РОДСТВЕННЫЕ ЗАЯВКИ
[001] Настоящая заявка испрашивает приоритет предварительной заявки на патент США 62/411,478, поданной 21 октября 2016 года, которая полностью включена в настоящий документ посредством отсылки.
УРОВЕНЬ ТЕХНИКИ
Область техники, к которой относится изобретение
[002] В настоящем описании предложено применение одного или более соединений индазол-3-карбоксамида или их солей или аналогов для лечения одного или более заболеваний или состояний, независимо выбранных из группы, состоящей из тендинопатии, дерматита, псориаза, бляшечной склеродермии, ихтиоза, синдрома Рейно и болезни Дарье; и/или для ускорения заживления ран. Способы включают введение субъекту (например, нуждающемуся в этом субъекту) терапевтически эффективного количества одного или более соединений индазол-3-карбоксамида или их солей или их аналогов, как описано в любой части настоящего документа.
Уровень техники
[003] Формирование паттерна представляет собой активность, с помощью которой эмбриональные клетки образуют упорядоченные пространственные структуры дифференцированных тканей. Предположение относительно механизмов, лежащих в основе этих эффектов формирования паттерна, обычно сосредоточено на секреции сигнальной молекулы, которая вызывает соответствующий ответ от тканей, формирующих паттерн. Недавняя работа, направленная на идентификацию таких сигнальных молекул, предполагает существование секретируемых белков, кодируемых отдельными представителями небольшого числа семейств генов.
[004] Семейство факторов роста Wnt включает более 10 генов, идентифицированных у мыши, и по меньшей мере 19 генов, идентифицированных у человека. Представители семейства Wnt сигнальных молекул опосредуют многие важные краткосрочные и долгосрочные процессы формирования паттернов во время развития беспозвоночных и позвоночных. Сигнальный путь Wnt известен своей важной ролью в индуктивных взаимодействиях, которые регулируют рост и дифференцировку, и играет важную роль в гомеостатическом поддержании целостности постэмбриональной ткани. Wnt стабилизирует цитоплазматический β-катенин, который стимулирует экспрессию генов, включающих c-myc, c-jun, fra-1 и циклин D1. Кроме того, нарушение регуляции сигнализации Wnt может вызывать дефекты развития и вовлечено в генез некоторых форм рака у человека. Недавно путь Wnt был связан с поддержанием стволовых клеток или клеток-предшественников в растущем списке зрелых тканей, который теперь включает кожу, кровь, кишечник, предстательную железу, мышцы и нервную систему.
[005] Также предполагают, что патологическая активация пути Wnt является первичным событием, приводящим к колоректальному раку в более чем 85% всех спорадических случаев в западных странах. Активацию пути Wnt также широко описывали при гепатоцеллюлярной карциноме, раке молочной железы, раке яичника, раке поджелудочной железы, меланомах, мезотелиомах, лимфомах и лейкозах. В дополнение к раку ингибиторы пути Wnt могут применяться для исследования стволовых клеток или для лечения каких-либо заболеваний, характеризуемых аберрантной активацией Wnt, таких как диабетическая ретинопатия, фиброз легких, ревматоидный артрит, склеродермия, а также микозы и вирусные инфекции, и заболевания костной и хрящевой ткани. Таким образом, это - терапевтическая мишень, которая представляет большой интерес в этой области.
[006] В дополнение к раку существует множество случаев генетических заболеваний, вызванных мутациями в компонентах сигнального пути Wnt. Примерами некоторых из многих заболеваний являются болезнь Альцгеймера [Proc. Natl. Acad. Sci. U S A (2007), 104 (22), 9434-9], остеоартроз, полипоз толстой кишки [Science (1991), 253(5020), 665-669], нарушения плотности костной ткани и сосудистые дефекты в глазу (синдром псевдоглиомы-остеопороза, OPPG) [N. Engl. J. Med. (2002), 346(20), 1513-21], семейная экссудативная витреоретинопатия [Hum. Mutat. (2005), 26(2), 104-12], ретинальный ангиогенез [Nat. Genet. (2002), 32(2), 326-30], начальная коронарная болезнь [Science (2007), 315(5816), 1278-82], синдром тетраамелии [Am. J. Hum. Genet. (2004), 74(3), 558-63], регрессия и вирилизация мюллерова протока [Engl. J. Med. (2004), 351(8), 792-8], синдром SERKAL [Am. J. Hum. Genet. (2008), 82(1), 39-47], сахарный диабет 2-го типа [Am. J. Hum. Genet. (2004), 75(5), 832-43; N. Engl. J. Med. (2006), 355(3), 241-50, синдром Фурмана [Am. J. Hum. Genet. (2006), 79(2), 402-8], синдром фокомелии Аль-Авади/Рааса-Ротшильда/Шинцеля [Am. J. Hum. Genet. (2006), 79(2), 402-8], одонто-ониходермальная дисплазия [Am. J. Hum. Genet. (2007), 81(4), 821-8], ожирение [Diabetologia (2006), 49(4), 678-84], мальформация расщепленной кисти/стопы [Hum. Mol. Genet. (2008), 17(17), 2644-53], синдром дупликации каудальной части [Am. J. Hum. Genet. (2006), 79(1), 155-62], агенез зубов [Am. J. Hum. Genet. (2004), 74(5), 1043-50], опухоль Вильмса [Science (2007), 315(5812), 642-5], дисплазия скелета [Nat. Genet. (2009), 41(1), 95-100], очаговая дермальная гипоплазия [Nat. Genet. (2007), 39(7), 836-8], аутосомно-рециссивная анонихия [Nat. Genet. (2006), 38(11), 1245-7], дефекты нервной трубки [N. Engl. J. Med. (2007), 356(14), 1432-7], синдром альфа-талассемии (ATRX) [The Journal of Neuroscience (2008), 28(47), 12570-12580], синдром ломкой Х-хромосомы [PLoS Genetics (2010), 6(4), e1000898], синдром ICF, синдром Ангельмана [Brain Research Bulletin (2002), 57(1), 109-119], синдром Прадера-Вилли [Journal of Neuroscience (2006), 26(20), 5383-5392], синдром Беквита-Видемана [Pediatric and Developmental Pathology (2003), 6(4), 299-306] и синдром Ретта.
[007] Регуляция клеточной сигнализации посредством сигнального пути Wnt важна для образования нейронных цепей. Путь Wnt модулирует в нервной ткани, помимо прочего, аксональное наведение, дендритное развитие и сборку синапсов. С помощью различных рецепторов путь Wnt активирует и/или регулирует разные сигнальные пути и другие процессы, которые приводят к локальным изменениям цитоскелета или общим клеточным изменениям, затрагивающим функцию ядра. Недавно была установлена связь между нейронной активностью, необходимой для формирования и улучшения нейронных соединений, и сигнальным путем Wnt. Действительно, активность нейронов регулирует высвобождение различных белков Wnt и локализацию их рецепторов. Путь Wnt опосредует синаптические структурные изменения, вызванные нейрональной активностью или ощущением. Опыт показывает, что дисфункция сигнализации Wnt способствует развитию неврологических нарушений [Brain Research Reviews (2000), 33(1), 1-12; Oncogene (2006) 25(57), 7545-7553; Molecular Neurodegeneration (2008), 3, 9; Neurobiology of Disease (2010), 38(2), 148-153; Journal of Neurodevelopmental Disorders (2011), 3(2), 162-174 и Cold Spring Harbor Perspectives in Biology February (2012), 4(2)].
[008] Тендинопатии представляют собой хронические нарушения или повреждения сухожилий, которые обычно возникают в результате постепенного износа и разрыва сухожилия, например, вызванных перенапряжением или старением, и приводят к дегенерации, слабости, разрыву и боли в сухожилиях. У людей, которые часто совершают многократные повторяющиеся движения в своей работе, спортивных упражнениях или регулярных ежедневных занятиях, с высокой вероятностью могут развиваться тендинопатии. Тендинопатия обычно вызывает боль, скованность и потерю силы в пораженной области.
[009] Заболевания кожи являются распространенными патологиями у многих людей. Некоторыми из наиболее распространенных заболеваний являются дерматит (также известный как экзема) и псориаз. Как дерматит, так и псориаз могут вызывать серьезные физические и/или психологические страдания у субъекта независимо от области локализации на теле, в которой возникают такие состояния.
[010] В WO 2013/040215 описаны индазол-3-карбоксамиды, имеющие Формулу (I), и их применение в качестве ингибиторов сигнального пути Wnt/B-катенина.
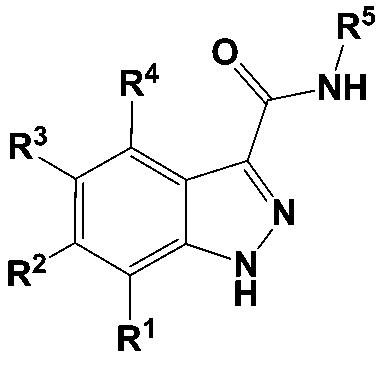 (I)
(I)
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[011] Настоящее описание относится к применению одного или более соединений индазол-3-карбоксамида или их солей или аналогов для лечения одного или более заболеваний или состояний, независимо выбранных из группы, состоящей из тендинопатии, дерматита, псориаза, бляшечной склеродермии, ихтиоза, синдрома Рейно и болезни Дарье; и/или для ускорения заживления ран. Способы включают введение субъекту (например, нуждающемуся в этом субъекту) терапевтически эффективного количества одного или более соединений индазол-3-карбоксамида или их солей или их аналогов, как описано в любой части настоящего документа.
[012] Один вариант осуществления, раскрытый в настоящем документе, включает введение соединения индазол-3-карбоксамида, имеющего структуру Формулы I:
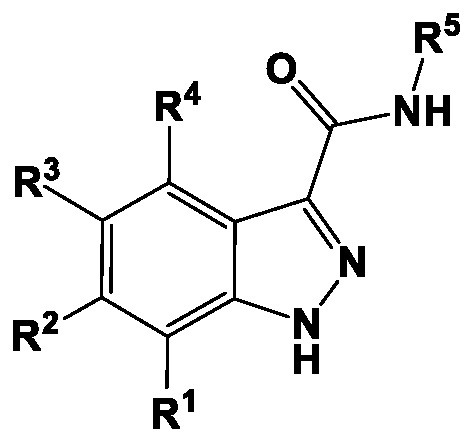
I
а также его пролекарств и фармацевтически приемлемых солей.
[013] В некоторых вариантах осуществления Формулы (I):
R1, R2 и R4 независимо выбраны из группы, состоящей из H, C1-9 алкила, галогенида, -N(R10)2, -XR10, CN, -OCF3 и -CF3;
R3 выбран из группы, состоящей из карбоциклилR6, гетероциклилR6, арилR6 и гетероарилR6;
R5 выбран из группы, состоящей из -(C1-9 алкил)nкарбоциклилR7, -(C1-9 алкил)nгетероциклилR7, -(C1-9 алкил)nарилR7 и -(C1-9 алкил)nгетероарилR7;
каждый R6 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-9 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR10, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8, -(C1-9 алкил)nгетероарилR8, -C(=O)R11, -N(R10)C(=O)R11, -(C1-9 алкил)nN(R10)2, -(C1-9 алкил)nN(R10)SO2R11 и -SO2R11;
каждый R7 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-9 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR10, -(C1-9 алкил)nкарбоциклилR9, -(C1-9 алкил)nгетероциклилR9, -(C1-9 алкил)nарилR9, -(C1-9 алкил)nгетероарилR9, -C(=O)R11, -N(R10)C(=O)R11, -(C1-9 алкил)nN(R10)2, -(C1-9 алкил)nN(R10)SO2R11 и -SO2R11;
каждый R8 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR12, -C(=O)R13, -N(R12)C(=O)R13, -(C1-9 алкил)nN(R12)2, -(C1-9 алкил)nN(R12)SO2R13 и -SO2R13;
каждый R9 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR12, -C(=O)R13, -N(R12)C(=O)R13, -(C1-9 алкил)nN(R12)2, -(C1-9 алкил)nN(R12)SO2R13 и -SO2R13;
каждый R10 независимо выбран из группы, состоящей из H, C1-9 алкила, -(C1-9 алкил)nN(R14)2, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8 и -(C1-9 алкил)nгетероарилR8;
каждый R11 независимо выбран из группы, состоящей из C1-9 алкила, -N(R14)2, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8 и -(C1-9 алкил)nгетероарилR8;
каждый R12 независимо выбран из группы, состоящей из H, C1-9 алкила, -(C1-9 алкил)nN(R14)2, -(C1-9 алкил)nкарбоциклила, -(C1-9 алкил)nгетероциклила, -(C1-9 алкил)nарила и -(C1-9 алкил)nгетероарила;
каждый R13 независимо выбран из группы, состоящей из C1-9 алкила, -N(R14)2, -(C1-9 алкил)nкарбоциклила, -(C1-9 алкил)nгетероциклила, -(C1-9 алкил)nарила и -(C1-9 алкил)nгетероарила;
каждый R14 независимо выбран из группы, состоящей из H, C1-3 алкила, карбоциклила и арила;
каждый X выбран из группы, состоящей из связи, -O- и -S-; и
каждое n является 0 или 1.
[014] В другом варианте осуществления Формулы (I):
R1, R2 и R4 независимо выбраны из группы, состоящей из H, C1-9 алкила, галогенида, -N(R10)2, -XR10, CN, -OCF3 и -CF3;
R3 выбран из группы, состоящей из карбоциклилR6, гетероциклилR6, арилR6 и гетероарилR6;
в некоторых вариантах осуществления при условии, что, когда R3 является гетероарилом, гетероарил не выбран из группы, состоящей из изохинолина, 1H-пирроло[2,3-c]пиридина и тетразола;
R5 выбран из группы, состоящей из -(C1-9 алкил)nкарбоциклилR7, -(C1-9 алкил)nгетероциклилR7, -(C1-9 алкил)nарилR7 и -(C1-9 алкил)nгетероарилR7;
в некоторых вариантах осуществления предусмотрено, что R5 не является 4-пиридилR7, когда R1, R2 и R4 является H, R3 выбран из группы, состоящей из 3-пиридилR6, 4-пиридилR6, 2-пиридилR6, фенилR6, тиазолR6, имидазолR6, пиримидинR6, оксазолR6, 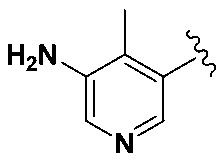 ,
, 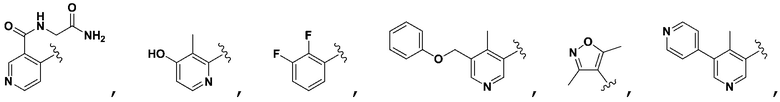
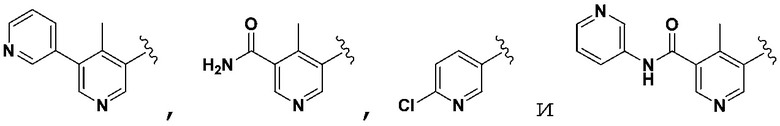 , и оба R6 и R7 являются H.
, и оба R6 и R7 являются H.
в некоторых вариантах осуществления предусмотрено, что R5 не является -(CH2)(3-пиридил)R7, когда R1, R2 и R4 являются H, R3 выбран из группы, состоящей из 3-пиридилR6, 4-пиридилR6 и тиазолR6, и оба R6 и R7 являются H;
в некоторых вариантах осуществления предусмотрено, что R5 не является фенилR7, когда R1, R2 и R4 являются H, R3 является 4-пиридилR6, и оба R6 и R7 являются H;
в некоторых вариантах осуществления предусмотрено, что R3 не является 3-пиридилR6, когда R1, R2 и R4 являются H, R5 выбран из группы, состоящей из фенилR7, 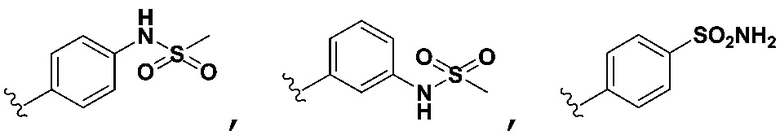 ,
, 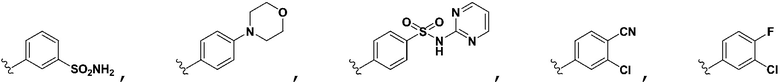 ,
, 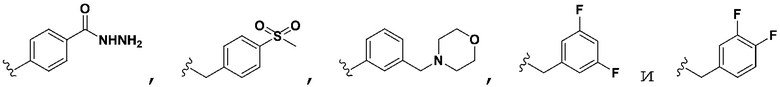 , и оба R6 и R7 являются H;
, и оба R6 и R7 являются H;
в некоторых вариантах осуществления предусмотрено, что R3 не оксазолR6, когда R1, R2 и R4 - H, R5 выбран из группы, состоящей из 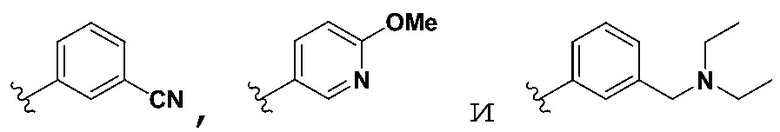 , и R6 является H;
, и R6 является H;
в некоторых вариантах осуществления предусмотрено, что R3 не тиазолR6, когда R1, R2 и R4 является H, R5 выбран из группы, состоящей из 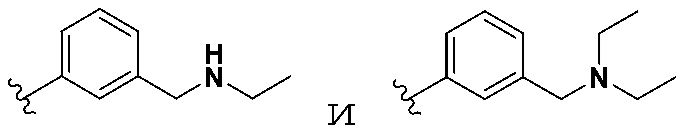 , и R6 является H;
, и R6 является H;
каждый R6 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-9 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR10, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8, -(C1-9 алкил)nгетероарилR8, -C(=O)R11, -N(R10)C(=O)R11, -(C1-9 алкил)nN(R10)2, -(C1-9 алкил)nN(R10)SO2R11 и -SO2R11;
каждый R7 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-9 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR10, -(C1-9 алкил)nкарбоциклилR9, -(C1-9 алкил)nгетероциклилR9, -(C1-9 алкил)nарилR9, -(C1-9 алкил)nгетероарилR9, -C(=O)R11, -N(R10)C(=O)R11, -(C1-9 алкил)nN(R10)2, -(C1-9 алкил)nN(R10)SO2R11 и -SO2R11;
каждый R8 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN -XR12, -C(=O)R13, -N(R12)C(=O)R13, -(C1-9 алкил)nN(R12)2, -(C1-9 алкил)nN(R12)SO2R13 и -SO2R13;
каждый R9 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR12, -C(=O)R13, -N(R12)C(=O)R13, -(C1-9 алкил)nN(R12)2, -(C1-9 алкил)nN(R12)SO2R13 и -SO2R13;
каждый R10 независимо выбран из группы, состоящей из H, C1-9 алкила, -(C1-9 алкил)nN(R14)2, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8 и -(C1-9 алкил)nгетероарилR8;
каждый R11 независимо выбран из группы, состоящей из C1-9 алкила, -N(R14)2, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8 и -(C1-9 алкил)nгетероарилR8;
каждый R12 независимо выбран из группы, состоящей из H, C1-9 алкила, -(C1-9 алкил)nN(R14)2, -(C1-9 алкил)nкарбоциклил, -(C1-9 алкил)nгетероциклил, -(C1-9 алкил)nарил и -(C1-9 алкил)nгетероарил;
каждый R13 независимо выбран из группы, состоящей из C1-9 алкила, -N(R14)2, -(C1-9 алкил)nкарбоциклила, -(C1-9 алкил)nгетероциклила, -(C1-9 алкил)nарила и -(C1-9 алкил)nгетероарила;
каждый R14 независимо выбран из группы, состоящей из H, C1-3 алкила, карбоциклила и арила;
каждый X выбран из группы, состоящей из связи, -O- и -S-; и
каждое n является 0 или 1.
[015] Некоторые варианты осуществления включают введение стереоизомеров и фармацевтически приемлемых солей соединения общей Формулы (I).
[016] Некоторые варианты осуществления включают введение пролекарств соединения общей Формулы (I).
[017] Некоторые варианты осуществления включают введение фармацевтических композиций, включающих соединение общей Формулы (I) в фармацевтически приемлемом носителе, разбавителе или вспомогательном веществе.
[018] Следует понимать, что предыдущее общее описание и следующее подробное описание являются лишь примерными и пояснительными и не ограничивают заявленное изобретение.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[019] На ФИГ. 1 представлен график, на котором показано, что воздействие на линию клеток колоректального рака человека (SW480) соединения 175 дозозависимо ингибирует активность Wnt/β-катенина в этих клетках (EC50=152,9 нМ). Линию клеток колоректального рака человека (SW480) с конститутивной активацией пути Wnt и модифицированную для экспрессии Wnt-чувствительного промотора, связанного с люциферазой, обрабатывали соединением 175 в тестируемых концентрациях 10, 3, 1, 0,3, 0,1, 0,03, 0,01, 0,003, 0,001 и 0,0003 мкМ.
[020] На ФИГ. 2A-C представлены графики процента мезенхимальных стволовых клеток человека (МСКч), экспрессирующих SCXA, тенацин C и теномодулин, соответственно, в зависимости от концентрации соединения 175. Мезенхимальные стволовые клетки человека обрабатывали соединением 175 в тестируемых концентрациях 750, 333,3, 166,6, 83,3, 41,7, 21,7, 10,8 и 5,8 нМ. Воздействие на клетки соединения 175 в течение 7 дней индуцировало экспрессию маркеров дифференцировки теноцитов - SCXA, тенацина C и теномодулина - в зависимости от дозы (EC50=139-189 нМ).
[021] ФИГ. 3 - изображения экспрессии SCXA, тенацина C и теномодулина в МСКч, обработанных ДМСО, костным морфогенетическим белком (BMP) и фактором роста фибробластов (FGF) и соединением 175 при концентрации 333 нМ.
[022] На ФИГ. 4A-B представлены графики концентрации фактора некроза опухоли альфа в клетках THP-1 в зависимости от логарифма концентрации соединения 175, воздействовавшего на клетки THP-1, и концентрации интерлейкина-6 в клетках THP-1 в зависимости от логарифма концентрации соединения 175, воздействовавшего на клетки THP-1, соответственно. Клетки THP-1, линию клеток человеческих моноцитов (6×10e4 клеток/лунка в 96-луночнос планшете), обрабатывали ДМСО (среда) или соединением 175 при концентрациях 10, 3,5, 1, 0,5, 0,1, 0,035, 0,01, 0,005 мкМ. Через 2 часа обработанные клетки стимулировали ЛПС (50 нг/мл в течение 5 часов [ФНОα] и 500 нг/мл в течение 22 часов [IL6]) при 37°C для индукции выработки цитокинов. Супернатанты (разведенные 1:1 или 1:4) собирали и исследовали на уровни ФНОα и IL6 при использовании наборов для ИФА ФНОα и IL6. Профиль ингибирования и EC50 вычисляли при использовании Prism 5. Репрезентативные изображения указывают, что воздействие соединения 175 на клетки приводило к дозозависимому ингибированию продукции ФНОα (4А) и IL6 (4B) в клетках THP-1 со средним значением EC50 342-547 нМ для ФНОα и 356-629 нМ для IL6 (2 независимых анализа и 3 повторности на анализ).
[023] ФИГ. 5 - сетка изображений ахиллова сухожилия крысы; ахиллово сухожилие крысы, обработанное коллагеназой с растворителем; ахиллово сухожилие крысы, обработанное коллагеназой, соединением 175 и бензиловым спиртом; и ахиллово сухожилие крысы, обработанное коллагеназой и соединением 175. Тендинопатию у крыс индуцировали инъекцией коллагеназы (50 мкл, 10 мг/мл типа IA в PBS, pH 7,4, ~469 единиц/мг) или ложной пункцией иглой для контроля в ахиллово сухожилие. Через 1 день крысам один раз в день в течение 21 дня путем наружного применения наносили контрольный растворитель или соединение 175 (10 мг/мл). Через 24 часа после последней дозы извлекали сухожилия, фиксировали 10% забуференным формалином, изготавливали срезы и окрашивали Г-Э. Группа 1 (ложная инъекция), Группа 2 (коллагеназа-растворитель), Группа 3 (коллагеназа-соединение 175 с 1% BA) и Группа 4 (Коллагеназа-соединение 175 с 0,5% Tween 80, без BA).
[024] ФИГ. 6 является диаграммой оценок гистологического исследования ахиллова сухожилия крыс; ахиллова сухожилия крысы, обработанного коллагеназой с носителем; ахиллова сухожилия крысы, обработанного коллагеназой, соединением 175 и бензиловым спиртом; и ахиллова сухожилия крысы, обработанного коллагеназой и соединением 175. Тендинопатию у крыс индуцировали инъекцией коллагеназы (50 мкл, 10 мг/мл типа IA в PBS, pH 7,4, ~469 единиц/мг) или ложной пункцией иглой для контроля в ахиллово сухожилие. Через 1 день крысам один раз в день в течение 21 дня путем местного применения наносили контрольный растворитель или соединение 175 (10 мг/мл). Через 24 часа после последней дозы извлекали сухожилия, фиксировали 10% забуференным формалином, изготавливали срезы и окрашивали Г-Э. Группа 1 (ложная инъекция), Группа 2 (коллагеназа-носитель), Группа 3 (коллагеназа-соединение 175 с 1% BA) и Группа 4 (коллагеназа-соединение 175 с 0,5% Tween 80, без BA). Слепая гистологическая оценка повреждения и воспаления сухожилия показала, что соединение 175 с или без консерванта BA значимо уменьшало тендинопатию, вызванную коллагеназой (**р<0,01 и *р<0,05 соответственно), при использовании критерия Стьюдента. В этом исследовании оценивали 64 среза для Группы 1 и ~96 секций для каждой из Групп 2-4.
[025] ФИГ. 7 - серия графиков зависимости концентраций KC/GRO в плазме у крыс от количества дней, прошедших после введения растворителя, соединения 175 с бензиловым спиртом и соединения 175. Тендинопатию у крыс индуцировали инъекцией коллагеназы (50 мкл, 10 мг/мл типа IA в PBS, pH 7,4, ~469 единиц/мг) в ахиллово сухожилие. Через 1 день крысам один раз в день в течение 21 дня путем наружного применения наносили контрольный растворитель или соединение 175 (10 мг/мл). Кровь забирали в различные временные точки и исследовали плазму на KC/GRO с помощью ИФА. Измерение воспалительного цитокина KC/GRO в плазме крыс в Группе 2 (коллагеназа-растворитель), Группа 3 (коллагеназа-соединение 175 10 мг/мл с 1% BA) и Группа 4 (коллагеназа-соединение 175 10 мг/мл без BA, с 0,5% Tween 80). Соединение 175 с или без консерванта BA значимо снижало уровни KC/GRO в плазме (p<0,05, t-критерий Стьюдента), что указывает на противовоспалительное действие соединения 175. Эти данные были получены с 3 повторностями на каждую временную точку для каждой группы (n=3).
[026] ФИГ. 8 - сетка изображений ахиллова сухожилия крысы; ахиллова сухожилия крысы, обработанного коллагеназой с растворителем; ахиллова сухожилия крысы, обработанного коллагеназой, 3 мг/мл соединения 175 и бензилового спирта; ахиллова сухожилия крысы, обработанного коллагеназой, 10 мг/мл соединения 175 и бензилового спирта; ахиллова сухожилия крысы, обработанного коллагеназой, 3 мг/мл соединения 175 и Phx; и ахиллова сухожилия крысы, обработанного коллагеназой, 10 мг/мл соединения 175 и Phx. Тендинопатию у крыс индуцировали инъекцией коллагеназы (50 мкл, 10 мг/мл типа IA в PBS, pH 7,4, ~469 единиц/мг) или ложной пункцией иглой для контроля в ахиллово сухожилие. Через 1 день крысам один раз в день в течение 21 дня путем наружного применения наносили растворитель или соединение 175 в лекарственных формах для наружного применения. Через 24 часа после последней дозы извлекали сухожилия, фиксировали 10% забуференным формалином, изготавливали срезы и окрашивали Г-Э. Группа 1 (ложная инъекция), Группа 2 (коллагеназа-растворитель с 0,5% Phx), Группа 3 (коллагеназа-соединение 175 3 мг/мл с 0,5% BA), Группа 4 (коллагеназа-соединение 175 10 мг/мл с 0,5% BA), Группа 5 (коллагеназа-соединение 175 3 мг/мл с 0,5% Phx) и Группа 6 (коллагеназа-соединение 175 10 мг/мл с 0,5% Phx).
[027] ФИГ. 9 - диаграмма оценки гистологического исследования ахиллова сухожилия крысы; ахиллова сухожилия крысы, обработанного коллагеназой с растворителем; ахиллова сухожилия крысы, обработанного коллагеназой, 3 мг/мл соединения 175 и бензиловым спиртом; ахиллова сухожилия крысы, обработанного коллагеназой, 10 мг/мл соединения 175 и бензиловым спиртом; ахиллова сухожилия крысы, обработанного коллагеназой, 3 мг/мл соединения 175 и Phx; и ахиллова сухожилия крысы, обработанного коллагеназой, 10 мг/мл соединения 175 и Phx. Тендинопатию у крыс индуцировали инъекцией коллагеназой (50 мкл, 10 мг/мл типа IA в PBS, pH 7,4, ~469 единиц/мг) или ложной пункцией иглой для контроля в ахиллово сухожилие. Через 1 день крысам один раз в день в течение 21 дня путем наружного применения наносили растворитель или лекарственную форму соединения 175 для наружного применения. Через 24 часа после последней дозы извлекали сухожилия, фиксировали 10% забуференным формалином, изготавливали срезы и окрашивали Г-Э. Группа 1 (ложная инъекция), Группа 2 (коллагеназа-растворитель с 0,5% Phx), Группа 3 (коллагеназа-соединение 175 3 мг/мл с 0,5% BA), Группа 4 (коллагеназа-соединение 175 10 мг/мл с 0,5% BA), Группа 5 (коллагеназа-соединение 175 3 мг/мл с 0,5% Phx) и Группа 6 (коллагеназа-соединение 175 10 мг/мл с 0,5% Phx). Слепая оценка гистологического исследования повреждения и воспаления сухожилий указывает, что соединение 175 в концентрации 3 и 10 мг/мл с BA или Phx в качестве консерванта значимо уменьшало тендинопатию, вызванную коллагеназой (**р<0,01 и ***р<0,001), при использовании t-критерия Стьюдента. В этом исследовании в общей сложности оценивали 94 среза для Группы 1 и 92-116 срезов для Групп 2-6.
[028] ФИГ. 10 - серия графиков зависимости концентраций KC/GRO в плазме у крыс от количества дней, прошедших после введения растворителя, 3 мг/мл соединения 175 с бензиловым спиртом, 10 мг/мл соединения 175 с бензиловым спиртом, 3 мг/мл соединения 175 с Phx и 10 мг/мл соединения 175 с Phx. Тендинопатию у крыс индуцировали инъекцией коллагеназы (50 мкл, 10 мг/мл типа IA в PBS, pH 7,4, ~469 единиц/мг) в ахиллово сухожилие. Через 1 день крысам один раз в день в течение 21 дня путем наружного применения наносили контрольный растворитель или соединение 175. Кровь забирали в различные временные точки и исследовали плазму на KC/GRO с помощью ИФА. Измерение воспалительного цитокина KC/GRO в плазме крыс в Группе 2 (коллагеназа-растворитель, содержащий 0,5% Phx), Группе 3 (коллагеназа-соединение 175 3 мг/мл с 0,5% BA), Группе 4 (коллагеназа-соединение 175 10 мг/мл с 0,5% BA), Группе 5 (коллагеназа-соединение 175 3 мг/мл с 0,5% Phx) и Группе 6 (коллагеназа-соединение 175 10 мг/мл с 0,5% Phx). Соединение 175 в обеих концентрациях дозы 3 и 10 мг/мл, с BA или Phx в качестве консерванта, значимо снижало уровни KC/GRO в плазме по сравнению с растворителем (p<0,05 и p<0,01, t-критерий Стьюдента, как показано в Таблице 5), что указывает на противовоспалительное действие соединения 175. Эти данные были получены в 3 повторностях на каждую временную точку для каждой группы (n=3).
[029] ФИГ. 11 - серия графиков зависимости концентраций соединения 175 от времени в сухожилиях, плазме и коже крыс линии Спрег-Доули после наружного применения 1 мг/мл соединения 175 и бензилового спирта, 10 мг/мл соединения 175 и бензилового спирта и 10 мг/мл соединения 175.
ПОДРОБНОЕ ОПИСАНИЕ
[030] Настоящее описание относится к применению одного или более соединений индазол-3-карбоксамида или их солей или аналогов для лечения одного или более заболеваний или состояний, независимо выбранных из группы, состоящей из тендинопатии, дерматита, псориаза, бляшечной склеродермии, ихтиоза, синдрома Рейно и болезни Дарье; и/или для ускорения заживления ран. Способы включают введение субъекту (например, нуждающемуся в этом субъекту) терапевтически эффективного количества одного или более соединений индазол-3-карбоксамида или их солей или аналогов, как описано в любой части настоящего документа.
Определения
[031] Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют такое же значение, которое обычно известно специалистам в области техники, к которой относится настоящее описание. Все патенты, заявки, опубликованные заявки и другие публикации полнотстью включены посредством отсылки. В случае, когда существует множество определений термина в настоящем документе, определения в данном разделе имеют преимущественную силу, если не указано иное.
[032] В настоящем описании и в формуле изобретения следующие термины имеют значения, определенные ниже. При использовании в настоящем документе "алкил" означает химическую группу с развевленной или нормальной цепью, содержащую только углерод и водород, такую как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил и пентил. Алкильные группы могут быть незамещенными или могут быть замещены одним или более заместителями, например, галогенидом, алкокси, ацилокси, амино, амидо, циано, нитро, гидроксилом, меркапто, карбокси, карбонилом, бензилокси, арилом, гетероарилом или другими функциональными группами, которые могут быть соответствующим образом блокированы защитными группами, если это необходимо в рамках изобретения. Алкильные группы могут быть насыщенными или ненасыщенными (например, содержащими субъединицы -C=C- или -C≡C-) по одному или нескольким положениям. Как правило, алкильные группы включают от 1 до 9 атомов углерода, предпочтительно от 1 до 6, более предпочтительно от 1 до 4 и, наиболее предпочтительно, от 1 до 2 атомов углерода.
[033] При использовании в настоящем документе "карбоциклил" означает циклическую кольцевую систему, содержащую только атомы углерода в скелете кольцевой системы, такую как циклопропил, циклобутил, циклопентил, циклогексил и циклогексенил. Карбоциклилы могут включать множество конденсированных колец. Карбоциклилы могут иметь любую степень насыщенности при условии, что по меньшей мере одно кольцо в кольцевой системе не является ароматическим. Карбоциклильные группы могут быть незамещенными или могут быть замещены одним или более заместителями, например, алкилом, галогенидом, алкокси, ацилокси, амино, амидо, циано, нитро, гидроксилом, меркапто, карбокси, карбонилом, бензилокси, арилом, гетероарилом или другими функциональными группами, которые могут быть соответствующим образом блокированы защитными группами, если это необходимо в рамках изобретения. Как правило, карбоциклильные группы включают от 3 до 10 атомов углерода, предпочтительно от 3 до 6.
[034] При использовании в настоящем документе "низший алкил" означает подтип алкила, содержащий от 1 до 3 атомов углерода, и, таким образом, представляет собой углеводородный заместитель, который является линейным или разветвленным. Примеры низшего алкила включают метил, этил, н-пропил и изопропил. Аналогичным образом, радикалы с использованием терминологии "низший" относятся к радикалам, предпочтительно содержащим от 1 до примерно 3 атомов углерода в алкильной части радикала.
[035] При использовании в настоящем документе "амидо" означает группу H-CON- или алкил-CON-, карбоциклил-CON-, арил-CON-, гетероарил-CON- или гетероциклил-CON, где алкильная, карбоциклильная, арильная или гетероциклильная группа являются такими, как описано в настоящем документе.
[036] При использовании в настоящем документе "арил" означает ароматический радикал, содержащий единственное кольцо (например, фенил) или множество конденсированных колец (например, нафтил или антрил), содержащих только атомы углерода в кольцевом скелете. Арильные группы могут быть незамещенными или могут быть замещены одним или более заместителями, например, алкилом, амино, циано, гидроксилом, низшим алкилом, гелогеналкилом, алкокси, нитро, гелогеном, меркапто и другими заместителями. Предпочтительным карбоциклическим арилом является фенил.
[037] При использовании в настоящем документе термин "гетероарил" означает ароматический радикал, содержащий один или более гетероатом (например, N, O или S) в кольцевом скелете, и может включать единственное кольцо (например, пиридин) или множество конденсированных колец (например, хинолин). Гетероарильные группы могут быть незамещенными или могут быть замещены одним или более заместителями, например, амино, циано, гидроксилом, низшим алкилом, галогеналкилом, алкокси, нитро, галогеном, меркапто и другими заместителями. Примеры гетероарила включают тиенил, пиридинил, фурил, оксазолил, оксадиазолил, пирролил, имидазолил, триазолил, тиодиазолил, пиразолил, изоксазолил, тиадиазолил, пиранил, пиразинил, пиримидинил, пиридазинил, триазинил, тиазолил, бензотиенил, бензоксадиазолил, бензофуранил, бензимидазолил, бензотриазолил, циннолинил, индазолил, индолил, изохинолинил, изотиазолил, нафтиридинил, пуринил, тиенопиридинил, пиридо[2,3-d]пиримидинил, пирроло[2,3-b]пиридинил, хиназолинил, хинолинил, тиено[2,3-c]пиридинил, пиразоло[3,4-b]пиридинил, пиразолo[3,4-c]пиридинил, пиразоло[4,3-c]пиридин, пиразолo[4,3-b]пиридинил, тетразолил и другие.
[038] В этих определениях прямо предусмотрено, что замещение на арильном и гетероарильном кольцах находится в рамках объема определенных вариантов осуществления. В случае, когда присутствует замещение, радикал называется замещенным арилом или замещенным гетероарилом. Предпочтительно на арильном кольце присутствуют от одного до трех, и более предпочтительно один или два заместителя. Хотя могут быть использоваться многие заместители, предпочтительные заместители включают такие, которые обычно присутствуют в арильных соединениях, такие как алкил, циклоалкил, гидрокси, алкокси, циано, галоген, галогеналкил, меркапто и т.п.
[039] При использовании в настоящем документе "амид" включает как RNR'CO- (в случае, когда R=алкил, алкаминокарбонил-), так и RCONR'- (в случае, когда R=алкил, алкилкарбониламино-).
[040] При использовании в настоящем документе термин "сложный эфир" включает как ROCO- (в случае, когда R=алкил, алкоксикарбонил-), так и RCOO- (в случае, когда R=алкил, алкилкарбонилокси-).
[041] При использовании в настоящем документе "ацил" означает группу H-CO- или алкил-CO-, карбоциклил-CO-, арил-O-, гетероарил-CO- или гетероциклил-CO-, где алкильная, карбоциклильная, арильная или гетероциклильная группа является такой, как описано в настоящем документе. Предпочтительные ацилы содержат низший алкил. Примеры алкилацильных групп включают формил, ацетил, пропаноил, 2-метилпропаноил, трет-бутилацетил, бутаноил и пальмитоил.
[042] При использовании в настоящем документе "гелоген", "галогенид" или "галоген" представляют собой радикал атома хлора, брома, фтора или иода. Хлор, бром и фтор являются предпочтительными галогенами. Наиболее предпочтительным галогеном является фтор.
[043] При использовании в настоящем документе "гелогеналкил" означает углеводородный заместитель, который является линейным или разветвленным или циклическим алкилом, алкенилом или алкинилом, который замещен атомом(ами) хлора, брома, фтора или иода. Наиболее предпочтительными из них являются фторалкилы, в которых один или более атомов водорода замещены фтором. Предпочтительные гелогеналкилы имеют длину от 1 до приблизительно 3 углеродов, более предпочтительные гелогеналкилы имеют длину от 1 до приблизительно 2 углеродов, и наиболее предпочтительные имеют длину 1 углерод. Специалисту в данной области будет известно, что при использовании в настоящем документе "галогеналкилен" означает дирадикальный вариант галогеналкила, при этом такие дирадикалы могут служить в качестве спейсеров между радикалами, другими атомами или между исходным кольцом и другой функциональной группой.
[044] При использовании в настоящем документе "гетероциклил" означает циклическую кольцевую систему, содержащую по меньшей мере один гетероатом в скелете кольцевой системы. Гетероциклилы могут включать множество конденсированных колец. Гетероциклилы могут иметь любую степень насыщенности при условии, что по меньшей мере одно кольцо в кольцевой системе не является ароматическим. Гетероциклилы могут быть незамещенными или могут быть замещены одним или более заместителями, например, алкилом, галогеном, алкокси, ацилокси, амино, амидо, циано, нитро, гидроксилом, меркапто, карбокси, карбонилом, бензилокси, арилом, гетероарилом и другими заместителями, и соединены с другими группами посредством любой доступной валентности, предпочтительно через любой доступный углерод или азот. Более предпочтительные гетероциклы являются 5-7-членными. В шестичленных моноциклических гетероциклах гетероатом(ы) выбран(ы) из одного и до трех O, N или S, и где в том случа, когда гетероцикл является пятичленным, он предпочтительно содержит один или два гетероатома, выбранные из O, N или S. Примеры гетероциклила включают азиринил, азиридинил, азетидинил, оксетанил, тиетанил, 1,4,2-дитиазолил, 1,3-бензодиоксолил, дигидроизоиндолил, дигидроизохинолинил, дигидроциннолинил, дигидробензодиоксинил, дигидро[1,3]оксазоло[4,5-b]пиридинил, бензотиазолил, дигидроиндолил, дигидропиридинил, 1,3-диоксанил, 1,4-диоксанил, 1,3-диоксоланил, изоиндолинил, морфолинил, тиоморфолинил, пиперазинил, пиранил, пирролидинил, тетрагидрофурил, тетрагидропиридинил, оксазинил, тиазинил, тиинил, тиазолидинил, изотиазолидинил, оксазолидинил, изоксазолидинил, пиперидинил, пиразолидинил, имидазолидинил, тиоморфолинил и другие.
[045] При использовании в настоящем документе "замещенный амино" означает аминорадикал, который замещен одним или двумя алкильными, циклоалкильными, арильными, гетероарильными или гетероциклильными группами, где алкил, арил, гетероарил или гетероциклил определены, как указано выше.
[046] При использовании в настоящем документе "замещенный тиол" означает RS- группу, где R является алкильной, арильной, гетероарильной или гетероциклильной группой, где алкил, циклоалкил, арил, гетероарил или гетероциклил определены, как указано выше.
[047] При использовании в настоящем документе "сульфонил" означает алкилSO2, арилSO2, гетероарилSO2, карбоциклилSO2 или гетероциклил-SO2 группу, где алкил, карбоциклил, арил, гетероарил или гетероциклил определены, как указано выше.
[048] При использовании в настоящем документе "сульфамидо" означает алкил-N-S(O)2N-, арил-NS(O)2N-, гетероарил-NS(O)2N-, карбоциклил-NS(O)2N или гетероциклил-NS(O)2N- группу, где алкильная, карбоциклильная, арильная, гетероарильная или гетероциклильная группа является такой, как описано в настоящем документе.
[049] При использовании в настоящем документе "сульфонамидо" означает алкил-S(O)2N-, арил-S(O)2N-, гетероарил-S(O)2N-, карбоциклил-S(O)2N- или гетероциклил-S(O)2N- группу, где алкильная, карбоциклильная, арильная, гетероарильная или гетероциклильная группа является такой, как описано в настоящем документе.
[050] При использовании в настоящем документе "уреидо" означает алкил-NCON-, арил-NCON-, гетероарил-NCON-, карбоциклил-NCON- или гетероциклил-NCON- группу, где алкильная, карбоциклильная, арильная, гетероарильная или гетероциклильная группа является такой, как описано в настоящем документе.
[051] При использовании в настоящем документе, когда две группы указаны как "соединенные" или "связанные" с образованием "кольца", следует понимать, что связь образуется между двумя группами и может включать замену атома водорода на одной или обеих группах связью, с образованием в результате карбоциклильного, гетероциклильного, арильного или гетероарильного кольца. Специалисту в данной области будет известно, что такие кольца могут легко образоваться и образуются в результате обычных химических реакций, при этом в компетенцию специалиста входят как такие кольца, так и способы их образования. Предпочтительными являются кольца, содержащие от 3-7 членов, более предпочтительно 5 или 6 членов. При использовании в настоящем документе термин "кольцо" или "кольца", при их образовании в результате объединения двух радикалов, относится к гетероциклическим, карбоциклическим, арильным или гетероарильным кольцам.
[052] Специалисту в данной области будет известно, что некоторые структуры, описанные в настоящем документе, могут быть резонансными формами или таутомерами соединений, которые могут быть фактически представлены другими химическими структурами, даже кинетически; специалисту будет известно, что такие структуры составляют лишь очень малую часть образца такого соединения(й). Такие соединения прямо предусмотрены в рамках объема настоящего изобретения, хотя такие резонансные формы или таутомеры могут не быть прямо представлены в настоящем описании.
[053] Соединения, предложенные в настоящем документе, могут включать различные стереохимические формы. Соединения также охватывают диастереомеры, как и оптические изомеры, например, смеси энантиомеров, в том числе рацемические смеси, а также индивидуальные энантиомеры и диастереомеры, которые возникают вследствие структурной асимметрии в некоторых соединениях. Разделение отдельных изомеров или селективный синтез отдельных изомеров осуществляют путем применения различных способов, которые хорошо известны специалистам в данной области техники. Если не указано иное, когда раскрытое соединение названо или изображено в виде структуры без указания стереохимии и имеет один или более хиральных центров, следует понимать, что присутствуют все возможные стереоизомеры соединения.
[054] Термин "введение" относится к способу предоставления дозы соединения или фармацевтической композиции позвоночным или беспозвоночным, в том числе млекопитающим, птицам, рыбам или земноводным, где способ осуществляют, например, перорально, подкожно, внутривенно, интраназально, наружно, трансдермально, внутрибрюшинно, внутримышечно, внутрилегочно, вагинально, ректально, онтологически, нейроотологически, внутриглазным путем, субконъюктивально, путем инъекции в переднюю камеру глаза, в стекловидное тело, внутрибрюшинно, интратекально, внутрикистозно, внутриплеврально, путем орошения раны, в слизистую ротовой полости, интраабдоминально, внутрисуставно, внутриушным путем, внутрибронхиально, интракапсулярно, интраменингеально, путем ингаляции, путем эндотрахеальной или эндобронхиальной инстилляции, путем прямой инстилляции в легочные полости, интраспинально, интрасиновиально, интраторакально, путем орошения при дренировании плевральной полости, эпидурально, внутригрудинно, интрацистернально, внутрисосудисто, интравентрикулярно, внутрикостно, путем орошения инфицированной кости или путем нанесения в виде компонента любой смеси на протезные устройства. Предпочтительный способ введения может изменяться в зависимости от различных факторов, например, компонентов фармацевтической композиции, участка заболевания, конкретного вовлеченного заболевания и тяжести заболевания.
[055] "Диагностическое средство" при использовании в настоящем документе является соединением, способом, системой или устройством, которое способствует идентификации и определению состояния здоровья или патологического состояния. Диагностическое средство может применяться в стандартных анализах, как известно в данной области техники.
[056] Термин "млекопитающее" используется в его обычном биологическом смысле. Таким образом, термин, в частности, включает людей, крупный рогатый скот, лошадей, собак и кошек, но также включает многие другие биологические виды.
[057] Термин "фармацевтически приемлемый носитель" или "фармацевтически приемлемое вспомогательное вещество" включает любые возможные растворители, сорастворители, комплексообразователи, дисперсионные среды, покрытия, антибактериальные и противогрибковые средства, изотонические и задерживающие абсорбцию вещества и т.п., которые не являются биологически или иным образом нежелательными. Применение таких сред и средств для фармацевтически активных веществ хорошо известно в данной области. За исключением любых стандартных сред или средств, несовместимых с действующим веществом, предусмотрено их применение в терапевтических композициях. В композиции также могут быть включены дополнительные действующие вещества. Кроме того, могут быть включены различные вспомогательные вещества, такие как обычно используемые в данной области. Эти и другие указанные соединения описаны в литературе, например, в Merck Index, Merck & Company, Rahway, NJ. Рекомендации по включению различных компонентов в фармацевтические композиции описаны, например, в Gilman et al. (Eds.) (2010); Goodman and Gilman's: The Pharmacological Basis of Therapeutics, 12th Ed., The McGraw-Hill Companies.
[058] Термин "фармацевтически приемлемая соль" относится к солям, которые сохраняют биологическую эффективность и свойства соединений предпочтительных вариантов осуществления, и которые не являются биологически или иным образом нежелательными. Во многих случаях соединения предпочтительных вариантов осуществления изобретения способны образовывать соли кислот и/или оснований благодаря присутствию аминогруппы и/или карбоксильной группы или подобной им группы, в присутствии аминогруппы и/или карбоксильной группы или подобной им группы. Фармацевтически приемлемые соли присоединения кислот могут быть образованы с неорганическими кислотами и органическими кислотами. Неорганические кислоты, с которыми могут быть получены соли, включают, например, соляную кислоту, бромоводородную кислоту, серную кислоту, азотную кислоту, фосфорную кислоту и т.п. Органические кислоты, с которыми могут быть получены соли, включают, например, уксусную кислоту, пропионовую кислоту, гликолевую кислоту, пировиноградную кислоту, щавелевую кислоту, малеиновую кислоту, малоновую кислоту, янтарную кислоту, фумаровую кислоту, винную кислоту, лимонную кислоту, бензойную кислоту, коричную кислота, миндальную кислоту, метансульфоновую кислоту, этансульфоновую кислоту, п-толуолсульфоновую кислоту, салициловую кислоту и т.п. Фармацевтически приемлемые соли присоединения оснований могут быть образованы с неорганическими и органическими основаниями. Неорганические основания, с которыми могут быть получены соли, включают, например, натрий, калий, литий, аммоний, кальций, магний, железо, цинк, медь, марганец, алюминий и т.п.; особенно предпочтительными являются соли аммония, калия, натрия, кальция и магния. Органические основания, с которыми могут быть получены соли, включают, например, первичные, вторичные и третичные амины, замещенные амины, в том числе природные замещенные амины, циклические амины, основные ионообменные смолы и т.п., в частности, такие как изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин и этаноламин. Многие такие соли известны в данной области, как описано в международной патентной публикации 87/05297, Johnston et al., опубликованной 11 сентября 1987 года (включенной в настоящее описание посредством отсылки).
[059] "Сольват" относится к соединению, образующемуся при взаимодействии растворителя и ингибитора пути Wnt, его метаболита или соли. Подходящие сольваты являются фармацевтически приемлемыми сольватами, в том числе гидратами.
[060] "Субъект" при использовании в настоящем документе означает человека или не относящегося к человеку млекопитающего, например, собаку, кошку, мышь, крысу, корову, овцу, свинью, козу, не относящегося к человеку примата или птицу, например, курицу, а также любое другое позвоночное или беспозвоночное.
[061] "Терапевтически эффективное количество" или "фармацевтически эффективное количество" является таким количеством, которое достаточно для достижения требуемого эффекта, при этом оно может изменяться в зависимости от природы и тяжести патологического состояния и эффективности соединения. Термин "терапевтически эффективное количество" также включает одно или более соединений формулы (I) в комбинации с одним или более другими средствами, которые являются эффективными для ингибирования связанных с Wnt заболеваний и/или состояний. Комбинация соединений предпочтительно является синергической комбинацией. Синергизм, как описано, например, Chou and Talalay, Advances in Enzyme Regulation (1984), 22, 27-55, наблюдается, когда эффект соединений при введении в комбинации превосходит аддитивный эффект соединений при отдельном введении в виде одного средства. Как правило, синергетический эффект наиболее четко проявляется при субоптимальных концентрациях соединений. Следует понимать, что для профилактики могут использоваться другие концентрации, нежели чем при лечении активного заболевания. Такое количество может также зависеть от роста, веса, пола, возраста пациента и сведений о перенесенных им заболеваниях.
[062] Терапевтический эффект облегчает, в некоторой степени, один или более симптомов заболевания и включает излечение заболевания. "Излечение" означает устранение симптомов активного заболевания. Однако некоторые долгосрочные или постоянные эффекты заболевания могут существовать даже после пройденного лечения (такие как обширное повреждение ткани).
[063] "Лечить" или "лечение" при использовании в настоящем документе относятся к введению фармацевтической композиции с терапевтическими целями. Термин "терапевтическое лечение" относится к введению препарата пациенту, уже страдающему заболеванием, в результате чего достигается терапевтически благоприятный эффект, например, облегчение имеющихся симптомов, предотвращение дополнительных симптомов, облегчение или предотвращение первичных метаболических причин симптомов, задержка или предотвращение дальнейшего развития нарушения и/или уменьшение тяжести симптомов, которые будут или предположительно могут развиваться.
[064] "Бляшечная склеродермия" при использовании в настоящем документе относится к заболеванию кожи, при котором обесцвеченные и/или затвердевшие пятна появляются на коже (например, одном или нескольких наружных слоях кожи) в результате чрезмерного отложения коллагена.
[065] "Синдром Рейно" при использовании в настоящем документе относится к заболеванию, при котором в некоторых частях тела (например, пальцах рук и/или пальцах ног) чувствуется оненемие и/или холод в ответ на различные стимулы (например, низкие температуры и/или стресс) из-за сужения артерий.
[066] "Болезнь Дарье" при использовании в настоящем документе относится к аутосомно-доминантному нарушению, характеризуемому появлением темных затвердевших пятен на коже (например, кератотических папул, фолликулярного кератоза или фолликулярного дискератоза), которые могут содержать гной.
[067] "Заживление ран" при использовании в настоящем документе относится к процессу, посредством которого кожа и/или другие ткани организма восстанавливаются, например, после перенесенного повреждения и/или травмы.
[068] "Ихтиоз" при использовании в настоящем документе относится к группе генетических заболеваний кожи, характеризуемых наличием сухой, чешуйчатой, потрескавшейся и/или шелушащейся кожи.
[069] "Тендинопатия" при использовании в настоящем документе относится к заболеванию или поражению сухожилия, характеризуемому воспалением, нарушением функции и/или повреждением сухожилия и/или ткани, контактирующей, граничащей или соединенной с сухожилием. Тендинопатия включает, например, воспаление сухожилия (например, тендинит), невоспалительную дегенерацию, например, структуры и/или состава сухожилия (например, тендиноз), воспаление паратенона около или контактирующего с сухожилием (например, паратенонит), микротравму сухожилия и разрыв сухожилия (например, острый, хронический, частичный и/или полный разрыв). Термин также охватывает тендовагинит, тендинопатию внешнего покрова сухожилия, которое происходит в некоторых сухожилиях, таких как сухожилия сгибателя и ахиллово сухожилие. Симптомы тендинопатии включают боль в покое, при пальпации сухожилия и/или при движении, например, сухожилия, ткани, сустава или кости рядом или соединенной с сухожилием; скованность в суставе; трудности при движении; слабость сустава или мышц, окружающих сухожилие; покраснение кожи около сухожилия; опухание сухожилия и/или ткани около сухожилия; и/или крепитацию.
[070] "Тендиноз" при использовании в настоящем документе относится к невоспалительному повреждению сухожилия, характеризующемуся внутрисухожильной дегенерацией сухожилия, обычно в форме микроразрывов в ткани внутри и вокруг сухожилия, вызванной чрезмерной нагрузкой, которая приводит к увеличению количества клеток, восстанавливающих сухожилие, вокруг области повреждения. Дегенерацию сухожилия вызывает повреждение или дезорганизация коллагеновых волокон, клеток и сосудистых компонентов сухожилия, что может уменьшить прочность сухожилия при растяжении и может привести к разрыву сухожилия, если его не лечить.
[071] "Тендинит", при использовании в настоящем документе относится к воспалительному повреждению сухожилия, характеризуемому дегенерацией наподобие наблюдаемой при тендинозе, но при этом также сопровождаемой воспалением сухожилия, повреждением сосудов и воспалительной репарационной реакцией. Тендинит часто связан с фибробластной и миофибробластной пролиферацией, а также с кровоизлиянием и организацией грануляционной ткани. Как правило, тендинит называют по вовлеченной части тела, такой как тендинит ахиллова сухожилия (при поражении ахиллова сухожилия) или тендинит надколенника (также известный как "колено прыгуна", поражающий надколенное сухожилие), хотя существуют некоторые исключения, такие как латеральный эпикондилит (также известный как "теннисный локоть", поражающий сухожилие короткого лучевого разгибателя запястья). Симптомы могут варьировать от ломоты или болей и локальной скованности до ощущения жжения, окружающего весь сустав вокруг воспаленного сухожилия. В некоторых случаях тендинит характеризуется отеком, иногда сопровождающимся жаром и покраснением; также могут присутствовать видимые узлы, окружающие сустав. У многих пациентов боль обычно усиливается во время и после движений, а сухожилие и область сустава могут стать более скованными на следующий день, когда мышцы напрягаются при движении сухожилия.
[072] "Псориаз" при использовании в настоящем документе относится к аутоиммунному заболеванию, при котором клетки кожи накапливаются и вызывают появление на коже приподнятых над поверхностью, красных, шелушащихся пятен.
[073] "Дерматит" (также известный как экзема) при использовании в настоящем документе относится к обычному воспалению кожи. Определенные типы дерматита включают атопический, контактный, монетовидный, фотоиндуцированный и застойный дерматит. Эти болезни характеризуются зудом, покраснением кожи и высыпанием.
Соединения
[074] Некоторые варианты осуществления настоящего изобретения включают соединения, их соли, фармацевтически приемлемые соли или пролекарство Формулы (I):
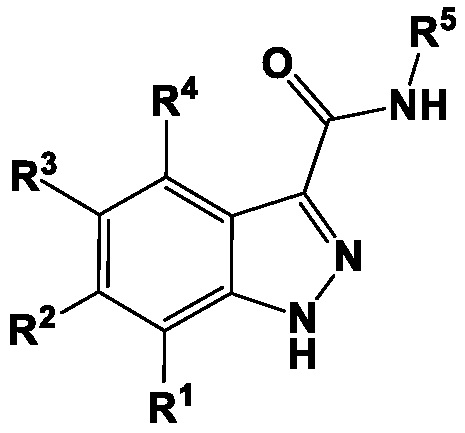
I
[075] В некоторых вариантах осуществления Формулы I, R1, R2 и R4 независимо выбраны из группы, состоящей из H, C1-9 алкила, галогенида, -N(R10)2, -XR10, CN, -OCF3 и -CF3.
[076] В некоторых вариантах осуществления Формулы I, R3 выбран из группы, состоящей из карбоциклилR6, гетероциклилR6, арилR6 и гетероарилR6.
[077] В некоторых вариантах осуществления Формулы I, когда R3 является гетероарилом, гетероарил не выбран из группы, состоящей из изохинолина, 1H-пирроло[2,3-c]пиридина и тетразола.
[078] В некоторых вариантах осуществления Формулы I, R5 выбран из группы, состоящей из -(C1-9 алкил)nкарбоциклилR7, -(C1-9 алкил)nгетероциклилR7, -(C1-9 алкил)nарилR7 и -(C1-9 алкил)nгетероарилR7.
[079] В некоторых вариантах осуществления Формулы I, R5 не является 4-пиридилR7, когда R1, R2 и R4 являются H, R3 выбран из группы, состоящей из 3-пиридилR6, 4-пиридилR6, 2-пиридилR6, фенилR6, тиазолR6, имидазолR6, пиримидинR6, оксазолR6,  ,
, 
 , и оба R6 и R7 являются H.
, и оба R6 и R7 являются H.
[080] В некоторых вариантах осуществления Формулы I, R5 не является -(CH2)(3-пиридил)R7, когда R1, R2 и R4 являются H, R3 выбран из группы, состоящей из 3-пиридилR6, 4-пиридилR6 и тиазолR6, и оба R6 и R7 являются H.
[081] В некоторых вариантах осуществления Формулы I, R5 не является фенилR7, когда R1, R2 и R4 являются H, R3 является 4-пиридилR6, и оба R6 и R7 являются H.
[082] В некоторых вариантах осуществления Формулы I, R3 не является 3-пиридилR6, когда R1, R2 и R4 являются H, R5 выбран из группы, состоящей из фенилR7,  ,
,  ,
,  , и оба R6 и R7 являются H.
, и оба R6 и R7 являются H.
[083] В некоторых вариантах осуществления Формулы I, R3 не является оксазолR6, когда R1, R2 и R4 являются H, R5 выбран из группы, состоящей из  , и R6 является H.
, и R6 является H.
[084] В некоторых вариантах осуществления Формулы I, R3 не является тиазолR6, когда R1, R2 и R4 являются H, R5 выбран из группы, состоящей из 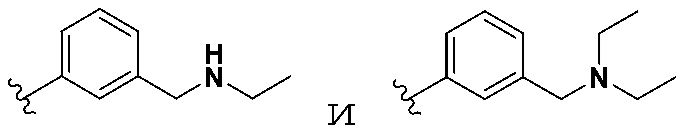 , и R6 является H.
, и R6 является H.
[085] В некоторых вариантах осуществления Формулы I каждый R6 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-9 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR10, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8, -(C1-9 алкил)nгетероарилR8, -C(=O)R11, -N(R10)C(=O)R11, -(C1-9 алкил)nN(R10)2, -(C1-9 алкил)nN(R10)SO2R11 и -SO2R11.
[086] В некоторых вариантах осуществления Формулы I каждый R7 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-9 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR10, -(C1-9 алкил)nкарбоциклилR9, -(C1-9 алкил)nгетероциклилR9, -(C1-9 алкил)nарилR9, -(C1-9 алкил)nгетероарилR9, -C(=O)R11, -N(R10)C(=O)R11, -(C1-9 алкил)nN(R10)2, -(C1-9 алкил)nN(R10)SO2R11 и -SO2R11.
[087] В некоторых вариантах осуществления Формулы I каждый R8 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN -XR12, -C(=O)R13, -N(R12)C(=O)R13, -(C1-9 алкил)nN(R12)2, -(C1-9 алкил)nN(R12)SO2R13 и -SO2R13.
[088] В некоторых вариантах осуществления Формулы I каждый R9 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN, -XR12, -C(=O)R13, -N(R12)C(=O)R13, -(C1-9 алкил)nN(R12)2, -(C1-9 алкил)nN(R12)SO2R13 и -SO2R13.
[089] В некоторых вариантах осуществления Формулы I каждый R10 независимо выбран из группы, состоящей из H, C1-9 алкила, -(C1-9 алкил)nN(R14)2, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8 и -(C1-9 алкил)nгетероарилR8.
[090] В некоторых вариантах осуществления Формулы I каждый R11 независимо выбран из группы, состоящей из C1-9 алкила, -N(R14)2, -(C1-9 алкил)nкарбоциклилR8, -(C1-9 алкил)nгетероциклилR8, -(C1-9 алкил)nарилR8 и -(C1-9 алкил)nгетероарилR8.
[091] В некоторых вариантах осуществления Формулы I каждый R12 независимо выбран из группы, состоящей из H, C1-9 алкила, -(C1-9 алкил)nN(R14)2, -(C1-9 алкил)nкарбоциклила, -(C1-9 алкил)nгетероциклила, -(C1-9 алкил)nарила и -(C1-9 алкил)nгетероарила.
[092] В некоторых вариантах осуществления Формулы I каждый R13 независимо выбран из группы, состоящей из C1-9 алкила, -N(R14)2, -(C1-9 алкил)nкарбоциклила, -(C1-9 алкил)nгетероциклила, -(C1-9 алкил)nарила и -(C1-9 алкил)nгетероарила.
[093] В некоторых вариантах осуществления Формулы I каждый R14 независимо выбран из группы, состоящей из H, C1-3 алкила, карбоциклила и арила.
[094] В некоторых вариантах осуществления Формулы I каждый X выбран из группы, состоящей из связи, -O- и -S-.
[095] В некоторых вариантах осуществления Формулы I каждое n является 0 или 1.
[096] В некоторых вариантах осуществления Формулы I, X является O.
[097] В некоторых вариантах осуществления Формулы I, R1, R2 и R4 являются H.
[098] Некоторые варианты осуществления настоящего изобретения включают соединения, их соли, фармацевтически приемлемые соли или пролекарство Формулы (Ia):
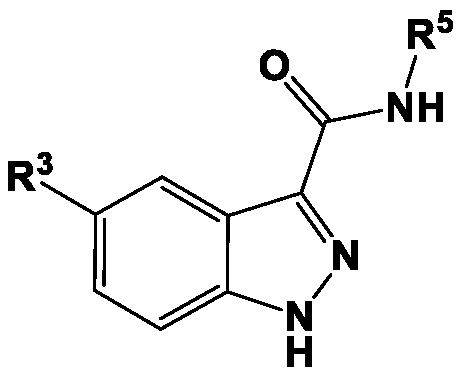
Ia
где:
R3 выбран из группы, состоящей из 3-пиридилR6, 5-пиримидинилR6, и 4-пиридазинилR6;
R5 выбран из группы, состоящей из -гетероарилR7;
R6 является заместителем, выбранным из группы, состоящей из -(C1-2 алкил)гетероциклилR8 и -гетероциклилR8;
R7 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H, C1-3 алкила, галогенида, -NH2, -OCF3, -CF3, -CN, -OR10, -(C1-2 алкил)гетероциклилR9, -гетероциклилR9 и -SO2R11;
R8 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H, C1-3 алкила, галогенида и -OR12;
каждый R9 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN и -OR12;
R10 выбран из группы, состоящей из H и C1-3 алкила;
R11 является C1-3 алкилом; и
каждый R12 независимо выбран из группы, состоящей из H и C1-3 алкила.
[099] Некоторые варианты осуществления настоящего изобретения включают соединения, их соли, фармацевтически приемлемые соли или пролекарство Формулы (Ia):

Ia
где:
R3 является 3-пиридилR6;
R5 выбран из группы, состоящей из пиридилR7, -пиримидинилR7, и -пиридазинилR7;
R6 является -CH2гетероциклилR8;
R7 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H, F, метила, -NH2, -CF3, -CN, -OMe, -SO2Me 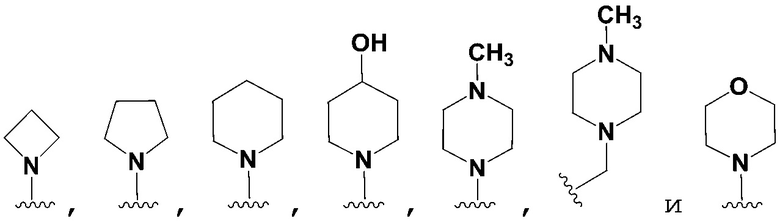 ; и
; и
R8 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H и галогенида.
[0100] В некоторых вариантах осуществления Формулы Ia R3 выбран из группы, состоящей из 3-пиридилR6, 5-пиримидинилR6 и 4-пиридазинилR6;
[0101] В некоторых вариантах осуществления Формулы Ia R5 выбран из группы, состоящей из -гетероарилR7.
[0102] В некоторых вариантах осуществления Формулы Ia R5 выбран из группы, состоящей из -пиперазинилR7, -тетрагидропиранилR7, -пиперидинилR7, пиразолилR7, пиримидинилR7, пиридазинилR7, бензо[d][1,3]диоксолилR7, 2,3-дигидробензо[b][1,4]диоксинилR7, пиразинилR7 и 3-пиридилR7.
[0103] В некоторых вариантах осуществления Формулы Ia R6 является заместителем, выбранным из группы, состоящей из -(C1-2 алкил)гетероциклилR8 и -гетероциклилR8.
[0104] В некоторых вариантах осуществления Формулы Ia каждый R6 является 1-2 заместителями, каждый из которых выбран из группы, состоящей из -(C1-2 алкил)гетероциклилR8, -гетероциклилR8, -(C1-2 алкил)арилR8, -N(R10)C(=O)R11 и -(C1-2 алкил)N(R10)2.
[0105] В некоторых вариантах осуществления Формулы Ia R7 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H, C1-3 алкила, галогенида, -NH2, -OCF3, -CF3, -CN, -OR10, -(C1-2 алкил)гетероциклилR9, -гетероциклилR9 и -SO2R11.
[0106] В некоторых вариантах осуществления Формулы Ia каждый R7 является 1-2 заместителями, каждый из которых выбран из группы, состоящей из незамещенного C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN, -OR10, -C(=O)R11, -N(R10)C(=O)R11, -N(R10)2, -(C1-2 алкил)N(R10)2 и -N(R10)SO2R11.
[0107] В некоторых вариантах осуществления Формулы Ia R8 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H, C1-3 алкила, галогенида и -OR12.
[0108] В некоторых вариантах осуществления Формулы Ia каждый R9 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN и -OR12.
[0109] В некоторых вариантах осуществления Формулы Ia R10 выбран из группы, состоящей из H и C1-3 алкила.
[0110] В некоторых вариантах осуществления Формулы Ia каждый R10 независимо выбран из группы, состоящей из H, C1-3 алкила, -(C1-3 алкил)N(R14)2 и -арилR8.
[0111] В некоторых вариантах осуществления Формулы Ia R11 является C1-3 алкилом.
[0112] В некоторых вариантах осуществления Формулы Ia каждый R11 независимо выбран из группы, состоящей из C1-3 алкила, -N(R14)2, -карбоциклилR8 и -гетероциклилR8.
[0113] В некоторых вариантах осуществления Формулы Ia каждый R12 независимо выбран из группы, состоящей из H и C1-3 алкила.
[0114] В некоторых вариантах осуществления Формулы Ia R3 выбран из группы, состоящей из арилR6 и гетероарилR6.
[0115] В некоторых вариантах осуществления Формулы Ia, когда R3 является гетероарилом, гетероарил не выбран из группы, состоящей из изохинолина, 1H-пирроло[2,3-c]пиридина и тетразола.
[0116] В некоторых вариантах осуществления Формулы Ia R5 выбран из группы, состоящей из-карбоциклилR7, -гетероциклилR7, -арилR7, -гетероарилR7, и -(C1-2 алкил)гетероарилR7.
[0117] В некоторых вариантах осуществления Формулы Ia R5 не является 4-пиридилR7, когда R3 выбран из группы, состоящей из 3-пиридилR6, 4-пиридилR6, 2-пиридилR6, фенилR6, тиазолR6, имидазолR6, пиримидинR6, оксазолR6, 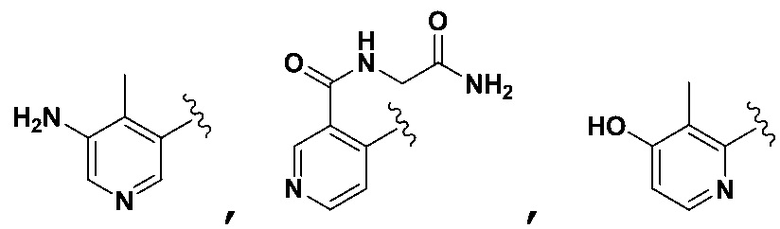 ,
, 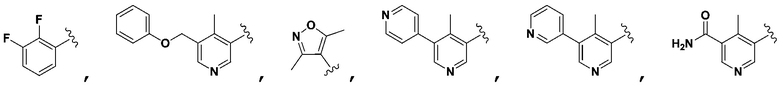 ,
, 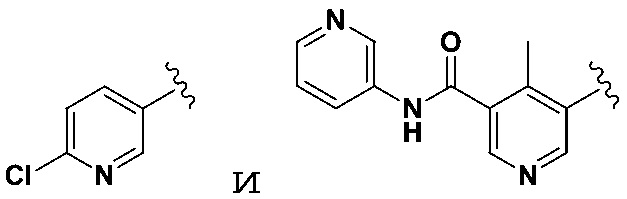 , и оба R6 и R7 являются H.
, и оба R6 и R7 являются H.
[0118] В некоторых вариантах осуществления Формулы Ia R5 не является -(CH2)(3-пиридил)R7, когда R3 выбран из группы, состоящей из 3-пиридилR6, 4-пиридилR6 и тиазолR6, и оба R6 и R7 являются H.
[0119] В некоторых вариантах осуществления Формулы Ia R5 не является фенилR7, когда R3 является 4-пиридилR6, и оба R6 и R7 являются H.
[0120] В некоторых вариантах осуществления Формулы Ia R3 не является 3-пиридилR6, когда R5 выбран из группы, состоящей из фенилR7, 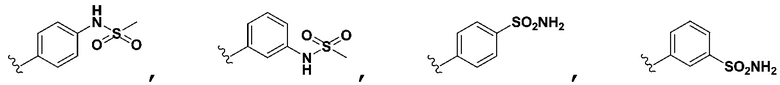 ,
, 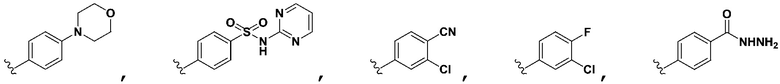 ,
, 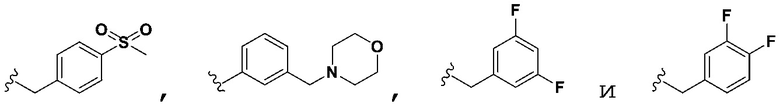 , и оба R6 и R7 являются H.
, и оба R6 и R7 являются H.
[0121] В некоторых вариантах осуществления Формулы Ia R3 не является оксазолR6, когда R5 выбран из группы, состоящей из  , и R6 является H.
, и R6 является H.
[0122] В некоторых вариантах осуществления Формулы Ia R3 не является тиазолR6, когда R5 выбран из группы, состоящей из 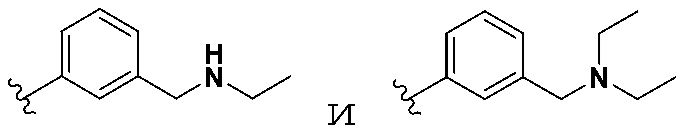 , и R6 является H.
, и R6 является H.
[0123] В некоторых вариантах осуществления Формулы Ia каждый R6 является 1-2 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN, -OR10, -(C1-2 алкил)гетероциклилR8, -гетероциклилR8, -(C1-2 алкил)арилR8, -C(=O)R11, -N(R10)C(=O)R11 и -(C1-2 алкил)N(R10)2.
[0124] В некоторых вариантах осуществления Формулы Ia каждый R7 является 1-2 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3, -CN, -OR10, -(C1-2 алкил)гетероциклилR9, -гетероциклилR9, -арилR9, -(C1-2 алкил)арилR9, -C(=O)R11, -N(R10)C(=O)R11, -N(R10)2, -(C1-2 алкил)N(R10)2, -N(R10)SO2R11 и -SO2R11.
[0125] В некоторых вариантах осуществления Формулы Ia каждый R8 является 1-2 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, OCF3, -CF3 -CN и -OR12.
[0126] В некоторых вариантах осуществления Формулы Ia каждый R9 является 1-2 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида, амино, -OCF3, -CF3 -CN и -OR12.
[0127] В некоторых вариантах осуществления Формулы Ia каждый R10 независимо выбран из группы, состоящей из H, C1-3 алкила, -(C1-3 алкил)N(R14)2 и -арилR8.
[0128] В некоторых вариантах осуществления Формулы Ia каждый R11 независимо выбран из группы, состоящей из C1-3 алкила, -N(R14)2, -карбоциклилR8 и -гетероциклилR8.
[0129] В некоторых вариантах осуществления Формулы Ia каждый R12 независимо выбран из группы, состоящей из H и C1-3 алкила.
[0130] В некоторых вариантах осуществления Формулы Ia каждый R14 независимо выбран из группы, состоящей из H, C1-3 алкила и карбоциклила.
[0131] В некоторых вариантах осуществления Формулы I или Формулы Ia галогенид является фтором.
[0132] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -арилR6.
[0133] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -гетероарилR6.
[0134] В некоторых вариантах осуществления Формулы I или Формулы Ia R5 является -арилR7.
[0135] В некоторых вариантах осуществления Формулы I или Формулы Ia R5 является -гетероарилR7.
[0136] В некоторых вариантах осуществления Формулы I или Формулы Ia R5-гетероциклилR7.
[0137] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -гетероарилR6, и R5 является -гетероарилR7.
[0138] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -фенилR6, и R5 является -гетероарилR7.
[0139] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -гетероарилR6, и R5 является -фенилR7.
[0140] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7.
[0141] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -CH2-3-пиридилR7.
[0142] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -пиридазинилR7.
[0143] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -пиразинилR7.
[0144] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -пиримидинилR7.
[0145] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является бензо[d][1,3]диоксолилом.
[0146] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является 2,3-дигидробензо[b][1,4]диоксинилом.
[0147] В некоторых вариантах осуществления Формулы I или Формулы Ia арил является фенилом.
[0148] В некоторых вариантах осуществления Формулы I или Формулы Ia, когда R3 является гетероарилом, гетероарил является 3-пиридилом.
[0149] В некоторых вариантах осуществления Формулы I или Формулы Ia, когда R5 является гетероарилом, гетероарил является 3-пиридилом.
[0150] В некоторых вариантах осуществления Формулы I или Формулы Ia, когда R5 является гетероарилом, гетероарил является 5-пиримидинилом.
[0151] В некоторых вариантах осуществления Формулы I или Формулы Ia, когда R5 является гетероарилом, гетероарил является 4-пиридазинилом.
[0152] В некоторых вариантах осуществления Формулы I или Формулы Ia, когда R5 является гетероарилом, гетероарил является пиразолилом.
[0153] В некоторых вариантах осуществления Формулы I или Формулы Ia, когда R5 является гетероарилом, гетероарил является бензо[d][1,3]диоксолилом.
[0154] В некоторых вариантах осуществления Формулы I или Формулы Ia, когда R5 является гетероарилом, гетероарил является 2,3-дигидробензо[b][1,4]диоксинилом.
[0155] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является гетероциклилом. Например, гетероциклил может быть выбран из группы, состоящей из морфолинила, пиперазинила, пиперидинила, тетрагидропиранила, азетидинила и пирролидинила. В некоторых вариантах осуществления R6 является морфолинилом. В другом варианте осуществления R6 является пиперазинилом. В другом варианте осуществления R6 является пиперидинилом. В другом варианте осуществления R6 является пирролидинилом.
[0156] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является гетероциклилом. Например, гетероциклил может быть выбран из группы, состоящей из морфолинила, пиперазинила, пиперидинила, тетрагидропиранила, азетидинила и пирролидинила. В некоторых вариантах осуществления R7 является морфолинилом. В другом варианте осуществления R7 является пиперазинилом. В другом варианте осуществления R7 является пиперидинилом. В другом варианте осуществления R7 является пирролидинилом. В другом варианте осуществления R7 является азетидинилом.
[0157] В некоторых вариантах осуществления Формулы I или Формулы Ia R10 является карбоциклилом. Например, карбоциклил может быть выбран из группы, состоящей из циклопропила, циклобутила, циклопентила и циклогексила. В некоторых вариантах осуществления R10 является циклопропилом. В другом варианте осуществления R10 является циклобутилом. В другом варианте осуществления R10 является циклопентилом. В другом варианте осуществления R10 является циклогексилом.
[0158] В некоторых вариантах осуществления Формулы I или Формулы Ia R11 является гетероциклилом. Например, гетероциклил может быть выбран из группы, состоящей из морфолинила, пиперазинила, пиперидинила, тетрагидропиранила, азетидинила и пирролидинила. В некоторых вариантах осуществления R11 является морфолинилом. В другом варианте осуществления R11 является пиперазинилом. В другом варианте осуществления R11 является пиперидинилом. В другом варианте осуществления R11 является пирролидинилом. В другом варианте осуществления R11 является азетидинилом.
[0159] В некоторых вариантах осуществления Формулы I или Формулы Ia R11 является карбоциклилом. Например, карбоциклил может быть выбран из группы, состоящей из циклопропила, циклобутила, циклопентила и циклогексила. В некоторых вариантах осуществления R11 является циклопропилом. В другом варианте осуществления R11 является циклобутилом. В другом варианте осуществления R11 является циклопентилом. В другом варианте осуществления R11 является циклогексилом.
[0160] В некоторых вариантах осуществления Формулы I или Формулы Ia R12 является карбоциклилом. Например, карбоциклил может быть выбран из группы, состоящей из циклопропила, циклобутила, циклопентила и циклогексила. В некоторых вариантах осуществления R12 является циклопропилом. В другом варианте осуществления R12 является циклобутилом. В другом варианте осуществления R12 является циклопентилом. В другом варианте осуществления R12 является циклогексилом.
[0161] В некоторых вариантах осуществления Формулы I или Формулы Ia R13 является гетероциклилом. Например, гетероциклил может быть выбран из группы, состоящей из морфолинила, пиперазинила, пиперидинила, тетрагидропиранила, азетидинила и пирролидинила. В некоторых вариантах осуществления R13 является морфолинилом. В другом варианте осуществления R13 является пиперазинилом. В другом варианте осуществления R13 является пиперидинилом. В другом варианте осуществления R13 является пирролидинилом. В другом варианте осуществления R13 является азетидинилом.
[0162] В некоторых вариантах осуществления Формулы I или Формулы Ia R13 является карбоциклилом. Например, карбоциклил может быть выбран из группы, состоящей из циклопропила, циклобутила, циклопентила и циклогексила. В некоторых вариантах осуществления R13 является циклопропилом. В другом варианте осуществления R13 является циклобутилом. В другом варианте осуществления R13 является циклопентилом. В другом варианте осуществления R13 является циклогексилом.
[0163] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем.
[0164] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является 1-2 заместителями.
[0165] В некоторых вариантах осуществления Формулы I R6 является 1-3 заместителями.
[0166] В некоторых вариантах осуществления Формулы I R6 является 1-4 заместителями.
[0167] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является H.
[0168] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является галогенидом.
[0169] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель-NH2.
[0170] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -OCF3.
[0171] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -OCH3.
[0172] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -CF3.
[0173] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -гетероциклилR8.
[0174] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -(CH2)гетероциклилR8.
[0175] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -(CH2)пирролидинилR8.
[0176] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -(CH2)пирролидинилR8, где R8 является двумя заместителями, и оба заместителя являются галогенидами.
[0177] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -(CH2)пиперидинилR8.
[0178] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -(CH2)фенилR8.
[0179] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -феноксиR8.
[0180] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является 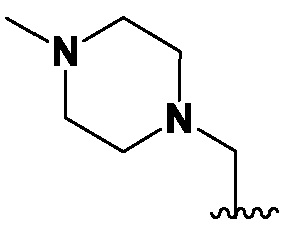 .
.
[0181] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -N(R10)2.
[0182] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -N(R10)2, где каждый R10 независимо выбран из C1-3 алкила.
[0183] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -(CH2)N(R10)2.
[0184] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -(CH2)N(R10)2, где каждый R10 независимо выбран из C1-3 алкила.
[0185] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -N(R10)SO2R11.
[0186] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -N(R10)C(=O)R11.
[0187] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -N(R10)C(=O)R11, где R11 является гетероциклилом.
[0188] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель является -N(R10)C(=O)R11, где R11 является карбоциклилом.
[0189] В некоторых вариантах осуществления Формулы I R6 является двумя заместителями, и заместители являются фтором и -(C1-9 алкил)nгетероциклилR8.
[0190] В некоторых вариантах осуществления Формулы Ia R6 является двумя заместителями, и заместители являются фтором и -гетероциклилR8.
[0191] В некоторых вариантах осуществления Формулы Ia R6 является двумя заместителями, и заместители являются фтором и -(C1-2 алкил)гетероциклилR8.
[0192] В некоторых вариантах осуществления Формулы I или Формулы Ia R6 является одним заместителем, и заместитель выбран из группы, состоящей из:
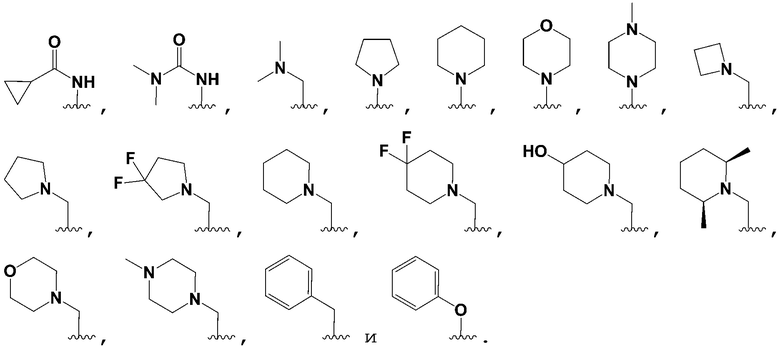
[0193] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем.
[0194] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является 1-2 заместителями.
[0195] В некоторых вариантах осуществления Формулы I R7 является 1-3 заместителями.
[0196] В некоторых вариантах осуществления Формулы I R7 является 1-4 заместителями.
[0197] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является галогенидом.
[0198] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -NH2.
[0199] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -OH.
[0200] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -CF3.
[0201] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -CN.
[0202] В некоторых вариантах осуществления Формулы I R7 является одним заместителем, и заместитель является -XR10, где X является O, и R10 является C1-3 алкилом.
[0203] В некоторых вариантах осуществления Формулы Ia R7 является одним заместителем, и заместитель является -OR10, и R10 является C1-3 алкилом.
[0204] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -фенилR9.
[0205] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -(CH2)N(R10)2.
[0206] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -(CH2)N(R10)2, где каждый R10 независимо выбран из C1-3 алкила.
[0207] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -(CH2)гетероциклилR9.
[0208] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -(CH2)пирролидинилR9.
[0209] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -гетероциклилR9.
[0210] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -феноксиR9.
[0211] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -(CH2)фенилR9.
[0212] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -фенилR9.
[0213] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -N(R10)C(=O)R11.
[0214] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -N(R10)C(=O)R11, где R11 является карбоциклилом.
[0215] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель-N(R10)2.
[0216] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -C(=O)R11, где R11 выбран из группы, состоящей из -гетероциклилR8 и -N(R10)2.
[0217] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -SO2R11.
[0218] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель является -SO2R11; и R11 является C1-3 алкилом.
[0219] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является двумя заместителями, и заместители являются C1-3 алкилом и -гетероциклилR9.
[0220] В некоторых вариантах осуществления Формулы I или Формулы Ia R7 является одним заместителем, и заместитель выбран из группы, состоящей из:
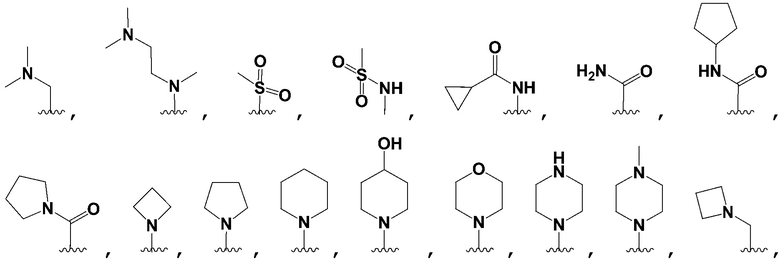
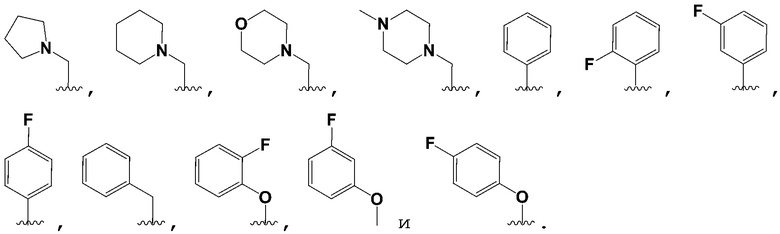
[0221] В некоторых вариантах осуществления Формулы I или Формулы Ia R8 является одним заместителем.
[0222] В некоторых вариантах осуществления Формулы I или Формулы Ia R8 является 1-2 заместителями.
[0223] В некоторых вариантах осуществления Формулы I R8 является 1-3 заместителями.
[0224] В некоторых вариантах осуществления Формулы I R8 является 1-4 заместителями.
[0225] В некоторых вариантах осуществления Формулы I или Формулы Ia R8 является H.
[0226] В некоторых вариантах осуществления Формулы I или Формулы Ia R8 является одним заместителем, и заместитель является C1-3 алкилом.
[0227] В некоторых вариантах осуществления Формулы I или Формулы Ia R8 является одним заместителем, и заместитель является -OH.
[0228] В некоторых вариантах осуществления Формулы I или Формулы Ia R8 является одним заместителем, и заместитель является галогенидом.
[0229] В некоторых вариантах осуществления Формулы I или Формулы Ia R8 является двумя заместителями, и заместители являются галогенидами.
[0230] В некоторых вариантах осуществления Формулы I R8 является тремя заместителями, и заместители является галогенидами.
[0231] В некоторых вариантах осуществления Формулы I или Формулы Ia R9 является одним заместителем.
[0232] В некоторых вариантах осуществления Формулы I или Формулы Ia R9 является 1-2 заместителями.
[0233] В некоторых вариантах осуществления Формулы I R9 является 1-3 заместителями.
[0234] В некоторых вариантах осуществления Формулы I R9 является 1-4 заместителями.
[0235] В некоторых вариантах осуществления Формулы I или Формулы Ia R9 является H.
[0236] В некоторых вариантах осуществления Формулы I или Формулы Ia R9 является одним заместителем, и заместитель является C1-3 алкилом.
[0237] В некоторых вариантах осуществления Формулы I или Формулы Ia R9 является одним заместителем, и заместитель является -OH.
[0238] В некоторых вариантах осуществления Формулы I или Формулы Ia R9 является одним заместителем, и заместитель является галогенидом.
[0239] В некоторых вариантах осуществления Формулы I или Формулы Ia R9 является двумя заместителями, и заместители являются галогенидами.
[0240] В некоторых вариантах осуществления Формулы I или Формулы Ia R8 является -C1-3 алкилом. Например, -C1-3 алкил может быть выбран из группы, состоящей из метила, этила, н-пропила и изопропила. В некоторых вариантах осуществления R8 является метилом. В другом варианте осуществления R8 является этилом.
[0241] В некоторых вариантах осуществления Формулы I или Формулы Ia R10 является -C1-3 алкилом. Например, -C1-3 алкил может быть выбран из группы, состоящей из метила, этила, н-пропила и изопропила. В некоторых вариантах осуществления R10 является метилом. В другом варианте осуществления R10 является этилом. В другом варианте осуществления R10 является н-пропилом. В другом варианте осуществления R10 является изопропилом.
[0242] В некоторых вариантах осуществления Формулы I или Формулы Ia R11 является -C1-3 алкилом. Например, -C1-3 алкил может быть выбран из группы, состоящей из метила, этила, н-пропила и изопропила. В некоторых вариантах осуществления R11 является метилом. В другом варианте осуществления R11 является этилом. В другом варианте осуществления R11 является н-пропилом. В другом варианте осуществления R11 является изопропилом.
[0243] В некоторых вариантах осуществления Формулы I или Формулы Ia R14 является -C1-3 алкилом. Например, -C1-3 алкил может быть выбран из группы, состоящей из метила, этила, н-пропила и изопропила. В некоторых вариантах осуществления R14 является метилом. В другом варианте осуществления R14 является этилом. В другом варианте осуществления R14 является н-пропилом. В другом варианте осуществления R14 является изопропилом.
[0244] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)N(R10)2; и R7 является одним заместителем, состоящим из -CF3; и каждый R10 является -C1-3 алкилом.
[0245] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; оба R7 и R8 являются H; и гетероцикл представляет собой 5-членное кольцо.
[0246] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; оба R7 и R8 являются H; и гетероцикл представляет собой 6-членное кольцо.
[0247] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из CN; R8 является H; и гетероцикл представляет собой 5-членное кольцо.
[0248] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из CN; R8 является H; и гетероцикл представляет собой 6-членное кольцо.
[0249] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из CF3; R8 является H; и гетероцикл представляет собой 6-членное кольцо.
[0250] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из-гетероциклилR8; каждый R8 является H; и гетероциклы независимо выбраны из 5- или 6-членного кольца.
[0251] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)N(R10)2; и R7 является одним заместителем, состоящим из -CN; и каждый R10 является -C1-3 алкилом.
[0252] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)N(R10)2; и R7 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R8 является H; каждый R10 является -C1-3 алкилом; и гетероцикл представляет собой 6-членное кольцо.
[0253] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из -гетероциклилR8; каждый R8 является одним заместителем, независимо выбранным из H и -OH; и гетероциклы независимо выбраны из 5- или 6-членного кольца.
[0254] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из-C(=O)R11; R11 является -гетероциклилR8; каждый R8 является H; и гетероциклы независимо выбраны из 5- или 6-членного кольца.
[0255] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из -гетероциклилR8; каждый R8 является 1-3 заместителями, независимо выбранными из H и F, при условии, что по меньшей мере один заместитель на одном гетероцикле является фтором; и каждый гетероцикл представляет собой 5-членное кольцо.
[0256] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из-C(=O)R11; R11 является -NHR10; R10 является гетероциклилR8; каждый R8 является H; и гетероциклы независимо выбраны из 5- или 6-членного кольца.
[0257] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является одним заместителем, состоящим из -SO2R11; R8 является H; R11 является -C1-3 алкилом; и гетероцикл представляет собой 6-членное кольцо.
[0258] В некоторых вариантах осуществления Формулы I или Формулы Ia R3 является -3-пиридилR6, и R5 является -3-пиридилR7; R6 является одним заместителем, состоящим из -(C1-2 алкил)гетероциклилR8; R7 является H; R8 является 1-4 заместителями, независимо выбранными из H и F, при условии, что по меньшей мере один заместитель является фтором; и гетероцикл представляет собой 5-членное кольцо.
[0259] Иллюстративные соединения Формулы (I) показаны в Таблице 1.
Таблица 1
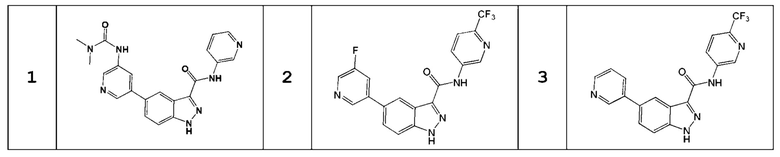
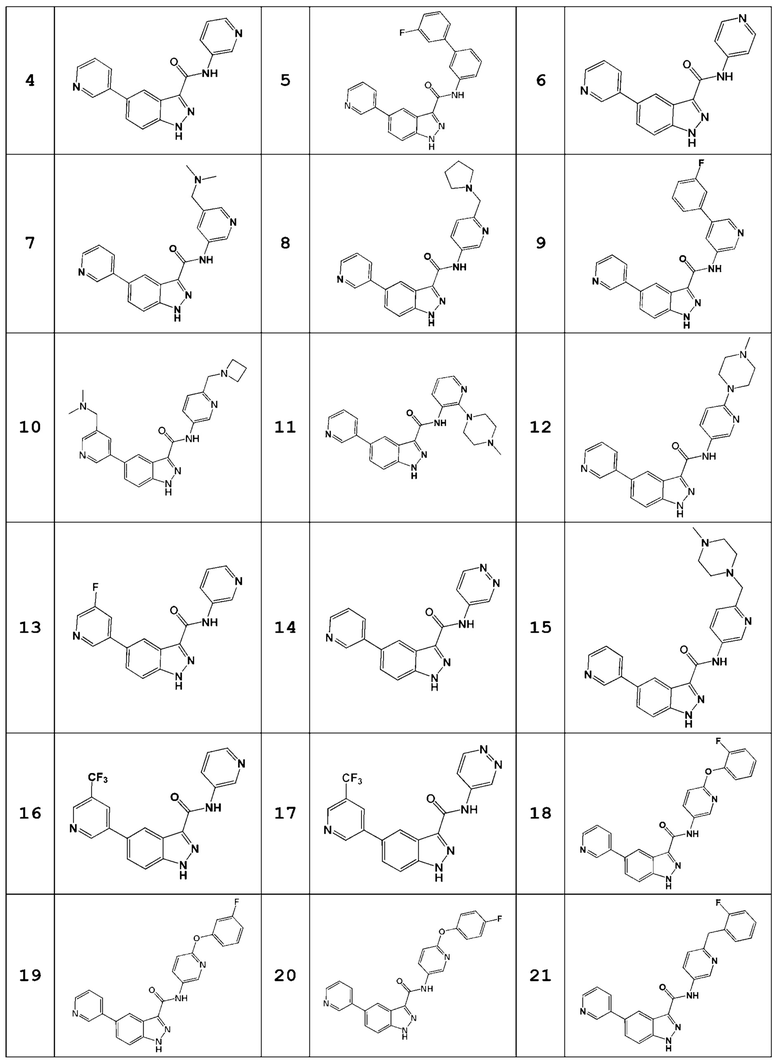
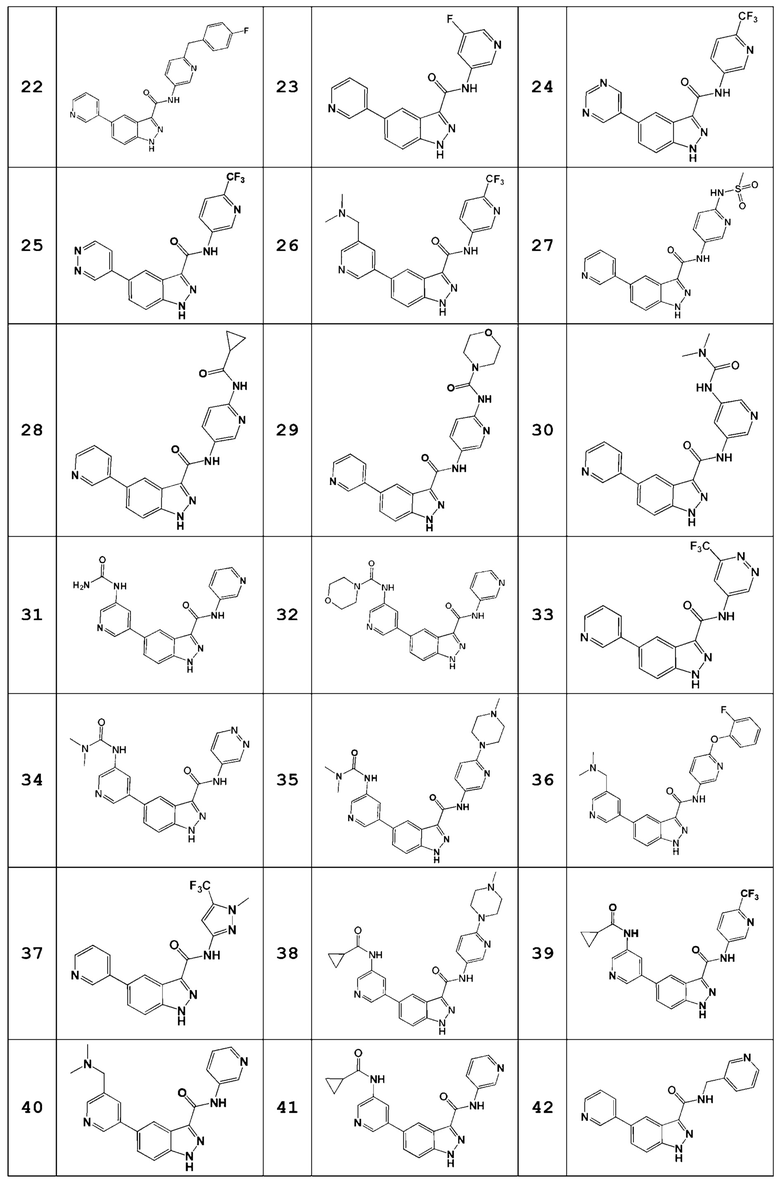
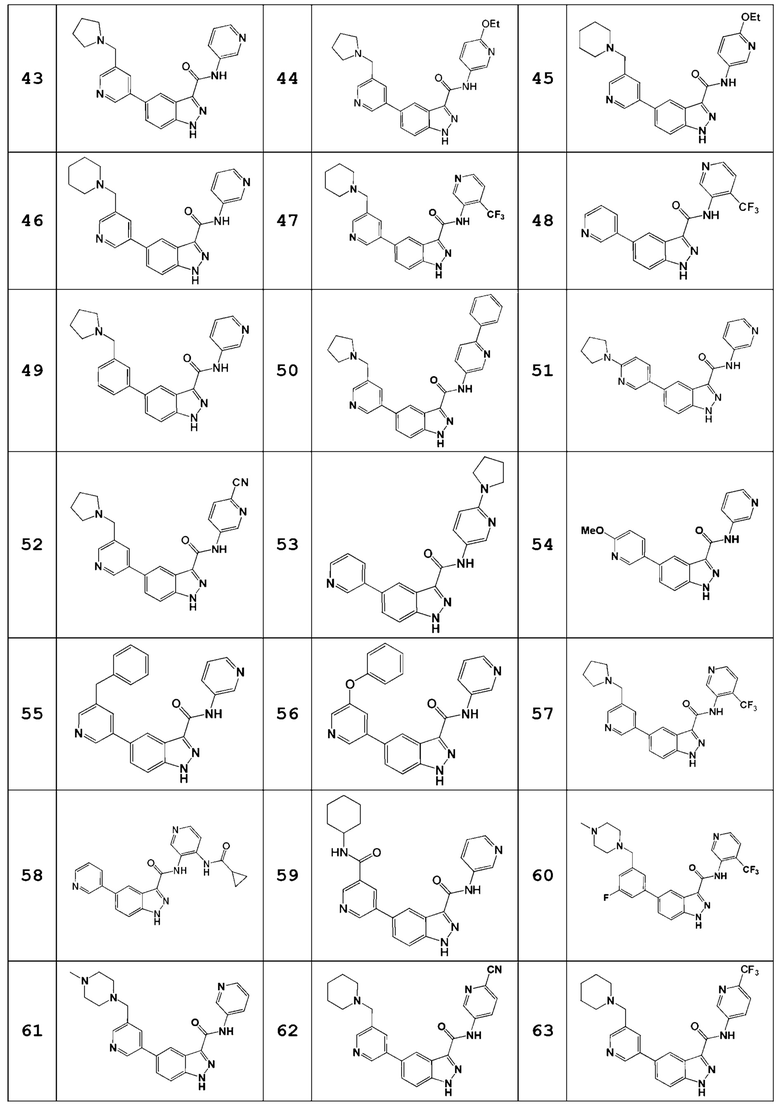
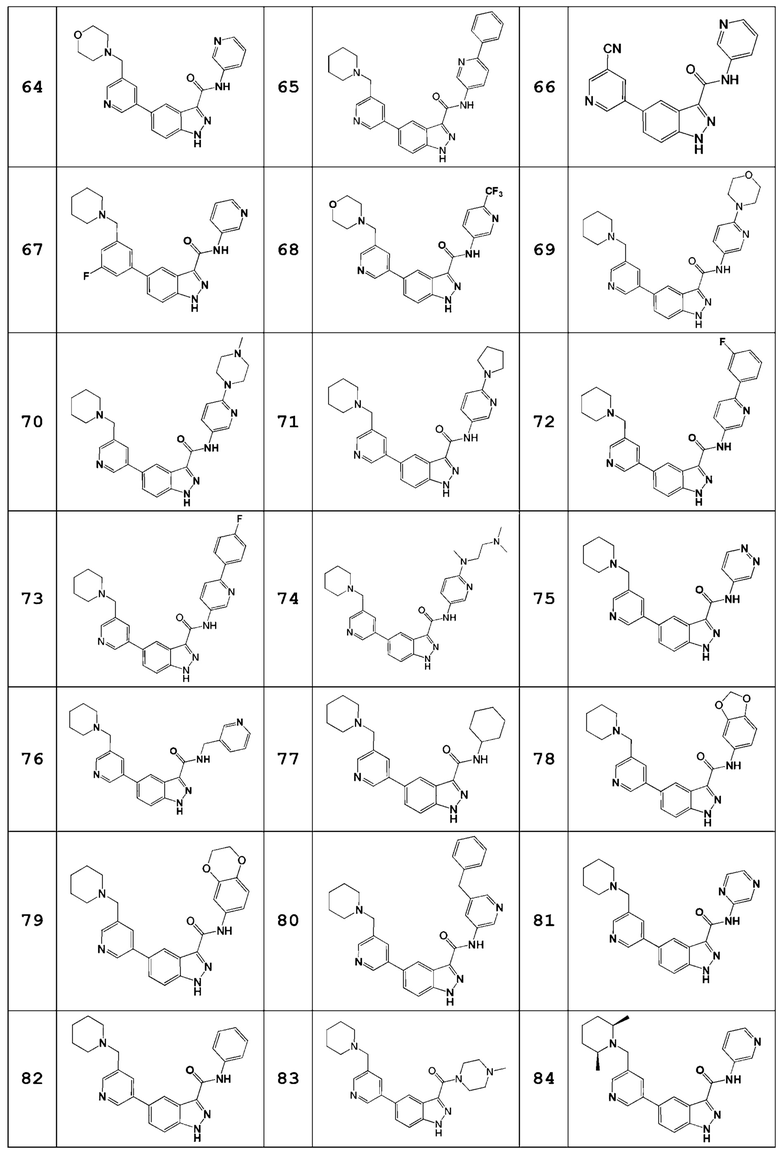
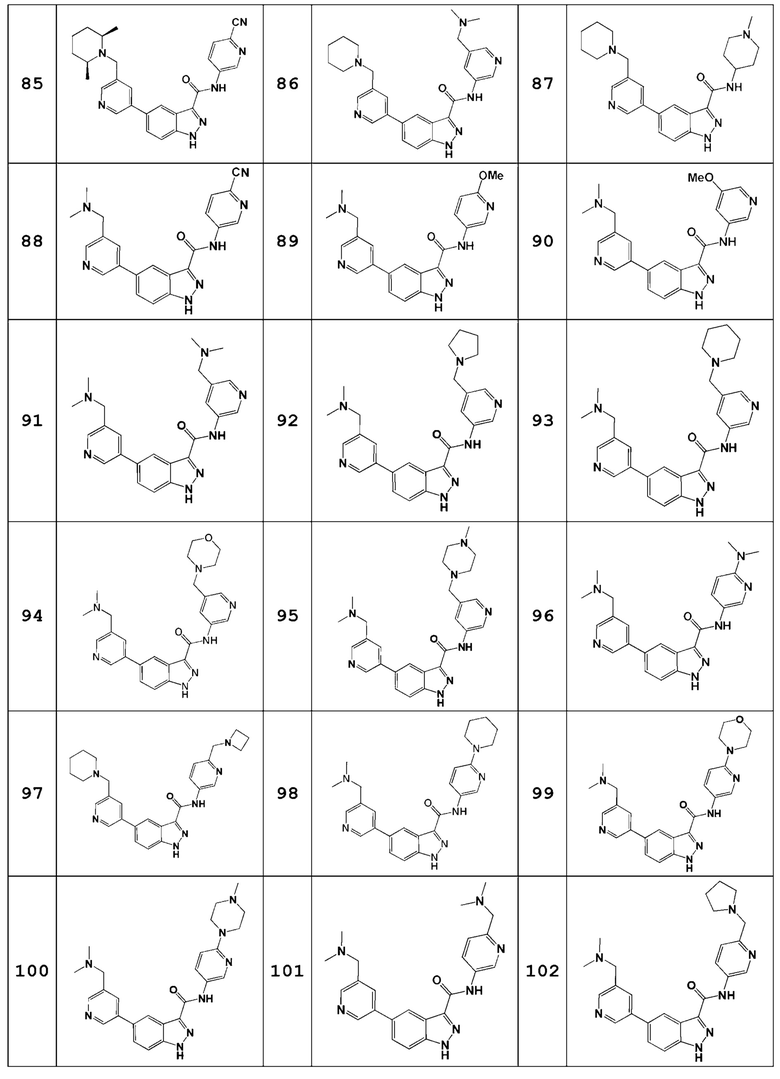
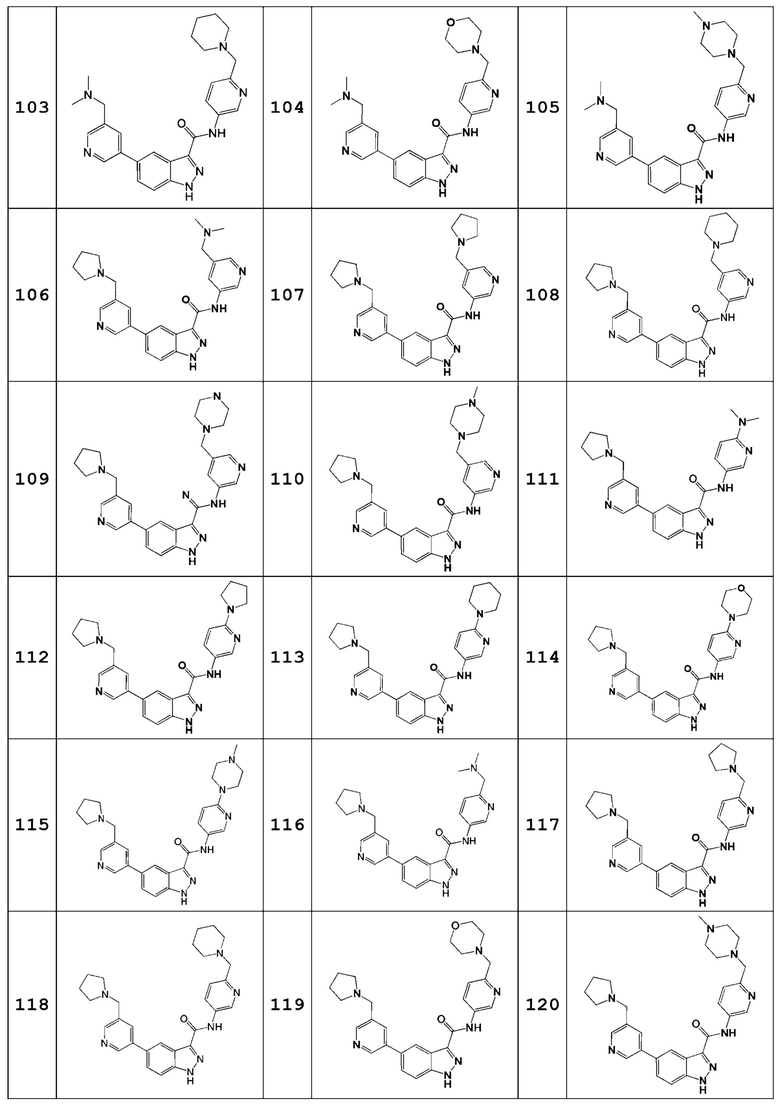
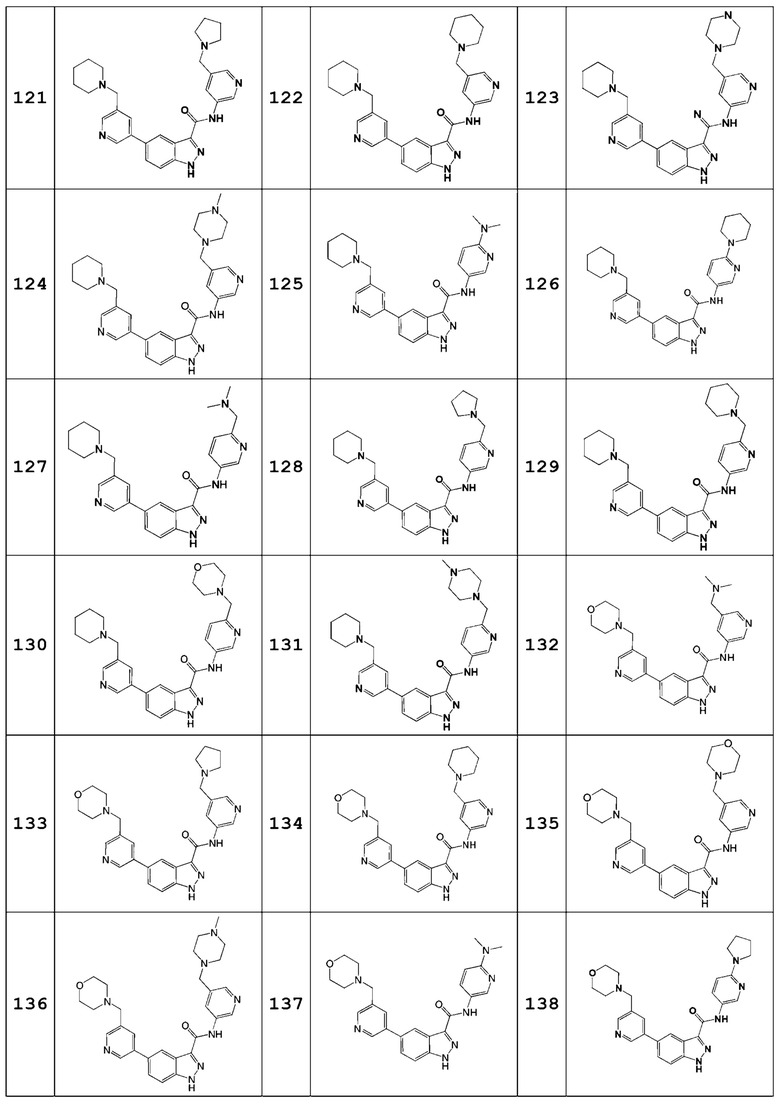
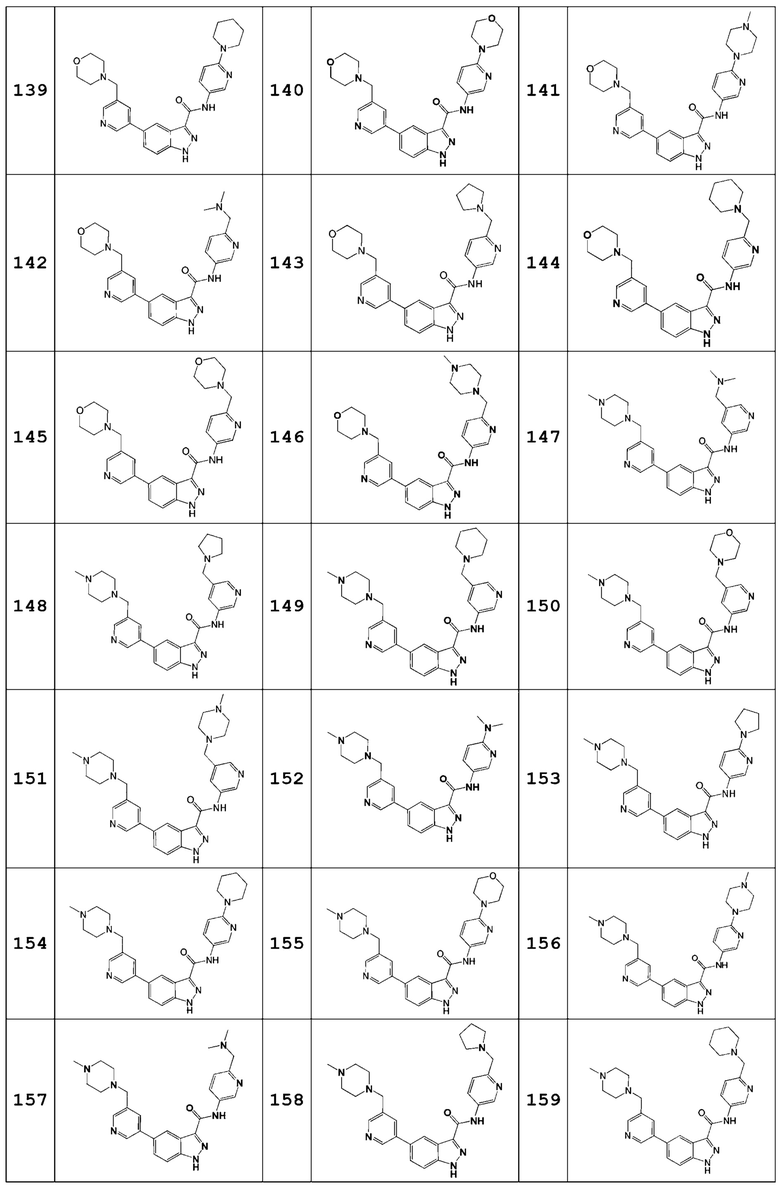
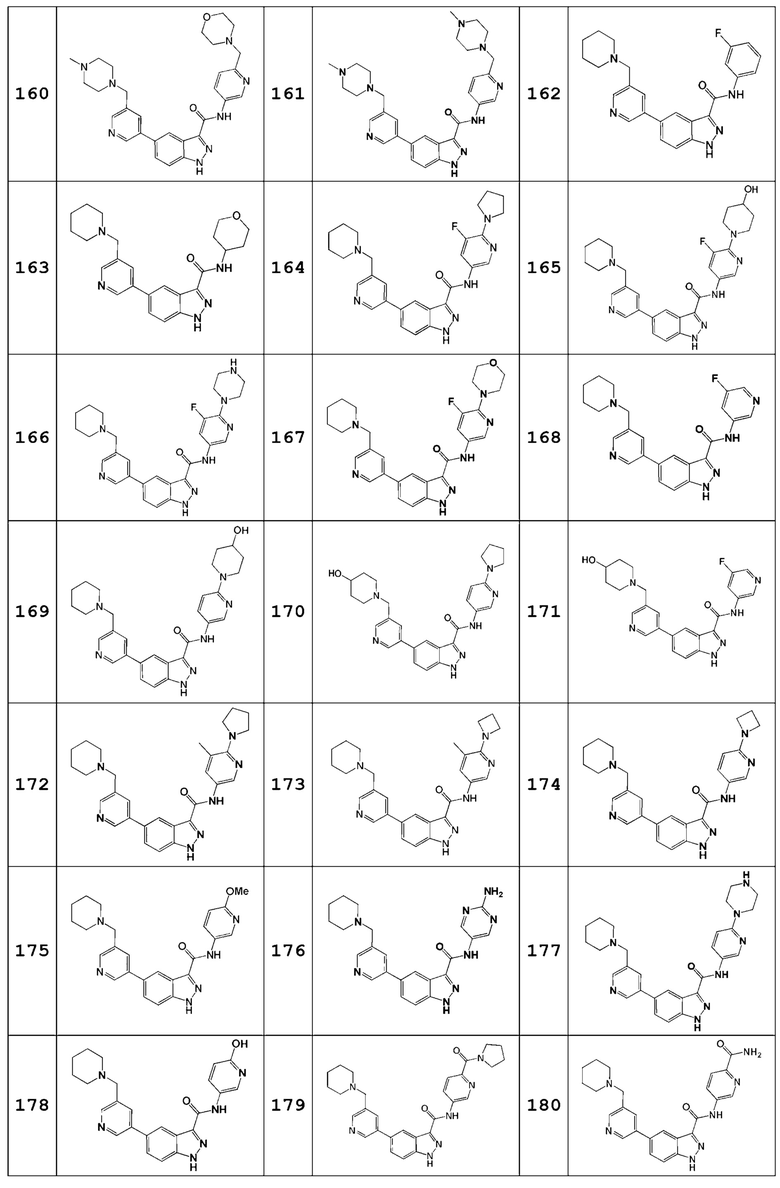
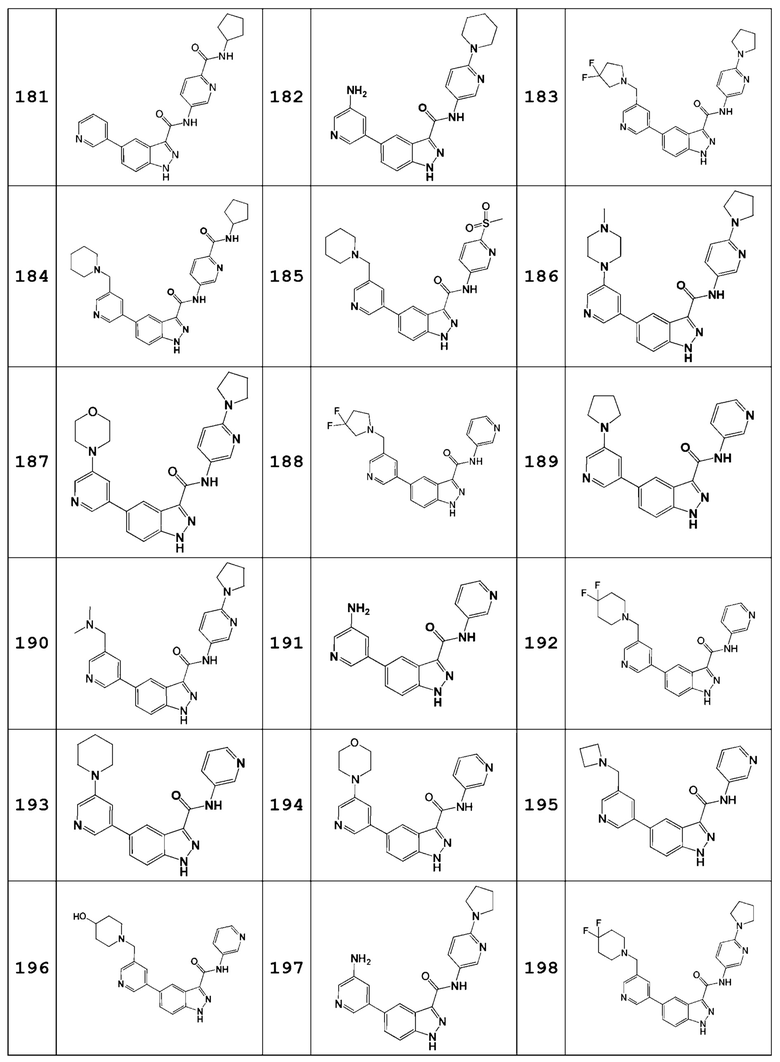
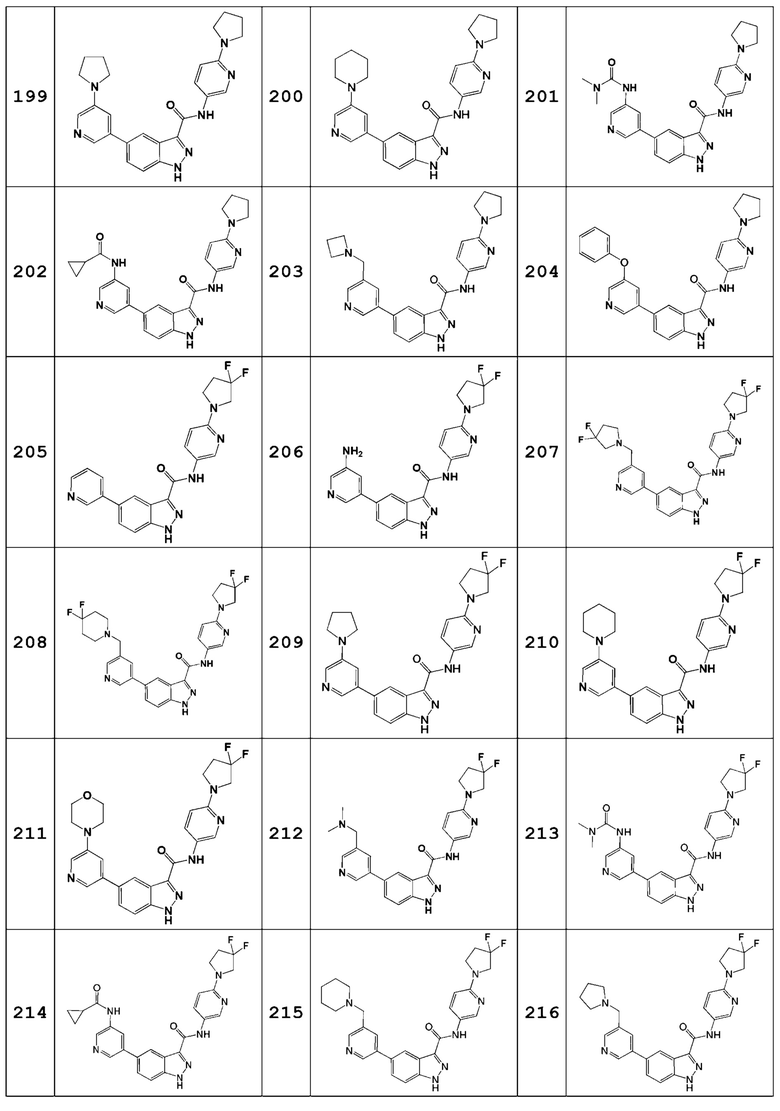
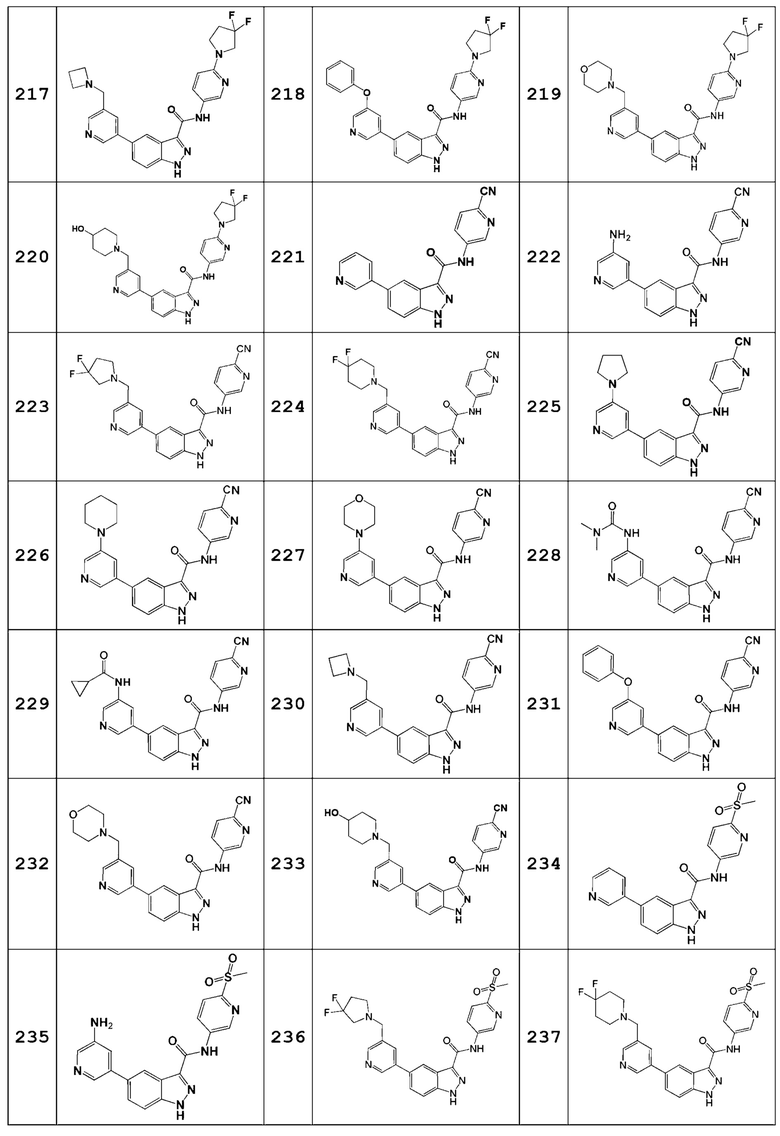
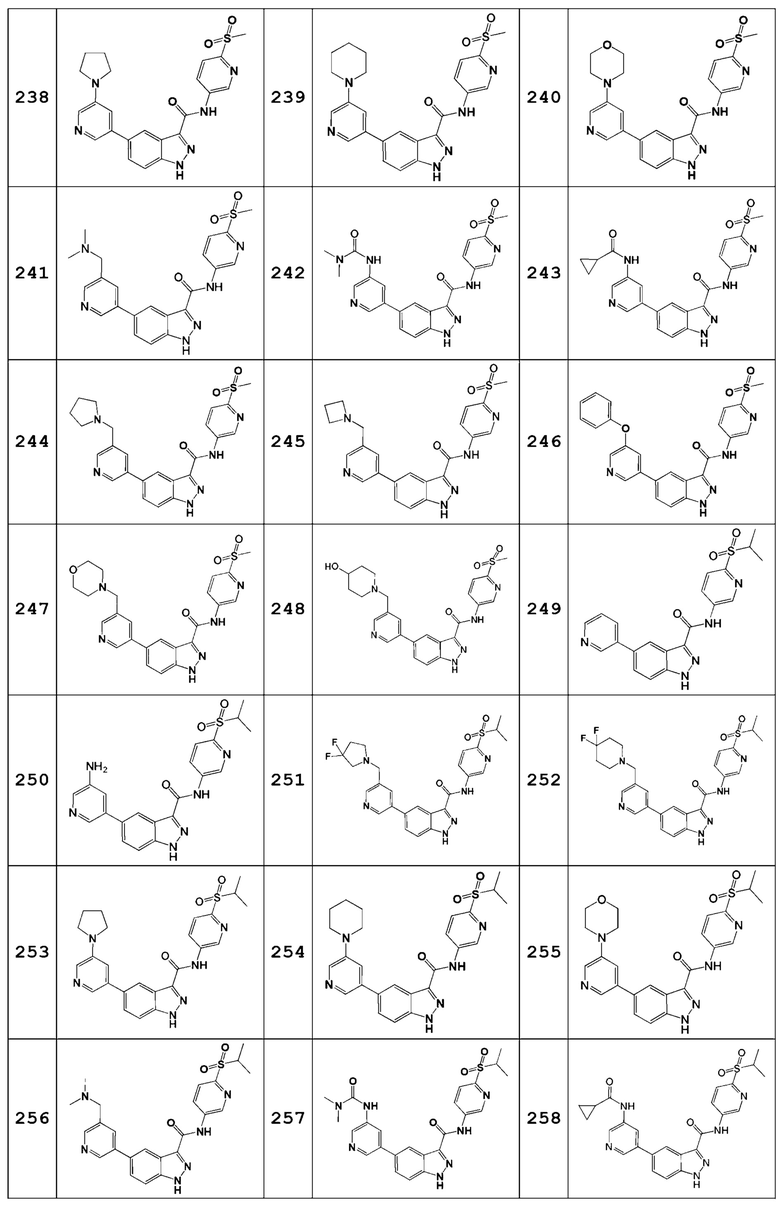
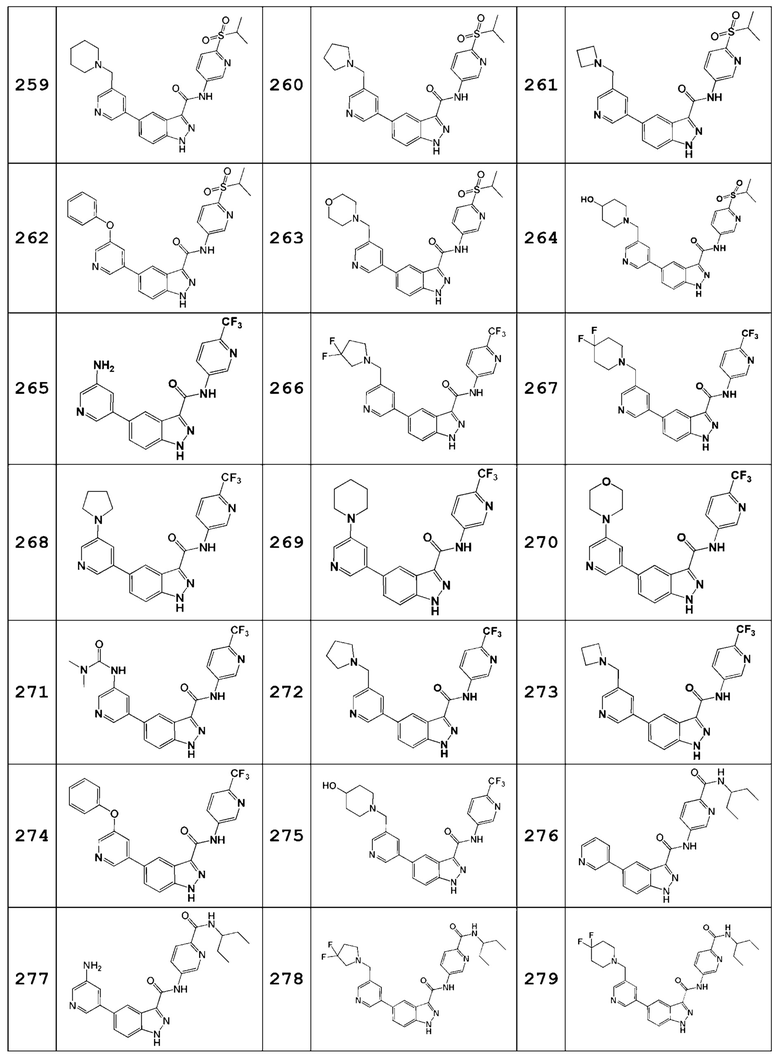
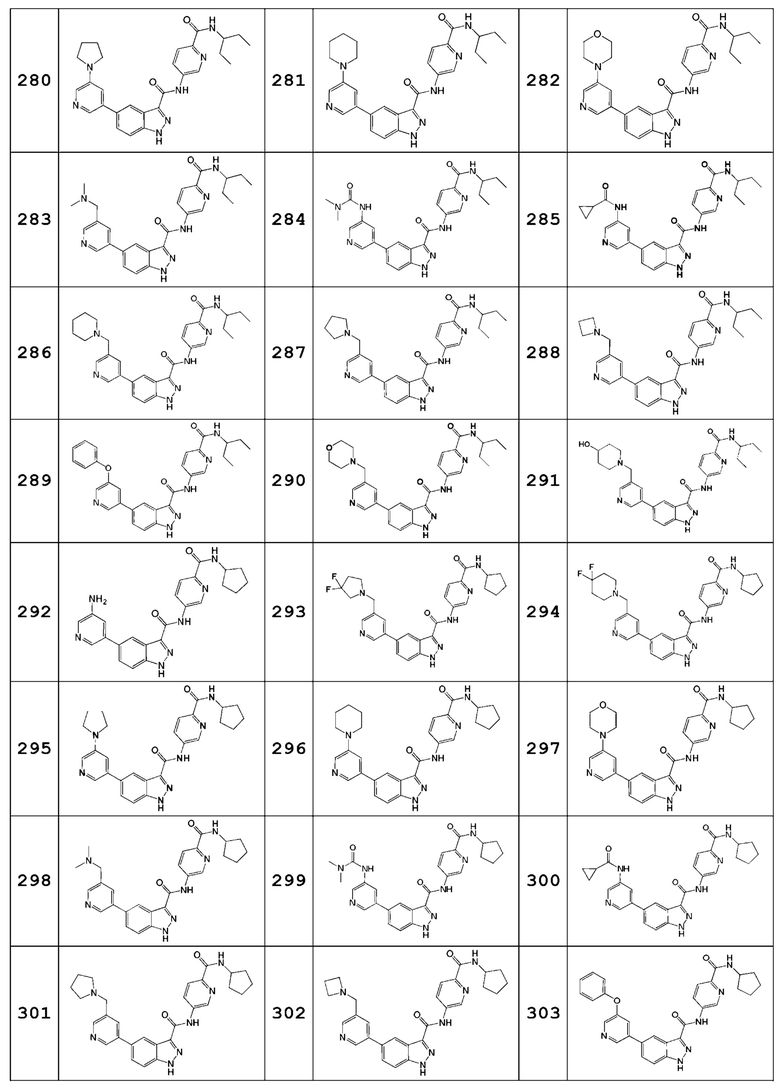
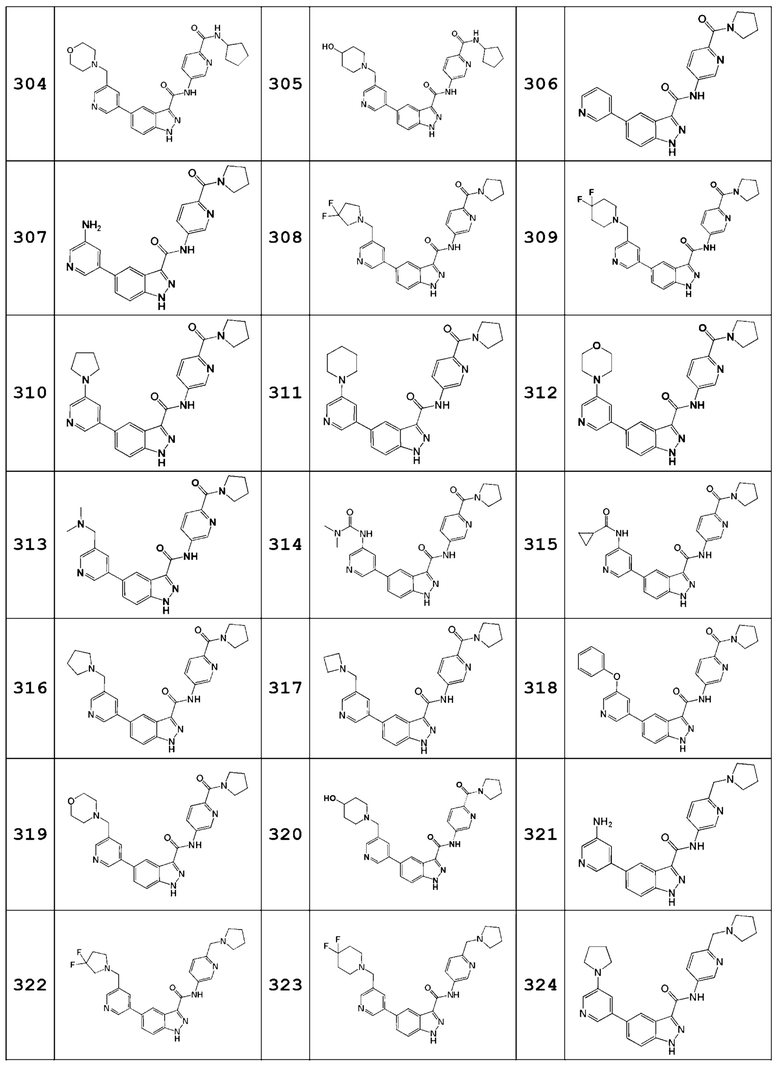
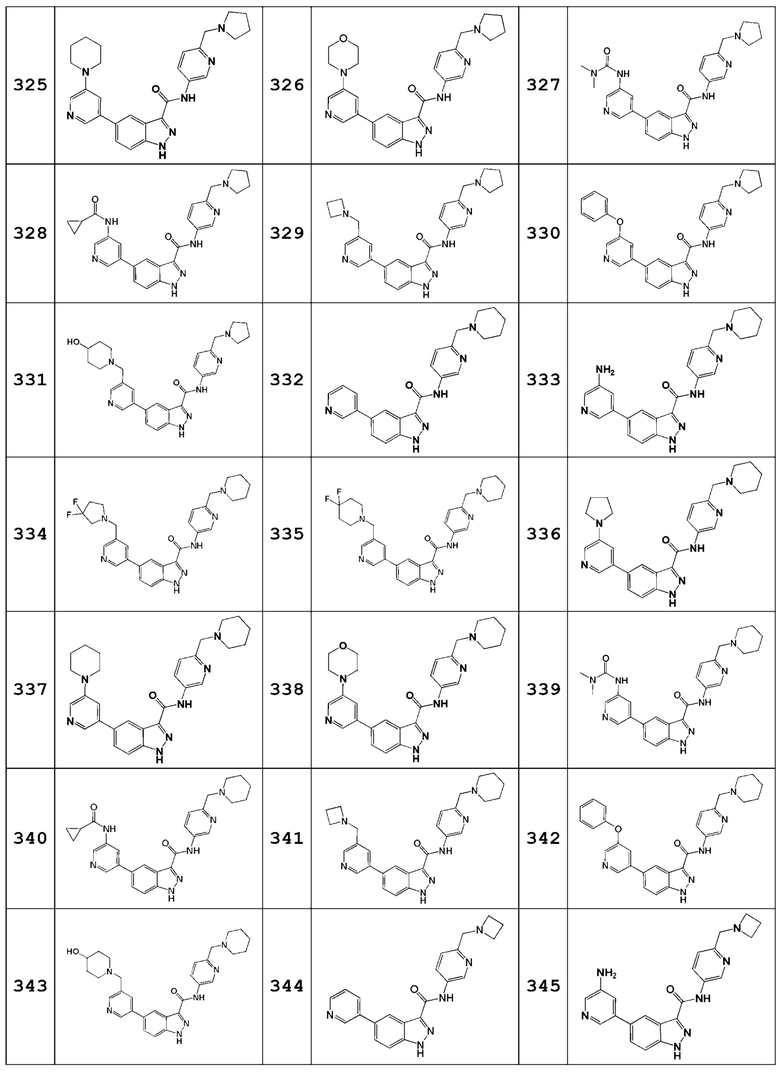
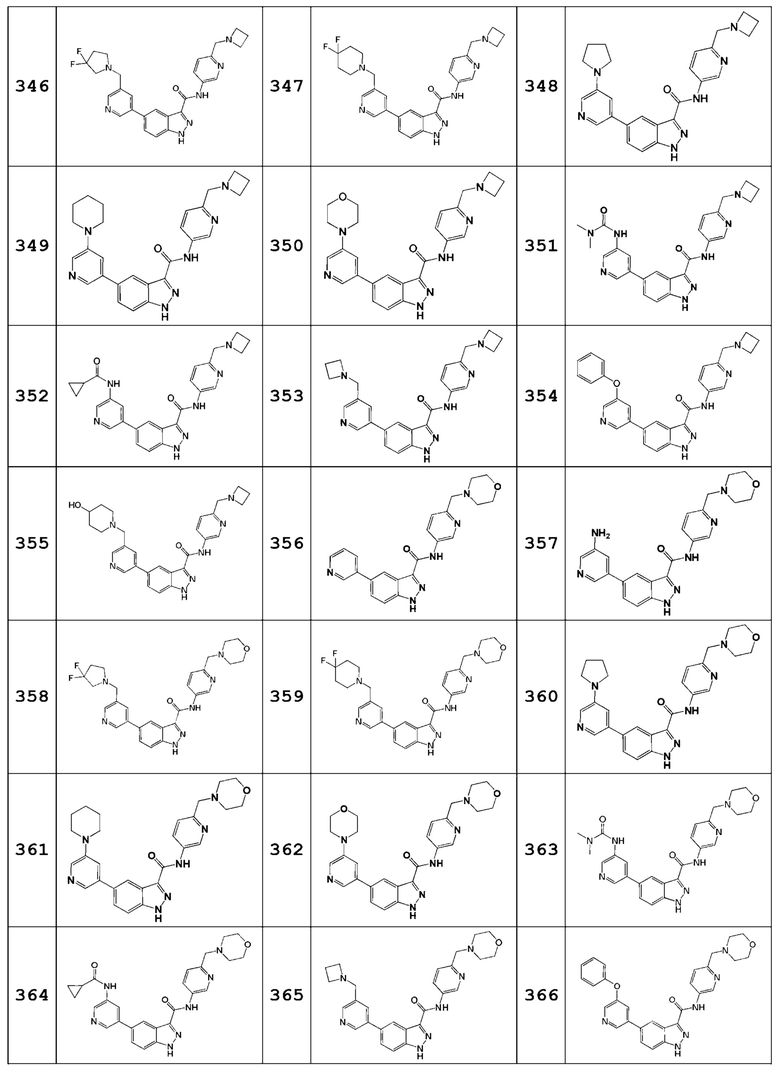
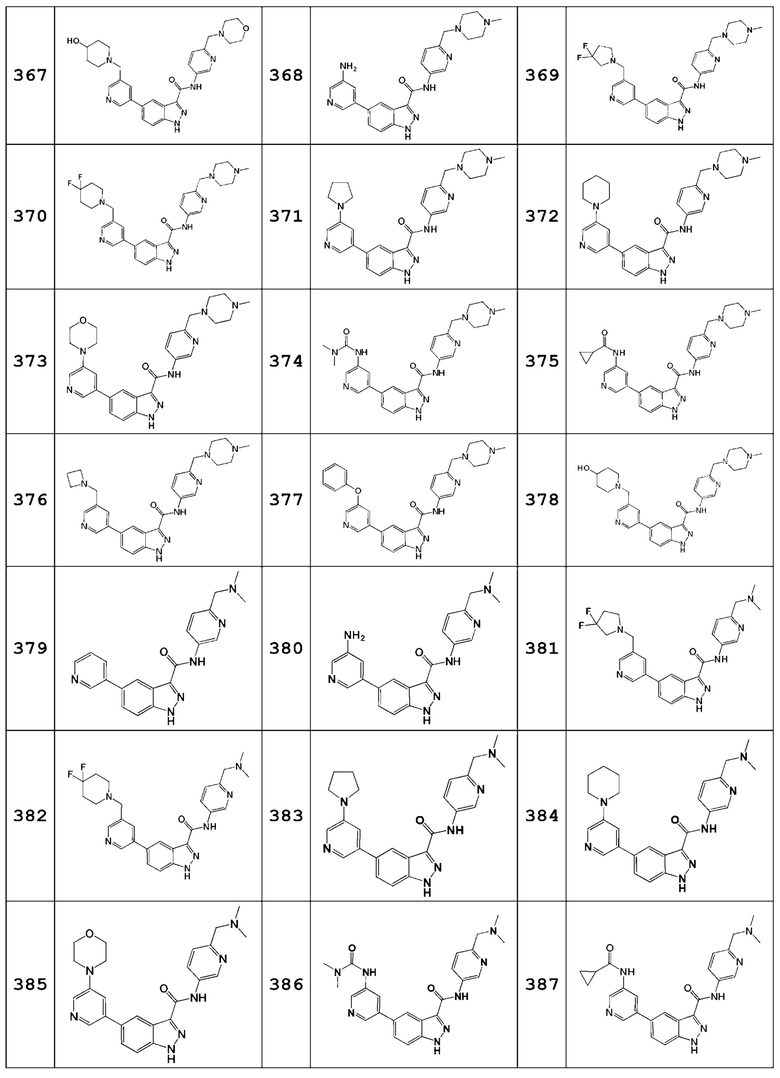
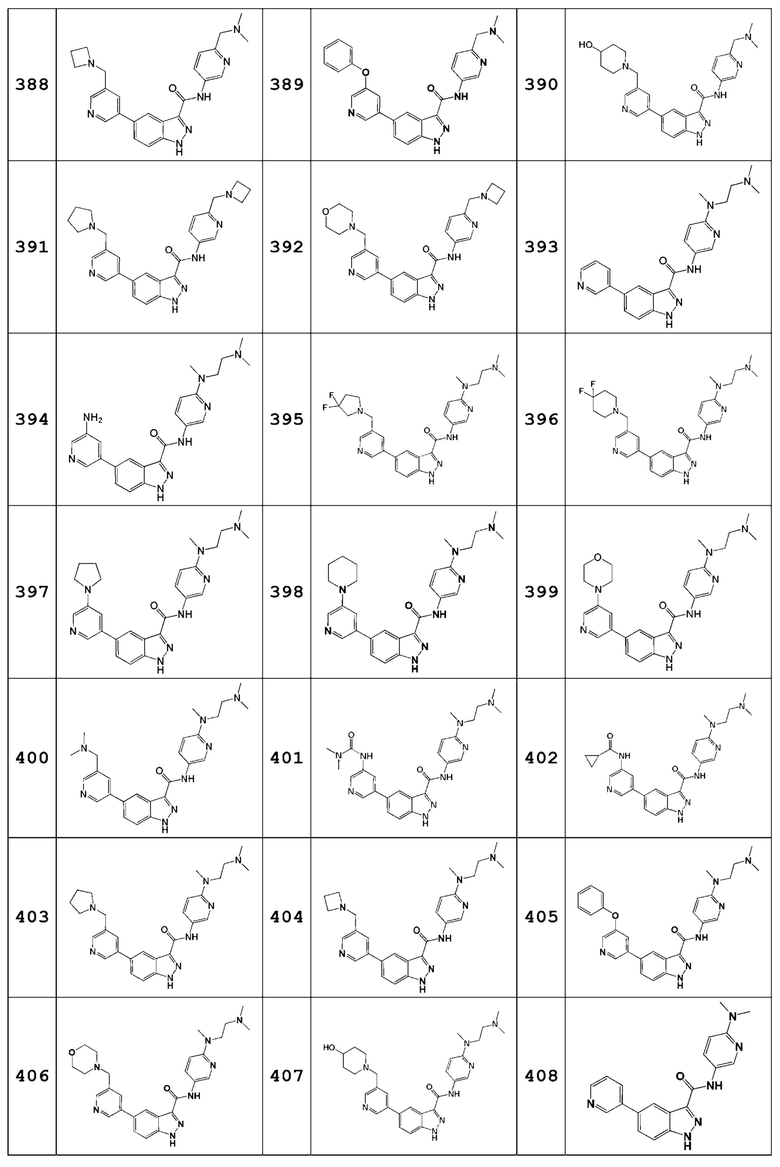
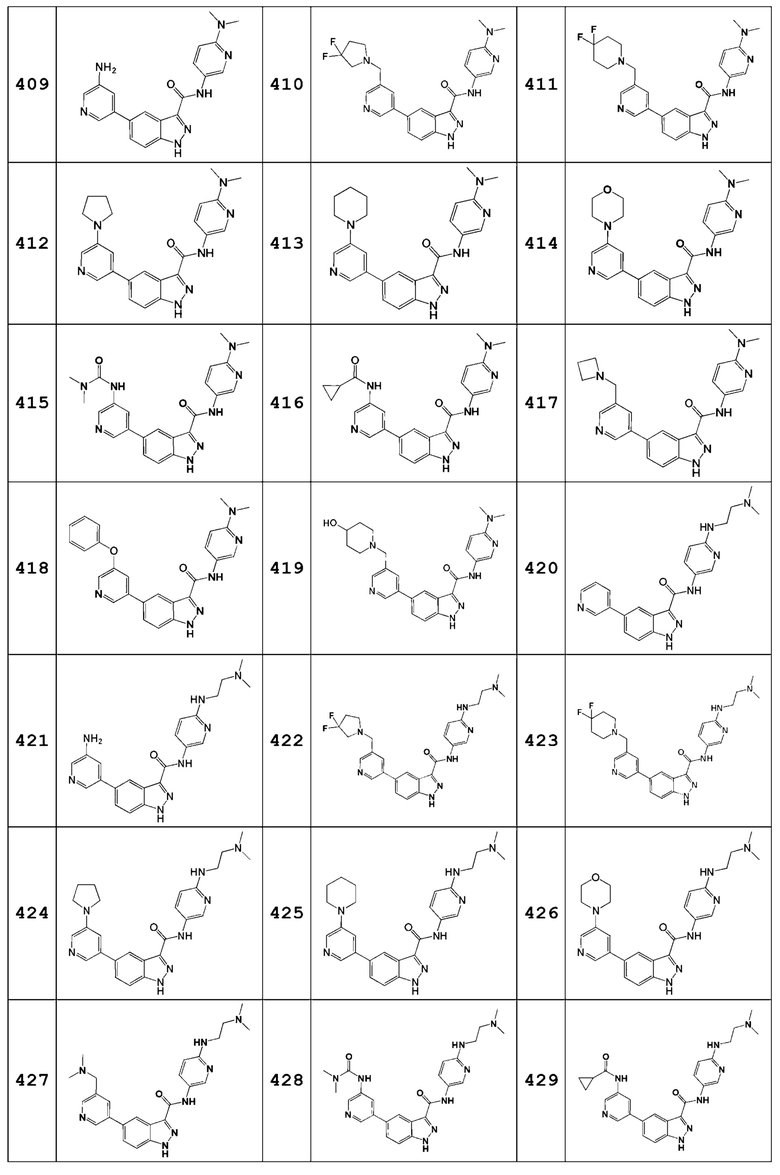
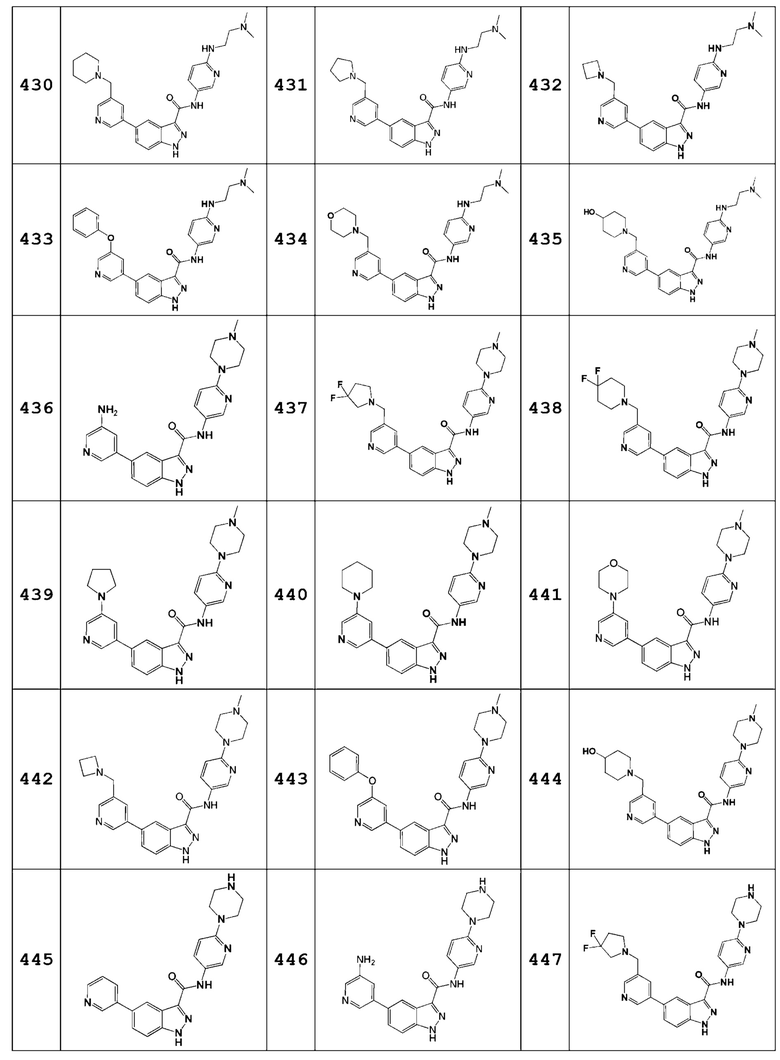
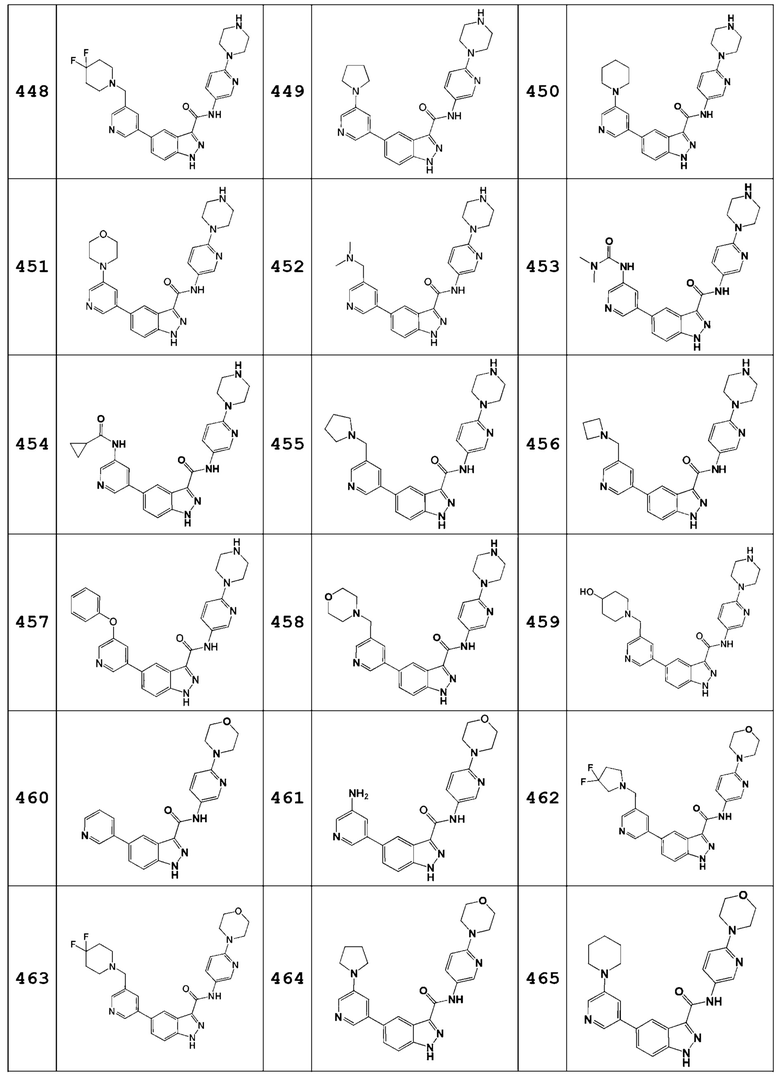
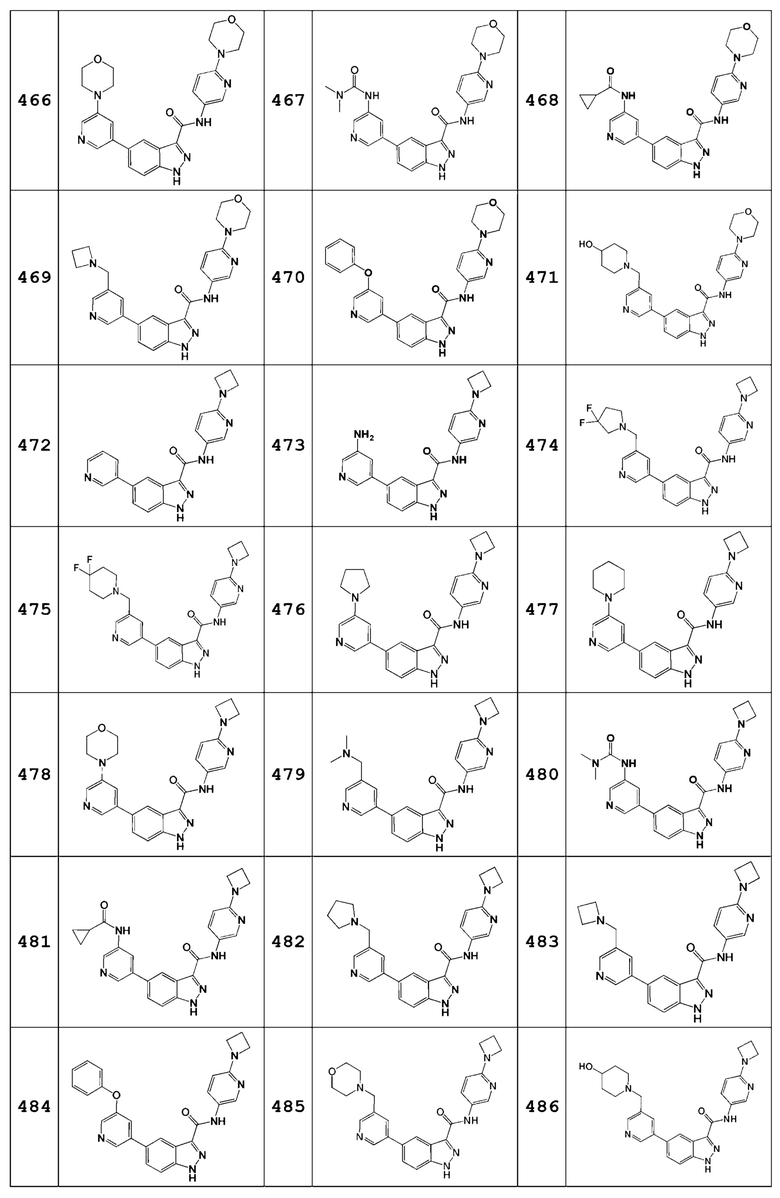
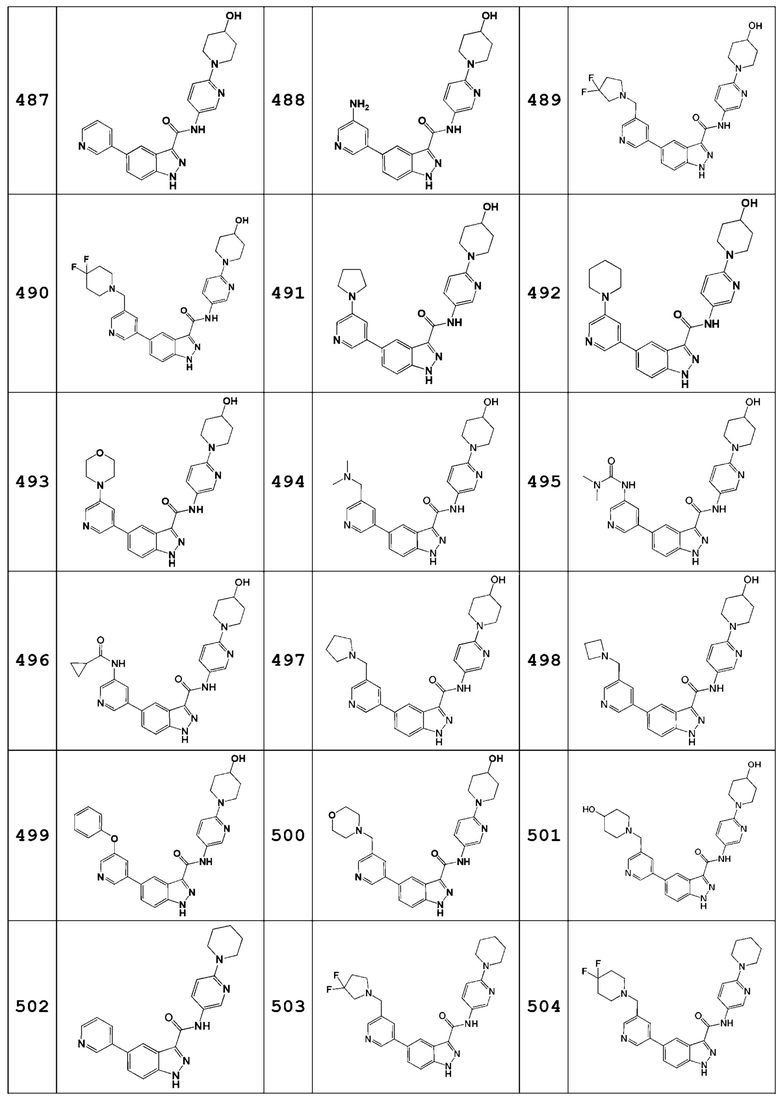
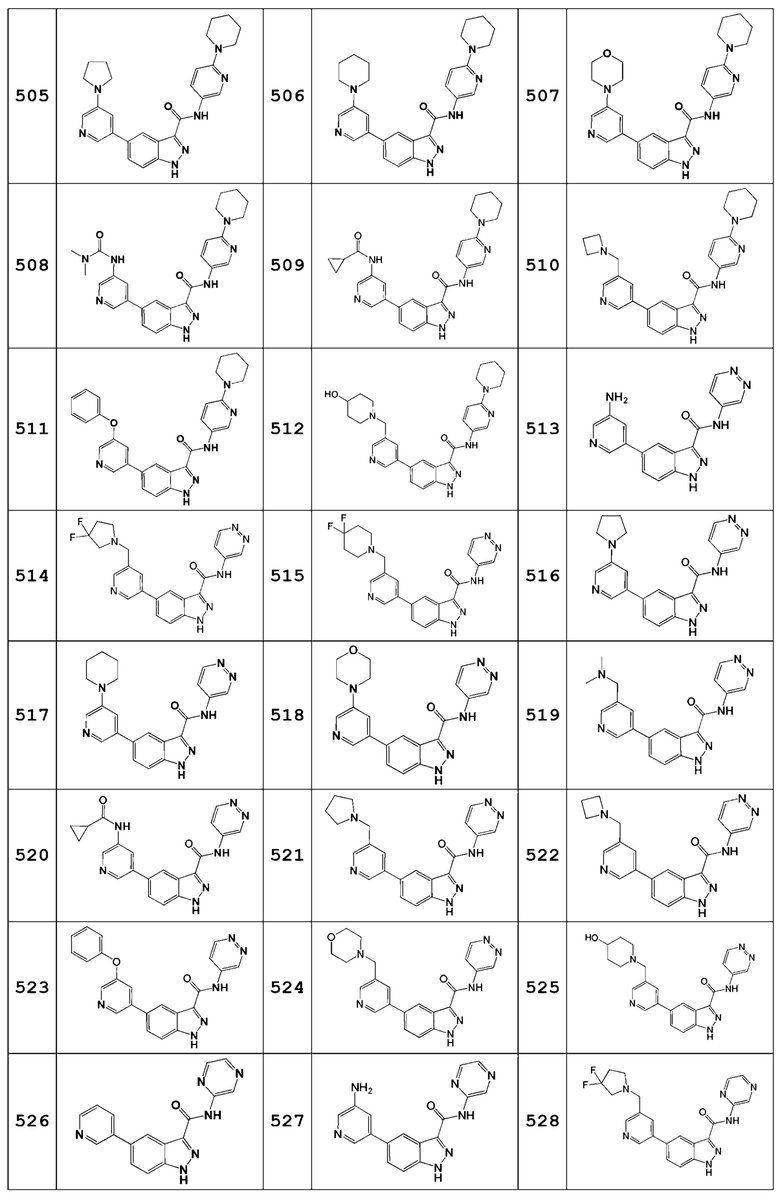
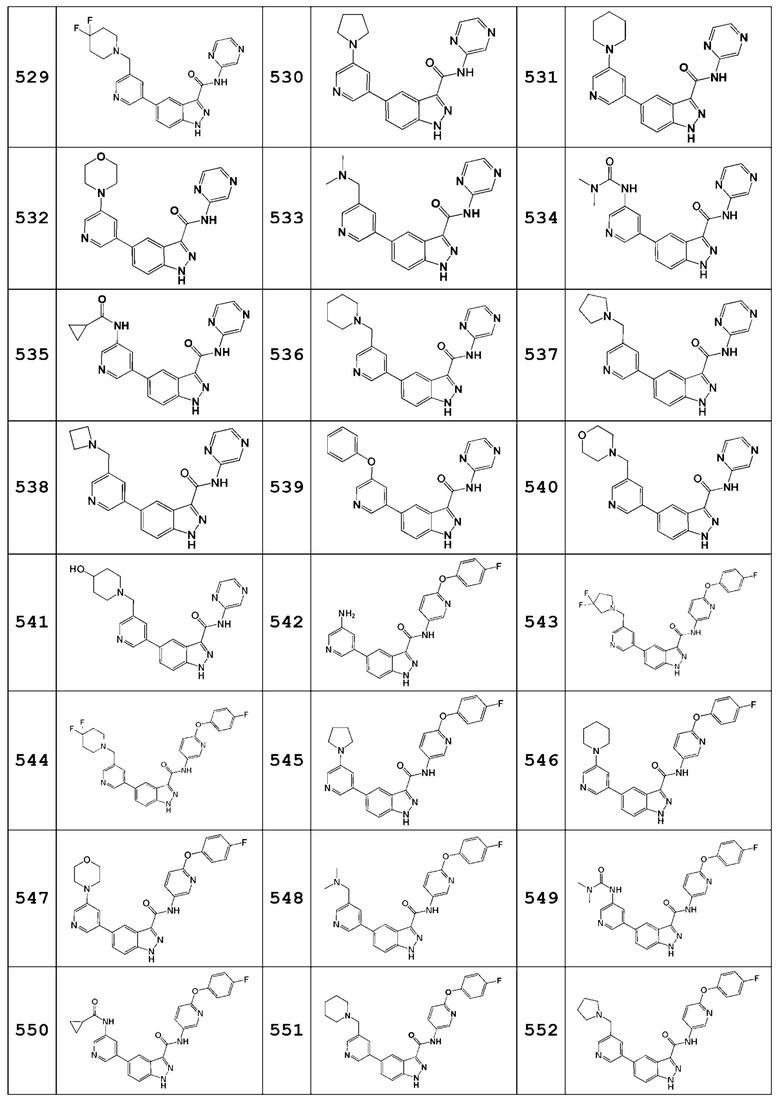
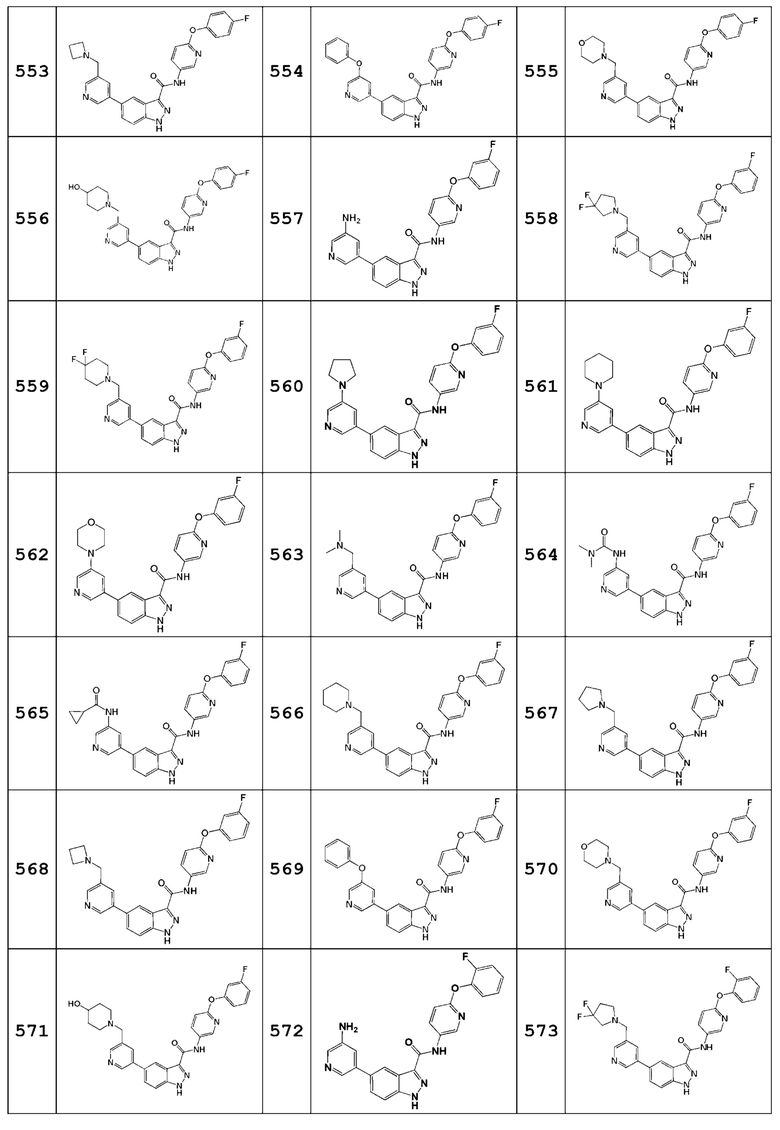
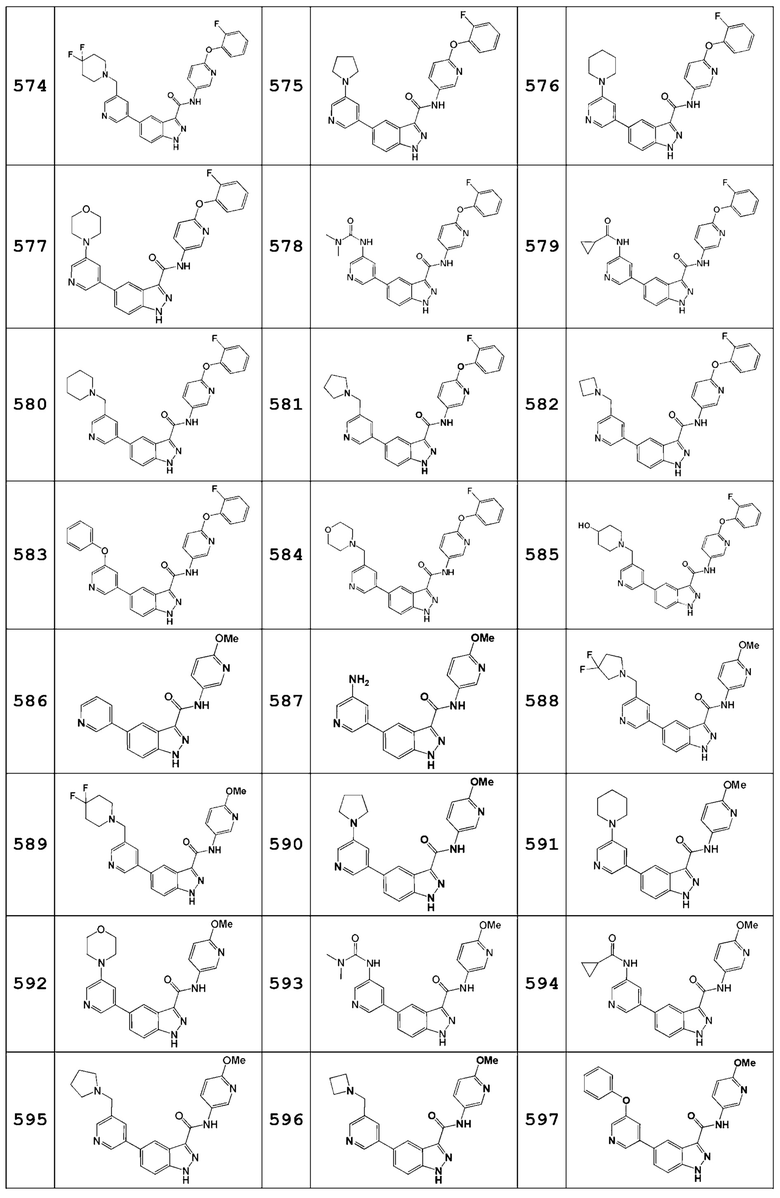
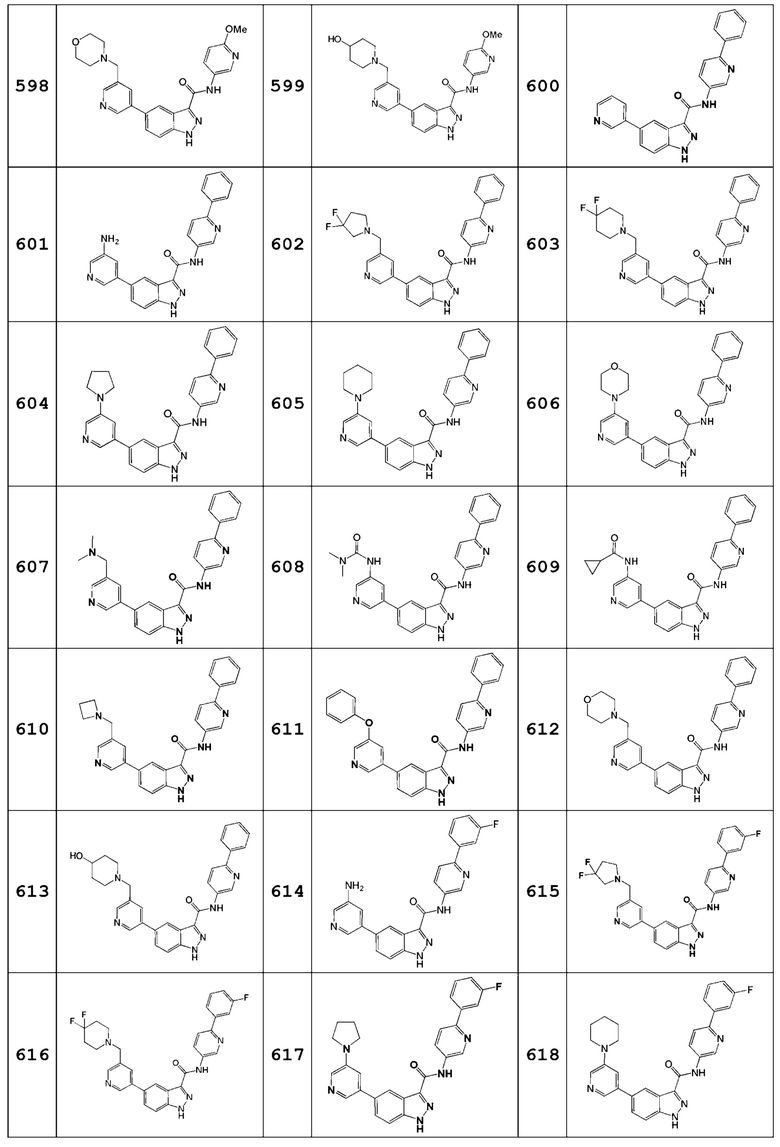
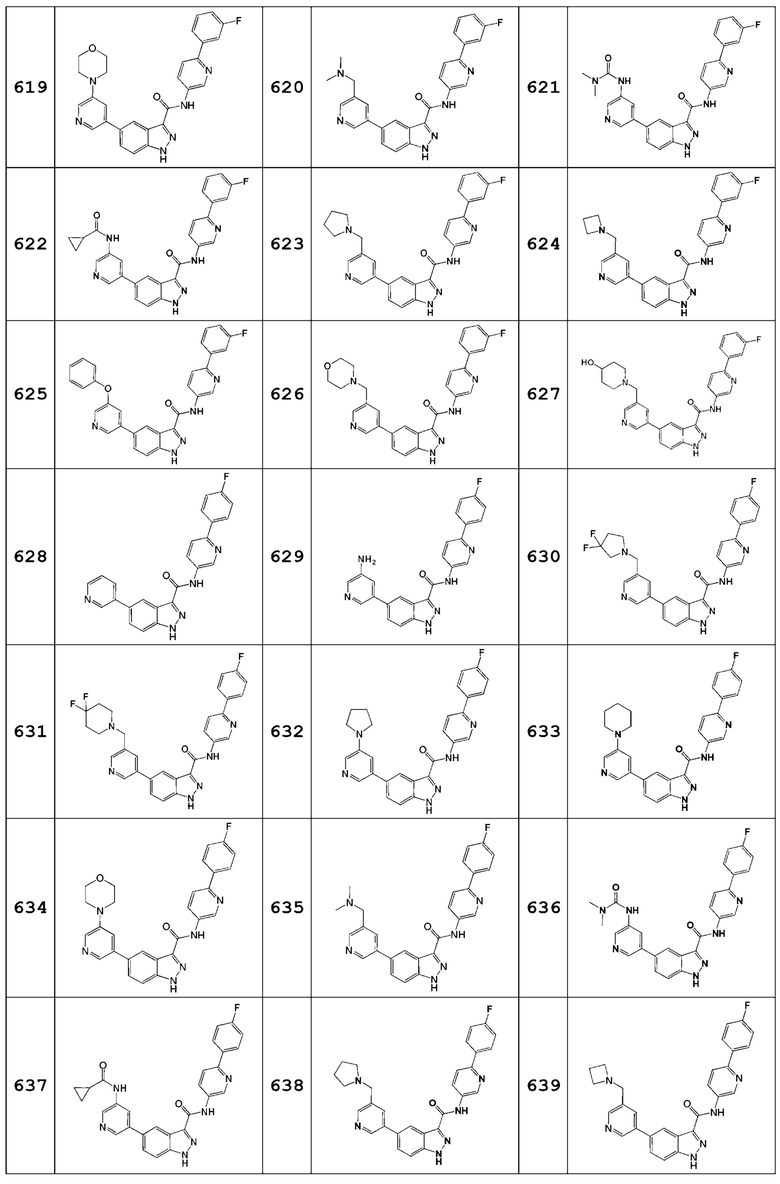
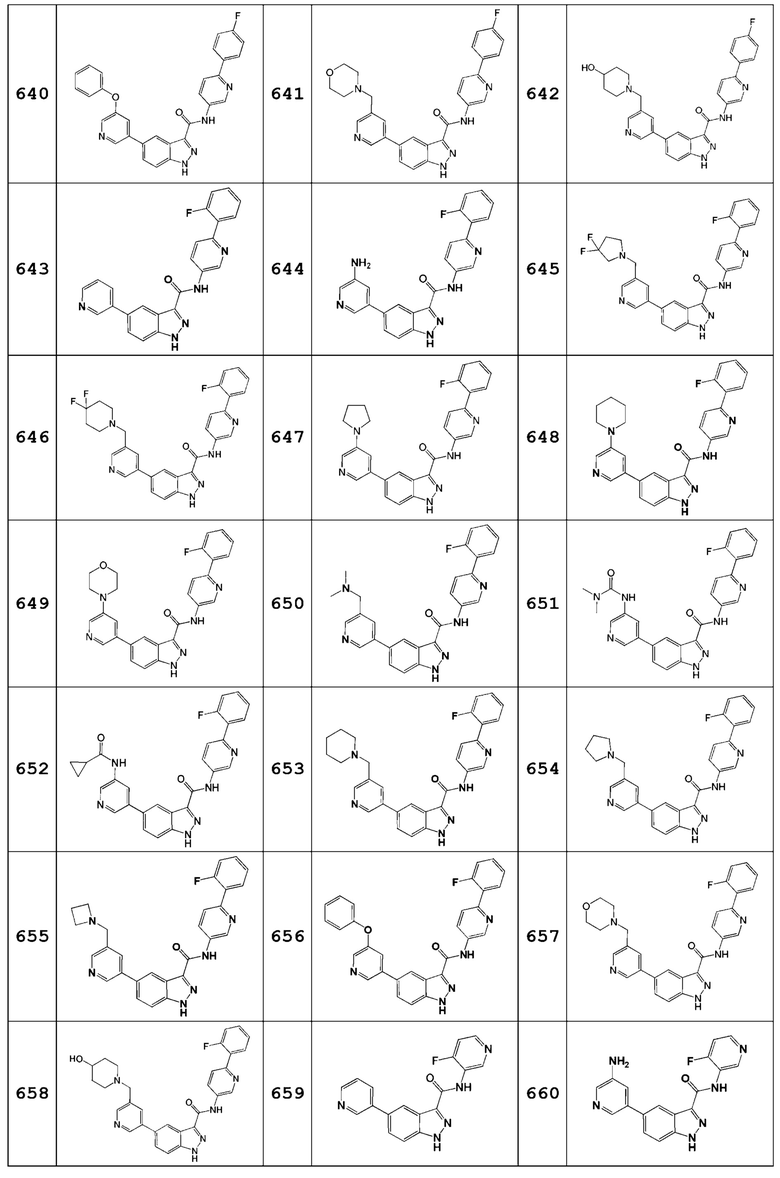
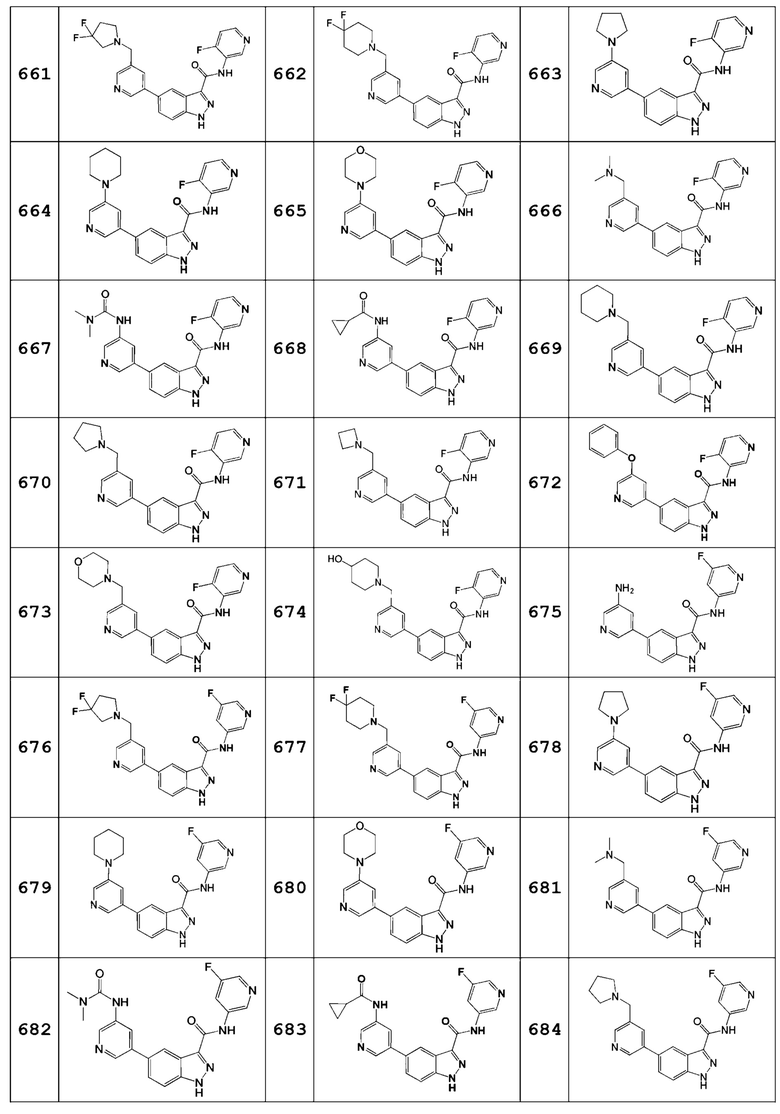
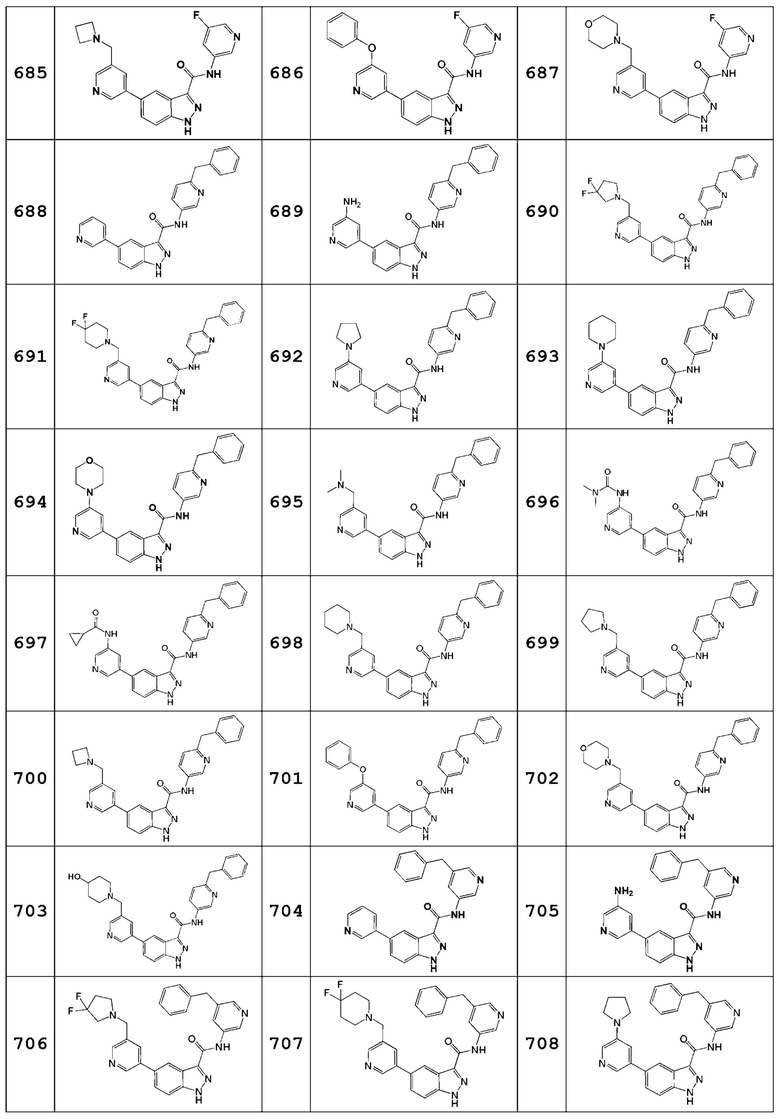
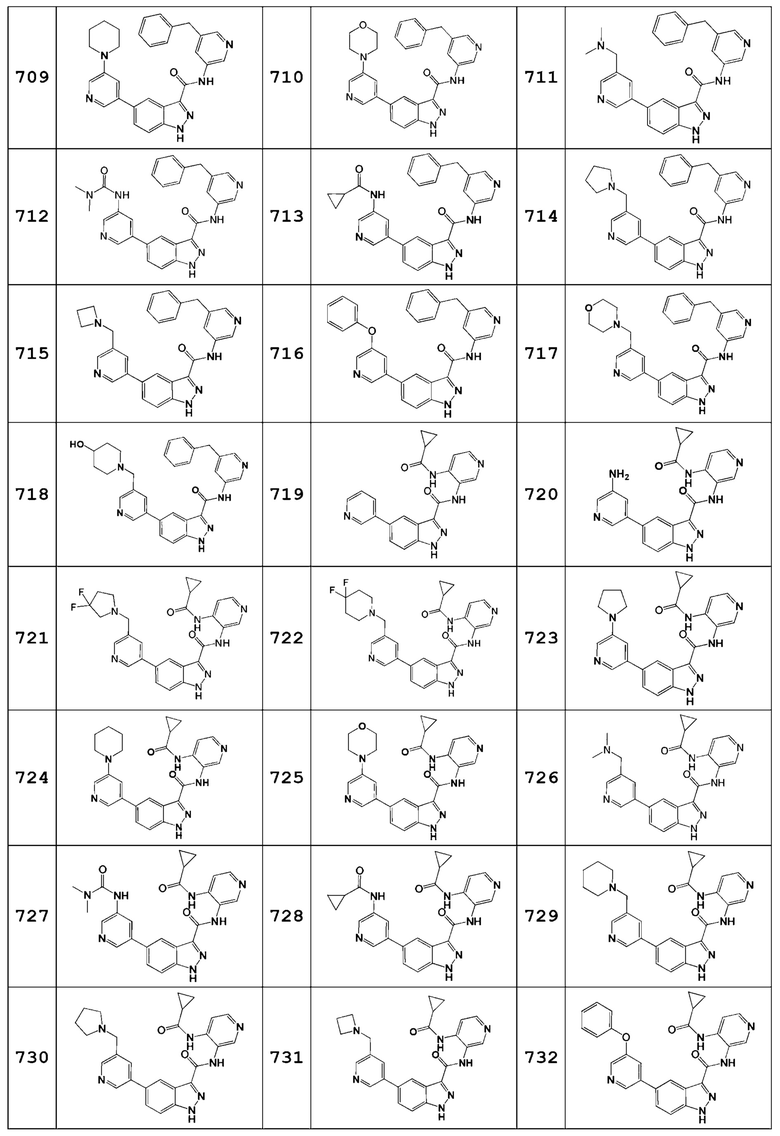
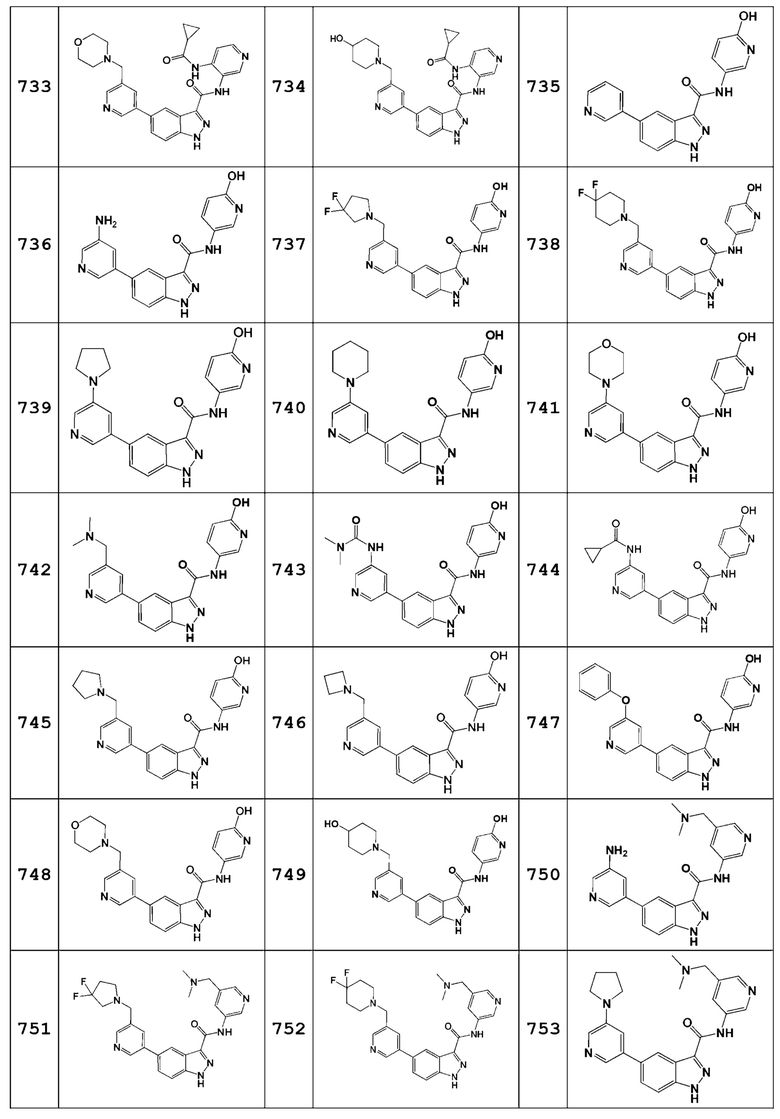
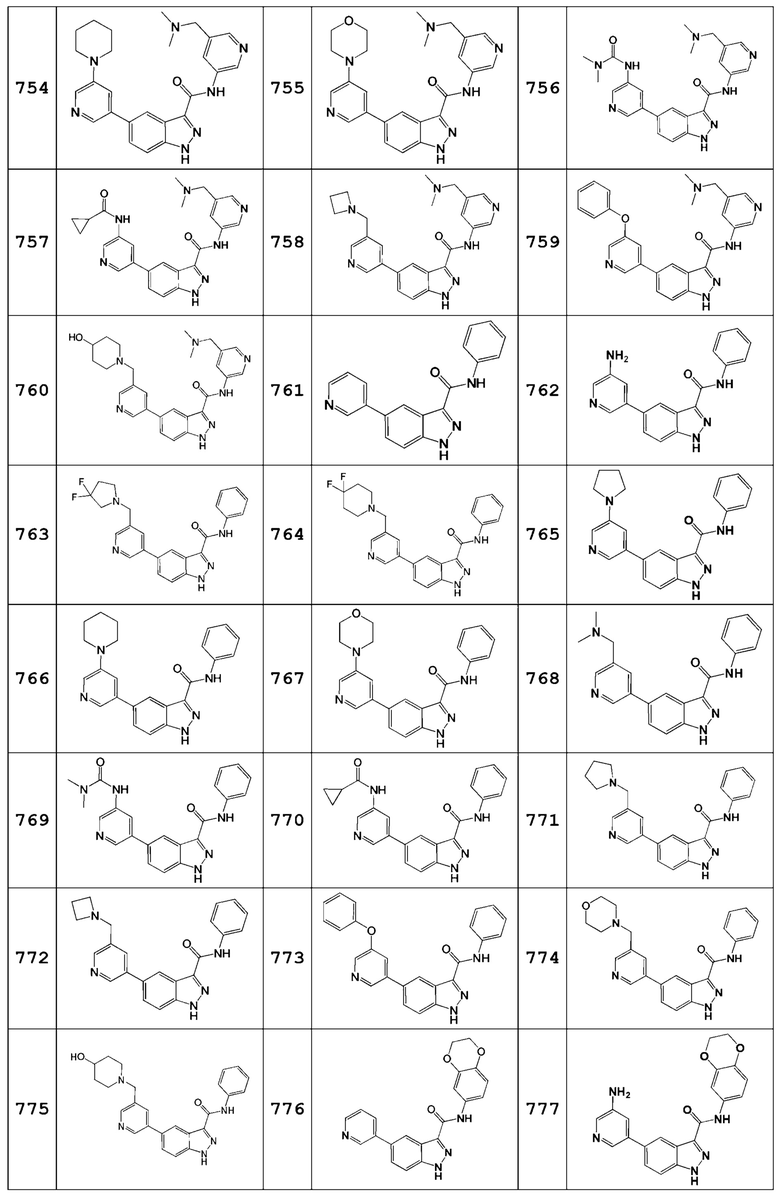
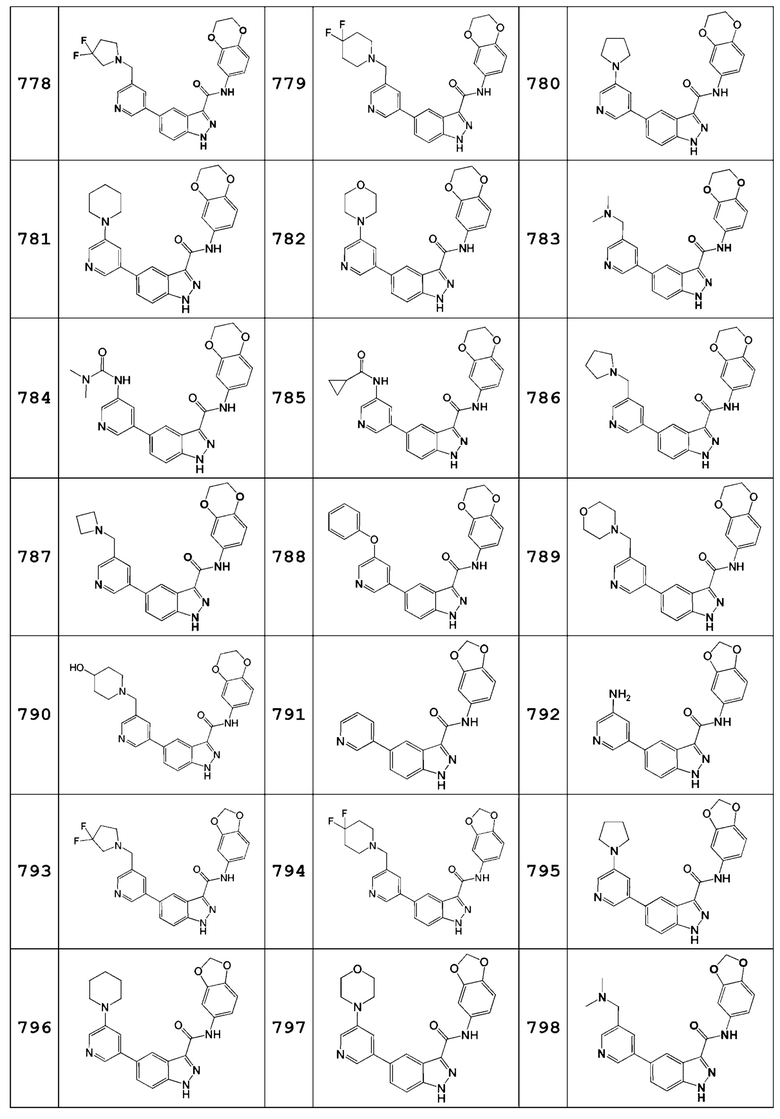
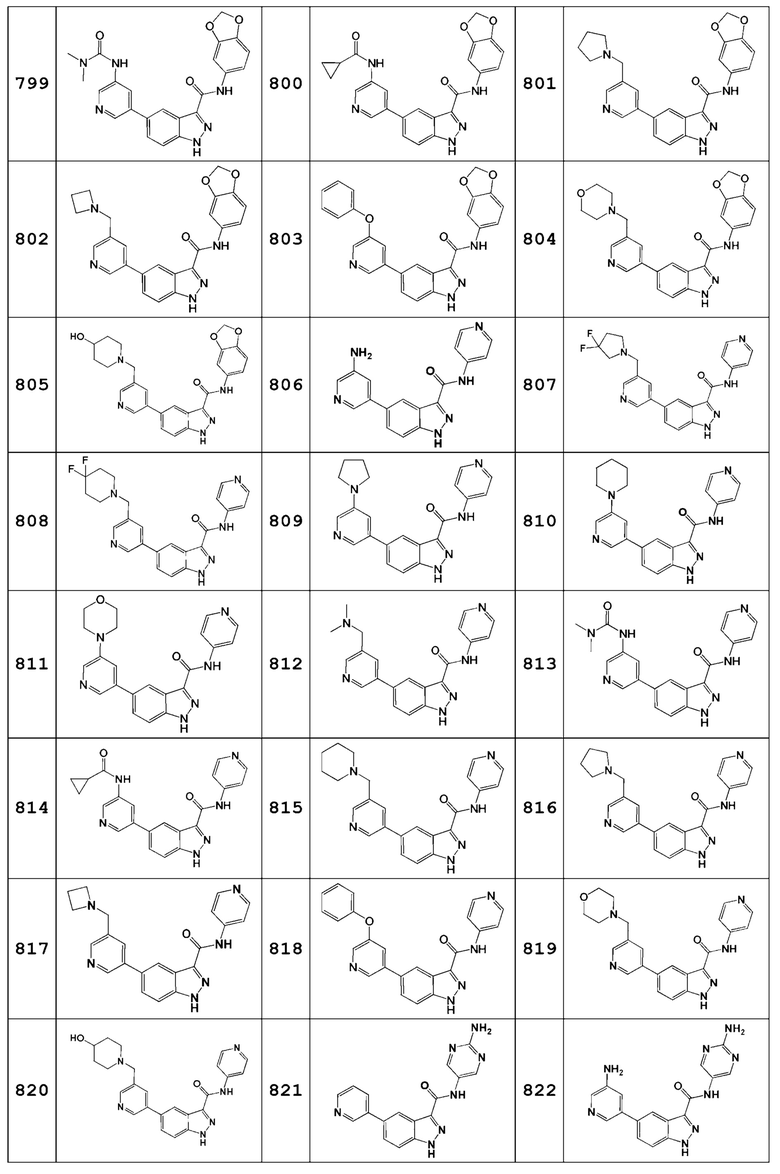
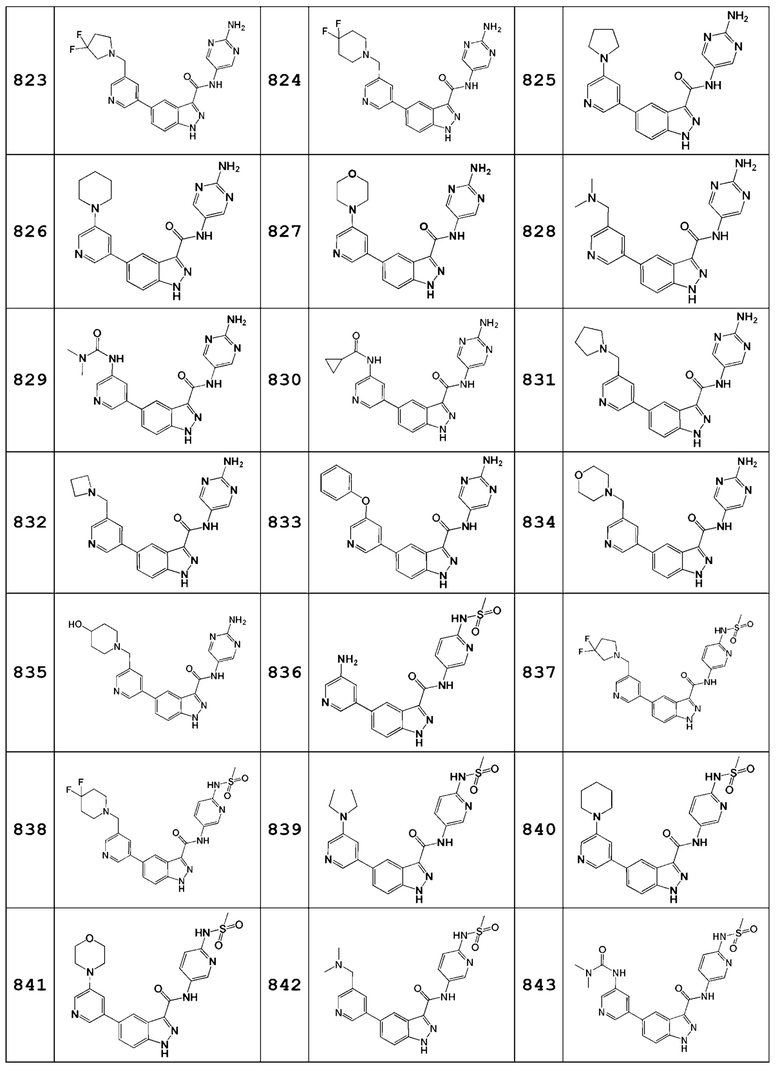
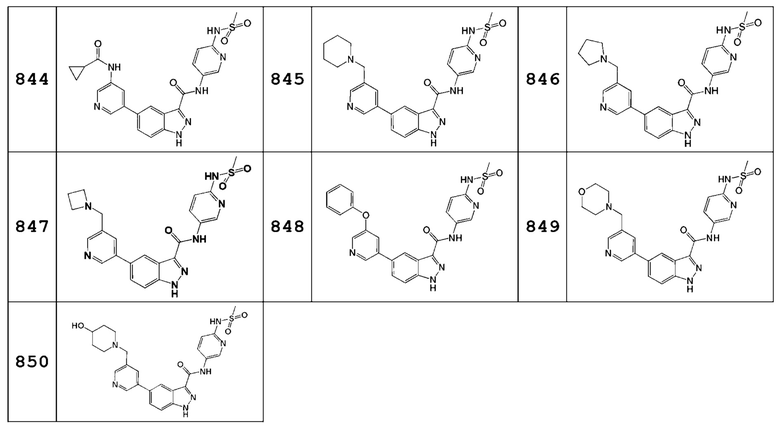
Получение соединений
[0260] Исходные вещества, используемые при получении соединений согласно настоящему изобретению, известны, могут быть получены известными способами или доступны в продаже. Специалисту в данной области будет очевидно, что способы получения предшественников и функциональных групп, относящиеся к заявленным в настоящем документе соединениям, как правило, описаны в литературе. Специалист в данной области на основе литературных сведений и настоящего описания сумеет легко получить любое из этих соединений.
[0261] Следует понимать, что специалист в области органической химии сможет легко произвести манипуляции без дополнительного указания, то есть проведение таких манипуляций находится в рамках компетенции и практических навыков специалиста в данной области. Они включают восстановление карбонильных соединений до соответствующих спиртов, окисление, ацилирование, ароматическое замещение, как электрофильное, так и нуклеофильное, этерификацию с получением простых и сложных эфиров, омыление и т.п. Подобные манипуляции обсуждаются в стандартных изданиях, таких как March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure 6th Ed., John Wiley & Sons (2007), Carey and Sundberg, Advanced Organic Chemistry 5th Ed., Springer (2007), Comprehensive Organic Transformations: A Guide to Functional Group Transformations, 2nd Ed., John Wiley & Sons (1999) (полностью включенных в настоящий документ посредством отсылки) и т.п.
[0262] Специалисту в данной области будет очевидно, что некоторые реакции лучше проводить, когда в молекуле другие функциональные группы замаскированы или защищены, что позволяет избежать нежелательных побочных реакций и/или повысить выход реакции. Часто специалист использует защитные группы для получения таких повышенных выходов и исключения нежелательных реакций. Такие реакции описаны в литературе, а также известны специалисту в данной области. Примеры многих таких манипуляций можно найти, например, в издании T. Greene and P. Wuts Protecting Groups in Organic Synthesis, 4th Ed., John Wiley & Sons (2007), полностью включеном в настоящий документ посредством отсылки.
[0263] Для дополнительной иллюстрации настоящего изобретения включены следующие примеры. Примеры, безусловно, не следует рассматривать как какое-либо ограничение изобретения. Вариации указанных примеров в рамках объема формулы изобретения находятся в пределах компетенции специалиста в данной области и считаются включенными в объем настоящего изобретения, как описано и заявлено в формуле изобретения. Читателю будет понятно, что специалист в данной области, ознакомившись с настоящим изобретением, сумеет подготовить и применить изобретение без исчерпывающих примеров.
[0263] Торговые наименования, используемые в настоящем документе, являются лишь примерами и отражают иллюстративные материалы, используемые на момент публикации изобретения. Специалисту в данной области будет известно, что можно ожидать изменений в партиях, производственных процессах и т.п. Следовательно, примеры и торговые наименования, используемые в них, не являются ограничивающими, и они не предназначены для ограничения, а являются лишь иллюстрацией того, как специалист в данной области может выбрать для реализации один или более вариантов осуществления изобретения.
[0265] (1H) спектры ядерного магнитного резонанса (ЯМР) были получены в указанных растворителях на ЯМР-спектрометре Bruker (Avance TM DRX300, 300 МГц для 1H или Avance TM DRX500, 500 МГц для 1H) или на ЯМР-спектрометре Varian (Mercury 400BB, 400 МГц для 1H). Положения пиков выражены в миллионных долях (м.д.) в сторону слабого поля от тетраметилсилана. Мультиплетность пиков обозначена следующим образом: с, синглет;, д, дублет; т, триплет; к, квартет; АВк, AB-квартет; квин, квинтет; сек, секстет; сеп, септет; нон, нонет; дд, дублет дублетов; д/ABкв, дублет AB-квартетов; дт, дублет триплетов; тд, триплет дублетов; м, мультиплет.
[0266] Следующие сокращения имеют указанные значения:
солевой раствор=насыщенный водный раствор хлорида натрия
CDCl3=дейтерированный хлороформ
ДХЭ=дихлорэтан
ДХМ=дихлорметан
DHP=дигидропиран
DIPEA=диизопропилэтиламин
ДМФА=N,N-диметилформамид
ДМСО-d6=дейтерированный диметилсульфоксид
ЭРИ-МС=масс-спектрометрия с электрораспылительной ионизацией
EtOAc=этилацетат
EtOH=этанол
ч=час
HATU=гексафторфосфат 2-(1H-7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония
HCl=соляная кислота
HOAc=уксусная кислота
H2SO4=серная кислота
iPrOH=изопропиловый спирт
KOAc=ацетат калия
K3PO4=фосфат калия
LAH=алюмогидрид лития
mCPBA=мета-хлорнадбензойная кислота
MeOH=метанол
MgSO4=сульфат магния
мин=минута
MW=микроволновое излучение
NaBH(OAc)3=триацетоксиборогидрид натрия
NaHCO3=бикарбонат натрия
NaHSO3=бисульфит натрия
NaHSO4=бисульфат натрия
NaOH=гидроксид натрия
NH4OH=гидроксид аммония
ЯМР=ядерный магнитный резонанс
Pd/C=палладий (0) на угле
PdCl2(dppf)2=хлорид 1,1'-бис(дифенилфосфино)ферроцен]-палладия (II)
Pd2(dba)3=трис(дибензилиденацетон)дипалладия (0)
Pd(PPh3)4=тетракис(трифенилфосфин)палладий (0)
PPTS=п-толуолсульфонат пиридиния
к.т.=комнатная температура
нас.=насыщенный
р-р=раствор
Дефлегм.=нагревание с обратным холодильником
ТЭА=триэтиламин
ТФУ=трифторуксусная кислота
ТГФ=тетрагидрофуран
ТСХ=тонкослойная хроматография
Tr-Cl=тритилхлорид или трифенилметилхлорид
[0267] Следующие примерные схемы представлены читателю для руководства, и в совокупности представляют собой примерный способ получения соединений, предложенных в настоящем документе. Более того, другие способы получения соединений согласно настоящему изобретению будут очевидны среднему специалисту в данной области с учетом следующих схем реакций и примеров. Специалист в данной области сумеет получить указанные соединения такими способам, которые представлены в литературе и в настоящем описании. Нумерация соединений, используемых в схемах синтеза, представленных ниже, предназначена только для данных конкретных схем, и не должна рассматриваться в качестве такой же нумерации в других разделах заявки или спутана с ней. Если не указано иное, все переменные являются такими, как определено выше.
Общие методики
[0268] Соединения Формулы I согласно настоящему изобретению могут быть получены, как показано на Схеме 1.
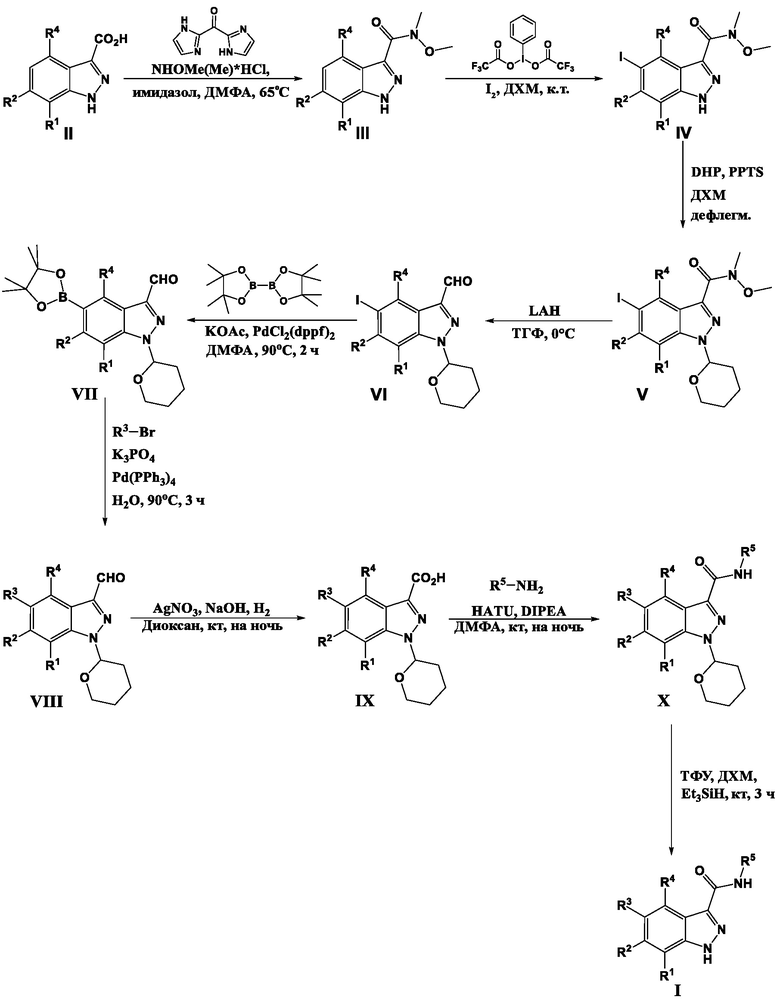
Схема 1
[0269] Схема 1 описывает способ получения производных индазол-3-карбоксамида (I) путем образования сначала амида Вайнреба (III) 1H-индазол-3-карбоновой кислоты (II). Амид Вайнреба (III) подвергают реакции с (бис(трифторацетокси)иод)-бензолом с получением 5-иод-1H-индазол-3-карбоновой кислоты (IV), после чего вводят THP защиту индазольного азота. Амид Вайнреба защищенного индазола V восстанавливают до альдегида VI с последующей реакцией с бис(пинаколато)дибором с получением сложного пинаколового эфира (VII). Конденсация по Сузуки с различными ароматическими и неароматическими бромидами дает R3 замещенный индазол VIII. Окисление альдегида до кислоты (IX) с последующей опосредованной HATU конденсацией различных аминов и удалением защиты дает требуемые производные индазол-3-карбоксамида (I).
[0270] Соединения Формулы I согласно настоящему изобретению могут быть также получены, как показано на Схеме 2.
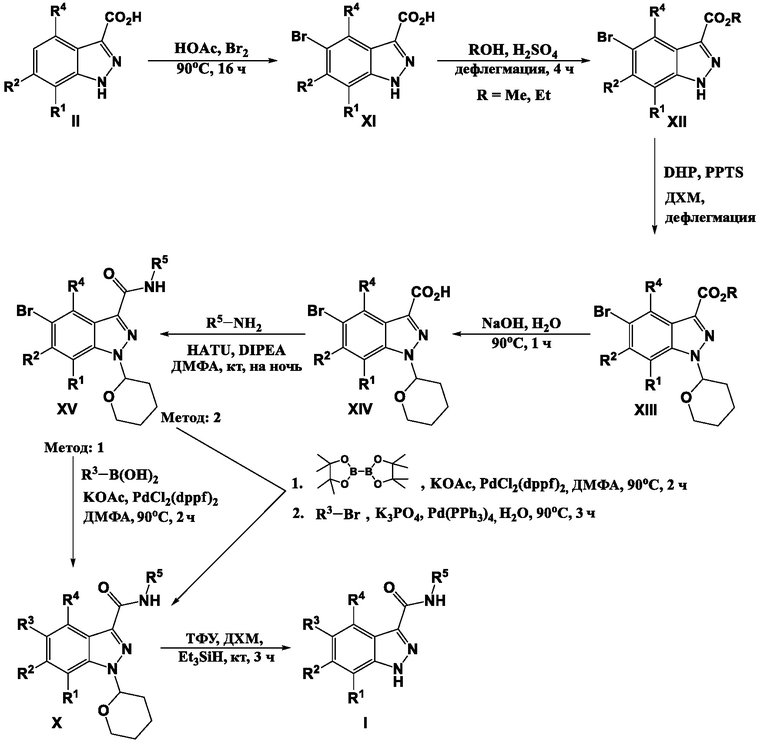
Схема 2
[0271] Схема 2 описывает альтернативный способ получения производных индазол-3-карбоксамида (I) путем бромирования индазола по 5-положении с последующей этерификацией и образованием сложного эфира XII. Азот индазола защищают THP и гидролизуют сложный эфир до кислоты XIV. Кислоту конденсируют с различными аминами с получением амида XV, который затем конденсируют с различными бороновыми кислотами (Метод 1) с получением X. В альтернативном методе XV может быть превращен в боронатный сложный эфир и затем подвергнут конденсации с различными бромидами (Метод 2) с получением X. Заключительное удаление защитных групп индазольного азота дает требуемые производные индазол-3-карбоксамида (I).
[0272] Соединения Формулы I согласно настоящему изобретению также могут быть получены, как показано на Схеме 3.
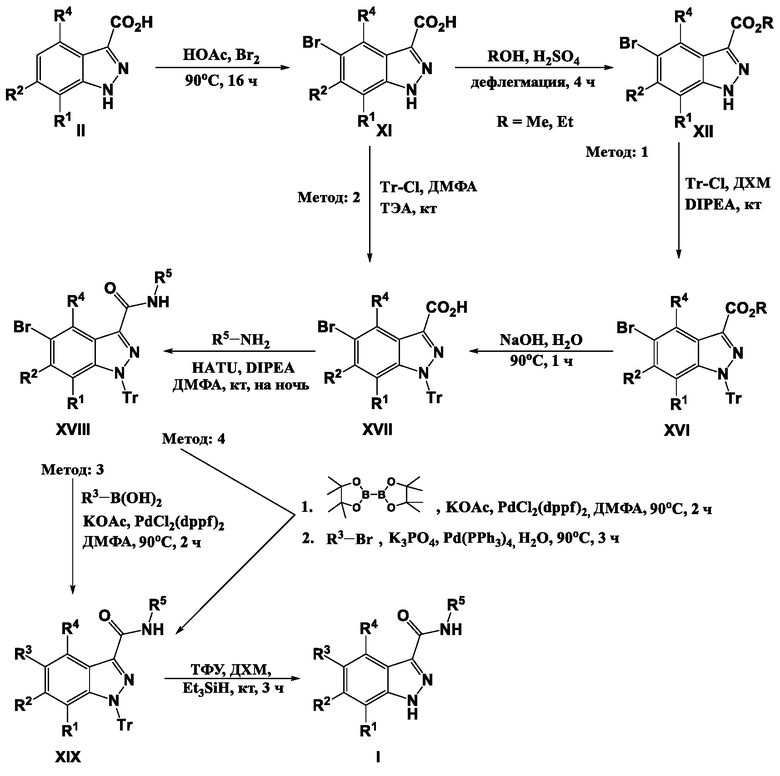
Схема 3
[0273] Схема 3 описывает другой альтернативный способ получения производных индазол-3-карбоксамида (I) путем бромирования 5 положения индазола, и затем либо согласно Методу 1: этерификация с образованием сложного эфира XII, затем тритильная защита индазольного азота и далее конечный гидролиз сложного эфира до кислоты XVII; или по Методу 2: тритильная защита индазольного азота непосредственно с получением кислоты XVII. Кислоту конденсируют с различными аминами с получением амида XVIII, который затем конденсируют с различными бороновыми кислотами (Метод 3) с получением XIX. В альтернативном методе, XVIII может быть превращен в боронатный сложный эфир и затем конденсирован с различными бромидами (Метод 4) с получением XIX. Заключительное удаление защитных групп индазольного азота дает требуемые производные индазол-3-карбоксамида (I).
Иллюстративные примеры соединений
[0274] Получение промежуточной 3-(5-бромпиридин-3-ил)-1,1-диметилмочевины (XXII) показано ниже на Схеме 4.

Схема 4
Стадия 1
[0275] 3-Амино-5-бром-пиридин (XX) (1,0 г, 5,78 ммоль) растворяли в пиридине и охлаждали до температуры 0°C, после чего добавляли диметилкарбамилхлорид (XXI) (0,683 г, 6,35 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов и затем нагревали в течение ночи при температуре 60°C в атмосфере аргона. Раствор охлаждали до комнатной температуры, вливали в воду со льдом и экстрагировали EtOAc. Органический экстракт сушили над MgSO4, фильтровали и выпаривали до остатка с получением 3-(5-бромпиридин-3-ил)-1,1-диметилмочевины (XXII) в виде коричневого твердого вещества (1,24 г, 5,09 ммоль, выход 88%). 1H-ЯМР (ДМСО-d6) δ м.д. 8,67-8,64 (м, 2H), 8,23 (д, J=7,8 Гц, 1H), 2,93 (с, 6H); ЭРИ-МС найдено для C8H10BrN3O m/z 245,05 (M+H).
[0276] Следующие промежуточные соединения получали в соответствии с методикой, описанной на Схеме 4 выше.
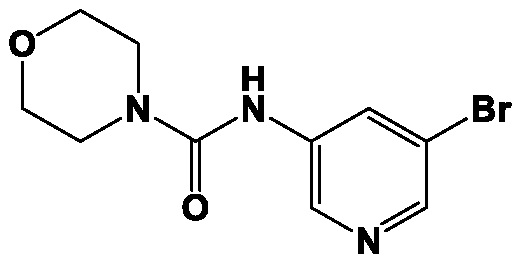
XXIII
[0277] N-(5-бромпиридин-3-ил)морфолин-4-карбоксамид (XXIII): Коричневое твердое вещество (0,82 г, 48%). 1H-ЯМР (ДМСО-d6) 3,43-3,45 (м, 4H), 3,60-3,62 (м, 4H), 8,21 (т, J=2,0 Гц, 1H), 8,26 (д, J=2,0 Гц, 1H), 8,62 (д, J=2,2 Гц, 1H), 8,91 (с, 1H); ЭРИ-МС найдено для C10H12BrN3O2 m/z 286 (M+H).
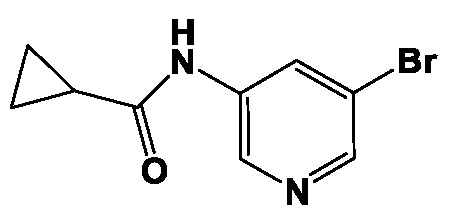
XXIV
[0278] N-(5-бромпиридин-3-ил)циклопропанкарбоксамид (XXIV): Почти белое твердое вещество (выход 83%), 1H-ЯМР (CDCl3, 400 МГц) δ м.д. 8,46-8,39 (м, 3H), 7,54 (шс, 1H), 1,56-1,50 (м, 1H), 1,13-1,07 (м, 2H), 0,96-0,90 (м, 2H); ЭРИ-МС найдено для C9H9BrN2O m/z 240,85 (M+H).
[0279] Получение промежуточного соединения (XXVI) показано на Схеме 5 ниже.
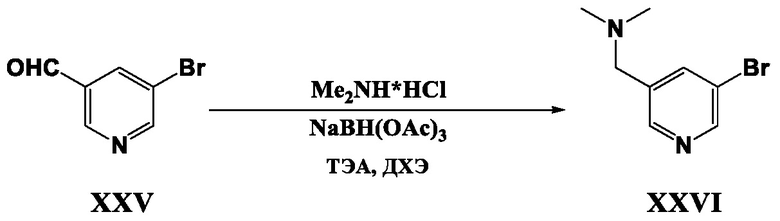
Схема 5
Стадия 1
[0280] К раствору 5-бромникотинальдегида (XXV) (5,0 г, 26,9 ммоль) в ДХЭ (108 мл) добавляли диметиламин-HCl (4,39 г, 53,8 ммоли) и ТЭА (7,5 г, 53,8 ммоль). Реакцию перемешивали при комнатной температуре в течение 1 ч. Добавляли NaBH(OAc)3 и реакцию перемешивали в течение ночи при комнатной температуре. Реакцию разбавляли ДХМ и нас. водным р-ром NaHCO3. Органический слой отделяли, промывали водой, солевым раствором, сушили и выпаривали в вакууме с получением 1-(5-бромпиридин-3-ил)-N,N-диметилметанамина (XXVI) в виде коричневой жидкости (выход 92,6%). 1H-ЯМР (CDCl3) δ м.д. 2,15 (с, 6H), 3,43 (с, 2H), 7,94 (с, 1H), 8,47 (д, J=2 Гц, 1H), 8,59 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C8H11BrN2 m/z 215 (MBr79+H) и 217 (MBr81+H).
[0281] Следующие промежуточные соединения получали в соответствии с методикой, описанной на Схеме 5 выше.
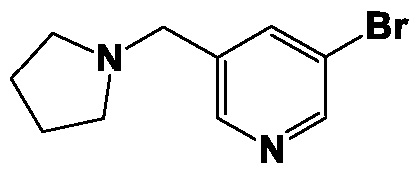
XXVII
[0282] 3-Бром-5-(пирролидин-1-илметил)пиридин (XXVII): Золотая жидкость (1,35 г, выход 97%). 1H-ЯМР (ДМСО-d6) 1,68-1,71 (м, 4H), 2,42-2,44 (м, 4H), 3,60 (с, 2H), 7,96 (с, 1H), 8,48 (д, J=2 Гц, 1H), 8,58 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C10H13BrN2 m/z 242 (M+H).
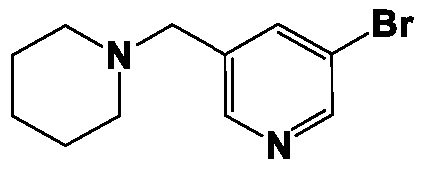
XXVIII
[0283] 3-Бром-5-(пиперидин-1-илметил)пиридин (XXVIII): Коричневая жидкость (13,1 г, выход 94%). 1H-ЯМР (ДМСО-d6) 1,36-1,39 (м, 2H), 1,46-1,51 (м, 4H), 2,31-2,32 (м, 4H), 3,46 (с, 2H), 7,94 (с, 1H), 8,47 (д, J=2 Гц, 1H), 8,58 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C11H15BrN2 m/z 257 (M+H).
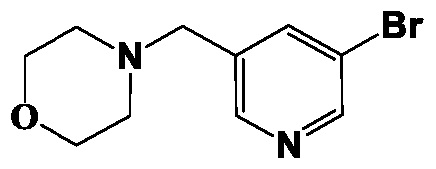
XXIX
[0284] 4-((5-Бромпиридин-3-ил)метил)морфолин (XXIX): Коричневое масло (1,02 г, выход 35,6%). ЭРИ-МС найдено для C10H13BrN2O m/z 258 (M+H).
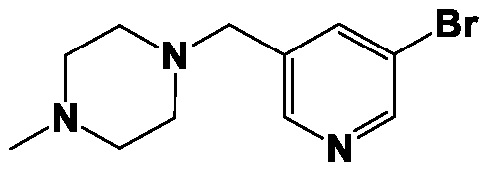
XXX
[0285] 1-((5-Бромпиридин-3-ил)метил)-4-метилпиперазин (XXX): Коричневое масло (0,93 г, выход 64%). 1H-ЯМР (ДМСО-d6) 2,14 (с, 3H), 2,27-2,37 (м, 8H), 3,49 (с, 2H), 7,95 (с, 1H), 8,47 (д, J=1,7 Гц, 1H), 8,59 (д, J=2,2 Гц, 1H); ЭРИ-МС найдено для C11H16BrN3 m/z 272 (M+H).
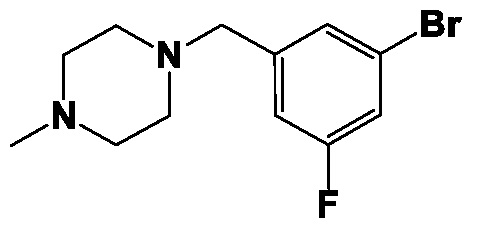
XXXI
[0286] 1-(3-Бром-5-фторбензил)-4-метилпиперазин (XXXI): Светло-желтое масло (2,07 г, выход 68%). 1H-ЯМР (ДМСО-d6) 2,14 (с, 3H), 2,28-2,40 (м, 8H), 3,46 (с, 2H), 7,15-7,17 (м, 1H), 7,35 (с, 1H), 7,40-7,42 (м, 1H); ЭРИ-МС найдено для C12H16BrFN2 m/z 288 (M+H).
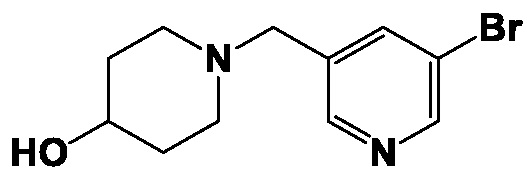
XXXII
[0287] 1-(5-бромпиридин-3-ил)пиперидин-4-ол (XXXII): Коричневое масло (2,15 г, 7,93 ммоль, выход 72,7%). 1H-ЯМР (ДМСО-d6) 1,34-1,41 (м, 2H), 1,67-1,71 (м, 2H), 2,03-2,07 (м, 2H), 2,62-2,64 (м, 2H), 3,42-3,46 (м, 1H), 3,47 (с, 2H), 4,55 (д, J=4,2 Гц, 1H), 7,93-7,94 (м, 1H), 8,46 (д, J=1,6 Гц, 1H), 8,58 (д, J=2,2 Гц, 1H); ЭРИ-МС найдено для C11H15BrN2O m/z 272 (M+H).
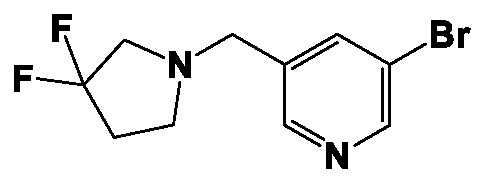
XXXIII
[0288] 3-Бром-5-((3,3-дифторпирролидин-1-ил)метил)пиридин (XXXIII): Коричневая жидкость (7,38 г, 26,64 ммоль, выход 94,9%). 1H-ЯМР (ДМСО-d6) 2,21-2,30 (м, 2H), 2,70 (т, J=7 Гц, 2H), 2,89 (т, J=13 Гц, 2H), 3,66 (с, 2H), 7,95-7,98 (м, 1H), 8,57 (д, J=1,7 Гц, 1H), 8,61 (д, J=2,2 Гц, 1H); ЭРИ-МС найдено для C10H11BrF2N2 m/z 276 (M+H).
[0289] Получение 3-бензил-5-бромпиридина (XXXVI) показано ниже на Схеме 6.
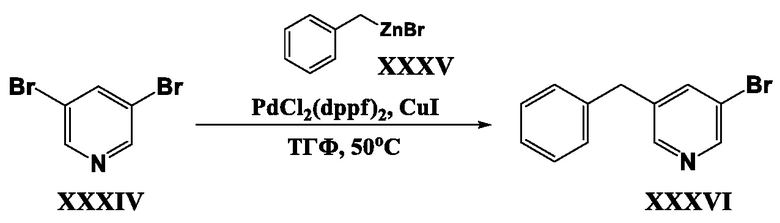
Схема 6
Стадия 1
[0290] К раствору 3,5-дибромпиридина (XXXIV) (1,03 г, 4,36 ммоль) в ТГФ (7 мл) под аргоном добавляли CuI (50 мг, 0,26 ммоль) и PdCl2(dppf)2 (178 мг, 0,22 ммоль). Бензилцинкабромид (II) (XXXV) (0,5М в ТГФ) (13,09 мл, 6,55 ммоль) медленно добавляли шприцем. Реакцию нагревали при 50°C в течение выходных. Реакцию останавливали водой и экстрагировали EtOAc. EtOAc отделяли, промывали водой, солевым раствором, сушили над MgSO4 и выпаривали в вакууме. Остаток очищали на колонке с силикагелем (100% смесь гексанов → 5:95 EtOAc:смесь гексанов) с получением 3-бензил-5-бромпиридина (XXXVI) (0,614 г, 2,47 ммоль, выход 57%) в виде светло-коричневого масла. 1H-ЯМР (ДМСО-d6) δ м.д. 3,98 (с, 2H), 7,19-7,23 (м, 1H), 7,27-7,32 (м, 4H), 7,92-7,93 (м, 1H), 8,51 (д, J=2 Гц, 1H), 8,54 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C12H10BrN m/z 248 (M+H).
[0291] Получение 3-бром-5-феноксипиридина (XXXIX) показано ниже на Схеме 7.
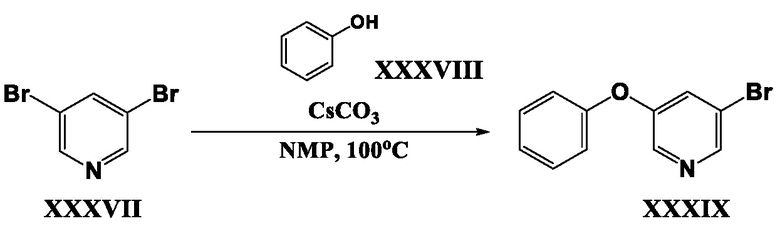
Схема 7
Стадия 1
[0292] К раствору 3,5-дибромпиридина (XXXVII) (1,00 г, 4,24 ммоль) в NMP (11 мл) добавляли фенол (XXXVIII) (398 мг, 4,24 ммоль) и CsCO3 (1,38 г, 4,24 ммоль). Реакцию нагревали при 100°C в течение выходных. Затем реакцию делили между Et2O/водой. Et2O отделяли, промывали 2× водой, солевым раствором, сушили над MgSO4 и выпаривали в вакууме. Остаток очищали на колонке с силикагелем (100% смесь гексанов → 2:98 EtOAc:смесь гексанов) с получением 3-бром-5-феноксипиридина (XXXIX) (535 мг, 2,14 ммоль, выход 50%) в виде прозрачного масла. 1H-ЯМР (ДМСО-d6) δ м.д. 7,13-7,15 (м, 2H), 7,23-7,26 (м, 1H), 7,43-7,46 (м, 2H), 7,69-7,70 (м, 1H), 8,37 (д, J=3 Гц, 1H), 8,49 (д, J=2 Гц, 1H); ЭРИ-МС найдено для C11H8BrNO m/z 250 (M+H).
[0293] Получение 1-(5-бромпиридин-3-ил)-4-метилпиперазина (XL) показано ниже на Схеме 8.
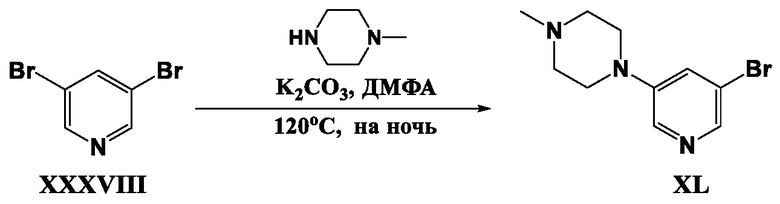
Схема 8
Стадия 1
[0294] К раствору 3,5-дибромпиридина (XXXVIII) (2,90 г, 12,24 ммоль) в сухом ДМФА (20 мл) добавляли 1-метилпиперазин (2,987 мл, 26,93 ммоль) и K2CO3 (5,58 г, 40,39 ммоль). Реакцию нагревали при 120°C в течение ночи. Добавляли дополнительную порцию 1-метилпиперазина (6 мл) и продолжали нагревание в течение еще 24 ч. Реакцию вливали в воду со льдом и фильтровали. Фильтрат экстрагировали 66% MeOH/CHCl3. Органический слой сушили нал MgSO4, фильтровали и выпаривали в вакууме с получением 1-(5-бромпиридин-3-ил)-4-метилпиперазина (XL) в виде коричневого вязкого масла (2,49 г, 9,76 ммоль, выход 79,8%). ЭРИ-МС найдено для C10H14BrN3 m/z 256 (M+H).
[0295] Следующее промежуточное соединение получали в соответствии с методикой, описанной на Схеме 8 выше.
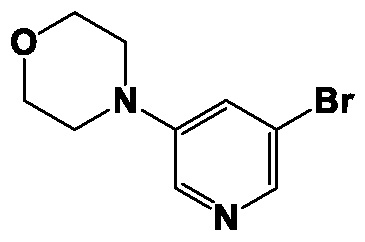
XLI
[0296] 4-(5-Бромпиридин-3-ил)морфолин (XLI): Желтое твердое вещество (1,12 г, 4,61 ммоль, выход 64,9%). ЭРИ-МС найдено для C9H11BrN2O m/z 244,1 (M+H).
[0297] Получение 5-бром-N-циклогексилникотинамида (XLIV) показано ниже на Схеме 9.
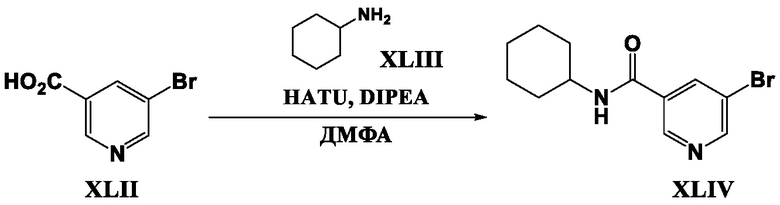
Схема 9
Стадия 1
[0298] К раствору 5-бромникотиновой кислоты (XLII) (500 мг, 2,49 ммоль) в ДМФА (8 мл) добавляли циклогексанамин (XLIII) (247 мг, 2,49 ммоль) и DIPEA (643 мг, 4,98 ммоль). Реакцию охлаждали до 0°C, после чего добавляли HATU (947 мг, 2,49 ммоль). Реакцию нагревали до комнатной температуры и перемешивали в течение 4 часов. Реакцию разбавляли EtOAc, промывали 2× водой, солевым раствором, сушили над MgSO4 и выпаривали в вакууме с получением неочищенного 5-бром-N-циклогексилникотинамида (XLIV). Продукт использовали без дополнительной очистки. ЭРИ-МС найдено для C12H15BrN2O m/z 283 (M+H).
[0299] Получение 3-бром-5-(((2R,6S)-2,6-диметилпиперидин-1-ил)метил)пиридина (XLVII) показано ниже на Схеме 10.
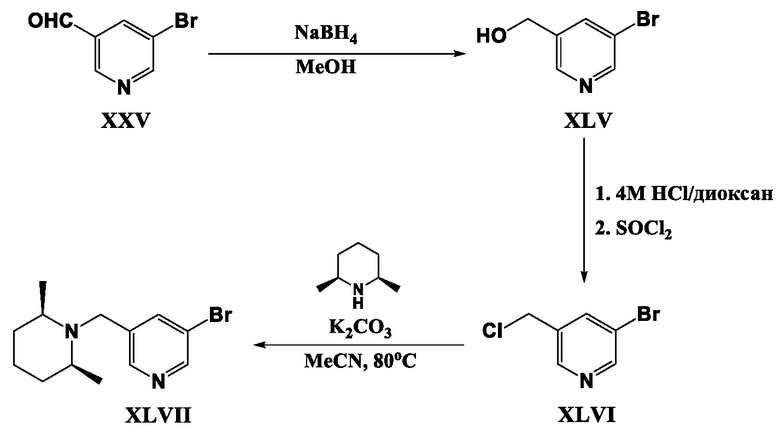
Схема 10
Стадия 1
[0300] К раствору 5-бромникотинальдегида (XXV) (2,05 г, 11,0 ммоль) в MeOH (85 мл) добавляли NaBH4 (832 мг, 21,99 ммоль). Реакцию перемешивали при комнатной температуре в течение 1 ч. Реакцию останавливали насыщенным водным р-ром NH4Cl (5 мл). Реакцию выпаривали в вакууме и делили остаток между насыщенным водным р-ром NH4Cl/EtOAc. Органический слой отделяли, промывали водой, солевым раствором, сушили над MgSO4 и выпаривали в вакууме с получением неочищенного (5-бромпиридин-3-ил)метанола (XLV) в виде золотистого масла (1,54 г, 8,2 ммоль, выход 74%). Продукт использовали без дополнительной очистки. ЭРИ-МС найдено для C6H6BrNO m/z 188 (M+H).
Стадия 2
[0301] (5-Бромпиридин-3-ил)метанол (XLV) (1,54 г, 8,2 ммоль) обрабатывали 4M HCl в диоксане (10 мл) при 0°C и затем выпаривали. Остаток растворяли в SOCl2 (4 мл) и нагревали с обратным холодильником в течение 2 часов, SOCl2 удаляли, а остаток растирали с гексаном с получением соли HCl 3-бром-5-(хлорметил)пиридина (XLVI) в виде коричневого твердого вещества (1,30 г, 5,4 ммоль, выход 66%). Продукт использовали без дополнительной очистки. ЭРИ-МС найдено для C6H5BrClN m/z 206 (M+H).
Стадия 3
[0302] К раствору 3-бром-5-(хлорметил)пиридина (XLVI) (1,17 г, 4,8 ммоль) в MeCN (0,2 мл) и (2S,6R)-2,6-диметилпиперидинe (2,6 мл, 19,3 ммоль) добавляли K2CO3 (667 мг, 4,8 ммоль). Реакцию нагревали с обратным холодильником в течение 5 часов. ТСХ показала присутствие исходного материала, поэтому добавляли дополнительное количество (2S,6R)-2,6-диметилпиперидина (2,0 мл, 14,8 ммоль) и нагревали реакцию с обратным холодильником еще в течение 5 часов. Растворитель удаляли, а остаток делили между EtOAc/водой. EtOAc отделяли и промывали солевым раствором, сушили над MgSO4 и выпаривали в вакууме. Остаток очищали на колонке с силикагелем (100% смеси гексанов → 6:94 EtOAc:смесь гексанов) с получением 3-бром-5-(((2R,6S)-2,6-диметилпиперидин-1-ил)метил)пиридина (XLVII) в виде прозрачного масла (728 мг, 2,57 ммоль, выход 53%). 1H-ЯМР (ДМСО-d6) δ м.д. 0,92 (д, J=8 Гц, 6H), 1,21-1,32 (м, 3H), 1,52-1,55 (м, 2H), 1,59-1,63 (м, 1H), 2,42-2,46 (м, 2H), 3,73 (с, 2H), 7,97-7,98 (м, 1H), 8,50 (д, J=3 Гц, 1H), 8,55-8,56 (м, 1H); ЭРИ-МС найдено для C13H19BrN2 m/z 283 (M+H).
[0303] Получение промежуточного 3'-фторбифенил-3-амина (LI) показано ниже на Схеме 11.
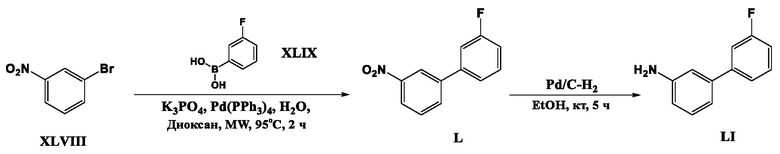
Схема 11
Стадия 1
[0304] В сосуд для микроволнового синтеза объемом 25 мл вносили 1-бром-3-нитробензол (XLVIII) (0,61 г, 3,0 ммоль), 3-фторфенилбороновую кислоту (XLIX) (0,46 г, 3,3 ммоль), трехосновный фосфат калия (0,95 г, 4,5 ммоль), 1,4-диоксан (15,0 мл) и воду (3,0 мл). Добавляли тетракис(трифенилфосфин)палладий (0) (0,17 г, 0,15 ммоль) и помещали реакцию в микроволновый реактор на 1 ч при 95°C. Добавляли дополнительное количество 3-фторфенилбороновой кислоты (0,20 г) и тетракис(трифенилфосфин)палладия (0) (0,05 г) и нагревали реакцию в течение еще 1 ч при 95°C в микроволновом реакторе. Органический растворитель отделяли от воды и выпаривали до остатка. Затем остаток очищали с помощью флеш-хроматографии при использовании 25 г нормально-фазового картриджа с силикагелем Thomson (100% смесь гексанов → 1:99 EtOAc:смесь гексанов) с получением 3'-фтор-3-нитробифенила (L) (0,63 г, 2,91 ммоль, выход 97%) в виде белого твердого вещества. 1H-ЯМР (ДМСО-d6) δ м.д. 8,48 (т, J=2,0 Гц, 1H), 8,26-8,24 (м, 1H), 8,20-8,18 (м, 1H), 7,78 (т, J=8 Гц, 1H), 7,70-7,68 (м, 1H), 7,67-7,65 (м, 1H), 7,59-7,56 (м, 1H), 7,32-7,28 (м, 1H).
Стадия 2
[0305] К раствору 3'-фтор-3-нитробифенила (L) (0,63 г, 2,88 ммоль) в EtOH (20,0 мл) добавляли 10% палладий на угле (0.095 г). Колбу вакуумировали и заполняли водородом. Раствор перемешивали при комнатной температуре в течение 5 часов в атмосфере водорода. Катализатор фильтровали через слой целита и удаляли растворитель при пониженном давлении. Остаток очищали с помощью флеш-хроматографии при использовании 40 г нормально-фазового картриджа с силикагелем Thomson (100% смесь гексанов → 15:85 EtOAc:смесь гексанов) с получением 3'-фторбифенил-3-амина (LI) (0,34 г, 1,81 ммоль, выход 63%) в виде светло-желтого масла. 1H-ЯМР (ДМСО-d6) δ м.д. 7,47-7,44 (м, 1H), 7,40-7,39 (м, 1H), 7,36-7,33 (м, 1H), 7,15-7,14 (м, 1H), 7,10 (т, J=7,7 Гц, 1H), 6,85-6,84 (м, 1H), 6,80-6,79 (м, 1H), 6,60-6,58 (м, 1H), 5,18 (с, 2H); ЭРИ-МС найдено для C12H10FN m/z 188 (M+H).
[0306] Получение промежуточного 5-(3-фторфенил)пиридин-3-амина (LIII) показано ниже на Схеме 12.
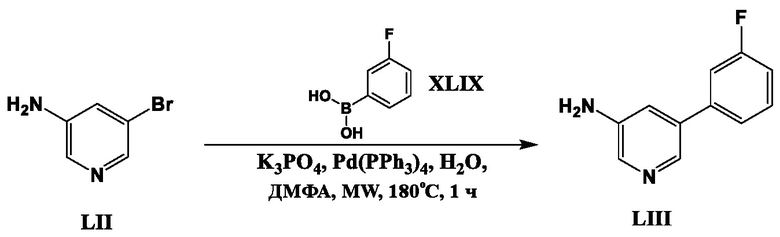
Схема 12
Стадия 1
[0307] Во флакон для микроволнового синтеза добавляли 3-амино-5-бромпиридин (LII) (0,400 г, 2,31 ммоль), 3-фторфенил-бороновую кислоту (XLIX) (0,356 г, 2,54 ммоль), тетракис(трифенилфосфин)палладий (0) (0,133 г, 0,116 ммоль), фосфат калия (0,736 г, 3,47 ммоль), воду (1 мл) и ДМФА (5 мл). Реакционный флакон закрывали, продували аргоном и нагревали при микроволновом облучении в течение 1 ч при 180°C. Раствор фильтровали через слой целита и выпаривали в вакууме. Остаток очищали с помощью колоночной хроматографии (4:6 EtOAc:смесь гексанов → 7:3 EtOAc:смесь гексанов) с получением 5-(3-фторфенил)пиридин-3-амина (LIII) (0,360 г, 1,92 ммоль, выход 83%) в виде желтовато-белого твердого вещества. ЭРИ-МС найдено для C11H9FN2 m/z 189,1 (M+H).
[0308] Получение промежуточного 5-((диметиламино)метил)-пиридин-3-амина (LVII) показано ниже на Схеме 13.
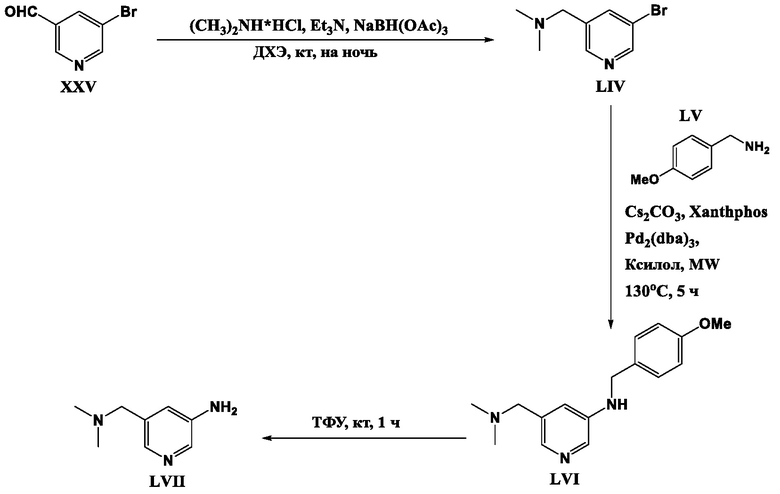
Схема 13
Стадия 1
[0309] 5-Бромникотинальдегид (XXV) (5.01 г, 26,9 ммоль) и гидрохлорид диметиламина (4,39 г, 53,8 ммоль) суспендировали в 1,2-дихлорэтане (108 мл). Добавляли триэтиламин (7,50 мл, 53,8 ммоль) и перемешивали реакцию при комнатной температуре в течение 1 ч. Добавляли триацетоксиборогидрид натрия (8,56 г, 40,4 ммоль) и затем перемешивали реакцию при комнатной температуре в течение ночи. Реакцию разбавляли насыщенным раствором бикарбоната натрия и ДХМ. Органический слой отделяли, последовательно промывали водой и солевым раствором, сушили над MgSO4, фильтровали и выпаривали с получением 1-(5-бромпиридин-3-ил)-N,N-диметилметанамина (LIV) (1,19 г, 23,9 ммоль, выход 89%) в виде коричневого масла: 1H-ЯМР (ДМСО-d6) δ м.д. 8,59 (д, J=3 Гц, 1H), 8,47 (д, J=2 Гц, 1H), 7,94 (с, 1H), 3,43 (с, 2H), 2,15 (с, 6H); ЭРИ-МС найдено для C8H11BrN2 m/z 215 (M+H).
Стадия 2
[0310] В сосуде для микроволнового синтеза объемом 25 мл 1-(5-бромпиридин-3-ил)-N,N-диметилметанамин (LIV) (1,27 г, 5,92 ммоль), 4-метоксибензиламин (LV) (0,77 мл, 5,92 ммоль), карбонат цезия (2,70 г, 8,29 ммоль) и Xanthphos (0.17 г, 0,30 ммоль) суспендировали в смеси ксилолов (12,0 мл). Растворитель дегазировали и добавляли трис(дибензилиденацетон)дипалладий (0) (0,27 г, 0,30 ммоль). Сосуд герметично закрывали и нагревали реакцию до 130°C в течение 5 ч в микроволновом реакторе. Растворитель собирали с осадка твердого материала и выпаривали до остатка. Остаток очищали с помощью хроматографии на силикагеле при использовании 40 г нормально-фазового картриджа с силикагелем Thomson (100% CHCl3 → 3:97 MeOH [7Н NH3]:CHCl3) с получением 5-((диметиламино)метил)-N-(4-метоксибензил)пиридин-3-амина (LVI) (0,68 г, 2,49 ммоль, выход 42%) в виде желтого твердого вещества. 1H-ЯМР (ДМСО-d6) δ м.д. 7,84 (д, J=3 Гц, 1H), 7,64 (д, J=2 Гц, 1H), 7,27 (д, J=11 Гц, 2H), 6,88 (д, J=11 Гц, 2H), 6,83-6,82 (м, 1H), 6,35 (т, J=8 Гц, 1H), 4,20 (д, J=8 Гц, 2H), 3,72 (с, 3H), 3,24 (с, 2H), 2,08 (с, 6H); ЭРИ-МС найдено для C16H21N3O m/z 272 (M+H).
Стадия 3
[0311] 5-(Диметиламино)метил)-N-(4-метоксибензил)пиридин-3-амин (LVI) (0,15 г, 0,56 ммоль) растворяли в ТФУ (2,0 мл) и перемешивали при комнатной температуре в течение 1 ч. ТФУ удаляли, а остаток обрабатывали 7Н аммиаком в смеси MeOH/хлороформа (7/93) для нейтрализации ТФУ и снова выпаривали до остатка. Остаток очищали с помощью флеш-хроматографии на силикагеле при использовании 4 г нормально-фазового картриджа с силикагелем Thomson (100% CHCl3 → 3:97 MeOH [7Н NH3]:CHCl3) с получением 5-(диметиламино)метил)пиридин-3-амина (LVII) (0,044 г, 0,29 ммоль, выход 52%) в виде коричневого масла. ЭРИ-МС найдено для C8H13N3 m/z 152 (M+H).
[0312] Следующее промежуточное соединение получали в соответствии с методкой, описанной выше на Схеме 13.
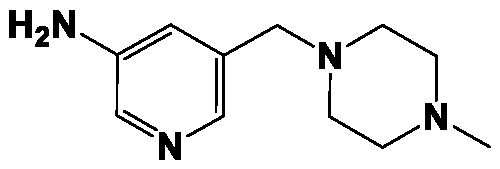
LVIII
[0313] 5-((4-Метилпиперазин-1-ил)метил)пиридин-3-амин (LVIII): Темно-желтое твердое вещество (138 мг, 0,67 ммоль, выход 71%). ЭРИ-МС найдено для C11H18N4 m/z 207 (M+H).
[0314] Получение промежуточного 6-(пирролидин-1-илметил)пиридин-3-амина (LXIII) показано ниже на Схеме 14.
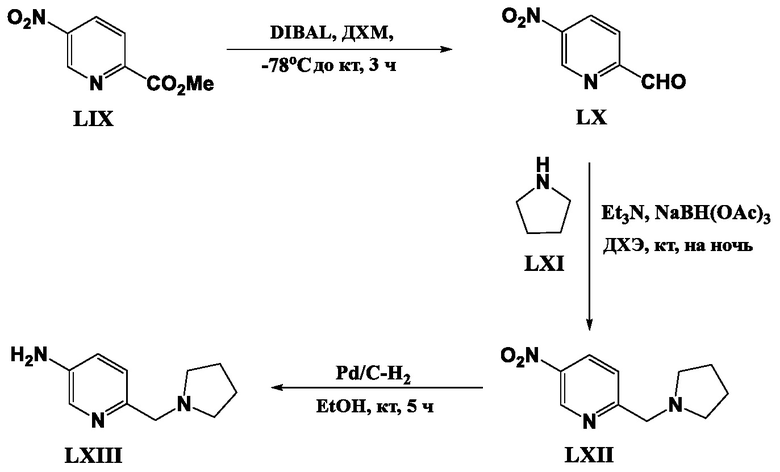
Схема 14
Стадия 1
[0315] К суспензии метил-5-нитропиколината (LIX) (1,282 г, 7,03 ммоль) в ДХМ (25 мл), перемешиваемой при -78°C под аргоном, медленно добавляли DIBAL (1M в толуоле) (9,14 мл, 9,14 ммоль). Раствор оставляли нагреваться до комнатной температуры на 3 ч. Добавляли водный раствор тартрата калия натрия, затем разбавляли водой и ДХМ. Раствор перемешивали при комнатной температуре еще в течение 30 мин, после чего органический слой отделяли. Водный слой экстрагировали 2× ДХМ, объединяли с органическим слоем, сушили над MgSO4, фильтровали и выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии с получением 5-нитропиколинальдегида (LX) в виде коричневого масла (0,64 г, 4,2 ммоль, выход 60%). 1H-ЯМР (ДМСО-d6) δ м.д. 8,17 (д, J=9 Гц, 1H), 8,81 (дд, J=9 Гц, J=2 Гц, 1H), 9,56 (д, J=2 Гц, 1H), 10,08 (с, 1H).
Стадия 2
[0316] Получение 5-нитро-2-(пирролидин-1-илметил)пиридина (LXII) проводили согласно методике, представленной на Схеме 5 в Стадии 1. Пурпурное масло (0,41 г, 1,98 ммоль, выход 86%). 1H-ЯМР (ДМСО-d6) δ м.д. 9,28 (д, J=3 Гц, 1H), 8,56 (дд, J=11 Гц, 3 Гц, 1H), 7,72 (д, J=11 Гц, 1H), 3,85 (с, 2H), 2,53-2,50 (м, 4H), 1,75-1,70 (м, 4H).
Стадия 3
[0317] Получение промежуточного 6-(пирролидин-1-илметил)пиридин-3-амина (LXIII) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Темно-коричневое масло (0,35 г, 1,97 ммоль, количественный выход). ЭРИ-МС найдено для C10H15N3 m/z 178 (M+H).
[0318] Следующее промежуточное соединение получали в соответствии с методикой, описанной выше на Схеме 14.
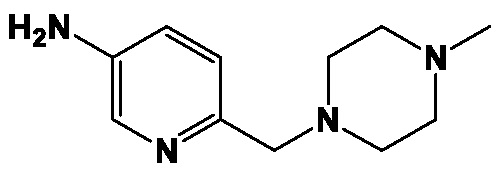
LXIV
[0319] 6-((4-Метилпиперазин-1-ил)метил)пиридин-3-амин (LXIV): Коричневое масло (120 мг, 0,58 ммоль, выход 100%). ЭРИ-МС найдено для C11H18N4 m/z 207 (M+H).
[0320] Получение промежуточного 6-(3-фторфенокси)пиридин-3-амина (LXVIII) представлено ниже на Схеме 15.
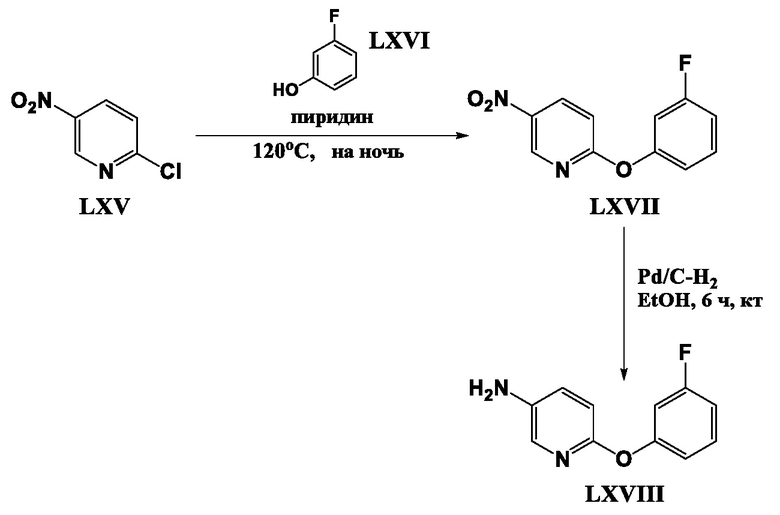
Схема 15
Стадия 1
[0321] Раствор 2-хлор-5-нитропиридина (LXV) (1,98 г, 12,5 ммоль) и 3-фторфенола (LXVI) (1,4 г, 12,5 ммоль) в пиридине (20 мл) нагревали при 120°C в течение ночи под аргоном. Раствор охлаждали до комнатной температуры и выпаривали в вакууме. Остаток растворяли в EtOAc, промывали водой, солевым раствором, сушили над MgSO4 и выпаривали. Остаток очищали с помощью колоночной хроматографии на силикагеле (100% гексан → 2:98 EtOAc:гексан) с получением 2-(3-фторфенокси)-5-нитропиридина (LXVII) в виде желтого вязкого масла (2,27 г, 9,7 ммоль, выход 77%). 1H-ЯМР (ДМСО-d6) δ м.д. 7,11 (дд, J=8 Гц, J=2 Гц, 1H), 7,17 (дт, J=8 Гц, J=6 Гц, 1H), 7,23 (тд, J=10 Гц, J=2 Гц, 1H), 7,31 (д, J=9 Гц, 1H), 7,52 (к, J=9 Гц, 1H), 8,64 (дд, J=9 Гц, J=3 Гц, 1H), 9,05 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C11H7FN2O3 m/z 234,9 (M+H).
Стадия 2
[0322] Получение промежуточного 6-(3-фторфенокси)пиридин-3-амина (LXVIII) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Черно-зеленое вязкое масло (1,90 г, 9,3 ммоль, выход 96%). 1H-ЯМР (ДМСО-d6) δ м.д. 5,18 (шс, 2H), 6,74-6,83 (м, 3H), 6,90 (дт, 1H), 7,09 (дд, J=9 Гц, J=3 Гц, 1H), 7,34 (к, J=7 Гц, 1H), 7,57 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C11H9FN2O m/z 204,4 (M +).
[0323] Следующие промежуточные соединения получали в соответствии с методикой, описанной выше на Схеме 15.
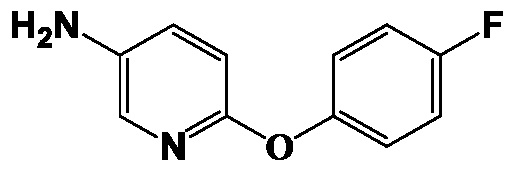
LXIX
[0324] 6-(4-Фторфенокси)пиридин-3-амин (LXIX): Темно-коричневое масло (870 мг, 4,3 ммоль, выход 100%). 1H-ЯМР (ДМСО-d6) δ м.д. 5,08 (шс, 2H), 6,75 (д, J=15 Гц, 1H), 6,90-7,01 (м, 2H), 7,07 (дд, J=9 Гц, J=3 Гц, 1H), 7,16 (т, 9 Гц, 1H), 7,26-7,30 (м, 1H), 7,73 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C11H9FN2O m/z 204,9 (M+H).
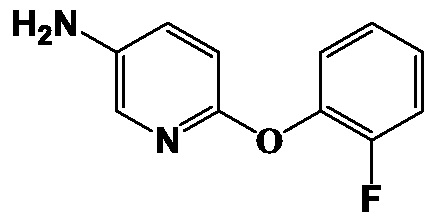
LXX
[0325] 6-(2-Фторфенокси)пиридин-3-амин (LXX): Темно-коричневое масло (611 мг, 3,0 ммоль, выход 91%). ЭРИ-МС найдено для C11H9FN2O m/z 204,9 (M+H).
[0326] Получение промежуточного 6-фенилпиридин-3-амина (LXXIV) представлено ниже на Схеме 16.
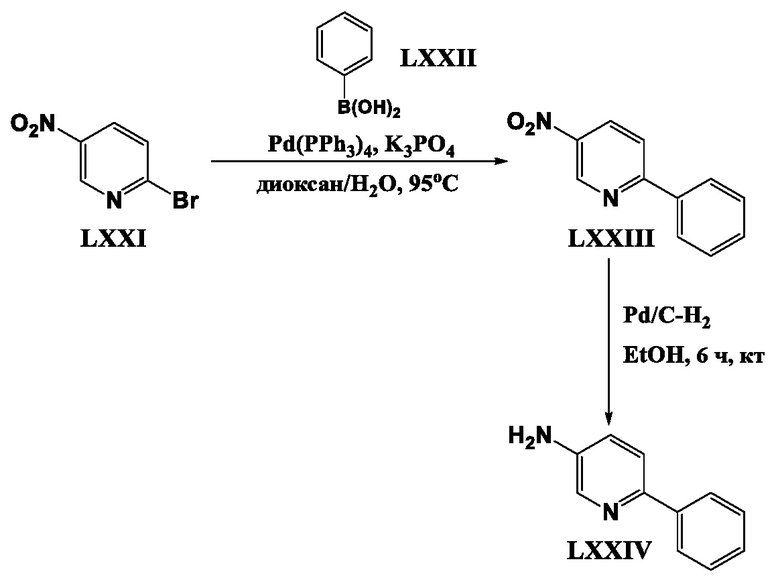
Схема 16
Стадия 1
[0327] К раствору 2-бром-5-нитропиридина (LXXI) (302 мг, 1,49 ммоль) в смеси диоксана (14 мл) и воды (3 мл) добавляли фенилбороновую кислоту (LXXII) (199 мг, 1,64 ммоль), Pd(PPh3)4 (86 мг, 0,74 ммоль) и K3PO4 (473 мг, 2,23 ммоль). Реакцию обрабатывали мироволновым излучением при 95°C в течение 1 ч. Реакцию охлаждали, органическую фазу отделяли, сушили над MgSO4 и выпаривали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле (100% гексан → 5:95 EtOAc:гексан) с получением 5-нитро-2-фенилпиридина (LXXIII) в виде почти белых игл (254 мг, 1,27 ммоль, выход 85%). ЭРИ-МС найдено для C11H8N2O2 m/z 200,9 (M+H).
Стадия 2
[0328] Получение промежуточного 6-фенилпиридин-3-амина (LXXIV) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Черно-зеленое вязкое масло (211 мг, 1,24 ммоль, выход 98%). 1H-ЯМР (ДМСО-d6) δ м.д. 5,45 (с, 2H), 6,99 (дд, J=11 Гц, J=3 Гц, 1H), 7,25-7,28 (м, 1H), 7,38-7,40 (м, 2H), 7,62 (д, J=11 Гц, 1H), 7,89-7,91 (м, 1H), 8,02 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C11H10N2 m/z 171 (M+H).
[0329] Следующие промежуточные соединения получали в соответствии с методикой, описанной выше на Схеме 16.
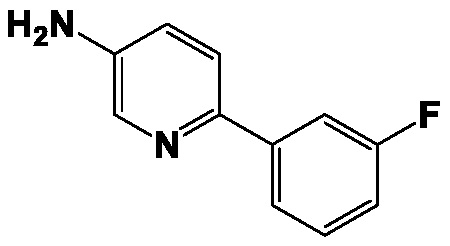
LXXV
[0330] 6-(3-Фторфенил)пиридин-3-амин (LXXV): Коричневое масло (252 мг, 1,34 ммоль, выход 98%). ЭРИ-МС найдено для C11H9FN2 m/z 189 (M+H).
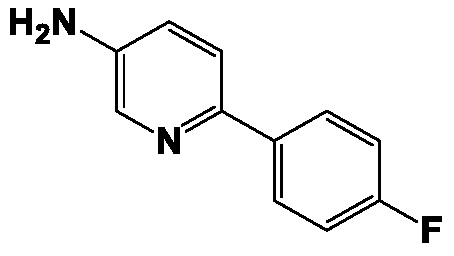
LXXVI
[0331] 6-(4-Фторфенил)пиридин-3-амин (LXXVI): Темно-пурпурное масло (202 мг, 1,07 ммоль, выход 98%). ЭРИ-МС найдено для C11H9FN2 m/z 189 (M+H).
[0332] Получение промежуточного 5-бензилпиридин-3-амина (LXXX) представлено ниже на Схеме 17.
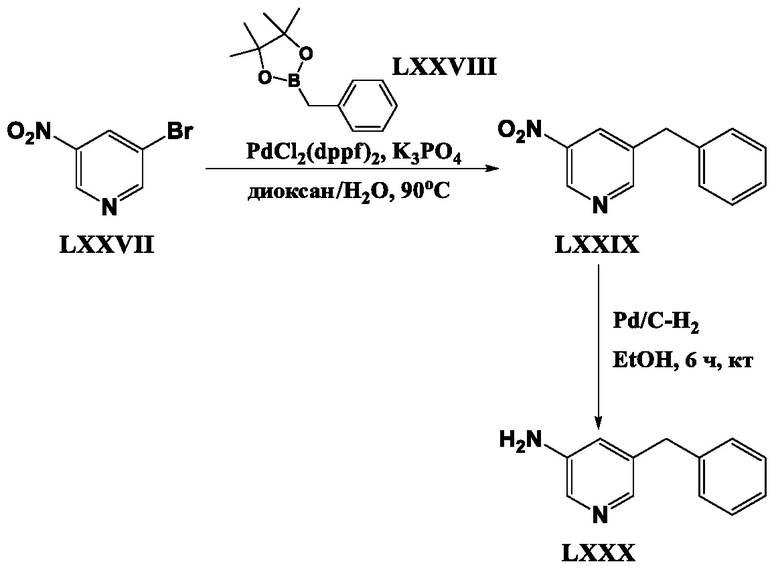
Схема 17
Стадия 1
[0333] К раствору 3-бром-5-нитропиридина (LXXVII) (295 мг, 1,45 ммоль) в диоксане (14 мл) добавляли 2-бензил-4,4,5,5-тетраметил-1,3,2-диоксаборолан (LXXVIII) (420 мкл, 1,89 ммоль), PdCl2(dppf)2, (120 мг, 0,15 ммоль) и 2М водный р-р K3PO4 (2,2 мл, 4,36 ммоль). Реакцию обрабатывали мироволновым излучением при 90°C в течение 2 ч. Реакцию охлаждали, и органическую фазу отделяли, сушили над MgSO4 и выпаривали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле (100% гексан → 6:94 EtOAc:гексан) с получением 3-бензил-5-нитропиридина (LXXIX) в виде коричневого масла (117 мг, 0,54 ммоль, выход 37%). 1H-ЯМР (ДМСО-d6) δ м.д. 4,16 (с, 2H), 7,21-7,25 (м, 1H), 7,31-7,33 (м, 4H), 8,45-8,46 (м, 1H), 8,93 (д, J=2 Гц, 1H), 9,21 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C12H10N2O2 m/z 215 (M+H).
Стадия 2
[0334] Получение 5-бензилпиридин-3-амина (LXXX) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Черно-зеленое вязкое масло (139 мг, 0,75 ммоль, выход 98%). ЭРИ-МС найдено для C12H12N2 m/z 185 (M+H).
[0335] Получение промежуточного 2-(4-метилпиперазин-1-ил)пиридин-3-амина (LXXXIV) представлено ниже на Схеме 18.
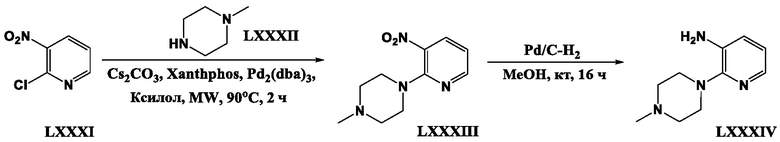
Схема 18
Стадия 1
[0336] Во флакон для микроволнового синтеза добавляли 2-хлор-3-нитропиридин (LXXXI) (1,00 г, 6,31 ммоль), 1-метилпиперазин (LXXXII) (0,758 г, 7,57 ммоль), карбонат цезия (2,88 г, 8,83 ммоль), Pd2(dba)3 (0,173 г, 0,189 ммоль), Xanthphos (0,109 г, 0,189 ммоль) и диоксан (5 мл). Реакционный флакон закрывали и продували аргоном. Раствор в реакционном флаконе нагревали при микроволновом облучении в течение 2 ч при 90°C. Раствор фильтровали через слой целита и выпаривали до остатка в вакууме. Остаток очищали с помощью колоночной хроматографии (1:99 MeOH:CHCl3 → 8:92 MeOH:CHCl3) с получением 1-метил-4-(3-нитро-пиридин-2-ил)-пиперазина (LXXXIII) (1,30 г, 5,85 ммоль, выход 93%) в виде коричневого масла.
Стадия 2
[0337] К перемешиваемому раствору 1-метил-4-(3-нитро-пиридин-2-ил)-пиперазина (LXXXIII) (1,30 г, 5,85 ммоль) в MeOH (15 мл) добавляли 10% Pd/C. Раствор барботировали водородом. Раствор перемешивали при комнатной температуре в течение 16 ч под водородом. Раствор фильтровали через слой целита и выпаривали до остатка в вакууме. Остаток очищали с помощью колоночной хроматографии (100% CHCl3 → 2:98 MeOH [7Н NH3]:CHCl3) с получением 2-(4-метилпиперазин-1-ил)пиридин-3-амина (LXXXIV) (0,466 г, 2,42 ммоль, выход 52%) в виде коричневого твердого вещества. ЭРИ-МС найдено для C10H16N4 m/z 192,4 (M+H).
[0338] Следующие промежуточные соединения получали в соответствии с методикой, описанной выше на Схеме 18.
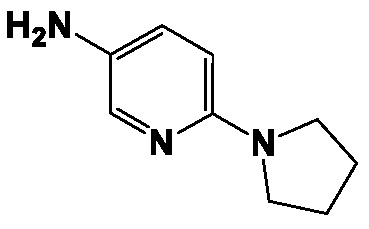
LXXXV
[0339] 6-(Пирролидин-1-ил)пиридин-3-амин (LXXXV): Темно-фиолетовое масло (1,43 г, 8,77 ммоль, выход 100%). ЭРИ-МС найдено для C9H13N3 m/z 164 (M+H).
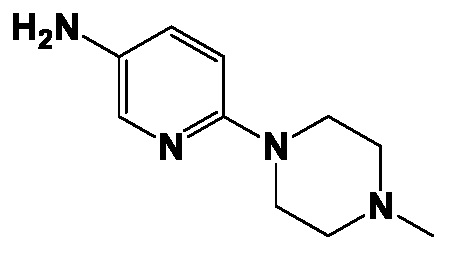
LXXXVI
[0340] 6-(4-Метилпиперазин-1-ил)пиридин-3-амин (LXXXVI): Фиолетовое твердое вещество (598 мг, 3,11 ммоль, выход 32%). ЭРИ-МС найдено для C10H16N4 m/z 193 (M+H).
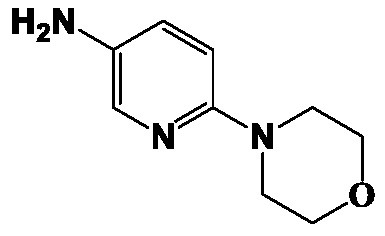
LXXXVII
[0341] 6-Морфолинопиридин-3-амин (LXXXVII): Фиолетовое твердое вещество (782 мг, 4,36 ммоль, выход 95%). ЭРИ-МС найдено для C9H13N3O m/z 180 (M+H).
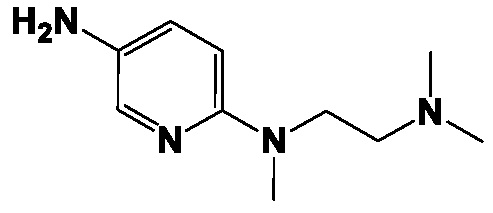
LXXXVIII
[0342] N2-(2-(Диметиламино)этил)-N2-метилпиридин-2,5-диамин (LXXXVIII): Темно-фиолетовое масло (1,55 г, 7,98 ммоль, выход 96%). ЭРИ-МС найдено для C10H18N4 m/z 195 (M+H).
[0343] Получение промежуточного 1-(5-аминопиридин-2-ил)пиперидин-4-ола (XCI) представлено ниже на Схеме 19.
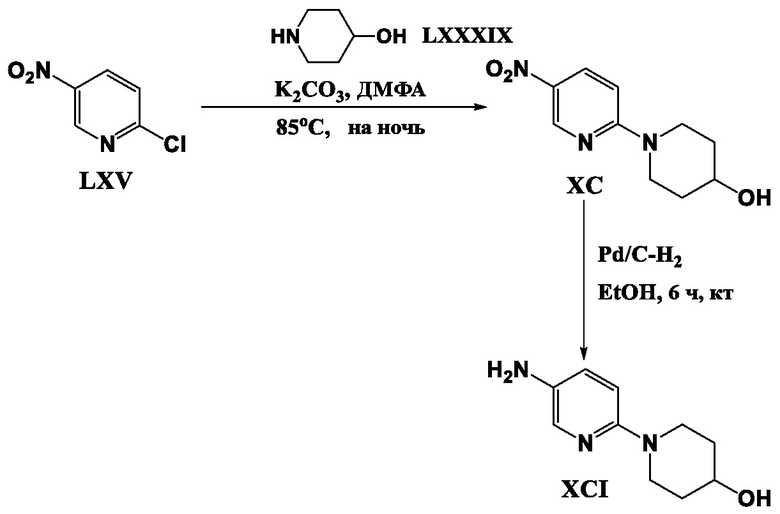
Схема 19
Стадия 1
[0344] К раствору 2-хлор-5-нитропиридина (LXV) (5,0 г, 31,5 ммоль) в ДМФА (50 мл) добавляли пиперидин-4-ол (LXXXIX) (3,5 г, 34,65 ммоль) и K2CO3 (8,7 г, 63,0 ммоль). Реакцию нагревали при 85°C в течение ночи. Раствор вливали в воду со льдом, перемешивали в течение 15 мин и затем фильтровали. Твердую фазу промывали холодной водой и сушили в вакууме с получением 1-(5 аминопиридин 2-ил)пиперидин-4-ола (XC) в виде желтого твердого вещества (6,62 г, 29,67 ммоль, выход 94,2%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,34-1,42 (м, 2H), 1,77-1,83 (м, 2H), 3,40-3,56 (м, 2H), 3,76-3,83 (м, 1H), 4,12 (шд, 2H), 4,81 (д, J=4 Гц, 1H), 6,94 (д, J=10 Гц, 1H), 8,17 (дд, J=10 Гц, J=3 Гц, 1H), 8,94 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C10H13N3O3 m/z 224,1 (M+H).
Стадия 2
[0345] Получение промежуточного 1-(5-аминопиридин-2-ил)пиперидин-4-ола (XCI) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Темно-коричневое масло (5,7 г, 29,5 ммоль, выход 99,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36 (тк, J=13 Гц, J=4 Гц, 2H), 1,72-1,76 (м, 2H), 2,79 (дт, J=13 Гц, J=3 Гц, 2H), 3,54-3,61 (м, 1H), 3,70-3,78 (м, 2H), 4,49 (с, 2H), 4,61 (д, J=4 Гц, 1H), 6,61 (д, J=9 Гц, 1H), 6,88 (дд, J=9 Гц, J=3 Гц, 1H), 7,57 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C10H15N3O m/z 194,1 (M+H).
[0346] Следующие промежуточные соединения получали в соответствии с методикой, описанной выше на Схеме 19.
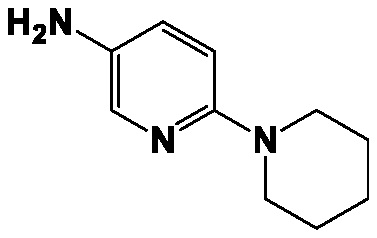
XCII
[0347] 6-(Пиперидин-1-ил)пиридин-3-амин (XCII): Темно-красное вязкое масло (4,93 г, 27,81 ммоль, выход 95,9%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,48-1,71 (м, 8H), 3,42-3,53 (м, 2H), 4,48 (шс, 2H), 6,59 (д, J=9 Гц, 1H), 6,89 (дд, J=9 Гц, J=3 Гц, 1H), 7,58 (д, J=3 Гц, 1H); ЭРИ-МС найдено для C10H15N3 m/z 178,0 (M+H).
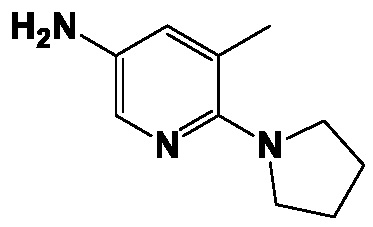
XCIII
[0348] 5-Метил-6-(пирролидин-1-ил)пиридин-3-амин (XCIII): Темно-синее вязкое масло (2,06 г, 12,62 ммоль, выход 100%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,76-1,82 (м, 4H), 2,13 (с, 3H), 3,15-3,20 (м, 4H), 4,53 (шс, 2H), 6,74 (д, J=3,5 Гц, 1H), 7,42 (д, J=2,7 Гц, 1H); ЭРИ-МС найдено для C10H15N3 m/z 178,1 (M+H).
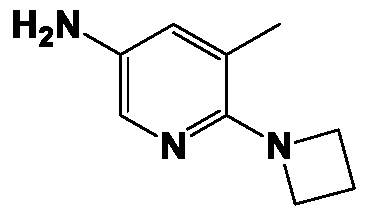
XCIV
[0349] 6-(Азетидин-1-ил)-5-метилпиридин-3-амин (XCIV): Темно-красное твердое вещество (2,0 г, 11,29 ммоль, выход 86,9%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,11 (квин, J=7 Гц, 2H), 3,76-3,87 (м, 4H), 4,50 (шс, 2H), 6,72 (д, J=2,5 Гц, 1H), 7,38 (д, J=2,5 Гц, 1H); ЭРИ-МС найдено для C9H13N3 m/z 164,4 (M+H).
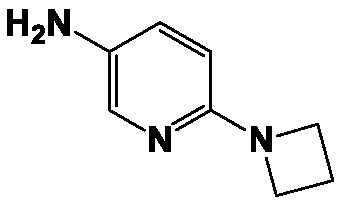
XCV
[0350] 6-(Азетидин-1-ил)пиридин-3-амин (XCV): Бордовый твердое вещество (1,45 г, 9,70 ммоль, выход 99,3%). ЭРИ-МС найдено для C8H11N3 m/z 149,0 (M+H).
[0351] Получение промежуточного трет-бутил-4-(5-аминопиридин-2-ил)пиперазин-1-карбоксилата (XCVIII) представлено ниже на Схеме 20.

Схема 20
Стадия 1
[0352] К раствору 2-хлор-5-нитропиридина (LXV) (2,0 г, 12,6 ммоль) в EtOH (20 мл) добавляли трет-бутил-пиперазин-1-карбоксилат (XCVI) (7,05 г, 37,9 ммоль). Реакцию нагревали при 70°C в течение 16 ч. Реакцию выпаривали в вакууме и затем растворяли в EtOAc. EtOAc промывали 1 М NaOH, солевым раствором и затем сушили над MgSO4 с получением трет-бутил-4-(5-нитропиридин-2-ил)пиперазин-1-карбоксилата (XCVII) в виде желтого твердого вещества (4,94 г). ЭРИ-МС найдено для C14H20N4O4 m/z 309,0 (M+H).
Стадия 2
[0353] Получение промежуточного трет-бутил-4-(5-аминопиридин-2-ил)пиперазин-1-карбоксилата (XCVIII) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Фиолетовое твердое вещество (990 мг, 3,56 ммоль, количественный выход). ЭРИ-МС найдено для C14H22N4O2 m/z 278,8 (M+H).
[0354] Получение промежуточного N-(3-аминопиридин-4-ил)циклопропанкарбоксамида (CII) представлено ниже на Схеме 21.
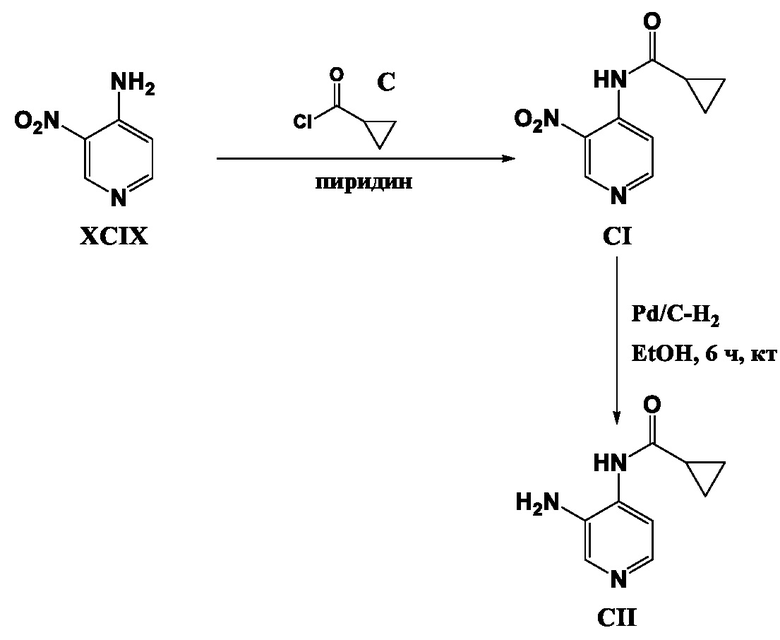
Схема 21
Стадия 1
[0355] Получение N-(3-нитропиридин-4-ил)циклопропанкарбоксамида (CI) проводили согласно методике, представленной на Схеме 4 в Стадии 1. Оранжевое твердое вещество (130 мг, 0,93 ммоль, выход 13%). ЭРИ-МС найдено для C9H9N3O3 m/z 207,8 (M+H).
Стадия 2
[0356] Получение промежуточного N-(3 аминопиридин 4-ил)циклопропанкарбоксамида (CII) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Темно-серое твердое вещество (100 мг, 0,56 ммоль, количественный выход). ЭРИ-МС найдено для C9H11N3O m/z 178,3 (M+H).
[0357] Получение промежуточного (5-аминопиридин-2-ил)(пирролидин-1-ил)метанона (CV) представлено ниже на Схеме 22.
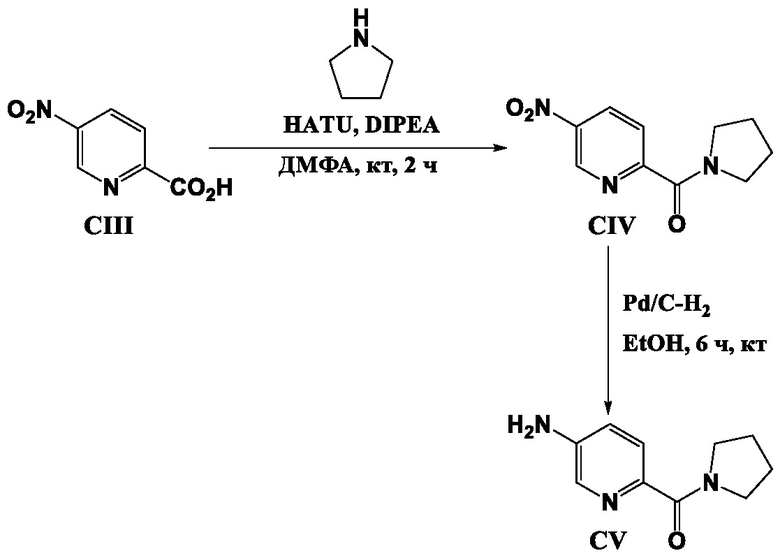
Схема 22
Стадия 1
[0358] К раствору 5-нитропиколиновой кислоты (CIII) (500 мг, 2,97 ммоль) в ДМФА (15 мл) добавляли пирролидин (244 мкл, 2,47 ммоль) и DIPEA (1,03 мл, 5,95 ммоль). Реакцию охлаждали при 0°C, после чего добавляли HATU (1,13 г, 2,47 ммоль). Реакцию нагревали до комнатной температуры и перемешивали в течение 2 ч. Реакцию выпаривали в вакууме и затем растворяли в смеси воды и 10% iPrOH/CHCl3. Органический слой отделяли и водную фазу снова промывали 10% iPrOH/CHCl3. Объединенные органические фазы промывали солевым раствором, сушили над MgSO4 и выпаривали с получением (5-нитропиридин-2-ил)(пирролидин-1-ил)метанона (CIV) в виде красного твердого вещества (849 мг). ЭРИ-МС найдено для C10H11N3O3 m/z 222,1 (M+H).
Стадия 2
[0359] Получение промежуточного (5-аминопиридин-2-ил)(пирролидин-1-ил)метанона (CV) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Желтое твердое вещество (708 мг, 7,3 ммоль, выход 96,4%). ЭРИ-МС найдено для C10H13N3O m/z 191,4 (M+H).
[0360] Следующее промежуточное соединение получали в соответствии с методикой, описанной выше на Схеме 22.
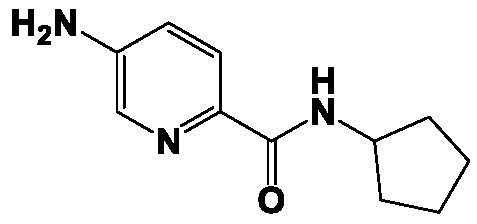
CVI
[0361] 5-Амино-N-циклопентилпиколинамид (CVI): Желтое твердое вещество (450 мг, 2,19 ммоль, выход 93,7%). ЭРИ-МС найдено для C11H15N3O m/z 206,1 (M+H).
[0362] Получение промежуточного 6-(метилсульфонил)пиридин-3-амина (CIX) представлено ниже на Схеме 23.
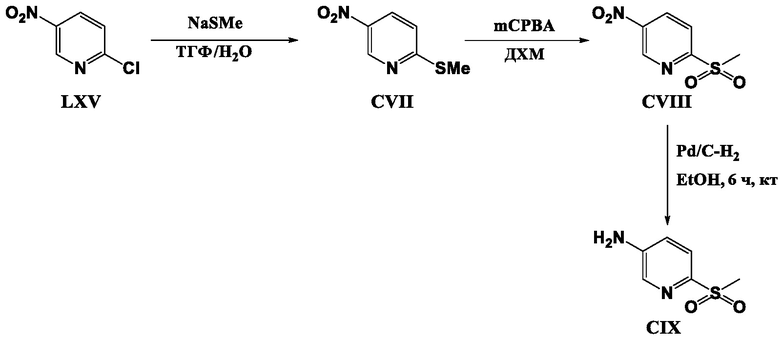
Схема 23
Стадия 1
[0363] К раствору тиометоксида натрия в ТГФ (53 мл) и H2O (20 мл), охлажденному до 0°C, добавляли 2-хлор-5-нитропиридин (LXV) (5,09 г, 32,09 ммоль). Реакцию нагревали до комнатной температуры и перемешивали в течение 2 часов. Реакцию вливали в воду со льдом и перемешивали в течение 10 минут, фильтровали, промывали водой, сушили в вакууме с получением 2-(метилтио)-5-нитропиридина (CVII) в виде желтого твердого вещества (5,14 г, 30,20 ммоль, 94,1%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,62 (с, 3H), 7,57 (д, J=8,9 Гц, 1H), 8,38 (д, J=8,9 Гц, 1H), 9,22 (д, J=2,7 Гц, 1H); ЭРИ-МС найдено для C6H6N2O2S m/z 171,1 (M+H).
Стадия 2
[0364] К раствору 2-(метилтио)-5-нитропиридина (CVII) (502 мг, 2,95 ммоль) в ДХМ (60 мл) добавляли mCPBA (1,33 г, 5,90 ммоль). Реакцию перемешивали при комнатной температуре в течение 1 часа. Две дополнительных порции mCPBA (2×250 мг) добавляли с интервалами 1 час в течение общего времени реакции 4 часа. Реакцию вливали в насыщенный водный р-р NaHCO3. Органическую фазу отделяли и промывали водой, солевым раствором, а затем сушили над MgSO4. Растворитель удаляли в вакууме с получением неочищенного 2-(метилсульфонил)-5-нитропиридина (CVIII) (854 мг), который использовали без очистки в стадии 3. ЭРИ-МС найдено для C6H6N2O4S m/z 203,0 (M+H).
Стадия 3
[0365] Получение промежуточного 6-(метилсульфонил)пиридин-3-амина (CIX) проводили согласно методике, представленной на Схеме 11 в Стадии 2. Неочищенный продукт использовали в таком виде без очистки. ЭРИ-МС найдено для C6H8N2O2S m/z 173,0 (M+H).
[0366] Получение промежуточного 5-иод-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбальдегида (CXIV) представлено ниже на Схеме 24.
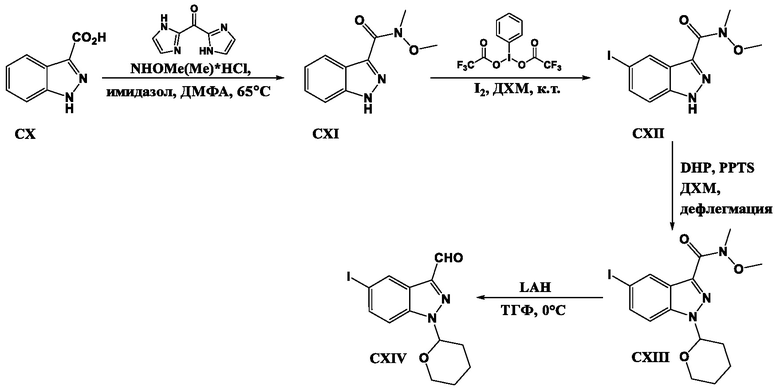
Схема 24
Стадия 1
[0367] 1H-индазол-3-карбоновую кислоту (CX) (100 г, 617 ммоль) в ДМФА обрабатывали карбонилдиимидазолом (110 г, 678 ммоль) при комнатной температуре до прекращения выделения газа (прибл. 15 минут). Реакцию нагревали до 60-65°C в течение 2 ч и затем позволяли охладиться до комнатной температуры. N,O-Диметилгидроксиламин-HCl (66,2 г, 678 ммоль) добавляли в твердом виде и нагревали смесь до 65°C в течение 3 ч. Реакцию выпаривали до пасты, собирали в ДХМ и затем промывали водой и 2 Н HCl. Можно было наблюдать выделение продукта из раствора. Твердую фазу отфильтровывали и отдельно промывали EtOAc. Слои EtOAc и ДХМ отдельно промывали бикарбонатом натрия, затем солевым раствором, сушили над MgSO4 и выпаривали при пониженном давлении. Полученные в результате твердые продукты объединяли, растирали со смесью 1:1 ДХМ-эфира, фильтровали и сушили с получением N-метокси-N-метил-1H-индазол-3-карбоксамида (CXI) в виде белого твердого вещества (100 г, 487 ммоль, выход 79%). 1H-ЯМР (ДМСО-d6) δ м.д. 3,46 (с, 3H), 3,69-3,85 (м, 3H), 7,13-7,31 (м, 1H), 7,41 (т, J=7,25 Гц, 1H), 7,56-7,65 (м, 1H), 7,93-8,08 (м, 1H); ЭРИ-МС найдено для C10H11N3O2 m/z 206 (M+H).
Стадия 2
[0368] К N-метокси-N-метил-1H-индазол-3-карбоксамиду (CXI) (20 г, 97,4 ммоль) в ДХМ (1 л) добавляли (бис(трифторацетокси)иод)бензол (46 г, 107 ммоль) с последующим добавлением иода (14,84 г, 58,5 ммоль) порциями при комнатной температуре. Через 1 ч добавляли насыщенный водный р-р NaHSO3 (600 мл), при этом начинал образовываться осадок, который отфильтровывали и промывали избытком ДХМ. Фильтрат промывали солевым раствором, сушили над MgSO4, выпаривали, а оставшееся твердое вещество растирали с минимальным количеством ДХМ. Объединенные твердые продукты сушили в вакууме над KOH с получением 5-иод-N-метокси-N-метил-1H-индазол-3-карбоксамида (CXII) в виде белого твердого вещества (23,2 г, 70 ммоль, выход 72%). 1H-ЯМР (ДМСО-d6) δ м.д. 3,45 (с, 3H), 3,77 (с, 3H), 7,45-7,54 (м, 1H), 7,66 (дд, J=8,81, 1,51 Гц, 1H), 8,40 (д, J=1,01 Гц, 1H); ЭРИ-МС найдено для C10H10IN3O2 m/z 331 (M+H).
Стадия 3
[0369] Смесь 5-иод-N-метокси-N-метил-1H-индазол-3-карбоксамида (CXII) (16,5 г, 50 ммоль), 3,4-дигидро-2H-пирана (10,3 мл, 113 ммоль) и PPTS (0,12 г, 0,6 ммоль) в ДХМ нагревали с обратным холодильником в течение 5 ч. Раствор вливали в насыщенный водный раствор NaHCO3, слои разделяли и экстрагировали водный слой ДХМ. Объединенные органические слои промывали 5% водной лимонной кислотой и солевым раствором, сушили над MgSO4 и выпаривали. Неочищенный продукт очищали на колонке с силикагелем (100% EtOAc → 3:97 MeOH:ДХМ) с получением 5-иод-N-метокси-N-метил-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксамида (CXIII) в виде белого вязкого масла (19,1 г, 46 ммоль, выход 92%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,28-1,84 (м, 6H), 3,43 (с, 3H), 3,60-4,04 (с, 5-й), 5,86-6,08 (м, 1H), 7,45-7,87 (м, 2H), 8,39 (с, 1H); ЭРИ-МС найдено для C15H18IN3O3 m/z 416 (M+H).
Стадия 4
[0370] Алюмогидрид лития (160 мг, 4,21 ммоль)порциями добавляли к охлажденному (0°C) раствору 5-иод-N-метокси-N-метил-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксамида (CXIII) (1,46 г, 3,5 ммоль) в ТГФ. Перемешивание продолжали при 0°C до полного завершения реакции, приблизительно 30 мин. Реакцию останавливали путем медленного добавления EtOAc при 0°C и всю смесь вливали в водный 0,4 Н р-р NaHSO4. Органический слой промывали солевым раствором, сушили над MgSO4, выпаривали и очищали на колонке с силикагелем (100% EtOAc → 3:97 MeOH:ДХМ) с получением 5-иод-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбальдегида (CXIV) в виде белого твердого вещества (0,90 г, 3,15 ммоль, выход 72%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,50-1,71 (м, 2H), 1,71-1,87 (м, 1H), 1,97-2,15 (м, 2H), 2,31-2,42 (м, 1H), 3,66-3,99 (м, 2H), 5,96-6,17 (м, 1H), 7,78 (д, J=6 Гц, 1H), 7,84 (д, J=6 Гц, 1H), 8,50 (с, 1H), 10,13 (с, 1H); ЭРИ-МС найдено для C13H13IN2O2 m/z 357 (M+H).
[0371] Получение промежуточной 5-бром-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXVIII) представлено ниже на Схеме 25.
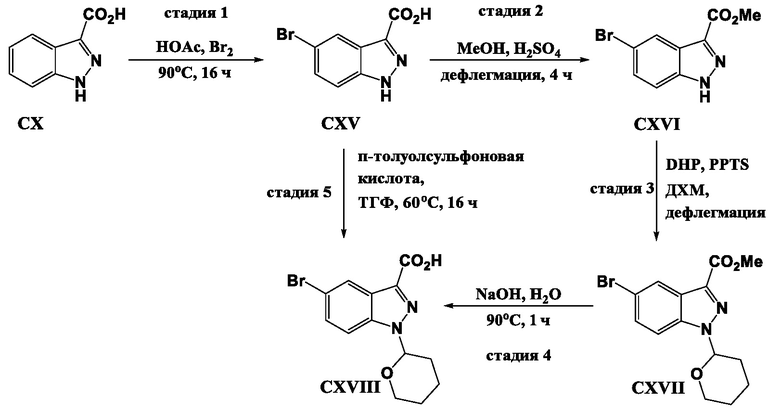
Схема 25
Стадия 1
[0372] Суспензию индазол-3-карбоновой кислоты (CX) (1,0 г, 6,16 ммоль) в ледяной уксусной кислоте (60 мл) нагревали при 120°C с получением прозрачного раствора. Раствор охлаждали до 90°C. К раствору при нагревании при 90°C медленно добавляли раствор брома (0,633 мл, 12,33 ммоль) в ледяной уксусной кислоте (2 мл). Затем раствор нагревали 16 ч при 90°C. Раствор охлаждали до комнатной температуры, вливали в воду со льдом и перемешивали при комнатной температуре еще в течение 15 мин. Образовавшееся твердое вещество отфильтровывали, промывали холодной водой и сушили в вакууме при комнатной температуре с получением 5-бром-1H-индазол-3-карбоновой кислоты (CXV) в виде белого твердого вещества (1,30 г, 5,39 ммоль, выход 87,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 13,95 (с, 1H), 13,18 (шс, 1H), 8,21 (д, J=1,2 Гц, 1H), 7,65 (д, J=7,0 Гц, 1H), 7,56 (дд, J=7,0, 1,2 Гц, 1H); ЭРИ-МС найдено для C8H4BrN2O2 m/z 242,0 (M+H).
Стадия 2
[0373] Концентрированную серную кислоту (1 мл) добавляли к суспензии 5-бром-1H-индазол-3-карбоновой кислоты (CXV) (1,30 г, 5,39 ммоль) в сухом MeOH (50 мл) и нагревали с обратным холодильником в течение 4 ч под аргоном. Раствор охлаждали до комнатной температуры и MeOH выпаривали в вакууме. Остаток растворяли в EtOAc и промывали водой. Органическую фазу сушили над Na2SO4, фильтровали и выпаривали с получением метил-5-бром-1H-индазол-3-карбоксилата (CXVI) в виде белого твердого вещества (1,35 г, 5,29 ммоль, выход 98%). 1H-ЯМР (ДМСО-d6) δ м.д. 14,13 (с, 1H), 8,21 (д, J=1,6 Гц, 1H), 7,67 (д, J=7,2 Гц, 1H), 7,59 (дд, J=7,2, 1,2 Гц, 1H), 3,92 (с, 3H); ЭРИ-МС найдено для C9H7BrN2O2 m/z 256,0 (M+H).
Стадия 3
[0374] Суспензию метил-5-бром-1H-индазол-3-карбоксилата (CXVI) (1,35 г, 5,29 ммоль), п-толуолсульфоната пиридиния (0,143 г, 0,56 ммоль) и 3,4-дигидро-2H-пирана (1,02 мл, 11,90 ммоль) в безводном дихлорэтане (20 мл) нагревали с обратным холодильником 5 ч под аргоном. Суспензия становилась прозрачным раствором. Раствор охлаждали, и избыток растворителя выпаривали в вакууме. Остаток растворяли в EtOAc и промывали разбавленным раствором NaHCO3 (нас. р-р NaHCO3/H2O: 1:9). Органический слой сушили над Na2SO4, фильтровали и выпаривали. Остаток очищали с помощью колоночной хроматографии (100% смесь гексанов → 5:95 EtOAc:смесь гексанов) с получением метил-5-бром-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксилата (CXVII) в виде белого твердого вещества (1,47 г, 4,34 ммоль, выход 82%). 1H-ЯМР (ДМСО-d6) δ м.д. 8,22 (д, J=1,4 Гц, 1H), 7,89 (д, J=7,2 Гц, 1H), 7,68 (дд, J=7,2, 1,6 Гц, 1H), 6,02 (дд, J=8,0, 2,4 Гц, 1H), 3,94 (с, 3H), 3,88 (м, 1H), 3,79 (м, 1H), 2,37-2,31 (м, 1H), 2,05-1,96 (м, 2H), 1,77-1,73 (м, 1H), 1,60-1,58 (м, 2H); ЭРИ-МС найдено для C14H15BrN2O3 m/z 340,0 (M+H).
Стадия 4
[0375] К суспензии метил-5-бром-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксилата (CXVII) (1,30 г, 3,83 ммоль) в воде (20 мл) добавляли 2Н водный раствор NaOH (10 мл) и нагревали при 90°C в течение 1 ч. Раствор охлаждали до комнатной температуры, разбавляли водой со льдом и подкисляли до pH 3,0 10% водной HCl. Образовавшееся твердое вещество отфильтровывали, промывали холодной водой и сушили в вакууме при комнатной температуре с получением 5-бром-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXVIII) в виде белого твердого вещества (0,87 г, 2,68 ммоль, выход 70%). ЭРИ-МС найдено для C13H13BrN2O3 m/z 326,0 (M+H).
Стадия 5
[0376] К раствору 5-бром-1H-индазол-3-карбоновой кислоты (CXV) (59,8 г, 248 ммоль) в ТГФ (800 мл) под аргоном добавляли 3,4-дигидро-2H-пиран (50,6 мл, 558 ммоль) и п-TsOH (4,72 г, 24,8 ммоль). Реакцию нагревали с обратным холодильником при 60°C в течение 16 ч. Добавляли дополнительную порцию п-TsOH (0,025 экв.) и 3,4-дигидро-2H-пирана (0,56 экв.) и продолжали нагревание с обратным холодильником в течение 5 ч. Раствор выпаривали в вакууме. К остатку добавляли EtOAc, и суспензию фильтровали и сушили в глубоком вакууме в течение ночи с получением 5-бром-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXVIII) в виде белого твердого вещества (49,07 г, 150,9 ммоль, выход 60,8%). ЭРИ-МС найдено для C13H13BrN2O3 m/z 326,3 (M+H).
[0377] Получение промежуточной 5-бром-1-тритил-1H-индазол-3-карбоновой кислоты (CXXI) представлено ниже на Схеме 26.
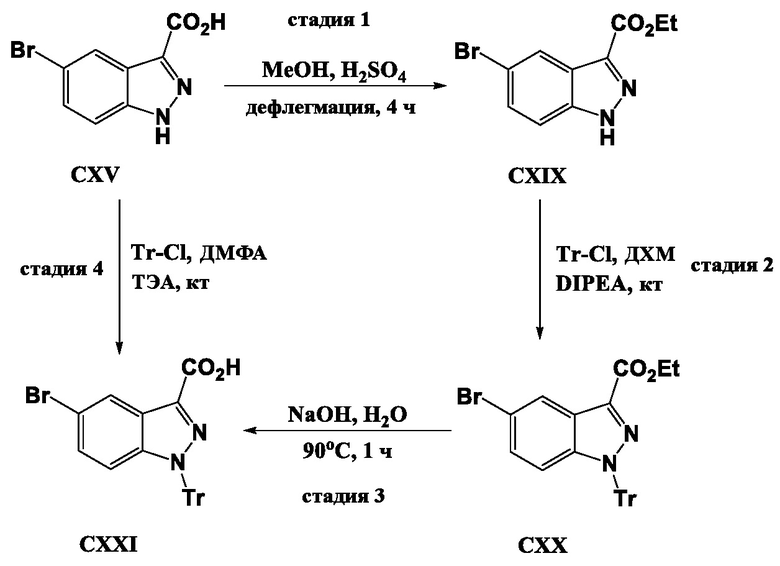
Схема 26
Стадия 1
[0378] Получение промежуточного этил-5-бром-1H-индазол-3-карбоксилата (CXIX) проводили согласно методике, представленной на Схеме 25 в Стадии 2. Белое твердое вещество (3,60 г, 13,38 ммоль, выход 64,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,37 (т, J=7 Гц, 3H), 4,40 (к, J=7 Гц, 2H), 7,57 (дд, J=9 Гц, J=2 Гц, 1H), 7,66 (д, J=9 Гц, 1H), 8,20 (д, J=2 Гц, 1H), 14,11 (шс, 1H); ЭРИ-МС найдено для C10H9BrN2O2 m/z 269,0 (M+H).
Стадия 2
[0379] К раствору этил-5-бром-1H-индазол-3-карбоксилата (CXIX) и тритилхлорида в ДХМ медленно добавляли DIPEA. Раствор перемешивали при комнатной температуре в течение ночи. Реакцию вливали в воду и перемешивали в течение 5 мин. Органический слой отделяли, сушили над MgSO4 и выпаривали в вакууме. Остаток очищали с помощью колоночной хроматографии при использовании системы ISCO 200RF с колонкой SiO2 (12 г) (100% смесь гексанов → 10:90 EtOAc:смесь гексанов) с получением белого твердого вещества (357 мг, 0,70 ммоль, выход 69,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,34 (т, J=7 Гц, 3H), 4,38 (к, J=7 Гц, 2H), 6,43 (д, J=9,5 Гц, 1H), 7,11-7,14 (м, 6H), 7,31-7,35 (м, 10H), 8,23 (д, J=2 Гц, 1H); ЭРИ-МС найдено для C29H23BrN2O2 m/z 511,0 (M+H).
Стадия 3
[0380] Получение промежуточного 5-бром-1-тритил-1H-индазол-3-карбоновой кислоты (CXXI) путем гидролиза этил-5-бром-1-тритил-1H-индазол-3-карбоксилата (CXX) может быть выполнено согласно методике, представленной на Схеме 25 в Стадии 3.
Стадия 4
[0381] Получение промежуточной 5-бром-1-тритил-1H-индазол-3-карбоновой кислоты (CXXI) путем тритилирования 5-бром-1H-индазол-3-карбоновой кислоты (CXV) может быть выполнено согласно методике, представленной в Journal of Medicinal Chemistry (2003), 46(25), 5458-5470.
Пример 1
[0382] Получение 5-(5-(3,3-диметилуреидо)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамида (1) представлено ниже на Схеме 27.
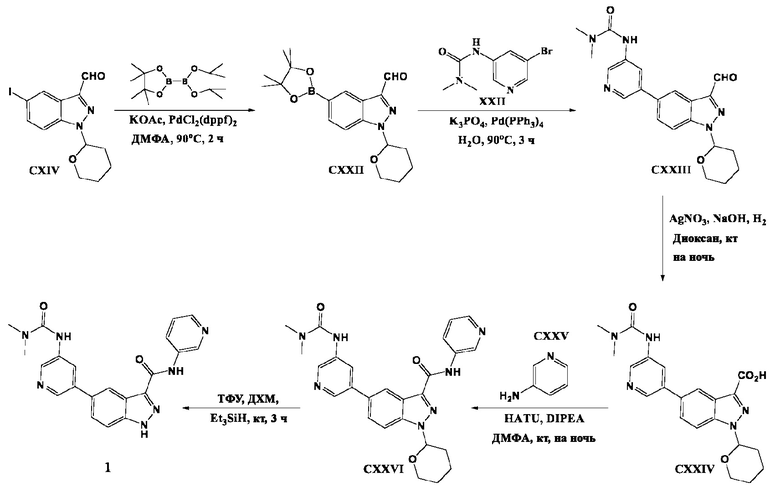
Схема 27
Стадия 1-2
[0383] Раствор 5-иод-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбальдегида (CXIV) (1,780 г, 5,0 ммоль), бис(пинаколато)дибора (1,523 г, 6,0 ммоль), KOAc (1,471 г, 15 ммоль) и сухого ДМФА (20 мл) барботировали аргоном. К реакционной смеси добавляли PdCl2(dppf)2 (0,245 г, 0,3 ммоль) и снова барботировали аргоном. Раствор нагревали при 90°C в течение 2 ч. Как только ТСХ показала исчезновение (CXIV), раствор охлаждали до комнатной температуры. К этому раствору добавляли K3PO4 (1,592 г, 7,5 ммоль), 3-(5-бромпиридин-3-ил)-1,1-диметилмочевину (XXII) (1,220 г, 5,0 ммоль), Pd(PPh3)4 (173 мг, 0,15 ммоль) и воду (2 мл). Раствор барботировали аргоном и нагревали при 90°C в течение 3 ч. Раствор охлаждали до комнатной температуры и затем выпаривали при пониженном давлении. Остаток растворяли в ДХМ и промывали водой, сушили над MgSO4, фильтровали и затем выпаривали в вакууме. Остаток очищали на колонке с силикагелем (100% ДХМ → 2:98 MeOH:ДХМ) с получением 3-(5-(3-формил-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-5-ил)пиридин-3-ил)-1,1-диметилмочевины (CXXIII) в виде коричневого вязкого масла, которое затвердевало в вакууме при комнатной температуре (354 мг, 0,90 ммоль, выход 18% в 2 стадиях). 1H-ЯМР (ДМСО-d6) δ м.д. 10,22 (с, 1H), 8,76 (д, J=1,6 Гц, 1H), 8,63 (с, 1H), 8,52 (д, J=1,6 Гц, 1H), 8,36 (с, 1H), 8,24 (м, 1H), 8,05 (д, J=7,2 Гц, 1H), 7,91 (дд, J=7,2, 1,4 Гц, 1H), 6,13 (дд, J=7,6, 2,0 Гц, 1H), 3,93 (м, 1H), 3,85 (м, 1H), 2,98 (с, 6H), 2,47-2,42 (м, 1H), 2,11-2,06 (м, 2H), 1,82-1,79 (м, 1H) 1,64 (м, 2H); ЭРИ-МС найдено для C21H23N5O3 m/z 394,0 (M+H).
Стадия 3
[0384] Раствор гидроксида натрия (0,173 г, 4,33 ммоль) в воде (5 мл) добавляли к раствору нитрата серебра (0,367 г, 2,16 ммоль) в воде (5 мл) с получением коричневого осадка. 3-(5-(3-Формил-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-5-ил)пиридин-3-ил)-1,1-диметилмочевину (CXXIII) (0,340 г, 0,86 ммоль) растворяли в 1,4-диоксане (10 мл) и добавляли к реакционной смеси, которую перемешивали в течение ночи при комнатной температуре. Раствор разбавляли водой и затем экстрагировали диэтиловым эфиром. Водный слой отделяли и осторожно доводили до pH=3 водной HCl. Затем водный слой экстрагировали 10% iPrOH/хлорформом. Объединенные органические слои затем сушили (Na2SO4), фильтровали и выпаривали с получением 5-(5-(3,3-диметилуреидо)пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXXIV) в виде коричневато-белого твердого вещества (246 мг, 0,60 ммоль, выход 70%). 1H-ЯМР (ДМСО-d6) δ м.д. 13,26 (шс, 1H), 8,87 (с, 1H), 8,63 (с, 1H), 8,41 (с, 1H), 8,34 (с, 1H), 8,03 (д, J=7,1 Гц, 1H), 7,86 (дд, J=7,2, 1,3 Гц, 1H), 6,06 (дд, J=8,0, 4,0 Гц, 1H), 3,92 (м, 1H), 3,80 (м, 1H), 2,98 (с, 6H), 2,42-2,39 (м, 1H), 2,03-2,02 (м, 2H), 1,79-1,77 (м, 1H) 1,61 (м, 2H); ЭРИ-МС найдено для C21H23N5O4 m/z 410,0 (M+H).
Стадия 4
[0385] HATU (0,190 г, 0,5 ммоль) добавляли к раствору 5-(5-(3,3-диметилуреидо)пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXXIV) (0,39 г, 1,21 ммоль) и диизопропилэтиламина (0,174 мл, 1,0 ммоль) в ДМФА, перемешиваемому при комнатной температуре под аргоном. После перемешивания в течение 5 мин, в раствор добавляли 3-аминопиридин (CXXV) (0,047 г, 0,5 ммоль). Раствор перемешивали в течение ночи при комнатной температуре под аргоном. ДМФА удаляли при пониженном давлении, а остаток обрабатывали водой, быстро обрабатывали ультразвуком и фильтровали. Сухие вещества промывали холодной водой и сушили при комнатной температуре. Продукт очищали с помощью колоночной хроматографии при использовании 4 г нормально-фазового картриджа с силикагелем Thomson (100% ДХМ → 5:95 MeOH:ДХМ) с получением 5-(5-(3,3-диметилуреидо)пиридин-3-ил)-N-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксамида (CXXVI) в виде почти белого твердого вещества (323 мг, 0,67 ммоль, выход 55%). 1H-ЯМР (ДМСО-d6) δ м.д. 10,56 (с, 1H), 9,06 (д, J=2,0 Гц, 1H), 8,75 (д, J=1,6 Гц, 1H), 8,64 (с, 1H), 8,53 (д, J=1,6 Гц, 1H), 8,46 (с, 1H), 8,34-8,29 (м, 2H), 8,26 (м, 1H), 8,03 (д, J=7,0 Гц, 1H), 7,88 (дд, J=7,0, 1,2 Гц, 1H), 7,43 (дд, J=6,64, 3,84 Гц, 1H), 6,07 (дд, J=8,0, 1,8 Гц, 1H), 3,98 (м, 1H), 3,82 (м, 1H), 2,98 (с, 6H), 2,63-2,60 (м, 1H), 2,11-2,06 (м, 2H), 1,83-1,81 (м, 1H) 1,52 (м, 2H); ЭРИ-МС найдено для C21H23N5O4 m/z 410,0 (M+H).
Стадия 5
[0386] ТФУ (5 мл) добавляли к раствору 5-(5-(3,3-диметилуреидо)пиридин-3-ил)-N-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксамида (CXXVI) (0,134 г, 0,27 ммоль) и триэтилсилана (0,110 мл, 0,69 ммоль) в ДХМ (5 мл) и перемешивали 3 ч при комнатной температуре. Растворитель удаляли в вакууме. Остаток обрабатывали водой, быстро обрабатывали ультразвуком, чтобы диспергировать твердую фазу, подщелачивали до pH 9,0 5 Н NH4OH и снова обрабатывали ультразвуком. Твердую фазу отфильтровывали, промывали холодной водой и очищали с помощью колоночной хроматографии (100% ДХМ → 5:95 MeOH [7Н NH3]:ДХМ) с получением 5-(5-(3,3-диметилуреидо)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамида (1) в виде белого твердого вещества (35,8 мг, 0,09 ммоль, выход 33%). 1H-ЯМР (ДМСО-d6) δ м.д. 13,99 (с, 1H), 10,69 (с, 1H), 9,08 (д, J=1,2 Гц, 1H), 8,74 (д, J=1,8 Гц, 1H), 8,63 (с, 1H), 8,51 (д, J=1,5 Гц, 1H), 8,47 (с, 1H), 8,33-8,30 (м, 2H), 8,26 (м, 1H), 7,80 (с, 2H), 7,41 (дд, J=6,6, 3,6 Гц, 1H), 2,98 (с, 6H); ЭРИ-МС найдено для C21H19N7O2 m/z 402,3 (M+H).
[0387] Следующее соединение получали в соответствии с методикой, описанной выше в Примере 1.
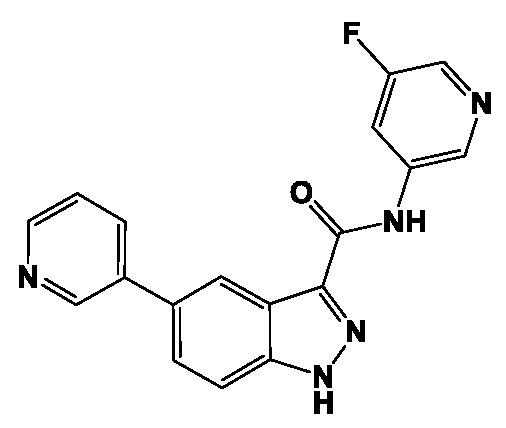
23
[0388] N-(5-Фторпиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 23.
[0389] Светло-коричневое твердое вещество. 1H-ЯМР (ДМСО-d6) δ м.д. 7,53 (дд, J=8 Гц, J=5 Гц, 1H), 7,82-7,86 (м, 2H), 8,13-8,15 (м, 1H), 8,31-8,34 (м, 2H), 8,47-8,48 (м, 1H), 8,60 (дд, J=5 Гц, J=2 Гц, 1H), 894 (д, J=2 Гц, 1H), 8,99 (д, J=2 Гц, 1H), 10,97 (с, 1H), 14,05 (с, 1H); ЭРИ-МС найдено для C18H12FN5O m/z 334 (M+1).
Пример 2
[0390] Получение 5-(5-фторпиридин-3-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (2) представлено ниже на Схеме 28.
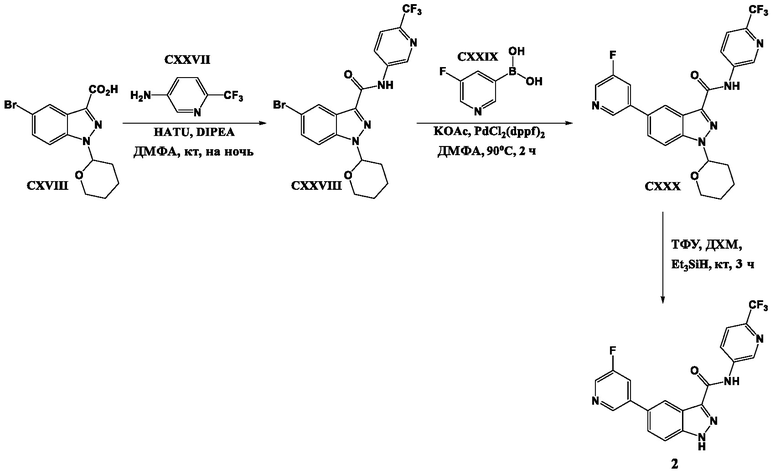
Схема 28
Стадия 1
[0391] HATU (1,125 г, 2,96 ммоль) добавляли к раствору 5-бром-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXVIII) (0,876 г, 2,69 ммоль) и диизопропилэтиламина (1,03 мл, 5,92 ммоль) в ДМФА, перемешиваемому при комнатной температуре под аргоном. После перемешивания в течение 5 мин, в раствор добавляли 5-амино-2-трифторметил-пиридин (CXXVII) (0,479 г, 2,96 ммоль). Раствор перемешивали 24 ч при комнатной температуре под аргоном. ДМФА удаляли при пониженном давлении, а остаток обрабатывали водой, быстро обрабатывали ультразвуком и фильтровали. Твердую фазу промывали холодной водой и сушили при комнатной температуре. Продукт очищали с помощью колоночной хроматографии на силикагеле (100% смесь гексанов → 7:93 EtOAc:смесь гексанов) с получением 5-бром-1-(тетрагидро-2H-пиран-2-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (CXXVIII) в виде белого твердого вещества (1,17 г, 2,50 ммоль, выход 93%). 1H-ЯМР (ДМСО-d6) δ м.д. 10,93 (с, 1H), 9,23 (д, J=1,9 Гц, 1H), 8,60 (дд, J=6,8, 1,4 Гц, 1H), 8,38 (д, J=4,4 Гц, 1H), 7,95 (м, 2H), 7,70 (дд, J=7,1, 1,5 Гц, 1H)), 6,04 (дд, J=8,1, 1,9 Гц, 1H), 3,98 (м, 1H), 3,82 (м, 1H), 2,59-2,54 (м, 1H), 2,08-2,03 (м, 2H), 1,81-1,77 (м, 1H), 1,66-1,61 (м, 2H); ЭРИ-МС найдено для C19H16BrF3N4O2 m/z 470,0 (M+H).
Стадия 2
[0392] Раствор 5-бром-1-(тетрагидро-2H-пиран-2-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (CXXVIII) (0,469 г, 1 ммоль), 5-фтор-пиридил-3-бороновой кислоты (CXXIX) (0,156 г, 1,1 ммоль), трехосновного фосфата калия (0,318 г, 1,5 ммоль) и воды (дегазированной, 1 мл) в ДМФА (10 мл) барботировали аргоном. Добавляли тетракис(трифенилфосфин)-палладий (0) (0,034 г, 0,03 ммоль) и раствор снова барботировали аргоном. Реакцию нагревали до 90°C в течение 3 ч, при этом ТСХ показала исчезновение исходного материала. Раствор охлаждали до комнатной температуры и удаляли избыток растворителя в вакууме. Остаток обрабатывали водой, быстро обрабатывали ультразвуком и отфильтровывали образовавшийся осадок. Твердую фазу промывали холодной водой и сушили в вакууме при комнатной температуре, после чего очищали с помощью колоночной хроматографии на силикагеле (2:8 EtOAc:смесь гексанов → 3:7 EtOAc:смесь гексанов) с получением 5-(5-фторпиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (CXXX) в виде белого твердого вещества (427 мг, 0,88 ммоль, выход 88%). 1H-ЯМР (ДМСО-d6) δ м.д. 10,95 (с, 1H), 9,25 (д, J=1,8 Гц, 1H), 8,85 (м, 1H), 8,63 (д, J=1,8 Гц, 1H), 8,61 (д, J=2,1 Гц, 1H), 8,53 (м, 1H), 8,16-8,13 (м, 1H), 8,08 (д, J=7,1 Гц, 1H), 7,97-7,94 (м, 2H), 6,11 (дд, J=8,1, 1,8 Гц, 1H), 4,01 (м, 1H), 3,88-3,83 (м, 1H), 2,63-2,60 (м, 1H), 2,11-2,07 (м, 2H), 1,83-1,80 (м, 1H), 1,69-1,65 (м, 2H); ЭРИ-МС найдено для C24H19F4N5O2 m/z 486,0 (M+H).
Стадия 3
[0393] ТФУ (10 мл) добавляли к раствору 5-(5-фторпиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (CXXX) (0,420 г, 0,86 ммоль) и триэтилсилана (0,345 мл, 2,16 ммоль) в ДХМ (10 мл) и перемешивали 5 ч при комнатной температуре. Растворитель удаляли в вакууме. Остаток обрабатывали водой, быстро обрабатывали ультразвуком, чтобы диспергировать твердую фазу, подщелачивали до pH 9,0 5 Н NH4OH и снова обрабатывали ультразвуком. Твердую фазу отфильтровывали, промывали холодной водой и сушили на воздухе при комнатной температуре. Твердое вещество суспендировали в смеси ДХМ:MeOH (1:1) и кипятили с получением прозрачного раствора. Раствор охлаждали до комнатной температуры. Образовавшийся осадок отфильтровывали, промывали ДХМ и сушили в вакууме при комнатной температуре с получением 5-(5-фторпиридин-3-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (2) в виде белого твердого вещества (72,9 мг, 0,18 ммоль, выход 21%). 1H-ЯМР (ДМСО-d6) δ м.д. 14,13 (шс, 1H), 11,11 (с, 1H), 9,27 (д, J=1,8 Гц, 1H), 8,84 (м, 1H), 8,63 (дд, J=6,8, 1,8 Гц, 1H), 8,60 (д, J=2,0 Гц, 1H), 8,53 (м, 1H), 8,14-8,11 (м, 1H), 7,94 (д, J=6,9 Гц, 1H), 7,90-7,83 (м, 2H); ЭРИ-МС найдено для C19H11F4N5O m/z 402,30 (M+H).
[0394] Следующее соединение получали в соответствии с методикой, описанной выше в Примере 2.
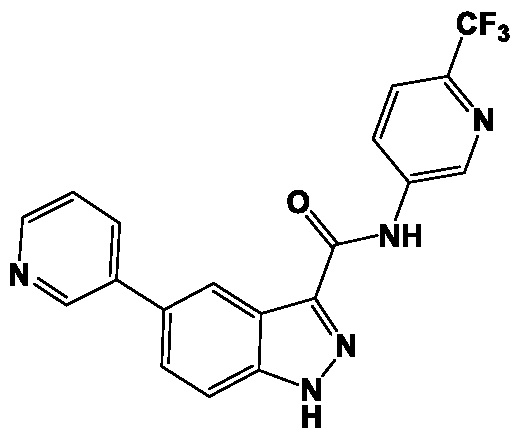
3
[0395] 5-(Пиридин-3-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 3.
[0396] Белое твердое вещество (выход 19%). 1H-ЯМР (ДМСО-d6) δ м.д. 14,03 (шс, 1H), 11,10 (с, 1H), 9,27 (д, J=1,8 Гц, 1H), 8,94 (д, J=1,6 Гц, 1H), 8,63 (дд, J=6,8, 1,7 Гц, 1H), 8,60 (м, 1H), 8,48 (с, 1H), 8,15-8,13 (м, 1H), 7,93 (д, J=6,9 Гц, 1H), 7,85 (с, 2H), 7,54 (м, 1H); ЭРИ-МС найдено для C19H12F3N5O m/z 384,0 (M+H).
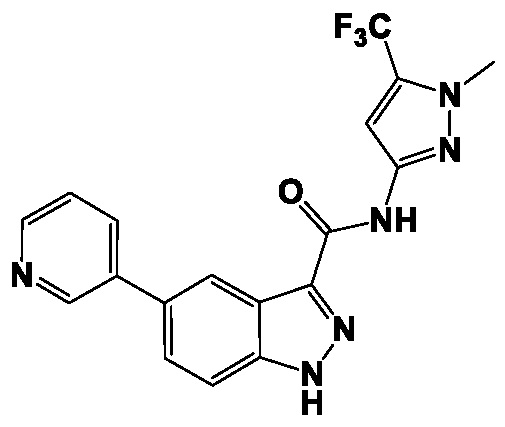
37
[0397] N-(1-Метил-5-(трифторметил)-1H-pyrazol-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 37.
[0398] Светло-зеленое твердое вещество (76,7 мг, 0,20 ммоль, выход 48,4%). 1H-ЯМР (ДМСО-d6) δ м.д. 3,93 (с, 3H), 7,18 (с, 1H), 7,55 (дт, J=8 Гц, J=3 Гц, 1H), 7,81 (дд, J=15 Гц, J=9 Гц, 2H), 8,16 (д, J=8 Гц, 1H), 8,45 (с, 1H), 8,61 (д, J=4 Гц, 1H), 8,95 (с, 1H), 10,81 (с, 1H), 13,96 (с, 1H); ЭРИ-МС найдено для C18H13F3N6O m/z 387,1 (M+H).
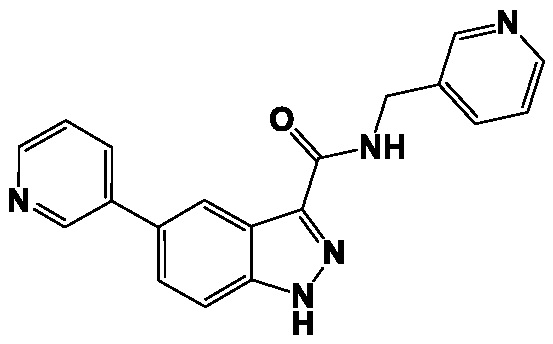
42
[0399] 5-(Пиридин-3-ил)-N-(пиридин-3-илметил)-1H-индазол-3-карбоксамид 42.
[0400] Белое твердое вещество (54,5 мг, 0,17 ммоль, выход 78%). 1H-ЯМР (ДМСО-d6) δ м.д. 4,53 (д, J=6 Гц, 2H), 7,35 (дд, J=8 Гц, J=5 Гц, 1H), 7,49-7,52 (м, 1H), 7,74-7,78 (м, 3H), 8,09-8,11 (м, 1H), 8,41-8,42 (м, 1H), 8,45 (дд, J=5 Гц, J=2 Гц, 1H), 8,57 (дд, J=5 Гц, J=2 Гц, 1H), 8,59 (д, J=2 Гц, 1H), 8,90 (д, J=2 Гц, 1H), 9,16 (т, J=6 Гц, 1H), 13,77 (с, 1H); ЭРИ-МС найдено для C19H15N5O m/z 330 (M+H).
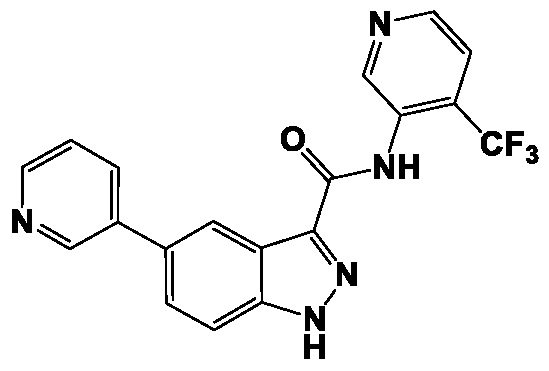
48
[0401] 5-(Пиридин-3-ил)-N-(4-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 48.
[0402] Белое твердое вещество (67 мг, 0,17 ммоль, выход 62%). 1H-ЯМР (ДМСО-d6) δ м.д. 7,52 (дд, J=8 Гц, J=5 Гц, 1H), 7,83-7,87 (м, 3H), 8,12 (тд, J=8 Гц, J=2 Гц, 1H), 8,41 (т, J=1 Гц, 1H), 8,59 (дд, J=5 Гц, J=2 Гц, 1H), 8,75 (д, J=5 Гц, 1H), 8,92 (д, J=3 Гц, 1H), 9,08 (с, 1H), 10,21 (с, 1H), 14,06 (шс, 1H); ЭРИ-МС найдено для C19H12F3N5O m/z 384,0 (M+H).
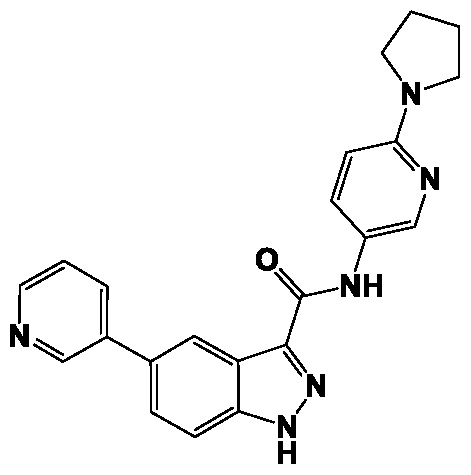
53
[0403] 5-(Пиридин-3-ил)-N-(6-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 53.
[0404] Бежевое твердое вещество (23,8 мг, 0,06 ммоль, выход 44,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,92-1,97 (м, 4H), 3,38 (т, J=7 Гц, 4H), 6,46 (д, J=9 Гц, 1H), 7,52 (дд, J=8 Гц, J=5 Гц, 1H), 7,80 (дк, J=9 Гц, J=2 Гц, 2H), 7,97 (дд, J=9 Гц, J=3 Гц, 1H), 8,12 (дд, J=8 Гц, J=4 Гц, 1H), 8,47 (с, 1H), 8,50 (д, J=3 Гц, 1H), 8,59 (дд, J=5 Гц, J=2 Гц, 1H), 8,92 (д, J=2 Гц, 1H), 10,22 (с, 1H), 13,86 (с, 1H); ЭРИ-МС найдено для C22H20N6O m/z 385,1 (M+H).
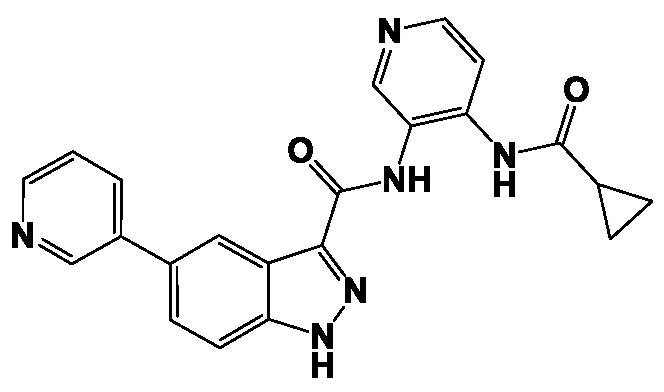
58
[0405] N-(4-(Циклопропанкарбоксамидо)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 58.
[0406] Белое твердое вещество (32,7 мг, 0,08 ммоль, выход 37,0%). 1H-ЯМР (ДМСО-d6) δ м.д. 0,84-0,88 (м, 2H), 0,88-0,92 (м, 2H), 1,91-1,99 (м, 1H), 7,52 (дд, J=8 Гц, J=5 Гц, 1H), 7,73 (д, J=6 Гц, 1H), 7,82 (дд, J=12 Гц, J=9 Гц, 2H), 8,12 (дт, J=9 Гц, J=4 Гц, 1H), 8,34 (д, J=6 Гц, 1H), 8,44 (с, 1H), 8,59 (дд, J=5 Гц, J=2 Гц, 1H), 8,80 (с, 1H), 8,92 (д, J=2 Гц, 1H), 10,03 (с, 1H), 10,31 (с, 1H), 13,98 (с, 1H); ЭРИ-МС найдено для C22H18N6O2 m/z 399,0 (M+H).
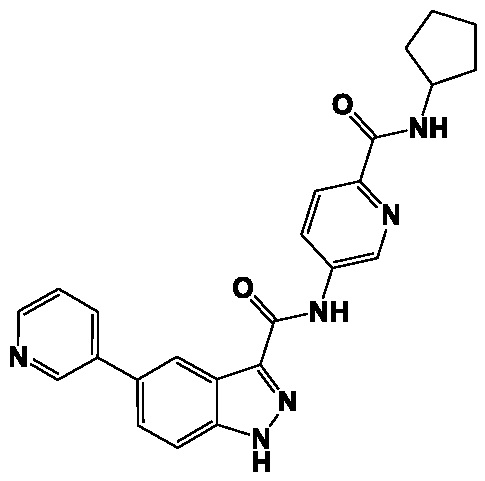
181
[0407] N-(6-(Циклопентилкарбамоил)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 181.
[0408] Светло-желтое твердое вещество (18 мг, 0,04 ммоль, выход 16,6%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,50-1,64 (м, 4H), 1,67-1,76 (м, 2H), 1,85-1,94 (м, 4H), 4,24 (квин, J=8 Гц, 1H), 7,53 (дд, J=8 Гц, J=5 Гц, 1H), 7,84 (ABк, 2H), 8,03 (д, J=9 Гц, 1H), 8,14 (д, J=8 Гц, 1H), 8,45 (д, J=8 Гц, 1H), 8,48 (с, 1H), 8,54 (дд, J=9 Гц, J=2,5 Гц, 1H), 8,60 (д, J=4 Гц, 1H), 8,94 (д, J=2 Гц, 1H), 9,16 (д, J=2 Гц, 1H), 10,97 (с, 1H), 14,08 (шс, 1H); ЭРИ-МС найдено для C24H22N6O2 m/z 427,1 (M+H).
Пример 3
[0409] Получение N,5-ди(пиридин-3-ил)-1H-индазол-3-карбоксамида (4) представлено ниже на Схеме 29.
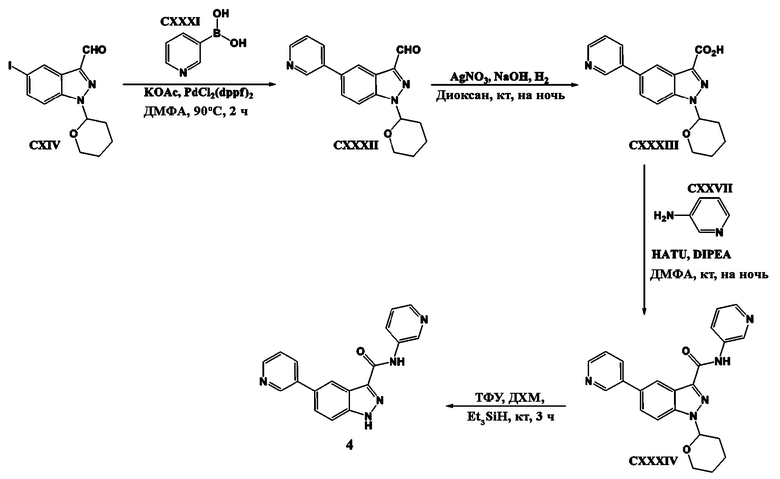
Схема 29
Стадия 1
[0410] 5-Иод-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбальдегид (CXIV) (1,53 г, 4,30 ммоль), пиридин-3-бороновую кислоту (CXXXI) (0,58 г, 4,73 ммоль) и трехосновный фосфат калия (1,37 г, 6,45 ммоль) растворяли в 1,4-диоксане (43,0 мл) и воде (9,0 мл). Добавляли тетракис(трифенилфосфин)палладий (0) (0,50 г, 0,4301 ммоль) и нагревали реакцию до 95°C в течение 2,5 ч. Растворитель удаляли, а остаток делили между EtOAc и водой. Органическую фазу отделяли и последовательно промывали водой и солевым раствором. Материал сушили (MgSO4), выпаривали и очищали с помощью флеш-хроматографии при использовании 40 г нормально-фазового картриджа с силикагелем Thomson (100% смесь гексанов → 1:1 EtOAc:смесь гексанов) с получением 5-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбальдегида (CXXXII) (0,62 г, 2,02 ммоль, выход 47%) в виде коричневого аморфного твердого вещества. 1H-ЯМР (ДМСО-d6) δ м.д. 10,23 (с, 1H), 8,95 (д, J=2,3 Гц, 1H), 8,61 (дд, J=4,8, 1,5 Гц, 1H), 8,39 (д, J=0,98 Гц, 1H), 8,17-8,14 (м, 1H), 8,06 (д, J=8,8 Гц, 1H), 7,95-7,93 (м, 1H), 7,64-7,60 (м, 1H), 6,13 (дд, J=9,4, 2,4 Гц, 1H), 3,93-3,90 (м, 1H), 3,86-3,81 (м, 1H), 2,45-2,41 (м, 1H), 2,11-2,07 (м, 2H), 1,82-1,78 (м, 1H), 1,66-1,62 (м, 2H); ЭРИ-МС найдено для C18H17N3O2 m/z 308 (M+H).
Стадия 2
[0411] К раствору нитрата серебра (0,55 г, 3,25 ммоль) в воде (10 мл) добавляли раствор гидроксида натрия (0,26 г, 6,50 ммоль) в воде (5 мл) с получением коричневого осадка. 5-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбальдегид (CXXXII) (0,40 г, 1,30 ммоль), растворенный в 1,4-диоксане (3 мл), добавляли к реакции, которую перемешивали при комнатной температуре в течение 2 ч. Затем реакцию экстрагировали диэтиловым эфиром. Водный слой отделяли и осторожно доводили до pH=3 10% водной HCl. Затем водный слой пять раз экстрагировали iPrOH/хлороформом (1/9). Объединенные органические слои затем сушили (MgSO4) и выпаривали с получением 5-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXXXIII) (0,30 г, 0,93 ммоль, выход 70%) в виде белого твердого вещества. 1H-ЯМР (ДМСО-d6) δ м.д. 13,28 (шс, 1H), 8,93 (с, 1H), 8,60 (д, J=4,1 Гц, 1H), 8,32 (д, J=0,83 Гц, 1H), 8,14-8,12 (м, 1H), 8,00 (д, J=8,8 Гц, 1H), 7,86 (дд, J=8,8, 1,7 Гц, 1H), 7,52 (дд, J=7,8, 4,7 Гц, 1H), 6,04 (дд, J=9,3, 2,3 Гц, 1H), 3,92-3,90 (м, 1H), 3,83-3,78 (м, 1H), 2,44-2,37 (м, 1H), 2,08-2,02 (м, 2H), 1,79-1,76 (м, 1H), 1,63-1,61 (м, 2H).
Стадия 3
[0412] К раствору 5-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXXXIII) (0,39 г, 1,21 ммоль) и 3-аминопиридина (CXXVII) (0,11 г, 1,21 ммоль) в ДМФА (4,0 мл) добавляли N,N-диизопропилэтиламин (0,42 мл, 1,21 ммоль). Раствор охлаждали до 0°C, после чего добавляли HATU (0,46 г, 1,21 ммоль). Ледяную баню убирали, нагревали реакцию до комнатной температуры и перемешивали в течение 2 ч. ДМФА удаляли при пониженном давлении, а остаток делили между хлороформом и водой. Органическую фазу отделяли и последовательно промывали водой и солевым раствором, сушили над MgSO4, фильтровали и выпаривали. Продукт очищали с помощью колоночной хроматографии при использовании 25 г нормально-фазового картриджа с силикагелем Thomson (100% CHCl3 → 2:98 MeOH:CHCl3) с получением N,5-ди(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксамида (CXXXIV) (0,36 г, 0,90 ммоль, выход 75%) в виде почти белого твердого вещества. 1H-ЯМР (ДМСО-d6) δ м.д. 10,56 (с, 1H), 9,06 (д, J=2,4 Гц, 1H), 8,94 (д, J=2,3 Гц, 1H), 8,60 (дд, J=4,8, 1,5 Гц, 1H), 8,47 (д, J=1,1 Гц, 1H), 8,34-8,33 (м, 1H), 8,31-8,29 (м, 1H), 8,16-8,14 (м, 1H), 8,04 (д, J=8,8 Гц, 1H), 7,90 (дд, J=8,8, 1,8 Гц, 1H), 7,54-7,52 (м, 1H), 7,43-7,41 (м, 1H), 7,43-7,41 (м, 1H), 6,08-6,06 (м, 1H), 4,01-3,99 (м, 1H), 3,87-3,82 (м, 1H), 2,64-2,57 (м, 1H), 2,11-2,06 (м, 2H), 1,84-1,80 (м, 1H), 1,69-1,65 (м, 2H); ЭРИ-МС найдено для C23H21N5O2 m/z 400 (M+H).
Стадия 4
[0413] ТФУ (5,0 мл) добавляли к раствору N,5-ди(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксамида (CXXXIV) (0,36 г, 0,90 ммоль) и триэтилсилана (0,29 мл, 1,81 ммоль) в ДХМ (5,0 мл). Раствор перемешивали в течение ночи при комнатной температуре. Добавляли еще 5,0 мл ТФУ и раствор снова перемешивали в течение ночи. Растворители удаляли, а остаток обрабатывали 7 Н аммиаком в MeOH. Растворители снова удаляли и очищали продукт с помощью флеш-хроматографии при использовании 12 г нормально-фазового картриджа с силикагелем Thomson (100% CHCl3 → 5:95 MeOH [7Н NH3]:CHCl3) с получением N,5-ди(пиридин-3-ил)-1H-индазол-3-карбоксамида (4) (0,23 г, 0,73 ммоль, выход 82%) в виде белого твердого вещества. 1H-ЯМР (ДМСО-d6) δ м.д. 14,00 (с, 1H), 10,69 (с, 1H), 9,08 (д, J=2,0 Гц, 1H), 8,93 (д, J=2,0 Гц, 1H), 8,60 (дд, J=4,8, 1,3 Гц, 1H), 8,48-8,47 (м, 1H), 8,33-8,31 (м, 2H), 8,15-8,12 (м, 1H), 7,85-7,81 (м, 2H), 7,54-7,51 (м, 1H), 7,41-7,39 (м, 1H); ЭРИ-МС найдено для C18H13N5O m/z 316 (M+H).
[0414] Следующие соединения получали в соответствии с методикой, описанной выше в Примере 3.
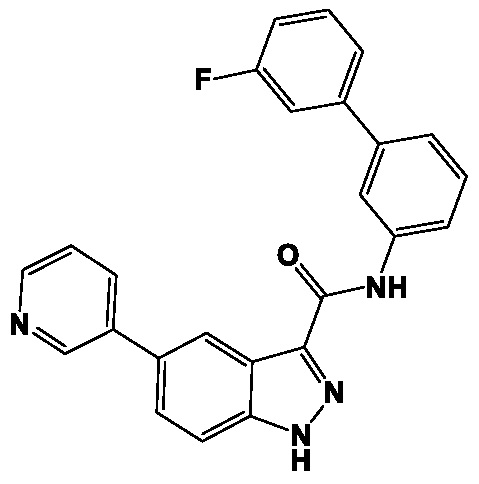
5
[0415] N-(3'-Фторбифенил-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 5.
[0416] Белое твердое вещество (77 мг, 0,19 ммоль, выход 69%). 1H-ЯМР (ДМСО-d6) δ м.д. 13,95 (с, 1H), 10,50 (с, 1H), 8,94 (д, J=2,3 Гц, 1H), 8,59 (дд, J=4,6, 1,5 Гц, 1H), 8,51 (д, J=1,0 Гц, 1H), 8,31-8,30 (м, 1H), 8,15-8,13 (м, 1H), 7,99-7,97 (м, 1H), 7,83-7,82 (м, 2H), 7,55-7,45 (м, 6H), 7,24-7,22 (м, 1H); ЭРИ-МС найдено для C25H17FN4O m/z 409 (M+H).
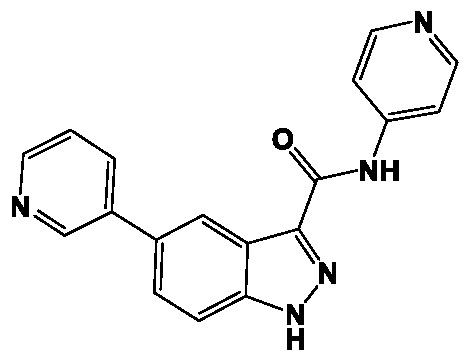
6
[0417] 5-(Пиридин-3-ил)-N-(пиридин-4-ил)-1H-индазол-3-карбоксамид 6.
[0418] Почти белое твердое вещество (52 мг, 0,16 ммоль, выход 77%). 1H-ЯМР (ДМСО-d6) δ м.д. 14,05 (шс, 1H), 10,83 (с, 1H), 8,94 (д, J=2,0 Гц, 1H), 8,60 (дд, J=4,6, 1,2 Гц, 1H), 8,48-8,47 (м, 3H), 8,15-8,13 (м, 1H), 7,94 (дд, J=5,0, 1,4 Гц, 2H), 7,86-7,82 (м, 2H), 7,54-7,52 (м, 1H); ЭРИ-МС найдено для C18H13N5O m/z 316 (M+H).
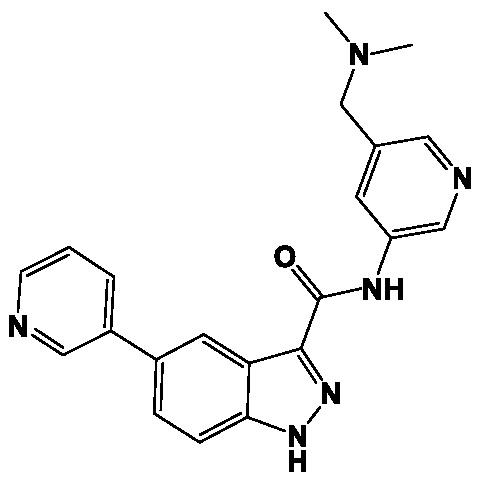
7
[0419] N-(5-((Диметиламино)метил)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 7.
[0420] Почти белое твердое вещество (37 мг, 0,10 ммоль, выход 47%). 1H-ЯМР (ДМСО-d6) δ м.д. 14,00 (с, 1H), 10,68 (с, 1H), 8,94 (д, J=2,0 Гц, 1H), 8,91 (д, J=2,3 Гц, 1H), 8,60 (дд, J=4,7, 1,2 Гц, 1H), 8,49-8,48 (м, 1H), 8,38-8,37 (м, 1H), 8,21 (д, J=2,2 Гц, 1H), 8,16-8,13 (м, 1H), 7,85-7,81 (м, 2H), 7,52 (дд, J=7,9, 4,9 Гц, 1H), 3,44 (с, 2H), 2,19 (с, 6H); ЭРИ-МС найдено для C21H20N6O m/z 373 (M+H).
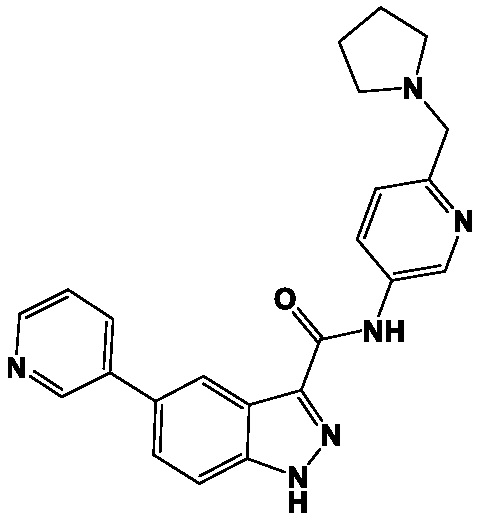
8
[0421] 5-(Пиридин-3-ил)-N-(6-(пирролидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 8.
[0422] Почти белое твердое вещество (38 мг, 0,10 ммоль, выход 77%). 1H-ЯМР (ДМСО-d6) δ м.д. 13,99 (шс, 1H), 10,64 (с, 1H), 8,96 (д, J=2,5 Гц, 1H), 8,93 (д, J=2,4 Гц, 1H), 8,59 (дд, J=4,8, 1,5 Гц, 1H), 8,48 (д, J=1,2 Гц, 1H), 8,27 (дд, J=8,5, 2,5 Гц, 1H), 8,16-8,12 (м, 1H), 7,84-7,80 (м, 2H), 7,54-7,51 (м, 1H), 7,41 (д, J=8,5 Гц, 1H), 2,37 (с, 2H), 2,50-2,47 (м, 4H), 1,72-1,70 (м, 4H); ЭРИ-МС найдено для C23H22N6O m/z 399 (M+H).
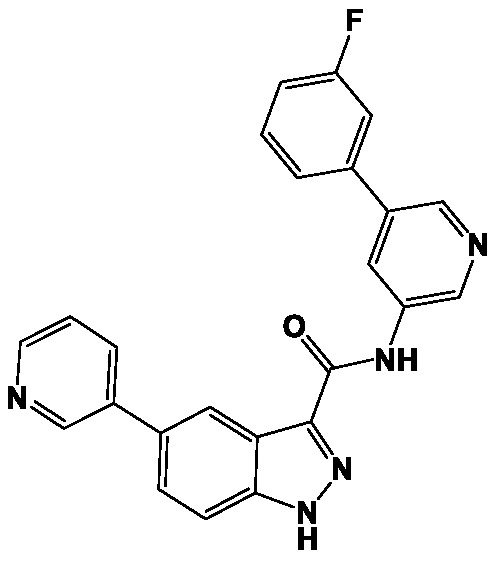
9
[0423] N-(5-(3-Фторфенил)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 9.
[0424] Белое твердое вещество (35 мг, 0,09 ммоль, выход 47%). 1H-ЯМР (ДМСО-d6) δ м.д. 14,05 (шс, 1H), 10,79 (с, 1H), 9,13 (д, J=2,0 Гц, 1H), 8,94 (д, J=1,9 Гц, 1H), 8,68-8,65 (м, 2H), 8,60 (дд, J=4,83, 4,83 Гц, 1H), 8,52-8,49 (м, 1H), 8,16-8,12 (м, 1H), 7,85-7,81 (м, 2H), 7,62-7,56 (м, 3H), 7,54-7,50 (м, 1H), 7,31-7,26 (м, 1H), ЭРИ-МС найдено для C24H16FN5O m/z 410,5 (M+H).
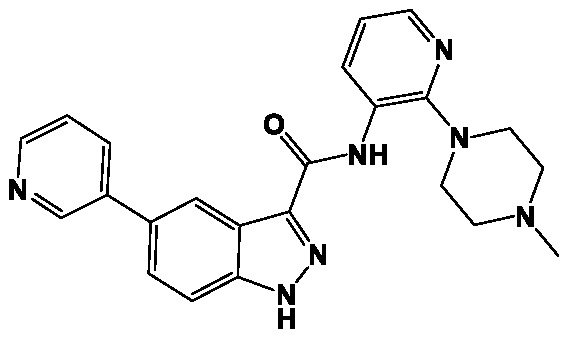
11
[0425] N-(2-(4-Метилпиперазин-1-ил)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 11.
[0426] Белое твердое вещество (11 мг, 0,03 ммоль, выход 65%). 1H-ЯМР (ДМСО-d6) δ м.д. 14,10 (с, 1H), 9,63 (с, 1H), 8,93 (д, J=2,1 Гц, 1H), 8,65-8,59 (м, 2H), 8,48 (с, 1H), 8,16-8,12 (м, 1H), 8,11-8,09 (м, 1H), 7,87-7,80 (м, 2H), 7,55-7,51 (м, 1H), 7,20-7,17 (м, 1H), 3,10-3,06 (м, 4H), 2,80-2,40 (м, 4H), 2,30 (с, 3H), ЭРИ-МС найдено для C23H23N7O m/z 414,0 (M+H).
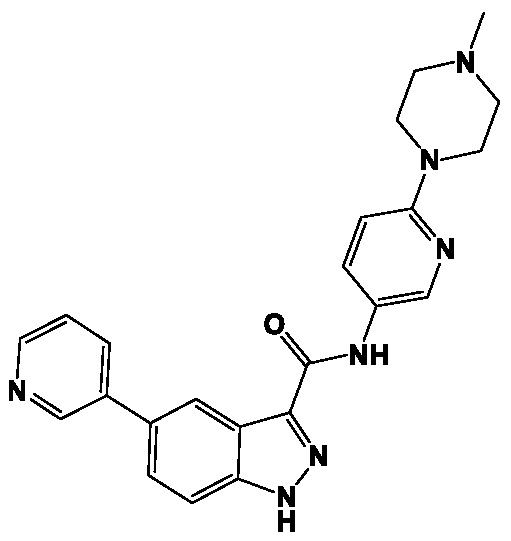
12
[0427] N-(6-(4-Метилпиперазин-1-ил)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 12.
[0428] Белое твердое вещество (31 мг, 0,07 ммоль, выход 39%). 1H-ЯМР (ДМСО-d6) δ м.д. 13,86 (шс, 1H), 10,33 (с, 1H), 8,92 (д, J=2,1 Гц, 1H), 8,60-8,58 (м, 2H), 8,46 (с, 1H), 8,14-8,11 (м, 1H), 8,10-8,02 (м, 1H), 7,83-7,78 (м, 2H), 7,54-7,50 (м, 1H), 6,86 (д, J=9,1 Гц, 1H), 3,45-3,42 (м, 4H), 2,42-2,39 (м, 4H), 2,21 (с, 3H), ЭРИ-МС найдено для C23H23N7O m/z 414,3 (M+H).
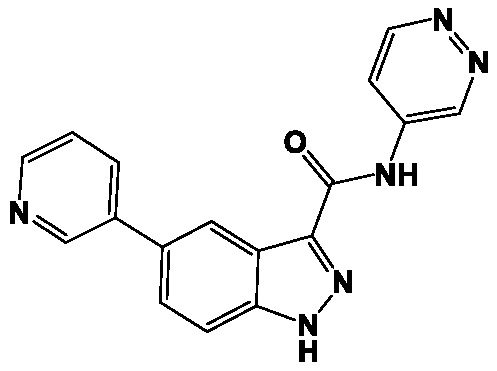
14
[0429] N-(Пиридазин-4-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 14.
[0430] Почти белое твердое вещество (50 мг, 0,16 ммоль, выход 99%). 1H-ЯМР (ДМСО-d6) δ м.д. 14,20-13,90 (шс, 1H), 11,15 (с, 1H), 9,71-9,70 (м, 1H), 9,09-9,08 (м, 1H), 8,94 (д, J=2,0 Гц, 1H), 8,61-8,60 (м, 1H), 8,47-8,46 (м, 1H), 8,25 (дд, J=5,9, 2,8 Гц, 1H), 8,16-8,13 (м, 1H), 7,86-7,85 (м, 2H), 7,53 (дд, J=7,8, 5,0 Гц, 1H); ЭРИ-МС найдено для C17H12N6O m/z 317 (M+H).
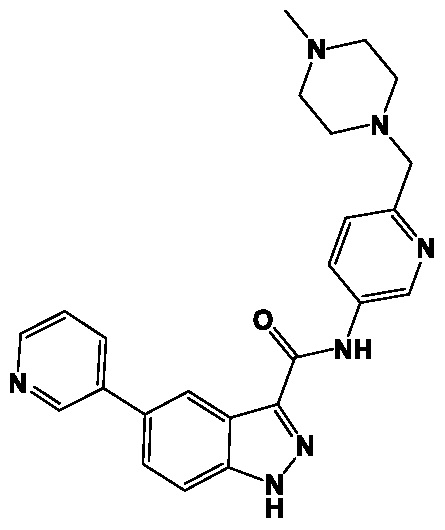
15
[0431] N-(6-((4-Метилпиперазин-1-ил)метил)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 15.
[0432] Белое твердое вещество (42 мг, 0,10 ммоль, выход 81%). 1H-ЯМР (ДМСО-d6) δ м.д. 13,97 (шс, 1H), 10,65 (с, 1H), 8,97 (д, J=2,4 Гц, 1H), 8,93 (д, J=2,1 Гц, 1H), 8,59 (дд, J=4,7, 1,5 Гц, 1H), 8,48-8,47 (м, 1H), 8,28 (дд, J=8,5, 2,5 Гц, 1H), 8,15-8,12 (м, 1H), 7,85-7,81 (м, 2H), 7,54-7,51 (м, 1H), 7,40 (д, J=8,5 Гц, 1H), 3,55 (с, 2H), 2,42-2,28 (м, 8H), 2,15 (с, 3); ЭРИ-МС найдено для C24H25N7O m/z 428 (M+H).
Пример 4
[0433] Получение 5-(5-фторпиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамида (13) представлено ниже на Схеме 30.
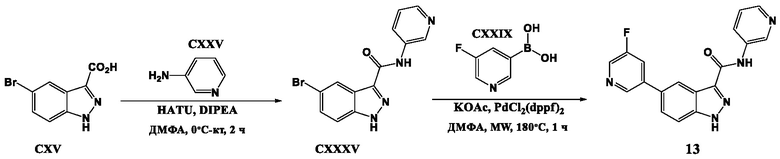
Схема 30
Стадия 1
[0434] К перемешиваемому раствору 3-аминопиридина (CXXV) (0,195 г, 2,07 ммоль) в ДМФА (10 мл) добавляли 5-бром-1H-индазол-3-карбоновую кислоту (CXV) (0,500 г, 2,07 ммоль) и N,N-диизопропилэтиламин (0,723 мл, 4,15 ммоль). Реакционную смесь охлаждали до 0°C и добавляли HATU (0,787 г, 2,07 ммоль). Реакционной смеси позволяли нагреться до комнатной температуры и перемешивали еще в течение 2 ч. Раствор выпаривали в вакууме. Остаток очищали с помощью колоночной хроматографии (1:99 MeOH [7Н NH3]:CHCl3 → 4:96 MeOH [7Н NH3]:CHCl3) с получением 5-бром-N-(пиридин-3-ил)-1H-индазол-3-карбоксамида (CXXXV) (0,200 г, 0,63 ммоль, выход 30%) в виде белого твердого вещества. ЭРИ-МС найдено для C13H9BrN4O m/z 318,0 (M+H).
Стадия 2
[0435] Во флакон для микроволнового синтеза добавляли 5-бром-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид (CXXXV) (0,200 г, 0,63 ммоль), 5-фторпиридин-3-бороновую кислоту (CXXIX) (0,098 г, 0,694 ммоль), тетракис(трифенилфосфин)палладий (0) (0,036 г, 0,032 ммоль), фосфат калия (0,201 г, 0,947 ммоль), воду (1 мл) и ДМФА (5 мл). Реакционный флакон закрывали, продували аргоном и нагревали при микроволновом облучении в течение 1 ч при 180°C. Раствор фильтровали через слой целита и выпаривали в вакууме. Неочищенный продукт очищали с помощью колоночной хроматографии (100% CHCl3 → 2:98 MeOH [7Н NH3]:CHCl3) с получением 5-(5-фторпиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамида (13) (4 мг, 0,01 ммоль, выход 2%) в виде белого твердого вещества. 1H-ЯМР (ДМСО-d6) δ м.д. 14,02 (шс, 1H), 10,70 (с, 1H), 9,08 (д, J=2,5 Гц, 1H), 8,83 (т, J=1,8 Гц, 1H), 8,60 (д, J=2,7 Гц, 1H), 8,53-8,52 (м, 1H), 8,34-8,29 (м, 2H), 8,14-8,09 (м, 1H), 7,89-7,81 (м, 2H), 7,42-7,38 (м, 1H), ЭРИ-МС найдено для C18H12FN5O m/z 334,0 (M+H).
Пример 5
[0436] Получение N-(пиридин-3-ил)-5-(5-(трифторметил)-пиридин-3-ил)-1H-индазол-3-карбоксамида (16) представлено ниже на Схеме 31.
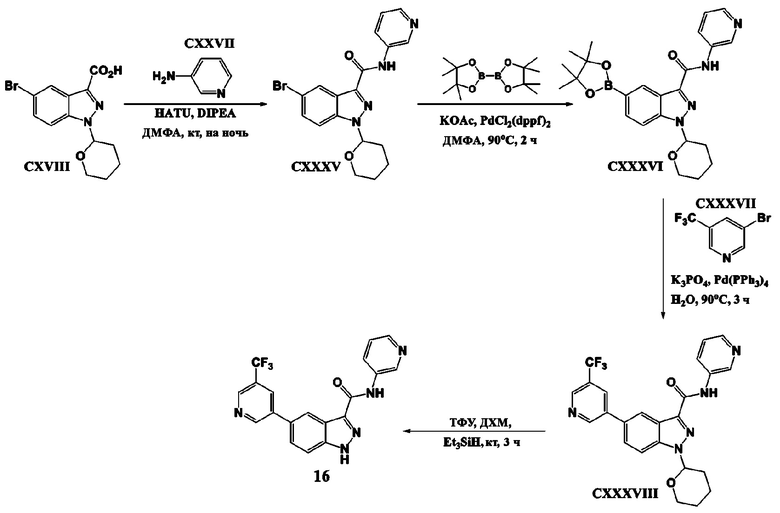
Схема 31
Стадия 1
[0437] Получение промежуточного 5-бром-N-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксамида (CXXXV) проводили согласно методике, представленной на Схеме 19 в Стадии 4. Светло-желтое твердое вещество (5,5 г, 13,7 ммоль, выход 88%). ЭРИ-МС найдено для C18H17BrN4O2 m/z 401,1 (M79Br+H) и 403,1 (M81Br+H).
Стадии 2-3
[0438] Получение промежуточного N-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-5-(5-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (CXXXVIII) проводили согласно методике, представленной на Схеме 26 в Стадиях 1-2. Коричневое твердое вещество (295 мг, 0,63 ммоль, выход 84%). ЭРИ-МС найдено для C24H20F3N5O2 m/z 468,1 (M+H).
Стадия 4
[0439] Получение N-(пиридин-3-ил)-5-(5-(трифторметил)-пиридин-3-ил)-1H-индазол-3-карбоксамида (16) проводили согласно методике, представленной на Схеме 28 в Стадии 4. Белое твердое вещество (95 мг, 0,25 ммоль, выход 39,3%). 1H-ЯМР (ДМСО-d6) δ м.д. 7,40 (дд, J=2,2 Гц, J=2 Гц, 1H), 7,84 (д, J=6,7 Гц, 1H), 7,93 (дд, J=1,5 Гц, J=7 Гц, 1H), 8,29-8,34 (м, 2H), 8,50 (с, 1H), 8,57 (с, 1H), 8,99 (с, 1H), 9,09 (д, J=2 Гц, 1H), 9,25 (д, J=1,6 Гц, 1H), 10,72 (шс, 1H); ЭРИ-МС найдено для C19H12F3N5O m/z 383,9 (M+H).
[0440] Следующие соединения получали в соответствии с методикой, описанной выше в Примере 5.
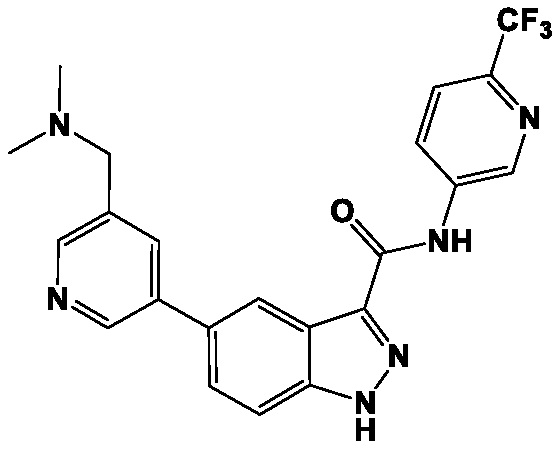
26
[0441] 5-(5-((Диметиламино)метил)пиридин-3-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 26.
[0442] Белое твердое вещество (93 мг, 0,21 ммоль, выход 78%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,24 (с, 6H), 3,57 (с, 2H), 7,86 (ABк, J=8 Гц, 2H), 7,93 (д, J=9 Гц, 1H), 8,04 (шс, 1H), 8,50 (д, J=7 Гц, 1H), 8,63 (дд, J=9 Гц, J=2 Гц, 1H), 8,85 (д, J=2 Гц, 1H), 9,27 (д, J=2 Гц, 1H), 11,11 (с, 1H), 14,11 (с, 1H); ЭРИ-МС найдено для C22H19F3N6O m/z 441,0 (M+H)
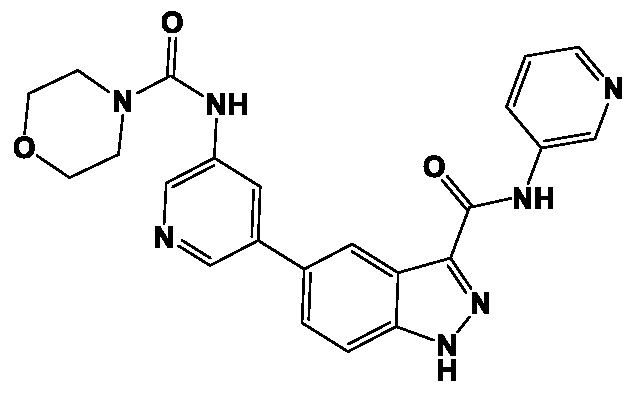
32
[0443] N-(5-(3-(Пиридин-3-илкарбамоил)-1H-индазол-5-ил)пиридин-3-ил)морфолин-4-карбоксамид 32.
[0444] Белое твердое вещество (132 мг, 0,30 ммоль, выход 56%). 1H-ЯМР (ДМСО-d6) δ м.д. 3,49 (т, J=5 Гц, 4H), 3,64 (т, J=5 Гц, 4H), 7,40 (дд, J=8 Гц, J=5 Гц, 1H), 7,82 (д, J=1 Гц, 1H), 8,26 (т, J=2 Гц, 1H), 8,30-8,34 (м, 2H), 8,47 (с, 1H), 8,54 (д, J=2 Гц, 1H), 8,72 (д, J=2 Гц, 1H), 8,87 (с, 1H), 9,09 (д, 2 Гц, 1H), 10,71 (с, 1H), 14,01 (с, 1H); ЭРИ-МС найдено для C23H21N7O3 m/z 444,3 (M+H).
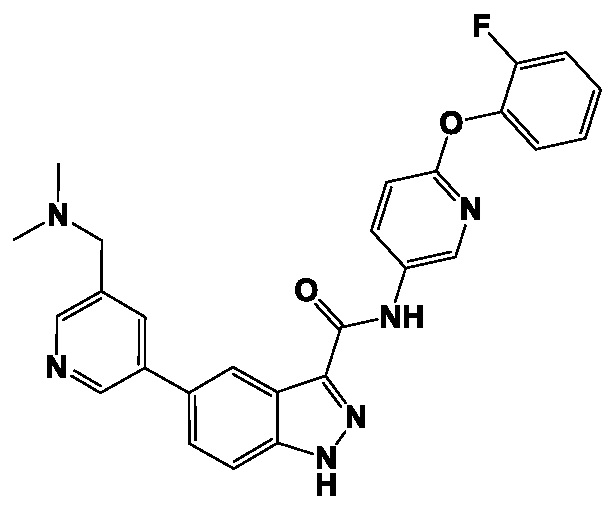
36
[0445] 5-(5-((Диметиламино)метил)пиридин-3-ил)-N-(6-(2-фторфенокси)пиридин-3-ил)-1H-индазол-3-карбоксамид 36.
[0446] Белое твердое вещество (137 мг, 0,28 ммоль, выход 53%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,20 (с, 6H), 3,53 (с, 2H), 7,16 (д, J=9 Гц, 1H), 7,22-7,40 (м, 4H), 7,82 (д/Abк, J=9 Гц, J=1 Гц, 2H), 8,00 (т, J=2 Гц, 1H), 8,38 (дд, J=9 Гц, J=3 Гц, 1H), 8,47 (с, 1H), 8,49 (д, J=2 Гц, 1H), 8,55 (д, J=3 Гц, 1H), 8,83 (д, J=2 Гц, 1H), 10,67 (с, 1H), 13,97 (шс, 1H); ЭРИ-МС найдено для C27H23FN6O2 m/z 383,1 (M+H).
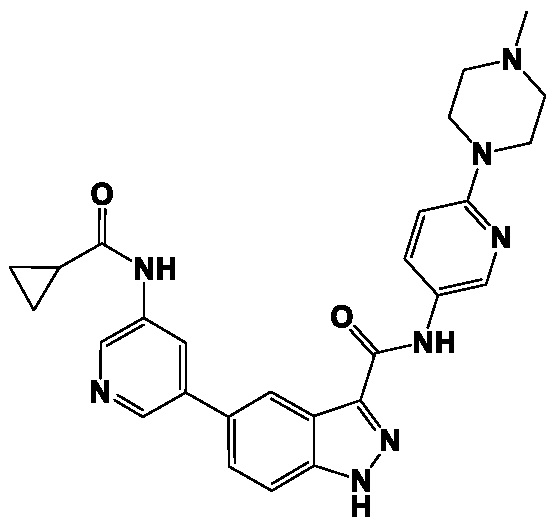
38
[0447] 5-(5-(Циклопропанкарбоксамидо)пиридин-3-ил)-N-(6-(4-метилпиперазин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 38.
[0448] Белое твердое вещество (39 мг, 0,08 ммоль, выход 61%). 1H-ЯМР (ДМСО-d6) δ м.д. 0,83-0,90 (м, 4H), 1,80-1,86 (м, 1H), 2,25 (шс, 3H), 2,45 (шс, 4H), 3,45 (шс, 4H), 6,86 (д, J=9 Гц, 1H), 7,79 (д, J=1 Гц, 1H), 8,04 (дд, J=9 Гц, J=3 Гц, 1H), 8,42 (т, J=2 Гц, 1H), 8,46 (с, 1H), 8,60 (дд, J=10 Гц, J=3 Гц, 2H), 8,76 (д, J=2 Гц, 1H), 10,34 (с, 1H), 10,56 (с, 1H), 13,90 (с, 1H); ЭРИ-МС найдено для C27H27N8O2 m/z 497,4 (M+H).
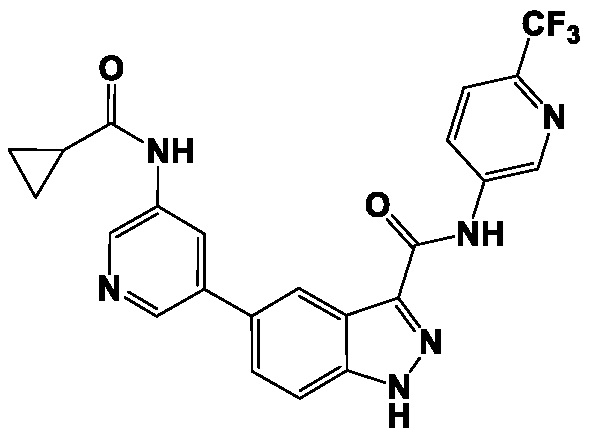
39
[0449] 5-(5-(Циклопропанкарбоксамидо)пиридин-3-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 39.
[0450] Белое твердое вещество (128 мг, 0,27 ммоль, выход 45%). 1H-ЯМР (ДМСО-d6) δ м.д. 0,82-0,90 (м, 4H), 1,80-1,86 (м, 1H), 7,84 (с, 2H), 7,92 (д, J=9 Гц, 1H), 8,43 (д, J=2 Гц, 1H), 8,48 (с, 1H), 8,61-8,65 (м, 2H), 8,77 (д, J=2 Гц, 1H), 9,27 (д, J=2 Гц, 1H), 10,57 (с, 1H), 11,11 (с, 1H), 14,11 (с, 1H); ЭРИ-МС найдено для C23H17F3N6O2 m/z 467,1 (M+H).
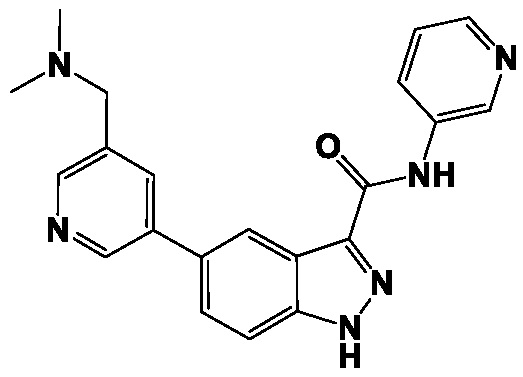
40
[0451] 5-(5-((Диметиламино)метил)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 40.
[0452] Белое твердое вещество (312 мг, 0,84 ммоль, выход 77%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,21 (с, 6H), 3,53 (с, 2H), 7,40 (дд, J=8 Гц, J=5 Гц, 1H), 7,83 (д/Abк, J=9 Гц, J=2 Гц, 2H), 8,01 (т, J=2 Гц, 1H), 8,29-8,34 (м, 2H), 8,48 (дд, J=4 Гц, J=1 Гц, 1H), 8,83 (д, J=2 Гц, 1H), 9,08 (д, J=3 Гц, 1H), 10,70 (с, 1H), 13,99 (шс, 1H); ЭРИ-МС найдено для C21H20N6O m/z 373,0 (M+H).
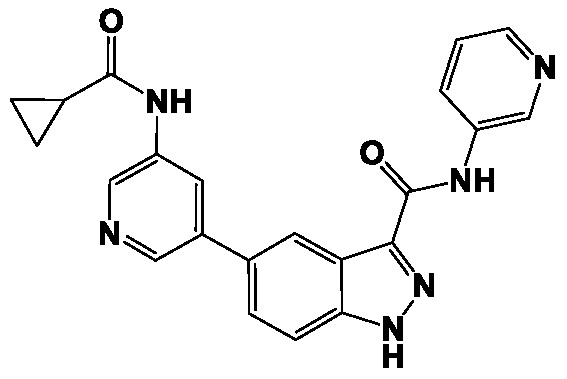
41
[0453] 5-(5-(Циклопропанкарбоксамидо)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 41.
[0454] Белое твердое вещество (148 мг, 0,37 ммоль, выход 71%). 1H-ЯМР (ДМСО-d6) δ м.д. 0,83-0,90 (м, 4H), 1,80-1,87 (м, 1H), 7,40 (дд, J=8 Гц, J=5 Гц, 1H), 7,82 (д, J=1 Гц, 1H), 8,29-8,34 (м, 2H), 8,43 (т, J=2 Гц, 1H), 8,47 (с, 1H), 8,62 (д, J=2 Гц, 1H), 8,76 (д, J=2 Гц, 1H), 9,08 (д, J=2 Гц, 1H), 10,57 (с, 1H), 10,70 (с, 1H), 14,01 (с, 1H); ЭРИ-МС найдено для C22H18N6O2 m/z 399,0 (M+H).
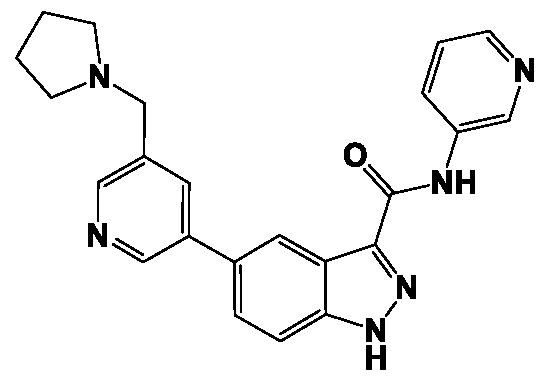
43
[0455] N-(Пиридин-3-ил)-5-(5-(пирролидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 43.
[0456] Белое твердое вещество (157 мг, 0,39 ммоль, выход 76%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,70-1,74 (м, 4H), 2,46-2,52 (м, 4H), 3,71 (с, 2H), 7,40 (дд, J=8 Гц, J=5 Гц, 1H), 7,83 (д/Abк, J=9 Гц, J=2 Гц, 2H), 8,02 (т, J=2 Гц, 1H), 8,29-8,34 (м, 2H), 8,48 (с, 1H), 8,51 (д, J=2 Гц, 1H), 8,82 (д, J=2 Гц, 1H), 9,08 (д, J=2 Гц, 1H), 10,70 (с, 1H), 14,00 (с, 1H); ЭРИ-МС найдено для C23H22N6O m/z 399,0 (M+H).
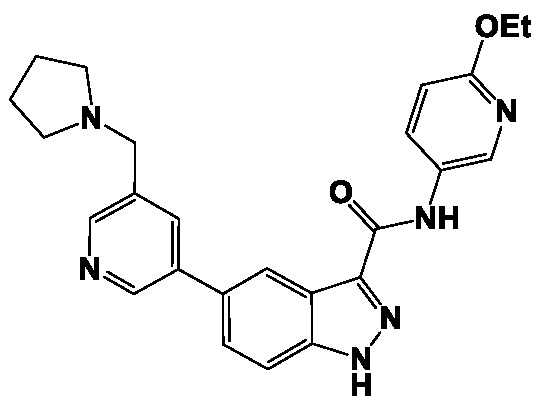
44
[0457] N-(6-Этоксипиридин-3-ил)-5-(5-(пирролидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 44.
[0458] Белое твердое вещество (62 мг, 0,14 ммоль, выход 39%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,32 (т, J=7 Гц, 3H), 1,70-1,74 (м, 4H), 2,47-2,52 (м, 4H), 3,71 (с, 2H), 4,29 (к, J=7 Гц, 2H), 6,81 (д, J=9 Гц, 1H), 7,82 (д/Abк, J=9 Гц, J=2 Гц, 2H), 8,01 (т, J=2 Гц, 1H), 8,16 (дд, J=9 Гц, J=3 Гц, 1H), 8,46 (с, 1H), 8,51 (д, J=2 Гц, 1H), 8,63 (д, J=2 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 10,51 (с, 1H), 13,94 (шс, 1H); ЭРИ-МС найдено для C25H26N6O2 m/z 443,4 (M+H).
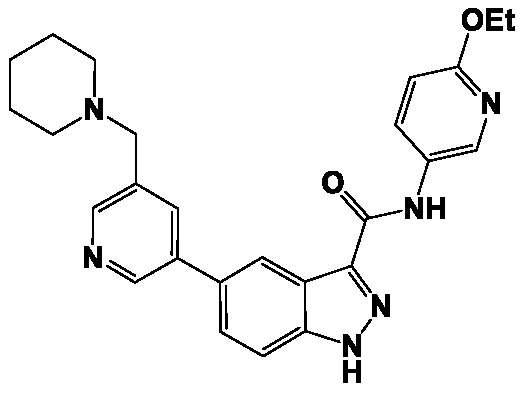
45
[0459] N-(6-Этоксипиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 45.
[0460] Белое твердое вещество (98 мг, 0,21 ммоль, выход 44%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,32 (т, J=7 Гц, 3H), 1,34-1,42 (м, 2H), 1,47-1,53 (м, 4H), 2,38 (шс, 4H), 3,56 (с, 2H), 4,29 (к, J=7 Гц, 2H), 6,81 (д, J=9 Гц, 1H), 7,81 (д/Abк, J=9 Гц, J=2 Гц, 2H), 7,99 (т, J=2 Гц, 1H), 8,16 (дд, J=9 Гц, J=3 Гц, 1H), 8,46 (д, J=1 Гц, 1H), 8,49 (д, J=2 Гц, 1H), 8,63 (д, J=2 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 10,51 (с, 1H), 13,92 (шс, 1H); ЭРИ-МС найдено для C26H28N6O2 m/z 457,3 (M+H).
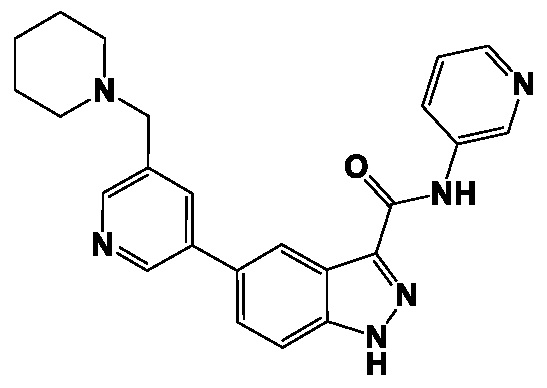
46
[0461] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 46.
[0462] Белое твердое вещество (126 мг, 0,31 ммоль, выход 52%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,42 (м, 2H), 1,48-1,55 (м, 4H), 2,39 (шс, 4H), 3,57 (с, 2H), 7,40 (дд, J=8 Гц, J=5 Гц, 1H), 7,83 (д/Abк, J=9 Гц, J=2 Гц, 2H), 7,99 (т, J=2 Гц, 1H), 8,30-8,34 (м, 2H), 8,48 (д, J=1 Гц, 1H), 8,49 (д, J=2 Гц, 1H), 8,82 (д, J=2 Гц, 1H), 9,08 (д, J=2 Гц, 1H), 10,70 (с, 1H), 14,00 (шс, 1H); ЭРИ-МС найдено для C24H24N6O m/z 413,0 (M+H).
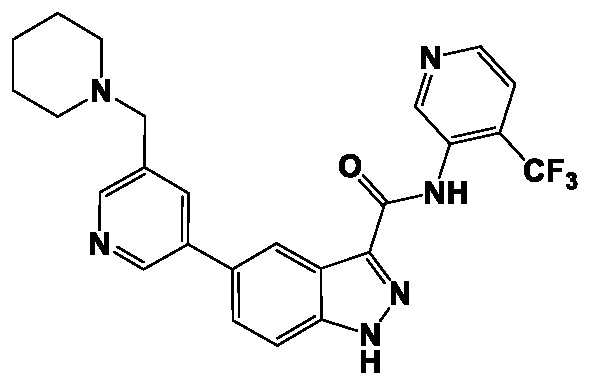
47
[0463] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(4-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 47.
[0464] Белое твердое вещество (150 мг, 0,31 ммоль, выход 71%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,34-1,42 (м, 2H), 1,46-1,53 (м, 4H), 2,37 (шс, 4H), 3,55 (с, 2H), 7,81-7,87 (м, 3H), 7,98 (с, 1H), 8,41 (с, 1H), 8,48 (д, J=2 Гц, 1H), 8,75 (д, J=5 Гц, 1H), 8,80 (д, J=2 Гц, 1H), 9,07 (с, 1H), 10,22 (с, 1H), 14,06 (шс, 1H); ЭРИ-МС найдено для C25H23F3N6O m/z 481,0 (M+H).
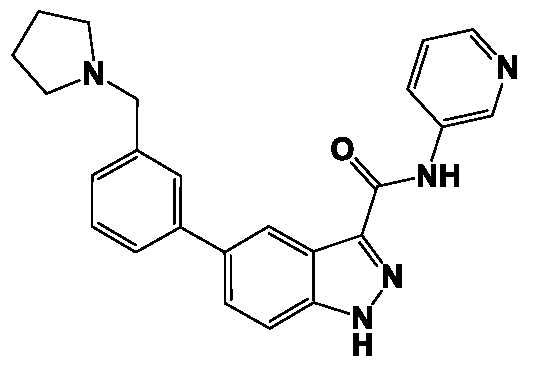
49
[0465] N-(Пиридин-3-ил)-5-(3-(пирролидин-1-илметил)фенил)-1H-индазол-3-карбоксамид 49.
[0466] Коричневое аморфное твердое вещество (53,4 мг, 0,13 ммоль, выход 72%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,70-1,71 (м, 4H), 2,47-2,49 (м, 4H), 3,67 (с, 2H), 7,31 (д, J=8 Гц, 1H), 7,40 (дд, J=8 Гц, J=5 Гц, 1H), 7,44 (т, J=8 Гц, 1H), 7,58-7,60 (м, 1H), 7,63-7,64 (м, 1H), 7,76-7,78 (м, 2H), 8,30-8,34 (м, 2H), 8,44 (с, 1H), 9,08 (д, J=2 Гц, 1H), 10,68 (с, 1H), 13,93 (с, 1H); ЭРИ-МС найдено для C24H23N5O m/z 398 (M+H).
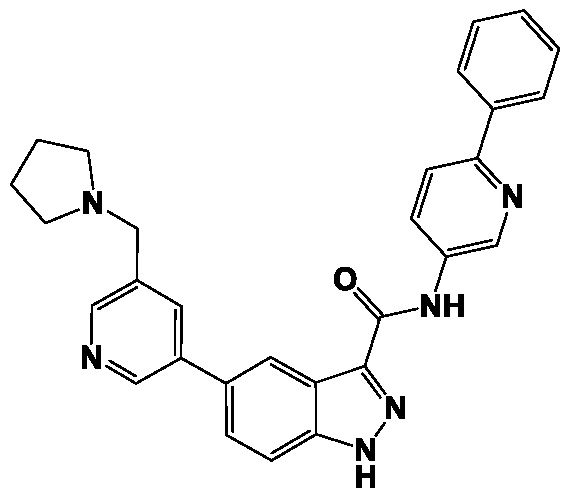
50
[0467] N-(6-Фенилпиридин-3-ил)-5-(5-(пирролидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 50.
[0468] Коричневое хлопьевидное твердое вещество (61,3 мг, 0,13 ммоль, выход 74%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,71-1,72 (м, 4H), 3,72 (с, 2H), 7,39-7,42 (м, 1H), 7,47-7,50 (м, 2H), 7,81-7,86 (м, 2H), 8,00 (д, J=9 Гц, 1H), 8,02-8,03 (м, 1H), 8,08-8,10 (м, 2H), 8,45 (дд, J=9 Гц, J=3 Гц, 1H), 8,49-8,50 (м, 1H), 8,51 (д, J=2 Гц, 1H), 8,83 (д, J=2 Гц, 1H), 9,18 (д, J=3 Гц, 1H), 10,81 (с, 1H), 14,03 (с, 1H); ЭРИ-МС найдено для C29H26N6O m/z 475 (M+H).
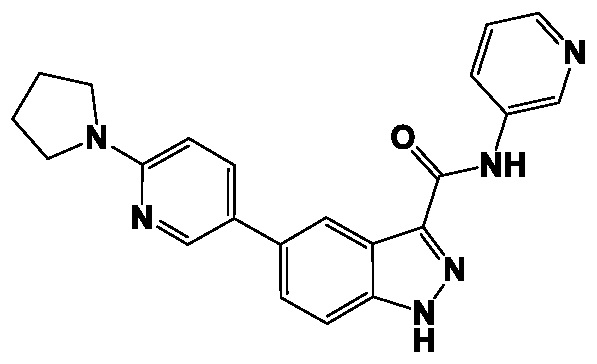
51
[0469] N-(Пиридин-3-ил)-5-(6-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 51.
[0470] Желтое твердое вещество (32 мг, 0,08 ммоль, выход 37,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,94-2,01 (м, 4H), 3,42-3,48 (м, 4H), 6,57 (д, J=9 Гц, 1H), 7,40 (дд, J=8 Гц, J=5 Гц, 1H), 7,72 (д, J=1 Гц, 2H), 7,85 (дд, J=9 Гц, J=3 Гц, 1H), 8,29-8,34 (м, 3H), 8,43 (д, J=2 Гц, 1H), 9,08 (д, J=2 Гц, 1H), 10,63 (с, 1H), 13,87 (с, 1H); ЭРИ-МС найдено для C22H20N6O m/z 385,0 (M+H).
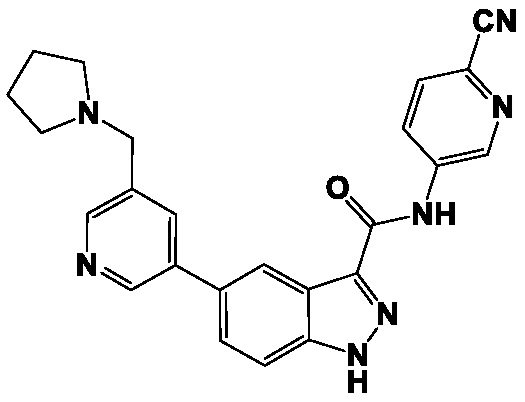
52
[0471] N-(6-Цианопиридин-3-ил)-5-(5-(пирролидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 52.
[0472] Бежевое твердое вещество (52 мг, 0,12 ммоль, выход 49,1%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,70-1,75 (м, 4H), 3,31-3,36 (м, 4H), 7,85 (дк, J=9 Гц, J=2 Гц, 2H), 8,02 (с, 1H), 8,05 (д, J=9 Гц, 1H), 8,47 (с, 1H), 8,52 (д, J=2 Гц, 1H), 8,58 (дд, J=9 Гц, J=3 Гц, 1H), 8,82 (д, J=2 Гц, 1H), 9,28 (д, J=2 Гц, 1H), 11,18 (с, 1H), 14,13 (шс, 1H); ЭРИ-МС найдено для C24H21N7O m/z 424,3 (M+H).
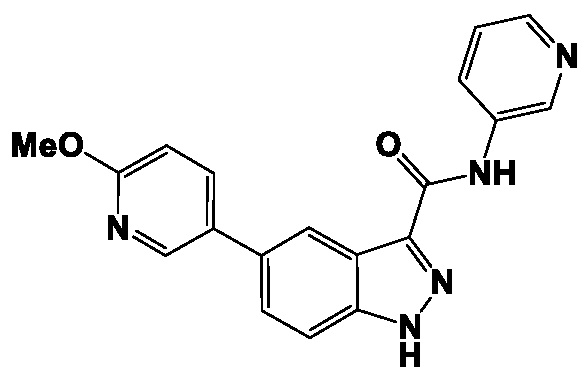
54
[0473] 5-(6-Метоксипиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 54.
[0474] Белое твердое вещество (79,7 мг, 0,23 ммоль, выход 44,2%). 1H-ЯМР (ДМСО-d6) δ м.д. 3,91 (с, 3H), 6,95 (д, J=9 Гц, 1H), 7,40 (дд, J=9 Гц, J=5 Гц, 1H), 7,78 (дд, J=11 Гц, J=2 Гц, 2H), 8,06 (дд, J=9 Гц, J=3 Гц, 1H), 8,29-8,34 (м, 2H), 8,39 (с, 1H), 8,51 (д, J=2 Гц, 1H), 9,08 (д, J=3 Гц, 1H), 10,67 (с, 1H), 13,91 (шс, 1H); ЭРИ-МС найдено для C19H15N5O2 m/z 346,0 (M+H).
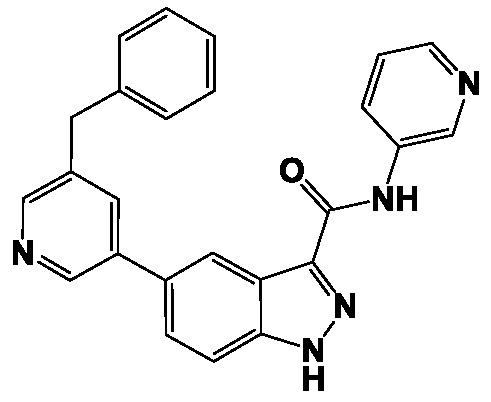
55
[0475] 5-(5-Бензилпиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 55.
[0476] Желтое твердое вещество (101,9 мг, 0,25 ммоль, выход 76%). 1H-ЯМР (ДМСО-d6) δ м.д. 4,09 (с, 2H), 7,19-7,23 (м, 1H), 7,30-7,35 (м, 4H), 7,39-7,41 (м, 1H), 7,78-7,82 (м, 2H), 7,99 (т, J=2 Гц, 1H), 8,31-8,33 (м, 2H), 8,45 (с, 1H), 8,51 (д, J=2 Гц, 1H), 8,76 (д, J=2 Гц, 1H), 9,08 (д, J=2 Гц, 1H), 10,69 (с, 1H), 14,00 (с, 1H); ЭРИ-МС найдено для C25H19N5O m/z 406 (M+H).
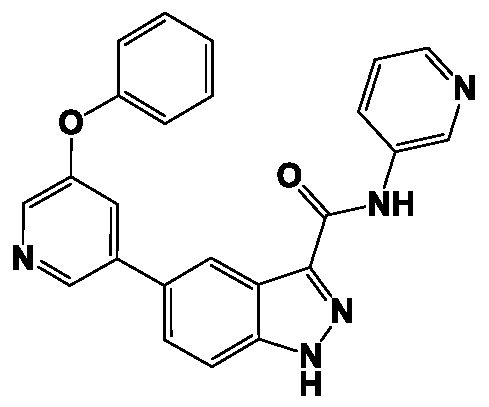
56
[0477] 5-(5-Феноксипиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 56.
[0478] Белое твердое вещество (73,6 мг, 0,18 ммоль, выход 75%). 1H-ЯМР (ДМСО-d6) δ м.д. 7,17-7,18 (м, 2H), 7,22-7,23 (м, 1H), 7,38-7,41 (м, 1H), 7,44-7,47 (м, 2H), 7,72-7,73 (м, 1H), 7,80-7,81 (м, 2H), 8,29-8,31 (м, 2H), 8,37-8,38 (м, 1H), 8,44-8,45 (м, 1H), 8,74 (д, J=2 Гц, 1H), 9,06 (д, J=2 Гц, 1H), 10,69 (с, 1H), 14,00 (с, 1H); ЭРИ-МС найдено для C24H17N5O2 m/z 408 (M+H).
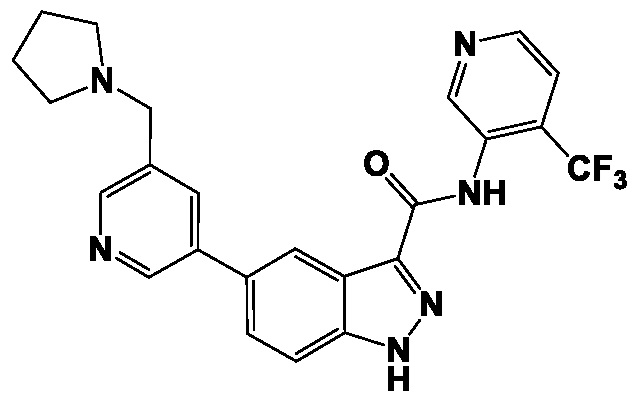
57
[0479] 5-(5-(Пирролидин-1-илметил)пиридин-3-ил)-N-(4-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 57.
[0480] Белое твердое вещество (64 мг, 0,14 ммоль, выход 35,2%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,67-1,74 (м, 4H), 2,44-2,52 (м, 4H), 3,70 (с, 2H), 7,81-7,88 (м, 3H), 8,00 (д, J=2 Гц, 1H), 8,41 (с, 1H), 8,50 (д, J=2 Гц, 1H), 8,75 (д, J=5 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 9,07 (с, 1H), 10,22 (с, 1H), 14,01 (шс, 1H); ЭРИ-МС найдено для C24H21F3N6O m/z 467,3 (M+H).
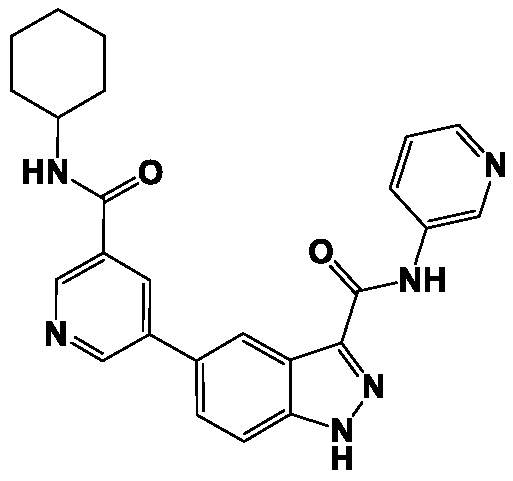
59
[0481] 5-(5-(Циклогексилкарбамоил)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 59.
[0482] Светло-коричневое твердое вещество (117 мг, 0,27 ммоль, выход 49,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,10-1,21 (м, 1H), 1,28-1,39 (м, 4H), 1,63 (д, J=12 Гц, 1H), 1,72-1,78 (м, 2H), 1,86-1,91 (м, 2H), 3,77-3,87 (м, 1H), 7,41 (дд, J=8 Гц, J=5 Гц, 1H), 7,84 (д, J=8 Гц, 1H), 7,91 (д, J=9 Гц, 1H), 8,30-8,36 (м, 2H), 8,48 (т, J=2 Гц, 1H), 8,55 (с, 1H), 8,59 (д, J=8 Гц, 1H), 8,99 (д, J=2 Гц, 1H), 9,04 (д, J=2 Гц, 1H), 9,09 (д, J=2 Гц, 1H), 10,72 (с, 1H), 14,04 (с, 1H); ЭРИ-МС найдено для C25H24N6O2 m/z 441,0 (M+H).
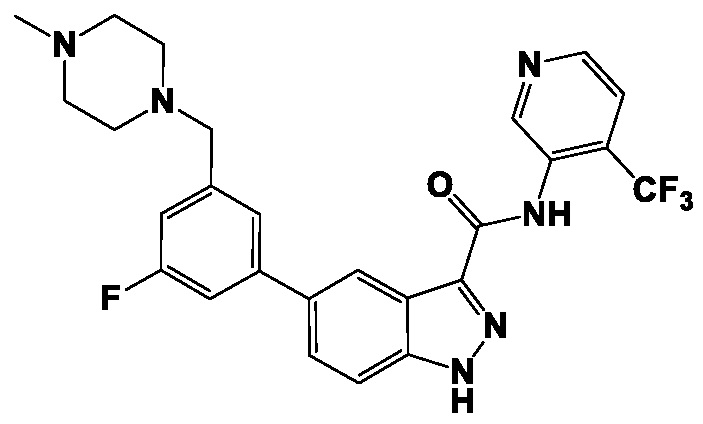
60
[0483] 5-(3-Фтор-5-((4-метилпиперазин-1-ил)метил)фенил)-N-(4-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 60.
[0484] Белое твердое вещество (43 мг, 0,08 ммоль, выход 76,3%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,23 (с, 3H), 2,22-2,50 (м, 8H), 3,56 (с, 2H), 7,12 (д, J=9 Гц, 1H), 7,42 (дд, J=8 Гц, J=2 Гц, 1H), 7,47 (с, 1H), 7,80 (д, J=1 Гц, 2H), 7,85 (д, J=5 Гц, 1H), 8,39 (с, 1H), 8,75 (д, J=5 Гц, 1H), 9,08 (с, 1H), 10,22 (с, 1H), 14,02 (шс, 1H); ЭРИ-МС найдено для C26H24F4N6O m/z 513,3 (M+H).
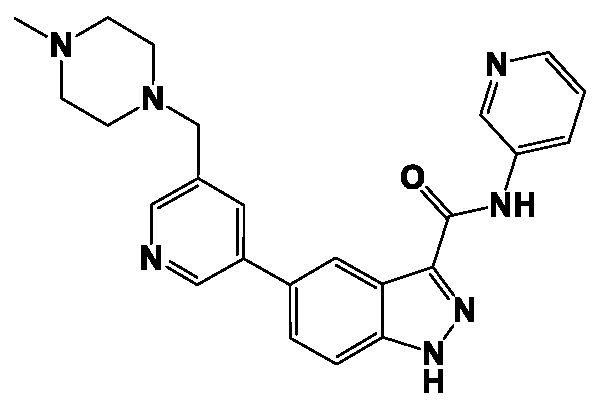
61
[0485] 5-(5-((4-метилпиперазин-1-ил)метил)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 61.
[0486] Белое твердое вещество (81,6 мг, 0,19 ммоль, выход 55%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,14 (с, 3H), 2,33-2,42 (м, 8H), 3,60 (с, 2H), 7,39-7,41 (м, 1H), 7,81-7,85 (м, 2H), 8,00-8,01 (м, 1H), 8,31-8,33 (м, 2H), 8,47-8,48 (м, 1H), 8,49 (д, J=2 Гц, 1H), 8,82 (д, J=2 Гц, 1H), 9,08 (д, J=3 Гц, 1H), 10,74 (с, 1H), 14,00 (с, 1H); ЭРИ-МС найдено для C24H25N7O m/z 427,8 (M+H).
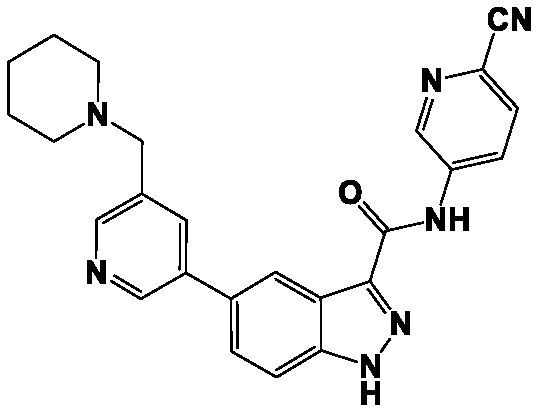
62
[0487] N-(6-Цианопиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 62.
[0488] Почти белое твердое вещество (42 мг, 0,10 ммоль, выход 36,9%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,42 (м, 2H), 1,47-1,54 (м, 4H), 2,38 (шс, 4H), 3,57 (с, 2H), 7,85 (д, J=1 Гц, 2H), 8,00 (т, J=2 Гц, 1H), 8,05 (д, J=9 Гц, 1H), 8,47 (д, J=1 Гц, 1H), 8,50 (д, J=2 Гц, 1H), 8,58 (дд, J=9 Гц, J=3 Гц, 1H), 8,82 (д, J=2 Гц, 1H), 9,28 (д, J=2 Гц, 1H), 11,18 (с, 1H), 14,12 (шс, 1H); ЭРИ-МС найдено для C25H23N7O m/z 438,1 (M+H).
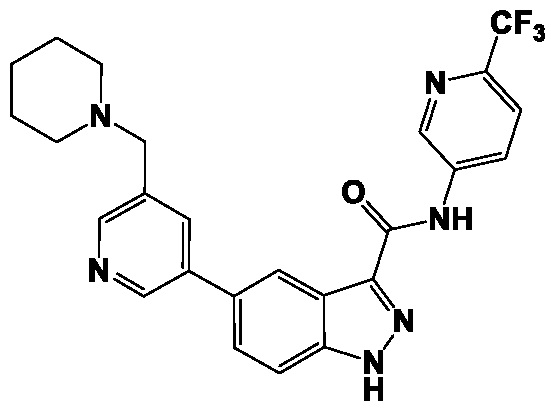
63
[0489] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(6-(трифторметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 63.
[0490] Белое твердое вещество (78 мг, 0,16 ммоль, выход 49%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,35-1,44 (м, 2H), 1,46-1,57 (м, 4H), 2,40 (шс, 4H), 3,59 (шс, 2H), 7,85 (с, 2H), 7,93 (д, J=9 Гц, 1H), 8,01 (с, 1H), 8,48 (с, 1H), 8,50 (с, 1H), 8,63 (д, J=8 Гц, 1H), 8,83 (с, 1H), 9,27 (с, 1H), 11,11 (с, 1H), 14,11 (шс, 1H); ЭРИ-МС найдено для C25H23F3N6O m/z 481,1 (M+H).
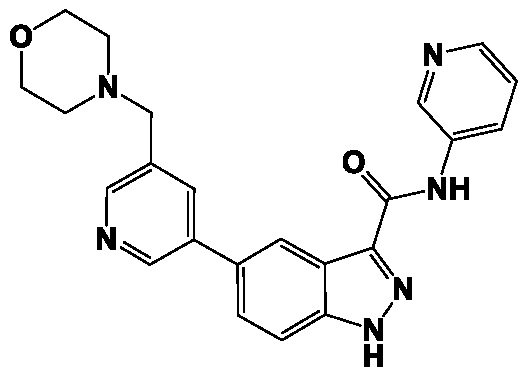
64
[0491] 5-(5-(Морфолинометил)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 64.
[0492] Белое твердое вещество (77 мг, 0,19 ммоль, выход 66%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,41-2,43 (м, 4H), 3,58-3,60 (м, 4H), 3,61 (с, 2H), 7,39-7,41 (м, 1H), 7,81-7,85 (м, 2H), 8,02-8,03 (м, 1H), 8,31-8,33 (м, 2H), 8,47-8,48 (м, 1H), 8,51 (д, J=2 Гц, 1H), 8,83 (д, J=2 Гц, 1H), 9,08 (д, J=2 Гц, 1H), 10,70 (с, 1H), 14,00 (с, 1H); ЭРИ-МС найдено для C23H22N6O2 m/z 415 (M+H).
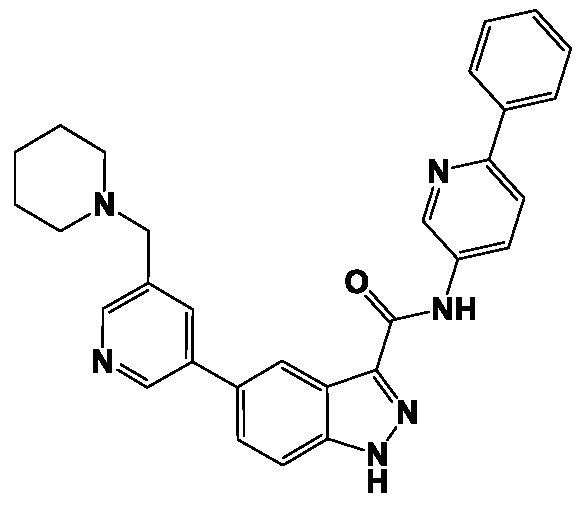
65
[0493] N-(6-Фенилпиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 65.
[0494] Белое твердое вещество (61,5 мг, 0,13 ммоль, выход 68%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39-1,40 (м, 2H), 1,49-1,53 (м, 4H), 2,38-2,39 (м, 4H), 3,57 (с, 2H), 7,39-7,43 (м, 1H), 7,47-7,50 (м, 2H), 7,82-7,86 (м, 2H), 7,99-8,01 (м, 2H), 8,08-8,10 (м, 2H), 8,44 (дд, J=9 Гц, J=3 Гц, 1H), 8,50-8,51 (м, 2H), 8,83 (д, J=2 Гц, 1H), 9,18 (д, J=3 Гц, 1H), 10,81 (с, 1H), 14,02 (с, 1H); ЭРИ-МС найдено для C30H28N6O m/z 489 (M+H).
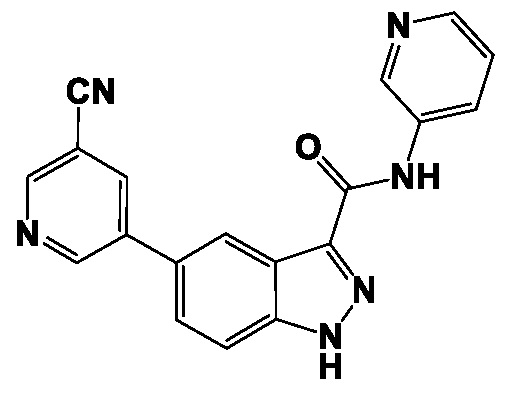
66
[0495] 5-(5-Цианопиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 66.
[0496] Бежевое твердое вещество (107 мг, 0,31 ммоль, выход 66,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 7,40 (дд, J=8 Гц, J=4 Гц, 1H), 7,84 (д, J=8 Гц, 1H), 7,91 (дд, J=9 Гц, J=2 Гц, 1H), 8,30-8,34 (м, 2H), 8,57 (с, 1H), 8,72 (т, J=2 Гц, 1H), 9,03 (д, J=2 Гц, 1H), 9,09 (д, J=2 Гц, 1H), 9,23 (д, J=2 Гц, 1H), 10,72 (с, 1H), 14,06 (с, 1H); ЭРИ-МС найдено для C19H12N6O m/z 340,8 (M+H).
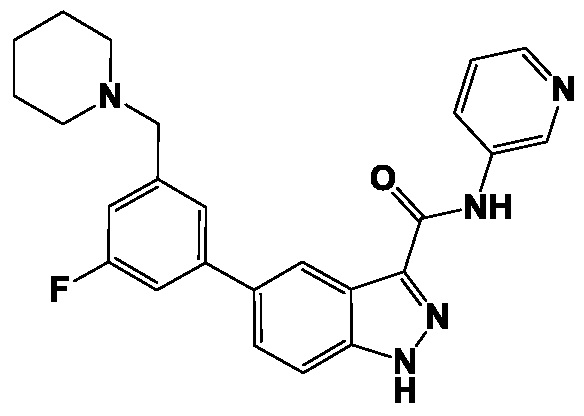
67
[0497] 5-(3-Фтор-5-(пиперидин-1-илметил)фенил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 67.
[0498] Желтое твердое вещество (84 мг, 0,20 ммоль, выход 66%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,37-1,39 (м, 2H), 1,49-1,54 (м, 4H), 2,37-2,38 (м, 4H), 3,54 (с, 2H), 7,12-7,13 (м, 1H), 7,39-7,43 (м, 2H), 7,47-7,48 (м, 1H), 7,77-7,81 (м, 2H), 8,31-8,33 (м, 2H), 8,44-8,45 (м, 1H), 9,08 (д, J=2 Гц, 1H), 10,69 (с, 1H), 13,97 (с, 1H); ЭРИ-МС найдено для C25H24FN5O m/z 430 (M+H).
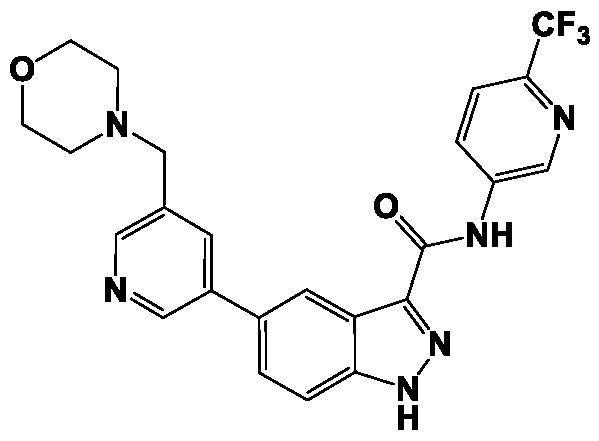
68
[0499] 5-(5-(Морфолинометил)пиридин-3-ил)-N-(6-(трифтор-метил)пиридин-3-ил)-1H-индазол-3-карбоксамид 68.
[0500] Белое твердое вещество (72 мг, 0,15 ммоль, выход 30,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,43 (шс, 4H), 3,56-3,63 (м, 4H), 3,62 (с, 2H), 7,85 (ABк, J=9 Гц, 2H), 7,93 (д, J=9 Гц, 1H), 8,04 (с, 1H), 8,49 (с, 1H), 8,52 (д, J=1 Гц, 1H), 8,63 (дд, J=9 Гц, J=3 Гц, 1H), 8,84 (д, J=2 Гц, 1H), 9,27 (д, J=2 Гц, 1H), 11,11 (с, 1H), 14,11 (шс, 1H); ЭРИ-МС найдено для C24H21F3N6O2 m/z 483,3 (M+H).
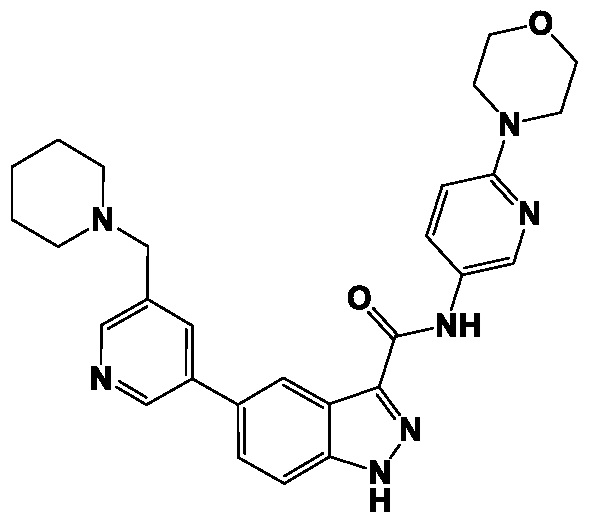
69
[0501] N-(6-Морфолинопиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 69.
[0502] Светло-желтое твердое вещество (58 мг, 0,12 ммоль, выход 36,4%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,37-1,44 (м, 2H), 1,51 (квин, J=5 Гц, 4H), 2,33-2,40 (м, 4H), 3,40 (т, J=5 Гц, 4H), 3,56 (с, 2H), 3,71 (т, 5 Гц, 4-х), 6,89 (д, J=9 Гц, 1H), 7,78 (д, J=8 Гц, 1H), 7,81 (д, J=9 Гц, 1H), 7,97 (т, J=2 Гц, 1H), 8,06 (дд, J=9 Гц, J=2 Гц, 1H), 8,46 (д, J=10 Гц, 1H), 8,60 (д, J=2 Гц, 1H), 8,79 (д, J=2 Гц, 1H), 10,35 (с, 1H), 13,90 (шс, 1H); ЭРИ-МС найдено для C28H31N7O2 m/z 498,0 (M+H).
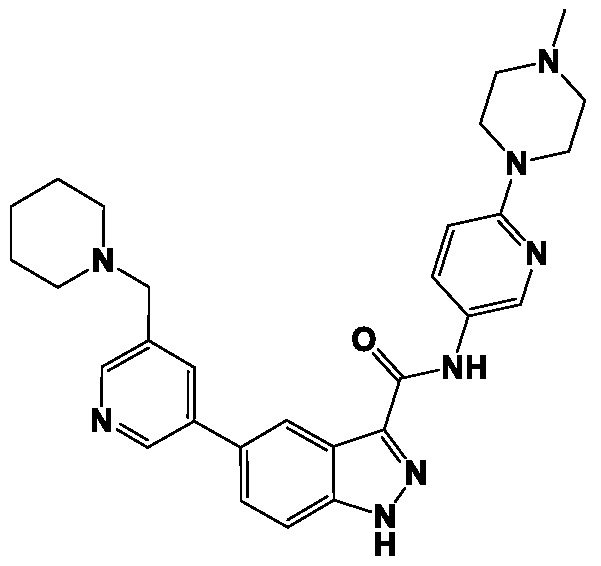
70
[0503] N-(6-(4-метилпиперазин-1-ил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 70.
[0504] Светло-желтое твердое вещество (37 мг, 0,07 ммоль, выход 39,2%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,37-1,44 (м, 2H), 1,51 (квин, J=5 Гц, 4H), 2,22 (с, 3H), 2,35-2,42 (м, 8H), 3,44 (т, J=5 Гц, 4H), 3,56 (с, 2H), 6,86 (д, J=9 Гц, 1H), 7,79 (д, J=9 Гц, 1H), 7,82 (д, J=10 Гц, 1H), 7,98 (д, J=2 Гц, 1H), 8,03 (дд, J=9 Гц, J=3 Гц, 1H), 8,48 (д, J=11 Гц, 1H), 8,58 (д, J=3 Гц, 1H), 8,81 (д, J=3 Гц, 1H), 10,34 (с, 1H), 13,89 (шс, 1H); ЭРИ-МС найдено для C29H34N8O m/z 511,5 (M+H).
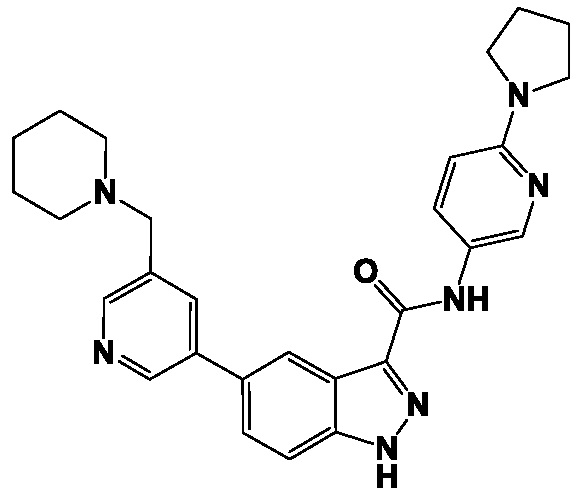
71
[0505] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(6-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 71.
[0506] Коричневое твердое вещество (53,9 мг, 0,11 ммоль, выход 53%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,38-1,39 (м, 2H), 1,51-1,52 (м, 4H), 1,93-1,96 (м, 4H), 2,36-2,38 (м, 4H), 3,36-3,39 (м, 4H), 3,56 (с, 2H), 6,46 (д, J=9 Гц, 1H), 7,78-7,83 (м, 2H), 7,96 (дд, J=9 Гц, J=3 Гц, 1H), 7,98-7,99 (м, 1H), 8,46-8,47 (м, 2H), 8,49 (д, J=3 Гц, 1H), 8,80-8,81 (м, 1H), 10,23 (с, 1H), 13,87 (с, 1H); ЭРИ-МС найдено для C28H31N7O m/z 482 (M+H).
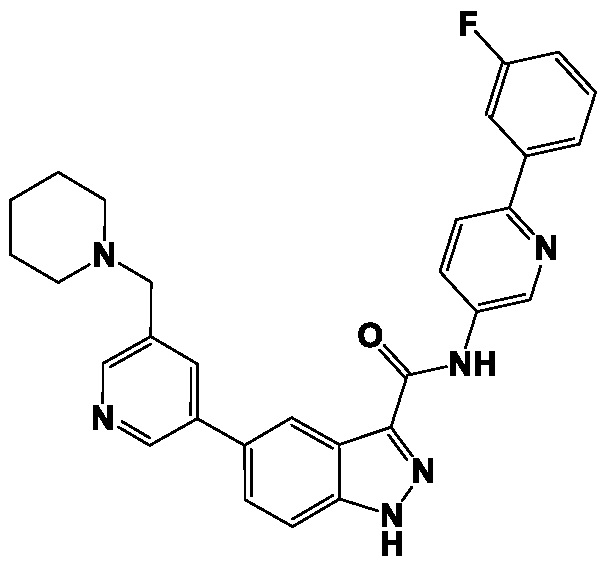
72
[0507] N-(6-(3-Фторфенил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 72.
[0508] Белое твердое вещество (54,8 мг, 0,11 ммоль, выход 64%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39-1,40 (м, 2H), 1,50-1,54 (м, 4H), 2,38-2,39 (м, 4H), 3,57 (с, 2H), 7,22-7,26 (м, 1H), 7,51-7,55 (м, 1H), 7,82-7,86 (м, 2H), 7,88-7,91 (м, 1H), 7,94-7,96 (м, 1H), 8,00-8,01 (м, 1H), 8,06 (д, J=9 Гц, 1H), 8,46 (дд, J=9 Гц, J=3 Гц, 1H), 8,50 (с, 2H), 8,82 (д, J=2 Гц, 1H), 9,20 (д, J=2 Гц, 1H), 10,86 (с, 1H), 14,03 (с, 1H); ЭРИ-МС найдено для C30H27FN6O m/z 507 (M+H).
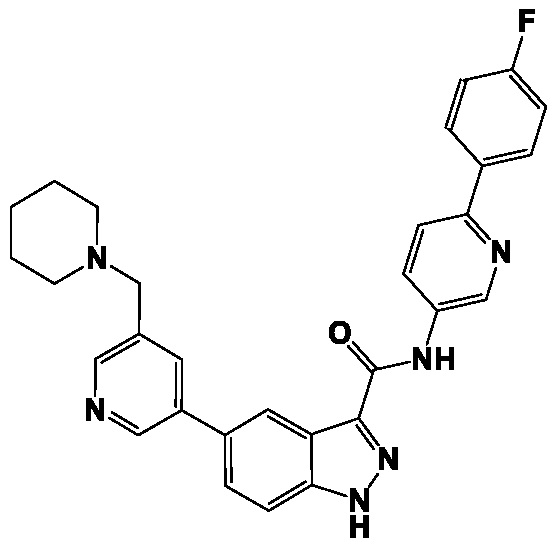
73
[0509] N-(6-(4-Фторфенил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 73.
[0510] Белое твердое вещество (50,8 мг, 0,10 ммоль, выход 55%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39-1,40 (м, 2H), 1,49-1,53 (м, 4H), 2,36-2,39 (м, 4H), 3,57 (с, 2H), 7,29-7,32 (м, 2H), 7,82-7,86 (м, 2H), 7,98-8,01 (м, 2H), 8,12-8,15 (м, 2H), 8,43 (дд, J=9 Гц, J=3 Гц, 1H), 8,49 (с, 2H), 8,82 (д, J=2 Гц, 1H), 9,17 (д, J=3 Гц, 1H), 10,81 (с, 1H), 14,02 (с, 1H); ЭРИ-МС найдено для C30H27FN6O m/z 507 (M+H).
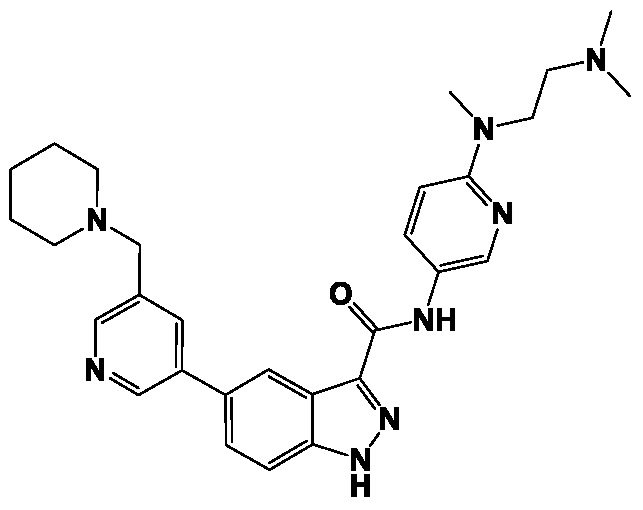
74
[0511] N-(6-((2-(Диметиламино)этил)(метил)амино)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 74.
[0512] Светло-желтое твердое вещество (88,5 мг, 0,17 ммоль, выход 61,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,38-1,42 (м, 2H), 1,51 (квин, J=5 Гц, 4H), 2,18 (с, 6H), 2,34-2,40 (м, 6H), 2,99 (с, 3H), 3,56 (с, 2H), 3,61 (т, J=7 Гц, 2H), 6,61 (д, J=9 Гц, 1H), 7,79 (д, J=9 Гц, 1H), 7,81 (д, J=9 Гц, 1H), 7,95 (дд, J=9 Гц, J=3 Гц, 1H), 7,98 (т, J=2 Гц, 1H), 8,46 (с, 1H), 8,48 (д, J=2 Гц, 2H), 8,81 (д, J=2 Гц, 1H), 10,24 (с, 1H), 13,84 (шс, 1H); ЭРИ-МС найдено для C29H36N8O m/z 513,5 (M+H).
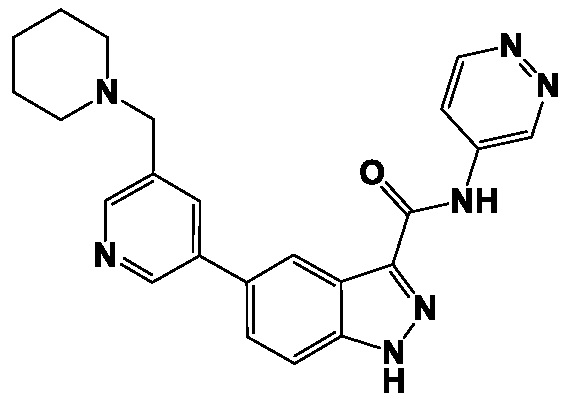
75
[0513] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(пиридазин-4-ил)-1H-индазол-3-карбоксамид 75.
[0514] Белое твердое вещество (53 мг, 0,13 ммоль, выход 33,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,43 (м, 2H), 1,47-1,54 (м, 4H), 2,33-2,42 (м, 4H), 3,57 (с, 2H), 7,85 (с, 2H), 8,00 (т, J=2 Гц, 1H), 8,25 (дд, J=6 Гц, J=3 Гц, 1H), 8,47 (т, J=1 Гц, 1H), 8,50 (д, J=2 Гц, 1H), 8,82 (д, J=2 Гц, 1H), 9,09 (д, J=6 Гц, 1H), 9,71 (дд, J=3 Гц, J=1 Гц, 1H), 11,16 (с, 1H), 14,16 (шс, 1H); ЭРИ-МС найдено для C23H23N7O m/z 414,1 (M+H).
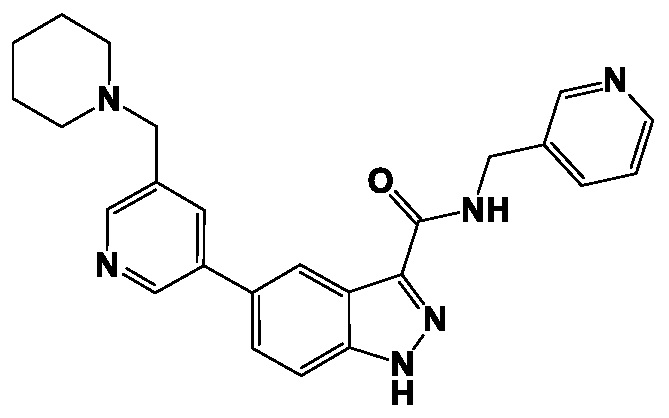
76
[0515] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(пиридин-3-илметил)-1H-индазол-3-карбоксамид 76.
[0516] Белое твердое вещество (26,8 мг, 0,06 ммоль, выход 27%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,38-1,39 (м, 2H), 1,49-1,51 (м, 4H), 2,36-2,37 (м, 4H), 3,55 (с, 2H), 4,53 (д, J=6 Гц, 2H), 7,35 (дд, J=8 Гц, J=5 Гц, 1H), 7,74-7,80 (м, 3H), 7,95-7,96 (м, 1H), 8,41-8,42 (м, 1H), 8,45-8,46 (м, 1H), 8,48-8,49 (м, 1H), 8,58-8,59 (м, 1H), 8,78 (д, J=2 Гц, 1H), 9,17 (т, J=6 Гц, 1H), 13,77 (с, 1H); ЭРИ-МС найдено для C25H26N6O m/z 427 (M+H).
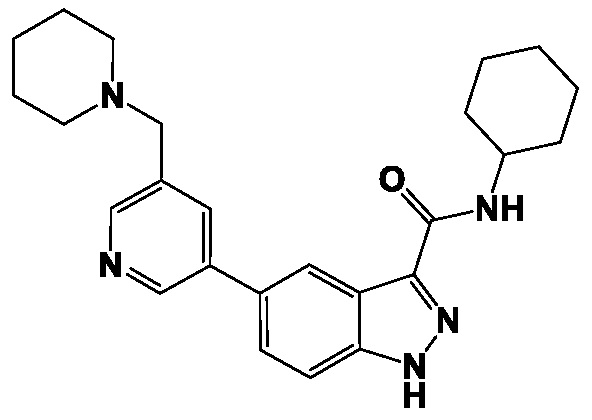
77
[0517] N-Циклогексил-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 77.
[0518] Белое твердое вещество (50,4 мг, 0,12 ммоль, выход 72,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,12-1,47 (м, 7H), 1,50-1,53 (м, 4H), 1,60-1,63 (м, 1H), 1,73-1,75 (м, 2H), 1,83-1,84 (м, 2H), 2,37-2,38 (м, 4H), 3,55 (с, 2H), 3,81-3,87 (м, 1H), 7,73-7,78 (м, 2H), 7,95-7,96 (м, 1H), 8,14 (д, J=8 Гц, 1H), 8,41-8,42 (м, 1H), 8,47 (д, J=2 Гц, 1H), 8,78 (д, J=2 Гц, 1H), 13,67 (с, 1H); ЭРИ-МС найдено для C25H31N5O m/z 418 (M+H).
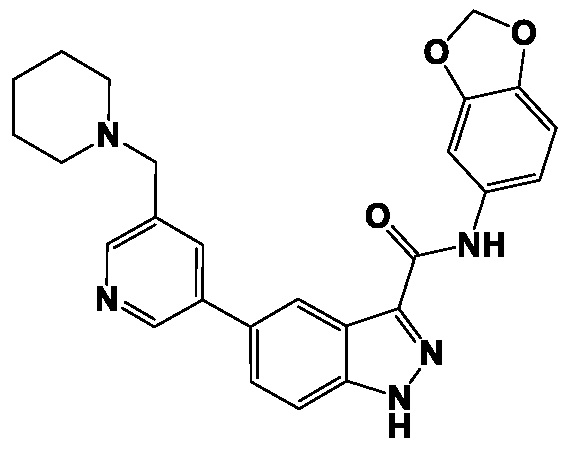
78
[0519] N-(Бензо[d][1,3]диоксол-5-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 78.
[0520] Белое твердое вещество (48,6 мг, 0,11 ммоль, выход 22,1%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,37-1,43 (м, 2H), 1,51 (квин, J=5 Гц, 4H), 2,36-2,42 (м, 4H), 3,56 (с, 2H), 6,01 (с, 2H), 6,90 (д, J=9 Гц, 1H), 7,37 (дд, J=9 Гц, J=2 Гц, 1H), 7,57 (д, J=2 Гц, 1H), 7,91 (дд, J=9 Гц, J= Гц, 1H), 7,82 (дд, J=9 Гц, J=1 Гц, 1H), 7,99 (т, J=2 Гц, 1H), 8,47 (дд, J=12 Гц, J=2 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 10,34 (с, 1H), 13,89 (с, 1H); ЭРИ-МС найдено для C26H25N5O3 m/z 456,0 (M+H).
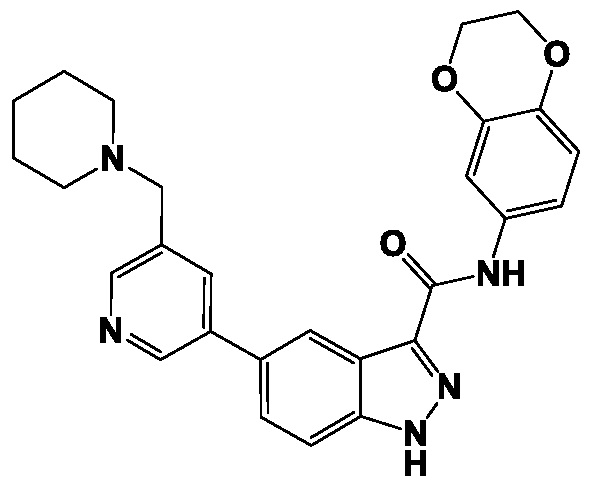
79
[0521] N-(2,3-Дигидробензо[b][1,4]диоксин-6-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 79.
[0522] Белое твердое вещество (98,4 мг, 0,21 ммоль, выход 38,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,42 (м, 2H), 1,51 (квин, J=5 Гц, 4H), 2,34-2,41 (м, 4H), 3,56 (с, 2H), 4,20-4,27 (м, 4H), 6,82 (д, J=9 Гц, 1H), 7,35 (дд, J=9 Гц, J=3 Гц, 1H), 7,51 (д, J=3 Гц, 1H), 7,78 (дд, J=9 Гц, J=1 Гц, 1H), 7,81 (дд, J=9 Гц, J=1 Гц, 1H), 7,98 (т, J=2 Гц, 1H), 8,47 (дд, J=12 Гц, J=2 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 10,26 (с, 1H), 13,87 (шс, 1H); ЭРИ-МС найдено для C27H27N5O3 m/z 470,4 (M+H).
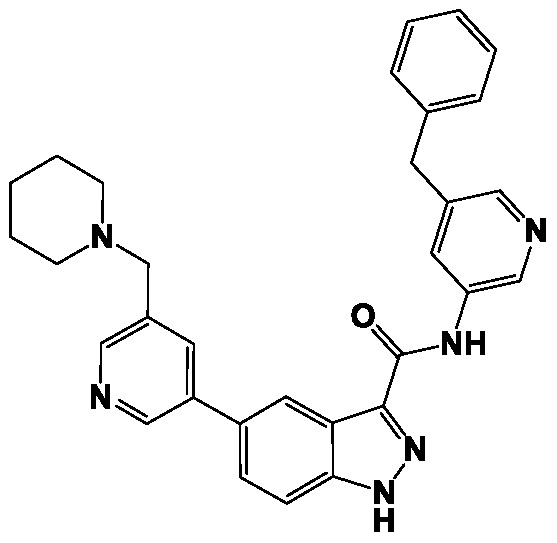
80
[0523] N-(5-Бензилпиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 80.
[0524] Белое твердое вещество (81,9 мг, 0,16 ммоль, выход 59%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39-1,41 (м, 2H), 1,49-1,53 (м, 4H), 2,37-2,39 (м, 4H), 3,56 (с, 2H), 4,00 (с, 2H), 7,20-7,23 (м, 1H), 7,28-7,34 (м, 4H), 7,79-7,84 (м, 2H), 7,98-7,99 (м, 1H), 8,23-8,24 (м, 1H), 8,25 (д, J=2 Гц, 1H), 8,45-8,46 (м, 1H), 8,49 (д, J=2 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 8,89 (д, J=2 Гц, 1H), 10,65 (с, 1H), 13,97 (с, 1H); ЭРИ-МС найдено для C31H30N6O m/z 503 (M+H).
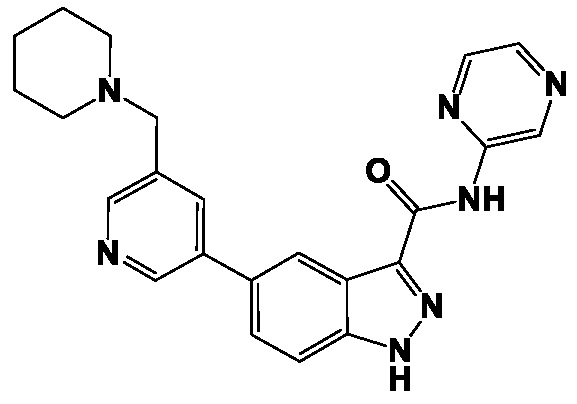
81
[0525] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(пиразин-2-ил)-1H-индазол-3-карбоксамид 81.
[0526] Белое твердое вещество (104 мг, 0,25 ммоль, выход 41,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,35-1,42 (м, 2H), 1,51 (квин, J=5 Гц, 4H), 2,33-2,42 (м, 4H), 3,57 (с, 2H), 7,83 (д, J=9 Гц, 1H), 7,85 (д, J=9 Гц, 1H), 8,00 (с, 1H), 8,45 (д, J=2 Гц, 1H), 8,46 (с, 1H), 8,50 (с, 1H), 8,83 (д, J=2 Гц, 1H), 9,50 (с, 1H), 10,36 (с, 1H), 14,11 (шс, 1H); ЭРИ-МС найдено для C23H23N7O m/z 413,9 (M+H).
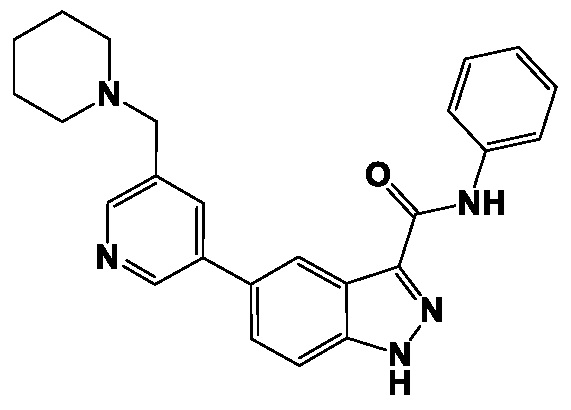
82
[0527] N-Фенил-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 82.
[0528] Белое твердое вещество (97,8 мг, 0,24 ммоль, выход 81%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39-1,40 (м, 2H), 1,49-1,53 (м, 4H), 2,37-2,39 (м, 4H), 3,57 (с, 2H), 7,09-7,12 (м, 1H), 7,34-7,37 (м, 2H), 7,80 (д, J=9 Гц, 1H), 7,83 (дд, J=9 Гц, 2 Гц, 1H), 7,907,92 (м, 2H), 7,99-8,00 (м, 1H), 8,47-8,48 (м, 1H), 8,49 (д, J=2 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 10,40 (с, 1H), 13,92 (с, 1H); ЭРИ-МС найдено для C25H25N5O m/z 412 (M+H).
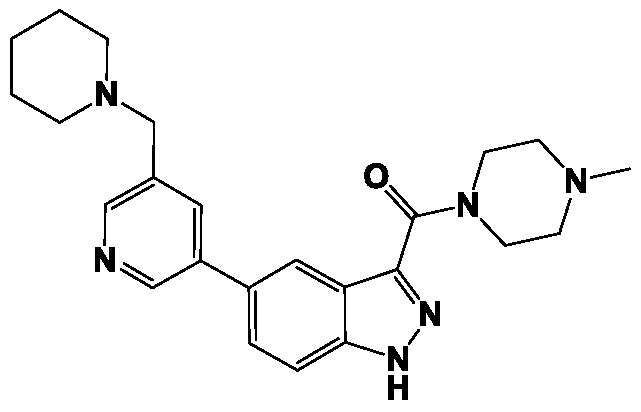
83
[0529] (4-Метилпиперазин-1-ил)(5-(5-(пиперидин-1-илметил)-пиридин-3-ил)-1H-индазол-3-ил)метанон 83.
[0530] Светло-желтое аморфное твердое вещество (74,6 мг, 0,18 ммоль, выход 93%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,38-1,39 (м, 2H), 1,48-1,53 (м, 4H), 2,22 (с, 3H), 2,36-2,41 (м, 8H), 3,55 (с, 2H), 3,72-3,73 (м, 2H), 4,01-4,02 (м, 2H), 7,73 (д, J=9 Гц, 1H), 7,79 (дд, J=9 Гц, J=2 Гц, 1H), 7,95-7,96 (м, 1H), 8,22 (д, J=1 Гц, 1H), 8,46 (д, J=2 Гц, 1H), 8,78 (д, J=2 Гц, 1H), 13,64 (с, 1H); ЭРИ-МС найдено для C24H30N6O m/z 419 (M+H).
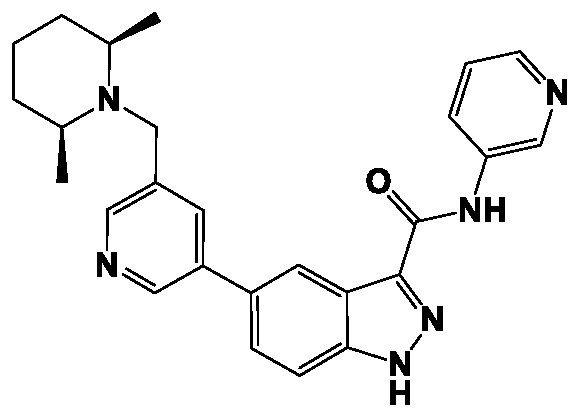
84
[0531] 5-(5-(((2R,6S)-2,6-Диметилпиперидин-1-ил)метил)-пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 84.
[0532] Бежевое твердое вещество (76,5 мг, 0,17 ммоль, выход 75,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,00 (д, J=6 Гц, 6H), 1,21-1,35 (м, 3H), 1,55 (д, J=11 Гц, 2H), 1,60-1,65 (м, 1H), 2,45-2,53 (м, 2H), 3,84 (с, 1H), 7,40 (дд, J=7 Гц, 3 Гц, 1H), 7,79 (дд, J=9 Гц, J=2 Гц, 1H), 7,83 (дд, J=9 Гц, J=1 Гц, 1H), 8,04 (с, 1H), 8,29-8,35 (м, 2H), 8,46 (с, 1H), 8,60 (д, J=2 Гц, 1H), 8,73 (д, J=2 Гц, 1H), 9,08 (д, J=3 Гц, 1H), 10,70 (с, 1H), 14,00 (шс, 1H); ЭРИ-МС найдено для C26H28N6O m/z 441,3 (M+H).
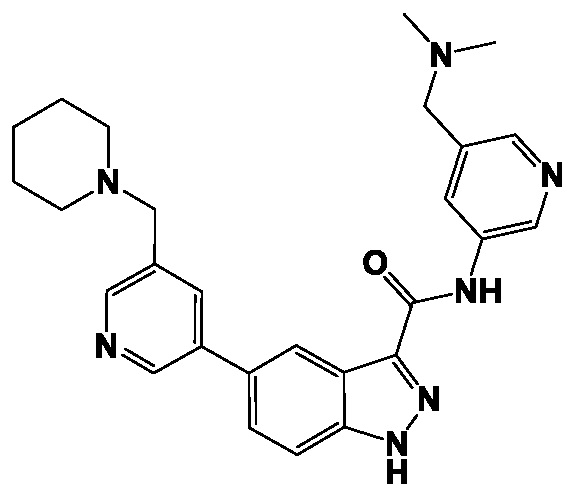
86
[0533] N-(5-((Диметиламино)метил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 86.
[0534] Белое твердое вещество (41,5 мг, 0,09 ммоль, выход 72%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39-1,40 (м, 2H), 1,49-1,54 (м, 4H), 2,19 (с, 6H), 2,36-2,39 (м, 4H), 3,44 (с, 2H), 3,58 (с, 2H), 7,81 (д, J=9 Гц, 1H), 7,85 (дд, J=9 Гц, J=2 Гц, 1H), 8,00-8,01 (м, 1H), 8,21 (д, J=2 Гц, 1H), 8,37-8,38 (м, 1H), 8,49-8,50 (м, 2H), 8,83 (д, J=2 Гц, 1H), 8,91 (д, J=2 Гц, 1H), 10,69 (с, 1H), 14,01 (шс, 1H); ЭРИ-МС найдено для C27H31N7O m/z 470 (M+H).
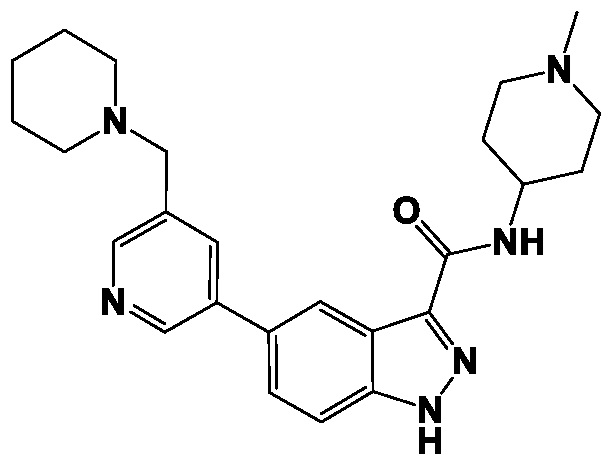
87
[0535] N-(1-Метилпиперидин-4-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 87.
[0536] Белое аморфное твердое вещество (18,2 мг, 0,04 ммоль, выход 59,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39-1,40 (м, 2H), 1,49-1,53 (м, 4H), 1,66-1,75 (м, 4H), 1,95-2,00 (м, 2H), 2,18 (с, 3H), 2,37-2,38 (м, 4H), 2,77 (д, J=11 Гц, 2H), 3,55 (с, 2H), 3,81-3,83 (м, 1H), 7,73-7,75 (м, 1H), 7,77-7,79 (м, 1H), 7,95-7,96 (м, 1H), 8,25 (д, J=8 Гц, 1H), 8,41-8,42 (м, 1H), 8,47 (д, J=2 Гц, 1H), 8,78 (д, J=2 Гц, 1H), 13,70 (с, 1H); ЭРИ-МС найдено для C25H32N6O m/z 433 (M+H).
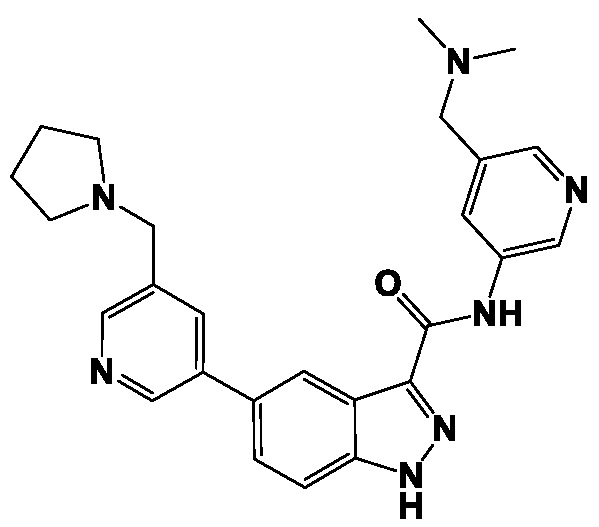
106
[0537] N-(5-((Диметиламино)метил)пиридин-3-ил)-5-(5-(пирролидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 106.
[0538] Белое твердое вещество (39,4 мг, 0,09 ммоль, выход 74%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,71-1,73 (м, 4H), 2,49-2,50 (м, 4H), 2,18 (с, 6H), 3,43 (с, 2H), 3,71 (с, 2H), 7,81 (д, J=9 Гц, 1H), 7,84 (ABк, J=9 Гц, 1H), 8,02-8,03 (м, 1H), 8,21 (д, J=2 Гц, 1H), 8,37-8,38 (м, 1H), 8,48-8,49 (м, 1H), 8,51 (д, J=2 Гц, 1H), 8,83 (д, J=2 Гц, 1H), 8,91 (д, J=2 Гц, 1H), 10,68 (с, 1H), 13,98 (с, 1H); ЭРИ-МС найдено для C26H29N7O m/z 456 (M+H).
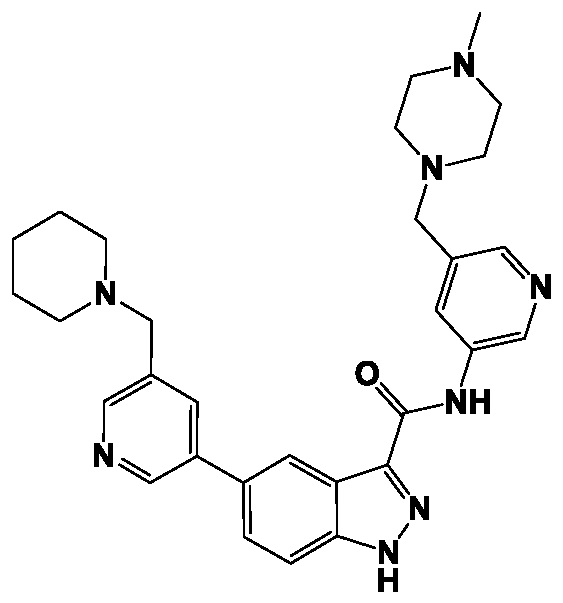
124
[0539] N-(5-((4-Метилпиперазин-1-ил)метил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 124.
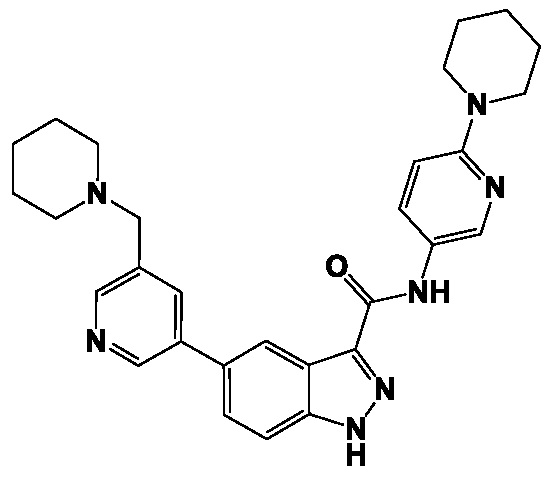
126
[0540] N-(6-(Пиперидин-1-ил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 126.
[0541] Серое тело (92,7 мг, 0,19 ммоль, выход 29,0%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,48-1,64 (м, 12H), 2,32-2,43 (м, 4H), 3,48 (т, J=4,5 Гц, 4H), 3,56 (с, 2H), 6,83 (д, J=9 Гц, 1H), 7,80 (ABк, J=10 Гц, 2H), 7,98 (с, 1H), 8,00 (д, J=2,4 Гц, 1H), 8,47 (д, J=10 Гц, 2H), 8,55 (д, J=2,5 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 10,27 (с, 1H), 13,86 (с, 1H); ЭРИ-МС найдено для C29H33N7O m/z 496,5 (M+H).
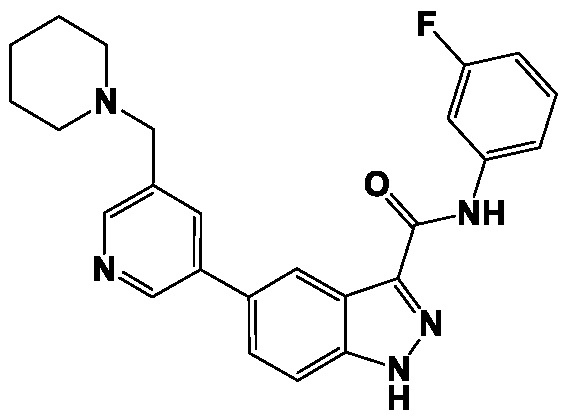
162
[0542] N-(3-Фторфенил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 162.
[0543] Белое твердое вещество (176 мг, 0,41 ммоль, выход 56,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,43 (м, 2H), 1,47-1,55 (м, 4H), 2,38 (шс, 4H), 3,56 (с, 2H), 6,93 (дт, J=9 Гц, J=3 Гц, 1H), 7,39 (к, J=8 Гц, 1H), 7,75 (дд, J=8 Гц, J=1 Гц, 1H), 7,82 (д/Abк, J=9 Гц, J=1 Гц, 2H), 7,89 (тд, J=12 Гц, J=2 Гц, 1H), 7,99 (т, J=2 Гц, 1H), 8,47 (с, 1H), 8,49 (д, J=2 Гц, 1H), 8,82 (д, J=2 Гц, 1H), 10,66 (с, 1H), 13,97 (шс, 1H); ЭРИ-МС найдено для C25H24FN5O m/z 430,0 (M+H).
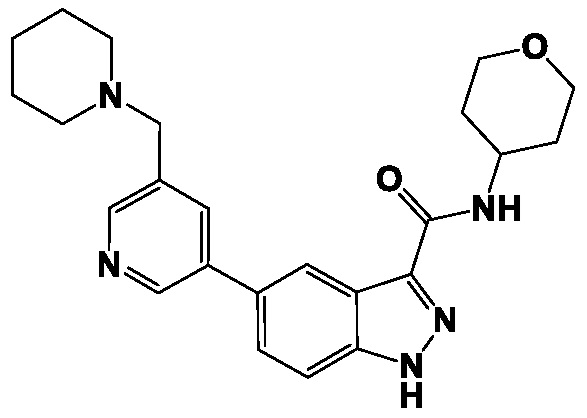
163
[0544] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(тетрагидро-2H-пиран-4-ил)-1H-индазол-3-карбоксамид 163.
[0545] Коричневое аморфное твердое вещество (88 мг, 0,21 ммоль, выход 88%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39-1,40 (м, 2H), 1,49-1,53 (м, 4H), 1,69-1,76 (м, 4H), 2,37-2,38 (м, 4H), 3,39-3,42 (м, 2H), 3,56 (с, 2H), 3,88-3,90 (м, 2H), 4,05-4,10 (м, 1H), 7,74 (д, J=9 Гц, 1H), 7,77-7,79 (м, 1H), 7,95-7,96 (м, 1H), 8,37 (д, J=8 Гц, 1H), 8,41-8,42 (м, 1H), 8,47 (д, J=2 Гц, 1H), 8,79 (д, J=2 Гц, 1H), 13,72 (с, 1H); ЭРИ-МС найдено для C24H29N5O2 m/z 420 (M+H).
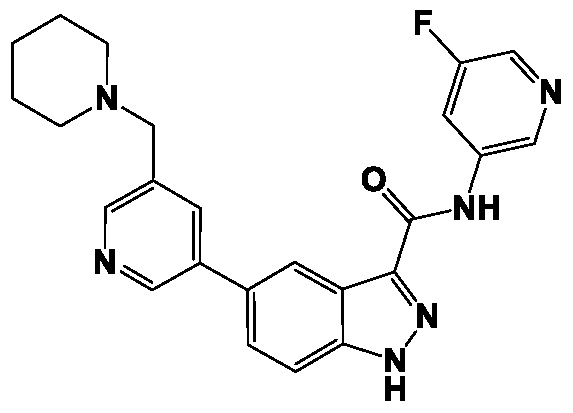
168
[0546] N-(5-Фторпиридин-3-ил)-5-(5-(пиперидин-1-илметил)-пиридин-3-ил)-1H-индазол-3-карбоксамид 168.
[0547] Белое твердое вещество (286 мг, 0,66 ммоль, выход 56%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,39 (м, 2H), 1,49-1,53 (м, 4H), 2,38 (шс, 4H), 3,56 (с, 2H), 7,81-7,86 (м, 2H), 7,99 (с, 1H), 8,31-8,34 (м, 2H), 8,47 (с, 1H), 8,49 (д, J=1,3 Гц, 1H), 8,82 (д, J=1,7 Гц, 1H), 8,99 (с, 1H), 10,97 (с, 1H), 14,07 (шс, 1H); ЭРИ-МС найдено для C24H23FN6O m/z 431,4 (M+H).
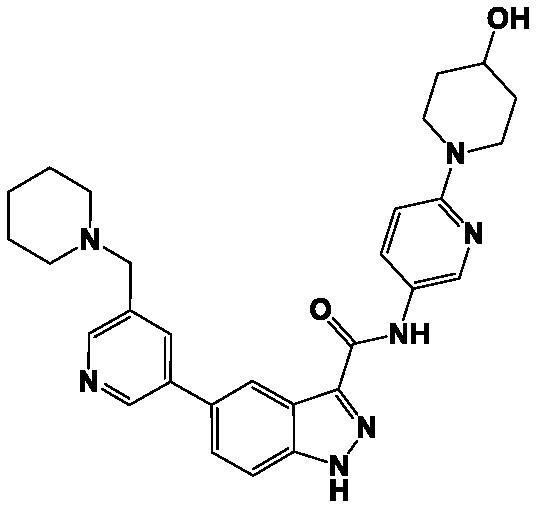
169
[0548] N-(6-(4-Гидроксипиперидин-1-ил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 169.
[0549] Почти белое твердое вещество (33 мг, 0,06 ммоль, выход 53,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,32-1,43 (м, 4H), 1,45-1,57 (м, 4H), 1,74-1,83 (м, 2H), 2,33-2,44 (м, 4H), 3,04 (т, J=10 Гц, 2H), 3,56 (с, 2H), 3,63-3,73 (м, 1H), 3,93-4,02 (м, 2H), 4,72 (с, 1H), 6,85 (д, J=9 Гц, 1H), 7,80 (ABк, J=10 Гц, 2H), 7,99 (д, J=7 Гц, 2H), 8,47 (д, J=10 Гц, 2H), 8,54 (с, 1H), 8,81 (с, 1H), 10,28 (с, 1H), 13,87 (с, 1H); ЭРИ-МС найдено для C29H33N7O2 m/z 512,3 (M+H).
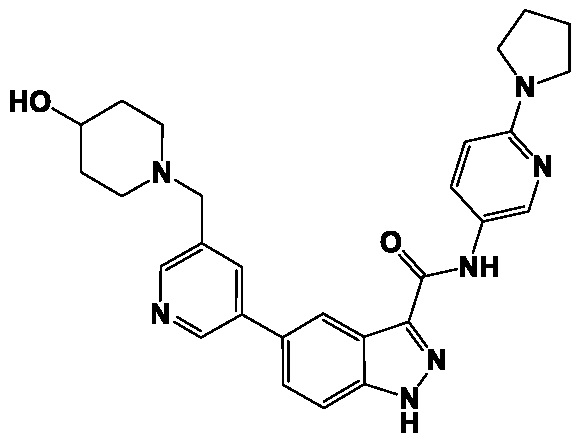
170
[0550] 5-(5-((4-Гидроксипиперидин-1-ил)метил)пиридин-3-ил)-N-(6-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 170.
[0551] Почти белое твердое вещество (125,4 мг, 0,25 ммоль, выход 73,2%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,93-1,96 (м, 4H), 2,09-2,12 (м, 2H), 2,70-2,72 (м, 2H), 3,37-3,39 (м, 4H), 3,46-3,47 (м, 1H), 3,58 (с, 1H), 4,52 (д, J=4 Гц, 1H), 6,46 (д, J=9 Гц, 1H), 7,77-7,82 (м, 2H), 7,95-7,98 (м, 2H), 8,44-8,48 (м, 2H), 8,49 (д, J=2,5 Гц, 1H), 8,80 (д, J=2,1 Гц, 1H), 10,20 (с, 1H), 13,85 (с, 1H); ЭРИ-МС найдено для C28H31N7O2 m/z 498 (M+H).
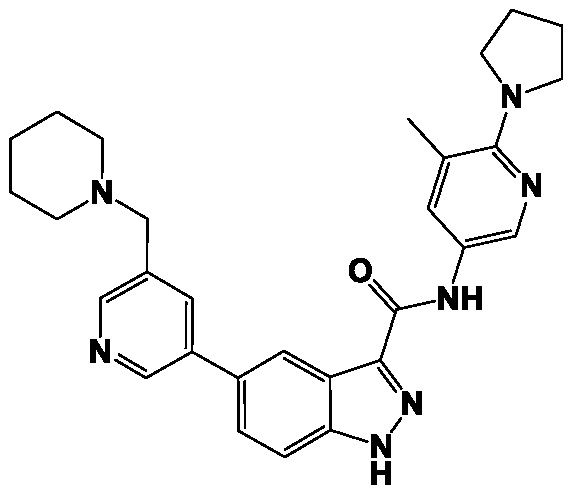
172
[0552] N-(5-Метил-6-(пирролидин-1-ил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 172.
[0553] Почти белое твердое вещество (186 мг, 0,38 ммоль, выход 72,2%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,34-1,43 (м, 2H), 1,47-1,55 (м, 4H), 1,82-1,89 (м, 4H), 2,30 с, 3H), 2,33-2,42 (м, 4H), 3,43 (т, J=6,6 Гц, 4H), 3,56 (с, 2H), 7,81 (ABк, J=10 Гц, 2H), 7,89 (д, J=2 Гц, 1H), 7,98 (с, 1H), 8,38 (д, J=2 Гц, 1H), 8,47 (д, J=8 Гц, 2H), 8,81 (д, J=2 Гц, 1H), 10,24 (с, 1H), 13,86 (с, 1H); ЭРИ-МС найдено для C29H33N7O m/z 496,4 (M+H).
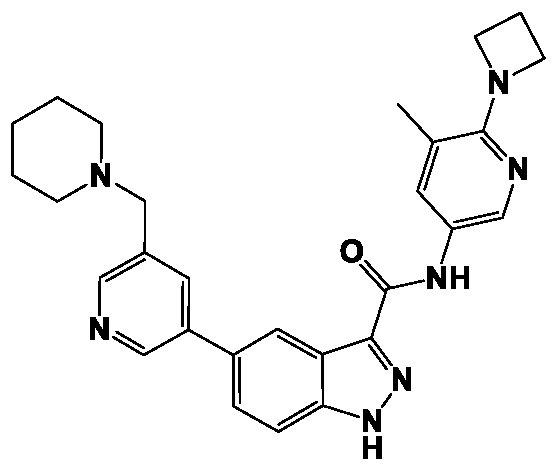
173
[0554] N-(6-(Азетидин-1-ил)-5-метилпиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 173.
[0555] Почти белое твердое вещество (184 мг, 0,38 ммоль, выход 62,6%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,35-1,43 (м, 2H), 1,47-1,54 (м, 4H), 2,16 (с, 3H), 2,22 (квин, J=7 Гц, 2H), 2,34-2,42 (м, 4H), 3,56 (с, 2H), 4,00 (т, J=7 Гц, 4H), 7,81 (ABк, J=10 Гц, 2H), 7,85 (д, J=2 Гц, 1H), 8,39 (д, J=2 Гц, 1H), 8,47 (д, J=10 Гц, 2H), 8,81 (д, J=2 Гц, 1H), 10,24 (с, 1H), 13,87 (с, 1H); ЭРИ-МС найдено для C28H31N7O m/z 482,0 (M+H).
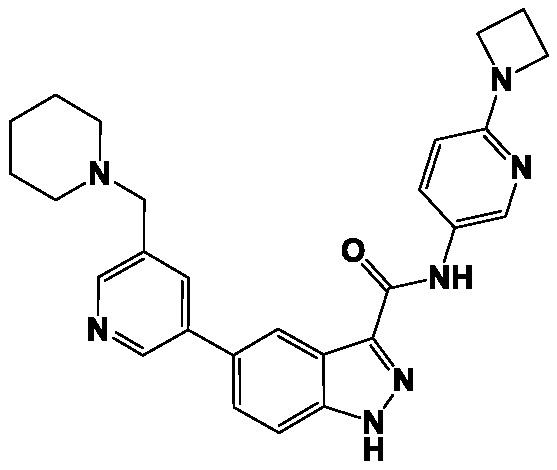
174
[0556] N-(6-(Азетидин-1-ил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 174.
[0557] Белое твердое вещество (14,9 мг, 0,03 ммоль, выход 11,0%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,43 (м, 2H), 1,47-1,54 (м, 4H), 2,32 (квин, J=7 Гц, 2H), 2,35-2,42 (м, 4H), 3,56 (с, 2H), 3,92 (т, J=7 Гц, 4H), 6,39 (д, J=9 Гц, 1H), 7,77-7,83 (м, 2H), 7,98 (дд, J=9 Гц, J=2 Гц, 2H), 8,42-8,53 (м, 3H), 8,78-8,84 (м, 1H), 10,27 (с, 1H), 13,87 (с, 1H); ЭРИ-МС найдено для C27H29N7O m/z 468,0 (M+H).
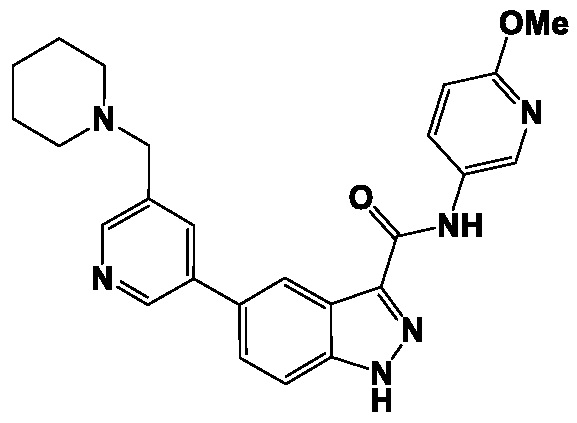
175
[0558] N-(6-Метоксипиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 175.
[0559] Белое твердое вещество (31,2 мг, 0,07 ммоль, выход 25,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,43 (м, 2H), 1,47-1,55 (м, 4H), 2,33-2,42 (м, 4H), 3,56 (с, 2H), 3,85 (с, 3H), 6,84 (д, J=9 Гц, 1H), 7,81 (ABк, J=12 Гц, 2H), 7,98 (с, 1H), 8,18 (дд, J=9 Гц, J=2,7 Гц, 1H), 8,47 (дд, J=10 Гц, J=1 Гц, 2H), 8,65 (д, J=2,6 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 10,50 (с, 1H), 13,91 (шс, 1H); ЭРИ-МС найдено для C25H26N6O2 m/z 443,4 (M+H).
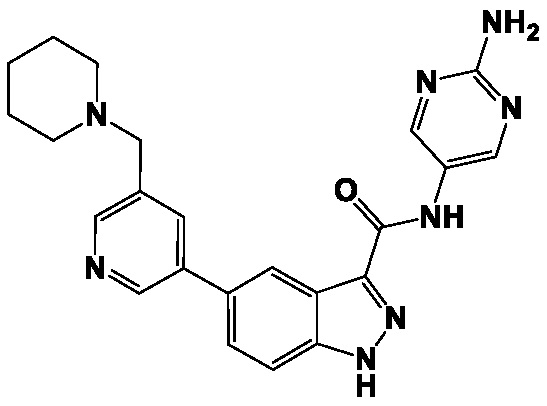
176
[0560] N-(2-Аминопиримидин-5-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 176.
[0561] Желтое твердое вещество (412 мг, 0,96 ммоль, выход 52,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,37-1,43 (м, 2H), 1,47-1,54 (м, 4H), 2,35-2,41 (м, 4H), 3,56 (с, 2H), 6,49 (с, 2H), 7,81 (ABк, J=10 Гц, 2H), 7,98 (с, 1H), 8,47 (дд, J=12 Гц, J=2 Гц, 2H), 8,63 (с, 1H), 8,81 (д, J=2 Гц, 1H), 10,32 (с, 1H), 13,91 (с, 1H); ЭРИ-МС найдено для C23H24N8O m/z 429,3 (M+H).
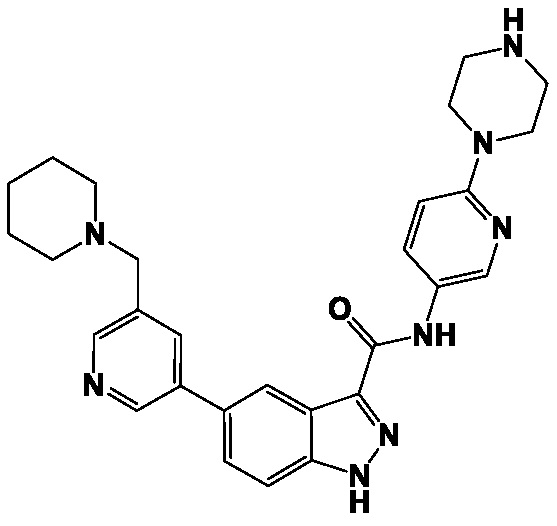
177
[0562] N-(6-(Пиперазин-1-ил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 177.
[0563] Коричневое твердое вещество (160 мг, 0,32 ммоль, выход 28,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,37-1,43 (м, 2H), 1,48-1,54 (м, 4H), 2,34-2,41 (м, 4H), 2,79 (т, J=5 Гц, 4H), 3,36 (т, J=5 Гц, 4H), 3,56 (с, 2H), 6,82 (д, J=9 Гц, 1H), 7,81 (ABк, J=10 Гц, 2H), 7,98 (с, 1H), 8,02 (дд, J=9 Гц, J=2,7 Гц, 1H), 8,47 (дд, J=9 Гц, J=2 Гц, 2H), 8,57 (д, J=2,5 Гц, 1H), 8,81 (д, J=2 Гц, 1H), 10,29 (с, 1H); ЭРИ-МС найдено для C28H32N8O m/z 497,1 (M+H).
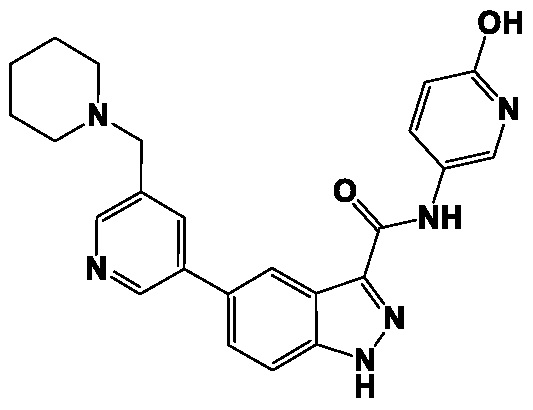
178
[0564] N-(6-Гидроксипиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 178.
[0565] Почти белое твердое вещество (78,3 мг, 0,18 ммоль, выход 52,4%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,43 (м, 2H), 1,48-1,54 (м, 4H), 2,35-2,42 (м, 4H), 3,56 (с, 2H), 6,38 (д, J=10 Гц, 1H), 7,80 (ABк, J=11 Гц, 2H), 7,83 (дд, J=10 Гц, J=3 Гц, 1H), 7,97 (с, 1H), 8,04 (д, J=2,5 Гц, 1H), 8,44 (с, 1H), 8,48 (д, J=2 Гц, 1H), 8,80 (д, J=2 Гц, 1H), 10,27 (с, 1H), 11,42 (шс, 1H), 13,87 (шс, 1H); ЭРИ-МС найдено для C24H24N6O2 m/z 429,1 (M+H).
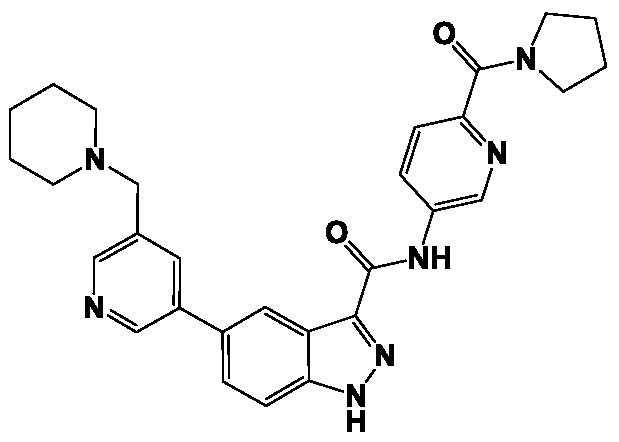
179
[0566] 5-(5-(Пиперидин-1-илметил)пиридин-3-ил)-N-(6-(пирролидин-1-карбонил)пиридин-3-ил)-1H-индазол-3-карбоксамид 179.
[0567] Светло-желтое твердое вещество (61 мг, 0,12 ммоль, выход 37,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,37-1,43 (м, 2H), 1,48-1,55 (м, 4H), 1,82-1,90 (м, 4H), 2,38 (шс, 4H), 3,17 (д, J=5 Гц, 2H), 3,51 (т, J=7 Гц, 2H), 3,57 (с, 2H), 3,70 (т, J=7 Гц, 2H), 7,79 (д, J=9 Гц, 1H), 7,84 (ABк, J=11 Гц, 2H), 8,00 (с, 1H), 8,46 (дд, J=9 Гц, J=2,5 Гц, 1H), 8,48 (дд, J=9 Гц, J=2 Гц, 2H), 8,82 (д, J=2 Гц, 1H), 9,10 (д, J=2 Гц, 1H), 10,91 (с, 1H), 14,05 (шс, 1H); ЭРИ-МС найдено для C29H31N7O2 m/z 510,6 (M+H).
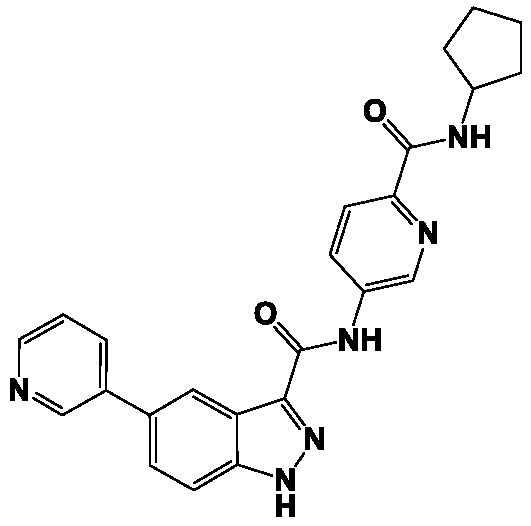
181
[0568] N-(6-(Циклопентилкарбамоил)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 181.
[0569] Светло-желтое твердое вещество (18 мг, 0,04 ммоль, выход 16,6%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,50-1,64 (м, 4H), 1,67-1,76 (м, 2H), 1,85-1,94 (м, 4H), 4,24 (квин, J=8 Гц, 1H), 7,53 (дд, J=8 Гц, J=5 Гц, 1H), 7,84 (ABк, 2H), 8,03 (д, J=9 Гц, 1H), 8,14 (д, J=8 Гц, 1H), 8,45 (д, J=8 Гц, 1H), 8,48 (с, 1H), 8,54 (дд, J=9 Гц, J=2,5 Гц, 1H), 8,60 (д, J=4 Гц, 1H), 8,94 (д, J=2 Гц, 1H), 9,16 (д, J=2 Гц, 1H), 10,97 (с, 1H), 14,08 (шс, 1H); ЭРИ-МС найдено для C24H22N6O2 m/z 427,1 (M+H).
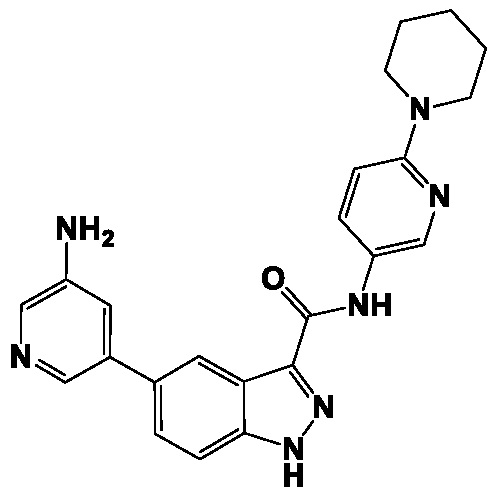
182
[0570] 5-(5-Аминопиридин-3-ил)-N-(6-(пиперидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 182.
[0571] Почти белое твердое вещество (23,4 мг, 0,06 ммоль, выход 19,4%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,51-1,63 (м, 6H), 3,47 (т, J=5 Гц, 4H), 5,45 (с, 2H), 6,83 (д, J=10 Гц, 1H), 7,24 (т, J=2 Гц, 1H), 7,73 (дк, J=9 Гц, J=2 Гц, 2H), 7,94 (д, J=2,5 Гц, 1H), 8,00 (дд, J=9 Гц, J=2,5 Гц, 1H), 8,08 (д, J=2 Гц, 1H), 8,40 (с, 1H), 8,56 (д, J=2,5 Гц, 1H), 10,27 (с, 1H), 13,84 (с, 1H); ЭРИ-МС найдено для C23H23N7O m/z 414,3 (M+H).
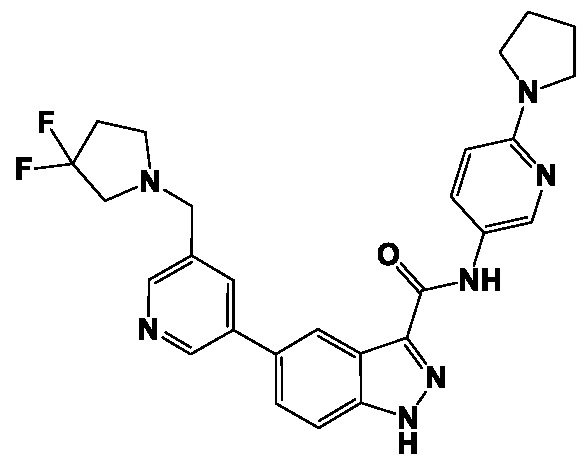
183
[0572] 5-(5-((3,3-Дифторпирролидин-1-ил)метил)пиридин-3-ил)-N-(6-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 183.
[0573] Почти белое твердое вещество (307 мг, 0,61 ммоль, выход 39,6%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,95 (т, J=6,5 Гц, 4H), 2,28 (тт, J=13,5 Гц, J=7 Гц, 2H), 2,76 (т, J=7 Гц, 2H), 2,94 (т, J=13,5 Гц, 2H), 3,38 (т, J=6,5 Гц, 4H), 3,77 (с, 2H), 6,46 (д, J=9 Гц, 1H), 7,81 (дк, J=8,5 Гц, J=1,5 Гц, 2H), 7,97 (дд, J=9 Гц, J=2,5 Гц, 1H), 8,03 (с, 1H), 8,48 (с, 1H), 8,49 (д, J=2,5 Гц, 1H), 8,52 (с, 1H), 8,84 (д, J=2 Гц, 1H), 10,23 (с, 1H), 13,87 (с, 1H); ЭРИ-МС найдено для C27H27F2N7O m/z 504,0 (M+H).
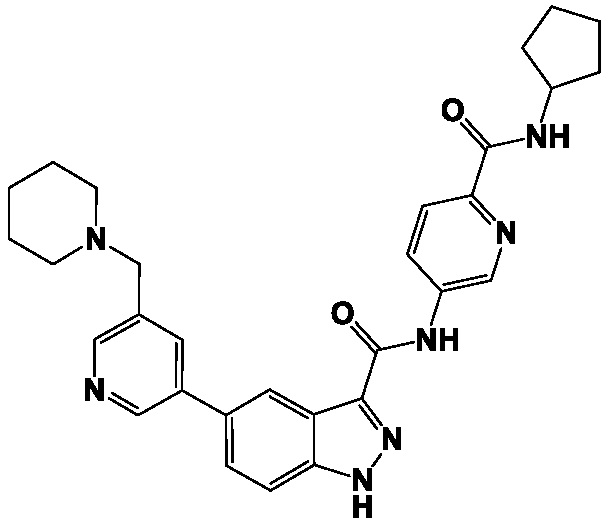
184
[0574] N-(6-(Циклопентилкарбамоил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 184.
[0575] Белое твердое вещество (3,2 мг, 0,01 ммоль, выход 18,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,43 (м, 2H), 1,43-1,64 (м, 8H), 1,64-1,76 (м, 2H), 1,82-1,93 (м, 2H), 2,38 (шс, 4H), 3,57 (с, 2H), 4,24 (квин, J=7 Гц, 1H), 7,84 (ABк, J=10 Гц, 2H), 8,00 (с, 1H), 8,03 (д, J=9 Гц, 1H), 8,44 (д, J=8 Гц, 1H), 8,48 (дд, J=8 Гц, J=2 Гц, 2H), 8,55 (дд, J=9 Гц, J=2,5 Гц, 1H), 8,82 (д, J=2,5 Гц, 1H), 9,16 (д, J=2,5 Гц, 1H), 10,98 (с, 1H), 14,06 (шс, 1H); ЭРИ-МС найдено для C30H33N7O2 m/z 524,5 (M+H).
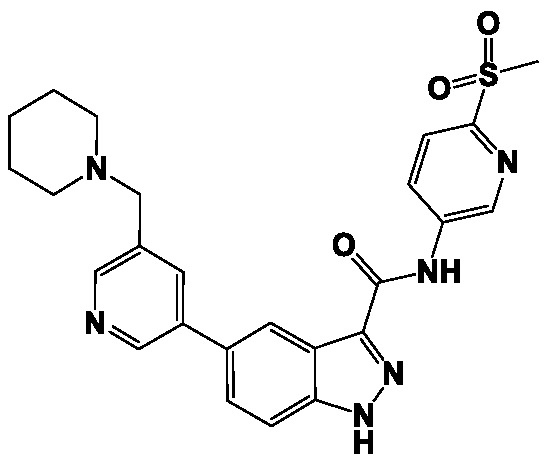
185
[0576] N-(6-(Метилсульфонил)пиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамид 185.
[0577] Белое твердое вещество (72 мг, 0,15 ммоль, выход 56,4%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,43 (м, 2H), 1,48-1,55 (м, 4H), 2,39 (шс, 4H), 3,27 (с, 3H), 3,57 (с, 2H), 7,85 (с, 2H), 8,00 (с, 1H), 8,08 (д, J=8,5 Гц, 1H), 8,49 (дд, J=10 Гц, J=1,5 Гц, 2H), 8,83 (д, J=2,5 Гц, 1H), 9,26 (д, J=2,5 Гц, 1H), 11,19 (с, 1H), 14,13 (шс, 1H); ЭРИ-МС найдено для C25H26N6O3S m/z 491,1 (M+H).
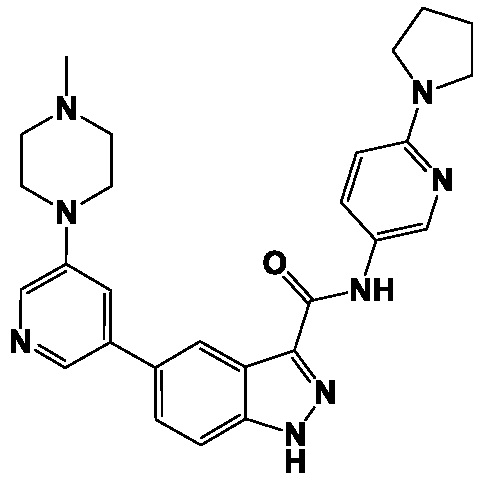
186
[0578] 5-(5-(4-метилпиперазин-1-ил)пиридин-3-ил)-N-(6-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 186.
[0579] Почти белое твердое вещество (196 мг, 0,41 ммоль, выход 47,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,89-1,98 (м, 4H), 2,27 (шс, 3H), 3,25-3,42 (м, 12H), 6,45 (д, J=9 Гц, 1H), 7,53 (с, 1H), 7,77 (к, J=8,5 Гц, 2H), 7,96 (д, J=6,5 Гц, 1H), 8,31 (д, J=5,5 Гц, 2H), 8,43 (с, 1H), 8,48 (с, 1H), 10,21 (с, 1H), 13,83 (с, 1H); ЭРИ-МС найдено для C27H30N8O m/z 483,4 (M+H).
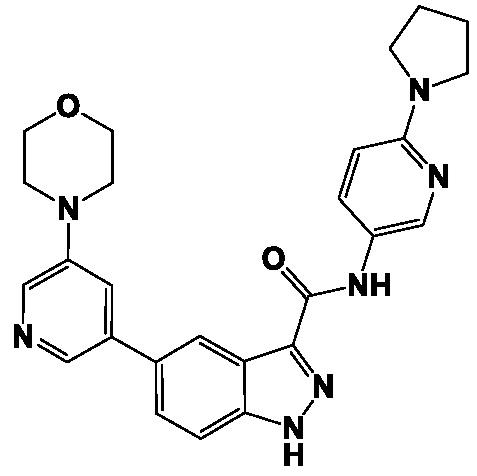
187
[0580] 5-(5-Морфолинопиридин-3-ил)-N-(6-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 187.
[0581] Белое твердое вещество (92 мг, 0,20 ммоль, выход 43,5%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,94 (т, J=6,5 Гц, 4H), 3,28 (т, J=4,5 Гц, 4H), 3,38 (т, J=6,5 Гц, 4H), 3,78 (т, J=4,5 Гц, 4H), 6,45 (д, J=9 Гц, 1H), 7,55 (с, 1H), 7,77 (дк, J=8,5 Гц, J=1,5 Гц, 2H), 7,96 (дд, J=9 Гц, J=2,5 Гц 1H), 8,33 (дд, J=6,5 Гц, J=3 Гц, 2H), 8,44 (с, 1H), 8,49 (д, J=2,5 Гц, 1H), 10,21 (с, 1H), 13,83 (с, 1H); ЭРИ-МС найдено для C26H27N7O2 m/z 470,5 (M+H).
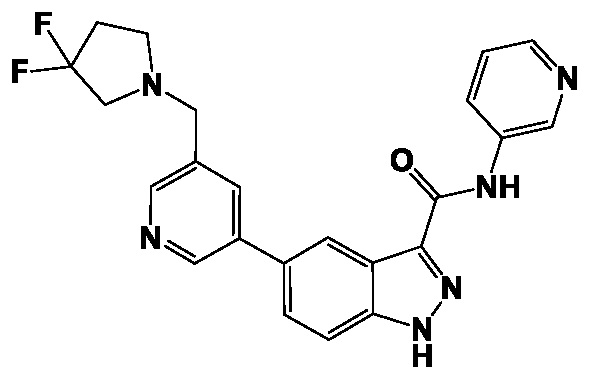
188
[0582] 5-(5-((3,3-Дифторпирролидин-1-ил)метил)пиридин-3-ил)-N-(пиридин-3-ил)-1H-индазол-3-карбоксамид 188.
[0583] Белое твердое вещество (209 мг, 0,48 ммоль, выход 56,6%). 1H-ЯМР (ДМСО-d6) δ м.д. 2,23-2,32 (м, 2H), 2,76 (т, J=7 Гц, 2H), 2,94 (т, J=13,5 Гц, 2H), 3,77 (с, 2H), 7,40 (к, J=8 Гц, 1H), 7,83 (дк, J=8 Гц, J=2 Гц, 2H), 8,04 (с, 1H), 8,31-8,34 (м, 2H), 8,49 (с, 1H), 8,53 (д, J=2 Гц, 1H), 8,85 (д, J=2,5 Гц, 1H), 9,08 (д, J=2 Гц, 1H), 10,70 (с, 1H), 14,01 (шс, 1H); ЭРИ-МС найдено для C23H20F2N6O m/z 435,2 (M+H).
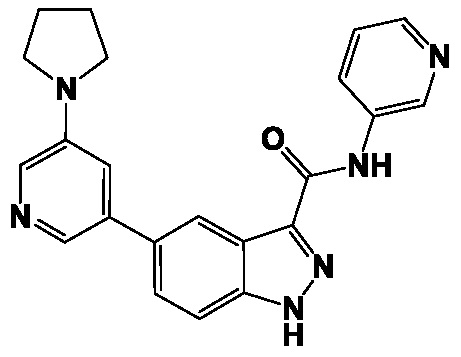
189
[0584] N-(Пиридин-3-ил)-5-(5-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 189.
[0585] Белое твердое вещество (30 мг, 0,08 ммоль, выход 26,0%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,91-2,05 (м, 4H), 3,33-3,39 (м, 4H), 7,09 (с, 1H), 7,40 (к, J=8 Гц, 1H), 7,79 (с, 2H), 7,96 (д, J=2,5 Гц, 1H), 8,14 (с, 1H), 8,30-8,34 (м, 2H), 8,44 (с, 1H), 9,07 (д, J=2 Гц, 1H), 10,68 (с, 1H), 13,97 (шс, 1H); ЭРИ-МС найдено для C22H20N6O m/z 385,2 (M+H).
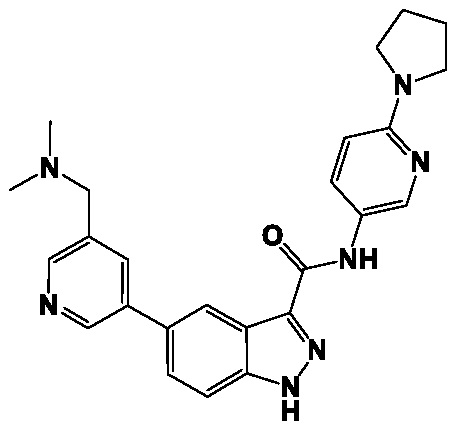
190
[0586] 5-(5-((Диметиламино)метил)пиридин-3-ил)-N-(6-(пирролидин-1-ил)пиридин-3-ил)-1H-индазол-3-карбоксамид 190.
[0587] Белое твердое вещество (142 мг, 0,32 ммоль, выход 39,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,92-1,97 (м, 4H), 2,20 (с, 6H), 3,35-3,40 (м, 4H), 3,53 (с, 2H), 6,46 (д, J=9 Гц, 1H), 7,80 (дк, J=9 Гц, J=1,5 Гц, 2H), 7,97 (дд, J=9 Гц, J=3 Гц, 1H), 8,00 (с, 1H), 8,46-8,50 (м, 3H), 8,82 (д, J=2,5 Гц, 1H), 10,22 (с, 1H), 13,86 (шс, 1H); ЭРИ-МС найдено для C25H27N7O m/z 442,4 (M+H).
Пример 6
[0588] Получение N-(6-(2-фторфенокси)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамида (18) представлено ниже на Схеме 32.
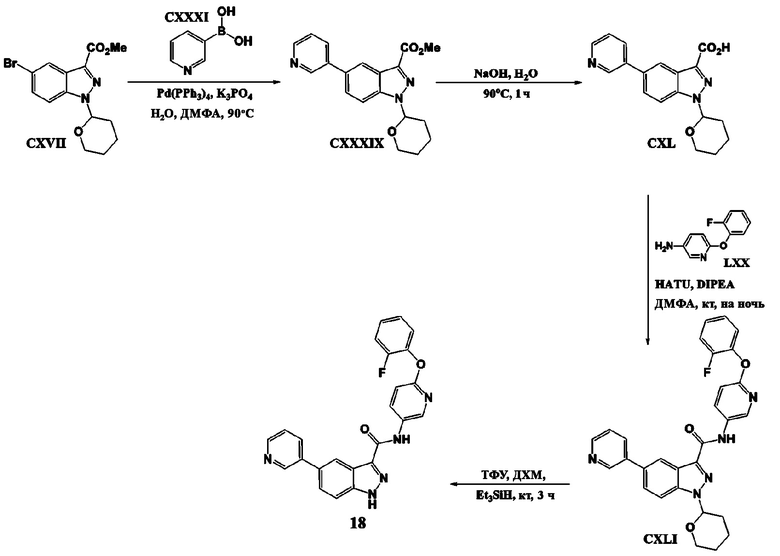
Схема 32
Стадия 1
[0589] К раствору метил-5-бром-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксилата (CXVII) (7,0 г, 20,6 ммоль) в ДМФА (80 мл) и воде (16 мл) добавляли K3PO4 (6,56 г, 30,9 ммоль), пиридин-3-илбороновую кислоту (CXXXI) (2,79 г, 22,7 ммоль) и Pd(PPh3)4 (1,19 г, 1,03 ммоль). Раствор барботировали аргоном и нагревали при 90°C в течение 3 ч. Раствор охлаждали до комнатной температуры и затем выпаривали при пониженном давлении. Остаток растворяли в ДХМ и промывали водой, сушили над MgSO4, фильтровали и затем выпаривали в вакууме. Остаток очищали на колонке с силикагелем (100% ДХМ → 1,5:98,5 MeOH:ДХМ) с получением метил-5-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксилата (CXXXIX) в виде оранжевого масла, которое затвердевало при кт (6,28 г, 18,6 ммоль, выход 90%). ЭРИ-МС найдено для C19H19N3O3 m/z 338,0 (M+H).
Стадия 2
[0590] Получение промежуточной 5-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоновой кислоты (CXL) проводили согласно методике, представленной на Схеме 25 в Стадии 4. Белое твердое вещество (900 мг, 2,78 ммоль, выход 15%). ЭРИ-МС найдено для C18H17N3O3 m/z 324,1 (M+H).
Стадия 3
[0591] Получение промежуточного N-(6-(2-фторфенокси)-пиридин-3-ил)-5-(пиридин-3-ил)-1-(тетрагидро-2H-пиран-2-ил)-1H-индазол-3-карбоксамида (CXLI) проводили согласно методике, представленной на Схеме 28 в Стадии 3. Почти белое твердое вещество (207 мг, 0,41 ммоль, выход 66%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,60-1,69 (м, 2H), 1,76-1,87 (м, 1H), 2,03-2,13 (м, 2H), 2,56-2,65 (м, 1H), 3,84 (дт, J=11 Гц, J=4 Гц, 1H), 3,99 (т, J=11 Гц, 1H), 6,07 (дд, J=10 Гц, J=2 Гц, 1H), 6,98 (дд, J=3 Гц, J=2 Гц, 1H), 7,03-7,08 (м, 2H), 7,14 (д, J=9 Гц, 1H), 7,46 (т, J=7 Гц, 1H), 7,61 (дд, J=8 Гц, J=5 Гц, 1H), 7,91 (дд, J=9 Гц, J=2 Гц, 1H), 8,05 (д, J=9 Гц, 1H), 8,25 (д, J=8 Гц, 1H), 8,37 (дд, J=9 Гц, J=3 Гц, 1H), 8,49 (с, 1H), 8,64 (дд, J=5 Гц, J=2 Гц, 1H), 8,66 (д, J=3 Гц, 1H), 9,00 (д, J=2 Гц, 1H), 10,59 (с, 1H); ЭРИ-МС найдено для C29H24FN5O3 m/z 509,2 (M+H).
Стадия 4
[0592] Получение N-(6-(2-фторфенокси)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамида (18) проводили согласно методике, представленной на Схеме 28 в Стадии 4. Белое твердое вещество (128 мг, 0,30 ммоль, выход 54,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 7,16 (д, J=9 Гц, 1H), 7,23-7,39 (м, 4H), 7,52 (дд, J=8 Гц, J=5 Гц, 1H), 7,79-7,85 (м, 2H), 8,13 (тд, J=8 Гц, J=2 Гц, 1H), 8,38 (дд, J=9 Гц, J=3 Гц, 1H), 8,46 (с, 1H), 8,56 (д, J=3 Гц, 1H), 8,59 (дд, J=5 Гц, J=1 Гц, 1H), 8,93 (д, J=2 Гц, 1H), 10,65 (с, 1H), 13,96 (шс, 1H); ЭРИ-МС найдено для C24H16FN5O2 m/z 426,0 (M+H).
[0593] Следующие соединения получали в соответствии с методикой, описанной выше в Примере 6.
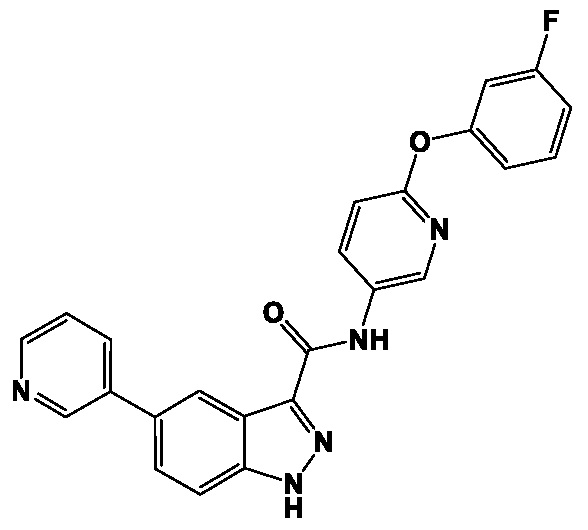
19
[0594] N-(6-(3-Фторфенокси)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 19.
[0595] Почти белое твердое вещество (148 мг, 0,35 ммоль, выход 89,3%). 1H-ЯМР (ДМСО-d6) δ м.д. 6,98 (дд, J=8 Гц, J=2 Гц, 1H), 7,01-7,06 (м, 2H), 7,13 (д, J=9 Гц, 1H), 7,44 (к, J=7 Гц, 1H), 7,53 (дд, J=8 Гц, J=5 Гц, 1H), 7,80-7,85 (м, 2H), 8,14 (тд, J=6 Гц, J=2 Гц, 1H), 8,40 (дд, J=9 Гц, J=3 Гц, 1H), 8,47 (с, 1H), 8,60 (дд, J=5 Гц, J=1 Гц, 1H), 8,69 (д, J=3 Гц, 1H), 8,93 (д, J=2 Гц, 1H), 10,71 (с, 1H), 13,99 (с, 1H); ЭРИ-МС найдено для C24H16FN5O2 m/z 426,0 (M+H).
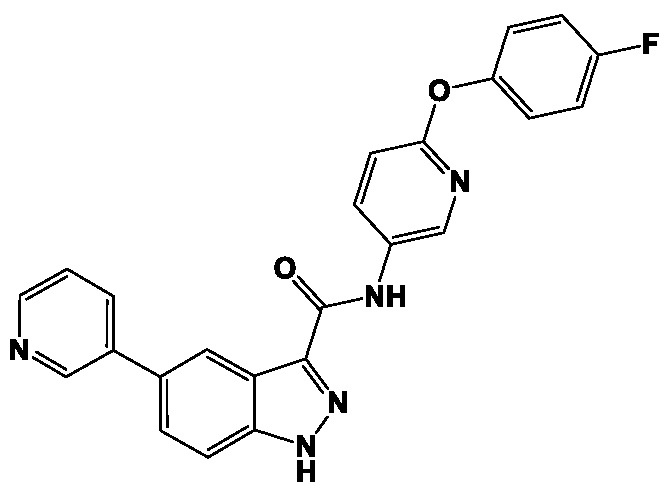
20
[0596] N-(6-(4-Фторфенокси)пиридин-3-ил)-5-(пиридин-3-ил)-1H-индазол-3-карбоксамид 20.
[0597] Белое твердое вещество (82 мг, 0,19 ммоль, выход 91,8%). 1H-ЯМР (ДМСО-d6) δ м.д. 7,08 (д, J=9 Гц, 1H), 7,15-7,21 (м, 2H), 7,22-7,27 (м, 2H), 7,67 (дд, J=8 Гц, J=5 Гц, 1H), 7,81-7,88 (м, 2H), 8,31 (д, J=8 Гц, 1H), 8,36 (дд, J=9 Гц, J=3 Гц, 1H), 8,51 (с, 1H), 8,63 (д, J=3 Гц, 1H), 8,66 (дд, J=5 Гц, J=1 Гц, 1H), 9,02 (д, 2 Гц, 1H), 10,67 (с, 1H), 14,00 (с, 1H); ЭРИ-МС найдено для C24H16FN5O2 m/z 426,0 (M+H).
Пример 7
[0598] Получение N-(6-карбамоилпиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (180) представлено ниже на Схеме 33.
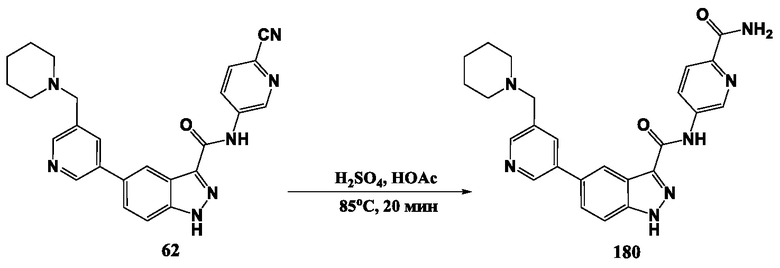
Схема 33
Стадия 1
[0599] К раствору N-(6-цианопиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (62) (200 мг, 0,45 ммоль) в ледяной уксусной кислоте (2 мл), нагреваемому при 85°C, осторожно по каплям добавляли серную кислоту (2 мл). Реакцию нагревали при 85°C еще в течение 20 минут, после чего выливали в лед. Раствор подщелачивали холодным 5Н NH4OH. Образовавшее твердое вещество отфильтровывали, промывали холодной водой и сушили в вакууме. Сухое твердое вещество суспендировали в ДХМ и добавляли несколько капель MeOH. Нерастворимое твердое вещество отфильтровывали и отбрасывали. Фильтрат выпаривали и снова суспендировали в ДХМ, кипятили в течение 15 минут и фильтровали. Твердое вещество сушили в вакууме с получением N-(6-карбамоилпиридин-3-ил)-5-(5-(пиперидин-1-илметил)пиридин-3-ил)-1H-индазол-3-карбоксамида (180) в виде белого твердого вещества (192 мг, 0,42 ммоль, выход 93,7%). 1H-ЯМР (ДМСО-d6) δ м.д. 1,36-1,42 (м, 2H), 1,48-1,55 (м, 4H), 2,38 (шс, 4H), 3,56 (с, 2H), 7,49 (с, 1H), 7,65 (д, J=9 Гц, 1H), 7,80 (д, J=9 Гц, 1H), 7,97 (с, 1H), 8,03 (с, 2H), 8,41 (с, 1H), 8,45 (д, J=2 Гц, 1H), 8,54 (дд, J=9 Гц, J=2,5 Гц, 1H), 8,80 (д, J=2 Гц, 1H), 9,15 (д, J=2 Гц, 1H), 10,83 (шс, 1H); ЭРИ-МС найдено для C25H25N7O2 m/z 456,4 (M+H).
Введение и фармацевтические композиции
[0600] Некоторые варианты осуществления включают фармацевтические композиции, включающие: (a) безопасное и терапевтически эффективное количество индазол-3-карбоксамида или его соответствующего энантиомера, диастереоизомера или таутомера, или фармацевтически приемлемой соли; и (b) фармацевтически приемлемый носитель.
[0601] В некоторых вариантах осуществления способы, описанные в настоящем документе, дополнительно включают введение соединений настоящего изобретения в комбинации (вводимых вместе или последовательно) с другими известными средствами.
[0602] Введение соединений, раскрытых в настоящем документе, или их фармацевтически приемлемых солей может быть выполнено любыми приемлемыми способами введения средств, которые имеют аналогичное назначение, в том числе, без ограничения перечисленным, перорально, подкожно, внутривенно, интраназально, наружно, трансдермально, внутрибрюшинно, внутримышечно, внутрилегочно, вагинально, ректально, онтологически, нейроотологически, интраокулярно, субконъюктивально, путем инъекции в переднюю камеру глаза, интравитреально, интраперитонеально, интратекально, внутрикистозно, внутриплеврально, путем орошения раны, интрабуккально, интраабдоминально, внутрисуставно, в ухо, внутрибронхиально, интракапсулярно, интраменингеально, ингаляционно, путем эндотрахеальной или эндобронхиальной инстилляции, путем прямой инстилляции в легочные полости, интраспинально, интрасиновиально, интраторакально, путем орошения при дренировании плевральной полости, эпидурально, внутригрудинно, интрацистернально, внутрисосудисто, интравентрикулярно, внутрикостно, путем орошения инфицированной кости или путем нанесения в виде компонента любой смеси на протезные устройства. Пероральное и парентеральное введение является стандартным при лечении показаний.
[0603] Соединения согласно изобретению, предназначенные для фармацевтического применения, могут быть введены в виде кристаллических или аморфных продуктов. Фармацевтически приемлемые композиции могут включать твердые вещества, полутвердые вещества, жидкости, растворы, коллоидные вещества, липосомы, эмульсии, суспензии, комплексы, коацерваты и аэрозоли. Лекарственные формы, такие как, например, таблетки, капсулы, порошки, жидкости, суспензии, суппозитории, аэрозоли, имплантаты, формы с контролируемым высвобождением и т.п. Они могут быть получены, например, в виде прессованной массы, порошков или пленок такими способами, как осаждение, кристаллизация, размол, измельчение, обработка сверхкритической жидкостью, коацервация, комплексная коацервация, инкапсулирование, эмульгирование, комплексообразование, лиофильная сушка, распылительная сушка или сушка выпариванием. Для этой цели может использоваться микроволновая или радиочастотная сушка. Соединения также могут быть введены в лекарственных формах с пролонгированным или контролируемым высвобождением, включая депо-инъекции, осмотические насосы, пилюли (таблетки и/или капсулы), трансдермальные (включая электроперенос) пластыри, имплантаты и т.п., для пролонгированного и/или регулируемого по времени импульсного введения с заданной скоростью.
[0604] Соединения могут быть введены либо отдельно, либо, что более обычно, в комбинации со стандартным фармацевтическим носителем, вспомогательным веществом и т.п. Термин "вспомогательное вещество" используется в настоящем документе для описания любого другого ингредиента кроме соединения(й) согласно изобретению. Фармацевтически приемлемые вспомогательные вещества включают, без ограничения перечисленными, ионообменные материалы, оксид алюминия, стеарат алюминия, лецитин, самоэмульгируемые системы доставки лекарственных средств (SEDDS), такие как D-α-токоферола полиэтиленгликоль 1000 сукцинат, поверхностно-активные вещества, используемые в лекарственных формах, такие как Tween, полоксамеры или другие подобные полимерные матрицы доставки, сывороточные белки, такие как человеческий сывороточный альбумин, буферные вещества, такие как фосфаты, трис, глицин, сорбиновая кислота, сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как протамина сульфат, динатрия гидрофосфат, калия гидрофосфат, натрия хлорид, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натрий-карбоксиметилцеллюлозу, полиакрилаты, воски, блокполимеры полиэтилена-полиоксипропилена и ланолин. Циклодекстрины, такие как α-, β- и γ-циклодекстрин, или химически модифицированные производные, такие как гидроксиалкилциклодекстрины, включая 2- и 3-гидроксипропил-b-циклодекстрины, или другие солюбилизированные производные, также могут эффективно использоваться для улучшения доставки соединений формул, описанных в настоящем документе. Могут быть изготовлены лекарственные формы или композиции, содержащие соединение, как описано в настоящем документе, в пределах от 0,005% до 100%, при этом остальная часть состоит из нетоксичного носителя. Предполагаемые композиции могут содержать 0,001%-100% действующего вещества, в одном варианте осществления - 0,1-95%, в другом варианте осуществления - 75-85%, в другом варианте осуществления - 20-80%. Применяемые в настоящее время способы изготовления таких лекарственных форм известны или будут очевидны для специалистов в данной области техники, например, см. Remington: The Science and Practice of Pharmacy, 21st Edition (Lippincott Williams & Wilkins. 2005).
[0605] В одном предпочтительном варианте осуществления композиции будут иметь форму стандартной лекарственной формы, такой как пилюля или таблетка, и, таким образом, композиция наряду с действующим веществом может содержать разбавитель, такой как лактозу, сахарозу, фосфат дикальция и т.п.; смазывающее вещество, такое как стеарат магния и т.п.; и связующее вещество, такое как крахмал, гуммиарабик, поливинилпирролидон, желатин, целлюлозу, производные целлюлозы и т.п. В другой твердой лекарственной форме порошок, марумеризированные гранулы, раствор или суспензия (например, в пропиленкарбонате, растительных маслах, ПЭГ, полоксамере 124 или триглицеридах) заключены в капсулу (желатиновую или целлюлозную капсулу). Также предусмотрены стандартные лекарственные формы, в которых два действующих вещества разделены физически; например, капсулы с гранулами (или таблетками в капсуле) каждого лекарственного средства; двухслойные таблетки; двухкамерные желатиновые капсулы и т.д. Также предусмотрены лекарственные формы для приема внутрь с кишечнорастворимым покрытием или с отсроченным высвобождением.
[0606] Жидкие фармацевтически вводимые композиции могут быть изготовлены, например, путем растворения, диспергирования и т.д. активного соединения, как определено выше, и, необязательно, фармацевтических вспомогательных веществ в носителе (например, в воде, физиологическом растворе, водном растворе декстрозы, глицерине, гликолях, этаноле и т.п.) с получением раствора, коллоида, липосомы, эмульсии, комплексов, коацервата или суспензии. При необходимости фармацевтическая композиция может также содержать небольшие количества нетоксичных вспомогательных веществ, таких как смачивающие вещества, эмульгирующие вещества, сорастворители, солюбилизирующие вещества, рН-буферные вещества и т.п. (например, ацетат натрия, цитрат натрия, производные циклодекстрина, сорбитанмонолаурат, ацетат триэтаноламина, олеат триэтаноламин и т.п.).
[0607] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 0,25 мг/кг до 50 мг/кг.
[0608] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 0,25 мг/кг до 20 мг/кг.
[0609] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 0,50 мг/кг до 19 мг/кг.
[0610] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 0,75 мг/кг до 18 мг/кг.
[0611] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 1,0 мг/кг до 17 мг/кг.
[0612] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 1,25 мг/кг до 16 мг/кг.
[0613] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 1,50 мг/кг до 15 мг/кг.
[0614] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 1,75 мг/кг до 14 мг/кг.
[0615] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 2,0 мг/кг до 13 мг/кг.
[0616] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 3,0 мг/кг до 12 мг/кг.
[0617] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 4,0 мг/кг до 11 мг/кг.
[0618] В некоторых вариантах осуществления однократная доза соединений Формулы (I) при медицинском применении составляет от 5,0 мг/кг до 10 мг/кг.
[0619] В некоторых вариантах осуществления композиции представлены в единичных лекарственных формах, подходящих для однократного введения точной дозы.
[0620] В некоторых вариантах осуществления композиции представлены в единичных лекарственных формах, подходящих для введения точной дозы два раза в день.
[0621] В некоторых вариантах осуществления композиции представлены в единичных лекарственных формах, подходящих для введения точной дозы три раза в день.
[0622] Препараты для инъекций могут быть изготовлены в стандартных формах, либо в виде жидких растворов, коллоида, липосом, комплексов, коацервата или суспензий, в виде эмульсий, либо в твердых формах, пригодных для восстановления в жидкость перед инъекцией. Процентное содержание активного соединения, содержащегося в такой композиции для парентерального введения, в значительной степени зависит от его природы, а также от активности соединения и потребностей субъекта. В любом случае, используемое процентное содержание действующего вещества в растворе составляет от 0,01% до 10% и может быть выше, если композиция представляет собой твердое вещество или суспензию, которые могут быть впоследствии разбавлены до вышеуказанного процентного содержания.
[0623] В некоторых вариантах осуществления инъекция может быть внутрисухожильной инъекцией.
[0624] В некоторых вариантах осуществления композиция будет включать 0,1-10% действующего вещества в растворе.
[0625] В некоторых вариантах осуществления композиция будет включать 0,1-5% действующего вещества в растворе.
[0626] В некоторых вариантах осуществления композиция будет включать 0,1-4% действующего вещества в растворе.
[0627] В некоторых вариантах осуществления композиция будет включать 0,15-3% действующего вещества в растворе.
[0628] В некоторых вариантах осуществления композиция будет включать 0,2-2% действующего вещества в растворе.
[0629] В некоторых вариантах осуществления композиции представлены в лекарственных формах, подходящих для непрерывного введения путем внутривенной инфузии в течение 1-96 часов.
[0630] В некоторых вариантах осуществления композиции представлены в лекарственных формах, подходящих для непрерывного введения путем внутривенной инфузии в течение 1-72 часов.
[0631] В некоторых вариантах осуществления композиции представлены в лекарственных формах, подходящих для непрерывного введения путем внутривенной инфузии в течение 1-48 часов.
[0632] В некоторых вариантах осуществления композиции представлены в лекарственных формах, подходящих для непрерывного введения путем внутривенной инфузии в течение 1-24 часов.
[0633] В некоторых вариантах осуществления композиции представлены в лекарственных формах, подходящих для непрерывного введения путем внутривенной инфузии в течение 1-12 часов.
[0634] В некоторых вариантах осуществления композиции представлены в лекарственных формах, подходящих для непрерывного введения путем внутривенной инфузии в течение 1-6 часов.
[0635] В некоторых вариантах осуществления эти композиции могут вводить путем внутривенной инфузии людям в дозах от 5 мг/м2 до 300 мг/м2.
[0636] В некоторых вариантах осуществления эти композиции могут вводить путем внутривенной инфузии людям в дозах от 5 мг/м2 до 200 мг/м2.
[0637] В некоторых вариантах осуществления эти композиции могут вводить путем внутривенной инфузии людям в дозах от 5 мг/м2 до 100 мг/м2.
[0638] В некоторых вариантах осуществления эти композиции могут вводить путем внутривенной инфузии людям в дозах от 10 мг/м2 до 50 мг/м2.
[0639] В некоторых вариантах осуществления эти композиции могут вводить путем внутривенной инфузии людям в дозах от 50 мг/м2 до 200 мг/м2.
[0640] В некоторых вариантах осуществления эти композиции могут вводить путем внутривенной инфузии людям в дозах от 75 мг/м2 до 175 мг/м2.
[0641] В некоторых вариантах осуществления эти композиции могут вводить путем внутривенной инфузии людям в дозах от 100 мг/м2 до 150 мг/м2.
[0642] В одном предпочтительном варианте осуществления композиции могут вводить в дыхательные пути (в том числе назально и пульмонально), например, с помощью небулайзера, дозирующих ингаляторов, атомайзера, мелкокапельного распылителя, аэрозоля, порошкового ингалятора, инсуффлятора, инсталяции жидкости или другого подходящего устройства или способа.
[0643] В некоторых вариантах осуществления аэрозоли, предназначенные для доставки на слизистую оболочку носа, предусматривают ингаляцию через нос. Для оптимальной доставки в полости носа подходящим является размер вдыхаемых частиц от приблизительно 5 до приблизительно 100 микронов, и предпочтительным является размер частиц от приблизительно 10 до приблизительно 60 микрон. В случае назальной доставки необходим больший размер вдыхаемых частиц, чтобы максимально увеличить воздействие на слизистую оболочку носа и свести к минимуму или исключить накопление введенной композиции в легких. В некоторых вариантах осуществления аэрозоли, предназначенные для доставки в легкие, предусматривают вдыхание через нос или рот. Для оптимальной доставки в легкие подходящим является аэродинамический размер вдыхаемых частиц, меньший или равный 10 мкм, и предпочтительным является аэродинамический размер частиц от приблизительно 0,1 до 10 мкм. Вдыхаемые частицы могут быть определены как капли жидкости, содержащей растворенное лекарственное средство, капли жидкости, содержащей суспендированные частицы лекарственного средства (в случаях, когда лекарственное средство нерастворимо в суспендирующей среде), сухие частицы чистой лекарственной субстанции, лекарственная субстанция, объединенная со вспомогательными веществами, липосомами, эмульсиями, коллоидными системами, коацерватами, агрегатами наночастиц лекарственного средства, или сухие частицы разбавителя, которые содержат включенные наночастицы лекарственного средства.
[0644] В некоторых вариантах осуществления соединения Формулы (I), раскрытые в настоящем документе, предназначенные для доставки в дыхательные пути (системной или местной), могут быть введены в виде водных композиций, в виде неводных растворов или суспензий, в виде суспензий или растворов в галогенированных углеводородных пропеллентах со спиртом или без него, в виде коллоидной системы, в виде эмульсий, коацерватов или в виде сухих порошков. Водные препараты могут распылять в виде аэрозоля с помощью небулайзеров для жидкостей, в которых используется гидравлическое или ультразвуковое распыление, или с помощью модифицированных микронасосных систем (например, ингаляторов Soft mist, систем Aerodose® или AERx®). В системах на основе пропеллентов могут использоваться подходящие дозирующие ингаляторы под давлением (pMDI). Для сухих порошков могут использоваться порошковые ингаляторные устройства (DPI), которые способны эффективно диспергировать лекарственную субстанцию. Требуемый размер и распределение частиц могут быть получены путем выбора соответствующего устройства.
[0645] В некоторых вариантах осуществления композиции Формулы (I), раскрытые в настоящем документе, могут вводить в ухо различными способами. Например, может использоваться катетер для круглого окна улитки (например, патенты США 6,440,102 и 6,648,873).
[0646] В альтернативе, композиции могут быть включены в тампон для использования между наружным ухом и средним ухом (например, патент США 6,120,484) или абсорбированы на коллагеновой губке или другой твердой подложке (например, патент США 4,164,559).
[0647] При необходимости композиции согласно изобретению могут быть включены в гелевую композицию (например, патенты США 4,474,752 и 6,911,211).
[0648] В некоторых вариантах осуществления соединения Формулы (I), раскрытые в настоящем документе, предназначенные для доставки в ухо, могут быть введены с помощью имплантируемого насоса и системы доставки через иглу, непосредственно в среднее или внутреннее ухо (улитку), или через канал стилетного электрода кохлеарного имплантата, или альтернативный подготовленный канал для доставки лекарственных средств, такой как, без ограничения, игла через височную кость, в улитку.
[0649] Другие варианты включают доставку с помощью насоса через тонкую пленку, нанесенную на многоканальный электрод или электрод со специально встроенным каналом (путями) доставки лекарственного средства, вырезанным в тонкой пленке для этой цели. В других вариантах осуществления кислотный или основной твердый гациклидин может быть доставлен из резервуара внешней или внутренней имплантируемой насосной системы.
[0650] Композиции согласно изобретению также могут вводить в ухо путем интратимпанальной инъекции в среднее ухо, внутреннее ухо или в улитку (например, патент США 6,377,849 и заявка 11/337,815).
[0651] Интратимпанальная инъекция лекарственных средств является способом введения лекарственного средства за барабанную перепонку в среднее и/или внутреннее ухо. В одном из вариантов осуществления композиции, описанные в настоящем документе, наносят непосредственно на мембрану круглого окна улитки с помощью инъекции через барабанную перепонку. В другом варианте осуществления приемлемые для введения в ухо композиции средства, модулирующего ионный канал, описанные в настоящем документе, наносят на мембрану круглого окна улитки путем нетранстимпанального доступа во внутреннее ухо. В дополнительных вариантах осуществления композицию, описанную в настоящем документе, наносят на мембрану круглого окна улитки путем хирургического доступа к мембране круглого окна улитки, включающего модификацию гребня круглого окна улитки.
[0652] В некоторых вариантах осуществления соединения Формулы (I) включены в композиции для ректального введения, такие как спринцовки, ректальные гели, ректальные пены, ректальные аэрозоли, суппозитории, желеобразные суппозитории, суппозитории или удерживаемые клизмы, содержащие обычные основы для суппозиториев, такие как масло какао или другие глицериды, а также синтетические полимеры, такие как поливинилпирролидон, ПЭГ (например, мази на основе ПЭГ) и т.п. В суппозиторных формах композиций воск с низкой температурой плавления, например, без ограничения, смесь глицеридов жирных кислот, необязательно в комбинации с маслом какао, сначала расплавляют.
[0653] Суппозитории для ректального введения лекарственного средства (в виде раствора, коллоида, суспензии или комплекса) могут быть изготовлены путем смешивания лекарственного средства с подходящим, не вызывающим раздражение вспомогательным веществом, который является твердым при обычных температурах, но является жидким при ректальной температуре, и поэтому будет плавиться или разрушаться/растворяться в прямой кишке и высвобождать лекарственное средство. Такие материалы включают масло какао, глицеринизированный желатин, гидрогенированные растительные масла, полоксамеры, смеси полиэтиленгликолей разной молекулярной массы и сложные эфиры жирных кислот и полиэтиленгликоля.
[0654] В некоторых вариантах осуществления композиции могут вводить с помощью трансдермального пластыря.
[0655] Другие способы доставки включают применение биоразлагаемых или небиоразлагаемых каркасов.
[0656] Следует отметить, что значения концентраций и доз могут также изменяться в зависимости от тяжести состояния, подлежащего облегчению. Следует также понимать, что для каждого конкретного пациента определенные схемы применения нужно корректировать с течением времени в соответствии с индивидуальной потребностью и профессиональным решением лица, производящего или контролирующего введение композиции, и что диапазоны концентраций, представленные в настоящем документе, являются лишь примерными и не ограничивают объем изобретения или практическое применение заявленных композиций.
[0657] Твердые композиции могут быть предоставлены в различных типах лекарственных форм в зависимости от физико-химических свойств лекарственного средства, требуемой скорости растворения, факторов стоимости и других критериев. В одном из вариантов осуществления твердая композиция представляет собой отдельную единицу. Это подразумевает, что одна однократная доза лекарственного средства содержится в отдельной, физически оформленной твердой форме или продукте. Другими словами, твердая композиция является монолитной, в отличие от дозированной лекарственной формы, образованной множественными единицами, в которой единицы не являются связанными.
[0658] Примеры отдельных единиц, которые могут использоваться в качестве лекарственных форм для твердой композиции, включают таблетки, такие как прессованные таблетки, единицы в форме пленки, единицы в форме фольги, облатки, лиофилизированные матричные единицы и т.п. В предпочтительном варианте осуществления твердая композиция представляет собой лиофилизированную форму с высокой пористостью. Такие лиофилизаты, иногда также называемые облатками или лиофилизированными таблетками, в частности, используют из-за их быстрого распада, что также способствует быстрому растворению активного соединения.
[0659] С другой стороны, для некоторых применений, твердая композиция также может быть изготовлена в виде дозированной лекарственной формы, образованной множественными единицами, как определено выше. Примерами множественных единиц являются порошки, гранулы, микрочастицы, пеллеты, минитаблетки, сферы, лиофилизированные порошки и т.п. В одном варианте осуществления твердая композиция является лиофилизированным порошком. Такая дисперсная лиофилизированная система содержит множество частиц в виде порошка, и, вследствие использования процесса лиофилизации при получении порошка, каждая частица имеет нерегулярную пористую микроструктуру, посредством которой порошок способен очень быстро поглощать воду, что приводит к быстрому растворению. Шипучие композиции также предумотрены для быстрого образования дисперсии и абсорбции соединения.
[0660] Другой тип системы в форме множества частиц, которая также способна обеспечивать быстрое растворение лекарственного средства, представляет собой системы порошков, гранул или драже из водорастворимых вспомогательных веществ, которые покрыты лекарственным средством, в результате чего лекарственное средство расположено на внешней поверхности отдельных частиц. В таком типе системы водорастворимое низкомолекулярное вспомогательное вещество применяют для изготовления ядер таких покрытых оболочкой частиц, которые затем могут быть покрыты композицией для получения покрытия, содержащей лекарственное средство и, предпочтительно, один или более дополнительных вспомогательных веществ, таких как связывающее вещество, порообразователь, сахарид, сахароспирт, пленкообразующий полимер, пластификатор или другие вспомогательные вещества, используемые в фармацевтических композициях для получения покрытий.
[0661] Также в настоящем документе предложены наборы. Обычно набор включает одно или более соединений или композиций, описанных в настоящем документе. В некоторых вариантах осуществления набор может включать одну или более систем доставки, например, для доставки или введения соединения, как представлено выше, а также инструкцию по применению набора (например, инструкции для лечения пациента). В другом варианте осуществления набор может включать соединение или композицию, как описано в настоящем документе, и этикетку, которая указывает, что содержимое следует вводить пациенту со злокачественной опухолью. В другом варианте осуществления набор может включать соединение или композицию, как описано в настоящем документе, и этикетку, которая указывает, что содержимое следует вводить пациенту с одним или более заболеваниями или состояниями, независимо выбранными из группы, состоящей из тендинопатии, дерматита, псориаза, бляшечной склеродермии, ихтиоза, синдрома Рейно и болезни Дарье; и/или для ускорения заживления раны.
[0662] Фактическая доза активных соединений согласно настоящему изобретению зависит от конкретного соединения и от состояния, подлежащего лечению; подбор подходящей дозы находится в рамках знаний квалифицированного специалиста.
Способы лечения
[0663] Соединения и композиции, предложенные в настоящем документе, могут применяться в качестве ингибиторов и/или модуляторов одного или более компонентов пути Wnt, который может включать один или более белков Wnt, и, таким образом, могут применяться для лечения различных нарушений и заболеваний, при которых нарушена сигнализация Wnt. Неограничивающие примеры включают одно или более заболеваний или состояний, независимо выбранных из группы, состоящей из тендинопатии, дерматита, псориаза, бляшечной склеродермии, ихтиоза, синдрома Рейно и болезни Дарье. В некоторых вариантах осуществления соединения и композиции, предложенные в настоящем документе, могут применяться для ускорения заживления ран.
[0664] В некоторых вариантах осуществления способы дополнительно включают введение нуждающемуся в таком лечении пациенту эффективного количества одного или более соединений Формулы (I) в комбинации (одновременно или последовательно) по меньшей мере с еще одним средством.
[0665] В некоторых вариантах осуществления способы дополнительно включают введение фармацевтической композиции, которая включает терапевтически эффективное количество соединения Формулы (I) или его фармацевтически приемлемой соли и фармацевтически приемлемое вспомогательное вещество, и, необязательно, по меньшей мере еще одного средства.
[0666] В некоторых вариантах осуществления одним или более заболеваниями или состояниями является тендинопатия. В некоторых вариантах осуществления тендинопатия является тендинозом. В некоторых вариантах осуществления тендинопатия является тендинитом. В некоторых вариантах осуществления тендинопатия является тендовагинитом.
[0667] Сухожилие представляет собой образование из волокнистой соединительной ткани, которое обычно соединяет мышцы с костью. Здоровые сухожилия включают параллельные пучки коллагеновых волокон I типа, плотно упакованные вместе, но также включают небольшое количество эластина и протеогликанов. Сухожилия могут медленно восстанавливаться при повреждении, и иногда не могут восстановить свою первоначальную прочность. Частичные разрывы заживают благодаря быстрой выработке дезорганизованного коллагена III типа, который обладает меньшей прочностью, чем нормальное сухожилие. Повторная травма в поврежденной области сухожилия является распространенным явлением.
[0668] Сухожилия, которые можно лечить способами согласно изобретению, включают любое сухожилие тела человека или млекопитающего. Неограничивающие примеры сухожилий включают сухожилие надколенника, сухожилие передней большеберцовой мышцы, ахиллово сухожилие, подколенное сухожилие, сухожилие полусухожильной мышцы, сухожилие тонкой мышцы, сухожилие отводящей мышцы, сухожилие приводящей мышцы, сухожилие надостной мышцы, сухожилие подостной мышцы, сухожилие подлопаточной мышцы, сухожилие малой круглой мышцы, сухожилие сгибателя, сухожилие прямой мышцы бедра, сухожилие задней большеберцовой мышцы и сухожилие четырехглавой мышцы бедра.
[0669] В некоторых вариантах осуществления сухожилие является сухожилием стопы или лодыжки; например, длинного разгибателя большого пальца стопы, длинного сгибателя большого пальца стопы, длинного разгибателя пальцев, короткого разгибателя пальцев, длинной малоберцовой мышцы, короткой малоберцовой мышцы, короткого сгибателя большого пальца стопы, длинного сгибателя пальцев, задней большеберцовой мышцы, ахилловым сухожилием и плантарной фасцией.
[0670] В некоторых вариантах осуществления сухожилие является сухожилием ноги; например, сухожилием надколенника, сухожилием передней большеберцовой мышцы, ахилловым сухожилием, подколенным сухожилием, сухожилием полусухожильной мышцы, сухожилием тонкой мышцы, сухожилием отводящей мышцы, сухожилием приводящей мышцы, сухожилием сгибателя, сухожилием прямой мышцы бедра, сухожилием задней большеберцовой мышцы и сухожилием четырехглавой мышцы бедра.
[0671] В некоторых вариантах осуществления сухожилие является сухожилием плеча; например, сухожилием надостной мышцы, сухожилием подостной мышцы, сухожилием подлопаточной мышцы и сухожилием малой круглой мышцы (комплекса вращательной манжеты).
[0672] В некоторых вариантах осуществления сухожилие является сухожилием локтя; например, сухожилием бицепса, сухожилием трицепса, короткого лучевого разгибателя запястья, сухожилием общего разгибателя, разгибателя пальцев, разгибателя мизинца, локтевого разгибателя запястья, супинатора, сухожилием общего сгибателя, круглого пронатора, лучевого сгибателя запястья, длинной ладонной мышцы, локтевого сгибателя запястья и поверхностного сгибателя пальцев. В некоторых вариантах осуществления сухожилие является сухожилием запястья. В некоторых вариантах осуществления сухожилие запястья выбрано из группы, состоящей из сухожилия бицепса, сухожилия трицепса, короткого лучевого разгибателя запястья, сухожилия общего разгибателя, разгибателя пальцев, разгибателя мизинца, локтевого разгибателя запястья, супинатора, сухожилия общего сгибателя, круглого пронатора, лучевого сгибателя запястья, длинной ладонной мышцы, локтевого сгибателя запястья, поверхностного сгибателя пальцев, короткого сгибателя большого пальца, длинного сгибателя большого пальца, короткой отводящей мышцы большого пальца, длинной отводящей мышцы большого пальца, глубокого сгибателя пальцев, поверхностного сгибателя пальцев, короткого разгибателя большого пальца и длинного разгибателя большого пальца. В некоторых вариантах осуществления сухожилие является сухожилием кисти. В некоторых вариантах осуществления сухожилие кисти выбрано из группы, состоящей из короткого сгибателя большого пальца, длинного сгибателя большого пальца, короткой отводящей мышцы большого пальца, длинной отводящей мышцы большого пальца, глубокого сгибателя пальцев, поверхностного сгибателя пальцев, короткого разгибателя большого пальца и длинного разгибателя большого пальца.
[0673] Неограничивающие примеры тендинопатий включают: ключичную или пателлярную тендинопатию, пателлярный тендинит; синдром напряжения медиальной поверхности большеберцовой кости; тендинопатию ахиллова сухожилия, латеральный эпикондилит или "теннисный локоть"; медиальный эпикондилит или "локоть гольфиста"; плантарный фасциит; и тендинопатию вращательной манжеты плечевого сустава.
[0674] В некоторых вариантах осуществления тендинопатия является тендинопатией вращательной манжеты; например, тендинопатией надостной мышцы, тендинопатией подостной мышцы, тендинопатией подлопаточной мышцы и тендинопатией малой круглой мышцы.
[0675] В некоторых вариантах осуществления тендинопатия является латеральным эпикондилитом или "теннисным локтем" в начале группы мышц-разгибателей в боковом прикреплении плечевого мыщелка, преимущественно в сухожилии короткого лучевого разгибателя запястья (ECRB). В некоторых вариантах осуществления тендинопатия является медиальным эпикондилитом или "локтем гольфиста" в области контакта между круглым пронатором и началом лучевого сгибателя запястья в медиальной части плечевого мыщелка.
[0676] В некоторых вариантах осуществления тендинопатия является пателлярной тендинопатией. В некоторых вариантах осуществления тендинопатия является тендинопатией ахиллова сухожилия. В некоторых вариантах осуществления тендинопатия является плантарным фасциитом. В некоторых вариантах осуществления тендинопатия является медиальным плантарным фасциитом. В некоторых вариантах осуществления тендинопатия является латеральным плантарным фасциитом.
[0677] В некоторых вариантах осуществления тендинопатия является тендинозом. В некоторых вариантах осуществления тендиноз выбран из группы, состоящей из тендиноза длинного разгибателя большого пальца стопы, тендиноза длинного сгибателя большого пальца стопы, тендиноза длинного разгибателя пальцев, тендиноза короткого разгибателя пальцев, тендиноза длинной малоберцовой мышцы, тендиноза короткой малоберцовой мышцы, тендиноза короткого сгибателя большого пальца стопы, тендиноза длинного сгибателя пальцев, тендиноза задней большеберцовой мышцы, тендиноза ахиллова сухожилия и тендиноза плантарной фасции. В некоторых вариантах осуществления тендиноз выбран из группы, состоящей из пателлярного тендиноза, тендиноза передней большеберцовой мышцы, тендиноза подколенного сухожилия, тендиноза полусухожильной мышцы, тендиноза тонкой мышцы, тендиноза отводящей мышцы и тендиноза приводящей мышцы. В некоторых вариантах осуществления тендиноз выбран из группы, состоящей из тендиноза сгибателя, тендиноза прямой мышцы бедра, тендиноза задней большеберцовой мышцы и тендиноза квадрицепса бедра. В некоторых вариантах осуществления тендиноз выбран из группы, состоящей из тендиноза надостной мышцы, тендиноза подостной мышцы, тендиноза подлопаточной мышцы и тендиноза малой круглой мышцы.
[0678] В некоторых вариантах осуществления тендиноз выбран из группы, состоящей из тендиноза бицепса, тендиноза трицепса, тендиноза короткого лучевого разгибателя запястья, тендиноза общего разгибателя, тендиноза разгибателя пальцев, тендиноза разгибателя мизинца, тендиноза локтевого разгибателя запястья, тендиноза супинатора, тендиноза общего сгибателя, тендиноза круглого пронатора, тендиноза лучевого сгибателя запястья, тендиноза длинной ладонной мышцы, тендиноза локтевого сгибателя запястья и тендиноза поверхностного сгибателя пальцев. В некоторых вариантах осуществления тендиноз выбран из группы, состоящей из тендиноза бицепса, тендиноза трицепса, тендиноза короткого лучевого разгибателя запястья, тендиноза общего разгибателя, тендиноза разгибателя пальцев, тендиноза разгибателя мизинца, тендиноза локтевого разгибателя запястья, тендиноза супинатора, тендиноза общего сгибателя, тендиноза круглого пронатора, тендиноза лучевого сгибателя запястья, тендиноза длинной ладонной мышцы, тендиноза локтевого сгибателя запястья, тендиноза поверхностного сгибателя пальцев, тендиноза короткого сгибателя большого пальца, тендиноза длинного сгибателя большого пальца, тендиноза короткой отводящей мышцы большого пальца, тендиноз длинной отводящей мышцы большого пальца, тендиноза глубокого сгибателя пальцев, тендиноза поверхностного сгибателя пальцев, тендиноза короткого разгибателя большого пальца и тендиноза длинного разгибателя большого пальца. В некоторых вариантах осуществления тендиноз выбран из группы, состоящей из тендиноза короткого сгибателя большого пальца, тендиноза длинного сгибателя большого пальца, тендиноза короткой отводящей мышцы большого пальца, тендиноза длинной отводящей мышцы большого пальца, тендиноза глубокого сгибателя пальцев, тендиноза поверхностного сгибателя пальцев, тендиноза короткого разгибателя большого пальца и тендиноза длинного разгибателя большого пальца.
[0679] В некоторых вариантах осуществления тендинопатия является тендинитом. В некоторых вариантах осуществления тендинит выбран из группы, состоящей из тендинита длинного разгибателя большого пальца стопы, тендинита длинного сгибателя большого пальца стопы, тендинита длинного разгибателя пальцев, тендинита короткого разгибателя пальцев, тендинита длинной малоберцовой мышцы, тендинита короткой малоберцовой мышцы, тендинита короткого сгибателя большого пальца стопы, тендинита длинного сгибателя пальцев, тендинита задней большеберцовой мышцы, тендинита ахиллова сухожилия и тендинита плантарной фасции. В некоторых вариантах осуществления тендинит выбран из группы, состоящей из пателлярного тендинита, тендинита передней большеберцовой мышцы, тендинита подколенного сухожилия, тендинита полусухожильной мышцы, тендинита тонкой мышцы, тендинита отводящей мышцы и тендинита приводящей мышцы. В некоторых вариантах осуществления тендинит выбран из группы, состоящей из тендинита сгибателя, тендинита прямой мышцы бедра, тендинита задней большеберцовой мышцы и тендинита квадрицепса бедра. В некоторых вариантах осуществления тендинит выбран из группы, состоящей из тендинита надостной мышцы, тендинита подостной мышцы, тендинита подлопаточной мышцы и тендинита малой круглой мышцы.
[0680] В некоторых вариантах осуществления тендинит выбран из группы, состоящей из тендинита бицепса, тендинита трицепса, тендинита короткого лучевого разгибателя запястья, тендинита общего разгибателя, тендинита разгибателя пальцев, тендинита разгибателя мизинца, тендинита локтевого разгибателя запястья, тендинита супинатора, тендинита общего сгибателя, тендинита круглого пронатора, тендинита лучевого сгибателя запястья, тендинита длинной ладонной мышцы, тендинита локтевого сгибателя запястья и тендинита поверхностного сгибателя пальцев. В некоторых вариантах осуществления тендинит выбран из группы, состоящей из тендинита бицепса, тендинита трицепса, тендинита короткого лучевого разгибателя запястья, тендинита общего разгибателя, тендинита разгибателя пальцев, тендинита разгибателя мизинца, тендинита локтевого разгибателя запястья, тендинита супинатора, тендинита общего сгибателя, тендинита круглого пронатора, тендинита лучевого сгибателя запястья, тендинита длинной ладонной мышцы, тендинита локтевого сгибателя запястья, тендинита поверхностного сгибателя пальцев, тендинита короткого сгибателя большого пальца, тендинита длинного сгибателя большого пальца, тендинита короткой отводящей мышцы большого пальца, тендинита длинной отводящей мышца большого пальца, тендинита глубокого сгибателя пальцев, тендинита поверхностного сгибателя пальцев, тендинита короткого разгибателя большого пальца и тендинита длинного разгибателя большого пальца. В некоторых вариантах осуществления тендинит выбран из группы, состоящей из тендинита короткого сгибателя большого пальца, тендинита длинного сгибателя большого пальца, тендинита короткой отводящей мышцы большого пальца, тендинита длинной отводящей мышцы большого пальца, тендинита глубокого сгибателя пальцев, тендинита поверхностного сгибателя пальцев, тендинита короткого разгибателя большого пальца, кальцифицирующего тендинита и тендинита длинного разгибателя большого пальца.
[0681] В некоторых вариантах осуществления тендинит вызван хроническими травмами сухожилия при перенапряжении, препятствующими заживлению.
[0682] В некоторых вариантах осуществления травма или повреждение локализованы очень близко к мышечно-сухожильному соединению (миосухожильному соединению).
[0683] В некоторых вариантах осуществления тендинит приводит к рубцеванию и фиброзу.
[0684] Способы согласно изобретению могут привести к улучшению одного или более из следующего: уменьшению боли в пораженном суставе или конечности, уменьшению скованности пораженного сустава или конечности, увеличению подвижности пораженного сустава или конечности, повышению прочности пораженного сустава или конечности, снижению скорости прогрессирования тендинопатии, уменьшению воспаления, увеличению прочности сухожилия или повышению скорости восстановления прочности сухожилия. Различные способы измерения эффективности лечения включают, без ограничения перечисленным: Опросник для оценки результатов нарушения функции руки, плеча и кисти (DASH), Визуальную аналоговую шкалу (VAS) и тест на силу хвата.
[0685] В некоторых вариантах осуществления лечение приводит к увеличению прочности сухожилия. В некоторых вариантах осуществления лечение приводит к ускорению восстановления прочности сухожилия. В некоторых вариантах осуществления лечение приводит к увеличению прочности сухожилия приблизительно на 30%, приблизительно на 40%, приблизительно на 50%, приблизительно на 60%, приблизительно на 70%, приблизительно на 80%, приблизительно на 90% в течение приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 дня после введения соединения согласно изобретению, по сравнению с исходным показателем.
[0686] Способы согласно изобретению могут включать профилактическое лечение.
[0687] В некоторых вариантах осуществления введение осуществляют путем прямой инъекции в поврежденную область. В некоторых вариантах осуществления прямую инъекцию выполняют при использовании "методики выстрела дробью" под УЗ контролем или без него. "Методика выстрела дробью" является инъекционным методом, при котором после введения иглы в болезненную область производят многократные небольшие инъекции путем извлечения, перенаправления и повторного введения иглы без полного извлечения из кожи.
[0688] В некоторых вариантах осуществления способы могут дополнительно включать применение одной или более других терапевтических схем и/или средств, эффективных для лечения тендинопатии, например, паллиативную терапию, при которой лечение направлено на противовоспалительные меры, включая лечение нестероидными противовоспалительными средствами (НПВС), инъекциями стероидов, инъекциями кортизона, инъекциями богатой тромбоцитами плазмы (БоТП), физиотерапией, ударно-волновой терапией, лазерной терапией с низким уровнем излучения (фототерапией), клеточной терапией и склеротерапией.
[0689] В некоторых вариантах осуществления одним или более заболеваниями или состояниями является псориаз. Неограничивающие примеры включают: псориаз (в том числе монетовидный псориаз и бляшечный псориаз); генерализованный пустулезный псориаз (в том числе герпетиформное импетиго и болезнь фон Цумбуша); персистирующий акродерматит; ладонно-подошвенный пустулез; каплевидный псориаз; артропатический псориаз; другой псориаз (включая обратный псориаз).
[0690] В некоторых вариантах осуществления одним или более заболеваниями или состояниями является дерматит. Неограничивающие примеры включают: атопический дерматит, контактный дерматит (например, аллергический контактный дерматит, ирритантный контактный дерматит), стазисный дерматит, дерматит, который привел к стероидному дерматиту, стероид-резистентный дерматит, дерматит, при котором нельзя применять такролимус, хронический дерматит, эритродермию (например, постэкзематозную эритродермию и вторичную эритродермию при дерматозах, токсическую эритродермию, десквамативную эритродермию новорожденных и паранеопластическую эритродермию), экзему, монетовидную экзему, дисгидротическую экзему, астеатотическую экзему, себорейный дерматит, аутосенсибилизационный дерматит, стазисный дерматит, крапивницу, лекарственную эритему, кожный васкулит, пруриго, кожный зуд, эритему (например, узловатую или мультиформную), розацеа, розацеа-подобный дерматит, красный плоский лишай, фотоиндуцированный дерматит или фолликулярный кератоз. В некоторых вариантах осуществления дерматит является контактным дерматитом, например аллергическим контактным дерматитом, например, возникающим в результате непосредственного контакта кожи с таким веществом, как ядовитый плющ, ядовитый дуб или ядовитый сумах.
[0691] В некоторых вариантах осуществления одним или более заболеваниями или состояниями является бляшечная склеродермия.
[0692] В некоторых вариантах осуществления одним или более заболеваниями или состояниями является ихтиоз.
[0693] В некоторых вариантах осуществления одним или более заболеваниями или состояниями является болезнь Дарье.
[0694] В некоторых вариантах осуществления способы могут дополнительно включать применение одной или более других терапевтических схем и/или средств, эффективных при лечении заболевания кожи, описанного в настоящем документе, например, кортикостероидов, иммуномодуляторов, витамина D3 и его аналогов, ретиноевых кислот и их фармацевтически активных производных или их комбинаций. Конкретные неограничивающие примеры лекарственных средств включают бетаметазона дипропионат, клобетазола пропионат, галобетазола пропионат, дифлоразона диацетат, амцинонид, дезоксиметазон, флуоцинонид, галцинонид, мометазона фуроат, бетаметазона валерат, флуоцинонид, флутиказона пропионат, триамцинолона ацетонид, флуоцинолона ацетонид, флурандренолид, десонид, гидрокортизона бутират, гидрокортизона валерат, алклометазона дипропионат, флуметазона пиволат, гидрокортизон, гидрокортизона ацетат, преднизолон, бенадрил, такролимус, пикролимус, тазаротен, изотретиноин, циклоспорин, антралин, витамин D3, холекальциферол, кальцитриол, кальципотриол, такальцитол, кальципотриен, госсипол, 4-гидроксиэстрадиол, 2-гидроксиэстрадиол, 2-гидроксиэстрон, 2-бензимидазолилтиоацетамид-N-этил-2-бензил (KH7.102), антитело, нуклеиновую кислоту или их комбинации.
[0695] В некоторых вариантах осуществления одним или более заболеваниями или состояниями является синдром Рейно.
[0696] В некоторых вариантах осуществления пациентом является человек.
[0697] В некоторых вариантах осуществления соединение Формулы (I) ингибирует один или более белков в пути Wnt.
[0698] В некоторых вариантах осуществления соединение Формулы (I) ингибирует сигнализацию, индуцированную одним или более белками Wnt.
[0699] В некоторых вариантах осуществления белки Wnt выбраны из: WNT1, WNT2, WNT2B, WNT3, WNT3A, WNT4, WNT5A, WNT5B, WNT6, WNT7A, WNT7B, WNT8A, WNT8B, WNT9A, WNT9B, WNT10A, WNT10B, WNT11 и WNT16.
[0700] В некоторых вариантах осуществления соединение Формулы (I) ингибирует киназную активность.
[0701] В некоторых вариантах осуществления соединение Формулы (I) ингибирует один или более белков Wnt.
Оценка биологической активности
[0702] Биологическая активность соединений, описанных в настоящем документе, может быть исследована с использованием любого подходящего анализа, известного специалистам в данной области, например, WO 2001/053268 или WO 2005/009997. Например, активность соединения может быть исследована с использованием одного или более методов анализа, описанных ниже.
[0703] В другом примере можно использовать анализы биологической активности Wnt in vitro, например, стабилизации β-катенина и стимуляции роста стволовых клеток. Исследования биологической активности Wnt включают стабилизацию β-катенина, которая может быть измерена, например, при серийных разведениях композиции кандидатного ингибитора. В примере исследования биологической активности Wnt производят контакт композиции Wnt в присутствии кандидатного ингибитора с клетками, например, мышиными L-клетками. Клетки культивируют в течение периода времени, достаточного для стабилизации β-катенина, обычно в течение по меньшей мере приблизительно 1 часа, и лизируют. Клеточный лизат разделяют с помощью ДСН-ПААГЭ, затем переносят на нитроцеллюлозу и метят антителами, специфичными к β-катенину.
[0704] В дополнительном примере активность кандидатного соединения может быть измерена в биоанализе образования дополнительной оси тела у Xenopus (Leyns, L. et al. Cell (1997), 88(6), 747-756).
Пример 8
[0705] Другой метод скрининга активности Wnt описан следующим образом. Линии репортерных клеток могут быть получены путем стабильной трансдукции клеток клеточных линий злокачественных опухолей (например, рака толстой кишки) лентивирусной конструкцией, которая включает Wnt-чувствительный промотор, направляющий экспрессию гена люциферазы светляка.
[0706] Могут быть получены лентивирусные конструкции, в которых промотор SP5, промотор, имеющий восемь участков связывания TCF/LEF, полученный из промотора SP5, связан слева с геном люциферазы светляка. Лентивирусные конструкции могут также включать ген устойчивости к гигромицину в качестве селективного маркера. Конструкция с промотором SP5 может использоваться для трансдукции клеток SW480, линии клеток рака толстой кишки, имеющей мутантный ген APC, который дает усеченный белок APC, что приводит к дерегулированному накоплению β-катенина. Контрольная клеточная линия может быть получена при использовании другой лентивирусной конструкции, содержащей ген люциферазы под контролем промотора SV40, для активации которого не требуется β-катенин.
[0707] Культивирумые клетки SW480, несущие репортерную конструкцию, можно распределить в 96- или 384-луночные планшеты при плотности примерно 10000 клеток на лунку. Затем соединения из библиотеки низкомолекулярных соединений можно добавить в лунки в серии полулогарифмических разведений при использовании максимальной концентрации десять микромоль. В серию контрольных лунок для каждого типа клеток добавляют только буфер и растворитель для соединения. Через двадцать четыре - сорок часов после добавления соединения можно провести анализ репортерной активности люциферазы, например, при добавлении люминесцентного реагента BrightGlo (Promega) и использовании планшетного анализатора Victor3 (Perkin Elmer). Показания прибора могут быть нормализованы по клеткам, обработанным только ДМСО, и затем нормализованные активности можно использовать при вычислениях EC50. В Таблице 2 показана активность выбранных аналогов индазол-3-карбоксамида.
Таблица 2
Пример 9
[0708] Скрининг репрезентативных соединений проводили при использовании первичных человеческих мезенхимальных стволовых клеток (МСКч) с целью определения их способности вызывать дифференцировку теноцитов (процесс, в котором развивается сухожилие).
[0709] Культура человеческих мезенхимальных стволовых клеток: Первичные человеческие мезенхимальные стволовые клетки (МСКч) приобретали в Lonza (Walkersville, MD) и размножали в средах для выращивания мезенхимальных стволовых клеток (Lonza). Для экспериментов использовали клетки между пассажами 3 и 6.
[0710] Скрининг соединений: Каждое соединение растворяли в ДМСО в виде 10 мМ стока и использовали для приготовления исходных планшетов с соединениями. Для анализа дифференровки теноцитов подготавливали серийное разведение (1:2, 10-точечные кривые зависимости доза-эффект, от 10 мкМ до 19,5 нМ) и производили перенос соединения при использовании ECHO 550 (Labcyte, Sunnyvale, CA) в 384-луночные черные аналитические планшеты с прозрачным (Greiner Bio-One) с соответствующим обратным наполнением ДМСО до конечной концентрации ДМСО 0,17%. МСКч сеяли при плотности 3000 клеток/лунка в 70 мкл/лунка модифицированной по Дульбекко среды Игла (DMEM, Life Technologies, Carlsbad, CA) с 1% фетальной бычьей сывороткой (FBS, Life Technologies). Костный морфогенетический фактор (BMP) и фактор роста плода (FGF) (по 10 нг/мл каждого, Peprotech, Inc., Rocky Hill, NJ) использовали в качестве положительного контроля дифференцировки, тогда как лунки отрицательного контроля обрабатывали 120 нл DMSO для нормализации и вычисления значений EC50. Клетки инкубировали при 37°C и 5% CO2 в течение 4 дней. Клетки фиксировали с использованием 4% формальдегида (Electron Microscopy Sciences) и окрашивали антителами против scleraxis гомолога A (SCXA) (Abgent, San Diego, CA) [Webb S., et.al., Retinoic acid receptor signaling preserves tendon stem cell characteristics and prevents spontaneous differentiation in vitro, Stem Cell Research & Therapy 2016, 7:45] в течение ночи при 4°C. Клетки промывали фосфатно-солевым буфером (PBS, Life Technologies) и инкубировали с вторичными Alexa-fluor 647-конъюгированными антителами против иммуноглобулина кролика (Life Technologies) и DAPI (Life Technologies) в течение 1 часа при комнатной температуре. Клетки промывали с использованием PBS и визуализировали при использовании CellInsight CX5 (Life Technologies, фильтр 594/633 нм). Количество клеток, положительных на SCXA, количественно определяли в каждой лунке с помощью CellInsight CX5. Данные нормализовали по среднему значению 12 обработанных ДМСО лунок на одном планшете с использованием модуля Dotmatics Studies. Были вычислены нормализованные средние значения (кратное изменение по сравнению с ДМСО) для лунок в тройной повторности для каждой концентрации соединения. Из-за ограничений по растворимости некоторых соединений, значения для более высоких доз корректировали вручную, а аппроксимацию кривых и определения EC50 выполняли с использованием Dotmatics Studies.
[0711] Приведены EC50 для каждого соединения. В Таблице 3 показана измеренная активность для репрезентативных соединений Формулы I, как описано в настоящем документе.
Таблица 3
Пример 10
Ингибировние сигнализации Wnt
[0712] Культура клеток. Клетки SW480 (ATCC) культивировали в модифицированной по Дульбекко среде Игла (DMEM, ThermoFisher) с 1% Glutamax (Life Technologies), 1% пенициллина-стрептомицина (Life Technologies), 150 мкг/мл гигромицина (Life Technologies) с 10% эмбриональной бычьей сывороткой (FBS) (Hyclone) при 37°C, 5% CO2.
[0713] Wnt репортерный анализ. Линию человеческих клеток колоректального рака SW480, стабильно экспрессирующую Wnt-чувствительный промотор, связанный с геном люциферазы, сеяли на ночь при плотности 4×10e4 клеток/лунка в среду DMEM с высоким содержанием глюкозы, без глутамина, без фенолового красного (Life Technologies), 1% Glutamax (Life Technologies), 1% пирувата натрия (Life Technologies), 1% пенициллина-стрептомицина (Life Technologies) с 1% эмбриональной бычьей сывороткой (Hyclone). Затем клетки обрабатывали ДМСО (контроль среды) или соединением 175 при максимальной концентрации 10 мкМ и полулогарифмическом разведении до 10 концентраций (10, 3, 1, 0,3, 0,1, 0,03, 0,01, 0,003, 0,001 и 0,0003 мкМ). Клетки инкубировали в течение 48 часов при 37°C. 15 мкл Bright-Glo (система люциферазного анализа Bright-Glo™, Promega) добавляли к клеткам и измеряли люминесценцию при использовании планшетного анализатора Cytation 3 (Biotek). Данные нормализовали при использовании профиля ДМСО контроля и ингибирования, и EC50 вычисляли при использовании Prism 4 (GraphPad Software Inc, La Jolla, CA, USA). Prism 4.0 использовали для вычисления EC50 в Wnt репортерном анализе ингибирования.
[0714] Воздействие на клетки SW480 соединения 175 при концентрациях 10, 3, 1, 0,3, 0,1, 0,03, 0,01, 0,003, 0,001 и 0,0003 мкМ показало, что соединение 175 дозозависимо ингибировало активность пути Wnt в этих клетках с EC50 ~152,9 нМ (см. ФИГ. 1).
Пример 11
Дифференцировка сухожилия
[0715] Культура клеток. Первичные человеческие мезенхимальные стволовые клетки (МСКч; Lonza Inc.) культивировали в Среде для выращивания мезенхимальных стволовых клеток MSCGM™ с 10% FBS (Lonza), 10% эмбриональной бычьей сыворотки (FBS) (Hyclone) при 37°C, 5% CO2. МСКч использовали между пассажами 2 и 6 и никогда не позволяли достичь конфлюэнтности, чтобы сохранить наивное состояние.
[0716] Анализ дифференцировки теноцитов. Для дифференцировки теноцитов, МСКч сеяли в 384-луночные планшеты при плотности 1×104 клеток/лунка в модифицированной по Дульбекко среде Игла (DMEM, ThermoFisher) с 1% фетальной бычьей сывороткой (FBS) (Hyclone). Затем клетки обрабатывали ДМСО (контроль среды) или соединением 175 при максимальной концентрации 750 нМ и 2-кратном разведении до 8 концентраций (750, 333,3, 166,6, 83,3, 41,7, 21,7, 10,8 и 5,8 нМ) и инкубировали в течение 7 дней при 37°С. Комбинацию BMP и FGF (по 10 нг/мл каждого, Peprotech, Inc.) использовали в качестве положительного контроля. По истечении 7 дней клетки фиксировали при использовании 4% формальдегида без метанола (Electron Microscopy Sciences) в течение 10 минут, промывали фосфатно-солевым буфером (PBS) 3 раза, пермеабилизировали в PBS, содержащем 0,3% Triton X-100 (Sigma) в течение 5 мин, блокировали PBST (PBS, содержащим 0,3% Triton X-100) с 3% бычьего сывороточного альбумина (BSA; Sigma) в течение 1 часа при комнатной температуре с последующим инкубированием с первичными антителами в PBST+BSA в течение ночи при 4°C. Клетки 3 раза промывали PBS и инкубировали с вторичным антителом, конъюгированным с флуорофором, в PBST+BSA и DAPI в течение 1 часа при комнатной температуре, и 3 раза промывали PBS. Планшеты визуализировали при использовании сканера для высокопроизводительного скрининга CX5 (ThermoFisher), и определяли % положительно окрашенных клеток при использовании алгоритма подсчета клеток (ThermoFisher). Данные наносили на график и вычисляли EC50 при использовании Prism 5 (GraphPad Software Inc, La Jolla, CA, USA). Prism 5.0 использовали для вычисления ЕС50 в анализе дифференцировки теноцитов.
[0717] Воздействие на МСКч соединения 175 при концентрациях 750, 333,3, 166,6, 83,3, 41,7, 21,7, 10,8 и 5,8 нМ показало, что соединение 175 дозозависимо индуцировало экспрессию SCXA, тенацина C и теномодулина с EC50 в пределах 139-189 нМ (см. ФИГ. 2A-C и 3), указывая на дифференцировку МСКч в теноциты.
Противовоспалительное действие
[0718] Культура клеток. Клетки THP-1 (номер по кат. TIB-202, ATCC, Manassas, VA) культивировали в среде Roswell Park Memorial Institute (RPMI) 1640 (номер по кат. 21870-100, Buffalo, NY) с 1% L-глутамина, 1% HEPES, 1% пирувата натрия, 2% бикарбоната натрия, с добавкой 100 единиц/мл пенициллина, 50 мкг/мл стрептомицина, 2-меркаптоэтанола (0,05 мМ) [минимальная среда] и 10% эмбриональной бычьей сыворотки (номер по кат. 16140089, Life Technologies, Carlsbad, CA) при 37°C и 5% CO2.
[0719] Анализ продукции цитокинов. Клетки THP-1 культивировали в минимальных средах с 1% FBS в течение 24 часов до начала анализа. Клетки THP-1 сеяли при плотности 6×10e4 клеток/лунка и обрабатывали ДМСО (контроль среды) или соединением 175 при наибольшей тестируемой концентрации 10 мкМ и в 2-3,5-кратных серийных разведениях до 8 концентраций (10, 3,5, 1, 0,5, 0,1, 0,035, 0,01, 0,005 мкм). Для анализа ФНОα, 50 нг/мл ЛПС добавляли в лунки через 2 часа, чтобы вызвать продукцию цитокина, и инкубировали клетки в течение 5 часов при 37°C. Для анализа IL6, 500 нг/мл ЛПС добавляли через 2 часа и инкубировали клетки в течение 22 часов при 37°C. Планшеты центрифугировали в течение 1 минуты при 10000 об/мин и собирали супернатанты для ИФА. Супернатанты разбавляли 1:1 для анализа ФНОα и 1:4 для анализа IL6, используя среду для анализа. ИФА проводили с использованием наборов для анализа человеческого ФНО-α ELISA MAX™ Deluxe (номер по кат. 430204, Biolegend, San Diego, CA) и человеческого IL-6 ELISA MAX™ Deluxe (номер по кат. 430504, Biolegend, San Diego, CA). Коротко, 96-луночные планшеты покрывали подходящим захватывающим антителом в течение ночи и промывали для удаления избытка антитела. Добавляли блокирующий буфер и инкубировали в течение 1 часа для устранения неспецифического связывания. Разбавленные супернатанты инкубировали в покрытых пластинах в течение 2 часов при комнатной температуре. После промывки для удаления несвязавшихся белков, добавляли биотинилированное детектирующее антитело и инкубировали в течение 30 мин при комнатной температуре, с последующей промывкой для удаления несвязавшегося избыточного антитела. Затем добавляли авидин-HRP и инкубировали в течение 30 мин при комнатной температуре. После нескольких промывок для удаления несвязавшегося авидина-HRP, добавляли субстрат TMB и считывали планшеты на планшетном анализаторе Cytation 3 (Biotek Inc., Winooski, VT) при длине волны поглощения 450 нм с коррекцией при 570 нм. Все образцы обрабатывали в тройной повторности. Профиль ингибирования и EC50 вычисляли при использовании Prism 5 (GraphPad Software Inc, La Jolla, CA, USA). Prism 5.0 использовали для вычисления EC50 в анализах ингибирования ФНОα и IL6.
[0720] Воздействие ЛПС на клетки THP-1 вызывало продукцию и ФНОα и IL6. Обработка Соединением 175 дозозависимо ингибировала индуцированную ЛПС продукцию цитокинов в этих клетках со средней EC50 в пределах 342-547 нм для ФНОα и 356-629 нм для IL6 (см. ФИГ. 4A-B), при этом результы были получены в двух независимых анализах в тройной повторности на анализ.
Пример 12
Модель тендинопатии на крысах (1)
[0721] Модель вызванного коллагеназой тендинита на крысах. Пятьдесят (50 мкл) коллагеназы типа IA (10 мг/мл в PBS, pH 7,4, приблизительно 469 единиц/мг) (номер по кат. C5138, Sigma, St. Louis, MO) вводили в ахиллово сухожилие обеих лодыжек около остеосухожильного соединения самцам крыс Sprague Dawley CD ®IGS (CRL, Inc.) при использовании инсулиновых шприцев с иглой 28,5 G.
[0722] Доставка соединения 175 при наружном применении. Крыс распределяли в 6 групп, по 5 животных в группе: Группа 1 (ложная инъекция); Группа 2 (коллагеназа-растворитель); Группа 3 (коллагеназа-соединение 175 10 мг/мл с 1% BA) и Группа 4 (коллагеназа-СОЕДИНЕНИЕ 175 10 мг/мл с 0,5% Tween 80). СОЕДИНЕНИЕ 175, разведенное в 1% ГПМЦ 40-0101/20% PG/1% BA или 1% ГПМЦ 40-0101/20% PG/0,5% Tween 80, или растворитель (1% ГПМЦ 40-0101/20% PG/1% BA) наносили в объеме дозы 30 мкл/см2 на участке площадью 2 см2 на кожу в области ахиллова сухожилия обеих лодыжек крыс, которым вводили коллагеназу, при использовании аппликатора и втирали в кожу в течение 10 секунд. Всех крыс периодически наблюдали на любые проявления боли, недомогания или патологий. В различные временные точки кровь забирали для выделения плазмы в покрытые гепарином лития пробирки при надрезе из подкожной вены задней лапы. Для гистологического исследования крыс усыпляли с использованием изофлурана, сухожилия извлекали (n=6 сухожилий/группа), фиксировали в 10% буферизованном формалине (номер по кат. SF93-4, Fisher, Pittsburgh PA) и окрашивание Г-Э гистологических препаратов выполняли в другом центре (Pacific Pathology, San Diego, CA). Для биохимического исследования сухожилия извлекали (n=4 сухожилия/группа), быстро замораживали в жидком азоте и затем хранили при -80°C для последующего биохимического исследования (не указано).
[0723] Гистологическая оценка сухожилий. Существует биологическая вариабельность в реакции на коллагеназу при инъекции непосредственно в сухожилия. Это приводит к различным степеням тяжести и переменной локализации воспаления, а также к дегенерации сухожилий (Urdzikova et al., Human multipotent mesenchymal stem cells improve healing after collagenase tendon injury in the rat. Biomed Eng Online. 2014 Apr 9; 13:42). Следовательно, все сухожилие извлекали, помещали в кассету для тканей и заливали в парафин. Делали срезы по пять (5) мкм, и в среднем 3 среза фиксировали на одном стекле, минимум с восемью (8) стеклами на каждое сухожилие, и подвергали окрашиванию гематоксилином и эозином (Г-Э). Препараты исследовали под прямым оптическим микроскопом (EVOS AMEX-1200) при 10-кратном увеличении и оценивали вслепую, используя шкалу оценки от 1 до 4: 1 соответствует тяжелому повреждению, а 4 соответствует нормальному сухожилию, по Линейности структуры волокон, Форме сухожильных клеток, Плотности сухожильных клеток, воспалению и Кровоизлиянию, с общим баллом двадцать (20), при использовании модификации, описанной ранее (Urdzikova et al., 2014 - см. Таблицу 3). После завершения анализа исследователь, проводивший оценку, получал доступ к расшифровке идентификационных кодов, после чего оценки по каждому критерию были снабжены комментариями, суммированы, и общие оценки по каждому срезу усредняли вместе, с получением окончательного балла для каждой крысы с последующим усреднением показателей для данной группы лечения.
[0724] Анализы биомаркеров в плазме. Согласно инструкциям производителя, уровни KC/GRO в плазме определяли при использовании набора для иммуноанализа KC/GRO (номер по кат. 900-K57, Peprotech, Rocky Hill, NJ). Коротко, 96-луночные планшеты покрывали захватывающим антителом против крысиного KC/GRO в течение ночи и промывали для удаления избытка антитела. Образцы плазмы инкубировали в покрытых планшетах в течение 2 часов при комнатной температуре. После промывки для удаления несвязавшихся белков, добавляли биотинилированное детектирующее антитело против крысиного KC/GRO и инкубировали в течение 30 мин при комнатной температуре. После промывки для удаления несвязавшегося избыточного антитела, добавляли авидин-HRP и инкубировали в течение 30 мин при комнатной температуре. После промывки для удаления несвязавшегося авидина-HRP, добавляли субстрат ABTS и считывали планшеты на планшетном анализаторе Cytation 3 (Biotek Inc., Winooski, VT) при длине волны поглощения 525 нм с коррекцией при 450 нм. Все образцы обрабатывали в тройной повторности.
[0725] Анализ данных. Для оценки сухожилий каждый срез исследовали по шкале оценки от 1 до 4, как описано ранее (Urdzikova et al., 2014) с исключением одной переменной, Толщины эпитенона, из-за сложности при различении слоя эпитенона на гистологических препаратах. В Таблице 4 ниже кратко описана шкала оценки.
Таблица 4
2=20-50% линейных
3=>50% линейных
4=линейные (нормальные)
2=умеренно круглые
3=слегка овальные
4=линейные (нормальные)
2=умеренное увеличение
3=легкое увеличение
4=рассеянные (нормальные)
2=легкое увеличение
3=легкое увеличение
4=нет
2=множество областей в каждом поле
3=рассеянное или очаговое
4=нет
[0726] aГистологическая оценка была модифицирована Samumed для исключения одной переменной, Толщины эпитенона.
[0727] В данном исследовании в общей сложности 64 среза оценивали для Группы 1 (группа ложной инъекции) и приблизительно по 96 срезов для Группы 2 (коллагеназа-растворитель), Группы 3 (коллагеназа-соединение 175 с консервантом BA) и Группы 4 (коллагеназа-соединение 175 без консерванта). Для определения статистической значимости между группами использовали t-критерий Стьюдента, уровень p<0,05 считали значимым для гистологической оценки и анализа биомаркеров.
[0728] Соединение 175 облегчает вызванную коллагеназой тендинопатию. Вызванный коллагеназой тендинит у крыс воспроизводит острое поражение сухожилия у людей с воспалением, развивающимся в течение нескольких часов (Urdzikova et al., 2014). Используя интервенционный метод, композицию соединения 175 для наружного применения вводили в ахиллово сухожилие через 24 часа после инъекции коллагеназы. Крысам после инъекции коллагеназы вводили только растворитель или соединение 175 (10 мг/мл) в композиции с или без BA в качестве консерванта, в течение 21 дня подряд. Крысы в Группе 1, которые получали ложные инъекции, служили в качестве контроля без индукции болезни.
[0729] Как показано на ФИГ. 5, значительное присутствие воспалительных клеток наблюдалось в группе Коллагеназы-растворителя. Следовательно, имелись признаки дегенерации и повреждения сухожилий в группе Коллагеназы-растворителя по сравнению с нормальными сухожилиями, обнаруженными в контрольной группе ложной инъекции. Уменьшение воспаления, как и дегенерации сухожилия, соединением 175 показано на ФИГ. 5. Патогистология сухожилия в группах лечения выявила сухожилия с уменьшенным воспалением, а также улучшенной структурой волокон и сухожильных клеток по линейности, форме и плотности. Это наблюдение дополнительно подтверждалось слепой оценкой гистологии. Как показано на ФИГ. 6, при наружном лечении соединением 175 обе группы лечения соединением 175 продемонстрировали статистически значимое увеличение показателей сухожилия, достигнув оценки 14,0 (±0,217) в Группе 3 (коллагеназа-соединение 175 с BA) и оценки 12,2 (±0,284) в Группе 4 (коллагеназа-соединение 175 без BA), в сравнении с оценкой 9,14 (±2,43) в Группе 2 (коллагеназа-растворитель), с р-значением <0,01 и <0,05, соответственно, при использовании t-критерия Стьюдента
[0730] Соединение 175 снижает биомаркер KC/GRO в плазме в модели вызванного коллагеназой повреждения сухожилия. KC/GRO является воспалительным биомаркером, который, согласно некоторым сообщениям, связан с развитием тендинита. В данном исследовании концентрации KC/GRO в плазме анализировали в различные временные точки исследования. Как показано в Таблице 4 и на ФИГ. 7, уровни KC/GRO были повышены в Группе 2 (коллагеназа-растворитель) в дни 5-21, в пределах от 814 до 1483 пг/мл, тогда как в обеих группах, обработанных СОЕДИНЕНИЕМ 175, с или без BA, наблюдали более низкие уровни KC/GRO в плазме, от 400 до 480 пг/мл и от 347 до 451 пг/мл, соответственно. Обе группы, обработанные соединением 175 (Группы 3 и 4), продемонстрировали статистически значимое снижение уровней KC/GRO в плазме по сравнению с контролем Коллагеназа-растворитель в дни 7 и 21 (р<0,05 согласно t-критерию Стьюдента, Таблица 5). В целом, снижение биомаркера воспаления в плазме подтверждает способность соединения 175 облегчать тендинит.
Таблица 5
(0 мг/мл)
(10 мг/мл с 0,5% BA)
(10 мг/мл без BA, с 0,5% Tween 80)
[0731] aСредние значения превышали предел количественного определения (AQL>1000 пг/мл) и приведены в приближении.
[0732] *p<0,05 (t-критерий Стьюдента) в группах, обработанных соединением 175 (Группы 3 и 4), по сравнению с Группой 2 (Растворитель) в Дни 7 и 21.
[0733] Тендинопатия - острая травма сухожилия, которая включает воспаление и повреждение сухожилия. Если ее не лечить, повторная травма может привести к разрывам сухожилий и потребовать хирургического вмешательства. Присутствие или отсутствие консерванта, бензилового спирта, не влияет на эффективность соединения 175. Лечение соединением 175 облегчает тендинопатию согласно слепой гистологической оценке сухожилия. Для дальнейшего подтверждения данного результата было показано, что соединение 175 также приводит к снижению воспалительного биомаркера плазмы, KC/GRO.
Пример 13
Модель тендинопатии на крысах (2)
[0734] Пятьдесят (50 мкл) коллагеназы IA типа (10 мг/мл в PBS, pH 7,4, приблизительно 469 единиц/мг) (номер по кат. C5138, Sigma, St. Louis, MO) вводили в ахиллово сухожилие обеих лодыжек около остеосухожильного соединения самцам крыс Sprague Dawley CD ®IGS (CRL, Inc.) при использовании инсулиновых шприцев с иглами 28,5 G.
[0735] Доставка соединения 175 при наружном применении. Крыс распределяли в 6 групп, по 6 животных в группе, за исключением 8 животных в Группе 2: Группа 1 (ложная инъекция), Группа 2 (коллагеназа-растворитель с 0,5% Phx), Группа 3 (коллагеназа-соединение 175 3 мг/мл с 0,5% BA), Группа 4 (коллагеназа-соединение 175 10 мг/мл с 0,5% BA), Группа 5 (коллагеназа-соединение 175 3 мг/мл с 0,5% Phx) и Группа 6 (коллагеназа-соединение 175 10 мг/мл с 0,5% Phx). СОЕДИНЕНИЕ 175, в концентрации 3 или 10 мг/мл, приготовленное в 1% ГПМЦ 40-0101/20% PG/0,5% BA или 1% HPMC 40-0101/20% PG/0,5% Phx, или растворитель (1% ГПМЦ 40-0101/20% PG/0,5% Phx) наносили в количестве 30 мкл/см2 на участок площадью 2 см2 на кожу в области ахиллова сухожилия обеих лодыжек крыс, которым вводили коллагеназу, при использовании аппликатора и втирали в кожу в течение 10 секунд. Всех крыс периодически наблюдали на любые проявления боли, недомогания или патологий. В различные временные точки кровь забирали для выделения плазмы в покрытые гепарином лития пробирки при надрезе из подкожной вены задней лапы. Для гистологического исследования крыс усыпляли при использовании изофлурана, сухожилия извлекали (n=8 сухожилий/группа), фиксировали в 10% буферизованном формалине (номер по кат. SF93-4, Fisher, Pittsburgh, PA) и окрашивание Г-Э гистологических препаратов выполняли в другом центре (Pacific Pathology, San Diego, CA). Для биохимического исследования сухожилия извлекали (n=4 сухожилия/группа), быстро замораживали в жидком азоте и затем хранили при -80°C для последующего биохимического исследования (не указано). Кроме того, через один (1) день после инъекции коллагеназы, 4 сухожилия собирали в Группе 2 (растворитель) для наблюдения индукции воспаления (не указано).
[0736] Существует биологическая вариабельность в реакции на коллагеназу при инъекции непосредственно в сухожилия. Это приводит к различным степеням тяжести и переменной локализации воспаления, а также к дегенерации сухожилий (Urdzikova et al., 2014). Следовательно, все сухожилие извлекали, помещали в кассету для тканей и заливали в парафин. Делали срезы толщиной пять (5) мкм, и в среднем 3 среза фиксировали на одном стекле, минимум с восемью (8) срезами на каждое сухожилие, и подвергали окрашиванию гематоксилином и эозином (Г-Э). Препараты исследовали под прямым оптическим микроскопом (EVOS AMEX-1200) при 10-кратном увеличении и оценивали вслепую, используя шкалу оценки тяжести от 1 до 4 баллов: 1 соответствует тяжелому повреждению, а 4 соответствует нормальному сухожилию, по Линейности структуры волокон, Форме сухожильных клеток, Плотности сухожильных клеток, Воспалению и Кровоизлиянию, с общим баллом двадцать (20), при использовании модификации, описанной ранее (Urdzikova et al., 2014 - см. Таблицу 3). После завершения анализа исследователь, проводивший оценку, получал доступ к расшифровке идентификационных кодов, после чего оценки по каждому критерию были снабжены комментариями, суммированы, и общие оценки по каждому срезу усредняли вместе, с получением окончательного балла для каждой крысы с последующим усреднением показателей для данной группы лечения.
[0737] Анализы биомаркеров в плазме. Согласно инструкциям производителя, уровни KC/GRO в плазме определяли при использовании набора для иммуноанализа KC/GRO (номер по кат. 900-K57, Peprotech, Rocky Hill, NJ). Коротко, 96-луночные планшеты покрывали захватывающим антителом против крысиного KC/GRO в течение ночи и промывали для удаления избытка антитела. Образцы плазмы инкубировали в покрытых планшетах в течение 2 часов при комнатной температуре. После промывки для удаления несвязавшихся белков, добавляли биотинилированное детектирующее антитело против крысиного KC/GRO и инкубировали в течение 30 мин при комнатной температуре. После промывки для удаления несвязавшегося избыточного антитела, добавляли авидин-HRP и инкубировали в течение 30 мин при комнатной температуре. После промывки для удаления несвязавшегося авидина-HRP, добавляли субстрат ABTS и считывали планшеты на планшетном анализаторе Cytation 3 (Biotek Inc., Winooski, VT) при длине волны поглощения 525 нм с коррекцией при 450 нм. Все образцы обрабатывали в тройной повторности.
[0738] Анализ данных. Для оценки сухожилий каждый срез исследовали по шкале оценки 1-4, как описано ранее (Urdzikova et al., 2014) с исключением одной переменной, Толщины эпитенона, из-за сложности при различении слоя эпитенона в на гистологических препаратах. В Таблице 2 ниже кратко описана шкала оценки. В данном исследовании в общей сложности 94 среза оценивали для Группы 1 (ложная инъекция, контрольная группа) и в пределах 92-116 срезов для Группы 2 (коллагеназа-растворитель с 0,5% Phx); Группы 3 (коллагеназа-соединение 175 3 мг/мл с 0,5% BA), Группы 4 (коллагеназа-соединение 175 10 мг/мл с 0,5% BA), Группы 5 (коллагеназа-соединение 175 3 мг/мл с 0,5% Phx) и Группы 6 (коллагеназа-соединение 175 10 мг/мл с 0,5% Phx).
[0739] Соединение 175 облегчает вызванную коллагеназой тендинопатию. Вызванный коллагеназой тендинит у крыс воспроизводит острое повреждение сухожилия у людей с воспалением, развивающимся в течение нескольких часов (Urdzikova et al., 2014). Используя интервенционный метод, композицию соединения 175 для наружного применения вводили через день (~24 часа) после инъекции коллагеназы в ахиллово сухожилие. Крысам после инъекции коллагеназы вводили только растворитель (содержащий 0,5% Phx) или соединение 175 (3 или 10 мг/мл) в композиции с 0,5% BA или с 0,5% Phx в качестве консерванта, в течение двадцати одного (21) дня подряд. Крысы в Группе 1 (ложные инъекции) служили в качестве контрольных животных без индукции болезни.
[0740] Как показано на ФИГ. 8, значительное присутствие воспалительных клеток наблюдалось в группе Коллагеназы-растворителя (Группа 2). Следовательно, имелись признаки дегенерации и повреждения сухожилий в группе Коллагеназы-растворителя по сравнению с нормальными сухожилиями, обнаруженными в контрольной группе ложной инъекции (Группа 1). Уменьшение воспаления, как и дегенерации сухожилий, соединением 175 продемонстрировано на ФИГ. 8. Патогистология сухожилия в группах лечения, получавших соединение 175, выявила сухожилия с уменьшенным воспалением, а также улучшенной структурой волокон и сухожильных клеток по линейности, форме и плотности. Это наблюдение дополнительно подтверждалось слепой оценкой гистологии. Как показано на ФИГ. 9, после наружного лечения соединением 175, все четыре (4) группы, получавшие соединение 175, продемонстрировали статистически значимое увеличение показателей сухожилия, достигнув оценки 14,5 (±1,15) в Группе 3 (коллагеназа-соединение 175 3 мг/мл с 0,5% BA), оценки 14,8 (±0,968) в Группе 4 (коллагеназа-соединение 175 10 мг/мл с 0,5% BA), оценки 15,1 (±0,506) в Группе 5 (коллагеназа-соединение 175 3 мг/мл с 0,5% Phx) и оценки 13,2 (±0,855) в Группе 6 (коллагеназа-соединение 175 10 мг/мл с 0,5% Phx), по сравнению с оценкой 8,57 (±0,672) в Группе 2 (коллагеназа-растворитель), с p-значениями <0,001 (Группы 3, 4 и 5) и <0,01 (Группа 6) в сравнении с Группой 2, при использовании t-критерия Стьюдента.
[0741] Соединение 175 снижает биомаркер KC/GRO в плазме в модели вызванного коллагеназой повреждения сухожилия. KC/GRO является воспалительным биомаркером, который, согласно некоторым сообщениям, связан с развитием тендинита. В данном исследовании концентрации KC/GRO в плазме анализировали в различные временные точки исследования. Как показано в Таблице 5 и на ФИГ. 10, уровни KC/GRO были повышены в Группе 2 (коллагеназа-растворитель с 0,5% Phx) в Дни 5-21, в пределах от 488 до 778 пг/мл, тогда как во всех четырех группах, получавших соединение 175, уровни KC/GRO в плазме были снижены, в пределах от 150-561 пг/мл. Соединение 175 при обеих концентрациях дозы 3 и 10 мг/мл, с BA или с Phx в качестве консерванта (Группы 3-6), продемонстрировало статистически значимое снижение уровней KC/GRO в плазме по сравнению с контролем растворителем (Группа 2) в Дни 5, 7 и 21 (p<0,05, t-критерий Стьюдента), как показано в Таблице 6. В целом, снижение биомаркера воспаления в плазме подтверждает способность соединения 175 облегчать тендинит.
Таблица 6
[0742] *p<0,05 (t-критерий Стьюдента) в День 7 (Группа 6) и в День 21 (Группа 3) по сравнению с Группой 2 (Растворитель) в Дни 7 и 21.
[0743] **p<0,01 (t-критерий Стьюдента) в День 5 в группах, получавших соединение 175 (Группы 4, 5 и 6), по сравнению с Группой 2 (Растворитель).
[0744] Тендинопатия - острая травма сухожилия, которая включает воспаление и повреждение сухожилия. Если ее не лечить, повторная травма может привести к разрывам сухожилий и потребовать хирургического вмешательства. Обе дозы соединения 175 (3 и 10 мг/мл, с консервантами BA или Phx) были эффективными в модели тендинита на крысах. На основе ранее полученных результатов ни один из консервантов, BA или Phx, как оказалось, не улучшал эффективность соединения 175. Результаты демонстрируют, что лечение соединением 175 облегчало тендинопатию согласно слепой гистологической оценке сухожилия. Для дальнейшего подтверждения данного результата было показано, что соединение 175 также приводит к снижению воспалительного биомаркера плазмы, KC/GRO.
Пример 14
Фармакокинетика
[0745] Тридцать (30) наивных самцов крыс Sprague Dawley распределяли в три группы дозы (Группы 1-3; 10 животных/группа). Соединение 175 разводили в 1% р-ре гидроксипропилметилцеллюлозы (ГПМЦ) 40-0101/20% пропиленгликоля в концентрации 1 или 10 мг/мл, содержащем 1% бензилового спирта (BA) в качестве консерванта (Группы 1 и 2), или в концентрации 10 мг/мл, содержащем 0,5% Tween 80 (использовавшегося в более ранних исследованиях на крысах) без консерванта BA (Группа 3). Композицию Соединения 175 наносили однократко на каждую лодыжку задней конечности каждого животного в объеме 60 мкл (30 мкл/см2×2 см2) в области ахиллова сухожилия. Схема исследования представлена в Таблице 7 ниже.
Таблица 7
[0746] a Наружное применение на левой и правой лодыжках задних конечностей в области ахиллова сухожилия
[0747] b Композиции соединения 175 для наружного применения: 1% ГПМЦ 40-0101/20% пропиленгликоля, содержащая 1% бензилового спирта (BA) в качестве консерванта (Группы 1 и 2), и без консерванта BA, но с 0,5% Tween 80 (Группа 3).
[0748] Сбор образцов крови. Образцы крови (~0,5 мл) собирали при кардиальной пункции в пробирки, содержащие K2ЭДТА в качестве антикоагулянта, через 1, 2, 4, 7 и 24 часа после введения дозы, у 2 животных на каждую временную точку (n=2). Плазму получали и замораживали при -80°C для биоанализа.
[0749] Сбор образцов ткани. Ахилловы сухожилия из обеих лодыжек собирали после усыпления животных, через 1, 2, 4, 7 и 24 часа после введения дозы, у 2 животных на каждую временную точку (n=4) из всех групп. Образцы кожной ткани забирали из участка введения дозы через 7 и 24 часа после введения, у 2 животных на каждую временную точку (n=4) в Группе 2. Ткани замораживали при -80°C для биоанализа. График сбора крови и тканей представлен в Таблице 8 ниже.
Таблица 8
[0750] NS=Образцы не забирали.
[0751] 1) n=2/временная точка/группа для забора крови.
[0752] b n=4/временная точка/группа для забора сухожилий и кожи (2 животных на каждую временную точку ×2 лодыжки).
[0753] Методики эксперимента. Образцы кожной ткани обрабатывали при использовании следующих методик: 1) Взвешивают ткань и гомогенизируют с помощью cryoPrep (Covaris); 2) Добавляют 9× объем ацетонитрила:метанола (70:30) и встряхивают в течение одного часа; 3) Отбирают аликвоты по 100 мкл гомогената ткани в полипропиленовый планшет-штатив с 96 микропробирками; 4) Добавляют 10 мкл рабочего стандарта к каждому стандарту; 5) Добавляют 10 мкл метанола во все образцы и пустые пробирки; 6) Добавляют 10 мкл внутреннего стандарта (IS) во все пробирки, кроме пустых пробирок; 7) Центрифугируют при 3000 об/мин в течение 10 минут; и 8) Переносят 100 мкл супернатанта в 96-луночный планшет, содержащий 150 мкл воды. Закрывают крышку и встряхивают для ЖХ/МС/МС анализа
[0754] Биоаналитический и фармакокинетический анализ. Хроматограммы образцов интегрировали и калибровали при использовании Analyst 1.6.2 (AB Sciex, Redwood City, CA). Для стандартной калибровки использовали линейную регрессию с 1/x2 взвешиванием и внутренней стандартизацией, с критерием приемлемости ± 30% от номинальной стандартной концентрации. Нижний предел количественного определения (LLOQ) составлял 2,00 нг/мл (плазма), 6,00 нг/г (сухожилие) и 25,0 нг/г (кожа). Фармакокинетические параметры оценивали с помощью некомпартментного анализа на основе индивидуальных профилей зависимости концентрации от времени при использовании Pheonix WinNonlin версии 6.3 (Certara, Inc., Princeton, NJ). Время достижения максимальной концентрации (tmax) и максимальную концентрацию (Cmax) определяли по измеренным концентрациям в плазме и тканях. Площадь под кривой (AUC0-last) вычисляли при использовании линейного правила трапеций.
[0755] Системная экспозиция. Системная экспозиция соединения 175 была низкой по сравнению с тканями сухожилия и кожи после однократного наружного применения композиции 1 или 10 мг/мл с BA или Tween 80. Уровни в плазме в Группах 1 и 2 (композиция 1 и 10 мг/мл, содержащая BA) составляли: 1,30 и 10,6 нг/мл Cmax и 0,650 и 36,1 ч⋅нг/мл AUC(0-last) соответственно, демонстрируя пропорциональное дозе увеличение Cmax и превышающее пропорциональное дозе увеличение общей экспозиции (AUC(0- last)). Экспозиция в Группе 3 (композиция 10 мг/мл без BA, но содержащая Tween 80) составляла 1,94 нг/мл Cmax и 6,79 ч⋅нг/мл AUC(0-last), что составило ~0,2× для Группы 2 (10 мг/мл с BA).
[0756] Экспозиция в сухожилиях. Экспозиция соединения 175 в ахилловом сухожилии в Группах 1 и 2 (композиция 1 и 10 мг/мл, содержащая BA) составила 519 и 1930 нг/г Cmax и 2164 и 7270 ч⋅нг/г AUC(0-last) соответственно, что указывает на меньшее, чем пропорциональное дозе увеличение экспозиции: 3,4-кратное увеличение AUC(0-last) при увеличении дозы в 10 раз. Уровни в сухожилии в Группе 3 (10 мг/мл без BA) составляли 7053 нг/г Cmax и 28077 ч⋅нг/г AUC(0-last), что было в ~4 раза больше, чем в Группе 2 (10 мг/мл с BA). Отношения уровней в сухожилиях к уровням в плазме (AUC(0-last)) составляли 3329 и 202 в Группах 1 и 2 (композиции 1 и 10 мг/мл, содержащие BA) и 4135 в Группе 3 (10 мг/мл без BA).
[0757] Концентрации в коже в Группе 2 (10 мг/мл с BA) приведены в приближении, поскольку все значения превышали предел количественного определения (AQL>25000 нг/г). Средние концентрации в коже через 7 и 24 часа после введения дозы составляли ~208600 и 113375 нг/г, примерно в 1000× выше концентраций в сухожилиях в эти временные точки. Параметры ФК в плазма, сухожилиях и коже представлены ниже в Таблице 9, и профили зависимости концентрации от времени показаны на ФИГ. 11.
Таблица 9
[0758] Общий объем дозы=60 мкл/лодыжка задней конечности; n=2 (плазма), n=4 (сухожилие, кожа; 2).
[0759] NC=не вычисляли из-за отсутствия достаточного количества временных точек для вычисления AUC.
[0760] 1) Значение выше предела количественного определения (AQL>25000 нг/г) приведено в приближении.
[0761] Системная экспозиция соединения 175 у крыс после однократного наружного применения была низкой во всех группах дозы по сравнению с уровнями в сухожилиях, с изменением отношения концентраций в сухожилиях к концентрациям в плазме в пределах 202-4135 между группами. Дозозависимое увеличение концентраций в плазме и сухожилиях было отмечено для композиций 1 и 10 мг/мл, содержащих BA. Тогда как композиция 10 мг/мл без BA (содержащая Tween 80) показала более низкие системные экспозиции (0,2×) по сравнению с композицией, содержащей BA, концентрация в сухожилиях была в 4 раза выше, чем для композиции 10 мг/мл, содержащей BA.
[0762] Термин "включающий" при использовании в настоящем документе является синонимом "содержащего" или "отличающегося тем, что", и является включительным или открытым и не исключает дополнительные, неуказанные элементы или стадии способа.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНДАЗОЛ-3-КАРБОКСАМИДЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ СИГНАЛЬНОГО ПУТИ WNT/b-КАТЕНИНА | 2012 |
|
RU2627693C2 |
| ИНГИБИТОРЫ HPK1 И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2839132C2 |
| АНИЛИДЫ АМИНОКИСЛОТ В КАЧЕСТВЕ НИЗКОМОЛЕКУЛЯРНЫХ МОДУЛЯТОРОВ IL-17 | 2019 |
|
RU2815505C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ MAT2A И СПОСОБЫ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2019 |
|
RU2809987C2 |
| 1Н-ПИРАЗОЛО[3,4-B]ПИРИДИНЫ И ИХ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2013 |
|
RU2689141C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2681849C2 |
| ИНДАЗОЛЬНЫЕ ИНГИБИТОРЫ СИГНАЛЬНОГО ПУТИ WNT И ИХ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2017 |
|
RU2682245C1 |
| 6-5 КОНДЕНСИРОВАННЫЕ КОЛЬЦА КАК ИНГИБИТОРЫ С5а | 2018 |
|
RU2780338C2 |
| ИНДАЗОЛЬНЫЕ ИНГИБИТОРЫ СИГНАЛЬНОГО ПУТИ WNT И ИХ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2013 |
|
RU2638932C2 |
| ЗАМЕЩЕННЫЕ ХРОМАНЫ | 2015 |
|
RU2718060C2 |
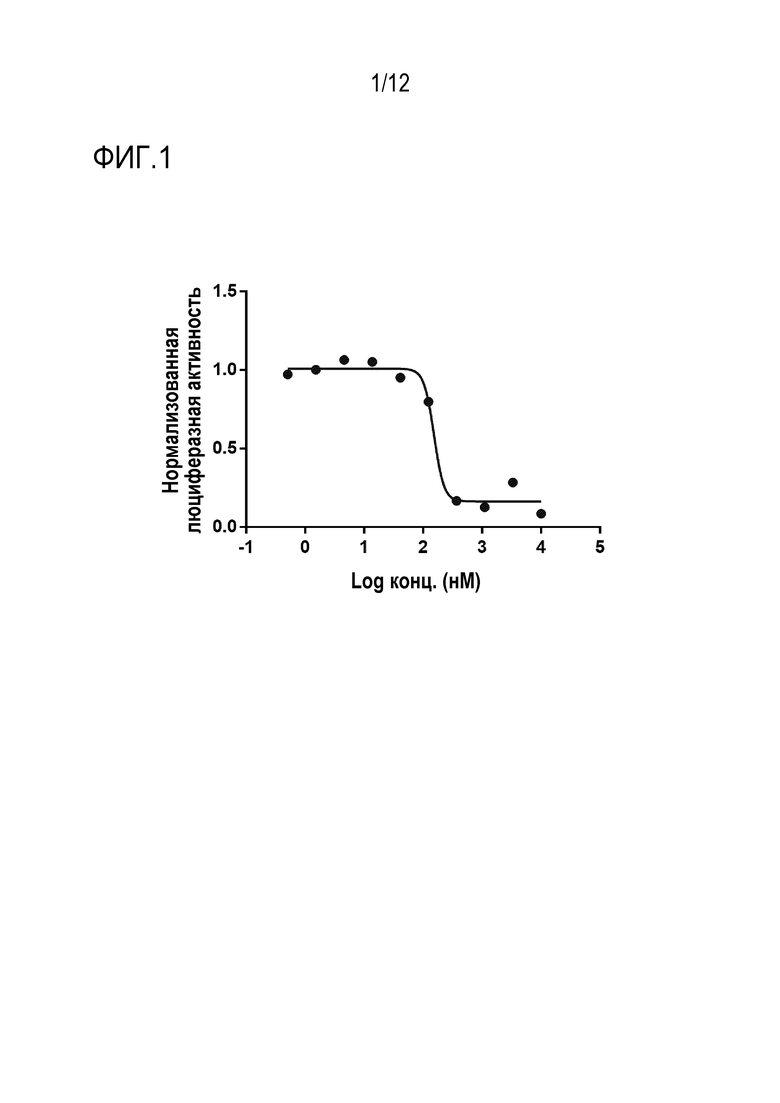
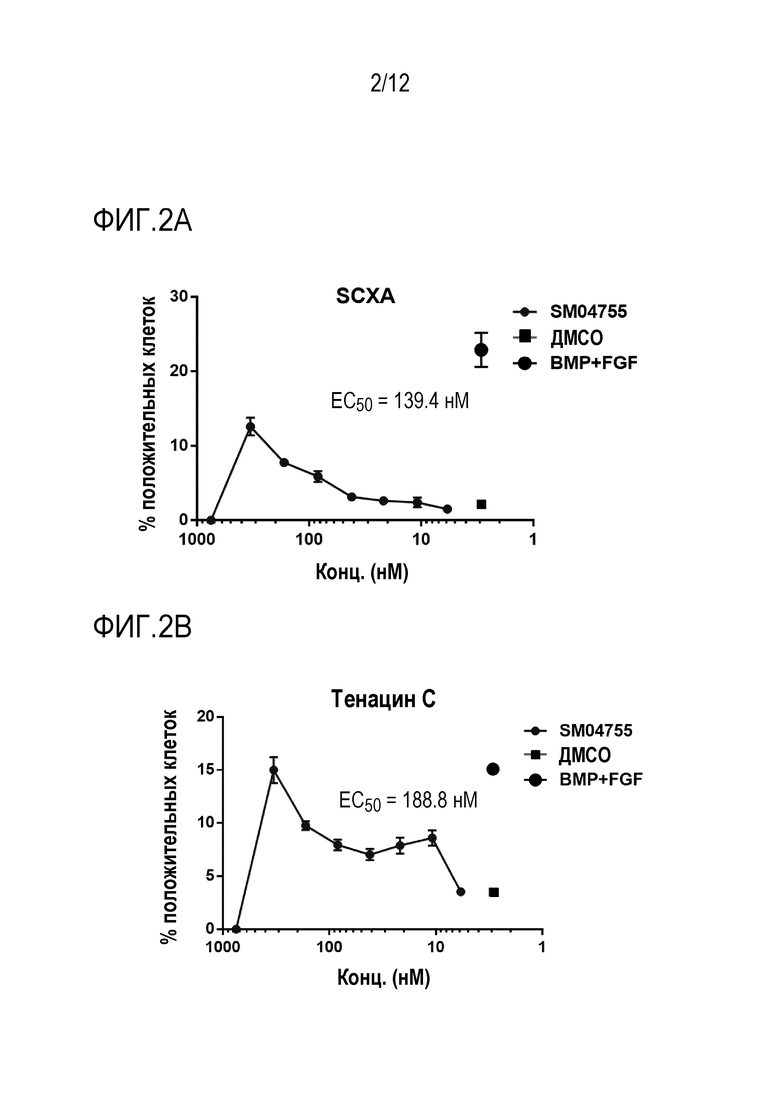
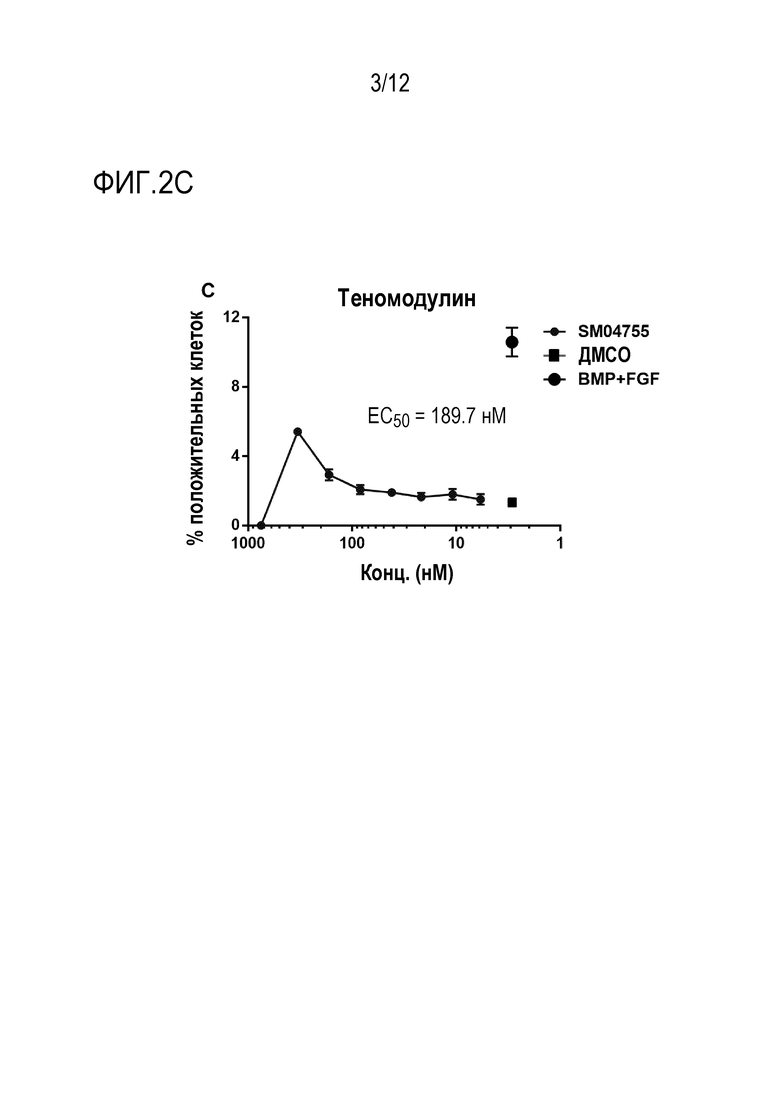
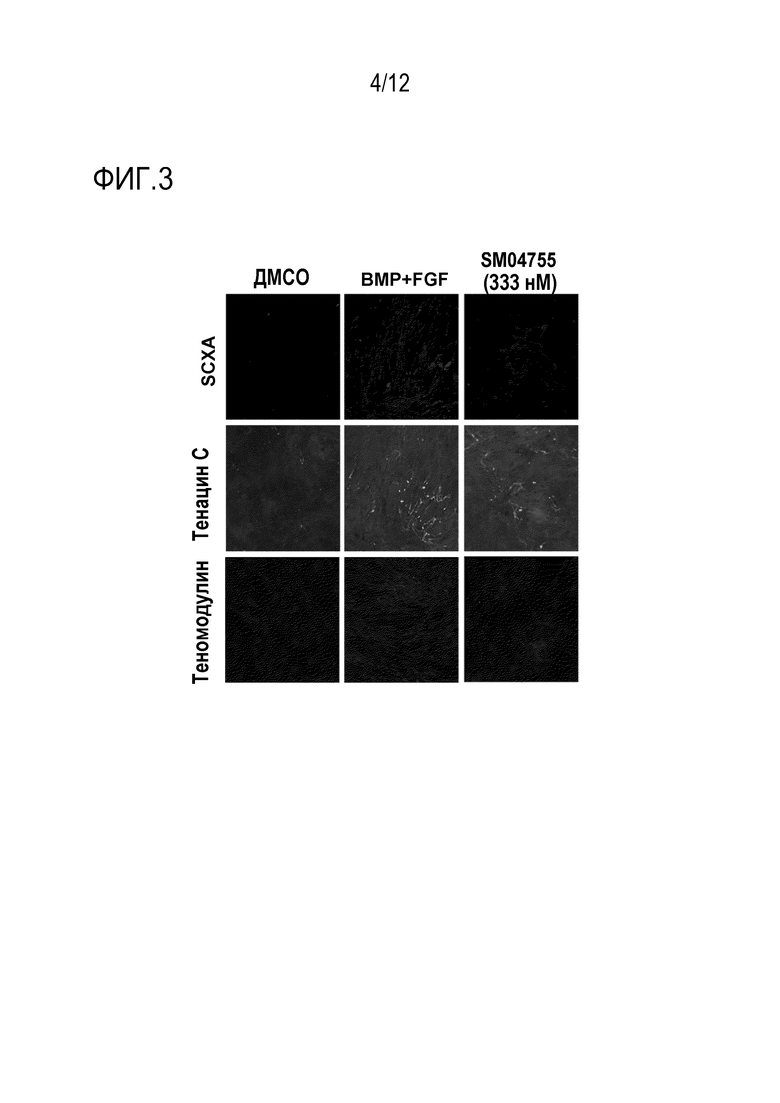
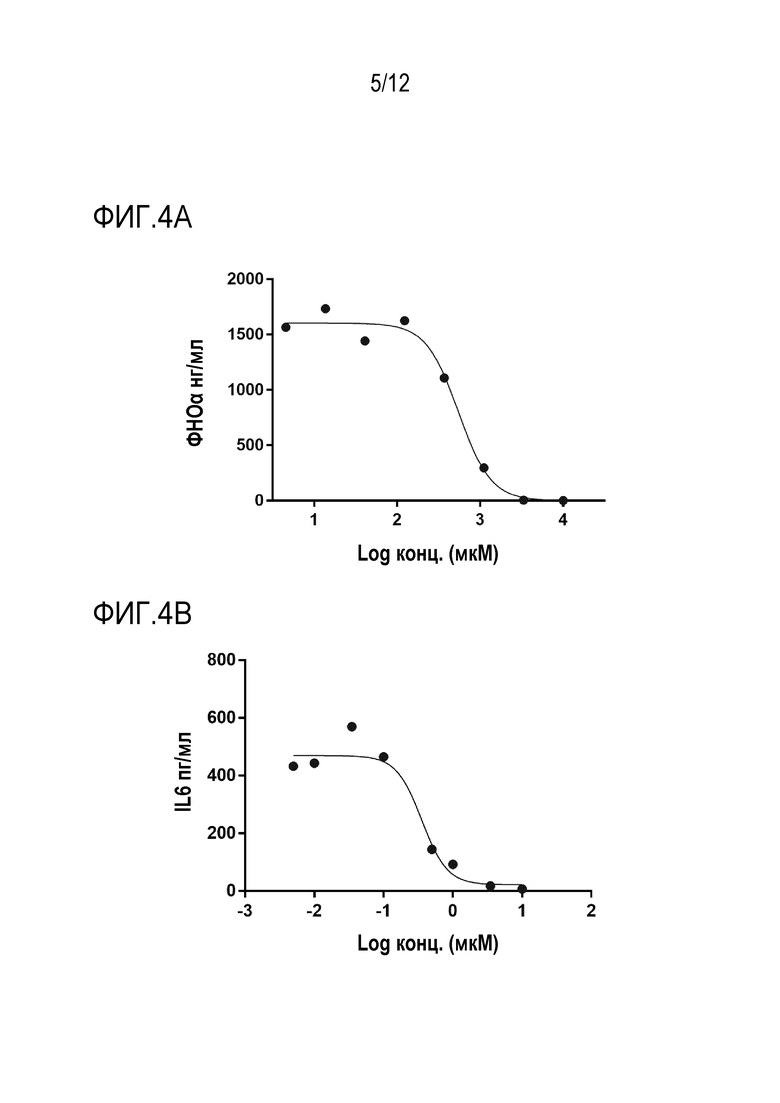

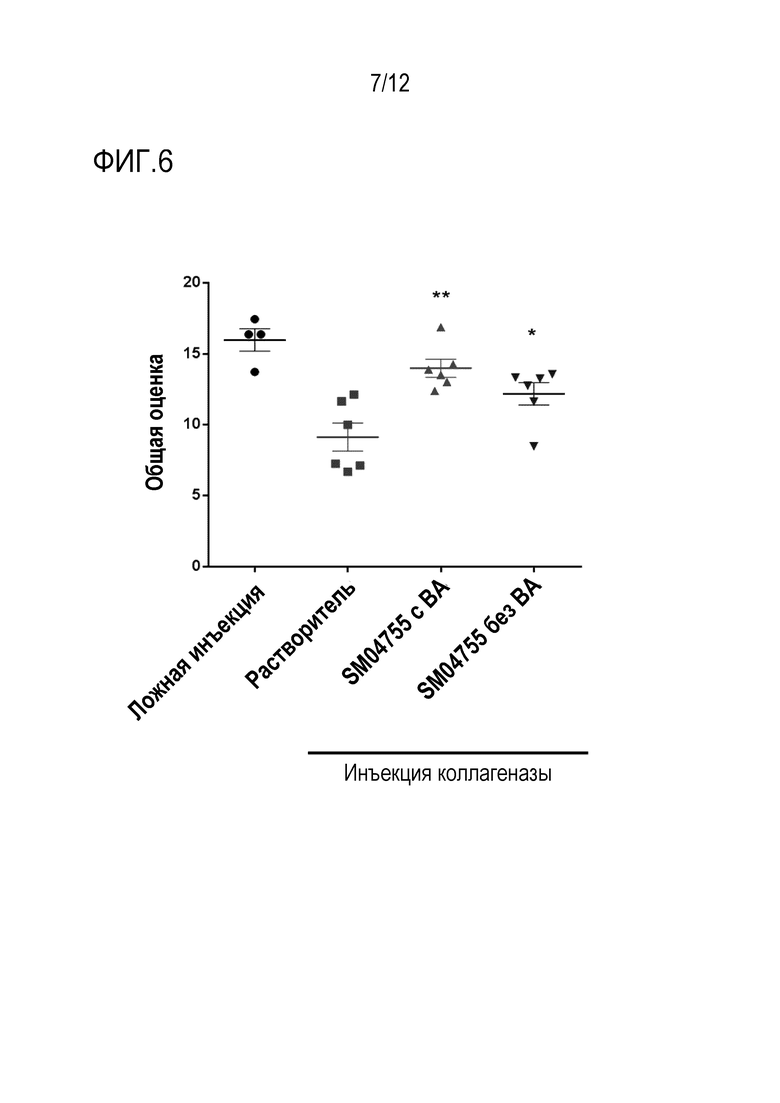
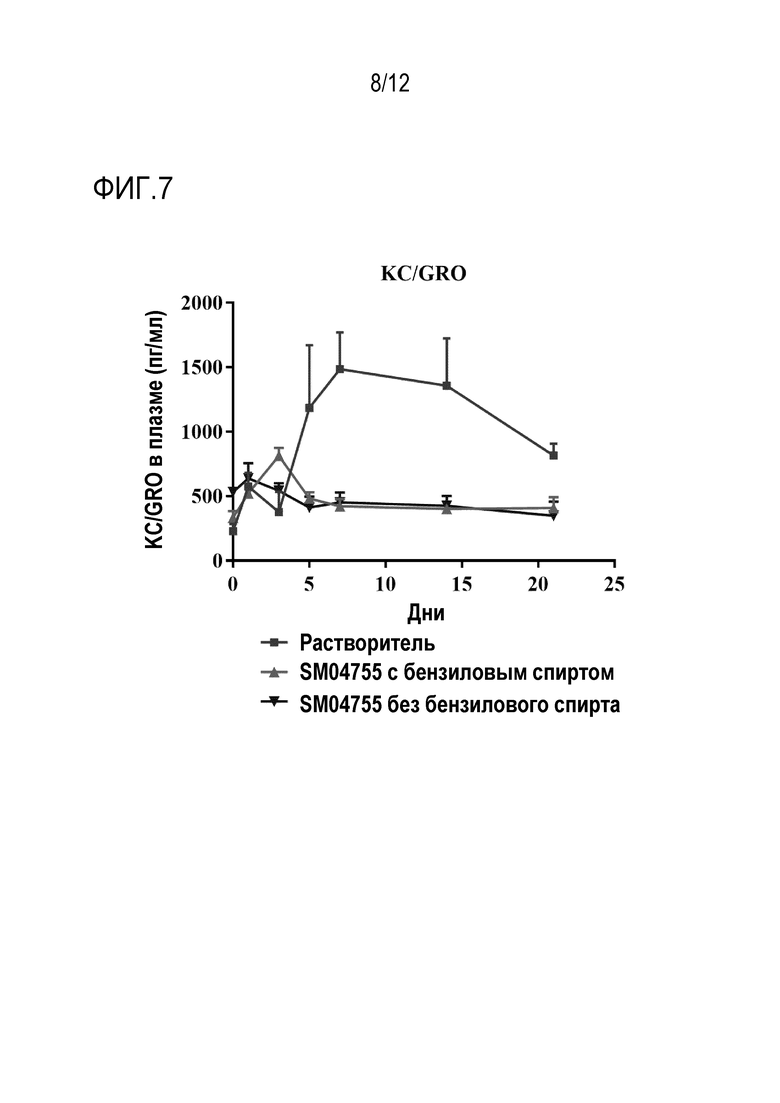
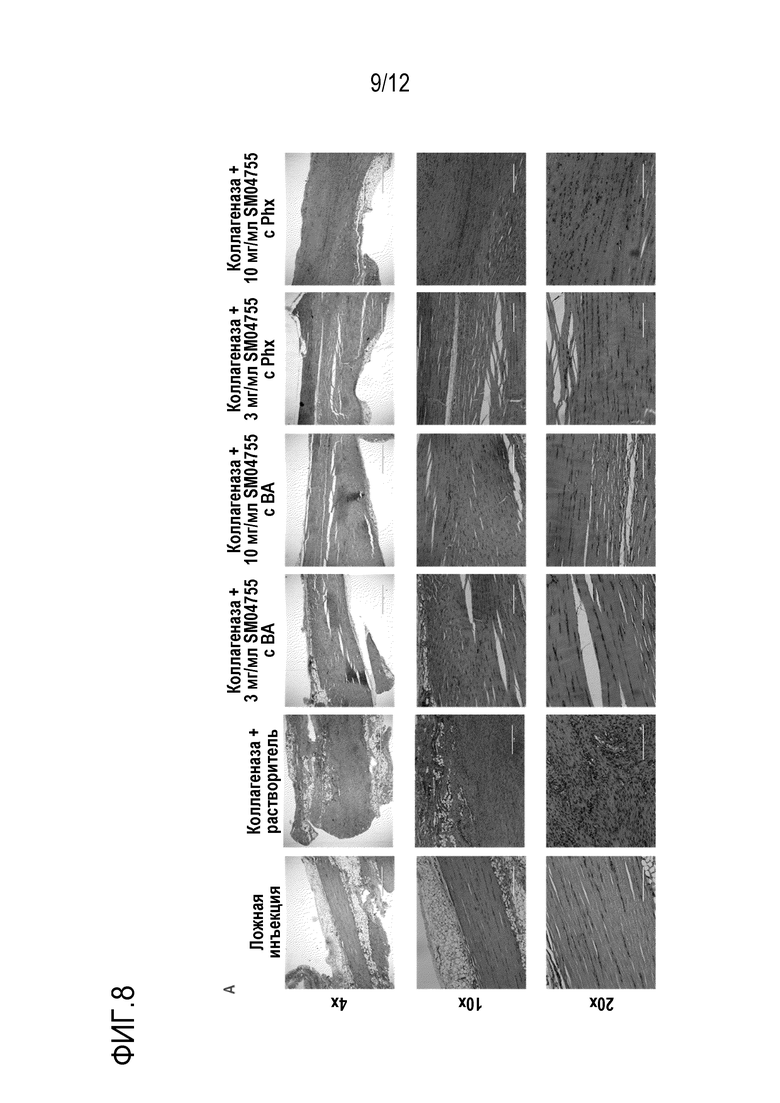
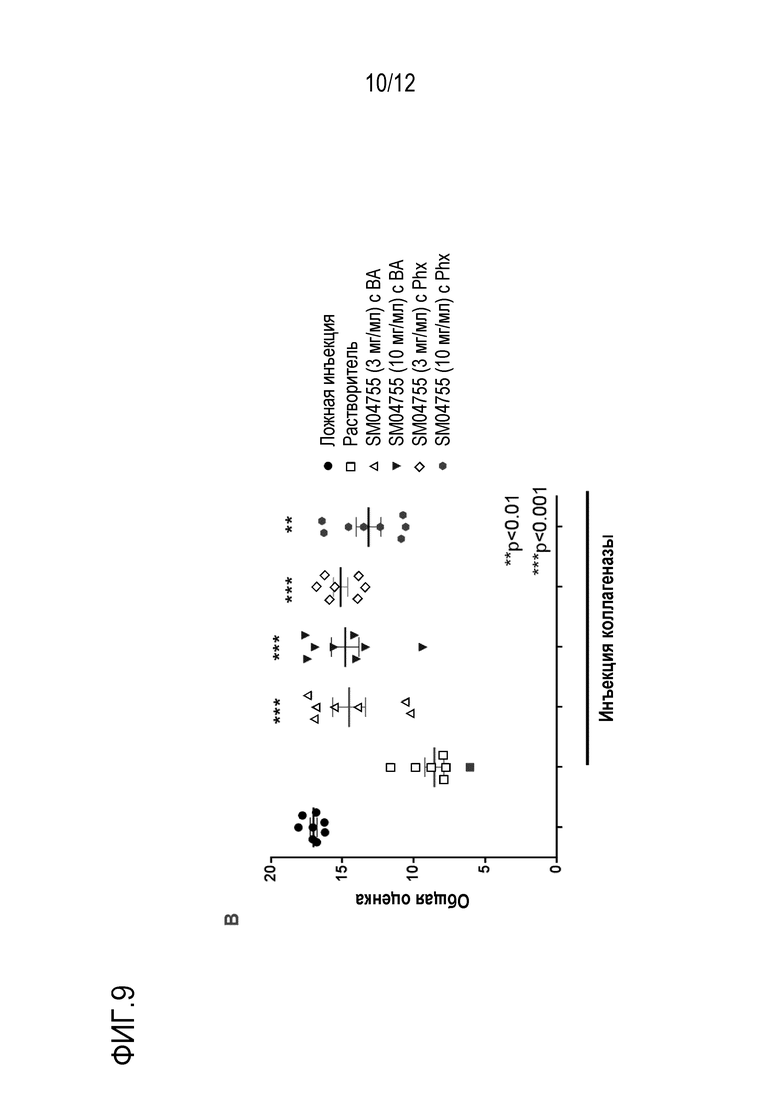
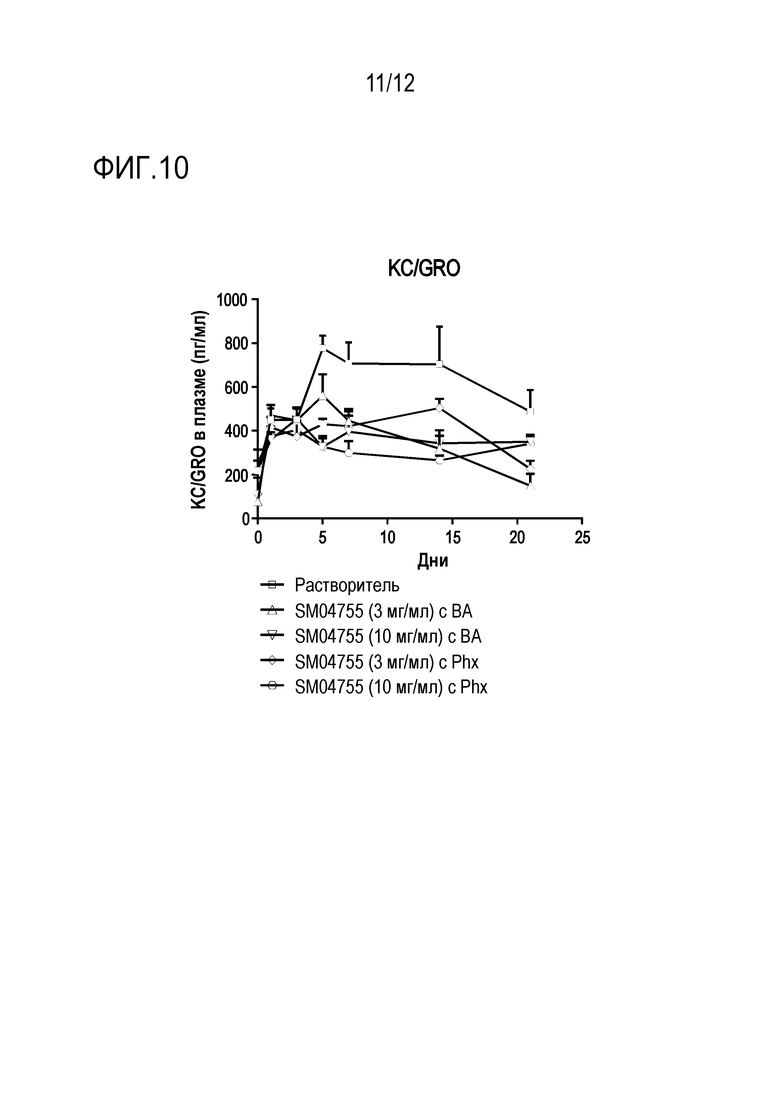
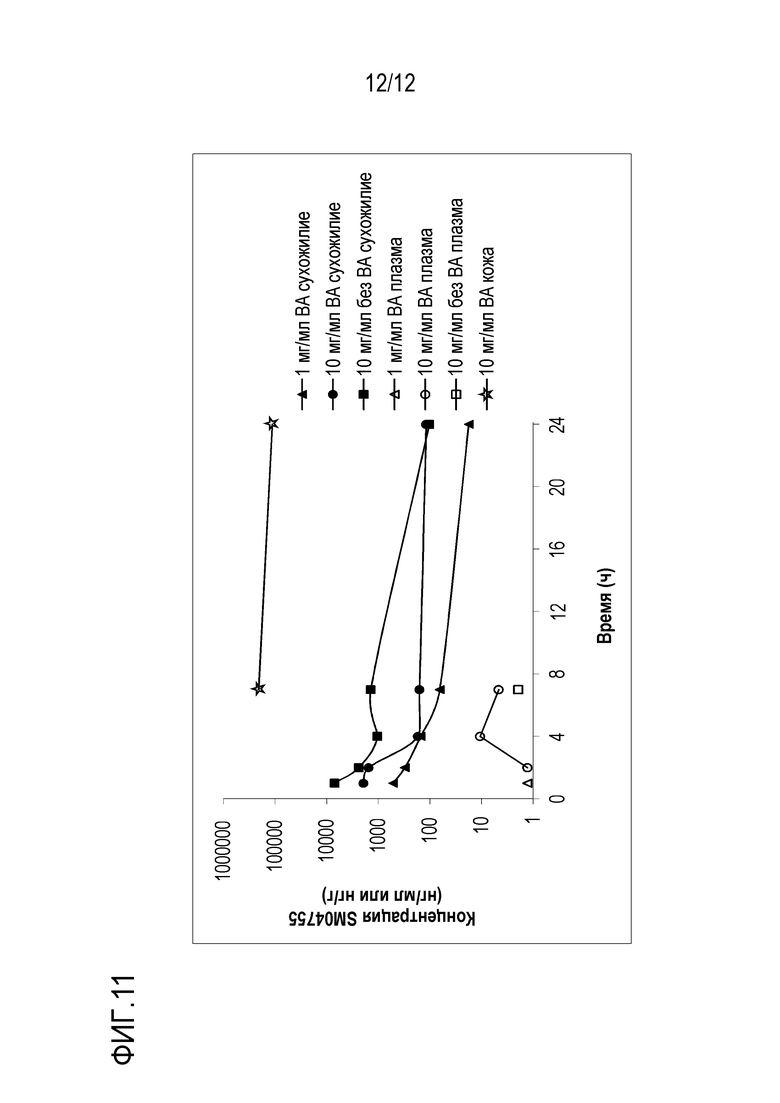
Группа изобретений относится к области фармацевтики и медицины и направлена на лечение тендинопатии. В частности, описаны способы лечения тендинопатии, включающие введение субъекту терапевтически эффективного количества соединений, имеющих структурные Формулы I и Iа (значения радикалов такие, как указано в формуле изобретения), а кроме того, ряда индивидуальных соединений или их фармацевтически приемлемых солей. Технический результат: эффективное лечение тендинопатии. 5 н. и 31 з.п. ф-лы, 11 ил., 9 табл., 14 пр.
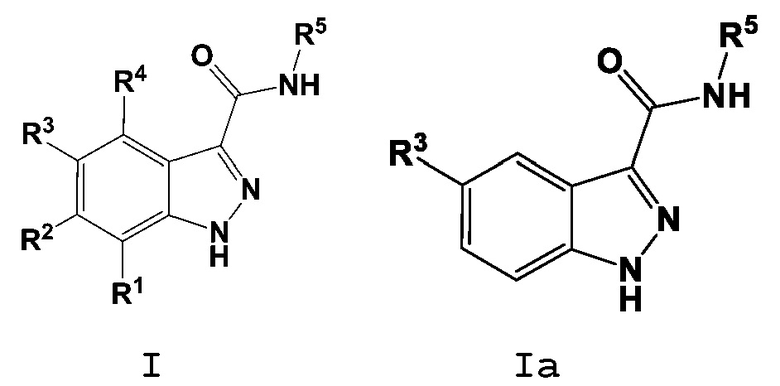
1. Способ лечения тендинопатии, включающий введение нуждающемуся в этом субъекту соединения или его фармацевтически приемлемой соли, имеющего структурную Формулу I
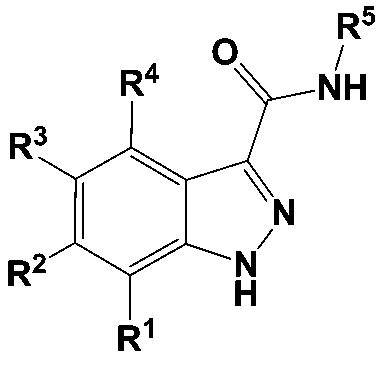
I,
где R1, R2 и R4 означают H;
R3 выбран из группы, состоящей из фенилR6 и 6-членного гетероарилR6;
R5 выбран из группы, состоящей из -(3-6-членный карбоциклил)R7, -(3-10-членный гетероциклил)R7, -фенилR7 и -(C1-9 алкил)n(5-6-членный гетероарил)R7;
каждый R6 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-9 алкила, галогенида, амино, -CF3, -CN, -XR10, -(C1-9 алкил)n(3-6-членный гетероциклил)R8, -C(=O)R11, -N(R10)C(=O)R11 и -(C1-9 алкил)nN(R10)2;
каждый R7 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-9 алкила, галогенида, амино, -CF3, -CN, -XR10, -(C1-9 алкил)n(3-6-членный гетероциклил)R9, -(C1-9 алкил)nфенилR9, -C(=O)R11, -N(R10)C(=O)R11, -(C1-9 алкил)nN(R10)2 и -N(R10)SO2R11;
каждый R8 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида и -XR12;
каждый R9 является 1-5 заместителями, каждый из которых выбран из группы, состоящей из H, C1-3 алкила, галогенида и -XR12;
каждый R10 независимо выбран из группы, состоящей из H, C1-9 алкила, -(C1-9 алкил)nN(R14)2 и фенилR8;
каждый R11 независимо выбран из группы, состоящей из C1-9 алкила, -N(R14)2, -(3-6-членный карбоциклил)R8, -(3-6-членный гетероциклил)R8 и -(5-6-членный гетероарил)R8;
каждый R12 независимо выбран из группы, состоящей из H и C1-9 алкила;
каждый R14 независимо выбран из группы, состоящей из H, C1-3 алкила и (3-6-членного карбоциклила);
каждый X представляет собой -O-; и
каждое n является 0 или 1.
2. Способ по п.1, где R3 является 3-пиридилR6.
3. Способ по п.1, где R3 является 5-пиримидинилR6.
4. Способ по п.1, где R3 является 4-пиридазинилR6.
5. Способ по п.2, где R6 является одним заместителем и является -N(R9)C(=O)R10.
6. Способ по п.2, где R6 является одним заместителем и является -(CH2)гетероциклилR8.
7. Способ по п.6, где R6 гетероциклил независимо выбран из группы, состоящей из азетидинилR8, пирролидинилR8, пиперидинилR8, пиперазинилR8 и морфолинилR8.
8. Способ по п.1, где R5 является 3-пиридилR7.
9. Способ по п.2, где R5 является 3-пиридилR7.
10. Способ по п.1, где R5 является 5-пиримидинилR7.
11. Способ по п.1, где R5 является 4-пиридазинилR7.
12. Способ по п.8, где R7 является одним заместителем и выбран из группы, состоящей из галогенида, -CF3, -(C1-9 алкил)nN(R10)2, N(R10)SO2R11 и -N(R10)C(=O)R11.
13. Способ по п.9, где R7 является одним заместителем и выбран из группы, состоящей из галогенида, -CF3, -(C1-9 алкил)nN(R10)2, N(R10)SO2R11 и -N(R10)C(=O)R11.
14. Способ по п.8, где R7 является одним заместителем и выбран из группы, состоящей из-OR10 и -C(=O)R11, где R11 является -N(R10)2 и каждый R10 независимо выбран из группы, состоящей из H, метила и карбоциклилR8, где каждый R8 является 1-2 заместителями, независимо выбранными из H или галогенида.
15. Способ по п.9, где R7 является одним заместителем и выбран из группы, состоящей из -OR10 и -C(=O)R11, где R11 является -N(R10)2 и каждый R10 независимо выбран из группы, состоящей из H, метила и карбоциклилR8, где каждый R8 является 1-2 заместителями, независимо выбранными из H или галогенида.
16. Способ по п.1, где соединение имеет структуру, выбранную из группы, состоящей из:
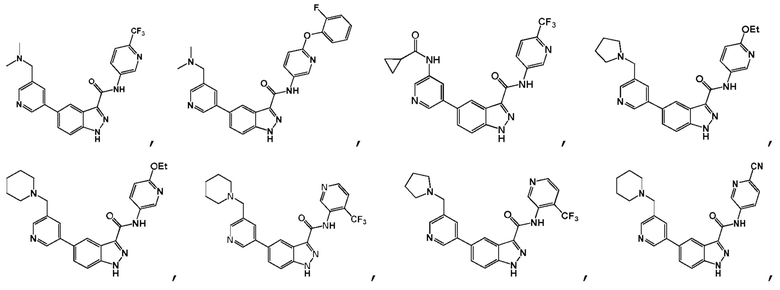
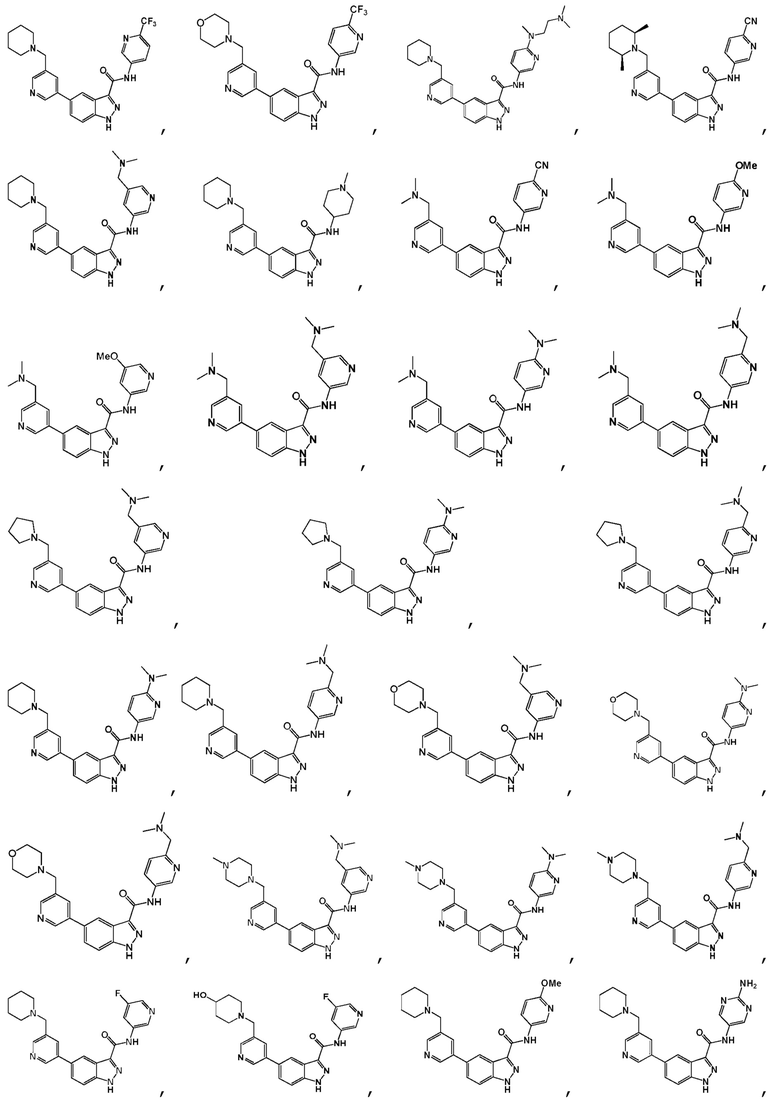


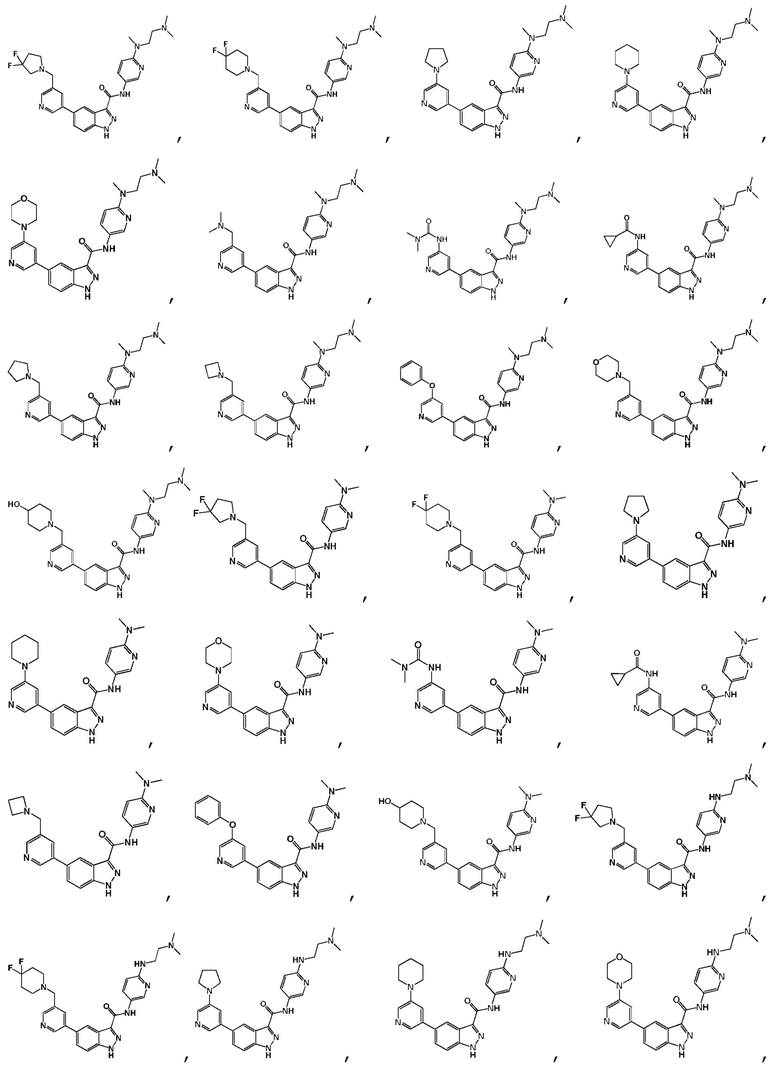




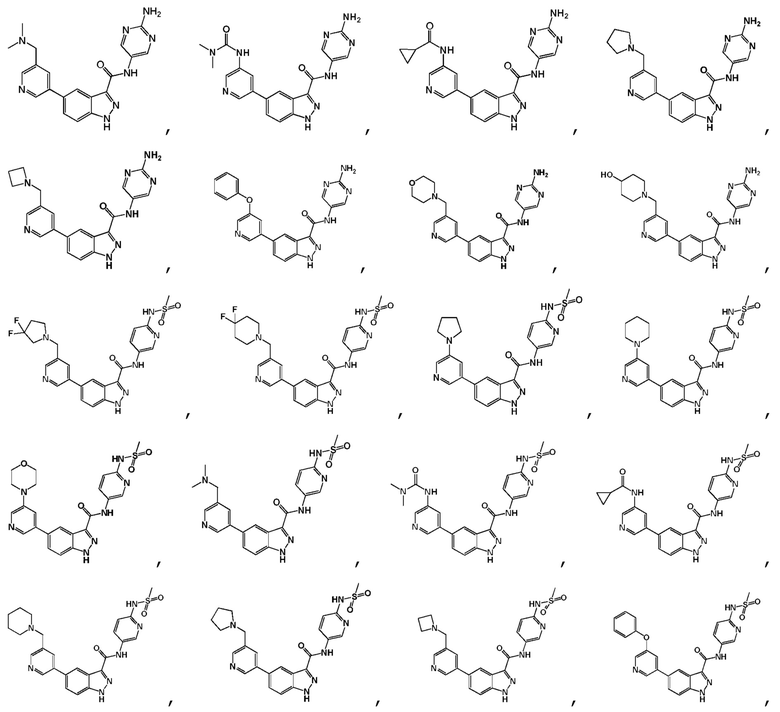
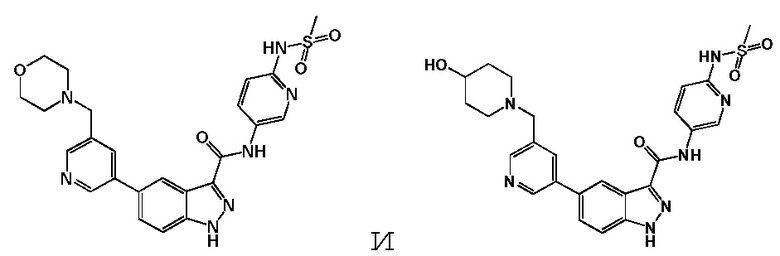 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
17. Способ по п.16, где соединение имеет структуру, выбранную из группы, состоящей из:
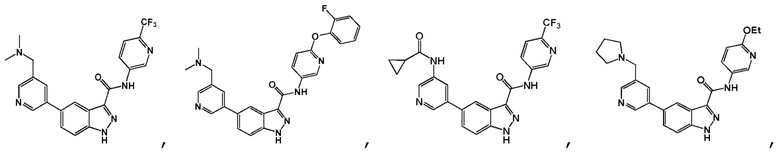

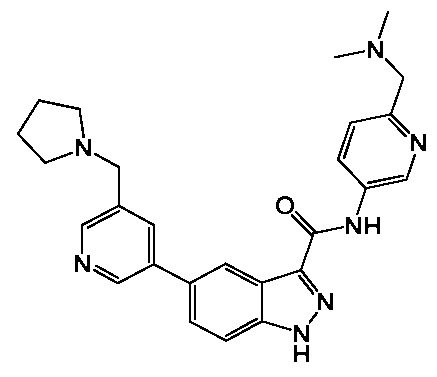 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
18. Способ по п.16, где соединение имеет структуру, выбранную из группы, состоящей из:
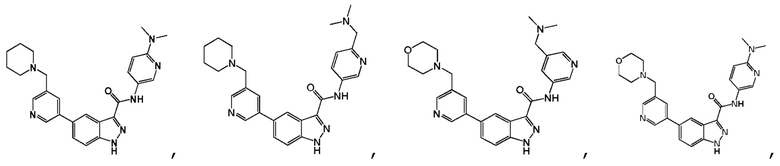
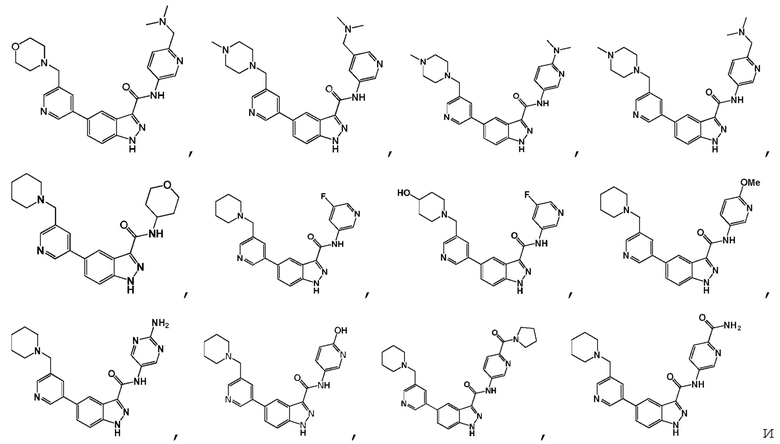
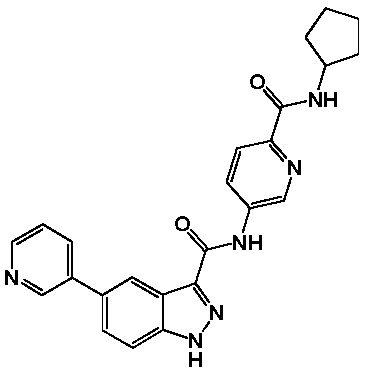 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
19. Способ по п.16, соединение имеет структуру, выбранную из группы, состоящей из:
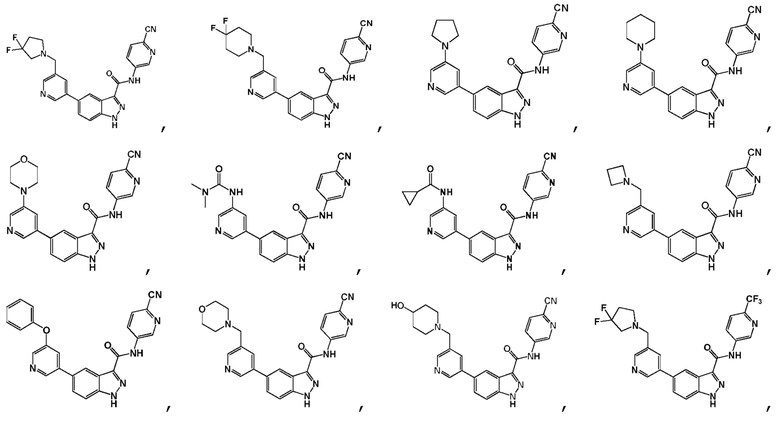

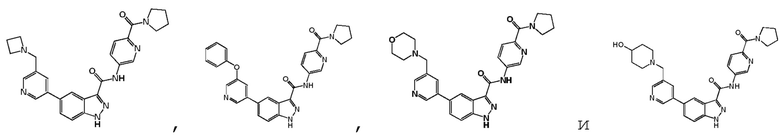 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
20. Способ по п.16, где соединение имеет структуру, выбранную из группы, состоящей из:

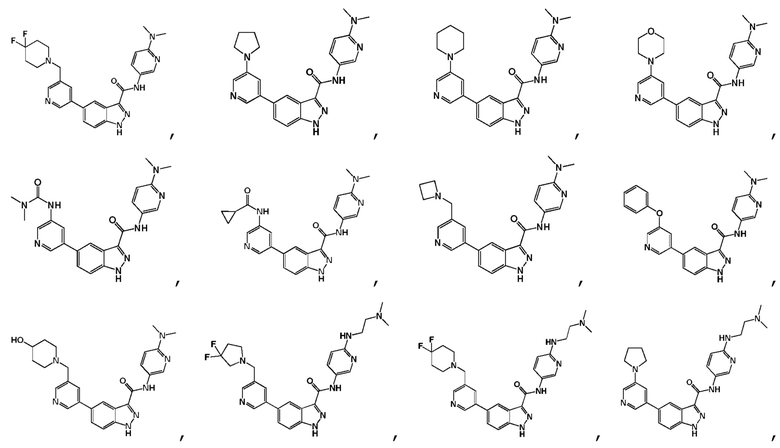
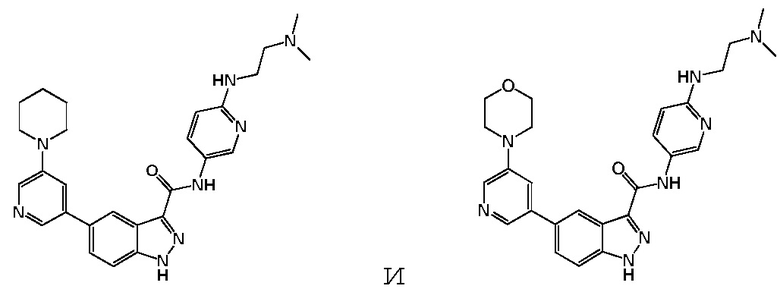 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
21. Способ по п.16, где соединение имеет структуру, выбранную из группы, состоящей из:
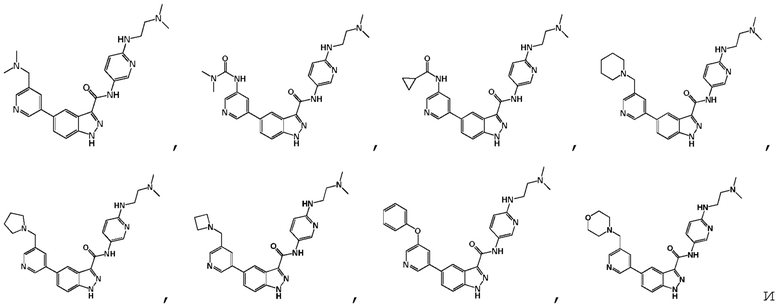
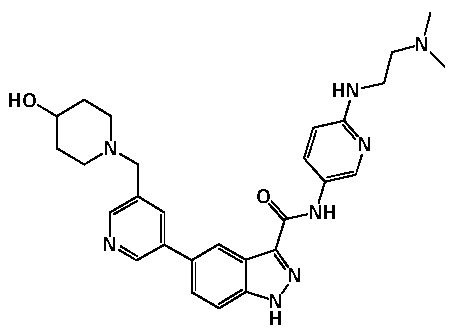 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
22. Способ по п.16, где соединение имеет структуру, выбранную из группы, состоящей из:


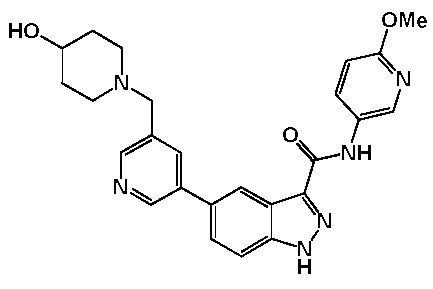 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
23. Способ по п.16, где соединение имеет структуру, выбранную из группы, состоящей из:
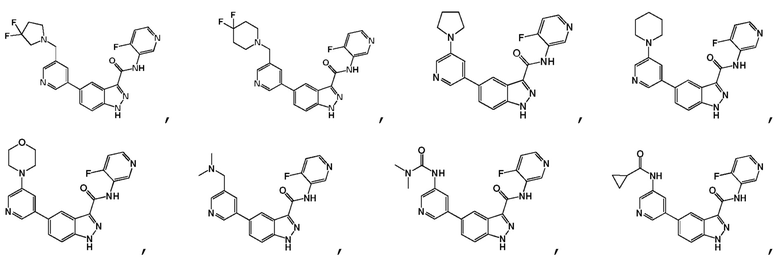

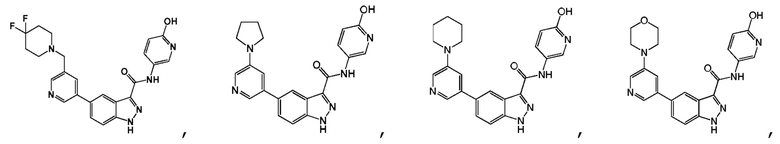
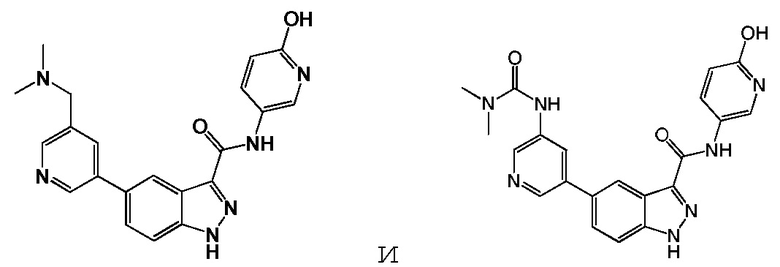 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
24. Способ по п.16, где соединение имеет структуру, выбранную из группы, состоящей из:


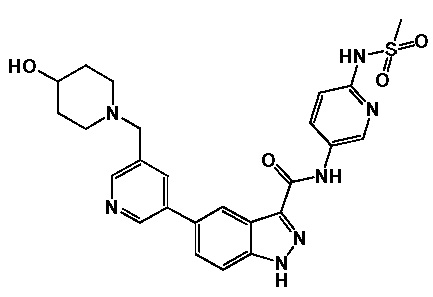 , или его фармацевтически приемлемая соль.
, или его фармацевтически приемлемая соль.
25. Способ лечения тендинопатии, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли, имеющего структурную Формулу Ia
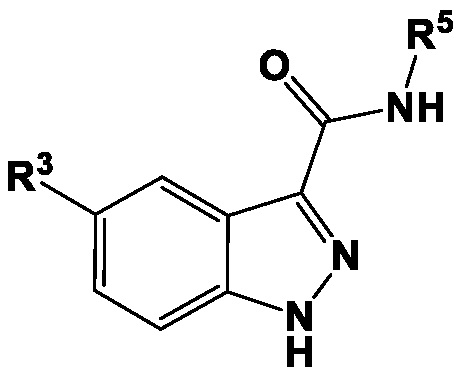
Ia,
где R3 является 3-пиридилR6;
R5 выбран из группы, состоящей из пиридилR7, -пиримидинилR7 и -пиридазинилR7;
R6 является -CH2(3-6-членный гетероциклил)R8;
R7 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H, F, метила, -NH2, -CF3, -CN, -OMe, 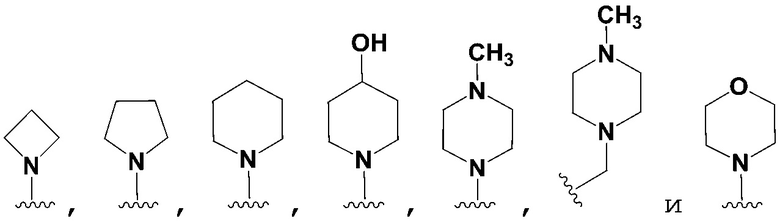 ; и
; и
R8 является 1-2 заместителями, каждый из которых независимо выбран из группы, состоящей из H и галогенида.
26. Способ по п.25, где R6 гетероциклил выбран из группы, состоящей из азетидинилR8, пирролидинилR8, пиперидинилR8, пиперазинилR8 и морфолинилR8.
27. Способ по п.25, где R6 является -CH2пиперидинилR8.
28. Способ по п.25, где R7 выбран из группы, состоящей из H, -CF3, -OMe, -CN, 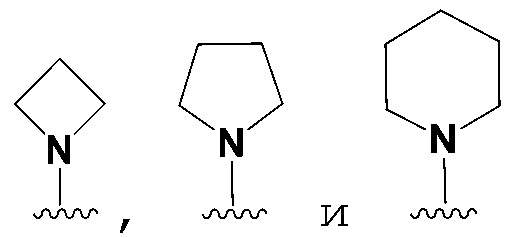 .
.
29. Способ по п.26, где R8 является H.
30. Способ по п.27, где R8 является H.
31. Способ лечения тендинопатии, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли, имеющего структуру 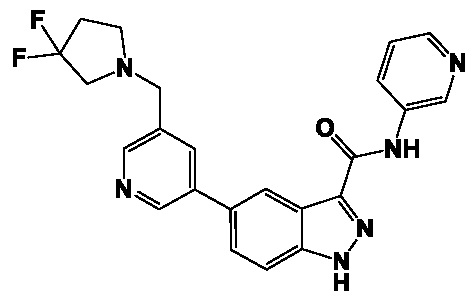 .
.
32. Способ лечения тендинопатии, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли, имеющего структуру 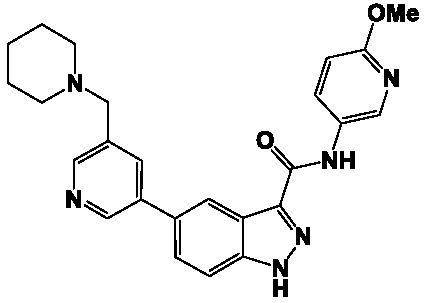 .
.
33. Способ лечения тендинопатии, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества соединения или его фармацевтически приемлемой соли, имеющего структуру 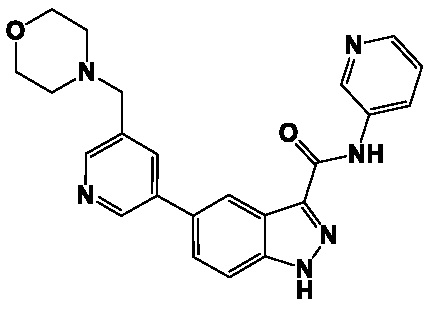 .
.
34. Способ по любому одному из пп. 1, 25 и 31-33, где тендинопатия является тендинозом.
35. Способ по любому одному из пп. 1, 25 и 31-33, где тендинопатия является тендинитом.
36. Способ по любому одному из пп. 1, 25 и 31-33, где тендинопатия является тендовагинитом.
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| P.P.Y | |||
| LUI | |||
| Histopathological changes in tendinopathy—potential roles of BMPs?, Rheumatology, vol | |||
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
| Сердечник для отливки полых металлических предметов | 1915 |
|
SU2116A1 |
| EA 200200768, 27.02.2003. | |||
Авторы
Даты
2022-04-19—Публикация
2017-10-20—Подача