ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к определенным новым способам отбора эпитопов белков-мишеней, применяемых для получения антитела (например, функционального антитела), но не ограничиваясь указанным. Настоящее изобретение, таким образом, согласно некоторым аспектам относится к способу получения антитела. Такие способы, как правило, включают идентификацию антигенного эпитопа и получение (индукцию синтеза) антитела против указанного антигенного эпитопа. Настоящее изобретение также относится к антигенным эпитопам и к антителам, которые связываются с такими антигенными эпитопами.
УРОВЕНЬ ТЕХНИКИ
Терапевтические средства на основе антител становятся все более распространенными, во многом благодаря клинической эффективности, который наблюдается в случае некоторых вариантов терапии на основе моноклональных антител (МАТ), включающей антитела Хумира, Авастин, Герцептин, и благодаря потенциалу, например, новых вариантов лечения для снижения уровня холестерола на основе МАТ, нацеленных на PCSK9, таких как алирокумаб и эволокумаб. Однако все антитела, которые на сегодняшний день присутствуют на рынке, и все антитела, находящиеся на поздних стадиях клинической разработки, как правило, нацелены на внеклеточные мишени, и данные антитела обычно обнаруживают и разрабатывают с применением платформ скрининга, основное внимание в которых уделяется силе аффинности или связывания. Однако разработка действующих внутри клеток антител и антител, направленных на «сложные мишени», т.е. мишени, в случае которых традиционная методика обнаружения антител оказалась неудачной, представляет собой крайне серьезную проблему, для решения которой требуется применение новых достижений технического прогресса с целью обнаружения и разработки эффективных антител. В случае действующих внутри клеток антител также необходимы новые инструменты для интернализации антител в клетки в правильных органах-мишенях. Более того, в существующих платформах для обнаружения и разработки антител, как правило, отсутствуют функциональные, фармакологические соотношения и соотношения механизма действия, которые позволяют прогнозировать работу конкретного антитела в данной биологической системе, например, при патологическом состоянии.
На сегодняшний день стратегии разработки и обнаружения эффективных терапевтических средств на основе антител не ограничены полноразмерными моноклональными антителами. Благодаря достижениям в белковой инженерии в течение двух последних десятилетий было получено широкое множество сконструированных фрагментов антител, включая Fab-фрагменты, ScFv-фрагменты, диатела, тетратела, функционализированные конъюгатами белков фрагменты антител, а также биспецифичные фрагменты, связывающиеся с двумя антигенами. Данные новые конструкции обеспечивают значительно больший набор инструментов для возможностей разработки антител и биологических средств на основе антител с высокой специфичностью и аффинностью, глубоким проникновением в ткани, высокой стабильностью и низкой токсичностью. Однако все еще сохраняется одно из главных препятствий в случае терапевтических средств на основе антител, которое заключается в том, что указанные терапевтические средства ограничены внеклеточными мишенями. Антитела являются слишком большими и крайне полярными, чтобы проходить через клеточную мембрану. Дополнительно, антитела, как правило, являются нестабильными в восстановительной среде цитозоля. Для изучения внутриклеточных мишеней было разработано несколько методик, включая транспортирование антител через клеточную мембрану с помощью различных транспортирующих векторов, например, реактивов для трансфекции и доменов белковой трансдукции (protein transduction domains, PTD), а также экспрессия антитела непосредственно внутри клетки-мишени, что приводит к образованию так называемых интрател. Также применяли методики электропорации, хотя в случае антител и не так широко, как в случае малых молекул и генетического материала. Интратела могут быть сконструированы для нацеливания на различные компартменты клетки посредством слияния генетической последовательности интратела с сигналами внутриклеточного транспорта. Потребность в эффективных векторах доставки, тем не менее, является критически важным этапом терапии интрателами, поскольку генетический материал, кодирующий интратело, еще должен быть доставлен в клетку-мишень.
Получение моноклональных антител с применением гибридомных технологий впервые было разработано в 1975 году. Вкратце, млекопитающим инъецируют антиген, представляющий интерес, который запускает у указанных млекопитающих иммунный ответ. Затем из селезенки животного отбирают спленоциты, которые сливают с иммортализованными клетками миеломы. Клетки разбавляют до степени разведения в одну клетку и разделяют на многолуночных планшетах. Поскольку начало каждой отдельной колонии дает одна клетка, наработанные антитела в одной лунке будут являться моноклональными. Следующий этап заключается в скрининге всех различных лунок для выбора наилучшего кандидата для связывания с антигеном.
Огромное преимущество фрагментов антител меньшего размера по сравнению с полноразмерными антителами заключается в том, что такие фрагменты можно получить в различных системах экспрессии, например, в Escherichia coli, дрожжах и клетках млекопитающих, и данные фрагменты больше не ограничены получением с помощью гибридомной технологии. Данное преимущество делает возможной крупномасштабную наработку при меньших затратах и обеспечивает множество возможностей для модуляции свойств антитела генетическим способом. Фрагменты антитела могут быть экспонированы на поверхности нитевидного бактериофага, так называемый фаговый дисплей, что можно использовать для создания больших библиотек антител, скрининг которых проводят в отношении целевого антигена. В ходе процедуры скрининга оценивают антитела-кандидаты, которые связываются с антигеном. Такой скрининг часто повторяют в ходе нескольких циклов по причине неспецифичного связывания на первых циклах. Условия в ходе циклов скрининга можно менять для обнаружения кандидатов, наиболее подходящих для определенных условий, например, посредством применения агрессивных условий можно выбрать более стабильные антитела. Другой способ выбора антител с очень высокой аффинностью заключается в осуществлении скрининга с очень низкой концентрацией антигена, в результате чего при таких условиях останутся исключительно антитела, способные к связыванию. Некоторые компании разработали свои собственные технологии скрининга и часто имеют обширные библиотеки антител, см., например, Regeneron (regeneron.com) или Alligator bioscience (alligatorscience.se).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно одному аспекту в настоящем изобретении предложен способ создания антитела против белка, причем указанный способ включает:
(i) идентификацию антигенного эпитопа в указанном белке посредством воздействия на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной (разобранной) или усеченной версии указанного белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от указанного белка под действием указанной протеазы, и создание антигенного эпитопа на основе указанного экспонированного на поверхности пептида; и
(ii) получение антитела против указанного антигенного эпитопа.
Согласно другому аспекту в настоящем изобретении предложен способ создания антитела против белка, причем указанный способ включает:
(i) воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта указанного белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии указанного белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от указанного белка под действием указанной протеазы; и
(ii) идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в области белка, которая приводит к утрате или существенному изменению биологической функции указанного белка, когда пептид отщепляют или удаляют от указанного белка в течение ограниченного или частичного протеолиза; или выбор по меньшей мере одной области-мишени в указанном белке на основании биоинформационных данных и/или известных данных о биологической функции указанного белка и идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в указанной по меньшей мере одной области-мишени; и
(iii) получение антитела против указанного антигенного эпитопа.
Согласно другому аспекту в настоящем изобретении предложен способ идентификации антигенного эпитопа, причем указанный способ включает:
(i) воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта указанного белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от указанного белка под действием указанной протеазы; и
(ii) идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в области указанного белка, которая приводит к утрате или существенному изменению биологической функции указанного белка, когда пептид отщепляют или удаляют от указанного белка в течение ограниченного или частичного протеолиза; или
выбор по меньшей мере одной области-мишени в указанном белке на основании биоинформационных данных и/или известных данных о биологической функции указанного белка и идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в указанной по меньшей мере одной области-мишени.
Настоящее изобретение относится к способам обнаружения и идентификации аминокислотных последовательностей в белках, причем указанные аминокислотные последовательности являются значительно экспонированными и соответствующими с функциональной точки зрения, по меньшей мере, данные последовательности являются значительно экспонированными. Таким образом, данные аминокислотные последовательности, которые авторы настоящего изобретения называют «горячими точками», можно применять в качестве антигенных эпитопов, направляющих нацеливание, обнаружение и разработку антител. Более того, данные аминокислотные последовательности можно классифицировать в зависимости от их появления после протеолитического расщепления и в зависимости от функциональной значимости на основании уже известных биоинформационных данных или данных функционального/фармакологического исследования. Таким образом, из перечня нескольких аминокислотных последовательностей, полученных в результате протеолитического расщепления, можно выбрать наиболее подходящие аминокислотные последовательности (на основании функциональных и структурных данных) для обнаружения и разработки антигенного эпитопа. Протеолитическое расщепление проводят при лимитирующих условиях, т.е. активность протеазы или нескольких протеаз является очень низкой, в результате чего лишь один или несколько экспонированных на поверхности пептидов отщепляются от белка-мишени в данный момент времени. Таким образом, протеазы используют в качестве зондов для определения возможности применения антитела, связывающегося с белком-мишенью, в качестве лекарственного препарата.
Согласно варианту реализации настоящего изобретения антитела являются фармакологически активными. Согласно другому варианту реализации настоящего изобретения антитела являются фармакологически активными и разработанными для терапевтического применения. Более конкретно, такие способы включают применение инструментов протеомики для выявления эпитопов горячих точек белков-мишеней.
Согласно аспекту настоящего изобретения белок расщепляют, деконструируют (обеспечивают его разборку) и/или усекают под действием протеазы, и все значительно экспонированные аминокислотные последовательности используют для создания антигенного эпитопа, и антитела, разработанные на основе указанных антигенных эпитопов, изучают в отношении биологической активности, эффективности, фармакологического профилирования и других тестов, которые являются общепринятыми при обнаружении антител, используемых в фармацевтической промышленности.
Согласно аспекту настоящего изобретения белок расщепляют, деконструируют и/или усекают под действием протеазы и параллельно исследуют в функциональном анализе расщепленного, деконструированного и/или усеченного белка для определения функционально важных областей белка. Соответствующий белок иногда называют в настоящей заявке белком-мишенью.
Согласно варианту реализации настоящего изобретения расщепление, деконструирование и/или усечение белка-мишени проводят параллельно с функциональным анализом для определения функционально важных областей белка-мишени для направления селекции эпитопов с целью создания антитела.
Согласно варианту реализации настоящего изобретения расщепление, деконструирование и/или усечение и функциональный анализ расщепленного, деконструированного и/или усеченного белка и нативного белка-мишени объединяют с другими биоинформационными данными и другими известными фактами о функции белка для определения функционально важных областей белка-мишени для направления селекции эпитопов с целью создания антитела.
Согласно варианту реализации настоящего изобретения для расщепления, деконструирования и/или усечения белка-мишени можно использовать одну протеазу. Согласно другому варианту реализации настоящего изобретения для расщепления, деконструирования и/или усечения белка-мишени можно использовать несколько протеаз, последовательно по одной в данный момент времени или параллельно. Примерами таких протеаз являются, не ограничиваясь указанным, протеиназа Arg-C, эндопептидаза Asp-N, клострипаин, глутамилэндопептидаза, Lys-C, Lys-N, трипсин, химотрипсин, протеиназа K и термолизин. Область, которую легко расщепляют несколько протеаз, должна располагаться в экспонированной области белка, и область, которая расщепляется исключительно одной протеазой, вероятно, располагается в более скрытой области. В качестве альтернативы, протеаза обладает уникальной специфичностью расщепления или/и физико-химическими свойствами или/и структурными свойствами, в результате чего может идентифицировать экспонированные на поверхности пептиды на белке-мишени, что не свойственно другим протеазам. Таким образом, применение нескольких протеаз является предпочтительным, и каждая отличная протеаза может привести к получению комплементарной или уникальной информации о пригодности экспонированных на поверхности пептидов в качестве антигенных эпитопов.
Варианты реализации настоящего изобретения делают возможной новую методологию/технологию для быстрой и точной разработки фармакологически активных антител, которые можно использовать для фармакологических исследований, например, которые можно использовать в качестве инструмента для обнаружения биологических соединений, например, в анализах на клетках или in vitro. Более важно то, что указанные антитела можно использовать для лечения медицинского состояния у людей и животных. Варианты реализации настоящего изобретения можно применять в отношении всех белков, растворимых или мембраносвязанных, внеклеточных или внутриклеточных. Более того, варианты реализации настоящего изобретения можно использовать для получения нового фундаментального понимания функции белка.
В настоящем изобретении также предложено антитело, созданное способом согласно настоящему изобретению.
В настоящем изобретении также предложен антигенный эпитоп, идентифицированный способом согласно настоящему изобретению.
В настоящем изобретении также предложено антитело против антигенного эпитопа согласно настоящему изобретению.
Другие свойства и преимущества настоящего изобретения будут очевидны из следующего подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Варианты реализации настоящего изобретения вместе с дополнительными целями и преимуществами указанного изобретения станут более понятными посредством ссылки на следующее описание, которое следует рассматривать вместе с прилагаемыми чертежами, на которых:
Фигура 1
Пептиды, обнаруженные в TRPV1 (transient receptor potential vanilloid 1, ваниллоидном ионном канале типа 1 с транзиторным рецепторным потенциалом) после ограниченного протеолиза под действием 5 мкг/мл трипсина при комнатной температуре, n=6. А: Расположение обнаруженных пептидов показано на 3D-модели TRPV1. Пептиды были обнаружены через 0,5 мин. (пурпурный цвет), 5 мин. (оранжевый цвет) и 15 мин. (синий цвет) В: Расположение обнаруженных пептидов показано на схематическом изображении TRPV1. Пептиды были обнаружены через 0,5 мин. (пурпурный цвет), 5 мин. (оранжевый цвет) и 15 мин. (синий цвет). С: Столбчатый график обнаруженных пептидов, полученных в результате расщепления TRPV1 после ограниченного протеолиза под действием 5 мкг/мл трипсина, с указанием, в какие временные точки данные пептиды были подтверждены.
Фигура 2
Пептиды, полученные в результате расщепления TRPV1 через 5 мин. воздействия 5 мкг/мл, 20 мкг/мл или 40 мкг/мл трипсина (Тр.), и изменение ответа тока после удаления трипсина. А-С: Расположение расщепленных пептидов TRPV1, демонстрирующее пептиды, расщепленные в проточной ячейке (голубой цвет), и пептиды, расщепленные в проточной ячейке с последующим полным расщеплением в течение ночи (желтый цвет). D: Иллюстративные кривые результатов анализа TRPV1 методом «наружная сторона внутри» при активации 1 мкМ капсайцином (Кап.) с последующим воздействием в течение 5 мин. буфером или трипсином и дополнительной активацией капсайцином. Сверху вниз: 5 мин. воздействия буфером, 5 мкг/мл, 20 мкг/мл и 40 мкг/мл трипсина, соответственно. Кривые фильтровали цифровым способом при 100 Гц исключительно для лучшей визуализации фигуры.
Фигура 3
Результаты анализа функции TRPV1 методом электрофизиологического пэтч-клампа (фиксации потенциала), демонстрирующие интеграл времени кривой тока для второй активации капсайцином, рассчитанный в виде процента интеграла для первой активации капсайцином после обработки буфером, n=11, или антителом, n=6. Данные представлены в виде среднего значения ± С.О.С. (стандартная ошибка среднего).
Фигура 4
Расположение антигенной детерминанты (красный цвет) для OTV1, пептида аа96-117, визуализированного на модели поверхности hTRPV1 (TRPV1 человека). А: Боковая проекция TRPV1, на которой каждый мономер окрашен в синий или пурпурный цвет. В: TRPV1, вид сверху, на котором каждый мономер окрашен в синий или пурпурный цвет.
Фигура 5
Расположение антигенной детерминанты (красный цвет) для OTV2, пептида аа785-799, визуализированного на модели поверхности hTRPV1. А: Боковая проекция TRPV1, на которой два мономера были опущены с целью лучшей визуализации. В: TRPV1, вид снизу, на котором каждый мономер окрашен в синий или пурпурный цвет.
Фигура 6
Локализация OTV1 (слева) и OTV2 (справа) в фиксированных клетках с экспрессией (А) и без экспрессии (В) TRPV1. OTV1 и OTV2 визуализировали с применением вторичного антитела козы против иммуноглобулинов кролика Alexa 488. Значения интенсивности вдоль линейного сегмента (черный цвет), пересекающего ячейку, приведены под каждым изображением. В случае OTV1 и OTV2 использовали различные настройки лазера, поэтому не следует проводить сравнения между антителами.
Фигура 7
Результаты анализа функции TRPV1 методом электрофизиологического пэтч-клампа после обработки антителом. А: Интеграл времени кривой тока для второй активации капсайцином, рассчитанный в виде процента интеграла для первой активации капсайцином после обработки буфером (n=11) или OTV1 (n=6). В: Интеграл времени кривой тока для второй активации капсайцином в присутствии кальмодулина (СаМ) и OTV2, рассчитанный в виде процента интеграла для первой активации капсайцином, после обработки исключительно кальмодулином (n=11) или кальмодулином и OTV2. Обработка OTV2 разделена на измерения в течение 15 минут после кратковременной обработки ультразвуком (n=4) и измерения в течение 30 минут после кратковременной обработки ультразвуком (n=7). Данные представлены в виде среднего значения ± С.О.С.
Фигура 8
А: Опосредованное TRPV1 поглощение YO-PRO после электропорации OTV1 в ФБР (фосфатном буферном растворе), не содержащем кальция. Верхний чертеж: Интенсивность флуоресценции в случае OTV1 (n=11) и контроля (n=11). Нижний чертеж: Соответствующая степень интенсивности флуоресценции в случае OTV1 и контроля. В: Опосредованное TRPV1 поглощение YO-PRO после электропорации OTV2 в присутствии 50 мкМ Са2+. Верхний чертеж: Интенсивность флуоресценции в случае OTV2 (n=9) и контроля (n=7). Нижний чертеж: Соответствующая степень интенсивности флуоресценции в случае OTV2 (зеленый цвет) и контроля (красный цвет). Данные представлены в виде среднего значения ± С.О.С.
Фигура 9
Валидация интернализации антител посредством электропорации с применением флуоресценции. Клетки подвергали электропорации, фиксировали, пермебеализовали и инкубировали с вторичным антителом козы против иммуноглобулинов кролика Alexa 488. Интенсивности флуоресценции измеряли методом конфокальной микроскопии. Интенсивности сравнивали между клетками, подвергавшимися и не подвергавшимися электропорации, после воздействия OTV1 или OTV2, а также клетками, на которые воздействовали исключительно вторичным антителом. В случае OTV1 и OTV2 использовали различные настройки лазера, поэтому не следует проводить сравнения значений интенсивности. Данные представлены в виде среднего значения ± С.О.С.
Фигура 10
Пептиды, обнаруженные в TRPV1 после ограниченного протеолиза трипсином. Расположение обнаруженных пептидов показано на 3D-модели TRPV1. Детали эксперимента приведены в примере 3. Пептиды, отщепленные первыми, показаны черным цветом. Пептиды, отщепленные позже, показаны серым цветом.
Фигура 11
Пептиды, обнаруженные в TRPV1 после ограниченного протеолиза Asp-N. Расположение обнаруженных пептидов показано на 3D-модели TRPV1. Детали эксперимента приведены в примере 3. Пептиды, отщепленные первыми, показаны черным цветом. Пептиды, отщепленные позже, показаны серым цветом.
Фигура 12
Пептиды, обнаруженные в TRPV1 после ограниченного протеолиза химотрипсином. Расположение обнаруженных пептидов показано на 3D-модели TRPV1. Детали эксперимента приведены в примере 3. Пептиды, отщепленные первыми, показаны черным цветом. Пептиды, отщепленные позже, показаны серым цветом.
Фигура 13
Пептиды, обнаруженные в TRPV1 после ограниченного протеолиза пепсином. Расположение обнаруженных пептидов показано на 3D-модели TRPV1. Детали эксперимента приведены в примере 3. Пептиды, отщепленные первыми, показаны черным цветом. Пептиды, отщепленные позже, показаны серым цветом.
Фигура 14
Пептиды, обнаруженные в TRPV1 после ограниченного протеолиза протеиназой K. Расположение обнаруженных пептидов показано на 3D-модели TRPV1. Детали эксперимента приведены в примере 3. Пептиды, отщепленные первыми, показаны черным цветом. Пептиды, отщепленные позже, показаны серым цветом.
Фигура 15
На данной фигуре представлены подобные внешние размеры протеазы и Fab-области антитела. Верхний чертеж: часть кристаллической структуры Fab НММ5, участок, содержащий паратоп, отмечен красным цветом, К (PDB: 5I8O). Нижний чертеж: кристаллическая структура бычьего трипсина, участок, содержащий активный карман, отмечен красным цветом, К (PDB:1MCT). Масштабная шкала=10 
Фигура 16
На данной фигуре представлен иллюстративный рабочий процесс для идентификации доступных для протеазы/разрезаемых протеазой, но не высвобождающихся эпитопов на основании моделирования in silico, гомологичного связывания Fab-протеаза и мультижидкостного расщепления несколькими протеазами/обнаружения методом МС-МС. (a) Расщепление in silico сочетали с моделированием белков по гомологии и докингом Fab-протеаза для прогнозирования сайтов разрезания протеазой на нативной структуре белка. (b) Протеолипосомы, содержащие нативный белок, иммобилизовали и расщепляли набором протеаз с применением микрожидкостной платформы, и полученные в результате пептиды идентифицировали методом ЖХ-МС/МС. Это позволило провести картирование доступных для протеазы сайтов разрезания. Пептиды протеазы 1 отмечены красным цветом (К), пептиды протеазы 2 отмечены синим цветом (С), пептиды протеазы 3 отмечены зеленым цветом (3) (с) Определенные экспериментальным путем сайты разрезания сравнивали с предсказанными in silico сайтами для определения неожиданных пропущенных расщеплений, (d) Для исследования пропущенных сайтов разрезания нарабатывали антитела против последовательностей длиной 7-8 аминокислот, содержащих пропущенные сайты разрезания, с применением подхода сдвига рамки с целью охвата подходящей области (например, от -20 до +20 аминокислот, окружающих сайт разрезания). Проводили скрининг антител для обнаружения антител, которые связывались наилучшим образом, (е) Антитела, которые связывались наилучшим образом, использовали для исследования нативного и частично расщепленного белка в отношении структурной информации. Например, если антитело связывается с пропущенным сайтом разрезания на нативном белке, это может свидетельствовать о том, что протеаза связывается, но по какой-либо причине не разрезает белок. Антитела можно также использовать для исследования в отношении разрывов пептидов, усечений или утраты локальной структуры в доменах, например, под действием протеазы. Также возможно обнаружение структурных реаранжировок, вызванных лиганд- или белок-белковым взаимодействием.
Фигура 17
На данной фигуре представлена иллюстративная платформа расщепления несколькими протеазами для идентификации эпитопов-кандидатов. (а) Протеолипосомы, содержащие мишень, выделяли из клеток и подвергали ограниченному протеолизу с помощью нескольких протеаз параллельно. Применяли различные параметры реакции (длительность, концентрации фермента). Расщепленные пептиды из каждой реакции элюировали и идентифицировали с применением ЖХ-МС/МС. (b) Доступность поверхности классифицировали в зависимости от параметра реакции, например, категория, в которой пептиды расщепляются с применением наиболее медленной кинетики, расположена в экспонированных на поверхности областях, и вследствие этого таким пептидам присваивали высокий класс. (с) Пептиды дополнительно классифицировали в зависимости от функциональной значимости с применением биоинформационных и экспериментальных данных в зависимости от того, эффект какого типа является желательным (агонизм, антагонизм или простое связывание). Эпитопы, подходящие для разработки антитела, характеризуются хорошей доступностью и соответствующей функцией. (d) Эпитопы оптимизировали и подтверждали in silico, например, посредством имитаций докинга с Fab-фрагментами с эпитопом. Наконец, эпитопы применяли в качестве иммуногенов для получения антитела у животных.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Вышеизложенные и другие аспекты настоящего изобретения теперь будут описаны более подробно в отношении описания и методологий, представленных в настоящей заявке. Следует понимать, что настоящее изобретение может быть реализовано в различных формах, и данное изобретение не следует истолковывать как ограниченное вариантами реализации, изложенными в настоящей заявке. Напротив, данные варианты реализации предложены для того, чтобы данное описание изобретения являлось обстоятельным и полным и полностью отражало объем настоящего изобретения для специалистов в данной области техники.
Если не определено обратное, все технические и научные термины, используемые в настоящей заявке, имеют то же значение, которое обычно понимается средним специалистом в области техники, к которой относится настоящее изобретение. В настоящем описании формы единственного числа также включают множественное число, если контекст однозначно не диктует обратное. Несмотря на то, что при реализации на практике или тестировании настоящего изобретения можно использовать способы и материалы, подобные или эквивалентные таковым, описанным в настоящей заявке, подходящие способы и материалы описаны ниже. Все публикации, заявки на патенты, патенты и другие источники, упомянутые в настоящей заявке, включены в настоящую заявку посредством ссылки. Источники, ссылки на которые содержатся в настоящей заявке, не признаются предшествующим уровнем техники в отношении заявленного изобретения. В случае конфликта настоящее описание, включая определения, будет являться определяющим. Кроме того, материалы, способы и примеры являются исключительно иллюстративными и не подразумеваются как ограничивающие.
Терминология, используемая в описании настоящего изобретения в настоящей заявке, предназначена исключительно для описания конкретных вариантов реализации и не предназначена для ограничения настоящего изобретения. В описании вариантов реализации настоящего изобретения формы единственного числа предназначены для включения также форм множественного числа, если контекст однозначно не указывает обратное. Также в настоящей заявке термин «и/или» означает и охватывает любые и все возможные комбинации одного или более связанных перечисленных элементов. Более того, термин «приблизительно» в настоящей заявке при использовании в отношении измеряемого значения, такого как количество соединения, доза, время, температура и т.п., предназначен для включения вариаций на 20%, 10%, 5%, 1%, 0,5% или даже 0,1% от указанного количества. Когда применяется диапазон (например, диапазон от х до у), это означает, что измеряемое значение представляет собой диапазон от приблизительно х до приблизительно у или любой диапазон в пределах указанного диапазона, такой как от приблизительно х1 до приблизительно у1 и т.д. Следует также понимать, что термины «содержит», «включает» и/или «содержащий», «включающий» в настоящем описании обозначают наличие указанных свойств, целых чисел, этапов, операций, элементов и/или компонентов, но не исключают наличия или добавления одного или более других свойств, целых чисел, этапов, операций, элементов, компонентов и/или их групп. Если не определено обратное, все термины, включая технические и научные термины, используемые в настоящем описании, имеют то же значение, которое обычно понимается средним специалистом в области техники, к которой относится настоящее изобретение.
Согласно одному аспекту в настоящем изобретении предложен способ создания антитела против белка, причем указанный способ включает:
(i) идентификацию антигенного эпитопа в указанном белке посредством воздействия на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от белка под действием указанной протеазы, и создание антигенного эпитопа на основе указанного экспонированного на поверхности пептида; и
(ii) получение антитела против антигенного эпитопа.
Согласно другому аспекту в настоящем изобретении предложен способ создания антитела против белка, причем указанный способ включает:
(i) воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от белка под действием указанной протеазы; и
(ii) идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в области белка, которая приводит к утрате или существенному изменению биологической функции белка, когда пептид отщепляют или удаляют от белка в течение ограниченного или частичного протеолиза; или
выбор по меньшей мере одной области-мишени в белке на основании биоинформационных данных и/или известных данных о биологической функции белка и идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в указанной по меньшей мере одной области-мишени; и
(iii) получение антитела против антигенного эпитопа.
В качестве альтернативы, в настоящем изобретении предложен способ создания антитела против белка, причем указанный способ включает:
(i) воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от белка под действием указанной протеазы; и
(ii) идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности пептида, который отщепляется, содержащего аминокислотную последовательность, которая обладает или которая согласно прогнозу обладает функциональной важностью в отношении указанного белка, и создание антигенного эпитопа на основе указанного экспонированного на поверхности пептида; и
(iii) получение антитела против указанного антигенного эпитопа.
Согласно другому аспекту в настоящем изобретении предложен способ создания антитела против белка, причем указанный способ включает:
(i) идентификацию экспонированного на поверхности пептида в указанном белке посредством воздействия на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного пептида, который отщепляется от белка под действием указанной протеазы; и
(ii) конструирование линейного или конформационного антигенного эпитопа на основе по меньшей мере одного экспонированного на поверхности пептида; и
(iii) получение антитела против антигенного эпитопа.
Согласно другому аспекту в настоящем изобретении предложен способ создания антитела против белка, причем указанный способ включает:
(i) идентификацию экспонированного на поверхности пептида в указанном белке посредством воздействия на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от белка под действием указанной протеазы; и
(ii) идентификацию экспонированного на поверхности пептида, который при отщеплении или удалении от белка в течение ограниченного или частичного протеолиза приводит к утрате или существенному изменению биологической функции указанного белка; или
выбор по меньшей мере одного из идентифицированных экспонированных на поверхности пептидов согласно (i) на основании соотнесения указанных экспонированных на поверхности пептидов с биоинформационными и/или известными данными о биологической функции белка; и
(iii) конструирование линейного или конформационного антигенного эпитопа на основе по меньшей мере одного экспонированного на поверхности пептида; и
(iv) получение антитела против антигенного эпитопа.
Согласно другому аспекту в настоящем изобретении предложен способ создания антитела против белка, причем указанный способ включает:
(i) идентификацию антигенного эпитопа в указанном белке посредством воздействия на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от белка под действием указанной протеазы; и
(ii) получение антитела против антигенного эпитопа.
Согласно другому аспекту способ создания антитела согласно настоящему изобретению может представлять собой, в качестве альтернативы, способ получения антитела, которое специфично связывается с белком. Иллюстративные и предпочтительные варианты реализации способов создания антитела, описанные в настоящей заявке, с соответствующими изменениями также применяют в отношении способов получения антитела, которое специфично связывается с белком.
Согласно другому аспекту в настоящем изобретении предложен способ идентификации антигенного эпитопа, причем указанный способ включает:
(i) воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от белка под действием указанной протеазы; и
(ii) идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в области белка, которая приводит к утрате или существенному изменению биологической функции белка, когда пептид отщепляют или удаляют от белка в течение ограниченного или частичного протеолиза; или
выбор по меньшей мере одной области-мишени в белке на основании биоинформационных данных и/или известных данных о биологической функции белка и идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в указанной по меньшей мере одной области-мишени.
Необязательно данный способ также включает этап получения антитела против указанного антигенного эпитопа.
В качестве альтернативы, в настоящем изобретении предложен способ идентификации антигенного эпитопа, причем указанный способ включает:
(i) воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от белка под действием указанной протеазы; и
(ii) идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности пептида, который отщепляется, содержащего аминокислотную последовательность, которая обладает или которая согласно прогнозу обладает функциональной важностью в отношении указанного белка, и создание антигенного эпитопа на основе указанного экспонированного на поверхности пептида.
Необязательно данный способ также включает этап получения антитела против указанного антигенного эпитопа.
Подробная информация относительно экспонированных на поверхности функционально активных эпитопов в белке может способствовать разработке эффективных антител и может уменьшить потребность в сложных процедурах скрининга посредством уменьшения количества антител-кандидатов. Возможным способом изучения топологии поверхности белка является ограничение активности протеазы для расщепления исключительно наиболее гибких и экспонированных на поверхности частей белка посредством осуществления ограниченного и контролируемого протеолиза. Идея заключается в замедлении кинетики активности протеазы настолько, чтобы пептиды отщеплялись по одному в течение определенного периода времени или не более чем по несколько в течение определенного периода времени. Затем отщепленные пептиды можно классифицировать на основании порядка их появления после воздействия протеазы. Пептиды, которые отщепляются от белка первыми, являются значительно экспонированными белком и являются легкодоступными для протеазы. Авторы настоящего изобретения отнесли данные пептиды к наивысшему классу и выдвинули гипотезу, что пептиды, легко отщепляемые протеазой, также легко распознаются антителом. Пептиды, которые отщепляются позже, авторы настоящего изобретения отнесли к низшему классу, и всем пептидам между указанными пептидами присваивали показатели от высокого до низкого в зависимости от их появления во времени после воздействия протеазы. Таким образом, способ основан на аминокислотной последовательности, и, поскольку авторам настоящего изобретения известна последовательность, конкретно известно, где именно антитело будет связываться с указанным белком-мишенью. На втором этапе, поскольку авторам настоящего изобретения известны конкретные аминокислотные последовательности, которые являются мишенями в белке, можно исследовать функциональную значимость указанной аминокислотной последовательности на основании опубликованных данных или других известных биоинформационных данных либо данных фармакологических исследований усеченных белков. Если аминокислотная последовательность совпадает или является близкой либо перекрывается с известной аминокислотной последовательностью, имеющей функциональную важность, например, сайтом связывания, сайтом модулирования, сайтом, важным со структурной точки зрения, областью канала и т.д., тогда указанному пептиду присваивают высокий показатель, и данный пептид считают хорошим кандидатом на роль антигенного эпитопа и для последующей разработки антитела. Такого результата можно достичь, в частности, посредством контроля активности протеазы с использованием, например, низких температур, низких концентраций и/или короткого времени расщепления. Когда ограниченный протеолиз проводили в отношении белков с известной структурой, главным образом, были распознаны три структурные детерминанты, которые оказывают влияние на то, где возникает протеолитическая активность. Данные детерминанты включают гибкость, экспонирование на поверхности и количество локальных взаимодействий. Для того чтобы цепь пептида поступила в активный сайт протеазы, требуется гибкость и способность белка к локальному развертыванию. Экспонирование на поверхности, более вероятно, обеспечивает сайт расщепления для протеолиза, поскольку области на поверхности имеют тенденцию более легко разворачиваться, а также создают меньшее количество стерических препятствий. Количество локальных взаимодействий применительно к водородным связям и дисульфидным мостикам также является важным. Меньшее количество локальных взаимодействий способствует протеолизу. Все три данные структурные детерминанты обычно соотносятся в белке. Вследствие этого в ходе ограниченного протеолиза, главным образом, отщепляются экспонированные на поверхности области при условии, что цепь белка может локально разворачиваться. Данный факт был использован в качестве способа определения экспонированных на поверхности областей в белках, подробная структура которых неизвестна.
Технология иммобилизации белка на основе липидов (lipid-based protein immobilization, LPI) делает возможной осуществление гибкой химии на мембранных белках. Посредством получения протеолипосом из клеток и их иммобилизации в проточной ячейке создают неподвижную фазу мембранных белков, которую можно подвергнуть взаимодействию с несколькими сериями растворов и различными типами химических модуляций, например, с помощью ферментов. Был разработан протокол поэтапного триптического расщепления для протеомной характеризации, в котором пептиды, полученные в результате ступенчатого ферментативного расщепления протеолипосом, анализируют методом жидкостной хроматографии стандемной масс-спектрометрией (ЖХ-МС/МС) [1-3].
Согласно некоторым вариантам реализации способов согласно настоящему изобретению белок представляет собой белок (например, мембранный белок), который присутствует (например, в липидном двойном слое) в протеолипосоме (например, в протеолипосоме, полученной из клеток, например, из клеток человека). Соответственно, согласно некоторым вариантам реализации настоящего изобретения ограниченный протеолиз проводят в отношении протеолипосом. Протеолипосомы представляют собой липидные везикулы, содержащие белки. Протеолипосомы могут быть восстановлены из очищенных мембранных белков и липидов или могут быть получены напрямую из мембраны клетки (например, посредством пузырения) либо посредством лизиса клетки. Предпочтительно, протеолипосомы получают (готовят) из клеточных мембран лизированных клеток. Протеолипосомы можно получить из любого типа клеток, представляющих интерес. Подходящий тип клеток представляет собой клетки яичников китайского хомячка (Chinese hamster ovary, СНО).
Способы получения протеолипосом известны в данной области техники, и можно использовать любой из таких способов (например, способ, описанный в публикации Jansson et al. Anal. Chem., 2012, 84: 5582-5588). Иллюстративный и предпочтительный способ получения протеолипосом описан в примерах в настоящей заявке. Как правило, предпочтительными являются протеолипосомы диаметром от приблизительно 50 нм до приблизительно 150 нм.
Использование протеолипосом, полученных (приготовленных) из клеточных мембран лизированных клеток, является предпочтительным, поскольку протеолипосомы, полученные таким образом (например, с применением способа, указанного в примерах), могут представлять внутриклеточные части (или домены) мембранных белков на внешней стороне протеолипосомы, что делает доступными для протеолитического расщепления (и, следовательно, для идентификации антигенного эпитопа) некоторые части белка, которые в противном случае будут недоступны для протеазы.
Согласно одному аспекту авторы настоящего изобретения разработали технологию адресных антител посредством применения микрожидкостной платформы LPI [1, 4] для создания потенциальных эпитопов-кандидатов. Данная методология скорее основана на механизме, чем на скрининге. Вкратце, технология LPI делает возможной осуществление гибкой химии, такой как ограниченный протеолиз, на мембранных белках. Посредством получения протеолипосом из клеток и их иммобилизации в проточной ячейке создают неподвижную фазу мембранных белков. Был разработан протокол поэтапного расщепления для протеомной характеризации, в котором пептиды, полученные в результате ступенчатого ферментативного расщепления протеолипосом, анализируют методом ЖХ-МС/МС. Такие пептиды, созданные в процессе кинетически контролируемого расщепления в проточной ячейке LPI, позволяют выявить в белке-мишени экспонированные и доступные области, области, которые потенциально могут быть доступными для связывания с антителом. Затем данные потенциальные эпитопы соотносят с известными функциональными данными с целью обнаружения эпитопов, которые позволяют получить антитела с одинаково превосходными характеристиками связывания и биологической эффективностью. Наконец, выбранные эпитопы/пептиды можно использовать для иммунизации животного-хозяина с целью получения антител. Следует упомянуть, что в данной области техники известны другие способы и методики для осуществления ограниченного протеолитического расщепления, которые также можно использовать, например, в случае растворимых белков.
Согласно некоторым вариантам реализации настоящего изобретения белок (например, мембранный белок) иммобилизуют (например, на твердой подложке) перед ограниченным или частичным протеолизом для получения неподвижной фазы белка. Таким образом, согласно некоторым вариантам реализации настоящего изобретения белок является связанным с поверхностью.
Согласно некоторым вариантам реализации настоящего изобретения белок (например, мембранный белок) присутствует в (или присутствует на) протеолипосоме (например, протеолипосоме, полученной из клеток), и указанную протеолипосому иммобилизуют (например, на твердой подложке) перед ограниченным или частичным протеолизом для получения неподвижной фазы белка.
Согласно некоторым вариантам реализации способов согласно настоящему изобретению белок представляет собой мембранный белок, который присутствует в протеолипосоме, полученной из клеток, причем указанную протеолипосому иммобилизуют в проточной ячейке для получения неподвижнной фазы мембранных белков. Подходящие проточные ячейки известны в данной области техники, например, проточная ячейка, описанная в публикации Jansson et al. (Anal. Chem., 2012, 84: 5582-5588).
Согласно некоторым вариантам реализации настоящего изобретения белок (например, мембранный белок) присутствует в (или присутствует на) протеолипосоме (например, протеолипосоме, полученной из клеток), и указанные протеолипосомы находятся в суспензии (например, суспендированы в растворе).
Согласно некоторым вариантам реализации настоящего изобретения указанный белок находится в (или присутствует на) липидной везикуле, содержащей белок, которая является связанной с поверхностью или находится в суспензии (например, суспендирована в растворе).
Согласно некоторым вариантам реализации настоящего изобретения указанный белок может представлять собой часть любой соответствующей структуры либо может быть представлен на любой соответствующей структуре, в результате чего сохраняется функциональная или природная конформация белка, например, белок может представлять собой часть липидного бислоя или мембраны либо может быть представлен на каркасе или частице.
Согласно некоторым вариантам реализации настоящего изобретения указанный белок находится в (или представлен на) частице, такой как наночастица или любая другая коллоидная частица, которая является связанной с поверхностью или находится в суспензии (например, суспендирована в растворе).
Согласно некоторым вариантам реализации настоящего изобретения указанный белок находится в (или представлен на) каркасе или другой химической структуре, такой как каркасные соединения, которая является связанной с поверхностью или находится в суспензии (например, суспендирована в растворе).
Согласно некоторым вариантам реализации настоящего изобретения указанный белок находится в (или представлен на) интактной клетке (биологической клетке, например, клетке человека), которая является связанной с поверхностью или находится в суспензии (например, суспендирована в растворе).
«В» в контексте белков в протеолипосомах, везикулах, содержащих белок, или интактных клетках включает белки, которые простираются до внешней поверхности протеолипосомы, липидной везикулы, содержащей белок, или клетки (и которые, таким образом, экспонированы на указанной внешней поверхности).
Согласно некоторым вариантам реализации настоящего изобретения указанный белок находится в растворе. Раствор может представлять собой раствор очищенного белка или может содержать смесь белков.
Согласно некоторым вариантам реализации настоящего изобретения клетки (например, клетки СНО) сверхэкспрессируют белок, например, посредством индуцибельной (например, индуцибельной тетрациклином) системы экспрессии. Согласно некоторым вариантам реализации настоящего изобретения используют протеолипосомы, полученные из таких клеток.
Авторы настоящего изобретения изучали пептиды, полученные в результате ограниченного протеолиза ваниллоидного ионного канала типа 1 с транзиторным рецепторным потенциалом (transient receptor potential vanilloid 1, TRPV1), с целью обнаружения потенциальных эпитопов для разработки биологически активных антител, которые обладают способностью модулировать функции данного ионного канала. TRPV1 подвергали ограниченному протеолизу двумя различными протеазами, и отщепленные пептиды соотносили с функциональными данными. Авторы настоящего изобретения, используя данную информацию, разработали два поликлональных антитела, OTV1 и OTV2, действующие на внутриклеточной стороне ионного канала TRPV1 человека (hTRPV1, human TRPV1). Оба антитела являются фармакологически активными, и области-мишени эпитопа указанных антител были выбраны на основании простоты отщепления (или экспонирования на поверхности (пептиды высокого класса после ограниченного протеолиза)), а также функциональной важности. OTV1 демонстрирует мощное ингибирующее действие в отношении белка при стимуляции агонистом капсайцином. OTV2 препятствует кальмодулин/Са2+-зависимой десенсибилизации TRPV1, представляющей собой процесс, который запускается притоком кальция через TRPV1. Эффективность OTV1 и OTV2 исследовали методом пэтч-кламп «наружная сторона внутри», в ходе которого внутриклеточную сторону TRPV1 можно экспонировать в раствор антитела, а также посредством анализа поглощения опосредованной TRPV1 флуоресценции после того, как антитела электропорировали внутрь живых клеток.
Способы, в которых используют проточную ячейку LPI в сочетании с микрожидкостной проточной ячейкой открытого объема для быстрой смены раствора, подходящие для экспериментов с применением метода пэтч-кламп, были описаны ранее. Преимущество данного подхода заключается в том, что мембраны клеток можно вывернуть наизнанку и можно непосредственно исследовать внутриклеточные домены ионного канала. С помощью данного подхода можно получить согласованные структурные и функциональные данные, используя ограниченный и контролируемый протеолиз. TRPV1 представляет собой катионный канал, который экспрессируется в ноцицептивных первичных сенсорных нейронах. Подробная кристаллическая структура полноразмерного белка отсутствует, но для TRPV1 крысы был успешно кристаллизован домен анкириновых повторов (ankyrin repeat domain, ARD) N-конца. Пептиды, отщепленные в течение коротких периодов времени при осуществлении ограниченного протеолиза TRPV1, сравнивали с известными функционально активными областями. Треть обнаруженных пептидов содержала остатки, которые, как было предположено, являются функционально важными.
Скрининг топологии поверхности TRPV1, как описано в исследованиях в данной области техники, осуществляли посредством иммобилизации протеолипосом, содержащих TRPV1, в проточной ячейке и посредством последующего воздействия на протеолипосомы ограниченного протеолиза трипсином [1, 4]. Активность трипсина контролировали посредством применения различных времен расщепления при комнатной температуре. Использовали поэтапный протокол с нарастающими временами инкубации, и отщепленные пептиды обнаруживали методом ЖХ-МС/МС. Увеличивающееся количество пептидов было обнаружено в зависимости от времени, что позволило выявить области белка, которые были доступны и легко расщеплялись, а также более устойчивые области. Данные результаты проиллюстрированы на фигуре 1. Несколько областей, которые были обнаружены методом ЖХ-МС/МС в качестве отщепленных пептидов после ограниченного протеолиза TRPV1 в проточной ячейке LPI, согласовывались с известными сайтами взаимодействия с кальмодулином, АТФ и PIP2.
Авторы настоящего изобретения также исследовали функциональность TRPV1 после удаления различных структурных сегментов посредством расщепления трипсином [4]. Активность ионного канала TRPV1 исследовали с помощью анализа методом пэтч-кламп «наружная сторона внутри» и расщеплений в проточной ячейке, после чего следовал протеомный анализ, в котором оценивали структурные эффекты химического усечения. Авторы настоящего изобретения использовали конфигурацию анализа пэтч-кламп «наружная сторона внутри», которая позволяет подвергать воздействию трипсина внутриклеточную часть TRPV1, и определяли уменьшение ответа тока при увеличении концентрации трипсина (фигура 2).
Авторы настоящего изобретения продемонстрировали, что ионный канал TRPV1 можно подвергнуть ограниченному и контролируемому протеолизу трипсином в двух различных микрожидкостных проточных ячейках в идентичных условиях эксперимента. В одном случае анализ методом пэтч-кламп проводили с целью фармакологических исследований, которые позволили получить информацию о динамике функции канала в микрожидкостном устройстве открытого объема. Данный дизайн позволяет с помощью пипетки для пэтч-кламп и фрагмента клетки получить доступ к перфузионным каналам. В другом случае использовали эквивалентную проточную ячейку закрытого объема для отщепления пептидов от ионного канала, не вызывая разведения образца. Отщепленные пептиды идентифицировали методом ЖХ-МС/МС. Затем сравнивали данные, полученные в двух экспериментах, и оценивали отношение структура-функция. Используя данный методологический подход, авторы настоящего изобретения идентифицировали в высокой степени гибкие области TRPV1, а также ключевые области, которые влияют на функциональные свойства канала в ходе активации последнего агонистом капсайцином.
Данный тип методологии можно также использовать для других белков (т.е. белков, отличных от TRPV1).
Аминокислотная последовательность hTRPV1 представлена ниже (SEQ ID NO: 1).

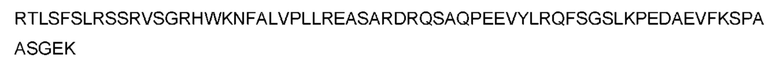
Вследствие этого настоящее изобретение делает возможным проведение функциональных исследований специфичных эпитопов или оценку предполагаемых сайтов связывания новых антител для мембранного белка-мишени, находящегося в нативном липидном окружении.
Согласно настоящему изобретению антигенный эпитоп, как правило, основан на экспонированном на поверхности пептиде, который был отщеплен от белка в процессе ограниченного или частичного протеолиза. В качестве альтернативы, экспонированный на поверхности пептид, как правило, используют для получения антигенного эпитопа.
В этой связи антигенный эпитоп может содержать аминокислотную последовательность экспонированного на поверхности пептида или последовательность, по существу гомологичную указанной последовательности. Антигенный эпитоп может состоять из аминокислотной последовательности экспонированного на поверхности пептида или последовательности, по существу гомологичной указанной последовательности. Антигенный эпитоп может перекрываться с аминокислотной последовательностью экспонированного на поверхности пептида или последовательностью, по существу гомологичной указанной последовательности.
Аминокислотные последовательности, которые являются «по существу гомологичными» экспонированным на поверхности пептидам, включают последовательности, имеющие, или последовательности, содержащие последовательность, которая содержит 1, 2 или 3 замены аминокислот (предпочтительно, 1 или 2, более предпочтительно, 1) по сравнению с аминокислотной последовательностью данного экспонированного на поверхности пептида.
Аминокислотные последовательности, которые являются «по существу гомологичными» экспонированным на поверхности пептидам, включают последовательности, которые содержат по меньшей мере 5 или по меньшей мере 6 последовательных аминокислот экспонированных на поверхности пептидов либо которые состоят из указанных аминокислот (или которые содержат по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 15, по меньшей мере 20 или по меньшей мере 25 последовательных аминокислот экспонированного на поверхности пептида либо которые состоят из указанных аминокислот). Шесть аминокислот составляют типичную длину последовательности пептида/белка, которая распознается или связывается антителом.
Аминокислотные последовательности, которые являются «по существу гомологичными» экспонированным на поверхности пептидам, включают последовательности, имеющие, или последовательности, содержащие последовательность, которая характеризуется идентичностью последовательности по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 98% данной последовательности экспонированного на поверхности пептида. Предпочтительными являются идентичности последовательностей, составляющие по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 98%.
Антигенный эпитоп может содержать удлиненную версию экспонированного на поверхности пептида или удлиненную версию аминокислотной последовательности, по существу гомологичной экспонированному на поверхности пептиду (или может состоять из указанных последовательностей). Например, одна или более дополнительных аминокислот (например, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8 или по меньшей мере 9, по меньшей мере 10, по меньшей мере 15 или по меньшей мере 20 аминокислот) могут присутствовать на одном конце или на обоих концах последовательности экспонированного на поверхности пептида (или последовательности, по существу гомологичной указанной последовательности). Согласно некоторым вариантам реализации до 2, до 3, до 4, до 5, до 6, до 7, до 8, до 9, до 10, до 15 или до 20 аминокислот могут присутствовать на одном конце или на обоих концах последовательности экспонированного на поверхности пептида (или последовательности, по существу гомологичной указанной последовательности).
Антигенный эпитоп может содержать усеченную версию экспонированного на поверхности пептида или усеченную версию аминокислотной последовательности, по существу гомологичной экспонированному на поверхности пептиду (или может состоять из указанных последовательностей). Например, одна или более аминокислот (например, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8 или 9, по меньшей мере 10) могут отсутствовать с одного или обоих концов последовательности экспонированного на поверхности пептида (или последовательности, по существу гомологичной указанной последовательности). Согласно некоторым вариантам реализации настоящего изобретения до 2, до 3, до 4, до 5, до 6, до 7, до 8, до 9 или до 10, до 15 или до 20 аминокислот могут отсутствовать с одного или обоих концов последовательности экспонированного на поверхности пептида (или последовательности, по существу гомологичной указанной последовательности).
Антигенный эпитоп может представлять собой циклический пептид, например, по существу гомологичный одному или нескольким экспонированным на поверхности пептидам, причем экспонированные на поверхности пептиды расположены близко друг к другу в пространстве.
Антигенные эпитопы могут составлять по меньшей мере 5 или по меньшей мере 6, или по меньшей мере 7 аминокислот в длину, например, от 6 до 10, от 6 до 12, от 6 до 15, от 6 до 20, от 6 до 25, от 6 до 30, от 6 до 40, от 6 до 50, от 6 до 60 или от 6 до 75 аминокислот в длину. Антигенные эпитопы могут составлять, например, до 7, до 8, до 9, до 10, до 15, до 20, до 25 или до 30 аминокислот в длину. Антигенные эпитопы могут составлять, например, от 5 до 30, от 6 до 30, от 7 до 30, от 5 до 25, от 6 до 25 или от 7 до 25 аминокислот в длину. Антигенные эпитопы могут составлять, например, от 5 до 7, или от 5 до 8, или от 5 до 9 (например, от 7 до 9 аминокислот) в длину. Во избежание разночтений отметим, что более длинные белки или полипептиды, например, таковые длиной более 100 аминокислот, не считают эпитопами согласно настоящему изобретению.
Гомологию (например, идентичность последовательности) можно оценить любым подходящим способом. Однако пригодными для определения степени гомологии (например, идентичности) между последовательностями являются компьютерные программы, которые позволяют проводить множественные выравнивания последовательностей, например Clustal W (Thompson, Higgins, Gibson, Nucleic Acids Res., 22: 4673-4680, 1994). При необходимости, алгоритм Clustal W можно использовать вместе с матрицей замен BLOSUM 62 (Henikoff and Henikoff, Proc. Natl. Acad. Sci. USA, 89: 10915-10919, 1992), а также штрафом за открытие пропуска 10 и штрафом за удлинение пропуска 0,1, для получения соответствия наивысшего порядка между двумя последовательностями, причем, чтобы по меньшей мере 50% общей длины одной из последовательностей было вовлечено в выравнивание. Другие способы, которые можно использовать для выравнивания последовательностей, представляют собой способ выравнивания Нидлмана и Вунша (Needleman and Wunsch, J. Mol. Biol., 48: 443, 1970), пересмотренный Смитом и Вотерманом (Smith and Waterman, Adv. Appl. Math., 2: 482, 1981), для получения соответствия наивысшего порядка между двумя последовательностями и для определения количества идентичных аминокислот между двумя последовательностями. Другие способы расчета процента идентичности между двумя аминокислотными последовательностями, как правило, известны в данной области техники и включают, например, таковые, описанные в публикации Carillo and Lipton (Carillo and Lipton, SIAM J. Applied Math., 48: 1073, 1988), и таковые, описанные в руководстве Computational Molecular Biology, Lesk, e.d. Oxford University Press, New York, 1988, Biocomputing: Informatics and Genomics Projects.
Как правило, для таких расчетов будут использовать компьютерные программы. Пригодными для данной цели также являются программы, которые сравнивают и выравнивают пары последовательностей, такие как ALIGN (Myers and Miller, CABIOS, 4: 11-17, 1988), FASTA (Pearson and Lipman, Proc. Natl. Acad. Sci. USA, 85: 2444-2448, 1988; Pearson, Methods in Enzymology, 183: 63-98, 1990) и gapped BLAST (Altschul et al., Nucleic Acids Res., 25: 3389-3402, 1997), BLASTP, BLASTN или GCG (Devereux, Haeberli, Smithies, Nucleic Acids Res., 12: 387, 1984). Более того, сервер Dali Европейского института биоинформатики предлагает выравнивания на основании структуры последовательностей белка (Holm, Trends in Biochemical Sciences, 20: 478-480, 1995; Holm, J. Mol. Biol., 233: 123-38, 1993; Holm, Nucleic Acid Res., 26: 316-9, 1998).
Антигенные эпитопы согласно настоящему изобретению могут являться линейными эпитопами или конформационными эпитопами.
Согласно некоторым вариантам реализации настоящего изобретения антигенные эпитопы согласно настоящему изобретению могут являться циклизированными эпитопами.
Общепринятая методика, используемая для получения линейных антигенных эпитопов, применяемых для иммунизации, представляет собой ТФПС (твердофазный пептидный синтез) на основе Fmoc. В ТФПС небольшие пористые бусины обрабатывают функциональными линкерами, на которых могут быть построены цепи пептидов с использованием повторяющихся циклов промывки - сочетания - промывки. Затем синтезированный пептид освобождают от бусин с использованием химического отщепления. Для синтеза циклических пептидов в общепринятых способах используют циклизацию посредством образования дисульфидного мостика (причем мостик образуется между двумя цистеинами) или посредством образования мостика по типу «голова-хвост», причем мостик состоит из типичных пептидных связей. Циклические пептиды могут быть образованы на твердой подложке. Антитела против конформационных эпитопов обычно синтезируют с использованием целого белка или больших частей белка.
Ограниченный или частичный протеолиз включает протеолитическое расщепление белка, которое проходит не до конца. Таким образом, посредством ограниченного или частичного протеолиза данный белок может быть расщеплен только частично (или частично деконструирован или частично усечен). Ограниченный или частичный протеолиз можно рассматривать как неполный протеолиз. Если данный белок содержит определенное количество потенциальных точек расщепления данной протеазой (т.е. сайтов, распознаваемых данной протеазой для расщепления), при ограниченном или частичном протеолизе протеаза может расщеплять исключительно часть данных сайтов расщепления.
Ограниченный или частичный протеолиз также включает протеолиз, проводимый при лимитирующих условиях, посредством чего кинетика активности протеазы замедляется до такой степени, что пептиды отщепляются от белка по одному в данный момент времени или не более чем по несколько в данный момент времени. Согласно некоторым вариантам реализации настоящего изобретения кинетическая активность указанной по меньшей мере одной протеазы замедляется настолько, что указанные экспонированные на поверхности пептиды отщепляются по одному в данный момент времени или не более чем по несколько в данный момент времени, например, не более чем 8 (1, 2, 3, 4, 5, 6, 7 или 8) в данный момент времени (например, не более чем 8 пептидов или не более чем 8 уникальных пептидов в образце, например, как описано в другом месте в настоящей заявке), или не более чем 7 (1, 2, 3, 4, 5, 6 или 7) в данный момент времени (например, не более чем 7 пептидов или не более чем 7 уникальных пептидов в образце, например, как описано в другом месте в настоящей заявке), или не более чем 5 (1, 2, 3, 4 или 5) в данный момент времени (например, не более чем 5 пептидов или не более чем 5 уникальных пептидов в образце, например, как описано в другом месте в настоящей заявке). Согласно некоторым таким вариантам реализации настоящего изобретения реакция протеолиза может проходить до завершения, в результате чего в белке исчерпываются пептиды, которые могут отщепляться данной протеазой.
Как описано в другом месте в настоящей заявке, как правило, ограниченный или частичный протеолиз приводит к тому, что протеазой расщепляются исключительно наиболее гибкие и/или экспонированные на поверхности части белка.
Согласно некоторым вариантам реализации настоящего изобретения указанную по меньшей мере одну протеазу используют в условиях, которые приводят к получению не более чем 8 экспонированных на поверхности пептидов (например, 1, 2, 3, 4, 5, 6, 7 или 8 экспонированных на поверхности пептидов), отщепленных от белка под действием указанной протеазы (например, не более чем 8 пептидов или не более чем 8 уникальных пептидов в образце, например, как описано в другом месте в настоящей заявке).
Согласно предпочтительному варианту реализации настоящего изобретения указанную по меньшей мере одну протеазу используют в условиях, которые приводят к получению не более чем 7 экспонированных на поверхности пептидов (например, 1, 2, 3, 4, 5, 6 или 7 экспонированных на поверхности пептидов) или не более чем 5 экспонированных на поверхности пептидов (например, 1, 2, 3, 4 или 5 экспонированных на поверхности пептидов), отщепленных от белка под действием указанной протеазы (например, не более чем 7 или не более чем 5 пептидов, или не более чем 7 или не более чем 5 уникальных пептидов в образце, например, как описано в другом месте в настоящей заявке).
Ограниченного или частичного протеолиза согласно настоящему изобретению можно, как правило, достичь посредством уменьшения активности протеазы, например, посредством замедления кинетики активности протеазы до такой степени, что пептиды отщепляются от белка по одному в данный момент времени или не более чем по несколько в данный момент времени. Согласно некоторым вариантам реализации настоящего изобретения кинетическая активность указанной по меньшей мере одной протеазы замедляется настолько, что указанные экспонированные на поверхности пептиды отщепляются по одному в данный момент времени или не более чем по несколько в данный момент времени, например, не более чем 8 (1, 2, 3, 4, 5, 6, 7 или 8) в данный момент времени или не более чем 7 в данный момент времени (1, 2, 3, 4, 5, 6 или 7), или не более чем 5 (1, 2, 3, 4 или 5) в данный момент времени, например, как описано выше.
Для ограниченного или частичного протеолиза можно использовать любые подходящие условия для получения исключительно наиболее гибких и/или экспонированных на поверхности частей белка, отщепляемых протеазой, например, для получения не более чем 8 экспонированных на поверхности пептидов или не более чем 7 экспонированных на поверхности пептидов, или не более чем 5 экспонированных на поверхности пептидов, отщепляемых протеазой. Условия, которые приводят к ограниченному или частичному протеолизу, можно установить посредством варьирования температуры реакции расщепления и/или концентрации протеазы, и/или продолжительности реакции расщепления, и/или буферных условий. Количество пептидов, отщепляемых от пептида в конкретных условиях, может определить специалист в данной области техники (например, методом масс-спектрометрии или химии белка либо биохимии). Подходящие способы установления соответствующих условий ограниченного или частичного протеолиза также описаны в другом месте в настоящей заявке. Соответствующие условия для ограниченного или частичного протеолиза можно установить для различных белков или для различных протеаз либо для конкретной комбинации используемых белка и протеазы. В особенности предпочтительные условия для ограниченного или частичного протеолиза описаны в примерах в настоящей заявке. Условия, используемые для ограниченного или частичного протеолиза, как правило, не изменяют (или значительно не изменяют) нативную конфигурацию (нативную форму) белка. Кофакторы белка могут присутствовать, но не обязательно присутствуют в течение ограниченного или частичного протеолиза.
Соответствующие условия для ограниченного или частичного протеолиза могут отличаться в зависимости от протеазы и/или белка, но представляют собой, как правило, условия, которые не являются оптимальными для протеазы, о которой идет речь, например, в результате чего кинетика активности протеазы значительно замедляется или уменьшается.
Как правило, используют условия, которые предоставляют (или обеспечивают) низкую протеолитическую активность протеазы (например, меньшую или значительно меньшую, чем оптимальная протеолитическая активность). Такие условия включают, но не ограничены указанными, использование низкой концентрации протеазы и/или рабочей температуры, которая не является оптимальной для протеазы, о которой идет речь, и/или нестандартного или неоптимального буфера для протеазы, о которой идет речь, и/или короткого времени контакта (инкубации) протеазы с белком.
Согласно некоторым вариантам реализации настоящего изобретения ограниченный или частичный протеолиз (например, при использовании трипсина или, например, при использовании протеазы с оптимальной рабочей температурой, составляющей, например, 37°С или выше) проводят при комнатной температуре (например, приблизительно 20°С или 17-23°С).
Согласно некоторым вариантам реализации настоящего изобретения ограниченный или частичный протеолиз проводят при температуре, которая по меньшей мере на 2°С, по меньшей мере на 5°С, по меньшей мере на 10°С или по меньшей мере на 20°С выше или ниже либо значительно выше или ниже (предпочтительно, ниже) оптимальной рабочей температуры используемой протеазы. Согласно некоторым вариантам реализации ограниченный или частичный протеолиз проводят при температуре, которая по меньшей мере на 2°С-5°С, 2°С-10°С, 2°С-20°С, 2°С-30°С, 5°С-10°С, 5°С-20°С, 5°С-30°С, 10°С-20°С, 10°С-30°С, 20°С-30°С выше или ниже (предпочтительно, ниже) оптимальной рабочей температуры используемой протеазы.
Согласно некоторым вариантам реализации настоящего изобретения для ограниченного или частичного протеолиза используют концентрации до 5 мкг/мл протеазы (например, трипсина). Согласно некоторым вариантам реализации для ограниченного или частичного протеолиза используют концентрации до 0,5 мкг/мл, до 1 мкг/мл, до 2 мкг/мл, до 10 мкг/мл или до 20 мкг/мл протеазы. Согласно некоторым вариантам реализации настоящего изобретения реакции ограниченного протеолиза позволяют протекать в течение не более чем или менее чем 5 минут, 10 минут, 15 минут, 30 минут, одного часа или пяти часов, причем более короткие времена инкубации, как правило, являются предпочтительными. Например, согласно некоторым вариантам реализации настоящего изобретения реакции ограниченного протеолиза позволяют протекать в течение не более чем или менее чем 5 минут, 10 минут, 15 минут или 30 минут. Согласно некоторым таким вариантам реализации настоящего изобретения ограниченный протеолиз проводят при комнатной температуре. Таким образом, согласно некоторым вариантам реализации настоящего изобретения ограниченный протеолиз проводят с концентрацией не более чем 5 мкг/мл протеазы (например, приблизительно 5 мкг/мл протеазы) в течение не более чем приблизительно 5 минут (например, приблизительно 5 минут) при комнатной температуре.
Согласно некоторым вариантам реализации настоящего изобретения реакции протеолитического расщепления можно остановить с использованием муравьиной кислоты или водного аммиака. Например, активность трипсина, Asp-N, протеиназы K и химотрипсина можно остановить с использованием муравьиной кислоты, а активность пепсина можно остановить с использованием водного аммиака.
Согласно некоторым вариантам реализации настоящего изобретения отщепленные экспонированные на поверхности пептиды классифицируют на основании порядка их появления после осуществления контакта с указанной по меньшей мере одной протеазой, причем экспонированным на поверхности пептидам, которые отщепляются первыми (или раньше) и обнаруживаются в первых (или ранних) точках отбора образца, присваивают высокий класс, и экспонированным на поверхности пептидам, которые отщепляются позже и обнаруживаются в последующих точках отбора образца, присваивают низкий класс. Пептиды высокого класса, которые быстро отделяются от белка-мишени, а также характеризуются функциональной значимостью, можно, как правило, использовать для разработки эпитопа, иммунизации и последующего создания антитела.
Согласно некоторым вариантам реализации настоящего изобретения экспонированным на поверхности пептидам, которые отщепляются в условиях низкой (менее жесткой) протеолитической активности, как описано в настоящей заявке (например, при (более) низкой концентрации протеазы, при (более) низкой температуре инкубации и/или при (более) коротком времени инкубации, как правило, легко расщепляемым пептидам), присваивают высокий класс, и экспонированным на поверхности пептидам, которые отщепляются в условиях высокой (более жесткой) протеолитической активности, как описано в настоящей заявке (например, при (более) высокой концентрации протеазы, при (более) высокой температуре инкубации и/или при (более) длительной температуре инкубации, как правило, менее легко расщепляемым пептидам), присваивают низкий класс.
Согласно некоторым вариантам реализации настоящего изобретения несколько образцов расщепленного протеолитическим способом материала (или элюата реакции протеолитического расщепления) можно отобрать в течение реакции ограниченного или частичного протеолиза (например, последовательно), и/или несколько образцов (например, несколько реакций ограниченного или частичного протеолиза) можно обрабатывать (или анализировать) по отдельности (например, обрабатывать или анализировать параллельно).
Согласно некоторым вариантам реализации настоящего изобретения несколько образцов расщепленного протеолитическим способом материала (или элюата реакции протеолитического расщепления) отбирают (или получают) через определенные интервалы времени (например, с интервалами в 1 минуту, 2,5 минут или 5 минут) в течение ограниченного или частичного протеолиза белка. Согласно некоторым таким вариантам реализации настоящего изобретения протеаза и/или (как правило, «и») концентрация протеазы (и/или другие условия, которые могут оказывать влияние на протеолиз, как описано в другом месте в настоящей заявке) могут являться постоянными для каждого (или в каждом) из образцов, а варьировать будет время (или продолжительность) контакта (или инкубации) с протеазой. Согласно некоторым таким вариантам реализации настоящего изобретения образцы можно получить последовательно (последовательное расщепление).
Согласно некоторым вариантам реализации настоящего изобретения несколько образцов (например, несколько реакций ограниченного или частичного расщепления) обрабатывают (или анализируют) по отдельности, причем каждый образец характеризуется различными протеолитическими условиями или протеолитическими активностями для ограниченного или частичного протеолиза белка, например, как обсуждается в другом месте в настоящей заявке, например, для различных образцов можно использовать различные протеазы и/или различные концентрации протеазы, и/или различные температуры, и/или различные времена инкубации. Согласно некоторым таким вариантам реализации настоящего изобретения время (или продолжительность) контакта (или инкубации) с протеазой, как правило (и предпочтительно) являются постоянными для каждого (или в каждом) из образцов. Согласно некоторым таким вариантам реализации настоящего изобретения образцы можно обрабатывать (или анализировать) параллельно.
Согласно некоторым вариантам реализации способов согласно настоящему изобретению количество экспонированных на поверхности пептидов, отщепленных от белка под действием указанной протеазы, контролируют посредством времени при постоянной концентрации протеазы, и несколько образцов отбирают в течение времени, либо количество экспонированных на поверхности пептидов, отщепленных от белка под действием указанной протеазы, контролируют посредством концентрации протеазы при постоянном времени, и некоторые образцы можно отбирать (или анализировать) при нескольких различных концентрациях протеазы, либо количество экспонированных на поверхности пептидов, отщепленных от белка под действием указанной протеазы, контролируют посредством как времени, так и концентрации указанной протеазы.
Каждый образец (или предпочтительные образцы) может, предпочтительно, содержать один или несколько пептидов (например, не более 8 пептидов или не более 8 уникальных пептидов), которые были отщеплены от белка. Таким образом, в каждом образце можно обнаружить один или несколько пептидов (например, не более 8 пептидов или не более 8 уникальных пептидов), которые были отщеплены от белка. Уникальный пептид представляет собой пептид, который не присутствует в предшествующем образце или не присутствует в образце с более слабыми (или менее жесткими) протеолитическими условиями (например, отличный или отличающийся от пептидов, присутствующих в предшествующем образце или в образце с более слабыми протеолитическими условиями). Соответственно, образец, который содержит не более 8 уникальных пептидов, может содержать более 8 различных пептидов, но один или более из данных пептидов могли быть обнаруженными в предшествующем образце или в образце с более слабыми протеолитическими условиями (и, таким образом, один или более из данных пептидов могут являться неуникальными пептидами).
В идеальном случае и предпочтительно, каждый образец будет содержать исключительно один отщепленный пептид. Например, один отщепленный пептид может быть обнаружен в первом образце (или точке отбора образца), и один отщепленный пептид может быть обнаружен в одном или более последующих образцах (или точках отбора образца). В других примерах несколько отщепленных пептидов (например, не более 8 пептидов или не более 8 уникальных пептидов) могут быть обнаружены в первом и/или последующих образцах (точках отбора образца). Условия, которые приводят к получению одного или нескольких отщепленных пептидов на образец (например, не более 8 пептидов или не более 8 уникальных пептидов на образец), можно установить посредством применения коротких интервалов отбора образца, различных концентраций протеазы, различных составов буфера, различных температур, различных концентраций соли или ингибиторов протеазы (или комбинации указанных факторов). Отщепленные пептиды можно классифицировать в зависимости от образца (точки отбора образца), в котором появляются данные пептиды. Например, в условиях, которые приводят к обнаружению исключительно одного пептида на точку отбора образца, пептиду в первом отобранном образце присваивают наивысший класс, пептиду во втором отобранном образце присваивают класс 2 и т.д. При использовании условий, посредством которых в каждой точке отбора образца обнаруживают исключительно один отщепленный пептид, возможно классифицировать отдельные пептиды. При использовании условий, посредством которых в каждой точке отбора образца обнаруживают несколько отщепленных пептидов, возможно классифицировать группы пептидов.
Согласно некоторым вариантам реализации настоящего изобретения экспонированные на поверхности пептиды (отщепленные пептиды) высокого класса являются предпочтительными. Согласно некоторым вариантам реализации настоящего изобретения экспонированный на поверхности пептид (например, пептид высокого класса) согласно настоящему изобретению представляет собой отщепленный пептид, который обнаруживают (или который присутствует) в первом отобранном образце. Согласно некоторым вариантам реализации настоящего изобретения экспонированный на поверхности пептид согласно настоящему изобретению (например, пептид высокого класса) представляет собой отщепленный пептид, который представляет собой один из пептидов первых 8 классов (например, уникальных пептидов первых 8 классов), или присутствует в образце, содержащем один из пептидов первых 8 классов (например, первых 7 классов или первых 5 классов) пептидов (например, первых 8, первых 7 или первых 5 классов уникальных пептидов), на основании порядка появления пептидов в образце (образцах), отобранных в течение ограниченного или частичного протеолиза белка. Такие пептиды могут быть обнаружены (или могут присутствовать) в первом отобранном образце или могут присутствовать в одном или более последовательно отобранных образцах.
Пептиды, которые отщепляются от белка первыми (или раньше) (например, таковые из первого отобранного образца (из первой точки отбора образца), как описано выше, или таковые, которые классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше), являются, как правило, значительно экспонированными (например, экспонированными на поверхности), и, таким образом, легкодоступными для протеазы. Таким первым (или ранее) отщепляемым пептидам присваивают высокий класс (например, пептиду, который появляется первым, присваивают класс 1, второму присваивают класс 2 и т.д.). Пептиды, которые отщепляются от белка позже (например, в более поздней точке отбора образца, чем ранние пептиды), не являются, как правило, значительно экспонированными, и, таким образом, не являются легкодоступными для протеазы. Таким позже отщепляемым пептидам присваивают более низкий класс. В настоящем изобретении пептиды высокого класса являются, как правило, предпочтительными.
Согласно некоторым вариантам реализации настоящего изобретения отщепленные пептиды (экспонированные на поверхности пептиды), содержащие аминокислотные последовательности, наиболее экспонированные на поверхности белка, являются предпочтительными для разработки антигенного эпитопа.
Согласно некоторым вариантам реализации настоящего изобретения пептиды (отщепленные пептиды) можно классифицировать на основании функциональной важности или прогнозируемой функциональной важности данных пептидов в отношении белка. Как правило, таким пептидам, содержащим аминокислотные последовательности, которые являются или которые согласно прогнозу являются функционально важными в отношении белка, присваивают более высокий класс, чем таковым, которые не являются или которые согласно прогнозу не являются функционально важными. Согласно некоторым вариантам реализации настоящего изобретения пептиды высокого класса являются предпочтительными.
Согласно некоторым вариантам реализации настоящего изобретения пептиды, содержащие аминокислотные последовательности, которые являются или которые согласно прогнозу являются функционально важными в отношении белка (например, характеризуются высоким классом функциональной важности) и которые дополнительно характеризуются высоким классом на основании экспонирования на поверхности (например, пептид из первого отобранного образца (из первой точки отбора образца), как описано выше, или таковые, которые классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше), являются предпочтительными для разработки антигенного эпитопа (или, другими словами, являются предпочтительными пептидами, на основе которых можно получить антигенный эпитоп).
Согласно некоторым вариантам реализации настоящего изобретения пептиды, содержащие аминокислотные последовательности, которые являются или которые согласно прогнозу являются функционально важными в отношении белка (например, характеризуются высоким классом функциональной важности), но которые дополнительно не характеризуются высоким классом на основании экспонирования на поверхности (например, не являются пептидами из первого отобранного образца (из первой точки отбора образца), как описано выше, или таковые, которые классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше), можно использовать для разработки антигенного эпитопа.
Согласно некоторым вариантам реализации настоящего изобретения пептиды, содержащие аминокислотные последовательности, которые не являются или которые согласно прогнозу не являются функционально важными в отношении белка (например, характеризуются низким классом функциональной важности), но которые характеризуются высоким классом на основании экспонирования на поверхности (например, пептид из первого отобранного образца (из первой точки отбора образца), как описано выше, или таковые, которые классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше), можно использовать для разработки антигенного эпитопа.
Согласно некоторым вариантам реализации настоящего изобретения антигенный эпитоп основан на экспонированном на поверхности пептиде, который отщепляется первым (или раньше) от указанного белка (например, на пептиде из первого отобранного образца (из первой точки отбора образца), как описано выше, или на пептиде, который классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов), на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше), вне зависимости от функциональной важности или прогнозируемой функциональной важности аминокислотной последовательности отщепленного пептида.
Согласно некоторым вариантам реализации настоящего изобретения антигенный эпитоп основан на экспонированном на поверхности пептиде, который классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, среди таковых пептидов, дополнительно содержащих аминокислотную последовательность, которая является или которая согласно прогнозу является функционально важной в отношении белка. Данные пептиды не обязательно должны быть (но могут являться) теми же, что и набор пептидов первых 8 классов на основании порядка появления самого по себе (как описано выше).
Согласно некоторым вариантам реализации настоящего изобретения в белке идентифицируют или выявляют область, представляющую интерес, которая является или которая согласно прогнозу является функционально важной в отношении белка, и антигенный эпитоп основан на экспонированном на поверхности пептиде, который классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, среди таковых пептидов, дополнительно содержащих аминокислотную последовательность, которая отщепляется от указанной области, представляющей интерес. Данные пептиды не обязательно должны быть (но могут являться) теми же, что и набор пептидов первых 8 классов на основании порядка появления самого по себе (как описано выше).
Согласно некоторым вариантам реализации настоящего изобретения антигенные эпитопы для получения антитела основаны на аминокислотной последовательности пептида (экспонированного на поверхности пептида), который был отщеплен первым (или раньше) (например, пептида из первого отобранного образца (из первой точки отбора образца), как описано выше, или пептида, который классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше) от указанного белка под действием протеазы в течение ограниченного протеолиза, и, таким образом, который характеризуется высоким классом.
Таким образом, согласно некоторым вариантам реализации настоящего изобретения способы согласно настоящему изобретению включают выбор экспонированного на поверхности пептида, который характеризуется высоким классом (например, пептида из первого отобранного образца (из первой точки отбора образца), как описано выше, или пептида, который классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше), для разработки антигенного эпитопа и получения антитела против указанного антигенного эпитопа, который основан на указанном экспонированном на поверхности пептиде (или разработан из указанного пептида).
Согласно некоторым вариантам реализации настоящего изобретения способы согласно настоящему изобретению включают выбор экспонированного на поверхности пептида, который характеризуется высоким классом (например, пептида из первого отобранного образца (из первой точки отбора образца), как описано выше, или пептида, который классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше), конструирование антигенного эпитопа на основе указанного экспонированного на поверхности пептида и получение антитела против указанного антигенного эпитопа.
Согласно некоторым вариантам реализации настоящего изобретения способы согласно настоящему изобретению включают выбор экспонированного на поверхности пептида, который характеризуется высоким классом (например, пептида из первого отобранного образца (из первой точки отбора образца), как описано выше, или пептида, который классифицируют в первые 8 пептидов (например, уникальные пептиды первых 8 классов) на основании порядка появления в течение ограниченного или частичного протеолиза, как описано выше), и соотнесение указанного пептида с определенным биологическим свойством (или биологической функцией) белка, конструирование антигенного эпитопа на основе указанного экспонированного на поверхности пептида и получение антитела против указанного антигенного эпитопа. Пептиды, содержащие аминокислотную последовательность, которая соотносится с определенным биологическим свойством (или биологической функцией) белка, являются, как правило, предпочтительными.
Для идентификации отщепленных пептидов (экспонированных на поверхности пептидов) можно применять любые средства. Согласно некоторым вариантам реализации настоящего изобретения отщепленные пептиды идентифицируют с использованием масс-спектрометрии. Согласно некоторым вариантам реализации настоящего изобретения используют жидкостную хроматографию в сочетании с масс-спектрометрией. Предпочтительно, отщепленные пептиды (экспонированные на поверхности пептиды) идентифицируют методом ЖХ-МС/МС (жидкостной хроматографии - тандемной масс-спектрометрии). Иллюстративные и предпочтительные методологии масс-спектрометрии описаны в примерах. Поиск в тандемных масс-спектрах можно проводить с помощью программного обеспечения MASCOT (Matrix Science, Лондон, Великобритания) по сравнению с соответствующей базой данных, например, как описано в примерах.
Расщепленный, деконструированный или усеченный белок, как указано в настоящей заявке, представляет собой белок, который был расщеплен в одном или более сайтах по всей его длине протеазой. Такое протеолитическое расщепление приводит к тому, что один или более пептидов (экспонированных на поверхности пептидов) отщепляются (т.е. высвобождаются) от белка. Таким образом, экспонированный на поверхности пептид представляет собой пептид, который был отщеплен от белка под действием протеазы. Термин «экспонированный на поверхности» отражает тот факт, что, как правило, в контексте полноразмерного белка (т.е. нерасщепленного белка) часть белка, которая соответствует последовательности отщепленного (высвободившегося) пептида, является значительно экспонированной и доступной для протеазы.
В настоящем изобретении предложены новые способы обнаружения терапевтических антител и новые фармакологически активные антитела, направленные на белок TRPV1 человека.
Настоящее изобретение относится к способам обнаружения эпитопов на белках, которые являются значительно экспонированными и которые, таким образом, можно использовать в качестве ориентиров для нацеливания антитела.
Некоторые способы согласно настоящему изобретению включают этап идентификации антигенного эпитопа посредством идентификации экспонированного на поверхности пептида, который отщепляется, содержащего аминокислотную последовательность, которая характеризуется или которая согласно прогнозу характеризуется функциональной важностью (например, биологической важностью) в отношении указанного белка, и создание антигенного эпитопа на основе такого экспонированного на поверхности пептида. Согласно некоторым вариантам реализации настоящего изобретения получают антитела против такого антигенного эпитопа.
Обнаружение того, содержит или не содержит экспонированный на поверхности пептид, который отщепляется от указанного белка, аминокислотную последовательность, которая является или которая согласно прогнозу является функционально важной в отношении указанного белка, можно провести посредством любых подходящих средств, и специалист в данной области техники способен с легкостью осуществить такое обнаружение.
Например, согласно некоторым вариантам реализации настоящего изобретения белок, который расщепляют, деконструируют или усекают в течение ограниченного или частичного протеолиза, исследуют в функциональном анализе для оценки того, была ли изменена функция или функциональные активности данного белка (например, биологическая функция). Данную оценку можно провести посредством сравнения уровня функциональной активности расщепленного, деконструированного или усеченного белка с уровнем функциональной активности белка, который не подвергали ограниченному или частичному протеолизу (уровень функциональной активности белка, который не подвергали ограниченному или частичному протеолизу, можно считать контрольным уровнем). Если биологическая функция белка изменяется после (или в течение) ограниченного или частичного протеолиза, это свидетельствует, что отщепленный пептид (пептиды) (экспонированный на поверхности пептид (пептиды)), были отщеплены (высвободились) из области белка, которая обладает функциональной значимостью в отношении белка (например, из области, обладающей биологической важностью). Соответственно, отщепленные экспонированные на поверхности пептиды можно соотнести с функциональными данными для оценки функциональной важности экспонированных на поверхности пептидов в отношении белка. Отщепленный пептид (пептиды) можно идентифицировать (например, последовательность (последовательности) отщепленного пептида (пептидов) можно идентифицировать), например, в параллельном эксперименте, как описано в другом месте в настоящей заявке (например, методом ЖХ-МС/МС). Если отщепление пептида (экспонированного на поверхности пептида) от белка приводит к изменению функциональной активности белка, это свидетельствует, что экспонированный на поверхности пептид может быть в особенности пригодным для создания антигенного эпитопа согласно настоящему изобретению. В качестве альтернативы, антигенный эпитоп на основе такого экспонированного на поверхности пептида может быть в особенности пригодным и предпочтительным для создания антитела.
Согласно одному варианту реализации настоящего изобретения белок представляет собой TRPV1, и анализ для определения функциональной важности отщепленных пептидов в отношении TRPV1 представляет собой анализ методом пэтч-кламп «наружная 35 сторона внутри», как описано в другом месте в настоящей заявке.
«Измененная» или «изменение» функции или функциональной активности может представлять собой любое измеряемое изменение, предпочтительно, значимое изменение, более предпочтительно, статистически значимое изменение. «Измененная» функция или «изменение функции» может представлять собой увеличение или уменьшение функции. Иллюстративные изменения функции представляют собой изменения ≥2% ≥3% ≥5% ≥10% ≥25% ≥50% ≥75% ≥100% ≥200% ≥300% ≥400% ≥500% ≥600% ≥700% ≥800% ≥900% ≥1000% ≥2000% ≥5000% или>10000%. Изменения, как правило, оценивают по сравнению с соответствующим контрольным уровнем функции или функциональной активности, например, по сравнению с функцией или функциональной активностью эквивалентного белка, который не подвергали ограниченному или частичному протеолизу.
Согласно некоторым вариантам реализации настоящего изобретения антигенный эпитоп основан на аминокислотной последовательности экспонированного на поверхности пептида, которая при отщеплении от белка приводит к изменению функции или функциональной активности белка.
Согласно некоторым вариантам реализации настоящего изобретения то, характеризуется или не характеризуется экспонированная на поверхности пептида последовательность функциональной важностью (например, биологической важностью), прогнозируют или определяют посредством биоинформационных средств и/или посредством применения другой уже известной информации (например, из научной литературы) относительно функционально важных областей белка. Соответственно, отщепленные экспонированные на поверхности пептиды можно соотнести с известными данными относительно функционально важных областей белка для прогнозирования или определения функциональной важности отщепленного пептида в отношении белка. Если известно, что аминокислотная последовательность экспонированного на поверхности пептида характеризуется (или согласно прогнозу характеризуется) функциональной важностью, это свидетельствует, что экспонированный на поверхности пептид может быть в особенности пригодным для создания антигенного эпитопа согласно настоящему изобретению. В качестве альтернативы, антигенный эпитоп на основе такого экспонированного на поверхности пептида может быть в особенности пригодным и предпочтительным для создания антитела.
Таким образом, согласно некоторым вариантам реализации настоящего изобретения антигенный эпитоп основан на аминокислотной последовательности экспонированного на поверхности пептида, которая, как известно, является (или согласно прогнозу является) функционально важной, например, на основании биоинформационного анализа и/или на основании другой уже известной информации (например, из научной литературы) относительно функционально важных областей белка.
Согласно некоторым вариантам реализации настоящего изобретения антигенный эпитоп представляет собой антигенный эпитоп TRPV1, основанный на аминокислотной последовательности экспонированного на поверхности пептида, которая соотносится с последовательностью TRPV1, связывающей кальмодулин, или с сайтом связывания капсайцина TRPV1 (или соответствует указанным последовательностям).
Согласно некоторым вариантам реализации настоящего изобретения функциональный анализ для определения функциональной важности экспонированного на поверхности пептида проводят дополнительно к прогнозированию или определению функциональной важности экспонированного на поверхности пептида с помощью биоинформационных средств и/или посредством применения другой уже известной информации (например, из научной литературы) относительно функционально важных областей белка.
«Биоинформационные средства», «биоинформационный анализ», «биоинформационные данные» и «биоинформационная информация» включают, но не ограничены указанными, проведение поиска в базах данных (например, проведение поиска в базе данных BLAST), структурное моделирование или структурную биологию, а также данные/информацию, которые получают посредством указанных способов.
Функция (например, биологическая функция) может включать любую соответствующую с биологической или физиологической точки зрения функцию белка, о котором идет речь. Функция (например, биологическая функция) включает, но не ограничена указанными, способность белка связываться с мишенью (такой как лиганд или рецептор) или с другим партнером связывания, например, кофактором, активность по передаче сигналов, ферментативную активность белка и активность ионного канала, активность транспортера, высвобождение, например, механизмы высвобождения и поглощения инсулина, и т.д. Таким образом, соответствующие с функциональной точки зрения или функционально важные области белка включают, но не ограничены указанными, области, которые обеспечивают способность белка к связыванию с мишенью (такой как лиганд или рецептор) или с другим партнером связывания, например, кофактором, области, которые обеспечивают активность передачи сигналов, области, которые обладают ферментативной активностью белка, области, которые обеспечивают активность ионного канала, области, обеспечивающие активность транспортера, и области, обеспечивающие высвобождение и поглощение молекул (например, инсулина).
Согласно одному варианту реализации способ согласно настоящему изобретению также включает этап создания in silico набора предполагаемых пептидов (например, всех предполагаемых пептидов), которые могут быть отщеплены от белка одной или более протеазами (например, посредством применения компьютерной программы, способной идентифицировать точки расщепления в белке на основании известной последовательности (последовательностей) распознавания указанной одной или более протеаз), и необязательно фильтрацию указанного набора созданных in silico предполагаемых пептидов для удаления пептидов, которые были описаны ранее (например, в базах данных последовательностей, например, посредством поиска в базе данных BLAST или в другой литературе), в результате чего получают отфильтрованный перечень предполагаемых пептидов, сравнение указанного отфильтрованного перечня предполагаемых пептидов с перечнем пептидов, идентифицированных в результате ограниченного или частичного протеолиза белка, идентификацию пептидов, которые присутствуют как в указанном отфильтрованном перечне, так и в указанном перечне пептидов, идентифицированных в результате ограниченного или частичного протеолиза белка, идентификацию (или конструирование) антигенного эпитопа на основе пептида, присутствующего в обоих перечнях, и необязательно получение антитела против указанного антигенного эпитопа.
Согласно другому аспекту в настоящем изобретении предложен способ идентификации антигенного эпитопа, причем указанный способ включает:
(i) воздействие на первый белок ограниченного или частичного протеолиза путем осуществления контакта первого белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии первого белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от первого белка под действием указанной протеазы;
(ii) идентификацию аминокислотной последовательности области (или доли либо части) второго белка, которая является идентичной или по существу гомологичной аминокислотной последовательности экспонированного на поверхности пептида, который отщепляется от первого белка; и
(iii) создание антигенного эпитопа на основании аминокислотной последовательности указанной области (или доли либо части) указанного второго белка, которая является идентичной или по существу гомологичной аминокислотной последовательности экспонированного на поверхности пептида, который отщепляется от первого белка; и необязательно
(iv) получение антитела против антигенного эпитопа.
Иллюстративные типы по существу гомологичной последовательности обсуждаются в другом месте в настоящей заявке. Такой способ может облегчить создание антигенного эпитопа для белка (второго белка) на основании ограниченного или частичного протеолиза, который проводят на отличном белке (первом белке). Данный подход может быть в особенности пригодным, когда первый и второй белки относятся к одному и тому же семейству белков или являются иным способом связанными, например, данные от ограниченного или частичного протеолиза, проведенного в отношении TRPV1, можно использовать для идентификации антигенного эпитопа TRPV2. Определение (или идентификацию) по существу гомологичных белков на втором белке можно проводить с использованием любых подходящих средств (например, компьютерных программ), которые известны специалисту. Исключительно в качестве примера, подходящей компьютерной программой является программа EMBOSS Needle, предоставленная EMBL-EBI. EMBOSS Needle считывает две входные последовательности и записывает оптимальное всеобщее выравнивание последовательности с помощью вычисления с использованием алгоритма выравнивания Нидлмана и Вунша для обнаружения оптимального выравнивания (включая пропуски) двух последовательностей по всей длине.
Согласно некоторым вариантам реализации настоящего изобретения антигенный эпитоп не основан на экспонированном на поверхности пептиде, содержащем аминокислотную последовательность, которая является консервативной в отношении другого белка (белков) (например, консервативную в ходе эволюции последовательность или последовательность, идентичную или по существу гомологичную аминокислотной последовательности экспонированного на поверхности пептида). Данный факт может минимизировать перекрестную реактивность (или неспецифичное связывание) антител, синтез которых был индуцирован против таких антигенных эпитопов. Другими словами, согласно некоторым вариантам реализации настоящего изобретения можно использовать антигенные эпитопы на основе уникальных аминокислотных последовательностей (или последовательностей, не обнаруженных в других белках).
Настоящее изобретение относится к способам обнаружения эпитопов на белках, которые являются соответствующими с функциональной точки зрения и которые, таким образом, можно применять в качестве ориентиров для нацеливания антитела. Более конкретно, такие способы включают применение инструментов протеомики для выявления эпитопов горячих точек белков-мишеней. Данные эпитопы, которые потенциально можно использовать в качестве антигенов при получении антител, обозначены в настоящей заявке как антигенные эпитопы.
Согласно аспекту настоящего изобретения белок расщепляют, деконструируют и/или усекают под действием протеазы и параллельно проводят один или более функциональных анализов расщепленного, деконструированного и/или усеченного белка для определения функционально важной области (областей) белка.
Согласно варианту реализации настоящего изобретения расщепление, деконструирование и/или усечение белка можно проводить параллельно с функциональным анализом (анализами) для определения функционально важных областей белка для направления селекции эпитопов с целью создания антитела.
Согласно варианту реализации настоящего изобретения для расщепления, деконструирования и/или усечения белка можно использовать одну протеазу. Согласно другому варианту реализации настоящего изобретения для расщепления, деконструирования и/или усечения белка-мишени можно использовать несколько протеаз, последовательно по одной или параллельно. Примерами таких протеаз являются, не ограничиваясь указанным, протеиназа Arg-C, эндопептидаза Asp-N, клострипаин, глутамилэндопептидаза, Lys-C, Lys-N, трипсин, химотрипсин, протеиназа K и термолизин. Область, которую легко расщепляют несколько протеаз, должна располагаться в экспонированной области белка, и область, которая расщепляется исключительно одной протеазой, вероятно, располагается в более скрытой области. В качестве альтернативы, протеаза обладает уникальной специфичностью расщепления или/и физико-химическими свойствами или/и структурными свойствами, в результате чего может идентифицировать экспонированные на поверхности пептиды на белке-мишени, что не свойственно другим протеазам. Таким образом, применение нескольких протеаз является предпочтительным, и каждая отличная протеаза может привести к получению комплементарной или уникальной информации о пригодности экспонированных на поверхности пептидов в качестве антигенных эпитопов.
Последовательное применение нескольких протеаз означает, что различные протеазы инкубируют с белком одну за другой, т.е. инкубируют одну протеазу, после чего в более позднюю временную точку инкубируют другую, и необязательно в более позднюю временную точку (или точки) - одну или более других различных протеаз.
Последовательное применение одной протеазы означает, что одну и ту же протеазу (например, ту же концентрацию протеазы) инкубируют с белком несколько раз, например, в нескольких различных (последовательных) временных точках, или что из реакции протеолитического расщепления в течение времени отбирают несколько образцов, и появление новых или уникальных пептидов, полученных в реакции, обнаруживают и отслеживают в течение времени.
Параллельное применение означает, что проводят несколько отдельных реакций расщепления одной протеазой, каждую реакцию с различной протеазой или с одной и той же протеазой, но в различных протеолитических условиях, например, как описано в другом месте в настоящей заявке, например, при различных концентрациях протеазы и/или температурах, и/или временных точках.
С целью идентификации перекрывающихся, комплементарных или уникальных экспонированных на поверхности пептидов можно использовать несколько протеаз. В данном контексте «перекрывающийся» означает, что экспонированный на поверхности пептид, идентифицированный посредством ограниченного или частичного протеолиза одной протеазой, содержит аминокислотную последовательность, которая перекрывается (частично или полностью) с аминокислотной последовательностью экспонированного на поверхности пептида, идентифицированного посредством ограниченного или частичного протеолиза одной или более другими (т.е. отличными) протеазами. В данном контексте «комплементарный» означает, что экспонированный на поверхности пептид, идентифицированный посредством ограниченного или частичного протеолиза одной протеазой, содержит аминокислотную последовательность, которая в контексте последовательности всего белка (т.е. последовательности всего белка до ограниченного или частичного протеолиза) лежит следом за аминокислотной последовательностью экспонированного на поверхности пептида, идентифицированного посредством ограниченного или частичного протеолиза одной или более другими (т.е. отличными) протеазами, или поблизости от указанной последовательности (или даже частично перекрывается с указанной последовательностью). «Уникальный» экспонированный на поверхности пептид представляет собой экспонированный на поверхности пептид, который был идентифицирован исключительно после ограниченного или частичного протеолиза одной или несколькими (меньшей частью) исследованных протеаз.
Не опираясь на какую-либо теорию, считают, что область белка, которая отщепляется более чем одной протеазой, вероятно, находится в значительно экспонированной (например, экспонированной на поверхности) области белка, и, таким образом, экспонированные на поверхности пептиды из области белка, которая отщепляется более чем одной протеазой, могут представлять собой в особенности пригодные экспонированные на поверхности пептиды, на основе которых можно получить антигенные эпитопы.
Использование нескольких протеаз включает, но не ограничено указанным, использование 2, 3, 4, 5 протеаз.
Согласно некоторым вариантам реализации способов согласно настоящему изобретению протеаза выбрана из группы, состоящей из трипсина, протеиназы Arg-C, эндопептидазы Asp-N, клострипаина, глутамилэндопептидазы, Lys-C, Lys-N, химотрипсина, протеиназы K, термолизина, пепсина, каспазы 1, каспазы 2, каспазы 3, каспазы 4, каспазы 5, каспазы 6, каспазы 7, каспазы 8, каспазы 9, каспазы 10, энтерокиназы, фактора Ха, гранзима В, нейтрофильной эластазы, пролинэндопептидазы, стафилококковой пептидазы I и тромбина (или включающей указанные протеазы).
Согласно некоторым предпочтительным вариантам реализации настоящего изобретения протеаза выбрана из группы, состоящей из трипсина, Asp-N эндопептидазы, химотрипсина, пепсина и протеиназы K (или включающей указанные протеазы). Согласно предпочтительным вариантам реализации настоящего изобретения протеаза представляет собой трипсин.
Согласно еще одному аспекту настоящего изобретения коктейль нескольких протеаз используют вместе в одном или нескольких воздействиях, разделенных во времени, при постоянных или варьирующих концентрациях одной или нескольких протеаз. Таким образом, согласно некоторым вариантам реализации настоящего изобретения используют единый коктейль (смесь) нескольких протеаз.
Если используют несколько протеаз, упорядоченный по классам перечень может быть получен для каждой отдельной протеазы.
Данный способ позволяет получить новое фундаментальное понимание функции белка и новую методологию/технологию для быстрой и точной разработки фармакологически активных антител, которые можно использовать для лечения медицинского состояния у людей и/или животных. Способ может быть распространен на белки, растворимые или мембраносвязанные, внеклеточные или внутриклеточные.
Перечень эпитопов, полученный с помощью предлагаемого способа, предпочтительно, сортируют в зависимости от специально подобранных биоинформационных данных и функционального анализа (анализов). В способе, предпочтительно, используют входящие данные из обоих экспериментов, а также биоинформационную информацию. Согласно варианту реализации настоящего изобретения основное внимание будет уделено мембранным и мембраносвязанным белкам. Примерами таких белков являются, не ограничиваясь указанными, ноцицептор TRPV1 человека, другие ионные каналы суперсемейства TRP, а также некоторые рецепторы возбуждающей аминокислоты, включая NMDA-рецептор, и G-белки. Данные белки (например, ионные каналы) обладают тем преимуществом, что данные белки можно непосредственно подробно исследовать с использованием, например, метода пэтч-кламп. Другие классы белков, представляющих интерес, относятся конкогенным белкам, включая онкогенные малые ГТФазы KRAS, NRAS и HRAS. KRAS представляет собой ключевой белок при некоторых метастатических злокачественных новообразованиях, включая карциному поджелудочной железы, карциному толстой кишки и карциному легких. ГТФазную активность можно исследовать, например, посредством радиоизотопного мечения ГТФ с последующим измерением свободного 32Р после гидролиза ГТФ до ГДФ или с применением анализов преобразования с последующим анализом методом вестернблоттинга. Другие представляющие интерес классы белка представляют собой иммуномодулирующие белки, вовлеченные в иммуномодуляцию при противораковой терапии, такие как PD1, PDL1, CD40 в качестве лишь нескольких примеров.
«Белок» согласно настоящему изобретению может представлять собой любой белок.
Согласно некоторым вариантам реализации настоящего изобретения белок представляет собой мембраносвязанный белок, растворимый (например, циркулирующий) белок, внеклеточный белок или внутриклеточный белок.
Согласно некоторым вариантам реализации настоящего изобретения белок представляет собой мембранный или мембраносвязанный белок.
Согласно некоторым вариантам реализации настоящего изобретения белок представляет собой ионный канал, например, ионный канал суперсемейства TRP (например, TRPV1 или TRPV2). Согласно предпочтительным вариантам реализации настоящего изобретения белок представляет собой TRPV1.
Согласно некоторым вариантам реализации настоящего изобретения белок представляет собой рецептор возбуждающей аминокислоты. Согласно некоторым таким вариантам реализации настоящего изобретения белок представляет собой NMDA-рецептор или G-белок.
Согласно некоторым вариантам реализации настоящего изобретения белок представляет собой онкогенный белок. Согласно некоторым таким вариантам реализации настоящего изобретения белок представляет собой онкогенную малую ГТФазу, которая выбрана из группы, состоящей из KRAS, NRAS и HRAS.
Согласно некоторым вариантам реализации настоящего изобретения белок представляет собой иммуномодулирующий белок. Согласно некоторым таким вариантам реализации настоящего изобретения белок выбран из группы, состоящей из PD1, PDL1, CD40, ОХ40, VISTA, LAG-3, TIM-3, GITR и CD20.
Согласно некоторым вариантам реализации настоящего изобретения белок не является рецептором активатора плазминогена урокиназного типа (urokinase plasminogen activator receptor, u-PAR), трансглутаминазой 3 (transglutaminase, TGase3), белком Neisseria meningitidis или каннабиноидным рецептором (например, СВ1).
Согласно некоторым вариантам реализации настоящего изобретения белок представляет собой эукариотический белок. Например, согласно некоторым вариантам реализации настоящего изобретения белок представляет собой белок млекопитающего, предпочтительно, белок человека.
Согласно некоторым вариантам реализации настоящего изобретения белок представляет собой любой белок протеома человека. Другими словами, белки человека являются предпочтительными.
Применение протокола ограниченного расщепления одной или несколькими протеазами в отношении данных мишеней приведет к обнаружению новых антител, направленных на эпитопы горячих точек. Различные протеазы будут образовывать различные отщепленные пептиды. Согласно варианту реализации настоящего изобретения мембранные белки деконструируют, и эффекты данного усечения по частям исследуют в отношении влияния на функцию белка. Редкие точки, наблюдаемые исключительно при применении определенных протеаз, также будут идентифицированы. Затем идентифицированные данные будут анализировать в зависимости от специально подобранных биоинформационных данных, а также данных функциональных анализов усеченных белков для выявления функционально важных областей белка, о котором идет речь.
Аспект вариантов реализации настоящего изобретения относится к способу идентификации антигенного эпитопа в белке. Способ включает воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида. Согласно другому варианту реализации настоящего изобретения способ также включает исследование по меньшей мере одной расщепленной, деконструированной или усеченной версии белка в функциональном анализе, в котором изучают, проверяют или подтверждают по меньшей мере одну биологическую функцию белка. Способ также включает идентификацию антигенного эпитопа в белке как экспонированного на поверхности пептида среди по меньшей мере одного экспонированного на поверхности пептида и присутствующего в области белка, вовлеченной в выполнение биологической функции белка, что определено на основании функционального анализа.
Согласно варианту реализации настоящего изобретения воздействие на белок ограниченного или частичного протеолиза включает осуществление контакта белка с по меньшей мере одной протеазой i) при выбранной температуре или диапазоне температуры, ii) при выбранной концентрации или диапазоне концентрации по меньшей мере одной протеазы (относительно концентрации белка) и/или и) в течение выбранной продолжительности времени. Данный подход, в свою очередь, позволяет по меньшей мере одной протеазе отщеплять экспонированные на поверхности области белка, но не негибкие и/или внутренние области белка.
Воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой предусматривает, что белок подвергают мягкому протеолизу. Как следствие, в особенности экспонированная на поверхности и гибкая пептидная часть (части) белка будет отщеплена от аминокислотной последовательности под действием по меньшей мере одной протеазы. Температура, концентрация и/или продолжительность, применяемые для протеолиза, как правило, зависят от конкретной протеазы (протеаз) и используемого белка. Таким образом, согласно варианту реализации настоящего изобретения сначала исследуют набор потенциальных условий протеолиза с целью выбрать или идентифицировать подходящую температуру, концентрацию протеазы и/или продолжительность, используемые для расщепления, и буферных условий для деконструирования или усечения белка и получения по меньшей мере одного экспонированного на поверхности пептида. Например, протеолиз можно провести при нескольких, т.е. по меньшей мере двух различных температурах реакции, при нескольких различных концентрациях протеазы (относительно концентрации белка) и/или при нескольких различных длительностях реакции, включая различные буферные условия, как показано на фигуре 1, с целью идентифицировать наиболее соответствующие условия протеолиза для текущей комбинации белка и протеазы (протеаз).
Подходящие условия для протеазы представляют собой, например, температуру, концентрацию и/или продолжительность, которые приводят к расщеплению, деконструированию или усечению белка на один или не более чем N экспонированных на поверхности пептидов. Типичное значение параметра N составляет 7, предпочтительно, 6 или 5, более предпочтительно, 4 или 3 или, еще более предпочтительно, 2 или 1.
Согласно варианту реализации настоящего изобретения в функциональном анализе изучают, проверяют или подтверждают по меньшей мере одну биологическую функцию белка. Неограничивающие примеры такой биологической функции включают способность белка связываться с мишенью, такой как лиганд или рецептор; ферментативную активность белка; активность ионного канала; и т.д.
Согласно варианту реализации настоящего изобретения воздействие на белок ограниченного или частичного протеолиза включает воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта белка с несколькими протеазами с образованием нескольких отщепленных, деконструированных или усеченных версий белка и нескольких экспонированных на поверхности пептидов. Согласно конкретному варианту реализации настоящего изобретения осуществляют контакт белка с несколькими протеазами последовательно, т.е. одной за другой. Согласно другому конкретному варианту реализации настоящего изобретения осуществляют контакт белка с несколькими протеазами параллельно.
Согласно варианту реализации настоящего изобретения идентификация антигенного эпитопа включает идентификацию экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в области, которая приводит к утрате или существенному изменению биологической функции белка, когда область отщепляют или удаляют от белка в течение ограниченного или частичного протеолиза.
Согласно варианту реализации настоящего изобретения способ также включает выбор по меньшей мере одной области-мишени в белке на основании биоинформационных данных и/или известных данных о биологической функции белка. В данном случае идентификация антигенного эпитопа включает идентификацию экспонированного на поверхности пептида среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в области белка среди по меньшей мере одной области-мишени.
Согласно данному варианту реализации настоящего изобретения биоинформационные и/или другие известные данные о биологической функции используют для направления селекции антигенных эпитопов. Это означает, что в качестве кандидатов при идентификации или выборе антигенного эпитопа используют исключительно экспонированные на поверхности пептиды, которые присутствуют в выбранной области-мишени (или областях-мишенях). Соответственно, количество кандидатов можно уменьшить посредством удаления или пропуска экспонированных на поверхности пептидов, которые присутствуют в областях, в которых, как известно, отсутствует любая биологическая функция, и/или которые, как известно, не вовлечены в осуществление биологической функции белка.
Другой аспект вариантов реализации настоящего изобретения относится к антигенному эпитопу, идентифицированному согласно вышеописанному способу идентификации антигенного эпитопа в белке.
Согласно одному варианту реализации в настоящем изобретении предложен антигенный эпитоп TRPV1, содержащий аминокислотную последовательность (или состоящий из аминокислотной последовательности), которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности.
Согласно другому варианту реализации в настоящем изобретении предложен антигенный эпитоп TRPV1, содержащий аминокислотную последовательность (или состоящий из аминокислотной последовательности), которая выбрана из группы, состоящей из:

Согласно одному варианту реализации в настоящем изобретении предложен антигенный эпитоп TRPV1, содержащий аминокислотную последовательность (или состоящий из аминокислотной последовательности) LVENGADVQAAAHGDF (SEQ ID NO: 7) или последовательность, по существу гомологичную указанной последовательности.
Согласно другому варианту реализации в настоящем изобретении предложен антигенный эпитоп TRPV1, содержащий аминокислотную последовательность (или состоящий из аминокислотной последовательности), которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности.
Согласно другому варианту реализации в настоящем изобретении предложен антигенный эпитоп TRPV1, содержащий аминокислотную последовательность (или состоящий из аминокислотной последовательности), которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности.
Согласно одному варианту реализации в настоящем изобретении предложен антигенный эпитоп TRPV1, содержащий аминокислоту (или состоящий из аминокислоты), которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности.
Согласно некоторым вариантам реализации в настоящем изобретении предложен антигенный эпитоп TRPV1, содержащий аминокислотную последовательность, представленную под вторым заголовком (заголовком, отмеченным двумя звездочками (**)) в каждой из таблиц 2, 3, 4, 5 и 6 в примере 3 в настоящей заявке, или последовательность, по существу гомологичную указанной последовательности. Такие пептиды, отщепляемые с использованием более высокой протеолитической активности (или более жестких или строгих протеолитических условий), являются, как правило, менее предпочтительными, чем пептиды, отщепляемые с использованием меньшей протеолитической активности (или менее жестких или слабых протеолитических условий) (например, более короткого времени и/или меньшей концентрации, например, представленные под первыми заголовком (заголовком, помеченным одной звездочкой (*) в каждой из таблиц 2, 3, 4, 5 и 6); однако особенный интерес представляет, если данные пептиды характеризуются или согласно прогнозу характеризуются функциональной важностью в отношении белка. Пептиды, представленные под вторыми заголовками в таблицах 2, 3, 4, 5 и 6 (**), можно считать пептидами, которые отщепляются позже, и пептиды, представленные под первыми заголовками в таблицах 2, 3, 4, 5 и 6 (*), можно считать пептидами, которые отщепляются первыми.
В контексте вышеописанных антигенных эпитопов TRPV1 указанная по существу гомологичная последовательность может представлять собой последовательность, содержащую 1, 2, 3, 4, 5 или 6 (предпочтительно, 1, 2 или 3) замен или делеций аминокислот по сравнению с данной аминокислотной последовательностью, или представляет собой последовательность, которая характеризуется идентичностью последовательности по меньшей мере 70% данной аминокислотной последовательности, или представляет собой последовательность, содержащую по меньшей мере 6 последовательных аминокислот данной аминокислотной последовательности. Другие примеры «по существу гомологичных» последовательностей описаны в другом месте в настоящей заявке в отношении аминокислотных последовательностей, которые являются «по существу гомологичными» экспонированным на поверхности пептидам, и данные примеры «по существу гомологичных» последовательностей также применимы к специфичным последовательностям пептидов, упомянутым выше. Специфичные последовательности пептидов, упомянутые выше, представляют собой последовательности экспонированного на поверхности пептида.
Согласно некоторым вариантам реализации в настоящем изобретении предложен антигенный эпитоп, который содержит удлиненную, усеченную или циклическую версию последовательности пептида, упомянутой выше (или состоит из указанной последовательности), или последовательность, по существу гомологичную указанной последовательности. Удлиненная, усеченная и циклическая версии пептидов обсуждаются в другом месте в настоящей заявке в контексте удлиненных, усеченных и циклических экспонированных на поверхности пептидов, и данное обсуждение также применимо к последовательностям пептидов, упомянутым выше. Конкретные последовательности пептида, упомянутые выше, представляют собой экспонированные на поверхности последовательности пептида.
Согласно одному варианту реализации в настоящем изобретении предложен антигенный эпитоп TRPV2, содержащий аминокислоту (или состоящий из аминокислоты), которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности. Иллюстративные по существу гомологичные последовательности обсуждаются в другом месте в настоящей заявке.
Следующий аспект вариантов реализации настоящего изобретения относится к конъюгату, конфигурированному для использования с целью получения антител. Конъюгат содержит по меньшей мере один антигенный эпитоп, как определено выше, присоединенный к пептиду-носителю или смешанный с пептидом-носителем.
Таким образом, согласно одному аспекту в настоящем изобретении предложен конъюгат, содержащий антигенный эпитоп согласно настоящему изобретению или идентифицированный согласно настоящему изобретению (либо полученный согласно настоящему изобретению). Конъюгаты могут содержать антигенный эпитоп и любую отличную структуру (т.е. любую структуру, отличную от антигенного эпитопа), например, метку или пептид-носитель. Конъюгаты, как правило, содержат антигенный эпитоп и пептид-носитель, причем указанный антигенный эпитоп присоединен к пептиду-носителю или смешан с пептидом-носителем.
Согласно варианту реализации настоящего изобретения пептид-носитель выбран из группы, состоящей из гемоцианина фисуреллы (keyhole limpet hemocyanin, KLH) и овальбумина (или включающей указанные пептиды). Присоединение может, например, представлять собой ковалентное присоединение или дисульфидный мостик. Согласно одному варианту реализации настоящего изобретения гемоцианин фисуреллы является предпочтительным пептидом-носителем. Согласно некоторым вариантам реализации настоящего изобретения может быть обеспечен антигенный эпитоп с остатком цистеина на N- или С- конце (предпочтительно, на N-конце). Такой остаток цистеина может облегчить присоединение антигенного эпитопа к пептиду-носителю (например, KLH).
Другой аспект вариантов реализации настоящего изобретения относится к применению антигенного эпитопа и/или конъюгата согласно вышеуказанному аспекту для получения антитела, которое специфично связывается с белком.
Еще один аспект вариантов реализации настоящего изобретения относится к способу получения антитела, которое специфично связывается с белком. Способ включает получение антитела против антигенного эпитопа и/или конъюгата согласно вышеуказанному аспекту и выделение антитела. Выделение антитела может включать выделение антитела из клетки (например, клетки-хозяина), в которой антитело было получено или наработано, и/или из среды роста/супернатанта.
Согласно конкретному варианту реализации настоящего изобретения способ включает воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии белка и по меньшей мере одного экспонированного на поверхности пептида. Способ также включает исследование по меньшей мере одной расщепленной, деконструированной или усеченной версии белка в функциональном анализе, в котором изучают, проверяют или подтверждают по меньшей мере одну биологическую функцию белка. Способ также включает идентификацию антигенного эпитопа в белке как экспонированного на поверхности пептида среди по меньшей мере одного экспонированного на поверхности пептида и присутствующего в области белка, вовлеченной в осуществление биологической функции белка, что определено на основании функционального анализа. Способ также включает получение антитела против антигенного эпитопа и выделение антитела.
Получение антитела против антигенного эпитопа можно осуществить согласно методикам, известным в данной области техники, включая, например, методику гибридомы, технологию фагового дисплея и т.д., как было описано в настоящей заявке ранее.
Следующий аспект вариантов реализации настоящего изобретения относится к антителу против антигенного эпитопа и/или конъюгата согласно вышеуказанному аспекту. Антитело специфично связывается с белком.
Таким образом, согласно одному аспекту в настоящем изобретении предложено антитело, созданное (или полученное) посредством способа согласно настоящему изобретению.
Согласно другому аспекту в настоящем изобретении предложено антитело против антигенного эпитопа согласно настоящему изобретению. В качестве альтернативы, в настоящем изобретении предложено антитело, которое связывается с антигенным эпитопом согласно настоящему изобретению. В качестве альтернативы, в настоящем изобретении предложено антитело, которое специфично связывается с антигенным эпитопом согласно настоящему изобретению.
В качестве примера, в настоящем изобретении предложено антитело против антигенного эпитопа, содержащего аминокислотную последовательность, которая выбрана из группы, состоящей из LLSQDSVAASTEKTLRLYDRRS (SEQ ID NO: 5) и GRHWKNFALVPLLRE (SEQ ID NO: 6), или состоящего из указанной последовательности. Согласно одному варианту реализации настоящего изобретения антитело против антигенного эпитопа, содержащего аминокислотную последовательность LLSQDSVAASTEKTLRLYDRRS (SEQ ID NO: 5), или состоящего из указанной последовательности, представляет собой антагонистическое (ингибиторное) антитело против TRPV1, предпочтительно, обладающее одним или более из функциональных свойств, описанных в разделе примеров в отношении антитела OTV1. Данный эпитоп соответствует аминокислотной последовательности, которая расположена в N-концевом внутриклеточном домене TRPV1. Согласно одному варианту реализации настоящего изобретения антитело против антигенного эпитопа, содержащего аминокислотную последовательность GRHWKNFALVPLLRE (SEQ ID NO: 6), или состоящего из указанной последовательности, представляет собой агонистическое антитело против TRPV1, предпочтительно, обладающее одним или более из функциональных свойств, описанных в разделе примеров в отношении антитела OTV2. Данный эпитоп соответствует аминокислотной последовательности, которая расположена в С-концевом внутриклеточном домене TRPV1.
Согласно некоторым вариантам реализации настоящего изобретения антитело может быть направлено против внутриклеточного эпитопа (или домена) TRPV1. Согласно некоторым таким вариантам реализации настоящего изобретения антитело может представлять собой антагонистическое (ингибиторное) антитело против внутриклеточного эпитопа (или домена) TRPV1. Согласно другим таким вариантам реализации настоящего изобретения антитело может представлять собой агонистическое антитело против внутриклеточного эпитопа (или домена) TRPV1.
Согласно варианту реализации настоящего изобретения связывание антитела с белком приводит к отсутствию или существенному изменению биологической функции белка.
Таким образом, антитело может представлять собой функциональное антитело, например, агонистическое антитело или антагонистическое антитело (например, антагонистическое или агонистическое антитело против TRPV1 или TRPV2). Антагонистическое антитело способно к связыванию с белком и ингибированию или уменьшению функции белка. Агонистическое антитело способно к связыванию с белком и усилению или увеличению функции белка. В случае TRPV1 или TRPV2 (или любого другого ионного канала) функция, о которой идет речь, может представлять собой активность транспорта ионов. Например, можно оценить способность антитела блокировать (уменьшать) или усиливать (увеличивать) связывание с капсайцином или кальмодулином. Антитела с такими свойствами составляют предпочтительные варианты реализации настоящего изобретения.
Связанный аспект вариантов реализации настоящего изобретения определяет антитело согласно вышеуказанному аспекту для применения в качестве лекарственного препарата.
Антитело против антигенного эпитопа и/или конъюгата можно получить посредством иммунизации животного одним или более антигенными эпитопами и/или одним или более конъюгатами согласно вариантам реализации настоящего изобретения. Иммунизированное животное можно выбрать из группы, состоящей из людей, мышей, крыс, кроликов, овец, нечеловекообразных приматов, коз, лошадей и сельскохозяйственных птиц.
Антитело согласно вариантам реализации настоящего изобретения можно также получить посредством способов иммунизации in vitro с использованием одного или более антигенных эпитопов и/или одного или более конъюгатов согласно вариантам реализации настоящего изобретения.
Антитело согласно настоящему изобретению может представлять собой поликлональное антитело или моноклональное антитело.
Антитело может представлять собой лиганд, один или более фрагментов антитела, такие как Fab-фрагмент (fragment antigen binding, антигенсвязывающий фрагмент), F(ab)'2-фрагмент (фрагмент, содержащий два Fab), ScFv-фрагмент (single-chain variable fragment, одноцепочечный вариабельный фрагмент), диатело, тетратело или интактное антитело.
Антитело согласно настоящему изобретению, как правило, способно к связыванию (например, специфичному связыванию) с полноразмерной версией белка, против которого направлено данное антитело, например, с полноразмерной версией белка в нативной форме (например, в клетке или на клетке).
Согласно некоторым вариантам реализации настоящего изобретения антитело представляет собой антитело против одного из белков (или типов белков), описанных в другом месте в настоящей заявке.
Антитела и антигенные эпитопы можно выделить или очистить. Термин «выделенный» или «очищенный» в данном контексте означает такие молекулы, которые выделены, очищены из своего природного окружения или по существу свободны от своего природного окружения, например, выделены или очищены из организма (если данные молекулы действительно существуют в природе), или означает такие молекулы, которые были получены в результате технологического процесса, т.е. включает рекомбинантные и полученные синтетическим путем молекулы. Таким образом, термин «выделенный» или «очищенный», как правило, означает антитело или антигенный эпитоп, по существу свободный от клеточного материала или других белков того источника, из которого были получены антитело или антигенный эпитоп. Согласно некоторым вариантам реализации настоящего изобретения такие выделенные или очищенные молекулы являются по существу свободными от культуральной среды при получении с помощью рекомбинантных методик или от химических исходных веществ или других химических веществ, когда данные молекулы являются синтезированными химическим способом.
Можно оценить функциональный эффект антител, полученных в настоящем изобретении, в отношении белка-мишени, и специалист с легкостью определит подходящие для применения анализы, например, исходя из природы белка-мишени. Например, если антитело представляет собой антитело против TRPV1 (или любого другого ионного канала), функциональный эффект антитела можно оценить, например, с использованием электрофизиологии и/или анализа поглощения YO-PRO, описанного в примере 2 в настоящей заявке.
Способы согласно настоящему изобретению можно использовать для создания антитела, которое затем можно выделить, получить или произвести для различных последующих применений. Таким образом, согласно следующему аспекту в настоящем изобретении предложен способ получения или производства и/или выделения антитела.
После того как одно или более антител были созданы, получены, выбраны, идентифицированы, выделены и/или очищены с применением способов согласно настоящему изобретению, данные антитела или компонент, фрагмент, вариант или производное указанных антител можно произвести и при необходимости приготовить в состав с по меньшей мере одним фармацевтически приемлемым носителем или вспомогательным веществом. Такие произведенные молекулы или компоненты, фрагменты, варианты или производные указанных молекул также охватываются настоящим изобретением. В качестве альтернативы, данные молекулы могут принимать форму нуклеиновых кислот, кодирующих указанные антитела, причем указанные нуклеиновые кислоты могут, в свою очередь, быть встроенными в соответствующий вектор экспрессии и/или могут содержаться в подходящих клетках-хозяевах. Таким образом, молекулы нуклеиновой кислоты, кодирующие указанные антитела, или векторы экспрессии, содержащие указанные молекулы нуклеиновой кислоты, образуют следующие аспекты настоящего изобретения.
После того как конкретное антитело или компонент, фрагмент, вариант или производное указанного антитела было создано или получено согласно настоящему изобретению, вектор экспрессии, кодирующий антитело, можно с легкостью применять (или приспособить для применения) с целью получения достаточных количеств молекулы посредством экспрессии в соответствующих клетках-хозяевах или системах и посредством выделения антител из клетки-хозяина или системы либо из среды роста или супернатанта указанной среды, в зависимости от обстоятельств. В случае поликлональных антител антитела можно выделить или очистить из сыворотки иммунизированного животного.
Таким образом, согласно следующему аспекту настоящего изобретения предложен способ получения или производства антитела, включающий этапы создания или получения антитела согласно способам согласно настоящему изобретению, как описано выше, производства или получения указанного антитела или компонента, фрагмента, варианта или производного указанного антитела, и необязательно приготовления в состав указанного произведенного антитела с по меньшей мере одним фармацевтически приемлемым носителем или вспомогательным веществом.
Указанные варианты или производные антитела включают пептоидные эквиваленты, молекулы с непептидным синтетическим остовом и полипептиды, родственные или полученные из исходного идентифицированного полипептида, в которых аминокислотная последовательность была модифицирована на одну или несколько замен, добавлений и/или делеций аминокислот, которые могут, в качестве альтернативы или дополнительно, содержать замены или добавления аминокислот, которые были модифицированы химическим способом, например, посредством дегликозилирования или гликозилирования. Для удобства такие производные или варианты могут характеризоваться идентичностью последовательности по меньшей мере 60, 70, 80, 90, 95 или 99% исходному полипептиду, из которого были получены данные производные.
Поскольку настоящее изобретение относится к получению антител, указанные варианты или производные также включают преобразование одного формата молекулы антитела в другой формат (например, преобразование из Fab в scFv или наоборот либо преобразование между любыми форматами молекул антитела, описанными в другом месте в настоящей заявке, например, преобразование в любой другой тип фрагмента антитела, как описано в настоящей заявке), или преобразование молекулы антитела в молекулу антитела конкретного класса (например, преобразование молекулы антитела в IgG или подкласс указанного класса, например, IgG1 или IgG3, которые являются в особенности подходящими для терапевтических антител) либо гуманизацию или образование химерной версии любого антитела.
Указанные варианты или производные также включают объединение антител с другими функциональными компонентами, которые могут, например, являться пригодными в последующих применениях указанных антител. Например, антитела можно объединить с компонентами, которые нацеливают данные антитела к конкретному участку тела, или с обнаруживаемыми группами, пригодными, например, при визуализации или других диагностических применениях, или с грузом, таким как радиоактивный изотоп, токсин или химиотерапевтическое средство в форме иммуноконъюгата.
Очевидно, что основное требование к таким компонентам, фрагментам, вариантам или производным, которые являются партнерами связывания молекул или структур-мишеней, заключается в том, что данные компоненты сохраняют свою исходную функциональную активность в отношении способности к связыванию или обладают улучшенными функциональными активностями.
Молекулы антитела, созданные или полученные либо произведенные с применением способов согласно настоящему изобретению, можно использовать в любых способах, в которых необходимы антитела, специфичные к структуре-мишени (например, антитела, специфичные к конкретному антигену). Таким образом, антитела можно использовать в качестве молекулярных инструментов, и согласно следующему аспекту настоящего изобретения предложен реактив, который содержит такие антитела, как определено в настоящей заявке. Кроме того, такие молекулы можно использовать для терапевтических или профилактических применений in vivo, диагностики или применений для визуализации in vivo или in vitro либо для анализов in vitro.
Некоторые конкретные варианты реализации настоящего изобретения изложены ниже:
1. Способ создания антитела против белка, причем указанный способ включает:
(i) идентификацию антигенного эпитопа в указанном белке посредством воздействия на белок ограниченного или частичного протеолиза путем осуществления контакта белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии указанного белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от указанного белка под действием указанной протеазы, и создание антигенного эпитопа на основе указанного экспонированного на поверхности пептида; и
(ii) получение антитела против указанного антигенного эпитопа.
2. Способ создания антитела против белка, причем указанный способ включает:
(i) воздействие на белок ограниченного или частичного протеолиза путем осуществления контакта указанного белка с по меньшей мере одной протеазой с образованием по меньшей мере одной расщепленной, деконструированной или усеченной версии указанного белка и по меньшей мере одного экспонированного на поверхности пептида, который отщепляется от указанного белка под действием указанной протеазы; и
(ii) идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в области белка, которая приводит к утрате или существенному изменению биологической функции указанного белка, когда пептид отщепляют или удаляют от указанного белка в течение ограниченного или частичного протеолиза; или
выбор по меньшей мере одной области-мишени в указанном белке на основании биоинформационных данных и/или известных данных о биологической функции указанного белка и идентификацию антигенного эпитопа посредством идентификации экспонированного на поверхности эпитопа среди по меньшей мере одного экспонированного на поверхности пептида, присутствующего в указанной по меньшей мере одной области-мишени; и
(iii) получение антитела против указанного антигенного эпитопа.
3. Способ согласно варианту реализации 1 или варианту реализации 2, отличающийся тем, что указанную по меньшей мере одну протеазу используют в условиях, которые приводят к получению не более чем 8, или не более чем 7, или не более чем 5 экспонированных на поверхности пептидов, или не более чем 7, или не более чем 5 уникальных экспонированных на поверхности пептидов, отщепленных от белка под действием указанной протеазы в образце материала, расщепляемого протеолитическим способом, и при этом несколько образцов необязательно отбирают или анализируют последовательно или параллельно, необязательно через различные периоды времени и/или при различных концентрациях указанной протеазы.
4. Способ согласно любому из вариантов реализации 1-3, отличающийся тем, что указанную по меньшей мере одну протеазу используют в условиях, которые приводят к получению не более чем 8 или не более чем 7, или не более чем 5 экспонированных на поверхности пептидов, отщепленных от указанного белка под действием указанной протеазы.
5. Способ согласно любому из вариантов реализации 1-4, отличающийся тем, что кинетическая активность указанной по меньшей мере одной протеазы замедляется настолько, что указанные экспонированные на поверхности пептиды отщепляются по одному в данный момент времени или не более чем по несколько в данный момент времени, например, не более чем 8 или не более чем 7, или не более чем 5 в данный момент времени в образце, и при этом несколько образцов необязательно отбирают или анализируют последовательно или параллельно.
6. Способ согласно любому из вариантов реализации 1-5, отличающийся тем, что указанные отщепленные экспонированные на поверхности пептиды классифицируют на основании порядка их образования после осуществления контакта с указанной по меньшей мере одной протеазой, причем экспонированным на поверхности пептидам, которые отщепляются первыми или при меньших концентрациях указанной протеазы, присваивают высокий класс, и экспонированным на поверхности пептидам, которые отщепляются позже или при более высоких концентрациях указанной протеазы, присваивают низкий класс, и экспонированные на поверхности пептиды, которые отщепляются в промежутке между отщеплением указанных пептидов, необязательно можно классифицировать в порядке их возникновения.
7. Способ согласно варианту реализации 6, отличающийся тем, что указанный способ включает выбор экспонированного на поверхности пептида, который характеризуется высоким классом, для разработки антигенного эпитопа и получение антитела против указанного антигенного эпитопа.
8. Способ согласно варианту реализации 6, отличающийся тем, что указанный способ включает выбор экспонированного на поверхности пептида, который характеризуется высоким классом, конструирование антигенного эпитопа на основе указанного экспонированного на поверхности пептида и получение антитела против указанного антигенного эпитопа.
9. Способ согласно варианту реализации 6, отличающийся тем, что указанный способ включает выбор экспонированного на поверхности пептида, который характеризуется высоким классом, соотнесение указанного экспонированного на поверхности пептида с определенным биологическим свойством указанного белка, конструирование антигенного эпитопа на основе указанного экспонированного на поверхности пептида и получение антитела против указанного антигенного эпитопа.
10. Способ согласно любому из вариантов реализации 1-9, отличающийся тем, что для расщепления, деконструирования и/или усечения указанного белка используют одну протеазу.
11. Способ согласно любому из вариантов реализации 1 - 9, отличающийся тем, что для расщепления, деконструирования и/или усечения указанного белка используют несколько протеаз.
12. Способ согласно варианту реализации 11, отличающийся тем, что указанные несколько протеаз используют последовательно по одной, используют параллельно или используют в едином коктейле из нескольких протеаз.
13. Способ согласно варианту реализации 11 или варианту реализации 12, отличающийся тем, что указанные несколько протеаз используют для идентификации перекрывающихся, комплементарных или уникальных экспонированных на поверхности пептидов.
14. Способ согласно любому из вариантов реализации 1-13, отличающийся тем, что указанная протеаза выбрана из группы, состоящей из: трипсина, протеиназы Arg-C, эндопептидазы Asp-N, клострипаина, глутамилэндопептидазы, Lys-C, Lys-N, химотрипсина, протеиназы K, термолизина, пепсина, каспазы 1, каспазы 2, каспазы 3, каспазы 4, каспазы 5, каспазы 6, каспазы 7, каспазы 8, каспазы 9, каспазы 10, энтерокиназы, фактора Ха, гранзима В, нейтрофильной эластазы, пролинэндопептидазы, стафилококковой пептидазы I и тромбина.
15. Способ согласно любому из вариантов реализации 1-14, отличающийся тем, что указанная протеаза представляет собой трипсин.
16. Способ согласно любому из вариантов реализации 1-15, отличающийся тем, что указанный белок представляет собой мембранный белок, который присутствует в протеолипосоме, полученной из клеток.
17. Способ согласно любому из вариантов реализации 1-16, отличающийся тем, что указанную протеолипосому иммобилизуют в проточной ячейке для получения неподвижной фазы мембранных белков.
18. Способ согласно любому из вариантов реализации 1-15, отличающийся тем, что указанный белок находится в белок-содержащей липидной везикуле, которая является связанной с поверхностью или суспендированной в растворе.
19. Способ согласно любому из вариантов реализации 1-15, отличающийся тем, что указанный белок находится в интактной клетке, которая является связанной с поверхностью или суспендированной в растворе.
20. Способ согласно любому из вариантов реализации 1-15, отличающийся тем, что указанный белок находится в растворе.
21. Способ согласно любому из вариантов реализации 1-20, отличающийся тем, что указанный белок представляет собой любой белок протеома человека.
22. Способ согласно любому из вариантов реализации 1-21, отличающийся тем, что указанный белок представляет собой мембраносвязанный белок, растворимый белок, внеклеточный белок или внутриклеточный белок.
23. Способ согласно любому из вариантов реализации 1-22, отличающийся тем, что указанный белок представляет собой мембранный или мембраносвязанный белок.
24. Способ согласно любому из вариантов реализации 1-23, отличающийся тем, что указанный белок представляет собой ионный канал суперсемейства TRP.
25. Способ согласно варианту реализации 24, отличающийся тем, что указанный белок представляет собой TRPV1 или TRPV2.
26. Способ согласно любому из вариантов реализации 1-23, отличающийся тем, что указанный белок представляет собой рецептор возбуждающей аминокислоты.
27. Способ согласно варианту реализации 26, отличающийся тем, что указанный белок представляет собой NMDA-рецептор или G-белок.
28. Способ согласно любому из вариантов реализации 1-23, отличающийся тем, что указанный белок представляет собой онкогенный белок.
29. Способ согласно варианту реализации 28, отличающийся тем, что указанный белок представляет собой онкогенную малую ГТФазу, которая выбрана из группы, состоящей из KRAS, NRAS и HRAS.
30. Способ согласно любому из вариантов реализации 1-23, отличающийся тем, что указанный белок представляет собой иммуномодулирующий белок.
31. Способ согласно варианту реализации 30, отличающийся тем, что указанный белок выбран из группы, состоящей из PD1, PDL1, CD40, ОХ40, VISTA, LAG-3, TIM-3, GITR и CD20.
32. Способ согласно любому из вариантов реализации 1-31, отличающийся тем, что указанные отщепленные пептиды идентифицируют путем масс-спектрометрии.
33. Способ согласно варианту реализации 24, отличающийся тем, что указанные отщепленные пептиды идентифицируют путем ЖХ-МС/МС.
34. Способ согласно любому из вариантов реализации 2-33, отличающийся тем, что указанная биологическая функция выбрана из группы, состоящей из способности указанного белка связываться с мишенью, такой как лиганд или рецептор, ферментативной активности указанного белка, активности ионного канала, активности транспортера и высвобождения, такого как механизм высвобождения и поглощения инсулина.
35. Способ согласно любому из вариантов реализации 1-34, отличающийся тем, что получение антитела против указанного антигенного эпитопа осуществляют посредством гибридомной технологии, технологии фагового дисплея или посредством иммунизации животного указанным антигенным эпитопом.
36. Способ согласно любому из вариантов реализации 1-35, отличающийся тем, что указанное антитело представляет собой моноклональное или поликлональное антитело.
37. Антитело, полученное способом согласно любому из вариантов реализации 1-36.
38. Антигенный эпитоп TRPV1, содержащий аминокислотную последовательность, которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности,
причем указанная по существу гомологичная последовательность представляет собой последовательность, содержащую 1, 2 или 3 замены или делеции аминокислот по сравнению с данной аминокислотной последовательностью, или представляет собой последовательность, которая по меньшей мере на 70% идентична данной аминокислотной последовательности, или представляет собой последовательность, содержащую по меньшей мере 6 последовательных аминокислот данной аминокислотной последовательности.
39. Антигенный эпитоп TRPV1, содержащий аминокислотную последовательность, которая выбрана из группы, состоящей из:

40. Антигенный эпитоп TRPV1, содержащий аминокислотную последовательность LVENGADVQAAAHGDF (SEQ ID NO: 7) или последовательность, по существу гомологичную указанной последовательности,
причем указанная по существу гомологичная последовательность представляет собой последовательность, содержащую 1, 2 или 3 замены или делеции аминокислот по сравнению с данной аминокислотной последовательностью, или представляет собой последовательность, которая по меньшей мере на 70% идентична данной аминокислотной последовательности, или представляет собой последовательность, содержащую по меньшей мере 6 последовательных аминокислот данной аминокислотной последовательности.
41. Антигенный эпитоп TRPV1, содержащий аминокислотную последовательность, которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности,
причем указанная по существу гомологичная последовательность представляет собой последовательность, содержащую 1, 2 или 3 замены или делеции аминокислот по сравнению с данной аминокислотной последовательностью, или представляет собой последовательность, которая по меньшей мере на 70% идентична данной аминокислотной последовательности, или представляет собой последовательность, содержащую по меньшей мере 6 последовательных аминокислот данной аминокислотной последовательности.
42. Антигенный эпитоп TRPV1, содержащий аминокислоту, которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности,
причем указанная по существу гомологичная последовательность представляет собой последовательность, содержащую 1, 2 или 3 замены или делеции аминокислот по сравнению с данной аминокислотной последовательностью, или представляет собой последовательность, которая по меньшей мере на 70% идентична данной аминокислотной последовательности, или представляет собой последовательность, содержащую по меньшей мере 6 последовательных аминокислот данной аминокислотной последовательности.
43. Антигенный эпитоп TRPV1, содержащий аминокислоту, которая выбрана из группы, состоящей из:
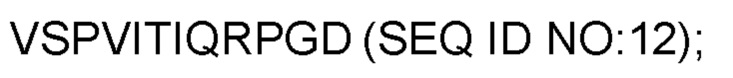

или последовательность, по существу гомологичную указанной последовательности,
причем указанная по существу гомологичная последовательность представляет собой последовательность, содержащую 1, 2 или 3 замены или делеции аминокислот по сравнению с данной аминокислотной последовательностью, или представляет собой последовательность, которая по меньшей мере на 70% идентична данной аминокислотной последовательности, или представляет собой последовательность, содержащую по меньшей мере 6 последовательных аминокислот данной аминокислотной последовательности.
44. Антигенный эпитоп TRPV2, содержащий аминокислоту, которая выбрана из группы, состоящей из:

или последовательность, по существу гомологичную указанной последовательности,
причем указанная по существу гомологичная последовательность представляет собой последовательность, содержащую 1, 2 или 3 замены или делеции аминокислот по сравнению с данной аминокислотной последовательностью, или представляет собой последовательность, которая по меньшей мере на 70% идентична данной аминокислотной последовательности, или представляет собой последовательность, содержащую по меньшей мере 6 последовательных аминокислот данной аминокислотной последовательности.
45. Антитело против антигенного эпитопа согласно любому из вариантов реализации 38-44.
Как отмечается выше, авторы настоящего изобретения разработали методологию для идентификации экспонированных на поверхности антигенных эпитопов, которая позволяет получать фармакологически активные антитела с применением кинетически контролируемого протеолиза. В идеальном случае протеолитический этап осуществляют настолько медленно, что под действием протеазы в данный момент времени от антигена отрывается один или несколько пептидов. Пептиды, которые появляются первыми, являются экспонированными на поверхности и легкодоступными для антитела, и вследствие этого, как правило, являются предпочтительными по сравнению с пептидами, которые появляются позже. Затем данные пептиды можно перекрестно соотнести для определения функциональной значимости на основании последовательности с использованием специально подобранных биоинформационных данных, а также функциональных анализов, которые проводят с усеченными белками.
Однако в настоящем изобретении также предложены способы, которые характеризуются улучшениями по сравнению со способами, описанными выше, которые делают возможной дальнейшую оптимизацию дизайна эпитопа и/или идентификацию следующих (дополнительных) эпитопов. Такие улучшенные способы обозначены как способы А и В.
Подобно другим способам, описанным в настоящей заявке, в данных улучшенных способах можно применять несколько протеаз параллельно с целью максимизации числа полученных эпитопов. На ионном канале TRPV1 исследовали 5 протеаз, и диапазон подходящих протеаз можно расширить в случае, если предложенные протеазы характеризуются различной специфичностью расщепления, для получения большего числа уникальных пептидов из нативных и минимально расщепленных белков.
В целом, данные улучшенные способы должны улучшить разработку антитела и позволить получить новые терапевтически и фармакологически активные антитела для борьбы с заболеванием. Фармакологически активные антитела, действующие как внутри-, так и внеклеточно, можно получить с применением способов, описанных в настоящей заявке.
В способах согласно настоящему изобретению, в отличие от множества известных методик обнаружения новых антител, антитело можно сконструировать с самого начала для связывания с конкретным сайтом и необязательно для выполнения конкретной функции вместо получения вслепую, когда изначальным приоритетом, как правило, является аффинность, а не функциональность, а затем подмножество антител, демонстрирующих хорошие характеристики связывания, исследуют для определения биологических эффектов.
Способ А
Таким образом, согласно одному аспекту в настоящем изобретении предложен способ идентификации эпитопа, с которым может связываться антитело, на белке, причем указанный способ включает:
(i) идентификацию сайтов, в которых одна или более протеаз разрезали указанный белок после того, как указанный белок подвергся воздействию ограниченного или частичного протеолиза указанной одной или более протеазами; и
(ii) исследование совокупности эпитопов на указанном белке, которые расположены между сайтами разрезания, которые перекрываются с сайтом разрезания или которые расположены в области, фланкирующей сайт разрезания, с помощью антител, направленных против указанных эпитопов, посредством этого идентифицируя один или более эпитопов, с которыми может связываться антитело.
Можно использовать любую соответствующую протеазу, и подходящие протеазы, которые можно использовать в таком способе, описаны в другом месте в настоящей заявке. Таким образом, можно использовать одну или несколько протеаз, как описано в другом месте в настоящей заявке. Если используют несколько протеаз, тогда согласно некоторым вариантам реализации их можно использовать параллельно, как описано в другом месте в настоящей заявке. Ограниченный или частичный протеолиз также описан в другом месте в настоящей заявке. Согласно данному аспекту (способу А) можно использовать любое из условий ограниченного или частичного протеолиза, описанных в настоящей заявке.
Сайты, идентифицированные в части (i) описанного выше способа, можно обозначить как сайты разрезания (сайты, в которых протеаза разрезала или согласно прогнозу разрежет и отщепет экспонированный на поверхности пептид). Для идентификации сайтов, в которых одна или более протеаз разрезали (или разрежут) указанный белок (сайтов разрезания), можно использовать любой соответствующий способ/методику. Одна из подходящих методик представляет собой масс-спектрометрию. Данные о последовательностях пептида или пептидов, которые высвободились (или отщепились) от белка в результате ограниченного или частичного протеолиза (например, идентифицированных методом масс-спектрометрии), являются источником информации о сайтах разрезания. В этой связи остатки на концах высвободившегося пептида или пептидов (отщепленных пептидов) являются источником информации о сайте разрезания в белке (например, в нативном или полноразмерном белке).
Во избежание разночтений отметим, что «сайт разрезания» на этапе (ii) описанного выше способа (способа А) можно также рассматривать как сайт (или положение) в аминокислотной последовательности белка (например, в нативном белке или полноразмерном белке, или белке дикого типа), соответствующий сайту, который был (или будет) разрезан (или расщеплен) в соответствии с этапом (i) (соответствует сайту, идентифицированному на этапе (i)). Этап (ii) способа А, таким образом, как правило, включает исследование совокупности эпитопов на нативном белке (или полноразмерном белке, или белке дикого типа), которые расположены между сайтами разрезания, которые перекрываются с сайтом разрезания или которые расположены в области, фланкирующей сайт разрезания, с помощью антител, направленных против указанных эпитопов, посредством этого идентифицируя один или более эпитопов, с которыми может связываться антитело.
Во избежание разночтений отметим, что «между сайтами разрезания», предпочтительно, обозначает «между смежными сайтами разрезания». Таким образом, «между сайтами разрезания», предпочтительно, обозначает «между данным сайтом разрезания и следующим (или предыдущим) сайтом разрезания» в аминокислотной последовательности белка (например, в нативном белке, или полноразмерном белке, или белке дикого типа). Таким образом, «между сайтами разрезания», предпочтительно, обозначает «между сайтами разрезания, смежными друг с другом в первичной аминокислотной последовательности».
Согласно некоторым вариантам реализации настоящего изобретения способ может дополнительно включать (до этапа (ii)) этап образования (или синтеза) совокупности (например, 2 или более, 3 или более, 5 или более, 10 или более, 20 или более, 50 или более) выделенных эпитопов, последовательности которых соответствуют эпитопам (или последовательностям) на указанном белке, которые расположены между сайтами разрезания, которые перекрываются с сайтом разрезания или которые расположены в области, фланкирующей сайт разрезания, и образования (получения) антител, направленных на выделенные эпитопы или связывающихся с указанными выделенными эпитопами. Такие антитела затем можно использовать на этапе (ii) описанного выше способа для исследования совокупности эпитопов на указанном белке (например, нативном или полноразмерном белке), которые расположены между сайтами разрезания, которые перекрываются с сайтом разрезания или которые расположены в области, фланкирующей сайт разрезания. Можно использовать любой соответствующий способ/методику образования выделенных эпитопов или образования антител (например, как описано в другом месте в настоящей заявке), и специалисту известны такие способы и методики.
Согласно некоторым вариантам реализации настоящего изобретения эпитопы характеризуются различными длинами и/или последовательностями. Таким образом, среди совокупности (или группы) эпитопов могут присутствовать эпитопы, которые отличаются друг от друга длинами и/или последовательностями. Согласно другим вариантам реализации настоящего изобретения эпитопы характеризуются одинаковыми (или подобными) длинами и обычно различными последовательностями. Таким образом, согласно некоторым вариантам реализации настоящего изобретения среди совокупности (или группы) эпитопов эпитопы характеризуются одинаковой (или подобной) длиной.
Эпитопы могут характеризоваться любой соответствующей длиной. Согласно некоторым вариантам реализации настоящего изобретения выделенные эпитопы составляют 7-8 аминокислот в длину или характеризуются длиной, как описано в другом месте в настоящей заявке.
Согласно предпочтительным вариантам реализации настоящего изобретения эпитопы перекрываются с сайтом разрезания (или содержат сайт разрезания, или окружают сайт разрезания).
Как правило, эпитопы (или по меньшей мере часть любого данного эпитопа) будут находиться в пределах 50 аминокислот от сайта разрезания, т.е. от +50 до -50 аминокислот относительно сайта разрезания. Предпочтительно, эпитопы (или по меньшей мере часть любого данного эпитопа) будут находиться в пределах 20 аминокислот от сайта разрезания, т.е. от +20 до -20 аминокислот относительно сайта разрезания, или будут находиться в пределах 10 аминокислот от сайта разрезания, т.е. от +10 до -10 аминокислот относительно сайта разрезания, или будут находиться в пределах 5 аминокислот от сайта разрезания, т.е. от +5 до -5 аминокислот относительно сайта разрезания.
Согласно некоторым вариантам реализации настоящего изобретения совокупность эпитопов представляет собой множество (или группу) эпитопов, причем последовательность каждого эпитопа во множестве смещена по сравнению с другим эпитопом во множестве на одну или несколько (например 1, 2 или 3), предпочтительно, одну, аминокислоту. Иными словами, согласно некоторым вариантам реализации настоящего изобретения во множестве (совокупности) эпитопов последовательность каждого эпитопа сдвинута на одну или несколько (например 1, 2 или 3), предпочтительно, одну, аминокислоту относительно последовательности другого эпитопа во множестве. Таким образом, совокупность эпитопов может представлять собой вложенное множество эпитопов, например, как проиллюстрировано на фигуре 16d. Как правило, такое вложенное множество эпитопов будет охватывать до приблизительно 50 аминокислот последовательности белка в любом направлении (или в обоих направлениях) относительно (или в окружении) сайта разрезания. Предпочтительно, такое вложенное множество эпитопов будет охватывать до приблизительно 20 или 10, или 5 аминокислот последовательности белка в любом направлении (или в обоих направлениях) относительно (или в окружении) сайта разрезания.
Когда используют вложенное множество эпитопов, согласно предпочтительным вариантам реализации настоящего изобретения значительное число эпитопов будет содержать сайт разрезания, предпочтительно, по существу все из эпитопов во вложенном множестве будут содержать сайт разрезания, более предпочтительно, все эпитопы во вложенном множестве будут содержать сайт разрезания.
Согласно некоторым вариантам реализации настоящего изобретения проводят этап активного осуществления ограниченного или частичного протеолиза. Согласно другим вариантам реализации настоящего изобретения активный этап осуществления ограниченного или частичного протеолиза не проводят, вместо этого проводят идентификацию сайтов, в которых одна или более протеаз разрезали указанный белок, на основании данных проведенных ранее экспериментов по ограниченному или частичному протеолизу (например, архивных данных, например, данных масс-спектрометрии, содержащих последовательности пептидов, высвободившихся из белка, из предшествующих экспериментов по ограниченному или частичному протеолизу). Вновь, предпочтительные и подходящие способы осуществления ограниченного или частичного протеолиза описаны в другом месте в настоящей заявке.
Исследование совокупности эпитопов означает, что несколько (например, 2 или более, 3 или более, 5 или более, 10 или более, 20 или более, 50 или более, или более одного, но до 4, 5, 10, 20 или 50) эпитопов (или потенциальных эпитопов) на белке (например, нативном или полноразмерном белке) анализируют (или оценивают) в отношении их способности быть связанными антителами, которые были образованы против выделенных эпитопов (или которые связываются с выделенными эпитопами), соответствующих эпитопу (или потенциальному эпитопу) на белке.
Как описано выше, исследование совокупности эпитопов на белке, которые расположены между сайтами разрезания, которые перекрываются с сайтом разрезания или которые расположены в области, фланкирующей сайт разрезания, можно провести с помощью антител, направленных против указанных эпитопов (т.е. антитела выступают в качестве зондов). В действительности, исследование с помощью антител (например, Fab-фрагментов или других фрагментов антитела) является предпочтительным. Однако, в качестве альтернативы, другие связывающие молекулы можно использовать в качестве зондов (например, можно использовать другие аффинные зонды). Антитела представляют собой один из примеров аффинного зонда, который можно использовать.
Предпочтительные белки описаны в другом месте в настоящей заявке.
Согласно одному аспекту в настоящем изобретении предложен эпитоп (или антигенный эпитоп), идентифицированный способом идентификации эпитопа, с которым может связываться антитело, на белке, как описано выше (способ А). Согласно одному аспекту в настоящем изобретении предложено антитело, которое связывается с таким эпитопом на белке. Согласно некоторым вариантам реализации настоящего изобретения антитела, которые связываются в непосредственной близости от сайта разрезания, как описано в настоящей заявке, например, в пределах 5, 10, 20 или 50 аминокислот от сайта разрезания, являются предпочтительными. Специалисту в данной области техники известны способы или методики образования антител против данных эпитопов, и можно использовать любой соответствующий способ (например, как описано в другом месте в настоящей заявке). Предпочтительные типы антител также описаны в другом месте в настоящей заявке.
Согласно некоторым вариантам реализации настоящего изобретения способ (способ А) также включает этап образования (или получения, или продуцирования) антитела против эпитопа, идентифицированного способом А (идентифицированного на этапе (ii)), или которое связывается с указанным эпитопом. Необязательно можно осуществить следующий этап приготовления антитела в состав с по меньшей мере одним фармацевтически приемлемым носителем или вспомогательным веществом.
Таким образом, согласно одному аспекту в настоящем изобретении предложен способ получения или изготовления антитела, которое связывается с эпитопом, идентифицированным способом А (идентифицированным на этапе (ii)). Необязательно можно осуществить следующий этап приготовления указанного полученного или изготовленного антитела в состав с по меньшей мере одним фармацевтически приемлемым носителем или вспомогательным веществом. Способы получения или изготовления антител описаны в другом месте в настоящей заявке и применимы с соответствующими изменениями к данному аспекту настоящего изобретения.
Согласно одному аспекту в настоящем изобретении предложен конъюгат, содержащий по меньшей мере один эпитоп, идентифицированный способом А, присоединенный к пептидному носителю или смешанный с ним. Конъюгаты описаны в другом месте в настоящей заявке, и указанное обсуждение применимо с соответствующими изменениями к данному аспекту настоящего изобретения.
Антитела, которые связываются с эпитопами, идентифицированными способом А (или эпитопами, идентифицированными способом А, или конъюгатами, содержащими такие эпитопы), можно использовать в терапии.
Антитела (например, одно или более, или панель или матрицу антител, или большое число антител), нацеленные на совокупность эпитопов на белке, можно исследовать в отношении их способности связываться с белком, например, для оценки их аффинности связывания или другого функционального эффекта (например, как описано в другом месте в настоящей заявке) в отношении белка. Таким образом, можно провести скрининг антител для идентификации антител, которые связываются наилучшим образом. Таким образом, можно идентифицировать в особенности подходящие эпитопы (например, для нацеливания на них антител), например, эпитопы, которые являются в особенности подходящими для нацеливания на них высокоаффинных антител, или нацеливание на которые приводит к значительному или измеряемому функциональному эффекту в отношении белка-мишени (например, антагонистическому или агонистическому эффекту). Соответственно, можно идентифицировать оптимальные эпитопы (например, для нацеливания на них антител, например, для вариантов терапевтического применения). Таким образом, в качестве альтернативы, в настоящем изобретении предложен способ оптимизации дизайна эпитопа или выбора оптимального эпитопа (например, для антител, которые получают против данного эпитопа или которые нацелены на данный эпитоп). Способ может позволить определять оптимальную длину и положение эпитопа относительно сайта разрезания.
Применение ограниченного протеолиза в качестве инструмента для подтверждения доступных областей для связывания антитела основывается на высвобождении пептидов из белка, т.е. на том, что протеазы расщепляют в двух доступных сайтах, окружающих последовательность правильного размера, для обнаружения, например, методом масс-спектрометрии. Информация, полученная в таком эксперименте, является подтверждением доступности двух сайтов разрезания, которые были расщеплены, что привело к высвобождению пептида. Однако размер и положение доступной области, окружающей сайт разрезания, могут являться неизвестными. В способе А применяют антитела (или другие связывающие белки) для проверки доступности областей, окружающих сайт разрезания. Например, посредством разработки антител, нацеленных на эпитопы, окружающие сайт разрезания, и последующего исследования их аффинности связывания и или функции, можно определить длину и положение оптимального эпитопа относительно сайта разрезания. Способы могут включать разработку панели (более одного) или большого числа антител, нацеленных на эпитопы различных длин и различных положений, в последовательности относительно сайта разрезания. Как правило, каждый эпитоп будет сдвинут на одну аминокислоту относительно каждого другого и будет охватывать от -20 до +20 аминокислот, окружающих сайт разрезания. Для экспериментального подтверждения доступных сайтов разрезания с применением ограниченного протеолиза можно использовать различные протеазы параллельно. Оптимальный дизайн эпитопа может варьировать среди сайтов разрезания, которые были проверены различными протеазами, поскольку для различных протеаз может требоваться больше или меньше доступных областей для получения возможности связаться и расщепить сайт разрезания. Вследствие этого оптимальный дизайн эпитопа можно определить для любого типа протеазы посредством исследования каждого подтвержденного сайта разрезания с помощью описанной выше методологии (способа А).
Предпочтительные характеристики других способов, описанных в настоящей заявке, можно применять с соответствующими изменениями к данному аспекту настоящего изобретения (способу А).
Как упомянуто выше, авторы настоящего изобретения разработали дополнительные и улучшенные способы, поскольку при применении предшествующих способов несколько потенциальных связывающих антитело сайтов могут быть пропущены, так как некоторые пептиды не высвобождаются. Это может произойти, например, если протеаза расщепляет только один из двух сайтов расщепления, окружающих определенную аминокислотную последовательность. В улучшенном способе, описанном ниже (способе В), посредством разработки новых алгоритмов поиска на основании данных in silico, гомологичного связывания Fab-протеаза и наборов данных расщепления несколькими протеазами, можно обнаружить уникальные и новые связывающие антитело сайты и, кроме того, можно получить новые структурные данные для нативных, а также частично расщепленных белков. Данная методика (в сочетании со способом А, описанным выше), таким образом, может обеспечить комплексные инструменты для исследования структуры и функции белка.
Способ В
Согласно другому аспекту в настоящем изобретении предложен способ идентификации эпитопа, с которым может связываться антитело, на белке, причем указанный способ включает:
(i) осуществление протеолитического расщепления указанного белка in silico одной или более протеазами для идентификации сайтов на белке, которые согласно прогнозу разрезаются указанной одной или более протеазами, и необязательно осуществление моделирования белков по гомологии для прогнозирования, какие спрогнозированные in silico сайты разрезания протеазой, вероятно, являются экспонированными, и/или необязательно осуществление докинга in silico фрагментов антитела или протеаз для прогнозирования, какие спрогнозированные in silico сайты разрезания, вероятно, будут разрезаны in vitro;
(ii) осуществление протеолитического расщепления указанного белка in vitro одной или более протеазами;
(iii) идентификацию пептидов, высвободившихся из указанного белка в результате протеолитического расщепления in vitro на этапе (ii), и посредством этого -идентификацию сайтов разрезания;
(iv) сравнение спрогнозированных in silico сайтов разрезания, идентифицированных на этапе (i), с сайтами разрезания, идентифицированными на этапе (iii);
(v) исследование одного или более эпитопов в области белка, содержащей или фланкирующей сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii) с помощью одного или более антител; и
(vi) определение того, связывается или нет указанное одно или более антител с указанным одним или более эпитопами, и посредством этого идентификацию эпитопа на белке, с которым может связываться антитело.
В вышеописанном способе (способе В) осуществляют этап расщепления протеазой in silica Однако, в качестве альтернативы, для прогнозирования расщепления белка протеазой можно использовать любой другой способ или методику. Например, аминокислотную последовательность белка можно осмотреть визуально, и спрогнозированные сайты разрезания (т.е. сайты, которые согласно прогнозу будут разрезаны протеазой) можно идентифицировать на основании информации о специфичности данной протеазы и правил. Для прогнозирования расщепления протеазой белка на основании информации о специфичности данной протеазы и правил можно использовать любой способ или методику. Таким образом, согласно некоторым вариантам реализации способа прогнозирование с помощью компьютерных способов не является необходимым, хотя компьютеризированные способы и являются предпочтительными.
Можно использовать любую соответствующую протеазу, и подходящие протеазы описаны в другом месте в настоящей заявке. Таким образом, можно использовать одну или несколько протеаз, как описано в другом месте в настоящей заявке.
Способ необязательно включает осуществление моделирования (например, моделирования in silico), например, моделирования белков, такого как моделирование белков по гомологии, для прогнозирования, какие спрогнозированные in silico сайты разрезания протеазой, вероятно, являются экспонированными (например, экспонированными в раствор или экспонированными на поверхности).
Способ необязательно включает осуществление докинга (или связывания) in silico фрагментов антитела (например, Fab-фрагментов или других фрагментов антитела, описанных в другом месте в настоящей заявке) или протеаз для прогнозирования, какие спрогнозированные in silico сайты разрезания, вероятно, будут разрезаны in vitro. Специалист в данной области техники способен с легкостью осуществить такой анализ докинга или моделирования in silico.
Моделирование (например, моделирование по гомологии) можно осуществить с применением любых подходящих способов, например, модуля моделирования гомологии в программном обеспечении МОЕ (Molecular Operating Environment (МОЕ) 2015. 10. Chemical Computing Group Inc., 1010 Шербрук стрит Вест, офис №910, Монреаль, Квебек, Канада, H3A2R7. 2016).
Для построения и моделирования модели белка и/или для осуществления моделирования белок-белкового докинга (докинга in silico) можно использовать программное обеспечение, такое как программное обеспечение МОЕ. Данное программное обеспечение позволяет прогнозировать конфигурации белок-белкового связывания и может позволить получить состыкованные структуры белков. Таким образом, можно получить модели белков, состыкованных (или связанных) с антителами (или фрагментами антитела) или состыкованных (или связанных) с протеазами.
Согласно предпочтительным вариантам реализации настоящего изобретения протеолитическое расщепление белка in vitro одной или более протеазами представляет собой ограниченный или частичный протеолиз. Ограниченный или частичный протеолиз описан в другом месте в настоящей заявке.
Когда используют несколько протеаз, протеазы, предпочтительно, используют отдельно (например, параллельно).
Идентификацию пептидов (последовательностей пептидов), высвободившихся из указанного белка в результате расщепления протеазой in vitro на этапе описанного выше способа (способа В), можно осуществить любым соответствующим способом или методикой, например, методом масс-спектрометрии (например ЖХ-МС/МС). Идентифицировав пептиды (последовательности пептидов), высвободившиеся из указанного белка, легко идентифицировать сайты, в которых одна или более протеаз разрезали указанный белок (сайты разрезания), поскольку данные о последовательности пептида или пептидов, которые высвободились от белка в результате ограниченного или частичного протеолиза (например, идентифицированные методом масс-спектрометрии), являются источником информации о сайтах разрезания. В этой связи, остатки на концах высвободившегося пептида или пептидов (отщепленных пептидов) являются источником информации о сайте разрезания в белке (например, в нативном или полноразмерном белке).
Этап (v) способа В обозначает исследование одного или более эпитопов в области белка, содержащей или фланкирующей сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii) с помощью одного или более антител. Как очевидно из описания в другом месте в настоящей заявке, и во избежание разночтений отметим, что сайт разрезания (который перекрывается или фланкируется одним или более эпитопами) можно рассматривать как сайт (или положение) в аминокислотной последовательности белка (например, в нативном белке, или полноразмерном белке, или белке дикого типа), соответствующий сайту, который согласно прогнозу будет разрезаться (который идентифицируют) на этапе (i), но который не идентифицируют на этапе (iii).
Исследование одного или более (например, совокупности) эпитопов означает, что один или более эпитопов (или потенциальных эпитопов) на белке (например, нативном или полноразмерном белке) анализируют (или оценивают) в отношении их способности быть связанными антителами, которые были получены против выделенных эпитопов (или связываются с выделенными эпитопами), соответствующих эпитопу (или потенциальному эпитопу) на белке. Согласно предпочтительному варианту реализации исследуют совокупность (или матрицу) эпитопов.
Этап (v) способа В, таким образом, как правило, включает исследование одного или более эпитопов в области нативного белка (или полноразмерного белка, или белка дикого типа), содержащего или фланкирующего сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii) с помощью одного или более антител. В качестве альтернативы, этап (v) способа В, как правило, включает исследование нативного белка (или полноразмерного белка, или белка дикого типа) в области указанного белка, содержащей или фланкирующей сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii) с помощью одного или более антител.
Согласно некоторым вариантам реализации настоящего изобретения способ может дополнительно включать этап (до этапа (v)) образования (или синтеза) одного или более (например, совокупности, например, 2 или более, 3 или более, 5 или более, 10 или более, 20 или более, 50 или более, например, до 3, до 4, до 5, до 10, до 20 или до 50) выделенных эпитопов, последовательности которых соответствуют одному или более эпитопам (или последовательностям) на указанном белке, которые расположены в области белка, содержащей или фланкирующей сайт разрезания (сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii)), и образование (получение) антител (например, поликлональных антител), направленных на выделенные эпитопы или связывающихся с указанными выделенными эпитопами. Согласно предпочтительному варианту реализации настоящего изобретения получают совокупность (или матрицу) эпитопов и получают совокупность (или матрицу) антител. Такие антитела затем можно использовать на этапе (v) описанного выше способа для исследования одного или более эпитопов на указанном белке (например, в нативном или полноразмерном белке). Можно использовать любой соответствующий способ или методику образования выделенных эпитопов или образования антител (например, как описано в другом месте в настоящей заявке), и специалисту известны такие способы и методики.
Согласно некоторым вариантам реализации настоящего изобретения эпитопы характеризуются различными длинами и/или последовательностями. Таким образом, среди совокупности (или группы) эпитопов могут присутствовать эпитопы, которые отличаются друг от друга длинами и/или последовательностями. Согласно другим вариантам реализации настоящего изобретения эпитопы характеризуются одинаковыми (или подобными) длинами и обычно различными последовательностями. Таким образом, согласно некоторым вариантам реализации настоящего изобретения среди совокупности (или группы) эпитопов эпитопы характеризуются одинаковой (или подобной) длиной.
Эпитопы могут характеризоваться любой соответствующей длиной. Согласно некоторым вариантам реализации настоящего изобретения выделенные эпитопы составляют 7-8 аминокислот в длину или характеризуются длиной, как описано в другом месте в настоящей заявке.
Согласно предпочтительным вариантам реализации настоящего изобретения эпитопы содержат сайт разрезания (или перекрываются с сайтом разрезания, или окружают сайт разрезания).
Как правило, эпитопы (или по меньшей мере часть любого данного эпитопа) будут находиться в пределах 50 аминокислот от сайта разрезания (сайта разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii)), т.е. от +50 до -50 аминокислот относительно сайта разрезания. Предпочтительно, эпитопы (или по меньшей мере часть любого данного эпитопа) будут находиться в пределах 20 аминокислот от сайта разрезания (сайта разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii)), т.е. от +20 до -20 аминокислот относительно сайта разрезания, или в пределах 10 аминокислот от сайта разрезания, т.е. от +10 до -10 аминокислот относительно сайта разрезания, или в пределах 5 аминокислот от сайта разрезания, т.е. от +5 до -5 аминокислот относительно сайта разрезания.
Согласно некоторым вариантам реализации настоящего изобретения совокупность эпитопов представляет собой множество (или группу) эпитопов, причем последовательность каждого эпитопа во множестве смещена по сравнению с другим эпитопом во множестве на одну или несколько (например 1, 2 или 3), предпочтительно, одну, аминокислоту. Иными словами, согласно некоторым вариантам реализации настоящего изобретения во множестве (совокупности) эпитопов последовательность каждого эпитопа сдвинута на одну или несколько (например 1, 2 или 3), предпочтительно, одну, аминокислоту относительно последовательности другого эпитопа во множестве. Таким образом, совокупность эпитопов может представлять собой вложенное множество эпитопов, например, как проиллюстрировано на фигуре 16d. Как правило, такое вложенное множество эпитопов будет охватывать до приблизительно 50 аминокислот последовательности белка в любом направлении (или в обоих направлениях) относительно (или в окружении) сайта разрезания (сайта разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii)). Предпочтительно, такое вложенное множество эпитопов будет охватывать до приблизительно 20 аминокислот последовательности белка в любом направлении (или в обоих направлениях) относительно (или в окружении) сайта разрезания (сайта разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii)). Согласно некоторым вариантам реализации настоящего изобретения такое вложенное множество эпитопов будет охватывать до приблизительно 6 аминокислот последовательности белка в любом направлении (или в обоих направлениях, предпочтительно, в обоих направлениях) относительно (или в окружении) сайта разрезания (сайта разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii)).
Когда используют вложенное множество эпитопов, согласно предпочтительным вариантам реализации настоящего изобретения значительное число эпитопов будет содержать сайт разрезания, предпочтительно, по существу все из эпитопов во вложенном множестве будут содержать сайт разрезания, более предпочтительно, все эпитопы во вложенном множестве будут содержать сайт разрезания.
Как описано выше, исследование эпитопов на белке, которые расположены между сайтами разрезания, которые перекрываются с сайтом разрезания или которые расположены в области, фланкирующей сайт разрезания, можно провести с помощью антител, направленных против указанных эпитопов (т.е. антитела выступают в качестве зондов). В действительности, исследование с помощью антител (например, Fab-фрагментов или других фрагментов антитела) является предпочтительным. Однако, в качестве альтернативы, другие связывающие молекулы можно использовать в качестве зондов (например, можно использовать другие аффинные зонды). Антитела представляют собой один из примеров аффинного зонда, который можно использовать.
Предпочтительные белки описаны в другом месте в настоящей заявке.
Согласно другому аспекту, в качестве альтернативы активному осуществлению расщепления протеазой in vitro на этапе (ii) способа В активный этап расщепления белка (этап in vitro) не проводят, вместо этого проводят идентификацию пептидов, высвободившихся из белка, и, таким образом, идентификацию сайтов разрезания на этапе (iii) проводят на основании данных проведенных ранее экспериментов по протеолизу (например, архивных данных, например, данных масс-спектрометрии, содержащих последовательности пептидов, высвободившихся из белка, из предшествующих экспериментов по протеолизу). Однако согласно предпочтительным способам проводят этап активного осуществления расщепления протеазой in vitro (предпочтительно, ограниченного или частичного протеолиза).
Согласно одному аспекту в настоящем изобретении предложен эпитоп (или антигенный эпитоп), например, выделенный эпитоп, идентифицированный способом идентификации эпитопа, с которым может связываться антитело, на белке, как описано выше (способ В). Согласно одному аспекту в настоящем изобретении предложено антитело, которое связывается с таким эпитопом на белке. Согласно некоторым вариантам реализации антитела, которые связываются в непосредственной близости от сайта разрезания, как описано в настоящей заявке, например, в пределах 5, 10, 20 или 50 аминокислот от сайта разрезания, являются предпочтительными. Специалисту в данной области техники известны способы или методики создания эпитопов (например, выделенных эпитопов) и антител против данных эпитопов, и можно использовать любой соответствующий способ (например, как описано в другом месте в настоящей заявке). Предпочтительные типы антител также описаны в другом месте в настоящей заявке.
Согласно одному аспекту в настоящем изобретении предложено антитело, которое связывается с эпитопом на белке, содержащем или фланкирующем (предпочтительно, содержащем) сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, но который не является сайтом разрезания, идентифицированным посредством протеолиза in vitro (например, ограниченного или частичного протеолиза).
Антитела (например, панель, или матрицу, или большое число антител), нацеленные на эпитопы (предпочтительно, совокупность эпитопов) на белке, можно исследовать в отношении их способности связываться с белком, например, для оценки их аффинности связывания или другого функционального эффекта (например, как описано в другом месте в настоящей заявке) в отношении белка. Таким образом, можно провести скрининг антител для идентификации антител, которые связываются наилучшим образом. Таким образом, можно идентифицировать в особенности подходящие эпитопы (например, для нацеливания на них антител), например, эпитопы, которые являются в особенности подходящими для нацеливания на них высокоаффинных антител или нацеливание на которые приводит к значительному или измеряемому функциональному эффекту в отношении белка-мишени (например, антагонистическому или агонистическому эффекту). Соответственно, можно идентифицировать оптимальные эпитопы (например, для нацеливания на них антител). Таким образом, в качестве альтернативы, в настоящем изобретении предложен способ оптимизации дизайна эпитопа или выбора оптимального эпитопа (например, для антител, которые получают против данного эпитопа или которые нацелены на данный эпитоп). Способ может позволить определять оптимальную длину и положение эпитопа относительно сайта разрезания.
Согласно некоторым вариантам реализации настоящего изобретения способ (способ В) также включает этап образования (или получения, или продуцирования) антитела против эпитопа, идентифицированного способом В (идентифицированного на этапе (vi)), или которое связывается с указанным эпитопом. Необязательно можно осуществить следующий этап приготовления антитела в состав с по меньшей мере одним фармацевтически приемлемым носителем или вспомогательным веществом.
Таким образом, согласно одному аспекту в настоящем изобретении предложен способ получения или изготовления антитела, которое связывается с эпитопом, идентифицированным способом В (идентифицированным на этапе (vi)). Необязательно можно осуществить следующий этап приготовления указанного полученного или изготовленного антитела в состав с по меньшей мере одним фармацевтически приемлемым носителем или вспомогательным веществом. Способы получения или изготовления антител описаны в другом месте в настоящей заявке и применимы с соответствующими изменениями к данному аспекту настоящего изобретения.
Согласно одному аспекту в настоящем изобретении предложен конъюгат, содержащий по меньшей мере один эпитоп, идентифицированный способом В, присоединенный к пептидному носителю или смешанный с ним. Конъюгаты описаны в другом месте в настоящей заявке, и указанное обсуждение применимо с соответствующими изменениями к данному аспекту настоящего изобретения.
Антитела, которые связываются с эпитопами, идентифицированными способом В (или эпитопами, идентифицированными способом В, или конъюгатами, содержащими такие эпитопы), можно использовать в терапии.
Способ В можно использовать для идентификации доступных для протеазы/разрезаемых протеазой, но не высвобождающихся эпитопов на поверхности белков. В способе можно применять алгоритмы поиска на основании расщепления протеазой in silico и моделирование по гомологии (например, гомологии связывания Fab-протеаза с белком-мишенью) с целью предсказания сайтов разрезания протеазой на поверхности белка. В способе применяют расщепление протеазой in vitro, необязательно с применением нескольких протеаз (например, параллельно). В способе можно применять микрожидкостную платформу для расщепления. Для идентификации пептидов, высвобождаемых протеазами из белка-мишени, можно использовать масс-спектрометрию (МС), предпочтительно, ЖХ-МС/МС. Определенные экспериментальным путем сайты разрезания выясняют на основании пептидных карт, например, получаемых методом МС. Спрогнозированные in silico сайты разрезания на поверхности белков можно сравнить с наблюдаемыми в эксперименте сайтами разрезания. Спрогнозированные in silico сайты разрезания, которые не наблюдаются в эксперименте, можно исследовать с применением антител против последовательностей, охватывающих сайты разрезания (например, от -20 до +20 аминокислот, окружающих сайты разрезания). Антитела можно классифицировать в зависимости от силы связывания (например, аффинности) и/или активности (например, антагонистического или агонистического эффекта в отношении белка-мишени). Антитела можно изучить в отношении связывания с нативным белком и расщепленным белком. Если связывание антитела с сайтом разрезания достигается как для нативного белка, так и для расщепленного белка, можно сделать заключение, что протеаза не разрезает в данном сайте. Если, напротив, антитело связывается с нативным белком, но не с расщепленным белком, можно сделать заключение, что сайт был действительно расщеплен протеазой in vitro, но высвобождение пептидов невозможно обнаружить. Это позволяет предположить, что антитело не может связываться с последовательностью, о которой идет речь, после ее разрезания.
Целью данного способа является идентификация сайтов связывания антитела и/или установление структуры белка с применением новых процедур и алгоритмов, в которых антитела используют для идентификации доступных для протеазы/разрезаемых протеазой, но не высвобождающихся эпитопов. Способ основан на расщеплении in silico и необязательно на моделировании структуры белка и/или имитации докинга фрагментов антитела (например, Fab-фрагментов) и/или протеазы для нацеливания на белки. Можно использовать мультижидкостное расщепление несколькими протеазами (например, несколько протеаз, применяемых параллельно, как описано в другом месте в настоящей заявке) с обнаружением методом МС-МС. Процедуры делают возможным обнаружение уникальных и новых сайтов связывания антитела и могут позволить получить новые структурные данные для нативных, а также частично расщепленных белков.
Оценка протеолиза с применением масс-спектрометрии основывается на высвобождении пептидов из белка, т.е. на том, что протеазы разрезают в двух сайтах, окружающих последовательность правильного размера, для обнаружения методом масс-спектрометрии. Однако некоторые области в белке, представляющие интерес, могут не удовлетворять данным критериям. Протеаза может разрезать только один сайт, создавая разрыв, но не высвобождая пептид. Для высвобождения пептида необходимо два разреза. Поскольку пептид не высвободился, вследствие этого отсутствует основанное на МС доказательство события связывания или протеолитической активности. Один разрез остается необнаруженным. Другие причины необнаружения могут включать гликозилирование на пептиде или то, что пептид остается связанным с белком ионными или ковалентными связями. Один из путей обхода данной проблемы заключается в создании антител против последовательностей, в которых расположен такой сайт разрезания. Принимая во внимание в высокой степени подобные размеры Fab-области антитела и протеазы (фигура 1), протеазы могут быть подходящими для исследования поверхности в отношении сайтов связывания антитела, и наоборот.
Если связывание антитела подтверждено для сайта в нативном белке, тогда будет известно, что, на основании подобия размера протеаза тоже должна связываться в этом месте. Если провести тот же анализ связывания антитела в отношении расщепленного белка, отсутствие связывания с сайтом после протеолиза будет свидетельствовать, что последовательность-мишень была действительно разрезана, поскольку специфичный эпитоп, который распознает антитело, был уничтожен протеазой.
Рабочий процесс для идентификации молчащих, необнаруженных сайтов разрезания представлен на фигуре 16.
Авторы настоящего изобретения использовали расщепление последовательности белка in silico с применением одной или более различных протеаз. При этом принимали во внимание специфичность протеазы и правила, например, трипсин будет разрезать только по аргинину или лизину в С-концевом положении. Правила и исключения при расщеплении для большинства протеаз известны, см., например, компьютерную программу Peptidecutter (Expasy, SIB, Swiss Institute of Bioinformatics, Швейцарский институт биоинформатики). Таким образом, для осуществления расщепления протеазой in silico можно использовать компьютерные программы, такие как Peptidecutter. Затем с применением моделирования (например, моделирования белков по гомологии) можно необязательно оценить, какие сайты разрезания будут, вероятно, экспонированы в раствор, и посредством сочетания данного этапа с докингом фрагментов антитела in silico (например, Fab-фрагментов) или протеаз вдоль поверхности можно предсказать, какие сайты разрезания, вероятно, будут расщеплены in vitro (фигура 16а). Модели гомологии можно получить с применением сверхгибкого и прозрачного модуля моделирования гомологии в программном обеспечении МОЕ (Molecular Operating Environment (МОЕ) 2015. 10. Chemical Computing Group Inc., 1010 Шербрук стрит Вест, офис №910, Монреаль, Квебек, Канада, Н3А 2R7. 2016). Например, модель гомологии TRPV1 человека можно сконструировать с применением структур TRPV1 крысы, полученных методом криоэлектронной микроскопии (делеционные мутанты, учетные записи PDB 3J5P29 и 5IRZ30). На основании данных структур и с использованием МОЕ авторы настоящего изобретения сконструировали модель гомологии TRPV1 человека для применения в способе разработки.
После предсказания сайтов разрезания протеазой, например, сайтов разрезания протеазой на поверхности, проводят эксперименты по протеолизу in vitro. В случае мембраносвязанных белков протеолипосомы, содержащие нативный белок, можно расщепить в микрожидкостной проточной ячейке (LPI, Nanoxis Consulting АВ). Технология проточной ячейки обеспечивает возможность проведения гибкой химии, такой как ограниченный протеолиз, на мембранных белках, содержащихся в неподвижной фазе (Jansson ЕТ, Trkulja CL, Olofsson J, et al. Microfluidic flow cell for sequential digestion of immobilized proteoliposomes. Anal Chem. 2012; 84(13):5582-5588), которые можно подвергнуть воздействию нескольких раундов растворов и различным типам химических модуляций, например, с помощью ферментов. Клеточные мембраны можно вывернуть наизнанку, и как внутриклеточные, так и внеклеточные домены пронизывающих мембрану белков можно подробно исследовать напрямую. Растворимые белки можно подвергнуть ограниченному протеолизу с применением стандартных методик в растворе.
Можно использовать несколько протеаз с различными специфичностями в параллельных реакциях с целью охвата как можно большего числа последовательностей. Ограничивающие условия уже установлены, например, для ограничения протеолиза поверхностью белка можно использовать концентрации протеазы в диапазоне 2-5 мкг/мл и 5 минут расщепления (фигура 16b). Другие ограничивающие условия (условия ограниченного или частичного протеолиза) обсуждаются в другом месте в настоящей заявке, и согласно данному аспекту (способу В) можно использовать любые из них. Высвободившиеся пептиды можно идентифицировать методом масс-спектрометрии (например, ЖХ-МС/МС), предпочтительно, с применением масс-спектрометра с высоким разрешением (например, Q Exactive, Thermo Fisher) и идентификации пептидов/белков в базе данных Mascot. Затем, получив пептидные карты, можно определить, какие сайты разрезания являлись физически доступными для протеаз.
С целью точного определения сайтов, которые являются доступными для протеазы/разрезаемыми протеазой, но не высвобождаются, авторы настоящего изобретения сравнивали подтвержденные экспериментальным способом сайты разрезания с перечнем спрогнозированных сайтов, и выбирали те спрогнозированные сайты, которые отсутствовали в данных МС (фигура 16с). Последовательности пептидов, предпочтительно, составляющие 7-8 аминокислот в длину, содержащие данные сайты, можно синтезировать и применять для получения поликлональных антител (ПАТ). Причина выбора длины заключается в том, что последовательность-мишень необходимо минимизировать для минимизации поликлональности ПАТ, но данная последовательность не должна быть настолько короткой, чтобы стать слабо иммуногенной.
Сдвиги рамки на одну аминокислоту можно использовать для выбора линейных последовательностей данной длины в пределах установленного расстояния на каждой стороне сайта разрезания (например, 6 аминокислот). После этого данные последовательности можно использовать для создания матрицы нацеленных на последовательность ПАТ, скрининг которых можно затем провести в отношении связывания с нативным интактным белком с применением, например, метода ELISA.
Подтвержденные события связывания показывают, что сайт является доступным для антитела, и вследствие этого должен быть также доступен для протеазы, и наоборот. Затем полученные результаты позволяют предположить, что протеаза должна разрезать в данном сайте, но пептид не высвобождается. Подтверждение можно обеспечить с применением в отношении расщепленного белка той же матрицы антител, причем снижение связывания с сайтом разрезания подтверждает, что произошел протеолиз (фигура 16е). Это позволяет предположить, что антитело не связывается с разрушенной последовательностью, но, как правило, антитела являются в высокой степени специфичными в отношении конфигурации аминокислот, используемой в качестве эпитопа.
Данная методология характеризуется потенциалом применения не только для определения разрезов протеазы, но также в качестве инструмента для обнаружения усечений или вырезаний и утраты локальной структуры домена. Подтверждение усечения будет подходящим, когда данное усечение нельзя оценить с применением масс-спектрометрии, например, поскольку высвободившаяся последовательность слишком коротка или длинна для обнаружения методом МС, или если пептид содержит гликозилирование, или остается связанным с белком посредством одной или более ионных либо ковалентных связей. Авторы настоящего изобретения соотнесли вырезание пептидов с функциональными анализами для TRPV1. Также с применением данных антител можно исследовать изменения локальной структуры, вызванные связыванием лиганда или белок-белковым взаимодействием. Антитела, полученные данным способом, можно также использовать в качестве нацеленных на последовательность функциональных антител для терапевтического применения.
Во избежание разночтений отметим, что в способах согласно настоящему изобретению не обязательно использовать алгоритмы поиска, однако такие алгоритмы можно использовать. Например, можно использовать алгоритмы, которые анализируют (или обрабатывают) один или более наборов данных in silico (например, данных о расщеплении протеазой in silico, и/или данных моделирования гомологии белков, и/или данных о структуре и функции белка, причем данные о структуре и функции содержатся в компьютерной модели (или предсказаны посредством компьютерной модели)), один или более наборов данных о гомологичном связывании Fab-протеаза (например, полученных посредством белок-белкового докинга in silico), одной или более других моделей белок-белкового докинга in silico (таких как модели докинга белок-антитело, модели докинга белок-фрагмент антитела и/или модели докинга белок-протеаза), и/или один или более наборов данных о расщеплении протеазой (например, расщеплении несколькими протеазами) (например, данных масс-спектрометрии). Алгоритм поиска может сочетать и обрабатывать входящие данные из одного или более различных наборов данных с целью обнаружения (или предсказания) областей структуры белка, которые являются функционально доступными для антитела и функционально значимыми с точки зрения функции белка (например, изменение в данной области изменит функцию белка).
Предпочтительные свойства других способов, описанных в настоящей заявке, можно применять с соответствующими изменениями к данному аспекту настоящего изобретения (способу В).
Согласно вариантам реализации настоящего изобретения, в которых применяют несколько протеаз, соответствующие примеры описаны в другом месте в настоящей заявке. Согласно некоторым вариантам реализации настоящего изобретения предпочтительные протеазы представляют собой одну или более протеаз, выбранных из группы, состоящей из трипсина, Asp-N, химотрипсина, пепсина, протеиназы K, Lys-C, Arg-C, клострипаина, глутамилэндопептидазы, Lys-N и термолизина, или включающей указанные протеазы.
Другие свойства и преимущества настоящего изобретения станут очевидными на основании примеров, представленных ниже. Приведенные примеры иллюстрируют различные компоненты и методологии, пригодные при реализации настоящего изобретения на практике. Примеры не ограничивают заявленное изобретение. На основании представленного описания изобретения специалист может обнаружить и применять другие компоненты и методологию, пригодные для реализации настоящего изобретения на практике.
ПРИМЕРЫ
ПРИМЕР 1
В данном примере описан эффективный подход, с помощью которого авторы настоящего изобретения обнаружили и разработали поликлональное антитело OTV1, действующее на внутриклеточной стороне ионного канала TRPV1 человека, на основе предложенного изобретения, включая способы. Антитело является фармакологически активным и демонстрирует мощное ингибирующее действие в отношении белка при стимуляции агонистом капсайцином. Насколько известно авторам настоящего изобретения, впервые было обнаружено ингибиторное антитело, нацеленное на внутриклеточные домены TRPV1. Это подтверждает, что данная идея характеризуется высокой вероятностью использования, и что даже лучшие и оптимизированные антитела можно идентифицировать, если будет доступна исходная матрица эпитопов, полученных из гораздо более богатого набора данных от множества протеаз. Антитело было выбрано из множества совпадений при поиске после ограниченного протеолиза и биоинформационного анализа. Сначала было выбрано антитело, после чего было продемонстрировано убедительное доказательство его эффективности. Данный подход представляет собой значительное достижение и дополняет имеющиеся на сегодняшний день попытки идентификации антитела, ведь в данном подходе отсутствует необходимость в этапе скрининга, поскольку подход непосредственно приводит к идентификации уникальных эпитопов, которые могут стать мишенями фармакологически активного антитела.
Область-мишень эпитопа выбирали на основании ограниченного расщепления белка-мишени с использованием оптимизированных протоколов на микрожидкостной платформе LPI и дополнительно оптимизировали. Поликлональное антитело было создано посредством модификации пептидного эпитопа-мишени остатком цистеина и присоединения к последнему гемоцианина фисуреллы (KLH). Получение специфичного антитела проводили посредством иммунизации специфичных свободных от патогенной флоры (СПФ) кроликов после инъекции KLH с присоединенным специфичным пептидом. Антитела очищали и подвергали анализу методом ELISA (enzyme-linked immunosorbent assay, твердофазного иммуноферментного анализа) согласно стандартным протоколам. Титр антитела против линейного эпитопа определяли методом ELISA, что привело к определению концентрации 0,25 мкг/мл. Эффективность антитела против нативного TRPV1 исследовали методом пэтч-кламп «наружная сторона внутри», в котором внутриклеточную сторону TRPV1 можно экспонировать в раствор антитела. Анализ методом «наружная сторона внутри» проводили с использованием микрожидкостного устройства для анализа методом пэтч-кламп (Dynaflow, Cellectricon АВ, Гетеборг, Швеция). Амплитуды тока измеряли посредством воздействия на фрагменты, содержащие несколько ионных каналов, капсайцином с антителом и без антитела. На контроли воздействовали 1 мкМ капсайцина в течение 30 с с последующим воздействием буфером в течение 70 с, а затем снова воздействовали 1 мкМ капсайцина в течение 30 с. На обработанные антителом фрагменты воздействовали 1 мкМ капсайцина в течение 30 с с последующим воздействием 0,14 мг/мл антитела в течение 70 с, а затем воздействовали 1 мкМ капсайцина вместе с 0,14 мг/мл антитела в течение 30 с. Для всех измерений активность антитела сравнивали с активностью после воздействия исключительно буфера с целью исключить любые эффекты десенсибилизации или потенцирования. Рассчитывали проинтегрированные площади ток - время, и соотношение между проинтегрированными площадями для второго и первого тока рассчитывали и сравнивали между обработками. В случае клеток, обработанных антителом, наблюдалось уменьшение ответа тока на 50% по сравнению клетками, с обработанными исключительно буфером (фигура 3). Статистическую значимость рассчитывали с помощью t-критерия Стьюдента (р>0,05).
ПРИМЕР 2
Рынок терапевтических МАТ быстро растет и, согласно прогнозу, в 2020 году его объем составит приблизительно 125 миллиардов долларов США. Новые МАТ непрерывно получают регуляторное одобрение, и на сегодняшний день интенсивно обсуждаются МАТ на иммунной основе, такие как ингибиторы PD1, поскольку данные МАТ значительно улучшают исходы при определенных типах сложных метастатических вариантов рака. Однако обнаружение новых антител для терапевтических целей основано, главным образом, на скрининге и проводится вслепую. Основное внимание уделяют аффинности, а затем подмножество антител, демонстрирующих хорошие характеристики связывания, исследуют для определения биологических эффектов. Детали относительно взаимодействия связывания, антигенных детерминант и механизмов действия остаются неизвестными.
Авторы настоящего изобретения представляют способ, который позволяет выбирать эпитопы антигена на основании ограниченного протеолитического кинетического воздействия с использованием подхода на основе микрожидкостных технологий и масс-спектрометрии. Протеолитический этап проводят настолько медленно, что после воздействия протеазы в данный момент времени от антигена отрывается один или несколько пептидов. Пептиды, которые появляются первыми, являются легкодоступными для ПАТ (поликлональных антител) или МАТ, и вследствие этого являются предпочтительными по сравнению с пептидами, которые появляются позже и находятся в более труднодоступных областях белка. Затем данные пептиды классифицируют и перекрестно соотносят для определения функциональной значимости на основании последовательности с использованием специально подобранных биоинформационных данных. Пептиды высокого класса, быстро поступающие от белка-мишени, также обладающие функциональной значимостью, используют для разработки эпитопа, иммунизации и последующего создания антитела. Усеченные белки также можно использовать для фармакологического исследования. Данный способ основан на информации, полученной на основании последовательности, и представляет собой фармакологический, основанный на механизме действия подход для обнаружения антитела, который можно использовать как для внутриклеточных, так и для циркулирующих и внеклеточных мишеней. Авторы настоящего изобретения использовали данный способ для разработки двух антител: активирующего, нацеленного на кальмодулин-связывающую последовательность, и ингибиторного, нацеленного на сайт связывания капсайцина на N-конце внутриклеточной области ионного канала TRPV1 человека.
Двумя важными параметрами при разработке терапевтических антител являются аффинность связывания и биологическая эффективность. Антитела представляют собой большие белки молекулярной массой приблизительно 150 кДа и связываются в первую очередь с антигенными сайтами, расположенными на поверхности белка. Локализация аминокислот в непосредственной близости от поверхности структур нативного белка может направлять идентификацию и прогнозирование данных сайтов. Авторы настоящего изобретения использовали ограниченный протеолиз для анализа экспонирования на поверхности и гибкости белка. В данном способе активность протеазы ограничена контролем температуры, концентрации и/или времени расщепления. В таких условиях будут расщепляться исключительно гибкие области, которые могут локально разворачиваться и обеспечивать размещение протеазы, экспонированные на поверхности области и области с несколькими локальными взаимодействиями, такими как водородные связи и дисульфидные мостики. Авторы настоящего изобретения последовательно использовали несколько протеаз с целью увеличить до максимума поиск структурной информации. Области, которые легко расщепляются несколькими протеазами, должны располагаться в наиболее экспонированных, наиболее доступных областях белка и должны характеризоваться высокой пригодностью для последующей разработки антитела. Области, которые расщепляются исключительно одной протеазой, вероятно, расположены в скрытой области белка, и являются менее доступными. В таких случаях физико-химические свойства протеазы, способность достигать и расщеплять данные области может потенциально направлять разработку антитела. Авторы настоящего изобретения классифицировали отщепленные пептиды на основании простоты их отщепления в зависимости оттого, какие параметры использовали для ограничения протеолиза. Данные параметры могут представлять собой временную точку, в которую были отщеплены пептиды, использованную концентрацию или температуру. Затем пептиды, полученные в результате расщепления каждой протеазой, соотносили друг с другом с целью обнаружения пептидов, происходящих из наиболее доступных областей белка.
В процессе общепринятой разработки антител биологическую эффективность, как правило, исследуют и подтверждают после положительного связывания между антителом и антигеном. Авторы настоящего изобретения считают, что ранний механистически управляемый подход будет полезным при разработке антитела благодаря фокусированию иммунизации на доступных сайтах в биологически активном сайте или в непосредственной близости от указанного сайта вместо создания антител, нацеленных на все возможные антигенные сайты. Данный подход минимизирует процедуры скрининга, а также риск необходимости оптимизации антител, которые обладают высокой аффинностью связывания с областями, отдаленными от биологически активного сайта. Целью авторов настоящего изобретения был поиск доступных эпитопов, которые также обладают функциональной важностью в отношении белка-мишени. Данного результата достигли посредством соотнесения классифицированных пептидов после ограниченного протеолиза с биоинформационными данными.
Авторы настоящего изобретения продемонстрировали свой механистически управляемый подход с использованием в качестве модельного белка ионного канала TRPV1 человека. TRPV1 представляет собой ионный канал, чувствительный к вредным стимулам, таким как низкий уровень рН, высокая температура (Т>42°С), капсайцин и некоторые воспалительные медиаторы. Ионный канал TRPV1, главным образом, расположен в ноцицептивных нейронах периферической нервной системы и организован в тетрамерную конформацию. Каждый из четырех мономеров данного канала состоит из шести трансмембранных областей, N- и С-концы которых обращены к внутриклеточной стороне плазматической мембраны. Область поры состоит из 5ой и 6ой трансмембранных областей. Внутриклеточная часть TRPV1 содержит множество регуляторных областей, важных для тепловой активации, сенсибилизации и десенсибилизации.
Создание эпитопа
Протеолипосомы, содержащие TRPV1, получали из клеток СНО и подвергали ограниченному протеолизу в проточной ячейке LPI с использованием трипсина и Asp-N по отдельности. Активность протеаз ограничивали до такой степени, что отщеплялось исключительно несколько пептидов, с применением комнатной температуры и низких концентраций. Затем отщепленные пептиды обнаруживали методом жидкостной хроматографии с тандемной масс-спектрометрией (ЖХ-МС/МС). Три пептида были обнаружены после протеолиза трипсином, и один пептид - после протеолиза Asp-N. Пептиды сравнивали с известными функциональными данными, и несколько пептидов соотносились с функционально важными областями, перечисленными в таблице 1. Для последующей разработки антитела были выбраны два пептида, аа96-117 и аа785-799, названные OTV1 и OTV2, соответственно. Визуализация эпитопов в структуре TRPV1 представлена на фигурах 4 и 5. Последовательность пептида OTV1 содержит arg115 (arg114 в случае rTRPVI), который, как было показано, является важным для активации капсайцином или протонами. Обе протеазы расщепляли области в непосредственной близости от данной аминокислоты, что подтверждало вероятность того, что в третичной структуре белка данная область является экспонированной. Последовательность пептида OTV2 содержит сайт связывания кальмодулина аа786- аа798 (аа785-аа797 в случае rTRPV1) и расщепляется исключительно трипсином. Сайты расщепления Asp-N, который отщепляет Asp и Cys с N-концевой стороны, в данной части TRPV1 отсутствовали. Синтетические пептиды аа96-117 и аа785-799 связывали с гемоцианином фисуреллы (KLH), а затем использовали для получения поликлональных антител посредством иммунизации кроликов после инъекции пептидов, связанных с KLH. Полученные антитела демонстрируют тенденцию к агрегации в процессе замораживания и со временем в растворе. Вследствие этого свежеоттаянные антитела перед применением подвергали кратковременной обработке ультразвуком, и все эксперименты проводили в течение 30 минут после кратковременной обработки ультразвуком.
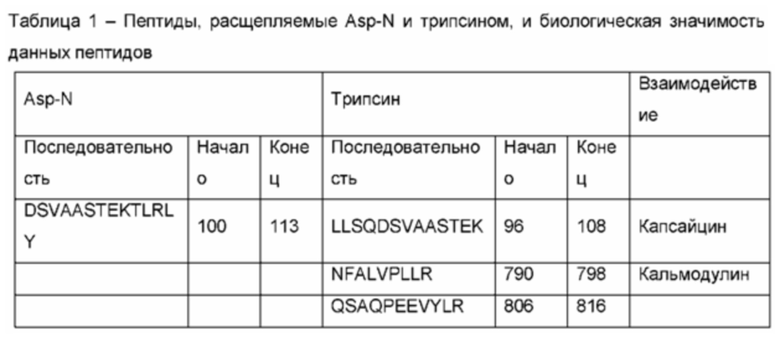
Иммуноцитохимия
Исследование методом иммуноцитохимии проводили с целью визуализации распределения антитела в клетках СНО, экспрессирующих TRPV1 (фигура 6). Неиндуцированные клетки выступали в качестве контроля неспецифичного связывания. Клетки фиксировали и окрашивали OTV1 или OTV2 с последующим окрашиванием вторичным антителом козы против иммуноглобулинов кролика Alexa 488. Четкое окрашивание плазматической мембраны, которое было видимым исключительно в индуцированных клетках, наблюдали как в случае OTV1, так и в случае OTV2. Неспецифичное связывание вторичного антитела являлось незначительным (данные не показаны).
Электрофизиология
Функциональный эффект OTV1 на индуцированную капсайцином активность TRPV1, а также эффект OTV2 на кальмодулин/Са2+-зависимую десенсибилизацию оценивали с использованием анализа методом пэтч-кламп «наружная сторона внутри». Фрагменты мембраны, содержащие несколько ионных каналов, вырезали из клеток СНО, делая возможным воздействие антитела на внутриклеточные области TRPV1. В случае OTV1 TRPV1 активировали капсайцином, затем обрабатывали OTV1, после чего следовала активация капсайцином в присутствии OTV1. Контроли активировали капсайцином, обрабатывали буфером и снова активировали капсайцином. Наблюдали уменьшение опосредованных капсайцином токов на 50% при сравнении обработки OTV1 с обработкой исключительно буфером (фигура 7). Исследовали способность OTV2 препятствовать кальмодулин/Са2+-зависимой десенсибилизации. TRPV1 активировали капсайцином, затем обрабатывали кальмодулином, Са2+ и OTV2, после чего следовала активация капсайцином в присутствии кальмодулина, Са2+ и OTV2. Контроли активировали капсайцином, обрабатывали кальмодулином и Са2+ и активировали капсайцином в присутствии кальмодулина и Са2+. Кальмодулин десентизировал TRPV1 в присутствии кальция. Обработка OTV2 уменьшала данный эффект на 45% (фигура 7).
Анализ опосредованного TRPV1 поглощения YO-PRO
Эффективности антител в цельных клетках исследовали с использованием электропорации в качестве способа доставки с последующим измерением опосредованного TRPV1 поглощения YO-PRO методом лазерной сканирующей конфокальной микроскопии. Клетки подвергали электропорации с использованием системы трансфекции Neon (Life Technologies) в присутствии OTV1, OTV2 или буфера. На клетки, которые подвергали электропорации с использованием OTV1 или буфера, воздействовали капсайцином и YO-PRO в ФБР (фосфатном буферном растворе), содержащем хелатор кальция. Затем контролировали внутриклеточное увеличение флуоресценции в связи с опосредованным TRPV1 поглощением YO-PRO. Наблюдали уменьшение степени поглощения на 60% в случае клеток, обработанных OTV1, в течение первых 12 с активации, и наибольшая скорость поглощения в случае клеток, обработанных OTV1, наблюдалась через 20 с по сравнению с 8 с в случае контроля (фигура 8). Клетки, которые подвергали электропорации с использованием OTV2 или буфера, подвергали воздействию капсайцина и YO-PRO в ФБР, содержащем кальций, опираясь на десенсибилизацию посредством эндогенного кальмодулина, который запускался наносимым кальцием. В случае клеток, обработанных OTV2, наблюдали увеличение скорости поглощения на 80% через 15 с активации. Интернализацию антител в результате электропорации валидировали с использованием метода иммуноцитохимии (фигура 9).
Авторы настоящего изобретения разработали микрожидкостный способ создания антитела, который позволяет определять местонахождение экспонированных и доступных антигенных сайтов в функционально важных областях белка-мишени и/или в непосредственной близости от указанных областей. Доступные области исследуют с использованием частичного с кинетической точки зрения протеолиза в проточной ячейке LPI. Белок-мишень поддерживают в нативном состоянии, при этом сложность его окружения можно тщательно контролировать, например, посредством присутствия кофакторов. Данный подход позволяет получить лучшее понимание доступности антигенных сайтов по сравнению с анализами связывания с использованием очищенных белков. Способ хорошо подходит для трансмембранных мишеней, которые в противном случае сложно очистить и использовать в анализах связывания без добавления детергентов. При использовании данного подхода мишенями могут выступать как внутриклеточные, так и внеклеточные домены.
Информация о расположении антигенного сайта, а также его биологической функции имеет огромное значение для прогнозирования и оценки неспецифичного связывания и перекрестной реактивности с другими белками. Эпитопы, расположенные в очень консервативных областях, можно исключить из анализа потенциальных эпитопов-кандидатов с целью минимизации перекрестной реактивности.
Антитела, разработанные в настоящей заявке, являются поликлональными, несмотря на то, что не были получены в результате иммунизации целым белком. Предложенный способ совместим с общепринятыми протоколами получения моноклональных антител с использованием гибридом и последующими процедурами скрининга. Использование поликлональных антител в качестве первого этапа экспериментальной валидации биологической эффективности для нескольких многообещающих эпитопов-кандидатов с последующим получением моноклональных антител с использованием наилучшего эпитопа/эпитопов и процедуры скрининга для выявления высокой аффинности связывания объединяет лучшее от двух подходов.
Подтверждение интернализации антитела
Интернализацию антител посредством электропорации валидировали через 24 часа после электропорации методом иммуноцитохимии. Клетки подвергали электропорации в присутствии 0,14 мг/мл OTV1 или 0,27 мг/мл OTV2 в ФБР. Затем электропорированные клетки культивировали в течение 24 часов в чашках со стеклянным дном (Willco wells). Готовили два различных контроля. Один контроль не подвергали электропорации, но на всех остальных этапах обрабатывали эквивалентным способом и подвергали воздействию тех же растворов антитела; второй контроль не подвергали воздействию OTV1 и OTV2. Последний использовали, чтобы количественно подсчитать неспецифичное связывание вторичного антитела. Через 24 часа культивирования клетки тщательно промывали ФБР для удаления каких-либо остатков антител, которые в противном случае могли поступить в клетки в течение фиксации. Затем клетки фиксировали и пермебеализовали с использованием набора для фиксации и пермебеализации Image-iT® (Invitrogen). Фиксированные и пермебеализованные клетки инкубировали с вторичным антителом козы против иммуноглобулинов кролика Alexa 488 (Invitrogen) в течение 30 мин. при комнатной температуре. Клетки визуализировали после этапа финальной промывки, и сравнивали интенсивности флуоресценции в случае клеток, которые подвергали электропорации, клеток, которые не подвергали электропорации, и клеток, которые подвергали воздействию исключительно вторичных антител (фигура 9). Наблюдали очевидное различие в значениях интенсивности между клетками, которые подвергали электропорации, и клетками, которые не подвергали электропорации. Статистический анализ проводили с применением t-критерия Стьюдента, и р<0,05 считали статистически значимым. В клетках, которые подвергали электропорации, были обнаружены низкие уровни первичных антител, которые, вероятно, представляют собой остаточные антитела, поступившие в течение фиксации и пермебеализации.
Авторы настоящего изобретения в настоящей заявке предложили способ создания высокоаффинных биологически активных антител с применением комбинации микрожидкостных технологий и ограниченного протеолиза. Способ валидировали с использованием ионного канала TRPV1 человека, и были разработаны два антитела. Оба антитела вызывали прогнозируемое изменение ответа TRPV1 на основании функциональной важности соответствующей области эпитопа указанных антител.
Материалы и методы
Химические реактивы
Среду для культивирования клеток (DMEM/среду Хэма F12 с глутамином), эмбриональную телячью сыворотку и аккутазу заказывали в компании РАА. Зеоцин, Na4BAPTA, K4ВАРТА и вторичное антитело козы против иммуноглобулинов кролика Alexa 488 заказывали в компании Invitrogen. Модифицированный трипсин степени чистоты для секвенирования и Asp-N степени чистоты для секвенирования заказывали в компании Promega. Все другие химические реактивы заказывали в компании Sigma. Использовали следующие буферы: А: 300 мМ NaCl, 10 мМ Tris, рН 8,0, В: 20 мМ NH4HCO3, рН 8,0. С: 140 мМ NaCl, 5 мМ KCl, 1 мМ MgCl2 10 мМ HEPES, 10 мМ D-глюкоза, 10 мМ Na4BAPTA рН 7,4, D: 140 мМ NaCl, 2,7 мМ KCl, 10 мМ Na2HPO4, 10 мМ K4ВАРТА рН 7,2, Е: 140 мМ NaCl, 2,7 мМ KCl, 10 мМ Na2HPO4, рН 7,2. F: 140 мМ NaCl, 2,7 мМ KCl, 10 мМ Na2HPO4, рН 7,4. G: 120 мМ KCl, 2 мМ MgCl2, 10 мМ HEPES, 10 мМ K4ВАРТА рН 8,0
Культура клеток
Адгерентные клетки яичников китайского хомячка (СНО) с регулируемой тетрациклином системой экспрессии (T-REx) культивировали в среде (DMEM/F12 с глутамином) с добавлением 10% эмбриональной телячьей сыворотки, зеоцина (350 мкг/мл) и бластицидина (5 мкг/мл) в культуральных колбах или культуральных чашках (Nunc) со стеклянными пластинами и без таковых. За 18-24 часа до применения клетки инкубировали в среде (DMEM/F12 с глутамином) с добавлением 10% эмбриональной телячьей сыворотки и доксициклина (1 мкг/мл) с целью индукции экспрессии TRPV1 человека. Линию клеток исследовали общепринятым способом для инфицирования микоплазмой.
Получение протеолипосом
Протеолипосомы получали, как описано ранее в публикации [1], в буфере А. Каждый препарат протеолипосом происходил из нескольких различных культуральных колб.
Протоколы расщепления
Однократные расщепления в проточной ячейке проводили, как описано в публикации [1]. 5 мкг/мл трипсина и 5 мкг/мл Asp-N растворяли в буферах G и В, соответственно. Расщепления в проточной ячейке каждой протеазой проводили при комнатной температуре в течение 5 мин. Последующие расщепления в элюатах ингибировали добавлением муравьиной кислоты до конечной концентрации 12%.
Жидкостная хроматография с тандемной масс-спектрометрией
Образцы пептида после расщепления протеолипосом СНО анализировали с помощью системы Proteomics Core Facility в Гетеборгском университете, Гетеборг, Швеция, как описано ранее [1]. Поиски во всех тандемных масс-спектрах проводили с помощью программного обеспечения MASCOT (Matrix Science, Лондон, Великобритания) по сравнению с базой знаний UniProtKB, выпуск 2013_04 (человек, [Homo sapiens]) в случае расщепления трипсином и выпуск 2015_06 (человек, [Homo sapiens]) в случае расщепления Asp-N. Программное обеспечение Thermo Proteome Discoverer v. 1.3 (Thermo Scientific) использовали для валидации идентификации пептида и белка на основе МС/МС. Уровень ложноположительных результатов, составляющий 0,01 на уровне пептида, использовали и определяли посредством поиска в обратной базе данных.
Разработка антитела
Синтезировали и очищали синтетические пептиды аа96-117 и аа785-799 на основании аминокислотной последовательности hTRPV1, включая дополнительный остаток цистеина на N-концевой стороне. Затем пептиды присоединяли посредством остатка цистеина к гемоцианину фисуреллы (KLH), после чего использовали для получения поликлональных антител посредством иммунизации специфичных свободных от патогенной флоры (СПФ) кроликов после инъекции пептидов, связанных с KLH. Антитела очищали и подвергали анализу методом ELISA. Получение как синтетических пептидов, так и поликлональных антител проводили с помощью компании Innovagen АВ (Лунд, Швеция).
Антитела использовали свежеоттаянными и в течение 30 мин. после кратковременной обработки ультразвуком. Антитела обрабатывали ультразвуком при амплитуде 14% три раза, с интервалами с перерывом в 1 мин. с использованием ультразвукового гомогенизатора Vibra Cell VCX 600 от компании Sonics & Materials Inc. (Ньютаун, Коннектикут, США). Суммарное время обработки ультразвуком составило 40 с, причем время поступления импульса составляло 0,5 с, и время покоя составляло 0,5 с с целью уменьшения нагревания пробы.
Электрофизиология
Анализ методом «наружная сторона внутри» проводили с использованием микрожидкостного устройства для анализа методом пэтч-кламп (Dynaflow, Cellectricon АВ, Гетеборг, Швеция) и амплификатора для пэтч-кламп HEKA ЕРС10 (Heka Elektronik, Германия). Омывающий раствор и раствор для пипетирования содержали буфер С. Фрагменты фиксировали при +60 мВ, и сигналы тока регистрировали при частоте замеров 20 кГц и фильтрации низких частот при 5 кГц.
В случае OTV1 амплитуды тока измеряли посредством воздействия на фрагменты, содержащие несколько ионных каналов, капсайцином с антителом и без антитела. На контроли воздействовали 1 мкМ капсайцина в буфере D в течение 30 с с последующим воздействием буфером D в течение 70 с, а затем снова воздействовали 1 мкМ капсайцина в буфере D в течение 30 с. На фрагменты, обработанные OTV1, воздействовали 1 мкМ капсайцина в буфере D в течение 30 с с последующим воздействием 0,14 мг/мл антитела в буфере D в течение 70 с, а затем воздействовали 1 мкМ капсайцина вместе с 0,14 мг/мл антитела в буфере D в течение 30 с. В случае OTV2 амплитуды тока измеряли посредством воздействия на фрагменты капсайцина с антителом и без антитела и кальмодулина/Са2+. На контроли воздействовали 1 мкМ капсайцина в буфере Е в течение 30 с с последующим воздействием 0,5 мкМ кальмодулина и 50 мкМ Са2+ в буфере Е в течение 70 с, а затем снова воздействовали 1 мкМ капсайцина в буфере Е в течение 30 с. На фрагменты, обработанные антителом, воздействовали 1 мкМ капсайцина в буфере Е в течение 30 с с последующим воздействием 0,14 мг/мл антитела, 0,5 мкМ кальмодулина и 50 мкМ Са2+ в буфере Е в течение 70 с, а затем воздействовали 1 мкМ капсайцина вместе с 0,14 мг/мл антитела, 0,5 мкМ кальмодулина и 50 мкМ Са2+ в буфере Е в течение 30 с. Измерения, которые после обработки в значительной степени смещались в сопротивление уплотнения, исключали из последующего анализа.
Анализ данных электрофизиологии
Для всех измерений активность после обработки антителом сравнивали с активностью после воздействия исключительно буфера с целью исключить любые эффекты десенсибилизации или потенцирования, обусловленные повторным активированием. В случае данных, содержащих кривые тока, проинтегрированные площади ток - время рассчитывали с использованием программного обеспечения Fitmaster (HEKA Elektronik, Германия) и Matlab (Mathworks, Массачусетс, США) для каждой активации капсайцином между нанесением и удалением OTV1 и между полной активацией (через 10 с) и удалением в случае OTV2. Соотношение между проинтегрированными площадями для второго и первого тока рассчитывали и сравнивали между обработками. В случае OTV2 данные наблюдений группировали на две категории (<15 мин. после кратковременной обработки ультразвуком и <30 мин. после кратковременной обработки ультразвуком) в связи с зависимым от времени уменьшением эффекта.
Статистический анализ проводили с помощью однофакторного дисперсионного анализа в сочетании с апостериорным критерием Даннетта и t-критерием Стьюдента, где применимо. р<0,05 считали статистически значимым. Данные представлены в виде среднего значения ±С.О.С.
Электропорация
Доставку антитела в цитозоль проводили с использованием системы трансфекции Neon (Life Technologies). Адгерентные клетки СНО отсоединяли с использованием аккутазы и промывали буфером F. 105 клеток осаждали центрифугированием и ресуспендировали в буфере F, 0,14 мг/мл OTV1 в буфере F или 0,27 мг/мл OTV2 в буфере F. 10 мкл суспензии клеток/антитела пипетировали с использованием микродозатора Neon и подвергали электропорации в системе станции для пипетирования. Использовали протокол, оптимизированный для доставки антител [5], в котором клетки подвергали воздействию 1550 В в течение 10 мс и в течение 3 импульсов. Клетки, которые подвергали электропорации, переносили на чашки со стеклянным дном (Willco wells).
Визуализация
Локализацию антитела посредством иммуноцитохимии и опосредованного TRPV1 поглощения YO-PRO измеряли с использованием измерения области, представляющий интерес (region of interest, ROI), на флуоресцентных микроснимках. Микроснимки получали с использованием системы Thorlabs CLS, оснащенной сканером Galvo:Resonant и высокочувствительными фотоэлектронными умножительными трубками на основе арсенида-фосфида галлия (gallium arsenide phosphide photomultiplier tubes, GaAsP PMT), и регистрировали в программном обеспечении ThorlmageLS (Thorlabs Inc, Нью-Джерси, США). Устройство для сканирования устанавливали на микроскоп Leica DMIRB, оснащенный объективом с масляной иммерсией 63× NA 1,47 Leica НСХ PL АРО. Флуоресцентную детекцию проводили от одной клетки с возбуждением при 488 нм с использованием лазера Coherent Sapphire 488 LP (Coherent Inc., Калифорния, США), и эмиссию регистрировали при длине волны 500-550 нм. Данные ROI анализировали с использованием программного обеспечения Image J и Matlab (Mathworks, Массачусетс, США).
Иммуноцитохимия
Клетки культивировали на чашках со стеклянным дном (Willco wells), и за 18-24 часа до применения в некоторых чашках индуцировали экспрессию TRPV1. Чашки, содержащие как клетки, экспрессирующие TRPV1, так и неиндуцированные клетки, промывали буфером F, а затем фиксировали и пермебеализовали с использованием набора для фиксации и пермеабилизации Image-iT® (Invitrogen). Фиксированные и пермебеализованные клетки подвергали воздействию 25 мкг/мл антитела в буфере F в течение 30 мин. при температуре 37°С, затем промывали буфером F, после чего следовала инкубация с вторичным антителом козы против иммуноглобулинов кролика Alexa 488 в течение 30 мин. при комнатной температуре. Клетки визуализировали после этапа финальной промывки, и распределение антитела сравнивали в случае индуцированных и неиндуцированных клеток.
Опосредованное TRPV1 поглощение YO-PRO
Чашки со стеклянным дном, содержащие 10 мкл клеток, которые подвергали электропорации, устанавливали на микроскоп. Регистрацию начинали при скорости 0,5 Гц. В случае OTV1 на клетки после электропорации аккуратно пипетировали каплю объемом 20 мкл, содержащую капсайцин, YO-PRO и K4ВАРТА в буфере F, с целью минимизации отсоединения, что приводило к получению конечной концентрации 1 мкМ капсайцина, 1 мкМ YO-PRO и 10 мМ K4ВАРТА. В случае OTV2 на клетки после электропорации аналогичным способом пипетировали каплю объемом 20 мкл, содержащую капсайцин, YO-PRO и Са2+ в буфере F, что приводило к получению конечной концентрации 1 мкМ капсайцина, 1 мкМ YO-PRO и 50 мкМ Са2+.
Варианты реализации настоящего изобретения, описанные выше, следует понимать как несколько иллюстративных примеров настоящего изобретения. Специалисту в данной области техники очевидно, что в пределах объема настоящего изобретения в варианты реализации настоящего изобретения могут быть внесены различные модификации, комбинации и изменения. В частности, различные части растворов в различных вариантах реализации настоящего изобретения можно объединить в других конфигурациях, когда это технически возможно.
ПЕРЕЧЕНЬ ЛИТЕРАТУРНЫХ ИСТОЧНИКОВ:
1 Jansson, Е.Т.; et. al., Anal. Chem. 2012, 84: 5582-5588.
2 Международная заявка на патент № WO 2006/068619.
3 Европейская заявка на патент № ЕР 2174908.
4 Trkulja, С.L., et al., J. Am. Chem. Soc. 2014, 136: 14875-14882.
5 Freund, G. et al., MAbs, 2013, 5: 518-522.
ПРИМЕР 3
Идентификация пептида посредством ограниченного расщепления и масс-спектрометрии ионного канала TRPV1, экспрессированного в клетках СНО, с использованием нескольких протеаз
В данном примере описано параллельное применение нескольких протеаз для идентификации специфичных к протеазе наборов пептидов TRPV1. Протеазы, использованные в данном примере, представляли собой трипсин, Asp-N, пепсин, протеиназу K и химотрипсин. По сравнению друг с другом, специфичные к протеазе наборы пептидов могут являться перекрывающимися, комплементарными или уникальными. Различные протеолитические активности обеспечивали посредством применения различных концентраций протеазы, а в нескольких примерах - посредством применения различных времен инкубации.
Материалы и методы
Культура клеток
Вкратце, клетки СНО культивировали согласно публикации Trkulja et al. (J. Am. Chem. Soc. 2014, 136, 14875-14882). Вкратце, адгерентные клетки яичников китайского хомячка (СНО) с регулируемой тетрациклином системой экспрессии (T-REx) культивировали в среде (DMEM/F12 с глутамином) с добавлением 10% ФБР, зеоцина (350 мкг/мл) и бластицидина (5 мкг/мл) в культуральных колбах Т175 или Т500 (Nunc) или на стеклянных чашках. Перед применением (за 18-24 ч) клетки инкубировали в среде (DMEM/F12 с глутамином) с добавлением 10% ФБР и доксициклина (1 мкг/мл) с целью индукции экспрессии TRPV1 человека. Линию клеток исследовали общепринятым способом для инфицирования микоплазмой. После сбора клетки замораживали и хранили при температуре -80 градусов. Затем клетки обрабатывали, как описано ниже.
Лизис и гомогенизция клеток
Суспензии клеток центрифугировали при 580g в течение 3 минут. Супернатант отбрасывали, и пробирки аккуратно наполняли 4 мл ледяного ФБР. Осадки клеток аккуратно ресуспендировали, а затем в пробирки наливали до 14 мл ледяного ФБР. Суспензии клеток снова центрифугировали при 580g в течение 3 минут, и процедуру повторяли дважды.
Осадки клеток (~800 мл по объему) ресуспендировали в приблизительно 6 мл лизирующего буфера (10 мМ NaHCO3, рН 7,4) и выдерживали на льду в течение 10 минут.
Клетки в лизирующем буфере переносили в гомогенизатор Даунса (7 мл), один для каждой суспензии клеток. Затем клетки подвергали гомогенизации с помощью жесткого пестика с использованием 20 движений. После гомогенизации лизированные клетки подвергали этапу центрифугирования при 580g в течение 3 минут. Супернатант собирали, осадок клеток отбрасывали. Супернатанты подвергали второму этапу центрифугирования при 580g в течение 3 минут, и осадок клеток (небольшой) отбрасывали.
Супернатанты объединяли и переносили в пробирку для центрифугирования Beckman (50 мл), добавляли лизирующий буфер до 20 мл. Супернатанты центрифугировали в течение 10 минут при 7300g для удаления митохондрий и дебриса клеток. Супернатант разделяли на две пробирки Falcon (по 10 мл каждая) и замораживали в морозильной камере при температуре -80 для последующей обработки.
Ультрацентрифугирование
Супернатанты оттаивали на льду и переносили в две чистые пробирки для ультрацентрифугирования Beckman (Beckman Coulter, артикул 344057). Пробирки заполняли ледяным буфером (10 мМ Tris, 300 мМ NaCl, рН 8) и тщательно уравновешивали перед центрифугированием при 100000g (32900 об./мин.) в течение 45 минут с использованием ротора SW55 Ti (Beckman Coulter). Супернатанты отбрасывали, осадки ресуспендировали в ледяном буфере (10 мМ Tris, 300 мМ NaCl, рН 8), а затем пробирки заливали тем же ледяным буфером. После тщательного уравновешивания и центрифугирования при 100000g (32900 об./мин.) в течение 45 минут супернатант отбрасывали, осадки ресуспендировали в ледяном буфере (10 мМ Tris, 300 мМ NaCl, рН 8), приблизительно по 800 мкл на осадок. Собирали препарат мембран с суммарным объемом приблизительно 1,6 мл и замораживали при температуре -80 градусов.
Кратковременная обработка ультразвуком
Замороженный препарат мембран оттаивали на льду и объединяли перед обработкой ультразвуком в ледяной конической виале с использованием ультразвукового аппарата (Vibracell). Препарат мембран сначала разводили до объема 4 мл ледяным буфером (10 мМ Tris, 300 мМ NaCl, рН 8) и подвергали 30 секундам обработки ультразвуком с использованием амплитуды 15% и цикла импульса/покоя 0,5 секунд. После этого коническую виалу и препарат мембран охлаждали на льду в течение нескольких минут, а затем препарат мембран подвергали воздействию другого цикла с использованием амплитуды 15% и импульса/покоя 0,5 секунд в течение 30 секунд, процедуру повторяли снова. Полученный в результате препарат мембран (протеолипосомы) замораживали в виде аликвот объемом 310 мкл при температуре -80 градусов.
Протеазы
Все протеазы заказывали в компании Promega. Все растворы готовили с использованием воды степени чистоты для ЖХ-МС от компании Fisher Scientific.
Кат. № V1621
Asp-N степени чистоты для секвенирования, 2 мкг.
Кат. № V1959
Пепсин, 250 мг.
Кат. № V3021
Протеиназа K, 100 мг.
Кат. № V1062
Химотрипсин степени чистоты для секвенирования, 25 мкг.
Кат. № V5111
Модифицированный трипсин степени чистоты для секвенирования, 20 мкг.
Трипсин
Трипсин растворяли в 100 мМ бикарбонате аммония, Ambic, рН 8.
Asp-N
Asp-N растворяли в 100 мМ бикарбонате аммония, Ambic, рН 8.
Пепсин
Пепсин растворяли в 100 мМ бикарбонате аммония, Ambic, рН 8.
Протеиназа K
Протеиназу K растворяли в 100 мМ бикарбонате аммония, Ambic, рН 8.
Химотрипсин
Химотрипсин растворяли в 100 мМ Tris-HCl, 10 мМ CaCl2, рН 8.
Использование LPI
Эксперименты проводили с использованием для расщепления датчиков LPI HexaLane. Одну дорожку на каждом датчике использовали для одного расщепления. Вкратце, аликвоты протеолипосом оттаивали при комнатной температуре, вручную инжектировали на дорожки с применением пипетки объемом 100 мкл и иммобилизовали в течение 1 часа.
Промывку дорожек также проводили вручную с использованием пипетки объемом 100 мкл. Каждую из ячеек промывали по 200 мкл буфера для промывки (такого же, что и буфер для расщепления, за исключением протокола расщепления пепсином, в котором в качестве буфера для промывки использовали 100 мМ Ambic, рН 8. Данный подход применяли во избежание низкого значения рН в проточной ячейке в течение длительного времени). Затем дорожки промывали по 4×100 мкл буфера для промывки с использованием пипетки объемом 100 мкл.
После этого в дорожку инжектировали протеазу и проводили инкубацию согласно инструкциям, приведенным ниже. Инкубации (расщепления) проводили при комнатной температуре. После расщепления пептиды элюировали с дорожки с использованием 200 мкл буфера для расщепления (2×100 мкл). Активность протеазы останавливали посредством добавления 4 мкл муравьиной кислоты в результате окисления полученного раствора пептида до значения рН приблизительно 2. Данный этап проводили для всех образцов, за исключением пепсина, в который вместо этого добавляли 16 мкл раствора аммиака (25%), чтобы сделать раствор основным (рН 9).
Использовали следующие условия расщепления, по одному в каждой дорожке:
Трипсин:
0,5 мкг/мл в течение 2,5 мин.
0,5 мкг/мл в течение 5 мин.
2 мкг/мл в течение 5 мин.
5 мкг/мл в течение 5 мин.
10 мкг/мл в течение 5 мин.
20 мкг/мл в течение 5 мин.
Asp-N
20 мкг/мл в течение 5 мин.
2 мкг/мл в течение 24 часов
Химотрипсин
5 мкг/мл в течение 5 мин.
10 мкг/мл в течение 5 мин.
20 мкг/мл в течение 5 мин.
Протеиназа K
5 мкг/мл в течение 5 мин.
10 мкг/мл в течение 5 мин.
20 мкг/мл в течение 5 мин.
Пепсин
2 мкг/мл в течение 5 мин.
5 мкг/мл в течение 5 мин.
10 мкг/мл в течение 5 мин.
20 мкг/мл в течение 5 мин.
Образцы метили и замораживали при температуре -80°С.
Анализ методом МС
Триптические пептиды обессоливали на спин-колонках PepClean С18 (Thermo Fisher Scientific, Inc., Уолтем, Массачусестс, США) согласно руководствам производителя, высушивали и восстанавливали с помощью 15 микролитров 0,1% муравьиной кислоты (Sigma Aldrich, Сент-Луис, Миссури) в 3% ацетонитриле градиентной чистоты (Merck KGaA, Дармштадт, Германия). Инжекцию двух микролитров образца вносили с помощью автоматического дозатора Easy-nLC (Thermo Fisher Scientific, Inc., Уолтем, Массачусестс, США) и анализировали на гибридном масс-спектрометре Q Exactive, снабженном интерфейсом (Thermo Fisher Scientific). Пептиды удерживали на предколонке (внутр. диаметр 45 × 0,075 мм) и разделяли на колонке с обращенной фазой, 200 × 0,075 мм, самостоятельно упакованной частицами Reprosil-Pur C18-AQ размером 3 мкм (Dr. Maisch, Аммербух, Германия). Градиент nanoLC (жидкостная хроматография) анализировали при 200 нг/мин., начиная с 7% ацетонитрила (ACN) в 0,2% муравьиной кислоте, увеличивая до 27% ACN в течение 25 мин., затем увеличивая до 40% в течение 5 мин. и, наконец, до 80% ACN в течение 5 мин., и поддерживали при 80% ACN в течение 10 мин.
Ионы получали и распыляли в масс-спектрометр под напряжением 1,8 кВ и при температуре капилляра 320 градусов по Цельсию в информационно-зависимом режиме определения положительных ионов. Спектры полного сканирования (MS1) получали в орбитальной ионной ловушке Orbitrap в диапазоне m/z (масса/заряд) 400-1600, диапазоне заряда 2-6 при разрешении 70000 до целевого значения AGC (Automatic Gain Control, автоматический выбор числа уловленных ионов) 1е6 при максимуме 250 мс. Спектры МС/МС получали с использованием диссоциации, индуцируемой высокоэнергетическим соударением (higher energy collision dissociation, HCD), при 30% от m/z 110 для десяти наиболее распространенных родительских ионов при разрешении 35000 с использованием окна выделения предшественников 2 Да до целевого значения AGC 1е5 в течение времени инжекции 110 мс. Динамическое исключение в течение 30 с после выбора МС/МС было включено для обнаружения как можно большего количества возможных предшественников.
Краткое изложение результатов
На фигуре 10 представлено расположение пептидов, обнаруженных после ограниченного протеолиза трипсином, на 3D-модели TRPV1. Последовательности обнаруженных пептидов после ограниченного протеолиза трипсином показаны ниже в таблице 2. Пептиды, расщепленные 0,5 мкг/мл трипсина в течение 2,5 мин., показаны первыми. Пептиды, расщепленные 0,5 мкг/мл трипсина в течение 5 мин., 2 мкг/мл трипсина в течение 5 мин., 5 мкг/мл трипсина в течение 5 мин., 10 мкг/мл трипсина в течение 5 мин. и 20 мкг/мл трипсина в течение 5 мин., соответственно, были объединены с целью лучшей визуализации и показаны вторыми.

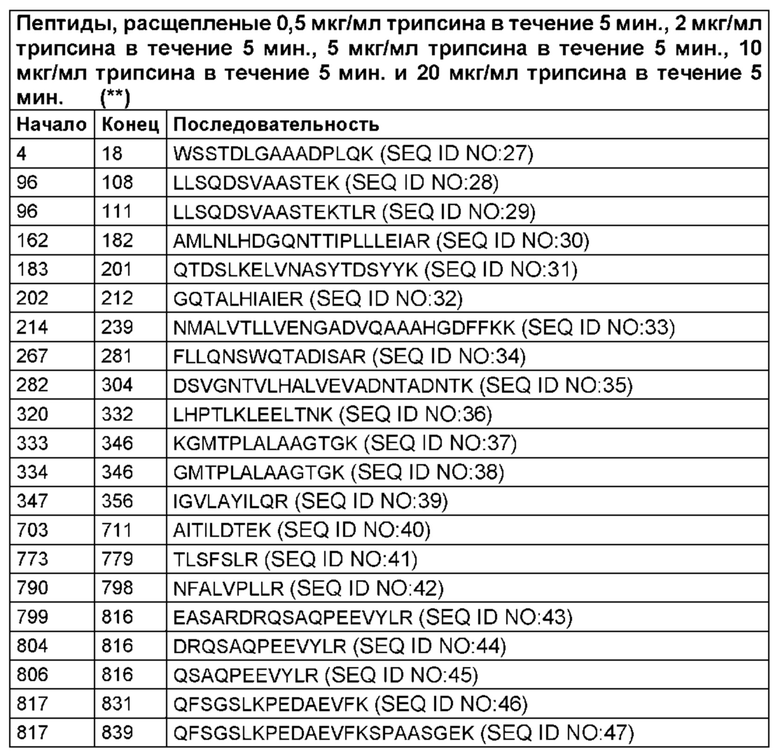
На фигуре 11 представлено расположение пептидов, обнаруженных после ограниченного протеолиза Asp-N, на 3D-модели TRPV1. Последовательности обнаруженных пептидов после ограниченного протеолиза Asp-N показаны ниже в таблице 3. Пептиды, расщепленные 20 мкг/мл Asp-N в течение 5 мин., показаны первыми. Пептиды, расщепленные 2 мкг/мл Asp-N в течение 24 часов, показаны вторыми.


На фигуре 12 представлено расположение пептидов, обнаруженных после ограниченного протеолиза химотрипсином, на 3D-модели TRPV1. Последовательности обнаруженных пептидов после ограниченного протеолиза химотрипсином показаны ниже в таблице 4. Пептиды, расщепленные 5 мкг/мл химотрипсина в течение 5 мин., показаны первыми. Пептиды, расщепленные 10 мкг/мл химотрипсина в течение 5 мин. и 20 мкг/мл химотрипсина в течение 5 мин., соответственно, были объединены с целью лучшей визуализации и показаны вторыми.
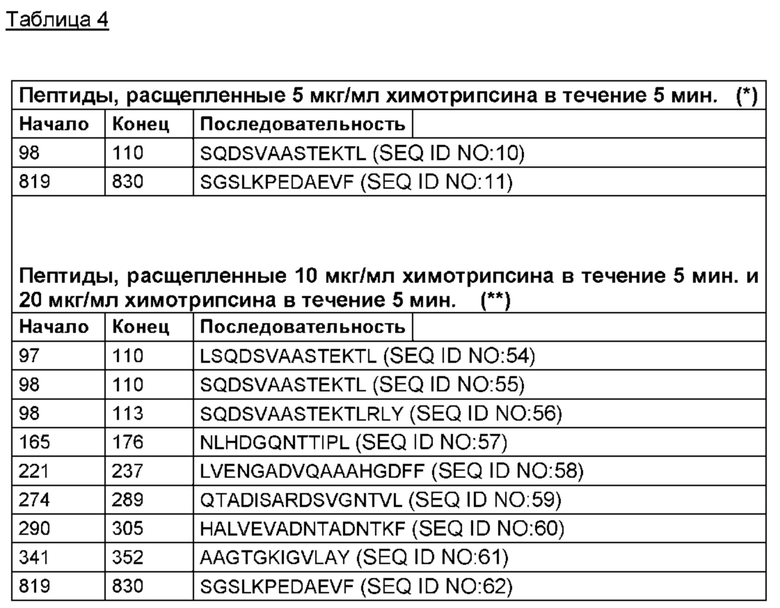
На фигуре 13 представлено расположение пептидов, обнаруженных после ограниченного протеолиза пепсином, на 3D-модели TRPV1. Последовательности обнаруженных пептидов после ограниченного протеолиза пепсином показаны ниже в таблице 5. Пептиды, расщепленные 2 мкг/мл пепсина в течение 5 мин., показаны первыми. Пептиды, расщепленные 5 мкг/мл пепсина в течение 5 мин., 10 мкг/мл пепсина в течение 5 мин. и 20 мкг/мл пепсина в течение 5 мин., соответственно, были объединены с целью лучшей визуализации и показаны вторыми.
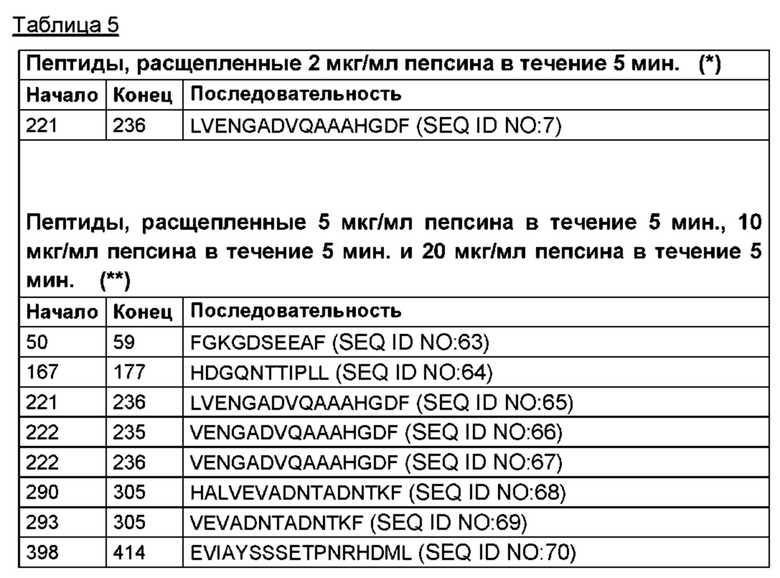
На фигуре 14 представлено расположение пептидов, обнаруженных после ограниченного протеолиза протеиназой K, на 3D-модели TRPV1. Последовательности обнаруженных пептидов после ограниченного протеолиза протеиназой K показаны ниже в таблице 6. Пептиды, расщепленные 5 мкг/мл протеиназы K в течение 5 мин., показаны первыми. Пептиды, расщепленные 10 мкг/мл протеиназы K в течение 5 мин. и 20 мкг/мл протеиназы K в течение 5 мин., соответственно, были объединены с целью лучшей визуализации и показаны вторыми.

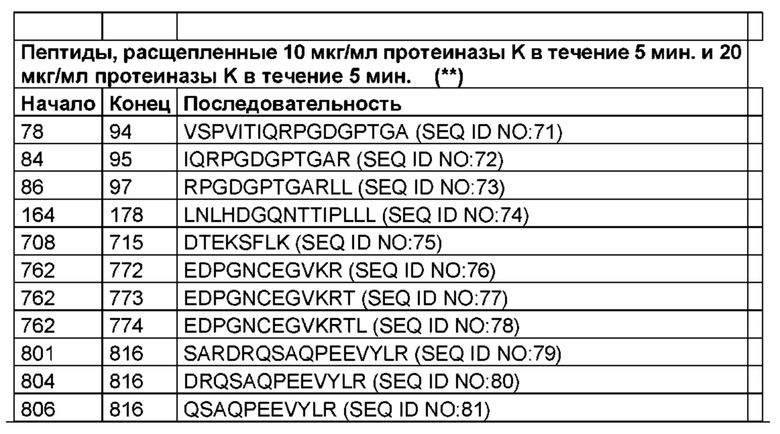
В таблицах 2, 3, 4, 5 и 6 термины «начало» и «конец» означают положения остатков аминокислот в последовательности TRPV1.
В процессе оценки данных для Фильтров результатов (пептид) был установлен порог значимости Mascot, составляющий 0,01.
Трипсин позволял получить увеличенное количество пептидов и увеличенный доверительный интервал с увеличением концентрации протеазы.
Как пепсин, так и химотрипсин давали начало множеству пептидов и при низких, и при более высоких концентрациях.
| название | год | авторы | номер документа |
|---|---|---|---|
| МУЛЬТИПРОТЕАЗНЫЙ СПОСОБ | 2017 |
|
RU2774157C2 |
| НОВЫЕ СПОСОБЫ СЕЛЕКЦИИ ЭПИТОПОВ | 2016 |
|
RU2764992C2 |
| НОВЫЕ ГЕНЫ, КОДИРУЮЩИЕ НОВЫЕ ПРОТЕОЛИТИЧЕСКИЕ ФЕРМЕНТЫ | 2002 |
|
RU2423525C2 |
| НОВЫЕ ГЕНЫ, КОДИРУЮЩИЕ НОВЫЕ ПРОТЕОЛИТИЧЕСКИЕ ФЕРМЕНТЫ | 2002 |
|
RU2296160C2 |
| АНТИГЕННЫЕ МАТРИЦЫ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ КОСТЕЙ | 2002 |
|
RU2322258C2 |
| ЧАСТИЦЫ С РАСЩЕПЛЕННЫМ ЯДРОМ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ПРЕЗЕНТАЦИИ ЧУЖЕРОДНЫХ МОЛЕКУЛ, ПРЕЖДЕ ВСЕГО ДЛЯ ПРИМЕНЕНИЯ В ВАКЦИНАХ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2454462C2 |
| КОМПОЗИЦИЯ ДЛЯ ИММУНИЗАЦИИ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ АЛЛЕРГИЧЕСКИХ ЭОЗИНОФИЛЬНЫХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2319503C2 |
| РОТАВИРУСНЫЕ ЧАСТИЦЫ С ХИМЕРНЫМИ ПОВЕРХНОСТНЫМИ БЕЛКАМИ | 2014 |
|
RU2698049C2 |
| КОНЪЮГАТЫ ПЕПТИДА Melan-A, АНАЛОГА ВИРУСОПОДОБНОЙ ЧАСТИЦЫ | 2004 |
|
RU2351362C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ ДЛЯ ОПРЕДЕЛЕНИЯ НЕ4А | 2011 |
|
RU2650778C2 |
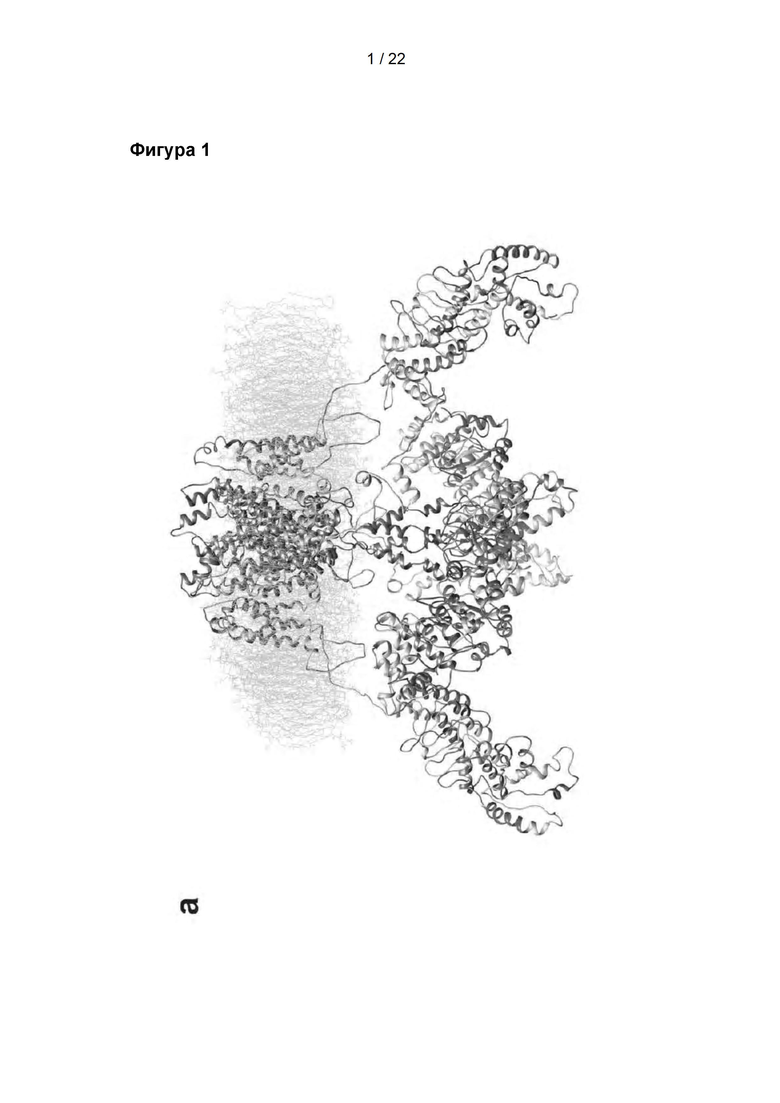
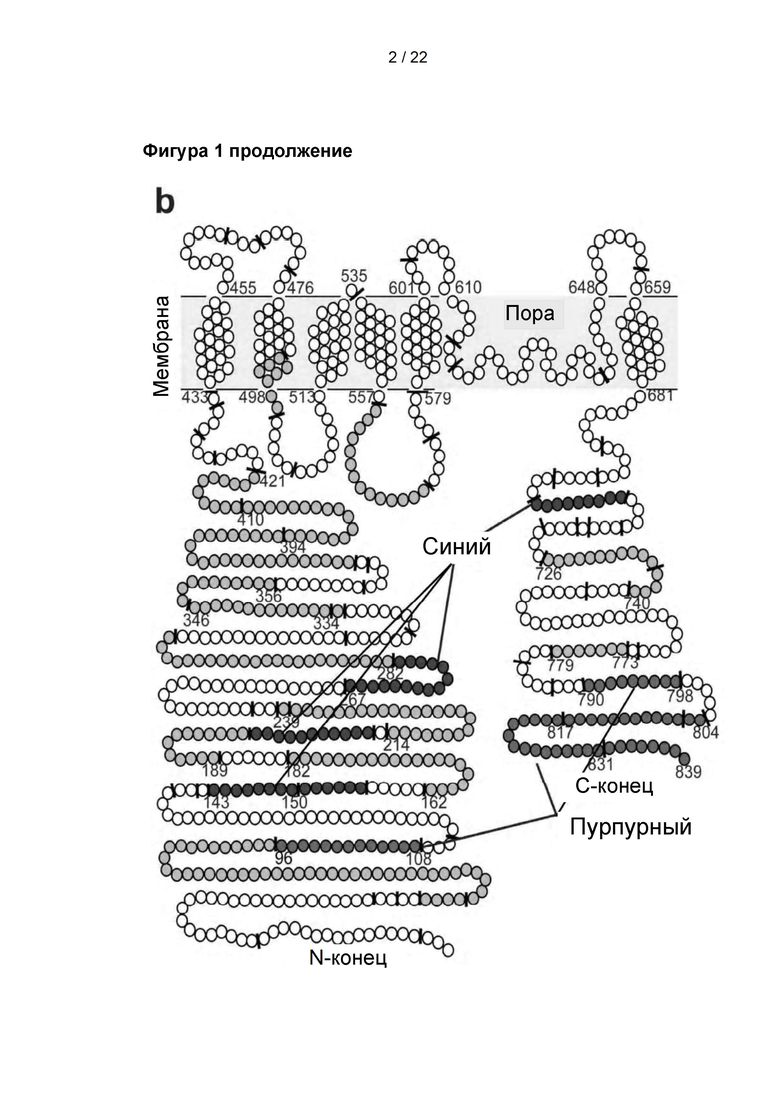
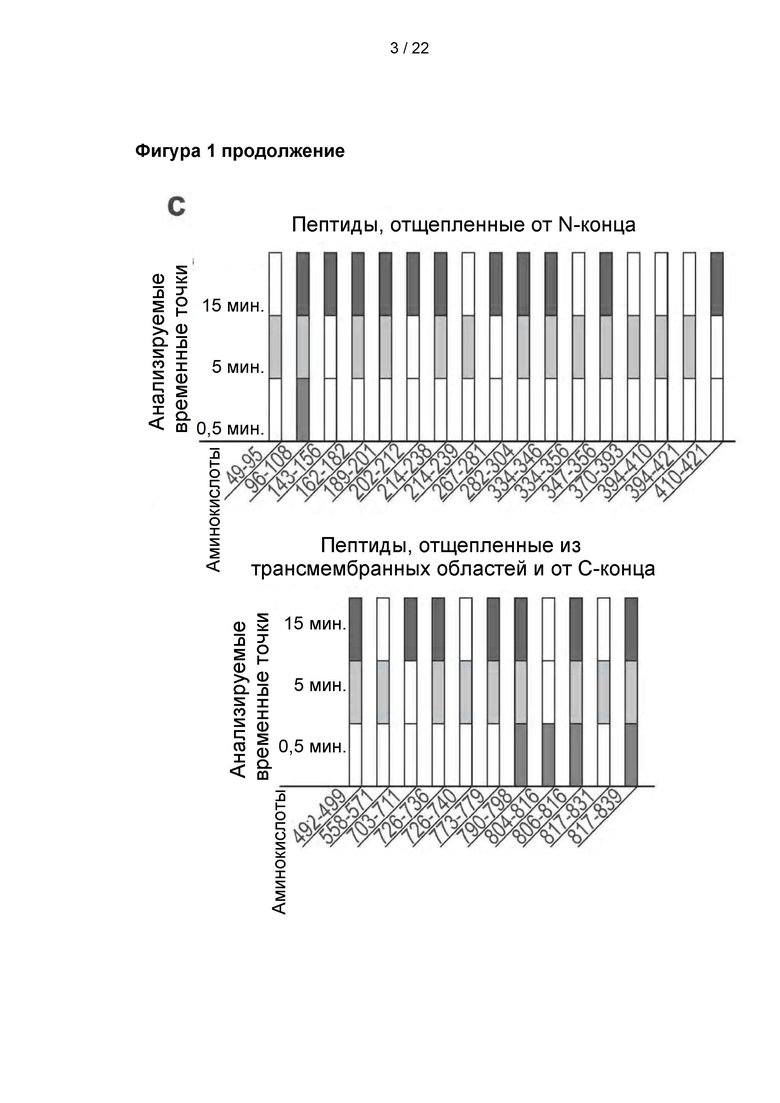
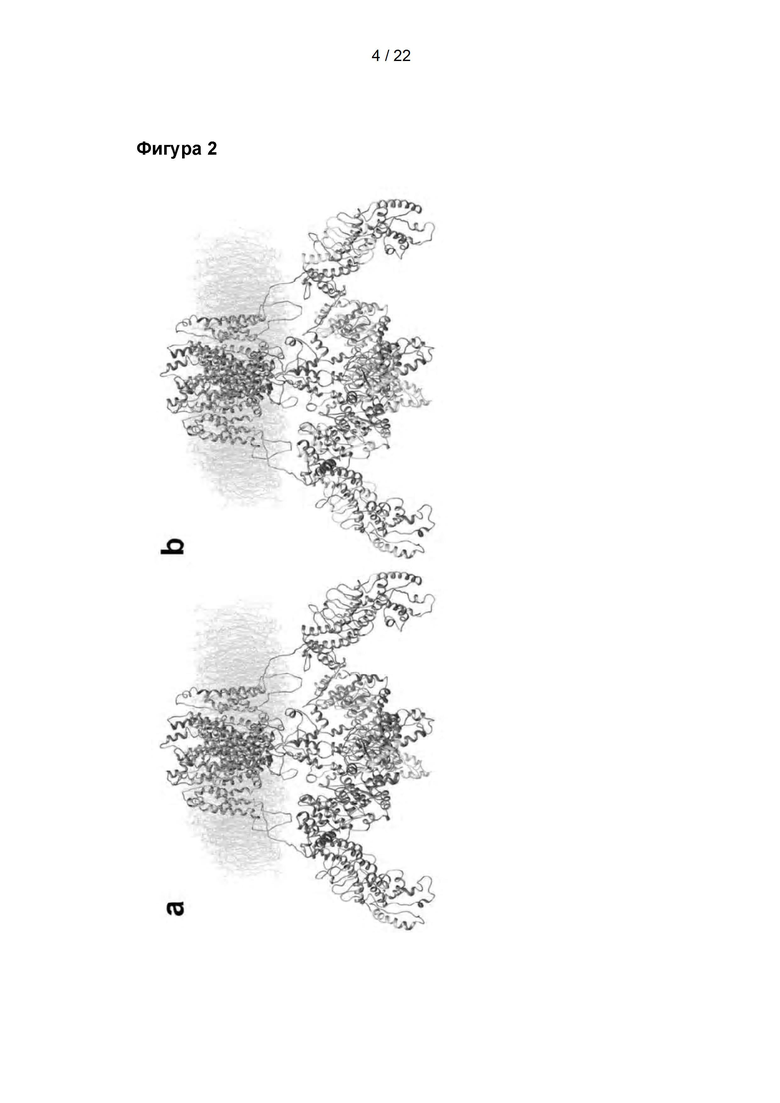
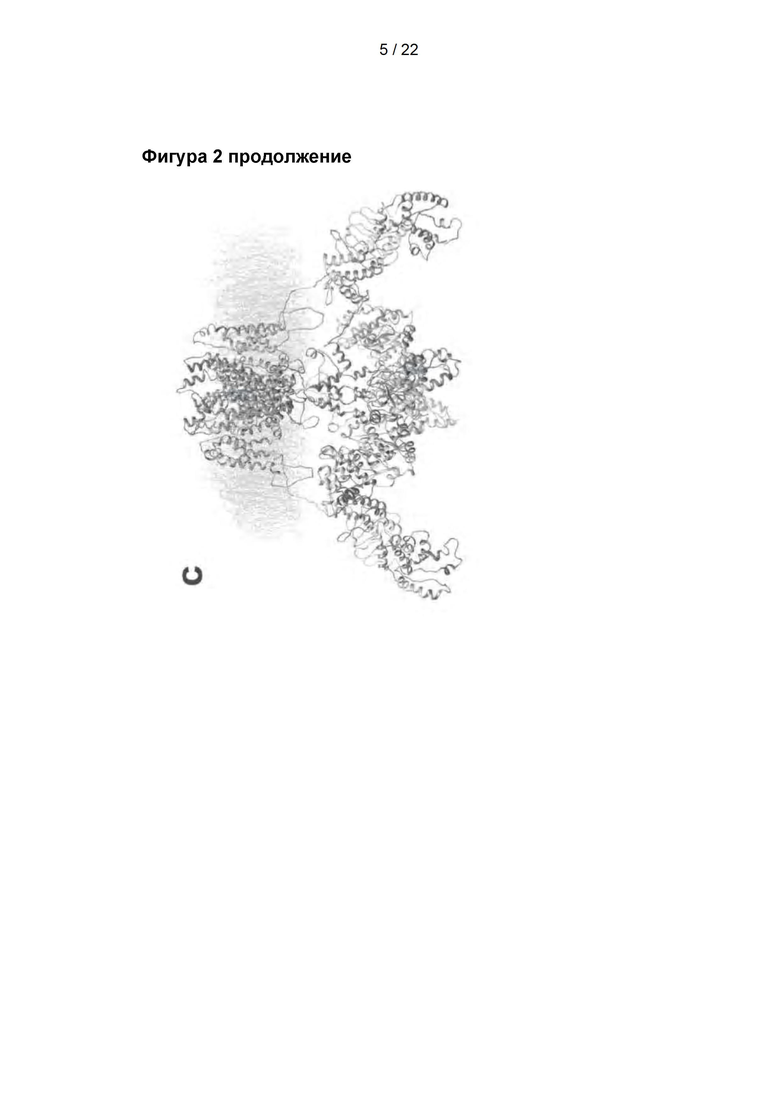
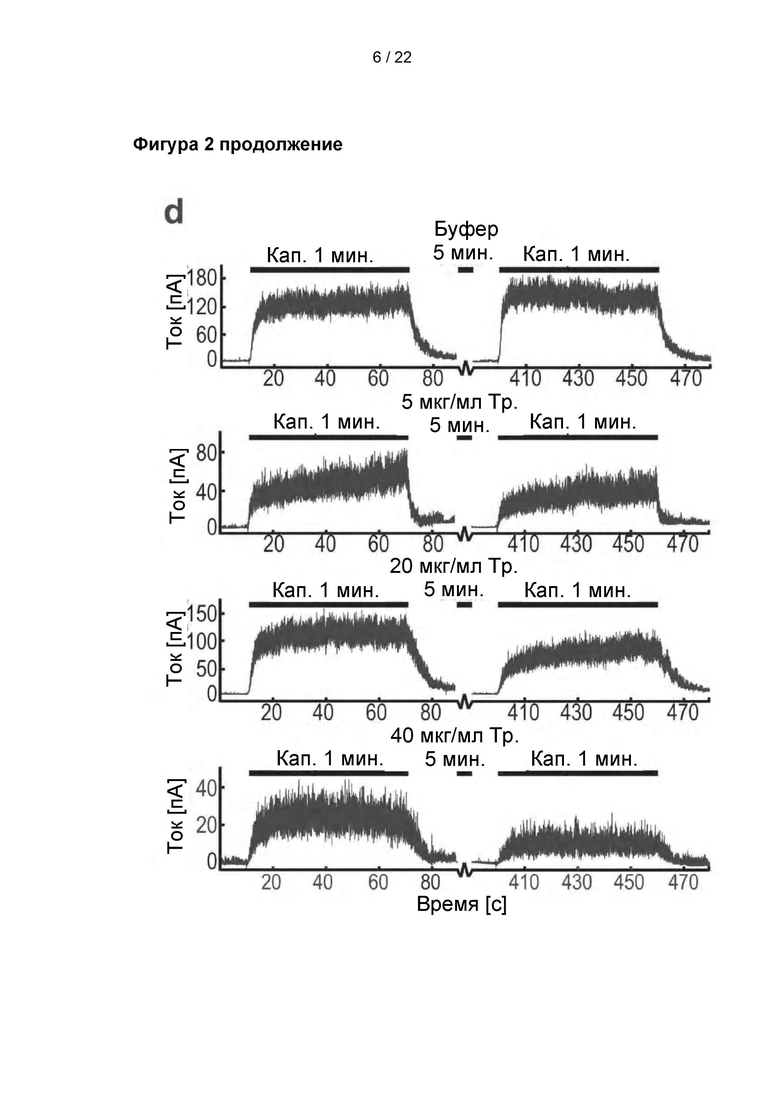
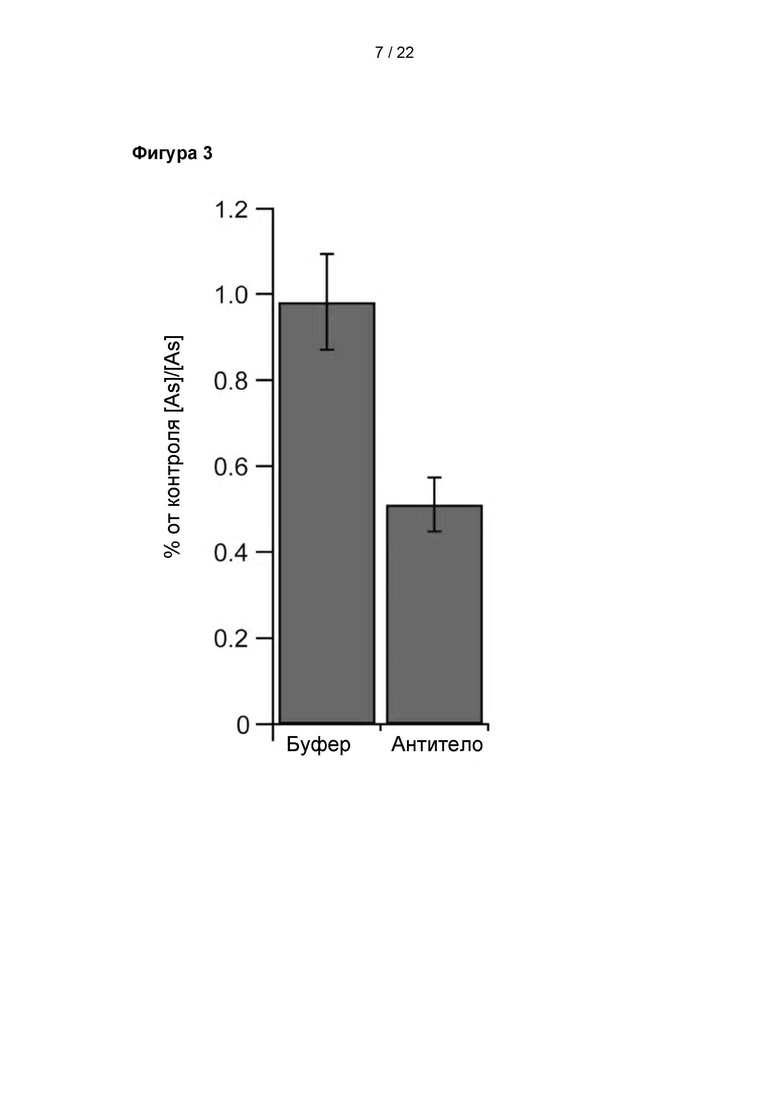
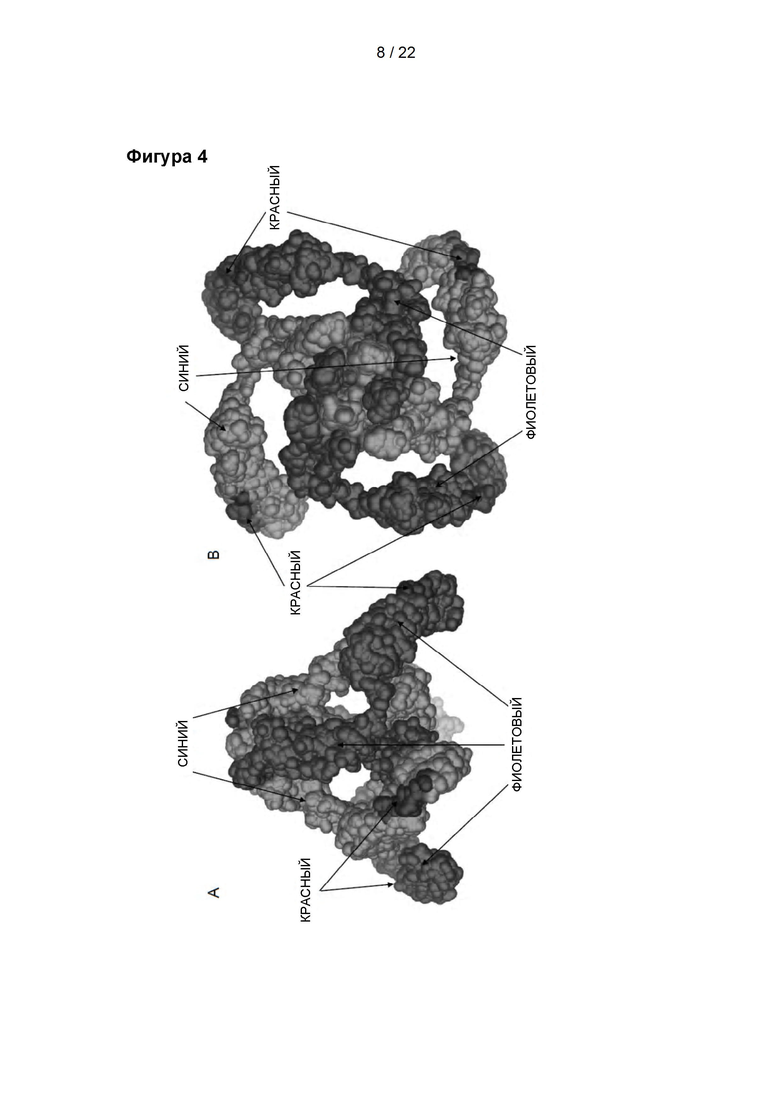
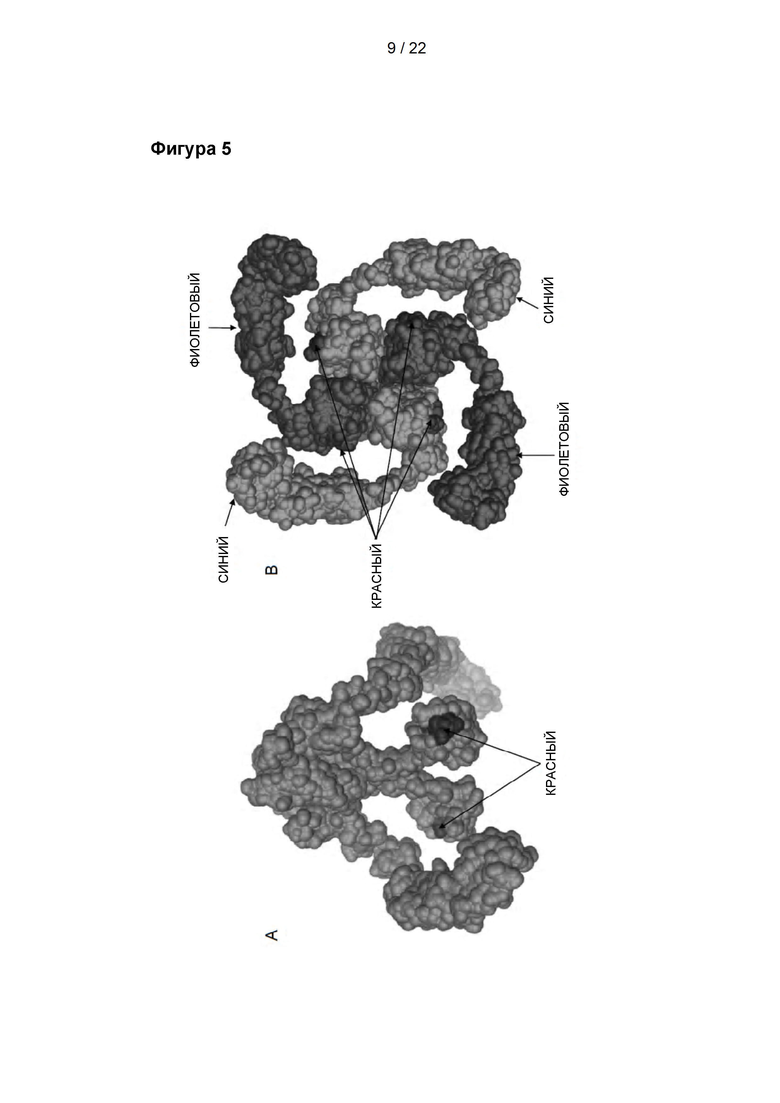
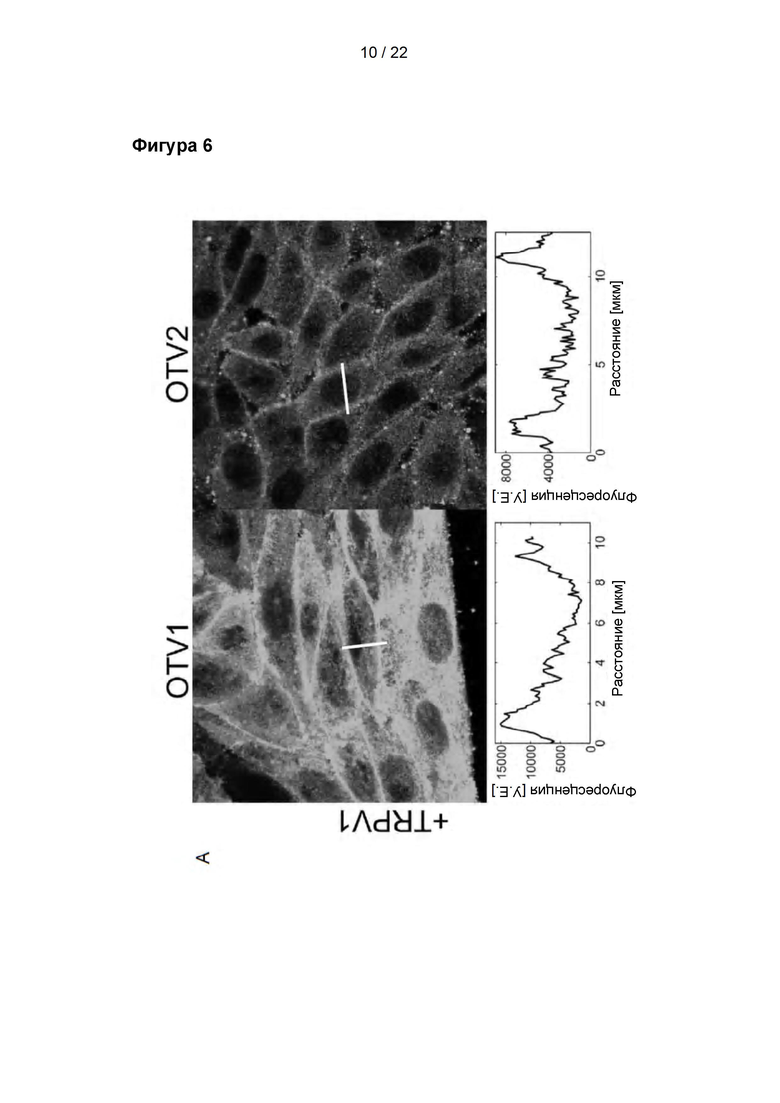
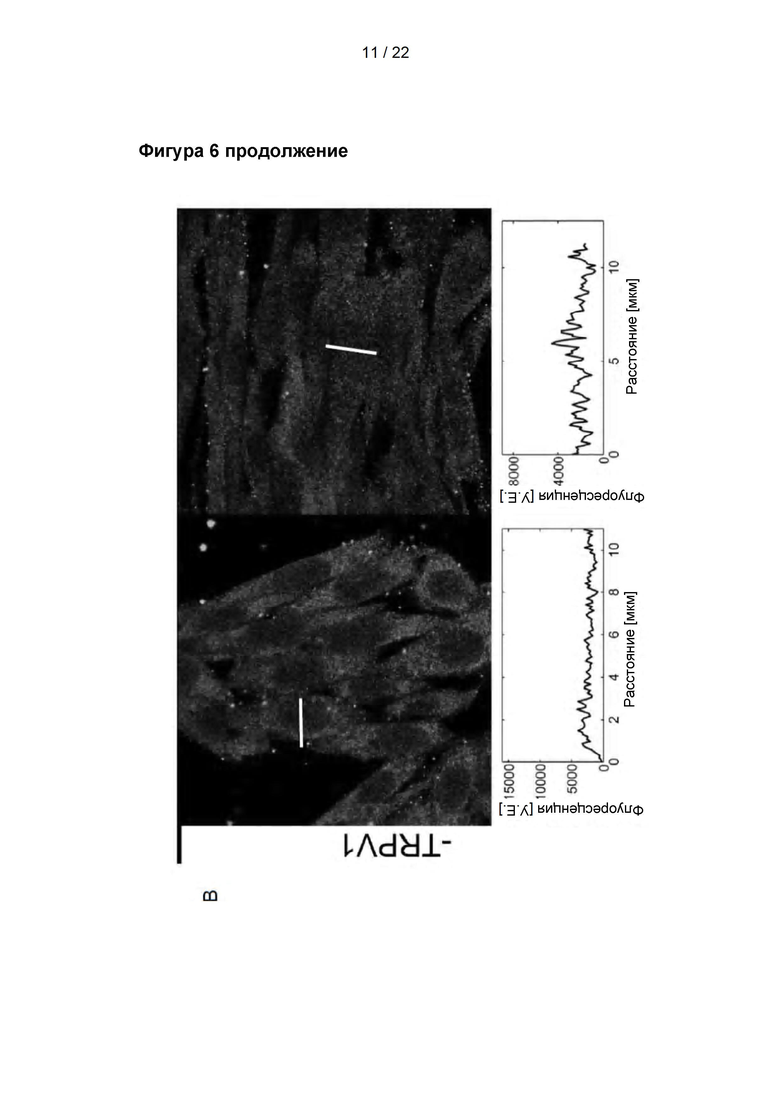
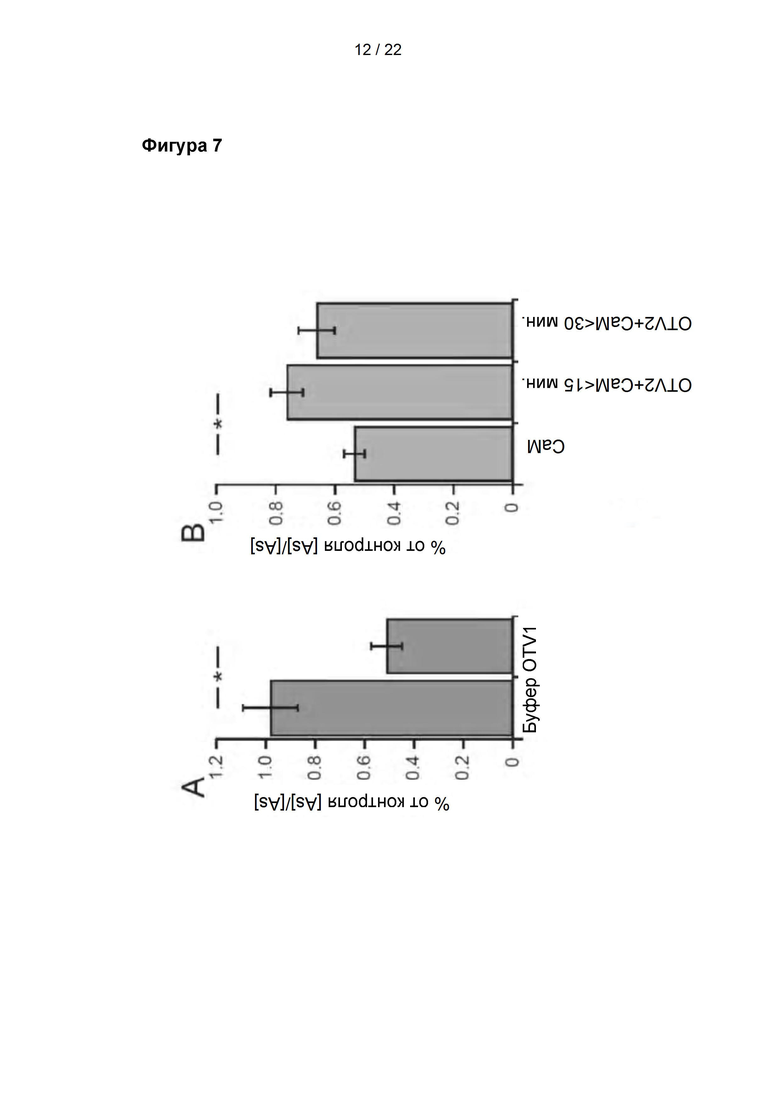

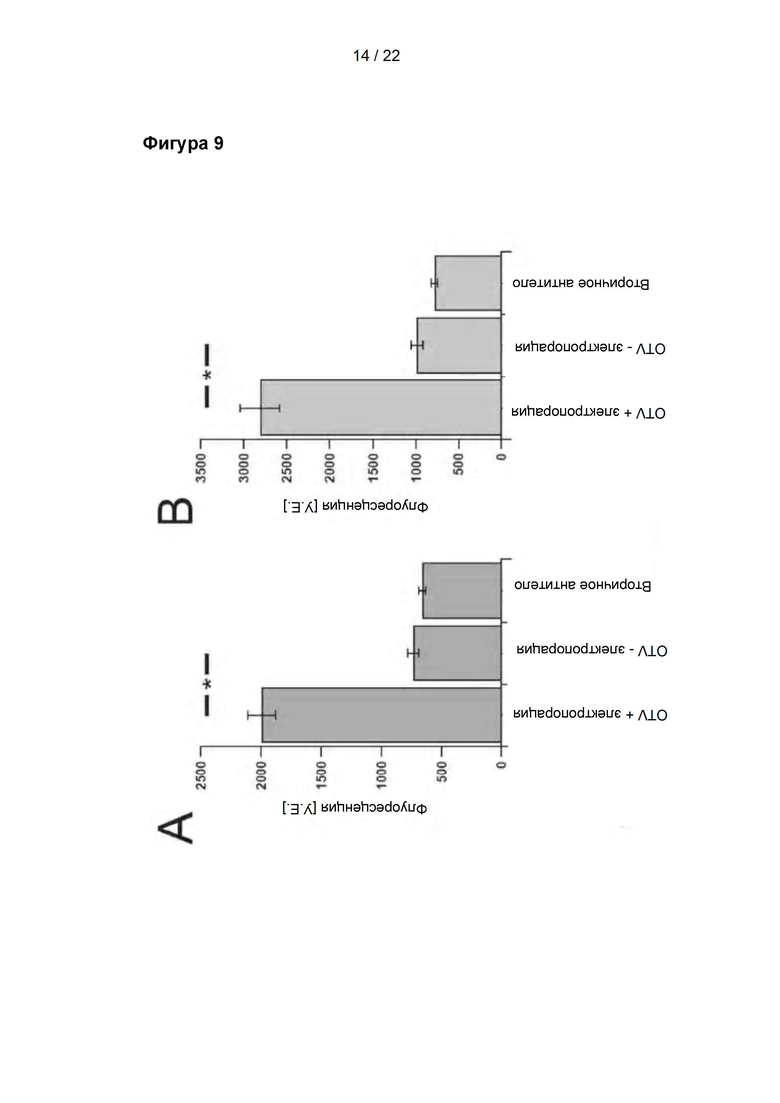

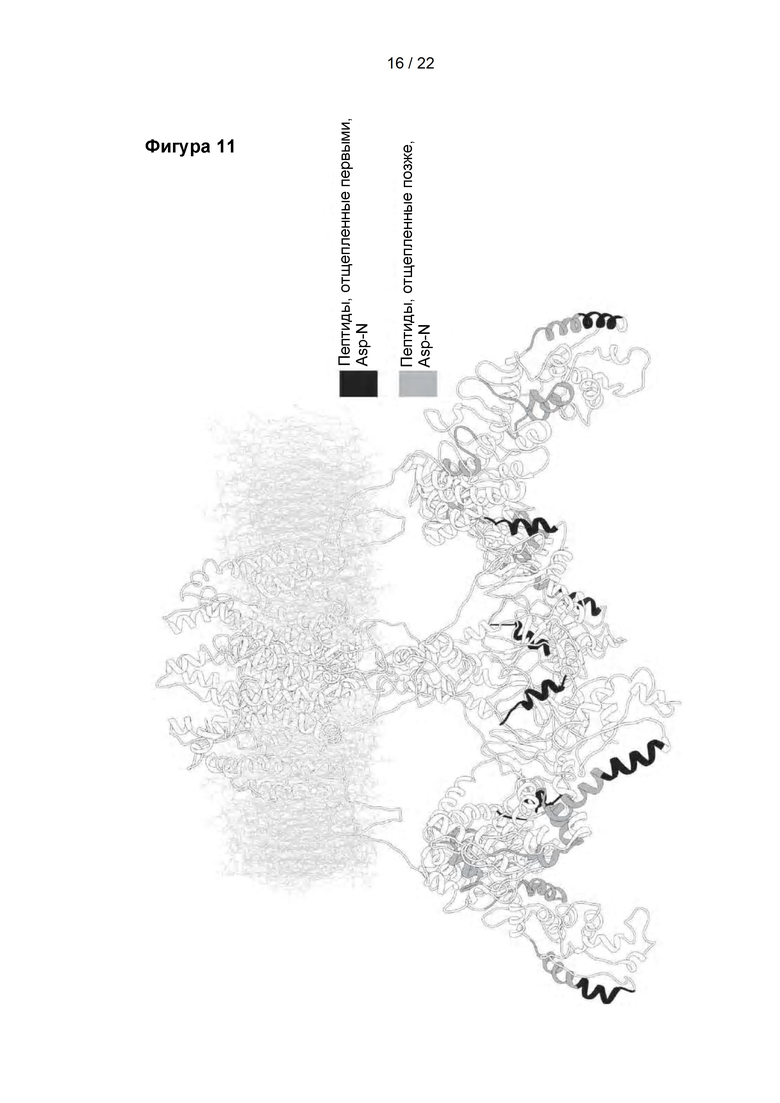
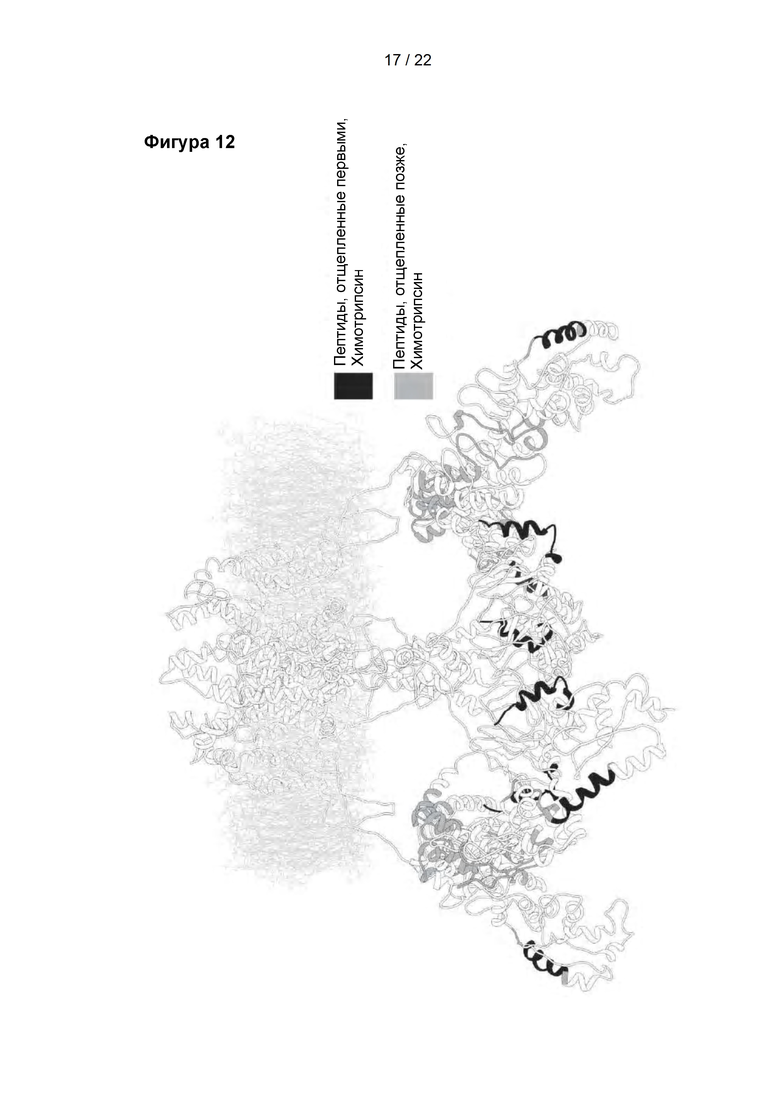
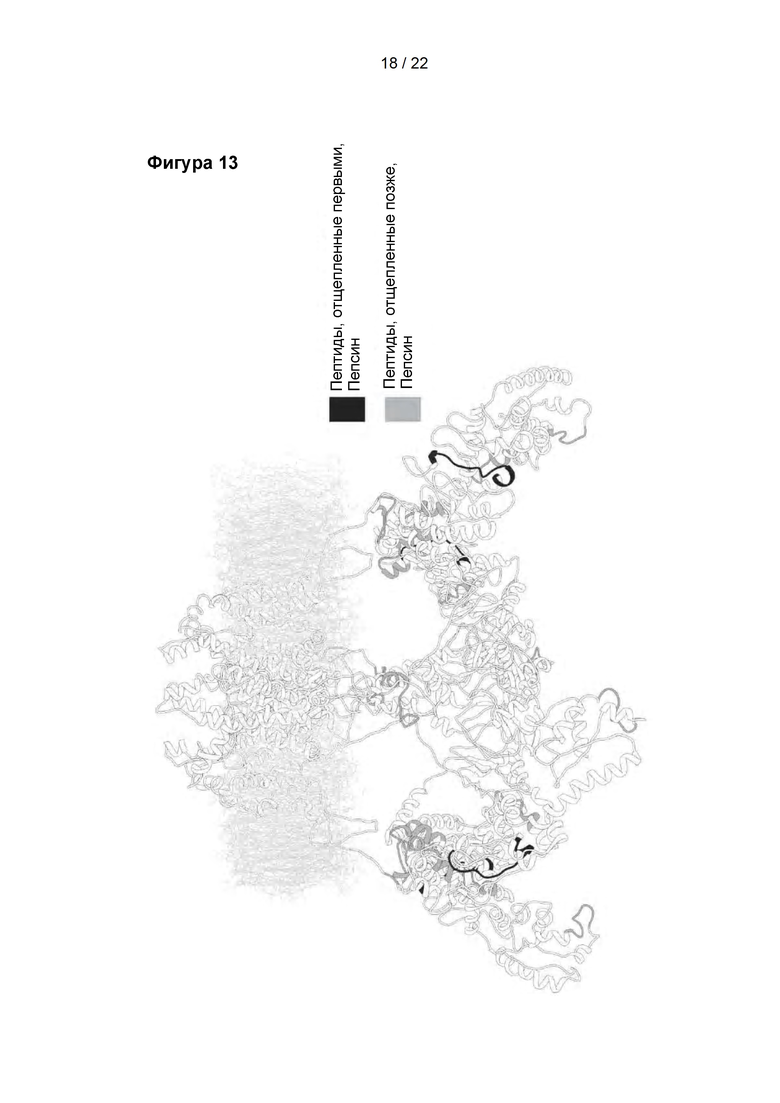

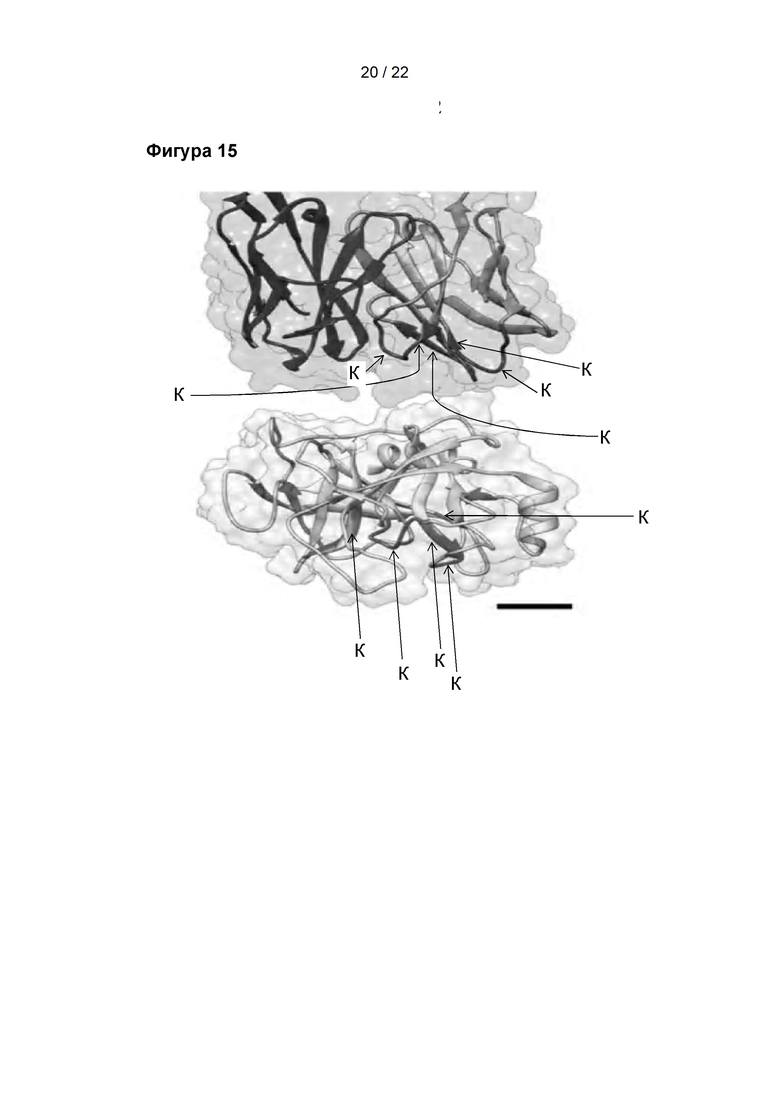


Настоящее изобретение относится к способам идентификации эпитопа, с которым может связываться антитело, на белке. Предложен способ идентификации эпитопа, с которым может связываться антитело, на белке, причем указанный способ включает: (i) осуществление протеолитического расщепления указанного белка in silico одной или более протеазами для идентификации сайтов на белке, которые согласно прогнозу разрезаются указанной одной или более протеазами и a. осуществление моделирования белков по гомологии для прогнозирования, какие спрогнозированные in silico сайты разрезания протеазой, вероятно, являются экспонированными, и/или b. осуществление докинга фрагментов антитела или протеаз in silico для прогнозирования, какие спрогнозированные in silico сайты разрезания, вероятно, будут разрезаны in vitro; (ii) осуществление ограниченного или частичного протеолиза указанного белка in vitro одной или более протеазами; (iii) идентификацию пептидов, высвободившихся из указанного белка в результате протеолитического расщепления in vitro на этапе (ii), и посредством этого идентификацию сайтов разрезания; (iv) сравнение спрогнозированных in silico сайтов разрезания, идентифицированных согласно прогнозу как экспонированные или разрезаемые in vitro на этапе (i), с сайтами разрезания, идентифицированными на этапе (iii); (v) исследование одного или более эпитопов в области белка, содержащей или фланкирующей сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный согласно прогнозу как экспонированный или разрезаемый in vitro на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii) с помощью одного или более антител; и (vi) определение того, связывается или нет указанное одно или более антител с указанным одним или более эпитопами, и посредством этого идентификацию эпитопа на белке, с которым может связываться антитело. 2 н. и 22 з.п. ф-лы, 17 ил., 6 табл., 3 пр.
1. Способ идентификации эпитопа, с которым может связываться антитело, на белке, причем указанный способ включает:
(i) осуществление протеолитического расщепления указанного белка in silico одной или более протеазами для идентификации сайтов на белке, которые согласно прогнозу разрезаются указанной одной или более протеазами, и
a. осуществление моделирования белков по гомологии для прогнозирования, какие спрогнозированные in silico сайты разрезания протеазой, вероятно, являются экспонированными, и/или
b. осуществление докинга фрагментов антитела или протеаз in silico для прогнозирования, какие спрогнозированные in silico сайты разрезания, вероятно, будут разрезаны in vitro;
(ii) осуществление ограниченного или частичного протеолиза указанного белка in vitro одной или более протеазами;
(iii) идентификацию пептидов, высвободившихся из указанного белка в результате протеолитического расщепления in vitro на этапе (ii), и посредством этого идентификацию сайтов разрезания;
(iv) сравнение спрогнозированных in silico сайтов разрезания, идентифицированных согласно прогнозу как экспонированные или разрезаемые in vitro на этапе (i), с сайтами разрезания, идентифицированными на этапе (iii);
(v) исследование одного или более эпитопов в области белка, содержащей или фланкирующей сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный согласно прогнозу как экспонированный или разрезаемый in vitro на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii) с помощью одного или более антител; и
(vi) определение того, связывается или нет указанное одно или более антител с указанным одним или более эпитопами, и посредством этого идентификацию эпитопа на белке, с которым может связываться антитело.
2. Способ по п. 1, отличающийся тем, что применяют одну протеазу.
3. Способ по п. 1, отличающийся тем, что применяют несколько протеаз.
4. Способ по любому из пп. 1–3, отличающийся тем, что указанная протеаза выбрана из группы, состоящей из: трипсина, протеиназы Arg-C, эндопептидазы Asp-N, клострипаина, глутамилэндопептидазы, Lys-C, Lys-N, химотрипсина, протеиназы K, термолизина, пепсина, каспазы 1, каспазы 2, каспазы 3, каспазы 4, каспазы 5, каспазы 6, каспазы 7, каспазы 8, каспазы 9, каспазы 10, энтерокиназы, фактора Xa, гранзима B, нейтрофильной эластазы, пролинэндопептидазы, стафилококковой пептидазы I и тромбина.
5. Способ по любому из пп. 1–4, отличающийся тем, что указанная протеаза выбрана из группы, состоящей из: трипсина, эндопептидазы Asp-N, химотрипсина, пепсина и протеиназы K.
6. Способ по любому из пп. 1–5, отличающийся тем, что указанный белок представляет собой мембранный белок, который присутствует в протеолипосоме, полученной из клеток.
7. Способ по п. 6, отличающийся тем, что указанная протеолипосома иммобилизована в проточной ячейке для создания неподвижной фазы мембранных белков.
8. Способ по любому из пп. 1–7, отличающийся тем, что идентификацию пептидов, высвободившихся из указанного белка в результате протеолитического расщепления in vitro на этапе (ii), и посредством этого идентификацию сайтов разрезания осуществляют методом масс-спектрометрии.
9. Способ по любому из пп. 1–8, отличающийся тем, что указанный способ дополнительно включает до этапа (v) этап создания одного или более выделенных эпитопов, последовательности которых соответствуют одному или более эпитопам на указанном белке, которые расположены в области белка, содержащей или фланкирующей сайт разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный согласно прогнозу как экспонированный или разрезаемый in vitro на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii), и образования антител, которые связываются с указанными выделенными эпитопами, и применения указанных антител на этапе (v) для исследования указанного одного или более эпитопов указанного белка.
10. Способ по любому из пп. 1–9, отличающийся тем, что исследуют совокупность эпитопов.
11. Способ по любому из пп. 1–10, отличающийся тем, что указанный эпитоп находится в пределах 20 аминокислот от указанного сайта разрезания, который представляет собой сайт разрезания протеазой, спрогнозированный in silico, идентифицированный согласно прогнозу как экспонированный или разрезаемый in vitro на этапе (i), но который не является сайтом разрезания, идентифицированным на этапе (iii).
12. Способ по любому из пп. 1–11, отличающийся тем, что исследуют совокупность эпитопов и что указанная совокупность эпитопов представляет собой множество (группу) эпитопов, причем последовательность каждого эпитопа во множестве смещена по сравнению с другим эпитопом во множестве на 1, 2 или 3 аминокислоты.
13. Способ идентификации эпитопа, с которым может связываться антитело, на белке, причем указанный способ включает:
(i) идентификацию сайтов, в которых одна или более протеаз разрезали указанный белок после того, как указанный белок подвергся воздействию ограниченного или частичного протеолиза указанной одной или более протеазами; и
(ii) исследование совокупности эпитопов на указанном белке, которые расположены между сайтами разрезания, которые перекрываются с сайтом разрезания или которые расположены в области, фланкирующей сайт разрезания, с помощью антител, направленных против указанных эпитопов, посредством этого идентифицируя один или более эпитопов, с которыми может связываться антитело.
14. Способ по п. 13, отличающийся тем, что применяют одну протеазу.
15. Способ по п. 13, отличающийся тем, что применяют несколько протеаз.
16. Способ по любому из пп. 13–15, отличающийся тем, что указанная протеаза выбрана из группы, состоящей из: трипсина, протеиназы Arg-C, эндопептидазы Asp-N, клострипаина, глутамилэндопептидазы, Lys-C, Lys-N, химотрипсина, протеиназы K, термолизина, пепсина, каспазы 1, каспазы 2, каспазы 3, каспазы 4, каспазы 5, каспазы 6, каспазы 7, каспазы 8, каспазы 9, каспазы 10, энтерокиназы, фактора Xa, гранзима B, нейтрофильной эластазы, пролинэндопептидазы, стафилококковой пептидазы I и тромбина.
17. Способ по любому из пп. 13–16, отличающийся тем, что указанная протеаза выбрана из группы, состоящей из: трипсина, эндопептидазы Asp-N, химотрипсина, пепсина и протеиназы K.
18. Способ по любому из пп. 13–17, отличающийся тем, что указанный белок представляет собой мембранный белок, который присутствует в протеолипосоме, полученной из клеток.
19. Способ по п. 18, отличающийся тем, что указанная протеолипосома иммобилизована в проточной ячейке для создания неподвижной фазы мембранных белков.
20. Способ по любому из пп. 13–19, отличающийся тем, что указанные сайты, в которых одна или более протеаз разрезали указанный белок, идентифицируют с применением масс-спектрометрии.
21. Способ по любому из пп. 13–20, отличающийся тем, что указанный способ дополнительно включает до этапа (ii) этап создания совокупности выделенных эпитопов, последовательности которых соответствуют эпитопам на указанном белке, которые расположены между сайтами разрезания, которые перекрываются с сайтом разрезания или которые расположены в области, фланкирующей сайт разрезания, и образования антител, которые связываются с указанными выделенными эпитопами, и применения указанных антител на этапе (ii) для исследования указанной совокупности эпитопов на указанном белке.
22. Способ по любому из пп. 13–21, отличающийся тем, что указанный эпитоп находится в пределах 20 аминокислот от указанного сайта разрезания.
23. Способ по любому из пп. 13–22, отличающийся тем, что указанная совокупность эпитопов представляет собой множество (группу) эпитопов, причем последовательность каждого эпитопа во множестве смещена по сравнению с другим эпитопом во множестве на 1, 2 или 3 аминокислоты.
24. Способ по любому из пп. 1–23, отличающийся тем, что указанный способ дополнительно включает этап получения антитела против эпитопа, идентифицированного по любому из пп. 1–23.
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| "Probing structure and function of ion channels using limited | |||
Авторы
Даты
2022-05-06—Публикация
2017-09-01—Подача