Изобретение относится к области онкологии, генетики человека и может быть использовано для прогнозирования риска возникновения плоскоклеточного рака легких (РЛ) у мужчин. В 60-80% случаев РЛ выявляется уже на поздних стадиях, с метастазами. Несмотря на внедрение химиотерапевтических препаратов нового поколения и методов таргетной терапии, 5-летняя общая выживаемость по-прежнему крайне низкая. Ежегодный скрининг РЛ с использованием низкодозной компьютерной томографии показал высокую чувствительность метода и снижение смертности на 20%, однако специфичность такой диагностики не велика (даже в ведущих скрининговых центрах мира). К основной причине формирования РЛ относят курение (de Groot, P. & Munden, R. F. Lung cancer epidemiology, risk factors, and prevention. Radiol. Clin. North. Am. 50, 863-876, https://doi.org/10.1016/j.rcl.2012.06.006 (2012)). В то же время от 15 до 25% случаев РЛ регистрируются у некурящих. Риск злокачественной трансформации увеличивается с возрастом, чаще встречается у мужчин, превалирует у лиц, контактировавших с производственными канцерогенами. Свой вклад вносит контакт с канцерогенами в бытовых условиях и общее состояние бронхолегочной системы (хронические заболевания легочной системы) (Schwartz, A.G. Epidemiology of Lung Cancer / A.G. Schwartz, MX. Cote // Adv Exp Med Biol. - 2016. - V. 893. - P. 21-41; Wu, M.F. Post-inhaled corticosteroid pulmonary tuberculosis and pneumonia increases lung cancer in patients with COPD / MJF. Wu, ZJL Jian, LY. Huang et al. // BMC Cancer. -2016. - V. 16(1). - P. 778; De Groot, P.M. The epidemiology of lung cancer / P.M. de Groot, C.C. Wu, B.W. Carter et al. // Transl Lung Cancer Res. - 2018. - V. 7(3). - P. 220-233).
Различные гистопатологические, клинические характеристики РЛ, а также отличия в этиологии подтипов заболевания, свидетельствуют о гетерогенности, и требуют индивидуального подхода в его исследованиях (De Sousa, V.M.L. Heterogeneity in Lung Cancer / V.M.L. De Sousa, L. Carvalho // Pathobiology. - 2018. - V. 85(1-2). - P. 96-107). Однако до сих пор непонятен комплекс факторов, способных модулировать канцерогенные эффекты и тем самым определять индивидуальную чувствительность к риску формирования онкопатологии легкого.
Применение биологических онкомаркеров может обеспечить более раннее и точное выявление заболевания и прогнозировать развитие РЛ в группах высокого риска. Поиски оптимальных онкомаркеров ведутся не только в опухолевых тканях, но и в легкодоступном биологическом материале (кровь, мокрота, лаваж, выдыхаемый воздух и др.), что дает возможность проводить раннюю диагностику до оперативных вмешательств и позволяет избежать проблем, связанных с генетической гетерогенностью опухолей. Активно изучаются такие молекулярные маркеры, как специфические протеины, антитела к опухолевым антигенам, микроРНК, профиль метилирования ДНК, циркулирующая опухолевая ДНК, фрагменты системы комплемента, хромосомные аберрации, однонуклеотидные замены (SNPs) (Ooki A, Maleki Z, Tsay JJ, Goparaju С, Brait M, Turaga N, Nam HS, Rom WN, Pass HI, Sidransky D, Guerrero-Preston R, Hoque MO A Panel of Novel Detection and Prognostic Methylated DNA Markers in Primary Non-Small Cell Lung Cancer and Serum DNA. Clin Cancer Res. 2017 23(22):7141-7152. doi:10.1158/1078-0432.CCR-17-1222). Большинство из этих методов ориентированы на ранее выявление опухолевых клеток, но не на обнаружение маркеров канцерогенеза в стадии инициации и промоции.
Известны способы биологической индикации повышенного риска рака различных локализаций, основанные на определении в лимфоцитах периферической крови обследуемого повышенного уровня хромосомных аберраций (ХА) (Bonassi, S. Chromosomal aberration frequency in lymphocytes predicts the risk of cancer: results from a pooled cohort study of 22 358 subjects in 11 countries / S. Bonassi, H. Norppa, M. Ceppi et al // Carcinogenesis. - 2008 - V. 29(6). - P. 1178-1183. - doi:10.1093/carcin/bgn075; Vodicka, P. Chromosomal damage in peripheral blood lymphocytes of newly diagnosed cancer patients and healthy controls / P. Vodicka, Z. Polivkova, S. Sytarova etal // Carcinogenesis. - 2010. - V. 31. - P. 1238-1241; Vodenkova, S. Structural chromosomal aberrations as potential risk markers in incident cancer patients / S. Vodenkova, Z. Polivkova, L. Musak, et al. // Mutagenesis. - 2015. - V. 30(4). - P. 557-620). Исследования предиктивной значимости ХА в отношении риска рака легкого у населения угледобывающего региона свидетельствуют о том, что превышение фонового уровня ХА даже на 1% может приводить к возрастанию риска немелкоклеточного РЛ на 70% (Minina, V.I. Polymorphisms in DNA repair genes in lung cancer patients living in a coal-mining region / Minina V.I, Bakanova M.L., Soboleva O.A., Ryzhkova A.V., Titov R.A., Savchenko Y.A., Sinitsky M.Y., Voronina E.N., Titov V.A., Glushkov A.N. II Eur J Cancer Prev. - 2019. - V. 28(6) - P. 522-528. doi:10.1097/CEJ.0000000000000504). Недостатком такого подхода можно считать необходимость забора крови из вены (инвазивный метод).
Известен способ прогнозирования возникновения рака легкого у больных хронической обструктивной болезнью легких (RU 2407013 С1, Кл. G01N 33/53, опубл. 20.12.2010). Сущность способа заключается в том, что в крови больных с хронической обструктивной болезнью легких определяют содержание CD3+ CD16-, IgE, спонтанную пролиферацию Т-лимфоцитов (активированные клетки), процент лимфоцитов с увеличением количества ДНК (G1-фаза), фагоцитарный индекс, проводят стимулированный зимозаном тест с нитросиним тетразолием (НСТ-индуцированный). При значениях содержания CD3+ CD16- выше 1,85⋅103, IgE более 330 МЕ/мл, спонтанной пролиферации ниже 20%, процента лимфоцитов с увеличением количества ДНК (G1-фаза) менее 1,9, фагоцитарного индекса более 52, стимулированного зимозаном теста с нитросиним тетразолием выше 38% прогнозируют развитие рака легкого. Существенным ограничением данного метода является то, что его диагностическая значимость доказана лишь для пациентов с хронической обструктивной болезнью легких (диагноз, который сам по себе уже является значимым фактором риска развития рака легкого).
Известен еще один способ определения риска рака с таким же недостатком - способ прогнозирования возникновения рака легкого у больных хронической обструктивной болезнью легких путем оценки содержания антител острого периода класса М и G к вирусам семейства Herpesviridae, а именно IgM к вирусу простого герпеса типа 1 и 2; IgM к цитомегаловирусу; IgG и IgM к предраннему белку цитомегаловируса, IgM к капсидному белку вируса Эпштейн-Барра и IgG к раннему антигену вируса Эпштейн-Барра (RU 2437102 С1, Кл. G01N 33/577, опубл. 20.12.2011). При выявлении антител острого периода одновременно к двум и более вирусам семейства Herpesviridae прогнозируют развитие рака легкого.
Известен способ определения предрасположенности к онкологическим заболеваниям, в том числе к раку легкого (RU 2475184 С2, Кл. А61В 5/103, опубл. 20.02.2013) на основе анализа дерматоглифических параметров. Определяют на фалангах пальцев - тип узора и гребневой счет; на ладонях -гребневой счет ab, be, cd; величину угла atd, направление окончания главных ладонных линий А, В, С и Д в ладонные поля; расположение ладонных и осевых трирадиусов; характер рисунков на тенаре, гипотенаре и в межпальцевых полях. На основании выявленных параметров диагностируют генетическую предрасположенность к раку легких, желудка или молочной железы. Данный метод позволяет оценивать вероятность развития онкозаболеваний, однако риск непосредственно рака легкого остается не известным.
Известен способ прогнозирования риска возникновения рака или диагностирования рака легкого у женщин на основе определения уровня проэнкефалина или его фрагментов и установления корреляции между указанным уровнем проэнкефалина (PENK) или его фрагментов и риском возникновения рака (RU 2671578 С2, Кл. G01N 33/574, опубл. 27.11.2016). Недостатком данного способа может служить его сфокусированность на прогнозировании риска рака легкого только у женщин, тогда как заболеваемость этой патологией у мужчин значительно выше, чем у женщин.
Наиболее близким способом определения риска развития рака легкого может служить способ прогнозирования развития РЛ у лиц, проживающих в экологически неблагоприятных условиях на основе определения ряда систем наследственного полиморфизма, в частности - генетического маркера иммуноглобулина Gml (RU 2260799 С1, Кл. G01N 33/48, опубл. 20.09.2005). Суть способа заключается в том, что у испытуемого забирают кровь из локтевой вены и исследуют наличие генетического маркера иммуноглобулина Gml в сыворотке крови методом торможения агглютинации эритроцитов с последующей микроскопической оценкой. При наличии генетического маркера иммуноглобулина Gml (+) прогнозируют предрасположенность к развитию рака легкого, а при наличии генетического маркера иммуноглобулина Gml (-) прогнозируют резистентность к развитию рака легкого.
К недостаткам данного способа следует отнести: инвазивность метода (необходим забор крови), определение только одного из множества известных генетических маркеров человека устаревшими методами (типирование маркеров генетического полиморфизма целесообразнее проводить методами секвенирования или полимеразной цепной реакции). Это существенно сужает точность и информативность способа. Кроме того, в настоящее время уже известно, что рак легкого - высоко гетерогенное заболевание. Механизмы предрасположенности, индукции и промоции канцерогенеза значительно отличаются для различных гистологических форм рака легкого. Поэтому способы оценки риска должны быть специфическими для разных патоморфологических форм рака легкого.
В связи с успехами молекулярной медицины и разработкой методов высокопроизводительного секвенирования в последние годы стало возможным проведение детального анализа не только генома человека, но и анализ генома бактериальной микробиоты различных органов. Большинство бактерий не могут быть исследованы с использованием традиционных методов микробиологического культивирования, а изучение бактериальных геномов позволяет компенсировать данные ограничения. Исследования в данной области указали на значимую роль микробиоты при различных состояниях здоровья и жизнедеятельности человеческого организма.
В результате исследований, сравнивающих респираторную микробиоту у больных с различными заболеваниями легких и здоровых людей, были обнаружены значительные различия в составе микробного сообщества [Dickson RP, Erb-Downward JR, Huffnagle GB. The role of the bacterial microbiome in lung disease. Expert Rev Respir Med. 2013;7:245-257]. Описано увеличение количества видов при хронических заболеваниях воздухоносных путей, чаще со сдвигом в составе сообщества от типа Bacteroidetes, доминирующего в микробиоме здоровых легких, к типу Proteobacteria, содержащему множество родственных легочных грамотрицательных бактерий. Недавние исследования показали, что некоторые отдельные бактерии, а также дисбиоз респираторной микробиоты коррелируют с развитием РЛ [Мао Q, Jiang F, Yin R, Wang J, Xia W, Dong G, et al. Interplay between the lung microbiome and lung cancer. Cancer Lett. 2018;415:40-48].
Результаты нескольких исследований указывают на возможную роль бактерий в стимулировании развития РЛ. Например, таким фактором может быть повышенная бактериальная колонизация при хронической обструктивной болезни легких (ХОБЛ) [Pragman АА, Kim НВ, Reilly CS, Wendt С, Isaacson RE. The lung microbiome in moderate and severe chronic obstructive pulmonary disease. PLoS ONE. 2012;7:e47305], которая является известным фактором риска для развития РЛ. Уже существуют доказательства того, что бактерии, присутствующие в легких и респираторном тракте, играют роль в этиологии ХОБЛ и бронхиальной астмы [Lin KW, Li J, Finn PW. Emerging pathways in asthma: Innate and adaptive interactions. Biochim Biophys Acta. 2011;1810:1052-1058; Han MK, Huang YJ, Lipuma JJ, Boushey HA, Boucher RC, Cookson WO, et al. Significance of the microbiome in obstructive lung disease. Thorax. 2012;67:456-463]. В частности, у пациентов, страдающих тяжелой формой ХОБЛ, было обнаружено существенное изменение бактериального состава легких по сравнению со здоровыми индивидами [Engel М, Endesfelder D, Schloter-Hai В, Kublik S, Granitsiotis MS, Boschetto P, et al. Influence of lung CT changes in chronic obstructive pulmonary disease (COPD) on the human lung microbiome. PLoS One. 2017; 12(7): e0180859]. Повышенная секреция слизи, характерная для респираторной патологии, приводит к появлению локальных очагов повышенной температуры, понижает снабжение этих участков кислородом, что также избирательно благоприятствует росту известных болезнетворных бактерий [Goleva Е, Jackson LP, Harris JK, Robertson СЕ, Sutherland ER, Hall CF, et al. The effects of airway microbiome on corticosteroid responsiveness in asthma. Am J Respir Crit Care Med. 2013;188:1193-1201]. Кроме того, было показано, что генерация катехоламинов и воспалительных цитокинов, наблюдаемая при респираторных заболеваниях, способствует росту отдельных видов бактерий, обладающих ДНК-повреждающим действием (например, P. aeruginosa, S. pneumoniae, Staphylococcus aureus, E.coli) [Freestone PP, Hirst RA, Sandrini SM, Sharaff F, Fry H, Hyman S, et al. Pseudomonas aeruginosa - catecholamine inotrope interactions: a contributory factor in the development of ventilator associated pneumonia? Chest. 2012;142:1200-1210].
Состав микробиома мокроты как возможного источника неинвазивных бактериальных биомаркеров для выявления рака легких был определен в недавнем исследовании. Было показано увеличение содержания в мокроте больных с подтвержденным диагнозом РЛ представителей Streptococcus viridans и 16 других видов бактерий, включая Neisseria gonorrhoeae, которые были выявлены только в мокроте больных раком легкого, но не в контроле [Cameron SJS, Lewis KE, Huws SA, Hegarty MJ, Lewis PD, Pachebat JA, et al. A pilot study using metagenomic sequencing of the sputum microbiome suggests potential bacterial biomarkers for lung cancer. PLoS One. 2017;12(5):e0177062]. Инфицирование N. gonorrhoeae вызывает двойные и одиночные разрывы ДНК с образованием репарационных фокусов, содержащих γН2АХ и 53 ВР1. Кроме этого, наблюдается повышение уровней р21 и р27 ингибиторов циклинзависимой киназы, в то время как увеличения уровня р53 не происходит. Все это в конечном итоге приводит к задержке инфицированных клеток на стадии G1, способствуя тем самым выживаемости клеток хозяина, несмотря на присутствие повреждений ДНК, что, в свою очередь, может стимулировать их злокачественную трансформацию [Vielfort К, Soderholm N, Weyler L, Vare D, Lofmark S, Aro H, et al. Neisseria gonorrhoeae infection causes DNA damage and affects the expression of p21, p27 and p53 in non-tumor epithelial cells. J Cell Sci. 2013;126(1):339-347].
Основной задачей предложенного изобретения является: создание неинвазивного способа определения индивидуального риска формирования плоскоклеточного рака легкого у мужчин на основе анализа микробиома мокроты.
Технический результат данного изобретения заключается в разработке комплекса характеристик микробиома мокроты мужчин, оценка совокупности которых необходима и достаточна для более эффективного определения индивидуального риска формирования плоскоклеточного рака легкого у мужчин.
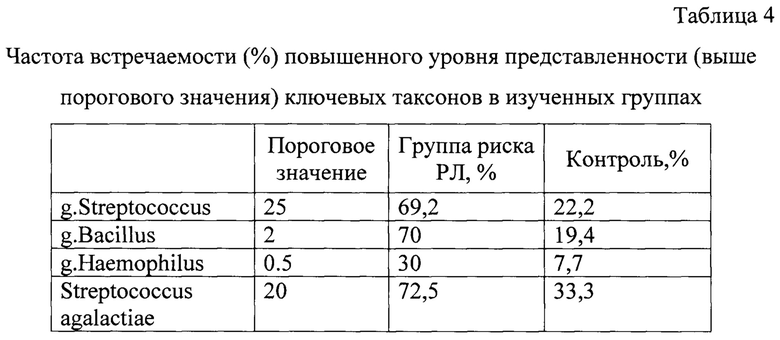
Это достигается за счет того, что в предложенном способе определения индивидуального риска формирования плоскоклеточного рака легкого выполняют высокопроизводительное секвенирование гипервариабельной (V3-V4) области гена 16S рРНК, оценивают таксономический состав микробиоты мокроты и определяют наличие предрасполагающих (содержание g. Streptococcus 25% и более; g.Bacillus 2% и более; g.Haemophilus - 0,5% и более; Streptococcus agalactiae 20% и более) и протективных маркеров (содержание g.Streptococcus ниже 25%; g.Bacillus выше 2%; g.Haemophilus ниже 0,5%; Streptococcus agalactiae ниже 20%) и делают заключение о высоком индивидуальном риске рака легкого при количественном преобладании предрасполагающих маркеров или равном количестве предрасполагающих и протективных маркеров, а при количественном преобладании протективных маркеров прогнозируют резистентность к развитию рака.
Способ выполняют в следующей последовательности:
1. Формируют группы наблюдений.
Для этого формируют две группы доноров: опытная (с высоким риском формирования плоскоклеточного РЛ) и контрольная (низкий риск). В нашем исследовании были обследованы 76 мужчин, проживающих в одной местности. У них был проведен забор мокроты в асептических условиях. Все образцы сразу замораживались и отправлялись на хранение в биобанк. Все процедуры выполнялись в соответствии с этическими стандартами, определенными Хельсинской декларацией (1964). После детального инструментального обследования в условиях онкологического диспансера у 40 человек был диагностирован плоскоклеточный рак легкого (подтвержден после биопсии тканей), у 36 мужчин не было выявлено злокачественной трансформации тканей легкого. В обследование не включали индивидов, получающих медикаментозное лечение, а также проходивших рентгенологическое обследование в течение 3 мес до сбора материала. На каждого обследуемого был оформлен протокол информированного согласия. Характеристика групп представлена в таблице 1.


ДНК выделяли из каждого образца с помощью набора FastDNA Spin Kit For Soil в соответствии с рекомендациями производителя (MP Biomedicals). Из 50 нг экстрагированной и очищенной ДНК (каждого образца) были приготовлены библиотеки ампликонов гена 16S рРНК с помощью ПЦР-амплификации 467 п. н. в гипервариабельной (V3-V4) области гена 16S рРНК (в соответствии с протоколом подготовки библиотек для метагеномного секвенирования Illumina 16S).
Обработка результатов проводилась с помощью программы QIIME2. Была проведена проверка качества и создана библиотека последовательностей. Последовательности были объединены в операционные таксономические единицы (OTU) на основе сходства нуклеотидов (порог 99%) с использованием библиотек референсных последовательностей Greengenes (версии 13-8) и SILVA (version 132). Расчет показателей альфа и бета-разнообразия проводился по методике UniFrac. Чтобы оценить значимость различий в проценте отдельных бактериальных таксонов определяли U-критерий Манна-Уитни. Расчеты выполнялись с использованием программного пакета STATISTICA.10t (Statsoft, США).
В использованном подходе к секвенированию (16S рРНК V3-V6) были идентифицированы в общей сложности более 100 таксонов с относительной частотой выше 0,1% (124 таксона в группе контроля и 109 - в группе больных РЛ). Метод UniFrac позволил выявить значимые отличия в сообществах прокариот мокроты здоровых и больных плоскоклеточным раком легкого (pseudo-F=1.94; р=0.005) и снижение бета-разнообразия у больных РЛ.
Сравнение частоты представленности ключевых таксонов в двух группах проводят по критерию Манна-Уитни с помощью ППП Statistica 10.0.
Результаты проведенного исследования показали статистически значимое повышение представленности четырех таксонов в группе больных РЛ (табл. 2).

Далее при помощи ROC-анализа (Zweig, Campbell, 1993) были рассчитаны пороговые значения представленности микроорганизмов (табл.3), что позволило условно разделить исследуемую группу на выборки с высоким и низким риском РЛ. Для оценки прогностического качества уровня представленности таксона, как маркера риска, рассчитывали его разрешающую способность AUC (Area Under Curve), которая определяется по площади под характеристической кривой:
AUC=(SP+SE)/2;
При AUC=0,90-1,0 качество модели признается отличным, при 0,80-0,89 - очень хорошим, при 0,70-0,79 - хорошим, 0,60-0,69 - средним, 0,50-0,59 - неудовлетворительным.


2. Формируют таблицу относительного риска
Проводят сравнение уровней представленности выделенных ключевых таксонов в опытной и контрольной группах.
Относительный риск и доверительный интервал рассчитывают по формулам:

где: а+0,5 - количество доноров с высоким риском РЛ носителей данного маркера; б+0,5 - количество носителей данного маркера с низким риском РЛ; с+0,5 - количество доноров с высоким риском РЛ без данного маркера; d+0,5 - количество доноров с низким риском РЛ без данного маркера (с поправкой на малое число наблюдений).
Для построения доверительного интервала берут величину L=lnOP, которую приближенно можно считать нормально распределенной со средним значением:
или 
и стандартным отклонением:

Нижней и верхней доверительными границами показателя, между которыми его показатели находятся с вероятностью 1-α, соответственно составляют величины:


где, t ∞(α) - значение критерия Стьюдента, соответствующее вероятности ошибки α; в частности, при построении 95% доверительного интервала α=0,05 и t ∞(α)=1,96; при 99% доверительного интервала α=0,01 и t ∞(α)=2,58; а при 99,9% доверительного интервала α=0,001 и t ∞(α)=3,29.
В качестве нижней и верхней доверительных границ берут антилогарифмы от величин 

где е=2,718.
Если доверительный интервал не включает значения 1,0, то ассоциацию маркер-заболевание считают статистически значимой.
Значения относительного риска для всех маркеров приведены в таблице 5. При относительном риске более 1,5 делают заключение о предрасположенности, при относительном риске менее 0,7 - о низком риске РЛ.

3. Формируют таблицу протективных и предрасполагающих маркеров (табл. 6).

4. Детальное описание способа.
Пример 1.
У обследуемого Г. 60 лет мокроту собрали в одноразовую лабораторную посуду и поместили в низкотемпературный холодильник (-80°С) до проведения анализа. Далее проводили выделение бактериальной (метагеномной) ДНК из мокроты и определение представленности ключевых таксонов. Полученные значения маркеров представлены в таблице 7. Установлено наличие 4 предрасполагающих маркеров.

Исходя из полученных результатов сделано заключение о существовании высокого риска плоскоклеточного рака легкого. Это заключение подтвердилось позднее после выполнения инструментального анализа.
Пример 2.
У обследуемого Ф. 58 лет типирование маркеров проводили так же, как описано в примере 1. Полученные результаты представлены в таблице 8.

Выявлено преобладание протективных маркеров (3 протективных и 1 предрасполагающий). Сделано заключение о генетически детерминированной устойчивости к формированию плоскоклеточного РЛ. Это заключение подтвердилось позднее после выполнения инструментального анализа.
5. Эффективность способа.
Определяли маркеры риска рака в группе мужчин, проживающих в промышленно развитом регионе (Кемеровской области). Обнаружили, что из 76 человек с относительно небольшой частотой хромосомных аберраций (2,96±0,29%) у 27 человек имело место преобладание предрасполагающих маркеров или равное количество предрасполагающих и протективных маркеров. Это свидетельствует о том, что их индивидуальный риск плоскоклеточного РЛ повышен.
Средняя частота ХА у них (4,16%) оказалась выше, чем у остальных индивидов с преобладанием протективных маркеров и обладающих индивидуальной устойчивостью к действию канцерогенов (2,38%). Очевидно, что с увеличением времени у 27 человек с выявленным риском вероятность РЛ будет возрастать в большей степени, чем у остальных индивидов.
Таким образом, группа с повышенным риском РЛ (18 человек), сформированная с помощью известного метода анализа ХА (индивиды с уровнем ХА выше 3%), увеличилась на 9 человек за счет применения предлагаемого способа, включающего в себя определение маркеров представленности ключевых микробных таксонов. То есть эффективность способа повысилась на 12%.
6. Вывод.
Предложенный способ обладает большей прогностической значимостью и применимостью, т.к. позволяет проводить оценку предрасположенности к формированию плоскоклеточного РЛ с большей эффективностью и не инвазивным способом - путем анализа предложенного комплекса характеристик микробиоты мокроты мужчин.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки риска развития рака легкого на фоне хронической обструктивной болезни легких | 2022 |
|
RU2790302C1 |
| Способ прогнозирования риска рецидива заболевания плоскоклеточным раком легкого IIб - IIIа стадии у пациентов, получивших адъювантную полихимиотерапию после радикальной операции | 2023 |
|
RU2815575C1 |
| СПОСОБ ДИАГНОСТИКИ ПЛОСКОКЛЕТОЧНОГО РАКА ЛЕГКОГО И НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2014 |
|
RU2586779C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ГЕМАТОГЕННЫХ МЕТАСТАЗОВ У БОЛЬНЫХ НЕМЕЛКОКЛЕТОЧНЫМ РАКОМ ЛЕГКОГО ПОСЛЕ ОПЕРАЦИИ | 2019 |
|
RU2733160C1 |
| СПОСОБ СКРИНИНГА НА РАК ЛЕГКИХ | 2023 |
|
RU2817246C1 |
| Способ выявления и оценки уровня патогенности возбудителей оппортунистических инфекций у женщин репродуктивного возраста и новорожденных детей для прогнозирования течения и развития осложнений инфекционных заболеваний | 2016 |
|
RU2638453C1 |
| Способ определения ответа пациента с диагнозом меланома кожи на анти-PD1-терапию | 2020 |
|
RU2771080C2 |
| Способ прогнозирования риска летального исхода в первые 4 года от начала противоопухолевого лечения у больных плоскоклеточным раком легкого | 2023 |
|
RU2817940C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЗЛОКАЧЕСТВЕННОЙ ТРАНСФОРМАЦИИ ЭРОЗИВНО-ЯЗВЕННОЙ ФОРМЫ КРАСНОГО ПЛОСКОГО ЛИШАЯ СЛИЗИСТОЙ ОБОЛОЧКИ ПОЛОСТИ РТА | 2015 |
|
RU2580222C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ ЧЕЛОВЕКА К РАЗВИТИЮ АГРЕССИВНЫХ НЕХОДЖКИНСКИХ ЛИМФОМ | 2008 |
|
RU2373862C1 |
Изобретение относится к области онкологии, генетики человека и может быть использовано для прогнозирования риска возникновения плоскоклеточного рака легких у мужчин. Проводят генетическое исследования мокроты и определяют предрасполагающие и протективные маркеры: содержание g. Streptococcus 25% и более - предрасполагающий маркер, содержание g.Streptococcus менее 25% - протективный маркер; содержание g.Bacillus 2% и более - предрасполагающий маркер, содержание g.Bacillus менее 2% - протективный маркер; содержание g.Haemophilus 0,5% и более - предрасполагающий маркер, а содержание g.Haemophilus менее 0,5% - протективный маркер; содержание Streptococcus agalactiae 20% и более - предрасполагающий маркер, содержание Streptococcus agalactiae ниже 20% - протективный маркер. Делают заключение о высоком индивидуальном риске плоскоклеточного рака легкого при количественном преобладании предрасполагающих маркеров или равном количестве предрасполагающих и протективных маркеров, а при количественном преобладании протективных маркеров прогнозируют резистентность к развитию рака. Способ обеспечивает более эффективное определение индивидуального риска формирования плоскоклеточного рака легкого у мужчин. 8 табл., 2 пр.
Способ определения индивидуального риска формирования плоскоклеточного рака легкого у мужчин, включающий анализ микробиоты мокроты путем высокопроизводительного секвенирования гипервариабельной V3-V4 области гена 16S рРНК, и при выявлении g.Streptococcus 25% и более, g.Bacillus 2% и более, g.Haemophilus - 0,5% и более, Streptococcus agalactiae 20% и более делают заключение о высоком индивидуальном риске плоскоклеточного рака легкого; при выявлении g.Streptococcus ниже 25%, g.Bacillus ниже 2%, g.Haemophilus ниже 0,5%, Streptococcus agalactiae ниже 20% прогнозируют резистентность к развитию рака.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПРЕДРАСПОЛОЖЕННОСТИ К РАКУ ЛЕГКОГО У ЛИЦ, ПРОЖИВАЮЩИХ В ЭКОЛОГИЧЕСКИ НЕБЛАГОПОЛУЧНЫХ УСЛОВИЯХ | 2004 |
|
RU2260799C1 |
| БАГИРОВА Н.С | |||
| и др | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| БЕЛЬСКАЯ Л | |||
| В | |||
| Возможности применения слюны для диагностики онкологических заболеваний //Клиническая лабораторная диагностика | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Т | |||
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| N | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| A.MADDI et al., The microbiome and lung cancer // J | |||
Авторы
Даты
2022-05-12—Публикация
2020-10-26—Подача