Настоящее изобретение относится к искусственным молекулам нуклеиновой кислоты, которые содержат открытую рамку считывания, элемент 3'-нетранслируемой области (3'-UTR-элемент) и/или элемент 5'-нетранслируемой области (5'-UTR-элемент) и необязательно поли(А)-последовательность и/или сигнал полиаденилирования. Изобретение относится также к вектору, содержащему 3'-UTR-элемент и/или 5'-UTR-элемент, к клетке, содержащей искусственную молекулу нуклеиновой кислоты или вектор, к фармацевтической композиции, содержащей искусственную молекулу нуклеиновой кислоты или вектор, и к набору, содержащему искусственную молекулу нуклеиновой кислоты, вектор и/или фармацевтическую композицию, предпочтительно предназначенным для применения в области генной терапии и/или генетической вакцинации.
Генная терапия и генетическая вакцинация относятся к наиболее перспективным и быстро развивающимся методам современной медицины. Их можно применять при разработке высокоспецифических и индивидуальных подходов для лечения широкого разнообразия заболеваний. Мишенью для таких подходов к лечению могут являться, прежде всего, врожденные генетические заболевания, а также злокачественные или связанные с опухолью заболевания и также воспалительные заболевания. Подразумевается, что с помощью указанных подходов можно предупреждать раннее начало таких заболеваний.
Основная концептуальная идея генной терапии заключается в осуществлении соответствующей модуляции нарушенной генной экспрессии, ассоциированной с патологическими состояниями при конкретных заболеваниях. Патологически измененная генная экспрессия может приводить к недостатку или сверхпроизводству имеющих важное значение генных продуктов, например, сигнальных факторов, таких как гормоны, факторы, обусловленные генами «домашнего хозяйства», метаболические ферменты, структурные белки или т.п. Измененная генная экспрессия может быть обусловлена не только нарушением регуляции транскрипции и/или трансляции, но также и мутациями в ОРС, кодирующей конкретный белок. Патологические мутации могут вызываться, например, хромосомной аберрацией или более специфическими мутациями, такими как точечные мутации или мутации, приводящие к сдвигу рамки считывания, которые все приводят к ограничению функциональности и возможно к полной потере функции генного продукта. Однако нарушение регуляции транскрипции или трансляции может иметь место также в том случае, если мутации воздействуют на гены, кодирующие белки, которые участвуют в механизме транскрипции или трансляции в клетке. Такие мутации могут приводить к патологической повышающей или понижающей регуляции генов, которые сами по себе являются функциональными. Гены, кодирующие генные продукты, которые обладают такими регуляторными функциями, могут представлять собой, например, гены факторов транскрипции, сигнальных рецепторов, белков-мессенджеров или т.п. Однако, потеря функции таких генов, кодирующих регуляторные белки, при определенных обстоятельствах может быть восстановлена путем искусственной интродукции других факторов, функционирующих по ходу транскрипции относительно нарушенного генного продукта. Такие дефекты генов можно компенсировать также с помощью генной терапии посредством замены самого поврежденного гена.
Генетическая вакцинация позволяет вызывать требуемый иммунный ответ на выбранные антигены, такие как обладающие определенными характеристиками компоненты бактериальных поверхностей, вирусные частицы, опухолевые антигены или т.п. В целом, вакцинация представляет собой одно из наиболее важных достижений современной медицины. Однако, в настоящее время эффективные вакцины доступны только для ограниченного количества заболеваний. Поэтому инфекции, которые нельзя предупреждать путем вакцинации, все еще поражают каждый год миллионы людей.
В целом, вакцины можно подразделять на вакцины «первого», «второго» и «третьего» поколения. Вакцины «первого поколения», как правило, представляют собой вакцины, содержащие цельные организмы. Они основаны либо на живых и ослабленных, либо на убитых патогенах, например, вирусах, бактериях или т.п. Основным недостатком живых и ослабленных вакцин является риск реверсии с образованием угрожающих жизни вариантов. Таким образом, указанные патогены, хотя они и являются ослабленными, все еще могут нести присущие им непредсказуемые риски. Убитые патогены могут не являться достаточно эффективными для создания специфического иммунного ответа. Для того чтобы минимизировать указанные риски, были разработаны вакцины «второго поколения». Как правило, они представляют собой субъединичные вакцины, состоящие из компонентов определенных антигенов или рекомбинантных белков, происходящих из патогенов.
Генетические вакцины, т.е. вакцины для генетической вакцинации, как правило, называют вакцинами «третьего поколения». Они, как правило, состоят из созданных методами генной инженерии молекул нуклеиновой кислоты, которые обеспечивают экспрессию in vivo фрагментов пептида или белка (антигена), характерных для патогена или опухолевого антигена. При введении пациенту экспрессия генетических вакцин происходит после поглощения клетками-мишенями. Экспрессия введенных нуклеиновых кислот приводит к производству кодируемых белков. В том случае, когда эти белки распознаются иммунной системой пациента как чужие, запускается иммунный ответ.
Как следует из вышеизложенного, оба метода, и генная терапия, и генетическая вакцинация, по существу основаны на введении молекул нуклеиновой кислоты пациенту и последующей транскрипции и/или трансляции кодируемой генетической информации. Альтернативно этому, генетическая вакцинация или генная терапия может включать также методы, которые предусматривают выделение специфических клеток из организма пациента, подлежащего лечению, последующую трансфекцию ех vivo указанных клеток и повторное введение обработанных клеток пациенту.
В контексте генной терапии или генетической вакцинации в качестве молекул нуклеиновой кислоты можно вводить как ДНК, так и РНК. Известно, что ДНК является относительно стабильной и с ней проще манипулировать. Однако применение ДНК сопряжено с риском нежелательного встраивания введенных ДНК-фрагментов в геном пациента, что может приводить к мутагенным действиям, таким как потеря функции нарушенных генов. Другим риском является то, что происходит нежелательное возникновение антител к ДНК. Еще одним недостатком является ограниченный уровень экспрессии кодируемого пептида или белка, достижимый при введении ДНК, поскольку ДНК должна проникнуть в ядро для того, чтобы произошла ее транскрипция перед тем, как могла осуществляться трансляция полученной в результате этого мРНК. Уровень экспрессии введенной ДНК может зависеть, среди прочего, от присутствия специфических факторов транскрипции, которые регулируют транскрипцию ДНК. В случае отсутствия таких факторов транскрипция ДНК не приводит к получению ДНК в достаточных количествах. В результате достигаемый уровень транслированного пептида или белка является ограниченным.
При использовании РНК вместо ДНК для генной терапии или генетической вакцинации риск нежелательной интеграции в геном и образования антител к ДНК сводится к минимуму или устраняется. Однако считается, что РНК являться относительно нестабильной молекулой, которая может легко расщепляться под действием повсеместно присутствующих РНКаз.
Расщепление РНК in vivo вносит вклад в регулирование времени полужизни РНК. Этот эффект был изучен, и было установлено, что он строго регулирует экспрессию эукариотических генов (Friedel и др., Conserved principles of mammalian transcriptional regulation revealed by RNA half-life, Nucleic Acid Research 37(17), 2009, сс. 1-12). Таким образом, каждая встречающаяся в естественных условиях мРНК имеет свое индивидуальное время полужизни, зависящее от гена, из которого происходит мРНК, и от типа клетки, в которой происходит экспрессия. Оно вносит вклад в регуляцию уровня экспрессии рассматриваемого гена. Нестабильные РНК важны для реализации кратковременной генной экспрессии в определенные моменты времени. Однако РНК с продолжительным временем жизни могут ассоциироваться с накоплением различных белков или с непрерывной экспрессией генов. Время полужизни мРНК in vivo может зависеть также от факторов окружающей среды, таких как обработка гормонами, что продемонстрировано, например, для мРНК инсулин-подобного фактора роста I, актина, и альбумина (Johnson и др.. Newly synthesized RNA: Simultaneous measurement in intact cells of transcription rates и RNA стабильность insulin-like growth factor I, actin, и albumin in growth hormone-stimulated hepatocytes, Proc. Natl. Acad. Sci., т. 88, 1991, сс. 5287-5291).
Для генной терапии и генетической вакцинации, как правило, требуется стабильная РНК. Это обусловлено, с одной стороны, тем фактом, что, как правило, требуется, чтобы in vivo происходило накопление продукта, кодируемого последовательностью РНК. С другой стороны, РНК должна сохранять свою структурную и функциональную целостность при приготовлении пригодной лекарственной формы, в процессе ее хранения и при введении. Поэтому предпринимались усилия для создания стабильных молекул РНК для генной терапии или генетической вакцинации с целью предупреждения их от раннего разложения или расщепления.
Опубликованы данные о том, что содержание G/C в молекулах нуклеиновой кислоты может оказывать влияние на ее стабильность. Так, нуклеиновые кислоты, содержащие в большем количестве остатки гуанина (G) и/или цитозина (С), могут быть функционально более стабильными, чем нуклеиновые кислоты, содержащие большое количество адениновых (А) и тиминовых (Т) или урациловых (U) нуклеотидов. В этом контексте в WO 02/098443 предложена фармацевтическая композиция, содержащая мРНК, которая стабилизирована посредством модификаций последовательности в кодирующей области. Такая модификация последовательности является возможной благодаря вырожденности генетического кода. В соответствии с этим кодоны, содержащие менее предпочтительную комбинацию нуклеотидов (менее предпочтительную с точки зрения стабильности РНК), могут быть заменены на альтернативные кодоны без изменения кодируемой аминокислотной последовательности. Такой метод стабилизации РНК ограничен тем, что для каждой отдельной молекулы РНК нужно получать конкретную нуклеотидную последовательность, которая не приводит к получению аминокислотной последовательности, отклоняющейся от требуемой. Указанный подход ограничен также тем, что его применяют к кодирующим областям РНК.
При поиске альтернативного подхода к стабилизации мРНК было установлено, что встречающиеся в естественных условиях молекулы эукариотической мРНК содержат характерные стабилизирующие элементы. Например, они могут содержать так называемые нетранслируемые области (UTR) на своем 5'-конце (5'-UTR) и/или на своем 3'-конце (3'-UTR), а также другие структурные особенности, такие как 5'-кэп-структура или 3'-поли(А)-хвост. Как 5'-UTR, так и 3'-UTR, как правило, транскрибируются с геномной ДНК и, следовательно, представляют собой элемент незрелой мРНК. Характерные структурные особенности зрелой мРНК, такие как 5'-кэп и 3'- поли(А)-хвост (которые обозначают так же, как поли(А)-хвост или поли(А)-последовательность), как правило, добавляются к транскрибированной (незрелой) мРНК в ходе процессинга мРНК.
3'-поли(А)-хвост, как правило, представляет собой монотонный участок последовательности, который состоит из аденозиновых нуклеотидов, добавленный к 3'-концу транскрибированной мРНК. Он может содержать вплоть до примерно 400 аденозиновых нуклеотидов. Установлено, что длина такого 3'-поли(А)-хвоста может являться элементом, имеющим решающее значение для стабильности индивидуальной мРНК.
Было продемонстрировано также, что 3'-UTR мРНК α-глобина может являться важным фактором, обеспечивающим хорошо известную стабильность мРНК α-глобина (Rodgers и др., Regulated α-globin mRNA decay is a cytoplasmic еще t proceeding through 3'-to-5' exosome-dependent decapping, RNA, 8, 2002, сс. 1526-1537). 3'-UTR мРНК α-глобина, по-видимому, участвует в формировании специфического рибонуклеопротеинового комплекса, α-комплекса, присутствие которого коррелирует со стабильностью мРНК in vitro (Wang и др., An mRNA стабильность complex functions with poly(A)-binding protein to stabilize mRNA in vitro. Molecular и Cellular biology, том 19, №7, июль 1999 г., сс. 4552-4560).
Кроме того, для UTR в мРНК рибосомального белка была выявлена важная регуляторная функция: хотя 5'-UTR мРНК рибосомального белка контролирует ассоциированную с ростом трансляцию мРНК, строгость указанной регулировки обеспечивается соответствующей 3'-UTR в мРНК рибосомального белка (Ledda и др.. Effect of the 3'-UTR length on the translational regulation of 5'-terminal oligopyrimidine mRNAs, Gene, т.344, 2005, сс. 213-220). Этот механизм оказывает влияние на специфическую схему экспрессии рибосомальных белков, которые, как правило, транскрибируются постоянным образом, вследствие чего мРНК некоторых рибосомальных белков, таких как рибосомальный белок S9 или рибосомальный белок L32, называют генами «домашнего хозяйства» (Janovick-Guretzky и др.. Housekeeping Gene Expression in Bovine Liver is Affected by Physiological State, Feed Intake, и Dietary Treatment, J. Dairy Sci., т. 90, 2007, сс. 2246-2252). Таким образом, ассоциированная с ростом схема экспрессии рибосомальных белков в основном обусловлена регуляцией на уровне трансляции.
В WO 2014/164253 A1 описаны некоторые специфические молекулы нуклеиновой кислоты, имеющие 5'-UTR и/или 3'-UTR, но не указаны подробности, касающиеся эффективности трансляции таких молекул.
Вне зависимости от факторов, влияющих на стабильность мРНК, эффективность трансляции введенных молекул нуклеиновой кислоты клетками-мишенями или тканью имеет решающее значение для любого подхода с использованием молекул нуклеиновой кислоты для генной терапии или генетической вакцинации. Как следует из процитированных выше примеров, структурные особенности, такие как UTR, 5'-кэп и 3'-поли(А)-хвост, наряду с регуляцией стабильности, регулируют также трансляцию большинства мРНК. В этом контексте, опубликованы данные о том, что длина поли(А)-хвоста может играть важную роль также и для эффективности трансляции. Однако стабилизирующие 3'-элементы могут оказывать также ослабляющее действие на трансляцию.
В основу настоящего изобретения была положена задача создать молекулы нуклеиновой кислоты, которые можно применять для генной терапии и/или генетической вакцинации. Задача изобретения заключалась, прежде всего, в том, чтобы создать виды мРНК, которые стабилизированы для защиты от преждевременного разложения или расщепления, но которые не характеризуются значительной функциональной потерей с точки зрения эффективности трансляции. Задачей изобретения являлось также создание искусственной молекулы нуклеиновой кислоты, предпочтительно мРНК, отличающейся высокой эффективностью трансляции. Одна из конкретных задач изобретения заключалась в создании мРНК, позволяющей повышать эффективность трансляции (производства рибосомами соответствующего кодируемого белка), например, по сравнению с референс-молекулой нуклеиновой кислоты (референс-мРНК). Другая задача настоящего изобретения заключалась в том, чтобы создать молекулы нуклеиновой кислоты, кодирующие такие обладающие преимуществами виды мРНК, которые могут быть пригодными для применения в генной терапии и/или генетической вакцинации. Следующая задача настоящего изобретения заключалась в том, чтобы создать фармацевтическую композицию для применения в генной терапии и/или генетической вакцинации. В целом, задача настоящего изобретения заключалась в создании усовершенствованных видов нуклеиновой кислоты, которые позволяют преодолевать указанные выше недостатки существующего уровня техники с использованием экономичного и простого подхода.
Задача, положенная в основу настоящего изобретения, решается с помощью объектов изобретения, представленных в формуле изобретения. В частности, при создании настоящего изобретения были идентифицированы UTR-элементы (5'-UTR-элементы и 3'-UTR-элементы), которые обеспечивают высокую эффективность трансляции. Общей характерной особенностью предпочтительных молекул нуклеиновой кислоты, предлагаемых в настоящем изобретении, является то, что все они характеризуются эффективностью трансляции, которая превышает эффективность трансляции известных ранее молекул нуклеиновой кислоты. Предложен также анализ для определения высокой эффективности трансляции относительно референс-молекулы нуклеиновой кислоты.
Настоящее изобретение было создано при поддержке правительства США в рамках соглашения № HR 0011-11-3-0001, подписанного DARPA (Агентство передовых оборонных исследовательских проектов). Правительство США обладает определенными правами на изобретение.
Для целей ясности и удобочитаемости ниже даны следующие определения. Любые технические характеристики, указанные в этих определениях, применимы к каждому и всем вариантам осуществления изобретения. В контексте этих вариантов осуществления изобретения специально могут быть даны дополнительные определения и пояснения.
Адаптивный иммунный ответ: Как правило, под адаптивным иммунным ответом понимают антигенспецифический ответ иммунной системы. Специфичность в отношении антигена позволяет вырабатывать ответы, приспособленные к специфическим патогенам или инфицированным патогеном клеткам. Способность создавать такие приспособленные ответы, как правило, поддерживается в организме «клетками памяти». Если патоген инфицирует организм более одного раза, то указанные специфические клетки памяти используются для его быстрой элиминации. В этом контексте первая стадия адаптивного иммунного ответа представляет собой активацию наивных антигенспецифических Т-клеток или других иммунных клеток, способных индуцировать антигенспецифический иммунный ответ, антигенпрезентирующими клетками. Это происходит в лимфоидных тканях и органах, через которые постоянно проходят наивные Т-клетки. Три типа клеток, которые могут служить в качестве антигенпрезентирующих клеток, представляют собой дендритные клетки, макрофаги и В-клетки. Каждая из указанных клеток выполняет отдельную функцию при вызывании иммунных ответов. Дендритные клетки могут поглощать антигены посредством фагоцитоза и макропиноцитоза, и они могут стимулироваться при контакте, например, с чужим антигеном, к миграции в местную лимфоидную ткань, где может происходить их дифференцировка в зрелые дендритные клетки. Макрофаги поглощают находящиеся в форме частиц антигены, такие как бактерии, и могут индуцироваться инфекционными агентами или другими соответствующими стимулами и экспрессировать в результате этого молекулы ГКГС. Уникальная способность В-клеток к связыванию и интернализации растворимых белковых антигенов посредством своих рецепторов также может иметь важное значение для индукции Т-клеток. ГКГС-молекулы, как правило, ответственны за презентацию антигена Т-клеткам. При этом презентация антигена на молекулах ГКГС приводит к активации Т-клеток, что индуцирует их пролиферацию и дифференцировку в «вооруженные» эффекторные Т-клетки. Наиболее важной функцией эффекторных Т-клеток является уничтожение (цитолиз) инфицированных клеток цитотоксическими CD8+-Т-клетками и активация макрофагов Th1-клетками, что в совокупности создает опосредованный клетками (клеточный) иммунитет, а активация В-клеток как Th2-, так и Th1-клетками, приводящая к образованию различных классов антител, запускает гуморальный иммунный ответ. Т-клетки распознают антиген посредством своих Т-клеточных рецепторов, которые не распознают антиген и не связываются с ним непосредственно, но вместо этого распознают короткие пептидные фрагменты, например, выведенных из патогена белковых антигенов, например, так называемые эпитопы, которые связываются с молекулами ГКГС на поверхностях других клеток.
Адаптивная иммунная система: Адаптивная иммунная система в основном предназначена для устранения или предупреждения роста патогенов. Как правило, она регулирует адаптивный иммунный ответ, придавая иммунной системе позвоночных способность распознавать и запоминать специфические патогены (для создания иммунитета) и организовывать более сильную атаку в каждом случае при обнаружении патогена. Система обладает высокой способностью к адаптации вследствие соматической гипермутации (процесс ускоренных соматических мутаций) и V(D)J-рекомбинации (необратимая генетическая рекомбинация сегментов гена рецептора антигена). Этот механизм позволяет небольшому количеству генов создавать огромное количество различных рецепторов антигенов, которые затем уникальным образом экспрессируются на каждом индивидуальном лимфоците. Поскольку реаранжировка гена приводит к необратимому изменению ДНК каждой клетки, то все потомство такой клетки должно затем наследовать гены, кодирующие ту же самую рецепторную специфичность, включая В-клетки памяти и Т-клетки памяти, которые имеют решающее значение для долговременного специфического иммунитета.
Адъювант/адъювантный компонент: Адъювант или адъювантный компонент в наиболее широком смысле, как правило, представляет собой фармакологический и/или иммунологический агент, который может модифицировать, например, усиливать, действие других агентов, таких как лекарственное средство или вакцина. Это понятие следует рассматривать в широком смысле, и оно относится к широкому спектру субстанций. Как правило, указанные субстанции обладают способностью повышать иммуногенность антигенов. Например, адъюванты могут распознаваться врожденными иммунными системами и, например, могут вызывать врожденный иммунный ответ. «Адъюванты», как правило, не вызывают адаптивный иммунный ответ. Таким образом, «адъюванты» нельзя классифицировать как антигены. Механизм их действия отличен от механизма действий, запускаемых антигенами, которые приводят к адаптивному иммунному ответу.
Антиген: В контексте настоящего изобретения понятие «антиген» относится, как правило, к субстанции, которая может распознаваться иммунной системой, предпочтительно адаптивной иммунной системой, и которая обладает способностью запускать антигенспецифический иммунный ответ, например, посредством образования антител и/или антигенспецифических Т-клеток, в качестве компонента адаптивного иммунного ответа. Как правило, антиген может представлять собой или содержать пептид или белок, который может презентироваться ГКГС Т-клеткам. В контексте настоящего изобретения антиген может представлять собой продукт трансляции предложенной молекулы нуклеиновой кислоты, предпочтительно мРНК, представленной в настоящем описании. В этом контексте под антигенами подразумевают также фрагменты, варианты и производные пептидов и белков, содержащие по меньшей мере один эпитоп. В контексте настоящего изобретения наиболее предпочтительными являются опухолевые антигены и патогенные антигены.
Иными словами, искусственную молекулу нуклеиновой кислоты можно рассматривать как молекулу нуклеиновой кислоты, не встречающуюся в естественных условиях. Такая молекула нуклеиновой кислоты может не встречаться в естественных условиях из-за своей индивидуальной последовательности (которая не встречается в естественных условиях) и/или из-за других модификаций, например, структурных модификаций нуклеотидов, которые не встречаются в естественных условиях. Искусственная молекула нуклеиновой кислоты может представлять собой молекулу ДНК, молекулу РНК или гибридную молекулу, содержащую участки ДНК и РНК. Как правило, искусственные молекулы нуклеиновой кислоты можно конструировать и/или создавать методами генетической инженерии таким образом, чтобы они соответствовали требуемой искусственной последовательности нуклеотидов (гетерологичной последовательности). В этом контексте искусственная последовательность, как правило, представляет собой последовательность, которая не может встречаться в естественных условиях, т.е. отличается от последовательности дикого типа по меньшей мере одним нуклеотидом. Можно считать, что понятие «дикий тип» относится к последовательности, встречающейся в природе. Кроме того, не следует понимать, что понятие «искусственная молекула нуклеиновой кислоты» обозначает «одну единственную молекулу», как правило, оно включает группу идентичных молекул. Следовательно, оно может относиться к множеству идентичных молекул, содержащихся в аликвоте.
Бицистронная РНК. полицистронная РНК: Бицистронная или полицистронная РНК, как правило, представляет собой РНК, предпочтительно мРНК, которая, как правило, может иметь две (бицистронная) или большее количество (полицистронная) открытых рамок считывания (ОРС). В этом контексте открытая рамка считывания представляет собой последовательность, состоящую из нескольких кодонов, которые могут транслироваться в пептид или белок.
Носитель/полимерный носитель: В контексте изобретения носитель, как правило, может представлять собой соединение, которое облегчает транспорт и/или включение в комплекс другого соединения (карго, полезный груз). Полимерный носитель, как правило, представляет собой носитель, образующий полимер. Носитель может быть связан со своим полезным грузом посредством ковалентного или нековалентного взаимодействия. Носитель может транспортировать нуклеиновые кислоты, например, РНК или ДНК, к клеткам-мишеням. Носитель может (в некоторых вариантах осуществления изобретения) представлять собой катионный компонент.
Катионный компонент: Понятие «катионный компонент», как правило, относится к заряженной молекуле, которая является положительно заряженной (катион) при значении рН, составляющем, как правило, от 1 до 9, предпочтительно при значении рН, равном или ниже 9 (например, от 5 до 9), равном или ниже 8 (например, от 5 до 8), равном или ниже 7 (например, от 5 до 7), наиболее предпочтительно при физиологическом значении рН, например, от 7,3 до 7.4. Таким образом, катионный компонент может представлять собой любое положительно заряженное соединение или полимер, предпочтительно катионный пептид или белок, который является положительно заряженным в физиологических условиях, прежде всего в физиологических условиях in vivo. «Катионный пептид или белок» может содержать по меньшей мере одну положительно заряженную аминокислоту, или более чем одну положительно заряженную аминокислоту, например, выбранную из Arg, His, Lys или Orn. Следовательно, «поликатионные» соединения также подпадают под указанное определение, если они несут более одного положительного заряда в указанных условиях.
5'-Кэп: 5'-Кэп представляет собой структуру, как правило, модифицированную нуклеотидную структуру, которая обычно «завершает (кэпирует)» 5'-конец зрелой мРНК. 5'-Кэп может, как правило, быть образован модифицированным нуклеотидом, прежде всего производным гуанинового нуклеотида. Предпочтительно 5'-кэп связан с 5'-концом через 5'-5'-трифосфатную связь. 5'-кэп может быть метилирован, например, может представлять собой m7GpppN, где N обозначает концевой 5'-нуклеотид нуклеиновой кислоты, несущей 5'-кэп, как правило, 5'-конец РНК. Другими примерами структур 5'-кэпа являются глицерил, инвертированная дезоксигруппа (фрагмент), лишенная азотистого основания, 4',5'-метиленовой нуклеотид, 1-(бета-D-эритрофуранозильный) нуклеотид, 4'-тионуклеотид, карбоциклический нуклеотид, 1,5-ангидрогекситольный нуклеотид, L-нуклеотиды, альфа-нуклеотид, нуклеотид с модифицированным основанием, треопентофуранозильный нуклеотид, ациклический 3',4'-секонуклеотид, ациклический 3,4-дигидроксибутильный нуклеотид, ациклический 3,5-дигидроксипентильный нуклеотид, 3'-3'-инвертированный нуклеотидный фрагмент, 3'-3'-инвертированный лишенный азотистого основания фрагмент, 3'-2'-инвертированный нуклеотидный фрагмент, 3'-2'-инвертированный лишенный азотистого основания фрагмент, 1,4-бутандиолфосфатный, 3'-фосфороамидатный, гексилфосфатный, аминогексилфосфатный, 3'-фосфатный, 3'-фосфоротиоатный, фосфородитиоатный или связанный мостиком или не связанный мостиком метилфосфонатный фрагмент.
Клеточный иммунитет/клеточный иммунный ответ: Клеточный иммунитет относится, как правило, к активации макрофагов, естественных клеток-киллеров (NK), антигенспецифических цитотоксических Т-лимфоцитов и высвобождению различных цитокинов в ответ на антиген. В более общем смысле клеточный иммунитет основан не на антителах, а на активации клеток иммунной системы. Как правило, клеточный иммунный ответ может характеризоваться, например, активацией антигенспецифических цитотоксических Т-лимфоцитов, которые способны индуцировать апоптоз клеток, например, специфических иммунных клеток типа дендритных клеток или других клеток, экспонирующих эпитопы чужих генов на своей поверхности. Такие клетки могут представлять собой инфицированные вирусом или инфицированные внутриклеточными бактериями, или раковые клетки, экспонирующие опухолевые антигены. Другими характеристиками могут являться активация макрофагов и естественных клеток-киллеров, позволяющая им разрушать патогены, и стимуляция клеток к секреции различных цитокинов, которые влияют на функцию других клеток, участвующих в адаптивных иммунных ответах и врожденных иммунных ответах.
ДНК: ДНК является общепринятым сокращением дезоксирибонуклеиновой кислоты. Она представляет собой молекулу нуклеиновой кислоты, т.е. полимер, состоящий из нуклеотидов. Указанные нуклеотиды, как правило, представляют собой мономеры дезоксиаденозинмонофосфата, дезокситимидинмонофосфата, дезоксигуанозинмонофосфата и дезоксицитидинмонофосфата, которые сами состоят из сахарного фрагмента (дезоксирибоза), фрагмента, представляющего собой основание, и фосфатного фрагмента, и образуют полимеры с характерной каркасной структурой. Каркасная структура, как правило, образована с помощью фосфодиэфирных связей между сахарным фрагментом нуклеотида, т.е. дезоксирибозы, первого мономера и фосфатным фрагментом второго смежного мономера. Специфический порядок мономеров, т.е. порядок оснований, сцепленных с сахарным/фосфатным каркасом, называют ДНК-последовательностью. ДНК может быть одноцепочечной или двухцепочечной. В двухцепочечной форме нуклеотиды первой цепи, как правило, гибридизуются с нуклеотидами второй цепи, например, путем спаривания оснований А/Т и спаривания оснований G/C.
Эпитоп: Эпитопы (которые называют также «антигенными детерминантами») можно подразделить на Т-клеточные эпитопы и В-клеточные эпитопы. В контексте настоящего изобретения Т-клеточные эпитопы или части белков могут содержать фрагменты, предпочтительно имеющие длину от примерно 6 до примерно 20 или даже более аминокислот, например, фрагменты, процессируемые и презентируемые молекулами ГКГС класса I, предпочтительно имеют длину от примерно 8 до примерно 10 аминокислот, например, 8, 9 или 10, (или даже 11 или 12 аминокислот), или фрагменты, процессируемые и презентируемые молекулами ГКГС класса II, предпочтительно имеют длину примерно 13 аминокислот или более, например, 13, 14, 15, 16, 17, 18, 19, 20 или даже большее количество аминокислот, при этом указанные фрагменты можно выбирать из любой части аминокислотной последовательности. Указанные фрагменты, как правило, распознаются Т-клетками в форме комплекса, состоящего из пептидного фрагмента и молекулы ГКГС, т.е. фрагменты, как правило, не распознаются в их нативной форме. В-клеточные эпитопы, как правило, представляют собой фрагменты, локализованные на внешней поверхности (нативных) белковых или пептидных антигенов, указанных в настоящем описании, предпочтительно состоящих из 5-15 аминокислот, более предпочтительно состоящих из 5-12 аминокислот, еще более предпочтительно состоящих из 6-9 аминокислот, которые могут распознаваться антителами, т.е. в их нативной форме.
Такие эпитопы белков или пептидов можно, кроме того, выбирать из любых указанных вариантов таких белков или пептидов. В этом контексте антигенные детерминанты могут представлять собой конформационные или прерывистые эпитопы, состоящие из сегментов указанных в настоящем описании белков или пептидов, которые расположены с перерывами в аминокислотной последовательности белков или пептидов, указанных в настоящем описании, но которые находятся вблизи друг от друга в трехмерной структуре, или непрерывные или линейные эпитопы, состоящие из одной полипептидной цепи.
Фрагмент последовательности: фрагмент последовательности, как правило, представляет собой укороченный участок полноразмерной последовательности, например, молекулы нуклеиновой кислоты или аминокислотной последовательности. Следовательно, фрагмент, как правило, состоит из последовательности, которая идентична соответствующему сегменту полноразмерной последовательности. В контексте настоящего изобретения предпочтительный фрагмент последовательности состоит из непрерывного сегмента, содержащего такие элементы, как нуклеотиды или аминокислоты, который соответствует непрерывному состоящему из указанных элементов сегменту молекулы, из которой происходит фрагмент, длина которого составляет по меньшей мере 30%, более предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 50%, еще более предпочтительно по меньшей мере 60%, еще более предпочтительно по меньшей мере 70%, и наиболее предпочтительно по меньшей мере 80% от всей (т.е. полноразмерной) молекулы, из которой происходит фрагмент.
G/C-модифицированная: G/C-модифицированная нуклеиновая кислота, как правило, может представлять собой нуклеиновую кислоту, предпочтительно искусственную молекулу нуклеиновой кислоты, указанную в настоящем описании, созданную на основе модифицированной последовательности дикого типа, которая содержит предпочтительно повышенное количество гуанозиновых и/или цитозиновых нуклеотидов по сравнению с последовательностью дикого типа. Для получения указанного повышенного количества можно осуществлять замену кодонов, содержащих аденозиновые или тимидиновые нуклеотиды, на кодоны, содержащие гуанозиновые или цитозиновые нуклеотиды. При повышенном содержании G/C в кодирующей области ДНК или РНК, при заменах можно использовать вырожденность генетического кода. Таким образом, замены кодонов предпочтительно не изменяют кодируемые аминокислотные остатки, но исключительно увеличивают содержание G/C в молекуле нуклеиновой кислоты.
Генная терапия: Генная терапия, как правило, может представлять собой лечение организма пациента или выделенных элементов организма пациента, например, выделенных тканей/клеток, с помощью нуклеиновых кислот, кодирующих пептид или белок. Как правило, она может включать по меньшей мере одну из следующих стадий а) введение нуклеиновой кислоты, предпочтительно искусственной молекулы нуклеиновой кислоты, указанной в настоящем описании, непосредственно пациенту - любым путем введения - либо in vitro в выделенные клетки/ткани пациента, что приводит к трансфекции клеток пациента, либо in vivo/ex vivo, либо in vitro; б) транскрипция и/или трансляция интродуцированной молекулы нуклеиновой кислоты; и необязательно в) повторное введение выделенных трансфектированных клеток пациенту, если нуклеиновую кислоту не вводили непосредственно пациенту.
Генетическая вакцинация: Генетическая вакцинация, как правило, может представлять собой вакцинацию, осуществляемую путем введения молекулы нуклеиновой кислоты, кодирующей антиген или иммуноген или его фрагменты. Молекулу нуклеиновой кислоты можно вводить в организм индивидуума или в выделенные клетки индивидуума. После трансфекции определенных клеток организма или после трансфекции выделенных клеток антиген или иммуноген может экспрессироваться указанными клетками и затем презентироваться иммунной системе, вызывая адаптивный, т.е. антигенспецифический иммунный ответ. Таким образом, генетическая вакцинация, как правило, включает по меньшей мере одну из следующих стадий: а) введение нуклеиновой кислоты, предпочтительно искусственной молекулы нуклеиновой кислоты, указанной в настоящем описании, индивидууму, предпочтительно пациенту, или в выделенные клетки индивидуума, предпочтительно пациента, что обычно приводит к трансфекции клеток индивидуума in vivo или in vitro; б) транскрипцию и/или трансляцию интродуцированной молекулы нуклеиновой кислоты; и необязательно в) повторное введение выделенных трансфектированных клеток индивидууму, предпочтительно пациенту, если нуклеиновую кислоту не вводили непосредственно пациенту.
Гетерологичная последовательность: Как правило, считается, что две последовательности являются «гетерологичными», если они не происходят из одного и того же гена. Это означает, что, хотя гетерологичные последовательности могут происходить из одного и того же организма, они в естественных условиях (в природе) не встречаются в одной и той же молекуле, например, в одной и той же молекуле нуклеиновой кислоты.
Гуморальный иммунитет/гуморальный иммунный ответ: Гуморальный иммунитет, как правило, относится к производству антител и необязательно к вспомогательным процессам, которые могут сопровождать его. Гуморальный иммунный ответ, как правило, может характеризоваться, например, активацией Th2 и производством цитокинов, образованием зародышевого центра и переключением изотипа, созреванием аффинности и образованием клеток памяти. Гуморальный иммунитет, как правило, может относиться также к эффекторным функциям антител, включая нейтрализацию патогенов и токсинов, классическую активацию комплемента и стимулирование опсонинами фагоцитоза и элиминации патогенов.
Иммуноген: В контексте настоящего изобретения под иммуногеном, как правило, понимают соединение, которое обладает способностью стимулировать иммунный ответ. Предпочтительно иммуноген представляет собой пептид, полипептид или белок. В наиболее предпочтительном варианте осуществления изобретения иммуноген в контексте настоящего изобретения представляет собой продукт трансляции применяемой молекулы нуклеиновой кислоты, предпочтительно искусственной молекулы нуклеиновой кислоты, указанной в настоящем описании. Как правило, иммуноген вызывает по меньшей мере адаптивный иммунный ответ.
Иммуностимулирующая композиция: В контексте изобретения иммуностимулирующая композиция, как правило, может представлять собой композицию, содержащую по меньшей мере один компонент, который обладает способностью индуцировать иммунный ответ или из которого может происходить компонент, обладающий способностью индуцировать иммунный ответ. Такой иммунный ответ предпочтительно может представлять собой врожденный иммунный ответ или комбинацию адаптивного и врожденного иммунного ответа. В контексте настоящего описания иммуностимулирующая композиция предпочтительно содержит по меньшей мере одну искусственную молекулу нуклеиновой кислоты, более предпочтительно РНК, например, молекулу мРНК. Иммуностимулирующий компонент, такой как мРНК, может находиться в составе комплекса с пригодным носителем. Таким образом, иммуностимулирующая композиция может содержать комплекс мРНК/носитель. Кроме того, иммуностимулирующая композиция может содержать адъювант и/или пригодный наполнитель для иммуностимулирующего компонента, такого как мРНК.
Иммунный ответ: Иммунный ответ может, как правило, представлять собой либо специфическую реакцию адаптивной иммунной системы на конкретный антиген (так называемый специфический или адаптивный иммунный ответ), либо неспецифическую реакцию врожденной иммунной системы (так называемый неспецифический или врожденный иммунный ответ), либо их комбинацию.
Иммунная система: Иммунная система может защищать организмы от инфекции. Если патогену удалось преодолеть физический барьер организма и попасть в указанный организм, то врожденная иммунная система обеспечивает немедленный, но неспецифический ответ. Если патоген ускользает от этого врожденного ответа, у позвоночных имеется второй уровень защиты, представляющий собой адаптивную иммунную систему. В этом случае иммунная система адаптирует свой ответ в процессе инфекции для улучшения распознавания патогена. Затем этот улучшенный ответ сохраняется после элиминации патогена в форме иммунологической памяти и позволяет адаптивной иммунной системе организовывать более быстрые и сильные атаки каждый раз при проникновении указанного патогена. Таким образом, иммунная система включает врожденную и адаптивную иммунную систему. Каждая из этих двух частей, как правило, включает так называемые гуморальный и клеточный компоненты.
Иммуностимулирующая РНК: Иммуностимулирующая РНК (isPHK) в контексте изобретения, как правило, может представлять собой РНК, которая обладает способностью индуцировать врожденный иммунный ответ. Обычно она не имеет открытой рамки считывания и, таким образом, не кодирует пептид-антиген или иммуноген, но вызывает иммунный ответ, например, посредством связывания со специфическим типом Толл-подобного рецептора (TLR) или другими приемлемыми рецепторами. Однако, естественно, также и мРНК, имеющие открытую рамку считывания и кодирующие пептид/белок, могут индуцировать врожденный иммунный ответ и, следовательно, могут являться иммуностимулирующими РНК.
Врожденная иммунная система: Врожденная иммунная система, которую называют также неспецифической иммунной системой, как правило, включает клетки и механизмы, которые неспецифически защищают хозяина от заражения другими организмами. Это означает, что клетки врожденной системы могут распознавать патогены и реагировать на них обычным путем, но, в отличие от адаптивной иммунной системы, она не обеспечивает долговременный или защитный иммунитет хозяину. Врожденная иммунная система может, например, активироваться лигандами патоген-ассоциированных распознающих молекулярные паттерны (РАМР) рецепторов, например, Толл-подобных рецепторов (TLR), или другими вспомогательными субстанциями, такими как липополисахариды, TNF-альфа, лиганд CD40 или цитокины, монокины, лимфокины, интерлейкины или хемокины, IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-25, IL-26, IL-27, IL-28, IL-29, IL-30, IL-31, IL-32, IL-33, IFN-альфа, IFN-бета, IFN-гамма, GM-CSF, G-CSF, M-CSF, LT-бета, TNF-альфа, факторы роста и hGH, лиганд человеческого Толл-подобного рецептора TLR1, TLR2, TLR3, TLR4, TLR5, TLR6, TLR7, TLR8, TLR9, TLR10, лиганд мышиного Толл-подобного рецептора TLR1, TLR2, TLR3, TLR4, TLR5, TLR6, TLR7, TLR8, TLR9, TLR10, TLR11, TLR12 или TLR13, лиганд NOD-подобного рецептора, лиганд RIG-1-подобного рецептора, Иммуностимулирующая нуклеиновая кислота, Иммуностимулирующая РНК (isPHK), CpG-ДНК, антибактериальный агент или противовирусный агент. Как правило, ответ врожденной иммунной системы включает рекрутинг иммунных клеток к областям заражения посредством производства химических факторов, включая специализированные химические медиаторы, которые называют цитокинами; активацию каскада комплемента; идентификацию и удаление чужих субстанций, присутствующих в органах, тканях, крови и лимфе, специализированными лейкоцитами; активацию адаптивной иммунной системы посредством процесса, известного как презентация антигена; и/или функционирование в качестве физического и химического барьера для инфекционных агентов.
Сайт клонирования: Под сайтом клонирования, как правило, понимают сегмент молекулы нуклеиновой кислоты, пригодный для встраивания нуклеотидной последовательности, например, нуклеотидной последовательности, содержащей открытую рамку считывания. Встраивание можно осуществлять с помощью любого метода молекулярной биологии, известного специалисту в данной области, например, посредством рестрикции и лигирования. Сайт клонирования, как правило, содержит один или несколько сайтов, распознаваемых рестриктазами (сайты рестрикции). Указанные один или несколько сайтов рестрикции могут распознаваться рестриктазами, расщепляющими ДНК в этих сайтах. Сайт клонирования, который содержит более одного сайта рестрикции, можно обозначать также как множественный сайт клонирования (MCS) или полилинкер.
Молекула нуклеиновой кислоты: Молекула нуклеиновой кислоты представляет собой молекулу, которая содержит, предпочтительно состоит из компонентов нуклеиновой кислоты. Понятие «молекула нуклеиновой кислоты» предпочтительно относится к молекулам ДНК или РНК. Его предпочтительно применяют в качестве синонима понятия «полинуклеотид». Предпочтительно молекула нуклеиновой кислоты представляет собой полимер, содержащий или состоящий из нуклеотидных мономеров, которые ковалентно связаны друг с другом фосфодиэфирными связями сахарного/фосфатного каркаса. Понятие «нуклеиновая кислота» включает также модифицированные молекулы нуклеиновой кислоты, такие как молекулы ДНК или РНК с модифицированным основанием, модифицированным сахарным фрагментом или модифицированным каркасом.
Открытая рамка считывания: Открытая рамка считывания (ОРС) в контексте изобретения, как правило, может представлять собой состоящую из нескольких нуклеотидных триплетов последовательность, которая может транслироваться в пептид или белок. Открытая рамка считывания предпочтительно содержит на своем 5'-конце стартовый кодон, т.е. комбинацию трех последовательно расположенных нуклеотидов, кодирующих, как правило, аминокислоту метионин (ATG или AUG), и следующую за ним область, длина которой, как правило, кратна 3 нуклеотидам. ОРС предпочтительно оканчивается стоп-кодоном (например, ТАА, TAG, TGA). Как правило, в открытой рамке считывания присутствует только один стоп-кодон. Таким образом, открытая рамка считывания в контексте настоящего изобретения предпочтительно представляет собой нуклеотидную последовательность, состоящую из кратного трем количества нуклеотидов, которая начинается стартовым кодоном (например, ATG или AUG), и которая предпочтительно заканчивается стоп-кодоном (например, ТАА, TGA или TAG, или UAA, UAG, UGA соответственно). Открытая рамка считывания может быть выделена или она может быть встроена в более длинную нуклеотидную последовательность, например, в вектор или мРНК. Открытую рамку считывания можно называть также «кодирующей белок областью».
Пептид: Пептид или полипептид, как правило, представляет собой полимер, состоящий из аминокислотных мономеров, связанных пептидными связями. Он, как правило, содержит менее 50 мономерных звеньев. Однако понятие «пептид» не исключает молекулы, имеющие более 50 мономерных звеньев. Длинные пептиды называют также полипептидами, как правило, они имеют от 50 до 600 мономерных звеньев.
Фармацевтически эффективное количество: В контексте изобретения под фармацевтически эффективным количеством, как правило, понимают количество, достаточное для того, чтобы индуцировать фармацевтическое действие, такое как иммунный ответ, измененный патологический уровень экспрессируемого пептида или белка, или замену недостающего генного продукта, например, в случае наличия патологической ситуации.
Белок: Белок, как правило, содержит один или несколько пептидов или полипептидов. Белок, как правило, уложен с образованием 3-мерной структуры, которая может требоваться для проявления биологической функции белка.
Поли(А)-последовательность: Поли(А)-последовательность, которую называют также поли(А)-хвостом или 3'-поли(А)-хвостом, как правило, представляет собой последовательность аденозиновых нуклеотидов, содержащую, например, вплоть до примерно 400 аденозиновых нуклеотидов, например, от примерно 25 до примерно 400, предпочтительно от примерно 50 до примерно 400, более предпочтительно от примерно 50 до примерно 300, еще более предпочтительно от примерно 50 до примерно 250, наиболее предпочтительно от примерно 60 до примерно 250 аденозиновых нуклеотидов. Поли(А)-последовательность, как правило, локализована на 3'-конце мРНК. В контексте настоящего изобретения поли(А)-последовательность может быть локализована внутри мРНК или любой другой молекулы нуклеиновой кислоты, например, внутри вектора, например, вектора, служащего в качестве матрицы для создания РНК, предпочтительно мРНК, например, при транскрипции вектора.
Полиаденилирование: Под полиаденилированием, как правило, понимают добавление поли(А)-последовательности к молекуле нуклеиновой кислоты, такой как молекула РНК, например, незрелая мРНК. Полиаденилирование может индуцироваться так называемым сигналом полиаденилирования. Указанный сигнал предпочтительно локализован в сегменте нуклеотидов на 3'-конце молекулы нуклеиновой кислоты, такой как молекула РНК, подлежащая полиаденилированию. Сигнал полиаденилирования, как правило, содержит гексамер, состоящий из адениновых и/или урациловых/тиминовых нуклеотидов, предпочтительно последовательность гексамера AAUAAA. Также возможны другие последовательности, предпочтительно гексамерные последовательности. Полиаденилирование, как правило, имеет место во время процессинга пре-мРНК (которую называют также незрелой мРНК). Как правило, созревание РНК (превращение пре-мРНК в зрелую мРНК) включает стадию полиаденилирования.
Сайт рестрикции: Сайт рестрикции, который называют также как сайт, распознаваемый рестриктазой, представляет собой нуклеотидную последовательность, распознаваемую рестрктазой. Сайт рестрикции, как правило, представляет собой короткую, предпочтительно палиндромную нуклеотидную последовательность, например, последовательность, содержащую от 4 до 8 нуклеотидов. Сайт рестрикции предпочтительно специфически распознается рестриктазой. Рестриктаза, как правило, расщепляет нуклеотидную последовательность, содержащую сайт рестрикции, в этом сайте. В двухцепочечной нуклеотидной последовательности, такой как двухцепочечная последовательность ДНК, рестриктаза, как правило, расщепляет обе цепи нуклеотидной последовательности.
РНК, мРНК: РНК является общепринятым сокращением для рибонуклеиновой кислоты. Она представляет собой молекулу нуклеиновой кислоты, т.е. полимер, состоящий из нуклеотидов. Указанные нуклеотиды представляют собой, как правило, мономеры аденозинмонофосфата, уридинмонофосфата, гуанозинмонофосфата и цитидинмонофосфата, соединенные друг с другом вдоль так называемого каркаса. Каркас формируется с помощью фосфодиэфирных связей между сахаром, т.е. рибозой, первого мономера и фосфатным фрагментом второго смежного мономера. Конкретную последовательность мономеров называют РНК-последовательностью. Как правило, РНК можно получать путем транскрипции ДНК-последовательности, например, внутри клетки. В эукариотических клетках транскрипция, как правило, происходит в ядре или в митохондрии. In vivo транскрипция ДНК, как правило, приводит к образованию так называемой незрелой РНК, которая в результате процессинга должна превратиться в так называемую матричную (информационную) РНК, которую сокращенно обозначают как мРНК. Процессинг незрелой РНК, например, в эукариотических организмах, включает ряд различных пост-транскрипционных модификаций, таких как сплайсинг, 5'-кэпирование, полиаденилирование, экспорт из ядра или митохондрии и т.п. Совокупность указанных процессов называют также созреванием РНК. Зрелая матричная РНК, как правило, представляет собой нуклеотидную последовательность, которая может транслироваться в аминокислотную последовательность конкретного пептида или белка. Как правило, зрелая мРНК содержит 5'-кэп, 5'UTR, открытую рамку считывания, необязательно 3'UTR и поли(А)-последовательность. Помимо матричной РНК существует несколько некодирующих типов РНК, которые могут участвовать в регуляции транскрипции и/или трансляции.
Последовательность молекулы нуклеиновой кислоты: Под последовательностью молекулы нуклеиновой кислоты, как правило, понимают конкретный и индивидуальный порядок расположения, т.е. последовательный ряд входящих в нее нуклеотидов. Под последовательностью белка или пептида, как правило, понимают порядок расположения, т.е. последовательный ряд входящих в него аминокислот.
Идентичность последовательности: Две или большее количество последовательностей являются идентичными, если они имеют одинаковую длину и порядок расположения нуклеотидов или аминокислот. Процент идентичности, как правило, характеризует степень идентичности двух последовательностей, т.е. он, как правило, характеризует процент нуклеотидов, которые соответствуют по своему положению идентичным нуклеотидам референс-последовательности. При определении степени идентичности считается, что подлежащие сравнению последовательности имеют одну и ту же длину, т.е. длину наиболее длинной последовательности из подлежащих сравнению последовательностей. Это означает, что первая последовательность, состоящая из 8 нуклеотидов, идентична на 80% второй последовательности, состоящей из 10 нуклеотидов, которая содержит первую последовательность. Другими словами, в контексте настоящего изобретения идентичность последовательностей предпочтительно относится к проценту нуклеотидов в последовательности, которые находятся в одних и тех же положениях в двух или большем количестве последовательностей, имеющих одинаковую длину. При сравнительном анализе первичной структуры последовательностей бреши обычно рассматривают как неидентичные положения безотносительно к их действительному положению.
Стабилизированная молекула нуклеиновой кислоты: Стабилизированная молекула нуклеиновой кислоты представляет собой молекулу нуклеиновой кислоты, предпочтительно молекулу ДНК или РНК, модифицированную таким образом, чтобы она обладала большей стабильностью к расщеплению или разрушению, например, факторами окружающей среды, или ферментативному расщеплению, такому как расщепление экзо- или эндонуклеазами, чем молекула нуклеиновой кислоты без модификации. Предпочтительно стабилизированная молекула нуклеиновой кислоты в контексте настоящего изобретения является стабилизированной в клетке, такой как прокариотическая или эукариотическая клетка, предпочтительно в клетке млекопитающего, такой как человеческая клетка. Стабилизирующее действие можно оказывать также вне клеток, например, в буферном растворе и т.д., например, в процессе производства фармацевтической композиции, которая содержит стабилизированную молекулу нуклеиновой кислоты.
Трансфекция: Понятие «трансфекция» относится к интродукции молекул нуклеиновой кислоты, таких как молекулы ДНК или РНК (например, мРНК), в клетки, предпочтительно в эукариотические клетки. В контексте настоящего изобретения под понятие «трансфекция» подпадает любой известный специалисту в данной области метод интродукции молекул нуклеиновой кислоты в клетки, предпочтительно в эукариотические клетки, такие как клетки млекопитающих. Такие методы включают, например, электропорацию, липофекцию, например, на основе катионных липидов и/или липосом, осаждение фосфатом кальция, трансфекцию на основе наночастиц, трансфекцию на основе вирусов или трансфекцию на основе катионных полимеров, таких как ДЭАЭ-декстран или полиэтиленимин, и т.д. Предпочтительно интродукцию осуществляют без использования вирусов.
Трансляционная эффективность (или эффективность трансляции): В контексте настоящего описания указанное понятие, как правило, относится к свойству молекулы нуклеиновой кислоты (например, мРНК), содержащей открытую рамку считывания (ОРС). Эффективность трансляции поддается количественной оценке. Эффективность трансляции, как правило, измеряют путем определения количества белка, транслированного с ОРС. При экспериментальной количественной оценке эффективности трансляции предпочтительно ОРС кодирует репортерный белок или любой другой белок, поддающийся количественной оценке. Однако, не вдаваясь в какую-либо конкретную теорию, можно считать, что высокая эффективность трансляции, как правило, обеспечивается специфическим UTR-элементом (специфическим 5'-UTR-элементом или специфическим 3'-UTR-элементом). Таким образом, в контексте настоящего изобретения понятие «эффективность трансляции» используют, прежде всего, применительно к молекулам нуклеиновой кислоты, которые содержат помимо ОРС по меньшей мере один 5'-UTR-элемент и/или по меньшей мере один 3'-UTR-элемент, предпочтительно представленный в настоящем описании. Хотя для целей экспериментальной количественной оценки эффективности трансляции следует использовать ОРС, кодирующую репортерный белок или любой другой белок, который можно количественно оценивать, настоящее изобретение не ограничивается такими целями; следовательно, по меньшей мере один 5'-UTR-элемент и/или по меньшей мере один 3'-UTR-элемент, предлагаемый в изобретении (который обеспечивает высокую эффективность трансляции), может содержаться в молекуле нуклеиновой кислоты, содержащей ОРС, которая не кодирует репортерный белок.
Эффективность трансляции является относительным понятием. Так, можно определять и сравнивать эффективность трансляции различных, например, двух или большего количества молекул нуклеиновой кислоты, например, путем экспериментальной количественной оценки белка, колируемого ОРС. Это можно осуществлять в стандартизованных условиях, например, с помощью стандартизованного анализа, представленного в настоящем описании. Таким образом, эффективность трансляции, определенная в стандартизованных условиях, является объективной характеристикой. Предпочтительно определяют и сравнивают эффективность трансляции двух молекул нуклеиновой кислоты. Первую из указанных двух молекул нуклеиновой кислоты можно обозначить как «рассматриваемая молекула нуклеиновой кислоты» или «рассматриваемая конструкция», а вторую из указанных двух молекул нуклеиновой кислоты можно обозначить как «референс-молекула нуклеиновой кислоты» или «референс-конструкция». Рассматриваемая молекула нуклеиновой кислоты может представлять собой искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении. Для рассматриваемой цели референс-молекула нуклеиновой кислоты и рассматриваемая молекула нуклеиновой кислоты должны иметь одну и ту же ОРС (имеющую идентичную нуклеотидную последовательность); и предпочтительно нуклеотидная последовательность рассматриваемой молекулы нуклеиновой кислоты идентична нуклеотидной последовательности референс-молекулы нуклеиновой кислоты за исключением UTR-элемента, подлежащего тестированию, т.е. либо 5'-ЦТК--элемента, либо 3'-UTR-элемента; иными словами, рассматриваемая молекула нуклеиновой кислоты и референс-молекула нуклеиновой кислоты предпочтительно отличаются друг от друга только тем, что либо их 5'-UTR-элементы, либо их 3'-UTR-элементы имеют отличную друг от друга нуклеотидную последовательность; таким образом, 5'-UTR-элемент или 3'-UTR-элемент представляет собой единственную структурную особенность, которая отличает рассматриваемую молекулу нуклеиновой кислоты от референс-молекулы нуклеиновой кислоты.
В представленном в настоящем описании анализе рассматриваемой молекулой нуклеиновой кислоты и референс-молекулой нуклеиновой кислоты трансфектируют клетки млекопитающего и определяют эффективность трансляции. Если эффективность трансляции рассматриваемой молекулы нуклеиновой кислоты выше, чем эффективность трансляции референс-молекулы нуклеиновой кислоты, то считается, что рассматриваемая молекула нуклеиновой кислоты должна характеризоваться высокой эффективностью трансляции. В этом случае считается, что 5'-UTR-элемент или 3'-UTR-элемент, которым различаются рассматриваемая молекула нуклеиновой кислоты и референс-молекула нуклеиновой кислоты, обеспечивает высокую эффективность трансляции (рассматриваемой молекулы нуклеиновой кислоты). Иными словами, считается, что высокая эффективность трансляции должна «обеспечиваться» специфическим 5'-UTR-элементом или 3'-UTR-элементом, который присутствует в рассматриваемой молекуле нуклеиновой кислоты, но не присутствует в референс-молекуле нуклеиновой кислоты; и считается, что рассматриваемая молекула нуклеиновой кислоты (или искусственная молекула нуклеиновой кислоты), которая содержит такую 5'-UTR или 3'-UTR и по меньшей мере одну ОРС, «должна характеризоваться» высокой эффективностью трансляции.
Вакцина: Под вакциной, как правило, понимают предназначенный для профилактики или терапии продукт, содержащий по меньшей мере один антиген, предпочтительно иммуноген. Антиген или иммуноген может иметь происхождение из любого материала, пригодного для вакцинации. Например, антиген или иммуноген может происходить из патогена, такого как бактерии или вирусные частицы и т.д., или из опухолевой или раковой ткани. Антиген или иммуноген стимулирует адаптивную иммунную систему организма вырабатывать адаптивный иммунный ответ.
Вектор: Понятие «вектор» относится к молекуле нуклеиновой кислоты, предпочтительно к искусственной молекуле нуклеиновой кислоты. В контексте настоящего изобретения вектор можно применять для встраивания или хранения требуемой нуклеотидной последовательности, такой как нуклеотидная последовательность, содержащая открытую рамку считывания. Таким векторы могут представлять собой векторы для хранения, экспрессионные векторы, клонирующие векторы, векторы для переноса и т.д. Вектор для хранения представляет собой вектор, который позволяет удобно хранить молекулу нуклеиновой кислоты, например, молекулу мРНК. Так, вектор может содержать последовательность, соответствующую, например, требуемой последовательности мРНК или ее части, такой как последовательность, соответствующая открытой рамке считывания и 3'-UTR и/или 5'-UTR мРНК. Экспрессионный вектор можно применять для производства продуктов экспрессии, таких как РНК, например, мРНК, или пептиды, полипептиды или белки. Например, экспрессионный вектор может содержать последовательности, необходимые для транскрипции сегмента последовательности вектора, такой как промоторная последовательность, например, промоторная последовательность РНК-полимеразы. Клонирующий вектор, как правило, представляет собой вектор, который содержит сайт клонирования, который можно применять для встраивания нуклеотидных последовательностей в вектор. Клонирующий вектор может представлять собой, например, плазмидный вектор или вектор на основе бактериофага. Вектор для переноса может представлять собой вектор, который пригоден для переноса молекул нуклеиновой кислоты в клетки или организмы, например, вирусные векторы. В контексте настоящего изобретения вектор может представлять собой, например, РНК-вектор или ДНК-вектор. Предпочтительно вектор представляет собой молекулу ДНК. В контексте настоящего описания предпочтительно вектор содержит сайт клонирования, маркер для селекции, такой как фактор, обусловливающий устойчивость к антибиотикам, и последовательность, пригодную для размножения вектора, такую как сайт инициации репликации. В контексте настоящего описания предпочтительно вектор представляет собой плазмидный вектор.
Наполнитель: Под наполнителем, как правило, понимают материал, пригодный для хранения, транспортирования и/или введения соединения, такого как фармацевтически активное соединение. Он может представлять собой, например, физиологически приемлемую жидкость, пригодную для хранения, транспортирования и/или введения соединения, такого как фармацевтически активное соединение.
3'-нетранслируемая область (3'-UTR): Как правило, понятие «3'-UTR» относится к части искусственной молекулы нуклеиновой кислоты, которая локализована с 3'-стороны (т.е. «по ходу транскрипции») открытой рамки считывания и которая не транслируется в белок. Как правило, 3'-UTR представляет собой часть мРНК, которая локализована между кодирующей белок областью (открытой рамкой считывания (ОРС) или кодирующей последовательностью (CDS)) и поли(А)-последовательностью мРНК. В контексте изобретения понятие «3'-UTR» может включать также элементы, которые не кодируются в матрице, с которой транскрибируется РНК, но которые добавляются после транскрипции в процессе созревания, например, поли(А)-последовательность. 3'-UTR мРНК не транслируется в аминокислотную последовательность. Последовательность 3'-UTR, как правило, кодируется геном, который транскрибируется в соответствующую мРНК в процессе экспрессии гена. Геномная последовательность сначала транскрибируется в незрелую мРНК, которая содержит необязательные интроны. Незрелая мРНК затем дополнительно процессируется с образованием зрелой мРНК в процессе созревания. Указанный процесс созревания включает стадии 5'-кэпирования, сплайсинга незрелой мРНК с вырезанием необязательных интронов и модификаций 3'-конца, таких как полиаденилирование 3'-конца незрелой мРНК, и необязательные расщепления эндо-/или экзонуклеазами и т.д. В контексте настоящего изобретения 3'-UTR соответствует последовательности зрелой мРНК, которая локализована между стоп-кодоном кодирующей области белка, предпочтительно непосредственно примыкает с 3'-стороны к стоп-кодону кодирующей белок области, и поли(А)-последовательностью мРНК. Понятие «соответствует» означает, что последовательность 3'-UTR может представлять собой последовательность РНК, такую как в последовательности мРНК, указанной в определении последовательности 3'UTR, или последовательность ДНК, которая соответствует указанной последовательности РНК. В контексте настоящего изобретения понятие «3'-UTR гена» означает последовательность, которая соответствует 3'-UTR зрелой мРНК, полученной из указанного гена, т.е. мРНК, полученной путем транскрипции гена и созревания незрелой мРНК. Понятие «3'-UTR гена» включает последовательность ДНК и последовательность РНК (как смысловую, так и антисмысловую цепи, и как зрелые, так и незрелые последовательности) 3'-UTR. Предпочтительно 3'-UTR имеют длину более 20, 30, 40 или 50 нуклеотидов.
5'-нетранслируемая область (5'-UTR): Понятие «5'-UTR», как правило, относится к части искусственной молекулы нуклеиновой кислоты, которая локализована с 5'-стороны (т.е. «в обратном направлении») относительно открытой рамки считывания мРНК и которая не транслируется в белок. Под 5'-UTR, как правило, понимают конкретный сегмент матричной РНК (мРНК), который локализован с 5'-стороны открытой рамки считывания мРНК. Как правило, 5'-UTR начинается с сайта инициации транскрипции и заканчивается за один нуклеотид до стартового кодона открытой рамки считывания. Предпочтительно 5'-UTR имеет длину более 20, 30, 40 или 50 нуклеотидов. 5'-UTR может содержать элементы, предназначенные для контроля генной экспрессии, так называемые регуляторные элементы. Указанные регуляторные элементы могут представлять собой, например, сайты связывания рибосом. 5'-UTR может подвергаться пост-транскрипционным модификациям, например, путем добавления 5'-кэпа. 5'-UTR не транслируется в аминокислотную последовательность. Последовательность 5'-UTR, как правило, кодируется геном, который транскрибируется в соответствующую мРНК в процессе генной экспрессии. Геномная последовательность сначала транскрибируется в незрелую мРНК, которая содержит необязательные интроны. Незрелая мРНК затем дополнительно процессируется с образованием зрелой мРНК в процессе созревания. Указанный процесс созревания включает стадии 5'-кэпирования, сплайсинга незрелой мРНК с вырезанием необязательных интронов и модификаций 3'-конца, таких как полиаденилирование 3'-конца незрелой мРНК, и необязательные расщепления эндо-/или экзонуклеазами и т.д. В контексте настоящего изобретения 5'-UTR соответствует последовательности зрелой мРНК, локализованной между стартовым кодоном и, например, 5'-кэпом. Предпочтительно 5'-UTR соответствует последовательности, которая простирается от нуклеотида, расположенного с 3'-стороны 5'-кэпа, более предпочтительно от нуклеотида, непосредственно примыкающего с 3'-стороны к 5'-кэпу, до нуклеотида, расположенного с 5'-стороны стартового кодона кодирующей белок области, предпочтительно до нуклеотида, непосредственно примыкающего с 5'-стороны к стартовому кодону кодирующей белок области. Нуклеотид, непосредственно примыкающий с 3'-стороны к 5'-кэпу зрелой мРНК, как правило, соответствует сайту инициации транскрипции. Понятие «соответствует» означает, что последовательность 5'-UTR может представлять собой последовательность РНК, такую как в последовательности мРНК, указанной при определении последовательности 5'UTR, или последовательность ДНК, которая соответствует указанной последовательности РНК. В контексте настоящего изобретения понятие «5'-UTR гена» обозначает последовательность, которая соответствует 5'-UTR зрелой мРНК, полученной из этого гена, т.е. мРНК, полученной путем транскрипции гена и созревания незрелой мРНК. Понятие «5'UTR гена» включает последовательность ДНК и последовательность РНК (как смысловую, так и антисмысловую цепи, и как зрелые, так и незрелые последовательности) 5'-UTR.
5'-концевой олигопиримидиновый тракт (ТОР): 5'-концевой олигопиримидиновый тракт (ТОР), как правило, обозначает сегмент пиримидиновых нуклеотидов, локализованный в 5'-концевой области молекулы нуклеиновой кислоты, например, в 5'-концевой области некоторых молекул мРНК или в 5'-концевой области функционального элемента, например, транскрибируемой области некоторых генов. Последовательность начинается с цитидина, который, как правило, соответствует сайту инициации транскрипции, и за которым следует сегмент, как правило, состоящий примерно из 3-30 пиримидиновых нуклеотидов. Например, ТОР может содержать 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или даже большее количество нуклеотидов. Пиримидиновый сегмент и, следовательно, 5'-ТОР, заканчивается одним нуклеотидом, расположенным в 5'-направлении относительно первого пуринового нуклеотида, локализованного по ходу транскрипции относительно ТОР. Матричную РНК, которая содержит 5'-концевой олигопиримидиновый тракт, часто обозначают как ТОР-мРНК. Таким образом, гены, из которых получают указанные матричные РНК, обозначают как ТОР-гены. Последовательности ТОР, например, обнаружены в генах и мРНК, кодирующих пептидные факторы элонгации и рибосомальные белки.
ТОР-мотив: В контексте настоящего изобретения ТОР-мотив представляет собой нуклеотидную последовательность, которая соответствует 5'-ТОР, описанному выше. Таким образом, ТОР-мотив в контексте настоящего изобретения предпочтительно обозначает состоящий из пиримидиновых нуклеотидов сегмент длиной 3-30 нуклеотидов. Предпочтительно ТОР-мотив состоит по меньшей мере из 3 пиримидиновых нуклеотидов, предпочтительно по меньшей мере 4 пиримидиновых нуклеотидов, предпочтительно по меньшей мере 5 пиримидиновых нуклеотидов, более предпочтительно по меньшей мере 6 нуклеотидов, более предпочтительно по меньшей мере 7 нуклеотидов, наиболее предпочтительно по меньшей мере 8 пиримидиновых нуклеотидов, при этом сегмент пиримидиновых нуклеотидов предпочтительно начинается на его 5'-конце с цитозинового нуклеотида. В ТОР-генах и ТОР-мРНК ТОР-мотив предпочтительно начинается на его 5'-конце с сайта инициации транскрипции и заканчивается на расстоянии одного нуклеотида в 5'-направлении относительно первого пуринового остатка в указанном гене или мРНК. В контексте настоящего изобретения ТОР-мотив предпочтительно локализован на 5'-конце последовательности, которая представляет собой 5'-UTR, или на 5'-конце последовательности, которая кодирует 5'-UTR. Таким образом, в контексте настоящего изобретения сегмент из 3 или большего количества пиримидиновых нуклеотидов предпочтительно называют «ТОР-мотивом», если сегмент локализован на 5'-конце соответствующей последовательности, такой как искусственная молекула нуклеиновой кислоты, 5'UTR-элемент искусственной молекулы нуклеиновой кислоты или нуклеотидная последовательность, которая происходит из 5'-UTR ТОР-гена, представленной в настоящем описании. Другими словами, сегмент, состоящий из 3 или большего количества пиримидиновых нуклеотидов, который не локализован на 5'-конце 5'-UTR или 5'-UTR-элемента, но локализован где-либо внутри 5'-UTR или 5'-UTR-элемента, предпочтительно не обозначают как «ТОР-мотив».
ТОР-ген: ТОР-гены, как правило, характеризуются присутствием 5'-концевого олигопримидинового тракта. Кроме того, большинство ТОР-генов характеризуются связанной с ростом регуляцией трансляции. Однако известны также ТОР-гены с тканеспецифической регуляцией трансляции. Как указано выше, 5'-UTR ТОР-гена соответствует последовательности 5'-UTR зрелой мРНК, происходящей из ТОР-гена, которая предпочтительно простирается от нуклеотида, примыкающего с 3'-стороны к 5'-кэпу, до нуклеотида, примыкающего с 5'-стороны к стартовому кодону. 5'-UTR ТОР-гена, как правило, не содержит никаких стартовых кодонов, предпочтительно не содержит расположенных в обратном направлении AUG (uAUG) или расположенных в обратном направлении открытых рамок считывания (uOPC). В данном контексте под расположенными в обратном направлении AUG и расположенными в обратном направлении открытыми рамками считывания, как правило, понимают AUG и открытые рамки считывания, которые находятся в 5'-направлении относительно стартового кодона (AUG) открытой рамки считывания, которая должна транслироваться. 5'-UTR ТОР-генов, как правило, являются относительно короткими. Длины 5'-UTR ТОР-генов могут варьироваться от 20 нуклеотидов вплоть до 500 нуклеотидов и, как правило, они содержат менее чем примерно 200 нуклеотидов, предпочтительно менее чем примерно 150 нуклеотидов, более предпочтительно менее чем примерно 100 нуклеотидов. Примерами 5'-UTR ТОР-генов в контексте настоящего изобретения являются нуклеотидные последовательности, простирающиеся от нуклеотида в положении 5 до нуклеотида, непосредственно примыкающего к 5'-концу стартового кодона (например, ATG) в последовательностях, которые представлены в SEQ ID NO: 1-1363 заявки на патент РСТ/ЕР 2012/002448, содержание которой включено в настоящее описание в качестве ссылки. В этом контексте наиболее предпочтительным фрагментом 5'-UTR ТОР-гена является 5'-UTR ТОР-гена без 5'ТОР-мотива. Понятия «5'-UTR ТОР-гена» или «5'-ТОР UTR» предпочтительно относится к 5'-UTR встречающегося в естественных условиях ТОР-гена. Предпочтительным примером является SEQ ID NO: 208 (5'-UTR большой субъединицы человеческого рибосомального белка 32 без 5'-концевого олигопиримидинового тракта); которая соответствует SEQ ID NO: 1368, представленной в заявке на патент WO 2013/143700).
Дикий тип, например, молекула нуклеиновой кислоты дикого типа: Понятие «дикий тип» может относиться к последовательности, встречающейся в естественных условиях. Под молекулой нуклеиновой кислоты дикого типа, как правило, следует понимать молекулу нуклеиновой кислоты, например, ДНК или РНК, которая встречается в естественных условиях. Иными словами, под искусственной молекулой нуклеиновой кислоты можно понимать встречающуюся в естественных условиях молекулу нуклеиновой кислоты. Такая молекула нуклеиновой кислоты может рассматриваться как встречающаяся в естественных условиях благодаря ее индивидуальной последовательности (которая встречается в естественных условиях) и/или вследствие наличия других модификаций, например, структурных модификаций нуклеотидов, которые встречаются в естественных условиях. Молекула нуклеиновой кислоты дикого типа может представлять собой молекулу ДНК, молекулу РНК или гибридную молекулу, содержащую ДНК- и РНК-сегменты. В контексте настоящего описания понятие «дикий тип» относится к любой последовательности, если она встречается в природе, при этом не требуется, чтобы она имелась в публично доступных коллекциях последовательностей, таких как GenBank. Национальные институты здоровья (NIH) располагают публично доступной аннотированной коллекцией публично доступных нуклеотидных последовательностей («GenBank», доступной с помощью системы поиска NCBI Entrez: http://www.ncbi.nlm.nih.gov), (Nucleic Acids Research; 41(D1), 2013, D36-42), которая включает публично доступные последовательности дикого типа. Каждой единице записи в GenBank приписан уникальный постоянный идентификатор, называемый кодом доступа и присутствующий в строке ACCESSION единицы записи в GenBank; а изменения в данных о последовательности отслеживаются с помощью численного расширения кода доступа, присутствующего в строке VERSION единицы записи в GenBank. Кроме того, понятие «молекула нуклеиновой кислоты дикого типа» не сводится к понятию «одна единственная молекула», а, как правило, подразумевается, что оно включает совокупность идентичных молекул. Следовательно, оно относится к множеству идентичных молекул, содержащихся в аликвоте.
Подробное описание
Изобретение относится к искусственной молекуле нуклеиновой кислоты, содержащей по меньшей мере одну открытую рамку считывания и по меньшей мере один элемент 3'-нетранслируемой области (3'-UTR-элемент), и/или по меньшей мере один элемент 5'-нетранслируемой области (5'-UTR-элемент), где указанная искусственная молекула нуклеиновой кислоты характеризуется высокой эффективностью трансляции. Эффективность трансляции обусловлена, по меньшей мере частично, 5'-UTR-элементом или 3'-UTR-элементом, или и 5'-UTR-элементом и 3'-UTR-элементом. Изобретение относится также к применению такой искусственной молекулы нуклеиновой кислоты в генной терапии и/или генетической вакцинации. Кроме того, предложены новые 3'-UTR-элементы и 5'-UTR-элементы.
Первый объект настоящего изобретения относится к искусственной молекуле нуклеиновой кислоты, содержащей
а. по меньшей мере одну открытую рамку считывания (ОРС); и
б. по меньшей мере один элемент, представляющий собой 3'-нетранслируемую область (3'-UTR-элемент), и/или по меньшей мере один элемент, представляющий собой 5'-нетранслируемую область (5'-UTR-элемент),
где указанная искусственная молекула нуклеиновой кислоты характеризуется высокой эффективностью трансляции.
Например, искусственная молекула нуклеиновой кислоты, предлагаемая в изобретении, может отличаться от других (например, дикого типа или искусственных) молекул нуклеиновой кислоты тем, что по меньшей мере один 3'-UTR-элемент (предпочтительно один 3'-UTR-элемент) заменен по меньшей мере на один неидентичный 3'-UTR-элемент (предпочтительно на один 3'-UTR-элемент), или тем, что по меньшей мере один 5'-UTR-элемент (предпочтительно один 5'-UTR-элемент) заменен по меньшей мере на один неидентичный 5'-UTR-элемент (предпочтительно на один 5'-UTR-элемент).
В целом, замена одного (или по меньшей мере одного) 3'-UTR-элемента или замена одного (или по меньшей мере одного) 5'-UTR-элемента (в исходной молекуле нуклеиновой кислоты или референс-молекуле нуклеиновой кислоты), как правило, означает, что последовательность, содержащую по меньшей мере некоторые нуклеотиды указанного 3'-UTR-элемента или указанного 5'-UTR-элемента, заменяют на неидентичную последовательность нуклеиновой кислоты. Предпочтительно, когда заменяют 5'-UTR-элемент, то непрерывную последовательность нуклеотидов 5'-UTR-элемента заменяют на неидентичную непрерывную последовательность (элемент) нуклеотидов; а когда заменяют 3'-UTR-элемент, то непрерывную последовательность нуклеотидов 3'-UTR-элемента заменяют на неидентичную непрерывную последовательность (элемент) нуклеотидов. Непрерывная последовательность нуклеотидов исходного (подлежащего замене) элемента и заменяющего элемента, каждая независимо может иметь любую длину, например, от 1 до более чем 500 нуклеотидов, от 20 до 500 нуклеотидов, от 40 до 400 нуклеотидов, от 60 до 300 нуклеотидов, от 80 до 200 нуклеотидов или от 100 до 150 нуклеотидов. Когда заменяют (5'- или 3'-) UTR-элемент, это не означает, что необходимо заменять все нуклеотиды, расположенные с 5'-стороны от стартового кодона или все нуклеотиды, расположенные с 3'-стороны от стоп-кодона. В предпочтительных вариантах осуществления изобретения заменяют непрерывную последовательность, которая представляет собой поднабор всех нуклеотидов, локализованных с 5'-стороны от стартового кодона, или поднабор всех нуклеотидов, локализованных с 3'-стороны от стоп-кодона соответственно. Такие примеры представлены на фиг. 1Б (5') и 1В (3'). Можно заменять строго известный 5'-UTR-элемент или известный 3'-UTR-элемент, присутствующий в исходной последовательности или референс-последовательности. Например, если нуклеиновая кислота (например, нуклеиновая референс-кислота) содержит 5'-UTR-элемент, соответствующий последовательности, представленной в SEQ ID NO: 208, то искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, можно создавать путем замены строго всей непрерывной последовательности, представленной в SEQ ID NO: 208, на неидентичный непрерывный 5'-UTR-элемент, предлагаемый в настоящем изобретении, т.е. на 5'-UTR-элемент, который обеспечивает высокую эффективность трансляции. Альтернативно этому, можно заменять не только (строго) известный UTR-элемент, например, заменять непрерывную нуклеотидную последовательность, содержащую дополнительные нуклеотиды, т.е. являющиеся дополнительными по отношению к известному UTR-элементу, или, например, заменять только часть известного UTR-элемента (как правило, основную часть, т.е. 90% его длины или более). Хотя эти возможности проиллюстрированы в настоящем описании для случая 5'-UTR-элементов, те же самые возможности существуют также и для 3'-UTR-элементов. Иными словами, замещенный UTR-элемент не обязательно должен строго соответствовать границам известного UTR-элемента. Эти возможности дополнительно проиллюстрированы с помощью примера на фиг. 1Б и фиг. 1В соответственно, в каждом случае в сравнении с фиг. 1А. Аналогично этому замещающий UTR-элемент не обязательно должен строго соответствовать границам известного UTR-элемента.
Предпочтительно искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, не содержит 3'-UTR (элемент) и/или 5'-UTR (элемент) рибосомального белка S6, RPL36AL, rps16 или рибосомального белка L9. Более предпочтительно искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, не содержит 3'-UTR (элемент) и/или 5'-UTR (элемент) рибосомального белка S6, RPL36AL, rps16 или рибосомального белка L9 и открытая рамка считывания искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, не кодирует белок GFP. Еще более предпочтительно искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, не содержит 3'-UTR (элемент) и/или 5'-UTR (элемент) рибосомального белка S6, RPL36AL, rps16 или рибосомального белка L9 и открытая рамка считывания искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, не кодирует репортерный белок, например, выбранный из группы, которая состоит из белков глобина (прежде всего, бета-глобина), белка люциферазы, белков GFP, белков глюкуронидазы (прежде всего, бета-глюкуронидазы) или их вариантов, например, вариантов, последовательности которых идентичны по меньшей мере на 70% последовательности белка глобина, белка люциферазы, белка GFP или белка глюкуронидазы.
Понятие «3'-UTR-элемент» относится к нуклеотидной последовательности, которая содержит или состоит из нуклеотидной последовательности, полученной из 3'-UTR или из варианта или фрагмента 3'-UTR. Понятие «3'-UTR-элемент» предпочтительно относится к нуклеотидной последовательности, которая содержится в 3'-UTR искусственной нуклеотидной последовательности, такой как искусственная мРНК. Следовательно, в контексте настоящего изобретения 3'-UTR-элемент предпочтительно может представлять собой 3'-UTR мРНК, предпочтительно искусственной мРНК, или может содержаться в 3'-UTR соответствующей матрицы для транскрипции. Предпочтительно 3'-UTR-элемент представляет собой нуклеотидную последовательность, которая соответствует 3'-UTR мРНК, предпочтительно 3'-UTR искусственной мРНК, такой как мРНК, полученная в результате транскрипции созданной генетическими методами векторной конструкции. Предпочтительно 3'-UTR-элемент в контексте настоящего изобретения функционирует в качестве 3'-UTR или кодирует нуклеотидную последовательность, которая выполняет функцию 3'-UTR.
Соответственно понятие «5'-UTR-элемент» относится к нуклеотидной последовательности, которая содержит или состоит из нуклеотидной последовательности, полученной из 5'-UTR или из варианта или фрагмента 5'-UTR. Понятие «5'-UTR-элемент» предпочтительно относится к нуклеотидной последовательности, которая содержится в 5'-UTR искусственной нуклеотидной последовательности, такой как искусственная мРНК. Следовательно, в контексте настоящего изобретения 5'-UTR-элемент предпочтительно может представлять собой 5'-UTR мРНК, предпочтительно искусственной мРНК, или может содержаться в 5'-UTR соответствующей матрицы для транскрипции. Предпочтительно 5'-UTR-элемент представляет собой нуклеотидную последовательность, которая соответствует 5'-UTR мРНК, предпочтительно 5'-UTR искусственной мРНК, такой как мРНК, полученной в результате транскрипции созданной генетическими методами векторной конструкции. Предпочтительно 5'-UTR-элемент в контексте настоящего изобретения функционирует в качестве 5'-UTR или кодирует нуклеотидную последовательность, которая выполняет функцию 5'-UTR.
3'-UTR-элемент и/или 5'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении, обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты. Так, искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может, в частности, содержать:
3'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты,
5'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты,
3'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, и 5'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты.
Предпочтительно искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, содержит 3'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, и/или 5'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты.
Предпочтительно искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, содержит по меньшей мере один 3'-UTR-элемент и по меньшей мере один 5'-UTR-элемент, а именно, по меньшей мере один 3'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, и по меньшей мере один 5'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты.
Как подробно описано ниже, указанный по меньшей мере один 3'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, или указанный по меньшей мере один 5'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, может быть выбран из встречающихся в естественных условиях (предпочтительно гетерологичных) 3'-UTR-элементов и 5'-UTR-элементов (в совокупности обозначены как встречающиеся в естественных условиях UTR-элементы или UTR-элементы дикого типа), и из искусственных 3'-UTR-элементов и искусственных 5'-UTR-элементов (в совокупности обозначены как искусственные UTR-элементы). UTR-элементы дикого типа можно выбирать из группы, состоящей из UTR-элементов дикого типа, известных из литературы и имеющихся в публично доступных базах данных, таких как GenBank (NCBI), и UTR-элементов дикого типа, которые не были ранее опубликованы. Последние можно идентифицировать путем секвенирования мРНК, присутствующих в клетках, предпочтительно в клетках млекопитающих. С использованием такого подхода при создании изобретения было идентифицировано несколько не опубликованных ранее UTR-элементов дикого типа, и UTR-элементы этого типа предложены в настоящем изобретении. Понятие «искусственный UTR-элемент» не накладывает специальных ограничений и может относиться к любой нуклеотидной последовательности, которая не обнаружена в естественных условиях, т.е. не является идентичной UTR-элементу дикого типа. Однако, в предпочтительных вариантах осуществления изобретения искусственный UTR-элемент, применяемый согласно настоящему изобретению, представляет собой нуклеотидную последовательность, которая обладает определенной степенью идентичности с последовательностью UTR-элемента дикого типа, например, составляющей от 10 до 99,9%, от 20 до 99%, от 30 до 98%, от 40 до 97%, от 50 до 96%, от 60 до 95%, от 70 до 90%. В предпочтительных вариантах осуществления изобретения искусственная UTR, применяемая согласно настоящему изобретению, идентична UTR дикого типа за исключением того, что один или два, или три, или четыре, или пять или более пяти нуклеотидов заменены таким же количеством нуклеотидов (например, один нуклеотид заменен на один нуклеотид). Предпочтительно замена одного нуклеотида представляет собой замену на соответствующий комплементарный нуклеотид. Предпочтительные искусственные UTR-элементы соответствуют UTR-элементам дикого типа за исключением того, что (I) некоторые или все триплеты ATG в 5'-UTR-элементе дикого типа (если они присутствуют) превращены в триплет TAG; и/или (II) выбранный(е) сайт(ы) расщепления конкретной рестриктазой в 5'-UTR-элементе дикого типа или в 3'-UTR-элементе дикого типа (если он присутствует) элиминированы путем замены одного нуклеотида в сайте расщепления указанной специфической рестриктазой на комплементарный нуклеотид, что приводит к удалению сайтов расщепления указанной специфической рестриктазой. Последнее, как правило, требуется в том случае, когда UTR-элемент (например, дикого типа) содержит сайт расщепления указанной специфической рестриктазой, и когда указанную конкретную рестриктазу используют (планируют использовать) на последующих стадиях клонирования.
Поскольку такое расщепление внутри 5'-UTR-элементов и 3'-UTR-элементов является нежелательным, то можно создавать искусственный UTR-элемент, в котором элиминирован сайт рестрикции, расщепляемый указанной специфической рестриктазой. Такую замену можно осуществлять с помощью любого пригодного метода, известного специалисту в данной области, например, с помощью ПЦР с использованием модифицированных праймеров.
Искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, необязательно содержит по меньшей мере один 3'-UTR-элемент и по меньшей мере один 5'-ЦТК-элемент, а именно, по меньшей мере один 3'-UTR-элемент, который пролонгирует и/или повышает производство белка, кодируемого указанной искусственной молекулой нуклеиновой кислоты, и по меньшей мере один 5'-UTR-элемент, который пролонгирует и/или повышает производство белка, кодируемого указанной искусственной молекулой нуклеиновой кислоты.
Производство белка: Анализ для определения того, имеет ли место пролонгирование и/или повышение производства белка
«Пролонгирование и/или повышение производства белка с указанной искусственной молекулы нуклеиновой кислоты» в целом относится к количеству белка, продуцируемого с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, которая содержит соответствующий 3'-UTR-элемент и/или 5'-UTR-элемент, по сравнению с количеством белка, продуцируемого с соответствующей нуклеиновой референс-кислоты, которая не содержит 3'-UTR и/или 5'-UTR или содержит референс-3'-UTR и/или референс-5'-UTR, такую как 3'-UTR и/или 5'-UTR, встречающаяся в естественных условиях в комбинации с ОРС.
В частности, по меньшей мере один 3'-UTR-элемент и/или 5'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, пролонгирует производство белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, например, с мРНК, предлагаемой в настоящем изобретении, по сравнению с соответствующей нуклеиновой кислотой, которая не содержит 3'-UTR и/или 5'-UTR или содержит референс-3'-UTR и/или референс-5'- UTR, такую как 3'-UTR и/или 5'-UTR, встречающаяся в естественных условиях в комбинации с ОРС.
В частности, по меньшей мере один 3'-UTR-элемент и/или 5'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, повышает производство белка, прежде всего экспрессию белка или общее производство белка, с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, например, с мРНК, предлагаемой в настоящем изобретении, по сравнению с соответствующей нуклеиновой кислотой, которая не содержит 3'-UTR и/или 5'-UTR или содержит референс-3'-UTR и/или референс-5'-UТР, такую как 3'-UTR и/или 5'-UTR, встречающаяся в естественных условиях в комбинации с ОРС.
Предпочтительно по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, не оказывает отрицательного влияния на эффективность трансляции нуклеиновой кислоты по сравнению с эффективностью трансляции соответствующей нуклеиновой кислоты, которая не содержит 3'-UTR и/или 5'-UTR или содержит референс-3'-UTR и/или референс-5'-UTR, такую как 3'-UTR и/или 5'-UTR, встречающаяся в естественных условиях в комбинации с ОРС. В альтернативном варианте 3'-UTR и/или 5'-UTR повышают эффективность трансляции по сравнению с эффективностью трансляции белка, кодируемого соответствующей ОРС в ее естественной окружении.
Понятие «соответствующая молекула нуклеиновой кислоты» или «референс-молекула нуклеиновой кислоты», используемое в настоящем описании, означает, что за исключением различных 3'-UTR и/или 5'-UTR, референс-молекула нуклеиновой кислоты сопоставима, предпочтительно идентична, искусственной молекуле нуклеиновой кислоты, предлагаемой в изобретении, которая содержит 3'-UTR-элемент и/или 5'-UTR-элемент.
Для оценки производства белка с предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты in vivo или in vitro, как указано в настоящем описании (т.е. in vitro относится к («живым») клеткам и/или ткани, включая ткань живого индивидуума; клетки включают, в частности, клеточные линии, первичные клетки, клетки в ткани или в организме индивидуумов, предпочтительными являются клетки млекопитающих, например, человеческие клетки и мышиные клетки, и наиболее предпочтительными являются человеческие линии клеток HeLa, HEPG2 и U-937 и мышиные линии клеток NIH3T3, JAWSII и L929, кроме того, наиболее предпочтительными являются первичные клетки, в наиболее предпочтительных вариантах осуществления изобретения - человеческие кожные фибробласты (HDF)), определяют экспрессию кодируемого белка после осуществления инъекции/трансфекции предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты в клетки-/ткани-мишени и сравнения с экспрессией белка, индуцируемой нуклеиновой референс-кислотой. В данной области известны количественные методы определения экспрессии белка (например, вестерн-блоттинг, FACS, ELISA, масс-спектрометрия). В рассматриваемом контексте наиболее пригодным является определение экспрессии репортерных белков типа люциферазы, зеленого флуоресцентного белка (GFP) или секретируемой щелочной фосфатазы (SEAP). Для этого искусственную нуклеиновую кислоту, предлагаемую в изобретении, или нуклеиновую референс-кислоту интродуцируют в ткань-мишень или клетку-мишень, например, посредством трансфекции или инъекции, предпочтительно в систему экспрессии млекопитающих, такую как клетки млекопитающих, например, в клетки линии HDF, L929, HepG2 и/или Hela. Через несколько часов или через несколько дней (например, через 6, 12, 24, 48 или 72 ч) после инициации экспрессии или после интродукции молекулы нуклеиновой кислоты берут образец клеток-мишеней и проводят измерения с помощью FACS и/или лизируют. После этого лизаты можно использовать для обнаружения экспрессированного белка (и определения тем самым эффективности экспрессии белка) с помощью нескольких методов, например, вестерн-блоттинга, FACS, ELISA, масс-спектрометрии или путем измерения флуоресценции или люминесценции.
Следовательно, если экспрессию белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, сравнивают с экспрессией белка с референс-молекулы нуклеиновой кислоты в определенные моменты времени (например, через 6, 12, 24, 48 или 72 ч после инициации экспрессии или после интродукции молекулы нуклеиновой кислоты), то обе молекулы нуклеиновой кислоты интродуцируют по отдельности в ткани-/клетки-мишени, берут образец ткани/клеток в определенный момент времени, приготавливают белковые лизаты согласно конкретному протоколу, скорректированному для конкретного метода обнаружения (например, для вестерн-блоттинга, ELISA, измерения флуоресценции или люминесценции и т.д., как это известно в данной области) и проводят обнаружение белка с помощью выбранного метода обнаружения. В качестве альтернативы измерениям количеств экспрессируемого белка в клеточных лизатах, или в дополнение к измерениям количеств белка в клеточных лизатах, с помощью FACS-анализа можно определять количества белка также до лизиса собранных клеток или параллельно с использованием аликвот.
Понятие «пролонгирование производства белка» с искусственной молекулы нуклеиновой кислоты, такой как искусственная мРНК, предпочтительно означает, что производство белка с искусственной молекулы нуклеиновой кислоты, такой как искусственная мРНК, пролонгируется по сравнению с производством белка с референс-молекулы нуклеиновой кислоты, такой как референс-мРНК, например, которая содержит референс-3'-UTR и/или референс-5'-UTR или в которой отсутствует 3'-UTR и/или референс-5'-UTR, предпочтительно в экспрессионной системе млекопитающих, такой как HDF, L929, HEP2G или HeLa-клетки. Так, белок, продуцируемый с искусственной молекулы нуклеиновой кислоты, такой как искусственная мРНК, можно обнаруживать в течение более длительного периода времени, чем тот, в течение которого можно обнаруживать белок, продуцируемый с референс-молекулы нуклеиновой кислоты. Иными словами, количество белка, продуцированного с искусственной молекулы нуклеиновой кислоты, такой как искусственная мРНК, измеренное в более поздний момент времени, например, через 48 ч или 72 ч после трансфекции, больше, чем количество белка, продуцированного с референс-молекулы нуклеиновой кислоты, такой как референс-мРНК, в соответствующий более поздний момент времени. Такой «более поздний момент времени» может представлять собой, например, любой момент времени по истечении 24 ч после инициации экспрессии, такой как трансфекция молекулой нуклеиновой кислоты, например, через 36, 48, 60, 72, 96 ч после инициации экспрессии, т.е. после трансфекции. Кроме того, для одной и той же нуклеиновой кислоты количество белка, продуцированного в более поздний момент времени, можно стандартизовать относительно количества, продуцированного в более ранний (референс) момент времени, например, количество белка, продуцированного в более поздний момент времени, можно выражать в виде процента от количества белка через 24 ч после трансфекции.
Предпочтительно эффект пролонгирования производства белка определяют путем (I) измерения количеств белка, например, полученных в результате экспрессии кодируемого репортерного белка, такого как люцифераза, предпочтительно в экспрессионной системе млекопитающих, такой как клетки линии HDF, L929, HEP2G или HeLa, в зависимости от времени, (II) определения количества белка, обнаруженного в «референс-момент» времени t1, например, t1=24 ч после трансфекции, при этом указанное количество белка принимают за 100%, (III) измерения количества белка, обнаруженного в один или несколько более поздних моментов времени t2, t3 и т.д., например, t2=48 ч и t3=72 ч после трансфекции, и расчета относительного количества белка, обнаруженного в более поздний момент времени в виде процента от количества белка в момент времени t1. Например, для белка, экспрессированного в момент времени t1 в количестве «80», в момент времени t2 в количестве «20» и в момент времени t3 в количестве «10», относительное количество белка в момент времени t2 будет составлять 25%, а в момент времени t3 12,5%. Затем эти относительные количества в более поздний момент времени можно сравнивать на стадии (IV) с относительными количествами белка в соответствующие моменты времени, полученными в случае молекулы нуклеиновой кислоты, не содержащей 3'- и/или 5'-UTR соответственно или содержащей референс-3'-UTR и/или референс-5'-UTR соответственно. Путем сравнения относительного количества белка, продуцированного с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, с относительным количеством белка, продуцированного с референс-молекулы нуклеиновой кислоты, т.е. молекулы, не содержащей 3'- и/или 5'-UTR соответственно или содержащей референс-3'-UTR и/или референс-5'-UTR соответственно, можно определять коэффициент, характеризующий, во сколько раз пролонгируется производство белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, по сравнению с производством белка с референс-молекулы нуклеиновой кислоты.
Предпочтительно по меньшей мере один 3'- и/или 5'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в изобретении, пролонгирует производство белка с указанной искусственной молекулы нуклеиновой кислоты по меньшей мере в 1,2 раза, предпочтительно по меньшей мере в 1,5 раза, более предпочтительно по меньшей мере в 2 раза, еще более предпочтительно по меньшей мере в 2,5 раза по сравнению с производством белка с референс-молекулы нуклеиновой кислоты, которая не содержит 3'- и/или 5'-UTR соответственно или содержит референс-3'-UTR и/или референс-5'-UTR соответственно. Иными словами, (относительное) количество белка, продуцированного с искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, в определенный более поздний момент времени, указанный выше, повышается на коэффициент, составляющий по меньшей мере 1,2, предпочтительно по меньшей мере 1,5, более предпочтительно по меньшей мере 2, еще более предпочтительно по меньшей мере 2,5, по сравнению с (относительным) количеством белка, продуцированным с референс-молекулы нуклеиновой кислоты, которая не содержит 3'- и/или 5'-UTR соответственно или содержит референс-3'-UTR и/или референс-5'-UTR соответственно, в тот же самый более поздний момент времени.
Альтернативно этому пролонгирующее действие на производство белка можно определять также путем (I) измерения количеств белка, например, полученных в результате экспрессии кодируемого репортерного белка, такого как люцифераза, предпочтительно в экспрессионной системе млекопитающих, такой как клетки линии HDF, L929, HEP2G или HeLa, в зависимости от времени, (II) определения момента времени, в который количество белка становится ниже количества белка, обнаруженного, например, через 1, 2, 3, 4, 5 или 6 ч после инициации экспрессии, например, через 1, 2, 3, 4, 5 или 6 ч после трансфекции искусственной молекулой нуклеиновой кислоты, и (III) сравнения момента времени, который количество белка становится ниже количества белка, обнаруженного, например, через 1, 2, 3, 4, 5 или 6 ч после инициации экспрессии, с указанным моментом времени, определенным для молекулы нуклеиновой кислоты, в которой отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно.
Например, производство белка с искусственной молекулы нуклеиновой кислоты, такой как искусственная мРНК, в количестве, представляющем собой по меньшей мере количество, обнаруженное на начальной фазе экспрессии, например, через 1, 2, 3, 4, 5 или 6 ч после инициации экспрессии, например, после трансфекции молекулой нуклеиновой кислоты, пролонгируется по меньшей мере примерно на 5 ч, предпочтительно по меньшей мере примерно на 10 ч, более предпочтительно по меньшей мере примерно на 24 ч по сравнению с производством белка с референс-молекулы нуклеиновой кислоты, такой как референс-мРНК, в экспрессионной системе млекопитающих, такой как клетки млекопитающих, например, в клетках линии HDF, L929, HEP2G или HeLa. Так, искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, предпочтительно позволяет пролонгировать производство белка в количестве, которое представляет собой по меньшей мере количество, обнаруженное на начальной фазе экспрессии, например, через 1, 2, 3, 4, 5 или 6 ч после инициации экспрессии, например, после трансфекции, по меньшей мере примерно на 5 ч, предпочтительно по меньшей мере примерно на 10 ч, более предпочтительно по меньшей мере примерно на 24 ч по сравнению с производством белка с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно.
В предпочтительных вариантах осуществления изобретения период производства белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, удлинен по меньшей мере в 1,2 раза, предпочтительно по меньшей мере в 1,5 раза, более предпочтительно по меньшей мере в 2 раза, еще более предпочтительно по меньшей мере в 2,5 раза по сравнению с периодом производства белка с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно.
Предпочтительно указанное пролонгирующее действие на производство белка достигается, когда общее количество белка, продуцированное с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, например, в течение периода времени, составляющего 48 или 72 ч, соответствует по меньшей мере количеству белка, продуцированного с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-ЦТК и/или референс-5'-UTR соответственно, такую как 3'-UTR и/или 5'-UTR, встречающаяся в естественных условиях с ОРС искусственной молекулы нуклеиновой кислоты. Так, в настоящем изобретении предложена искусственная молекула нуклеиновой кислоты, которая обеспечивает пролонгированное производство белка в экспрессионной системе млекопитающих, такой как клетки млекопитающих, например, в клетках линии HDF, L929, HEP2G или HeLa, как указано выше, при этом общее количество белка, продуцированного с указанной искусственной молекулы нуклеиновой кислоты, например, в течение периода времени, составляющего 48 или 72 ч, представляет собой по меньшей мере общее количество белка, продуцированного, например, в течение указанного периода времени, с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно, такую как 3'-UTR и/или 5'-UTR, встречающаяся в естественных условиях с ORF искусственной молекулы нуклеиновой кислоты.
Кроме того, понятие «пролонгированная экспрессия белка» включает также понятие «стабилизированная экспрессия белка», при этом «стабилизированная экспрессия белка» предпочтительно означает, что имеет место более равномерное производство белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, в течение заранее определенного периода времени, например, в течение 24 ч, более предпочтительно в течение 48 ч, еще более предпочтительно в течение 72 ч, по сравнению с референс-молекулой нуклеиновой кислоты, например, мРНК, которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно или в которой отсутствует 3'-UTR и/или 5'-UTR соответственно.
Следовательно, уровень производства белка, например, в системе млекопитающих, с искусственной молекулы нуклеиновой кислоты, содержащей 3'-UTR-элемент и/или 5'-UTR-элемент, предлагаемый в настоящем изобретении, например, с мРНК, предлагаемой в настоящем изобретении, предпочтительно не снижается до уровня, обнаруженного для референс-молекулы нуклеиновой кислоты, такой как референс-мРНК, указанная выше. Для оценки того, до какой степени снижается производство белка со специфической молекулы нуклеиновой кислоты, можно сравнивать, например, количество белка (кодируемого соответствующей ОРС), обнаруженное через 24 ч после инициации экспрессии, например, через 24 ч после трансфекции искусственной молекулой нуклеиновой кислоты, предлагаемой в настоящем изобретении, клетки, такой как клетка млекопитающего, с количеством белка, обнаруженного через 48 ч после инициации экспрессии, например, через 48 ч после трансфекции. Так, отношение количества белка, кодируемого ОРС искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, такое как количество репортерного белка, например, люциферазы, обнаруженного в более поздний момент времени, например, через 48 ч после инициации экспрессии, например, после трансфекции, к количеству белка, обнаруженного в более ранний момент времени, например, через 24 ч после инициации экспрессии, например, после трансфекции, предпочтительно больше, чем соответствующее отношение (определенное для тех же самых моментов времени) для референс-молекулы нуклеиновой кислоты, содержащей референс-3'- и/или референс-5'-UTR соответственно или в которой отсутствует 3'-UTR и/или 5'-UTR соответственно.
Предпочтительно отношение количества белка, кодируемого ОРС искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, например, количество репортерного белка, например, люциферазы, обнаруженное в более поздний момент времени, например, через 48 ч после инициации экспрессии, например, после трансфекции, к количеству белка, обнаруженному в более ранний момент времени, например, через 24 ч после инициации экспрессии, например, после трансфекции, предпочтительно составляет по меньшей мере 0,2, более предпочтительно по меньшей мере примерно 0,3, еще более предпочтительно по меньшей мере примерно 0,4, еще более предпочтительно по меньшей мере примерно 0,5, и наиболее предпочтительно по меньшей мере примерно 0,7. Для соответствующей референс-молекулы нуклеиновой кислоты, например, мРНК, которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно, или в которой отсутствует 3'-UTR и/или 5'-UTR соответственно, указанное отношение может составлять, например, от примерно 0,05 до примерно 0,35.
Таким образом, в настоящем изобретении предложена искусственная молекула нуклеиновой кислоты, содержащая ОРС и 3'-UTR-элемент и/или 5'-UTR-элемент, описанный выше, при этом отношение количества белка, например, количество люциферазы, обнаруженное через 48 ч после инициации экспрессии, к количеству белка, обнаруженному через 24 ч после инициации экспрессии, предпочтительно в системе экспрессии млекопитающих, такой как клетки млекопитающих, например, в HDF-клетках или HeLa-клетках, предпочтительно составляет по меньшей мере 0,2, более предпочтительно по меньшей мере примерно 0,3, более предпочтительно по меньшей мере примерно 0,4, еще более предпочтительно по меньшей мере примерно 0,5, еще более предпочтительно по меньшей мере примерно 0,6, и наиболее предпочтительно по меньшей мере примерно 0,7. Таким образом, предпочтительно общее количество белка, продуцированного с указанной искусственной молекулы нуклеиновой кислоты, например, в течение периода времени, составляющего 48 ч, по меньшей мере соответствует общему количеству белка, продуцированного, например, в течение указанного периода времени, с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно, такую как 3'-UTR и/или 5'-UTR, встречающаяся в естественных условиях с ОРС искусственной молекулы нуклеиновой кислоты.
Предпочтительно в настоящем изобретении предложена искусственная молекула нуклеиновой кислоты, содержащая ОРС и 3'-UTR-элемент и/или 5'-UTR-элемент, описанный выше, при этом отношение количества белка, например, количество люциферазы, обнаруженное через 72 ч после инициации экспрессии, к количеству белка, обнаруженному через 24 ч после инициации экспрессии, предпочтительно в системе экспрессии млекопитающих, такой, например, как клетки линии HeLa или HDF, предпочтительно превышает примерно 0,05, более предпочтительно превышает примерно 0,1, более предпочтительно превышает примерно 0,2, еще более предпочтительно превышает примерно 0,3, при этом предпочтительно общее количество белка, продуцированного с указанной искусственной молекулы нуклеиновой кислоты, например, в течение периода времени, составляющего 72 ч, представляет собой по меньшей мере общее количество белка, продуцированного, например, в течение указанного периода времени с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно, такую как 3'-UTR и/или 5'-UTR, встречающаяся в естественных условиях c OPC искусственной молекулы нуклеиновой кислоты.
«Увеличенная экспрессия белка» или «повышенная экспрессия белка» в контексте настоящего изобретения предпочтительно обозначает увеличенную/повышенную экспрессию белка в один из моментов времени после инициации экспрессии или увеличенное/повышенное общее количество экспрессированного белка, по сравнению с экспрессией, индуцированной референс-молекулой нуклеиновой кислоты. Так, уровень белка, обнаруженный в определенный момент времени после инициации экспрессии, например, после трансфекции искусственной молекулой нуклеиновой кислоты, предлагаемой в настоящем изобретении, например, после трансфекции мРНК, предлагаемой в настоящем изобретении, например, через 6, 12, 24, 48 или 72 ч после трансфекции, предпочтительно превышает уровень белка, обнаруженный в этот же самый момент времени после инициации экспрессии, например, после трансфекции референс-молекулой нуклеиновой кислоты, такой как референс-мРНК, которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно или в которой отсутствует 3'-UTR и/или 5'-UTR соответственно. В предпочтительном варианте осуществления изобретения максимальное количество белка (определенное, например, по активности или массе белка), экспрессированного с искусственной молекулы нуклеиновой кислоты, увеличено по сравнению с количеством белка, экспрессированного с нуклеиновой референс-кислоты, которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно или в которой отсутствует 3'-UTR и/или 5'-UTR соответственно. Пиковые уровни экспрессии предпочтительно достигаются в пределах 48 ч, более предпочтительно в пределах 24 ч и еще более предпочтительно в пределах 12 ч после, например, трансфекции.
Предпочтительно понятие «увеличенное общее производство белка» или «повышенное общее производство белка», с искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, относится к увеличенному/повышенному производству белка в течение периода времени, в течение которого белок продуцируется с искусственной молекулы нуклеиновой кислоты, например, в течение 48 ч или 72 ч, предпочтительно в системе экспрессии млекопитающих, такой как клетки млекопитающих, например, в клетках линии HDF, L929, HEP2G или HeLa, по сравнению с референс-молекулой нуклеиновой кислоты, в которой отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-UTR и/или референс-5'-UTR соответственно. Согласно предпочтительному варианту осуществления изобретения кумулятивное количество белка, экспрессированного в течение периода времени, увеличивается, если применяют искусственную молекулу нуклеиновой кислоты, предлагаемую в изобретении.
Общее количество белка в течение определенного периода времени можно определять путем (I) сбора ткани или клеток в несколько моментов времени после интродукции искусственной молекулы нуклеиновой кислоты (например, через 6, 12, 24, 48 и 72 ч после инициации экспрессии или после интродукции молекулы нуклеиновой кислоты), и можно определять количество белка в каждый момент времени как указано выше. Для расчета кумулятивного количества белка можно применять математический метод определения общего количества белка, например, можно определять площадь под кривой (AUC) согласно следующей формуле:
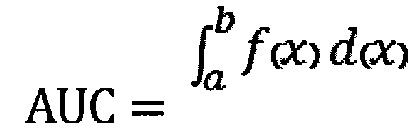
Для расчета площади под кривой для общего количества белка вычисляют интеграл уравнения кривой экспрессии между каждыми конечными точками (а и b).
Таким образом, понятие «общее производство белка» предпочтительно относится к площади под кривой (AUC), описывающей производство белка в зависимости от времени.
Предпочтительно по меньшей мере один 3'-UTR-элемент или 5'-UTR-элемент, предлагаемый в настоящем изобретении повышает производство белка с указанной искусственной молекулы нуклеиновой кислоты по меньшей мере 1,5 раза, предпочтительно по меньшей мере в 2 раза, более предпочтительно по меньшей мере в 2,5 раза, по сравнению с производством белка с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3'- UTR и/или 5'-UTR соответственно. Иными словами, общее количество белка, продуцированного с искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, в определенный момент времени, например, через 48 ч или 72 ч после инициации экспрессии, например, после трансфекции, повышается на коэффициент, составляющий по меньшей мере 1,5, предпочтительно по. меньшей мере 2, более предпочтительно по меньшей мере 2,5, по сравнению с (относительно) количеством белка, продуцированного с референс-молекулы нуклеиновой кислоты, в которой, например, отсутствует 3'-UTR и/или 5'-UTR соответственно или которая содержит референс-3'-UTR и/или референс-5'-ЦТР соответственно, в соответствующий более поздний момент времени.
Пролонгирующее производство мРНК и/или белка действие и эффективность и/или повышающее производство белка действие и эффективность вариантов, фрагментов и/или вариантов фрагментов 3'-UTR и/или 5'-UTR, а также пролонгирующее действие на мРНК и/или производство белка и эффективность и/или повышающее производство белка действие и эффективность по меньшей мере одного 3'-UTR-элемента и/или по меньшей мере одного 5'-UTR-элемента искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, можно определять с помощью любого пригодного для этой цели метода, известного специалисту в данной области.
Например, можно создавать искусственные молекулы мРНК, содержащие кодирующую последовательность/открытую рамку считывания (ОРС) репортерного белка, такого как люцифераза, и 3'-UTR-элемент, предлагаемый в настоящем изобретении, а именно, такой, который пролонгирует и/или повышает производство белка с указанной искусственной молекулы мРНК. Кроме того, такая предлагаемая в изобретении молекула мРНК может содержать также 5'-UTR-элемент, предлагаемый в настоящем изобретении, а именно, такой, который пролонгирует и/или повышает производство белка с указанной искусственной молекулы мРНК, не содержать 5'-UTR-элемент или 5'-UTR-элемент, не предлагаемый в настоящем изобретении, например, референс-5'-UTR. Следовательно можно создавать искусственные молекулы мРНК, содержащие кодирующую последовательность/открытую рамку считывания (ОРС) репортерного белка, такого как люцифераза, и 5'-UTR-элемент, предлагаемый в настоящем изобретении, а именно, такой, который пролонгирует и/или повышает производство белка с указанной искусственной молекулы мРНК. Кроме того, такая предлагаемая в изобретении молекула мРНК может содержать также 3'-UTR-элемент, предлагаемый в настоящем изобретении, а именно, такой, который пролонгирует и/или повышает производство белка с указанной искусственной молекулы мРНК, не содержать 3'-UTR-элемент или 3'-UTR-элемент, не предлагаемый в настоящем изобретении, например, референс-3'-UTR
Согласно настоящему изобретению можно создавать мРНК, например, путем транскрипции in vitro соответствующих векторов, таких как плазмидные векторы, например, таких, которые содержат промотор Т7 и последовательность, кодирующую соответствующие последовательности мРНК. Созданными молекулами мРНК можно трансфектировать клетки с помощью любого метода трансфекции, пригодного для трансфекции мРНК, например, их можно встраивать посредством липофекции в клетки млекопитающих, такие как клетки HeLa или клетки HDF, и образцы можно анализировать в определенные моменты времени после трансфекции, например, через 6 ч, 24 ч, 48 ч и 72 ч после трансфекции. Указанные образцы можно анализировать для определения количеств мРНК и/или количеств белка с помощью методов, хорошо известных специалисту в данной области. Например, количества репортерной мРНК, присутствующей в клетках в определенные моменты времени можно определять с помощью методов количественной ПЦР. Количества репортерного белка, кодируемого соответствующими мРНК, можно определять, например, с помощью вестерн-блоттинга, ELISA-анализов, FACS-анализов или репортерных анализов, таких как анализы люциферазы, в зависимости от применяемого репортерного белка. Эффект стабилизации экспрессии белка и/или пролонгирования экспрессии белка можно анализировать, например, путем определения отношения уровня белка, обнаруженного через 48 ч после трансфекции, к уровню белка, обнаруженного через 24 ч после трансфекции. Чем ближе указанная величина к 1, тем более стабильна экспрессия белка в течение этого периода времени. Такие измерения для определения стабильности экспрессии белка можно, естественно, осуществлять также и через 72 или большее количество часов и можно определять отношение уровня белка, обнаруженного через 72 ч после трансфекции, к уровню белка, обнаруженного через 24 ч после трансфекции.
Эффективность трансляции: Анализ для определения эффективности трансляции
Как подробно описано выше, эффективность трансляции представляет собой характеристику молекулы нуклеиновой кислоты (например, мРНК), которая содержит открытую рамку считывания (ОРС), и, как правило, она обеспечивается специфическим UTR-элементом (специфическим 5'-UTR-элементом или специфическим 3'-UTR-элементом), который содержится в молекуле нуклеиновой кислоты. Эффективность трансляции, как правило, измеряют по количеству белка, транслированного с ОРС. Касательно этого в настоящем изобретении предложены общие методы, а также специфический анализ. Эффективность трансляции различных, например, двух или большего количества молекул нуклеиновой кислоты можно сравнивать, например, путем экспериментальной количественной оценки белка, кодируемого ОРС.
В целом, для оценки эффективности трансляции применяют методы, основанные на применении клеток. Эффективность трансляции предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты экспериментально тестируют in vivo или in vitro, как указано в настоящем описании (т.е. in vitro относится к («живым») клеткам и/или ткани, включая ткань живого индивидуума; клетки включают, в частности, клеточные линии, первичные клетки, клетки в ткани или в организме индивидуумов, предпочтительными являются клетки млекопитающих, например, человеческие клетки и мышиные клетки, и наиболее предпочтительными являются человеческие линии клеток HeLa, HEPG2 и U-937 и мышиные линии клеток NIH3T3, JAWSII и L929, кроме того, наиболее предпочтительными являются первичные клетки, в наиболее предпочтительных вариантах осуществления изобретения - человеческие кожные фибробласты (HDF)), экспрессию кодируемого белка определяют после осуществления инъекции/трансфекции предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты в клетки-/ткани-мишени и сравнивают с экспрессией белка, индуцируемой нуклеиновой референс-кислотой. В данной области известны количественные методы определения экспрессии белка (например, вестерн-блоттинг, FACS, ELISA, масс-спектрометрия). В рассматриваемом контексте наиболее пригодным является определение экспрессии репортерных белков типа люциферазы, зеленого флуоресцентного белка (GFP) или секретируемой щелочной фосфатазы (SEAP). Так, искусственную нуклеиновую кислоту, предлагаемую в изобретении, или нуклеиновую референс-кислоту интродуцируют в ткань-мишень или клетку-мишень, например, посредством трансфекции или инъекции, предпочтительно в систему экспрессии млекопитающих, такую как клетки млекопитающих, например, в клетки линии HDF, L929, HepG2 и/или Hela. Через несколько часов или через несколько дней (например, через 6, 12, 24, 48 или 72 ч) после инициации экспрессии или после интродукции молекулы нуклеиновой кислоты берут образец клеток-мишеней и проводят измерения с помощью FACS и/или лизируют. После этого лизаты можно использовать для обнаружения экспрессированного белка (и определения тем самым эффективности экспрессии белка) с помощью нескольких методов, например, вестерн-блоттинга, FACS, ELISA, масс-спектрометрии или путем измерения флуоресценции или люминесценции.
Так, если экспрессию белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, сравнивают с экспрессией белка с референс-молекулы нуклеиновой кислоты в конкретный момент времени (например, через 6, 12, 24, 48 или 72 ч после инициации экспрессии или после интродукции молекулы нуклеиновой кислоты), то обе молекулы нуклеиновой кислоты вводят независимо в ткань-мишень/клетки-мишени, берут образец ткани-мишени/клеток-мишеней после определенного момента времени, приготавливают белковые лизаты согласно конкретному протоколу, адаптированному к конкретному методу обнаружения (такому, например, как вестерн-блоттинг, ELISA, измерение флуоресценции или люминесценции и т.д., известному в данной области) и проводят обнаружение белка с помощью выбранного метода обнаружения. В качестве альтернативы измерению количеств экспрессированного белка в клеточных лизатах, или в дополнение к измерению количеств экспрессированного белка в клеточных лизатах можно определять также количества белка с помощью метода FACS до лизиса собранных клеток или параллельно с использованием аликвот.
Другие общие объекты соответствуют объектам, представленным выше при описании производства белка, если из контекста не следует иное.
Предпочтительно высокая эффективность трансляции искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, обеспечивается за счет по меньшей мере одного элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или по меньшей мере одного элемента 5'-нетранслируемой области (5'-UTR-элемента). Выражение «обеспечивается» означает, что при отсутствии по меньшей мере одного элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или по меньшей мере одного элемента 5'-нетранслируемой области (5'-UTR-элемента) эффективность трансляции не является высокой, как указано в настоящем описании.
Понятие «высокая эффективность трансляции» можно использовать для сравнения эффективности трансляции искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, с референс-молекулой нуклеиновой кислоты. Понятие «референс-молекула нуклеиновой кислоты» в контексте настоящего описания означает, что за исключением различных 3'-UTR и/или 5'-UTR референс-молекула нуклеиновой кислоты сопоставима, предпочтительно идентична, искусственной молекуле нуклеиновой кислоты, предлагаемой в изобретении, которая содержит 3'-UTR-элемент и/или 5'-UTR-элемент. Таким образом, можно сравнивать эффективность трансляции искусственной молекулы нуклеиновой кислоты с эффективностью трансляции референс-молекулы нуклеиновой кислоты. Соответствующий способ сравнения эффективности трансляции представлен в настоящем описании.
Все объекты, представленные выше при описании определения производства белка, применимы также к способу сравнения эффективности трансляции, если из контекста не следует иное. Поскольку в способе сравнения эффективности трансляции используют сравнение двух молекул нуклеиновой кислоты, то осуществляют два параллельных эксперимента, единственное различие между указанными двумя экспериментами состоит в природе молекулы нуклеиновой кислоты. Иными словами, все остальные условия, такие, например, как среда для роста, температура, значение рН, в экспериментах являются идентичными. Специалист в данной области с помощью общепринятых подходов может выбрать пригодные условия на основе общей компетенции и представленного в настоящем описании руководства, при условии, что для обоих параллельных экспериментов должны быть выбраны идентичные условия. Как правило, один из параллельных экспериментов проводят с использованием референс-молекулы нуклеиновой кислоты (которая может представлять собой молекулу дикого типа или искусственную молекулу), а другой проводят с искусственной молекулой нуклеиновой кислоты (которую обозначают также как рассматриваемая молекула нуклеиновой кислоты). Этот способ позволяет сравнивать, характеризуется ли рассматриваемая молекула нуклеиновой кислоты высокой эффективностью трансляции; т.е., представляет ли она собой искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении. Конкретные аспекты способа, предназначенного для сравнения эффективности трансляции, заключаются в следующем:
В рассматриваемом способе референс-молекула нуклеиновой кислоты содержит по меньшей мере одну открытую рамку считывания (ОРС), которая является идентичной по меньшей мере одной открытой рамке считывания (ОРС) искусственной молекулы нуклеиновой кислоты; и референс-молекула нуклеиновой кислоты не содержит по меньшей мере один элемент 3'-нетранслируемой области (3'-UTR-элемент) искусственной молекулы нуклеиновой кислоты и/или по меньшей мере один элемент 5'-нетранслируемой области (5'-UTR-элемент) искусственная молекула нуклеиновой кислоты. Эффективность трансляции искусственной молекулы нуклеиновой кислоты и эффективность трансляции референс-молекулы нуклеиновой кислоты сравнивают с помощью способа, включающего стадии, на которых:
(I) трансфектируют клетки млекопитающих искусственной молекулой нуклеиновой кислоты и измеряют количества экспрессированного белка, кодируемого ОРС искусственной молекулы нуклеиновой кислоты, в определенный момент времени после трансфекции (например, через 24 или 48 ч),
(II) трансфектируют клетки млекопитающих референс-молекулой нуклеиновой кислоты и измеряют количества экспрессированного белка, кодируемого ОРС референс-молекулы нуклеиновой кислоты в тот же самый момент времени после трансфекции,
(III) рассчитывают отношение количества белка, экспрессированного с искусственной молекулы нуклеиновой кислоты, к количеству белка, экспрессированного с референс-молекулы нуклеиновой кислоты,
где отношение, рассчитанное на стадии (III), составляет ≥1, предпочтительно >1.
Таким образом, путем сравнения относительного количества белка, продуцированного с рассматриваемой молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, с относительным количеством белка, продуцированного с референс-молекулы нуклеиновой кислоты, можно определять коэффициент, на который повышается эффективность трансляции искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, по сравнению с эффективностью трансляции референс-молекулы нуклеиновой кислоты.
Понятие «после трансфекции» используют для ссылки на момент времени, в который была осуществлена трансфекция клеток рассматриваемой молекулой нуклеиновой кислоты и референс-молекулой нуклеиновой кислоты.
Предпочтительно по меньшей мере один 3'- и/или 5'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в изобретении, повышает эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты по меньшей мере в 1,2 раза, предпочтительно по меньшей мере в 1,5 раза, более предпочтительно по меньшей мере в 2 раза, еще более предпочтительно по меньшей мере в 2,5 раза, по сравнению с производством белка с референс-молекулы нуклеиновой кислоты, содержащей референс-3'-UTR и/или референс-5'-UTR, соответственно (т.е. отношение, рассчитанное на стадии (III), составляет по меньшей мере 1,2, предпочтительно по меньшей мере 1,5, более предпочтительно по меньшей мере 2, еще более предпочтительно по меньшей мере 2,5). Иными словами, эффективность трансляции повышается на коэффициент, составляющий по меньшей мере 1,2, предпочтительно по меньшей мере 1,5, более предпочтительно по меньшей мере 2, еще более предпочтительно по меньшей мере 2,5, по сравнению с эффективностью трансляции референс-молекулы нуклеиновой кислоты в тот же самый момент времени.
Высокая эффективность трансляции обеспечивается 5'-UTR или 3'-UTR, которой рассматриваемая молекула нуклеиновой кислоты отличается от референс-молекулы нуклеиновой кислоты.
В предпочтительном варианте способа сравнения эффективности трансляции, предлагаемого в настоящем изобретении, (I) референс-молекула нуклеиновой кислоты содержит 3'-UTR-элемент, который не присутствует в искусственной молекуле нуклеиновой кислоты, или (II) референс-молекула нуклеиновой кислоты содержит 5'-UTR-элемент, который не присутствует в искусственной молекуле нуклеиновой кислоты. В более предпочтительных вариантах осуществления изобретения, (I) референс-молекула нуклеиновой кислоты содержит 3'-UTR-элемент, который получен из 3'-UTR гена альбумина, предпочтительно 3'-UTR, которая соответствует последовательности, представленной в SEQ ID NO: 207, или (II) референс-молекула нуклеиновой кислоты содержит 5'-UTR-элемент, который получен из 5'-UTR ТОР-гена, предпочтительно 5'-UTR человеческого рибосомального белка большой субъединицы 32 без 5'-концевого олигопиримидинового тракта, предпочтительно 5'-UTR, которая соответствует последовательности, представленной в SEQ ID NO: 208.
В альтернативном предпочтительном варианте осуществления изобретения (I) референс-молекула нуклеиновой кислоты не содержит никакого элемента 3'-нетранслируемой области (3'-UTR-элемента), или (II) референс-молекула нуклеиновой кислоты не содержит никакого элемента 5'-нетранслируемой области (5'-UTR-элемента).
В предпочтительном варианте осуществления изобретения клетки, применяемые на стадии трансфекции искусственной молекулой нуклеиновой кислоты и референс-молекулой нуклеиновой кислоты, представляют собой клетки млекопитающих, предпочтительно выбранные из группы клеток линий HDF, L929, HEP2G и HeLa. Кроме того, предпочтительно способ осуществляют параллельно на более чем одном типе клеток млекопитающих, например, параллельно на комбинации любых двух, предпочтительно любых трех, более предпочтительно всех четырех из указанных выше клеточных линий. Когда способ осуществляют параллельно на более чем одном типе клеток млекопитающих, то можно считать, что рассматриваемая молекула нуклеиновой кислоты должна характеризоваться высокой эффективностью трансляции, если отношение, рассчитанное на стадии (III) составляет ≥ 1, предпочтительно > 1, по меньшей мере для одного из использованных типов клеток млекопитающих. Однако предпочтительно считать, что рассматриваемая молекула нуклеиновой кислоты характеризуется высокой эффективностью трансляции, если отношение, рассчитанное на стадии (III) составляет ≥ 1, предпочтительно > 1, по меньшей мере для двух типов, например, по меньшей мере для трех типов, например, для четырех типов использованных клеток млекопитающих.
Количества экспрессированного белка, кодируемого ОРС искусственной молекулы нуклеиновой кислоты и референс-молекулы нуклеиновой кислоты, измеряют в определенный момент времени после трансфекции (например, через 12 ч, 24 ч, 36 ч, 48 ч или 72 ч). Предпочтительно количества экспрессированного белка, кодируемого ОРС, измеряют через 24 ч после трансфекции.
В настоящем изобретении предложена также специфическая предпочтительная референс-конструкция, которую можно применять в способе, предлагаемом в настоящем изобретении. Наиболее предпочтительно, чтобы референс-молекула нуклеиновой кислоты представляла собой мРНК, имеющую SEQ ID NO: 205 (фиг. 1А). В этом случае предпочтительно также, чтобы референс-молекула нуклеиновой кислоты отличалась от искусственной молекулы нуклеиновой кислоты только тем, что по меньшей мере один 3'-UTR-элемент заменен по меньшей мере на один другой 3'-UTR-элемент (предпочтительно на один 3'-UTR-элемент), или тем, что по меньшей мере один 5'-UTR-элемент заменен по меньшей мере на один другой 5'-UTR-элемент (предпочтительно на один 5'-UTR-элемент). В любом случае это позволяет осуществлять непосредственное тестирование того, обеспечивает ли указанный другой 3'-UTR-элемент или другой 5'-UTR-элемент соответственно высокую эффективность трансляции.
Наиболее предпочтительно способ определения эффективности трансляции характеризуется также тем, что:
(а) на стадии трансфекции клетки представляют собой клетки млекопитающих, выбранные из группы клеток линий HDF, L929, HEP2G и HeLa; и
(б) момент времени для измерения представляет собой момент времени, наступивший через 24 ч после трансфекции; и
(в) референс-молекула нуклеиновой кислоты представляет собой мРНК, имеющую SEQ ID NO: 205 (фиг. 1А); и
предпочтительно (г) референс-молекула нуклеиновой кислоты отличается от искусственной молекулы нуклеиновой кислоты только тем, что (I) по меньшей мере один 3'-UTR-элемент (предпочтительно один 3'-UTR-элемент) заменен по меньшей мере на один другой 3'-UTR-элемент (предпочтительно один 3'-UTR-элемент), или (II) по меньшей мере один 5'-UTR-элемент (предпочтительно один 5'-UTR-элемент)) заменен по меньшей мере на один другой 5'-UTR-элемент (предпочтительно один 5'-UTR-элемент); иными словами, рассматриваемая молекула нуклеиновой кислоты идентична референс-молекуле нуклеиновой кислоты, за исключением того, что по меньшей мере один 5'-UTR-элемент отличается от 5'-UTR, представленной на фиг. 1А, или тем, что по меньшей мере один 3'-UTR-элемент отличается от 3'-UTR, представленной на фиг. 1А. Пример замены 5'-UTR-элемента представлен на фиг. 1Б; пример замены 3'-UTR-элемента представлен на фиг. 1В.
Если выполнены все условия от (а) до (г), то способ обозначают также как «стандартизованный анализ для определения эффективности трансляции» или просто «анализ для определения эффективности трансляции». Наиболее предпочтительно, когда искусственная молекула нуклеиновой кислоты, предлагаемая в изобретении, характеризуется высокой эффективностью трансляции, которая может быть определена с помощью указанного стандартного анализа для определения эффективности трансляции. Этот стандартный анализ позволяет осуществлять непосредственную идентификацию обладающих наибольшим преимуществом искусственных молекул нуклеиновой кислоты.
Стандартный анализ применяли в примере 3 настоящего изобретения. Таким путем при создании настоящего изобретения было установлено, что группа новых искусственных нуклеиновых кислот обладает дающим преимущество свойством, заключающимся в высокой эффективности трансляции, а именно, более высокой, чем эффективность трансляции референс-молекулы нуклеиновой кислоты, проиллюстрированной на фиг. 1А (см. пример 3.5). Это является очень неожиданным и дающим преимущество открытием, прежде всего по той причине, что указанная референс-молекула нуклеиновой кислоты содержит 3'-UTR-элемент, который получен из 3'-UTR гена альбумина (3'-UTR соответствует последовательности ДНК, представленной в SEQ ID NO: 207), и 5'-UTR-элемент, который получении из 5'-UTR ТОР-гена, прежде всего 5'-UTR человеческого белка большой субъединицы рибосомы 32 без 5'-концевого олигопиримидинового тракта (5'-UTR соответствует последовательности ДНК, представленной в SEQ ID NO: 208). Известно, что такие 3'-UTR-элементы и 5'-UTR-элементы обладают преимуществом с точки зрения трансляции белка в клетке (данные для 3'-UTR, полученной из гена альбумина представлены в WO 2013/143700; для 5'-TOP-UTR представлены в WO 2013/143700). В настоящем изобретении предложено дополнительное усовершенствование.
В некоторых вариантах осуществления изобретения ОРС искусственной молекулы нуклеиновой кислоты кодирует белок, который можно количественно оценивать, предпочтительно репортерный белок. Эти варианты осуществления изобретения являются предпочтительными для применения в способе сравнения эффективности трансляции, предлагаемом в настоящем изобретении. В других вариантах осуществления изобретения ОРС искусственной молекулы нуклеиновой кислоты не кодирует белок, который можно количественно оценивать, предпочтительно репортерный белок. Например, если с помощью способа, предлагаемого в изобретении, с использованием ОРС искусственной молекулы нуклеиновой кислоты, кодирующей белок, который можно количественно оценивать, определили конкретную 5'-UTR или 3'-UTR, обеспечивающую высокую эффективность трансляции, то указанную 5'-UTR или 3'-UTR можно рекомбинировать с любой ОРС. Например, когда в стандартизованном анализе для определения эффективность трансляции ОРС кодирует репортерный белок, то искусственные нуклеиновые кислоты, предлагаемые в настоящем изобретении, не ограничены ОРС, применяемой в стандартизованном анализе.
Указанные способы можно применять итерационно; а именно, искусственную молекулу нуклеиновой кислоты, для которой с помощью способа, представленного в настоящем описании, было установлено, что она характеризуется высокой эффективностью трансляции, саму можно применять в качестве «референс-конструкции» для последующего раунда, представленного в настоящем описании способа. Это позволяет тестировать, характеризуется ли другая искусственная молекула нуклеиновой кислоты еще более высокой эффективностью трансляции (или то, обеспечивает ли UTR, содержащаяся в другой искусственной молекуле нуклеиновой кислоты, еще более высокую эффективность трансляции). Это позволяет идентифицировать еще более усовершенствованные искусственные молекулы нуклеиновой кислоты и UTR.
Стабильная мРНК
В некоторых вариантах осуществления изобретения по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении, получают из стабильной мРНК. В данном случае «полученный (имеющий происхождение)» из стабильной мРНК означает, что последовательность по меньшей мере одного 3'-UTR-элемента и/или по меньшей мере одного 5'-UTR-элемента идентична по меньшей мере на 50%, предпочтительно по меньшей мере на 60%, предпочтительно по меньшей мере на 70%, более предпочтительно по меньшей мере на 75%, более предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 85%, еще более предпочтительно по меньшей мере на 90%, еще более предпочтительно по меньшей мере на 95%, и наиболее предпочтительно по меньшей мере на 98% последовательности 3'-UTR-элемента и/или 5'-UTR-элемента стабильной мРНК. Предпочтительно стабильная мРНК представляет собой встречающуюся в естественных условиях мРНК и, таким образом, 3'-UTR-элемент и/или 5'-UTR-элемент стабильной мРНК относится к 3'-UTR и/или 5'-UTR встречающейся в естественных условиях мРНК, или их фрагментам или вариантам. Кроме того, 3'-UTR-элемент и/или 5'-UTR-элемент полученный из стабильной мРНК, предпочтительно относится также к 3'-UTR-элементу и/или 5'-UTR-элементу, который модифицирован по сравнению с встречающимся в естественных условиях 3'-UTR-элементом и/или 5'-UTR-элементом, например, для того, чтобы еще больше повышать стабильность РНК и/или для того, чтобы пролонгировать и/или увеличивать производство белка. Само собой разумеется, что предпочтительными являются такие модификации, которые не ухудшают стабильность РНК, например, по сравнению с встречающимся в естественных условиях (немодифицированным) 3'-UTR-элементом и/или 5'-UTR-элементом. В частности, понятие «мРНК» в контексте настоящего описания относится к молекуле мРНК, однако, оно может относиться также и к представленным в настоящем описании видам мРНК.
Предпочтительно стабильность мРНК, т.е. время расщепления и/или полужизни мРНК, оценивают в стандартных условиях, например, в стандартных условиях (стандартная среда, инкубация и т.д.) для определенной применяемой клеточной линии.
Понятие «стабильная мРНК» в контексте настоящего описания относится в целом к мРНК, характеризующейся медленным расщеплением мРНК. Таким образом, «стабильная мРНК», как правило, обладает продолжительным временем полужизни. Время полужизни мРНК представляет собой время, необходимое для расщепления 50% молекул мРНК, присутствующих в условиях in vivo или in vitro. Следовательно, стабильность мРНК, как правило, оценивают in vivo или in vitro. В данном случае in vitro относится, в частности, к («живым») клеткам и/или ткани, включая ткань живого индивидуума. Клетки включают, в частности, клеточные линии, первичные клетки, клетки в ткани или организме индивидуумов. В конкретных вариантах осуществления изобретения пригодными для применения согласно настоящему изобретению могут быть типы клеток, позволяющие осуществлять культивирование клеток. Наиболее предпочтительными являются клетки млекопитающих, например, человеческие клетки и мышиные клетки. В наиболее предпочтительных вариантах осуществления изобретения применяют человеческие клеточные линии HeLa, HEPG2 и U-937 и мышиные клеточные линии NIH3T3, JAWSII и L929. Кроме того, наиболее пригодными являются первичные клетки, в наиболее предпочтительных вариантах осуществления изобретения можно применять человеческие кожные фибробласты (HDF). В альтернативном варианте можно применять также ткань индивидуума.
Предпочтительно время полужизни «стабильной мРНК» составляет по меньшей мере 5 ч, по меньшей мере 6 ч, по меньшей мере 7 ч, по меньшей мере 8 ч, по меньшей мере 9 ч, по меньшей мере 10 ч, по меньшей мере 11 ч, по меньшей мере 12 ч, по меньшей мере 13 ч, по меньшей мере 14 ч, и/или по меньшей мере 15 ч. Время полужизни представляющей интерес мРНК можно определять различными методами, известными специалисту в данной области. Как правило, время полужизни представляющей интерес мРНК определяют путем определения константы расщепления, при этом, как правило, предполагается, что имеет место идеальная ситуация in vivo (или in vitro, как указано выше), в которой транскрипция представляющей интерес мРНК может быть полностью «выключена» (или снижена пo-меньшей мере до не поддающегося обнаружению уровня). В такой идеальной ситуации, как правило, предполагается, что такое расщепление мРНК происходит в соответствии с кинетикой первого порядка. Следовательно, расщепление мРНК, как правило, может быть описано следующим уравнением:
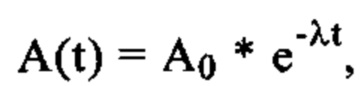
где А0 представляет собой количество (или концентрацию) представляющей интерес мРНК в момент времени 0, т.е. перед началом расщепления, A(t) представляет собой количество (или концентрацию) представляющей интерес мРНК в момент времени t в процессе расщепления, а λ представляет собой константу расщепления. Таким образом, если известны количество (или концентрация) представляющей интерес мРНК в момент времени 0 (А0) и количество (или концентрацию) представляющей интерес мРНК в момент времени t в процессе расщепления (A(t) и t), то можно рассчитать константу расщепления λ. На основе константы расщепления λ можно рассчитать время полужизни t1/2 согласно следующему уравнению:
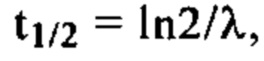
поскольку по определению A(t)/A0=1/2 при t1/2. Таким образом, для оценки времени полужизни представляющей интерес мРНК, как правило, определяют количество или концентрацию мРНК в процессе расщепления РНК in vivo (или in vitro, как указано выше).
Для определения количества или концентрации мРНК в процессе расщепления РНК in vivo (или in vitro, как указано выше) можно применять различные методы, известные специалисту в данной области. Примеры таких методов включают (но, не ограничиваясь только ими) общее ингибирование транскрипции, например, с помощью ингибитора транскрипции, такого как актиномицин D, применение индуцибельных промоторов для специфического усиления кратковременной транскрипции, например, индуцируемая сывороткой промоторная система c-fos и регуляторная промоторная система Tet-off, и кинетические методы мечения, например, импульсного мечения, например, с использованием 4-тиоуридина (4sU), 5-этинилуридина (EU) или 5'-бромуридина (BrU). Другие подробности и предпочтительные варианты, касающиеся того, как определять количество или концентрацию мРНК в процессе расщепления РНК, описаны ниже в контексте способа идентификации 3'-UTR-элемента и/или по меньшей мере одного 5'-UTR-элемента, предлагаемого в настоящем изобретении. Соответствующее описание и предпочтительные варианты того, как определять количество или концентрацию мРНК в процессе расщепления РНК применимы также и в данном случае.
Предпочтительно «стабильная мРНК» в контексте настоящего изобретения характеризуется более медленным расщеплением мРНК по сравнению с усредненной мРНК, которое предпочтительно оценивают in vivo (или in vitro, как указано выше). Например, «расщепление усредненной мРНК» можно оценивать путем исследования расщепления мРНК для множества видов мРНК, предпочтительно для 100, по меньшей мере 300, по меньшей мере 500, по меньшей мере 1000, по меньшей мере 2000, по меньшей мере 3000, по меньшей мере 4000, по меньшей мере 5000, по меньшей мере 6000, по меньшей мере 7000, по меньшей мере 8000, по меньшей мере 9000, по меньшей мере 10000, по меньшей мере 11000, по меньшей мере 12000, по меньшей мере 13000, по меньшей мере 14000, по меньшей мере 15000, по меньшей мере 16000, по меньшей мере 17000, по меньшей мере 18000, по меньшей мере 19000, по меньшей мере 20000, по меньшей мере 21000, по меньшей мере 22000, по меньшей мере 23000, по меньшей мере 24000, по меньшей мере 25000, по меньшей мере 26000, по меньшей мере 27000, по меньшей мере 28000, по меньшей мере 29000, по меньшей мере 30000 видов мРНК. Наиболее предпочтительно оценивать весь транскриптом или максимально возможное количество видов мРНК в транскриптоме. Это можно осуществлять, например, с использованием микромассива, обеспечивающего охват всех транскриптов.
Понятие «виды мРНК» в контексте настоящего описания соответствует геномной транскрипционной единице, а именно, как правило, к гену. Так, в одном «виде мРНК» могут присутствовать различные транскрипты, например, обусловленные процессингом мРНК. Виды мРНК можно вносить в виде пятен на микромассив. Следовательно, микромассив представляет собой предпочтительный «инструмент» определения количества для множества видов мРНК, например, в определенный момент времени в процессе расщепления мРНК. Однако можно применять также и другие методы, известные специалисту в данной области, например, секвенирование РНК, количественную ПЦР и т.д.
Согласно настоящему изобретению наиболее предпочтительно, когда стабильная мРНК характеризуется таким расщеплением мРНК, при котором отношение количества указанной мРНК во второй момент времени к количеству указанной мРНК в первый момент времени составляет по меньшей мере 0,5 (50%), по меньшей мере 0,6 (60%), по меньшей мере 0,7 (70%), по меньшей мере 0,75 (75%), по меньшей мере 0,8 (80%), по меньшей мере 0,85 (85%), по меньшей мере 0,9 (90%) или по меньшей мере 0,95 (95%). При этом подразумевается, что второй момент времени наступает позднее первого момента времени в процессе расщепления.
Предпочтительно первый момент времени выбирают таким образом, чтобы рассматривать только мРНК, которая подвергается процессу расщепления, т.е. чтобы не рассматривать мРНК, возникающую, например, в процессе транскрипции. Например, если применяют кинетические методы мечения, например, импульсное мечение, то первый момент времени предпочтительно выбирают таким образом, чтобы при этом было завершено включение метки в мРНК, т.е. не имело место продолжение включения метки в мРНК. Таким образом, если применяют кинетическое мечение, то первый момент времени может наступать по меньшей мере через 10 мин, по меньшей мере 20 мин, по меньшей мере через 30 мин, по меньшей мере 40 мин, по меньшей мере 50 мин, по меньшей мере 60 мин, по меньшей мере через 70 мин, по меньшей мере через 80 мин или по меньшей мере через 90 мин после завершения экспериментальной процедуры мечения, например, после завершения инкубации клеток с меткой.
Например, первый момент времени может наступать предпочтительно в период от 0 до 6 ч после прекращения транскрипции (например, с помощью ингибитора транскрипции), прекращения индукции промотора в случае индуцибельных промоторов или после прекращения подачи импульса или метки, например, после окончания мечения. Более предпочтительно первый момент времени может наступать в период от 30 мин до 5 ч, еще более предпочтительно от 1 ч до 4 ч и наиболее предпочтительно примерно через 3 ч после прекращения транскрипции (например, с помощью ингибитора транскрипции), прекращения индукции промотора в случае индуцибельных промоторов или после прекращения подачи импульса или метки, например, после окончания мечения.
Предпочтительно, в качестве второго момента времени выбирают по возможности максимально поздний момент времени в процессе расщепления мРНК. Однако, если рассматривают множество видов мРНК, то второй момент времени предпочтительно выбирают таким образом, чтобы все еще присутствовало значительное количество из множества видов мРНК, предпочтительно по меньшей мере 10% видов мРНК, в поддающемся обнаружению количестве, т.е. в количестве, превышающем 0. Предпочтительно второй момент времени наступает по меньшей мере через 5 ч, по меньшей мере 6 ч, по меньшей мере 7 ч, по меньшей мере 8 ч, по меньшей мере 9 ч, по меньшей мере 10 ч, по меньшей мере 11 ч, по меньшей мере 12 ч, по меньшей мере 13 ч, по меньшей мере 14 ч или по меньшей мере 15 ч после окончания транскрипции или после окончания экспериментальной процедуры мечения.
Таким образом, промежуток времени между первым моментом времени и вторым моментом времени предпочтительно является по возможности максимально большим в указанных выше пределах. Следовательно, промежуток времени между первым моментом времени и вторым моментом времени предпочтительно составляет по меньшей мере 4 ч по меньшей мере 5 ч, по меньшей мере 6 ч, по меньшей мере 7 ч, по меньшей мере 8 ч, по меньшей мере 9 ч, по меньшей мере 10 ч, по меньшей мере 11 ч или по меньшей мере 12 ч.
Кроме того, можно идентифицировать по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении, с помощью способа идентификации 3'-UTR-элемента и/или 5'-UTR-элемента, предлагаемого в настоящем изобретении, который представлен в настоящем описании. Наиболее предпочтительно по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении, идентифицировать с помощью представленного в настоящем описании способа идентификации 3'-UTR-элемента и/или 5'-UTR-элемента, который обеспечивает высокую эффективность трансляции искусственной молекулы нуклеиновой кислоты.
Предпочтительные варианты искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении
Предпочтительно по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении, содержит или состоит из нуклеотидной последовательности, которая получена из 3'-UTR и/или 5'-UTR гена, кодирующего эукариотический белок, предпочтительно из 3'-UTR и/или 5'-UTR гена, кодирующего белок позвоночного, более предпочтительно из 3'-UTR и/или 5'-UTR гена, кодирующего белок млекопитающего, например, из генов, кодирующих мышиный и человеческий белок, еще более предпочтительно из 3'-UTR и/или 5'-UTR гена, кодирующего белок примата или грызуна, прежде всего 3'-UTR и/или 5'-UTR гена, кодирующего человеческий или мышиный белок.
В целом, следует иметь в виду, что по меньшей мере один 3'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении, содержит или состоит из нуклеотидной последовательности, которая предпочтительно получена из встречающейся в естественных условиях (в природе) 3'-UTR, в то время как по меньшей мере один 5'-UTR-элемент в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении, содержит или состоит из нуклеотидной последовательности, которая предпочтительно получена из встречающейся в естественных условиях (в природе) 5'-UTR.
Предпочтительно по меньшей мере одна открытая рамка считывания является гетерологичной по меньшей мере одному 3'-UTR-элементу и/или по меньшей мере одному 5'-UTR-элементу. Понятие «гетерологичный» в этом контексте означает, что два элемента последовательности, содержащиеся в искусственной молекуле нуклеиновой кислоты, такие как открытая рамка считывания и 3'-UTR-элемент и/или открытая рамка считывания и 5'-UTR-элемент, не встречаются в естественных условиях (в природе) в рассматриваемой комбинации. Как правило, они являются рекомбинантными. Предпочтительно 3'-UTR-элемент и/или 5'-UTR-элемент получены/получен из гена, отличного от того, из которого получена открытая рамка считывания. Например, ОРС может быть получена из гена, отличного от того, из которого получен 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент, например, кодирующего другой белок или такой же белок, но из другого вида и т.д. Т.е. открытая рамка считывания получена из гена, который отличен от гена, из которого получен 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент. В предпочтительном варианте осуществления изобретения ОРС не кодирует человеческий рибосомальный белок или растительный рибосомальный белок (например, из Arabidopsis), предпочтительно не кодирует человеческий рибосомальный белок S6 (RPS6), белок, подобный человеческому рибосомальному белку L36a (RPL36AL) или рибосомальный белок S16 Arabidopsis (RPS16). В другом предпочтительном варианте осуществления изобретения открытая рамка считывания (ОРС) не кодирует рибосомальный белок S6 (RPS6), белок, подобный рибосомальному белку L36a (RPL36AL) или рибосомальный белок S16 (RPS16).
В конкретных вариантах осуществления изобретения предпочтительно открытая рамка считывания не кодирует репортерный белок, например, выбранный из группы, состоящей из белков глобина (прежде всего, бета-глобина), белка люциферазы, белков GFP или их вариантов, например, вариантов, последовательности которых идентичны по меньшей мере на 70% последовательности белка глобина, белка люциферазы или белка GFP. При этом наиболее предпочтительно, чтобы открытая рамка считывания (ОРС) не кодировала белок GFP. Наиболее предпочтительно также, чтобы открытая рамка считывания (ОРС) не кодировала репортерный ген или не происходила из репортерного гена, где репортерный ген предпочтительно не выбран из группы, состоящей из (генов) белков глобина (прежде всего бета-глобина), белка люциферазы, бета-глюкуронидазы (GUS) и белков GFP или их вариантов, предпочтительно не выбирают из EGFP или из вариантов любого из вышеуказанных генов, последовательности которых, как правило, идентичны по меньшей мере на 70% последовательности любого из вышеуказанных репортерных генов, предпочтительно генов белка глобина, белка люциферазы или белка GFP.
Еще более предпочтительно 3'-UTR-элемент и/или 5'-UTR-элемент является гетерологичным относительно любого другого элемента, содержащегося в искусственной нуклеиновой кислоте, представленной в настоящем описании. Например, если искусственная нуклеиновая кислота, предлагаемая в изобретении, содержит 3'-UTR-элемент из рассматриваемого гена, то она предпочтительно не содержит никакой другой нуклеотидной последовательности, прежде всего никакой функциональной нуклеотидной последовательности (например, элемента кодирующей или регуляторной последовательности) из этого же гена, включая его регуляторные последовательности на 5'- и 3'-конце ОРС гена. Следовательно, например, если искусственная нуклеиновая кислота, предлагаемая в изобретении, содержит 5'-UTR-элемент из рассматриваемого гена, то она предпочтительно не содержит никакой другой нуклеотидной последовательности, прежде всего никакой функциональной нуклеотидной последовательности (например, элемента кодирующей или регуляторной последовательности) из этого же гена, включая его регуляторные последовательности на 5'- и 3'-конце ОРС гена.
Кроме того, предпочтительно, когда искусственная нуклеиновая кислота, предлагаемая в настоящем изобретении, содержит по меньшей мере одну открытую рамку считывания, по меньшей мере одну 3'-UTR (элемент) и по меньшей мере одну 5'-UTR (элемент), при этом или по меньшей мере одна 3'-UTR (элемент) представляет собой 3'-UTR-элемент, предлагаемый в настоящем изобретении, и/или по меньшей мере одна 5'-UTR (элемент) представляет собой 5'-UTR-элемент, предлагаемый в настоящем изобретении. В такой предпочтительной искусственной нуклеиновой кислоте, предлагаемой в настоящем изобретении, которая содержит по меньшей мере одну открытую рамку считывания, по меньшей мере одна 3'-UTR (элемент) и по меньшей мере одна 5'-UTR (элемент), наиболее предпочтительно, когда каждая/каждый из по меньшей мере одной открытой рамки считывания, по меньшей мере одной 3'-UTR (элемента) и по меньшей мере одной 5'-UTR (элемента) являются гетерологичными, т.е. ни по меньшей мере одна 3'-UTR (элемент) и по меньшей мере одна 5'-UTR (элемент), ни открытая рамка считывания и 3'-UTR (элемент) или 5'-UTR (элемент) соответственно, не встречаются в естественных условиях (в природе) в рассматриваемой комбинации. Это означает, что искусственная молекула нуклеиновой кислоты содержит ОРС, 3'-UTR (элемент) и 5'-UTR (элемент), которые все являются гетерологичными друг другу, например, они являются рекомбинантными, поскольку каждый из указанных элементов происходит из различных генов (и их 5'- и 3'-UTR). В другом предпочтительном варианте осуществления изобретения 3'-UTR (элемент) не происходит из 3'-UTR (элемента) вирусного гена или не имеет происхождения из вируса.
Предпочтительно по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент функционально связан с ОРС. Это означает, что предпочтительно 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент ассоциирован с ОРС таким образом, что он может осуществлять функцию, такую как функция повышения или стабилизации экспрессии кодируемого пептида или белка, или функцию стабилизации искусственной молекулы нуклеиновой кислоты. Предпочтительно ОРС и 3'-UTR-элемент ассоциированы в направлении 5'→3' и/или 5'-UTR-элемент и ОРС ассоциированы в направлении 5'→3'. Таким образом, предпочтительно искусственная молекула нуклеиновой кислоты содержит, как правило, структуру 5'-[5'-UTR-элемент]-(необязательный)-линкер-ОРС-[3'-UTR-элемент]-3', при этом искусственная молекула нуклеиновой кислоты может содержать только 5'-UTR-элемент и не содержать 3'-UTR-элемент, только 3'-UTR-элемент и не содержать 5'-UTR-элемент, или оба, и 3'-UTR-элемент, и 5'-UTR-элемент. Кроме того, линкер может присутствовать или отсутствовать. Например, линкер может состоять из одного или нескольких нуклеотидов, например, представлять собой сегмент, состоящий из 1-50 или 1-20 нуклеотидов, например, содержащий или состоящий из одного или нескольких сайтов, распознаваемых рестриктазами (сайтов рестрикции).
Предпочтительно по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент содержит или состоит из нуклеотидной последовательности, которая получена из 3'-UTR и/или 5'-UTR транскрипта гена, выбранного из группы, которая состоит из ZNF460, TGM2, IL7R, BGN, TK1, RAB3B, СВХ6, FZD2, COL8A1, NDUFS7, PHGDH, PLK2, TSPO, PTGS1, FBXO32, NID2, ATP5D, EXOSC4, NOL9, UBB4B, VPS18, ORMDL2, FSCN1, ТМЕМ33, TUBA4A, ЕМР3, ТМЕМ201, CRIP2, BRAT1, SERPINH1, CD9, DPYSL2, CDK9, TFRC, PSMB3 5'-UTR, FASN, PSMB6, PRSS56, KPNA6, SFT2D2, PARD6B, LPP, SPARC, SCAND1, VASN, SLC26A1, LCLAT1, FBXL18, SLC35F6, RAB3D, MAP1B, VMA21, CYBA, SEZ6L2, PCOLCE, VTN, ALDH16A1, RAVER1, KPNA6, SERINC5, JUP, CPN2, CRIP2, EPT1, PNPO, SSSCA1, POLR2L, LIN7C, UQCR10, PYCRL, AMN, MAP1S, NDUFS7, PHGDH, TSPO, ATP5D, EXOSC4, TUBB4B, TUBA4A, EMP3, CRIP2, BRAT1, CD9, CDK9, PSMB3, PSMB6, PRSS56, SCAND1, AMN, CYBA, PCOLCE, MAP1S, VTN, ALDH16A1 (предпочтительно все человеческие) и Dpysl2, Ccnd1, Acox2, Cbx6, Ubc, Ldlr, Nudt22, Pcyoxl1, Ankrd1, Tmem37, Tspyl4, Slc7a3, Cst6, Aacs, Nosip, Itga7, Ccnd2, Ebp, Sf3b5, Fasn, Hmgcs1, Osr1, Lmnb1, Vma21, Kif20a, Cdca8, Slc7a1, Ubqln2, Prps2, Shmt2, Aurkb, Fignl1, Cad, Anln, Slfn9, Ncaph, Pole, Uhrf1, Gja1, Fam64a, Kif2c, Tspan10, Scand1, Gpr84, Fads3, Cers6, Cxcr4, Gprc5c, Fen1, Cspg4, Mrpl34, Comtd1, Armc6, Emr4, Atp5d, 1110001J03Rik, Csf2ra, Aarsd1, Kif22, Cth, Tpgs1, Ccl17, Alkbh7, Ms4a8a, Acox2, Ubc, Slpi, Pcyox1l, Igf2bp1, Tmem37, Slc7a3, Cst6, Ebp, Sf3b5, Plk1, Cdca8, Kif22, Cad, Cth, Pole, Kif2c, Scand1, Gpr84, Tpgs1, Ccl17, Alkbh7, Ms4a8a, Mrpl34, Comtd1, Armc6, Atp5d, 1110001J03Rik, Nudt22, Aarsd1 (предпочтительно все мышиные).
Предпочтительно по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, содержит или состоит из «функционального фрагмента», «функционального варианта» или «функционального фрагмента варианта» 3'-UTR и/или 5'-UTR транскрипта гена.
Предпочтительно по меньшей мере один 5'-UTR-элемент содержит нуклеотидную последовательность, которая получена из 5'-UTR транскрипта гена, выбранного из группы, которая состоит из ZNF460-5'-UTR, TGM2-5'-UTR, IL7R-5'-UTR, BGN-5'-UTR, TK1-5'-UTR, RAB3B-5'-UTR, CBX6-5'-UTR, FZD2-5'-UTR, COL8A1-5'-UTR, NDUFS7-5'-UTR, PHGDH-5'-UTR, PLK2-5'-UTR, TSPO-5'-UTR, PTGS1-5'-UTR, FBXO32-5'-UTR, NID2-5'-UTR, ATP5D-5'-UTR, EXOSC4-5'-UTR, NOL9-5'-UTR, UBB4B-5'-UTR, VPS18-5'-UTR, ORMDL2-5'-UTR, FSCN1-5'-UTR, TMEM33-5'-UTR, TUBA4A-5'-UTR, EMP3-5'-UTR, TMEM201-5'-UTR, CRIP2-5'-UTR, BRAT1-5'-UTR, SERPINH1-5'-UTR, CD9-5'-UTR, DPYSL2-5'-UTR, CDK9-5'-UTR, TFRC-5'-UTR, PSMB3 5'-UTR, FASN-5'-UTR, PSMB6-5'-UTR, PRSS56-5'-UTR, KPNA6-5'-UTR, SFT2D2-5'-UTR, PARD6B-5'-UTR, LPP-5'-UTR, SPARC-5'-UTR, SCAND1-5'-UTR, VASN-5'-UTR, SLC26A1-5'-UTR, LCLAT1-5'-UTR, FBXL18-5'-UTR, SLC35F6-5'-UTR, RAB3D-5'-UTR, MAP1B-5'-UTR, VMA21-5'-UTR, CYBA-5'-UTR, SEZ6L2-5'-UTR, PCOLCE-5'-UTR, VTN-5'-UTR, ALDH16A1-5'-UTR, RAVER1-5'-UTR, KPNA6-5'-UTR, SERINC5-5'-UTR, JUP-5'-UTR, CPN2-5'-UTR, CRIP2-5'-UTR, EPT1-5'-UTR, PNPO-5'-UTR, SSSCA1-5'-UTR, POLR2L-5'-UTR, LIN7C-5'-UTR, UQCR10-5'-UTR, PYCRL-5'-UTR, AMN-5'-UTR, MAP1S-5'-UTR, (предпочтительно все человеческие) и Dpysl2-5'-UTR, Ccnd1-5'-UTR, Acox2-5'-UTR, Cbx6-5'-UTR, Ubc-5'-UTR, Ldlr-5'-UTR, Nudt22-5'-UTR, Pcyox1l-5'-UTR, Ankrd1-5'-UTR, Tmem37-5'-UTR, Tspyl4-5'-UTR, Slc7a3-5'-UTR, Cst6-5'-UTR, Aacs-5'-UTR, Nosip-5'-UTR, Itga7-5'-UTR, Ccnd2-5'-UTR, Ebp-5'-UTR, Sf3b5-5'-UTR, Fasn-5'-UTR, Hmgcs1-5'-UTR, Osr1-5'-UTR, Lmnb1-5'-UTR, Vma21-5'-UTR, Kif20a-5'-UTR, Cdca8-5'-UTR, Slc7a1-5'-UTR, Ubqln2-5'-UTR, Prps2-5'-UTR, Shmt2-5'-UTR, Aurkb-5'-UTR, Fignl1-5'-UTR, Cad-5'-UTR, Anln-5'-UTR, Slfn9-5'-UTR, Ncaph-5'-UTR, Pole-5'-UTR, Uhrf1-5'-UTR, Gja1-5'-UTR, Fam64a-5'-UTR, Kif2c-5'-UTR, Tspan10-5'-UTR, Scand1-5'-UTR, Gpr84-5'-UTR, Fads3-5'-UTR, Cers6-5'-UTR, Cxcr4-5'-UTR, Gprc5c-5'-UTR, Fen1-5'-UTR, Cspg4-5'-UTR, Mrpl34-5'-UTR, Comtd1-5'-UTR, Armc6-5'-UTR, Emr4-5'-UTR, Atp5d-5'-UTR, 1110001J03Rik-5'-UTR, Csf2ra-5'-UTR, Aarsd1-5'-UTR, Kif22-5'-UTR, Cth-5'-UTR, Tpgs1-5'-UTR, Ccl17-5'-UTR, Alkbh7-5'-UTR, Ms4a8a-5'-UTR (предпочтительно все мышиные).
Предпочтительно по меньшей мере один 3'-UTR-элемент содержит или состоит из нуклеотидной последовательности, которая получена из 3'-UTR транскрипта гена, выбранного из группы, которая состоит из NDUFS7-3'-UTR, PHGDH-3'-UTR, TSPO-3'-UTR, ATP5D-3'-UTR, EXOSC4-3'-UTR, TUBB4B-3'-UTR, TUBA4A-3'-UTR, EMP3-3'-UTR, CRIP2-3'-UTR, BRAT1-3'-UTR, CD9-3'-UTR, CDK9-3'-UTR, PSMB3-3'-UTR, PSMB6-3'-UTR, PRSS56-3'-UTR, SCAND1-3'-UTR, AMN-3'-UTR, CYBA-3'-UTR, PCOLCE-3'-UTR, MAP1S-3'-UTR, VTN-3'-UTR, ALDH16A1-3'-UTR (предпочтительно все человеческие) и Асох2-3'-UTR, Ubc-3'-UTR, Slpi-3'-UTR, Pcyox1l-3'-UTR, Igf2bp1-3'-UTR, Tmem37-3'-UTR, Slc7a3-3'-UTR, Cst6-3'-UTR, Ebp-3'-UTR, Sf3b5-3'-UTR, Plk1-3'-UTR, Cdca8-3'-UTR, Kif22-3'-UTR, Cad-3'-UTR, Cth-3'-UTR, Pole-3'-UTR, Kif2c-3'-UTR, Scand1-3'-UTR, Gpr84-3'-UTR, Tpgs1-3'-UTR, Ccl17-3'-UTR, Alkbh7-3'-UTR, Ms4a8a-3'-UTR, Mrpl34-3'-UTR, Comtd1-3'-UTR, Armc6-3'-UTR, Atp5d-3'-UTR, 1110001J03Rik-3'-UTR, Nudt22-3'-UTR, Aarsd1-3'-UTR (предпочтительно все мышиные).
Предпочтительно также, чтобы искусственная нуклеиновая кислота, предлагаемая в изобретении, содержала и (I) по меньшей мере одну предпочтительную 5'-UTR, и (I) по меньшей мере одну предпочтительную 3'-UTR.
В наиболее предпочтительном варианте осуществления изобретения по меньшей мере один 5'-UTR-элемент содержит нуклеотидную последовательность, которая получена из 5'-UTR транскрипта гена, выбранного из группы, которая состоит из ZNF460-5'-UTR, TGM2-5'-UTR, IL7R-5'-UTR, COL8A1-5'-UTR, NDUFS7-5'-UTR, PLK2-5'-UTR, FBXO32-5'-UTR, ATP5D-5'-UTR, TUBB4B-5'-UTR, ORMDL2-5'-UTR, FSCN1-5'-UTR, CD9-5'-UTR, PYSL2-5'-UTR, PSMB3-5'-UTR, PSMB6-5'-UTR, KPNA6-5'-UTR, SFT2D2-5'-UTR, LCLAT1-5'-UTR, FBXL18-5'-UTR, SLC35F6-5'-UTR, VMA21-5'-UTR, SEZ6L2-5'-UTR, PCOLCE-5'-UTR, VTN-5'-UTR, ALDH16A1-5'-UTR, KPNA6-5'-UTR, JUP-5'-UTR, CPN2-5'-UTR, PNPO-5'-UTR, SSSCA1-5'-UTR, POLR2L-5'-UTR, LIN7C-5'-UTR, UQCR10-5'-UTR, PYCRL-5'-UTR, AMN-5'-UTR, MAP1S-5'-UTR (все человеческие), Dpysl2-5'-UTR, Acox2-5'-UTR, Ubc-5'-UTR, Nudt22-5'-UTR, Pcyox1l-5'-UTR, Ankrd1-5'-UTR, Tspyl4-5'-UTR, Slc7a3-5'-UTR, Aacs-5'-UTR, Nosip-5'-UTR, Itga7-5'-UTR, Ccnd2-5'-UTR, Ebp-5'-UTR, Sf3b5-5'-UTR, Fasn-5'-UTR, Hmgcs1-5'-UTR, Osr1-5'-UTR, Lmnb1-5'-UTR, Vma21-5'-UTR, Kif20a-5'-UTR, Cdca8-5'-UTR, Slc7a1-5'-UTR, Ubqln2-5'-UTR, Prps2-5'-UTR, Shmt2-5'-UTR, Fignl1-5'-UTR, Cad-5'-UTR, Anln-5'-UTR, Slfn9-5'-UTR, Ncaph-5'-UTR, Pole-5'-UTR, Uhrf1-5'-UTR, Gja1-5'-UTR, Fam64a-5'-UTR, Tspan10-5'-UTR, Scand1-5'-UTR, Gpr84-5'-UTR, Cers6-5'-UTR, Cxcr4-5'-UTR, Gprc5c-5'-UTR, Fen1-5'-UTR, Cspg4-5'-UTR, Mrpl34-5'-UTR, Comtd1-5'-UTR, Armc6-5'-UTR, Emr4-5'-UTR, Atp5d-5'-UTR, Csf2ra-5'-UTR, Aarsd1-5'-UTR, Cth-5'-UTR, Tpgs1-5'-UTR, Ccl17-5'-UTR, Alkbh7-5'-UTR, Ms4a8a-5'-UTR (все мышиные).
Установлено, что такие UTR-элементы способствуют высокой эффективности трансляции.
В наиболее предпочтительном варианте осуществления изобретения по меньшей мере один 3'-UTR-элемент содержит нуклеотидную последовательность, которая получена из 3'-UTR транскрипта гена, выбранного из группы, которая состоит из NDUFS7-3'-UTR, PHGDH-3'-UTR, TSPO-3'-UTR, ATP5D-3'-UTR, EXOSC4-3'-UTR, TUBB4B-3'-UTR, TUBA4A-3'-UTR, EMP3-3'-UTR, CRIP2-3'-UTR, BRAT1-3'-UTR, CD9-3'-UTR, CDK9-3'-UTR, PSMB3-3'-UTR, PSMB6-3'-UTR, PRSS56-3'-UTR, SCAND1-3'-UTR, AMN-3'-UTR, CYBA-3'-UTR, PCOLCE-3'-UTR, MAP1S-3'-UTR, VTN-3'-UTR, ALDH16A1-3'-UTR (предпочтительно все человеческие) и Acox2-3'-UTR, Ubc-3'-UTR, Slpi-3'-UTR, Pcyox1l-3'-UTR, Igf2bp1-3'-UTR, Tmem37-3'-UTR, Slc7a3-3'-UTR, Cst6-3'-UTR, Ebp-3'-UTR, Sf3b5-3'-UTR, Plk1-3'-UTR, Cdca8-3'-UTR, Kif22-3'-UTR, Cad-3'-UTR, Cth-3'-UTR, Pole-3'-UTR, Kif2c-3'-UTR, Scand1-3'-UTR, Gpr84-3'-UTR, Tpgs1-3'-UTR, Ccl17-3'-UTR, Alkbh7-3'-UTR, Ms4a8a-3'-UTR, Mrpl34-3'-UTR, Comtd1-3'-UTR, Armc6-3'-UTR, Atp5d-3'-UTR, 1110001J03Rik-3'-UTR, Nudt22-3'-UTR, Aarsd1-3'-UTR, (предпочтительно все мышиные). Установлено, что такие UTR-элементы способствуют высокой эффективности трансляции.
Указанные наиболее предпочтительные варианты осуществления изобретения можно комбинировать таким образом, чтобы искусственная нуклеиновая кислота, предлагаемая в изобретении, содержала и (I) по меньшей мере одну наиболее предпочтительную 5'-UTR, и (I) по меньшей мере одну наиболее предпочтительную 3'-UTR.
Фраза «нуклеотидная последовательность, которая получена из 3'-UTR и/или 5'-UTR транскрипта гена» предпочтительно относится к нуклеотидной последовательности, основой которой является последовательность 3'-UTR гена и/или последовательность 5'-UTR транскрипта гена или его фрагмента или участка, предпочтительно встречающегося в естественных условиях гена или его фрагмента или участка. В этом контексте понятие «встречающийся в естественных условиях» является синонимом понятию «дикий тип». Указанная фраза включает последовательности, соответствующие полной последовательности 3'-UTR и/или полной последовательности 5'-UTR, т.е. полноразмерной последовательности 3'-UTR и/или 5'-UTR транскрипта гена, и последовательности, соответствующие фрагменту последовательности 3'-UTR и/или последовательности 5'-UTR транскрипта гена. Предпочтительно фрагмент 3'-UTR и/или 5'-UTR транскрипта гена состоит из непрерывного сегмента нуклеотидов, соответствующего непрерывному сегменту нуклеотидов полноразмерной 3'-UTR и/или 5'-UTR транскрипта гена, который включает по меньшей мере 5%, 10%, 20%, предпочтительно по меньшей мере 30%, более предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 50%, еще более предпочтительно по меньшей мере 60%, еще более предпочтительно по меньшей мере 70%, еще более предпочтительно по меньшей мере 80% и наиболее предпочтительно по меньшей мере 90% полноразмерной 3'-UTR и/или 5'-UTR транскрипта гена. В контексте настоящего изобретения такой фрагмент предпочтительно представляет собой функциональный фрагмент, представленный в настоящем описании. Предпочтительно фрагмент сохраняет функцию регулирования трансляции ОРС, сцепленной с 3'-UTR и/или 5'-UTR или ее фрагментом.
Понятия «вариант 3'-UTR и/или вариант 5'-UTR транскрипта гена и «его вариант» в контексте 3'-UTR и/или 5'-UTR транскрипта гена относятся к варианту 3'-UTR и/или 5'-UTR транскрипта встречающегося в естественных условиях гена, предпочтительно к варианту 3'-UTR и/или 5'-UTR транскрипта гена позвоночных, более предпочтительно к варианту 3'-UTR и/или 5'-UTR транскрипта гена млекопитающих, еще более предпочтительно к варианту 3'-UTR и/или 5'-UTR транскрипта гена приматов, прежде всего гена человека, представленного выше. Такой вариант может представлять собой модифицированную 3'-UTR и/или 5'-UTR транскрипта гена. Например, вариант 3'-UTR и/или вариант 5'-UTR может иметь одну или несколько делеций, инсерций, добавлений и/или замен нуклеотидов по сравнению с встречающейся в естественных условиях 3'-UTR и/или 5'-UTR, из которой получен вариант. Предпочтительно вариант 3'-UTR и/или вариант 5'-UTR транскрипта гена по меньшей мере на 40%, предпочтительно по меньшей мере на 50%, более предпочтительно по меньшей мере на 60%, более предпочтительно по меньшей мере на 70%, еще более предпочтительно по меньшей мере на 80%, еще более предпочтительно по меньшей мере на 90%, наиболее предпочтительно по меньшей мере на 95% идентичен встречающейся в естественных условиях 3'-UTR и/или 5'-UTR, из которой происходит вариант. Предпочтительно вариант представляет собой функциональный вариант, представленный в настоящем описании, из которой происходит вариант.
Фраза «нуклеотидная последовательность, которая получена из варианта 3'-UTR и/или из варианта 5'-UTR транскрипта гена» предпочтительно относится к нуклеотидной последовательности, основой которой является вариант последовательности 3'-UTR и/или 5'-UTR транскрипта гена или его фрагмент или участок, представленный выше. Эта фраза включает последовательности, соответствующие полной последовательности варианта 3'-UTR и/или 5'-UTR транскрипта гена, т.е. полноразмерной последовательности варианта 3'-UTR и/или полноразмерной последовательности варианта 5'-UTR транскрипта гена, и последовательности, соответствующие фрагменту варианта последовательности 3'-UTR и/или фрагменту варианта последовательности 5'-UTR транскрипта гена. Предпочтительно фрагмент варианта 3'-UTR и/или 5'-UTR транскрипта гена состоит из непрерывного сегмента нуклеотидов, соответствующего непрерывному сегменту нуклеотидов полноразмерного варианта 3'-UTR и/или 5'-UTR транскрипта гена, который включает по меньшей мере 20%, предпочтительно по меньшей мере 30%, более предпочтительно по меньшей мере 40%, более предпочтительно по меньшей мере 50%, еще более предпочтительно по меньшей мере 60%, еще более предпочтительно по меньшей мере 70%, еще более предпочтительно по меньшей мере 80%, и наиболее предпочтительно по меньшей мере 90% полноразмерного варианта 3'-UTR и/или 5'-UTR транскрипта гена. В контексте настоящего изобретения такой фрагмент варианта предпочтительно представляет собой функциональный фрагмент варианта, представленного в настоящем описании.
В контексте настоящего описания понятия «функциональный вариант» «функциональный фрагмент» и «функциональный фрагмент варианта» (который обозначают также как «функциональный вариантный фрагмент») означают, что фрагмент 3'-UTR и/или 5'-UTR, вариант 3'-UTR и/или 5'-UTR или фрагмент варианта 3'-UTR и/или 5'-UTR транскрипта гена выполняет по меньшей мере одну, предпочтительно более чем одну функцию встречающейся в естественных условиях 3'-UTR и/или 5'-UTR транскрипта гена, из которой получен вариант, фрагмент или фрагмент варианта. Такая функция может заключаться, например, в стабилизации мРНК и/или увеличении, стабилизации и/или пролонгировании производства белка с мРНК, и/или увеличении экспрессии белка или общего производства белка с мРНК, предпочтительно в клетке млекопитающего, такой как человеческая клетка. Предпочтительно функция 3'-UTR и/или 5'-UTR касается трансляции белка, кодируемого ОРС. Более предпочтительно функция включает повышение эффективности трансляции ОРС, связанной с 3'-UTR и/или 5'-UTR, или ее фрагментом или вариантом. В контексте настоящего изобретения наиболее предпочтительно, чтобы вариант, фрагмент и вариант фрагмента выполнял функцию стабилизации мРНК, предпочтительно в клетке млекопитающего, такой как человеческая клетка, по сравнению с мРНК, которая содержит референс-3'-UTR и/или референс-5'-UTR, или в которой отсутствует 3'-UTR и/или 5'-UTR, и/или функцию повышения, стабилизации и/или пролонгирования производства белка с мРНК, предпочтительно в клетке млекопитающего, такой как человеческая клетка, по сравнению с мРНК, которая содержит референс-3'-UTR и/или референс-5'-UTR, или в которой отсутствует 3'-UTR и/или 5'-UTR, и/или функцию увеличения производства белка с мРНК, предпочтительно в клетке млекопитающего, такой как человеческая клетка, по сравнению с мРНК, которая содержит референс-3'-UTR и/или референс-5'-UTR, или в которой отсутствует 3'-UTR и/или 5'-UTR. Референс-3'-UTR и/или референс-5'-UTR может представлять собой, например, 3'-UTR и/или 5'-UTR, встречающуюся в естественных условиях в комбинации с ОРС. Кроме того, функциональный вариант, функциональный фрагмент или функциональный вариант фрагмента 3'-UTR и/или 5'-UTR транскрипта гена предпочтительно не оказывает существенного понижающего действия на эффективность трансляции мРНК, которая содержит такой вариант, фрагмент или вариант фрагмента 3'-UTR и/или 5'-UTR, по сравнению с 3'-UTR дикого типа и/или 5'-UTR дикого типа, из которой получен вариант, фрагмент или вариант фрагмента. В контексте настоящего изобретения наиболее предпочтительная функция «функционального фрагмента», «функционального варианта» или «функционального варианта фрагмента» 3'-UTR и/или 5'-UTR транскрипта гена заключается в увеличении, стабилизации и/или пролонгировании производства белка посредством экспрессии мРНК, несущей функциональный вариант, функциональный фрагмент или функциональный вариант фрагмента, представленный выше.
Предпочтительно эффективность одной или нескольких функций, осуществляемых функциональным вариантом, функциональным фрагментом или функциональным вариантом фрагмента, такую как обеспечение эффективности трансляции, повышают по меньшей мере на 5%, более предпочтительно по меньшей мере на 10%, более предпочтительно по меньшей мере на 20%, более предпочтительно по меньшей мере на 30%, более предпочтительно по меньшей мере на 40%, более предпочтительно по меньшей мере на 50%, более предпочтительно по меньшей мере на 60%, еще более предпочтительно по меньшей мере 70%, еще более предпочтительно по меньшей мере 80%, наиболее предпочтительно по меньшей мере на 90% по сравнению с эффективностью трансляции, обеспечиваемой встречающейся в естественных условиях 3'-UTR и/или 5'-UTR транскрипта гена, из которого получен вариант, фрагмент или вариант фрагмента.
В контексте настоящего изобретения фрагмент 3'-UTR и/или 5'-UTR транскрипта гена или вариант 3'-UTR и/или 5'-UTR транскрипта гена предпочтительно имеет длину по меньшей мере примерно 3 нуклеотида, предпочтительно по меньшей мере примерно 5 нуклеотидов, более предпочтительно по меньшей мере примерно 10, 15, 20, 25 или 30 нуклеотидов, еще более предпочтительно по меньшей мере примерно 50 нуклеотидов, наиболее предпочтительно по меньшей мере примерно 70 нуклеотидов. Предпочтительно такой фрагмент 3'-UTR и/или 5'-UTR транскрипта гена или вариант 3'-UTR и/или 5'-UTR транскрипта гена представляет собой функциональный фрагмент, описанный выше. В предпочтительном варианте осуществления изобретения 3'-UTR и/или 5'-UTR транскрипта гена или его фрагмент или вариант имеет длину от 3 до примерно 500 нуклеотидов, предпочтительно от 5 до примерно 150 нуклеотидов, более предпочтительно от 10 до 100 нуклеотидов, еще более предпочтительно от 15 до 90, наиболее предпочтительно от 20 до 70 нуклеотидов. Как правило, 3'-UTR-элемент и/или 5'-UTR-элемент отличается тем, что содержит менее чем 500, 400, 300, 200, 150 или менее чем 100 нуклеотидов.
5'-UTR-элементы
Предпочтительно по меньшей мере один 5'-UTR-элемент содержит или состоит из нуклеотидной последовательности, которая идентична по меньшей мере примерно на 1, 2, 3, 4, 5, 10, 15, 20, 30 или 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% нуклеотидной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 1-151, или соответствующей последовательности РНК соответственно, или по меньшей мере один 5'-UTR-элемент содержит или состоит из фрагмента нуклеотидной последовательности, который идентичен по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% нуклеотидной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 1-151, или соответствующей последовательности РНК соответственно.
Среди последовательностей, подробно описанных ниже, SEQ ID NO: 1-136 можно рассматривать как последовательности 5'-UTR дикого типа, a SEQ ID NO: 136-151 можно рассматривать как искусственные последовательности 5'-UTR.
SEQ ID NO: 1 - 5'-UTR ZNF460 Homo sapiens
NM_006635.3
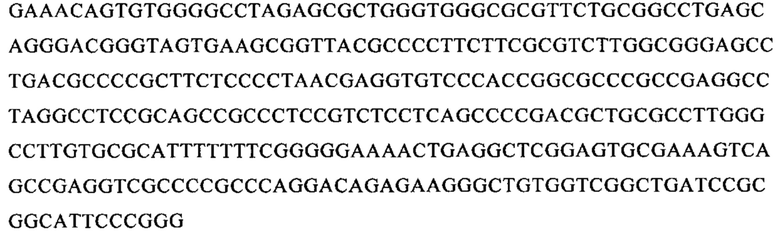
SEQ ID NO: 2 - 5'-UTR TGM2 Homo sapiens
NM_004613.2
SEQ ID NO: 3 - 5'-UTR IL7R Homo sapiens
NM_002185.3
SEQ ID NO: 4 - 5'-UTR BGN Homo sapiens
NM_001711.4
SEQ ID NO: 5 - 5'-UTR TK1 Homo sapiens
NM_003258.4
SEQ ID NO: 6 - 5'-UTR RAB3B Homo sapiens
NM_002867.3
SEQ ID NO: 7 - 5'-UTR CBX6 Homo sapiens
NM_014292.3
SEQ ID NO: 8 - 5'-UTR FZD2 Homo sapiens
NM_001466.3
SEQ ID NO: 9 - 5'-UTR COL8A1 Homo sapiens
NM_001850.4
SEQ ID NO: 10 - 5'-UTR NDUFS7 Homo sapiens
NM_024407.4
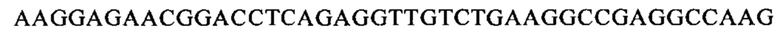
SEQ ID NO: 11 - 5'-UTR PHGDH Homo sapiens
NM_006623.3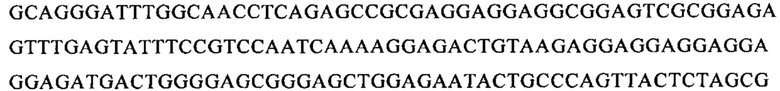
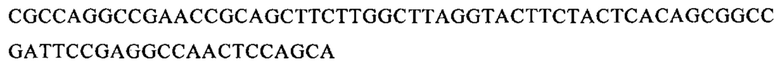
SEQ ID NO: 12 - 5'-UTR PLK2 Homo sapiens
NM_006622.3
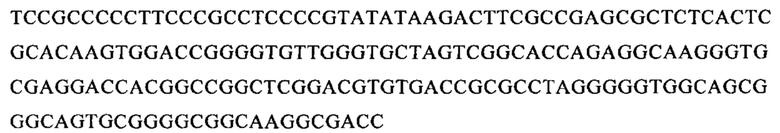
SEQ ID NO: 13 - 5'-UTR TSPO Homo sapiens
NM_000714.5
SEQ ID NO: 14 - 5'-UTR PTGS1 Homo sapiens
NM_000962.3
SEQ ID NO: 15 - 5'-UTR FBXO32 Homo sapiens
NM_058229.3
SEQ ID NO: 16 - 5'-UTR NID2 Homo sapiens
NM_007361.3
SEQ ID NO: 17 - 5'-UTR ATP5D Homo sapiens
NM_001687.4
SEQ ID NO: 18 - 5'-UTR EXOSC4 Homo sapiens
NM_019037.2
SEQ ID NO: 19 - 5'-UTR NOL9 Homo sapiens
NM_024654.4
SEQ ID NO: 20 - 5'-UTR TUBB4B Homo sapiens
NM_006088.5
SEQ ID NO: 21 - 5'-UTR VPS18 Homo sapiens
NM_020857.2
SEQ ID NO: 22 - 5'-UTR ORMDL2 Homo sapiens
NM_014182
SEQ ID NO: 23 - 5'-UTR FSCN1 Homo sapiens
NM_003088.3
SEQ ID NO: 24 - 5'-UTR TMEM33 Homo sapiens
NM_018126.2

SEQ ID NO: 25 - 5'-UTR TUBA4A Homo sapiens
NM_006000.2
SEQ ID NO: 26 - 5'-UTR EMP3 Homo sapiens
NM_001425.2
SEQ ID NO: 27 - 5'-UTR TMEM201 Homo sapiens
NM_001010866.3
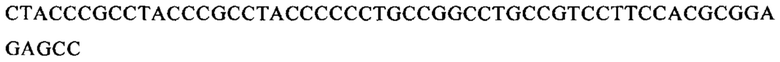
SEQ ID NO: 28 - 5'-UTR CRIP2 Homo sapiens
NM_001312.3
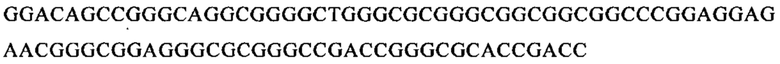
SEQ ID NO: 29 - 5'-UTR BRAT1 Homo sapiens
NM_152743.3
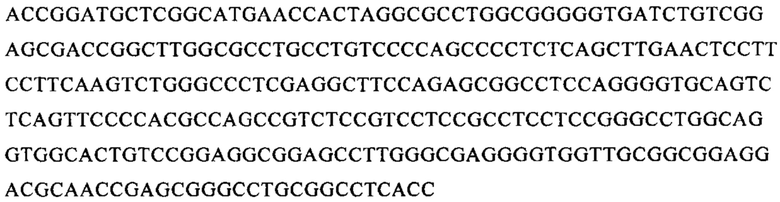
SEQ ID NO: 30 - 5'-UTR SERPINH1 Homo sapiens
NM_001235.3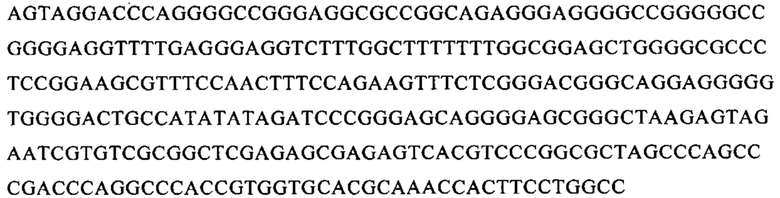
SEQ ID NO: 31 - 5'-UTR CD9 Homo sapiens
NM_001769.3
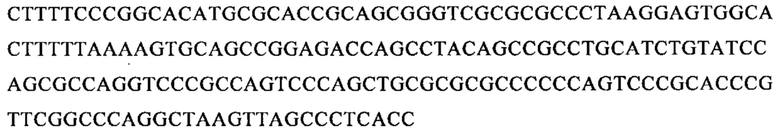
SEQ ID NO: 32 - 5'-UTR DPYSL2 Homo sapiens
NM_001386.5
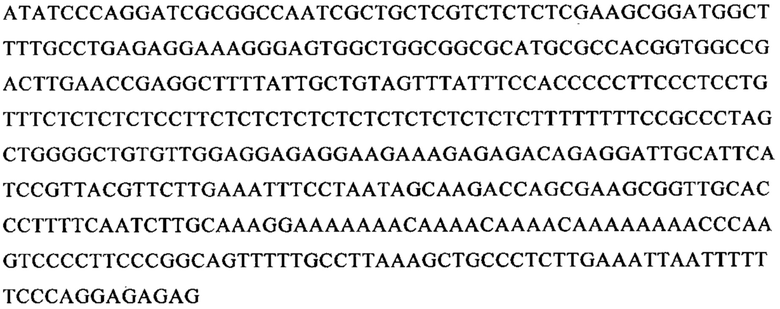
SEQ ID NO: 33 - 5'-UTR CDK9 Homo sapiens
NM_001261.3
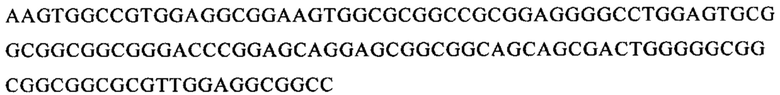
SEQ ID NO: 34 - 5'-UTR SSSCA1 Homo sapiens
NM_006396.1
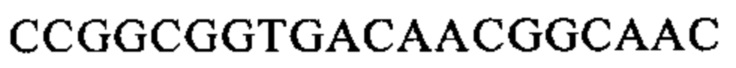
SEQ ID NO: 35 - 5'-UTR POLR2L Homo sapiens
NM_021128.4
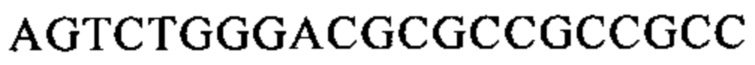
SEQ ID NO: 36 - 5'-UTR LIN7C Homo sapiens
NM_018362
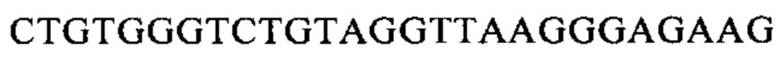
SEQ ID NO: 37 - 5'-UTR UQCR10 Homo sapiens
NM_001003684.1
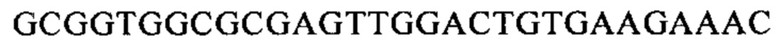
SEQ ID NO: 38 - 5'-UTR TFRC Homo sapiens
NM_001128148.1
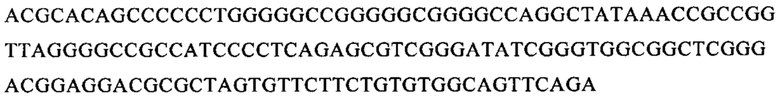
SEQ ID NO: 39 - 5'-UTR PSMB3 Homo sapiens
NM_002795.2
SEQ ID NO: 40 - 5'-UTR FASN Homo sapiens
NM_004104.4
SEQ ID NO: 41 - 5'-UTR PSMB6 Homo sapiens
NM_002798.2
SEQ ID NO: 42 - 5'-UTR PYCRL Homo sapiens
NM_023078.3
SEQ ID NO: 43 - 5'-UTR PRSS56 Homo sapiens
NM_001195129.1
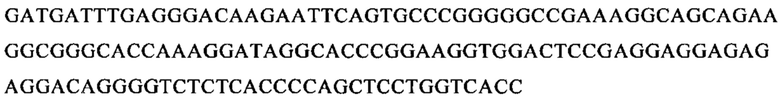
SEQ ID NO: 44 - 5'-UTR KPNA6 Homo sapiens
NM_012316.4
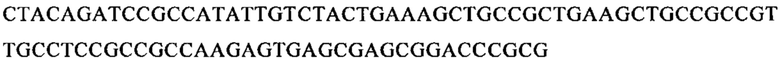
SEQ ID NO: 45 - 5'-UTR SFT2D2 Homo sapiens
NM_199344.2
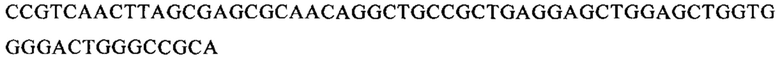
SEQ ID NO: 46 - 5'-UTR PARD6B Homo sapiens
NM_032521.2
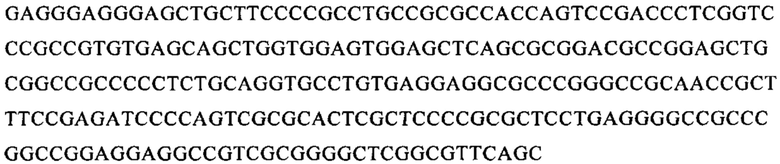
SEQ ID NO: 47 - 5'-UTR LPP Homo sapiens
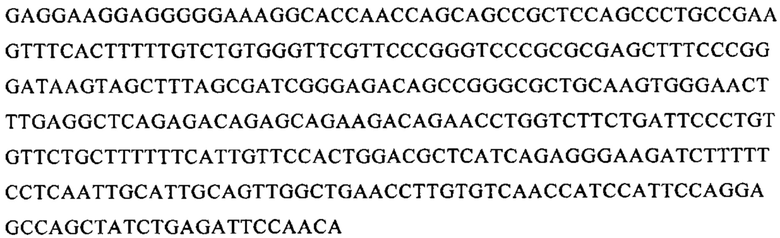
SEQ ID NO: 48 - 5'-UTR SPARC Homo sapiens
NM_003118.3
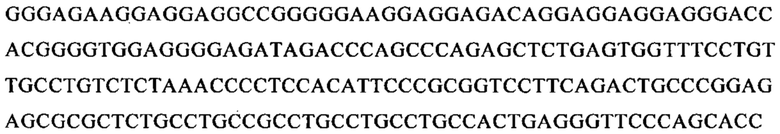
SEQ ID NO: 49 - 5'-UTR SCAND1 Homo sapiens
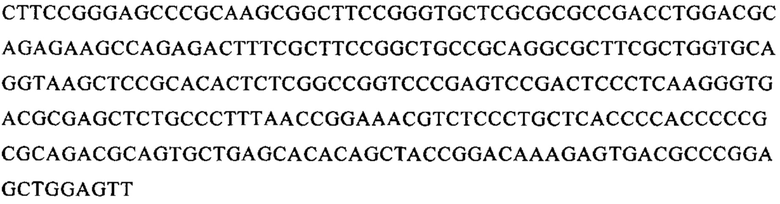
SEQ ID NO: 50 - 5'-UTR VASN Homo sapiens
NM_138440.2
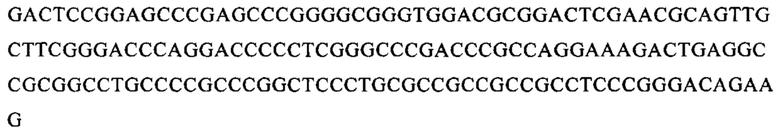
SEQ ID NO: 51 - 5'-UTR SLC26A1 Homo sapiens
NM_022042.3
SEQ ID NO: 52 - 5'-UTR LCLAT1 Homo sapiens
NM_182551.3
SEQ ID NO: 53 - 5'-UTR FBXL18 Homo sapiens
NM_024963.4
SEQ ID NO: 54 - 5'-UTR SLC35F6 Homo sapiens
NM_017877.3
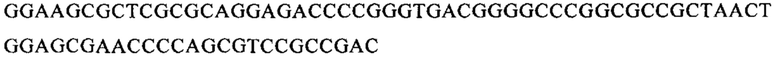
SEQ ID NO: 55 - 5'-UTR RAB3D Homo sapiens
NM_004283.3
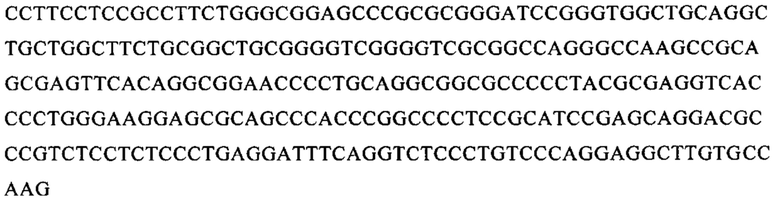
SEQ ID NO: 56 - 5'-UTR MAP1B Homo sapiens
NM_005909.3
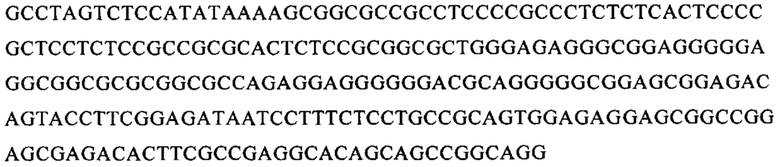
SEQ ID NO: 57 - 5'-UTR VMA21 Homo sapiens
NM_001017980.3
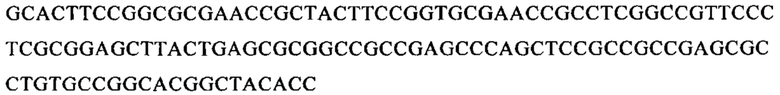
SEQ ID NO: 58 - 5'-UTR AMN Homo sapiens
NM_030943.3
SEQ ID NO: 59 - 5'-UTR CYBA Homo sapiens
NM_000101.3
SEQ ID NO: 60 - 5'-UTR SEZ6L2 Homo sapiens
NM_012410.3
SEQ ID NO: 61 - 5'-UTR PCOLCE Homo sapiens
NM_002593.3
SEQ ID NO: 62 - 5'-UTR MAP1S Homo sapiens
NM_018174.4
SEQ ID NO: 63 - 5'-UTR VTN Homo sapiens
NM_000638.3
SEQ ID NO: 64 - 5'-UTR ALDH16A1 Homo sapiens
NM_001145396.1
SEQ ID NO: 65 - 5'-UTR RAVER1 Homo sapiens
NM_133452.2
SEQ ID NO: 66 - 5'-UTR KPNA6 Homo sapiens (идентична SEQ ID NO: 44)
NM_012316.4
SEQ ID NO: 67 - 5'-UTR SERINC5 Homo sapiens
NM_178276.5
SEQ ID NO: 68 - 5'-UTR JUP Homo sapiens
NM_002230.2
SEQ ID NO: 69 - 5'-UTR CPN2 Homo sapiens
NM_001080513.2
SEQ ID NO: 70 - 5'-UTR CRIP2 Homo sapiens
NM_001312.3
SEQ ID NO: 71 - 5'-UTR EPT1 Homo sapiens
NM_033505.2
SEQ ID NO: 72 - 5'-UTR PNPO Homo sapiens
NM_018129.3
SEQ ID NO: 73 - 5'-UTR Dpysl2 Mus musculus
NM_009955.3
SEQ ID NO: 74 - 5'-UTR Ccnd1 Mus musculus
NM_007631.2
SEQ ID NO: 75 - 5'-UTR Acox2 Mus musculus
NM_001161667.1
SEQ ID NO: 76 - 5'-UTR Cbx6 (Npcd) Mus musculus
NM_001013360.2
SEQ ID NO: 77 - 5'-UTR Ubc Mus musculus
SEQ ID NO: 78 - 5'-UTR Ldlr Mus musculus
NM_001252659.1
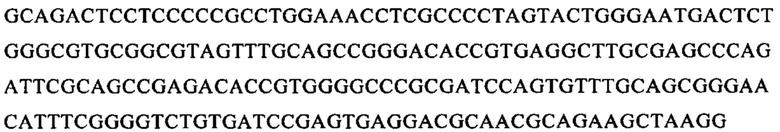
SEQ ID NO: 79 - 5'UTR Nudt22 Mus musculus
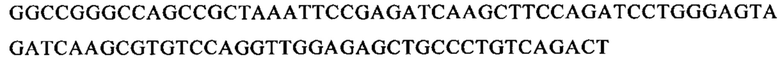
SEQ ID NO: 80 - 5'-UTR Pcyox11 Mus musculus
NM_172832.4
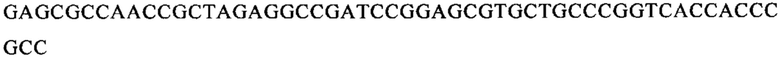
SEQ ID NO: 81 - 5'-UTR Ankrdl Mus musculus
NM_013468.3
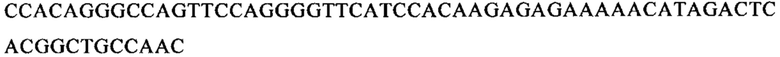
SEQ ID NO: 82 - 5'-UTR Tmem37 Mus musculus
NM_019432.2
SEQ ID NO: 83 - 5'-UTR Tspyl4 Mus musculus
NM_030203.2
SEQ ID NO: 84 - 5'-UTR Slc7a3 Mus musculus
SEQ ID NO: 85 - 5'-UTR Cst6 Mus musculus
SEQ ID NO: 86 - 5'-UTR Aacs Mus musculus
NM_030210.1
SEQ ID NO: 87 - 5'-UTR Nosip Mus musculus
NM_001163684.1
SEQ ID NO: 88 - 5'-UTR Itga7 Mus musculus
NM_008398.2
SEQ ID NO: 89 - 5'-UTR Ccnd2 Mus musculus
NM_009829.3
SEQ ID NO: 90 - 5'-UTR Ebp Mus musculus
SEQ ID NO: 91 - 5'-UTR Sf3b5 Mus musculus
NM_009829.3
SEQ ID NO: 92 - 5'-UTR Fasn Mus musculus
SEQ ID NO: 93 - 5'-UTR Hmgcs1 Mus musculus
SEQ ID NO: 94 - 5'-UTR Osr1 Mus musculus
NM_011859.3
SEQ ID NO: 95 - 5'-UTR Lmnb1 Mus musculus
NM_011121.3
SEQ ID NO: 96 - 5'-UTR Aarsd1 Mus musculus
NM_144829.1
SEQ ID NO: 97 - 5'-UTR Vma21 Mus musculus
NM_001081356.2
SEQ ID NO: 98 - 5'-UTR Kif20a Mus musculus
SEQ ID NO: 99 - 5'-UTR Cdca8 Mus musculus
NM_026560.4
SEQ ID NO: 100 - 5'-UTR Slc7a1 Mus musculus
NM_007513.4
SEQ ID NO: 101 - 5'-UTR Ubqln2 Mus musculus
NM_018798.2
SEQ ID NO: 102 - 5'-UTR Prps2 Mus musculus
NM_026662.4
SEQ ID NO: 103 - 5'-UTR Shmt2 Mus musculus
NM_026662.4
SEQ ID NO: 104 - 5'-UTR Kif22 Mus musculus
NM_145588.1
SEQ ID NO: 105 - 5'-UTR Aurkb Mus musculus
NM_011496.1
SEQ ID NO: 106 - 5'-UTR Fign11 Mus musculus
SEQ ID NO: 107 - 5'-UTR Cad Mus musculus
NM_023525.2
SEQ ID NO: 108 - 5'-UTR Anln Mus musculus
NM_028390.3
SEQ ID NO: 109 - 5'-UTR Slfn9 Mus musculus
SEQ ID NO: 110 - 5'-UTR Ncaph Mus musculus
NM_144818.3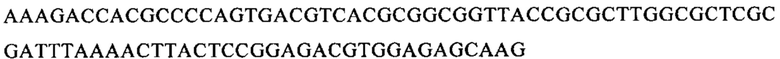
SEQ ID NO: 111 - 5'-UTR Cth Mus musculus
NM_145953.2
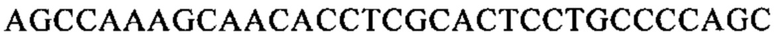
SEQ ID NO: 112 - 5'-UTR Pole Mus musculus
NM_011132.2
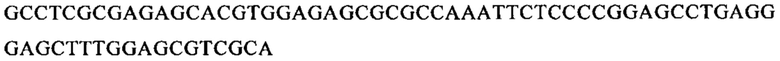
SEQ ID NO: 113 - 5'-UTR Uhrf1 Mus musculus
NM_001111079.1
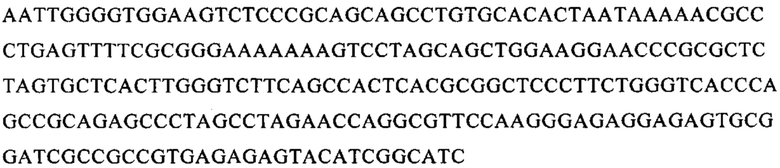
SEQ ID NO: 114 - 5'-UTR Gja1 Mus musculus
NM_010288.3
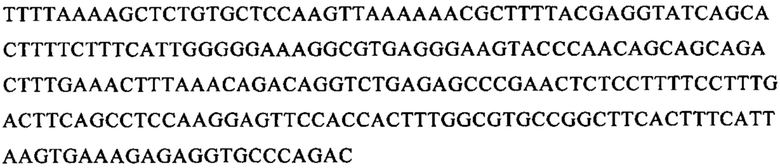
SEQ ID NO: 115 - 5'-UTR Fam64a Mus musculus
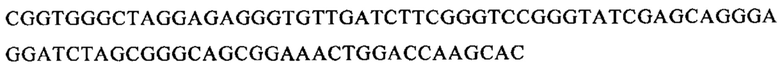
SEQ ID NO: 116 - 5'-UTR Kif2c Mus musculus
NM_134471.4
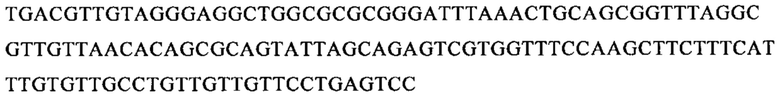
SEQ ID NO: 117 - 5'-UTR Tspan10 Mus musculus
NM_145363.2
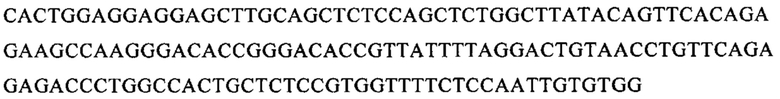
SEQ ID NO: 118 - 5'-UTR Scand1 Mus musculus
SEQ ID NO: 119 - 5'-UTR Gpr84 Mus musculus
NM_030720.1
SEQ ID NO: 120 - 5'-UTR Tpgs1 Mus musculus
BC138516.1
SEQ ID NO: 121 - 5'-UTR Ccl17 Mus musculus
NM_011332.3
SEQ ID NO: 122 - 5'-UTR Fads3 Mus musculus
NM_021890.3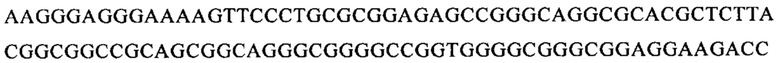
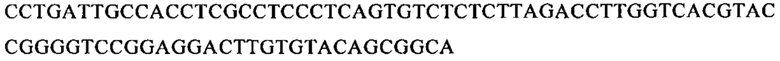
SEQ ID NO: 123 - 5'-UTR Cers6 Mus musculus
NM_172856.3
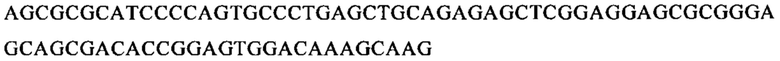
SEQ ID NO: 124 - 5'-UTR Alkbh7 Mus musculus
NM_027372.1
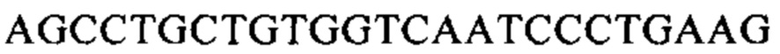
SEQ ID NO: 125 - 5'-UTR Ms4a8a Mus musculus
SEQ ID NO: 126 - 5'-UTR Cxcr4 Mus musculus
NM_009911.3
SEQ ID NO: 127 - 5'-UTR Gprc5c Mus musculus
SEQ ID NO: 128 - 5'-UTR Fen1 Mus musculus
NM_007999.4
SEQ ID NO: 129 - 5'-UTR Cspg4 Mus musculus
NM_139001.2
SEQ ID NO: 130 - 5'-UTR Mrpl34 Mus musculus
NM_053162.2
SEQ ID NO: 131 - 5'-UTR Comtd1 Mus musculus
SEQ ID NO: 132 - 5'-UTR Armc6 Mus musculus
NM_133972.2
SEQ ID NO: 133 - 5'-UTR Emr4 Mus musculus
NM_139138.3
SEQ ID NO: 134 - 5'-UTR Atp5d Mus musculus
NM_025313.2
SEQ ID NO: 135 - 5'-UTR 1110001J03Rik Mus musculus
SEQ ID NO: 136 - 5'-UTR Csf2ra Mus musculus
Некоторые из указанных 5'-UTR-элементов дикого типа имеют последовательности, которые отличаются от публично доступных последовательностей 5'-UTR, представленных в GenBank NCBI, см. таблицу 1 (пример 1). В этой таблице отражены результаты секвенирования, полученные при создании настоящего изобретения.
Так, 5'-UTR-элементы, выбранные из группы, которая состоит из SEQ ID NO: 45, SEQ ID NO: 47, SEQ ID NO: 49, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 84, SEQ ID NO: 85, SEQ ID NO: 90, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO:98, SEQ ID NO: 106, SEQ ID NO: 109, SEQ ID NO: 115, SEQ ID NO: 118, SEQ ID NO: 125, SEQ ID NO: 127, SEQ ID NO: 131, SEQ ID NO: 135, представляют собой элементы, предлагаемые в настоящем изобретении, и их можно применять в любом из объектов настоящего изобретения.
Примеры искусственных 5'-UTR-элементов, которые можно применять согласно настоящему изобретению
В некоторых вариантах осуществления изобретения 5'-UTR-элемент, предлагаемой в настоящем изобретении, отличается от 5'-UTR-элемента дикого типа. Такие 5'-UTR-элементы обозначают как «искусственные 5'-UTR-элементы».
Предпочтительно, чтобы искусственный 5'-UTR-элемент обладал степенью идентичности последовательности с 5'-UTR-элементом дикого типа, составляющей (а) менее 100%, и чтобы, в то же самое время, она составляла (б) более чем 10%, более чем 20%, более чем 30%, более чем 40%, более чем 50%, более чем 60%, более чем 70%, более чем 80%, более чем 90%, более чем 95%, такой 5'-UTR-элемент дикого типа выбирают из группы, которая состоит из SEQ ID NO: 1-136. Как правило, искусственный 5'-UTR-элемент отличается от 5'-UTR-элемента дикого типа тем, что в нем заменен(ы) по меньшей мере один нуклеотид, например, два нуклеотида, три нуклеотида, четыре нуклеотида, пять нуклеотидов, шесть нуклеотидов, семь нуклеотидов, восемь нуклеотидов, девять нуклеотидов, десять нуклеотидов или более чем десять нуклеотидов. Например, такую замену нуклеотидов можно рекомендовать в том случае, когда 5'-UTR-элемент дикого типа содержит нуклеотидный элемент, который рассматривается как «невыгодный». Например, в некоторых вариантах осуществления изобретения нуклеотидный элемент, который рассматривается как «невыгодный», выбирают из (I) внутреннего триплета ATG (т.е. триплета ATG, отличного от стартового кодона открытой рамки считывания нуклеиновой кислоты, предлагаемой в изобретении) или (II) сайта, распознаваемого рестриктазой (сайт расщепления), прежде всего сайта, распознаваемого рестриктазой (сайт расщепления), который распознается (может расщепляться) рестриктазой, применяемой в процессе создания (клонирования) искусственной нуклеиновой кислоты, предлагаемой в настоящем изобретении. Таким образом, можно специально интродуцировать определенное(ые) основание(я) (для обмена, предпочтительно замены, соответствующего(их) основания(й) дикого типа), так чтобы искусственный 5'-UTR-элемент не содержал нуклеотидный элемент, который рассматривается как «невыгодный». В конкретных вариантах осуществления изобретения искусственные 5'-UTR-элементы выбирают из группы, которая состоит из SEQ ID NO: 137-151:
SEQ ID NO: 137 - Искусственная последовательность (на основе SEQ ID NO: 3)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 138 - Искусственная последовательность (на основе SEQ ID NO: 9)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 139 - Искусственная последовательность (на основе SEQ ID NO: 14)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 140 - Искусственная последовательность (на основе SEQ ID NO: 17)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 141 - Искусственная последовательность (на основе SEQ ID NO: 18)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 142 - Искусственная последовательность (на основе SEQ ID NO: 29)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что два  заменены на два
заменены на два  оба подчеркнуты выше для большей выразительности]
оба подчеркнуты выше для большей выразительности]
SEQ ID NO: 143 - Искусственная последовательность (на основе SEQ ID NO: 31)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 144 - Искусственная последовательность (на основе SEQ ID NO: 42)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 145 - Искусственная последовательность (на основе SEQ ID NO: 43)
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что (I)  заменен на
заменен на  и что (II)
и что (II)  заменен на
заменен на  каждый подчеркнут выше для большей выразительности]
каждый подчеркнут выше для большей выразительности]
SEQ ID NO: 146 - Искусственная последовательность (на основе SEQ ID NO: 52)
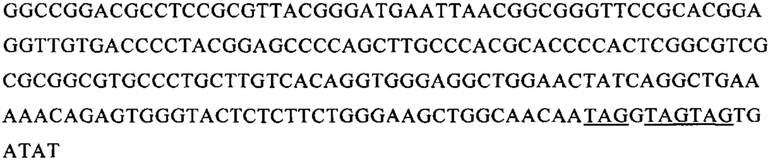
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что каждый из трех  заменен на
заменен на  каждый подчеркнут выше для большей выразительности]
каждый подчеркнут выше для большей выразительности]
SEQ ID NO: 147 - Искусственная последовательность (на основе SEQ ID NO: 109)
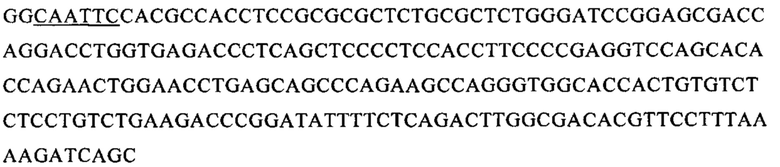
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 148 - Искусственная последовательность (на основе SEQ ID NO: 110)
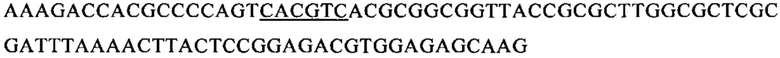
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что 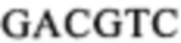 заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 149 - Искусственная последовательность (на основе SEQ ID NO: 119)
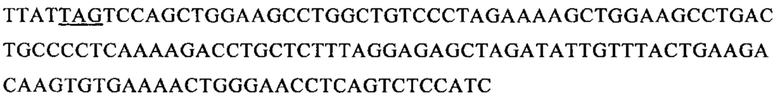
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 150 - Искусственная последовательность (на основе SEQ ID NO: 120)
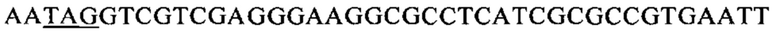
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
SEQ ID NO: 151 - Искусственная последовательность (на основе SEQ ID NO: 136)
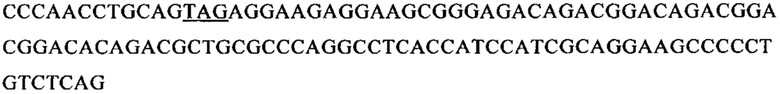
[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что  заменен на
заменен на  подчеркнут выше для большей выразительности]
подчеркнут выше для большей выразительности]
3'-UTR-элементы
Предпочтительно по меньшей мере один 3'-UTR-элемент содержит или состоит из нуклеотидной последовательности, которая идентична по меньшей мере примерно на 1, 2, 3, 4, 5, 10, 15, 20, 30 или 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% нуклеотидной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 152-204, или соответствующей последовательности ДНК или РНК соответственно, или по меньшей мере один 3'-UTR-элемент содержит или состоит из фрагмента нуклеотидной последовательности, который идентичен по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% нуклеотидной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 152-204, или соответствующей последовательности ДНК или РНК соответственно.
Среди последовательностей, подробно описанных ниже, SEQ ID NO: 152-203 можно рассматривать как последовательности 3'-UTR дикого типа, a SEQ ID NO: 204 можно рассматривать как искусственную последовательность 3'-UTR.
SEQ ID NO: 152 - 3'-UTR NDUFS7 Homo sapiens
NM_024407.4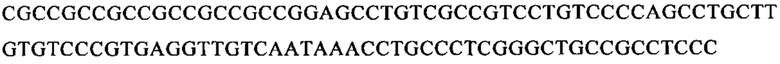
SEQ ID NO: 153 - 3'-UTR PHGDH Homo sapiens
NM_006623.3

SEQ ID NO: 154 - 3'-UTR TSPO Homo sapiens
NM_000714.5
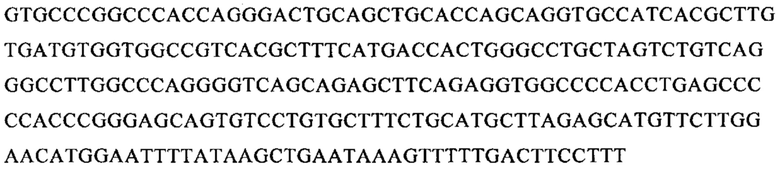
SEQ ID NO: 155 - 3'-UTR ATP5D Homo sapiens
NM_001687.4
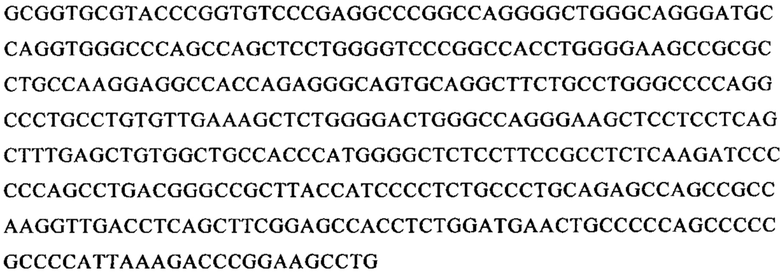
SEQ ID NO: 156 - 3'-UTR EXOSC4 Homo sapiens
NM_019037.2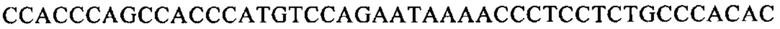
SEQ ID NO: 157 - 3'-UTR TUBB4B Homo sapiens
NM_006088.5
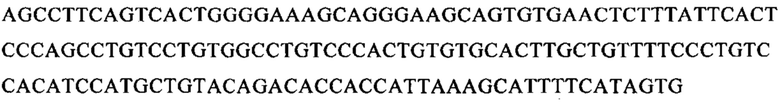
SEQ ID NO: 158 - 3' -UTR TUBA4A Homo sapiens
NM_006000.1
SEQ ID NO: 159 - 3'-UTR EMP3 Homo sapiens
SEQ ID NO: 160 - 3'-UTR CRIP2 Homo sapiens
NM_001312.3

SEQ ID NO: 161 - 3'-UTR BRAT1 Homo sapiens
NM_152743.3
SEQ ID NO: 162 - 3'-UTR CD9 Homo sapiens
NM_001769.3

SEQ ID NO: 163 - 3'-UTR CDK9 Homo sapiens
NM_001261.3

SEQ ID NO: 164 - 3'-UTR PSMB3 Homo sapiens
NM_002795.2
SEQ ID NO: 165 - 3'-UTR PSMB6 Homo sapiens
NM_002798.2
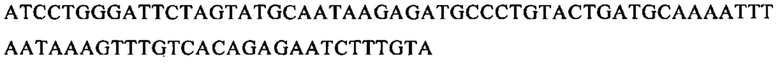
SEQ ID NO: 166 - 3'-UTR PRSS56 Homo sapiens
NM_001195129.1
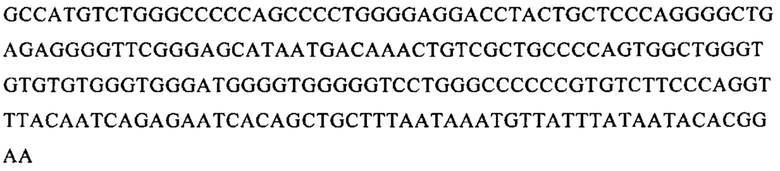
SEQ ID NO: 167 - 3'-UTR SCAND1 Homo sapiens
NM_016558
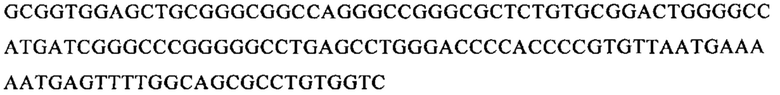
SEQ ID NO: 168 - 3'-UTR AMN Homo sapiens
NM_030943.3
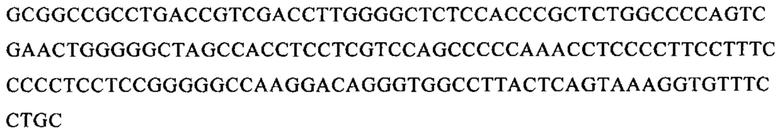
SEQ ID NO: 169 - 3'-UTR CYBA Homo sapiens
NM_000101.3
SEQ ID NO: 170 - 3'-UTR PCOLCE Homo sapiens
NM_002593.3
SEQ ID NO: 171 - 3'-UTR MAP1S Homo sapiens
NM_018174.4
SEQ ID NO: 172 - 3'-UTR VTN Homo sapiens
NM_000638.3
SEQ ID NO: 173 - 3'-UTR ALDH16A1 Homo sapiens
NM_001145396.1
SEQ ID NO: 174 - 3'-UTR Acox2 Mus musculus
NM_001161667.1
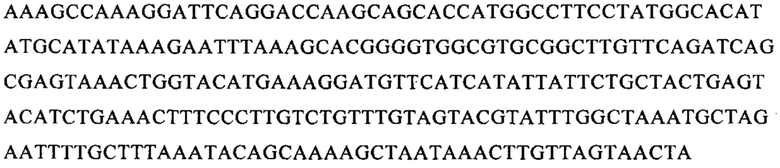
SEQ ID NO: 175 - 3'-UTR Ubc Mus musculus
BC006680.1

SEQ ID NO: 176 - 3'-UTR Slpi Mus musculus
NM_011414.3
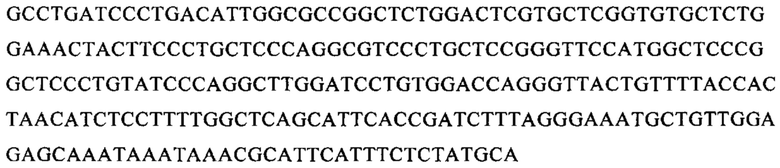
SEQ ID NO: 177 - 3'-UTR Nudt22 Mus musculus
NM_026675.2
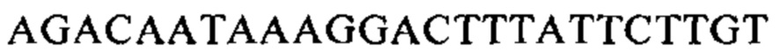
SEQ ID NO: 178 - 3'-UTR Pcyox11 Mus musculus
NM_172832.4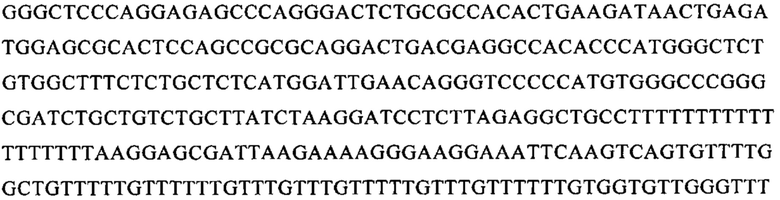
SEQ ID NO: 179 - 3'-UTR Igf2bp1 Mus musculus
SEQ ID NO: 180 - 3'-UTR Tmem37 Mus musculus
SEQ ID NO: 181 - 3'-UTR (240) Slc7a3 Mus musculus
NM_007515
SEQ ID NO: 182 - 3'-UTR Cst6 Mus musculus
SEQ ID NO: 183 - 3'-UTR Ebp Mus musculus
SEQ ID NO: 184 - 3'-UTR Sf3b5 Mus musculus
NM_009829.3
SEQ ID NO: 185 - 3'-UTR Plk1 Mus musculus
NM_011121.3
SEQ ID NO: 186 - 3'-UTR Aarsd1 Mus musculus
NM_144829.1
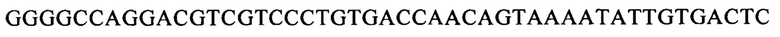
SEQ ID NO: 187 - 3'-UTR Cdca8 Mus musculus
NM_026560.4
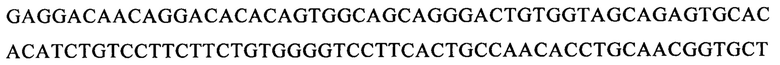

SEQ ID NO: 188 - 3'-UTR Kif22 Mus musculus
NM_145588.1
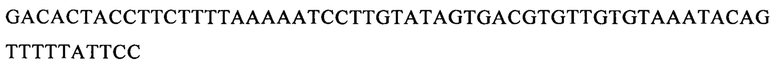
SEQ ID NO: 189 - 3'-UTR Cad Mus musculus
NM_023525.2
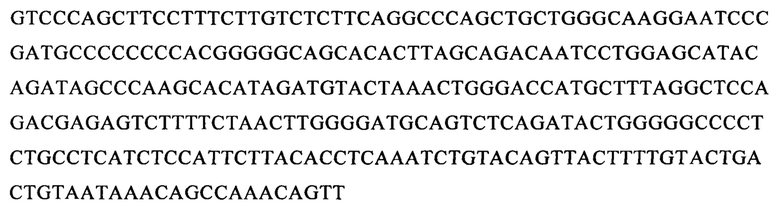
SEQ ID NO: 190 - 3'-UTR Cth Mus musculus
NM_145953.2

SEQ ID NO: 191 - 3'-UTR Pole Mus musculus
NM_011132.2
SEQ ID NO: 192 - 3'-UTR Kif2c
Mus musculus NM_134471.4

SEQ ID NO: 193 - 3'-UTR Scand1 Mus musculus
NM_020255.3
SEQ ID NO: 194 - 3'-UTR Gpr84 Mus musculus
NM_030720.1
SEQ ID NO: 195 - 3'-UTR Tpgs1 Mus musculus
NM_148934.2
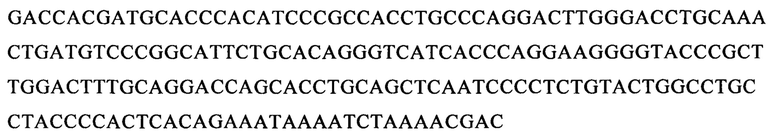
SEQ ID NO: 196 - 3'-UTR Cel17 Mus musculus
NM_011332.3
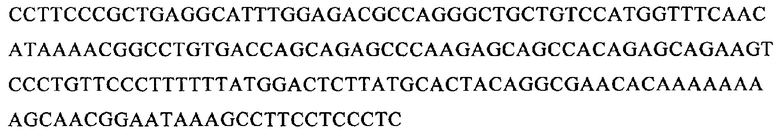
SEQ ID NO: 197 - 3'-UTR Alkbh7 Mus musculus
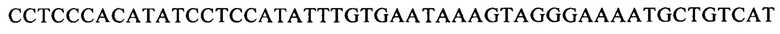
SEQ ID NO: 198 - 3'-UTR Ms4a8a Mus musculus
NM_022430.2
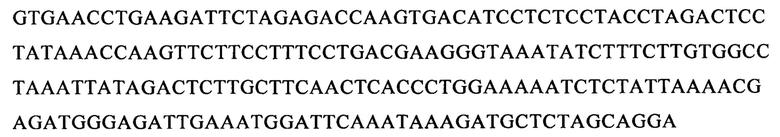
SEQ ID NO: 199 - 3'-UTR Mrp134 Mus musculus
NM_053162.2
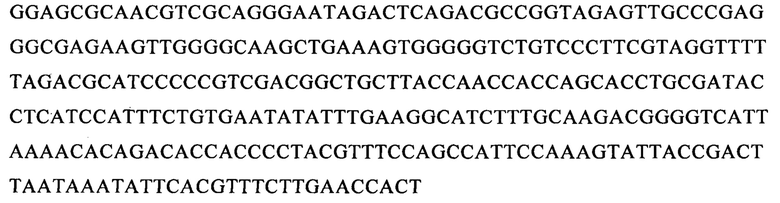
SEQ ID NO: 200 - 3'-UTR Comtd1 Mus musculus
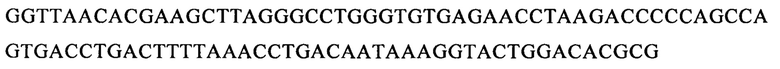
SEQ ID NO: 201 - 3'-UTR Armc6 Mus musculus
NM_133972.2

SEQ ID NO: 202 - 3'-UTR Atp5d Mus musculus
NM_025313.2
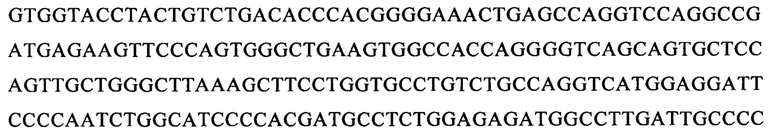
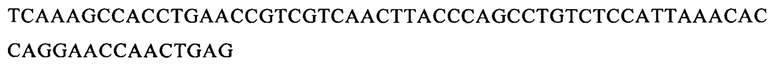
SEQ ID NO: 203 - 3'-UTR 1110001J03Rik Mus musculus
NM_025363.3

Некоторые из указанных 3'-UTR-элементов дикого типа отличаются от публично доступных последовательностей 3'-UTR, представленных в GenBank NCBI, см. таблицу 2 (пример 1). В указанной таблице отражены результаты секвенирования, полученные при создании настоящего изобретения.
Так, 3'-UTR-элементы, выбранные из группы, которая состоит из SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 197, SEQ ID NO: 200, представляют собой элементы, предлагаемые в настоящем изобретении, и их можно применять в любом из объектов настоящего изобретения.
Пример искусственных 3'-UTR-элементов, которые можно применять согласно настоящему изобретению
В некоторых вариантах осуществления изобретения 3'-UTR-элемент, предлагаемой в настоящем изобретении, отличается от 3'-UTR-элемента дикого типа. Такие 3'-UTR-элементы обозначены как «искусственные 3'-UTR-элементы».
Предпочтительно, чтобы искусственный 3'-UTR-элемент обладал степенью идентичности с 3'-UTR-элементом дикого типа, составляющей (а) менее 100%, и чтобы, в то же самое время, она составляла (В) более чем 10%, более чем 20%, более чем 30%, более чем 40%, более чем 50%, более чем 60%, более чем 70%, более чем 80%, более чем 90%, более чем 95%, такой 3'-UTR-элемент дикого типа выбирают из группы, которая состоит из SEQ ID NO: 152-203. Как правило, искусственный 3'-UTR-элемент отличается от 3'-UTR-элемента дикого типа тем, что в нем заменен(ы) по меньшей мере один нуклеотид, например, два нуклеотида, три нуклеотида, четыре нуклеотида, пять нуклеотидов, шесть нуклеотидов, семь нуклеотидов, восемь нуклеотидов, девять нуклеотидов, десять нуклеотидов или более чем десять нуклеотидов. Например, такую замену нуклеотидов можно рекомендовать в том случае, когда 3'-UTR-элемент дикого типа содержит нуклеотидный элемент, который рассматривается как невыгодный. Например, в некоторых вариантах осуществления изобретения нуклеотидный элемент, который рассматривается как невыгодный, представляет собой сайт, распознаваемый рестриктазой (сайт расщепления), прежде всего сайт, распознаваемый рестриктазой (сайт расщепления), который распознается (может расщепляться) рестриктазой, применяемой в процессе создания (клонирования) искусственной нуклеиновой кислоты, предлагаемой в настоящем изобретении. Таким образом, можно специально интродуцировать определенное(ые) основание(я) (для обмена, предпочтительно замены, соответствующего(их) основания(й) дикого типа), так чтобы искусственный 3'-UTR-элемент не содержал нуклеотидный элемент, который рассматривается как невыгодный. В конкретных вариантах осуществления изобретения искусственные 3'-UTR-элементы имеют последовательность SEQ ID NO: 204:
SEQ ID NO: 204 - Искусственная последовательность (на основе SEQ ID NO: 192)

[Указанная последовательность соответствует служащей для нее основой последовательности дикого типа, за исключением того, что AGATCT заменен TGATCT, подчеркнут выше для большей выразительности]
Новые 5'-UTR-элементы и новые 3'-UTR-элементы
В настоящем изобретении предложены также новые 5'-UTR-элементы и новые 3'-UTR-элементы, т.е. 5'-UTR-элементы и 3'-UTR-элементы, которые были обнаружены при создании настоящего изобретения в человеческих клетках и мышиных клетках соответственно, но которые не представлены в публичных базах данных (см. пример 1). Любая 5'-UTR, выбранная из группы, которая состоит из SEQ ID NO: 45, SEQ ID NO: 47, SEQ ID NO: 49, может являться предпочтительной в некоторых вариантах осуществления настоящего изобретения. Любая 5'-UTR, выбранная из группы, которая состоит из SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 84, SEQ ID NO: 85, SEQ ID NO: 90, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 98, SEQ ID NO: 106, SEQ ID NO: 109, SEQ ID NO: 115, SEQ ID NO: 118, SEQ ID NO: 125, SEQ ID NO: 127, SEQ ID NO: 131, SEQ ID NO: 135, может являться предпочтительной в некоторых вариантах осуществления настоящего изобретения. Любая 3'-UTR, выбранная из группы, которая состоит из SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 197, SEQ ID NO: 200, может являться предпочтительной в некоторых вариантах осуществления настоящего изобретения.
Описание 5'-UTR-элементов и предпочтительных 3'-UTR-элементов
Предпочтительно по меньшей мере один 3'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, содержит или состоит из нуклеотидной последовательности, которая идентична по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99%, наиболее предпочтительно на 100% последовательности 3'-UTR транскрипта гена, выбранного из группы, которая состоит из NDUFS7-3'-UTR, PHGDH-3'-UTR, TSPO-3'-UTR, ATP5D-3'-UTR, EXOSC4-3'-UTR, TUBB4B-3'-UTR, TUBA4A-3'-UTR, EMP3-3'-UTR, CRIP2-3'-UTR, BRAT1-3'-UTR, PSMB3-3'-UTR, PSMB6-3'-UTR, SCAND1-3'-UTR, AMN-3'-UTR, CYBA-3'-UTR, PCOLCE-3'-UTR, MAP1S-3'-UTR, VTN-3'-UTR, ALDH16A1-3'-UTR (все человеческие), Acox2-3'-UTR, Ubc-3'-UTR, Slpi-3'-UTR, Igf2bp1-3'-UTR, Tmem37-3'-UTR, Slc7a3-3'-UTR, Cst6-3'-UTR, Ebp-3'-UTR, Sf3b5-3'-UTR, Cdca8-3'-UTR, Kif22-3'-UTR, Cad-3'-UTR, Pole-3'-UTR, Kif2c-3'-UTR, Scand1-3'-UTR, Gpr84-3'-UTR, Tpgs1-3'-UTR, Ccl17-3'-UTR, Alkbh7-3'-UTR, Ms4a8a-3'-UTR, Mrpl34-3'-UTR, Comtd1-3'-UTR, Armc6-3'-UTR, Atp5d-3'-UTR, 1110001 J03Rik-3'-UTR, Nudt22-3'-UTR (все мышиные). Наиболее предпочтительно по меньшей мере один 3'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, содержит или состоит из нуклеотидной последовательности, которая идентична по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99%, наиболее предпочтительно на 100% последовательности, выбранной из группы, которая состоит из SEQ ID NO: 152, SEQ ID NO: 153, SEQ ID NO: 154, SEQ ID NO: 155, SEQ ID NO: 156, SEQ ID NO: 157, SEQ ID NO: 158, SEQ ID NO: 159, SEQ ID NO: 160, SEQ ID NO: 161, SEQ ID NO: 164, SEQ ID NO: 165, SEQ ID NO: 167, SEQ ID NO: 168, SEQ ID NO: 169, SEQ ID NO: 170, SEQ ID NO: 171, SEQ ID NO: 172, SEQ ID NO: 173; SEQ ID NO: 174, SEQ ID NO: 175, SEQ ID NO: 176, SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 181, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 184, SEQ ID NO: 187, SEQ ID NO: 188, SEQ ID NO: 189, SEQ ID NO: 191, SEQ ID NO: 204 (в альтернативном варианте SEQ ID NO: 192), SEQ ID NO: 193, SEQ ID NO: 194, SEQ ID NO: 195, SEQ ID NO: 196, SEQ ID NO: 197, SEQ ID NO: 198, SEQ ID NO: 199, SEQ ID NO: 200, SEQ ID NO: 201, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 177, или соответствующих последовательностей РНК соответственно.
Предпочтительно по меньшей мере один 5'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, содержит или состоит из нуклеотидной последовательности, которая идентична по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99%, наиболее предпочтительно на 100% последовательности 5'-UTR транскрипта ZNF460-5'-UTR, TGM2-5'-UTR, IL7R-5'-UTR, COL8A1-5'-UTR, NDUFS7-5'-UTR, PLK2-5'-UTR, FBXO32-5'-UTR, ATP5D-5'-UTR, TUBB4B-5'-UTR, ORMDL2-5'-UTR, FSCN1-5'-UTR, CD9-5'-UTR, PYSL2-5'-UTR, PSMB3-5'-UTR, PSMB6-5'-UTR, KPNA6-5'-UTR, SFT2D2-5'-UTR, LCLAT1-5'-UTR, FBXL18-5'-UTR, SLC35F6-5'-UTR, VMA21-5'-UTR, SEZ6L2-5'-UTR, PCOLCE-5'-UTR, VTN-5'-UTR, ALDH16A1-5'-UTR, KPNA6-5'-UTR, JUP-5'-UTR, CPN2-5'-UTR, PNPO-5'-UTR, SSSCA1-5'-UTR, POLR2L-5'-UTR, LIN7C-5'-UTR, UQCR10-5'-UTR, PYCRL-5'-UTR, AMN-5'-UTR, MAP1S-5'-UTR (все человеческие), Dpysl2-5'-UTR, Acox2-5'-UTR, Ubc-5'-UTR, Nudt22-5'-UTR, Pcyox1l-5'-UTR, Ankrd1-5'-UTR, Tspyl4-5'-UTR, Slc7a3-5'-UTR, Aacs-5'-UTR, Nosip-5'-UTR, Itga7-5'-UTR, Ccnd2-5'-UTR, Ebp-5'-UTR, Sf3b5-5'-UTR, Fasn-5'-UTR, Hmgcs1-5'-UTR, Osr1-5'-UTR, Lmnb1-5'-UTR, Vma21-5'-UTR, Kif20a-5'-UTR, Cdca8-5'-UTR, Slc7a1-5'-UTR, Ubqln2-5'-UTR, Prps2-5'-UTR, Shmt2-5'-UTR, Fignl1-5'-UTR, Cad-5'-UTR, Anln-5'-UTR, Slfn9-5'-UTR, Ncaph-5'-UTR, Pole-5'-UTR, Uhrf1-5'-UTR, Gja1-5'-UTR, Fam64a-5'-UTR, Tspan10-5'-UTR, Scand1-5'-UTR, Gpr84-5'-UTR, Cers6-5'-UTR, Cxcr4-5'-UTR, Gprc5c-5'-UTR, Fen1-5'-UTR, Cspg4-5'-UTR, Mrpl34-5'-UTR, Comtd1-5'-UTR, Armc6-5'-UTR, Emr4-5'-UTR, Atp5d-5'-UTR, Csf2ra-5'-UTR, Aarsd1-5'-UTR, Cth-5'-UTR, Tpgs1-5'-UTR, Ccl17-5'-UTR, Alkbh7-5'-UTR, Ms4a8a-5'-UTR (все мышиные). Наиболее предпочтительно по меньшей мере один 5'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, содержит или состоит из нуклеотидной последовательности, которая идентична по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99%, наиболее предпочтительно на 100% последовательности, представленной в SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 137 (в альтернативном варианте SEQ ID NO: 3), SEQ ID NO: 138 (в альтернативном варианте SEQ ID NO: 9), SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 15, SEQ ID NO: 140 (в альтернативном варианте SEQ ID NO: 17), SEQ ID NO: 20, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 143 (в альтернативном варианте SEQ ID NO: 31), SEQ ID NO: 32, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 146 (в альтернативном варианте SEQ ID NO: 52), SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 57, SEQ ID NO: 60, SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 66, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 72, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 144 (в альтернативном варианте SEQ ID NO: 42), SEQ ID NO: 58, SEQ ID NO: 62; SEQ ID NO: 73, SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 80, SEQ ID NO: 81, SEQ ID NO: 83, SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 89, SEQ ID NO: 90, SEQ ID NO: 91, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 97, SEQ ID NO: 98, SEQ ID NO: 99, SEQ ID NO: 100, SEQ ID NO: 101, SEQ ID NO: 102, SEQ ID NO: 103, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 147 (в альтернативном варианте SEQ ID NO: 109), SEQ ID NO: 148 (в альтернативном варианте SEQ ID NO: 110), SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 149 (в альтернативном варианте SEQ ID NO: 119), SEQ ID NO: 123, SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO: 130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134, SEQ ID NO: 151 (в альтернативном варианте SEQ ID NO: 136), SEQ ID NO: 96, SEQ ID NO: 111, SEQ ID NO: 150 (на основе SEQ ID NO: 120), SEQ ID NO: 121, SEQ ID NO: 124, SEQ ID NO: 125 или соответствующей последовательности РНК соответственно.
По меньшей мере один 3'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, может также содержать или состоять из фрагмента нуклеотидной последовательности, идентичного по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99%, наиболее предпочтительно на 100% нуклеотидной последовательности 3'-UTR транскрипта гена, такой как последовательность 3'-UTR, представленная в SEQ ID NO: 152-204, при этом фрагмент предпочтительно представляет собой функциональный фрагмент или функциональный вариант фрагмента, описанный выше. Такой фрагмент предпочтительно имеет длину по меньшей мере примерно 3 нуклеотида, предпочтительно по меньшей мере примерно 5 нуклеотидов, более предпочтительно по меньшей мере примерно 10, 15, 20, 25 или 30 нуклеотидов, еще более предпочтительно по меньшей мере примерно 50 нуклеотидов, наиболее предпочтительно по меньшей мере примерно 70 нуклеотидов. В предпочтительном варианте осуществления изобретения фрагмент или его вариант имеет длину от 3 до примерно 500 нуклеотидов, предпочтительно от 5 до примерно 150 нуклеотидов, более предпочтительно от 10 до 100 нуклеотидов, еще более предпочтительно от 15 до 90, наиболее предпочтительно от 20 до 70 нуклеотидов. Предпочтительно указанные варианты, фрагменты или варианты фрагментов представляют собой функциональные варианты, функциональные фрагменты или функциональные варианты фрагментов 3'-UTR, которые пролонгируют производство белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, с эффективностью, составляющей по меньшей мере 30%, предпочтительно с эффективностью, составляющей по меньшей мере 40%, более предпочтительно по меньшей мере 50%, более предпочтительно по меньшей мере 60%, еще более предпочтительно по меньшей мере 70%, еще более предпочтительно по меньшей мере 80%, наиболее предпочтительно по меньшей мере 90% от эффективности пролонгирования производства белка, обеспечиваемой искусственной молекулой нуклеиновой кислоты, которая содержит нуклеотидную последовательность, выбранную из группы, которая состоит из SEQ ID NO: 152, SEQ ID NO: 153, SEQ ID NO: 154, SEQ ID NO: 155, SEQ ID NO: 156, SEQ ID NO: 157, SEQ ID NO: 158, SEQ ID NO: 159, SEQ ID NO: 160, SEQ ID NO: 161, SEQ ID NO: 164, SEQ ID NO: 165, SEQ ID NO: 167, SEQ ID NO: 168, SEQ ID NO: 169, SEQ ID NO: 170, SEQ ID NO: 171, SEQ ID NO: 172, SEQ ID NO: 173; SEQ ID NO: 174, SEQ ID NO: 175, SEQ ID NO: 176, SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 181, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 184, SEQ ID NO: 187, SEQ ID NO: 188, SEQ ID NO: 189, SEQ ID NO: 191, SEQ ID NO: 204 (в альтернативном варианте SEQ ID NO: 192), SEQ ID NO: 193, SEQ ID NO: 194, SEQ ID NO: 195, SEQ ID NO: 196, SEQ ID NO: 197, SEQ ID NO: 198, SEQ ID NO: 199, SEQ ID NO: 200, SEQ ID NO: 201, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 177.
По меньшей мере один 5'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, может также содержать или состоять из фрагмента нуклеотидной последовательности, идентичного по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99%, наиболее предпочтительно на 100% нуклеотидной последовательности 5'-UTR транскрипта гена, такой как последовательность 5'-UTR, представленная в SEQ ID NO: 1-151, при этом фрагмент предпочтительно представляет собой функциональный фрагмент или функциональный вариант фрагмента, описанный выше. Такой фрагмент предпочтительно имеет длину по меньшей мере примерно 3 нуклеотида, предпочтительно по меньшей мере примерно 5 нуклеотидов, более предпочтительно по меньшей мере примерно 10, 15, 20, 25 или 30 нуклеотидов, еще более предпочтительно по меньшей мере примерно 50 нуклеотидов, наиболее предпочтительно по меньшей мере примерно 70 нуклеотидов. В предпочтительном варианте осуществления изобретения фрагмент или его вариант имеет длину от 3 до примерно 500 нуклеотидов, предпочтительно от 5 до примерно 150 нуклеотидов, более предпочтительно от 10 до 100 нуклеотидов, еще более предпочтительно от 15 до 90, наиболее предпочтительно от 20 до 70 нуклеотидов. Предпочтительно указанные варианты, фрагменты или варианты фрагментов представляют собой функциональные варианты, функциональные фрагменты или функциональные варианты фрагментов 3'-UTR, которые пролонгируют производство белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, с эффективностью, составляющей по меньшей мере 30%, предпочтительно с эффективностью, составляющей по меньшей мере 40%, более предпочтительно по меньшей мере 50%, более предпочтительно по меньшей мере 60%, еще более предпочтительно по меньшей мере 70%, еще более предпочтительно по меньшей мере 80%, наиболее предпочтительно по меньшей мере 90% от эффективности пролонгирования производства белка, обеспечиваемой искусственной молекулой нуклеиновой кислоты, которая содержит нуклеотидную последовательность, выбранную из группы, которая состоит из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 137 (в альтернативном варианте SEQ ID NO: 3), SEQ ID NO: 138 (в альтернативном варианте SEQ ID NO: 9), SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 15, SEQ ID NO: 140 (в альтернативном варианте SEQ ID NO: 17), SEQ ID NO: 20, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 143 (в альтернативном варианте SEQ ID NO: 31), SEQ ID NO: 32, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 146 (в альтернативном варианте SEQ ID NO: 52), SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 57, SEQ ID NO: 60, SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 66, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 72, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 144 (в альтернативном варианте SEQ ID NO: 42), SEQ ID N0:58, SEQ ID NO: 62; SEQ ID NO: 73, SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 80, SEQ ID NO: 81, SEQ ID NO: 83, SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 89, SEQ ID NO: 90, SEQ ID NO: 91, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 97, SEQ ID NO: 98, SEQ ID NO: 99, SEQ ID NO: 100, SEQ ID NO: 101, SEQ ID NO: 102, SEQ ID NO: 103, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 147 (в альтернативном варианте SEQ ID NO: 109), SEQ ID NO: 148 (в альтернативном варианте SEQ ID NO: 110), SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 149 (в альтернативном варианте SEQ ID NO: 119), SEQ ID NO: 123, SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO: 130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134, SEQ ID NO: 151 (в альтернативном варианте SEQ ID NO: 136), SEQ ID NO: 96, SEQ ID NO: 111, SEQ ID NO: 150 (на основе SEQ ID NO: 120), SEQ ID NO: 121, SEQ ID NO: 124, SEQ ID NO: 125.
Другие предпочтительные варианты осуществления изобретения
Предпочтительно по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, имеет длину по меньшей мере примерно 3 нуклеотида, предпочтительно по меньшей мере примерно 5 нуклеотидовв, более предпочтительно по меньшей мере примерно 10, 15, 20, 25 или 30 нуклеотидов, еще более предпочтительно по меньшей мере примерно 50 нуклеотидов, наиболее предпочтительно по меньшей мере примерно 70 нуклеотидов. Верхний предел длины по меньшей мере одного 3'-UTR-элемента и/или по меньшей мере одного 5'-UTR-элемента может составлять 500 нуклеотидов или менее, например, 400, 300, 200, 150 или 100 нуклеотидов. В других вариантах осуществления изобретения верхний предел можно выбирать в диапазоне от 50 до 100 нуклеотидов. Например, его фрагмент или вариант может иметь длину от 3 до примерно 500 нуклеотидов, предпочтительно от 5 до примерно 150 нуклеотидов, более предпочтительно от 10 до 100 нуклеотидов, еще более предпочтительно от 15 до 90, наиболее предпочтительно от 20 до 70 нуклеотидов.
Может оказаться предпочтительным также, чтобы UTR-элемент, содержащийся в искусственной молекуле нуклеиновой кислоты, содержал (или состоял из) непрерывной последовательности, которая короче любой последовательности, выбранной из SEQ ID NO: 1-204, представленных в настоящем описании, при условии, что она все еще идентична на 70% или более, 80% или более, 90% или более или 95% или более соответствующей последовательности любой последовательности, выбранной из SEQ ID NO: 1-204. В таком случае предпочтительно замещающий UTR-элемент содержит непрерывную последовательность, которая по всей длине идентична любой последовательности, выбранной из SEQ ID NO: 1-204; однако, замещающий UTR-элемент является более коротким, например, имеет длину, составляющую 70% или более, 80% или более, 90% или более или 95% или более по сравнению со всей длиной последовательности, а в остальном является идентичным указанной последовательности, которая выбрана из SEQ ID NO: 1-204.
Кроме того, искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может содержать более одного 3'-UTR-элемента и/или более одного 5'-UTR-элемента, описанного выше. Например, искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может содержать один, два, три, четыре или большее количество 3'-UTR-элементов, и/или один, два, три, четыре или большее количество 5'-UTR-элементов, при этом индивидуальные 5'-UTR-элементы могут быть одинаковыми или они могут быть различными, и аналогично этому индивидуальные 5'-UTR-элементы могут быть одинаковыми или они могут быть различными. Например, искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может содержать два практически идентичных 3'-UTR-элемента, описанные выше, например, два 3'-UTR-элемента, содержащие или состоящие из нуклеотидной последовательности, которая получена из 3'-UTR транскрипта гена, например, из последовательности, представленной в SEQ ID NO: 152-204, или из фрагмента или варианта 3'-UTR транскрипта гена, его функциональных вариантов, его функциональных фрагментов или его функциональных вариантов фрагментов, описанных выше. Следовательно, например, искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может содержать два практически идентичных 5'-UTR-элемента, описанных выше, например, два 5'-UTR-элемента, содержащие или состоящие из нуклеотидной последовательности, которая получена из 5'-UTR транскрипта гена, such например, из последовательности, представленной в SEQ ID NO: 1-151, или из фрагмента или варианта 5'-UTR транскрипта гена, его функциональных вариантов, его функциональных фрагментов или его функциональных вариантов фрагментов, описанных выше.
При создании изобретения неожиданно было установлено, что искусственная молекула нуклеиновой кислоты, содержащая 3'-UTR-элемент, описанный выше, и/или 5'-UTR-элемент, описанный выше, может представлять собой или может позволять создавать молекулу мРНК, которая обеспечивает высокую эффективность трансляции. Так, 3'-UTR-элемент, представленный в настоящем описании, и/или 5'-UTR-элемент, представленный в настоящем описании, может повышать эффективность трансляции молекулы мРНК.
В частности, искусственная молекула нуклеиновой кислоты, предлагаемая в изобретении, может содержать (I) по меньшей мере один 3'-UTR-элемент и по меньшей мере один 5'-UTR-элемент, которые обеспечивают высокую эффективность трансляции; (II) по меньшей мере один 3'-UTR-элемент, который обеспечивает высокую эффективность трансляции, но не содержать 5'-UTR-элемент, который обеспечивает высокую эффективность трансляции; или (III) по меньшей мере один 5'-UTR-элемент, который обеспечивает высокую эффективность трансляции, но не содержать 3'-UTR-элемент, который обеспечивает высокую эффективность трансляции.
Однако, прежде всего, в случаях (II) и (III), но, возможно, также и в случае (I), искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может содержать дополнительно один или большее количество «дополнительных 3'-UTR-элементов и/или 5'-UTR-элементов», т.е. 3'-UTR-элементов и/или 5'-UTR-элементов, которые не удовлетворяют описанным выше требованиям. Например, искусственная молекула нуклеиновой кислоты, предлагаемая в изобретении, которая содержит 3'-UTR-элемент, предлагаемый в настоящем изобретении, т.е. 3'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, может дополнительно содержать любую дополнительную 3'-UTR и/или любую дополнительную 5'-UTR, в частности, дополнительную 5'-UTR, например, 5'-ТОР UTR, или любую другую 5'-UTR или другой 5'-UTR-элемент. Аналогично этому, например, искусственная молекула нуклеиновой кислоты, предлагаемая в изобретении, которая содержит 5'-UTR-элемент, предлагаемый в настоящем изобретении, т.е. 5'-UTR-элемент, который обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, может дополнительно содержать любую дополнительную 3'-UTR и/или любую дополнительную 5'-UTR, в частности, дополнительную 3'-UTR, например, 3'-UTR, полученную из 3'-UTR гена альбумина, наиболее предпочтительно 3'-UTR, содержащую последовательность, представленную в SEQ ID NO: 206 или 207, прежде всего SEQ ID NO: 207, или любую другую 3'-UTR или другой 3'-UTR-элемент.
Если помимо предлагаемого в изобретении по меньшей мере одного 5'-UTR-элемента и/или предлагаемого в изобретении по меньшей мере одного 3'-UTR-элемента, который обеспечивает высокую эффективность трансляции, в искусственной молекуле нуклеиновой кислоты, предлагаемой в изобретении, присутствуют дополнительная 3'-UTR (элемент) и/или дополнительная 5'-UTR (элемент), то дополнительная 5'-UTR (элемент) и/или дополнительная 3'-UTR (элемент) могут взаимодействовать с предлагаемым в изобретении 3'-UTR-элементом и/или предлагаемым в изобретении 5'-UTR-элементом и, таким образом, поддерживать воздействие на эффективность трансляции предлагаемого в изобретении 3'-UTR-элемента и/или предлагаемого в изобретении 5'-UTR-элемента соответственно. Такие дополнительная 3'-UTR и/или 5'-UTR (элементы) могут дополнительно поддерживать стабильность и эффективность трансляции. Кроме того, если в искусственной молекуле нуклеиновой кислоты, предлагаемой в изобретении, присутствуют оба, и предлагаемый в изобретении 3'-UTR-элемент, и предлагаемый в изобретении 5'-UTR-элемент, то предпочтительно имеет место синергетический эффект на воздействие предлагаемого в изобретении 3'-UTR-элемента и/или предлагаемого в изобретении 5'-UTR-элемента в отношении обеспечения эффективности трансляции.
Предпочтительно дополнительная 3'-UTR содержит или состоит из нуклеотидной последовательности, которая получена из 3'-UTR гена, выбранного из группы, которая состоит из гена альбумина, гена α-глобина, гена β-глобина, гена тирозингидроксилазы, гена липоксигеназы и гена коллагена альфа, такого как ген коллагена альфа 1(I), или из варианта 3'-UTR гена, выбранного из группы, которая состоит из гена альбумина, гена α-глобина, гена β-глобина, гена тирозингидроксилазы, гена липоксигеназы и гена коллагена альфа, такого как ген коллагена альфа 1(I), представленных в SEQ ID NO: 1369-1390 заявки на патент WO 2013/143700, содержание которой включено в настоящее описание в качестве ссылки. В наиболее предпочтительном варианте осуществления изобретения другая 3'-UTR содержит или состоит из нуклеотидной последовательности, которая получена из 3'-UTR гена альбумина, предпочтительно гена альбумина позвоночного, более предпочтительно гена альбумина млекопитающего, наиболее предпочтительно человеческого гена альбумина, имеющего SEQ ID NO: 206:
SEQ ID NO: 206:

(3'-UTR человеческого альбумина; соответствующая SEQ ID NO: 1369, представленной в заявке на патент WO 2013/143700).
В другом наиболее предпочтительном варианте осуществления изобретения другая 3'-UTR содержит или состоит из нуклеотидной последовательности, которая получена из 3'-UTR гена α-глобина, предпочтительно гена α- или β-глобина позвоночного, более предпочтительно гена α- или β-глобина млекопитающего, наиболее предпочтительно человеческого гена α- или β-глобина, имеющего SEQ ID NO: 1370, представленную в заявке на патент WO 2013/143700 (3'-UTR гемоглобина альфа 1 (НВА1) Homo sapiens), или SEQ ID NO: 1371, представленную в заявке на патент WO 2013/143700 (3'-UTR гемоглобина альфа 2 (НВА2) Homo sapiens), и/или SEQ ID NO: 1372, представленную в заявке на патент WO 2013/143700 (3'-UTR гемоглобина бета (НВВ) Homo sapiens).
Например, дополнительная 3'-UTR может содержать или состоять из центрального, α-комплекс-связывающего фрагмента 3'-UTR гена α-глобина, имеющего SEQ ID NO: 1393, представленную в заявке на патент WO 2013/143700.
В этом контексте наиболее предпочтительно, когда предлагаемая в изобретении молекула нуклеиновой кислоты содержит дополнительный 3'-UTR-элемент, полученный из нуклеиновых кислот, имеющих SEQ ID NO: 1369-1390, которые представлены в заявке на патент WO 2013/143700, или их фрагментов, гомологов или вариантов.
Наиболее предпочтительно дополнительная 3'-UTR содержит нуклеотидную последовательность, полученную из фрагмента человеческого гена альбумина, имеющего SEQ ID NO: 207:
SEQ ID NO: 207:
(3'-UTR. альбумина7; соответствующая SEQ ID NO: 1376, представленной в заявке на патент WO 2013/143700)
В этом контексте наиболее предпочтительно, когда дополнительная 3'-UTR предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты содержит или состоит из нуклеотидной последовательности, имеющей SEQ ID NO: 207, или соответствующей последовательности РНК.
В некоторых вариантах осуществления изобретения дополнительная 3'-UTR содержит или состоит из нуклеотидной последовательности, полученной из гена, кодирующего рибосомальный белок, предпочтительно описанного в международных заявках на патент WO 2015/101414 или WO 2015/101415, содержание которых включено в настоящее описание в качестве ссылки.
Дополнительная 3'-UTR может также содержать или состоять из нуклеотидной последовательности, полученной из гена, кодирующего рибосомальный белок, где гены, кодирующие рибосомальный белок, из которых можно получать дополнительную 3'-UTR, включают (но, не ограничиваясь только ими) гены рибосомального белка L9 (RPL9), рибосомального белка L3 (RPL3), рибосомального белка L4 (RPL4), рибосомального белка L5 (RPL5), рибосомального белка L6 (RPL6), рибосомального белка L7 (RPL7), рибосомального белка L7a (RPL7A), рибосомального белка L11 (RPL11), рибосомального белка L12 (RPL12), рибосомального белка L13 (RPL13), рибосомального белка L23 (RPL23), рибосомального белка L18 (RPL18), рибосомального белка L18a (RPL18A), рибосомального белка L19 (RPL19), рибосомального белка L21 (RPL21), рибосомального белка L22 (RPL22), рибосомального белка L23a (RPL23A), рибосомального белка L17 (RPL17), рибосомального белка L24 (RPL24), рибосомального белка L26 (RPL26), рибосомального белка L27 (RPL27), рибосомального белка L30 (RPL30), рибосомального белка L27a (RPL27A), рибосомального белка L28 (RPL28), рибосомального белка L29 (RPL29), рибосомального белка L31 (RPL31), рибосомального белка L32 (RPL32), рибосомального белка L35a (RPL35A), рибосомального белка L37 (RPL37), рибосомального белка L37a (RPL37A), рибосомального белка L38 (RPL38), рибосомального белка L39 (RPL39), рибосомального белка, большой субъединицы, Р0 (RPLP0), рибосомального белка, большой субъединицы, P1 (RPLP1), рибосомального белка, большой субъединицы, Р2 (RPLP2), рибосомального белка S3 (RPS3), рибосомального белка S3A (RPS3A), рибосомального белка S4, Х-сцепленного (RPS4X), рибосомального белка S4, Y-сцепленного 1 (RPS4Y1), рибосомального белка S5 (RPS5), рибосомального белка S6 (RPS6), рибосомального белка S7 (RPS7), рибосомального белка S8 (RPS8), рибосомального белка S9 (RPS9), рибосомального белка S10 (RPS10), рибосомального белка S11 (RPS11), рибосомального белка S12 (RPS12), рибосомального белка S13 (RPS13), рибосомального белка S15 (RPS15), рибосомального белка S15a (RPS15A), рибосомального белка S16 (RPS16), рибосомального белка S19 (RPS19), рибосомального белка S20 (RPS20), рибосомального белка S21 (RPS21), рибосомального белка S23 (RPS23), рибосомального белка S25 (RPS25), рибосомального белка S26 (RPS26), рибосомального белка S27 (RPS27), рибосомального белка S27a (RPS27a), рибосомального белка S28 (RPS28), рибосомального белка S29 (RPS29), рибосомального белка L15 (RPL15), рибосомального белка S2 (RPS2), рибосомального белка L14 (RPL14), рибосомального белка S14 (RPS14), рибосомального белка L10 (RPL10), рибосомального белка L10a (RPL10A), рибосомального белка L35 (RPL35), рибосомального белка L13a (RPL13A), рибосомального белка L36 (RPL36), рибосомального белка L36a (RPL36A), рибосомального белка L41 (RPL41), рибосомального белка S18 (RPS18), рибосомального белка S24 (RPS24), рибосомального белка L8 (RPL8), рибосомального белка L34 (RPL34), рибосомального белка S17 (RPS17), рибосомального белка SA (RPSA), продукта 1 слияния: остаток убиквитина А-52-рибосомальный белок (UBA52), повсеместно экспрессируемого (FAU) вируса мышиной саркомы Финкеля-Бискиса-Рейли, белка 1, подобного рибосомальному белку L22 (RPL22L1), белка, подобного рибосомальному белку L39 (RPL39L), белка, подобного рибосомальному белку L10 (RPL10L), белка, подобного рибосомальному белку L36a (RPL36AL), белка, подобного рибосомальному белку L3 (RPL3L), белка, подобного рибосомальному белку S27 (RPS27L), белка 1, подобного рибосомальному белку L26 1 (RPL26L1), белка 1, подобного рибосомальному белку L7 (RPL7L1), псевдогена рибосомального белка L13a (RPL13AP), псевдогена 8 рибосомального белка L37a (RPL37AP8), псевдогена 5 рибосомального белка S10 (RPS10P5), псевдогена 11 рибосомального белка S26 (RPS26P11), псевдогена 5 рибосомального белка L39 (RPL39P5), псевдогена 6 рибосомального белка, большой субъединицы, Р0 (RPLP0P6) и псевдогена 14 рибосомального белка L36 (RPL36P14).
Предпочтительно, дополнительная 5'-UTR содержит или состоит из нуклеотидной последовательности, которая получена из 5'-UTR ТОР-гена, или которая получена из фрагмента, гомолога или варианта 5'-UTR ТОР-гена.
Наиболее предпочтительно, чтобы 5'-UTR-элемент не содержал ТОР-мотив или 5'-ТОР, указанный выше. В частности, предпочтительно, чтобы 5'-UTR ТОР-гена представляла собой 5'-UTR ТОР-гена без ТОР-мотива.
Нуклеотидную последовательность, которая происходит из 5'UTR ТОР-гена, получают из эукариотического ТОР-гена, предпочтительно ТОР-гена растения или животного, более предпочтительно ТОР-гена хордовых, еще более предпочтительно ТОР-гена позвоночных, наиболее предпочтительно ТОР-гена млекопитающих, такого как человеческий ТОР-ген.
Например, дополнительный 5'UTR-элемент предпочтительно выбирают из 5'-UTR-элементов, содержащих или состоящих из нуклеотидной последовательности, которая происходит из нуклеотидной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-1363, SEQ ID NO: 1395, SEQ ID NO: 1421 и SEQ ID NO: 1422, представленных в заявке на патент WO 2013/143700, описание которой включено в настоящее описание в качестве ссылки, из гомологов SEQ ID NO: 1-1363, SEQ ID NO: 1395, SEQ ID NO: 1421 и SEQ ID NO: 1422, представленных в заявке на патент WO 2013/143700, из ее варианта или предпочтительно из соответствующей последовательности РНК. Понятие «гомологи SEQ ID NO: 1-1363, SEQ ID NO: 1395, SEQ ID NO: 1421 и SEQ ID NO: 1422, представленные в заявке на патент WO 2013/143700» относится к последовательностям из видов кроме Homo sapiens, которые гомологичны последовательностям SEQ ID NO: 1-1363, SEQ ID NO: 1395, SEQ ID NO: 1421 и SEQ ID NO: 1422, представленным в заявке на патент WO 2013/143700.
В предпочтительном варианте осуществления изобретения дополнительная 5'UTR содержит или состоит из нуклеотидной последовательности, которая происходит из нуклеотидной последовательности, простирающейся от нуклеотидного положения 5 (т.е. нуклеотида, находящегося в последовательности в положении 5) до нуклеотидного положения, непосредственно примыкающего с 5'-стороны к стартовому кодону (находящемуся на 3'-конце последовательностей), например, до нуклеотидного положения, непосредственно примыкающего с 5'-стороны к последовательности ATG нуклеотидной последовательности, выбранной из SEQ ID NO: 1-1363, SEQ ID NO: 1395, SEQ ID NO: 1421 и SEQ ID NO: 1422, представленных в заявке на патент WO 2013/143700, из гомологов SEQ ID NO: 1-1363, SEQ ID NO: 1395, SEQ ID NO: 1421 и SEQ ID NO: 1422, представленных в заявке на патент WO 2013/143700, из ее варианта, или соответствующей последовательности РНК. Наиболее предпочтительно дополнительную 5' UTR получают из нуклеотидной последовательности, простирающейся от нуклеотидного положения, непосредственно примыкающего с 3'-стороны к 5'-ТОР, до нуклеотидного положения, непосредственно примыкающего с 5'-стороны к стартовому кодону (находящемуся на 3'-конце последовательностей), например, до нуклеотидного положения, непосредственно примыкающего с 5'-стороны к последовательности ATG нуклеотидной последовательности выбранной из SEQ ID NO: 1-1363, SEQ ID NO: 1395, SEQ ID NO: 1421 и SEQ ID NO: 1422, представленных в заявке на патент WO 2013/143700, из гомологов SEQ ID NO: 1-1363, SEQ ID NO: 1395, SEQ ID NO: 1421 и SEQ ID NO: 1422, представленных в заявке на патент WO 2013/143700, из ее варианта, или соответствующей последовательности РНК.
В наиболее предпочтительном варианте осуществления изобретения дополнительная 5'-UTR содержит или состоит из нуклеотидной последовательности, происходящей из 5'-UTR ТОР-гена, кодирующего рибосомальный белок, или из варианта 5'-UTR ТОР-гена, кодирующего рибосомальный белок. Например, 5'-UTR-элемент содержит или состоит из нуклеотидной последовательности, полученной из 5'-UTR нуклеотидной последовательности, представленной в любой из SEQ ID NO: 170, 232, 244, 259, 1284, 1285, 1286, 1287, 1288, 1289, 1290, 1291, 1292, 1293, 1294, 1295, 1296, 1297, 1298, 1299, 1300, 1301, 1302, 1303, 1304, 1305, 1306, 1307, 1308, 1309, 1310, 1311, 1312, 1313, 1314, 1315, 1316, 1317, 1318, 1319, 1320, 1321, 1322, 1323, 1324, 1325, 1326, 1327, 1328, 1329, 1330, 1331, 1332, 1333, 1334, 1335, 1336, 1337, 1338, 1339, 1340, 1341, 1342, 1343, 1344, 1346, 1347, 1348, 1349, 1350, 1351, 1352, 1353, 1354, 1355, 1356, 1357, 1358, 1359 или 1360, представленных в заявке на патент WO 2013/143700, соответствующей последовательности РНК, ее гомолога или ее варианта, представленного в настоящем описании, предпочтительно без 5'-ТОР-мотива. Как описано выше, последовательность, простирающаяся от положения 5 до нуклеотида, непосредственно примыкающего с 5'-стороны к ATG (который находится на 3'-конце последовательностей), соответствует 5'-UTR указанных последовательностей.
Предпочтительно дополнительная 5'UTR содержит или состоит из нуклеотидной последовательности, которая происходит из 5'-UTR ТОР-гена, кодирующего рибосомальный белок большой субъединицы (RPL), или из гомолога или варианта 5'-UTR ТОР-гена, кодирующего рибосомальный белок большой субъединицы (RPL). Например, 5'-UTR-элемент содержит или состоит из нуклеотидной последовательности, происходящей из 5'-UTR нуклеотидной последовательности, представленной в любой из SEQ ID NO: 67, 259, 1284-1318, 1344, 1346, 1348-1354, 1357, 1358, 1421 и 1422, описанных в заявке на патент WO 2013/143700, соответствующей последовательности РНК, ее гомолога или ее варианта, представленного в настоящем описании, предпочтительно без 5'-ТОР-мотива.
В наиболее предпочтительном варианте осуществления изобретения 5'-UTR-элемент содержит или состоит из нуклеотидной последовательности, происходящей из 5'-UTR гена рибосомального белка большой субъединицы 32, предпочтительно из гена рибосомального белка большой субъединицы 32 (L32) позвоночных, более предпочтительно гена рибосомального белка большой субъединицы 32 (L32) млекопитающих, наиболее предпочтительно из гена рибосомального белка большой субъединицы 32 (L32) человека, или из варианта 5'-UTR гена рибосомального белка большой субъединицы 32, предпочтительно из гена рибосомального белка большой субъединицы 32 (L32) позвоночных, более предпочтительно из гена рибосомального белка большой субъединицы 32 (L32) млекопитающих, наиболее предпочтительно из гена рибосомального белка большой субъединицы 32 (L32) человека, где предпочтительно дополнительная 5'-UTR не содержит 5'-ТОР указанного гена.
Следовательно, в наиболее предпочтительном варианте осуществления изобретения, дополнительная 5'-UTR содержит или состоит из нуклеотидной последовательности, идентичной по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% нуклеотидной последовательности, представленной в SEQ ID NO: 208 (5'-UTR рибосомального белка большой субъединицы 32 человека без 5'-концевого олигопиримидинового тракта:
 (SEQ ID NO: 208); соответствующая SEQ ID NO: 1368, указанной в заявке на патент WO 2013/143700) или предпочтительно соответствующей последовательности РНК, или где по меньшей мере одна дополнительная 5'UTR содержит или состоит из фрагмента нуклеотидной последовательности, идентичного по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% нуклеотидной последовательности, представленной в SEQ ID NO: 208, или более предпочтительно соответствующей последовательности РНК, где предпочтительно фрагмент представляет собой описанный выше фрагмент, непрерывный сегмент нуклеотидов, представляющий собой по меньшей мере 20% и т.д. полноразмерной 5'-UTR. Предпочтительно фрагмент имеет длину по меньшей мере примерно 20 нуклеотидов или более, предпочтительно по меньшей мере примерно 30 нуклеотидов или более, более предпочтительно по меньшей мере примерно 40 нуклеотидов или более. Предпочтительно фрагмент представляет собой функциональный фрагмент, представленный в настоящем описании.
(SEQ ID NO: 208); соответствующая SEQ ID NO: 1368, указанной в заявке на патент WO 2013/143700) или предпочтительно соответствующей последовательности РНК, или где по меньшей мере одна дополнительная 5'UTR содержит или состоит из фрагмента нуклеотидной последовательности, идентичного по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% нуклеотидной последовательности, представленной в SEQ ID NO: 208, или более предпочтительно соответствующей последовательности РНК, где предпочтительно фрагмент представляет собой описанный выше фрагмент, непрерывный сегмент нуклеотидов, представляющий собой по меньшей мере 20% и т.д. полноразмерной 5'-UTR. Предпочтительно фрагмент имеет длину по меньшей мере примерно 20 нуклеотидов или более, предпочтительно по меньшей мере примерно 30 нуклеотидов или более, более предпочтительно по меньшей мере примерно 40 нуклеотидов или более. Предпочтительно фрагмент представляет собой функциональный фрагмент, представленный в настоящем описании.
В некоторых вариантах осуществления изобретения искусственная молекула нуклеиновой кислоты содержит дополнительную 5'-UTR, которая содержит или состоит из нуклеотидной последовательности, происходящей из 5'-UTR ТОР-гена позвоночных, например, млекопитающих, например, ТОР-гена человека, выбранного из RPSA, RPS2, RPS3, RPS3A, RPS4, RPS5, RPS6, RPS7, RPS8, RPS9, RPS10, RPS11, RPS12, RPS13, RPS14, RPS15, RPS15A, RPS16, RPS17, RPS18, RPS19, RPS20, RPS21, RPS23, RPS24, RPS25, RPS26, RPS27, RPS27A, RPS28, RPS29, RPS30, RPL3, RPL4, RPL5, RPL6, RPL7, RPL7A, RPL8, RPL9, RPL10, RPL10A, RPL11, RPL12, RPL13, RPL13A, RPL14, RPL15, RPL17, RPL18, RPL18A, RPL19, RPL21, RPL22, RPL23, RPL23A, RPL24, RPL26, RPL27, RPL27A, RPL28, RPL29, RPL30, RPL31, RPL32, RPL34, RPL35, RPL35A, RPL36, RPL36A, RPL37, RPL37A, RPL38, RPL39, RPL40, RPL41, RPLP0, RPLP1, RPLP2, RPLP3, RPLP0, RPLP1, RPLP2, EEF1A1, EEF1B2, EEF1D, EEF1G, EEF2, EIF3E, EIF3F, EIF3H, EIF2S3, EIF3C, EIF3K, EIF3EIP, EIF4A2, РАВРС1, HNRNPA1, ТРТ1, TUBB1, UBA52, NPM1, ATP5G2, GNB2L1, NME2, UQCRB или из его гомолога или варианта, где предпочтительно дополнительная 5'-UTR не содержит ТОР-мотив или 5'-ТОР указанных генов, и где необязательно 5'-UTR-элемент начинается на своем 5'-конце с нуклеотида, находящегося в положении 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 по ходу транскрипции относительно 5'-концевого олигопиримидинового тракта (ТОР), и где необязательно также дополнительная 5'-UTR, происходящая из 5'-UTR ТОР-гена, заканчивается на своем 3'-конце нуклеотидом, находящимся в положении 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 в обратном направлении относительно стартового кодона (A(U/T)G) гена, из которого она происходит.
В конкретных вариантах осуществления изобретения дополнительная 5'-UTR содержит или состоит из нуклеотидной последовательности, которая получена из 5'-UTR, описанной в международной заявке на патент WO 2016/107877, содержание которой включено в настоящее описание в качестве ссылки.
Искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может представлять собой РНК, такую как мРНК или вирусная РНК, или репликон, ДНК, такую как плазмидная ДНК или вирусная ДНК, или может представлять собой модифицированную молекулу РНК или ДНК. Она может представлять собой двухцепочечную молекулу, имеющую смысловую цепь и антисмысловую цепь, например, молекулу ДНК, имеющую смысловую цепь и антисмысловую цепь.
Искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, необязательно может содержать также 5'-кэп. Необязательный 5'-кэп предпочтительно локализован с 5'-стороны относительно ОРС, более предпочтительно с 5'-стороны относительно по меньшей мере одной 5'-UTR или любой дополнительной 5'-UTR в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении.
Предпочтительно искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, содержит также поли(А)-последовательность и/или сигнал полиаденилирования. Предпочтительно необязательная поли(А)-последовательность локализована с 3'-стороны относительно по меньшей мере одного 3'-UTR-элемента или любой дополнительной 3'-UTR, более предпочтительно необязательная поли(А)-последовательность соединена с 3'-концом 3'-UTR-элемента. Соединение может быть непосредственным или косвенным, например, с помощью сегмента, состоящего из 2, 4, 6, 8, 10, 20 и т.д. нуклеотидов, например, с помощью линкера, состоящего из 1-50, предпочтительно 1-20 нуклеотидов, например, содержащего или состоящего из одного или большего количества сайтов рестрикции. Однако, даже если искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, не содержит 3'-UTR, например, если она содержит только по меньшей мере один 5'-UTR-элемент, то предпочтительно она все же содержит поли(А)-последовательность и/или сигнал полиаденилирования.
В одном из вариантов осуществления изобретения необязательный сигнал полиаденилирования расположен по ходу транскипции с 3'-стороны 3'-UTR-элемента. Предпочтительно сигнал полиаденилирования содержит консенсусную последовательность NN(U/T)ANA, в которой N = А или U, предпочтительно AA(U/T)AAA или A(U/T)(U/T)AAA. Такая консенсусная последовательность может распознаваться большинством клеточных систем животных и бактериальных клеточных систем, например, факторами полиаденилирования, такими как фактор специфичности расщепления/полиаденилирования (CPSF), в сочетании с CstF, PAP, РАВ2, CFI и/или CFII. Предпочтительно сигнал полиаденилирования, предпочтительно представляющий собой консенсусную последовательность NNUANA, расположен на расстоянии менее чем примерно 50 нуклеотидов, более предпочтительно менее чем примерно 30 оснований, наиболее предпочтительно менее чем примерно 25 оснований, например, на расстоянии 21 основания, по ходу транскрипции относительно 3'-конца 3'-UTR-элемента или ОРС, если не присутствует 3'-UTR-элемент.
Транскрипция искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, например, искусственной молекулы ДНК, содержащей сигнал полиаденилирования, расположенный по ходу транскрипции относительно 3'-UTR-элемента (или ОРС), должна приводить к получению незрелой РНК, содержащей сигнал полиаденилирования, по ходу транскрипции относительно ее 3'-UTR-элемента (или ОРС).
Затем при использовании соответствующей системы транскрипции должно происходить присоединение поли(А)-последовательности к незрелой РНК. Например, предлагаемая в изобретении искусственная молекула нуклеиновой кислоты может представлять собой молекулу ДНК, содержащую 3'-UTR-элемент, описанный выше, и сигнал полиаденилирования, который может приводить к полиаденилированию РНК после транскрипции указанной молекулы ДНК. Следовательно, образовавшаяся РНК может содержать комбинацию предлагаемого в изобретении 3'-UTR-элемента, за которым располагается поли(А)-последовательность.
Возможными системами транскрипции являются системы транскрипции in vitro или клеточные системы транскрипции и т.д. Таким образом, транскрипция искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, например, транскрипция искусственной молекулы нуклеиновой кислоты, содержащей открытую рамку считывания, 3'-UTR-элемент и/или 5'-UTR-элемент и необязательно сигнал полиаденилирования, может приводить к получению молекулы мРНК, содержащей открытую рамку считывания, 3'-UTR-элемент и необязательно поли(А)-последовательность.
Таким образом, в изобретении предложена также искусственная молекула нуклеиновой кислоты, которая представляет собой молекулу мРНК, содержащую открытую рамку считывания, 3'-UTR-элемент, описанный выше, и/или 5'-UTR-элемент, описанный выше, и необязательно поли(А)-последовательность.
В другом варианте осуществления изобретения 3'-UTR искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, не содержит сигнал полиаденилирования или поли(А)-последовательность. Кроме того, предпочтительно искусственная молекула нуклеиновой кислоты, предлагаемая в изобретении, не содержит сигнал полиаденилирования или поли(А)-последовательность. Более предпочтительно 3'-UTR искусственной молекулы нуклеиновой кислоты или сама предлагаемая в изобретении искусственная молекула нуклеиновой кислоты не содержит сигнал полиаденилирования, прежде всего не содержит сигнал полиаденилирования AAU/TAAA.
В предпочтительном варианте осуществления изобретения предложена искусственная молекула нуклеиновой кислоты, которая представляет собой искусственную молекулу РНК, содержащую открытую рамку считывания и последовательность РНК, соответствующую последовательности ДНК, выбранной из группы, которая состоит из последовательностей, представленных в SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 137 (в альтернативном варианте SEQ ID NO: 3), SEQ ID NO: 138 (в альтернативном варианте SEQ ID NO: 9), SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 15, SEQ ID NO: 140 (в альтернативном варианте SEQ ID NO: 17), SEQ ID NO: 20, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 143 (в альтернативном варианте SEQ ID NO: 31), SEQ ID NO: 32, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 146 (в альтернативном варианте SEQ ID NO: 52), SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 57, SEQ ID NO: 60, SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 66, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 72, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 144 (в альтернативном варианте SEQ ID NO: 42), SEQ ID NO: 58, SEQ ID NO: 62; SEQ ID NO: 73, SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 80, SEQ ID NO: 81, SEQ ID NO: 83, SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 89, SEQ ID NO: 90, SEQ ID NO: 91, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 97, SEQ ID NO: 98, SEQ ID NO: 99, SEQ ID NO: 100, SEQ ID NO: 101, SEQ ID NO: 102, SEQ ID NO: 103, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 147 (в альтернативном варианте SEQ ID NO: 109), SEQ ID NO: 148 (в альтернативном варианте SEQ ID NO: 110), SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 149 (в альтернативном варианте SEQ ID NO: 119), SEQ ID NO: 123, SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO: 130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134, SEQ ID NO: 151 (в альтернативном варианте SEQ ID NO: 136), SEQ ID NO: 96, SEQ ID NO: 111, SEQ ID NO: 150 (на основе SEQ ID NO: 120), SEQ ID NO: 121, SEQ ID NO: 124, SEQ ID NO: 125 или ее фрагмент, описанный выше. Кроме того, предложена соответствующая искусственная молекула ДНК.
В другом предпочтительном варианте осуществления изобретения предложена искусственная молекула нуклеиновой кислоты, которая представляет собой искусственную молекулу ДНК, содержащую открытую рамку считывания и последовательность, выбранную из группы, которая состоит из последовательностей, представленных в SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 137 (в альтернативном варианте SEQ ID NO: 3), SEQ ID NO: 138 (в альтернативном варианте SEQ ID NO: 9), SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 15, SEQ ID NO: 140 (в альтернативном варианте SEQ ID NO: 17), SEQ ID NO: 20, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 143 (в альтернативном варианте SEQ ID NO: 31), SEQ ID NO: 32, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 146 (в альтернативном варианте SEQ ID NO: 52), SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 57, SEQ ID NO: 60, SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 66, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 72, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 144 (в альтернативном варианте SEQ ID NO: 42), SEQ ID NO: 58, SEQ ID NO: 62; SEQ ID NO: 73, SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 80, SEQ ID NO: 81, SEQ ID NO: 83, SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 89, SEQ ID NO: 90, SEQ ID NO: 91, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 97, SEQ ID NO: 98, SEQ ID NO: 99, SEQ ID NO: 100, SEQ ID NO: 101, SEQ ID NO: 102, SEQ ID NO: 103, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 147 (в альтернативном варианте SEQ ID NO: 109), SEQ ID NO: 148 (в альтернативном варианте SEQ ID NO: 110), SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 149 (в альтернативном варианте SEQ ID NO: 119), SEQ ID NO: 123, SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO: 130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134, SEQ ID NO: 151 (в альтернативном варианте SEQ ID NO: 136), SEQ ID NO: 96, SEQ ID NO: 111, SEQ ID NO: 150 (на основе SEQ ID NO: 120), SEQ ID NO: 121, SEQ ID NO: 124, SEQ ID NO: 125.
Таким образом, в изобретении предложена искусственная молекула нуклеиновой кислоты, которая может служить в качестве матрицы для молекулы РНК, предпочтительно для молекулы мРНК, которая характеризуется высокой эффективностью трансляции. Иными словами, искусственная молекула нуклеиновой кислоты может представлять собой ДНК, которую можно применять в качестве матрицы для получения мРНК. мРНК, которую можно получать таким путем, может, в свою очередь, транслироваться с получением требуемого пептида или белка, кодируемого открытой рамкой считывания. Если искусственная молекула нуклеиновой кислоты представляет собой ДНК, то ее можно, например, использовать в качестве двухцепочечной формы хранения для продолжения и повторения производства мРНК in vitro или in vivo. В данном случае in vitro относится, в частности, к («живым») клеткам и/или ткани, включая ткань живого индивидуума. Клетки включают, в частности, клеточные линии, первичные клетки, клетки в ткани или организме индивидуумов. В конкретных вариантах осуществления изобретения пригодными для применения согласно настоящему изобретению могут быть типы клеток, позволяющие осуществлять культивирование клеток. Наиболее предпочтительными являются клетки млекопитающих, например, человеческие клетки и мышиные клетки. В наиболее предпочтительных вариантах осуществления изобретения применяют человеческие клеточные линии HeLa, HEPG2 и U-937 и мышиные клеточные линии NIH3T3, JAWSII и L929. Кроме того, наиболее предпочтительными являются первичные клетки, в наиболее предпочтительных вариантах осуществления изобретения можно применять человеческие кожные фибробласты (HDF). В альтернативном варианте можно применять также ткань индивидуума.
В одном из вариантов осуществления изобретения искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, содержит также поли(А)-последовательность. Например, молекула ДНК, содержащая ОРС, за которой необязательно следует 3'-UTR, может содержать состоящий из тимидиновых нуклеотидов сегмент, который может транскрибироваться в поли(А)-последовательность в образующейся мРНК. Длина поли(А)-последовательности может варьироваться. Например, поли(А)-последовательность может иметь длину от примерно 20 адениновых нуклеотидов вплоть до 300 адениновых нуклеотидов, предпочтительно от примерно 40 до примерно 200 адениновых нуклеотидов, более предпочтительно от примерно 50 до примерно 100 адениновых нуклеотидов, например, примерно 60, 70, 80, 90 или 100 адениновых нуклеотидов. Наиболее предпочтительно предлагаемая в изобретении нуклеиновая кислота содержит поли(А)-последовательность, содержащую от примерно 60 до примерно 70 нуклеотидов, наиболее предпочтительно 64 адениновых нуклеотида.
Искусственные молекулы РНК можно также получать in vitro с помощью обычных методов химического синтеза, при этом не требуется осуществлять транскрипцию с ДНК-предшественника.
В наиболее предпочтительном варианте осуществления изобретения искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, представляет собой молекулу РНК, предпочтительно молекулу РНК, содержащую в 5'→3'-направлении открытую рамку считывания, 3'-UTR-элемент, описанный выше, и поли(А)-последовательность, или содержащую в 5'→3'-направлении 5'-UTR-элемент, описанный выше, открытую рамку считывания и поли(А)-последовательность.
В предпочтительном варианте осуществления изобретения открытую рамку считывания получают из гена, отличного от гена, из которого получают 3'-UTR-элемент и/или 5'-UTR-элемент предлагаемой в изобретении искусственной нуклеиновой кислоты. В некоторых других предпочтительных вариантах осуществления изобретения открытая рамка считывания не кодирует ген, выбранный из группы, которая состоит из ZNF460, TGM2, IL7R, BGN, TK1, RAB3B, СВХ6, FZD2, COL8A1, NDUFS7, PHGDH, PLK2, TSPO, PTGS1, FBXO32, NID2, ATP5D, EXOSC4, NOL9, UBB4B, VPS18, ORMDL2, FSCN1, TMEM33, TUBA4A, ЕМР3, TMEM201, CRIP2, BRAT1, SERPINH1, CD9, DPYSL2, CDK9, TFRC, PSMB3, FASN, PSMB6, PRSS56, KPNA6, SFT2D2, PARD6B, LPP, SPARC, SCAND1, VASN, SLC26A1, LCLAT1, FBXL18, SLC35F6, RAB3D, MAP1B, VMA21, CYBA, SEZ6L2, PCOLCE, VTN, ALDH16A1, RAVER1, KPNA6, SERINC5, JUP, CPN2, CRIP2, EPT1, PNPO, SSSCA1, POLR2L, LIN7C, UQCR10, PYCRL, AMN, MAP1S, NDUFS7, PHGDH, TSPO, ATP5D, EXOSC4, TUBB4B, TUBA4A, EMP3, CRIP2, BRAT1, CD9, CDK9, PSMB3, PSMB6, PRSS56, SCAND1, AMN, CYBA, PCOLCE, MAP1S, VTN, ALDH16A1 (предпочтительно все человеческие) и Dpysl2, Ccnd1, Acox2, Cbx6, Ubc, Ldlr, Nudt22, Pcyox1l, Ankrd1, Tmem37, Tspyl4, Slc7a3, Cst6, Aacs, Nosip, Itga7, Ccnd2, Ebp, Sf3b5, Fasn, Hmgcs1, Osr1, Lmnb1, Vma21, Kif20a, Cdca8, Slc7a1, Ubqln2, Prps2, Shmt2, Aurkb, Fignl1, Cad, Anln, Slfn9, Ncaph, Pole, Uhrf1, Gja1, Fam64a, Kif2c, Tspan10, Scand1, Gpr84, Fads3, Cers6, Cxcr4, Gprc5c, Fen1, Cspg4, Mrpl34, Comtd1, Armc6, Emr4, Atp5d, 1110001J03Rik, Csf2ra, Aarsd1, Kif22, Cth, Tpgs1, Cel17, Alkbh7, Ms4a8a, Acox2, Ubc, Slpi, Pcyox1l, Igf2bp1, Tmem37, Slc7a3, Cst6, Ebp, Sf3b5, Plk1, Cdca8, Kif22, Cad, Cth, Pole, Kif2c, Scand1, Gpr84, Tpgs1, Ccl17, Alkbh7, Ms4a8a, Mrpl34, Comtd1, Armc6, Atp5d, 1110001J03Rik, Nudt22, Aarsd1 (предпочтительно все мышиные), или их вариантов, при условии, что 3'-UTR-элемент и/или 5'-UTR-элемент имеет последовательность, выбранную из группы, которая состоит из последовательностей, представленных в SEQ ID NO: 1-204.
В предпочтительном варианте осуществления изобретения ОРС не кодирует рибосомальные белки человека или растения, прежде всего Arabidopsis, прежде всего не кодирует человеческий рибосомальный белок S6 (RPS6), белок, подобный человеческому рибосомальному белку L36a (RPL36AL), или рибосомальный белок Arabidopsis S16 (RPS16). В другом предпочтительном варианте осуществления изобретения открытая рамка считывания (ОРС) не кодирует рибосомальный белок S6 (RPS6), белок, подобный рибосомальному белку L36a (RPL36AL) или рибосомальный белок S16 (RPS16) вне зависимости от его происхождения.
В одном из вариантов осуществления изобретения предложена искусственная молекула ДНК, содержащая открытую рамку считывания, предпочтительно открытую рамку, полученную из гена, отличного от гена, из которого получен 3'-UTR-элемент и/или 5'-UTR-элемент; при этом 3'-UTR-элемент содержит или состоит из последовательности, идентичной по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%; еще более предпочтительно по меньшей мере на 99%; еще более предпочтительно на 100% последовательности ДНК, выбранной из группы, которая состоит из последовательностей, представленных в SEQ ID NO: 152, SEQ ID NO: 153, SEQ ID NO: 154, SEQ ID NO: 155, SEQ ID NO: 156, SEQ ID NO: 157, SEQ ID NO: 158, SEQ ID NO: 159, SEQ ID NO: 160, SEQ ID NO: 161, SEQ ID NO: 164, SEQ ID NO: 165, SEQ ID NO: 167, SEQ ID NO: 168, SEQ ID NO: 169, SEQ ID NO: 170, SEQ ID NO: 171, SEQ ID NO: 172, SEQ ID NO: 173; SEQ ID NO: 174, SEQ ID NO: 175, SEQ ID NO: 176, SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 181, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 184, SEQ ID NO: 187, SEQ ID NO: 188, SEQ ID NO: 189, SEQ ID NO: 191, SEQ ID NO: 204 (в альтернативном варианте SEQ ID NO: 192), SEQ ID NO: 193, SEQ ID NO: 194, SEQ ID NO: 195, SEQ ID NO: 196, SEQ ID NO: 197, SEQ ID NO: 198, SEQ ID NO: 199, SEQ ID NO: 200, SEQ ID NO: 201, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 177, и/или 5'-UTR-элемент содержит или состоит из последовательности, идентичной по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%; еще более предпочтительно по меньшей мере на 99%; еще более предпочтительно на 100% последовательности ДНК, выбранной из группы, которая состоит из последовательностей, представленных в SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 137 (в альтернативном варианте SEQ ID NO: 3), SEQ ID NO: 138 (в альтернативном варианте SEQ ID NO: 9), SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 15, SEQ ID NO: 140 (в альтернативном варианте SEQ ID NO: 17), SEQ ID NO: 20, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 143 (в альтернативном варианте SEQ ID NO: 31), SEQ ID NO: 32, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 146 (в альтернативном варианте SEQ ID NO: 52), SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 57, SEQ ID NO: 60, SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 66, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 72, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 144 (в альтернативном варианте SEQ ID NO: 42), SEQ ID NO: 58, SEQ ID NO: 62; SEQ ID NO: 73, SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 80, SEQ ID NO: 81, SEQ ID NO: 83, SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 89, SEQ ID NO: 90, SEQ ID NO: 91, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 97, SEQ ID NO: 98, SEQ ID NO: 99, SEQ ID NO: 100, SEQ ID NO: 101, SEQ ID NO: 102, SEQ ID NO: 103, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 147 (в альтернативном варианте SEQ ID NO: 109), SEQ ID NO: 148 (в альтернативном варианте SEQ ID NO: 110), SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 149 (в альтернативном варианте SEQ ID NO: 119), SEQ ID NO: 123, SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO: 130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134, SEQ ID NO: 151 (в альтернативном варианте SEQ ID NO: 136), SEQ ID NO: 96, SEQ ID NO: 111, SEQ ID NO: 150 (на основе SEQ ID NO: 120), SEQ ID NO: 121, SEQ ID NO: 124, SEQ ID NO: 125; и сигнал полиаденилирования и/или поли(А)-последовательность.
Кроме того, в изобретении предложена искусственная молекула РНК, предпочтительно искусственная молекула мРНК или искусственная молекула вирусной РНК, содержащая открытую рамку считывания, предпочтительно открытую рамку считывания, полученную из гена, отличного от гена, из которого получен 3'-UTR-элемент и/или 5'-UTR-элемент; при этом 3'-UTR-элемент содержит или состоит из последовательности, идентичной по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%; еще более предпочтительно по меньшей мере на 99%; еще более предпочтительно на 100% последовательности РНК, которая соответствует последовательности ДНК, выбранной из группы, которая состоит из последовательностей, представленных в SEQ ID NO: 152, SEQ ID NO: 153, SEQ ID NO: 154, SEQ ID NO: 155, SEQ ID NO: 156, SEQ ID NO: 157, SEQ ID NO: 158, SEQ ID NO: 159, SEQ ID NO: 160, SEQ ID NO: 161, SEQ ID NO: 164, SEQ ID NO: 165, SEQ ID NO: 167, SEQ ID NO: 168, SEQ ID NO: 169, SEQ ID NO: 170, SEQ ID NO: 171, SEQ ID NO: 172, SEQ ID NO: 173; SEQ ID NO: 174, SEQ ID NO: 175, SEQ ID NO: 176, SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 181, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 184, SEQ ID NO: 187, SEQ ID NO: 188, SEQ ID NO: 189, SEQ ID NO: 191, SEQ ID NO: 204 (в альтернативном варианте SEQ ID NO: 192), SEQ ID NO: 193, SEQ ID NO: 194, SEQ ID NO: 195, SEQ ID NO: 196, SEQ ID NO: 197, SEQ ID NO: 198, SEQ ID NO: 199, SEQ ID NO: 200, SEQ ID NO: 201, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 177, и/или 5'-UTR-элемент содержит или состоит из последовательности, идентичной по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%; еще более предпочтительно по меньшей мере на 99%; еще более предпочтительно на 100% последовательности РНК, которая соответствует последовательности ДНК, выбранной из группы, которая состоит из последовательностей, представленных в SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 137 (в альтернативном варианте SEQ ID NO: 3), SEQ ID NO: 138 (в альтернативном варианте SEQ ID NO: 9), SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 15, SEQ ID NO: 140 (в альтернативном варианте SEQ ID NO: 17), SEQ ID NO: 20, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 143 (в альтернативном варианте SEQ ID NO: 31), SEQ ID NO: 32, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 146 (в альтернативном варианте SEQ ID NO: 52), SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 57, SEQ ID NO: 60, SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 66, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 72, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 144 (в альтернативном варианте SEQ ID NO: 42), SEQ ID NO: 58, SEQ ID NO: 62; SEQ ID NO: 73, SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 80, SEQ ID NO: 81, SEQ ID NO: 83, SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 89, SEQ ID NO: 90, SEQ ID NO: 91, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 97, SEQ ID NO: 98, SEQ ID NO: 99, SEQ ID NO: 100, SEQ ID NO: 101, SEQ ID NO: 102, SEQ ID NO: 103, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 147 (в альтернативном варианте SEQ ID NO: 109), SEQ ID NO: 148 (в альтернативном варианте SEQ ID NO: 110), SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 149 (alternatively SEQ ID NO: 119), SEQ ID NO: 123, SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO: 130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134, SEQ ID NO: 151 (в альтернативном варианте SEQ ID NO: 136), SEQ ID NO: 96, SEQ ID NO: 111, SEQ ID NO: 150 (на основе SEQ ID NO: 120), SEQ ID NO: 121, SEQ ID NO: 124, SEQ ID NO: 125; и сигнал полиаденилирования и/или поли(А)-последовательность.
В изобретении предложена искусственная молекула нуклеиновой кислоты, предпочтительно искусственная мРНК, которая характеризуется высокой эффективностью трансляции. Не вдаваясь в какую-либо теорию, можно считать, что высокая эффективность трансляции может быть обусловлена снижением расщепления искусственной молекулы нуклеиновой кислоты, такой как искусственная молекула мРНК, предлагаемая в настоящем изобретении. Следовательно, предлагаемый в изобретении 3'-UTR-элемент и/или предлагаемый в изобретении 5'-UTR-элемент может предупреждать расщепление и разложение искусственной нуклеиновой кислоты.
Предпочтительно искусственная молекула нуклеиновой кислоты может дополнительно содержать гистоновую структуру типа «стебель-петля». Так, искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может содержать, например, расположенные в 5'→3'-направлении ОРС, 3'-UTR-элемент, необязательную последовательность гистоновой структуры типа «стебель-петля», необязательную поли(А)-последовательность или сигнал полиаденилирования и необязательную поли(С)-последовательность, или расположенные в 5'→3'-направлении 5'-UTR-элемент, ОРС, необязательную последовательность гистоновой структуры типа «стебель-петля», необязательную поли(А)-последовательность или сигнал полиаденилирования и необязательную поли(С)-последовательность, или расположенные в 5'→3'-направлении 5'-UTR-элемент, ОРС, 3'-UTR-элемент, необязательную последовательность гистоновой структуры типа «стебель-петля», необязательную поли(А)-последовательность или сигнал полиаденилирования и необязательную поли(С)-последовательность. Она может содержать также расположенные в 5'→3'-направлении ОРС, 3'-UTR-элемент, необязательную поли(А)-последовательность, необязательную поли(С)-последовательность и необязательную последовательность гистоновой структуры типа «стебель-петля», или расположенные в 5'→3'-направлении 5'-UTR-элемент, ОРС, необязательную поли(А)-последовательность, необязательную поли(С)-последовательность и необязательную последовательность гистоновой структуры типа «стебель-петля», или расположенные в 5'→3'-направлении 5'-UTR-элемент, ОРС, 3'-UTR-элемент, необязательную поли(А)-последовательность, необязательную поли(С)-последовательность и необязательную последовательность гистоновой структуры типа «стебель-петля.
В предпочтительном варианте осуществления изобретения искусственная молекула нуклеиновой кислоты, предлагаемой в изобретении, дополнительно содержит по меньшей мере одну последовательность гистоновой структуры типа «стебель-петля».
Такие последовательности гистоновой структуры типа «стебель-петля» предпочтительно выбирают из последовательностей гистоновой структуры типа «стебель-петля», представленных в WO 2012/019780, содержание которой включено в настоящее описание в качестве ссылки.
Последовательность гистоновой структуры типа «стебель-петля», которую можно применять в настоящем изобретении, предпочтительно выбирают по меньшей мере из одной из следующих формул (I) или (II):
формула (I) (последовательность структуры типа «стебель-петля» без пограничных элементов стебля):
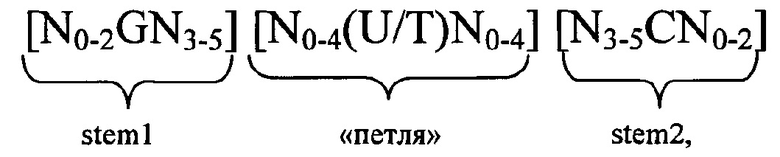
формула (II) (последовательность структуры типа «стебель-петля» с пограничными элементами стебля):
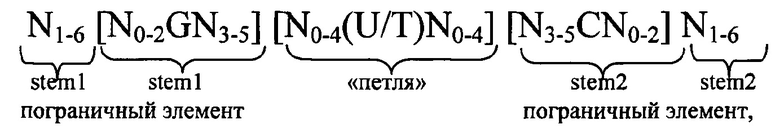
в которых:



где
у элементов stem1 и stem2 может происходить спаривание оснований друг с другом с образованием обратно комплементарной последовательности, где спаривание оснований может иметь место между stem1 и stem2, например, посредством спаривания оснований по Уотсону-Крику нуклеотидов А и U/T или G и С, или посредством спаривания оснований не по Уотсону-Крику, например, посредством спаривания «качающихся» оснований («качающегося» спаривания оснований), обратного спариванию оснований по Уотсону-Крику, посредством хугстиновского спаривания оснований, посредством обратного хугстиновскому спаривания оснований, или у них может происходить спаривание оснований друг с другом с образованием частично обратно комплементарной последовательности, при этом неполное спаривание оснований может иметь место между stem1 и stem2, вследствие того, что для одного или нескольких оснований в одном стебле не имеется комплементарного основания в обратно комплементарной последовательности другого стебля.
Согласно другому предпочтительному варианту осуществления изобретения в качестве последовательности гистоновой структуры типа «стебель-петля» можно выбирать последовательность, соответствующую по меньшей мере одной из следующих конкретных формул (Ia) или (IIa):
формула (Ia) (последовательность структуры типа «стебель-петля» без пограничных элементов стебля):
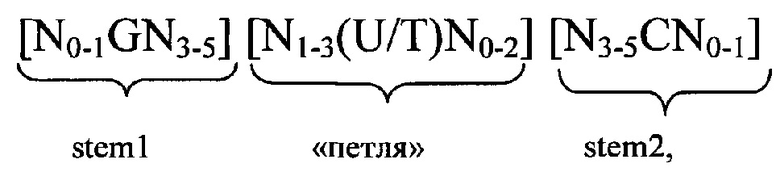
формула (IIa) (последовательность структуры типа «стебель-петля» с пограничными элементами стебля):
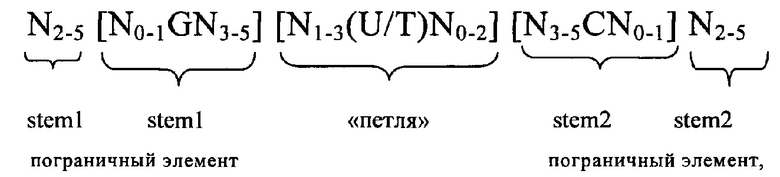
в которой:
N, С, G, T и U имеют указанные выше значения.
Согласно другому предпочтительному варианту осуществления изобретения мРНК, предлагаемая в настоящем изобретении, может содержать или кодировать по меньшей мере одну последовательность гистоновой структуры типа «стебель-петля», соответствующую по меньшей мере одной из следующих конкретных формул (Ib) или (IIb):
формула (Ib) (последовательность структуры типа «стебель-петля» без пограничных элементов стебля):
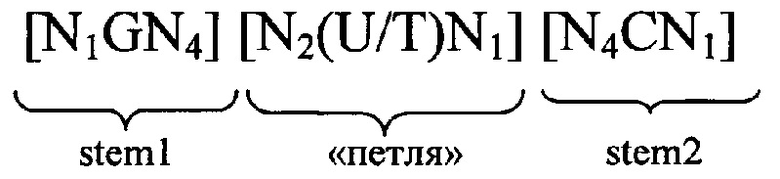
формула (IIb) (последовательность структуры типа «стебель-петля» с пограничными элементами стебля):
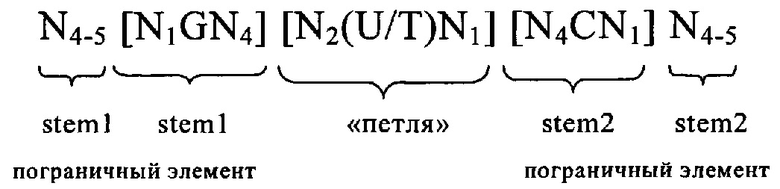
в которой:
N, С, G, Т и U имеют указанные выше значения.
Наиболее предпочтительной последовательностью гистоновой структуры типа «стебель-петля» является последовательность, представленная в 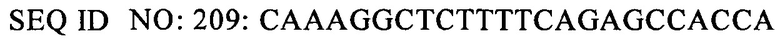 или более предпочтительно последовательность РНК, соответствующая нуклеотидной последовательности, представленной в SEQ ID NO: 209.
или более предпочтительно последовательность РНК, соответствующая нуклеотидной последовательности, представленной в SEQ ID NO: 209.
Например, отдельные элементы могут присутствовать в искусственной молекуле нуклеиновой кислоты в следующем порядке:
5'-кэп - 5'-UTR (элемент) - ОРС - 3'-UTR (элемент) - гистоновая структура типа «стебель-петля» - поли(А)/(С)-последовательность;
5'-кэп - 5'-UTR (элемент) - ОРС - 3'-UTR (элемент) - поли(А)/(С)-последовательность - гистоновая структура типа «стебель-петля»;
5'-кэп - 5'-UTR (элемент) - ОРС - IRES - ОРС - 3'-UTR (элемент) - гистоновая структура типа «стебель-петля» - поли(А)/(С)-последовательность;
5'-кэп - 5'-UTR (элемент) - ОРС - IRES - ОРС - 3'-UTR (элемент) - гистоновая структура типа «стебель-петля» - поли(А)/(С)-последовательность - поли(А)/(С)-последовательность;
5'-кэп - 5'-UTR (элемент) - ОРС - IRES - ОРС - 3'-UTR (элемент) - поли(А)/(С)-последовательность - гистоновая структура типа «стебель-петля»;
5'-кэп - 5'-UTR (элемент) - ОРС - IRES - ОРС - 3'-UTR (элемент) - поли(А)/(С)-последовательность - поли(А)/(С)-последовательность - гистоновая структура типа «стебель-петля»;
5'-кэп - 5'-UTR (элемент) - ОРС - 3'-UTR (элемент) - поли(А)/(С)-последовательность - поли(А)/(С)-последовательность;
5'-кэп - 5'-UTR (элемент) - ОРС - 3'-UTR (элемент) - поли(А)/(С)-последовательность - поли(А)/(С)-последовательность - гистоновая структура типа «стебель-петля»; и т.д.
В некоторых вариантах осуществления изобретения искусственная молекула нуклеиновой кислоты содержит дополнительные элементы, такие как 5'-кэп, поли(С)-последовательность и/или IRES-мотив. 5'-кэп может быть добавлен в процессе транскрипции или после транскрипции к 5'-концу РНК. Кроме того, предлагаемую в изобретении искусственную молекулу нуклеиновой кислоты, прежде всего в том случае, когда нуклеиновая кислота находится в форме мРНК или кодирует мРНК, можно модифицировать с помощью последовательности, состоящей по меньшей мере из 10 цитидинов, предпочтительно по меньшей мере из 20 цитидинов, более предпочтительно по меньшей мере из 30 цитидинов (так называемая «поли(С)-последовательность»). В частности, предлагаемая в изобретении искусственная молекула нуклеиновой кислоты может содержать, прежде всего в том случае, когда нуклеиновая кислота находится в форме мРНК или кодирует мРНК, поли(С)-последовательность которая, как правило, содержит примерно от 10 до 200 цитозиновых нуклеотидов, предпочтительно примерно от 10 до 100 цитидиновых нуклеотидов, более предпочтительно примерно от 10 до 70 цитидиновых нуклеотидов или еще более предпочтительно примерно от 20 до 50 или даже от 20 до 30 цитидиновых нуклеотидов. Наиболее предпочтительно, предлагаемая в изобретении нуклеиновая кислота содержит поли(С)-последовательность, состоящую из 30 цитидиновых остатков. Так, предпочтительно искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, содержит, предпочтительно расположенные в 5'→3' направлении, по меньшей мере один 5'-UTR-элемент, описанный выше, ОРС, по меньшей мере один 3'-UTR-элемент, описанный выше, поли(А)-последовательность или сигнал полиаденилирования и поли(С)-последовательность, или расположенные в 5'→3' направлении необязательно дополнительную 5'-UTR, ОРС, по меньшей мере один 3'-UTR-элемент, описанный выше, поли(А)-последовательность или сигнал полиаденилирования и поли(С)-последовательность, или расположенные в 5'→3' направлении по меньшей мере один 5'-UTR-элемент, описанный выше, ОРС, необязательно дополнительную 3'-UTR, поли(А)-последовательность или сигнал полиаденилирования и поли(С)-последовательность.
Последовательность внутреннего сайта связывания рибосом (IRES) или IRES-мотив может разделять несколько открытых рамок считывания, например в том случае, когда искусственная молекула нуклеиновой кислоты кодирует два или большее количество пептидов или белков. IRES-последовательность может быть наиболее полезной в том случае, когда искусственная молекула нуклеиновой кислоты представляет собой би- или полицистронную молекулу нуклеиновой кислоты.
Кроме того, искусственная молекула нуклеиновой кислоты может содержать дополнительные 5'-элементы, предпочтительно промотор или последовательность, содержащую промотор. Промотор может контролировать или регулировать транскрипцию искусственной молекулы нуклеиновой кислоты предлагаемой в настоящем изобретении, например, искусственной молекулы ДНК, предлагаемой в настоящем изобретении.
Предпочтительно в искусственной молекуле нуклеиновой кислоты, предлагаемой в настоящем изобретении, предпочтительно в открытой рамке считывания, модифицируют по меньшей мере содержание G/C. Так, предлагаемую в изобретении искусственную молекулу нуклеиновой кислоты можно стабилизировать с точки зрения ее термодинамических характеристик путем модификации содержания G (гуанозин)/С (цитидин) в молекуле. Содержание G/C в открытой рамке считывания искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, можно повышать по сравнению с содержанием G/C в открытой рамке считывания соответствующей последовательности дикого типа, предпочтительно на основе вырожденности генетического кода. Так, аминокислотную последовательность, кодируемую искусственной молекулой нуклеиновой кислоты, предпочтительно не модифицируют посредством модификации содержания G/C по сравнению с конкретной кодируемой аминокислотной последовательностью дикого типа. Таким образом, можно варьировать кодоны кодирующей последовательности или всей искусственной молекулы нуклеиновой кислоты, например, мРНК, по сравнению с кодирующей последовательностью дикого типа таким образом, чтобы они содержали большее количество G/C-нуклеотидов, сохраняя при этом транслируемую аминокислотную последовательность. Благодаря тому факту, что несколько кодонов кодируют одну и ту же аминокислоту (так называемая вырожденность генетического кода), можно изменять кодоны, не изменяя кодируемую последовательность пептида/белка (использование так называемых альтернативных часто встречающихся кодонов). Следовательно, можно специально интродуцировать определенные кодоны (осуществляя обмен соответствующих кодонов дикого типа, кодирующих ту же самую аминокислоту), которые являются более предпочтительными с точки зрения стабильности РНК и/или с точки зрения часто встречающихся кодонов в организме индивидуума (так называемая оптимизация кодонов).
В зависимости от аминокислоты, которая должна кодироваться кодирующей областью предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты, представленной в настоящем описании, существуют различные возможности для модификации нуклеотидной последовательности, например, открытой рамки считывания, по сравнению с ее кодирующей областью дикого типа. В случае аминокислот, которые кодируются кодонами, содержащими только нуклеотиды G или С, модификации кодонов не требуется. Таким образом, кодоны для Pro (ССС или CCG), Arg (CGC или CGG), Ala (GCC или GCG) и Gly (GGC или GGG) не требуют модификации, поскольку в них отсутствуют А или U/T.
В противоположность этому, кодоны, которые содержат нуклеотиды А и/или U, можно модифицировать путем замены на другие кодоны, которые кодируют эти же аминокислоты, но не содержат А и/или U. Например,
кодирующие Pro кодоны CC(U/T) или ССА можно модифицировать на ССС или CCG;
кодирующие Arg кодоны CG(U/T) или CGA, или AGA, или AGG можно модифицировать на CGC или CGG;
кодирующие Ala кодоны GC(U/T) или GCA можно модифицировать на GCC или GCG;
кодирующие Gly кодоны GG(U/T) или GGA можно модифицировать на GGC или GGG.
В других случаях, когда нуклеотиды А или U нельзя элиминировать из кодонов, можно снижать содержание А и U с использованием кодонов, которые содержат нуклеотиды А и/или U в более низком количестве. Примерами указанных кодонов являются:
кодирующие Phe кодоны (U/T)(U/T)(U/T) можно модифицировать на (U/T) (U/T)C;
кодирующие Leu кодоны (U/T) (U/T)A, (U/T) (U/T)G, C(U/T) (U/T) или C(U/T)A можно модифицировать на C(U/T)C или C(U/T)G;
кодирующие Ser кодоны (U/T)C(U/T) или (U/T)CA, или AG(U/T) можно модифицировать на (U/T)CC, (U/T)CG или AGC;
кодирующий Tyr кодон (U/T)A(U/T) можно модифицировать на (U/T)AC;
кодирующий Cys кодон (U/T)G(U/T) можно модифицировать на (U/T)GC;
кодирующий His кодон СА(U/Т) можно модифицировать на САС;
кодирующий Gin кодон САА можно модифицировать на CAG;
кодирующие Ile кодоны A(U/T)(U/T) или A(U/T)A можно модифицировать на A(U/T)C
кодирующие Thr кодоны АС(U/T) или АСА можно модифицировать на АСС или ACG
кодирующий Asn кодон AA(U/T) можно модифицировать на ААС;
кодирующий Lys кодоны AAA можно модифицировать на AAG;
кодирующие Val кодоны G(U/T)(U/T) или G(U/T)A можно модифицировать на G(U/T)C или G(U/T)G;
кодирующий Asp кодон GA(U/T) можно модифицировать на GAC;
кодирующий Glu кодон GAA можно модифицировать на GAG;
стоп-кодон (U/T)AA можно модифицировать на (U/T)AG или (U/T)GA.
С другой стороны, в случае кодонов Met (AUG) и Trp (UGG), отсутствует возможность модификации последовательности без изменения кодируемой аминокислотной последовательности.
Перечисленные выше замены можно использовать либо индивидуально, либо в любых возможных комбинациях для повышения содержания G/C в открытой рамке считывания в предлагаемой в настоящем изобретении искусственной молекуле нуклеиновой кислоты, представленной в настоящем описании, по сравнению с конкретной открытой рамкой считывания дикого типа (т.е. исходной последовательности). Так, например, все кодоны Thr, встречающиеся в последовательности дикого типа, можно модифицировать на АСС (или ACG).
Предпочтительно содержание G/C в открытой рамке считывания в предлагаемой в настоящем изобретении искусственной молекуле нуклеиновой кислоты, представленной в настоящем описании, повышают по меньшей мере на 7%, более предпочтительно по меньшей мере на 15%, наиболее предпочтительно по меньшей мере на 20%, по сравнению с содержанием G/C в кодирующей области мРНК дикого типа без изменения кодируемой аминокислотной последовательности, т.е. используя вырожденность генетического кода. В конкретном варианте осуществления изобретения заменяют по меньшей мере 5%, 10%, 20%, 30%, 40%, 50%, 60%, более предпочтительно по меньшей мере 70%, еще более предпочтительно по меньшей мере 80% и наиболее предпочтительно по меньшей мере 90%, 95% или даже 100% пригодных для замены кодонов в открытой рамке считывания в предлагаемой в изобретении искусственной молекуле нуклеиновой кислоты или ее фрагменте, варианте или производном, повышая тем самым содержание G/C в указанной открытой рамке считывания.
В этом контексте наиболее предпочтительно повышать содержание G/C в открытой рамке считывания в предлагаемой в изобретении искусственной молекуле нуклеиновой кислоты, представленной в настоящем описании, до максимума (т.е. до 100% пригодных для замещения кодонов) по сравнению с открытой рамкой считывания дикого типа без изменения кодируемой аминокислотной последовательности.
Кроме того, в открытой рамке считывания предпочтительно осуществляют по меньшей мере частично оптимизацию кодонов. Оптимизация кодонов основана на открытии того факта, что эффективность трансляции может определяться также различной частотой встречаемости транспортных РНК (тРНК) в клетках. Таким образом, если в кодирующей области предлагаемой в изобретении искусственной молекуле нуклеиновой кислоты, представленной в настоящем описании, присутствуют в повышенном количестве так называемые «редкие кодоны», то уровень трансляции соответствующей модифицированной нуклеотидной последовательности является более низким, чем в том случае, когда присутствуют кодоны, кодирующие относительно «часто встречающуюся» тРНК.
Так, открытую рамку считывания предлагаемой в изобретении искусственной молекуле нуклеиновой кислоты предпочтительно модифицируют по сравнению с соответствующей кодирующей областью дикого типа таким образом, чтобы по меньшей мере один кодон в последовательности дикого типа, который кодирует тРНК, которая является относительно редкой в клетке, был заменен на кодон, который кодирует тРНК, которая встречается в клетке относительно часто и «несет» такую же аминокислоту, что и относительно редко встречающаяся тРНК. Посредством такой модификации открытую рамку считывания предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты, представленной в настоящем описании, модифицируют таким образом, чтобы кодонами, для которых доступны часто встречающиеся тРНК, заменять кодоны, которые соответствуют редким тРНК. Иными словами, согласно изобретению с помощью такой модификации все кодоны в открытой рамке считывания дикого типа, которые кодируют тРНК, являющуюся редкой в клетке, можно заменять на кодон, который кодируют тРНК, более часто встречающуюся в клетке, и которая в каждом случае «несет» такую же аминокислоту, что и редко встречающаяся тРНК. тРНК, встречающиеся относительно часто в клетке, и наоборот, встречающиеся относительно редко, известны специалистам в данной области, см., например, Akashi, Curr. Opin. Genet. Dev., 11(6), 2001, cc. 660-666. Таким образом, предпочтительно открытая рамка считывания имеет оптимизированные кодоны, предпочтительно применительно к системе, в которой должна экспрессироваться искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, предпочтительно применительно к системе, в которой должна транслироваться искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении. Предпочтительно, оптимизацию кодонов для часто встречающихся кодонов в открытой рамке считывания осуществляют в соответствии с часто встречающимися кодонами млекопитающих, более предпочтительно в соответствии с часто встречающимися кодонами человека. Предпочтительно, в открытой рамке считывания осуществляют и оптимизацию кодонов и модификацию содержания G/C.
Для дополнительного повышения устойчивости к расщеплению, например, устойчивости к расщеплению in vivo (или in vitro, как указано выше) экзо- или эндонуклеазой, и/или для дополнительного повышения стабильности экспрессии белка с искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, можно осуществлять дополнительные модификации искусственной молекулы нуклеиновой кислоты, такие как модификации каркаса, модификации Сахаров и/или модификации оснований, например, липидные модификации или т.п. Предпочтительно, такие модификации не приводят к значимому ухудшению транскрипции и/или трансляции искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении.
Как правило, искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может содержать любой нативный (встречающийся в естественных условиях) нуклеотид, например, гуанозин, урацил, аденозин и/или цитозин, или их аналоги. В этом контексте нуклеотидные аналоги классифицируют как встречающиеся в естественных условиях и не встречающиеся в естественных условиях варианты встречающихся в естественных условиях нуклеотидов аденозина, цитозина, тимидина, гуанозина и уридина. Таким образом, аналоги представляют собой, например, химически дериватизированные нуклеотиды, несущие не встречающиеся в естественных условиях функциональные группы, которые предпочтительно добавляют или изымают путем делеции из встречающегося в естественных условиях нуклеотида, или которыми заменяют встречающиеся в естественных условиях функциональные группы нуклеотида. Следовательно, можно модифицировать каждый компонент встречающегося в естественных условиях нуклеотида, а именно, компонент, представляющий собой основание, компонент, представляющий собой сахар (рибоза), и/или компонент, представляющий собой фосфат, формирующий каркас (см. выше) последовательности РНК. Аналоги гуанозина, уридина, аденозина, тимидина и цитозина включают (но, не ограничиваясь только ими) любой встречающийся в естественных условиях или не встречающийся в естественных условиях гуанозин, уридин, аденозин, тимидин или цитозин, который был изменен химически, например, ацетилированием, метилированием, гидроксилированием и т.д., включая, например, 1-метиладенозин, 1-метилгуанозин, 1-метилинозин, 2,2-диметилгуанозин, 2,6-диаминопурин, 2'-амино-2'-дезоксиаденозин, 2'-амино-2'-дезоксицитидин, 2'-амино-2'-дезоксигуанозин, 2'-амино-2'-дезоксиуридин, 2-амино-6-хлорпуринорибозид, 2-аминопуринрибозид, 2'-арааденозин, 2'-арацитидин, 2'-арауридин, 2'-азидо-2'-дезоксиаденозин, 2'-азидо-2'-дезоксицитидин, 2'-азидо-2'-дезоксигуанозин, 2'-азидо-2'-дезоксиуридин, 2-хлораденозин, 2'-фтор-2'-дезоксиаденозин, 2'-фтор-2'-дезоксицитидин, 2'-фтор-2'-дезоксигуанозин, 2'-фтор-2'-дезоксиуридин, 2'-фтортимидин, 2-метиладенозин, 2-метилгуанозин, 2-метилтио-N6-изопенениладенозин, 2'-O-метил-2-аминоаденозин, 2'-O-метил-2'-дезоксиаденозин, 2'-O-метил-2'-дезоксицитидин, 2'-O-метил-2'-дезоксигуанозин, 2'-O-метил-2'-дезоксиуридин, 2'-O-метил-5-метилуридин, 2'-O-метилинозин, 2'-O-метилпсевдоуридин, 2-тиоцитидин, 2-тиоцитозин, 3-метилцитозин, 4-ацетилцитозин, 4-тиоуридин, 5-(карбоксигидроксиметил)урацил, 5,6-дигидроуридин, 5-аминоаллилцитидин, 5-аминоаллилдезоксиуридин, 5-бромуридин, 5-карбоксиметиламинометил-2-тиоурацил, 5-карбоксиметиламинометилурацил, 5-хлор-арацитозин, 5-фторуридин, 5-йодуридин, 5-метоксикарбонилметилуридин, 5-метоксиуридин, 5-метил-2-тиоуридин, 6-азацитидин, 6-азауридин, 6-хлор-7-деазагуанозин, 6-хлорпуринорибозид, 6-меркаптогуанозин, 6-метилмеркаптопуринрибозид, 7-деаза-2'-дезоксигуанозин, 7-деазааденозин, 7-метилгуанозин, 8-азааденозин, 8-броаденозин, 8-бромгуанозин, 8-меркапторгуанозин, 8-оксогуанозин, бензимидазолрибозид, бета-D-маннозилквеозин, дигидроурацил, инозин, N1-метиладенозин, N6-([6-аминогексил]карбамоилметил)аденозин, N6-изопентениладенозин, N6-метиладенозин, N7-метилксантозин, метиловый эфир N-урацил-5-оксиуксусной кислоты, пуромицин, квеозин, урацил-5-оксиуксусная кислота, метиловый эфир урацил-5-оксиуксусной кислоты, вибутоксозин, ксантозин и ксилоаденозин. Получение таких аналогов известно специалисту в данной области, например, описано в US 4373071, US 4401796, US 4415732, US 4458066, US 4500707, US 4668777, US 4973679, US 5047524, US 5132418, US 5153319, US 5262530 и 5700642. Касательно аналогов, описанных выше, наиболее предпочтительными согласно некоторым вариантам осуществления изобретения могут быть те аналоги, которые увеличивают белковую экспрессию кодируемого пептида или белка, или повышают иммуногенность искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, и/или не взаимодействуют с другой интродуцированной модификацией искусственной молекулы нуклеиновой кислоты.
Согласно конкретному варианту осуществления изобретения искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может содержать липидную модификацию.
В предпочтительном варианте осуществления изобретения искусственная молекула нуклеиновой кислоты содержит, предпочтительно в 5'→3'-направлении, следующие элементы:
5'-UTR-элемент, обеспечивающий высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, предпочтительно нуклеотидную последовательность, представленную в одной из SEQ ID NO: 1-151; или дополнительную 5'-UTR, предпочтительно 5'-TOP UTR;
по меньшей мере одну открытую рамку считывания (ОРС), где ОРС предпочтительно содержит по меньшей мере одну модификацию по сравнению с последовательностью дикого типа;
3'-UTR-элемент, обеспечивающий высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, предпочтительно нуклеотидную последовательность, представленную в одной из SEQ ID NO: 152-204; или дополнительную 3'-UTR, предпочтительно 3'-UTR альбумина7;
поли(А)-последовательность, предпочтительно содержащую 64 аденилата;
поли(С)-последовательность, предпочтительно содержащую 30 цитидилатов;
последовательность гистоновой структуры типа «стебель-петля».
В наиболее предпочтительном варианте осуществления изобретения искусственная молекула нуклеиновой кислоты, предлагаемая в изобретении, может содержать также одну или несколько описанных ниже модификаций:
Химические модификации:
В контексте настоящего описания понятие «модификация» применительно к искусственной молекуле нуклеиновой кислоты может относиться к химическим модификациям, включающим модификации каркаса, а также модификации сахара или модификации основания.
В этом контексте искусственная молекула нуклеиновой кислоты, предпочтительно молекула РНК, представленная в настоящем описании, может содержать нуклеотидные аналоги/модификации, например, модификации каркаса, модификации сахара или модификации основания. Модификация каркаса согласно настоящему изобретению представляет собой модификацию, при которой химически модифицируют фосфаты каркаса нуклеотидов, содержащихся в молекуле нуклеиновой кислоты, представленной в настоящем описании. Модификация сахара согласно настоящему изобретению представляет собой химическую модификацию сахара нуклеотидов в молекуле нуклеиновой кислоты, представленной в настоящем описании. Кроме того, модификация основания согласно настоящему изобретению представляет собой химическую модификацию основного фрагмента нуклеотидов в молекуле нуклеиновой кислоты. В этом контексте нуклеотидные аналоги или модификации предпочтительно выбирают из нуклеотидных аналогов, пригодных для транскрипции и/или трансляции.
Модификации сахара:
Модифицированные нуклеозиды и нуклеотиды, которые могут быть включены в искусственную молекулу нуклеиновой кислоты, предпочтительно РНК, представленную в настоящем описании, могут быть модифицированы в сахарном фрагменте. Например, 2'-гидроксигруппу (ОН) в молекуле РНК можно модифицировать или заменять многочисленными «окси»- или «дезокси»-заместителями. Примерами модификаций, включающих «окси»-2'-гидроксигруппы, являются (но, не ограничиваясь только ими) алкоксигруппы или арилоксигруппы (-OR, например, R=Н, алкил, циклоалкил, арил, аралкил, гетероарил или сахар); полиэтиленгликоли (PEG), -O(CH2CH2O)nCH2CH2OR; «замкнутые» нуклеиновые кислоты (LNA), в которых 2'-гидроксил присоединен, например, с помощью метиленового мостика к 4'-углероду в том же самом сахарном фрагменте, представляющем собой рибозу; и аминогруппы (-O-аминогруппы, в которых аминогруппа, например, NRR, может представлять собой алкиламиногруппу, диалкиламиногруппу, гетероциклил, ариламиногруппу, диариламиногруппу, гетероариламиногруппу или дигетероариламиногруппу, этилендиамин, полиаминогруппу) или аминоалкоксигруппу.
«Дезокси»-модификация включает водород, аминогруппу (например, NH2; алкиламиногруппу, диалкиламиногруппу, гетероциклил, ариламиногруппу, диариламиногруппу, гетероариламиногруппу, дигетероариламиногруппу или аминокислоту); или аминогруппу можно присоединять к сахару через линкер, где линкер содержит один или несколько атомов С, N и О.
Сахарная группа может содержать также один или несколько атомов углерода, которые могут находиться в стереохимической конфигурации, отличной от конфигурации соответствующего атома углерода в рибозе. Так, модифицированная молекула нуклеиновой кислоты может включать, например, в качестве сахара арабинозу.
Модификации каркаса:
Можно модифицировать также фосфатный каркас в модифицированных нуклеозидах и нуклеотидах, которые могут быть встроены в искусственную молекулу нуклеиновой кислоты, предпочтительно РНК, представленную в настоящем описании. Фосфатные группы в каркасе можно модифицировать посредством замены одного или нескольких атомов кислорода на различные заместители. Кроме того, в модифицированных нуклеозидах и нуклеотидах не модифицированный фосфатный фрагмент может быть полностью заменен на модифицированный фосфат, представленный в настоящем описании. Примеры модифицированных фосфатных групп включают (но, не ограничиваясь только ими) фосфоротиоаты, фосфороселенаты, боранофосфаты, сложные боранофосфатные эфиры, первичные фосфонаты, фосфороамидаты, алкил- или арилфосфонаты и сложные фосфотриэфиры. В фосфородитиоатах оба несвязывающих атома кислорода заменены серой. Фосфатный линкер также можно модифицировать путем замены связывающего атома кислорода на азот (мостиковые фосфороамидаты), серу (мостиковые фосфоротиоаты) и углерод (мостиковые метиленфосфонаты).
Модификации основания:
Модифицированные нуклеозиды и нуклеотиды, которые можно встраивать в искусственную молекулу нуклеиновой кислоты, предпочтительно молекулу РНК, представленную в настоящем описании, можно модифицировать также во фрагменте, представляющем собой нуклеооснование. Примерами нуклеооснований, входящих в РНК, являются (но, не ограничиваясь только ими) аденин, гуанин, цитозин и урацил. Например, нуклеозиды и нуклеотиды, представленные в настоящем описании, можно химически модифицировать на поверхности главной бороздки. В некоторых вариантах осуществления изобретения химические модификации в главной бороздке включают аминогруппу, тиольную группу алкильную группу или галогруппу.
В наиболее предпочтительных вариантах осуществления настоящего изобретения нуклеотидные аналоги/модификации выбирают из модификаций основания, которые предпочтительно выбирают из 2-амино-6-хлорпуринрибозид-5'-трифосфат, 2-аминоаденозин-5'-трифосфат, 2-тиоцитидин-5'-трифосфат, 2-тиоуридин-5'-трифосфат, 4-тиоуридин-5'-трифосфат, 5-аминоаллилцитидин-5'-трифосфат, 5-аминоаллилуридин-5'-трифосфат, 5-бромцитидин-5'-трифосфат, 5-бромуридин-5'-трифосфат, 5-йодцитидин-5'-трифосфат, 5-йодуридин-5'-трифосфат, 5-метилцитидин-5'-трифосфат, 5-метилуридин-5'-трифосфат, 6-азацитидин-5'-трифосфат, 6-азауридин-5'-трифосфат, 6-хлорпуринрибозид-5'-трифосфат, 7-деазааденозин-5'-трифосфат, 7-деазагуанозин-5'-трифосфат, 8-азааденозин-5'-трифосфат, 8-азидоаденозин-5'-трифосфат, бензимидазолрибозид-5'-трифосфат, N1-метиладенозин-5'-трифосфат, N1-метилгуанозин-5'-трифосфат, N6-метиладенозин-5'-трифосфат, O6-метилгуанозин-5'-трифосфат, псевдоуридин-5'-трифосфат или пуромицин-5'-трифосфат, ксантозин-5'-трифосфат. Наиболее предпочтительные нуклеотиды для модификаций оснований выбирают из группы нуклеотидов с модифицированными основаниями, включающей 5-метилцитидин-5'-трифосфат, 7-деазагуанозин-5'-трифосфат, 5-бромцитидин-5'-трифосфат и псевдоуридин-5'-трифосфат.
В некоторых вариантах осуществления изобретения модифицированные нуклеозиды включают пиридин-4-оновый рибонуклеозид, 5-азауридин, 2-тио-5-азауридин, 2-тиоуридин, 4-тиопсевдоуридин, 2-тиопсевдоуридин, 5-гидроксиуридин, 3-метилуридин, 5-карбоксиметилуридин, 1-карбоксиметилпсевдоуридин, 5-пропинилуридин, 1-пропинилпсевдоуридин, 5-тауринометилуридин, 1-тауринометилпсевдоуридин, 5-тауринометил-2-тиоуридин, 1-тауринометил-4-тиоуридин, 5-метилуридин, 1-метилпсевдоуридин, 4-тио-1-метилпсевдоуридин, 2-тио-1-метилпсевдоуридин, 1-метил-1-деазапсевдоуридин, 2-тио-1-метил-1-деазапсевдоуридин, дигидроуридин, дигидропсевдоуридин, 2-тиодигидроуридин, 2-тиодигидропсевдоуридин, 2-метоксиуридин, 2-метокси-4-тиоуридин, 4-метоксипсевдоуридин и 4-метокси-2-тиопсевдоуридин.
В некоторых вариантах осуществления изобретения модифицированные нуклеозиды включают 5-азацитидин, псевдоизоцитидин, 3-метилцитидин, N4-ацетилцитидин, 5-формилцитидин, N4-метилцитидин, 5-гидроксиметилцитидин, 1-метилпсевдоизоцитидин, пирролоцитидин, пирролопсевдоизоцитидин, 2-тиоцитидин, 2-тио-5-метилцитидин, 4-тиопсевдоизоцитидин, 4-тио-1-метилпсевдоизоцитидин, 4-тио-1-метил-1-деазапсевдоизоцитидин, 1-метил-1-деазапсевдоизоцитидин, зебуларин, 5-азазебуларин, 5-метилзебуларин, 5-аза-2-тиозебуларин, 2-тиозебуларин, 2-метоксицитидин, 2-метокси-5-метилцитидин, 4-метоксипсевдоизоцитидин и 4-метокси-1-метилпсевдоизоцитидин.
В других вариантах осуществления изобретения модифицированные нуклеозиды включают 2-аминопурин, 2, 6-диаминопурин, 7-деазааденин, 7-деаза-8-азааденин, 7-деаза-2-аминопурин, 7-деаза-8-аза-2-аминопурин, 7-деаза-2,6-диаминопурин, 7-деаза-8-аза-2,6-диаминопурин, 1-метиладенозин, N6-метиладенозин, N6-изопентениладенозин, N6-(цис-гидроксиизопентенил)аденозин, 2-метилтио-N6-(цис-гидроксиизопентенил) аденозин, N6-глицинилкарбомоиладенозин, N6-треонилкарбамоиладенозин, 2-метилтио-N6-треонилкарбамоиладенозин, N6,N6-диметиладенозин, 7-метиладенин, 2-метилтиоаденин и 2-метоксиаденин.
В других вариантах осуществления изобретения модифицированные нуклеозиды включают инозин, 1-метилинозин, виозин, вибутозин, 7-деазагуанозин, 7-деаза-8-азагуанозин, 6-тиогуанозин, 6-тио-7-деазагуанозин, 6-тио-7-деаза-8-азагуанозин, 7-метилгуанозин, 6-тио-7-метилгуанозин, 7-метилинозин, 6-метоксигуанозин, 1-метилгуанозин, N2-метилгуанозин, N2,N2-диметилгуанозин, 8-оксогуанозин, 7-метил-8-оксогуанозин, 1-метил-6-тиогуанозин, N2-метил-6-тиогуанозин и N2,N2-диметил-6-тиогуанозин.
В некоторых вариантах осуществления изобретения нуклеотид можно модифицировать на поверхности главной бороздки и модификация может включать замену атома водорода на С-5 урацила метальной группой или галогруппой. В конкретных вариантах осуществления изобретения модифицированный нуклеозид представляет собой 5'-O-(1-тиофосфат)-аденозин, 5'-O-(1-тиофосфат)-цитидин, 5'-O-(1-тиофосфат)-гуанозин, 5'-O-(1-тиофосфат)-уридин или 5'-O-(1-тиофосфат)-псевдоуридин.
В других конкретных вариантах осуществления изобретения искусственная молекула нуклеиновой кислоты, предпочтительно молекула РНК, может содержать нуклеозидные модификации, выбранные из 6-азацитидина, 2-тиоцитидина, альфа-тиоцитидина, псевдоизоцитидина, 5-аминоаллилуридина, 5-йодуридина, N1-метилпсевдоуридина, 5,6-дигидроуридина, альфа-тиоуридина, 4-тиоуридина, 6-азауридина, 5-гидроксиуридина, дезокситимидина, 5-метилуридина, пирролоцитидина, инозина, альфа-тиогуанозина, 6-метилгуанозина, 5-метилцитидина, 8-оксогуанозина, 7-деазагуанозина, N1-метиладенозина, 2-амино-6-хлорпурина, N6-метил-2-аминопурина, псевдоизоцитидина, 6-хлорпурина, N6-метиладенозин, альфа-тиоаденозина, 8-азидоаденозина, 7-деазааденозина.
Липидная модификация:
Согласно следующему варианту осуществления изобретения искусственная молекула нуклеиновой кислоты, предпочтительно РНК, представленная в настоящем описании, может содержать липидную модификацию. Такая модифицированная липидами РНК, как правило, содержит РНК, представленную в настоящем описании. Такая модифицированная липидами молекула РНК, представленная в настоящем описании, как правило, дополнительно содержит по меньшей мере один линкер, ковалентно связанный с указанной молекулой РНК, и по меньшей мере один липид, ковалентно связанный с соответствующим линкером. Альтернативно этому, модифицированная липидами молекула РНК содержит (по меньшей мере одну) молекулу РНК, указанную в настоящем описании, и по меньшей мере один (бифункциональный) липид, ковалентно связанный (без линкера) с указанной молекулой РНК. Согласно третьей альтернативе модифицированная липидами молекула РНК содержит искусственную молекулу нуклеиновой кислоты, предпочтительно молекулу РНК, указанную в настоящем описании, по меньшей мере один линкер, ковалентно связанный с указанной молекулой РНК, и по меньшей мере один липид, ковалентно связанный с соответствующим линкером, и также по меньшей мере один (бифункциональный) липид, ковалентно связанный (без линкера) с указанной мРНК. В этом контексте наиболее предпочтительно липидную модификацию осуществляют на концах линейной последовательности РНК.
Модификация 5'-конца модифицированной РНК:
Согласно другому предпочтительному варианту осуществления изобретения искусственную молекулу нуклеиновой кислоты, предпочтительно молекулу РНК, представленную в настоящем описании, можно модифицировать путем добавления так называемой «5'-кэп»-структуры.
5'-кэп представляет собой структуру, как правило, структуру, состоящую из модифицированных нуклеотидов, которая, как правило, «кэпирует» 5'-конец зрелой мРНК. 5'-кэп, как правило, может быть сформирован модифицированным нуклеотидом, прежде всего производным гуанинового нуклеотида.
Предпочтительно 5'-кэп связан с 5'-концом с помощью 5'-5'-трифосфатной связи. 5'-кэп может быть метилирован, например, m7GpppN, где N представляет собой концевой 5'-нуклеотид нуклеиновой кислоты, несущей 5'-кэп, как правило, 5'-конец РНК. m7GpppN представляет собой 5'-кэп-структуру, которая встречается в естественных условиях в мРНК, транскрибируемой полимеразой II, и, следовательно, не рассматривается как модификация, содержащаяся в модифицированной РНК, предлагаемой в изобретении. Это означает, что искусственная молекула нуклеиновой кислоты, предпочтительно молекула РНК, предлагаемая в настоящем изобретении, может содержать m7GpppN в качестве 5'-кэпа, но при этом дополнительно искусственная молекула нуклеиновой кислоты, предпочтительно молекула РНК, содержит по меньшей мере одну дополнительную модификацию, представленную в настоящем описании.
Другими примерами 5'-кэп-структур являются глицерил, инвертированная дезоксигруппа (фрагмент), лишенная азотистого основания, 4',5'-метиленовой нуклеотид, 1-(бета-D-эритрофуранозильный) нуклеотид, 4'-тионуклеотид, карбоциклический нуклеотид, 1,5-ангидрогекситольный нуклеотид, L-нуклеотиды, альфа-нуклеотид, нуклеотид с модифицированным основанием, треопентофуранозильный нуклеотид, ациклический 3',4'-секонуклеотид, ациклический 3,4-дигидроксибутильный нуклеотид, ациклический 3,5-дигидроксипентильный нуклеотид, 3'-3'-инвертированный нуклеотидный фрагмент, 3'-3'-инвертированный лишенный азотистого основания фрагмент, 3'-2'-инвертированный нуклеотидный фрагмент, 3'-2'-инвертированный лишенный азотистого основания фрагмент, 1,4-бутандиолфосфатный, 3'-фосфороамидатный, гексилфосфатный, аминогексилфосфатный, 3'-фосфатный, 3'-фосфоротиоатный, фосфородитиоатный или связанный мостиком или несвязанный мостиком метилфосфонатный фрагмент. Эти модифицированные 5'-кэп-структуры рассматриваются в качестве по меньшей мере одной модификации, содержащейся в искусственной молекуле нуклеиновой кислоты, предпочтительно в молекуле РНК, предлагаемой в настоящем изобретении.
Наиболее предпочтительными модифицированными 5'-кэп-структурами являются САР1 (метилирование рибозы соседнего с m7GpppN нуклеотида), САР2 (метилирование рибозы 2-ого нуклеотида, расположенного по ходу транскрипции относительно m7GpppN), САР3 (метилирование рибозы 3-его нуклеотида, расположенного по ходу транскрипции относительное m7GpppN), САР4 (метилирование рибозы 4-ого нуклеотида, расположенного по ходу транскрипции относительно m7GpppN), ARCA (аналог кэп-структуры с правильной ориентацией, модифицированный ARCA (например, модифицированный фосфотиоатом ARCA), инозин, N1-метилгуанозин, 2'-фторгуанозин, 7-деазагуанозин, 8-оксогуанозин, 2-аминогуанозин, ЗНК-гуанозин и 2-азидогуанозин.
В предпочтительном варианте осуществления изобретения по меньшей мере одна открытая рамка считывания кодирует терапевтический белок или пептид. В другом варианте осуществления изобретения по меньшей мере одной открытой рамкой считывания кодируется антиген, такой как патогенный антиген, опухолевый антиген, аллергенный антиген или аутоиммунный антиген. Таким образом, введение искусственной молекулы нуклеиновой кислоты, кодирующей антиген, применяют в подходе, заключающемся в генетической вакцинации против заболевания, в котором участвует указанный антиген.
В альтернативном варианте осуществления изобретения по меньшей мере одной открытой рамкой считывания искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении, кодируется антитело или антиген-специфический Т-клеточный рецептор, или его фрагмент.
Антигены:
Патогенные антигены:
Искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может кодировать белок или пептид, который содержит патогенный антиген или его фрагмент, вариант или производное. Такие патогенные антигены происходят из патогенных организмов, прежде всего, бактерий, вирусов или простейших (многоклеточных) патогенных организмов, которые вызывают иммунологическую реакцию у индивидуума, прежде всего у млекопитающего, более предпочтительно у человека. Более конкретно, патогенные антигены предпочтительно представляют собой поверхностные антигены, например, белки (или фрагменты белков, например, находящуюся снаружи часть поверхностного антигена), локализованные на поверхности вируса или бактерии или простейшего.
Патогенные антигены представляют собой пептидные или белковые антигены, предпочтительно происходящие из патогенов, ассоциированных с инфекционным заболеванием, которые предпочтительно выбирают из антигенов, происходящих из патогенов Acinetobacter baumannii, рода Anaplasma, Anaplasma phagocytophilum, Ancylostoma braziliense, Ancylostoma duodenale, Arcanobacterium haemolyticum, Ascaris lumbricoides, рода Aspergillus, Astroviridae, рода Babesia, Bacillus anthracis, Bacillus cereus, Bartonella henselae, вируса BK, Blastocystis hominis, Blastomyces dermatitidis, Bordetella pertussis, Borrelia burgdorferi, рода Borrelia, Borrelia spp, рода Brucella, Brugia malayi, семейства Bunyaviridae, Burkholderia cepacia и других видов Burkholderia, Burkholderia mallei, Burkholderia pseudomallei, семейства Caliciviridae, рода Campylobacter, Candida albicans, Candida spp, Chlamydia trachomatis, Chlamydophila pneumoniae, Chlamydophila psittaci, приона CJD, Clonorchis sinensis, Clostridium botulinum, Clostridium difficile, Clostridium perfringens, Clostridium perfringens, Clostridium spp, Clostridium tetani, Coccidioides spp, коронавирусов, Coryneb acterium diphtheriae, Coxiella burnetii, вируса геморрагической лихорадки Крым-Конго, Cryptococcus neoformans, рода Cryptosporidium, Cytomegalovirus (CMV), вирусов Денге (DEN-1, DEN-2, DEN-3 и DEN-4), Dientamoeba fragilis, вируса Эбола (EBOV), рода Echinococcus, Ehrlichia chaffeensis, Ehrlichia ewingii, рода Ehrlichia, Entamoeba histolytica, рода Enterococcus, рода Enterovirus, энтеровирусов, прежде всего вируса Коксаки А и энтеровируса 71 (EV71), Epidermophyton spp, вируса Эпштейна-Барра (EBV), Escherichia coli O157:Н7, O111 и О104:Н4, Fasciola hepatica и Fasciola gigantica, приона FFI, суперсемейства Filarioidea, флавивирусов, Francisella tularensis, рода Fusobacterium, Geotrichum candidum, Giardia intestinalis, Gnathostoma spp, приона GSS, вируса Гуанарито, Haemophilus ducreyi, Haemophilus influenzae, Helicobacter pylori, генипавируса (вирус Гендра и вирус Нипа), вируса гепатита А, вируса гепатита В (HBV), вируса гепатита С (HCV), вируса гепатита D, вируса гепатита, вируса герпеса простого 1 и 2 (HSV-1 и HSV-2), Histoplasma capsulatum, HIV (вирус иммунодефицита человека), Hortaea werneckii, человеческого бокавируса (HBoV), человеческого вируса герпеса 6 (HHV-6) и человеческого вируса герпеса 7 (HHV-7), человеческого вируса метапенвмонии (hMPV), вируса папилломы человека (HPV), человеческих вирусов парагриппа (HPIV), вируса японского энцефалита, вируса JC, вируса Джунин, Kingella kingae, Klebsiella granulomatis, приона Куру, вируса Ласса, Legionella pneumophila, рода Leishmania, рода Leptospira, Listeria monocytogenes, вируса лимфоцитарного хориоменингита (LCMV), вируса Мачупо, Malassezia spp, вируса Марбурга, вируса кори, Metagonimus yokagawai, Microsporidia phylum, вируса контагиозного моллюска (MCV), вируса паротита, Mycobacterium leprae и Mycobacterium lepromatosis, Mycobacterium tuberculosis, Mycobacterium ulcerans, Mycoplasma pneumoniae, Naegleria fowleri, Necator americanus, Neisseria gonorrhoeae, Neisseria meningitidis, Nocardia asteroides, Nocardia spp, Onchocerca volvulus, Orientia tsutsugamushi, семейства Orthomyxoviridae (грипп), Paracoccidioides brasiliensis, Paragonimus spp, Paragonimus westermani, парвовируса В19, рода Pasteurella, рода Plasmodium, Pneumocystis jirovecii, полиовируса, вируса бешенства, респираторно-синтициального вируса (RSV), риновируса, риновирусов, Rickettsia akari, рода Rickettsia, Rickettsia prowazekii, Rickettsia rickettsii, Rickettsia typhi, вируса долины Рифта, ротавируса, вируса краснухи, вируса Сабиа, рода Salmonella, Sarcoptes scabiei, коронавируса SARS, рода Schistosoma, рода Shigella, вируса Син Номбре, хантавируса, Sporothrix schenckii, рода Staphylococcus, Streptococcus agalactiae, Streptococcus pneumoniae, Streptococcus pyogenes, Strongyloides stercoralis, рода Taenia, Taenia solium, вируса клещевого энцефалита (TBEV), Toxocara canis или Toxocara cati, Toxoplasma gondii, Treponema pallidum, Trichinella spiralis, Trichomonas vaginalis, Trichophyton spp, Trichuris trichiura, Trypanosoma brucei, Trypanosoma cruzi, Ureaplasma urealyticum, вируса ветряной оспы (VZV), Variola major или Variola minor, приона vCJD, вируса венесуэльского энцефалита лошадей, Vibrio cholerae, вируса Западного Нила, вируса западного энцефалита лошадей, Wuchereria bancrofti, вируса желтой лихорадки, Yersinia enterocolitica, Yersinia pestis и Yersinia pseudotuberculosis.
В этом контексте наиболее предпочтительными являются антигены из патогенов, выбранных из вируса гриппа, респираторно-синтициального вируса (RSV), вируса герпеса простого (HSV), вируса папилломы человека (HPV), вируса иммунодефицита человека (HIV), Plasmodium, Staphylococcus aureus, вируса Денге, Chlamydia trachomatis, цитомегаловируса (CMV), вируса гепатита В (HBV), Mycobacterium tuberculosis, вируса бешенства и вируса желтой лихорадки.
Опухолевые антигены:
В другом варианте осуществления изобретения искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, может кодировать белок или пептид, который содержит пептид или белок, содержащий опухолевый антиген, фрагмент, вариант или производное указанного опухолевого антигена, где предпочтительно, опухолевый антиген представляет собой меланоцит-специфический антиген, раково-тестикулярный антиген или опухоль-специфический антиген, предпочтительно СТ-Х-антиген, не-Х-СТ-антиген, партнер, связывающий СТ-Х-антиген или партнер, связывающий не-Х-СТ-антиген, или опухоль-специфический антиген, более предпочтительно СТ-Х-антиген, партнер, связывающий не-Х-СТ-антиген или опухоль-специфический антиген, или фрагмент, вариант или производное указанного опухолевого антигена; и где каждая из нуклеотидных последовательностей кодирует отличный от других пептид или белок; и где по меньшей мере одна из нуклеотидных последовательностей кодирует 5Т4, 707-АР, 9D7, AFP, AlbZIP HPG1, альфа-5-бета-1-интегрин, альфа-5-бета-6-интегрин, альфа-актинин-4/m, альфа-метилацил-кофермент А-рацемазу, ART-4, ARTC1/m, В7Н4, BAGE-1, BCL-2, bcr/abl, бета-катенин/m, BING-4, BRCA1/m, BRCA2/m, CA 15-3/CA 27-29, CA19-9, CA72-4, CA125, калретикулин, CAMEL, CASP-8/m, катепсин В, катепсин L, CD19, CD20, CD22, CD25, CDE30, CD33, CD4, CD52, CD55, CD56, CD80, CDC27/m, CDK4/m, CDKN2A/m, CEA, CLCA2, CML28, CML66, COA-1/m, коактозин-подобный белок, коллаген XXIII, COX-2, CT-9/BRD6, Cten, циклин B1, циклин D1, cyp-B, CYPB1, DAM-10, DAM-6, DEK-CAN, EFTUD2/m, EGFR, ELF2/m, EMMPRIN, EpCam, EphA2, EphA3, ErbB3, ETV6-AML1, EZH2, FGF-5, FN, Frau-1, G250, GAGE-1, GAGE-2, GAGE-3, GAGE-4, GAGE-5, GAGE-6, GAGE7b, GAGE-8, GDEP, GnT-V, gp100, GPC3, GPNMB/m, HAGE, HAST-2, гепсин, Her2/neu, HERV-K-MEL, HLA-A*0201-R17I, HLA-A11/m, HLA-A2/m, HNE, гомеобокс NKX3.1, HOM-TES-14/SCP-1, HOM-TES-85, HPV-E6, HPV-E7, HSP70-2M, HST-2, hTERT, iCE, IGF-1R, IL-13Ra2, IL-2R, IL-5, незрелый ламининовый рецептор, каллекреин-2, каллекреин-4, Ki67, KIAA0205, KIAA0205/m, KK-LC-1, K-Ras/m, LAGE-A1, LDLR-FUT, MAGE-A1, MAGE-A2, MAGE-А3, MAGE-A4, MAGE-A6, MAGE-A9, MAGE-A10, MAGE-A12, MAGE-B1, MAGE-B2, MAGE-B3, MAGE-B4, MAGE-B5, MAGE-B6, MAGE-B10, MAGE-B16, MAGE-B17, MAGE-C1, MAGE-C2, MAGE-C3, MAGE-D1, MAGE-D2, MAGE-D4, MAGE-E1, MAGE-E2, MAGE-F1, MAGE-H1, MAGEL2, маммоглобин A, MART-1/мелан-А, MART-2, MART-2/m, матриксный белок 22, MC1R, M-CSF, ME1/m, мезотелин, MG50/PXDN, MMP11, MN/CA IX-антиген, MRP-3, MUC-1, MUC-2, MUM-1/m, MUM-2/m, MUM-3/m, миозин класса I/m, NA88-A, N-ацетилглюкозаминилтрансферазу-V, Neo-PAP, Neo-PAP/m, NFYC/m, NGEP, NMP22, NPM/ALK, N-Ras/m, NSE, NY-ESO-1, NY-ESO-B, OA1, OFA-iLRP, OGT, OGT/m, OS-9, OS-9/m, остеокальцин, остеопонтин, p15, p190 минорный bcr-abl, p53, p53/m, PAGE-4, PAI-1, PAI-2, PART-1, PATE, PDEF, Pim-1-киназу, Pin-1, Pml/PARальфа, POTE, PRAME, PRDX5/m, простеин, протеиназу-3, PSA, PSCA, PSGR, PSM, PSMA, PTPRK/m, RAGE-1, RBAF600/m, RHAMM/CD168, RU1, RU2, S-100, SAGE, SART-1, SART-2, SART-3, SCC, SIRT2/m, Sp17, SSX-1, SSX-2/HOM-MEL-40, SSX-4, STAMP-1, STEAP, сурвивин, сурвивин-2В, SYT-SSX-1, SYT-SSX-2, TA-90, TAG-72, TARP, TEL-AML1, TGFбета, TGFбетаRII, TGM-4, TPI/m, TRAG-3, TRG, TRP-1, TRP-2/6b, TRP/INT2, TRP-p8, тирозиназу, UPA, VEGF, VEGFR-2/FLK-1, WT1 и иммуноглобулиновый идиотип лимфоидной кровяной клетки или идиотип Т-клеточного рецептора, или фрагмент, вариант или производное указанного опухолевого антигена; предпочтительно сурвивин или его гомолог, антиген семейства MAGE или его связывающий партнер или фрагмент, вариант или производное указанного опухолевого антигена. Наиболее предпочтительными в этом контексте являются опухолевые антигены NY-ESO-1, 5Т4, MAGE-C1, MAGE-C2, сурвивин, Muc-1, PSA, PSMA, PSCA, STEAP и РАР.
В предпочтительном варианте осуществления изобретения искусственная молекула нуклеиновой кислоты кодирует белок или пептид, который содержит терапевтический белок или его фрагмент, вариант или производное.
В контексте настоящего описания терапевтические белки представляют собой пептиды или белки, которые оказывают полезное действие при лечении любого врожденного или приобретенного заболевания или которые улучшают состояние индивидуума. В частности, терапевтические белки имеют важное значение для создания терапевтических средств, которые могут помимо осуществления других функций модифицировать и осуществлять репарацию генетических ошибок, разрушать раковые клетки или инфицированные патогеном клетки, лечить нарушения иммунной системы, лечить метаболические или эндокринные нарушения. Например, эритропоэтин (ЕРО), белковый гормон, можно применять для лечения пациентов с дефицитом эритроцитов, который является обычной причиной почечных осложнений. Кроме того, под понятие «терапевтические белки» подпадают адъювантные белки, терапевтические антитела, а также средства гормонзаместительной терапии, которую применяют, например, при лечении женщин в период менопаузы. В более современных подходах используют соматические клетки пациента для перепрограммирования их в плюрипотентные стволовые клетки, что является заменой спорной терапии на основе стволовых клеток. Такие белки, применяемые для перепрограммирования соматических клеток или применяемые для дифференцировки стволовых клеток, также рассматриваются как терапевтические белки в контексте настоящего описания. Кроме того, терапевтические белки можно применять и для других целей, например, для заживления ран, регенерации тканей, ангиогенеза и т.д. Кроме того, в контексте настоящего описания антигенпрезентирующие В-клеточные рецепторы и их фрагменты и варианты рассматриваются как терапевтические белки.
Таким образом, терапевтические белки можно применять для различных целей, включая лечение различных заболеваний, таких, например, как инфекционные заболевания, неоплазмы (например, раковые или опухолевые заболевания), заболевания крови или кроветворных органов, эндокринных, связанных с питанием или метаболических заболеваний, заболеваний нервной системы, заболеваний системы кровообращения, заболеваний дыхательной системы, заболеваний пищеварительной системы, заболеваний кожи и подкожной ткани, заболеваний скелетно-мышечной системы и соединительной ткани, и заболеваний мочеполовой системы, независимо от того, являются ли они врожденными или приобретенными.
В этом контексте наиболее предпочтительными терапевтическими белками, которые можно применять, среди прочего, для лечения метаболических или эндокринных нарушений, являются (в скобках указано конкретное заболевание, для лечения которого применяют терапевтический белок): кислая сфингомиелиназа (болезнь Нимана-Пика), адипотид (ожирение), агалзидаза-бета (человеческая галактозидаза А) (болезнь Фабри; препятствует накоплению липидов, которое может приводить к почечным и сердечно-сосудистым осложнениям), алглукозидаза (болезнь Помпе (гликогеноз (накопление гликогена) типа II)), альфа-галактозидаза А (альфа-GAL А, агалзидаза-альфа) (болезнь Фабри), альфа-глюкозидаза (гликогеноз (GSD), болезнь Помпе), альфа-L-идуронидаза (мукополисахаридоз (MPS), синдром Гурлер, синдром Шейе), альфа-N-ацетилглюкозаминидаза (синдром Санфилиппо), амфирегулин (рак, метаболическое нарушение), ангиопоэтин ((Ang1, Ang2, Ang3, Ang4, ANGPTL2, ANGPTL3, ANGPTL4, ANGPTL5, ANGPTL6, ANGPTL7) (ангиогенез, стабилизирует сосуды), бетацеллюлин (метаболическое нарушение), бета-глюкуронидаза (синдром Слая), костный морфогенетический белок BMP (ВМР1, ВМР2, ВМР3, ВМР4, ВМР5, ВМР6, ВМР7, ВМР8а, BMP8b, ВМР10, BMP15) (регенеративное действие, состояния, связанные с костной тканью, хроническое заболевание почек (CKD)), белок CLN6 (болезнь, вызванная мутациями в локусе CLN6 - атипичный поздний инфантилизм, вариант с поздним началом, ранний ювенильный, нейрональный цероид-липофусциноз (NCL)), эпидермальный фактор роста (EGF) (заживление ран, регуляция роста, пролиферации и дифференцировки клеток), эпиген (метаболическое нарушение), эпирегулин (метаболическое нарушение), фактор роста фибробластов (FGF, FGF-1, FGF-2, FGF-3, FGF-4, FGF-5, FGF-6, FGF-7, FGF-8, FGF-9, FGF-10, FGF-11, FGF-12, FGF-13, FGF-14, FGF-16, FGF-17, FGF-17, FGF-18, FGF-19, FGF-20, FGF-21, FGF-22, FGF-23) (заживление ран, ангиогенез, эндокринные нарушения, регенерация ткани), галсульфаза (мукополисахаридоз типа VI), грелин (синдром раздраженного кишечника (IBS), ожирение, синдром Прадера-Вилли, сахарный диабет типа II), глюкоцереброзидаза (болезнь Гоше), GM-CSF (регенеративное действие, производство лейкоцитов, рак), гепаринсвязывающий EGF-подобный фактор роста (HB-EGF) (заживление ран, гипертрофия сердца и развитие и функция сердца), фактор роста гепатоцитов HGF (регенеративное действие, заживление ран), гепсидин (нарушения метаболизма железа, бета-талассемия), человеческий альбумин (пониженное производство альбумина (гипопротеинемия), повышенная потеря альбумина (нефротический синдром), гиповолемия, гипербилирубинемия), идурсульфаза (идуронат-2-сульфатаза) (мукополисахаридоз типа II (синдром Хантера)), интегрины αVβ3, αVβ5 и α5β1 (связывают матриксные макромолекулы и протеиназы, ангиогенез), идуронатсульфатаза (синдром Хантера), ларонидаза (мукополисахаридоз типа I, формы Гурлер и Гурлер-Шайе), N-ацетилгалактозамин-4-сульфатаза (rhASB; галсульфаза, арилсульфатаза A (ARSA), арилсульфатаза В (ARSB)) (дефицит арилсульфатазы В, синдром Марото-Лами, мукополисахаридоз типа VI), N-ацетилглюкозамин-6-сульфатаза (синдром Санфилиппо), фактор роста нервов (NGF, мозговой нейротрофический фактор (BDNF), нейротрофин-3 (NT-3) и нейротрофин 4/5 (NT-4/5) (регенеративное действие, сердечно-сосудистые заболевания, коронарный атеросклероз, ожирение, диабет типа 2, метаболический синдром, острые коронарные синдромы, деменция, депрессия, шизофрения, аутизм, синдром Ретта, нервная анорексия, нервная булимия, заживление ран, кожные язвы, изъязвления роговицы, болезнь Альцгеймера), нейрегулин (NRG1, NRG2, NRG3, NRG4) (метаболическое нарушение, шизофрения), нейропилин (NRP-1, NRP-2) (ангиогенез, управление аксонами, выживание, миграция клеток), обестатин (синдром раздраженного кишечника (IBS), ожирение, синдром Прадера-Вилли, сахарный диабет типа II), фактор роста тромбоцитов (PDGF (PDFF-A, PDGF-B, PDGF-C, PDGF-D) (регенеративное действие, заживление ран, нарушение ангиогенеза, артериосклероз, фиброз, рак), рецепторы TGF-бета (эндоглин, рецептор TGF-бета 1, рецептор TGF-бета 2, рецептор TGF-бета 3) (почечный фиброз, заболевание почек, диабет, терминальная стадия почечной болезни (ESRD), ангиогенез), тромбопоэтин (ТНРО) (фактор роста и развития мегакариоцитов (MGDF)) (тромбоцитарные нарушения, тромбоциты для донорской сдачи, восстановление уровня тромбоцитов после миелосупрессорной химиотерапии), трансформирующий фактор роста (TGF (TGF-альфа, TGF-бета (TGFбета1, TGFбета2 и TGFбета3))) (регенеративное действие, заживление ран, иммунитет, рак, заболевание сердца, диабет, синдром Марфана, синдром Лоеса-Дитца), VEGF (VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGF-E, VEGF-F и PIGF) (регенеративное действие, ангиогенез, заживление ран, рак, проницаемость), несритид (острая декомпенсированная застойная сердечная недостаточность), трипсин (декубитальная язва, варикозная язва, санация струпа, спонтанно раскрывающаяся рана, солнечный ожог, мекониевая непроходимость кишечника), адренокортикотропный гормон (АСТН) (болезнь Аддисона, мелкоклеточная саркома, адренолейкодистрофия, врожденная гиперплазия надпочечников, синдром Кушинга, синдром Нельсона, детские спазмы), предсердный натрийуретический пептид (ANP) (эндокринные нарушения), холецистокинин (различной длины), гастрин (гипогастринемия), лептин (диабет, гиперглицинемия, ожирение), окситоцин (стимулирует грудное кормление, ненаступление родов), соматостатин (симптоматическое лечение карционоидного синдрома, острое варикозное кровотечение и акромегалия, поликистозные заболевания печени и почек, акромегалия и симптомы, вызываемые нейроэндокринными опухолями), вазопрессин (антидиуретический гормон) (несахарный диабет), кальцитонин (постменопаузальный остеопороз, гиперкальциемия, болезнь Пэджета, метастазы в костную ткань, фантомная боль к конечностях, спинальный стеноз), экзенатид (диабет типа 2, устойчивый к обработке метформином и сульфонилмочевиной), гормон роста (GH), соматотропин (нарушение роста вследствие дефицита GH или хронической печеночной недостаточности, синдром Прадера-Вилли, синдром Турнера, обусловленное СПИДом истощение или кахексия при осуществлении противовирусной терапии), инсулин (сахарный диабет, диабетический кетоацидоз, гиперкалиемия), инсулиноподобный фактор роста 1 IGF-1 (нарушение роста у детей с делецией гена GH или серьезным первичным дефицитом IGF1, нейродегенеративное заболевание, сердечно-сосудистые заболевания, сердечная недостаточность), мекасермин ринфабат, аналог IGF-1 (нарушение роста у детей с делецией гена GH или серьезным первичным дефицитом IGF1, нейродегенеративное заболевание, сердечно-сосудистые заболевания, сердечная недостаточность), мегасермин, аналог IGF-1 (нарушение роста у детей с делецией гена GH или серьезным первичным дефицитом IGF1, нейродегенеративное заболевание, сердечно-сосудистые заболевания, сердечная недостаточность), пэгвисомант (акромегалия), прамлинтид (сахарный диабет, в комбинации с инсулином), терипаратид (человеческий паратиреоидный гормон, остатки 1-34) (серьезный остеопороз), бекаплермин (вспомогательное средство при санации диабетических язв), диботермин-альфа (костный морфогенный белок 2) (хирургическая операция по закреплению позвоночника (Spinal Fusion), восстановление кости при повреждении), гистрелина ацетат (гонадотропин-рилизинг гормон; GnRH) (преждевременное половое созревание), октреотид (акромегалия, симптоматическое ослабление VIP-секретирующей аденомы и метастатических карциноидных опухолей) ипалифермин (фактор роста кератиноцитов; KGF) (серьезный оральный мукозит у пациентов, подвергающихся химиотерапии, заживление ран).
Указанные и другие белки рассматриваются как терапевтические, поскольку они предназначены для лечения индивидуума путем возмещения нарушенного эндогенного производства в его организме функционального белка в достаточных количествах. Следовательно, такие терапевтические белки, как правило, представляют собой белки млекопитающих, прежде всего человеческие белки.
Для лечения нарушений крови, заболеваний системы кровообращения, заболеваний дыхательной системы, раковых или опухолевых заболеваний, инфекционных заболеваний или иммунодефицитов можно применять такие терапевтические белки, как: альтерплаза (активатор тканевого плазминогена; tPA) (легочная эмболия, инфаркт миокарда, острый ишемический инсульт («удар»), окклюзия устройств центрального венозного доступа), анистреплаза (тромболизис), антитромбин III (АТ-III) (наследственный дефицит АТ-III, тромбоэмболия), бивалирудин (снижает риск свертывания крови при коронарной ангиопластике и индуцированной гепарином тромбоцитопении), дарбепоэтин-альфа (лечение анемии у пациентов с хронической почечной недостаточностью и хроническим почечным нарушением (+/- диализ)), дротрекогин-альфа (активированный белок С) (серьезный сепсис с высоким риском смерти), эритропоэтин, эпоэтин-альфа, эритропоэтин, эритропоетин (анемия при хроническом заболевании, миелодисплазия, анемия при почечной недостаточности или при осуществлении химиотерапии, предоперационная подготовка), фактор IX (гемофилия В), фактор VIIa (кровоизлияние у пациентов с гемофилией А или В и при применении ингибиторов фактора VIII или фактора IX), фактор VIII (гемофилия А), лепирудин (индуцируемая гепарином тромбоцитопения), концентрат белка С (венозный тромбоз, молниеносная пурпура), ретеплаза (делеция мутеина в tPA) (лечение острого инфаркта миокарда, улучшение функции желудочков), стрептокиназа (остро развивающийся трансмуральный инфаркт миокарда, легочная эмболия, тромбоз глубоких вен, артериальный тромбоз или эмболия, окклюзия артериовенозной канюли), тенестеплаза (острый инфаркт миокарда), урокиназа (легочная эмболия), ангиостатин (рак), анти-CD22 иммунотоксин (рецидивирующий острый миелоидный CD33+-лейкоз), денилейкин дифтитокс (кожная Т-клеточная лимфома (CTCL)), иммуноцианин (рак мочевого пузыря и предстательной железы), MPS (металлопанстимулин) (рак), афлиберцепт (немелкоклеточный рак легкого (NSCLC), метастатический колоректальный рак (mCRC), гормон-устойчивый метастатический рак предстательной железы, влажная форма дегенерации желтого пятна), эндостатин (рак, воспалительные заболевания типа ревматоидного артрита, а также болезнь Крона, диабетическая ретинопатия, псориаз и эндометриоз), коллагеназа (санация хронических кожных язв и областей серьезных ожогов, контрактура Дюпюитрена, болезнь Пейрони), человеческая дезоксирибонуклеаза I, дорназа (муковисцидоз; уменьшение инфекций респираторного тракта у выбранных пациентов с FVC, превышающим более чем на 40% предсказанную величину), гиалуронидаза (применяется в качестве адъюванта для повышения абсорбции и диспергирования инъецированных лекарственных средств, прежде всего анестезирующих средств при глазной хирургии и определенных визуализирующих агентов), папаин (санация некротической ткани или разжижение отторгающихся некротических масс при острых и хронических повреждениях, таких как пролежни, варикозные и диабетические язвы, ожоги, послеоперационные раны, пилонидальные кистозные раны, карбункулы и другие раны), L-аспарагиназа (острый лимфоцитарный лейкоз, требующий экзогенного аспарагина для пролиферации), пэг-аспарагиназа (острый лимфоцитарный лейкоз, требующий экзогенного аспарагина для пролиферации), расбуриказа (пациенты детского возраста с лейкозом, лимфомой и солидными опухолями, подвергающиеся противораковой терапии, которая может вызывать синдром лизиса опухоли), человеческий хорионный гонадотропин (HCG) (улучшает репродуктивную функцию), человеческий фолликулостимулирующий гормон (FSH) (улучшает репродуктивную функцию), лутропин-альфа (бесплодие, сопровождающееся дефицитом лютениизирующего гормона), пролактин (гипопролактинемия, дефицит сывороточного пролактина, дисфункция яичника у женщин, состояние страха, артериогенная эректильная дисфункция, преждевременное семяизвержение, олигозооспермия, астеноспермия, пониженная функция семенных пузырьков, гипоандрогенизм у мужчин), ингибитор альфа-1-протеиназы (врожденный дефицит антитрипсина), лактаза (газообразование, вздутие, спазмы и диарея вследствие неспособности расщеплять лактозу), панкреатические ферменты (липаза, амилаза, протеиназа) (муковисцидоз, хронический панкреатит, панкреатическая недостаточность, состояние после операции желудочного шунтирования по Билльрот типа II (Billroth II), обструкция протоков поджелудочной железы, стеаторрея, недостаточное пищеварение, газообразование, вздутие), аденозиндеаминаза (бычья пегадемаза, PEG-ADA) (заболевания с серьезным комбинированным иммунодефицитом вследствие дефицита аденозиндеаминазы), абатецепт (ревматоидный артрит (прежде всего, рефракторный в отношении ингибирования TNF-альфа)), алефацепт (бляшковидный псориаз), анакинра (ревматоидный артрит), этанецепт (ревматоидный артрит, многосуставной юношеский ревматоидный артрит, псориатический артрит, анкилоизирующий спондилит, бляшковидный псориаз, анкилоизирующий спондилит), антагонист рецептора интерлейкина-1 (IL-1), анакинра (воспаление и деградация хряща, ассоциированная с ревматоидным артритом), тимулин (нейродегенеративные заболевания, ревматизм, нервная анорексия), антагонист TNF-альфа (аутоиммунные заболевания, такие как ревматоидный артрит, анкилоизирующий спондилит, болезнь Крона, псориаз, гнойный гидраденит, рефрактерная астма), энфувиртид (HIV-1-инфекция) и тимозин α1 (гепатит В и С)
(в скобках указано конкретное заболевание, для лечения которого применяют терапевтический белок).
Следующим объектом настоящего изобретения является вектор, содержащий
а. открытую рамку считывания (ОРС) и/или сайт клонирования, например, предназначенный для встраивания открытой рамки считывания или последовательности, содержащей открытую рамку считывания; и
б. по меньшей мере один элемент 3'-нетранслируемой области (3'-UTR-элемент) и/или по меньшей мере один элемент 5'-нетранслируемой области (5'-UTR-элемент), при этом указанная искусственная нуклеиновая кислота характеризуется высокой эффективностью трансляции.
Как правило, вектор, предлагаемой в настоящем изобретении, может содержать искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, которая описана выше. В частности, предпочтительные варианты осуществления изобретения, указанные выше при описании искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, применимы также и для искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, которая содержится в векторе, предлагаемом в настоящем изобретении. Например, в предлагаемом в изобретении векторе по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент и ОРС представляют собой структуры, указанные выше при описании искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, включая предпочтительные варианты осуществления изобретения. Например, в векторе, предлагаемом в настоящем изобретении, стабильная мРНК, из которой получен по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент предпочтительно может характеризоваться тем, что обеспечивает такое расщепление мРНК, при котором отношение количества указанной мРНК во второй момент времени к количеству указанной мРНК в первый момент времени составляет по меньшей мере 0,5 (50%), по меньшей мере 0,6 (60%), по меньшей мере 0,7 (70%), по меньшей мере 0,75 (75%), по меньшей мере 0,8 (80%), по меньшей мере 0,85 (85%), по меньшей мере 0,9 (90%) или по меньшей мере 0,95 (95%).
Сайт клонирования может представлять собой любую последовательность, пригодную для встраивания открытой рамки считывания или последовательности, содержащей открытую рамку считывания, например, один или несколько сайтов рестрикции. Таким образом, вектор содержит сайт клонирования, предпочтительно пригодный для встраивания открытой рамки считывания в вектор, предпочтительно для встраивания открытой рамки считывания с 3'-стороны относительно 5'-UTR-элемента и/или с 5'-стороны относительно 3'-UTR-элемента. Предпочтительно сайт клонирования или ОРС расположен/расположена с 3'-стороны относительно 5'-UTR-элемента и/или с 5'-стороны относительно 3'-UTR-элемента, предпочтительно в непосредственной близости от 3'-конца 5'-UTR-элемента и/или 5'-конца 3'-UTR-элемента. Например, сайт клонирования или ОРС могут быть непосредственно присоединены к 3'-концу 5'-UTR-элемента и/или к 5'-концу 3'-UTR-элемента, или они могут быть присоединены с помощью нуклеотидного сегмента, например, сегмента, состоящего из 2, 4, 6, 8, 10, 20 и т.д. нуклеотидов, как указано выше при описании искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении.
Предпочтительно вектор, предлагаемой в настоящем изобретении, можно применять для производства искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, предпочтительно производства искусственной мРНК, предлагаемой в настоящем изобретении, например, необязательно путем встраивания открытой рамки считывания или последовательности, содержащей открытую рамку считывания, в вектор и транскрибирования вектора. Так, предпочтительно вектор содержит элементы, необходимые для транскрипции, такие как промотор, например, промотор РНК-полимеразы. Предпочтительно вектор пригоден для транскрипции с использованием эукариотической, прокариотической, вирусной или фаговой систем транскрипции, таких как эукариотические клетки, прокариотические клетки или эукариотические, прокариотические, вирусные или фаговые системы транскрипции in vitro. Так, например, вектор может содержать промоторную последовательность, которая распознается полимеразой, такой как РНК-полимераза, например, эукариотической, прокариотической, вирусной или фаговой РНК-полимеразой. В предпочтительном варианте осуществления изобретения вектор содержит промотор РНК-полимеразы фага, такой как промотор фага SP6, Т3 или Т7, предпочтительно промотор фага Т7. Предпочтительно вектор пригоден для транскрипции in vitro с использованием системы транскрипции in vitro на основе фага, такой как система транскрипции in vitro на основе РНК-полимеразы фага Т7.
В другом предпочтительном варианте осуществления изобретения вектор можно применять непосредственно для экспрессии кодируемого пептида или белка в клетках или ткани. Для этой цели вектор содержит конкретные элементы, необходимые для экспрессии в указанных клетках/ткани, например, конкретные последовательности промотора, такого как промотор CMV.
Вектор может содержать также поли(А)-последовательность и/или сигнал полиаденилирования, описанные выше для искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении.
Вектор может представлять собой РНК-вектор или ДНК-вектор. Предпочтительно вектор представляет собой ДНК-вектор. Вектор может представлять собой любой вектор, известный специалисту в данной области, такой как вирусный вектор или плазмидный вектор. Предпочтительно вектор представляет собой плазмидный вектор, предпочтительно плазмидный ДНК-вектор.
В предпочтительном варианте осуществления изобретения вектор, предлагаемый в настоящем изобретении, содержит искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении.
Предпочтительно ДНК-вектор, предлагаемой в изобретении, содержит нуклеотидную последовательность, идентичную по меньшей мере примерно на 1, 2, 3, 4, 5, 10, 15, 20, 30 или 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99%, наиболее предпочтительно на 100% нуклеотидной последовательности 3'-UTR транскрипта гена, например, нуклеотидных последовательностей, представленных в SEQ ID NO: 152-204.
Предпочтительно ДНК-вектор, предлагаемой в изобретении, содержит нуклеотидную последовательность, идентичную по меньшей мере примерно на 1, 2, 3, 4, 5, 10, 15, 20, 30 или 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99%, наиболее предпочтительно на 100% нуклеотидной последовательности 5'-UTR транскрипта гена, например, нуклеотидных последовательностей, представленных в SEQ ID NO: 1-151.
Предпочтительно ДНК-вектор, предлагаемой в настоящем изобретении, содержит последовательность, выбранную из группы, которая состоит из последовательностей ДНК, соответствующих 5'-UTR-элементам, представленным в SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 137 (в альтернативном варианте SEQ ID NO: 3), SEQ ID NO: 138 (в альтернативном варианте SEQ ID NO: 9), SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 15, SEQ ID NO: 140 (в альтернативном варианте SEQ ID NO: 17), SEQ ID NO: 20, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 143 (в альтернативном варианте SEQ ID NO: 31), SEQ ID NO: 32, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 146 (в альтернативном варианте SEQ ID NO: 52), SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 57, SEQ ID NO: 60, SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 66, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 72, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, SEQ ID NO: 144 (в альтернативном варианте SEQ ID NO: 42), SEQ ID NO: 58, SEQ ID NO: 62; SEQ ID NO: 73, SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 80, SEQ ID NO: 81, SEQ ID NO: 83, SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 89, SEQ ID NO: 90, SEQ ID NO: 91, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 97, SEQ ID NO: 98, SEQ ID NO: 99, SEQ ID NO: 100, SEQ ID NO: 101, SEQ ID NO: 102, SEQ ID NO: 103, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 147 (в альтернативном варианте SEQ ID NO: 109), SEQ ID NO: 148 (в альтернативном варианте SEQ ID NO: 110), SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 149 (в альтернативном варианте SEQ ID NO: 119), SEQ ID NO: 123, SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO: 130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134, SEQ ID NO: 151 (в альтернативном варианте SEQ ID NO: 136), SEQ ID NO: 96, SEQ ID NO: 111, SEQ ID NO: 150 (на основе SEQ ID NO: 120), SEQ ID NO: 121, SEQ ID NO: 124, SEQ ID NO: 125, и 3'-UTR-элементов, представленных в SEQ ID NO: 152, SEQ ID NO: 153, SEQ ID NO: 154, SEQ ID NO: 155, SEQ ID NO: 156, SEQ ID NO: 157, SEQ ID NO: 158, SEQ ID NO: 159, SEQ ID NO: 160, SEQ ID NO: 161, SEQ ID NO: 164, SEQ ID NO: 165, SEQ ID NO: 167, SEQ ID NO: 168, SEQ ID NO: 169, SEQ ID NO: 170, SEQ ID NO: 171, SEQ ID NO: 172, SEQ ID NO: 173; SEQ ID NO: 174, SEQ ID NO: 175, SEQ ID NO: 176, SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 181, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 184, SEQ ID NO: 187, SEQ ID NO: 188, SEQ ID NO: 189, SEQ ID NO: 191, SEQ ID NO: 204 (в альтернативном варианте SEQ ID NO: 192), SEQ ID NO: 193, SEQ ID NO: 194, SEQ ID NO: 195, SEQ ID NO: 196, SEQ ID NO: 197, SEQ ID NO: 198, SEQ ID NO: 199, SEQ ID NO: 200, SEQ ID NO: 201, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 177, или последовательность, идентичную по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%; еще более предпочтительно по меньшей мере примерно на 99% одной из указанных последовательностей, или ее фрагменту, описанному выше, предпочтительно ее функциональному фрагменту.
Предпочтительно РНК-вектор, предлагаемой в настоящем изобретении, содержит последовательность, выбранную из группы, которая состоит из последовательностей, представляющих собой последовательности РНК, соответствующие последовательностям ДНК, указанным выше при описании ДНК-вектора, предлагаемого в настоящем изобретении.
Предпочтительно вектор представляет собой кольцевую молекулу. Предпочтительно вектор представляет собой двухцепочечную молекулу, такую как двухцепочечная молекула ДНК. Такую кольцевую, предпочтительно двухцепочечную молекулу ДНК можно использовать в качестве удобной формы хранения предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты. Кроме того, ее можно применять для трансфекции клеток, например, культивируемых клеток. Ее можно использовать также для транскрипции in vitro для получения искусственной молекулы РНК, предлагаемой в изобретении.
Предпочтительно вектор, предпочтительно кольцевой вектор, можно линеаризовать, например, путем расщепления рестриктазой. В предпочтительном варианте осуществления изобретения вектор содержит сайт расщепления, такой как сайт рестрикции, предпочтительно уникальный сайт расщепления, непосредственно примыкающий с 3'-стороны к ОРС, или непосредственно примыкающий с 3'-стороны к 3'-UTR-элементу, если он присутствует, или расположенный с 3'-стороны относительно поли(А)-последовательности или сигнала полиаденилирования, если она/он присутствует, или с 3'-стороны относительно поли(С)-последовательности, если она присутствует, или с 3'-стороны относительно гистоновой структуры типа «стебель-петля», если она присутствует. Так, предпочтительно продукт, полученный в результате линеаризации вектора, заканчивается на 3'-конце 3'-концом ОРС или 3'-концом 3'-UTR-элемента, если он присутствует, или 3'-концом поли(А)-последовательности или сигналом полиаденилирования, если она/он присутствует, или 3'-концом поли(С)-последовательности, если она присутствует. В варианте осуществления изобретения, в котором вектор, предлагаемый в настоящем изобретении, содержит искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, сайт рестрикции, предпочтительно уникальный сайт рестрикции, предпочтительно примыкает непосредственно с 3'-стороны к 3'-концу искусственной молекулы нуклеиновой кислоты.
Следующий объект настоящего изобретения относится к клетке, содержащей искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, или вектор, предлагаемый в настоящем изобретении. Клетка может представлять собой любую клетку, такую как бактериальная клетка, клетка насекомого, клетка растения, клетка позвоночного, например, клетка млекопитающего. Такую клетку можно применять, например, для репликации вектора, предлагаемого в настоящем изобретении, например, в клетке бактерии. Кроме того, клетку можно применять для осуществления транскрипции искусственной молекулы нуклеиновой кислоты или вектора, предлагаемой/предлагаемого в настоящем изобретении, и/или для трансляции открытой рамки считывания искусственной молекулы нуклеиновой кислоты или вектора, предлагаемой/предлагаемого в настоящем изобретении. Например, клетку можно применять для производства рекомбинантного белка.
Клетки, предлагаемые в настоящем изобретении, можно получать, например, с помощью стандартных методов переноса нуклеиновой кислоты, таких как стандартные методы трансфекции, трансдукции или трансформации. Например, искусственную молекулу нуклеиновой кислоты или вектор, предлагаемую/предлагаемый в настоящем изобретении, можно переносить в клетку путем электропорации, липофекции, например, с использованием катионных липидов и/или липосом, осаждения фосфатом кальция, трансфекции на основе наночастиц, трансфекции, основанной на применении вирусов или на основе катионных полимеров, таких как DEAE-декстран или полиэтиленимин и т.д.
Предпочтительно клетка представляет собой клетку млекопитающего, такую как клетка человека, домашнего животного, лабораторного животного, такую как клетка мыши или крысы. Предпочтительно клетка представляет собой человеческую клетку. Клетка может представлять собой клетку широко применяемой клеточной линии, такой как СНО, BHK, 293Т, COS-7, HELA, HEK и т.д. или клетка может представлять собой первичную клетку, такую как человеческая кожная фибробластная (HDF) клетка и т.д., предпочтительно клетку, выделенную из организма. В предпочтительном варианте осуществления изобретения клетка представляет собой выделенную клетку млекопитающего, предпочтительно человека. Например, клетка может представлять собой иммунную клетку, такую как дендритная клетка, раковую или опухолевую клетку, или любую соматическую клетку и т.д., предпочтительно млекопитающего, предпочтительно человека.
Следующим объектом настоящего изобретения является фармацевтическая композиция, содержащая искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, или клетку, предлагаемую в настоящем изобретении. Фармацевтическую композицию, предлагаемую в изобретении, можно применять, например, в качестве вакцины, например, для генетической вакцинации. Так, ОРС может, например, кодировать антиген, предназначенный для введения пациенту с целью вакцинации. Так, в предпочтительном варианте осуществления изобретения фармацевтическая композиция, предлагаемая в настоящем изобретении, представляет собой вакцину. Кроме того, фармацевтическую композицию, предлагаемую в настоящем изобретении, можно применять, например, для генной терапии.
Предпочтительно фармацевтическая композиция содержит также один или несколько фармацевтически приемлемых наполнителей, разбавителей и/или эксципиентов и/или один или несколько адъювантов. В контексте настоящего изобретения фармацевтически приемлемый наполнитель, как правило, включает жидкую или нежидкую основу предлагаемой в изобретении фармацевтической композиции. В одном из вариантов осуществления изобретения фармацевтическая композиция находится в жидкой форме. В этом случае предпочтительно носитель представляет собой носитель на водной основе, например, может представлять собой свободную от пирогенов воду; изотонический соляной раствор или забуференные (водные) растворы, например, растворы, забуференные фосфатом, цитратом и т.д. Буфер может быть гипертоническим, изотоническим или гипотоническим относительно конкретной референс-среды, т.е. содержание в буфере солей может быть выше, идентичным или ниже их содержания в конкретной референс-среде, при этом предпочтительно можно применять такие концентрации вышеуказанных солей, которые не приводят к повреждению клеток в результате осмоса или других связанных с концентрацией воздействий. Референс-среды могут представлять собой, например, жидкости, применяемые в методах «in vivo», такие как кровь, лимфа, цитозольные жидкости или другие жидкости организма, или, например, жидкости, которые можно использовать в качестве референс-сред в методах «in vitro», такие как обычные буферы или жидкости. Указанные обычные буферы или жидкости известны специалисту в данной области. Наиболее предпочтительной жидкой основой является лактированный раствор Рингера.
В предлагаемой в изобретении фармацевтической композиции можно использовать также один или несколько совместимых твердых или жидких наполнителей или разбавителей или капсулирующих соединений, которые можно применять для введения пациенту. Понятие «совместимые» в контексте настоящего описания означает, что указанные компоненты предлагаемой в изобретении фармацевтической композиции можно смешивать с предлагаемой в изобретении искусственной нуклеиновой кислотой, вектором или клетками, указанными в настоящем описании, таким образом, чтобы не происходило взаимодействия, которое могло бы существенно снижать фармацевтическую эффективность предлагаемой в изобретении фармацевтической композиции в обычных условиях применения.
Фармацевтическая композиция, предлагаемая в настоящем изобретении, может необязательно содержать также один или несколько дополнительных фармацевтически активных компонентов. В данном контексте фармацевтически активный компонент представляет собой соединение, которое обладает терапевтическим действием в отношении лечения, облегчения или предупреждения конкретного показания или заболевания. Такие соединения включают (но, не ограничиваясь только ими) пептиды или белки, нуклеиновые кислоты, (терапевтически активные) низкомолекулярные органические или неорганические соединения (с молекулярной массой менее 5000, предпочтительно менее 1000), сахара, антигены или антитела, терапевтические агенты, уже известные из существующего уровня техники, антигенные клетки, антигенные клеточные фрагменты, клеточные фракции; компоненты клеточной оболочки (например, полисахариды), модифицированные, ослабленные или дезактивированные (например, химическим путем или путем облучения) патогены (вирусы, бактерии и т.д.).
Кроме того, предлагаемая в изобретении фармацевтическая композиция может содержать носитель для искусственной молекулы нуклеиновой кислоты или вектора. Такой носитель может быть пригоден для облегчения растворения в физиологически приемлемых жидкостях, транспортировки и поглощения клеткой фармацевтически активной искусственной молекулы нуклеиновой кислоты или вектора. Следовательно, такой носитель может представлять собой компонент, который может быть пригоден для хранения и доставки искусственной молекулы нуклеиновой кислоты или вектора, предлагаемой/предлагаемого в изобретении. Такие компоненты могут представлять собой, например, катионные или поликатионные носители или соединения, которые могут служить в качестве агентов для трансфекции или комплексообразования.
В предпочтительном варианте осуществления изобретения искусственную молекулу нуклеиновой кислоты или вектор включают в комплекс с одним или несколькими катионными или поликатионными соединениями, предпочтительно с катионными или поликатионными полимерами, катионными или поликатионными пептидами или белками, например, протамином, катионными или поликатионными полисахаридами и/или катионными или поликатионными липидами.
Согласно предпочтительному варианту осуществления изобретения искусственную молекулу нуклеиновой кислоты или вектор можно включать в комплекс с липидами с образованием одной или большего количества липосом, липоплексов или липидных наночастиц. Следовательно, в одном из вариантов осуществления изобретения, предлагаемая в изобретении фармацевтическая композиция содержит липосомы, липоплексы или липидные наночастицы, которые содержат искусственную молекулу нуклеиновой кислоты или вектор, предпочтительно РНК, более предпочтительно мРНК.
Возрастает количество данных о том, что препаративные формы на основе липидов следует рассматривать в качестве одной из наиболее перспективных систем доставки нуклеиновых кислот, прежде всего РНК, благодаря их биосовместимости и простоты крупномасштабного производства. Катионные липиды широко изучены в качестве синтетических материалов для доставки РНК. После перемешивания нуклеиновые кислоты конденсируются катионными липидами с образованием комплексов липид/нуклеиновая кислота, известных как липоплексы. Указанные липидные комплексы могут защищать генетический материал от воздействия нуклеаз и доставляться в клетки путем взаимодействия с отрицательно заряженной клеточной мембраной. Липоплексы можно получать непосредственно путем смешения положительно заряженных липидов при физиологических значениях рН с отрицательно заряженными нуклеиновыми кислотами.
Общепринятые липосомы состоят из липидного бислоя, который может состоять из катионных, анионных или нейтральных (фосфо)липидов и холестерина, который окружает водное ядро. Как липидный бислой, так и водное пространство могут включать гидрофобные или гидрофильные соединения соответственно. Характеристики и поведение липосом in vivo можно модифицировать путем добавления гидрофильного полимерного покрытия, например, из полиэтиленгликоля (ПЭГ), на поверхность липосом для придания стерической стабилизации. Кроме того, липосомы можно применять для специфического таргетинга путем присоединения лигандов (например, антител, пептидов и углеводов) к их поверхности или к концам присоединенных цепей ПЭГ (Front Pharmacol., 6, 1 декабря 2015 г., с. 286).
Липосомы представляют собой коллоидные системы доставки на основе липидов и на основе поверхностно-активных веществ, состоящие из фосфолипидного бислоя, окружающего водный компартмент. Они могут иметь форму сферических пузырьков, и диапазон их размера может составлять от 20 нм до нескольких мкм. Липосомы на основе катионных липидов могут образовывать комплекс с отрицательно заряженными нуклеиновыми кислотами посредством электростатических взаимодействий, что приводит к образованию комплексов, отличающихся биосовместимостью, низкой токсичностью и возможностью их крупномасштабного производства, необходимого для клинических применений in vivo. Липосомы могут сливаться с плазматической мембраной для проникновения; находясь внутри клетки, липосомы подвергаются процессингу посредством эндоцитозного пути и после этого генетический материал высвобождается из эндосомы/носителя в цитоплазму. Липосомы в течение долгого времени рассматриваются в качестве носителей для доставки лекарственных средств благодаря их очень высокой биосовместимости, основанной на том, что липосомы являются в целом аналогами биологических мембран и их можно получать из встречающихся в естественных условиях и синтетических фосфолипидов (Int J Nanomedicine. 9, 2014, сс. 1833-1843).
Катионные липосомы традиционно наиболее широко применяли в качестве невирусных систем доставки для олигонуклеотидов, включая плазмидную ДНК, антисмысловые олигонуклеотиды и siPHK/малую РНК-шпильку (shPHK)). Катионные липиды, такие как DOTAP (1,2-диолеоил-3-триметиламмонийпропан) и DOTMA (метилсульфат N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония) могут образовывать комплексы или липоплексы с отрицательно заряженными нуклеиновыми кислотами с образованием наночастиц посредством электростатического взаимодействия, что обеспечивает высокую эффективность трансфекции in vitro. Кроме того, разработаны нанолипосомы для доставки РНК на основе нейтрального липида, например, нанолипосомы на основе нейтрального 1,2-диолеоил-sn-глицеро-3-фосфатидилхолина (DOPC) (Adv Drug Deliv Rev. 66, февраль 2014 г., сс. 110-116).
Таким образом, в одном из вариантов осуществления изобретения искусственную молекулу нуклеиновой кислоты или вектор, предпочтительно РНК, входящую в фармацевтическую композицию, предлагаемую в настоящем изобретении, включают в комплекс с катионными липидами и/или нейтральными липидами и тем самым образуют липосомы, липидные наночастицы, липоплексы или нанолипосомы на основе нейтральных липидов.
В других вариантах осуществления изобретения наиболее предпочтительными агентами для трансфекции или комплексообразования являются катионные или поликатионные соединения, включая протамин, нуклеолин, спермин или спермидин, или другие катионные пептиды или белки, такие как поли-L-лизин (PLL), полиаргинин, основные полипептиды, обладающие способностью проникать в клетку пептиды (СРР), такие как ВИЧ-связывающие пептиды, Tat ВИЧ-1 (ВИЧ), выведенные из Tat пептиды, пенетратин, полученные из VP22 пептиды или аналоги, VP22 HSV (вирус герпеса простого), MAP, KALA или домены трансдукции белков (PTD), РрТ620, богатые пролином пептиды, богатые аргинином пептиды, богатые лизином пептиды, MPG-пептид(ы), Рер-1, L-олигомеры, пептид(ы) кальцитонина, выведенные из Antennapedia пептиды (прежде всего, выведенные из Drosophila antennapedid), pAntp, pIsl, FGF, лактоферрин, транспортан, буфорин-2, Вас715-24, SynB, SynB(1), pVEC, выведенные из hCT пептиды, SAP или гистоны.
Кроме того, такие катионные или поликатионные соединения могут представлять собой катионные или поликатионные пептиды или белки, которые предпочтительно содержат или дополнительно модифицированы так, чтобы они содержали по меньшей мере одну -SH-группу. Предпочтительно катионный или поликатионный носитель выбирают из катионных пептидов, имеющих следующую общую формулу (I):
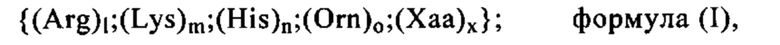
в которой l+m+n+о+х=3-100 и l, m, n или о независимо друг от друга обозначают любое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80, 81-90 и 91-100, при условии, общее содержание Arg (аргинин), Lys (лизин), His (гистидин) и Orn (орнитин) составляет по меньшей мере 10% от общего содержания аминокислот в олигопептиде; а Хаа может обозначать любую аминокислоту, выбранную из нативных (т.е. встречающихся в естественных условиях) или не встречающихся в естественных условиях аминокислот за исключением Arg, Lys, His или Orn; и х может обозначать любое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80, 81-90, при условии, что общее содержание Хаа не превышает 90% от общего содержания аминокислот в олигопептиде. Любую из аминокислот Arg, Lys, His, Orn и Хаа можно помещать в любое положение пептида. В этом контексте наиболее предпочтительными являются катионные пептиды или белки, содержащие 7-30 аминокислот. Предпочтительные катионные пептиды и белки описаны также в международной заявке на патент WO 2009/030481, содержание которой включено в настоящее описание в качестве ссылки.
Кроме того, катионный или поликатионный пептид или белок, определяемый формулой 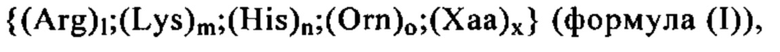 представленной выше, который содержит или дополнительно модифицирован так, что он содержал по меньшей мере одну -SH-группу, можно выбирать (но, не ограничиваясь только этим) из соединений подформулы (Ia):
представленной выше, который содержит или дополнительно модифицирован так, что он содержал по меньшей мере одну -SH-группу, можно выбирать (но, не ограничиваясь только этим) из соединений подформулы (Ia):
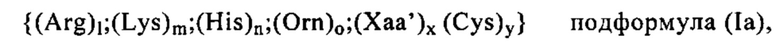
в которой (Arg)1; (Lys)m; (His)n; (Orn)o; и х имеют указанные выше значения, Хаа' обозначает любую аминокислоту, выбранную из нативных (т.е. встречающихся в естественных условиях) или не встречающихся в естественных условиях аминокислот за исключением Arg, Lys, His, Orn или Cys, и у обозначает любое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21-30, 31-40, 41-50, 51-60, 61-70, 71-80 и 81-90, при условии, что общее содержание Arg (аргинин), Lys (лизин), His (гистидин) и Orn (оринитин) составляет по меньшей мере 10% от общего содержания аминокислот в олигопептиде. Кроме того, катионный или поликатионный пептид можно выбирать из соединений подформулы (Iб):
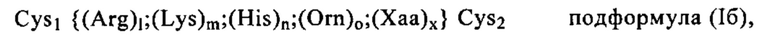
в которой эмпирическая формула 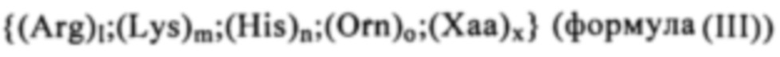 представлена в настоящем описании и образует ядро аминокислотной последовательности, представленной (полуэмпирической) формулой (III), и в которой Cys1 и Cys2 обозначают остатки цистеина, расположенные проксимально или терминально относительно (Arg)1;(Lys)m;(His)n;(Orn)o;(Xaa)x. В этом контексте содержание WO 2011/026641 включено в настоящее описание в качестве ссылки.
представлена в настоящем описании и образует ядро аминокислотной последовательности, представленной (полуэмпирической) формулой (III), и в которой Cys1 и Cys2 обозначают остатки цистеина, расположенные проксимально или терминально относительно (Arg)1;(Lys)m;(His)n;(Orn)o;(Xaa)x. В этом контексте содержание WO 2011/026641 включено в настоящее описание в качестве ссылки.
Другие предпочтительные катионные или поликатионные соединения, которые можно применять в качестве агентов для трансфекции, могут представлять собой катионные полисахариды, например, хитозан, полибрен, катионные полимеры, например, полиэтиленимин (PEI), катионные липиды, например, DOTMA: хлорид [1-(2,3-сиолеилокси)пропил)]-N,N,N-триметиламмония, DMRIE, ди-С14-амидин, DOTIM, SAINT, DC-Chol, BGTC, СТАР, DOPC, DODAP, DOPE: диолеилфосфатидилэтаноламин, DOSPA, DODAB, DOIC, DMEPC, DOGS: диоктадециламидоглицилспермин, DIMRI: бромид димиристооксипропилдиметилгидроксиэтиламмония, DOTAP: диолеоилокси-3-(триметиламмонио)пропан, DC-6-14: хлорид O,O-дитетрадеканоил-N-(α-триметиламмониоацетил)диэтаноламина, CLIP1: хлорид рац-[(2,3-диоктадецилоксипропил)(2-гидроксиэтил)]диметиламмония, CLIP6: рац-[2(2,3-дигексадецилоксипропилоксиметилокси)этил]триметиламмоний, CLIP9: рац-[2(2,3-дигексадецилоксипропилоксисукцинилокси)этил]триметиламмоний, олигофектамин, или катионные или поликатионные полимеры, например, модифицированные полиаминокислоты, такие как полимеры β-аминокислот, или обратимые полиамиды и т.д., модифицированные полиэтилены, такие как PVP (бромид поли(N-этил-4-винилпиридиния)) и т.д. модифицированные акрилаты, такие как pDMAEMA (поли(диметиламиноэтилметилакрилат)) и т.д., модифицированные амидоамины, такие как рАМАМ (поли(амидоамин)) и т.д., модифицированный сложный полибетааминоэфир (РВАЕ), например, с модифицированным диаминовым концом сополимеры 1,4-бутандиолдиакрилата и 5-амино-1-пентанола, и т.д. дендримеры, например, дендримеры полипропиламина или дендримеры на основе рАМАМ, и т.д. полиимин(ы), например, PEI: поли(этиленимин), поли(пропиленимин) и т.д., полиаллиламин, полимеры на основе сахарного каркаса, такие как полимеры на основе циклодекстрина, полимеры на основе декстрана, хитозан и т.д. полимеры на основе силанового каркаса, например, сополимеры PMOXA-PDMS и т.д., блок-сополимеры, состоящие из комбинации одного или несколько катионных блоков (например, выбранных из катионного полимера, указанного выше) и одного или нескольких гидрофильных или гидрофобных блоков (например, полиэтиленгликоль); и т.д.
Согласно другому варианту осуществления изобретения фармацевтическая композиция, предлагаемая в изобретении, может содержать адъювант для повышения иммуностимулирующих свойств фармацевтической композиции. В данном контексте под адъювантом можно понимать любое соединение, которое пригодно для облегчения введения и доставки компонентов, таких как искусственная молекула нуклеиновой кислоты или вектор, которая/который содержится в фармацевтической композиции, предлагаемой в изобретении. Кроме того, такой адъювант может (но, не ограничиваясь только этим) инициировать или усиливать иммунный ответ врожденной иммунной системы, т.е. неспецифический иммунный ответ. Иными словами, после введения фармацевтическая композиция, предлагаемая в изобретении, как правило, инициирует адаптивный иммунный ответ, направленный на антиген, кодируемый искусственной молекулой нуклеиновой кислоты. Кроме того, фармацевтическая композиция, предлагаемая в изобретении, может вызывать (поддерживающий) врожденный иммунный ответ благодаря добавлению адъюванта, указанного в настоящем описании, к фармацевтической композиции, предлагаемой в изобретении.
Такой адъювант можно выбирать из любого адъюванта, известного специалисту в данной области и пригодного для рассматриваемого случая, т.е. для поддержания индукции иммунного ответа у млекопитающего. Предпочтительно адъювант можно выбирать из группы, включающей (но, не ограничиваясь только ими) TDM, MDP, мурамилдипептид, плюроники, раствор квасцов, гидроксид алюминия, ADJUMER™ (полифосфазен); гель фосфата алюминия; глюканы, выделенные из водорослей; алгаммулин; гель гидроксида алюминия (квасцы); высокоадсорбирующий белки гель гидроксида алюминия; обладающий низкой вязкостью гель гидроксида алюминия; AF или SPT (эмульсия, содержащая сквалан (5%), Твин 80 (0.2%), плюроник L121 (1,25%), забуференный фосфатом физиологический раствор, рН 7,4); AVRIDINE™ (пропандиамин); BAY R1005™ ((N-(2-дезокси-2-L-леуциламиноб-D-глюкопиранозил)-N-октадециламида гидроацетат); CALCITRIOL™ (1-альфа,25-дигидрокси-витамин D3); гель фосфата кальция; САР™ (наночастицы фосфата кальция); холерный голотоксин, слитый белок холерный токсин-A1-белок-А-D-фрагмент, субъединица В холерного токсина; CRL 1005 (блок-сополимер Р1205); содержащие цитокин липосомы; DDA (диметилдиоктадециламмония бромид); DHEA (дегидроэпиандростерон); DMPC (димиристоилфосфатидилхолин); DMPG (димиристоилфосфатидилглицерин); комплекс DOC/квасцы (натриевая соль дезоксихолиновой кислоты); полный адъювант Фрейнда; неполный адъювант Фрейнда; инулин-гамма; адъювант Гербу (смесь, содержащая: I) N-ацетилглюкозаминил-(Р1-4)-N-ацетилмурамоил-L-аланил-D35 глутамин (GMDP), II) диметилдиоктадециламмония хлорид (DDA), III) комплекс цинк-соль L-пролина (ZnPro-8); GM-CSF); GMDP (N-ацетилглюкозаминил-(b1-4)-N-ацетилмурамил-L47 аланил-D-изоглутамин); имиквимод (1-(2-метилпропил)-1Н-имидазо[4,5-с]хинолин-4-амин); ImmTher™ (N-ацетилглюкозаминил-N-ацетилмурамил-L-Ala-D-изоGlu-L-Ala-глицерина дипальмитат); DRV (иммунолипосомы, приготовленные из везикул, полученных методом гидратации-регидратации); интерферон-гамма; интерлейкин-1бета; интерлейкин-2; интерлейкин-7; интерлейкин-12; ISCOMSTM; ISCOPREP 7.0.3. ТМ; липосомы; LOXORIBINE™ (7-аллил-8-оксогуанозин); оральный адъювант LT 5 (лабильный энтеротоксин-протоксин из E. coli); микросферы и микрочастицы любого состава; MF59TM; (водная эмульсия сквалена); MONTANIDE ISA 51™ (очищенный неполный адъювант Фрейнда); MONTANIDE ISA 720™ (метаболизируемый масляный адъювант); MPL™ (3-Q-дезацил-4'-монофосфорил-липид А); липосомы МТР-РЕ и МТР-РЕ (N-ацетил-L-аланил-D-изоглутаминил-L-аланин-2-(1,2-дипальмитоил-sn-глицеро-3-(гидроксифосфорилокси))этиламид, однонатриевая соль); MURAMETIDE™ (Nac-Mur-L-Ala-D-Gln-OCH3); MURAPALMITINE™ и DMURAPALMITINE™ (Nac-Mur-L-Thr-D-изоGIn-sn-глицериндипальмитоил); NAGO (нейраминидаза-галактозооксидаза); наносферы или наночастицы любого состава; NISV (везикулы из неионогенного поверхностно-активного вещества); PLEURAN™ (β-глюкан); PLGA, PGA и PLA (гомо- и сополимеры молочной кислоты и гликолевой кислоты; микросферы/наносферы); ПЛЮРОНИК L121™; РММА (полиметилметакрилат); PODDS™ (протеноидные микросферы); полиэтиленкарбаматные производные; поли-rА:поли-rU (комплекс полиадениловая кислота-полиуридиновая кислота); полисорбат 80 (Твин 80); белковые кохлеаты (фирма Avanti Polar Lipids, Inc., Алабастер, шт. Алабама); STIMULON™ (QS-21); Quil-A (сапонин Quil-A); S-28463 (4-аминоотекдиметил-2-этоксиметил-1Н-имидазо[4,5-с]хинолин-1-этанол); SAF-1™ («композиция адъювантов фирмы Syntex»); протеолипосомы вируса Сендаи и липидные матрицы, содержащие вирус Сендаи; Спан-85 (сорбитантриолеат); Specol (эмульсия Marcol 52, Спан 85 и Твин 85); сквален или Robane® (2,6,10,15,19,23-гексаметилтетракозан и 2,6,10,15,19,23-гексаметил-2,6,10,14,18,22-тетракозагексан); стеарилтирозин (октадецилтирозина гидрохлорид); Theramid® (М-ацетилглюкозаминил-N-ацетилмурамил-L-Ala-D-isoGlu-L-Ala-дипальмитоксипропиламид); Theronyl-MDP (Termurtide™ или [thr 1]-MDP; N-ацетилмурамил-L-треонил-D-изоглутамин); Ту-частицы (Ту-ВПЧ или вирусоподобные частицы); липосомы Уолтера-Рида (липосомы, содержащие липид А, адсорбированный на гидроксиде алюминия) и липопептиды, включая Pam3Cys, прежде всего соли алюминия, такие как адъю-фос (Adju-phos), алгидрогель, регидрагель и т.д., эмульсии, такие как CFA, SAF, IFA, MF59, провакс, TiterMax, монтанид, ваксфектин и т.д., сополимеры, такие как оптивакс (Optivax, CRL1005), L121, полоксамер 4010) и т.д., липосомы, такие как «липосомы-невидимки (Stealth)» и т.д., кохлеаты, такие как BIORAL, и т.д., адъюванты растительного происхождения, такие как QS21, Quil A, Iscomatrix, ISCOM; адъюванты, пригодные для костимуляции, включая томатин, биополимеры, такие как PLG, РММ, инулин и т.д., адъюванты микробного происхождения, такие как ромуртид, DETOX, MPL, CWS, манноза, нуклеотидные последовательности CpG, CpG7909, лиганды человеческого TLR 1-13, ISS-1018, 35 IC31, имидазохинолины, амплиген, Ribi529, IMOxine, IRIV, ВПЧ, холерный токсин, термолабильный токсин, Pam3Cys, флагеллин, GPI (гликозилфосфатидилинозитол)-якорь, LNFPIII/Lewis X, противомикробные пептиды, UC-1V150, слитый белок RSV, cdiGMP; и адъюванты, пригодные в качестве антагонистов, включая нейропептид CGRP.
Пригодные адъюванты можно выбирать также из катионных или поликатионных соединений, при этом адъювант предпочтительно получают путем образования комплекса, включающего искусственную молекулу нуклеиновой кислоты или вектор, входящую/входящий в фармацевтическую композицию, и катионное или поликатионное соединение. Ассоциация или образование комплекса, включающего искусственную молекулу нуклеиновой кислоты или вектор входящую/входящий в фармацевтическую композицию, и катионные или поликатионные соединения, указанные в настоящем описании, предпочтительно обеспечивает присущие адъюванту свойства и оказывает стабилизирующее действие на искусственную молекулу нуклеиновой кислоты или вектор, входящую/входящий в фармацевтическую композицию. Наиболее предпочтительно такие катионные или поликатионные соединения выбирают из катионных или поликатионных пептидов или белков, включая протамин, нуклеолин, спермин или спермидин, или другие катионные пептиды или белки, такие как поли-L-лизин (PLL), полиаргинин, основные полипептиды, обладающие способностью проникать в клетку пептиды (СРР), такие как ВИЧ-связывающие пептиды, Tat ВИЧ-1 (ВИЧ), выведенные из Tat пептиды, пенетратин, полученные из VP22 пептиды или аналоги, VP22 HSV (вирус герпеса простого), MAP, KALA или домены трансдукции белков (PTD), РрТ620, богатые пролином пептиды, богатые аргинином пептиды, богатые лизином пептиды, MPG-пептид(ы), Рер-1, L-олигомеры, пептид(ы) кальцитонина, выведенные из Antennapedia пептиды (прежде всего, выведенные из Drosophila antennapedia), pAntp, pIsl, FGF, лактоферрин, транспортан, буфорин-2, Вас715-24, SynB, SynB(1), pVEC, выведенные из hCT пептиды, SAP или гистоны. Другими предпочтительными катионными или поликатионными соединениями могут являться катионные полисахариды, например хитозан, полибрен, катионные полимеры, например, полиэтиленимин (PEI), катионные липиды, например, DOTMA: хлорид [1-(2,3-сиолеилокси)пропил)]-N,N,N-триметиламмония, DMRIE, ди-С14-амидин, DOTIM, SAINT, DC-Chol, BGTC, СТАР, DOPC, DODAP, DOPE: диолеилфосфатидилэтаноламин, DOSPA, DODAB, DOIC, DMEPC, DOGS: диоктадециламидоглицилспермин, DIMRI: бромид димиристооксипропилдиметилгидроксиэтиламмония, DOTAP: диолеоилокси-3-(триметиламмонио)пропан, DC-6-14: хлорид O,O-дитетрадеканоил-N-(α-триметиламмониоацетил)диэтаноламина, CLIP1: хлорид рац-[(2,3-диоктадецилоксипропил)(2-гидроксиэтил)]диметиламмония, CLIP6: рац-[2(2,3-дигексадецилоксипропилоксиметилокси)этил]триметиламмоний, CLIP9: рац-[2(2,3-дигексадецилоксипропилоксисукцинилокси)этил]триметиламмоний, олигофектамин, или катионные или поликатионные полимеры, например, модифицированные полиаминокислоты, такие как полимеры β-аминокислот, или обратимые полиамиды и т.д., модифицированные полиэтилены, такие как PVP (бромид поли(N-этил-4-винилпиридиния)) и т.д. модифицированные акрилаты, такие как pDMAEMA (поли(диметиламиноэтилметилакрилат)) и т.д., модифицированные амидоамины, такие как рАМАМ (поли(амидоамин)) и т.д., модифицированный сложный полибетааминоэфир (РВАЕ), например, с модифицированным диаминовым концом сополимеры 1,4-бутандиолдиакрилата и 5-амино-1-пентанола, и т.д. дендримеры, например, дендримеры полипропиламина или дендримеры на основе рАМАМ, и т.д. полиимин(ы), например, PEI: поли(этиленимин), поли(пропиленимин) и т.д., полиаллиламин, полимеры на основе сахарного каркаса, такие как полимеры на основе циклодекстрина, полимеры на основе декстрана, хитозан и т.д. полимеры на основе силанового каркаса, например, сополимеры PMOXA-PDMS и т.д., блок-сополимеры, состоящие из комбинации одного или несколько катионных блоков (например, выбранных из катионного полимера, указанного выше) и одного или нескольких гидрофильных или гидрофобных блоков (например, полиэтиленгликоль); и т.д.
Кроме того, предпочтительные катионные или поликатионные белки или пептиды, которые можно применять в качестве адъюванта путем образования комплекса с искусственной молекулой нуклеиновой кислоты или вектором, предпочтительно РНК, включенной/включенным в композицию, можно выбирать из представленных ниже белков или пептидов, имеющих следующую общую формулу (I): (Arg)1;(Lys)m;(His)n;(Orn)o;(Xaa)x, в которой l+m+n+о+х=8-15 и l, m, n или о независимо друг от друга могут обозначать любое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15, при условии, что общее содержание Arg, Lys, His и Orn составляет по меньшей мере 50% от общего содержания аминокислот в олигопептиде; и Хаа может обозначать любую аминокислоту, выбранную из нативных (т.е. встречающихся в естественных условиях) или ненативных аминокислот за исключением Arg, Lys, His или Orn; и х может обозначать любое число, выбранное из 0, 1, 2, 3 или 4, при условии, что общее содержание Хаа не должно превышать 50% от всех аминокислот в олигопептиде. Наиболее предпочтительными олигоаргининами в данном контексте являются, например, Arg7, Arg8, Arg9, Arg7, H3R9, R9H3, H3R9H3, YSSR9SSY, (RKH)4, Y(RKH)2R и т.д.
Соотношение между искусственной нуклеиновой кислотой или вектором и катионным или поликатионным соединением можно рассчитывать на основе отношения содержания азота к содержанию фосфата (N/P-отношение) во всем включающем нуклеиновую кислоту комплексе. Например, 1 мкг РНК, как правило, содержит примерно 3 нмоля остатков фосфата, при условии, что для РНК характерно статистическое распределение оснований. Кроме того, 1 мл пептида, как правило, содержит примерно х нмолей остатков азота в зависимости от молекулярной массы и количества основных аминокислот. Если в качестве примера сделать расчет для (Arg)9 (молекулярная масса 1424 г/моль, 9 атомов азота), то 1 мкг (Arg)9 содержит примерно 700 пмолей (Arg)9 и, следовательно, 700×9=6300 пмолей основных аминокислот, т.е. 6,3 нмолей атомов азота. Можно рассчитать, что для массового соотношения PHK/(Arg)9, составляющего примерно 1:1, отношение N/P должно составлять примерно 2. Если в качестве примера сделать расчет для протамина (молекулярная масса примерно 4250 г/моль, 21 атом азота, если применяют протамин из лосося) при массовом соотношении, составляющем примерно 2:1, то для 2 мкг РНК дает 6 нмолей фосфата; 1 мкг протамина содержит примерно 235 пмолей молекул протамина и, следовательно, 235×21=4935 пмолей основных атомов азота, т.е. 4,9 нмолей атомов азота. Можно рассчитать, что для массового соотношения РНК/протамин, составляющего примерно 2:1, отношение N/P должно составлять примерно 0,81. Можно рассчитать, что для массового соотношения РНК/протамин, составляющего примерно 8:1, отношение N/P должно составлять примерно 0,2. В контексте настоящего изобретения касательно соотношения нуклеиновая кислота:пептид в комплексе N/P-отношение предпочтительно находится примерно в пределах 0,1-10, предпочтительно примерно в пределах 0,3-4, и наиболее предпочтительно примерно в пределах 0,5-2 или 0,7-2, и наиболее предпочтительно примерно в пределах 0,7-1,5.
В заявке на патент WO 2010/037539, содержание которой включено в настоящее описание в качестве ссылки, описана иммуностимулирующая композиция и методы получения иммуностимулирующей композиции. Так, в предпочтительном варианте осуществления изобретения композицию получают, осуществляя две отдельные стадии для достижения и эффективного иммуностимулирующего действия, и эффективной трансляции искусственной молекулы нуклеиновой кислоты, предлагаемой в изобретении. Для этого на первой стадии получают так называемый «адъювантный компонент» путем образования комплекса, включающего искусственную молекулу нуклеиновой кислоты или вектор, предпочтительно РНК, входящую в адъювантный компонент, и катионное или поликатионное соединение в конкретном соотношении для формирования стабильного комплекса. В этом контексте важно, чтобы в адъювантном компоненте отсутствовало или сохранялось лишь в ничтожно малых количествах свободное катионное или поликатионное соединение после образования комплекса с нуклеиновой кислотой. Таким образом, соотношение между нуклеиновой кислотой и катионным или поликатионным соединением в адъювантном компоненте, как правило, выбирают в таком диапазоне, чтобы нуклеиновая кислота была полностью включена в комплекс и отсутствовало или сохранялось лишь в ничтожно малых количествах свободное катионное или поликатионное соединение. Предпочтительно соотношение в адъювантном компоненте, т.е. соотношение между мРНК и катионным или поликатионным соединением, выбирают из диапазона, составляющего от примерно 6:1 (мас./мас.) до примерно 0,25:1 (мас./мас.), более предпочтительно от примерно 5:1 (мас./мас.) до примерно 0,5:1 (мас./мас.), еще более предпочтительно от примерно 4:1 (мас./мас.) до примерно 1:1 (мас./мас.) или от примерно 3:1 (мас./мас.) до примерно 1:1 (мас./мас.) и наиболее предпочтительно от примерно 3:1 (мас./мас.) до примерно 2:1 (мас./мас).
Согласно предпочтительному варианту осуществления изобретения искусственную молекулу нуклеиновой кислоты или вектор, предпочтительно молекулу РНК, предлагаемую/предлагаемый в изобретении, добавляют на второй стадии к входящей в комплекс молекуле нуклеиновой кислоты, предпочтительно РНК, адъювантного компонента для получения (иммуностимулирующей) композиции, предлагаемой в изобретении. При этом искусственную молекулу нуклеиновой кислоты или вектор, предпочтительно молекулу РНК, предлагаемые в изобретении, добавляют в виде свободной нуклеиновой кислоты, т.е. нуклеиновой кислоты, которая не входит в комплекс с другими соединениями. Перед добавлением свободную искусственную молекулу нуклеиновой кислоты или вектор не включают в комплекс и предпочтительно после добавления адъювантного компонента она/он не должна/должен подвергаться какой-либо поддающейся обнаружению или значимой реакции комплексообразования.
Приемлемые адъюванты можно выбирать также из нуклеиновых кислот, имеющих формулу (II): GlXmGn, в которой: G обозначает гуанозин (гуанин), уридин (урацил) или аналог гуанозина (гуанина) или уридина (урацила); X обозначает гуанозин (гуанин), уридин (урацил), аденозин (аденин), тимидин (тимин), цитидин (цитозин) или аналог вышеуказанных нуклеотидов (нуклеозидов); l обозначает целое число от 1 до 40, при этом, когда l=1, то G представляет собой гуанозин или его аналог, когда l>1, то по меньшей мере 50% нуклеотидов представляют собой гуанозин (гуанин) или его аналог; m обозначает целое число и обозначает по меньшей мере 3; при этом, когда m=3, то X представляет собой уридин (урацил) или его аналог, когда m>3, то по присутствуют меньшей мере 3 последовательно расположенных уридинов (урацилов) или аналогов уридина (урацила); n обозначает целое число от 1 до 40, при этом, когда n=1, то G представляет собой гуанозин (гуанин) или его аналог, когда n>1, то по меньшей мере 50% нуклеотидов (нуклеозидов) представляет собой гуанозин (гуанин) или его аналог.
Другие приемлемые адъюванты можно выбирать также из нуклеиновых кислот, имеющих формулу (III): ClXmCn, в которой: С обозначает цитидин (цитозин), уридин (урацил) или аналог цитидинва (цитозина) или уридина (урацила); X обозначает гуанозин (гуанин), уридин (урацил), аденозин (аденин), тимидин (тимин), цитидин (цитозин) или аналог вышеуказанных нуклеотидов (нуклеозидов); l обозначает целое число от 1 до 40, при этом, когда l=1, то С представляет собой цитидин (цитозин) или его аналог, когда l>1, то по меньшей мере 50% нуклеотидов (нуклеозидов) представляют собой цитидин (цитозин) или его аналог; m обозначает целое число и обозначает по меньшей мере 3; когда m=3, X представляет собой уридин (урацил) или его аналог, когда m>3, то присутствуют по меньшей мере 3 последовательно расположенных уридина (урацила) или аналогов уридина (урацила); n обозначает целое число от 1 до 40, при этом, когда n=1, то С представляет собой цитидин (цитозин) или его аналог, когда n>1, то по меньшей мере 50% нуклеотидов (нуклеозидов) представляют собой цитидин (цитозин) или его аналог.
Предлагаемая в настоящем изобретении фармацевтическая композиция предпочтительно содержит в «безопасном и эффективном количестве» компоненты фармацевтической композиции, прежде всего предлагаемую в изобретении искусственную молекулу нуклеиновой кислоты, вектор и/или клетки, представленные в настоящем описании. В контексте настоящего описания понятие «безопасное и эффективное количество» обозначает количество, достаточное для значимой индукции положительной модификации заболевания или нарушения, указанного в настоящем описании. Однако в то же время «безопасное и эффективное количество» должно быть таким, чтобы избегать серьезных побочных действий и обеспечивать разумное соотношение между преимуществом и риском. Определение этих пределов, как правило, находится в компетенции осуществляющего лечение врача.
Следующим объектом настоящего изобретения является искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетка, предлагаемая в настоящем изобретении, или фармацевтическая композиция, предлагаемая в настоящем изобретении, предназначенные для применения в качестве лекарственного средства, например, в качестве вакцины (для генетической вакцинации), или в генной терапии.
Искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетка, предлагаемая в настоящем изобретении, или фармацевтическая композиция, предлагаемая в настоящем изобретении, наиболее пригодны для любого медицинского применения, в котором используется терапевтическое действие или эффект пептидов, полипептидов или белков, или в котором требуется добавление конкретного пептида или белка. Таким образом, в настоящем изобретении предложены искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетка, предлагаемая в настоящем изобретении, или фармацевтическая композиция, предлагаемая в настоящем изобретении, предназначенные для применения при лечении или предупреждении заболеваний или нарушений, поддающихся лечению посредством терапевтического действия или эффекта пептидов, полипептидов или белков, или поддающихся лечению путем добавления конкретного пептида, полипептида или белка. Например, искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетку, предлагаемую в настоящем изобретении, или фармацевтическую композицию, предлагаемую в настоящем изобретении, можно применять для лечения или предупреждения генетических заболеваний, аутоиммунных заболеваний, раковых или связанных с опухолью заболеваний, инфекционных заболеваний, хронических заболеваний или т.п., например, путем генетической вакцинации или генной терапии.
В частности, такие терапевтические обработки, польза от которых определяется увеличенным количеством и пролонгированным присутствием терапевтических пептидов, полипептидов или белков в организме индивидуума, подлежащего лечению, являются наиболее пригодными в качестве медицинского подхода в контексте настоящего изобретения, поскольку предлагаемый в изобретении 3'-UTR-элемент обеспечивает стабильную и пролонгированную экспрессию пептида или белка, кодируемого предлагаемой в изобретении искусственной молекулой нуклеиновой кислоты или предлагаемым в изобретении вектором, и/или предлагаемый в изобретении 5'-UTR-элемент обеспечивает повышенную экспрессию пептида или белка, кодируемого предлагаемой в изобретении искусственной молекулой нуклеиновой кислоты или предлагаемым в изобретении вектором. Так, наиболее пригодным медицинским применением искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, вектора, предлагаемого в настоящем изобретении, клетки, предлагаемой в настоящем изобретении, или фармацевтической композиции, предлагаемой в настоящем изобретении, является вакцинация. Таким образом, в настоящем изобретении предложены искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетка, предлагаемая в настоящем изобретении, или фармацевтическая композиция, предлагаемая в настоящем изобретении, для вакцинации индивидуума, предпочтительно млекопитающего, более предпочтительно человека. Предпочтительными видами вакцинации являются вакцинация против инфекционных заболеваний, таких как бактериальные, протозойные или вирусные инфекции, и противоопухолевая вакцинация. Такие виды вакцинации можно осуществлять в профилактических или терапевтических целях.
Можно выбирать ОРС в зависимости от заболевания, подлежащего лечению. Например, открытая рамка считывания может кодировать белок, который требуется поставлять в организм пациента, страдающего от полной потери или по меньшей мере от частичной потери функции белка, например, в организм пациента, страдающего генетическим заболеванием. Кроме того, открытую рамку считывания можно выбирать из ОРС, кодирующих пептид или белок, который оказывает благоприятное действие на заболевание или состояние пациента. Кроме того, открытая рамка считывания может кодировать пептид или белок, который осуществляет понижающую регуляцию патологического сверхпроизводства встречающегося в естественных условиях пептида или белка или элиминацию клеток, патологически экспрессирующих белок или пептид. Такое отсутствие, потеря функции или сверхпроизводство могут иметь место, например, в случае опухоли и неоплазии, при аутоиммунных заболеваниях, аллергиях, инфекциях, хронических заболеваниях или т.п. Кроме того, открытая рамка считывания может кодировать антиген или иммуноген, например, эпитоп патогена или опухолевого антигена. Так, в предпочтительных вариантах осуществления изобретения искусственная молекула нуклеиновой кислоты или вектор, предлагаемая/предлагаемый в настоящем изобретении, содержит ОРС, кодирующую аминокислотную последовательность, содержащую или состоящую из последовательности антигена или иммуногена, например, эпитопа патогена или опухоль-ассоциированного антигена, 3'-UTR-элемент, указанный выше, и/или 5'-UTR-элемент, указанный выше, и необязательно дополнительные компоненты, такие как поли(А)-последовательность и т.п.
В контексте медицинского применения, прежде всего в контексте вакцинации, предпочтительно, чтобы искусственная молекула нуклеиновой кислоты, предлагаемая в настоящем изобретении, представляла собой РНК, предпочтительно мРНК, поскольку ДНК несет риск вызывания иммунного анти-ДНК-ответа и имеет тенденцию к встраиванию в геномную ДНК. Однако в некоторых вариантах осуществления изобретения, например, когда применяют вирусный носитель для доставки, такой как аденовирусный носитель для доставки, для доставки искусственной молекулы нуклеиновой кислоты или вектора, предлагаемой/предлагаемого в настоящем изобретении, например, в контексте различных видов генного терапии, может оказаться желательным, чтобы искусственная молекула нуклеиновой кислоты или вектор представляла/представлял собой молекулу ДНК.
Искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетку, предлагаемую в настоящем изобретении, или фармацевтическую композицию, предлагаемую в настоящем изобретении, можно вводить орально, парентерально, путем ингаляции с использованием спрея, местно, ректально, интраназально, трансбуккально, вагинально, с использованием имплантированного резервуара или посредством струйной инъекции. В контексте настоящего описания понятие «парентерально» включает методы подкожной, внутривенной, внутримышечной, внутрисуставной, интрасиновиальной, надчревной, внутриоболочечной, внутрипеченочной, осуществляемой в область повреждения, внутричерепной, чрескожной, внутрикожной, внутрилегочной, внутрибрюшинной, внутрисердечной, внутриартериальной и подъязычной инъекции или инфузии. В предпочтительном варианте осуществления изобретения искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетку, предлагаемую в настоящем изобретении, или фармацевтическую композицию, предлагаемую в настоящем изобретении, вводят посредством безыгольной инъекции (например, струйной инъекции).
Предпочтительно искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетку, предлагаемую в настоящем изобретении, или фармацевтическую композицию, предлагаемую в настоящем изобретении, вводят парентерально, например, путем парентеральной инъекции, более предпочтительно с помощью методов подкожной, внутривенной, внутримышечной, внутрисуставной, интрасиновиальной, надчревной, внутриоболочечной, внутрипеченочной, осуществляемой в область повреждения, внутричерепной, чрескожной, внутрикожной, внутрилегочной, внутрибрюшинной, внутрисердечной, внутриартериальной, подъязычной инъекции или инфузии. Наиболее предпочтительными являются внутрикожная и внутримышечная инъекции. Стерильные инъекционные формы предлагаемой в изобретении фармацевтической композиции могут представлять собой водную или масляную суспензию. Такие суспензии можно приготавливать с помощью методов, известных в данной области, с применением пригодных диспергирующих или смачивающих средств и суспендирующих средств. Предпочтительно, растворы или суспензии вводят посредством безыгольной инъекции (например, струйной инъекции).
Искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетку, предлагаемую в настоящем изобретении, или фармацевтическую композицию, предлагаемую в настоящем изобретении, можно вводить также орально в любой пригодной для орального введения лекарственной форме, включая (но, не ограничиваясь только ими) капсулы, таблетки, водные суспензии или растворы.
Искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетку, предлагаемую в настоящем изобретении, или фармацевтическую композицию, предлагаемую в настоящем изобретении, можно применять также местно, прежде всего в тех случаях, когда мишень для лечения включает области или органы, легкодоступные для местного нанесения, включая, например, заболевания кожи или любой другой доступной эпителиальной ткани. Для каждой из таких областей или органов можно легко приготавливать пригодные для местной обработки композиции. Для местного нанесения искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетку, предлагаемую в настоящем изобретении, или фармацевтическую композицию, предлагаемую в настоящем изобретении, можно приготавливать в виде пригодной мази, суспендированной или растворенной в одном или нескольких носителях.
В одном из вариантов осуществления изобретения применение в качестве лекарственного средства включает стадию трансфекции клеток млекопитающих, предпочтительно трансфекцию in vitro или ex vivo клеток млекопитающих, более предпочтительно трансфекцию in vitro клеток, выделенных из организма пациента, подлежащего лечению лекарственным средством. Если применение в качестве лекарственного средства включает трансфекцию in vitro выделенных клеток, то применение может предусматривать также повторное введение трансфектированных клеток пациенту. Применение предлагаемых в изобретении искусственных молекул нуклеиновой кислоты или вектора в качестве лекарственного средства может включать также стадию отбора успешно трансфектированных выделенных клеток. Таким образом, может оказаться целесообразным, чтобы вектор содержал также маркер для селекции. Применение в качестве лекарственного средства может включать также трансфекцию in vitro выделенных клеток и очистку продукта экспрессии, т.е. кодируемого пептида или белка из указанных клеток. Этот очищенный пептид или белок можно затем вводить индивидууму, нуждающемуся в этом.
В настоящем изобретении предложен также способ лечения или предупреждения заболевания или нарушения, указанного выше, заключающийся в том, что вводят искусственную молекулу нуклеиновой кислоты, предлагаемую в настоящем изобретении, вектор, предлагаемый в настоящем изобретении, клетку, предлагаемую в настоящем изобретении, или фармацевтическую композицию, предлагаемую в настоящем изобретении, индивидууму, нуждающемуся в этом.
Кроме того, предложен способ лечения или предупреждения заболевания или нарушения, заключающийся в том, что осуществляют трансфекцию клетки искусственной молекулой нуклеиновой кислоты, предлагаемой в настоящем изобретении, или вектором, предлагаемым в настоящем изобретении. Указанную трансфекцию можно осуществлять in vitro, ex vivo или in vivo. В предпочтительном варианте осуществления изобретения трансфекцию клетки осуществляют in vitro и трансфектированную клетку вводят индивидууму, нуждающемуся в этом, предпочтительно больному человеку. Предпочтительно клетка, которую требуется трансфектировать in vitro, представляет собой клетку, выделенную из организма индивидуума, предпочтительно больного человека. Таким образом, в настоящем изобретении предложен способ лечения, заключающийся в том, что осуществляют стадии, на которых выделяют клетку из организма индивидуума, предпочтительно из организма больного человека, трансфектируют выделенную клетку искусственной нуклеиновой кислотой, предлагаемой в настоящем изобретении, или вектором, предлагаемым в настоящем изобретении, и вводят трансфектированную клетку индивидууму, предпочтительно больному человеку.
Способ лечения или предупреждения нарушения, предлагаемый в настоящем изобретении, предпочтительно представляет собой способ вакцинации или способ генной терапии, описанный выше.
Как описано выше, предлагаемый в изобретении 3'-UTR-элемент и/или предлагаемый в изобретении 5'-UTR-элемент обладает способностью пролонгировать и/или повышать производство белка с мРНК. Таким образом, следующий объект настоящего изобретения относится к способу повышения и/или пролонгирования производства белка с искусственной молекулы нуклеиновой кислоты, предпочтительно с молекулы мРНК или вектора, где способ включает стадию, на которой осуществляют ассоциацию открытой рамки считывания с 3'-UTR-элементом и/или 5'-UTR-элементом, где 3'-UTR-элемент и/или 5'-UTR-элемент обеспечивает высокую эффективность трансляции полученной искусственной молекулы нуклеиновой кислоты, с получением искусственной молекулы нуклеиновой кислоты, предпочтительно молекулы мРНК, предлагаемой в настоящем изобретении, которая описана выше, или вектора, предлагаемого в настоящем изобретении, который описан выше.
Предпочтительно, в способе повышения и/или пролонгирования производства белка с искусственной молекулы нуклеиновой кислоты, предпочтительно с молекулы мРНК или вектора, предлагаемой/предлагаемого в настоящем изобретении, 3'-UTR-элемент и/или 5'-UTR-элемент содержит или состоит из нуклеотидной последовательности, которая получена из 3'-UTR и/или 5'-UTR транскрипта гена, выбранного из группы, которая состоит из ZNF460, TGM2, IL7R, BGN, TK1, RAB3B, СВХ6, FZD2, COL8A1, NDUFS7, PHGDH, PLK2, TSPO, PTGS1, FBXO32, NID2, ATP5D, EXOSC4, NOL9, UBB4B, VPS18, ORMDL2, FSCN1, ТМЕМ33, TUBA4A, ЕМР3, ТМЕМ201, CRIP2, BRAT1, SERPINH1, CD9, DPYSL2, CDK9, TFRC, PSMB3, FASN, PSMB6, PRSS56, KPNA6, SFT2D2, PARD6B, LPP, SPARC, SCAND1, VASN, SLC26A1, LCLAT1, FBXL18, SLC35F6, RAB3D, MAP1B, VMA21, CYBA, SEZ6L2, PCOLCE, VTN, ALDH16A1, RAVER1, KPNA6, SERINC5, JUP, CPN2, CRIP2, EPT1, PNPO, SSSCA1, POLR2L, LIN7C, UQCR10, PYCRL, AMN, MAP1S, NDUFS7, PHGDH, TSPO, ATP5D, EXOSC4, TUBB4B, TUBA4A, EMP3, CRIP2, BRAT1, CD9, CDK9, PSMB3, PSMB6, PRSS56, SCAND1, AMN, CYBA, PCOLCE, MAP1S, VTN, ALDH16A1 (предпочтительно все человеческие) и Dpysl2, Ccnd1, Acox2, Cbx6, Ubc, Ldlr, Nudt22, Pcyox1l, Ankrd1, Tmem37, Tspyl4, Slc7a3, Cst6, Aacs, Nosip, Itga7, Ccnd2, Ebp, Sf3b5, Fasn, Hmgcs1, Osr1, Lmnb1, Vma21, Kif20a, Cdca8, Slc7a1, Ubqln2, Prps2, Shmt2, Aurkb, Fignl1, Cad, An1n, Slfn9, Ncaph, Pole, Uhrf1, Gja1, Fam64a, Kif2c, Tspan10, Scand1, Gpr84, Fads3, Cers6, Cxcr4, Gprc5c, Fen1, Cspg4, Mrpl34, Comtd1, Armc6, Emr4, Atp5d, 1110001J03Rik, Csf2ra, Aarsd1, Kif22, Cth, Tpgs1, Cel17, Alkbh7, Ms4a8a, Acox2, Ubc, Slpi, Pcyox1l, Igf2bp1, Tmem37, Slc7a3, Cst6, Ebp, Sf3b5, Plk1, Cdca8, Kif22, Cad, Cth, Pole, Kif2c, Scand1, Gpr84, Tpgs1, Cel17, Alkbh7, Ms4a8a, Mrpl34, Comtd1, Armc6, Atp5d, 1110001J03Rik, Nudt22, Aarsd1 (предпочтительно все мышиные); предпочтительно из группы, состоящей из ZNF460-5'-UTR, TGM2-5'-UTR, IL7R-5'-UTR, BGN-5'-UTR, TK1-5'-UTR, RAB3B-5'-UTR, CBX6-5'-UTR, FZD2-5'-UTR, COL8A1-5'-UTR, NDUFS7-5'-UTR, PHGDH-5'-UTR, PLK2-5'-UTR, TSPO-5'-UTR, PTGS1-5'-UTR, FBXO32-5'-UTR, NID2-5'-UTR, ATP5D-5'-UTR, EXOSC4-5'-UTR, NOL9-5'-UTR, UBB4B-5'-UTR, VPS18-5'-UTR, ORMDL2-5'-UTR, FSCN1-5'-UTR, TMEM33-5'-UTR, TUBA4A-5'-UTR, EMP3-5'-UTR, TMEM201-5'-UTR, CRIP2-5'-UTR, BRAT1-5'-UTR, SERPINH1-5'-UTR, CD9-5'-UTR, DPYSL2-5'-UTR, CDK9-5'-UTR, TFRC-5'-UTR, PSMB3-5'-UTR, FASN-5'-UTR, PSMB6-5'-UTR, PRSS56-5'-UTR, KPNA6-5'-UTR, SFT2D2-5'-UTR, PARD6B-5'-UTR, LPP-5'-UTR, SPARC-5'-UTR, SCAND1-5'-UTR, VASN-5'-UTR, SLC26A1-5'-UTR, LCLAT1-5'-UTR, FBXL18-5'-UTR, SLC35F6-5'-UTR, RAB3D-5'-UTR, MAP1B-5'-UTR, VMA21-5'-UTR, CYBA-5'-UTR, SEZ6L2-5'-UTR, PCOLCE-5'-UTR, VTN-5'-UTR, ALDH16A1-5'-UTR, RAVER1-5'-UTR, KPNA6-5'-UTR, SERINC5-5'-UTR, JUP-5'-UTR, CPN2-5'-UTR, CRIP2-5'-UTR, EPT1-5'-UTR, PNPO-5'-UTR, SSSCA1-5'-UTR, POLR2L-5'-UTR, LIN7C-5'-UTR, UQCR10-5'-UTR, PYCRL-5'-UTR, AMN-5'-UTR, MAP1S-5'-UTR, (предпочтительно все человеческие) и Dpysl2-5'-UTR, Ccnd1-5'-UTR, Acox2-5'-UTR, Cbx6-5'-UTR, Ubc-5'-UTR, Ldlr-5'-UTR, Nudt22-5'-UTR, Pcyox1l-5'-UTR, Ankrd1-5'-UTR, Tmem37-5'-UTR, Tspyl4-5'-UTR, Slc7a3-5'-UTR, Cst6-5'-UTR, Aacs-5'-UTR, Nosip-5'-UTR, Itga7-5'-UTR, Ccnd2-5'-UTR, Ebp-5'-UTR, Sf3b5-5'-UTR, Fasn-5'-UTR, Hmgcs1-5'-UTR, Osr1-5'-UTR, Lmnb1-5'-UTR, Vma21-5'-UTR, Kif20a-5'-UTR, Cdca8-5'-UTR, Slc7a1-5'-UTR, Ubqln2-5'-UTR, Prps2-5'-UTR, Shmt2-5'-UTR, Aurkb-5'-UTR, Fignl1-5'-UTR, Cad-5'-UTR, Anln-5'-UTR, Slfn9-5'-UTR, Ncaph-5'-UTR, Pole-5'-UTR, Uhrf1-5'-UTR, Gja1-5'-UTR, Fam64a-5'-UTR, Kif2c-5'-UTR, Tspan10-5'-UTR, Scand1-5'-UTR, Gpr84-5'-UTR, Fads3-5'-UTR, Cers6-5'-UTR, Cxcr4-5'-UTR, Gprc5c-5'-UTR, Fen1-5'-UTR, Cspg4-5'-UTR, Mrpl34-5'-UTR, Comtd1-5'-UTR, Armc6-5'-UTR, Emr4-5'-UTR, Atp5d-5'-UTR, 1110001J03Rik-5'-UTR, Csf2ra-5'-UTR, Aarsd1-5'-UTR, Kif22-5'-UTR, Cth-5'-UTR, Tpgs1-5'-UTR, Ccl17-5'-UTR, Alkbh7-5'-UTR, Ms4a8a-5'-UTR (предпочтительно все мышиные); и NDUFS7-3'-UTR, PHGDH-3'-UTR, TSPO-3'-UTR, ATP5D-3'-UTR, EXOSC4-3'-UTR, TUBB4B-3'-UTR, TUBA4A-3'-UTR, EMP3-3'-UTR, CRIP2-3'-UTR, BRAT1-3'-UTR, CD9-3'-UTR, CDK9-3'-UTR, PSMB3-3'-UTR, PSMB6-3'-UTR, PRSS56-3'-UTR, SCAND1-3'-UTR, AMN-3'-UTR, CYBA-3'-UTR, PCOLCE-3'-UTR, MAP1S-3'-UTR, VTN-3'-UTR, ALDH16A1-3'-UTR (предпочтительно все человеческие) и Acox2-3'-UTR, Ubc-3'-UTR, Slpi-3'-UTR, Pcyox1l-3'-UTR, Igf2bp1-3'-UTR, Tmem37-3'-UTR, Slc7a3-3'-UTR, Cst6-3'-UTR, Ebp-3'-UTR, Sf3b5-3'-UTR, Plk1-3'-UTR, Cdca8-3'-UTR, Kif22-3'-UTR, Cad-3'-UTR, Cth-3'-UTR, Pole-3'-UTR, Kif2c-3'-UTR, Scand1-3'-UTR, Gpr84-3'-UTR, Tpgs1-3'-UTR, Cel17-3'-UTR, Alkbh7-3'-UTR, Ms4a8a-3'-UTR, Mrpl34-3'-UTR, Comtd1-3'-UTR, Armc6-3'-UTR, Atp5d-3'-UTR, 1110001J03Rik-3'-UTR, Nudt22-3'-UTR, Aarsd1-3'-UTR, (предпочтительно все мышиные).
Понятие «ассоциация искусственной молекулы нуклеиновой кислоты или вектора с 3'-UTR-элементом и/или с 5'-UTR-элементом» в контексте настоящего изобретения предпочтительно означает функциональную ассоциацию или функциональное объединение искусственной молекулы нуклеиновой кислоты или вектора с 3'-UTR-элементом и/или с 5'-UTR-элементом. Это означает, что осуществляют ассоциацию или связывание искусственной молекулы нуклеиновой кислоты или вектора с 3'-UTR-элементом и/или с 5'-UTR-элементом, предпочтительно с 3'-UTR-элементом и/или с 5'-UTR-элементом, описанным выше, таким образом, чтобы осуществлялась функция 3'-UTR-элемента и/или 5'-UTR-элемента, например, функция пролонгирования и/или повышения производства РНК и/или белка. Как правило, это означает, что 3'-UTR-элемент и/или 5'-UTR-элемент интегрируют в искусственную молекулу нуклеиновой кислоты или вектор, предпочтительно в молекулу мРНК, с 3'-стороны и/или 5'-стороны относительно открытой рамки считывания соответственно, предпочтительно так, чтобы он непосредственно примыкал с 3'-стороны к открытой рамке считывания и/или непосредственно примыкал с 5'-стороны к открытой рамке считывания, чтобы 3'-UTR-элемент предпочтительно располагался между открытой рамкой считывания и поли(А)-последовательностью или сигналом полиаденилирования. Предпочтительно 3'-UTR-элемент и/или 5'-UTR-элемент интегрируют в искусственную молекулу нуклеиновой кислоты или вектор, предпочтительно в мРНК, в качестве 3'-UTR и/или 5'-UTR соответственно, т.е. так, чтобы 3'-UTR-элемент и/или 5'-UTR-элемент представлял собой 3'-UTR и/или 5'-UTR соответственно искусственной молекулы нуклеиновой кислоты или вектора, предпочтительно мРНК, т.е. так, чтобы 5'-UTR-концы находились непосредственно перед 5'-концом ОРС и 3'-UTR простирался от 3'-стороны открытой рамки считывания до 5'-стороны поли(А)-последовательности или сигнала полиаденилирования, необязательно был присоединен с помощью короткого линкера, такого как последовательность, содержащая или состоящая из одного или нескольких сайтов рестрикции. Таким образом, предпочтительно понятие «ассоциация искусственной молекулы нуклеиновой кислоты или вектора с 3'-UTR-элементом и/или 5'-UTR-элементом» означает функциональную ассоциацию 3'-UTR-элемента и/или 5'-UTR-элемента с открытой рамкой считывания, локализованной в искусственной молекуле нуклеиновой кислоты или векторе, предпочтительно в молекуле мРНК. 3'-UTR и/или 5'-UTR и ОРС представляют собой конструкции, описанные выше для искусственной молекулы нуклеиновой кислоты, предлагаемой в настоящем изобретении, например, предпочтительно ОРС и 3'-UTR являются гетерологичными и/или ОРС и 5'-UTR являются гетерологичными соответственно, например, происходят из различных генов, как описано выше. Ассоциацию с 3'-UTR-элементом и/или 5'-UTR-элементом можно осуществлять либо посредством de novo ассоциации индивидуальных элементов, либо путем модификации уже существующей нуклеиновой кислоты (матрицы). В последнем случае, в качестве примера и в качестве иллюстрации молекулу нуклеиновой кислоты, предлагаемой в настоящем изобретении, можно получать путем (I) использования нуклеиновой кислоты, имеющей соответствующую последовательность, которая представлена на фиг. 1А, в качестве матрицы, (II) модификации указанной матрицы путем замены по меньшей мере одного (а) подчеркнутого 5'-UTR-элемента (подчеркнут на фиг. 1А) или (б) 3'-UTR-элемента (подчеркнут двойной линией на фиг. 1А) на (а) другой 5'-UTR-элемент или (б) другой 3'-UTR-элемент, осуществляя тем самым ассоциацию искусственной молекулы нуклеиновой кислоты с указанным 5'-UTR-элементом или 3'-UTR-элементом.
Другой объект настоящего изобретения относится к применению 3'-UTR-элемента и/или 5'-UTR-элемента, предпочтительно 3'-UTR-элемента, описанного выше, и/или 5'-UTR-элемента, описанного выше, для повышения и/или пролонгирования производства белка с искусственной молекулы нуклеиновой кислоты, предпочтительно с молекулы мРНК или вектора, где 3'-UTR-элемент и/или 5'-UTR-элемент содержит или состоит из нуклеотидной последовательности, полученной из 3'-UTR и/или 5'-UTR транскрипта гена, выбранного из группы, которая состоит из ZNF460, TGM2, IL7R, BGN, TK1, RAB3B, СВХ6, FZD2, COL8A1, NDUFS7, PHGDH, PLK2, TSPO, PTGS1, FBXO32, NID2, ATP5D, EXOSC4, NOL9, UBB4B, VPS18, ORMDL2, FSCN1, ТМЕМ33, TUBA4A, ЕМР3, ТМЕМ201, CRIP2, BRAT1, SERPINH1, CD9, DPYSL2, CDK9, TFRC, PSMB3 5'-UTR, FASN, PSMB6, PRSS56, KPNA6, SFT2D2, PARD6B, LPP, SPARC, SCAND1, VASN, SLC26A1, LCLAT1, FBXL18, SLC35F6, RAB3D, MAP1B, VMA21, CYBA, SEZ6L2, PCOLCE, VTN, ALDH16A1, RAVER1, KPNA6, SERINC5, JUP, CPN2, CRIP2, EPT1, PNPO, SSSCA1, POLR2L, LIN7C, UQCR10, PYCRL, AMN, MAP1S, NDUFS7, PHGDH, TSPO, ATP5D, EXOSC4, TUBB4B, TUBA4A, ЕМР3, CRIP2, BRAT1, CD9, CDK9, PSMB3, PSMB6, PRSS56, SCAND1, AMN, CYBA, PCOLCE, MAP1S, VTN, ALDH16A1 (предпочтительно все человеческие) и Dpysl2, Ccnd1, Acox2, Cbx6, Ubc, Ldlr, Nudt22, Pcyox1l, Ankrd1, Tmem37, Tspyl4, Slc7a3, Cst6, Aacs, Nosip, Itga7, Ccnd2, Ebp, Sf3b5, Fasn, Hmgcs1, Osr1, Lmnb1, Vma21, Kif20a, Cdca8, Slc7a1, Ubqln2, Prps2, Shmt2, Aurkb, Fignl1, Cad, Anln, Slfn9, Ncaph, Pole, Uhrf1, Gja1, Fam64a, Kif2c, Tspan10, Scand1, Gpr84, Fads3, Cers6, Cxcr4, Gprc5c, Fen1, Cspg4, Mrpl34, Comtd1, Armc6, Emr4, Atp5d, 1110001J03Rik, Csf2ra, Aarsd1, Kif22, Cth, Tpgs1, Cel17, Alkbh7, Ms4a8a, Acox2, Ubc, Slpi, Pcyox1l, Igf2bp1, Tmem37, Slc7a3, Cst6, Ebp, Sf3b5, Plk1, Cdca8, Kif22, Cad, Cth, Pole, Kif2c, Scand1, Gpr84, Tpgs1, Ccl17, Alkbh7, Ms4a8a, Mrpl34, Comtd1, Armc6, Atp5d, 1110001J03Rik, Nudt22, Aarsd1 (предпочтительно все мышиные); предпочтительно из группы, состоящей из ZNF460-5'-UTR, TGM2-5'-UTR, IL7R-5'-UTR, BGN-5'-UTR, TK1-5'-UTR, RAB3B-5'-UTR, CBX6-5'-UTR, FZD2-5'-UTR, COL8A1-5'-UTR, NDUFS7-5'-UTR, PHGDH-5'-UTR, PLK2-5'-UTR, TSPO-5'-UTR, PTGS1-5'-UTR, FBXO32-5'-UTR, NID2-5'-UTR, ATP5D-5'-UTR, EXOSC4-5'-UTR, NOL9-5'-UTR, UBB4B-5'-UTR, VPS18-5'-UTR, ORMDL2-5'-UTR, FSCN1-5'-UTR, TMEM33-5'-UTR, TUBA4A-5'-UTR, EMP3-5'-UTR, TMEM201-5'-UTR, CRIP2-5'-UTR, BRAT1-5'-UTR, SERPINH1-5'-UTR, CD9-5'-UTR, DPYSL2-5'-UTR, CDK9-5'-UTR, TFRC-5'-UTR, PSMB3 5'-UTR, FASN-5'-UTR, PSMB6-5'-UTR, PRSS56-5'-UTR, KPNA6-5'-UTR, SFT2D2-5'-UTR, PARD6B-5'-UTR, LPP-5'-UTR, SPARC-5'-UTR, SCAND1-5'-UTR, VASN-5'-UTR, SLC26A1-5'-UTR, LCLAT1-5'-UTR, FBXL18-5'-UTR, SLC35F6-5'-UTR, RAB3D-5'-UTR, MAP1B-5'-UTR, VMA21-5'-UTR, CYBA-5'-UTR, SEZ6L2-5'-UTR, PCOLCE-5'-UTR, VTN-5'-UTR, ALDH16A1-5'-UTR, RAVER1-5'-UTR, KPNA6-5'-UTR, SERINC5-5'-UTR, JUP-5'-UTR, CPN2-5'-UTR, CRIP2-5'-UTR, EPT1-5'-UTR, PNPO-5'-UTR, SSSCA1-5'-UTR, POLR2L-5'-UTR, LIN7C-5'-UTR, UQCR10-5'-UTR, PYCRL-5'-UTR, AMN-5'-UTR, MAP1S-5'-UTR (предпочтительно все человеческие) и Dpysl2-5'-UTR, Ccnd1-5'-UTR, Acox2-5'-UTR, Cbx6-5'-UTR, Ubc-5'-UTR, Ldlr-5'-UTR, Nudt22-5'-UTR, Pcyox1l-5'-UTR, Ankrd1-5'-UTR, Tmem37-5'-UTR, Tspyl4-5'-UTR, Slc7a3-5'-UTR, Cst6-5'-UTR, Aacs-5'-UTR, Nosip-5'-UTR, Itga7-5'-UTR, Ccnd2-5'-UTR, Ebp-5'-UTR, Sf3b5-5'-UTR, Fasn-5'-UTR, Hmgcs1-5'-UTR, Osr1-5'-UTR, Lmnb1-5'-UTR, Vma21-5'-UTR, Kif20a-5'-UTR, Cdca8-5'-UTR, Slc7a1-5'-UTR, Ubqln2-5'-UTR, Prps2-5'-UTR, Shmt2-5'-UTR, Aurkb-5'-UTR, Fignl1-5'-UTR, Cad-5'-UTR, Anln-5'-UTR, Slfn9-5'-UTR, Ncaph-5'-UTR, Pole-5'-UTR, Uhrf1-5'-UTR, Gja1-5'-UTR, Fam64a-5'-UTR, Kif2c-5'-UTR, Tspan10-5'-UTR, Scand1-5'-UTR, Gpr84-5'-UTR, Fads3-5'-UTR, Cers6-5'-UTR, Cxcr4-5'-UTR, Gprc5c-5'-UTR, Fen1-5'-UTR, Cspg4-5'-UTR, Mrpl34-5'-UTR, Comtd1-5'-UTR, Armc6-5'-UTR, Emr4-5'-UTR, Atp5d-5'-UTR, 1110001J03Rik-5'-UTR, Csf2ra-5'-UTR, Aarsd1-5'-UTR, Kif22-5'-UTR, Cth-5'-UTR, Tpgs1-5'-UTR, Ccl17-5'-UTR, Alkbh7-5'-UTR, Ms4a8a-5'-UTR (предпочтительно все мышиные); и NDUFS7-3'-UTR, PHGDH-3'-UTR, TSPO-3'-UTR, ATP5D-3'-UTR, EXOSC4-3'-UTR, TUBB4B-3'-UTR, TUBA4A-3'-UTR, EMP3-3'-UTR, CRIP2-3'-UTR, BRAT1-3'-UTR, CD9-3'-UTR, CDK9-3'-UTR, PSMB3-3'-UTR, PSMB6-3'-UTR, PRSS56-3'-UTR, SCAND1-3'-UTR, AMN-3'-UTR, CYBA-3'-UTR, PCOLCE-3'-UTR, MAP1S-3'-UTR, VTN-3'-UTR, ALDH16A1-3'-UTR (предпочтительно все человеческие) и Acox2-3'-UTR, Ubc-3'-UTR, Slpi-3'-UTR, Pcyox11-3'-UTR, Igf2bp1-3'-UTR, Tmem37-3'-UTR, Slc7a3-3'-UTR, Cst6-3'-UTR, Ebp-3'-UTR, Sf3b5-3'-UTR, Plk1-3'-UTR, Cdca8-3'-UTR, Kif22-3'-UTR, Cad-3'-UTR, Cth-3'-UTR, Pole-3'-UTR, Kif2c-3'-UTR, Scand1-3'-UTR, Gpr84-3'-UTR, Tpgs1-3'-UTR, Ccl17-3'-UTR, Alkbh7-3'-UTR, Ms4a8a-3'-UTR, Mrpl34-3'-UTR, Comtd1-3'-UTR, Armc6-3'-UTR, Atp5d-3'-UTR, 1110001J03Rik-3'-UTR, Nudt22-3'-UTR, Aarsd1-3'-UTR, (предпочтительно все мышиные).
Варианты применения, предлагаемые в настоящем изобретении, предпочтительно включают ассоциацию искусственной молекулы нуклеиновой кислоты, вектора или РНК с 3'-UTR-элементом, описанным выше, и/или с 5'-UTR-элементом, описанным выше.
Соединения и ингредиенты предлагаемой в изобретении фармацевтической композиции можно также изготавливать и продавать по отдельности друг от друга. Таким образом, изобретение относится также к набору или набору компонентов, содержащему искусственную молекулу нуклеиновой кислоты, предлагаемой в изобретении, вектор, предлагаемый в изобретении, клетку, предлагаемую в изобретении, и/или фармацевтическую композицию, предлагаемую в изобретении. Предпочтительно такой набор или наборы компонентов могут дополнительно содержать инструкции по применению, клетки для трансфекции, адъювант, средства для введения фармацевтической композиции, фармацевтически приемлемый носитель и/или фармацевтически приемлемый раствор для растворения или разведения искусственной молекулы нуклеиновой кислоты, вектора, клеток или фармацевтической композиции.
Способ идентификации элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или элемента 5'-нетранслируемой области (5'-UTR-элемента)
Другим объектом настоящего изобретения является способ идентификации элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или элемента 5'-нетранслируемой области (5'-UTR-элемента), включающий следующие стадии, на которых:
а) анализируют стабильность мРНК, осуществляя следующие подстадии, на которых:
I. определяют количество указанной мРНК в первый момент времени в процессе расщепления указанной мРНК,
II. определяют количество указанной мРНК во второй момент времени в процессе расщепления указанной мРНК, и
III. рассчитывают отношение количества указанной мРНК, определенное на стадии (I), к количеству указанной мРНК, определенному на стадии (II);
б) Отбирают стабильную мРНК, характеризующуюся тем, что отношение, рассчитанное на подстадии (III), составляет по меньшей мере 0,5 (50%), по меньшей мере 0,6 (60%), по меньшей мере 0,7 (70%), по меньшей мере 0,75 (75%), по меньшей мере 0,8 (80%), по меньшей мере 0,85 (85%), по меньшей мере 0,9 (90%) или по меньшей мере 0,95 (95%); и
в) Определяют нуклеотидную последовательность 3'- и/или 5'-UTR-элемента указанной стабильной мРНК.
При этом стабильность мРНК предпочтительно оценивают в стандартных условиях, например, в стандартных условиях (стандартная среда, инкубация и т.д.) для конкретной применяемой клеточной линии или применяемого типа клеток.
Для анализа стабильности мРНК процесс расщепления указанной мРНК оценивают путем определения количества или концентрации указанной мРНК в первый и второй моменты времени в процессе расщепления указанной мРНК (смотри стадии а) I. и а) II.).
Для определения количества или концентрации мРНК в процессе расщепления РНК in vivo или in vitro, как указано выше (т.е. in vitro относится, в частности, к («живым») клеткам и/или ткани, включая ткань живого индивидуума; клетки включают, в частности, клеточные линии, первичные клетки, клетки в ткани или в организме индивидуумов, предпочтительными являются клетки млекопитающих, например, человеческие клетки и мышиные клетки, и наиболее предпочтительно применяют человеческие линии клеток HeLa, HEPG2 и U-937 и мышиные линии клеток NIH3T3, JAWSII и L929, кроме того, наиболее предпочтительными являются первичные клетки, в наиболее предпочтительных вариантах осуществления изобретения - человеческие кожные фибробласты (HDF)), можно применять различные методы, известные специалисту в данной области. Примеры таких методов включают (но, не ограничиваясь только ими) общее ингибирование транскрипции, например, с помощью ингибитора транскрипции, такого как актиномицин D, применение индуцибельных промоторов для специфического усиления кратковременной транскрипции, например, индуцируемой сывороткой промоторной системы c-fos и регуляторной промоторной системы Tet-off, и кинетические методы мечения, например, импульсного мечения.
Например, если для определения количества или концентрации мРНК в процессе расщепления РНК in vivo или in vitro, как указано выше, применяют опосредуемое ингибитором транскрипции прекращение транскрипции на стадии а), то можно применять ингибиторы транскрипции, такие как актиномицин D (ActD), 5,6-дихлор-1-D-рибофуранозилбензимидазол (DRB) или -аманитин (α-Am). В этом случае для оценки расщепления мРНК, как правило, ингибиторы транскрипции добавляют к клеткам и тем самым обычно ингибируют транскрипцию, и при этом можно выявлять расщепление РНК без помех, обусловленных происходящей транскрипцией.
В альтернативном варианте на стадии а) можно применять индуцибельные промоторы для специфического усиления кратковременной транскрипции, в этом случае идея заключается в том, чтобы обеспечить стимул, который активирует транскрипцию и приводит к всплеску синтеза мРНК, после чего стимул удаляют для «выключения» транскрипции и осуществляют мониторинг расщепления мРНК. При этом применение индуцибельного промотора позволяет осуществлять строгий контроль, благодаря чему индукция и прекращение транскрипции происходят в узком временном окне. Известно, что в случае клеток млекопитающих, для указанной цели полезным является промотор c-fos, поскольку он поддается быстрой и кратковременной индукции в ответ на добавление сыворотки, что обеспечивает надежный и простой путь достижения кратковременной вспышки транскрипции. Промоторная система Tet-off представляет собой другую возможность, которая еще больше расширяет применение подхода, основанного на импульсном усилении транскрипции, для изучения обмена мРНК в клетках млекопитающих.
Однако, в настоящем изобретении на стадии а) для определения количества мРНК в процессе расщепления РНК in vivo или in vitro, как указано выше, предпочтительно применяют кинетические методы мечения. В кинетических методах мечения, как правило, осуществляют мечение РНК, при этом метки включают, прежде всего, меченые нуклеотиды и меченые нуклеозиды, наиболее предпочтительными являются меченый уридин и меченый урацил. Примеры предпочтительных меток включают 4-тиоуридин (4sU), 2-тиоуридин, 6-тиогуанозин, 5-этинилуридин (EU), 5-бромуридин (BrU), биотин-16-аминоаллилуридин, 5-аминоаллилуридин, 5-аминоаллилцитидин и т.д., при этом 4-тиоуридин (4sU), 5-этинилуридин (EU) или 5'-бромуридин (BrU) являются более предпочтительными. Наиболее предпочтительным является 4-тиоуридин (4sU). 4-тиоуридин (4sU) предпочтительно применяют в концентрации 100-500 мкМ. Кроме того, можно применять также радиоактивно меченые нуклеотиды, например, уридин-3Н. Можно применять также комбинации указанных выше меченых нуклеотидов, при этом наиболее предпочтительными является комбинация 4-тиоуридина и 6-тиогуанозина.
При кинетическом мечении, как правило, метят образующуюся РНК, например, путем включения меченого уридина или урацила в процессе транскрипции. Спустя некоторое время прекращают добавление метки, и после этого можно обнаруживать расщепление РНК путем оценки специфически меченой РНК, не осуществляя общее ингибирования транскрипции.
Для определения количества мРНК в процессе расщепления РНК на стадии а) предпочтительно применяют импульсное мечение, при этом наиболее предпочтительной является методология вытеснения метки. В контексте настоящего описания понятие «импульсное мечение» относится к методу, в котором применяют метку, например, описанные выше метки, для измерения скоростей синтеза и/или расщепления соединений в живых клетках. Как правило, клетки приводят в контакт с небольшим количеством метки в течение короткого периода времени, поэтому используют понятие «импульс». В методологии вытеснения метки после импульсного мечения, как правило, после необходимого периода времени контактирования с меткой добавляют в намного большем количестве немеченое соединение, соответствующее «импульсу» (соединению, используемому для импульсного мечения) (например, немеченый уридин, если в качестве импульса применяли меченый уридин). Воздействие конкуренции между меченым и немеченым соединениями должно приводить к снижению дальнейшего поглощения меченого соединения до пренебрежимо малого уровня, отсюда понятие «вытеснение».
Для определения количества или концентрации мРНК, как правило, необходимо выделять мРНК. Специалисту в данной области известны различные методы выделения РНК, например, с помощью экстракции гуанидин-тиоцианат-фенол-хлороформом или экстракции с использованием силикагелевой колонки. Можно применять также поступающие в продажу наборы, например, набор RNeasy Kit фирмы Qiagen.
Кроме того, может потребоваться стадия экстракции, в частности, в том случае, когда применяют кинетический метод мечения (в отличие от ингибитора транскрипции, когда общая РНК представляет собой «расщепляющуюся» РНК, поскольку осуществляют общее ингибирование транскрипции). На стадии экстракции меченую РНК (т.е. представляющую собой «расщепляющуюся» РНК) экстрагируют из общей выделенной РНК. Таким образом, средства экстракции можно выбирать в зависимости от применяемой метки. Например, можно применять иммунную очистку с использованием антител к метке.
Кроме того, например, для экстракции несущей тио-метку, например, меченой 4-тиоуридином (4sU) РНК, можно осуществлять инкубацию HPDP-биотин (пиридилдитиол-активированный, сульфгидрил-реактивный реагент для биотинилирования, конъюгация с которым происходит посредством расщепляемой (обратимой) дисульфидной связи) с выделенной «общей РНК». Этот реагент специфически взаимодействует с восстановленными тиолами (-SH) в меченой 4-тиоуридином (4sU) РНК с образованием обратимых дисульфидных связей. Биотинилирование позволяет осуществлять связывание несущей тио-метку, например, меченой 4-тиоуридином (4sU) РНК со стрептавидином и, следовательно, ее можно экстрагировать из общей РНК путем восстановления дисульфидной связи с помощью дитиотреитола или бета-меркаптоэтанола (или любого другого восстановителя).
В случае меченых биотином нуклеотидов, например, биотин-16-аминоаллилуридина, можно применять непосредственно стрептавидин для экстракции меченой РНК из общей РНК.
Например, для экстракции новых транскрибированных меченных 5-этинилуридином (EU) клеточных РНК из общей РНК можно применять биотинилирование EU в катализируемой медью реакции циклоприсоединения (часто обозначают как «клик-химия»), после чего осуществлять очистку на основе аффинности к стрептавидину. Этот метод осуществляют с использованием поступающего в продажу набора Click-iT Nascent RNA Capture (каталожный номер С10365, фирма Invitrogen). В инструкции производителя рекомендовано применять время импульсного мечения от 30 до 60 мин для дозы 0,5 мМ EU или от 1 до 24 ч для дозы 0,1 или 0,2 мМ EU.
Например, меченные BrU молекулы РНК можно экстрагировать посредством иммуноочистки с использованием антитела к бромдезоксиуридину (например, клона 2 В1, каталожный номер MI-11-3, фирма MBL) и белок G сефарозы.
Затем можно измерять количество или концентрацию мРНК, т.е. уровень (число копий) транскрипта, с помощью различных методов, известных специалисту в данной области. Примерами таких методов являются (но, не ограничиваясь только ими) анализ с использованием микромассивов, анализ методом нозерн-блоттинга, количественная ПЦР или технология секвенирования следующего поколения (высокоэффективное секвенирование). Наиболее предпочтительными являются анализ с использованием микромассивов и технология секвенирования следующего поколения. Кроме того, наиболее предпочтительными являются подходы на основе анализа полного генома/полного транскриптома, например, при анализе на основе микромассивов - анализ полногеномного микромассива, например, Affymetrix Human Gene 1.0 ST или 2.0 ST, или Affymetrix Mouse Gene 1.0 ST или 2.0 ST, или анализ полного транскрипта путем секвенирования следующего поколения.
На подстадиях I. и II. стадии а) определяют количество мРНК в первый и во второй моменты времени в процессе расщепления мРНК. Как правило, это означает, что мРНК, прежде всего, выделяют в первый и во второй моменты времени в процессе расщепления мРНК для определения соответствующих количеств. Следовательно, «первый момент времени» и «второй момент времени» представляют собой определенные моменты времени в процессе расщепления РНК, в которые выделяют РНК для определения количества РНК. Как правило, «второй момент времени» наступает позднее в процессе расщепления РНК, чем «первый момент времени».
Предпочтительно первый момент времени выбирают таким образом, чтобы рассматривать только мРНК, подвергающуюся процессу расщепления, т.е. чтобы избегать образующейся мРНК, например, в процессе транскрипции. Например, если применяют кинетические методы мечения, например, импульсное мечение, то первый момент времени предпочтительно выбирают таким образом, чтобы было завершено включение метки в мРНК, т.е. более не происходило включение метки в мРНК. Так, если применяют кинетическое мечение, то первый момент времени может наступать по меньшей мере через 10 мин, по меньшей мере через 20 мин, по меньшей мере через 30 мин, по меньшей мере через 40 мин, по меньшей мере через 50 мин, по меньшей мере через 60 мин, по меньшей мере через 70 мин, по меньшей мере через 80 мин или по меньшей мере через 90 мин после окончания экспериментальной процедуры мечения, например, после окончания инкубации клеток с меткой.
Например, первый момент времени может наступать предпочтительно через 0-6 ч после прекращения транскрипции (например, с помощью ингибитора транскрипции), прекращения индукции промотора в случае применения индуцибельных промоторов или после прекращения подачи импульса или метки, например, после окончания мечения. Более предпочтительно первый момент времени может наступать по истечении периода, составляющего от 30 мин до 5 ч, еще более предпочтительно от 1 до 4 ч и наиболее предпочтительно примерно через 3 ч после прекращения транскрипции (например, с помощью ингибитора транскрипции), прекращения индукции промотора в случае применения индуцибельных промоторов или после прекращения подачи импульса или метки, например, после окончания мечения.
Предпочтительно второй момент времени выбирают таким образом, чтобы он наступал максимально позже в процессе расщепления мРНК. Однако, если рассматривают множество видов мРНК, то второй момент времени предпочтительно выбирают таким образом, чтобы все еще имелось значительное количество видов мРНК, предпочтительно по меньшей мере 10% видов мРНК, присутствующих в поддающемся обнаружению количестве, т.е. в количестве, превышающем 0. Предпочтительно, второй момент времени наступает по меньшей мере через 5 ч, по меньшей мере через 6 ч, по меньшей мере через 7 ч, по меньшей мере через 8 ч, по меньшей мере через 9 ч, по меньшей мере через 10 ч, по меньшей мере через 11 ч, по меньшей мере через 12 ч, по меньшей мере через 13 ч, по меньшей мере через 14 ч или по меньшей мере через 15 ч после прекращения транскрипции (например, с помощью ингибитора транскрипции), прекращения индукции промотора в случае применения индуцибельных промоторов или после прекращения подачи импульса или метки, например, после окончания мечения.
Например, второй момент времени предпочтительно может наступать через 3-48 ч после прекращения транскрипции (например, с помощью ингибитора транскрипции), прекращения индукции промотора в случае применения индуцибельных промоторов или после прекращения подачи импульса или метки, например, после окончания мечения. Более предпочтительно второй момент времени может наступать по истечении периода времени, составляющего от 6 мин до 36 ч, еще более предпочтительно от 10 до 24 ч и наиболее предпочтительно примерно через 15 ч после прекращения транскрипции (например, с помощью ингибитора транскрипции), прекращения индукции промотора в случае применения индуцибельных промоторов или после прекращения подачи импульса или метки, например, после окончания мечения.
Таким образом, промежуток времени между первым моментом времени и вторым моментом времени предпочтительно должен быть максимально большим в указанных выше пределах. Следовательно, промежуток времени между первым моментом времени и вторым моментом времени предпочтительно должен составлять по меньшей мере 4 ч, по меньшей мере 5 ч, по меньшей мере 6 ч, по меньшей мере 7 ч, по меньшей мере 8 ч, по меньшей мере 9 ч, по меньшей мере 10 ч, по меньшей мере 11 ч или по меньшей мере 12 ч, при этом наиболее предпочтителен промежуток времени, составляющий примерно 12 ч. Как правило, второй момент времени наступает по меньшей мере на 10 мин позднее чем первый момент времени.
На подстадии III. стадии а) рассчитывают отношение количества мРНК, определенного на стадии (I), к количеству мРНК, определенному на стадии (II). Для этой цели количество мРНК (число копий транскрипта), определенное как указано выше во второй момент времени, делят на количество мРНК (число копий транскрипта), определенное как указано выше в первый момент времени. Использование указанного отношения препятствует тому, что стабильные виды мРНК, которые уже в первый момент времени присутствуют лишь в очень малых количествах, не будут учтены при сравнении с видами мРНК, которые присутствуют в больших количествах.
На стадии б) отбирают такую мРНК, для которой отношение, рассчитанное на подстадии (III) стадии а), составляет по меньшей мере 0,5 (50%), по меньшей мере 0,6 (60%), по меньшей мере 0,7 (70%), по меньшей мере 0,75 (75%), по меньшей мере 0,8 (80%), по меньшей мере 0,85 (85%), по меньшей мере 0,9 (90%) или по меньшей мере 0,95 (95%). Такая мРНК рассматривается согласно настоящему изобретению как наиболее стабильная мРНК.
На стадии в) определяют нуклеотидную последовательность 3'- и/или 5'-UTR-элемента указанной мРНК, т.е. мРНК, отобранной на стадии б). Для этой цели можно применять различные методы, известные специалисту в данной области, например, секвенирование или выбор из публично доступных баз данных, таких, например, как NCBI (Национальный центр биотехнологической информации). Например, можно осуществлять поиск последовательности мРНК отобранной на стадии б) мРНК в базе данных и затем можно 3'- и/или 5'-UTR выделять из последовательности мРНК, имеющейся в базе данных.
В частности, в описанном выше способе идентификации элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или элемента 5'-нетранслируемой области (5'-UTR-элемента) понятие «мРНК» и/или «стабильная мРНК» соответственно могут относиться также и к видам мРНК, представленным в настоящем описании, и/или к стабильным видам мРНК соответственно.
Кроме того, в контексте настоящего описания предпочтительно «стабильная мРНК» может характеризоваться более медленным расщеплением по сравнению со средним расщеплением мРНК, которое предпочтительно оценивают in vivo или in vitro как описано выше. При этом «среднее расщепление мРНК» можно оценивать путем исследования расщепления мРНК для множества видов мРНК.
Следовательно, другим объектом настоящего изобретения является способ идентификации элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или элемента 5'-нетранслируемой области (5'-UTR-элемента), включающий следующие стадии, на которых:
а) анализируют стабильность множества видов мРНК, осуществляя следующие подстадии, на которых:
I. определяют количество каждого вида мРНК из указанного множества видов мРНК в первый момент времени в процессе расщепления указанных видов мРНК,
II. определяют количество каждого вида мРНК из указанного множества видов мРНК во второй времени в процессе расщепления указанных видов мРНК и
III. рассчитывают для каждого вида мРНК из указанного множества видов мРНК отношение количества указанного вида мРНК, определенного на стадии (I), к количеству указанного вида мРНК, определенному на стадии (II);
б) ранжируют виды мРНК из множества видов мРНК в зависимости от величины отношения, рассчитанного на подстадии (III) для каждого вида мРНК;
в) отбирают один или большее количество видов мРНК, характеризующихся наибольшей величиной отношения или наибольшими величинами отношения, рассчитанного(ыми) на подстадии (III); и
г) определяют нуклеотидную последовательность 3'- и/или 5'-UTR-элемента указанной мРНК.
Понятие «виды мРНК» в контексте настоящего описания соответствует геномной транскрипционной единице, т.е. гену. Так, в одном «виде мРНК» могут присутствовать различные транскрипты, например, обусловленные процессингом мРНК. Виды мРНК, например, могут быть представлены в виде пятен на микромассиве. Следовательно, микромассив представляет собой предпочтительный «инструмент» для определения количества множества видов мРНК, например, в определенный момент времени в процессе расщепления мРНК. Однако можно применять также и другие методы, известные специалисту в данной области, например, секвенирование РНК (называемое также секвенированием полного транскриптома по методу дробовика (шотган-секвенирование), что представляет собой технологию, в которой используются возможности секвенирования следующего поколения для выявления на основе моментальных снимков присутствия и количества РНК в геноме в данный момент времени), количественную ПЦР и т.д.
Предпочтительно выражение «множество видов мРНК» относится к по меньшей мере 100, по меньшей мере 300, по меньшей мере 500, по меньшей мере 1000, по меньшей мере 2000, по меньшей мере 3000, по меньшей мере 4000, по меньшей мере 5000, по меньшей мере 6000, по меньшей мере 7000, по меньшей мере 8000, по меньшей мере 9000, по меньшей мере 10000, по меньшей мере 11000, по меньшей мере 12000, по меньшей мере 13000, по меньшей мере 14000, по меньшей мере 15000, по меньшей мере 16000, по меньшей мере 17000, по меньшей мере 18000, по меньшей мере 19000, по меньшей мере 20000, по меньшей мере 21000, по меньшей мере 22000, по меньшей мере 23000, по меньшей мере 24000, по меньшей мере 25000, по меньшей мере 26000, по меньшей мере 27000, по меньшей мере 28000, по меньшей мере 29000, по меньшей мере 30000 видам мРНК. Наиболее предпочтительно оценивать весь транскриптом или максимально возможное количество видов мРНК в транскриптоме. Это можно осуществлять, например, с использованием микромассива, обеспечивающего охват всех транскриптов.
В этом способе стадия а), включая ее подстадии I.-III., практически соответствует стадии а), включая ее подстадии I.-III., описанного ранее способа, предлагаемого в изобретении, но отличается только тем, что количество каждого вида мРНК из множества видов мРНК определяют в первый и второй моменты времени, и тем, что величину отношения рассчитывают для каждого вида мРНК. Следовательно, подробно описанные выше способы и предпочтительные варианты осуществления изобретения применимы также и в данном случае и величину отношения для индивидуальных видов мРНК (и каждый из индивидуальных видов мРНК соответственно) можно определять согласно процедуре, описанной выше для «мРНК».
Однако, в отличие от указанного выше способа стабильность мРНК оценивают не по абсолютной величине отношения, а путем ранжирования видов мРНК из множества видов мРНК, в зависимости от величины отношения, рассчитанного на подстадии (III) стадии а) для каждого из видов мРНК. Затем отбирают на подстадии в) один или большее количество видов мРНК, характеризующихся наибольшей величиной отношения или наибольшими величинами отношения, рассчитанного на подстадии (III) стадии а).
В данном контексте наиболее предпочтительно на стадии в) отбирают 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,8%, 0,9%, 1%, 2%, 3%, 4%, 5%, 10%, 15%, 20% наиболее стабильных видов мРНК. Альтернативно этому или дополнительно можно отбирать на стадии в) такие виды мРНК, которые характеризуются величиной отношения, рассчитанного на подстадии III. стадии а), которое соответствует по меньшей мере 100% средней величины отношения, рассчитанной для всех проанализированных видов мРНК. Более предпочтительно отбирают такие виды мРНК, которые характеризуются величиной отношения, составляющей меньшей мере 150%, еще более предпочтительно по меньшей мере 200% и наиболее предпочтительно по меньшей мере 300% от средней величины отношения, рассчитанной для всех проанализированных видов мРНК.
На стадии г) определяют нуклеотидную последовательность 3'- и/или 5'-UTR-элемента мРНК, отобранной на стадии в), согласно процедуре, описанной выше для стадии в) описанного ранее способа, предлагаемого в изобретении.
Предпочтительно в обоих описанных выше способах идентификации 3'-UTR-элемента и/или 5'-UTR-элемента, предлагаемого в настоящем изобретении, период времени между первым моментом времени и вторым моментом времени составляет по меньшей мере 5 ч, предпочтительно по меньшей мере 6 ч, предпочтительно по меньшей мере 7 ч, более предпочтительно по меньшей мере 8 ч, более предпочтительно по меньшей мере 9 ч, еще более предпочтительно по меньшей мере 10 ч, еще более предпочтительно по меньшей мере 11 ч и наиболее предпочтительно по меньшей мере 12 ч.
Предпочтительно в обоих описанных выше способах идентификации 3'-UTR-элемента и/или 5'-UTR-элемента, предлагаемого в настоящем изобретении, стабильность мРНК анализируют с помощью импульсного мечения, предпочтительно с использованием методологии вытеснения метки.
Способ идентификации элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или элемента 5'-нетранслируемой области (5'-UTR-элемента)
Другим объектом настоящего изобретения является также способ идентификации элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или элемента 5'-нетранслируемой области (5'-UTR-элемента), который обеспечивает высокую эффективность трансляции искусственной молекулы нуклеиновой кислоты, включающий следующие стадии, на которых:
а) идентифицируют 3'-UTR-элемент и/или 5'-UTR-элемент, полученный из стабильной мРНК, с помощью способа идентификации 3'-UTR-элемента и/или 5'-UTR-элемента, соответствующего одному из способов, которые описаны выше;
б) синтезируют искусственную молекулу нуклеиновой кислоты, содержащую по меньшей мере одну открытую рамку считывания и по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент, который соответствует или содержится в 3'-UTR-элементе и/или 5'-UTR-элементе, идентифицированном на стадии а);
в) анализируют экспрессию белка, кодируемого по меньшей мере одной открытой рамкой считывания (ОРС) искусственной молекулы нуклеиновой кислоты, синтезированной на стадии б);
г) анализируют экспрессию белка, кодируемого по меньшей мере одной открытой рамкой считывания (ОРС) искусственной референс-молекулы нуклеиновой кислоты, в которой отсутствует 3'-UTR-элемент и/или 5'-UTR-элемент;
д) сравнивают экспрессию белка с искусственной молекулы нуклеиновой кислоты, проанализированной на стадии в), с экспрессией белка с искусственной референс-молекулы нуклеиновой кислоты, проанализированной на стадии г); и
е) отбирают 3'-UTR-элемент и/или 5'-UTR-элемент, если экспрессия белка с искусственной молекулы нуклеиновой кислоты, проанализированной на стадии в), пролонгирована и/или повышена по сравнению с экспрессией белка с искусственной референс-молекулы нуклеиновой кислоты, проанализированной на стадии г).
В этом способе первый 3'-UTR-элемент и/или 5'-UTR-элемент идентифицируют с помощью описанного выше способа, предлагаемого в настоящем изобретении. Это позволяет осуществлять синтез 3'- и/или 5'-UTR-элемента с помощью методов, известных специалисту в данной области, например, с помощью ПЦР-амплификации. Праймеры, применяемые для такой ПЦР, предпочтительно могут содержать сайты рестрикции для клонирования. Альтернативно этому 3'- и/или 5'-UTR-элемент можно синтезировать, например, с помощью химического синтеза или отжига олигонуклеотидов. Таким образом, на стадии б) синтезируют искусственную молекулу нуклеиновой кислоты, содержащую по меньшей мере одну открытую рамку считывания и по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент, который соответствует или содержится в 3'-UTR-элементе и/или 5'-UTR-элементе, идентифицированном на стадии а). В частности, по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент, как правило, объединяют с открытой рамкой считывания, что приводит к получению искусственной нуклеиновой кислоты, содержащей 3'- и/или 5'-UTR-элемент, предлагаемый в настоящем изобретении, если 3'- и/или 5'-UTR-элемент удовлетворяют(ет) соответствующим требованиям, а именно, если они пролонгируют и/или повышают экспрессию белка. Для тестирования этого 3'-и/или 5'-UTR-элемент, идентифицированный на стадии а), или ПЦР-фрагмент или синтезированную последовательность соответственно можно клонировать в конкретном векторе, предпочтительно в экспрессионном векторе, для оценки экспрессии белка с соответствующей ОРС.
Затем, как описано выше, на стадии в) оценивают экспрессию белка с искусственной молекулы нуклеиновой кислоты, содержащей по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент, и сравнивают с оцененной на стадии г), экспрессией белка с соответствующей искусственной референс-молекулы нуклеиновой кислоты, которая не содержит 3'-UTR-элемент и/или 5'-UTR-элемент, как описано на стадии д).
После этого на стадии е) отбирают такой 3'-UTR-элемент и/или 5'-UTR-элемент, который повышает экспрессию белка с искусственной молекулы нуклеиновой кислоты, проанализированной на стадии в), по сравнению с экспрессией белка с искусственной референс-молекулы нуклеиновой кислоты, проанализированной на стадии г). Сравнение экспрессии белка с предлагаемой в изобретении молекулы нуклеиновой кислоты с экспрессией белка с референс-молекулы нуклеиновой кислоты осуществляют согласно процедуре, представленной в настоящем описании, прежде всего в контексте предлагаемой в изобретении искусственной молекулы нуклеиновой кислоты.
Кроме того, в настоящем изобретении предложен наиболее предпочтительный способ идентификации элемента 3'-нетранслируемой области (3'-UTR-элемента) и/или элемента 5'-нетранслируемой области (5'-UTR-элемента), который обеспечивает высокую эффективность трансляции искусственной молекулы нуклеиновой кислоты, включающий следующие стадии, на которых:
а) подпитывают/инкубируют клетки с меченым нуклеотидом для его включения в новые транскрибированные молекулы РНК (мечение с вытеснением метки);
б) выделяют общую РНК из клеток в первый момент времени и по меньшей мере в один второй более поздний момент времени;
в) экстрагируют меченые молекулы РНК из общей РНК, выделенной на стадии б);
г) измеряют количество/число копий транскрипта различных видов мРНК, присутствующих в меченой РНК;
д) рассчитывают отношение количества/числа копий транскрипта видов мРНК, присутствующих по меньшей мере в один второй более поздний момент времени, к количеству/числу копий транскрипта видов мРНК, присутствующих в первый момент времени;
е) ранжируют виды мРНК в зависимости от величины отношения, определенного на стадии д);
ж) отбирают наиболее стабильные виды мРНК;
з) определяют нуклеотидную последовательность 3'- и/или 5'-UTR наиболее стабильных видов мРНК, отобранных на стадии ж);
и) синтезируют 3'- и/или 5'-UTR-элемент, содержащийся в 3'- и/или 5'-UTR, определенной на стадии з);
к) комбинируют 3'- и/или 5'-UTR-элемент, синтезированный на стадии и), с открытой рамкой считывания с получением предлагаемой в изобретении нуклеиновой кислоты, указанной в настоящем описании; и
л) необязательно сравнивают экспрессию открытой рамки считывания, присутствующей в предлагаемой в изобретении нуклеиновой кислоте, с экспрессией открытой рамки считывания, присутствующей в нуклеиновой референс-кислоте, не содержащей 3'- и/или 5'-UTR-элемент, указанный в настоящем описании.
При этом подробное описание и предпочтительные варианты осуществления изобретения, представленные выше для предлагаемых в изобретении способов, можно применять и в данном случае с учетом соответствующих ограничений, указанных для стадий а)-л).
В частности, для подпитки на стадии а) предлагаемого в изобретении способа предпочтительно применяют следующие меченые нуклеотиды: 4-тиоуридин (4sU), 2-тиоуридин, 6-тиогуанозин, 5-этинилуридин (EU), 5-бромуридин (BrU), биотин-16-аминоаллилуридин, 5-аминоаллилуридин, 5-аминоаллилцитидин и т.д. Наиболее предпочтительным является 4-тиоуридин (4sU). 4-тиоуридин предпочтительно применяют в концентрации 100-500 мкМ. В альтернативном варианте можно применять радиоактивно меченые нуклеотиды, например, уридин-3Н. Можно применять комбинации указанных выше меченых нуклеотидов. Наиболее предпочтительной является комбинация 4-тиоуридина и 6-тиогуанозина.
Инкубацию клеток с меченым нуклеотидом на стадии а) можно варьировать. Наиболее предпочтительно продолжительность инкубации (время подпитки) составляет от 10 мин до 24 ч. Наиболее предпочтительным является период времени от 2 до 6 ч, более предпочтительно от 2 до 3 ч.
Клетки, которые можно применять в способе, предлагаемом в изобретении, включают, в частности, клеточные линии, первичные клетки, клетки в ткани или организме индивидуумов. В конкретных вариантах осуществления изобретения пригодными для применения согласно настоящему изобретению могут быть типы клеток, позволяющие осуществлять культивирование клеток. Наиболее предпочтительными являются клетки млекопитающих, например, человеческие клетки и мышиные клетки. В наиболее предпочтительных вариантах осуществления изобретения применяют человеческие клеточные линии HeLa, HEPG2 и U-937 и мышиные клеточные линии NIH3T3, JAWSII L929. Кроме того, наиболее пригодными являются первичные клетки, в наиболее предпочтительных вариантах осуществления изобретения можно применять человеческие кожные фибробласты (HDF). В альтернативном варианте мечеными нуклеотидами можно обрабатывать также ткань индивидуума и после периода инкубации выделять РНК из ткани согласно стадии в).
Для определения наиболее стабильных мРНК в клетке (типе) общую РНК экстрагируют в первый момент времени, указанный выше, например, через 0-6 ч после мечения, предпочтительно через 3 ч после мечения, и во второй более поздний момент времени, указанный выше, например, через 3-48 ч после мечения, предпочтительно через 10-24 ч, наиболее предпочтительно через 15 ч после мечения. Второй более поздний момент времени наступает по меньшей мере через 10 мин после первого момента времени.
На стадии е) виды мРНК ранжируют в зависимости от величины отношения, рассчитанного на стадии д). В этом контексте наиболее предпочтительно отбирают 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,8%, 0,9%, 1%, 2%, 3%, 4%, 5%, 10%, 15%, 20% наиболее стабильных видов мРНК.
В этом контексте предпочтительно также отбирают такие виды мРНК, для которых число копий транскрипта/количество видов мРНК во второй более поздний момент времени по сравнению с первым моментом времени составляет по меньшей мере 50% (0,5-кратное), по меньшей мере 60% (0,6-кратное), по меньшей мере 70% (0,7-кратное), по меньшей мере 90% (0,9-кратное) или по меньшей мере 95% (0,95-кратное). Этот вариант осуществления изобретения является наиболее предпочтительным, если РНК выделяют через 3 ч (первый момент времени) и через 15 ч (второй момент времени) после мечения.
В альтернативном варианте или дополнительно отбирают такие виды мРНК, которые характеризуются величиной отношения, рассчитанного на стадии д), соответствующего по меньшей мере 100% средней величины отношения, рассчитанной для всех проанализированных видов мРНК. Более предпочтительно отбирают такие виды мРНК, которые характеризуются величиной отношения, составляющей по меньшей мере 150% и более предпочтительно по меньшей мере 200%, и наиболее предпочтительно по меньшей мере 300% средней величины отношения, рассчитанной для всех проанализированных видов мРНК.
На следующей стадии предлагаемого в изобретении способа определяют нуклеотидную последовательность 3'- и/или 5'-UTR наиболее стабильных видов мРНК, отобранных на стадии ж), и на стадии и) синтезируют 3'- и/или 5'-UTR-элемент, например, с помощью ПЦР-амплификации. Праймеры, применяемые для ПЦР, предпочтительно могут содержать сайты рестрикции для клонирования. Альтернативно этому можно синтезировать 3'- и/или 5'-UTR-элемент (например, путем химического синтеза или отжига олигонуклеотидов).
На стадии к) предлагаемого в изобретении способа комбинируют ПЦР-фрагмент или синтезированную последовательность с открытой рамкой считывания, получая искусственную нуклеиновую кислоту, содержащую 3'-и/или 5'-UTR-элемент, предлагаемый в изобретении. Предпочтительно ПЦР-фрагмент или последовательность можно клонировать в векторе.
Наиболее предпочтительный вариант осуществления изобретения относится к включающему стадии а)-л) способу идентификации элементов 3'-нетранслируемой области (3'-UTR-элементов) и/или элементов 5'-нетранслируемой области (5'-UTR-элементов), где 3'-UTR-элементы и/или 5'-UTR-элементы пролонгируют производство белка с искусственной молекулы нуклеиновой кислоты, содержащей по меньшей мере один из 3'-UTR-элементов и/или по меньшей мере один из 5'-UTR-элементов.
Следующий объект настоящего изобретения относится также к способу создания искусственной молекулы нуклеиновой кислоты, в котором синтезируют искусственную молекулу нуклеиновой кислоты, содержащую по меньшей мере одну открытую рамку считывания и по меньшей мере один 3'-UTR-элемент и/или по меньшей мере один 5'-UTR-элемент, идентифицированный с помощью предлагаемого в настоящем изобретении способа идентификации 3'-UTR-элемента и/или 5'-UTR-элемента, указанного в настоящем описании. Синтез искусственной молекулы нуклеиновой кислоты, как правило, осуществляют с помощью методов, известных специалисту в данной области, например, методов клонирования, например, общеизвестных методов или представленных в настоящем описании.
Предпочтительно вектор, предлагаемый в настоящем изобретении, который представлен в настоящем описании, применяют в таком предлагаемом в изобретении способе создания искусственной молекулы нуклеиновой кислоты.
Предпочтительно искусственная молекула нуклеиновой кислоты, созданная с помощью такого способа получения искусственной молекулы нуклеиновой кислоты, представляет собой предлагаемую в настоящем изобретении молекулу нуклеиновой кислоты, указанную в настоящем описании.
Кроме того, в настоящем изобретении предложена также искусственная молекула нуклеиновой кислоты, которую можно получать с помощью предлагаемого в настоящем изобретении способа создания искусственной молекулы нуклеиновой кислоты, представленного в настоящем описании.
Представленные ниже чертежи, последовательности и примеры предназначены для дополнительной иллюстрации изобретения. Они не направлены на ограничение сущности изобретения.
На чертежах показано:
на фиг. 1 - последовательности, кодирующие мРНК (т.е. искусственные молекулы нуклеиновой кислоты), которые можно получать путем транскрипции in vitro;
Используются следующие сокращения:
• PpLuc (GC): последовательность мРНК с высоким содержанием GC (GC-обогащенная), кодирующая люциферазу Photinus pyralis; ОРС PpLuc (GC) выделена курсивом;
• А64: поли(А)-последовательность, содержащая 64 аденилата;
• С30: поли(С)-последовательность, содержащая 30 цитидилатов;
• hSL: последовательность гистоновой структуры типа «стебель-петля», взятая из публикации Cakmakci, Lerner, Wagner, Zheng и William F. Marzluff, Mol. Cell. Biol. 28(3), 2008, cc. 1182-1194;
• 32L4: искусственный вариант 5'-нетранслируемой области 5'-UTR человеческого рибосомального белка большой субъединицы 32, в которой отсутствует 5'-концевой олигопиримидиновый тракт. 5'-UTR получают из человеческого рибосомального белка большой субъединицы 32, в которой отсутствует 5'-концевой олигопиримидиновый тракт;
• альбумин7: искусственный вариант 3'-нетранслируемой области (3'-UTR) человеческого альбумина, содержащий три единичные точечные мутации, интродуцированные для того, чтобы удалить сигнал терминации Т7, а также сайты рестрикции HindIII и XbaI.
на фиг. 1А - референс-конструкция, SEQ ID NO: 205, т.е. последовательность мРНК 32L4 - PpLuc(GC) - альбумин7 - А64 - С30 - hSL (R3111);
Описание UTR-элементов человеческого происхождения, которые подвергали экспериментальному тестированию, представлено в таблице 3. Описание UTR-элементов мышиного происхождения, которые подвергали экспериментальному тестированию, представлено в таблице 4;
На фиг. 1Б - Искусственная нуклеиновая кислота (SEQ ID NO: 210), указанная искусственная нуклеиновая кислота содержит протестированную 5'-UTR, соответствующую SEQ ID NO: 1 (подчеркнута одной линией). Все элементы последовательности, представленной на данном чертеже, за исключением подчеркнутого одной линией элемента, идентичны SEQ ID NO: 205. Таким образом, SEQ ID NO: 210 отличается от SEQ ID NO: 205 тем, что содержит другой 5'-UTR-элемент.
[5'-UTR, соответствующая SEQ ID NO: 1] - PpLuc(GC) - альбумин7 - А64 - С30 - hSL;
На фиг. 1В - Искусственная нуклеиновая кислота (SEQ ID NO: 211), указанная искусственная нуклеиновая кислота содержит протестированную 3'-UTR, соответствующую SEQ ID NO: 152 (подчеркнута двойной линией). Все элементы последовательности, представленной на данном чертеже, за исключением подчеркнутого двойной линией элемента, идентичны SEQ ID NO: 205. Таким образом, SEQ ID NO: 211 отличается от SEQ ID NO: 205 тем, что содержит другой 3'-UTR-элемент.
32L4 - PpLuc(GC) - [3'-UTR, соответствующая SEQ ID NO: 152] - А64 - С30 -hSL;
На фиг. 2-9 - средние уровни экспрессии люциферазы и SEM для мРНК, которые анализировали в трех повторностях; т.е. относительные уровни экспрессии PpLuc, стандартизованные относительно RrLuc (представлены средние значения по трем независимым экспериментам и стандартная ошибка среднего (SEM)). Исследовали влияние 5'-UTR-элементов и 3'-UTR-элементов человеческого происхождения (таблица 3) и 5'-UTR-элементов и 3'-UTR-элементов мышиного происхождения (таблица 4) на экспрессию люциферазы с мРНК в сравнении с экспрессией люциферазы с мРНК, представленной на фиг. 1 (референс-конструкция). Данные о конструкциях, содержащих протестированные 5'-UTR-элементы и 3'-UTR-элементы, описанные в таблицах 3 и 4, представлены в примере 3, прежде всего в разделах 3.3 и 3.4. Для этой цели линии клеток, указанные на чертежах, трансфектировали различными мРНК посредством липофекции (фиг. 2: клетки HDF трансфектировали мРНК, имеющими 5'-UTR-элементы и 3'-UTR-элементы человеческого происхождения, указанными в таблице 3; на фиг. 3: клетки HDF трансфектировали мРНК, имеющими 5'-UTR-элементы и 3'-UTR-элементы мышиного происхождения, указанными в таблице 4; на фиг. 4: клетки L929 трансфектировали мРНК, имеющими 5'-UTR-элементы и 3'-UTR-элементы человеческого происхождения, указанными в таблице 3; на фиг. 5: клетки L929 трансфектировали мРНК, имеющими 5'-UTR-элементы и 3'-UTR-элементы мышиного происхождения, указанными в таблице 4; на фиг. 6: клетки HEPG2 трансфектировали мРНК, имеющими 5'-UTR-элементы и 3'-UTR-элементы человеческого происхождения, указанными в таблице 3; на фиг. 7: клетки HEPG2 трансфектировали мРНК, имеющими 5'-UTR-элементы и 3'-UTR-элементы мышиного происхождения, указанными в таблице 4; на фиг. 8: клетки HeLa трансфектировали мРНК, имеющими 5'-UTR-элементы и 3'-UTR-элементы человеческого происхождения, указанными в таблице 3; на фиг. 9: клетки HeLa трансфектировали мРНК, имеющими 5'-UTR-элементы и 3'-UTR-элементы мышиного происхождения, указанными в таблице 4). Более подробные сведения представлены в примере 3, прежде всего в разделе 3.5. На каждой из фиг. 2-9 представлены 96 столбиков, соответствующих 96 лункам в анализе, описанном в примере 3. На фиг. 2-9 96 столбиков расположены друг за другом в следующем порядке A1, B1, C1, D1, […], F12, G12, Н12.
RLU = относительные световые единицы (используются при измерении люциферазной активности).
Примеры
Пример 1: UTR-элементы - кандидаты
Экспрессию мРНК в человеческих и мышиных клетках оценивали экспериментально. Это позволило идентифицировать мРНК, которые экспрессировались в соответствующих клетках. Нуклеотидную последовательность 5'- и/или 3'-UTR видов мРНК определяли путем поиска в базе данных, проверяли и корректировали на основе полученных путем высокопроизводительного секвенирования данных о клеточных транскриптомах, и амплифицировали с помощью ПЦР или синтезировали с помощью отжига олигонуклеотидов.
Поскольку идентифицированные мРНК происходят из их нативного клеточного окружения, то эти мРНК рассматривались в качестве мРНК дикого типа:
SEQ ID NO: 1-72 соответствуют человеческим 5'-UTR-элементам дикого типа;
SEQ ID NO: 73-136 соответствуют мышиным 5'-UTR-элементам дикого типа;
SEQ ID NO: 152-173 соответствуют человеческим 3'-UTR-элементам дикого типа;
SEQ ID NO: 174-203 соответствуют мышиным 3'-UTR-элементам дикого типа.
Хотя несколько из этих UTR-элементов являлись известными (например, они присутствуют в их окружении дикого типа), данный подход позволил идентифицировать также новые 5'-UTR-элементы и новые 3'-UTR-элементы, т.е. 5'-UTR-элементы и 3'-UTR-элементы, которые, как было установлено при создании изобретения, экспрессируются в человеческих клетках и мышиных клетках соответственно, но которые не были известны из публичных баз данных (NCBI):
В частности, в группе, состоящей из человеческих 5'-UTR-элементов, имеющих SEQ ID NO: 1-72, следующие 5'-UTR-элементы дикого типа отличаются от 5'-UTR-элементов, известных из публичных баз данных (NCBI): SEQ ID NO: 45, SEQ ID NO: 47, SEQ ID NO: 49.
В группе, состоящей из мышиных 5'-UTR-элементов, имеющих SEQ ID NO: 73-136, следующие 5'-UTR-элементы дикого типа отличаются от 5'-UTR-элементов, известных из публичных баз данных (NCBI): SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 84, SEQ ID NO: 85, SEQ ID NO: 90, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 98, SEQ ID NO: 106, SEQ ID NO: 109, SEQ ID NO: 115, SEQ ID NO: 118, SEQ ID NO: 125, SEQ ID NO: 127, SEQ ID NO: 131, SEQ ID NO: 135.
В группе, состоящей из мышиных 3'-UTR-элементов, имеющих SEQ ID NO: 174-203, следующие 3'-UTR-элементы дикого типа отличаются от 3'-UTR-элементов, известных из публичных баз данных (NCBI): SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 197, SEQ ID NO: 200.
Отличия новых идентифицированных 5'-UTR-элементов и новых идентифицированных 3'-UTR-элементов от известных 5'-UTR-элементов и известных 3'-UTR-элементов соответственно представлены в таблицах 1 и 2. В частности, эти новые идентифицированные элементы не были ранее описаны в качестве 3'-UTR-элементов или 5'-UTR-элементов соответственно.
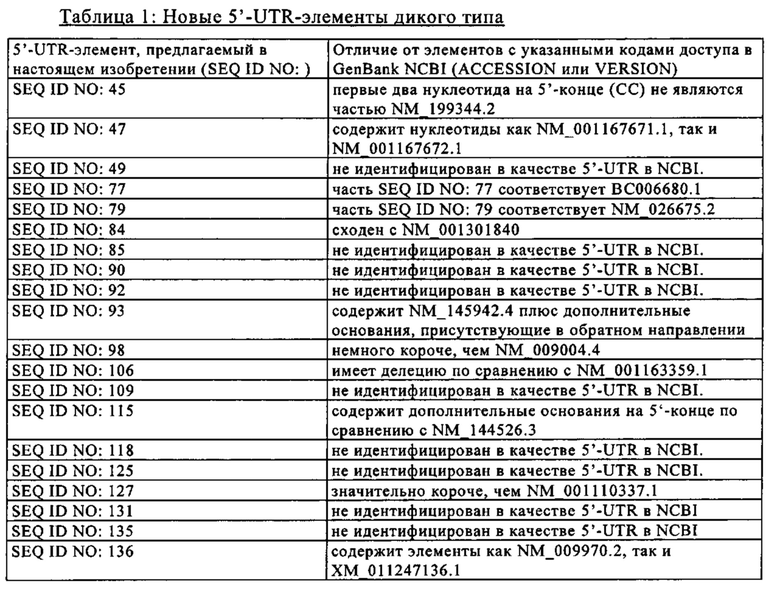
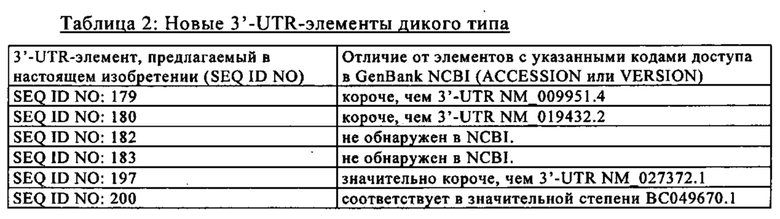
Искусственные 5'-UTR-элементы и искусственные 3'-UTR-элементы
В некоторых случаях получали искусственные 5'-UTR-элементы и искусственные 3'-UTR-элементы. Это осуществляли путем модификации 5'-UTR-элементов и 3'-UTR-элементов дикого типа с помощью основанного на ПЦР подхода с использованием модифицированных праймеров следующим образом:
(I) Некоторые триплеты ATG в последовательностях 5'-UTR (если они присутствовали) конвертировали в триплет TAG. (II) Кроме того, наличие определенного сайта, расщепляемого специфической рестриктазой (если он присутствовал), рассматривали как нежелательное, в том случае, когда считали, что указанный определенный сайт расщепления будет мешать последующим экспериментам по клонированию. Считали, что сайт расщепления, присутствующий в последовательности дикого типа, будет мешать последующим экспериментам по клонированию (таким, которые описаны в примерах 2 и 3), если рестриктаза применяемая в последующих экспериментах по клонированию, может распознавать и расщеплять 3'-UTR-элемент дикого типа или 5'-UTR-элемент дикого типа. Поскольку такое внутреннее расщепление 5'-UTR-элементов и 3'-UTR-элементов было нежелательным, то сайты, расщепляемые указанной специфической рестриктазой, удаляли путем замены одного нуклеотида в сайте, расщепляемом указанной специфической рестриктазой, на комплементарный нуклеотид, удаляя тем самым сайт, расщепляемый указанной специфической рестриктазой.
SEQ ID NO: 137 (на основе SEQ ID NO: 3), SEQ ID NO: 138, (на основе SEQ ID NO: 9), SEQ ID NO: 139 (на основе SEQ ID NO: 14), SEQ ID NO: 140 - (на основе SEQ ID NO: 17), SEQ ID NO: 141 (на основе SEQ ID NO: 18), SEQ ID NO: 142 (на основе SEQ ID NO: 29),SEQ ID NO: 143 (на основе SEQ ID NO: 31), SEQ ID NO: 144 (на основе SEQ ID NO: 42), SEQ ID NO: 145 (на основе SEQ ID NO: 43), SEQ ID NO: 146 (на основе SEQ ID NO: 52), SEQ ID NO: 147 (на основе SEQ ID NO: 109), SEQ ID NO: 148 (на основе SEQ ID NO: 110), SEQ ID NO: 149 (на основе SEQ ID NO: 119), SEQ ID NO: 150 (на основе SEQ ID NO: 120) и SEQ ID NO: 151 (на основе SEQ ID NO: 136) представляют собой искусственные 5'-UTR-элементы. SEQ ID NO: 204 (на основе SEQ ID NO: 192) представляет собой искусственный 3'-UTR-элемент. Точные отличия от соответствующих последовательностей дикого типа указаны выше.
В целом, SEQ ID NO: 1-136 можно рассматривать как 5'-UTR последовательности дикого типа, a SEQ ID NO: 137-151 можно рассматривать как искусственные последовательности 5'-UTR; SEQ ID NO: 152-203 можно рассматривать как 3'-UTR последовательности дикого типа, a SEQ ID NO: 204 можно рассматривать как искусственную последовательность 3'-UTR.
В целом, в данном примере представлены несколько 5'-UTR-элементов и 3'-UTR-элементов (дикого типа и искусственные), каждый из которых можно тестировать в отношении их относительного влияния на эффективность трансляции, по сравнению с референс-UTR-элементами (как описано ниже в примерах 2 и 3).
Пример 2: Референс-UTR-элементы и содержащая их референс-конструкция
На фиг. 1А представлена последовательность РНК референс-конструкции, используемой в настоящем изобретении. Конструировали также вектор для транскрипции in vitro, содержащий последовательность ДНК, соответствующую последовательности РНК, представленной на фиг. 1А. Вектор содержал промотор Т7, искусственный вариант 5'-нетранслируемой области (5'-UTR) 32L4 (рибосомальный белок большой субъединицы 32), GC-обогащенную последовательность (открытую рамку считывания, ОРС), кодирующую ген люциферазы Photinus pyralis (PpLuc(GC)), искусственный вариант 3'-нетранслируемой области (3'-UTR) человеческого альбумина (ALB), альбумин7. Поли(А)-последовательность А64, за которой следовали С30 и последовательность гистоновой структуры типа «стебель-петля», располагались с 3'-стороны относительно альбумина7. За последовательностью гистоновой структуры типа «стебель-петля» находился сайт рестрикции, используемый для линеаризации вектора перед осуществлением транскрипции in vitro.
ПЦР-фрагменты, соответствующие последовательностям, описанным в примере 1, индивидуально клонировали в векторе, содержащем последовательность ДНК, которая соответствовала последовательности РНК, представленной на фиг. 1. В тех случаях, когда последовательности дикого типа, описанные в примере 1, содержали триплеты ATG в 5'-UTR и/или нежелательные сайты рестрикции в 5'-UTR или 3'-UTR, применяли соответствующие искусственные последовательности, идентифицированные в примере 1 (например, SEQ ID NO: 137 применяли вместо SEQ ID NO: 3).
Более подробно, для создания конструкции для тестирования 5'-UTR-элемента-кандидата, подчеркнутый одной линией 5'-UTR-элемент, представленный на фиг. 1А, заменяли на подлежащий тестированию (дикого типа или искусственный) 5'-UTR-элемент-кандидат (пример 1) (соответствующий пример представлен на фиг. 1Б); и для создания конструкции для тестирования 3'-UTR-элемента-кандидата, подчеркнутый двойной линией 3'-UTR-элемент, представленный на фиг. 1А, заменяли на подлежащий тестированию (дикого типа или искусственный) 5'-UTR-элемент-кандидат (пример 1) (соответствующий пример представлен на фиг. 1В). Полученные векторы или плазмиды (содержащие ДНК, соответствующую, например, последовательности РНК, например, РНК, представленной на фиг. 1А-В) можно обозначать также как ДНК-матрицы.
ДНК-матрицы линеаризовали и транскрибировали in vitro с использованием РНК-полимеразы Т7 (WO 2015/101416). Затем ДНК-матрицу расщепляли путем обработки ДНКазой. Транскрипты мРНК содержали 5'-кэп-структруру, полученную путем добавления избытка N7-метилгуанозин-5'-трифосфат-5'-гуанозина к реакционной смеси для транскрипции. Полученную таким путем мРНК очищали и ресуспендировали в воде. Полученные таким путем мРНК для тестирования UTR-элементов соответствовали мРНК, представленной на фиг. 1А (референс-конструкция), за исключением того, что 5'-UTR-элемент или 3'-UTR-элемент референс-конструкции был заменен на соответствующий подлежащий тестированию UTR-элемент.
Пример 3: Эффективность трансляции UTR-элементов-кандидатов в сравнении с референс-конструкцией
Экспериментально тестировали 5'-UTR-элементы человеческого происхождения или мышиного происхождения или 3'-UTR-элементы человеческого происхождения или мышиного происхождения. В контексте данного примера понятие «человеческое происхождение» может относиться либо к человеческой последовательности дикого типа (например, SEQ ID NO: 1), либо к искусственной последовательности, сконструированной на основе человеческой последовательности дикого типа путем замены одного или большего количества оснований (например, SEQ ID NO: 137), соответствующим образом применяют и понятие «мышиное происхождение». Более подробные данные о том, каким образом искусственные последовательности созданы на основе последовательностей дикого типа, представлены в таблицах 3 и 4 в примере 1.
Экспериментально тестировали, оказывают ли 5'- или 3'-UTR (таблицы 3 и 4, ниже) благоприятное действие на эффективность трансляции. Это осуществляли с помощью способа, включающего стадии, на которых:
(I) трансфектируют клетки млекопитающих искусственной молекулой нуклеиновой кислоты и измеряют количества экспрессированного белка, кодируемого ОРС искусственной молекулы нуклеиновой кислоты в один или два определенных момента времени после трансфекции (через 24 и 48 ч),
(II) трансфектируют клетки млекопитающих референс-молекулой нуклеиновой кислоты (фиг. 1А) и измеряют количества экспрессированного белка, кодируемого ОРС референс-молекулы нуклеиновой кислоты в те же самые один или два момента времени после трансфекции (через 24 и 48 ч),
(III) рассчитывают отношение количества белка, экспрессированного с искусственной молекулы нуклеиновой кислоты, к количеству белка, экспрессированного с референс-молекулы нуклеиновой кислоты,
При этом величина отношения, рассчитанного на стадии (III), составляет ≥1.
Указанное отношение ассоциировано с высокой эффективностью трансляции.
Все последовательности UTR, экспериментально тестированные в рассматриваемом примере, обозначали также как «экспериментально тестированные UTR-элементы» или «тестированные UTR-элементы», или «экспериментально тестированные UTR» или «тестированные UTR».
Искусственная молекула нуклеиновой кислоты, указанная в пункте (I), содержала тестированный UTR-элемент. В частности, искусственная молекула нуклеиновой кислоты (мРНК) не отличалась по своей структуре от референс-молекулы нуклеиновой кислоты (фиг. 1А), за исключением того, что либо 5'-UTR-элемент, либо 3'-UTR-элемент референс-молекулы нуклеиновой кислоты заменен на тестированный UTR-элемент (иллюстративные примеры представлены на фиг. 1Б и 1В).
3.1 UTR-элементы человеческого происхождения
Подробные данные о UTR-элементах человеческого происхождения, которые подвергали экспериментальному тестированию, представлены ниже в таблице 3. Экспериментальное тестирование осуществляли, проводя сравнение с референс-конструкцией, подробно описанной выше и в разделе «Подробное описание конструкции».
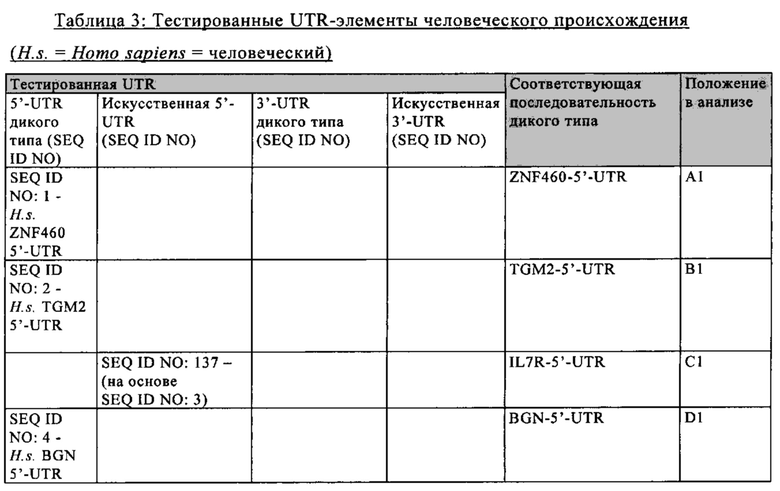
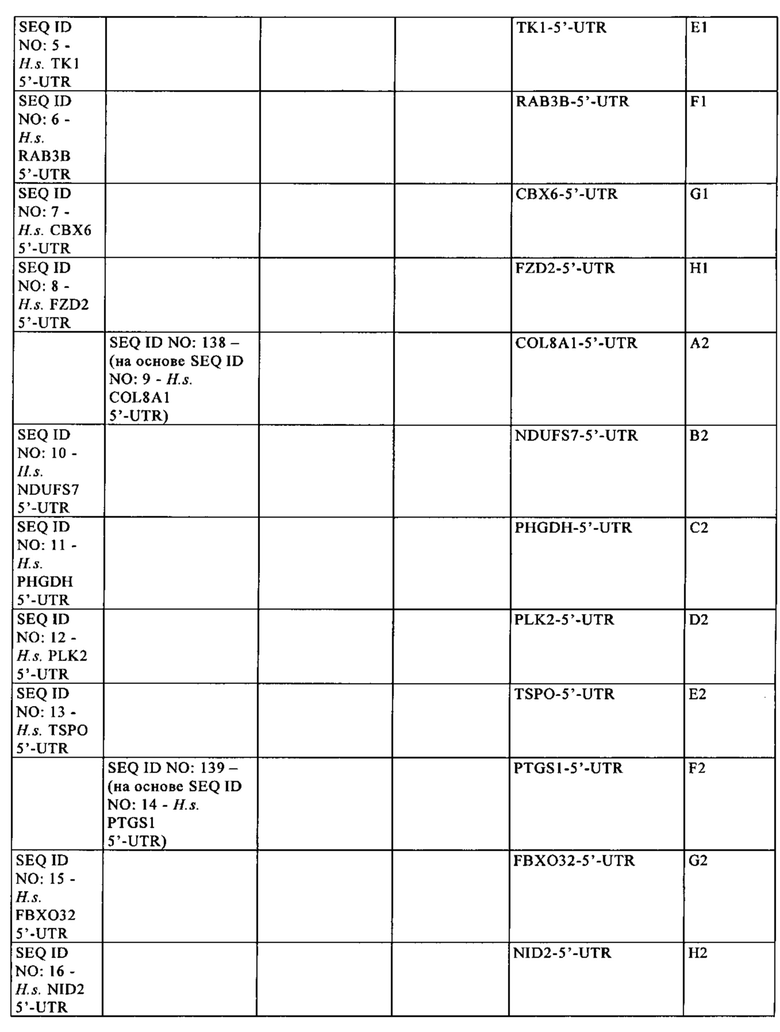
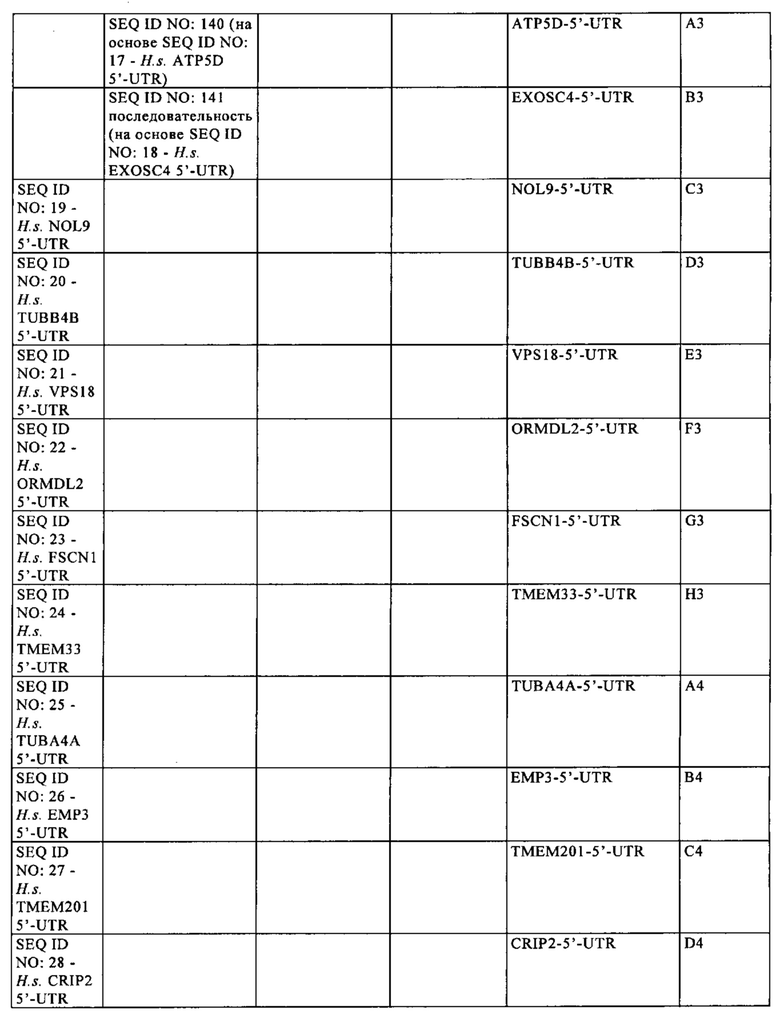
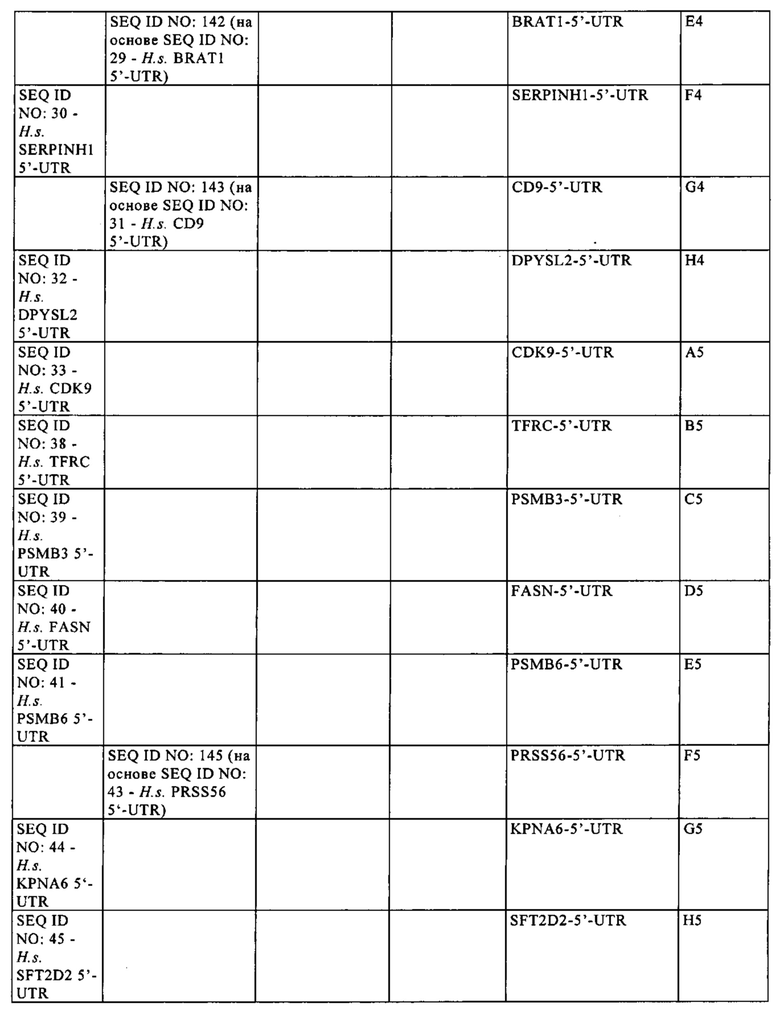
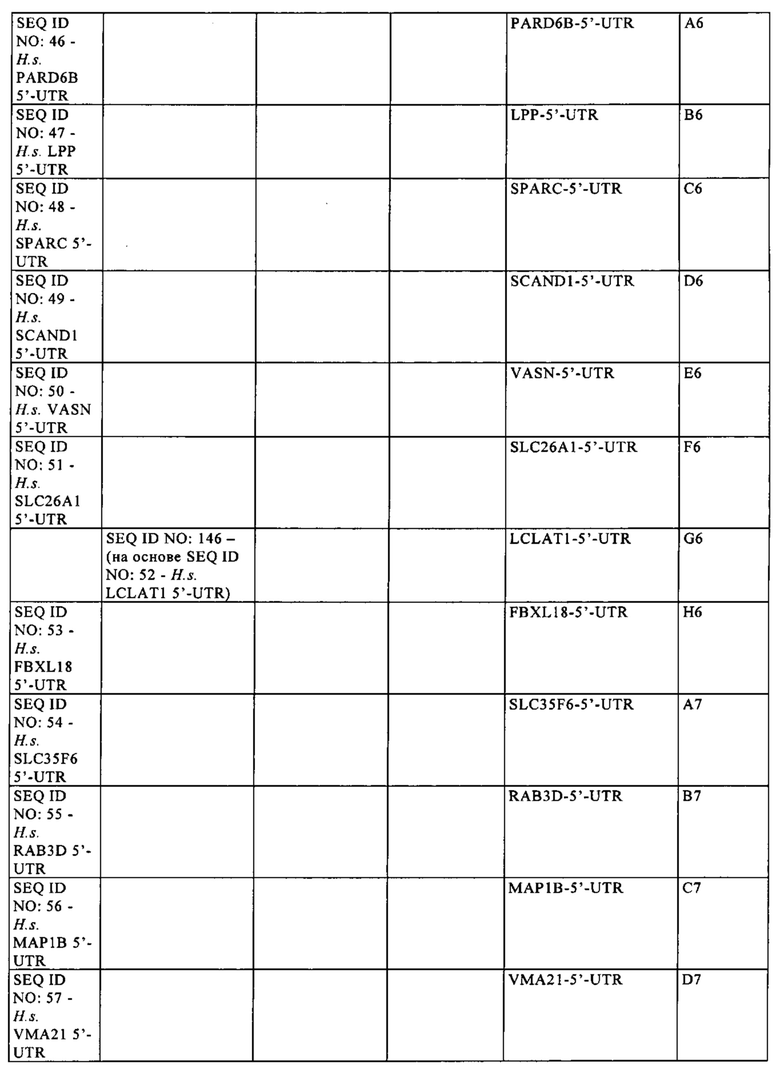
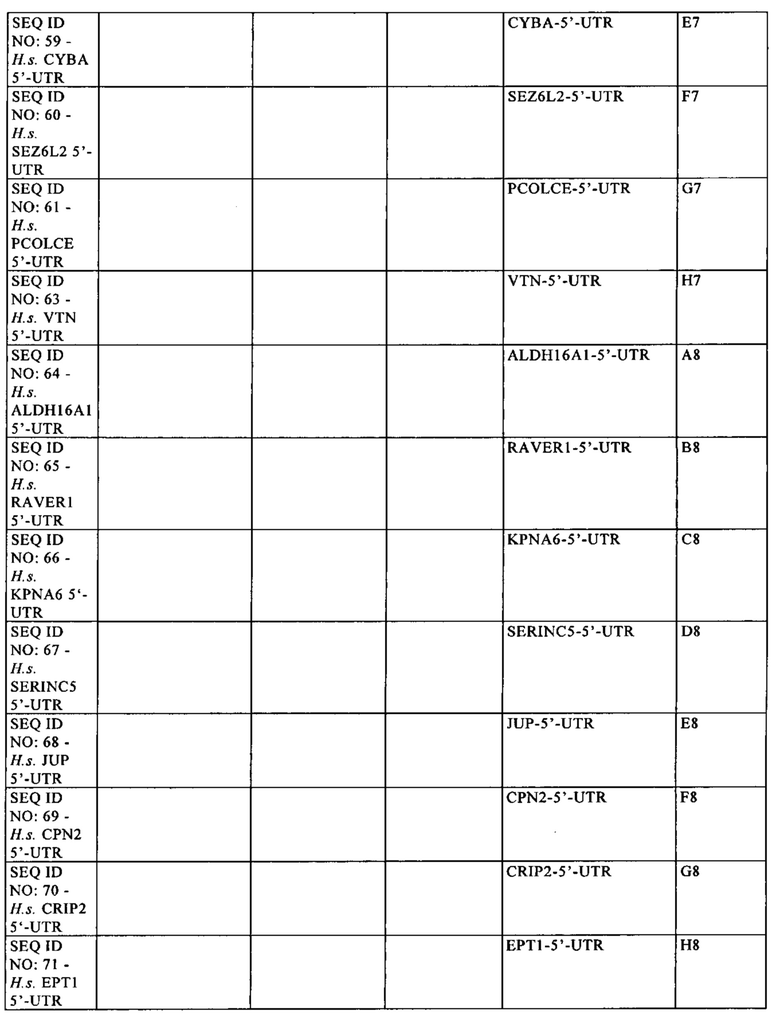
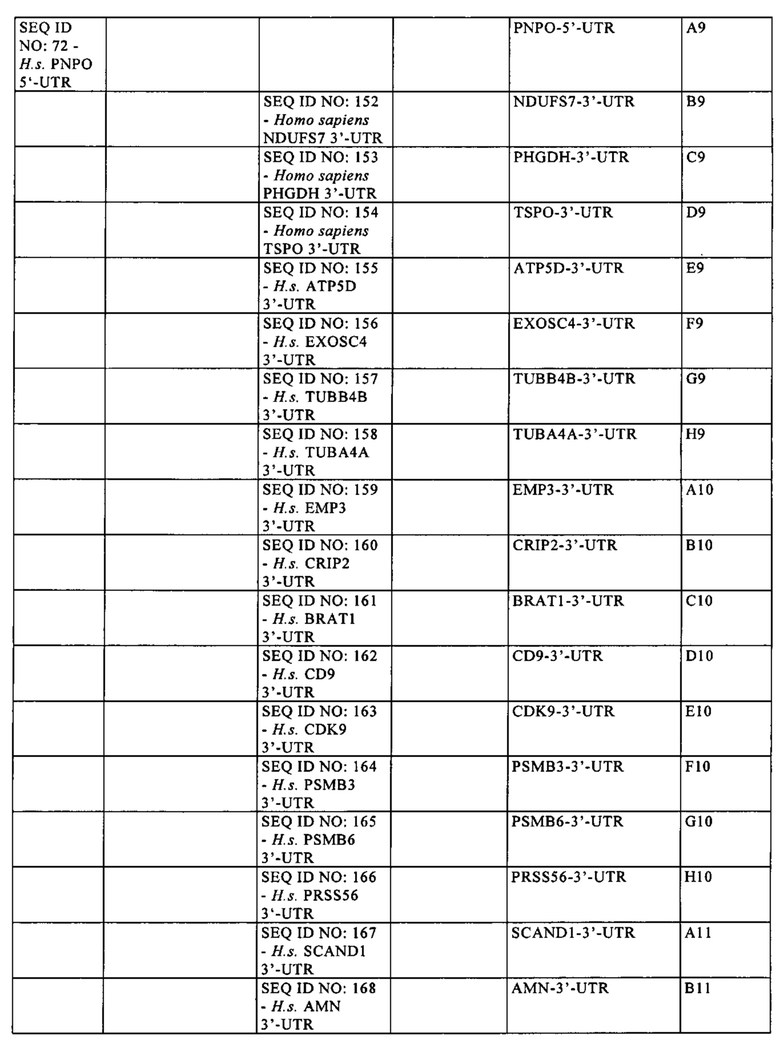
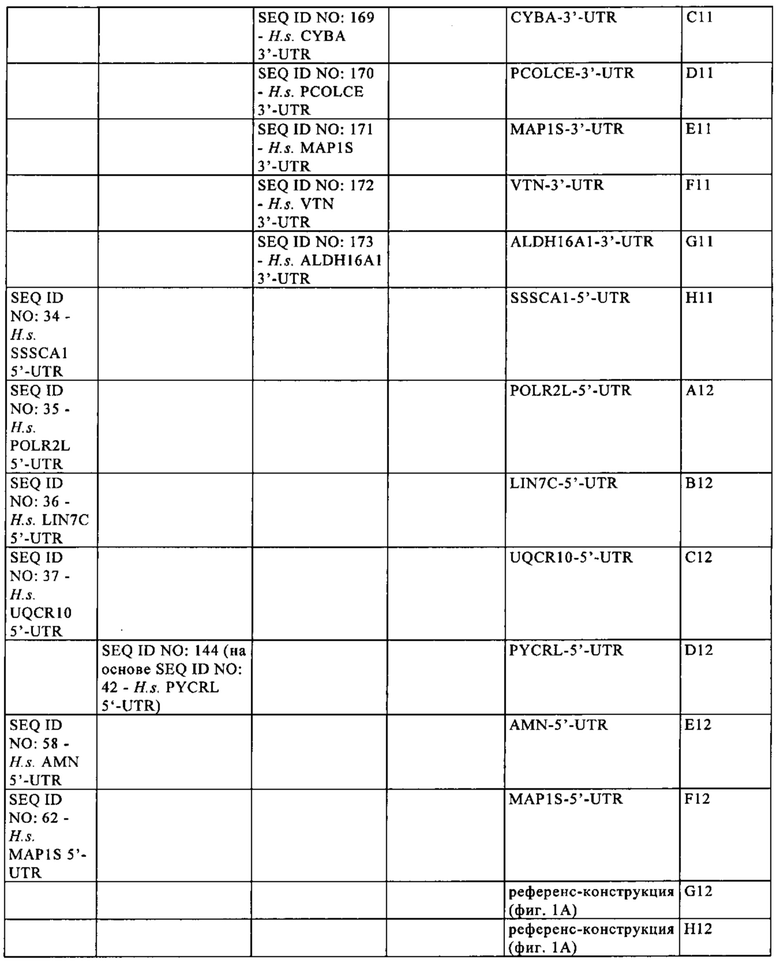
3.2 UTR-элементы мышиного происхождения
Подробные данные о UTR-элементах мышиного происхождения, которые подвергали экспериментальному тестированию, представлены ниже в таблице 4.
Экспериментальное тестирование осуществляли, проводя сравнение с референс-конструкцией, подробно описанной выше и в разделе «Подробное описание конструкции».
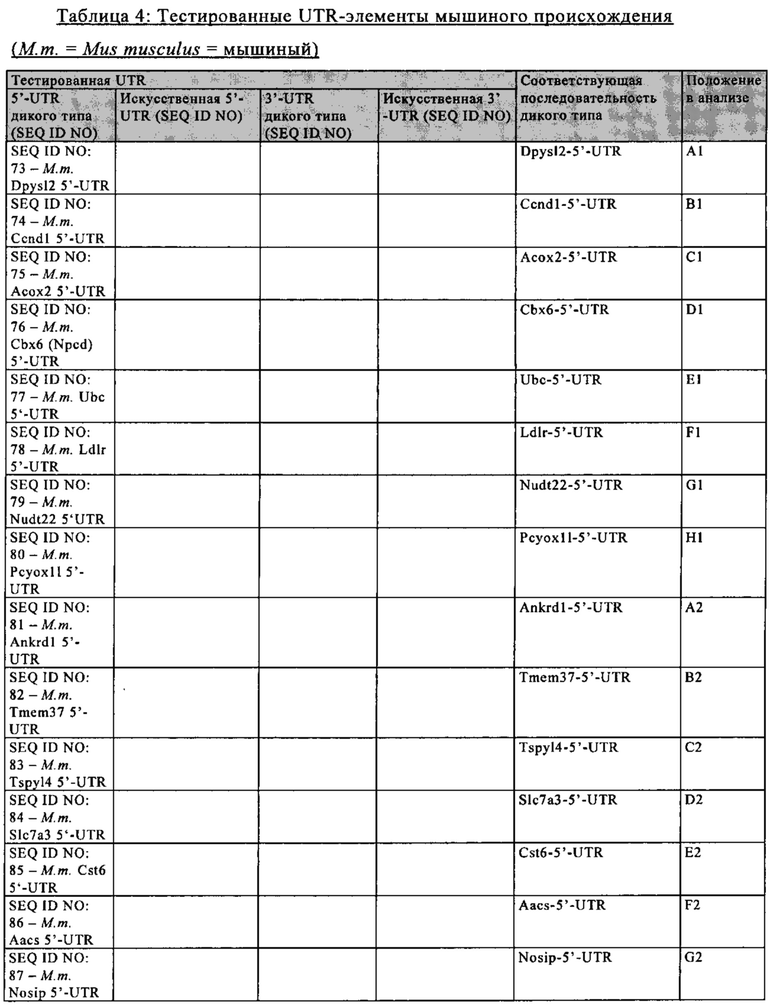
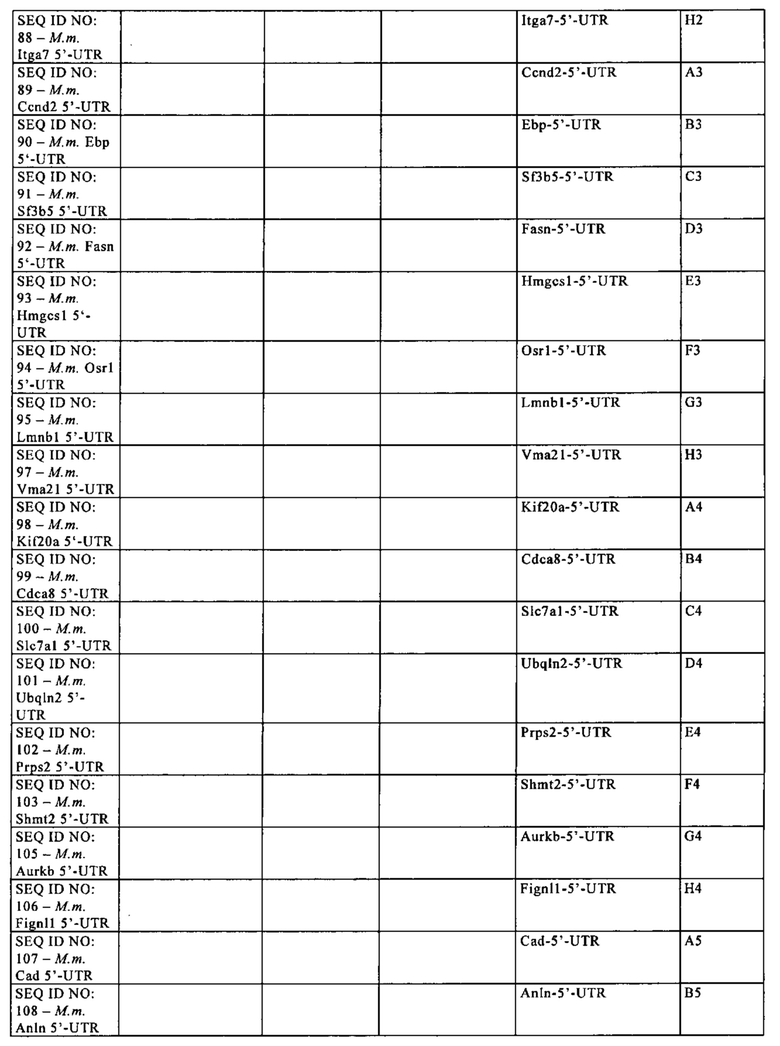
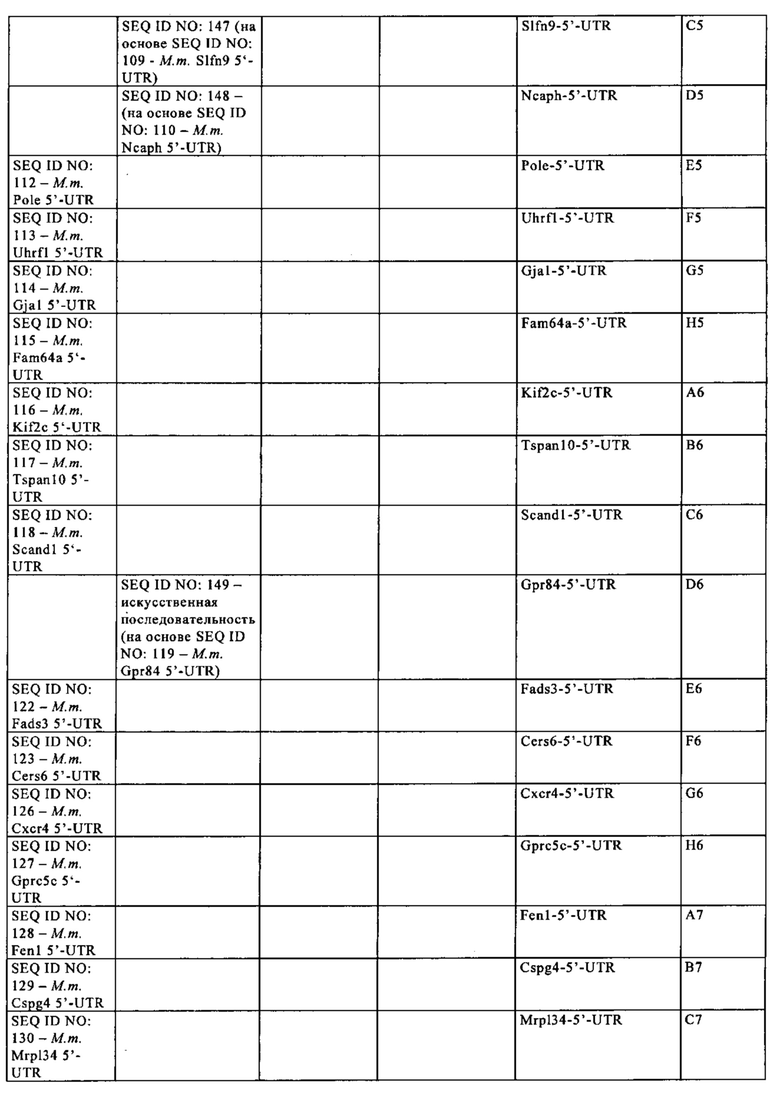
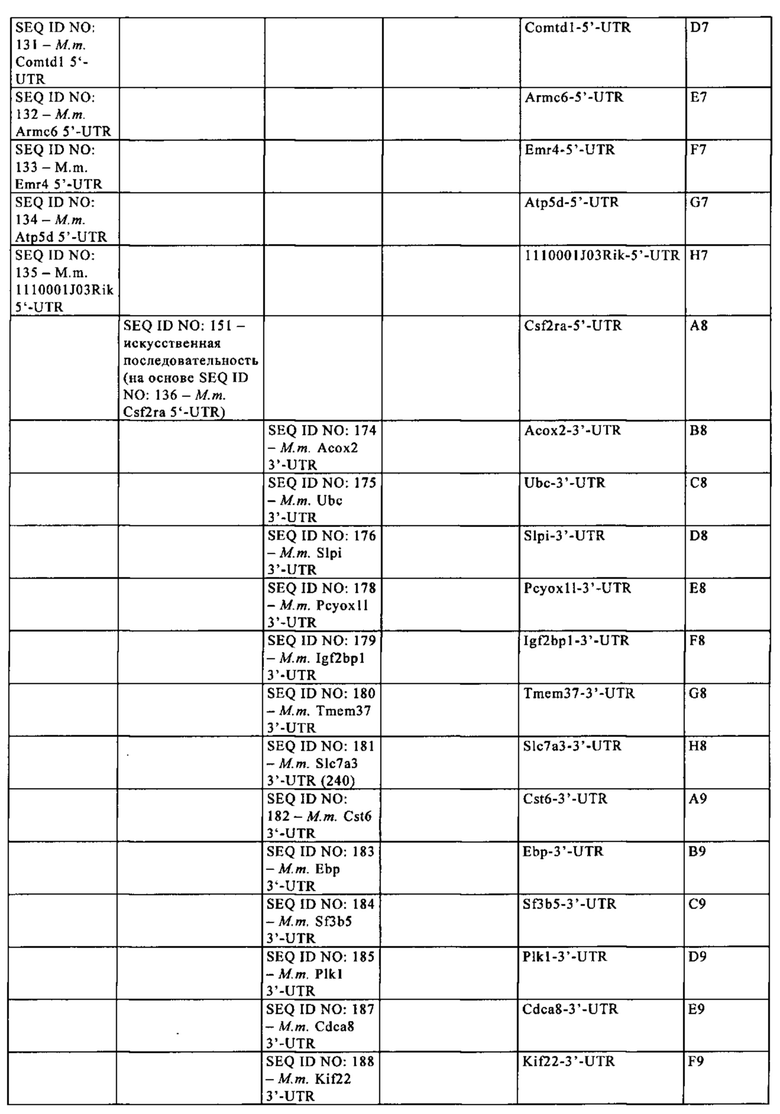
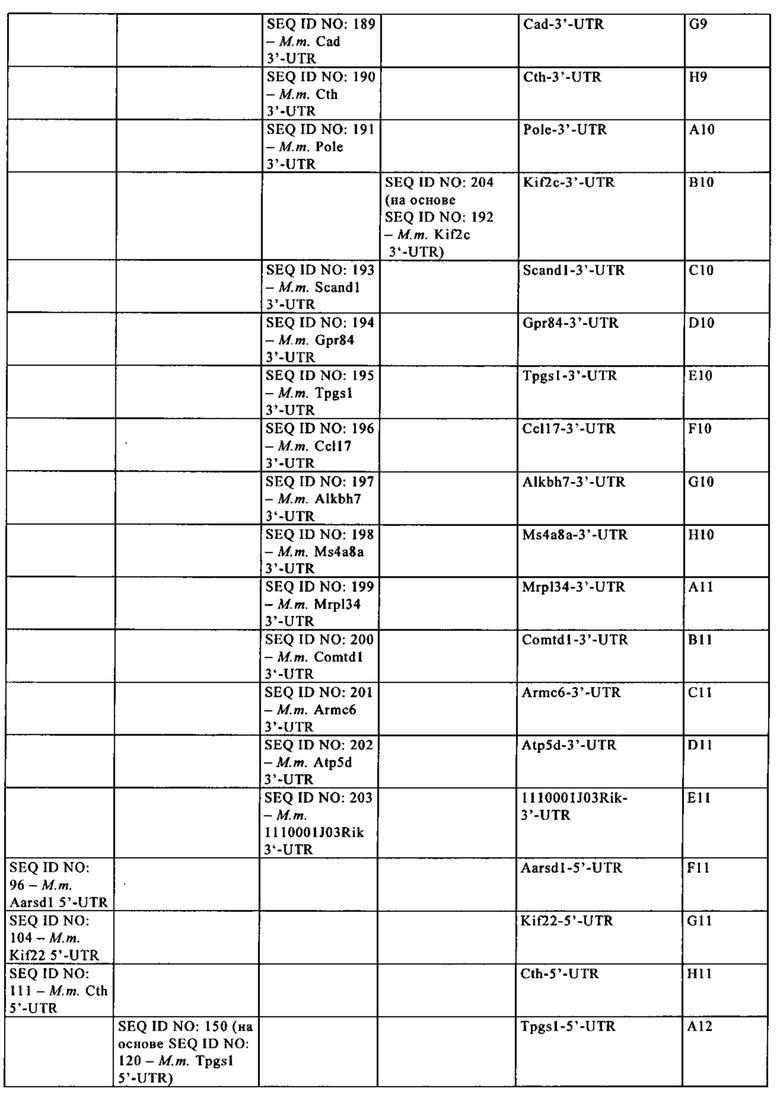
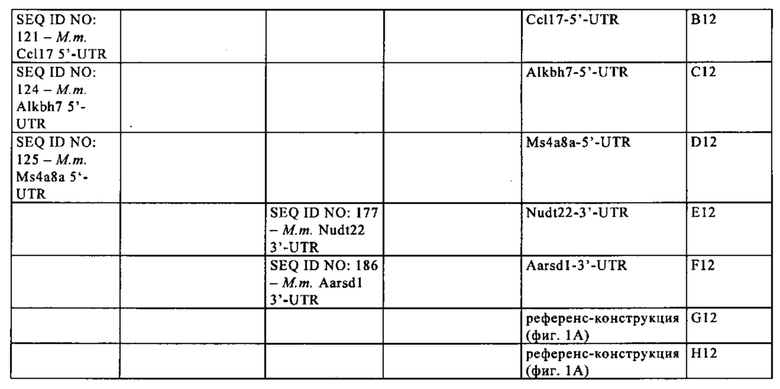
3.3 Подробное описание конструкции
При тестировании 5'-UTR заменяли 5'-UTR референс-конструкции (т.е. 32L4 - PpLuc(GC) - альбумин7- А64 - С30 - hSL; фиг. 1) на «тестируемую» 5'-UTR - т.е. либо на последовательность 5'-UTR дикого типа (последовательность мРНК, соответствующая последовательности ДНК, представленная в таблице 3 или 4, первый столбец), либо на искусственную последовательность 5'-UTR, созданную на ее основе (последовательность мРНК, соответствующая последовательности ДНК, представленная в таблице 3 или 4, второй столбец). Остальные элементы последовательности референс-конструкции оставались без изменений.
В свою очередь, при тестировании 3'-UTR заменяли 3'-UTR референс-конструкции (т.е. 32L4 - PpLuc(GC) - альбумин7- А64 - С30 - hSL; фиг. 1) на «тестируемую» 3'-UTR - т.е. либо на последовательность 3'-UTR дикого типа (последовательность мРНК, соответствующая последовательности ДНК, представленная в таблице 3 или 4, третий столбец), либо на искусственную последовательность 5'-UTR, созданную на ее основе (последовательность мРНК, соответствующая последовательности ДНК, представленная в таблице 3 или 4, четвертый столбец). Остальные элементы последовательности референс-конструкции оставались без изменений.
3.4. Анализ люциферазной активности для определения эффективности трансляции
Эффективность трансляции тестировали экспериментально с помощью анализа на основе трансфекции клеток с использованием различных линий клеток млекопитающих (человеческих, мышиных), а именно, HDF, L929, HepG2 и Hela (см. фиг. 2-9).
Человеческие кожные фибробласты (HDF), L929-клетки, HepG2-клетки и HeLa-клетки высевали в 86-луночные планшеты с плотностью 1×104 клеток на лунку. На следующий день клетки промывали в среде Opti-MEM и затем трансфектировали, используя по 25 нг на лунку мРНК, кодирующей PpLuc, включенной в комплекс с липофектамином 2000, в среде Opti-MEM. Нетрансфектированые клетки служили в качестве контроля. Для контроля эффективности трансфекции наряду с мРНК PpLuc (1 нг мРНК RrLuc на лунку) осуществляли трансфекцию мРНК, кодирующей люциферазу Renilla reniformis (RrLuc). Через 90 мин после начала трансфекции осуществляли замены среды Opti-MEM. Через 24 и 48 ч после трансфекции среду удаляли путем аспирации и клетки лизировали в 100 мкл буфера для лизиса (буфер для пассивного лизиса, фирма Promega). Лизаты хранили при -80° до осуществления измерений люциферазной активности.
Люциферазную активность измеряли в относительных световых единицах (RLU) с помощью ридера для планшетов Hidex Chameleon. Активности Ppluc и Rrluc измеряли последовательно в одном образце с помощью двойного анализа люциферазы. Сначала измеряли активность PpLuc в течение периода измерения, равного 2 с с использованием 20 мкл лизата и 50 мкл буферной системы Beetle-Juice (фирма PJK GmbH). Спустя 1500 мс, измеряли активность RrLuc с использованием 50 мкл буферной системы Renilla-Juice (фирма PJK GmbH).
Эту процедуру осуществляли в 96-луночных планшетах, и каждый тестируемый UTR-элемент (в каркасе содержащей его конструкции, см. раздел 3.3) помещали в соответствующее положение на 96-луночном планшете. Использовали два 96-луночных планшета, один для тестирования UTR-элементов человеческого происхождения и один для тестирования UTR-элементов мышиного происхождения. В каждом планшете референс-конструкция (соответствующая последовательности мРНК, представленной на фиг. 1А) находилась в положениях G12 и Н12. Тестируемые UTR-элементы находились в положениях, указанных в последней колонке в Таблицах 3 и 4 соответственно. Например, конструкция, содержащая 3'-UTR мышиного Aarsd1 (SEQ ID NO: 186) находилась в положении F12 (см. таблицу 4).
Люциферазную активность измеряли через 24 ч (1d, 24 ч) после трансфекции клеток и затем еще раз через 48 ч (2d, 48 ч) после трансфекции клеток.
Результаты этого анализа описаны ниже в разделе 3.5.
3.5 Результаты - Определение UTR-элементов, ассоциированных с высокой эффективностью трансляции
Результаты оценки экспрессии с помощью указанного анализа (см. раздел 3.4, выше), измеренные через 24 ч (1d, 24 ч) и еще раз через 48 ч (2d, 48 ч) после трансфекции в различных линиях клеток млекопитающих (HDF, L929, HepG2 и Hela), представлены на фиг. 2-9. Следует отметить, что в данном случае применяли два набора 96-луночных планшетов, один был предназначен для UTR-элементов человеческого происхождения и один был предназначен для UTR-элементов мышиного происхождения.
В то время как данные на фиг. 2-9 относятся к конкретным положениям на 96-луночном планшете (например, А1), в таблицах 3 и 4 конкретные протестированные 5'- или 3'-UTR-элементы соотнесены с конкретными положениями на 96-луночном планшете. Например, из таблицы 3 можно установить, что в положении А1 96-луночного планшета с протестированными человеческими UTR-элементами, тестировали ZNF460-5'-UTR-элемент (SEQ ID NO: 1) и т.д.
Определяли группу наиболее предпочтительных UTR-элементов (которые обозначали также как группу «конечного отбора»). Эта группа содержала 5'-UTR-элементы и 3'-UTR-элементы, которые характеризовались эффективностью трансляции, измеренной через 1 день (24 ч), равной или более высокой, предпочтительно более высокой, чем эффективность референс-конструкции (фиг. 1А), по меньшей мере для одной из протестированных клеточных линий. Эту группа подразделяли на четыре подгруппы: (I) 5'-UTR-элементы человеческого происхождения (см. таблицу 5), (II) 3'-UTR-элементы человеческого происхождения (см. таблицу 6), (III) 5'-UTR-элементы мышиного происхождения (см. таблицу 7), (IV) 3'-UTR-элементы мышиного происхождения (см. таблицу 8)
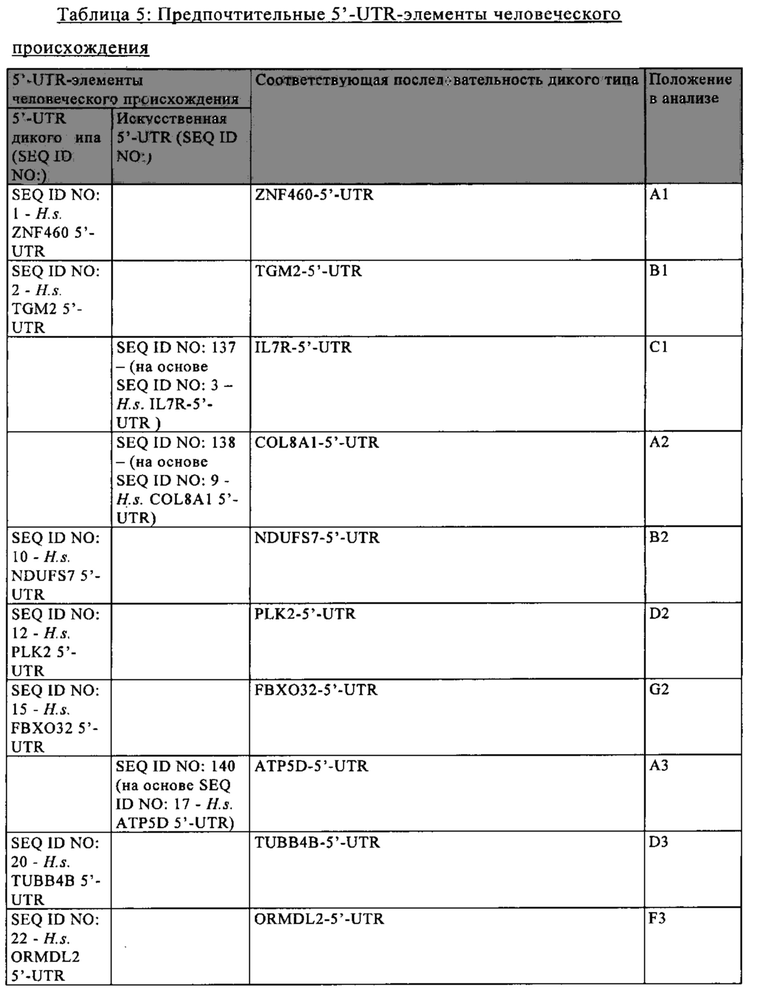
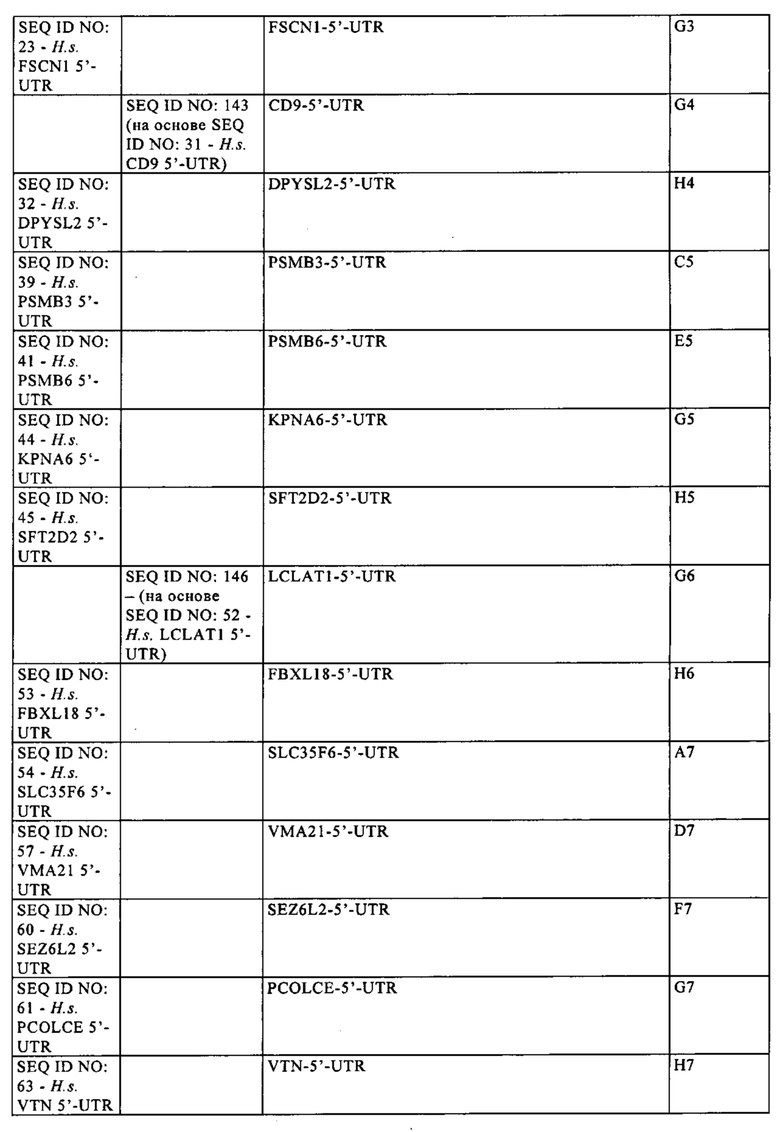
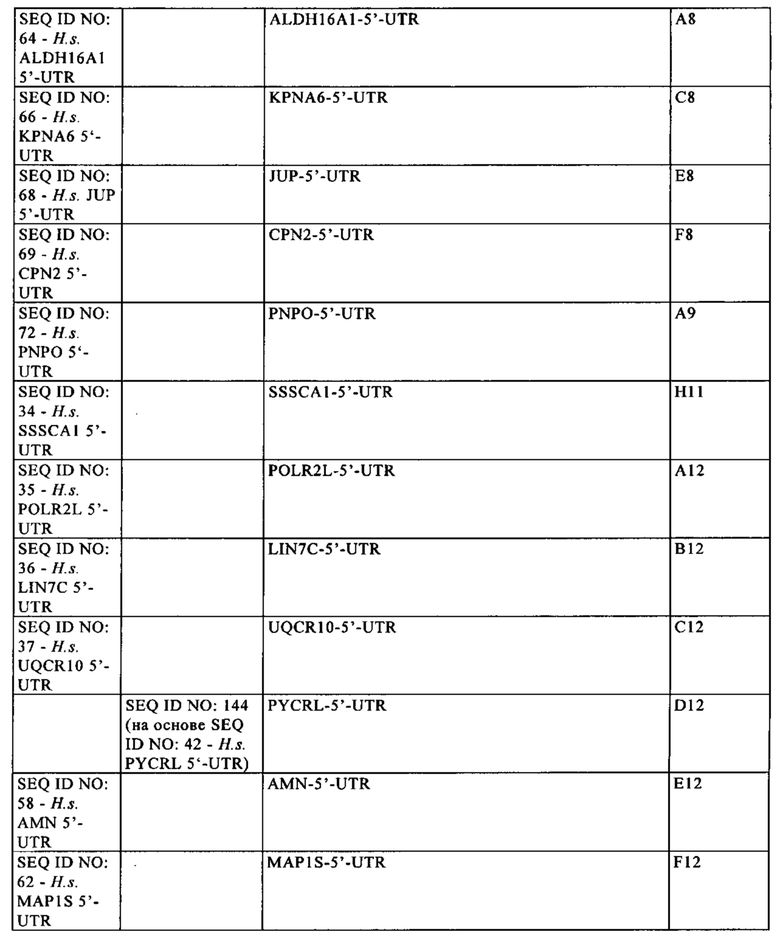
Таким образом, 5'-UTR человеческих генов из группы, состоящей из ZNF460-5'-UTR, TGM2-5'-UTR, IL7R-5'-UTR, COL8A1-5'-UTR, NDUFS7-5'-UTR, PLK2-5'-UTR, FBXO32-5'-UTR, ATP5D-5'-UTR, TUBB4B-5'-UTR, ORMDL2-5'-UTR, FSCN1-5'-UTR, CD9-5'-UTR, PYSL2-5'-UTR, PSMB3-5'-UTR, PSMB6-5'-UTR, KPNA6-5'-UTR, SFT2D2-5'-UTR, LCLAT1-5'-UTR, FBXL18-5'-UTR, SLC35F6-5'-UTR, VMA21-5'-UTR, SEZ6L2-5'-UTR, PCOLCE-5'-UTR, VTN-5'-UTR, ALDH16A1-5'-UTR, KPNA6-5'-UTR, JUP-5'-UTR, CPN2-5'-UTR, PNPO-5'-UTR, SSSCA1-5'-UTR, POLR2L-5'-UTR, LIN7C-5'-UTR, UQCR10-5'-UTR, PYCRL-5'-UTR, AMN-5'-UTR, MAP1S-5'-UTR, рассматривали как обеспечивающие высокую эффективность трансляции.
Также считали, что 5'-UTR, имеющие SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 137 (или ее эквивалент дикого типа SEQ ID NO: 3), SEQ ID NO: 138 (или ее эквивалент дикого типа SEQ ID NO: 9), SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 15, SEQ ID NO: 140 (или ее эквивалент дикого типа SEQ ID NO: 17), SEQ ID NO: 20, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 143 (или ее эквивалент дикого типа SEQ ID NO: 31), SEQ ID NO: 32, SEQ ID NO: 39, SEQ ID NO: 41, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 146 (или ее эквивалент дикого типа SEQ ID NO: 52), SEQ ID NO: 53, SEQ ID NO: 54, SEQ ID NO: 57, SEQ ID NO: 60, SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 64, SEQ ID NO: 66, SEQ ID NO: 68, SEQ ID NO: 69, SEQ ID NO: 72, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO:37, SEQ ID NO: 144 (или ее эквивалент дикого типа SEQ ID NO: 42), SEQ ID NO: 58, SEQ ID NO: 62, обеспечивают высокую эффективность трансляции.
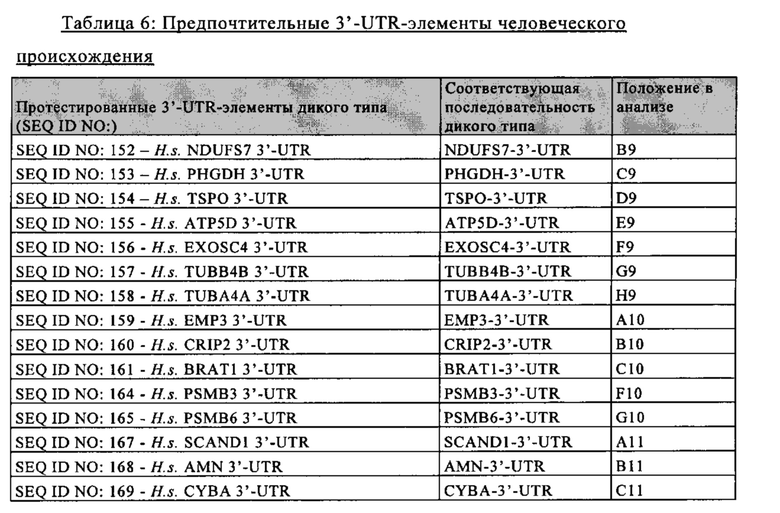
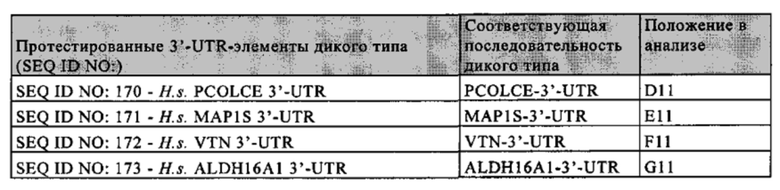
Таким образом, 3'-UTR человеческих генов из группы, состоящей из NDUFS7-3'-UTR, PHGDH-3'-UTR, TSPO-3'-UTR, ATP5D-3'-UTR, EXOSC4-3'-UTR, TUBB4B-3'-UTR, TUBA4A-3'-UTR, EMP3-3'-UTR, CRIP2-3'-UTR, BRAT1-3'-UTR, PSMB3-3'-UTR, PSMB6-3'-UTR, SCAND1-3'-UTR, AMN-3'-UTR, CYBA-3'-UTR, PCOLCE-3'-UTR, MAP1S-3'-UTR, VTN-3'-UTR, ALDH16A1-3'-UTR рассматривали как обеспечивающие высокую эффективность трансляции.
Также считали, что 3'-UTR, имеющие SEQ ID NO: 152, SEQ ID NO: 153, SEQ ID NO: 154, SEQ ID NO: 155, SEQ ID NO: 156, SEQ ID NO: 157, SEQ ID NO: 158, SEQ ID NO: 159, SEQ ID NO: 160, SEQ ID NO: 161, SEQ ID NO: 164, SEQ ID NO: 165, SEQ ID NO: 167, SEQ ID NO: 168, SEQ ID NO: 169, SEQ ID NO: 170, SEQ ID NO: 171, SEQ ID NO: 172, SEQ ID NO: 173, обеспечивают высокую эффективность трансляции.
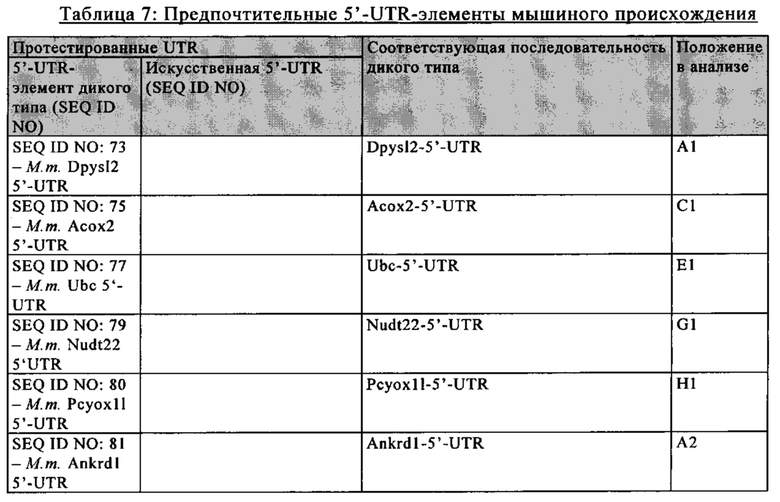
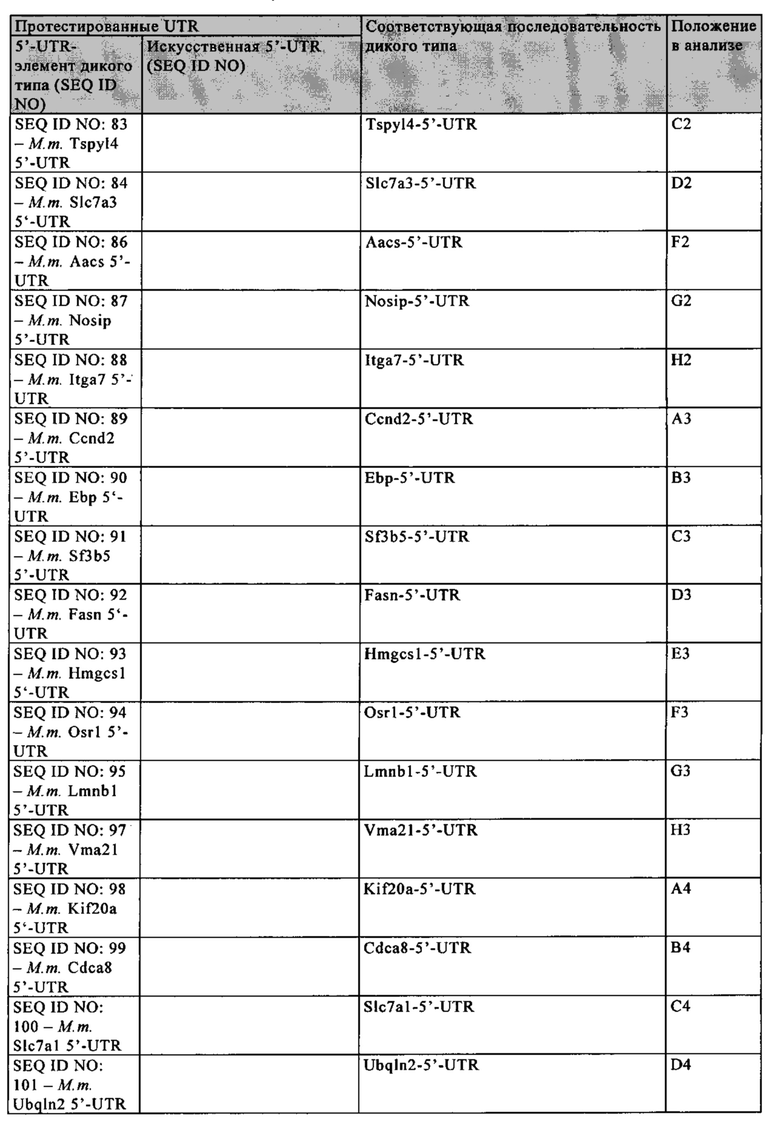
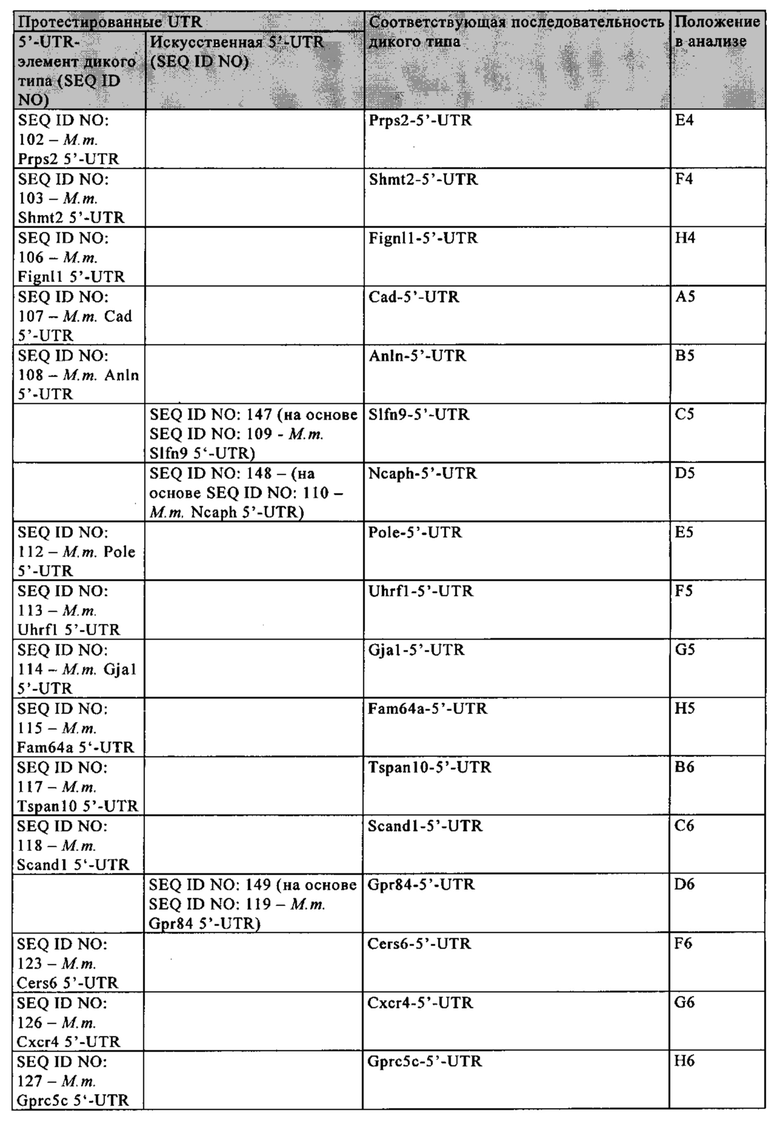
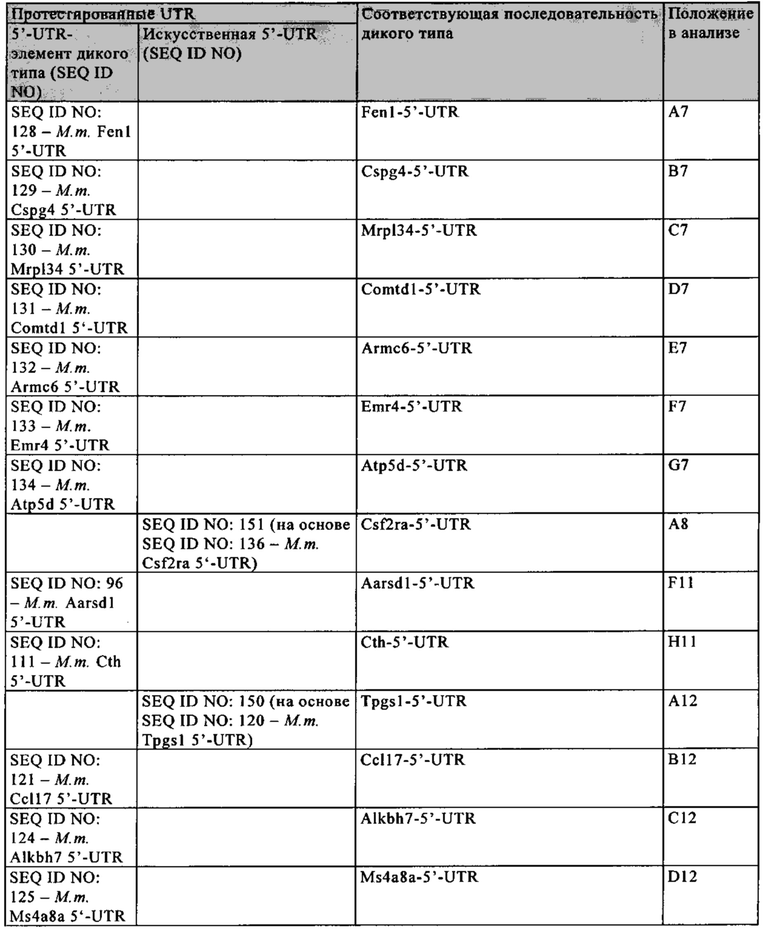
Таким образом, 5'-UTR мышиных генов из группы, состоящей из Dpysl2-5'-UTR, Acox2-5'-UTR, Ubc-5'-UTR, Nudt22-5'-UTR, Pcyox1l-5'-UTR, Ankrd1-5'-UTR, Tspyl4-5'-UTR, Slc7a3-5'-UTR, Aacs-5'-UTR, Nosip-5'-UTR, Itga7-5'-UTR, Ccnd2-5'-UTR, Ebp-5'-UTR, Sf3b5-5'-UTR, Fasn-5'-UTR, Hmgcs1-5'-UTR, Osr1-5'-UTR, Lmnb1-5'-UTR, Vma21-5'-UTR, Kif20a-5'-UTR, Cdca8-5'-UTR, Slc7a1-5'-UTR, Ubqln2-5'-UTR, Prps2-5'-UTR, Shmt2-5'-UTR, Fignl1-5'-UTR, Cad-5'-UTR, Anln-5'-UTR, Slfn9-5'-UTR, Ncaph-5'-UTR, Pole-5'-UTR, Uhrf1-5'-UTR, Gja1-5'-UTR, Fam64a-5'-UTR, Tspan10-5'-UTR, Scand1-5'-UTR, Gpr84-5'-UTR, Cers6-5'-UTR, Cxcr4-5'-UTR, Gprc5c-5'-UTR, Fen1-5'-UTR, Cspg4-5'-UTR, Mrpl34-5'-UTR, Comtd1-5'-UTR, Armc6-5'-UTR, Emr4-5'-UTR, Atp5d-5'-UTR, Csf2ra-5'-UTR, Aarsd1-5'-UTR, Cth-5'-UTR, Tpgs1-5'-UTR, Ccl17-5'-UTR, Alkbh7-5'-UTR, Ms4a8a-5'-UTR, рассматривали как обеспечивающие высокую эффективность трансляции.
Также 5'-UTR, имеющие SEQ ID NO: 73, SEQ ID NO: 75, SEQ ID NO: 77, SEQ ID NO: 79, SEQ ID NO: 80, SEQ ID NO: 81, SEQ ID NO: 83, SEQ ID NO: 84, SEQ ID NO: 86, SEQ ID NO: 87, SEQ ID NO: 88, SEQ ID NO: 89, SEQ ID NO: 90, SEQ ID NO: 91, SEQ ID NO: 92, SEQ ID NO: 93, SEQ ID NO: 94, SEQ ID NO: 95, SEQ ID NO: 97, SEQ ID NO: 98, SEQ ID NO: 99, SEQ ID NO: 100, SEQ ID NO: 101, SEQ ID NO: 102, SEQ ID NO: 103, SEQ ID NO: 106, SEQ ID NO: 107, SEQ ID NO: 108, SEQ ID NO: 147 (или ее эквивалент дикого типа SEQ ID NO: 109), SEQ ID NO: 148 (или ее эквивалент дикого типа SEQ ID NO: 110), SEQ ID NO: 112, SEQ ID NO: 113, SEQ ID NO: 114, SEQ ID NO: 115, SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 149 (или ее эквивалент дикого типа SEQ ID NO: 119), SEQ ID NO: 123, SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO: 130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134, SEQ ID NO: 151 (или ее эквивалент дикого типа SEQ ID NO: 136), SEQ ID NO: 96, SEQ ID NO: 111, SEQ ID NO: 150 (на основе SEQ ID NO: 120), SEQ ID NO: 121, SEQ ID NO: 124, SEQ ID NO: 125, рассматривали как обеспечивающие высокую эффективность трансляции.
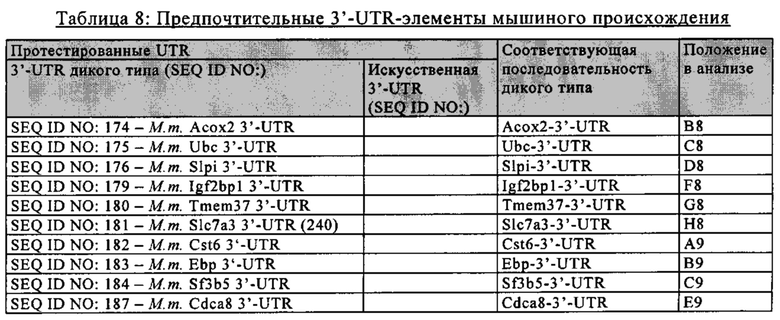
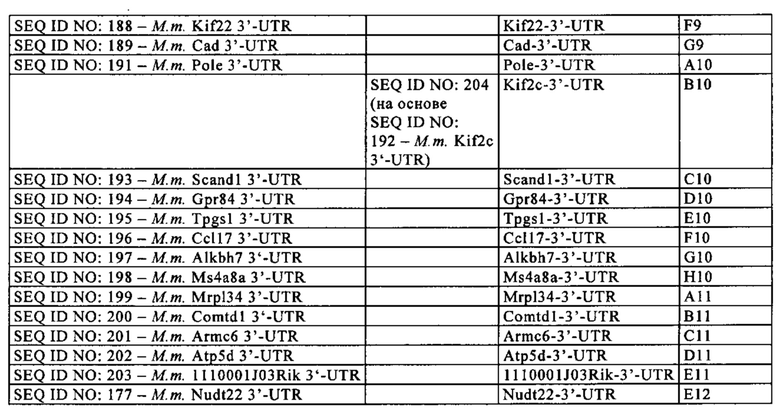
Таким образом, 3'-UTR мышиных генов из группы, состоящей из Асох2-3'-UTR, Ubc-3'-UTR, Slpi-3'-UTR, Igf2bp1-3'-UTR, Tmem37-3'-UTR, Slc7a3-3'-UTR, Cst6-3'-UTR, Ebp-3'-UTR, Sf3b5-3'-UTR, Cdca8-3'-UTR, Kif22-3'-UTR, Cad-3'-UTR, Pole-3'-UTR, Kif2c-3'-UTR, Scand1-3'-UTR, Gpr84-3'-UTR, Tpgs1-3'-UTR, Ccl17-3'-UTR, Alkbh7-3'-UTR, Ms4a8a-3'-UTR, Mrpl34-3'-UTR, Comtd1-3'-UTR, Armc6-3'-UTR, Atp5d-3'-UTR, 1110001J03Rik-3'-UTR, Nudt22-3'-UTR, рассматривали как обеспечивающие высокую эффективность трансляции.
Также 3'-UTR, имеющие SEQ ID NO: 174, SEQ ID NO: 175, SEQ ID NO: 176, SEQ ID NO: 179, SEQ ID NO: 180, SEQ ID NO: 181, SEQ ID NO: 182, SEQ ID NO: 183, SEQ ID NO: 184, SEQ ID NO: 187, SEQ ID NO: 188, SEQ ID NO: 189, SEQ ID NO: 191, SEQ ID NO: 204 (или ее эквивалент дикого типа SEQ ID NO: 192), SEQ ID NO: 193, SEQ ID NO: 194, SEQ ID NO: 195, SEQ ID NO: 196, SEQ ID NO: 197, SEQ ID NO: 198, SEQ ID NO: 199, SEQ ID NO: 200, SEQ ID NO: 201, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 177, рассматривали как обеспечивающие высокую эффективность трансляции.































































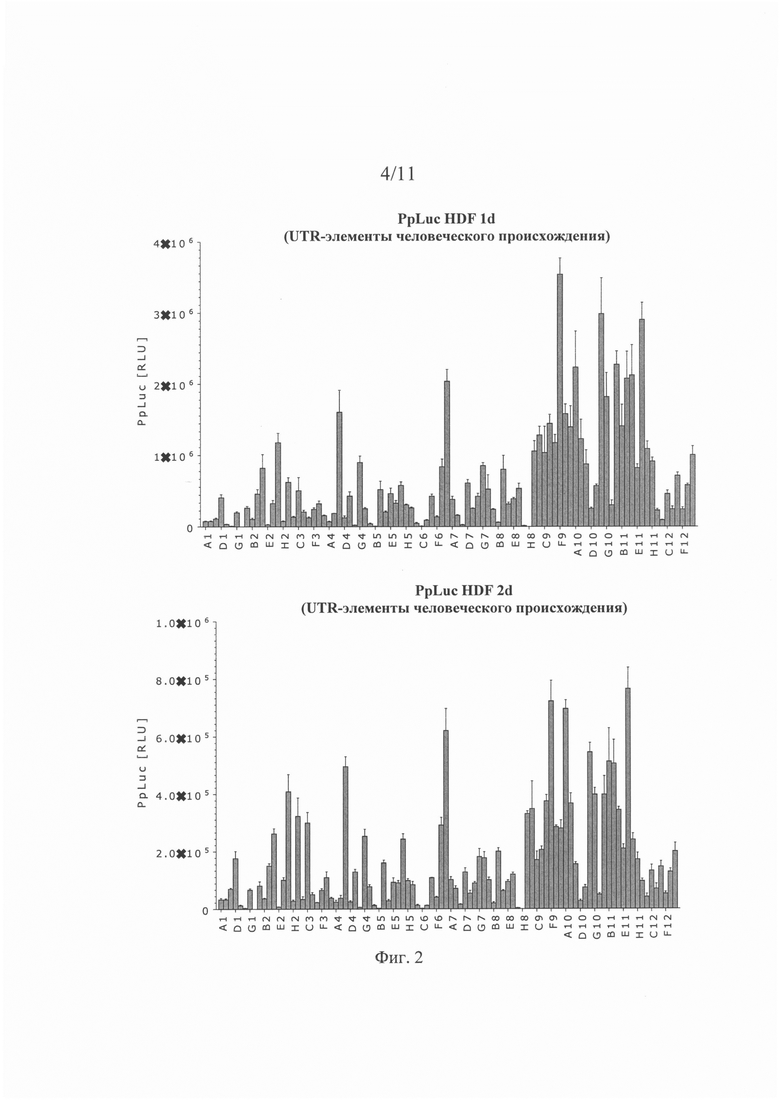
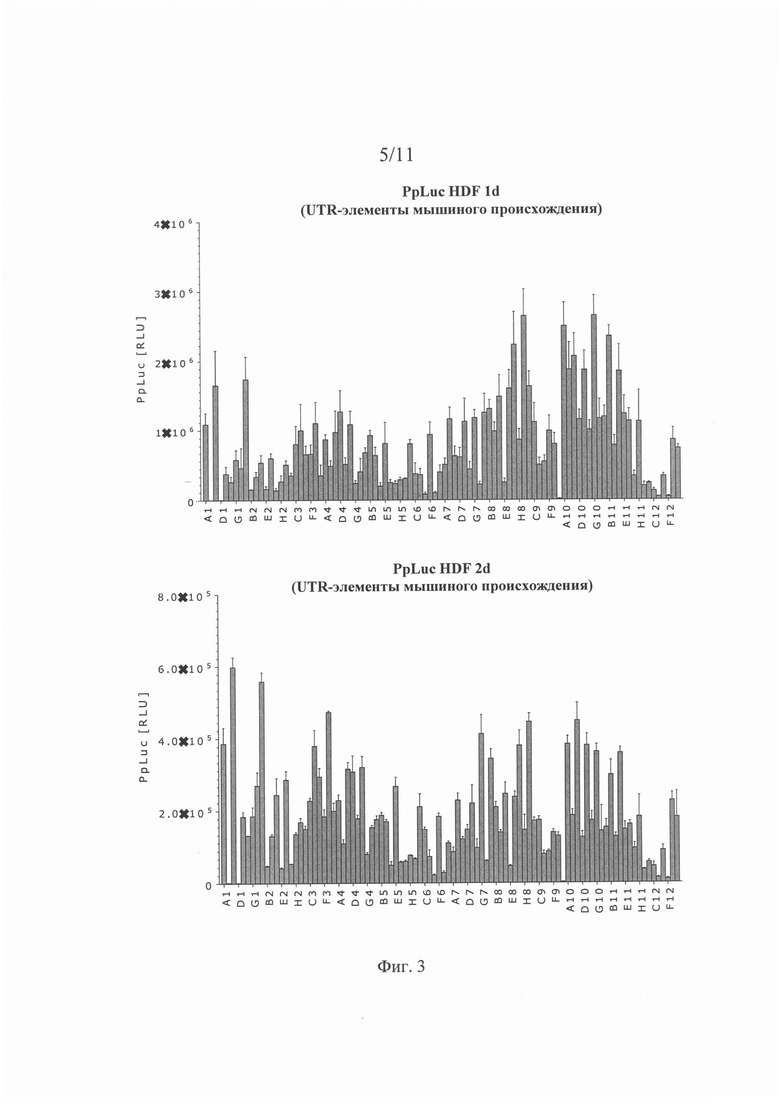
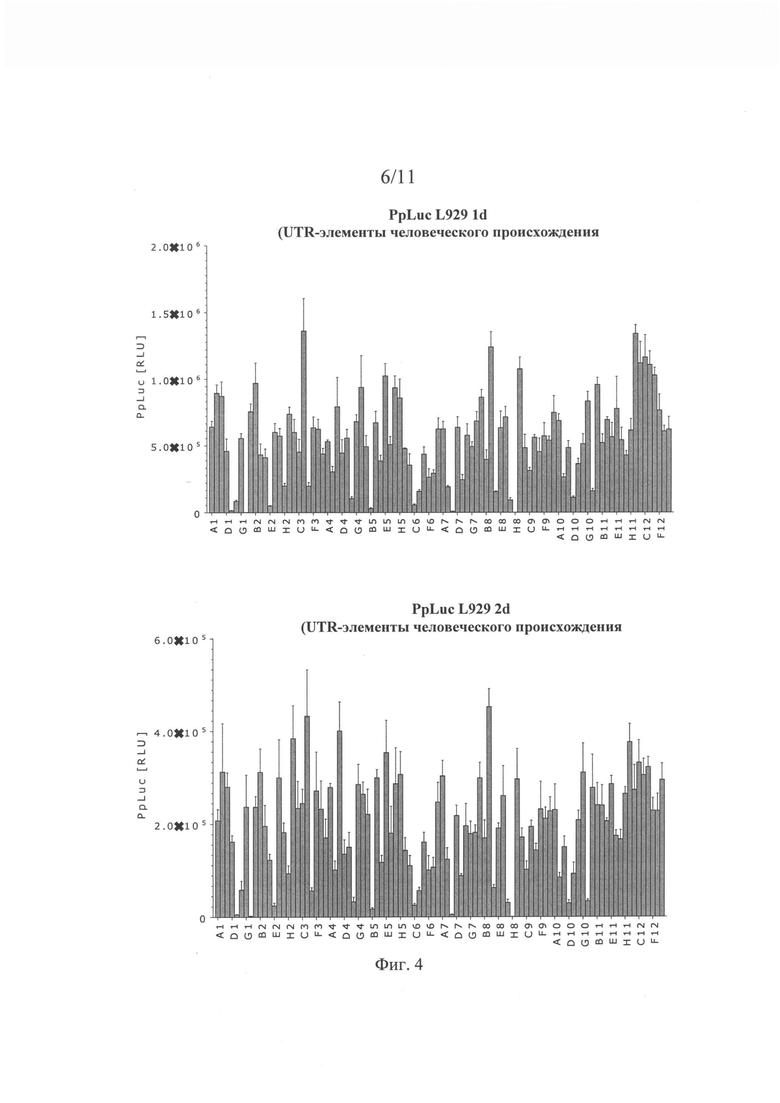
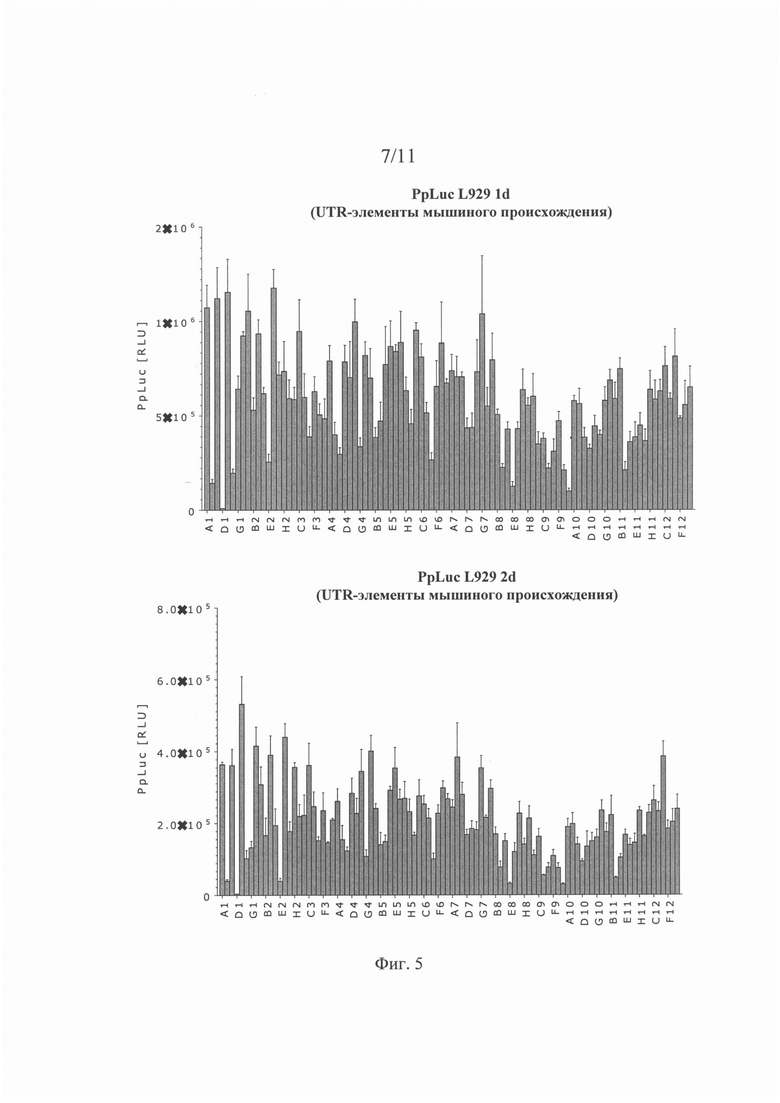
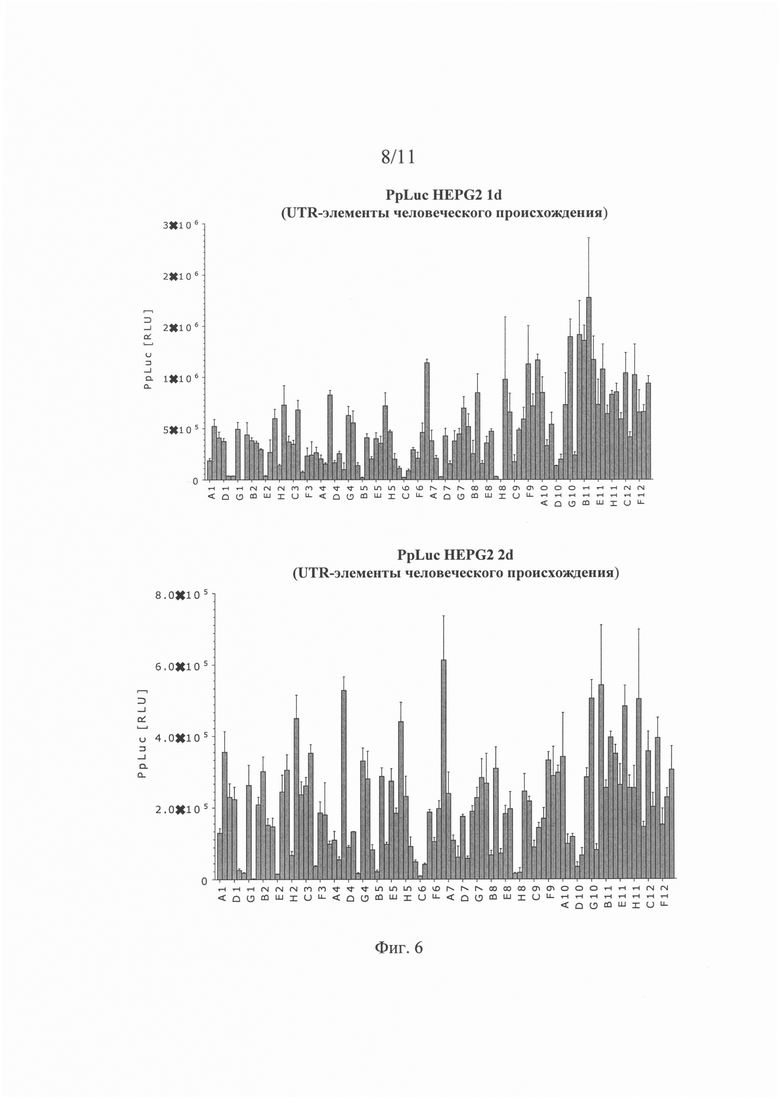
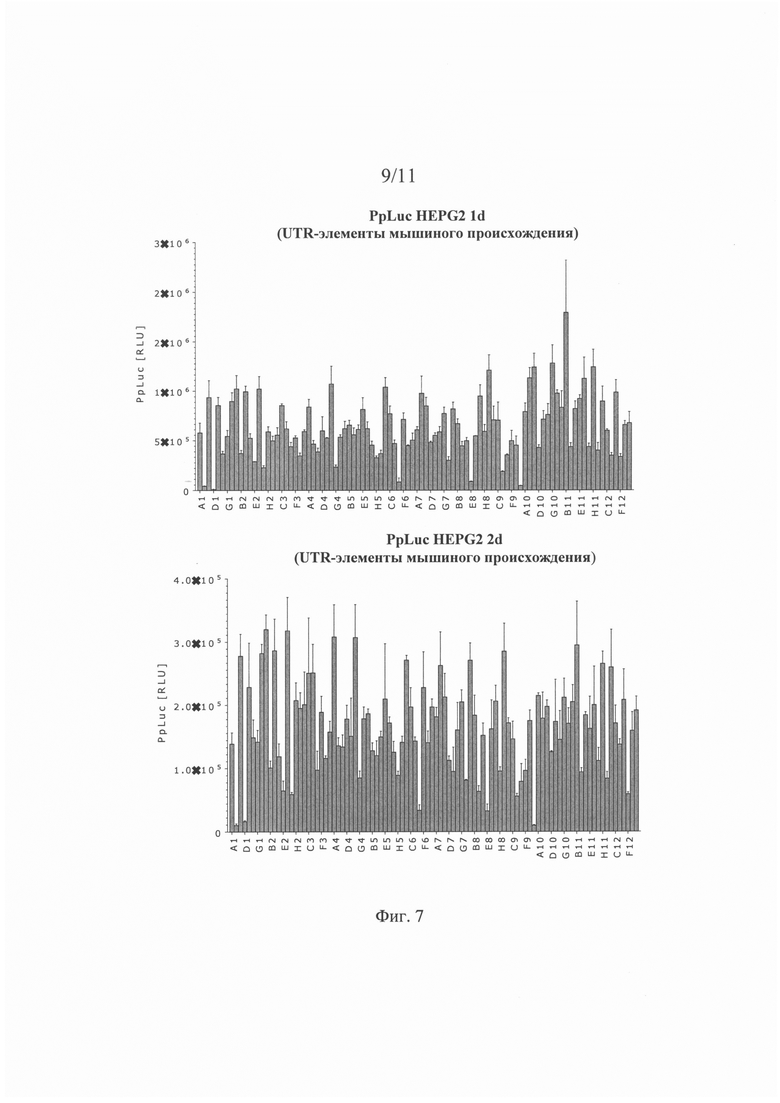
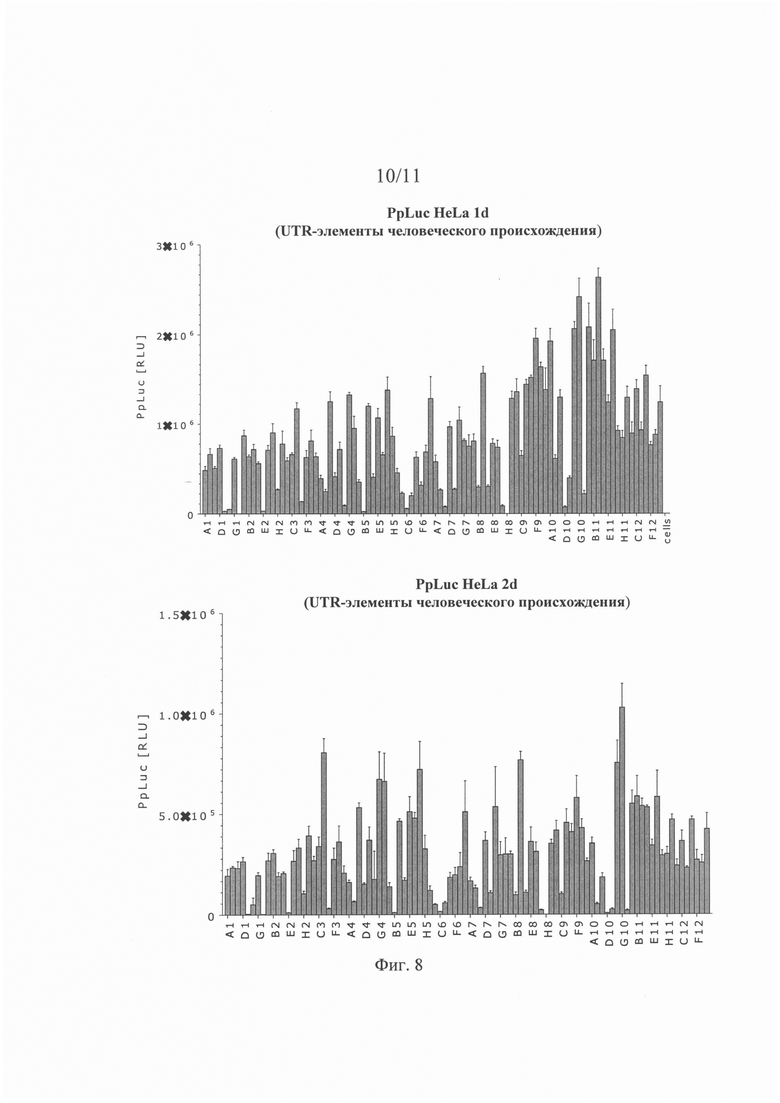
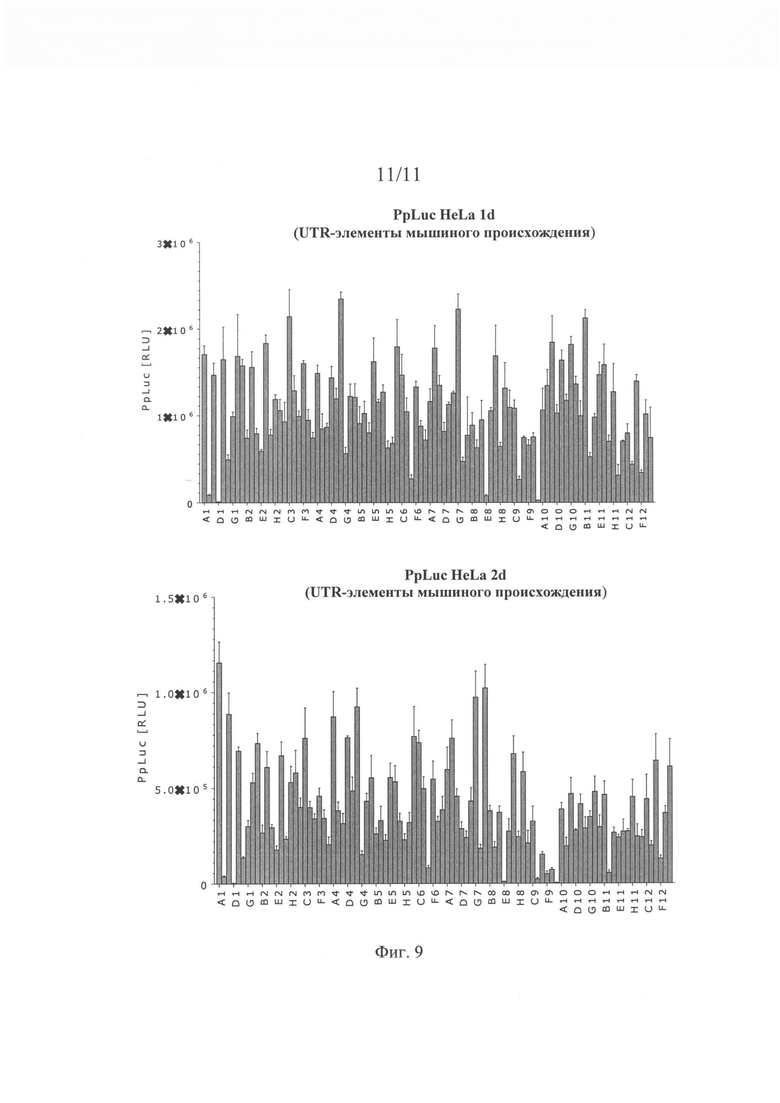
Изобретение относится к биотехнологии, а именно к искусственной молекуле нуклеиновой кислоты, содержащей по меньшей мере одну открытую рамку считывания и по меньшей мере один 3'-UTR-элемент и необязательно меньшей мере один 5'-UTR-элемент, где указанная искусственная молекула нуклеиновой кислоты отличается высокой эффективностью трансляции по сравнению с эффективностью трансляции референс-молекулы нуклеиновой кислоты, которая идентична искусственной молекуле нуклеиновой кислоты за исключением 3’-UTR-элемента. Также изобретение относится к вектору экспрессии, клетке для получения полипептида или пептида, фармацевтическим композициям для вакцинации или генной терапии, их применению в качестве вакцины или генной терапии, способу получения искусственной молекулы, способу обеспечения повышенной эффективности трансляции, набору для вакцинации, набору для генной терапии и применению 3’-UTR-элемента. 18 н. и 13 з.п. ф-лы, 9 ил., 8 табл., 3 пр.
1. Искусственная молекула нуклеиновой кислоты для обеспечения высокой эффективности трансляции полипептида или пептида, содержащая
a. по меньшей мере одну открытую рамку считывания - ОРС;
б. по меньшей мере один элемент 3’-нетранслируемой области -3’-UTR-элемент, который содержит нуклеотидную последовательность, полученную из 3’-UTR транскрипта гена, выбранного из группы, которая состоит из NDUFS7-3’-UTR, PHGDH-3’-UTR, TSPO-3’-UTR, ATP5D-3’-UTR, EXOSC4-3’-UTR, TUBB4B-3’-UTR, TUBA4A-3’-UTR, EMP3-3’-UTR, CRIP2-3’-UTR, BRAT1-3’-UTR, CD9-3’-UTR, CDK9-3’-UTR, PSMB3-3’-UTR, PSMB6-3’-UTR, PRSS56-3’-UTR, SCAND1-3’-UTR, AMN-3’-UTR, CYBA-3’-UTR, PCOLCE-3’-UTR, MAP1S-3’-UTR, VTN-3’-UTR, ALDH16A1-3’-UTR - предпочтительно все человеческие, и Acox2-3’-UTR,Ubc-3’-UTR, Slpi-3’-UTR, Pcyox1l-3’-UTR, Igf2bp1-3’-UTR, Tmem37-3’-UTR, Slc7a3-3’-UTR, Cst6-3’-UTR, Ebp-3’-UTR, Sf3b5-3’-UTR, Plk1-3’-UTR, Cdca8-3’-UTR, Kif22-3’-UTR, Cad-3’-UTR, Cth-3’-UTR, Pole-3’-UTR, Kif2c-3’-UTR, Scand1-3’-UTR, Gpr84-3’-UTR, Tpgs1-3’-UTR, Ccl17-3’-UTR, Alkbh7-3’-UTR, Ms4a8a-3’-UTR, Mrpl34-3’-UTR, Comtd1-3’-UTR, Armc6-3’-UTR, Atp5d-3’-UTR, 1110001J03Rik-3’-UTR, Nudt22-3’-UTR, Aarsd1-3’-UTR - предпочтительно все мышиные; и
в. необязательно по меньшей мере один элемент 5’-нетранслируемой области-5’-UTR-элемент, в которой по меньшей мере одна открытая рамка считывания является гетерологичной по отношению к 3’-UTR и/или 5’-UTR-элементу, и где указанная искусственная молекула нуклеиновой кислоты отличается высокой эффективностью трансляции по сравнению с эффективностью трансляции референс-молекулы нуклеиновой кислоты, которая идентична искусственной молекуле нуклеиновой кислоты за исключением 3’-UTR-элемента, а эффективность трансляции искусственной молекулы нуклеиновой кислоты и эффективность трансляции референс-молекулы нуклеиновой кислоты сравнивают с помощью способа, включающего стадии, на которых:
(I) трансфектируют клетки млекопитающих искусственной молекулой нуклеиновой кислоты и измеряют количества экспрессированного белка, кодируемого ОРС искусственной молекулы нуклеиновой кислоты после трансфекции,
(II) трансфектируют клетки млекопитающих референс-молекулой нуклеиновой кислоты и измеряют количества экспрессируемого белка, кодируемого ОРС референс-молекулы нуклеиновой кислоты, в тот же самый момент времени после трансфекции,
(III) рассчитывают отношение количества белка, экспрессированного с искусственной молекулы нуклеиновой кислоты, к количеству белка, экспрессированного с референс-молекулы нуклеиновой кислоты, где величина отношения, рассчитанного на стадии III, составляет > 1.
2. Искусственная молекула нуклеиновой кислоты по п. 1, в которой по меньшей мере один 3’-UTR-элемент содержит или состоит из нуклеотидной последовательности SEQ ID NO: 164 или соответствующей последовательности РНК.
3. Искусственная молекула нуклеиновой кислоты по п. 1, в которой по меньшей мере один 3’-UTR-элемент содержит или состоит из нуклеотидной последовательности, идентичной по меньшей мере на 95%, еще более предпочтительно по меньшей мере на 99% нуклеотидной последовательности SEQ ID NO: 164 или соответствующей последовательности РНК.
4. Искусственная молекула нуклеиновой кислоты по п. 1, где 3’-UTR-элемент референс-молекулы нуклеиновой кислоты имеет последовательность, представленную в SEQ ID NO: 207, или соответствующую последовательность РНК.
5. Искусственная молекула нуклеиновой кислоты по любому из пп. 1-4, в которой по меньшей мере один 3’-UTR-элемент и/или по меньшей мере один 5’-UTR-элемент повышает эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты по меньшей мере в 1,2 раза, предпочтительно по меньшей мере в 1,5 раза, более предпочтительно по меньшей мере в 2 раза, еще более предпочтительно по меньшей мере в 2,5 раза по сравнению с производством белка с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3’-UTR и/или по меньшей мере одна 5’-UTR соответственно, и/или в которой по меньшей мере один 3’-UTR-элемент и/или по меньшей мере один 5’-UTR-элемент обеспечивает высокую эффективность трансляции указанной искусственной молекулы нуклеиновой кислоты, превышающую по меньшей мере в 1,5 раза, предпочтительно по меньшей мере в 2 раза, более предпочтительно по меньшей мере в 2,5 раза производство белка с референс-молекулы нуклеиновой кислоты, в которой отсутствует 3’-UTR и/или по меньшей мере одна 5’-UTR соответственно.
6. Искусственная молекула нуклеиновой кислоты по любому из пп. 1-5, в которой по меньшей мере один 5’-UTR-элемент содержит или состоит из нуклеотидной последовательности, которая получена из 5’-UTR транскрипта гена, выбранного из группы, которая состоит из ZNF460, TGM2, IL7R, BGN, TK1, RAB3B, CBX6, FZD2, COL8A1, NDUFS7, PHGDH, PLK2, TSPO, PTGS1, FBXO32, NID2, ATP5D, EXOSC4, NOL9, UBB4B, VPS18, ORMDL2, FSCN1, TMEM33, TUBA4A, EMP3, TMEM201, CRIP2, BRAT1, SERPINH1, CD9, DPYSL2, CDK9, TFRC, PSMB3 5’-UTR, FASN, PSMB6, PRSS56, KPNA6, SFT2D2, PARD6B, LPP, SPARC, SCAND1, VASN, SLC26A1, LCLAT1, FBXL18, SLC35F6, RAB3D, MAP1B, VMA21, CYBA, SEZ6L2, PCOLCE, VTN, ALDH16A1, RAVER1, KPNA6, SERINC5, JUP, CPN2, CRIP2, EPT1, PNPO, SSSCA1, POLR2L, LIN7C, UQCR10, PYCRL, AMN, MAP1S, NDUFS7, PHGDH, TSPO, ATP5D, EXOSC4, TUBB4B, TUBA4A, EMP3, CRIP2, BRAT1, CD9, CDK9, PSMB3, PSMB6, PRSS56, SCAND1, AMN, CYBA, PCOLCE, MAP1S, VTN, ALDH16A1 - предпочтительно все человеческие, и Dpysl2, Ccnd1, Acox2, Cbx6, Ubc, Ldlr, Nudt22, Pcyox1l, Ankrd1, Tmem37, Tspyl4, Slc7a3, Cst6, Aacs, Nosip, Itga7, Ccnd2, Ebp, Sf3b5, Fasn, Hmgcs1, Osr1, Lmnb1, Vma21, Kif20a, Cdca8, Slc7a1, Ubqln2, Prps2, Shmt2, Aurkb, Fignl1, Cad, Anln, Slfn9, Ncaph, Pole, Uhrf1, Gja1, Fam64a, Kif2c, Tspan10, Scand1, Gpr84, Fads3, Cers6, Cxcr4, Gprc5c, Fen1, Cspg4, Mrpl34, Comtd1, Armc6, Emr4, Atp5d, 1110001J03Rik, Csf2ra, Aarsd1, Kif22, Cth, Tpgs1, Ccl17, Alkbh7, Ms4a8a, Acox2, Ubc, Slpi, Pcyox1l, Igf2bp1, Tmem37, Slc7a3, Cst6, Ebp, Sf3b5, Plk1, Cdca8, Kif22, Cad, Cth, Pole, Kif2c, Scand1, Gpr84, Tpgs1, Ccl17, Alkbh7, Ms4a8a, Mrpl34, Comtd1, Armc6, Atp5d, 1110001J03Rik, Nudt22, Aarsd1 - предпочтительно все мышиные.
7. Искусственная молекула нуклеиновой кислоты по любому из пп. 1-6, в которой по меньшей мере один 5’-UTR-элемент содержит или состоит из нуклеотидной последовательности, идентичной по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% нуклеотидной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 1-151 или соответствующей последовательности РНК, или в которой по меньшей мере один 5’-UTR-элемент содержит или состоит из фрагмента нуклеотидной последовательности, идентичного по меньшей мере примерно на 40%, предпочтительно по меньшей мере примерно на 50%, предпочтительно по меньшей мере примерно на 60%, предпочтительно по меньшей мере примерно на 70%, более предпочтительно по меньшей мере примерно на 80%, более предпочтительно по меньшей мере примерно на 90%, еще более предпочтительно по меньшей мере примерно на 95%, еще более предпочтительно по меньшей мере примерно на 99% фрагменту нуклеотидной последовательности, выбранной из группы, которая состоит из SEQ ID NO: 1-151 или соответствующей последовательности РНК.
8. Искусственная молекула нуклеиновой кислоты по любому из пп. 1-7, дополнительно содержащая
г. поли(A)-последовательность и/или сигнал полиаденилирования, который находится с 3’-стороны относительно 3’-UTR-элемента.
9. Искусственная молекула нуклеиновой кислоты по любому из пп. 1-8, дополнительно содержащая 5’-кэп-структуру, поли(C)-последовательность, гистоновую структуру типа «стебель-петля» и/или IRES-мотив.
10. Искусственная молекула нуклеиновой кислоты по любому из пп. 1–9, в которой нуклеотидная последовательность содержит 5’-TOP UTR.
11. Искусственная молекула нуклеиновой кислоты по любому из пп. 1-10, в открытой рамке считывания которой по меньшей мере частично модифицировано содержание G/C, где предпочтительно содержание G/C открытой рамки считывания повышено по сравнению с открытой рамкой считывания дикого типа и/или в которой открытая рамка считывания содержит область с оптимизированными кодонами, предпочтительно в которой открытая рамка считывания имеет оптимизированные кодоны.
12. Искусственная молекула нуклеиновой кислоты по любому из пп. 1-11, которая представляет собой РНК, предпочтительно молекулу мРНК.
13. Вектор экспрессии полипептида или пептида, содержащий искусственную молекулу нуклеиновой кислоты по любому из пп. 1-12.
14. Клетка для получения полипептида или пептида, содержащая искусственную молекулу нуклеиновой кислоты по любому из пп. 1-12 или вектор по п. 13.
15. Фармацевтическая композиция для вакцинации, содержащая эффективное количество искусственной молекулы нуклеиновой кислоты по любому из пп. 1-12, или вектора по п. 13, или клетки по п. 14 и один или более фармацевтически приемлемых носителей, разбавителей и/или эксципиентов и/или один или большее количество адъювантов.
16. Фармацевтическая композиция для генной терапии, содержащая эффективное количество искусственной молекулы нуклеиновой кислоты по любому из пп. 1-12, или вектора по п. 13, или клетки по п. 14 и один или более фармацевтически приемлемых носителей, разбавителей и/или эксципиентов и/или один или большее количество адъювантов.
17. Применение искусственной молекулы нуклеиновой кислоты по любому из пп. 1-12 в качестве вакцины.
18. Применение искусственной молекулы нуклеиновой кислоты по любому из пп. 1-12 в генной терапии.
19. Применение вектора по п. 13 в качестве вакцины.
20. Применение вектора по п. 13 в генной терапии.
21. Применение клетки по п. 14 в качестве вакцины.
22. Применение клетки по п. 14 в генной терапии.
23. Применение фармацевтической композиции по п. 15 в качестве вакцины.
24. Применение фармацевтической композиции по п. 16 в генной терапии.
25. Способ получения искусственной молекулы нуклеиновой кислоты по любому из пп. 1-12, предусматривающий объединение
a. по меньшей мере одной открытой рамки считывания - ОРС;
б. по меньшей мере одного элемента 3’-нетранслируемой области -3’-UTR-элемента, который содержит нуклеотидную последовательность, которая получена из 3’-UTR транскрипта человеческого гена, выбранного из группы, которая состоит из NDUFS7-3’-UTR, PHGDH-3’-UTR, TSPO-3’-UTR, ATP5D-3’-UTR, EXOSC4-3’-UTR, TUBB4B-3’-UTR, TUBA4A-3’-UTR, EMP3-3’-UTR, CRIP2-3’-UTR, BRAT1-3’-UTR, CD9-3’-UTR, CDK9-3’-UTR, PSMB3-3’-UTR, PSMB6-3’-UTR, PRSS56-3’-UTR, SCAND1-3’-UTR, AMN-3’-UTR, CYBA-3’-UTR, PCOLCE-3’-UTR, MAP1S-3’-UTR, VTN-3’-UTR, ALDH16A1-3’-UTR - предпочтительно все человеческие, и Acox2-3’-UTR, Ubc-3’-UTR, Slpi-3’-UTR, Pcyox1l-3’-UTR, Igf2bp1-3’-UTR, Tmem37-3’-UTR, Slc7a3-3’-UTR, Cst6-3’-UTR, Ebp-3’-UTR, Sf3b5-3’-UTR, Plk1-3’-UTR, Cdca8-3’-UTR, Kif22-3’-UTR, Cad-3’-UTR, Cth-3’-UTR, Pole-3’-UTR, Kif2c-3’-UTR, Scand1-3’-UTR, Gpr84-3’-UTR, Tpgs1-3’-UTR, Ccl17-3’-UTR, Alkbh7-3’-UTR, Ms4a8a-3’-UTR, Mrpl34-3’-UTR, Comtd1-3’-UTR, Armc6-3’-UTR, Atp5d-3’-UTR, 1110001J03Rik-3’-UTR, Nudt22-3’-UTR, Aarsd1-3’-UTR - предпочтительно все мышиные, и
в. необязательно по меньшей мере одного элемента 5’-нетранслируемой области -5’-UTR-элемента, причем по меньшей мере одна открытая рамка считывания является гетерологичной по отношению 3’-UTR и/или 3’-UTR –элементу.
26. Способ по п. 25, в котором применяют вектор по п. 13.
27. Способ обеспечения повышенной эффективности трансляции полипептида или пептида, предусматривающий получение искусственной молекулы нуклеиновой кислоты по любому из пп. 1-12.
28. Набор для вакцинации, содержащий искусственную молекулу нуклеиновой кислоты по любому из пп. 1-12, или вектор по п. 13, или клетку по п. 14, или фармацевтическую композицию по п. 15 и инструкцию по его применению.
29. Набор для генной терапии, содержащий искусственную молекулу нуклеиновой кислоты по любому из пп. 1-12, или вектор по п. 13, или клетку по п. 14, или фармацевтическую композицию по п. 16 и инструкцию по его применению.
30. Набор по п. 28 или 29, который содержит адьювант, средства для трансфекции клетки, средства для введения фармацевтической композиции, фармацевтически приемлемый носитель и/или фармацевтически приемлемый раствор для растворения или разведения искусственной молекулы нуклеиновой кислоты, или вектора, или клеток, или фармацевтической композиции.
31. Применение 3’-UTR-элемента, содержащегося в молекуле искусственной нуклеиновой кислоты по любому из пп. 1-12 или в векторе по п. 13, для обеспечения высокой эффективности трансляции полипептида или пептида.
| МОЛЕКУЛЫ ИСКУССТВЕННОЙ НУКЛЕИНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИЕ 5'UTR ГЕНА TOP | 2013 |
|
RU2660565C2 |
| GAVIN S.WILKIE et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| КИМИССЕ М.Г | |||
| и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Агрономия и | |||
Авторы
Даты
2022-05-19—Публикация
2016-08-22—Подача