ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА СВЯЗАННЫЕ ПАТЕНТНЫЕ ЗАЯВКИ
Эта заявка в соответствии с параграфом 119(a) раздела 35 Свода законов США испрашивает приоритет предварительной заявки на патент США №63/058,205, поданной 29 июля 2020 г., и предварительной заявки на патент США №63/087,563, поданной 5 октября 2020 г., полное содержание которых таким образом включено в данную заявку для любых целей посредством ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к способу повышения безопасности литиевых батарей, в частности к способу подавления теплового убегания литиевых батарей путем пассивации слоя активного вещества положительного электрода и слоя активного вещества отрицательного электрода.
Предшествующий уровень техники
Поскольку литий-ионные батареи широко используются в различных продуктах, таких как транспортные средства, носимые устройства для потребительского и промышленного применения, портативные устройства, устройства хранения энергии и т.д., то они применяются почти во всех сферах повседневной жизни человека. Тем не менее, время от времени все еще появляется информация об инцидентах, связанных с литий-ионными аккумуляторными батареями, таких как пожары или взрывы аккумуляторных батарей мобильных телефонов и электромобилей. Все это связано с тем, что литиевые батареи до сих пор не имеют комплексных и эффективных решений проблем безопасности. Основная причина таких небезопасных происшествий, как возгорания или взрывы литиевых батарей это тепловое убегание. И основной причиной теплового убегания литиевых батарей является тепло, которое представляет собой результат экзотермических реакций, возникающих в результате термического растрескивания пленки SEI (разделяющей твердый электролит), самого электролита, связующего вещества, а также активных веществ положительного и отрицательного электродов в батарее, вызванного повышенной температурой. Существующие способы подавления теплового убегания можно разделить на два типа: находящиеся снаружи аккумуляторного элемента и внутри него, в зависимости от выбранного расположения. В качестве средства подавления, располагающегося снаружи аккумуляторного элемента, применяется система мониторинга, которая использует цифровое арифметическое моделирование. Средства подавления, располагающиеся внутри аккумуляторного элемента, можно далее разделить на физические или химические. В цифровой системе мониторинга, расположенной снаружи аккумуляторного элемента, для улучшения контроля безопасности аккумулятора во время процесса использования используются специальная схема защиты и специальная система управления, находящиеся снаружи аккумуляторного элемента. Используемые внутри аккумуляторного элемента средства подавления физического типа, такие как сепаратор с защитой от перегрева, при повышенной температуре аккумуляторной ячейки закрывают отверстия сепаратора, блокируя прохождение ионов.
Используемые внутри аккумуляторного элемента средства подавления теплового убегания химического типа делятся на средства контроля масштаба убегания и средства, основанные на электрохимических реакциях. В качестве средства контроля масштаба теплового убегания используется добавление в электролит огнезащитного состава, ограничивающего нагрев. Средства подавления, основанные на электрохимических реакциях, предусматривают использование следующих их типов:
а. В электролит добавляют мономер или олигомер. В этом случае, при повышении температуры будет происходить полимеризация, снижающая скорость миграции ионов. Следовательно, ионная проводимость уменьшается с повышением температуры, и скорость электрохимической реакции в ячейке замедляется;
б. Между слоем положительного электрода или слоем отрицательного электрода и соседним токосъемным слоем располагается резистивный материал с положительным температурным коэффициентом (ПТК). Когда температура аккумуляторного элемента повышается, улучшается электроизоляционная способность этого материала. Эффективность передачи электроэнергии между слоем положительного электрода или слоем отрицательного электрода и соседним токосъемным слоем снижается, как и скорость электрохимической реакции; а также
с. На поверхности активного вещества положительного электрода формируется модифицированный слой. Когда температура аккумуляторного элемента повышается, модифицированный слой превращается в плотную пленку, которая увеличивает сопротивление переносу заряда и снижает скорость электрохимической реакции.
Например, в соответствии с патентом США 9711774, термочувствительный слой может быть расположен между электродами и сепаратором. Когда литий-ионная аккумуляторная батарея находится в состоянии теплового убегания и внутренняя температура повышается до критического значения, частицы полимера претерпевают процесс теплового перехода (плавление) для образования изолирующего барьера на электродах, который блокирует перенос ионов лития между электродами и отключает внутренний ток батареи.
Однако вышеперечисленные способы нацелены только на пассивное блокирование пути миграции ионов или электронов для уменьшения тепловыделения, не позволяя основному источнику, главному реагенту всей электрохимической реакции, т.е. активным веществам электродов, генерировать максимальную энергию, что и вызывает тепловое убегание. Следовательно, настоящее изобретение обеспечивает способ подавления теплового убегания литиевых батарей путем уменьшения тепловой энергии, приводящей к тепловому убеганию, неуправляемому нагреву активных веществ, для уменьшения или устранения вышеупомянутых проблем.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является предоставление совершенно нового способа подавления теплового убегания литиевых батарей, который заключается в пассивации активных веществ положительного и отрицательного электродов с целью заблокировать протекание электрохимической реакции, чтобы эффективно избежать теплового убегания батареи.
Для реализации описанного выше, в настоящем изобретении раскрывается способ подавления теплового убегания литиевых батарей, который включает в себя следующие этапы: этап (а): обеспечение литиевой батареи, способной заряжаться и разряжаться, которая содержит в себе электрохимическую реакционную систему; и этап (b): нанесение ионов металла (А) и ионов амфотерного металла (В) на слой активного вещества положительного электрода и слой активного вещества отрицательного электрода литиевой батареи, когда температура литиевой батареи достигает заданного значения, для пассивации слоя активного вещества положительного электрода и слоя активного вещества отрицательного электрода, чтобы заблокировать протекание электрохимической реакции и эффективно избежать теплового убегания батареи. Ионы металлов (А) выбираются из ионов щелочных металлов, отличных от лития, ионов щелочноземельных металлов или их сочетаний.
Дальнейший объем применимости настоящего изобретения станет очевидным из подробного описания, приведенного ниже. Однако следует понимать, что подробное описание и конкретные примеры, хотя и показывают предпочтительные варианты осуществления изобретения, даны только в качестве иллюстрации, поскольку различные изменения и модификации в пределах сущности и объема изобретения станут очевидными для специалистов в данной области техники из этого подробного описания.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Настоящее изобретение станет более понятным из подробного описания, приведенного ниже только в качестве иллюстрации, и, таким образом, не ограничивающего настоящее изобретение, и в котором:
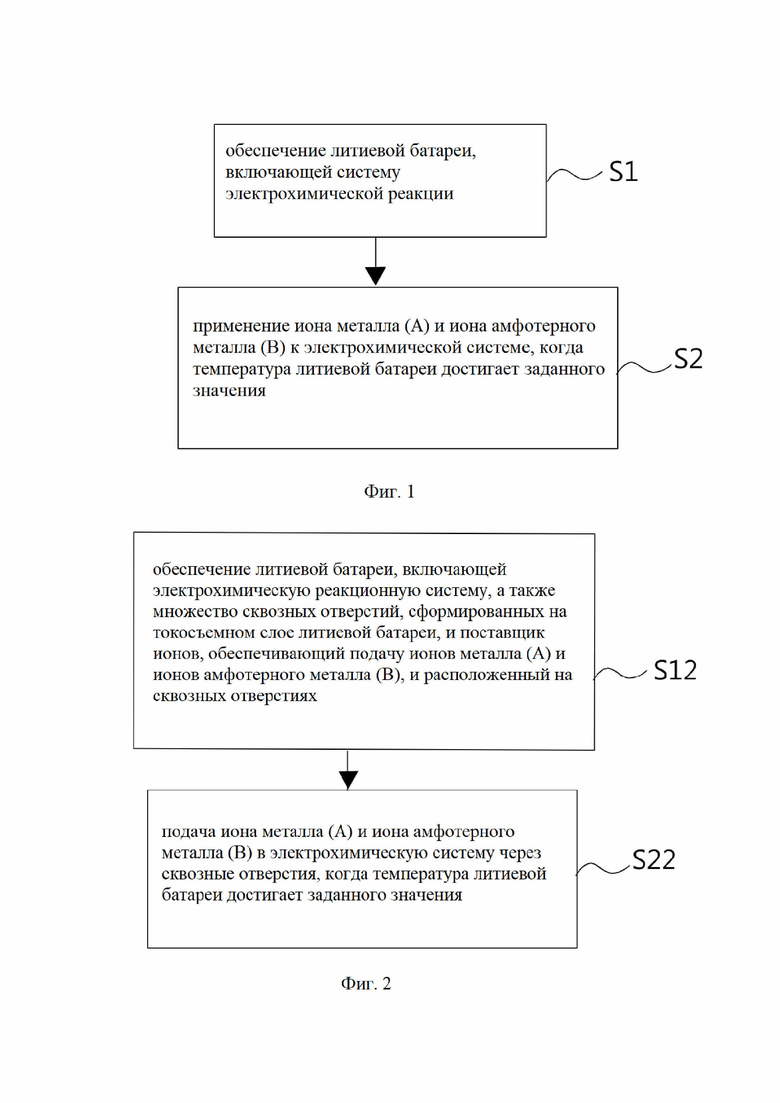
Фигура 1 представляет собой блок-схему, показывающую пример этапов способа подавления теплового убегания литиевых батарей в соответствии с настоящим изобретением.
Фигура 2 представляет собой блок-схему, показывающую другой пример этапов способа подавления теплового убегания литиевых батарей в соответствии с настоящим изобретением.
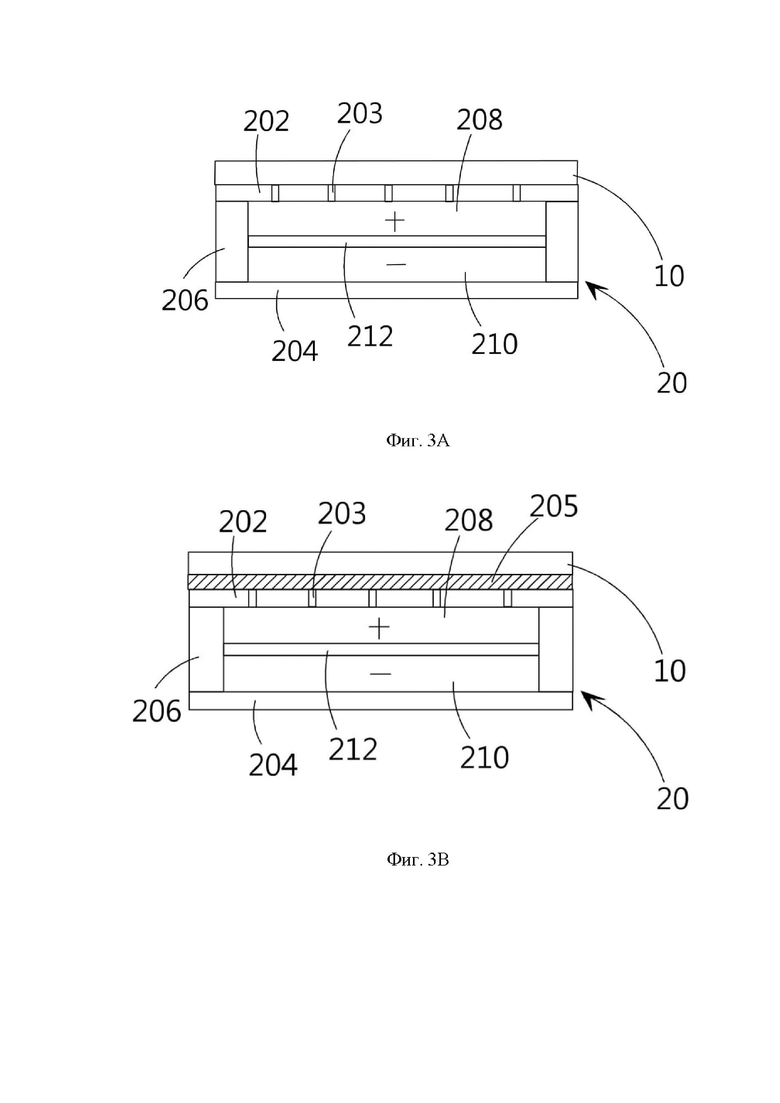
Фигуры 3А и 3В являются принципиальными схемами аккумуляторных элементов в соответствии с фигурой 2.
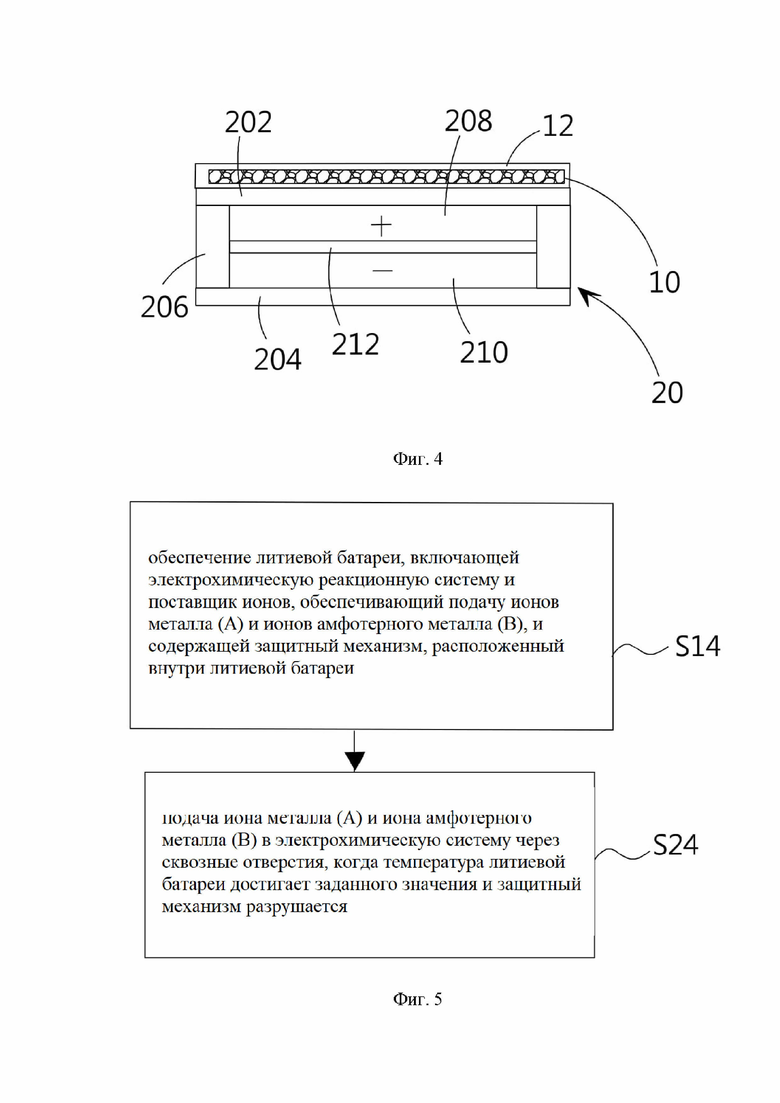
Фигура 4 - принципиальная схема другого варианта осуществления аккумуляторных элементов в соответствии с фигурой 2.
Фигура 5 блок-схема, показывающая другой пример этапов способа подавления теплового убегания литиевых батарей в соответствии с настоящим изобретением.
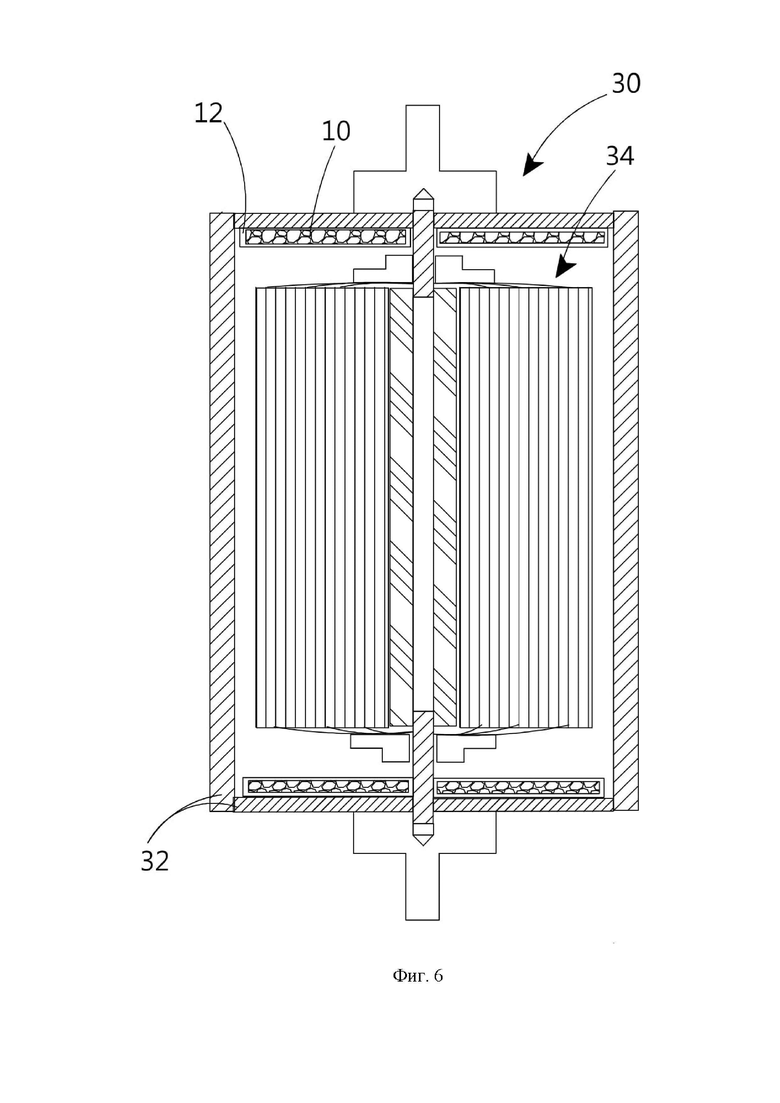
Фигура 6 - принципиальная схема варианта осуществления литиевой батареи с подавлением теплового убегания в соответствии с настоящим изобретением.
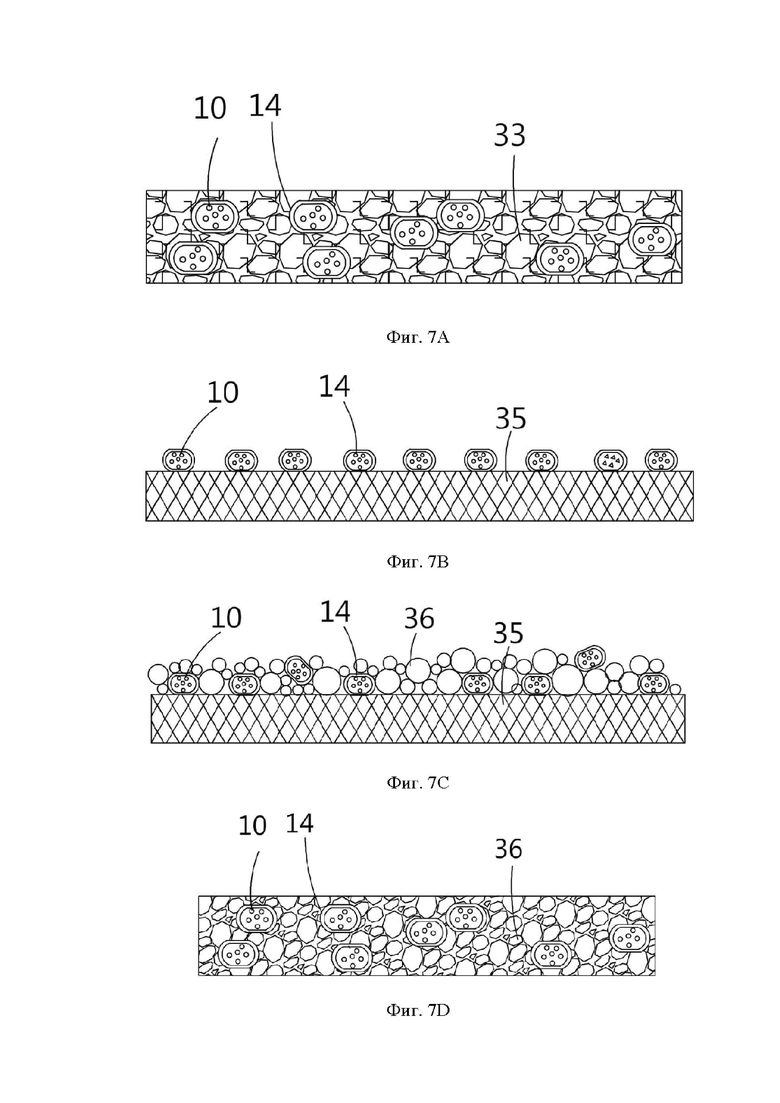
Фигура 7А принципиальная схема слоя активного вещества с поставщиком ионов для применения ионов металлов (А) и (В) в соответствии с настоящим изобретением.
Фигура 7В - принципиальная схема сепаратора, покрытого поставщиком ионов, для применения ионов металлов (А) и (В) в соответствии с настоящим изобретением.
Фигура 7С - принципиальная схема сепаратора в соответствии с настоящим изобретением, поверхность которого содержит керамические порошки и поставщик ионов.
Фигура 7D - принципиальная схема керамических порошков, смешанных с поставщиком ионов, для применения ионов металлов (А) и (В) в соответствии с настоящим изобретением.
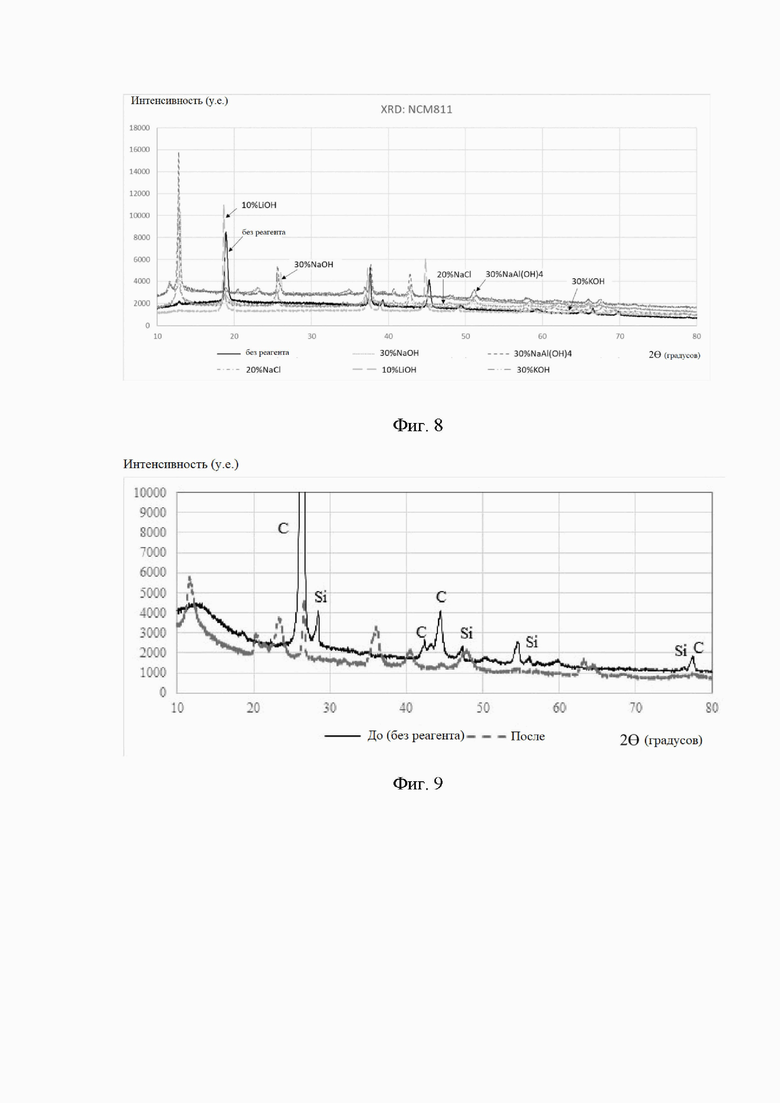
Фигура 8 представляет собой рентгеновскую дифрактограмму, на которой концентрации 30% NaOH(aq), 30% NaAl(OH)4(aq), 30% NaCl(aq), 10% LiOH(aq) и 30% KOH(aq) реагируют с активным веществом положительного электрода с выделением ионов лития.
Фигура 9 представляет собой рентгеновскую дифрактограмму до и после того, как активное вещество отрицательного электрода с введением ионов лития подвергается воздействию ионов натрия/калия и ионов алюминия.
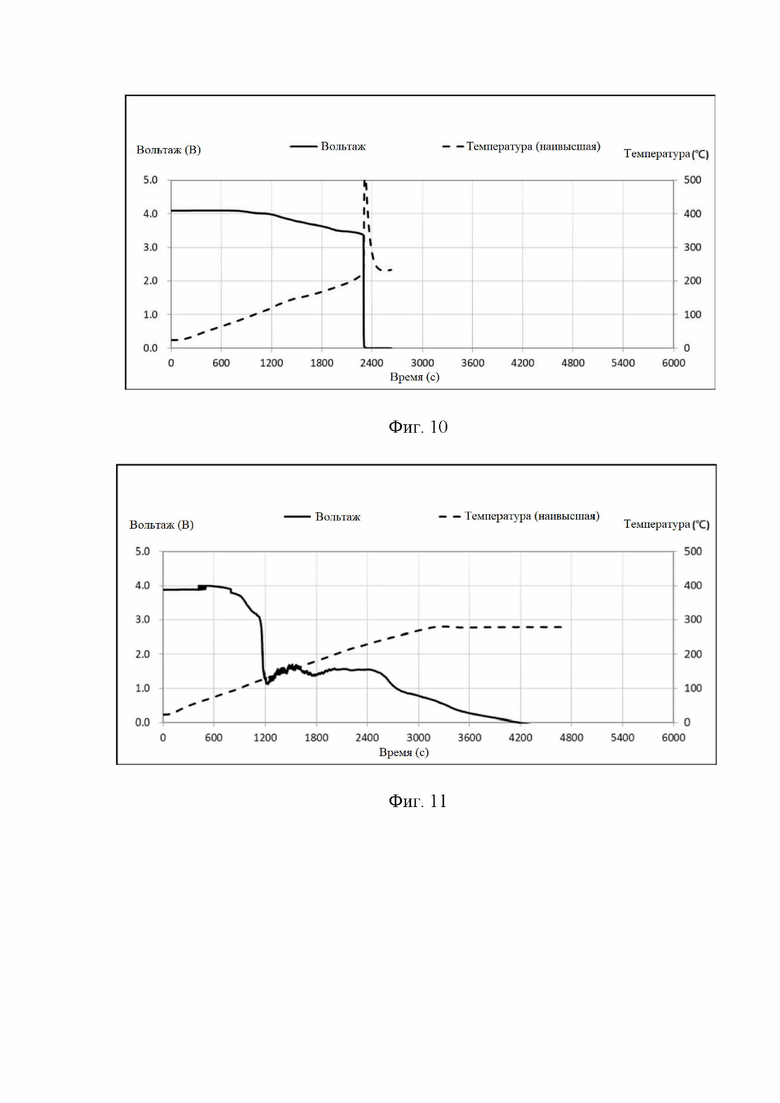
Фигура 10 показывает кривую напряжения и температуры для испытания на тепловое убегание обычного элемента литиевой батареи.
Фигура 11 показывает кривую напряжения и температуры для элемента литиевой батареи с подавлением теплового убегания в соответствии с настоящим изобретением.
Фигуры 12А-12С являются изображениями результатов капания различных растворов, выбранных, соответственно, из чистой воды, NaOH(aq) и NaAl(OH)4(aq), на катод со 100% состоянием зарядки.
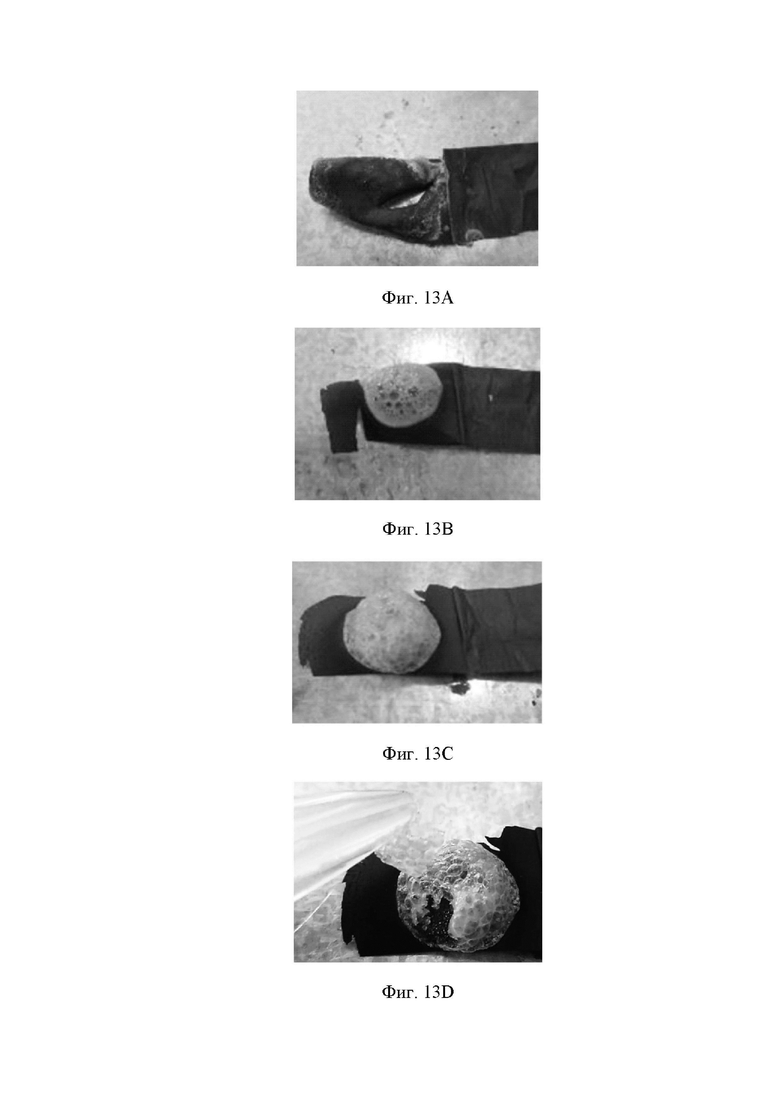
Фигуры 13А-13С являются изображениями результатов капания различных растворов, выбранных, соответственно, из чистой воды, NaOH(aq) и NaAl(OH)4(aq), на анод со 100% состоянием зарядки.
Фигура 13D изображение фигуры 13С, на котором пена зажимается зажимным приспособлением.
Фигуры 14А и 14В представляют собой изображения со сканирующего электронного микроскопа катода батареи, заряженной на 40% и 100%, соответственно, на который 30% водный раствор гидроксида натрия капал в течение примерно 1 часа.
Фигуры 15А и 15В представляют собой изображения со сканирующего электронного микроскопа анода батареи, заряженной на 40% и 100%, соответственно, на который 30% водный раствор гидроксида натрия капал в течение примерно 1 часа.
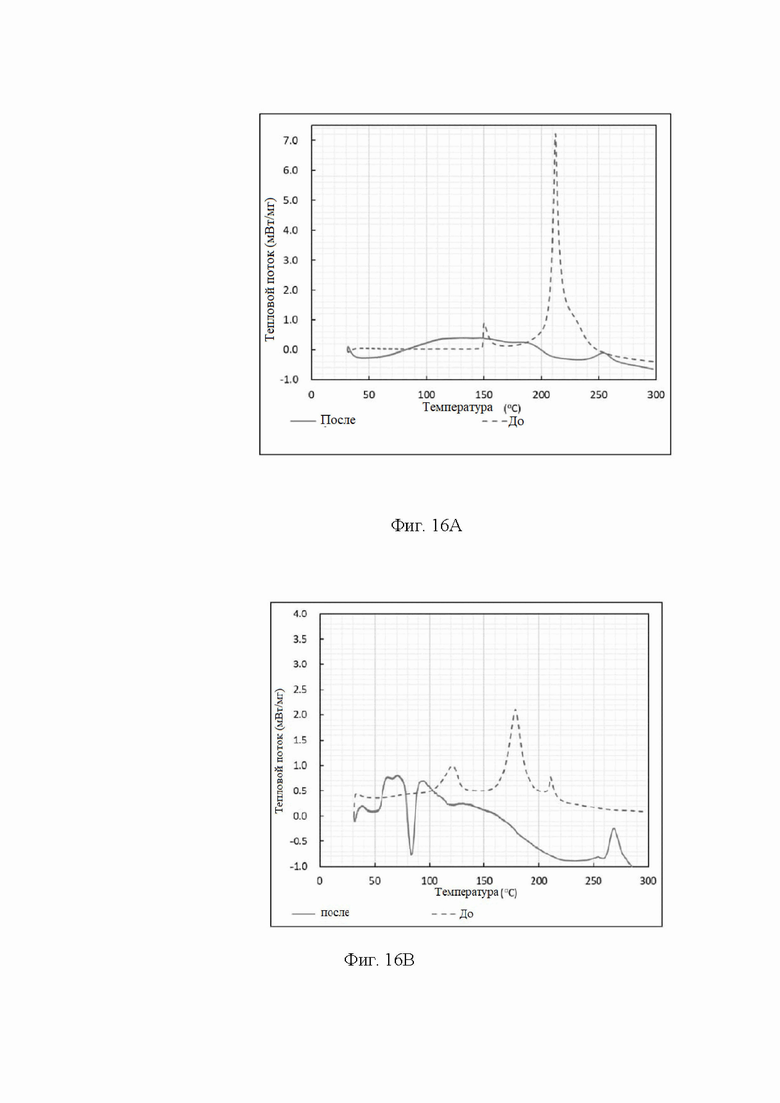
Фигуры 16А и 16В термограммы с дифференциального сканирующего калориметра для катода и анода с использованием 20% NaAl(OH4)(aq).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение будет описано в отношении конкретных вариантов осуществления и со ссылкой на определенные фигуры, но изобретение не ограничивается ими, а только своей патентной формулой. Любые ссылочные позиции в формуле изобретения не должны рассматриваться как ограничение объема изобретения. Описанные фигуры являются только схематическими и не ограничивают объем изобретения. На фигурах размеры некоторых элементов могут быть преувеличены и не отображаться в масштабе в иллюстративных целях.
Используемая здесь терминология предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения общей концепции изобретения. Используемые здесь формы единственного числа предназначены для включения также и форм множественного числа, если контекст явно не подразумевает иное. Если не указано иное, все термины (включая технические и научные), используемые в данном документе, имеют то же значение, которое обычно понимается специалистом в данной области техники, к которой относятся примерные варианты осуществления. Далее следует понимать, что термины, такие как те, которые определены в широко применяемых словарях, должны интерпретироваться как имеющие значение, которое согласуется с их значением в контексте соответствующей области науки и техники, и не должны интерпретироваться в идеализированном или чрезмерно формальном смысле, если только это прямо не определено в данном документе.
Ссылка во всем этом описании на «один вариант осуществления» или «вариант осуществления» означает, что конкретный признак, структура или характеристика, описанные в связи с вариантом осуществления, включены по крайней мере в один вариант осуществления настоящего изобретения. Таким образом, появление фраз «в одном варианте осуществления» или «в варианте осуществления» в различных местах данного описания не обязательно относится к одному и тому же варианту осуществления, хотя это возможно. Кроме того, конкретные признаки, структуры или характеристики могут быть объединены любым подходящим образом, как будет очевидно специалисту в данной области техники из этого раскрытия, в одном или нескольких вариантах осуществления. Прежде всего, обратитесь к фигуре 1, которая представляет собой блок-схему, показывающую пример этапов способа подавления теплового убегания литиевых батарей в соответствии с настоящим изобретением. Как показано на фигуре, первым шагом S1 является «обеспечение литиевой батареи, содержащей в себе электрохимическую реакционную систему». Литиевая батарея способна заряжаться и разряжаться. Это означает, что литиевая батарея может иметь активное вещество положительного электрода с выделением ионов лития и активное вещество отрицательного электрода с введением ионов лития. Затем этап S2 представляет собой «применение дополнительных ионов металла (А) и дополнительных ионов амфотерного металла (В) к литиевой батарее, когда температура литиевой батареи достигает заданного значения». Ионы металла (А) и ионы амфотерного металла (В) будут вступать в химические реакции с активным веществом положительного электрода с выделением ионов лития и активным веществом отрицательного электрода с введением ионов лития, чтобы перевести активное вещество положительного электрода и активное вещество отрицательного электрода электрохимической реакционной системы в пассивированное состояние с более низким уровнем энергии по сравнению с исходными состояниями. Таким образом, протекание электрохимической реакции блокируется, что позволяет эффективно избежать теплового убегания батареи. Ионы металла (А) выбираются из ионов щелочных металлов, отличных от лития, ионов щелочноземельных металлов или их сочетания. Заданная температура составляет 70-130°С. Кроме того, упомянутое выше слово «дополнительные ионы» означает, что литиевая батарея уже имеет необходимые материалы для выполнения зарядки и разрядки, а ионы металла (А) и ионы амфотерного металла (В) дополнительно добавляются в литиевую батарею или в эти материалы.
Когда ионы металла (А) выбираются из ионов щелочных металлов, отличных от лития, предпочтительно выбирать их из ионов натрия, ионов калия или их сочетания. Когда ионы металла (А) выбираются из ионов щелочноземельных металлов, предпочтительно выбирать их из ионов бериллия, ионов магния или ионов кальция. Ионы амфотерных металлов (В) представляет собой ионы алюминия или ионы цинка. Вышеупомянутая электрохимическая реакционная система включает в себя слой активного вещества положительного электрода, слой активного вещества отрицательного электрода, сепаратор, расположенный между слоем активного вещества положительного электрода и слоем активного вещества отрицательного электрода, а также систему электролита, заполненную электрохимической реакционной системой. Система электролита может быть жидкой, твердой или их сочетанием.
После того, как ионы металла (А) и ионы амфотерного металла (В) вводятся в электрохимическую реакционную систему литиевой батареи, для активного вещества положительного электрода, ионы металла (А) будут получать электроны от активного вещества положительного электрода и осаждаться на поверхность активного вещества положительного электрода, а затем мигрировать, чтобы захватывать избыточную часть выделяемых ионов лития. Активное вещество положительного электрода посредством выделения ионов лития переводится из исходного состояния с более высоким электрическим потенциалом и более высокой энергией в состояние пассивации с более низким электрическим потенциалом и более низкой энергией. Кроме того, его структура нестабильна и легко выделяет кислород в различном виде (О2, O2-, О-) из-за потери атомов лития в исходном состоянии активного вещества положительного электрода. Атомы металла, такого как натрий, образованные ионами металла (А) с электронами, будут приводиться в движение тепловой энергией, чтобы заполнить пространство, освобождаемое выделяемыми ионами лития, то есть будет происходить интеркаляция, и перестраивать пространственную решетку таким образом, чтобы сформировать новое стабильное состояние, при этом расходуется тепловая энергия. Кроме того, когда атомы металла, образованные ионами металла (А), такого как натрий, заполняют освобождаемое выделяемыми ионами лития пространство, эта новая структура, имеющая стабильное состояние, будет демонстрировать некоторые характеристики натрия, из-за содержания в ней натрия, например, повышенную адсорбцию влаги. Это повысит изолирующие свойства электродов и приведет к снижению производительности. Аналогичным образом, для активного вещества отрицательного электрода, ионы металла (А) и ионы амфотерного металла (В) будут реагировать с активным веществом отрицательного электрода с введением ионов лития. Активное вещество отрицательного электрода с введением ионов лития переводится из исходного состояния с более низким электрическим потенциалом и более высокой энергией в состояние пассивации с более высоким электрическим потенциалом и более низкой энергией. Следовательно, это изобретение позволяет достичь пассивации активных веществ положительного и отрицательного электродов, применяя дополнительные ионы металла (А) и дополнительные ионы амфотерного металла (В), чтобы заблокировать протекание электрохимической реакции, с целью эффективного избегания теплового убегания батареи.
Что касается этапа S2 применения дополнительных ионов металла (А) и дополнительных ионов амфотерного металла (В) к литиевой батарее, то он имеет следующие типы: 1) ионы металла (А) и ионы амфотерного металла (В) подаются снаружи литиевой батареи в электрохимическую реакционную систему; и 2) ионы металла (А) и ионы амфотерного металла (В) подаются изнутри литиевой батареи в электрохимическую реакционную систему.
В отношении упомянутого выше способа подачи ионов металла (А) и ионов амфотерного металла (В) снаружи литиевой батареи в электрохимическую реакционную систему, можно использовать такие каналы подачи ионов, как клапан сброса давления, выполненный непосредственно на корпусе литиевой батареи, отверстия, возникающие при вспухании литиевой батареи, или же прорывы, вызываемые проколом. Кроме того, каналы могут быть сформированы специально с целью подачи ионов металла (А) и ионов амфотерного металла (В) снаружи литиевой батареи в электрохимическую реакционную систему. Следующее описание иллюстрирует пример такого формирования. Пожалуйста, обратитесь к фигуре 2 и фигуре 3А, этап S12 это «обеспечение литиевой батареи 20, включающей в себя электрохимическую реакционную систему, а также множество сквозных отверстий 203, сформированных на токосъемном слое 202 литиевой батареи 20, и поставщик ионов 10, обеспечивающий подачу ионов металла (А) и ионов амфотерных металлов (В), располагаемый на сквозных отверстиях 203». Литиевая батарея 20 имеет множество сквозных отверстий 203, сформированных на токосъемном слое 202. Одни концы сквозных отверстий 203 выходят наружу литиевой батареи 20, а другие концы соединены с электрохимической реакционной системой, т.е. со слоями активного вещества 208, 210 и сепаратором 212. Поставщик ионов 10 расположен на внешней поверхности литиевой батареи 20 и закрывает сквозные отверстия 203. При таком строении, поскольку поставщик ионов 10 расположен снаружи литиевой батареи 20, это не повлияет на эффективность или состав электрохимической реакционной системы литиевой батареи 20. Диаметр сквозных отверстий составляет от 5 до 250 микрометров. Затем, когда температура литиевой батареи 20 достигает заданного значения, поставщик ионов 10 подает ионы металла (А) и ионы амфотерного металла (В) в электрохимическую реакционную систему через сквозные отверстия 203 (этап S22).
Кроме того, для описанного выше процесса, когда активное вещество положительного электрода переводится из состояния с более высоким электрическим потенциалом и более высокой энергией в состояние с более низким электрическим потенциалом и более низкой энергией, подробное описание приводится ниже. Активное вещество положительного электрода находится в состоянии выделения ионов лития, а его электрический потенциал более высок. Кроме того, из-за нестабильности кристаллической решетки она легко разрушается и имеет более высокую способность выделять кислород и большие объемы тепловой энергии. Следовательно, как определено выше, активное вещество положительного электрода находится в состоянии с более высоким электрическим потенциалом и более высокой энергией, что может вызвать тепловое убегание. Когда ионы металла (А) заполняют позиции, откуда выделились ионы лития, т.е. происходит интеркаляция, электрический потенциал активного вещества положительного электрода снижается, и кристаллическая решетка активного вещества положительного электрода становится относительно стабильной. Кроме того, стабильность кристаллической решетки активного вещества положительного электрода повышается, а способность выделять кислород снижается, как и способность резко выделять тепловую энергию. Следовательно, как определено выше, активное вещество положительного электрода находится в состоянии пассивации после реакции с ионами металла (А), что определяет его кристаллическое состояние с более низким электрическим потенциалом и более низкой энергией.
Для описанного выше процесса, когда активное вещество отрицательного электрода переводится из состояния с более низким электрическим потенциалом и более высокой энергией, которое может стать причиной теплового убегания, в состояние с более высоким электрическим потенциалом и более низкой энергией, подробное описание приводится ниже. Активное вещество отрицательного электрода находится в состоянии с введением ионов лития, и его электрический потенциал ниже. Кроме того, поскольку активное вещество отрицательного электрода поглощает кислород, высвобождаемый из активного вещества положительного электрода, активное вещество отрицательного электрода склонно к интенсивному горению и высвобождению тепловой энергии. Следовательно, активное вещество отрицательного электрода нестабильно и имеет более высокую способность выделять тепловую энергию. Соответственно, как определено выше, активное вещество отрицательного электрода находится в состоянии с более низким электрическим потенциалом и более высокой энергией. Когда ионы металла (А) и ионы амфотерного металла (В) взаимодействуют с активным веществом отрицательного электрода с введением ионов лития, ионы лития извлекаются и образуют полимерное соединение с основным компонентом активного вещества отрицательного электрода, таким как кремний-углерод. Наряду с уменьшением способности активного вещества положительного электрода выделять кислород, способность активного вещества отрицательного электрода бурно выделять тепловую энергию также снижается. Следовательно, как определено выше, активное вещество отрицательного электрода после взаимодействия с ионами металла (А) и ионами амфотерного металла (В) находится в состоянии пассивации, которое определяется как состояние полимерного соединения с более высоким электрическим потенциалом и более низкой энергией. Поставщиком ионов 10 может быть соединение, способное обеспечивать подачу ионов металла (А), и соединение, способное обеспечивать подачу ионов амфотерного металла (В). Например, соединение, способное предоставлять ионы металла (А), может представлять собой NaOH, KOH, NaCl, NaNO3, KNO3 или другое подобное. Соединение, способное предоставлять ионы амфотерных металлов (В), может представлять собой AlCl3, AlBr3, AlI3, Al(NO3)3, AlClO4, AlF3, AlH3, Zn(OH)2 или другое подобное. Также поставщик ионов 10 может быть соединением, способным обеспечивать подачу как ионов металла (А), так и ионов амфотерного металла (В), такое как NaAl(OH)4 или другое подобное.
Литиевая батарея 20 в соответствии с этим вариантом осуществления включает в себя первый токосъемный слой 202, второй токосъемный слой 204, клеевой каркас 206, электрохимическую реакционную систему, сепаратор 212 и систему электролита. Клеевой каркас 206 расположен между первым токосъемным слоем 202 и вторым токосъемным слоем 204. Один конец клеевого каркаса 206 приклеен к первому токосъемному слою 202, а другой конец клеевого каркаса 206 приклеен ко второму токосъемному слою 204. Первый токосъемный слой 202, второй токосъемный слой 204 и клеевой каркас 206 образуют замкнутое пространство (сквозные отверстия 203 здесь не рассматриваются). Электрохимическая реакционная система, расположенная в замкнутом пространстве, включает в себя первый слой активного вещества 208, примыкающий к первому токосъемному слою 202, и второй слой активного вещества 210, примыкающий ко второму токосъемному слою 204. Первый слой активного вещества 208 и второй слой активного вещества 210 представляют собой, соответственно, активные вещества положительного и отрицательного электродов. Сепаратор 212 расположен между первым слоем активного вещества 208 и вторым слоем активного вещества 210 и имеет характеристики ионной проводимости и электроизоляционные свойства. Система электролита расположена в замкнутом пространстве и пропитывает или смешана с первым слоем активного вещества 208 и вторым слоем активного вещества 210, и используется для переноса ионов. Кроме того, первый слой активного вещества 208 и второй слой активного вещества 210 могут дополнительно включать в себя электропроводящие материалы и адгезивные материалы. Поскольку эти части не являются техническими особенностями данного изобретения, подробное описание здесь не приводится.
Также, материал сепаратора 212 может быть выбран из различных типов материалов, используемых в аккумуляторной промышленности. Например, сепаратор 212 может состоять из твердого электролита или электроизоляционного слоя с отверстиями, сформированного из полимерного материала, с покрытием из керамических порошков на его поверхности. Кроме того, сепаратор 212 также может быть сформирован путем укладки только керамических порошков с использованием связующего вещества. Керамические порошки могут не обладать ионной проводимостью или же могут иметь ионную проводимость. Сквозные отверстия 203 проходят через первый токосъемный слой 202 для соединения его верхней и нижней поверхностей. Следовательно, один конец сквозных отверстий 203 открыт во внешнюю среду литиевой батареи 20, а другой конец соединен с электрохимической реакционной системой литиевой батареи 20. Первый токосъемный слой 202 может быть положительным токосъемным слоем или отрицательным токосъемным слоем. Полярность первого токосъемного слоя 202 отличается от полярности второго токосъемного слоя 204. Например, когда первый токосъемный слой 202 является положительным токосъемным слоем, второй токосъемный слой 204 является отрицательным токосъемным слоем. Первый токосъемный слой 202, второй токосъемный слой 204 и клеевой каркас 206 используются в качестве упаковочного компонента батареи. Иными словами, если не учитываются сквозные отверстия 203, электрохимическая реакционная система литиевой батареи 20 защищена от внешней среды этим упаковочным компонентом.
Клеевой каркас 206 изготавливается из полимерного материала без особых требований к нему, если он способен приклеиваться к поверхностям первого и второго токосъемных слоев 202, 204 и быть достаточно прочным для системы электролита. Однако предпочтительным является использование термореактивной смолы, например, силикона. Активное вещество отрицательного электрода может быть углеродным материалом, материалом на основе кремния или их сочетанием. Примеры углеродных материалов включают графитированные углеродные материалы и аморфные углеродные материалы, такие как природный графит, модифицированный графит, частицы графитированного мезофазного углерода, мягкие углеродные материалы, такие как кокс, и некоторые твердые углероды. Материалы на основе кремния включают кремний, оксиды кремния, кремний-углеродные композитные материалы и кремниевые сплавы.
Способ формирования сквозных отверстий 203 в токосъемном слое 202 может заключаться в их непосредственной пробивке и предварительном формовании в токосъемном слое 202. Кроме того, чтобы предотвратить взаимодействие поставщика ионов 10, являющегося источником ионов металла (А) и ионов амфотерного металла (В), с электрохимической реакционной системой, через заранее сформированные сквозные отверстия 203, например, утечку электролита в поставщик ионов 10, или проникновение поставщика ионов 10 внутрь электрохимической реакционной системы, поверх сквозных отверстий 203 расположен удаляемый затворный слой 205 для временного закрытия отверстий, как показано на фигуре 3В. При разрушении затворного слоя 205 сквозные отверстия 203 открываются. Например, затворный слой 205 может быть изготовлен из материалов, которые могут быть разрушены травлением, а материалы для травления затворного слоя 205 могут содержаться в поставщике 10 ионов металла (А) и ионов амфотерного металла (В), или же применяться дополнительно. Затворный слой 205 также может быть изготовлен из термочувствительного материала, который может плавиться при нагреве, выступающем в качестве разрушающего механизма, или затворный слой 205 может быть изготовлен из деполимеризуемого материала, а материал, вызывающий деполимеризацию, может содержаться в поставщике 10 ионов металла (А) и ионов амфотерного металла (В) или же применяться дополнительно.
Другой способ формирования сквозных отверстий 203 в токосъемном слое 202 травление, например, поставщик 10 ионов металла (А) и ионов амфотерного металла (В) может иметь способность к травлению, и способность к травлению будет активироваться высокой температурой. Например, внешняя поверхность поставщика ионов 10 может быть покрыта защитным слоем 12, состоящим из термочувствительного материала, разлагающегося при перегреве. Как показано на фигуре 4, когда температура приближается к заданному значению, защитный слой 12 будет разлагаться, открывая/высвобождая поставщик ионов 10, и заставляя поставщик ионов 10 проявлять способность к травлению внешнего компонента (токосъемного слоя 202). С другой стороны, поставщик ионов 10 может иметь разлагаемый состав, активируемый высокой температурой, как, например, высвобождающие воду материалы. При высоких температурах высвобождающие воду материалы эндотермически разлагаются с выделением воды, чтобы отрегулировать концентрацию или характеристики ионов поставщика ионов 10, активируя его способность к травлению.
Пожалуйста, обратитесь к фигуре 5, которая используется для иллюстрации того, каким образом ионы металла (А) и ионы амфотерного металла (В) подаются внутрь литиевой батареи и поступают в электрохимическую реакционную систему. Как показано на фигуре, литиевая батарея 20 дополнительно включает в себя поставщик ионов 10, обеспечивающий ионы металла (А) и ионы амфотерного металла (В), и расположенный внутри литиевой батареи 20, при этом поверхность поставщика ионов 10 включает удаляемый защитный механизм (этап S14). Например, защитный слой может быть нанесен на поверхность поставщика ионов 10 пленочного типа, или поставщик ионов 10 может быть разделен на части в оболочке, чтобы избежать неправильного взаимодействия между электрохимической реакционной системой и поставщиком ионов 10. Затем, на этапе S24, когда температура литиевой батареи 20 достигает заданного значения, удаляемый защитный слой разрушается, и поставщик ионов 10 подает ионы металла (А) и ионы амфотерного металла (В) в электрохимическую реакционную систему. Далее, ионы металла (А) и ионы амфотерного металла (В) реагируют с активным веществом положительного и отрицательного электродов, вызывая их пассивацию. В отношении механизма защиты, например, поставщик ионов 10, обеспечивающий ионы металла (А) и ионы амфотерного металла (В), может быть покрыт вышеупомянутым защитным слоем 12 и размещен в упаковочном корпусе 32 литиевой батареи 30. Как показано на фигуре 6, поставщик ионов 10 не располагается в слоях активного вещества или в сепараторе электрохимической реакционной системы.
Поставщик ионов 10 содержится в оболочке 14 и смешивается со слоем активного вещества 33 электрохимической реакционной системы, как показано на фигуре 7А, или наносится на поверхность сепаратора 35, как показано на фигуре 7В. Кроме того, поверхность сепаратора 35 может быть также покрыта армирующим материалом, например, керамическим порошком 36, как показано на фигуре 7С, или, в случае отсутствия подложки, оболочки, наполненные поставщиком ионов 10, могут быть смешаны с керамическим порошком 36 сепаратора 35, как показано на фигуре 7D. Эти керамические порошки 36 могут обладать ионной проводимостью или не обладать ею. Кроме того, оболочки 14 могут быть смешаны с электролитом (жидким или твердым). В этом варианте осуществления оболочка 14 используется в качестве механизма защиты поставщика ионов 10, чтобы предотвратить реакцию поставщика ионов 10 с компонентами электрохимической реакционной системы, когда заданная температура не достигнута. Этот способ может быть применен к конструкции литиевой батареи с клеевым каркасом и токосъемным слоем, служащими в качестве упаковочной конструкции, а также может быть применен к литиевой батарее, которая не использует токосъемный слой и клеевой каркас в качестве упаковочной конструкции, когда, например, используется металлический кожух, как показано на фигуре 6, или же литиевые батареи упакованы в алюминиево-пластиковую пленку.
Термочувствительный разлагающийся материал защитного слоя 12 выбирается из парафинового масла, микрокристаллического воска, полиэтиленового воска, полиэтилена низкой плотности, поли(транс-1,4-бутадиена), политетраметиленоксида, изотактического полиметилметакрилата, полиэтиленоксида, полиэтиленадипата, изотактического поли(1-бутена), полиэтилена. Кроме того, термочувствительный разлагающийся материал может быть смешан с минеральным маслом для снижения температуры размягчения. Материал оболочки 14 определяется содержащимся в ней соединением. Например, когда разлагаемый состав, который разлагается под воздействием высокой температуры поставщика ионов 10, выбирается из высвобождающих воду материалов, материал оболочки 14 выбирается из материалов, легко растворяемых в полярных растворах, таких как вода, желатин, гуммиарабик, хитозан, казеинат натрия, крахмал, лактоза, мальтодекстрин, поли-L-лизин/альгинат, полиэтиленимин/альгинат, альгинат кальция, поливиниловый спирт. Когда материалом оболочки 14 является термочувствительный разлагающийся материал, он выбирается из этилцеллюлозы, полиэтилена, полиметакрилата, нитроцеллюлозы, силиконов, парафина, карнаубского воска, стеариновой кислоты, жирных спиртов, стеарилового спирта, жирных кислот, углеводородной смолы, моноацилглицерола, диацилглицерина и триацилглицерина. Когда поставщик ионов 10 выбирается из материалов, которые проявляют способность к травлению при определенной температуре, материал оболочки 14 выбирается из травимых материалов. Однако эти описания являются лишь примерами. Специалисты в данной области техники поймут, что в конкретные варианты осуществления могут быть внесены изменения, не выходящие за рамки сущности и объема изобретения. Продолжая, необходимо убедиться, что способ в соответствии с настоящим изобретением может воздействовать на активные вещества положительного и отрицательного электродов и изменять структуру активных веществ положительного и отрицательного электродов для подавления теплового убегания. В этом эксперименте активным веществом положительного электрода является NMC811, а активным веществом отрицательного электрода кремний-углерод. Ионы металла (А) представляют собой ионы натрия или калия, а ионы амфотерного металла (В) представляют собой ионы алюминия.
Пожалуйста, обратитесь к фигуре 8, которая представляет собой рентгеновскую дифрактограмму, на которой концентрации 30% NaOH, 30% NaAl(OH)4, 30% NaCl, 10% LiOH, and 30% KOH реагируют с активным веществом положительного электрода с выделением ионов лития. Из фигуры видно, что после того, как NMC811 с выделением ионов лития прореагирует с ионами натрия или калия, характеристический пик (указанный стрелками) NMC811 больше не существует, а структура решетки изменилась из-за введения ионов натрия или калия. Это может быть связано с тем, что ионы натрия/калия, имеющие более крупный размер, больший вес и более высокую потенциальную энергию, поглощают электроны на поверхности активного вещества положительного электрода с образованием атомов натрия/калия. И за счет поглощения тепловой энергии они будут перемещаться на места выделяемых ионов лития, т.е. будет происходить интеркаляция, формируя более стабильную структуру с более стабильной и низкой энергией.
Пожалуйста, обратитесь к фигуре 9, которая представляет собой рентгеновскую дифрактограмму до и после того, как активное вещество отрицательного электрода с введением ионов лития подвергается воздействию ионов натрия/калия и ионов алюминия. Очевидно, что характерные пики, представляющие сплавы лития и кремния, полностью исчезли. Это означает, что сплавы лития и кремния превратились в полимерные соединения с более низкой энергией.
Обратитесь к фигурам 10 и 11. Фигура 10 показывает кривую напряжения и температуры для испытания на тепловое убегание обычного элемента литиевой батареи. Фигура 11 показывает кривую напряжения и температуры для элемента литиевой батареи с подавлением теплового убегания в соответствии с настоящим изобретением. Как показано на фигурах, при возникновении теплового убегания, выделяющего тепло, напряжение обычного литиевого аккумуляторного элемента начинает падать после того, как температура достигает примерно 500°С. Однако для элемента литиевой батареи с подавлением теплового убегания в соответствии с настоящим изобретением напряжение начинает падать после того, как температура достигает около 100°С, блокируя протекание электрохимической реакции, чтобы эффективно избежать теплового убегания. Фигуры 12А-12С представляют собой изображения результатов капания различных растворов, выбранных из, соответственно, чистой воды, NaOH(aq) и NaAl(OH4)(aq) на катод батареи, заряженной на 100%. На фигуре 12А видно, что катод не вступает в реакцию с чистой водой. На фигурах 12В и 12С видно, что NaOH(aq) и NaAl(OH4)(aq) образуют на поверхности катода капли в гидрофобном состоянии, и в каплях присутствует множество крошечных пузырьков.
Фигуры 13А-13С являются изображениями результатов капания различных растворов, выбранных из, соответственно, чистой воды, NaOH(aq) и NaAl(OH4)(aq), на анод батареи, заряженной на 100%. На фигуре 13А видно, что оставшийся в аноде литий вступает в интенсивную реакцию с чистой водой, что приводит к растрескиванию анода. На фигурах 13В и 13С можно видеть, что NaOH(aq) и NaAl(OH4)(aq) образуют на поверхности анода неорганический полимер с пузырьками, похожими на пену. Кроме того, часть неорганического полимера может быть зажата зажимом, как показано на фигуре 13D. Фигуры 14А и 14В представляют собой изображения со сканирующего электронного микроскопа катода батареи, заряженной на 40% и 100%, соответственно, при этом 30% гидроксид натрия капал на него в течение примерно 1 часа, для очистки поверхности использовались DMC (диметилкарбонат) и чистая вода, и затем он просушивался в течение 8 часов при 60°С. Как показано на фигурах, для катода батареи, заряженной на 40%, из-за более низкой степени выделения ионов лития, введение ионов натрия на место выделенных ионов лития в катоде не оказывает на него существенного влияния. Однако неровности топографии поверхности катода уже становятся значительными. Для катода батареи, заряженной на 100%, из-за более высокой степени выделения ионов лития, введение ионов натрия на место выделенных ионов лития в катоде уже оказывает на него существенное влияние. Смещение решетки и неровность топографии поверхности катода батареи, заряженной на 100%, также очень значительны. И можно заметить, что некоторые части поверхности даже имеют следы растрескивания.
Фигуры 15А и 15В представляют собой изображения со сканирующего электронного микроскопа анода батареи, заряженной на 40% и 100%, соответственно, при этом 30% гидроксид натрия капал на него в течение примерно 1 часа, для очистки поверхности использовались DMC (диметилкарбонат) и чистая вода, и затем он просушивался в течение 8 часов при 60°С. Как показано на фигурах, гидроксид натрия превращает части анода батареи, заряженной на 40%, в неорганический полимер (геополимер), а также он имеет игольчатую структуру коллоидной кремнеземной кислоты. Для анода батареи, заряженной на 100%, игольчатая структура еще более очевидна.
Кроме того, чтобы удостовериться в упомянутой выше более низкой энергии катода и анода, обратитесь к фигурам 16А и 16В, которые представляют собой термограммы с дифференциального сканирующего калориметра для катода и анода с использованием 20% NaAl(OH4)(aq). На фигуре 16А можно ясно видеть, что пик теплового потока катода при температуре около 210°С, очевидно, исчез, и пик теплового потока анода при температуре около 180°С, как видно на фигуре 16В, очевидно, также исчез. Соответственно, настоящее изобретение обеспечивает способ подавления теплового убегания литиевых батарей. Когда температура литиевой батареи достигает заданного значения, ионы металла (А) и ионы амфотерного металла (В) наносятся на активное вещество положительного электрода и активное вещество отрицательного электрода для проведения реакций. Активное вещество положительного электрода с выделением ионов лития и активное вещество отрицательного электрода с введением ионов лития переводятся в состояние пассивации с более низкой энергией. Протекание электрохимической реакции блокируется, чтобы эффективно избежать теплового убегания батареи. Ионы металла (А) выбираются из ионов щелочных металлов, отличных от лития, ионов щелочноземельных металлов или их сочетания. Более того, по сравнению с традиционными способами, способ подавления теплового убегания в соответствии с настоящим изобретением выполняется непосредственно на поверхности активных веществ, которые генерируют максимальную энергию, вызывающую тепловое убегание, и являются основными реагентами всей электрохимической реакции. Кроме того, ионы металла (А) будут приводиться в движение полученной тепловой энергией, заполняя или интеркалируя выделенные ионы лития, и перестраивая кристаллическую решетку таким образом, чтобы сформировать новое стабильное ее состояние, в то же время потребляя тепловую энергию. Ионы металла (А) и ионы амфотерного металла (В) будут вступать в реакцию с активным веществом отрицательного электрода с введением ионов лития, чтобы перевести его в состояние пассивации. Следовательно, как активное вещество положительного электрода, так и активное вещество отрицательного электрода в результате останутся в состоянии с более низкой энергией, повышая безопасность литиевых батарей.
Из описанного таким образом изобретения будет очевидно, что оно может быть изменено многими способами. Такие изменения не следует рассматривать как отступление от сущности и объема изобретения, и все такие модификации, которые будут очевидны специалисту в данной области техники, предназначены для включения в объем следующей патентной формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕМЕНТ ПОДАВЛЕНИЯ ТЕПЛОВОГО УБЕГАНИЯ И ЕГО СООТВЕТСТВУЮЩЕЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2772946C1 |
| ЛИТИЕВЫЕ АККУМУЛЯТОРЫ | 2022 |
|
RU2810614C1 |
| ЛИТИЕВЫЕ АККУМУЛЯТОРЫ | 2022 |
|
RU2810612C1 |
| ПЕРЕЗАРЯЖАЕМЫЙ ЭЛЕМЕНТ АККУМУЛЯТОРНОЙ БАТАРЕИ | 2007 |
|
RU2438212C2 |
| ПЕРЕЗАРЯЖАЕМЫЙ ЭЛЕКТРОХИМИЧЕСКИЙ ЭЛЕМЕНТ | 2011 |
|
RU2569328C2 |
| Горизонтальная составная группа элементов электоропитания | 2019 |
|
RU2733271C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ОКСИДНОГО ТВЕРДОГО ЭЛЕКТРОЛИТА С ИСХОДНОЙ ФАЗОЙ, СПОСОБ ПРОИЗВОДСТВА ЛИТИЕВОЙ БАТАРЕИ И ЭКОЛОГИЧНАЯ БАТАРЕЯ ИЗ НЕГО | 2020 |
|
RU2741877C1 |
| КОМПОЗИТНЫЙ РАЗДЕЛИТЕЛЬНЫЙ СЛОЙ | 2021 |
|
RU2763581C1 |
| АКТИВНЫЙ МАТЕРИАЛ ОТРИЦАТЕЛЬНОГО ЭЛЕКТРОДА НА ОСНОВЕ КРЕМНИЕВОГО СПЛАВА ДЛЯ ЭЛЕКТРИЧЕСКОГО УСТРОЙСТВА | 2010 |
|
RU2508579C2 |
| КОНСТРУКЦИЯ БАТАРЕИ | 2018 |
|
RU2721216C1 |


Изобретение относится к способу подавления теплового убегания литиевых батарей путем пассивации слоя активного вещества положительного электрода и слоя активного вещества отрицательного электрода. Изобретение обеспечивает способ, который включает этап обеспечения литиевой батареи, способной заряжаться и разряжаться, которая включает с себя электрохимическую реакционную систему. Когда температура литиевой батареи достигает заданного значения, ионы металла (А) и ионы амфотерного металла (В) наносятся на слой активного вещества положительного электрода и слой активного вещества отрицательного электрода литиевой батареи для пассивации слоя активного вещества положительного электрода и слоя активного вещества отрицательного электрода. Ионы металла (А) выбираются из ионов щелочных металлов, отличных от лития, ионов щелочноземельных металлов или их сочетания. Техническим результатом является повышение безопасности литиевых батарей за счет подавления теплового убегания литиевых батарей путем уменьшения тепловой энергии, приводящей к тепловому убеганию, неуправляемому нагреву активных веществ. 15 з.п. ф-лы, 16 ил. 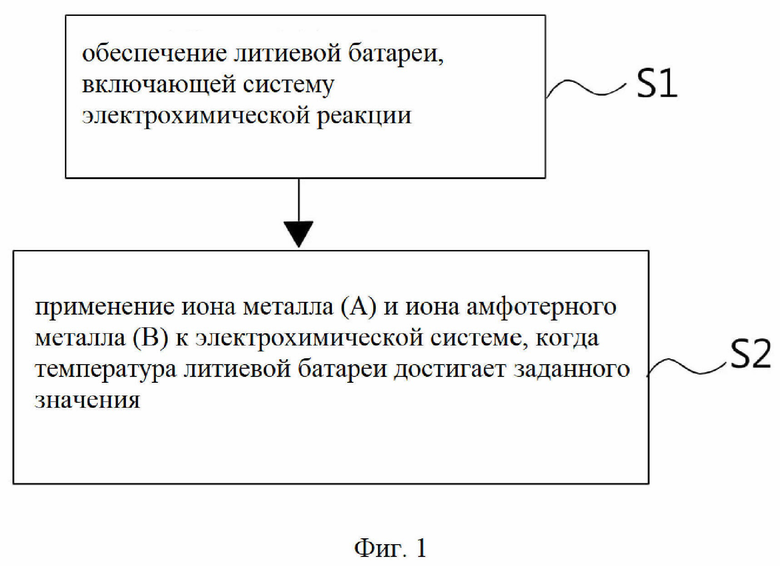
1. Способ подавления теплового убегания литиевых батарей, содержащий следующие этапы:
этап (а): обеспечение литиевой батареи, способной заряжаться и разряжаться, которая включает в себя электрохимическую реакционную систему; а также
этап (b): нанесение ионов металла (A) и ионов амфотерного металла (B) на слой активного вещества положительного электрода и слой активного вещества отрицательного электрода литиевой батареи, когда температура литиевой батареи достигает заданного значения, для пассивации слоя активного вещества положительного электрода и слоя активного вещества отрицательного электрода; причем ионы металла (А) выбираются из ионов щелочных металлов, отличных от лития, ионов щелочноземельных металлов или их сочетания.
2. Способ по п. 1, в котором ионы металла (А) выбираются из ионов натрия, ионов калия или их сочетания.
3. Способ по п. 2, в котором поступление ионов металла (A) обеспечивается соединениями NaOH, KOH, NaCl, KCl, NaNO3, KNO3 или NaAl(OH)4.
4. Способ по п. 1, в котором ионы амфотерных металлов (В) представляют собой ионы алюминия.
5. Способ по п. 1, в котором поступление ионов амфотерного металла (B) обеспечивается соединениями AlCl3, AlBr3, AlI3, Al(NO3)3, AlClO4, AlF3, AlH3, Zn(OH)2 или NaAl(OH)4.
6. Способ по п. 1, в котором литиевая батарея на этапе (а) дополнительно содержит:
сквозное отверстие, соединяющее электрохимическую реакционную систему с наружной частью литиевой батареи; а также
поставщик ионов, обеспечивающий поступление ионов металла (A) и ионов амфотерного металла (B), расположенный на внешней поверхности литиевой батареи и накрывающий сквозное отверстие.
7. Способ по п. 6, в котором диаметр сквозного отверстия составляет от 5 до 250 мкм.
8. Способ по п. 6, в котором литиевая батарея на этапе (а) дополнительно содержит удаляемый затворный слой, закрывающий сквозное отверстие, при этом поставщик ионов расположен на внешней поверхности затворного слоя.
9. Способ по п. 8, в котором затворный слой удаляется посредством термического разложения, травления или деполимеризационного разложения.
10. Способ по п. 1, в котором литиевая батарея на этапе (а) дополнительно включает в себя поставщик ионов, обеспечивающий поступление ионов металла (А) и ионов амфотерного металла (В) и расположенный внутри литиевой батареи, при этом поверхность поставщика ионов включает в себя удаляемый защитный механизм.
11. Способ по п. 10, в котором защитный механизм представляет собой защитный слой, который удаляется путем термического разложения или растворяется в полярном растворе.
12. Способ по п. 10, в котором поставщик ионов расположен внутри электрохимической реакционной системы.
13. Способ по п. 10, в котором защитный механизм представляет собой оболочку, которая удаляется путем термического разложения или растворяется в полярном растворе.
14. Способ по п. 13, в котором поставщик ионов расположен в слоях активного вещества электрохимической реакционной системы, нанесен на сепаратор электрохимической реакционной системы или добавлен в электролит электрохимической реакционной системы.
15. Способ по п. 13, в котором сепаратор электрохимической реакционной системы покрыт множеством слоев керамических порошков, а поставщик ионов перемешан с керамическими порошками.
16. Способ по п. 1, в котором заданная температура составляет 70-130 °C.
| US 2016141720 A1, 19.05.2016 | |||
| US 9711774 B2, 18.07.2017 | |||
| ОРГАНИЧЕСКИЙ/НЕОРГАНИЧЕСКИЙ КОМПОЗИТНЫЙ СЕПАРАТОР И ЭЛЕКТРОХИМИЧЕСКОЕ УСТРОЙСТВО, ЕГО СОДЕРЖАЩЕЕ | 2008 |
|
RU2460177C2 |
| Способ шлифования желоба на круглой детали | 1989 |
|
SU1731601A2 |
| CN 208336379 U, 04.01.2019. | |||
Авторы
Даты
2022-06-01—Публикация
2021-07-23—Подача