ПРЕДПОСЫЛКИ СОЗДАНИЯ ДАННОГО ИЗОБРЕТЕНИЯ
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка в соответствии с §119(a) тома 35 Свода законов США испрашивает приоритет предварительной заявки на патент США № 63/296,315, поданной 4 января 2022 г., содержание которой для любых целей полностью включено в настоящий документ путем ссылки.
Область техники
Данное изобретение относится к литиевому аккумулятору, в частности, к литиевому аккумулятору, способному подавлять тепловой разгон.
Уровень техники
Поскольку литий-ионные аккумуляторы широко используются в различных изделиях, таких как транспортные средства, носимые изделия для потребителей и промышленного применения, портативные устройства и устройства хранения энергии и прочее, они применяются практически во всех областях повседневной жизни человека. Тем не менее, время от времени происходят несчастные случаи с литий-ионными аккумуляторами, например, возгорание или взрыв аккумуляторов мобильных телефонов и электромобилей. Все это связано с тем, что в литий-ионных аккумуляторах до сих пор отсутствуют комплексные и эффективные решения вопросов безопасности.
Основной причиной возгорания или взрыва в литиевых аккумуляторах является тепловой разгон. Основной причиной теплового разгона литиевых аккумуляторов является тепло, которое представляет собой экзотермические реакции, возникающие в результате термического растрескивания, вызванного повышенной температурой, пленки SEI (интерфейс электролит-твёрдое тело), электролита, связующего вещества, а также активных материалов положительного и отрицательного электродов в аккумуляторе. Существующие способы подавления теплового разгона можно разделить на два типа: снаружи аккумуляторного элемента и внутри аккумуляторного элемента в зависимости от участка активации защитного механизма. Для типа вне аккумуляторного элемента используется система мониторинга с цифровым арифметическим моделированием. Для типа внутри аккумуляторного элемента эти способы можно дополнительно разделить на физические или химические. Для улучшения контроля безопасности аккумулятора в процессе использования в цифровой системе контроля снаружи аккумуляторного элемента используется специальная схема защиты и специальная система контроля снаружи аккумуляторного элемента. Для физического типа внутри аккумуляторного элемента, такого как сепаратор с тепловым отключением, при повышенной температуре для аккумуляторного элемента отверстия сепаратора закрываются, блокируя прохождение ионов.
Для химического типа внутри аккумуляторного элемента его можно определить как тип с управлением по уровню или тип электрохимической реакции. В типе с управлением по уровню в электролит добавляют антипирен для управления уровнем теплового разгона. Примеры типов электрохимических реакций приведены ниже.
a) Мономер или олигомер добавляют в электролит. Полимеризация будет происходить при повышении температуры с целью уменьшить скорость миграции ионов. Поэтому при повышении температуры ионная проводимость уменьшается, а скорость электрохимических реакций в элементе замедляется.
b) Материал сопротивления с положительным температурным коэффициентом (ПТК) помещен между положительным электродным слоем или отрицательным электродным слоем, и соседним токосъемным слоем. При повышении температуры аккумуляторного элемента повышается способность к электроизоляции. Эффективность передачи электроэнергии между положительным электродным слоем или отрицательным электродным слоем между соседними токосъемными слоями снижается, и скорость электрохимической реакции также снижается.
c) На поверхности активного материала положительного электрода формируется модифицированный слой. При повышении температуры аккумуляторного элемента модифицированный слой превращается в плотную пленку, что увеличивает сопротивление переноса заряда и снижает скорость электрохимической реакции.
Тем не менее, вышеперечисленные способы направлены только на пассивное блокирование пути миграции ионов/электронов для уменьшения выделения тепла, но не на основной источник генерирования максимальной энергии для обеспечения теплового разгона и основной реакционной массы всей электрохимической реакции, т.е. активных материалов.
Таким образом, данное изобретение предлагает принципиально новый литиевый аккумулятор для решения проблемы теплового разгона из активных материалов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Задача данного изобретения состоит в разработке литиевого аккумулятора, который содержит источник ионов, размещенный в положительном электроде. Источник ионов не участвует в операциях зарядки и разрядки. Источник ионов способен поглощать тепловую энергию с высвобождением реакционноспособной анионной группы. Реакционноспособная анионная группа будет взаимодействовать с активным материалом положительного электрода, что уменьшает обратимость данного активного материала положительного электрода. Кроме того, под действием некоторой специфической реакционноспособной анионной группы структура решетки активного материала положительного электрода будет переходить из состояния с более высокой энергией в состояние с более низкой энергией с выведением ионов лития. Следовательно, положительный электрод, из которого ушли ионы лития, стабилизируется и будет более эффективно подавлять тепловой разгон литиевого аккумулятора.
Другая задача данного изобретения состоит в разработке литиевого аккумулятора, который содержит источник ионов, размещенный в положительном электроде, и приемник лития, размещенный в отрицательном электроде. Источник ионов может поглощать тепловую энергию с высвобождением реакционноспособной анионной группы, которая взаимодействует с активным материалом положительного электрода, улучшая способность к связыванию кислорода в активном материале положительного электрода с выведением ионов лития. Таким образом, удается избежать высвобождения большого количества атомарного кислорода из участков выведения ионов лития. В случае отрицательного электрода избыточный литий, который встроен в отрицательный электрод, будет диффундировать в приемник лития, в результате чего уменьшается концентрация лития в отрицательном электроде. Поэтому он будет представлять собой стабильное состояние для эффективного подавления теплового разгона.
Для реализации вышеупомянутого данное изобретение раскрывает литиевый аккумулятор, содержащий положительный электрод, отрицательный электрод и систему электролита, обеспечивающую ионную проводимость между положительным электродом и отрицательным электродом. Ионы лития могут перемещаться между положительным и отрицательным электродами для осуществления электрохимической реакции для зарядки и разрядки. Источник ионов, неактивный во время электрохимической реакции, добавлен к положительному электроду. Источник ионов содержит реакционноспособную анионную группу и катион, связанный с реакционноспособной анионной группой. Источник ионов способен высвобождать реакционноспособную анионную группы путем поглощения тепловой энергии. Реакционноспособная анионная группа взаимодействует с активным материалом положительного электрода, что уменьшает обратимость данного активного материала положительного электрода. Кроме того, под действием некоторой специфической реакционноспособной анионной группы структура решетки активного материала положительного электрода переходит из состояния с более высокой энергией в состояние с более низкой энергией с выведением ионов лития. Следовательно, положительный электрод, из которого ушли ионы лития, стабилизируется, и предотвращается возникновение явлений теплового разгона.
Дополнительный объем применения согласно данному изобретению будет очевиден из подробного описания ниже. Тем не менее, следует понимать, что подробное описание и конкретные примеры, хотя в них указаны предпочтительные примеры осуществления изобретения, представлены только в иллюстративных целях, так как различные изменения и модификации в рамках сущности и объема данного изобретения будут очевидны специалистам в данной области техники из данного подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Данное изобретение станет более понятным на основании приведенного ниже подробного описания, носящего исключительно иллюстративный, а не ограничивающий данное изобретение характер.
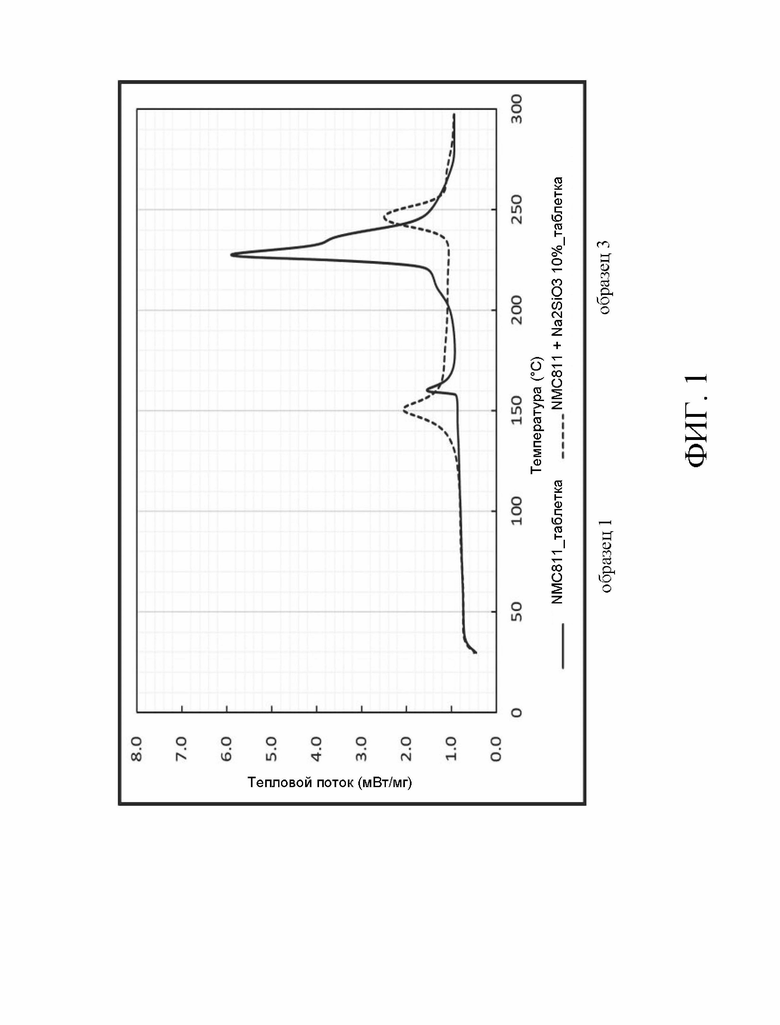
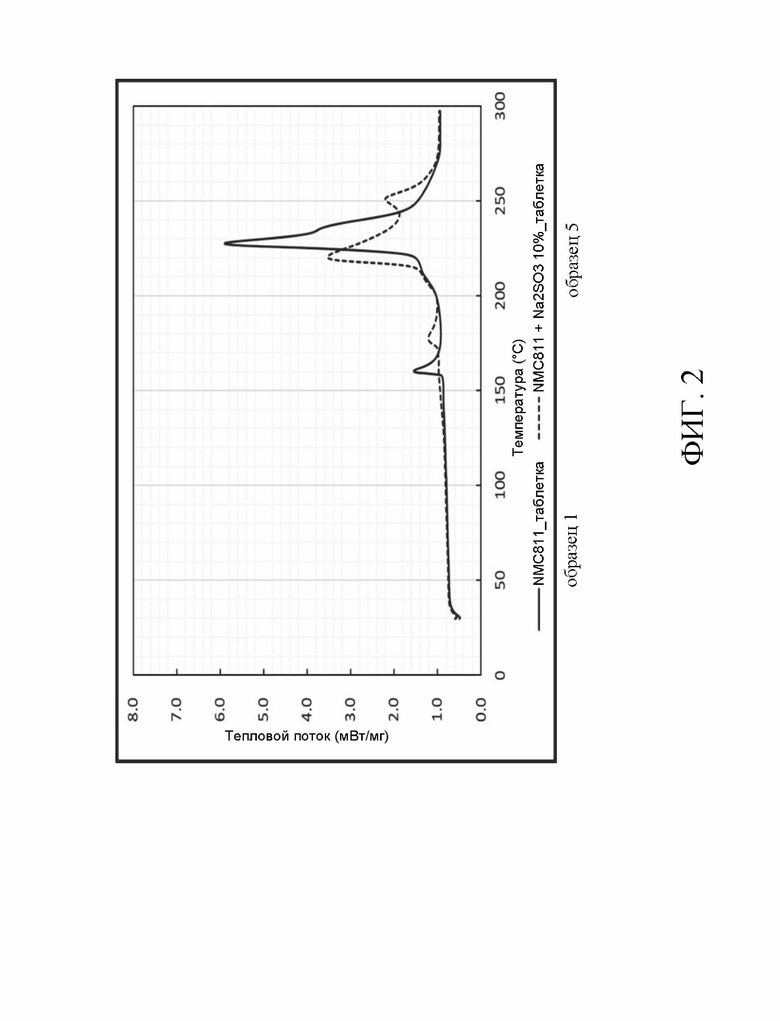
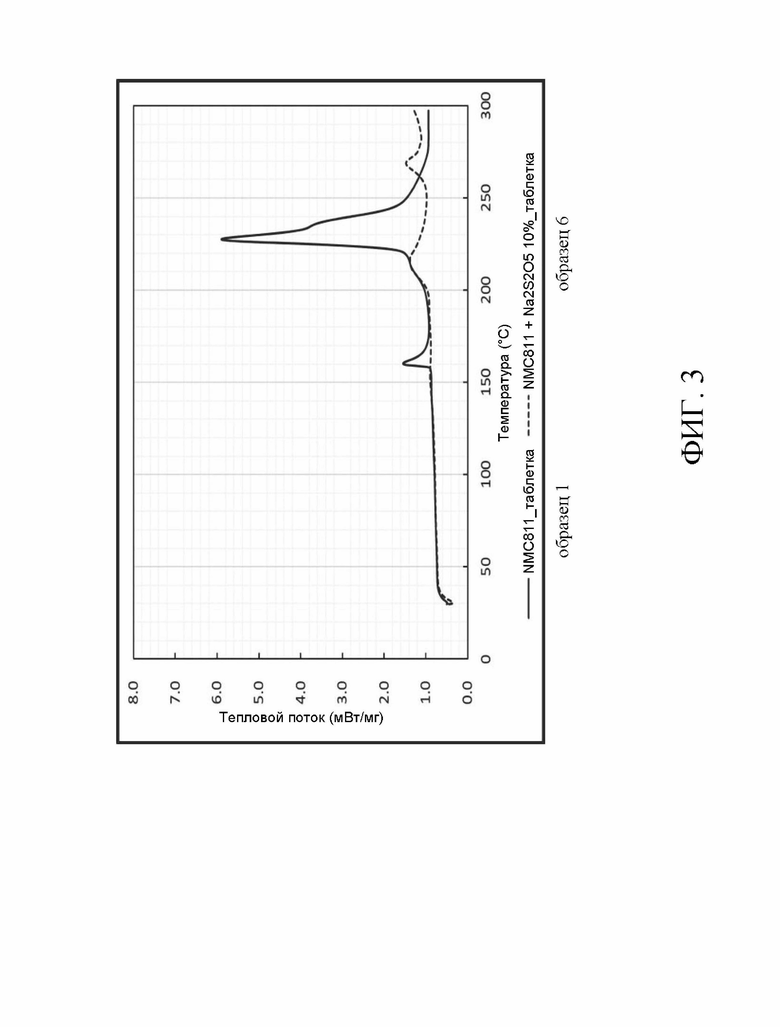
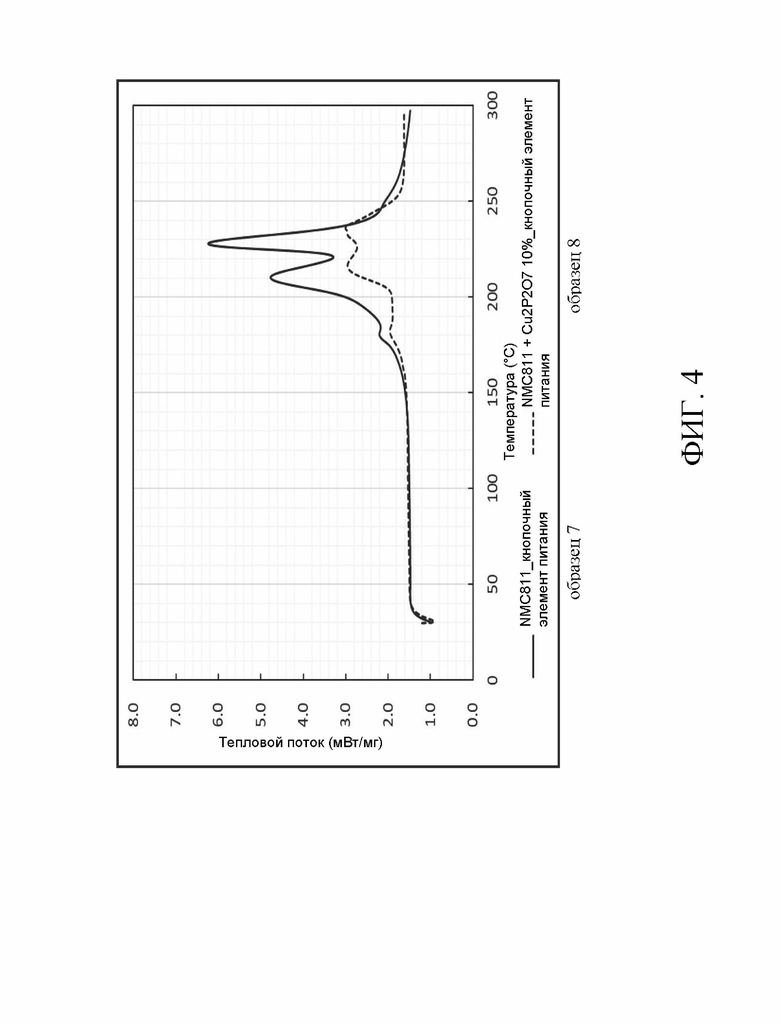
На Фиг. 1-7 представлены термограммы дифференциального сканирующего калориметра с источником ионов или без него в соответствии с данным изобретением.
ПОДРОБНОЕ ОПИСАНИЕ ДАННОГО ИЗОБРЕТЕНИЯ
Данное изобретение раскрыто ниже на конкретных примерах осуществления изобретения и со ссылкой на определенные чертежи, но данное изобретение ограничено не ими, а только формулой изобретения. Любые ссылочные обозначения в формуле изобретения не следует истолковывать как ограничивающие объем изобретения. Раскрытые чертежи носят исключительно схематический характер и не имеют ограничительного характера. В иллюстративных целях размеры некоторых элементов на чертежах могут быть преувеличены и вычерчены не в масштабе.
Используемая в настоящем описании терминология предназначена только для описания конкретных вариантов осуществления изобретения и не носит ограничительного характера для общей концепции настоящего изобретения. Форма единственного числа подразумевает как единственное, так и множественное число существительных, за исключением случаев, если контекстом явно не указано иное. Если не определено иное, все термины (включая технические и научные термины), используемые в настоящем документе, имеют значение, обычно используемое специалистами в области техники, к которой относятся примеры осуществления изобретения. Кроме того, термины, такие как те, которые определены в обычно используемых словарях, должны интерпретироваться как имеющие значение, которое согласуется с их значением в контексте уровня техники, и не будут интерпретироваться в идеализированном или чрезмерно формальном смысле, если это явно не определено в тексте.
Ссылка в данном описании на «один пример осуществления изобретения» или «пример осуществления изобретения» означает, что конкретный признак, структура или характеристика, раскрытые в связи с этим примером осуществления изобретения, содержатся в, по меньшей мере, одном примере осуществления данного изобретения. Таким образом, наличие фраз «в одном примере осуществления изобретения» или «в примере осуществления изобретения» в различных местах данного описания может относиться, но не обязательно относится к одному и тому же примеру осуществления изобретения. Более того, конкретные признаки, структуры или характеристики могут быть объединены каким-либо соответствующим образом в одном или нескольких примерах осуществления изобретения, что очевидно для специалиста в данной области техники из настоящего описания.
Данное изобретение раскрывает литиевый аккумулятор, выполненный с возможностью эффективно подавлять тепловой разгон и содержащий положительный электрод, содержащий активный материал положительного электрода, отрицательный электрод, содержащий активный материал отрицательного электрода, и систему электролита, обеспечивающую ионную проводимость между положительным электродом и отрицательным электродом. Ионы лития могут перемещаться между положительным и отрицательным электродами для осуществления электрохимической реакции зарядки и разрядки. Источник ионов добавлен к положительному электроду. Источник ионов неактивен во время электрохимической реакции, т.е. не участвует в электрохимической реакции. Источник ионов содержит реакционноспособную анионную группу и катион, связанный с реакционноспособной анионной группой. Источник ионов высвобождает реакционноспособную анионную группу после поглощения тепловой энергии. Реакционноспособная анионная группа будет взаимодействовать с активным материалом положительного электрода, что уменьшает обратимость/активность данного активного материала положительного электрода. Кроме того, благодаря некоторой специфичной реакционноспособной анионной группе структура решетки активного материала положительного электрода стабилизируется. Следовательно, активный материал положительного электрода будет переходить из состояния с более высокой энергией в состояние с более низкой энергией с выведением ионов лития, которое подавляет тепловой разгон аккумулятора литиевого перезаряжаемого. Тепловую энергию, поглощенную источником ионов, может обеспечивать литиевый аккумулятор, когда его температура достигает первой температуры. Прочность связи между катионом и реакционноспособной анионной группой можно регулировать путем выбора их материалов специалистами в данной области техники. При первой температуре источник ионов способен получить достаточно кинетической энергии, чтобы разорвать связь между катионом и реакционноспособной анионной группой, так что реакционноспособная анионная группа может свободно перемещаться. Таким образом, согласно данному изобретению источник ионов не диссоциируется в полярном растворе с высвобождением реакционноспособной анионной группы, т.е. источник ионов не способен диссоциироваться в полярном растворе. Реакционноспособная анионная группа приводится в действие тепловой энергией с ионизацией реакционноспособной анионной группы.
Реакционноспособная анионная группа может иметь по меньшей мере связь бор-кислород, связь сера-кислород, связь кремний-кислород, связь алюминий-кислород или связь фосфор-кислород. Источник ионов размещен на положительном электроде литиевого аккумулятора, и источник ионов примыкает к частицам активного материала положительного электрода или непосредственно контактирует с ними. Например, источник ионов смешан с частицами активного материала положительного электрода с формированием случайного распределения между частицами активного материала положительного электрода. В качестве альтернативы источник ионов покрывает поверхность положительного электрода. Система электролита может представлять собой твердый электролит, полутвердый электролит, жидкий электролит или их комбинацию. Источник ионов не растворяется в системе электролита.
Реакционноспособная анионная группа с по меньшей мере связью бор-кислород, связью сера-кислород, связью кремний-кислород, связью алюминий-кислород или связью фосфор-кислород может взаимодействовать с активным материалом положительного электрода, что делает положительный электрод непригодным к эффективному подавлению теплового разгона. Для данного варианта осуществления изобретения реакционноспособная анионная группа выбрана из AlO2-, PO43-, P2O74-, AlSiO4-, B4O72-, SO3-R-, SO2-R-, SiO3-, HPO42-, SO32-, H2PO2-, HPO32-, P2O6-, P3O93-, BO2-, BO3-, P4O136-, SO72-, S2O32-, SO52-, S2O82-, S2O62-, S2O42-, P3O105-, B2O54-, H2PO4-, или S2O52-. R выбран из любой группы заместителей. Например, R выбран из группы заместителей, содержащей водород, алкил, арил, аралкил или алкарил. Реакционноспособная анионная группа может быть симметричной или асимметричной. Асимметричная реакционноспособная анионная группа предпочтительнее симметричной реакционноспособной анионной группы. Так, например, серосодержащий оксид, например SO72- или SO32-, имеет более асимметричную структуру, чем SO42-, а SO72- имеет более асимметричную структуру, чем SO32-. Следовательно, SO72- предпочтительнее SO32-, а SO32- предпочтительнее SO42-. P2O74- фосфора оксида имеет более асимметричную структуру, чем PO43-. P2O74- предпочтительнее PO43-. SO42- имеет симметричную структуру, его практически невозможно отделить от действия. Следовательно, его сложно использовать в качестве реакционноспособной анионной группы данного изобретения. Кроме того, в случае взаимодействия активного материала положительного электрода с реакционноспособной анионной группой выбор катиона может быть более разнообразным, например, можно выбрать ионы металлов с валентностью от +1 до +3, такие как ионы натрия, калия, меди, магния, кальция или железа и т. д. Следовательно, для этого могут быть приспособлены такие соединения, как меди пирофосфат (Cu2P2O7) или железа пирофосфат (Fe4(P2O7)3).
Кроме того, источник ионов может также иметь анионную группу основной цепи с большей молекулярной массой, чем у реакционноспособной анионной группы. Реакционноспособная анионная группа расположена в концевом или боковом положении от анионной группы основного каркаса.
В данном изобретении приемник лития, или так называемая новая литиевая управляющая система, дополнительно размещен в отрицательном электроде литиевого аккумулятора. Приемник лития выполнен с возможностью взаимодействовать с литием с формированием литиевого сплава или соединения лития, но не участвует в электрохимической реакции положительного и отрицательного электродов литиевого аккумулятора во время зарядки и разрядки. Это означает, что приемник лития неактивен во время сплавления лития или введения иона лития в отрицательный электрод. Электрический потенциал, при котором приемник лития взаимодействует с литием, отличается от электрического потенциала, при котором активный материал отрицательного электрода взаимодействует с литием. Например, электрический потенциал, при котором приемник лития взаимодействует с литием с формированием литиевого сплава или соединения лития, выше, чем электрический потенциал, при котором активный материал отрицательного электрода взаимодействует с литием с формированием литиевого сплава или соединения лития. Поэтому приемник лития не участвует в зарядке и разрядке аккумулятора литиевого перезаряжаемого. Приемник лития расположен на отрицательном электроде литиевого аккумулятора, и приемник лития примыкает к активному материалу отрицательного электрода или непосредственно контактирует с ним. Например, приемник лития смешан с частицами активного материала отрицательного электрода с распределением между частицами активного материала отрицательного электрода, либо покрывает поверхность отрицательного электрода.
Во время зарядки литиевого аккумулятора происходит чрезмерное осаждение и диффузия ионов лития к отрицательному электроду. Отрицательный электрод будет демонстрировать материальные характеристики лития на основании характеристик исходного сырья. Этот процесс крайне нестабилен. Тем не менее, атомы лития будут диффундировать от отрицательного электрода к приемнику лития под действием разности концентраций и тепловой энергии литиевого аккумулятора при второй температуре. Концентрация лития на отрицательном электроде снижается, что демонстрирует свойства материала, близкие к свойствам исходного сырья. Поэтому будет иметь место стабильное состояние с более низкой энергией. Вторая температура может быть такой же, как и первая или отличаться от нее. Активный материал отрицательного электрода может представлять собой углерод, кремний или металл литий. Приемник лития может быть неорганическим материалом, таким как Li4Ti5O12, Fe4(P2O7)3, FeS2, Cu2P2O7, TiS2 или их смесь. Например, FeS2 сплавляется с литием при напряжении от 1,5 до 2,5 вольт, а углерод, кремний или металл литий вступают в электрохимическую реакцию с литием при напряжении от 0 до 0,1 вольт. Таким образом, приемник лития неактивен во время легирования лития или введения иона лития в отрицательный электрод.
В качестве альтернативы приемник лития может представлять собой органический полимер, который выдерживает температуру выше 150 градусов С. Органический полимер сплавляется с литием при напряжении от 1,5 до 3,5 вольт. Активный материал отрицательного электрода может быть подвергнуто предварительной обработке, чтобы избежать вышеуказанного рабочего напряжения органического полимера. В случае, если активным материалом отрицательного электрода является углерод или кремний, углерод или кремний литируется, чтобы избежать вышеуказанного рабочего напряжения органического полимера. Кроме того, органический полимер может представлять собой полиимид (ПИ), производные полиимида, такие как полиэфиримид (ПЭИ), полиарилэфиркетон (ПАЭК) или их смесь. Например, ПИ сплавляется с литием при напряжении 2,5 вольт.
Литиевый аккумулятор может содержать источник ионов или приемник ионов. Литиевый аккумулятор по данному изобретению может дополнительно содержать сепаратор, который состоит из электроизоляционного материала с отверстиями для прохождения ионов или ионопроводящего и электроизоляционного материала, такого как твердый электролит. Активный материал отрицательного электрода может представлять собой углеродный материал, материал на основе кремния, смесь обоих материалов или металлический литий. Примеры углеродного материала могут содержать графитированные углеродные материалы и аморфные углеродные материалы, такие как природный графит, модифицированный графит, графитированные мезоуглеродные микрошарики, мягкий углерод (например, кокс) и твердый углерод. Материал на основе кремния содержит кремний, оксид кремния, композиты кремний-углерод и кремниевый сплав. Активный материал положительного электрода может представлять собой оксид лития-кобальта-марганца, в котором массовый процент никеля составляет более 75%, например, NCM811.
Ниже представлены различные эксперименты для проверки действия данного изобретения. Электролит, используемый в данном эксперименте, является безводным электролитом, таким как органический электролит, коллоидный электролит, полимерный электролит или карбонатный растворитель, такой как ЭК (этиленкарбонат), ПК (поликарбонат), дополненный солями, такими как LiPF6, LiBF4, и т.д.
В таблице 1 ниже представлены разности генерируемого кислорода между образцами с источником и без источника ионов. Состав образца 1 содержал 76,61 весовых % NCM811, 3,26 весовых % электропроводящего вещества, 1,63 весовых % клея и 18,5 весовых % электролита. Способ изготовления образца 1 заключался в смешивании 76,61 весовых % NCM811, 3,26 весовых % электропроводящего вещества, 1,63 весовых % клея и 18,5 весовых % электролита и нанесении покрытия на токосъемник положительного электрода, чтобы сформировать слой активного материала положительного электрода. Затем на поверхность активного материала положительного электрода последовательно уложили сепаратор, слой активного материала отрицательного электрода и токосъемник отрицательного электрода. Уплотнительную рамку, помещенную между токосъемником положительного электрода и токосъемником отрицательного электрода, использовали для герметизации слоя активного материала положительного электрода, сепаратора и слоя активного материала отрицательного электрода между токосъемником положительного электрода, уплотнительной рамкой и токосъемником отрицательного электрода для формирования слоистого аккумуляторного листа. Слоистый электрохимический элемент формировали при 100% SOC (уровень заряда). Затем сформированный слой активного материала положительного электрода соскоблили и прессовали под давлением 0,9 Н в течение 1 минуты для формирования листа с получением образца 1. Способ изготовления образца 2 заключался в смешивании 76,61 весовых % NCM811, 3,26 весовых % электропроводящего вещества, 1,63 весовых % клея и 18,5 весовых % электролита по массе и нанесении покрытия на токосъемник положительного электрода, чтобы сформировать слой активного материала положительного электрода. Затем на поверхность активного материала положительного электрода последовательно уложили сепаратор, слой активного материала отрицательного электрода и токосъемник отрицательного электрода. Уплотнительную рамку, помещенную между токосъемником положительного электрода и токосъемником отрицательного электрода, использовали для герметизации слоя активного материала положительного электрода, сепаратора и слоя активного материала отрицательного электрода между токосъемником положительного электрода, уплотнительной рамкой и токосъемником отрицательного электрода для формирования слоистого аккумуляторного листа. Слоистый элемент аккумулятора формировали при 100% SOC (уровень заряда). Затем сформированный слой активного материала положительного электрода соскоблили для смешивания и измельчения с Na2B4O7 с такой же массой. Смесь прессовали под давлением 0,9 Н в течение 1 минуты, чтобы сформировать лист, с получением образца 2. В образце 2 источником ионов является Na2B4O7. Образцы 3-6 получали таким же образом, как описано для образца 2, за исключением того, что источник ионов, т.е. Na2B4O7, заменили на Na2SiO3, NaAlSiO4, Na2SO3 и Na2S2O5. Анализ образцов 1-6 проводили методом ГХ-МС (газовая хроматография-масс-спектрометрия) соответственно. В этом анализе образцы 1-6 помещали в специальные флаконы для ГХ-МС анализа. В перчаточной камере кислород во флаконах с образцами заменяли аргоном. Затем бутылки с образцами закрывали парафильмом для обеспечения герметичности. При анализе методом ГХ-МС температура экстракции паровой фазы составляла 200°C, а время экстракции составляло 20 минут. Затем образец 1 мл нагревали от 40°C до 250°C. Как следует из таблицы 1, после вышеупомянутого анализа ГХ-МС количество генерируемого кислорода в образцах с источником ионов могло быть значительно снижено.
Рассмотрим Фиг. 1-3, которые представляют собой термограммы дифференциального сканирующего калориметра для образцов 3, 5 или 6 в сравнении с образцом 1. Соответствующее количество этих образцов было отобрано лопаткой. Затем их поместили на специальный лоток для образцов дифференциальной сканирующей калориметрии (ДСК) и запечатали лоток для образцов. Испытание ДСК проводили на образцах при повышении температуры от 30°C дo 300°C со скоростью 5°C/мин. Из чертежей видно, что в образцах с источником ионов можно сдвинуть в обратном направлении температуру начала экзотермической реакции. Поэтому литиевый аккумулятор способен выдерживать более высокую температуру.
В таблице 2 ниже представлены разности генерируемого кислорода между образцами с приемником лития и без него.
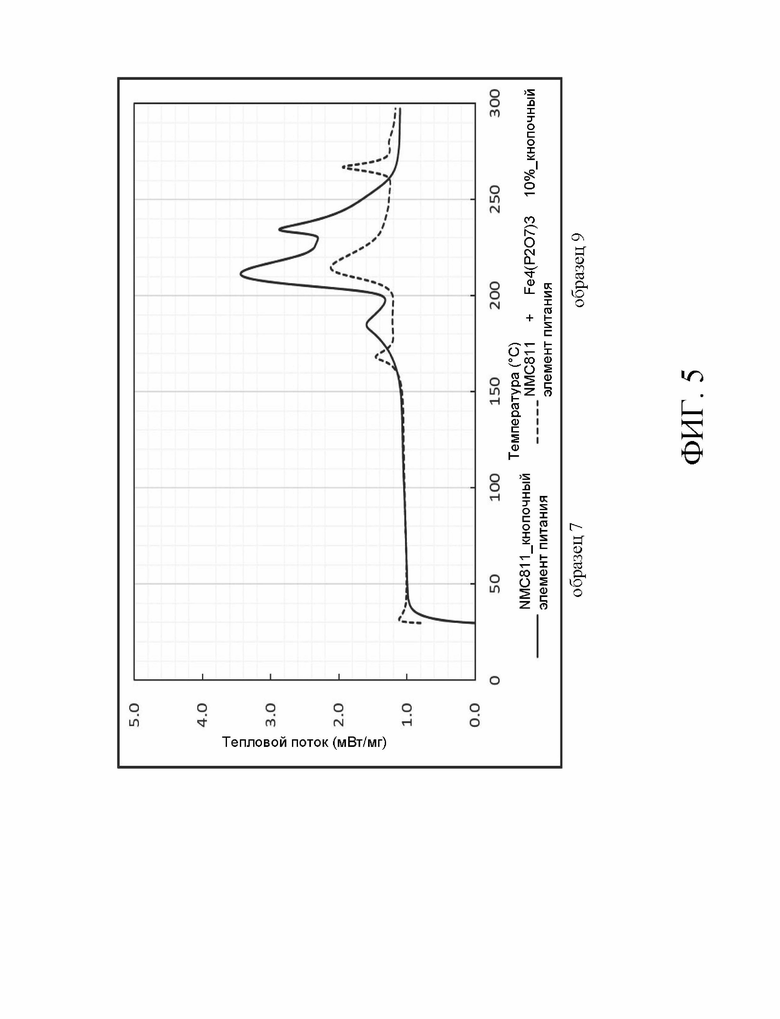
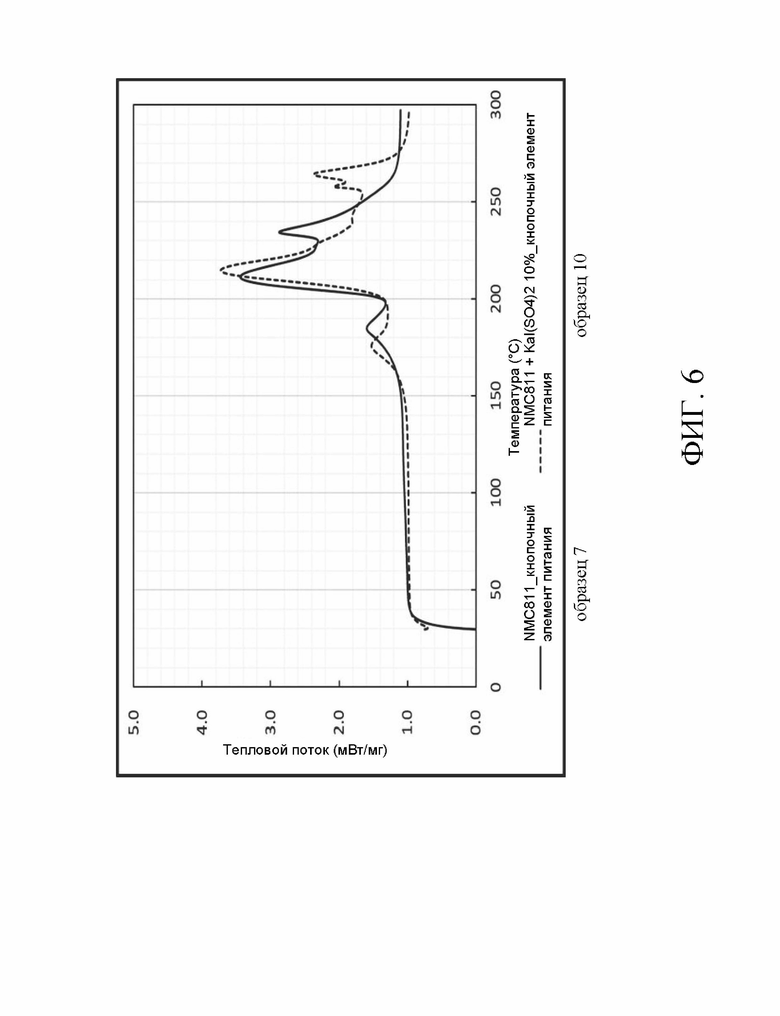
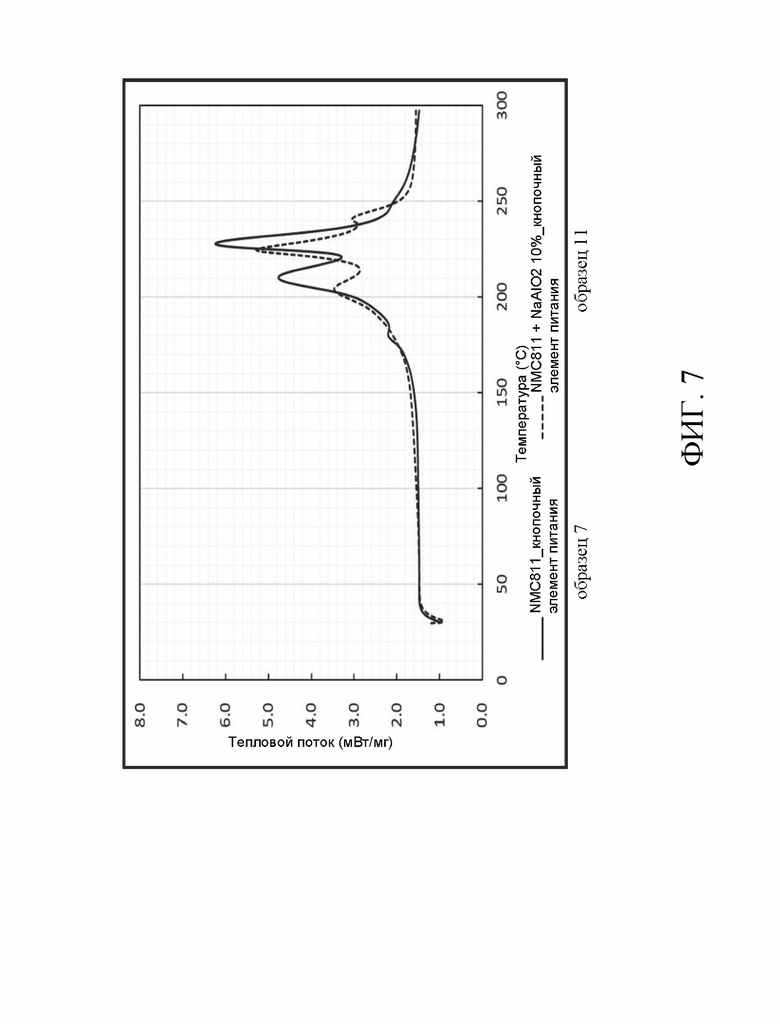
Состав образца 7 содержал 76,61 весовых % NCM811, 3,26 весовых % электропроводящего вещества, 1,63 весовых % клея и 18,5 весовых % электролита по весу. Способ изготовления образца 7 заключался в смешивании NCM811, электропроводящего вещества, клея и электролита, чтобы сформировать электродную пленку. Электродную пленку использовали в качестве положительного электрода кнопочного элемента питания. Кнопочный элемент питания сформировали при 100% SOC (уровень заряда). Затем электродную пленку отобрали непосредственно как образец 7. Состав образца 8 содержал 66,61 весовых % NCM811, 3,26 весовых % электропроводящего вещества, 1,63 весовых % клея и 18,5 весовых % электролита и 10% Cu2P2O7 по массе. Способ изготовления образца 8 заключается в смешивании 66,61% NCM811, 3,26% электропроводящего вещества, 1,63 весовых % клея, 18,5 весовых % электролита и 10 весовых % Cu2P2O7, чтобы сформировать электродную пленку. Электродную пленку использовали в качестве положительного электрода кнопочного элемента питания. Кнопочный элемент питания сформировали при 100% SOC (уровень заряда). Затем электродную пленку отобрали непосредственно как образец 8. В образце 8 источником ионов является Cu2P2O7. Образцы 9-11 получали таким же образом, как описано для образца 8, за исключением замены источника ионов, т.е. Cu2P2O7. В образце 9 источником ионов является Fe4(P2O7)3. В образце 10 источником ионов является KAl(SO4)2. В образце 11 источником ионов является NaAlO2. Анализ данных образцов проводили методом ГХ-МС (газовая хроматография-масс-спектрометрия), соответственно. В этом анализе образцы помещали в специальные флаконы для анализа методом ГХ-МС. В перчаточной камере кислород во флаконах с образцами заменяют аргоном. Затем бутылки с образцами закрыли парафильмом для обеспечения герметичности. При анализе методом ГХ-МС температура экстракции паровой фазы составляла 200°C, а время экстракции составляло 20 минут. Затем образец 1 мл нагрели от 40°C до 250°C. Как следует из таблицы 2, после вышеупомянутого анализа ГХ-МС количество генерируемого кислорода в образцах с источником ионов может быть значительно снижено по сравнению с образцом 7.
Рассмотрим Фиг. 4-7, которые представляют собой термограммы дифференциального сканирующего калориметра образцов 8, 9, 10 или 11 в сравнении с образцом 7. Соответствующее количество этих образцов отобрали лопаткой. Затем их поместили на специальный лоток для образцов дифференциальной сканирующей калориметрии (ДСК) и запечатали лоток для образцов. Испытание ДСК проводили на образцах при повышении температуры от 30°C дo 300°C со скоростью 5°C/мин. Из чертежей видно, что для образцов с источником ионов можно сдвинуть в обратном направлении температуру начала экзотермической реакции. Поэтому литиевый аккумулятор способен выдерживать более высокую температуру.
В таблице 3 ниже представлены разности генерируемого газа между образцами с приемником лития и без него. Состав образца 12 включал 62,153 весовых % C/SiO, 2,049 весовых % электропроводящего вещества, 4,098 весовых % клея и 31,7 весовых % электролита. Способ изготовления образца 12 заключался в смешивании 62,153 весовых % C/SiO, 2.049 весовых % электропроводящего вещества, 4,098 весовых % клея и 31,7 весовых % электролита и в нанесении покрытия на токоприемник отрицательного электрода, чтобы сформировать слой активного материала отрицательного электрода. Затем на поверхность активного материала отрицательного электрода последовательно уложили сепаратор, слой активного материала положительного электрода и токосъемник отрицательного электрода. Уплотнительную рамку, помещенную между токосъемником положительного электрода и токосъемником отрицательного электрода, использовали для герметизации слоя активного материала положительного электрода, сепаратора и слоя активного материала отрицательного электрода между токосъемником положительного электрода, уплотнительной рамкой и токосъемником отрицательного электрода для формирования слоистого аккумуляторного листа. Слоистый элемент аккумулятора формировали при 100% SOC (уровень заряда). Затем сформированный слой активного материала отрицательного электрода соскоблили и прессовали под давлением 0,9 Н в течение 1 минуты для формирования листа с получением образца 12. Состав образца 13 содержал 31,0765 весовых % C/SiO, 1,0245 весовых % электропроводящего вещества, 2,049 весовых % клея и 15,85 весовых % электролита и 50 весовых % CaHPO4. Способ изготовления образца 13 заключался в смешивании 62,153 весовых % C/SiO, 2,049 весовых % электропроводящего вещества, 4,098 весовых % клея и 31,7 весовых % электролита и нанесении покрытия на токосъемник отрицательного электрода, чтобы сформировать слой активного материала отрицательного электрода. Затем на поверхность активного материала отрицательного электрода последовательно уложили сепаратор, слой активного материала положительного электрода и токосъемник отрицательного электрода. Уплотнительную рамку, помещенную между токосъемником положительного электрода и токосъемником отрицательного электрода, использовали для герметизации слоя активного материала положительного электрода, сепаратора и слоя активного материала отрицательного электрода между токосъемником положительного электрода, уплотнительной рамкой и токосъемником отрицательного электрода для формирования слоистого аккумуляторного листа. Слоистый элемент аккумулятора формировали при 100% SOC (уровень заряда). Затем сформированный слой активного материала отрицательного электрода соскоблили для смешивания и измельчения с CaHPO4 с такой же массой. Смесь прессовали под давлением 0,9 Н в течение 1 минуты, чтобы сформировать лист с получением образца 13.
Способ изготовления образца 14 практически не отличался от способа изготовления образца 13. Только CaHPO4 заменили на Cu2P2O7. ГХ-МС использовали для анализа кислорода, монооксида углерода и газообразных алканов, а ГХ-ТПД - для анализа водорода. При анализе температура экстракции паровой фазы составляла 200°C, а время экстракции - 20 минут. Затем образец 1 мл нагрели от 40°C до 250°C. Как следует из таблицы 3, из вышеописанного анализа следует, что количество генерируемого кислорода у образца 13 без источника ионов увеличилось по сравнению с образцом 12, а количество генерируемого кислорода у образца 14 с источником ионов уменьшилось по сравнению с образцом 12.
В таблице 4 ниже представлены различия в количествах генерируемого газа между образцами с приемником лития и без него. Состав образца 15 содержит 62,153 весовых % C/SiO, 2,049 весовых % электропроводящего вещества, 4,098 весовых % клея и 31,7 весовых % электролита. Способ изготовления образца 15 заключался в смешивании 62,153 весовых % C/SiO, 2,049 весовых % электропроводящего вещества, 4,098 весовых % клея и 31,7 весовых % электролита, чтобы сформировать электродную пленку. Электродную пленку использовали в качестве положительного электрода кнопочного элемента питания. Кнопочный элемент питания формировали при 100% SOC (уровень заряда). Затем электродную пленку отобрали непосредственно как образец 15. Состав образца 16 содержит 52,153 весовых % C/SiO, 2,049 весовых % электропроводящего вещества, 4,098 весовых % клея и 31,7 весовых % электролита и 10 весовых % Cu2P2O7. Способ изготовления образца 16 заключался в смешивании всех вышеупомянутых веществ для формирования электродной пленки. Электродную пленку использовали в качестве положительного электрода кнопочного элемента питания. Кнопочный элемент питания формировали при 100% SOC (уровень заряда). Затем электродную пленку отобрали непосредственно как образец 16. Способ изготовления образца 17 практически не отличался от способа изготовления образца 16. Только Cu2P2O7 заменен на Fe4(P2O7)3. Образцы 15-17 анализировали с помощью ГХ-МС/ГХ-ТПД (газовая хроматография - теплопроводный детектор) соответственно. В этом анализе образцы 15-17 помещали в специальные флаконы для анализа ГХ-МС/ГХ-ТПД. В перчаточной камере кислород во флаконах с образцами заменили аргоном. Затем бутылки с образцами закрыли парафильмом для обеспечения герметичности. ГХ-МС использовали для анализа кислорода, монооксида углерода и газообразных алканов, а ГХ-ТПД - для анализа водорода. При анализе температура экстракции паровой фазы составляла 200°C, а время экстракции - 20 минут. Затем образец 1 мл нагрели от 40°C до 250°C. Как следует из таблицы 4, количество генерируемого газа для образцов 16-17 с источником ионов может быть значительно ниже по сравнению с образцом 15.
Соответственно, данное изобретение предлагает литиевый аккумулятор, имеющий возможность подавлять тепловой разгон. К положительному электроду добавлен источник ионов или к отрицательному электроду добавлен литиевый приемник. Источник ионов способен поглощать тепловую энергию, вызванную повышением температуры литиевого аккумулятора, с высвобождением реакционноспособной анионной группы. Реакционноспособная анионная группа взаимодействует с активным материалом положительного электрода, что уменьшает обратимость/активность данного активного материала положительного электрода. Кроме того, под действием некоторой специфической реакционноспособной анионной группы структура решетки активного материала положительного электрода будет переходить из состояния с более высокой энергией в состояние с более низкой энергией с выведением ионов лития. Следовательно, положительный электрод, из которого ушли ионы лития, стабилизируется. Для отрицательного электрода приемник лития используется для приема избыточного лития, чтобы продемонстрировать свойства материала, близкие к свойствам исходного сырья отрицательного электрода. Поэтому он будет представлять собой стабильное состояние для эффективного подавления теплового разгона.
Данное изобретение, раскрытое таким образом, может быть изменено различными способами. Такие изменения не должны считаться отступлением от сущности и объема данного изобретения, и все подобные модификации, очевидные специалисту в данной области техники, входят в объем приведенной ниже формулы изобретения.
Изобретение относится к области электротехники, а именно к литий-ионному аккумулятору с безводным электролитом, содержащему источник ионов, добавленный к положительному электроду, и может быть использовано для подавления теплового разгона аккумулятора во время его эксплуатации. Повышение надежности работы литиевого аккумулятора является техническим результатом изобретения, который достигается за счет того, что к положительному электроду добавлен источник ионов, неактивный во время электрохимической реакции, при этом источник ионов содержит реакционноспособную анионную группу и катион, связанный с реакционноспособной анионной группой, причем источник ионов способен высвобождать реакционноспособную анионную группу путем поглощения тепловой энергии для взаимодействия с активным материалом положительного электрода, при этом реакционноспособная анионная группа имеет по меньшей мере одну связь, выбранную из связи бор-кислород, связи сера-кислород, связи кремний-кислород, связи алюминий-кислород и связи фосфор-кислород. Источник ионов не участвует в электрохимической реакции литиевого аккумулятора во время зарядки и разрядки и способен поглощать тепловую энергию, вызванную повышением температуры литиевого аккумулятора, что эффективно подавляет тепловой разгон литиевого аккумулятора. 10 з.п. ф-лы, 7 ил., 4 табл.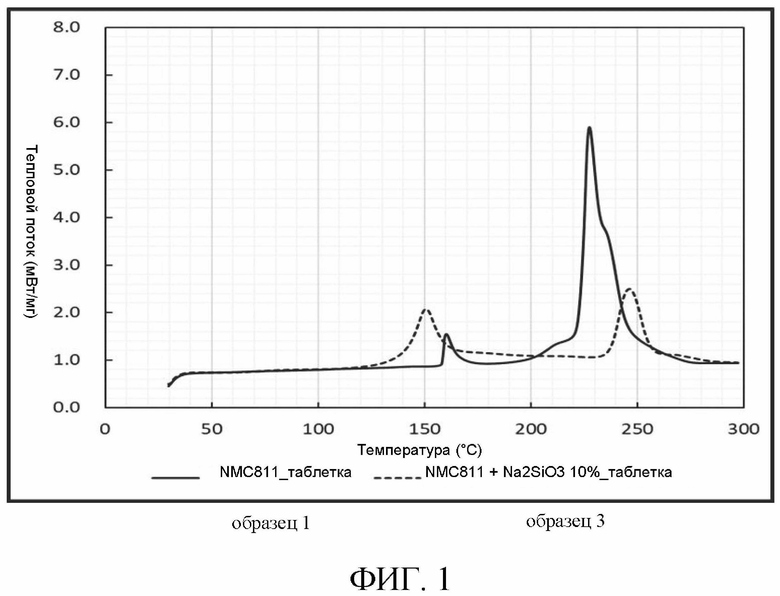
1. Литиевый аккумулятор, способный подавлять тепловой разгон, содержащий: положительный электрод, содержащий активный материал положительного электрода; отрицательный электрод, содержащий активный материал отрицательного электрода; систему безводного электролита, обеспечивающую ионную проводимость между положительным электродом и отрицательным электродом, чтобы позволить ионам лития перемещаться между положительным электродом и отрицательным электродом для осуществления электрохимической реакции для зарядки и разрядки; и
источник ионов, добавленный к положительному электроду, но не участвующий в электрохимической реакции для зарядки и разрядки, при этом источник ионов состоит из реакционноспособной анионной группы и катиона, связанного с реакционноспособной анионной группой, при этом реакционноспособная анионная группа представляет собой AlO2-, РО43-, Р2О74-, AlSiO4-, В4О72-, SO3-R-, SO2-R-, SiO3-, НРО42-, SO32-, Н2РО2-, НРО32-, P2O6-, Р3О93-, BO2-, ВО3-, Р4О136-, SO72-, S2O32-, SO52-, S2O82-, S2O62-, S2O42-, Р3О105-, B2O54-, Н2РО4- или S2O52-, при этом R выбран из группы заместителей, состоящей из водорода, алкила, арила, аралкила и алкарила, при этом
катион представляет собой натрий, калий, медь, магний, кальций или железо и имеет валентность в диапазоне от +1 до +3, при условии, что источник ионов не является фосфатом железа,
причем источник ионов способен поглощать тепловую энергию с высвобождением реакционноспособной анионной группы для взаимодействия с активным материалом положительного электрода.
2. Литиевый аккумулятор по п. 1, в котором активный материал положительного электрода представляет собой оксид лития-кобальта-марганца, в котором процентная доля никеля превышает 75 весовых %.
3. Литиевый аккумулятор по п. 1, в котором реакционноспособная анионная группа является асимметричной.
4. Литиевый аккумулятор по п. 3, в котором реакционноспособная анионная группа представляет собой SO72- или SO32-.
5. Литиевый аккумулятор по п. 3, в котором реакционноспособная анионная группа представляет собой SO72-.
6. Литиевый аккумулятор п. 3, в котором реакционноспособная анионная группа представляет собой Р2О74-.
7. Литиевый аккумулятор по п. 1, в котором источник ионов имеет анионную группу основной цепи с большей молекулярной массой, чем у реакционноспособной анионной группы, и реакционноспособная анионная группа расположена в концевом или боковом положении от анионной группы основной решетки.
8. Литиевый аккумулятор по п. 1, в котором источник ионов распределен между частицами активного материала положительного электрода или покрывает поверхность положительного электрода.
9. Литиевый аккумулятор по п. 1, дополнительно содержащий приемник лития, распределенный между частицами активного материала отрицательного электрода или покрывающий поверхность отрицательного электрода, при этом приемник лития выполнен с возможностью взаимодействовать с литием с формированием литиевого сплава или соединения лития, но не участвует в электрохимической реакции для зарядки и разрядки; при этом электрический потенциал, при котором приемник лития взаимодействует с литием с формированием литиевого сплава или соединения лития, выше, чем электрический потенциал, при котором активный материал отрицательного электрода взаимодействует с литием с формированием литиевого сплава или соединения лития, при этом
приемник лития представляет собой неорганический материал или органический полимер, при этом неорганический материал содержит Li4Ti5O12, Fe4(P2O7)3, FeS2, Cu2P2O7, TiS2 или их смесь; при этом
органический полимер содержит полиимид (ПИ), производные полиимида, такие как полиэфиримид (ПЭИ) полиарилэфиркетон (ПАЭК), или их смесь.
10. Литиевый аккумулятор по п. 1, в котором источник ионов не диссоциирует в полярном растворе.
11. Литиевый аккумулятор по п. 1, в котором активный материал отрицательного электрода представляет собой углерод, кремний или металл литий.
| US 20160013518 A1, 14.01.2016 | |||
| US 20120244439 A1, 27.09.2012 | |||
| CN 113471424 A, 01.10.2021 | |||
| CN 113140782 A, 20.07.2021 | |||
| CN 113707935 A, 26.11.2021 | |||
| CN 108123175 A, 05.06.2018 | |||
| US 20160204418 A1, 14.07.2016 | |||
| Электрод с защитным подслоем для предотвращения разрушения при возгорании литий-ионных аккумуляторов | 2019 |
|
RU2726938C1 |
Авторы
Даты
2023-12-28—Публикация
2022-12-28—Подача