Область изобретения
Согласно настоящему изобретению предложены соединения, которые представляют собой селективные аллостерические ингибиторы TMLR-, TMLRCS-, LR-, LRCS-содержащих мутантов EGFR, их получение, фармацевтические композиции, содержащие их, и их применение в качестве терапевтически активных веществ.
Предшествующий уровень техники
Рецепторные тирозинкиназы HER-семейства являются медиаторами клеточного роста, дифференцировки и выживаемости. Данное семейство рецепторов включает в себя четыре отдельных члена, т.е. рецептор эпидермального фактора роста (EGFR, ErbB1 или HER1), HER2 (ErbB2), HER3 (ErbB3) и HER4 (ErbB4). После связывания с лигандом рецепторы образуют гомо- и гетеродимеры, и последующая активация собственной тирозинкиназной активности приводит к аутофосфорилированию рецепторов и активации нижестоящих сигнальных молекул (Yarden и др.1). Нарушение регуляции EGFR в результате сверхэкспрессии или мутации вовлечено во многие типы рака человека, включая колоректальный рак, рак поджелудочной железы, глиомы, рак головы и шеи и рак легкого, в частности, немелкоклеточный рак легкого (NSCLC), и за многие годы разработаны различные EGFR-направленные агенты (Ciardiello и др.2). Эрлотиниб (Tarceva®), обратимый ингибитор тирозинкиназы EGFR, был одобрен к применению для лечения рецидивирующего NSCLC во многих странах.
В подгруппе пациентов с NSCLC, чьи опухоли несут соматические мутации в киназном домене, наблюдается впечатляющая активность ингибиторов тирозинкиназы EGFR при использовании их в качестве единственных агентов, тогда как клиническая польза в случае пациентов с EGFR дикого типа значительно снижена (Paez и др.3). Самыми распространенными соматическими мутациями EGFR являются делеции в экзоне 19, при этом самой распространенной мутацией является дельта 746-750, и замены аминокислот в экзоне 21 с наиболее часто встречающейся мутацией L858R (Sharma и др.4).
Невосприимчивость к лечению часто возникает вследствие вторичной мутации Т790М в АТФ-связывающем сайте рецептора. Некоторые разработанные мутант-селективные необратимые ингибиторы являются высокоактивными в отношении мутанта с Т790М, но их эффективность может быть снижена в результате приобретения мутации C797S, то есть замены остатка цистеина, с которым они образуют ключевую ковалентную связь (Thress и др.5). Wang также сообщил, что мутация C797S является основной причиной устойчивости к ингибиторам, нацеленным на EGFR с мутацией Т790М (Wang и др.6). Дополнительные мутации, которые вызывают устойчивость к осимертинибу, описаны Yang, например, L718Q (Yang и др.7).
Поскольку большинство доступных ингибиторов тирозинкиназы EGFR нацелены на АТФ-связывающий сайт киназы, существует потребность в новых терапевтических агентах, которые действуют по-другому, например, путем направленного действия на лекарственно устойчивые мутанты EGFR. Рецептор дикого типа, однако, остается незатронутым.
Недавние исследования подтверждают, что изучение целенаправленного воздействия на аллостерические сайты может привести к разработке мутант-селективных ингибиторов (Jia и др.8).
Имеется обоснованная необходимость в разработке селективных молекул, которые специфично ингибируют TMLR-, TMLRCS-, LR-, LRCS-содержащие мутанты EGFR, полезных для терапевтического и/или профилактического лечения рака, в частности, Т790М- и C797S-содержащих мутантов EGFR.
В WO 20091583699 описываются некоторые гетероциклические антибактериальные агенты. В WO 201618353410 описываются некоторые гетероциклические соединения, подходящие в качестве ингибиторов EBNA1 (ядерный антиген 1 вируса Эпштейна-Барр). В WO 2011128279 описываются некоторые гетероциклические соединения, подходящие в качестве модуляторов LR 772 (Я-120): метаботропного глутаматного рецептора, подтипа 5 (mGluR5).
Краткое описание сущности изобретения
Согласно настоящему изобретению предложен изоиндолин-ацетилен формулы I или его фармацевтически приемлемая соль,
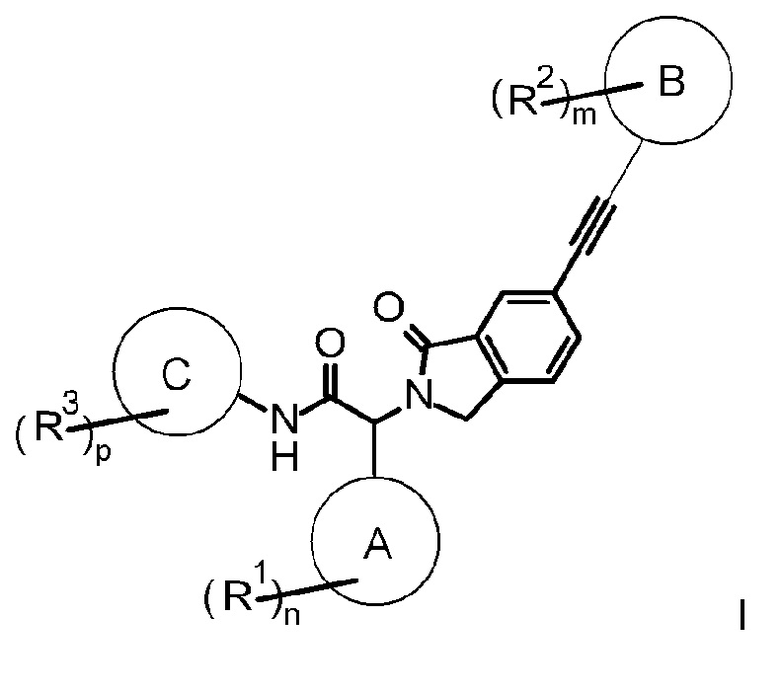
где заместители и переменные являются такими, как описано ниже и в формуле изобретения, или его фармацевтически приемлемая соль.
Соединения по настоящему изобретению полезны для терапевтического и/или профилактического лечения рака.
Подробное описание изобретения
Согласно настоящему изобретению предложены соединения формулы I и их фармацевтически приемлемые соли, получение вышеупомянутых соединений, лекарственные средства, содержащие их, и их приготовление, а также применение вышеупомянутых соединений для терапевтического и/или профилактического лечения рака, в частности, немелкоклеточного рака легкого.
Следующие далее определения общих терминов, использованных в описании настоящего изобретения, применяются независимо от того, встречаются ли рассматриваемые термины по отдельности или в комбинации с другими группами.
Если не указано иное, приведенные ниже термины, использованные в этой заявке, включая описание и формулу изобретения, имеют указанные ниже определения. Необходимо отметить, что, как использовано в описании и прилагаемой формуле изобретения, формы единственного числа включают объекты в форме множественного числа, если контекст ясно не предусматривает иное.
Термин "С1-6-алкил", по отдельности или в комбинации с другими группами, означает углеводородный радикал, который может быть линейным или разветвленным, с одним или несколькими ветвлениями, при этом алкильная группа обычно содержит 1-6 атомов углерода, например, метил (Me), этил (Et), пропил, изопропил (i-пропил), н-бутил, изобутил (i-бутил), 2-бутил (втор-бутил), трет-бутил (t-бутил), изопентил, 2-этил-пропил (2-метил-пропил), 1,2-диметил-пропил и тому подобное. Конкретной группой является метил.
Термин "галоген-С1-6-алкил", по отдельности или в комбинации с другими группами, относится к C1-6-алкилу, определенному в данном описании, который замещен одним или несколькими атомами галогена, в частности 1-5 атомами галогена, более конкретно 1-3 атомами галогена. В частности, галогеном является фтор. В частности, "галоген-С1-6-алкилом" является фтор-С1-6-алкил и, в частности, "галоген-С1-3-алкилом" является фтор-С1-3-алкил. Примерами являются трифторметил, дифторметил, фторметил и тому подобное.
Термин "циано", по отдельности или в комбинации с другими группами, относится к N≡C-(NC-).
Термин "амино", по отдельности или в комбинации с другими группами, относится к NH2.
Термин "гидрокси", по отдельности или в комбинации с другими группами, относится к ОН.
Термин "галоген", по отдельности или в комбинации с другими группами, означает атом хлора (Cl), иода (I), фтора (F) и брома (Br). Конкретной группой является F.
Термин "гетероарил", по отдельности или в комбинации с другими группами, относится к ароматической карбоциклической группе, имеющей одиночное 4-8-членное кольцо, в частности, 5-8-членное, или несколько конденсированных колец, содержащих 6-14, в частности, 6-10 атомов в кольце, и содержащей 1, 2 или 3 гетероатома, по отдельности выбранных из N, О и S, в частности, 1 атом N или 2 атома N, при этом в данной группе по меньшей мере одно гетероциклическое кольцо является ароматическим. Термин "5-членный гетероарил" относится к одиночному 5-членному ароматическому кольцу, содержащему 1 или 2 гетероатома, выбранных из N, О и S, в частности, один атом N и один атом S, например тиазолилу. Конкретной группой является тиазол-2-ил. Термин "6-членный гетероарил" относится к одиночному 6-членному ароматическому кольцу, содержащему 1 или 2 гетероатома, выбранных из N, О и S, в частности, один атом N, например, пиридинилу. Конкретной группой является 2-пиридил. Примеры "гетероарила" включают бензофурил, бензоимидазолил, 1Н-бензоимидазолил, бензооксазинил, бензоксазолил, бензотиазинил, бензотиазолил, бензотиенил, бензотриазолил, фурил, имидазолил, индазолил, 1Н-индазолил, индолил, изохинолинил, изотиазолил, изоксазолил, оксазолил, пиразинил, пиразолил (пиразил), 1Н-пиразолил, пиразоло[1,5-а]пиридинил, пиридазинил, пиридинил, пиримидинил, пирролил, хинолинил, тетразолил, тиазолил, тиенил, триазолил, 6,7-дигидро-5Н-[1]пириндинил и тому подобное. Конкретными группами являются пиридинил и тиазолил.
Термин "C1-6-алкокси", по отдельности или в комбинации с другими группами, означает -O-C1-6-алкильный радикал, который может быть линейным или разветвленным, с одним или несколькими ветвлениями, при этом алкильная группа обычно содержит 1-6 атомов углерода, например, метокси (ОМе, МеО), этокси (OEt), пропокси, изопропокси (i-пропокси), н-бутокси, изобутокси (i-бутокси), 2-бутокси (втор-бутокси), трет-бутокси (t-бутокси), изопентилокси (i-пентилокси) и тому подобное. В частности, группами "C1-6-алкокси" являются группы с 1-4 атомами углерода. Конкретной группой является метокси.
Термин "галоген-С1-6-алкокси", по отдельности или в комбинации с другими группами, относится к группе C1-6-алкокси, определенной в данном описании, которая замещена одним или несколькими атомами галогена, в частности, 1-5 атомами галогена, более конкретно 1-3 атомами галогена. В частности, галогеном является фтор. В частности, группой "галоген-С1-6-алкокси" является фтор-С1-6-алкокси, и, в частности, группой "галоген-С1-3-алкокси" является фтор-С1-3-алкокси. Конкретной группой является -O-CF3.
Термин "N-содержащий гетероциклил" или "гетероциклил" относится к одновалентной насыщенной или частично ненасыщенной моно- или бициклической кольцевой системе из 4-9 атомов в кольце, содержащей в кольце 1, 2 или 3 гетероатома, которые представляют собой атомы N, причем остальные атомы в кольце представляют собой атом углерода. Термин "бициклический" означает "состоящий из двух циклов", имеющих два общих атома в кольце, т.е. мостик между этими двумя кольцами представляет собой либо одинарную связь, либо цепочку из одного или двух атомов в кольце. Примерами являются пирролидинил, пиперидинил и пиперазинил.
Термин "арил" означает одновалентную ароматическую карбоциклическую моно- или бициклическую кольцевую систему, содержащую 6-10 атомов углерода в кольце. Примеры арильных группировок включают фенил и нафтил. Конкретным "арилом" является фенил.
Термин "фармацевтически приемлемый" означает характерную особенность вещества, используемого при изготовлении фармацевтической композиции, то есть, что оно, как правило, является безопасным, нетоксичным и не является нежелательным ни в биологическом, ни в каком-либо ином отношении, и является приемлемым для использования в производстве фармацевтических продуктов для ветеринарии, а также для людей.
Термин "фармацевтически приемлемая соль" относится к соли, которая подходит для применения в контакте с тканями людей и животных. Примерами подходящих солей с неорганическими и органическими кислотами являются, но не ограничиваются этим, соли с такими кислотами, как уксусная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, соляная кислота, молочная кислота, малеиновая кислота, яблочная кислота, метансульфоновая кислота, азотная кислота, фосфорная кислота, п-толуолсульфоновая кислота, янтарная кислота, серная кислота, винная кислота, трифторуксусная кислота и тому подобное. В частности, кислотами являются муравьиная кислота, трифторуксусная кислота и соляная кислота. Конкретными кислотами являются соляная кислота, трифторуксусная кислота и фумаровая кислота.
Термин "фармацевтически приемлемое вспомогательное вещество" относится к таким носителям и вспомогательным веществам, как разбавители или эксципиенты, которые совместимы с другими ингредиентами композиции.
Термин "фармацевтическая композиция" охватывает продукт, содержащий конкретно указанные ингредиенты в предварительно заданных количествах или соотношениях, а также любой продукт, который получается, непосредственно или опосредованно, в результате объединения конкретно указанных ингредиентов в конкретно указанных количествах. В частности, он охватывает продукт, включающий в себя один или несколько активных ингредиентов и возможный носитель, содержащий инертные ингредиенты, а также любой продукт, который получается, непосредственно или опосредованно, в результате объединения, комплексообразования или агрегации двух или более ингредиентов, либо в результате диссоциации одного или более ингредиентов, либо в результате реакций или взаимодействий другого типа между одним или несколькими ингредиентами.
Термин "ингибитор" означает соединение, которое конкурирует за связывание, ослабляет связывание или предотвращает связывание конкретного лиганда с конкретным рецептором либо которое ослабляет или предотвращает ингибирование функции конкретного белка.
Термин "концентрация, вызывающая половину от максимального ингибирования", (IC50) означает концентрацию конкретного соединения, необходимую для достижения 50% ингибирования биологического процесса in vitro. Значения IC50 можно преобразовать логарифмически в значения pIC50 (-log IC50), при этом их более высокие значения указывают на экспоненциально более высокую эффективность. Значение IC50 не является абсолютным значением, а зависит от экспериментальных условий, например, применяемых концентраций. Значение IC50 можно преобразовать в абсолютную константу ингибирования (Ki), используя уравнение Ченга-Прусоффа11.
"Терапевтически эффективное количество" означает количество соединения, которое при введении субъекту для лечения болезненного состояния, является достаточным для осуществления такого лечения в отношении данного болезненного состояния. "Терапевтически эффективное количество" будет варьировать в зависимости от соединения, подвергаемого лечению болезненного состояния, тяжести или подвергаемого лечению заболевания, возраста и относительного состояния здоровья субъекта, пути и формы введения, заключения лечащего врача или ветеринара и других факторов.
Термины "те, которые определены в данном описании" и "те, которые описаны в данной заявке", когда они имеют отношение к переменной величине, включают в себя посредством ссылки широкое определение для данной переменной величины, а также конкретное, более конкретное и наиболее конкретное определения, если таковые имеются.
Термины "обработка", "приведение в контакт" и приведение во взаимодействие", когда они имеют отношение к химической реакции, означают добавление или смешивание двух или более реагентов в соответствующих условиях с целью получения указанного и/или желаемого продукта. Должно быть очевидно, что взаимодействие, в результате которого образуется указанный и/или желаемый продукт, не обязательно должна быть результатом непосредственного объединения двух первоначально добавленных реагентов, т.е. в смеси могут образовываться и присутствовать одно или более промежуточных соединений, что в конечном итоге приводит к образованию указанного и/или желаемого продукта.
Термин "ароматический" относится к общепринятой идее ароматичности, как она определена в литературе, в частности, в IUPAC (Международный союз по теоретической и прикладной химии) - Compendium of Chemical Terminology, 2nd, A.D. McNaught & A. Wilkinson (Eds). Blackwell Scientific Publications, Oxford (1997).
Термин "фармацевтически приемлемый эксципиент" означает любой ингредиент, не обладающий никакой терапевтической активностью и являющийся нетоксичным, такой как разрыхлители, связующие вещества, наполнители, растворители, буферы, вещества, регулирующие тоничность, стабилизаторы, антиоксиданты, поверхностно-активные вещества или смазывающие вещества, используемый в технологии приготовления фармацевтических продуктов.
Всякий раз, когда в химической структуре присутствует хиральный атом углерода, подразумевается, что все стереоизомеры, ассоциированные с данным хиральным атомом углерода, охватываются данной структурой как чистые стереоизомеры, а также их смеси.
Согласно изобретению также предложены фармацевтические композиции, способы применения и способы получения вышеупомянутых соединений.
Все отдельные воплощения можно комбинировать.
Согласно одному из воплощений изобретения предложено соединение формулы I,
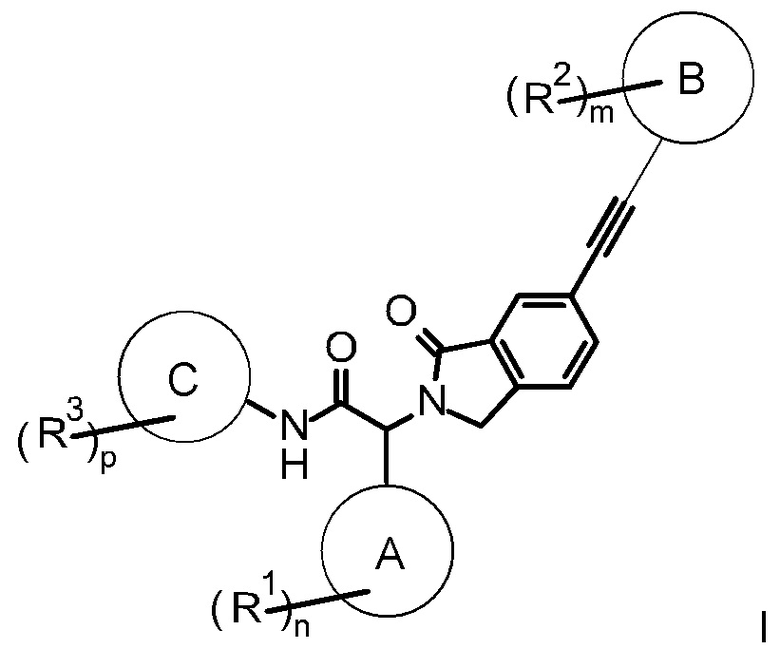
где
А представляет собой арил или гетероарил,
В представляет собой арил или гетероарил,
С представляет собой гетероарил,
R1 каждый независимо выбран из группы, состоящей из
1) амино,
2) С1-6-алкила,
3) C1-6-алкокси,
4) циано,
5) галогена,
6) галоген-С1-6-алкила,
7) галоген-С1-6-алкокси и
8) гидрокси;
R2 каждый независимо выбран из группы, состоящей из
1) -(CH2)k-N(R4,R5),
2) -(C=O)-N(R4,R5),
3) галогена,
4) -NH-(С=O)-С1-6-алкила и
5) С1-6-алкила;
R3 каждый независимо выбран из группы, состоящей из
1) амино,
2) С1-6-алкила,
3) С1-6-алкокси,
4) циано,
5) галогена,
6) галоген-С1-6-алкила,
7) галоген-С1-6-алкокси и
8) гидрокси;
R4 каждый независимо выбран из группы, состоящей из
1) Н и
2) C1-6-алкила;
R5 каждый независимо выбран из группы, состоящей из
1) Н,
2) C1-6-алкила и
3) -(С=O)-С1-6-алкила;
или R4 и R5 вместе с атомом N, к которому они присоединены, образуют гетероциклил, при этом гетероциклил возможно замещен группой R6;
R6 каждый независимо выбран из группы, состоящей из
1) -OH,
2) С1-6-алкила и
3) -(С=O)-С1-6-алкила;
k равно 0, 1 или 2,
n равно 0, 1, 2 или 3;
m равно 0, 1 или 2
р равно 0 или 1;
или его фармацевтически приемлемая соль.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где
А представляет собой арил или гетероарил,
В представляет собой арил или гетероарил,
С представляет собой гетероарил,
R1 каждый независимо выбран из группы, состоящей из
1) амино,
2) C1-6-алкила,
3) C1-6-алкокси,
4) циано,
5) галогена,
6) галоген-С1-6-алкила,
7) галоген-С1-6-алкокси и
8) гидрокси;
R2 каждый независимо выбран из группы, состоящей из
1) -(CH2)k-N(R4,R5),
2) -(C=O)-N(R4,R5),
3) -NH-(С=O)-С1-6-алкила и
4) C1-6-алкила;
R3 каждый независимо выбран из группы, состоящей из
1) амино,
2) С1-6-алкила,
3) C1-6-алкокси,
4) циано,
5) галогена,
6) галоген-С1-6-алкила,
7) галоген-С1-6-алкокси и
8) гидрокси;
R4 каждый независимо выбран из группы, состоящей из
1) Н и
2) C1-6-алкила;
R5 каждый независимо выбран из группы, состоящей из
1) Н,
2) С1-6-алкила и
3) -(С=O)-С1-6-алкила;
или R4 и R5 вместе с атомом N, к которому они присоединены, образуют гетероциклил;
k равно 0, 1 или 2;
n равно 0, 1, 2 или 3;
m равно 0, 1 или 2;
р равно 0 или 1.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где А представляет собой арил, в частности, фенил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где А представляет собой арил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где А представляет собой фенил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где А представляет собой пиридинил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где В представляет собой арил, в частности, фенил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где В представляет собой арил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где В представляет собой фенил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где В представляет собой гетероарил, в частности, пиридинил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где В представляет собой гетероарил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где В представляет собой пиридинил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где В представляет собой фенил или пиридинил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где С представляет собой гетероарил, в частности, тиазолил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где С представляет собой гетероарил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где С представляет собой гетероарил, в частности, тиазолил или пиридинил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где С представляет собой тиазолил или пиридинил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где С представляет собой пиридинил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где n равно 0, 1 или 2.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где n равно 0.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где n равно 1.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где n равно 2.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где m равно 1.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где m равно 0.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где р равно 0.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где р равно 1.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где R1 представляет собой галоген.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где R1 представляет собой F.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где R2 представляет собой -(С=O)-морфолинил, -(C=O)N(H,CH3), -СН2-(4-метилпиперазинил), -СН2-(4-ацетилпиперазинил), -СН2-(4-этилпиперазинил), -СН2-(4-гидрокси-пиперидил), -СН2-(морфолинил), -CH2NH2, -СН2-пиперазинил, Cl, -N(H,C=OCH3) или -NH2, в частности, -С=O-морфолинил, -(C=O)N(H,CH3), -СН2-(4-ацетилпиперазинил), -СН2-(4-этилпиперазинил), -СН2-морфолинил, -CH2-NH2, -СН2-пиперазинил, -N(H,(C=O)CH3) или -NH2.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где R2 представляет собой -(С=O)-морфолинил, -(C=O)N(H,CH3), -СН2-(4-метилпиперазинил), -СН2-(4-ацетилпиперазинил), -СН2-(4-этилпиперазинил), -СН2-(4-гидрокси-пиперидил), -СН2-(морфолинил), -CH2NH2, -СН2-пиперазинил, Cl, -N(H,C=OCH3) или -NH2.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где R2 представляет собой -С=O-морфолинил, -(C=O)N(H,CH3), -СН2-(4-ацетилпиперазинил), -СН2-(4-этилпиперазинил), -СН2-морфолинил, -CH2-NH2, -СН2-пиперазинил, -N(H,(C=O)CH3) или -NH2.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где R2 представляет собой -NH2.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где R3 представляет собой -NH2.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где А представляет собой фенил, n равно 0, В представляет собой фенил, m равно 0, и С представляет собой тиазолил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где А представляет собой фенил, n равно 0, В представляет собой пиридил, m равно 0, и С представляет собой тиазолил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где А представляет собой фенил, n равно 1, R2 представляет собой -NH2, В представляет собой фенил, m равно 0, и С представляет собой тиазолил.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, где А представляет собой фенил, n равно 1, R2 представляет собой -NH2, В представляет собой пиридил, m равно 0, и С представляет собой тиазолил.
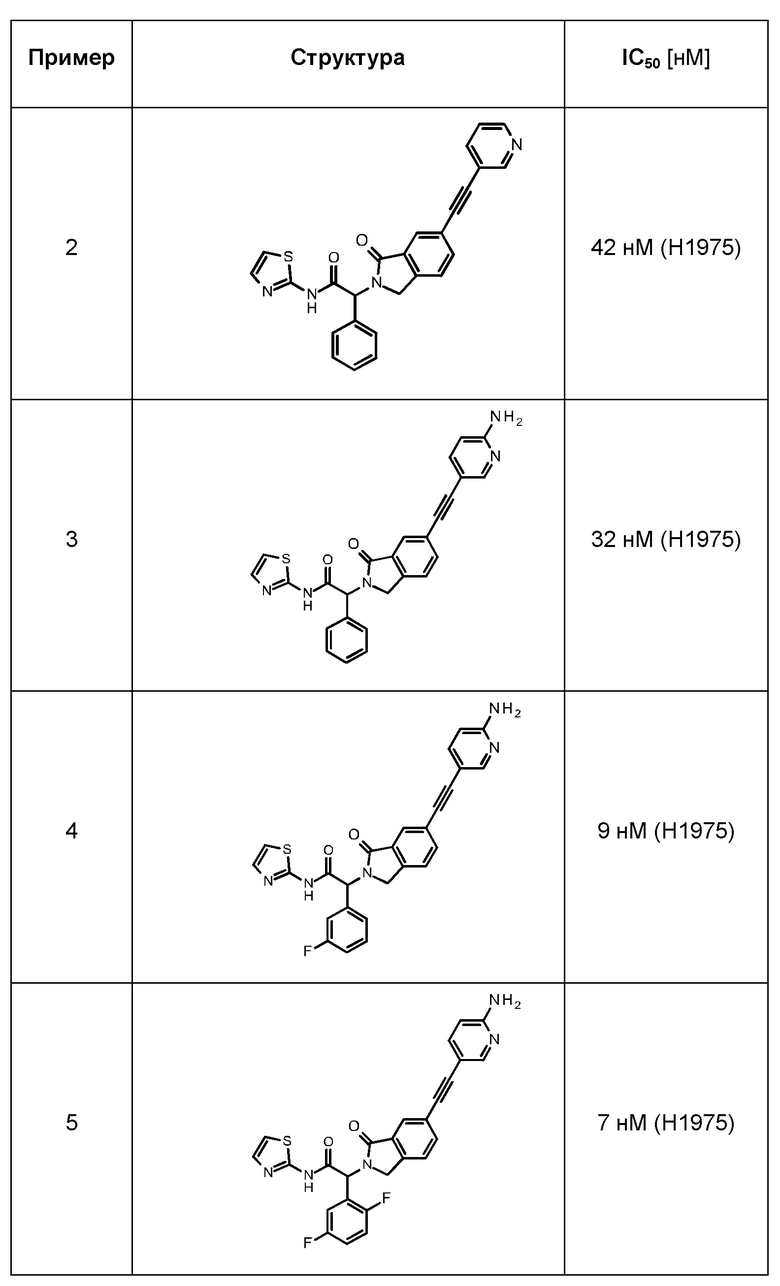
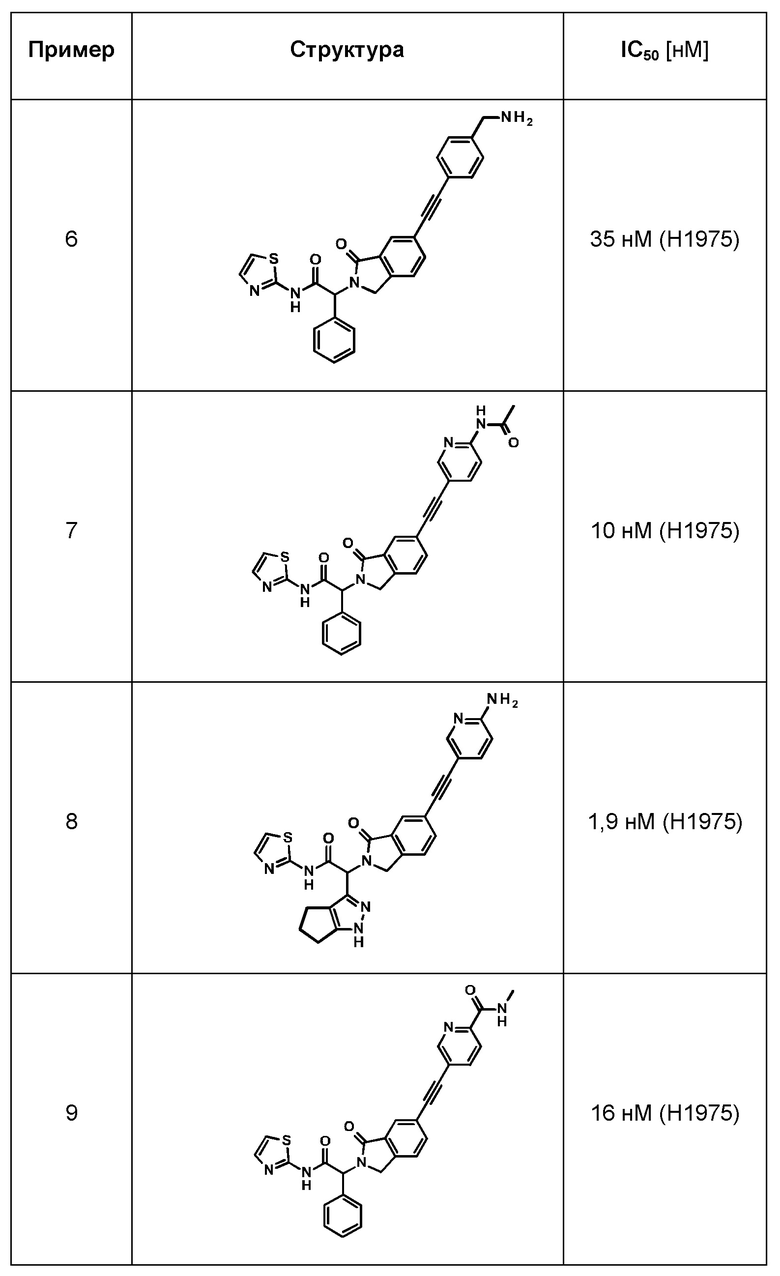
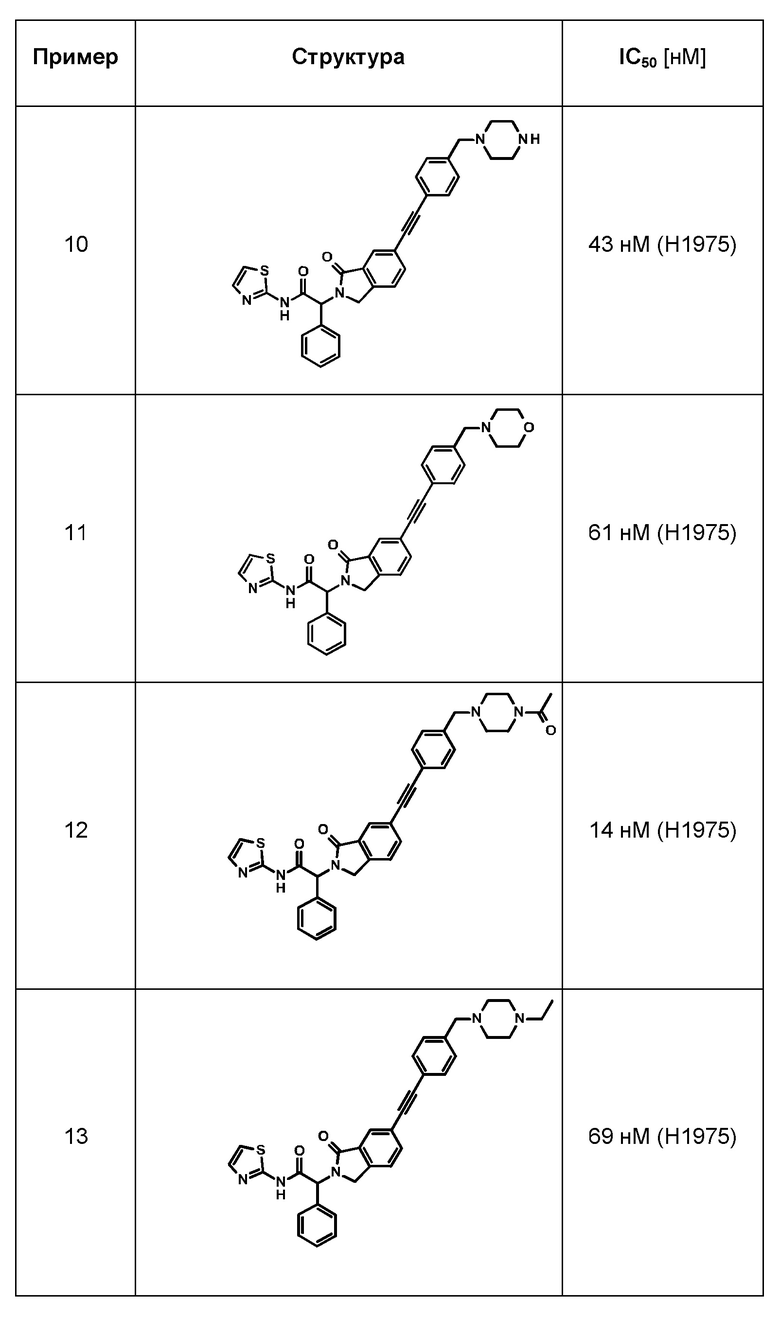
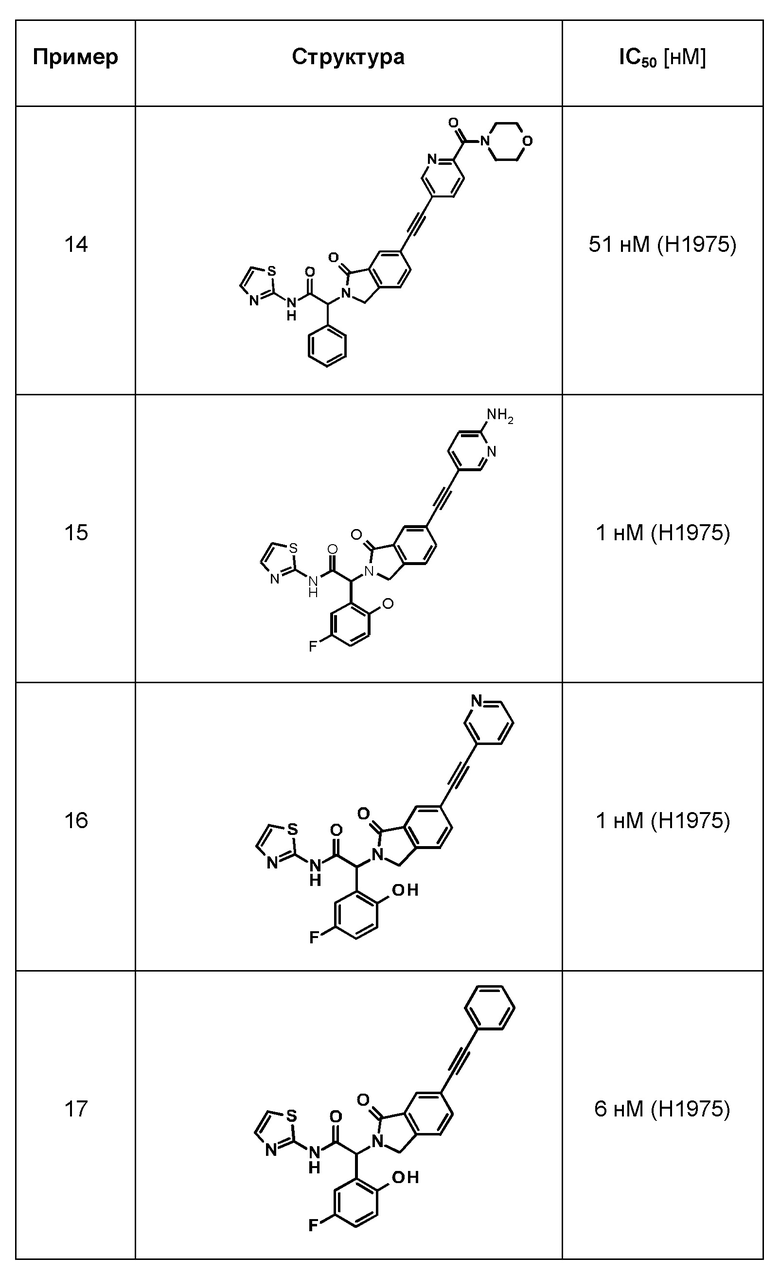
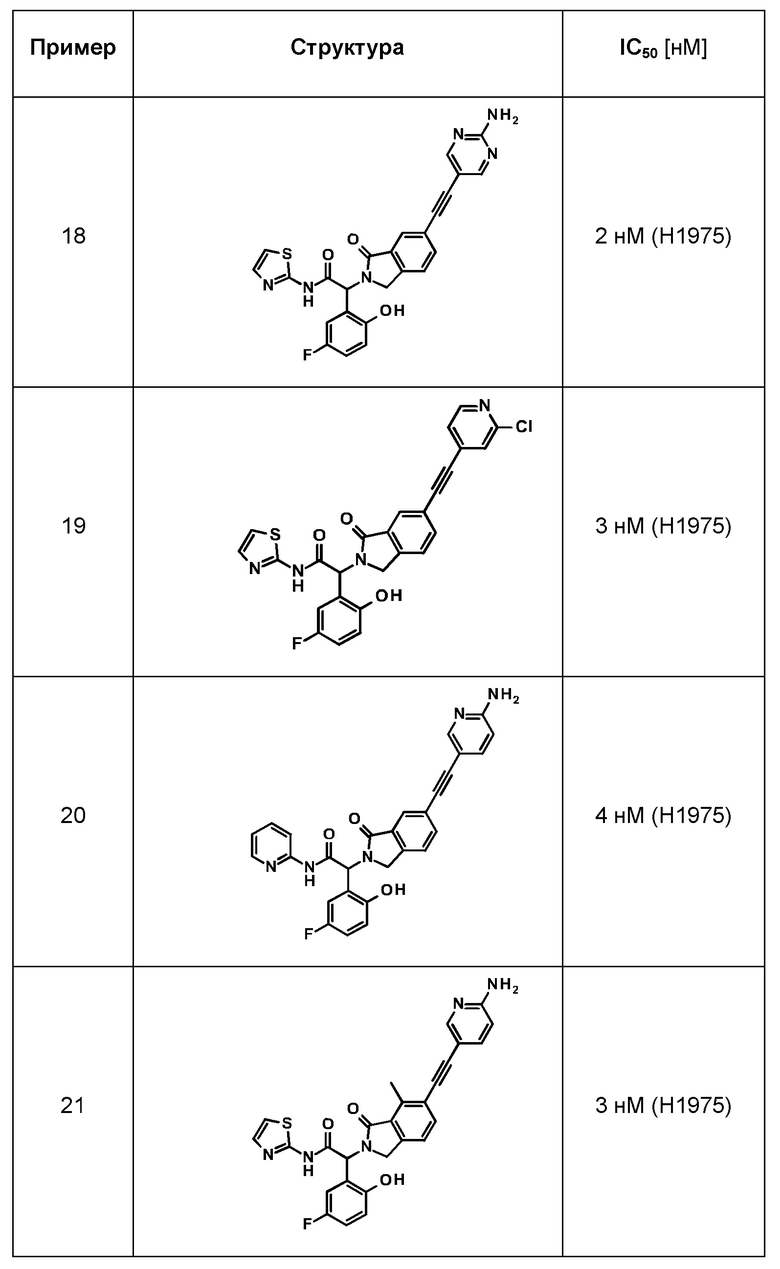
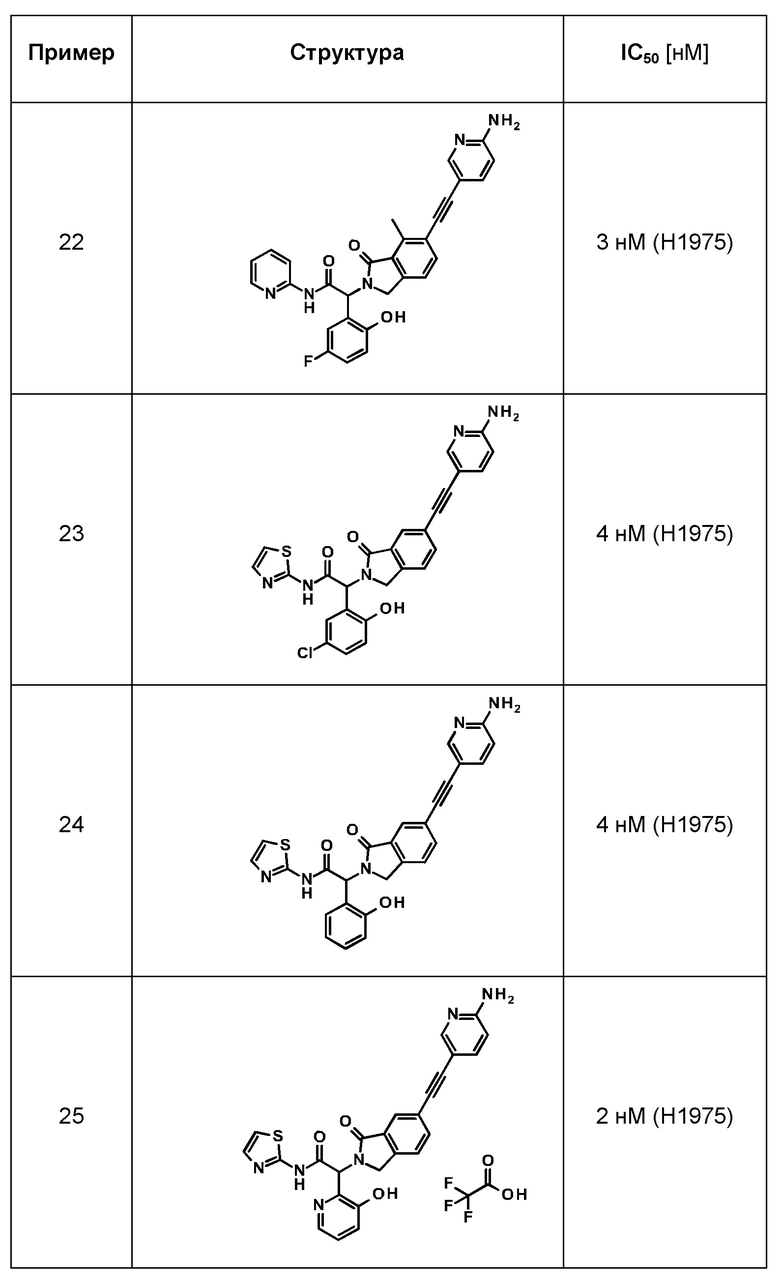
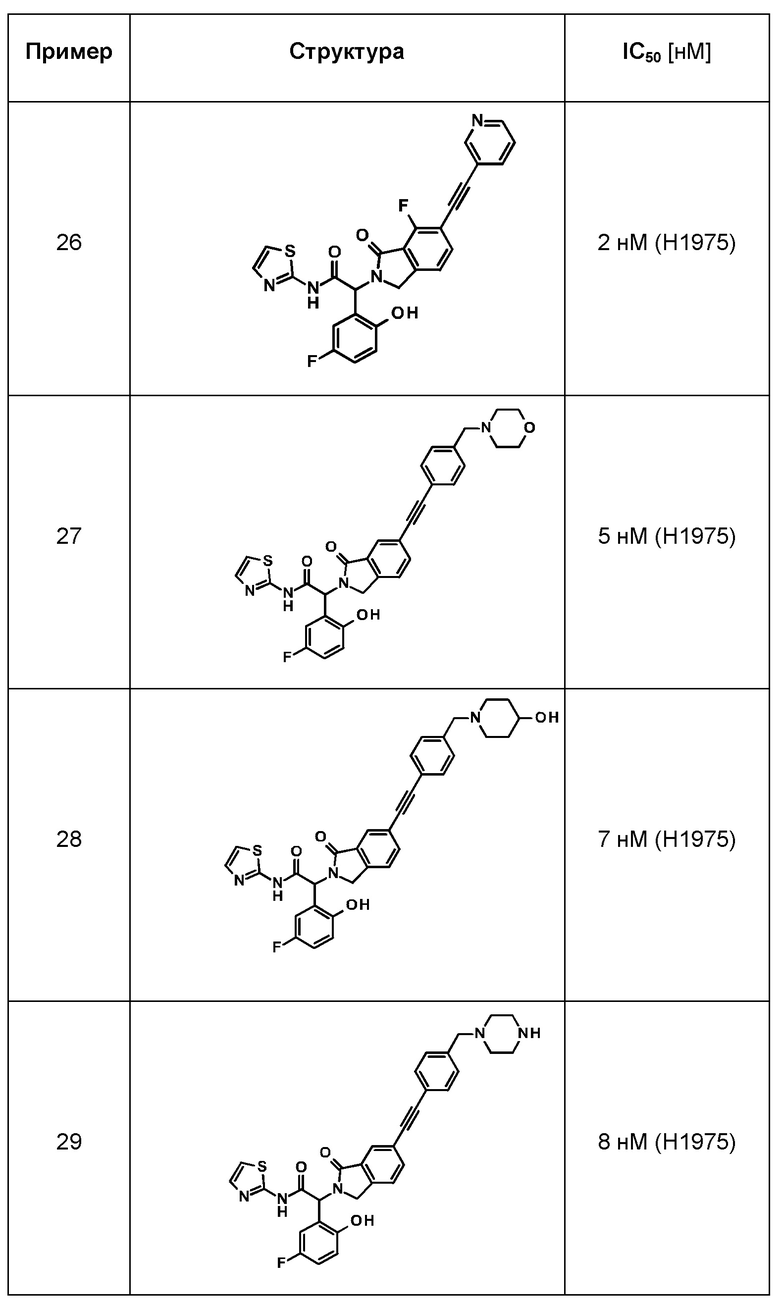
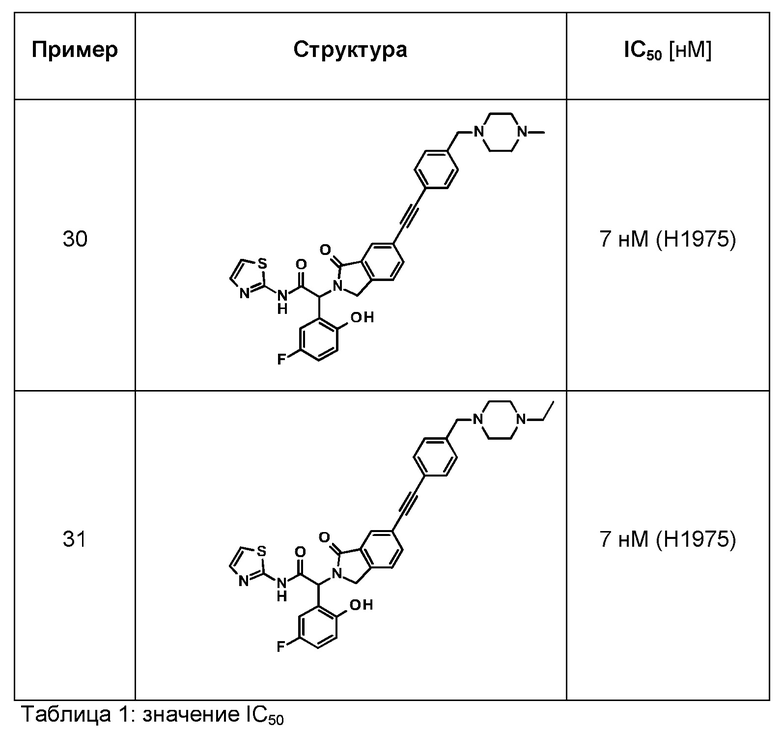
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, которые выбраны из группы, состоящей из
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-[(4-гидрокси-1-пиперидил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-[(4-метилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[7-фтор-1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(2-аминопиримидин-5-ил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(2-хлор-4-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-ацетамидо-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-фторфенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(1,4,5,6-тетрагидроциклопента[с]пиразол-3-ил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-(2-пиридил)ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-хлор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2-гидроксифенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-гидрокси-2-пиридил)-N-тиазол-2-ил-ацетамида трифторацетата,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-(2-пиридил)ацетамида,
(2RS)-2-[6-[2-[4-(аминометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-ацетилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[6-(морфолин-4-карбонил)-3-пиридил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида и
N-метил-5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоксамида.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, которые выбраны из группы, состоящей из
(2RS)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-ацетамидо-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-фторфенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(1,4,5,6-тетрагидроциклопента[с]пиразол-3-ил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-(аминометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-ацетилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[6-(морфолин-4-карбонил)-3-пиридил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
N-метил-5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоксамида и
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли, которые выбраны из группы, состоящей из
(2RS)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-ацетамидо-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-фторфенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(1,4,5,6-тетрагидроциклопента[с]пиразол-3-ил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-(аминометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-ацетилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[6-(морфолин-4-карбонил)-3-пиридил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида и
N-метил-5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоксамида.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли для применения в качестве терапевтически активного вещества.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли для применения при терапевтическом и/или профилактическом лечении рака, в частности, немелкоклеточного рака легкого.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли для применения при терапевтическом и/или профилактическом лечении немелкоклеточного рака легкого.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли для приготовления лекарственного средства для терапевтического и/или профилактического лечения рака, в частности, немелкоклеточного рака легкого.
Одно из воплощений изобретения относится к фармацевтической композиции, содержащей соединение формулы I, как оно описано в данной заявке, или его фармацевтически приемлемую соль и фармацевтически приемлемое вспомогательное вещество.
Одно из воплощений изобретения относится к способу терапевтического и/или профилактического лечения рака, в частности, немелкоклеточного рака легкого, путем введения пациенту соединения формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли для применения в качестве лекарственного средства при терапевтическом и/или профилактическом лечении пациента с EGFR-активирующими мутациями, страдающего от рака, в частности, немелкоклеточного рака легкого, включающего определение статуса EGFR-активирующих мутаций у указанного пациента и затем введение указанному пациенту соединения формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли.
Одно из воплощений изобретения относится к соединению формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли для применения в качестве лекарственного средства при терапевтическом и/или профилактическом лечении пациента с EGFR-активирующими мутациями, которые определены с использованием теста для определения мутаций в EGFR "cobas® EGFR Mutation Test v2", страдающего от рака, в частности, немелкоклеточного рака легкого, включающего определение статуса EGFR-активирующих мутаций у указанного пациента и затем введение указанному пациенту соединения формулы I, как оно описано в данной заявке, или его фармацевтически приемлемой соли.
Кроме того, изобретение включает все оптические изомеры соединений формулы I, т.е. их диастереоизомеры, диастереомерные смеси, рацемические смеси, все соответствующие им энантиомеры и/или таутомеры, а также сольваты.
Соединения формулы I могут содержать один или более асимметрических центров и поэтому могут присутствовать в виде рацематов, рацемических смесей, одиночных энантиомеров, диастереомерных смесей и индивидуальных диастереомеров. В зависимости от природы различных заместителей в молекуле могут присутствовать дополнительные асимметрические центры. Благодаря наличию каждого такого асимметрического центра будут независимо образовываться два оптических изомера, и подразумевается, что все возможные оптические изомеры и диастереомеры в виде смесей и в виде чистых или частично очищенных соединений включены в данное изобретение. Подразумевается, что настоящее изобретение охватывает все такие изомерные формы этих соединений. С использованием соответствующей модификации методологии, изложенной в данном описании, могут быть выполнены независимые процедуры синтеза этих диастереомеров или их хроматографические разделения, известные в данной области техники. Их абсолютную стереохимическую конфигурацию можно определить, используя рентгеноструктурную кристаллографию кристаллических продуктов или кристаллических промежуточных соединений, которые при необходимости модифицируют с использованием реагента, содержащего асимметрический центр с известной абсолютной конфигурацией. При желании можно выполнить разделение рацемических смесей соединений, чтобы выделить индивидуальные энантиомеры. Разделение может быть осуществлено методами, хорошо известными в данной области техники, такими как проведение реакции сочетания рацемической смеси соединений с энантиомерно чистым соединением для образования диастереомерной смеси, затем разделение индивидуальных диастереомеров стандартными методами, такими как фракционная кристаллизация или хроматография.
В тех воплощениях, где предложены оптически чистые энантиомеры, термин "оптически чистый энантиомер означает", что соединение содержит более 90% (по массе) желаемого изомера, в частности, более 95% (по массе) желаемого изомера или, конкретнее, более 99% (по массе) желаемого изомера, при этом указанный процент по массе приводится из расчета на общую массу изомера(ов) данного соединения. Хирально чистые или хирально обогащенные соединения могут быть получены с использованием хирально-селективного синтеза или путем разделения энантиомеров. Разделение энантиомеров может быть выполнено на стадии получения конечного продукта или, альтернативно, на стадии получения подходящего промежуточного соединения.
Соединения формулы I могут быть получены в соответствии со схемами, описанными в разделе Примеры. Исходное вещество имеется в продаже или может быть получено в соответствии с известными методами.
Получение соединений формулы I далее описано более подробно на схеме 1 и в разделе Примеры.
Схема 1
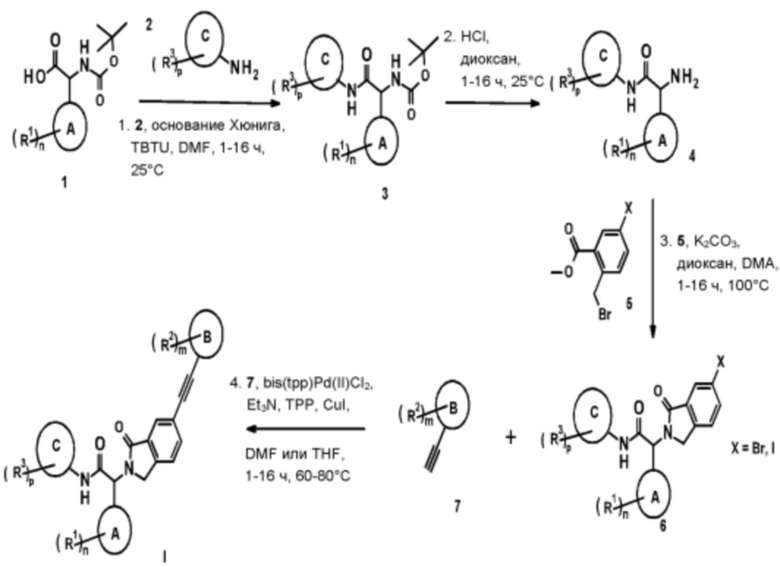
Соединение на основе изоиндолин-ацетилена общей формулы I может быть получено, например, посредством амидного сочетания соответствующим образом замещенной кислоты формулы 1 и соответствующим образом замещенного амина формулы 2 с использованием агента сочетания, такого как TBTU (тетрафторборат 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония), с получением желаемых амидных производных формулы 3. После удаления защитных групп с последующей циклизацией в кольцевую форму с использованием иод- или бромметил-2-(бромметил)бензоата формулы 5 получают желаемый изоиндолин 6. В результате реакции сочетания Соногаширы с соответствующим образом замещенным ацетиленом формулы 7 образуется желаемое соединение на основе изоиндолин-ацетилена общей формулы I (схема 1).
Вообще говоря, последовательность стадий, используемых для синтеза соединений формулы I, в некоторых случаях также может быть модифицирована.
Соответствующие фармацевтически приемлемые соли с кислотами могут быть получены стандартными методами, известными специалисту в данной области техники, например, путем растворения соединения формулы I в подходящем растворителе, таком как, например, диоксан или тетрагидрофуран, и добавления соответствующего количества соответствующей кислоты. Обычно продукты могут быть выделены фильтрованием или хроматографией. Превращение соединения формулы I в фармацевтически приемлемую соль с основанием можно осуществить посредством обработки такого соединения таким основанием. Один из возможных методов образования такой соли заключается, например, в добавлении 1/n эквивалентов основания, такого как, например, М(ОН)n, где М означает катион металла или аммония, а n означает число гидроксид-анионов, к раствору соединения в подходящем растворителе (например, этаноле, смеси этанол-вода, смеси тетрагидрофуран-вода) и удалении растворителя посредством выпаривания или лиофилизации. Конкретными солями являются гидрохлорид, формиат и трифторацетат.
В случаях, когда их получение не описано в разделе Примеры, соединения формулы I, а также все промежуточные продукты могут быть получены в соответствии с аналогичными способами или в соответствии со способами, приведенными в данном описании. Исходные вещества имеются в продаже, известны в данной области техники или могут быть получены способами, известными в данной области техники, или по аналогии с ними.
Будет очевидно, что соединения общей формулы I по данному изобретению могут быть модифицированы по функциональным группам с получением производных, которые способны превращаться обратно в исходное соединение in vivo.
Фармакологические тесты
Соединения формулы I и их фармацевтически приемлемые соли обладают полезными фармакологическими свойствами. Соединения исследовали в соответствии с приведенным далее тестом.
Анализ (на клетках) фосфо-EGFR с использованием гомогенной флуоресценции с разрешением по времени (HTRF)
Клеточная линия и среды
Клеточную линию Н1975 получали из Американской коллекции типовых культур (Manassas, VA, USA). Клетки поддерживали при 37°С, 5% CO2 в полной среде RPMI 1640 без фенолового красного, содержащей глутамин (0,3 мг/мл), пенициллин (100 международных единиц (МЕ)/мл) и стрептомицин (100 мг/мл) (Gibco), дополненной 10% фетальной телячьей сыворотки (FBS) (Gibco). Соединения разбавляли в "голодной" среде RPMI 1640 без фенолового красного, содержащей глутамин (0,3 мг/мл), пенициллин (100 МЕ/мл) и стрептомицин (100 мг/мл) (Gibco).
Протокол
Клетки культивировали в течение ночи в 384-луночном белом планшете (8000 клеток/лунка), используя по 8 мкл полной среды/лунка. Клетки промывали два раза, используя по 20 мкл "голодной" среды. Среды удаляли путем вытряхивания из планшетов на ткань и после этого добавляли свежую "голодную" среду из расчета 8 мкл/лунка. Затем к клеткам добавляли 3х раствор соединения в количестве 4 мкл/лунка в серии полулогарифмических разведений соединения или DMSO (диметилсульфоксид) в "голодной" среде. Через 6 часов инкубирования при 37°С, 5% CO2 клетки подвергали лизизу, добавляя к смеси с соединением дополняющий лизирующий буфер из расчета 4 мкл/лунка, затем инкубировали в течение 30 мин при комнатной температуре со встряхиванием. Лизаты хранили при -20°С в течение ночи. На следующий день планшеты размораживали и добавляли по 2 мкл раствора меченного криптатом антитела к фосфо-EGFR и по 2 мкл раствора антитела к фосфо-EGFR-d2, приготовленных в буфере для детекции. Затем планшеты инкубировали в течение по меньшей мере 4 ч при комнатной температуре, после чего прочитывали интенсивность испускаемой флуоресценции при 620 и 665 нм, используя планшетный ридер PHERAstar FX (BMG Labtech).
Фармацевтические композиции
LR 772 (Я-120): Соединения формулы I и фармацевтически приемлемые соли могут быть использованы в качестве терапевтически активных веществ, например, в форме фармацевтических препаратов. Эти фармацевтические препараты можно вводить перорально, например, в форме таблеток, таблеток, покрытых оболочкой, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако, введение также может быть осуществлено ректально, например, в форме суппозиториев, или парентерально, например, в форме растворов для инъекций.
В процессе приготовления фармацевтических препаратов соединения формулы I и их фармацевтически приемлемые соли можно обрабатывать совместо с фармацевтически инертными неорганическими или органическими носителями. Например, в качестве таких носителей для таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул можно использовать лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли и тому подобное. Подходящими носителями для мягких желатиновых капсул являются, например растительные масла, воски, жиры, полутвердые и жидкие полиолы и тому подобное. Однако, в случае мягких желатиновых капсул никаких носителей обычно не требуется, но это зависит от природы активного вещества. Подходящими носителями для приготовления растворов и сиропов являются, например, вода, полиолы, глицерин, растительное масло и тому подобное. Подходящими носителями для суппозиториев являются, например, природные или отвержденные жиры, воски, жиры, полужидкие или жидкие полиолы и тому подобное.
Помимо этого фармацевтические препараты могут содержать фармацевтически приемлемые вспомогательные вещества, такие как консерванты, солюбилизаторы, стабилизаторы, увлажняющие агенты, эмульгаторы, подсластители, красители, корригенты, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать другие дополнительные терапевтически полезные вещества.
Согласно настоящему изобретению также предложены лекарственные средства, содержащие соединение формулы I или его фармацевтически приемлемую соль и терапевтически инертный носитель, равно как и способ их получения, который включает приведение одного или более чем одного соединения формулы I и/или одной или более чем одной их фармацевтически приемлемой соли и, при желании, одного или более чем одного другого терапевтически полезного вещества в форму галенова препарата вместе с одним или более чем одним терапевтически инертным носителем.
Дозировка может варьировать в широких пределах и, несомненно, в каждом конкретном случае должна быть подобрана с учетом индивидуальных потребностей. В случае перорального введения дозировка соединения общей формулы I или соответствующего количества его фармацевтически приемлемой соли для взрослых может варьировать от примерно 0,01 мг до примерно 1000 мг в сутки. Суточную дозировку можно вводить в виде разовой дозы или в разделенных дозах, и помимо этого, если на то имеется показание, также может быть превышен верхний предел.
Следующие далее примеры иллюстрируют настоящее изобретение без его ограничения, но являются всего лишь репрезентативными. Фармацевтические препараты подходящим образом содержат примерно 1-500 мг, в частности, 1-100 мг соединения формулы I. Примерами композиций по изобретению являются приведенные далее композиции.
Пример А
Таблетки следующего состава готовят обычным образом.
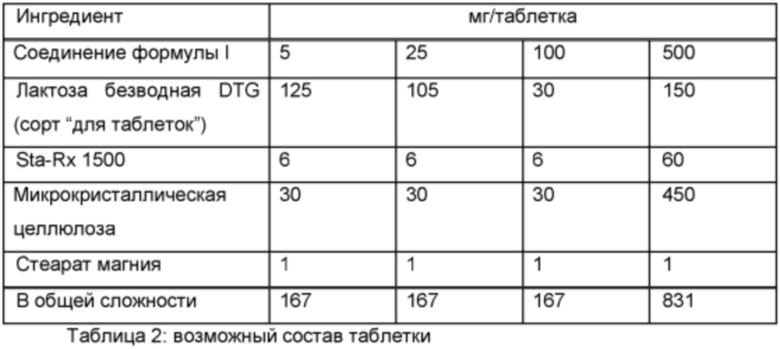
Методика приготовления
1. Смешать ингредиенты 1, 2, 3 и 4 и гранулят с очищенной водой.
2. Высушить гранулы при 50°С.
3. Пропустить гранулы через подходящее для измельчения оборудование.
4. Добавить ингредиент 5 и перемешать в течение трех минут; подвергнуть прессованию на подходящем прессе.
Пример В-1
Готовят капсулы следующего состава:
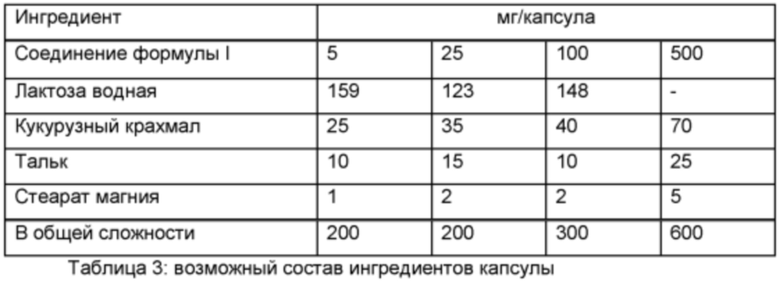
Методика приготовления
1. Смешать ингредиенты 1, 2 и 3 в подходящем смесителе в течение 30 минут.
2. Добавить ингредиенты 4 и 5 и перемешать в течение 3 минут.
3. Заполнить подходящую капсулу.
Соединение формулы I, лактозу и кукурузный крахмал сначала смешивают в смесителе и затем измельчают в измельчителе. Смесь возвращают в смеситель; к ней добавляют тальк и тщательно перемешивают. Используя автомат, смесью заполняют подходящие капсулы, например, твердые желатиновые капсулы.
Пример В-2
Готовят мягкие желатиновые капсулы следующего состава:
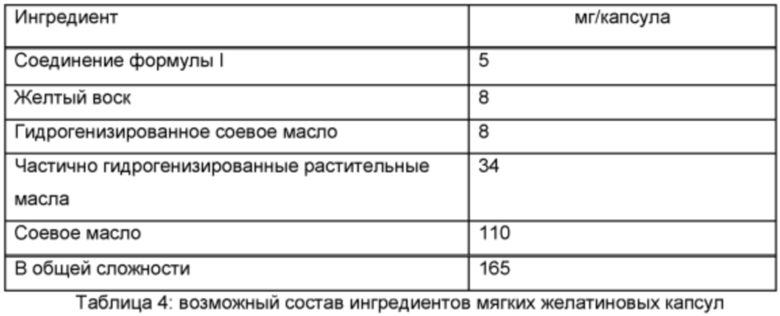
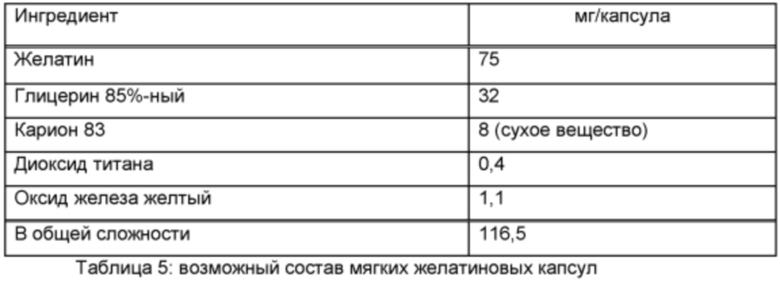
Методика приготовления
Соединение формулы I растворяют в теплом расплаве других ингредиентов и данной смесью заполняют мягкие желатиновые капсулы соответствующего размера. Заполненные мягкие желатиновые капсулы обрабатывают в соответствии с обычными методиками.
Пример С
Готовят суппозитории следующего состава:
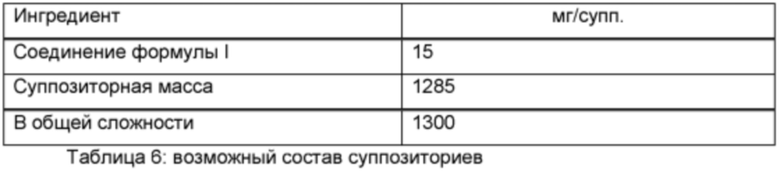
Методика приготовления
Суппозиторную массу расплавляют в стеклянном или стальном сосуде, тщательно перемешивают и охлаждают до 45°С. После этого к ней добавляют тонкоизмельченное соединение формулы I и перемешивают до тех пор, пока оно не будет полностью диспергировано. Смесь выливают в формы для суппозиториев подходящего размера, оставляют охлаждаться; затем суппозитории извлекают из форм и по отдельности упаковывают в парафинированную бумагу или металлическую фольгу.
Пример D
Готовят растворы для инъекций следующего состава:
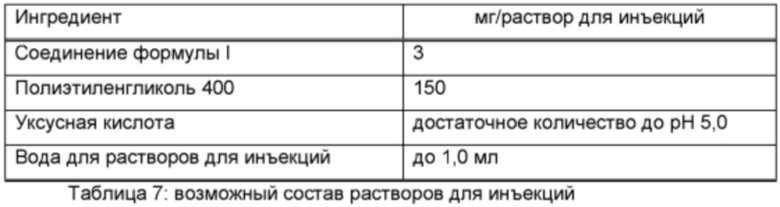
Методика приготовления
Соединение формулы I растворяют в смеси полиэтиленгликоля 400 и воды для инъекций (ее части). Значение рН подводят до 5,0 уксусной кислотой. Объем подводят до 1,0 мл, добавляя оставшееся количество воды. Раствор фильтруют, разливают во флаконы, используя соответствующий избыток, и стерилизуют.
Пример Е
Готовят саше следующего состава:
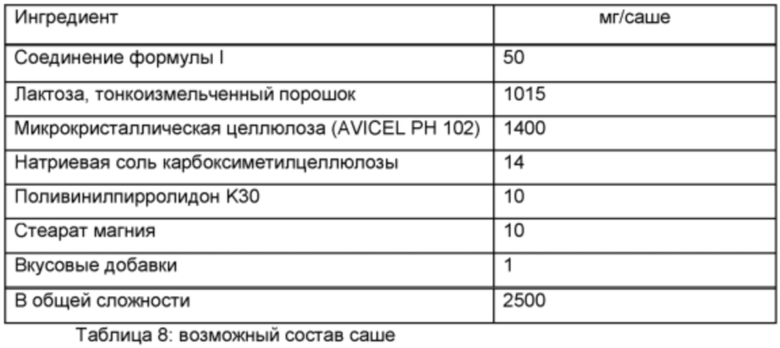
Методика приготовления
Соединение формулы I смешивают с лактозой, микрокристаллической целлюлозой и натриевой солью карбоксиметилцеллюлозы и подвергают гранулированию со смесью поливинилпирролидона в воде. Гранулят смешивают со стеаратом магния и вкусовыми добавками и этим заполняют саше.
Экспериментальная часть
Следующие далее примеры приведены для иллюстрации изобретения. Их не следует рассматривать в качестве ограничивающих объем данного изобретения, а всего лишь как являющихся репрезентативными.
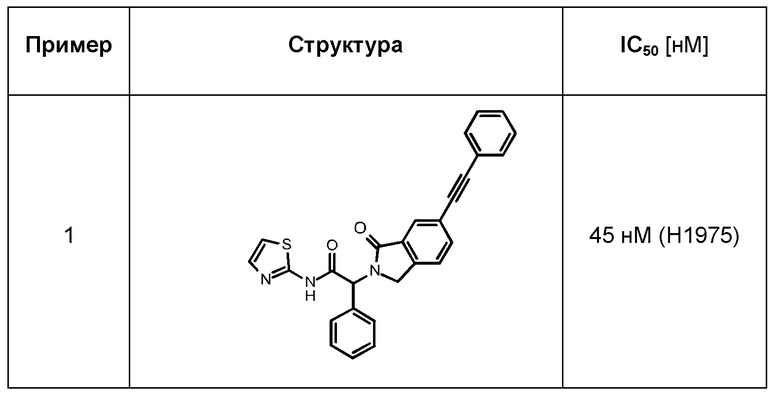
Пример 1
(2RS)-2-[1-Оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Стадия 1: трет-бутил-N-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]карбамат
(2RS)-2-(трет-Бутоксикарбониламино)-2-фенил-уксусную кислоту (9,5 г; 37,8 ммоль) растворяли в 75 мл этилацетата и 10 мл DMF (диметилформамид). По каплям добавляли тиазол-2-амин (3,79 г; 37,8 ммоль; 1 экв.), основание Хюнига (14,7 г; 19,8 мл; 113 ммоль; 3 экв.) и раствор пропилфосфонового ангидрида (50%-ный в этилацетате) (36,1 г; 33,8 мл; 56,7 ммоль; 1,5 экв.) при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь экстрагировали насыщенным раствором NaHCO3 и два раза этилацетатом. Органические слои экстрагировали водой, сушили над сульфатом натрия и упаривали досуха. Желаемый трет-бутил-N-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]карбамат (12 г; выход 95%) получали в виде светло-желтого твердого вещества, MS: m/e = 334,5 (М+Н+).
Стадия 2: (2RS)-2-амино-2-фенил-N-тиазол-2-ил-ацетамида гидрохлорид
трет-Бутил-N-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]карбамат (пример 1, стадия 1) (12 г; 37 ммоль) растворяли в 100 мл МеОН и добавляли HCl (4 н. раствор в диоксане) (27,7 мл; 111 ммоль; 3 экв.) при комнатной температуре. Смесь перемешивали в течение 5 часов при комнатной температуре. Реакционную смесь упаривали досуха и использовали непосредственно на следующей стадии. Желаемый (2RS)-2-амино-2-фенил-N-тиазол-2-ил-ацетамида гидрохлорид (количественный выход) получали в виде серого твердого вещества, MS: m/e = 234,4 (М+Н+).
Стадия 3: (2RS)-2-(6-иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамид
(2RS)-2-Амино-2-фенил-N-тиазол-2-ил-ацетамида гидрохлорид (пример 1, стадия 2) (1,22 г; 4,51 ммоль) растворяли в 15 мл диоксана и 2,5 мл DMA (диметилацетамид). Добавляли метил-2-(бромметил)-5-иодбензоат (CAS (химическая реферативная служба) 1310377-56-0) (1,6 г; 4,51 ммоль; 1 экв.) и триэтиламин (2,28 г; 3,14 мл; 22,5 ммоль; 5 экв.) при комнатной температуре. Смесь перемешивали при 100°С в течение 2 часов. Реакционную смесь экстрагировали водой и два раза этилацетатом. Органические слои экстрагировали рассолом, сушили над сульфатом натрия и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом этилацетат : гептан от 0:100 до 100:0, получая желаемый (2RS)-2-(6-иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамид (870 мг; выход 41%) в виде желтого твердого вещества, MS: m/e = 475,9 (М+Н+).
Стадия 4: (2RS)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил1-2-фенил-N-тиазол-2-ил-ацетамид
(2RS)-2-(6-Иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамид (пример 1, стадия 3) (50 мг; 0,105 ммоль) и фенилацетилен (16,1 мг; 17,3 мкл; 0,158 ммоль; 1,5 экв.) растворяли в 2 мл THF (тетрагидрофуран). Добавляли триэтиламин (16 мг; 22 мкл; 0,158 ммоль; 1,5 экв.), дихлорид бис-(трифенилфосфин)-палладия(II) (3,7 мг; 0,005 ммоль; 0,05 экв.), трифенилфосфин (2,8 мг; 0,01 ммоль; 0,1 экв.) и иодид меди(I) (0,2 мг; 0,001 ммоль; 0,01 экв.) и смесь перемешивали в течение 2 часов при 60°С. Реакционную смесь упаривали досуха и неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом этилацетат : гептан от 0:100 до 100:0. Желаемый (2RS)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид (30 мг; выход 63%) получали в виде светло-коричневого твердого вещества, MS: m/e = 450,0 (М+Н+).
Пример 2
(2RS)-2-[1-Оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 451,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамида (пример 1, стадия 3) и 3-этинилпиридина.
Пример 3
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белой пены, MS: m/e = 466,6 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамида (пример 1, стадия 3) и 5-этинилпиридин-2-амина.
Пример 4
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-фторфенил)-N-тиазол-2-ил-ацетамид
Стадия 1: трет-бутил-N-[(1RS)-1-(3-фторфенил)-2-оксо-2-(тиазол-2-иламино)этил]карбамат
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 352,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 1, исходя из (2RS)-2-(трет-бутоксикарбониламино)-2-(3-фторфенил)уксусной кислоты и тиазол-2-амина.
Стадия 2: (2RS)-2-амино-2-(3-фторфенил)-N-тиазол-2-ил-аиетамида гидрохлорид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 252,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 2, исходя из трет-бутил-N-[(1RS)-1-(3-фторфенил)-2-оксо-2-(тиазол-2-иламино)этил]карбамата (пример 4, стадия 1).
Стадия 3: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(3-фторфенил)-N-тиазол-2-ил-аиетамид
Указанное в заголовке соединение получали в виде светло-желтой пены, MS: m/e = 446,4/448,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 3, исходя из (2RS)-2-амино-2-(3-фторфенил)-N-тиазол-2-ил-ацетамида гидрохлорида (пример 4, стадия 2) и метил-5-бром-2-(бромметил)бензоата.
Стадия 4: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-фторфенил)-N-тиазол-2-ил-аиетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 484,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(3-фторфенил)-N-тиазол-2-ил-ацетамида (пример 4, стадия 3) и 5-этинилпиридин-2-амина.
Пример 5
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамид
Стадия 1: трет-бутил-N-[(1RS)-1-(2,5-дифторфенил)-2-оксо-2-(тиазол-2-иламино)этил]карбамат
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 370,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 1, исходя из (2RS)-2-(трет-бутоксикарбониламино)-2-(2,5-дифторфенил)уксусной кислоты и тиазол-2-амина.
Стадия 2: (2RS)-2-амино-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамида гидрохлорид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 270,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 2, исходя из трет-бутил-N-[(1RS)-1-(2,5-дифторфенил)-2-оксо-2-(тиазол-2-иламино)этил]карбамата (пример 5, стадия 1).
Стадия 3: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтой пены, MS: m/e = 464,4/466,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 3, исходя из (2RS)-2-амино-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамида гидрохлорида (пример 5, стадия 2) и метил-5-бром-2-(бромметил)бензоата.
Стадия 4: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2,5-дифторфенил)-N-тиазол-2-ил-аиетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 502,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамида (пример 5, стадия 3) и 5-этинилпиридин-2-амина.
Пример 6
(2RS)-2-[6-[2-[4-(Аминометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 479,6 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамида (пример 1, стадия 3) и (4-этинилфенил)метанамина гидрохлорида.
Пример 7
(2RS)-2-[6-[2-(6-Ацетамидо-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого полутвердого вещества, MS: m/e = 508,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 1, исходя из (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида (пример 3) и уксусной кислоты.
Пример 8
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(1,4,5,6-тетрагидроциклопента[с]пиразол-3-ил)-N-тиазол-2-ил-ацетамид
Стадия 1: 1-((2-(триметилсилил)этокси)метил)-1,4,5,6-тетрагидроциклопента[с]пиразол-3-карбальдегид
1,4,5,6-Тетрагидроциклопента[с]пиразол-3-карбальдегид (1 г; 7,53 ммоль) растворяли в 10 мл DCM (дихлорметан). По каплям добавляли основание Хюнига (1,95 г; 2,63 мл; 15,1 ммоль; 2 экв.) и (2-(хлорметокси)этил)триметилсилан (1,63 г; 1,73 мл; 9,8 ммоль; 1,3 экв.) при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 70 часов. Реакционную смесь экстрагировали насыщенным раствором NaHCO3 и два раза DCM. Органические слои сушили над сульфатом натрия и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом этилацетат : гептан от 0:100 до 50:50, получая желаемый 1-((2-(триметилсилил)этокси)метил)-1,4,5,6-тетрагидроциклопента[с]пиразол-3-карбальдегид (1,6 г; выход 80%) в виде бесцветного масла, MS: m/e = 267,4 (М+Н+).
Стадия 2: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]ацетонитрил
1-((2-(Триметилсилил)этокси)метил)-1,4,5,6-тетрагидроцикло-пента[с]пиразол-3-карбальдегид (пример 8, стадия 1) (1,6 г; 6,02 ммоль) растворяли в 20 мл ацетонитрила. Добавляли метил-2-(аминометил)-5-бромбензоата гидрохлорид (1,69 г; 6,02 ммоль; 1 экв.), основание Хюнига (1,95 г; 2,63 мл; 15,1 ммоль; 2,5 экв.) и триметилсилилцианид (0,7 г; 0,96 мл; 7,22 ммоль; 1,2 экв.) при комнатной температуре. Смесь перемешивали в течение 17 часов при 75°С. Реакционную смесь экстрагировали насыщенным раствором NH4Cl и два раза этилацетатом. Органические слои экстрагировали водой и рассолом, сушили над сульфатом натрия и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом этилацетат : гептан от 0:100 до 50:50, получая желаемый (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]ацетонитрил (1,66 г; выход 57%) в виде желтого твердого вещества, MS: m/e = 487,5/489,5 (М+Н+).
Стадия 3: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]уксусная кислота
(2RS)-2-(6-Бром-1-оксо-изоиндолин-2-ил)-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]ацетонитрил (пример 8, стадия 2) (1,66 г; 3,4 ммоль) растворяли в 12 мл этанола. Добавляли KOH (2 М раствор в воде) (8,5 мл; 17 ммоль; 5 экв.) при комнатной температуре. Смесь перемешивали в течение 4 часов при 100°С. Реакционную смесь охлаждали до комнатной температуры и нейтрализовали до рН 5, используя 8 мл уксусной кислоты. Смесь экстрагировали два раза водой и два раза этилацетатом. Органические слои сушили над сульфатом натрия и упаривали досуха. Желаемую (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]уксусную кислоту (1,7 г; выход 78%; чистотой 80%) получали в виде светло-желтой пены, MS: m/e = 506,4/508,5 (М+Н+).
Стадия 4: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-2-[1-(2-триметилсилилэтокси метил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]ацетамид
Указанное в заголовке соединение получали в виде желтой пены, MS: m/e = 588,5/590,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 1, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]уксусной кислоты (пример 8, стадия 3) и тиазол-2-амина.
Стадия 5: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]ацетамид
Указанное в заголовке соединение получали в виде белого полутвердого вещества, MS: m/e = 626,7 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]ацетамида (пример 8, стадия 4) и 5-этинилпиридин-2-амина.
Стадия 6: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(1,4,5,6-тетрагидроциклопента[с]пиразол-3-ил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого полутвердого вещества, MS: m/e = 496,1 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 2, исходя из (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-2-[1-(2-триметилсилилэтоксиметил)-5,6-дигидро-4Н-циклопента[с]пиразол-3-ил]ацетамида (пример 8, стадия 5).
Пример 9
N-Метил-5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоксамид
Стадия 1: 5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоновая кислота
Указанное в заголовке соединение получали в виде светло-зеленого твердого вещества, MS: m/e = 495,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамида (пример 1, стадия 3) и 5-этинилпиколиновой кислоты.
Стадия 2: N-метил-5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоксамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 508,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 1, исходя из 5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоновой кислоты (пример 9, стадия 1) и метиламина.
Пример 10
(2RS)-2-[1-Оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида гидрохлорид
Стадия 1: трет-бутил-4-(4-этинилбензил)пиперазин-1-карбоксилат
4-Этинилбензальдегид (400 мг; 3,07 ммоль) растворяли в 15 мл DCM. Добавляли трет-бутил-пиперазин-1-карбоксилат (687 мг; 3,7 ммоль; 1,2 экв.) и триацетоксигидроборат натрия (780 мг; 3,7 ммоль; 1,2 экв.) при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь экстрагировали водой и два раза DCM. Органические слои экстрагировали рассолом, сушили над сульфатом натрия и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом этилацетат : гептан от 0:100 до 50:50, получая желаемый трет-бутил-4-(4-этинилбензил)пиперазин-1-карбоксилат (670 мг; выход 73%) в виде бесцветного масла, MS: m/e = 301,5 (М+Н+).
Стадия 2: трет-бутил-4-[[4-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]фенил]метил]пиперазин-1-карбоксилат
Указанное в заголовке соединение получали в виде оранжевого твердого вещества, MS: m/e = 648,9 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамида (пример 1, стадия 3) и трет-бутил-4-(4-этинилбензил)пиперазин-1-карбоксилата (пример 10, стадия 1).
Стадия 3: (2RS)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида гидрохлорид
Указанное в заголовке соединение получали в виде светло-коричневого твердого вещества, MS: m/e = 546,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 2, исходя из трет-бутил-4-[[4-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]фенил]метил]пиперазин-1-карбоксилата (пример 10, стадия 2).
Пример 11
(2RS)-2-[6-[2-[4-(Морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Стадия 1: (2RS)-2-[6-[2-(4-формилфенил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде оранжевого твердого вещества, MS: m/e = 478,6 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(6-иод-1-оксо-изоиндолин-2-ил)-2-фенил-N-тиазол-2-ил-ацетамида (пример 1, стадия 3) и 4-этинилбензальдегида.
Стадия 2: (2RS)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 549,7 (М+Н+), используя химические реакции, аналогичные описанным в примере 10 на стадии 1, исходя из (2RS)-2-[6-[2-(4-формилфенил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида (пример 11, стадия 1) и морфолина.
Пример 12
(2RS)-2-[6-[2-[4-[(4-Ацетилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 588,6 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 1, исходя из (2RS)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида гидрохлорида (пример 10) и уксусной кислоты.
Пример 13
(2RS)-2-[6-[2-[4-[(4-Этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
(2RS)-2-[1-Оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида гидрохлорид (пример 10) (30 мг; 0,05 ммоль) растворяли в 1 мл ацетонитрила. Добавляли карбонат калия (57 мг; 0,41 ммоль; 8 экв.) и иодэтан (9,6 мг; 0,06 ммоль; 1,2 экв.) при комнатной температуре. Смесь перемешивали при 65°С в течение 4 часов. Реакционную смесь экстрагировали водой и два раза DCM. Органические слои экстрагировали рассолом, сушили над сульфатом натрия и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом дихлорметан : метанол от 100:0 до 85:15, получая желаемый (2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид (13 мг; выход 44%) в виде бесцветного твердого вещества, MS: m/e = 576,8 (М+Н+).
Пример 14
(2RS)-2-[6-[2-[6-(Морфолин-4-карбонил)-3-пиридил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 564,6 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 1, исходя из 5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоновой кислоты (пример 9, стадия 1) и морфолина.
Пример 15
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Стадия 1: трет-бутил-[(1RS)-1-(5-фтор-2-метоксифенил)-2-оксо-2-(тиазол-2-иламино)этил]карбамат
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 382,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 1, исходя из (2RS)-2-((трет-бутоксикарбонил)амино)-2-(5-фтор-2-метоксифенил)уксусной кислоты.
Стадия 2: (2RS)-2-амино-2-(5-фтор-2-метоксифенил)-N-(тиазол-2-ил)ацетамида гидрохлорид
Указанное в заголовке соединение получали в виде светло-зеленого твердого вещества, MS: m/e = 282,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 2, исходя из трет-бутил-[(1RS)-1-(5-фтор-2-метоксифенил)-2-оксо-2-(тиазол-2-иламино)этил]карбамата (пример 15, стадия 1).
Стадия 3: (2RS)-2-(5-фтор-2-метоксифенил)-2-(6-иод-1-оксоизоиндолин-2-ил)-N-(тиазол-2-ил)ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 524,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 3, исходя из (2RS)-2-амино-2-(5-фтор-2-метоксифенил)-N-(тиазол-2-ил)ацетамида гидрохлорида (пример 15, стадия 2) и метил-2-(бромметил)-5-иодбензоата.
Стадия 4: (2RS)-2-(6-((6-аминопиридин-3-ил)этинил)-1-оксоизоиндолин-2-ил)-2-(5-фтор-2-метоксифенил)-N-(тиазол-2-ил)ацетамид
Указанное в заголовке соединение получали в виде светло-желтого масла, MS: m/e = 514,6 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-(5-фтор-2-метоксифенил)-2-(6-иод-1-оксоизоиндолин-2-ил)-N-(тиазол-2-ил)ацетамида (пример 15, стадия 3) и 5-этинилпиридин-2-амина.
Стадия 5: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-аиетамид
(2RS)-2-(6-((6-Аминопиридин-3-ил)этинил)-1-оксоизоиндолин-2-ил)-2-(5-фтор-2-метоксифенил)-N-(тиазол-2-ил)ацетамид (пример 15, стадия 4) (80 мг; 0,16 ммоль) растворяли в 2,5 мл дихлорметана. Добавляли BBr3 (1 М раствор в дихлорметане) (0,62 мл; 0,62 ммоль; 4 экв.) при комнатной температуре. Смесь перемешивали при 25°С в течение 1 часа. Реакционную смесь гасили водой (56 мг; 3,1 ммоль; 20 экв.) и раствор неочищенного продукта очищали непосредственно флэш-хроматографией на колонке с силикагелем с элюированием градиентом дихлорметан : метанол от 100:0 до 80:20, получая желаемый (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид (56 мг; выход 72%) в виде светло-желтого твердого вещества, MS: m/e = 500,0 (М+Н+).
Пример 16
(2RS)-2-(5-Фтор-2-гидрокси-фенил)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Стадия 1: метил-(2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)ацетат
6-Бромизоиндолин-1-он (CAS 675109-26-9) (1,61 г; 7,58 ммоль; 1,05 экв.) суспендировали в 32 мл THF и охлаждали до 0-5°С. Добавляли гидрид натрия (60%-ную дисперсию в минеральном масле) (318 мг; 7,94 ммоль; 1,1 экв.) при 0-5°С. Реакционную смесь перемешивали при комнатной температуре в течение 15 минут и затем охлаждали до 0-5°С. По каплям добавляли метил-(2RS)-2-бром-2-(5-фтор-2-метоксифенил)ацетат (CAS 1368458-30-3) (2,00 г; 7,22 ммоль), растворенный в 8,0 мл THF, при 0-5°С. По завершении добавления ледяную баню удаляли и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь гасили насыщенным раствором NH4Cl и экстрагировали этилацетатом. Водный слой повторно экстрагировали этилацетатом. Органические слои промывали водой и рассолом. Органические слои объединяли, сушили над сульфатом натрия, фильтровали и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом этилацетат : гептан от 0:100 до 50:0, получая желаемый метил-(2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)ацетат (2,202 г; выход 75%) в виде желтой пены, MS: m/e = 408,0/410,0 (М+Н+).
Стадия 2: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)уксусная кислота
Метил-(2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)ацетат (пример 16, стадия 1) (2,200 г; 5,39 ммоль) растворяли в 10 мл THF и 10 мл метанола. Добавляли гидроксид лития моногидрат (678 мг; 16,2 ммоль; 3 экв.), затем 10 мл воды и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Органические растворители удаляли при пониженном давлении. Водный остаток подкисляли 5%-ным раствором лимонной кислоты и затем экстрагировали этилацетатом. Водный слой повторно экстрагировали этилацетатом. Органические слои промывали водой и рассолом. Органические слои объединяли, сушили над сульфатом натрия, фильтровали и упаривали досуха. Желаемую (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)уксусную кислоту (2,056 г; выход 97%) получали в виде желтого твердого вещества, MS: m/e = 394,1/396,1 (М+Н+).
Стадия 3: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид
(2RS)-2-(6-Бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)уксусную кислоту (пример 16, стадия 2) (2,050 г; 5,2 ммоль) и тиазол-2-амин (651 мг; 6,5 ммоль; 1,3 экв.) растворяли в 13 мл DMF. Добавляли основание Хюнига (2,81 г; 3,8 мл; 21,8 ммоль; 4,2 экв.), затем TBTU (2 г; 6,24 ммоль; 1,2 экв.). Реакционную смесь перемешивали при комнатной температуре в течение 4 суток. Реакционную смесь разбавляли водой (образовывался осадок). Суспензию охлаждали до 0-5°С и перемешивали в течение 30 минут. Охлажденную суспензию фильтровали, промывали водой и этилацетатом в минимальном количестве. Полученное беловатое твердое вещество сушили с использованием роторного вакуумного испарителя и затем помещали под высокий вакуум, получая (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид (2,210 г; выход 89%), MS: m/e = 476,0/478,0 (М+Н+).
Стадия 4: (2RS)-2-(5-фтор-2-метокси-фенил)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
(2RS)-2-(6-Бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид (пример 16, стадия 3) (110 мг; 0,231 ммоль) растворяли в 2,3 мл DMF, добавляли 3-этинилпиридин (35 мг; 0,339 ммоль; 1,5 экв.), триэтиламин (72,6 мг; 0,10 мл; 0,717 ммоль; 3,1 экв.), трифенилфосфин (6 мг; 0,023 ммоль; 0,10 экв.), дихлорид бис(трифенилфосфин)палладия(II) (8 мг; 0,0114 ммоль; 0,05 экв.) и иодид меди(I) (2 мг; 0,0105 ммоль; 0,05 экв.) и реакционную смесь перемешивали при 90°С в течение 6 часов. Реакционную смесь охлаждали до комнатной температуры и экстрагировали этилацетатом и водой. Водный слой повторно дважды экстрагировали этилацетатом. Органические слои промывали четыре раза водой и один раз рассолом. Органические слои объединяли, сушили над сульфатом натрия, фильтровали и упаривали досуха. Неочищенный продукт адсорбировали на Isolute® и очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом дихлорметан : метанол от 100:0 до 95:5, получая желаемый (2RS)-2-(5-фтор-2-метокси-фенил)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид (61 мг; выход 53%) в виде светло-желтого твердого вещества, MS: m/e = 499,2 (М+Н+).
Стадия 5: (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде беловатого твердого вещества, MS: m/e = 485,1 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 16, стадия 4).
Пример 17
(2RS)-2-(5-Фтор-2-гидрокси-фенил)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Стадия 1: (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-(6-иод-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде беловатого твердого вещества, MS: m/e = 510,0 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-(6-иод-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-ацетамида (пример 15, стадия 3).
Стадия 2: (2RS)-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-2-(6-иод-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-ацетамид
(2RS)-2-(5-Фтор-2-гидрокси-фенил)-2-(6-иод-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-ацетамид (пример 17, стадия 1) (315 мг; 0,619 ммоль) растворяли в 2,0 мл DMF. Добавляли трет-бутилдиметилхлорсилан (103 мг; 0,680 ммоль; 1,1 экв.), затем имидазол (50 мг; 0,734 ммоль; 1,2 экв.). Реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Добавляли дополнительно трет-бутилдиметилхлорсилан (34 мг; 0,226 ммоль; 0,365 экв.), затем имидазол (17 мг; 0,250 ммоль; 0,404 экв.). Реакционную смесь перемешивали при комнатной температуре в течение 5 часов. Реакционную смесь экстрагировали МТВЕ (метил-трет-бутиловый эфир) и водой. Водный слой повторно экстрагировали МТВЕ. Органические слои промывали три раза водой и один раз рассолом. Органические слои объединяли, сушили над сульфатом натрия, фильтровали и упаривали досуха. Неочищенный продукт адсорбировали на Isolute® и очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом этилацетат : гептан от 0:100 до 50:50, получая желаемый (2RS)-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-2-(6-иод-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-ацетамид (282 мг; выход 73%) в виде беловатого твердого вещества, MS: m/e = 624,3 (М+Н+).
Стадия 3: (2RS)-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде желтого твердого вещества, MS: m/e = 598,3 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-2-(6-иод-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-ацетамида (пример 17, стадия 2) и фенилацетилена.
Стадия 4: (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
(2RS)-2-[2-[трет-Бутил(диметил)силил]окси-5-фтор-фенил]-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид (пример 17, стадия 3) (45 мг; 0,075 ммоль) растворяли в 1,2 мл THF. Добавляли фторид тетрабутиламмония (1,0 М раствор в THF) (79 мкл; 0,079 ммоль; 1,05 экв.) при комнатной температуре и реакционную смесь перемешивали при комнатной температуре в течение 60 минут. Реакционную смесь экстрагировали этилацетатом и водой. Водный слой повторно экстрагировали этилацетатом. Органические слои промывали три раза водой и один раз рассолом. Органические слои объединяли, сушили над сульфатом натрия, фильтровали и упаривали досуха. Неочищенный продукт адсорбировали на Isolute® и очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом дихлорметан : метанол от 100:0 до 95:5, получая желаемый (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид (27 мг; выход 74%) в виде светло-желтого твердого вещества, MS: m/e = 484,2 (М+Н+).
Пример 18
(2RS)-2-[6-[2-(2-Аминопиримидин-5-ил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Стадия 1: (2RS)-2-[6-[2-(2-аминопиримидин-5-ил)этинил]-1-оксо-изоиндолин-2-ил]-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 615,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-2-(6-иод-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-ацетамида (пример 17, стадия 2) и 5-этинилпиримидин-2-амина (CAS 857265-74-8).
Стадия 2: (R2S)-2-[6-[2-(2-аминопиримидин-5-ил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде беловатого порошка, MS: m/e = 501,3 (М+Н+), используя химические реакции, аналогичные описанным в примере 17 на стадии 4, исходя из (2RS)-2-[6-[2-(2-аминопиримидин-5-ил)этинил]-1-оксо-изоиндолин-2-ил]-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-N-тиазол-2-ил-ацетамида (пример 18, стадия 1).
Пример 19
(2RS)-2-[6-[2-(2-Хлор-4-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Стадия 1: (2RS)-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-2-[6-[2-(2-хлор-4-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде желтого твердого вещества, MS: m/e = 633,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4, исходя из (2RS)-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-2-(6-иод-1-оксо-изоиндолин-2-ил)-N-тиазол-2-ил-ацетамида (пример 17, стадия 2) и 2-хлор-4-этинилпиридина (CAS 945717-09-9).
Стадия 2: (2RS)-2-[6-[2-(2-хлор-4-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде беловатого твердого вещества, MS: m/e = 519,1 (М+Н+), используя химические реакции, аналогичные описанным в примере 17 на стадии 4, исходя из ((2RS)-2-[2-[трет-бутил(диметил)силил]окси-5-фтор-фенил]-2-[6-[2-(2-хлор-4-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 19, стадия 1).
Пример 20
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-(2-пиридил)ацетамид
Стадия 1: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-(2-пиридил)ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 470,2/472,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 3, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)уксусной кислоты (пример 16, стадия 2) и пиридин-2-амина (CAS 504-29-0).
Стадия 2: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-метокси-фенил)-N-(2-пиридил)ацетамид
Указанное в заголовке соединение получали в виде беловатого твердого вещества, MS: m/e = 508,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-(2-пиридил)ацетамида (пример 20, стадия 1) и 5-этинилпиридин-2-амина (CAS 82454-61-3).
Стадия 3: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-(2-пиридил)ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 494,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-метокси-фенил)-N-(2-пиридил)ацетамида (пример 20, стадия 2).
Пример 21
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Стадия 1: метил-(2RS)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)ацетат
Указанное в заголовке соединение получали в виде желтой пены, MS: m/e = 422,0/424,0 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 1, исходя из метил-(2RS)-2-бром-2-(5-фтор-2-метоксифенил)ацетата (CAS 1368458-30-3) и 6-бром-7-метил-изоиндолин-1-она (CAS 1427394-72-6).
Стадия 2: (2RS)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)уксусная кислота
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 408,0/410,0 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 2, исходя из метил-(2RS)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)ацетата (пример 21, стадия 1).
Стадия 3: (2S)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде беловатого твердого вещества, MS: m/e = 490,0/492,0 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 3, исходя из (2RS)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)уксусной кислоты (пример 21, стадия 2) и тиазол-2-амина.
Стадия 4: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-коричневого твердого вещества, MS: m/e = 528,3 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 4, исходя из (2RS)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамида (пример 21, стадия 3) и 5-этинилпиридин-2-амина (CAS 82454-61-3).
Стадия 5: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 514,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамида (пример 21, стадия 4).
Пример 22
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-(2-пиридил)ацетамид
Стадия 1: (2RS)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-(2-пиридил)ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 484,2/486,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 3, исходя из (2RS)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)уксусной кислоты (пример 21, стадия 2) и пиридин-2-амина (CAS 504-29-0).
Стадия 2: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-метокси-фенил)-N-(2-пиридил)ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 522,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 4, исходя из (2RS)-2-(6-бром-7-метил-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-(2-пиридил)-ацетамида (пример 22, стадия 1) и 5-этинилпиридин-2-амина (CAS 82454-61-3).
Стадия 3: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-(2-пиридил)ацетамид
Указанное в заголовке соединение получали в виде беловатого твердого вещества, MS: m/e = 508,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-метокси-фенил)-N-(2-пиридил)ацетамида (пример 22, стадия 2).
Пример 23
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-хлор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Стадия 1: метил-(2RS)-2-бром-2-(5-хлор-2-метокси-фенил)ацетат
Метил-2-(5-хлор-2-метоксифенил)ацетат (CAS 26939-01-5) (1,14 г; 5,31 ммоль) растворяли в 20 мл α,α,α-трифтортолуола (CAS 98-08-08). Добавляли N-бромсукцинимид (1,13 г; 6,37 ммоль; 1,2 экв.), затем 2,2'-азобис(2-метилпропионитрил) (AIBN) (88 мг; 0,536 ммоль; 0,10 экв.). Реакционную смесь перемешивали при 110°С в течение 90 минут. Реакционную смесь охлаждали до комнатной температуры, адсорбировали на Isolute® и очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом этилацетат : гептан от 0:100 до 20:80, получая желаемый метил-(2RS)-2-бром-2-(5-хлор-2-метокси-фенил)ацетат (1,367 г; выход 88%) в виде светло-желтого масла, MS: m/e = 293,1/295,1 (М+Н+).
Стадия 2: метил-(2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-хлор-2-метокси-фенил)ацетат
Указанное в заголовке соединение получали в виде желтой пены, MS: m/e = 424,0/425,9 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 1, исходя из метил-(2RS)-2-бром-2-(5-хлор-2-метокси-фенил)ацетата (пример 23, стадия 1) и 6-бромизоиндолин-1-она (CAS 675109-26-9).
Стадия 3: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-хлор-2-метокси-фенил)уксусная кислота
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 409,9/411,9 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 2, исходя из метил-(2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-хлор-2-метокси-фенил)ацетата (пример 23, стадия 2).
Стадия 4: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-хлор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде беловатого твердого вещества, MS: m/e = 492,0/494,0 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 3, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-хлор-2-метокси-фенил)уксусной кислоты (пример 23, стадия 3) и тиазол-2-амина.
Стадия 5: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-хлор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде желтого твердого вещества, MS: m/e = 530,2/532,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-хлор-2-метокси-фенил)-N-тиазол-2-ил-ацетамида (пример 23, стадия 4) и 5-этинилпиридин-2-амина (CAS 82454-61-3).
Стадия 6: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-хлор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 516,2/518,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-хлор-2-метокси-фенил)-N-тиазол-2-ил-ацетамида (пример 23, стадия 5).
Пример 24
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2-гидроксифенил)-N-тиазол-2-ил-ацетамид
Стадия 1: трет-бутил-N-[(1RS)-1-(2-метоксифенил)-2-оксо-2-(тиазол-2-иламино)этил]карбамат
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 364,3 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 3, исходя из (2RS)-2-(трет-бутоксикарбониламино)-2-(2-метоксифенил)уксусной кислоты (CAS 179417-69-7) и тиазол-2-амина.
Стадия 2: (2RS)-2-амино-2-(2-метоксифенил)-N-тиазол-2-ил-ацетамида гидрохлорид
трет-Бутил-N-[(1RS)-1-(2-метоксифенил)-2-оксо-2-(тиазол-2-иламино)этил]карбамат (пример 24, стадия 1) (190 мг; 0,523 ммоль) растворяли в 2 мл дихлорметана и добавляли HCl (4 н. раствор в диоксане) (1,31 мл; 5,23 ммоль; 10 экв.) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь упаривали досуха и использовали непосредственно на следующей стадии. Желаемый (2RS)-2-амино-2-(2-метоксифенил)-N-тиазол-2-ил-ацетамида гидрохлорид (количественный выход) получали в виде белого твердого вещества, MS: m/e = 264,3 (М+Н+).
Стадия 3: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(2-метоксифенил)-N-тиазол-2-ил-ацетамид
(2RS)-2-Амино-2-(2-метоксифенил)-N-тиазол-2-ил-ацетамида гидрохлорид (пример 24, стадия 2) (160 мг; 0,534 ммоль) растворяли в 3 мл DMF. Добавляли метил-5-бром-2-(бромметил)бензоат (CAS 79670-17-0) (197 мг; 0,640 ммоль; 1,2 экв.) и триэтиламин (270 мг; 0,37 мл; 2,67 ммоль; 5 экв.) при комнатной температуре. Реакционную смесь перемешивали при 80°С в течение 16 часов. Реакционную смесь экстрагировали водой и два раза этилацетатом. Органические слои промывали водой и рассолом, сушили над сульфатом натрия и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем с элюированием градиентом дихлорметан : метанол от 100:0 до 90:10, получая желаемый (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(2-метоксифенил)-N-тиазол-2-ил-ацетамид (140 мг; выход 57%) в виде светло-желтого твердого вещества, MS: m/e = 458,3/460,3 (М+Н+).
Стадия 4: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2-метоксифенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 496,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(2-метоксифенил)-N-тиазол-2-ил-ацетамида (пример 24, стадия 3) и 5-этинилпиридин-2-амина (CAS 82454-61-3).
Стадия 5: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2-гидроксифенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 482,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2-метоксифенил)-N-тиазол-2-ил-ацетамида (пример 24, стадия 4).
Пример 25
(2RS)-2-[6-[2-(6-Амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-гидрокси-2-пиридил)-N-тиазол-2-ил-ацетамида трифторацетат
Стадия 1: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(3-метокси-2-пиридил)ацетонитрил
Указанное в заголовке соединение получали в виде светло-красного твердого вещества, MS: m/e = 357,9/359,9 (М+Н+), используя химические реакции, аналогичные описанным в примере 8 на стадии 2, исходя из 3-метоксипиколинальдегида и метил-2-(аминометил)-5-бромбензоата гидрохлорида.
Стадия 2: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(3-метокси-2-пиридил)ацетат натрия
Указанное в заголовке соединение получали в виде желтого твердого вещества, MS: m/e = 376,9/378,9 (М+Н+), используя химические реакции, аналогичные описанным в примере 8 на стадии 3, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(3-метокси-2-пиридил)ацетонитрила (пример 25, стадия 1) и используя гидроксид натрия вместо гидроксида калия.
Стадия 3: (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(3-метокси-2-пиридил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде беловатого твердого вещества, MS: m/e = 458,9/460,9 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 3, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(3-метокси-2-пиридил)ацетата натрия (пример 25, стадия 2) и тиазол-2-амина.
Стадия 4: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-метокси-2-пиридил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-коричневого твердого вещества, MS: m/e = 495,1 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(3-метокси-2-пиридил)-N-тиазол-2-ил-ацетамида (пример 25, стадия 3) и 5-этинилпиридин-2-амина (CAS 82454-61-3).
Стадия 5: (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-гидрокси-2-пиридил)-N-тиазол-2-ил-ацетамида трифторацетат
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 481,3 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-метокси-2-пиридил)-N-тиазол-2-ил-ацетамида (пример 25, стадия 4) и очищая обращенно-фазовой хроматографией (колонка С18, от 10% до 90% ацетонитрила в воде + 0,1% трифторуксусной кислоты).
Пример 26
(2RS)-2-(5-Фтор-2-гидрокси-фенил)-2-[7-фтор-1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Стадия 1: этил-3-бром-6-(бромметил)-2-фторбензоат
Указанное в заголовке соединение получали в виде бесцветного масла, используя химические реакции, аналогичные описанным в примере 23 на стадии 1, исходя из этил-3-бром-2-фтор-6-метилбензоата и используя метилацетат в качестве растворителя.
Стадия 2: (2RS)-2-(6-бром-7-фтор-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 494,1/496,1 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 3, исходя из (2RS)-2-амино-2-(5-фтор-2-метоксифенил)-N-(тиазол-2-ил)ацетамида гидрохлорида (пример 15, стадия 2) и этил-3-бром-6-(бромметил)-2-фторбензоата (пример 26, стадия 1).
Стадия 3: (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[7-фтор-1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 503,2 (М+Н+), используя химические реакции, аналогичные описанным в примере 1 на стадии 4 и примере 15 на стадии 5, исходя из (2RS)-2-(6-бром-7-фтор-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамида (пример 26, стадия 2) и 3-этинилпиридина.
Пример 27
(2RS)-2-(5-Фтор-2-гидрокси-фенил)-2-[6-[2-[4-(морфолинометил)фенил]-этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Стадия 1: (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-(4-формилфенил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-коричневого твердого вещества, MS: m/e = 526,3 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамида (пример 16, стадия 3) и 4-этинилбензальдегида (CAS 63697-96-1).
Стадия 2: (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белой пены, MS: m/e = 597,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 10 на стадии 1, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-(4-формилфенил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 27, стадия 1) и морфолина.
Стадия 3: (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 583,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 27, стадия 2).
Пример 28
(2RS)-2-(5-Фтор-2-гидрокси-фенил)-2-[6-[2-[4-[(4-гидрокси-1-пиперидил)-метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Стадия 1: (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-[4-[(4-гидрокси-1-пиперидил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид Указанное в заголовке соединение получали в виде белой пены, MS: m/e = 611,5 (М+Н+), используя химические реакции, аналогичные описанным в примере 10 на стадии 1, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-(4-формилфенил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 27, стадия 1) и пиперидин-4-ола (CAS 5382-16-1).
Стадия 2: (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-[(4-гидрокси-1-пиперидил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 597,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-[4-[(4-гидрокси-1-пиперидил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 28, стадия 1).
Пример 29
(2RS)-2-(5-Фтор-2-гидрокси-фенил)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Стадия 1: трет-бутил-4-[[4-[2-[3-оксо-2-[(1RS)-1-(5-фтор-2-метокси-фенил)-2-оксо-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]фенил]метил]пиперазин-1-карбоксилат
Указанное в заголовке соединение получали в виде беловатой пены, MS: m/e = 696,7 (М+Н+), используя химические реакции, аналогичные описанным в примере 16 на стадии 4, исходя из (2RS)-2-(6-бром-1-оксо-изоиндолин-2-ил)-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамида (пример 16, стадия 3) и трет-бутил-4-[(4-этинилфенил)метил]пиперазин-1-карбоксилата (пример 10, стадия 1).
Стадия 2: (2RS)-2-(5-фтор-2-метокси-фенил)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
трет-Бутил-4-[[4-[2-[3-оксо-2-[(1RS)-1-(5-фтор-2-метокси-фенил)-2-оксо-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]фенил]метил]пиперазин-1-карбоксилат (пример 29, стадия 1) (248 мг; 0,356 ммоль) объединяли с 9 мл метанола. Добавляли HCl (4 н. раствор в диоксане) (891 мкл; 3,56 ммоль; 10 экв.). Реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь упаривали досуха. Остаток разбавляли водой, выливали в насыщенный раствор NaHCO3 и три раза экстрагировали смесью дихлорметан:метанол (9:1). Органические слои объединяли, сушили над сульфатом натрия, фильтровали и упаривали досуха, получая желаемый (2RS)-2-(5-фтор-2-метокси-фенил)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид (количественный выход) в виде беловатой пены, MS: m/e = 596,5 (М+Н+).
Стадия 3: (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 582,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 29, стадия 2).
Пример 30
(2RS)-2-(5-Фтор-2-гидрокси-фенил)-2-[6-[2-[4-[(4-метилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Стадия 1: (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-[4-[(4-метилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде оранжевого твердого вещества, MS: m/e = 610,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 10 на стадии 1, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-(4-формилфенил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 27, стадия 1) и 1-метилпиперазина (CAS 109-01-3).
Стадия 2: (2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-[(4-метилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 596,3 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-[4-[(4-метилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 30, стадия 1).
Пример 31
(2RS)-2-[6-[2-[4-[(4-Этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Стадия 1: (2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде светло-желтого твердого вещества, MS: m/e = 624,4 (М+Н+), используя химические реакции, аналогичные описанным в примере 10 на стадии 1, исходя из (2RS)-2-(5-фтор-2-метокси-фенил)-2-[6-[2-(4-формилфенил)этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида (пример 27, стадия 1) и 1-этилпиперазина (CAS 5308-25-8).
Стадия 2: (2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамид
Указанное в заголовке соединение получали в виде белого твердого вещества, MS: m/e = 610,3 (М+Н+), используя химические реакции, аналогичные описанным в примере 15 на стадии 5, исходя из (2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-метокси-фенил)-N-тиазол-2-ил-ацетамида (пример 31, стадия 1).
Источники информации
1. Yarden, Y., Sliwkowski, MX. Untangling the ErbB signalling network. Nature Review Mol Cell Biol. 2001 Feb, 2(2): 127-37.
2. Ciardiello, F., and Tortora, G. (2008). EGFR antagonists in cancer treatment. The New England journal of medicine, 358, 1160-1174.
3. Paez, J. et al. (2004). EGFR mutations in lung cancer: correlation with clinical response to gefitinib therapy. Science, New York, NY, 304, 1497-1500.
4. Sharma SV, Bell DW, Settleman J, Haber DA. Epidermal growth factor receptor mutations in lung cancer. Nat. Rev. Cancer, 2007 Mar, 7(3): 169-81.
5. Thress, K.S. et al. Acquired EGFR C797S mutation mediates resistance to AZD9291 in non-small cell lung cancer harboring EGFR T790M. Nat. Med., 21, 560-562 (2015).
6. Wang et al. EGFR C797S mutation mediates resistance to third-generation inhibitors in T790M-positive non-small cell lung cancer. J. Hematol. Oncol., 2016, 9: 59.
7. Yang et al. Investigating Novel Resistance Mechanisms to Third-Generation EGFR Tyrosine Kinase Inhibitor Osimertinib in Non-Small Cell Lung Cancer Patients, Clinical Cancer Research, DOI: 10.1158/1078-0432.CCR-17-2310.
8. Jia et al. Overcoming EGFR(T790M) and EGFR(C797S) resistance with mutant-selective allosteric inhibitors. June 2016, Nature, 534, 129-132.
9. WO 2009158369.
10. WO 2016183534.
11. Biochem. Pharmacol. (1973) 22: 3099.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ | 2019 |
|
RU2800278C2 |
| ПИРИДИЛПИРИДОНЫ | 2018 |
|
RU2805334C2 |
| ПРОИЗВОДНЫЕ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБЫ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ И ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2001 |
|
RU2265011C2 |
| БИАРИЛЬНЫЕ МОНОБАКТАМНЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2016 |
|
RU2746129C2 |
| Новые соединения | 2016 |
|
RU2734256C2 |
| ИНГИБИТОР, ПРЕДСТАВЛЯЮЩИЙ СОБОЙ ПРОИЗВОДНОЕ ПИРИДАЗИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2807611C2 |
| НОВЫЕ 3,4-ДИГИДРО-2Н-ИЗОХИНОЛИН-1-ОНЫ И 2,3-ДИГИДРО-ИЗОИНДОЛ-1-ОНЫ | 2014 |
|
RU2689421C2 |
| СОЕДИНЕНИЯ БЕНЗАЗЕПИНА ДИКАРБОКСАМИДА | 2016 |
|
RU2712248C2 |
| 2, 5-ДИОКСОИМИДАЗОЛИДИН-4-ИЛ-МЕТИЛКАРБОНИЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ В ИЗГОТОВЛЕНИИ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2003 |
|
RU2326117C2 |
| Спироконденсированные пирролидиновые производные в качестве ингибиторов деубиквитилирующих ферментов (DUB) | 2017 |
|
RU2730552C2 |
Изобретение относится к соединениям, которые представляют собой селективные аллостерические ингибиторы TMLR-, TMLRCS-, LR-, LRCS-содержащих мутантов EGFR - рецептор эпидермального фактора роста, фармацевтическим композициям, содержащим их, и их применению в качестве терапевтически активных веществ для лечения немелкоклеточного рака легкого. 4 н. и 11 з.п. ф-лы, 31 пр., 8 табл.
1. Соединение формулы I,
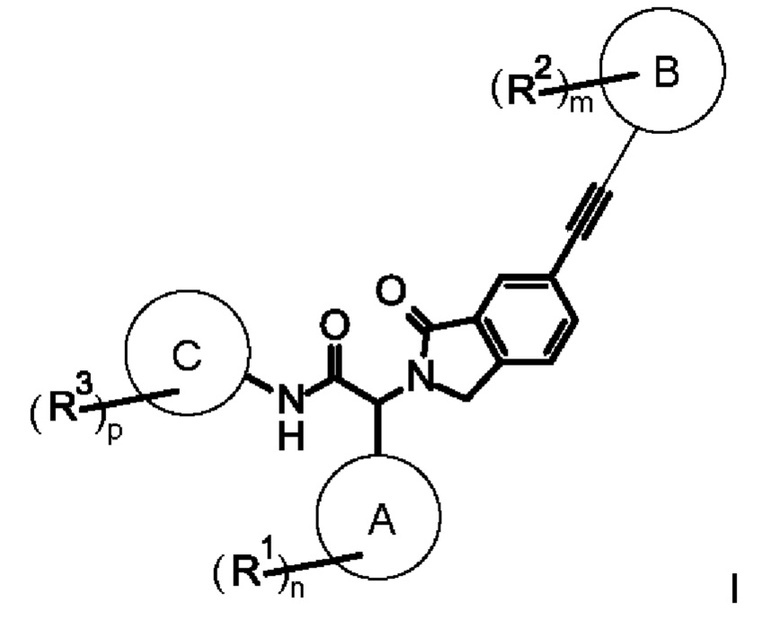
где
А представляет собой моноарил, содержащий 6-10 атомов углерода в кольце, или гетероарил, содержащий одиночное 4-8-членное кольцо и 1 гетероатом азота или несколько конденсированных колец, содержащих 6-14 атомов углерода в кольце и 2 гетероатома азота;
В представляет собой моноарил, содержащий 6-10 атомов углерода в кольце, или гетероарил, содержащий одиночное 4-8-членное кольцо и 1, 2 гетероатома азота;
С представляет собой гетероарил, содержащий одиночное 4-8-членное кольцо и 1, 2 гетероатома, выбранных из азота и серы;
R1 каждый независимо выбран из группы, состоящей из
i) галогена,
ii) гидрокси;
R2 каждый независимо выбран из группы, состоящей из
i) -(CH2)k-N(R4,R5),
ii) -(C=O)-N(R4,R5),
iii) галогена,
iv) -NH-(С=O)-С1.6-алкила;
R4 каждый независимо представляет собой Н;
R5 каждый независимо выбран из группы, состоящей из
i) Н,
ii) С1-6-алкила;
или R4 и R5 вместе с атомом N, к которому они присоединены, образуют насыщенный моногетероциклил, содержащий 4-9 атомов в кольце, где 1, 2 гетероатома выбраны из азота и кислорода, остальные атомы в кольце представляют собой атом углерода, при этом насыщенный моногетероциклил возможно замещен группой R6;
R6 каждый независимо выбран из группы, состоящей из
i) -ОН,
ii) С1-6-алкила и
iii) -(С=O)-С1-6-алкила;
k равно 0, 1,
n равно 0, 1, 2; m равно 0, 1;
р равно 0;
или его фармацевтически приемлемая соль.
2. Соединение формулы I или его фармацевтически приемлемая соль по п. 1, где А представляет собой моноарил, содержащий 6-10 атомов углерода в кольце, в частности фенил.
3. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1, 2, где В представляет собой моноарил, содержащий 6-10 атомов углерода в кольце, в частности фенил.
4. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-3, где В представляет собой гетероарил, содержащий одиночное 4-8-членное кольцо и 1, 2 гетероатома азота, в частности пиридинил.
5. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-4, где С представляет собой гетероарил, содержащий одиночное 4-8-членное кольцо и 1, 2 гетероатома, выбранных из азота и серы, в частности тиазолил.
6. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-5, где n равно 0, 1 или 2, в частности 0 или 2, более конкретно 2.
7. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-6, где m равно 1.
8. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-7, где R2 представляет собой -(С=O)-морфолинил, -(C=O)N(H,CH3), -СН2-(4-метилпиперазинил), -СН2-(4-ацетилпиперазинил), -СН2-(4-этилпиперазинил), -СН2-(4-гидрокси-пиперидил), -СН2-(морфолинил), -CH2NH2, -СН2-пиперазинил, Cl, -N(H,C=OCH3) или -NH2, в частности -С=O-морфолинил, -(C=O)N(H,CH3), -СН2-(4-ацетилпиперазинил), -СН2-(4-этилпиперазинил), -СН2-морфолинил, -CH2-NH2, -СН2-пиперазинил, -N(H, (C=O)CH3) или -NH2.
9. Соединение формулы I или его фармацевтически приемлемая соль, выбранные из группы, состоящей из:
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-[(4-гидрокси-1-пиперидил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[6-[2-[4-[(4-метилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-(5-фтор-2-гидрокси-фенил)-2-[7-фтор-1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-(2-фенилэтинил)изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-[2-(3-пиридил)этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[1-оксо-6-[2-[4-(пиперазин-1-илметил)фенил]этинил]изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(2-аминопиримидин-5-ил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(2-хлор-4-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-ацетамидо-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-фторфенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2,5-дифторфенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(1,4,5,6-тетрагидроциклопента[с]пиразол-3-ил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-(2-пиридил)ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(5-хлор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(2-гидроксифенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-1-оксо-изоиндолин-2-ил]-2-(3-гидрокси-2-пиридил)-N-тиазол-2-ил-ацетамида трифторацетата,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-(6-амино-3-пиридил)этинил]-7-метил-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-(2-пиридил)ацетамида,
(2RS)-2-[6-[2-[4-(аминометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-(морфолинометил)фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-ацетилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[4-[(4-этилпиперазин-1-ил)метил]фенил]этинил]-1-оксо-изоиндолин-2-ил]-2-(5-фтор-2-гидрокси-фенил)-N-тиазол-2-ил-ацетамида,
(2RS)-2-[6-[2-[6-(морфолин-4-карбонил)-3-пиридил]этинил]-1-оксо-изоиндолин-2-ил]-2-фенил-N-тиазол-2-ил-ацетамида и
N-метил-5-[2-[3-оксо-2-[(1RS)-2-оксо-1-фенил-2-(тиазол-2-иламино)этил]изоиндолин-5-ил]этинил]пиридин-2-карбоксамида.
10. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-9 для применения в качестве терапевтически активного вещества.
11. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-9 для применения при терапевтическом и/или профилактическом лечении рака, в частности немелкоклеточного рака легкого.
12. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-9 для применения при изготовлении лекарственного средства для терапевтического и/или профилактического лечения рака, в частности немелкоклеточного рака легкого.
13. Фармацевтическая композиция для лечения немелкоклеточного рака легкого, содержащая соединение формулы I или его фармацевтически приемлемую соль по любому из пп. 1-9 в эффективном количестве и фармацевтически приемлемое вспомогательное вещество.
14. Способ терапевтического и/или профилактического лечения немелкоклеточного рака легкого путем введения пациенту соединения формулы I или его фармацевтически приемлемой соли по любому из пп. 1-9.
15. Соединение формулы I или его фармацевтически приемлемая соль по любому из пп. 1-9 для применения в качестве лекарственного средства при терапевтическом и/или профилактическом лечении пациента с активирующими EGFR мутациями, страдающего от рака, в частности немелкоклеточного рака легкого, включающего определение статуса EGFR-активирующих мутаций у указанного пациента и затем введение указанному пациенту соединения формулы I или его фармацевтически приемлемой соли по любому из пп. 1-9.
| WO 2016183534 A1, 17.11.2016 | |||
| WO 2009158369 A1, 30.12.2009 | |||
| EA 201491727 A1, 30.01.2015 | |||
| Беликов В.Г | |||
| "Фармацевтическая химия" | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| - М.: МЕДпресс-информ, 2007, с | |||
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| интернет-источник | |||
Авторы
Даты
2022-06-24—Публикация
2018-06-01—Подача