ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к фармацевтическим составам, к способам их получения и к их применению для лечения и профилактики заболеваний у млекопитающих, в частности, у человека.
УРОВЕНЬ ТЕХНИКИ, К КОТОРОМУ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Фармацевтические дозированные формы, которые быстро растворяются, когда их помещают в полость рта пациента, тем самым доставляя желаемую дозу фармацевтически активных веществ, являются особенно пригодными, когда дозированная форма может быть принята без воды. Такие дозированные формы обычно являются предпочтительными для детей и пожилых людей, а также для людей с затрудненным глотанием и/или приемом таблеток или капсул.
Быстро растворяющиеся дозированные формы обычно получают с использованием многостадийного процесса. В некоторых из этих процессов используется стадия лиофилизации, в ходе которой растворитель удаляют из раствора и/или суспензии, содержащей фармацевтически активное вещество, материал носителя и растворитель.
Фармацевтические составы, изготавливаемые посредством лиофилизации, имеют различные преимущества, а также различные проблемы, такие как проблемы свободной текучести, впитывания влаги, горького вкуса, единообразия дозы и единообразия содержимого. Настоящее изобретение нацелено на преодоление этих проблем.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новой композиции смеси сорбита и вазелинового масла для применения для улучшения свойств фармацевтических составов по нескольким параметрам, т.е. свойствам текучести, защите от влаги, антистатическим свойствам и прессуемости (индекс Карра). Композиция смеси также может содержать лимонную кислоту и обладает способностью смягчать вкус горьких лекарственных средств.
Таким образом, настоящее изобретение относится к свободнотекучему твердому фармацевтическому составу, содержащему один или несколько активных ингредиентов и композицию смеси, содержащую или состоящую из сорбита, вазелинового масла и необязательно лимонной кислоты.
Кроме того, настоящее изобретение относится к смеси, содержащей или состоящей из сорбита, вазелинового масла и необязательно лимонной кислоты, для применения для изготовления фармацевтического состава, содержащего один или несколько активных ингредиентов.
Настоящее изобретение также относится к способам изготовления твердого фармацевтического состава по изобретению, включающим:
(a) получение лиофилизированного порошка путем возгонки растворителя из препарата, содержащего один или несколько активных ингредиентов и растворитель;
(b) получение композиции смеси, содержащей или состоящей из сорбита, вазелинового масла и необязательно лимонной кислоты;
(c) смешение композиции смеси, полученной на стадии (b), с лиофилизированным порошком, полученным на стадии (a).
ЧЕРТЕЖИ
На фиг.1 сравнивается коэффициент прессуемости (индекс Карра) составов согласно примеру 1 и сравнительным примерам A-E.
На фиг.2 сравнивается отношение Хауснера для составов согласно примеру 1 и сравнительным примерам A-E.
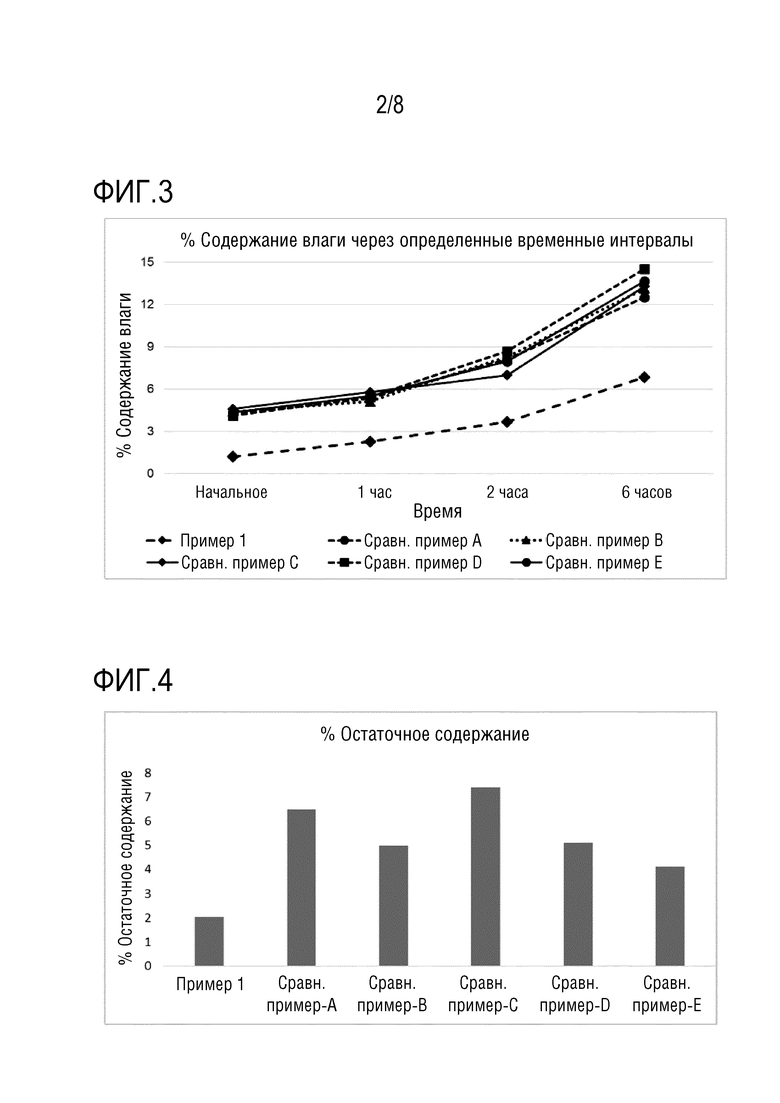
На фиг.3 представлено % содержание влаги в составах согласно примеру 1 и сравнительным примерам A-E в зависимости от времени хранения.
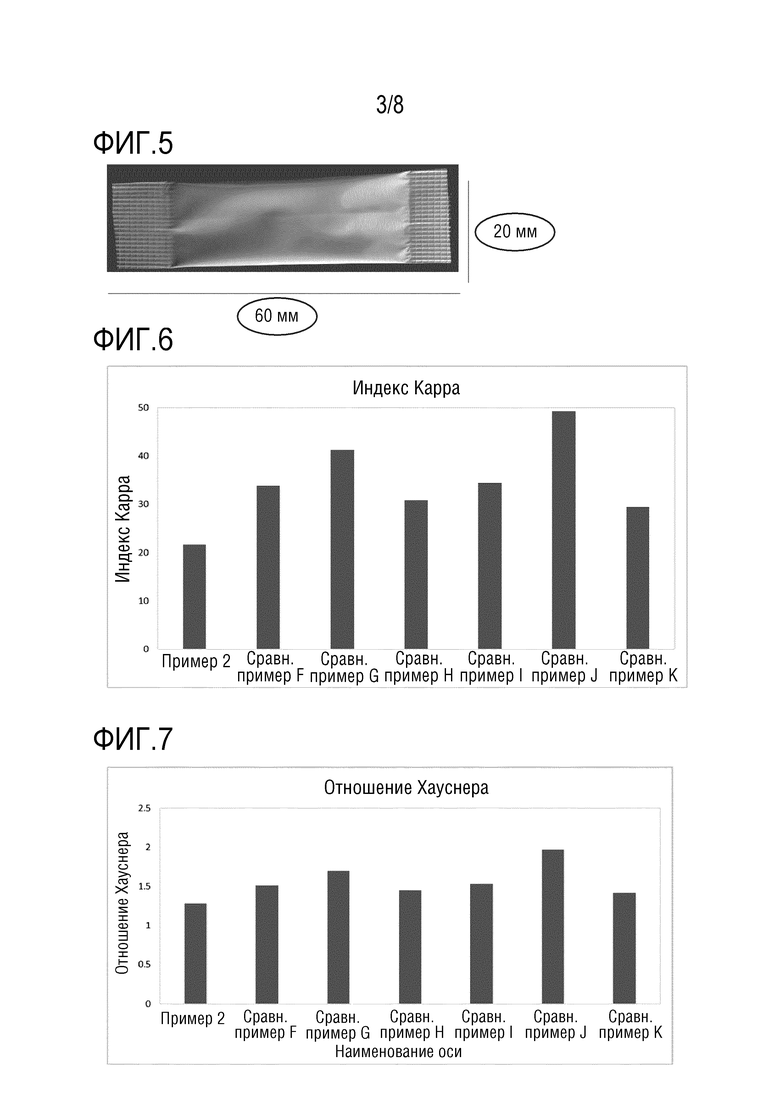
На фиг.4 сравнивается % остаточное содержание составов согласно примеру 1 и сравнительным примерам A-E.
На фиг.5 представлена фотография стик-пакета по изобретению.
На фиг.6 сравнивается коэффициент прессуемости (индекс Карра) составов согласно примеру 2 и сравнительным примерам F-K.
На фиг.7 сравнивается отношение Хауснера для составов согласно примеру 2 и сравнительным примерам F-K.
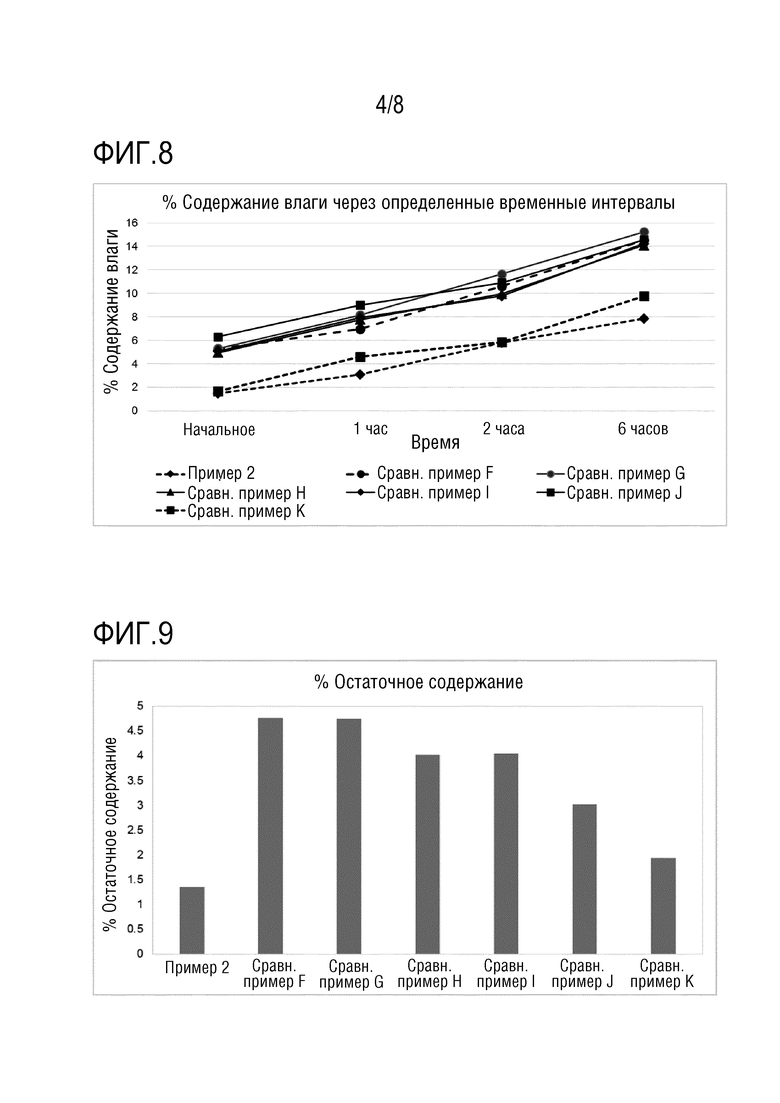
На фиг.8 представлено % содержание влаги в составах согласно примеру 2 и сравнительным примерам F-K в зависимости от времени хранения.
На фиг.9 сравнивается % остаточное содержание составов согласно примеру 2 и сравнительным примерам F-K.
На фиг.9 сравнивается % остаточное содержание составов согласно примеру 2 и сравнительным примерам F-K.
На фиг.10 сравнивается индекс прессуемости (индекс Карра) составов согласно примерам 3-4 и сравнительным примерам L-Q.
На фиг.11 сравнивается отношение Хауснера для составов согласно примерам 3-4 и сравнительным примерам L-Q.
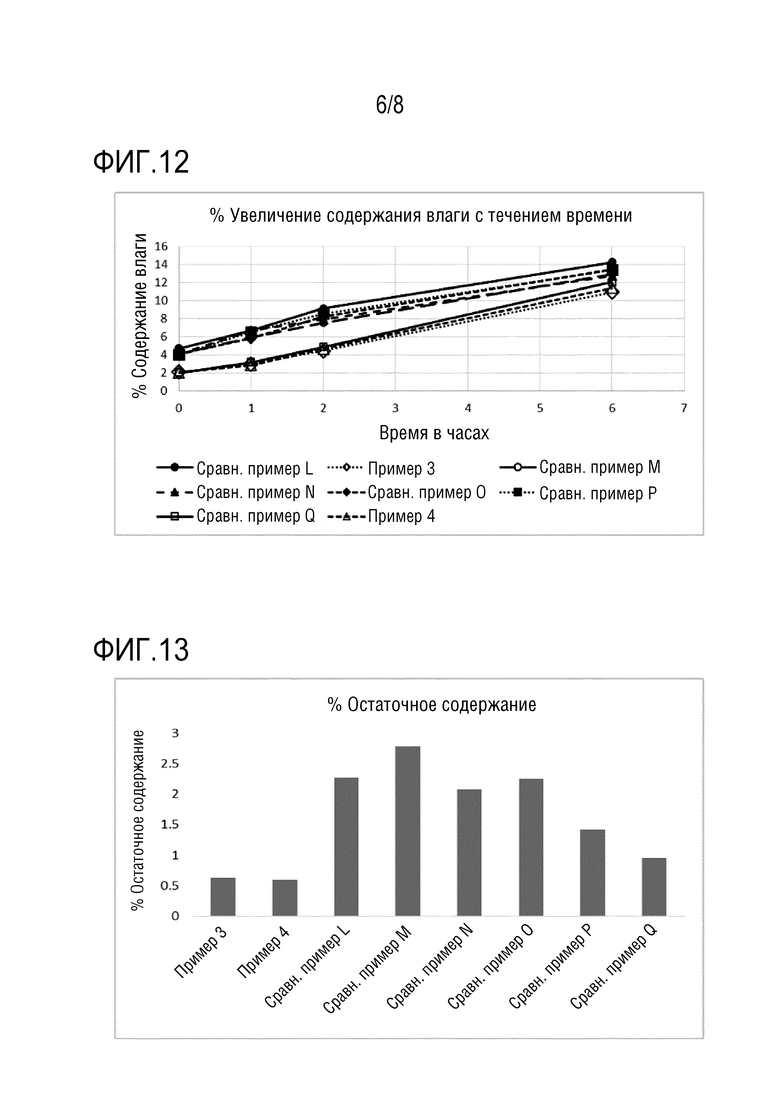
На фиг.12 представлено % содержание влаги в составах согласно примерам 3-4 и сравнительным примерам L-Q в зависимости от времени хранения.
На фиг.13 сравнивается % остаточное содержание составов согласно примерам 3-4 и сравнительным примерам L-Q
На фиг.14 сравнивается коэффициент прессуемости (индекс Карра) составов согласно примеру 5 и сравнительным примерам R-W.
На фиг.15 сравнивается отношение Хауснера составов согласно примеру 5 и сравнительным примерам R-W.
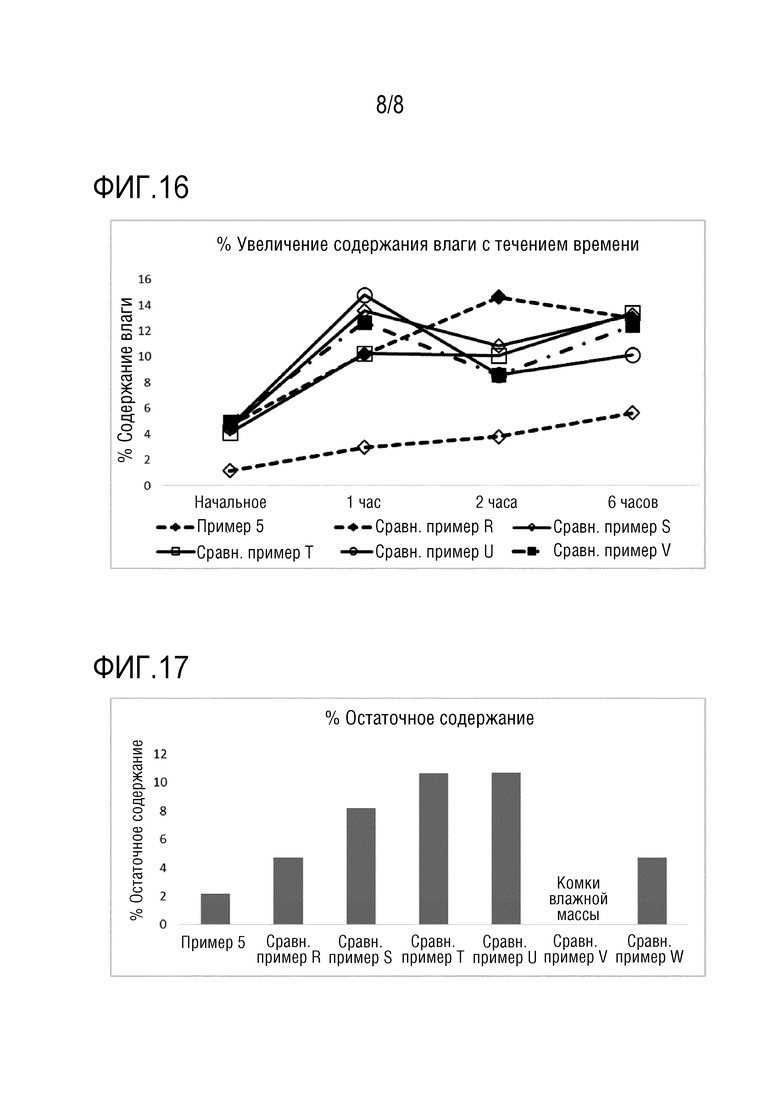
На фиг.16 представлено % содержание влаги в составах согласно примеру 5 и сравнительным примерам R-W в зависимости от времени хранения.
На фиг.17 сравнивается % остаточное содержание составов согласно примеру 5 и сравнительным примерам R-W.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новой композиции смеси сорбита и вазелинового масла для применения для улучшения свойств фармацевтических составов по нескольким параметрам, т.е. свойствам текучести, защите от влаги, антистатическим свойствам и прессуемости. Композиция смеси также может содержать лимонную кислоту и обладает способностью смягчать вкус горьких лекарственных средств.
Новая смесь, когда она смешана с лиофилизированным порошком, обеспечивает фармацевтический состав с улучшенными свойствами, например, свойствами текучести, защиты от влаги, антистатическими свойствами и прессуемостью.
Таким образом, настоящее изобретение относится к свободнотекучему твердому фармацевтическому составу, содержащему один или несколько активных ингредиентов и композицию смеси, содержащую или состоящую из сорбита, вазелинового масла и необязательно лимонной кислоты.
Состав предпочтительно содержит от 0,01% до 30% по массе одного или нескольких активных ингредиентов, от 70% до 99,99% по массе композиции смеси, и от 0% до 30% по массе одного или нескольких других фармацевтически приемлемых эксципиентов. Более предпочтительно, состав содержит от 0,1% до 28% по массе одного или нескольких активных ингредиентов, от 72% до 99,9% по массе композиции смеси, и от 5% до 30% по массе одного или нескольких других фармацевтически приемлемых эксципиентов. В одном варианте осуществления изобретения состав получают посредством процесса, включающего стадии получения композиции смеси посредством смешения сорбита, вазелинового масла и необязательно лимонной кислоты, и добавления композиции смеси к активному ингредиенту(ам), который предпочтительно представляет собой лиофилизированный порошок.
Кроме того, настоящее изобретение относится к композиции смеси, содержащей или состоящей из сорбита, вазелинового масла и необязательно лимонной кислоты для применения для изготовления фармацевтического состава, содержащего один или несколько активных ингредиентов. Композиция смеси предпочтительно содержит от 95 до 99,9% по массе сорбита, от 0,1% до 5% по массе вазелинового масла, и от 0 до 4% по массе лимонной кислоты. Более предпочтительно, композиция смеси содержит от 96 до 99,5% по массе сорбита, от 0,5% до 4% по массе вазелинового масла, и от 0,5 до 2% по массе лимонной кислоты. В одном варианте осуществления композиция смеси состоит из указанных компонентов в указанных предпочтительных и более предпочтительных соотношениях.
Также настоящее изобретение относится к способу изготовления твердого фармацевтического состава по изобретению, включающему:
(a) получение лиофилизированного порошка посредством возгонки растворителя из препарата, содержащего один или несколько активных ингредиентов и растворитель;
(b) получение композиции смеси, содержащей или состоящей из сорбита, вазелинового масла и необязательно лимонной кислоты;
(c)смешение композиции смеси, полученной на стадии (b), с лиофилизированным порошком, полученным на стадии (a).
Способ по изобретению позволяет получение твердого фармацевтического состава в форме свободнотекучего порошка.
Предпочтительные доли активного ингредиента(ов), сорбита, вазелинового масла, лимонной кислоты и композиции смеси в способе по настоящему изобретению являются такими же, как и в фармацевтическом составе по настоящему изобретению.
Растворитель, используемый в препарате, подлежащим лиофилизации, содержащем активный ингредиент(ы) и растворитель, как правило, представляет собой воду.
Термины "активный ингредиент" и "фармацевтически активный ингредиент" используют в настоящем описании взаимозаменяемо.
Фармацевтический состав по настоящему изобретению содержит один или несколько фармацевтически активных ингредиентов. Они могут быть выбраны, например, из олигопептидов, полипептидов (белков), нуклеотидов, полинуклеотидов и "низкомолекулярных соединений". Неограничивающими примерами фармацевтически активных ингредиентов, которые можно использовать в рамках настоящего изобретения, являются обезболивающие средства, альфа-блокаторы, противоаллергические средства, противоастматические средства, средства против ринита, средства против крапивницы, противовоспалительные средства, антиаритмические средства, антибактериальные средства, антипсихотические средства, антидиабетические средства, антидиуретики, противоэпилептические средства, противогрибковые средства, противоподагрические средства, антигипертензивные средства, средства против недержания мочи, средства против мигрени, антимускариновые средства и иммунодепрессанты, противовирусные средства, анксиолитики, седативные средства, снотворные средства и нейролептики, средства против доброкачественной гиперплазии (средства против BPH), средства, уменьшающие застой, диуретики, ферменты, средства против паркинсонизма, желудочно-кишечные средства, антагонисты рецепторов гистамина, средства от бесплодия, средства против эндометриоза, средства гормон-заместительной терапии, регулирующие липиды средства, местные анестетики, нервно-мышечные средства, средства против укачивания, питательные вещества, пероральные вакцины, белки, пептиды и рекомбинантные лекарственные средства, ингибиторы протонного насоса, средства против шизофрении, гормоны, контрацептивы, средства против судорожных припадков/панических расстройств, средства против половой дисфункции (мужской и женской) и т.д.
Конкретными неограничивающими примерами этих активных ингредиентов являются:
Противоаллергические средства: деслоратидин, лоратидин, монтелукаст, монтелукаст натрий, цетиризин, фексофенадин, эбастин.
Альфа-блокаторы: тамсулозин, силодозин.
Обезболивающие и противовоспалительные средства: аспирин, алоксиприн, ауранофин, азапропазон, бенорилат, дифлунизал, этодолак, фенбуфен, фенопрофен кальций, флубипрофен, ибупрофен, индометацин, кетопрофен, меклофенаминовая кислота, мефенаминовая кислота, набуметон, напроксен, оксапрозин, оксифенбутазон, фенилбутазон, пироксикам, сулиндак, парацетамол.
Антиаритмические средства: амиодарон HCl, дизопирамид, флецианида ацетат, хинидина сульфат.
Антибактериальные средства: бенэтамин пенициллин, циноксацин, ципрофлоксацин HCl, кларитромицин, клофазимин, клооксициллин, демеклоциклин, доксицилин, эритромицин, этионамид, имипенем, налидиксовая кислота, нитрофурантоин, рифампицин, спирамицин, сульфабензамид, сульфадоксин, сульфамеразин, сульфацетамид, сульфадиазин, сульфафуразол, сульфаметоксазол, сульфапиридин, тетрациклин, триметоприм.
Антипсихотические средства: амоксапин, циклазиндол, мапротилин HCl, миансерин HCl, нортриптилин HCl, тразодон HCl, триимипрамина малеат.
Антидиабетические средства: ацетогексамид, хлорпропамид, глибенкламид, гликлазид, глипизид, толазамид, толбутамид.
Антидиуретики: десмопрессин и его аналог, десмопрессина ацетат.
Противоэпилептические средства: бекламид, карбамазепин, клонезепам, этотоин, метоин, метсуксимид, метилфенобарбитон, окскарбазепин, параметадион, фенацемид, фенобарбитон, фенитоин, фенсуксимид, примидон, султиам, вальпроевая кислота.
Противогрибковые средства: амфотерицин, бутоконазола нитрат, клотримазол, эконазола нитрат, флуконазол, флуцитозин, гризеофульвин, итраконазол, кетоконазол, миконазол, натамицин, нистатин, сульконазола нитрат, тербинафин HCl, терконазол, тиоконазол, ундеценовая кислота.
Противоподагрические средства: аллопуринол, пробенецид, сульфинпиразон.
Антигипертензивные средства: амлодипин, бенидипин, дародипин, дилтиазем HCl, диазоксид, фелодипин, гуанабенца ацетат, индорамин, израдипин, миноксидил, никардипин HCl, нифедипин, нимодипин, феноксибензамин HCl, празосин HCl, резерпин, теразозин HCl.
Средства против мигрени: ризатриптан, дигидроэрготамина мезилат, эрготамина тартрат, метисергида малеат, пизотифена малеат, суматриптана сукцинат, кофеин.
Антимускариновые средства: оксибутинин, толтеродин, атропин, бензгексол HCl, бипериден, этопропазин HCl, гиосцина бутилбромид, хиосциамин, мепензолата бромид, орфенадрин, оксифенциклимин HCl, тропикамид.
Средства против ринита, средства против крапивницы: цетризин, фексофенадин, эбастин, лоратидин, монтелукаст.
Противовирусные средства: ацикловир, амантадина гидрохлорид, фамицикловир, зидовадин, диданозин, зальцитабин, фоскарнет натрий.
Анксиолитические средства, седативные средства, снотворные средства и нейролептики: альпразолам, амилобарбитон, барбитон, бентазепам, бромазепам, бромперидол, бротизолам, бутобарбитон, карбромал, хлордиазепоксид, хлорфенирамин, хлорметиазол, хлорпромазин, клобазам, клоназепан, клотиазепам, клозапин, диазепам, дроперидол, этинамат, флунанизон, флунитразепам, флуопромазин, флупентиксола деканоат, флуфеназина деканоат, флуразепам, галоперидол, лоразепам, лорметазепам, медазепам, мепробамат, метаквалон, мидазолам, нитразепам, оксазепам, пентобарбитон, перфеназин фенилэфрин, пимозид, прохлорперазин, псевдоэфедрин HCL, сульпирид, темазепам, тиоридазин, триазолам, зопиклон.
Контрацептивы: кломифена цитрат, даназол, дезогестрел, этинилоэстрадиол, этиндиол, этиндиол диацетат, левоноргестерел, медроксипрогестерона ацетат, местранол, метилтестостерон, норэтистерон, норэтистерона энантат, норгестрел, эстрадиол, конъюгированные эстрогены, дигидрогестерон, прогестерон, станозолол, стилбоэстрол, тестостерон, тиболон.
Средства, уменьшающие застой: псевдоэфедрина гидрохлорид.
Диуретики: ацетазоламид, амилорид, бендрофлуазид, буметанид, хлортиазид, хлорталидон, этакриновая кислота, фрусемид, метолазон, спиронолактон, триамтерен.
Ферменты: панкреатин, пепсин, липаза.
Эпилепсия: габапентин
Средства против паркинсонизма: бромкриптина мезилат, лизурида малеат, селегилин, пара-фторселегилин, лазабемид, разагилин, 2-BUMP [N-(2-бутил)-N-метилпропаргиламин], M-2-PP [N-метил-N-(2-пентил)-пропаргиламин], MDL-72145 [бета-(фторметилен)-3,4-диметокси-бензолэтанамин], мофегилин, apoморфин, N-пропилнорапорфин, каберголин, метерголин, наксаголид, перголид, пирибедил, ропинирол, тергурид, хинаголид.
Желудочно-кишечные средства: бисакодил, циметидин, цисаприд, дифеноксилат HCl, домперидон, метоклопрамид, фамотидин, лоперамид, месалазин, низатидин, эзомепразол, метопимазин, пантопразол, ондансетрон HCl, гранизетрон, трописетрон, долазетрон, ранитидин HCl, сульфасалазин, ланзопразол.
Антагонисты рецепторов гистамина: акривастин, астемизол, циннаризин, циклизин, ципрогептадин HCl, дименгидринат, флунаризин HCl, лоратидин, меклозин HCl, оксатомид, терфенадин, трипролидин.
Гормоны: агонисты или антагонисты гормона роста человека (HGH), фолликулостимулирующего гормона (FSH), гонадотропин-рилизинг гормона (GnRH), нафарелин, трипторелин, цетрореликс, атосибан.
Средства гормон-заместительной терапии: дигидрогестерон.
Антигипертензивные средства: эналаприл.
Средства для лактации: окситоцин, агонисты окситоцина.
Регулирующие липиды средства: безафибрат, клофибрат, фенофибрат, гемфиброзил, пробукол.
Местные анестетики: аметокаин, амилокаин, бензокаин, букрокаин, бупивакаин, бутакаин, бутаниликаин, бутоксикаин, бутиламинобензоат, картикаин, хлорпрокаин, цинхокаин, клибукаин, клормекаин, кока, какаин, циклометикаин, диметизоквин, диперодон, диклокаин, этилхлорид, этил п-пиперидинoацетиламинобензоат, этидокаин, гексилкаин, изобутамбен, кетокаин, лигнокаин, мепивакаин, меприлкаин, миртекаин, октакаин, оксетазаин, оксибупрокаин, парэтоксикаин, прамоксин, прилокаин, прокаин, пропранокаин, пропоксикаин, проксиметакаин, ропивакаин, толикаин, трикаин, тримекаин, вадокаин.
Средства против укачивания: дифенгидрамин.
Нервно-мышечные средства: пиридостигмин.
Нестероидные антиандрогены: энзалутамид.
Питательные вещества: бета-каротин, витамины, такие как витамин A, витамин B2, витамин D, витамин E, витамин K, минералы.
Пероральные вакцины: для предупреждения или снижения симптомов заболеваний, таких как грипп, туберкулез, менингит, гепатит, коклюш, полиомиелит, столбняк, дифтерия, малярия, холера, герпес, тиф, ВИЧ, СПИД, корь, болезнь Лайма, диарея путешественников, гепатит A, B и C, отит среднего уха, лихорадка Денге, бешенство, парагрипп, краснуха, желтая лихорадка, дизентерия, болезнь легионеров, токсоплазмоз, Q-лихорадка, геморрагическая лихорадка, аргентинская геморрагическая лихорадка, кариес, болезнь Шагаса, инфекции мочевыводящих путей, вызванные E. coli, пневмококковое заболевание, свинка, чикунгунья, сенная лихорадка, астма, ревматоидный артрит, карциномы, кокцидоз, болезнь Ньюкасла, энзоотическая пневмония, кошачий лейкоз, атрофический ринит, рожистое воспаление, ящур и пневмония свиней, или для предупреждения или снижения симптомов заболеваний, вызываемых видами Vibrio, видами Salmonella, видами Bordetella, видами Haemophilus, Toxoplasmosis gondii, цитомегаловирусом, видами Chlamydia, видами стрептококков, вирусом Норволк, Escherischia coli, Helicobacter pylori, ротавирусом, Neisseria gonorrhae, Neisseria meningiditis, аденовирусом, вирусом Эпштейна-Барр, вирусом японского энцефалита, Pneumocystis carini, Herpes simplex, видами Clostridia, респираторно-синцитиальным вирусом, видами Klebsiella, видами Shigella, Pseudomonas aeruginosa, парвовирусом, видами Campylobacter, видами Rickettsia, Varicella zoster, видами Yersinia, вирусом реки Росс, вирусом J.C., Rhodococcus equi, Moraxella catarrhalis, Borrelia burgdorferi и Pasteurella haemolytica, БЦЖ.
Средства против дисфнукций мочеиспускания: тамсулозин, троспия хлорид, толтеродин, оксибутинин, солифенацин.
Белки, пептиды и рекомбинантные лекарственные средства: рекомбинантные гормоны и изогормоны, рекомбинантные цитокины, рекомбинантные плазминогены, слитый белок рецептора TNF, моноклональные антитела, нуклеиновые кислоты, антисмысловые олигонуклеотиды, олигонуклеотиды, гликопротеины и молекулы адгезии, кальцитонин, октреотид, инсулин и аналоги инсулина, этанерцепт, пегфилграстим, лираглутид, бивалирудин, несиритид, церулетид, бантиромид, эксенатид, гонадорелин, энфувиртид, ванкомицин, икатибант, секретин, леупролид, рекомбинантный глюкагон, окситоцин, серморелин, грамицидин D, инсулин рекомбинантный, капреомицин, вазопрессин, козинотропин, бацитрацин, абареликс, вапреотид, тималфазин, мекасермин, терипаратид, кортикотропин, прамлитинид.
Связывающие фосфаты средства: севеламер.
Средства против половой дисфункции: каберголин, окситоцин, тадалафил, силденафил, варденафил.
Стимуляторы: амфетамин, дексамфетамин, дексфенфлурамин, фенфлурамин.
В конкретном варианте осуществления активный ингредиент состава по изобретению выбран из группы, состоящей из деслоратидина, монтелукаста, солифенацина, силодозина, силденафила и любой их фармацевтически приемлемой соли.
В конкретном варианте осуществления активный ингредиент состава по изобретению представляет собой деслоратидин.
В конкретном варианте осуществления активный ингредиент состава по изобретению представляет собой силденафил.
В конкретном варианте осуществления активный ингредиент состава по изобретению представляет собой солифенацин.
В дополнение к описанным выше компонентам, состав также может включать другие эксципиенты (вспомогательные вещества, дополнительные вещества), такие как, но не ограничиваясь ими, наполнители, загустители (включая, но не ограничиваясь ими, гуаровую камедь и ксантановую смолу), связующие вещества, разбавители, смазывающие вещества, pH-корректирующие средства, защитные средства, усилители вязкости, средства, способствующие впитыванию влаги, нешипучие разрыхлители, шипучие разрыхлители, поверхностно-активные вещества, антиоксиданты, смачивающие вещества, красители, вкусовые добавки, маскирующие вкус вещества, подсластители, консерванты и т.д.
Подходящим путем введения дозированной формы по настоящему изобретению является пероральное введение.
В одном варианте осуществления фармацевтически состава по изобретению можно вводить пациенту в форме порошка.
В другом аспекте фармацевтически состав по изобретению находится в упаковке, распределяющей однократную дозу состава, также называемой единичной дозированной формой. Неограничивающими примерами упаковки/единичной дозированной формы являются саше и стик-пакет.
В другом варианте осуществления фармацевтически состав по изобретению, например, в форме порошка, упакован в множественную дозированную форму, т.е. дозированную форму, позволяющую отбор множества доз произвольного размера. Неограничивающими примерами множественной дозированной формы являются бутылка и любой другой контейнер, способный вмещать порошок.
Пациент, который принимает состав в свободнотекучей форме, может быть уверен, что он получает всю дозировку, т.е. в упаковке/единичной дозированной форме не останется остатка.
В одном варианте осуществления пероральное введение проводят путем опустошения саше, стик-пакета или (любой другой) единичной упаковки, содержащей порошок, на язык и проглатывания содержимого.
В другом варианте осуществления пероральное введение проводят путем растворения порошка в растворителе (например, стакане воды), а затем выпивания раствора.
Точная доза и режим введения дозированной формы обязательно зависят от терапевтического эффекта, которого хотят достигнуть, и они могут варьироваться в зависимости от конкретного активного ингредиента, пути введения, возраста и состояния конкретного индивидуума, которому намереваются вводить состав. Иногда пациенты могут быть проинструктированы принимать две или любое количество единичных дозированных форм, например, стик-пакетов, за одно введение, или только часть, такую как половина или четверть, единичной дозированной формы за одно введение.
Составы по изобретению являются уникальными тем, что они обладают улучшенными свойствами текучести, содержания влаги, антистатическими свойствами и прессуемостью.
Фармацевтический состав по изобретению можно получать посредством:
(a) получения лиофилизированного порошка путем возгонки растворителя (например, воды), например в процессе лиофилизации, из препарата, который содержит активный ингредиент(ы) и растворитель;
(b) получения композиции смеси, содержащей сорбит и вазелиновое масло. Композиция смеси необязательно может содержать лимонную кислоту;
(c) смешения композиции смеси с лиофилизированным порошком, полученным на стадии (a), с получением фармацевтической композиции с улучшенными свойствами текучести, защитой от влаги, антистатическими свойствами и прессуемостью.
Согласно одному варианту осуществления, полученная свободнотекучая композиция находится в стик-пакете.
Согласно другому варианту осуществления, полученная свободнотекучая композиция находится в саше.
Свободнотекучая композиция смеси сорбита и вазелинового масла смешивают с лиофилизированным порошком способами, известными в данной области, такими как геометрическое смешение или смешение с использованием любого типа блендера.
ПРИМЕРЫ
Изобретение дополнительно описано в приведенных ниже примерах, которые не предназначены для ограничения объема заявленного изобретения.
Материалы и способы
Пример 1: Состав плацебо
Состав (плацебо) получали с использованием следующих ингредиентов:
Методика изготовления:
I. Лиофилизированные гранулы
1. Лимонную кислоту растворяли в 200 г воды с использованием магнитной/верхнеприводной мешалки в течение 5 минут.
2. Добавляли смолу при непрерывном перемешивании и образующуюся дисперсию продолжали перемешивать в течение 1 часа.
3. Добавляли мальтодекстрин при непрерывном перемешивании.
4. Конечную массу раствора/дисперсии доводили до 400 г с использованием очищенной воды.
5. Перемешивание раствора/дисперсии продолжали в течение 10 минут с использованием магнитной/верхнеприводной мешалки.
6. Этим раствором/дисперсией заполняли лоток из нержавеющей стали и лиофилизировали в лиофилизаторе.
7. После завершения лиофилизации лиофилизированный кек просеивали через сито #40 с получением лиофилизированных гранул.
II. Композиция смеси
8. Сорбит пропускали через сито #40 и смешивали с измельченной и просеянной лимонной кислотой в двухконусном барабанном смесителе в течение 2 минут при 10 об/мин.
9. К 40 г смеси стадии 8 капельно добавляли вазелиновое масло и перемешивали вручную с получением однородно распределенной композиции смеси.
10. Композицию смеси просеивали через сито #60, а затем смешивали с оставшейся смесью со стадии 8 с использованием двухконусного смесителя в течение 3 минут при 10 об/мин с получением конечной композиции смеси.
III. Состав
11. Лиофилизированные гранулы со стадии 7 смешивали с конечной композицией смеси со стадии 10 в двухконусном барабанном смесителе в течение 5 минут при 10 об/мин с получением свободнотекучей композиции (плацебо).
12. Свободнотекучей композицией заполняли стик-пакеты и запечатывали, в количестве 500 мг на стик-пакет (см. фиг.5).
Пример 2: Композиция деслоратидина
Состав деслоратидина получали с использованием следующих ингредиентов:
Методика изготовления
I. Лиофилизированные гранулы
1. Лимонную кислоту растворяли в 200 г воды с использованием магнитной/верхнеприводной мешалки в течение 5 минут.
2. Добавляли деслоратидин при непрерывном перемешивании с использованием магнитной/верхнеприводной мешалки.
3. Добавляли смолу при непрерывном перемешивании и полученную дисперсию продолжали перемешивать в течение 1 часа.
4. Добавляли мальтодекстрин при непрерывном перемешивании.
5. Конечную массу раствора/дисперсии доводили 400 г с использованием очищенной воды.
6. Перемешивание раствора/дисперсии продолжали в течение 10 минут с использованием магнитной/верхнеприводной мешалки.
7. Этим раствором/дисперсией заполняли лоток из нержавеющей стали и лиофилизировали в лиофилизаторе.
8. После завершения лиофилизации лиофилизированный кек просеивали через сито #40 с получением лиофилизированных гранул.
II. Композиция смеси
9. Сорбит пропускали через сито #40 и смешивали с измельченной и просеянной лимонной кислотой в двухконусном барабанном смесителе в течение 2 минут при 10 об/мин.
10. К 40 г смеси со стадии 9 капельно добавляли вазелиновое масло и перемешивали вручную с получением однородно распределенной композиции смеси.
11. Композицию смеси просеивали через сито #60, а затем смешивали с остальной смесью со стадии 9 с использованием двухконусного смесителя в течение 3 минут при 10 об/мин с получением конечной композиции смеси.
III. Состав
12. Лиофилизированные гранулы со стадии 8 смешивали с конечной композицией смеси со стадии 11 в двухконусном барабанном смесителе в течение 5 минут при 10 об/мин с получением свободнотекучего состава деслоратидина.
13. Свободнотекучей композицией заполняли стик-пакеты и запечатывали, в количестве 500 мг на стик-пакет (см. фиг.5).
Сравнительный пример A
Состав гранул получали, по существу как описано в примере 1, с использованием следующих ингредиентов:
Сравнительный пример B
Сравнительный фармацевтический состав получали, по существу как описано в примере 1, с использованием композиции смеси, содержащей тальк и следующие другие ингредиенты:
Сравнительный пример C
Сравнительный фармацевтический состав получали, по существу как описано в примере 1, с использованием композиции смеси, содержащей стеарат магния и следующие другие ингредиенты:
Сравнительный пример D
Сравнительный фармацевтический состав получали, по существу как описано в примере 1, с использованием композиции смеси, содержащей тальк, стеарат магния и следующие другие ингредиенты:
Сравнительный пример E
Сравнительный фармацевтический состав получали, по существу как описано в примере 1, с использованием композиции смеси, содержащей только вазелиновое масло и следующие другие ингредиенты:
Сравнительный пример F
Состав гранул получали, по существу как описано в примере 2, с использованием следующих ингредиентов:
Сравнительный пример G
Сравнительный фармацевтический состав получали, по существу как описано в примере 2, с использованием композиции смеси, содержащей тальк и следующие другие ингредиенты:
Сравнительный пример H
Сравнительный фармацевтический состав получали, по существу как описано в примере 2, с использованием композиции смеси, содержащей стеарат магния и следующие другие ингредиенты:
Сравнительный пример I
Сравнительный фармацевтический состав получали, по существу как описано в примере 2, с использованием композиции смеси, содержащей тальк, стеарат магния и следующие другие ингредиенты:
Сравнительный пример J
Сравнительный фармацевтический состав получали, по существу как описано в примере 2, с использованием композиции смеси, содержащей только вазелиновое масло и следующие другие ингредиенты:
Сравнительный пример K
Сравнительный фармацевтический состав получали, по существу как описано в примере 2, с использованием композиции смеси, содержащей только сорбит и следующие другие ингредиенты:
Пример 3: Композиция силденафила
Состав силденафила получали с использованием следующих ингредиентов:
Методика изготовления
I. Лиофилизированные гранулы
1. Гидроксид натрия растворяли в 370 мл очищенной воды при перемешивании с использованием верхнеприводной мешалки в течение 10 мин при 1000 об/мин.
2. Силденафила цитрат диспергировали однородно в растворе стадии 1 при перемешивании в течение 30 мин.
3. Дисперсию, полученную на стадии 2, гомогенизировали при 10000 об/мин в течение 60 мин с использованием гомогенизатора и верхнеприводной мешалки.
4. Гидроксипропилцеллюлозу L растворяли в воде (166,5 г) и раствор добавляли к дисперсии стадии 2 при перемешивании.
5. К дисперсии добавляли маннит.
6. Конечную массу раствора/дисперсии доводили 1000 г с использованием очищенной воды.
7. Перемешивание раствора/дисперсии продолжали в течение 10 минут с использованием магнитной/верхнеприводной мешалки.
8. Этим раствором/дисперсией заполняли лоток из нержавеющей стали и лиофилизировали в лиофилизаторе.
9. После завершения лиофилизации лиофилизированный кек просеивали через сито #40 с получением лиофилизированных гранул.
II. Композиция смеси
10. Сорбит пропускали через сито #40 и смешивали с измельченной и просеянной лимонной кислотой в двухконусном барабанном смесителе в течение 2 минут при 10 об/мин.
11. Вазелиновое масло капельно добавляли к 40 г смеси стадии 10, и перемешивали вручную с получением однородно распределенной композиции смеси.
12. Композицию смеси просеивали через сито #60, а затем смешивали с остальной смесью со стадии 9 с использованием двухконусного смесителя в течение 3 минут при 10 об/мин с получением конечной композиции смеси.
III. Состав
13. Лиофилизированные гранулы со стадии 9 смешивали с конечной композицией смеси со стадии 12 в двухконусном барабанном смесителе в течение 5 минут при 10 об/мин с получением свободнотекучего состава силденафила цитрата.
14. Свободнотекучим составом заполняли стик-пакеты и запечатывали, в количестве 500 или 1000 мг на стик-пакет (см. фиг.5).
Пример 4: Композиция силденафила
Состав силденафила получали, по существу как описано в примере 3, с использованием следующих ингредиентов:
Сравнительный пример L
Состав гранул получали, по существу как описано в примере 3 с использованием следующих ингредиентов:
Сравнительный пример M
Сравнительный фармацевтический состав получали, по существу как описано в примере 3, с использованием композиции смеси, содержащей тальк и следующие другие ингредиенты:
Сравнительный пример N
Сравнительный фармацевтический состав получали, по существу как описано в примере 3, с использованием композиции смеси, содержащей стеарат магния и следующие другие ингредиенты:
Сравнительный пример O
Сравнительный фармацевтический состав получали, по существу как описано в примере 3, с использованием композиции смеси, содержащей тальк, стеарат магния и следующие другие ингредиенты:
Сравнительный пример P
Сравнительный фармацевтический состав получали, по существу как описано в примере 3, с использованием композиции смеси, содержащей вазелиновое масло и следующие другие ингредиенты:
Сравнительный пример Q
Сравнительный фармацевтический состав получали, по существу как описано в примере 3, с использованием композиции смеси, содержащей сорбит и следующие другие ингредиенты:
Пример 5: Композиция солифенацина
Состав солифенацина получали с использованием следующих ингредиентов:
Методика изготовления
I. Лиофилизированные гранулы
1. Солифенацин растворяли в 140 г воды с использованием магнитной/верхнеприводной мешалки в течение 5 минут.
2. Добавляли лимонную кислоту при непрерывном перемешивании с использованием магнитной/верхнеприводной мешалки.
3. Добавляли смолу при непрерывном перемешивании и полученную дисперсию продолжали перемешивать в течение 1 часа.
4. Мальтодекстрин растворяли в 140 г воды в отдельном стакане, а затем добавляли к смеси стадии 3 при непрерывном перемешивании.
5. Конечную массу раствора/дисперсии доводили 400 г с использованием очищенной воды.
6. Перемешивание раствора/дисперсии продолжали в течение 10 минут с использованием магнитной/верхнеприводной мешалки.
7. Этим раствором/дисперсией заполняли лоток из нержавеющей стали и лиофилизировали в лиофилизаторе.
8. После завершения лиофилизации лиофилизированный кек просеивали через сито #40 с получением лиофилизированных гранул.
II. Композиция смеси
9. Сорбит пропускали через сито #40 и смешивали с измельченной и просеянной лимонной кислотой в двухконусном барабанном смесителе в течение 2 минут при 10 об/мин.
10. Вазелиновое масло капельно добавляли к 40 г смеси стадии 9 и перемешивали вручную с получением однородно распределенной композиции смеси.
11. Композицию смеси просеивали через сито #60, а затем смешивали с остальной смесью со стадии 9 с использованием двухконусного смесителя в течение 3 минут при 10 об/мин с получением конечной композиции смеси.
III. Состав
12. Лиофилизированные гранулы со стадии 8 смешивали с конечной композицией смеси со стадии 11 в двухконусном барабанном смесителе в течение 5 минут при 10 об/мин с получением свободнотекучего состава солифенацина.
13. Свободнотекучей композицией заполняли стик-пакеты и запечатывали, в количестве 500 мг на стик-пакет (см. фиг.5).
Сравнительный пример R
Состав гранул получали, по существу как описано в примере 5, с использованием следующих ингредиентов:
Сравнительный пример S
Сравнительный фармацевтический состав получали, по существу как описано в примере 5, с использованием композиции смеси, содержащей тальк и следующие другие ингредиенты:
Сравнительный пример T
Сравнительный фармацевтический состав получали, по существу как описано в примере 5, с использованием композиции смеси, содержащей стеарат магния и следующие другие ингредиенты:
Сравнительный пример U
Сравнительный фармацевтический состав получали, по существу как описано в примере 5, с использованием композиции смеси, содержащей тальк, стеарат магния и следующие другие ингредиенты:
Сравнительный пример V
Сравнительный фармацевтический состав получали, по существу как описано в примере 5, с использованием композиции смеси, содержащей вазелиновое масло и следующие другие ингредиенты:
Сравнительный пример W
Сравнительный фармацевтический состав получали, по существу как описано в примере 5, с использованием композиции смеси, содержащей сорбит и следующие другие ингредиенты:
Пример 6: Результаты исследования объемной плотности и насыпной плотности
Объемная и насыпная плотность являются важными для понимания свойств текучести составов. Объемная плотность материала представляет собой соотношение массы и объема (включая объем пустот между частицами) образца порошка образца неуплотненного порошка. Насыпная плотность представляет собой увеличенную объемную плотность, достигнутую после механического уплотнения постукивания по контейнеру, содержащему образец порошка. Насыпную плотность определяют путем механического постукивания по градуированному цилиндру, содержащему образец, до тех пор, пока не наблюдают, что дальнейшее изменение объема является малым. Поскольку взаимодействия между частицами, влияющие на свойства объема порошка, также являются взаимодействиями, которые препятствую текучести порошка, сравнение объемной и насыпной плотности может давать меру относительной важности этих взаимодействий в данном порошке. Такое сравнение часто используют в качестве показателя способности порошка течь, как например, коэффициент прессуемости или отношение Хауснера:
Индекс прессуемости (индекс Карра):
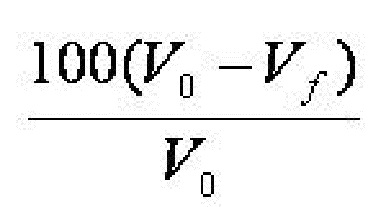
Отношение Хауснера:
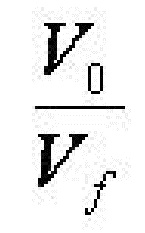 ,
,
V0=кажущийся объем без уплотнения (общий объем) Vf=конечный объем после уплотнения
Чем ниже величины коэффициента прессуемости и отношения Хауснера, тем лучше свойства текучести порошка.
Методика определения объемной плотности:
Согласно способу Фармакопеи США (USP), глава <616>, способ I, с использованием 100-мл цилиндра с ценой деления до 1 мл и количества порошка, при котором кажущийся объем без уплотнения составляет от 50 и 100 мл.
Методика определения насыпной плотности:
Согласно Фармакопее США (USP), глава <616>, способ I, со следующими деталями:
- 100-мл градуированный цилиндр (с ценой деления до 1 мл) массой 130 ± 16 г устанавливают на штатив массой 240 ± 12 г.
- Проводят 10, 500 и 1250 постукиваний по образцу порошка и определят соответствующие объемы V10, V500 и V1250 по ближайшей градуированной единице.
- Если разность между V500 и V1250 меньше или равна 1 мл, то насыпной объем равен V1250.
- Если разность между V500 и V1250 превышает 1 мл, измерение повторяют с шагом, таким как 1250 постукиваний, до тех пор, пока разность между последовательными измерениями не составит меньше или равно 1 мл.
Результаты:
Пример 7: Угол естественного откоса:
Угол естественного откоса используют для охарактеризации свойств текучести твердых веществ. Угол естественного откоса представляет собой характеристику, связанную с трением между частицами или устойчивости к движению между частицами. Угол естественного откола представляет собой постоянный трехмерный угол (относительно горизонтального основания), который имеет подобная конусу горстка материала.
Методика (согласно USP, общая глава <1174>):
Угол естественного откоса образуется на фиксированном основании с удерживающим выступом для удержания слой порошка на основании. Основание должно быть свободно от вибрации. Высоту воронки меняют, чтобы осторожно сформировать симметричный конус порошка. Следует следить, чтобы не было вибрации по мере движения воронки. Высоту воронки следует поддерживать на уровне приблизительно 2-4 см от вершины горстки порошка по мере ее формирования, для минимизации влияния падающего порошка на вершину конуса. Если симметричный конус порошка не может быть успешно и воспроизводимым образом сформирован, этот способ не пригоден. Угол естественного откоса определяют путем высоты конуса порошка и вычисления угла естественного откоса (a) по следующему уравнению:
tan (a) = высота/0,5 основание.
Результаты:
(градус)
Пример 8: Содержание влаги:
Фармацевтические составы помещали на открытые чашки Петри, которые затем помещали в Climacel, поддерживаемый при 25ºC/75% RH, для имитации воздействия высокой влажности. Содержание влаги в каждом составе анализировали через 1, 2 и 6 часов в Climacel. Содержание влаги оценивали с использованием USP, общая глава 921 - Способ определения содержания воды.
Результаты:
(масс.%)
Пример 9: Свойства уменьшения липкости
Свойства уменьшения липкости состава определяли путем определения остаточного содержания с использованием следующей методики:
Методика:
Фармацевтическими составами единообразно заполняли 10 стик-пакетов из гибких ламинированных материалов, как представлено на фиг.5. Массу содержимого каждого стик-пакета записывали для дальнейшего сравнения. Заполненные стик-пакеты закрывали с использованием запечатывающего устройства. Запечатанные стик-пакеты держали на вибрирующем устройстве сдвига в течение 30 минут для размещения составов в углах стик-пакета. Каждый стик-пакет открывали посредством разрезания с одной запечатанной стороны. Состав из каждого стик-пакета извлекали и взвешивали на откалиброванных весах для определения количества состава, извлеченного из каждого стик-пакета. Остаточное содержание вычисляли с использованием следующей формулы:
(Масса заполнения стик-пакета) - (содержимое, извлеченное из стик-пакета) = Остаточное содержание
Результаты
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ СОЛИФЕНАЦИНА ИЛИ ЕГО СОЛИ ДЛЯ ИСПОЛЬЗОВАНИЯ В ТВЕРДОМ ПРЕПАРАТЕ | 2005 |
|
RU2359670C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ С МАСКИРОВАННЫМ ВКУСОМ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2012 |
|
RU2583935C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ СИЛДЕНАФИЛА ЦИТРАТА В ФОРМЕ СУСПЕНЗИИ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ | 2016 |
|
RU2649834C1 |
| ФАРМАЦЕВТИЧЕСКИЕ И/ИЛИ ПИЩЕВЫЕ КОМПОЗИЦИИ НА ОСНОВЕ КОРОТКОЦЕПОЧЕЧНЫХ ЖИРНЫХ КИСЛОТ | 2010 |
|
RU2528106C2 |
| БЫСТРО РАСПАДАЮЩАЯСЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2018 |
|
RU2751193C2 |
| СТАБИЛИЗИРУЮЩАЯ КОМПОЗИЦИЯ ДЛЯ БИОЛОГИЧЕСКИХ МАТЕРИАЛОВ | 2013 |
|
RU2666601C2 |
| СОСТОЯЩАЯ ИЗ МНОГИХ ЧАСТЕЙ ВНУТРИРОТОВАЯ ЛЕКАРСТВЕННАЯ ФОРМА С ОРГАНОЛЕПТИЧЕСКИМИ СВОЙСТВАМИ | 2010 |
|
RU2490010C2 |
| ПОЛНОСТЬЮ НАТУРАЛЬНЫЕ НЕТОКСИЧНЫЕ СУБЛИНГВАЛЬНЫЕ СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2014 |
|
RU2733468C2 |
| КОМБИНИРОВАННАЯ ЖИДКАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ НЕОЧИЩЕННЫЙ ВЫСУШЕННЫЙ ПОРОШОК, СТАБИЛИЗИРУЮЩИЙ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2703734C1 |
| ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 2011 |
|
RU2565731C2 |



Группа изобретений относится к фармацевтике. Предложен свободнотекучий фармацевтический состав, содержащий (1) лиофилизированные гранулы, содержащие один или несколько активных ингредиентов, и (2) композицию смеси, содержащую сорбит и вазелиновое масло, где состав содержит от 0,01% до 30% по массе активного ингредиента(ов), от 70% до 99,99% по массе композиции смеси и от 0% до 29,99% по массе других фармацевтически приемлемых эксципиентов. При этом композиция смеси содержит от 95% до 99,9% по массе сорбита, от 0,1 до 5% по массе вазелинового масла и от 0% до 4% по массе лимонной кислоты. Предложены также упаковка, содержащая указанный фармацевтический состав, способ изготовления указанного состава и применение твердой смеси, содержащей сорбит и вазелиновое масло в указанном количестве, для изготовления фармацевтического состава. Полученный состав обладает улучшенными свойствами текучести, защиты от влаги, антистатическими свойствами, а также высокой однородностью антиадгезионных свойств, препятствующих слипанию. 4 н. и 12 з.п. ф-лы, 17 ил., 9 пр.
1. Свободнотекучий фармацевтический состав, содержащий (1) лиофилизированные гранулы, содержащие один или несколько активных ингредиентов и (2) композицию смеси, содержащую сорбит и вазелиновое масло, где состав содержит от 0,01% до 30% по массе активного ингредиента(ов), от 70% до 99,99% по массе композиции смеси и от 0% до 29,99% по массе других фармацевтически приемлемых эксципиентов, и
композиция смеси содержит от 95% до 99,9% по массе сорбита, от 0,1 до 5% по массе вазелинового масла и от 0% до 4% по массе лимонной кислоты.
2. Состав по п.1, содержащий от 0,1% до 28% по массе активного ингредиента(ов), от 72% до 99,9% по массе композиции смеси и от 5% до 27,9% по массе одного или нескольких других фармацевтически приемлемых эксципиентов.
3. Состав по п.1 или 2, где композиция смеси содержит от 96 до 99,5% по массе сорбита, от 0,5% до 4% по массе вазелинового масла и от 0% до 2% по массе лимонной кислоты.
4. Состав по п.1 или 2, где композиция смеси состоит из от 95 до 99,9% по массе сорбита, от 0,1% до 5% по массе вазелинового масла и от 0 до 4% по массе лимонной кислоты.
5. Состав по п.4, где композиция смеси состоит из от 96 до 99,5% по массе сорбита, от 0,5% до 4% по массе вазелинового масла и от 0% до 2% по массе лимонной кислоты.
6. Состав по любому из пп.1-5, где активный ингредиент выбран из группы, состоящей из деслоратидина, монтелукаста, солифенацина, силодосина, силденафила и фармацевтически приемлемых солей вышеуказанных активных ингредиентов, и десмопрессина и ацетата десмопрессина.
7. Состав по любому из пп.1-5, где активный ингредиент представляет собой деслоратидин или его фармацевтически приемлемую соль.
8. Состав по любому из пп.1-5, где активный ингредиент представляет собой монтелукаст или его фармацевтически приемлемую соль.
9. Состав по любому из пп.1-5, где активный ингредиент представляет собой силодосин или его фармацевтически приемлемую соль.
10. Состав по любому из пп.1-5, где активный ингредиент представляет собой силденафил или его фармацевтически приемлемую соль.
11. Состав по любому из пп.1-5, где активный ингредиент представляет собой солифенацин или его фармацевтически приемлемую соль.
12. Состав по любому из пп.1-5, где активный ингредиент представляет собой десмопрессин или ацетат десмопрессина.
13. Упаковка, содержащая состав по любому из предшествующих пунктов.
14. Упаковка по п.13, выбранная из группы, состоящей из саше и стик-пакета.
15. Применение твердой смеси, содержащей от 95% до 99,9% по массе сорбита, от 0,1% до 5% по массе вазелинового масла и от 0% до 4% по массе лимонной кислоты для изготовления фармацевтического состава, определенного в п.1.
16. Способ изготовления фармацевтического состава по любому из пп.1-12, включающий:
(a) получение лиофилизированного порошка путем возгонки растворителя из препарата, содержащего один или несколько активных ингредиентов и растворитель;
(b) получение композиции смеси, содержащей или состоящей из сорбита, вазелинового масла и необязательно лимонной кислоты;
(c) смешение композиции смеси, полученной на стадии (b), с лиофилизированным порошком, полученным на стадии (a).
| WO 2009112156 A1, 17.09.2009 | |||
| US 7122198 B1, 17.10.2006 | |||
| WO 2010021607 A2, 25.02.2010 | |||
| US 20160128944 A1, 12.05.2016 | |||
| ОРАЛЬНЫЙ ПРЕПАРАТ ИНТЕРФЕРОНА В ВИДЕ ТАБЛЕТОК | 1999 |
|
RU2175554C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРОТИВОВИРУСНОГО СРЕДСТВА | 2010 |
|
RU2454221C2 |
Авторы
Даты
2022-08-08—Публикация
2019-04-25—Подача