Область техники, к которой относится изобретение
Изобретение относится к области медицинской диагностики, а именно к способам региональной биоимпедансометрии участка челюстно-лицевой области, а именно щечной области с использованием электрического тока в качестве зондирующего сигнала. Изобретение может быть использовано в восстановительной медицине, функциональной диагностике, хирургической стоматологии и челюстно-лицевой хирургии.
Уровень техники
Способ заключается в последовательном измерении импеданса на исследуемом участке тела, а именно щечной области. Для этого на пациента накладывают токовые электроды, подключенные к генератору высокочастотного тока, и потенциальные электроды, подключенные к измерителю высокочастотного напряжения. Измеряют электрическое сопротивление на разных сроках реабилитации и рассчитывают разницу полученных значений сопротивления в динамике.
Как известно, любое оперативное вмешательство сопровождается повреждением покровных и подлежащих тканей с развитием в последствии воспаления, протекающего через последовательно сменяющиеся фазы альтерации, экссудации и пролиферации. Экссудация в очаге воспаления возникает в результате нарушения местной микроциркуляции. Экссудация представляет собой выпотевание белоксодержащей жидкой части крови через сосудистую стенку в окружающую соединительную ткань.
За выход жидкой части крови из сосудов и задержку жидкости в межклеточных пространствах отвечают несколько основных механизмов: повышенная проницаемость сосудов микроциркуляторного русла, увеличенное фильтрационное давление крови, повышенное осмотическое и онкотическое давление в очаге воспаления, фильтрация плазмы через трансцеллюлярные каналы клеток и посредством микровезикулярного транспорта.
Скопление жидкости в мягких тканях в результате экссудации приводит к возникновению внешнего признака воспаления - отека [1].
Любое оперативное вмешательство в полости рта, включающее отслаивание слизисто-надкостничного лоскута и остеотомию костной ткани, приводит к разной степени послеоперационного отека. Выраженный отек не только ухудшает самочувствие пациента после операции и удлиняет сроки восстановительного периода, но и повышает риск развития воспалительных осложнений, включая нагноение операционной раны, дальнейшее распространение воспалительного процесса на прилежащие ткани с возможным развитием абсцессов и флегмон. Выраженность отечных явлений при хирургических операциях в полости рта и челюстно-лицевой области обусловлена особенностями анатомии челюстно-лицевой области, заключающимися в наличии обширной сети кровеносных и лимфатических сосудов, располагающихся в мягких тканях лица и шеи, а также наличием выраженной подкожно-жировой клетчатки в челюстно-лицевой области и жирового тела щеки, которые также вовлекаются в очаг постоперационного воспаления [2].
Адекватная оценка состояния пациента в значительной мере является гарантией его полного восстановления и реабилитации. Контроль развития и динамики изменения отека мягких тканей щечной области при операциях в полости рта и челюстно-лицевой области позволяет достоверно оценивать направленность адаптивных реакций организма и адекватно корректировать проводимый лечебный процесс.
Несмотря на большое количество методик, которые возможно использовать для контроля послеоперационного отека челюстно-лицевой области, все они имеют определенные недостатки, важнейшими из которых является невысокая точность некоторых методов и невозможность использования их в амбулаторных условиях врачом-стоматологом из-за высокой стоимости процедуры, отсутствия возможности проведения исследования непосредственно в стоматологическом кабинете, необходимости привлечения сторонних специалистов. Надежный и простой метод контроля отека, применяемый в стоматологическом кабинете, позволил бы облегчить оценку коллатерального отека для клиницистов и исследователей. Таким образом, это может способствовать объективизации оценки отека в рутинной клинической практике, развитию дальнейших исследований о причинах, последствиях и методах устранения отеков в раннем послеоперационном периоде.
Для определения гидратации участка тела возможно применение диагностических устройств, использующих переменный ток в качестве зондирующего сигнала. Эта методика является наиболее неинвазивной и доступной среди современных технических средств. Описанные выше устройства позволяют регистрировать сопротивление тканей (импеданс) при прохождении через этот участок переменного тока. Для измерения электрического сопротивления участка тела используется тетраполярный метод, в котором зондирующий ток пропускается через токовые электроды, а падение напряжения на исследуемом участке тела измеряется с помощью потенциальных электродов [3].
Описан способ определения импеданса и последующего расчета объемов жидкости в сегментах тела, осуществляемый путем наложения потенциальных и токовых электродов на дистальные части конечностей, и последовательном измерении импеданса рук, туловища и ног, и определении, основываясь на измеренных параметрах, импеданса отдельных регионов тела. [3]. Описанный выше способ и аналогичные ему обладают одним существенным недостатком, а именно низкой точностью измерения импеданса отдельных сегментов тела за счет неравномерного распределения переменного тока на больших участках тела, а также не имеют технической возможности измерения отдельного участка головы, а только позволяют определить импеданс всей головы или одного полушария.
Методом, позволяющим проводить измерение импеданса на выбранном локальном участке тела, является способ региональной биоимпедансометрии, заключающийся в пропускании зондирующего тока через участок тела человека и измерении величины напряжения на нем, используемой для расчета импеданса исследуемого участка, расположенного на пути протекания зондирующего переменного тока [4]. Явным недостатком описанного метода является недостаточно высокая точность измерения импеданса исследуемого сегмента, связанная с тем, что электроды должны быть размещены непосредственно на границах исследуемого участка тела, и, в некоторых случаях становится практически невозможно точно воспроизвести расположение электродов при повторном исследовании того же пациента. Это вызывает изменение объема реально исследуемого региона тела и существенно искажает результаты сравнительного анализа. Описанный способ не применялся ранее для оценки гидратации сегмента челюстно-лицевой области в связи с ее сложным анатомическим строением и невозможностью произвести фиксацию электродов в строго определенных точках.
Метод региональной биоимпедансометрии с использованием внутриротовых электродов применялся ранее в диагностике заболеваний пародонта для оценки активного и реактивного сопротивления тканей полости рта для оценки выраженности воспалительного процесса в пародонте. Описанный метод позволяет определять импеданс небольшого участка в полости рта с достаточно высокой точностью благодаря нивелированию потерь напряжения при прохождении тока от токовых электродов, расположенных на больших расстояниях. Однако данный метод используется для определения импеданса только участка альвеолярного отростка, покрытого слизистой оболочкой. В то время как наибольшее изменение содержания внеклеточной жидкости после операций в полости рта происходит в поверхностных тканях подкожной жировой клетчатки, подслизистого и слизистого слоя, а применение внутриротовых электродов в раннем послеоперационном периоде может быть затруднено. [5].
Наиболее близким аналогом предлагаемого метода является описанный ранее способ прогнозирования ранних осложнений дентальной имплантации посредством проведения биоимпедансной спектрометрии для определения биоимпеданса тканей альвеолярного отростка на разных частотах. Согласно этому способу, оценка проницаемости мембран клеток костной ткани в области планируемой имплантации посредством измерения отношения импеданса на частоте 10 кГц к импедансу на частоте 100 кГц позволяет прогнозировать эффективность остеоинтеграции. В основу данного способа положена методика тетраполярной биоимпедансной спектрометрии, предполагающая фиксацию показаний импеданса в системе из 2 потенциальных и 2 токовых электродов на линейном участке, при непосредственном наложении электродов на дистальные границы исследуемой области альвеолярного отростка [6].
Все описанные методы применения региональной биоимпедансометрии в челюстно-лицевой области предполагают применение внутриротовых электродов, что становится затруднительным в условиях выраженного отека мягких тканей и наличия болевых ощущений у пациента в послеоперационном периоде. Применение метода локальной биоимпедансометрии для определения импеданса участка челюстно-лицевой области с использованием накожных электродов ранее не описывалось.
В основу настоящего изобретения положена задача создать способ применения региональной биоимпедансометрии для определения импеданса участка челюстно-лицевой области, а именно щечной области, который позволил бы объективно определять изменения импеданса на исследуемом участке у пациентов при хирургических операциях в ротовой полости и челюстно-лицевой области, что косвенно свидетельствовало бы об изменении в динамике объема внеклеточной жидкости мягких тканей челюстно-лицевой области.
Данная задача может быть решена применением метода региональной биоимпедансометрии, адаптированного для использования в щечной области.. Основной принцип электрического биоимпеданса состоит в анализе изменений напряжения, возникающего при пропускании зондирующего переменного тока, вводимого через электроды через тело или сегмент тела. Как известно, сопротивление рассчитывается как отношение силы тока к напряжению на участке, через который прошел электрический ток. Значение сопротивления прямо пропорционально длине исследуемого участка и обратно пропорционально площади поперечного сечения этого участка. При увеличении объема жидкости в участке тела изменяются его геометрические параметры, а именно происходит увеличение объема этого участка, а значит и увеличение площади его поперечного сечения. Таким образом, сопротивление электрическому току уменьшается при увеличении объема жидкости, а следовательно, импеданс участка тела снижается в случаях возникновения отека в исследуемой области в сравнении с обычным состоянием этого участка. Таким образом, биоимпедансометрия может применяться, помимо других диагностических целей, для мониторинга динамики изменения импеданса участка тела с дальнейшим расчетом изменения гидратации на данном участке. Данное предположение с успехом подтверждается исследованиями по оценке послеоперационного отека методом биоимпедансометрии коленного сустава после тотального эндопротезирования коленного сустава, локального отека при ожогах конечностей, оценке локальной лимфэдемы руки после резекции молочной железы [7, 8].
Послеоперационный отек при операциях в ротовой полости и челюстно-лицевой области представляет собой увеличение объема межклеточной жидкости за счет коллатерального отека межклеточных пространств подслизистого слоя, подкожной жировой клетчатки, жирового тела щеки и межмышечных прослоек соединительной ткани, а также образующейся гематомой, что приводит к изменению объема исследуемой области и, как следствие, падению напряжения и уменьшению импеданса на данном участке. Для оценки локального отека исследуемого участка тела наибольший интерес представляет показатель изменения импеданса тканей исследуемого участка на низких частотах (5 кГц), напрямую зависящий от изменения объема внеклеточной жидкости в указанном участке. Эту переменную можно непосредственно измерить с помощью прибора для биоимпедансной спектрометрии. Таким образом, получаемое значение изменения импеданса можно считать потенциально достоверным параметром, определяющим динамику изменения объемов внеклеточной жидкости. При этом получаемый параметр импеданса и его разница будут индивидуальны для каждого пациента и динамика его изменений в послеоперационном периоде позволит судить о процессах, происходящих в постоперационной области.
Для наиболее точной регистрации изменения импеданса на исследуемом участке челюстно-лицевой области, а именно щечной области, в предлагаемом способе использована методика тетраполярной региональной биоимпедансометрии, при которой потенциальные и токовые электроды располагаются на границах исследуемой области в строго определенных точках, что позволяет получать значения линейного напряжения на относительно однородном участке без значительных искажений.
Техническим результатом является расширение области применения способа региональной биоимпедансометрии за счет обеспечения возможности измерения импеданса участка челюстно-лицевой области, а именно щечной области, у пациентов при хирургических операциях в полости рта и челюстно-лицевой области.
Раскрытие сущности изобретения
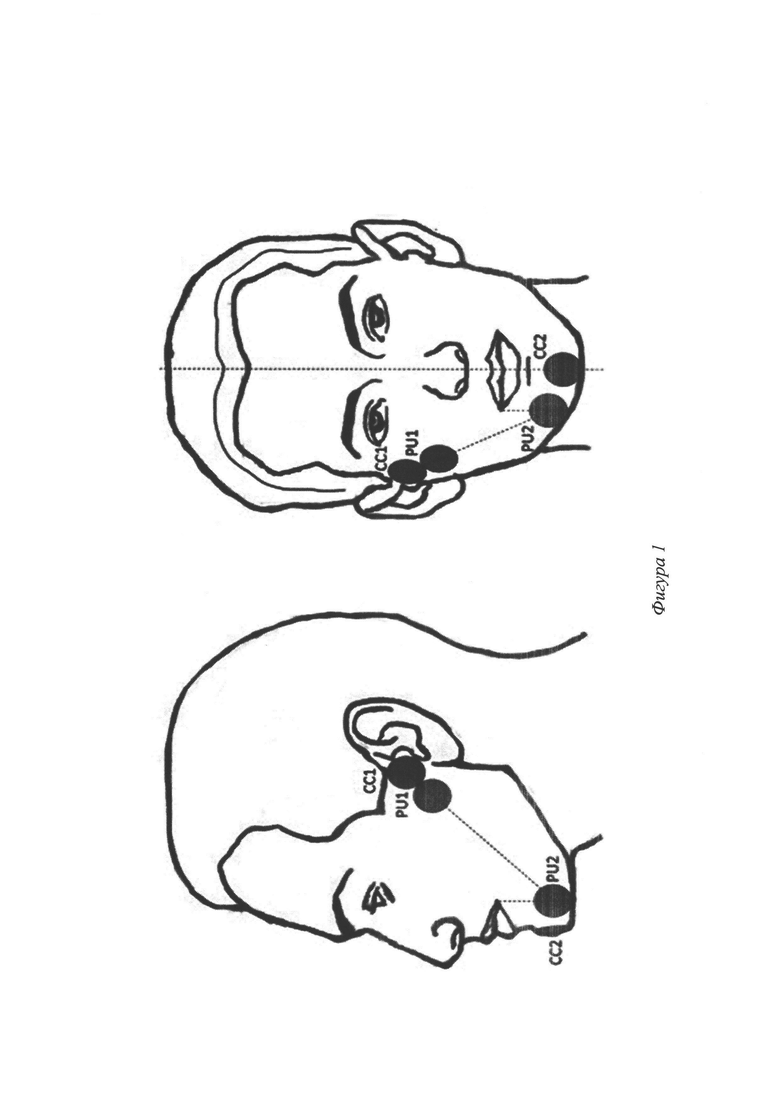
Для решения поставленной технической задачи разработан способ применения региональной биоимпедансометрии щечной области,, осуществляемый методом тетраполярной биоимпедансометрии с расположением потенциальных и токовых электродов непосредственно на границах исследуемой области, определенных четкими анатомическими ориентирами. Для измерения электрического сопротивления щечной области лица используют два токовых электрода, из которых один накладывают на дистальном участке скуловой дуги выше и кпереди от козелка уха, касаясь его задним краем клеящей части электрода, второй располагают по центру подбородка, при этом центр электрода ориентирован через центральную линию лица, нижним краем клеящей части касаясь нижнего края подбородка; и два потенциальных электрода, которые накладывают на границе исследуемой области таким образом, что центр одного электрода располагается на линии, являющейся перпендикуляром, опущенным к нижнему краю нижней челюсти от угла рта соответствующей стороны, а нижний край клеящей части электрода касается нижнего края подбородка, и центр второго электрода располагается на линии, соединяющей первый токовый и первый потенциальный электрод, задним краем клеящей части касаясь первого токового электрода. Схема расположения электродов представлена на фиг. 1, где СС1, СС2 - токовые электроды; PU1, PU2 - потенциальные электроды. При подобном расположении электродов в область исследования попадает участок щеки, включающий следующие анатомические образования: кожу и подкожную жировую клетчатку, мышечный слой, образованный волокнами щечной мышцы, слизистую оболочку и подслизистый слой, а также образования, располагающиеся в толще щеки - жировое тело щеки и крупные сосуды: лицевая артерия и вена.
Для проведения исследования используются одноразовые самоклеящиеся неонатальные кардиографические электроды с уменьшенным диаметром клеящей части, диаметр основы которых составляет 26 мм. Подобные электроды благодаря их небольшому размеру позволяют разместить их на ограниченном участке челюстно-лицевой области без наложения, а благодаря наличию самоклеящейся части дают хорошую фиксацию с постоянным давлением на участке лица со сложной конфигурацией.
Таким образом, измерение импеданса выполняется на одном и том же участке щечной области, определенном четкими анатомическими параметрами, что позволяет уменьшить погрешность измерений. Кроме того, обеспечивается более точное определение сопротивления на исследуемом участке щечной области за счет фиксации показаний сопротивления на границах исследуемого региона в отличие от методов, предполагающих оценку импеданса всей головы относительно туловища человека. Предложенный способ позволяет осуществлять измерение электрического сопротивления тканей челюстно-лицевой области без использования внутриротовых электродов, доставляющих дискомфорт пациенту.
Осуществление изобретения
Предложенный способ применения региональной биоимпедансометрии был апробирован на 30 пациентах, перенесших операции сложного удаления третьих моляров нижней челюсти. Полученные значения импеданса и их разница до операции, на 1-е, 3-й, 5-е, 7-е и 14-е сутки показали снижение сопротивления тканей щечной области на 1-е сутки после операции, с дальнейшим уменьшением значений импеданса к 3-им суткам и постепенным восстановлением этих значений в дни последующих измерений, что коррелировало с данными клинических наблюдений степени выраженности коллатерального отека щечной области при внешнем осмотре врачом-стоматологом.
Клинический пример.
Пациент А., 26 лет обратился с жалобами на периодически возникающие боли в области угла нижней челюсти справа. При внешнем осмотре конфигурация лица не изменена. Регионарные лимфатические узлы не увеличены, безболезненные. Открывание рта свободное, в объеме до 5 см. В полости рта слизистая оболочка альвеолярных отростков бледно-розового цвета, умеренно увлажнена, без видимых патологических изменений. Слизистая оболочка в области зуба 4.8 незначительно гиперемирована, умеренно увлажнена, при пальпации безболезненна. Зуб 4.8 частично прорезался через слизистую оболочку. На ортопантомограмме: зуб 4.8 имеет мезиальный наклон. Коронковая часть зуба 4.8 прилежит к дистальной поверхности зуба 4.7. Рентгенологически верхушки корней зуба 4.8 накладываются на нижнечелюстной канал. Костных деструктивных изменений не выявлено.
Диагноз (МКБ-10): Ретенированный зуб 4.8
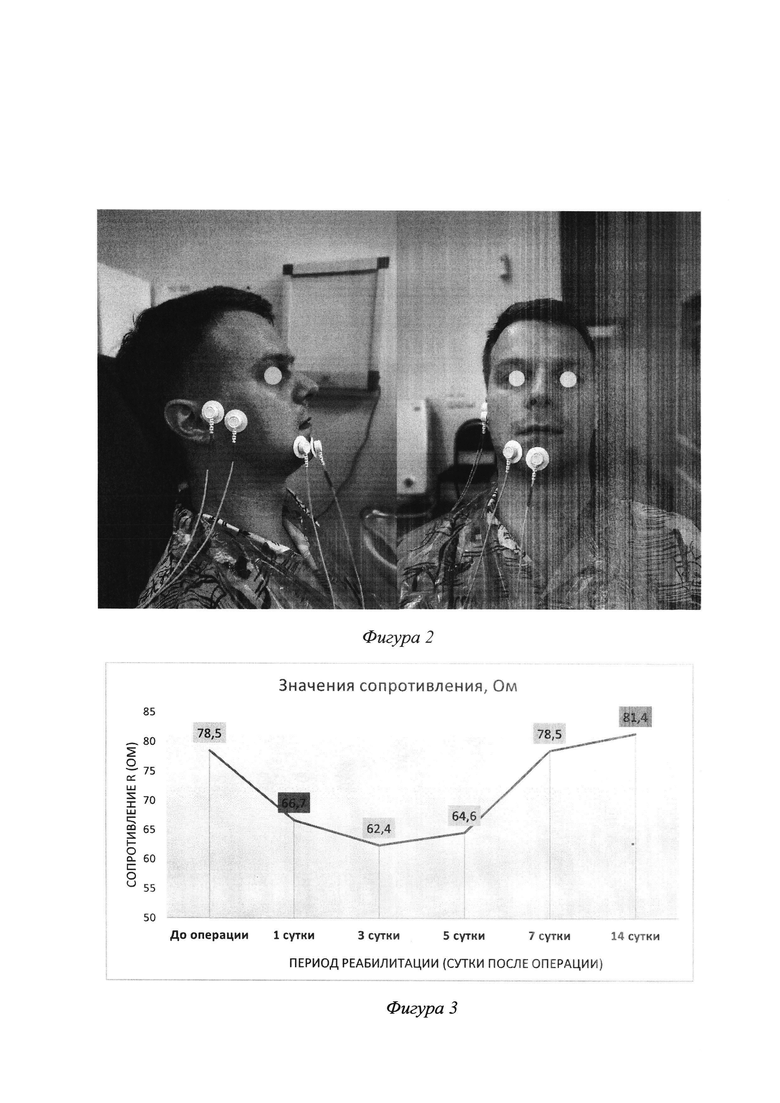
Контрольные биоимпедансные измерения сопротивления тканей челюстно-лицевой области на стороне предполагаемого оперативного вмешательства произведены с помощью аппарата для биоимпедансной спектроскопии и программного обеспечения АВС-01 «МЕДАСС» в соответствии с описанной выше схемой расположения электродов (Фигура 2).
Протокол операции: под инфильтрационной и проводниковой анестезией 4% раствором артикаина 3,4 мл с вазоконстриктором в концентрации 1:100000, произведен разрез из ретромолярной области правой стороны до дистальной поверхности зуба 4.7, внутрибороздковый разрез по вестибулярной поверхности зуба 4.7, далее опущен до переходной складки. Отслоен слизисто-надкостничный лоскут. Зуб 4.8 визуализирован. При помощи фрез и физиодиспенсера под водяным охлаждением физиологическим раствором NaCl 0.9% произведена остеотомия компактной пластинки нижней челюсти с вестибулярной стороны. Зуб 4.8 сегментирован и фрагментарно удален. Кюретаж. Антисептическая обработка операционной области 0,05% раствором хлоргексидина биглюконата. Гемостаз. Кровяной сгусток в лунке сформировался. Лоскут мобилизован и уложен на место. Ушит простыми узловыми швами нитью Монофил 4-0. В лунку 4.8 введена йодоформная турунда.
В послеоперационном периоде пациенту назначен антибиотик «Амоксиклав» 625 мг по 1 таб. 2 раза в день в течение 7 дней, нестероидный противовоспалительный препарат «Нимесил» 100 мг по 1 дозе 1 раз в день в течение 3 дней, ротовые ванночки 0,05% раствором хлоргексидина биглюконата 3 раза в день в течение 14 дней. Послеоперационное течение без особенностей, динамическое наблюдение и замена йодоформной турунды проводилось на 1-е, 3-й, 5-е, 7-е и 14-е сутки. Швы сняты на 7-е сутки.
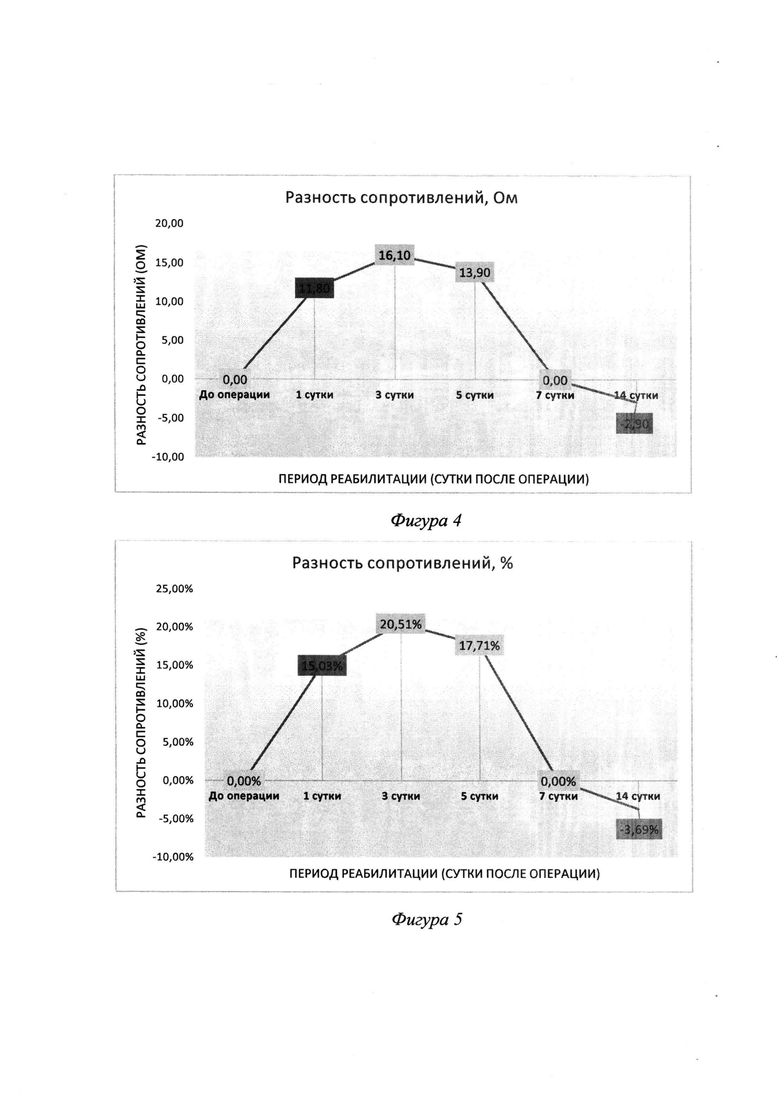
Значения импеданса тканей челюстно-лицевой области на стороне оперативного вмешательства на частоте 5 кГц составляли: до операции - 78,5 Ом, на 1-е сутки - 66,7 Ом, на 3-й сутки - 62,4 Ом, на 5-е сутки - 64,6 Ом, на 7-е сутки - 78,5 Ом, на 14-е сутки - 81,4 Ом (Фиг. 3). Также приведены графики абсолютной и относительной разности импедансов щечной области в указанные периоды, представленные на диаграммах (Фиг. 4, 5).
Приведенный клинический пример, а также измерения, проведенные с использованием описанного способа применения региональной биоимпедансометрии щечной области у 30 пациентов, перенесших операции сложного удаления зубов, показывают возможность применения предложенного способа для определения импеданса щечной области.
Краткое описание чертежей
Фигура 1. Представлена схема расположения электродов на коже лица человека для проведения реиональной биоимпедансометрии щечной области.
Фигура 2. На фотографии наглядно показана фиксация электродов на лице пациента А.
Фигура 3. Представлена диаграмма полученных значений импеданса щечной области до операции, на 1-е, 3-й, 5-е, 7-е и 14-е сутки у пациента А.
Фигура 4. Диаграмма абсолютной разности импедансов щечной области на исследуемом участке до операции, на 1-е, 3-й, 5-е, 7-е и 14-е сутки у пациента А.
Фигура 5. Диаграмма относительной разности импедансов щечной области до операции, на 1-е, 3-й, 5-е, 7-е и 14-е сутки у пациента А.
Список литературы
1. Литвицкий П.Ф., Патофизиология. В 2 т. Т. 2: учебник / П.Ф. Литвицкий. - 5-е изд., перераб. и доп.- М.: ГЭОТАР-Медиа, 2016. - с. 351-380.
2. Хирургическая стоматология: учебник / В.В. Афанасьев [и др.]; под общ. ред. В.В. Афанасьева. - 3-е изд., перераб. - М.: ГЭОТАР-Медиа, 2016. - 400 с.
3. Патент РФ RU2204938 C1, 27.05.2003
4. Патент США №4291708, кл. А61В 5/05
5. Патент РФ 2016152108, 28.02.2018
6. Патент РФ RU2578908 C1, 27.03.2016
7. Dylke E.S., Ward L.C. Three Decades of Bioelectrical Impedance Spectroscopy in Lymphedema Assessment: An Historical Perspective. Lymphat Res Biol. №19(3), 2021, p. 206-214.
8. Pichonnaz C., Bassin J.P., Currat D., Martin E., Jolles B.M. Bioimpedance for oedema evaluation after total knee arthroplasty. Physiother Res Int. №18(3), 2013, p. 140-147.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЕРИОПЕРАЦИОННОГО ВЕДЕНИЯ ПАЦИЕНТОВ С ИСПОЛЬЗОВАНИЕМ НУТРИТИВНОЙ ПОДДЕРЖКИ В СИПИНГОВОЙ ФОРМЕ В СОЧЕТАНИИ С ИНЪЕКЦИЯМИ ГЛЮКОКОРТИКОИДОВ ПРИ ХИРУРГИЧЕСКИХ СТОМАТОЛОГИЧЕСКИХ ВМЕШАТЕЛЬСТВАХ | 2022 |
|
RU2783692C1 |
| СПОСОБ УСТРАНЕНИЯ ОРОАНТРАЛЬНОГО СОУСТЬЯ С ПОМОЩЬЮ ЖИРОВОГО ТЕЛА ЩЕКИ ТОННЕЛЬНЫМ МЕТОДОМ | 2022 |
|
RU2803983C1 |
| СПОСОБ НАЛОЖЕНИЯ КИНЕЗИОЛОГИЧЕСКОЙ ПОВЯЗКИ ДЛЯ ЛИМФОДРЕНАЖНОЙ ФУНКЦИИ В ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ ПОСЛЕ ОРТОГНАТИЧЕСКИХ ОПЕРАЦИЙ | 2023 |
|
RU2817472C1 |
| Пенная композиция для склерозирующей терапии венозных мальформаций головы и шеи у детей и способ проведения терапии с ее применением | 2021 |
|
RU2777202C1 |
| СПОСОБ РЕГИОНАЛЬНОЙ БИОИМПЕДАНСОМЕТРИИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1996 |
|
RU2094013C1 |
| СПОСОБ ЛЕЧЕНИЯ КИСТ ЧЕЛЮСТЕЙ | 2014 |
|
RU2578161C2 |
| Способ динамической коррекции паралича мышц, иннервируемых краевой нижнечелюстной ветвью лицевого нерва | 2020 |
|
RU2743846C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСТРАКРАНИАЛЬНЫХ АРТЕРИОВЕНОЗНЫХ МАЛЬФОРМАЦИЙ ГОЛОВЫ И ШЕИ | 2023 |
|
RU2841253C2 |
| СПОСОБ ЛЕЧЕНИЯ ФЛЕГМОН ГЛУБОКОЙ ОБЛАСТИ ЛИЦА | 1991 |
|
RU2068655C1 |
| Способ реваскуляризации аутотрансплантата в челюстно-лицевой области | 2018 |
|
RU2678040C1 |
Изобретение относится к области медицинской диагностики, а именно к способам региональной биоимпедансометрии для определения импеданса щечной области у пациентов при операциях в полости рта и челюстно-лицевой области, и может быть использовано в восстановительной медицине, функциональной диагностике, хирургической стоматологии и челюстно-лицевой хирургии. При этом на пациента накладывают токовые электроды, подключенные к генератору высокочастотного тока, и потенциальные электроды, подключенные к измерителю высокочастотного напряжения. Измеряют импеданс тканей и определяют разницу импеданса на разных этапах до- и послеоперационного периода. Используют два токовых электрода, из которых один накладывают на дистальном участке скуловой дуги выше и кпереди от козелка уха, касаясь его задним краем клеящей части электрода. Второй электрод располагают по центру подбородка. Центр электрода ориентирован через центральную линию лица, нижним краем клеящей части касаясь нижнего края подбородка. Два потенциальных электрода накладывают на границе исследуемой области таким образом, что центр одного электрода располагается на линии, являющейся перпендикуляром, опушенным к нижнему краю нижней челюсти от угла рта соответствующей стороны, а нижний край клеящей части электрода касается нижнего края подбородка. Центр второго электрода располагается на линии, соединяющей первый токовый и первый потенциальный электрод, задним краем клеящей части касаясь первого токового электрода. Достигается расширение области применения способа региональной биоимпедансометрии с более точной регистрацией изменения импеданса за счет расположения электродов на границах исследуемой области в строго определенных точках, что позволяет получать значения линейного напряжения на относительно однородном участке без значительных искажений с уменьшенной погрешностью измерений, а также без использования внутриротовых электродов, доставляющих дискомфорт пациенту. 5 ил., 1 пр.
Способ применения региональной биоимпедансометрии для определения импеданса щечной области у пациентов при операциях в полости рта и челюстно-лицевой области, заключающийся в том, что на пациента накладывают токовые электроды, подключенные к генератору высокочастотного тока, и потенциальные электроды, подключенные к измерителю высокочастотного напряжения, измеряют импеданс тканей на этом участке и определяют разницу импеданса на разных этапах до- и послеоперационного периода; отличающийся тем, что используют два токовых электрода, из которых один накладывают на дистальном участке скуловой дуги выше и кпереди от козелка уха, касаясь его задним краем клеящей части электрода, второй располагают по центру подбородка, при этом центр электрода ориентирован через центральную линию лица, нижним краем клеящей части касаясь нижнего края подбородка; и два потенциальных электрода, которые накладывают на границе исследуемой области таким образом, что центр одного электрода располагается на линии, являющейся перпендикуляром, опушенным к нижнему краю нижней челюсти от угла рта соответствующей стороны, а нижний край клеящей части электрода касается нижнего края подбородка, и центр второго электрода располагается на линии, соединяющей первый токовый и первый потенциальный электрод, задним краем клеящей части касаясь первого токового электрода.
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАННИХ ОСЛОЖНЕНИЙ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ | 2015 |
|
RU2578908C1 |
| УСТРОЙСТВО ДЛЯ ИЗМЕРЕНИЯ ИМПЕДАНСА | 1998 |
|
RU2140190C1 |
| ИЗМЕРИТЕЛЬ ВЛАГОСОДЕРЖАНИЯ | 2011 |
|
RU2601104C2 |
| US 5772605 A, 30.06.1998 | |||
| CN 208447812 U, 01.02.2019 | |||
| US 2018161136 A1, 14.06.2018 | |||
| KR 20180047088 A, 10.05.2018 | |||
| WO 2017034368 A1, 02.03.2017 | |||
| US 2010069779 A1, 18.03.2010 | |||
| Предохранительное устройство для внутрикуркового спускового механизма спортивно-охотничьего ружья | 1978 |
|
SU727969A2 |
Авторы
Даты
2022-08-15—Публикация
2022-01-20—Подача