Настоящее изобретение относится к нанокомпозитам, обладающим диагностическими, терапевтическими и тераностическими свойствами, то есть способными одновременно реализовывать диагностические (двухканальная диагностика) и терапевтические эффекты и способу их изготовления, а именно, к магнитным наночастицам, сформированным на основе гадолиний-содержащих соединений, в том числе и биметаллических, которые инкапсулированы в макромолекулы полисахаридов (арабиногалактана и арабиногалактана-сырца) и способам их изготовления. Магнитные нанокомпозиты, согласно настоящему изобретению, обладают растворимостью воде и коллоидной стабильностью, а также одновременно отличаются эффектом контрастирования МРТ и эффектом лечения опухоли, тем самым могут эффективно использоваться в качестве диагностических, терапевтических и тераностических нанокомпозитов, способных одновременно выполнять диагностику (двухканальную) и лечение.
Онкологические заболевания занимают одно из первых мест среди причин смертности населения как экономически развитых, так и отстающих стран. На практике это миллионы человеческих жертв каждый год, сопоставимые с непрекращающейся мировой войной. В связи с такой остротой актуальности проблемы онкозаболеваний, уже созданы и постоянно разрабатываются многочисленные новые подходы к ее решению (основанные на разнообразных химиотерапевтических, радиационно-лучевых, биологических и др. принципах).
Одним из наиболее используемых методов лечения злокачественных опухолей является проникающая лучевая терапия, вызывающая дегенерацию опухолевой ткани и подавление роста ее клеток. При этом также наблюдаются серьезное побочное воздействие на здоровые ткани и системы органов человека в виде локальных и отдаленных последствий, включая вторичный радиационно-стимулированный онкогенез по всему организму вдоль канала ионизирующего радиационного луча (как перед опухолью, так и после нее) [«Bioinorganic Medicinal Chemistry». Wiley-VCH, Weinheim., 2011, 422 p., Cancer J. Clinic., 2012, 62, 75].
Принципиально выгодной альтернативой классической ионизирующей лучевой терапии является использование терано-статической магнитно-резонансной томографии (МРТ) - системы, которая может одновременно выполнять диагностику и лечение МРТ на одной платформе. Контрастные вещества для тераностатической МРТ делятся на две группы: Т1 (положительные) и Т2 (отрицательные) в зависимости от контрастного вещества. Контрастные вещества Т2 обычно состоят из суперпарамагнитных наночастиц оксида железа и демонстрирует темновое МР-изображение. С другой стороны, контрастные вещества T1 обычно включают парамагнитный гадолиний (Gd) в качестве основного металла, который существует в различных формах. Например, (1) наночастицы органического полимера, заполненные или окруженные ионами гадолиния или хелатными комплексами гадолиния, (2) дендримеры, ковалентно связанные с хелатными комплексами гадолиния, (3) липосомы, окруженные ионами гадолиния или хелатными комплексами гадолиния, и (4) хелатные комплексы гадолиния, например, Gd-DTPA (где DTPA - это диэтилентриаминпентауксусная кислота) [«Neutron capture therapy with Gd-DTPA in tumor-bearing rats.» New York: Plenum Press., 1996, Р. 865; Chem. Rev., 1999, 99, 2293].
Хотя каждому типу вышеописанных систем соответствуют определенные преимущества, существует серьезная проблема, заключающаяся в том, что ионы гадолиния быстро диффундируют из опухолей из-за его сильно гидрофильных свойств [Pure Appl. Chem., 2015, 87(2), 123; Future Med. Chem., 2016, 8, 899]. Было сделано много попыток соответствовать требованиям доставки и удерживания достаточного количества Gd в участках опухолей, таких как прямые внутриопухолевые инъекции комплекса гадопентеновая кислота/хитозан и Gd-содержащих эмульсий и микросфер [Biomaterials, 2012, 33, 247; J. Mater. Chem. B., 2013, 1, 6359]; артериальное введение Gd-микрокапсул [Pure Appl. Chem., 2015, 87(2), 123; Future Med. Chem., 2016, 8, 899] или системная инъекция Gd, нацеленнная на опухоль [Eur. J. Pharm. Biopharm., 2002, 54, 119; Злокач. опух., 2015, 1(10-23), 1028]. Согласно литературным данным, высвобождающиеся ионы гадолиния способствуют развитию нефротоксических и нейротоксических эффектов, панкреатиту, гемолизу эритроцитов и, в ряде случаев, развитию анафилактической реакции [American Journal of Roentgenology, 1996, 167(4), 847; Clinical Radiology, 2006, 61(11), 905; Медицинская визуализация, 2004, 5, 130; Вестник рентгенологии и радиологии, 2006, 5, 54; ЕДИАТР, 2016, 7(1), 97].
Кроме того, известно, что существует целый ряд заболеваний, которые, в силу своей локализации, принципиально плохо поддаются своевременной диагностике и лечению. Прежде всего - это заболевания головного мозга, на пути кровоснабжения которого существует гематоэнцефалический барьер, защищающий от попадания из кровотока в мозг чужеродных соединений и объектов [Curr. Pharm. Design., 2017, 23, 1]. Таким образом, в головной мозг потенциально трудно или невозможно вообще доставить многие традиционные терапевтические и диагностические агенты [Curr. Pharm. Design., 2017, 23, 1; Curr. Neuropharm., 2008, 6, 179]. Более того, заболевания головного мозга, например, онкологические, также трудно поддаются и оперативному лечению, так как крайне сложно осуществить оперативное вмешательство в головной мозг, не нарушив какую-либо из его функций.
Одним из наиболее перспективных способов преодоления гематоэнцефалического барьера на сегодняшний день считается использование наноразмерных частиц определенного размера [Sci. Rep., 2020, 10, 18220; Nanomedicine, 2018, 13(13), 1513; Pharmaceutics, 2018, 10, 269], а именно, диаметром от 3 до 10 нм. Но, несмотря на то, что такие частицы демонстрируют скорость релаксации r1, которая почти вдвое больше, чем у Gd-DTPA, они обычно не отличаются высокой растворимостью в воде и коллоидной стабильностью, а синтез таких частиц технически сложен.
Например, наиболее часто используемый метод синтеза наночастиц гадолиния - это стабилизация формирующихся или уже сформированных наночастиц с помощью диоксида кремния [ACS Appl. Nano Mater. 2021, 4(4), 3767; Nanomaterials 2020, 10, 1341; Journal of Physics: Conf. Series., 2020, 1461, 012111]. Однако, кремнеземом не только выполняет защитно-стабилизирующие свойства по отношению к наночастицам оксида гадолиния, но и ингибирует возможности взаимодействие Gd2O3 с водой, что приводит к ухудшению скорости релаксации.
Известен способ получения наночастиц гадолиния, инкапсулированных углеродом [US10548993B2]. Результирующие Gd@C-структуры растворяются в воде, биологически инертны и препятствуют выбросу металла в биологические среды. Кроме того, несмотря на размеры, превышающие общепризнанный порог почечного клиренса, данные наночастицы могут эффективно выводиться с мочой после систематических инъекций. К сожалению, авторы патента не привели никаких данных о способности наночастиц проходить через гематоэнцефалический барьер, а используемые ими методики синтеза сложны и требуют применения высоких температур (300°С).
Известен способ покрытия наночастиц Gd2O3 полимерами, например, полиакриловой кислотой (Mw 5100 Да) [RSC Adv., 2018, 8, 3189]. Авторы отметили, что в данном случае полиакриловая кислота выполняет роль не только стабилизатора, но и способствует гидрофилизации поверхности наночастиц. Было показано, что коллоидная суспензия Gd2O3 позволяет получить высококонтрастные МРТ-изображения T1 в различных органах мыши после внутривенного введения и, в конечном итоге, выводиться через почечную систему. Данные о возможном накоплении рассматриваемых нанокомпозитов в мозге, а также их детальные магнитные параметры в работе не приводятся.
Известен способ стабилизации наночастиц Gd2O3 с помощью полисахаридов, например, декстрозой и ее модифицированных аналогов [Journal of Magnetism and Magnetic Materials, 2016, 403, 118]. Причем было показано, что молекулярная масса декстрозы влияет на стабильность, размер и морфологию Gd2O3 наночастиц, а также на эффективность покрытия. Исследования цитотоксичности показали, что концентрации Gd 0.2 мМ и ниже не были токсичными. К сожалению, данные о магнитных характеристиках наночастиц, а также о значениях релаксивности r1 и r2 были получены при значительно более высоких концентрациях Gd.
Для минимизации высвобождения ионов гадолиния из структуры при сохранении высокой полезной нагрузки был предложен метод легированные наночастицы гадолиния (GdNP) другими металлами [например, US10786582; US2018/0264145A1]. Хотя такие частицы отличаются приемлемыми значениями T1, их редко используют в качестве контрастных агентов для МРТ in vivo. Это связано с тем, что метод модификации поверхности для образования достаточно хорошо водорастворимых и стабильных гадолиний-содержащих наночастиц пока не известен.
С другой стороны, были предприняты попытки легирования наночастиц с помощью гадолиния, например, легирование наночастиц магнетита. Недостатком данного способа является то, что полученные модифицированные нанокомпозиты магнетита обладают относительно низкими значениями скорости релаксации r1 и r2, что затрудняет проведение эффективной МРТ-диагностики, даже с учетом того, что биметаллические наночастицы, содержащие Fe и Gd, позволяют реализовать двухканальную диагностику.
Например, известен способ легирования наночастиц магнетита гадолинием [JACS, 2009, 131, 6336] путем смешивания Fe(acac)3 и Gd(acac)3 с 1,2-гексадекандиолом в диэтиловом эфире, перемешивания смеси в течении 20 мин при комнатной температуре, нагревания полученной смеси до 100°С в атмосфере инертного газа до образования оранжевого раствора, добавления в смесь олеиновой кислоты и олеиламина с последующим повышением температуры до 260°С и выдерживания при данной температуре 22 часа, охлаждения до комнатной температуры, добавления спирта, отделения наночастиц, их редиспергирования в неполярном растворителе. Недостаток данного способа заключается в том, что рассматриваемые легированные гадолинием наночастицы магнетита обладают относительно невысокой намагниченностью насыщения, процедура синтеза требует довольно жестких условий (выдерживание реакционной смеси при 260°С 22 часа), а также отсутствуют какие-либо сведения как о токсичности данных наночастиц, так и о возможности преодоления данными наночастицами гематоэнцефалического барьера.
Известен способ легирования наночастиц магнетита гадолинием [Advanced Materials, 2012, 24, 6223] путем смешения смеси олеата железа (III) и олеата гадолиния (III) с олеиновой кислотой в октадецене, нагрева смеси до температуры кипения в атмосфере инертного газа (скорость тока газа 5°С/мин), выдерживания при данной температуре 2 часа, охлаждения до комнатной температуры, добавления спирта, отделения наночастиц, их редиспергирования в неполярном растворителе и обработка наночастиц органическим гидрофильным модификатором. Недостаток данного метода заключается низкой гидрофильности результирующих нанокомпозитов, а также достаточно низкими значениями скорости релаксации r1 и r2.
Известен способ получения модифицированных наночастиц магнетита, легированных гадолинием [№2738118C1 RU от 17.06.2020. (Бюл. №34. МПК C01G 49/08, B82B 3/00, A61K 103/34, B82Y 40/00)], путем смешения водного раствора, содержащего смесь FeCl2⋅4H2O и GdCl3⋅6H2O (FeCl2⋅4H2O/GdCl3⋅6H2O=2.5/1.2), с водным раствором бензоата натрия, добавление в полученный раствор ацетонитрила, перемешивание смеси до образования осадка, отделение образовавшегося осадка от надосадочной жидкости, промывку осадка диэтиловым эфиром, сушку осадка на воздухе, его смешение с олеиламином, олеиновой кислотой и дибензиловым эфиром, нагрев полученной смеси до 110°С в атмосфере инертного газа с последующим повышением температуры до 310°С и выдерживанием при этой температуре 30 мин, охлаждение смеси до комнатной температуры в атмосфере инертного газа, добавление спирта, отделение частиц, их редиспергирование в гексане и обработку наночастиц органическим гидрофильным модификатором (Pluronic F-127, представляющий собой блок-сополимер полиоксиэтилена и полиоксипропилена). Недостаток данного способа заключается в слишком громоздкой методике синтеза, недостаточно хорошей растворимости результирующих наночастиц, невысокими значениями скорости релаксации r1 и r2, а также отсутствии данных о токсичности рассматриваемых нанокомпозитов и возможности преодоления гематоэнцефалического барьера.
Можно согласиться с литературным выводом [Поверхн., 2010, 2, 355], что основная проблема эффективной магнитно-резонансной томографии злокачественных новообразований вообще - получение новых малотоксичных препаратов, обладающих высокими нейтроннозахватными свойствами и способностью селективно накапливаться в опухоли. Кроме того, становится понятным, что, несмотря на впечатляющие успехи в тераностики опухолей различной локализации с помощью, например, гадолиний-содержащих препаратов, онкологические заболевания с локализацией конкретно в головном мозге еще практически не охвачены этими перспективным методом вследствие трудной преодолимости гематоэнцефалического барьера и слабой накапливаемости в опухоли многих существующих нейтрон-чувствительных тераностических препаратов. Практически не реализованы также перспективные возможности по двухканальной (гадолиний-, бор-нейтронозахватной и магнито-гипертермической) терапии и параллельной визуализирующей диагностике (тераностике) опухолей головного мозга.
С другой стороны известно, что молекулы, подобные арабиногалактану (AG) лиственницы сибирской, обладают способностью как проникать в головной мозг через гематоэнцефалический барьер, так и выполнять роль транспортной полимерной матрицы, которая позволяет наночастицам металлов проникать в мозг, а также выступать в качестве их стабилизатора [Nanotechnologies in Russia, 2015, 10(7-8), 640; Nano Hybrids and Composites, 2017, 13, 263; RU 2611999].
Сущность заявляемого решения заключается в том, что в качестве водорастворимых магнитных нанокомпозитов предлагается использовать гадолиний-содержащие наночастицы (Gd2O3, GdBO3), в том числе и биметаллические (содержащие Gd и Fe), способность которых к преодолению гематоэнцефалического барьера, а значит и реализации возможности параллельной многоканальной диагностики и терапии онкологических заболеваний головного мозга обеспечивается применением макромолекул полисахарида, выбранного из арабиногалактана и арабиногалактана-сырца, в качестве стабилизирующей и транспортной матрицы.
Ближайшим известным решением аналогичной задачи по технической сущности являются водорастворимые магнитоактивные нанобиокомпозиты флавоноидных комплексов гадолиния на основе природного конъюгата арабиногалактана с биофлавоноидами, описанный в патенте №2706705 RU от 28.03.2019 (Бюл. №32. МПК C08B 37/00, A61K 9/14, A61K 49/00, A61K 49/06, A61K 49/10, A61K 49/18, B82Y 5/00). Водорастворимые нанокомпозиты, представляющие собой наночастицы металлокомплексных соединений биофлавоноидов, содержащихся в арабиногалактане-сырце (природном конъюгате арабиногалактана и биофлованоидов), и Gd(III), инкапсулированные в макромолекулы арабиногалактана (обладающие магнитными свойствами, в частности, высокой способностью сокращать время магнитной релаксации протонов воды, в виде стабильных водорастворимых порошков с размером наночастиц комплексов гадолиния 1-100 нм и содержанием гадолиния в композите 0.8-9.1%) получали через взаимодействие водного раствора соли гадолиния с водным раствором арабиногалактана-сырца в присутствии водного раствора аммиака для создания нейтральной среды при комнатной температуре 20-25°С и последующее осаждение в ацетон или этанол, или другой смешивающийся с водой органический растворитель и фильтрование. Основной недостаток данной методики заключается в том, что, являясь одноэлементными нанокомпозитами (содержат только гадолиний), они не могут реализовывать возможности двухканальной тераностики. Кроме того, в патенте отсутствует подробное описание магнитных параметров рассматриваемых нанокомпозитов.
Поставленная задача достигается следующим образом:
1) к водному раствору, содержащему макромолекулы полисахарида (арабиногалактан или арабиногалактан-сырец), при комнатной температуре (20-25°С) добавляют водный раствор хлорида гадолиния(III) или смесь хлоридов гадолиния(III) и железа(III). Далее по каплям добавляют 25%-ный водный раствор аммиака до достижения pH=7.0 результирующим раствором. Затем полученный раствор перемешивают в течение 2-х часов, а образовавшийся целевой гибридный нанобиокомпозит выделяется осаждением в этанол или другой смешивающийся с водой органический растворитель, осадок фильтруется, промывается тем же растворителем и сушится в эксикаторе (рисунок 1 и 2, таблица 1, примеры 1-4, 7).
2) к водному раствору, содержащему наночастицы Gd2O3, находящиеся в макромолекулах арабиногалактана (см. пункт 1), при комнатной температуре (20-25°С) добавляют водный раствор H3BO3. Результирующий целевой раствор при комнатной температуре перемешивается 2 часа, а образовавшийся целевой гибридный нанобиокомпозит выделяется осаждением в этанол или другой смешивающийся с водой органический растворитель, осадок фильтруется, промывается тем же растворителем и сушится в эксикаторе (рисунок 1 и 2, таблица 1, пример 6).
Содержание гадолиния, бора и железа в полученных образцах, определенное элементным анализом и рентгеновским энергодисперсионным микроанализом, варьируется в зависимости от исходного соотношения соли гадолиния к H3BO3 или соли железа, а также к содержанию полисахарида (арабиногалактана или арабиногалактана-сыреца) (Примеры 1-7). Диапазон содержания гадолиния в нанокомпозитах составляет 1,7-18 мас. %. По данным просвечивающей электронной микроскопии, размеры металлокомплексных наночастиц составляют 1-100 нм (Рисунок 1).
Показано, что рассматриваемые нанобиокомпозиты уже при комнатной температуре являются магнетиками с интенсивным сигналом электронного парамагнитного резонанса (ЭПР) ΔH<900 Гс (Рисунок 2).
Для всех образцов получены полевые зависимости намагниченности при 5 и 320 K в магнитных полях до 15 кЭ, и исследована температурная зависимость магнитной восприимчивости в интервале температуры 5-320 K в магнитном поле 10 кЭ (см. Таблица 1, Пример 8). Полученные данные о намагниченности образцов и их магнитной восприимчивости свидетельствуют о том, что все синтезированные нанобиокомпозиты, а именно, Gd2O3, инкапсулированные в макромолекулы арабиногалактана и арабиногалактана-сырца, а также GdBO3 и биметаллические структуры, содержащие Fe и Gd, инкапсулированные в макромолекулы арабиногалактана, в этом интервале температуры являются парамагнетиками.
Установлено, что синтезированные магнитные нанобиокомпозиты описываются одинаковым по сравнению с традиционно используемой в качестве МРТ-контраста гадопентетовой кислотой (т.н. Magnevist [American Journal of Roentgenology., 1996, 167, 847]) значением Т1, что является главной характеристикой при использовании подобных субстанций в МРТ (Пример 9).
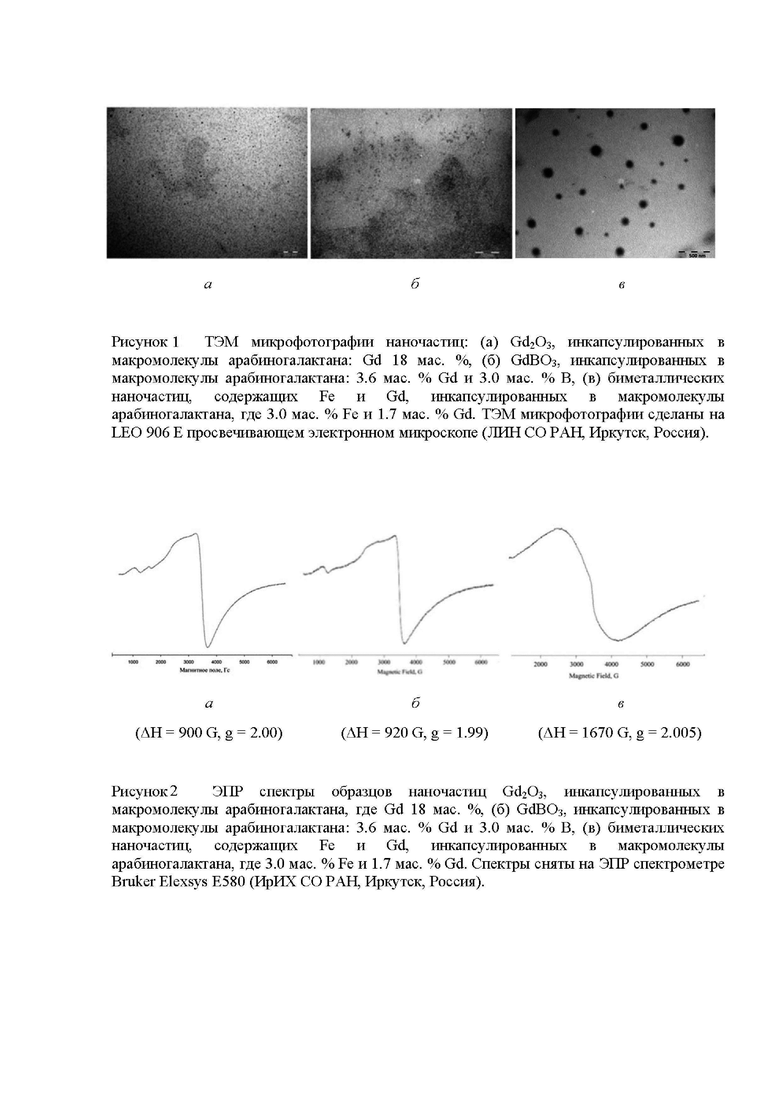
На рисунке 1 представлены ТЭМ микрофотографии (1) наночастиц Gd2O3, инкапсулированных в макромолекулы: (а) арабиногалактана, где Gd 18 мас.%, (б) арабиногалактан-сырца, где Gd 11.5 мас.%; (2) GdBO3, инкапсулированных в макромолекулы арабиногалактана: 3.6 мас.% Gd и 3.0 мас.% B; (3) биметаллических наночастиц, содержащих Fe и Gd, инкапсулированных в макромолекулы арабиногалактана, где 3.0 мас.% Fe и 1.7 мас.% Gd.
На рисунке 2 представлены типичные ЭПР спектры, полученных гибридных нанокомпозитов: (а) арабиногалактана, где Gd 18 мас.%, (б) арабиногалактан-сыреца, где Gd 11.5 мас.% и (в) биметаллических наночастиц, содержащих Fe и Gd, инкапсулированных в макромолекулы арабиногалактана, где 3.0 мас.% Fe и 1.7 мас.% Gd, (г) GdBO3, инкапсулированных в макромолекулы арабиногалактана: 3.6 мас.% Gd и 3.0 мас.% B.
В таблице 1 представлены результаты СКВИД магнетометрии синтезированных образцов (по методикам, описанным в примерах 1-3, 6, 7).
Заявителем не выявлены источники, содержащие информацию о технических решениях, идентичных настоящему изобретению, что позволяет сделать вывод о его соответствии критерию «новизна».
Отличительной особенностью настоящего изобретения является:
- простота (исходные вещества - это коммерчески доступные компоненты, не требующие предварительной подготовки и обработки; все манипуляции проводятся на воздухе, при комнатной температуре (20-25°С) в одном реакционном сосуде);
- конечный продукт, а именно гадолиний-содержащие гибридные нанокомпозиты (Gd2O3, GdBO3 и биметаллические, содержащие Fe и Gd, инкапсулированные в макромолекулы полисахарида (арабиногалактан или арабиногалактан-сырец) - это стабильные порошкообразные вещества, сохраняющие свои физико-химические параметры в течение длительного промежутка времени;
- возможность одновременной реализации диагностических (магнитоконтрастных и люминесцентных, необходимых для дополнительной реализации принципов визуальной диагностики “в окне прозрачности" биотканей) и терапевтических (нейтронозахватных и магнито-гипертермических) методов;
- возможность реализации двухканальной тераностики благодаря наличию в одном образце наночастиц, содержащих сразу два элемента, например, бор и гадолиний, или железо и гадолиний.
Заявителем не обнаружены какие-либо источники информации, содержащие сведения о влиянии заявленных отличительных признаков на достигаемый вследствие их реализации технический результат. Это, по мнению заявителя, свидетельствует о соответствии данного технического решения критерию «изобретательский уровень».
Следующие примеры иллюстрируют изобретение.
Пример 1.
Навеску арабиногалактана массой 1 г растворяли в 3 мл воды и к полученному раствору прикапывали растворенный GdCl3⋅6H2O (0.83 г) в 2 мл деионизированной воды при постоянном перемешивании. Раствор перемешивали в течении 15 мин, при этом никаких видимых изменений с раствором не происходило. Далее значение рН раствора доводили до нейтрального (рН=7.0), прикапывая водный раствор аммиака (25% раствор). Контроль за значением рН среды проводили при помощи ионометра ЭВ-74. При этом цвет реакционного раствора практически мгновенно изменялся до темно-коричневого. Реакционную смесь перемешивали при комнатной температуре (20-25°С) в течение 2 часов. Полученный продукт осаждали в 18 мл этилового спирта с последующим фильтрованием через воронку Шотта на вакууме. Готовый порошок нанокомпозита промывали на воронке Шотта этиловым спиртом порциями по 15 мл (шесть раз) и высушивали полученный продукт в эксикаторе над безводным CaCl2.
Выход полученного нанокомпозита составил 95,6% (в пересчете на гадолиний) с содержанием гадолиния 18 мас.%.
Пример 2.
Навеску арабиногалактана массой 1 г растворяли в 3 мл воды и к полученному раствору прикапывали растворенный GdCl3⋅6H2O (0.32 г) в 2 мл деионизированной воды при постоянном перемешивании. Раствор перемешивали в течение 15 мин, при этом никаких видимых изменений с раствором не происходило. Далее значение рН раствора доводили до нейтрального (рН=7.0), прикапывая водный раствор аммиака (25% раствор). Контроль за значением рН среды проводили при помощи ионометра ЭВ-74. При этом цвет реакционного раствора практически мгновенно изменялся до темно-коричневого. Реакционную смесь перемешивали при комнатной температуре (20-25°С) в течение 2 часов. Полученный продукт осаждали в 18 мл этилового спирта с последующим фильтрованием через воронку Шотта на вакууме. Готовый порошок нанокомпозита промывали на воронке Шотта этиловым спиртом порциями по 15 мл (шесть раз) и высушивали полученный продукт в эксикаторе над безводным CaCl2.
Выход полученного нанокомпозита составил 94,0% (в пересчете на гадолиний) с содержанием гадолиния 8 мас.%.
Пример 3.
Навеску арабиногалактана-сырца массой 1 г растворяли в 3 мл воды и к полученному раствору прикапывали растворенный GdCl3⋅6H2O (0.44 г) в 2 мл деионизированной воды при постоянном перемешивании. Раствор перемешивали в течение 15 мин, при этом никаких видимых изменений с раствором не происходило. Далее значение рН раствора доводили до нейтрального (рН=7.0), прикапывая водный раствор аммиака (25% раствор). Контроль за значением рН среды проводили при помощи ионометра ЭВ-74. При этом цвет реакционного раствора практически мгновенно изменялся до темно-коричневого. Реакционную смесь перемешивали при комнатной температуре (20-25°С) в течение 2 часов. Полученный продукт осаждали в 18 мл этилового спирта с последующим фильтрованием через воронку Шотта на вакууме. Готовый порошок нанокомпозита промывали на воронке Шотта этиловым спиртом порциями по 15 мл (шесть раз) и высушивали полученный продукт в эксикаторе над безводным CaCl2.
Выход полученного нанокомпозита составил 95% (в пересчете на гадолиний) с содержанием гадолиния 11.5 мас.%.
Пример 4.
Навеску арабиногалактана-сырца массой 1 г растворяли в 3 мл воды и к полученному раствору прикапывали растворенный GdCl3⋅6H2O (0.33 г) в 2 мл деионизированной воды при постоянном перемешивании. Раствор перемешивали в течение 15 мин, при этом никаких видимых изменений с раствором не происходило. Далее значение рН раствора доводили до нейтрального (рН=7.0), прикапывая водный раствор аммиака (25% раствор). Контроль за значением рН среды проводили при помощи ионометра ЭВ-74. При этом цвет реакционного раствора практически мгновенно изменялся до темно-коричневого. Реакционную смесь перемешивали при комнатной температуре (20-25°С) в течение 2 часов. Полученный продукт осаждали в 18 мл этилового спирта с последующим фильтрованием через воронку Шотта на вакууме. Готовый порошок нанокомпозита промывали на воронке Шотта этиловым спиртом порциями по 15 мл (шесть раз) и высушивали полученный продукт в эксикаторе над безводным CaCl2.
Выход полученного нанокомпозита составил 94% (в пересчете на гадолиний) с содержанием гадолиния 8.5 мас.%.
Пример 5.
Навеску арабиногалактана массой 1 г растворяли в 3 мл деионизированной воды и к полученному раствору прикапывали растворенный GdCl3⋅6H2O (0.15 г) в 2 мл деионизированной воды при постоянном перемешивании. Раствор перемешивали в течение 15 мин, при этом никаких видимых изменений с раствором не происходило. Далее значение рН раствора доводили до нейтрального (рН=7.0), прикапывая водный раствор аммиака (25% раствор). Контроль за значением рН среды проводили при помощи ионометра ЭВ-74. При этом цвет реакционного раствора практически мгновенно изменялся до темно-коричневого. Реакционную смесь перемешивали при комнатной температуре (20-25°С) в течение 2 часов. Полученный продукт осаждали в 18 мл этилового спирта с последующим фильтрованием через воронку Шотта на вакууме. Готовый порошок нанокомпозита промывали на воронке Шотта этиловым спиртом порциями по 15 мл (шесть раз) и высушивали полученный продукт в эксикаторе над безводным CaCl2.
Выход полученного нанокомпозита составил 95.4% (в пересчете на гадолиний) с содержанием гадолиния 3.6 мас.%.
Пример 6.
Навеску нанокомпозита, полученного в примере 2, массой 1 г растворяли в 3 мл деионизированной воды и к полученному раствору прикапывали раствор Н3⋅ВО3 (0.034 г, массовое отношение B/Gd=2.5) в 2 мл деионизированной воды при постоянном перемешивании. Реакционную смесь перемешивали при комнатной температуре (20-25°С) в течение 2 часов. Полученный продукт осаждали в 15 мл этилового спирта с последующим фильтрованием через воронку Шотта на вакууме. Готовый порошок нанокомпозита промывали на воронке Шотта этиловым спиртом порциями по 15 мл (шесть раз) и высушивали полученный продукт в эксикаторе над безводным CaCl2.
Выход полученного нанокомпозита составил 95% (в пересчете на гадолиний) с содержанием гадолиния 3.6 мас.% и бора 3.0 мас.%.
Пример 7.
Навеску арабиногалактана массой 1 г растворяли в 3 мл воды и к полученному раствору прикапывали растворенный GdCl3⋅6H2O (0.044 г) и FeCl3⋅6H2O (0.178 г) в 3 мл деионизированной воды при постоянном перемешивании (мас. отношение Fe/Gd=1.8). Раствор перемешивали в течение 15 мин, при этом никаких видимых изменений с раствором не происходило. Далее значение рН раствора доводили до нейтрального (рН=7.0), прикапывая водный раствора аммиака (25% раствор). Контроль за значением рН среды проводили при помощи ионометра ЭВ-74. При этом цвет реакционного раствора практически мгновенно изменялся до коричневого. Реакционную смесь перемешивали при комнатной температуре (20-25°С) в течение 2 часов. Полученный продукт осаждали в 18 мл этилового спирта с последующим фильтрованием через воронку Шотта на вакууме. Готовый порошок нанокомпозита промывали на воронке Шотта этиловым спиртом порциями по 15 мл (шесть раз) и высушивали полученный продукт в эксикаторе над безводным CaCl2.
Выход полученного нанокомпозита составил 95,3% (в пересчете на гадолиний) с содержанием гадолиния 1.7 мас.% и железа 3.0 мас.%.
Пример 8.
Магнитные свойства нанокомпозитов, синтезированных в примерах 1-5, были измерены с помощью СКВИД магнетометра (MPMS-XL фирмы «Quantum Design») МТЦ СО РАН (Новосибирск, Россия). Для всех образцов получены полевые зависимости намагниченности при 5 и 320 K в магнитных полях до 15 кЭ, и исследована температурная зависимость магнитной восприимчивости в интервале температуры 5-320 K в магнитном поле 10 кЭ. Полученные данные о намагниченности образцов и их магнитной восприимчивости (см. Таблица 1) свидетельствуют, что все синтезированные нанобиокомпозиты, а именно Gd2O3, инкапсулированные в макромолекулы полисахарида (арабиногалактана и арабиногалактана-сырца), GdBO3 и биметаллические нанокомпозиты, содержащие Fe и Gd, инкапсулированные в макромолекулы арабиногалактана, в этом интервале температуры являются парамагнетиками.
Пример 9.
В 2 мл воды (или дейтерированной воды D2O) растворяли 0.030 г нанокомпозита с содержанием гадолиния 8.5 массовых % (Пример 4) и определяли время релаксации Т1 протонов воды (или остаточных протонов дейтерированной воды D2O) на ЯМР спектрометре Bruker DPX-400 по стандартной методике «инверсия-восстановление» сигнала. Время Т1=11.5 мс, что соответствует значению Т1 для гадопентеновой кислоты с таким же содержанием гадолиния.
1 С, K⋅см3/г - значение постоянной Кюри.
2 Θ, К - значение постоянной Вейсса.
3χ0, см3/г - значение магнитной восприимчивости.
| название | год | авторы | номер документа |
|---|---|---|---|
| Водорастворимые магнитоактивные нанобиокомпозиты флавоноидных комплексов гадолиния на основе природного конъюгата арабиногалактана с биофлавоноидами и способ получения этих нанобиокомпозитов | 2019 |
|
RU2706705C1 |
| Средство, обладающее противоопухолевой активностью на основе нанокомпозитов арабиногалактана с селеном, и способы получения таких нанобиокомпозитов | 2015 |
|
RU2614363C2 |
| Способ оценки токсического действия биметаллического феррум-гадолиниевого нанокомпозита, инкапсулированного в природную полимерную матрицу арабиногалактана, на лабораторных животных | 2019 |
|
RU2733504C1 |
| Нанокомпозит серебра на основе конъюгата арабиногалактана и флавоноидов, обладающий антимикробным и противоопухолевым действием, и способ его получения | 2015 |
|
RU2611999C2 |
| Микрофлюидный синтез нанокомпозита на основе люминофора BaGdF:Tb и фотосенсибилизатора бенгальского розового для применения в рентгеновской фотодинамической терапии опухолей | 2023 |
|
RU2822425C1 |
| Углеродные наночастицы и способ их изготовления | 2024 |
|
RU2841407C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНЫХ МЕТАЛЛИЧЕСКИХ И МЕТАЛЛОКСИДНЫХ ЧАСТИЦ | 2004 |
|
RU2260500C1 |
| Способ оценки процесса апоптоза в ткани головного мозга лабораторных животных | 2016 |
|
RU2621122C1 |
| Способ получения композиционного материала биотехнологического назначения | 2018 |
|
RU2687283C1 |
| Способ получения антиоксидантной наноразмерной формы эссенциального микроэлемента селена | 2024 |
|
RU2834305C1 |
Изобретение может быть использовано для получения водорастворимых магнитоконтрастных средств для проведения диагностики, терапии и тераностики онкологических заболеваний головного мозга. Магнитоконтрастные средства представляют собой гадолинийсодержащие нанокомпозиты, стабилизирующая и транспортная матрица которых состоит из макромолекул полисахарида, выбранного из арабиногалактана и арабиногалактана-сырца. Наночастицы, инкапсулированные в матрице, состоят из Gd2O3, GdBO3 или представляют собой биметаллические наночастицы, содержащие Gd и Fe. Размер наночастиц составляет 1-100 нм. Диапазон содержания гадолиния в нанокомпозитах 1,7-18 мас.%. Предложены способы получения нанокомпозитов, содержащих Gd2O3, GdBO3 или биметаллические наночастицы Gd и Fe. Изобретения позволяют упростить получение стабильных магнитоконтрастных средств, которые не теряют свои свойства в течение длительного промежутка времени и пригодны для двухканальной тераностики новообразований. 4 н.п. ф-лы, 2 ил., 1 табл., 9 пр.
1. Водорастворимые магнитоконтрастные средства, пригодные для проведения диагностики, терапии и тераностики онкологических заболеваний головного мозга, представляющие собой гадолинийсодержащие нанокомпозиты, стабилизирующая и транспортная матрица которых состоит из макромолекул полисахарида, выбранного из арабиногалактана и арабиногалактана-сырца, а инкапсулированные в них наночастицы отличаются тем, что состоят из Gd2O3, GdBO3 или биметаллических структур, содержащих Gd и Fe, при этом размер наночастиц составляет 1-100 нм, а диапазон содержания гадолиния в нанокомпозитах составляет 1,7-18 мас.%.
2. Способ получения магнитных водорастворимых нанокомпозитов Gd2О3 по п. 1, включающий взаимодействие водного раствора хлорида гадолиния(III) с водным раствором макромолекул полисахарида, выбранного из арабиногалактана и арабиногалактана-сырца, в присутствии водного раствора аммиака для создания нейтральной среды при комнатной температуре 20-25°С, последующее осаждение в этанол или другой смешивающийся с водой органический растворитель и фильтрование.
3. Способ получения магнитных водорастворимых нанокомпозитов GdBO3, включающий получение магнитных водорастворимых нанокомпозитов Gd2О3, инкапсулированных в арабиногалактан, по п. 2, с дальнейшим их превращением в GdBO3 под действием водного раствора Н3ВО3 при комнатной температуре 20-25°С, последующее осаждение в этанол или другой смешивающийся с водой органический растворитель и фильтрование.
4. Способ получения магнитных водорастворимых биметаллических нанокомпозитов, содержащих Fe и Gd, инкапсулированных в арабиногалактан, по п. 1, включающий взаимодействие водных растворов хлорида гадолиния(III) и хлорида железа(III) с водным раствором арабиногалактана в присутствии водного раствора аммиака для создания нейтральной среды при комнатной температуре 20-25°С, последующее осаждение в этанол или другой смешивающийся с водой органический растворитель и фильтрование.
| Водорастворимые магнитоактивные нанобиокомпозиты флавоноидных комплексов гадолиния на основе природного конъюгата арабиногалактана с биофлавоноидами и способ получения этих нанобиокомпозитов | 2019 |
|
RU2706705C1 |
| Способ получения модифицированных наночастиц магнетита, легированных гадолинием | 2020 |
|
RU2738118C1 |
| RU 2396207 C2, 10.08.2010 | |||
| US 6770261 B2, 03.08.2004 | |||
| US 8357545 B2, 22.01.2013 | |||
| YU KIMURA et al., Size-Controlled and Biocompatible Gd2O3 Nanoparticles for Dual Photoacoustic and MR Imaging, Advanced Healthcare Materials, 2012, v | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Конденсатор | 1923 |
|
SU657A1 |
Авторы
Даты
2022-08-29—Публикация
2021-07-27—Подача