ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к нанотехнологии и наномедицине, более конкретно к микрофолюидному способу получения нанокомпозита на основе люминофора BaGdF5:Tb и фотосенсибилизатора бенгальского розового для получения нанолюминофора со средним размером частиц 7-8 нм и максимальной интенсивностью люминесценции на длине волны 545 нм и фотосенсибилизатора бенгальского розового с поглощением в области излучения люминофора, и может быть использовано в рентгеновской фотодинамической терапии злокачественных опухолей.
Существующие методы лучевой и химиотерапии помимо разрушения злокачественных клеток разрушают и здоровые клетки. Таким образом, необходимость разработки альтернативных и более безопасных методов терапии является важной проблемой. Одним из перспективных методов неинвазивной и малотоксичной терапии является рентгеновская фотодинамическая терапия (РФДТ), основанная на подавлении роста глубоко лежащей злокачественной опухоли за счет генерации активных форм кислорода (АФК) при облучении светочувствительного вещества, фотосенсибилизатора [1-2]. Для активации системы «фотосенсибилизатор-АФК» необходимо добавить дополнительный компонент, который поглощает рентгеновские лучи и переизлучает накопленную энергию в ультрафиолетовом-видимом диапазоне электромагнитного спектра, то есть в области поглощения фотосенсибилизатора [3]. Одними из наиболее перспективных и изученных являются рентгеновские люминофоры на основе NaGdF4 и BaGdF5, допированные Eu3+, Tb3+ или другими лантанидами.
Люминесцентные наноматериалы, допированные редкоземельными ионами являются перспективными для биомедицинского применения. Эти материалы характеризуются такими физико-химическими свойствами, как длительное время свечения, большие стоксовы и/или антистоксовы сдвиги, узкие полосы люминесценции, высокая фотостабильность и низкая токсичность. Данные материалы можно рассматривать как новое поколение биосенсоров наряду с такими традиционными молекулярными зондами, как органические красители [4].
Возможно получение наночастиц люминофора BaGdF5:Tb микроволновым и сольвотермальным методом синтеза. Исследования, проведенные авторами настоящего изобретения, показали, что микроволновым синтезом получают более мелкие частицы для всего широкого диапазона рассматриваемых температур синтеза по сравнению с сольвотермальным синтезом. Таким образом, варьируя состав растворителя, а также способ нагрева системы, можно варьировать размер наночастиц рентгеновского люминофора BaGdF5:Tb. В результате было показано, что сольвотермальный метод синтеза позволяет получить наночастицы со средним размером от 13 до 49 нм, микроволновый - от 7 до 26 нм в зависимости от состава растворителя. Этот факт соответствует требованиям, предъявляемым к нанофосфорам в составе нанокомпозитов, которые могут быть использованы в РФДТ [5].
Известный нанокомпозитный материал со структурой ядро-оболочка (CN 105031669 (A), опубл. 23.06.2016) [6], имеющий структуру BaGdF5 с оболочкой из мезопористого кремния, в которую встроен фотосенсибилизатор дигидроксифталоцианин кремния и молекулы гиалуроновой кислоты. Маслорастворимые наночастицы пентафторида гадолиния-бария получают сольвотермальным методом и подвергают модификации его водорастворимость; затем на мезопористый кремния наносят золь-гель-методом молекулы гиалуроновой кислоты, поверхность мезопористого кремния имеет большое количество аминогрупп, которые можно комбинировать с целевой молекулой гиалуроновой кислоты, и в то же время поверхность мезопористого кремния связывается с фотосенсибилизатором дигидроксифталоцианином кремния. Приготовленный материал имеет однородный размер частиц и хорошую дисперсность. Наночастицы такой структуры могут быть использованы в качестве контрастного вещества в рентгеновской компьютерной томографии, а также для ФДТ.
Однако, известный нанокомпозит имеет очень слабую эмиссионную способность в области видимого излучения, что снижает потенциал его использования в качестве эффективных материалов для применения в фотодинамической терапии. Кроме того, процесс создания нанокомпозита подразумевает несколько стадий с использованием физико-химических процессов в закрытых автоклавах, протекающих в водных растворах при температуре свыше 100°С и давлении выше 1 атмосферы. Модифицированные люминесцентные наночастицы синтезируют гидротермальным методом в одном реакторе с одновременной модификацией поверхности наночастиц. Рассматривается применение наночастиц в различных областях биомедицинского применения благодаря их преимуществам при мультимодальной биовизуализации in vitro и in vivo, таким как малый размер частиц до 15 нм, а также содержанию тяжелых элементов, способных эффективно поглощать рентгеновское излучение.
В известном биозонде на основе наночастиц для мультимодальной биовизуализации (US2014147391 (A1) опубл. 29.05.2014) [7] люминесцентные наночастицы BaGdF5:Yb/Er с модифицированной поверхностью синтезируют гидротермальным методом в одном реакторе с одновременной модификацией поверхности наночастиц с использованием физико-химических процессов в закрытых системах, протекающих в водных растворах при температурах свыше 100°С и давлениях выше 1 атмосферы. Наночастицы потенциально применимы для магнитно-резонансной томографии (МРТ) и компьютерной рентгеновской томографии (КТ) благодаря их преимуществам при мультимодальной биовизуализации in vitro и in vivo, таким как малый размер частиц до 15 нм, а также содержанию тяжелых элементов, способных эффективно поглощать рентгеновское излучение. Полученные частицы активируются на длине волны ближнего инфракрасного диапазона (NIR) и преобразуют излучение в видимый диапазон.
Однако синтез полученных наночастиц не включает этап конъюгации с молекулами фотосенсибилизатора для применения в рентгеновской фотодинамический терапии злокачественных новообразований. Более того, получение наночастиц характеризуется длительным периодом (24 часа) термостатирования реакционной смеси при температуре 190°С.
В патенте (CN113278420 (A) - 20.08.2021) [8] молекулярная формула нанокристаллического материала с ап-конверсией в ближнем инфракрасном диапазоне имеет вид: BaGdF5:Na/Yb/Tm-CaLuF5:Yb. Способ получения включает следующие стадии: растворение карбоната щелочноземельного металла или оксида редкоземельного элемента в трифторуксусной кислоте и деионизированной воде и получение предшественника трифторацетата щелочноземельного и редкоземельного элементов путем растворения и сушки путем дистилляции; в трехгорлую колбу добавляют трифторацетат бария, трифторацетат гадолиния, трифторацетат натрия, трифторацетат иттербия, трифторацетат тулия, олеиновую кислоту, олеиламин и октадецен, удаляют воду, затем быстро нагревают полученную смесь до заданной температуры, сохраняя тепло, и после окончания реакцию, осуществляющую центробежную промывку с использованием смешанного раствора этанола и циклогексана с получением сферических нанокристаллов BaGdF5: Na/Yb/Tm. Затем следует добавление трифторацетата кальция, трифторацетата лютеция, трифторацетата иттербия, олеиновой кислоты, олеиламина и октадецена в трехгорлую колбу, удаление воды, добавление нанокристаллов ядра, непрерывное поддержание температуры в течение определенного периода времени, быстрый нагрев до заданной температуры, поддержание температуры, замена растворителя центробежной промывкой с использованием смешанного раствора этанола и циклогексана после завершения реакции и, наконец, сушка полученного продукта с получением нанокристаллов ядро-оболочка BaGdF5: Na/Yb/Tm-CaLuF5: Yb.
Однако синтез полученных наночастиц не включает последующей стадии присоединения фотосенсибилизатора для применения в РФДТ злокачественных новообразований. Кроме того, синтез занимает относительно много времени - более 5 часов, а также требует нагревания реакционной смеси до 310°С.
Известен способ получения нанокристаллического люминофора типа ядро-оболочка ближнего инфракрасного диапазона (CN112457849 (A)) [9]. Приготовление состава Ca0,3Ba0,7GdF5 @ CeBaGdF5 @ NdSrF2 последовательно включает следующие стадии: добавление трифторацетата кальция, трифторацетата бария, трифторацетата гадолиния, трифторацетата церия, олеиновой кислоты и октадецена в трехгорлую бутыль, осуществляя нагревание и выдерживая температуру в течение 1 часа при 110°С под защитой азота и естественным образом охлаждая материалы до комнатной температуры; и промывание материалов смешанным раствором этанола и циклогексана для получения нанокристалла ядро-оболочка и приготовление нанокристалла ядро-оболочка методом послойного эпитаксиального выращивания. Преимуществами метода, как указывают авторы, являются простота, низкая стоимость и высокий выход; и продукт имеет характеристику, проявляющую эффективную люминесценцию в ближнем инфракрасном диапазоне, возбуждаемую рентгеновскими лучами. Стоит отметить, что синтез наночастиц не включает присоединение фотосенсибилизатора для применения в рентгеновской ФДТ злокачественных новообразований. Кроме того, синтез нанолюминофора топологии ядро-оболочка-оболочка Ca0,3Ba0,7GdF5:Ce @ BaGdF5:Nd @ SrF2 занимает больше 1 час.
Наиболее близким по назначению, составу и достигаемому результату к заявляемому способу является [10], в котором проведен синтез люминофоров с разным содержанием допирующего элемента, а также конъюгация полученных частиц с молекулами фотосенсибилизатора, бенгальского розового. Наночастицы β-NaGdF4: x% Tb, модифицированные олеиновой кислотой (ОК), были синтезированы по методу соосаждения, адаптированному из литературы. Вкратце, GdCl3·6H2O (1-x ммоль) и TbCl3·6H2O (x ммоль) смешивали с 6 мл олеиновой кислоты и 15 мл 1-октадецена в трехгорлую круглую колбу емкостью 100 мл, затем полученную смесь нагревали до 160°С в течение 60 мин в инертной атмосфере аргона до образования гомогенного раствора. После охлаждения раствора до комнатной температуры к смеси по каплям добавляли 10 мл раствора метанола, содержащего NH4F (4 ммоль) и NaOH (2,5 ммоль). Реакционную смесь перемешивали еще 60 мин, медленно нагревали до 60°С в течение 60 мин для удаления метанола, а затем дегазировали при 120°С в течение 20 мин. После этого раствор дополнительно нагревали до 290°С с возрастающей скоростью 15°С/мин, а затем выдерживали при этой температуре в течение 60 мин под защитой газа аргона. Конечный раствор охлаждали до комнатной температуры и продукт осаждали добавлением избыточного количества этанола, собранного центрифугированием при 9000 оборотах в течение 10 мин. Осадок трижды промывали смесью этанол/гексан (3:1 по объему), стабилизированные олеиновой кислотой наночастицы диспергировали в гексане для дальнейшего использования. Для оценки влияния легирования Tb на эффективность люминесценции были синтезированы НЧ β-NaGdF4: x% Tb (x = 5, 10, 15, 20 и 25 % соответственно) по методикам, аналогичным описанным выше, за исключением того, что добавляли разные количества TbCl3·6H2O. Водный раствор NH2-модифицированных наночастиц β-NaGdF4: 15% Tb с концентрацией 1 мг/мл смешивали с 0,05 мл розового бенгальского, растворенного в диметилсульфоксиде (ДМСО) с концентрацией 10 мг/мл, с интенсивным перемешиванием. К смеси добавляли 10 мг N-(3-диметиламинопропил) -N-этилкарбодиимида кристаллического гидрохлорида и продолжали перемешивать в течение ночи при комнатной температуре. Затем наночастицы БР промывали в ДМСО один раз и еще два раза деионизированной водой для удаления избытка БР.
Известный способ получения нанокомпозита является многостадийным и требует использования высоких температур при синтезе, до 290 °С и время синтеза составляет 4 часа, имеет большой расход реактивов, присутствие человеческого фактора, Все эти факторы отрицательно влияют на повторяемость результатов, скорость получения конечного продукта, присущие всем известным стандартным способам синтеза.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Технической задачей настоящего изобретения является возможность получения нанокомпозита путем конъюгирования синтезированных наночастиц рентгеновского люминофора на основе матрицы BaGdF5 допированной редкоземельным металлом Tb с молекулами фотосенсибилизатора бенгальского розового в процессе одностадийного микрофлюидного синтеза.
Синтез реализуется в проточной системе и включает первичное смешивание 4-х реактивов в микрореакторе топологии меандр (при комнатной температуре) с поперечным квадратным сечением каналов 500 мкм, и последующем нагревом реакционной смеси в тефлоновой трубке с круглым сечением диаметром 2 мм в масляной бане при 100 °С. Затем полученная реакционная смесь проходит через водяную баню, охлаждается до комнатной температуры и смешивается с водным раствором фотосенсибилизатора в микрореакторе.
Оборудование: проточная система синтеза с возможностью подачи жидкостных реактивов в диапазоне скоростей потоков от 0.5 μл/с до 300 μл/с, содержащая микрофлюидные реакторы топологии меандр с возможностью смешивания четырех и двух компонентов, с поперечным сечением каналов 500 мкм, изготовленные из фотополимерной смолы методом DLP 3D печати. Реактивы: водные растворы солей BaCl2 (анал. чистоты 99.99%), GdCl3 (анал. чистоты 99.99%), TbCl3 (анал. чистоты 99.99%), NH4F (анал. чистоты 98 %); этилен гликоль, деионизированная вода (18 МОм·см).
Указанная техническая задача решена тем, что микрофлюидный синтез нанокомпозита на основе люминофора BaGdF5:Tb и его последующая конъюгация фотосенсибилизатора бенгальского розового для применения в рентгеновской фотодинамической терапии опухолей, характеризуется следующей последовательностью действий:
а) приготовление прекурсоров для синтеза люминофора соответствующего химической формуле BaGd 0.75F 5: Tb 0.25 путем растворения в отдельных колбах в смеси этиленгликоль-вода, взятой в объемном соотношении 3:1, хлоридов BaCl2, GdCl3 и NH4F в объеме 50 мл с концентрацией 0.1 М и допирующего прекурсора TbCl3 в объеме 10 мл с концентрацией 0.1 М;
б) приготовление водного раствора фотосенсибилизатора красителя бенгальского розового для пропитки наночастиц в оптимальной концентрации, соответствующей максимальной чувствительности измерительного прибора к используемому фотосенсибилизатору;
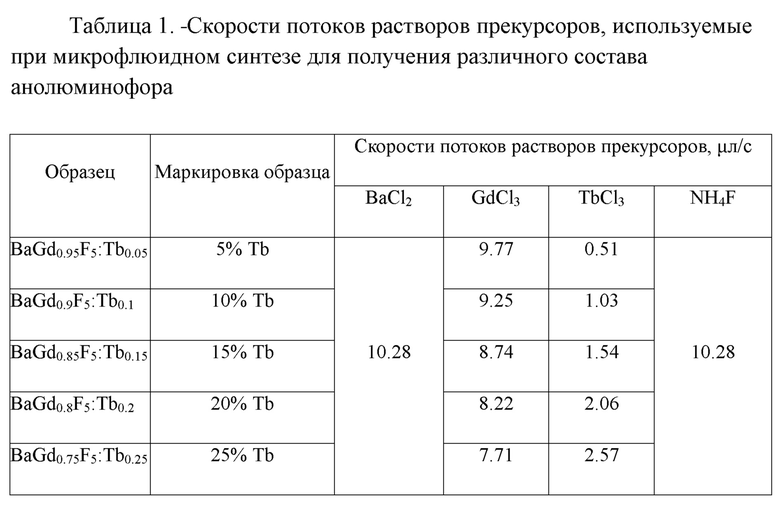
в) введение с помощью системы шприцевых насосов подготовленных растворов прекурсоров BaCl2, GdCl3, NH4F, TbCl3 отдельно в каждый канал четырехканального микрореактора с заданными скоростями потоков, в μл/с:BaCl2 - 10.28, GdCl3 - 7.71, TbCl3 - 2.57, NH4F - 10.28;
г) смешивание всех растворов прекурсоров в меандре четырехканального микрореактора с суммарной скоростью потока реакционной смеси 30.84 μл/с;
д) термостатирование полученной реакционной смеси в масляной бане при температуре 100°С для получения суспензии кристаллов люминофора;
е) охлаждение в водяной бане, полученной после термостатирования реакционной смеси до комнатной температуры;
ж) введение с помощью шприцевого насоса водного раствора фотосенсибилизатора бенгальского розового в один канал двухканального микрореактора со скоростью потока 30.84 μл/с, эквивалентной скорости потока результирующей реакционной смеси;
з) одновременное введение суспензии кристаллов люминофора в другой канал двухканального микрореактора;
и) смешивание полученной суспензии кристаллов люминофора с водным раствором фотосенсибилизатора красителя бенгальского розового в меандре упомянутого двухканального микрореактора с последующим поступлением суспензии нанокомпозита в колбу-приемник;
к) центрифугирование собранного продукта при 13000 оборотов в течение 5 минут для удаления слабо связанных или не связанных молекул фотосенсибилизатора;
л) четырехразовое промывание синтезированных наночастиц композитного материала дважды дистиллированной водой с целью удаления молекул растворителя - этиленгликоля, а также слабо связанных молекул фотосенсибилизатора бенгальского розового.
В результате проведения теоретических и экспериментальных исследований выбран люминофор, соответствующий химической формуле BaGd0.75F5:Tb0.25 с максимальным значением интенсивности люминесценции в диапазоне 545 нм, возбуждаемой индуцированном рентгеновским излучением.
Суммарная скорость потока реакционной смеси при распространении в микрореакторе составляет 30.84 μл/с и определяется суммой скоростей потоков растворов четырех исходных реагентов, используемых в синтезе. Процентное содержание ионов допирующего элемента Tb3+ определяется путем изменения соотношений скоростей потоков исходных растворов солей GdCl3 и TbCl3 подаваемых на вход микрореактора.
ПЕРЕЧЕНЬ ФИГУР ГРАФИЧЕСКОГО ИЗОБРАЖЕНИЯ
Изобретение иллюстрируется фигурами чертежей и таблицами.
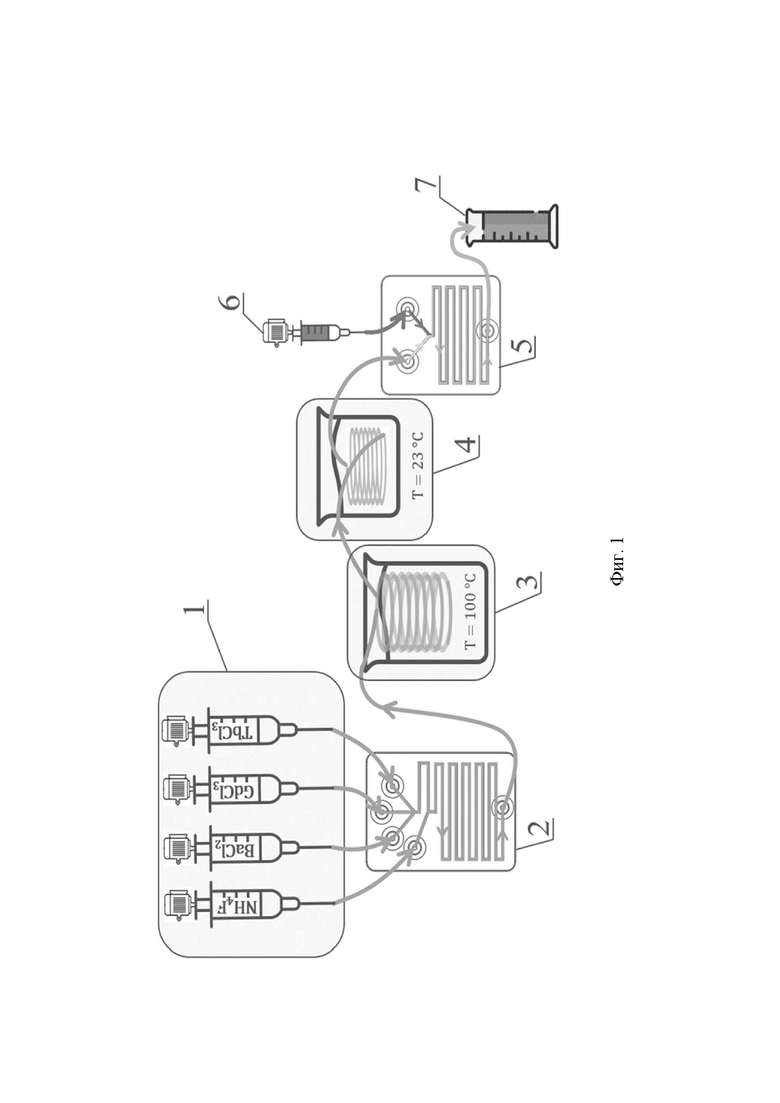
Фиг. 1. Структурная схема установки для микрофлюидного синтеза нанокомпозита.
Фиг. 2. Спектры поглощения в УФ-видимой области, полученные для серии исходных растворов фотосенсибилизаторов с различной концентрацией и маточного раствора, собранного после пропитки наночастиц BaGdF5:Tb раствором фотосенсибилизатора бенгальского розового.
Фиг. 3. Профили порошковой рентгеновской дифракции образцов серии наночастиц BaGdF5, допированных редкоземельными ионами Tb3+ с различной концентрацией замещений Gd-Tb (приведено в процентах из расчета скоростей потоков для прекурсоров Gd и Tb), полученных проточным микрофлюидным синтезом.
Фиг. 4. ПЭМ-изображения серии люминофоров BaGd1-xF5: Tbx - а) и их распределение по размерам - б).
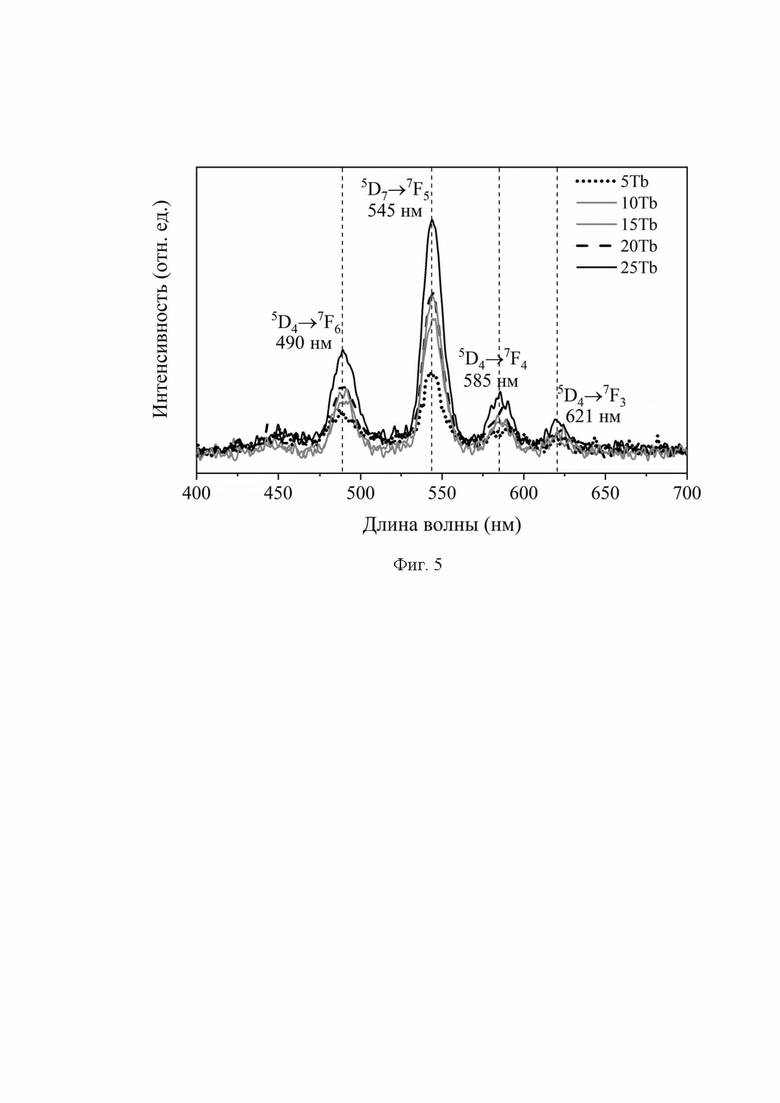
Фиг. 5. Спектры излучения в оптическом диапазоне при возбуждении рентгеновским излучением серии наночастиц-люминофоров BaGdF5 допированных редкоземельными ионами Tb3+ при варьировании скоростей потоков прекурсоров Gd и Tb (параметры работы рентгеновской трубки: U = 35 кВ, I = 1.6 мА).
Таблица 1. Скорости потоков растворов прекурсоров, используемые при микрофлюидном синтезе для получения различного состава нанолюминофора.
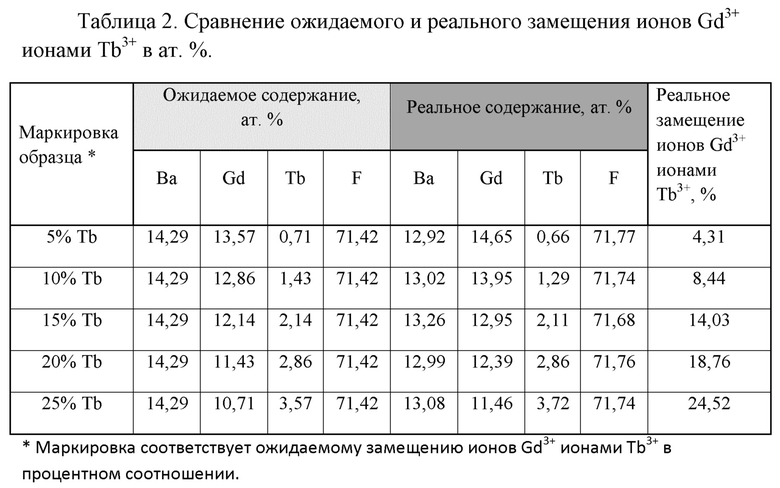
Таблица 2. Сравнение ожидаемого и реального замещения ионов Gd3+ ионами Tb3+ в ат. %.
ПРИМЕР КОНКРЕТНОГО ВЫПОЛНЕНИЯ
1. Подготовка прекурсоров для синтеза нанокомпозита, состоящего из люминофора BaGd0.75 F5:Tb0.25 и фотосенсибилизатора бенгальского розового.
Для приготовления необходимых прекурсоров использовались соответствующие соли высокой аналитической чистоты BaCl2, GdCl3, TbCl3 (произв. Sigma Aldrich, анал. чистота 99.99 %), NH4F (произв. Alfa Aesar, чистота 98%). Для приготовления растворов использовали дистиллированную воду с высокой степенью очистки (очищенную с помощью системы Simplicity с УФ лампой) и этилен гликоль (произв. ЭКРОС, анал. чистота 99.99 %). Для синтезов использовался растворитель этиленгликоль-вода с объемным соотношением 3:1 для предотвращения закупоривания каналов микрочипа кристаллами BaGdF5:Tb на начальной стадии синтеза.
Отдельно были приготовлены три раствора прекурсоров BaCl2, GdCl3, NH4F в объеме 50 мл, с концентрацией 0.1 М. Для этого взвешенные в количестве, в мг 1231.5 BaCl2, 1858.4 GdCl3 и 1017.5 NH4F, растворяли поочередно в трех цилиндрических колбах в водном растворе этиленгликоля в количестве 12.5 мл воды и 37.5 мл этиленгликоля.
Также был приготовлен раствор допирующего прекурсора TbCl3 в 10 мл растворителя с концентрацией 0.1 М. Для этого TbCl3 в количестве 1120,32 мг растворяли в одной цилиндрической колбе в водном растворе этиленгликоля в соотношении 7.5 мл этиленгликоля и 2.5 мл воды.
Для приготовления раствора фотосенсибилизатора предварительно был приготовлен водный раствор красителя бенгальского розового с оптимальной для пропитки концентрацией 62.5 μг/мл в 50 мл, соответствующей максимальной чувствительности измерительного прибора к используемому фотосенсибилизатору.
2. Оборудование, использованное для одностадийного проточного синтеза нанокомпозита.
Синтез нанокомпозита проводили в установке микрофлюидного одностадийного проточного синтеза, собранной из известных узлов, схема которой представлена на фиг. 1, которая содержит шприцевой насос 1, входной четырехканальный микрореактор 2 с шириной каналов 500 мкм для смешивания прекурсоров металлов и фторида аммония, масляную баню 3 для термостатирования реакционной смеси, водяную баню 4 для охлаждения реакционной смеси, выходной двухканальный микрореактор 5 с шириной каналов 300 мкм, шприцевой насос 6, подключенный к выходному микрореактору 5 для введения водного раствора красителя бенгальского розового, стеклянную колбу - приемник 7 для сбора продуктов синтеза. Для синтеза использовались: система насосов 1 - установка микрофлюидного синтеза МФ-1 (разработанная в МИИ «Интеллектуальных материалов», ЮФУ) и шприцевой инфузионный насос (BYZ-810, изготовитель Hunan Beyond Medical Technology Co,Ltd (Китай). Установка микрофлюидного синтеза МФ-1 содержит стеклянные шприцы из боросиликатного стекла и нержавеющей стали (объем шприцов - 10 мл, ход поршня - 60 мм. (производитель Runze Fluid, Китай) с фторопластовым носиком с нарезанной резьбой для подключения трубок на резьбовом соединении.
Входной микрореактор 2 представляет собой четырехкомпонентный микрочип с пассивным микромиксером топологии меандр с шириной каналов 500 мкм для смешивания растворов прекурсоров BaCl2, GdCl3, TbCl3 и прекурсора NH4F.
Выходной микрореактор 5 представляет собой двухкомпонентный микрочип с пассивным микромиксером топологии меандр с шириной каналов 500 мкм и предназначен для смешивания люминофора, допированного тербием и фотосенсибилизатора БР.
Для осуществления дозированной подачи реактива в микрореактор 2 на малых скоростях потоков использованы модули линейного перемещения на базе шаговых двигателей и шарико-винтовой передачи, приводимые в движение коммерчески доступными шаговыми электродвигателями стандарта NEMA 23 (произв. США). С помощью специальной системы креплений для корпуса шприцов и поршней шприцов система позволяет подавать реактивы в точку смешивания в диапазоне скоростей от 1 μл/с до 325 μл/с.
3. Последовательность действий при микрофлюидном синтезе нанокомпозита, содержащего люминофор BaGd0.75F5:Tb0.25 и фотосенсибилизатор бенгальский розовый.
Подготовленные растворы прекурсоров BaCl2, GdCl3, NH4F, TbCl3 вводились с помощью системы насосов 1 отдельно в каждый канал микрореактора 2 с заданными скоростями потоков, представленными в таблице для образца BaGd0.75F5:Tb0.25: BaCl2 - 10.28 μл/с, GdCl3 - 7.71 μл/с, TbCl3 - 2.57 μл/с, NH4F - 10.28 μл/с.
Далее в микрореакторе 2 топологии меандр происходит смешивание всех растворов прекурсоров с получением реакционной смеси, которая распространяется с совокупной скоростью подачи всех реактивов 30.84 μл/с и сопровождается начальной стадией кристаллизации. Затем реакционная смесь перетекает в тефлоновую трубку, находящуюся в масляной бане 3, где нагревается до 100°С и далее через тефлоновую трубку поступает в водяную баню 4, где происходит ее охлаждение до комнатной температуры.
Затем реакционная смесь поступает в первый вход двухканального выходного микрореактора 5, на второй вход которого с помощью шприцевого насоса подают водный раствор красителя бенгальского розового в концентрации 0.064 мМ со скоростью потока 30.84 μл/с, где происходит смешивание наночастиц люминофора и фотосенсибилизатора БР. После смешивания компоненты через силиконовую трубку длиной 15 см и затем синтезированный продукт в виде суспензии поступает в колбу-приемник 7. При этом время синтеза 8 мл продукта составило 6 минут.
Затем собранный продукт центрифугировали при 13000 оборотов в минуту с целью удаления слабо связанных или не связанных молекул фотосенсибилизатора, затем четырежды промывали полученные образцы наночастиц композитного материала дважды дистиллированной водой. Полученный после центрифугирования маточный раствор использовали для количественной оценки степени пропитки наночастиц молекулами ФС путем регистрации спектров поглощения в оптическом диапазоне.
Для определения содержания фотосенсибилизатора на поверхности нанокомпозита проводились измерения оптических спектров на двухлучевом спектрофотометре Shimadzu UV-2600 в диапазоне длин волн от 200 до 700 нм.
Исходя из данных УФ-видимых спектров поглощения (Фиг. 2) маточный раствор (МР) образца содержал молекулы фотосенсибилизатора в меньшем количестве, чем в изначальном растворе с концентрацией 500 μг/мл. Для дальнейшей количественной оценки была использована калибровочная кривая, которая отражает зависимость между концентрацией фотосенсибилизатора БР и интенсивностью сигнала на 520 нм. Таким образом, концентрация маточного раствора составила 127 μг/мл, это говорит нам о том, что остальная часть фотосенсибилизатора была осаждена на поверхности наночастиц.
В результате получено оптимальное сочетание двух основных составляющих нанокомпозита: люминофора, способного эффективно поглощать энергию рентгеновских фотонов и переизлучать ее в оптическом диапазоне, а также фотосенсибилизатора, с целью достижения максимального перекрытия спектра поглощения фотосенсибилизатора и эмиссионного спектра наночастиц люминофора.
В результате микрофлюидного синтеза получен нанокомпозит, состоящий из люминофоров со средним размером 7-8 нм (фиг. 4) и максимальной интенсивностью на длине волны 545 нм (фиг. 5), а также фотосенсибилизатора бенгальского розового с поглощением в области излучения люминофора (фиг. 2).
Так как мелкие капилляры кровеносной системы человека имеют диаметр около 3 мкм, то наночастицы размером 7-8 нм могут свободно транспортироваться по кровеносной системе для воздействия на глубоколежащие злокачественные опухоли.
3. Экспериментальное подтверждение существенности состава нанокомпозита BaGd0.75F5:Tb0.25 для получения люминофора со средним размером 7-8 нм и максимальным излучением на длине волны 545 нм, что соответствует области поглощения фотосенсибилизатора бенгальского розового.
Для этого проведен синтез люминофоров с разным процентным содержанием допирующего элемента BaGd1-xF5:Tbx.
Отдельно были приготовлены три раствора прекурсоров BaCl2, GdCl3, NH4F в 50 мл растворителя, с концентрацией 0.3 М. Для этого поочередно были взвешены 3694,5 мг BaCl2, 5575,2 мг GdCl3 и 3052,5 мг NH4F, растворены в трех цилиндрических колбах в 12.5 мл воды с добавлением 37.5 мл этиленгликоля. Также был приготовлен раствор допирующего прекурсора TbCl3 в 10 мл растворителя с концентрацией 0.3М. Для этого был взвешен TbCl3 с массой 1120,32 мг и растворен в двух цилиндрических колбах в растворителе с 7.5 мл этиленгликоля и 2,5 мл воды.
Микрофлюидный синтез пяти образцов нанолюминофоров BaGd1-xF5:Tbx проводили на установке (фиг. 1) в соответствии с процессом, приведенным выше в разделе 2. Для этого с помощью четырех независимых насосов в систему запускались 0.3 M растворы BaCl2, GdCl3, TbCl3 и NH4F со скоростями представленными в табл. 1 для определенного состава люминофора. При заданной скорости потока реакционной смеси 30.84 μл/с прохождение участка тефлоновой трубки, подверженного температурному воздействию, составляет 6 минут. После прохождения участка с масляной баней трубка отсоединяется и происходит сбор результатов синтеза нанолюминофора в пластиковую тару. Далее для получения остальных составов люминофоров, в программе задавались скорости из таблицы 1 для необходимого состава и синтез запускается заново.
Для подбора идеальных условий синтеза экспериментально было выявлено путем варьирования состава растворителя, времени синтеза, определяемого скоростями подачи потоков реактивов, и концентрация прекурсора, что увеличение концентрации прекурсоров, а также снижение общей скорости потока и вязкости приводят к засорению микрофлюидного чипа в месте смешивания с фторидом аммония, где происходил быстрый и неконтролируемый рост кристаллов фторидов металлов, блокирующих поток.
Для дальнейшего исследования конечных продуктов - наночастиц рентгеновских люминофоров BaGd1-xF5:Tbx результирующая реакционная смесь центрифугировалась при скорости 13000 оборотов в минуту в течение 5 минут, затем смесь трижды промывалась дистиллированной водой.
На фиг. 3 приведены профили порошковой рентгеновской дифракции образов серии наночастиц BaGdF5, допированных редкоземельными ионами Tb3+ с различной концентрацией замещений Gd-Tb (приведено в процентах из расчета скоростей потоков для прекурсоров Gd и Tb) и полученных с помощью проточного микрофлюидного синтеза. Качественное исследование профилей рентгеновской дифракции выявило образование однофазного материала для всех образцов со структурой, аналогичной структурам, указанным для нелегированной структуры BaGdF5 в базе данных PDF JCPDS № 24-0098, пространственная группа Fm-3m и параметр ячейки a = 6,023 Å, V = 218,49 Å.
На фиг. 4 а) приведены изображения ПЭМ серии люминофоров BaGd1-xF5: Tbx, а на фиг. 4 б) - их распределение по размерам.
Согласно результатам анализа изображений просвечивающей электронной микроскопии (ПЭМ) (Фиг. 4 - а) и распределений частиц по размерам (Фиг. 4 - б) был получен монодисперсный образец в виде сферических наночастиц с усредненным размером в диапазоне от 7 до 8 нм. Гистограммы распределения были построены на основании оценки диаметра 600 частиц на ПЭМ снимках для каждого образца. Кроме того, биологические макромолекулы крупнее наночастиц. Размер наночастиц обычно составляет порядка десятков нанометров, что в 1000 раз меньше размера раковой клетки. То есть, в отличие от микрочастиц, наночастицы хорошо усваиваются клетками. Это делает их идеальными кандидатами для доставки противоопухолевых препаратов. Из-за своего небольшого размера наноматериалы могут преодолевать биологические барьеры. Мелкие капилляры имеют диаметр около 3 микрометров, а наночастицы размером 7-8 нм могут свободно транспортироваться по кровеносной системе и нести фармацевтически активные вещества [11].
С помощью рентгенофлуоресцентного анализа (РФА) был оценен состав синтезированных нанокомпозитов. В таблице 2 показано ожидаемое (т. е. оцененное в соответствии с исходной загрузкой прекурсора) и фактическое измеренное содержание ионов Tb для каждого синтезированного образца. Как видно из таблицы, расхождения теоретических и экспериментальных данных небольшое. Таким образом, с помощью скоростей потоков прекурсоров Gd и Tb действительно были получены нанолюминофоры с заданным процентным содержанием этих элементов.
Оптические спектры, снятые под рентгеновским излучением (Фиг. 5) для серии образцов BaGd1-xF5: Tbx демонстрируют типичную форму спектра для структуры BaGdF5:Tb. Для BaGdF5:Tb характерны четыре сильные узкие полосы, соответствующие Tb3+ переходам: 5D4 → 7F6 (λ = 490 нм), 5D4 → 7F5 (λ = 545 нм), 5D4 → 7F4 (λ = 585 нм) и 5D3 → 7F6 (λ = 621 нм). Оптимальное содержание редкоземельного элемента Tb3+ наблюдается в образце BaGd0.75F5: Tb0.25, эмиссионный спектр которого показывает максимум интенсивности люминесценции среди полученной серии образцов при варьировании концентрации допирующего элемента. На основе анализа интенсивности люминисценции, для получения нанокомпозитов проточным одностадийным микрофлюидным синтезом доказаны значения скоростей потоков вышеуказанных компонент, соответствующих образцу состава BaGd0.75F5: Tb0.25.
В результате микрофлюидного синтеза нанокомпозита на основе люминофора BaGdF5:Tb и фотосенсибилизатора бенгальского розового получен нанолюминофор со средним размером частиц 7-8 нм и максимальной интенсивностью люминесценции на длине волны 545 нм и фотосенсибилизатор бенгальского розового с поглощением в области излучения люминофора для использования в рентгеновской фотодинамической терапии злокачественных опухолей.
Источники информации:
1. Yang Y., Bazhin A., Werner J., Karakhanova S. Reactive oxygen species in the immune system // International Reviews of Immunology. - 2013. - T. 32, № 3. - C. 1563-5244
2. Yang Y., Karakhanova S., Werner J., Bazhin A. Reactive Oxygen Species in Cancer Biology and Anticancer Therapy // Current Medicinal Chemistry. - 2013. - T. 20, № 30. - C. 3677-3692.
3. Gadzhimagomedova Z., Zolotukhin P., Kit O., Kirsanova D., Soldatov A. Nanocomposites for X-Ray Photodynamic Therapy // International Journal of Molecular Sciences. - 2020. - T. 21, № 11. - C. 1422-0067.
4. Бажукова И. Н., Пустоваров В. А., Мышкина А. В., Улитко М. В. Люминесцентные наноматериалы, допированные редкоземельными ионами, и перспективы их биомедицинского применения (обзор) // Оптика и спектроскопия. - 2020. - T. 128, № 12.
5. Polyakov V., Gadzhimagomedova Z., Kirsanova D., Soldatov A. Synthesis Optimization of BaGdF5:x%Tb3+ Nanophosphors for Tunable Particle Size // Materials. - 2022. - T. 15, № 23.
6. CN 105031669 (A), опубл. 23.06.2016, Core-shell structured nano composite material and a preparing method and application thereof // МПК: A61K47/48, A61K41/00, A61K47/04, A61K47/36, A61K49/04, A61K49/12, A61P35/00.
7. US2014147391 (A1), опубл. 29.05.2014, Bioprobe based on single-phase upconversion nanoparticles (UCNPs) for multi-modal bioimaging // МПК: A61K49/00, A61K49/04, A61K49/18.
8. CN113278420 (A), опубл. 20.08.2021, Efficient near-infrared up-conversion nanocrystalline material and preparation method thereof // МПК: B82Y20/00, B82Y30/00, C09K11/02, C09K11/85.
9. CN112457849 (A), 09.03.2021, Near-infrared fluoride core-shell nanocrystalline scintillator // МПК B82Y20/00, B82Y30/00, C09K11/02, C09K11/85.
10. Zhang W., Zhang X., Shen Y., Shi F., Song C., Liu T., Gao P., Lan B., Liu M., Wang S., Fan L., Lu H. Ultra-high FRET efficiency NaGdF4: Tb3+-Rose Bengal biocompatible nanocomposite for X-ray excited photodynamic therapy application // Biomaterials. - 2018. - T. 184. - C. 31-40.
11. Teleanu R. I., Chircov C., Grumezescu A. M., Teleanu D. M. Tumor Angiogenesis and Anti-Angiogenic Strategies for Cancer Treatment // Journal of Clinical Medicine - 2019. - T. 9, № 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИМЕР-НЕОРГАНИЧЕСКИЕ НАНОКОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ НА ОСНОВЕ ПОЛИМЕТИЛМЕТАКРИЛАТА С НАСТРАИВАЕМЫМ СПЕКТРОМ ФОТОЛЮМИНЕСЦЕНЦИИ | 2012 |
|
RU2537603C2 |
| Материал для температурного сенсора на основе измерения эффективного времени затухания люминесценции | 2024 |
|
RU2836516C1 |
| ЛЮМИНЕСЦЕНТНЫЕ НАНОЧАСТИЦЫ С ЯДРОМ И ОБОЛОЧКОЙ | 2004 |
|
RU2346022C2 |
| СИНТЕЗ НАНОЧАСТИЦ, СОДЕРЖАЩИХ ВАНАДАТ МЕТАЛЛА (III) | 2004 |
|
RU2344162C2 |
| Способ получения ортоборатов лантана, допированных европием и висмутом | 2021 |
|
RU2762551C1 |
| Способ получения боратов лантана, легированных европием и тербием | 2021 |
|
RU2761209C1 |
| Способ получения нанокристаллических порошков оксида гадолиния, допированного редкоземельными элементами | 2023 |
|
RU2817028C1 |
| Способ синтеза нанокомпозитов Ag/C | 2018 |
|
RU2686223C1 |
| Нанокомпозитный магнитный материал на основе полисопряженного полимера и смеси магнитных наночастиц и способ его получения | 2021 |
|
RU2768158C1 |
| Нанокомпозиты на основе гадолинийсодержащих соединений для диагностики, терапии и тераностики онкологических заболеваний головного мозга и способы их получения | 2021 |
|
RU2778928C1 |


Изобретение предназначено для получения агента, используемого в медицине при рентгеновской фотодинамической терапии опухолей. При микрофлюидном синтезе нанокомпозита на основе люминофора BaGdF5:Tb и фотосенсибилизатора бенгальского розового сначала готовят прекурсоры путём растворения в отдельных колбах хлоридов BaCl2, GdCl3 и NH4F в 50 мл смеси этиленгликоль-вода при объёмном соотношении её компонентов, составляющем 3:1, и концентрации 0,1 М, а также прекурсора допирующего элемента TbCl3 в 10 мл указанной смеси. Также готовят водный раствор бенгальского розового с концентрацией 62,5 μг/мл в 50 мл указанной смеси. Подготовленные растворы прекурсоров вводят с помощью системы шприцевых насосов 1 отдельно в каждый канал четырехканального микрореактора 2 с заданными скоростями потоков в μл/с: BaCl2 – 10,28, GdCl3 – 7,71, TbCl3 – 2,57, NH4F – 10,28 и смешивают их в меандре указанного микрореактора 2 со скоростью распространения реакционной смеси 30,84 μл/с. Приготовленную реакционную смесь термостатируют в масляной бане 3 при температуре 100°С для получения суспензии кристаллов люминофора, соответствующего химической формуле BaGd0,75F5:Tb0,25, а затем охлаждают в водяной бане 4. С помощью шприцевого насоса 6 в один канал двухканального микрореактора 5 вводят водный раствор бенгальского розового со скоростью распространения 30,84 μл/с с одновременным введением охлаждённой суспензии кристаллов люминофора в другой канал и смешивают их в меандре упомянутого двухканального микрореактора 5 с получением нанокомпозита на основе указанного люминофора и фотосенсибилизатора бенгальского розового. Затем суспензию нанокомпозита подают в колбу-приемник 7. Собранный продукт центрифугируют при 13000 об/мин для удаления слабо связанных или не связанных молекул фотосенсибилизатора. Синтезированные наночастицы промывают четыре раза дважды дистиллированной водой. Изобретение позволяет получить указанный нанокомпозит путём конъюгирования синтезированных наночастиц люминофора с молекулами фотосенсибилизатора в процессе одностадийного микрофлюидного синтеза. 2 табл., 5 ил.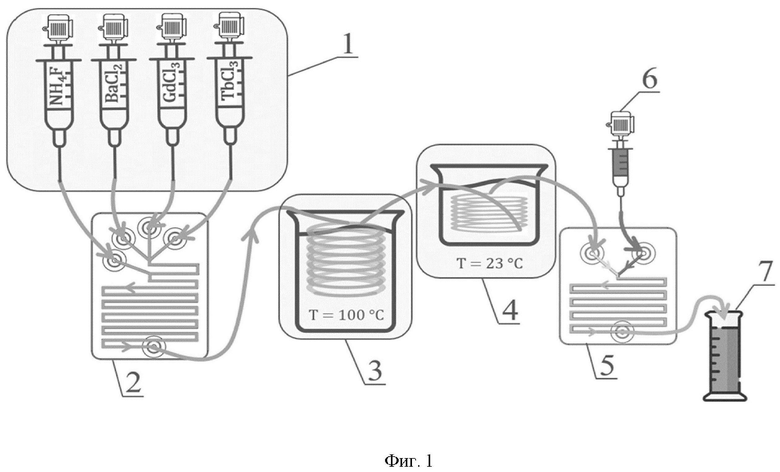
Микрофлюидный синтез нанокомпозита на основе люминофора BaGdF5:Tb и фотосенсибилизатора бенгальского розового для применения в рентгеновской фотодинамической терапии опухолей, характеризующийся следующей последовательностью действий:
а) приготовление прекурсоров для синтеза люминофора, соответствующего химической формуле BaGd0,75F5:Tb0,25, путем растворения в отдельных колбах в смеси этиленгликоль-вода, взятой в объемном соотношении 3:1, хлоридов BaCl2, GdCl3 и NH4F в объеме 50 мл с концентрацией 0,1 М и допирующего прекурсора TbCl3 в объеме 10 мл с концентрацией 0,1 М;
б) приготовление водного раствора фотосенсибилизатора красителя бенгальского розового с концентрацией 62,5 μг/мл в объеме 50 мл;
в) введение с помощью системы шприцевых насосов подготовленных растворов прекурсоров BaCl2, GdCl3, NH4F, TbCl3 отдельно в каждый канал четырехканального микрореактора с заданными скоростями потоков в μл/с: BaCl2 – 10,28, GdCl3 – 7,71, TbCl3 – 2,57, NH4F – 10,28;
г) смешивание всех растворов прекурсоров в меандре четырехканального микрореактора со скоростью распространения реакционной смеси 30,84 μл/с;
д) термостатирование полученной реакционной смеси в масляной бане при температуре 100°С для получения суспензии кристаллов люминофора;
е) охлаждение в водяной бане, полученной после термостатирования реакционной смеси, до комнатной температуры;
ж) введение с помощью шприцевого насоса водного раствора фотосенсибилизатора красителя бенгальского розового в один канал двухканального микрореактора со скоростью распространения 30,84 μл/с;
з) одновременное введение суспензии кристаллов люминофора в другой канал двухканального микрореактора;
и) смешивание полученной суспензии кристаллов люминофора с водным раствором фотосенсибилизатора красителя бенгальского розового в меандре упомянутого двухканального микрореактора с последующим поступлением суспензии нанокомпозита в колбу-приемник;
к) центрифугирование собранного продукта при 13000 оборотов в минуту для удаления слабо связанных или не связанных молекул фотосенсибилизатора;
л) четырехразовое промывание синтезированных наночастиц композитного материала дважды дистиллированной водой.
| WENLI ZHANG et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Переносная печь-плита | 1920 |
|
SU184A1 |
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| CN 105031669 A, 11.11.2015 | |||
| CN 112457849 A, 09.03.2021 | |||
| CN 113278420 A, 20.08.2021 | |||
| БАХМЕТЬЕВ В.В | |||
| и др | |||
| Нанолюминофоры на | |||
Авторы
Даты
2024-07-05—Публикация
2023-12-12—Подача