ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0001] Настоящее изобретение относится к фармацевтическому составу слитого белка, который регулирует лимфоцитопоэз и дифференцировку лимфоцитов, и относится к области лекарственных средств против аутоиммунных заболеваний.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002] Лимфоцитопоэз и дифференцировка лимфоцитов регулируются цитокинами. Стимулятор В-лимфоцитов (BlyS, также известный как фактор активации В-клеток, BAFF) и лиганд, индуцирующий пролиферацию (APRIL), представляют собой цитокины, оказывающие важное регулирующее действие на иммунный ответ человека. Они могут способствовать развитию и пролиферации В-лимфоцитов и увеличивать экспрессию иммуноглобулина в крови. BlyS и APRIL также имеют ключевое регулирующее влияние на созревание Т-лимфоцитов, поэтому они также имеют важное влияние на клеточный иммунитет.
[0003] BlyS и APRIL регулируют иммунный ответ лимфоцитов через рецепторы на поверхности лимфоцитов. Они связываются с рецепторами клеточных мембран, TACI (трансмембранный активатор и CAML-интерактор) и BCMA (антиген созревания В-клеток). Кроме того, BlyS также может связываться с другим рецептором BAFF-R. В-лимфоциты экспрессируют TACI, BCMA и BAFF-R, а зрелые Т-лимфоциты экспрессируют TACI. BlyS и APRIL регулируют активацию, пролиферацию и развитие лимфоцитов посредством передачи сигналов этих рецепторов и вызывают иммунный ответ. Кроме того, для лимфоцитарных опухолей BlyS и APRIL также обладают эффектами стимулирования деления опухолевых клеток и ингибирования апоптоза опухолевых клеток, таким образом ускоряя прогрессирование опухолей.
[0004] Ряд исследований показал, что избыточная экспрессия BlyS и APRIL является одной из причин множества аутоиммунных заболеваний. Эти заболевания включают системную красную волчанку, ревматоидный артрит, синдром Шегрена и тому подобное. Клинические исследования показали, что концентрация BlyS часто положительно коррелирует с тяжестью аутоиммунных заболеваний. Следовательно, подавление продукции BlyS и APRIL или снижение их концентрации в организме становится эффективным способом лечения аутоиммунных заболеваний. Между тем, поскольку BlyS и APRIL могут ускорять процесс опухолей B-лимфоцитов, ингибирование BlyS и APRIL также может быть использовано для лечения опухолей B-лимфоцитов, таких как хронический лимфолейкоз, множественная миелома и B-лимфоцитарная лимфома.
[0005] Поскольку TACI имеет высокое сродство к BlyS и APRIL, растворимый TACI (внеклеточная часть TACI) используется для предотвращения взаимодействия между BlyS или APRIL и рецепторами клеточной мембраны (TACI, BCMA и BAFF-R), чтобы достичь цели блокирования биологической активности BlyS и APRIL и лечения аутоиммунных заболеваний или опухолей. Многочисленные исследования показали, что слитый белок (TACI-Fc) с внеклеточной частью связывания TACI с фрагментом Fc IgG может эффективно ингибировать заболевания, связанные с BlyS и APRIL. Например, клинические результаты слитого белка TACI Atacicept, разработанного ZymoGenetics и Merck Serono, показывают, что он оказывает терапевтическое действие на СКВ, ревматоидный артрит, лимфому и другие заболевания.
[0006] Кроме того, в патенте CN101323643B описан слитый белок, состоящий из усеченного TACI и иммуноглобулина Fc. Часть TACI слитого белка включает последовательность аминоконцевой области, начинающуюся с аминокислотного остатка 13 во внеклеточной области TACI, всю богатую цистеином область и частичную последовательность области стебля. Fc-часть иммуноглобулина слитого белка включает шарнирную область, область CH2 и область CH3. Последовательность TACI и последовательность Fc сливаются напрямую или через линкерную последовательность. Кроме того, его часть TACI выбрана из положений 13-108 или 13-118 аминокислотной последовательности TACI, линкерной последовательностью является 9Gly, и фрагмент Fc иммуноглобулина выбран из Fc иммуноглобулина человека или животного, который выбран из IgG, IgM, IgD и IgA, причем каждый тип иммуноглобулина включает каждый подтип, такой как IgG1. В патенте CN102085368B описан вышеупомянутый слитый белок TACI-Fc, полезный при лечении аутоиммунных заболеваний, таких как системная красная волчанка. В заявке на патент CN201810512508.8 доказывалось использование слитого белка TACI-Fc для лечения расстройства спектра зрительного нерва (NMOSD) и рассеянного склероза (MS). NMOSD включает оптический нейромиелит, рецидивирующий неврит зрительного нерва, продольно распространяющийся поперечный миелит, оптико-спинальную форму рассеянного склероза, длительный поперечный миелит, односторонний или двусторонний неврит зрительного нерва, неврит зрительного нерва или миелит, сопровождающий аутоиммунное заболевание, неврит зрительного нерва или миелит, сопровождающийся симптоматические или бессимптомные внутричерепные поражения.
[0007] Часть составов других лекарственных препаратов на основе антител и гибридных белков, которые были на рынке, являются следующими:
[0008] Из композиций вспомогательных ингредиентов вышеуказанного препарата антитела и слитого белка также можно видеть, что композиция слитого белка и препарата антитела имеет свою собственную уникальность. С одной стороны, из-за низкой стабильности и сложной структуры лекарств с моноклональными антителами производство и хранение таких лекарств чрезвычайно сложно. Из-за гетерогенной структуры антител, особенно областей, определяющих комплементарность (CDR), и гликозилирования Fc, разработку различных композиций моноклональных антител необходимо проводить индивидуально в зависимости от конкретного случая. При разработке составов антител возникают проблемы, связанные с конформацией, коллоидом или химической структурой антитела, такими как окисление, изомеризация, дезамидирование, агрегация, денатурация и фрагментация. При воздействии различных температур, влажности, pH и стрессовых условий стереоструктура mAb может измениться, особенно в гипервариабельных областях (HVR). Плохие продукты могут проявлять пониженную активность и, что более важно, повышенная иммуногенность может представлять опасность для пациента. Следовательно, жизненно важно выбрать лучшие адъюванты для защиты антитела (Ссылка 1: Monoclonal antibodies: formulations of marketed products and recent advances in novel delivery system, Yanan Cui et al., Drug Development and Industrial Pharmacy, Volume 43, Issue 4, Pages 519-530, 2017). С другой стороны, легкая агрегация и низкая стабильность продуктов слияния белков вызывают неблагоприятные иммунные ответы или мешают процессу очистки, что всегда было проблемой, которую необходимо решить в этой области. Более того, факторы, влияющие на агрегацию гибридных белков, также являются сложными, которые можно разделить на внешние и внутренние факторы. К внешним факторам в основном относятся температура, физическое давление и факторы растворителя (pH, ионная сила, концентрация, ионы металлов и т.д.); а внутренние факторы в основном включают структурные характеристики слитого белка, чувствительные остатки и непарный цистеин и т.д. Эти факторы будут влиять на агрегацию слитого белка, тем самым влияя на его стабильность и время хранения. Следовательно, выбор вспомогательных веществ для слитых белков требует обширных экспериментальных исследований (Ссылка 2: Production Challenges for Complex Biologics: Fusion Proteins, Stefan R. Schmidt, American Pharmaceutical Review, pages 1-5, 2017).
[0009] Таким образом, целью настоящего изобретения является получение комбинации состава слитого белка TACI-Fc посредством широкого диапазона скрининга и исследования диапазона концентраций доступных вспомогательных веществ для биологических составов для достижения следующих технических эффектов: слитый белок TACI-Fc может хорошо растворяться до и после лиофилизации, при этом нерастворимые микрочастицы и видимые посторонние вещества соответствуют стандартам инъекций для использования человеком, и при этом остается стабильным в течение длительного времени в процессе лиофилизации и хранения и не склонен к полимеризации или деградация после повторного растворения с сохранением хорошей биологической активности.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0010] Настоящее изобретение относится к водному жидкому фармацевтическому составу слитого белка TACI-Fc, содержащему слитый белок TACI-Fc, невосстанавливающий сахар и аминокислоту; где невосстанавливающий сахар выбран из маннита, сахарозы, трегалозы и их комбинации; и аминокислота выбрана из гистидина, аланина, аргинина, глицина, глутаминовой кислоты и их комбинации.
[0011] В некоторых вариантах осуществления изобретения гистидин представляет собой гидрохлорид гистидина в концентрации 1-100 ммоль/л, предпочтительно, 5-50 ммоль/л, 5-20 ммоль/л, 8-12 ммоль/л или около 10 ммоль/л; и аргинин представляет собой гидрохлорид аргинина в концентрации 10-160 ммоль/л, предпочтительно, 20-120 ммоль/л, 50-100 ммоль/л, 70-95 ммоль/л, 75-90 ммоль/л или около 90 ммоль/л или около 75 ммоль/л.
[0012] В некоторых вариантах осуществления изобретения концентрация сахарозы составляет 1-300 ммоль/л, предпочтительно, 5-200 ммоль/л, 10-100 ммоль/л, 35-45 ммоль/л или около 40 ммоль/л.
[0013] В некоторых вариантах осуществления изобретения концентрация маннита составляет 10-300 ммоль/л, предпочтительно, 10-200 ммоль/л, 60-150 ммоль/л, 85-125 ммоль/л, 90-120 ммоль/л или около 120 ммоль/л или около 90 ммоль/л.
[0014] В некоторых вариантах осуществления изобретения слитый белок TACI-Fc имеет аминокислотную последовательность, показанную в SEQ ID NO. 1. Белок содержит аминокислоты 13-118 TACI и оптимизированный фрагмент Fc, который снижает эффекты ADCC и CDC.
[0015] В слитом белке TACI-Fc, показанном в SEQ ID NO. 1, чтобы избежать эффекта антителозависимой клеточно-опосредованной токсичности (ADCC), вызванного мембраносвязанным BlyS или лигандом, индуцирующим пролиферацию (APRIL), фрагмент Fc, полученный из IgG1, был оптимизирован для секвенирования, где аминокислоты 120-123 в области CH2 фрагмента Fc были мутированы из лейцин (L)-лейцин (L)-глицин (G)-глицин (G) в аланин (A)-глутаминовая кислота (E)-глицин (G)-аланин (A), чтобы снизить сродство рецепторов Fcγ. Кроме того, область CH2 последовательности Fc также была мутирована (аминокислотные остатки 216~217 были мутированы из аланин (A)-пролина (P) на серин (S)-серин (S)) для уменьшения связывания или фиксации комплемента, тем самым снижая эффекты комплемент-зависимой цитотоксичности (CDC).
[0016] Последовательность SEQ ID NO: 1 является следующей:

[0017] В жидком составе два мономера слитого белка TACI-Fc могут образовывать двухцепочечную структуру из-за образования межцепочечной дисульфидной связи в шарнирной области Fc.
[0018] В некоторых вариантах осуществления изобретения концентрация слитого белка TACI-Fc составляет 5-240 мг/мл, предпочтительно, от около 50 мг/мл до около 100 мг/мл и, наиболее предпочтительно, от около 80 мг/мл до около 100 мг/мл.
[0019] В некоторых вариантах осуществления изобретения невосстанавливающий сахар представляет собой 90-120 ммоль/л маннита и/или 35-45 ммоль/л сахарозы, аминокислота представляет собой 75-125 ммоль/л гидрохлорида аргинина и/или 8-12 ммоль/л гидрохлорида гистидина, концентрация слитого белка TACI-Fc составляет 80-100 мг/мл; и концентрация гидрохлорида гистидина, более предпочтительно, составляет около 10 ммоль/л.
[0020] В некоторых вариантах осуществления изобретения содержание слитого белка TACI-Fc составляет от около 1% до около 10% (мас./об., г/100 мл), предпочтительно, содержание слитого белка TACI-Fc составляет около 6-10% (мас./об., г/100 мл).
[0021] В некоторых вариантах осуществления изобретения невосстанавливающий сахар представляет собой около 90 ммоль/л маннита и около 40 ммоль/л сахарозы, аминокислота представляет собой около 90 ммоль/л гидрохлорида аргинина и около 10 ммоль/л гидрохлорида гистидина и концентрация слитого белка TACI-Fc составляет около 80 мг/мл.
[0022] В некоторых вариантах осуществления изобретения невосстанавливающий сахар представляет собой около 120 ммоль/л маннита и около 40 ммоль/л сахарозы, аминокислота представляет собой около 75 ммоль/л гидрохлорида аргинина и около 10 ммоль/л гидрохлорида гистидина и концентрация слитого белка TACI-Fc составляет около 80 мг/мл.
[0023] В некоторых вариантах осуществления изобретения композиция имеет pH от 4,0 до 8,0, предпочтительно, от 4,5 до 7,0, от 5,0 до 6,0 или около 5,5. Значение pH раствора регулируется NaOH или соляной кислотой.
[0024] В другом аспекте настоящее изобретение относится к лиофилизированному фармацевтическому составу, полученному лиофилизацией водного жидкого фармацевтического состава.
[0025] В некоторых вариантах лиофилизированного фармацевтического состава жидкий водный фармацевтический состав содержит около 90 ммоль/л маннита, около 40 ммоль/л сахарозы, около 90 ммоль/л гидрохлорида аргинина, около 10 ммоль/л гидрохлорида гистидина и около 80 мг/мл слитого белка TACI-Fc, и водный жидкий фармацевтический состав имеет pH от 5,0 до 6,0.
[0026] В некоторых вариантах лиофилизированного фармацевтического состава жидкий водный фармацевтический состав содержит около 120 ммоль/л маннита, около 40 ммоль/л сахарозы, около 75 ммоль/л гидрохлорида аргинина, около 10 ммоль/л гидрохлорида гистидина и около 80 мг/мл слитого белка TACI-Fc, и водный жидкий фармацевтический состав имеет pH от 5,0 до 6,0.
[0027] В некоторых вариантах лиофилизированного фармацевтического состава невосстанавливающие сахара в жидком водном фармацевтическом составе представляют собой маннит и сахарозу в концентрациях около 16,4 мг/мл и около 13,7 мг/мл, соответственно; и аминокислоты в жидком водном фармацевтическом составе представляют собой гидрохлорид аргинина и гидрохлорид гистидина в концентрациях около 19,0 мг/мл и около 2,1 мг/мл, соответственно.
[0028] В некоторых вариантах лиофилизированного фармацевтического состава невосстанавливающие сахара в жидком водном фармацевтическом составе представляют собой маннит и сахарозу в концентрациях около 21,9 мг/мл и около 13,7 мг/мл, соответственно; и аминокислоты в водном жидком фармацевтическом составе представляют собой гидрохлорид аргинина и гидрохлорид гистидина в концентрациях около 15,8 мг/мл и около 2,1 мг/мл, соответственно.
[0029] Настоящее изобретение дополнительно относится к применению фармацевтического состава при изготовлении лекарственного средства для лечения аутоиммунного заболевания, и аутоиммунное заболевание включает системную красную волчанку, ревматоидный артрит, расстройство спектра нейромиелита зрительного нерва (NMOSD), рассеянный склероз (РС) и синдром Шегрена, при этом расстройство спектра нейромиелита зрительного нерва включает нейромиелит зрительного нерва, рецидивирующий неврит зрительного нерва, продольно распространяющийся поперечный миелит, оптико-спинальная форма рассеянного склероза, долговременный поперечный миелит, односторонний или двусторонний неврит зрительного нерва, неврит зрительного нерва или миелит, сопровождающий аутоиммунное заболевание, неврит зрительного нерва или миелит, сопровождающийся симптоматическими или бессимптомными внутричерепными поражениями, и лимфома включает хронический лимфолейкоз, множественную миелому и лимфому B-лимфоцитов.
[0030] Настоящее изобретение также относится к способу получения фармацевтического состава слитого белка TACI-Fc, включающему: (1) приготовление состава, как описано выше; и (2) оценку стабильности слитого белка TACI-Fc в составе.
[0031] В другом аспекте настоящее изобретение также относится к способу приготовления фармацевтического состава, как описано выше, включающему следующие стадии: получение исходного раствора белка, предварительное замораживание, первичную сушку, вторичную сушку и субупаковку.
[0032] В некоторых вариантах осуществления изобретения стадия получения исходного раствора белка включает:
[0033] 1. Культивирование генетически рекомбинантных клеток СНО, способных экспрессировать слитый белок TACI-Fc, и когда жизнеспособность клеток достигает приемлемого нижнего предела, отделение клеток центрифугированием или фильтрацией и сбор супернатанта;
2. Выполнение первой стадии очистки с использованием колонки для аффинной хроматографии с протеином А и элюирование полученного целевого белка для ультрафильтрации и концентрирования. Затем проводят вторую стадию очистки на хроматографической колонке с композитной насадкой и собирают пик целевого белка. Наконец, выполнение третьей стадии очистки на третьей колонке в режиме проникновения целевого белка.
[0034] В некоторых вариантах осуществления изобретения стадия получения исходного раствора белка дополнительно включает: после прохождения теста очищенный белок смешивают с «5× буфером для приготовления состава» для ультрафильтрации и концентрирования для получения исходного раствора белка.
[0035] В некоторых вариантах осуществления изобретения полученный исходный раствор белка необходимо точно разбавить до требуемой концентрации белка с помощью буфера для приготовления состава, не содержащего белка, чтобы получить раствор-полуфабрикат белка, который затем разделяют по флаконам для вакуумной лиофилизации. Основной технический эффект, достигаемый настоящим изобретением, заключается в том, что белок TACI-Fc после высокой степени очистки имеет чистоту более 99% невосстанавливающего SDS-PAGE, и белок клетки-хозяина CHO, ДНК-хозяин клетки CHO, бактериальный эндотоксин и другие индикаторы соответствуют требованиям стандарта «Китайской фармакопеи» (издание 2005 г.). Фармацевтический состав, содержащий слитый белок TACI-Fc, полученный в соответствии с настоящим описанием, достиг превосходных стандартов с точки зрения содержания влаги, количества частиц, количества видимых посторонних материалов и нерастворимых микрочастиц, а фармацевтический состав имеет стабильность при длительном хранении.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
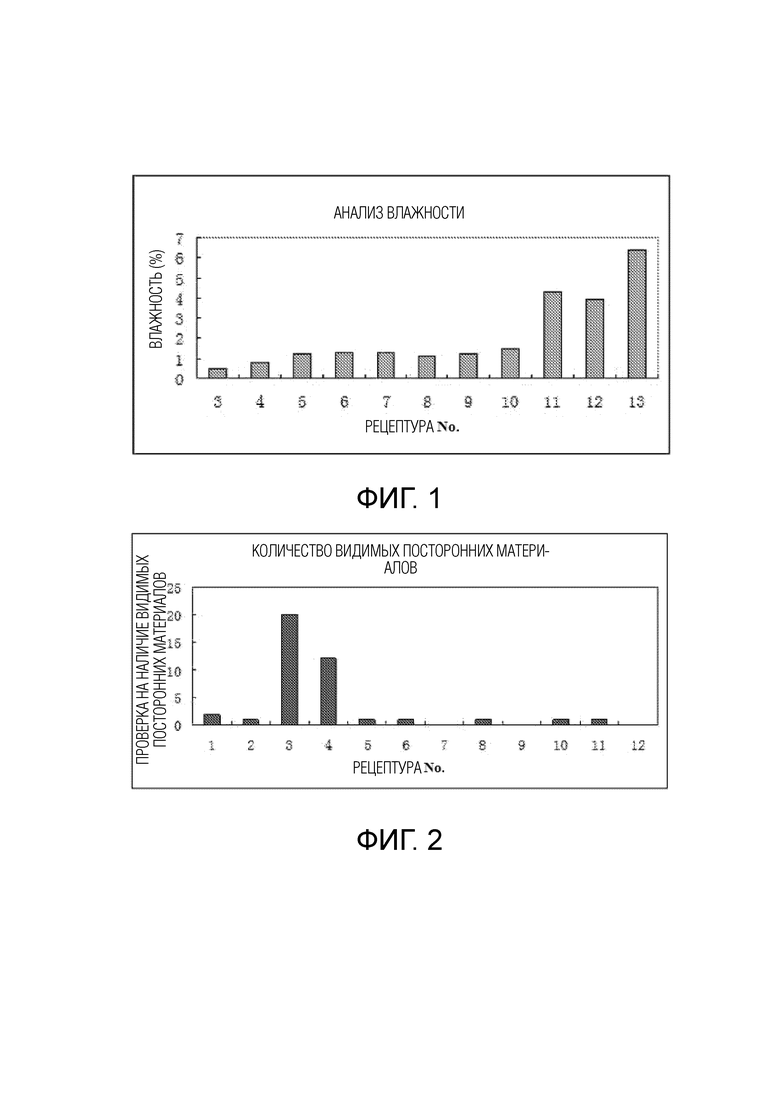
[0036] ФИГ. 1: Определение влажности. Результаты показывают, что лиофилизированные порошки рецептур 11, 12 и 13 очень легко впитывают воду, а содержание влаги не соответствует требованиям. Рецептуры с 3 по 9 соответствуют требованиям теста на влажность.
[0037] ФИГ. 2: Анализ видимых посторонних материалов. Результаты показывают, что рецептуры 3 и 4 не соответствуют требованиям теста на наличие видимых посторонних материалов.
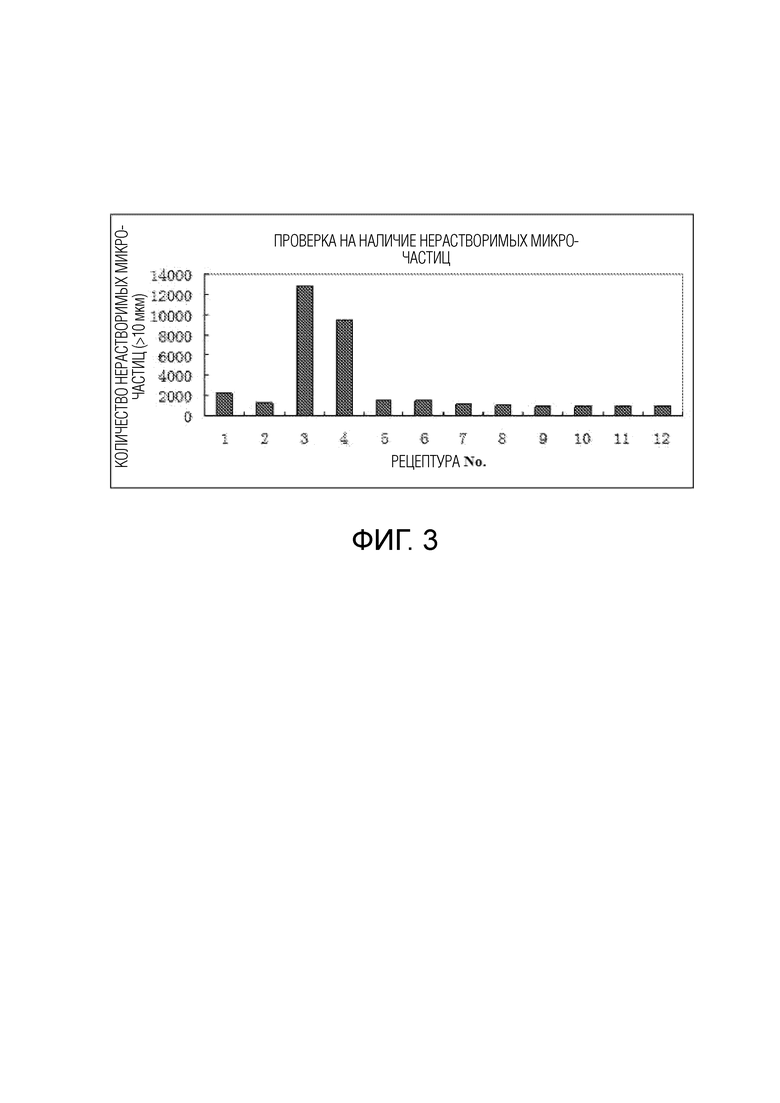
[0038] ФИГ. 3: Анализ нерастворимых микрочастиц. Результаты показывают, что рецептуры 3 и 4 не соответствуют требованиям проверки нерастворимых микрочастиц.
ПОДРОБНОЕ ОПИСАНИЕ
[0039] Пример 1: Получение и очистка слитого белка TACI-Fc
[0040] Тотальную РНК экстрагировали из мононуклеарных клеток периферической крови человека с помощью набора для экстракции РНК Qiagen. Затем из РНК с помощью обратной транскриптазы была синтезирована кДНК, далее для амплификации желаемых фрагментов TACI проводили полимеразную цепную реакцию с праймерами (прямой: 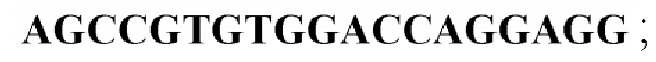 обратный:
обратный: 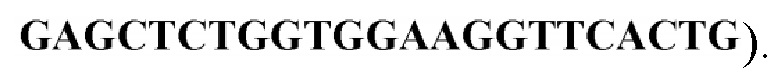 Фрагмент Fc иммуноглобулина получали с помощью ПЦР-амплификации из клонированной плазмиды Fc с оптимизированной последовательностью IgG1 со сниженными эффектами ADCC и CDC. Наконец, последовательности TACI и Fc были слиты с помощью ПЦР для конструирования последовательности ДНК слитого белка TACI-Fc (его аминокислотная последовательность показана в SEQ ID NO. 1). Позже, используя набор для клонирования ТА, продукты ПЦР TACI и Fc были клонированы в плазмиду pCR2.1, соответственно, которую затем трансфицировали в E. coli. После этого отбирали белые колонии и добавляли среду LB для ночного культивирования. Затем плазмиду экстрагировали с помощью набора для экстракции плазмид Qiangen, и последовательности TACI и Fc идентифицировали расщеплением рестрикционным ферментом и секвенированием. Наконец, кДНК TACI и IgG Fc лигировали вместе методом ПЦР сплайсинга. Фрагмент TACI-Fc вставляли в экспрессионную плазмиду. Впоследствии рекомбинантную плазмиду трансфицировали в E. coli, затем отбирали положительные колонии с последующей экстракцией плазмиды, и последовательности-мишени идентифицировали расщеплением рестрикционным ферментом и секвенированием. Затем плазмиду трансфицировали в клетки СНО, и генетически рекомбинированные клетки СНО культивировали в стандартных условиях. Когда питательные вещества в среде были исчерпаны и клетки переставали расти, культуральную смесь собирали. Затем клетки разделяли центрифугированием или фильтрацией, и супернатант, содержащий белок TACI-Fc, собирали и наносили на колонку для аффинной хроматографии с белком А для первой очистки. Элюированный целевой белок затем концентрировали ультрафильтрацией до целевой концентрации белка 30-50 мг/мл и загружали в хроматографическую колонку с композитной насадкой для второй очистки. Целевой белок собирали и затем загружали в третью колонку для третьей очистки в режиме проникновения целевого белка. Очищенный белок, прошедший испытание по различным показателям, смешивали с «5× буфером для приготовления состава» в объемном соотношении 4:1, и затем концентрировали ультрафильтрацией для получения белка с концентрацией около 100 мг/мл, который был исходным раствором белка и мог храниться при -80°C в течение длительного времени.
Фрагмент Fc иммуноглобулина получали с помощью ПЦР-амплификации из клонированной плазмиды Fc с оптимизированной последовательностью IgG1 со сниженными эффектами ADCC и CDC. Наконец, последовательности TACI и Fc были слиты с помощью ПЦР для конструирования последовательности ДНК слитого белка TACI-Fc (его аминокислотная последовательность показана в SEQ ID NO. 1). Позже, используя набор для клонирования ТА, продукты ПЦР TACI и Fc были клонированы в плазмиду pCR2.1, соответственно, которую затем трансфицировали в E. coli. После этого отбирали белые колонии и добавляли среду LB для ночного культивирования. Затем плазмиду экстрагировали с помощью набора для экстракции плазмид Qiangen, и последовательности TACI и Fc идентифицировали расщеплением рестрикционным ферментом и секвенированием. Наконец, кДНК TACI и IgG Fc лигировали вместе методом ПЦР сплайсинга. Фрагмент TACI-Fc вставляли в экспрессионную плазмиду. Впоследствии рекомбинантную плазмиду трансфицировали в E. coli, затем отбирали положительные колонии с последующей экстракцией плазмиды, и последовательности-мишени идентифицировали расщеплением рестрикционным ферментом и секвенированием. Затем плазмиду трансфицировали в клетки СНО, и генетически рекомбинированные клетки СНО культивировали в стандартных условиях. Когда питательные вещества в среде были исчерпаны и клетки переставали расти, культуральную смесь собирали. Затем клетки разделяли центрифугированием или фильтрацией, и супернатант, содержащий белок TACI-Fc, собирали и наносили на колонку для аффинной хроматографии с белком А для первой очистки. Элюированный целевой белок затем концентрировали ультрафильтрацией до целевой концентрации белка 30-50 мг/мл и загружали в хроматографическую колонку с композитной насадкой для второй очистки. Целевой белок собирали и затем загружали в третью колонку для третьей очистки в режиме проникновения целевого белка. Очищенный белок, прошедший испытание по различным показателям, смешивали с «5× буфером для приготовления состава» в объемном соотношении 4:1, и затем концентрировали ультрафильтрацией для получения белка с концентрацией около 100 мг/мл, который был исходным раствором белка и мог храниться при -80°C в течение длительного времени.
Скрининг вспомогательных веществ
[0041] Посредством анализа большого количества информации и экспериментального скрининга на ранней стадии сахароза, маннит, глицерин, гистидин, аргинин, полисорбат 80 (т.е. Твин 80) и т.п. были предварительно идентифицированы как кандидаты во вспомогательные вещества для дальнейшего скрининга, и далее были проведены следующие испытания.
[0042] Пример 2: Исследование стимулирования растворения белка TACI-Fc аргинином
[0043] После культивирования в течение ночи белка TACI-Fc в буфере без аргинина (например, 20 ммоль/л NaH2PO4-Na2HPO4 120 ммоль/л NaCl, pH 5,5) при концентрации белка выше 5 мг/мл при температуре 4°C холодильника, на дне контейнера будет появляться хлопьевидный осадок, и проверка видимых посторонних материалов и нерастворимых микрочастиц не может быть выполнена из-за плавающего осадка при осторожном встряхивании. Чем выше концентрация белка, тем серьезнее осаждается белок. Предварительные экспериментальные исследования показывают, что добавление гидрохлорида аргинина к раствору белка может привести к быстрому исчезновению осадка.
[0044] Дальнейшие эксперименты: 1) 7290 мг очищенного белка TACI-Fc диализовали в 10 ммоль/л гистидинового (pH 5,5) буфера с концентрацией белка 5 мг/мл; 2) Белковый раствор делили на 9 групп, 7 порций в группе, всего 63 порции, с содержанием 7 порций белка в каждой группе по 10, 20, 40, 100, 160, 200, 300 мг, соответственно, и в каждую из 9 групп добавляли раствор 1 моль/л гидрохлорида аргинина (pH 5,5) до тех пор, пока конечная концентрация гидрохлорида аргинина не становилась 0, 10, 20, 30, 40, 50, 75, 100, 125 ммоль/л, соответственно, а затем концентрировали с помощью центробежной ультрафильтрационной пробирки с размером пор 30 кД до конечного объема 2 мл. Наблюдали за явным осаждением белка. Если были очевидные осадки, дальнейшая процедура требовалась, и в таблице прямо указывалось «-». Если осаждение не было очевидным, раствор белка фильтровали в стерильный флакон объемом 2 мл со стерильным шприцевым фильтром 0,22 мкм на сверхчистом столе. Каждый флакон закрывали стерильной резиновой пробкой, надевали алюминиевый колпачок и хранили в холодильнике при 4°C в течение 24 часов, чтобы наблюдать, будет ли выпадать осадок.
[0045] Стандарт контроля: наблюдение под детектором прозрачности YB-II. Полностью четкие или не более 3-х белых пятен помечаются знаком «-». Если есть осадки, они помечаются как «+», «++» и «+++» в зависимости от количества выпавших осадков. Больше знаков «+» означает большее количество осадков. Результаты экспериментов, представленные в таблице 1, показывают, что оптимальная концентрация гидрохлорида аргинина составляет от 75 ммоль/л до 125 ммоль/л.
[0046]
[0047] Таблица 1. Влияние концентрации гидрохлорида аргинина на растворимость белка TACI-Fc
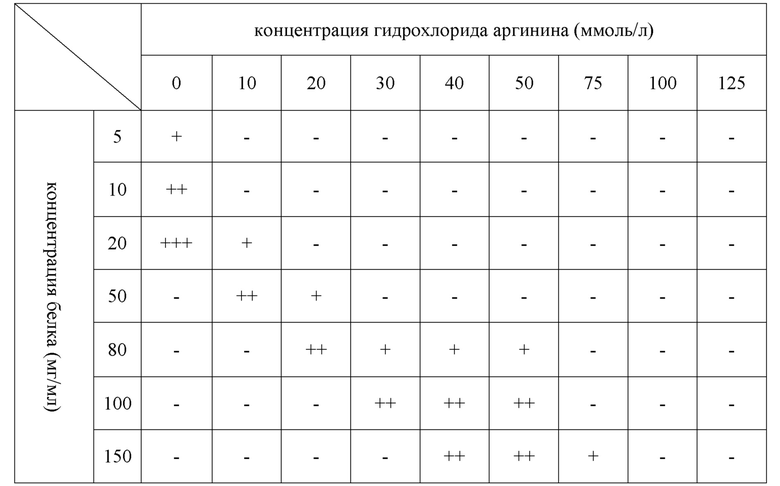
[0048] Пример 3: Определение влияния концентрации маннита на содержание влаги и внешний вид лиофилизированного порошка
[0049] Посредством тех же стадий, что и в примере 2, исследовали содержание влаги и внешний вид лиофилизированного порошка, приготовленного с различными концентрациями слитого белка TACI-Fc в присутствии различных концентраций маннита. Эксперименты показывают, что, когда содержание маннита составляет менее 60 ммоль/л, это влияет на содержание влаги и внешний вид лиофилизированного порошка.
[0050] Пример 4: Влияние сахарозы на защитный эффект слитого белка TACI-Fc
[0051] Стабильность лиофилизированных порошков фармацевтических составов, содержащих различные концентрации сахарозы в условиях 4°C, 25°C и 35°C была исследована посредством экспериментов, которые показали, что, когда концентрация сахарозы в лиофилизированном исходном растворе составляет ниже 10 ммоль/л, маточный раствор теряет активность слитого белка TACI-Fc во время лиофилизации и не проявляет эффективного защитного эффекта от лиофилизации.
[0052] Пример 5: Приготовление пробного раствора состава
[0053] На основе вышеупомянутых экспериментов были разработаны различные рецептуры состава для дальнейшего исследования.
[0054] Приготовление раствора гидрохлорида гистидина:
В соответствии с рецептурами, приведенными в таблице 2, были приготовлены 1× буферы для приготовления состава рецептур №1-13. Взяв в качестве примера рецептуру №1 в таблице 2:
1) Путем расчета, отвешивая 2,10 г гидрохлорида гистидина, 0 г маннита, 15,80 г гидрохлорида аргинина и 54,77 г сахарозы в чистый стакан емкостью 1 л;
2) Добавление соответствующего количества воды для инъекций для растворения и корректировка pH после растворения;
3) Регулировка объема в соответствии с плотностью раствора методом взвешивания, а затем точная регулировка pH до 5,5.
Другие рецептуры были приготовлены в соответствии с вышеуказанными этапами в соответствии с количеством каждой рецептуры.
[0055] Приготовление буфера для диализа: 10 ммоль/л гидрохлорида гистидина, pH 5,5.
[0056] Приготовление буфера для приготовления состава:
[0057] 1× буфер для приготовления состава: он был приготовлен в соответствии с таблицей рецептур буфера для приготовления состава (таблица 2);
[0058] 5× буфер для приготовления состава: рецептура представлена в таблице 3, где концентрация гидрохлорида гистидина составляла 10 ммоль/л, концентрация гидрохлорида аргинина составляла CArg×5 ммоль/л, концентрация маннита составляла CMan×5 ммоль/л, и концентрация сахарозы составляла CSuc×5 ммоль/л при фиксированном pH 5,5. CArg, CMan и CSuc представляют собой концентрацию аргинина, маннита и сахарозы в соответствующей рецептуре в 1× буфере для приготовления состава, соответственно.
[0059] Величину pH вышеуказанных растворов доводили с помощью 6 моль/л гидроксида натрия или 6 моль/л соляной кислоты, и растворы использовали после ультрафильтрации с ультрафильтрационной мембраной с размером пор не более 10 кД для удаления эндотоксинов.
Таблица 2. Таблица рецептур 1× буфера для приготовления состава
[0060] Инструкции по составлению рецептур:
[0061] 1. Гидрохлорид гистидина представляет собой буферный агент для pH. Согласно проведенной ранее экспериментальной проверке в качестве концентрации использовалась 10 ммоль/л; и на основании приведенных выше примеров было определено, что минимальная концентрация маннита в каждой рецептуре составляла 60 ммоль/л, минимальная концентрация гидрохлорида аргинина составляла 75 ммоль/л, а минимальная концентрация сахарозы составляла 10 ммоль/л.
[0062] 2. Объединяли по четыре концентрации маннита, гидрохлорида аргинина и сахарозы. 60, 90, 120 и 150 ммоль/л маннита, 75, 90, 105 и 120 ммоль/л гидрохлорида аргинина и 10, 40, 70, 100 ммоль/л сахарозы составляют 10 различных комбинаций (рецептуры 4-13). Кроме того, рецептура 1 содержит только гидрохлорид аргинина и маннит, рецептура 2 содержит только гидрохлорид аргинина, а рецептура 3 содержит только гидрохлорид аргинина и сахарозу.
Таблица 3. Таблица рецептур 5× буфера для приготовления состава
[0063] Пример 6: Вакуумная сублимационная сушка
[0064] Исходный раствор белка извлекали из холодильника с температурой -80°C, размораживали, точно разбавляли «1× буфером для приготовления состава» до концентрации белка 80 мг/мл и субупаковывали в стерильный апирогенный стандартный лиофилизированный флакон объемом 20 мл, по 1 мл на флакон, а затем подвергали сублимационной сушке в вакууме.
[0065] Условия сублимационной сушки
[0066] Предварительное замораживание: -45°C в течение 5 часов;
[0067] Первичная сушка: -26°C в течение 40 часов при степени вакуума 10-15 Па; и
[0068] Вторичная сушка: 25°C в течение 10 часов при степени вакуума 10-15 Па.
[0069] После лиофилизации флаконы закрывали резиновой пробкой в вакууме, вынимали из лиофилизатора и надевали алюминиевый колпачок.
[0070] Пример 7: Проверка внешнего вида и содержания влаги в лиофилизированном порошке
[0071] Стандарты приемлемости для внешнего вида лиофилизированных порошков следующие: однородный цвет, ровные и плотные поры, а объем и форма до и после лиофилизации остаются в основном неизменными, показывая структуру блоков или губчатой массы.
Таблица 4. Наблюдение за внешним видом лиофилизированного порошка
Примечание: «--» означает, что объем массы был уменьшен до менее чем половины ее объема перед лиофилизацией; «-» означает, что объем массы был уменьшен до более чем половины ее объема перед лиофилизацией; «+» указывает на то, что только краевая часть имела небольшую усадку, и объем массы был в основном таким же, как и до лиофилизации; а «++» означает, что объемной усадки вообще не было, и объем продукта был таким же, как до лиофилизации.
[0072] Экспериментальные результаты, приведенные в таблице 4, показывают, что внешний вид лиофилизированного порошка рецептуры 1, рецептуры 2, рецептуры 10 и рецептуры 13 не соответствует требованиям и исключен. Внешний вид лиофилизированного порошка других рецептур соответствует требованиям.
[0073] Стандарт испытаний для анализа содержания влаги:
[0074] Влажность лиофилизированного порошка измеряли с помощью анализатора микровлажности типа SF-6 (кулонометрический метод Карла Фишера), и стандарт приемлемости составляет не более 3%.
Таблица 5. Результаты измерения влажности
[0075] Результаты экспериментов показывают, что лиофилизированные порошки рецептур 11, 12 и 13 очень легко впитывают воду, и содержание влаги не соответствует требованиям. Рецептуры 3-9 соответствуют требованиям теста на влажность.
[0076] Пример 8: Проверка видимых посторонних материалов и нерастворимых микрочастиц
[0077] Лиофилизированный порошок повторно растворяли во флаконах в стерильной воде для инъекций, каждый объемом 1 мл. Перед повторным растворением его удаляли из вакуума, и затем медленно добавляли воду по внутренней стенке флакона.
[0078] Для проверки видимых посторонних материалов использовался детектор прозрачности YB-II. В соответствии с «Методом проверки на видимые посторонние предметы - методом проверки с помощью лампы» в «Китайской фармакопее» (издание 2005 г.), Приложение VB и соответствующими положениями «Уведомления о выпуске дополнительных положений метода проверки на предмет обнаружения посторонних материалов» Национальным отделом пищевых продуктов и медикаментов Администрацией [Регистрация Национального управления по санитарному надзору за качеством пищевых продуктов и медикаментов [2005] № 37] было проверено 20 флаконов для каждой рецептуры и было рассчитано среднее содержание видимых посторонних материалов в каждом флаконе.
[0079] Стандарты приемки для проверки видимых посторонних материалов: среди 5 проверенных образцов (флаконов) не должно быть обнаружено никаких посторонних материалов, таких как осколки стекла, волокна, цветные пятна, цветные блоки, и не более 3 других видимых посторонних материалов (белые пятна, мелкие белковые хлопья или белковые частицы).
[0080] Исследование нерастворимых микрочастиц проводили с использованием детектора нерастворимых микрочастиц ZWJ-3. В соответствии с «Методом исследования нерастворимых микрочастиц - методом фоторезистентности» в «Китайской фармакопее» (издание 2005 г.), приложение IXC, исследовали количество нерастворимых микрочастиц размером более 10 микрон и более 25 микрон в каждом миллилитре белкового раствора. Для каждой рецептуры проверяли 3 флакона и рассчитывали среднее содержание нерастворимых микрочастиц в каждом флаконе.
[0081] Нормы приемлемости для проверки нерастворимых микрочастиц: каждый испытательный контейнер должен содержать не более 6000 микрочастиц размером 10 мкм или более и не более 600 микрочастиц размером 25 мкм или более.
Таблица 6. Результаты проверки на наличие видимых посторонних материалов и нерастворимых микрочастиц
[0082] Согласно данным, представленным в таблице 6, можно видеть, что рецептуры 3 и 4 не соответствуют требованиям для проверки видимых посторонних материалов и нерастворимых микрочастиц.
[0083] Пример 9. Длительное (1-12 месяцев) исследование стабильности лиофилизированного порошка
[0084] Рецептуры 1, 2, 10 и 13 были исключены по результатам проверки внешнего вида лиофилизированного порошка, рецептуры 11 и 12 были исключены по результатам проверки содержания влаги, и рецептуры 3 и 4 были исключены по результатам проверки видимых посторонних веществ и нерастворимых микрочастиц. Исследование стабильности проводилось для остальных рецептур 5, 6, 7, 8 и 9. Лиофилизированный порошок каждой рецептуры хранили при 37°C, 25°C и 4°C, соответственно, и отбирали пробы в разное время для таких анализов, как SDS-PAGE, ВЭЖХ с обращенной фазой, биологическая активность методом связывания лиганда, содержание влаги, внешний вид, pH, видимые инородные тела и нерастворимые микрочастицы. Результаты представлены в таблицах 7, 8 и 9.
[0085] Результаты показывают, что рецептура с концентрацией сахарозы 10 ммоль/л имела плохую стабильность, а рецептура 8 и рецептура 9 с концентрацией сахарозы 40 ммоль/л имели лучшую стабильность при длительном хранении. Во всех аспектах рецептуры 8-9 соответствуют требованиям в отношении содержания влаги, видимых посторонних материалов, внешнего вида, нерастворимых микрочастиц и стабильности.
Таблица 7. Результаты исследования стабильности после хранения при 37°C в течение 1 месяца
(%)
Таблица 8. Результаты исследования стабильности после хранения при 25°C в течение 3 месяца
(%)
Таблица 9. Результаты исследования стабильности после хранения при 4°C в течение 12 месяца
(%)
[0086] На основании приведенных выше экспериментальных данных можно видеть, что, с одной стороны, выбор конкретных вспомогательных веществ в классе веществ, таких как невосстанавливающие сахара и аминокислоты, оказывает непредсказуемое влияние на конечный состав. Для слитого белка по настоящему изобретению необходимо большое количество экспериментов для тестирования различных свойств, чтобы наконец получить хорошее сочетание компонентов. Например, согласно экспериментальным данным, хотя все рецептуры 1-13 содержат гидрохлорид гистидина, маннит, гидрохлорид аргинина и сахарозу, из-за разницы в содержании этих компонентов результаты окончательной проверки содержания влаги, видимых посторонних материалов, внешнего вида, нерастворимых микрочастиц и стабильности значительно различались, и только рецептуры 8 и 9 смогли пройти вышеуказанные тесты. По существу, выбор типов и содержания вспомогательных компонентов фармацевтических составов имеет решающее значение, и его предсказуемость оставляет желать лучшего.
[0087] С другой стороны, из-за гетерогенной структуры антител, особенно областей, определяющих комплементарность (CDR), и гликозилирования Fc, разработку различных композиций моноклональных антител необходимо проводить индивидуально в зависимости от конкретного случая. При разработке составов антител возникают проблемы, связанные с конформацией, коллоидом или химической структурой антитела, такими как окисление, изомеризация, деамидирование, агрегация, денатурация и фрагментация. На основании приведенной выше информации можно увидеть, что компоненты рецептур ранее продаваемых лекарственных средств на основе антител и гибридных белков обладают собственной уникальностью. Когда специалисты в данной области сталкиваются с выбором вспомогательных веществ для лекарственных препаратов на основе антител, четкие указания, полученные из продуктов предшествующего уровня техники, не являются достаточно показательными и по-прежнему нуждаются в большом количестве тестов для определения подходящих протоколов составления. На основе обширных и долгосрочных экспериментальных исследований в настоящем описании получена композиция, подходящая для составов слитых белков TACI-Fc, которые хорошо растворяются до и после лиофилизации, при этом нерастворимые микрочастицы и видимые посторонние вещества соответствуют стандартам инъекций для использования человеком, и при этом остаются стабильными в течение длительного времени в процессе лиофилизации и хранения, даже при длительном хранении в условиях высоких температур 25°C или 37°C. Лиофилизированный состав не был склонен к полимеризации или разложению после повторного растворения, сохранял хорошую биологическую активность и достигал неожиданных технических эффектов.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> REMEGEN CO., LTD.
<120> ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ СЛИТОГО БЕЛКА TACI-FC
<130> 2020
<160> 1
<170> PatentIn version 3.3
<210> 1
<211> 333
<212> PRT
<213> искусственная последовательность
<220>
<223> RC18 аминокислотная последовательность
<400> 1
Ser Arg Val Asp Gln Glu Glu Arg Phe Pro Gln Gly Leu Trp Thr Gly
1 5 10 15
Val Ala Met Arg Ser Cys Pro Glu Glu Gln Tyr Trp Asp Pro Leu Leu
20 25 30
Gly Thr Cys Met Ser Cys Lys Thr Ile Cys Asn His Gln Ser Gln Arg
35 40 45
Thr Cys Ala Ala Phe Cys Arg Ser Leu Ser Cys Arg Lys Glu Gln Gly
50 55 60
Lys Phe Tyr Asp His Leu Leu Arg Asp Cys Ile Ser Cys Ala Ser Ile
65 70 75 80
Cys Gly Gln His Pro Lys Gln Cys Ala Tyr Phe Cys Glu Asn Lys Leu
85 90 95
Arg Ser Pro Val Asn Leu Pro Pro Glu Leu Asp Lys Thr His Thr Cys
100 105 110
Pro Pro Cys Pro Ala Pro Glu Ala Glu Gly Ala Pro Ser Val Phe Leu
115 120 125
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
130 135 140
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
145 150 155 160
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
165 170 175
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
180 185 190
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
195 200 205
Val Ser Asn Lys Ala Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
210 215 220
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
225 230 235 240
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
245 250 255
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
260 265 270
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
275 280 285
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
290 295 300
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
305 310 315 320
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<---
Группа изобретений относится к области медицины и фармацевтики. Первое изобретение группы: водный жидкий фармацевтический состав слитого белка TACI-Fc для лечения аутоиммунного заболевания или лимфомы, содержащий слитый белок TACI-Fc, невосстанавливающий сахар и аминокислоту; где слитый белок TACI-Fc имеет аминокислотную последовательность SEQ ID NO.1, невосстанавливающий сахар представляет собой 90-120 ммоль/л маннита и/или 35-45 ммоль/л сахарозы, аминокислота представляет собой 75-125 ммоль/л гидрохлорида аргинина и/или 8-12 ммоль/л гидрохлорида гистидина, и концентрация слитого белка TACI-Fc составляет 80-100 мг/мл. Также группа изобретений относится к лиофилизированному составу, полученному из указанного водного состава; к применению фармацевтических составов при изготовлении лекарственного средства для лечения аутоиммунного заболевания или лимфомы; к способу получения фармацевтического состава слитого белка TACI-Fc. Группа изобретений обеспечивает высокую растворимость слитого белка TACI-Fc до и после лиофилизации, соответствие стандартам инъекций для человека в отношении содержания нерастворимых микрочастиц и видимых посторонних веществ, стабильность в процессе лиофилизации и хранения без полимеризации или деградации после повторного растворения с сохранением биологической активности. 5 н. и 11 з.п. ф-лы, 9 табл., 9 пр., 3 ил.
1. Водный жидкий фармацевтический состав слитого белка TACI-Fc для лечения аутоиммунного заболевания или лимфомы, содержащий слитый белок TACI-Fc, невосстанавливающий сахар и аминокислоту; где слитый белок TACI-Fc имеет аминокислотную последовательность SEQ ID NO.1, невосстанавливающий сахар представляет собой 90-120 ммоль/л маннита и/или 35-45 ммоль/л сахарозы, аминокислота представляет собой 75-125 ммоль/л гидрохлорида аргинина и/или 8-12 ммоль/л гидрохлорида гистидина, и концентрация слитого белка TACI-Fc составляет 80-100 мг/мл.
2. Водный жидкий фармацевтический состав по п.1, в котором концентрация гидрохлорида гистидина составляет около 10 ммоль/л.
3. Водный жидкий фармацевтический состав по любому из пп.1, 2, содержащий от около 1% до около 10 мас./об.% (г/100 мл) слитого белка TACI-Fc, предпочтительно, около 6-10 мас./об.% (г/100 мл) слитого белка TACI-Fc.
4. Водный жидкий фармацевтический состав по п.1 или 3, в котором невосстанавливающий сахар представляет собой около 90 ммоль/л маннита и около 40 ммоль/л сахарозы, аминокислота представляет собой около 90 ммоль/л гидрохлорида аргинина и около 10 ммоль/л гидрохлорида гистидина, и концентрация слитого белка TACI-Fc составляет около 80 мг/мл.
5. Водный жидкий фармацевтический состав по п.1 или 3, в котором невосстанавливающий сахар представляет собой около 120 ммоль/л маннита и около 40 ммоль/л сахарозы, аминокислота представляет собой около 75 ммоль/л гидрохлорида аргинина и около 10 ммоль/л гидрохлорида гистидина, и концентрация слитого белка TACI-Fc составляет около 80 мг/мл.
6. Водный жидкий фармацевтический состав по любому из пп.1-5, где состав имеет pH от 4,0 до 8,0, предпочтительно, от 4,5 до 7,0, от 5,0 до 6,0 или около 5,5.
7. Водный жидкий фармацевтический состав по любому из пп.1-6, где два из слитых белков TACI-Fc в водном жидком фармацевтическом составе образуют двухцепочечную структуру через связывающую дисульфидную связь, образованную в шарнирной области Fc.
8. Лиофилизированный фармацевтический состав для лечения аутоиммунного заболевания или лимфомы, полученный лиофилизацией водного жидкого фармацевтического состава по любому из пп.1-7.
9. Лиофилизированный фармацевтический состав по п.8, в котором жидкий водный фармацевтический состав содержит около 90 ммоль/л маннита, около 40 ммоль/л сахарозы, около 90 ммоль/л гидрохлорида аргинина, около 10 ммоль/л гидрохлорида гистидина и около 80 мг/мл слитого белка TACI-Fc, и имеет pH от 5,0 до 6,0.
10. Лиофилизированный фармацевтический состав по п.8, где жидкий водный фармацевтический состав содержит около 120 ммоль/л маннита, около 40 ммоль/л сахарозы, около 75 ммоль/л гидрохлорида аргинина, около 10 ммоль/л гидрохлорида гистидина и около 80 мг/мл слитого белка TACI-Fc, и имеет pH от 5,0 до 6,0.
11. Лиофилизированный фармацевтический состав по п.8, где невосстанавливающие сахара в водном жидком фармацевтическом составе представляют собой маннит и сахарозу в концентрациях около 16,4 мг/мл и около 13,7 мг/мл, соответственно; и аминокислоты в жидком водном фармацевтическом составе представляют собой гидрохлорид аргинина и гидрохлорид гистидина в концентрациях около 19,0 мг/мл и около 2,1 мг/мл, соответственно.
12. Лиофилизированный фармацевтический состав по п.8, где невосстанавливающие сахара в водном жидком фармацевтическом составе представляют собой маннит и сахарозу в концентрациях около 21,9 мг/мл и около 13,7 мг/мл, соответственно; и аминокислоты в водном жидком фармацевтическом составе представляют собой гидрохлорид аргинина и гидрохлорид гистидина в концентрациях около 15,8 мг/мл и около 2,1 мг/мл, соответственно.
13. Применение фармацевтического состава по любому из пп.1-12 при изготовлении лекарственного средства для лечения аутоиммунного заболевания, где аутоиммунное заболевание включает системную красную волчанку, ревматоидный артрит, расстройство оптического спектра нейромиелита (NMOSD), рассеянный склероз (МС) и синдром Шегрена.
14. Применение по п.13, где расстройство оптического спектра нейромиелита включает оптический нейромиелит, рецидивирующий неврит зрительного нерва, продольно распространяющийся поперечный миелит, зрительно-спинномозговую форму рассеянного склероза, длительный поперечный миелит, односторонний или двусторонний неврит зрительного нерва, неврит зрительного нерва или миелит, сопровождающий аутоиммунное заболевание, неврит зрительного нерва или миелит, сопровождающийся симптоматическими или бессимптомными внутричерепными поражениями.
15. Применение фармацевтического состава по любому из пп.1-12 при изготовлении лекарственного средства для лечения лимфомы, где лимфома включает хронический лимфоцитарный лейкоз, множественную миелому и лимфому B-лимфоцитов.
16. Способ получения фармацевтического состава слитого белка TACI-Fc, включающий: (1) приготовление состава по любому из пп.1-12; и (2) оценку стабильности слитого белка TACI-Fc в составе.
| ОРГАНИЧЕСКОЕ СВЯЗУЮЩЕЕ ДЛЯ МЕТАЛЛИЗАЦИОННЫХ ПАСТ НАРУЖНЫХ ЭЛЕКТРОДОВ МНОГОСЛОЙНЫХ КЕРАМИЧЕСКИХ КОНДЕНСАТОРОВ | 1990 |
|
RU2018183C1 |
| STRINGER J.L | |||
| DRUG, in: Ecyclopedia Britannica // материалы сайта: https://www.britannica.com, сохраненная версия статьи от 24.06.2015: https://web.archive.org/web/20150624085903/http://www.britannica.com/science/drug-chemical-agent | |||
| The Pursuit of Responsible Use of Medicines | |||
| Sharing and Learning from Country | |||
Авторы
Даты
2022-09-06—Публикация
2020-12-09—Подача