Область техники, к которой относится изобретение
Изобретение относится к области медицины, фармакологии и химико-фармацевтической промышленности, а именно, к новой кристаллической форме 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3Н-1,4-бензодиазепин-2-она, и включающей ее фармацевтической композиции и лекарственной форме, которые могут использоваться в качестве анксиолитического средства.
Уровень техники
Разные кристаллические и аморфные формы определенного активного вещества, могут обладать различными свойствами, такими как профиль растворения, температура плавления, стабильность, гигроскопичность, форма частиц, плотность, биодоступность, электризуемость, прессуемость, сыпучесть и т.д. Данные свойства тщательно анализируются и учитываются при изготовлении лекарственных средств. В частности, сильная электризуемость и низкая прессуемость не позволяют получить лекарственную форму, такую как таблетка. Лекарственные соединения должны обладать способностью хорошо растворяться и храниться в течение длительных периодов времени, не проявляя значительного изменения физико-химических свойств, например, не обводняться, что может приводить как к изменению химического состава лекарственно средства, так и к разрыхлению и рассыпанию лекарственной формы, например, таблетки.
Метод порошковой рентгеновской дифрактометрии позволяет идентифицировать даже небольшие изменения в состоянии атомной решетки кристалла, не детектируемые другими методами. Рентгенография поликристаллических образцов позволяет определять состояния твердого тела (кристаллическое, разные его формы, аморфное, или их комбинации). Значение структурных исследований весьма велико. Определение связи между атомной структурой и свойствами вещества позволяет устанавливать рациональный контроль за технологическими процессами, раскрывать причины изменения этих свойств под действием того или иного фактора, дает возможность более сознательно управлять технологическим процессом создания фармацевтических субстанций и изменять его в нужном направлении.
Ранее методом рентгеноструктурного анализа установлена кристаллическая и молекулярная структура 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3Н-1,4-бензодиазепин-2-она [1].
При этом до настоящего времени нет информации о возможном существовании других кристаллических форм 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3Н-1,4-бензодиазепин-2-она, а также их получении и свойствах.
Таким образом, задачей настоящего изобретения является разработка стабильной при хранении, негигроскопичной новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3Н-1,4-бензодиазепин-2-она.
Авторы изобретения неожиданно обнаружили, что полученная кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3Н-1,4-бензодиазепин-2-он, ранее неизвестная в уровне техники, обладает пониженной гигроскопичностью и повышенной стабильностью при хранении, а активная фармацевтическая субстанция, содержащая указанную новую кристаллическую форму, обладает улучшенной прессуемостью с хорошими показателями сыпучести без заметных электростатических явлений, при этом по меньшей мере не теряя свою терапевтическую эффективность.
Таким образом, техническими результатами настоящего изобретения являются:
- повышение стабильности при хранении (в течение 3 лет) новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она;
- повышение долгосрочной (в течение 10 лет) стабильности новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она;
- уменьшение гигроскопичности новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она;
- улучшение прессуемости с сохранением хороших показателей сыпучести без заметных электростатических явлений фармацевтической субстанции, содержащей новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она;
- улучшение биодоступности и увеличение терапевтической эффективности.
- расширение арсенала средств, проявляющих анксиолитическое действие.
Поставленная задача решается, а заявленный технический результат достигается получением новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, охарактеризованной посредством порошковой рентгенограммы, имеющей дифракционные максимумы характеристических пиков при значениях 2θ (±0,2°), составляющих: 11.7, 16.5, 20.1, 22.0, 26.4
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
Если не указано иное, все технические и специальные термины, использованные в данном контексте, имеют общепринятое в данной области техники значение.
Термин «эксципиент» в контексте настоящего изобретения характеризует вещества неорганического или органического происхождения, используемые в процессе производства, изготовления лекарственных препаратов для придания им необходимых физико-химических свойств.
«Фармацевтическая композиция» в контексте настоящего изобретения обозначает композицию, включающую в себя новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она и, по крайней мере, один из эксципиентов, применяемых в данной области техники, где «эксципиент» в контексте настоящего изобретения выбран из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых носителей, вспомогательных средств, таких как растворители, разбавители, консерванты, стабилизаторы, наполнители, дезинтегранты, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от их природы, способа введения композиции и дозировки. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как бензиловый спирт, уротропин, этилендиаминтетрауксусная кислота, бензойная кислота, хлорбутанол, сорбиновая кислота, парабены, алкилпиридиний, бензетоний и их фармацевтически приемлемые соли и подобные им соединения. Фармацевтическая композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, таких как гидрофильные полимерные замедлители высвобождения, например, производные целлюлозы, в частности, гидроксипропилметилцеллюлоза, полиэтиленоксид, желатин, поливиниловый спирт, полив инилпирролидон, альгинаты, карбомеры, гидрофобные замедлители высвобождения, такие как глицерилбегенат, моностеарат алюминия. Примерами подходящих носителей, растворителей и разбавителей являются вода, этанол, полиспирты, буферные растворы, а также их смеси, растительные масла (такие, например, как оливковое масло) и инъекционные органические сложные эфиры (такие, например, как этилолеат). Примерами наполнителей являются лактоза, микрокристаллическая целлюлоза, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль. Примерами скользящих агентов являются кремния диоксид коллоидный, крахмал, тальк и тому подобное. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, капсулы, пеллеты, драже, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, ректальные, интраназальные или внутриглазные формы введения.
Термин «фармацевтически приемлемый» в контексте настоящего изобретения означает, что данное вещество или композиция, в отношении которых применяется этот термин, должны быть совместимы с точки зрения химии и/или токсикологии с другими ингредиентами, входящими в состав препарата, и безопасны для того, кого лечат (снимают симптомы) этим веществом или композицией.
«Фармацевтически приемлемая соль» в контексте настоящего изобретения означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валераты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные [2].
Термин «лекарственное средство» (препарат) в контексте настоящего изобретения означает вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и других готовых лекарственных форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции и прочего.
Выражение «находится в твердой форме» в данном контексте характеризует фармацевтические композиции и лекарственные средства твердой, плотной или вязкой консистенции, в которых частицы не могут свободно перемещаться, а могут только совершать малые колебания около положения равновесия, при этом частицы активно взаимодействуют между собой.
Термин активная фармацевтическая субстанция (АФС) в контексте настоящего изобретения означает продукт синтеза, содержащий любое вещество или смесь веществ синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, предназначенный для производства лекарственных средств, который в процессе производства лекарственного средства (препарата) становится активным ингредиентом этого лекарственного средства. Такие продукты предназначены для проявления фармакологической активности или другого прямого эффекта при диагностике, лечении, облегчении симптомов или профилактике болезни, или для воздействия на структуру или функцию организма.
Термины «содержащий», «содержит» в контексте настоящего изобретения означает, что указанные фармацевтические композиции и лекарственные средства включают перечисленные компоненты, но не исключают включение других компонентов.
Термин «эффективное количество» в контексте настоящего изобретения относится к количеству фармацевтической композиции или лекарственного средства, которое при введении субъекту для лечения заболевания или по меньшей мере одного из клинических симптомов заболевания или нарушения является достаточным для воздействия такого лечения на заболевание, нарушение или симптом. «Эффективное количество» может изменяться в зависимости от того, в какой форме находится вещество (какая его полиморфная форма, изомер, соль и т.д.), заболевания, нарушения и/или симптомов заболевания или нарушения, тяжести заболевания, нарушения и/или симптомов заболевания или нарушения, возраста субъекта, подлежащего лечению, и/или веса субъекта, подлежащего лечению. Надлежащее количество в каждом конкретном случае будет очевидно специалисту в данной области или может быть определено путем стандартных экспериментов.
Термин «дозировка», используемый здесь, характеризует содержание одного или нескольких действующих веществ в количественном выражении на единицу дозы, или единицу объема, или единицу массы в соответствии с лекарственной формой либо для некоторых видов лекарственных форм количество высвобождаемого из лекарственной формы действующего вещества за единицу времени.
«Кристаллическая фаза» в контексте настоящего изобретения определяет пространственно однородное, равновесное состояние вещества, характеризуемое определенным элементным составом и структурой. Кристаллическая фаза может быть представлена различными кристаллическими формами, имеющими одинаковый химический состав, но характеризующимися различными структурой и размером кристалла.
«Порошковая рентгеновская дифракция» - это аналитический метод, с помощью которого измеряют и определяют углы связей и расстояния в кристаллических веществах, используя дифракцию рентгеновского излучения. Порошковая рентгеновская дифракция является эффективным инструментом для идентификации различных кристаллических фаз за счет их уникальных дифрактограмм.
Термин «значение 2 тета», или «2θ», относится к позиции пика на основе экспериментальной настройки выполняемого опыта по дифракции рентгеновских лучей и представляет собой общепринятую единицу по оси абсцисс на дифракционных картинах. Входящий рентгеновский луч образует угол тета (θ) с определенной плоскостью решетки исследуемого кристалла, отраженный луч записывают при угле 2 тета (2θ), который принято использовать для характеристики и сравнения данных полученных дифранктограмм.
Используемый в тексте термин «примерно» обозначает приблизительно плюс или минус десять процентов от указанной величины.
Раскрытие сущности изобретения
Поставленная задача решается, а заявленный технический результат достигается получением новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющей дифракционные максимумы пиков на рентгеновской порошковой дифрактограмме при величинах углов дифракции 2θ (±0,2°), составляющих: 11.7, 16.5, 20.1, 22.0, 26.4.
Одним из вариантов настоящего изобретения является кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющая дополнительно дифракционный максимум при значении 2θ (±0,2°), составляющем 12.8.
Другим вариантом настоящего изобретения является кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющая дополнительно дифракционный максимум при значении 2θ (±0,2°), составляющем 21.4.
Еще одним вариантом настоящего изобретения является кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющая дополнительно дифракционный максимум при значении 2θ (±0,2°), составляющем 23.5.
Предметом настоящего изобретения также является фармацевтическая композиция, обладающая анксиолитической активностью для лечения невротических и психических расстройств, содержащая кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющую дифракционные максимумы пиков на рентгеновской порошковой дифрактограмме при величинах углов дифракции 2θ (±0,2°), составляющих: 11.7, 16.5, 20.1, 22.0, 26.4 и, по меньшей мере, один фармацевтически приемлемый эксципиент.
В другом варианте предметом настоящего изобретения является фармацевтическая композиция, обладающая анксиолитической активностью для лечения невротических и психических расстройств, содержащая кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющую дифракционные максимумы пиков на рентгеновской порошковой дифрактограмме при величинах углов дифракции 2θ (±0,2°), составляющих: 11.7, 16.5, 20.1, 22.0, 26.4, также дополнительные максимумы пиков при значениях 12.8, 21.4, и/или 23.5, и по меньшей мере, один фармацевтически приемлемый эксципиент.
Более предпочтительной является фармацевтическая композиция, обладающая анксиолитической активностью для лечения невротических и психических расстройств, где невротические и психические расстройства включают эмоциональное напряжение, тревогу, страх, беспокойство, психомоторное возбуждение.
Фармацевтическую композицию, содержащую новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она по настоящему изобретению, можно вводить (не ограничиваясь указанным) посредством перорального, парентерального, ингаляционного, ректального, или местного введения субъекту, который нуждается в лечении или уменьшении клинических симптомов. Для перорального введения фармацевтическая композиция по настоящему изобретению может представлять собой стандартный состав в виде твердой лекарственной формы, такой как (не ограничиваясь указанным) таблетки, гранулы, порошок, капсулы, жевательные капсулы и т.п., жидкий препарат, такой как (не ограничиваясь указанным) водная или масляная суспензия, такие как сироп, раствор или т.п. Для парентерального введения фармацевтическая композиция по настоящему изобретению может представлять собой (не ограничиваясь указанным) водный раствор, масляной концентрат, лиофилизированный порошок или подобное. В качестве неограничивающего примера предпочтительный состав фармацевтической композиции по настоящему изобретению выбран из таблетки, покрытой оболочкой таблетки или капсулы.
В некоторых вариантах осуществления фармацевтическую композицию согласно настоящему изобретению можно получить с помощью известных общепринятых способов в области фармацевтики.
Предметом настоящего изобретения также является лекарственное средство, обладающее анксиолитической активностью для лечения невротических и психических расстройств, в форме таблеток или капсул, содержащее кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющую дифракционные максимумы пиков на рентгеновской порошковой дифрактограмме при величинах углов дифракции 2θ (±0,2°), составляющих: 11.7, 16.5, 20.1, 22.0, 26.4 или фармацевтическую композицию, содержащую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющую дифракционные максимумы пиков на рентгеновской порошковой дифрактограмме при величинах углов дифракции 2θ (±0,2°), составляющих: 11.7, 16.5, 20.1, 22.0, 26.4 и, по меньшей мере, один фармацевтически приемлемый эксципиент.
В одном из вариантов кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она согласно настоящему изобретению применяют для лечения и/или профилактики невротических и неврозоподобных состояний (тревожность, страх, раздражительность, эмоциональная лабильность, бессонница, психопатия); вегетативной лабильности (в т.ч. диэнцефальная патология); мигрени; логоневроза; абстинентного алкогольного синдрома, алкоголизма.
Наиболее предпочтительным является лекарственное средство, обладающее анксиолитической активностью, для лечения невротических и психических расстройств, где невротические и психические расстройства включают эмоциональное напряжение, тревогу, страх, беспокойство, психомоторное возбуждение.
Дозировка кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она согласно настоящему изобретению, при использовании в качестве активного ингредиента (действующего вещества), находится в диапазоне от 1 мг до 1909 мг в сутки, предпочтительно от 60 мг до 500 мг, наиболее предпочтительно от 60 мг до 150 мг в сутки. Указанная дозировка может быть введена как одной дозой, так и разделена на несколько приемов в течение суток, например, 2, 3 или 4 раза в сутки, предпочтительно 3 раза в сутки. Предпочтительный режим дозирования составляет от 20 до 50 мг три раза в сутки.
Лекарственные формы по настоящему изобретению включают, но не ограничиваются указанным, таблетки, в частности, буккальные таблетки, шипучие таблетки, таблетки, покрытые оболочкой, таблетки с замедленным высвобождением, обычные таблетки, таблетки с контролируемым высвобождением, диспергируемые в полости рта таблетки, лиофилизированные быстрорастворимые таблетки и т.п.; капсулы, такие как твердые капсулы, мягкие капсулы, желатиновые капсулы и т.п.; порошки для инъекций, такие как лиофилизированные порошки для инъекций, обычные порошки для инъекций и тп.; растворы, аэрозоли, спреи, трансдермальные лекарственные средства, например, пластыри, гранулы, суппозитории и другие лекарственные формы.
Лекарственные средства по настоящему изобретению могут вводиться (не ограничиваясь указанным) перорально, парентерально, ингаляционно, подкожно, внутрибрюшинно, местно, ректально. Терапевтическая дозировка лекарственного средства, содержащего новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, или активную фармацевтическую субстанцию, или фармацевтическую композицию по настоящему изобретению или фармацевтической композиции для лечения невротических и психопатических расстройств, которая содержит в терапевтически эффективном количестве новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она по настоящему изобретению, у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента.
Предметом настоящего изобретения также является применение вышеуказанной кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она для получения фармацевтической композиции или лекарственного средства.
Осуществление изобретения
Настоящее изобретение дополнительно поясняется, но не ограничивается следующими примерами, которые иллюстрируют настоящее изобретение.
Пример 1. Способ получения новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она.
Синтез 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3Н-1,4-бензодиазепин-2-она осуществляли по методике, приведенной в UA81277.
Новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она получали способом, описанным ниже.
1 г 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она растворяли в 10 мл ацетонитрила при температуре 20°С. Полученный раствор медленно добавляли к воде при комнатной температуре (10 мл раствора на 100 мл воды) при перемешивании. Наблюдали образование суспензии. Данную суспензию перемешивали в течение 30 минут. Затем суспензию оставляли при температуре 10°С на 3 часа. Полученный осадок фильтровали под вакуумом, промывали 100 мл воды три раза. Затем осадок сушили при температуре 110-140°С.
Картину порошковой рентгеновской дифракции новой кристаллической формы получали с помощью дифрактометра, оборудованного германиевым монохроматором и системой щелей для монохроматизации и фокусировки (λ[CuKα]=1.5406 Å), а также позиционно-чувствительным детектором, в угловом диапазоне 6-60° с шагом 0.02° по углу 2θ с использованием геометрии на пропускание.
На спектре порошковой рентгеновской дифракции кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она наблюдали следующие интенсивные пики при углах дифракции 2θ,° (±0.2°):

Характеристическими пиками являлись пики при углах дифракции 2θ,° (±0.2°) 11.7, 16.5, 20.1, 22.0, 26.4.
Полученную новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она использовали для получения активной фармацевтической субстанции (АФС) посредством дополнительной стадии сушки (сушка в потоке СО2, метод распылительной сушки, сушки под вакуумом и т.д.) до постоянной массы. На выходе получали мелкодисперсный белый порошок. Готовую фармацевтическую субстанцию помещали в герметично закрытый флакон.
Пример 2. Исследование стабильности при хранении новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она.
Стабильность новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она оценивали по количественному содержанию исследуемого вещества в фармацевтической субстанции и сравнивали со стабильностью прототипа методом ускоренного старения по методике согласно ОФС.1.1.0009.15 (Государственная фармакопея РФ XIII издание).
Все образцы хранили в стеклянных флаконах, укупоренных резиновыми пробками с алюминиевыми колпачками, в климатической камере в условиях ускоренных испытаний. Содержание действующего вещества определяли методом ВЭЖХ с использованием стандартов.
В результате исследований было обнаружено, что новая кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, полученная согласно примеру 1, обладает статистически достоверно увеличенной стабильностью при хранении по сравнению с прототипом (таблица 1). Субстанцию кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она согласно настоящему изобретению получали способу согласно примеру 1, а субстанцию 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она (прототип) получали способом, раскрытым в UA81277. Полученные субстанции смешивали с лактозой моногидратом, добавляли картофельный крахмал, кальция стеарат и поливинилпирролидон, тщательно перемешивали итоговую смесь и прессовали ее до получения таблеток.
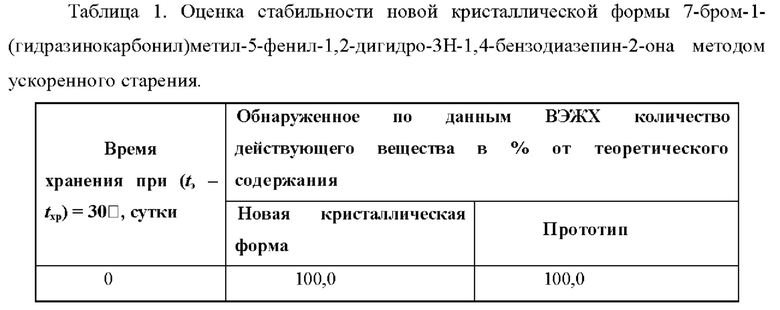
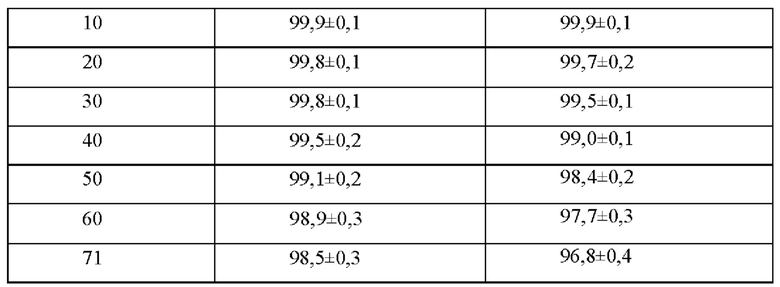
Установлено, что после 71 суток хранения в условиях метода ускоренного старения кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она по настоящему изобретению обладала статистически достоверно увеличенной стабильностью и оставалась химически чистой. Субстанция прототипа оставалась химически чистой в течение менее 10 суток, к концу эксперимента содержание действующего вещества уменьшалось более чем на 3%. Таким образом, новая кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она согласно настоящему изобретению является статистически значимо более стабильной при хранении по сравнению с прототипом. Использование новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она согласно настоящему изобретению, обладающего повышенной стабильностью, может обеспечить увеличение срока годности лекарственного средства.
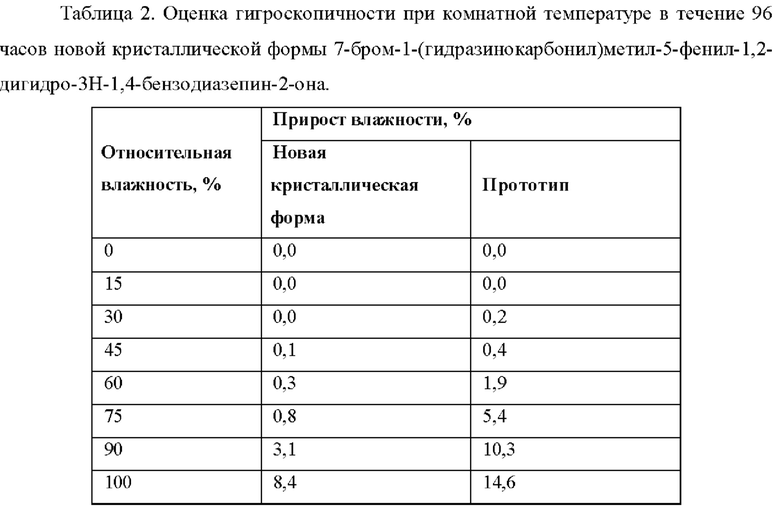
Пример 3. Определение гигроскопичности новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она.
Пониженная гигроскопичность является большим преимуществом при получении и хранении субстанции. В частности, при повышенной гигроскопичности к концу срока годности может наблюдаться обводнение таблеток, что приводит к их разрушению. Гигроскопичность оценивают при хранении твердого соединения в камерах с постоянной относительной влажностью при комнатной температуре в течение 96 часов.
Субстанцию кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она согласно настоящему изобретению получали способом согласно примеру 1, а субстанцию 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она получали способом, раскрытым в UA81277. Сравнение субстанции 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она (прототипа) и новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она согласно настоящему изобретению при комнатной температуре показало, что прототип достоверно является более гигроскопичным и демонстрирует большее увеличение влажности при хранении, начиная с 60% относительной влажности. В новой кристаллической форме 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-он согласно настоящему изобретению заметное увеличения влажности было выявлено при хранении с относительной влажностью 90%. Результаты исследования представлены ниже в таблице 2.
Пример 4. Определение сыпучести и прессуемости активной фармацевтической субстанции, содержащей кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она.
Улучшение прессуемости и сохранение хорошей сыпучести является большим преимуществом фармацевтических субстанций, содержащих новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, полученную в примере 1, при получении и хранении лекарственных форм, например, таких, как таблетки. В частности, если прессуемость фармацевтической субстанции низкая, таблетка получается непрочной, а иногда полностью разрушается при выталкивании из матрицы. Достижение хорошей сыпучести порошков фармацевтических субстанции позволяет повысить производительность таблеточных машин, улучшить качество таблеток, а также влияет на смешиваемость порошков.
Сыпучесть определяли на вибрационном устройстве для снятия характеристик сыпучих материалов.
Навески фармацевтической субстанции кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она и навеску фармацевтической субстанции 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она (прототип) получали в соответствии со способами, описанными в примере 1. Далее отбирали навеску соответствующей фармацевтической субстанций массой 50,0 г (с точностью до 0,01 г), смешивали с лактозой моногидратом в соотношении 1:2,5, добавляли крахмал картофельный, кальция стеарат и поливинилпирролидон, и тщательно перемешивали до получения однородной таблетировочной смеси, после чего полученную смесь засыпали в воронку при закрытой заслонке, включали прибор и секундомер. После 20 секунд утряски, необходимой для получения стабильных показаний, открывали заслонку и фиксировали время истечения материала из воронки. Показатель сыпучести рассчитывали, как среднюю величину, выраженную в граммах в секунду.
При определении прессуемости фармацевтической субстанции, содержащей новую кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, брали навеску порошка указанных субстанций массой 0,3 г, прессовали в матрице с помощью пуансонов диаметром 9 мм на гидравлическом прессе при давлении 120 МПа. Полученную таблетку взвешивали на весах, высоту таблетки измеряли микрометром. Далее, используя измеренные величины, рассчитывали коэффициент прессуемости. Результаты исследований представлены в таблице 3.


Исследования прессуемости, приведенные выше, показали, что показатели прессуемости фармацевтической субстанции по настоящему изобретению достоверно выше, чем у фармацевтической субстанции по прототипу. При этом фармацевтическая субстанция по настоящему изобретению неожиданно сохраняет хорошие показатели сыпучести без заметных электростатических явлений.
Пример 5. Исследование анксиолитической активности новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она в тесте «приподнятый крестообразный лабиринт».
Эксперимент проводили на 45 взрослых беспородных мышах. Животных содержали в стандартных условиях вивария на обычном пищевом рационе, со свободным доступом к воде.
Животные были рандомизированно разделены на 3 группы по 15 особей в каждой: первая группа контроль (носитель - лактозы моногидрат); 2 группа кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, полученная согласно примеру 1, в количестве 20 мг; 3 группа - кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, полученная согласно примеру 1, в количестве 50 мг (все дозы приведены в пересчете на человека). Составы вводили однократно внутрижелудочно с помощью зонда за 30 минут до начала тестирования.
Анксиолитическую активность новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она изучали по поведению мышей в приподнятом крестообразном лабиринте с открытыми и замкнутыми рукавами. До начала исследования крыс помещали в темный бокс с отверстиями для вентиляции на 5 минут. Далее животное помещали в центр лабиринта мордочкой к открытому рукаву и в течение пяти минут наблюдали за его передвижениями (регистрировали время пребывания животного в открытых рукавах, на центральной площадке лабиринта, количество заходов в открытые рукава) [М. Komada, К. Takao, and Т. Miyakawa «Elevated Plus Maze for Mice» // J. Vis. Exp.2008, 22, p.1088]. Полученные результаты приведены в таблице 4. Перед началом эксперимента исходные уровни тревожности, оцениваемые в приподнятом крестообразном лабиринте, в подопытных группах статистически значимых различий не имели, что свидетельствует об их адекватном формировании.

Результаты, представленные в таблице 4, демонстрируют увеличение времени нахождения животных групп 2 и 3 в открытых рукавах и числа заходов в них по сравнению с контрольной 1 группой, что свидетельствует о наличии анксиолитического эффекта у новой кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она.
Таким образом, по результатам эксперимента по изучению поведенческой реакции новая кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она согласно настоящему изобретению в тесте «приподнятый крестообразный лабиринт» можно заключить, что новая кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она обладает выраженным анксиолитическим действием.
Изобретение может быть использовано в медицине, химии, фармакологии и химико-фармацевтической промышленности.
Список литературы
1. Ю.А. Симонов и др. КРИСТАЛЛИЧЕСКАЯ И МОЛЕКУЛЯРНАЯ СТРУКТУРА ГИДАЗЕПАМА // ОРГАНИЧЕСКАЯ ХИМИЯ. - УКР. ХИМ. ЖУРН. 2009. Т. 75, №3
2. Berge S.M., Bighley L.D., Monkhouse D.C.: «Pharmaceutical Salts» // Journal of Pharmaceutical Sciences, V. 66, №1, 1977, P. 1-19.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛИЧЕСКАЯ ФОРМА МАЛАТА 6-МЕТИЛ-2-ЭТИЛПИРИДИН-3-ОЛА И СОДЕРЖАЩИЕ ЕЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2022 |
|
RU2803255C1 |
| Фармацевтическая композиция на основе N-бензил-N-метил-1-фенилпирроло [1,2-a] пиразин-3-карбоксамида | 2017 |
|
RU2689396C2 |
| ПРОИЗВОДНОЕ 6,7-ДИГИДРОПИРАЗОЛО[1,5-a]ПИРАЗИНОНА И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2018 |
|
RU2792694C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА АЗОЛБЕНЗОЛЬНОГО ПРОИЗВОДНОГО | 2015 |
|
RU2675854C2 |
| ПРОИЗВОДНЫЕ 1,4-БЕНЗОДИАЗЕПИНА, ОБЛАДАЮЩИЕ СЕЛЕКТИВНОЙ АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2133248C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СНОТВОРНОЙ, СЕДАТИВНОЙ И ТРАНКВИЛИЗИРУЮЩЕЙ АКТИВНОСТЬЮ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2001 |
|
RU2183121C1 |
| ИМИДАЗОДИАЗЕПИНОВОЕ СОЕДИНЕНИЕ | 2016 |
|
RU2777915C2 |
| СОЛЬ ПРОИЗВОДНОГО ПИРАЗОЛОХИНОЛИНА И ЕЕ КРИСТАЛЛ | 2014 |
|
RU2655171C2 |
| СОЛЬ МЕТАНСУЛЬФОНОВОЙ КИСЛОТЫ ПИРАЗОЛПИРИМИДИНОВОГО СОЕДИНЕНИЯ, ЕГО КРИСТАЛЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2345995C2 |
| ИМИДАЗОДИАЗЕПИНОВОЕ СОЕДИНЕНИЕ | 2016 |
|
RU2712968C2 |
Изобретение относится к области медицины, фармакологии и химико-фармацевтической промышленности, а именно к новой кристаллической форме 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она и включающей ее фармацевтической композиции и лекарственной форме, обладающих анксиолитической активностью для лечения невротических и психических расстройств. Кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющая дифракционные максимумы пиков на рентгеновской порошковой дифрактограмме при величинах углов дифракции 2θ (± 0,2°), составляющих 11.7, 16.5, 20.1, 22.0, 26.4. Также изобретение относится к фармацевтической композиции, обладающей анксиолитической активностью для лечения невротических и психических расстройств, содержащей кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она в эффективном количестве и, по меньшей мере, один фармацевтически приемлемый эксципиент. Изобретение относится к лекарственному средству, обладающему анксиолитической активностью для лечения невротических и психических расстройств, в твердой форме, содержащему кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она в эффективном количестве или фармацевтическую композицию в эффективном количестве. Технический результат - кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она для лечения невротических и психических расстройств. 4 н. и 7 з.п. ф-лы, 3 табл., 5 пр.
1. Кристаллическая форма 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она, имеющая дифракционные максимумы пиков на рентгеновской порошковой дифрактограмме при величинах углов дифракции 2θ (± 0,2°), составляющих 11.7, 16.5, 20.1, 22.0, 26.4.
2. Кристаллическая форма по п. 1, имеющая дополнительно дифракционный максимум при значении 2θ (± 0,2°), составляющем 12.8.
3. Кристаллическая форма по п. 1, имеющая дополнительно дифракционный максимум при значении 2θ (± 0,2°), составляющем 21.4.
4. Кристаллическая форма по п. 1, имеющая дополнительно дифракционный максимум при значении 2θ (± 0,2°), составляющем 23.5.
5. Фармацевтическая композиция, обладающая анксиолитической активностью для лечения невротических и психических расстройств, содержащая кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она по пп. 1-4 в эффективном количестве и, по меньшей мере, один фармацевтически приемлемый эксципиент.
6. Фармацевтическая композиция по п. 5, где невротические и психические расстройства включают эмоциональное напряжение, тревогу, страх, беспокойство, психомоторное возбуждение.
7. Лекарственное средство, обладающее анксиолитической активностью для лечения невротических и психических расстройств, в твердой форме, содержащее кристаллическую форму 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она по пп. 1-4 в эффективном количестве или фармацевтическую композицию по п. 5 в эффективном количестве.
8. Лекарственное средство по п. 7, где твердая форма представляет собой таблетку или капсулу.
9. Лекарственное средство по п. 7, где невротические и психические расстройства включают эмоциональное напряжение, тревогу, страх, беспокойство, психомоторное возбуждение.
10. Применение кристаллической формы 7-бром-1-(гидразинокарбонил)метил-5-фенил-1,2-дигидро-3H-1,4-бензодиазепин-2-она по пп. 1-4 для лечения невротических и психических расстройств.
11. Применение по п. 10, где невротические и психические расстройства включают эмоциональное напряжение, тревогу, страх, беспокойство, психомоторное возбуждение.
| 1-(Гидразинокарбонил)алкил-1,2-дигидро-3Н-1,4-бенздиазепин-2-оны, обладающие транквилизирующими и противосудорожными свойствами | 1980 |
|
SU953819A1 |
| Н.Я | |||
| Головенко, И.А | |||
| Кравченко, Биохимическая фармакология пролекарств | |||
| Одесса "Астропринт", 2007, 181 с | |||
| Регистр Лекарственных средств России, Энциклопедия лекарств, 2004, 11, ООО "РЛС-2004", с.233 | |||
| MINO R | |||
| CAIRA "Crystalline Polymorphism of Organic Compounds", TOPICS IN CURRENT CHEMISTRY, 1998, vol.198, pp.163-208 | |||
Авторы
Даты
2022-09-28—Публикация
2021-06-28—Подача