ОБЛАСТЬ ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Моющие композиции для стирки, а именно жидкие моющие композиции для стирки для удаления смешанных пятен от пищевых продуктов.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Моющие композиции для стирки составляются так, чтобы обеспечить качественную очистку тканей: т.е. чтобы белые ткани оставались белыми, а цветные ткани оставались яркими. Моющие композиции для стирки обычно также составляются так, чтобы они удаляли пятна. Пятно представляет собой легко различимый участок ткани с измененным цветом. Поскольку пятна приводят к изменению цвета так, что испачканные участки резко контрастируют с незапачканными тканями, они очень хорошо заметны на тканях.
Удаление некоторых смешанных пятен от пищевых продуктов, таких как готовые соусы, остается затруднительным, особенно при низких температурах. Более того, как оказалось, такие пятна во время стирки повторно осаждаются на ткани, несмотря на использование средств, препятствующих повторному осаждению. Хотя увеличение концентраций активных веществ, таких как средства, препятствующие повторному осаждению, поверхностно-активные вещества и компоненты моющих средств, может повысить эффективность удаления подобных пятен, это увеличит стоимость состава и может повлиять на другие характеристики, такие как стабильность.
Следовательно, сохраняется потребность в моющей композиции для стирки, обладающей повышенной эффективностью удаления смешанных пятен от пищевых продуктов, таких как готовые соусы, но при этом стабильной и не требующей увеличения концентрации активных веществ, используемых для удаления пятен.
Патент WO2019/038059 относится к моющим композициям, содержащим варианты эндоглюканазы, и способам использования указанных композиций. Патент WO2019/038060 относится к моющим композициям, содержащим варианты ксантанлиазы, и способам использования указанных композиций.
Изложение сущности изобретения
Настоящее изобретение относится к моющей композиции для стирки, содержащей: моющее поверхностно-активное вещество, причем моющее поверхностно-активное вещество содержит комбинацию анионных и неионных поверхностно-активных веществ; ферментную систему, содержащую: ксантанэндоглюканазу, причем указанная ксантанэндоглюканаза содержит полипептид с последовательностью, по меньшей мере на 60% идентичной SEQ ID NO: 1; ксантанлиазу, причем указанная ксантанлиаза содержит полипептид с последовательностью, по меньшей мере на 60% идентичной SEQ ID NO: 2, и маннаназу, причем указанная маннаназа содержит полипептид с последовательностью, по меньшей мере на 85% идентичной остаткам 27-331 SEQ ID NO: 3, и/или с последовательностью, по меньшей мере на 80% идентичной SEQ ID NO: 4.
Настоящее изобретение также относится к способу стирки ткани, предпочтительно ткани, содержащей пятно, содержащее комбинацию маннан и полисахаридов, причем способ включает следующие стадии: обеспечение моющей композиции для стирки настоящего изобретения; разбавление моющей композиции для стирки с обеспечением промывочной жидкости, обладающей суммарной концентрацией поверхностно-активного вещества свыше 300 м. д.; и стирку ткани промывочной жидкостью.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Неожиданно было обнаружено, что устойчивость некоторых смешанных пятен от пищевых продуктов, таких как некоторые готовые соусы, обусловлена комбинацией маннан и других полисахаридов. Такие соусы могут включать в себя пасты чили, уксусные заправки и некоторые виды мороженого. Указанные маннаны могут содержаться, например, в бобах рожкового дерева, камеди тары, гуаровой камеди и т.п., а также в их смесях. Полисахариды содержатся, например, в ксантановой камеди. Предполагается, что при высыхании загрязнения комбинация маннан и полисахаридов формирует гели, в результате чего удаление пятен становится затруднительным. Кроме того, устойчивость подобных гелей может быть увеличена в присутствии остатков жира или масла, таких как животные жиры (например, жир из бекона, свиное сало, кондитерский жир, масло) или растительные масла (например, подсолнечное масло, рапсовое масло, хлопковое масло, оливковое масло, кукурузное масло). Кроме того, даже после удаления пятна гелеобразная структура в процессе цикла стирки способствует сохранению пятен в суспензии, в результате чего усиливается повторное осаждение. Предполагается, что ферментная система, используемая в настоящем изобретении, в большей мере способна разрушать эти гелевые структуры, более эффективно чем только маннаназа или только эндоглюканазы, даже в том случае, когда гелевые структуры содержат остатки жира или масла, и, следовательно, обеспечивает улучшенное удаление подобных пятен. Кроме того, поскольку ферментная система обладает большей способностью к разрушению этих гелевых структур, то также достигается уменьшение повторного осаждения загрязнений.
Если не указано иное, все концентрации компонента или композиции относятся к активной части данного компонента или композиции и исключают примеси, например остаточные растворители или побочные продукты, которые могут присутствовать в доступных в продаже источниках таких компонентов или композиций.
Все процентные показатели и отношения рассчитывают по массе, если не указано иное. Все процентные показатели и отношения рассчитывают в расчете на всю композицию, если не указано иное.
Если не указано иное, все измерения проводят при 25 °C.
В контексте настоящего документа термины в единственном числе следует понимать, как означающие один или более из заявленных или описанных объектов.
Моющая композиция для стирки
Моющая композиция для стирки может иметь любую приемлемую форму, такую как жидкость, паста, гранулированная форма, твердая форма, порошок, или быть связанной с носителем, таким как субстрат. Предпочтительные моющие композиции для стирки имеют жидкую или гранулированную форму, более предпочтительно жидкую форму.
В контексте настоящего документа термин «жидкая моющая композиция» относится к жидкой моющей композиции, представленной текучей средой и предпочтительно способной смачивать и очищать ткань, например одежду, в бытовой стиральной машине. В контексте настоящего документа термин «моющая композиция для стирки» относится к композициям, приемлемым для стирки одежды. Композиция может включать твердые вещества или газы в приемлемым образом разделенной форме, но суммарная композиция исключает формы продукта, которые в целом не являются текучими, такие как таблетки или гранулы. Жидкая моющая композиция для стирки предпочтительно имеет плотность в диапазоне от 0,9 до 1,3 грамма на кубический сантиметр, более конкретно от 1,00 до 1,10 грамма на кубический сантиметр, исключая любые твердые добавки, но включая любые пузырьки, если они присутствуют.
Предпочтительными являются жидкие моющие композиции для стирки на водной основе. В таких жидких моющих композициях для стирки на водной основе концентрация воды может составлять от 5% до 99%, предпочтительно от 15% до 90%, более предпочтительно от 25% до 80% по массе жидкой моющей композиции.
Диапазон pH моющей композиции составляет от 6,0 до 8,9, предпочтительно от pH 7 до 8,8.
Моющая композиция может быть также заключена в водорастворимую пленку с образованием изделия с единичной дозой. Такие изделия с единичной дозой содержат моющую композицию настоящего изобретения, содержание воды в которой составляет менее 20%, предпочтительно менее 15%, более предпочтительно менее 10% по массе, при этом моющая композиция заключена в водорастворимую или диспергируемую пленку. Такие изделия с единичной дозой могут быть изготовлены с применением любых способов, известных в данной области.
Приемлемые материалы для водорастворимого мешочка включают полимеры, сополимеры или их производные. Предпочтительные полимеры, сополимеры или их производные могут быть выбраны из группы, состоящей из поливиниловых спиртов, поливинилпирролидона, полиалкиленоксидов, акриламида, акриловой кислоты, целлюлозы, простых эфиров целлюлозы, сложных эфиров целлюлозы, амидов целлюлозы, поливинилацетатов, поликарбоновых кислот и солей, полиаминокислот или пептидов, полиамидов, полиакриламида, сополимеров малеиновой/акриловой кислот, полисахаридов, включая крахмал и желатин, природных камедей, таких как ксантановая камедь и карраген. Более предпочтительные полимеры выбраны из полиакрилатов и водорастворимых акрилатных сополимеров, метилцеллюлозы, натрийкарбоксиметилцеллюлозы, декстрина, этилцеллюлозы, гидроксиэтилцеллюлозы, гидроксипропилметилцеллюлозы, мальтодекстрина, полиметакрилатов, а наиболее предпочтительно выбраны из поливиниловых спиртов, сополимеров поливинилового спирта и гидроксипропилметилцеллюлозы (ГПМЦ) и их комбинаций.
Моющие поверхностно-активные вещества
Моющее поверхностно-активное вещество в контексте настоящего документа обозначает поверхностно-активные вещества или смеси поверхностно-активных веществ, обеспечивающих эффект очистки, удаления пятен или отстирывания загрязненного материала. Приемлемыми моющими поверхностно-активными веществами могут быть: анионное поверхностно-активное вещество, неионное поверхностно-активное вещество, цвиттерионное поверхностно-активное вещество и их комбинации. Моющее поверхностно-активное вещество содержит комбинацию анионного и неионного поверхностно-активных веществ.
Композиция для стирки может содержать моющее поверхностно-активное вещество в концентрации от 3 мас.% до 50 мас.%, предпочтительно от 10 мас.% до 37,5 мас.%, более предпочтительно от 15 мас.% до 30 мас.%.
Приемлемые анионные поверхностно-активные вещества могут быть выбраны из группы, состоящей из: алкилсульфатов, алкилэтоксисульфатов, алкилсульфонатов, алкилбензолсульфонатов, жирных кислот и их солей, а также их смесей. Однако в силу своих свойств может быть использовано любое анионное поверхностно-активное вещество, известное в области моющих композиций, как указано в Surfactant Science Series, том 7, под редакцией W.M. Linfield, Marcel Dekker. Однако композиция предпочтительно содержит по меньшей мере поверхностно-активное вещество с сульфоновой кислотой, такой как линейная алкилбензолсульфоновая кислота, но также могут быть использованы формы водорастворимых солей. Также предпочтительны алкилэтоксисульфаты или их смеси.
Анионные поверхностно-активные вещества, содержащие сульфонат или сульфоновую кислоту, приемлемые для использования в контексте настоящего документа, включают кислотные и солевые формы линейных или разветвленных алкилбензолсульфонатов, алкилсульфонатов сложных эфиров, алкансульфонатов, алкилсульфонированных поликарбоновых кислот и их смесей. Приемлемые анионные поверхностно-активные вещества, содержащие сульфонат или сульфоновую кислоту, включают: алкилбензолсульфонаты С5-С20, более предпочтительно алкилбензолсульфонаты С10-С16, более предпочтительно алкилбензолсульфонаты С11-С13, алкилсульфонаты С5-С20 сложных эфиров, первичные или вторичные алкансульфонаты С6-С22, сульфонированные поликарбоновые кислоты С5-С20 и любые их смеси, но предпочтительно алкилбензолсульфонаты С11-С13. Перечисленные выше поверхностно-активные вещества могут варьироваться в широком диапазоне по содержанию 2-фенил изомера. Такие поверхностно-активные вещества, содержащие сульфонат или сульфоновую кислоту, могут присутствовать в концентрации от 1,0% до 20%, более предпочтительно от 5,0% до 15%, и более предпочтительно от 6,5% до 12,5% по массе композиции.
Анионные сульфатные соли, приемлемые для использования в композиции настоящего изобретения, включают первичные и вторичные алкилсульфаты с линейной или разветвленной алкильной или алкенильной группой, содержащей от 9 до 22 атомов углерода или более предпочтительно от 12 до 18 атомов углерода. Также пригодны поверхностно-активные вещества с бета-разветвленным алкилсульфатом или со смесью доступных на рынке материалов, имеющих средневесовую степень разветвленности (поверхностно-активного вещества или смеси) по меньшей мере 50%.
Другие анионные поверхностно-активные вещества, приемлемые для использования в контексте настоящего документа, включают сульфонаты метилового эфира жирной кислоты и/или алкилалкоксилированные сульфаты, такие как алкилэтоксисульфаты (AES) и/или алкилполиалкоксилированные карбоксилаты (AEC). При использовании поверхностно-активного вещества с алкилалкоксилированным сульфатом последний предпочтительно является смесью одного или более алкилэтоксилированных сульфатов. Приемлемые алкилалкоксилированные сульфаты включают алкилэтоксилат С10-С18, более предпочтительно алкилэтоксилат С12-С15 со степенью этоксилирования от 1 до 5, предпочтительно от 2 до 3. Такие алкилалкоксилированные сульфаты присутствуют предпочтительно в концентрации от 1,0% до 10%, более предпочтительно от 2,0% до 7,5% и наиболее предпочтительно от 3,0% до 5% по массе композиции.
Приемлемые жирные кислоты включают «натуральные» жирные кислоты, например кокосовое масло, пальмоядровое масло, оливковое масло или жирная кислота топленого жира и их смеси. Такие содержащие жирную кислоту поверхностно-активные вещества могут присутствовать в концентрации от 1,0% до 15%, более предпочтительно от 2,0% до 12,5% и наиболее предпочтительно от 5,0% до 10% по массе композиции.
Анионные поверхностно-активные вещества обычно присутствуют в виде солей с алканоламинами или щелочными металлами, такими как натрий и калий.
Жидкая моющая композиция может содержать неионное поверхностно-активное вещество. Концентрация неионного поверхностно-активного вещества в жидкой моющей композиции может составлять от 1,0% до 20%, предпочтительно от 2,5% до 15%, более предпочтительно от 5,0% до 12,5% по массе композиции.
Приемлемые неионные поверхностно-активные вещества включают, без ограничений, алкилэтоксилаты (АЕ) С12-С18, включая так называемые алкилэтоксилаты с узкими пиками, алкилфенолалкоксилаты С6-С12 (особенно этоксилаты и смешанные этоксилаты/пропоксилаты), блок алкиленоксидный конденсат алкилфенолов С6-С12, алкиленоксидные конденсаты алканолов С8-С22 и блок-полимеры этиленоксида/пропиленоксида (Pluronic производства BASF Corp.), а также полуполярные неионные вещества (например, аминоксиды и фосфиноксиды), и могут быть использованы в настоящих композициях. Подробное раскрытие информации об этих типах поверхностно-активных веществ можно найти в патенте США № 3,929,678, Laughlin et al., выданном 30 декабря 1975 г.
Алкилполисахариды, такие как описанные в патенте США № 4,565,647, Llenado, также являются неионными поверхностно-активными веществами, пригодными для использования в композициях настоящего изобретения.
Также приемлемыми являются алкильные полиглюкозидные поверхностно-активные вещества.
Пригодные неионные поверхностно-активные вещества включают неионные поверхностно-активные вещества формулы R1(OC2H4)nOH, где R1 представляет собой C10-C16 алкильную группу или C8-C12 алкилфенильную группу и n составляет от предпочтительно 3 до 80. В некоторых вариантах осуществления неионные поверхностно-активные вещества могут быть продуктами конденсации спиртов C12-C15 с от 5 до 20 моль этиленоксида на моль спирта, например спирта С12-С13, конденсированного с 6,5 моль этиленоксида на моль спирта.
Приемлемыми поверхностно-активными веществами с аминоксидами являются аминоксиды, имеющие следующую формулу: R1R2R3NO, где R1 представляет собой углеводородную цепь, содержащую от 1 до 30 атомов углерода, предпочтительно от 6 до 20, более предпочтительно от 8 до 16, а R2 и R3 представляют собой независимо насыщенные или ненасыщенные, замещенные или незамещенные, линейные или разветвленные углеводородные цепи, содержащие от 1 до 4 атомов углерода, предпочтительно от 1 до 3 атомов углерода, и более предпочтительно являются метильными группами. R1 может представлять собой насыщенную или ненасыщенную, замещенную или незамещенную линейную или разветвленную углеводородную цепь.
Приемлемыми аминоксидами для использования в контексте настоящего документа являются, например, предпочтительно диметиламиноксид C12-C14, поставляемый на рынок компанией Albright & Wilson, аминоксиды C12-C14, поставляемые на рынок под торговым названием Genaminox® LA от компании Clariant, или AROMOX® DMC от компании AKZO Nobel.
Дополнительные приемлемые неионные поверхностно-активные вещества включают амиды полигидрокси жирных кислот с формулой:
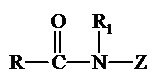 ,
,
где R представляет собой C9-C17 алкил или алкенил, R1 представляет собой метильную группу и Z представляет собой глицидил, полученный из восстановленного сахара или его алкоксилированного производного. Примеры представляют собой N-метил N-1-дезоксиглицитил кокоамид и N-метил N-1-дезоксиглицитилолеамид. Способы получения амидов полигидрокси жирных кислот известны и могут быть найдены в патенте США № 2,965,576, Wilson, и в патенте США № 2,703,798, Schwartz.
Жидкая моющая композиция может содержать цвиттерионное вещество. Цвиттерионное вещество может присутствовать в концентрации от 0,1 мас.% до 5 мас.%, предпочтительно от 0,2 мас.% до 2 мас.%, более предпочтительно от 0,4 мас.% до 1 мас.%.
Приемлемые амфотерные или цвиттерионные моющие поверхностно-активные вещества включают вещества, широко используемые в качестве средств для очистки при уходе за волосами и личной гигиене. Не имеющие ограничительного характера цвиттерионные или амфотерные моющие поверхностно-активные вещества описаны в патенте США № 5,104,646 (Bolich Jr. et al.), в патенте США № 5,106,609 (Bolich Jr. et al.). Приемлемые амфотерные моющие поверхностно-активные вещества включают поверхностно-активные вещества, подробно описанные как производные вторичных и третичных алифатических аминов, в которых алифатический радикал может иметь неразветвленную или разветвленную цепь и в которых один из алифатических заместителей содержит от 8 до 18 атомов углерода и еще один содержит анионную группу, такую как карбокси, сульфонат, сульфат, фосфат или фосфонат. Приемлемые амфотерные моющие поверхностно-активные вещества для использования в настоящем изобретении включают, без ограничений, следующими веществами: кокоамфоацетат, кокоамфодиацетат, лауроамфоацетат, лауроамфодиацетат и их смеси.
Предпочтительно используют поверхностно-активные вещества, содержащие насыщенные алкильные цепи.
Ферментная система
Моющая композиция для стирки настоящего изобретения содержит ферментный коктейль, в котором коктейль содержит ксантанэндоглюканазу, ксантанлиазу и маннаназу.
Определения ферментов
Родительский. Термин «родительский» обозначает фермент, в который вносят изменение для получения вариантов фермента. Родитель может представлять собой полипептид природного происхождения (дикого типа) или его вариант.
Идентичность последовательности. Сходство между двумя аминокислотными последовательностями или между двумя нуклеотидными последовательностями описывается параметром «идентичность последовательности». Для целей настоящего изобретения степень идентичности последовательностей между двумя аминокислотными последовательностями определяют с помощью алгоритма Нидлмана-Вунша (Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443-453), реализованного в программе Needle из пакета EMBOSS (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, Trends Genet. 16: 276-277), предпочтительно версия 3.0.0 или более поздняя. Необязательными параметрами являются штраф за открытие гэпа, составляющий 10, штраф за продление гэпа, составляющий 0,5, и матрица замен EBLOSUM62 (версия BLOSUM62 пакета EMBOSS). Выходной параметр программы Needle, помеченный как «самая длинная идентичность» (получаемый с помощью опции nobrief), используют в качестве процента идентичности и рассчитывают следующим образом:
(идентичные остатки x 100) / (длина выравниваемого участка - общее число гэпов в выравниваемом участке)
В альтернативном варианте осуществления применяемыми параметрами могут быть штраф за открытие гэпа, составляющий 10, штраф за продление гэпа, составляющий 0,5, и матрица замен EDNAFULL (версия NCBI NUC4.4 пакета EMBOSS). Выходной параметр программы Needle, помеченный как «наиболее длинная идентичность» (получаемый с помощью опции «nobrief»), используют в качестве процента идентичности и рассчитывают следующим образом:
(идентичные дезоксирибонуклеотиды x 100) / (длина выравниваемого участка - общее число гэпов в выравниваемом участке)
Вариант. Термин «вариант» обозначает полипептид, обладающий ферментной активностью, содержащий изменение/мутацию, т.е. замену, вставку и/или делецию в одном или более (например, нескольких) положениях относительно родительского фермента. Замена означает замену аминокислоты, занимающей некоторое положение, другой аминокислотой; делеция означает удаление аминокислоты, занимающей некоторое положение; а вставка означает добавление 1-3 аминокислоты в положение, смежное с положением, занимаемым аминокислотой, и непосредственно следующим за этим положением. Изменения/мутации обычно описывают с помощью однобуквенных кодов аминокислот и условных обозначений, известных специалистам в данной области. Например, S23D обозначает замену серинового (S) остатка аспарагиновой кислотой (D) в положении 23; Y30* обозначает делецию тирозинового остатка в положении 30. G34GW обозначает вставку триптофанового остатка после глицина в положении 34.
Фермент дикого типа: термином «дикого типа» обозначают фермент, кодируемый ДНК существующих в природе организмов, таких как встречающиеся в природе бактерия, дрожжи или нитевидный грибок.
Ксантанэндоглюканаза
В контексте настоящего документа термин ксантанэндоглюканаза обозначает фермент, проявляющий эндо-бета-1,4-глюканазную активность, которая катализирует гидролиз 1,4-связанной β-D-глюкозы полимерного каркаса ксантановой камеди в сочетании с приемлемым ферментом ксантанлиазой. Ксантанэндоглюканаза в соответствии с изобретением обладает эндо-бета-1,4-глюканазной активностью и содержит полипептид с по меньшей мере 60% идентичностью с SEQ ID NO: 1. SEQ ID NO: 1 соответствует аминокислотной последовательности ксантанэндоглюканазы, эндогенной по отношению к Paenibacillus sp-62047.
В последующих вариантах осуществления изобретения ксантанэндоглюканаза представлена вариантом с по меньшей мере 61%, по меньшей мере 62%, по меньшей мере 63%, по меньшей мере 64%, по меньшей мере 65%, по меньшей мере 66%, по меньшей мере 67%, по меньшей мере 68%, по меньшей мере 69%, по меньшей мере 70%, по меньшей мере 71%, по меньшей мере 72%, по меньшей мере 73%, по меньшей мере 74%, по меньшей мере 75%, по меньшей мере 76%, по меньшей мере 77%, по меньшей мере 78%, по меньшей мере 79%, по меньшей мере 80%, по меньшей мере 81%, по меньшей мере 82%, по меньшей мере 83%, по меньшей мере 84%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, или по меньшей мере 99% идентичностью последовательности, представленной SEQ ID NO: 1.
В дополнительных вариантах осуществления изобретения ксантанэндоглюканаза имеет замещения в одном или нескольких из положений 17, 20, 51, 53, 55, 56, 60, 63, 79, 87, 186, 192, 302, 311, 313, 387, 388, 390, 403, 408, 410, 416, 448, 451, 471, 472, 476, 489, 507, 512, 515, 538, 598, 599, 602, 605, 609, 676, 688, 690, 694, 697, 698, 699, 711, 719, 754, 756, 760, 781, 786, 797, 833, 834, 835 и 1048, представленных в SEQ ID NO: 1.
В дополнительных вариантах осуществления изобретения ксантанэндоглюканаза имеет замещения в одном или нескольких из положений S17A, F20P, F20N, F20G, F20Y, K51Q, K51H, E53P, E53G, Y55M, V56M, Y60F, S63F, T87R, A186P, K192N, I320D, I302H, I302V, I302M, H311N, S313D, I387T, K388R, K390Q, I403Y, E408D, E408S, E408P, E408A, E408G, E408N, P410G, Q416S, Q416D, A448E, A448W, A448S, K451S, G471S, S472Y, D476R, Q489P, K507R, K512P, S515V, S538C, Y579W, S598Q, A599S, I602T, I602D, V603P, S605T, G609E, D676H, A688G, Y690F, T694A, T697G, R698W, T699A, T711V, T711Y, W719R, K754R, V756H, V756Y, S760G, T781M, N786K, T797S, A824D, N833D, Q834E, S835D и F1048W
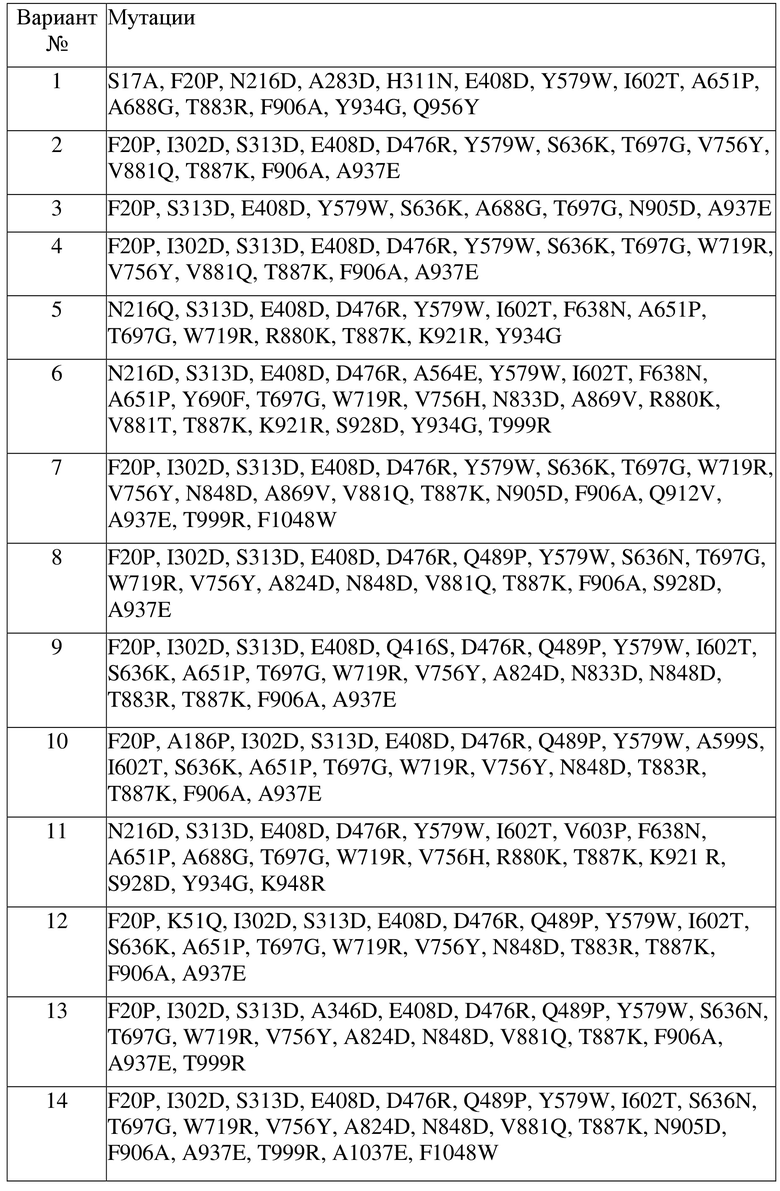
Примеры приемлемых ксантанэндоглюканаз в соответствии с изобретением указаны ниже, при этом замещения соответствуют положениям в SEQ ID NO: 1:
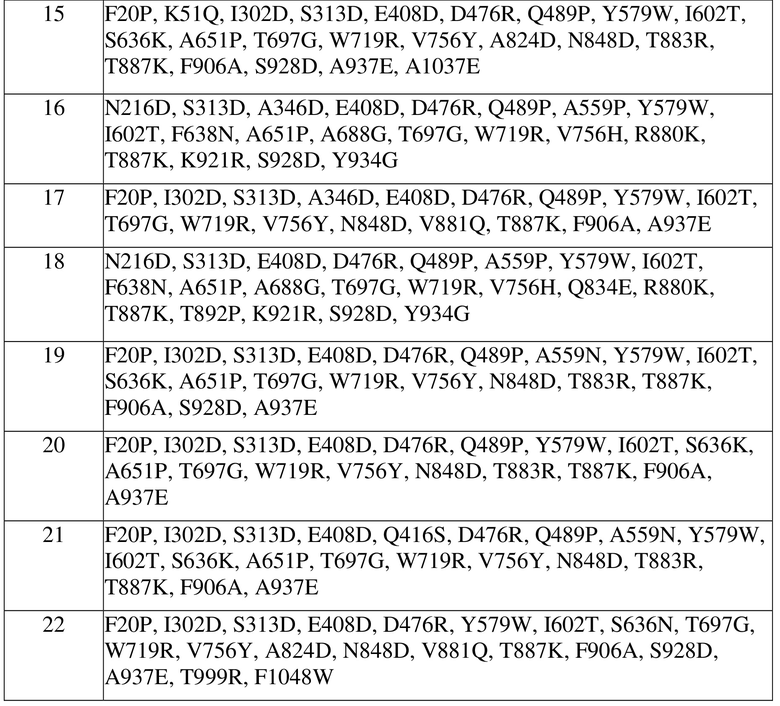
Ксантанлиаза
В контексте настоящего документа термин «ксантанлиаза» обозначает фермент, который разрывает β-D-маннозил-β-D-1,4-глюкуронозильную связь ксантана и был описан в литературе. В соответствии с номенклатурой ферментов ксантанлиазы классифицируются как EC 4.2.2.12 и образуются многими бактериями, расщепляющими ксантан, включая виды Bacillus, Corynebacterium и Paenibacillus. Ксантанлиаза в соответствии с изобретением обладает ксантанлиазной активностью и представляет собой полипептид, имеющий по меньшей мере 60% идентичность с SEQ ID NO: 2. SEQ ID NO: 2 соответствует аминокислотной последовательности ксантанлиазы, эндогенной по отношению к Paenibacillus sp.
В дополнительных вариантах осуществления изобретения ксантанлиаза представлена вариантом, имеющим по меньшей мере 61%, по меньшей мере 62%, по меньшей мере 63%, по меньшей мере 64%, по меньшей мере 65%, по меньшей мере 66%, по меньшей мере 67%, по меньшей мере 68%, по меньшей мере 69%, по меньшей мере 70%, по меньшей мере 71%, по меньшей мере 72%, по меньшей мере 73%, по меньшей мере 74%, по меньшей мере 75%, по меньшей мере 76%, по меньшей мере 77%, по меньшей мере 78%, по меньшей мере 79%, по меньшей мере 80%, по меньшей мере 81%, по меньшей мере 82%, по меньшей мере 83%, по меньшей мере 84%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичность последовательности, представленной SEQ ID NO: 2.
В другом варианте осуществления изобретения ксантанлиаза представлена вариантом с изменениями в одной или более позициях, выбранных из группы, состоящей из позиций: 9, 15, 46, 58, 66, 89, 95, 100, 106, 109, 183, 188, 190, 203, 204, 221, 229, 234, 238, 240, 242, 243, 257, 258, 291, 293, 316, 320, 324, 329, 333, 339, 341, 352, 354, 360, 377, 399, 400, 419, 440, 450, 451, 454, 458, 481, 492, 567, 568, 578, 579, 582, 664, 672, 703, 728, 843, 855, 887, 892, 1008 и 1016, представленных в SEQ ID NO: 2.
В другом варианте осуществления изобретения ксантанлиаза представлена вариантом с изменениями в одной или более позициях, выбранных из группы, состоящей из позиций 624, 631, 635, 649, 656, 752, 752, 754, 757, 769, 775, 777, 800, 801, 875, 911 и 915, представленных в SEQ ID NO: 2.
В другом варианте осуществления изобретения ксантанлиаза представлена вариантом с одной или более заместителями, выбранными из группы, состоящей из: K9R, N15T, L46D, A58L, S66H, Q89Y, K95E, S100D, N106Y, Q109R, Q109D, Q109F, Q109K, Q109A, K183Q, K183R, V188I, A190Q, A203P, K204R, A221 P, E229N, E229S, I234V, I238W, I238L, I238M, I240W, N242S, G243V, Y257W, R258E, K291 R, A293G, A293P, K316R, K320R, L324Q, K329R, K333R, L339M, 1341 P, V352I, S354P, K360G, K360R, F377Y, N399K, K400R, F419Y, N440K, D450P, K451 E, K451 R, A454V, D458S, K481 R, A492L, A492H, K567R, G568A, S578K, S578R, S579R, S579K, S582K, A624E, T631 N, S635E, T649K, I656V, T664K, N672D, I703L, M728V, G738L, P752K, P752R, G753E, S754E, S754R, S757D, A769D, L775A, D777R, V800P, D801 G, A843P, K855R, K875T, K887R, N892Y, N892W, N892F, A911V, T915A, N1008D и K1016T, представленных в SEQ ID NO: 2.
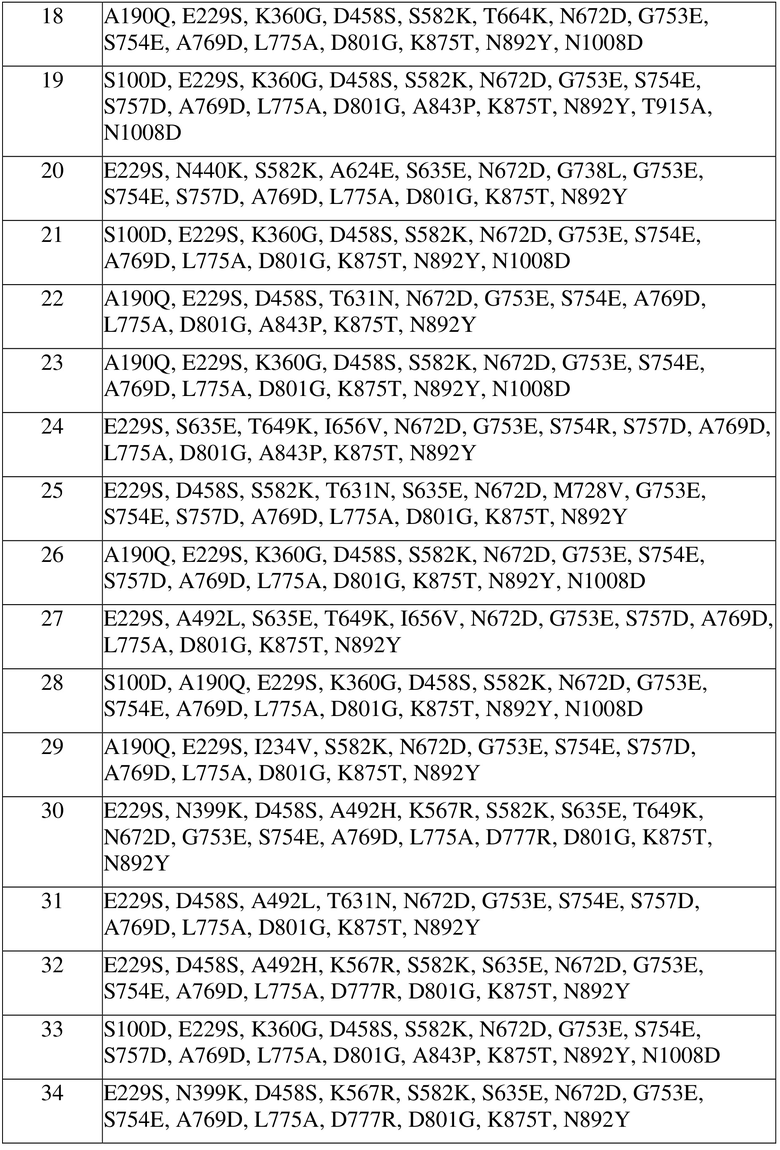
В другом варианте осуществления изобретения ксантанлиаза представлена вариантом с одним из следующих наборов заместителей, основанных на SEQ ID NO: 2.

Маннаназа
В контексте настоящего документа термин «маннаназа» или «галактоманнаназа» обозначает фермент маннаназу, определяемый в соответствии с ферментом, известным в данной области техники как маннан-эндо-1,4-бета-маннозидаза, и имеющий альтернативные названия бета-маннаназа и эндо-1,4-маннаназа, и катализирующий гидролиз 1,4-бета-D-маннозидных связей в маннанах, галактоманнанах, глюкоманнанах и галактоглюкоманнанах. В соответствии с номенклатурой ферментов маннаназы классифицируют как EC 3.2.1.78.
Приемлемая маннаназа может быть выбрана из группы, состоящей из:
a) маннаназы, обладающей маннаназной активностью и содержащей полипептид с последовательностью, по меньшей мере на 85% идентичной остаткам 27-331, представленным в SEQ ID NO: 3. SEQ ID NO: 3 соответствует полноразмерной аминокислотной последовательности маннаназы Man7, эндогенной по отношению к Bacillus hemicellulosilyticus, включая сигнальную последовательность;
b) маннаназы, обладающей маннаназной активностью и содержащей полипептид с по меньшей мере 60% идентичностью с SEQ ID NO: 4. В одном варианте осуществления изобретения маннаназа обладает маннаназной активностью и содержит полипептид с по меньшей мере 80% идентичностью с SEQ ID NO: 4. SEQ ID NO: 4 соответствует полноразмерной аминокислотной последовательности маннаназы Man4, эндогенной по отношению к Paenibacillus sp;
c) и их смесей.
Таким образом, приемлемая маннаназа может иметь маннаназную активность и содержать полипептид с последовательностью, по меньшей мере на 85% идентичной остаткам 27-331, представленным в SEQ ID NO: 3. SEQ ID NO: 3 соответствует полноразмерной аминокислотной последовательности маннаназы Man7, эндогенной по отношению к Bacillus hemicellulosilyticus, включая сигнальную последовательность. В одном варианте осуществления изобретения маннаназа имеет последовательность, по меньшей мере на 90% идентичную остаткам 27-331, представленным в SEQ ID NO: 3. В другом варианте осуществления изобретения маннаназа представляет собой вариант SEQ ID NO: 3, содержащий по меньшей мере один заместитель в позициях 123, 158, 180, 272, 285 или 307 или их комбинацию. В другом варианте осуществления изобретения маннаназа представляет собой вариант SEQ ID NO: 3, содержащий по меньшей мере один заместитель в позициях M123, A158, F180, G272, T285 или T307 или их комбинацию. В другом варианте осуществления изобретения маннаназа представляет собой вариант SEQ ID NO: 3, содержащий по меньшей мере один заместитель в позициях M123, A158, F180, G272, T307 или L316 или их комбинацию. В варианте осуществления вариант содержит один дополнительный заместитель, два дополнительных заместителя, три дополнительных заместителя или четыре дополнительных заместителя.
В альтернативном или дополнительном варианте осуществления приемлемая маннаназа может иметь маннаназную активность и представлять собой полипептид с по меньшей мере 60% идентичностью с SEQ ID NO: 4. В одном варианте осуществления изобретения маннаназа обладает маннаназной активностью и содержит полипептид с по меньшей мере 80% идентичностью с SEQ ID NO: 4. SEQ ID NO: 4 соответствует полноразмерной аминокислотной последовательности маннаназы Man4, эндогенной по отношению к Paenibacillus sp.
Маннаназа может представлять собой вариант SEQ ID NO: 4, содержащий одну, две, три, четыре, пять, шесть, семь или более вариаций по сравнению с SEQ ID NO: 4, выбранных из:
(i) N10Q/T, P19E/V, S30T, T38E/I/L/M/Q/R/V, S59D/G/K/N/Q/T, L60F/M/V, T62E/I/Q/V, K63L, L66C/T/V, N67A/D/E/G/P/Q/S/V, A68L/M/R/S/W, K70R/V, N71D/H, N74E/C/Q/V, V75I, Q78A/D/L/M, N79E/F/W, K80Q/T, N97E/L/P/Q, V103I, Y129M, T131P, S135A/C/Q, A136E, K143Q/R, F167L/S/W/Y, P168A/E/G/L/M/S/T, Q184D/F/H/L/M/P, N213E, K214C/Q, G225A/C/P/W, T228A/G/H/I/K/S/V/Y, Y235G/I/L/Q/S/V, Q242S/E, K244A/C/G/L/M/P/S, S258A/D/E/G/M/N/P/T, G259A/E/R/S/W, N261I/M/P/Q/R/S/T/V/W/Y и D283G/H/T; или
(ii) P19E/V, T38E/I/L/M/Q/R/V, N67A/D/E/G/P/Q/S/V, N97E/L/P/Q, Y129M, K143Q/R, P168A/E/G/L/M/S/T, Q184D/F/H/L/M/P, G225A/C/P/W, T228A/G/H/I/K/S/V/Y, Y235G/I/L/Q/S/V, K244A/C/G/L/M/P/S, S258A/D/E/G/M/N/P/T и N261I/M/P/Q/R/S/T/V/W/Y; или
(iii) P19E/V, T38E/I/L/M/Q/R/V, N67A/D/E/G/P/Q/S/V, L85L, Y129M, P168A/E/G/L/M/S/T, Q184D/F/H/L/M/P, G225A/C/P/W, K244A/C/G/L/M/P/S, S258A/D/E/G/M/N/P/T и N261I/M/P/Q/R/S/T/V/W/Y; или
(iv) P19E, S30T, T38E, S59V, L60Q, K63R, N67D, N97D, V103I, Y129M, F167Y, P168S, Q184L, G225C, T228V, Y235L, K244L, S258D и N261R;
при условии, что один или более указанных вариаций не встречаются в природе; и в котором аминокислотные позиции указанного варианта маннаназы или рекомбинантного полипептида или активного фрагмента последнего пронумерованы в соответствии с аминокислотной последовательностью, представленной в SEQ ID NO:4.
В альтернативном или дополнительном варианте осуществления маннаназа может представлять собой вариант SEQ ID NO: 4, содержащий комбинацию вариаций SEQ ID NO:4, выбранных из P19E-T38E-N67D-N97D-Y129M-P168S-Q184L-K244L-S258D-N261R; N10T-P19E-G28S-S30T-T38E-N67D-N71D-N97D-Y129M-P168S-Q184L-G225C-Y235L-K244L-S258D-N261R-F297FQ; P19E-S30T-T38E-S59V-L60Q-K63R-N67D-N97D-V103I-Y129M-F167Y-Q184L-G225C-T228V-Y235L-K244L-S258D-N261R-F297FQ; N10T-P19E-S30T-T38E-S59V-L60Q-K63R-N67D-N97D-Y129M-K143Q-P168S-Q184L-G225C-T228V-Y235L-K244L-S258D-N261R-F297FQ; N10T-P19E-S30T-T38E-S59V-L60Q-K63R-N67D-N97D-Y129M-K143Q-P168S-Q184L-G225P-T228V-Y235L-K244L-S258D-N261R-F297FQ; N10T-P19E-S30T-T38E-S59V-L60Q-K63R-N67D-N71D-N97D-V103I-Y129M-K143Q-P168S-Q184L-G225P-T228V-Y235L-K244L-S258D-N261R-F297FQ; A2S-P19E-G28S-S30T-T38E-K63R-N67D-N71D-N74E-K93R-N97D-Y129M-N150T-P168S-Q184L-N213A-G225C-Y235L-K244L-S258D-N261Q-F297FQ; T3R-N10T-P19E-G28A-S30T-T38E-T62E-N67D-N71D-K93R-N97L-E111S-Y129M-D139M-P168S-Q184L-G225C-Y235L-K244L-S258D-N261Q-F297FQ; и N10T-P19E-G28A-S30T-T38E-S59D-N67D-A68S-N71D-K93R-N97D-Y129M-K143Q-P168S-Q184D-G225C-Y235L-K244L-S258D-N261R-T284E-F297FQ; и в котором аминокислотные позиции указанного варианта маннаназы пронумерованы в соответствии с аминокислотной последовательностью, представленной в SEQ ID NO:4.
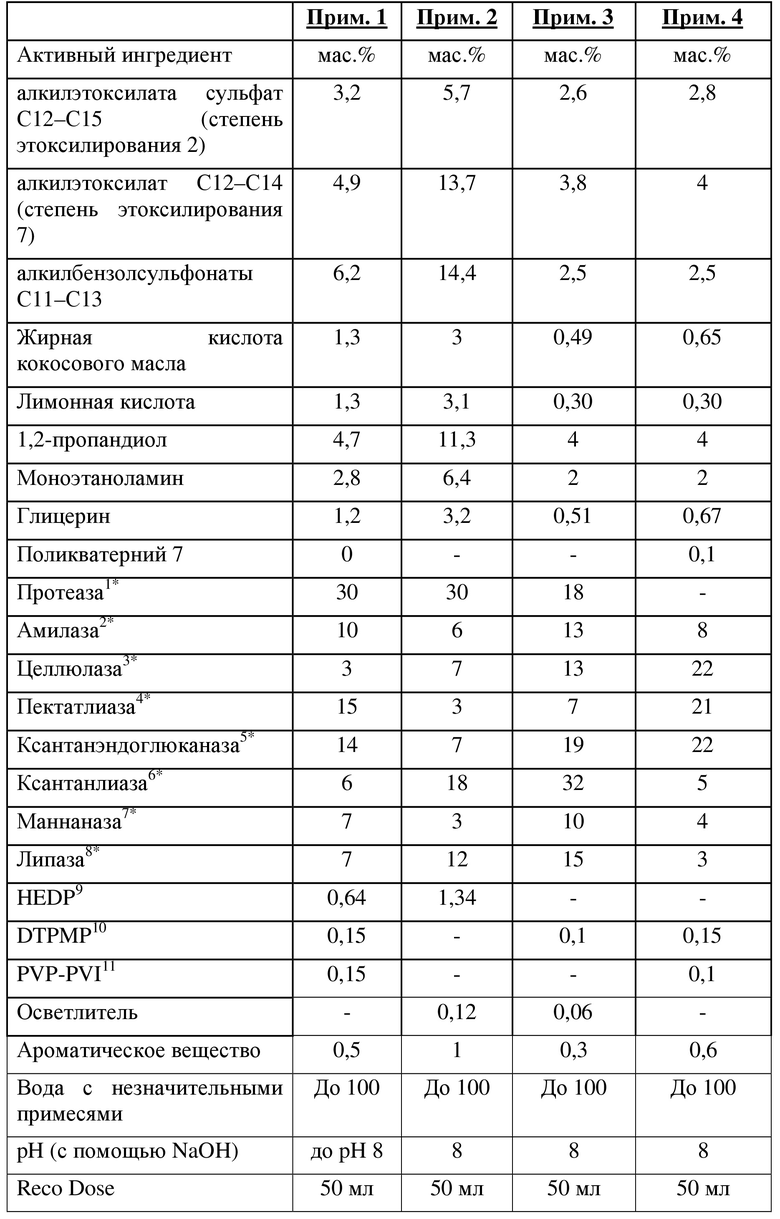
Маннаназная активность может быть подтверждена с помощью общедоступных наборов реактивов, включая доступные в продаже реактивы от компаний Megazyme, Bray, Ирландия и Glycospot,  , Дания.
, Дания.
Липаза
Ферментная система предпочтительно дополнительно содержит липазу. Присутствие масел и/или жиров может дополнительно увеличить устойчивость пятен, содержащих маннаны и другие полисахариды. Таким образом, присутствие липазы в составе ферментного комплекса может дополнительно повысить эффективность удаления таких пятен. Подходящие липазы включают липазы бактериального, грибкового или синтетического происхождения и их варианты. Кроме того, приемлемыми вариантами являются химически модифицированные или полученные с помощью белковой инженерии мутанты. Примеры приемлемых липаз включают липазы из Humicola (синоним Thermomyces), например из H. lanuginosa (T. lanuginosus).
Липаза может представлять собой «липазу первого цикла», например, как описано в WO06/090335 и WO13/116261. В одном аспекте липаза представляет собой липазу первой отмывки, предпочтительно вариант липазы дикого типа из Thermomyces lanuginosus, содержащий мутации T231R и/или N233R.
Предпочтительные липазы включают продаваемые под торговыми наименованиями Lipex®, Lipolex® и Lipoclean® производства компании Novozymes, г. Багсвэрд, Дания.
Другие подходящие липазы включают: Liprl 139, например, как описано в WO2013/171241; TfuLip2, например, как описано в WO2011/084412 и WO2013/033318; липаза Pseudomonas stutzeri, например, как описано в WO2018228880; липаза Microbulbifer thermotolerans, например, как описано в WO2018228881; липаза Sulfobacillus acidocaldarius, например, как описано в EP3299457; липаза LIP062, например, как описано в WO2018209026; липаза PinLip, например, как описано в WO2017036901, и липаза Absidia sp, например, как описано в WO2017005798.
Приемлемой липазой является вариант SEQ ID NO:5, содержащий:
(а) заместитель T231R
и
(b) заместитель N233R или N233C
и
(c) по меньшей мере три дополнительных заместителя, выбранных из E1C, D27R, N33Q, G38A, F51V, G91Q, D96E, K98L, K98I, D111A, G163K, H198S, E210Q, Y220F, D254S, I255A и P256T;
где позиции соответствуют позициям в SEQ ID NO:5 и при этом вариант липазы имеет последовательность, по меньшей мере на 90%, но менее чем на 100% идентичную полипептиду, имеющему аминокислотную последовательность SEQ ID NO: 5, и при этом вариант обладает липазной активностью.
Одной предпочтительной липазой является вариант SEQ ID NO: 5, содержащий следующие заместители: T231R, N233R, D27R, G38A, D96E, D111A, G163K, D254S и P256T
Одной предпочтительной липазой является вариант SEQ ID NO: 5, содержащий следующие заместители: T231R, N233R, N33Q, G91Q, E210Q, I255A.
Приемлемые липазы доступны в продаже от компании Novozymes, например, такие как Lipex Evity 100L, Lipex Evity 200L (обе представляют собой жидкое сырье) и Lipex Evity 105T (гранулят). Структура этих липаз отличается от структуры продуктов Lipex 100L, Lipex 100T и Lipex Evity 100T, которые не входят в объем изобретения.
Другие ферменты
Ферментная система может содержать другие ферменты. Приемлемые ферменты обеспечивают очищающие характеристики и/или полезные эффекты ухода за тканью. Примеры других приемлемых ферментов включают, без ограничений, гемицеллюлазы, пероксидазы, протеазы, целлюлазы, ксиланазы, липазы, фосфолипазы, эстеразы, кутиназы, пектиназы, кератаназы, редуктазы, оксидазы, фенолоксидазы, липоксигеназы, лигниназы, пуллуланазы, танназы, пентосаназы, маланазы, β-глюканазы, арабинозидазы, гиалуронидазу, хондроитиназу, лакказу и известные амилазы или их комбинации. Предпочтительная ферментная система дополнительно содержит коктейль из традиционных моющих ферментов, таких как протеаза, липаза, кутиназа и/или целлюлаза в сочетании с амилазой. Моющие ферменты более подробно описаны в патенте США № 6,579,839.
Необязательные ингредиенты
Моющая композиция может дополнительно содержать один или более из следующих необязательных ингредиентов: внешнего структурообразующего средства или загустителя, ферментов, стабилизаторов ферментов, очищающих полимеров, отбеливающих систем, оптических осветлителей, окрашивающих пигментов, материала в виде частиц, ароматических веществ и других средств контроля запаха, гидротропов, подавителей пенообразования, полезных средств ухода за тканью, средств, регулирующих pH, средств, ингибирующих перенос красителя, консервантов, прямых красителей не для тканей и их смесей. В более предпочтительных вариантах осуществления моющая композиция для стирки не содержит отбеливающее вещество.
Внешнее структурообразующее средство или загуститель: Предпочтительными внешними структурообразующими средствами и загустителями являются те из них, которые обеспечивают структурирующий эффект независимо от взаимодействий между зарядами. Таким образом, особенно предпочтительными внешними структурообразующими средствами являются незаряженные внешние структурообразующие средства, такие как средства, выбранные из группы, состоящей из: неполимерных кристаллических, гидроксифункциональных структурообразующих средств, таких как гидрогенизированное касторовое масло; микрофибриллированная целлюлоза; незаряженная гидроксиэтилцеллюлоза; незаряженная гидрофобно-модифицированная гидроксиэтилцеллюлоза; гидрофобно-модифицированные этоксилированные уретаны; гидрофобно-модифицированные неионные полиолы; и их смеси.
Приемлемые полимерные структурообразующие средства включают полученные природным путем и/или синтетические полимерные структурообразующие средства.
Примеры полученных природным путем пригодных полимерных структурообразующих средств включают: микрофибриллированную целлюлозу, гидроксиэтилцеллюлозу, гидрофобно-модифицированную гидроксиэтилцеллюлозу, карбоксиметилцеллюлозу, производные полисахаридов и их смеси. Не имеющие ограничительного характера примеры микрофибриллированной целлюлозы описаны в WO 2009/101545 А1. Приемлемые производные полисахаридов включают: пектин, альгинат, арабиногалактан (гуммиарабик), каррагинан, геллановую камедь, ксантановую камедь, гуаровую камедь и их смеси.
Примеры пригодных синтетических полимерных структурообразующих средств или загустителей для применения в настоящем изобретении включают: поликарбоксилаты, гидрофобно-модифицированные этоксилированные уретаны (HEUr), гидрофобно-модифицированные неионные полиолы и их смеси.
Предпочтительно жидкая моющая композиция на водной основе имеет вязкость от 50 до 5000, предпочтительно от 75 до 1000, более предпочтительно от 100 до 500 мПа⋅с, измеренную при скорости сдвига 100 с-1, при температуре 20 °C. Для повышения устойчивости фазы, а также повышения стабильности суспендированных ингредиентов жидкая моющая композиция на водной основе имеет вязкость от 50 до 250000, предпочтительно от 5000 до 125000, более предпочтительно от 10000 до 35000 мПа⋅с, измеренную при скорости сдвига 0,05 с-1, при температуре 20 °C.
Очищающие полимеры. Моющая композиция предпочтительно содержит очищающий полимер. Такие очищающие полимеры по меньшей мере частично удаляют пятно с текстильных волокон и позволяют ферментным системам эффективнее разрушать комплексы, содержащие маннан и другой полисахарид. Приемлемые очищающие полимеры обеспечивают широкий диапазон очистки поверхностей и тканей от грязи и/или перевод частиц загрязнений во взвешенное состояние. Не имеющие ограничительного характера примеры приемлемых очищающих полимеров включают: амфифильные алкоксилированные очищающие жир полимеры, очищающие глинистые загрязнения полимеры, удаляющие загрязнения полимеры и суспендирующие загрязнения полимеры. Предпочтительный очищающий полимер получают путем свободнорадикальной сополимеризации по меньшей мере одного соединения формулы (I),
 ,
,
в которой n больше или равно 3, причем в это число входит
по меньшей мере одно соединение формулы (II),
 ,
,
в которой А- представляет анион, в частности выбранный из галогенидов, таких как фторид, хлорид, бромид, йодид, сульфата, гидросульфата, алкилсульфата, такого как метилсульфат, и их смесей. Такие полимеры дополнительно описаны в EP3196283A1.
По тем же причинам удаляющие загрязнения полимеры на основе сложного полиэфира, такие как SRA300, поставляемые компанией Clariant, являются также особо предпочтительными.
Другие полезные очищающие полимеры описаны в USPN 2009/0124528A1. Моющая композиция может содержать амфифильные алкоксилированные очищающие жир полимеры, которые могут иметь сбалансированные гидрофильные и гидрофобные свойства, которые позволяют им удалять частицы жира с тканей и поверхностей. Амфифильные алкоксилированные очищающие жир полимеры могут иметь сердцевинную структуру и множество алкоксилатных групп, связанных с этой сердцевинной структурой. Они могут содержать, например, алкоксилированные полиалкиленимины. Такие соединения могут содержать, без ограничений, этоксилированный полиэтиленимин, этоксилированный гексаметилендиамин и их сульфатированные версии. Также могут быть включены полипропоксилированные производные. Целый ряд аминов и полиалкилениминов могут быть алкоксилированы до различных степеней. Полезным примером является этоксилированная полиэтилениминовая основа с молекулярной массой 600 г/моль, содержащая до 20 этоксилатных (EO) групп на -NH-группу и поставляемая компанией BASF. Алкоксилированные полиалкиленимины могут иметь внутренний полиэтиленоксидный блок и наружный полипропиленоксидный блок. Моющие композиции могут содержать очищающий полимер в концентрации от 0,1% до 10%, предпочтительно от 0,1% до 8%, более предпочтительно от 0,1% до 2% по массе моющей композиции.
Ингибитор переноса красителя. Моющая композиция может содержать ингибитор переноса красителя. Приемлемые ингибиторы переноса красителя могут быть выбраны из группы, состоящей из поливинилпирролидона (PVP), поливинилимидазола (PVI), сополимеров винилпирролидона и винилимидазола (PVP/PVI), поливинилпиридин-N-оксида, поли-N-карбоксиметил-4-винилпиридиумхлорида и их смесей, и особо предпочтительно поливинилпирролидона (PVP), поливинилимидазола (PVI), сополимеров винилпирролидона и винилимидазола (PVP/PVI) и их смесей. Ингибитор переноса красителя может присутствовать в концентрации от 0,05% до 5%, предпочтительно от 0,1% до 3% и более предпочтительно от 0,2% до 2,5% по массе моющей композиции.
Полимерное осаждающее средство. Моющая композиция для стирки может содержать от 0,1% до 7%, более предпочтительно от 0,2% до 3% полимерного осаждающего средства. В контексте настоящего документа термин «полимерное осаждающее средство» обозначает любой катионный полимер или комбинацию катионных полимеров, которые существенно усиливают осаждение на ткани полезного средства ухода за тканью во время стирки. Приемлемые полимерные осаждающие средства могут содержать катионный полисахарид и/или сополимер, или предпочтительно катионный полисахарид, или наиболее предпочтительно поликватерний 7. Термин «полезное средство ухода за тканью» в контексте настоящего документа обозначает любой материал, обеспечивающий полезный эффект ухода за тканью. Не имеющие ограничительного характера примеры полезных средств ухода за тканью включают: силиконовые производные, масляные производные сахара, диспергируемые полиолефины, полимерные латексы, катионные поверхностно-активные вещества и их комбинации. Предпочтительно осаждающее средство является катионным или амфотерным полимером. Плотность катионного заряда полимера предпочтительно варьируется в пределах от 0,05 миллиэквивалент/г до 6 миллиэквивалент/г. Плотность заряда рассчитывают путем деления количества суммарных зарядов в повторяющемся звене на молекулярную массу повторяющегося звена. В одном варианте осуществления изобретения плотность заряда варьируется от 0,1 миллиэквивалент/г до 3 миллиэквивалент/г. Положительные заряды могут быть расположены на каркасе полимеров или боковых цепях полимеров.
Органический структурообразователь и/или хелатообразующий агент. Моющая композиция для стирки может содержать от 0,6% до 10%, предпочтительно от 2% до 7% по массе одного или более органических структурообразователей и/или хелатообразующих агентов. Приемлемые органические структурообразователи и/или хелатообразующие агенты выбирают из группы, состоящей из: МЭА-цитрата, лимонной кислоты, аминоалкиленполи(алкиленфосфонатов), этан-1-гидроксидифосфонатов щелочных металлов и нитрилотриметилена, фосфонатов, диэтилентриаминпента(метиленфосфоновой кислоты) (DTPMP), этилендиамин тетра(метиленфосфоновой кислоты) (DDTMP), гексаметилендиамин тетра(метиленфосфоновой кислоты), гидроксиэтилен-1,1-дифосфоновой кислоты (HEDP), гидроксиэтандиметиленфосфоновой кислоты, этилендиаминдиянтарной кислоты (EDDS), этилендиаминтетрауксусной кислоты (EDTA), гидроксиэтилэтилендиаминтриацетата (HEDTA), нитрилотриацетата (NTA), метилглициндиацетата (MGDA), иминодисукцината (IDS), гидроксиэтилиминодисукцината (HIDS), гидроксиэтилиминодиацетата (HEIDA), глициндиацетата (GLDA), диэтилентриаминпентауксусной кислоты (DTPA), катехолсульфонатов, таких как Tiron™ и их смесей.
Стабилизатор ферментов. Ферменты можно стабилизировать с помощью любой известной системы стабилизаторов, такой как соединения кальция и/или магния, соединения бора и замещенных борных кислот, ароматические боратные сложные эфиры, пептиды и пептидные производные, полиолы, низкомолекулярные карбоксилаты, относительно гидрофобные органические соединения [например, определенные сложные эфиры, диалкилгликольные эфиры, спирты или спиртовые алкоксилаты], алкилэфиркарбоксилат в дополнение к источнику ионов кальция, гипохлорит бензамидина, низшие алифатические спирты и карбоновые кислоты, N,N-бис(карбоксиметил)сериновые соли; сополимер (мет)акриловой кислоты - сложного эфира (мет)акриловой кислоты и ПЭГ; соединение лигнина, полиамидный олигомер, гликолевая кислота или ее соли; полигексаметиленбигуанид или N,N-бис-3-аминопропилдодециламин или соль; и их смеси.
Окрашивающие пигменты. Моющая композиция может содержать окрашивающее средство для тканей (иногда называемое оттеняющим, подсинивающим или отбеливающим средством). Как правило, окрашивающее средство придает ткани синий или фиолетовый оттенок. Окрашивающие средства можно использовать либо отдельно, либо в комбинации для создания конкретного подкрашивающего оттенка и/или для придания оттенка разным типам ткани. Это можно обеспечить, например, путем смешивания красного и зелено-синего красителя для получения синего или фиолетового оттенка. Окрашивающие средства могут быть выбраны из любого известного химического класса красителей, включая, без ограничений, акридин, антрахинон (включая полициклические хиноны), азин, азо (например, моноазо, диазо, триазо, тетракисазо, полиазо), включая предварительно металлизированный азо, бензодифуран и бензодифуранон, каротиноид, кумарин, цианин, диазагемицианин, дифенилметан, формазан, гемицианин, индигоиды, метан, нафталимиды, нафтохинон, нитро и нитрозо, оксазин, фталоцианин, пиразолы, стильбен, стирил, триарилметан, трифенилметан, ксантены и их комбинации.
Оптические осветлители. Моющая композиция может содержать от 0,005% до 2%, предпочтительно от 0,01% до 0,1% флуоресцентного средства (оптического осветлителя) в расчете на общую массу моющей композиции. Флуоресцентные средства хорошо известны, и многие флуоресцентные средства доступны на рынке. Обычно эти флуоресцентные средства поставляют и используют в виде щелочных солей металла, например солей натрия. Предпочтительными классами флуоресцентных средств являются: соединения дистирилбифенила, например Tinopal (торговый знак) CBS-X, соединения диаминостильбен-дисульфоновой кислоты, например Tinopal DMS pure Xtra и Blankophor (торговый знак) HRH, и соединения пиразолина, например Blankophor SN. Предпочтительными флюоресцентными веществами являются: натрий 2-(4-стирил-3-сульфофенил)-2H-нафтол[1,2-d]триазол, динатрий 4,4'-бис{[(4-анилино-6-(N-метил-N-2-гидроксиэтил)амино-1,3,5-триазин-2-ил)]амино}стильбен-2-2'-дисульфонат, динатрий-4,4'-бис{[(4-анилино-6-морфолино-1,3,5-триазин-2-ил)]амино}стильбен-2-2'-дисульфонат и динатрий 4,4'-бис(2-сульфостирил)бифенил.
Гидротроп. Моющая композиция может содержать в расчете на общую массу моющей композиции от 0% до 30%, предпочтительно от 0,5% до 5%, более предпочтительно от 1,0% до 3,0% гидротропа, способного предотвращать формирование жидких кристаллов. Таким образом, добавление гидротропа способствует обеспечению чистоты/прозрачности композиции. Приемлемые гидротропы содержат, без ограничений, мочевину, соли бензолсульфоната, толуолсульфоната, ксиленсульфоната или куменсульфоната. Для обеспечения оптимального эффекта гидротроп предпочтительно выбирают из группы, состоящей из пропиленгликоля, ксиленсульфоната, этанола и мочевины.
Частицы. Композиция может также содержать частицы, особенно если композиция дополнительно содержит структурообразующее средство или загуститель. Композиция может содержать от 0,02% до 10%, предпочтительно от 0,1% до 4%, более предпочтительно от 0,25% до 2,5% частиц в расчете на общую массу композиции. Указанные частицы включают гранулы, перлесцентные агенты, микрокапсулы и их смеси.
Микрокапсулы. Приемлемые капсулы обычно образованы таким образом, что они по меньшей мере частично, предпочтительно полностью окружают полезное средство, формируя вокруг них оболочку. Предпочтительно капсула представлена капсулой ароматического вещества, в которой указанное полезное средство содержит один или более сырьевых материалов ароматического вещества. Материал оболочки капсулы может содержать: меламин, полиакриламид, силиконы, кремнезем, полистирол, полимочевина, полиуретаны, материалы на основе полиакрилата, материалы на основе эфиров полиметакрилатовой кислоты, желатин, малеиновый ангидрид стирола, полиамиды, ароматические спирты, поливиниловый спирт, материалы на основе резорцина, материалы на основе полиизоцианата, ацетали (такие как бензол-1,3,5-триол-глутаральдегид и бензол-1,3,5-триол-меламин), крахмал, ацетатфталат целлюлозы и их смеси. Предпочтительно оболочка капсулы содержит меламин и/или материал на основе полиакрилата. Капсула ароматического вещества может быть покрыта слоем осаждающего средства, катионного полимера, неионного полимера, анионного полимера или их смесей. Предпочтительно капсулы ароматического вещества имеют средневзвешенный размер частиц от 0,1 микрон до 100 микрон, предпочтительно от 0,5 микрон до 60 микрон. Особенно если композиция содержит капсулы с оболочкой, образованной по меньшей мере частично из формальдегида, композиция может дополнительно содержать поглотители формальдегида.
Способ получения жидкой моющей композиции для стирки
Моющие композиции для стирки могут быть получены с помощью любого известного специалисту приемлемого способа. Обычно ингредиенты смешивают друг с другом в любом приемлемом порядке. Предпочтительно моющие поверхностно-активные вещества добавляют в составе концентрированной готовой смеси, к которой добавляют другие необязательные ингредиенты. Предпочтительно растворитель добавляют либо в последнюю очередь, либо, если предполагается добавление внешнего структурообразующего средства, то непосредственно перед ним, при этом структурообразующее средство добавляют в качестве последнего ингредиента.
Способ стирки тканей
Моющие композиции для стирки настоящего изобретения могут быть использованы для стирки тканей. В таких способах моющую композицию для стирки разбавляют для обеспечения промывочной жидкости с общей концентрацией поверхностно-активного вещества более 300 м.д., предпочтительно от 400 м.д. до 2500 м.д., более предпочтительно от 600 м.д. до 1000 м.д. После этого ткань стирают в промывочной жидкости и предпочтительно прополаскивают.
Способ настоящего изобретения, в частности, подходит для удаления пятен, в частности когда пятно содержит комбинацию маннан и других полисахаридов, и особенно когда пятно дополнительно содержит масла и/или жиры, такие как натуральные масла и/или натуральные жиры, такие как животный жир, растительный жир или их смеси.
СПОСОБЫ
А) Измерение рН
pH измеряют при температуре 25 °C с помощью pH-метра Santarius PT-10P с заполненным гелем зондом (таким как зонд Toledo, кат. номер 52 000 100), откалиброванным в соответствии с инструкцией. pH измеряют при 10% разведении в деминерализованной воде (т.е. 1 часть моющей композиции для стирки и 9 частей деминерализованной воды).
В) Способ измерения вязкости
Вязкость измеряют с помощью реометра AR 2000 от компании TA instruments плоскоконической формы диаметром 40 мм и углом 1°. Вязкость при различных скоростях сдвига измеряют посредством логарифмической развертки скоростей сдвига от 0,1 с-1 до 1200 с-1 через 3 минуты при 20 °C. Вязкость при малых усилиях сдвиге измеряют при постоянной скорости сдвига 0,05 с-1.
ПРИМЕРЫ
Ниже приведены примеры жидких моющих композиций для стирки настоящего изобретения.
* Концентрации фермента приведены в мг активного белка фермента на 100 г готового продукта
1 Lavergy® Pro 104L, поставляемый компанией BASF
2 Amplify® 24L, поставляемый компанией Novozymes
3 Biotouch® FLX1, поставляемый компанией AB Enzymes
4 XPect® 100L, поставляемый компанией Novozymes
5 Ксантанэндоглюканаза, содержащая полипептид с последовательностью, по меньшей мере на 60% идентичной SEQ ID NO: 1, например вариант SEQ ID NO: 1 с заместителями в F20P, I302D, S313D, E408D, D476R, Y579W, I602T, S636N, T697G, W719R, V756Y, A824D, N848D, V881Q, T887K, F906A, S928D, A937E, T999R, F1048W.
6 Ксантанлиаза, содержащая полипептид с последовательностью, по меньшей мере на 60% идентичной SEQ ID NO: 2, например вариант SEQ ID NO: 2 с заместителями в E229S, N399K, D458S, K567R, S582K, S635E, N672D, G753E, S754E, A769D, L775A, D777R, D801G, K875T, N892Y.
7 Маннаназа, содержащая вариант SEQ ID NO: 4, например вариант SEQ ID NO: 4, содержащий вариации в N10T-P19E-G28A-S30T-T38E-S59D-N67D-A68S-N71D-K93R-N97D-Y129M-K143Q-P168S-Q184D-G225C-Y235L-K244L-S258D-N261R-T284E-F297FQ.
8 Вариант липазы, представленный SEQ ID NO: 5, такой как Lipex Evity 100L или 200L
9 Гидроксиэтилидендифосфоновая кислота
10 Диэтилентриаминпента(метиленфосфоновая кислота)
11 Поливинилпирролидон-поливинилимидазол, в котором относительное содержание N-винилпирролидона составляет по меньшей мере 50 мас.%, со средневзвешенной молекулярной массой около 40000
Ниже приведена жидкая моющая композиция для стирки с низким содержанием воды, которая может быть инкапсулирована в водорастворимую пленку с обеспечением водорастворимого изделия с единичной дозой в соответствии с настоящим изобретением. Обычно 24 г жидкой моющей композиции для стирки с низким содержанием воды может быть инкапсулировано в поливинилспиртовую пленку с обеспечением водорастворимого изделия с единичной дозой. Концентрации фермента приведены в мг активного белка фермента на 100 г готового продукта.

* Концентрации фермента приведены в мг активного белка фермента на 100 г готового продукта
11 Диэтилентриаминпентауксусная кислота, натриевая соль
12 Этоксилированная основа из разветвленного полиэтиленимина со средневзвешенной молекулярной массой 600 г/моль, содержащая до 20 этоксилатных (EO) групп на -NH-группу и поставляемая компанией BASF
13 Амфифильный привитый полимер на основе водорастворимого полиэтиленоксида (A) в качестве основы для прививки и боковых цепей, образованных полимеризацией винилэфирного компонента (В), при этом указанный полимер имеет ≤1 участка прививки на 50 единиц алкиленоксида и средневзвешенную молекулярную массу от 3000 до 100000
Размеры и величины, описанные в настоящем документе, не следует понимать как строго ограниченные перечисленными точными числовыми значениями. Напротив, если не указано иное, каждый такой размер должен обозначать как указанное значение, так и функционально эквивалентный диапазон, в который входит это значение. Например, размер, описанный как «40 мм», подразумевает «около 40 мм».
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Дзе Проктер Энд Гэмбл Компани
Дзе Проктер Энд Гэмбл Компани
<120> МОЮЩИЕ КОМПОЗИЦИИ ДЛЯ СТИРКИ С УДАЛЕНИЕМ ПЯТЕН
<130> CM05071
<160> 5
<170> PatentIn, версия 3.5
<210> 1
<211> 1050
<212> PRT
<213> Paenibacillus sp-62047
<400> 1
Ile Ala Gly Val Val Gln Ser Val Asn Val Ser Gln Ala Gly Tyr Ser
1 5 10 15
Ser Asn Asp Phe Lys Thr Ala Thr Val Thr Ala Ser Asp Lys Leu Ser
20 25 30
Asp Thr Ser Tyr Gln Ile Leu Gln Gly Thr Thr Val Ile Ala Thr Gly
35 40 45
Thr Met Lys Asp Glu Gly Tyr Val Trp Gly Lys Tyr Val Tyr Ser Ile
50 55 60
Asp Phe Ser Ser Val Thr Ala Thr Gly Thr Asn Phe Thr Ile Arg Ser
65 70 75 80
Asn Gly Val Ser Ser Tyr Thr Phe Pro Ile Gln Thr Asn Met Trp Asn
85 90 95
Glu Tyr Lys Asp Glu Met Thr Ala Phe Tyr Arg Leu Leu Arg Thr Thr
100 105 110
Asp Thr Phe Ala Ala Tyr Pro Ala Gly Tyr Ser Asn Ile Ala Pro Ser
115 120 125
Asn Lys Ile Leu His Pro Asp Ser Phe Leu Asp Asp Ala Phe Ser Pro
130 135 140
Asp Arg Thr Thr His Tyr Asp Leu Thr Gly Gly Trp Phe Asp Ala Gly
145 150 155 160
Asp Tyr Gly Lys Tyr Gly Gly Asn Gln Trp Val Gln Gly Asn Ile Ala
165 170 175
Ile Ser Tyr Leu Arg His Ala Ser Ser Ala Ala Val Asn Phe Asp Lys
180 185 190
Asp Thr Asn Gly Ile Pro Asp Leu Val Asp Glu Ala Ile Phe Gly Ser
195 200 205
Gln Tyr Leu Val Lys Phe Ala Asn Gln Leu Gly Gly Ala Ile His Asn
210 215 220
Ile Leu Arg Lys Gly Gly Phe Val Leu Pro His Lys Val Thr Asp Asn
225 230 235 240
Val Pro Gly Asn Thr Asp Asp Arg Ala Leu Glu Ala Val Glu Ala Val
245 250 255
Gly Gly Ser Gly Lys Ser Ser Gly Ser Leu Ala Ala Thr Ala Arg Ala
260 265 270
Ile Arg Thr Ala Ile Ala Gly Gly Lys Val Ala Ala Asn Lys Val Ala
275 280 285
Gln Leu Gln Thr Leu Ala Asn Glu Phe Gln Ala Ala Ala Ile Ile Phe
290 295 300
Tyr Asn Tyr Thr Leu Thr His Gln Ser Gly Asn His Gly Ser Tyr Gly
305 310 315 320
Thr Met Asn Asn Gly Gly Ile Ala Asn Pro Leu Leu Trp Ala Glu Val
325 330 335
Gln Leu Tyr Leu Leu Thr Gly Asp Ala Ala Tyr Lys Thr Gln Ala Gln
340 345 350
Thr Arg Ile Asn Ala Ile Asn Glu Ala Tyr Val Ser Ser Thr Asn Tyr
355 360 365
Trp Asp Met His Pro Ile Ala Leu Ala Glu Phe Tyr Pro Val Ala Asp
370 375 380
Ser Ala Ile Lys Thr Lys Ile Gln Ser Ile Leu Lys His Gln Ala Tyr
385 390 395 400
Tyr Phe Ile Thr Leu Met Asp Glu Thr Pro Tyr Gly Val Leu Asn Gln
405 410 415
Phe Gly Asn Phe Gly Val Asn Glu Pro His Ala Ser Tyr Met Ala Asp
420 425 430
Leu Leu Arg Tyr Tyr Glu Leu Phe Asn Asp Pro Val Ala Leu Arg Ala
435 440 445
Ala Lys Lys Ala Leu Tyr Trp Ile Val Gly Asn Asn Pro Trp Asn Ile
450 455 460
Ser Trp Val Ser Gly Val Gly Ser Asn Phe Thr Asp Phe Leu His Thr
465 470 475 480
Arg Leu Asp Glu Glu Ala Tyr Ser Gln Thr Asn Thr Gly Val Val Leu
485 490 495
Pro Gly Ala Met Val Ser Gly Pro Asn Ile Lys Asp Pro Asn Asn Lys
500 505 510
Leu Ser Ser Ser Pro Trp Tyr Glu Asp Lys Pro Ile Trp Ala Asp Asp
515 520 525
Thr Asn Gln Trp Arg Tyr Asn Glu Tyr Ser Val Ser Ile Gln Thr Gly
530 535 540
Leu Phe Tyr Thr Ile Met Gly Leu Ser Ala Leu Gly Gly Asn Ala Ser
545 550 555 560
Thr Gly Gly Ala Glu Pro Val Lys Leu Pro Ile Thr Trp Pro Ile Ile
565 570 575
Gly Asp Tyr Val Thr Gly Asp Val Thr Val Phe Ala Gln Pro Glu Gly
580 585 590
Ser Leu Ser Asn Val Ser Ala Asn Gly Ile Val Leu Ser Pro Ser Asp
595 600 605
Gly Val Tyr Thr Thr Thr Val Ser Thr Ser Ala Asp Ala Pro Tyr Thr
610 615 620
Glu Arg Lys Val Gln Ile Lys Gly Thr Asp Asp Ser Gly Phe Thr Thr
625 630 635 640
Tyr Ser Asn Thr His Phe Thr Val Ala Pro Ala Leu Pro Asp Pro Ser
645 650 655
His Pro Leu Leu Phe Asp Asp Phe Asn Gln Lys Gly Ile Trp Gly Ser
660 665 670
Gln Lys Leu Asp Trp Val Asn Trp Tyr Asn Gln Asn Gly Gly Thr Ala
675 680 685
Ser Tyr Thr Arg Thr Thr Val Asp Thr Arg Thr Val Gly Lys Phe Ala
690 695 700
His Thr Pro Ala Ala Thr Thr Ser Lys Ala Lys Phe Gln Pro Trp Lys
705 710 715 720
Tyr Asn Ala Asn Leu Asn Gly Tyr Arg Tyr Leu Asn Phe Thr Met Lys
725 730 735
Asn Pro Gly Tyr Pro Asn Thr Lys Ile Arg Ile Ala Ala Asn Asp Gly
740 745 750
Thr Lys Ser Val Asn Leu Thr Ser Gly Glu Val Ala Ile Ser Ser Thr
755 760 765
Trp Thr Thr Tyr Gln Tyr Asp Leu Asn Leu His Pro Thr Leu Asn Lys
770 775 780
Ser Asn Val Leu Ile Glu Val Trp Leu Ser Asn Pro Thr Ala Gly Ala
785 790 795 800
Tyr Gly Glu Ile Leu Ile Asp Glu Ile Ser Ala Val Asn Thr Asn Ser
805 810 815
Gly Thr Ala Pro Thr Leu Ser Ala Thr Gly Val Asn Ala Ser Ile Gly
820 825 830
Asn Gln Ser Thr Val Phe Thr Tyr Thr Ala Thr Tyr Thr Asp Ala Asn
835 840 845
Asn Gln Ala Pro Phe Asp Val Gln Val Val Ile Asp Gly Val Ile Arg
850 855 860
Ser Met Thr Ala Ala Asp Pro Thr Asp Thr Thr Tyr Ser Asp Gly Arg
865 870 875 880
Val Tyr Thr Tyr Ala Thr Thr Leu Pro Val Gly Thr His Lys Phe Tyr
885 890 895
Phe Arg Thr Thr Asp Thr Thr Thr Asn Phe Val Ser Thr Ser Val Gln
900 905 910
Thr Gly Pro Thr Val Ile Arg Asn Lys Leu Glu Ala Glu Val Leu Ser
915 920 925
Ile Asn Leu Thr Asn Tyr Thr His Ala Val Lys Asp Asn Ala Asp Ala
930 935 940
Ser Gly Gly Lys Tyr Arg Leu Phe Asn Gly Arg Gln Ala Asn Asp Tyr
945 950 955 960
Ile Glu Tyr Ala Val Asn Val Pro Lys Ala Gly Thr Tyr Gln Val Ser
965 970 975
Ala Arg Ala Met Arg Leu Ser Asp Asn Gly Ile Tyr Gln Leu Gln Ile
980 985 990
Asn Gly Ser Asn Gln Gly Thr Pro Phe Asp Thr Tyr Gln Ser Ser Gly
995 1000 1005
Lys Tyr Leu Asp Tyr Ala Leu Gly Asn Val Thr Ile Thr Ser Pro
1010 1015 1020
Gly Thr Gln Leu Phe Arg Phe Lys Val Thr Gly Lys Asn Ala Ser
1025 1030 1035
Ser Leu Gly Tyr Lys Leu Pro Leu Asp Phe Ile Gln
1040 1045 1050
<210> 2
<211> 1037
<212> PRT
<213> Paenibacillus sp.
<400> 2
Asp Glu Phe Asp Thr Leu Arg Glu Lys Tyr Lys Ala Met Leu Asn Gly
1 5 10 15
Gly Thr Thr Tyr Asn Leu Ser Asp Pro Asp Ile Ala Ala Arg Val Asn
20 25 30
Ala Ile Thr Val Thr Ala Gln Gly Tyr Trp Asp Ser Met Leu Lys Asp
35 40 45
Pro Asn Arg Asn Arg Leu Trp Asn Asp Ala Pro Phe Gly Ser Asp Ser
50 55 60
Thr Ser Ile Thr Thr Thr Tyr Arg His Leu Tyr Asp Met Ala Leu Ala
65 70 75 80
Tyr Thr Thr Tyr Gly Ser Ser Leu Gln Gly Asn Ala Ala Leu Lys Ala
85 90 95
Asp Ile Ile Ser Gly Leu Asp Trp Met Asn Ala Asn Gln Phe Tyr Asn
100 105 110
Gly Cys Ser Gln Tyr Gln Asn Trp Trp His Trp Gln Ile Gly Gly Pro
115 120 125
Met Ala Leu Asn Asp Ile Val Ala Leu Met Tyr Thr Glu Leu Thr Ala
130 135 140
Thr Gln Ile Ser Asn Tyr Met Ala Ala Ile Tyr Tyr Thr Gln Ala Ser
145 150 155 160
Val Thr Met Thr Gly Ala Asn Arg Leu Trp Glu Ser Gln Val Ile Ala
165 170 175
Ile Ser Gly Ile Leu Asn Lys Asp Ser Ala Arg Val Ala Ala Gly Arg
180 185 190
Asp Gly Ile Ser Ala Leu Leu Pro Tyr Val Ala Lys Gly Asp Gly Phe
195 200 205
Tyr Asn Asp Gly Ser Phe Val Gln His Thr Tyr Tyr Ala Tyr Asn Gly
210 215 220
Gly Tyr Gly Ser Glu Leu Leu Ser Gly Ile Ala Asp Leu Ile Phe Ile
225 230 235 240
Leu Asn Gly Ser Ser Trp Gln Val Thr Asp Pro Asn Lys Asn Asn Val
245 250 255
Tyr Arg Trp Ile Tyr Asp Ser Tyr Glu Pro Phe Ile Tyr Lys Gly Asn
260 265 270
Leu Met Asp Met Val Arg Gly Arg Glu Ile Ser Arg His Gly Leu Gln
275 280 285
Asp Asp Lys Ala Ala Val Thr Val Met Ala Ser Ile Ile Arg Leu Ser
290 295 300
Gln Thr Ala Ala Ser Ala Asp Ala Thr Ala Phe Lys Arg Met Val Lys
305 310 315 320
Tyr Trp Leu Leu Leu Asp Thr Asp Lys Thr Phe Leu Lys Ala Val Ser
325 330 335
Ile Asp Leu Ile Ile Ala Ala Asn Gln Leu Val Asn Asp Ser Thr Val
340 345 350
Thr Ser Arg Gly Glu Leu Val Lys Tyr Lys Gln Phe Ser Gly Met Asp
355 360 365
Arg Ala Val Gln Leu Arg Pro Gly Phe Gly Phe Gly Leu Ser Met Phe
370 375 380
Ser Ser Arg Ile Gly Asn Tyr Glu Ser Ile Asn Ala Glu Asn Asn Lys
385 390 395 400
Gly Trp His Thr Gly Asp Gly Met Thr Tyr Leu Tyr Asn Thr Asp Leu
405 410 415
Ser Gln Phe Asn Asp His Phe Trp Ala Thr Val Asp Asn Tyr Arg Leu
420 425 430
Pro Gly Thr Thr Val Leu Gln Asn Thr Thr Gln Thr Ala Asn Ser Arg
435 440 445
Ser Asp Lys Ser Trp Ala Gly Gly Thr Asp Ile Leu Gly Gln Tyr Gly
450 455 460
Val Ser Gly Met Glu Leu His Thr Val Gly Lys Ser Leu Thr Ala Lys
465 470 475 480
Lys Ser Trp Phe Met Phe Asp Asp Glu Ile Val Ala Leu Gly Ser Gly
485 490 495
Ile Ala Ser Thr Asp Gly Ile Ala Thr Glu Thr Ile Val Glu Asn Arg
500 505 510
Lys Leu Asn Ser Ser Gly Asn Asn Ala Leu Ile Val Asn Gly Thr Ala
515 520 525
Lys Pro Gly Ser Leu Gly Trp Ser Glu Thr Met Thr Gly Thr Asn Tyr
530 535 540
Ile His Leu Ala Gly Ser Val Pro Gly Ser Asp Ile Gly Tyr Tyr Phe
545 550 555 560
Pro Gly Gly Ala Ala Val Lys Gly Leu Arg Glu Ala Arg Ser Gly Ser
565 570 575
Trp Ser Ser Leu Asn Ser Ser Ala Ser Trp Lys Asp Ser Thr Leu His
580 585 590
Thr Arg Asn Phe Met Thr Leu Trp Phe Asp His Gly Met Asn Pro Thr
595 600 605
Asn Gly Ser Tyr Ser Tyr Val Leu Leu Pro Asn Lys Thr Ser Ser Ala
610 615 620
Val Ala Ser Tyr Ala Ala Thr Pro Gln Ile Ser Ile Leu Glu Asn Ser
625 630 635 640
Ser Ser Ala Gln Ala Val Lys Glu Thr Gln Leu Asn Val Thr Gly Ile
645 650 655
Asn Phe Trp Asn Asp Glu Pro Thr Thr Val Gly Leu Val Thr Ser Asn
660 665 670
Arg Lys Ala Ser Val Met Thr Lys Glu Thr Ala Ser Asp Phe Glu Ile
675 680 685
Ser Val Ser Asp Pro Thr Gln Ser Asn Val Gly Thr Ile Tyr Ile Asp
690 695 700
Val Asn Lys Ser Ala Thr Gly Leu Ile Ser Lys Asp Asn Glu Ile Thr
705 710 715 720
Val Ile Gln Tyr Tyr Pro Thr Met Lys Phe Lys Val Asn Val Asn Asn
725 730 735
Ser Gly Gly Lys Ser Tyr Lys Val Lys Phe Ser Leu Thr Gly Thr Pro
740 745 750
Gly Ser Asn Pro Ser Pro Ile Pro Ile Pro Asn Pro Tyr Glu Ala Glu
755 760 765
Ala Leu Pro Ile Asn Ala Leu Thr Asp Thr Pro Val Val Tyr Asn Asp
770 775 780
Ala Asn Ala Ser Gly Gly Lys Lys Leu Gly Phe Asn Asn Asn Ala Val
785 790 795 800
Asp Asp Tyr Val Glu Phe Ser Leu Asp Val Thr Gln Pro Gly Thr Tyr
805 810 815
Asp Val Lys Ser Arg Ile Met Lys Ser Thr Asn Ser Gly Ile Tyr Gln
820 825 830
Leu Ser Ile Asn Gly Thr Asn Val Gly Ser Ala Gln Asp Met Phe Trp
835 840 845
Thr Thr Ser Glu Leu Ser Lys Glu Phe Thr Met Gly Ser Tyr Ser Phe
850 855 860
Ser Thr Pro Gly Ser Tyr Leu Phe Arg Leu Lys Thr Thr Gly Lys Asn
865 870 875 880
Val Ser Ser Ser Gly Tyr Lys Leu Met Leu Asp Asn Phe Ser Leu Val
885 890 895
Ser Thr Gly Ile Asp Thr Thr Val Ile Val Asp Asn Ala Asp Ala Ala
900 905 910
Gly Val Thr Lys Val Gly Thr Trp Thr Gly Thr Asn Thr Gln Thr Asp
915 920 925
Arg Tyr Gly Ala Asp Tyr Ile His Asp Gly Asn Thr Gly Lys Gly Thr
930 935 940
Lys Ser Val Thr Phe Thr Pro Asn Val Pro Ile Ser Gly Thr Tyr Gln
945 950 955 960
Val Tyr Met Met Trp Ala Ala His Thr Asn Arg Ala Thr Asn Val Pro
965 970 975
Val Asp Val Thr His Ser Gly Gly Thr Ala Thr Leu Asn Val Asn Gln
980 985 990
Gln Gly Asn Gly Gly Val Trp Asn Leu Leu Gly Thr Tyr Ser Phe Asn
995 1000 1005
Ala Gly Ser Thr Gly Ala Ile Lys Ile Arg Thr Asp Ala Thr Asn
1010 1015 1020
Gly Tyr Val Val Ala Asp Ala Val Lys Leu Val Lys Val Pro
1025 1030 1035
<210> 3
<211> 490
<212> PRT
<213> Bacillus hemicellulosilyticus
<400> 3
Met Arg Asn Phe Gly Lys Leu Ile Val Ser Ser Cys Leu Leu Phe Ser
1 5 10 15
Phe Phe Leu Phe Ala Ser Asp Gly His Ser Gln Thr His Ser Gly Phe
20 25 30
Tyr Ile Glu Gly Ser Thr Leu Tyr Asp Ala Asn Gly Glu Pro Phe Val
35 40 45
Met Arg Gly Ile Asn His Gly His Ala Trp Tyr Lys His Asp Ser Asn
50 55 60
Val Ala Ile Pro Ala Ile Ala Asn Gln Gly Ala Asn Thr Ile Arg Ile
65 70 75 80
Val Leu Ser Asp Gly Gly Gln Trp Ala Lys Asp Asp Ile Asn Thr Leu
85 90 95
Asn Gln Val Leu Asp Leu Ala Glu Glu His Glu Met Ile Ala Val Val
100 105 110
Glu Val His Asp Ala Thr Gly Ser Asn Ser Met Ala Asp Leu Asn Arg
115 120 125
Ala Val Asp Tyr Trp Ile Glu Met Lys Asp Ala Leu Ile Gly Lys Glu
130 135 140
Asp Arg Val Ile Ile Asn Ile Ala Asn Glu Trp Tyr Gly Ala Trp Asp
145 150 155 160
Gly Gln Gly Trp Ala Asn Gly Tyr Lys Glu Val Ile Pro Arg Leu Arg
165 170 175
Asn Ala Gly Phe Thr His Thr Leu Met Val Asp Ala Ala Gly Trp Gly
180 185 190
Gln Tyr Pro Gln Ser Ile His Asp Tyr Gly Gln Glu Val Phe Asn Ala
195 200 205
Asp Pro Leu Ala Asn Thr Met Phe Ser Ile His Met Tyr Glu Tyr Ala
210 215 220
Gly Gly Asn Ala Ser Met Val Gln Ser Asn Ile Asp Gly Val Val Asp
225 230 235 240
Gln Gly Leu Ala Leu Val Ile Gly Glu Phe Gly His Met His Thr Asp
245 250 255
Gly Asp Val Asp Glu Ala Thr Ile Leu Ser Tyr Ser Gln Gln Arg Gly
260 265 270
Val Gly Trp Leu Ala Trp Ser Trp Lys Gly Asn Gly Thr Gln Trp Glu
275 280 285
Tyr Leu Asp Leu Ser Tyr Asp Trp Gln Gly Thr Asn Leu Thr Ser Trp
290 295 300
Gly Asn Thr Ile Val His Gly Pro Asn Gly Leu Leu Glu Thr Ser Ile
305 310 315 320
Pro Ser Ser Ile Phe His Thr Ala Pro Asn Asn Gly Asp Pro Pro Pro
325 330 335
His Asn Gly Asn Glu Thr Ile Leu Tyr Asp Phe Glu His Gly Thr Gln
340 345 350
Gly Trp Ser Gly Ser Ser Leu Leu Gly Gly Pro Trp Thr Thr Asn Glu
355 360 365
Trp Ser Thr Asn Gly Asn His Ser Leu Lys Ala Asp Ile Phe Leu Ser
370 375 380
Ala Asn Ser Lys His Glu Leu Ala Lys Val Glu Asn Arg Asn Leu Ser
385 390 395 400
Gly Tyr Ser Thr Leu Gln Ala Thr Val Arg His Ala His Trp Gly Asn
405 410 415
Val Gly Asn Leu Thr Ala Arg Met Tyr Val Lys Thr Gly Ser Asn Tyr
420 425 430
Ser Trp Phe Asn Gly Asp Pro Ile Pro Val Asn Ser Ala Asn Gly Thr
435 440 445
Thr Val Thr Leu Pro Leu Ser Ser Ile Pro Asn Leu Asn Asp Val Lys
450 455 460
Glu Ile Gly Val Glu Phe Ile Gly Ala Ser Asn Ser Asn Gly Gln Thr
465 470 475 480
Ala Ile Tyr Leu Asp His Val Thr Ile Gln
485 490
<210> 4
<211> 297
<212> PRT
<213> Paenibacillus sp.
<400> 4
Met Ala Thr Gly Phe Tyr Val Ser Gly Asn Lys Leu Tyr Asp Ser Thr
1 5 10 15
Gly Lys Pro Phe Val Met Arg Gly Val Asn His Gly His Ser Trp Phe
20 25 30
Lys Asn Asp Leu Asn Thr Ala Ile Pro Ala Ile Ala Lys Thr Gly Ala
35 40 45
Asn Thr Val Arg Ile Val Leu Ser Asn Gly Ser Leu Tyr Thr Lys Asp
50 55 60
Asp Leu Asn Ala Val Lys Asn Ile Ile Asn Val Val Asn Gln Asn Lys
65 70 75 80
Met Ile Ala Val Leu Glu Val His Asp Ala Thr Gly Lys Asp Asp Tyr
85 90 95
Asn Ser Leu Asp Ala Ala Val Asn Tyr Trp Ile Ser Ile Lys Glu Ala
100 105 110
Leu Ile Gly Lys Glu Asp Arg Val Ile Val Asn Ile Ala Asn Glu Trp
115 120 125
Tyr Gly Thr Trp Asn Gly Ser Ala Trp Ala Asp Gly Tyr Lys Lys Ala
130 135 140
Ile Pro Lys Leu Arg Asn Ala Gly Ile Lys Asn Thr Leu Ile Val Asp
145 150 155 160
Ala Ala Gly Trp Gly Gln Phe Pro Gln Ser Ile Val Asp Tyr Gly Gln
165 170 175
Ser Val Phe Ala Ala Asp Ser Gln Lys Asn Thr Val Phe Ser Ile His
180 185 190
Met Tyr Glu Tyr Ala Gly Lys Asp Ala Ala Thr Val Lys Ala Asn Met
195 200 205
Glu Asn Val Leu Asn Lys Gly Leu Ala Leu Ile Ile Gly Glu Phe Gly
210 215 220
Gly Tyr His Thr Asn Gly Asp Val Asp Glu Tyr Ala Ile Met Arg Tyr
225 230 235 240
Gly Gln Glu Lys Gly Val Gly Trp Leu Ala Trp Ser Trp Tyr Gly Asn
245 250 255
Ser Ser Gly Leu Asn Tyr Leu Asp Met Ala Thr Gly Pro Asn Gly Ser
260 265 270
Leu Thr Ser Phe Gly Asn Thr Val Val Asn Asp Thr Tyr Gly Ile Lys
275 280 285
Asn Thr Ser Gln Lys Ala Gly Ile Phe
290 295
<210> 5
<211> 269
<212> PRT
<213> Thermomyces lanuginosus
<400> 5
Glu Val Ser Gln Asp Leu Phe Asn Gln Phe Asn Leu Phe Ala Gln Tyr
1 5 10 15
Ser Ala Ala Ala Tyr Cys Gly Lys Asn Asn Asp Ala Pro Ala Gly Thr
20 25 30
Asn Ile Thr Cys Thr Gly Asn Ala Cys Pro Glu Val Glu Lys Ala Asp
35 40 45
Ala Thr Phe Leu Tyr Ser Phe Glu Asp Ser Gly Val Gly Asp Val Thr
50 55 60
Gly Phe Leu Ala Leu Asp Asn Thr Asn Lys Leu Ile Val Leu Ser Phe
65 70 75 80
Arg Gly Ser Arg Ser Ile Glu Asn Trp Ile Gly Asn Leu Asn Phe Asp
85 90 95
Leu Lys Glu Ile Asn Asp Ile Cys Ser Gly Cys Arg Gly His Asp Gly
100 105 110
Phe Thr Ser Ser Trp Arg Ser Val Ala Asp Thr Leu Arg Gln Lys Val
115 120 125
Glu Asp Ala Val Arg Glu His Pro Asp Tyr Arg Val Val Phe Thr Gly
130 135 140
His Ser Leu Gly Gly Ala Leu Ala Thr Val Ala Gly Ala Asp Leu Arg
145 150 155 160
Gly Asn Gly Tyr Asp Ile Asp Val Phe Ser Tyr Gly Ala Pro Arg Val
165 170 175
Gly Asn Arg Ala Phe Ala Glu Phe Leu Thr Val Gln Thr Gly Gly Thr
180 185 190
Leu Tyr Arg Ile Thr His Thr Asn Asp Ile Val Pro Arg Leu Pro Pro
195 200 205
Arg Glu Phe Gly Tyr Ser His Ser Ser Pro Glu Tyr Trp Ile Lys Ser
210 215 220
Gly Thr Leu Val Pro Val Thr Arg Asn Asp Ile Val Lys Ile Glu Gly
225 230 235 240
Ile Asp Ala Thr Gly Gly Asn Asn Gln Pro Asn Ile Pro Asp Ile Pro
245 250 255
Ala His Leu Trp Tyr Phe Gly Leu Ile Gly Thr Cys Leu
260 265
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ МОЮЩЕГО СРЕДСТВА ДЛЯ СТИРКИ | 2017 |
|
RU2716130C1 |
| КОМПОЗИЦИЯ МОЮЩЕГО СРЕДСТВА ДЛЯ СТИРКИ | 2017 |
|
RU2719358C1 |
| КОМПОЗИЦИЯ МОЮЩЕГО СРЕДСТВА ДЛЯ СТИРКИ С НИЗКИМ ПОКАЗАТЕЛЕМ PH | 2017 |
|
RU2715886C1 |
| КОМПОЗИЦИЯ МОЮЩЕГО СРЕДСТВА ДЛЯ СТИРКИ С НИЗКИМ ПОКАЗАТЕЛЕМ PH | 2017 |
|
RU2719356C1 |
| КОМПОЗИЦИЯ МОЮЩЕГО СРЕДСТВА ДЛЯ СТИРКИ С НИЗКИМ ПОКАЗАТЕЛЕМ PH | 2017 |
|
RU2716255C1 |
| ВАРИАНТЫ ПРОТЕАЗ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2790443C2 |
| ВАРИАНТЫ ПРОТЕАЗЫ КЛАДЫ APRL И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2733987C2 |
| СПОСОБЫ УЛУЧШЕНИЯ ЗДОРОВЬЯ РАСТЕНИЯ С ПРИМЕНЕНИЕМ СВОБОДНЫХ ФЕРМЕНТОВ И МИКРООРГАНИЗМОВ, ЭКСПРЕССИРУЮЩИХ ФЕРМЕНТЫ НА ПОВЫШЕННОМ УРОВНЕ | 2017 |
|
RU2802848C2 |
| Слитые молекулы, происходящие от Cholix-токсина, для пероральной доставки биологически активных нагрузок | 2015 |
|
RU2723178C2 |
| Композиции для получения глюкозных сиропов | 2015 |
|
RU2706297C2 |
Изобретение относится к моющим композициям для стирки. Описана моющая композиция для стирки, содержащая: a) моющее поверхностно-активное вещество, содержащее комбинацию анионного и неионного поверхностно-активных веществ, где анионное поверхностно-активное вещество выбрано из линейного алкилбензолсульфоната и алкилалкоксилированного сульфата, а неионное поверхностно-активное вещество выбрано из группы, состоящей из алкилэтоксилатов С12-С18, алкилфенолалкоксилатов С6-С12, блок алкиленоксидного конденсата алкилфенолов С6-С12, алкиленоксидных конденсатов алканолов С8-С22, блок-полимеров этиленоксида/пропиленоксида, полуполярных неионных веществ, алкилполисахаридов, алкильных полиглюкозидных поверхностно-активных веществ, неионных поверхностно-активных веществ формулы R1(ОС2Н4)nOH, где R1 представляет собой С10-С16 алкильную группу или С8-С12 алкилфенильную группу и n составляет от предпочтительно 3 до 80, продуктов конденсации спиртов С12-С15 с от 5 до 20 моль этиленоксида на моль спирта; при этом концентрация моющего поверхностно-активного вещества в композиции для стирки составляет от 1 до 70 мас.%; b) ферментную систему, содержащую: i) ксантанэндоглюканазу, причем указанная ксантанэндоглюканаза содержит полипептид с последовательностью, по меньшей мере на 85% идентичной SEQ ID NO: 1; ii) ксантанлиазу, причем указанная ксантанлиаза содержит полипептид с последовательностью, по меньшей мере на 85% идентичной SEQ ID NO: 2, и iii) маннаназу, причем указанная маннаназа выбрана из группы, состоящей из: а) маннаназы, обладающей маннаназной активностью и содержащей полипептид с последовательностью, по меньшей мере на 85% идентичной остаткам 27-331, представленным в SEQ ID NO: 3, SEQ ID NO: 3 соответствует полноразмерной аминокислотной последовательности маннаназы Man7, эндогенной по отношению к Bacillus hemicellulosilyticus, включая сигнальную последовательность; b) маннаназы, обладающей маннаназной активностью и содержащей полипептид с по меньшей мере 85% идентичностью с SEQ ID NO: 4, SEQ ID NO: 4 соответствует полноразмерной аминокислотной последовательности маннаназы Man4, эндогенной по отношению к Paenibacillus sp; c) и их смесей. Технический результат - ферментная система обладает большей способностью к разрушению гелевых структур, а также достигается уменьшение повторного осаждения загрязнений. 2 н. и 18 з.п. ф-лы.
1. Моющая композиция для стирки, содержащая:
a) моющее поверхностно-активное вещество, содержащее комбинацию анионного и неионного поверхностно-активных веществ,
где анионное поверхностно-активное вещество выбрано из линейного алкилбензолсульфоната и алкилалкоксилированного сульфата, а неионное поверхностно-активное вещество выбрано из группы, состоящей из алкилэтоксилатов С12-С18, алкилфенолалкоксилатов С6-С12, блок алкиленоксидного конденсата алкилфенолов С6-С12, алкиленоксидных конденсатов алканолов С8-С22, блок-полимеров этиленоксида/пропиленоксида, полуполярных неионных веществ, алкилполисахаридов, алкильных полиглюкозидных поверхностно-активных веществ, неионных поверхностно-активных веществ формулы R1(ОС2Н4)nOH, где R1 представляет собой С10-С16 алкильную группу или С8-С12 алкилфенильную группу и n составляет от предпочтительно 3 до 80, продуктов конденсации спиртов С12-С15 с от 5 до 20 моль этиленоксида на моль спирта;
при этом концентрация моющего поверхностно-активного вещества в композиции для стирки составляет от 1 до 70 мас.%;
b) ферментную систему, содержащую:
i) ксантанэндоглюканазу, причем указанная ксантанэндоглюканаза содержит полипептид с последовательностью, по меньшей мере на 85% идентичной SEQ ID NO: 1;
ii) ксантанлиазу, причем указанная ксантанлиаза содержит полипептид с последовательностью, по меньшей мере на 85% идентичной SEQ ID NO: 2, и
iii) маннаназу, причем указанная маннаназа выбрана из группы, состоящей из:
а) маннаназы, обладающей маннаназной активностью и содержащей полипептид с последовательностью, по меньшей мере на 85% идентичной остаткам 27-331, представленным в SEQ ID NO: 3, SEQ ID NO: 3 соответствует полноразмерной аминокислотной последовательности маннаназы Man7, эндогенной по отношению к Bacillus hemicellulosilyticus, включая сигнальную последовательность;
b) маннаназы, обладающей маннаназной активностью и содержащей полипептид с по меньшей мере 85% идентичностью с SEQ ID NO: 4, SEQ ID NO: 4 соответствует полноразмерной аминокислотной последовательности маннаназы Man4, эндогенной по отношению к Paenibacillus sp;
c) и их смесей.
2. Моющая композиция для стирки по п. 1, в которой моющее поверхностно-активное вещество выбрано из группы, состоящей из: неионного поверхностно-активного вещества, анионного поверхностно-активного вещества, амфотерного поверхностно-активного вещества и их смесей.
3. Моющая композиция для стирки по п. 2, в которой моющее поверхностно-активное вещество содержит анионное поверхностно-активное вещество, причем анионное поверхностно-активное вещество содержит линейный алкилбензолсульфонат и алкилалкоксилированный сульфат, а соотношение поверхностно-активного вещества с линейным алкилбензолсульфонатом и поверхностно-активного вещества с алкилалкоксилированным сульфатом составляет от 0,1 до 5, предпочтительно от 0,25 до 3, более предпочтительно от 0,6 до 1,1.
4. Моющая композиция для стирки по любому из предшествующих пунктов, в которой концентрация моющего поверхностно-активного вещества в композиции для стирки составляет от 10 до 50 мас.%, предпочтительно от 15 до 35 мас.%.
5. Моющая композиция для стирки по любому из предшествующих пунктов, в которой ксантанэндоглюканаза представляет собой вариант с по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности, представленной SEQ ID NO: 1.
6. Моющая композиция для стирки по любому из предшествующих пунктов, в которой ксантанэндоглюканаза имеет заместители в одной или более из позиций 17, 20, 51, 53, 55, 56, 60, 63, 79, 87, 186, 192, 302, 311, 313, 387, 388, 390, 403, 408, 410, 416, 448, 451, 471, 472, 476, 489, 507, 512, 515, 538, 598, 599, 602, 605, 609, 676, 688, 690, 694, 697, 698, 699, 711, 719, 754, 756, 760, 781, 786, 797, 833, 834, 835 и 1048, представленных в SEQ ID NO: 1.
7. Моющая композиция для стирки по любому из предшествующих пунктов, в которой ксантанэндоглюканаза имеет заместители в одной или более из позиций S17A, F20P, F20N, F20G, F20Y, K51Q, K51H, Е53Р, E53G, Y55M, V56M, Y60F, S63F, T87R, А186Р, K192N, I320D, I302H, I302V, I302M, H311N, S313D, I387T, K388R, K390Q, 1403Y, E408D, E408S, Е408Р, Е408А, E408G, E408N, P410G, Q416S, Q416D, А448Е, A448W, A448S, K451S, G471S, S472Y, D476R, Q489P, K507R, К512Р, S515V, S538C, Y579W, S598Q, A599S, I602T, I602D, V603P, S605T, G609E, D676H, A688G, Y690F, Т694А, T697G, R698W, Т699А, T711V, T711Y, W719R, K754R, V756H, V756Y, S760G, Т781М, N786K, T797S, A824D, N833D, Q834E, S835D и F1048W.
8. Моющая композиция для стирки по любому из предшествующих пунктов, в которой ксантанлиаза представляет собой вариант с по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% идентичностью последовательности, представленной в SEQ ID NO: 2.
9. Моющая композиция для стирки по любому из предшествующих пунктов, в которой ксантанлиаза представляет собой вариант с изменениями в одной или более из позиций, выбранных из группы, состоящей из позиций: 9, 15, 46, 58, 66, 89, 95, 100, 106, 109, 183, 188, 190, 203, 204, 221, 229, 234, 238, 240, 242, 243, 257, 258, 291, 293, 316, 320, 324, 329, 333, 339, 341, 352, 354, 360, 377, 399, 400, 419, 440, 450, 451, 454, 458, 481, 492, 567, 568, 578, 579, 582, 664, 672, 703, 728, 843, 855, 887, 892, 1008 и 1016, представленных в SEQ ID NO: 2.
10. Моющая композиция для стирки по любому из предшествующих пунктов, в которой ксантанлиаза представляет собой вариант с изменениями в одной или более из позиций, выбранных из группы, состоящей из позиций 624, 631, 635, 649, 656, 752, 754, 757, 769, 775, 777, 800, 801, 875, 911 и 915, представленных в SEQ ID NO: 2.
11. Моющая композиция для стирки по любому из предшествующих пунктов, в которой маннаназа имеет последовательность, по меньшей мере на 90% идентичную остаткам 27-331, представленным в SEQ ID NO: 3.
12. Моющая композиция для стирки по любому из предшествующих пунктов, в которой маннаназа представляет собой вариант SEQ ID NO: 3, содержащий по меньшей мере один заместитель в позициях 123, 158, 180, 272, 285 или 307 или их комбинацию.
13. Моющая композиция для стирки по любому из предшествующих пунктов, в которой маннаназа представляет собой вариант SEQ ID NO: 3, содержащий по меньшей мере один заместитель в позициях М123, А158, F180, G272, Т285 или Т307 или их комбинацию.
14. Моющая композиция для стирки по любому из предшествующих пунктов, в которой маннаназа содержит полипептид с последовательностью, по меньшей мере на 85% идентичной остаткам 27 - 331, представленным в SEQ ID NO: 3, и/или по меньшей мере на 85% идентичной последовательности SEQ ID NO: 4.
15. Моющая композиция для стирки по п. 14, в которой маннаназа представляет собой вариант SEQ ID NO: 3, содержащий по меньшей мере один заместитель в позициях М123, А158, F180, G272, Т307 или L316 или их комбинацию.
16. Моющая композиция для стирки по п. 14, в которой маннаназа содержит по меньшей мере одну, две, три, четыре, пять, шесть, семь или более вариаций по сравнению с SEQ ID NO: 4, выбранных из:
(a) N10Q/T, P19E/V, S30T, T38E/I/L/M/Q/R/V, S59D/G/K/N/Q/T, L60F/M/V, T62E/I/Q/V, K63L, L66C/T/V, N67A/D/E/G/P/Q/S/V, A68L/M/R/S/W, K70R/V, N71D/H, N74E/C/Q/V, V75I, Q78A/D/L/M, N79E/F/W, K80Q/T, N97E/L/P/Q, V103I, Y129M, Т131Р, S135A/C/Q, А136Е, K143Q/R, F167L/S/W/Y, P168A/E/G/L/M/S/T, Q184D/F/H/L/M/P, N213E, K214C/Q, G225A/C/P/W, T228A/G/H/I/K/S/V/Y, Y235G/I/L/Q/S/V, Q242S/E, K244A/C/G/L/M/P/S, S258A/D/E/G/M/N/P/T, G259A/E/R/S/W, N261I/M/P/Q/R/S/T/V/W/Y и D283G/H/T; или
(b) P19E/V, T38E/I/L/M/Q/R/V, N67A/D/E/G/P/Q/S/V, N97E/L/P/Q, Y129M, K143Q/R, P168A/E/G/L/M/S/T, Q184D/F/H/L/M/P, G225A/C/P/W, T228A/G/H/I/K/S/V/Y, Y235G/I/L/Q/S/V, K244A/C/G/L/M/P/S, S258A/D/E/G/M/N/P/T и N261I/M/P/Q/R/S/T/V/W/Y; или
(c) P19E/V, T38E/I/L/M/Q/R/V, N67A/D/E/G/P/Q/S/V, L85L, Y129M, P168A/E/G/L/M/S/T, Q184D/F/H/L/M/P, G225A/C/P/W, K244A/C/G/L/M/P/S, S258A/D/E/G/M/N/P/T и N261I/M/P/Q/R/S/T/V/W/Y; или
(d) Р19Е, S30T, Т38Е, S59V, L60Q, K63R, N67D, N97D, V103I, Y129M, F167Y, P168S, Q184L, G225C, T228V, Y235L, K244L, S258D и N261R.
17. Моющая композиция для стирки по п. 14, в которой маннаназа представляет собой вариант SEQ ID NO: 4, содержащий ряд вариаций SEQ ID NO: 4, выбранных из: P19E-T38E-N67D-N97D-Y129M-P168S-Q184L-K244L-S258D-N261R; N10T-P19E-G28S-S30T-T38E-N67D-N71D-N97D-Y129M-P168S-Q184L-G225C-Y235L-K244L-S258D-N261R-F297FQ; P19E-S30T-T38E-S59V-L60Q-K63R-N67D-N97D-V1031-Y129M-F167Y-Q184L-G225C-T228V-Y235L-K244L-S258D-N261R-F297FQ; N10T-P19E-S30T-T38E-S59V-L60Q-K63R-N67D-N97D-Y129M-K143Q-P168S-Q184L-G225C-T228V-Y235L-K244L-S258D-N261R-F297FQ; N10T-P19E-S30T-T38E-S59V-L60Q-K63R-N67D-N97D-Y129M-K143Q-P168S-Q184L-G225P-T228V-Y235L-K244L-S258D-N261R-F297FQ; N10T-Р19Е-S30T-T38E-S59V-L60Q-K63R-N67D-N71D-N97D-V103I-Y129M-K143Q-P168S-Q184L-G225P-T228V-Y235L-K244L-S258D-N261R-F297FQ; A2S-P19E-G28S-S30T-T38E-K63R-N67D-N71D-N74E-K93R-N97D-Y129M-N150T-P168S-Q184L-N213A-G225C-Y235L-K244L-S258D-N261Q-F297FQ; T3R-N10T-P19E-G28A-S30T-T38E-T62E-N67D-N71D-K93R-N97L-E111S-Y129M-D139M-P168S-Q184L-G225C-Y235L-K244L-S258D-N261Q-F297FQ и N10T-P19E-G28A-S30T-T38E-S59D-N67D-A68S-N71D-K93R-N97D-Y129M-K143Q-P168S-Q184D-G225C-Y235L-K244L-S258D-N261R-T284E-F297FQ.
18. Моющая композиция для стирки по любому из предшествующих пунктов, в которой ферментная система композиции дополнительно содержит липазу, предпочтительно вариант липазы, представленный в SEQ ID NO: 5, содержащий:
(a) заместитель T231R;
(b) заместитель N233R или N233C; и
(c) по меньшей мере три дополнительных заместителя, выбранных из E1C, D27R, N33Q, G38A, F51V, G91Q, D96E, K98L, K98I, D111A, G163K, H198S, E210Q, Y220F, D254S, I255A и Р256Т;
где позиции соответствуют позициям в SEQ ID NO: 5, и при этом вариант липазы имеет последовательность, по меньшей мере на 90%, но менее чем на 100% идентичную полипептиду, имеющему аминокислотную последовательность SEQ ID NO: 5, и при этом вариант обладает липазной активностью.
19. Моющая композиция для стирки по любому из предшествующих пунктов, в которой композиция дополнительно содержит очищающий полимер, причем предпочтительно очищающий полимер получают путем свободнорадикальной сополимеризации по меньшей мере одного соединения формулы (I),

в которой n больше или равно 3, причем в это число входит по меньшей мере одно соединение формулы (II),
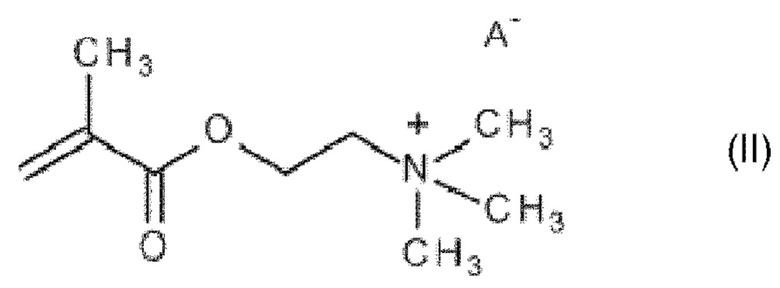
в которой А- представляет анион, в частности выбранный из галогенидов, таких как фторид, хлорид, бромид, йодид, сульфата, гидросульфата, алкилсульфата, такого как метилсульфат, и их смесей.
20. Способ стирки ткани, содержащей пятно, причем пятно содержит комбинацию маннан и других полисахаридов, включающий в себя стадии, на которых:
a) обеспечивают моющую композицию для стирки по любому из пп. 1-19;
b) разбавляют моющую композицию для стирки с обеспечением промывочной жидкости с суммарной концентрацией поверхностно-активного вещества более 300 м. д.; и
c) стирают ткань в промывочной жидкости.
| WO 2017021515 A1, 09.02.2017 | |||
| WO 2019028059 A1, 28.02.2019 | |||
| Трансмиттер к буквопечатающему телефонному аппарату с многозначным кодом | 1934 |
|
SU42146A1 |
| КОМПОЗИЦИЯ ДЛЯ СТИРКИ | 2007 |
|
RU2415908C2 |
| МОЮЩАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ВАРИАНТ КСИЛОГЛЮКАНАЗЫ СЕМЕЙСТВА 44 | 2009 |
|
RU2525669C2 |
| WO 200042157 A1, 20.07.2000. | |||
Авторы
Даты
2022-09-28—Публикация
2020-03-25—Подача