ОБЛАСТЬ ТЕХНИКИ
[0001]
Настоящее изобретение относится к гетероциклическому соединению, обладающему ингибирующим действием на моноацилглицеринлипазу (иногда обозначаемую как «MAGL» в настоящем описании), лекарственному средству, содержащему его, и тому подобному.
[0002]
(Уровень техники)
Сообщалось, что арахидоновая кислота (иногда обозначаемая в настоящем описании как «АА») и ее in vivo продукт, эйкозаноид, вызывают воспаление в центральной и периферической нервной системе [непатентный документ 1: Science, vol. 294, pages 1871-1875, 2001]. Ингибитор, который подавляет путь продуцирования арахидоновой кислоты и путь продуцирования эйкозаноидов, является перспективным в качестве терапевтического лекарственного средства при воспалительных заболеваниях, и нестероидные противовоспалительные лекарственные средства, такие как ингибитор циклооксигеназы и тому подобное, используются в качестве терапевтических лекарственных средств для воспалительной боли. Однако, когда ингибитор циклооксигеназы используется в течение длительного времени, расстройства пищеварительного тракта иногда развиваются как побочные эффекты, что создает проблему. Кроме того, проблемы с кровообращением, такие как инфаркт миокарда, церебральный инфаркт и тому подобное, также создают проблемы в последние годы.
[0003]
Предполагается, что воспаление мозга, сопровождаемое активацией глиальных клеток, является патологическим изменением, характерным для нейродегенеративных заболеваний (например, болезнь Альцгеймера и т. д.) [непатентный документ 2: Molecular Neurobiology (Mol. Neurobiol), vol. 41, pages 115-128, 2010]. Сообщалось, что противовоспалительные препараты подавляют активацию глиальных клеток и подавляют нейродегенеративное прогрессирование на животной модели сверхэкспрессии тау-белка (человеческий вариант тау-трансгенной мыши и т. д.), которая является патологической характеристикой болезни Альцгеймера [непатентный документ 3: Neuron, vol. 53, pages 337-351, 2007]. Кроме того, была предложена эффективность подавления воспаления головного мозга для лечения нейродегенеративных заболеваний, таких как болезнь Альцгеймера и тому подобное [непатентный документ 4: Nature Reviews Neurology (Nat. Rev. Neurol.), vol. 6, pages 193-201, 2010], и терапевтический препарат, который подавляет воспаление мозга, перспективен в качестве терапевтического или профилактического препарата при нейродегенеративных заболеваниях.
[0004]
Моноацилглицеринлипаза (MAGL) представляет собой фермент, который гидролизует моноацилглицерин в жирную кислоту и глицерин. В центральной нервной системе субстратом MAGL является 2-арахидоноилглицерин (также называемый 2-AG в настоящем описании), который разлагается на арахидоновую кислоту и глицерин [непатентный документ 5: Chemistry and Physics of Lipids (Chem phys Lipids) vol. 121, pages 149-158, 2002]. В последние годы подавление выработки арахидоновой кислоты и эйкозаноидов, подавление активации глиальных клеток, подавление продуцирования воспалительных цитокинов и уменьшение действия на накопление бляшек Aβ, что является патологическим диагнозом болезни Альцгеймера, были зарегистрированы в кроссбредном животном с дефицитом MAGL и амилоида β (в настоящем описании также обозначаемый как Aβ) со сверхэкспрессирующей моделью животного (двойная трансгенная мышь APP/PS1 и т. д.) [непатентный документ 6: Cell Report (Cell Rep.), vol. 1, pages 617-623, 2012], и ингибитор и т. д., которые подавляют действие MAGL, являются перспективными в качестве терапевтического или профилактического препарата при болезни Альцгеймера.
[0005]
Кроме того, в качестве рецепторов 2-AG, который является субстратом MAGL, идентифицировали каннабиноидный рецептор 1 (в настоящем описании обозначается как CB1) и каннабиноидный рецептор 2 (в настоящем описании упоминаемый как CB2) [непатентный документ 7: Biochemical Pharmacology (Biochem. Pharmcol.) vol. 50, 83-90, 1995]. CB1 в основном экспрессируется в области мозга [непатентный документ 8: Molecular Pharmacology (Mol. Pharmacol.), vol. 34, pages 605-613, 1988], и CB2 экспрессируется в иммуноцитах и глиальных макрофагов в области мозга [непатентный документ 9: Neuroscience Letters (Neurosci. Lett.), vol. 396, pages 113-116, 2006]. В последние годы сообщалось, что агонист рецептора CB1 улучшает познавательную функцию [непатентный документ 10: Journal of Alzheimer’s Disease (J. Alzheimers. Dis.), vol. 30, pages 439-459, 2012], и 2-AG, который является субстратом MAGL, проявляет защитное действие против гибели нервных клеток из-за Aβ [непатентный документ 11: Neuroscience, vol. 178, pages 159-168, 2011]. Следовательно, ингибитор MAGL, который подавляет разложение 2-AG, является перспективным в качестве терапевтического или профилактического лекарственного средства, которое оказывает воздействие не только на облегчение симптомов, но также на подавление прогрессирования заболевания, подавляя воспаление в мозге, гибель нервных клеток, накопление Aβ и тому подобное, наблюдаемое при болезни Альцгеймера.
[0006]
Болезнь Паркинсона, которая является одним из нейродегенеративных заболеваний, представляет собой заболевание, связанное с двигательными расстройствами, вызванными дегенерацией дофаминовых нервных клеток среднего мозга, при которой сообщается об активации глиальной клетки [непатентный документ 12: Annals of Neurology (Ann. Neurol.) vol. 57, pages 168-175, 2005]. Хотя известно, что 1-метил-4-фенил-1,2,3,6-тетрагидропиридин индуцирует клеточную гибель дофаминового нейрона черной субстанции среднего мозга, было показано, что он обладает защитным действием против гибели нервных клеток у мышей с дефицитом MAGL [непатентный документ 13: Science, vol. 334, pages 809-813, 2011]. Следовательно, ингибиторы и т. д., которые подавляют действие MAGL, являются перспективными в качестве новых терапевтических лекарств от болезни Паркинсона.
[0007]
Латеральный амиотрофический склероз (в настоящем описании обозначаемый как ALS) представляет собой заболевание, связанное с дегенерацией двигательного нейрона, и в настоящее время не существует эффективного лечения. Сообщалось об активации глиальной клетки в ALS [непатентный документ 14: Neurobiology of Disease (Neurobiol. Dis.) vol. 15, pages 601-609, 2004]. Также сообщалось, что активация CB2 подавляет прогрессирование заболевания у мутантной мыши с избыточной экспрессией супероксиддисмутазы, которая является животной моделью ALS [непатентный документ 15: European Journal of Pharmacology (Eur. J. Pharmacol.), vol. 542, pages 100-105, 2006]. Кроме того, сообщалось, что воспаление мозга у мышей с дефицитом MAGL подавляется снижением арахидоновой кислоты, которая является продуктом MAGL in vivo [непатентный документ 13: Science, vol. 334, pages 809-813, 2011]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения ALS.
[0008]
Болезнь Хантингтона, которая является одним из нейродегенеративных заболеваний, представляет собой заболевание, при котором неврологическая функция теряется в результате гибели нервных клеток и воспаления головного мозга вследствие агрегации полиглутамина. Сообщалось, что активация CB2 подавляет воспаление мозга и проявляет нейропротекторное действие у мыши R6/2, которая является моделью болезни Хантингтона на животных [непатентный документ 16: Brain, vol. 132, pages 3152-3164, 2009]. Кроме того, сообщалось, что воспаление головного мозга подавляется снижением арахидоновой кислоты, которая является продуктом MAGL, у мышей с дефицитом MAGL [непатентный документ 13: Science, vol. 334, pages 809-813, 2011]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения болезни Хантингтона.
[0009]
Сообщалось, что 2-AG, который является субстратом MAGL, подавляет прогрессирование болезненного состояния на модели аутоиммунного энцефаломиелита, то есть на модели рассеянного склероза на животных, которая является одним из центральных заболеваний демиелинизации [непатентный документ 17: Brain Research (Brain Res.), vol. 1390, pages 126-141, 2011]. Кроме того, сообщалось, что воспаление головного мозга подавляется снижением арахидоновой кислоты, которая является продуктом MAGL, у мышей с дефицитом MAGL [непатентный документ 13: Science, vol. 334, pages 809-813, 2011]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения рассеянного склероза.
[0010]
Травматическое повреждение головного мозга (TBI -Traumatic brain injury) представляет собой патологическое состояние, оказывающее чрезвычайно вредное влияние на здоровье людей, и в настоящее время не существует эффективного лечения. Сообщалось, что 2-AG, являющийся субстратом MAGL, обладает защитным действием против гибели нервных клеток на модели животных с закрытой травмой черепа [непатентный документ 18: Nature, vol. 413, pages 527-531, 2001]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического или профилактического препарата для черепно-мозговой травмы.
[0011]
Глаукома чаще всего вызывает потерю зрения и считается серьезной социальной проблемой. Сообщалось, что 2-AG, который является субстратом MAGL, активирует отток воды в модели внутриглазной перфузии [непатентный документ 19: Experimental Eye Research (Exp. Eye Res.), vol. 87, pages 106-114, 2008]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического или профилактического препарата для лечения глаукомы.
[0012]
Тревожное расстройство представляет собой психическое заболевание, которое встречается очень часто и сильно влияет на качество жизни. Сообщалось, что 2-AG, который является субстратом MAGL, проявляет анти-тревожное действие в тесте с приподнятым крестообразным лабиринтом, который является эффективной тест-системой тревожного расстройства [непатентный документ 20: Behavioural Brain Research (Behav. Brain Res.), vol. 252, pages 10-17, 2013]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения тревожных расстройств.
[0013]
2-AG, который является субстратом MAGL, показал антиноцицептивный эффект в формалиновом тесте [непатентный документ 21: British Journal of Pharmacology, vol. 150, pages 693-701, 2007]. Кроме того, сообщалось, что 2-AG демонстрирует эффект в тесте механической гипералгезии, который является моделью карциноматозной боли [непатентный документ 22: Pharmacological Research (Pharmacol. Res.), vol. 64, pages 60-67, 2011]. Поэтому ингибитор MAGL является перспективным в качестве нового терапевтического лекарственного средства при воспалительной боли и нервной боли.
[0014]
Эпилепсия сильно влияет на повседневную жизнь. Известно, что воспаление головного мозга было индуцировано в гиппокампе пациентов с эпилепсией височной доли, и воспаление головного мозга, сопровождаемое активацией глиальных клеток, участвует в судорожном приступе [непатентный документ 23: Nature Medicine (Nature Med.), vol. 16, pages 413-419, 2010]. 2-AG, являющийся субстратом MAGL, оказывает подавляющее действие на судорожный приступ, вызванный пентилентетразолом, который является моделью острой судороги [непатентный документ 24: Neurochemical Research (Neurochem. Res.), vol. 36, pages 1520-1525, 2011]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения эпилепсии.
[0015]
Депрессия представляет собой заболевание, которое очень часто встречается в современном обществе и сильно влияет на качество жизни. Сообщалось, что 2-AG, который является субстратом MAGL, проявляет антидепрессивное действие на модели хронического стресса, которая является эффективной тест-системой депрессии [непатентный документ 25: Neuropsychopharmacology, vol. 39, pages 1763-1776, 2014]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения депрессии.
[0016]
Мигрень представляет собой заболевание, которое очень часто встречается в современном обществе и сильно влияет на качество жизни. Одним из факторов развития мигрени является воспаление мозга. Сообщалось, что активация CB2 оказывает обезболивающее действие у крыс, которым вводили нитроглицерин, что является эффективной тест-системой для лечения мигрени [непатентный документ 26: Journal of Headache and Pain, vol. 15, No. 14, 2014]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения мигрени.
[0017]
Отек мозга представляет собой заболевание, развивающееся в связи с различными энцефалопатиями. Одной из причин отека мозга является разрушение гематоэнцефалического барьера. Известно, что арахидоновая кислота и эйкозаноиды разрушают гематоэнцефалический барьер [непатентный документ 27: Brain Research, vol. 1298, pages 13-23, 2009]. Ингибитор, который подавляет действие MAGL, уменьшает выработку арахидоновой кислоты MAGL. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения отека мозга.
[0018]
Ишемия головного мозга является одним из факторов, вызывающих возникновение инфаркта головного мозга. Сообщалось, что 2-AG, который является субстратом MAGL, обладает защитным действием на мозг в тест-системе, эффективной для лечения ишемии головного мозга [непатентный документ 28: Brain Research, vol. 1474, pages 91-99, 2012]. Поэтому ингибитор MAGL перспективен в качестве нового терапевтического препарата для лечения ишемии головного мозга.
[0019]
В качестве гетероциклических соединений известны следующие соединения. Патентный документ 1 описывает, что соединение представлено следующей формулой (I):
[0020]
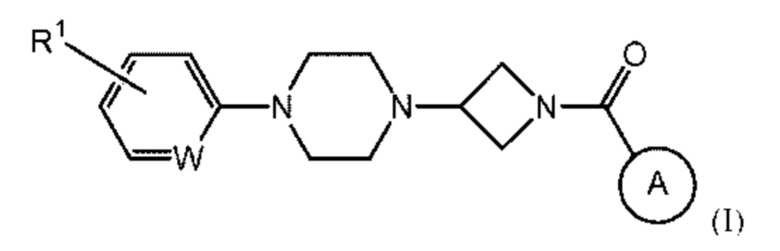
[0021]
где каждый символ такой, как определено в патентном документе 1,
представляет собой ингибитор MAGL и пригоден для лечения боли и тому подобного.
Патентный документ 2 описывает, что соединение представлено следующей формулой (I):
[0022]
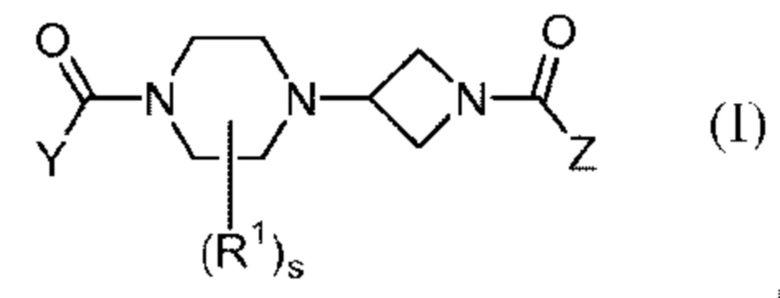
[0023]
где каждый символ такой, как определено в патентном документе 2,
представляет собой ингибитор MAGL и пригоден для лечения боли и тому подобного.
Патентный документ 3 описывает, что соединение представлено следующей формулой (I):
[0024]
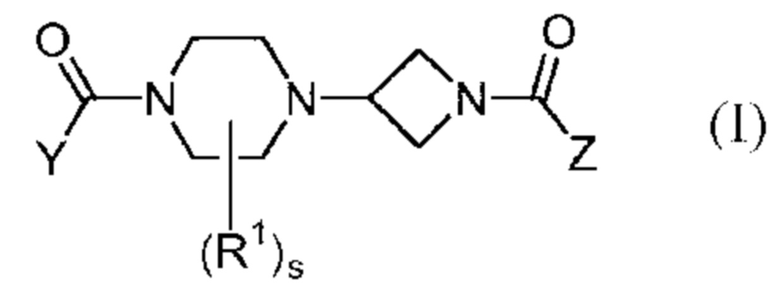
[0025]
где каждый символ такой, как определено в патентном документе 3,
представляет собой ингибитор MAGL и пригоден для лечения боли и тому подобного.
Патентный документ 4 описывает, что соединение представлено следующей формулой (I):
[0026]

[0027]
где каждый символ такой, как определено в патентном документе 4,
представляет собой ингибитор MAGL и пригоден для лечения боли и тому подобного.
Патентный документ 5 описывает, что соединение представлено следующей формулой:
[0028]
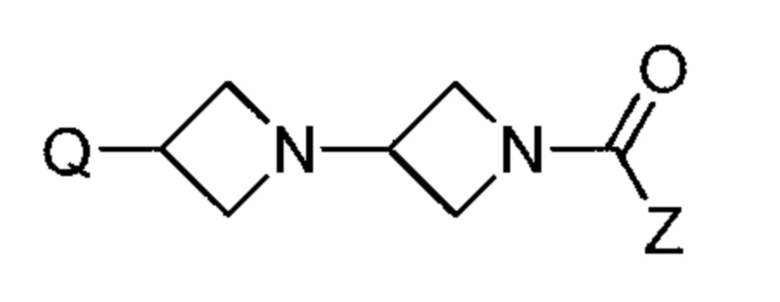
[0029]
где каждый символ такой, как определено в патентном документе 5,
пригодно в качестве ингибитора MAGL.
Патентный документ 6 описывает, что соединение представлено следующей формулой:
[0030]
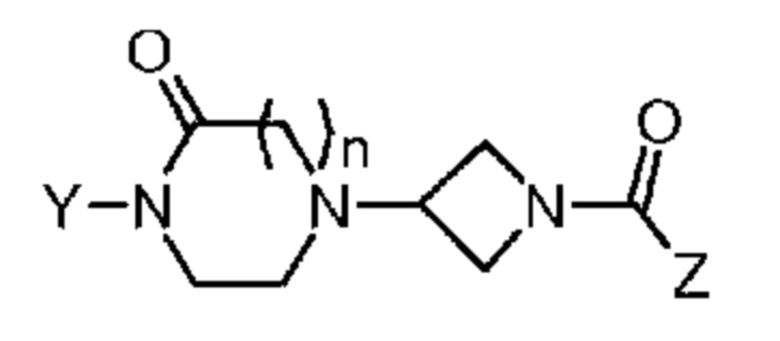
[0031]
где каждый символ такой, как определено в патентном документе 6, и соединение, представленное следующей формулой:
[0032]
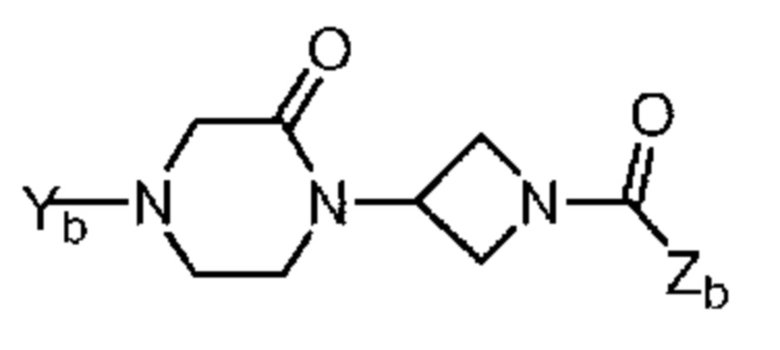
[0033]
где каждый символ такой, как определено в патентном документе 6,
пригодно в качестве ингибитора MAGL.
Патентный документ 7 описывает, что соединение представлено следующей формулой:
[0034]
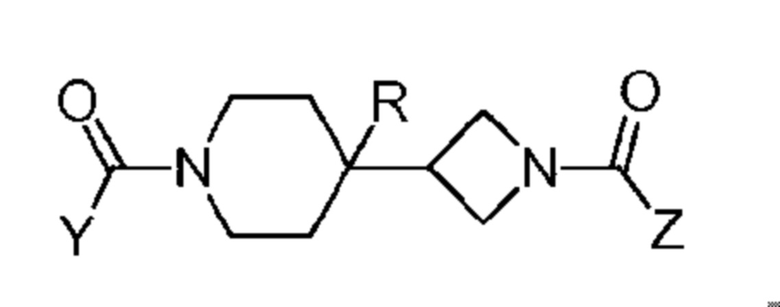
[0035]
где каждый символ такой, как определено в патентном документе 7,
пригодно в качестве ингибитора MAGL.
Патентный документ 8 описывает, что соединение представлено следующей формулой (I):
[0036]
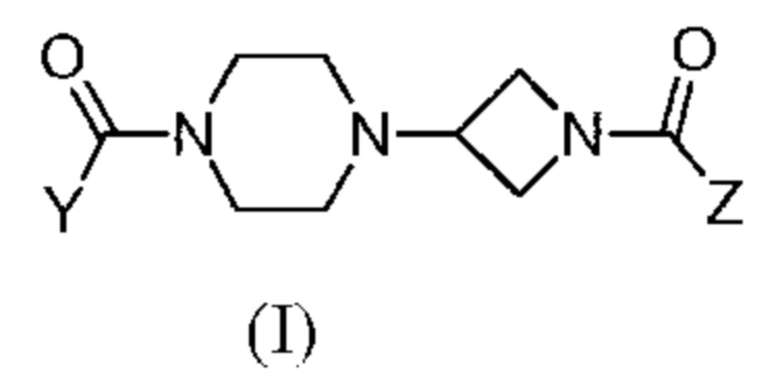
[0037]
где каждый символ такой, как определено в патентном документе 8,
представляет собой ингибитор MAGL и пригодно для лечения, улучшения или профилактики метаболических заболеваний (ожирение, диабет).
Патентный документ 9 описывает, что соединение представлено следующей формулой (I):
[0038]
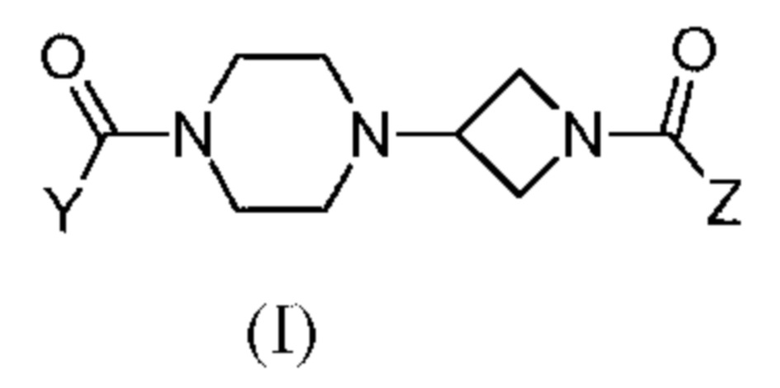
[0039]
где каждый символ такой, как определено в патентном документе 9,
представляет собой ингибитор MAGL и пригодно для лечения, улучшения или профилактики метаболических заболеваний (ожирение, диабет).
[0040]
Патентный документ 10 описывает, что соединение представлено следующей формулой (I):
[0041]
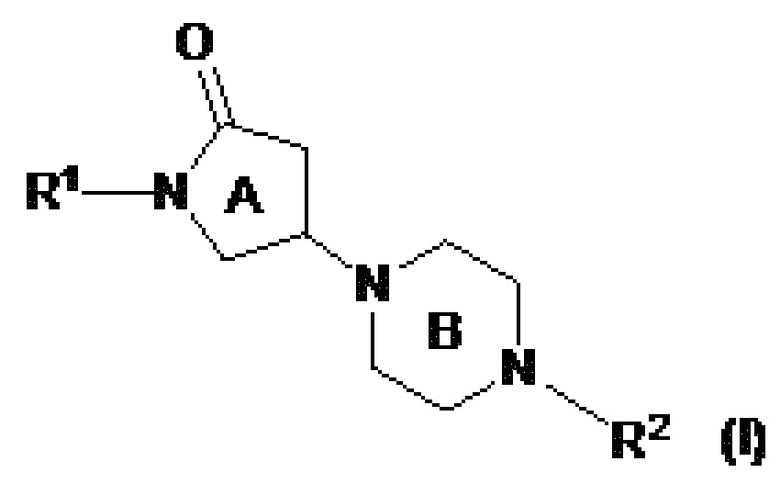
[0042]
где каждый символ такой, как определено в патентном документе 10,
представляет собой ингибитор MAGL и пригоден для лечения, улучшения или профилактики нейродегенеративных заболеваний, тревожных расстройств, боли и эпилепсии.
Патентный документ 11 описывает, что соединение представлено следующей формулой (I):
[0043]
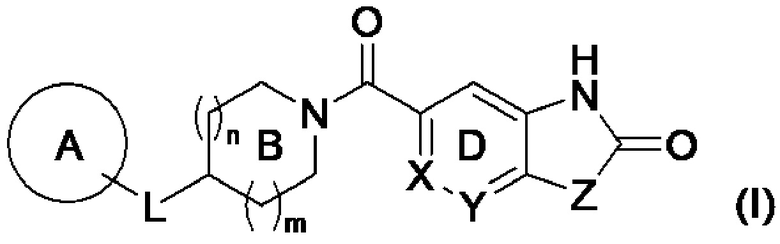
[0044]
где каждый символ такой, как определено в патентном документе 11,
представляет собой ингибитор MAGL и пригоден для профилактики или лечения нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, травматического повреждения головного мозга, глаукомы, рассеянного склероза и т. д.), тревожного расстройства, боли (например, воспалительной боли, раковой боли, нервной боли и т. д.), эпилепсии, депрессии и тому подобного.
Патентный документ 12 описывает, что соединение представлено следующей формулой (I):
[0045]
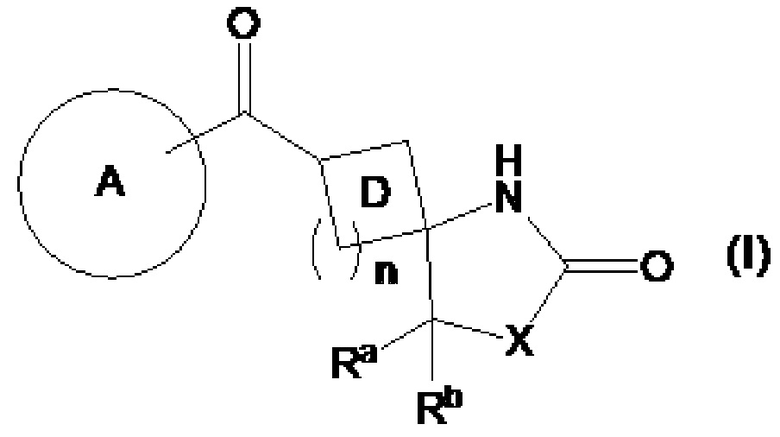
[0046]
где каждый символ такой, как определено в патентном документе 12,
представляет собой ингибитор MAGL и пригоден для профилактики или лечения нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, травматического повреждения головного мозга, глаукомы, рассеянного склероза и т. д.), тревожного расстройства, боли (например, воспалительной боли, раковой боли, нервной боли и т. д.), эпилепсии, депрессии и тому подобного.
Патентный документ 13 описывает, что соединение представлено следующей формулой (I):
[0047]

[0048]
где каждый символ такой, как определено в патентном документе 13,
представляет собой ингибитор MAGL и пригоден для профилактики или лечения нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, травматического повреждения головного мозга, глаукомы, рассеянного склероза и т. д.), тревожного расстройства, боли (например, воспалительной боли, раковой боли, нервной боли и т. д.), эпилепсии, депрессии и тому подобного.
Список документов
Патентный документ
[0049]
Патентный документ 1: WO 2010/124122
Патентный документ 2: WO 2010/124082
Патентный документ 3: WO 2010/124086
Патентный документ 4: WO 2010/124121
Патентный документ 5: WO 2012/030907
Патентный документ 6: WO 2012/044613
Патентный документ 7: WO 2012/054716
Патентный документ 8: WO 2013/049289
Патентный документ 9: WO 2013/049293
Патентный документ 10: WO 2015/099196
Патентный документ 11: WO 2016/158956
Патентный документ 12: WO 2017/171100
Патентный документ 13: WO 2017/170830
Непатентный документ
[0050]
Непатентный документ 1: Science, vol. 294, pages 1871-1875, 2001
Непатентный документ 2: Molecular Neurobiology (Mol. Neurobiol), vol. 41, pages 115-128, 2010
Непатентный документ 3: Neuron, vol. 53, pages 337-351, 2007
Непатентный документ 4: Nature Reviews Neurology (Nat. Rev. Neurol.), vol. 6, pages 193-201, 2010
Непатентный документ 5: Chemistry and Physics of Lipids (Chem phys Lipids) vol. 121, pages 149-158, 2002
Непатентный документ 6: Cell Report (Cell Rep.), vol. 1, page 617-623, 2012
Непатентный документ 7: Biochemical Pharmacology (Biochem. Pharmcol.) vol. 50, 83-90, 1995
Непатентный документ 8: Molecular Pharmacology (Mol. Pharmacol.), vol. 34, pages 605-613, 1988
Непатентный документ 9: Neuroscience Letters (Neurosci. Lett.), vol. 396, pages 113-116, 2006
Непатентный документ 10: Journal of Alzheimer’s Disease (J. Alzheimers. Dis.), vol. 30, pages 439-459, 2012
Непатентный документ 11: Neuroscience, vol. 178, pages 159-168, 2011
Непатентный документ 12: Annals of Neurology (Ann. Neurol.) vol. 57, pages 168-175, 2005
Непатентный документ 13: Science, vol. 334, pages 809-813, 2011
Непатентный документ 14: Neurobiology of Disease (Neurobiol. Dis.) vol. 15, pages 601-609, 2004
Непатентный документ 15: European Journal of Pharmacology (Eur. J. Pharmacol.), vol. 542, pages 100-105, 2006
Непатентный документ 16: Brain, vol. 132, pages 3152-3164, 2009
Непатентный документ 17: Brain Research (Brain Res.), vol. 1390, pages 126-141, 2011
Непатентный документ 18: Nature, vol. 413, pages 527-531, 2001
Непатентный документ 19: Experimental Eye Research (Exp. Eye Res.), vol. 87, pages 106-114, 2008
Непатентный документ 20: Behavioural Brain Research (Behav. Brain Res.), vol. 252, pages 10-17, 2013
Непатентный документ 21: British Journal of Pharmacology, vol. 150, pages 693-701, 2007
Непатентный документ 22: Pharmacological Research (Pharmacol. Res.), vol. 64, pages 60-67, 2011
Непатентный документ 23: Nature Medicine (Nature Med.), vol. 16, pages 413-419, 2010
Непатентный документ 24: Neurochemical Research (Neurochem. Res.), vol. 36, pages 1520-1525, 2011
Непатентный документ 25: Neuropsychopharmacology, vol. 39, pages 1763-1776, 2014
Непатентный документ 26: Journal of Headache and Pain, vol. 15, No. 14, 2014
Непатентный документ 27: Brain Research, vol. 1298, pages 13-23, 2009
Непатентный документ 28: Brain Research, vol. 1474, pages 91-99, 2012
Сущность изобретения
Проблемы, которые должны быть решены данным изобретением
[0051]
Задачей настоящего изобретения является обеспечение соединения, обладающего ингибирующим действием на MAGL, которое, как ожидается, будет пригодным в качестве агента для профилактики или лечения нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, черепно-мозговой травмы, глаукомы, рассеянного склероза и т. д.), тревожного расстройства, боли (например, воспалительной боли, раковой боли, нейрогенной боли и т. д.), эпилепсии, депрессии и тому подобного.
Способы решения проблем
[0052]
Авторы настоящего изобретения провели интенсивные исследования в попытке решить вышеупомянутые проблемы и обнаружили, что соединение, представленное следующей формулой (I), обладает ингибирующим действием на MAGL, и, следовательно, ожидается, что оно будет пригодным в качестве средства для профилактики или лечения нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, черепно-мозговой травмы, глаукомы, рассеянного склероза и т. д.), тревожного расстройства, болей (например, воспалительной боли, раковой боли, нейрогенной боли и т. д.), эпилепсии, депрессии и тому подобного, что привело к завершению настоящего изобретения.
[0053]
Соответственно, в настоящем изобретении предложено следующее.
[1] Соединение, представленное формулой (I):
[0054]

[0055]
где
A представляет собой необязательно замещенную насыщенную циклическую группу,
L представляет собой связь или C1-3 алкиленовую группу, необязательно замещенную атомом(ами) галогена,
Кольцо D представляет собой кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами), необязательно замещенной атомом(ами) галогена,
n равно 1 или 2,
X представляет собой -O-, -CR1R2- или -NR3-,
Ra и Rb, каждый независимо представляет собой атом водорода или C1-6 алкильную группу, необязательно замещенную атомом(ами) галогена, и
R1, R2 и R3, каждый независимо представляет собой атом водорода или заместитель,
или его соль (далее иногда упоминается как соединение (I)).
[0056]
[2] Соединение или соль вышеуказанного [1], где
A представляет собой C3-10 циклоалкильную группу
замещенную 1-3 заместителями, выбранными из
(a) C6-14 арилоксигруппы, необязательно замещенной 1-4 заместителями, выбранными из
(i) атома галогена и
(ii) необязательно галогенированной C1-6 алкильной группы,
(b) C6-14 арилокси-C1-6 алкильной группы, необязательно замещенной 1-4 заместителями, выбранными из
(i) атома галогена и
(ii) необязательно галогенированной C1-6 алкильной группы,
(c) C7-16 аралкилоксигруппы, необязательно замещенной 1-4 заместителями, выбранными из
(i) атома галогена и
(ii) необязательно галогенированной C1-6 алкильной группы и
(d) C7-16 аралкилокси-C1-6 алкильной группы, необязательно замещенной 1-4 заместителями, выбранными из
(i) атома галогена и
(ii) необязательно галогенированной C1-6 алкильной группы и
необязательно дополнительно замещенной 1-3 С1-6 алкильными группами;
L представляет собой связь или C1-3 алкиленовую группу;
кольцо D представляет собой 4- или 5-членный азотсодержащий гетероцикл;
n равно 1 или 2;
X представляет собой -O- или -CH2-; и
оба Ra и Rb представляют собой атомы водорода.
[0057]
[3] Соединение или соль вышеуказанного [1], где
A представляет собой циклобутильную группу, замещенную одним заместителем, выбранным из
(a) феноксигруппы, замещенной 3 атомами галогена, и
(b) феноксиметильной группы, замещенной 3 атомами галогена;
L представляет собой связь;
кольцо D представляет собой азетидиновое кольцо;
n равно 1;
X представляет собой -O-; и
оба Ra и Rb представляют собой атомы водорода.
[0058]
[4] цис-3-((2,3,4-Трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат или его соль.
[5] цис-3-((2,4,6-Трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат или его соль.
[6] цис-3-(2,4,6-Трифторфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат или его соль.
[0059]
[7] Лекарственное средство, содержащее соединение или соль вышеупомянутого [1].
[8] Лекарственное средство вышеупомянутого [7], которое является ингибитором моноацилглицеринлипазы.
[9] Лекарственное средство вышеупомянутого [7], которое является агентом для профилактики или лечения болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, рассеянного склероза, тревожного расстройства, боли, эпилепсии или депрессии.
[0060]
[10] Способ ингибирования моноацилглицеринлипазы у млекопитающего, включающий введение млекопитающему эффективного количества соединения или соли вышеупомянутого [1].
[11] Способ профилактики или лечения болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, рассеянного склероза, тревожного расстройства, боли, эпилепсии или депрессии у млекопитающего, включающий введение млекопитающему эффективного количества соединения или соли вышеупомянутого [1].
[0061]
[12] Соединение или соль вышеупомянутого [1] для применения в профилактике или лечении болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, рассеянного склероза, тревожного расстройства, боли, эпилепсии или депрессии.
[13] Применение соединения или соли вышеупомянутого [1] для изготовления агента для применения в профилактике или лечении болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, рассеянного склероза, тревожного расстройства, боли, эпилепсии или депрессии.
Эффект изобретения
[0062]
Согласно настоящему изобретению соединение, обладающее превосходным ингибирующим действием на MAGL, которое, как ожидается, будет пригодно в качестве агента для профилактики или лечения нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, черепно-мозговой травмы, глаукомы, рассеянного склероза и т. д.), тревожного расстройства, болей (например, воспалительной боли, раковой боли, нейрогенной боли и т. д.), эпилепсии, депрессии и тому подобного.
[0063]
(Подробное описание сущности изобретения)
Настоящее изобретение подробно объясняется следующим.
[0064]
Определение каждого заместителя, используемого в данном описании, подробно описано ниже. Если не указано иное, каждый заместитель имеет следующее определение.
В данном описании примеры «атома галогена» включают фтор, хлор, бром и иод.
В данном описании примеры «C1-6 алкильной группы» включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, 1-этилпропил, гексил, изогексил, 1,1-диметилбутил, 2,2-диметилбутил, 3,3-диметилбутил и 2-этилбутил.
В данном описании примеры «необязательно галогенированной C1-6 алкильной группы» включают C1-6 алкильную группу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5 атомов галогена. Ее конкретные примеры включают метил, хлорметил, дифторметил, трихлорметил, трифторметил, этил, 2-бромэтил, 2,2,2-трифторэтил, тетрафторэтил, пентафторэтил, пропил, 2,2-дифторпропил, 3,3,3-трифторпропил, изопропил, бутил, 4,4,4-трифторбутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, 5,5,5-трифторпентил, гексил и 6,6,6-трифторгексил.
В данном описании примеры «C2-6 алкенильной группы» включают этенил, 1-пропенил, 2-пропенил, 2-метил-1-пропенил, 1-бутенил, 2-бутенил, 3-бутенил, 3-метил-2-бутенил, 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 4-метил-3-пентенил, 1-гексенил, 3-гексенил и 5-гексенил.
В данном описании примеры «C2-6 алкинильной группы» включают этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 1-пентинил, 2-пентинил, 3-пентинил, 4-пентинил, 1-гексинил, 2-гексинил, 3-гексинил, 4-гексинил, 5-гексинил и 4-метил-2-пентинил.
В данном описании примеры «C3-10 циклоалкильной группы» включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, бицикло[2.2.1]гептил, бицикло[2.2.2]октил, бицикло [3.2.1]октил и адамантил.
В данном описании примеры «необязательно галогенированной C3-10 циклоалкильной группы» включают C3-10 циклоалкильную группу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5 атомов галогена. Ее конкретные примеры включают циклопропил, 2,2-дифторциклопропил, 2,3-дифторциклопропил, циклобутил, дифторциклобутил, циклопентил, циклогексил, циклогептил и циклооктил.
В данном описании примеры «C3-10 циклоалкенильной группы» включают циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклогептенил и циклооктенил.
В данном описании примеры «C6-14 арильной группы» включают фенил, 1-нафтил, 2-нафтил, 1-антрил, 2-антрил и 9-антрил.
В данном описании примеры «C7-16 аралкильной группы» включают бензил, фенетил, нафтилметил и фенилпропил.
[0065]
В данном описании примеры «C1-6 алкоксигруппы» включают метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси и гексилокси.
В данном описании примеры «необязательно галогенированной C1-6 алкоксигруппы» включают C1-6 алкоксигруппу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5 атомов галогена. Ее конкретные примеры включают метокси, дифторметокси, трифторметокси, этокси, 2,2,2-трифторэтокси, пропокси, изопропокси, бутокси, 4,4,4-трифторбутокси, изобутокси, втор-бутокси, пентилокси и гексилокси.
В данном описании примеры «C3-10 циклоалкилоксигруппы» включают циклопропилокси, циклобутилокси, циклопентилокси, циклогексилокси, циклогептилокси и циклооктилокси.
В данном описании примеры «C1-6 алкилтиогруппы» включают метилтио, этилтио, пропилтио, изопропилтио, бутилтио, втор-бутилтио, трет-бутилтио, пентилтио и гексилтио.
В данном описании примеры «необязательно галогенированной C1-6 алкилтиогруппы» включают C1-6 алкилтиогруппу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5 атомов галогена. Ее конкретные примеры включают метилтио, дифторметилтио, трифторметилтио, этилтио, пропилтио, изопропилтио, бутилтио, 4,4,4-трифторбутилтио, пентилтио и гексилтио.
В данном описании примеры «C1-6 алкил-карбонильной группы» включают ацетил, пропаноил, бутаноил, 2-метилпропаноил, пентаноил, 3-метилбутаноил, 2-метилбутаноил, 2,2-диметилпропаноил, гексаноил и гептаноил.
В данном описании примеры «необязательно галогенированной C1-6 алкил-карбонильной группы» включают C1-6 алкил-карбонильную группу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5 атомов галогена. Ее конкретные примеры включают ацетил, хлорацетил, трифторацетил, трихлорацетил, пропаноил, бутаноил, пентаноил и гексаноил.
В данном описании примеры «C1-6 алкокси-карбонильной группы» включают метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, пентилоксикарбонил и гексилоксикарбонил.
В данном описании примеры «C6-14 арил-карбонильной группы» включают бензоил, 1-нафтоил и 2-нафтоил.
В данном описании примеры «C7-16 аралкил-карбонильной группы» включают фенилацетил и фенилпропионил.
В данном описании примеры «5-14-членной ароматической гетероциклилкарбонильной группы» включают никотиноил, изоникотиноил, теноил и фуроил.
В данном описании примеры «3-14-членной неароматической гетероциклилкарбонильной группы» включают морфолинилкарбонил, пиперидинилкарбонил и пирролидинилкарбонил.
[0066]
В данном описании примеры «моно- или ди-C1-6 алкил-карбамоильной группы» включают метилкарбамоил, этилкарбамоил, диметилкарбамоил, диэтилкарбамоил и N-этил-N-метилкарбамоил.
В данном описании примеры «моно- или ди-C7-16 -арилкил-карбамоильной группы» включают бензилкарбамоил и фенетилкарбамоил.
В данном описании примеры «C1-6 алкилсульфонильной группы» включают метилсульфонил, этилсульфонил, пропилсульфонил, изопропилсульфонил, бутилсульфонил, втор-бутилсульфонил и трет-бутилсульфонил.
В данном описании примеры «необязательно галогенированной C1-6 алкилсульфонильной группы» включают C1-6 алкилсульфонильную группу, необязательно имеющую от 1 до 7, предпочтительно, от 1 до 5, атомов галогена. Ее конкретные примеры включают метилсульфонил, дифторметилсульфонил, трифторметилсульфонил, этилсульфонил, пропилсульфонил, изопропилсульфонил, бутилсульфонил, 4,4,4-трифторбутилсульфонил, пентилсульфонил и гексилсульфонил.
В данном описании примеры «C6-14 арилсульфонильной группы» включают фенилсульфонил, 1-нафтилсульфонил и 2-нафтилсульфонил.
[0067]
В данном описании примеры «заместителя» включают атом галогена, цианогруппу, нитрогруппу, необязательно замещенную углеводородную группу, необязательно замещенную гетероциклическую группу, ацильную группу, необязательно замещенную аминогруппу, необязательно замещенную карбамоильную группу, необязательно замещенную тиокарбамоильную группу, необязательно замещенную сульфамоильную группу, необязательно замещенную гидроксигруппу, необязательно замещенную сульфанильную (SH) группу и необязательно замещенную силильную группу.
В данном описании примеры «углеводородной группы» (включая «углеводородную группу» из «необязательно замещенной углеводородной группы») включают C1-6 алкильную группу, C2-6 алкенильную группу, C2-6 алкинильную группу, C3-10 циклоалкильную группу, C3-10 циклоалкенильную группу, C6-14 арильную группу и C7-16 аралкильную группу.
[0068]
В данном описании примеры «необязательно замещенной углеводородной группы» включают углеводородную группу, необязательно имеющую заместитель(и), выбранный из следующей группы заместителей А.
[Группа заместителей A]
(1) атом галогена,
(2) нитрогруппа,
(3) цианогруппа,
(4) оксогруппа,
(5) гидроксигруппа,
(6) необязательно галогенированная C1-6 алкоксигруппа,
(7) C6-14 арилоксигруппа (например, фенокси, нафтокси),
(8) C7-16 аралкилоксигруппа (например, бензилокси),
(9) 5-14-членная ароматическая гетероциклилоксигруппа (например, пиридилокси),
(10) 3-14-членная неароматическая гетероциклилоксигруппа (например, морфолинилокси, пиперидинилокси),
(11) C1-6 алкил-карбонилоксигруппа (например, ацетокси, пропаноилокси),
(12) C6-14 арил-карбонилоксигруппа (например, бензоилокси, 1-нафтоилокси, 2-нафтоилокси),
(13) C1-6 алкокси-карбонилоксигруппа (например, метоксикарбонилокси, этоксикарбонилокси, пропоксикарбонилокси, бутоксикарбонилокси),
(14) моно- или ди-C1-6 алкил-карбамоилоксигруппа (например, метилкарбамоилокси, этилкарбамоилокси, диметилкарбамоилокси, диэтилкарбамоилокси),
(15) C6-14 арил-карбамоилоксигруппа (например, фенилкарбамоилокси, нафтилкарбамоилокси),
(16) 5-14-членная ароматическая гетероциклилкарбонилоксигруппа (например, никотиноилокси),
(17) 3-14-членная неароматическая гетероциклилкарбонилоксигруппа (например, морфолинилкарбонилокси, пиперидинилкарбонилокси),
(18) необязательно галогенированная C1-6 алкилсульфонилоксигруппа (например, метилсульфонилокси, трифторметилсульфонилокси),
(19) C6-14 арилсульфонилоксигруппа, необязательно замещенная C1-6 алкильной группой (например, фенилсульфонилокси, толуолсульфонилокси),
(20) необязательно галогенированная C1-6 алкилтиогруппа,
(21) 5-14-членная ароматическая гетероциклическая группа,
(22) 3-14-членная неароматическая гетероциклическая группа,
(23) формильная группа,
(24) карбоксигруппа,
(25) необязательно галогенированная C1-6 алкил-карбонильная группа,
(26) C6-14 арил-карбонильная группа,
(27) 5-14-членная ароматическая гетероциклилкарбонильная группа,
(28) 3-14-членная неароматическая гетероциклилкарбонильная группа,
(29) C1-6 алкокси-карбонильная группа,
(30) C6-14 арилокси-карбонильная группа (например, фенилоксикарбонил, 1-нафтилоксикарбонил, 2-нафтилоксикарбонил),
(31) C7-16 аралкилокси-карбонильная группа (например, бензилоксикарбонил, фенэтилоксикарбонил),
(32) карбамоильная группа,
(33) тиокарбамоильная группа,
(34) моно- или ди-C1-6 алкил-карбамоильная группа,
(35) C6-14 арил-карбамоильная группа (например, фенилкарбамоил),
(36) 5-14-членная ароматическая гетероциклилкарбамоильная группа (например, пиридилкарбамоил, тиенилкарбамоил),
(37) 3-14-членная неароматическая гетероциклилкарбамоильная группа (например, морфолинилкарбамоил, пиперидинилкарбамоил),
(38) необязательно галогенированная C1-6 алкилсульфонильная группа,
(39) C6-14 арилсульфонильная группа,
(40) 5-14-членная ароматическая гетероциклилсульфонильная группа (например, пиридилсульфонил, тиенилсульфонил),
(41) необязательно галогенированная C1-6 алкилсульфинильная группа,
(42) C6-14 арилсульфинильная группа (например, фенилсульфинил, 1-нафтилсульфинил, 2-нафтилсульфинил),
(43) 5-14-членная ароматическая гетероциклилсульфинильная группа (например, пиридилсульфинил, тиенилсульфинил),
(44) аминогруппа,
(45) моно- или ди-C1-6 алкиламиногруппа (например, метиламино, этиламино, пропиламино, изопропиламино, бутиламино, диметиламино, диэтиламино, дипропиламино, дибутиламино, N-этил-N-метиламино),
(46) моно- или ди-C6-14 ариламиногруппа (например, фениламино),
(47) 5-14-членная ароматическая гетероциклиламиногруппа (например, пиридиламино),
(48) C7-16 аралкиламиногруппа (например, бензиламино),
(49) формиламиногруппа,
(50) C1-6 алкил-карбониламиногруппа (например, ацетиламино, пропаноиламино, бутаноиламино),
(51) (C1-6 алкил)(C1-6 алкил-карбонил)аминогруппа (например, N-ацетил-N-метиламино),
(52) C6-14 арил-карбониламиногруппа (например, фенилкарбониламино, нафтилкарбониламино),
(53) C1-6 алкокси-карбониламиногруппа (например, метоксикарбониламино, этоксикарбониламино, пропоксикарбониламино, бутоксикарбониламино, трет-бутоксикарбониламино),
(54) C7-16 аралкилокси-карбониламиногруппа (например, бензилоксикарбониламино),
(55) C1-6 алкилсульфаниламиногруппа (например, метилсульфониламино, этилсульфониламино),
(56) C6-14 арилсульфониламиногруппа, необязательно замещенная C1-6 алкильной группой (например, фенилсульфониламино, толуолсульфониламино),
(57) необязательно галогенированная C1-6 алкильная группа,
(58) C2-6 алкенильная группа,
(59) C2-6 алкинильная группа,
(60) C3-10 циклоалкильная группа,
(61) C3-10 циклоалкенильная группа и
(62) C6-14 арильная группа.
[0069]
Число вышеупомянутых заместителей в «необязательно замещенной углеводородной группе» составляет, например, от 1 до 5, предпочтительно, от 1 до 3. Когда число заместителей равно двум или более, соответствующие заместители могут быть одинаковыми или разными.
В данном описании примеры «гетероциклической группы» (включая «гетероциклическую группу» в «необязательно замещенной гетероциклической группе») включают (i) ароматическую гетероциклическую группу, (ii) неароматическую гетероциклическую группу и (iii) 7-10-членную мостиковую гетероциклическую группу, каждая из которых содержит в качестве кольцевого атома, кроме атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода.
[0070]
В данном описании примеры «ароматической гетероциклической группы» (включая «5-14-членную ароматическую гетероциклическую группу») включают 5-14-членную (предпочтительно 5-10-членную) ароматическую гетероциклическую группу, содержащую в качестве кольцевого атома, кроме атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода.
Предпочтительные примеры «ароматической гетероциклической группы» включают 5- или 6-членные моноциклические ароматические гетероциклические группы, такие как тиенил, фурил, пирролил, имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, изоксазолил, пиридил, пиразинил, пиримидинил, пиридазинил, 1,2,4-оксадиазолил, 1,3,4-оксадиазолил, 1,2,4-тиадиазолил, 1,3,4-тиадиазолил, триазолил, тетразолил, триазинил и тому подобное; и
8-14-членные конденсированные полициклические (предпочтительно би или трициклические) ароматические гетероциклические группы, такие как бензотиофенил, бензофуранил, бензимидазоил, бензоксазолил, бензизоксазолил, бензотиазолил, бензизотиазолил, бензотриазолил, имидазопиридинил, тиенопиридинил, фуропиридинил, пирролопиридинил, пиразолопиридинил, оксазолопиридинил, тиазолoпиридинил, имидазопиразинил, имидазопиримидинил, тиенопиримидинил, фуропиримидинил, пирролопиримидинил, пиразолопиримидинил, оксазолопиримидинил, тиазолoпиримидинил, пиразолотриазинил, нафто[2,3-b] тиенил, феноксантинил, индолил, изоиндолил, 1H-индазолил, пуринил, изохинолил, хинолил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинили, карбазолил, β-карболинил, фенантридинил, акридинил, феназинил, фенотиазинил, феноксазинил и тому подобное
[0071]
В данном описании примеры «неароматической гетероциклической группы» (включая «3-14-членную неароматическую гетероциклическую группу») включают 3-14-членную (предпочтительно 4-10-членную) неароматическую гетероциклическую группу, содержащую, в качестве кольцевого атома, кроме атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атома кислорода.
Предпочтительные примеры «неароматической гетероциклической группы» включают 3-8-членные моноциклические неароматические гетероциклические группы такие как азиридинил, оксиранил, тииранил, азетидинил, оксетанил, тиетанил, тетрагидротиенил, тетрагидрофуранил, пирролинил, пирролидинил, имидазолинил, имидазолидинил, оксазолинил, оксазолидинил, пиразолинил, пиразолидинил, тиазолинил, тиазолидинил, тетрагидроизотиазолил, тетрагидрооксазолил, тетрагидроизоксазолил, пиперидинил, пиперазинил, тетрагидропиридинил, дигидропиридинил, дигидротиопиранил, тетрагидропиримидинил, тетрагидропиридазинил, дигидропиранил, тетрагидропиранил, тетрагидротиопиранил, морфолинил, тиоморфолинил, азепанил, диазепанил, азепинил, оксепанил, азоканил, диазоканил и.т.п; и
9-14-членные конденсированные полициклические (предпочтительно би или трициклические) неароматические гетероциклические группы, такие как дигидробензофуранил, дигидробензимидазолил, дигидробензоксазолил, дигидробензотиазолил, дигидробензизотиазолил, дигидронафто[2,3-b]тиенил, тетрагидроизохинолил, тетрагидрохинолил, 4Н-хинолизинил, индолинил, изоиндолинил, тетрагидротиено[2,3-с]пиридинил, тетрагидробензазепинил, тетрагидрохиноксалинил, тетрагидрофенантридинил, гексагидрофенотиазинил, гексагидрофеноксазинил, тетрагидрофталазинил, тетрагидронафтиридинил, тетрагидрохиназолинил, тетрагидроциннолинил, тетрагидрокарбазолил, тетрагидро-β-карболинил, тетрагидроакридинил, тетрагидрофеназинил, тетрагидротиоксантенил, октагидроизохинолил и тому подобное.
[0072]
В данном описании предпочтительные примеры «7-10-членной мостиковой гетероциклической группы» включают хинуклидинил и 7-азабицикло[2,2,1]гептанил.
В данном описании примеры «азотсодержащей гетероциклической группы» включают «гетероциклическую группу», содержащую по меньшей мере один атом азота в качестве кольцевого атома.
В данном описании примеры «необязательно замещенная гетероциклическая группа» включает гетероциклическую группу, необязательно имеющую заместитель(и), выбранный из вышеупомянутой «группы заместителей А».
Число заместителей в «необязательно замещенной гетероциклической группе» равно, например, от 1 до 3. Когда число заместителей равно двум или более, соответствующие заместители могут быть одинаковыми или разными.
[0073]
В данном описании примеры «ацильной группы» включает формильную группу, карбоксигруппу, карбамоильную группу, тиокарбамоильную группу, сульфиногруппу, сульфогруппу, сульфамоильную группу и фосфоногруппу, каждая из которых необязательно имеет «1 или 2 заместителя, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C3-10 циклоалкенильной группы, C6-14 арильной группы, C7-16 аралкильной группы, 5-14-членной ароматической гетероциклической группы и 3-14-членной неароматической гетероциклической группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из атома галогена, необязательно галогенированной C1-6 алкоксигруппы, гидроксигруппы, нитрогруппы, цианогруппы, аминогруппы и карбамоильной группы».
Примеры «ацильной группы» также включают углеводород-сульфонильную группу, гетероциклилсульфонильную группу, углеводород-сульфинильную группу и гетероциклилсульфинильную группу.
Здесь углеводород-сульфонильная группа означает связанную с углеводородной группой сульфонильную группу, гетероциклилсульфонильная группа означает связанную с гетероциклической группой сульфонильную группу, углеводород-сульфинильная группа означает связанную с углеводородной группой сульфинильную группу, гетероциклилсульфинильная группа означает связанную с гетероциклической группой сульфинильную группу.
Предпочтительные примеры «ацильной группы» включают формильную группу, карбоксигруппу, C1-6 алкил-карбонильную группу, C2-6 алкенил-карбонильную группу (например, кротоноил), C3-10 циклоалкил-карбонильную группу (например, циклобутанкарбонил, циклопентанкарбонил, циклогексанкарбонил, циклогептанкарбонил), C3-10 циклоалкенил-карбонильную группу (например, 2-циклогексенкарбонил), C6-14 арил-карбонильную группу, C7-16 аралкил-карбонильную группу, 5-14-членную ароматическую гетероциклилкарбонильную группу, 3-14-членную неароматическую гетероциклилкарбонильную группу, C1-6 алкокси-карбонильную группу, C6-14 арилокси-карбонильную группу (например, фенилоксикарбонил, нафтилоксикарбонил), C7-16 аралкилокси-карбонильную группу (например, бензилоксикарбонил, фенэтилоксикарбонил), карбамоильную группу, моно- или ди-C1-6 алкил-карбамоильную группу, моно- или ди-C2-6 алкенил-карбамоильную группу (например, диaллилкарбамоил), моно- или ди-C3-10 циклоалкил-карбамоильную группу (например, циклопропилкарбамоил), моно- или ди-C6-14 арил-карбамоильную группу (например, фенилкарбамоил), моно- или ди-C7-16 аралкил-карбамоильную группу, 5-14-членную ароматическую гетероциклилкарбамоильную группу (например, пиридилкарбамоил), тиокарбамоильную группу, моно- или ди-C1-6 алкил-тиокарбамоильную группу (например, метилтиокарбамоил, N-этил-N-метилтиокарбамоил), моно- или ди-C2-6 алкенил-тиокарбамоильную группу (например, диaллилтиокарбамоил), моно- или ди-C3-10 циклоалкил-тиокарбамоильную группу (например, циклопропилтиокарбамоил, циклогексилтиокарбамоил), моно- или ди-C6-14 арил-тиокарбамоильную группу (например, фенилтиокарбамоил), моно- или ди-C7-16 аралкил-тиокарбамоильную группу (например, бензилтиокарбамоил, фенэтилтиокарбамоил), 5-14-членную ароматическую гетероциклилтиокарбамоильную группу (например, пиридилтиокарбамоил), сульфиногруппу, C1-6 алкилсульфинильную группу (например, метилсульфинил, этилсульфинил), сульфогруппу, C1-6 алкилсульфонильную группу, C6-14 арилсульфонильную группу, фосфоногруппу и моно- или ди-C1-6 алкилфосфоногруппу (например, диметилфосфоно, диэтилфосфоно, диизопропилфосфоно, дибутилфосфоно).
[0074]
В данном описании примеры «необязательно замещенной аминогруппы» включают аминогруппу, необязательно имеющую «1 или 2 заместителей, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкил-карбонильной группы, C6-14 арил-карбонильной группы, C7-16 аралкил-карбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкокси-карбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкил-карбамоильной группы, моно- или ди-C7-16 аралкил-карбамоильной группы, C1-6 алкилсульфонильной группы и C6-14 арилсульфонильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной аминогруппы включают аминогруппу, моно- или ди-(необязательно галогенированную C1-6 алкил) аминогруппу (например, метиламино, трифторметиламино, диметиламино, этиламино, диэтиламино, пропиламино, дибутиламино), моно- или ди-C2-6 алкениламиногруппу (например, диaллиламино), моно- или ди-C3-10 циклоалкиламиногруппу (например, циклопропиламино, циклогексиламино), моно- или ди-C6-14 ариламиногруппу (например, фениламино), моно- или ди-C7-16 аралкиламиногруппу (например, бензиламино, дибензиламино), моно- или ди-(необязательно галогенированную C1-6 алкил)-карбониламиногруппу (например, ацетиламино, пропиониламино), моно- или ди-C6-14 арил-карбониламиногруппу (например, бензоиламино), моно- или ди-C7-16 аралкил-карбониламиногруппу (например, бензилкарбониламино), моно- или ди-5-14-членную ароматическую гетероциклилкарбониламиногруппу (например, никотиноиламино, изоникотиноиламино), моно- или ди-3-14-членную неароматическую гетероциклилкарбониламиногруппу (например, пиперидинилкарбониламино), моно- или ди-C1-6 алкокси-карбониламиногруппу (например, трет-бутоксикарбониламино), 5-14-членную ароматическую гетероциклиламиногруппу (например, пиридиламино), карбамоиламиногруппу, (моно- или ди-C1-6 алкил-карбамоил)аминогруппу (например, метилкарбамоиламино), (моно- или ди-C7-16 аралкил-карбамоил)аминогруппу (например, бензилкарбамоиламино), C1-6 алкилсульфониламиногруппу (например, метилсульфониламино, этилсульфониламино), C6-14 арилсульфониламиногруппу (например, фенилсульфониламино), (C1-6 алкил)(C1-6 алкил-карбонил) аминогруппу (например, N-ацетил-N-метиламино) и (C1-6 алкил)(C6-14 арил-карбонил)аминогруппу (например, N-бензоил-N-метиламино).
[0075]
В данном описании примеры «необязательно замещенной карбамоильной группы» включают карбамоильную группу, необязательно имеющую «1 или 2 заместителей, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкил-карбонильной группы, C6-14 арил-карбонильной группы, C7-16 аралкил-карбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкокси-карбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкил-карбамоильной группы и моно- или ди-C7-16 аралкил-карбамоильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной карбамоильной группы включают карбамоильную группу, моно- или ди-C1-6 алкил-карбамоильную группу, моно- или ди-C2-6 алкенил-карбамоильную группу (например, диaллилкарбамоил), моно- или ди-C3-10 циклоалкил-карбамоильную группу (например, циклопропилкарбамоил, циклогексилкарбамоил), моно- или ди-C6-14 арил-карбамоильную группу (например, фенилкарбамоил), моно- или ди-C7-16 аралкил-карбамоильную группу, моно- или ди-C1-6 алкил-карбонил-карбамоильную группу (например, ацетилкарбамоил, пропионилкарбамоил), моно- или ди-C6-14 арил-карбонил-карбамоильную группу (например, бензоилкарбамоил) и 5-14-членную ароматическую гетероциклилкарбамоильную группу (например, пиридилкарбамоил).
[0076]
В данном описании примеры «необязательно замещенной тиокарбамоильной группы» включают тиокарбамоильную группу, необязательно имеющую «1 или 2 заместителей, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкил-карбонильной группы, C6-14 арил-карбонильной группы, C7-16 аралкил-карбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкокси-карбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкил-карбамоильной группы и моно- или ди-C7-16 аралкил-карбамоильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной тиокарбамоильной группы включают тиокарбамоильную группу, моно- или ди-C1-6 алкил-тиокарбамоильную группу (например, метилтиокарбамоил, этилтиокарбамоил, диметилтиокарбамоил, диэтилтиокарбамоил, N-этил-N-метилтиокарбамоил), моно- или ди-C2-6 алкенил-тиокарбамоильную группу (например, диaллилтиокарбамоил), моно- или ди-C3-10 циклоалкил-тиокарбамоильную группу (например, циклопропилтиокарбамоил, циклогексилтиокарбамоил), моно- или ди-C6-14 арил-тиокарбамоильную группу (например, фенилтиокарбамоил), моно- или ди-C7-16 аралкил-тиокарбамоильную группу (например, бензилтиокарбамоил, фенэтилтиокарбамоил), моно- или ди-C1-6 алкил-карбонил-тиокарбамоильную группу (например, ацетилтиокарбамоил, пропионилтиокарбамоил), моно- или ди-C6-14 арил-карбонил-тиокарбамоильную группу (например, бензоилтиокарбамоил) и 5-14-членную ароматическую гетероциклилтиокарбамоильную группу (например, пиридилтиокарбамоил).
[0077]
В данном описании примеры «необязательно замещенной сульфамоильной группы» включают сульфамоильную группу, необязательно имеющую «1 или 2 заместителей, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкил-карбонильной группы, C6-14 арил-карбонильной группы, C7-16 аралкил-карбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкокси-карбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкил-карбамоильной группы и моно- или ди-C7-16 аралкил-карбамоильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной сульфамоильной группы включают сульфамоильную группу, моно- или ди-C1-6 алкил-сульфамоильную группу (например, метилсульфамоил, этилсульфамоил, диметилсульфамоил, диэтилсульфамоил, N-этил-N-метилсульфамоил), моно- или ди-C2-6 алкенил-сульфамоильную группу (например, диaллилсульфамоил), моно- или ди-C3-10 циклоалкил-сульфамоильную группу (например, циклопропилсульфамоил, циклогексилсульфамоил), моно- или ди-C6-14 арил-сульфамоильную группу (например, фенилсульфамоил), моно- или ди-C7-16 аралкил-сульфамоильную группу (например, бензилсульфамоил, фенэтилсульфамоил), моно- или ди-C1-6 алкил-карбонил-сульфамоильную группу (например, ацетилсульфамоил, пропионилсульфамоил), моно- или ди-C6-14 арил-карбонил-сульфамоильную группу (например, бензоилсульфамоил) и 5-14-членную ароматическую гетероциклилсульфамоильную группу (например, пиридилсульфамоил).
[0078]
В данном описании примеры «необязательно замещенной гидроксигруппы» включают гидроксигруппу, необязательно имеющую «заместитель, выбранный из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкил-карбонильной группы, C6-14 арил-карбонильной группы, C7-16 аралкил-карбонильной группы, 5-14-членной ароматической гетероциклилкарбонильной группы, 3-14-членной неароматической гетероциклилкарбонильной группы, C1-6 алкокси-карбонильной группы, 5-14-членной ароматической гетероциклической группы, карбамоильной группы, моно- или ди-C1-6 алкил-карбамоильной группы, моно- или ди-C7-16 аралкил-карбамоильной группы, C1-6 алкилсульфонильной группы и C6-14 арилсульфонильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной гидроксигруппы включают гидроксигруппу, C1-6 алкоксигруппу, C2-6 алкенилоксигруппу (например, alллилокси, 2-бутенилокси, 2-пентенилокси, 3-гексенилокси), C3-10 циклоалкилоксигруппу (например, циклогексилокси), C6-14 арилоксигруппу (например, фенокси, нафтилокси), C7-16 аралкилоксигруппу (например, бензилокси, фенэтилокси), C1-6 алкил-карбонилоксигруппу (например, ацетилокси, пропионилокси, бутирилокси, изобутирилокси, пивалоилокси), C6-14 арил-карбонилоксигруппу (например, бензоилокси), C7-16 аралкил-карбонилоксигруппу (например, бензилкарбонилокси), 5-14-членную ароматическую гетероциклилкарбонилоксигруппу (например, никотиноилокси), 3-14-членную неароматическую гетероциклилкарбонилоксигруппу (например, пиперидинилкарбонилокси), C1-6 алкокси-карбонилоксигруппу (например, трет-бутоксикарбонилокси), 5-14-членную ароматическую гетероциклилоксигруппу (например, пиридилокси), карбамоилоксигруппу, C1-6 алкил-карбамоилоксигруппу (например, метилкарбамоилокси), C7-16 аралкил-карбамоилоксигруппу (например, бензилкарбамоилокси), C1-6 алкилсульфонилоксигруппу (например, метилсульфонилокси, этилсульфонилокси) и C6-14 арилсульфонилоксигруппу (например, фенилсульфонилокси).
[0079]
В данном описании примеры «необязательно замещенной сульфанильной группы» включают сульфанильную группу, необязательно имеющую «заместитель, выбранный из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы, C7-16 аралкильной группы, C1-6 алкил-карбонильной группы, C6-14 арил-карбонильной группы и 5-14-членной ароматической гетероциклической группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A», и галогенированную сульфанильную группу.
Предпочтительные примеры необязательно замещенной сульфанильной группы включают сульфанильную (-SH) группу, C1-6 алкилтиогруппу, C2-6 алкенилтиогруппу (например, aллилтио, 2-бутенилтио, 2-пентенилтио, 3-гексенилтио), C3-10 циклоалкилтиогруппу (например, циклогексилтио), C6-14 арилтиогруппу (например, фенилтио, нафтилтио), C7-16 аралкилтиогруппу (например, бензилтио, фенэтилтио), C1-6 алкил-карбонилтиогруппу (например, ацетилтио, пропионилтио, бутирилтио, изобутирилтио, пивалоилтио), C6-14 арил-карбонилтиогруппу (например, бензоилтио), 5-14-членную ароматическую гетероциклилтиогруппу (например, пиридилтио) и галогенированную тиогруппу (например, пентафтортио).
[0080]
В данном описании примеры «необязательно замещенной силильной группы» включают силильную группу, необязательно имеющую «1-3 заместителя, выбранных из C1-6 алкильной группы, C2-6 алкенильной группы, C3-10 циклоалкильной группы, C6-14 арильной группы и C7-16 аралкильной группы, каждая из которых необязательно имеет от 1 до 3 заместителей, выбранных из группы заместителей A».
Предпочтительные примеры необязательно замещенной силильной группы включают три-C1-6 алкилсилильную группу (например, триметилсилил, трет-бутил(диметил)силил).
[0081]
В настоящем описании примеры «гетероцикла» включают ароматический гетероцикл и неароматический гетероцикл, каждый из которых содержит в качестве кольцевого атома, кроме атома углерода, от 1 до 4 гетероатомов, выбранных из атома азота, атома серы и атом кислорода.
[0082]
В настоящем описании примеры «ароматического гетероцикла» включают 5-14-членный (предпочтительно, 5-10-членный) ароматический гетероцикл, содержащий в качестве кольцевого атома, кроме атома углерода, от 1 до 4 гетероатомов, выбранных из атом азота, атом серы и атом кислорода. Предпочтительные примеры «ароматического гетероцикла» включают 5- или 6-членные моноциклические ароматические гетероциклы, такие как тиофен, фуран, пиррол, имидазол, пиразол, тиазол, изотиазол, оксазол, изоксазол, пиридин, пиразин, пиримидин, пиридазин, 1,2,4-оксадиазол, 1,3,4-оксадиазол, 1,2,4-тиадиазол, 1,3,4-тиадиазол, триазол, тетразол, триазин и т. п.; и
8-14-членные конденсированные полициклические (предпочтительно би- или трициклические) ароматические гетероциклы, такие как бензотиофен, бензофуран, бензимидазол, бензоксазол, бензизоксазол, бензотиазол, бензизотиазол, бензотриазол, имидазопиридин, тиенопиридин, фуропиридин, пирролопиридин, пиразолопиридин, оксазолопиридин, тиазолопиридин, имидазопиразин, имидазопиримидин, тиенопиримидин, фуропиримидин, пирролопиримидин, пиразолопиримидин, оксазолопиримидин, тиазолопиримидин, пиразолопиримидин, пиразолотриазин, нафто[2,3-b]тиофен, феноксатиин, индол, изоиндол, 1Н-индазол, пурин, изохинолин, хинолин, фталазин, нафтиридин, хиноксалин, хиназолин, циннолин, карбазол, β-карболин, фенантридин, акридин, феназин, фенотиазин, феноксазин и тому подобное.
[0083]
В настоящем описании примеры «неароматического гетероцикла» включают 3-14-членный (предпочтительно, 4-10-членный) неароматический гетероцикл, содержащий в качестве кольцевого атома, кроме атома углерода, от 1 до 4 гетероатомов, выбранных из атом азота, атом серы и атом кислорода. Предпочтительные примеры «неароматического гетероцикла» включают 3-8-членные моноциклические неароматические гетероциклы, такие как азиридин, оксиран, тииран, азетидин, оксетан, тиетан, тетрагидротиофен, тетрагидрофуран, пирролин, пирролидин, имидазолин, имидазолидин, оксазолин, оксазолидин, пиразолин, пиразолидин, тиазолин, тиазолидин, тетрагидроизотиазол, тетрагидрооксазол, тетрагидроизоксазол, пиперидин, пиперазин, тетрагидропиридин, дигидропиридин, дигидротиопиран, тетрагидропиримидин, тетрагидропиридазин, дигидропиран, тетрагидропиран, тетрагидротиопиран, морфолин, тиоморфолин, азепан, диазепан, азепин, азокан, диазокан, оксепан и тому подобное; и
9-14-членные конденсированные полициклические (предпочтительно би или трициклические) неароматические гетероциклы, такие как дигидробензoфуран, дигидробензимидазол, дигидробензоксазол, дигидробензoтиазол, дигидробензизотиазол, дигидронафто[2,3-b] тиофен, тетрагидроизохинолин, тетрагидрохинолин, 4H-хинолизин, индолин, изоиндолин, тетрагидротиено[2,3-c]пиридин, тетрагидробензазепин, тетрагидрохиноксалин, тетрагидрофенантридин, гексагидрофенотиазин, гексагидрофеноксазин, тетрагидрофталазин, тетрагидронафтиридин, тетрагидрохиназолин, тетрагидроциннолин, тетрагидрокарбазол, тетрагидро-β-карболин, тетрагидроакридин, тетрагидрофеназин, тетрагидротиоксантен, октагидроизохинолин и тому подобное.
В данном описании примеры «азотсодержащего гетероцикликла» включают «гетероцикл», содержащий по меньшей мере один атом азота в качестве кольцевого атома.
[0084]
Определение каждого символа в формуле (I) подробно объясняется далее.
[0085]
A представляет собой необязательно замещенную насыщенную циклическую группу.
Примеры «насыщенной циклической группы» «необязательно замещенной насыщенной циклической группы», представленной A, включают C3-10 циклоалкильную группу и насыщенную гетероциклическую группу. Примеры «насыщенной гетероциклической группы» включают насыщенные группы из числа «неароматической гетероциклической группы», и ее конкретные примеры включают 3-8-членные насыщенные моноциклические неароматические гетероциклические группы, такие как азиридинил, азетидинил, пирролидинил, пиперидил, пиперазинил, морфолинил, тиоморфолинил, имидазолидинил, оксазолидинил, пиразолидинил, тиазолидинил, тетрагидроизотиазолил, тетрагидроизоксазолил, тетрагидропиримидинил, тетрагидропиридазинил, азепанил, диазепанил, азоканил, диазоканил, оксиранил, оксетанил, тетрагидрофурил, тетрагидропиранил, тииранилтират, тетрагидратиенил, тетрагидратиопиранил и тому подобное.
[0086]
«Насыщенная циклическая группа» «необязательно замещенной насыщенной циклической группы», представленной A, представляет собой C3-10 циклоалкильную группу, более предпочтительно C3-6 циклоалкильную группу (например, циклобутил, циклогексил), еще более предпочтительно циклическую группу или циклогексильную группу, в частности, циклобутильную группу.
[0087]
«Насыщенная циклическая группа» «необязательно замещенной насыщенной циклической группы», представленной A, необязательно замещена, например, заместителем (ями), выбранными из вышеупомянутых заместителей группы A. Число заместителей составляет, например, от 1 до 3. Когда число заместителей равно 2 или более, соответствующие заместители могут быть одинаковыми или разными. Кроме того, группа заместителей А необязательно дополнительно замещена заместителем (ями), выбранным из вышеупомянутой группы заместителей А. Число заместителей составляет, например, от 1 до 3. Когда число заместителей равно 2 или более, соответствующие заместители могут быть одинаковыми или разными.
[0088]
Предпочтительные примеры заместителя включают
(a) необязательно замещенную C6-14 арилоксигруппу (например, фенокси),
(b) необязательно замещенную C6-14 арилокси-C1-6 алкильную группу (предпочтительно C6-14 арилоксиметильную группу (например, феноксиметил)),
(c) необязательно замещенную C7-16 аралкилоксильную группу (например, бензилокси),
(d) необязательно замещенную C7-16 аралкилокси-C1-6 алкильную группу (предпочтительно C7-16 аралкилоксиметильную группу (например, бензилоксиметил)), и
(e) C1-6 алкильную группу (например, метил).
Более предпочтительные примеры заместителя включают
(a) необязательно замещенную C6-14 арилоксигруппу (например, фенокси),
(b) необязательно замещенную C6-14 арилокси-C1-6 алкильную группу (предпочтительно C6-14 арилоксиметильную группу (например, феноксиметил)), и
(c) C1-6 алкильную группу (например, метил).
Конкретные предпочтительные примеры заместителя включают
(a) необязательно замещенную C6-14 арилоксигруппу (например, фенокси), и
(b) необязательно замещенную C6-14 арилокси-C1-6 алкильную группу (предпочтительно C6-14 арилоксиметильную группу (например, феноксиметил)).
[0089]
Предпочтительные примеры заместителя «необязательно замещенной C6-14 арилоксигруппы», «необязательно замещенной C6-14 арилокси-C1-6 алкильной группы», «необязательно замещенной C7-16 аралкилоксигруппы» и «необязательно замещенной C7-16 аралкилокси-C1-6 алкильной группы» содержат атом галогена (например, атом фтора, атом хлора) и необязательно галогенированной C1-6 алкильной группы (например, метил, трифторметил).
[0090]
A предпочтительно представляет собой необязательно замещенную C3-10 циклоалкильную группу (предпочтительно, C3-6 циклоалкильную группу (например, циклобутил, циклогексил), особенно предпочтительно, циклобутил).
[0091]
A более предпочтительно представляет собой C3-10 циклоалкильную группу (предпочтительно C3-6 циклоалкильную группу (например, циклобутил, циклогексил), особенно предпочтительно, циклобутил)
замещенную 1-3 (предпочтительно 1) заместителями, выбранными из
(a) необязательно замещенную C6-14 арилоксигруппу (например, фенокси),
(b) необязательно замещенную C6-14 арилокси-C1-6 алкильную группу (предпочтительно C6-14 арилоксиметильную группу (например, феноксиметил)),
(c) необязательно замещенную C7-16 аралкилоксигруппу (например, бензилокси), и
(d) необязательно замещенную C7-16 аралкилокси-C1-6 алкильную группу (предпочтительно C7-16 аралкилоксиметильную группу (например, бензилоксиметил)), и
необязательно дополнительно замещенную 1-3 (предпочтительно 1) заместителями, выбранными из
(e) C1-6 алкильной группу (например, метил).
[0092]
A еще более предпочтительно представляет собой C3-10 циклоалкильную группу (предпочтительно, C3-6 циклоалкильную группу (например, циклобутил, циклогексил), особенно предпочтительно, циклобутил)
замещенную 1-3 (предпочтительно 1) заместителями, выбранными из
(a) C6-14 арилоксигруппы (например, фенокси), необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил),
(b) C6-14 арилокси-C1-6 алкильной группы (предпочтительно, C6-14 арилоксиметильной группы (например, феноксиметил)), необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил),
(c) C7-16 аралкилоксигруппы (например, бензилокси), необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил), и
(d) C7-16 аралкилокси-C1-6 алкильной группы (предпочтительно, C7-16 аралкилоксиметильной группы (например, бензилоксиметил)), необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил), и
необязательно дополнительно замещенных от 1 до 3 (предпочтительно 1) C1-6 алкильных групп (например, метил).
[0093]
A еще более предпочтительно представляет собой
(1) циклобутильную группу
замещенную 1-3 (предпочтительно 1) заместителями, выбранными из
(a) феноксигруппы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил),
(b) феноксиметильной группы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил),
(c) бензилоксигруппы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил), и
(d) бензилоксиметильной группы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил), и
необязательно дополнительно замещенных от 1 до 3 (предпочтительно 1) C1-6 алкильных групп (например, метил), или
(2) циклогексильной группы, замещенной 1-3 (предпочтительно 1) заместителями, выбранными из
(a) феноксигруппы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, трифторметил).
[0094]
A даже более предпочтительно представляет собой циклобутильную группу
замещенную одним заместителем, выбранным из
(a) феноксигруппы, замещенной 2 или 3 заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) C1-6 алкильной группы (например, метил), и
(b) феноксиметильной группы, замещенной 2 или 3 заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) C1-6 алкильной группы (например, метил), и
необязательно дополнительно замещенных от 1 до 3 (предпочтительно 1) C1-6 алкильных групп (например, метил).
[0095]
A особенно предпочтительно представляет собой циклобутильную группу, замещенную одним заместителем, выбранным из
(a) феноксигруппы, замещенной 3 атомами галогена (например, атом фтора), и
(b) феноксиметильной группы, замещенной 3 атомами галогена (например, атом фтора).
[0096]
В другом варианте осуществления изобретения, когда A представляет собой замещенную циклобутильную группу, один заместитель Y выбирают из
(a) необязательно замещенной C6-14 арилоксигруппы (например, фенокси),
(b) необязательно замещенной C6-14 арилокси-C1-6 алкильной группы (предпочтительно C6-14 арилоксиметильной группы (например, феноксиметил)),
(c) необязательно замещенной C7-16 аралкилоксигруппы (например, бензилокси), и
(d) необязательно замещенной C7-16 аралкилокси-C1-6 алкильной группы (предпочтительно, C7-16 аралкилоксиметильной группы (например, бензилоксиметил)),
предпочтительно замещенной в 3-положении в циклобутановом кольце, как показано на следующей частичной структуре.
[0097]
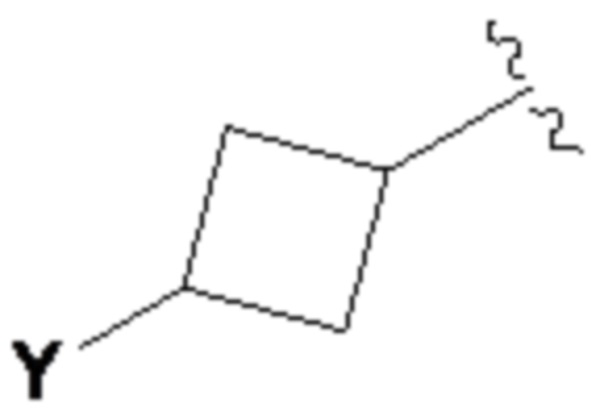
[0098]
В этом случае циклобутильная группа необязательно дополнительно замещена 1-3 (предпочтительно 1) заместителями, выбранными из
(e) C1-6 алкильной группы (например, метил).
Вышеупомянутая частичная структура предпочтительно представляет собой
[0099]
 .
.
[0100]
[0101]
L представляет собой связь или C1-3 алкиленовую группу, необязательно замещенную атомом(ами) галогена.
[0102]
Примеры «C1-3 алкиленовой группы» «необязательно замещенной C1-3 алкиленовой группы», представленной L, включают -CH2-, -(CH2)2-, -(CH2)3-, -CH(CH3)-, -C(CH3)2-, -CH(C2H5)-, -CH2-CH(CH3)-, -CH(CH3)-CH2- и тому подобное.
[0103]
L предпочтительно представляет собой связь или C1-3 алкиленовую группу (например, -CH2-).
L предпочтительно представляет собой связь.
[0104]
Кольцо D представляет собой кольцо, необязательно дополнительно замещенное C1-6 алкильной группой(ами), необязательно замещенной атомом(ами) галогена.
[0105]
Примеры «кольца» из «кольца, необязательно дополнительно замененной С1-6 алкильной групп(ы), необязательно замещенной атомом(ами) галогена», представлены кольцом D, включающим 4- или 5-членный азотсодержащий гетероцикл и тому подобное. Примеры «4- или 5-членного азотсодержащего гетероцикла» включают 4- или 5-членные кольца, содержащие по меньшей мере один атом азота в качестве образующего кольцо атома, из числа «гетероциклов», и их конкретные примеры включают азетидин, пирролидин и тому подобное.
[0106]
«Кольцо» из «кольца, необязательно дополнительно замещенного С1-6 алкильной группой(ами), необязательно замещенной атомом(ами) галогена», представленное кольцом D, предпочтительно представляет собой 4- или 5-членный азотсодержащий гетероцикл (например, азетидин, пирролидин), более предпочтительно азетидиновое кольцо или пирролидиновое кольцо, особенно предпочтительно азетидиновое кольцо.
[0107]
Кольцо D предпочтительно представляет собой 4- или 5-членный азотсодержащий гетероцикл (например, азетидин, пирролидин), необязательно дополнительно замещенный С1-6 алкильной группой(ами), необязательно замещенной атомом(ами) галогена.
Кольцо D более предпочтительно представляет собой 4- или 5-членный азотсодержащий гетероцикл (например, азетидин, пирролидин).
Кольцо D еще более предпочтительно представляет собой азетидиновое кольцо или пирролидиновое кольцо.
Кольцо D особенно предпочтительно представляет собой азетидиновое кольцо.
[0108]
n равно 1 или 2.
n предпочтительно равно 1.
[0109]
X представляет собой -O-, -CR1R2- или -NR3-.
R1, R2 и R3, каждый независимо, представляют собой атом водорода или заместитель. Примеры «заместителя» включают заместитель (и), выбранный из группы заместителей A.
[0110]
X предпочтительно представляет собой -O- или -CR1R2-.
Оба R1 и R2 предпочтительно представляют собой атомы водорода.
X более предпочтительно представляет собой -O- или -CH2-.
X еще более предпочтительно представляет собой -O-.
[0111]
Ra и Rb, каждый независимо, представляют собой атом водорода или C1-6 алкильную группу, необязательно замещенную атомом(ами) галогена.
Оба Ra и Rb предпочтительно представляют собой атомы водорода.
[0112]
Комбинация кольца D, n, X, Ra и Rb предпочтительно представляет собой
Кольцо D представляет собой 4 или 5-членный азотсодержащий гетероцикл (например, азетидин, пирролидин);
n равно 1 или 2;
X представляет собой -O- или -CH2-; и
оба Ra и Rb представляют собой атомы водорода,
более предпочтительно
кольцо D представляет собой азетидиновое кольцо или пирролидиновое кольцо;
n равно 1 или 2;
X представляет собой -O- или -CH2-; и
оба Ra и Rb представляют собой атомы водорода,
особенно предпочтительно
кольцо D представляет собой азетидиновое кольцо;
n равно 1;
X представляет собой -O-; и
оба Ra и Rb представляют собой атомы водорода.
[0113]
Предпочтительные примеры соединения (I) включают следующие соединения.
[0114]
[Соединение A]
Соединение (I), где
A представляет собой C3-10 циклоалкильную группу (предпочтительно C3-6 циклоалкильную группу (например, циклобутил, циклогексил), более конкретно, предпочтительно циклобутил)
замещенную 1-3 (предпочтительно 1) заместителями, выбранными из
(a) необязательно замещенную C6-14 арилоксигруппу (например, фенокси),
(b) необязательно замещенную C6-14 арилокси-C1-6 алкильную группу (предпочтительно C6-14 арилоксиметильную группу (например, феноксиметил)),
(c) необязательно замещенную C7-16 аралкилоксигруппу (например, бензилокси), и
(d) необязательно замещенную C7-16 аралкилокси-C1-6 алкильную группу (предпочтительно C7-16 аралкилоксиметильную группу (например, бензилоксиметил)), и
необязательно дополнительно замещенную 1-3 (предпочтительно 1) заместителями, выбранными из
(e) C1-6 алкильной группы (например, метил);
L представляет собой связь или C1-3 алкиленовую группу, необязательно замещенную атомом(ами) галогена;
Кольцо D представляет собой 4 или 5-членный азотсодержащий гетероцикл (например, азетидин, пирролидин), необязательно дополнительно замещенный С1-6 алкильной группой(ами), необязательно замещенной атомом(ами) галогена;
n равно 1 или 2;
X представляет собой -O- или -CR1R2-;
R1 и R2, каждый независимо, представляют собой атом водорода или заместитель; и
Ra и Rb, каждый независимо, представляют собой атом водорода или C1-6 алкильную группу, необязательно замещенную атомом(ами) галогена.
[0115]
[Соединение B]
Соединение (I), где
A представляет собой C3-10 циклоалкильную группу (предпочтительно C3-6 циклоалкильную группу (например, циклобутил, циклогексил), более конкретно, предпочтительно циклобутил)
замещенную 1-3 (предпочтительно 1) заместителями, выбранными из
(a) C6-14 арилоксигруппы (например, фенокси), необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил),
(b) C6-14 арилокси-C1-6 алкильной группы (предпочтительно, C6-14 арилоксиметильной группы (например, феноксиметил)), необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил),
(c) C7-16 аралкилоксигруппы (например, бензилокси), необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил), и
(d) C7-16 аралкилокси-C1-6 алкильной группы (предпочтительно, C7-16 аралкилоксиметильной группы (например, бензилоксиметил)), необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил), и
необязательно дополнительно замещенных от 1 до 3 (предпочтительно 1) C1-6 алкильных групп (например, метил);
L представляет собой связь или C1-3 алкиленовую группу (например, -CH2-);
Кольцо D представляет собой 4 или 5-членный азотсодержащий гетероцикл (например, азетидин, пирролидин);
n равно 1 или 2;
X представляет собой -O- или -CH2-; и
оба Ra и Rb представляют собой атомы водорода.
[0116]
[Соединение C]
Соединение (I), где
A представляет собой
(1) циклобутильную группу
замещенную 1-3 (предпочтительно 1) заместителями, выбранными из
(a) феноксигруппы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил),
(b) феноксиметильной группы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил),
(c) бензилоксигруппы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил), и
(d) бензилоксиметильной группы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, метил, трифторметил), и
необязательно дополнительно замещенных от 1 до 3 (предпочтительно 1) C1-6 алкильных групп (например, метил), или
(2) циклогексильной группы, замещенной 1-3 (предпочтительно 1) заместителями, выбранными из
(a) феноксигруппы, необязательно замещенной 1-4 (предпочтительно, 1-3, более предпочтительно, 2-3) заместителями, выбранными из
(i) атома галогена (например, атом фтора), и
(ii) необязательно замещенной C1-6 алкильной группы (например, трифторметил);
L представляет собой связь или C1-3 алкиленовую группу (например, -CH2-);
кольцо D представляет собой азетидиновое кольцо или пирролидиновое кольцо;
n равно 1 или 2;
X представляет собой -O- или -CH2-; и
оба Ra и Rb представляют собой атомы водорода.
[0117]
[Соединение D]
Соединение (I), где
A представляет собой циклобутильную группу,
замещенную одним заместителем, выбранным из
(a) феноксигруппы, замещенной 2 или 3 заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) C1-6 алкильной группы (например, метил), и
(b) феноксиметильной группы, замещенной 2 или 3 заместителями, выбранными из
(i) атома галогена (например, атом фтора, атом хлора), и
(ii) C1-6 алкильной группы (например, метил), и
необязательно дополнительно замещенных от 1 до 3 (предпочтительно 1) C1-6 алкильных групп (например, метил);
L представляет собой связь;
кольцо D представляет собой азетидиновое кольцо;
n равно 1;
X представляет собой -O-; и
оба Ra и Rb представляют собой атомы водорода.
[0118]
[Соединение E]
Соединение (I), где
A представляет собой циклобутильную группу, замещенную одним заместителем, выбранным из
(a) феноксигруппы, замещенной 3 атомами галогена (например, атом фтора), и
(b) феноксиметильной группы, замещенной 3 атомами галогена (например, атом фтора);
L представляет собой связь;
кольцо D представляет собой азетидиновое кольцо;
n равно 1;
X представляет собой -O-; и
оба Ra и Rb представляют собой атомы водорода.
[0119]
Конкретные примеры соединения (I) включают соединения из примеров от 1 до 64.
Среди них,
цис-3-((2,3,4-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат (Пример 16) или его соль;
цис-3-((2,4,6-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат (Пример 18) или его соль; и
цис-3-(2,4,6-трифторфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат (Пример 46) или его соль
являются предпочтительными.
[0120]
Когда соединение (I) представляет собой соль, примеры соли включают соли металлов, соли аммония, соли с органическим основанием, соли с неорганической кислотой, соли с органической кислотой и соли с основной или кислой аминокислотой. Предпочтительные примеры соли металла включают соли щелочных металлов, такие как соли натрия, соли калия и тому подобное; соли щелочноземельных металлов, такие как соли кальция, соли магния, соли бария и тому подобное; и соли алюминия. Предпочтительные примеры соли с органическим основанием включают соли с триметиламином, триэтиламином, пиридином, пиколином, 2,6-лутидином, этаноламином, диэтаноламином, триэтаноламином, циклогексиламином, дициклогексиламином, N, N'-дибензилэтилендиамином и тому подобное. Предпочтительные примеры соли с неорганической кислотой включают соли с соляной кислотой, бромистоводородной кислотой, азотной кислотой, серной кислотой, фосфорной кислотой и тому подобное. Предпочтительные примеры соли с органической кислотой включают соли с муравьиной кислотой, уксусной кислотой, трифторуксусной кислотой, фталевой кислотой, фумаровой кислотой, щавелевой кислотой, винной кислотой, малеиновой кислотой, лимонной кислотой, янтарной кислотой, яблочной кислотой, метансульфоновой кислотой, бензолсульфоновой кислотой, п-толуолсульфоновой кислотой и тому подобное. Предпочтительные примеры солей с основной аминокислотой включают соли с аргинином, лизином, орнитином и тому подобное. Предпочтительные примеры солей с кислой аминокислотой включают соли с аспарагиновой кислотой, глутаминовой кислотой и тому подобное. Среди них фармацевтически приемлемая соль является предпочтительной. Например, когда соединение имеет кислотную функциональную группу, примеры соли включают неорганические соли, такие как соли щелочных металлов (например, соль натрия, соль калия и т. д.), соли щелочноземельных металлов (например, соль кальция, соль магния и т. д.). и тому подобное, соль аммония и т. д., и когда соединение имеет основную функциональную группу, примеры соли включают соли с неорганической кислотой, такой как соляная кислота, бромистоводородная кислота, азотная кислота, серная кислота, фосфорная кислота и тому подобное, и соли с органической кислотой, такой как уксусная кислота, фталевая кислота, фумаровая кислота, щавелевая кислота, винная кислота, малеиновая кислота, лимонная кислота, янтарная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и тому подобное.
Когда соединение (I) содержит изомеры, такие как таутомеры, оптические изомеры, стереоизомеры, позиционные изомеры и вращательные изомеры, любой изомер или смесь также включаются в соединение по настоящему изобретению. Кроме того, когда соединение (I) содержит оптический изомер, данный оптический изомер, отделенный от рацемата, включается в соединение (I).
Соединение (I) может быть получено в кристаллической форме. Любая монокристаллическая форма или кристаллическая смесь могут быть включены в соединение (I).
Соединение (I) может представлять собой фармацевтически приемлемую сокристаллическую или сокристаллическую соль. В контексте данного документа сокристаллическая или сокристаллическая соль означает кристаллический материал, состоящий из двух или более уникальных твердых частиц при комнатной температуре, каждая из которых имеет отличительные физические характеристики, такие как структура, температура плавления и теплоты плавления, гигроскопичность, растворимость и стабильность. Сокристаллическая или сокристаллическая соль может быть получена согласно способу совместной кристаллизации, известному per se.
Соединение (I) может представлять собой сольват (например, гидрат) или несольват, и оба они включены в соединение (I).
Соединения, меченные или замещенные изотопами (например, 2H, 3H, 11C, 14C, 18F, 35S, 125I и т. д.) также включены в соединение (I). Соединение, меченное или замещенное изотопами, может использоваться, например, в качестве индикатора, используемого для позитронно-эмиссионной томографии (PET) (PET-индикатор), и ожидается, что он будет пригодным в области медицинской диагностики и тому подобном.
[0121]
Способ получения соединения по данному изобретению объяснен ниже.
[0122]
Соединение исходного материала и используемый реагент, а также соединение, полученное на каждой стадии в следующем способе получения, могут каждый находиться в форме соли, и примеры такой соли включают соли, аналогичные солям соединения по данному изобретению, и тому подобное.
[0123]
Когда соединение, полученное на каждой стадии, находится в свободной форме, оно может быть превращено в целевую соль в соответствии со способом, известным per se. Когда соединение, полученное на каждой стадии, представляет собой соль, оно может быть преобразовано в целевую свободную форму или другую соль в соответствии со способом, известным per se.
[0124]
Соединение, полученное на каждой стадии, можно использовать непосредственно в качестве используемой смеси или в качестве сырого продукта для следующей реакции. Альтернативно, соединение, полученное на каждой стадии, может быть выделено и очищено из реакционной смеси в соответствии со способом, известным per se, например, способами выделения, такими как концентрирование, кристаллизация, перекристаллизация, дистилляция, экстракция растворителем, фракционная перегонка, колоночная хроматография и тому подобное
[0125]
Когда исходное соединение и реагент, используемые на каждой стадии, являются коммерчески доступными, коммерчески доступный продукт также можно использовать непосредственно.
[0126]
В реакции на каждой стадии, хотя время реакции изменяется в зависимости от используемого реагента и растворителя, оно обычно составляет 1 мин - 48 ч, предпочтительно, 10 мин - 8 ч, если не указано иное.
[0127]
В реакции на каждой стадии, хотя температура реакции изменяется в зависимости от типа используемого реагента и растворителя, обычно она составляет -78°C - 300°C, предпочтительно -78°C - 150°C, если не указано иное.
[0128]
В реакции на каждой стадии, хотя давление изменяется в зависимости от типа используемого реагента и растворителя, оно обычно составляет 1-20 атм, предпочтительно, 1-3 атм, если не указано иное.
[0129]
Микроволновый синтезатор, такой как Initiator производства Biotage и тому подобное, может быть использован для реакции на каждой стадии. Хотя температура реакции меняется в зависимости от типа используемого реагента и растворителя, обычно комнатная температура составляет - 300°C, предпочтительно 50°C - 250°C, если не указано иное. Хотя время реакции меняется в зависимости от типа используемого реагента и растворителя, оно обычно составляет 1 мин - 48 ч, предпочтительно, 1 мин - 8 ч, если не указано иное.
[0130]
В реакции на каждой стадии реагент используется в количестве 0,5 эквивалента - 20 эквивалентов, предпочтительно 0,8 эквивалента - 5 эквивалентов относительно субстрата, если не указано иное. Когда реагент используется в качестве катализатора, реагент используется в количестве 0,001 эквивалента - 1 эквивалент, предпочтительно 0,01 эквивалента - 0,2 эквивалента относительно субстрата. Когда реагент используется в качестве реакционного растворителя, реагент используется в количестве растворителя.
[0131]
Если не указано иное, реакцию на каждой стадии проводят без растворителя или путем растворения или суспендирования исходного соединения в подходящем растворителе. Примеры растворителя включают описанные в Примерах и следующие растворители.
спирты: метанол, этанол, трет-бутиловый спирт, 2-метоксиэтанол и тому подобное;
простые эфиры: диэтиловый эфир, дифениловый эфир, тетрагидрофуран, 1,2-диметоксиэтан и тому подобное;
ароматические углеводороды: хлорбензол, толуол, ксилол и тому подобное;
насыщенные углеводороды: циклогексан, гексан и тому подобное;
амиды: N, N-диметилформамид, N-метилпирролидон и тому подобное;
галогенированные углеводороды: дихлорметан, четыреххлористый углерод и тому подобное;
нитрилы: ацетонитрил и тому подобное;
сульфоксиды: диметилсульфоксид и тому подобное;
ароматические органические основания: пиридин и тому подобное;
ангидриды: уксусный ангидрид и тому подобное;
органические кислоты: муравьиная кислота, уксусная кислота, трифторуксусная кислота и тому подобное;
неорганические кислоты: соляная кислота, серная кислота и тому подобное;
сложные эфиры: этилацетат и тому подобное;
кетоны: ацетон, метилэтилкетон и тому подобное;
вода.
Вышеупомянутый растворитель можно использовать в смеси двух или более его видов в соответствующем соотношении.
[0132]
Когда для реакции на каждой стадии используют основание, его примеры включают описанные в Примерах и следующих основаниях.
неорганические основания: гидроксид натрия, гидроксид магния, карбонат натрия, карбонат кальция, гидрокарбонат натрия и тому подобное;
органические основания: триэтиламин, диэтиламин, пиридин, 4-диметиламинопиридин, N, N-диметиланилин, 1,4-диазабицикло[2.2.2]октан, 1,8-диазабицикло[5.4.0]-7-ундецен, имидазол, пиперидин и тому подобное;
алкоксиды металлов: этоксид натрия, трет-бутоксид калия и тому подобное;
гидриды щелочных металлов: гидрид натрия и тому подобное;
амиды металлов: амид натрия, диизопропиламид лития, гексаметилдисилазид лития и тому подобное;
литий органические соединения: н-бутиллитий и тому подобное.
[0133]
Когда для реакции на каждой стадии используют кислоту или кислотный катализатор, их примеры включают те, которые описаны в примерах и следующих кислотах и кислотных катализаторах.
неорганические кислоты: соляная кислота, серная кислота, азотная кислота, бромистоводородная кислота, фосфорная кислота и тому подобное;
органические кислоты: уксусная кислота, трифторуксусная кислота, лимонная кислота, п-толуолсульфоновая кислота, 10-камфорсульфоновая кислота и тому подобное;
Кислота Льюиса: комплекс трифторида бора и диэтилового эфира, иодид цинка, безводный хлорид алюминия, безводный хлорид цинка, безводный хлорид железа и тому подобное.
[0134]
Если не указано иное, реакцию на каждой стадии проводят в соответствии со способом, известным per se, например способом, описанным в Jikken Kagaku Kouza, 5-е изд., том 13-19 (the Chemical Society of Japan ed.); Shin Jikken Kagaku Kouza, том 14-15 (the Chemical Society of Japan ed.); Fine Organic Chemistry, 2-е исправленное издание (L. F. Tietze, Th. Eicher, Nankodo); Organic Name Reactions, the Reaction Mechanism and Essence, исправленное издание (Hideo Togo, Kodansha); ORGANIC SYNTHESES Collective том I-VII (John Wiley & Sons Inc); Modern Organic Synthesis in the Laboratory A Collection of Standard Experimental Procedures (Jie Jack Li, OXFORD UNIVERSITY); Comprehensive Heterocyclic Chemistry III, том 1 -том 14 (Elsevier Japan); Strategic Applications of Named Reactions in Organic Synthesis (переведен Kiyoshi Tomioka, Kagakudojin); Comprehensive Organic Transformations (VCH Publishers Inc.), 1989 или т. п., или способом, описанным в примерах.
[0135]
На каждом этапе реакцию введения защитной группы или снятия защитной функциональной группы проводят в соответствии со способом, известным per se, например способом, описанным в «Protective Groups in Organic Synthesis, 4-е изд.», Wiley-Interscience, Inc., 2007 (Theodora W. Greene, Peter G. M. Wuts); «Protecting Groups 3-е изд.» Thieme, 2004 (P.J. Kocienski), или т. п., или способом, описанным в примерах.
Примеры защитной группы для гидроксигруппы спирта и тому подобное, фенольной гидроксигруппы включают защитные группы эфирного типа, такие как метоксиметиловый эфир, бензиловый эфир, трет-бутилдиметилсилиловый эфир, тетрагидропираниловый эфир и тому подобное; защитные группы типа сложного эфира карбоксилата, такие как уксусный эфир и тому подобное; защитные группы типа сульфонатного эфира, такие как метансульфонатный эфир и тому подобное; защитные группы типа карбонатного эфира, такие как трет-бутилкарбонат и тому подобное, и тому подобное
Примеры защитной группы для карбонильной группы альдегида включают защитные группы ацетального типа, такие как диметилацеталь и тому подобное; циклические защитные группы ацетального типа, такие как 1,3-диоксан и тому подобное, и тому подобное
Примеры защитной группы для карбонильной группы кетона включают защитные группы кетального типа, такие как диметилкеталь и тому подобное; защитные группы циклического типа кеталя, такие как 1,3-диоксан и тому подобное; защитные группы оксимного типа, такие как O-метилоксим и тому подобное; защитные группы гидразонового типа, такие как N, N-диметилгидразон и тому подобное, и тому подобное
Примеры защитной группы для карбоксигруппы включают защитные группы типа сложного эфира, такие как сложный метиловый эфир и тому подобное; защитные группы амидного типа, такие как N, N-диметиламид и тому подобное, и тому подобное
Примеры защитной группы для тиола включают защитные группы эфирного типа, такие как бензилтиоэфир и тому подобное; защитные группы типа сложного эфира, такие как тиоацетатный эфир, тиокарбонат, тиокарбамат и тому подобное, и тому подобное
Примеры защитной группы для аминогруппы и ароматического гетероцикла, такого как имидазол, пиррол, индол и тому подобное, включают защитные группы карбаматного типа, такие как бензилкарбамат и тому подобное; защитные группы амидного типа, такие как ацетамид и тому подобное; защитные группы типа алкиламина, такие как N-трифенилметиламин и тому подобное; защитные группы сульфонамидного типа, такие как метансульфонамид и тому подобное, и тому подобное.
Защитные группы могут быть удалены в соответствии со способом, известным per se, например, с использованием способа с применением кислоты, основания, облучения ультрафиолетом, гидразина, фенилгидразина, N-метилдитиокарбамат натрия, фторид тетрабутиламмония, ацетат палладия, триалкилсилилгалогенида (например, триметилсилилиодида, триметилсилилбромида) и тому подобного, способа восстановления и тому подобного.
[0136]
Когда реакцию восстановления проводят на каждой стадии, примеры используемого восстановителя включают гидриды металлов, такие как литийалюминийгидрид, триацетоксиборгидрид натрия, цианоборгидрид натрия, диизобутилалюминийгидрид (DIBAL-H), боргидрид натрия, триацетоксиборгидрид тетраметиламмония и тому подобное; бораны, такие как комплекс борана с тетрагидрофураном и тому подобное; никель Ренея; кобальт Ренея; водород; муравьиная кислота; триэтилсилан и тому подобное Когда углерод-углеродная двойная связь или тройная связь восстанавливается, может быть использован способ с применением катализатора, такого как палладий на угле, катализатор Линдлара и тому подобное.
[0137]
Когда реакцию окисления проводят на каждой стадии, примеры окислителя, которые следует использовать, включают пероксиды, такие как м-хлорпербензойная кислота (мХПБК), пероксид водорода, трет-бутилгидропероксид и тому подобное; перхлораты, такие как перхлорат тетрабутиламмония и тому подобное; хлораты, такие как хлорат натрия и тому подобное; хлориты, такие как хлорит натрия и тому подобное; периодаты, такие как периодат натрия и тому подобное; реагенты со гипервалентным иодом, такие как иодозилбензол и тому подобное; реагенты, содержащие марганец, такие как диоксид марганца, перманганат калия и тому подобное; производтсва свинца, такие как тетраацетат свинца и тому подобное; реагенты, содержащие хром, такие как хлорхромат пиридиния (PCC), дихромат пиридиния (PDC), реагент Джонса и тому подобное; соединения галогенов, такие как N-бромсукцинимид (NBS) и тому подобное; кислород; озон; комплекс триоксид серы-пиридин; тетраоксид осмия; диоксид селена; 2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ) и тому подобное
[0138]
Когда радикальную реакцию циклизации проводят на каждой стадии, примеры используемого инициатора радикальной реакции включают азосоединения, такие как азобисизобутиронитрил (AIBN) и тому подобное; водорастворимые радикальные инициаторы, такие как 4-4'-азобис-4-цианопентановая кислота (ACPA) и тому подобное; триэтилбор в присутствии воздуха или кислорода; бензоилпероксид и тому подобное. Примеры используемого радикального реагента включают трибутилстаннан, тристриметилсилилсилан, 1,1,2,2-тетрафенилдисилан, дифенилсилан, иодид самария и тому подобное.
[0139]
Когда реакцию Виттига проводят на каждой стадии, примеры используемого реагента Виттига включают алкилиденфосфораны и тому подобное. Алкилиденфосфораны могут быть получены в соответствии со способом, известным per se, например, путем взаимодействия соли фосфония с сильным основанием.
[0140]
Когда реакцию Хорнера-Эммонса проводят на каждой стадии, примеры используемых реагентов включают фосфоноацетаты, такие как метил-диметилфосфоноацетат, этил-диэтилфосфоноацетат и тому подобное; и основания, такие как гидриды щелочных металлов, литийорганические соединения и тому подобное.
[0141]
Когда реакцию Фриделя-Крафтса проводят на каждой стадии, в качестве реагента используют комбинацию кислоты Льюиса и хлорангидрида кислоты или комбинацию кислоты Льюиса и алкилирующего агента (например, алкилгалогенида, спирта, олефина). Альтернативно, вместо кислоты Льюиса также может быть использована органическая кислота или неорганическая кислота и ангидрид, такой как уксусный ангидрид и тому подобное, также он может быть использован вместо хлорангидрида кислоты.
[0142]
Когда ароматическую реакцию нуклеофильного замещения проводят на каждой стадии, в качестве реагента используются нуклеофил (например, амин, имидазол и т. д.) и основание (например, органическое основание и т. д.).
[0143]
Когда проводят реакцию нуклеофильного присоединения с карбанионом, реакцию нуклеофильного 1,4-присоединения (реакцию присоединения Михаэля) с карбанионом или реакцию нуклеофильного замещения карбанионом, и примеры оснований, которые будут использоваться для образования карбаниона, включают литийорганические соединения, алкоксиды металлов, неорганические основания, органические основания и тому подобное.
[0144]
Когда реакцию Гриньяра проводят на каждой стадии, примеры используемого реактива Гриньяра включают арилмагнийгалогениды, такие как фенилмагнийбромид и тому подобное; и алкилмагнийгалогениды, такие как метилмагнийбромид и тому подобное. Реагент Гриньяра может быть получен в соответствии со способом, известным per se, например, путем взаимодействия алкилгалогенида или арилгалогенида с металлическим магнием в эфире или тетрагидрофуране в качестве растворителя.
[0145]
Когда реакцию конденсации Кновенагеля проводят на каждой стадии, в качестве реагента используют соединение, имеющее активированную метиленовую группу с двумя электроноакцепторными группами (например, малоновая кислота, диэтилмалонат, малонодинитрил и т. д.) и основание (например, органическое основание, алкоксид металла, неорганическое основание).
[0146]
Когда реакцию Вильсмейера-Хаака проводят на каждой стадии, в качестве реагента используют фосфорилхлорид и производное амида (например, N, N-диметилформамид и т. д.).
[0147]
Когда реакцию азидирования спирта, алкилгалогенида или сульфоната проводят на каждой стадии, примеры азидирующего агента, который следует использовать, включают дифенилфосфорилазид (DPPA), триметилсилилазид, азид натрия и тому подобное. Например, для реакции азидирования спирта используют метод с использованием дифенилфосфорилазида и 1,8-диазабицикло[5.4.0]ундец-7-ена (DBU), метод с использованием триметилсилилазида и кислоты Льюиса и тому подобное.
[0148]
Когда реакцию восстановительного аминирования проводят на следующей стадии, примеры используемого восстановителя включают триацетоксиборгидрид натрия, цианоборогидрид натрия, водород, муравьиную кислоту и тому подобное. Когда субстрат представляет собой соединение амина, примеры используемого карбонильного соединения включают параформальдегид, альдегиды, такие как ацетальдегид и тому подобное, и кетоны, такие как циклогексанон и тому подобное. Когда субстрат представляет собой карбонильное соединение, примеры амина, которые следует использовать, включают аммиак, первичные амины, такие как метиламин и тому подобное; вторичные амины, такие как диметиламин и тому подобное.
[0149]
Когда реакцию Мицунобу проводят на следующей стадии, в качестве реагента используют азодикарбоксилат (например, диэтилазодикарбоксилат (DEAD), диизопропилазодикарбоксилат (DIAD) и т. д.) и трифенилфосфин.
[0150]
Когда реакцию этерификации, реакцию амидирования или реакцию образования мочевины проводят на следующей стадии, примеры используемых реагентов включают ацилгалогениды, такие как хлорангидриды кислот, бромангидриды кислот и тому подобное; активированные карбоновые кислоты, такие как ангидриды, активированные сложные эфиры, сульфаты и тому подобное Примеры активирующего агента карбоновой кислоты включают карбодиимидные конденсирующие агенты, такие как 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (WSCD) и тому подобное; триазиновые конденсирующие агенты, такие как n-гидрат 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиний хлорида (DMT-MM) и тому подобное; карбонатные конденсирующие агенты, такие как 1,1-карбонилдиимидазол (CDI) и тому подобное; дифенилфосфорилазид (DPPA); соль бензотриазол-1-илокси-трисдиметиламинофосфония (реагент BOP); иодид 2-хлор-1-метилпиридиния (реагент Мукайяма); тионилхлорид; низшие алкилгалогенформиаты, такие как этилхлорформиат и тому подобное; гексафторфосфорат O-(7-азабензотриазол-1-ил)-N, N,N',N'-тетраметилурония (HATU); серная кислота; их комбинации и тому подобное. Когда используют карбодиимидный конденсирующий агент, в реакционную систему можно добавить добавку, такую как 1-гидроксибензотриазол (HOBt), N-гидроксисукцинимид (HOSu), диметиламинопиридин (DMAP) и тому подобное.
[0151]
Когда реакции сочетания проводят на каждой стадии, примеры используемых металлических катализаторов включают соединения палладия, такие как ацетат палладия (II), тетракис(трифенилфосфин)палладий(0), дихлорбис(трифенилфосфин)палладий(II), дихлорбис(триэтилфосфин)палладий(II), трис(дибензил иденацетон)дипалладий(0), 1,1'-бис(дифенилфосфино)ферроценпалладий (II) хлорид и тому подобное; соединения никеля, такие как тетракис(трифенилфосфин)никель(0) и тому подобное; соединения родия, такие как трис(трифенилфосфин)родий (III) хлорид и тому подобное; соединения кобальта; соединения меди, такие как оксид меди, иодид меди (I) и тому подобное; соединения платины и тому подобное. Кроме того, основание может быть добавлено в реакционную систему, и его примеры включают неорганические основания и тому подобное.
[0152]
Когда реакцию тиокарбонилирования проводят на каждой стадии, в качестве тиокарбонилирующего агента обычно используют пентасульфид фосфора. Альтернативно, реагент, имеющий 1,3,2,4-дитиадифосфетан-2,4-дисульфидную структуру (например, 2,4-бис(4-метоксифенил)-1,3,2,4-дитиадифосфетан-2,4- дисульфид (реагент Лауссона) и т. д.) также можно использовать вместо пентасульфида фосфора.
[0153]
Когда реакцию галогенирования проводят на каждой стадии, примеры галогенирующего агента, который следует использовать, включают N-иодсукцинимид, N-бромсукцинимид (NBS), N-хлорсукцинимид (NCS), бром, сульфурилхлорид и тому подобное. Кроме того, реакция может быть ускорена путем воздействия инициатора радикальной реакции, такого как тепло, свет, бензоилпероксид, азобисизобутиронитрил и тому подобное на реакционную систему.
[0154]
Когда реакцию галогенирования гидроксигруппы проводят на каждой стадии, примеры галогенирующего агента, который следует использовать, включают галогеноводородные кислоты и галогенангидриды неорганических кислот, в частности, соляную кислоту, тионилхлорид, оксихлорид фосфора и тому подобное для хлорирования, 48% бромистоводородную кислоту и тому подобное для бромирования. Кроме того, может быть использован способ получения алкилгалогенида путем введения в реакцию спирта с трифенилфосфином и четыреххлористым углеродом или четырехбромистым углеродом или тому подобное. Альтернативно, также может быть использован двухстадийный способ получения алкилгалогенида, включающий превращение спирта в соответствующий сульфонат с последующим взаимодействием сульфоната с бромидом лития, хлоридом лития или иодидом натрия.
[0155]
Когда реакцию Арбузова проводят на каждой стадии, примеры используемых реагентов включают алкилгалогениды, такие как этилбромацетат и т. п.; и фосфиты, такие как триэтилфосфит, три(изопропил)фосфит и т. п.
[0156]
Когда реакцию этерификации сульфоната проводят на каждой стадии, примеры используемого сульфирующего агента включают метансульфонилхлорид, п-толуолсульфонилхлорид, метансульфоновый ангидрид, трифторметансульфоновый ангидрид, п-толуолсульфоновый ангидрид и т. п.
[0157]
Когда реакцию гидролиза проводят на каждой стадии, в качестве реагента используют кислоту или основание. Для реакции кислотного гидролиза трет-бутильного сложного эфира муравьиная кислота, триэтилсилан и т. п. могут быть добавлены к катиону трет-бутильной восстановительной ловушке, которая является побочным продуктом.
[0158]
Когда реакцию дегидратации проводят на каждой стадии, примеры используемого дегидратирующего агента включают серную кислоту, пентаоксид дифосфора, оксихлорид фосфора, N, N'-дициклогексилкарбодиимид, оксид алюминия, полифосфорную кислоту и тому подобное.
[0159]
Когда реакцию карбонилирования проводят на каждой стадии, примеры используемого реагента включают трифосген, 1,1'-карбонилбис-1Н-имидазол, дифосген, фенилхлорформиат и тому подобное.
[0160]
Соединение (I) может быть синтезировано в соответствии со следующими схемами. Каждый символ в формулах схем является таким, как определено выше, если не указано иное. P1 является «защитной группой для аминогруппы». Примеры «защитной группы для аминогруппы» включают трет-бутоксикарбонильную группу и тому подобное, в дополнение к приведенным в качестве примера вышеупомянутой защитной группы для аминогруппы. R4 представляет собой необязательно замещенную C1-6 алкильную группу (например, метил).
[0161]
Соединение (I) можно получить, подвергая соединение (2) и соединение (3) реакции карбонилирования.
[0162]
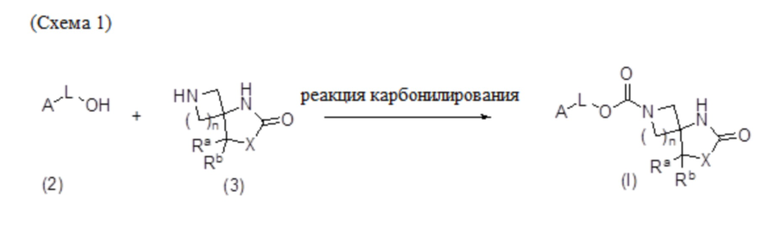
[0163]
Кроме того, при желании соединение (I) может быть синтезировано путем проведения реакции снятия защиты, реакции ацилирования, реакции алкилирования, реакции Мицунобу, реакции гидрирования, реакции окисления, реакции восстановления, реакции удлинения углеродной цепи, реакции галогенирования, реакции обмена заместителей, реакции сочетания, реакции нуклеофильного присоединения карбоаниона, реакция Гриньяра, реакция дезоксофторирования и тому подобное отдельного и одного или двух, или более из них в комбинации.
[0164]
Среди соединения (3), используемого на Схеме реакции 1, соединение (3-1), которое представляет собой соединение (3), где X представляет собой -O-, может быть получено из соединения (4) согласно следующему способу.
[0165]
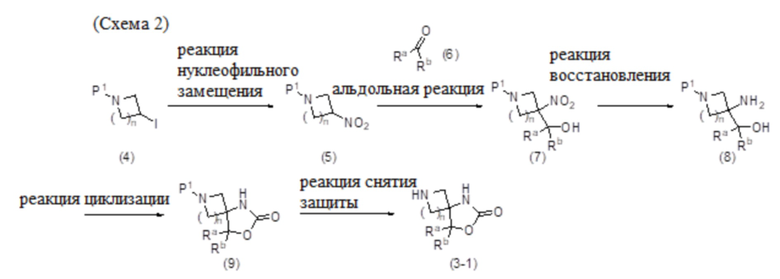
[0166]
Соединение (5) можно получить, подвергая соединение (4) реакции нуклеофильного замещения. Примеры нуклеофила включают нитрит натрия и тому подобное.
Соединение (7) можно получить, подвергая соединение (5) альдольной реакции с соединением (6) в присутствии основания. Примеры основания включают триэтиламин и тому подобное
Соединение (8) можно получить, подвергая соединение (7) реакции восстановления.
Соединение (9) можно получить, подвергая соединение (8) реакции циклизации с использованием реакции карбонилирования в присутствии основания. Примеры основания включают триэтиламин и тому подобное
Соединение (3-1) можно получить, подвергая соединение (9) реакции снятия защитной группы.
[0167]
Среди соединения (3), используемого на Схеме реакции 1, соединение (3-2), которое представляет собой соединение (3), где X представляет собой -CH2-, может быть получено из соединения (5) согласно следующему способу.
[0168]

[0169]
Соединение (11) можно получить, подвергая соединение (5) реакции Михаэля с соединением (10) в присутствии основания. Примеры основания включают DBU, карбонат калия и тому подобное.
Соединение (12) можно получить, подвергая соединение (11) реакции восстановления. В качестве условия реакции можно использовать комбинированное использование борогидрида натрия и гексагидрата хлорида никеля (II), использование никеля Ренея в атмосфере водорода и тому подобное.
Соединение (13) можно получить, подвергая соединение (12) реакции циклизации в присутствии основания. Примеры основания включают карбонат калия и тому подобное.
Соединение (3-2) можно получить, подвергая соединение (13) реакции снятия защитной группы.
[0170]
Среди соединения (3), используемого на Схеме реакции 1, соединение (3-3), которое представляет собой соединение (3), где X представляет собой -NR3-, может быть получено из соединения (7) согласно следующему способу. R5 представляет собой метил, п-метилфенил или трифторметил.
[0171]
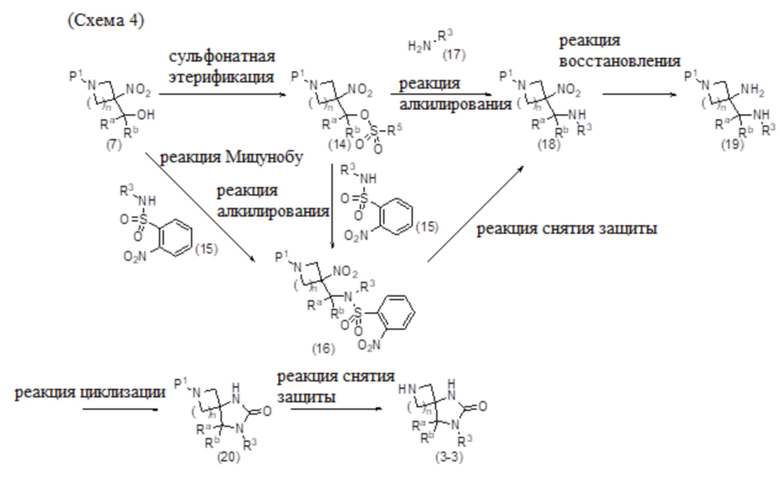
[0172]
Соединение (14) можно получить, подвергая соединение (7) сульфонатной этерификации в присутствии основания. Примеры основания включают триэтиламин, пиридин и тому подобное.
Соединение (16) можно получить, подвергая соединение (7) реакции Мицунобу с соединением (15). Соединение (16) также можно получить, подвергая соединение (14) реакции алкилирования соединением (15) в присутствии основания. Примеры основания включают вышеуказанные органические основания, неорганические основания, алкоксиды металлов, гидриды щелочных металлов и амиды металлов.
Соединение (18) можно получить, подвергая соединение (14) реакции алкилирования соединением (17) в присутствии основания. Примеры основания включают основания, приведенные в качестве примера в вышеупомянутой реакции алкилирования. Соединение (18) также можно получить, подвергая соединение (16) реакции снятия защиты в присутствии основания и нуклеофила. Примеры используемого нуклеофила включают тиогликолевую кислоту, тиофенол и тому подобное. Примеры основания включают триэтиламин, гидроксид лития, карбонат калия и тому подобное.
Соединение (20) можно получить, подвергая соединение (19) реакции циклизации. Реакция циклизации может быть проведена с использованием основания. Примеры используемого основания включают триэтиламин и тому подобное.
[0173]
Соединения (2), (4), (6), (10), (15) и (17), которые используются в качестве исходных материалов в каждой схеме, могут быть коммерчески доступными продуктами или могут быть получены в соответствии с известным per se способом.
[0174]
Исходное соединение и/или промежуточный продукт получения соединения (I) может образовывать соль. Соль конкретно не ограничена, если реакция может быть выполнена. Их примеры включают соли, подобные солям, необязательно образованным соединением (I), и тому подобное.
Что касается конфигурационных изомеров (E, Z-форм) соединения (I), они могут быть выделены и очищены, когда происходит изомеризация, например, в соответствии с обычными способами разделения, такими как экстракция, перекристаллизация, дистилляция, хроматография и тому подобное, для получения чистого соединения. Кроме того, соответствующий чистый изомер также может быть получен путем изомеризации двойной связи с использованием нагревания, кислотного катализатора, комплекса переходного металла, металлического катализатора, радикального катализатора, облучения светом, сильноосновного катализатора и тому подобного в соответствии с методом, описанным в Shin Jikken Kagaku Kouza 14 (The Chemical Society of Japan ed.), pages 251 to 253, 4th Edition Jikken Kagaku Kouza 19 (The Chemical Society of Japan ed.), pages 273 to 274 или аналогичным ему способом.
[0175]
Соединение (I) содержит стереоизомер в зависимости от типа заместителя, и каждый стереоизомер и их смесь включены в настоящее изобретение.
Соединение (I) может являться гидратом или негидратом.
Когда целевой продукт получают в свободной форме в результате вышеупомянутой реакции, его можно превратить в соль в соответствии с обычным способом, или когда целевой продукт получают в виде соли, его можно преобразовать в свободную форму или другую соль в соответствии с традиционно принятым способом. Полученное таким образом соединение (I) также может быть выделено и очищено из реакционной смеси в соответствии с известным способом, таким как перенос, концентрирование, экстракция растворителем, дистилляция, кристаллизация, перекристаллизация, хроматография и тому подобное.
Когда соединение (I) содержит конфигурационный изомер, диастереомер, конформер и тому подобное, при жедании каждый из них может быть выделен в соответствии с вышеупомянутыми способами разделения и очистки. Кроме того, когда соединение (I) является рацемическим, d-форма и l-форма могут быть выделены в соответствии с традиционно принятым оптическим разделением.
[0176]
Полученное таким образом соединение (I), другие промежуточные продукты его реакции и его исходные соединения могут быть выделены и очищены из реакционной смеси в соответствии со способом, известным per se, например, экстракцией, концентрированием, нейтрализацией, фильтрацией, дистилляцией, перекристаллизацией, колоночной хроматографией, тонкослойной хроматографией, препаративной высокоэффективной жидкостной хроматографией (препаративная ВЭЖХ), препаративной жидкостной хроматографией среднего давления (препаративная ЖХ среднего давления) и тому подобное.
[0177]
Соль соединения (I) может быть получена в соответствии со способом, известным per se. Например, когда соединение (I) представляет собой основное соединение, она может быть получена путем добавления неорганической кислоты или органической кислоты, или когда соединение (I) представляет собой кислотное соединение, путем добавления органического основания или неорганического основания.
Когда соединение (I) содержит оптический изомер, каждый оптический изомер и их смесь включены в объем настоящего изобретения, и при желании эти изомеры могут подвергаться оптическому разделению или могут быть получены соответственно в соответствии со способом, известным per se.
[0178]
Когда соединение (I) содержит конфигурационный изомер, диастереомер, конформер и тому подобное, при жедании каждый из них может быть выделен в соответствии с вышеупомянутыми способами разделения и очистки. Кроме того, когда соединение (I) является рацемическим, S-форма и R-форма могут быть выделены в соответствии с традиционно принятым оптическим разделением.
Когда соединение (I) содержит стереоизомер, каждый изомер и их смесь включены в настоящее изобретение.
[0179]
Ожидается, что соединение по данному изобретению будет пригодно для млекопитающих (например, мыши, крысы, хомяка, кролика, кошки, собаки, крупного рогатого скота, овцы, обезьяны, человека и т. д.) в качестве агента для профилактики или лечения заболеваний, например,
(1) психических заболеваний [например, депрессии, большой депрессии, биполярной депрессии, дистимического расстройства, эмоционального расстройства (сезонного аффективного расстройства и тому подобное), рецидивирующей депрессии, послеродовой депрессии, стрессового расстройства, симптома депрессии, мании, тревожности, генерализованного тревожного расстройства, синдрома тревоги, панического расстройства, фобии, социофобии, социального тревожного расстройства, обсессивного расстройства, посттравматического стрессового синдрома, посттравматического стрессового расстройства, синдрома Туретта, аутизм, синдрома ломкой Х-хромосомы, синдрома Ретта, расстройства адаптации, биполярного расстройства, невроза, шизофрении (например, положительного симптома, отрицательного симптома, когнитивного нарушения), синдрома хронической усталости, невроза тревоги, невроза навязчивых состояний, панического расстройства, эпилепсии, тревожного расстройства, тревоги, тревожного психического состояния, эмоциональной аномалии, циклотимии, нервного эретизма, слабости, зависимости, низкого полового влечения, синдрома дефицита внимания и гиперактивности (ADHD), психотической большой депрессии, резистентной к лечению депрессии, депрессивного расстройства, каталепсии, гебефренической шизофрении, параноидной шизофрении],
(2) нейродегенеративных заболеваний [например, болезни Альцгеймера, старческого слабоумия типа Альцгеймера, болезни Паркинсона, болезни Хантингтона, мультиинфарктной деменции, лобно-височной деменции, деменции по типу Паркинсона, прогрессирующего надъядерного паралича, синдрома Пика, синдрома Ниманна-Пика, кортико-базальной дегенерации, болезни Дауна, сосудистой деменции, постэнцефалитического паркинсонизма, деменции с тельцами Леви, ВИЧ-деменции, бокового амиотрофического склероза (ALS), болезни моторного нейрогенеза (MND), болезни Крейтцфельда-Якоба или прионовой болезни, церебрального паралича, прогрессирующего надъядерного паралича, черепно-мозговой травмы, глаукомы, рассеянного склероза, нейромиелита зрительного нерва (NMO), послеоперационной познавательной дисфункции (POCD), послеоперационного бреда (POD), бреда],
(3) возрастных когнитивных расстройств памяти [например, возрастных расстройств памяти, старческого слабоумия],
(4) расстройства сна [например, врожденные расстройства сна (например, психофизиологической бессонницы и тому подобного), приобретенного расстройства сна, расстройства циркадного ритма (например, синдрома смены часового пояса (jet lag), расстройства сна в сменную работу, нерегулярного характера бодрствования во сне, синдрома отсроченного наступления фаз сна, синдрома фазового опережения сна, 24-часового бодрствования без сна и тому подобное), парасомнии, нарушений сна, связанных с врожденным медицинским или психическим расстройством (например, хронических обструктивных заболеваний легких, болезни Альцгеймера, болезни Паркинсона, цереброваскулярной деменции, шизофрении, депрессии, невроза тревоги), стрессовой бессонницы, бессонницы, инсомнического невроза, синдрома апноэ во сне],
(5) угнетения дыхания, вызванного анестетиками, травматическим заболеванием или нейродегенеративным заболеванием и тому подобного,
(6) черепно-мозговой травмы, апоплексии головного мозга, невротической анорексии, расстройства пищевого поведения, нервной анорексии, гиперорексии, другого расстройства пищевого поведения, алкогольной зависимости, алкогольной зависимости, алкогольной амнезии, алкогольной паранойи, алкогольных предпочтений, алкогольной абстиненции, алкогольного безумия, алкогольного отравления, алкогольной ревности, алкогольной мании, алкогольно-зависимого психического расстройства, алкогольного безумия, фармакофилии, фармакофобии, фармакомании, отмены лекарственного средства, стрессовой головной боли, кататонической головной боли, диабетической невропатии, ожирения, диабета, мышечного спазма, болезни Меньера, вегетативной атаксии, алопеции, глаукомы, гипертонии, болезни сердца, тахикардии, застойной сердечной недостаточности, гипервентиляции, бронхиальной астмы, апноэ, синдрома внезапной детской смерти, воспалительного заболевания, аллергического заболевания, импотенции, климактерического расстройства, бесплодия, новообразования (например, рака, новообразований печени, новообразований толстой кишки, новообразований молочной железы, новообразований предстательной железы, нейробластомы, новообразований кости, новообразований полости рта, мастоцитомы, холангиокарциномы, карциномы легких Льюис и т. д.), синдрома иммунодефицита, вызванного ВИЧ-инфекцией, синдрома иммунодефицита, вызванного стрессом, цереброспинального менингита, акромегалии, недержания мочи, метаболического синдрома, остеопороза, язвенной болезни желудка, синдрома раздраженного кишечника, воспалительного заболевания кишечника, язвенного колита, болезни Крона, стрессового желудочно-кишечного расстройства, стрессовой рвоты, диареи, запора, послеоперационных гнойников, ревматоидного артрита, остеоартрита, функциональной диспепсии, гипералгезии, резистентности к инсулину, деменции боксеров, тошноты, рвоты, метастазирования новообразований, травм головного мозга, припадка, изменений массы тела, увеличения массы тела, потери веса, колита, алкоголизма, гипотермии, ожирения печени, атеросклероза, инфекции, мышечной спастичности, гипертонии, инсульта, злокачественных мигрирующих парциальных припадков в младенчестве, сахарного диабета, сахарного диабета 2 типа, дислипидемии, висцерального ожирения, глазной гипотензии, анорексии, фиброза, инфаркта миокарда, кахексии, индуцированного психотического расстройства, атаксии, синдрома истощения СПИДа, цирротической кардиомиопатии, уремического зуда, нейроповеденческих проявлений, синдрома тубулоинтерстициального нефрита и увеита, интерстициального цистита, пигментного ретинита, аутоиммунных заболеваний, болезни коронарных артерий, аспирин-индуцированной астмы, дефицита пула тромбоцитов, диабетической эмбриопатии, крапивницы Артуса, астмы, синдрома токсического масла, отита и тому подобного,
(7) боли (например, воспалительной боли, раковой боли, невропатической боли, острой боли, боли, связанной с периферической невропатией, центральной боли, фибромиалгии, сосудисто-болезненных кризов при серповидноклеточной анемии, рассеянной склероз-опосредованной спастичности или боли, функциональной боли в груди, синдрома сложной регионарной боли и т. д.),
(8) мигрени,
(9) отека мозга,
(10) церебральной ишемии, ишемии и тому подобного.
[0180]
Поскольку соединение по настоящему изобретению обладает превосходным ингибирующим действием на MAGL, можно ожидать превосходного профилактического или терапевтического эффекта для вышеупомянутых заболеваний.
[0181]
Поскольку соединение по настоящему изобретению обладает превосходным ингибирующим действием на MAGL, можно ожидать превосходный профилактический или терапевтический эффект при нейродегенеративных заболеваниях (например, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, боковом амиотрофическом склерозе, черепно-мозговой травме, глаукоме, рассеянном склерозе и т. д.), тревожном расстройстве, болях (например, воспалительной боли, раковой боли, нейрогенной боли и т. д.), эпилепсии, депрессии и тому подобном, в частности болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, боковом амиотрофическом склерозе, рассеянном склерозе, тревожном расстройстве, боли, эпилепсии или депрессии.
[0182]
Соединение (I) может быть использовано в качестве пролекарства.
[0183]
Пролекарство соединения (I) означает соединение, которое превращается в соединение (I) по реакции под действием фермента, желудочной кислоты и т. д. в физиологических условиях в живом организме, то есть соединение, которое превращается в соединение (I) с помощью окисления, восстановления, гидролиза и т. д. ферментом; соединение, которое превращается в соединение (I) путем гидролиза и т. д. желудочной кислотой и т. д.
[0184]
Пролекарством для соединения (I) может быть соединение, полученное путем подвергания аминогруппы в соединении (I) ацилированию, алкилированию или фосфорилированию (например, соединение, полученное путем подвергания аминогруппы в соединении (I) эйкозаноилированию, аланилированию, пентиламинокарбонилированию, (5-метил-2-оксо-1,3-диоксолен-4-ил)метоксикарбонилированию, тетрагидрофуранилированию, пирролидилметилированию, пивалоилоксиметилированию или трет-бутиированию и т. д.); соединение, полученное путем подвергания гидроксигруппы в соединении (I) ацилированию, алкилированию, фосфорилированию или борированию (например, соединение, полученное путем подвергания гидроксигруппы в соединении (I) ацетилированию, пальмитоилированию, пропаноилированию, пивалоилированию, сукцинилированию, фумарилированию, аланилированию или диметиламинометилкарбонилированию и т. д.); соединение, полученное подверганием карбоксильной группы в соединении (I) этерификации или амидированию (например, соединение, полученное подверганием карбоксильной группы в соединении (I) этил-этерификации, фенилэтерификации, карбоксиметил-этерификации, диметиламинометил-этерификации, пивалоилоксиметил-этерификации, этоксикарбонилоксиэтил-этерификации, фталидил-этерификации, (5-метил-2-оксо-1,3-диоксолен-4-ил)-этерификации, циклогексилоксикарбонилэтил-этерификации или метиламидированию и т. д.) и тому подобное. Любое из этих соединений может быть получено из соединения (I) известным per se способом. Пролекарство соединения (I) может представлять собой соединение, которое превращается в соединение (I) в физиологических условиях, как описано в Development of Pharmaceutical Products, vol. 7, Molecule Design, 163-198, Hirokawa Shoten (1990).
[0185]
Соединение по настоящему изобретению обладает превосходной кинетикой in vivo (например, время полужизни лекарственного средства в плазме, внутримозговая переносимость, метаболическая стабильность), показывает низкую токсичность (например, более высокое качество лекарственного средства с точки зрения острой токсичности, хронической токсичности, генетической токсичности, репродуктивной токсичности, кардиотоксичности, лекарственного взаимодействия, канцерогенности и т. д.). Соединение по настоящему изобретению непосредственно используется в качестве лекарственного средства или фармацевтической композиции, смешанной с фармацевтически приемлемым носителем или тому подобным, для безопасного перорального или парентерального введения млекопитающим (например, людям, обезьянам, коровам, лошадям, свиньям, мышам, крысам, хомякам, кроликам, кошкам, собакам, овцам и козам). Примеры «парентерального» включают внутривенное, внутримышечное, подкожное, внутриорганное, интраназальное, внутрикожное, инстилляционное, интрацеребральное, интраректальное, интравагинальное, внутрибрюшинное и внутриопухолевое введения, введение в окрестности опухоли и т. д. и прямое введение в поражение.
[0186]
Хотя доза соединения по настоящему изобретению варьируется в зависимости от пути введения, симптома и тому подобного, когда, например, соединение вводят перорально пациенту с болезнью Альцгеймера (взрослый, масса тела, например, 40-80 кг, например, 60 кг), она представляет, например, 0,001-1000 мг/кг масса тела/день, предпочтительно 0,01-100 мг/кг масса тела/день, более предпочтительно 0,1-10 мг/кг масса тела/день. Это количество можно вводить от 1 до 3 порций в день.
[0187]
Лекарственное средство, содержащее соединение по настоящему изобретению, можно использовать отдельно или в виде фармацевтической композиции, содержащей соединение по настоящему изобретению и фармацевтически приемлемый носитель, в соответствии со способом, известным per se, как и способ получения фармацевтического препарата (например, способ описано в японской фармакопее и т. д.). Лекарственное средство, содержащее соединение по настоящему изобретению, можно безопасно вводить в форме, например, таблетки (включая таблетку, покрытую сахаром, таблетку, покрытую оболочкой, подязычную таблетку, таблетку для перорального распада, буккальную и тому подобное), пилюли, порошка, гранулы, капсулы (включая мягкую капсулу, микрокапсулу), троше, сиропа, жидкости, эмульсии, суспензии, препарата с контролируемым высвобождением (например, препарат с немедленным высвобождением, препарат с отсроченным высвобождением, микрокапсула с замедленным высвобождением), аэрозоля, пленки (например, перорально распадающаяся пленка, адгезивная пленка к слизистой оболочки полости рта), инъекции (например, подкожная инъекция, внутривенная инъекция, внутримышечная инъекция, внутрибрюшинная инъекция), капельной инфузии, препарата трансдермального абсорбционного типа, мази, лосьони, адгезивного препарата, суппозитория (например, ректальный суппозиторий, вагинальный суппозиторий), пеллет, назального препарата, препарата для легких (ингалянт), глазных капель и тому подобного, перорально или парентерально (например, внутривенно, внутримышечно, подкожно, внутриорганно, интраназально, внутрикожно, инстилляционно, интрацеребрально, интраректально, интравагинально, внутрибрюшинно и вводят в очаг поражения).
[0188]
В качестве вышеупомянутого «фармацевтически приемлемого носителя» могут быть использованы различные органические или неорганические носители, обычно используемые в качестве материалов для приготовления (исходных материалов). Например, наполнитель, смазывающее вещество, связующее, дезинтегрант и тому подобное используют для твердых препаратов, а растворитель, солюбилизирующий агент, суспендирующий агент, изотонический агент, буфер, успокаивающий агент и тому подобное используют для жидких препаратов. Там, где это необходимо, также могут быть использованы добавки для подготовки, такие как консервант, антиоксидант, краситель, подсластитель и тому подобное.
Примеры эксципиента включают лактозу, сахарозу, D-маннит, крахмал, кукурузный крахмал, кристаллическую целлюлозу, легкую безводную кремниевую кислоту и тому подобное.
Примеры смазывающего вещества включают стеарат магния, стеарат кальция, тальк, коллоидный диоксид кремния и тому подобное.
Примеры связующего вещества включают кристаллическую целлюлозу, белый сахар, D-маннит, декстрин, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон, крахмал, сахарозу, желатин, метилцеллюлозу, карбоксиметилцеллюлозу натрия и тому подобное.
Примеры разрыхлителя включают крахмал, карбоксиметилцеллюлозу, карбоксиметилцеллюлозу кальция, карбоксиметилкрахмал натрия, L-гидроксипропилцеллюлозу и тому подобное.
Примеры растворителя включают воду для инъекций, спирт, пропиленгликоль, макрогол, кунжутное масло, кукурузное масло, оливковое масло и тому подобное.
Примеры солюбилизирующего агента включают полиэтиленгликоль, пропиленгликоль, D-маннит, бензилбензоат, этанол, трисаминометан, холестерин, триэтаноламин, карбонат натрия, цитрат натрия и тому подобное.
Примеры суспендирующего агента включают поверхностно-активные вещества, такие как стеарилтриэтаноламин, лаурилсульфат натрия, лауриламинопропионовая кислота, лецитин, хлорид бензалкония, хлорид бензетония, моностеарат глицерина и тому подобное; гидрофильные полимеры, такие как поливиниловый спирт, поливинилпирролидон, натрий-карбоксиметилцеллюлоза, метилцеллюлоза, гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза и тому подобное; и тому подобное.
Примеры агента изотоничности включают глюкозу, D-сорбит, хлорид натрия, глицерин, D-маннит и тому подобное.
Примеры буфера включают буферные растворы, такие как фосфаты, ацетаты, карбонаты, цитраты и тому подобное.
Примеры успокаивающего агента включают бензиловый спирт и тому подобное.
Примеры консерванта включают п-оксибензоаты, хлорбутанол, бензиловый спирт, фенилэтиловый спирт, дегидроуксусную кислоту, сорбиновую кислоту и тому подобное.
Примеры антиоксиданта включают сульфит, аскорбиновую кислоту, α-токоферол и тому подобное.
[0189]
Хотя фармацевтическая композиция варьируется в зависимости от лекарственной формы, способа введения, носителя и тому подобного, она может быть получена в соответствии с обычным способом путем добавления соединения по настоящему изобретению в пропорции обычно 0,01-100% (масс./масс.), предпочтительно, 0,1-95% (масс./масс.) от общего количества препарата.
[0190]
Соединение по настоящему изобретению можно использовать в сочетании с другими активными ингредиентами (далее в настоящем документе оно будет сокращено как сопутствующее лекарственное средство).
[0191]
Примеры сопутствующего лекарственного средства включают следующие. бензодиазепин (хлордиазепоксид, диазепам, клоразепат калия, лоразепам, клоназепам, алпразолам и т. д.), ингибитор кальциевых каналов L-типа (прегабалин и т. д.), трициклический или тетрациклический антидепрессант (имипрамин гидрохлорид, амитриптилин гидрохлорид, дезипрамин гидрохлорид) селективный ингибитор обратного захвата серотонина (малеат флувоксамина, флуоксетин гидрохлорид, циталопрам гидробромид, сертралин гидрохлорид, пароксетин гидрохлорид, эсциталопрам оксалат и т. д.), ингибитор обратного захвата серотонина-норадреналина (венлафаксин гидрохлорид, дулоксетин гидрохлорид, десвенлафаксин гидрохлорид и т. д.), ингибитор обратного захвата норадреналина (ребоксетин мезилат и т. д.),ингибитор обратного захвата норадреналина-дофамина (бупропион гидрохлорид и т. д.), миртазапин, тразодон гидрохлорид, нефазодон гидрохлорид, бупропион гидрохлорид, септипилин малеат, агонист 5-НТ1A (буспирон гидрохлорид, тандоспирон цитрат, осемозотан гидрохлорид и т. д.), антагонист 5-HT3 (циамемазин и т. д.), неселективный сердечный β-ингибитор (пропранолол гидрохлорид, окспренолол гидрохлорид и т. д.), антагонист гистамина Н1 (гидроксизин гидрохлорид и т. д.), терапевтическое лекарственное средство для лечения шизофрении (хлорпромазин, галоперидол, сульпирид, клозапин, трифлуоперазин гидрохлорид, флуфеназин гидрохлорид, оланзапин, кветиапина фумарат, рисперидон, арипипразол и т. д.), антагонист CRF, другой препарат против тревожности (мепробамат и т. д.), антагонист тахикинина (MK-869, саридутант и т. д.), медикамент, действующий на метаботропный рецептор глутамата, антагонист CCK, β3 антагонист адреналина (амибегрон гидрохлорид и т. д.), ингибитор GAT-1 (тиагабин гидрохлорид и т. д.), ингибитор кальциевых каналов N-типа, ингибитор карбоангидразы II, агонист глициновой группы NMDA, антагонист NMDA (мемантин и т. д.), агонист периферических бензодиазепиновых рецепторов, антагонист вазопрессина, антагонист вазопрессина V1b, антагонист вазопрессина V1a, ингибитор фосфодиэстеразы, антагонист опиоидов, агонист опиоидов, уридин, агонист рецепторов никотиновой кислоты, гормон щитовидной железы (T3, T4), TSH, TRH, ингибитор MAO (фенелзин сульфат, транилципромин сульфат, моклобемид и т. д.), антагонист 5-HT2A, обратный агонист 5-HT2A, ингибитор COMT (энтакапон и т. д.), терапевтический препарат для лечения биполярного расстройства (карбонат лития, вальпроат натрия, ламотриджин, рилузол, фелбамат и т. д.), антагонист каннабиноида CB1 (римонабант и т. д.), ингибитор FAAH, ингибитор натриевых каналов, препарат против ADHD (метилфенидат гидрохлорид), метамфетамин гидрохлорид и т. д.), терапевтический препарат от алкоголизма, терапевтический препарат от аутизма, терапевтический препарат от синдрома хронической усталости, терапевтический препарат от спазма, терапевтический препарат от синдрома фибромиалгии, терапевтический препарат от головной боли, терапевтическое лекарство от бессонницы (этизолам, зопиклон, триазолам, золпидем, рамелтеон, индиплон и т. д.), терапевтическое лекарство от курения, терапевтическое лекарство от миастении, лекарственное средство от инфаркта мозга, терапевтическое лекарство от мании, лекарственное средство от гиперсомнии, лечебное лекарство от боли, терапевтическое лекарство от дистимии, терапевтическое лекарство от вегетативной атаксии, терапевтическое лекарство от сексуальной дисфункции у мужчин и женщин, терапевтическое лекарство от мигрени, терапевтическое лекарство от патологического игрока, терапевтическое лекарство от синдрома беспокойных ног, терапевтическое лекарство от наркотической зависимости, терапевтическое лекарство от алкогольного синдрома, лекарственное средство для лечения синдрома раздраженного кишечника, лекарственное средство для лечения болезни Альцгеймера (донепезил, галантамин, мемантин, ривастигмин и т.д.), терапевтическое лекарственное средство для лечения болезни Паркинсона (леводопа, карбидопа, бенсеразид, селегилин, зонисамид, энтакапон, амантадин, талипексол, прамипексол, апоморфин, каберголин, бромкриптин, истрадефиллин, тригексифенидил, прометазин, перголид, и т. д.), терапевтический препарат для лечения болезни Хантингтона (хлорпромазин, гидрохлорид, галоперидол, резерпин и т. д.), терапевтический препарат для лечения ALS (рилузол и т. д., нейротрофический фактор и т. д.), терапевтический препарат для лечения рассеянного склероза (молекулярно-таргетный препарат, такой как финголимод, интерферон бета 1b, натализумаб и тому подобное, и т.д.), противоэпилептический препарат (фенитоин, карбамазепин, фенобарбитал, примидон, зонисамид, вальпроат натрия, этосуксимид, диазепам, нитразепам, клоназепам, клобазам, габапентин, топирамат, ламотриджин, леветирацетам, стирипентол, руфинамид, и т.д.), терапевтическое лекарственное средство для нарушения липидов, такое как понижающее холестерин лекарственное средство (ряд статинов (правастатин натрия, атровастатин, симвастатин, розувастатин и т. д.), фибрат (клофибрат и т. д.), ингибитор сквален-синтетазы), терапевтическое лекарственное средство для ненормального поведения или подавления дромомании вследствие слабоумия (седативные средства, лекарство от тревожности и т. д.), ингибитор апоптоза, лекарство от ожирения, лекарственное средство для лечения диабета, лекарственное средство для лечения гипертонии, лекарственное средство для лечения гипотонии, лекарственное средство для лечения ревматизма (DMARD), противораковое средство, лекарственное средство для лечения паращитовидной железы (PTH), антагонист кальциевого рецептора, половой гормон или его производное (прогестерон, эстрадиол, эстрадиол бензоат и т. д.), стимулятор дифференцировки нейронов, стимулятор регенерации нервов, нестероидный противовоспалительный препарат (мелоксикам, теноксикам, индометацин, ибупрофен, целекоксиб, рофекоксиб, аспирин и т. д.), стероид (дексаметазон, ацетат кортизона и т. д.), анти-цитокиновый препарат (ингибитор TNF, ингибитор киназы MAP и т. д.), лекарственное средство на основе антител, нуклеиновая кислота или производное нуклеиновой кислоты, аптамерное лекарственное средство и тому подобное.
[0192]
Комбинируя соединение по настоящему изобретению и сопутствующее лекарственное средство, достигается превосходный эффект, такой как
(1) доза может быть уменьшена по сравнению с однократным введением соединения по настоящему изобретению или сопутствующего лекарственного средства,
(2) лекарственное средство для комбинирования с соединением по настоящему изобретению может быть выбрано в соответствии с патологическим состоянием пациентов (легкий случай, тяжелый случай и тому подобное),
(3) период лечения может быть установлен более длительным путем выбора сопутствующего лекарственного средства, обладающего другим действием и механизмом, из соединения по настоящему изобретению,
(4) длительный лечебный эффект может быть достигнут путем выбора сопутствующего лекарственного средства, обладающего другим действием и механизмом, из соединения по настоящему изобретению,
(5) синергетический эффект может быть достигнут при комбинированном использовании соединения по настоящему изобретению и сопутствующего лекарственного средства и тому подобного.
[0193]
Здесь и далее соединение по настоящему изобретению и сопутствующее лекарственное средство, используемое в комбинации, называют «комбинированным агентом по настоящему изобретению».
При использовании комбинированного агента по настоящему изобретению время введения соединения по настоящему изобретению и сопутствующего лекарственного средства не ограничено, и соединение по настоящему изобретению или его фармацевтическую композицию и сопутствующее лекарственное средство или его фармацевтическую композицию могут вводить субъекту введения одновременно или могут быть введены в разное время. Дозировка сопутствующего лекарственного средства может быть определена в соответствии с клинически использованной дозой и может быть соответствующим образом выбрана в зависимости от субъекта введения, пути введения, заболевания, комбинации и тому подобное
Способ введения сопутствующего лекарственного средства по настоящему изобретению конкретно не ограничен, и достаточно, чтобы соединение по настоящему изобретению и сопутствующее лекарственное средство были объединены при введении. Примеры такого режима администрирования включают следующие способы:
(1) введение одного препарата, полученного одновременной обработкой соединения по настоящему изобретению и сопутствующего лекарственного средства, (2) одновременное введение двух видов препаратов соединения по настоящему изобретению и сопутствующего лекарственного средства, которые были получены отдельно, одним и тем же путем введения, (3) введение двух видов препаратов соединения по настоящему изобретению и сопутствующего лекарственного средства, которые были получены отдельно, одним и тем же путем введения в шахматном порядке, (4) одновременное введение двух видов препаратов соединения по настоящему изобретению и сопутствующего лекарственного средства, которые были получены отдельно, различными путями введения, (5) введение двух видов препаратов соединения по настоящему изобретению и сопутствующего лекарственного средства, которые были получены отдельно, различными путями введения в шахматном порядке (например, введение в порядке соединения по настоящему изобретению и сопутствующего лекарственного средства или в обратном порядке) и тому подобное.
[0194]
Комбинированный агент по настоящему изобретению проявляет низкую токсичность. Например, соединение по настоящему изобретению или (и) вышеупомянутое сопутствующее лекарственное средство может быть объединено с фармакологически приемлемым носителем в соответствии с известным способом для приготовления фармацевтической композиции, такой как таблетки (включая таблетку с сахарным покрытием и таблетку с пленочным покрытием), порошки, гранулы, капсулы (включая мягкие капсулы), жидкости, инъекции, суппозитории, агенты замедленного высвобождения и т. д. Эти композиции можно безопасно вводить перорально или неперорально (например, местно, ректально, внутривенно и т. д.). Инъекцию можно вводить внутривенно, внутримышечно, подкожно или путем внутриорганного введения или непосредственно в очаг поражения.
Примеры фармакологически приемлемых носителей, используемых для получения комбинированного агента по настоящему изобретению, включают аналогичные вышеупомянутым носителям.
[0195]
Соотношение смешивания соединения по настоящему изобретению с сопутствующим лекарственным средством в комбинированном средстве по настоящему изобретению может быть соответствующим образом выбрано в зависимости от субъекта введения, пути введения, заболеваний и тому подобного.
Например, содержание соединения по настоящему изобретению в комбинированном агенте по настоящему изобретению различается в зависимости от формы препарата и обычно от около 0,01 до около 100% масс., предпочтительно, от около 0,1 до около 50% масс., еще более предпочтительно, от около 0,5 до около 20% масс. в расчете на препарат. Содержание сопутствующего лекарственного средства в комбинированном агенте по настоящему изобретению различается в зависимости от формы препарата и обычно от около 0,01 до около 100% масс., предпочтительно, от около 0,1 до около % 50 масс., еще более предпочтительно, от около 0,5 до около 20% масс. в расчете на препарат.
Примеры
[0196]
Настоящее изобретение подробно поясняется ниже со ссылкой на примеры, экспериментальные примеры и примеры препаратов, которые не должны рассматриваться как ограничивающие, и изобретение может быть изменено в рамках объема настоящего изобретения.
В следующих примерах «комнатная температура» обычно означает от около 10°C до около 35°C. Соотношения, указанные для смешанных растворителей, представляют собой объемные соотношения, если не указано иное. % означает % масс., если не указано иное.
Элюирование колоночной хроматографией в примерах проводили под наблюдением с помощью ТСХ (тонкослойной хроматографии), если не указано иное. При наблюдении ТСХ использовали пластины 60 F254 для ТСХ производства Merck, растворитель, используемый в качестве элюирующего растворителя в колоночной хроматографии, использовали в качестве проявляющего растворителя, а УФ-детектор использовали для обнаружения. В колоночной хроматографии на силикагеле указание NH означает использование связанного с аминопропилсиланом силикагеля, а указание диола означает использование связанного с 3-(2,3-дигидроксипропокси)пропилсиланом силикагеля. В препаративной ВЭЖХ (высокоэффективная жидкостная хроматография) указание C18 означает использование октадецил-связанного силикагеля. Соотношение для элюирующего растворителя составляет, если не указано иное, объемное соотношение смешивания.
Для анализа 1H ЯМР использовали программное обеспечение ACD/SpecManager (торговое наименование) и тому подобное. Пики гидроксильной группы, аминогруппы и тому подобное, имеющие очень мягкий протонный пик, иногда не описываются.
МС измеряли методом ЖХ/МС. В качестве метода ионизации использовался метод ИЭР или метод APCI. Данные указывают на фактическое измеренное значение (найдено). Хотя обычно наблюдается пик молекулярного иона, иногда наблюдается фрагментный ион. В случае соли обычно наблюдается пик молекулярного иона или пик фрагментарного иона свободной формы.
Измеряли порошковую рентгенограмму с использованием характеристического излучения Cu-Kα от Rigaku Ultima IV описывали характерные пики.
В примерах используются следующие условные сокращения.
т.пл.: точка плавления
MС: масс-спектр
M: молярная концентрация
CDCl3: дейтерохлороформ
ДМСО-d6: дейтеродиметилсульфоксид
1H ЯМР: протонный ядерный магнитный резонанс
ЖХ/MС: жидкостная хроматография-масс-спектрометрия
ИЭР: Ионизация электрораспылением
APCI: Химическая ионизация при атмосферном давлении
DIAD: диизопропилазодикарбоксилат
ДМСО: диметилсульфоксид
DMA: N, N-диметилацетамид
DMAP: N, N-диметил-4-аминопиридин
ДМФА: N, N-диметилформамид
TBAF: фторид тетрабутиламмония
TEA : триэтиламин
ТГФ: тетрагидрофуран
[0197]
Пример 1
цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0198]
A) трет-бутил((цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутил)окси)диметилсилан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (500 мг), 1,2-дифтор-4-(трифторметил)бензола (0,383 мл) и ТГФ (10 мл) прибавляли трет-бутоксид калия (333 мг) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 16 ч. Смесь разбавляли этилацетатом, промывали водой насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Раствор пропускали через силикагель NH, элюировали этилацетатом и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (900 мг) в виде неочищенного продукта.
1H ЯМР (300 МГц, ДМСО-д6) δ 0,05 (6H, с), 0,86 (9H, с), 1,90-2,04 (2H, м), 2,87-3,00 (2H, м), 3,98-4,11 (1H, м), 4,41-4,54 (1H, м), 7,18 (1H, т, J=8,4 Гц), 7,50 (1H, д, J=8,5 Гц), 7,67 (1H, дд, J=11,3, 2,1 Гц).
[0199]
B) цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутанол
К смеси трет-бутил((цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутил)окси)диметилсилана (неочищенный продукт, 900 мг) и ТГФ (10 мл) прибавляли TBAF (1 M ТГФ раствор, 3,7 мл). Смесь перемешивали при комнатной температуре в течение 1 ч. Смесь разбавляли этилацетатом, промывали водой насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Раствор пропускали через силикагель NH, элюировали этилацетатом и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (486 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,89-2,02 (2H, м), 2,81-2,92 (2H, м), 3,79-3,93 (1H, м), 4,37-4,49 (1H, м), 5,24 (1H, д, J=6,8 Гц), 7,19 (1H, т, J=8,5 Гц), 7,50 (1H, д, J=8,7 Гц), 7,67 (1H, дд, J=11,3, 2,1 Гц).
[0200]
C) трет-бутил-3-(гидроксиметил)-3-нитроазетидин-1-карбоксилат
К смеси трет-бутил-3-нитроазетидин-1-карбоксилата (90 г) и ацетонитрила (1,25 л) прибавляли формальдегид (37% водный раствор, 73 мл), а затем по каплям прибавляли к ней TEA (60 мл) при комнатной температуре, и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/петролейный эфир) с получением указанного в заголовке соединения (85 мг).
1H ЯМР (500 МГц, CDCl3) δ 1,45 (9H, с), 2,68 (1H, уш. c), 4,11 (2H, д, J=10,4 Гц), 4,19-4,21 (2H, м), 4,39-4,46 (2H, м).
[0201]
D) трет-бутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси трет-бутил-3-(гидроксиметил)-3-нитроазетидин-1-карбоксилата (85 г), никеля Ренея (9 г) и метанола (1,5 л) подвергли гидрированию под 60 фунтов на кв. дюйм при комнатной температуре в течение 16 ч. Реакционную смесь отфильтровали через целит, и фильтрат концентрировали при пониженном давлении с получением промежуточного соединения (68 г). К смеси полученного промежуточного соединения (68 г), TEA (100 мл) и ТГФ (1,5 L) прибавляли трифосген (40 г) при 0°C, и реакционную смесь перемешивали при 0°C в течение 30 мин. Затем реакционную смесь перемешивали при комнатной температуре в течение 2 ч. Реакционную смесь вылили в насыщенный водный раствор гидрокарбоната натрия и экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/петролейный эфир) с получением указанного в заголовке соединения (58 g).
1H ЯМР (500 МГц, CDCl3) δ 1,43 (9H, с), 4,03 (2H, д, J=10,1 Гц), 4,13 (2H, д, J=9,5 Гц), 4,53 (2H, с), 6,52 (1H, уш. c).
[0202]
E) 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат
К смеси трет-бутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилата (58 г) и этилацетата (1,2 л) прибавляли гидрат тозиловой кислоты (58 г) при комнатной температуре, и смесь нагревали при кипячении в течение 2 ч. Реакционную смесь охладили до комнатной температуры, гидрат тозиловой кислоты (14,5 г) прибавляли к ней, и смесь нагревали при кипячении в течение дополнительных 2 ч. Реакционную смесь охладили до комнатной температуры, и твердое вещество собирали фильтрованием, промывали диэтиловым эфиром, и сушили при пониженном давлении с получением указанного в заголовке соединения (62 г).
1H ЯМР (400 МГц, ДМСО-д6) δ 2,29 (3H, с), 4,05-4,15 (4H, м), 4,54 (2H, с), 7,13 (2H, д, J=7,8 Гц), 7,50 (2H, д, J=7,8 Гц), 8,51-8,54 (3H, м).
[0203]
F) цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутанола (486 мг), TEA (1,08 мл) и ацетонитрила (16 мл) прибавляли трифосген (202 мг). Реакционную смесь перемешивали при 0°C в течение 30 мин и прибавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (583 мг). Смесь перемешивали при той же температуре в течение 16 ч. Смесь разбавляли этилацетатом, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Раствор пропускали через силикагель NH, элюировали этилацетатом и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (605 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,06-2,21 (2H, м), 2,93-3,07 (2H, м), 3,92-4,17 (4H, м), 4,47 (2H, с), 4,54-4,71 (2H, м), 7,20 (1H, т, J=8,5 Гц), 7,51 (1H, д, J=7,7 Гц), 7,69 (1H, дд, J=11,4, 2,0 Гц), 8,40 (1H, с).
[0204]
Пример 2
цис-3-(бензилокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(бензилокси)циклобутанола (328 мг), TEA (1,03 мл) и ацетонитрила (15 мл) прибавляли трифосген (191 мг). Реакционную смесь перемешивали при 0°C в течение 30 мин и прибавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (553 мг). Смесь перемешивали при той же температуре в течение 16 ч. Смесь разбавляли этилацетатом, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Раствор пропускали через силикагель NH, элюировали этилацетатом и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из диизопропилового эфира с получением указанного в заголовке соединения (436 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,80-1,95 (2H, м), 2,59-2,72 (2H, м), 3,65-3,78 (1H, м), 3,89-4,16 (4H, м), 4,36 (2H, с), 4,43-4,45 (3H, м), 7,24-7,40 (5H, м), 8,39 (1H, с).
[0205]
Пример 3
цис-3-((3-хлор-4-метилбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0206]
A) трет-бутил((цис-3-((3-хлор-4-метилбензил)окси)циклобутил)окси)диметилсилан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (500 мг) и ДМФА (9,3 мл) прибавляли гидрид натрия (60%, 109 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и прибавляли к ней смесь 4-(бромметил)-2-хлор-1-метилбензола (597 мг) и ДМФА (3,1 мл). Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (782 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,00 (6H, с), 0,83 (9H, с), 1,67-1,81 (2H, м), 2,30 (3H, с), 2,52-2,64 (2H, м), 3,55 (1H, квинт, J=7,0 Гц), 3,88 (1H, квинт, J=7,1 Гц), 4,29 (2H, с), 7,16 (1H, дд, J=7,9, 1,5 Гц), 7,26-7,37 (2H, м).
[0207]
B) цис-3-((3-хлор-4-метилбензил)окси)циклобутанол
К смеси трет-бутил((цис-3-((3-хлор-4-метилбензил)окси)циклобутил)окси)диметилсилана (782 мг) и ТГФ (12 мл) прибавляли TBAF (1 M ТГФ раствор, 4,6 мл). Смесь перемешивали при комнатной температуре в течение 64 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (461 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,65-1,80 (2H, м), 2,31 (3H, с), 2,45-2,58 (2H, м), 3,46-3,59 (1H, м), 3,60-3,74 (1H, м), 4,30 (2H, с), 4,99 (1H, д, J=6,6 Гц), 7,13-7,20 (1H, м), 7,27-7,36 (2H, м).
[0208]
C) цис-3-((3-хлор-4-метилбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((3-хлор-4-метилбензил)окси)циклобутанола (461 мг), TEA (1,13 мл) и ацетонитрила (10 мл) добавляли трифосген (211 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (641 мг). Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (575 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,88 (2H, дтд, J=9,8, 7,3, 2,9 Гц), 2,31 (3H, с), 2,65 (2H, дтд, J=9,7, 6,6, 2,9 Гц), 3,71 (1H, квинт, J=6,8 Гц), 3,89-4,01 (2H, м), 4,08 (2H, д, J=8,7 Гц), 4,33 (2H, с), 4,40-4,57 (3H, м), 7,18 (1H, дд, J=7,6, 1,4 Гц), 7,32 (1H, д, J=7,7 Гц), 7,35 (1H, д, J=1,5 Гц), 8,38 (1H, с).
[0209]
Пример 4
цис-3-((4-хлор-3-метилбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0210]
A) трет-бутил((цис-3-((4-хлор-3-метилбензил)окси)циклобутил)окси)диметилсилан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (500 мг) и ДМФА (9,3 мл) добавляли гидрид натрия (60%, 109 мг) в атмосфере аргона при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и добавляли к ней смесь 4-(бромметил)-1-хлор-2-метилбензола (597 мг) и ДМФА (3,1 мл) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (833 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,01 (6H, с), 0,85 (9H, с), 1,67-1,83 (2H, м), 2,32 (3H, с), 2,59 (2H, дтд, J=9,0, 6,4, 2,9 Гц), 3,57 (1H, квинт, J=7,0 Гц), 3,89 (1H, квинт, J=7,1 Гц), 4,30 (2H, с), 7,15 (1H, дд, J=8,2, 1,8 Гц), 7,28 (1H, с), 7,36 (1H, д, J=8,1 Гц).
[0211]
B) цис-3-((4-хлор-3-метилбензил)окси)циклобутанол
К смеси трет-бутил((цис-3-((4-хлор-3-метилбензил)окси)циклобутил)окси)диметилсилана (833 мг) и ТГФ (12 мл) добавляли TBAF (1 M ТГФ раствор, 4,9 мл). Смесь перемешивали при комнатной температуре в течение 64 ч. Смесь разбавляли этилацетатом, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (511 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,64-1,80 (2H, м), 2,32 (3H, с), 2,47-2,59 (2H, м), 3,47-3,59 (1H, м), 3,60-3,75 (1H, м), 4,29 (2H, с), 4,99 (1H, д, J=6,6 Гц), 7,14 (1H, дд, J=8,1, 1,7 Гц), 7,28 (1H, с), 7,36 (1H, д, J=8,1 Гц).
[0212]
C) цис-3-((4-хлор-3-метилбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((4-хлор-3-метилбензил)окси)циклобутанола (511 мг), TEA (1,26 мл) и ацетонитрила (11 мл) добавляли трифосген (234 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (711 мг). Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (651 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,80-1,95 (2H, м), 2,32 (3H, с), 2,65 (2H, дтд, J=9,7, 6,6, 3,0 Гц), 3,71 (1H, квинт, J=6,8 Гц), 3,91-4,01 (2H, м), 4,08 (2H, д, J=9,3 Гц), 4,32 (2H, с), 4,42-4,57 (3H, м), 7,16 (1H, дд, J=8,1, 1,7 Гц), 7,29 (1H, д, J=1,5 Гц), 7,37 (1H, д, J=8,1 Гц), 8,38 (1H, с).
[0213]
Пример 5
цис-3-((2,3-дифтор-4-метилбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0214]
A) трет-бутил((цис-3-((2,3-дифтор-4-метилбензил)окси)циклобутил)окси)диметилсилан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (400 мг) и ДМФА (5 мл) добавляли гидрид натрия (60%, 87 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и прибавляли к ней 1-(бромметил)-2,3-дифтор-4-метилбензол (481 мг) при комнатной температуре. Смесь перемешивали в течение ночи в атмосфере аргона при комнатной температуре. Смесь выливали в воду и экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (636 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,00-0,02 (6H, м), 0,84 (9H, с), 1,65-1,81 (2H, м), 2,27 (3H, д, J=2,1 Гц), 2,54-2,66 (2H, м), 3,58 (1H, квинт, J=7,0 Гц), 3,89 (1H, квинт, J=7,1 Гц), 4,38 (2H, д, J=7,1 Гц), 7,01-7,18 (2H, м).
[0215]
B) цис-3-((2,3-дифтор-4-метилбензил)окси)циклобутанол
К смеси трет-бутил((цис-3-((2,3-дифтор-4-метилбензил)окси)циклобутил)окси)диметилсилана (636 мг) и ТГФ (10 мл) добавляли TBAF (1 M ТГФ раствор, 2,8 мл) при комнатной температуре. Смесь перемешивали при той же температуре в течение 3 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (302 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ1,63-1,79 (2H, м), 2,27 (3H, д, J=2,1 Гц), 2,51-2,58 (2H, м), 3,54 (1H, квинт, J=7,1 Гц), 3,61-3,74 (1H, м), 4,38 (2H, д, J=1,1 Гц), 5,00 (1H, д, J=6,8 Гц), 6,88-7,29 (2H, м).
[0216]
C) цис-3-((2,3-дифтор-4-метилбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси 3-((2,3-дифтор-4-метилбензил)окси)циклобутанола (302 мг), TEA (0,74 мл) и ацетонитрила (10 мл) добавляли трифосген (137 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (417 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 4 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (300 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,77-1,92 (2H, м), 2,27 (3H, д, J=2,1 Гц), 2,59-2,71 (2H, м), 3,60-3,81 (1H, м), 3,89-4,02 (2H, м), 4,02-4,13 (2H, м), 4,41 (2H, с), 4,45-4,54 (3H, м), 6,96-7,20 (2H, м), 8,38 (1H, с).
[0217]
Пример 6
цис-3-((2,3,4-трифторбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0218]
A) трет-бутил(диметил)((цис-3-((2,3,4-трифторбензил)окси)циклобутил)окси)силан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (400 мг) и ДМФА (6,0 мл) добавляли гидрид натрия (60%, 95,0 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и добавляли к ней 1-(бромметил)-2,3,4-трифторбензол (534 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (716 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,01 (6H, с), 0,84 (9H, с), 1,64-1,90 (2H, м), 2,53-2,67 (2H, м), 3,59 (1H, квинт, J=7,1 Гц), 3,90 (1H, квинт, J=7,1 Гц), 4,40 (2H, с), 7,23-7,40 (2H, м).
[0219]
B) цис-3-((2,3,4-трифторбензил)окси)циклобутанол
К смеси трет-бутил(диметил)((цис-3-((2,3,4-трифторбензил)окси)циклобутил)окси)силана (715 мг) и ТГФ (7,0 мл) добавляли TBAF (1 M ТГФ раствор, 3,1 мл) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (413 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,64-1,79 (2H, м), 2,51-2,60 (2H, м), 3,50-3,61 (1H, м), 3,61-3,78 (1H, м), 4,40 (2H, с), 5,02 (1H, д, J=6,4 Гц), 7,23-7,38 (2H, м).
[0220]
C) цис-3-((2,3,4-трифторбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2,3,4-трифторбензил)окси)циклобутанола (250 мг), TEA (0,898 мл) и ацетонитрила (5,0 мл) добавляли трифосген (112 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (340 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 4 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан и метанол/этилацетат) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (176 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,76-1,98 (2H, м), 2,57-2,79 (2H, м), 3,74 (1H, квинт, J=6,8 Гц), 3,87-4,21 (4H, м), 4,36-4,61 (5H, м), 7,21-7,43 (2H, м), 8,39 (1H, с).
[0221]
Пример 7
цис-3-((2,4,5-трифторбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0222]
A) трет-бутил(диметил)((цис-3-((2,4,5-трифторбензил)окси)циклобутил)окси)силан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (500 мг) и ДМФА (5 мл) добавляли гидрид натрия (60%, 109 мг) при 0°C. Реакционную смесь перемешивали при комнатной температуре в течение 30 мин и добавляли к ней 1-(бромметил)-2,4,5-трифторбензол (0,358 мл) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 3 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (428 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,01 (6H, с), 0,85 (9H, с), 1,69-1,80 (2H, м), 2,54-2,65 (2H, м), 3,54-3,65 (1H, м), 3,84-3,95 (1H, м), 4,35 (2H, с), 7,47-7,59 (2H, м).
[0223]
B) цис-3-((2,4,5-трифторбензил)окси)циклобутанол
К смеси трет-бутил(диметил)((цис-3-((2,4,5-трифторбензил)окси)циклобутил)окси)силана (428 мг) и ТГФ (8 мл) добавляли TBAF (1 M ТГФ раствор, 1,5 мл) при комнатной температуре. Смесь перемешивали при той же температуре в течение 1 ч. К данной смеси добавляли насыщенный водный раствор хлорида натрия при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (126 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,65-1,79 (2H, м), 2,51-2,59 (2H, м), 3,56 (1H, квинт, J=7,0 Гц), 3,62-3,75 (1H, м), 4,35 (2H, с), 5,01 (1H, д, J=6,6 Гц), 7,52 (2H, ддт, J=10,8, 9,5, 6,7 Гц).
[0224]
C) цис-3-((2,4,5-трифторбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2,4,5-трифторбензил)окси)циклобутанола (126 мг), TEA (0.333 мл) и ацетонитрила (3 мл) добавляли трифосген (56.4 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (163 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (77,3 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,81-1,94 (2H, м), 2,60-2,72 (2H, м), 3,74 (1H, квинт, J=6,8 Гц), 3,92-4,14 (4H, м), 4,34-4,55 (5H, м), 7,48-7,61 (2H, м), 8,39 (1H, с).
[0225]
Пример 8
цис-3-((2,4,6-трифторбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0226]
A) трет-бутил(диметил)((цис-3-((2,4,6-трифторбензил)окси)циклобутил)окси)силан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (400 мг) и ДМФА (7,4 мл) добавляли гидрид натрия (60%, 87 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и добавляли к ней смесь 2-(бромметил)-1,3,5-трифторбензола (489 мг) и ДМФА (2,5 мл) при 0°C. Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (682 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,00 (6H, с), 0,84 (9H, с), 1,63-1,77 (2H, м), 2,52-2,65 (2H, м), 3,57 (1H, квинт, J=6,9 Гц), 3,90 (1H, квинт, J=7,1 Гц), 4,36 (2H, с), 7,13-7,27 (2H, м).
[0227]
B) цис-3-((2,4,6-трифторбензил)окси)циклобутанол
К смеси трет-бутил(диметил)((цис-3-((2,4,6-трифторбензил)окси)циклобутил)окси)силана (682 мг) и ТГФ (9,8 мл) добавляли TBAF (1 M ТГФ раствор, 3,9 мл). Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (397 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,60-1,75 (2H, м), 2,44-2,57 (2H, м), 3,53 (1H, квинт, J=7,0 Гц), 3,60-3,75 (1H, м), 4,35 (2H, с), 5,00 (1H, д, J=6,8 Гц), 7,13-7,27 (2H, м).
[0228]
C) цис-3-((2,4,6-трифторбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2,4,6-трифторбензил)окси)циклобутанола (397 мг), TEA (0,953 мл) и ацетонитрила (8,5 мл) добавляли трифосген (178 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (539 мг). Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из диизопропилового эфира с получением указанного в заголовке соединения (218 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,71-1,91 (2H, м), 2,56-2,78 (2H, м), 3,71 (1H, квинт, J=6,8 Гц), 3,89-4,01 (2H, м), 4,02-4,15 (2H, м), 4,39 (2H, с), 4,43-4,56 (3H, м), 7,15-7,28 (2H, м), 8,38 (1H, с).
[0229]
Пример 9
цис-3-((3,4-дихлорбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0230]
A) трет-бутил((цис-3-((3,4-дихлорбензил)окси)циклобутил)окси)диметилсилан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (270 мг) и ДМФА (3 мл) добавляли гидрид натрия (60%, 58,7 мг) при 0°C. Реакционную смесь перемешивали при комнатной температуре в течение 30 мин и добавляли к ней 4-(бромметил)-1,2-дихлорбензол (0,213 мл) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 3 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (240 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,01 (6H, с), 0,85 (9H, с), 1,71-1,83 (2H, м), 2,54-2,65 (2H, м), 3,53-3,64 (1H, м), 3,90 (1H, квинт, J=7,1 Гц), 4,35 (2H, с), 7,31 (1H, дд, J=8,3, 1,9 Гц), 7,57 (1H, д, J=1,9 Гц), 7,60 (1H, д, J=8,3 Гц).
[0231]
B) цис-3-((3,4-дихлорбензил)окси)циклобутанол
К смеси трет-бутил((цис-3-((3,4-дихлорбензил)окси)циклобутил)окси)диметилсилана (240 мг) и ТГФ (3 мл) добавляли TBAF (1 M ТГФ раствор, 0,66 мл) при комнатной температуре. Смесь перемешивали при той же температуре в течение 1 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (100 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,67-1,80 (2H, м), 2,51-2,59 (2H, м), 3,49-3,61 (1H, м), 3,61-3,75 (1H, м), 4,35 (2H, с), 4,97-5,03 (1H, м), 7,31 (1H, дд, J=8,3, 1,9 Гц), 7,56 (1H, д, J=1,9 Гц), 7,60 (1H, д, J=8,1 Гц).
[0232]
C) цис-3-((3,4-дихлорбензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((3,4-дихлорбензил)окси)циклобутанола (100 мг), TEA (0,186 мл) и ацетонитрила (2 мл) добавляли трифосген (42,0 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (122 мг) при 0°C. Смесь перемешивали при 0°C в течение 2 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан), а затем очищали ВЭЖХ (C18, подвижная фаза: вода/ацетонитрил (содержащая 0,1% ТФУ)). К полученной фракции добавили насыщенный водный раствор гидрокарбоната натрия, и экстрагировали смесь этилацетатом. Экстракт сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток перекристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (18,5 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,89 (2H, дтд, J=9,8, 7,3, 2,9 Гц), 2,60-2,71 (2H, м), 3,73 (1H, квинт, J=6,9 Гц), 3,92-4,14 (4H, м), 4,35-4,56 (5H, м), 7,32 (1H, дд, J=8,3, 1,9 Гц), 7,56-7,64 (2H, м), 8,39 (1H, с).
[0233]
Пример 10
цис-3-((2-фтор-4-(трифторметил)бензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0234]
A) цис-3-((2-фтор-4-(трифторметил)бензил)окси)циклобутанол
К смеси цис-3-((трет-бутил(дифенил)силил)окси)циклобутанола (352 мг) и ДМФА (4,0 мл) добавляли гидрид натрия (60%, 51,8 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и добавляли к ней смесь 1-(бромметил)-2-фтор-4-(трифторметил)бензола (277 мг) и ДМФА (1,5 мл) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 дней. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) с получением промежуточного соединения (315 мг) в виде неочищенного продукта. К смеси полученного промежуточного соединения (неочищенный продукт, 310 мг) и ТГФ (4,0 мл) добавляли TBAF (1 M ТГФ раствор, 0,27 мл) при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 4 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (132 мг).
1H ЯМР (300 МГц, CDCl3) δ 1,70 (1H, д, J=6,4 Гц), 1,88-2,03 (2H, м), 2,69-2,85 (2H, м), 3,67 (1H, квинт, J=6,9 Гц), 3,96 (1H, секст, J=7,0 Гц), 4,52 (2H, с), 7,31 (1H, д, J=9,8 Гц), 7,42 (1H, д, J=7,9 Гц), 7,52-7,64 (1H, м).
[0235]
B) цис-3-((2-фтор-4-(трифторметил)бензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2-фтор-4-(трифторметил)бензил)окси)циклобутанола (131 мг), TEA (0,275 мл) и ацетонитрила (3,5 мл) добавляли трифосген (51,3 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (156 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 4 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан и метанол/этилацетат) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (73,6 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,82-2,03 (2H, м), 2,61-2,78 (2H, м), 3,78 (1H, квинт, J=6,9 Гц), 3,90-4,19 (4H, м), 4,41-4,61 (5H, м), 7,57-7,77 (3H, м), 8,39 (1H, с).
[0236]
Пример 11
цис-3-((3-хлор-4-(трифторметил)бензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0237]
A) трет-бутил((цис-3-((3-хлор-4-(трифторметил)бензил)окси)циклобутил)окси)диметилсилан
К смеси цис-3-((трет-бутил(диметил)силил)окси)циклобутанола (416 мг) и ДМФА (7,7 мл) добавляли гидрид натрия (60%, 90 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин, и добавляли к ней смесь 3-хлор-4-(трифторметил)бензилметансульфоната (653 мг) и ДМФА (2,6 мл) при 0°C. Смесь перемешивали при комнатной температуре в течение 2 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (549 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,02 (6H, с), 0,85 (9H, с), 1,72-1,86 (2H, м), 2,55-2,68 (2H, м), 3,62 (1H, квинт, J=7,0 Гц), 3,91 (1H, квинт, J=7,1 Гц), 4,45 (2H, с), 7,49 (1H, д, J=8,1 Гц), 7,64 (1H, с), 7,83 (1H, д, J=8,1 Гц).
[0238]
B) цис-3-((3-хлор-4-(трифторметил)бензил)окси)циклобутанол
К смеси трет-бутил((цис-3-((3-хлор-4-(трифторметил)бензил)окси)циклобутил)окси)диметилсилана (549 мг) и ТГФ (7,0 мл) добавляли TBAF (1 M ТГФ раствор, 2,8 мл). Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (293 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,67-1,83 (2H, м), 2,50-2,61 (2H, м), 3,52-3,76 (2H, м), 4,45 (2H, с), 5,03 (1H, д, J=6,6 Гц), 7,49 (1H, дд, J=8,1, 0,8 Гц), 7,64 (1H, с), 7,83 (1H, д, J=8,1 Гц).
[0239]
C) цис-3-((3-хлор-4-(трифторметил)бензил)окси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((3-хлор-4-(трифторметил)бензил)окси)циклобутанола (293 мг), TEA (0,582 мл) и ацетонитрила (5,2 мл) добавляли трифосген (108 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (329 мг). Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (метанол/этилацетат) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (46,0 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,83-2,03 (2H, м), 2,60-2,79 (2H, м), 3,76 (1H, квинт, J=6,9 Гц), 3,89-4,02 (2H, м), 4,09 (2H, д, J=8,7 Гц), 4,39-4,59 (5H, м), 7,50 (1H, д, J=7,9 Гц), 7,66 (1H, с), 7,84 (1H, д, J=8,3 Гц), 8,39 (1H, с).
[0240]
Пример 12
цис-3-((2-фтор-4-метилфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0241]
A) (цис-3-(бензилокси)циклобутил)метил-4-метилбензолсульфонат
К смеси (цис-3-(бензилокси)циклобутил)метанола (1,78 г), 4-метилбензолсульфонилхлорида (1,94 г) и ацетонитрила (20 мл) по каплям прибавляли TEA (1,93 мл) при 0°C и прибавляли к ней триметиламин гидрохлорид (88 мг). Смесь перемешивали при той же температуре в течение 40 мин и разделили между насыщенным водным раствором хлорида натрия и этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (2,97 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,46-1,63 (2H, м), 2,02-2,28 (3H, м), 2,42 (3H, с), 3,86 (1H, квинт, J=7,2 Гц), 3,99 (2H, д, J=6,0 Гц), 4,31 (2H, с), 7,21-7,39 (5H, м), 7,48 (2H, д, J=7,9 Гц), 7,70-7,85 (2H, м).
[0242]
B) 1-((цис-3-(бензилокси)циклобутил)метокси)-2-фтор-4-метилбензол
Смесь (цис-3-(бензилокси)циклобутил)метил-4-метилбензолсульфоната (300 мг), 2-фтор-4-метилфенола (131 мг), карбоната калия (239 мг) и ДМФА (3,0 мл) перемешивали при 80°C в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Раствор пропускали через силикагель NH, элюировали этилацетатом и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (260 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,67-1,80 (2H, м), 2,15-2,39 (6H, м), 3,88-3,99 (3H, м), 4,37 (2H, с), 6,86-6,93 (1H, м), 6,97-7,06 (2H, м), 7,23-7,39 (5H, м).
[0243]
C) цис-3-((2-фтор-4-метилфенокси)метил)циклобутанол
Смесь 1-((цис-3-(бензилокси)циклобутил)метокси)-2-фтор-4-метилбензола (260 мг), палладия/угля (Pd 10%, 50% влаги, 184 мг) и метанола (20 мл) перемешивали при атмосферном давлении атмосферы водорода при комнатной температуре в течение 2 ч. Катализатор удалили фильтрованием, и фильтрат концентрировали при пониженном давлении. Остаток растворяли в этилацетате, и раствор пропускали через силикагель NH и элюировали этилацетатом с получением указанного в заголовке соединения (182 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,55-1,69 (2H, м), 2,01-2,18 (1H, м), 2,23 (3H, с), 2,24-2,35 (2H, м), 3,90-4,07 (3H, м), 5,00 (1H, д, J=6,4 Гц), 6,86-6,93 (1H, м), 6,96-7,05 (2H, м).
[0244]
D) цис-3-((2-фтор-4-метилфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2-фтор-4-метилфенокси)метил)циклобутанола (182 мг), TEA (0,483 мл) и ацетонитрила (9 мл) добавляли трифосген (90 мг). Реакционную смесь перемешивали при 0°C в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (260 мг). Смесь перемешивали при той же температуре в течение 16 ч. Смесь разбавляли этилацетатом, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Раствор пропускали через силикагель NH и элюировали этилацетатом. Раствор концентрировали, и остаток кристаллизовали из этилацетата/гексана (3/1) с получением указанного в заголовке соединения (238 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,75-1,93 (2H, м), 2,23 (3H, с), 2,26-2,47 (3H, м), 3,90-4,14 (6H, м), 4,47 (2H, с), 4,70-4,85 (1H, м), 6,86-6,95 (1H, м), 6,97-7,06 (2H, м), 8,34-8,42 (1H, м).
[0245]
Пример 13
цис-3-((4-фтор-2-метилфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0246]
A) 1-((цис-3-(бензилокси)циклобутил)метокси)-4-фтор-2-метилбензол
К смеси 4-фтор-2-метилфенола (120 мг), карбоната калия (263 мг) и DMA (5 мл) добавляли (цис-3-(бензилокси)циклобутил)метил-4-метилбензолсульфонат (300 мг) при комнатной температуре. Смесь перемешивали при 80°C в течение 3 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (215 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,67-1,88 (2H, м), 2,15 (3H, с), 2,19-2,41 (3H, м), 3,79-4,01 (3H, м), 4,38 (2H, с), 6,79-7,07 (3H, м), 7,18-7,46 (5H, м).
[0247]
B) цис-3-((4-фтор-2-метилфенокси)метил)циклобутанол
Смесь 1-((цис-3-(бензилокси)циклобутил)метокси)-4-фтор-2-метилбензола (215 мг), палладия/угля (Pd 10%, 50% влаги, 100 мг) и метанола (20 мл) перемешивали в течение ночи при атмосферном давлении атмосферы водорода при комнатной температуре. Катализатор удалили фильтрованием, и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (145 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,57-1,74 (2H, м), 2,03-2,14 (1H, м), 2,15 (3H, с), 2,23-2,35 (2H, м), 3,87 (2H, д, J=6,0 Гц), 3,91-4,05 (1H, м), 5,00 (1H, уш. c), 6,72-7,13 (3H, м).
[0248]
C) цис-3-((4-фтор-2-метилфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((4-фтор-2-метилфенокси)метил)циклобутанола (145 мг), TEA (0,38 мл) и ацетонитрила (5 мл) добавляли трифосген (71,6 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (217 мг). Смесь перемешивали при комнатной температуре в течение 4 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (125 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,80-1,98 (2H, м), 2,17 (3H, с), 2,26-2,45 (3H, м), 3,91 (2H, д, J=5,1 Гц), 3,94-4,02 (2H, м), 4,03-4,12 (2H, м), 4,47 (2H, с), 4,66-4,88 (1H, м), 6,80-7,10 (3H, м), 8,38 (1H, с).
[0249]
Пример 14
цис-3-((2-хлор-4-фторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0250]
A) этил-цис-3-((трет-бутил(диметил)силил)окси)циклобутанкарбоксилат
К смеси 2,6-диметилпиридина (9,44 мл), этил-цис-3-гидроксициклобутанкарбоксилата (5,84 г) и ДМФА (50 мл) добавляли трет-бутил(диметил)силилтрифторметансульфонат (11 мл) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (10,4 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,02 (6H, с), 0,85 (9H, с), 1,17 (3H, т, J=7,1 Гц), 1,89-2,02 (2H, м), 2,37-2,47 (2H, м), 2,53-2,65 (1H, м), 4,05 (2H, q, J=7,2 Гц), 4,11-4,22 (1H, м).
[0251]
B) (цис-3-((трет-бутил(диметил)силил)окси)циклобутил)метанол
К смеси этил-цис-3-((трет-бутил(диметил)силил)окси)циклобутанкарбоксилата (10,4 г) и ТГФ (100 мл) добавляли литийалюминийгидрид (1,69 г) при 0°C. Смесь перемешивали при той же температуре в течение 30 мин. К данной смеси добавляли 10 водный сульфат натрия при 0°C, и смесь перемешивали при комнатной температуре в течение 30 мин. Смесь отфильтровывали через целит, и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (5,66 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,01 (6H, с), 0,85 (9H, с), 1,48-1,62 (2H, м), 1,71-1,86 (1H, м), 2,11-2,24 (2H, м), 3,27-3,38 (2H, м), 4,03-4,15 (1H, м), 4,42 (1H, т, J=5,5 Гц).
[0252]
C) (цис-3-((трет-бутил(диметил)силил)окси)циклобутил)метил-4-метилбензолсульфонат
К смеси (цис-3-((трет-бутил(диметил)силил)окси)циклобутил)метанола (3,25 г), TEA (2,71 мл) и ацетонитрила (35 мл) добавляли 4-метилбензолсульфонилхлорид (3,01 г) и триметиламин гидрохлорид (144 мг) при 0°C. Смесь перемешивали при той же температуре в течение 10 мин, а затем при комнатной температуре в течение 1 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (5,12 г).
1H ЯМР (300 МГц, ДМСО-д6) δ -0,02 (6H, с), 0,82 (9H, с), 1,40-1,54 (2H, м), 1,92-2,07 (1H, м), 2,10-2,29 (2H, м), 2,42 (3H, с), 3,97 (2H, д, J=6,4 Гц), 4,08 (1H, квинт, J=7,3 Гц), 7,48 (2H, д, J=7,9 Гц), 7,73-7,84 (2H, м).
[0253]
D) трет-бутил((цис-3-((2-хлор-4-фторфенокси)метил)циклобутил)окси)диметилсилан
Смесь (цис-3-((трет-бутил(диметил)силил)окси)циклобутил)метил-4-метилбензолсульфоната (678 мг), 2-хлор-4-фторфенола (349 мг), карбоната калия (379 мг) и ДМФА (5,0 мл) перемешивали в течение ночи при 80°C. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (338 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,00 (6H, с), 0,83 (9H, с), 1,65-1,80 (2H, м), 2,05-2,20 (1H, м), 2,24-2,40 (2H, м), 3,97 (2H, д, J=6,0 Гц), 4,15 (1H, квинт, J=7,3 Гц), 7,07-7,18 (2H, м), 7,33-7,45 (1H, м).
[0254]
E) цис-3-((2-хлор-4-фторфенокси)метил)циклобутанол
К смеси трет-бутил((цис-3-((2-хлор-4-фторфенокси)метил)циклобутил)окси)диметилсилана (337 мг) и ТГФ (4,0 мл) добавляли TBAF (1 M ТГФ раствор, 1,5 мл) при комнатной температуре. Смесь перемешивали при той же температуре в течение 2 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (214 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,58-1,74 (2H, м), 2,04-2,21 (1H, м), 2,22-2,39 (2H, м), 3,87-4,09 (3H, м), 5,01 (1H, д, J=6,4 Гц), 7,07-7,26 (2H, м), 7,31-7,52 (1H, м).
[0255]
F) цис-3-((2-хлор-4-фторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2-хлор-4-фторфенокси)метил)циклобутанола (213 мг), TEA (0,770 мл) и ацетонитрила (4,0 мл) добавляли трифосген (96,0 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (291 мг). Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан), и кристаллизовали из этилацетата/гексана. Полученное твердое вещество очищали ВЭЖХ (C18, подвижная фаза: вода/ацетонитрил (содержащая 10 мM NH4HCO3)). Полученную фракцию частично концентрировали при пониженном давлении, и остаток экстрагировали этилацетатом. Экстракт промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, и концентрировали при пониженном давлении. Остаток перекристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (235 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,81-2,01 (2H, м), 2,24-2,46 (3H, м), 3,89-4,15 (6H, м), 4,47 (2H, с), 4,69-4,88 (1H, м), 7,03-7,24 (2H, м), 7,34-7,56 (1H, м), 8,39 (1H, с).
[0256]
Пример 15
цис-3-((4-хлор-2-фторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0257]
A) этил-цис-3-((трет-бутил(дифенил)силил)окси)циклобутанкарбоксилат
К смеси этил-цис-3-гидроксициклобутанкарбоксилата (500 мг), имидазола (283 мг), DMAP (21,2 мг) и ДМФА (12 мл) добавляли трет-бутил(дифенил)хлорсилан (1,05 г). Смесь перемешивали при комнатной температуре в течение 5 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (1,23 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,98 (9H, с), 1,12-1,22 (3H, м), 2,05-2,18 (2H, м), 2,27-2,41 (2H, м), 2,52-2,59 (1H, м), 3,94-4,09 (2H, м), 4,10-4,22 (1H, м), 7,36-7,52 (6H, м), 7,53-7,66 (4H, м).
[0258]
B) (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метанол
К смеси этил-цис-3-((трет-бутил(дифенил)силил)окси)циклобутанкарбоксилата (4,3 г) и ТГФ (50 мл) по каплям добавляли смесь литийалюминийгидрида (469 мг) и ТГФ (50 мл) при 0°C. Смесь перемешивали при той же температуре в течение 15 мин. К данной смеси добавляли 10 водный сульфат натрия, и смесь перемешивали в течение 15 мин. Нерастворимое вещество удалили фильтрованием, и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (3,54 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,97 (9H, с), 1,64-1,82 (3H, м), 2,06-2,17 (2H, м), 3,31-3,36 (2H, м), 4,04-4,16 (1H, м), 4,43 (1H, т, J=5,4 Гц), 7,31-7,51 (6H, м), 7,55-7,67 (4H, м).
[0259]
C) (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метил-4-метилбензолсульфонат
К смеси (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метанола (900 мг), 4-метилбензолсульфонилхлорида (554 мг) и ацетонитрила (9,0 мл) добавляли TEA (0,551 мл) и триметиламин гидрохлорид (25,3 мг) при 0°C. Смесь перемешивали при той же температуре в течение 1 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (1,29 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,95 (9H, с), 1,54-1,73 (2H, м), 1,82-1,97 (1H, м), 2,03-2,21 (2H, м), 2,39 (1H, с), 2,42 (3H, с), 3,98 (2H, д, J=6,0 Гц), 7,37-7,51 (8H, м), 7,53-7,62 (4H, м), 7,77 (2H, д, J=8,3 Гц).
[0260]
D) трет-бутил((цис-3-((4-хлор-2-фторфенокси)метил)циклобутил)окси)дифенилсилан
Смесь (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метил-4-метилбензолсульфоната (500 мг), 4-хлор-2-фторфенола (178 мг), карбоната калия (210 мг) и ДМФА (4,0 мл) перемешивали при 80°C в течение 4 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (439 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,98 (9H, с), 1,74-1,94 (2H, м), 2,01-2,15 (1H, м), 2,17-2,35 (2H, м), 4,00 (2H, д, J=6,0 Гц), 4,17 (1H, квинт, J=7,2 Гц), 7,08-7,24 (2H, м), 7,35-7,52 (7H, м), 7,56-7,71 (4H, м).
[0261]
E) цис-3-((4-хлор-2-фторфенокси)метил)циклобутанол
К смеси трет-бутил((цис-3-((4-хлор-2-фторфенокси)метил)циклобутил)окси)дифенилсилана (430 мг) и ТГФ (4,0 мл) добавляли TBAF (1 M ТГФ раствор, 0,41 мл) при комнатной температуре. Смесь перемешивали при той же температуре в течение 2 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (202 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,52-1,72 (2H, м), 2,02-2,20 (1H, м), 2,22-2,40 (2H, м), 3,89-4,08 (3H, м), 5,03 (1H, д, J=6,4 Гц), 7,10-7,23 (2H, м), 7,35-7,46 (1H, м).
[0262]
F) цис-3-((4-хлор-2-фторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((4-хлор-2-фторфенокси)метил)циклобутанола (200 мг), TEA (0,723 мл) и ацетонитрила (4,0 мл) добавляли трифосген (90,0 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (273 мг). Смесь перемешивали при комнатной температуре в течение 2 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан), и кристаллизовали из этилацетата/гексана. Полученное твердое вещество очищали ВЭЖХ (колонка: CHIRALPAK AD, 50 мм ID x 500 мл, произведенная Daicel Corporation, подвижная фаза: гексан/этанол (400/600 (об./об.))), и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (170 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,76-1,94 (2H, м), 2,22-2,46 (3H, м), 3,88-4,23 (6H, м), 4,47 (2H, с), 4,66-4,91 (1H, м), 7,11-7,27 (2H, м), 7,37-7,50 (1H, м), 8,39 (1H, с).
[0263]
Пример 16
цис-3-((2,3,4-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0264]
A) трет-бутил(диметил)((цис-3-((2,3,4-трифторфенокси)метил)циклобутил)окси)силан
Смесь (цис-3-((трет-бутил(диметил)силил)окси)циклобутил)метил-4-метилбензолсульфоната (53,3 г), 2,3,4-трифторфенола (22,6 г), карбоната цезия (70,3 г) и ДМФА (290 мл) перемешивали в течение ночи при комнатной температуре. К данной смеси добавляли раствор 2,3,4-трифторфенола (8,52 г) в ДМФА (50 мл) при комнатной температуре, и смесь перемешивали в течение 3 дней. Смесь разбавляли водой и экстрагировали толуолом/этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (45,6 г).
1H ЯМР (300 МГц, CDCl3) δ 0,05 (6H, с), 0,88 (9H, с), 1,70-1,89 (2H, м), 2,09-2,30 (1H, м), 2,37-2,52 (2H, м), 3,97 (2H, д, J=6,4 Гц), 4,12-4,25 (1H, м), 6,56-6,73 (1H, м), 6,77-6,96 (1H, м).
[0265]
B) цис-3-((2,3,4-трифторфенокси)метил)циклобутанол
К смеси трет-бутил(диметил)((цис-3-((2,3,4-трифторфенокси)метил)циклобутил)окси)силана (46,6 г) и ТГФ (270 мл) порциями добавляли TBAF гидрат (42,2 г) при 0°C, и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Смесь разбавляли водой и экстрагировали этилацетатом. Органический слой отделяли и промывали водой и насыщенным водным раствором хлорида натрия. Водный слой повторно экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия. Органические слои объединили, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (31,2 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,52-1,72 (2H, м), 2,03-2,21 (1H, м), 2,24-2,38 (2H, м), 3,91-4,09 (3H, м), 5,04 (1H, д, J=6,4 Гц), 6,94-7,10 (1H, м), 7,13-7,35 (1H, м).
[0266]
C) цис-3-((2,3,4-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2,3,4-трифторфенокси)метил)циклобутанола (2,25 г), TEA (6,73 мл) и ацетонитрила (24 мл) добавляли трифосген (1,01 г) при 0°C, и реакционную смесь перемешивали при той же температуре в течение 1 ч. К данной смеси добавляли 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (2,91 г) при 0°C, и реакционную смесь нагревали до комнатной температуры. Смесь перемешивали при комнатной температуре в течение 16 ч, разбавляли водой и экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан и метанол/этилацетат) и кристаллизовали из этилацетата/гексана. Полученное твердое вещество перекристаллизовали из этанола/воды/гептана с получением указанного в заголовке соединения (2,54 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,78-2,00 (2H, м), 2,24-2,47 (3H, м), 3,91-4,20 (6H, м), 4,47 (2H, с), 4,72-4,87 (1H, м), 6,96-7,09 (1H, м), 7,19-7,32 (1H, м), 8,39 (1H, с).
Т. пл. 145°C
порошковая рентгенограмма кристалла (угол дифракции 2θ): 9,8°, 13,6°, 14,4°, 15,2°, 18,2°, 19,6°, 22,0°, 24,3°, 25,4° и 29,1°
[0267]
Пример 17
цис-3-((2,4,5-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0268]
A) 1-((цис-3-(бензилокси)циклобутил)метокси)-2,4,5-трифторбензол
К смеси 2,4,5-трифторфенола (282 мг), карбоната калия (527 мг) и ДМФА (6 мл) добавляли (цис-3-(бензилокси)циклобутил)метил-4-метилбензолсульфонат (600 мг) при комнатной температуре. Смесь перемешивали при 80°C в течение 3 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (455 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,67-1,80 (2H, м), 2,16-2,40 (3H, м), 3,94 (1H, квинт, J=7,3 Гц), 4,02 (2H, д, J=6,0 Гц), 4,37 (2H, с), 7,23-7,45 (6H, м), 7,57 (1H, тд, J=10,9, 7,9 Гц).
[0269]
B) цис-3-((2,4,5-трифторфенокси)метил)циклобутанол
Смесь 1-((цис-3-(бензилокси)циклобутил)метокси)-2,4,5-трифторбензола (455 мг), палладия/угля (Pd 10%, 50% влаги, 100 мг) и метанола (5 мл) перемешивали в течение ночи при атмосферном давлении атмосферы водорода при комнатной температуре. Катализатор удалили фильтрованием, и фильтрат концентрировали при пониженном давлении. К данному остатку добавляли палладий/угле (Pd 10%, 50% влаги, 100 мг) и метанол (5 мл), и смесь перемешивали при атмосферном давлении атмосферы водорода при комнатной температуре в течение 2 ч. Катализатор удаляли фильтрованием, и фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (307 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,56-1,68 (2H, м), 2,02-2,19 (1H, м), 2,24-2,35 (2H, м), 3,94-4,02 (3H, м), 5,03 (1H, уш. c), 7,38 (1H, дт, J=12,4, 8,0 Гц), 7,56 (1H, тд, J=11,0, 7,9 Гц).
[0270]
C) цис-3-((2,4,5-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2,4,5-трифторфенокси)метил)циклобутанола (307 мг), TEA (0,737 мл) и ацетонитрила (6 мл) добавляли трифосген (157 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (397 мг). Смесь перемешивали при комнатной температуре в течение 4 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (219 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,78-1,92 (2H, м), 2,27-2,47 (3H, м), 3,94-4,13 (6H, м), 4,47 (2H, с), 4,72-4,85 (1H, м), 7,39 (1H, дт, J=12,3, 8,0 Гц), 7,58 (1H, тд, J=10,9, 7,5 Гц), 8,39 (1H, с).
[0271]
Пример 18
цис-3-((2,4,6-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0272]
A) 2-((цис-3-(бензилокси)циклобутил)метокси)-1,3,5-трифторбензол
К смеси (цис-3-(бензилокси)циклобутил)метил-4-метилбензолсульфоната (350 мг), 2,4,6-трифторфенола (180 мг) и ДМФА (4,0 мл) добавляли карбонат калия (209 мг) при комнатной температуре. Смесь перемешивали в течение ночи при 80 ºC. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (298 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,63-1,84 (2H, м), 2,07-2,24 (1H, м), 2,24-2,41 (2H, м), 3,86-3,97 (1H, м), 4,01 (2H, д, J=6,0 Гц), 4,36 (2H, с), 7,17-7,40 (7H, м).
[0273]
B) цис-3-((2,4,6-трифторфенокси)метил)циклобутанол
Смесь 2-((цис-3-(бензилокси)циклобутил)метокси)-1,3,5-трифторбензола (294 мг), гидроксида палладия/угля (Pd 20%, 50% влаги, 30,0 мг) и этилацетата (4,0 мл) перемешивали при атмосферном давлении атмосферы водорода при комнатной температуре в течение 4 ч. Катализатор удаляли фильтрованием, и фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (211 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,52-1,73 (2H, м), 1,96-2,15 (1H, м), 2,17-2,35 (2H, м), 3,89-4,07 (3H, м), 4,99 (1H, д, J=6,4 Гц), 7,02-7,40 (2H, м).
[0274]
C) цис-3-((2,4,6-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-((2,4,6-трифторфенокси)метил)циклобутанола (209 мг), TEA (0,751 мл) и ацетонитрила (4,0 мл) добавляли трифосген (93,0 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (284 мг). Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (266 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,75-2,02 (2H, м), 2,17-2,46 (3H, м), 3,89-4,20 (6H, м), 4,47 (2H, с), 4,76 (1H, квинт, J=7,3 Гц), 7,16-7,37 (2H, м), 8,38 (1H, с).
Т. пл. 111°C
порошковая рентгенограмма кристалла (угол дифракции 2θ): 3,7°, 7,4°, 14,8°, 18,1°, 20,6°, 22,3° и 24,4°
[0275]
Пример 19
цис-3-((2-фтор-4-(трифторметил)фенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0276]
A) цис-3-(этоксикарбонил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси этил-цис-3-гидроксициклобутанкарбоксилата (324 мг), TEA (1,04 мл) и ацетонитрила (19 мл) добавляли трифосген (233 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (562 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (370 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,17 (3H, т, J=7,1 Гц), 2,04-2,18 (2H, м), 2,44-2,57 (2H, м), 2,69-2,84 (1H, м), 3,90-4,15 (6H, м), 4,47 (2H, с), 4,78 (1H, квинт, J=7,6 Гц), 8,39 (1H, с).
[0277]
B) цис-3-((2-фтор-4-(трифторметил)фенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси литийалюминийгидрида (70,6 мг) и ТГФ (6,2 мл) по каплям добавляли смесь цис-3-(этоксикарбонил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат (370 мг) и ТГФ (6,2 мл) при 0°C. Смесь перемешивали в атмосфере аргона при той же температуре в течение 30 мин. К данной смеси последовательно прибавляли воду, 15% водный раствор гидроксида натрия и воду при 0°C, и смесь перемешивали при комнатной температуре в течение 30 мин. Нерастворимое вещество удаляли фильтрованием, и фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) с получением промежуточного соединения (67,7 мг) в виде неочищенного продукта. К смеси полученного промежуточного соединения (неочищенный продукт, 67,7 мг), 2-фтор-4-(трифторметил)фенола (47,6 мг) и ТГФ (5,3 мл) прибавляли трифенилфосфин (на полимерной подложке, 3 ммоль/г, 440 мг) и бис(2-метоксиэтил) (E)-диазен-1,2-дикарбоксилат (124 мг). Смесь перемешивали при комнатной температуре в течение 3 ч. Нерастворимое вещество удалили фильтрованием, и фильтрат разделяли между водой и этилацетата. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан и метанол/этилацетат) с получением указанного в заголовке соединения (28,5 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,79-1,95 (2H, м), 2,27-2,46 (3H, м), 3,90-4,02 (2H, м), 4,03-4,19 (4H, м), 4,47 (2H, с), 4,72-4,87 (1H, м), 7,30-7,40 (1H, м), 7,53 (1H, д, J=8,9 Гц), 7,67 (1H, дд, J=11,2, 2,0 Гц), 8,39 (1H, с).
[0278]
Пример 20
цис-3-((2-хлор-4-(трифторметил)фенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0279]
A) цис-3-((((4-метилфенил)сульфонил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(гидроксиметил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилата (67,9 мг) и пиридина (2 мл) добавляли 4-метилбензолсульфонилхлорид (60,6 мг). Смесь перемешивали при комнатной температуре в течение 16 ч. Смесь разбавляли этилацетатом, промывали 1 М соляной кислотой и сушили над безводным сульфатом натрия. Раствор пропускали через силикагель NH, элюировали этилацетатом, и концентрировали при пониженном давлении с получением указанного в заголовке соединения (109 мг) в виде неочищенного продукта.
MС: [M+H]+ 411,2
[0280]
B) цис-3-((2-хлор-4-(трифторметил)фенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
Смесь цис-3-((((4-метилфенил)сульфонил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилата (неочищенный продукт, 109 мг), 2-хлор-4-(трифторметил)фенола (78 мг), карбоната калия (110 мг) и ДМФА (3 мл) перемешивали при 80°C в течение 1 ч. Смесь разбавляли этилацетатом при комнатной температуре, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Раствор пропускали через силикагель NH, элюировали этилацетатом и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из диизопропилового эфира с получением указанного в заголовке соединения (19,4 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,85-2,02 (2H, м), 2,30-2,54(3H, м), 3,91-4,19 (6H, м), 4,47 (2H, с), 4,71-4,87 (1H, м), 7,32 (1H, д, J=8,7 Гц), 7,68 (1H, дд, J=8,9, 2,1 Гц), 7,84 (1H, д, J=1,9 Гц), 8,39 (1H, с).
[0281]
Пример 21
транс-3-((2,3,4-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0282]
A) (транс-3-(бензилокси)циклобутил)метил-4-метилбензолсульфонат
К смеси (транс-3-(бензилокси)циклобутил)метанола (236 мг), TEA (0,256 мл) и ацетонитрила (4,0 мл) добавляли 4-метилбензолсульфонилхлорид (281 мг) и триметиламин гидрохлорид (11,7 мг) при 0°C. Смесь перемешивали при той же температуре в течение 45 мин. К данной смеси добавляли воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (425 мг).
1H ЯМР (300 МГц, CDCl3) δ 1,99-2,24 (4H, м), 2,45 (3H, с), 2,48-2,64 (1H, м), 4,02 (2H, д, J=6,8 Гц), 4,05-4,16 (1H, м), 4,36 (2H, с), 7,27-7,44 (7H, м), 7,72-7,84 (2H, м).
[0283]
B) 1-((транс-3-(бензилокси)циклобутил)метокси)-2,3,4-трифторбензол
Смесь (транс-3-(бензилокси)циклобутил)метил-4-метилбензолсульфоната (417 мг), 2,3,4-трифторфенола (214 мг), карбоната калия (250 мг) и ДМФА (4,0 мл) перемешивали при 80°C в течение 8 ч. К данной реакционной смеси прибавляли 2,3,4-трифторфенол (428 мг) и карбонат калия (499 мг),и смесь перемешивали при 100°C в течение 6 ч, а затем при 80°C в течение 14 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом/толуолом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан), а затем очищали колоночной хроматографии на силикагеле (NH, этилацетат/гексан) с получением указанного в заголовке соединения (352 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,12 (4H, т, J=6,6 Гц), 2,61 (1H, дт, J=13,5, 6,6 Гц), 4,08 (2H, д, J=6,8 Гц), 4,21 (1H, квинт, J=6,7 Гц), 4,36 (2H, с), 7,04 (1H, тдд, J=9,2, 4,9, 2,6 Гц), 7,18-7,43 (6H, м).
[0284]
C) транс-3-((2,3,4-трифторфенокси)метил)циклобутанол
Смесь 1-((транс-3-(бензилокси)циклобутил)метокси)-2,3,4-трифторбензола (346 мг), гидроксида палладия/угля (Pd 20%, 50% влаги, 35,0 мг) и этилацетата (5,0 мл) перемешивали в течение ночи при атмосферном давлении атмосферы водорода при комнатной температуре. Катализатор удалили фильтрованием, и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (212 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,92-2,16 (4H, м), 4,05 (2H, д, J=7,2 Гц), 4,27 (1H, секст, J=6,8 Гц), 5,03 (1H, д, J=6,0 Гц), 6,97-7,10 (1H, м), 7,18-7,34 (1H, м).
[0285]
D) транс-3-((2,3,4-трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси транс-3-((2,3,4-трифторфенокси)метил)циклобутанола (100 мг), TEA (0,299 мл) и ацетонитрила (4,0 мл) добавляли трифосген (44,7 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (136 мг) при 0°C. Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан и метанол/этилацетат), и кристаллизовали из этилацетата/диизопропилового эфира с получением указанного в заголовке соединения (130 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,13-2,31 (4H, м), 2,58-2,77 (1H, м), 3,92-4,22 (6H, м), 4,48 (2H, с), 5,02 (1H, квинт, J=7,1 Гц), 6,98-7,12 (1H, м), 7,19-7,34 (1H, м), 8,40 (1H, с).
[0286]
Пример 22
транс-3-((2-фтор-4-(трифторметил)фенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0287]
A) транс-3-(этоксикарбонил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси этил-транс-3-гидроксициклобутанкарбоксилата (329 мг), TEA (1,04 мл) и ацетонитрила (19 мл) добавляли трифосген (233 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (562 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 16 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (330 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,07-1,27 (3H, м), 2,19-2,36 (2H, м), 2,38-2,48 (2H, м), 2,98-3,13 (1H, м), 3,88-4,19 (6H, м), 4,47 (2H, с), 4,96 (1H, квинт, J=7,1 Гц), 8,40 (1H, с).
[0288]
B) транс-3-((2-фтор-4-(трифторметил)фенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси литийалюминийгидрида (63,0 мг) и ТГФ (5,5 мл) по каплям добавляли смесь транс-3-(этоксикарбонил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилата (330 мг) и ТГФ (5,5 мл) при 0°C. Смесь перемешивали в атмосфере аргона при 0°C в течение 30 мин. К данной смеси добавляли последовательно воду, 15% водный раствор гидроксида натрия и воду при 0°C, и смесь перемешивали при комнатной температуре в течение 30 мин. Нерастворимое вещество удалили фильтрованием, и фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (метанол/этилацетат) с получением промежуточного соединения (49,3 мг) в виде неочищенного продукта. К смеси полученного промежуточного соединения (неочищенный продукт, 49,3 мг), 2-фтор-4-(трифторметил)фенола (34,6 мг) и ТГФ (3,9 мл) прибавляли трифенилфосфин (на полимерной подложке, 3 ммоль/г, 320 мг) и бис(2-метоксиэтил)(E)-диазен-1,2-дикарбоксилат (90 мг). Смесь перемешивали при комнатной температуре в течение 3 ч. Нерастворимое вещество удалили фильтрованием, и фильтрат разделили между этилацетатом и водой. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат) и кристаллизовали из этилацетата/диизопропилового эфира с получением указанного в заголовке соединения (5,4 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,17-2,31 (4H, м), 2,59-2,78 (1H, м), 3,92-4,03 (2H, м), 4,05-4,14 (2H, м), 4,19 (2H, д, J=6,8 Гц), 4,48 (2H, с), 5,04 (1H, квинт, J=6,9 Гц), 7,31-7,43 (1H, м), 7,54 (1H, д, J=8,5 Гц), 7,61-7,73 (1H, м), 8,40 (1H, с).
[0289]
Пример 23
(цис-3-(2,4,6-трифторфенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0290]
A) этил-3-(2,4,6-трифторфенокси)циклобутанкарбоксилат
Смесь этил-3-((метилсульфонил)окси)циклобутанкарбоксилата (1,5 г), иодида натрия (2,53 г) и ацетона (15 мл) облучали микроволновым излучением при 130°C в течение 2 ч. Нерастворимое вещество удалили фильтрованием, и фильтрат концентрировали при пониженном давлении. К данному остатку прибавляли диизопропиловый эфир, нерастворимое вещество удалили фильтрованием, и фильтрат концентрировали. К данному остатку прибавляли ДМФА (7 мл), и смесь 2,4,6-трифторфенола (999 мг), карбоната калия (2,05 г) и ДМФА (7 мл) добавляли к ней при комнатной температуре. Смесь перемешивали при 80°C в течение 3 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (1,04 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,18 (3H, т, J=7,2 Гц), 2,19-3,17 (5H, м), 4,03-4,13 (2H, м), 4,48-4,80 (1H, м), 7,19-7,34 (2H, м).
[0291]
B) (3-(2,4,6-трифторфенокси)циклобутил)метанол
К смеси литийалюминийгидрида (215 мг) и ТГФ (10 мл) по каплям прибавляли смесь этил-3-(2,4,6-трифторфенокси)циклобутанкарбоксилата (1,04 г) и ТГФ (10 мл) при 0°C. Смесь перемешивали в атмосфере аргона при той же температуре в течение 2 ч. К данной смеси добавляли 10% водный раствор тартрата калия натрия и этилацетат при 0°C, и нерастворимое вещество удаляли фильтрованием. Органические слой фильтрата удаляли, а водный слой экстрагировали этилацетатом. Органические слои объединили, промывали водой насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (566 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,81-1,93 (1H, м), 2,05-2,40 (4H, м), 3,33-3,43 (2H, м), 4,41-4,75 (2H, м), 7,17-7,31 (2H, м).
[0292]
C) (3-(2,4,6-трифторфенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси (3-(2,4,6-трифторфенокси)циклобутил)метанола (251 мг), TEA (0,497 мл) и ацетонитрила (6 мл) добавляли трифосген (112 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (325 мг) при 0°C. Смесь перемешивали при той же температуре в течение 1 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (160 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,82-1,94 (1H, м), 2,01-2,19 (2H, м), 2,19-2,38 (2H, м), 3,94-4,01 (4H, м), 4,05-4,13 (2H, м), 4,42-4,56 (2H, м), 4,73 (1H, квинт, J=6,5 Гц), 7,18-7,32 (2H, м), 8,39 (1H, д, J=2,6 Гц).
[0293]
D) (цис-3-(2,4,6-трифторфенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
(3-(2,4,6-Трифторфенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат (150 мг) разделяли ВЭЖХ (колонка: CHIRALCEL OJ (торговая марка), 50 мм ID×500 мл, произведенная Daicel Corporation, подвижная фаза: гексан/этанол=45/55), и фракцию, имеющую более короткое время удержания, концентрировали. Остаток перекристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (26,8 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,80-1,95 (2H, м), 1,98-2,16 (1H, м), 2,27-2,39 (2H, м), 3,92-4,03 (4H, м), 4,03-4,13 (2H, м), 4,45-4,56 (3H, м), 7,18-7,33 (2H, м), 8,40 (1H, с).
[0294]
Пример 24
(цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутил)метил 6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0295]
A) этил-цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутанкарбоксилат
К смеси этил-цис-3-гидроксициклобутанкарбоксилата (1 г) и ДМФА (10 мл) добавляли гидрид натрия (60%, 305 мг) при 0°C. Реакционную смесь перемешивали в атмосфере аргона при комнатной температуре в течение 30 мин, и смесь 1,2-дифтор-4-(трифторметил)бензола (1,26 г) и ДМФА (10 мл) по каплям прибавляли к ней при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 4 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (386 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,19 (3H, т, J=7,2 Гц), 2,18-2,33 (2H, м), 2,72-2,95 (3H, м), 4,09 (2H, q, J=7,1 Гц), 4,77-4,89 (1H, м), 7,21 (1H, т, J=8,5 Гц), 7,51 (1H, д, J=8,7 Гц), 7,69 (1H, дд, J=11,5, 2,1 Гц).
[0296]
B) (цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутил)метанол
К смеси литийалюминийгидрида (52,6 мг) и ТГФ (4 мл) по каплям добавляли смесь этил-цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутанкарбоксилата (386 мг) и ТГФ (4 мл) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 2 ч. К данной смеси добавляли 10% водный раствор тартрата калия натрия и этилацетат при комнатной температуре, и нерастворимое вещество удаляли фильтрованием. Органические слой фильтрата удаляли, а водный слой экстрагировали этилацетатом. Органические слои объединили, промывали водой насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (367 мг) в виде неочищенного продукта.
1H ЯМР (300 МГц, ДМСО-д6) δ 1,80-1,94 (2H, м), 2,01-2,16 (1H, м), 2,43-2,56 (2H, м), 3,40 (2H, т, J=5,5 Гц), 4,58 (1H, т, J=5,4 Гц), 4,75 (1H, квинт, J=7,2 Гц), 7,20 (1H, т, J=8,5 Гц), 7,50 (1H, дд, J=8,6, 0,8 Гц), 7,66 (1H, дд, J=11,4, 2,0 Гц).
[0297]
C) (цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси (цис-3-(2-фтор-4-(трифторметил)фенокси)циклобутил)метанола (215 мг), TEA (0,374 мл) и ацетонитрила (5 мл) добавляли трифосген (85 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (244 мг). Смесь перемешивали при комнатной температуре в течение 3 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (45,4 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,80-1,95 (2H, м), 2,19-2,35 (1H, м), 2,53-2,68 (2H, м), 3,93-4,14 (6H, м), 4,47 (2H, с), 4,77 (1H, квинт, J=7,1 Гц), 7,20 (1H, т, J=8,5 Гц), 7,50 (1H, д, J=8,7 Гц), 7,67 (1H, дд, J=11,4, 2,0 Гц), 8,39 (1H, с).
[0298]
Пример 25
(транс-3-(2,4,6-трифторфенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
(3-(2,4,6-Трифторфенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат (150 мг) разделяли ВЭЖХ (колонка: CHIRALCEL OJ (торговая марка), 50 мм ID×500 мл, произведенная Daicel Corporation, подвижная фаза: гексан/этанол=45/55), и фракцию, имеющую более длительное время удержания, концентрировали. Остаток перекристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (66,2 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,07-2,19 (2H, м), 2,19-2,32 (2H, м), 3,35-3,39 (1H, м), 3,92-4,02 (4H, м), 4,05-4,12 (2H, м), 4,47 (2H, с), 4,73 (1H, квинт, J=6,5 Гц), 7,18-7,34 (2H, м), 8,39 (1H, с).
[0299]
Пример 26
(цис-3-(2-хлор-4-(трифторметил)фенокси)циклобутил)метил 6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0300]
A) этил-цис-3-(2-хлор-4-(трифторметил)фенокси)циклобутанкарбоксилат
К смеси этил-цис-3-гидроксициклобутанкарбоксилата (1 г) и ТГФ (20 мл) добавляли гидрид натрия (60%, 305 мг) при 0°C. Реакционную смесь перемешивали при комнатной температуре в течение 30 мин и добавляли к ней 2-хлор-1-фтор-4-(трифторметил)бензол (0,950 мл) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 2 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (352 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,19 (3H, т, J=7,1 Гц), 2,19-2,30 (2H, м), 2,74-2,95 (3H, м), 4,09 (2H, кв, J=7,1 Гц), 4,81-4,91 (1H, м), 7,17 (1H, д, J=8,7 Гц), 7,66 (1H, дд, J=8,7, 1,5 Гц), 7,84 (1H, д, J=1,7 Гц).
[0301]
B) (цис-3-(2-хлор-4-(трифторметил)фенокси)циклобутил)метанол
К смеси этил-цис-3-(2-хлор-4-(трифторметил)фенокси)циклобутанкарбоксилата (352 мг) и ТГФ (4 мл) добавляли смесь литийалюминийгидрида (62,1 мг) и ТГФ (4 мл) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 4 ч. К данной смеси добавляли 10% водный раствор тартрата калия натрия и этилацетат при 0°C, и нерастворимое вещество удаляли фильтрованием. Органические слой фильтрата удаляли, а водный слой экстрагировали этилацетатом. Органические слои объединили, промывали водой насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (195 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,80-1,93 (2H, м), 2,01-2,17 (1H, м), 2,44-2,56 (2H, м), 3,41 (2H, т, J=5,4 Гц), 4,59 (1H, т, J=5,5 Гц), 4,76 (1H, квинт, J=7,2 Гц), 7,17 (1H, д, J=8,5 Гц), 7,64 (1H, дд, J=8,7, 1,7 Гц), 7,82 (1H, д, J=2,1 Гц).
[0302]
C) (цис-3-(2-хлор-4-(трифторметил)фенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси (цис-3-(2-хлор-4-(трифторметил)фенокси)циклобутил)метанола (195 мг), 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилата (230 мг), TEA (0,320 мл) и ТГФ (12 мл) добавляли трифосген (72,2 мг) при 0°C. Смесь перемешивали при 0°C в течение 2 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан), а затем очищали ВЭЖХ (C18, подвижная фаза: вода/ацетонитрил (содержащая 0,1% ТФУ)). К полученной фракции добавили насыщенный водный раствор гидрокарбоната натрия, и экстрагировали смесь этилацетатом. Экстракт сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток перекристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (13,2 мг).
1H ЯМР (300 МГц, CDCl3) δ 2,05-2,12 (2H, м), 2,28-2,44 (1H, м), 2,58-2,71 (2H, м), 4,09-4,13 (4H, м), 4,20-4,26 (2H, м), 4,54 (2H, с), 4,61-4,73 (1H, м), 6,73 (1H, с), 6,81 (1H, д, J=8,5 Гц), 7,44 (1H, дд, J=8,6, 1,6 Гц), 7,63 (1H, д, J=2,1 Гц).
[0303]
Пример 27
(транс-3-(2-хлор-4-(трифторметил)фенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0304]
A) этил-транс-3-(2-хлор-4-(трифторметил)фенокси)циклобутанкарбоксилат
К смеси этил-цис-3-(((4-метилфенил)сульфонил)окси)циклобутанкарбоксилата (1 г), 2-хлор-4-(трифторметил)фенола (725 мг) и ДМФА (20 мл) прибавляли карбонат калия (695 мг) при комнатной температуре. Смесь перемешивали при 80°C в течение 16 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (473 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,22 (3H, т, J=7,1 Гц), 2,36-2,48 (2H, м), 2,68-2,79 (2H, м), 3,14-3,26 (1H, м), 4,13 (2H, q, J=7,1 Гц), 5,02 (1H, квинт, J=6,6 Гц), 7,11 (1H, д, J=8,7 Гц), 7,61-7,68 (1H, м), 7,85 (1H, д, J=1,7 Гц).
[0305]
B) (транс-3-(2-хлор-4-(трифторметил)фенокси)циклобутил)метанол
К смеси этил-транс-3-(2-хлор-4-(трифторметил)фенокси)циклобутанкарбоксилата (473 мг) и ТГФ (5 мл) прибавляли смесь литийалюминийгидрида (61,2 мг) и ТГФ (5 мл) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 1 ч. К данной смеси добавляли 10% водный раствор тартрата калия натрия и этилацетат при 0°C. Нерастворимое вещество удаляли фильтрованием, органический слой фильтрата отделяли, а водный слой экстрагировали этилацетатом. Органические слои объединили, промывали водой насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (277 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,10-2,24 (2H, м), 2,28-2,45 (3H, м), 3,48 (2H, т, J=5,8 Гц), 4,69 (1H, т, J=5,3 Гц), 4,94 (1H, квинт, J=6,5 Гц), 7,08 (1H, д, J=8,5 Гц), 7,61-7,68 (1H, м), 7,83 (1H, д, J=1,7 Гц).
[0306]
C) (транс-3-(2-хлор-4-(трифторметил)фенокси)циклобутил)метил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилата (296 мг), (транс-3-(2-хлор-4-(трифторметил)фенокси)циклобутил)метанола (277 мг), TEA (0,454 мл) и ТГФ (6 мл) прибавляли трифосген (103 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 2 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/диизопропилового эфира/гексана с получением указанного в заголовке соединения (29,7 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,19-2,29 (2H, м), 2,31-2,40 (2H, м), 2,54-2,66 (1H, м), 3,97-4,17 (6H, м), 4,49 (2H, с), 5,00 (1H, квинт, J=6,6 Гц), 7,10 (1H, д, J=8,7 Гц), 7,66 (1H, дд, J=8,7, 1,7 Гц), 7,84 (1H, д, J=1,9 Гц), 8,42 (1H, с).
[0307]
Пример 28
цис-3-(((3-хлор-4-метилбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0308]
A) цис-3-(((3-хлор-4-метилбензил)окси)метил)циклобутанол
К смеси (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метанола (395 мг) и ДМФА (5 мл) добавляли гидрид натрия (60%, 60,3 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 15 мин и добавляли к ней смесь 4-(бромметил)-2-хлор-1-метилбензола (280 мг) и ДМФА (2 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) с получением промежуточного соединения (317 мг) в виде неочищенного продукта. К смеси полученного промежуточного соединения (неочищенный продукт, 316 мг) и ТГФ (6,6 мл) добавляли TBAF (1 M ТГФ раствор, 0,79 мл) при 0°C. Реакционную смесь перемешивали в течение ночи при комнатной температуре и добавляли к ней TBAF (1 M ТГФ раствор, 0,33 мл) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (83,9 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,42-1,58 (2H, м), 1,80-1,99 (1H, м), 2,10-2,28 (2H, м), 2,31 (3H, с), 3,34 (2H, д, J=6,2 Гц), 3,85-3,99 (1H, м), 4,41 (2H, с), 4,92 (1H, д, J=6,6 Гц), 7,17 (1H, дд, J=7,6, 1,4 Гц), 7,28-7,41 (2H, м).
[0309]
B) цис-3-(((3-хлор-4-метилбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(((3-хлор-4-метилбензил)окси)метил)циклобутанола (83 мг), TEA (0,192 мл) и ацетонитрила (3,5 мл) добавляли трифосген (43,0 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (104 мг) при 0°C. Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (69,9 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,65-1,82 (2H, м), 2,11 (1H, д, J=6,8 Гц), 2,25-2,40 (5H, м), 3,38 (2H, д, J=5,9 Гц), 3,87-4,15 (4H, м), 4,44 (4H, д, J=10,0 Гц), 4,72 (1H, т, J=7,5 Гц), 7,13-7,22 (1H, м), 7,28-7,38 (2H, м), 8,37 (1H, с).
[0310]
Пример 29
цис-3-(((4-хлор-3-метилбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0311]
A) цис-3-(((4-хлор-3-метилбензил)окси)метил)циклобутанол
К смеси (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метанола (0,8 г) и ДМФА (20 мл) добавляли гидрид натрия (60%, 122 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 15 мин и добавляли к ней смесь 4-(бромметил)-1-хлор-2-метилбензола (567 мг) и ДМФА (2 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) с получением промежуточного соединения (770 мг) в виде неочищенного продукта. К смеси полученного промежуточного соединения (неочищенный продукт, 769 мг) и ТГФ (16 мл) прибавляли TBAF (1 M ТГФ раствор, 2,4 мл) при 0°C. Реакционную смесь перемешивали в течение ночи при комнатной температуре и добавляли к ней TBAF (1 M ТГФ раствор, 0,80 мл). Смесь перемешивали при комнатной температуре в течение 3 ч. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (241 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ1,41-1,61 (2H, м), 1,81-2,02 (1H, м), 2,10-2,27 (2H, м), 2,32 (3H, с), 3,35 (2H, д, J=6,2 Гц), 3,81-4,02 (1H, м), 4,40 (2H, с), 4,92 (1H, д, J=6,6 Гц), 7,15 (1H, дд, J=8,1, 1,7 Гц), 7,28 (1H, д, J=1,1 Гц), 7,37 (1H, д, J=8,1 Гц).
[0312]
B) цис-3-(((4-хлор-3-метилбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(((4-хлор-3-метилбензил)окси)метил)циклобутанола (241 мг), TEA (0,558 мл) и ацетонитрила (10 мл) добавляли трифосген (125 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (301 мг) при 0°C. Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (291 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,65-1,84 (2H, м), 2,03-2,20 (1H, м), 2,24-2,40 (5H, м), 3,38 (2H, д, J=5,9 Гц), 3,87-4,15 (4H, м), 4,42 (2H, с), 4,46 (2H, с), 4,72 (1H, т, J=7,6 Гц), 7,15 (1H, дд, J=8,2, 1,6 Гц), 7,28 (1H, с), 7,38 (1H, д, J=8,1 Гц), 8,37 (1H, с).
[0313]
Пример 30
цис-3-(((2-хлор-4-фторбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0314]
A) трет-бутил((цис-3-(((2-хлор-4-фторбензил)окси)метил)циклобутил)окси)диметилсилан
К смеси (цис-3-((трет-бутил(диметил)силил)окси)циклобутил)метанола (400 мг) и ДМФА (4,0 мл) добавляли гидрид натрия (60%, 89,0 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 10 мин и добавляли к ней 1-(бромметил)-2-хлор-4-фторбензол (496 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (602 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,01 (6H, с), 0,84 (9H, с), 1,49-1,73 (2H, м), 1,86-2,13 (1H, м), 2,19-2,38 (2H, м), 3,43 (2H, д, J=6,0 Гц), 4,12 (1H, квинт, J=7,3 Гц), 4,49 (2H, с), 7,16-7,33 (1H, м), 7,39-7,55 (2H, м).
[0315]
B) цис-3-(((2-хлор-4-фторбензил)окси)метил)циклобутанол
К смеси трет-бутил((цис-3-(((2-хлор-4-фторбензил)окси)метил)циклобутил)окси)диметилсилана (600 мг) и ТГФ (5,0 мл) добавляли TBAF (1 M ТГФ раствор, 2,0 мл) при комнатной температуре. Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (364 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,46-1,63 (2H, м), 1,85-2,03 (1H, м), 2,16-2,31 (2H, м), 3,42 (2H, д, J=6,4 Гц), 3,78-3,99 (1H, м), 4,49 (2H, с), 4,94 (1H, д, J=6,4 Гц), 7,24 (1H, тд, J=8,5, 2,6 Гц), 7,44 (1H, дд, J=8,7, 2,6 Гц), 7,52 (1H, дд, J=8,7, 6,4 Гц).
[0316]
C) цис-3-(((2-хлор-4-фторбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(((2-хлор-4-фторбензил)окси)метил)циклобутанола (240 мг), TEA (0,818 мл) и ацетонитрила (4,0 мл) добавляли трифосген (102 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 20 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (309 мг). Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (301 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,68-1,85 (2H, м), 2,06-2,23 (1H, м), 2,26-2,42 (2H, м), 3,46 (2H, д, J=6,0 Гц), 3,89-4,18 (4H, м), 4,49 (4H, д, J=12,1 Гц), 4,73 (1H, квинт, J=7,5 Гц), 7,24 (1H, тд, J=8,5, 2,6 Гц), 7,40-7,61 (2H, м), 8,38 (1H, с).
[0317]
Пример 31
цис-3-(((2,3,4-трифторбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0318]
A) цис-3-(((2,3,4-трифторбензил)окси)метил)циклобутанол
К смеси (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метанола (1,01 г) и ДМФА (15 мл) добавляли гидрид натрия (60%, 154 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 15 мин и добавляли к ней 1-(бромметил)-2,3,4-трифторбензол (734 мг). Смесь перемешивали при комнатной температуре в течение 2 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) с получением промежуточного соединения (1,08 г) в виде неочищенного продукта. К смеси полученного промежуточного соединения (неочищенный продукт, 1,08 г) и ТГФ (22 мл) добавляли TBAF (1 M ТГФ раствор, 3,3 мл) при 0°C. Смесь перемешивали в течение ночи при комнатной температуре. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (291 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,39-1,60 (2H, м), 1,77-2,00 (1H, м), 2,14-2,33 (2H, м), 3,38 (2H, д, J=6,2 Гц), 3,79-3,98 (1H, м), 4,50 (2H, с), 4,92 (1H, д, J=6,6 Гц), 7,13-7,45 (2H, м).
[0319]
B) цис-3-(((2,3,4-трифторбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(((2,3,4-трифторбензил)окси)метил)циклобутанола (290 мг), TEA (0,657 мл) и ацетонитрила (12 мл) добавляли трифосген (147 мг) при 0°C. Реакционную смесь перемешивали при комнатной температуре в течение 30 мин и добавляли к ней7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (354 мг) при 0°C. Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (351 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,64-1,83 (2H, м), 1,99-2,19 (1H, м), 2,21-2,43 (2H, м), 3,37-3,52 (2H, м), 3,83-4,19 (4H, м), 4,36-4,58 (4H, м), 4,72 (1H, квинт, J=7,5 Гц), 7,17-7,42 (2H, м), 8,38 (1H, с).
[0320]
Пример 32
цис-3-(((2,4,5-трифторбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0321]
A) трет-бутил(дифенил)((цис-3-(((2,4,5-трифторбензил)окси)метил)циклобутил)окси)силан
К смеси (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метанола (1,00 г) и ДМФА (15 мл) добавляли гидрид натрия (60%, 129 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 15 мин и добавляли к ней 1-(бромметил)-2,4,5-трифторбензол (793 мг). Смесь перемешивали при комнатной температуре в течение 3 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (981 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 0,97 (9H, с), 1,61-1,80 (2H, м), 1,81-1,97 (1H, м), 2,07-2,25 (2H, м), 3,40 (2H, д, J=6,0 Гц), 4,06-4,19 (1H, м), 4,45 (2H, с), 7,36-7,67 (12H, м).
[0322]
B) цис-3-(((2,4,5-трифторбензил)окси)метил)циклобутанол
К смеси трет-бутил(дифенил)((цис-3-(((2,4,5-трифторбензил)окси)метил)циклобутил)окси)силана (981 мг) и ТГФ (4 мл) добавляли TBAF (1 M ТГФ раствор, 3,0 мл) при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 4 ч. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (296 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,40-1,59 (2H, м), 1,85-1,98 (1H, м), 2,13-2,31 (2H, м), 3,39 (2H, д, J=6,2 Гц), 3,82-3,98 (1H, м), 4,45 (2H, с), 4,92 (1H, д, J=6,6 Гц), 7,38-7,64 (2H, м).
[0323]
C) цис-3-(((2,4,5-трифторбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(((2,4,5-трифторбензил)окси)метил)циклобутанола (301 мг), TEA (0,68 мл) и ацетонитрила (5 мл) добавляли трифосген (127 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (385 мг). Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделили, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (105 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,65-1,81 (2H, м), 2,02-2,20 (1H, м), 2,26-2,37 (2H, м), 3,42 (2H, д, J=5,9 Гц), 3,90-4,00 (2H, м), 4,02-4,12 (2H, м), 4,46 (2H, с), 4,47 (2H, с), 4,72 (1H, квинт, J=7,4 Гц), 7,35-7,71 (2H, м), 8,37 (1H, с).
[0324]
Пример 33
цис-3-(((2,4,6-трифторбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0325]
A) цис-3-(((2,4,6-трифторбензил)окси)метил)циклобутанол
К смеси (цис-3-((трет-бутил(дифенил)силил)окси)циклобутил)метанола (804 мг) и ДМФА (10 мл) добавляли гидрид натрия (60%, 123 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 15 мин и добавляли к ней смесь 2-(бромметил)-1,3,5-трифторбензола (584 мг) и ДМФА (2 мл). Смесь перемешивали при комнатной температуре в течение 2 ч. К данной смеси добавляли воду при 0°C, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) с получением промежуточного соединения (1,11 г) в виде неочищенного продукта. К смеси полученного промежуточного соединения (неочищенный продукт, 1,1 г) и ТГФ (11 мл) добавляли TBAF (1 M ТГФ раствор, 4,5 мл) при 0°C. Смесь перемешивали в течение ночи при комнатной температуре. К данной смеси добавляли воду при комнатной температуре, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (82 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,29-1,56 (2H, м), 1,77-1,95 (1H, м), 2,12-2,30 (2H, м), 3,35 (2H, д, J=6,2 Гц), 3,79-4,05 (1H, м), 4,44 (2H, с), 4,90 (1H, д, J=6,6 Гц), 7,21 (2H, дд, J=9,3, 8,0 Гц).
[0326]
B) цис-3-(((2,4,6-трифторбензил)окси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси цис-3-(((2,4,6-трифторбензил)окси)метил)циклобутанола (352 мг), TEA (0,797 мл) и ацетонитрила (14 мл) добавляли трифосген (178 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (429 мг) при 0°C. Смесь перемешивали в течение ночи при комнатной температуре. К смеси прибавили воду, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (409 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,59-1,78 (2H, м), 2,01-2,17 (1H, м), 2,22-2,36 (2H, м), 3,39 (2H, д, J=6,0 Гц), 3,90-3,98 (2H, м), 4,01-4,13 (2H, м), 4,42-4,50 (4H, м), 4,70 (1H, квинт, J=7,6 Гц), 7,11-7,34 (2H, м), 8,37 (1H, с).
[0327]
Пример 39
транс-3-(2,3,4-трифторфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0328]
A) 1-((транс-3-(бензилокси)циклобутил)окси)-2,3,4-трифторбензол
К смеси цис-3-(бензилокси)циклобутанола (250 мг), 2,3,4-трифторфенола (249 мг), трифенилфосфина (552 мг) и ТГФ (5,0 мл) добавляли DIAD (40% толуольный раствор, 1,14 мл) при комнатной температуре. Смесь перемешивали при 60°C в течение 3 ч. Реакционную смесь концентрировали при пониженном давлении, и остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (426 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,28-2,41 (2H, м), 2,46 (2H, дд, J=6,8, 4,5 Гц), 4,28 (1H, тт, J=7,0, 4,7 Гц), 4,40 (2H, с), 4,94 (1H, тт, J=6,9, 4,2 Гц), 6,84 (1H, тдд, J=9,2, 4,5, 2,6 Гц), 7,12-7,48 (6H, м).
[0329]
B) транс-3-(2,3,4-трифторфенокси)циклобутанол
Смесь 1-((транс-3-(бензилокси)циклобутил)окси)-2,3,4-трифторбензола (417 мг), гидроксида палладия/угля (Pd 20%, 50% влаги, 40,0 мг) и этилацетата (6,0 мл) перемешивали в течение ночи при атмосферном давлении атмосферы водорода при комнатной температуре. Катализатор удалили фильтрованием, и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (287 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,19-2,41 (4H, м), 4,28-4,44 (1H, м), 4,85-4,97 (1H, м), 5,20 (1H, д, J=5,3 Гц), 6,80 (1H, тдд, J=9,2, 4,8, 2,6 Гц), 7,12-7,31 (1H, м).
[0330]
C) транс-3-(2,3,4-трифторфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси транс-3-(2,3,4-трифторфенокси)циклобутанола (280 мг), TEA (0,892 мл) и ТГФ (6,0 мл) добавляли трифосген (133 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (385 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 2 дней. Смесь пропускали через силикагель NH, элюировали этилацетатом/метанолом (10/1), и кристаллизовали из этилацетата/диизопропилового эфира с получением указанного в заголовке соединения (405 мг).
1H ЯМР (300 МГц, CDCl3) δ 2,44-2,77 (4H, м), 4,05-4,28 (4H, м), 4,56 (2H, с), 4,78-4,93 (1H, м), 5,19 (1H, тт, J=7,2, 4,5 Гц), 6,02 (1H, с), 6,33-6,58 (1H, м), 6,71-6,96 (1H, м).
[0331]
Пример 44
цис-3-(2-хлор-4-фторфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0332]
A) транс-3-(бензилокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
Смесь транс-3-(бензилокси)циклобутанола (9,65 г), TEA (37,6 мл) и ТГФ (120 мл) охладили до -10°C на ледяной бане с солью. При поддержании внутренней температуры реакционной смеси 5°C или ниже, смесь трифосгена (5,62 г) и ТГФ (40 мл) по каплям добавляли к ней в течение 30 мин. К реакционной смеси добавляли ТГФ (50 мл), смесь перемешивали при -10°C в течение 30 мин и добавляли к ней малыми порциями 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилата (16,3 г). Реакционную смесь перемешивали при 0°C в течение 1 ч, а затем при комнатной температуре в течение 3 дней. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/диизопропиловый эфир с получением указанного в заголовке соединения (15,6 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,15-2,41 (4H, м), 3,91-4,13 (4H, м), 4,15-4,27 (1H, м), 4,37 (2H, с), 4,47 (2H, с), 4,87-5,02 (1H, м), 7,21-7,46 (5H, м), 8,39 (1H, с).
[0333]
B) транс-3-гидроксициклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси транс-3-(бензилокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилата (7,50 г), этилацетата (50 мл) и метанола (50 мл) добавляли гидроксид палладия/угля (Pd 20%, 50% влаги, 750 мг) в атмосфере азота при комнатной температуре. Реакционную смесь перемешивали при атмосферном давлении атмосферы водорода при комнатной температуре в течение 4 ч. Катализатор удаляли фильтрованием, и фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (5,47 г).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,07-2,27 (4H, м), 3,91-4,15 (4H, м), 4,22-4,36 (1H, м), 4,47 (2H, с), 4,85-4,99 (1H, м), 5,11 (1H, д, J=5,3 Гц), 8,40 (1H, с).
[0334]
C) цис-3-(2-хлор-4-фторфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси транс-3-гидроксициклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилата (250 мг), 2-хлор-4-фторфенола (0,165 мл), трифенилфосфина (на полимерной подложке, 3 ммоль/г, 1,03 г) и ТГФ (5,0 мл) добавляли DIAD (0,305 мл) при комнатной температуре. Смесь перемешивали при 60°C в течение 3 ч. Реакционную смесь пропускали через силикагель NH и элюировали этилацетатом/метанолом (10/1), и фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан), кристаллизовали из этилацетата/диизопропилового эфира, промывали этилацетатом/диизопропиловым эфиром (1/10) и сушили при пониженном давлении при 80°C в течение 2 ч с получением указанного в заголовке соединения (245 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,99-2,20 (2H, м), 2,90-3,06 (2H, м), 3,88-4,22 (4H, м), 4,40-4,53 (3H, м), 4,63 (1H, квинт, J=7,1 Гц), 6,94-7,07 (1H, м), 7,15 (1H, тд, J=8,6, 3,0 Гц), 7,44 (1H, дд, J=8,3, 3,0 Гц), 8,39 (1H, с).
[0335]
Пример 46
цис-3-(2,4,6-трифторфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси транс-3-гидроксициклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилата (250 мг), 2,4,6-трифторфенола (229 мг), трифенилфосфина (на полимерной подложке, 3 ммоль/г, 1,03 г) и ТГФ (5,0 мл) прибавляли DIAD (0,305 мл) при комнатной температуре. Смесь перемешивали при той же температуре в течение 1 ч, а затем при 60°C в течение 1 ч. Реакционную смесь пропускали через силикагель NH и элюировали этилацетатом/метанолом (9/1), и фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/диизопропилового эфира с получением указанного в заголовке соединения (327 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 2,05-2,25 (2H, м), 2,67-2,86 (2H, м), 3,90-4,19 (4H, м), 4,34 (1H, квинт, J=6,9 Гц), 4,43-4,56 (3H, м), 7,20-7,40 (2H, м), 8,40 (1H, с).
Т. пл. 160°C
порошковая рентгенограмма кристалла (угол дифракции 2θ): 4,1°, 8,2°, 12,3°, 16,4°, 18,6°, 21,5°, 23,4° и 24,7°
[0336]
Пример 50
цис-3-(4-фтор-3-метилфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси транс-3-гидроксициклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилата (250 мг), 4-фтор-3-метилфенола (0,172 мл), трифенилфосфина (на полимерной подложке, 3 ммоль/г, 1,03 г) и ТГФ (5,0 мл) прибавляли DIAD (0,305 мл) при комнатной температуре. Смесь перемешивали при той же температуре в течение 1 ч, а затем при 60°C в течение 1 ч. Реакционную смесь пропускали через силикагель NH и элюировали этилацетатом/метанолом (9/1), и фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) и кристаллизовали из этилацетата/диизопропилового эфира с получением неочищенного продукта (257 мг). Полученный неочищенный продукт (243 мг) перекристаллизовали из этанола/воды с получением указанного в заголовке соединения (216 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ1,92-2,11 (2H, м), 2,19 (3H, д, J=1,9 Гц), 2,83-3,05 (2H, м), 3,92-4,21 (4H, м), 4,36 (1H, квинт, J=6,7 Гц), 4,47 (2H, с), 4,61 (1H, квинт, J=7,2 Гц), 6,66 (1H, дт, J=8,7, 3,6 Гц), 6,76 (1H, дд, J=6,5, 2,9 Гц), 7,02 (1H, т, J=9,2 Гц), 8,40 (1H, с).
[0337]
Пример 63
цис-3-(2-хлор-4-фторфенокси)-3-метилциклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
[0338]
A) 1-((3-(бензилокси)-1-метилциклобутил)окси)-4-фтор-2-нитробензол
К смеси 3-(бензилокси)-1-метилциклобутанола (0,89 г) и ДМФА (10 мл) добавляли гидрид натрия (60%, 204 мг) в атмосфере аргона при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 1,4-дифтор-2-нитробензола (0,552 мл) при 0°C. Смесь перемешивали в атмосфере аргона при комнатной температуре в течение 1 ч, 60°C в течение 3 ч, а затем в течение ночи при комнатной температуре. К реакционной смеси прибавили 0,1 М соляную кислоту, и смесь экстрагировали этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан), а затем очищали колоночной хроматографии на силикагеле NH (этилацетат/гексан) с получением указанного в заголовке соединения (629 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,45 (3H, с), 2,17-2,27 (2H, м), 2,61-2,70 (2H, м), 3,89 (1H, квинт, J=6,9 Гц), 4,39 (2H, с), 7,17 (1H, дд, J=9,4, 4,5 Гц), 7,24-7,39 (5H, м), 7,43-7,52 (1H, м), 7,86 (1H, дд, J=7,9, 3,2 Гц).
[0339]
B) 2-((3-(бензилокси)-1-метилциклобутил)окси)-5-фторанилин
Смесь 1-((3-(бензилокси)-1-метилциклобутил)окси)-4-фтор-2-нитробензола (629 мг), палладия/угля (этилендиаминовый комплекс, Pd 3,5-6,5%, 202 мг) и метанола (12 мл) перемешивали в течение ночи при атмосферном давлении атмосферы водорода при комнатной температуре. Катализатор удаляли фильтрованием, и фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (483 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,33-1,41 (3H, м), 2,14-2,24 (2H, м), 2,42-2,48 (2H, м), 3,81 (1H, квинт, J=6,9 Гц), 4,36 (2H, с), 4,97 (2H, с), 6,19 (1H, тд, J=8,6, 3,1 Гц), 6,43 (1H, дд, J=10,9, 3,1 Гц), 6,61 (1H, дд, J=8,7, 5,7 Гц), 7,24-7,37 (5H, м).
[0340]
C) 1-((3-(бензилокси)-1-метилциклобутил)окси)-2-хлор-4-фторбензол
К смеси 2-((3-(бензилокси)-1-метилциклобутил)окси)-5-фторанилина (483 мг) и соляной кислоты (6 M, 10 мл) добавляли смесьнитрита натрия (133 мг) и воды (1 мл) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и прибавляли к ней хлорид меди (I) (190 мг) при 0°C. Смесь перемешивали при той же температуре в течение 3 ч. К реакционной смеси добавили воду, и экстрагировали смесь этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (209 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,42 (3H, с), 2,15-2,27 (2H, м), 2,55-2,65 (2H, м), 3,87 (1H, квинт, J=6,9 Гц), 4,38 (2H, с), 6,98-7,05 (1H, м), 7,09-7,17 (1H, м), 7,25-7,38 (5H, м), 7,44 (1H, дд, J=8,5, 3,0 Гц).
[0341]
D) цис-3-(2-хлор-4-фторфенокси)-3-метилциклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат
К смеси иодида натрия (187 мг) и ацетонитрила (2 мл) добавляли хлортриметилсилан (0,159 мл) при 0°C. Смесь перемешивали при той же температуре в течение 30 мин, и добавляли к ней смесь 1-((3-(бензилокси)-1-метилциклобутил)окси)-2-хлор-4-фторбензола (200 мг) и ацетонитрила (2 мл) при 0°C. Смесь перемешивали при 0 °C в течение 1 ч, а затем при комнатной температуре в течение ночи. К реакционной смеси добавили воду, и экстрагировали смесь этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат/гексан) с получением промежуточного соединения (93 мг). К смеси полученного промежуточного соединения (93 мг), TEA (0,287 мл) и ацетонитрила (2 мл) добавляли трифосген (64,8 мг) при 0°C. Реакционную смесь перемешивали при той же температуре в течение 30 мин и добавляли к ней 7-окса-2,5-диазаспиро[3.4]октан-6-онтозилат (187 мг) при 0°C. Смесь перемешивали при комнатной температуре в течение 3 ч. К реакционной смеси добавили воду, и экстрагировали смесь этилацетатом. Органический слой отделяли, промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан). Остаток очищали ВЭЖХ (C18, подвижная фаза: вода/ацетонитрил (содержащая 0,1% ТФУ)). К полученной фракции добавили насыщенный водный раствор гидрокарбоната натрия, и экстрагировали смесь этилацетатом. Экстракт сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток перекристаллизовали из этилацетата/гексана с получением указанного в заголовке соединения (74,7 мг).
1H ЯМР (300 МГц, ДМСО-д6) δ 1,45 (3H, с), 2,24-2,37 (2H, м), 2,65-2,76 (2H, м), 3,91-4,01 (2H, м), 4,01-4,13 (2H, м), 4,46 (2H, с), 4,68 (1H, квинт, J=7,1 Гц), 6,97-7,05 (1H, м), 7,08-7,17 (1H, м), 7,45 (1H, дд, J=8,4, 3,1 Гц), 8,37 (1H, с).
[0342]
Соединения из примеров приведены в Таблице 1 далее. MС в таблицах означает фактическое измеренное значение. Соединения Примеров 34-38, 40-43, 45, 47-49, 51-62 и 64 в следующих таблицах были получены в соответствии со способами, описанными в вышеупомянутых примерах, или способах, аналогичных им.
[0343]
Таблица 1-1

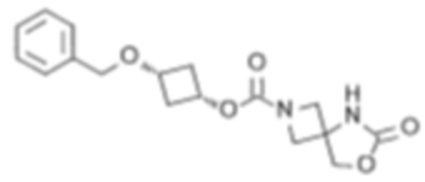


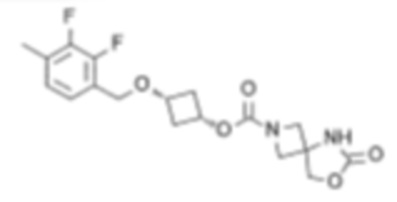



[0344]
Таблица 1-2

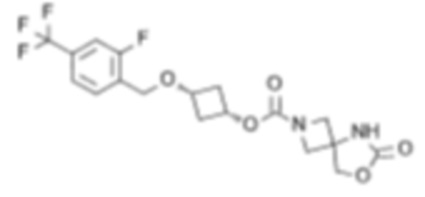

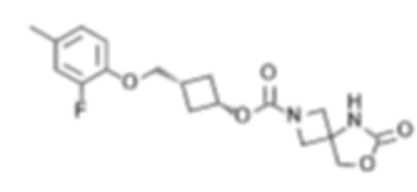

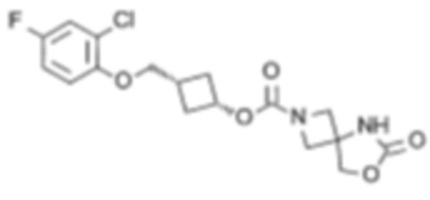
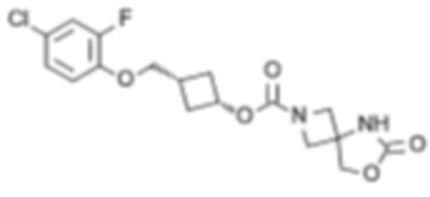
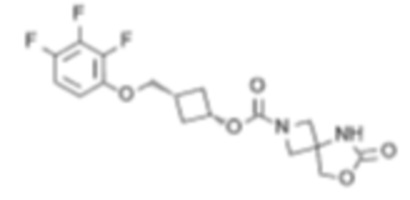
[0345]
Таблица 1-3


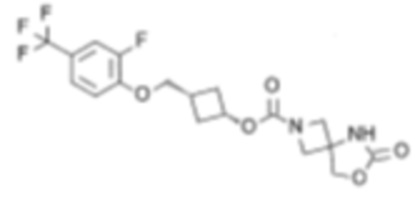
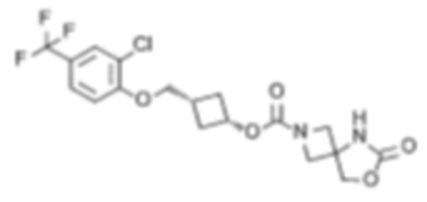
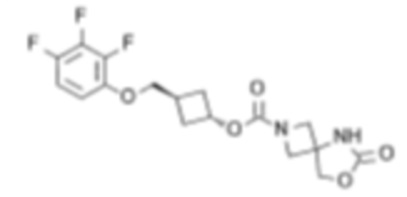
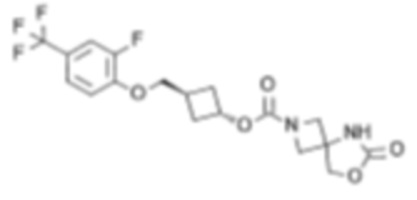


[0346]
Таблица 1-4

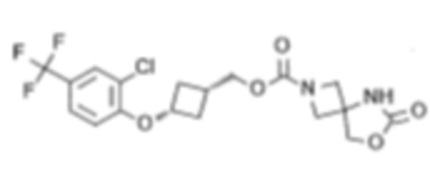

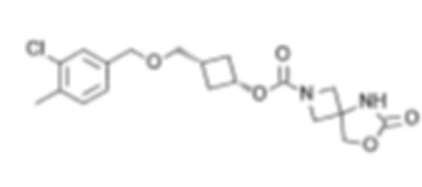
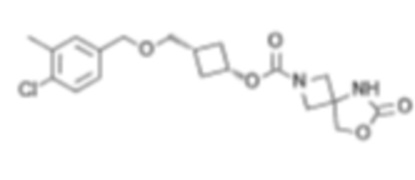

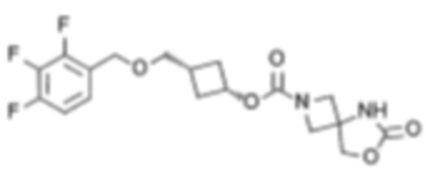
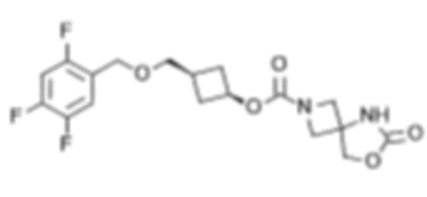
[0347]
Таблица 1-5
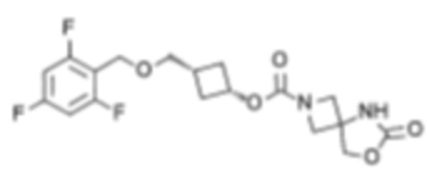




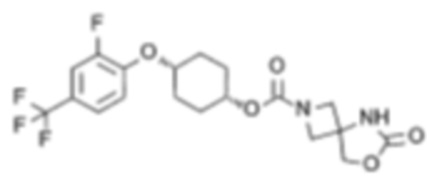
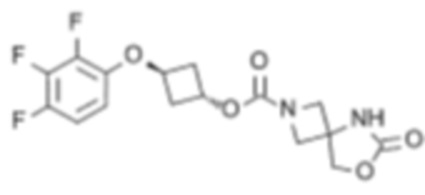

[0348]
Таблица 1-6
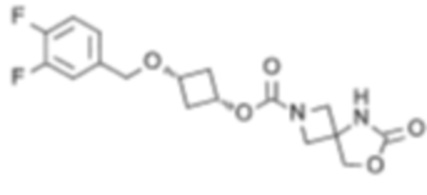

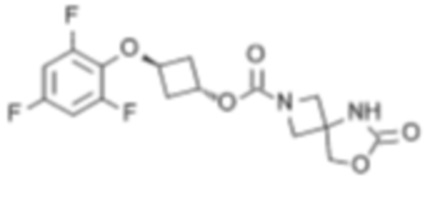
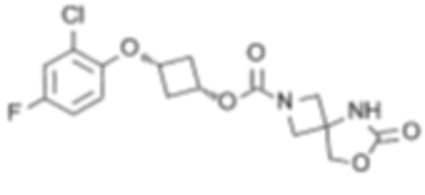

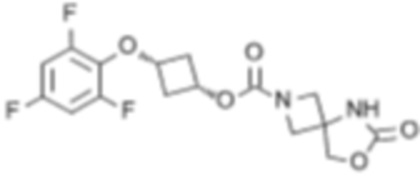


[0349]
Таблица 1-7
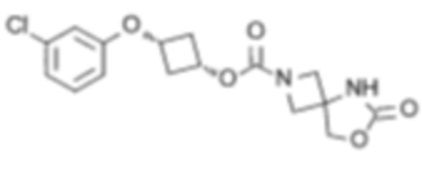
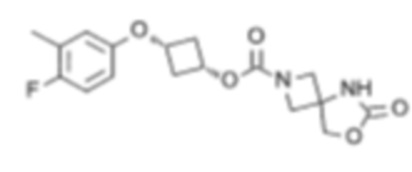


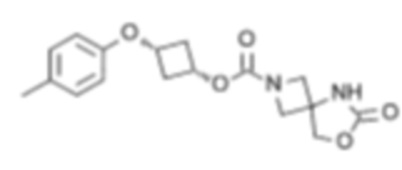

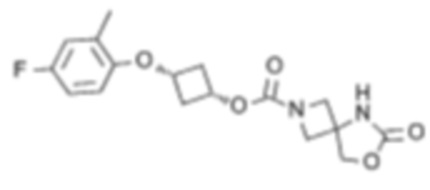
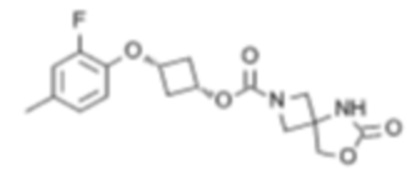
[0350]
Таблица 1-8
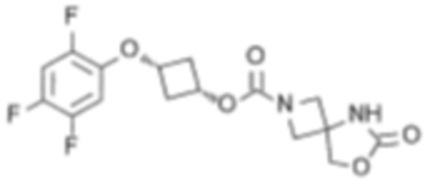

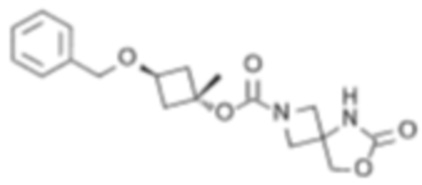
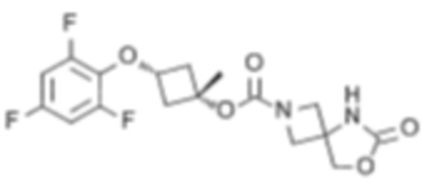


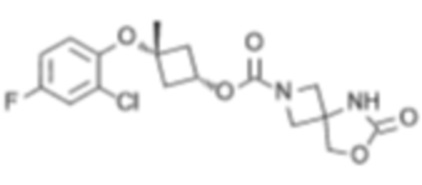
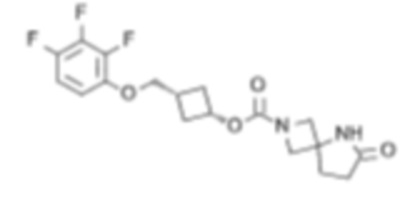
[0351]
Сравнительный пример 1
(1r,3r)-3-(бензилокси)циклобутан-1-ол (идентичен транс-3-(бензилокси)циклобутанолу)
[0352]
A) (1r,3r)-3-(бензилокси)циклобутил-4-нитробензоат
К смеси 3-(бензилокси)циклобутанона (24,7 г) и метанола (300 мл) прибавляли малыми порциями борогидрид натрия (5,30 г) при 0°C, и смесь перемешивали при 23°C в течение 2 ч. Метанол выпаривали при пониженном давлении и остаток разбавляли 0,5 М соляной кислотой (200 мл). Смесь экстрагировали этилацетатом. Экстракт промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением неочищенного продукта (21,8 г). Данный неочищенный продукт разделяли ВЭЖХ (колонка: CHIRALPAK AD (торговое наименование), 50 мм ID x 500 мл, произведенная Daicel Corporation, подвижная фаза: гексан/этанол (900/100 (об./об.))) с получением (1s,3s)-3-(бензилокси)циклобутан-1-ола (17,7 г). К полученной смеси (1s,3s)-3-(бензилокси)циклобутан-1-ола (10,0 г), 4-нитробензойной кислоты (14,07 г), трифенилфосфина (22,07 г) и ТГФ (125 мл) по каплям прибавляли DIAD (18,91 г) при 0°C, и смесь нагревали до комнатной температуры. Смесь перемешивали в течение ночи при комнатной температуре, разбавляли толуолом, и концентрировали при пониженном давлении до около 100 мл. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (18,45 г).
1H ЯМР (300 МГц, ДМСО-д6) δ2,42-2,49 (4H, м), 4,34 (1H, квин, J=5,8 Гц), 4,42 (2H, с), 5,21-5,40 (1H, м), 7,18-7,42 (5H, м), 8,15-8,27 (2H, м), 8,30-8,46 (2H, м).
[0353]
B) (1r,3r)-3-(бензилокси)циклобутан-1-ол
К смеси (1r,3r)-3-(бензилокси)циклобутил-4-нитробензоата (18,37 г) и ТГФ (100 мл)/метанола (20,0 мл) по каплям добавляли 2M водный раствор гидроксида натрия (84 мл) при 0°C, и смесь перемешивали в течение ночи при комнатной температуре. Органический растворитель выпаривали при пониженном давлении, и остаток разделяли между водой и этилацетатом. Экстракт промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (этилацетат/гексан) с получением указанного в заголовке соединения (9,65 г).
1H ЯМР (300 МГц, ДМСО-д6) δ1,95-2,08 (2H, м), 2,12-2,25 (2H, м), 4,09-4,20 (1H, м), 4,27 (1H, тк, J=7,1, 4,9 Гц), 4,33 (2H, с), 4,98 (1H, д, J=5,3 Гц), 7,21-7,42 (5H, м).
[0354]
Экспериментальный пример 1: Клонирование MGLL человека, кодирующего белок MAGL, и конструирование плазмиды экспрессии
кДНК MGLL человека получали с помощью ПЦР с использованием клона ORF человека (форма ДНК; идентификатор клона: 100004585) в качестве матрицы. Для ПЦР использовали два вида праймеров:
5’-CCACCATCATCACGGATCCATGCCAGAGGAAAGTTCCCCCA-3’
[SEQ ID NO: 1]
и
5’-TGGTGCTCGAGTGCGGCCGCTCAGGGTGGGGACGCAGTTC-3’
[SEQ ID NO: 2]
и ДНК-полимеразу PrimeSTAR MAX (Takara Bio Inc.) и (1) реакцию проводили при 98°C в течение 1 мин, (2) 25 циклов реакции при 98°C в течение 10 с и 68°C в течение 10 с за один цикл, и (3) реакцию проводили при 72°C в течение 1 мин. Полученный продукт ПЦР расщепляли Bam HI и Not I (Takara Bio Inc.), вставляли в сайт Bam HI/Not I pET21HH (V) (pET21a (Novagen), вставленный с последовательностью распознавания протеазы His x6 и TEV), используя Ligation High (Toyobo Co., Ltd.) и вводили в ECOSTM JM109 (Nippon Gene Co., Ltd.), посредством чего конструировали плазмиду экспрессии pET21HH(V)/His-hMGLLv2 для Escherichia coli.
[0355]
Экспериментальный пример 2: Получение рекомбинантного меченого полигистидином белка MAGL человека.
Рекомбинантный белок His-hMAGL был получен путем трансформации ECOSTM Competent E. coli BL21(DE3) (Nippon Gene Co., Ltd.) с плазмидой pET21HH(V)/His-hMGLLv2, полученной выше. Escherichia coli, полученный путем трансформации, инокулировали в 10 мл среды LB (1% пептона, 0,5% дрожжевого экстракта, 0,5% хлорида натрия, 0,01% ампициллина) и культивировали при 30°C в течение 16 ч. Полученную культуральную среду (5 мл) пересаживали в 2-литровую колбу Сакагучи, содержащую 1 л основной ферментационной среды (1,05% M9 MEDIUM BROTH (AMRESCO LLC), 0,5% дрожжевого экстракта, 1,5% сорбита, 1,5% казаминовой кислоты, 0,024% сульфата магния, 0,01% пеногасителя PE-L (Wako Pure Chemical Industries, Ltd.), 0,01% ампициллина) и начали встряхивать культуру при 37°C и 150 об./мин. Когда мутность культуральной среды достигала примерно 500 единиц Клетта, температуру культуры снижали до 16°C, прибавляли изопропил-β-D-тиогалактопиранозид (IPTG) до конечной концентрации 1 мМ, и смесь дополнительно культивировали для 19 ч. После завершения культивирования культуральную среду центрифугировали (4°C, 6000 об./мин, 10 мин) с получением His-hMAGL-экспрессированного Escherichia coli. Затем экспрессированную His-hMAGL Escherichia coli суспендировали в 50 мМ Трис-HCl (рН 8,0, 100 мл), содержащем 1% тритона Х-100, 20 мМ имидазола, 3 мМ DTT, 5 ед./мл бензоназы (Merck) и 150 мМ NaCl, и суспензию достаточно охладили и подвергли обработке ультразвуком при AMPLITUDE=60%, 15 с/вкл., 30 с/выкл. в течение 3 мин с использованием 3/4” дробленый рог твердого типа BRANSON Digital Sonifier 450 (Central Scientific Commerce, Inc.). Кроме того, гомогенат центрифугировали (4°C, 6000 об./мин, 20 мин) и получали супернатант. В качестве аппарата для очистки использовался AKTA explorer 10s (GE Healthcare Japan Corporation) при 4°C. К полученному супернатанту добавляли 5М NaCl до конечной концентрации соли 0,3 М, и смесь протекала через и адсорбировалась на 5 мл картриджах Ni-NTA Superflow (QIAGEN), заранее уравновешенных с буфером A (50 мM Трис-HCl (pH 8,0), содержащим 0,05% Тритон X-100, 1 мM DTT, 300 мM NaCl). Колонку достаточно промывали буфером A, содержащим 20 мМ имидазола, и His-hMAGL элюировали буфером A, содержащим имидазол в конечной концентрации 250 мМ. Затем элюат подвергали гель-фильтрации с использованием HiLoad 16/600 Superdex 200 пг (GE Healthcare Japan Corporation), уравновешенного 50 мМ Трис-HCl pH 8,0, содержащим 10% глицерина, 0,05% тритона X-100, 1 мМ DTT и 150 мм NaCl. Элюированную фракцию концентрировали с помощью Amicon Ultra-15 10K (Merck Millipore) с получением очищенного белка His-hMAGL. Концентрацию белка измеряли с помощью набора для анализа белка BCA (Thermo Fisher Scientific) с использованием BSA в качестве стандарта.
[0356]
Экспериментальный пример 3: Измерение ингибирующей активности MAGL
His-hMAGL, полученный выше, разбавляли ферментным реакционным буфером (10 мМ Трис-HCl, pH 7,5, 1 мМ ЭДТА, 0,025% (масс./об.) Тритон Х-100, 0,01% бычьего сывороточного альбумина) до концентрации 7,5 нг/мл. В каждую лунку 384-луночного аналитического планшета (Greiner 781280) добавляли раствор (5 мкл) тестируемого соединения, растворенного в диметилсульфоксиде (ДМСО), который разбавляли вышеупомянутым ферментным реакционным буфером, затем добавляли раствор His-hMAGL (5 мкл), разбавленный до концентрации 7,5 нг/мл, и смесь инкубировали при комнатной температуре в течение 60 мин. После этого в каждую лунку добавляли 5 мкл 150 мкМ 2-арахидонилглицерина (Tocris Bioscience), и смесь инкубировали при комнатной температуре в течение 10 мин. Затем добавляли 10 мкл 2% муравьиной кислоты (Wako Pure Chemical Industries, Ltd.), чтобы остановить реакцию. Кроме того, добавляли ацетонитрил (50 мкл), содержащий 3 мкМ арахидоновой кислоты-d8 (Cayman Chemical Company), и смесь перемешивали.
Количество арахидоновой кислоты в полученной ферментативной реакционной смеси рассчитывали путем измерения с помощью RapidFire-масс-спектрометрии и корректировки по количеству арахидоновой кислоты-d8. Высокопроизводительную твердофазную экстракцию в режиме онлайн проводили с использованием системы RapidFire 300TM (Agilent Technologies, Inc.). Образцы загружали на картридж SPE C4 (Agilent Technologies, Inc.) и обессоливали 0,2% (об./об.) уксусной кислотой (Wako Pure Chemical Industries, Ltd.) в сверхчистой воде/ацетонитриле (70/30, об./об. ) при скорости потока 1,5 мл/мин, элюировали при скорости потока 0,5 мл/мин 0,2% (об./об.) уксусной кислоты, растворенной в ацетонитриле/сверхчистой воде (90/10, об./об. ) и вводили в масс-спектрометрическую часть. Инъекционную иглу промывали сверхчистой водой (500 миллисекунд) и ацетонитрилом (500 миллисекунд), чтобы минимизировать перенос. Время всасывания (цикл впрыска 5 мкл), время загрузки/очистки, время элюирования и время повторного уравновешивания были доведены до 300, 3000, 4250 и 1000 миллисекунд соответственно, а общее время цикла привели до около 10,0 секунд. Систему RapidFire300 контролировали программным обеспечением RapidFire UI версии 3.6 (Agilent Technologies, Inc.).
Масс-спектрометрию полученного продукта проводили с использованием API4000TM тройного квадрупольного масс-спектрометра (AB SCIEX), оснащенного ионного источника для электрораспыления (TurboIon SprayTM) в негативном режиме контроля селективных реакций (SRM). Условия SRM показаны ниже. Параметры прибора были оптимизированы следующим образом: температура капилляра 600°C, напряжение распыления ионов -4,5 кВ, газ для соударений 8, газовая завеса 15 фунтов на кв. дюйм, газ источника ионов 1 60 фунтов на кв. дюйм, газ источника ионов 2 60 фунтов на кв. Масс-спектрометр контролировали с помощью программного обеспечения AnalystTM версии 1.5.1 (AB SCIEX). Интеграцию площади пика анализировали с использованием программного обеспечения интегратора RapidFire версии 3.6 (Agilent Technologies, Inc.).
Скорость ингибирования MAGL (%) рассчитывали в соответствии со следующей формулой расчета.
(1-(количество продуцируемой арахидоновой кислоты тестируемого соединения из прибавляемой группы - количество продуцируемой арахидоновой кислоты из группы, не содержащей ферментов) ÷ (количество продуцируемой арахидоновой кислоты из группы, не содержащей тестируемого соединения - количество продуцируемой арахидоновой кислоты из группы, не содержащей ферментов))×100
Результаты проиллюстрированы в следующей Таблице. 2.
[0357]
Таблица 2-1
[0358]
Таблица 2-2
[0359]
Как видно из Таблицы 2, соединение по настоящему изобретению обладает ингибирующей активностью в отношении MAGL.
[0360]
Экспериментальный пример 4: Измерение внутрицеребральных концентраций 2-AG и арахидоновой кислоты
В качестве мыши использовали 8-недельных самцов мышей C57BL/6J (CLEA Japan, Inc.) (6 мышей на группу). Растворы для введения готовили путем суспендирования тестируемых соединений (соединение 1 (соединение Примера 16), соединение 2 (соединение Примера 18) и соединение 3 (соединение Примера 46)) в 0,5% растворе метилцеллюлозы (Wako Pure Chemical Industries, Ltd.). Доза тестируемого соединения составляла 1 мг/кг массы тела/10 мл. Тестируемые соединения вводили через желудочный зонд в дозе 1 мг/кг массы тела. Мозг выделяли после введения испытуемого соединения (время выделения после введения тестируемого соединения проиллюстрировано в Таблице 3), а полушарие головного мозга экстрагировали. Полученное полушарие головного мозга замораживали на сухом льду и измеряли массу замороженной ткани.
[0361]
Ткань головного мозга гомогенизировали с 4-кратным (по объему) изопропанолом (IPA) и дважды разбавляли IPA. К разбавленному образцу (200 мкл) прибавляли раствор внутреннего стандарта (5 мкл) ([5,6,8,9,11,12,14,15-D8]-(5Z,8Z,11Z,14Z)5,8,11,14-эйкозатетраеновой кислоты (AA-d8, 0,5 нмоль/мл IPA) и [5,6,8,9,11,12,14,15-D8]-(5Z,8Z,11Z,14Z)-5,8,11,14-эйкозатетраеноил-2-глицериновый эфир (2-AG-d8, 0,5 нмоль/мл IPA)), и смесь центрифугировали при 15000 об./мин в течение 5 мин. Супернатант вводили в жидкостный хроматограф - масс-спектрометр для количественного анализа.
Для жидкостной хроматографии использовали систему Shimadzu LC20A (Shimadzu Corporation). Разделение проводили методом градиентного элюирования с подвижной фазой A (10 ммоль/л HCOONH4/HCOOH (100:0,2, об./об.)) и подвижной фазой B (этанол/IPA (3:2, об./об.)) с использованием Shim-pack XR-ODS (2,2 мкм, 2,0 × 30 мм, Shimadzu Corporation) при температуре колонки 50°C, при скорости потока 0,5 мл/мин. Условия градиента представлены ниже: 0-1 мин, 1% B; 1-1,2 мин, 1-55% B; 1,2-2,7 мин, 55-75% B; 2,7-3,5 мин, 75-99% B; 3,5-6 мин, 99% B; 6-8 мин, 1% B.
В качестве масс-спектрометра использовали API5000 (AB SCIEX). Элюат из жидкостной хроматографии непосредственно ионизировали методом ионизации турбоспреем, где (5Z,8Z,11Z,14Z)5,8,11,14-эйкозатетраеновую кислоту (AA) и AA-d8 измеряли в отрицательном режиме ионизации, и (5Z,8Z,11Z,14Z)5,8,11,14-эйкозатетраеноил-2-глицериновый эфир (2-AG) и 2-AG-d8 измеряли в положительном режиме ионизации. Условия обнаружения масс-спектрометра проиллюстрированы в Таблице 4.
Раствор для калибровочной кривой готовили до концентрации 2, 5, 10, 20, 50, 100, 200, 500, 1000 нмоль/мл ацетонитрила. Эти растворы (10 мкл) смешивали с 200 мкл IPA и 5 мкл раствора внутреннего стандарта, и смесь центрифугировали при 15000 об./мин в течение 5 мин, и супернатант вводили в жидкостный хроматограф-масс-спектрометр. Линейная регрессия с 1/x2 взвешиванием было использовано для подбора калибровочной кривой, а количественная оценка была подтверждена с точностью 100±20% и R2>0,99.
Результаты представлены в Таблице 5.
[0362]
Как видно из Таблицы 5, соединения 1, 2 и 3 мигрировали в мозг при пероральном введении мышам C57BL/6J, и эти соединения увеличивали внутрицеребральную концентрацию 2-AG и одновременно снижали внутрицеребральную концентрацию арахидоновой кислоты по сравнению с контролем.
[0363]
Таблица 3
[0364]
Таблица 4
параметр масс-спектрометра
DP︰ потенциал разложения
EP︰ входной потенциал
CE: энергия расщепления
CXP: напряжение на выходе ячейки соударений
[0365]
Таблица 5
[0366]
Примеры препарата
Лекарственные средства, содержащие соединение по данному изобретению в качестве активного компонента, могут быть получены, например, в виде следующих препаратов.
1. капсула
(1) соединение, полученное в Примере 1 10 мг
(2) лактоза 90 мг
(3) микрокристаллическая целлюлоза 70 мг
(4) стеарат магния 10 мг
1 капсула 180 мг
Общее количество вышеупомянутых (1), (2) и (3) и 5 мг (4) смешивают и гранулируют, и добавляют 5 мг оставшегося (4). Вся смесь запечатывается в желатиновую капсулу.
[0367]
2. таблетка
(1) соединение, полученное в Примере 1 10 мг
(2) лактоза 35 мг
(3) кукурузный крахмал 150 мг
(4) микрокристаллическая целлюлоза 30 мг
(5) стеарат магния 5 мг
1 таблетка 230 мг
Общее количество вышеуказанных (1), (2) и (3), 20 мг (4) и 2,5 мг (5) смешивают и гранулируют, а 10 мг оставшегося (4) и 2,5 мг оставшегося (5) добавляют в смесь для прессования в форме таблетки.
Промышленная применимость
[0368]
Согласно данному изобретению соединение, обладающее ингибирующим действием в отношении MAGL, которое, как ожидается, будет пригодно в качестве агента для профилактики или лечения нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, травматического повреждения головного мозга, глаукомы, рассеянного склероза и т. д.), тревожного расстройство, боли (например, воспалительной боли, раковой боли, нейрогенной боли и т. д.), эпилепсии, депрессии и тому подобное.
[0369]
Данная заявка основана на заявке на патент № 2017-190838, поданной 29 сентября 2017 г. в Японии, содержание которой полностью включено в настоящий документ.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОКСАДИАЗОЛЫ В КАЧЕСТВЕ АГОНИСТОВ МУСКАРИНОВОГО РЕЦЕПТОРА M1 И/ИЛИ M4 | 2019 |
|
RU2817018C2 |
| ИНГИБИТОРЫ УРИДИН-5-ДИФОСФАТ (UDP) ГЛИКОЗИЛТРАНСФЕРАЗЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2810928C2 |
| СПИРО-КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ПИПЕРИДИНА ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КАЛИЕВОГО КАНАЛА НАРУЖНОГО МЕДУЛЛЯРНОГО СЛОЯ | 2013 |
|
RU2642066C2 |
| ПРОИЗВОДНЫЕ 6-(ПИРИМИДИНОАМИНОПИРИДИН)БЕНЗОИМИДАЗОЛА, ПОЛЕЗНЫЕ ДЛЯ ЛЕЧЕНИЯ РАКА | 2014 |
|
RU2670762C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СПИРОСОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ MAGL | 2018 |
|
RU2726631C1 |
| АНТАГОНИСТЫ РЕЦЕПТОРА СОМАТОСТАТИНА ПОДТИПА 5 (SSTR5) | 2014 |
|
RU2671958C2 |
| ПРОИЗВОДНОЕ ДИГИДРОПИРИДАЗИН-3,5-ДИОНА | 2014 |
|
RU2662832C2 |
| ФАРМАЦЕВТИЧЕСКИЕ СОЕДИНЕНИЯ | 2018 |
|
RU2767857C2 |
| НОВОЕ СОЕДИНЕНИЕ БИФЕНИЛА ИЛИ ЕГО СОЛЬ | 2016 |
|
RU2726622C2 |
| КЛАСС БИФУНКЦИОНАЛЬНЫХ ХИМЕРНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ ДЛЯ НАПРАВЛЕННОГО РАЗРУШЕНИЯ АНДРОГЕННЫХ РЕЦЕПТОРОВ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2825000C2 |
Группа изобретений относится к области органической химии и фармацевтики и предназначена для использования в лечении нейродегенеративных заболеваний. Представлено новое соединение формулы (I), где A представляет собой C3-10 циклоалкильную группу, замещенную 1-3 заместителями, выбранными из (a) феноксигруппы, необязательно замещенной 1-4 заместителями, выбранными из (i) атома галогена и (ii) необязательно галогенированной C1-6 алкильной группы, (b) фенокси-C1-6 алкильной группы, необязательно замещенной 1-4 заместителями, выбранными из (i) атома галогена и (ii) необязательно галогенированной C1-6 алкильной группы, (c) бензилоксигруппы, необязательно замещенной 1-4 заместителями, выбранными из (i) атома галогена и (ii) необязательно галогенированной C1-6 алкильной группы, и (d) бензилокси-C1-6 алкильной группы, необязательно замещенной 1-4 заместителями, выбранными из (i) атома галогена и (ii) необязательно галогенированной C1-6 алкильной группы и необязательно дополнительно замещенной 1-3 С1-6 алкильными группами; L представляет собой связь или C1-3 алкиленовую группу; кольцо D представляет собой 4- или 5-членный азотсодержащий гетероцикл; n равно 1 или 2; X представляет собой -O- или -CH2-; и оба Ra и Rb представляют собой атомы водорода; или его фармацевтически приемлемая соль. Кроме того, описаны конкретные соединения-производные формулы (I), лекарственное средство, представляющее собой ингибитор моноацилглицеринлипазы и содержащее указанное соединение, а также способ ингибирования моноацилглицеринлипазы у млекопитающего, включающий введение млекопитающему эффективного количества соединения или соли по п. 1. Группа изобретений обеспечивает эффективное ингибирование моноацилглицеринлипазы у млекопитающего. 6 н. и 3 з.п. ф-лы, 5 табл., 67 пр.
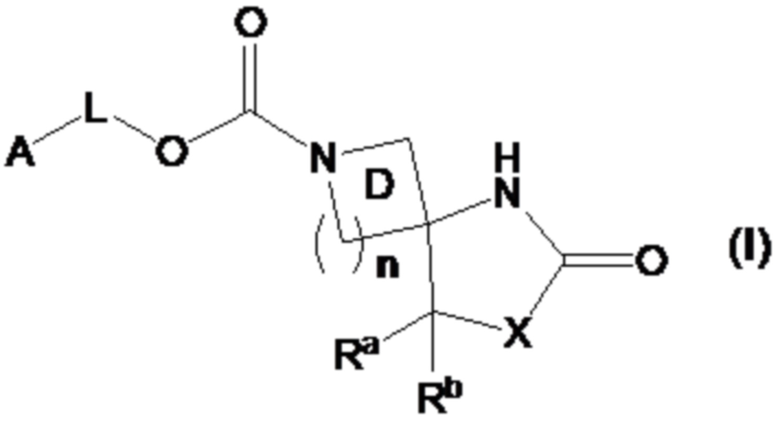
1. Соединение, представленное формулой (I):
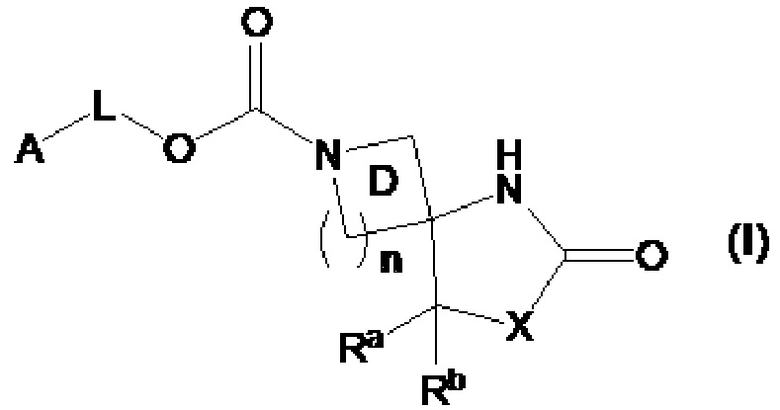
где
A представляет собой C3-10 циклоалкильную группу, замещенную 1-3 заместителями, выбранными из
(a) феноксигруппы, необязательно замещенной 1-4 заместителями, выбранными из
(i) атома галогена и
(ii) необязательно галогенированной C1-6 алкильной группы,
(b) фенокси-C1-6 алкильной группы, необязательно замещенной 1-4 заместителями, выбранными из
(i) атома галогена и
(ii) необязательно галогенированной C1-6 алкильной группы,
(c) бензилоксигруппы, необязательно замещенной 1-4 заместителями, выбранными из
(i) атома галогена и
(ii) необязательно галогенированной C1-6 алкильной группы, и
(d) бензилокси-C1-6 алкильной группы, необязательно замещенной 1-4 заместителями, выбранными из
(i) атома галогена и
(ii) необязательно галогенированной C1-6 алкильной группы и
необязательно дополнительно замещенной 1-3 С1-6 алкильными группами;
L представляет собой связь или C1-3 алкиленовую группу;
кольцо D представляет собой 4- или 5-членный азотсодержащий гетероцикл;
n равно 1 или 2;
X представляет собой -O- или -CH2-; и
оба Ra и Rb представляют собой атомы водорода;
или его фармацевтически приемлемая соль.
2. Соединение или фармацевтически приемлемая соль по п. 1, где
A представляет собой циклобутильную группу, замещенную одним заместителем, выбранным из
(a) феноксигруппы, замещенной 3 атомами галогена, и
(b) феноксиметильной группы, замещенной 3 атомами галогена;
L представляет собой связь;
кольцо D представляет собой азетидиновое кольцо;
n равно 1;
X представляет собой -O-; и
оба Ra и Rb представляют собой атомы водорода.
3. цис-3-((2,3,4-Трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат или его фармацевтически приемлемая соль.
4. цис-3-((2,4,6-Трифторфенокси)метил)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат или его фармацевтически приемлемая соль.
5. цис-3-(2,4,6-Трифторфенокси)циклобутил-6-оксо-7-окса-2,5-диазаспиро[3.4]октан-2-карбоксилат или его фармацевтически приемлемая соль.
6. Лекарственное средство, представляющее собой ингибитор моноацилглицеринлипазы, содержащее соединение или соль по п. 1.
7. Лекарственное средство по п. 6, отличающееся тем, что является агентом для профилактики или лечения болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, рассеянного склероза, тревожного расстройства, боли, эпилепсии или депрессии.
8. Способ ингибирования моноацилглицеринлипазы у млекопитающего, включающий введение млекопитающему эффективного количества соединения или соли по п. 1.
9. Соединение или соль по п. 1 для применения в профилактике или лечении болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона, бокового амиотрофического склероза, рассеянного склероза, тревожного расстройства, боли, эпилепсии или депрессии.
| WO 2017021805 A1, 09.02.2017 | |||
| PATEL J | |||
| et al., Loratadine analogues as MAGL inhibitors | |||
| Bioorganic & medicinal chemistry letters, 24.02.2015, vol | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| JP 2016525092 A, 22.08.2016 | |||
| JP 2015510938 A, 13.04.2015 | |||
| ПРОИЗВОДНЫЕ ДИАЗАСПИРОПИПЕРИДИНА | 2004 |
|
RU2355690C2 |
Авторы
Даты
2022-10-04—Публикация
2018-09-27—Подача