Перекрестная ссылка на родственную заявку
[01] Настоящая заявка испрашивает приоритет на основании патентной заявки США №62/479248, поданной 30 марта 2017 г. под названием "Модуляция гена сиртуина в эпидермальных кератиноцитах с помощью декапептида-12", которая включена в настоящую заявку посредством ссылки со всеми процитированными источниками.
Перечень последовательностей
[02] Настоящая заявка включает посредством ссылки перечень последовательностей под названием "ELLXP004US_ST25.txt» (3 килобайта), созданный 21 марта 2018 г. и поданный вместе с настоящей заявкой в электронном виде.
Уровень техники
[03] Настоящее изобретение относится к области новых биологических агентов.
Краткое описание изобретения
[04] В недавних сообщениях подробно описаны плейотропные роли сиртуинов в подавлении преждевременного старения, замедлении клеточного старения, увеличении продолжительности жизни и облегчении состояния при широком спектре нарушений старения. В настоящем документе мы приводим полученные нами данные о мощном активаторе сиртуина, декапептиде-12, и сравниваем его эффективность с хорошо описанным оксиресвератролом. Обработка предшественников эпидермальных кератиноцитов человека 100 мкМ декапептидом-12 усиливала транскрипцию SIRT1 на 141±11 процентов по сравнению с контрольными клетками, в то время как уровни SIRT3, SIRT6 и SIRT7 повышались на 121±13 процентов, 147±8 процентов и 95±14 процентов, соответственно. Декапептид-12 активировал транскрипцию сиртуина до уровня, аналогичного оксиресвератролу, но при пониженной цитотоксичности.
[05] Пептид в соответствии одним из вариантов реализации состоит из SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11 или SEQ. ID NO: 12.
[06] Пептид в соответствии с различными вариантами реализации состоит из SEQ ID NO: 9, модифицированной модифицирующей группой, причем указанная модифицирующая группа представляет собой пальмитоильную группу и/или ацетильную группу на N-конце или амидирование С-конца, или и то, и другое.
[07] Пептид в соответствии с различными вариантами реализации состоит из SEQ ID NO: 11, содержащей аминокислоту тирозин в положении 6 в виде D-изоформы, а все остальные аминокислоты представляют собой L-изоформы.
[08] Композиция в соответствии с одним из вариантов реализации содержит первый пептид, состоящий из SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11 или SEQ. ID NO: 12.
[09] Композиция в соответствии с различными вариантами реализации состоит из SEQ ID NO: 9, модифицированной модифицирующей группой, причем указанная модифицирующая группа представляет собой пальмитоильную группу и/или ацетильную группу на N-конце или амидирование С-конца, или и то, и другое.
[10] Композиция в соответствии с различными вариантами реализации состоит из SEQ ID NO: 11, содержащей аминокислоту тирозин в положении 6 в виде D-изоформы, а все остальные аминокислоты представляют собой L-изоформы.
[11] Композиция в соответствии с некоторыми из вариантов реализации содержит пептид в концентрации 1 мкМ или более.
[12] Вариант реализации способа лечения субъекта путем модуляции экспрессии гена сиртуина в клетке кожи с целью уменьшения симптомов старения кожи включает введение субъекту, нуждающемуся в этом, композиции, содержащей эффективное количество одного или более пептидов, причем указанные один или более пептидов состоят из SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11 или SEQ. ID NO: 12.
[13] В способе в соответствии с некоторыми из вариантов реализации указанный пептид состоит из SEQ ID NO: 9, модифицированной модифицирующей группой, причем указанная модифицирующая группа представляет собой пальмитоильную группу и/или ацетильную группу на N-конце или амидирование С-конца, или и то, и другое.
[14] В способе в соответствии с различными вариантами реализации указанный пептид состоит из SEQ ID NO: 11, содержащей аминокислоту тирозин в положении 6 в виде D-изоформы, а все остальные аминокислоты представляют собой L-изоформы.
[15] В способе в соответствии с различными вариантами реализации клетка кожи представляет собой предшественник.
[16] В соответствии с различными вариантами реализации предшественник представляет собой предшественник эпидермального кератиноцита, меланобласт, фибробласт, гистиобласт или дендробласт.
[17] В способе в соответствии с некоторыми из вариантов реализации клетка кожи является окончательно дифференцированной.
[18] В соответствии с различными вариантами реализации способа клетка кожи представляет собой кератиноцит, меланоцит, фиброцит, гистиоцит или дендроцит.
[19] В некоторых вариантах реализации способов пептид присутствует в концентрации 1 мкМ или более.
[20] В конкретных вариантах реализации ген сиртуина содержит SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6; или SEQ ID NO: 7.
[21] В некоторых вариантах реализации композиция дополнительно содержит оксиресвератрол.
[22] В определенных вариантах реализации клетка кожи представляет собой клетку млекопитающего.
[23] В некоторых вариантах реализации клетка кожи является клеткой человека.
[24] Вариант реализации способа модуляции экспрессии гена сиртуина в клетке кожи включает введение субъекту, нуждающемуся в этом, композиции, содержащей эффективное количество одного или более пептидов, причем указанные один или более пептидов состоят из SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11 или SEQ. ID NO: 12.
[25] Другие объекты, свойства и преимущества настоящего изобретения станут более очевидны при рассмотрении следующего подробного описания и прилагаемых чертежей, на которых аналогичные обозначения представляют собой аналогичные свойства на всех фигурах.
Краткое описание чертежей
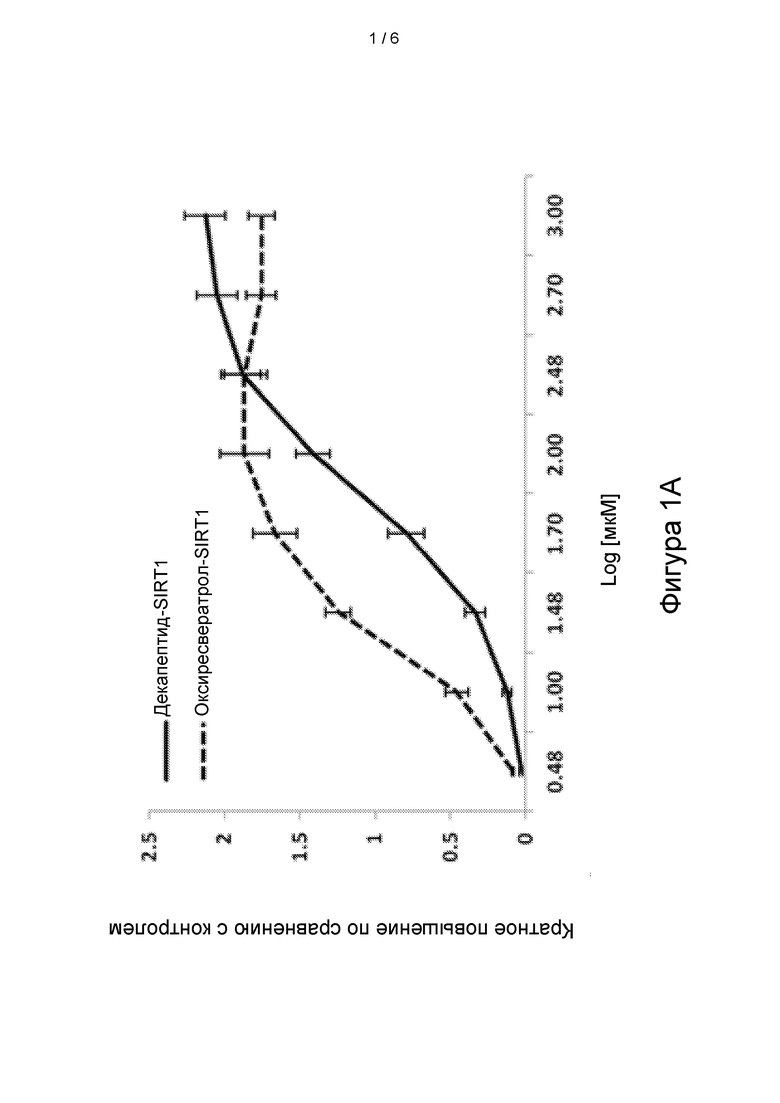
[26] На фигуре 1А показана стимуляция транскрипции SIRT1 в зависимости от дозы (a). Данные приведены в виде кратного увеличения по сравнению с внутренним контролем - геном 18S, и представляют собой средние значения ± SEM по 3 независимым экспериментам.
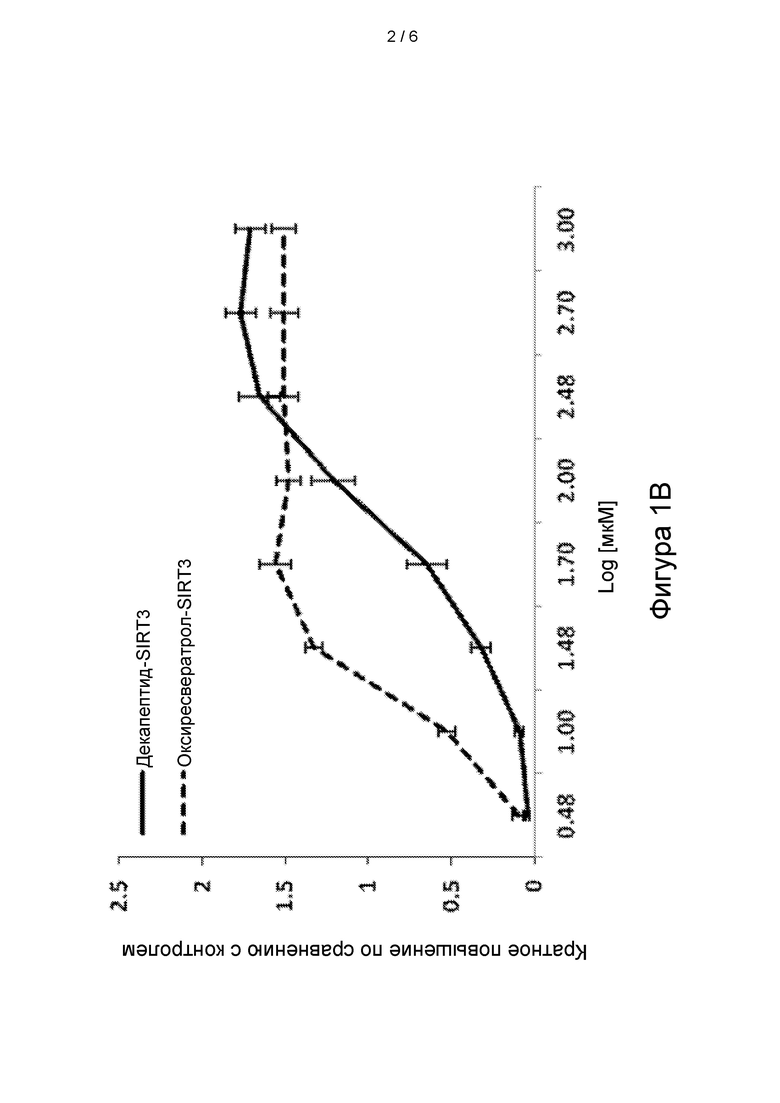
[27] На фигуре 1В показана стимуляция транскрипции SIRT3 в зависимости от дозы (b). Данные приведены в виде кратного увеличения по сравнению с внутренним контролем - геном 18S, и представляют собой средние значения ± SEM по 3 независимым экспериментам.
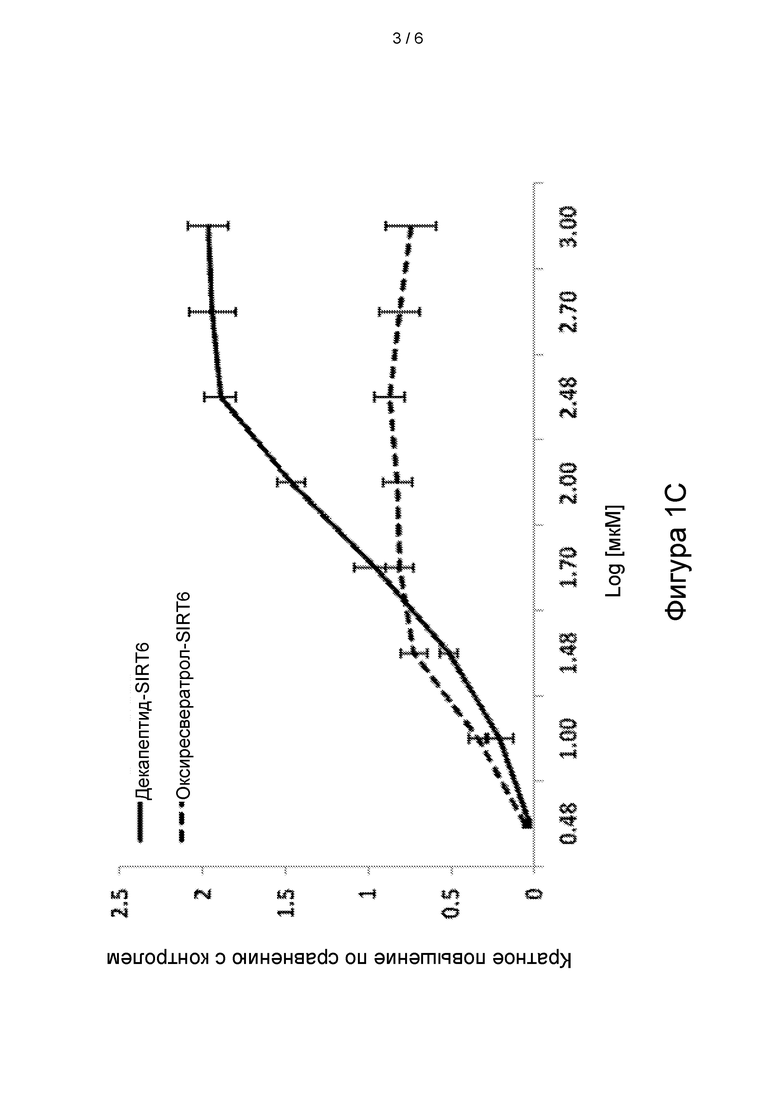
[28] На фигуре 1С показана стимуляция транскрипции SIRT6 в зависимости от дозы (c). Данные приведены в виде кратного увеличения по сравнению с внутренним контролем - геном 18S, и представляют собой средние значения ± SEM по 3 независимым экспериментам.
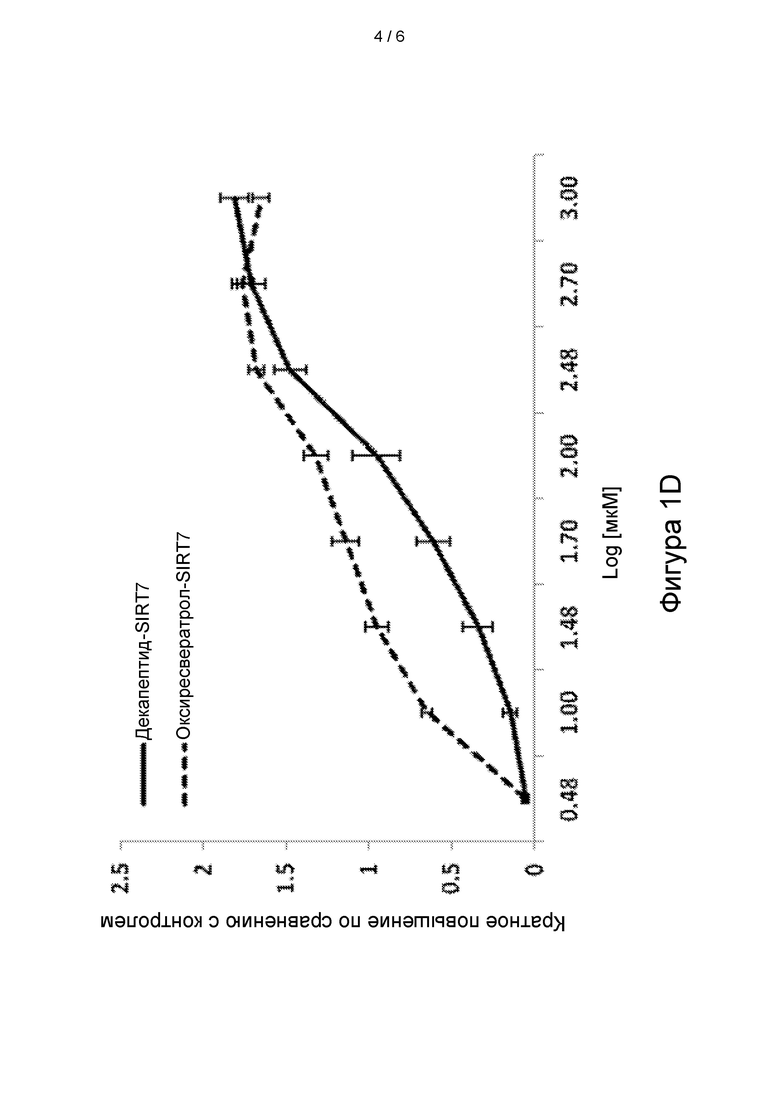
[29] На фигуре 1D показана стимуляция транскрипции SIRT7 в зависимости от дозы (d). Данные приведены в виде кратного увеличения по сравнению с внутренним контролем - геном 18S, и представляют собой средние значения ± SEM по 3 независимым экспериментам.
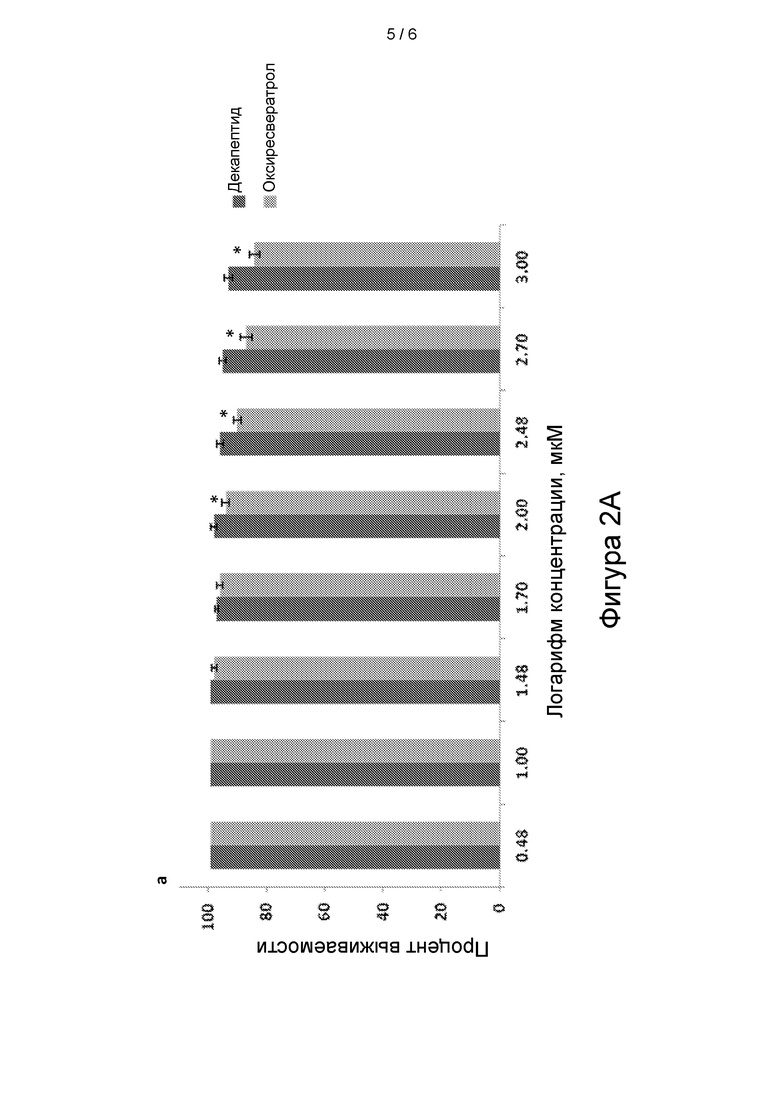
[30] На фигуре 2А показано цитотоксическое действие декапептида-12 и оксиресвератрола на эпидермальные кератиноциты. Данные приведены в виде процентного контроля и представляют собой средние значения ± SEM по 3 независимым экспериментам. *Р<0,05.
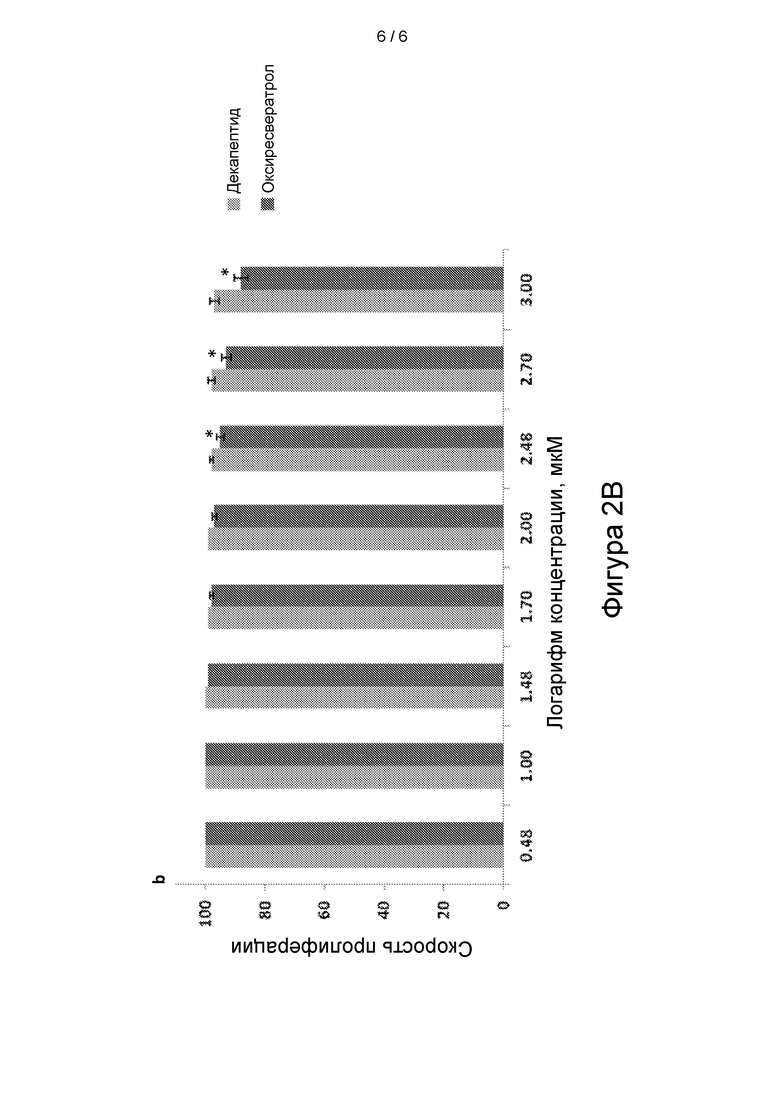
[31] На фигуре 2В показано действие декапептида-12 и оксиресвератрола на пролиферацию эпидермальных кератиноцитов. Данные приведены в виде процентного контроля и представляют собой средние значения ± SEM по 3 независимым экспериментам. *Р<0,05.
Подробное описание изобретения
[32] На коже проявляются последствия хронологического старения и фотостарения, что не дает нам забыть о процессе старения и стимулирует поиск средств замедления или купирования его воздействия. Старение кожи традиционно подразделяется на внешнее или внутреннее. Последние данные указывают на то, что для обоих этих типов характерны общие молекулярные особенности, включая изменение путей передачи сигнала, которые способствуют экспрессии матриксной металлопротеиназы, снижение синтеза проколлагена и повреждение соединительной ткани.
[33] В коже человека старение ассоциировано с увеличением количества стареющих клеток и снижением способности к клеточной пролиферации и дифференцировке. Значимые доказательства подтверждают теорию о том, что старение преимущественно является следствием повреждения свободными радикалами за счет различных эндогенных активных форм кислорода (АФК). Velarde et al. сообщали о полученном in vivo свидетельстве существования причинно-следственной связи между окислительным повреждением митохондрий, клеточным старением и фенотипами старения кожи. Кроме того, ультрафиолетовое (УФ) излучение стимулирует синтез АФК, которые участвуют в мутагенезе и фотостарении. В соответствии с этими данными, имеются указания на измененную экспрессию активности сиртуина при сравнении облучаемой ультрафиолетом и защищенной от солнца коже, и на то, что эти различия могут являться причиной определенных аспектов старения кожи.
[34] Клеточное старение описывает процесс, при котором клетки прекращают делиться и претерпевают характерные фенотипические изменения, в том числе глубокие изменения хроматина и секретома, а также активацию опухолевых супрессоров. Многочисленные сообщения помогли установить понятие о сиртуинах как белках - мощных антивозрастных агентах и подробно описать их плейотропные роли в задержке клеточного старения и преждевременного старения. Сиртуины являются ключевыми факторами в таких путях, как репарация повреждений ДНК, укорочение теломер, клеточный ответ на окислительный стресс и облегчение патологических нарушений, вызванных АФК.
[35] У млекопитающих есть семь генов сиртуинов (SIRT1-7), локализованных в разных клеточных компартментах иобладающих различной активностью. Биохимически сиртуины представляют собой класс белков, которые обладают в основном NAD+-зависимой лизиндеацетилазной активностью. Общепризнанно, что сиртуины являются важными регуляторами множественных метаболических путей, сенсоров энергии и окислительно-восстановительного статуса в клетках и модуляторов окислительного стресса.
[36] Эти результаты вызвали интерес к разработке низкомолекулярных активаторов или фармацевтических препаратов, помогающие замедлять прогрессирование старения и широкий спектр возрастных нарушений. Из семи сиртуинов млекопитающих SIRT1 наиболее изучен с точки зрения старения и долголетия. Например, антивозрастные эффекты ресвератрола в первую очередь связаны с активацией SIRT1. Действительно, Ido et al. сообщили, что ресвератрол за счет повышения активности АМФ-активированной протеинкиназы и сиртуинов улучшает клеточное старение и пролиферативную дисфункцию.
[37] Ранее мы сообщали о высокой эффективности декапептида-12 в гипопигментации кожи человека. Дальнейшие клинические исследования выявили общее улучшение внешнего вида кожи лица у пациентов с дисхромией, дважды в день получавших лечение кремом для наружного применения, содержащим 0,01 процента декапептида-12, в течение 8 недель. Эти результаты привели нас к гипотезе о том, что декапептид-12 может модулировать активность сиртуина для общего улучшения внешнего вида кожи. Для уточнения этой возможности мы выполнили оценку влияния декапептида-12 на транскрипцию сиртуина в эпидермальных предшественниках человека.
[38] Материалы и методы
[39] Реагенты
[40] Декапептид-12 (YRSRKYSSWY) SEQ ID NO: 9 синтезировали в Bio Basic, Inc. (Онтарио, Канада) с использованием твердофазных химических реакций FMOC. Оксиресвератрол приобрели в Sigma-Aldrich (Сент-Луис, штат Миссури, США).
[41] Культура клеток
[42] Неонатальные эпидермальные предшественники человека (Thermo Fisher Scientific, Нью-Йорк, США) сеяли на 6-луночные планшеты при плотности 2×105 клеток на лунку. В каждую лунку вносили 2 мл среды Epilife, содержащей 60 мкМ хлорида кальция (Thermo Fisher Scientific, Нью-Йорк, США). Планшеты инкубировали в камере с увлажнением при 37 градусах Цельсия и 5 процентах СО2. Через двадцать четыре часа клетки обрабатывали различными концентрациями оксиресвератрола или декапептида-12, растворенных в PBS, содержащем 5 процентов ДМСО. В контрольные лунки вносили только среду-носитель (5 процентов ДМСО и PBS). Конечная концентрация ДМСО в каждой лунке составляла 0,05 процента.
[43] Выделение, количественное определение общей РНК и синтез кДНК
[44] Через 72 часа инкубирования клетки трипсинизировали и выделяли общую РНК с использованием набора RNeasy (Qiagen, Валенсия, штат Калифорния, США) в соответствии с протоколом производителя.
[45] Концентрации РНК определяли с использованием спектрофотометра nanodrop (Thermo fisher scientific, Нью-Йорк, США). Два мкг общей РНК использовали для синтеза кДНК с использованием олиго-dT праймеров и реагентов TaqMan для обратной транскрипции (Thermo fisher scientific, Нью-Йорк, США). Реакцию выполняли в термоциклере DNA Engine Peltier Thermal Cycler (Bio-Rad, Херкулиз, штат Калифорния, США). Отжиг выполняли при температуре 25 градусов Цельсия в течение 10 минут, затем выполняли синтез первой цепи при 48 градусах Цельсия в течение 1 часа и термическую инактивацию при 95 градусах Цельсия в течение 5 минут.
[46] Полуколичественный анализ
[47] Праймеры SIRT1-7 (таблица 1) разработали с использованием Primer3. Полуколичественные реакции ПЦР выполняли в термоциклере DNA Engine Peltier Thermo Cycler (Bio-Rad, Херкулиз, штат Калифорния, США). ПЦР выполняли в следующих условиях: денатурация при 94 градусах Цельсия в течение 2 минут и удлинение праймеров при 54 градусах Цельсия в течение 30 секунд, 34 цикла для SIRT 1-7 и гена домашнего хозяйства 18S.
[48] Таблица 1: Последовательности праймеров для SIRT1-7 и 18S
[49]

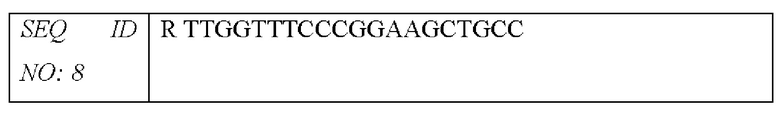
[50] Образцы исследовали и разделяли в 1,5-процентном агарозном геле, содержащем 0,5 мкг/мл бромида этидия, и визуализировали с помощью системы визуализации FluorChem HD2 Imaging System (Protein simple, Сан-Хосе, штат Калифорния, США). Денситометрический анализ выполняли с использованием программного обеспечения AlphaEase FC (Protein simple, Сан-Хосе, штат Калифорния, США). Отношения интенсивности рассчитывали как значение интенсивности для каждого гена, разделенное на значение интенсивности гена внутреннего контроля 18S.
[51] Анализ жизнеспособности/пролиферации и цитотоксичности
[52] Скорость пролиферации определяли с использованием набора для оценки пролиферации клеток TACS® МТТ Cell Proliferation Kit (R&D systems, Миннеаполис, штат Миннесота, США). Клетки сеяли из расчета 2,5×104/лунку в 96-луночные планшеты в увлажненной атмосфере с 5 процентами СО2 при 37 градусах Цельсия. Через двадцать четыре часа в соответствующие лунки добавляли декапептид-12 или оксиресвератрол в различных концентрациях (0, 3, 10, 30, 100, 300 и 1000 мкМ), а затем инкубировали культуры в течение 72 часов. Остальную часть процедуры выполняли в соответствии с протоколом производителя.
[53] Клеточную токсичность измеряли с использованием анализа вытеснения красителя трипановый синий. Клетки культивировали в 6-луночных планшетах при плотности 4×105 клеток/лунку. В каждую лунку вносили различные концентрации декапептида-12 или оксиресвератрола (0, 3, 10, 30, 100, 300 и 1000 мкМ). Планшеты инкубировали при 37 градусах Цельсия в увлажненной камере в атмосфере с 5 процентами СО2. Через 72 ч отбирали аликвоту и подсчитывали клетки с использованием гемоцитометра. Цитотоксичность измеряли в соответствии со следующей формулой: [1 - (кол-во клеток в контроле - кол-во живых клеток в тестируемом образце)/кол-во клеток в контроле] × 100 процентов.
[54] Статистический анализ
[55] Средние значения и их стандартные ошибки рассчитывали по 3 независимым анализам с использованием Microsoft Excel, статистическую значимость определяли с использованием парного дисперсионного анализа. Значения Р считали статистически значимыми при Р<0,05.
[56] Результаты
[57] Влияние декапептида на скорость пролиферации и цитотоксичность:
[58] Вначале мы оценивали цитотоксическое действие декапептида-12 и оксиресвератрола на эпидермальные клетки-предшественники человека. На фигуре 2А показано, что обработка с использованием 100 мкМ декапептида-12 или оксиресвератрола приводила к гибели 3±1 процента или 6±1 процентов клеток, соответственно. В концентрации 1 мкМ декапептид-12 или оксиресвератрол приводили к гибели 7±2 процентов или 16±2 процентов клеток, соответственно.
[59] Кроме того, мы оценивали действие декапептида-12 и оксиресвератрола на жизнеспособность и пролиферацию эпидермальных предшественников человека. На фигуре 2 В показано, что обработка с использованием 300 мкМ декапептида-12 или оксиресвератрола приводила к снижению пролиферации клеток на 2±1 процента или 5±1 процентов, соответственно. В то же время, в отличие от 1 мМ декапептида-12, который приводил к снижению пролиферации на 3±2 процента, 3-дневное инкубирование с оксиресвератролом снижало пролиферацию на 12±2 процентов.
[60] Транскрипция SIRT1-7, стимулированная декапептидом-12:
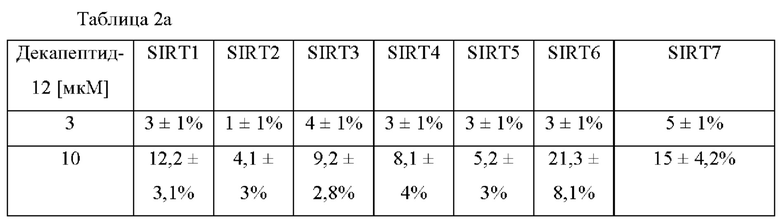
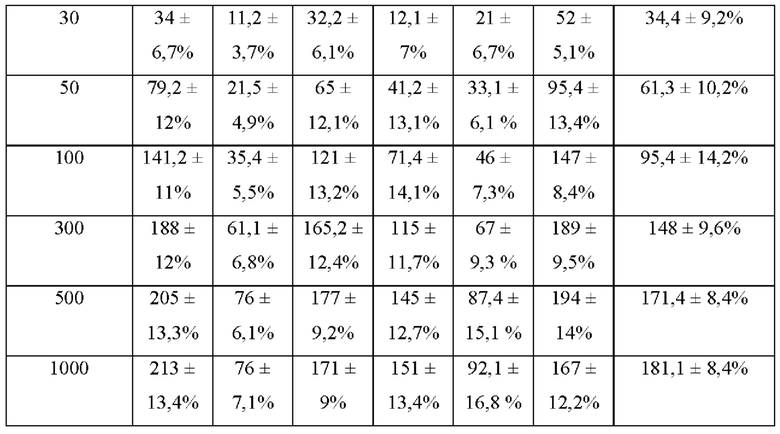
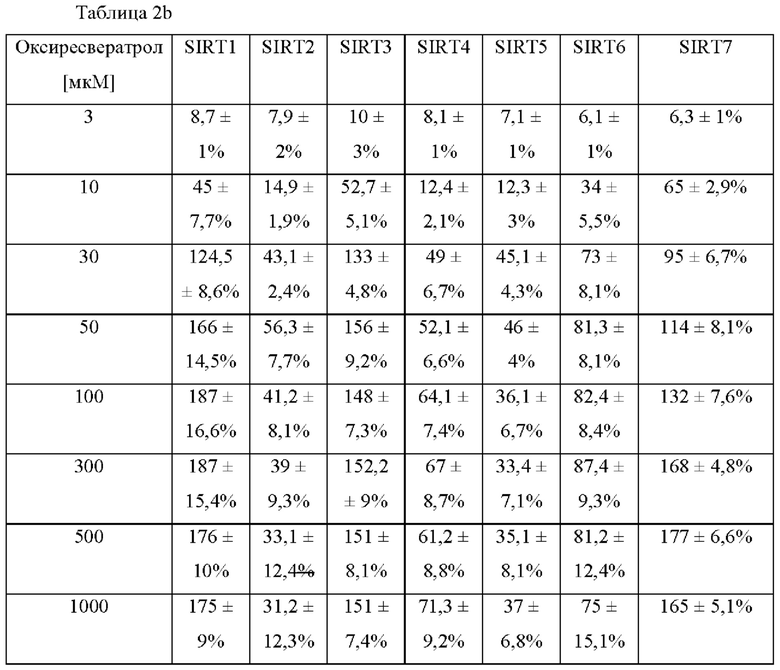
[61] Затем мы оценивали действие оксиресвератрола и декапептида-12 на экспрессию сиртуина в эпидермальных предшественниках человека. На фигурах 1А-1D и в таблице 2 показана транскрипция SIRT1-7, модулированная декапептидом-12 и оксиресвератролом в зависимости от дозы. При концентрации оксиресвератрола 30 мкМ уровень транскрипции SIRT1 повышался на 125±9 процентов по сравнению с контрольными клетками, в то время как уровни SIRT3, SIRT6 и SIRT7 повышались на 133±5 процентов, 73±8 процентов и 95±7 процентов, соответственно.
[62] Таблица 2. Профиль экспрессии генов SIRT 1-7 в ответ на обработку декапептидом-12 (а) и оксиресвератролом (b). Результаты представляют собой среднее значение по 3 независимым анализам.
[63]
[64]
[65] Данные демонстрируют, что 100 мкМ декапептид-12 усиливал транскрипцию SIRT1 на 141±11 процентов по сравнению с необработанными клетками, в то время транскрипция SIRT3, SIRT6 и SIRT7 повышалась на 121±13 процентов, 147±8 процентов и 95±14 процентов, соответственно (Фигуры 1А-1D).
[66] Обсуждение
[67] Плейотропные роли, которые сиртуины играют в задержке клеточного старения и блокаде развития преждевременного старения, помогли обосновать, что они являются мощными антивозрастными белками. Подробно изучено и документировано терапевтическое применение ресвератрола как активатора SIRT1 и потенциального антивозрастного агента. Ресвератрол защищает эндотелий человека от Н2О2-индуцированного окислительного стресса и старения за счет активации SIRT1. Аналогичным образом, оксиресвератрол также является мощным антиоксидантом и акцептором свободных радикалов. Однако в отличие от ресвератрола он обладает меньшей цитотоксичностью и лучшей растворимостью в воде. Поэтому мы решили использовать его в качестве положительного контроля, с которым сравнивали эффективность и способность декапептида-12 модулировать транскрипцию сиртуина в эпидермальных кератиноцитах человека.
[68] Несмотря на стимуляцию экспрессии всех 7 сиртуинов после обработки декапептидом-12, обсуждение будет сосредоточено на тех сиртуинах, которые непосредственно связаны со старением кожи.
[69] В концентрации 100 мкМ или 1 мМ декапептид-12 значительно усиливал транскрипцию SIRT1 - на 141 или 213 процентов, соответственно. SIRT1 прежде всего представляет собой ядерную деацетилазу. Он контролирует различные клеточные процессы, например, пролиферацию, дифференцировку, апоптоз, метаболизм, реакцию на стресс, стабильность генома и выживаемость клеток. Cao et al. сообщили, что SIRT1 обеспечивает защиту от гибели клеток, индуцированной UVB- и Н2О2, путем модуляции N-концевых киназ р53 и c-Jun в культивируемых кератиноцитах кожи, что указывает на возможность использования активаторов SIRT1 в качестве новых агентов против старения кожи. Другие исследователи сообщили, что SIRT1 может подавлять сигнальный путь NF-κВ и, таким образом, задерживать процесс старения и увеличивать продолжительность жизни. Активация SIRT1 ингибирует сигнальный путь NF-κВ непосредственно путем деацетилирования субъединицы р65 комплекса NF-κВ, усиливает окислительный метаболизм и способствует устранению воспаления. Следовательно, SIRT1 можно рассматривать как важнейший антивозрастной белок, опосредующий широкий спектр эффектов, направленных на предотвращении преждевременного старения и ускоренного старения за счет регуляции множества молекулярных путей.
[70] Транскрипция SIRT3 усиливалась на 121 процент после обработки 100 мкМ декапептида. SIRT3 главным образом связан с регуляцией различных митохондриальных процессов, например, β-окисления, образования АТФ и обезвреживание АФК. SIRT3 также участвует в поддержании регенеративной способности гемопоэтических стволовых клеток. SIRT3 подвергается супрессии при старении, а стимуляция экспрессии SIRT3 в старых гематопоэтических стволовых клетках улучшает их способность к регенерации. Это открытие устанавливает важную роль SIRT3 в поддержании стволовости и, что еще важнее, помогает при поиске способов будущих вмешательств на основе стволовых клеток при метаболических нарушениях, приводящих к преждевременному старению.
[71] SIRT6 можно рассматривать как важный антивозрастной белок, играющий разностороннюю роль в репарации повреждений ДНК, метаболической регуляции, воспалении и подавлении опухолей. SIRT6 стал известным, когда у модели мыши с нокаутом этого гена развились тяжелые фенотипы преждевременного старения с летальным исходом в течение месяца. Более того, SIRT6 является единственным сиртуином млекопитающих, при сверхэкспрессии которого во всем организме мыши наблюдается явное увеличение продолжительности жизни. Кроме того, Kawahara et al. сообщили, что SIRT6 ослабляет гиперактивность сигнального пути NF-кВ путем деацетилирования гистона Н3 в K9 на промоторах генов-мишеней NF-кВ, что усиливает роль SIRT6 как важного противовоспалительного белка.
[72] Baohua et al. показали, что SIRT6 играет ключевую роль в процессе старения кожи за счет модуляции метаболизма коллагена и сигнального пути NF-кВ. Они сообщили, что блокада SIRT6 значительно снижала содержание гидроксипролина за счет ингибирования транскрипции коллагена 1 типа, стимулирования секреции металлопротеиназы матрикса 1 и усиления сигнального пути NF-кВ. В совокупности эти результаты позволяют рассматривать SIRT6 в качестве ключевого модулятора антивозрастных процессов, регулирующего множество путей и вызывающего задержку клеточного старения и ускоренного старения. Следовательно, декапептид-12, усиливающий транскрипцию SIRT6 на 147 процентов в концентрации 100 мкМ, может являться перспективным антивозрастным кандидатом для устранения часто сопутствующих друг другу фенотипов преждевременного старения кожи и фотоповреждений кожи.
[73] Таким образом, в настоящем отчете показано, что декапептид-12 значительно повышает уровни транскрипции SIRT1, SIRT3 и SIRT6, которые играют важную роль в противодействии старению кожи и другим возрастным патологиям. В настоящее время разрабатываются клинические исследования различных наружных составов, содержащих декапептид-12, которые должны помочь подтвердить указанные результаты, полученные in vitro, и проверить эффективность этого мощного активатора сиртуина in vivo.
[74] ПРИМЕР
[75] В данном примере в декапептид Р4 внесены некоторые модификации, подробно описанные в следующей таблице 3.
[76]
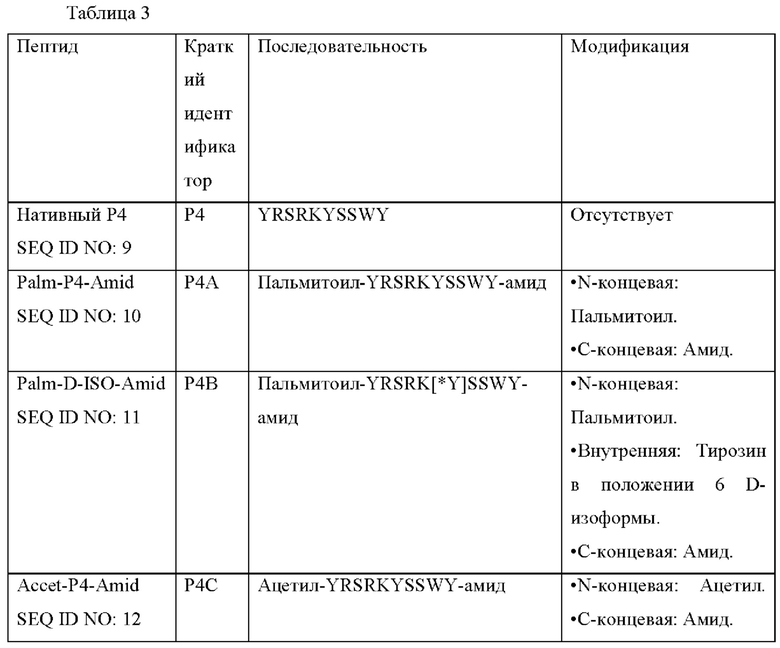
[77] Эти модификации декапептида Р4 можно использовать для улучшения стабильности против протеаз и для усиления чрескожного или чресклеточного проникновения, или их обоих.
[78] Пептиды согласно настоящему изобретению могут содержать остатки любых природных аминокислот или аминокислот, не встречающихся в природе. Эти встречающиеся и не встречающиеся в природе аминокислоты могут находиться в D- или L-конфигурации или могут включать обе правовращающие формы. Термины D- и L- используются в настоящей заявке, поскольку они известны в данной области техники. Пептиды согласно настоящему изобретению включают отдельные аминокислоты и короткие аминокислотные последовательности (например, из 1-20 аминокислот). Кроме того, модифицированные пептиды согласно настоящему изобретению также могут содержать мономер или димер.
[79] Стандартные однобуквенные и трехбуквенные коды для обозначения аминокислот используются в настоящей заявке и приведены ниже в таблице А.
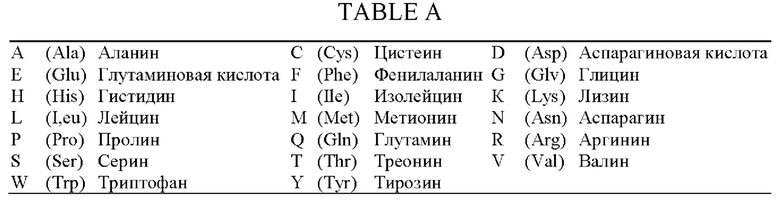
[80] Как описано выше, указанные остатки могут представлять собой встречающиеся в природе L-аминокислоты или их модификации, т.е. химическую модификацию, оптический изомер или связь с модифицирующей группой. Предполагается, что в пептид можно внести специфические модификации, поддерживающие способность пептидов согласно настоящему изобретению специфически модулировать экспрессию гена(ов) сиртуина.
[81] Выполнена оценка влияния декапептидов Р4, Р4А, Р4В и Р4С на уровень транскрипции сиртуинов 1-7. В таблице 4 приведена сводная информация об уровнях транскрипции соответствующих генов при воздействии всех четырех декапептидов в протестированных концентрациях, равных: 10, 30, 50, 100 и 300 (все концентрации приведены в мкМ).
[82]
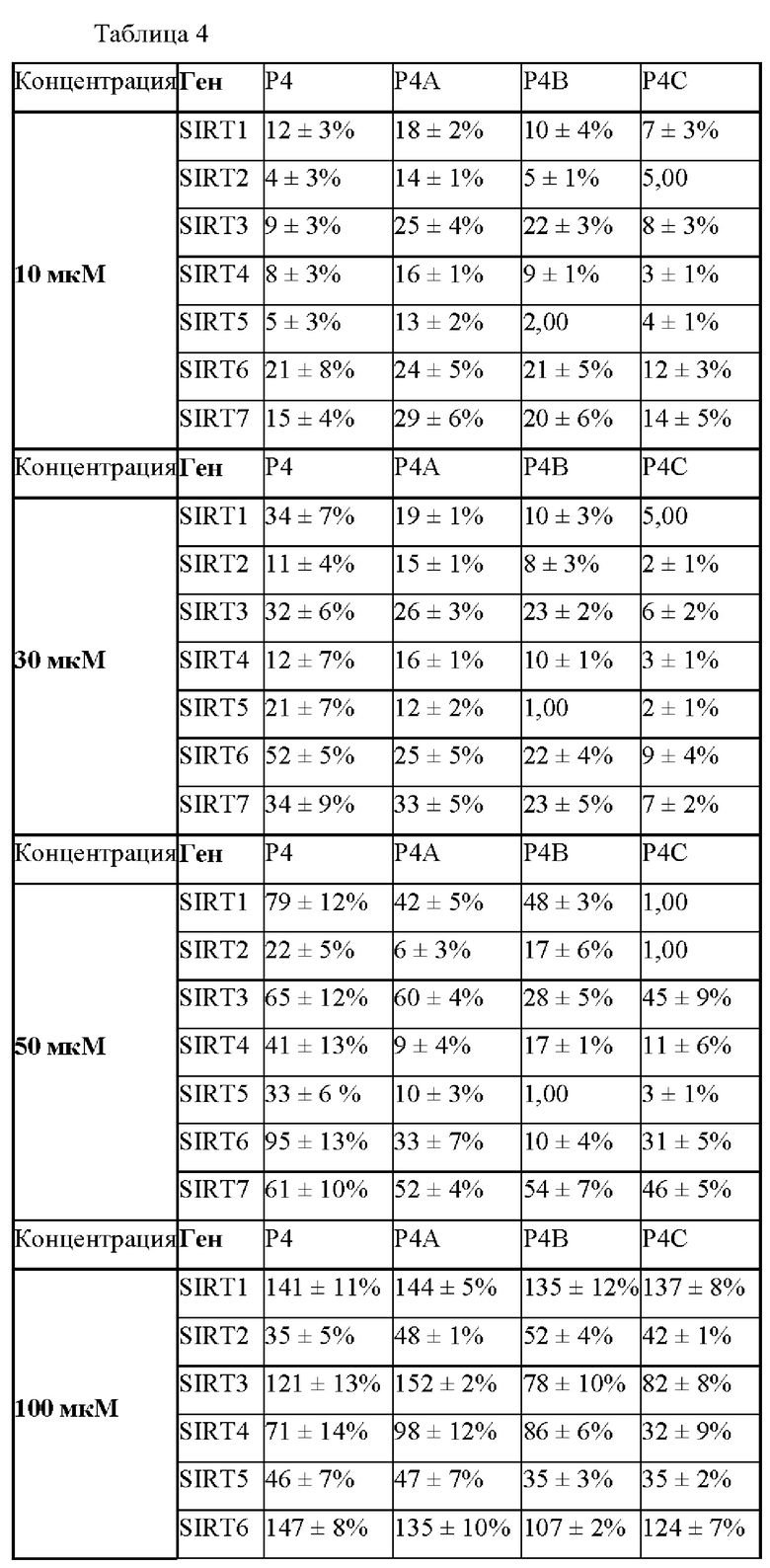
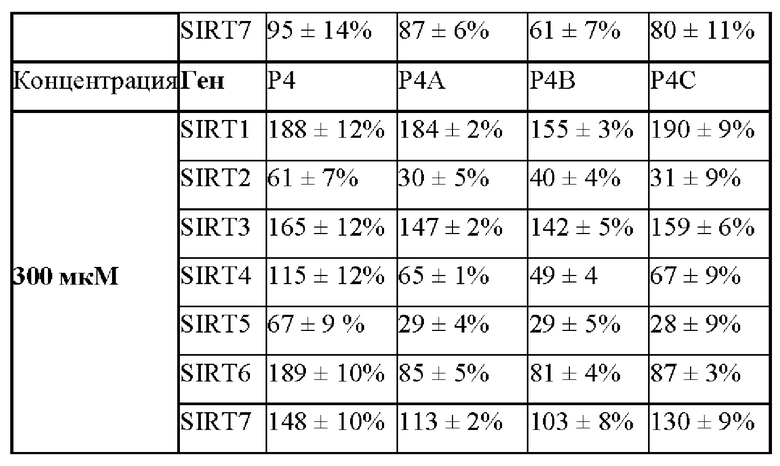
[83] В низких концентрациях нативный декапептид Р4 обеспечивал повышенный уровень транскрипции по сравнению с модифицированными декапептидами. В то же время каждый из трех модифицированных декапептидов (Р4А, Р4В и Р4С) стимулировал транскрипцию генов сиртуина по сравнению с контролем. В концентрации 100 мкМ влияние всех четырех декапептидов на уровень транскрипции было сопоставимым.
[84] Скорость пролиферации трех линий клеток человека (эпидермальных предшественников, меланобластов и фибробластов) определяли с использованием набора для оценки пролиферации TACS® МТТ Cell Proliferation Kit. Клетки сеяли из расчета 2,5×104/лунку в 96-луночные планшеты в увлажненной атмосфере с 5 процентами CO2 при 37 градусах Цельсия. Через двадцать четыре часа в соответствующие лунки добавляли декапептиды в различных концентрациях и инкубировали в течение 72 часов. Остальную часть процедуры выполняли в соответствии с протоколом производителя.
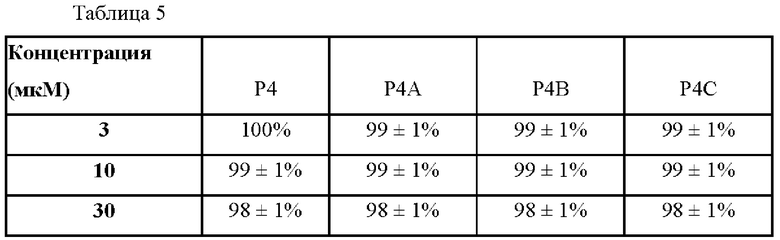
[85] В таблице 5 показана скорость пролиферации эпидермальных предшественников через 72 часа.
[86]
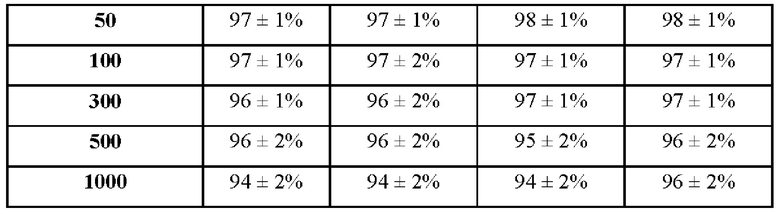
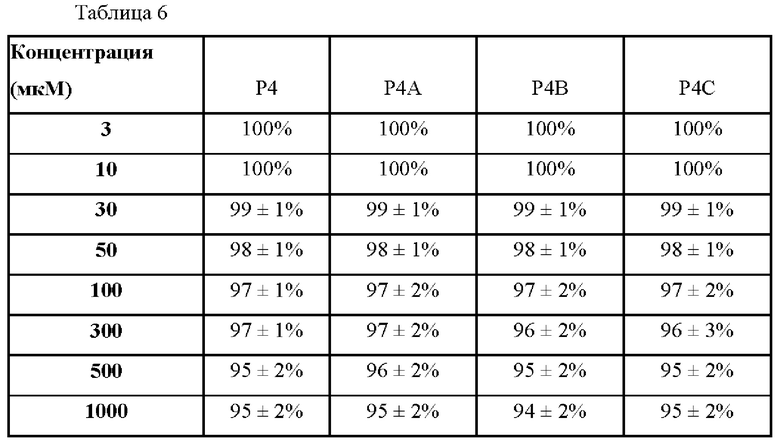
[87] В таблице 6 показана скорость пролиферации меланобластов через 72 часа.
[88]
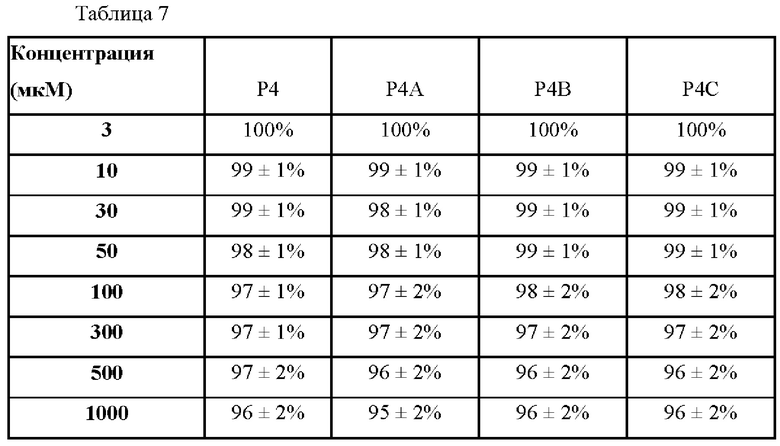
[89] В таблице 7 показана скорость пролиферации фибробластов через 72 часа.
[90]
[91] В результате 72-часового инкубирования эпидермальных предшественников, меланобластов и фибробластов с 100 мкМ декапептида Р4А скорость пролиферации всех трех клеточных линий снизилась на 3 процента.
[92] При концентрации 1000 мкМ скорость пролиферации эпидермальных предшественников снизилась на 6 процентов, тогда как скорость пролиферации меланобластов и фибробластов снизилась на 5 процентов и 4 процента, соответственно.
[93] Кроме того, протестировали влияние каждого из декапептидов на жизнеспособность клеток. В частности, клетки инкубировали с декапептидом в различных концентрациях и затем подсчитывали жизнеспособность по сравнению с контролем (необработанные клетки) с использованием трипанового синего. Цитотоксичность измеряли в соответствии со следующей формулой: [1 - (кол-во клеток в контроле - кол-во живых клеток в тестируемом образце)/кол-во клеток в контроле] × 100 процентов.
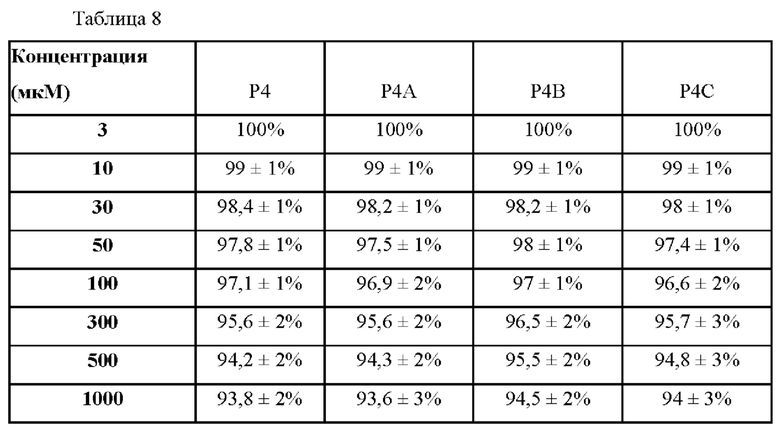
[94] В таблице 8 показана жизнеспособность эпидермальных предшественников через 7 дней.
[95]
[96] В таблице 9 показана жизнеспособность меланобластов через 7 дней.
[97]
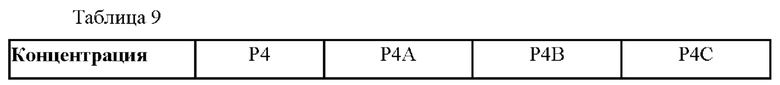
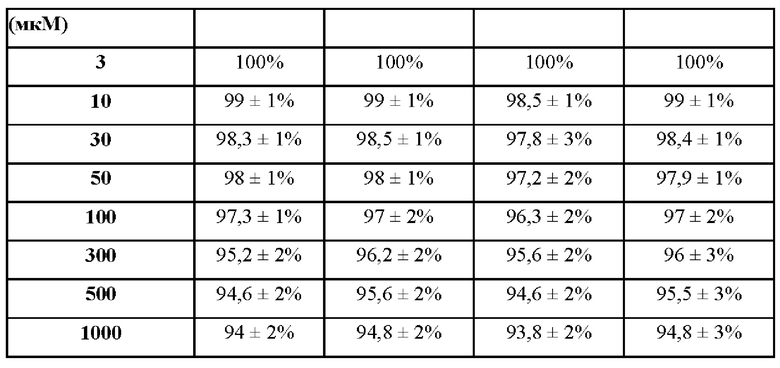
[98] В таблице 10 показана жизнеспособность фибробластов через 7 дней.
[99]
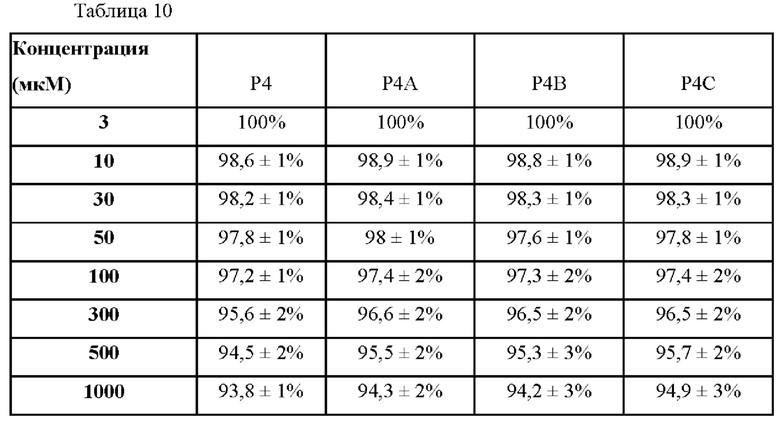
[100] При концентрации 100 мкМ жизнеспособность клеток всех трех линий клеток по-прежнему превышала 97 процентов. При концентрации 1000 мкМ жизнеспособность клеток падала на 6 процентов по сравнению с контролем.
[101] В заключение следует отметить, что в сообщениях подробно описаны плейотропные роли сиртуинов в подавлении преждевременного старения, замедлении клеточного старения, увеличении продолжительности жизни и облегчении состояния при широком спектре нарушения (расстройства) старения. В настоящем документе мы сообщаем о полученных нами данных о мощном активаторе сиртуина, декапептиде-12, и сравниваем его эффективность с хорошо описанным оксиресвератролом. Обработка эпидермальных предшественников 100 мкМ декапептида-12 усиливала транскрипцию SIRT1 на 141±11 процентов по сравнению с контрольными клетками, в то время как уровни SIRT3, SIRT6 и SIRT7 повышались на 121±13 процентов, 147±8 процентов и 95,4±14 процентов, соответственно. Декапептид-12 активировал транскрипцию сиртуина до уровня, аналогичного оксиресвератролу, но при пониженной цитотоксичности. Таким образом, декапептид-12 может оказаться перспективным и более безопасным терапевтическим средством против старения кожи и других возрастных патологий.
[102] Хотя в приведенном выше описании упоминается типичная концентрация декапептида 100 мкМ или более, как дающая очевидный эффект, результаты также демонстрируют, что более низкие концентрации также оказывали положительное влияние. Таким образом, в некоторых вариантах реализации можно использовать концентрацию декапептида 1 мкМ или более, причем в конкретных вариантах реализации используется диапазон концентраций пептида 100 мкМ или более. Примерами диапазонов концентраций пептидов в соответствии с различными вариантами реализации являются 1 мкМ или более, 5 мкМ или более, 10 мкМ или более, 30 мкМ или более, 50 мкМ или более, 100 мкМ или более, 300 мкМ или более, 500 мкМ или более и 1000 мкМ или более.
[103] Кроме того, следует отметить, что для достижения желательного эффекта конкретный декапептид можно применять в комбинации с другим(и) компонентом(ами). Например, конкретный декапептид можно применять в комбинации с другими пептидами, например, декапептидами Р4А, 4В и/или 4С, и/или с другими компонентами, например, оксиресвератролом. В соответствии с такими вариантами реализации синергетический эффект, реализуемый путем включения других компонентов, может в конечном итоге снизить концентрацию любого отдельного компонента (например, декапептида и др.), необходимую для достижения желательного результата.
[104] Хотя вышеуказанное конкретно относится к применению декапептидов и оксиресвератрола в качестве возможных дополнительных компонентов, варианты реализации не ограничиваются этим. Примеры других возможных добавок могут включать, в числе прочего, α-липоевую кислоту, биотин, кофеин, церамиды, кофермент Q10, гликолевую кислоту, зеленый чай, стволовые клетки человека, экстракты стволовых клеток человека, гиалуроновую кислоту, гидрохинон, масло хохобы, койевую кислоту, молочную кислоту, яблочную кислоту, ниацинамид, олигопептиды, пептиды, стволовые клетки растений, экстракты стволовых клеток растений, ресвератрол, ретинол, витамин С, витамин Е и витамин K, но не ограничиваются ими.
[105] Следует отметить, что варианты реализации можно применять для обработки различных типов клеток кожи. Примеры окончательно дифференцированных клеток кожи могут включать кератиноциты, фиброциты, меланоциты и клетки иммунной системы, например, клетки Лангерганса (например, гистиоциты или дендроциты), которые также стареют со временем, но не ограничиваются ими.
[106] Варианты реализации также можно применять для обработки клеток-предшественников кожи, с целью замедления старения кожи и обеспечения ее обновления в течение всей жизни. Примеры таких клеток-предшественников могут включать эпидермальные предшественники кератиноцитов, фибробласты, меланобласты, гистиобласты или дендробласты, которые являются предшественниками клеток Лангерганса, оседающих в эпидермисе, но не ограничиваются ими.
[107] Наконец, хотя вышеописанное описывает обработку клеток кожи человека, конкретные варианты реализации не ограничиваются такими подходами. В альтернативных вариантах реализации можно применять обработку клеток кожи других организмов, включая млекопитающих, например, коров (например, при производстве кожи), свиней и других животных (например, собак, кошек и других, конкурсная оценка которых зависит от внешнего вида их кожи), но не ограничиваясь этим.
[108] Настоящее описание изобретения представлено в иллюстрационных и описательных целях. Не следует подразумевать, что оно является исчерпывающим или ограничивает настоящее изобретение точной описанной формой, и в свете вышеизложенного можно внести большое количество модификаций и изменений. Указанные варианты реализации были выбраны и описаны с целью наилучшего разъяснения принципов настоящего изобретения и его практического применения. Это описание позволит другим специалистам в данной области техники наилучшим образом использовать и применять настоящее изобретение в различных вариантах реализации и с различными модификациями, которые подходят для конкретного применения. Рамки изобретения определяются следующей формулой изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Escape Therapeutics, Inc.
<120> Модуляция гена сиртуина с помощью декапептида-12 в эпидермальных
кератиноцитах
<130> ELIXP004US
<150> US 62/479 248
<151> 30.03.2017
<160> 12
<170> Версия PatentIn 3.5
<210> 1
<211> 24
<212> ДНК
<213> Homo sapiens
<400> 1
gccaatcata agatgttgct gaac 24
<210> 2
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 2
aacctccctc atctctaact 20
<210> 3
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 3
gttggttaca agatccagac 20
<210> 4
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 4
agagctgtga gagaatgaag 20
<210> 5
<211> 23
<212> ДНК
<213> Homo sapiens
<400> 5
tcttccatac actttactac ctt 23
<210> 6
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 6
cagcttaaac aggagtgaac 20
<210> 7
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 7
gacattttta gccatttgtc 20
<210> 8
<211> 24
<212> ДНК
<213> Homo sapiens
<400> 8
cggaggttcg aagacgatca gata 24
<210> 9
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<400> 9
Tyr Arg Ser Arg Lys Tyr Ser Ser Trp Tyr
1 5 10
<210> 10
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (1)..(10)
<223> N-концевой: Пальмитоил C-концевой: Амид
<400> 10
Tyr Arg Ser Arg Lys Tyr Ser Ser Trp Tyr
1 5 10
<210> 11
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (1)..(10)
<223> N-концевой:Пальмитоил Тирозин в положении 6 представляет собой
D-изоформу C-концевой:Амид
<400> 11
Tyr Arg Ser Arg Lys Tyr Ser Ser Trp Tyr
1 5 10
<210> 12
<211> 10
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> ВАРИАНТ
<222> (1)..(10)
<223> N-концевой:ацетил C-концевой:амид
<400> 12
Tyr Arg Ser Arg Lys Tyr Ser Ser Trp Tyr
1 5 10
<---
Изобретение относится к активатору сиртуина - декапептиду-12, который модулирует экспрессию гена сиртуина в клетке кожи. Обработка клеток-предшественников эпидермальных кератиноцитов 100 мкМ декапептидом-12 усиливала транскрипцию SIRT1 на 141±11% по сравнению с контрольными клетками, в то время как уровни SIRT3, SIRT6 и SIRT7 повышались на 121±13%, 147±8% и 95,4±14%, соответственно. Декапептид-12 активировал транскрипцию сиртуина до уровня, аналогичного оксиресвератролу, но при пониженной цитотоксичности. 4 н. и 16 з.п. ф-лы, 6 ил., 10 табл.
1. Применение пептида, состоящего из SEQ ID NO: 9 или модифицированной SEQ ID NO: 9, где указанная модификация включает пальмитоильную группу или ацетильную группу на N-конце, и/или амидирование С-конца, и/или D-тирозин в положении 6, для модулирования экспрессии гена сиртуина в клетке кожи.
2. Применение по п. 1, характеризующееся тем, что указанный пептид состоит из SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11 или SEQ. ID NO: 12.
3. Применение по любому из пп. 1, 2, в котором пептид состоит из SEQ ID NO: 11, содержащей аминокислоту тирозин в положении 6 в виде D-изоформы, а все остальные аминокислоты представляют собой L-изоформы.
4. Применение композиции, содержащей пептид, состоящий из SEQ ID NO: 9 или модифицированной SEQ ID NO: 9, где указанная модификация включает пальмитоильную группу или ацетильную группу на N-конце, и/или амидирование С-конца, и/или D-тирозин в положении 6, для модулирования экспрессии гена сиртуина в клетке кожи.
5. Применение по п. 4, характеризующееся тем, что указанный пептид состоит из SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11 или SEQ. ID NO: 12.
6. Применение по любому из пп. 4, 5, характеризующееся тем, что композиция состоит из SEQ ID NO: 11, содержащей аминокислоту тирозин в положении 6 в виде D-изоформы, а все остальные аминокислоты представляют собой L-изоформы.
7. Применение по любому из пп. 4-6, характеризующееся тем, что указанный пептид присутствует в композиции в концентрации 1 мкМ или более.
8. Способ лечения субъекта посредством модулирования экспрессии гена сиртуина в клетке кожи с целью уменьшения симптомов старения кожи, причем указанный способ включает введение субъекту, нуждающемуся в этом, композиции, содержащей эффективное количество одного или более пептидов, причем указанные один или более пептидов состоят из SEQ ID NO: 9 или модифицированной SEQ ID NO: 9, где указанная модификация включает пальмитоильную группу или ацетильную группу на N-конце, и/или амидирование С-конца, и/или D-тирозин в положении 6.
9. Способ по п. 8, характеризующийся тем, что указанный пептид состоит из SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11 или SEQ. ID NO: 12.
10. Способ по любому из пп. 8, 9, характеризующийся тем, что указанный пептид состоит из SEQ ID NO: 11, содержащей аминокислоту тирозин в положении 6 в виде D-изоформы, а все остальные аминокислоты представляют собой L-изоформы.
11. Способ по любому из пп. 8-10, характеризующийся тем, что указанная клетка является предшественником.
12. Способ по п. 11, характеризующийся тем, что предшественник представляет собой предшественник эпидермального кератиноцита, меланобласт, фибробласт, гистиобласт или дендробласт.
13. Способ по любому из пп. 8-10, характеризующийся тем, что клетка кожи является окончательно дифференцированной.
14. Способ по п. 13, характеризующийся тем, что клетка кожи представляет собой кератиноцит, меланоцит, фиброцит, гистиоцит или дендроцит.
15. Способ по любому из пп. 8-14, характеризующийся тем, что указанный пептид присутствует в концентрации 1 мкМ или более.
16. Способ по любому из пп. 8-15, характеризующийся тем, что ген сиртуина состоит из SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6 или SEQ ID NO: 7.
17. Способ по любому из пп. 8-16, характеризующийся тем, что композиция дополнительно содержит оксиресвератрол.
18. Способ по любому из пп. 8-17, характеризующийся тем, что клетка кожи является клеткой млекопитающего.
19. Способ по п. 18, характеризующийся тем, что клетка кожи является клеткой человека.
20. Способ модуляции экспрессии гена сиртуина в клетке кожи, причем указанный способ включает введение субъекту, нуждающемуся в этом, эффективного количества одного или более пептидов, причем указанные один или более пептидов состоят из SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 11 или SEQ. ID NO: 12.
| WO 2009003034 A1, 31.12.2008 | |||
| WO 2007032029 A1, 22.03.2007 | |||
| WO 2014140890 A2, 18.09.2014 | |||
| ПРОТИВОВОЗРАСТНЫЕ И РАНОЗАЖИВЛЯЮЩИЕ СОСТАВЫ | 2002 |
|
RU2318873C2 |
| Прибор для сигнализации о достижении наперед заданной температуры | 1930 |
|
SU18182A1 |
Авторы
Даты
2022-10-07—Публикация
2018-03-30—Подача