Изобретение относится к области медицины, а именно, к репродуктологии и может быть использовано для прогнозирования наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на контролируемую овариальную стимуляцию (КОС).
В настоящее время вспомогательная репродуктивная технология (ВРТ) занимает важное место в современной медицине, а число супружеских пар, проходящих на лечение бесплодия методом ЭКО, постоянно увеличивает.В то же время, встречаемость пациенток со сниженным (слабым и субоптимальным) ответом яичников на КОС гонадотропинами в протоколах ЭКО достаточно высокая. Известно, что низкая эффективность проведенных протоколов ЭКО со слабым ответом на КОС связана именно с получением малого числа ооцитов (≤3). С целью преодоления этой проблемы усилия многих исследователей были направлены на установление критериев прогнозирования развития слабого ответа [Ferraretti АР, La Marca A, Fauser ВС, et al. ESHRE consensus on the definition of 'poor response' to ovarian stimulation for in vitro fertilization: the Bologna criteria. Hum Reprod. 2011; 26(7):1616-1624. doi:10.1093/humrep/der092], а также разработку протоколов проведения стимуляции овуляции в циклах ВРТ, ориентированных на данную клиническую группу, включающие дозы применяемых препаратов, продолжительность стимуляции и рекомендации по возможному использованию различных лекарственных средств в качестве адъювантной терапии, а также методы определения эффективности программ ЭКО у пациенток, имеющих факторы риска развития слабого ответа. В отличии от когорты пациенток со слабым ответом, женщинам с субоптимальным ответом (4-9 ооцитов, полученных в результате стимуляции овуляции) посвящено существенно меньшее число работ, направленных на определение факторов риска, основных характеристик и методов повышения эффективности протоколов ВРТ. В то же время, частота субоптимального ответа на стимуляцию суперовуляции среди пациенток, проходящих лечение бесплодия методом ЭКО, более чем значима и составляет 43,3% согласно данным Human Fertilization and Embryology Authority (Великобритания). В большинстве ранее проведенных исследований было установлено, что частота имплантации, наступления клинической беременности и рождения живых новорожденных в результате ЭКО у пациентов с субоптимальным ответом на КОС значительно ниже, чем у женщин, имеющих нормальный ответ на стимуляцию овуляции (10-15 полученных ооцитов) [Туан Н.К., Джемлиханова Л.Х., Махмадалиева М.Р., Коган И.Ю., Ниаури Д.А., Крихели И.О., Объедкова К.В., Сафарян Г.Х., Мекина И.Д., Лесик Е.А., Ищук М.А., Гзгзян A.M. Основные характеристики протоколов ЭКО/ИКСИ у пациенток с субоптимальным ответом на контролируемую овариальную стимуляцию // Журнал акушерства и женских болезней. - 2021. - Т. 70. - №1. - С. 109-118. doi: 10.17816/JOWD55264; Sunkara SK, Rittenberg V, Raine-Fenning N, Bhattacharya S, Zamora J, Coomarasamy A. Association between the number of eggs and live birth in IVF treatment: an analysis of 400 135 treatment cycles. Hum Reprod. 2011; 26(7): 1768-1774. doi:10.1093/humrep/der106; Panagiotis Drakopoulos, Christophe Blockeel, Dominic Stoop, Michel Camus, Michel de Vos, Herman Tournaye, Nikolaos P. Polyzos, Conventional ovarian stimulation and single embryo transfer for IVFACSI. How many oocytes do we need to maximize cumulative live birth rates after utilization of all fresh and frozen embryos? Human Reproduction, Volume 31, Issue 2, February 2016, Pages 370-376, https://doi.org/10.1093/humrep/dev316].
В связи с вышеизложенным, проведение научных исследований, направленных на определение критериев диагностики, поиск методов преодоления субоптимального ответа на КОС, а также разработку способа прогнозирования эффективности программ ВРТ у женщин, имеющих факторы риска развития субоптимальной ответной реакции на стимуляцию яичников, имеет актуальную медико-социальную значимость.
Известен способ прогнозирования наступления беременности в программе ЭКО при селективном переносе эмбрионов путем оценки молекулярно-генетического профиля гамет с помощью ПЦР-РВ (патент RU 2550965 С1, дата публикации: 20.05.2015 г., Бюл. №14), заключающийся в том, что на основании данных ПЦР-амплификации исследуемых и референсных генов, полученных в день трансвагинальной пункции фолликулов методом ПЦР с обратной транскрипцией, об уровне экспрессии мРНК генов факторов роста (AREG, EREG, IGF1, IGFBP-4), ингибитора апоптоза (BIRC5) в клетках фолликулярной жидкости, соотношения уровня экспрессии мРНК протаминов (PRM2:PRM1) в сперме получают значения пороговых циклов (Ср) накопления продуктов реакции, вычисляют значение канонической линейной дискриминантной функции (КЛДФ) по определенной математической формуле.
Недостатками данного метода являются: многоэтапный, дорогостоящий и трудоемкий способ определения; сложная математическая формула не позволяет широко и удобно использовать данный способ в клинической практике.
Известен способ прогнозирования исхода программы ЭКО и ПЭ путем исследования фолликулярной жидкости (патент RU 2273031 С1, дата публикации: 27.03.2006 г., Бюл. №19), отличающийся тем, что в фолликулярной жидкости проводят количественное определение содержания ФНО-α и β-ФРФ, рассчитывают прогностический индекс по определенной математической формуле.
Недостатками данного способа являются: сложная математическая формула, не позволяющая широко использовать данный способ в клинической практике; не учитывает такие важные факторы, влияющие на эффективность программ ВРТ, как морфологические характеристики эмбрионов; отсутствуют данные о точности способа (чувствительность и специфичность).
Известен способ прогнозирования результативности программы экстракорпорального оплодотворения (патент RU 2646822 С1, дата публикации: 07.03.2018 г., Бюл. №7), включающий определение уровня макрофагального-колониестимулирующего фактора в периферической венозной крови иммуноферментным методом до начала стимуляции суперовуляции, в лейкоцитах - полиморфизма гена его рецептора rs386693509, rs3216780 3'UTR.
Недостатками данного способа являются: дорогостоящий способ; сложность в определении полиморфизма в структуре гена рецептора; также не учитывался важный фактор, влияющий на эффективность программ ВРТ-морфологические характеристики эмбрионов.
Наиболее близким к заявленному способу является способ прогнозирования успеха имплантации эмбрионов в программах ЭКО (патент ЕР 2857840 В1, дата публикации: 08.04.2015 г., Бюл. 2015/15) путем определения концентрации гранулоцитарного колониестимулирующего фактора (Г-КСФ) в фолликулярной жидкости, полученной из каждого фолликула во время трансвагинальной пункции.
Недостатками данного способа являются: необходимость определить концентрацию Г-КСФ в фолликулярной жидкости, полученной из каждого фолликула - высокая стоимость и трудоемкость; не учитывает важный фактор, влияющий на эффективность программ ВРТ - морфологические характеристики эмбрионов; отсутствие данных о чувствительности и специфичности способа.
Техническим результатом настоящего изобретения является прогнозирование наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС, повышение эффективности программ ВРТ у данной когорты женщин.
Указанный технический результат достигается в способе прогнозирования наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС, в котором у пациенток, имеющих суму баллов ≥9 по шкале прогнозирования развития субоптимального ответа на КОС: возраст пациентки ≥35 лет - 3 балла, наличие субоптимального ответа в анамнезе - 4,5 балла, уровень ФСГ в сыворотке крови ≥8,71 мМЕ/мл - 1 балл, уровень АМГ в сыворотке крови <2,56 нг/мл - 2 балла, количество антральных фолликулов <10 - 4 балла, определяют концентрацию Г-КСФ в фолликулярной жидкости с оценкой морфологических характеристик эмбрионов, и при уровне Г-КСФ в фолликулярной жидкости ≥410 пг/мл и наличии эмбрионов морфологически хорошего качества, характеризующихся стадией развития бластоцисты ≥3, внутренней клеточной массой типа А и В и трофэктодермой типа А и В, прогнозируют наступление клинической беременности.
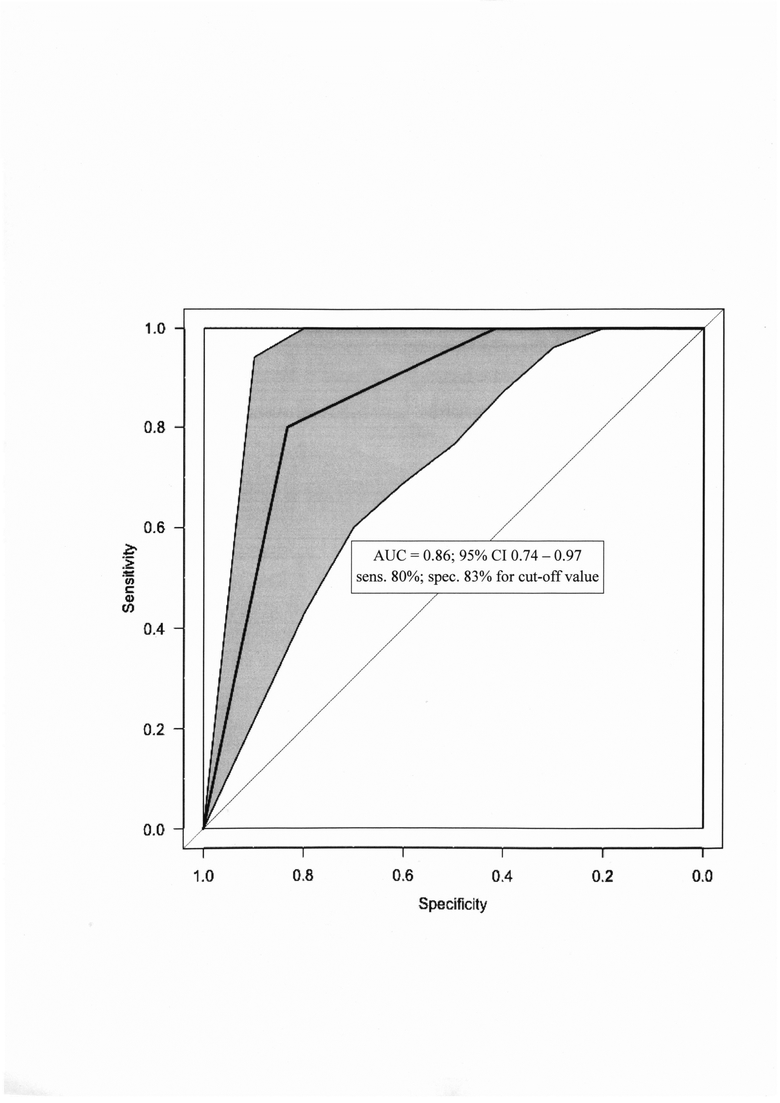
Способ иллюстрируется фиг., на которой представлена ROC-кривая прогнозирования наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС в заявляемом способе.
Способ основан на проспективном исследовании данных 40 пациенток, имеющих сумму баллов ≥9 по шкале прогнозирования развития субоптимального ответа на КОС: возраст пациентки ≥35 лет - 3 балла, наличие субоптимального ответа в анамнезе - 4,5 балла, уровень ФСГ в сыворотке крови ≥8,71 мМЕ/мл - 1 балл, уровень АМГ в сыворотке крови <2,56 нг/мл - 2 балла, количество антральных фолликулов <10-4 балла (патент RU 2774145 С1, дата публикации: 15.06.2022 г., Бюл. №17)
Всем пациенткам с 2-ого или 3-его дня менструального цикла проводили КОС гонадотропинами в стандартных протоколах с антагонистами ГнРГ. При достижении тремя фолликулами диаметра >17 мм вводили триггер; пункция фолликулов проводилась через 36 часов после введения триггера. Оплодотворение полученных ооцитов проводилось методом ЭКО или ICSI. По классификации, предложенной Gardner D.K. оцениваются морфологические характеристики эмбрионов. На пятый день культивирования с помощью катетера Cook производили перенос эмбрионов в полость матки под контролем УЗИ. У женщин с положительным тестом на ХГЧ наступление клинической беременности подтверждалось на основании результата ультразвуковой диагностики через 3-4 недели после переноса эмбрионов по факту наличия плодного яйца в полости матки и сердцебиения плода.
В день трансвагинальной пункции фолликулов проводили сбор образцов для определения уровня Г-КСФ в фолликулярной жидкости. Концентрация Г-КСФ в фолликулярной жидкости определялась иммуноферментным методом.
Проводилась статистическая обработка данных исследования с использованием отношения шансов (ОШ), 95% доверительного интервала (95% ДИ), логистической регрессии в статистическом пакете Stata Software, версия 14 (StataCorp, College Station, TX, США) для MacOS, которая позволила выделить основные факторы, значимо влияющие на частоту клинической беременности у пациенток с прогнозируемым субоптимальным ответом на КОС:
- Концентрация Г-КСФ в фолликулярной жидкости ≥410 пг/мл (ОШ=15,0; 95% ДИ 1,62-139; р=0,02).
- Наличие эмбрионов морфологически хорошего качества (ОШ=15,0; 95% ДИ 1,62-139; р=0,02).
На основании полученных результатов при использовании многофакторного статистического анализа с применением отношения шансов, метода логистической регрессии, Байесовского усреднения моделей, Байесовского информационного критерия, информационного критерия Акаике и ROC-анализа в статистическом пакете RStudio версия 1.3.1093 © 2009-2020 RStudio РВС для MacOS, был создан способ прогнозирования наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС.Указанный способ имеет следующее применение: при концентрации Г-КСФ в фолликулярной жидкости ≥410 пг/мл и наличии эмбрионов морфологически хорошего качества прогнозируют наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС.При проведении ROC-анализа определяются AUC=0,86; 95% ДИ 0,74-0,97; р<0,01; чувствительность - 80% и специфичность - 83% (фиг.).
Известно, что морфологические характеристики эмбрионов являются одним из важнейших факторов, определяющих эффективность программ ВРТ. При переносе эмбрионов с хорошим морфологическим качеством безусловно повышается частота имплантации и вероятность наступления клинической беременности. В то же время, существуют данные ранее проведенных исследований о том, что Г-КСФ участвует в регуляции функции репродуктивной системы, а его концентрация в фолликулярной жидкости имеет достоверную корреляционную взаимосвязь с уровнем ответной реакции яичников на КОС, а также с частотой имплантации и наступления клинической беременности в программах ВРТ [Lédéé N, Gridelet V, Ravet S, et al. Impact of follicular G-CSF quantification on subsequent embryo transfer decisions: a proof of concept study. Hum Reprod. 2013; 28(2):406-413. doi:10.1093/humrep/des354; Noël L, Donneau AF, Jouan C, et al. Absence of correlation between follicular fluid volume and follicular granulocyte colony-stimulating factor, a predictor of embryo implantation and successful delivery. Gynecol Endocrinol. 2020; 36(3):268-272. doi:10.1080/09513590.2019.1650341; Tournaye H, D'Hooghe T, Verheyen G, et al. Clinical performance of a specific granulocyte colony stimulating factor ELISA to determine its concentration in follicular fluid as a predictor of implantation success during in vitro fertilization. Gynecol Endocrinol. 2020; 36(1):44-48. doi:10.1080/09513590.2019.1631283].
Новизна заявленного способа заключается в том, что впервые разработан способ прогнозирования наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС на основе содержания Г-КСФ в фолликулярной жидкости и морфологических характеристик эмбрионов, пригодной к широкому использованию в практической деятельности.
Способ осуществляют, например, следующим образом.
1. При проведении трансвагинальной пункции собирают жидкость из фолликулов путем аспирации. Для определения концентрации Г-КСФ используют образцы с отсутствием крови. На следующем этапе проводят центрифугирование образцов биоматериала при 3000 оборотов в минуту в течение 15 минут. Полученную фолликулярную жидкость собирают в одноразовые стерильные пробирки Эппендорфа (Eppendorf) 1,5 мл. Определяют концентрацию Г-КСФ в фолликулярной жидкости иммуноферментным методом с помощью набора реагентов Invitrogen by Thermo Fisher Scientific G-CSF Human Instant ELISA™ Kit. При необходимости хранения, полученную фолликулярную жидкость содержат при температуре -80°С. Для сохранения биоактивности образцов запрещено проводить цикл замораживания/размораживания.
2. Согласно классификации, предложенной Gardner D.K., на пятый день культивирования проводят оценку морфологических характеристик эмбрионов у пациенток с прогнозируемым субоптимальным ответом на КОС по величине размеров полости бластоцисты и хетчинг-статусу; компактизации внутренней клеточной массы; характеристике трофэктодермы. Эмбрионы на стадии развития бластоцисты ≥3, с внутренней клеточной массой типа А и В, и трофэктодермой типа А и В, считаются морфологически хорошим качеством.
При концентрации Г-КСФ в фолликулярной жидкости ≥410 пг/мл и наличии эмбрионов морфологически хорошего качества прогнозируют наступление клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС.
Способ подтверждается следующими клиническими примерами.
Пример 1. Пациентка Б. 35 лет. Диагноз: Бесплодие II, обусловленное трубно-перитонеальным фактором. В анамнезе 1 протокол ЭКО с субоптимальным ответом на КОС (7 полученных ооцитов). Концентрация АМГ в сыворотке крови - 2,76 нг/мл, концентрация ФСГ в сыворотке крови - 6,81 мМЕ/мл и количество антральных фолликулов - 9.
С 3-его дня менструального цикла проведена КОС гонадотропинами (ФСГ) в протоколе с антагонистами ГнРГ. Длительность стимуляции - 8 дней. Стартовая доза - 250 ME, суммарная доза - 2000 ME. На 13-й день менструального цикла проведена трансвагинальная пункция и получено 7 ооцитов.
Концентрация Г-КСФ в фолликулярной жидкости - 673,6 нг/мл.
На пятый день культивирования имеет 4 эмбриона, из них 2 эмбриона морфологически хорошего качества 3АА, 4АВ. Был проведен перенос 1 эмбриона (4АВ) в полость матки, клиническая беременность наступила.
Прогноз, рассчитанный на основании заявленного способа, подтвердился.
Пример 2. Пациентка X. 32 года. Диагноз: Бесплодие I, обусловленное мужским фактором. Была лапароскопическая операция на левом яичнике: цистэктомия. В анамнезе 1 протокол ЭКО с субоптимальным ответом на КОС (8 полученных ооцитов). Концентрация АМГ в сыворотке крови - 2,16 нг/мл, концентрация ФСГ в сыворотке крови - 9,75 мМЕ/мл и количество антральных фолликулов - 7.
С 3-его дня менструального цикла проведена КОС гонадотропинами (ФСГ) в протоколе с антагонистами ГнРГ. Длительность стимуляции - 8 дней. Стартовая доза - 250 ME, суммарная доза - 2000 ME. На 13-й день менструального цикла проведена трансвагинальная пункция и получено 6 ооцитов.
Концентрация Г-КСФ в фолликулярной жидкости - 392,7 нг/мл.
На пятый день культивирования имеет 4 эмбриона, из них 2 эмбриона морфологически хорошего качества 3АВ, 3ВВ. Был проведен перенос 1 эмбриона (3АВ) в полость матки, клиническая беременность не наступила.
Прогноз, рассчитанный на основании заявленного способа, подтвердился.
Пример 3. Пациентка К. 33 года. Диагноз: Бесплодие I, обусловленное генитальным эндометриозом. В анамнезе 1 протокол ЭКО с субоптимальным ответом на КОС (9 полученных ооцитов). Была лапароскопическая операция на обеих яичниках: цистэктомия. Концентрация АМГ в сыворотке крови - 1,87 нг/мл, концентрация ФСГ в сыворотке крови - 8,39 мМЕ/мл и количество антральных фолликулов - 6.
С 3-его дня менструального цикла проведена КОС гонадотропинами (ФСГ) в протоколе с антагонистами ГнРГ. Длительность стимуляции - 7 дней. Стартовая доза - 300 ME, суммарная доза - 2100 ME. На 12-й день менструального цикла проведена трансвагинальная пункция и получено 5 ооцитов.
Концентрация Г-КСФ в фолликулярной жидкости - 462,9 нг/мл.
На пятый день культивирования имеет 3 эмбриона, при этом отсутствовали эмбрионы морфологически хорошего качества. Был проведен перенос 2 эмбрионов (2ВВ и 2ВС) в полость матки, беременность не наступила.
Прогноз, рассчитанный на основании заявленного способа, подтвердился.
Пример 4. Пациентка С. 35 лет. Диагноз: Бесплодие I сочетанное, обусловленное трубно-перитонеальным и мужским фактором. В анамнезе была лапароскопическая операция на правом яичнике: цистэктомия, тубэтомия. Концентрация АМГ в сыворотке крови - 2,38 нг/мл, концентрация ФСГ в сыворотке крови - 8,91 мМЕ/мл и количество антральных фолликулов - 9.
С 3-его дня менструального цикла проведена КОС гонадотропинами (ФСГ) в протоколе с антагонистами ГнРГ. Длительность стимуляции - 7 дней. Стартовая доза - 250 ME, суммарная доза - 1750 ME. На 12-й день менструального цикла проведена трансвагинальная пункция и получено 8 ооцитов.
Концентрация Г-КСФ в фолликулярной жидкости - 702,8 нг/мл.
На пятый день культивирования имеет 5 эмбрионов, из них 3 эмбриона морфологически хорошего качества 3АВ, 4ВВ, 3АА. Был проведен перенос 1 эмбриона (3АА) в полость матки, клиническая беременность наступила.
Прогноз, рассчитанный на основании заявленного способа, подтвердился.
Пример 5. Пациентка А. 39 лет. Диагноз: Бесплодие II, обусловленное ановуляцией и мужским фактором. В анамнезе 1 протокол ЭКО с субоптимальным ответом на КОС (8 полученных ооцитов). Концентрация АМГв сыворотке крови - 1,75 нг/мл, концентрация ФСГ в сыворотке крови - 10,47 мМЕ/мл и количество антральных фолликулов - 5.
С 3-его дня менструального цикла проведена КОС гонадотропинами (ФСГ) в протоколе с антагонистами ГнРГ. Длительность стимуляции - 8 дней. Стартовая доза - 300 ME, суммарная доза - 2400 ME. На 13-й день менструального цикла проведена трансвагинальная пункция и получено 4 ооцита.
Концентрация Г-КСФ в фолликулярной жидкости - 343,8 нг/мл.
На пятый день культивирования было получено 2 эмбриона, при этом отсутствовали эмбрионы морфологически хорошего качества. Был проведен перенос 1 эмбриона (2ВА) в полость матки, клиническая беременность не наступила.
Прогноз, рассчитанный на основании заявленного способа, подтвердился.
Заявляемый способ обладает простотой и доступностью выполнения, прост в интерпретации результатов, имеет высокую чувствительность и специфичность, помогает избегать безрезультатного переноса эмбрионов, способствует повышению эффективности ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ СУБОПТИМАЛЬНОГО ОТВЕТА НА КОНТРОЛИРУЕМУЮ ОВАРИАЛЬНУЮ СТИМУЛЯЦИЮ В ПРОГРАММАХ ЭКО/ИКСИ | 2021 |
|
RU2774145C1 |
| СПОСОБ ОТБОРА ПАЦИЕНТОК С СИНДРОМОМ "СЛАБОГО" ОТВЕТА ЯИЧНИКОВ ДЛЯ ПРОВЕДЕНИЯ ПРОГРАММЫ "ДОНАЦИЯ ООЦИТОВ" | 2014 |
|
RU2565449C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДОВ ПРОГРАММЫ ЭКО И ПЭ | 2015 |
|
RU2581027C1 |
| Способ прогнозирования исходов программ экстракорпорального оплодотворения и переноса эмбрионов | 2023 |
|
RU2813434C1 |
| Способ доклинической диагностики преждевременного истощения яичников у женщин репродуктивного возраста | 2016 |
|
RU2625723C1 |
| Способ иммунологического прогнозирования эффективности применения вспомогательных репродуктивных технологий | 2024 |
|
RU2836007C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СИНДРОМА "ПУСТЫХ" ФОЛЛИКУЛОВ | 2005 |
|
RU2302639C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ КАЧЕСТВА ЭМБРИОНА ПРИ ПРОВЕДЕНИИ ЭКО У ЖЕНЩИН С БЕСПЛОДИЕМ | 2010 |
|
RU2441243C1 |
| Способ прогнозирования наступления беременности в программе экстракорпорального оплодотворения | 2016 |
|
RU2648839C1 |
| Способ прогнозирования наступления беременности у женщин с «бедным» ответом с использованием сыворотки крови | 2023 |
|
RU2816049C1 |
Изобретение относится к области медицины, а именно к репродуктологии, и может быть использовано для прогнозирования наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на контролируемую овариальную стимуляцию (КОС). Определяют концентрацию гранулоцитарного колониестимулирующего фактора (Г-КСФ) в фолликулярной жидкости и морфологические характеристики эмбрионов. При уровне Г-КСФ в фолликулярной жидкости ≥410 пг/мл и наличии эмбрионов морфологически хорошего качества прогнозируют наступление клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС. Способ обладает простотой и доступностью выполнения, прост в интерпретации результатов, имеет высокую чувствительность и специфичность, помогает избегать безрезультатного переноса эмбрионов, способствует повышению эффективности ЭКО у пациенток с прогнозируемым субоптимальным ответом на КОС. 1 ил., 5 пр.
Способ прогнозирования наступления клинической беременности в циклах ЭКО у пациенток с прогнозируемым субоптимальным ответом на контролируемую овариальную стимуляцию (КОС), отличающийся тем, что у пациенток, имеющих сумму баллов ≥9 по шкале прогнозирования развития субоптимального ответа на КОС: возраст пациентки ≥35 лет - 3 балла, наличие субоптимального ответа в анамнезе - 4,5 балла, уровень ФСГ в сыворотке крови ≥8,71 мМЕ/мл - 1 балл, уровень АМГ в сыворотке крови <2,56 нг/мл - 2 балла, количество антральных фолликулов <10-4 балла, определяют концентрацию Г-КСФ в фолликулярной жидкости с оценкой морфологических характеристик эмбрионов, и при уровне Г-КСФ в фолликулярной жидкости ≥410 пг/мл и наличии эмбрионов морфологически хорошего качества, характеризующихся стадией развития бластоцисты ≥3, внутренней клеточной массой типа А и В и трофэктодермой типа А и В, прогнозируют наступление клинической беременности.
| СПОСОБ ПРОГНОЗА РЕЗУЛЬТАТА ЭКСТРАКОРПОРАЛЬНОГО ОПЛОДОТВОРЕНИЯ И ПЕРЕНОСА ЭМБРИОНОВ (ЭКО И ПЭ) | 2011 |
|
RU2476142C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДОВ ПРОГРАММЫ ЭКО И ПЭ | 2015 |
|
RU2581027C1 |
| RU 2193777 C2, 27.11.2002 | |||
| WO 2008009705 A1, 24.01.2008 | |||
| WO 2021028562 A1, 18.02.2021 | |||
| WO 2020118790 A1, 18.06.2020 | |||
| Н | |||
| О | |||
| Мотовилова и др | |||
| Секреция колониестимулирующих факторов в яичниках у больных с бесплодием в цикле ЭКО | |||
| Журнал акушерства и женских болезней | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2022-11-28—Публикация
2022-08-04—Подача