Изобретение относится к медицине, а именно к акушерству и гинекологии, клинической иммунологии, и может быть использовано для прогнозирования эффективности применения вспомогательных репродуктивных технологий (ВРТ).
Бесплодный брак является актуальной медико-биологической и социальной проблемой в связи с низким естественным приростом населения. По данным ВОЗ, каждый шестой человек в мире страдает от бесплодия (https://iris.who.int/bitstream/handle/10665/366700/9789240068315-eng.pdf?sequence=1). Применение ВРТ в последние годы стало ведущим методом лечения бесплодия. Основой для этих методов является процедура экстракорпорального оплодотворения преовуляторных фолликулов и перенос дробящихся эмбрионов в полость матки (ЭКО).
Эффективность ЭКО составляет примерно 37-39% наступивших вследствие применения ВРТ беременностей. В зависимости от возраста частота наступления беременности в группе женщин 35-39 лет в программах ЭКО составляет около 27%, в группе 40 лет и старше - 13%, что ниже аналогичных показателей в группе женщин моложе 35 лет - 30,4%. Низкая частота наступления беременности в программах ЭКО у женщин позднего репродуктивного возраста связана со снижением показателей овариального резерва и качества ооцитов, на которые влияют возраст, соматический и гинекологический анамнез (Ozcan P., Takmaz T. Identification of predictive factors for the probability of pregnancy following ovulation stimulation-intra-uterine insemination cycles in terms of female and male // The journal of obstetrics and gynaecology research. - 2021. - Vol. 47, №3. - P. 893-899).
При этом только 73% беременностей после ЭКО заканчивается рождением живых детей, доля преждевременных родов составляет треть, частота спонтанных абортов на ранних сроках беременности 21% (Calleja-Agius J., Jauniaux E., Pizzey A.R., Muttukrishna S. Investigation of systemic inflammatory in first trimester pregnancy failure // Human Reproduct. - 2012. - Vol. 27. - P. 349-358).
Учитывая высокую стоимость метода и достаточно низкую результативность, появляется необходимость в прогнозе результата ЭКО для определения реальных шансов наступления беременности в каждом конкретном случае. Оценке целесообразности проведения ЭКО и оптимизации тактики ведения пациенток как на этапе подготовки к процедуре, так и на этапе применения программы ЭКО или искусственной инсеминации, может способствовать детекция иммунных и гормональных параметров.
Исследование в сыворотке крови, фолликулярной жидкости яичников и эндометрии количественного уровня цитокинов как медиаторов межклеточных и межтканевых взаимодействий имеет несомненный научно-практический интерес в плане установления дискриминационных уровней иммунных параметров, специфичных для разных триместров нормально протекающей беременности, угрозы невынашивания, бесплодия. Трудности интерпретации содержания иммуномедиаторов с определением их диагностической и прогностической ценности обусловлены многообразием, плейотропностью и полифункциональностью цитокинов (Матвеева Л.В., Фоминова Г.В., Громова Е.В., Алямкина Е.А., Галыня А.С. Иммунологическое прогнозирование эффективности вспомогательных репродуктивных технологий // Вестник Российского университета дружбы народов. Серия: Медицина. 2023. Т. 27. №3. С. 342-353).
Известен способ прогнозирования степени риска отрицательных результатов ЭКО, учитывающий сывороточный уровень титра иммуноглобулина G к токсоплазменному антигену и количество предшествующих неудачных попыток ЭКО (RU 2773798, МПК A61B 5/00, G01N 33/53, опубл. 09.06.2022).
Но данный способ является узко специфичным и не учитывает ни уровень половых гормонов, ни иммуномедиаторов, ни инфекцию другими патогенами.
Известен способ прогноза развития синдрома гиперстимуляции яичников при применении ВРТ на основании измерения окружности талии, иммунологического исследования в крови уровней антимюллерового гормона (АМГ), пролактина, тиреотропного гормона, антител к тиреоидной пероксидазе с вычислением прогностического индекса (RU 2773798, МПК A61B 5/00, G01N 33/48, опубл. 13.03.2017).
Однако, применение данного способа не позволяет прогнозировать исход применения ВРТ в виде наступления беременности.
Ранее для прогноза ответа яичников в протоколах ЭКО было предложено применять многомерные модели, включающие возраст, количество антральных фолликулов и уровни лютеинизирующего и фолликулостимулирующего гормона (ФСГ) (Broekmans F.J.M., Verweij P., Eijkemans M.J., Mannaerts B., Witjes H. Prognostic models for high and low ovarian responses in controlled ovarian stimulation using a GnRH antagonist protocol // Hum. Reprod. - 2014. - Vol. 29 (8). - P. 1688-1697).
Также для прогнозирования ответа яичников предлагались многомерные модели, включающие АМГ, возраст, индекс массы тела, курение, тип и продолжительность бесплодия. При этом только индекс массы тела добавлял некоторую прогностическую ценность АМГ для прогнозирования как высокого, так и низкого ответа в протоколах ЭКО. При специфичности ~90% уровень АМГ при высоком и низком ответе, соответствующий пороговым значениям 4,5 и 0,8 мкг/л, показал чувствительность ~60% и ~45% соответственно (Hamdine O., Eijkemans M.J., Lentjes E.W., Torrance H.L., Macklon N.S., Fauser B.C., Broekmans F.J. Ovarian response prediction in GnRH antagonist treatment for IVF using anti-Müllerian hormone // Hum. Reprod. - 2015. - Vol. 30 (1). - P. 170-178).
Применение имеющихся аналогов с оценкой преимущественно только половых гормонов не позволяет оценить состояние иммунной реактивности женщины и спрогнозировать её вклад в эффективность процедуры ЭКО.
Известен способ отбора пациенток с синдромом слабого ответа яичников, нуждающихся в переводе на программу лечения с использованием донорских ооцитов, отличающийся тем, что у пациентки на 2-3-й дни менструального цикла, предшествующие проведению гонадотропной стимуляции, исследуют в сыворотке крови уровень АМГ и, при его уровне 0,1-0,5 нг/мл, дополнительно определяют концентрацию ФСГ, рассчитывают соотношение ФСГ/АМГ и, если величина полученного соотношения равна или превышает 51, проводят коррекцию лечения и перевод пациентки на программу лечения с использованием донорских ооцитов (RU 2565449, МПК G01N 33/53, G01N 33/74, опубл. 20.10.2015 г.).
Недостатками способа являются отсутствие данных о чувствительности и специфичности способа; пренебрежение оценкой иммунных параметров.
Известен способ прогнозирования исходов программы ЭКО и ПЭ путем исследования женщин с бесплодием трубно-перитонеального генеза до начала протокола ЭКО и ПЭ с оценкой в венозной крови уровня АМГ, и, если он 1,14 нг/мл и ниже, дополнительно определяют уровень тревожности по Спилбергу-Ханну, и, если он 45 и выше баллов, прогнозируют неблагоприятный исход программы ЭКО (RU 25810270, МПК G01N 33/68, опубл. 10.04.2016 г.).
Ограничениями применения данного способа являются узкий диапазон содержания АМГ и нозологического спектра, пренебрежение оценкой иммунных параметров.
Предлагаемый способ основывается на исследовании патогенетически значимых иммунных маркеров: комбинации провоспалительного медиатора межклеточных взаимодействий - интерлейкина (IL)-18, АМГ и секс-стероид-связывающего глобулина (ССГ), с помощью иммуноферментного анализа.
Ранее установлено, что усиление синтеза IL-18 приводит к блокированию роста и пролиферации эндотелиоцитов, угнетению ангиогенеза. IL-18 может прямо ингибировать fibroblast growth factor-индуцированную пролиферацию эндотелиоцитов, останавливать формирование новых сосудов, регрессировать растущие сосуды (Cao R., Farnebo J., Kurimoto M., Cao Y. Interleukin-18 acts as an angiogenesis and tumor suppressor // The FASEB Journal. - 1999. - Vol. 13 (15). - P. 2195-2202). Следовательно, логично предположить, что повышенный уровень IL-18 потенциально способен ухудшить васкулогенез и процесс имплантации.
У женщин АМГ вырабатывается исключительно гранулезными клетками фолликулов яичников на ранних стадиях развития фолликулов. Концентрация АМГ медленно снижается с возрастом, пока не становится неопределяемой примерно за 5 лет до менопаузы, когда запас примордиальных фолликулов истощается. Однако существует значительная индивидуальная вариабельность в темпах истощения пула фолликулов и исходном размере пула фолликулов. Индивидуальная концентрация АМГ в сыворотке достаточно верно отражает размер пула антральных фолликулов, представляя количество оставшихся примордиальных фолликулов. Соответственно, уровни АМГ могут значительно различаться у женщин одного и того же хронологического возраста, что позволяет прогнозировать продолжительность репродуктивной жизни женщины (Broer S.L., Broekmans F.J., Laven J.S., Fauser B.C. Anti-Müllerian hormone: ovarian reserve testing and its potential clinical implications // Hum. Reprod. Update. - 2014. - Vol. 20 (5). - P. 688-701). На современном этапе повышенный уровень АМГ предлагается считать критерием синдрома поликистозных яичников (Yong E.L., Teoh W.S., Huang Z.W. Polycystic ovary syndrome v.2023: Simplified diagnostic criteria for an East Asian phenotype // Ann. Acad. Med. Singap. - 2023. - Vol. 52 (12). - P. 669-678).
Известно, что ССГ поддерживает равновесие между свободной, биологически активной и связанной формами андрогенов и эстрогенов, регулируя их биологическую активность. Повышение уровня андрогенов и андрогенных прогестинов ингибирует синтез ССГ, напротив, высокие уровни эстрадиола, как и гормонов щитовидной железы, стимулируют. Количество ССГ зависит и от белоксинтезирующей функции печени. Повышение уровня ССГ сопровождает гиперэстрогению, гипертиреоз, гепатиты. С возрастом у женщин содержание ССГ снижается, что приводит к повышению свободных фракций тестостерона и клинике относительной гиперандрогении. Уменьшение количества ССГ может ассоциироваться с ожирением, инсулинорезистентностью, гипотиреозом, синдромом поликистозных яичников, системными коллагенозами, нефротическим синдромом (Zhu J.L., Chen Z., Feng W.J., Long S.L., Mo Z.C. Sex hormone-binding globulin and polycystic ovary syndrome // Clin. Chim. Acta. - 2019. - Vol. 499. - P. 142-148).
Техническим результатом предлагаемого изобретения является малоинвазивный, не требующий больших материальных затрат, способ иммунологического прогнозирования эффективности применения ВРТ.
Сущность изобретения заключается в том, что способ включает иммунологическое исследование факторов крови. Для этого определяют в сыворотке крови количественные уровни АМГ, IL-18 и ССГ, при комбинации значений АМГ включительно от 1,3 до 10 нг/мл, IL-18 меньших или равных 175 пг/мл, ССГ больших или равных 55 нмоль/л, прогнозируют благоприятный исход применения ВРТ.
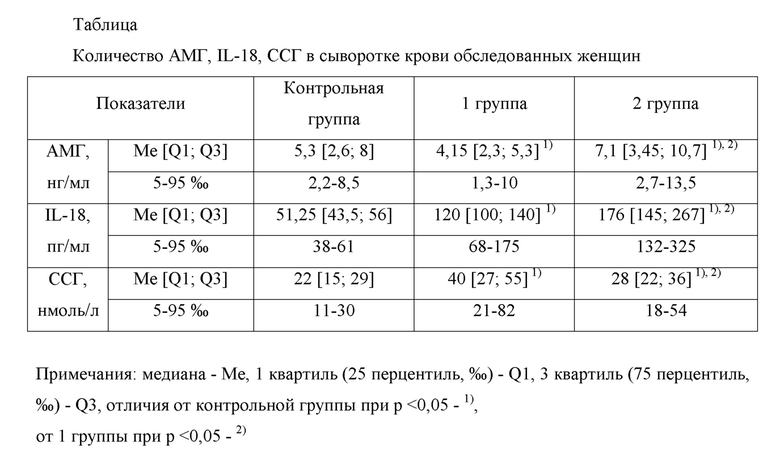
На фиг. 1 показана вариация сывороточного уровня АМГ, IL-18 и ССГ у обследованных женщин; в таблице отражено количество АМГ, IL-18 и ССГ в сыворотке крови обследованных женщин.
Способ осуществляют следующим образом: забор крови для исследования проводят в утренние часы натощак из локтевой вены в объеме 7 мл в пробирку с активатором свертывания, отделяют сыворотку с помощью центрифугирования при скорости 1500 оборотов в минуту в течение 10-12 минут. Определение количественного уровня сывороточных АМГ, IL-18 и ССГ проводят методом твердофазного иммуноферментного анализа с использованием соответствующих тест-систем.
В работе использовали наборы реагентов «АМГ-ИФА» и «ССГ-ИФА» ООО «ХЕМА», «Интерлейкин-18-ИФА-БЕСТ» АО «ВЕКТОР-БЕСТ», следуя инструкциям.
При определении концентрации АМГ в лунки планшета последовательно вносили калибровочные, контрольный, исследуемые образцы сыворотки крови, добавляли раствор конъюгата, инкубировали. После этого лунки планшета промывали промывочным раствором, затем вносили раствор тетраметилбензидина, инкубировали в темноте. Для остановки реакции во все лунки вносили стоп-реагент, содержимое лунок окрашивалось в желтый цвет разной интенсивности.
При определении концентрации ССГ в лунки планшета последовательно вносили буфер для разведения исследуемых образцов, калибровочные, контрольный, исследуемые образцы сыворотки крови, инкубировали. После инкубации лунки планшета промывали промывочным раствором, затем в лунки вносили раствор конъюгата, инкубировали. После этого лунки планшета промывали промывочным раствором, затем вносили раствор тетраметилбензидина, инкубировали в темноте. Для остановки реакции во все лунки вносили стоп-реагент, содержимое лунок окрашивалось в желтый цвет разной интенсивности.
После остановки реакции измеряли оптическую плотность в лунках с помощью спектрофотометра при длине волны 450 нм. Сывороточные концентрации АМГ и ССГ определяли при построении калибровочных графиков на трафарете. Достоверность результатов анализа оценивали по прогрессирующему нарастанию оптических плотностей калибровочных образцов, соответствию количества показателя в контрольном образце указанному.
При определении концентрации IL-18 в лунки планшета с иммобилизованными антителами к IL-18 вносили раствор для разведения образцов, калибровочные, контрольный и исследуемые образцы сыворотки крови, инкубировали. После чего лунки планшета промывали, затем вносили раствор конъюгата №1 (антителами к IL-18 с биотином), инкубировали. После 2-й инкубации лунки планшета промывали, затем добавляли раствор конъюгата №2 (стрептавидин с пероксидазой хрена), инкубировали. После 3-й инкубации лунки планшета промывали, затем вносили раствор тетраметилбензидина, инкубировали в темноте. Для остановки реакции во все лунки добавляли стоп-реагент, содержимое лунок окрашивалось в желтый цвет разной интенсивности. Измеряли оптическую плотность в лунках с помощью спектрофотометра при длине волны 450 нм. Сывороточную концентрацию IL-18 определяли при построении графика. Достоверность результатов анализа оценивали по прогрессирующему нарастанию оптических плотностей калибровочных образцов, соответствию количества показателя в контрольном образце указанному.
Способ апробирован на 80 женщинах с первичным бесплодием перед проведением процедур ВРТ в возрасте от 19 до 47 лет. Диагноз определяли на основании клинико-анамнестических данных, результатов инструментального исследования (ультразвуковое исследование (УЗИ) матки и придатков, молочных желёз). Обследуемые женщины впоследствии после применения ВРТ были распределены в группы сравнения: 1 группа - женщины с наступившей беременностью (n=51), 2 группа - женщины с ненаступившей беременностью (n=29). Средний возраст женщин 1 группы составил 35,41±3,45 года, 2 группы - 36,28±2,36 года. Статистически значимых возрастных различий среди женщин не наблюдалось.
Кровь для исследования брали при первичном обращении до применения ВРТ при получении информированного согласия обследуемых женщин. В качестве сравнения использовали серологические показатели, полученные в контрольной группе у здоровых женщин (n=10), имеющих в анамнезе беременность, наступившую без медицинских вмешательств и закончившуюся родами в срок, средний возраст которых составил 30,5±2,06 года.
Определение сывороточных концентраций АМГ, IL-18 и ССГ у здоровых женщин позволило установить интервал нормы, сопоставимый с референсными значениями.
Анализ изменений сывороточных уровней АМГ, IL-18 и ССГ у обследованных женщин выявил изменения их содержания, зависящие от фертильности (таблица).
Оценка диагностической ценности исследуемых параметров перед процедурой ВРТ относительно благоприятного её исхода в виде наступления беременности дала следующие результаты: у количества АМГ в предложенном диапазоне определилась чувствительность (Se) - 70,6%, специфичность (Sp) - 37,9%; у IL-18 - Se 100%, Sp 41,4%; у ССГ Se 29,4%, Sp 93,1%. В свою очередь, детекция комбинации АМГ, IL-18, ССГ относительно благоприятного исхода процедуры ВРТ показала Se 78,4%, Sp 62,1%.
Таким образом, результаты проведенного исследования позволяют прогнозировать исход применения ВРТ по сывороточным уровням АМГ, IL-18, ССГ.
Пример 1. Больная Ш., 47 лет, поступила на обследование и лечение в отделение вспомогательных репродуктивных технологий Перинатального центра ГБУЗ Республики Мордовия «Мордовская республиканская центральная клиническая больница» 05.09.2023 г. (на 2 день менструального цикла) с жалобами на отсутствие зачатия.
В анамнезе 3 беременности, 2 из которых закончились родами, 3-я - несостоявшимся выкидышем. Отсутствие зачатия беспокоит в течение 3 лет. Индекс массы тела - 26,17 кг/м2.
После проведенного обследования выставлен диагноз: Бесплодие женское, связанное с отсутствием овуляции. Рубец на матке после консервативной миомэктомии. Узловой зоб 1 степени. Эутиреоз.
УЗИ матки и придатков от 05.09.2023 г.: в обоих яичниках по 3-5 фолликулов размером по 2-3 мм, признаки аденомиоза.
УЗИ молочных желёз от 05.09.2023 г.: признаки фиброзной диффузной левосторонней мастопатии.
Иммунологическое исследование от 06.09.2023 г.: количество АМГ - 1,3 нг/мл, IL-18 - 145 пг/мл, ССГ - 103 нмоль/л.
После проведения ЭКО зафиксировано наступление беременности, что полностью соответствовало прогнозируемому результату.
Пример 2. Больная Н., 31 год, поступила на обследование и лечение в отделение вспомогательных репродуктивных технологий Перинатального центра ГБУЗ Республики Мордовия «Мордовская республиканская центральная клиническая больница» 11.12.2023 г. (на 3 день менструального цикла) с жалобами на отсутствие зачатия в течение 1 года.
В анамнезе беременность отсутствует, 1 протокол ЭКО с отрицательным результатом. Индекс массы тела - 31 кг/м2.
После проведенного обследования выставлен диагноз: Бесплодие женское, связанное с отсутствием овуляции. Диффузная кистозная мастопатия. Ожирение 1 ст. Гиперхолестеринемия.
УЗИ матки и придатков от 11.12.2023 г.: в правом яичнике 7 фолликулов размером до 7 мм, в левом яичнике 5 фолликулов размером до 8 мм, признаки аденомиоза.
УЗИ молочных желёз от 11.12.2023 г.: мелкая солитарная киста правой молочной железы.
Иммунологическое исследование от 12.12.2023 г.: количество АМГ -10 нг/мл, IL-18 - 133 пг/мл, ССГ - 117 нмоль/л.
После проведения ЭКО зафиксировано наступление беременности, что полностью соответствовало прогнозируемому результату.
Пример 3. Больная А., 31 год, поступила на обследование и лечение в отделение вспомогательных репродуктивных технологий Перинатального центра ГБУЗ Республики Мордовия «Мордовская республиканская центральная клиническая больница» 05.02.2024 г. (на 2 день менструального цикла) с жалобами на отсутствие зачатия.
В анамнезе 1 замершая беременность раннего срока, 3 протокола ЭКО с отрицательным результатом. Отсутствие зачатия беспокоит в течение 7 лет. Индекс массы тела - 27,71 кг/м2.
После проведенного обследования выставлен диагноз: Бесплодие женское. Эндометриоз матки. Субклинический гипотиреоз в стадии медикаментозной компенсации. Диффузная кистозная мастопатия.
УЗИ матки и придатков от 05.02.2024 г.: в правом яичнике 12 фолликулов размером до 6 мм, в левом яичнике 10 фолликулов размером до 6 мм, признаки поликистозных яичников.
УЗИ молочных желёз от 05.02.2024 г.: признаки мелких кистозных включений молочных желез.
Иммунологическое исследование от 06.02.2024 г.: количество АМГ -16,2 нг/мл, IL-18 - 325 пг/мл, ССГ - 19 нмоль/л.
После проведения ЭКО зафиксировано не наступление беременности, что полностью соответствовало прогнозируемому результату.
Пример 4. Больная П., 35 лет, поступила на обследование и лечение в отделение вспомогательных репродуктивных технологий Перинатального центра ГБУЗ Республики Мордовия «Мордовская республиканская центральная клиническая больница» 18.03.2024 г. (на 2 день менструального цикла) с жалобами на отсутствие зачатия.
В анамнезе беременность отсутствует, двусторонний гидросальпинкс, гиперплазия эндометрия, 2 протокола ЭКО с отрицательным результатом. Отсутствие зачатия беспокоит в течение 5 лет. Индекс массы тела - 23,37 кг/м2.
После проведенного обследования выставлен диагноз: Бесплодие женское, трубно-перитонеального генеза. Фиброаденома левой молочной железы.
УЗИ матки и придатков от 18.03.2024 г.: в правом яичнике 8 фолликулов размером до 7 мм, в левом яичнике 10 фолликулов размером до 7 мм, признаки диффузных изменений структуры матки по типу эндометриоза.
УЗИ молочных желёз от 18.03.2024 г.: фиброаденома левой молочной железы.
Иммунологическое исследование от 19.03.2024 г.: количество АМГ -1,15 нг/мл, IL-18 - 183 пг/мл, ССГ - 29 нмоль/л.
После проведения ЭКО зафиксировано не наступление беременности, что полностью соответствовало прогнозируемому результату.
При корреляционном анализе результатов определены статистически значимые взаимосвязи количества АМГ, IL-18 и ССГ с благоприятным прогнозом эффективности применения ВРТ. Коэффициент корреляции Пирсона составил для АМГ - -0,313, для IL-18 - -0,651, для ССГ - +0,361.
Способ предусматривает сочетанное определение в сыворотке крови количества АМГ, IL-18 и ССГ, при комбинации значений АМГ включительно от 1,3 до 10 нг/мл, IL-18 меньших или равных 175 пг/мл, ССГ больших или равных 55 нмоль/л, прогнозируют благоприятный исход применения ВРТ. Данный способ может быть использован для иммунодиагностики, прогнозирования исхода процедуры ВРТ, улучшения демографических показателей. Предлагаемый способ будет способствовать персонализированному определению шансов наступления беременности и оценке целесообразности проведения ЭКО и ИИ, оптимизации тактики ведения пациенток.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОТБОРА ПАЦИЕНТОК С СИНДРОМОМ "СЛАБОГО" ОТВЕТА ЯИЧНИКОВ ДЛЯ ПРОВЕДЕНИЯ ПРОГРАММЫ "ДОНАЦИЯ ООЦИТОВ" | 2014 |
|
RU2565449C1 |
| Способ доклинической диагностики преждевременного истощения яичников у женщин репродуктивного возраста | 2016 |
|
RU2625723C1 |
| Способ прогнозирования исходов вспомогательных репродуктивных технологий при трубном бесплодии | 2017 |
|
RU2672267C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НАСТУПЛЕНИЯ КЛИНИЧЕСКОЙ БЕРЕМЕННОСТИ В ЦИКЛАХ ЭКО У ПАЦИЕНТОК С ПРОГНОЗИРУЕМЫМ СУБОПТИМАЛЬНЫМ ОТВЕТОМ НА КОНТРОЛИРУЕМУЮ ОВАРИАЛЬНУЮ СТИМУЛЯЦИЮ | 2022 |
|
RU2784576C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДОВ ПРОГРАММЫ ЭКО И ПЭ | 2015 |
|
RU2581027C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ КАЧЕСТВА ЭМБРИОНА ПРИ ПРОВЕДЕНИИ ЭКО У ЖЕНЩИН С БЕСПЛОДИЕМ | 2010 |
|
RU2441243C1 |
| Способ прогноза развития синдрома гиперстимуляции яичников при применении вспомогательных репродуктивных технологий | 2015 |
|
RU2612839C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ СУБОПТИМАЛЬНОГО ОТВЕТА НА КОНТРОЛИРУЕМУЮ ОВАРИАЛЬНУЮ СТИМУЛЯЦИЮ В ПРОГРАММАХ ЭКО/ИКСИ | 2021 |
|
RU2774145C1 |
| Способ прогнозирования наступления беременности у женщин с «бедным» ответом с использованием сыворотки крови | 2023 |
|
RU2816049C1 |
| Способ прогнозирования эффективности программ вспомогательных репродуктивных технологий на основе нейронных сетей | 2022 |
|
RU2809429C1 |
Изобретение относится к медицине, а именно к акушерству и гинекологии, клинической иммунологии, и может быть использовано для иммунологического прогнозирования эффективности применения вспомогательных репродуктивных технологий (ВРТ) при определении иммунологических параметров крови. В сыворотке крови исследуют количества антимюллерова гормона (АМГ), интерлейкина-18 (IL-18) и секс-стероид-связывающего глобулина (ССГ). При комбинации значений АМГ включительно от 1,3 до 10 нг/мл, IL-18, меньших или равных 175 пг/мл, ССГ, больших или равных 55 нмоль/л, прогнозируют благоприятный исход применения ВРТ. Способ обеспечивает возможность малоинвазивного, не требующего больших материальных затрат иммунологического прогнозирования эффективности применения ВРТ, что способствует персонализированному определению шансов наступления беременности и оценке целесообразности проведения экстракорпорального оплодотворения, оптимизации тактики ведения пациенток за счет определения в сыворотке крови количественных уровней АМГ, IL-18 и ССГ. 1 ил., 1 табл., 4 пр.
Способ иммунологического прогнозирования эффективности применения вспомогательных репродуктивных технологий (ВРТ) при определении иммунологических параметров крови, отличающийся тем, что в сыворотке крови исследуют количества антимюллерова гормона (АМГ), интерлейкина-18 (IL-18) и секс-стероид-связывающего глобулина (ССГ), при комбинации значений АМГ включительно от 1,3 до 10 нг/мл, IL-18, меньших или равных 175 пг/мл, ССГ, больших или равных 55 нмоль/л, прогнозируют благоприятный исход применения ВРТ.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДОВ ПРОГРАММЫ ЭКО И ПЭ | 2015 |
|
RU2581027C1 |
| Способ прогнозирования эффективности вспомогательных репродуктивных технологий | 2023 |
|
RU2797507C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НАСТУПЛЕНИЯ КЛИНИЧЕСКОЙ БЕРЕМЕННОСТИ В ЦИКЛАХ ЭКО У ПАЦИЕНТОК С ПРОГНОЗИРУЕМЫМ СУБОПТИМАЛЬНЫМ ОТВЕТОМ НА КОНТРОЛИРУЕМУЮ ОВАРИАЛЬНУЮ СТИМУЛЯЦИЮ | 2022 |
|
RU2784576C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ПРОГРАММ ЭКО ПРИ ТРУБНО-ПЕРИТОНЕАЛЬНОМ БЕСПЛОДИИ, АССОЦИИРОВАННОМ С ХРОНИЧЕСКИМ ЭНДОМЕТРИТОМ | 2017 |
|
RU2677467C1 |
| Способ прогнозирования исходов вспомогательных репродуктивных технологий при трубном бесплодии | 2017 |
|
RU2672267C1 |
| Способ прогнозирования исходов программ экстракорпорального оплодотворения и переноса эмбрионов на основе оценки коморбидного статуса женщин | 2024 |
|
RU2828564C1 |
| WO 2015149129 A1, 08.10.2015 | |||
| FREOUR T | |||
| et al | |||
| Anti-mullerian hormone: clinical relevance in assisted reproductive therapy | |||
| Ann Endocrinol (Paris) | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| ДРОВОПИЛЬНО-ДРОВОКОЛЬНОЕ УСТРОЙСТВО | 1923 |
|
SU567A1 |
| LIU L | |||
| et | |||
Авторы
Даты
2025-03-10—Публикация
2024-07-22—Подача