ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По этой заявке испрашивается приоритет в соответствии с 35 U.S.C. § 119(c) на основании временной заявки на патент США с серийным номером 62/594342, поданной 4 декабря 2017 года.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым вакцинам против болезни Лайма у собак. Изобретение также относится к способам получения и применения вакцины индивидуально или в комбинациях с другими защитными средствами.
УРОВЕНЬ ТЕХНИКИ
Болезнь Лайма у собак вызывается инфекцией спирохетов вида Borrelia (spp.), включающих, в основном, B. burgdorferi sensu stricto (ss) в США и B. burgdorferi ss, B. garinii и B. afzelii в Европе [Baranton et al., Int. J. Sys. Bacteriol. 42:378-383 (1992); Hovius et al., J. Clin. Microbiol. 38:2611-2621(2000)]. Спирохеты передаются при получении инфицированными клещами Ixodes spp. крови в качестве пищи, причем инфекция вызывает у собак клинические симптомы, которые варьируют от субклинического синовита до острого артрита и артралгии [Jacobson et al., Semin. Vet. Med. Surg. 11:172-182 (1996); Summers et al., J. Comp. Path. 133:1-13 (2005)]. Важно отметить, что частота случаев болезни Лайма у собак продолжает увеличиваться ежегодно, что совпадает с увеличением числа случаев заболевания людей [Haninkova et al., Emerg. Infect. Dis. 12:604-610 (2006)]. Более того, у собак некоторых пород, особенно у ретриверов и бернских горных собак, развивается тяжелый гломерулонефрит [Dambach et al., Vet Pathol 34:85-96 (1997)], and fatalities from the complication have been reported [Littman et al., J Vet Intern Med. 20:422-434 (2006)].
Антитела, продуцируемые в ответ на заражение Borrelia spp. имеют две разные функции [Schwan, Biochem. Soc. Trans. 31:108-112 (2003); Tokarz et al., Infect. Immun. 72:5419-5432 (2004)]. Наиболее распространенный гуморальный иммунный ответ включает в себя продуцирование неспецифических связывающих/опсонизирующих (покрывающих) антител, которые "маркируют" спирохету для поглощения фагоцитарными клетками. Соответственно, указанный гуморальный иммунный ответ приводит к продукции антител, относящихся к иммуноглобулинам (Ig) M, которые связываются и индуцируют опосредованный комплементом мембраноатакующий комплекс, который убивает чужеродный антиген. Однако, в ответе, опосредованном антителами IgM, обычно класс антител переключается на IgG, которые связывают антиген, но больше не стимулируют опосредованное комплементом уничтожение. Скорее, антитела IgG связываются с антигеном-мишенью и эффективно "маркируют" спирохету для поглощения фагоцитарными клетками.
Этот более типичный ответ, опосредованный опсонизирующими антителами IgG, не обеспечивает эффективной защиты после вакцинации, прежде всего потому, что белки, которые индуцируют иммунный ответ, обычно являются общими для множества других микроорганизмов, а спирохеты, вызывающие болезнь Лайма, крайне редко обнаруживаются в кровотоке [Caine et al., Infect Immun 83: 3184-SI 94 (2015)], где взаимодействие с фагоцитарными клетками, вероятно, более эффективно. В действительности опсонизирующие антитела индуцируются несколькими белками, присутствующими также в других микроорганизмах (то есть белками размером 41 кДа, которые имеют бактериальные жгутики), что делает их значение для индуцированного вакцинацией и опосредованного антителами иммунитета, в лучшем случае сомнительным.
С другой стороны, несколько белков Borrelia spp. индуцируют опосредованный антителами ответ, при котором сохраняется способность фиксировать комплемент (боррелиацидный) даже после переключения на антитела IgG. Более конкретно, боррелиацидные антитела связываются со специфическим белком-мишенью и индуцируют комплемент, что приводит к образованию мембраноатакующего комплекса, который убивает организм, без необходимости утилизации фагоцитами. В отличие от опсонизирующих антител, указанный боррелиацидный ответ служит основой для наиболее эффективных бактериальных вакцин против болезни Лайма у собак.
Первые бактериальные вакцины против болезни Лайма у собак обеспечивали защиту путем индуцирования боррелиацидных антител, специфичных к белку внешней поверхности (Osp)A B. burgdorferi ss [Chu et al., JAVMA 201:403-411 (1992); Ma et al., Vaccine 14:1366-1374 (1996); Wikle et al., Intern. J. Appl. Res. Vet. Med. 4:23-28 (2006); and Straubinger et al., Vaccine 20:181-193 (2002)]. Этот подход может быть эффективным, однако сейчас понятно, что стратегия имеет существенные недостатки, которые могут привести к неудачной вакцинации. Например, антитела распознают только спирохеты B. burgdorferi ss, которые экспрессируют OspA [Jobe et al., J. Clin. Microbiol. 32:618-622 (1994); Lovrich et al., Infect. Immun. 63:2113-2119 (1995)], а клещи также обычно заражаются спирохетами B. burgdorferi ss, которые не экспрессируют OspA [Fikrig et al., Infect. Immun. 63:1658-1662 (1995); Ohnishi et al., Proc. Natl. Acad. Sci. 98:670-675 (2001)]. Кроме того, клещи также часто инфицируются другими Borrelia spp., такими как B. afzelii или B. garinii [Ornstein et al., J. Clin. Microbiol. 39:1294-1298(2001)], которые также вызывают болезнь Лайма, а антитела против OspA являются специфичными к геновиду [Lovrich et al., Infect. Immun. 63:2113-2119 (1995)]. Более того, "диапазон возможностей" для обеспечения защиты является кратким, поскольку экспрессия OspA, которая опосредует прикрепление к средней кишке клеща [Pal et al., J Clin Invest 106: 561-569 (2000)], отключается вскоре после того, как инфицированный клещ начинает питаться [Schwan et al., Proc. Natl. Acad. Sci. USA 92:2909-2913 (1995)].
Параллельно с разработкой вакцин против болезни Лайма на основе OspA исследователи показали, что белок OspC B. burgdorferi ss также индуцирует защитные боррелиацидные антитела [Rousselle et al., J. Infect. Dis. 178:733-741(1998); Ikushima et al., FEMS Immunol. Med. Microbiol. 29:15-21 (2000)], однако этот ответ не считается полезным для эффективной вакцины против болезни Лайма, поскольку OspC, даже среди изолятов B. burgdorferi ss, собранных из одного географического региона, является чрезвычайно гетерогенным [Ing-Nang et al., Genetics 151:15-30 (1999); Buckles et al., Clin. Vacc. Immunol. 13:1162-1165 (2006)]. Поэтому исследователи предполагают, что боррелиацидные антитела против OspC обеспечивают опосредованный антителами иммунитет лишь против небольшого числа спирохет, вызывающих болезнь Лайма.
В соответствии с вышесказанным Callister et al. [U.S. 6210676 и U.S. 6464985] предлагают использовать иммуногенный полипептидный фрагмент OspC, специфичный для карбокси (С) -конца Osp, индивидуально или в комбинации с полипептидом OspA для получения вакцины, защищающей людей и других млекопитающих от болезни Лайма. Конкретно стратегия заключается в том, чтобы индуцировать боррелиацидные антитела, которые специфически связываются с эпитопом из 7 аминокислот на карбокси (С)-конце OspC [Jobe et al., Clin. Diagn. Lab. Immuno. 10:573-578 (2003); Lovrich et al., Clin. Diagn. Lab. Immunol. 12:746-751 (2005)], поскольку этот эпитоп является консервативным среди разных штаммов B. burgdorferi ss, охарактеризованных к настоящему времени, а также присутствует у других патогенных видов Borrelia (которые можно найти с помощью поиска BLAST). Следовательно, можно ожидать, что вакцина, которая индуцирует боррелиацидные антитела OspC против консервативного эпитопа, обеспечит защиту против всех "штаммов" B. burgdorferi ss, независимо от филетической характеристики гена OspC, а также против других возбудителей болезни Лайма у собак, таких как B. garinii или B. afzelii. Livey et al. [U.S. 6872550] также предлагают вакцину для иммунизации против болезни Лайма, полученную с использованием сочетания рекомбинантных белков OspA, OspB и OspC.
На основании этой стратегии в 2009 году Merck Animal Health, Inc. получила одобрение USDA на цельноклеточную бактериальную вакцину Nobivac® Lyme, состоящую из смеси двух отдельных изолятов B. burgdorferi, которые экспрессируют либо OspA, либо OspC на внешней поверхности мембраны, соответственно [U.S. 8137678 B2; U.S. 8414901 B2]. Наиболее важно то, что подход Merck Animal Health к обеспечению более комплексной защиты собак от болезни Лайма с помощью ее вакцины Nobivac® Lyme тщательно проверен. Например, исследователи подтверждают, что вакцина индуцирует боррелиацидные антитела OspA и OspC, а также демонстрируют, что ответ, опосредованный антителами против OspC, включает значительную долю боррелиацидных антител, специфичных к консервативному эпитопу на С-конце [LaFleur et al., Clin Vaccine Immunol 16:253-259 (2009)]. Более того, исследователи подтверждают, что вакцина надежно защищает собак-реципиентов в течение одного года после вакцинации [LaFleur et al., Clin Vacc Immunol 17:870-874 (2010)], а также демонстрируют, что спирохеты, экспрессирующие OspC, вносят значительный вклад в высокий уровень защиты [LaFleur et al., Clin Vacc Immunol 22:836-839 (2015)]. Однако, несмотря на это улучшение, по-прежнему существует потребность в более комплексной и долгосрочной защите, особенно в связи с тем, что генетическое разнообразие спирохет, вызывающих болезнь Лайма, продолжает расти.
В последнее время исследователи используют другую стратегию для преодоления неоднородности OspC, и следовательно, обеспечения более полной защиты. Эта стратегия включает проведение филогенетического анализа OspC из многочисленных изолятов B. burgdorferi ss с целью идентификации участков последовательностей генов, которые являются гомогенными среди разных организмов [Earnhardt et al., Clin Vaccine Immunol 14:628-634 (2007)]. Затем исследователи конструируют "искусственный" ген, который содержит совокупность гомогенных участков, и используют его для получения химерного белка. Затем химерный белок можно использовать для получения вакцины, способной индуцировать боррелиацидные антитела против OspC, которые связываются со всеми включенными участками, что, в свою очередь, обеспечивает более полную защиту [Rhodes et al., Vet J 198:doi:10.1016/j.tvjl.2013.07.019 (2013)]. В результате получена утвержденная USDA в 2016 году коммерческая вакцина против болезни Лайма у собак (Vanguard® crLyme), состоящая из рекомбинантного (r)OspA и искусственно полученного химерного белка, который содержит эпитопы из 7 "типов" OspC [Zoetis technical bulletin - SAB-00233]. Однако из уровня техники не известно, как приготовить вакцину на основе субъединичного антигена OspC, которая могла бы индуцировать боррелиацидные антитела.
В течение ряда лет используют разные векторные стратегии, включающие применение альфавирусных частиц РНК-репликонов (RP) [Frolov et al., PNAS 93: 11371-11377 (1996); Vander Veen, et al. Anim Health Res Rev. 13(1):1-9. (2012) doi: 10.1017/S1466252312000011; Kamrud et al., J Gen Virol. 91(Pt 7):1723-1727 (2010)], полученных из нескольких разных альфавирусов, таких как вирус венесуэльского конского энцефалита (VEE) [Pushko et al., Virology 239:389-401 (1997)], вирус Синдбис (SIN) [Bredenbeek et al., Journal of Virology 67:6439-6446 (1993)] и вирус леса Семлики (SFV) [Liljestrom and Garoff, Biotechnology (NY) 9:1356- 1361 (1991)]. RP-вакцины доставляют не способные к размножению РНК-репликоны альфавирусов в клетки-хозяева и обеспечивают экспрессию целевого антигенного трансгена (трансгенов) in vivo [Pushko et al., Virology 239(2):389-401 (1997)]. RP обладают выгодным профилем безопасности и эффективности по сравнению с некоторыми традиционными вакцинными композициями [Vander Veen, et al. Anim Health Res Rev. 13(1):1-9. (2012)]. Платформу RP используют для кодирования патогенных антигенов и в качестве основы для нескольких лицензированных USDA вакцин для свиней и птиц. Кроме того, Gipson et al. [Vaccine. 21(25-26):3875-84. (2003)] используют платформу RP для кодирования антигена OpsA в исследованиях вакцинирования мышиных моделей, однако аналогичные исследования на собаках не проводились.
Соответственно, несмотря на повышенную эффективность вакцины Nobivac® Lyme и многие предполагаемые тупики и/или неудачи прошлого, все еще существует давняя потребность в дополнительно улучшенной вакцине против болезни Лайма, которая будет лучше защищать млекопитающих, особенно собак, от этой изнурительной болезни.
Цитирование любой ссылки в настоящем описании не должно истолковываться как допущение того, что такую ссылку можно использовать в качестве "уровня техники", предшествующего настоящей заявке.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Соответственно, настоящее изобретение относится к векторам, которые кодируют один или более антигенов Borrelia burgdorferi. Такие векторы можно использовать в иммуногенных композициях, содержащих эти векторы. Иммуногенные композиции по настоящему изобретению можно использовать для получения вакцин. В одном аспекте настоящего изобретения вакцина помогает защитить вакцинированного индивидуума (например, млекопитающего) от болезни Лайма. В конкретном варианте осуществления этого типа вакцинированный индивидуум представляет собой собаку. В другом варианте осуществления вакцинированный индивидуум представляет собой домашнюю кошку. Вакцины и/или способы по настоящему изобретению позволяют защищать и других домашних млекопитающих, таких как лошадиные (например, лошади) и/или крупный рогатый скот. Настоящее изобретение также относится к комбинированным вакцинам, обеспечивающим защитный иммунитет против болезни Лайма и других заболеваний, например, других инфекционных заболеваний у собак или лошадей. Изобретение также относится к способам получения и применения иммуногенных композиций и вакцин по настоящему изобретению.
В конкретных вариантах осуществления вектор представляет собой частицу РНК-репликона альфавируса, которая содержит конструкцию нуклеиновой кислоты, кодирующую антиген Borrelia burgdorferi. В более конкретных вариантах осуществления частица РНК-репликона альфавируса представляет собой частицу репликона альфавируса венесуэльского конского энцефалита (VEE). В еще более конкретных вариантах осуществления частица РНК-репликона альфавируса VEE представляет собой частицу РНК-репликона альфавируса VEE ТС-83. В других вариантах осуществления частица РНК-репликона альфавируса представляет собой частицу РНК-репликона вируса Синдбис (SIN). В других вариантах осуществления частица РНК-репликона альфавируса представляет собой частицу РНК-репликона альфавируса леса Семлики (SFV). В альтернативных вариантах осуществления вектор экспрессии, представляющий собой "оголенную" ДНК, содержит конструкцию нуклеиновой кислоты, которая кодирует антиген Borrelia burgdorferi. В других альтернативных вариантах осуществления вектор экспрессии, представляющий собой "оголенную" ДНК, содержит последовательность репликона альфавируса, которая сама кодирует антиген Borrelia burgdorferi. Настоящее изобретение включает все конструкции нуклеиновых кислот по настоящему изобретению, в том числе синтетическую матричную РНК, РНК-репликоны, а также все частицы РНК-репликонов альфавирусов по настоящему изобретению, векторы, представляющие собой "оголенную" ДНК, и иммуногенные композиции и/или вакцины, которые содержат конструкции нуклеиновых кислот (например, синтетическую матричную РНК, РНК-репликоны), частицы РНК-репликонов альфавирусов и/или векторы, представляющие собой "оголенную" ДНК по настоящему изобретению.
В конкретных вариантах осуществления нуклеотидная конструкция по настоящему изобретению кодирует один или более антигенов Borrelia burgdorferi. В одном таком варианте осуществления антиген Borrelia burgdorferi представляет собой белок A внешней поверхности (OspA), или его антигенный фрагмент. В другом варианте осуществления антиген Borrelia burgdorferi представляет собой белок С внешней поверхности (OspC), или его антигенный фрагмент. В других вариантах осуществления нуклеотидная конструкция кодирует от двух до четырех антигенов Borrelia burgdorferi или их антигенных фрагментов. В некоторых вариантах осуществления этого типа нуклеотидная конструкция кодирует один или более OspA, или один или более их антигенных фрагментов, и один или более OspC, или их антигенных фрагментов. В частности, нуклеотидная конструкция кодирует OspA, или его антигенный фрагмент, и OspC, или его антигенный фрагмент, где OspA, или его антигенный фрагмент, кодируется нуклеотидной последовательностью, расположенной выше нуклеотидной последовательности, кодирующей OspC, или его антигенный фрагмент. В другом конкретном варианте осуществления нуклеотидная конструкция кодирует OspC, или его антигенный фрагмент, и OspA, или его антигенный фрагмент, где OspC или его антигенный фрагмент кодируется нуклеотидной последовательностью, расположенной выше нуклеотидной последовательности, кодирующей OspA, или его антигенный фрагмент. В других вариантах осуществления нуклеотидная конструкция кодирует OspA, или его антигенный фрагмент, полученный из двух или более штаммов Borrelia burgdorferi. В других вариантах осуществления нуклеотидная конструкция кодирует OspC, или его антигенный фрагмент, полученный из двух или более штаммов Borrelia burgdorferi. Настоящее изобретение также относится к частицам РНК-репликона альфавируса, которые содержат любую из указанных нуклеотидных конструкций. В альтернативных вариантах осуществления вектор представляет собой оголенную ДНК, которая содержит одну или более из указанных нуклеотидных конструкций.
В конкретных вариантах осуществления иммуногенные композиции содержат частицы РНК-репликона альфавируса, которые содержат нуклеотидную конструкцию, кодирующую один или более антигенов Borrelia burgdorferi, или их антигенные фрагменты. В родственных вариантах осуществления иммуногенные композиции содержат частицы РНК-репликона альфавируса, которые содержат нуклеотидную конструкцию, кодирующую от двух до четырех антигенов Borrelia burgdorferi, или их антигенные фрагменты.
В конкретных вариантах осуществления иммуногенные композиции содержат частицы РНК-репликона альфавируса, которые содержат нуклеотидную конструкцию по настоящему изобретению. В конкретных вариантах осуществления этого типа частицы РНК-репликона альфавируса содержат нуклеотидную конструкцию, кодирующую OspA. В родственных вариантах осуществления частицы РНК-репликона альфавируса содержат нуклеотидную конструкцию, кодирующую антигенный фрагмент OspA. В других вариантах осуществления частицы РНК-репликона альфавируса содержат нуклеотидную конструкцию, кодирующую OspA, или его антигенные фрагменты, из двух или более разных штаммов Borrelia burgdorferi. В других вариантах осуществления частицы РНК-репликона альфавируса содержат нуклеотидную конструкцию, кодирующую OspC. В родственных вариантах осуществления частицы РНК-репликона альфавируса содержат нуклеотидную конструкцию, кодирующую антигенный фрагмент OspC. В других вариантах осуществления частицы РНК-репликонов альфавируса содержат нуклеотидную конструкцию, кодирующую OspC, или его антигенные фрагменты, из двух или более разных штаммов Borrelia burgdorferi.
В других вариантах осуществления иммуногенные композиции содержат частицы РНК-репликона альфавируса, которые содержат нуклеотидную конструкцию, кодирующую сочетание двух или более следующих антигенов Borrelia burgdorferi: OspA из одного или более штаммов, OspC из одного или более штаммов и/или антигенные фрагменты любого из этих белков. В конкретных вариантах осуществления иммуногенная композиция содержит частицы РНК-репликона альфавируса, которые представляют собой частицы РНК-репликона альфавируса венесуэльского конского энцефалита (VEE).
В родственных вариантах осуществления иммуногенная композиция содержит два или более наборов частиц РНК-репликона альфавируса. В конкретных вариантах осуществления этого типа один набор частиц РНК-репликона альфавируса содержит первую нуклеотидную конструкцию, а другой набор частиц РНК-репликона альфавируса содержит вторую нуклеотидную конструкцию. В других вариантах осуществления иммуногенная композиция содержит один набор частиц РНК-репликона альфавируса, который содержит первую нуклеотидную конструкцию, другой набор частиц РНК-репликона альфавируса, который содержит вторую нуклеотидную конструкцию, и третий набор частиц РНК-репликона альфавируса, который содержит третью нуклеотидную конструкцию. В следующих вариантах осуществления иммуногенная композиция содержит один набор частиц РНК-репликона альфавируса, который содержит первую нуклеотидную конструкцию, второй набор частиц РНК-репликона альфавируса, который содержит вторую нуклеотидную конструкцию, третий набор частиц РНК-репликона альфавируса, который содержит третью нуклеотидную конструкцию, и четвертый набор частиц РНК-репликона альфавируса, который содержит четвертую нуклеотидную конструкцию. В других вариантах осуществления иммуногенная композиция содержит набор частиц РНК-репликона альфавируса, который содержит первую нуклеотидную конструкцию, второй набор частиц РНК-репликона альфавируса, который содержит вторую нуклеотидную конструкцию, третий набор частиц РНК-репликона альфавируса, который содержит третью нуклеотидную конструкцию, четвертый набор частиц РНК-репликона альфавируса, который содержит четвертую нуклеотидную конструкцию, и пятый набор частиц РНК-репликона альфавируса, который содержит пятую нуклеотидную конструкцию. В таких вариантах осуществления нуклеотидные последовательности первой нуклеотидной конструкции, второй нуклеотидной конструкции, третьей нуклеотидной конструкции, четвертой нуклеотидной конструкции и пятой нуклеотидной конструкции являются разными.
Соответственно, настоящее изобретение относится к иммуногенным композициям, содержащим две или более частиц РНК-репликона альфавируса, каждая из которых по отдельности кодирует один или более антигенов Borrelia burgdorferi. В конкретных вариантах осуществления этого типа одна частица РНК-репликона альфавируса кодирует белок A внешней поверхности Borrelia burgdorferi (OspA), или его антигенный фрагмент. В некоторых вариантах осуществления одна частица РНК-репликона альфавируса кодирует белок C (OspC) внешней поверхности Borrelia burgdorferi, или его антигенный фрагмент. В следующем варианте осуществления одна частица РНК-репликона альфавируса кодирует OspA Borrelia burgdorferi, или его антигенный фрагмент, а вторая частица РНК-репликона альфавируса кодирует OspC Borrelia burgdorferi, или его антигенный фрагмент. В родственных вариантах осуществления иммуногенная композиция дополнительно содержит частицы РНК-репликона альфавируса, которые содержат нуклеотидную конструкцию, кодирующую два или более антигена Borrelia burgdorferi, или их антигенные фрагменты.
В частности, настоящее изобретение относится к иммуногенным композициям, содержащим первую и вторую частицу РНК-репликона альфавируса, каждая из которых отдельно кодирует OspA, или его антигенный фрагмент, и OspC, или его антигенный фрагмент (двойные конструкции), где первая частица РНК-репликона содержит нуклеотидную последовательность, кодирующую OspA, или его антигенный фрагмент, которая расположена перед нуклеотидной последовательностью, кодирующей OspC, или ее антигенный фрагмент, а вторая частица репликона РНК содержит нуклеотидную конструкцию, кодирующую OspC, или ее антигенный фрагмент, который расположен выше нуклеотидной последовательности, кодирующей OspA, или его антигенный фрагмент.
В конкретных вариантах осуществления нуклеотидная конструкция кодирует OspA, или его антигенный фрагмент, полученный из штамма 297 B. burgdorferi. В конкретных вариантах осуществления этого типа OspA содержит аминокислотную последовательность, которая на 95% или более идентична аминокислотной последовательности SEQ ID NO: 2. В более конкретных вариантах осуществления OspA содержит аминокислотную последовательность SEQ ID NO: 2. В еще более конкретных вариантах осуществления OspA кодируется нуклеотидной последовательностью SEQ ID NO: 1.
В родственном варианте осуществления нуклеотидная конструкция кодирует OspC, или его антигенный фрагмент, полученный из штамма 50772 B. burgdorferi (ATCC № PTA-439). В конкретных вариантах осуществления этого типа OspC содержит аминокислотную последовательность, которая на 95% или более идентична аминокислотной последовательности SEQ ID NO: 4. В более конкретных вариантах осуществления OspC содержит аминокислотную последовательность SEQ ID NO: 4. В еще более конкретных вариантах осуществления OspC кодируется нуклеотидной последовательностью SEQ ID NO: 3. В следующих вариантах осуществления нуклеотидная конструкция кодирует OspA, полученный из штамма 297 B. burgdorferi, и OspC, полученный из штамма 50772 B. burgdorferi.
Настоящее изобретение относится к вакцинам, содержащим иммуногенные композиции по настоящему изобретению, более конкретно, вакцины представляют собой не адъювантные вакцины. В конкретных вариантах осуществления вакцина помогает предотвращать заболевание, вызываемое B. burgdorferi. В конкретных вариантах осуществления заболевание, вызываемое B. burgdorferi, представляет собой болезнь Лайма. В более конкретных вариантах осуществления болезнь Лайма представляет собой болезнь Лайма у собак. В конкретных вариантах осуществления вакцина по настоящему изобретению эффективна для вакцинации здоровых собак возрастом 6-8 недель от болезни Лайма собак. В конкретных вариантах осуществления этого типа вакцина по настоящему изобретению эффективна для вакцинации здоровых собак возрастом 7 недель против болезни Лайма собак. В некоторых вариантах осуществления антитела индуцируются у собаки после ее иммунизации вакциной. В конкретных вариантах осуществления антитела представляют собой опсонизирующие IgG. В других вариантах осуществления индуцированные антитела являются боррелиацидными. В других вариантах осуществления индуцируются как опсонизирующие IgG, так и боррелиацидные антитела. В более конкретных вариантах осуществления индуцированные антитела против OspA представляют собой боррелиацидные и опсонизирующие IgG, и индуцированные антитела против OspC представляют собой боррелиацидные и опсонизирующие IgG.
В некоторых вариантах осуществления вакцина по настоящему изобретению дополнительно содержит по меньшей мере один отличный от Borrelia иммуноген, индуцирующий защитный иммунитет к отличному от Borrelia патогену. В конкретных вариантах осуществления вакцина по настоящему изобретению дополнительно содержит частицу РНК-репликона альфавируса, которая кодирует, по меньшей мере, один белковый антиген из отличного от Borrelia иммуногена, индуцирующий защитный иммунитет к отличному от Borrelia патогену. В некоторых вариантах осуществления отличный от Borrelia иммуноген получают из отличного от Borrelia патогена, такого как вирус чумы собак, собачий аденовирус, собачий парвовирус, вирус собачьего парагриппа, собачий коронавирус, вирус собачьего гриппа, серовар Leptospira, организм Leishmania, Bordetella bronchiseptica, виды Mycoplasma, вирус бешенства, Ehrlichia canis, организм Anaplasma и/или их сочетания.
В конкретных вариантах осуществления отличный от Borrelia иммуноген из серовара Leptospira представляет собой гриппотифозный серовар Leptospira kirschneri. В других вариантах осуществления иммуноген из серовара Leptospira представляет собой лептоспирозный серовар Leptospira interrogans. В следующих вариантах осуществления иммуноген из серовара Leptospira представляет собой иктерогеморрагический серовар Leptospira interrogans. В следующих вариантах осуществления иммуноген из серовара Leptospira представляет собой серовар pomona Leptospira interrogans. В следующих вариантах осуществления вакцина содержит иммуногены из нескольких сероваров Leptospira. В конкретных вариантах осуществления отличный от Borrelia иммуноген из вида Mycoplasma представляет собой Mycoplasma cynos.
Настоящее изобретение также относится к способам иммунизации млекопитающего против патогенных генотипов Borrelia, включающим введение млекопитающему иммунологически эффективного количества вакцины по настоящему изобретению. В конкретных вариантах осуществления вакцину вводят путем подкожной инъекции. В альтернативных вариантах осуществления вакцину вводят путем внутримышечной инъекции. В других вариантах осуществления вакцину вводят путем внутривенной инъекции. В следующих вариантах осуществления вакцину вводят путем внутрикожной инъекции. В следующих вариантах осуществления вакцину вводят перорально. В других вариантах осуществления вакцину вводят интраназально. В конкретных вариантах млекопитающее представляет собой собаку. В других вариантах осуществления млекопитающее относится к семейству лошадиных (например, оно представляет собой лошадь).
Вакцины по настоящему изобретению можно вводить в виде праймерной вакцины и/или в виде бустерной вакцины. В определенных вариантах осуществления, в случае введения как праймерной вакцины, так и бустерной вакцины, праймерную вакцину и бустерную вакцину можно вводить одинаковым способом. В некоторых вариантах этого типа праймерную вакцину и бустерную вакцину вводят путем подкожной инъекции. В альтернативных вариантах осуществления в случае введения как праймерной вакцины, так и бустерной вакцины, введение праймерной вакцины можно осуществлять одним способом, а введение бустерной вакцины - другим способом. В некоторых вариантах осуществления этого типа праймерную вакцину можно вводить путем подкожной инъекции, а бустерную вакцину можно вводить перорально.
Вакцинная композиция по настоящему изобретению может дополнительно включать иммунологически эффективное количество инактивированных организмов одного или более других штаммов (которые могут указываться здесь как второй штамм), относящихся к патогенному генотипу Borrelia. В конкретных вариантах осуществления второй штамм содержит антигены OspA и OspB. Примеры подходящих вторых штаммов включают один или более из следующих: B. burgdorferi ss S-1-10 (ATCC № PTA-1680), B. burgdorferi ss B-31 (ATCC № 35210), B. afzelii {например, доступный как ATCC № 51567), B. garinii (например, доступный как ATCC № 51383 и 51991), B. burgdorferi ss DK7, B. burgdorferi ss 61 BV3, B. burgdorferi ss ZS7, B. burgdorferi ss Pka, B. burgdorferi ss IP1, IP2, IP3, B. burgdorferi ss HII, B. burgdorferi ss P1F, B. burgdorferi ss Mil, B. burgdorferi ss 20006, B. burgdorferi ss 212, B. burgdorferi ss ESP1, B. burgdorferi ss Ne-56, B. burgdorferi ss Z136, B. burgdorferi ss ia, и/или любые их сочетания.
Настоящее изобретение также относится к способу иммунизации млекопитающего против патогенных видов Borrelia, в частности B. burgdorferi ss, включающему введение млекопитающему иммунологически эффективного количества описанных выше вакцин согласно изобретению. В конкретных вариантах осуществления вакцины могут содержать, например, примерно от 1×104 до 1×1010 RP или больше. В более конкретных вариантах осуществления вакцины могут содержать примерно от 1×105 до 1×109 RP. В еще более конкретных вариантах осуществления вакцины могут содержать примерно от 1×106 до 1×108 RP. В конкретных вариантах осуществления после вакцинации иммунизированное млекопитающее продуцирует боррелиацидные антитела. В конкретных воплощениях млекопитающее представляет собой собаку. В других вариантах осуществления млекопитающее относится к семейству лошадиных (например, оно представляет собой лошадь).
В некоторых воплощениях вакцины по настоящему изобретению вводят в дозах от 0,05 мл до 3 мл. В более конкретных вариантах осуществления вводимая доза составляет от 0,1 мл до 2 мл. В еще более конкретных вариантах осуществления вводимая доза составляет от 0,2 мл до 1,5 мл. В еще более конкретных вариантах осуществления вводимая доза составляет от 0,3 до 1,0 мл. В еще более конкретных вариантах осуществления вводимая доза составляет от 0,4 мл до 0,8 мл.
Настоящее изобретение также относится к комбинированным вакцинам, которые дополнительно содержат векторы (например, частицы РНК-репликонов альфавируса), кодирующие один или более иммуногенов других патогенов собак, такие как, например, иммуногены, индуцирующие иммунитет против вируса собачьей чумы, аденовируса собак, парвовируса собак, вируса собачьего парагриппа, собачьего коронавируса, вируса собачьего гриппа и/или сероваров Leptospira, например, гриппотифозный серовар Leptospira kirschneri, лептоспирозный серовар Leptospira interrogans, иктерогеморрагический серовар Leptospira interrogans, и/или серовар pomona Leptospira interrogans. Другие собачьи патогены, которые можно добавить в комбинированную вакцину по настоящему изобретению, включают организмы Leishmania, такие как Leishmania major и Leishmania infantum, Bordetella bronchiseptica, виды Mycoplasma (например, Mycoplasma cynos), вирус бешенства, виды анаплазмы, такие как Anaplasma phagocytophilum и Anaplasma platys; и Ehrlichia canis. В конкретных вариантах осуществления вакцина по настоящему изобретению дополнительно содержит частицу РНК-репликона альфавируса, которая кодирует по меньшей мере один или более антигенов из одного или более таких иммуногенов.
Нижеследующее подробное описание позволяет лучше понять приведенные и другие аспекты настоящего изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к иммуногенным композициям и/или вакцинам, которые содержат иммунологически эффективное количество частиц РНК-репликона альфавируса, кодирующих белок A внешней поверхности Borrelia burgdorferi (OspA), или его антигенный фрагмент, и белок C внешней поверхности Borrelia burgdorferi (OspC), или его антигенный фрагмент, иммунологически эффективное количество двух или более векторов, содержащих по меньшей мере одну частицу РНК-репликона альфавируса, кодирующую белок A внешней поверхности Borrelia burgdorferi (OspA), или его антигенный фрагмент, и по меньшей мере другую частицу РНК-репликона альфавируса, кодирующую белок C (OspC) внешней поверхности Borrelia burgdorferi, или его антигенный фрагмент, или сочетание частиц РНК-репликонов альфавируса, которые кодируют как Osp A, или его антигенный фрагмент, так и OspB, или его антигенный фрагмент, с частицами РНК-репликона альфавируса, которые кодируют Osp A, или его антигенный фрагмент, и/или Osp C, или его антигенный фрагмент. Все указанные иммуногенные композиции можно использовать для получения вакцин млекопитающих. В одном аспекте настоящего изобретения вакцина обеспечивает защиту вакцинированного индивидуума (например, млекопитающего) от болезни Лайма. В конкретном воплощении этого типа вакцинированный индивидуум представляет собой собаку. Соответственно, настоящее изобретение относится к новым иммунологическим композициям, которые повышают надежность вакцинации для предотвращения болезни Лайма у собак в результате того, что они (i) значительно снижают вероятность неблагоприятных побочных эффектов вследствие отсутствия вакцинации неродственными антигенами из бактериальных вакцин и (ii) по-прежнему обеспечивают всестороннюю защиту. Вакцинные композиции против болезни Лайма по настоящему изобретению также значительно увеличивают "окно эффективности", вызывая эффективный анамнестический вторичный иммунный ответ.
Нижеследующие определения приведены для более полного понимания изобретения.
Использование отдельных терминов для удобства описания никоим образом не подразумевает ограничения. Таким образом, например, ссылка на композицию, содержащую "полипептид", включает ссылку на один или более таких полипептидов. Кроме того, ссылка на "организм" включает ссылку на множество таких организмов, если не указано иное.
В настоящем описании термины "примерно" и "приблизительно", используемые как взаимозаменяемые, означают, что значение находится в пределах пятидесяти процентов от указанного значения, то есть композиция, содержащая "примерно" 1×108 частиц РНК-репликона альфавируса на миллилитр, содержит от 5×107 до 1,5×108 частиц РНК-репликона альфавируса на миллилитр.
Если не указано иное, используемый здесь термин "собачьи" включает всех домашних собак, Canis lupus familiaris или Canis familiaris.
Термин "геновид", который впервые использовали и определили G. Baranton et al., 1992, International J. of Systematic Bacteriology 42: 378-383, применяется здесь так же, как и термин "вид", для описания таксономии отличных от Borrelia организмов.
Термин "отличный от Borrelia" используют в применении к таким терминам, как организм, патоген и/или антиген (или иммуноген), для обозначения того, что соответствующий организм, патоген и/или антиген (или иммуноген) не является организмом Borrelia, не является патогеном Borrelia и/или не является антигеном (или иммуногеном) Borrelia соответственно, и что отличный от Borrelia белковый антиген (или иммуноген) получают не из организма Borrelia.
Термины "происходить из", "получают из" и "получаемый из" используются взаимозаменяемо в отношении конкретного белкового антигена и патогена, или штамма патогена, который его кодирует в природе, и в настоящем документе означают, что немодифицированная и/или усеченная аминокислотная последовательность конкретного белкового антигена кодируется указанным патогеном или штаммом указанного патогена. Последовательность нуклеотидной конструкции по настоящему изобретению, кодирующую белковый антиген, полученный из патогена, могла быть подвергнута генетическому изменению с достижением модификации и/или усечения аминокислотной последовательности экспрессируемого белкового антигена по сравнению с соответствующей последовательностью указанного белкового антигена, присутствующего в патогене или штамме патогена (включая природно-аттенуированные штаммы), из которого он происходит.
"Стандартные условия роста" для культивирования геновидов Borrelia включают выращивание при температуре в диапазоне примерно от 33°C до 35°C в среде BSK (Barbour Stoenner Kelly). Среду BSK, как описано здесь, получают по методу Callister et al. [Detection of Borreliacidal Antibodies by Flow Cytometry, Sections 11.5.1-11.5.12, Current Protocols in Cytometry, John Wiley and Sons, Inc. Supplement 26, (2003), включенному в настоящий документ посредством ссылки в полном объеме] (среду BSK также можно приобрести на коммерческой основе, например, в Sigma, St. Louis, MO).
Используемый здесь термин "OspC7" относится к иммунодоминантному эпитопу боррелиацидного антитела против OspC, расположенному в участке из 7 аминокислот [Lovrich et al., Clin. Diagn. Lab. Immunol., 12:746-751, (2005)] С-конца, состоящего из 50 аминокислот OspC, как описано Callister et al. [U.S. 6210676 B1 и U.S. 6464985 B1], который является консервативным среди известных патогенных видов Borrelia spp. Данная консервативность легко подтверждается поиском BLAST сегмента кодона, кодирующего сегмент из 7 аминокислот, как описано Lovrich et al. [Clin. Diagn. Lab. Immunol., 12:746-751, (2005)]. Такой поиск, проведенный 9 октября 2006 г., позволил получить список результатов из 100 видов Borrelia, содержащих указанный выше сегмент, кодирующий 7-мономерный эпитоп OspC. В конкретных вариантах осуществления частица РНК-репликона альфавируса кодирует антигенный фрагмент OspC, который включает OspC7.
Используемые здесь термины "защита" или "обеспечение защиты" или "индукция защитного иммунитета" и "способствует защите" не подразумевают наличие полной защиты от каких-либо признаков инфекции. Например, термин "способствует защите" может означать, что защита является достаточной для того, чтобы после заражения симптомы основной инфекции, по меньшей мере, уменьшались, и/или чтобы одна или более из основных клеточных, физиологических или биохимических причин или механизмов, вызывающих симптомы, уменьшались и/или устранялись. Следует понимать, что "уменьшенный" в данном контексте означает относительный статус инфекции, включая молекулярный статус инфекции, а не только физиологический статус инфекции.
Используемый здесь термин "вакцина" представляет собой композицию, подходящую для применения животному, например, представителю собачьих, кошачьих или лошадиных (включая, в некоторых вариантах осуществления, человека, хотя в других вариантах осуществления конкретно указано: не для людей), содержащую один или более антигенов, как правило, в сочетании с фармацевтически приемлемым носителем, таким как жидкость, содержащая воду, которая при введении животному вызывает достаточно сильный иммунный ответ, чтобы минимально способствовать защите от заболевания, возникающего в результате инфекции микроорганизма дикого типа, то есть достаточно сильный, чтобы способствовать профилактике заболевания и/или профилактике, ослаблению или излечению заболевания.
В настоящем описании поливалентная вакцина представляет собой вакцину, которая содержит два или более разных антигенов. В конкретном воплощении данного типа поливалентная вакцина стимулирует иммунную систему реципиента против двух или более разных патогенов.
Используемый здесь термин "репликон" относится к модифицированному геному РНК-вируса, в котором отсутствует один или более элементов (например, кодирующих последовательности структурных белков), которые, в случае присутствия, могли бы обеспечить успешное размножение исходного вируса в клеточных культурах или животных-хозяевах. В подходящем клеточном окружении репликон сам амплифицируется и может продуцировать один или более видов субгеномных РНК.
Используемый здесь термин "частица РНК-репликона альфавируса", сокращенно "RP", представляет собой полученный из альфавируса РНК-репликон, упакованный в структурные белки, например капсид и гликопротеины, которые также получены из альфавируса, например, как описано Pushko et al., [Virology 239(2):389-401 (1997)]. RP не может размножаться в клеточных культурах или животных-хозяевах (без херперной плазмиды или аналогичного компонента), поскольку репликон не кодирует структурные компоненты альфавируса (например, капсид и гликопротеины). Транскрипция гетерологичных нуклеиновых последовательностей РНК-RP, кодирующих OspA и/или OspC, или их антигенные фрагменты, находится под контролем субгеномного (sg) альфавирусного промотора, в частности промотора 26S sg, предпочтительно промотора VEEV 26S sg.
В случае двойных RP-конструкций последовательностей, кодирующих OspA и OspC, каждая из кодирующих последовательностей конструкции может находиться под транскрипционным контролем отдельного субгеномного промотора. В такой двойной конструкции расположенная выше по ходу считывания кодирующая последовательность соответствует 5'-позиции промотора, а расположенная ниже кодирующая последовательность соответствует 3'-позиции промотора (положительная смысловая РНК). Предпочтительно расположенные выше и ниже кодирующие последовательности являются смежными.
В настоящем описании термин "фармацевтически приемлемый" используют в качестве прилагательного для обозначения того, что модифицированное существительное подходит для применения в фармацевтическом продукте. При использовании, например, для описания вспомогательного вещества, входящего в состав фармацевтической вакцины, он характеризует вспомогательное вещество как совместимое с другими ингредиентами композиции и не являющееся излишне вредным для предполагаемого животного-реципиента, например собаки.
"Парентеральное введение" включает подкожные инъекции, субмукозальные инъекции, внутривенные инъекции, внутримышечные инъекции, внутрикожные инъекции и инфузию.
Термин "антигенный фрагмент", используемый здесь в применении к конкретному белку (например, белковому антигену), обозначает фрагмент этого белка (включающий большие фрагменты, в которых отсутствует только одна аминокислота полноразмерного белка), который обладает антигенными свойствами, то есть способностью специфически взаимодействовать с антиген-распознающей молекулой иммунной системы, такой как иммуноглобулин (антитело) или рецептор Т-клеточного антигена. Например, антигенный фрагмент белка A внешней поверхности (OspA) представляет собой фрагмент белка OspA, который обладает антигенными свойствами. Предпочтительно антигенный фрагмент по настоящему изобретению является иммунодоминантным для распознавания антителом и/или рецептором Т-клеток. В конкретных вариантах осуществления антигенный фрагмент по отношению к данному белковому антигену представляет собой фрагмент этого белка, который сохраняет по меньшей мере 25% антигенности полноразмерного белка. В предпочтительных вариантах осуществления антигенный фрагмент сохраняет по меньшей мере 50% антигенности полноразмерного белка. В более предпочтительных вариантах осуществления он сохраняет по меньшей мере 75% антигенности полноразмерного белка.
Антигенные фрагменты могут содержать всего 7-20 аминокислот (см. выше) или, с другой стороны, они могут представлять собой большие фрагменты, в которых по сравнению с полноразмерным белком отсутствует всего одна аминокислота. В конкретных вариантах осуществления антигенный фрагмент содержит от 25 до 150 аминокислотных остатков. В других вариантах осуществления антигенный фрагмент содержит от 50 до 250 аминокислотных остатков.
"OspC-специфическое боррелиацидное антитело" представляет собой антитело, присутствующее, например, в сыворотке животного, вакцинированного B. burgdorferi ss 50772 (ATCC № PTA-439), и способное избирательно связываться с любым эпитопом антигена OspC и уничтожать спирохеты, зависимо или независимо от комплемента. "OspC7-специфическое боррелиацидное антитело" представляет собой антитело, присутствующее, например, в сыворотке животного, вакцинированного B. burgdorferi ss 50772 (ATCC № PTA-439), и способное избирательно связываться с 7 C-концевыми аминокислотами OspC, как описано Lovrich et al. [Clin. Diagn. Lab. Immunol., 12:746-751, (2005)], и уничтожать спирохеты (обычно путем индукции комплемент-опосредованного мембраноатакующего комплекса). Специфичность OspC боррелиацидных антител хорошо известна. Например, боррелиацидные антитела OspC обычно детектируют в сыворотке пациентов с болезнью Лайма путем измерения чувствительности к B. burgdorferi ss 50772 в тесте на боррелиацидные антитела. Сыворотки пациентов-людей с близкородственными заболеваниями только в редких случаях (2%) содержат перекрестные антитела, способные также уничтожать штамм 50772 [подробно описано в Callister, et al., Clinical and Diagnostic Laboratory Immunology 3(4): 399-4021(1996)]. Более того, пептидный ELISA, в котором используется боррелиацидный эпитоп OspC7, позволяет точно обнаружить боррелиацидные антитела в сыворотке пациентов с болезнью Лайма, а сыворотка пациентов с другими близкородственными заболеваниями лишь иногда (<2%) содержит перекрестные антитела, которые также связывают пептид OspC7.
Если "значительная доля" индуцированных вакциной OspC-специфичных боррелиацидных антител в сыворотке специфична к консервативному эпитопу OspC7, это означает, что происходит заметное снижение OspC-специфичных боррелиацидных антител в сыворотке после абсорбции сыворотки на OspC7. Предпочтительно данный термин определяют как по меньшей мере 2-кратное снижение титра боррелиацидных антител в сыворотке, обнаруженное с использованием B. burgdorferi ss 50772, и более предпочтительно, как 2-4-кратное или более сильное снижение титра боррелиацидных антител сыворотки после абсорбции этой сыворотки на OspC7.
"Комплемент-специфичная реакция" представляет собой реакцию антитела, включающую уничтожение организма (организмов) Borrelia spp. под действием боррелиацидных антител, для которой требуется наличие комплемента в сыворотке.
В настоящем описании термин "инактивированный" микроорганизм используется взаимозаменяемо с термином "убитый" микроорганизм. В целях настоящего изобретения "инактивированный" организм Borrelia burgdorferi ss представляет собой организм, способный вызывать иммунный ответ у животного, но не способный инфицировать животное. Изоляты Borrelia burgdorferi ss можно инактивировать средством, выбранным из группы, состоящей из бинарного этиленимина, формалина, бета-пропиолактона, тимеросала или нагревания. В конкретном варианте осуществления изоляты Borrelia burgdorferi ss инактивируют бинарным этиленимином.
Используемый здесь термин "неадъювантная вакцина" относится к вакцине, или поливалентной вакцине, которая не содержит адъюванта.
B. burgdorferi ss 50772 (ATCC № PTA-439), описанный в US 6210676, и B. burgdorferi ss S-1-10 (ATCC № PTA-1680), описанный в US 6316005, помещены в Американскую коллекцию типовых культур, 10801 University Boulevard Manassas (VA) 20110, 30 июля 1999 г и 1 апреля 2000 г, соответственно.
В данном описании одна аминокислотная последовательность на 100% "идентична" второй аминокислотной последовательности или обладает 100% "идентичностью" со второй аминокислотной последовательностью, если аминокислотные остатки обеих последовательностей идентичны. Соответственно, аминокислотная последовательность на 50% "идентична" второй аминокислотной последовательности, если 50% аминокислотных остатков двух аминокислотных последовательностей являются идентичными. Сравнение последовательностей проводят по непрерывному блоку аминокислотных остатков, входящих в состав конкретного белка, например, сравниваемого белка или фрагмента полипептида. В конкретном варианте осуществления учитывают выбранные делеции или вставки, которые в противном случае могли бы изменить соответствие между двумя аминокислотными последовательностями.
Используемый здесь процент идентичности нуклеотидной и аминокислотной последовательности можно определить с помощью алгоритмов C MacVector (MacVector, Inc. Cary, NC 27519), Vector NTI (Informax, Inc. MD), Oxford Molecular Group PLC (1996) и Clustal W, используя параметры выравнивания по умолчанию и параметры идентичности по умолчанию. Указанные коммерчески доступные программы также можно использовать для определения подобия последовательностей с использованием таких же или аналогичных параметров по умолчанию. В качестве альтернативы можно использовать расширенный поиск Blast в условиях фильтра по умолчанию, например, с использованием программы для наложения GCG (Genetics Computer Group, Руководство по программе для пакета GCG, версия 7, Madison, Wisconsin) и параметров по умолчанию.
Также следует понимать, что настоящее изобретение не ограничивается конкретными конфигурациями, стадиями способов и материалами, описанными в настоящем описании, поскольку такие конфигурации, стадии способов и материалы могут немного варьировать. Также следует понимать, что приведенная здесь терминология используется только для описания конкретных вариантов осуществления и не предназначается для ограничения, поскольку объем настоящего изобретения ограничивается только прилагаемой формулой изобретения и ее эквивалентами.
Альтернативные штаммы OspA
Штаммы, содержащие антиген OspA, могут представлять собой обычные патогенные лабораторные изоляты B. burgdorferi ss [Barbour et al., J. Clin. Microbiol. 52: 478-484 (1985)], такого как B. burgdorferi ss B-31 (ATCC № 35210). Конкретным вторым организмом является представленный в качестве примера штамм B. burgdorferi ss S-1-10 (ATCC № PTA-1680). Другие штаммы, подходящие для использования в качестве второго организма в вакцинных композициях, оптимизированных для регионов за пределами Северной Америки, включают, например, следующие штаммы: B. burgdorferi ss B-31 (ATCC № 35210), B. afzelii (например, доступный как ATCC 51567) и B. garinii (например, доступный как ATCC № 51383 и 51991), а также перечисленные в таблице 1 ниже.
Таблица 1
1 Lagal et al., J. Clin. Microbiol. 41:5059-5065 (2003)
2 Heikkila et al., J. Clin. Microbiol. 40:1174-1180 (2002)
Композицию вакцины можно вводить любым стандартным способом, например, путем внутривенной, внутримышечной, подкожной, пероральной, интраназальной, внутрикожной и/или внутрибрюшинной вакцинации. Специалисту должно быть понятно, что вакцинную композицию предпочтительно получают соответствующим образом для каждого типа животного-реципиента и способа введения.
Таким образом, настоящее изобретение также относится к способам иммунизации собак против B. burgdorferi ss и других видов Borrelia. Один такой способ включает введение собакам иммунологически эффективного количества вакцины по настоящему изобретению, так чтобы собака продуцировала соответствующие OspA и/или OspC. В конкретных вариантах осуществления антитела представляют собой боррелиацидные антитела.
ПРИМЕРЫ
Нижеследующие примеры служат для дальнейшего понимания изобретения, но никоим образом не предназначаются для ограничения эффективного объема изобретения.
ПРИМЕР 1
КОНСТРУИРОВАНИЕ ВАКЦИН OspA и OspC, ДОСТАВЛЯЕМЫХ ЧАСТИЦАМИ РНК-РЕПЛИКОНОВ АЛЬФАВИРУСА
РНК-вирусы используют в качестве векторов-переносчиков для введения вакцинных антигенов, встроенных в их геномы посредством генетических манипуляций. Однако их использование до настоящего времени было ограничено, в основном, включением вирусных антигенов в РНК-вирус и затем введением вируса реципиенту-хозяину. Результатом является индукция защитных антител против включенных вирусных антигенов. Например, вектор на основе альфавирусного репликона используют для защиты мышей от нейротоксина ботулина и сибирской язвы посредством экспрессии нейротоксина HC C. botulinum или защитного антигена B. anthracis, соответственно [Lee et al., Vaccine 24 (47-48) 6886-6892 (2006)]. Частицы РНК-репликона альфавируса используют для кодирования патогенных антигенов. Такие платформы альфавирусных репликонов разработаны на основе нескольких разных альфавирусов, таких как вирус венесуэльского конского энцефалита (VEE) [Pushko et al., Virology 239: 389-401 (1997)], вирус Синдбис (SIN) [Bredenbeek et al., Journal of Virology 67:6439 -6446 (1993), содержание которого полностью включено в настоящий документ] и вирус леса Семлики (SFV) [Liljestrom and Garoff, Biotechnology (NY) 9:1356-1611 (1991), содержание которого настоящим включено в данный документ во всей полноте]. Кроме того, частицы РНК-репликона альфавируса являются основой нескольких лицензированных USDA вакцин для свиней и птицы. К ним относятся: вакцина против эпизоотической диареи свиней, РНК-частица (код продукта 19U5.P1), вакцина против свинного гриппа, РНК (код продукта 19A5.D0), вакцина против птичьего гриппа, РНК (код продукта 1905.D0) и рецептурный препарат, РНК-частица (код продукта 9PP0.00). Как описано ниже, исследована способность векторной системы на основе РНК-репликона альфавируса индуцировать у собак продуцирование боррелиацидных антител, специфичных к OspA, OspC и DbpA.
Включение последовательностей, кодирующих OspA или OspC в альфавирусный репликон:
Аминокислотные последовательности OspA (штамм 297) и OspC (штамм 50772) используют для получения оптимизированных по кодонам (частота использования кодонов у Canis lupus) нуклеотидных последовательностей путем компьютерного моделирования. Оптимизированные последовательности получает коммерческий поставщик в виде синтетической ДНК (ATUM, Newark, CA).
Векторы репликона VEE, предназначенные для экспрессии OspA или OspC, сконструированы по описанному ранее способу [см. US 9441247 B2; содержание которого настоящим включено в данный документ посредством ссылки], с нижеследующими модификациями. Вектор на основе репликона, полученного из TC-83 "pVEK" [раскрытый и описанный в U.S. 9441247 B2] расщепляют рестриктазами AscI и PacI. ДНК-плазмиду, содержащую оптимизированную по кодонам последовательность открытой рамки считывания OspA или OspC,
с 5'-фланкирующей последовательностью (5'-GGCGCGCCGCACC-3') [SEQ ID NO: 5] и
3’-фланкирующей последовательностью (5’-TTAATTAA-3’),
аналогичным образом расщепляют рестриктазами AscI и PacI. Затем синтетическую генную кассету лигируют в расщепленный вектор pVEK, и полученные клоны переименовывают в "pVHV-OspA" и "pVHV-OspC".
Получение частиц РНК-репликона ТС-83 (RP) проводят по описанным ранее способам [U.S. 9441247 B2 и US 8460913 B2; содержание которых включено в настоящее описание в качестве ссылки]. Коротко говоря, ДНК-вектор на основе репликона pVHV и хелперные ДНК-плазмиды линеаризуют с помощью рестриктазы NotI и затем подвергают транскрипции in vitro с использованием РНК-полимеразы MegaScript T7 и cap-аналога (Promega, Madison, WI). Важно, что хелперные РНК, используемые для продукции, не содержат субгеномную промоторную последовательность VEE, как описано ранее [Kamrud et al., J Gen Virol. 91 (Часть 7): 1723-1727 (2010)]. Очищенную РНК репликона и хелперные компоненты объединяют и смешивают с суспензией клеток Vero, проводят электропорацию в кюветах 4 мм и возвращают в бессывороточные среды для культивирования клеток, полученные от Thermo Fisher, Waltham MA, продаваемые под названием OptiPro SFM®. После инкубации в течение ночи частицы РНК-репликонов альфавируса очищают от клеток и среды путем пропускания суспензии через глубинный фильтр ZetaPlus BioCap (3M, Maplewood, MN), промывания фосфатно-солевым буфером, содержащим 5% сахарозы (масс./об.), и, наконец, элюирования оставшихся RP буфером, содержащим 400 мМ NaCl. Элюированные RP доводят до конечной концентрации сахарозы 5% (масс./об.), пропускают через мембранный фильтр 0,22 микрон и распределяют по аликвотам для хранения. Титр функциональных RP определяют с помощью иммунофлуоресцентного анализа на инфицированных монослоях клеток Vero. Партии RP идентифицируют в соответствии с геном, кодируемым упакованным репликоном: RP-OspA или RP-OspC.
ПРИМЕР 2
ВАКЦИНА, СОДЕРЖАЩАЯ КОНСТРУКЦИЮ RP-OspA
МАТЕРИАЛЫ И МЕТОДЫ
Конструкция: Конструкцию RP-OspA получают, как описано выше, с использованием нуклеотидной последовательности, кодирующей антиген, содержащий иммуногенные эпитопы белка А внешней поверхности.
Животные: Биглей возрастом пять месяцев (Marshall Bioresources) содержат совместно на приподнятых площадках для выгула собак, где еда и вода находятся в свободном доступе.
Получение вакцины RP-OspA: РНК OspA вместе с хелперными РНК вводят в клетки Vero путем электропорации. После совместной электропорации OspA упаковывается в RP, образуя RP- OspA. Затем RP-OspA смешивают со стабилизатором (сахароза, экстракт казеина, содержащий аминокислоты и белки, желатин), 0,9% солевым раствором, амфотерицином B и гентамицином, так чтобы доза в объеме 1,0 мл содержала 1,0×108 частиц репликона/мл. Затем вакцину лиофилизируют.
Вакцинация и сбор сыворотки: Собак вакцинируют подкожно в шею дозой вакцины RP-OspA 1 мл и в качестве повторной иммунизации вводят еще дозу 1 мл через 21 день. Целую кровь собирают на 7, 14, 20, 29, 35 и 42 дни исследования путем венопункции яремной вены. Сыворотку отделяют центрифугированием и хранят при -10°C или при более низкой температуре до тестирования.
Детекция боррелиацидных антител против OspA: Боррелиацидные антитела против OspA детектируют методом проточной цитометрии с использованием B. burgdorferi ss S-1-10 [Callister et al., Arch. Intern. Med. 154:1625-1632 (1994)].
Детекция антител IgG против OspA: Опсонизирующие антитела IgG против OspA детектируют методом ИФА.
РЕЗУЛЬТАТЫ
Вакцинация с использованием вакцины RP-OspA надежно индуцирует высокий уровень антител IgG, причем гуморальный ответ включает выработку значительного количества боррелиацидных антител против OspA через 2 недели после повторной вакцинации.
ТАБЛИЦА 2
Средние титры антител (n=5) после вакцинации RP-OspA
a ND=не обнаружены
Результаты, приведенные выше в таблице 2, демонстрируют способность вакцины, содержащей RP-OspA, индуцировать значительные уровни боррелиацидных антител против OspA.
ПРИМЕР 3
ВАКЦИНА, СОДЕРЖАЩАЯ КОНСТРУКЦИЮ RP-OspC
МАТЕРИАЛЫ И МЕТОДЫ
Конструкция: Конструкцию RP-OspC получают, как описано выше, с использованием нуклеотидной последовательности, кодирующей антиген, содержащий иммуногенные эпитопы белка С внешней поверхности.
Животные: Биглей возрастом пять месяцев (Marshall Bioresources) содержат совместно на приподнятых площадках для выгула собак, где еда и вода находятся в свободном доступе.
Получение вакцины RP-OspC: РНК OspC вместе с хелперными РНК вводят в клетки Vero путем электропорации. После совместной электропорации OspC упаковывается в RP, образуя RP-OspC. Затем RP-OspC смешивают со стабилизатором (сахароза, экстракт казеина, содержащий аминокислоты и белки, желатин), 0,9% солевым раствором, амфотерицином B и гентамицином, так чтобы доза в объеме 1,0 мл содержала 1,0×108 частиц репликона/мл. Затем вакцину лиофилизируют.
Вакцинация и сбор сыворотки: Собак вакцинируют подкожно в шею дозой вакцины RP-OspC 1 мл и в качестве повторной иммунизации вводят еще дозу 1 мл через 21 день. Целую кровь собирают на 7, 14, 20, 29, 35 и 42 дни исследования путем венопункции яремной вены. Сыворотку отделяют центрифугированием и хранят при -10°C или при более низкой температуре до тестирования.
Детекция боррелиацидных антител против OspC: Боррелиацидные антитела против OspC детектируют методом проточной цитометрии с использованием B. burgdorferi ss 50772 [Callister et al., Arch. Intern. Med. 154:1625-1632 (1994)].
Детекция антител IgG против OspC: Опсонизирующие антитела IgG против OspC детектируют методом ИФА.
РЕЗУЛЬТАТЫ
Вакцинация с использованием вакцины RP-OspC надежно индуцирует высокий уровень антител IgG, причем гуморальный ответ включает выработку значительного количества боррелиацидных антител против OspC через 2 недели после повторной вакцинации.
ТАБЛИЦА 3
Средние титры антител (n=5) после вакцинации RP-OspC
a ND=не обнаружены
Результаты демонстрируют способность вакцины, содержащей RP-OspC, индуцировать значительные уровни боррелиацидных антител против OspC.
ПРИМЕР 4
КОМБИНИРОВАННАЯ ВАКЦИНА, СОДЕРЖАЩАЯ RP-OspA и RP-OspC
МАТЕРИАЛЫ И МЕТОДЫ
Конструкция: Конструкции RP-OspA и RP-OspC получают по описанному выше способу.
Животные: Биглей возрастом пять месяцев (Marshall Bioresources) содержат совместно на приподнятых площадках для выгула собак, где еда и вода находятся в свободном доступе.
Получение комбинированной вакцины RP-OspA и RP-OspC: Антигены RP-OspA и RP-OspC смешивают со стабилизатором (сахароза, экстракт казеина, содержащий аминокислоты и белки, желатин), 0,9% солевым раствором, амфотерицином B и гентамицином, так чтобы доза в объеме 1,0 мл содержала 1,0×108 частиц репликона/мл. Затем вакцину лиофилизируют.
Вакцинация и сбор сыворотки: Собак вакцинируют подкожно в шею дозой комбинированной вакцины 1 мл и в качестве повторной иммунизации вводят еще дозу 1 мл через 21 день. Целую кровь собирают на 7, 14, 20, 29, 35 и 42 дни исследования путем венопункции яремной вены. Сыворотку отделяют центрифугированием и хранят при -10°C или при более низкой температуре до тестирования.
Детекция боррелиацидных антител: Боррелиацидные антитела против OspA and OspC детектируют методом проточной цитометрии с использованием B. burgdorferi ss S-1-10 или B. burgdorferi ss 50772, соответственно [Callister et al., Arch. Intern. Med. 154:1625-1632 (1994)].
Детекция антител IgG: Антитела IgG против OspA и OspC детектируют методом ИФА.
РЕЗУЛЬТАТЫ
Вакцинация с использованием комбинированной вакцины надежно индуцирует высокий уровень IgG и боррелиацидные антитела против OspA и OspC через 2 недели после повторной вакцинации.
Результаты демонстрируют способность комбинированной вакцины, содержащей RP-OspA и RP-OspC, индуцировать высокие уровни боррелиацидных антител против OspA и OspC и индуцировать высокие уровни опсонизирующих антител IgG против RP-OspC.
ПРИМЕР 5
КОМБИНИРОВАННАЯ ВАКЦИНА, СОДЕРЖАЩАЯ RP-OspA и RP-OspC
Конструкции: Конструкции RP-OspA и RP-OspC получают по описанному выше способу.
Животные: Биглей возрастом три месяца (Ridglan Farms) размещают совместно на площадках для выгула собак, где еда и вода находятся в свободном доступе.
Получение комбинированной вакцины RP-OspA и RP-OspC: Группа лечения А получает сочетание инактивированных бактериальных вакцин BEI штаммов S-1-10 и 50772 (смешанных с 5% раствором адъюванта Emulsigen-MVP Laboratories Inc., Omaha, US). Антигены RP-OspA и RP-OspC смешивают со стабилизатором (сахароза, экстракт казеина, содержащий аминокислоты и белки, желатин), 0,9% солевым раствором, амфотерицином B и гентамицином так, чтобы доза в объеме 1,0 мл содержала 5,0×107 (группа лечения B), 5,0×106 (группа лечения C) или 5,0×105 (группа лечения D) частиц репликона каждой конструкции/мл. Вакцины лиофилизируют.
Вакцинация и реакция в месте инъекции: Собак вакцинируют подкожно в шею дозой комбинированной вакцины 1 мл и в качестве повторной иммунизации вводят еще дозу 1 мл через 21 день. У собак регистрируют реакции в месте инъекции на 3 и 4 дни исследования после первой вакцинации и через 24 и 25 дней после второй вакцинации до тех пор, пока реакция не перестает ощущаться (таблица 4). Реакции в месте инъекции оценивают по типу и размеру. Реакции оценивают как видимые, утолщающие, мягкие, твердые или слабые, а размер реакции оценивают как S1 <1,0 см, S2=1,0-2,0 см или S3 >2,0 см.
РЕЗУЛЬТАТЫ
ТАБЛИЦА 4
Реакции в месте инъекции
Цельнокле-точная бактериальная вакцина
Мин. защитная доза
OspA, OspC7, DbpA-tpA
5,0×107
OspA, OspC7, DbpA-tPA
5,0×106
OspA, OspC7, Dbpa-tpA
5,0×105
S1 <1,0 см; S2=1,0-2,0 см; S3 >2,0 см; Т=утолщение; S=мягкий; H=жесткий; V=видимый
o=нет реакции
ПРИМЕР 6
КОМБИНИРОВАННАЯ ВАКЦИНА С ДВОЙНОЙ ВСТАВКОЙ КОНСТРУКЦИЙ RP-OspA/C
МАТЕРИАЛЫ И МЕТОДЫ
Включение последовательностей, кодирующих OspA и OspC, в альфавирусный репликон:
Вектор "pVEK" на основе репликона, полученного из TC-83, расщепленный AscI и PacI, получают по способу, описанному в примере 1. Две ДНК-плазмиды, содержащие оптимизированные по кодонам последовательности открытых рамок считывания как OspA, так и OspC, с 5'-фланкирующей последовательностью (5'-GGCGCGCCGCACC-3’) [SEQ ID NO: 5] и 3’-фланкирующей последовательностью (5’-TTAATTAA-3’), аналогичным образом расщепляют рестриктазами AscI и PacI. Конструкция кассеты синтетического гена содержит одну из последовательностей открытой рамки считывания (OspA или OspC), некодирующую последовательность, содержащую субгеномный промотор альфавируса и фланкирующие последовательности, а затем последовательность другой целевую открытой рамки считывания (OspA или OspC). Субгеномный промотор альфавируса и фланкирующие последовательности представляют собой
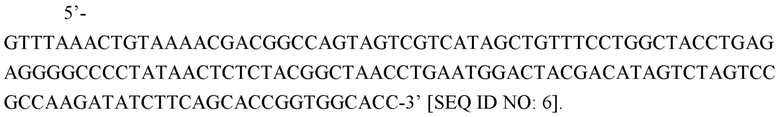
Этот дизайн дублирует короткую часть 3' nsP4 открытой рамки считывания, нативный субгеномный промотор альфавируса и 5'-нетранслируемый фрагмент нативной субгеномной последовательности. Также присутствуют участки распознавания рестрикционных ферментов, некодирующие случайные последовательности, участки связывания праймеров и консенсусная последовательность Козака, которая непосредственно примыкает к 5’-концу второй открытой рамки считывания. Затем синтетические генные кассеты лигируют в расщепленный вектор pVEK и полученным клонам дают новые названия "pVDG-OspA-OspC" или "pVDG-OspC-OspA", где названия приведены в порядке относительно 5'- и 3’-положения в кассете.
RP получают по способу, описанному в примере 1.
Животные: Биглей возрастом 7-8 недель (Ridglan Farms) содержат совместно на площадках для выгула собак, где еда и вода находятся в свободном доступе.
Получение вакцин RP-OspA/OspC или RP-OspC/OspA:
РНК-репликон каждой конструкции вместе с хелперными РНК (полученными из капсидных хелперных и гликопротеиновых последовательностей VEE) вводят методом электропорации в клетки Vero. Каждый репликон упаковывается в RP после совместной электропорации с образованием RP-антигенов. Полученные RP затем собирают в фосфатный буфер, содержащий 0,4 М NaCl и 5% (масс./об.) сахарозы, и количественно определяют путем иммунофлуоресцентного анализа.
Три отдельные вакцины смешивают со стабилизатором (сахароза, N-Z амин, желатин) и 0,9% солевым раствором так, чтобы 1 мл содержал 1 дозу. Целевая доза вакцины в группе лечения А составляет 5,0×107 каждого отдельного антигена RP-OspA и RP-OspC. Целевая доза вакцины в группе лечения B составляет 5,0×107 двойной антигенной конструкции RP-OspA/OspC. Целевая доза вакцины в группе лечения C составляет 5,0×107 двойной антигенной конструкции RP-OspC/OspA. Вакцины лиофилизируют.
Вакцинация и сбор сыворотки:
Собак вакцинируют подкожно в шею дозой вакцины 1 мл и в качестве повторной иммунизации вводят еще дозу 1 мл через 21 день. Целую кровь собирают на 1, 28, 35, 70, 92 и 119 дни исследования путем венопункции яремной вены. Сыворотку отделяют центрифугированием и хранят при -10°C или при более низкой температуре до тестирования.
Детекция боррелиацидных антител против OspA и OspC: Боррелиацидные антитела против OspA детектируют методом проточной цитометрии с использованием B. burgdorferi ss S-1-10 [Callister et al., Arch. Intern. Med. 154:1625-1632 (1994)]. Боррелиацидные антитела против OspC детектируют методом проточной цитометрии с использованием B. burgdorferi ss 50772 [Callister et al., Arch. Intern. Med. 154:1625-1632 (1994)].
РЕЗУЛЬТАТЫ
Вакцина, содержащая отдельные антигены RP-OspA и RP-OspC, индуцирует умеренные уровни боррелиацидных антител через 1 неделю после повторной вакцинации. Через 1 неделю после повторной вакцинации вакцина, содержащая двойную антигенную конструкцию RP-OspA/OspC, индуцирует высокие уровни боррелиацидных антител против OspC, но относительно низкие уровни боррелиацидных антител против OspA. И наоборот, вакцина, содержащая двойную антигенную конструкцию RP-OspC/OspA, индуцирует высокие уровни боррелиацидных антител против OspA, но относительно низкие уровни боррелиацидных антител против OspC. Полученные данные свидетельствуют о том, что более сильный ответ, опосредуемый боррелиацидными антителами против OspA или OspC, наблюдается в том случае, если этот ген находится в конструкции в нижестоящем положении (таблица 5).
ТАБЛИЦА 5
Результаты по боррелиацидным антителам
OspA+OspC
(отдельные конструкции)
OspA/OspC
(двойная конструкция)
OspA/OspC
(двойная конструкция)
Плацебо
*Значение 40 используют для определения среднего геометрического
Заражение клещами Ixodes scapularis, инфицированными B. burgdorferi:
Экспериментальное заражение клещами, инфицированными B. burgdorferi, проводят примерно через 2 недели после второй вакцинации. Коротко говоря, на выбритую сторону каждой собаки помещают 9 самок и 8 самцов взрослых клещей в резиновой чашке, которую фиксируют на месте с помощью ленты и бинтов. Клещам дают кормиться на собаках в течение 7 дней, после чего их удаляют. Через 1, 2 и 3 месяца после заражения у каждой собаки берут биопсию кожи с помощью пункционного устройства диаметром 4 мм в месте, прилегающем к месту прикрепления клеща, с целью выделения B. burgdorferi. Биопсийные образцы кожи инкубируют в среде, обогащенной BSA, и в течение 4 недель наблюдают рост B. burgdorferi. Образцы ткани с левой стороны собаки или с конечности, на которую припадает и/или прихрамывает собака, берут из локтя, запястья, колена и лапки и обрабатывают с целью выделения B. burgdorferi методом ПЦР (таблица 6).
ТАБЛИЦА 6
Число собак, у которых образцы кожи или суставов дают положительные результаты в анализе на B. burgdorferi
OspA/OspC
(двойная конструкция)
OspC/OspA
(двойная конструкция)
Плацебо
ТАБЛИЦА ПОСЛЕДОВАТЕЛЬНОСТЕЙ
ПОСЛЕДОВАТЕЛЬНОСТИ
Белок A внешней поверхности (SEQ ID NO: 1)
atgaaaaagtaccttttgggaatcggactcattctcgccctgatcgcctgcaagcaaaacgtgtcctccctcgacgaaaagaactcagtgtcggtggatctgcccggcgaaatgaaggtgctcgtgtccaaagagaagaacaaggatggaaaatacgacctgattgccaccgtggacaagctggagttgaagggcacctcagacaagaacaacgggtctggagtgctggaaggagtcaaagcggacaagtccaaggtcaagctgactatttcggacgacctgggccagactaccctggaagtgttcaaggaggacggaaagaccctggtgtccaagaaggtcacctccaaggataagtcgagcaccgaagagaagttcaatgagaagggagaagtgtcggagaagatcatcacccgcgccgatggaacccggctggagtacaccgagatcaagtccgatggttcggggaaggctaaggaagtcctgaagggctacgtgcttgagggtactctgactgcggaaaagaccactctggtggtcaaggaaggcaccgtgactctgtcaaagaacatctccaagagcggagaagtcagcgtggaactgaacgacacagattcctccgctgccacgaaaaagaccgccgcctggaacagcgggaccagcactctcaccattaccgtgaacagcaaaaagactaaggacctggtgttcaccaaggagaacacgatcaccgtgcagcagtatgactccaacggtaccaagctcgaagggtccgccgtggagatcactaagctggacgagattaagaatgcactgaagtga
Белок A внешней поверхности (SEQ ID NO: 2)
MKKYLLGIGLILALIACKQNVSSLDEKNSVSVDLPGEMKVLVSKEKNKDG
KYDLIATVDKLELKGTSDKNNGSGVLEGVKADKSKVKLTISDDLGQTTLE
VFKEDGKTLVSKKVTSKDKSSTEEKFNEKGEVSEKIITRADGTRLEYTEI
KSDGSGKAKEVLKGYVLEGTLTAEKTTLVVKEGTVTLSKNISKSGEVSVE
LNDTDSSAATKKTAAWNSGTSTLTITVNSKKTKDLVFTKENTITVQQYDS
NGTKLEGSAVEITKLDEIKNALK*
Белок C внешней поверхности (SEQ ID NO: 3)
atgaagaagaatactctctccgccattctgatgaccctgttcctgtttatctcctgcaacaactccgggaaggatggcaacacctcggccaactccgccgatgaaagcgtcaagggtcccaacctgactgagatctcgaagaaaatcaccgagtccaacgcggtggtgttggcagtgaaggaggtcgaaactctgctgactagcatcgacgagcttgccaaggccattggaaagaagattaagaacgacgtgtcactggacaacgaagctgaccataacggatctcttatctcgggcgcttacctgatttcgaccctcatcaccaagaagatctccgcgatcaaggacagcggggagctcaaggccgaaattgagaaagcaaagaagtgctccgaagagttcaccgcgaagctcaagggagaacacaccgacctgggaaaggaaggcgtcaccgatgataacgcgaagaaggccatcctcaaaaccaacaacgacaagacaaagggcgccgacgaactggagaagctgttcgagagcgtgaagaatctgtccaaggccgccaaggaaatgttgacgaacagcgtgaaggaactgacctcccctgtggtggccgagtcaccgaaaaagccatga
Белок C внешней поверхности (SEQ ID NO: 4)
MKKNTLSAILMTLFLFISCNNSGKDGNTSANSADESVKGPNLTEISKKIT
ESNAVVLAVKEVETLLTSIDELAKAIGKKIKNDVSLDNEADHNGSLISGA
YLISTLITKKISAIKDSGELKAEIEKAKKCSEEFTAKLKGEHTDLGKEGV
TDDNAKKAILKTNNDKTKGADELEKLFESVKNLSKAAKEMLTNSVKELTS
PVVAESPKKP*
Объем настоящего изобретения не ограничивается описанными здесь конкретными вариантами осуществления. Действительно, разные модификации изобретения, помимо описанных в настоящем описании, станут очевидными для специалистов в данной области техники из предшествующего описания. Предполагается, что такие модификации входят в объем прилагаемой формулы изобретения.
Кроме того, следует понимать, что все размеры оснований или размеры аминокислот и все значения молекулярных весов или молекулярных масс, приведенные для нуклеиновых кислот или полипептидов, являются приблизительными и представлены для описания.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ПРОТИВ ЛАЙМСКОЙ БОЛЕЗНИ СОБАК | 2007 |
|
RU2460538C2 |
| ВАКЦИНА ПРОТИВ ВИРУСА БЕШЕНСТВА | 2018 |
|
RU2782350C2 |
| УНИВЕРСАЛЬНАЯ ВАКЦИНА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БОЛЕЗНИ ЛАЙМА ДЛЯ ПРИМЕНЕНИЯ У ЛЮДЕЙ И В ВЕТЕРИНАРИИ И СПОСОБ ЕЕ ПРОИЗВОДСТВА | 2008 |
|
RU2472525C2 |
| ВАКЦИНАЦИЯ ЧАСТИЦАМИ РЕПЛИКОНА И МАСЛЯНЫМ АДЪЮВАНТОМ | 2018 |
|
RU2806690C2 |
| ХИМЕРНЫЕ ГЕНЫ OSPA, БЕЛКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2636455C2 |
| ХИМЕРНЫЕ ГЕНЫ OSPA, БЕЛКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2583289C2 |
| ПОЛИВАЛЕНТНАЯ ВАКЦИНА ДЛЯ ЖИВОТНЫХ СЕМЕЙСТВА КОШАЧЬИХ | 2018 |
|
RU2797538C2 |
| ВАКЦИНА К ВИРУСУ СВИНОГО ГРИППА A | 2018 |
|
RU2787596C2 |
| ХИМЕРНЫЕ ГЕНЫ OSPA, БЕЛКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2773402C2 |
| Нуклеотидная последовательность, кодирующая полипептид DBPAG, перспективный для серодиагностики клещевого боррелиоза, рекомбинантная плазмидная ДНК pETdbpagNH, кодирующая слитный полипептид DBPAG, рекомбинантный штамм бактерий Escherichia coli BL21(DE3)/ pETdbpagNH - продуцент полипептида DBPAG, полипептид DBPAG и способ его получения | 2017 |
|
RU2681229C1 |
Изобретение относится к биотехнологии и ветеринарии. Представлена вакцина, способствующая профилактике заболевания, вызываемого инфекцией Borrelia burgdorferi, содержащая две частицы РНК-репликона альфавируса; где одна частица РНК-репликона альфавируса кодирует белок A (OspA) внешней поверхности Borrelia burgdorferi и где другая частица РНК-репликона альфавируса кодирует белок C (OspC) внешней поверхности Borrelia burgdorferi; и фармацевтически приемлемый носитель. Представлена вакцина, способствующая профилактике заболевания, вызываемого инфекцией Borrelia burgdorferi, содержащая частицу РНК-репликона альфавируса, которая кодирует два антигена Borrelia burgdorferi; где один антиген Borrelia burgdorferi представляет собой белок A внешней поверхности (OspA) и где другой антиген Borrelia burgdorferi представляет собой белок С внешней поверхности (OspC); и фармацевтически приемлемый носитель. Представлен способ иммунизации животного семейства собачьих против патогенных геновидов Borrelia, включающий введение млекопитающему иммунологически эффективного количества вакцины. Изобретение направлено на дополнительное улучшение вакцины против болезни Лайма, которая будет лучше защищать млекопитающих, особенно собак, от этой изнурительной болезни. 3 н. и 9 з.п. ф-лы, 6 табл., 6 пр.
1. Вакцина, способствующая профилактике заболевания, вызываемого инфекцией Borrelia burgdorferi, содержащая две частицы РНК-репликона альфавируса;
где одна частица РНК-репликона альфавируса кодирует белок A (OspA) внешней поверхности Borrelia burgdorferi и где другая частица РНК-репликона альфавируса кодирует белок C (OspC) внешней поверхности Borrelia burgdorferi; и фармацевтически приемлемый носитель.
2. Вакцина, способствующая профилактике заболевания, вызываемого инфекцией Borrelia burgdorferi, содержащая частицу РНК-репликона альфавируса, которая кодирует два антигена Borrelia burgdorferi; где один антиген Borrelia burgdorferi представляет собой белок A внешней поверхности (OspA) и где другой антиген Borrelia burgdorferi представляет собой белок С внешней поверхности (OspC); и фармацевтически приемлемый носитель.
3. Вакцина по п.2, содержащая первую и вторую частицы РНК-репликона альфавируса, каждая из которых отдельно кодирует OspA и OspC, где первая частица РНК-репликона содержит нуклеотидную последовательность, кодирующую OspA, которая расположена выше нуклеотидной последовательности, кодирующей OspC, и вторая частица РНК-репликона содержит нуклеотидную последовательность, кодирующую OspC, которая расположена выше нуклеотидной последовательности, кодирующей OspA.
4. Вакцина по п.1, 2 или 3, где по меньшей мере одна из частиц РНК-репликона альфавируса представляет собой частицу РНК-репликона вируса Венесуэльского конского энцефалита (VEEV).
5. Вакцина по п.1-3 или 4, в которой все частицы РНК-репликона альфавируса представляют собой частицы РНК-репликона вируса Венесуэльского конского энцефалита (VEEV) .
6. Вакцина по п.1-4 или 5, где OspA получен из штамма B. burgdorferi 297 и OspC получен из штамма B. burgdorferi 50772.
7. Вакцина по п.6, где OspA содержит аминокислотную последовательность, идентичную по меньшей мере на 95% аминокислотной последовательности SEQ ID NO: 2, а OspC содержит аминокислотную последовательность, идентичную по меньшей мере на 95% аминокислотной последовательности SEQ ID NO: 4.
8. Вакцина по п.1-6 или 7, где как боррелиацидное антитело к OspA, так и боррелиацидное антитело к OspC индуцируются в организме собаки после иммунизации указанной собаки вакциной.
9. Вакцина по п.8, дополнительно содержащая по меньшей мере один отличный от Borrelia иммуноген, индуцирующий защитный иммунитет против отличного от Borrelia патогена.
10. Вакцина по п.8 или 9, дополнительно содержащая частицу РНК-репликона альфавируса, которая содержит нуклеотидную последовательность, кодирующую по меньшей мере один белковый антиген из отличного от Borrelia иммуногена.
11. Вакцина по любому из пп. 1-10, которая представляет собой неадъювантную вакцину.
12. Способ иммунизации животного семейства собачьих против патогенных геновидов Borrelia, включающий введение млекопитающему иммунологически эффективного количества вакцины по любому из пп. 1-11.
| EP 1939294 A1, 02.07.2008 | |||
| WO 2013158818 A2, 24.10.2013 | |||
| WO 2013116770 A1, 08.08.2013 | |||
| WO 2007047749 A1, 26.04.2007 | |||
| GIPSON C | |||
| L | |||
| et al | |||
| Evalution of Venezuelan Equine Encephalitis (VEE) replicon-based Outer surface protein A (OspA) vaccines in a tick challenge mouse model of Lyme disease, Vac, ELSEVIER, AMSTERDAM, NL, vol.21, no 25-26, |
Авторы
Даты
2022-12-09—Публикация
2018-12-03—Подача