[001] Настоящая заявка испрашивает приоритет заявки на патент Китая № CN201811363490.6, поданной 16 ноября 2018 г. Содержание заявки на патент Китая включено в данный документ посредством ссылки во всей своей полноте.
Область техники
[002] Настоящее изобретение относится к области фармацевтических составов, в частности относится к фармацевтической композиции, содержащей ингибиторы PARP, и способу ее получения.
Уровень техники
[003] Поли(АДФ-рибозо)полимеразы (PARP), характеризующиеся активностью полиаденозиндифосфатрибозилирования, составляют суперсемейство из 18 ядерных и цитоплазматических ферментов. Данное полиаденозиндифосфатрибозилирование модулирует каталитическую активность белка-мишени и взаимодействия между белками и регулирует многие фундаментальные биологические процессы, включая репарацию ДНК, гибель клеток, а также стабильность генома (см. D’ Amours et al. Biochem. J, 1999, 342, 249).
[004] Активность PARP-1 составляет примерно 80% от всей активности PARP в клетке, и данный фермент является членом семейства PARP, способным к репарации повреждений ДНК вместе с PARP-2, который наиболее подобен PARP-1. В качестве средства контроля повреждений ДНК и сигнального белка PARP-1 может быстро выявлять и связываться непосредственно с сайтами повреждений ДНК, а затем индуцировать агрегацию ряда белков, необходимых для репарации ДНК, тем самым позволяя восстановить повреждение ДНК. В случае дефицита PARP-1 в клетках PARP-2 может заменить PARP-1 для репарации повреждений ДНК.
[005] Исследования демонстрируют, что экспрессия белков PARP, как правило, усиливается в солидных опухолях по сравнению с нормальными клетками. Кроме того, опухоли (опухоли молочной железы и рак яичника) с делециями в генах, связанных с репарацией ДНК, таких как BRCA-1 или BRCA-2, демонстрируют чрезвычайную чувствительность к ингибитору PARP-1, что предполагает потенциальное применение ингибиторов PARP в качестве монотерапии при лечении так называемого трижды негативного рака молочной железы. (См. Plummer, E.R. Curr. Opin. Pharmacol. 2006, 6, 364; Ratnam, et al; Clin. Cancer Res. 2007, 13, 1383). В то же время PARP-1 рассматривается в качестве эффективной мишени для изучения новых вариантов терапии рака, поскольку механизм репарации повреждений ДНК является основным механизмом, с помощью которого опухолевые клетки развивают переносимость к химиотерапевтическим средствам и терапии ионизирующим излучением.
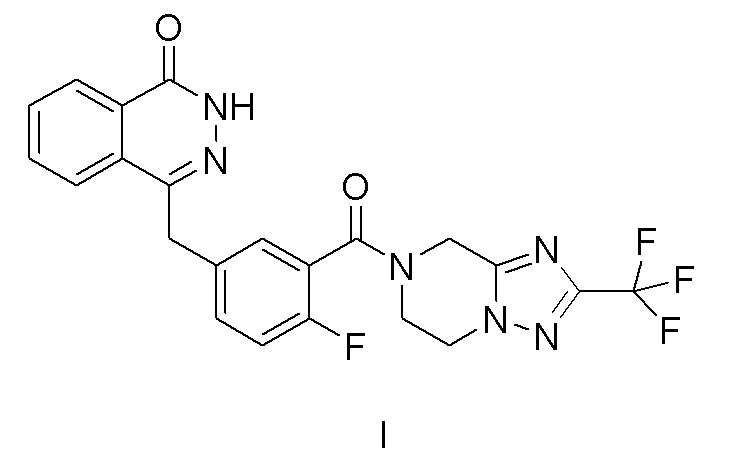
[006] В документе CN102372698A раскрыто новое производное фталазинона (формула I), которое проявляет сильное ингибирование поли(АДФ-рибозо)полимераз (PARP) и представляет собой вспомогательную терапию рака, показанное ниже:
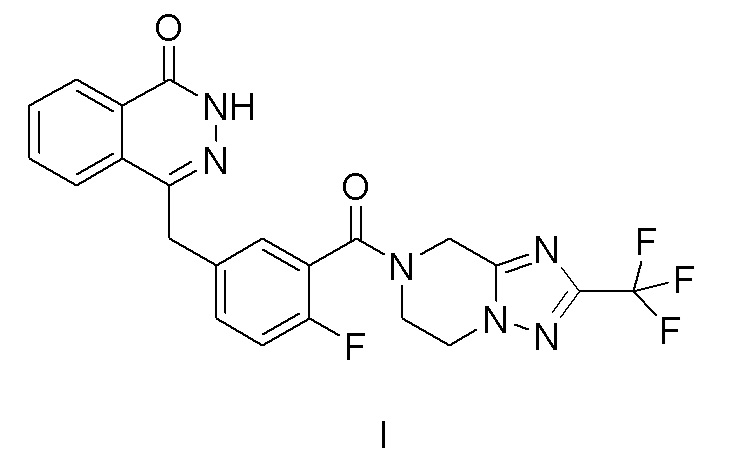 .
.
[007] В предшествующем уровне техники представлены некоторые композиции, содержащие ингибиторы PARP, и способы их получения. В документе CN102238945A описаны фармацевтические композиции, содержащие твердую дисперсию олапариба, где материалом-носителем для твердой дисперсии является коповидон, и указано, что твердая дисперсия характеризуется слабой стабильностью, если в качестве материала-носителя применяется PVP.
Содержание настоящего изобретения
[008] Целью настоящего изобретения является обеспечение твердой дисперсии, содержащей соединение, представленное формулой I, и фармацевтической композиции для улучшения лечебного эффекта лекарственных средств.
[009] В одном аспекте настоящего изобретения предусмотрена твердая дисперсия, содержащая соединение, представленное формулой I, и материал-носитель, где материал-носитель предусматривает поливинилпирролидон.
[0010] В некоторых вариантах осуществления соединение, представленное формулой I, находится в аморфной форме.
[0011] Весовое соотношение соединения, представленного формулой I, и поливинилпирролидона может составлять от 1:0,1 до 1:10, предпочтительно от 1:0,1 до 1:7, более предпочтительно от 1:0,5 до 1:5 и наиболее предпочтительно 1:3.
[0012] Поливинилпирролидон может относиться к зачастую применяемому при составлении типу поливинилпирролидона, который можно классифицировать исходя из значений K, такому как PVPK12, PVPK15, PVPK17, PVPK25, PVPK30, PVPK60, а также PVPK90, или исходя из сшитых полимеров, характеризующихся значениями молекулярной массы от 2500 до 1200000.
[0013] В некоторых вариантах осуществления твердая дисперсия может дополнительно содержать другие материалы-носители, где доля поливинилпирролидона может составлять более 40%, 50%, 60%, 70% или больше в пересчете на общий вес твердой дисперсии.
[0014] В некоторых вариантах осуществления твердая дисперсия состоит из соединения, представленного формулой I, и материала-носителя – поливинилпирролидона.
[0015] Твердую дисперсию можно дополнительно использовать для получения фармацевтической композиции, содержащей соединение, представленное формулой I, такой как состав для перорального применения, состав для инъекций, ингаляционный состав или состав для местного применения, например, таблетки, капсулы, инъекционные формы, лиофилизированный порошок для инъекции и т.д.
[0016] Фармацевтическая композиция по настоящему изобретению может представлять собой состав для перорального применения, состав для инъекций, ингаляционный состав или состав для местного применения, например, таблетки, капсулы, инъекционные формы и лиофилизированный порошок для инъекции.
[0017] Твердая дисперсия по настоящему изобретению может быть получена способами, хорошо известными в данной области техники, такими как экструзия расплава, высушивание распылением, выпаривание растворителя и т.д.
[0018] Например, способ включает стадию смешивания соединения, представленного формулой I, с поливинилпирролидоном и необязательным вспомогательным веществом в устройстве для экструзии расплава и стадию нагревания и перемешивания смеси, а также, наконец, экструдирования продукта в виде твердой дисперсии. Смесь нагревают в экструдере до температуры, достаточно высокой, чтобы расплавить смесь, но достаточно низкой, чтобы не разрушить активные компоненты.
[0019] В качестве альтернативы способ включает стадию смешивания соединения, представленного формулой I, с поливинилпирролидоном и растворителем и стадию удаления растворителя. Твердая дисперсия может быть получена путем смешивания с дополнительным вспомогательным веществом в случае необходимости. Способы удаления растворителя могут представлять собой выпаривание на роторном испарителе, высушивание распылением, лиофилизацию, пленочное испарение и т.д. Растворитель может представлять собой кетоновый растворитель и спиртовой растворитель, где кетоновый растворитель предпочтительно представляет собой ацетон, а спиртовой растворитель предпочтительно представляет собой этанол.
[0020] В другом аспекте настоящего изобретения предусмотрена фармацевтическая композиция, содержащая твердую дисперсию, которая содержит соединение, представленное формулой I, и одно или более фармацевтически приемлемых вспомогательных веществ.
[0021] В некоторых вариантах осуществления содержание соединения, представленного формулой I, составляет 0,01% - 50%, предпочтительно 1% - 40% (например, 4%, 22%) в пересчете на общий вес фармацевтической композиции.
[0022] В некоторых вариантах осуществления содержание соединения, представленного формулой I, составляет 0,1 мг - 1000 мг, например 1 мг - 500 мг, например 5 мг - 200 мг, например 10 мг, 40 мг, 100 мг.
[0023] В некоторых вариантах осуществления фармацевтическая композиция содержит наполнитель. Одно из фармацевтически приемлемых вспомогательных веществ в фармацевтической композиции может представлять собой наполнитель. Наполнитель по настоящему изобретению может включать без ограничения одно или более из микрокристаллической целлюлозы, гидрофосфата кальция, маннита, прежелатинизированного крахмала, лактозы, предпочтительно лактозу. Содержание наполнителя может составлять 5% - 90% (например, 81%) в пересчете на общий вес фармацевтической композиции.
[0024] В некоторых вариантах осуществления фармацевтическая композиция содержит разрыхлитель. Одно из фармацевтически приемлемых вспомогательных веществ в фармацевтической композиции может представлять собой разрыхлитель. Разрыхлитель может включать без ограничения одно или более из кроскармеллозы натрия, крахмала, натрий-карбоксиметилкрахмала и кросповидона, предпочтительно натрий-карбоксиметилкрахмал. Содержание разрыхлителя может составлять 1% - 20% (например, 2,2% и 11,9%) в пересчете на общий вес фармацевтической композиции.
[0025] В некоторых вариантах осуществления фармацевтическая композиция содержит смазывающее средство. Одно из фармацевтически приемлемых вспомогательных веществ в фармацевтической композиции может представлять собой смазывающее средство. Смазывающее средство может включать без ограничения одно или более из стеарата магния, стеарата цинка, глицерилбегената, лаурилсульфата натрия, гидрогенизированного растительного масла, микронизированного силикагеля, талька, диоксида кремния, предпочтительно одно или более из стеарата магния и диоксида кремния. Содержание смазывающего средства может составлять 0,5% - 5% (например, 1,3%, 3%) в пересчете на общий вес фармацевтической композиции.
[0026] Другие подходящие вспомогательные вещества включают адгезивы, суспендирующие средства, подсластители, ароматизаторы, консерванты, буферные средства, смачивающие средства, газообразующие вещества и т.д. Эти вспомогательные вещества хорошо известны в данной области техники.
[0027] В другом аспекте настоящего изобретения предусмотрена фармацевтическая композиция, содержащая:
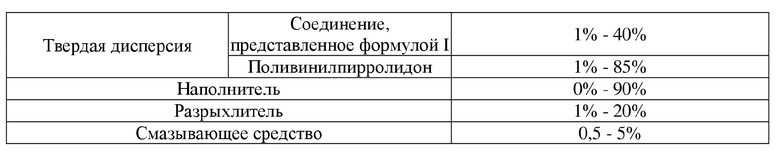
[0028] в пересчете на общий вес фармацевтической композиции; где наполнитель выбран из одного или более из микрокристаллической целлюлозы, гидрофосфата кальция, маннита, прежелатинизированного крахмала и лактозы, предпочтительно лактозы; разрыхлитель выбран из одного или более из кроскармеллозы натрия, крахмала, натрий-карбоксиметилкрахмала и кросповидона, предпочтительно натрий-карбоксиметилкрахмала; смазывающее средство выбрано из одного или более из стеарата магния, стеарата цинка, глицерилбегената, лаурилсульфата натрия, гидрогенизированного растительного масла, микронизированного силикагеля, талька и диоксида кремния, предпочтительно стеарата магния и/или диоксида кремния; при этом если смазывающим средством является стеарат магния и диоксид кремния, массовое соотношение стеарата магния и диоксида кремния составляет от 10:1 до 1:1, предпочтительно от 7:1 до 2:1.
[0029] В некоторых вариантах осуществления содержание соединения, представленного формулой I, в фармацевтической композиции составляет 4% - 22% в пересчете на общий вес фармацевтической композиции.
[0030] В некоторых вариантах осуществления содержание поливинилпирролидона в фармацевтической композиции составляет 12% - 64% в пересчете на общий вес фармацевтической композиции.
[0031] В некоторых вариантах осуществления содержание наполнителя в фармацевтической композиции составляет 0% - 80,3% в пересчете на общий вес фармацевтической композиции.
[0032] В некоторых вариантах осуществления содержание разрыхлителя в фармацевтической композиции составляет 2,2% - 11,9% в пересчете на общий вес фармацевтической композиции.
[0033] В некоторых вариантах осуществления содержание смазывающего средства в фармацевтической композиции составляет 1,3% - 3% в пересчете на общий вес фармацевтической композиции.
[0034] В другом аспекте настоящего изобретения предусмотрена фармацевтическая композиция, состоящая из вышеописанного соединения, представленного формулой I, вышеописанного поливинилпирролидона, вышеописанного наполнителя, вышеописанного разрыхлителя и вышеописанного смазывающего средства.
[0035] В другом аспекте настоящего изобретения предусмотрена фармацевтическая композиция, содержащая соединение, представленное формулой I, поливинилпирролидон, наполнитель, разрыхлитель и смазывающее средство, предпочтительно содержащая 1% - 40% соединения, представленного формулой I, 1% - 85% поливинилпирролидона, 0% - 90% наполнителя, 1% - 20% разрыхлителя и 0,5% - 5% смазывающего средства в пересчете на общий вес фармацевтической композиции; предпочтительно содержащая 4% соединения, представленного формулой I, 12,1% поливинилпирролидона, 80,3% лактозы, 2,2% натрий-карбоксиметилкрахмала, 0,2% диоксида кремния и 1,2% стеарата магния или содержащая 21,3% соединения, представленного формулой I, 63,8% поливинилпирролидона, 11,9% натрий-карбоксиметилкрахмала, 1% диоксида кремния и 2% стеарата магния в пересчете на общий вес фармацевтической композиции.
[0036] В другом аспекте настоящего изобретения предусмотрена фармацевтическая композиция, содержащая соединение, представленное формулой I, поливинилпирролидон, наполнитель, разрыхлитель и смазывающее средство, предпочтительно содержащая 1% - 40% соединения, представленного формулой I, 1% - 85% поливинилпирролидона, 0% - 90% наполнителя, 1% - 20% разрыхлителя и 0,5% - 5% смазывающего средства в пересчете на общий вес фармацевтической композиции; предпочтительно содержащая 4% соединения, представленного формулой I, 12,1% поливинилпирролидона, 80,3% лактозы, 2,2% натрий-карбоксиметилкрахмала, 0,2% диоксида кремния и 1,2% стеарата магния или содержащая 21,3% соединения, представленного формулой I, 63,8% поливинилпирролидона, 11,9% натрий-карбоксиметилкрахмала, 1% диоксида кремния и 2% стеарата магния в пересчете на общий вес фармацевтической композиции.
[0037] В другом аспекте настоящего изобретения предусмотрен способ получения фармацевтической композиции, содержащей соединение, представленное формулой I, по настоящему изобретению, где способ включает стадию смешивания твердой дисперсии по настоящему изобретению с одним или более фармацевтически приемлемыми вспомогательными веществами.
[0038] В некоторых вариантах осуществления фармацевтическая композиция по настоящему изобретению может быть получена в виде состава для перорального применения, состава для инъекций, ингаляционного состава или состава для местного применения, например, таблеток, капсул, инъекционных форм, лиофилизированного порошка для инъекции и т.д.
[0039] В некоторых вариантах осуществления фармацевтически приемлемое вспомогательное вещество предусматривает одно или более из наполнителя, разрыхлителя и смазывающего средства, где типы и количества наполнителя, разрыхлителя и смазывающего средства являются таковыми, как описано выше.
[0040] Другие подходящие вспомогательные вещества включают адгезивы, суспендирующие средства, подсластители, ароматизаторы, консерванты, буферные средства, смачивающие средства, газообразующие вещества и т.д. Эти вспомогательные вещества хорошо известны в данной области техники.
[0041] Способ получения может быть общепринятым в данной области техники, например, при получении состава для перорального применения, продукт может быть получен в виде гранул, например, на стадиях получения фармацевтической композиции в виде гранул путем гранулирования в сухом грануляторе, гранулирования с высокой скоростью сдвига, одностадийного гранулирования в псевдоожиженном слое и т.д., при этом его необязательно смешивают с другими вспомогательными веществами и затем таблетируют (наносят покрытие) или наполняют капсулы с получением таблеток, гранул или капсул.
[0042] В другом аспекте настоящего изобретения предусмотрена фармацевтическая композиция, содержащая соединение, представленное формулой I, диспергированное в материале-носителе и в одном или более фармацевтически приемлемых вспомогательных веществах, где соединение, представленное формулой I, находится в аморфной форме.
[0043] Содержание соединения, представленного формулой I, является таким же, как описано выше. Содержание и тип материала-носителя являются такими же, как описано выше. Содержание и тип вспомогательного вещества являются такими же, как описано выше.
[0044] Способ диспергирования соединения, представленного формулой I, в материале-носителе является таким же, что и способ получения твердой дисперсии по настоящему изобретению.
[0045] В некоторых вариантах осуществления твердую дисперсию по настоящему изобретению выдерживают при 25°C и 60% RH в течение 12 месяцев, и, в пересчете на общий вес твердой дисперсии, содержание соединения, представленного формулой I, составляет не менее 93%, например, содержание может составлять не менее 93,5%, 94%, 94,5%, 95%, 95,5%, 96%, 96,5%, 97%, 97,5%, 98%, 98,5% или больше, предпочтительно не менее 95% и более предпочтительно не менее 97%.
[0046] В некоторых вариантах осуществления твердую дисперсию по настоящему изобретению выдерживают при 40°C и 75% RH в течение 6 месяцев, и, в пересчете на общий вес твердой дисперсии, содержание соединения, представленного формулой I, составляет не менее 93%, например, содержание может составлять не менее 93,5%, 94%, 94,5%, 95%, 95,5%, 96%, 96,5%, 97%, 97,5%, 98%, 98,5% или больше, предпочтительно не менее 95% и более предпочтительно не менее 97%.
[0047] В некоторых вариантах осуществления фармацевтическую композицию по настоящему изобретению подвергают испытанию на растворение в соответствии с методом 2 (лопастная мешалка) для определения растворимости, описанным в приложении к Китайской фармакопее 2015 г. (том II), на следующих стадиях с применением 0,5% водного раствора Tween в качестве среды растворения, предпочтительно 1000 мл и при растворении при скорости вращения лопастной мешалки 50 об/мин при 37±0,5°C. Растворимость соединения, представленного формулой I, должна составлять более 90% в течение 60 минут, предпочтительно более 93%, более предпочтительно более 94% и еще более предпочтительно более 95%.
[0048] В некоторых вариантах осуществления фармацевтическую композицию по настоящему изобретению выдерживают при 40°C и 75% RH в течение 6 месяцев, и, в пересчете на общий вес твердой дисперсии, содержание соединения, представленного формулой I, составляет не менее 93%, например, содержание может составлять не менее 93,5%, 94%, 94,5%, 95%, 95,5%, 96%, 96,5%, 97%, 97,5%, 98%, 98,5% или больше, предпочтительно не менее 95%, более предпочтительно не менее 97% и наиболее предпочтительно не менее 98%.
[0049] В другом аспекте настоящего изобретения предусмотрено применение твердой дисперсии или фармацевтической композиции, содержащей соединение, представленное формулой I, по настоящему изобретению, при получении лекарственных средств для лечения различных видов рака. Виды рака выбраны из рака молочной железы, рака яичника, рака поджелудочной железы, рака предстательной железы, рака печени или рака толстой кишки и т.д.
[0050] В настоящем изобретении описан способ получения твердой дисперсии с применением поливинилпирролидона в качестве носителя, и, наконец, полученная фармацевтическая композиция характеризуется надлежащими показателями растворения. Кроме того, стабильность и растворимость композиции могут хорошо сохраняться после длительного хранения.
Краткое описание графических материалов
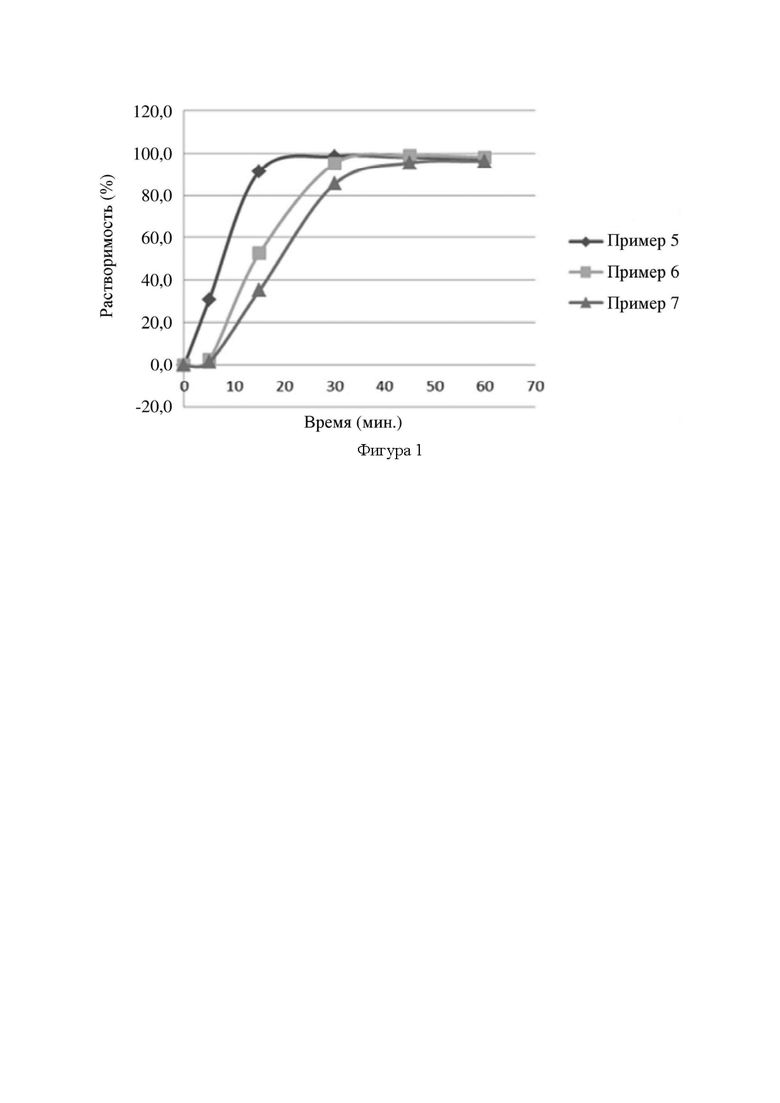
[0051] На фигуре 1 представлены профили растворения капсул из примеров 5-7.
Подробное описание варианта осуществления
[0052] Пример 1
[0053] Что касается испытаний в соответствии с Общими замечаниями Китайской фармакопеи 2010 г. (том II), избыток соединения, представленного формулой I, измельченного до состояния мелкого порошка, взвешивали, и переносили в определенное количество растворителя (25°C±2°C), и энергично встряхивали в течение 30 с каждые 5 мин. Растворение лекарственного средства наблюдали в течение 30 мин. Затем раствор фильтровали, первоначальный фильтрат удаляли и определяли концентрацию получаемого затем фильтрата. Рассчитывали растворимость.
Таблица 1. Растворимость соединения, представленного формулой I, в различных растворителях
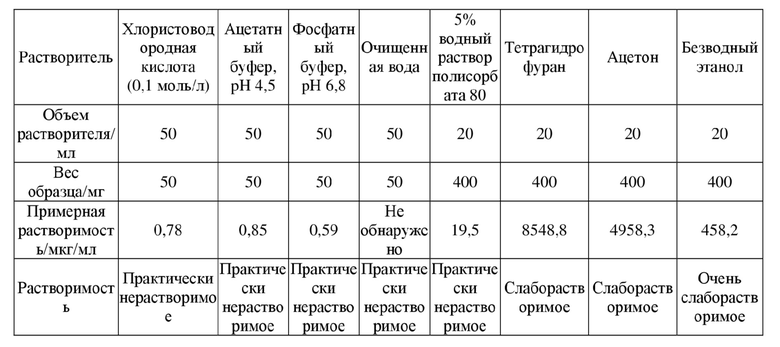
[0054] Как показывают результаты испытаний, соединение, представленное формулой I, является слаборастворимым в ацетоне и тетрагидрофуране, очень слаборастворимым в безводном этаноле и практически нерастворимым в традиционных водных растворителях, а солюбилизирующий эффект поверхностно-активного вещества на исходный материал был ограничен, поэтому получение составов традиционными способами не представляется возможным.
[0055] Примеры 2-3
Таблица 2. Компоненты твердой дисперсии
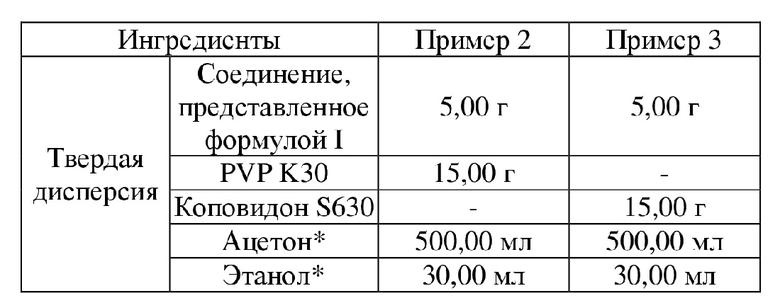
Примечание: *растворители удаляют в процессе производства.
[0056] Добавляли заданное количество коповидона S630 или PVPK30 и растворяли в этаноле. Добавляли заданное количество ацетона, смешивали и хорошо перемешивали. К вышеописанному раствору добавляли соединение, представленное формулой I. Раствор нагревали до 60°C и перемешивали до полного растворения соединения, представленного формулой I. После высушивания распылением раствора полученный порошок высушивали при 60°C с получением твердой дисперсии.
[0057] Пример 4
[0058] Исследовали физическую стабильность двух твердых дисперсий из примеров 2-3 при высокой температуре (40°C и 60°C) и влажности (25°C, RH 75±5%, 25°C, RH 90±5%), а также химическую стабильность в условиях ускоренного старения соответственно. Сравнивали внешний вид и изменения кристаллических форм двух твердых дисперсий на предметном стекле. Кроме того, определяли остаточные растворители в двух твердых дисперсиях.
[0059] Метод испытания для определения остаточных растворителей: газовая хроматография на капиллярной колонке DB-5 (30 м × 0,53 мм × 1,0 мкм) с пламенно-ионизационным детектором (FID) с использованием воды в качестве растворителя.
[0060] Методы испытания для определения содержания действующих веществ и общего содержания примесей (также представлены ниже): система для высокоэффективной жидкостной хроматографии с колонкой Phenomenex Luna C18 (4,6 мм × 200 мм, 5 мкм), подвижная фаза: раствор (0,02 моль/л) дигидрофосфата калия/ацетонитрил, при следующих длинах волн обнаружения: 254 нм и 200 нм.
Таблица 3. Испытания в стрессовых условиях
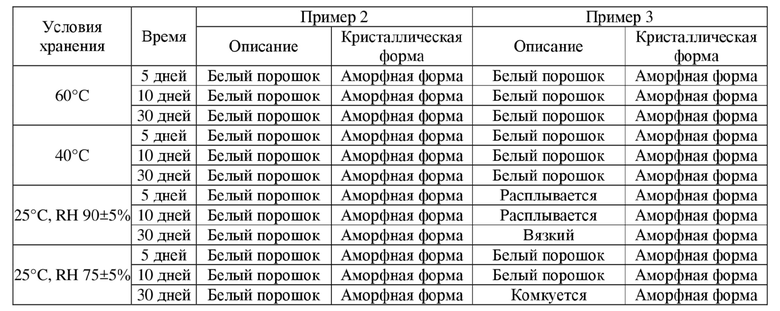
Таблица 4. Испытание для определения остаточных растворителей в твердых дисперсиях
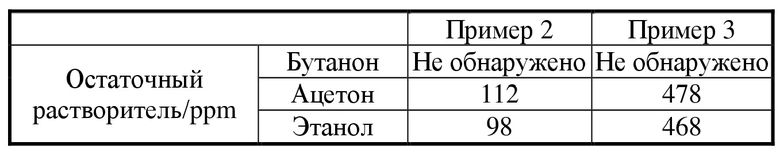
Таблица 5. Данные по испытаниям стабильности твердой дисперсии
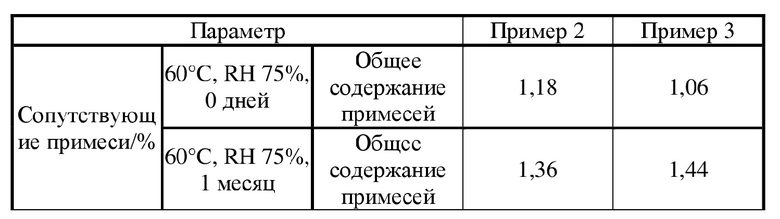
[0061] Твердая дисперсия, полученная с использованием коповидона, была более гигроскопичной, чем дисперсия, полученная с использованием PVP, и расплывалась через 5 дней, и становилась вязкой через 30 дней при RH 90±5%, при этом твердая дисперсия, полученная из PVP, была более стабильной по внешнему виду. Кроме того, твердая дисперсия, полученная из PVP, содержала меньшее количество остаточных растворителей. Через месяц испытаний в условиях ускоренного старения содержание примесей в твердой дисперсии, полученной с использованием PVP, выросло в меньшей мере, а содержание примесей в твердой дисперсии, полученной с использованием коповидона, выросло в большей мере.
[0062] Примеры 5-7
Таблица 6. Исходные и вспомогательные материалы для капсул различных дозировок
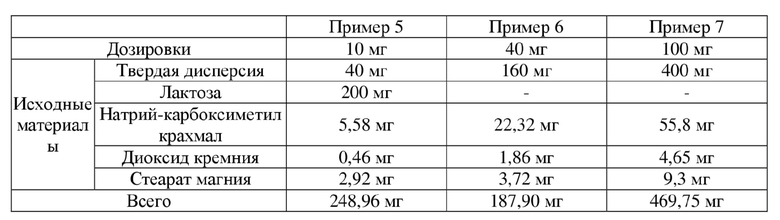
[0063] Твердую дисперсию из примера 2, содержащую соединение, представленное формулой I, лактозу (пример 5), натрий-карбоксиметилкрахмал, диоксид кремния с частью стеарата магния перемешивали надлежащим образом. Смесь помещали в сухой гранулятор для сухого гранулирования, хорошо перемешивали с оставшимся количеством стеарата магния после гранулирования и наполняли капсулы с получением капсул.
[0064] Пример 8.
[0065] Капсулы из примеров 5-7 подвергали испытанию на растворение в соответствии с методом 2 (лопастная мешалка) для определения растворимости, описанным в приложении к Китайской фармакопее 2015 г. (том II). Испытание на растворение для капсул из примеров 5, 6 и 7 проводили при скорости вращения лопастной мешалки 50 об/мин при 37±0,5°C с применением 1000 мл 0,5% водного раствора Tween в качестве среды растворения соответственно. Профили растворения представлены на фигуре 1. Результаты испытания на растворение показали, что все капсулы различной дозировки могут быть растворены быстро и полностью.
[0066] Пример 9
[0067] Образцы из примера 2 хранили в течение 12 месяцев в условиях долговременной стабильности (25°C/60% относительной влажности) и 6 месяцев в условиях ускоренного старения (40°C/75% относительной влажности) в упаковочном материале (в герметичных пакетах из фармацевтического полиэтилена низкой плотности, упакованных в пакет из алюминиевой фольги с осушителем) и периодически отбирали пробы для определения содержания действующих веществ, примесей, кажущейся растворимости (растворимость в 0,5% водном растворе полисорбата 80), а также кристаллизации. Результаты показаны в таблице ниже.
Таблица 7. Испытания стабильности образцов из примера 2 при различных условиях
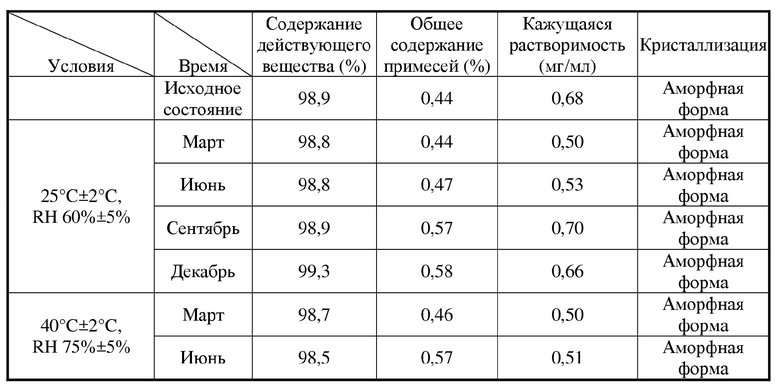
[0068] Как показано в результатах, твердая дисперсия, полученная с использованием PVP, оставалась стабильной после долговременного хранения, и растворимость может также сохраняться.
[0069] Пример 10
[0070] Капсулы из примера 7 помещали в листы из поливинилхлорида для фармацевтического применения в твердом виде и пакеты из алюминиевой фольги для упаковки фармацевтических средств, после термосваривания упаковывали в пакет из композитной пленки для упаковки фармацевтических средств, а затем помещали в картонную коробку после термосваривания. Периодически отбирали пробы после хранения при 40°C±2°C и RH 75%±5% в течение 6 месяцев и периодически отбирали пробы после хранения при 30°C±2°C и RH 65%±5% в течение 6 месяцев соответственно, для определения содержания действующих веществ, примесей и растворимости (через 45 мин, метод испытания на растворение такой же, что и в примере 8). Результаты показаны в таблице ниже.
Таблица 8. Испытания стабильности капсул из примера 7 при различных условиях
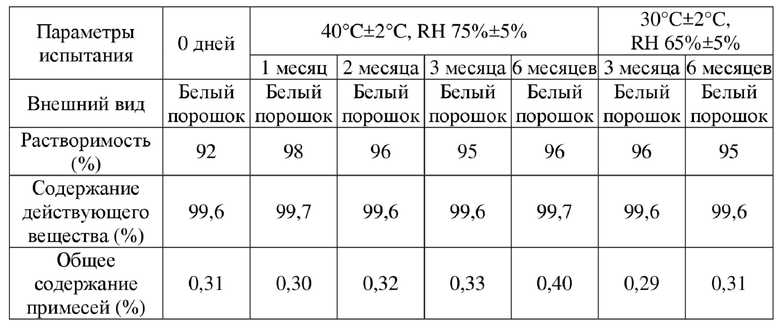
[0071] После испытаний стабильности образцов в условиях ускоренного старения и долговременного хранения при 40°C±2°C/RH 75%±5% и 30°C±2°C/RH 65±5% в течение 6 месяцев не наблюдалось никаких существенных изменений каждого из параметров, и стабильность была превосходной.
[0072] Хотя подробные варианты осуществления настоящего изобретения были описаны выше, специалисту в данной области техники будет понятно, что варианты осуществления являются всего лишь примерами, и в эти варианты осуществления можно вносить различные изменения или модификации без отступления от принципов и сути настоящего изобретения. Следовательно, объем защиты настоящего изобретения определяется прилагаемой формулой изобретения.
Твердая дисперсия для ингибиторов PARP, содержащая соединение, представленное формулой I, и материал-носитель, где материал-носитель предусматривает поливинилпирролидон. Фармацевтическая композиция, содержащая твердую дисперсию, наполнитель, разрыхлитель и смазывающее средство. Способ получения твердой дисперсии. Применение твердой дисперсии или фармацевтической композиции в изготовлении лекарственных средств, предназначенных для лечения видов рака. 5 н. и 5 з.п. ф-лы, 8 табл., 10 пр., 1 ил.
1. Твердая дисперсия для лечения рака молочной железы, рака яичника, рака поджелудочной железы или рака предстательной железы, содержащая соединение, представленное формулой I, и материал-носитель, где материал-носитель предусматривает поливинилпирролидон, где весовое соотношение соединения, представленного формулой I, и поливинилпирролидона составляет от 1:3 до 1:10, при этом доля поливинилпирролидона составляет более чем 70% в пересчете на общий вес твердой дисперсии,
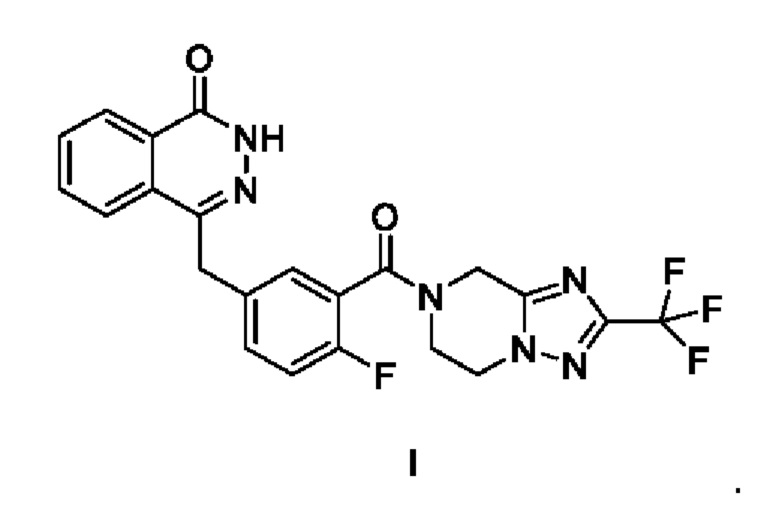
2. Твердая дисперсия по п. 1, где твердая дисперсия состоит из соединения, представленного формулой I, и материала-носителя поливинилпирролидона.
3. Твердая дисперсия по любому из пп. 1, 2, где весовое соотношение соединения, представленного формулой I, и поливинилпирролидона составляет от 1:3 до 1:7.
4. Твердая дисперсия по любому из пп. 1, 2, где весовое соотношение соединения, представленного формулой I, и поливинилпирролидона составляет от 1:3 до 1:5.
5. Твердая дисперсия по любому из пп. 1, 2, где весовое соотношение соединения, представленного формулой I, и поливинилпирролидона составляет 1:3.
6. Фармацевтическая композиция для лечения рака молочной железы, рака яичника, рака поджелудочной железы или рака предстательной железы, содержащая
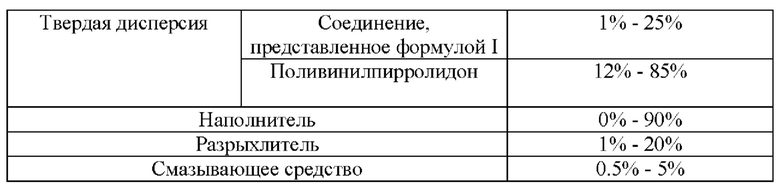
в пересчете на вес фармацевтической композиции, где наполнитель представляет собой лактозу; разрыхлитель представляет собой натрий-карбоксиметилкрахмал; смазывающее средство представляет собой стеарат магния и/или диоксид кремния.
7. Способ получения твердой дисперсии по любому из пп. 1-5, включающий способ (1), включающий стадию смешивания соединения, представленного формулой I, с поливинилпирролидоном и необязательным вспомогательным веществом в устройстве для экструзии расплава и стадию нагревания и перемешивания смеси и, наконец, экструдирования продукта в виде твердой дисперсии; или способ (2), включающий стадию смешивания соединения, представленного формулой I, с поливинилпирролидоном и растворителем и стадию удаления растворителя.
8. Способ по п. 7, где способ удаления растворителя выбран из одного или более из выпаривания на роторном испарителе, высушивания распылением, лиофилизации и пленочного испарения.
9. Способ получения фармацевтической композиции по п. 6, включающий стадию получения твердой дисперсии по п. 7 или 8 и стадию смешивания твердой дисперсии с одним или более наполнителем, разрыхлителем и смазывающим средством.
10. Применение твердой дисперсии по любому из пп. 1-5 или фармацевтической композиции по п. 6 в изготовлении лекарственного препарата, предназначенного для лечения рака молочной железы, рака яичника, рака поджелудочной железы или рака предстательной железы.
| CN 102372716 A, 2012.03.14 | |||
| CN 104434809 A, 2015.03.25 | |||
| БЕЗОПАСНАЯ РУКОЯТКА ДЛЯ ЛЕБЕДОК | 1930 |
|
SU20783A1 |
| US 9402909 B2, 2016.08.02 | |||
| US 9566277 B2, 2017.02.14. | |||
Авторы
Даты
2022-12-12—Публикация
2019-11-15—Подача