Изобретение относится к области ветеринарной медицины, а именно к способам лечения болезней бактериальной этиологии у животных.
Решение проблемы обеспечения населения продовольствием за счет собственных ресурсов, а именно эта задача поставлена Правительством Российской Федерации, зависит от надежного эпизоотического благополучия животных по инфекционным и незаразным болезням.
Одной из основных причин экономических потерь в животноводстве являются именно незаразные болезни бактериальной этиологии, так как они самые распространенные и способны снижать экономическую эффективность отрасли на 20-30%. Снижение экономической эффективности отрасли происходит из-за падежа, вынужденного убоя, снижения прироста живой массы, уменьшения продуктивности и снижения племенных качеств животных, а также затрат на лечебно-профилактические мероприятия. Поэтому поиск эффективных средств и способов защиты животных от болезней бактериальной этиологии является актуальным и перспективным направлением.
Известен способ лечения инфекций бактериальной этиологии у животных путем использования препарата на основе амоксициллина, а именно препарата Ремокс 500 (см. Инструкцию по применению Ремокса 500 для лечения свиней и сельскохозяйственных птиц при болезнях бактериальной этиологии, утверждена 03.12.2014).
Ремокс 500 содержит действующее вещество - амоксициллина тригидрат и вспомогательные вещества: натрий дегидроген фосфат безводный, натрий гексаметафосфат, кремний коллоидный безводный, натрий карбонат безводный.
Препарат применяют с лечебной целью свиньям и с лечебно-профилактической целью сельскохозяйственной птице при колибактериозе, сальмонеллезе, других бактериальных инфекциях желудочно-кишечного и респираторного тракта, вызванных чувствительными к амоксициллину возбудителями. Ремокс 500 свиньям применяют индивидуально или групповым способом перорально с питьевой водой или заменителем цельного молока. Птицам препарат применяют перорально с питьевой водой. Производитель препарата - "Industrial Veterinaria, S.A. "INVESA", Испания.
Известен также способ лечения инфекций бактериальной этиологии у животных путем использования препарата на основе амоксициллина-Амоксиклава. Амоксиклав представляет собой комбинацию амоксициллина и клавулановой кислоты (см. Инструкцию по применению Амоксиклава 62,5 водорастворимого порошка при болезнях бактериальной этиологии свиней и сельскохозяйственных птиц, утверждена 30.03.2016)
Порошок для орального применения Амоксиклав содержит амоксициллин в форме тригидрата и клавулановую кислоту в форме клавуланата калия и вспомогательные вещества: кремния диоксид коллоидный, кросповидон, кроскармеллоза натрия, стеарат магния, тальк, микрокристаллическая целлюлоза.
Объединение амоксициллина и клавулановой кислоты в один препарат дает возможность им работать синергически для лечения различных бактериальных инфекций в ветеринарной медицине, многие из которых в противном случае были бы устойчивы к одному амоксициллину. Перед применением готовят водный раствор препарата. С лечебно-профилактической и лечебной целью птице препарат применяют перорально с питьевой водой. Свиньям Амоксиклав применяют с лечебно-профилактической и лечебной целью перорально с водой, молоком или кормом.
Способ обладает хорошей эффективностью для терапии различных инфекций бактериального происхождения.
Данный способ является наиболее близким заявленному, однако препарат Амоксиклав также принадлежит иностранной компании, а именно компании «Сандоз д.д.», Словения.
Задачей изобретения является расширение ассортимента эффективных противобактериальных средств, т.е. создание отечественного противобактериального средства, и на его основе - разработка эффективного способа лечения болезней бактериальной этиологии у различных видов животных.
Поставленная задача решается тем, что, согласно изобретению, в способе лечения болезней бактериальной этиологии у животных, включающем введение препарата на основе амоксициллина тригидрата, животным вводят препарат, содержащий, в мг/г: амоксициллина тригидрат - 570,0-580,0, янтарную кислоту - 2,0-8,0, карбонат натрия - 100,0-300,0, аэросил - 2,0-8,0 и лактозу - до 1 г, при этом препарат животным вводят перорально с кормом или с водой для поения в дозе 17,5-35,0 мг/кг живой массы в течение 3-5 суток.
Поставленная задача решается также тем, что в качестве животных используют сельскохозяйственную птицу или свиней, и тем, что препарат вводят групповым способом или индивидуально.
Техническим результатом, полученным в результате реализации заявленного изобретения, является то, что заявленный способ позволяет эффективно лечить широкий спектр болезней бактериальной этиологии у животных, а используемый в данном способе препарат обладает широким спектром бактерицидной активности против большинства грамположительных и грамотрицательных микроорганизмов, включая антибиотикорезистентные, способные образовывать защитные биопленки штаммы, не обладает аллергенными свойствами, оказывает стимулирующее влияние на показатели гуморального иммунного ответа и стабилен при хранении.
Изобретение иллюстрируется следующими примерами, которые, однако, не ограничивают объем притязаний заявителя.
Пример 1. Заявленный препарат получают следующим образом:
В подготовленный контейнер для смешивания загружают 0,574 кг амоксициллина тригидрата, 0,005 кг янтарной кислоты, 0,2 кг карбоната натрия, 0,005 кг аэросила и 0,216 кг лактозы. Процесс смешивания осуществляют в течение 25 минут при скорости вращения 500 об/мин. Полученный препарат просеивают и измельчают.
Полученный порошок содержит, в мг/г: амоксициллина тригидрат - 574,0, янтарную кислоту - 5,0, карбонат натрия - 200,0, аэросил - 5,0 мг, лактозу - 216,0.
Механизм действия амоксициллина тригидрата заключается в подавлении функциональной активности бактериальных ферментов транспептидаз, локализующихся на цитоплазматической мембране микробной клетки. Связываясь с транспептидазами, амоксициллин ингибирует синтез муреина, основного материала для клеточной стенки бактерий. В результате осмотический баланс микробной клетки нарушается, внешняя оболочка становится менее стабильной и происходит лизис бактерий.
Янтарная кислота увеличивает чувствительность микроорганизмов к амоксициллину за счет увеличения проницаемости мембран бактериальных клеток. Янтарная кислота стимулирует разрушение бактериальных биопленок в организме животных, что увеличивает площадь контакта амоксициллина с бактериальными клетками. Кроме того, как показали исследования, янтарная кислота повышает стабильность полученного порошка при хранении.
Таким образом, комбинация амоксициллина тригидрата и янтарной кислоты, входящих в состав препарата, обладает широким спектром бактерицидной активности против большинства грамположительных и грамотрицательных микроорганизмов, включая антибиотикорезистентные, которые способны образовывать защитные биопленки.
Введение не описанного ранее в составах амоксициллина стабилизатора янтарной кислоты, а также нового соотношения вспомогательных веществ: карбоната натрия, аэросила и лактозы - обеспечивает стабильность заявленного фармацевтического состава в виде порошка в течение не менее трех лет, а также улучшает его технологические свойства при изготовлении.
Кроме того, янтарная кислота, как эндогенный метаболит, кроме стабилизации состава, участвует в энергетическом метаболизме клеточных мембран, повышает содержание восстановленного глутатиона - показателя антиоксидантной системы.
Далее во всех примерах выполнения заявленного изобретения использовали препарат, полученный по примеру 1, который содержит средние значения указанных в формуле изобретения ингредиентов. Препарат, содержащий ингредиенты в количестве ниже минимальных, указанных в формуле изобретения, в проведенных исследованиях показал сниженную эффективность при лечении болезней бактериальной этиологии, а при содержании ингредиентов в количестве выше максимальных, указанных в формуле изобретения - у препарата появляются побочные эффекты. Также у препаратов с количественным содержанием ингредиентов ниже или выше указанных в формуле изобретения, снижается стабильность при хранении.
Пример 2. Клиническая эффективность заявленного способа при заболеваниях бактериальной этиологии у сельскохозяйственных птиц.
Для проведения исследования отобрали клинически здоровую птицу, которая ранее в опытах не использовалась. Целевой вид: сельскохозяйственная птица, цыплята-бройлеры, кросс Кобб, возраст на начало эксперимента - 10 суток, масса тела - 165-180 г.
В суточном возрасте птица была провакцинирована против болезни Марека, инфекционного бронхита кур и Ньюкаслской болезни для предотвращения возможной контаминации вирусами в условиях вивария. Иммунизация инактивированными вакцинами не вызывает иммунодепрессии, что позволяет исключить влияние дополнительных негативных факторов на чистоту проведения эксперимента, и, соответственно, результаты исследований.
Птицу содержали клеточным способом в секциях по 15 голов. В помещении, где содержалась экспериментальная птица, параметры микроклимата соответствовали зоотехническим требованиям и нормам. Кормили цыплят полнорационным комбикормом, который не содержал антибиотиков. Доступ цыплят к корму и воде был постоянный.
Птица до начала исследования не получала антибактериальных препаратов и других лекарственных средств.
Формирование опытных и контрольной групп цыплят осуществляли по принципу аналогов, с учетом массы тела, кросса и возраста животных.
После недельного карантина птицу опытных и контрольной групп проверили на микробоносительство бактериальных культур Escherichia coli, Staphylococcus spp., Pseudomonas aeruginosa, Salmonella enteritidis и M. gallisepticum.
Для прижизненной диагностики бактериальных инфекций использовали классические микробиологические методы.
Было установлено, что цыплята не являются носителями Salmonella spp, Pseudomonas aeruginosa, M. gallisepticum, не содержат патогенных кишечных палочек и стафилококков выше допустимых количеств.
Затем цыплятам опытных и контрольной групп ввели перорально через желудочный зонд суточную бульонную культуру музейных штаммов: Salmonella spp. в дозе 1 млрд. микробных клеток на голову.
Для подтверждения процесса заражения, на вторые сутки после него отобрали пробы помета, а также исследовали внутренние органы с целью выделения из них возбудителя инфекции.
Факт заражения птицы подтверждали комплексно по наличию клинических признаков, выделения чистой культуры возбудителя и ее идентификации по культурально-морфологическим, биохимическим и серологическим признакам.
Перед началом лечения - на 1-ые сутки терапии - и по его окончании - на 5-ые сутки терапии - у птицы отбирали пробы крови для биохимического и морфологического исследования.
Исследование морфологического состава периферической крови включало подсчет количества эритроцитов и лейкоцитов, определение концентрации гемоглобина.
Температуру и клинические признаки контролировали два раза в день у птицы всех групп.
Критериями постановки диагноза являлись: клинические признаки, характерные для данного заболевания, бактериологическое подтверждение наличия возбудителя заболевания, результаты гематологических исследований.
Лечение назначали после появления характерной клинической картины и выявления возбудителя, которые регистрировали на третьи сутки после заражения.
В ходе исследований на третьи сутки после заражения, у цыплят отмечали клиническую картину кишечной инфекции: большинство цыплят-бройлеров находились в угнетенном состоянии, некоторые птицы большую часть времени проводили в стоячем или лежачем положении, были сильно ослаблены, наблюдалась потеря аппетита, жажда, диарея, перья у больных особей были взъерошены, тусклые, в области клоаки перья были сильно загрязнены фекалиями жидкой пенистой консистенции, светло-коричневого или желтоватого цвета с примесью слизи и крови и имели зловонный запах.
Далее все работы проводили на экспериментально зараженной птице. В течение всего периода эксперимента проводили наблюдения за общим состоянием и поведением птицы, потреблением корма и воды, реакцией на раздражители - звук, свет, проявлением симптомов заболевания и их угасанием, возможной гибелью.
Заявленный препарат применяли групповым способом с водой для поения в течение 3-5 суток в суточной дозе 17,5-35,0 мг/кг массы животного. Контрольной группе применяли препарат сравнения Амоксиклав 62,5% порошок, групповым способом с водой для поения в дозе 40 мг/кг массы животного согласно инструкции по его применению (см. табл. 1)
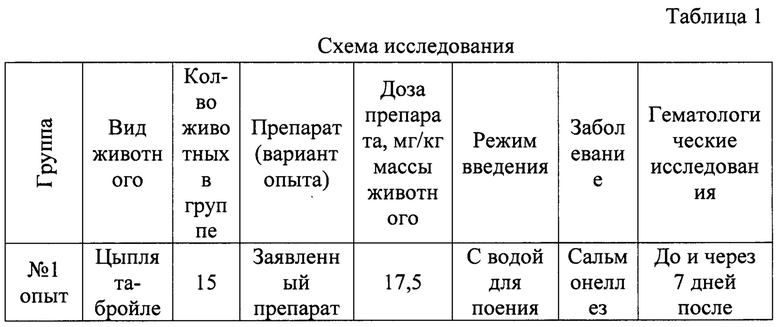
Критериями оценки эффективности заявленного способа являются: ослабление, а затем и исчезновение клинических признаков заболевания, нормализация гематологических показателей крови, отсутствие в биоматериале возбудителя заболевания.
Критериями оценки безопасности заявленного препарата являются: отсутствие побочного действия, осложнений, нежелательных явлений, аллергических реакций во время и после применения препарата.
Статистическую обработку полученных результатов по динамике прироста массы тела, изменений гематологических и биохимических показателей сыворотки крови проводили по стандартным процедурам с использованием критерия Стьюдента.
На вторые сутки с начала выпойки лекарственного препарата регистрировали положительную динамику у птиц опытных и контрольной групп. Так, у большего количества цыплят появился аппетит, они стали более активными и подвижными. К концу третьих суток регистрировали нормализацию работы желудочно-кишечного тракта - диарея исчезла, помет нормальной консистенции, без патологических примесей. К концу четвертых суток отмечали клиническое выздоровление всей птицы опытных групп.
Исследование морфологической картины крови после проведенного лечения выявило статистически достоверное снижение уровня лейкоцитов относительно первоначальных значений в опыте и контроле. Лейкоформула не претерпела значительных изменений после терапии, ее показатели находились в пределах нормы.
Исследования показали, что заявленный препарат при пероральном применении хорошо и быстро всасывается в желудочно-кишечном тракте и, поступая в кровь, проникает во все органы и ткани организма. Биодоступность препарата составляет 80%. Максимальная концентрация в сыворотке крови достигается через 2 часа после введения и находится на терапевтическом уровне в течение суток. Препарат выводится из организма в неизмененном виде, преимущественно с мочой и фекалиями.
Повторное бактериологическое исследование помета на 5-ые сутки терапии в опытных и контрольной группах, не подтвердило наличия патогенных микроорганизмов. Так, при повторном микробиологическом анализе помета регистрировали отсутствие роста Salmonella enteritidis на ксилоза-лизин-деоксихолатный агаре.
Таким образом, результаты микробиологического исследования подтверждают, что заявленный препарат позволяет в течение трех дней терапии нормализовать микрофлору кишечника птицы при бактериальной кишечной инфекции. Препарат проявляет 100%-ный клинический эффект в отношении патогенов Salmonella enteritidis.
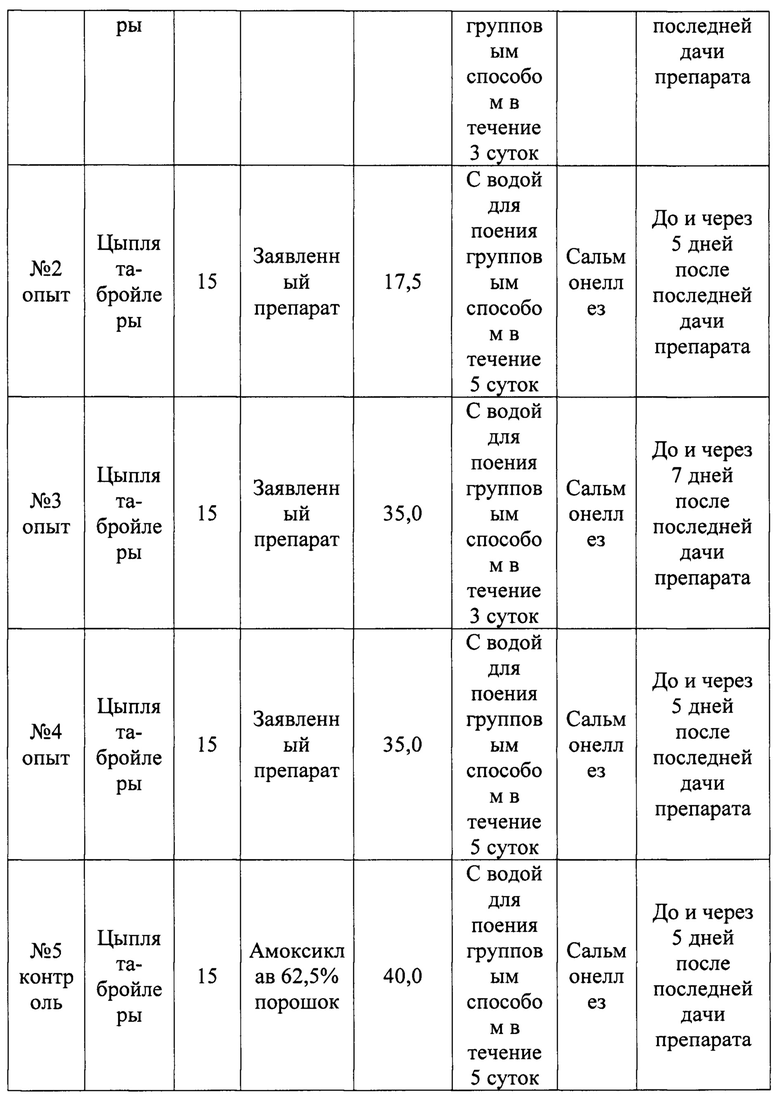
Динамика прироста массы тела не выявила достоверных различий между группами цыплят, однако не соответствовала породным критериям для данного кросса птицы и была значительно ниже требуемых параметров, но у цыплят опытных групп была несколько выше, чем у цыплят контрольной группы (см. табл. 2).
Сохранность цыплят при применении заявленного препарата составила 100%.
Таким образом, в результате проведенных исследований установлено, что заявленный способ, при введении препарата перорально в форме раствора с водой для поения в дозе 17,5 мг/кг и 35,0 мг/кг групповым способом в течение 3-5 дней, способствует полному выздоровлению цыплят-бройлеров при желудочно-кишечных заболеваниях бактериальной этиологии, вызываемых Salmonella spp., т.е. обеспечивает 100% клинический эффект при экспериментальном сальмонеллезе.
Заявленный препарат не оказывает отрицательного и побочного действий на организм цыплят-бройлеров при применении в исследуемых дозах, т.к. нежелательные реакции, осложнения, аллергические реакции со стороны цыплят-бройлеров во время и после применения препарата отсутствовали.
Полученные результаты позволяют сделать вывод о том, что заявленный препарат по своей эффективности не уступает препарату сравнения, и поэтому заявленный способ может быть использован в комплексных лечебно-профилактических и оздоровительных мероприятиях при сальмонеллезе у цыплят-бройлеров.
Пример 3. Терапевтическая эффективность заявленного способа при заболеваниях бактериальной этиологии у свиней.
В опыте использовали свинок и хрячков породы крупная белая двухмесячного возраста с массой тела 14-20 кг.
Экспериментальных животных содержали в одинаковых условиях в клетках по 10 голов. Корма и вода были безопасными для здоровья целевых животных, обеспечивали потребности целевых животных в питательных веществах и не влияли на результаты исследования.
Животных включали в эксперимент, если:
- подтвержден диагноз;
- животным не применяли какие-либо лекарственные препараты, влияющие на результаты эксперимента, не менее чем за месяц до его начала.
В ходе проведения диспансерного обследования поросят были выявлены животные со схожими клиническими признаками заболевания желудочно-кишечного тракта: общее угнетение, диарея, фекалии светло-коричневой окраски, мышечная слабость, иногда судороги, анорексия, в некоторых случаях акроцианоз, у большинства животных наблюдались признаки обезвоживания организма. Больные животные отставали в росте и развитии от здоровых поросят данного возраста.
С целью лабораторного подтверждения диагноза отобрали у животных образцы кала из прямой кишки. Лабораторные исследования биоматериала проводили по общепринятым методикам.
Микроскопия бактериальных мазков с окраской по методу Грама позволила определить следующие морфологические признаки выделенных бактерий: грамотрицательные палочки, одиночно расположенные, среднего размера, короткие, биполярно окрашенные, подвижные - Escherichia coli
При постановке реакции агглютинации с видоспецифической сывороткой было определено, что Escherichia coli относится к серогруппе O-8 - к энтеропатогенной группе кишечной палочки, вызывающей патологический процесс при ослаблении защитных сил организма.
Критериями постановки диагноза являлись: клинические признаки, характерные для данного заболевания, бактериологическое подтверждение наличия возбудителя заболевания, результаты гематологических исследований.
Контроль состояния животных осуществляли на протяжении всего опыта. В этот период проводили ежедневное наблюдение за поведением и состоянием животных, потреблением корма и воды, оценивали клинический статус - температура, учет симптомов заболевания, время наступления положительной динамики и срок выздоровления.
После подтверждения диагноза перед введением препарата брали кровь у животных опытных и контрольной групп для определения гематологических показателей. При исследовании крови на гематологические показатели учитывали количество эритроцитов, лейкоцитов, эозинофилов, базофилов, лимфоцитов, моноцитов, тромбоцитов, гемоглобин, скорость оседания эритроцитов - СОЭ.
При проведении общего анализа крови у больных поросят наблюдали повышение концентрации гемоглобина, числа эритроцитов, гематокритной величины и лейкоцитов, что указывает на сгущение крови вследствие развития диарейного синдрома. Повышение же концентрации лейкоцитов является следствием воспалительного процесса в желудочно-кишечном тракте и интоксикации организма продуктами метаболизма условно-патогенной флоры кишечника.
Схема исследования приведена в таблице 3.
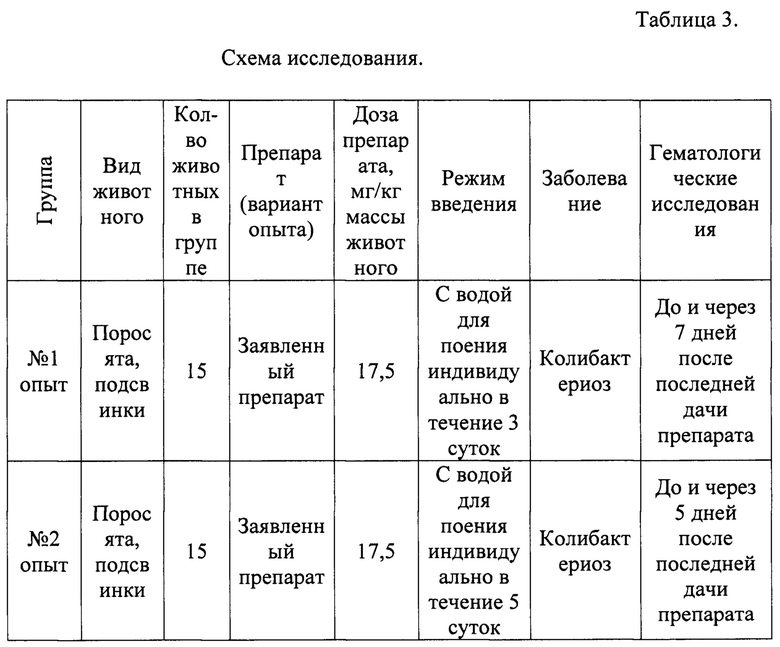

После проведенного лечения эффективность заявленного способа устанавливали по клиническим признакам и по результатам бактериологического исследования смыва кишечника. Смывы сделали через 5 дней после завершения лечения у животных. Через 5 дней после начала лечения у тех же животных повторно проводили анализ крови на гематологические показатели.
Критериями оценки эффективности заявленного способа являются: ослабление, а затем исчезновение клинических признаков заболевания, нормализация гематологических и биохимических показателей крови, отсутствие в биоматериале возбудителя заболевания.
Критериями оценки безопасности заявленного препарата являются: отсутствие побочного действия, осложнений, нежелательных явлений, аллергических реакций во время и после применения препарата.
В результате проведенных исследований установлена 100%-ая эффективность заявленного препарата при лечении колибактериоза свиней. У животных на 2-ой день после выпаивания препарата наблюдалось улучшение общего состояния, прекращение поноса, повышение аппетита. На 3-ий день общие физиологические показатели приближались к уровню нормы. Полное выздоровление животных всех групп наступало через 3-4 дня с момента назначения препаратов. Побочных действий препаратов на организм животных отмечено не было. При бактериальных посевах токсигенные штаммы кишечной палочки выявлены не были.
Вместе с этим через 10-ть дней после начала эксперимента отмечается положительная динамика общего анализа крови всех групп подопытных поросят. Отмечается снижение лейкоцитов, эритроцитов и гемоглобина, восстановление гематокритной величины до физиологических значений, что указывает на купирование воспалительной реакции и снятия интоксикации продуктами бактериальными метаболизма, а также на регидратацию организма подопытных поросят.
Полученные данные позволяют сделать вывод о том, что заявленный способ при введении препарата перорально как с питьевой водой, так и с кормом, в дозах 17,7 мг/кг и 35,0 мг/кг массы тела индивидуально или групповым способом, является эффективным при лечении желудочно-кишечных заболеваний поросят бактериальной этиологии. Установлено, что эффективность применения заявленного способа при колибактериозе поросят составляет 100%. Выздоровление поросят, больных колибактериозом, происходило в среднем на 3-4 сутки проведения терапевтических мероприятий. Клинические исследования, проведенные в течение опыта, показывают, что заявленный препарат не оказывает отрицательного и побочного действия на организм поросят при применении в рекомендуемой терапевтической дозе, Нежелательные реакции, осложнения, аллергические реакции со стороны поросят во время и после применения препарата отсутствуют. Таким образом, полученные результаты подтверждают, что заявленный способ обладает высокой активностью против патогенных бактерий кишечной группы, а заявленный препарат не уступает по своему действию препарату сравнения, и поэтому может быть использован в комплексных лечебно-профилактических и оздоровительных мероприятиях при желудочно-кишечных заболеваниях свиней бактериальной этиологии, вызванных Е. coli.
Пример 4. Эффективность заявленного способа при респираторных заболеваниях бактериальной этиологии у свиней.
В опыте использовали свинок и хрячков породы Дюрок четырехмесячного возраста с массой тела 38-42 кг
Животных не подвергали лекарственному воздействию не менее одного месяца до начала проведения эксперимента.
Экспериментальных животных содержали по 10 голов в одинаковых условиях, оптимальных для данного вида. Корма и вода были безопасными для здоровья целевых животных, обеспечивали потребности целевых животных в питательных веществах и не влияли на результаты исследования.
Диагностику заболевания осуществляли комплексно: учитывали анамнез, эпизоотологические и клинические данные, соответствующие респираторным заболеваниям: кашель, тахипное, одышка смешанного типа, истечения из носовых ходов, мелко- и средне пузырчатые хрипы, жесткое везикулярное дыхание. Также учитывали результаты гематологических исследований и бактериологического исследования смывов из носовых ходов на наличие патогенной микрофлоры дыхательных путей.
Пробы биоматериала отбирали до введения лекарственных препаратов и на 5-е или 7-е сутки после последнего введения препаратов в зависимости от группы животных.
В ходе проведения диспансерного обследования поросят экспериментального хозяйства были выявлены животные со схожими клиническими признаками респираторных заболеваний: общее угнетение, потеря аппетита, животные худели, отмечался громкий кашель, хрипы, серозное истечение из носовых ходов. У животных наблюдалось напряженное дыхание, смешанная одышка, серозно-катаральное или катаральное истечения из носовых отверстий, выделение во время кашля катарального экссудата. При аускультации в легких диагномтировали жесткое везикулярное дыхание, влажные мелкопузырчатые хрипы.
При проведении общего анализа крови у больных поросят диагностировали снижение концентрации гемоглобина, числа эритроцитов, гематокритной величины и достоверное увеличение лейкоцитов в основном за счет гранулоцитарных клеток, что указывает на прогрессирующую нормоцитарную анемию. Кроме того, лейкоцитоз является следствием воспалительного процесса в слизистой оболочки дыхательных путей и интоксикации организма продуктами метаболизма условно-патогенной флоры дыхательных путей.
Для постановки диагноза также важно было дифференцировать заболевания друг от друга с помощью бактериологических исследований биоматериала и патматериала в условиях лаборатории.
Проведенные исследования показали, что возбудителями инфекции являются Escherichia coli и Pseudomonas aeruginosa.
В опытные и контрольную группы отбирали животных по принципу аналогов с явными клиническими признаками респираторных заболеваний и положительным результатом бактериологических исследований смывов из носовых ходов и зева.
Сформировали 5 опытных и 1 контрольную группы свиней по 15 животных в каждой.
После подтверждения диагноза перед введением препаратов брали кровь у животных опытных и контрольной групп для определения гематологических показателей.
Контроль состояния животных осуществляли ежедневно на протяжении всего опыта, он включал наблюдение за поведением и состоянием животных, потреблением корма и воды, оценку клинического статуса, время наступления положительной динамики и срок выздоровления.
Схема введения заявленного препарата и препарата сравнения Амоксиклав указана в таблице 4.
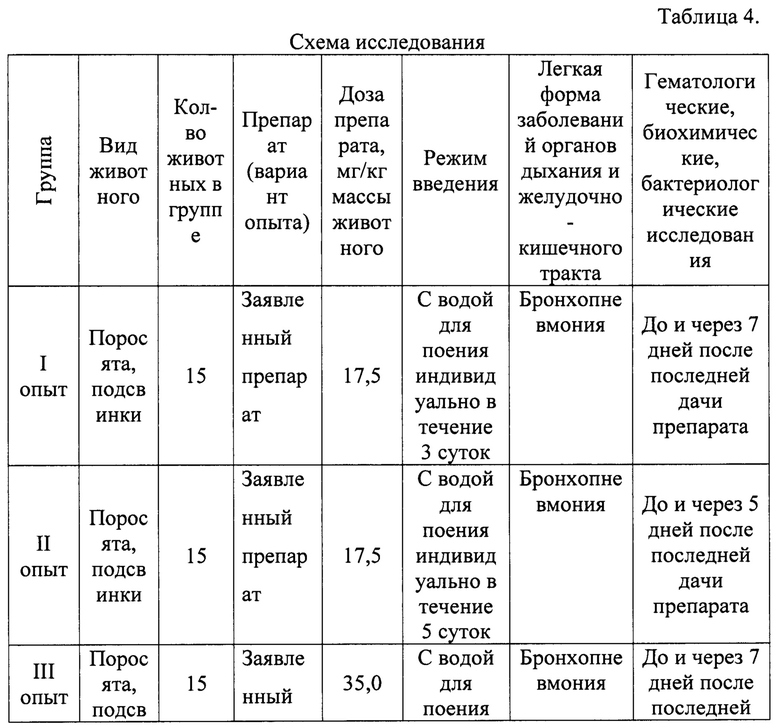
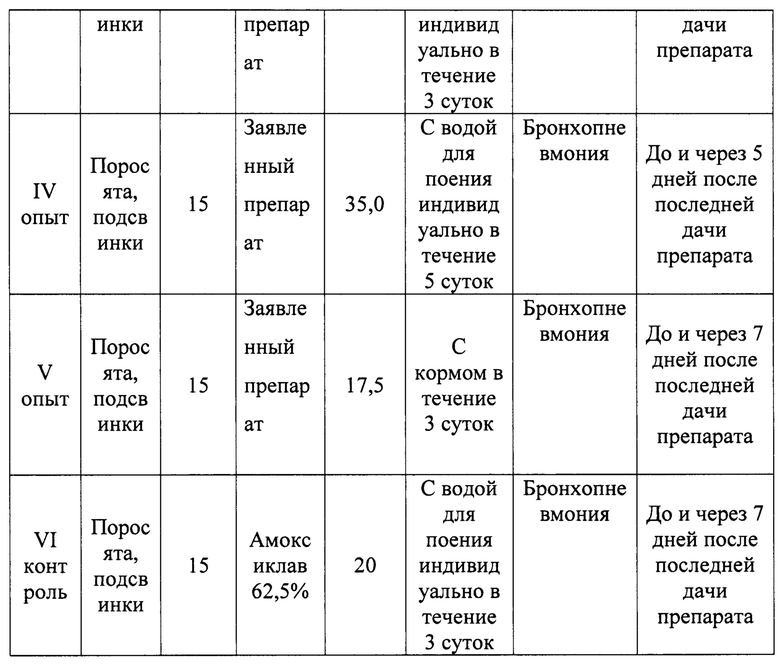
Критериями оценки эффективности заявленного способа являются: ослабление, а затем исчезновение клинических признаков заболевания, нормализация гематологических и биохимических показателей крови, отсутствие в биоматериале возбудителей заболевания.
Критериями оценки безопасности препарата являются: отсутствие побочного действия, осложнений, нежелательных явлений, аллергических реакций во время и после применения препарата.
В результате проведенных исследований установлена 100% эффективность заявленного способа при лечении респираторных заболеваний смешанной бактериальной этиологии у поросят. У животных на 3-ий день после выпаивания препарата наблюдалось улучшение общего состояния и повышение аппетита. На 5-ый день общие физиологические показатели приближались к норме. Полное выздоровление наступило через 7 дней. Побочных действий препарата на организм животных не отмечено. При бактериальных посевах из носовых ходов болезнетворной микрофлоры не выявлено
Вместе с этим на 10-ые сутки после начала эксперимента была отмечена положительная динамика общего анализа крови всех групп подопытных поросят. Отмечено снижение лейкоцитов, повышение эритроцитов и гемоглобина и гематокритной величины до физиологических значений, что указывает на нормализацию гемопоэза в организме поросят.
На основании полученных данных можно сделать вывод о том, что заявленный способ при пероральном введении препарата, как с питьевой водой, так и с кормом, в дозах 17,7 мг/кг и 35 мг/кг массы тела, как индивидуально, так и групповым способом, является эффективным средством при респираторных заболеваниях поросят бактериальной этиологии. Установлено, что эффективность применения заявленного препарата при бронхопневмонии поросят составляет 100%. Поросята, больные бронхопневмонией, выздоравливали в среднем на 3-4 сутки проведения терапевтических мероприятий. Заявленный препарат не оказывает отрицательного и побочного действий на организм поросят при применении в рекомендуемой терапевтической дозе. Нежелательные реакции, осложнения, аллергические реакции со стороны поросят во время и после применения препарата отсутствовали. Полученные результаты позволяют сделать вывод о том, что заявленный препарат не уступает по своей эффективности препарату сравнения, и поэтому может быть использован в комплексных лечебно-профилактических и оздоровительных мероприятиях в качестве средства с высокой активностью при респираторных заболеваниях поросят бактериальной этиологии, вызываемых Escherichia coli и Pseudomonas aeruginosa.
Пример 5. Эффективность заявленного способа при заболеваниях бактериальной этиологии у свиней.
Изучение эффективности заявленного способа проведено на 90 гибридных поросятах породы крупная белая-ландрас-дюрок группы доращивания 30-35 дневного возраста.
До начала лечения симптомы респираторных и желудочно-кишечных заболеваний, а именно снижение аппетита, двигательной активности, кашель, истечения из носовых отверстий, опухание суставов, повышение температуры тела, диарея, выявлены у всех 90 отобранных для исследований поросят.
При гематологическом исследовании крови у всех поросят диагностировали лимфоцитоз, эозинопению, умеренный моноцитоз, снижение гематокрита, эритроцитопению, гемоглобинемию, увеличение средней концентрации гемоглобина в эритроцитах, тромбоцитопению, ускорение СОЭ.
Также у всех поросят наблюдали симптомы поражения дыхательного тракта - апатичность, снижение аппетита и двигательной активности, повышение температуры тела, кашель, чихание, истечения из носовых отверстий, признаки поражения желудочно-кишечного тракта - диарея, у некоторых - опухание суставов.
Смывы со слизистой оболочки носа и слизистой прямой кишки от поросят опытных и контрольной групп получали индивидуально до начала опытов и через 5 суток после завершения лечения.
После клинического осмотра поросят и проведения бактериологического и молекулярно-биологического (ПЦР) исследования, по принципу аналогов сформировали пять опытных и одну контрольную группу поросят соответственно по 15 голов в каждой.
Поросят опытных групп содержали отдельно в специальных станках, поросят контрольной группы - в обособленном станке сектора.
Помещения, предназначенные для клинического исследования, соответствовали необходимым требованиям и были обеспечены необходимыми температурными и влажностными режимами.
Для кормления и ухода за животными использовали комбикорма, оборудование и инвентарь, которые хранились изолированно от мест содержания целевых животных. Рацион животных соответствовал установленным нормам для молодняка свиней соответствующего возраста, доступ к питьевой воде - без ограничения.
Заявленный препарат вводили животным с учетом клинических признаков, а также с учетом видов выделенных по результатам бактериологического и молекулярно-биологического исследований возбудителей инфекции. Схема исследований указана в таблице 5.

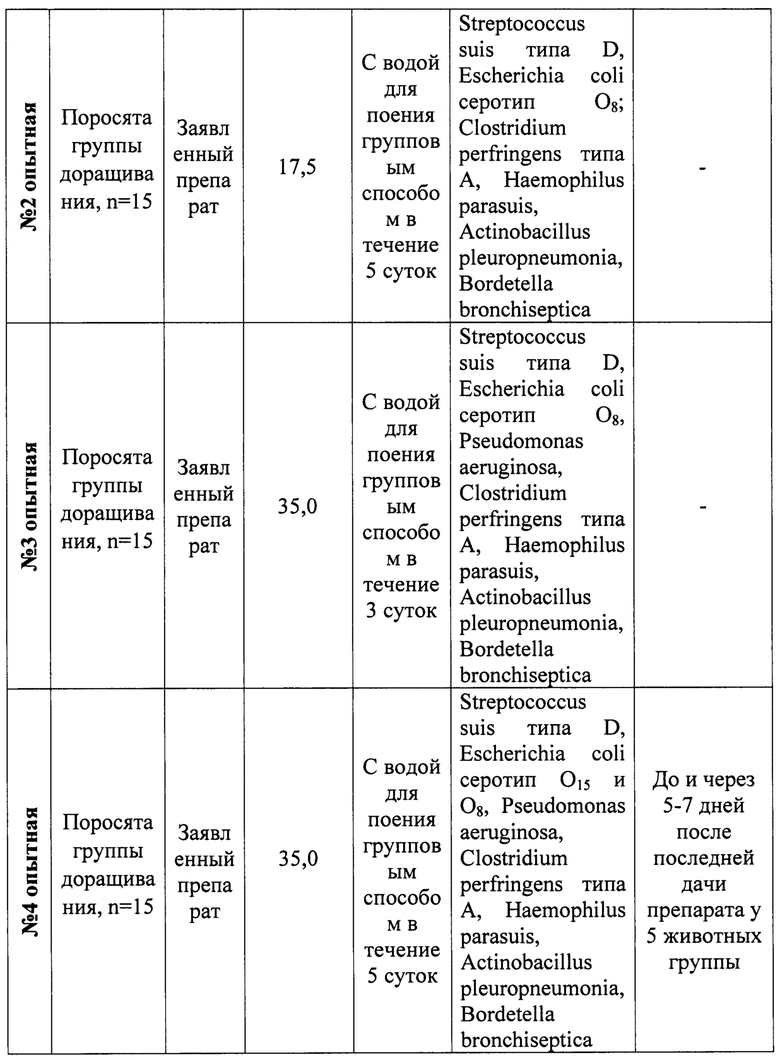

Эффективность лечения заявленным и препаратом сравнения оценивали по динамике клинического статуса, регрессии и отсутствию симптомов респираторных и желудочно-кишечных заболеваний у поросят, по результатам бактериологических и ПЦР исследований через 5 суток после завершения курса применения препарата.
Эффективность заявленного препарата сравнивали с эффективностью препарата сравнения Ремокс 500.
Проводили сравнение результатов клинического, бактериологического и молекулярно-биологического исследований животных опытных и контрольной групп до применения препарата и по окончании курсов терапии. Клинический статус животных оценивали по наличию или отсутствию клинических признаков поражения респираторного и желудочно-кишечного тракта в дни 0 и спустя 5 суток после завершения курсов дачи препарата, а также в процессе лечения.
Гематологические исследования поросят опытных и контрольной групп повторно проводили через 5 суток после завершения курсов лечения заявленным препаратом и Ремокс 500.
Результаты бактериологических и молекулярно-биологических исследований материала от поросят опытных и контрольной групп после лечения показали отсутствие патогенных бактерий в смывах со слизистой носовой полости и слизистой прямой кишки. При гематологическом скрининге установлена нормализация основных гематологических показателей.
Клинический осмотр поросят опытных и контрольной групп после курсов терапии показал нормализацию общего состояния, аппетита и двигательной активности, отсутствие кашля, носовых истечений, диареи и других симптомов расстройства органов дыхания и желудочно-кишечного тракта, а также постепенное увеличение среднесуточных привесов. Динамика клинического статуса животных опытных и контрольной групп в период наблюдения не отличалась.
Таким образом, на основании проведенного клинического исследования терапевтической эффективности заявленного способа при заболеваниях бактериальной этиологии у свиней установлено следующее:
- применение препарата групповым способом с водой для поения или с кормом в течение 3 суток в разовой суточной дозе 17,5 мг/кг живой массы, высокоэффективно при легкой форме заболеваний органов дыхания и желудочно-кишечного тракта свиней бактериальной этиологии;
- применение препарата групповым способом с водой для поения в течение 5 суток в разовой суточной дозе 17,5 мг/кг живой массы, высокоэффективно при тяжелой форме заболеваний органов дыхания и желудочно-кишечного тракта свиней бактериальной этиологии;
- применение препарата групповым способом с водой для поения в течение 3 суток или 5 суток в разовой суточной дозе 35,0 мг/кг живой массы, высокоэффективно при тяжелой форме заболеваний органов дыхания и желудочно-кишечного тракта свиней бактериальной этиологии;
При сравнении результатов бактериологического, молекулярно-биологического (ПЦР), гематологического и клинического исследований поросят опытных и контрольной групп статистически достоверных различий не установлено (р>0,05), из чего следует, что эффективность заявленного способа при бактериальных болезнях свиней не ниже эффективности известного способа с препаратом сравнения Ремокс 500.
Побочные явления и осложнения в виде беспокойства, зуда, отечности, гиперемии, раздражении кожи, гиперсаливации, аллергических реакций, а именно анафилаксии или гиперчувствительности замедленного типа, при применении поросятам заявленного препарата в испытанных дозах не выявлены.
Таким образом, полученные данные позволяют сделать вывод о том, что заявленный способ при использовании препарата в испытанных дозах обладает высокой активностью против широкого спектра возбудителей бактериальных болезней свиней и может быть использован в комплексных лечебно-профилактических мероприятиях по борьбе с респираторными и желудочно-кишечными болезнями свиней бактериальной этиологии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения болезней бактериальной этиологии у животных | 2022 |
|
RU2786919C1 |
| Способ лечения респираторных и желудочно-кишечных заболеваний сельскохозяйственных животных | 2022 |
|
RU2796827C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИЙ БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ У ЖИВОТНЫХ | 2013 |
|
RU2514647C1 |
| АНТИБАКТЕРИАЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И ПТИЦ | 2015 |
|
RU2570389C1 |
| КОМПЛЕКСНЫЙ АНТИБАКТЕРИАЛЬНЫЙ ПРЕПАРАТ ДЛЯ ЖИВОТНЫХ | 2014 |
|
RU2554797C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ДИСБИОЗОВ КИШЕЧНИКА В ПРОЦЕССЕ ПРОВЕДЕНИЯ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ У ТЕПЛОКРОВНЫХ ЖИВОТНЫХ: КРУПНОГО РОГАТОГО СКОТА, СВИНЕЙ, ДОМАШНИХ ЖИВОТНЫХ, В ЧАСТНОСТИ СОБАК, КОШЕК, И СЕЛЬСКОХОЗЯЙСТВЕННЫХ ПТИЦ И СПОСОБ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ДИСБИОЗОВ КИШЕЧНИКА В ПРОЦЕССЕ ПРОВЕДЕНИЯ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ У ТЕПЛОКРОВНЫХ ЖИВОТНЫХ: КРУПНОГО РОГАТОГО СКОТА, СВИНЕЙ, ДОМАШНИХ ЖИВОТНЫХ, В ЧАСТНОСТИ СОБАК, КОШЕК, И СЕЛЬСКОХОЗЯЙСТВЕННЫХ ПТИЦ | 2008 |
|
RU2415684C2 |
| Способ лечения болезней бактериальной этиологии у сельскохозяйственных животных и птиц | 2016 |
|
RU2611351C1 |
| ПРОБИОТИЧЕСКИЙ ПРЕПАРАТ ПРОТИВ ВИРУСНЫХ И БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ "ТОКСИСПОРИН", СПОСОБ ЕГО ПОЛУЧЕНИЯ, ШТАММ БАКТЕРИЙ BACILLUS LICHENIFORMIS, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ КОМПОНЕНТА ПРОБИОТИЧЕСКОГО ПРЕПАРАТА | 2011 |
|
RU2471864C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА ПТИЦЫ | 2016 |
|
RU2639544C1 |
| СПОСОБ ЛЕЧЕНИЯ ЦЫПЛЯТ-БРОЙЛЕРОВ ПРИ АССОЦИАТИВНОЙ КИШЕЧНОЙ ИНФЕКЦИИ | 2017 |
|
RU2677220C1 |
Изобретение относится к области ветеринарной медицины, а именно к способам лечения болезней бактериальной этиологии у животных. Способ заключается в том, что животным вводят препарат, содержащий в мг/г: амоксициллина тригидрат - 570,0-580,0, янтарную кислоту - 2,0-8,0, карбонат натрия - 100,0-300,0, аэросил - 2,0-8,0 и лактозу - до 1 г. При этом препарат животным вводят перорально с кормом или с водой для поения в дозе 17,5-35,0 мг/кг живой массы в течение 3-5 суток. Способ позволяет эффективно лечить широкий спектр болезней бактериальной этиологии у животных, а используемый в данном способе препарат обладает широким спектром бактерицидной активности против большинства грамположительных и грамотрицательных микроорганизмов, включая антибиотикорезистентные, не обладает аллергенными свойствами, оказывает стимулирующее влияние на показатели гуморального иммунного ответа и стабилен при хранении. 2 з.п. ф-лы, 5 табл., 5 пр.
1. Способ лечения болезней бактериальной этиологии у животных, включающий введение препарата на основе амоксициллина, отличающийся тем, что животным вводят препарат, содержащий в мг/г: амоксициллина тригидрат - 570,0-580,0, янтарную кислоту - 2,0-8,0 мг, карбонат натрия - 100,0-300,0, аэросил - 2,0-8,0 и лактозу - до 1 г, при этом препарат животным вводят перорально с кормом или с водой для поения в дозе 17,5-35,0 мг/кг живой массы в течение 3-5 суток.
2. Способ по п. 1, отличающийся тем, что в качестве животных используют сельскохозяйственную птицу или свиней.
3. Способ по п. 1, отличающийся тем, что препарат вводят групповым способом или индивидуально.
| Способ лечения болезней бактериальной этиологии у сельскохозяйственных животных и птиц | 2016 |
|
RU2611351C1 |
| АНТИБАКТЕРИАЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И ПТИЦ | 2015 |
|
RU2570389C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2676482C2 |
| ФИНАГЕЕВ Е.Ю | |||
| СПОСОБ ЛЕЧЕНИЯ ОВЕЦ С ГНОЙНО-НЕКРОТИЧЕСКИМИ ЯЗВАМИ ДИСТАЛЬНОГО ОТДЕЛА КОНЕЧНОСТЕЙ / Международный вестник ветеринарии, 2021, N 3, стр | |||
| Искусственный двухслойный мельничный жернов | 1921 |
|
SU217A1 |
| YUN J | |||
| et al | |||
| The effects of amoxicillin treatment of newborn piglets on the prevalence of hernias and | |||
Авторы
Даты
2022-12-20—Публикация
2022-04-14—Подача