Изобретение относится к медицине, а именно, к молекулярной онкологии, и может найти применение для неинвазивной диагностики глиальной опухоли головного мозга высокой степени злокачественности в случае невозможности оперативного вмешательства.
Глиобластома (ГБ) - одна из наиболее агрессивных и смертельных первичных опухолей центральной нервной системы, на долю которой приходится более 80% злокачественных глиом. За последние четыре десятилетия прогноз данного заболевания не улучшился.
Несмотря на прогресс, достигнутый в протоколах лечения, ГБ по-прежнему характеризуется высокой смертностью - средняя продолжительность жизни пациентов с ГБ составляет 1,5 года (см. Росторгуев, Э.Е. Новые подходы к диагностике и экспериментальной терапии глиальных опухолей высокой степени злокачественности: Автореф. дисс. … д-ра мед. наук: 14.01.12 - Ростов-на-Дону, 2021.).
Существует потребность в новых диагностических и прогностических маркерах (см. Van Meir E. G. et al. Exciting new advances in neuro-oncology: the avenue to a cure for malignant glioma // CA: a cancer journal for clinicians. - 2010. - Т. 60. - №. 3. - С. 166-193.). Наиболее перспективными выступают маркеры биологических жидкостей, особенно плазмы или сыворотки крови. В последние годы активно изучается возможность использования циркулирующих микроРНК в качестве маркеров малоинвазивной диагностики различных онкологических заболеваний, в том числе глиобластом (Birkó Z. et al. Novel molecular markers in glioblastoma-Benefits of liquid biopsy //International Journal of Molecular Sciences. - 2020. - Т. 21. - №. 20. - С. 7522.).
Анализ патентных источников показал наличие следующих изобретений близких по тематике к заявленному:
Известен способ диагностики злокачественных опухолей головного мозга, включающий взятие образца ткани мозга, выделение РНК и определение относительной экспрессии генов EGFR, MSI1 и микроРНК hsa-miR-92-1-5р методом ПЦР в реальном времени в образцах тканей опухоли и перифокальной зоны. При значениях «E-коэффициента» EGFR<0.5 или EGFR>1.5, MSI1<0.5 или MSI1>1.5, hsa-miR-92a-1-5p<0.5 или hsa-miR-92a-1-5p>1.5 хотя бы по одному локусу у пациента диагностируется глиома высокой степени злокачественности (GIII-IV) (см. патент RU 2709651 C1, опубл. 19.12.2019 г., Бюл. №35). Недостатками известного способа является необходимость наличия интраоперационного материала.
Наиболее близким к заявленному способу является способ диагностики глиом головного мозга человека высокой степени злокачественности, включающий определение уровней экспрессии микроРНК в образцах плазмы крови, где определяют экспрессию hsa-miR-22-3р, hsa-miR-122-5p, hsa-miR-107, hsa-miR-324-5p, hsa-miR-155-5p, hsamiR-21-5p, hsa-miR-330-3p, hsa-miR-146a-5p относительно экзогенной микроРНК cel-miR-39 (см. патент RU 2742413 C1, опубл. 05.02.2021 г, Бюл. №4). В способе используется подход с выделением фракции тотальной микроРНК из образца плазмы, что может негативно сказываться на информативности исследования из-за влияния эффективности выделения.
Способ малоинвазивной диагностики глиобластом является новым, так основан на оценке экспрессии микроРНК hsa-miR-5010-3p, hsa-miR-670-3p, hsa-miR-6782-5p, hsa-miR-1225-3p, hsa-miR-6720-5p, hsa-miR-654-5p, hsa-miR-1304-5p, hsa-miR-758-3p, hsa-miR-1180-3p, hsa-miR-6852-3p, hsa-miR-3180-3p методом секвенирования нового поколения в образце плазмы; метод не требует этапа выделения и используется 30 микролитров нативной плазмы; для наработки библиотек кДНК используют набор HTG EdgeSeq miRNA (HTG Molecular Diagnostics Inc., США); для получения показателей диагностически значимых микроРНК используются платформы секвенирования MiSeq, HiSeq 2500 или NextSeq 550 (Illumina, США); метод обладает специфичностью 95,3% и чувствительностью 97,6%.
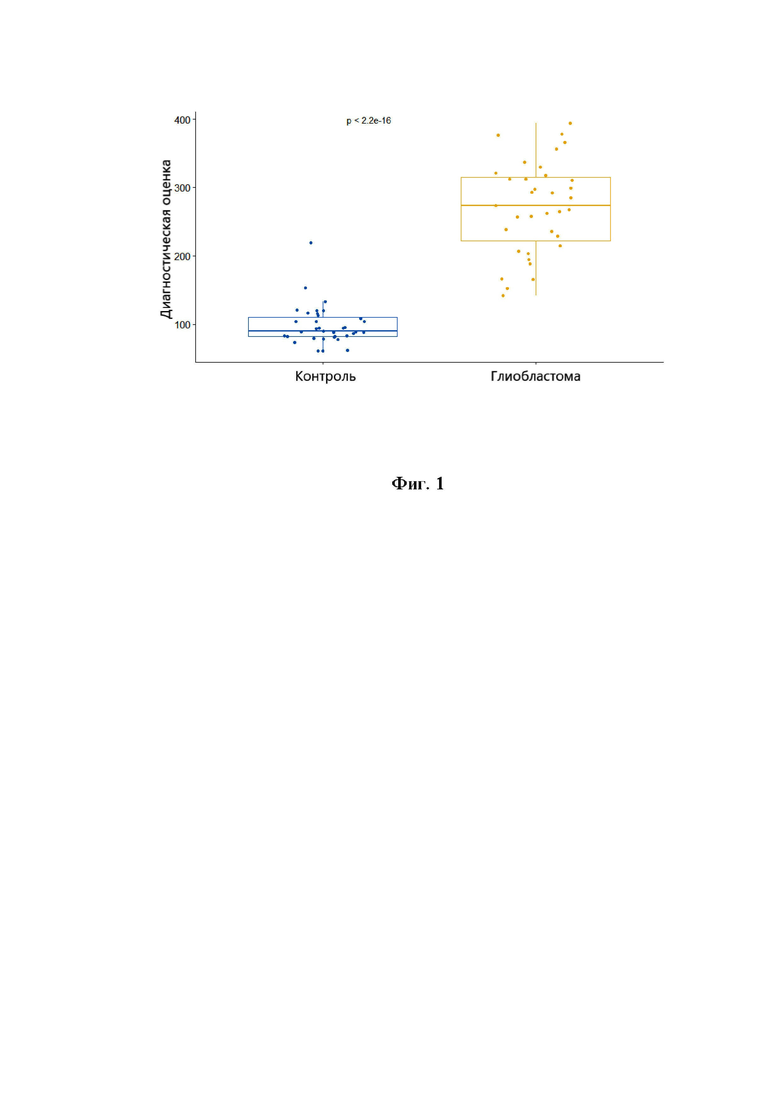
Нами было проведено исследование экспрессии циркулирующих микроРНК в образцах плазмы 70 человек - 35 пациентов с глиобластомой, 35 условно-здоровых доноров. В предварительном анализе с использованием логистической регрессии была получена формула расчета диагностического значения (R) на основе количества выровненных на геном (hg38) прочтений (The total number of mapped reads, RC) микроРНК hsa-miR-5010-3p, hsa-miR-670-3p, hsa-miR-6782-5p, hsa-miR-1225-3p, hsa-miR-6720-5p, hsa-miR-654-5p, hsa-miR-1304-5p, hsa-miR-758-3p, hsa-miR-1180-3p, hsa-miR-6852-3p, hsa-miR-3180-3p в 35 образцах плазмы пациентов с глиобластомой и 35 образцах плазмы условно-здоровой группы. Полученные данные демонстрируют высокий уровень статистической достоверности отличий диагностического значения между группой пациентов с глиобластомой и группой условно-здоровых доноров (p<2.2e-16) (см. фиг. 1).
Техническим результатом заявляемого изобретения является создание эффективного и специфичного способа малоинвазивной диагностики глиобластом.
Технический результат достигается тем, что проводят анализ экспрессии микроРНК в образце плазмы, затем выполняют расчет диагностической оценки R по формуле: R=0.201*RC'hsa-miR-5010-3p' + 0.143*RC'hsa-miR-670-3p' + 0.169*RC'hsa-miR-6782-5p' + 0.160*RC'hsa-miR-1225-3p' + 0.111*RC'hsa-miR-6720-5p' + 0.091*RC'hsa-miR-654-5p' + 0.121*RC'hsa-miR-1304-5p' + 0.121*RC'hsa-miR-758-3p' + 0.117*RC'hsa-miR-1180-3p' + 0.129*RC'hsa-miR-6852-3p' + 0.133*RC'hsa-miR-3180-3p, где RC - значения микроРНК, полученные в результате секвенирования нового поколения, 0.201, 0.143, 0.169, 0.160, 0.111, 0.091, 0.121, 0.121, 0.117, 0.129, 0.133 - коэффициенты, полученные в результате логистической регрессии. При значении R выше 137.554 диагностируют глиобластому.
На Фиг. 1 представлено распределение диагностического значения (R) в группе больных (глиобластома) и в группе- условно-здоровых доноров (контроль).
Реализацию заявленного способа выполняют следующим способом:
- На первом этапе образцы крови объемом 6 мл получают путем венепункции в вакутейнеры, содержащие K2ЭДТА. После взятия пробирки перемешивают переворачиванием в течение 10 сек. и хранят до обработки не более 30 минут при +4°C. Для получения плазмы кровь центрифугируют при 1500g, +4°C в течение 10 минут. Бесклеточную фракцию переносят в новую пробирку и центрифугируют при 12000g, +4°C в течение 10 минут, супернатант отбирают и хранят при -80°C.
- На втором этапе 30 мкл плазмы смешивают с буфером для лизиса в присутствии протеиназы K. Лизированные образцы инкубируют при 50°С в течение трех часов с периодическим пипетированием, после чего лизированные образцы гибридизуют с зондами микроРНК (HTG Molecular Diagnostics Inc., США) в течение 20 часов.
- На третьем этапе лизированые и гибридизованые образцы амплифицируют с использованием мастер-микса (10 мМ дезоксирибонуклеотидтрифосфата (dNTP), 10× Taq Turbo буфер буфер (Евроген, Россия), Taq ДНК-полимераза (Евроген, Россия), прямой и обратный праймеры (HTG Molecular Diagnostics Inc., США). Условия ПЦР реакции должны быть следующими: 95°С, 4 мин, (95°С, 15 с, 56°С, 45 с, 68°С, 45 с)х16, 68°C в течение 10 минут и хранение при 4 C. После ПЦР проводят очистку с помощью Ampure®Beats XP (Beckman Coulter Inc., США). Образцы перемешивают и инкубировают с гранулами при комнатной температуре в течение 5 мин. Связанные с шариками ампликоны дважды промывают 80% этанолом для удаления всех оставшихся реагентов ПЦР. После промывки образцы высушивают при комнатной температуре в течение 2 минут для удаления остаточного этанола. Затем ампликоны эллюируют в 10 мМ трис-гидрохлорида (трис-HCl), рН 8,0.
- На четвертом этапе ампликоны денатурируют 2Н растворе NaOH в течение 8 мин при комнатной температуре. NaOH гидролизуют 2Н HCl и разбавляют до 20 пМ буфером HT1 (Illumina Inc., США). Проводят секвенирование ампликонов c одноконцевым 50ч чтением c использованием MiSeq, HiSeq 2500 или NextSeq 550 (Illumina, США). Выполняют анализ данных секвенирования с использованием Small RNA Local Run Manager (Illumina, США) и на основе полученных значений RC микроРНК hsa-miR-5010-3p, hsa-miR-670-3p, hsa-miR-6782-5p, hsa-miR-1225-3p, hsa-miR-6720-5p, hsa-miR-654-5p, hsa-miR-1304-5p, hsa-miR-758-3p, hsa-miR-1180-3p, hsa-miR-6852-3p, hsa-miR-3180-3p проводят расчет диагностического значения R по формуле R=0.201*RC'hsa-miR-5010-3p' + 0.143*RC'hsa-miR-670-3p' + 0.169*RC'hsa-miR-6782-5p' + 0.160*RC'hsa-miR-1225-3p' + 0.111*RC'hsa-miR-6720-5p' + 0.091*RC'hsa-miR-654-5p' + 0.121*RC'hsa-miR-1304-5p' + 0.121*RC'hsa-miR-758-3p' + 0.117*RC'hsa-miR-1180-3p' + 0.129*RC'hsa-miR-6852-3p' + 0.133*RC'hsa-miR-3180-3p. При R> 137.554 ставится диагноз глиобластома.
Для доказательства диагностической ценности предлагаемого способа приводим 2 примера применения способа.
Пример №1.
Больной Г., 62 года, пол мужской, обратился к неврологу по месту жительства по поводу слабости в правых конечностях. Проводилось симптоматическая терапия по месту жительства. Лечение - без эффекта.
Обратился в ФГБУ «НМИЦ онкологии» Минздрава России, где была выполнена МРТ головного мозга в стандартных режимах с контрастным усилением и выявлена внемозговая опухоль левой теменной области.
При соматической оценке пациента патологии не выявлено. Предварительный диагноз: менингиома задней трети справа.
Пациенту выполнено исследование относительной экспрессии микроРНК в плазме крови (получена до лечения) методом секвенирования нового поколения. Результаты молекулярно-генетического исследования:
RC hsa-miR-5010-3p=0;
RC hsa-miR-670-3p=135.5;
RC hsa-miR-6782-5p=4.4;
RC hsa-miR-1225-3p=200.4;
RC hsa-miR-6720-5p=28;
RC hsa-miR-654-5p=54.5;
RC hsa-miR-1304-5p=2.9;
RC hsa-miR-758-3p=0;
RC hsa-miR-1180-3p=14.7;
RC hsa-miR-6852-3p=61.9;
RC hsa-miR-3180-3p=97.2.
R=0.201*0+0.143*135.5+0.169*4.4+0.160*200.4+0.111*28+0.091*54.5+0.121*2.9+0.121*0+0.117*14.7+0.129*61.9+0.133*97.2=83.2.
Значение R=83.2, что свидетельствуют об отсутствии у пациента глиобластомы.
В отделении нейроонкологии ФГБУ «НМИЦ онкологии» Минздрава России выполнена операция в объеме: костнопластическая краниотомия в правой теменной области, удаление опухоли (I степень радикальности по Симпсону). Иммуногистохимическое исследование охарактеризовало опухоль как менингиому.
Пример №2.
Больная Ж., 75 лет, пол женский, обратилась в ФГБУ «НМИЦ онкологии» Минздрава России с жалобами на диффузные головные боли в течение 2х месяцев. МРТ-исследование головного мозга в стандартных режимах с контрастным усилением выявило глиальную опухоль левой лобной доли. При комплексном обследовании других органов и систем патологии не выявлено. Предварительный диагноз: диффузная глиальная опухоль правой левой доли. Без стадии. Клиническая группа 2.
На этапе госпитализации выполнено исследование относительной экспрессии микроРНК в плазме крови (получена до лечения) методом секвенирования нового поколения. Результаты молекулярно-генетического исследования:
RC hsa-miR-5010-3p=14.9;
RC hsa-miR-670-3p=252.7;
RC hsa-miR-6782-5p=37.7;
RC hsa-miR-1225-3p=473.5;
RC hsa-miR-6720-5p=100;
RC hsa-miR-654-5p=223.5;
RC hsa-miR-1304-5p=20.8;
RC hsa-miR-758-3p=30.5;
RC hsa-miR-1180-3p=99.4;
RC hsa-miR-6852-3p=244.9;
RC hsa-miR-3180-3p=249.4.
R=0.201*14.9+0.143*252.7+0.169*37.7+0.160*473.5+0.111*100+0.091*223.5+0.121*20.8+0.121*30.5+0.117*99.4+0.129*244.9+0.133*249.4=235.2.
Значение R=235.2, что свидетельствуют о наличии у пациента глиобластомы.
В отделении нейроонкологии ФГБУ «НМИЦ онкологии» Минздрава России выполнена операция в объеме: костнопластическая краниотомия, циторедуктивное удаление глиальной опухоли с применением флуоресцентной микроскопии (5-аминолевулиновая кислота), оптической навигации границ опухоли, коммисуральных и проекционных трактов в условиях нейрофизиологического мониторинга. Иммуногистохимическое исследование характеризует опухоль как первичную глиобластому GIV IDH1/2 WT.
Клинические данные, полученные в результате амбулаторного обследования данных пациентов, впоследствии подтвердили поставленный диагноз в соответствии с диагностическим значением микроРНК в образцах плазмы крови пациентов, полученных до начала лечения.
Анализ представленных клинических случаев демонстрирует возможности малоинвазивной диагностики глиобластом с использованием оценки экспрессии hsa-miR-5010-3p, hsa-miR-670-3p, hsa-miR-6782-5p, hsa-miR-1225-3p, hsa-miR-6720-5p, hsa-miR-654-5p, hsa-miR-1304-5p, hsa-miR-758-3p, hsa-miR-1180-3p, hsa-miR-6852-3p, hsa-miR-3180-3p методом секвенирования нового поколения в образцах плазмы крови пациентов.
Перечень последовательностей нуклеотидов микроРНК указан в таблице 1.
Технико-экономическая эффективность способа заключается в том, что его применение позволяет эффективно проводить малоинвазивную диагностику глиобластом, в том числе, в случае невозможности оперативного вмешательства.
Изобретение относится к медицине, а именно к молекулярной онкологии, и может быть использовано для малоинвазивной диагностики глиобластом. Проводят анализ экспрессии микроРНК в образце плазмы. Рассчитывают диагностическое значение R по формуле: R=0.201*RC`hsa-miR-5010-3p` + 0.143*RC`hsa-miR-670-3p` + 0.169*RC`hsa-miR-6782-5p` + 0.160*RC`hsa-miR-1225-3p` + 0.111*RC`hsa-miR-6720-5p` + 0.091*RC`hsa-miR-654-5p` + 0.121*RC`hsa-miR-1304-5p` + 0.121*RC`hsa-miR-758-3p` + 0.117*RC`hsa-miR-1180-3p` + 0.129*RC`hsa-miR-6852-3p` + 0.133*RC`hsa-miR-3180-3p`, где RC – значения микроРНК, полученные в результате секвенирования нового поколения. При значении R выше 137.554 диагностируют глиобластому. Способ обеспечивает эффективную малоинвазивную диагностику глиобластом за счет использования оригинальной формулы расчета диагностического значения R на основе количества выровненных на геном прочтений микроРНК hsa-miR-5010-3p, hsa-miR-670-3p, hsa-miR-6782-5p, hsa-miR-1225-3p, hsa-miR-6720-5p, hsa-miR-654-5p, hsa-miR-1304-5p, hsa-miR-758-3p, hsa-miR-1180-3p, hsa-miR-6852-3p, hsa-miR-3180-3p. 1 ил., 1 табл., 2 пр.
Способ малоинвазивной диагностики глиобластом, заключающийся в том, что проводят анализ экспрессии микроРНК в образце плазмы, затем выполняют расчет диагностической оценки R по формуле: R=0.201*RC`hsa-miR-5010-3p` + 0.143*RC`hsa-miR-670-3p` + 0.169*RC`hsa-miR-6782-5p` + 0.160*RC`hsa-miR-1225-3p` + 0.111*RC`hsa-miR-6720-5p` + 0.091*RC`hsa-miR-654-5p` + 0.121*RC`hsa-miR-1304-5p` + 0.121*RC`hsa-miR-758-3p` + 0.117*RC`hsa-miR-1180-3p` + 0.129*RC`hsa-miR-6852-3p` + 0.133*RC`hsa-miR-3180-3p`, где RC – значения микроРНК, полученные в результате секвенирования нового поколения, 0.201, 0.143, 0.169, 0.160, 0.111, 0.091, 0.121, 0.121, 0.117, 0.129, 0.133 – коэффициенты, полученные в результате логистической регрессии, при значении R выше 137.554 диагностируют глиобластому.
| Способ диагностики глиальных опухолей головного мозга высокой степени злокачественности | 2020 |
|
RU2742413C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ГЛИОМ ГОЛОВНОГО МОЗГА ЧЕЛОВЕКА | 2015 |
|
RU2583871C1 |
| WO 2017085287 A1, 26.05.2017 | |||
| US 2014088170 A1, 27.03.2014. | |||
Авторы
Даты
2023-01-24—Публикация
2022-06-09—Подача