Область техники, к которой относится изобретение
Настоящее изобретение относится к композиции для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, содержащей двухцепочечную мкрРНК в качестве активного ингредиента, и, более конкретно, к фармацевтической или косметической композиции для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, содержащей в качестве активного ингредиента двухцепочечную мкрРНК, такую как miR-3139, miR-3189, miR-3199 или miR-8485, двухцепочечную олигонуклеотидную конструкцию, включающую ее, или наночастицы, включающие указанную конструкцию.
Сведения о предшествующем уровне техники
Поседение волос у человека является явлением физиологического старения и, как известно, вызвано уменьшением пигмента меланина вследствие функционального ухудшения и истощения меланоцитов или стволовых клеток меланоцитов в волосяных фолликулах. Пигмент меланин является важным фактором, определяющим цвет волос, и меланин синтезируется в меланосомах и секретируется из меланосом, присутствующих в меланоцитах, переносится на близлежащие кератиноциты, фибробласты и т.д., а затем перемещается по мере роста волос и поддерживает цвет волос. В настоящее время в качестве решения проблемы поседения волос используется простая процедура окрашивания, но окрашивание является временным способом, и повторное окрашивание необходимо из-за роста седых волос, а ингредиенты, содержащиеся в красках для волос, имеют различные побочные эффекты, такие как раздражение кожи головы и волосяных фолликулов или вызывание аллергии или дерматита. Текущие исследования, связанные с контролем выработки пигмента меланина, ограничиваются разработкой материалов, обладающих эффектами отбеливания кожи, и идентификацией механизмов их действия путем подавления симптомов, таких как пигментация и т.д., из-за чрезмерной выработки меланина в коже, вызванной различными факторами, такими как генетические факторы, старение, гормоны, факторы роста, ультрафиолетовое излучение и т.п. Напротив, было проведено мало исследований, касающихся механизма действия и разработки материалов, связанных со стимулированием меланогенеза для преодоления поседения волос или пониженного синтеза меланина. Более того, меланогенез регулируется взаимодействиями различных сигналов (сигнальный путь SCF-KIT-RAS-ERK, сигнальный путь MC1R-cAMP-PKA, сигнальный путь Wnt-бета-катенин). Из-за такого сложного механизма действия непросто идентифицировать механизм действия и разработать новые материалы для предотвращения или уменьшения поседения волос.
В последнее время андрогенетическая алопеция (AGA), которая в основном встречается у мужчин среднего возраста и считается генетическим заболеванием мужчин, часто встречается у женщин, а также у молодых мужчин из-за сильного загрязнения окружающей среды, стресса, диетических изменений и быстрого старения населения. Поскольку интерес к выпадению волос возрастает, быстро растет рынок, связанный с проблемой выпадения волос. Известно, что выпадение волос вызывается различными факторами, такими как генетические факторы, мужские гормоны, старение, нарушения кровообращения и т.п. В настоящее время одобренные лекарственные средства включают только финастерид, который ингибирует выработку дигидротестостерона (DHT), который является мужским гормоном (андрогеном), и миноксидил, который улучшает расширение кровеносных сосудов и кровообращение. Однако эти лекарственные средства обладают временной и ограниченной эффективностью в зависимости от дозы и способа введения, и сопровождаются различными побочными эффектами. Следовательно, требуется разработка новых материалов, которые индуцируют активацию клеток волосяных фолликулов и пролиферацию клеток, чтобы стимулировать рост волос без побочных эффектов.
Цикл роста волос включает три стадии: фазу анагена, в которой волосы растут наиболее активно, фазу катагена, в которой рост волос прекращается и начинается дегенерация волос, и фазу телогена, в которой активность волосяных фолликулов приостанавливается, и выпадение волос относится к естественному выпадению волос, которые перестали расти в соответствии с циклом роста, и известно, что выпадение волос вызывают различные факторы. Хотя разработка лекарственных средств для уменьшения симптомов выпадения волос проводилась в течение длительного времени, существуют только финастерид, который является пероральным терапевтическим средством от выпадения волос, и миноксидил, который является местным терапевтическим средством от выпадения волос. Однако, поскольку эти лекарственные средства вызывают облегчение симптомов выпадения волос за счет механизма ингибирования выработки мужских гормонов, они имеют побочные эффекты и ограничения в эффективности. Следовательно, необходимо разработать материалы с новыми механизмами и стратегиями, которые демонстрируют эффективность без побочных эффектов. Важной стратегией разработки терапевтических агентов для лечения выпадения волос является индукция быстрого перехода волос из фазы телогена в фазу анагена путем стимулирования активации и пролиферации клеток волосяных фолликулов. Соответственно, необходимо разработать новые материалы, которые вызывают активацию клеток волосяных фолликулов и пролиферацию клеток для стимулирования роста волос.
Технология подавления экспрессии генов считается важным инструментом в разработке терапевтических агентов и проверки мишеней для лечения заболеваний, и разработку осуществляли различными способами, чтобы преодолеть ограничения, связанные со способами лечения традиционными лекарственными средствами, при этом одним из способов является использование РНК-интерференции (далее именуется как «РНКи») (Iorns, E., Lord, C.J., Turner, N. & Ashworth, A., Nat. Rev. Drug Discov. 6, 556-68. 2007). РНКи является способом, используемым для подавления экспрессии генов, и область его применения разнообразна, так как он просто и четко демонстрирует эффекты подавления генов с низкими затратами. миРНК представляет собой одноцепочечную РНК, состоящую из 16-27 нуклеотидов, и действует в клетках в качестве компонента рибонуклеопротеина, известного как РИСК (РНК-индуцированный комплекс сайленсинга). РИСК функционирует в качестве ферментных ножниц РНК и расщепляет информационную РНК (далее именуемую как «мРНК») для ингибирования выработки белка из мРНК. миРНК, включенная в РИСК, связывается с мРНК, имеющей последовательность, комплементарную последовательности миРНК, с образованием двухцепочечной РНК, и РИСК, служащий в качестве ферментных ножниц РНК, расщепляет мРНК-мишень, так что мРНК больше не может функционировать в качестве матрицы для выработки белка.
Таким образом, терапевтические средства на основе РНКи оцениваются как более совершенные, чем одномолекулярные терапевтические средства, поскольку они блокируют мРНК до стадии выработки белка и используют РНК и клеточную внутреннюю систему РИСК, но вызывают побочные эффекты, которые не могут быть устранены даже с помощью технологии на основе миРНК, что представляет собой явление, называемое нецелевым эффектом. Как описано выше, терапевтические средства на основе РНКи разрушают мРНК, которая комплементарно связывается с последовательностью миРНК, но связываются с мРНК, которая комплементарна только части последовательности миРНК, а не всей последовательности миРНК, вызывая деградацию, которую называют «нецелевым эффектом», поскольку индуцируется деградация нецелевой мРНК.
С целью преодоления описанных выше технических трудностей терапевтических средств на основе РНКи проводится тщательное исследование по применению микроРНК (далее именуемой как «мкрРНК») в качестве терапевтического агента (Agostini, M. & Knight, R.A., Oncotarget 5, 872-81, 2014; Dangwal, S. & Thum, T., Annu. Rev. PharmacolToxicol. 54, 185-203, 2014). мкрРНК представляет собой РНК, состоящую из 16-27 нуклеотидов, и классифицируется как белок-некодирующая РНК при получении мРНК, которая транслируется в белок (Carthew, R.W. & Sontheimer, E.J., Cell 136, 642-55, 2009; MacFarlane, L.-A. & Murphy, P.R., Current Genomics 11, 537-561, 2010; Bartel, D.P., Cell 136, 215-33, 2009). мкрРНК обнаружена в геномах высших животных и клетках растений и, как известно, играет важную роль в регулировании клеточного метаболизма и функций, включая продуцирование, рост, дифференцировку и гибель клеток. На сегодняшний день известно около 2000 типов мкрРНК в геноме человека, и среди них до сих пор неизвестны функции значительного числа мкрРНК.
мкрРНК транскрибируется в РНК РНК-полимеразой, называемой Pol II, из генома, и ее начальная длина не указана и варьируется (Carthew, R.W. & Sontheimer, E.J., Cell 136, 642-55, 2009; Brodersen, P. & Voinnet, O., Nat. Rev. Mol. Cell Biol. 10, 141-148, 2009). Это обусловлено разнообразием положений, в которых мкрРНК включена в геном, в частности, из-за различных путей продукции мкрРНК, например, в интроне, который является частью мРНК, не участвующей в выработке белка и транскрибируется одновременно с выработкой мРНК, или в межгенной области генома и транскрибируется независимо (Malone, C.D. & Hannon, G.J., Cell 136, 656-68, 2009). Матрица мкрРНК, первоначально созданная таким образом, называется первичной miR (первичной микроРНК), и первичная мкрРНК редактируется в предшественник мкрРНК (далее именуемый как «пре-miR») с помощью РНКазы, называемой Дроша, в ядре (Bartel, D.P., Cell 136, 215-33, 2009). Pre-miR образует шпилечную структуру РНК и состоит примерно из 70-80 нуклеотидов. Pre-miR внутри клеточного ядра перемещается из ядра в цитоплазму с помощью белков-экспортинов и т.д. и вторично процессируется другой РНКазой, называемой Дисер, в цитоплазме с образованием двухцепочечной зрелой мкрРНК, состоящей из 16-27 нуклеотидов (зрелая микроРНК, далее именуемая miR, описанная без других модификаторов, означает зрелую miR). В двухцепочечной miR выбирается одноцепочечная РНК, которая связывается с РИСК, являющимся рибонуклеопротеином, и, таким образом, становится активной, и связывается с мРНК-мишенью, используя последовательность miR.
Как правило, мРНК в основном подразделяется на три области в зависимости от их участия в выработке белка: кодирующая область, которая несет информацию о трансляции белка, а также 5'-UTR (нетранслируемая область) и 3'-UTR, которые не несут информацию о трансляции белка, в качестве соответствующих 5'- и 3'-концов кодирующей области. миРНК, которая индуцирует деградацию мРНК-мишени с применением комплементарных мРНК последовательностей, действует независимо от 5'- и 3'-UTR и кодирующей области мРНК, тогда как miR в основном связывается с 3'-UTR (Carthew, R.W. & Sontheimer, E.J., Cell 136, 642-55, 2009; Bartel, D.P., Cell 136, 215-33, 2009). Уникальной особенностью миРНК и мкрРНК, помимо различия в положении связывания с мРНК, является то, что миРНК связывается в основном с мРНК, включая последовательность, комплементарную всей последовательности миРНК, тогда как мкрРНК устроена так, что для распознавания мРНК-мишени в основном используется последовательность затравочной области ограниченного размера, расположенная в 2-8 нуклеотидах от 5'-конца мкрРНК, и, таким образом, даже когда вся последовательность мкрРНК не имеет полностью комплементарной последовательности гену-мишени и включает определенную часть некомплементарной последовательности, активность мкрРНК не затрагивается (Bartel, D.P., Cell 136, 215-33, 2009). Поскольку последовательность затравочной области имеет длину 6-8 нуклеотидов, существуют различные типы мРНК, имеющие комплементарные ей последовательности в 3'-UTR, и, следовательно, один тип мкрРНК способен одновременно контролировать несколько типов мРНК. Такая мкрРНК функционирует в качестве эффективного регулятора, участвующего в контроле многих аспектов клеточной физиологии, включая клеточное деление, рост, дифференцировку и гибель. Кроме того, функция мкрРНК в качестве регулятора имеет то преимущество, что ее можно эффективно применять при различных заболеваниях. В отличие от миРНК, которая нацелена на подавление экспрессии одного гена, мкрРНК способна одновременно ингибировать экспрессию нескольких генов, участвующих в различных сигнальных путях. Большое количество мРНК содержат область в 3'-UTR, в которой вероятно связывается по меньшей мере одна мкрРНК, и на основе биоинформатических расчетов известно, что выработка белка из примерно 30% всех мРНК регулируется мкрРНК.
Несмотря на превосходные эффекты и широкий спектр применения мкрРНК или миРНК, для разработки мкрРНК/миРНК в качестве терапевтического агента мкрРНК/миРНК должна быть эффективно доставлена в клетки-мишени за счет улучшения стабильности мкрРНК/миРНК в организме и повышения эффективности доставки в клетки (FY Xie., Drug Discov. Today. 2006 Jan; 11(1-2):67-73). Для повышения стабильности в организме и решения проблемы, связанной со стимуляцией мкрРНК/миРНК неспецифического врожденного иммунитета, продолжаются тщательные исследования в отношении модификации некоторых нуклеотидов или остовов мкрРНК/миРНК для придания им устойчивости к нуклеазам или в отношении применения носителей, таких как вирусные векторы, липосомы, наночастицы и т.д. Система доставки с применением вирусного вектора, такого как аденовирус или ретровирус, обладает высокой эффективностью трансфекции, но высокой иммуногенностью и онкогенностью. С другой стороны, невирусная система доставки, включающая наночастицы, имеет низкую эффективность доставки в клетки по сравнению с вирусной системой доставки, но она имеет преимущество из-за высокой стабильности in vivo, возможности мишень-специфической доставки, поглощения и интернализации содержащихся олигонуклеотидов РНКи в клетки или ткани, а также почти отсутствия цитотоксичности или стимуляции врожденного иммунитета, так что в настоящее время она считается более мощным методом доставки, чем вирусная система доставки (Akhtar S, J. Clin. Invest. 2007 December 3; 117(12): 3623-3632).
Что касается способа применения наноносителя в невирусной системе доставки, то наночастицы формируются с применением различных полимеров, таких как липосомы, комплексы катионных полимеров и т.п., и мкрРНК/миРНК нагружают на такую наночастицу, а именно наноноситель, и доставляют в клетки. Среди способов применения наноносителя в основном можно использовать полимерную наночастицу, полимерную мицеллу, липоплекс и т.д., и, в частности, липоплекс состоит из катионных липидов и взаимодействует с анионными липидами эндосом клеток, тем самым вызывая эффект дестабилизации эндосом, чтобы обеспечить внутриклеточную доставку. Кроме того, известно, что высокая эффективность in vivo достигается путем связывания химического материала с концом смысловой (пассажирской) цепи мкрРНК/миРНК, чтобы обеспечить улучшенные фармакокинетические характеристики (J. Soutschek, Nature 11; 432(7014):173-8, 2004). Таким образом, стабильность мкрРНК/миРНК может варьироваться в зависимости от свойств химического материала, связанного с концом смысловой или антисмысловой (направляющей) цепи мкрРНК/миРНК.
Например, миРНК, содержащая связанное с ней полимерное соединение, такое как полиэтиленгликоль (PEG), взаимодействует с анионной фосфатной группой мкрРНК/миРНК в присутствии катионных веществ с образованием комплекса, тем самым становясь носителем мкрРНК/миРНК, обладающим повышенной стабильностью (S.H. Kim, J. Control Release 129(2):107-16, 2008). В частности, мицеллы, состоящие из полимерных комплексов, имеют чрезвычайно малый размер по сравнению с другими системами, используемыми в качестве средств доставки лекарственных средств, такими как микросферы или наночастицы, но характеризуются очень однородным распределением по размеру и образуются спонтанно, тем самым облегчая управление качеством смеси и обеспечивая воспроизводимость составов. Для повышения эффективности внутриклеточной доставки мкрРНК/миРНК была разработана технология достижения стабильности мкрРНК/миРНК и эффективной проницаемости через клеточные мембраны с применением конъюгата мкрРНК/миРНК, в котором гидрофильный материал (например, полиэтиленгликоль (PEG)) в качестве биосовместимого полимера конъюгирован с мкрРНК/миРНК посредством простой ковалентной связи или ковалентной связи, опосредованной линкером (корейский патент № 883471).
Однако химическая модификация мкрРНК/миРНК и конъюгирование с полиэтиленгликолем (PEG) (ПЭГилирование) по-прежнему имеют недостатки, такие как низкая стабильность in vivo и неэффективная доставка в целевые органы. Для устранения этих недостатков была разработана конструкция с двухцепочечным олигонуклеотидом, в которой гидрофильные и гидрофобные материалы связаны с двухцепочечным олигонуклеотидом, в частности, двухцепочечной олиго РНК, например, мкрРНК/миРНК, причем конструкция образует самособирающиеся наночастицы, названные SAMiRNA™ SAMiRNA (самособирающиеся мицеллы с ингибирующей РНК), самособирающиеся за счет гидрофорбного взаимодействия гидрофобного материала (корейский патент 1224828). Преимущество технологии SAMiRNA™ заключается в возможности получения однородных, но очень маленьких по размеру наночастиц по сравнению с традиционными технологиями доставки.
В качестве конкретного примера технологии SAMiRNA™, используется PEG (полиэтиленгликоль) или HEG (гексаэтиленгликоль) в качестве гидрофильного материала, а PEG является синтетическим полимером и часто применяется для повышения растворимости фармацевтических препаратов, особенно белков, и для контроля фармакокинетики. PEG представляет собой полидисперсный материал, и партия полимера состоит из общей суммы различного количества мономеров и имеет гауссово распределение молекулярной массы, а степень однородности материала выражается в виде индекса полидисперсности (Mw/Mn). В частности, когда PEG имеет низкую молекулярную массу (3-5 кДа), он демонстрирует индекс полидисперсности около 1,01, а в случае высокой молекулярной массы (20 кДа) он проявляет высокий индекс полидисперсности около 1,2, поэтому чем больше молекулярная масса, тем ниже однородность материала. Таким образом, случай, когда PEG связан с фармацевтическим препаратом, является невыгодным, так как нелегко проверить отдельный материал, поскольку характерная полидисперсность PEG отражается в конъюгате. Поэтому существует тенденция к получению материалов с низким индексом полидисперсности путем улучшения процессов синтеза и очистки PEG. В частности, в случае, когда PEG связан с материалом, имеющим низкую молекулярную массу, возникают проблемы из-за характеристик полидисперсности материала, что неудобно с той точки зрения, что сложно проверить произошло ли связывание (Francesco M. VDRUG DISCOVERY TODAY(2005) 10(21):1451-1458). Соответственно, в последние годы в качестве усовершенствованной формы существующих самособирающихся наночастиц SAMiRNA™ из гидрофильного материала двухцепочечной олигонуклеотидной конструкции, составляющей SAMiRNA™, формируются блоки из базовых единиц, включающих от 1 до 15 однородных мономеров определенной молекулярной массы, а при необходимости и линкер, и при применении соответствующего количества блоков в зависимости от потребности была разработана новая форма технологии носителя для доставки меньших размеров, чем у существующих SAMiRNA™, и со значительно лучшей полидисперсностью.
Соответственно, авторы настоящего изобретения приложили большие усилия для обнаружения мкрРНК, способной уменьшать поседение волос, и установили, что miR-3139, miR-3189, miR-3199 или miR-8485 могут активировать меланоциты и стимулировать меланогенез, тем самым уменьшая поседение волос, а также что пролиферация клеток дермальной папиллы волосяных фолликулов, кератиноцитов и т.д. стимулируется дополнительно к активации меланоцитов, и наружная корневая оболочка (ORS) волосяных фолликулов и длина волос увеличиваются, таким образом завершая настоящее изобретение.
Патентная литература
(Патентный документ 1) Корейский патент № 883471
(Патентный документ 2) Корейский патент № 1224828
(Патентный документ 3) Корейский патент № 1862349
Непатентная литература
(Непатентный документ 1) Iorns, E., Lord, C.J., Turner, N. & Ashworth, A., Nat. Rev. Drug Discov. 6, 556-68. 2007
(Непатентный документ 2) Agostini, M. & Knight, R.A., Oncotarget 5, 872-81, 2014
(Непатентный документ 3) Dangwal, S. & Thum, T., Annu. Rev. PharmacolToxicol. 54, 185-203, 2014
(Непатентный документ 4) Carthew, R.W. & Sontheimer, E.J., Cell 136, 642-55, 2009
(Непатентный документ 5) MacFarlane, L.-A. & Murphy, P.R., Current Genomics 11, 537-561, 2010
(Непатентный документ 6) Bartel, D.P., Cell 136, 215-33, 2009
(Непатентный документ 7) Carthew, R.W. & Sontheimer, E.J., Cell 136, 642-55, 2009
(Непатентный документ 8) Brodersen, P. & Voinnet, O., Nat. Rev. Mol. Cell Biol. 10, 141-148, 2009
(Непатентный документ 9) Malone, C.D. & Hannon, G.J., Cell 136, 656-68, 2009
(Непатентный документ 10) Akhtar S, J. Clin Invest. 2007 December 3; 117(12): 3623-3632, 2007
(Непатентный документ 11) S.H. Kim, J. Control Release 129(2):107-16, 2008
Сущность изобретения
Целью настоящего изобретения является обеспечение новой композиции, способной уменьшать поседение волос за счет активации меланоцитов волосяных фолликулов и стимуляции меланогенеза, а также предотвращать или уменьшать выпадение волос и стимулировать рост волос за счет индукции пролиферации клеток волосяных фолликулов.
Для достижения вышеуказанной цели в настоящем изобретении предлагается фармацевтическая композиция для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, включающая в качестве активного ингредиента (i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечную олигонуклеотидную конструкцию, имеющую структуру приведенной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или
(iii) наночастицы, включающие такую двухцепочечную олигонуклеотидную конструкцию.
Кроме того, в настоящем изобретении предлагается косметическая композиция для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, включающая в качестве активного ингредиента (i) miR-3139, miR-3189, miR-3199 или miR-8485; (ii) двухцепочечную олигонуклеотидную конструкцию, имеющую структуру приведенной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет miR-3139, miR-3189, miR-3199 или miR-8485; или
(iii) наночастицы, включающие такую двухцепочечную олигонуклеотидную конструкцию.
Кроме того, в настоящем изобретении предлагается способ уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, включающий введение субъекту, нуждающемуся в уменьшении поседения волос, стимулировании роста волос и/или предотвращении или уменьшении выпадения волос,
(i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечной олигонуклеотидной конструкции, имеющей структуру представленной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или
(iii) наночастиц, включающих такую двухцепочечную олигонуклеотидную конструкцию.
Кроме того, в настоящем изобретении предлагается применение для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос,
(i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечной олигонуклеотидной конструкции, имеющей структуру структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или (iii) наночастиц, включающих такую двухцепочечную олигонуклеотидную конструкцию.
Кроме того, в настоящем изобретении предлагается применение для изготовления лекарственных средств или косметических средств для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос,
(i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечной олигонуклеотидной конструкции, имеющей структуру представленной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или (iii) наночастиц, включающих такую двухцепочечную олигонуклеотидную конструкцию.
Описание чертежей
На фиг. 1 показаны результаты первичного скрининга 1728 мкрРНК человека, нагруженных на SAMiRNA™, путем измерения количества меланина, вырабатываемого в клеточной линии рака кожи человека (М21);
на фиг. 2 показаны результаты вторичного скрининга 18 мкрРНК с высоким количеством вырабатываемого меланина, отобранных посредством скрининга в клеточной линии рака кожи человека (М21);
на фиг. 3 показаны результаты оценки воспроизводимости количества вырабатываемого меланина и эффективности изменения цвета в клеточной линии рака кожи человека (SK-MEL-28) с применением 9 мкрРНК с наибольшим количеством вырабатываемого меланина, отобранных посредством первичного и вторичного скрининга;
на фиг. 4 показаны результаты анализа изменений в передаче сигналов меланогенеза посредством кПЦР-РВ (кПЦР-РВ) для анализа механизма действия 9 мкрРНК, включающих miR-8485, miR-7978, miR-6074, miR-3132, miR-4644, miR-3139, miR-3189, miR-3199 и miR-933 с наибольшим количеством меланина, вырабатываемого в клеточной линии SK-MEL-28;
на фиг. 5 показаны результаты анализа изменений в передаче сигналов меланогенеза посредством кПЦР-РВ с применением 9 выбранных мкрРНК, включающих miR-8485, miR-7978, miR-6074, miR-3132, miR-4644, miR-3139, miR-3189, miR-3199 и miR-933, в клеточной линии эпидермальных меланоцитов человека;
на фиг. 6 показаны результаты, подтверждающие изменения в передаче сигналов меланогенеза посредством Вестерн-блоттинга для анализа механизма действия 9 выбранных мкрРНК, включающих miR-8485, miR-7978, miR-6074, miR-3132, miR-4644, miR-3139, miR-3189, miR-3199 и miR-933, в клеточной линии SK-MEL-28;
на фиг. 7 показаны результаты наблюдения за стимулированием пролиферации клеток наружной корневой оболочки (ORS) и волосяных фолликулов в выщипанных седых волосах человека с применением окончательно отобранных 4 мкрРНК, включающих miR-3139, miR-3189, miR-3199 и miR-8485;
на фиг. 8 показаны результаты наблюдения за эффективностью (изменением цвета) в выщипанных седых волосах человека с помощью окончательно отобранных 4 мкрРНК, включающих miR-3139, miR-3189, miR-3199 и miR-8485;
на фиг. 9а показаны результаты анализа изменения цвета клеток и количества меланина, вырабатываемого при обработке клеточной линии SK-MEL-28 с применением SAMiRNA-miR-3199;
на фиг. 9b показаны результаты, подтверждающие изменения в передаче сигналов меланогенеза посредством кПЦР-РВ при обработке клеточной линии SK-MEL-28 с применением SAMiRNA-miR-3199;
на фиг. 9c показаны результаты, подтверждающие изменения в передаче сигналов меланогенеза иммуноблоттингом с обработкой SAMiRNA-miR-3199 клеточной линии SK-MEL-28;
на фиг. 9d показаны результаты, подтверждающие эффективность изменений в передаче сигналов меланогенеза иммуноцитохимическим анализом с обработкой SAMiRNA-miR-3199 клеточной линии SK-MEL-28;
на фиг. 10а показаны результаты выбора GSK3бета в качестве гена-мишени miR-3199;
на фиг. 10b показаны результаты, подтверждающие эффективность в отношении ингибирования GSK3бета посредством кПЦР-РВ при обработке SAMiRNA-miR-3199 клеточной линии SK-MEL-28;
на фиг. 10c показаны результаты, подтверждающие эффективность в отношении ингибирования GSK3бета иммуноблоттингом с обработкой SAMiRNA-miR-3199 клеточной линии SK-MEL-28;
на фиг. 10d показаны результаты, подтверждающие эффективность в отношении ингибирования GSK3бета иммуноцитохимическим анализом с обработкой SAMiRNA-miR-3199 клеточной линии SK-MEL-28;
на фиг. 10е показаны результаты, подтверждающие действие miR-3199 путем прямого связывания с 3'-UTR мРНК GSK3бета посредством анализа репортерного гена люциферазы;
на фиг. 11а показаны результаты анализа изменения цвета клеток и количества меланина, вырабатываемого при обработке SAMiRNA-miR-3199 эпидермальных меланоцитов человека;
на фиг. 11b показаны результаты, подтверждающие изменения в передаче сигналов меланогенеза посредством кПЦР-РВ при обработке SAMiRNA-miR-3199 эпидермальных меланоцитов человека;
на фиг. 11c показаны результаты, подтверждающие изменения в передаче сигналов меланогенеза иммуноблоттингом с обработкой SAMiRNA-miR-3199 эпидермальных меланоцитов человека;
на фиг. 12а показаны результаты оценки цитотоксичности SAMiRNA-miR-3199 в клетках дермальной папиллы фолликула человека, кератиноцитах и меланоцитах человека; и
на фиг. 12b показаны результаты оценки врожденной иммунотоксичности SAMiRNA-miR-3199 путем подтверждения увеличения содержания воспалительных цитокинов в мононуклеарных клетках периферической крови человека (РВМС).
Осуществление изобретения
Если не указано иное, все используемые в настоящем документе технические и научные термины имеют такие же значения, которые обычно понимаются специалистами в той области, к которой относится настоящее изобретение. В общем, используемая в настоящем документе номенклатура хорошо известна в данной области и является типичной.
В настоящем изобретении, в связи с необходимостью предотвращения или уменьшения поседения и выпадения волос, синтезировали скрининговую библиотеку на 1728 мкрРНК человека (таблица 2) и использовали для обработки клеточных линий рака кожи человека и эпидермальных меланоцитов человека, а также измеряли количество вырабатываемого меланина и анализировали изменение окрашивания клеток, в результате чего было выявлено четыре эффективные мкрРНК, включающие miR-3139, miR-3189, miR-3199 и miR-8485. Кроме того, было подтверждено, что мкрРНК способна уменьшать поседение волос за счет активации меланоцитов и стимулирования меланогенеза в выщипанных седых волосах человека, и был идентифицирован механизм действия стимулирования меланогенеза, а также посредством оценки цитотоксичности и врожденной иммунотоксичности было подтверждено, что мкрРНК способна стимулировать меланогенез в волосах без побочных эффектов. Кроме того, было подтверждено стимулирование пролиферации клеток, таких как клетки дермальной папиллы волосяного фолликула и кератиноциты, наряду с активацией меланоцитов, а также развивалась наружная корневая оболочка и увеличилась длина волос.
Соответственно, один аспект настоящего изобретения относится к фармацевтической композиции для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, включающей в качестве активного ингредиента:
(i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечную олигонуклеотидную конструкцию, имеющую структуру представленной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или
(iii) наночастицы, включающие такую двухцепочечную олигонуклеотидную конструкцию.
Другой аспект настоящего изобретения относится к косметической композиции для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, включающей в качестве активного ингредиента:
(i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечную олигонуклеотидную конструкцию, имеющую структуру представленной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или
(iii) наночастицы, включающие такую двухцепочечную олигонуклеотидную конструкцию.
В настоящем изобретении композиция способна уменьшать поседение волос, стимулировать рост волос и/или предотвращать или уменьшать выпадение волос путем активации меланоцитов и пролиферации клеток волосяных фолликулов, но настоящее изобретение не ограничивается этим.
В настоящем изобретении miR-3139 может включать нуклеотидную последовательность, представленную SEQ ID NO: 9, и нуклеотидную последовательность, представленную SEQ ID NO: 10, и предпочтительно представляет собой ДНК/ДНК, РНК/РНК или гибрид ДНК/РНК, состоящий из нуклеотидной последовательности, представленной SEQ ID NO: 9, и нуклеотидной последовательности, представленной SEQ ID NO: 10.
miR-3139
5’-CAGGCAUCUGUUGAGCUCCUAUU-3’ (SEQ ID NO: 9)
5’-UAGGAGCUCAACAGAUGCCUGUU-3’ (SEQ ID NO: 10)
В настоящем изобретении miR-3189 может включать нуклеотидную последовательность, представленную SEQ ID NO: 5, и нуклеотидную последовательность, представленную SEQ ID NO: 6, и предпочтительно представляет собой ДНК/ДНК, РНК/РНК или гибрид ДНК/РНК, состоящий из нуклеотидной последовательности, представленной SEQ ID NO: 5, и нуклеотидной последовательности, представленной SEQ ID NO: 6.
miR-3189
5’-UGCCCCAUCUGUGCCCUGGGUAGGA-3’ (SEQ ID NO: 5)
5’-CCCUUGGGUCUGAUGGGGUAG-3’ (SEQ ID NO: 6)
В настоящем изобретении miR-3199 может включать нуклеотидную последовательность, представленную SEQ ID NO: 15, и нуклеотидную последовательность, представленную SEQ ID NO: 16, и предпочтительно представляет собой ДНК/ДНК, РНК/РНК или гибрид ДНК/РНК, состоящий из нуклеотидной последовательности, представленной SEQ ID NO: 15, и нуклеотидной последовательности, представленной SEQ ID NO: 16.
miR-3199
5’-CUUUCUCCUAAGGCAGUCCCUUU-3’ (SEQ ID NO: 15)
5’-AGGGACUGCCUUAGGAGAAAGUU-3’ (SEQ ID NO: 16)
В настоящем изобретении miR-8485 может включать нуклеотидную последовательность, представленную SEQ ID NO: 1, и нуклеотидную последовательность, представленную SEQ ID NO: 2, и предпочтительно представляет собой ДНК/ДНК, РНК/РНК или гибрид ДНК/РНК, состоящий из нуклеотидной последовательности, представленной SEQ ID NO: 1, и нуклеотидной последовательности, представленной SEQ ID NO: 2.
miR-8485
5’-ACGUGUGUGUGUGUGUGUGUU-3’ (SEQ ID NO: 1)
5’-CACACACACACACACACGUAU-3’ (SEQ ID NO: 2)
В настоящем изобретении было подтверждено, что miR-3189, miR-3199 и miR-8485 повышают экспрессию фактора транскрипции, ассоциированного с микрофтальмом (MITF), тирозиназы (TYR), родственного тирозиназе белка 1 (TYRP1) и родственного тирозиназе белка 2 (TYRP2), а miR-3139 повышает экспрессию TYR и TYRP2.
Известно, что гены, экспрессия которых повышается с помощью мкрРНК по настоящему изобретению, выполняют следующие функции.
MITF, являющийся фактором транскрипции, регулирует экспрессию генов TYR, TYRP1 и TYRP2, которые являются ферментами, непосредственно участвующими в синтезе пигмента меланина, и известен как основной фактор транскрипции для развития и дифференцировки меланоцитов (D’Mello, S. A., Finlay, G. J., Baguley, B. C. & Askarian-Amiri, M. E. Signaling Pathways in Melanogenesis. Int. J. Mol. Sci. 17 (2016); Kawakami A, Fisher DE. The master role of microphthalmia-associated transcription factor in melanocyte and melanoma biology. Lab. Investig. (2017)).
TYR, TYRP1 и TYRP2 в основном участвуют в превращении тирозина в пигмент меланин и, в частности, известно, что TYR и TYRP2 являются важными ферментами, влияющими на количество и качество меланина (NIU, C., AISA, H.A., 2017: Upregulation of melanogenesis and tyrosinase activity: potential agents for vitiligo. Molecules 22, E1303. (2017); D’Mello, S. A., Finlay, G. J., Baguley, B. C. & Askarian-Amiri, M. E. Signaling Pathways in Melanogenesis. Int. J. Mol. Sci. 17 (2016)).
Как описано в предшествующем уровне техники, затравочная область в диапазоне от 2-го основания до 8-го-9-го оснований в активной последовательности мкрРНК является основным фактором активности. При получении двухцепочечного олигонуклеотида можно сконструировать и использовать длинный двухцепочечный олигонуклеотид, включающий ее.
Кроме того, мкрРНК может быть двухцепочечной и в другом варианте осуществления может включать одномолекулярный полинуклеотид. Например, это может быть антисмысловой олигонуклеотид или мкрРНК, но не ограничивается ими.
Между тем, miR-3139, miR-3189, miR-3199 или miR-8485 могут включать последовательность, в которой по меньшей мере одно основание заменено, удалено или вставлено в смысловую цепь, которая составляет ту же самую или комплементарную ей антисмысловую цепь.
Двухцепочечный олигонуклеотид в соответствии с настоящим изобретением может включать липкий конец, представляющий собой структуру, включающую один или несколько неспаренных нуклеотидов на 3’-конце одной или обеих цепей. Кроме того, смысловая цепь или антисмысловая цепь предпочтительно состоит из 19-31 нуклеотида, но не ограничивается этим.
В настоящем изобретении для олигоконъюгата, в котором гидрофильный материал и гидрофобный материал связываются с олигонуклеотидом РНК или ДНК, олигонуклеотид может быть эффективно доставлен in vivo, и его стабильность может быть повышена за счет конъюгата, в котором гидрофильный материал и гидрофобный материал конъюгированы с обоими концами олигонуклеотида РНК или ДНК.
Кроме того, самособирающиеся наночастицы образуются в результате гидрофобного взаимодействия гидрофобных материалов, и такие наночастицы обладают значительно более высокой эффективностью и стабильностью доставки in vivo, а также имеют очень однородный размер частиц благодаря структурным улучшениям, так что процесс изготовления лекарственного средства является простым, потому что QC (контроль качества) не составляет труда.
В одном варианте осуществления настоящего изобретения гидрофильный материал представлен (P)n, (Pm-J)n или (J-Pm)n, где P представляет собой мономер гидрофильного материала, n равно от 1 до 200, m равно от 1 до 15, и J представляет собой линкер, соединяющий m мономеров гидрофильного материала друг с другом или соединяющий m мономеров гидрофильного материала и олигонуклеотиды друг с другом.
В настоящем изобретении гидрофильный материал может иметь молекулярную массу от 200 до 10000.
В настоящем изобретении гидрофильный материал может быть любым материалом, выбранным из группы, состоящей из полиэтиленгликоля, поливинилпирролидона и полиоксазолина, но не ограничивается ими.
В настоящем изобретении мономер гидрофильного материала Р может иметь представленную ниже структуру соединения (1):
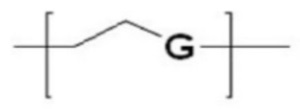 … соединение (1).
… соединение (1).
В соединении (1) G выбран из группы, состоящей из CH2, O, S и NH.
В настоящем изобретении линкер J может быть выбран из группы, состоящей из PO3-, SO3 и CO2.
В настоящем изобретении гидрофобный материал может иметь молекулярную массу от 250 до 1000, и гидрофобный материал может быть выбран из группы, состоящей из производного стероида, производного глицерида, эфира глицерола, полипропиленгликоля, ненасыщенного или насыщенного C12-С50 углеводорода, диацилфосфатидилхолина, жирной кислоты, фосфолипида и липополиамина, но не ограничивается ими.
В настоящем изобретении производное стероида может быть выбрано из группы, состоящей из холестерола, холестанола, холевой кислоты, холестерилформиата, холестанилформиата и холестериламина, но не ограничивается ими.
В настоящем изобретении производное глицерида может быть выбрано из группы, состоящей из моно-, ди- и триглицеридов, но не ограничивается ими.
В настоящем изобретении ковалентная связь, представленная X и Y, может быть либо нерасщепляемой связью, либо расщепляемой связью. В настоящем документе нерасщепляемой связью может быть амидная связь или фосфатная связь, и расщепляемой связью может быть дисульфидная связь, разлагаемая кислотой связь, сложноэфирная связь, ангидридная связь, биоразлагаемая связь или разлагаемая ферментами связь, но настоящее изобретение не ограничивается ими.
Когда гидрофильным материалом является А, двухцепочечная олигонуклеотидная конструкция по настоящему изобретению может иметь структуру представленной ниже структурной формулы (1’).
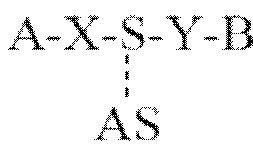 … структурная формула (1’).
… структурная формула (1’).
В структурной формуле (1’) A, B, X и Y имеют значения, определенные в структурной формуле (1), S представляет собой смысловую цепь мкрРНК, и AS представляет собой антисмысловую цепь мкрРНК.
В одном варианте осуществления настоящего изобретения двухцепочечная олигонуклеотидная конструкция, включающая мкрРНК, в соответствии с настоящим изобретением может представлять собой двухцепочечную олигонуклеотидную конструкцию, имеющую структуру представленной ниже структурной формулы (2).
A-X-5’ R 3’ Y-B … структурная формула (2).
В структурной формуле (2) A, B, X, Y и R являются такими, как определено в структурной формуле 1.
Более предпочтительно двухцепочечная олигонуклеотидная конструкция имеет структуру представленной ниже структурной формулы (2’).
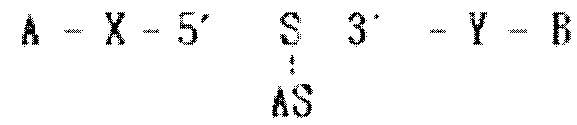 … структурная формула (2’)
… структурная формула (2’)
В одном варианте осуществления настоящего изобретения гидрофильный материал может представлять собой катионный или неионогенный полимерный материал с молекулярной массой от 200 до 10000, предпочтительно неионогенный полимерный материал с молекулярной массой от 1000 до 2000. Гидрофильный материал может представлять собой неионогенное гидрофильное полимерное соединение и может быть любым соединением, выбранным из группы, состоящей, например, из полиэтиленгликоля, поливинилпирролидона и полиоксазолина, но не ограничивается ими.
В другом варианте осуществления настоящего изобретения, когда гидрофильным материалом является (Pm-J)n или (J-Pm)n, двухцепочечная олигонуклеотидная конструкция в соответствии с настоящим изобретением имеет структуру представленной ниже структурной формулы (3) или структурной формулы (4).
(Pm-J)n-X-R-Y-B … структурная формула (3),
(J-Pm)n-X-R-Y-B … структурная формула (4).
В структурной формуле (3) и структурной формуле (4) P представляет собой мономер гидрофильного материала, n равно от 1 до 200, m равно от 1 до 15, J представляет собой линкер, соединяющий m мономеров гидрофильного материала друг с другом или соединяющий m мономеров гидрофильного материала и олигонуклеотиды друг с другом, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой специфическую мкрРНК по настоящему изобретению. Более предпочтительно двухцепочечная олигонуклеотидная конструкция, включающая мкрРНК в соответствии с настоящим изобретением имеет структуру представленной ниже структурной формулы (3’).
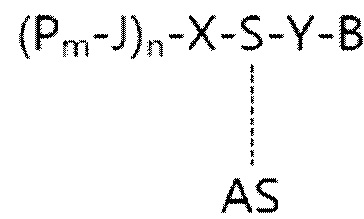 … структурная формула (3’).
… структурная формула (3’).
В структурной формуле (3') P, B, J, m, n, X и Y имеют значения, указанные в структурной формуле (3), S представляет собой смысловую цепь мкрРНК, и AS представляет собой антисмысловую цепь мкрРНК.
Более предпочтительно двухцепочечная олигонуклеотидная конструкция, включающая мкрРНК в соответствии с настоящим изобретением имеет структуру представленной ниже структурной формулы (4’).
 … структурная формула (4’).
… структурная формула (4’).
В структурной формуле (4') P, B, J, m, n, X и Y имеют значения, определенные в структурной формуле (4), S представляет собой смысловую цепь мкрРНК, и AS представляет собой антисмысловую цепь мкрРНК.
В качестве мономера гидрофильного материала P в структурной формуле (3) и структурной формуле (4) можно использовать любой мономер неионогенных гидрофильных полимеров без ограничений при условии, что он соответствует цели настоящего изобретения. Предпочтительно используют мономер, выбранный из соединения (1) - соединения (3), показанных в таблице 1 ниже, более предпочтительно используют мономер соединения (1), и G в соединении (1) предпочтительно выбирают из СН2, О, S и NH.
В частности, среди мономеров гидрофильных материалов мономер, представленный соединением (1), может включать различные введенные в него функциональные группы, может иметь превосходную биосовместимость, такую как хорошее сродство in vivo и низкий иммунный ответ, и может повышать стабильность in vivo олигонуклеотида, содержащегося в конструкции в соответствии со структурной формулой (3) и структурной формулой (4), а также эффективность его доставки, поэтому он очень подходит для изготовления конструкции в соответствии с настоящим изобретением.
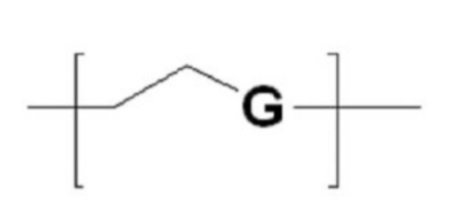
G представляет собой CH2, O, S или NH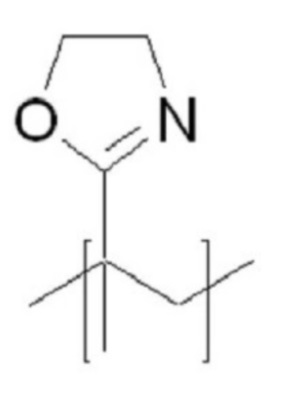
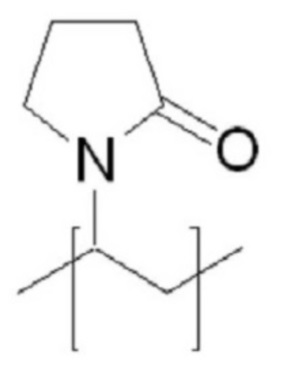
Предпочтительно, чтобы гидрофильный материал по структурной формуле (3) и структурной формуле (4) имел общую молекулярную массу в пределах от 1000 до 2000. Поэтому, например, при применении гексаэтиленгликоля в качестве соединения (1) в структурной формуле (3) и структурной формуле (4), то есть материала, в котором G означает О, а m равно 6, молекулярная масса гексаэтиленгликолевого спейсера равна 344, а число повторений n предпочтительно составляет от 3 до 5. Настоящее изобретение отличается тем, что повторяющееся звено гидрофильной группы, представленное в виде (Pm-J) или (J-Pm) в структурной формуле (3) и структурной формуле (4), то есть блок гидрофильного материала, может использоваться в соответствующем количестве, представленном n, по необходимости. Мономер P гидрофильного материала и линкер J, входящие в каждый из блоков гидрофильного материала, могут независимо быть одинаковыми или разными в блоках гидрофильного материала. В частности, при применении трех блоков гидрофильного материала (n=3), первый блок может включать мономер гидрофильного материала в соответствии с соединением (1), второй блок может включать мономер гидрофильного материала в соответствии с соединением (2), а третий блок может включать мономер гидрофильного материала в соответствии с соединением (3). Таким образом, можно использовать различные мономеры гидрофильного материала для всех блоков гидрофильного материала или же использовать какой-либо мономер гидрофильного материала, выбранный из мономеров гидрофильного материала в соответствии с соединением (1) - соединением (3), одинаковый для всех блоков гидрофильного материала. Точно также же в качестве линкера, который опосредует связывание мономеров гидрофильного материала, можно использовать один и тот же линкер для блоков гидрофильного материала или же разные линкеры для блоков гидрофильного материала. Кроме того, m, то есть количество мономеров гидрофильного материала, может быть одинаковым или различным в блоках гидрофильного материала. В частности, в первом блоке гидрофильного материала могут соединяться три мономера гидрофильного материала (m=3), во втором блоке гидрофильного материала могут соединяться пять мономеров гидрофильного материала (m=5) и в третьем блоке гидрофильного материала могут соединяться четыре мономера гидрофильного материала (m=4). Таким образом, можно использовать различные количества мономеров гидрофильного материала или же использовать одинаковое количество мономеров гидрофильного материала во всех блоках гидрофильного материала.
В настоящем изобретении линкер J предпочтительно выбирают из группы, состоящей из PO3-, SO3 и CO2, но не ограничиваются этим. Можно использовать любой линкер, если только он соответствует цели настоящего изобретения, в зависимости от используемого мономера гидрофильного материала, как это должно быть очевидно специалистам в данной области.
Все или часть мономеров гидрофильного материала могут быть модифицированы, чтобы иметь функциональную группу, необходимую для связывания с другими материалами, такими как мишень-специфический лиганд, по необходимости.
В некоторых случаях от одной до трех фосфатных групп могут связываться с 5'-концом антисмысловой цепи двухцепочечной олигонуклеотидной конструкции, включая ген-специфическую мкрРНК.
Например, двухцепочечная олигонуклеотидная конструкция, включающая мкрРНК, имеет структуру представленной ниже структурной формулы (3”) или структурной формулы (4”).
 … структурная формула (3”)
… структурная формула (3”)
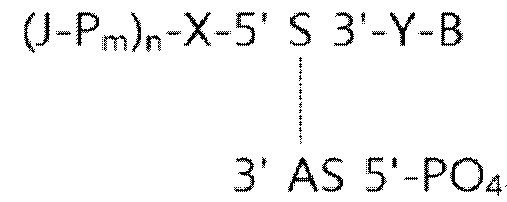 … структурная формула (4”)
… структурная формула (4”)
Гидрофобный материал В служит для формирования наночастиц, состоящих из олигонуклеотидной конструкции согласно структурной формуле (1), посредством гидрофобного взаимодействия.
Гидрофобный материал предпочтительно имеет молекулярную массу от 250 до 1000, и его примеры могут включать, но без ограничения, производное стероида, производное глицерида, эфир глицерина, полипропиленгликоль, ненасыщенный или насыщенный C12-C50 углеводород, диацилфосфатидилхолин, жирную кислоту, фосфолипид, липополиамин и т.п., а также любой гидрофобный материал может быть применен при условии, что он соответствует цели настоящего изобретения, как это будет очевидно для специалистов в области, к которой относится настоящее изобретение.
Производное стероидов может быть выбрано из группы, состоящей из холестерина, холестанола, холевой кислоты, холестерилформиата, холестанилформиата и холестериламина, а производное глицерида может быть выбрано из группы, состоящей из моно-, ди- и триглицерида. При этом жирная кислота глицерида предпочтительно представляет собой ненасыщенную или насыщенную C12-C50 жирную кислоту.
В частности, среди гидрофобных материалов предпочтительными являются насыщенные или ненасыщенные углеводороды или холестерин, так как они обладают тем преимуществом, что они способны легко связываться во время синтеза олигонуклеотидной конструкции по настоящему изобретению.
Гидрофобный материал может связываться с дистальным концом гидрофильного материала и может связываться с любым положением на смысловой или антисмысловой цепи мкрРНК.
В настоящем изобретении гидрофильный материал, блок гидрофильного материала или гидрофобный материал и олигонуклеотид связаны простой ковалентной связью или ковалентной связью, опосредованной линкером (X или Y). Ковалентная связь может быть нерасщепляемой связью или расщепляемой связью. При этом нерасщепляемой связью может быть амидная связь или фосфатная связь, а расщепляемой связью может быть дисульфидная связь, расщепляемая кислотой связь, сложноэфирная связь, ангидридная связь, биоразлагаемая связь или расщепляемая ферментами связь, но настоящее изобретение этим не ограничивается.
Последовательность мкрРНК, которую можно использовать в качестве активного ингредиента композиции для уменьшения поседения волос, предотвращения или уменьшения выпадения волос, стимулирования пролиферации клеток волосяных фолликулов и/или стимулирования роста волос путем активации меланоцитов и стимулирования меланогенеза, в соответствии с настоящим изобретением, может включать последовательности, происходящие из генома человека, или геном, из которого происходят мкрРНК, не ограничивается геномом человека, и также могут быть применены последовательности мкрРНК, происходящие из геномов других животных.
мкрРНК можно использовать в любой имитирующей мкрРНК форме, которая обеспечивает биоэквивалентную эффективность мкрРНК, и можно использовать модифицированную мкрРНК, включающую последовательность мкрРНК, содержащую ту же затравочную область. При этом длина смысловой и антисмысловой последовательностей мкрРНК может быть уменьшена, а также может быть применен короткий миметик длиной 15 нуклеотидов.
Миметик мкрРНК для мкрРНК может частично включать фосфоротиоатную структуру, которая представляет собой форму, в которой структура фосфатного остова РНК замещена другим элементом, таким как сера, и может быть применена в форме, в которой РНК является полностью или частично замещенной молекулами ДНК, PNA (пептидонуклеиновая кислота) или LNA (запертая нуклеиновая кислота). Более того, его можно использовать в форме, в которой 2’-гидроксильная группа РНК-сахара замещена различными функциональными структурами, которые включают, но без ограничения, метилирование, метоксилирование, фторирование и т.д.
мкрРНК не ограничивается двухцепочечной РНК зрелой мкрРНК и полученным из нее миметиком мкрРНК, и может использоваться в форме предшественника мкрРНК. Предшественник мкрРНК также может включать описанную выше структуру фосфатного остова РНК, частичную или полную замену РНК ДНК, PNA, LNA и т.д., модификацию 2’-гидроксильной группы молекулы РНК-сахара и т.п.
мкрРНК можно использовать в форме предшественника мкрРНК или первичной мкрРНК (пре-мкрРНК), которая может быть химически синтезирована или доставлена в клетки в форме плазмиды и, таким образом, экспрессирована.
В настоящем изобретении мкрРНК может быть доставлена в клетки, культивированные в чашке для культивирования, с помощью способов применения смеси с катионными липидами, путем электрической стимуляции или применения вируса. Различные способы, известные в данной области для доставки мкрРНК, могут быть легко осуществлены специалистами в данной области, и настоящее изобретение ими не ограничивается.
Еще один аспект настоящего изобретения относится к двухцепочечной олигонуклеотидной конструкции, включающей мкрРНК, такую как miR-3139, miR-3189, miR-3199 или miR-8485, и к наночастицам, включающим ее.
Как описано выше, двухцепочечная олигонуклеотидная конструкция, включающая мкрРНК, является амфифильной, содержащей как гидрофобные, так и гидрофильные материалы, и гидрофильная часть направлена наружу из-за сродства посредством взаимодействий, таких как водородные связи и т.д., с молекулами воды, присутствующими в организме, и гидрофобные материалы направлены внутрь за счет гидрофобного взаимодействия между ними с образованием термодинамически стабильных наночастиц. В частности, обеспечены наночастицы для защиты последовательности мкрРНК путем размещения гидрофобного материала в центре наночастиц и гидрофильного материала снаружи двухцепочечного олигонуклеотида, включающего мкрРНК.
Наночастицы в соответствии с настоящим изобретением могут быть составлены только с двухцепочечной олигонуклеотидной конструкцией, содержащей олигонуклеотиды с одинаковой последовательностью, или же они могут состоять из двухцепочечной олигонуклеотидной конструкции, содержащей олигонуклеотиды с разными последовательностями, и двухцепочечные олигонуклеотидные конструкции, включающие различные мкрРНК, нацеленные на гены, стимулирующие меланогенез и стимулирующие пролиферацию клеток волосяных фолликулов, могут быть включены в наночастицы в соответствии с настоящим изобретением. Например, наночастицы могут быть образованы путем смешивания двухцепочечной олигонуклеотидной конструкции, включающей miR-3139, и двухцепочечной олигонуклеотидной конструкции, включающей miR-8485.
Кроме того, композиция в соответствии с настоящим изобретением может дополнительно включать, в дополнение к двухцепочечной олигонуклеотидной конструкции, включающей мкрРНК, двухцепочечный олигонуклеотид, включающий мкрРНК, который активирует меланоциты и способствует меланогенезу и пролиферации клеток волосяных фолликулов, или двухцепочечную олигонуклеотидную конструкцию, включающую то же самое.
В настоящем изобретении было подтверждено, что двухцепочечная олигонуклеотидная конструкция (SAMiRNA™), включающая мкрРНК и наночастицы, эффективно активирует меланоциты и способствует меланогенезу, тем самым уменьшая поседение волос. Кроме того, в дополнение к активации меланоцитов был подтвержден эффект стимуляции пролиферации клеток дермальной папиллы волосяного фолликула и кератиноцитов.
Таким образом, настоящее изобретение позволяет использовать композицию для фармацевтического и косметического применения, при этом фармацевтическая композиция может быть применена в любом составе, выбранном из таких составов, как мази, пасты, гели, желе, сыворотки, аэрозольные спреи, неаэрозольные спреи, пены, кремы, лосьоны, растворы и суспензии, но не ограничиваются этим.
Когда композицию применяют в качестве косметического средства, ее можно использовать в любом составе, выбранном из составов, таких как тоники для волос, кондиционеры для волос, эссенции для волос, лосьоны для волос, питательные лосьоны для волос, шампуни для волос, ополаскиватели для волос, лечебные средства для волос, крема для волос, питательные крема для волос, крема для увлажнения волос, крема для массажа волос, воски для волос, аэрозоли для волос, маски для волос, питательные маски для волос, мыла для волос, очищающие пены для волос, масла для волос, средства для сушки волос, защитного средства для волос, краски для волос, средства для завивки волос, средства для обесцвечивания волос, гели для волос, блески для волос, средства для укладки волос, лаки для волос, увлажняющие средства для волос, муссы для волос и распылители для волос, но не ограничиваются ими.
Композиция по настоящему изобретению может быть получена путем включения по меньшей мере одного фармацевтически приемлемого носителя в дополнение к указанному выше активному ингредиенту. Такой фармацевтически приемлемый носитель должен быть совместим с активным ингредиентом по настоящему изобретению и может включать физиологический раствор, стерильную воду, раствор Рингера, забуференный физиологический раствор, раствор декстрозы, раствор мальтодекстрина, глицерин и этанол, которые можно использовать отдельно или в комбинации двух или более из них, и, при необходимости, могут быть добавлены другие типичные добавки, такие как антиоксиданты, буферы и бактериостатические агенты. Кроме того, могут быть дополнительно добавлены разбавители, диспергирующие, поверхностно-активные, связующие и смазывающие вещества для получения инъекционного состава, такого как водный раствор, суспензия, эмульсия и т.п. В частности, предпочтительно получение составов в лиофилизированной форме. Для приготовления лиофилизированного состава можно использовать способ, широко известный в той области, к которой относится настоящее изобретение, а также можно добавлять стабилизатор для лиофилизации. Кроме того, композицию предпочтительно составляют в зависимости от каждого заболевания или ингредиента подходящим методом из данной области или методом, описанным в Remington’s Pharmaceutical Science (Mack Publishing Company, Easton PA).
Количество и способ введения активного ингредиента и пр., включенных в композицию по настоящему изобретению, могут быть определены специалистами в данной области на основании количества меланоцитов, степени функционального ухудшения, симптомов поседения и тяжести седеющего участка обычного индивидуума. Кроме того, композиция может быть составлена в различных формах, таких как порошки, таблетки, инъекции, мази и функциональные косметические средства, и может поставляться в контейнерах для однократных или многократных доз, таких как запечатанные ампулы и флаконы.
Когда двухцепочечную олигонуклеотидную конструкцию, включающую мкрРНК в соответствии с настоящим изобретением, и композиции или наночастицы, включающие ее, применяют для изготовления функциональных косметических средств или препаратов для местного нанесения на кожу, состав функциональных косметических средств или препаратов для местного нанесения на кожу может быть выбран из группы, состоящей из кремов, лосьонов, гелей, водорастворимых жидкостей и эссенций, но не ограничивается этим.
Еще один аспект настоящего изобретения относится к способу уменьшения поседения волос, стимулированию роста волос и/или предотвращению или уменьшению выпадения волос, включающему введение субъекту, нуждающемуся в уменьшении поседения волос, стимулировании роста волос и/или предотвращении или уменьшении выпадения волос,
(i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечной олигонуклеотидной конструкции, имеющий структуру представленной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или
(iii) наночастиц, включающих такую двухцепочечную олигонуклеотидную конструкцию.
Еще один аспект настоящего изобретения относится к применению для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос,
(i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечной олигонуклеотидной конструкции, имеющей структуру представленной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или (iii) наночастиц, включающих такую двухцепочечную олигонуклеотидную конструкцию.
Еще один аспект настоящего изобретения относится к применению (i) miR-3139, miR-3189, miR-3199 или miR-8485;
(ii) двухцепочечной олигонуклеотидной конструкции, имеющей структуру приведенной ниже структурной формулы (1):
A-X-R-Y-B … структурная формула (1),
в структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, и R представляет собой miR-3139, miR-3189, miR-3199 или miR-8485; или (iii) наночастиц, включающих такую двухцепочечную олигонуклеотидную конструкцию, для изготовления лекарственных средств или косметических средств для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос.
Примеры
Лучше понять настоящего изобретения можно при помощи следующих примеров. Эти примеры приводятся просто для иллюстрации настоящего изобретения и не должны рассматриваться как ограничивающие объем настоящего изобретения, что должно быть ясно специалистам в данной области.
Пример 1. Скрининг для отбора мкрРНК, способствующих меланогенезу
1-1. Кандидаты в мкрРНК человека, способствующие меланогенезу
В качестве 21 версии последовательностей мкрРНК человека, предоставленных miRBase (www.mirbase.org), которая представляет собой базу данных мкрРНК, было синтезировано 1728 мкрРНК на основе структуры «стебель-петля» в форме, нагруженной на двухцепочечную олигонуклеотидную конструкцию (SAMiRNA™) (таблица 2). Для синтеза предполагаемой последовательности все синтезированные цепи мкрРНК были идентифицированы и подтверждены с применением масс-спектрометрии MALDI-TOF. Был проведен скрининг для обнаружения мкрРНК с самым высоким количеством меланина, вырабатываемого с применением 1728 мкрРНК в клеточных линиях рака кожи человека. Последовательности антисмысловых цепей 1728 человеческих мкрРНК, протестированных в настоящем изобретении, известны по miRbase (http://www.mirbase.org), и когда исходная область была предоставлена только на одной цепи, была синтезирована комплементарная ей последовательность для доставки к клеткам в двухцепочечной форме.
Например, мкрРНК miR-3139 получали следующим образом.
SEQ ID NO: 9: 5’-CAGGCAUCUGUUGAGCUCCUAUU-3’
SEQ ID NO: 10: 5’-UAGGAGCUCAACAGAUGCCUGUU-3’
Кроме того, когда затравочная последовательность обеспечена на обеих цепях, соответствующие цепи были синтезированы как смысловые и антисмысловые цепи. Например, мкрРНК miR-3189 получали следующим образом.
SEQ ID NO: 5: 5’-UGCCCCAUCUGUGCCCUGGGUAGGA-3’ (смысловая)
SEQ ID NO: 6: 5’-CCCUUGGGUCUGAUGGGGUAG-3’ (антисмысловая)
1-2. Клеточная культура и трансфекция мкрРНК
Для обнаружения мкрРНК, которые индуцируют выработку меланина, использовали меланому человека M21 (Корейский банк клеточных линий, KR), которая представляет собой клеточную линию рака кожи, полученную от человека. Клетки М21 культивировали при 37°C/5% CO2 в среде DMEM (Hyclone, США) с добавлением 10% эмбриональной бычьей сыворотки (FBS, Hyclone, США) и 1% пенициллина-стрептомицина (Hyclone, США). Клетки М21 распределяли по 4×104 клеток/лунку в 12-луночный планшет (Falcon, США) и на следующий день трансфицировали мкрРНК при концентрации 40 нМ с применением Lipofectamine RNAiMAX (Invitrogen, США) в соответствии с протоколом изготовителя.
1-3. Скрининг 1728 мкрРНК путем измерения количества вырабатываемого меланина
Клетки М21 трижды трансфицировали 1728 мкрРНК с помощью способа по примеру 1-2. После культивирования в течение 72 часов все клетки собирали и оставляли реагировать в 1 М растворе NaOH (Bioneer, KR) в течение 2 часов при 37°C в соответствии с протоколом экстракции меланина, после чего измеряли поглощение при длине волны 405 нм для сравнения изменения окрашивания и количества вырабатываемого меланина. После культивирования в течение 72 часов все клетки собирали и оставляли реагировать в 1 М растворе NaOH (Bioneer, KR) в течение 2 часов при 37°C в соответствии с протоколом экстракции меланина, после чего измеряли поглощение при длине волны 405 нм и, таким образом, анализировали количество вырабатываемого меланина. Для оценки воспроизводимости 9 лучших мкрРНК использовали для обработки клеток М21 с помощью способа по примеру 1-2. После культивирования в течение 72 часов все клетки собирали и оставляли реагировать в 1 М растворе NaOH (Bioneer, KR) в течение 2 часов при 37°C в соответствии с протоколом экстракции меланина, после чего измеряли поглощение при длине волны 405 нм и, таким образом, анализировали количество вырабатываемого меланина.
Таким образом, в клетках M21, обработанных в общей сложности 1728 мкрРНК, было отобрано 9 мкрРНК, демонстрирующих выработку меланина в количестве 13,0 мкг/мл или более (в 1,88 или более раз больше по сравнению с отрицательным контролем) и количество выработанного меланина, сходное с группой, обработанной положительным контролем IBMX (Sigma, США)/CuSO4 (Sigma, США) (фиг. 1). В повторных экспериментах для оценки воспроизводимости изменение окрашивания и меланогенез подтверждали в клеточной линии М21 с помощью выбранных 9 лучших мкрРНК по сравнению с группой отрицательного контроля (фиг. 2, таблица 3).
Пример 2. Окончательный отбор индуцирующих меланин мкрРНК путем оценки воспроизводимости 9 отобранных мкрРНК и анализа механизма меланогенеза
2-1. Клеточная культура и трансфекция мкрРНК
SK-MEL-28 (Корейский банк клеточных линий, KR), представляющая собой клеточную линию рака кожи, полученную от человека, использовали для оценки воспроизводимости 9 основных мкрРНК для меланогенеза. Клетки SK-MEL-28 культивировали при 37°C/5% CO2 в МЕМ (Hyclone, США) с добавлением 10% ФБС (Hyclone, США) и 1% пенициллина-стрептомицина (Hyclone, США). Клетки SK-MEL-28 распределяли по 4×104 клеток/лунку в 12-луночный планшет (Falcon, США) и на следующий день трансфицировали мкрРНК при концентрации 40 нМ с применением Lipofectamine RNAiMAX (Invitrogen, США) в соответствии с протоколом изготовителя.
2-2. Оценка воспроизводимости лучших 9 мкрРНК посредством анализа количества вырабатываемого меланина
Чтобы оценить воспроизводимость отобранных 9 лучших мкрРНК, изменение окрашивания и количество вырабатываемого меланина измеряли в клетках SK-MEL-28. Клетки SK-MEL-28 трижды трансфицировали каждой из miR-8485, miR-7978, miR-6074, miR-3132, miR-4644, miR-3139, miR-3189, miR-3199 и miR-933 с помощью способа по примеру 2-1. После культивирования в течение 72 часов все клетки собирали и наблюдали изменение окрашивания. Для измерения количества вырабатываемого меланина реакцию проводили в 1 М растворе NaOH (Bioneer, KR) в течение 2 часов при 37°C в соответствии с протоколом экстракции меланина, после чего измеряли поглощение при длине волны 405 нм и, таким образом, анализировали количество вырабатываемого меланина.
Таким образом, в группе, обработанной miR-8485, miR-7978, miR-6074, miR-3132, miR-4644, miR-3139, miR-3189, miR-3199 или miR-933, наблюдалось отчетливое изменение окрашивания и увеличение количества вырабатываемого меланина по сравнению с группой отрицательного контроля. Значительное изменение окрашивания и увеличение количества вырабатываемого меланина подтверждались при сравнении с положительным контрольным индуктором меланина (фиг. 3).
2-3. Анализ путей передачи сигналов, которые опосредуют меланогенез, с помощью кПЦР-РВ в клетках SK-MEL-28.
Чтобы проанализировать механизм действия выбранных лучших 9 мкрРНК для стимулирования меланогенеза, проводили кПЦР-РВ для анализа генов MITF, TYR, TYRP1 и TYRP2, которые являются ключевыми факторами меланогенеза. Клетки SK-MEL-28 распределяли по 4×104 клеток/лунку в 12-луночный планшет (Falcon, США) и затем культивировали при 37°C/5% CO2. На следующий день с помощью способа по примеру 2-1 клетки SK-MEL-28 трижды трансфицировали каждой из miR-8485, miR-7978, miR-6074, miR-3132, miR-4644, miR-3139, miR-3189, miR-3199 и miR-933. После культивирования в течение 96 часов общую РНК экстрагировали из клеточного лизата с применением набора Universal RNA extraction kit (Bioneer, KR) и, используя эту РНК в качестве матрицы, оценивали уровни экспрессии мРНК генов (набор Human qPCR panel kit, Bioneer, KR) и RPL13A (набор праймеров Human reference qPCR primer set, Bioneer, KR) с помощью количественной кПЦР-РВ с применением AccuPower GreenStar™ qRT-PCR Master Mix (Bioneer, KR) в соответствии с протоколом изготовителя. Значения Ct двух генов, полученные массовой кПЦР, подвергали относительной количественной оценке с помощью метода типа «два дельта Ct» [Livak KJ, Schmittgen TD. 2001. Methods. Dec;25(4):4 02-8], в результате чего рассчитывали относительное количество (кратное изменение) мРНК каждого гена в экспериментальной группе по сравнению с контрольной группой. Последовательности праймеров для отдельных генов показаны ниже (таблица 4).
Таким образом, было подтверждено, что экспрессия генов TYR, TYRP1 и TYRP2, которые представляют собой ферменты, непосредственно участвующие в синтезе меланина в меланосомах, увеличилась с помощью 9 мкрРНК (фиг. 4). В случае MITF, который является фактором транскрипции, наблюдалось слабое увеличение или отсутствие изменения экспрессии гена. Полагают, что это связано с наличием механизма регуляции MITF, влияющего не только на экспрессию генов, но также на стабильность и активность белка.
2-4. Анализ путей передачи сигналов, которые опосредуют меланогенез, с помощью кПЦР-РВ в меланоцитах человека
Экспрессию генов MITF, TYR, TYRP1 и TYRP2 с помощью 9 мкрРНК анализировали с применением эпидермальных меланоцитов человека, полученных из ткани кожи человека дикого типа. Эпидермальные меланоциты человека (Invitrogen, США) распределяли по 1×105 клеток/лунку в 12-луночный планшет (Falcon, США) с последующим культивированием при 37°C/5% CO2 в культуре клеток млекопитающих/культуре первичных клеток (Gibco, США), содержащий добавку-2 для роста меланоцитов человека (Gibco, США). На следующий день клетки обрабатывали каждой из miR-8485, miR-7978, miR-6074, miR-3132, miR-4644, miR-3139, miR-3189, miR-3199 и miR-933 при концентрации 5 мкМ. После культивирования в течение 96 часов общую РНК экстрагировали из клеточного лизата с применением набора Universal RNA extraction kit (Bioneer, KR) и, используя эту РНК в качестве матрицы, анализировали уровни экспрессии мРНК генов (набор Human qPCR panel kit, Bioneer, KR) и RPL13A (набор Human reference qPCR primer set, Bioneer, KR) с помощью кПЦР-РВ с применением AccuPower GreenStar™ qRT-PCR Master Mix (Bioneer, KR) в соответствии с протоколом изготовителя.
Таким образом, в меланоцитах человека дикого типа, в отличие от результатов для клеток меланомы М21, экспрессия гена MITF с применением miR-8485, miR-7978, miR-3139, miR-3189, miR-3199 или miR-933 увеличилась примерно в 1,2-1,7 раз по сравнению с группой отрицательного контроля. Кроме того, экспрессия TYR увеличилась примерно в 1,2-3,1 раза с применением 9 мкрРНК. Для TYRP1 и TYRP2 различия в паттернах экспрессии наблюдались для каждой из 9 мкрРНК. Для miR-8485, miR-7978, miR-3189, miR-3199 и miR-933, экспрессия как TYRP1, так и TYRP2 имела тенденцию к увеличению, а для miR-6074, miR-3139 и miR-4644 увеличилась только экспрессия TYRP2 (фиг. 5).
2-5. Анализ путей передачи сигналов, которые опосредуют меланогенез, с помощью вестерн-блоттинга в клетках SK-MEL-28
Вестерн-блоттинг проводили для анализа экспрессии белков MITF и TYR, которые являются важными факторами в процессе меланогенеза. Клетки SK-MEL-28 распределяли по 1×105 клеток/лунку в 6-луночный планшет (Falcon, США) и затем культивировали при 37°C/5% CO2. На следующий день клетки SK-MEL-28 трансфицировали каждой из miR-3139, miR-3189, miR-3199 и miR-8485 с помощью способа по примеру 2-1. После культивирования в течение 96 часов проводили анализ в соответствии с протоколом вестерн-блоттинга. В качестве первичных антител использовали MITF (Santa Cruz Biotechnology, Inc, США) и тирозиназу (Santa Cruz Biotechnology, Inc, США), а HRP-связанный анти-мышиный IgG (Cell Signaling Technology, США) и HRP-связанный анти-кроличий IgG (Cell Signaling Technology, США) использовали в качестве вторичных антител.
Таким образом, было подтверждено, что экспрессия белков MITF и TYR увеличилась с применением 9 мкрРНК, как и результаты кПЦР-РВ, представленные выше (фиг. 6). На основании результатов изменения окрашивания клеток, количества синтезированного меланина и экспрессии основных генов и белков в меланогенезе с обработкой выбранными лучшими 9 мкрРНК, были окончательно отобраны 4 типа miR-3139, miR-3189, miR-3199 и miR-8485 с самым высоким количеством синтезированного меланина и четкой экспрессией генов и белков MITF, TYR и TYRP1/2 (таблица 5).
Пример 3. Оценка меланогенной функции окончательно отобранных 4 мкрРНК на выщипанных седых волосах человека
Меланогенную функцию оценивали на выщипанных седых волосах человека с применением окончательно отобранных 4 мкрРНК. Волосы собирали путем выдергивания седых волос с их кончиков в день эксперимента, и волосы отрезали на расстоянии примерно 1-2 см от корня волоса и культивировали в 200 мкл среды DMEM/F12 (Gibco, США) с добавлением 10% ФБС (Hyclone, США) и 1% пенициллина-стрептомицина (Hyclone, США) в 24-луночном планшете (Falcon, США). Выщипанные седые волосы обрабатывали каждой из 4 мкрРНК при концентрации 5 мкМ в течение 35 дней с 2-дневными интервалами, и наблюдали за пролиферацией первичных клеток, происходящих из волосяного фолликула, изменением цвета волос и появлением седых волос.
Таким образом, в необработанных седых волосах в течение периода лечения не было значительных изменений, но у обработанных miR-3139, miR-3189, miR-3199 или miR-8485 седых волос внешняя корневая оболочка волосяных фолликулов со временем расширялись, и наблюдалась повышенная пролиферация или миграция первичных клеток, происходящих из волосяных фолликулов, включая клетки дермальной папиллы, меланоциты и кератиноциты, а также увеличение длины волосяных фолликулов (фиг. 7). Кроме того, было подтверждено, что седой волосяной фолликул постепенно менялся на коричневый цвет (фиг. 8).
Пример 4. Оценка меланогенной функции SAMiRNA-miR-3199 в клетках SK-MEL-28
4-1. Клеточная культура и обработка с применением SAMiRNA-miR-3199
SK-MEL-28 (Корейский банк клеточных линий, KR), которая представляет собой клеточную линию рака кожи человеческого происхождения, использовали для оценки эффекта SAMiRNA-miR-3199 на стимулирование меланогенеза. Клетки SK-MEL-28 культивировали при 37°C/5% CO2 в МЕМ (Hyclone, США) с добавлением 10% ФБС (Hyclone, США) и 1% пенициллина-стрептомицина (Hyclone, США). Клетки SK-MEL-28 распределяли по 4×104 клеток/лунку в 12-луночный планшет (Falcon, США), а затем на следующий день обрабатывали при концентрации 5 мкМ.
4-2. Анализ количества меланина, вырабатываемого при обработке SAMiRNA-miR-3199
Клетки SK-MEL-28 обрабатывали SAMiRNA-miR-3199 с помощью способа по примеру 4-1. После культивирования в течение 72 часов все клетки собирали и наблюдали за изменением окрашивания. Для измерения количества вырабатываемого меланина реакцию проводили в 1 М растворе NaOH (Bioneer, KR) в течение 2 часов при 37°C в соответствии с протоколом экстракции меланина, после чего измеряли поглощение при длине волны 405 нм и, таким образом, анализировали количество вырабатываемого меланина.
Таким образом, при обработке SAMiRNA-miR-3199 наблюдалось четкое изменение окрашивания и увеличение количества меланина по сравнению с отрицательным контролем (фиг. 9a).
4-3. Анализ сигнальных путей меланогенеза при обработке SAMiRNA-miR-3199
кПЦР-РВ проводили для анализа меланогенных генов MITF, TYR, TYRP1 и TYRP2 с обработкой SAMiRNA-miR-3199. Клетки SK-MEL-28 обрабатывали SAMiRNA-miR-3199 с помощью способа по примеру 4-1. После культивирования в течение 96 часов общую РНК экстрагировали из клеточного лизата с применением набора Universal RNA extraction kit (Bioneer, KR), и, используя эту РНК в качестве матрицы, анализировали уровни экспрессии мРНК генов (Human qPCR panel kit, Bioneer, KR) и RPL13A (Human reference qPCR primer set, Bioneer, KR) с помощью кПЦР-РВ с применением AccuPower GreenStar™ qRT-PCR Master Mix (Bioneer, KR) в соответствии с протоколом изготовителя. Значения Ct двух генов, полученные массовой кПЦР, подвергали относительной количественной оценке с помощью метода типа «два дельта Ct» [Livak KJ, Schmittgen TD. 2001. Methods. Dec; 25(4):4 02-8], в результате чего рассчитывали относительное количество (кратное изменение) мРНК каждого гена в экспериментальной группе по сравнению с контрольной группой.
Таким образом, было подтверждено, что экспрессия MITF, который является ключевым фактором транскрипции для синтеза меланина, была значительно увеличена при обработке SAMiRNA-miR-3199, а также была значительно увеличена экспрессия генов TYR, TYRP1 и TYRP2, которые являются ключевыми ферментами для синтеза меланина (фиг. 9b).
4-4. Анализ экспрессии меланогенного белка при обработке SAMiRNA-miR-3199
Иммуноблотинг проводили для анализа экспрессии белков MITF и TYR, которые являются ключевыми факторами меланогенеза. Клетки SK-MEL-28 распределяли по 1×105 клеток/лунку в 6-луночный планшет (Falcon, США) и затем культивировали при 37°C/5% CO2. На следующий день клетки SK-MEL-28 обрабатывали SAMiRNA-miR-3199. После культивирования в течение 96 часов проводили анализ в соответствии с протоколом иммуноблоттинга. В качестве первичных антител использовали MITF (Santa Cruz Biotechnology, Inc, US), тирозиназу (Santa Cruz Biotechnology, Inc, US) и альфа-тубулин (Cell Signaling Technology, US), а в качестве вторичных антител использовали HRP-связанный анти-мышиный IgG (Cell Signaling Technology, US) и HRP-связанный анти-кроличий IgG (Cell Signaling Technology, US).
Таким образом, было подтверждено, что экспрессия белков MITF и TYR значительно увеличилась при обработке SAMiRNA-miR-3199, как в случае результатов анализа экспрессии генов с помощью кПЦР-РВ (фиг. 9c).
4-5. Анализ внутриклеточной экспрессии меланогенного белка при обработке SAMiRNA-miR-3199
Иммуноцитохимический анализ проводили для анализа внутриклеточной экспрессии белков MITF и TYR, которые являются ключевыми факторами меланогенеза. Перед распределением клеток покровное стекло помещали в 12-луночный планшет (Falcon, US) и покрывали поли-L-лизином (Sigma, US) на 1 час, после чего клетки SK-MEL-28 распределяли при 2×104 клеток/лунку и культивировали при 37°C/5% CO2. На следующий день клетки SK-MEL-28 обрабатывали SAMiRNA-miR-3199 с помощью способа по примеру 4-1. После культивирования в течение 96 часов реакцию проводили в 0,1% растворе Triton-X100 в течение 10 минут для пермеабилизации клеток, а затем блокировали в растворе, содержащем 1% БСА (Sigma, US) в течение 1 часа. Здесь, MITF (Abcam, UK) и тирозиназу (Santa Cruz Biotechnology, Inc, US) использовали в качестве первичных антител, а в качестве вторичных антител использовали антитела против IgG мыши, конъюгированные с Alexa Fluor 594 (Cell Signaling Technology, US), и антитела против IgG кролика, конъюгированные с Alexa Fluor 488 (Cell Signaling Technology, US). Для флуоресцентного анализа окрашенных клеток изображения анализировали с применением конфокального микроскопа с вращающимся диском (Dragonfly high-speed confocal image platform, Andor).
Таким образом, было подтверждено, что с обработкой с применением SAMiRNA-miR-3199 экспрессия MITF, который является фактором транскрипции, значительно увеличилась в ядре, и экспрессия TYR, которая является ключевым ферментом для синтеза меланина, значительно увеличилась в цитоплазме с меланосомами (фиг. 9d).
Пример 5. Анализ механизма меланогенеза SAMiRNA-miR-3199
5-1. Идентификация целевого гена miR-3199
Среди многих генов, которые согласно прогнозам с применением программы прогнозирования генов-мишеней мкрРНК (TargetScan, http://www/targetscan.org/) могут связываться с затравочной последовательностью miR-3199, был выбран ген GSK3β, известный как ключевая сигнальная молекула в меланогенезе. Было предсказано связывание miR-3199 с 4153-4159 3'-UTR GSK3β (фиг. 10а).
5-2. Анализ ингибирующих эффектов SAMiRNA-miR-3199 на мРНК GSK3β
кПЦР-РВ проводили для анализа воздействия SAMiRNA-miR-3199 на ингибирование мРНК гена-мишени GSK3β. Клетки SK-MEL-28 распределяли по 4×104 клеток/лунку в 12-луночный планшет (Falcon, US) и затем культивировали при 37°C/5% CO2. На следующий день клетки SK-MEL-28 обрабатывали SAMiRNA-miR-3199 с помощью способа по примеру 4-1. После культивирования в течение 24 часов общую РНК экстрагировали из клеточного лизата с применением набора Universal RNA extraction kit (Bioneer, KR), и, используя эту РНК в качестве матрицы, анализировали уровни экспрессии мРНК GSK3β (Bioneer, KR) и RPL13A (Human reference qPCR primer set, Bioneer, KR) с помощью кПЦР-РВ с применением AccuPower GreenStar™ qRT-PCR Master Mix (Bioneer, KR) в соответствии с протоколом изготовителя. Значения Ct двух генов, полученные массовой кПЦР, подвергали относительной количественной оценке с помощью метода типа «два дельта Ct» [Livak KJ, Schmittgen TD. 2001. Methods. Dec; 25(4):4 02-8], в результате чего рассчитывали относительное количество (кратное изменение) мРНК каждого гена в экспериментальной группе по сравнению с контрольной группой. Ниже показаны последовательности праймеров для GSK3β (таблица 6).
Таким образом, было подтверждено, что экспрессия гена-мишени GSK3β значительно снижалась при обработке SAMiRNA-miR-3199 (фиг. 10b).
5-3. Анализ ингибирующих эффектов SAMiRNA-miR-3199 на белок GSK3β
Чтобы проанализировать эффекты SAMiRNA-miR-3199 на ингибирование белка GSK3β, проводили иммуноблоттинг. Клетки SK-MEL-28 распределяли по 1×105 клеток/лунку в 6-луночный планшет (Falcon, US) и затем культивировали при 37°C/5% CO2. Клетки SK-MEL-28 обрабатывали SAMiRNA-miR-3199 с помощью способа по примеру 4-1. После культивирования в течение 96 часов проводили анализ в соответствии с протоколом иммуноблоттинга. GSK3β (Cell Signaling Technology, Inc, US), бета-катенин (Becton, Dickinson and Company Inc, US) и альфа-тубулин (Cell Signaling Technology, US) использовали в качестве первичных антител, а в качестве вторичных антител использовали HRP-связанный анти-мышиный IgG (Cell Signaling Technology, US) и HRP-связанный анти-кроличий IgG (Cell Signaling Technology, US).
Таким образом, было подтверждено, что экспрессия белка GSK3β снижалась при обработке SAMiRNA-miR-3199, как и результаты анализа экспрессии гена GSK3β с помощью кПЦР-РВ. GSK3β фосфорилирует бета-катенин, чтобы способствовать деградации белка, снижая стабильность белка, а когда экспрессия GSK3β ингибируется, стабильность белка бета-катенина повышается. Следовательно, было подтверждено, что экспрессия белка бета-катенина повышалась при обработке SAMiRNA-miR-3199 (фиг. 10c).
5-4. Анализ внутриклеточной экспрессии белка GSK3β при обработке SAMiRNA-miR-3199
Иммуноцитохимический анализ проводили для анализа внутриклеточной экспрессии белка GSK3β с обработкой SAMiRNA-miR-3199. Перед распределением клеток покровное стекло помещали в 12-луночный планшет (Falcon, US) и покрывали поли-L-лизином (Sigma, US) на 1 час, после чего клетки SK-MEL-28 распределяли по 2×104 клеток/лунку и культивировали при 37°C/5% CO2. На следующий день клетки SK-MEL-28 обрабатывали SAMiRNA-miR-3199 с помощью способа по примеру 4-1. После культивирования в течение 48 часов реакцию проводили в 0,1% растворе Triton-X100 в течение 10 минут для пермеабилизации клеток с последующей блокировкой в растворе, содержащем 1% БСА, в течение 1 часа. Здесь, в качестве первичных антител использовали GSK3β (Cell Signaling Technology, Inc, US) и бета-катенин (Becton, Dickinson and Company Inc, US), а в качестве вторичных антител использовали антитела против IgG мыши, конъюгированные с Alexa Fluor 594 (Cell Signaling Technology, US), и антитела против IgG кролика, конъюгированные с Alexa Fluor 488 (Cell Signaling Technology, US). Для флуоресцентного анализа окрашенных клеток изображения анализировали с применением конфокального микроскопа с вращающимся диском (Dragonfly high-speed confocal image platform, Andor).
Таким образом, было подтверждено, что экспрессия гена-мишени GSK3β снижалась при обработке SAMiRNA-miR-3199, а также значительно повышалась экспрессия белка бета-катенина в ядре и цитоплазме (фиг. 10d).
5-5. Анализ прямого связывания SAMiRNA-miR-3199 с 3’-UTR мРНК GSK3β
Чтобы проанализировать, связывается ли miR-3199 напрямую с 3'-UTR мРНК GSK3β, был проведен анализ репортера люциферазы. Клетки SK-MEL-28 распределяли по 3×104 клеток/лунку в 12-луночный планшет (Falcon, US) и затем культивировали при 37°C/5% CO2. На следующий день клетки SK-MEL-28 трансфицировали конструкциями, в которые были вставлены GSK3β-дикого типа (WT) с сайтом связывания GSK3β дикого типа или GSK3β-мутант (MT) с мутированным сайтом связывания GSK3β с применением Lipofectamine RNAiMAX (Invitrogen, US). Одновременно клетки обрабатывали SAMiRNA-miR-3199. После культивирования в течение 96 часов активность люциферазы измеряли и анализировали в соответствии с протоколом изготовителя с применением Dual-Luciferase® Reporter Assay System (Promega™ Corporation, US).
Таким образом, было подтверждено, что когда клетки, экспрессирующие GSK3β-WT с сайтом связывания дикого типа, обрабатывали SAMiRNA-miR-3199, активность люциферазы значительно снижалась, и не было изменений в активности люциферазы при обработке SAMiRNA-miR-3199 в клетках, экспрессирующих GSK3β-MT с мутантным сайтом связывания (фиг. 10е). Это указывает на то, что miR-3199 ингибировала GSK3β путем прямого связывания с 3'-UTR (4153-4159) мРНК GSK3β.
Пример 6. Оценка меланогенной функции SAMiRNA-miR-3199 в меланоцитах человека
6-1. Клеточная культура и обработка SAMiRNA-miR-3199
Эпидермальные меланоциты человека (HEMs, Invitrogen, US), полученные из ткани кожи человека дикого типа, использовали для оценки эффективности SAMiRNA-miR-3199 в отношении стимулирования меланогенеза. HEM культивировали при 37°C/5% CO2 в культуре клеток млекопитающих/первичной среде для культивирования клеток (Gibco, US), содержащей добавку-2 для роста меланоцитов (Gibco, US). HEM распределяли по 1×105 клеток/лунку в 12-луночный планшет (Falcon, US) и на следующий день обрабатывали SAMiRNA-miR-3199 при концентрации 5 мкМ.
6-2. Анализ количества меланина, вырабатываемого при обработке SAMiRNA-miR-3199
Чтобы оценить эффективность SAMiRNA-miR-3199, изменение окрашивания и количество вырабатываемого меланина измеряли в HEM. HEM обрабатывали SAMiRNA-miR-3199 при концентрации 5 мкМ с помощью способа по примеру 6-1. После культивирования в течение 72 часов все клетки собирали и наблюдали изменение окрашивания. Для измерения количества вырабатываемого меланина реакцию проводили в 1 М NaOH (Bioneer, KR) в течение 2 часов при 37°C в соответствии с протоколом экстракции меланина, после чего измеряли поглощение при длине волны 405 нм и, таким образом, анализировали количество вырабатываемого меланина.
Таким образом, при обработке SAMiRNA-miR-3199 наблюдалось явное изменение цвета и увеличение количества меланина по сравнению с отрицательным контролем (фиг. 11a).
6-3. Анализ путей передачи сигнала, которые опосредуют меланогенез, при обработке SAMiRNA-miR-3199
кПЦР-РВ проводили для анализа экспрессии меланогенных генов MITF, TYR, TYRP1, TYRP2 и GSK3β после обработки SAMiRNA-miR-3199. HEM обрабатывали SAMiRNA-miR-3199 с помощью способа по примеру 6-1. После культивирования в течение 96 часов общую РНК экстрагировали из клеточного лизата с применением Universal RNA extraction kit (Bioneer, KR), и, используя эту РНК в качестве матрицы, анализировали уровни экспрессии мРНК генов (набор Human qPCR panel kit, Bioneer, KR) и RPL13A (набор праймеров Human reference qPCR primer set, Bioneer, KR) с помощью кПЦР-РВ с применением AccuPower GreenStar™ qRT-PCR Master Mix (Bioneer, KR) в соответствии с протоколом изготовителя. Значения Ct двух генов, полученные массовой кПЦР, подвергали относительной количественной оценке с помощью метода типа «два дельта Ct» [Livak KJ, Schmittgen TD. 2001. Methods. Dec; 25(4):4 02-8], в результате чего рассчитывали относительное количество (кратное изменение) мРНК каждого гена в экспериментальной группе по сравнению с контрольной группой.
Таким образом, было подтверждено, что экспрессия MITF, TYR, TYRP1 и TYRP2 была значительно увеличена при обработке SAMiRNA-miR-3199 (фиг. 11b), а также что экспрессия GSK3β, который является геном-мишенью miR-3199, была снижена (фиг. 11b).
6-4. Анализ экспрессии меланогенного белка при обработке SAMiRNA-miR-3199
Иммуноблотинг проводили для анализа экспрессии белков MITF и TYR, которые являются ключевыми факторами меланогенеза. HEM распределяли по 2×105 клеток/лунку в 6-луночный планшет (Falcon, US) и затем культивировали при 37°C/5% CO2. HEM обрабатывали SAMiRNA-miR-3199 с помощью способа по примеру 6-1. После культивирования в течение 96 часов проводили анализ в соответствии с протоколом иммуноблоттинга. Здесь, MITF (Santa Cruz Biotechnology, Inc, US), тирозиназу (Santa Cruz Biotechnology, Inc, US) и альфа-тубулин (Cell Signaling Technology, US) использовали в качестве первичных антител, а в качестве вторичного антитела использовали HRP-связанный анти-мышиный IgG (Cell Signaling Technology, US).
Таким образом, было подтверждено, что экспрессия белков MITF и TYR увеличивалась при обработке SAMiRNA-miR-3199, как в случае результатов анализа экспрессии генов с помощью кПЦР-РВ (фиг. 11c).
Пример 7. Оценка цитотоксичности и врожденной иммунотоксичности SAMiRNA-miR-3199
7-1. Оценка цитотоксичности SAMiRNA-miR-3199
Для оценки цитотоксичности SAMiRNA-miR-3199 использовали клетки дермальной папиллы фолликула человека (HFDPC, Promocell, DE), кератиноцит HaCaT (ATCC, US) и эпидермальные меланоциты человека (Invitrogen, US). HFDPC в количестве 3×103 клеток/лунку, HaCaT в количестве 4×103 клеток/лунку и HEM в количестве 5×103 клеток/лунку распределяли в 96-луночный планшет (Falcon, US) и затем культивировали при 37°C/5% CO2. На следующий день каждую клетку обрабатывали SAMiRNA-miR-3199 в разных концентрациях (0, 1, 5, 10 и 20 мкМ). После культивирования в течение 72 часов цитотоксичность анализировали в соответствии с протоколом изготовителя с применением набора WST assay kit (DOGEN, KR).
Таким образом, цитотоксичность не наблюдалась во всех клеточных линиях даже при применении SAMiRNA-miR-3199 в высокой концентрации 20 мкМ (фиг. 12a).
7-2. Оценка естественной иммунотоксичности SAMiRNA-miR-3199
Для оценки естественной иммунотоксичности SAMiRNA-miR-3199 использовали мононуклеарные клетки периферической крови человека (МКПК) (Cellular Technology Limited, US). Клетки распределяли по 5×105 клеток/лунку в 12-луночный планшет (Falcon, US) и затем культивировали при 37°C/5% CO2. На следующий день клетки обрабатывали SAMiRNA-miR-3199 в различных концентрациях (0, 5, 10 и 20 мкМ). После культивирования в течение 6 часов общую РНК экстрагировали из клеточного лизата с применением набора Universal RNA extraction kit (Bioneer, KR), и, используя эту РНК в качестве матрицы, оценивали уровни экспрессии мРНК генов воспалительных цитокинов (набор Human Immune кПЦР panel kit, Bioneer, KR) и RPL13A (набор праймеров Human reference qPCR primer set, Bioneer, KR) с помощью кПЦР-РВ с применением AccuPower GreenStar™ qRT-PCR Master Mix (Bioneer, KR) в соответствии с протоколом изготовителя. Последовательности праймеров для отдельных генов показаны ниже (таблица 7).
Таким образом, повышения уровня воспалительных цитокинов (IL-1β, IL-6, IL-12β, TNF-альфа, INF-гамма и др.) не наблюдалось даже при применении SAMiRNA-miR-3199 в высокой концентрации 20 мкМ, что указывает на отсутствие естественной иммунотоксичности (фиг. 12b).
Пример 8. Двухцепочечная олигонуклеотидная конструкция (SAMiRNA)
Двухцепочечная олигонуклеотидная конструкция, изготовленная в соответствии с настоящим изобретением, имеет структуру представленной ниже структурной формулы (5).
C18-S-S-C6-5’ S 3’-полиэтиленгликоль 2000
3’ AS 5’-PO4 … Структурная формула (5)
В структурной формуле (5) S представляет собой смысловую цепь мкрРНК, AS представляет собой антисмысловую цепь мкрРНК, PO4 представляет собой фосфатную группу, и полиэтиленгликоль представляет собой мономер гидрофильного материала, в котором полиэтиленгликоль 2000 связан через фосфатную группу (PO3-) в качестве линкера, C24 представляет собой гидрофобный материал и содержит дисульфидную связь, а 5' и 3' представляют концевые направления двухцепочечной олигоРНК.
Для смысловой цепи мкрРНК в структурной формуле (5) фосфодиэфирные связи, составляющие структуру остова РНК, соединяли с применением DMT-полиэтиленгликоля 2000-CPG в качестве носителя и с применением бета-цианоэтилфосфорамидита, в результате чего синтезировали конструкцию олигоРНК-гидрофильный материал, включающую смысловую цепь, в которой полиэтиленгликоль присоединен к 3'-концу, с последующим присоединением к 5'-концу гидрофобного C24, содержащего дисульфидную связь, в результате чего получали желаемую смысловую цепь конструкции РНК-полимер. Для отжига антисмысловой цепи со смысловой цепью фосфодиэфирные связи, составляющие структуру остова РНК, соединяли с применением бета-цианоэтилфосфорамидита с образованием антисмысловой цепи, имеющей последовательность, комплементарную смысловой цепи, с последующим присоединением фосфатной группы к 5'-концу с образованием антисмысловой цепи.
Промышленная применимость
Композиция в соответствии с настоящим изобретением может активировать меланоциты и способствовать меланогенезу, тем самым предотвращая поседение волос и замедляя его прогрессирование, и может преобразовывать волосы, которые уже подверглись поседению, в волосы до поседения, и, таким образом, может быть эффективно применена для фармацевтического применения и с косметической целью или для окрашивания волос без побочных эффектов, отличающегося от простых красителей, которые обычно многократно применяют для маскировки седых волос. Кроме того, композицию по настоящему изобретению можно применять в качестве фармацевтической или косметической композиции, которая может вызывать ослабление алопеции и стимулировать рост волос без побочных эффектов за счет стимулирования пролиферации клеток дермальной папиллы волосяного фолликула и кератиноцитов в дополнение к активации меланоцитов.
Хотя конкретные варианты осуществления настоящего изобретения были подробно описаны выше, специалистам в данной области техники будет очевидно, что описание представляет собой просто предпочтительные иллюстративные варианты осуществления и не должно толковаться как ограничивающее объем настоящего изобретения. Таким образом, по существу объем настоящего изобретения будет определяться прилагаемой формулой изобретения и ее эквивалентами.
Свободный текст списка последовательностей
Электронный файл прилагается.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> BIONEER CORPORATION
SIPHKGEN THERAPEUTICS CORPORATION
<120> КОМПОЗИЦИЯ ДЛЯ УМЕНЬШЕНИЯ ПОСЕДЕНИЯ ВОЛОС, СТИМУЛИРОВАНИЯ РОСТА ВОЛОС
И/ИЛИ ПРЕДОТВРАЩЕНИЯ ИЛИ УМЕНЬШЕНИЯ ВЫПАДЕНИЯ ВОЛОС, СОДЕРЖАЩАЯ
ДВУХЦЕПОЧЕЧНУЮ MIPHK В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА
<130> PF-B2916
<140> PCT/KR2022/002765
<141> 2022-02-25
<150> 10-2021-0025554
<151> 2021-02-25
<160> 40
<170> PatentIn version 3.5
<210> 1
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-8485
<400> 1
acgugugugu gugugugugu u 21
<210> 2
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-8485
<400> 2
cacacacaca cacacacgua u 21
<210> 3
<211> 24
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-3132
<400> 3
cucugagcuc cuucucuacc cauu 24
<210> 4
<211> 24
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-3132
<400> 4
uggguagaga aggagcucag agga 24
<210> 5
<211> 25
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-3189
<400> 5
ugccccaucu gugcccuggg uagga 25
<210> 6
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-3189
<400> 6
cccuuggguc ugauggggua g 21
<210> 7
<211> 20
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-6074
<400> 7
accuagccuc ugaauaucuu 20
<210> 8
<211> 20
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-6074
<400> 8
gauauucaga ggcuaggugg 20
<210> 9
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-3139
<400> 9
caggcaucug uugagcuccu auu 23
<210> 10
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-3139
<400> 10
uaggagcuca acagaugccu guu 23
<210> 11
<211> 22
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-933
<400> 11
gagaggucuc ccugcgcaca uu 22
<210> 12
<211> 22
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-933
<400> 12
ugugcgcagg gagaccucuc cc 22
<210> 13
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-7978
<400> 13
agcaacgcua uacaccagau u 21
<210> 14
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-7978
<400> 14
ucugguguau agcguugcuc a 21
<210> 15
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-3199
<400> 15
cuuucuccua aggcaguccc uuu 23
<210> 16
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-3199
<400> 16
agggacugcc uuaggagaaa guu 23
<210> 17
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-4644
<400> 17
ucugucucuu uucucucucc auu 23
<210> 18
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> hsa-miR-4644
<400> 18
uggagagaga aaagagacag aag 23
<210> 19
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hMITF-прямой
<400> 19
cgtctctcac tggattggtg 20
<210> 20
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hMITF-обратный
<400> 20
cttataaaat ccctgctgcc gt 22
<210> 21
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hTYR-прямой
<400> 21
ggatagcgga tgcctctcaa 20
<210> 22
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hTYR-обратный
<400> 22
ggagccactg ctcaaaaata c 21
<210> 23
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hTYRP1-прямой
<400> 23
ccacagccct cagtatccc 19
<210> 24
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hTYRP1-обратный
<400> 24
cagctcctct ccagccag 18
<210> 25
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hTYRP2-прямой
<400> 25
tcggatgtac aacatggttc c 21
<210> 26
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hTYRP2-обратный
<400> 26
ccaacctgga gtttcttcaa c 21
<210> 27
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hRPL13A-прямой
<400> 27
ccagcaatca agtttgccta 20
<210> 28
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> hRPL13A-обратный
<400> 28
gtggtggtgg tggtaattca 20
<210> 29
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 29
gcagcatgaa agttagcaga g 21
<210> 30
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 30
tgacttcttg tggcctgtc 19
<210> 31
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 31
ctgagctcgc cagtgaaat 19
<210> 32
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 32
ctgtagtggt ggtcggaga 19
<210> 33
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 33
agatgcaata accacccctg 20
<210> 34
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 34
tgcgcagaat gagatgagtt 20
<210> 35
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 35
attctggacg tttcacctgc 20
<210> 36
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 36
gtcccctctg actctctctg 20
<210> 37
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 37
ctgtagccca tgttgtagca 20
<210> 38
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 38
ggttatctct cagctccacg 20
<210> 39
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 39
gaatgtccaa cgcaaagcaa 20
<210> 40
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 40
acctcgaaac agcatctgac 20
<---
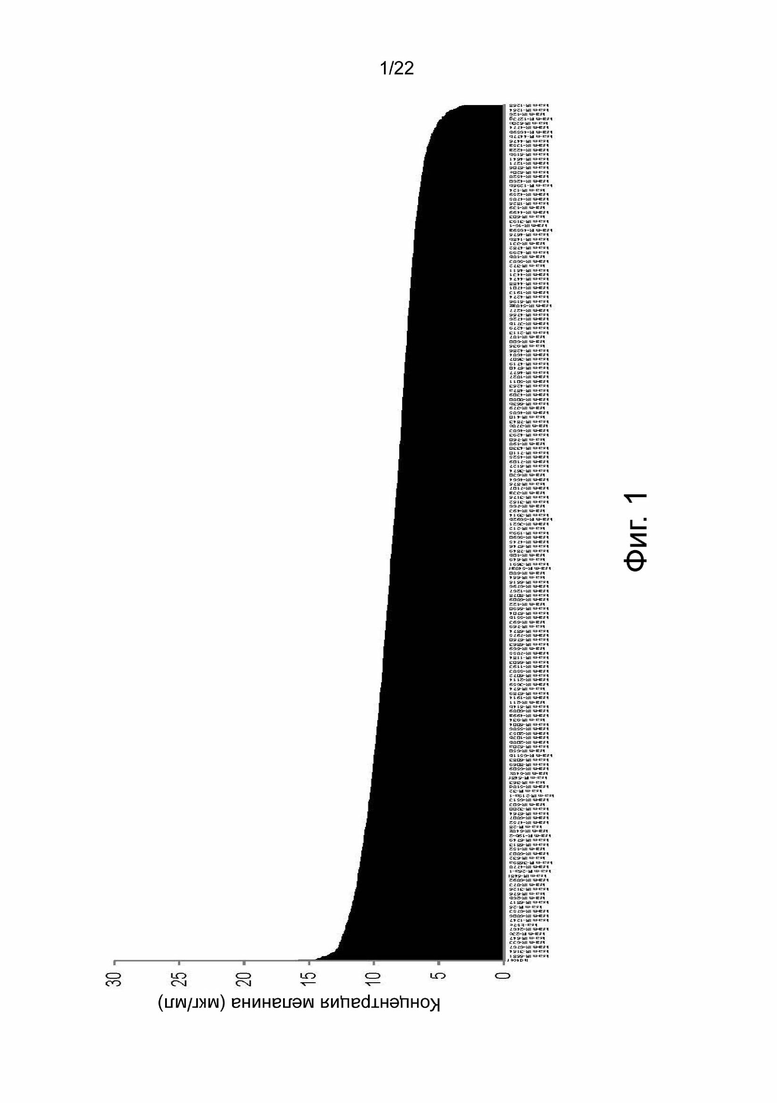




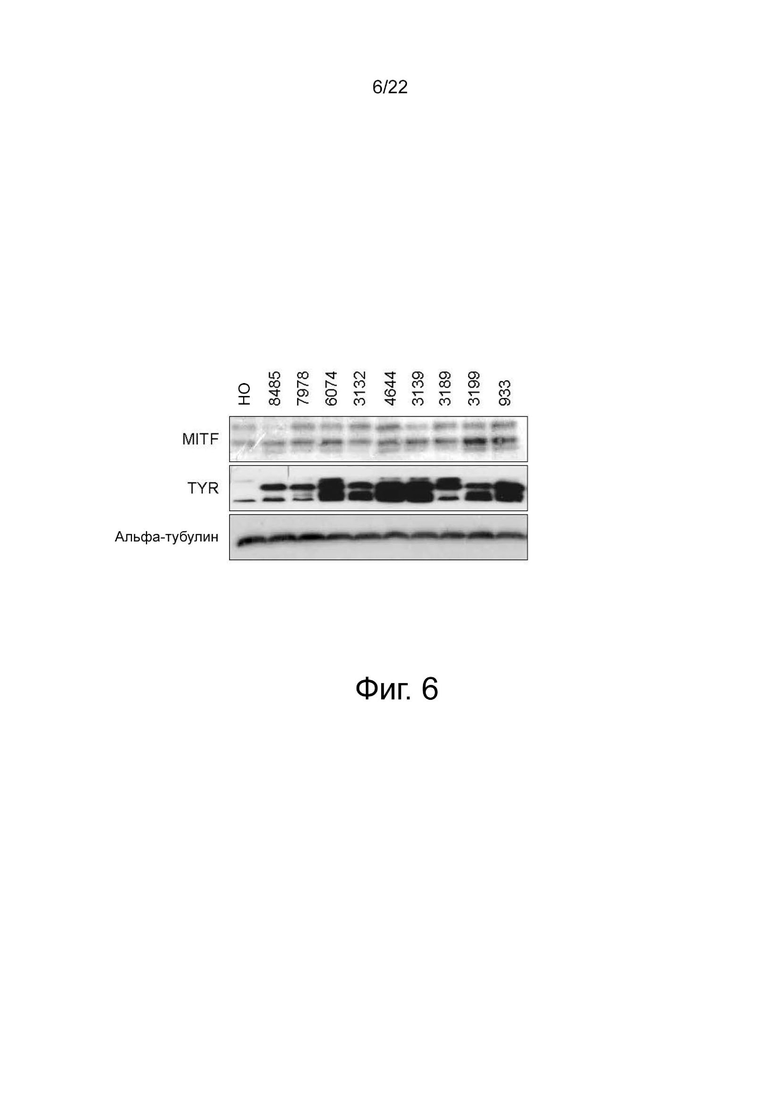
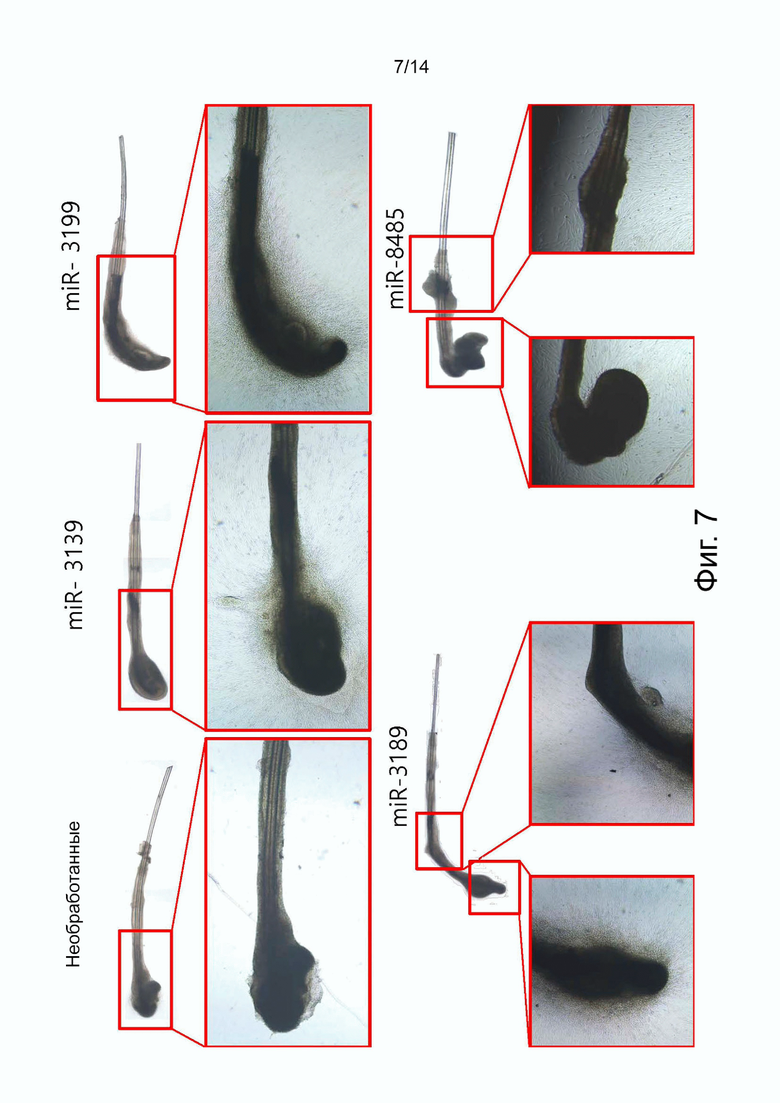
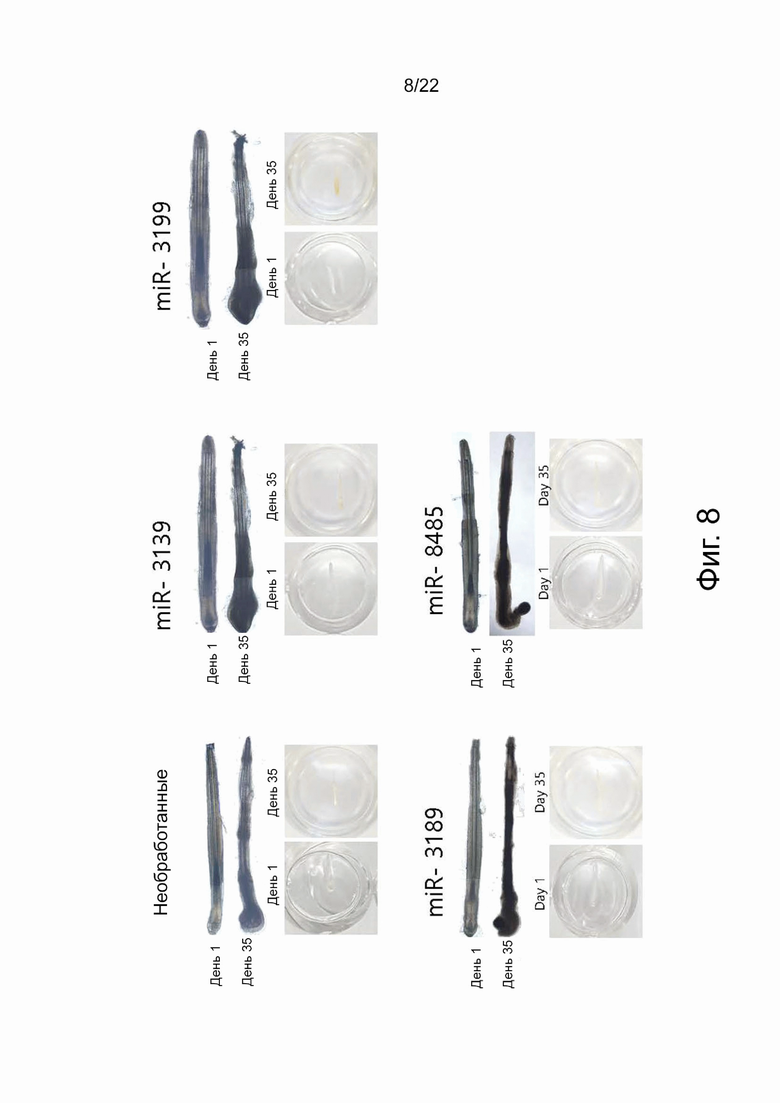
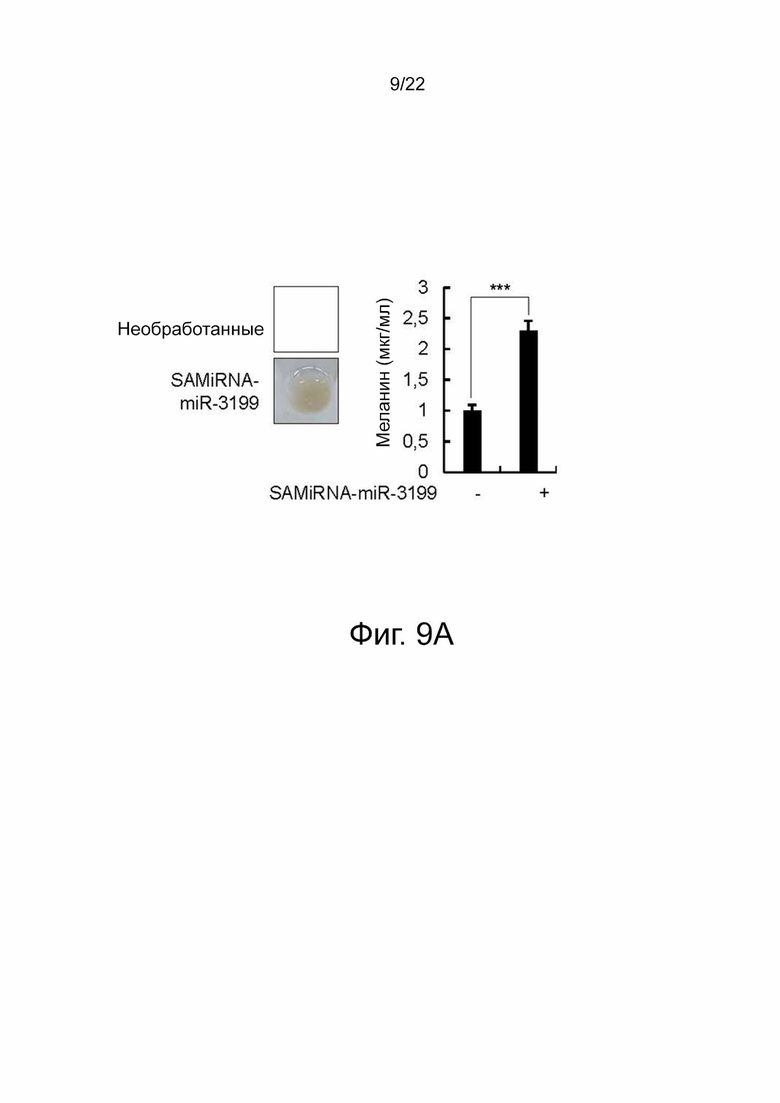
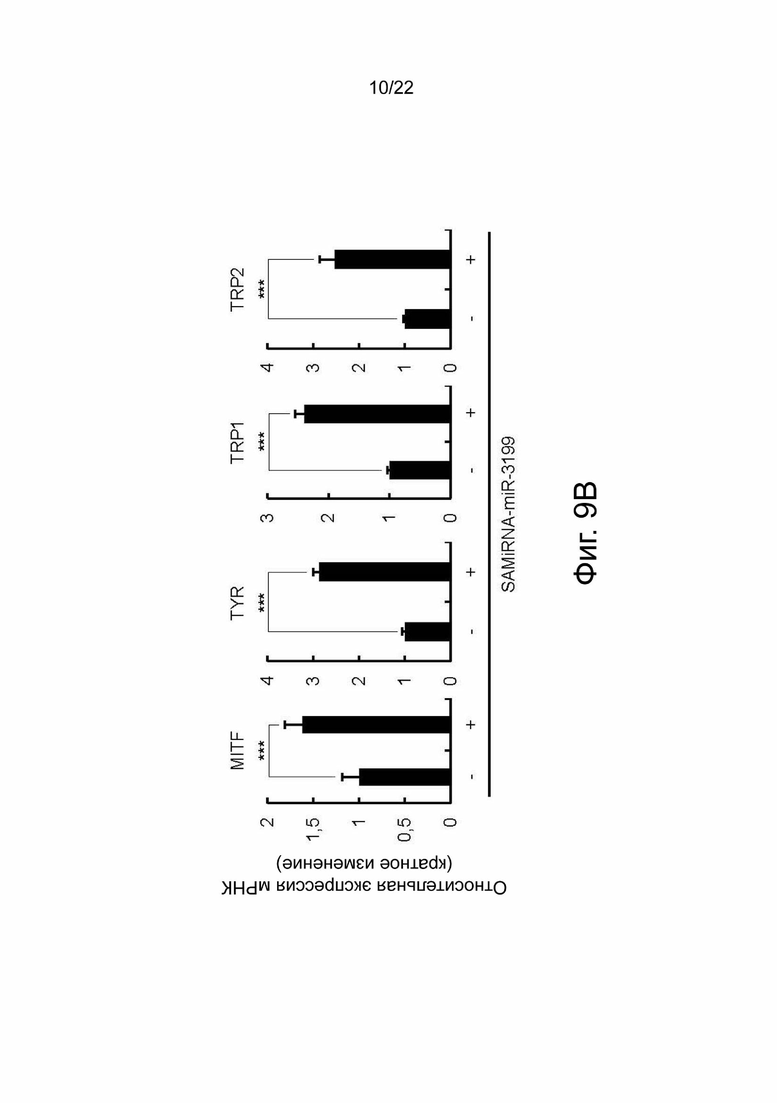

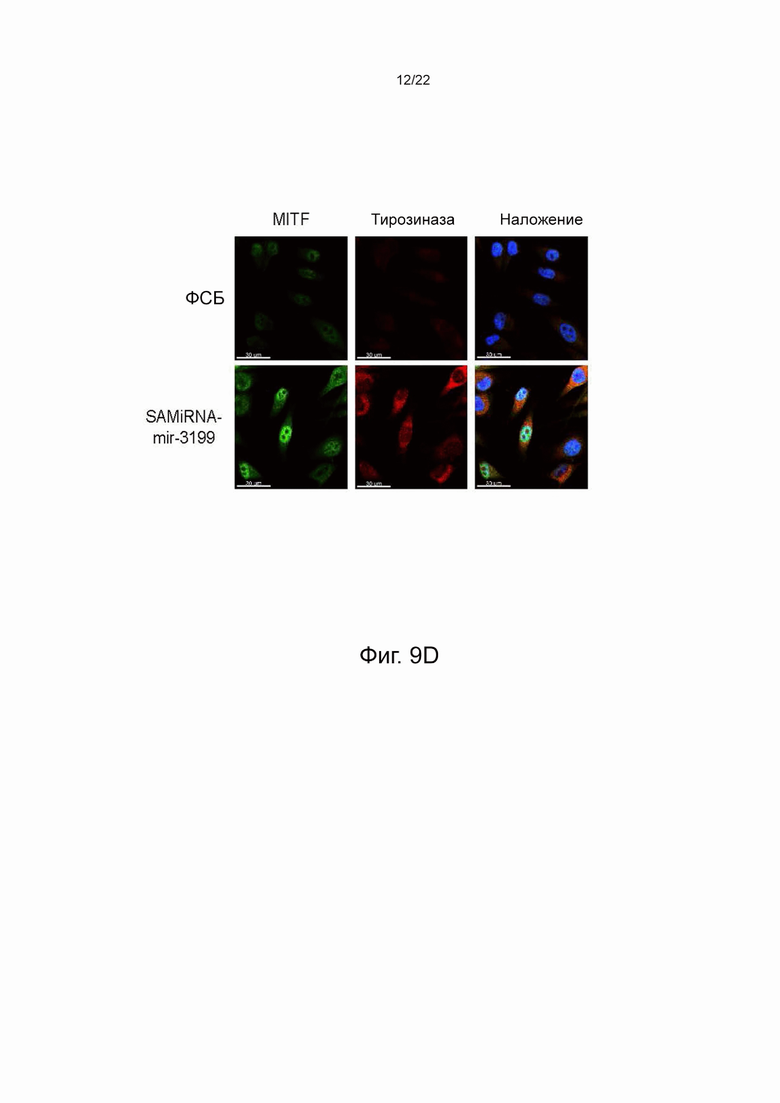

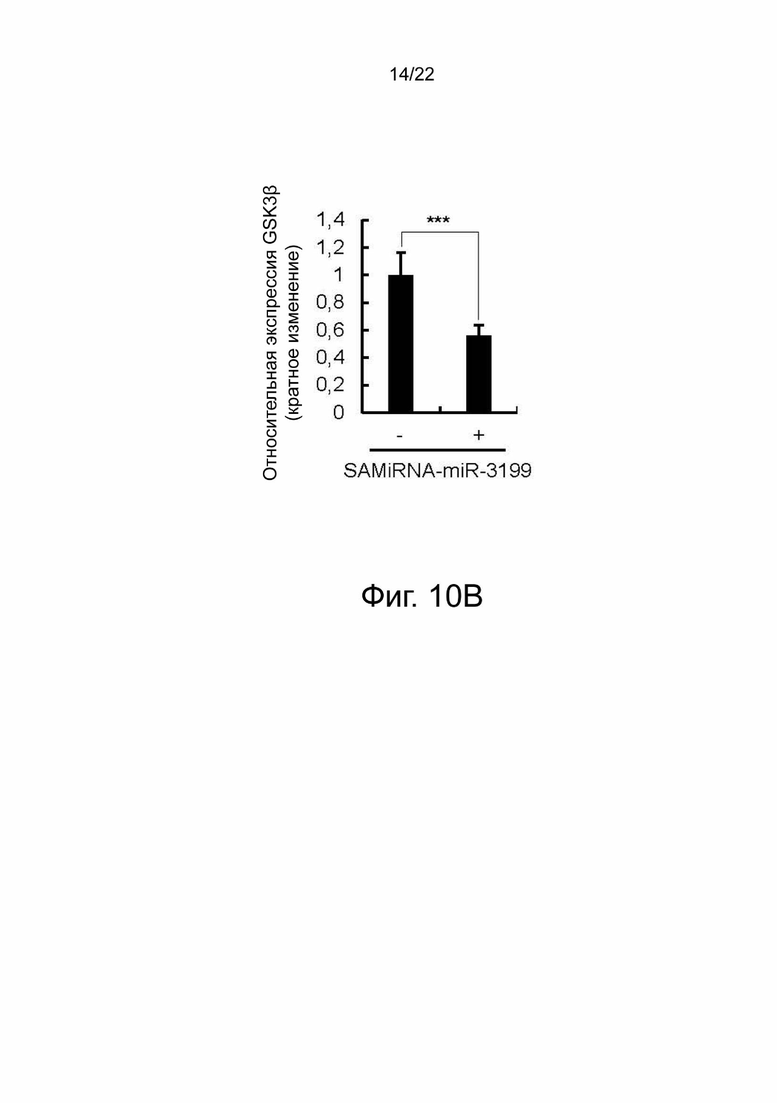
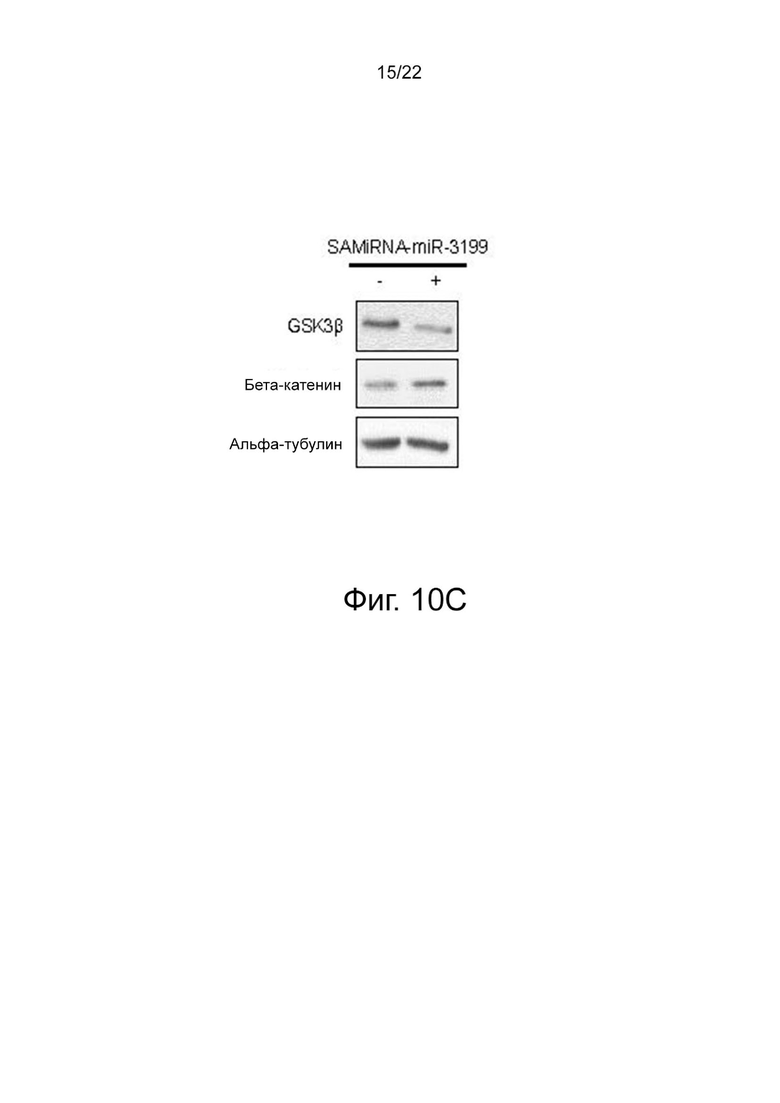
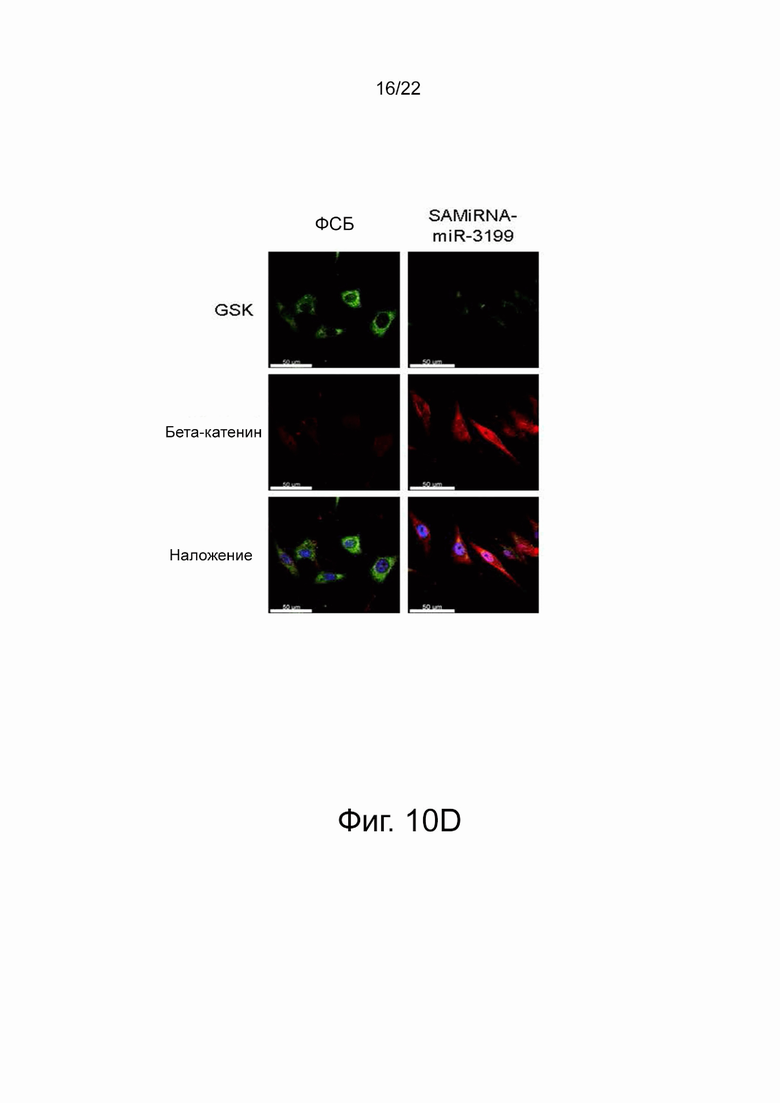


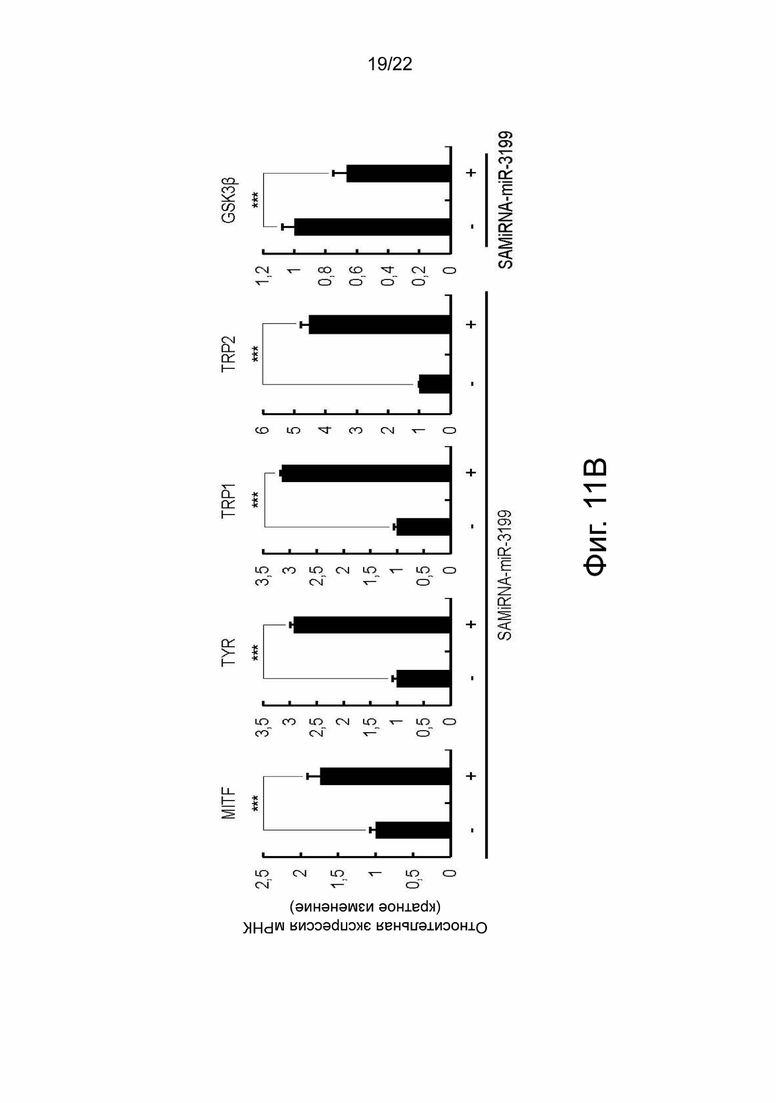
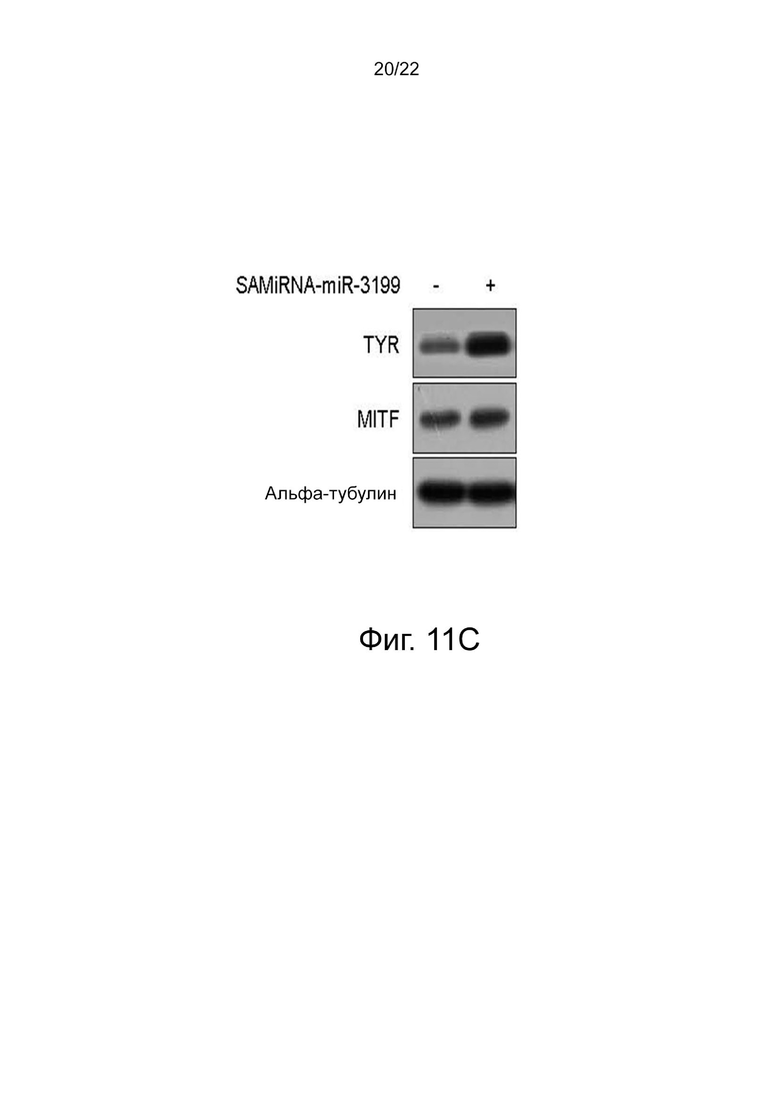
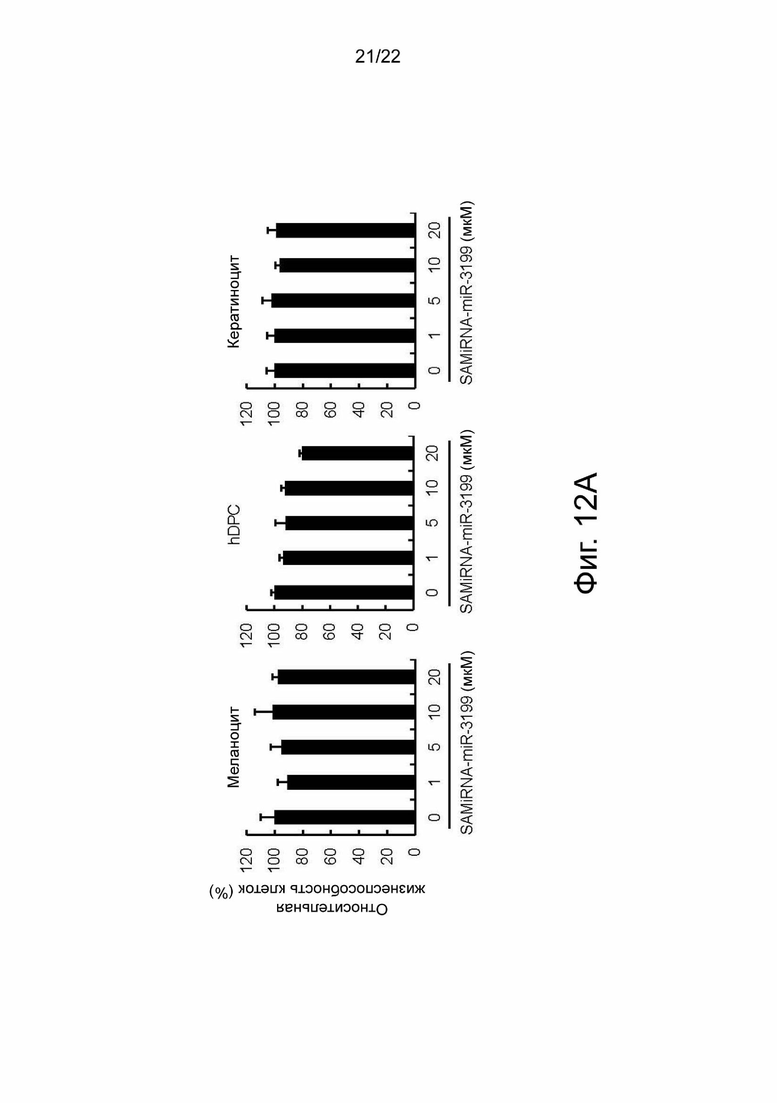
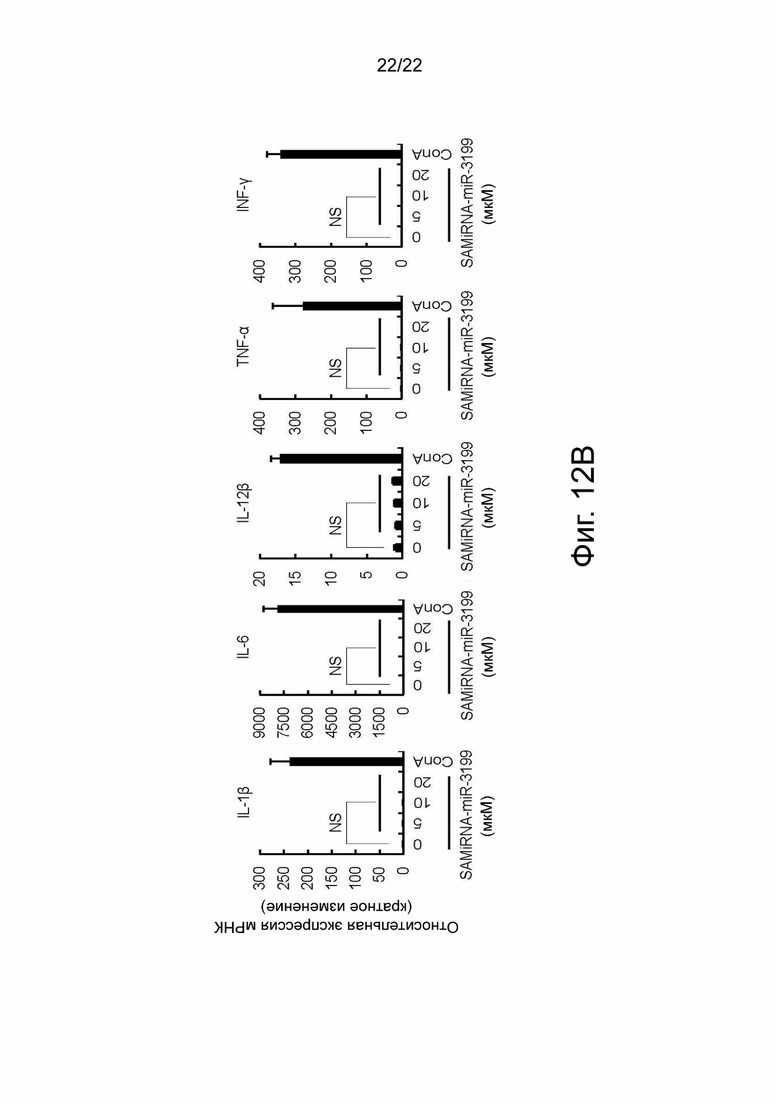
Группа изобретений относится к композициям для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос. Композиции содержат в качестве активного ингредиента двухцепочечный олигонуклеотид hsa-miR-3139, hsa-miR-3189, hsa-miR-3199 или hsa-miR-8485, двухцепочечную олигонуклеотидную конструкцию, включающую ее, или наночастицы, включающие указанную конструкцию. Композиции предотвращают поседение волос и снижают скорость его прогрессирования путем активации меланоцитов и стимулирования меланогенеза, а также обеспечивают улучшение состояния волос, уже затронутых поседением, до состояния, предшествующего поседению. Кроме того, композиции способствуют активации меланоцитов и пролиферации клеток дермальной папиллы и кератиноцитов, которые присутствуют в волосяных фолликулах, и индуцируют развитие наружного корневого влагалища и рост волос. 3 н. и 17 з.п. ф-лы, 12 ил., 7 табл., 8 пр.
1. Композиция для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, содержащая в качестве активного ингредиента:
(i) hsa-miR3139, hsa-miR3189, hsa-miR3199 или hsa-miR8485,
где hsa-miR-3139, hsa-miR-3189, hsa-miR-3199 и hsa-miR-8485 представляют собой двухцепочечный олигонуклеотид,
где hsa-miR-3139 содержит нуклеотидную последовательность, представленную SEQ ID NO: 9, и нуклеотидную последовательность, представленную SEQ ID NO: 10,
где hsa-miR-3189 содержит нуклеотидную последовательность, представленную SEQ ID NO: 5, и нуклеотидную последовательность, представленную SEQ ID NO: 6,
где hsa-miR-3199 содержит нуклеотидную последовательность, представленную SEQ ID NO: 15, и нуклеотидную последовательность, представленную SEQ ID NO: 16,
где hsa-miR-8485 содержит нуклеотидную последовательность, представленную SEQ ID NO: 1, и нуклеотидную последовательность, представленную SEQ ID NO: 2;
(ii) двухцепочечную олигонуклеотидную конструкцию, имеющую структуру представленной ниже структурной формулы (1'):
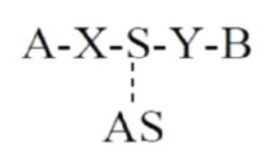 структурная формула (1'), в которой
структурная формула (1'), в которой
A представляет собой гидрофильный материал,
где гидрофильный материал представляет собой любой материал, выбранный из группы, состоящей из полиэтиленгликоля (ПЭГ), поливинилпирролидона и полиоксазолина, или
гидрофильный материал представлен (P)n, (Pm-J)n или (J-Pm)n, где P представляет собой мономер гидрофильного материала, n составляет от 1 до 200, m составляет от 1 до 15, а J представляет собой линкер, соединяющий m мономеров гидрофильного материала друг с другом или соединяющий m мономеров гидрофильного материала и олигонуклеотиды друг с другом,
при этом мономер гидрофильного материала (P) имеет структуру соединения (1), приведенного ниже:
 соединение (1), в котором
соединение (1), в котором
G выбран из группы, состоящей из CH2, O, S и NH,
B представляет собой гидрофобный материал,
где гидрофобный материал выбран из группы, состоящей из производного стероида, производного глицерида, эфира глицерина, полипропиленгликоля, ненасыщенного или насыщенного углеводорода C12-C50, диацилфосфатидилхолина, жирной кислоты, фосфолипида и липополиамина,
X и Y, каждый, независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь,
S представляет собой смысловую цепь hsa-miR-3139, hsa-miR-3189, hsa-miR-3199 или hsa-miR-8485, а
AS представляет собой антисмысловую цепь hsa-miR-3139, hsa-miR-3189, hsa-miR-3199 или hsa-miR-8485; или
(iii) наночастицы, содержащие такую двухцепочечную олигонуклеотидную конструкцию,
и эта композиция дополнительно содержит по меньшей мере один фармацевтически приемлемый носитель.
2. Фармацевтическая композиция для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, содержащая композицию по п.1 и по меньшей мере один фармацевтически приемлемый носитель.
3. Фармацевтическая композиция по п. 2, в которой гидрофильный материал имеет молекулярную массу от 200 до 10000.
4. Фармацевтическая композиция по п. 2, в которой линкер (J) выбран из группы, состоящей из PO3-, SO3 и CO2.
5. Фармацевтическая композиция по п. 2, в которой гидрофобный материал имеет молекулярную массу от 250 до 1000.
6. Фармацевтическая композиция по п. 2, в которой производное стероида выбрано из группы, состоящей из холестерина, холестанола, холевой кислоты, холестерилформиата, холестанилформиата и холестериламина.
7. Фармацевтическая композиция по п. 2, в которой производное глицерида выбрано из группы, состоящей из моно-, ди- и триглицеридов.
8. Фармацевтическая композиция по п. 2, в которой ковалентная связь, представленная X и Y, является нерасщепляемой связью или расщепляемой связью.
9. Фармацевтическая композиция по п. 8, в которой нерасщепляемая связь представляет собой амидную связь или фосфатную связь.
10. Фармацевтическая композиция по п. 8, в которой расщепляемая связь представляет собой дисульфидную связь, расщепляемую кислотой связь, сложноэфирную связь, ангидридную связь, биоразлагаемую связь или расщепляемую ферментами связь.
11. Косметическая композиция для уменьшения поседения волос, стимулирования роста волос и/или предотвращения или уменьшения выпадения волос, содержащая в качестве активного ингредиента:
(i) hsa-miR-3139, hsa-miR-3189, hsa-miR-3199 или hsa-miR-8485,
где hsa-miR-3139, hsa-miR-3189, hsa-miR-3199 и hsa-miR-8485 представляют собой двухцепочечный олигонуклеотид,
где hsa-miR-3139 содержит нуклеотидную последовательность, представленную SEQ ID NO: 9, и нуклеотидную последовательность, представленную SEQ ID NO: 10,
где hsa-miR-3189 содержит нуклеотидную последовательность, представленную SEQ ID NO: 5, и нуклеотидную последовательность, представленную SEQ ID NO: 6,
где hsa-miR-3199 содержит нуклеотидную последовательность, представленную SEQ ID NO: 15, и нуклеотидную последовательность, представленную SEQ ID NO: 16,
где hsa-miR-8485 содержит нуклеотидную последовательность, представленную SEQ ID NO: 1, и нуклеотидную последовательность, представленную SEQ ID NO: 2;
(ii) двухцепочечную олигонуклеотидную конструкцию, имеющую структуру структурной формулы (1'), приведенную ниже:
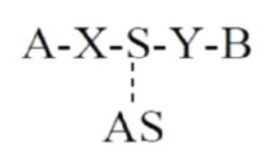 структурная формула (1'), в которой
структурная формула (1'), в которой
А – гидрофильный материал,
где гидрофильный материал представляет собой любой материал, выбранный из группы, состоящей из полиэтиленгликоля (ПЭГ), поливинилпирролидона и полиоксазолина, или
гидрофильный материал представлен (P)n, (Pm-J)n или (J-Pm)n, где P представляет собой мономер гидрофильного материала, n составляет от 1 до 200, m составляет от 1 до 15, а J представляет собой линкер, соединяющий m мономеров гидрофильного материала друг с другом или соединяющий m мономеров гидрофильного материала и олигонуклеотиды друг с другом,
где мономер гидрофильного материала (P) имеет структуру соединения (1), приведенного ниже:
 соединение (1), в котором
соединение (1), в котором
G выбран из группы, состоящей из CH2, O, S и NH,
B представляет собой гидрофобный материал,
где гидрофобный материал выбран из группы, состоящей из производного стероида, производного глицерида, эфира глицерина, полипропиленгликоля, ненасыщенного или насыщенного углеводорода C12-C50, диацилфосфатидилхолина, жирной кислоты, фосфолипида и липополиамина,
X и Y каждый независимо представляет собой простую ковалентную связь или ковалентную связь, опосредованную линкером,
S представляет собой смысловую цепь hsa-miR-3139, hsa-miR-3189, hsa-miR-3199 или hsa-miR-8485, а
AS представляет собой антисмысловую цепь hsa-miR-3139, hsa-miR-3189, hsa-miR-3199 или hsa-miR; или
(iii) наночастицы, содержащие двухцепочечную олигонуклеотидную конструкцию по (ii),
и эта композиция дополнительно содержит по меньшей мере один фармацевтически приемлемый носитель.
12. Косметическая композиция по п. 11, в которой гидрофильный материал имеет молекулярную массу от 200 до 10000.
13. Косметическая композиция по п. 11, в которой линкер (J) выбран из группы, состоящей из PO3-, SO3 и CO2.
14. Косметическая композиция по п. 11, в которой гидрофобный материал имеет молекулярную массу от 250 до 1000.
15. Косметическая композиция по п. 11, в которой производное стероида выбрано из группы, состоящей из холестерина, холестанола, холевой кислоты, холестерилформиата, холестанилформиата и холестериламина.
16. Косметическая композиция по п. 11, в которой производное глицерида выбрано из группы, состоящей из моно-, ди- и триглицеридов.
17. Косметическая композиция по п. 11, в которой ковалентная связь, представленная X и Y, является нерасщепляемой связью или расщепляемой связью.
18. Косметическая композиция по п. 17, в которой нерасщепляемая связь представляет собой амидную связь или фосфатную связь.
19. Косметическая композиция по п. 17, в которой расщепляемая связь представляет собой дисульфидную связь, расщепляемую кислотой связь, сложноэфирную связь, ангидридную связь, биоразлагаемую связь или разлагаемую ферментами связь.
20. Косметическая композиция по п. 11, где косметическая композиция выбрана из группы, состоящей из тоника для волос, кондиционера для волос, эссенции для волос, лосьона для волос, питательного лосьона для волос, шампуня для волос, ополаскивателя для волос, лечебных средств для волос, крема для волос, питательного крема для волос, крема для увлажнения волос, крема для массажа волос, воска для волос, аэрозоля для волос, маски для волос, питательной маски для волос, мыла для волос, очищающей пены для волос, масла для волос, средства для сушки волос, защитного средства для волос, краски для волос, средства для завивки волос, средства для обесцвечивания волос, геля для волос, блеска для волос, средства для укладки волос, лака для волос, увлажняющего средства для волос, мусса для волос и распылителя для волос.
| WO 2019103572 A1, 31.05.2019 | |||
| WO 2018038558 A1, 01.03.2018 | |||
| US 9649388 B2, 16.05.2017 | |||
| US 11123361 B2, 21.09.2021 | |||
| КОНЪЮГАТ МИРНК И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2558258C2 |
| УЛУЧШЕННАЯ ОЛИГОНУКЛЕОТИДНАЯ КОНСТРУКЦИЯ ТИПА НАНОЧАСТИЦЫ, ОБЛАДАЮЩАЯ ВЫСОКОЙ ЭФФЕКТИВНОСТЬЮ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2014 |
|
RU2670164C2 |
| WO 2007021142 A1, 02.22.2007 | |||
| CN 111662982 A, 15.09.2020 | |||
| CN111621573 A, 04.09.2020 | |||
| WO 2013124816 A2, 29.08.2013 | |||
| US 20200255906 A1, 13.08.2020. | |||
Авторы
Даты
2024-07-22—Публикация
2022-02-25—Подача