Изобретение относится к способам получения органических соединений, а именно азоксибензолов, которые содержат карбоксильную группу, отделенную от ароматического кольца фрагментом, содержащим, по меньшей мере, один атомом углерода.
Известно, что среди азоксибензолов значительное число соединений обладает практически значимыми свойствами: имеются вещества с жидкокристаллическими свойствами, различными видами биологической активности, а реакционная способность азокси-группы позволяет применять их как полупродукты для тонкого органического синтеза.
Известные к настоящему моменту способы получения карбоксилсодержащих азоокисей заключаются в восстановлении соответствующих нитросоединений. Способы отличаются используемыми восстановителями, реакционными средами и исходными нитросоединениями. Однако систематических данных о получении широкого ряда соединений относящихся к ряду азоксибензола и содержащих карбоксильную группу, отделенную от ароматического кольца фрагментом, содержащим, по меньшей мере, один атомом углерода, к настоящему моменту нет. Все известные способы опубликованы в источниках, относящихся к первой трети ХХ века, не подтверждены достаточным числом примеров, говорящих об общности методов и не содержат данных о чистоте образующихся соединений.
Известен способ получения 4-азоксикоричной кислоты восстановлением в водной среде 4-нитрокоричной кислоты арсенитом натрия, получаемым из мышьяковистого ангидрида и гидроокиси натрия в водной среде. Способ реализуется в соответствии со схемой:

(D. Vorländer. Ueber krystallinisch-flüssige Substanzen. Berichte der deutschen chemischen Gesellschaft. Volume39, Issue1, Januar-Februar 1906 Pages 803-810. DOI: 10.1002/cber.190603901126).
В описанном примере сообщается о практически количественном выходе целевого соединения, однако данные, подтверждающие его чистоту, отсутствуют. Кроме того, способ реализуется с использованием высокотоксичного соединения мышьяка, что делает его опасным.
Известен способ получения 4-азоксикоричной кислоты, реализующийся в две стадии. Способ включает восстановление эфиров 4-нитрокоричной кислоты (этилового или метилового) под действием бензоина в спиртовой среде в присутствии небольшого количества метоксида или этоксида натрия и последующий гидролиз эфиров 4-азоксикоричной кислоты. Способ реализуется в соответствии со схемой:
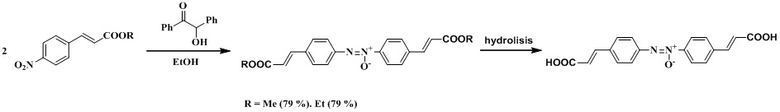
(H. B. Nisbet. CCLXXV.-The reduction of nitro-compounds by aromatic ketols. Part I. Some p-azoxy-compounds. J. Chem. Soc., 1927, 2081-2086. DOI: 10.1039/JR9270002081)
Указанный способ реализуется с использованием бензоина - синтетического продукта, получаемого при конденсации бензальдегида, удорожающего процесс восстановления. Кроме того, условия гидролиза и выход кислоты не приводятся.
Задачей предлагаемого изобретения является создание способа получения карбоксилсодержащих азоксибензолов, которые содержат карбоксильную группу, отделенную от ароматического кольца фрагментом, содержащим, по меньшей мере, один атомом углерода, которые представляют собой перспективные полупродукты для получения биологически активных соединений, жидкокристаллических веществ и др.
Техническим результатом настоящего изобретения является расширение ассортимента способов получения карбоксилсодержащих азоксибензолов, используемых в качестве многоцелевых органических соединений.
Технический результат достигается путем восстановления нитроарилсодержащих карбоновых кислот, в которых карбоксильная группа отделена от бензольного кольца фрагментом, содержащим, по меньшей мере, один атомом углерода, 200 мольными % глюкозы в присутствии гидроксида натрия в водно-этанольной среде при 50°С в течение 1 часа в соответствии со схемой:
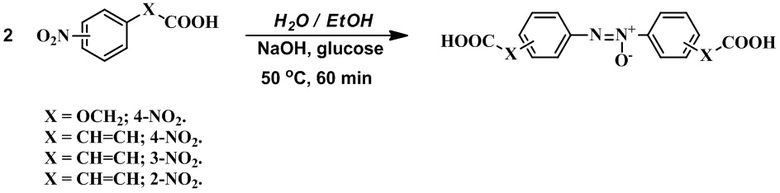
После завершения реакции, ход которой контролируется тонкослойной хроматографией (силикагель, хлороформ - метанол 10 : 0,5), реакционную массу охлаждают, выливают в 2 М раствор соляной кислоты, образовавшийся осадок отфильтровывают, промывают на фильтре дистиллированной водой и горячим этанолом.
В качестве нитроарилсодержащих карбоновых кислот, в которых карбоксильная группа отделена от бензольного кольца фрагментом, содержащим, по меньшей мере, один атомом углерода, используют соединения, например, содержащие оксиметиленовый фрагмент - 4-нитрофеноксиуксусную кислоту, а также этиленовый фрагмент - 4-нитрокоричную, 3-нитрокоричную и 2-нитрокоричную кислоты. Такого рода кислоты являются коммерчески доступными или могут быть легко получены известными методами.
Оптимальное время проведения реакции определяли мониторингом реакционной массы тонкослойной хроматографией по расходованию исходного соединения и установили, что время восстановления предпочтительно составляет 60 минут.
Чистота образующихся продуктов подтверждена тонкослойной хроматографией, а строение спектральными методами.
Пример 1. Получение 1,2-бис(4-(карбоксиметокси)фенил)диазен оксида
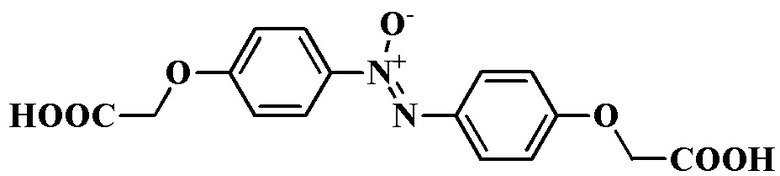
В колбу вносят 15 мл этанола, 19 мл 30% водного раствора гидроксида натрия и 1,5 г (0,0076 моль) 4-нитрофеноксиуксусной кислоты. Реакционную массу термостатируют при 50°С и вносят порциями 3 г (0,0152 моль) моногидрата глюкозы, после чего выдерживают 60 минут при указанной температуре. Затем реакционную массу охлаждают, выливают в стакан с 2 М раствором соляной кислоты, образовавшийся осадок отфильтровывают, промывают на фильтре дистиллированной водой и перекристаллизовывают из этанола. Выход 76 %. Тпл 247-248°С (с разложением).
ИК спектр (KBr), ν, см-1: 3554, 3464 (OH), 3068, 3051, (Csp2-H), 2918 (Csp3-H), 1743, 1712 (C=O), 1595, 1498 (Csp2-Csp2), 1467 (ассим. N=N(O)), 1373 (сим. N=N(O)).
Спектр ЯМР 1Н ((CD3)2SO, 399.78 МГц), δ, м.д.: 4.78 с (2H, CH2), 4.81 с (2H, CH2), 7.03 - 7.11 м (2H, CH), 8.15 - 8.20 м (2H, CH).
Спектр ЯМР 13C ((CD3)2SO, 100.5 МГц), δ, м.д.:64.6 (CH2), 64.8 (CH2), 114.6 (CH), 114.7 (CH), 123.5 (CH), 127.3 (CH), 137.6 (C), 141.2 (C), 158.4 (C), 160.3 (C), 169.7 (C), 169.9 (C).
Масс-спектр высокого разрешения (ESI TOF negative), m/z (Iотн. %): 345.0705 [M-H]- (345.0728 рассчитано для C16H14N2O7).
Пример 2. Получение 1,2-бис(4-(карбоксивинил)фенил)диазен оксида
В колбу вносят 15 мл этанола, 19 мл 30% водного раствора гидроксида натрия и 1,47 г (0,0076 моль) 4-нитрокоричной кислоты. Реакционную массу термостатируют при 50°С и вносят порциями 3 г (0,0152 моль) моногидрата глюкозы, после чего выдерживают 60 минут при указанной температуре. Затем реакционную массу охлаждают, выливают в стакан с 2 М раствором соляной кислоты, образовавшийся осадок отфильтровывают, промывают на фильтре дистиллированной водой и перекристаллизовывают из этанола. Выход 83 %. Желтый кристаллический порошок.
ИК спектр (KBr), ν, см-1: 3200-2400 широкая фоновая полоса (OH), 1687, 1676 (C=O), 1627 (Csp2-Csp2), 1456 (ассим. N=N(O)), 1323 (сим. N=N(O)).
Масс-спектр высокого разрешения (ESI TOF negative), m/z (Iотн. %): 337.0827 [M-H]- (337.0829 рассчитано для C18H14N2O5).
Пример 3. Получение 1,2-бис(3-(карбоксивинил)фенил)диазен оксида
В колбу вносят 15 мл этанола, 19 мл 30% водного раствора гидроксида натрия и 1,47 г (0,0076 моль) 3-нитрокоричной кислоты. Реакционную массу термостатируют при 50°С и вносят порциями 3 г (0,0152 моль) моногидрата глюкозы, после чего выдерживают 60 минут при указанной температуре. Затем реакционную массу охлаждают, выливают в стакан с 2 М раствором соляной кислоты, образовавшийся осадок отфильтровывают, промывают на фильтре дистиллированной водой и перекристаллизовывают из этанола. Выход 80 %. Желтый кристаллический порошок.
ИК спектр (KBr), ν, см-1: 3200-2500 широкая фоновая полоса (OH) (OH), 3070 (Csp2-H), 1685 (C=O), 1629 (Csp2-Csp2), 1454 (ассим. N=N(O)), 1338 (сим. N=N(O)).
Масс-спектр высокого разрешения (ESI TOF negative), m/z (Iотн. %): 337.0824 [M-H]- (337.0829 рассчитано для C18H14N2O5).
Пример 4. Получение 1,2-бис(2-(карбоксивинил)фенил)диазен оксида
В колбу вносят 15 мл этанола, 19 мл 30% водного раствора гидроксида натрия и 1,47 г (0,0076 моль) 3-нитрокоричной кислоты. Реакционную массу термостатируют при 50°С и вносят порциями 3 г (0,0152 моль) моногидрата глюкозы, после чего выдерживают 60 минут при указанной температуре. Затем реакционную массу охлаждают, выливают в стакан с 2 М раствором соляной кислоты, образовавшийся осадок отфильтровывают, промывают на фильтре дистиллированной водой и перекристаллизовывают из этанола. Выход 79 %. Желтый кристаллический порошок.
ИК спектр (KBr), ν, см-1: 3200-2500 широкая фоновая полоса (OH), 3068, 3034, (Csp2-H), 1699, 1687 (C=O), 1622 (Csp2-Csp2), 1456 (ассим. N=N(O)), 1327 (сим. N=N(O)).
Масс-спектр высокого разрешения (ESI TOF negative), m/z (Iотн. %): 337.0828 [M-H]- (337.0829 рассчитано для C18H14N2O5).
В предлагаемом способе восстановление осуществляют действием глюкозы в водно-этанольной среде, то есть с применение безопасных, дешевых реагентов, источником которых является доступное возобновляемое природное сырье, таким образом, условия реализации способа соответствуют принципам «зеленой химии».
На основании изложенного делаем вывод, что способ является новым, обладает изобретательским уровнем, и техническим результатом, т.е. является патентоспособным.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N-АДАМАНТИЛИРОВАННЫХ АМИДОВ | 2013 |
|
RU2549901C1 |
| Способ получения (1-адамантил)фуранов | 2017 |
|
RU2661482C1 |
| Способ получения производного неокупроина | 2022 |
|
RU2799334C1 |
| Способ получения 1,3-диоксациклоалкилсодержащих азоокисей | 2021 |
|
RU2767880C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ БЕТА-ДИКАРБОНИЛЬНЫХ СОЕДИНЕНИЙ | 2012 |
|
RU2496766C1 |
| Способ получения гидроксиалкилсодержащих азоокисей | 2021 |
|
RU2769996C1 |
| Способ получения 2-гидрокси-2-((5-метилфуран-2-ил)метил)-3,3,3-трифторпропановой кислоты | 2023 |
|
RU2813205C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИКАРБОНИЛЬНЫХ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ ДИБЕНЗОСУБЕРЕНИЛЬНЫЙ ФРАГМЕНТ | 2014 |
|
RU2560727C1 |
| Способ получения производных 5Н-фуро[3,2-c]изохромен-5-она | 2017 |
|
RU2657732C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(АМИНОАЛКИЛ)-3-(АМИНОФЕНИЛ)БИЦИКЛО[2.2.1]ГЕПТАНОВ | 2012 |
|
RU2493145C1 |
Изобретение относится к области органической химии, а именно к способу получения карбоксилсодержащих азоксибензолов общей формулы 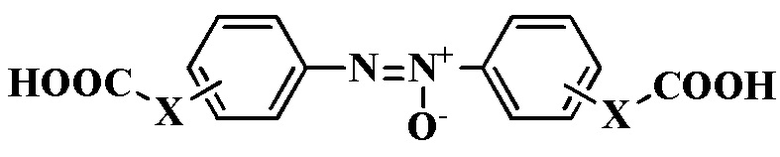 , где X означает OCH2 или CH=CH. Способ заключается в восстановлении нитроарилсодержащих карбоновых кислот общей формулы
, где X означает OCH2 или CH=CH. Способ заключается в восстановлении нитроарилсодержащих карбоновых кислот общей формулы 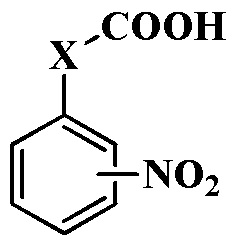 , где X=OCH2, 4-NO2; X=CH=CH, 4-NO2; X=CH=CH, 3-NO2; X=CH=CH, 2-NO2, которое проводят под действием 200 мольных % глюкозы в присутствии гидроокиси натрия в водно-этанольной среде при 50 °С в течение 1 часа. Технический результат: расширение ассортимента способов получения карбоксилсодержащих азоксибензолов, используемых в качестве многоцелевых органических соединений. 4 пр.
, где X=OCH2, 4-NO2; X=CH=CH, 4-NO2; X=CH=CH, 3-NO2; X=CH=CH, 2-NO2, которое проводят под действием 200 мольных % глюкозы в присутствии гидроокиси натрия в водно-этанольной среде при 50 °С в течение 1 часа. Технический результат: расширение ассортимента способов получения карбоксилсодержащих азоксибензолов, используемых в качестве многоцелевых органических соединений. 4 пр.
Способ получения карбоксилсодержащих азоксибензолов общей формулы
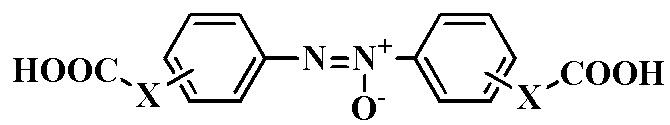
восстановлением нитроарилсодержащих карбоновых кислот общей формулы
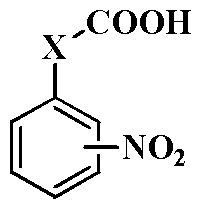 ,
,
где X = OCH2, 4-NO2; X = CH=CH, 4-NO2; X = CH=CH, 3-NO2; X= CH=CH, 2-NO2;
отличающийся тем, что восстановление проводят под действием 200 мольных % глюкозы в присутствии гидроокиси натрия в водно-этанольной среде при 50 °С в течение 1 часа.
| D | |||
| Vorlander., Ueber krystallinisch-flüssige Substanzen | |||
| Berichte der deutschen chemischen Gesellschaft, 1906, v.39, Issue 1, pp.803-810 | |||
| Способ получения гидроксиалкилсодержащих азоокисей | 2021 |
|
RU2769996C1 |
| Способ получения 1,3-диоксациклоалкилсодержащих азоокисей | 2021 |
|
RU2767880C1 |
| G.Heller, Reduction of Nitro Compounds by means of Zinc Dust and Acetic Acid | |||
| Berichte der Deutschen Chemischen Gesellschaft, 1910, v.43, pp.1907-1922 | |||
Авторы
Даты
2023-01-25—Публикация
2022-05-05—Подача