Настоящее изобретение относится к фармацевтической промышленности, в частности, к лекарственным препаратам для лечебного и профилактического применения и представляет собой фармацевтическую композицию активных фармацевтических субстанций для пероральной лекарственной формы в виде капсул.
Проблема лечения сердечно-сосудистых заболеваний (ССЗ) на данный момент является одной из актуальных, в виду высокой смертности и инвалидизации во всем мире. Каждый год в мире умирает 17,5 миллиона человек от ССЗ, и по прогнозам ВОЗ в 2030 году от ССЗ, в основном от болезней сердца и инсульта, умрет около 23,6 миллиона человек, и как предполагается, эти болезни останутся основными отдельными причинами смерти. Для снижения ССЗ используют комплексный подход в профилактике, направленный на повышение уровня физической активности, снижение употребления табака, алкоголя, продуктов с высоким содержанием жиров, сахара и соли. Для вторичной профилактики у лиц с уже имеющимся заболеванием, необходимо проведение лечения с использованием лекарственных средств (аспирин; бета-блокаторы; ингибиторы ангиотензинпревращающего фермента; статины).
В России активно используют препарат «Кардиомагнил», содержащий в качестве действующего вещества ацетилсалициловую кислоту и магния гидроксид, который обладает антиагрегантным действием. Однако, ацетилсалициловая кислота, относящаяся к группе нестероидных противовоспалительных препаратов (НПВП), способна проявлять системное побочное действие, не зависимо от применяемой лекарственной формы, в виде эрозивно-язвенных поражений желудка и двенадцатиперстной кишки.
Ряд авторов (Корнеева О.Н. и др. Доказательная гастроэнтерология. 2012;(2): 77-82.) описывают профилактику желудочно-кишечных осложнений при приеме антитромбоцитарных препаратов в виде добавления ингибиторов протонной помпы (ИПП) (омепразол в дозе 20 мг в сутки) к комбинации аспирина и клопидогрела, что сопровождается достоверным уменьшением риска желудочно-кишечных кровотечений на 45%. При этом авторы рекомендуют назначать пантопразол или рабепразол, поскольку последние не влияют на систему цитохрома 2C19 (CYP2C19) для пациентов с сердечно-сосудистой патологией, получающим антитромбоцитарные препараты.
Анализ литературы показывает, что пантопразол является нестабильным веществом. Поэтому данную его особенность необходимо учитывать при выборе вспомогательных веществ при разработке лекарственной формы, так как вещества в смеси могут влиять на стабильность друг друга. Например, пантопразол способен разрушаться, причем скорость деградации зависит от рН среды. Она будет выше, чем меньше значения рН среды (Шелехова В. А., и др., Физико-химические свойства и методы контроля пантопразола натрия сесквигидрата. Разработка и регистрация лекарственных средств. 2020; 9(1): 46-53). Также хорошо известно, что гигроскопичные добавки ухудшают высвобождение пантопразола после хранения (WO 2005/051348).
Целью настоящего изобретения является разработка композиции, содержащей НПВС (ацетилсалициловую кислоту), ИПП (пантопразол) и антацид (магния гидроксид) в одной лекарственной форме, а также разработка способа получения фармацевтической композиции, который позволит получить гранулы с улучшенным высвобождением действующих веществ, тем самым обеспечивая улучшенную оральную биодоступность.
Технические результаты, достигаемые изобретением, заключаются в том, что
- улучшается оральная биодоступность действующих веществ;
- уменьшаются побочные реакций.
Сущность настоящего изобретения заключается в том, что используют способ получения фармацевтической композиции включающий:
А) получение гранул пантопразола путем
- получения первого раствора покрытия при смешивании воды очищенной с фармацевтически приемлемым покрытием на основе гидроксипропилметилцеллюлозы и пантопразолом при скорости от 450 об/мин до 500 об/мин, при рН воды от 10 до 12, достигаемое путем прибавления 1 М раствора натрия гидроксида;
- получения второго раствора покрытия при перемешивании воды очищенной на скорости от 450 об/мин до 500 об/мин, в течении времени, равном от 30 до 60 минут с гипромелозой низкой вязкости, с добавлением талька;
- получения третьего раствора покрытия путем смешения метакриловой кислоты с водой очищенной и сополимера этилакрилата в соотношении 1:1 при скорости от 450 об/мин до 500 об/мин;
- нанесения первого, второго и третьего слоев покрытий, осуществляется последовательно с помощью установки псевдоожиженного слоя при температуре 40- 50 °С на инертные ядра-сферы из сахарозы или микрокристаллической целлюлозы;
Б) получение гранул ацетилсалициловой кислоты путем
- предварительного смешивания ацетилсалициловой кислоты с наполнителем, выбранным из лактозы моногидрата, или маннитола, или микрокристаллической целлюлозы или другого фармацевтически приемлемого наполнителя, увлажнения раствором поливинилпирролидона с последующим гранулированием и сушкой гранул при температуре 50-60° в течении времени равном от 10 мин до 30 мин;
или получение гранул ацетилсалициловой кислоты путем
- предварительного смешивания ацетилсалициловой кислоты с наполнителем, выбранным из лактозы моногидрата, или маннитола, или микрокристаллической целлюлозы или другого фармацевтически приемлемого наполнителя, увлажнения раствором поливинилпирролидона с последующим гранулированием и сушкой гранул при температуре 50-60° в течении времени равном от 10 мин до 30 мин;
- покрытия влагозащитной оболочкой, растворимой в желудке, диметиламиноэтилметакрилата, бутилметакрилата или метилметакрилата, или на основе диметиламиноэтилметакрилата, бутилметакрилата и метилметакрилата в соотношении 1:2:1;
В) получение гранул магния гидроксида путем
- предварительного смешивания магния гидроксида с наполнителем, выбранным из лактозы моногидрата, маннитола, микрокристаллической целлюлозы, крахмала или другого фармацевтически приемлемого наполнителя, увлажнения раствором поливинилпирролидона с последующим гранулированием и сушкой гранул при температуре 50-60° в течении времени равном от 10 мин до 30 мин;
или получение гранул магния гидроксида путем
- предварительного смешивания магния гидроксида с наполнителем, выбранным из лактозы моногидрата, маннитола, микрокристаллической целлюлозы, крахмала или другого фармацевтически приемлемого наполнителя, увлажнения раствором поливинилпирролидона с последующим гранулированием и сушкой гранул при температуре 50-60°С в течении времени равном от 10 мин до 30 мин;
- покрытия влагозащитной оболочкой, растворимой в желудке, на основе диметиламиноэтилметакрилата, бутилметакрилата или метилметакрилата, или на основе диметиламиноэтилметакрилата, бутилметакрилата и метилметакрилата в соотношении 1:2:1;
Г) смешение гранул, полученных стадией А с гранулами, полученными стадией Б, и гранулами, полученными стадией В, а также опудривание полученных смесей глидантом или тальком или коллоидным диоксидом кремния и последующее наполнение их в желатиновые капсулы.
Фармацевтическая композиция, полученная вышеописанным способом включает в себя :
Одним из неограничивающих вариантов изобретения является фармацевтическая композиция, полученная вышеописанным способом, может быть следующего состава:
Другим из неограничивающих вариантов изобретения является фармацевтическая композиция, полученная вышеописанным способом, может быть следующего состава::
Третьим неограничивающим вариантом изобретения может быть фармацевтическая композиция, полученная вышеописанным способом, включающая в себя:
Четвертым неограничивающим вариантом изобретения может быть фармацевтическая композиция, полученная вышеописанным способом, включающая в себя:
Полученные фармацевтические композиции применяют для лечения и профилактики сердечно-сосудистых заболеваний.
Пример 1. Состав композиции для лечения сердечно-сосудистых заболеваний: ацетилсалициловая кислота в количестве 15 - 20%, пантопразол в количестве 4,0 - 4,5%, магния гидроксид в количестве 3,0 - 3,5%, вспомогательные вещества, взятые в количестве, необходимом для получения гранул, массой 450 мг.
В качестве вспомогательных веществ для получения гранул пантопразола используются ядра-сферы диаметром от 255 мкм до 850 мкм из сахарозы или МКЦ, покрытие для таблеток на основе ГПМЦ, покрытие, растворимое в кишечнике, на основе метакриловой кислоты (метакриловая кислота и сополимер этилакрилата 1:1).
В качестве вспомогательных веществ для получения гранул ацетилсалициловой кислоты используется фармацевтически приемлемый наполнитель, в том числе лактозы моногидрат, маннитол, микрокристаллическая целлюлоза, крахмал. Для получения увляжнителя используется поливинилпирролидон К-30.
В качестве глиданта перед наполнением капсул для опудривания смеси используют тальк или коллоидный кремния диоксид.
Технологический процесс получения композиции на основе ИПП, НПВП и антацида заключается в раздельном изготовлении гранул, с последующим их наполнением в капсулы.
Получение гранул ИПП состоит из стадий получения растворов покрытий и непосредственно нанесение слоев покрытий на инертные ядра-сферы из сахарозы или микрокристаллической целлюлозы (МКЦ) или на другой фармацевтически приемлемый носитель.
Получение первого раствора покрытия заключается в смешении воды очищенной с фармацевтически приемлемым покрытием на основе гидроксипропилметилцеллюлозы и пантопразолом при скорости от 200 об/мин до 1000 об/мин, предпочтительно от 400 об/мин до 600 об/мин, наиболее предпочтительно от 450 об/мин до 500 об/мин, наиболее предпочтительно приблизительно 450 об/мин, при этом необходимым условием является значение рН воды, которое должно находиться в диапазоне предпочтительно от 10 до 12, достигаемое путем прибавления 1 М раствор натрия гидроксида.
Получение второго раствора покрытия состоит из перемешивания воды очищенной на скорости от 200 об/мин до 1000 об/мин, предпочтительно от 400 об/мин до 600 об/мин, наиболее предпочтительно от 450 об/мин до 500 об/мин, наиболее предпочтительно приблизительно 450 об/мин, в течении времени равном от 30 до 60 минут, предпочтительно 45±1 мин, с гипромелозой низкой вязкости, предпочтительно с добавлением талька, что является очевидным для специалистов в данной области.
Получение третьего раствора покрытия происходит за счет смешения готовой смеси из метакриловой кислоты или другого фармацевтически приемлемого вещества, очевидного для специалиста данной области (например, ACRYL-EZE (Colorcon) или EUDRAGIT (Evonik)) с водой очищенной при скорости от 200 об/мин до 1000 об/мин, наиболее предпочтительно от 450 об/мин до 500 об/мин, в течении времени, равном от 30 до 60 минут, предпочтительно 45±1 мин Нанесение покрытий, предварительно профильтрованных через сито, с размером отверстий не более 0,5 мм, осуществляется последовательно с помощью установки псевдоожиженного слоя (ПОС) с помощью форсунки (размер не менее 0,6 мм и не более 1,2 мм, предпочтительно от 0,8 мм до 1,0 мм) при температуре не выше 50°С.
Получение гранул НПВП состоит из стадий получения раствора увлажнителя, влажной грануляции с последующей сушкой гранул.
Получение увлажнителя заключается в растворении поливинилпирролидона (ПВП К-30) в воде при перемешивании. Процесс получения гранул ацетилсалициловой кислоты заключается в предварительном смешивании ацетилсалициловой кислоты с фармацевтически приемлемым наполнителем, увлажнении полученной смеси раствором ПВП К-30 с последующим гранулированием и сушкой гранул при температуре 60°С в течении времени равном от 10 мин до 30 мин, предпочтительно 15 мин. Процесс получения гранул магния гидроксида заключается в предварительном смешивании магния гидроксида с фармацевтически приемлемым наполнителем, увлажнении полученной смеси раствором ПВП К-30 с последующим гранулированием и сушкой гранул при температуре 60°С в течении времени равном от 10 мин до 30 мин, предпочтительно 15 мин.
Получение гранул гидроксида магния включает в себя предварительное смешивание магния гидроксида с наполнителем, выбранным из лактозы моногидрат, маннитол, микрокристаллическую целлюлозу, крахмал или другой фармацевтически приемлемый наполнитель, увлажнения раствором поливинилпирролидона с последующим гранулированием и сушкой гранул при температуре 50-60° в течении времени равном от 10 мин до 30 мин;
- покрытие влагозащитной оболочкой, растворимой в желудке, на основе диметиламиноэтилметакрилата, или бутилметакрилата или метилметакрилата в соотношении 1:2:1;
Или получение гранул магния гидроксида путем
- предварительного смешивания магния гидроксида с наполнителем, включающим в том числе лактозы моногидрат, маннитол, микрокристаллическую целлюлозу, крахмал или другой фармацевтически приемлемый наполнитель, увлажнения раствором поливинилпирролидона с последующим гранулированием и сушкой гранул при температуре 50-60° в течении времени равном от 10 мин до 30 мин;
- покрытие влагозащитной оболочкой, растворимой в желудке, диметиламиноэтилметакрилата, бутилметакрилата или метилметакрилата, или на основе диметиламиноэтилметакрилата, бутилметакрилата и метилметакрилата в соотношении 1:2:1;
Полученные гранулы ИПП, НПВП и антацида проходят стадию калибровки, взвешивания рассчитанного количества гранул и опудривания глидантом, тальком или диоксидом кремния и последующим наполнением в желатиновые капсулы.
Пример 2. Изучение композиции для профилактики и лечения сердечно-сосудистых заболеваний, содержащей НПВП, ИПП и антацид на модели артериального тромбоза у кроликов.
Проведенное доклиническое экспериментальное исследование проводилось при 10-дневном пероральном пути введения половозрелым самцам кроликов породы «Советская шиншилла» на модели артериального тромбоза, вызванной аппликацией хлорида железа, в соответствии с соблюдением норм этического обращения с животными и в соответствии с принципами GLP. Тестируемую композицию вводили перорально в дозах 1 капсула (одна терапевтическая доза) и 3 капсулы (три терапевтические дозы), без разрушения капсулы и препараты сравнения ацетилсалициловая кислота (препарат Кардиомагнил®) и пантопразол (Пантопразол® Канон) в течение 10 дней.
Выбор дозы препарата для доклинического исследования осуществлялся путем известных методик расчета (Шекунова ЕВ, Ковалева МА, Макарова МН, Макаров ВГ. Выбор дозы препарата для доклинического исследования: межвидовой перенос доз. Ведомости Научного центра экспертизы средств медицинского применения. 2020;10(1):19-28. https://doi.org/10.30895/1991-2919-2020-10-1-19-28)
Моделирование патологии осуществлялось через 3 дня от начала введения препаратов. Затем введение исследуемых препаратов было продолжено в течение 7 дней. В качестве критериев эффективности действия препаратов изучали параметры системы гемостаза (активированное частичное тромбопластиновое время (АЧТВ), протромбиновое время (ПВ) и клинический анализ крови) на трех временных точках: до введения исследуемых препаратов (исходный уровень), до индукции патологии в день моделирования патологии (4-й день); по окончании курса терапии (10-й день эксперимента).
Результаты оценки показателей системы гемостаза животных показали, что на фоне 10-дневной терапии тестируемой композиции наблюдалось увеличение протромбинового времени, вне зависимости от дозы препарата. Терапевтический эффект композиции был более выражен по сравнению с эффектами комбинации препаратов сравнения.
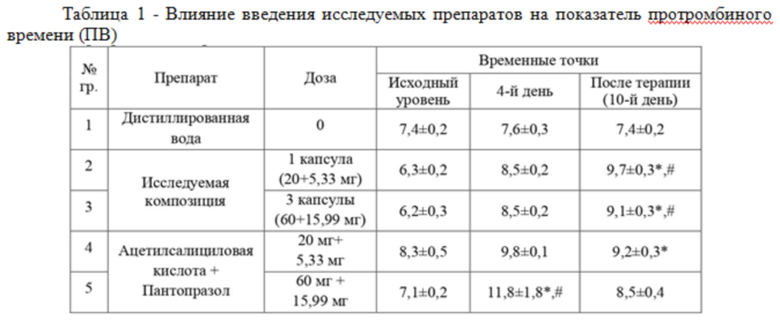
Примечания
1 - * - p<0,05, статистически значимы различия в сравнении с группой контроля в соответствующий день (критерий Тьюки);
2 - # - p<0,05, статистически значимы различия в сравнении с исходным уровнем в соответствующей группе (критерий Тьюки);
При анализе гистологических образцов ткани артерий, на фоне введения исследуемых препаратов, по сравнению с контрольной группой, наблюдалось снижение повреждений патоморфологической картины в группах, получавшие максимальные дозы.
Анализ образцов ткани желудка не выявил патологических изменений после введения исследуемых препаратов.
Пример 3. Проведено сравнительное доклиническое исследование токсических свойств композиции и зарегистрированных на территории РФ препаратов на кроликах при многократном пероральном введении. В данном исследовании осуществлено: анализ клинической картины интоксикации, анализ патологических изменений на основании данных клинико-лабораторных и морфологических показателей, выявление наиболее чувствительных систем и органов при многократном введении исследуемых препаратов, оценка местно-раздражающего действия и оценка обратимости выявленных патологических изменений. Препараты сравнения - Кардиомагнил таблетки, 75 + 15,2 мг (МНН: ацетилсалициловая кислота + магния гидроксид) и Пантопразол, таблетки, 20 мг (МНН: Пантопразол). Экспериментальные животные кролики породы «Белый Великан» (самцы и самки).
В результате исследования влияния на динамику массы тела, физико-химический состав мочи, систему гемостаза и биохимические показатели крови не обнаружено. Признаков местно-раздражающего действия исследуемых препаратов не обнаружено.
Исследуемые препараты не оказали влияния на гематологические показатели самок кроликов. У самцов выявлено снижение количества эритроцитов, уровня гемоглобина и уровня гематокрита в группах, получавших композицию и Кардиомагнил® в дозе 5 капсул/таблеток на животное по окончании периода введения. После периода отсроченного наблюдения регистрировали снижение количества тромбоцитов и тромбокрита у самцов группы максимальной дозы Кардиомагнил®.
По влиянию на гематологические показатели тестируемая композиция оказал сопоставимое действие, как и препарат сравнения Кардиомагнил®. По результатам оценки всех остальных исследованных в ходе изучения токсических свойств параметров тестируемая композиция и препараты сравнения не оказали клинически значимого влияние на организм лабораторных животных. Каких-либо неожидаемых нежелательных эффектов при применении комбинированного препарата не выявлено.
Группа изобретений относится к фармацевтической промышленности и касается способа получения фармацевтической композиции, композиции, полученной указанным способом, и ее применения для лечения и профилактики сердечно-сосудистых заболеваний. Предлагаемый способ получения композиции включает получение гранул пантопразола путем последовательного нанесения с помощью установки псевдоожиженного слоя при 40-50°С трех различных растворов покрытия на инертные ядра-сферы из сахарозы или микрокристаллической целлюлозы, получение гранул ацетилсалициловой кислоты и гранул гидроксида магния, покрытых влагозащитной оболочкой, растворимой в желудке. Полученные гранулы смешивают, опудривают глидантом и наполняют ими желатиновые капсулы. Предлагается также фармацевтическая композиция, полученная указанным выше способом, которая включает, в мг/капсулу: ацетилсалициловая кислота 65-85, пантопразол 10–30, магния гидроксид 10–20, ядра-сферы 100–150, гидроксипропилметилцеллюлоза 20–30, полимер метакриловой кислоты 40–70, поливинилпирролидон 5–25, маннитол 60–120, диметиламиноэтилметакрилат 40–70, тальк 5–10, и применение такой композиции для лечения и профилактики сердечно-сосудистых заболеваний. Использование способа позволяет получить композицию, содержащую в одной лекарственной форме гранулы трех действующих веществ - ацетилсалициловой кислоты (нестероидное противовоспалительное средство), пантопразола (ингибитор протонной помпы) и магния гидроксида (антацид) с улучшенным высвобождением, тем самым обеспечивая улучшенную оральную биодоступность. 3 н. и 1 з.п. ф-лы, 1 табл., 3 пр.
1. Способ получения фармацевтической композиции, включающий:
А) получение гранул пантопразола путем
- получения первого раствора покрытия при смешивании воды очищенной с фармацевтически приемлемым покрытием на основе гидроксипропилметилцеллюлозы и пантопразолом при скорости от 450 об/мин до 500 об/мин, при рН воды от 10 до 12, достигаемое путём прибавления 1 М раствора натрия гидроксида;
- получения второго раствора покрытия при перемешивании воды очищенной на скорости от 450 об/мин до 500 об/мин, в течение времени, равного от 30 до 60 мин с гипромелозой низкой вязкости, с добавлением талька;
- получения третьего раствора покрытия путем смешения метакриловой кислоты с водой очищенной и сополимера этилакрилата в соотношении 1:1 при скорости от 450 об/мин до 500 об/мин;
- нанесения первого, второго и третьего слоев покрытий, осуществляется последовательно с помощью установки псевдоожиженного слоя при температуре 40-50°С на инертные ядра-сферы из сахарозы или микрокристаллической целлюлозы;
Б) получение гранул ацетилсалициловой кислоты путем
- предварительного смешивания ацетилсалициловой кислоты с наполнителем, выбранным из лактозы моногидрата, или маннитола, или микрокристаллической целлюлозы, увлажнения раствором поливинилпирролидона с последующим гранулированием и сушкой гранул при температуре 50-60°С в течение времени равного от 10 мин до 30 мин;
- покрытие влагозащитной оболочкой, растворимой в желудке, на основе диметиламиноэтилметакрилата, бутилметакрилата и метилметакрилата в соотношении 1:2:1;
В) получение гранул магния гидроксида путем
получения гранул магния гидроксида путем
- предварительного смешивания магния гидроксида с наполнителем, выбранным из лактозы моногидрата, маннитола, микрокристаллической целлюлозы, крахмала, увлажнения раствором поливинилпирролидона с последующим гранулированием и сушкой гранул при температуре 50-60°С в течение времени равного от 10 мин до 30 мин;
- покрытия влагозащитной оболочкой, растворимой в желудке, на основе диметиламиноэтилметакрилата, бутилметакрилата или метилметакрилата, или на основе диметиламиноэтилметакрилата, бутилметакрилата и метилметакрилата в соотношении 1:2:1;
Г) смешение гранул, полученных стадией А, с гранулами, полученными стадией Б, и гранулами, полученными стадией В, а также опудривание полученных смесей глидантом или тальком или коллоидным диоксидом кремния и последующее наполнение ими желатиновых капсул.
2. Фармацевтическая композиция для лечения и профилактики сердечно-сосудистых заболеваний, полученная способом по п.1, включающая:
3. Фармацевтическая композиция по п.2, где ядра-сферы из сахарозы или микрокристаллической целлюлозы диаметром 255–850 нм.
4. Применение фармацевтической композиции по п.2 для лечения и профилактики сердечно-сосудистых заболеваний.
| CN 102406938 A, 11.04.2012 | |||
| JP 2005145894 A, 09.06.2005 | |||
| ФАРМАЦЕВТИЧЕСКИЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИЕМА, СОДЕРЖАЩИЕ ИНГИБИТОР ПРОТОННОГО НАСОСА И СРЕДСТВО НЕСТЕРОИДНОЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ ТЕРАПИИ | 1996 |
|
RU2158138C2 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
Авторы
Даты
2023-02-28—Публикация
2021-11-15—Подача