Область техники, к которой относится настоящее изобретение
[0001] Настоящее изобретение относится к трансдермальной терапевтической системе (TTS) для трансдермального введения гуанфацина в системный кровоток и к способам ее получения, способу лечения и к ее применениям.
Предшествующий уровень техники настоящего изобретения
[0002] Активное средство гуанфацин (так же известный как N-(аминоиминометил)-2,6-дихлор-бензолацетамид, C9H9Cl2N3O, № согласно CAS 29110-47-2) представляет собой симпатолитическое лекарственное средство, используемое для лечения гипертензии и синдрома дефицита внимания с гиперактивностью (ADHD). Он представляет собой агонист альфа(2)-адренорецепторов центрального действия. Он характеризуется следующей химической формулой:
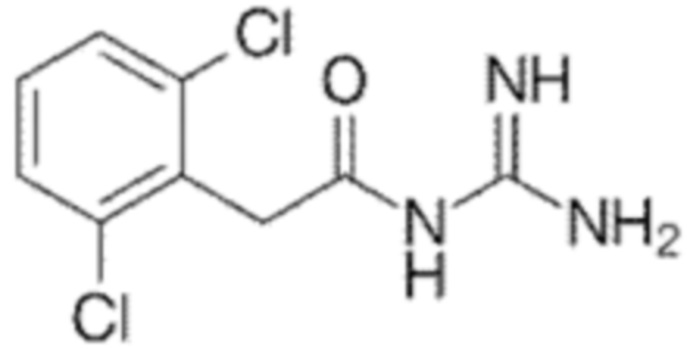
[0003] В настоящее время гуанфацин является коммерчески доступным, например, в форме таблеток с немедленным или контролируемым высвобождением, содержащих от 1 до 4 мг гуанфацина. Таблетки являются походящими для введения один раз в сутки.
[0004] Тем не менее, пероральное введение активных средств обладает недостатками, например, с точки зрения соблюдения пациентом режима и схемы лечения. Более того, невозможно быстро прекратить терапию, например, по причине передозировки или признаков непереносимости после приема внутрь таблетки с пролонгированным высвобождением.
[0005] Следовательно, существует потребность в трансдермальной терапевтической системе для трансдермального введения гуанфацина. В частности, существует потребность в TTS, которая является походящей для многодневной терапии с однократным применением, тем самым улучшая соблюдение пациентом режима и схемы лечения.
Цели и краткое раскрытие настоящего изобретения
[0006] Следовательно, целью настоящего изобретения является получение TTS для трансдермального введения гуанфацина. В частности, целью настоящего изобретения является получение TTS для трансдермального введения гуанфацина, обеспечивающей скорость чрескожного проникновения, которая является достаточной для достижения терапевтически эффективной дозы.
[0007] Дополнительной целью настоящего изобретения является получение TTS для трансдермального введения гуанфацина, обеспечивающей терапевтически эффективные количества гуанфацина в течение по меньшей мере 24 часов, предпочтительно по меньшей мере 72 часов, более предпочтительно приблизительно 84 часов. В частности, целью настоящего изобретения является то, чтобы терапевтически эффективные количества обеспечивались в течение всего периода времени, когда TTS нанесена на кожу, обеспечивая круглосуточное лечение путем замены TTS после определенного времени нанесения, составляющего, например, по меньшей мере 24 часа, предпочтительно по меньшей мере 72 часа, более предпочтительно приблизительно 84 часа.
[0008] Дополнительной целью настоящего изобретения является получение TTS для трансдермального введения гуанфацина, где колебание концентрации гуанфацина в плазме крови снижается по сравнению с пероральным введением, в частности в равновесном состоянии.
[0009] Дополнительной целью настоящего изобретения является получение TTS для трансдермального введения гуанфацина с высокой степенью использования действующего вещества.
[0010] Другой целью настоящего изобретения является получение TTS для трансдермального введения гуанфацина, которая удовлетворяет потребности в удобном применении с точки зрения размера и толщины и/или которую легко и экономически выгодно изготавливать.
[0011] Указанные и другие цели осуществляются с помощью настоящего изобретения, которое согласно одному аспекту относится к трансдермальной терапевтической системе для трансдермального введения гуанфацина, содержащей гуанфацин-содержащую слоистую структуру, причем указанная гуанфацин-содержащая слоистая структура содержит:
A) подложка; и
B) гуанфацин-содержащий слой;
причем трансдермальная терапевтическая система содержит по меньшей мере один силиконовый полимер.
[0012] Было обнаружено, что TTS согласно настоящему изобретению, которая содержит силиконовый полимер, обеспечивает благоприятные свойства в отношении постоянной и непрерывной доставки гуанфацина. В частности, TTS согласно настоящему изобретению обеспечивает походящие скорости проникновения и походящие проникшие количества гуанфацина в течение периода времени, составляющего по меньшей мере 24 часа, предпочтительно по меньшей мере 72 часа, более предпочтительно приблизительно 84 часа.
[0013] Согласно определенным вариантам осуществления настоящее изобретение также относится к трансдермальной терапевтической системе для трансдермального введения гуанфацина, как описано выше, в которой гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, содержащий:
i) гуанфацин, и
ii) по меньшей мере один силиконовый полимер.
[0014] Согласно определенным предпочтительным вариантам осуществления гуанфацин-содержащая слоистая структура дополнительно содержит по меньшей мере одно вспомогательное вещество, выбранное из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов.
[0015] Согласно одному конкретному аспекту настоящее изобретение относится к трансдермальной терапевтической системе для трансдермального введения гуанфацина, содержащей гуанфацин-содержащую слоистую структуру, причем указанная гуанфацин-содержащая слоистая структура содержит:
A) подложка; и
B) гуанфацин-содержащий слой, предпочтительно гуанфацин-содержащий матричный слой, содержащий:
i) гуанфацин в количестве 3-13% по массе в расчете на общую массу гуанфацин-содержащего слоя;
ii) по меньшей мере один силиконовый полимер в количестве 35-90% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iii) по меньшей мере один диспергирующий агент в количестве 2-6% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iv) по меньшей мере один усилитель проницаемости в количестве 2-10% по массе в расчете на общую массу гуанфацин-содержащего слоя; и
v) необязательно по меньшей мере один солюбилизатор в количестве 0,5-4% по массе в расчете на общую массу гуанфацин-содержащего слоя.
[0016] Согласно определенным вариантам осуществления настоящего изобретения трансдермальная терапевтическая система согласно настоящему изобретению предусмотрена для применения в способе лечения пациента-человека, предпочтительно для применения в способе лечения пациента-человека в возрасте, составляющем 6-17 лет. В частности, трансдермальная терапевтическая система согласно настоящему изобретению предусмотрена для применения в способе лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) и/или в качестве дополнительной терапии к лекарственным средствам-стимуляторам у пациента-человека, предпочтительно у пациента-человека в возрасте, составляющем 6-17 лет. В связи с этими медицинскими применениями TTS согласно настоящему изобретению предпочтительно наносят на кожу пациента в течение по меньшей мере 24 часов, более предпочтительно по меньшей мере 72 часов, наиболее предпочтительно приблизительно 84 часов.
[0017] Согласно определенным вариантам осуществления настоящее изобретение дополнительно относится к способу лечения пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем нанесения трансдермальной терапевтической системы согласно настоящему изобретению на кожу пациента. В частности, настоящее изобретение относится к способу лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) у пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем нанесения трансдермальной терапевтической системы согласно настоящему изобретению на кожу пациента. В связи с указанными способами предпочтительным является то, что TTS согласно настоящему изобретению наносят на кожу пациента в течение по меньшей мере 24 часов, более предпочтительно по меньшей мере 72 часов, наиболее предпочтительно приблизительно 84 часов.
[0018] Согласно другому аспекту настоящее изобретение относится к способу получения гуанфацин-содержащего слоя для применения в трансдермальной терапевтической системе согласно настоящему изобретению, предусматривающему стадии:
1) объединение по меньшей мере следующих компонентов:
i) гуанфацин; и
ii) по меньшей мере один силиконовый полимер
для получения композиции для покрытия;
2) нанесение композиции для покрытия на подложку или защитное покрытие для получения нанесенной композиции для покрытия; и
3) сушка нанесенной композиции для покрытия с образованием гуанфацин-содержащего слоя.
[0019] Предпочтительно силиконовый полимер представлен в виде раствора, причем растворитель представляет собой этилацетат или н-гептан, предпочтительно этилацетат.
[0020] Согласно другому аспекту настоящее изобретение относится к трансдермальной терапевтической системе, получаемой с помощью способа согласно настоящему изобретению.
Определения
[0021] Используемый в настоящем изобретении термин "трансдермальная терапевтическая система" (TTS) относится к системе, с помощью которой активное средство (например, гуанфацин) вводят в системный кровоток посредством трансдермальной доставки и относится ко всей отдельной единице дозирования, которую наносят, после удаления необязательно присутствующего защитного покрытия, на кожу пациента, и которая содержит терапевтически эффективное количество активного средства в содержащей активное средство слоистой структуре и необязательно дополнительный адгезивный слой поверх содержащей активное средство слоистой структуры. Содержащая активное средство слоистая структура может быть расположена на защитном покрытии (съемный защитный слой), таким образом, TTS может дополнительно содержать защитное покрытие. Используемый в настоящем изобретении термин "TTS", в частности, относится к системам, обеспечивающим трансдермальную доставку, исключая активную доставку, например, посредством ионтофореза или микропорации. Трансдермальные терапевтические системы могут также называться трансдермальными системами доставки лекарственного средства (TDDS) или трансдермальными системами доставки (TDS).
[0022] Используемый в настоящем изобретении термин "гуанфацин-содержащая слоистая структура" относится к слоистой структуре, содержащей терапевтически эффективное количество гуанфацина и содержащей подложку и по меньшей мере один гуанфацин-содержащий слой. Предпочтительно гуанфацин-содержащая слоистая структура представляет собой гуанфацин-содержащую самоклеящуюся слоистую структуру.
[0023] Используемый в настоящем изобретении термин "терапевтически эффективное количество" относится к количеству активного средства в TTS, которое при введении с помощью TTS пациенту, является достаточным для лечения, профилактики или снижения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) или которое является достаточным для дополнительной терапии к лекарственным средствам-стимуляторам у пациента-человека. TTS, как правило, содержит больше активного средства в системе, чем в действительности доставляется на кожу и в системный кровоток. Это избыточное количество активного средства, как правило, является необходимым для обеспечения достаточной движущей силы для доставки из TTS в системный кровоток.
[0024] Используемые в настоящем изобретении термины "активный агент", "активное средство" и тому подобное, а также термин "гуанфацин" относятся к гуанфацину в любой фармацевтически приемлемой химической и морфологической форме и физическом состоянии. Эти формы включают в себя без ограничения гуанфацин в форме его свободного основания, протонированный или частично протонированный гуанфацин, соли гуанфацина и, в частности, соли присоединения кислоты, образованные добавлением неорганической или органической кислоты, такие как гидрохлорид гуанфацина или тартрат гуанфацина, сольваты, гидраты, клатраты, сокристаллы, комплексы и т.д., а также гуанфацин в форме частиц, которые могут являться микронизированными, кристаллическими и/или аморфными, и любые смеси вышеупомянутых форм. Гуанфацин, если он содержится в среде, такой как растворитель, предпочтительно присутствует в дисперсной форме.
[0025] Когда упоминается, что гуанфацин используют в конкретной форме при изготовлении TTS, это не исключает взаимодействия между этой формой гуанфацина и другими ингредиентами гуанфацин-содержащей слоистой структуры, например, солеобразование или комплексообразование, в конечной TTS. Это означает, что, даже если гуанфацин включен в форме своего свободного основания, он может присутствовать в конечной TTS в протонированной или частично протонированной форме или в форме соли присоединения кислоты, или, если он включен в форме соли, его части могут присутствовать в виде свободного основания в конечной TTS. Если не указано иное, в частности, количество гуанфацина в слоистой структуре относится к количеству гуанфацина, включенного в TTS во время изготовления TTS, и рассчитывается на основе гуанфацина в форме свободного основания. Например, когда а) 0,1 ммоль (равно 24,61 мг) основания гуанфацина или b) 0,1 ммоль (равно 27,71 мг) гидрохлорида гуанфацина включено в TTS во время изготовления, количество гуанфацина в слоистой структуре составляет согласно настоящему изобретению в обоих случаях 24,06 мг, т.е. 0,1 ммоль.
[0026] Исходный материал гуанфацин, включенный в TTS во время изготовления TTS, может находиться в форме частиц. Гуанфацин может, например, присутствовать в содержащей активное средство слоистой структуре, в форме частиц, которые предпочтительно гомогенно диспергированы в содержащей активное средство слоистой структуре.
[0027] Используемый в настоящем изобретении термин "частицы" относится к твердому порошкообразному материалу, содержащему отдельные частицы, размеры которых являются незначительными по сравнению с материалом. В частности, частицы являются твердыми, включая в себя пластичные/деформируемые твердые вещества, включая в себя аморфные и кристаллические материалы.
[0028] В значении данного изобретения термин "диспергирование" относится к стадии или комбинации стадий, в которых исходный материал (например, гуанфацин) не растворяется или не растворяется полностью. Диспергирование согласно настоящему изобретению включает в себя растворение части исходного материала (например, частиц гуанфацина) в зависимости от растворимости исходного материала (например, растворимости гуанфацина в композиции для покрытия).
[0029] Существует два основных типа TTS для доставки активного средства, т.е. TTS матричного типа и TTS резервуарного типа. Высвобождение активного средства в TTS матричного типа в основном контролируется матрицей, включающей в себя само активное средство. В отличие от этого, TTS резервуарного типа, как правило, нуждается в мембране, контролирующей скорость, которая контролирует высвобождение активного средства. В принципе, TTS матричного типа также может содержать контролирующую скорость мембрану. Тем не менее, TTS матричного типа имеет то преимущество, что по сравнению с TTS резервуарного типа, как правило, не требуются мембраны, определяющие скорость, и не может произойти сброс дозы из-за разрыва мембраны. Таким образом, трансдермальные терапевтические системы матричного типа (TTS) являются менее сложными в изготовлении и простыми и удобными в использовании пациентами.
[0030] Согласно настоящему изобретению "TTS матричного типа" относится к системе или структуре, в которой активное средство гомогенно растворено и/или диспергировано в полимерном носителе, т.е. в матрице, которая образуется с активным средством и необязательно остальными ингредиентами матричный слой. В такой системе матричный слой контролирует высвобождение активного средства из TTS. Предпочтительно матричный слой имеет достаточную когезию, чтобы быть самоподдерживающимся, так что не требуется герметизация между другими слоями. Соответственно, содержащий активное средство слой согласно одному варианту осуществления настоящего изобретения может представлять собой содержащий активное средство матричный слой, где активное средство гомогенно распределено внутри полимерной матрицы. Согласно некоторым вариантам осуществления матричный слой, содержащий активное средство, может содержать два матричных слоя, содержащих активное средство, которые могут быть ламинированы вместе. TTS матричного типа, в частности, может находиться в форме TTS типа "лекарственное средство в адгезиве", относящейся к системе, в которой активное средство гомогенно растворено и/или диспергировано в приклеивающейся при надавливании адгезивной матрице. В связи с этим матричный слой, содержащий активное средство, также может называться приклеивающимся при надавливании адгезивным слоем, содержащим активное средство, или приклеивающимся при надавливании адгезивным матричным слоем, содержащим активное средство. TTS, содержащая активное средство, растворенное и/или диспергированное в полимерном геле, например, гидрогеле, также считается TTS матричного типа в соответствии с настоящим изобретением.
[0031] TTS с резервуаром, содержащим жидкое активное средство, обозначается термином "TTS резервуарного типа". В такой системе высвобождение активного средства предпочтительно контролируется мембраной, контролирующей скорость. В частности, резервуар герметизирован между подложкой и мембраной, регулирующей скорость. Соответственно, слой, содержащий активное средство, может согласно одному варианту осуществления представлять собой содержащий активное средство резервуарный слой, который предпочтительно содержит резервуар для жидкости, содержащий активное средство. Кроме того, TTS резервуарного типа, как правило, дополнительно содержит контактирующий с кожей слой, причем резервуарный слой и контактирующий с кожей слой могут быть разделены регулирующей скорость мембраной. В резервуарном слое активное средство предпочтительно растворяют в растворителе, таком как этанол или вода, или в силиконовом масле. Контактирующий с кожей слой, как правило, обладает адгезионными свойствами.
[0032] TTS резервуарного типа не следует понимать как матричный тип в значении согласно настоящему изобретению. Тем не менее, микрорезервуарные TTS (двухфазные системы, содержащие депо (например, сферы, капли) внутренней содержащей активное средство фазы, диспергированной во внешней полимерной фазе), считающиеся в настоящей области техники смешанной формой TTS матричного типа и TTS резервуарного типа, которая отличается от гомогенной однофазной TTS матричного типа и TTS резервуарного типа в концепции транспортировки лекарственного средства и доставки лекарственного средства, считаются матричными согласно настоящему изобретению. Размеры капель-микрорезервуаров можно определить с помощью измерения оптическим микроскопом (например, Leica MZ16, включающий в себя камеру, например, Leica DSC320) путем съемки микрорезервуаров в различных положениях с коэффициентом увеличения от 10 до 400 раз, в зависимости от требуемого предела обнаружения. Используя программное обеспечение для анализа изображений, можно определить размеры микрорезервуаров.
[0033] Используемый в настоящем изобретении термин "содержащий активное средство слой" относится к слою, содержащему активное средство и обеспечивающему площадь высвобождения. Термин охватывает матричные слои, содержащие активное средство, и резервуарные слои, содержащие активное средство. Если слой, содержащий активное средство, представляет собой матричный слой, содержащий активное средство, указанный слой присутствует в TTS матричного типа. Если полимер представляет собой приклеивающийся при надавливании адгезив, матричный слой может также представлять собой адгезивный слой TTS, так что дополнительный контактирующий с кожей слой отсутствует. Альтернативно, дополнительный контактирующий с кожей слой может присутствовать в качестве адгезивного слоя, и/или может присутствовать адгезивный верхний слой. Дополнительный контактирующий с кожей слой, как правило, изготавливают таким образом, что он не содержит активное средство. Тем не менее, из-за градиента концентрации активное средство со временем мигрирует из матричного слоя в дополнительный контактирующий с кожей слой, пока не будет достигнуто равновесие. Дополнительный контактирующий с кожей слой может присутствовать на матричном слое, содержащем активное средство, или быть отделенным от матричного слоя, содержащего активное средство, мембраной, предпочтительно контролирующей скорость мембраной. Предпочтительно матричный слой, содержащий активное средство, обладает достаточными адгезионными свойствами, так что дополнительный контактирующий с кожей слой отсутствует. Если слой, содержащий активное средство, представляет собой резервуарный слой, содержащий активное средство, указанный слой присутствует в TTS резервуарного типа, и этот слой содержит активное средство в резервуаре для жидкости. Кроме того, предпочтительно присутствует дополнительный контактирующий с кожей слой для обеспечения адгезионных свойств. Предпочтительно контролирующая скорость мембрана отделяет резервуарный слой от дополнительного контактирующего с кожей слоя. Дополнительный контактирующий с кожей слой может быть изготовлен таким образом, чтобы он не содержал активное средство или содержал активное средство. Если дополнительный контактирующий с кожей слой не содержит активное средство, активное средство будет мигрировать из-за градиента концентрации из резервуарного слоя в контактирующий с кожей слой с течением времени, пока не будет достигнуто равновесие. Кроме того, может быть предусмотрен адгезивный верхний слой.
[0034] Используемый в настоящем изобретении слой, содержащий активное средство, предпочтительно представляет собой матричный слой, содержащий активное средство, и относится к конечному отвердевшему слою. Предпочтительно матричный слой, содержащий активное средство, получают после нанесения покрытия и сушки композиции для покрытия, содержащей растворитель, как описано в настоящем документе. Альтернативно, матричный слой, содержащий активное средство, получают после нанесения покрытия из расплава и охлаждения. Матричный слой, содержащий активное средство, также можно изготовить путем ламинирования двух или более таких отвердевших слоев (например, высушенных или охлажденных слоев) одинакового состава для обеспечения требуемой массы поверхности. Матричный слой может являться самоклеящимся (в форме приклеивающегося при надавливании адгезивного матричного слоя), или TTS может содержать дополнительный контактирующий с кожей слой приклеивающегося при надавливании адгезива для обеспечения достаточной липкости. Предпочтительно матричный слой представляет собой приклеивающийся при надавливании адгезивный матричный слой. Необязательно может присутствовать адгезивный верхний слой.
[0035] Используемый в настоящем изобретении термин "приклеивающийся при надавливании адгезив" (также сокращенно обозначаемый как "PSA") относится к материалу, который, в частности, прилипает за счет давления пальца руки, является постоянно липким, оказывает сильное удерживающее усилие и должен удаляется с гладких поверхностей, не оставляя следов. Приклеивающийся при надавливании адгезивный слой при контакте с кожей является "самоклеящимся", т.е. обеспечивает адгезию к коже, поэтому обычно не требуется дополнительная помощь для фиксации на коже. "Самоклеящаяся" слоистая структура включает в себя приклеивающийся при надавливании адгезивный слой для контакта с кожей, который может быть выполнен в виде приклеивающегося при надавливании адгезивного матричного слоя или в форме дополнительного слоя, т.е. приклеивающегося при надавливании адгезивного контактирующего с кожей слоя. Для улучшения адгезии все еще можно использовать адгезивный верхний слой. Обеспечивающие приклеивание при надавливании адгезионные свойства приклеивающегося при надавливании адгезива зависят от используемого полимера или полимерной композиции.
[0036] Используемый в настоящем изобретении термин "силикон-акриловый гибридный полимер" относится к продукту полимеризации, включающему в себя повторяющиеся звенья силиконовых подвидов и акрилатных подвидов. Таким образом, силикон-акриловый гибридный полимер содержит силиконовую фазу и акриловую фазу. Предпочтительно силикон-акриловый гибридный полимер содержит силиконовую фазу и акрилатную фазу, т.е. силиконовые подвиды и акрилатные подвиды в определенном массовом отношении, например, от 60:40 до 40:60. Подразумевается, что термин "силикон-акриловый гибрид" обозначает больше, чем простую смесь подвидов на основе силикона и подвидов на основе акрилата. Вместо этого термин обозначает полимеризованные гибридные виды, которые включают в себя подвиды на основе силикона и подвиды на основе акрилата, которые были полимеризованы вместе. Силикон-акриловый гибридный полимер также может называться "силикон-акрилатный гибридный полимер", поскольку термины акрилат и акриловый обычно используют взаимозаменяемо в контексте гибридных полимеров, используемых в настоящем изобретении.
[0037] Используемый в настоящем изобретении термин "силикон-акриловый гибридный приклеивающийся при надавливании адгезив" относится к силикон-акриловому гибридному полимеру в форме приклеивающегося при надавливании адгезива. Силикон-акриловые гибридные приклеивающиеся при надавливании адгезивы описаны, например, в документах ЕР 2599847 и WO 2016/130408. Примеры силикон-акриловых гибридных приклеивающихся при надавливании адгезивов включают в себя PSA серии 7-6100 и 7-6300, производимые и поставляемые в н-гептане или этилацетате компанией Dow Coining (7-610Х и 7-630Х; X=1 на основе н-гептана/Х=2 на основе этилацетата). Было обнаружено, что в зависимости от растворителя, в котором поставляется силикон-акриловый гибридный PSA, расположение силиконовой фазы и акриловой фазы, обеспечивающих непрерывную внешнюю фазу из силикона или акрила и соответствующую дискретную внутреннюю фазу, различается. Если силикон-акриловый гибридный PSA поставляется в н-гептане, композиция содержит непрерывную силиконовую внешнюю фазу и дискретную акриловую внутреннюю фазу. Если силикон-акриловая гибридная PSA композиция поставляется в этилацетате, композиция содержит непрерывную акриловую внешнюю фазу и дискретную силиконовую внутреннюю фазу.
[0038] Используемый в настоящем изобретении термин "негибридный полимер" используют как синоним для полимера, который не включает в себя гибридные виды. Предпочтительно негибридный полимер представляет собой приклеивающийся при надавливании адгезив (например, приклеивающиеся при надавливании адгезивы на основе силикона или акрилата).
[0039] Используемый в настоящем изобретении термин "кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу" содержит продукт реакции конденсации силиконовой смолы, силиконового полимера и кремний-содержащего блокирующего агента, который обеспечивает указанную акрилатную или метакрилатную функциональную группу. Следует понимать, что кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, может включать в себя только акрилатную функциональную группу, только метакрилатную функциональную группу или как акрилатную функциональную группу, так и метакрилатную функциональную группу.
[0040] Используемый настоящем документе термин "содержащий активное средство матричный слой" представляет собой слой, содержащий активное средство, растворенное или диспергированное по меньшей мере в одном полимере, или содержащий активное средство, растворенное в растворителе с образованием смеси активного средства с растворителем, которая диспергирована в форме депо (в частности, капель) по меньшей мере в одном полимере. Предпочтительно по меньшей мере один полимер представляет собой приклеивающийся при надавливании адгезив на основе полимера (например, силиконовый приклеивающийся при надавливании адгезив). Используемый в настоящем изобретении термин "приклеивающийся при надавливании адгезивный слой" относится к приклеивающемуся при надавливании адгезивному слою, полученному из содержащей растворитель адгезивной композиции для покрытия после нанесения покрытия на пленку и испарения растворителей.
[0041] Используемый в настоящем изобретении термин "контактирующий с кожей слой" относится к слою, включенному в содержащую активное средство слоистую структуру, который находится в прямом контакте с кожей пациента во время нанесения. Это может быть содержащий активное средство слой. Когда TTS содержит дополнительный контактирующий с кожей слой, другие слои содержащей активное средство слоистой структуры не контактируют с кожей и не обязательно обладают самоклеящимися свойствами. Как указано выше, дополнительный контактирующий с кожей слой, прикрепленный к содержащему активное средство слою, может со временем абсорбировать части активного средства. Дополнительный контактирующий с кожей слой можно использовать для улучшения прилипания. Размеры дополнительного контактирующего с кожей слоя и содержащего активное средство слоя, как правило, являются одинаковыми и соответствуют площади высвобождения. Тем не менее, площадь дополнительного контактирующего с кожей слоя также может быть больше, чем площадь содержащего активное средство слоя. В таком случае площадь высвобождения все еще относится к площади содержащего активное средство слоя.
[0042] Используемый в настоящем изобретении термин "масса площади" относится к сухой массе конкретного слоя, например, матричного слоя, представленной в г/м2. Значения массы площади допускают отклонение, составляющее ± 10%, предпочтительно ± 7,5%, из-за изменчивости производственного процесса.
[0043] Если не указано иное, "%" относится к масс. % (% по массе).
[0044] Используемый в настоящем изобретении термин "полимер" относится к любому веществу, состоящему из так называемых повторяющихся звеньев, полученных полимеризацией одного или нескольких мономеров, и включает в себя гомополимеры, которые состоят из одного типа мономера, и сополимеры, которые состоят из двух или более типов мономеров. Полимеры могут характеризоваться любой архитектурой, такой как линейные полимеры, звездообразный полимер, гребенчатые полимеры, щеточные полимеры, характеризоваться любыми расположениями мономерных групп в случае сополимеров, например, чередующиеся, статистические, блок-сополимеры или привитые полимеры. Минимальная молекулярная масса варьируется в зависимости от типа полимера и известна специалисту в настоящей области техники. Полимеры могут, например, характеризоваться молекулярной массой, составляющей более 2000, предпочтительно более 5000 и более предпочтительно более 10000 дальтон. Соответственно, соединения с молекулярной массой ниже 2000, предпочтительно ниже 5000 или более предпочтительно ниже 10000 дальтон, как правило, называют олигомерами.
[0045] Используемый в настоящем изобретении термин "поперечно-сшивающий агент" относится к веществу, которое способно поперечно сшивать функциональные группы, содержащиеся в полимере.
[0046] Используемый в настоящем изобретении термин "адгезивный верхний слой" относится к самоклеящейся слоистой структуре, которая не содержит активное средство и больше по площади, чем содержащая активное средство структура, и обеспечивает дополнительную площадь, прилипающую к коже, но не площадь высвобождения активного средства. Он усиливает, тем самым, общие адгезионные свойства TTS. Адгезивный верхний слой содержит подложку, которая может обеспечивать окклюзивные или неокклюзивные свойства, и адгезивный слой. Предпочтительно подложка адгезивного верхнего слоя обеспечивает неокклюзивные свойства.
[0047] Используемый в настоящем изобретении термин "подложка" относится к слою, который поддерживает содержащий активное средство слой или образует основу адгезивного верхнего слоя. По меньшей мере одна подложка в TTS и, как правило, подложка содержащего активное средство слоя является по существу непроницаемой для активного средства, содержащегося в слое, в течение периода хранения и введения и, таким образом, предотвращает потерю активного средства или перекрестное загрязнение в соответствии с нормативными требованиями. Предпочтительно подложка также является окклюзивной, что означает, что она является по существу непроницаемой для воды и водяного пара. Походящие материалы для подложки включают в себя полиэтилентерефталат (PET), полиэтилен (РЕ), сополимер этилена-винилацетата (EVA), полиуретаны и их смеси. Походящие подложки представляют собой, таким образом, например, слоистые материалы PET, слоистые материалы EVA-PET и слоистые материалы РЕ-PET. Согласно предпочтительному варианту осуществления подложка представляет собой силиконизированную фольгу PET. Также походящие представляют собой тканые или нетканые материалы-подложки.
[0048] TTS согласно настоящему изобретению может характеризоваться определенными параметрами, измеренными в in vitro испытании на проницаемость кожи.
[0049] Как правило, in vitro испытание на проницаемость проводят в диффузионной ячейке Франца, на мембране EVA (например, 9% винилацетата и 50 мкм толщина, предпочтительно предоставленная 3М), и с использованием фосфатного буфера рН 5,5 или 7,4 в качестве рецепторной среды (32°C с 0,1% азидом натрия).
[0050] Кроме того, in vitro испытание на проницаемость можно проводить в диффузионной ячейке Франца, на коже человека или животного и предпочтительно на разделенной дерматомом по толщине коже человека с толщиной, составляющей 800 мкм, и неповрежденным эпидермисом, и с использованием фосфатного буфера рН 5,5 или 7,4 в качестве рецепторной среды (32°C с 0,1% азидом натрия) с добавлением или без максимум 40 об.% органического растворителя, например, этанола, ацетонитрила, изопропанола, дипропиленгликоля, PEG 400, так что рецепторная среда может, например, содержать 60 об.% фосфатного буфера с рН 5,5, 30 об.% дипропиленгликоля и 10 об.% ацетонитрила.
[0051] Если не указано иное, испытание на проницаемость in vitro проводят на разделенной дерматомом по толщине коже человека толщиной 800 мкм и неповрежденным эпидермисом и с фосфатным буфером рН 5,5 в качестве рецепторной среды (32°C с 0,1% азидом натрия). Количество активного средства, проникающего в рецепторную среду, определяют через регулярные промежутки времени с использованием валидированного способа ВЭЖХ с УФ-фотометрическим детектором, отбирая объем образца. Рецепторную среду полностью или частично заменяют свежей средой при взятии объема образца, и измеренное количество проникшего активного средства относится к количеству, проникшему между двумя последними точками отбора проб, а не к общему проникшему количеству до настоящего времени.
[0052] Таким образом, согласно настоящему изобретению параметр "проникшее количество" представляют в мкг/см2, и он относится к количеству активного средства, проникшего в интервале отбора образца за определенное истекшее время. Например, в испытании на проницаемость in vitro, как описано выше, где количество активного средства, проникшего в рецепторную среду, было, например, измерено в точках 0, 2, 4, 8, 12 и 24 часа, "проникшее количество" активного средства может быть представлено, например, для интервала отбора образца от 8 до 12 часов и соответствует измерению в точке 12 часов, причем рецепторную среду полностью заменяли в точке 8 часов.
[0053] Проникшее количество также можно представить как "кумулятивное проникшее количество", соответствующее накопленному количеству активного средства, проникшему в определенный момент времени. Например, в in vitro испытании на проницаемость, как описано выше, где количество активного средства, проникшего в рецепторную среду, было, например, измерено в точки 0, 2, 4, 8, 12 и 24 часа, "кумулятивное проникшее количество" активного средства в точке 12 часов соответствует сумме проникшего количества от 0 часов до 2 часов, от 2 часов до 4 часов, от 4 часов до 8 часов и от 8 часов до 12 часов.
[0054] Согласно настоящему изобретению параметр "скорость чрескожного проникновения" для определенного интервал отбора образца в определенное истекшее время представляют в мкг/(см2*ч) и рассчитывают из проникшего количества в указанном интервале отбора образца, как измерено с помощью in vitro испытания на проницаемость, как описано выше, в мкг/см2, деленного на часы указанного интервала отбора образца. Например, скорость чрескожного проникновения в in vitro испытании на проницаемость, как описано выше, где количество активного средства, проникшего в рецепторную среду, было, например, измерено в точки 0, 2, 4, 8, 12 и 24 часа, "скорость чрескожного проникновения" в точке 12 часов рассчитывают как проникшее количество в интервале отбора образца от 8 часов до 12 часов, деленное на 4 часа.
[0055] "Кумулятивную скорость чрескожного проникновения" можно рассчитать из соответственного кумулятивного проникшего количества путем деления кумулятивного проникшего количества на истекшее время. Например, в in vitro испытании на проницаемость, как описано выше, где количество активного средства, проникшего в рецепторную среду, было, например, измерено в точки 0, 2, 4, 8, 12 и 24 часа, "кумулятивную скорость чрескожного проникновения" в точке 12 часов рассчитывают как кумулятивное проникшее количество для точки 12 часов (см. выше), деленное на 12 часов.
[0056] Согласно настоящему изобретению представленные выше параметры "проникшее количество" и "скорость чрескожного проникновения" (а также "кумулятивное проникшее количество" и "кумулятивная скорость чрескожного проникновения") относятся к средним значениям, рассчитанным по меньшей мере из 3 экспериментов in vitro испытания на проницаемость. Если не указано иное, стандартное отклонение (SD) этих средних значений относится к скорректированному стандартному отклонению выборки, рассчитанному с использованием следующей формулы:
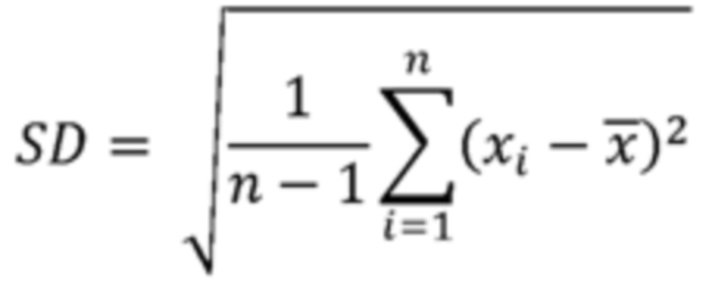
где n представляет собой размер выборки, {х1, х2, … xn} представляют собой наблюдаемые значения, и 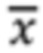 представляет собой среднее значение наблюдаемых значений.
представляет собой среднее значение наблюдаемых значений.
[0057] TTS согласно настоящему изобретению также может характеризоваться определенными параметрами, измеренными в in vivo клиническом исследовании.
[0058] Согласно настоящему изобретению параметр "средняя скорость высвобождения" относится к средней скорости высвобождения в мкг/ч (мкг/час) или в мг/день в течение периода введения (например, 1-7 дней), с которой активное средство высвобождается через кожу человека в системный кровоток, и она основана на значении AUC, полученном в течение указанного периода введения в клиническом исследовании.
[0059] Используемый в настоящем изобретении термин "продолжительный период времени" относится к периоду, составляющему по меньшей мере или приблизительно 24 ч, по меньшей мере или приблизительно 48 ч, по меньшей мере или приблизительно 72 ч, по меньшей мере или приблизительно 84 ч, по меньшей мере или приблизительно 1 день, по меньшей мере или приблизительно 2 дня, или по меньшей мере или приблизительно 3 дня, или по меньшей мере или приблизительно 3,5 дня, или к периоду, составляющему приблизительно 24 ч - приблизительно 168 ч, или 1-7 дней, или приблизительно 24 ч - приблизительно 84 ч, или 1-3,5 дня.
[0060] Для непрерывного лечения лекарственным средством частоту введения лекарственного средства предпочтительно поддерживают на достаточно высоком уровне, так чтобы поддерживать терапевтически эффективную концентрацию в плазме крови. Иными словами, интервал между двумя введениями лекарственной формы, также называемый интервалом между введениями доз, необходимо соответствующим образом адаптировать. Согласно настоящему изобретению термин "интервал между введениями доз" относится к периоду времени между двумя последовательными введениями TTS, т.е. интервал между двумя последовательными точками времени, когда TTS наносят на кожу пациента. После нанесения TTS, как правило, сохраняется на коже пациента в течение всего интервала между введениями доз, и ее удаляют только в конце интервала между введениями доз, после чего новую TTS наносят на кожу. Например, если интервал между введениями доз составляет 24 часа или 1 день, TTS наносится и сохраняется на коже пациента в течение 24 часов или 1 дня. Через 24 часа или 1 день TTS удаляют с кожи и наносят новую TTS. Таким образом, интервал между введениями доз, составляющий 24 часа или 1 день, обеспечивает режим ежедневной замены TTS при круглосуточном лечении. Согласно настоящему изобретению предпочтительным является интервал между введениями доз, составляющий по меньшей мере 72 часа, предпочтительно приблизительно 84 часа. Следует понимать, что время нанесения TTS на кожу пациента является предпочтительно идентичным времени интервала между введениями доз, что означает, что постоянное введение гуанфацина имеет место при замене TTS.
[0061] Используемый в настоящем изобретении термин "комнатная температура" относится к неизмененной температуре, обнаруженной в помещении лаборатории, где проводят эксперименты, и, как правило, она лежит в диапазоне от 15 до 35°С, предпочтительно приблизительно от 18 до 25°С.
[0062] Используемый в настоящем изобретении термин "пациент" относится к субъекту, у которого присутствует клиническое проявление определенного симптома или симптомов, указывающих на необходимость лечения, которого лечат превентивно или профилактически в отношении состояния или который был диагностирован с состоянием, подлежащим лечению. Предпочтительно возраст пациента составляет от 6 до 17 лет.
[0063] Используемый в настоящем изобретении термин "фармакокинетические параметры" относится к параметрам, описывающим кривую плазмы крови, например, Cmax, Ct и AUCt1-t2, полученным в клиническом исследовании, например, с помощью введения однократной дозы, многократных доз или стационарного введения TTS, содержащей активное средство, например, гуанфацин-содержащей TTS субъектам - здоровым людям. Фармакокинетические параметры отдельных субъектов суммируют с использованием арифметических и геометрических средств, например, среднее значение Cmax, среднее значение AUCt и среднее значение AUCINF, а также дополнительные статистические данные, такие как соответствующие стандартные отклонения и стандартные ошибки, минимальное значение, максимальное значение и среднее значение при ранжировании перечня значений (медиана). В контексте настоящего изобретения фармакокинетические параметры, например, Cmax, Ct и AUCt1-t2, относятся к средним геометрическим значениям, если не указано иное. Нельзя исключать, что абсолютные средние значения, полученные для определенной TTS в клиническом исследовании, варьируются в определенной степени от исследования к исследованию. Для сравнения абсолютных средних значений между исследованиями используют эталонный состав, например, в будущем любой продукт, основанный на настоящем изобретении, можно использовать в качестве внутреннего стандарта. Сравнение AUC по площади высвобождения соответствующего эталонного продукта в более раннем и более позднем исследовании можно использовать для получения коэффициента поправки, чтобы учесть различия от исследования к исследованию.
[0064] Клинические исследования согласно настоящему изобретению относятся к исследованиям, проводимым в полном соответствии с Международной конференцией по гармонизации клинических испытаний (ICH) и всеми применимыми местными стандартами надлежащей клинической практики (GCP) и правилами.
[0065] Используемый в настоящем изобретении термин "субъект - здоровый человек" относится к субъекту мужского или женского пола с массой тела в диапазоне от 55 кг до 100 кг и индексом массы тела (BMI) в диапазоне от 18 до 29,4 и нормальными физиологическими параметрами, такими как артериальное давление и т.д. Субъекты - здоровые люди для целей настоящего изобретения выбраны в соответствии с критериями включения и исключения в испытания, которые основаны и находятся в соответствии с рекомендациями ICH.
[0066] Используемый в настоящем изобретении термин "популяция субъектов" относится по меньшей мере к пяти, предпочтительно по меньшей мере к десяти отдельным субъектам - здоровым людям.
[0067] Используемый в настоящем изобретении термин "среднее геометрическое" относится к среднему значению логарифмически преобразованных данных, обратно преобразованных до исходного масштаба.
[0068] Используемый в настоящем изобретении термин "среднее арифметическое" относится к сумме всех значений наблюдения, деленной на общее количество наблюдений.
[0069] Согласно настоящему изобретению параметр "AUC" соответствует площади под кривой зависимости концентрации в плазме от времени. Значение AUC пропорционально количеству активного средства, абсорбированного в кровоток в целом, и, следовательно, является показателем биодоступности.
[0070] Согласно настоящему изобретению параметр "AUCt1-t2" представлен в (нг/мл) ч и относится к площади под кривой зависимости концентрации в плазме от времени от точки t1 часов до t2 часов и рассчитывается по линейному методу трапеций, если не указано иное. Другими способами расчета являются, например, логарифмический и линейный логарифмический метод трапеций.
[0071] Согласно настоящему изобретению параметр "Cmax" представлен в (нг/мл) и относится к максимальной наблюдаемой концентрации активного средства в плазме крови.
[0072] Согласно настоящему изобретению параметр "Ct" представлен в (нг/мл) и относится к концентрации активного средства в плазме крови, наблюдаемой в точке t часов.
[0073] Согласно настоящему изобретению параметр "tmax" представлен в часах и относится к моменту времени, в который достигается значение Cmax. Другими словами, tmax - это момент времени максимальной наблюдаемой концентрации в плазме.
[0074] Используемый в настоящем изобретении термин "средняя концентрация в плазме" представлена в (нг/мл) и представляет собой среднее значение отдельных концентраций активного средства в плазме, например, гуанфацина, в каждый момент времени.
[0075] Используемый в настоящем изобретении термин "композиция для покрытия" относится к композиции, содержащей все компоненты матричного слоя в растворителе, которая может быть нанесена на подложку или защитное покрытие для образования матричного слоя после сушки.
[0076] Используемый в настоящем изобретении термин "приклеивающаяся при надавливании адгезивная композиция" относится к приклеивающемуся при надавливании адгезиву по меньшей мере в смеси с растворителем (например, н-гептаном или этил ацетатом).
[0077] Используемый в настоящем изобретении термин "растворять" относится к процессу получения раствора, который является прозрачным и не содержит каких-либо частиц, видимых невооруженным глазом.
[0078] Используемый в настоящем изобретении термин "растворитель" относится к любому жидкому веществу, которое предпочтительно представляет собой летучую органическую жидкость, такую как метанол, этанол, изопропанол, ацетон, этилацетат, метиленхлорид, гексан, н-гептан, толуол и их смеси.
Краткое описание графических материалов
[0079] На фиг. 1 показано проникшее количество гуанфацина TTS, полученной согласно примерам 1a-d и сравнительному примеру 1.
[0080] На фиг. 2 показано проникшее количество гуанфацина TTS, полученной согласно примерам 2а-b.
[0081] На фиг. 3 показано проникшее количество гуанфацина TTS, полученной согласно примерам 3а-b.
[0082] На фиг. 4 показано проникшее количество гуанфацина TTS, полученной согласно сравнительным примерам 2а-b.
Подробное раскрытие настоящего изобретения
Структура TTS
[0083] Настоящее изобретение относится к трансдермальной терапевтической системе для трансдермального введения гуанфацина, содержащей гуанфацин-содержащую слоистую структуру, причем указанная гуанфацин-содержащая слоистая структура содержит: а) подложка, и b) гуанфацин-содержащий слой, причем трансдермальная терапевтическая система содержит по меньшей мере один силиконовый полимер. Эта гуанфацин-содержащая слоистая структура представляет собой предпочтительно гуанфацин-содержащую самоклеящуюся слоистую структуру и предпочтительно не содержит дополнительный контактирующий с кожей слой. В частности, силикон-акриловый гибридный полимер, который присутствует в трансдермальной терапевтической системе, предпочтительно в самоклеящейся слоистой структуре, предпочтительно обеспечивает адгезионные свойства.
[0084] TTS согласно настоящему изобретению может представлять собой TTS матричного типа или TTS резервуарного типа, и предпочтительно представляет собой TTS матричного типа.
[0085] В TTS матричного типа согласно настоящему изобретению гуанфацин предпочтительно гомогенно диспергирован в полимерном носителе, т.е. матрице, которая образует с гуанфацином и необязательно оставшимися ингредиентами матричный слой. Соответственно, гуанфацин-содержащий слой согласно одному варианту осуществления настоящего изобретения может представлять собой гуанфацин-содержащий матричный слой, где гуанфацин гомогенно диспергирован в полимерной матрице. Полимерная матрица предпочтительно содержит по меньшей мере один силиконовый полимер. Таким образом, согласно настоящему изобретению предпочтительным является то, что гуанфацин-содержащий матричный слой содержит гуанфацин и по меньшей мере один силиконовый полимер, который присутствует в TTS. В этой связи, также предпочтительным является то, что гуанфацин-содержащий матричный слой является самоклеящимся, так что отсутствует дополнительный контактирующий с кожей слой. Если гуанфацин-содержащий матричный слой получают путем ламинирования вместе двух гуанфацин-содержащих матричных слоев, которые по существу характеризуются одинаковым составом, полученный двойной слой следует рассматривать как один гуанфацин-содержащий матричный слой.
[0086] В TTS резервуарного типа согласно настоящему изобретению гуанфацин-содержащий слой представляет собой гуанфацин-содержащий резервуарный слой, который предпочтительно содержит резервуар для жидкости, содержащий гуанфацин. TTS резервуарного типа, как правило, дополнительно содержит контактирующий с кожей слой, где резервуарный слой и контактирующий с кожей слой предпочтительно разделены контролирующей скорость мембраной. По силикон-акриловый гибридный полимер затем обеспечивает адгезионные свойства. Предпочтительно контактирующий с кожей слой изготовлен так, что он не содержит гуанфацин.
[0087] Согласно предпочтительному варианту осуществления настоящего изобретения гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, содержащий:
i) гуанфацин, и
ii) по меньшей мере один силиконовый полимер.
[0088] Таким образом, согласно одному варианту осуществления настоящее изобретение относится к трансдермальной терапевтической системе для трансдермального введения гуанфацина, которая содержит гуанфацин-содержащую слоистую структуру, содержащую:
A) подложка; и
B) гуанфацин-содержащий слой, который представляет собой предпочтительно гуанфацин-содержащий матричный слой, содержащий:
i) гуанфацин, и
ii) по меньшей мере один силиконовый полимер.
[0089] Гуанфацин-содержащая слоистая структура представляет собой предпочтительно гуанфацин-содержащую самоклеящуюся слоистую структуру. В этой связи, предпочтительным также является то, что гуанфацин-содержащая слоистая структура не содержит дополнительный контактирующий с кожей слой. Вместо этого предпочтительным является то, что гуанфацин-содержащий слой, который представляет собой предпочтительно гуанфацин-содержащий матричный слой, является самоклеящимся. Таким образом, согласно предпочтительному варианту осуществления гуанфацин-содержащая слоистая структура представляет собой гуанфацин-содержащую самоклеящуюся слоистую структуру и предпочтительно не содержит дополнительный контактирующий с кожей слой. Альтернативно или дополнительно, предпочтительным является то, что гуанфацин-содержащий слой непосредственно прикреплен к подложке, так что отсутствует дополнительный слой между подложкой и гуанфацин-содержащим слоем. Следовательно, получают слоистую структуру низкой сложности, которая является благоприятной, например, с точки зрения затрат на изготовление.
[0090] В частности, предпочтительным является то, что гуанфацин-содержащая слоистая структура содержит не более чем 3, предпочтительно 2 слоя, т.е. предпочтительно только подложку и гуанфацин-содержащий слой. Достаточная адгезия между гуанфацин-содержащей самоклеящейся слоистой структурой и кожей пациента во время введения в этом случае обеспечивается гуанфацин-содержащим слоем, который представляет собой предпочтительно гуанфацин-содержащий матричный слой. Если присутствует дополнительный контактирующий с кожей слой, например, в качестве третьего слоя гуанфацин-содержащей слоистой структуры, адгезионные свойства могут обеспечиваться дополнительным контактирующим с кожей слоем. Тем не менее, согласно настоящему изобретению предпочтительным является то, что дополнительный контактирующий с кожей слой отсутствует.
[0091] Самоклеящиеся свойства гуанфацин-содержащей слоистой структуры предпочтительно обеспечены по меньшей мере одним силиконовым полимером, который присутствует в TTS, предпочтительно в гуанфацин-содержащем слое, более предпочтительно в гуанфацин-содержащем матричном слое. Таким образом, согласно предпочтительному варианту осуществления настоящего изобретения по меньшей мере один силиконовый полимер представляет собой силиконовый приклеивающийся при надавливании адгезив. Дополнительные детали в отношении силиконового полимера согласно настоящему изобретению приведены дополнительно ниже.
[0092] Следует понимать, что TTS, предпочтительно гуанфацин-содержащий слой, более предпочтительно гуанфацин-содержащий матричный слой также может содержать два силиконовых полимера.
[0093] Более того, TTS, предпочтительно гуанфацин-содержащий слой, более предпочтительно гуанфацин-содержащий матричный слой, может также содержать по меньшей мере один силиконовый полимер, и по меньшей мере один дополнительный полимер, выбранный из группы, состоящей из: акр штатные полимеры, силикон-акриловые гибридные полимеры, полиизобутилены и блок-сополимеры стирола-изопрена-стирола, предпочтительно выбранный из группы, состоящей из акрилатных полимеров и силикон-акриловых гибридных полимеров.
[0094] Например, первый полимер, обеспечивает преимущества с точки зрения интенсивного потока, при этом второй полимер, например, дополнительный силиконовый полимер или акрилатный полимер или силикон-акриловый гибридный полимер можно использовать для снижения и/или оптимизации потока для получения непрерывного и постоянного потока. Более того, липкость TTS можно модифицировать путем использования комбинации по меньшей мере двух полимеров. Дополнительные детали в отношении конкретных полимеров приведены дополнительно ниже.
[0095] Следует понимать, что TTS согласно настоящему изобретению содержит по меньшей мере терапевтически эффективное количество гуанфацина. Таким образом, согласно предпочтительному варианту осуществления настоящего изобретения гуанфацин-содержащая слоистая структура содержит терапевтически эффективное количество гуанфацина. Гуанфацин в гуанфацин-содержащей слоистой структуре предпочтительно присутствует в форме свободного основания, которое предпочтительно диспергировано в гуанфацин-содержащем слое. Предпочтительные варианты осуществления в отношении гуанфацина в TTS согласно настоящему изобретению приведены дополнительно ниже.
[0096] Согласно настоящему изобретению предпочтительным является то, что площадь высвобождения TTS находится в диапазоне от 1 до 100 см2, предпочтительно от 2,5 до 50 см2.
[0097] Согласно предпочтительному варианту осуществления настоящего изобретения подложка является по существу непроницаемой для гуанфацина. Более того, предпочтительным является то, что подложка является окклюзивной, как указано выше.
[0098] Согласно определенным вариантам осуществления настоящего изобретения TTS может дополнительно содержать адгезивный верхний слой. Этот адгезивный верхний слой, в частности, характеризуется большей площадью, чем гуанфацин-содержащая слоистая структура, и прикреплен к ней для усиления адгезионных свойств всей трансдермальной терапевтической системы. Указанный адгезивный верхний слой содержит подложку и адгезивный слой. Адгезивный верхний слой обеспечивает дополнительную площадь приклеивания к коже, но не добавляет площадь высвобождения гуанфацина. Адгезивный верхний слой содержит самоклеящийся полимер или смесь самоклеящихся полимеров, выбранных из группы, состоящей из: силикон-акриловые гибридные полимеры, акрилатные полимеры, силиконовые полимеры, полиизобутилены, сополимеры стирола-изопрена-стирола и их смеси, которые могут являться такими же или отличаться от любого полимера или смеси полимеров, включенных в гуанфацин-содержащую слоистую структуру.
[0099] Гуанфацин-содержащая слоистая структура согласно настоящему изобретению, такая как гуанфацин-содержащая самоклеящаяся слоистая структура, как правило, расположена на съемном защитном слое (защитное покрытие), с которого ее удаляют непосредственно перед нанесением на поверхность кожи пациента. Таким образом, TTS может дополнительно содержать защитное покрытие. TTS, защищенная таким образом, как правило, храниться в блистерной упаковке или пакете с герметичными швами. Упаковка может быть с функцией защиты от детей и/или являться легкой в обращении для пожилых людей.
Гуанфацин-содержащий слой
[0100] Как описано более подробно выше, TTS согласно настоящему изобретению содержит гуанфацин-содержащую слоистую структуру, содержащую гуанфацин-содержащий слой. Предпочтительно гуанфацин-содержащая слоистая структура представляет собой гуанфацин-содержащую самоклеящуюся слоистую структуру. Соответственно, предпочтительным также является то, что гуанфацин-содержащий слой представляет собой самоклеящийся гуанфацин-содержащий слой, более предпочтительно самоклеящийся гуанфацин-содержащий матричный слой. Согласно предпочтительному варианту осуществления гуанфацин-содержащий слой содержит терапевтически эффективное количество гуанфацина.
[0101] Согласно одному варианту осуществления настоящего изобретения гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой. Согласно другому варианту осуществления гуанфацин-содержащий слой представляет собой гуанфацин-содержащий резервуарный слой. Предпочтительным является то, что гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой.
[0102] Согласно одному варианту осуществления гуанфацин-содержащий слой содержит:
i) гуанфацин, предпочтительно в форме свободного основания; и
ii) по меньшей мере один силиконовый полимер.
Следует понимать, что по меньшей мере один силиконовый полимер, который представляет собой по меньшей мере один силиконовый полимер, который содержится в TTS согласно настоящему изобретению.
[0103] Согласно предпочтительному варианту осуществления гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, содержащий:
i) гуанфацин, предпочтительно в форме свободного основания; и
ii) по меньшей мере один силиконовый полимер.
Следует понимать, что по меньшей мере один силиконовый полимер, который представляет собой по меньшей мере один силиконовый полимер, который содержится в TTS согласно настоящему изобретению.
[0104] Согласно предпочтительному варианту осуществления гуанфацин-содержащий слой содержит по меньшей мере один силиконовый полимер, который представляет собой силиконовый приклеивающийся при надавливании адгезив. Таким образом, гуанфацин-содержащий слой представляет собой предпочтительно гуанфацин-содержащий матричный слой, и особенно предпочтительно гуанфацин-содержащий приклеивающийся при надавливании адгезивный матричный слой.
[0105] Согласно одному варианту осуществления настоящего изобретения гуанфацин-содержащий слой можно получить путем диспергирования гуанфацина, предпочтительно в форме свободного основания. В результате гуанфацин-содержащий слой TTS согласно настоящему изобретению, как правило, содержит гуанфацин в форме свободного основания. Кроме того, гуанфацин согласно определенным вариантам осуществления настоящего изобретения может частично присутствовать в протонированной форме. Тем не менее, предпочтительным является то, что по меньшей мере 50 моль %, предпочтительно по меньшей мере 75 моль % гуанфацина в гуанфацин-содержащем слое присутствуют в форме свободного основания. Согласно конкретному предпочтительному варианту осуществления по меньшей мере 90 моль %, предпочтительно по меньшей мере 95 моль %, более предпочтительно по меньшей мере 99 моль % гуанфацина в гуанфацин-содержащем слое присутствуют в форме свободного основания.
[0106] Согласно одному варианту осуществления настоящего изобретения гуанфацин-содержащая слоистая структура, предпочтительно гуанфацин-содержащий слой, более предпочтительно гуанфацин-содержащий матричный слой трансдермальной терапевтической системы согласно настоящему изобретению содержит гуанфацин в количестве 1-100 мг/TTS, предпочтительно 8-72 мг/TTS. Согласно предпочтительному варианту осуществления гуанфацин-содержащая слоистая структура, предпочтительно гуанфацин-содержащий слой, более предпочтительно гуанфацин-содержащий матричный слой содержит гуанфацин в количестве 8-30 мг/TTS, например, в количестве 8-10 мг/TTS или 17-19 мг/TTS. Другими словами, общее количество гуанфацина в гуанфацин-содержащей слоистой структуре находится в диапазоне от 1 до 100 мг/TTS, предпочтительно от 8 до 72 мг/TTS, более предпочтительно от 8 до 30 мг/TTS, например, от 8 до 10 мг/TTS или от 17 до 19 мг/TTS.
[0107] Согласно другому варианту осуществления нагрузка гуанфацина в гуанфацин-содержащей слоистой структуре находится в диапазоне от 0,2 до 1,6 мг/см2, предпочтительно от 0,4 до 1,2 мг/см2. Более того, предпочтительным является то, что площадь высвобождения TTS находится в диапазоне от 1 до 100 см2, предпочтительно от 2,5 до 50 см2.
[0108] Согласно одному варианту осуществления настоящего изобретения гуанфацин-содержащий слой содержит гуанфацин в количестве 1-20% по массе, предпочтительно 3-16% по массе, более предпочтительно 3-14% по массе, наиболее предпочтительно 3-13% по массе в расчете на общую массу гуанфацин-содержащего слоя. Например, гуанфацин-содержащий слой может содержать гуанфацин в количестве 3-8% по массе, предпочтительно 3-5 или 5-7% по массе, или в количестве 10-14% по массе, предпочтительно 11-13% по массе в расчете на общую массу гуанфацин-содержащего слоя, в зависимости от требуемой дозировки TTS.
[0109] Гуанфацин-содержащая слоистая структура и предпочтительно гуанфацин-содержащий слой содержит по меньшей мере один силиконовый полимер. Используемый в настоящем изобретении термин "силиконовый полимер" относится к полимеру на основе силикона или полимеру на основе полисилоксана, который можно предпочтительно получить, как описано ниже в настоящем документе. Предпочтительно силиконовый полимер представляет собой приклеивающийся при надавливании адгезивный полимер на основе силикона.
[0110] По меньшей мере один силиконовый полимер можно получить путем поликонденсации полидиметилсилоксана с блокированными концевыми силанольными группами с силикатной смолой. Концевая блокирующая группа предпочтительно представляет собой триметилсилильную группу. Предпочтительно по меньшей мере один силиконовый полимер представляет собой аминосовместимый силиконовый полимер. Аминосовместимые силиконовые полимеры могут быть получены путем реакции силиконового полимера с триметилсилилом (например, гексаметилдисилазаном) для снижения содержания силанола в полимере. Таким образом, в контексте по меньшей мере одного силиконового полимера, предпочтительным является то, что остаточная силанольная функциональная группа по меньшей мере одного силиконового полимера является по меньшей мере частично, предпочтительно в основном или полностью блокирована триметилсилоксигруппами.
[0111] Липкость по меньшей мере одного силиконового полимера можно модифицировать с помощью отношения смолы к полимеру, т.е. отношения полидиметилсилоксана с блокированной концевой силанольной группой к силикатной смоле, которое находится предпочтительно в диапазоне, составляющем 70:30 - 50:50, предпочтительно 65:35 - 55:45. Липкость будет увеличиваться с увеличением количеств полимера относительно смолы. Силиконовые полимеры с высокой липкостью предпочтительно характеризуются отношением смолы к полимеру, составляющим 55:45, силиконовые полимеры со средней липкостью предпочтительно характеризуются отношением смолы к полимеру, составляющим 60:40, и силиконовые полимеры с низкой липкостью предпочтительно характеризуются отношением смолы к полимеру, составляющим 65:35. Силиконовые полимеры с высокой липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×106 П, силиконовые полимеры со средней липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×107 П, и силиконовые полимеры с низкой липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×108 П. Аминосовместимые силиконовые полимеры с высокой липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×106 П, аминосовместимые силиконовые полимеры со средней липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×108 П, и аминосовместимые силиконовые полимеры с низкой липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×109 П. Предпочтительными согласно настоящему изобретению являются силиконовые полимеры со средней и высокой липкостью, в частности, аминосовместимые силиконовые полимеры со средней и высокой липкостью.
[0112] По меньшей мере один силиконовый полимер предпочтительно предусмотрен в форме раствора, причем растворитель представляет собой предпочтительно н-гептан или этилацетат.
[0113] Согласно предпочтительному варианту осуществления по меньшей мере один силиконовый полимер представляет собой силиконовый полимер, предпочтительно приклеивающийся при надавливании адгезив на основе силикона, который получают согласно следующей схеме:
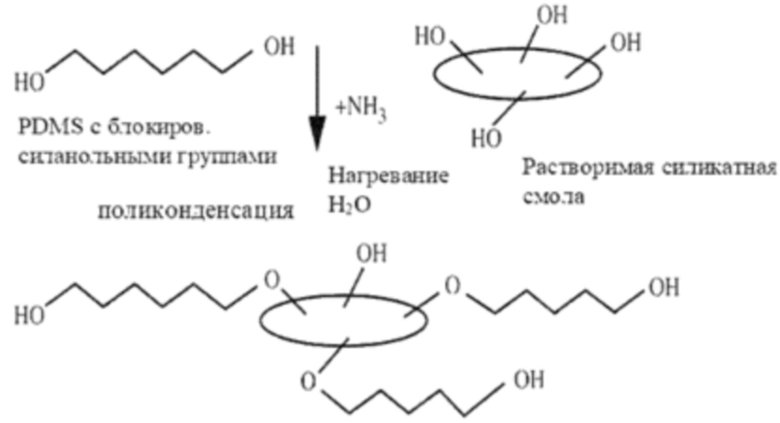
Такие силиконовые полимеры также носят название стандартного силиконового адгезива и являются доступными от Dow Corning, например, под торговыми марками BIO-PSA 7-4401, BIO-PSA-7-4501 или BIO-PSA 7-4601, которые поставляются в растворителе н-гептане (обозначено кодом "01"), или под торговыми марками BIO-PSA 7-4402, BIO-PSA 7-4502 и BIO 7-4602, которые поставляются в растворителе этилацетате (обозначено кодом "02"). Типичные содержания твердых веществ в растворителе находятся в диапазоне, составляющем 60-75%. Код "44" указывает на отношение смолы к полимеру, составляющее 65:35, что приводит к низкой липкости, код "45" указывает на отношение смолы к полимеру, составляющее 60:40, что приводит к средней липкости, код "46" указывает на отношение смолы к полимеру, составляющее 55:45, что приводит к высокой липкости.
[0114] Согласно более предпочтительному варианту осуществления по меньшей мере один силиконовый полимер представляет собой аминосовместимый силиконовый полимер, предпочтительно аминосовместимый приклеивающийся при надавливании адгезив на основе силикона, полученный согласно следующей схеме:

Такие аминосовместимые силиконовые полимеры доступны от Dow Corning, например, под торговыми марками BIO-PSA 7-4101, BIO-PSA-7-4201 или BIO-PSA 7-4301, которые поставляются в растворителе н-гептане (обозначено кодом "01"), или под торговыми марками BIO-PSA 7-4102, BIO-PSA 7-4202 и BIO 7-4302, которая которые поставляются растворителе этилацетате (обозначено кодом "02"). Типичные содержания твердых веществ в растворителе находятся в диапазоне, составляющем 60-75%. Код "41" указывает на отношение смолы к полимеру, составляющее 65:35, что приводит к низкой липкости, код "42" указывает на отношение смолы к полимеру, составляющее 60:40, что приводит к средней липкости, код "43" указывает на отношение смолы к полимеру, составляющее 55:45, что приводит к высокой липкости.
[0115] Согласно одному варианту осуществления настоящего изобретения гуанфацин-содержащий слой содержит по меньшей мере один силиконовый полимер, предпочтительно один или два силиконовых полимера.
[0116] Гуанфацин-содержащий слой также может содержать по меньшей мере один дополнительный полимер, выбранный из группы, состоящей из: акрилатные полимеры, силикон-акриловые гибридные полимеры, полиизобутилены и блок-сополимеры стирола-изопрена-стирола, предпочтительно выбранный из группы, состоящей из акрилатных полимеров и силикон-акриловых гибридных полимеров.
[0117] Акрилатные полимеры можно получить из одного или нескольких мономеров, выбранных из: акриловая кислота, бутилакрилат, 2-этилгексилакрилат, глицидилметакрилат, 2-гидроксиэтилакрилат, метилакрилат, метилметакрилат, т-октилакриламид и винилацетат, предпочтительно из одного или нескольких мономеров, выбранных из: этилгексилакрилат, глицидилметакрилат, 2-гидроксиэтилакрилат и винилацетат. Такие акрилатные полимеры являются доступными, например, от Henkel, как объяснено более подробно ниже.
[0118] Силикон-акриловые гибридные полимеры содержат силиконовую фазу и акрилатную фазу, предпочтительно в массовом отношении, составляющем от 60:40 до 40:60, наиболее предпочтительно в массовом отношении, составляющем 50:50. Силикон-акриловый гибридный полимер, как правило, содержит продукт реакции следующего: (а) кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, (b) этиленненасыщенный мономер; и (с) инициатор. Дополнительные подробности в отношении компонентов (а), (b) и (с) представлены дополнительно ниже. Следует понимать, что компонент (а) в основном образует силиконовую фазу, при этом компонент (b) в основном образует акрилатную фазу силикон-акрилового гибридного полимера. Акрилатная фаза влияет на липкость и вязкость силикон-акрилового гибридного полимера. Следовательно, предпочтительным является то, что этиленненасыщенный мономер, образующий акрилатную фазу, представляет собой комбинацию 2-этилгексилакрилата и метилакрилата, предпочтительно в отношении, составляющем от 40:60 до 70:30. Предпочтительным с точки зрения высокой липкости является отношение, составляющее 60:40, хотя вязкость при этом ниже. Предпочтительным с точки зрения повышенной вязкости является отношение, составляющее 50:50, хотя липкость при этом снижается. Силикон-акриловый гибридный полимер в гуанфацин-содержащем слое предпочтительно содержит непрерывную, акриловую внешнюю фазу и дискретную, силиконовую внутреннюю фазу.
[0119] Согласно одному варианту осуществления настоящего изобретения гуанфацин-содержащий слой содержит по меньшей мере один силиконовый полимер в количестве 20-99%, предпочтительно 30-97%, наиболее предпочтительно 35-90% по массе в расчете на общую массу гуанфацин-содержащего слоя. Представленные количества относятся к общему количеству одного или нескольких, предпочтительно одного или двух силиконовых полимеров в гуанфацин-содержащем слое. Тем не менее, как указано выше, гуанфацин-содержащий слой может дополнительно содержать по меньшей мере один дополнительный полимер, например, акрилатный полимер или силикон-акриловый гибридный полимер.
[0120] Согласно предпочтительному варианту осуществления настоящего изобретения гуанфацин-содержащий слой содержит первый полимер, который представляет собой силиконовый полимер, в количестве 35-70% по массе, и второй полимер, который выбран из группы, состоящей из силиконовых полимеров, акрилатных полимеров и силикон-акриловых гибридных полимеров, в количестве 15-45% по массе, в каждом случае в расчете на общую массу гуанфацин-содержащего слоя. Таким образом, гуанфацин-содержащий слой может содержать два различных силиконовых полимера, силиконовый полимер и акрилатный полимер или силиконовый полимер и силикон-акриловый гибридный полимер. Согласно особенно предпочтительному варианту осуществления гуанфацин-содержащий слой содержит первый силиконовый полимер в количестве 50-70% по массе в расчете на общую массу гуанфацин-содержащего слоя, и второй силиконовый полимер в количестве 15-25% по массе в расчете на общую массу гуанфацин-содержащего слоя.
[0121] Согласно определенным предпочтительным вариантам осуществления гуанфацин-содержащий слой может дополнительно содержать третий полимер, выбранный из группы, состоящей из силиконовых полимеров, акрилатных полимеров и силикон-акриловых гибридных полимеров, предпочтительно в количестве 1-5% по массе в расчете на общую массу гуанфацин-содержащего слоя.
[0122] Согласно одному варианту осуществления настоящего изобретения TTS согласно настоящему изобретению, и в частности гуанфацин-содержащий слой, содержит по меньшей мере одно вспомогательное вещество. Подходящие вспомогательные вещества описаны более подробно ниже, и каждое из них предпочтительно присутствует в количестве 0,5-10% по массе или 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя.
[0123] Согласно предпочтительному варианту осуществления настоящего изобретения гуанфацин-содержащий слой содержит по меньшей мере одно вспомогательное вещество, выбранное из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов. Согласно одному предпочтительному варианту осуществления по меньшей мере одно вспомогательное вещество, т.е. каждое отдельное вспомогательное вещество присутствует в количестве 0,5-10% по массе или 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Согласно одному предпочтительному варианту осуществления по меньшей мере одно вспомогательное вещество представляет собой диспергирующий агент. Согласно другому предпочтительному варианту осуществления по меньшей мере одно вспомогательное вещество представляет собой усилитель проницаемости. Согласно другому предпочтительному варианту осуществления по меньшей мере одно вспомогательное вещество представляет собой солюбилизатор. Согласно определенному предпочтительному варианту осуществления также предпочтительными являются комбинации вышеупомянутых вспомогательных веществ, например, комбинация диспергирующего агента и усилителя проницаемости, или комбинация диспергирующего агента и солюбилизатора, или комбинация усилителя проницаемости и солюбилизатора, или комбинация диспергирующего агента, усилителя проницаемости и солюбилизатора. Вышеупомянутые вспомогательные вещества характеризуются особым преимуществом для обеспечения гуанфацина в гомогенно диспергированной и высвобождаемой форме. Следует понимать, что диспергирующий агент также может действовать в качестве усилителя проницаемости и наоборот. Аналогично, солюбилизатор также может дополнительно действовать в качестве диспергирующего агента или усилителя проницаемости. Более того, солюбилизатор может стабилизировать дисперсию гуанфацина в TTS и предотвращать кристаллизацию. Более того, солюбилизатор может являться полезным в оптимизации когезии TTS. Согласно определенным предпочтительным вариантам осуществления гуанфацин-содержащий слой содержит по меньшей мере один диспергирующий агент, и по меньшей мере один усилитель проницаемости, и необязательно также по меньшей мере один солюбилизатор.
[0124] Согласно одному предпочтительному варианту осуществления по меньшей мере одно вспомогательное вещество представляет собой диспергирующий агент, который присутствует в количестве 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Предпочтительно диспергирующий агент присутствует в количестве 2-6% по массе, более предпочтительно 3-5% по массе в расчете на общую массу гуанфацин-содержащего слоя.
[0125] Согласно другому предпочтительному варианту осуществления по меньшей мере одно вспомогательное вещество представляет собой усилитель проницаемости, который присутствует в количестве 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Предпочтительно усилитель проницаемости присутствует в количестве 5-9% по массе в расчете на общую массу гуанфацин-содержащего слоя.
[0126] Согласно другому варианту осуществления по меньшей мере одно вспомогательное вещество представляет собой солюбилизатор, который присутствует в количестве 0,5-10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Предпочтительно солюбилизатор присутствует в количестве 0,5-4% по массе, более предпочтительно 0,5-3% по массе в расчете на общую массу гуанфацин-содержащего слоя.
[0127] Согласно одному варианту осуществления TTS согласно настоящему изобретению, и в частности гуанфацин-содержащий слой, более конкретно гуанфацин-содержащий матричный слой, содержит по меньшей мере два вспомогательные вещества, выбранных из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов.
[0128] Согласно одному предпочтительному варианту осуществления трансдермальная терапевтическая система, и в частности гуанфацин-содержащий слой, более конкретно гуанфацин-содержащий матричный слой, содержит по меньшей мере два вспомогательных вещества, причем первое вспомогательное вещество представляет собой диспергирующий агент, который присутствует в количестве 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя, и второе вспомогательное вещество представляет собой усилитель проницаемости, который присутствует в количестве 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Предпочтительно диспергирующий агент присутствует в количестве 1-6% по массе, и усилитель проницаемости присутствует в количестве 3-9% по массе. Более предпочтительно диспергирующий агент присутствует в количестве 3-5% по массе, и усилитель проницаемости присутствует в количестве 5-9% по массе.
[0129] Согласно другому предпочтительному варианту осуществления трансдермальная терапевтическая система, и в частности гуанфацин-содержащий слой, более конкретно гуанфацин-содержащий матричный слой, содержит по меньшей мере два вспомогательных вещества, причем первое вспомогательное вещество представляет собой диспергирующий агент, который присутствует в количестве 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя, и второе вспомогательное вещество представляет собой солюбилизатор, который присутствует в количестве 0,5-10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Предпочтительно диспергирующий агент присутствует в количестве 1-6% по массе, и солюбилизатор присутствует в количестве 0,5-4% по массе. Более предпочтительно диспергирующий агент присутствует в количестве 3-5% по массе, и солюбилизатор присутствует в количестве 0,5-3% по массе.
[0130] Согласно другому предпочтительному варианту осуществления трансдермальная терапевтическая система, и в частности гуанфацин-содержащий слой, более конкретно гуанфацин-содержащий матричный слой, содержит по меньшей мере два вспомогательных вещества, причем первое вспомогательное вещество представляет собой усилитель проницаемости, который присутствует в количестве 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя, и второе вспомогательное вещество представляет собой солюбилизатор, который присутствует в количестве 0,5-10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Предпочтительно усилитель проницаемости присутствует в количестве 3-9% по массе, и солюбилизатор присутствует в количестве 0,5-4% по массе. Предпочтительно усилитель проницаемости присутствует в количестве 5-9% по массе, и солюбилизатор присутствует в количестве 0,5-3% по массе.
[0131] Согласно одному варианту осуществления TTS согласно настоящему изобретению, и в частности гуанфацин-содержащий слой, более конкретно гуанфацин-содержащий матричный слой, содержит по меньшей мере три вспомогательных вещества, выбранных из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов.
[0132] Согласно одному варианту осуществления трансдермальная терапевтическая система, и в частности гуанфацин-содержащий слой, более конкретно гуанфацин-содержащий матричный слой, содержит по меньшей мере три вспомогательных вещества, причем первое вспомогательное вещество представляет собой диспергирующий агент, который присутствует в количестве 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя, второе вспомогательное вещество представляет собой усилитель проницаемости, который присутствует в количестве 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя, и третье вспомогательное вещество представляет собой солюбилизатор, который присутствует в количестве 0,5-10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Предпочтительно диспергирующий агент присутствует в количестве 1-6% по массе, усилитель проницаемости присутствует в количестве 3-9% по массе, и солюбилизатор присутствует в количестве 0,5-4% по массе. Более предпочтительно диспергирующий агент присутствует в количестве 3-5% по массе, усилитель проницаемости присутствует в количестве 5-9% по массе, и солюбилизатор присутствует в количестве 0,5-3% по массе.
[0133] В связи с приведенными выше вариантами осуществления в отношении числа вспомогательных веществ и количеств вспомогательных веществ в TTS согласно настоящему изобретению, и в частности в гуанфацин-содержащем слое, более конкретно гуанфацин-содержащем матричном слое следующие конкретные вспомогательные вещества являются предпочтительными.
[0134] Согласно предпочтительному варианту осуществления диспергирующий агент выбран из группы, состоящей из: сложные эфиры жирных кислот с многоатомными спиртами, жирные спирты, полиэтиленгликоли, характеризующиеся среднечисловой молекулярной массой, составляющей 300-400, алкилэфиры полиэтиленгликоля, и при этом диспергирующий агент представляет собой предпочтительно С8-С20-алкилэфир полиэтиленгликоля, содержащий 2-10 звеньев ЕО, предпочтительно 2-6 звеньев ЕО. Особенно предпочтительные диспергирующий агент представляет собой лауриловый эфир полиоксиэтилена (4) (С12Н25(ОСН2СН2)4OH). Этот диспергирующий агент, например, является доступным от Merck под торговой маркой Brij L4®.
[0135] Согласно предпочтительному варианту осуществления усилитель проницаемости выбран из группы, состоящей из: моноэтиловый эфир диэтиленгликоля (транскутол), олеиновая кислота, левулиновая кислота, триглицериды каприловой/каприновой кислоты, диизопропиладипат, изопропилмиристат, изопропилпальмитат, лауриллактат, триацетин, диметилпропиленмочевина и олеиловый спирт, и предпочтительно представляет собой олеиловый спирт. Олеиловый спирт, например, является доступным от BASF под торговой маркой Kollicream® OA.
[0136] Согласно предпочтительному варианту осуществления солюбилизатор выбран из группы, состоящей из: сополимеры, полученные из сложных эфиров акриловой и метакриловой кислоты, поливинилпирролидон, сополимеры винилпирролидона-винилацетата и привитые сополимеры поливинилкапролактама-поливинилацетата-полиэтиленгликоля. Предпочтительно солюбилизатор выбран из поливинилпирролидона и привитых сополимеров поливинилкапролактама-поливинилацетата-полиэтиленгликоля. Особенно предпочтительные солюбилизаторы представляют собой привитые сополимеры поливинилкапролактама-поливинилацетата-полиэтиленгликоля. Походящие привитые сополимеры поливинилкапролактама-поливинилацетата-полиэтиленгликоля, например, являются доступными от BASF под торговой маркой Soluplus®, и предпочтительно характеризуются следующей структурной формулой, где l, m и n выбирают так, что средняя молекулярная масса, определяемая с помощью гель-проникающей хроматографии, находится в диапазоне от 90000 до 140000 г/моль.
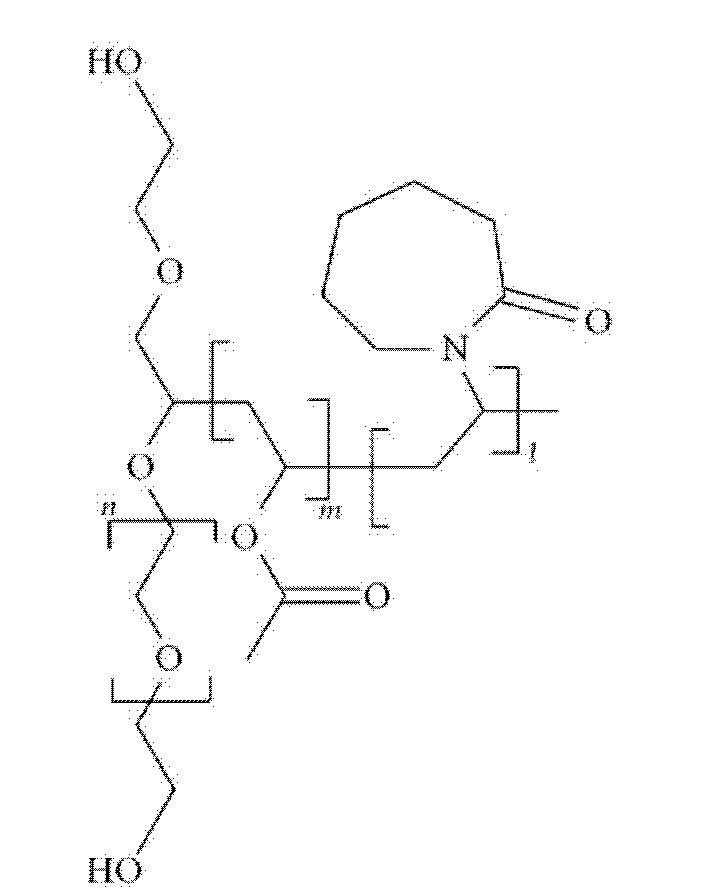
[0137] Согласно определенным предпочтительным вариантам осуществления гуанфацин-содержащий слой содержит по меньшей мере один диспергирующий агент в количестве 2-6% по массе, по меньшей мере один усилитель проницаемости в количестве 2-9% по массе, и необязательно по меньшей мере один солюбилизатор в количестве 0,5-4% по массе, в каждом случае в расчете на общую массу гуанфацин-содержащего слоя. Предпочтительно гуанфацин-содержащий слой содержит по меньшей мере один диспергирующий агент в количестве 3-5% по массе, по меньшей мере один усилитель проницаемости в количестве 3-5% по массе, и необязательно по меньшей мере один солюбилизатор в количестве 0,5-3% по массе, в каждом случае в расчете на общую массу гуанфацин-содержащего слоя. В связи с представленными выше предпочтительными мас.% количествами, представленные выше предпочтительные диспергирующие агенты, усилители проницаемости и солюбилизаторы являются предпочтительными.
[0138] Соответственно, согласно особенно предпочтительному варианту осуществления гуанфацин-содержащий слой содержит С8-С20-алкилэфир полиэтиленгликоля, характеризующийся 2-10 звеньями ЕО, предпочтительно лауриловый эфир полиоксиэтилена (4), в количестве 2-6% по массе, олеиловый спирт в количестве 3-9% по массе, и необязательно привитой сополимер поливинилкапролактама-поливинилацетата-полиэтиленгликоля, предпочтительно как указано выше, в количестве 0,5-4% по массе, в каждом случае в расчете на общую массу гуанфацин-содержащего слоя. Наиболее предпочтительно гуанфацин-содержащий слой содержит С8-С20-алкилэфир полиэтиленгликоля, характеризующийся 2-10 звеньями ЕО, предпочтительно лаур иловый эфир полиоксиэтилена (4), в количестве 3-5% по массе, олеиловый спирт в количестве 5-9% по массе, и необязательно привитой сополимер поливинилкапролактама-поливинилацетата-полиэтиленгликоля, предпочтительно как указано выше, в количестве 0,5-3% по массе, в каждом случае в расчете на общую массу гуанфацин-содержащего слоя.
[0139] Согласно одному варианту осуществления настоящего изобретения масса площади гуанфацин-содержащего слоя находится в диапазоне от 40 до 250 г/м2, предпочтительно от 50 до 180 г/м2, более предпочтительно от 70 до 180 г/м2, например, от 75 до 150 г/м2 или от 100 до 150 г/м2. Согласно определенным предпочтительным вариантам осуществления масса площади находится в диапазоне от 80 до 120 г/м2, предпочтительно от 90 до 100 г/м2.
[0140] С учетом вышеизложенного, настоящее изобретение согласно одному варианту осуществления относится к трансдермальной терапевтической системе для трансдермального введения гуанфацина, содержащей гуанфацин-содержащую слоистую структуру, причем указанная слоистая структура содержит:
A) подложка; и
B) гуанфацин-содержащий слой, предпочтительно гуанфацин-содержащий матричный слой, содержащий:
i) гуанфацин в количестве 3-13% по массе в расчете на общую массу гуанфацин-содержащего слоя;
ii) по меньшей мере один силиконовый полимер в количестве 35-90% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iii) по меньшей мере один диспергирующий агент в количестве 2-6% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iv) по меньшей мере один усилитель проницаемости в количестве 2-10% по массе в расчете на общую массу гуанфацин-содержащего слоя; и
v) необязательно по меньшей мере один солюбилизатор в количестве 0,5-4% по массе в расчете на общую массу гуанфацин-содержащего слоя.
В связи с указанным вариантом осуществления дополнительно предпочтительным является то, что гуанфацин-содержащая слоистая структура не содержит дополнительный контактирующий с кожей слой. Таким образом, гуанфацин-содержащий слой, предпочтительно гуанфацин-содержащий матричный слой, предпочтительно представляет контактирующий с кожей слой и обладает обеспечивающими приклеивание при надавливании адгезионными свойствами благодаря силиконовому полимеру.
[0141] Согласно предпочтительному варианту осуществления гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, который содержит:
i) гуанфацин в количестве 3-13% по массе в расчете на общую массу гуанфацин-содержащего слоя;
ii) по меньшей мере один силиконовый полимер в количестве 35-90% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iii) С8-С20-алкилэфир полиэтиленгликоля, характеризующийся 2-10 звеньями ЕО в количестве 2-6% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iv) олеиловый спирт в количестве 2-10% по массе в расчете на общую массу гуанфацин-содержащего слоя; и
v) необязательно привитой сополимер поливинилкапролактама-поливинилацетата-полиэтиленгликоля в количестве 0,5-4% по массе в расчете на общую массу гуанфацин-содержащего слоя.
Более того, предпочтительным является то, что масса площади гуанфацин-содержащего слоя находится в диапазоне от 80 до 120 г/м2, предпочтительно от 90 до 120 г/м2.
[0142] Согласно особенно предпочтительному варианту осуществления гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, который содержит:
i) гуанфацин в количестве 3-13% по массе в расчете на общую массу гуанфацин-содержащего слоя;
ii) первый силиконовый полимер в количестве 50-70% по массе в расчете на общую массу гуанфацин-содержащего слоя, и второй силиконовый полимер в количестве 15-25% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iii) С8-С20-алкилэфир полиэтиленгликоля, характеризующийся 2-10 звеньями ЕО, предпочтительно лауриловый эфир полиоксиэтилена (4), в количестве 3-5% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iv) олеиловый спирт в количестве 5-9% по массе в расчете на общую массу гуанфацин-содержащего слоя; и
v) необязательно привитой сополимер поливинилкапролактама-поливинилацетата-полиэтиленгликоля в количестве 0,5-3% по массе в расчете на общую массу гуанфацин-содержащего слоя.
Более того, предпочтительным является то, что масса площади гуанфацин-содержащего слоя находится в диапазоне от 80 до 120 г/м2, предпочтительно от 90 до 120 г/м2.
Гуанфацин
[0143] TTS согласно настоящему изобретению содержит гуанфацин-содержащую слоистую структуру, причем указанная гуанфацин-содержащая слоистая структура содержит: А) подложка; и В) гуанфацин-содержащий слой; причем трансдермальная терапевтическая система содержит по меньшей мере один силиконовый полимер. Гуанфацин-содержащий слой, который представляет собой предпочтительно гуанфацин-содержащий матричный слой, был описан подробнее выше.
[0144] Согласно одному варианту осуществления настоящего изобретения количество гуанфацина, содержащегося в гуанфацин-содержащей слоистой структуре, находится в диапазоне от 1 до 100 мг/TTS, предпочтительно 8-72 мг/TTS, более предпочтительно 8-30 мг/TTS, например, 8-10 мг/TTS или 17-19 мг/TTS. Дополнительные подробности в этом отношении были приведены выше.
[0145] Согласно одному варианту осуществления настоящего изобретения гуанфацин-содержащая слоистая структура предпочтительно содержит терапевтически эффективное количество гуанфацина. Более предпочтительно терапевтически эффективное количество гуанфацина присутствует в гуанфацин-содержащем слое гуанфацин-содержащей слоистой структуры. Предпочтительно гуанфацин в гуанфацин-содержащей слоистой структуре присутствует в форме свободного основания.
[0146] Согласно одному варианту осуществления настоящего изобретения по меньшей мере 50 моль %, предпочтительно по меньшей мере 75 моль % от общего количества гуанфацина в TTS присутствуют в форме свободного основания. Согласно конкретному предпочтительному варианту осуществления по меньшей мере 90 моль %, предпочтительно по меньшей мере 95 моль %, более предпочтительно по меньшей мере 99 моль % от общего количества гуанфацина в TTS присутствуют в форме свободного основания. Таким образом, предпочтительным является то, что по меньшей мере 50 моль %, предпочтительно по меньшей мере 75 моль % гуанфацина в гуанфацин-содержащем слое присутствуют в форме свободного основания. Согласно конкретному предпочтительному варианту осуществления по меньшей мере 90 моль %, предпочтительно по меньшей мере 95 моль %, более предпочтительно по меньшей мере 99 моль % гуанфацина в гуанфацин-содержащем слое присутствуют в форме свободного основания. Согласно определенным вариантам осуществления гуанфацин-содержащий слой не содержит солей гуанфацина.
[0147] Согласно определенным вариантам осуществления количество гуанфацина в гуанфацин-содержащем слое находится в диапазоне 1-20% по массе, предпочтительно 3-16% по массе, наиболее предпочтительно 3-14% по массе, например, 11-13% по массе или 7-9% по массе или 3-5% по массе в расчете на общую массу гуанфацин-содержащего слоя.
[0148] Согласно одному варианту осуществления настоящего изобретения гуанфацин-содержащий слой можно получить путем диспергирования гуанфацина в форме свободного основания. Если гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, указанный слой предпочтительно можно получить путем диспергирования гуанфацина в форме свободного основания в полимерном носителе, который особенно предпочтительно содержит силикон-акриловый гибридный полимер, и необязательно по меньшей мере одно вспомогательное вещество, как определено выше, в частности по меньшей мере один диспергирующий агент.
[0149] Согласно одному варианту осуществления гуанфацин-содержащий слой содержит фармацевтически приемлемую соль гуанфацина, такую как гидрохлорид гуанфацина или тартрат гуанфацина, предпочтительно гуанфацин гидрохлорид. Тем не менее, согласно настоящему изобретению предпочтительным является то, что гуанфацин в гуанфацин-содержащем слое присутствует в форме свободного основания.
[0150] Согласно определенным вариантам осуществления гуанфацин характеризуется чистотой, составляющей по меньшей мере 95%, предпочтительно по меньшей мере 98% и более предпочтительно по меньшей мере 99%, что определяют с помощью количественной ВЭЖХ. Количественную ВЭЖХ можно проводить с помощью обращенно-фазовой ВЭЖХ с УФ-обнаружением.
Силикон-акриловые гибридные полимер
[0151] TTS согласно настоящему изобретению может содержать силикон-акриловый гибридный полимер. Силикон-акриловый гибридный полимер содержит полимеризованный гибридный вид, который включает в себя подвид на основе силикона и подвид на основе акрилата, которые были полимеризованы вместе. Силикон-акриловый гибридный полимер, таким образом, содержит силиконовую фазу и акриловую фазу. Предпочтительно силикон-акриловый гибридный полимер представляет собой силикон-акриловые гибридный приклеивающийся при надавливании адгезив.
[0152] Силикон-акриловые гибридные приклеивающиеся при надавливании адгезивы, как правило, поставляют и используют в растворителях, таких как н-гептан и этилацетат. Содержание твердых веществ в приклеивающихся при надавливании адгезивах, как правило, составляет от 30% до 80%. Специалисту в настоящей области техники известно, что содержание твердых веществ можно модифицировать путем добавления походящего количества растворителя.
[0153] Предпочтительно массовое отношение силикона к акрилату в силикон-акриловом гибридном приклеивающемся при надавливании адгезиве составляет от 5:95 до 95:5 или от 20:80 до 80:20, более предпочтительно от 40:60 до 60:40 и наиболее предпочтительно отношение силикона к акрилату составляет приблизительно 50:50. Походящие силикон-акриловые гибридные приклеивающиеся при надавливании адгезивы, характеризующиеся массовым отношением силикона к акрилату, составляющим 50:50, представляют собой, например, коммерчески доступные силикон-акриловые гибридные приклеивающиеся при надавливании адгезивы 7-6102, отношение силикона к акрилату - 50/50, и 7-6302, отношение силикона к акрилату - 50/50, поставляемые в этилацетате Dow Coining.
[0154] Предпочтительные силикон-акриловые гибридные приклеивающиеся при надавливании адгезивы согласно настоящему изобретению характеризуются вязкостью раствора при 25°С и приблизительно 50% содержании твердых веществ в этилацетате, составляющей больше чем приблизительно 400 сП, или от приблизительно 500 сП до приблизительно 3500 сП, в частности, от приблизительно 1000 сП до приблизительно 3000 сП, более предпочтительно от приблизительно 1200 сП до приблизительно 1800, или наиболее предпочтительно приблизительно 1500 сП или альтернативно более предпочтительно от приблизительно 2200 сП до приблизительно 2800 сП, или наиболее предпочтительно приблизительно 2500 сП, предпочтительно, как измерено с использованием вискозиметра Brookfield RVT, оборудованного измерительным наконечником №5 при 50 об/мин.
[0155] Указанные силикон-акриловые гибридные приклеивающиеся при надавливании адгезивы также могут характеризоваться комплексной вязкостью при 0,1 рад/с при 30°С, составляющей меньше чем приблизительно 1,0е9 П (пуаз), или от приблизительно 1,0е5 П до приблизительно 9,0е8 П, или более предпочтительно от приблизительно 9,0е5 П до приблизительно 1,0е7 П, или наиболее предпочтительно приблизительно 4,0е6 П, или альтернативно более предпочтительно от приблизительно 2,0е6 П до приблизительно 9,0е7 П, или наиболее предпочтительно приблизительно 1,0е7 П, предпочтительно, как измерено с использованием реометра Rheometrics ARES, при этом реометр снабжен 8 мм пластинами, и зазор равен нулю.
[0156] Для получения образцов для измерения реологических свойств с использованием реометра Rheometrics ARES, от 2 до 3 г раствора адгезива можно налить на защитное покрытие фторполимера SCOTCH-РАК 1022 и дать отстояться в течение 60 минут в условиях окружающей среды. Чтобы получить практически не содержащие растворителя пленки адгезива, их можно поместить в сушильный шкаф при 110°С+/-10°С на 60 минут. Вынув из сушильного шкафа, дают уравновеситься до комнатной температуры. Пленки можно удалить с защитного покрытия и сложить, чтобы сформировать квадрат. Для устранения пузырьков воздуха пленки можно сжать с использованием пресса Carver. Затем образцы можно загрузить между пластинами и сжать до 1,5+/- 0,1 мм при 30°С. Избыток адгезива обрезают и регистрируют окончательный зазор. Размах частот от 0,01 до 100 рад/с можно выполнить со следующими настройками: температура = 30°С; деформация = 0,5-1% и данные, собранные в 3 точках на декаду.
[0157] Походящие силикон-акриловые гибридные приклеивающиеся при надавливании адгезивы, которые являются коммерчески доступными, включают в себя PSA серий 7-6100 и 7-6300, изготовленные и поставляемые в н-гептане или этилацетате компанией Dow Corning (7-610Х и 7-630X; X=1 - на основе н-гептана / Х=2 - на основе этилацетата). Например, силикон-акриловые гибридный PSA серии 7-6102, характеризующийся отношением силикона к акрилату, составляющим 50/50, характеризуется вязкостью раствора при 25°С и приблизительно 50% содержании твердых веществ в этилацетате, составляющей 2500 сП, и комплексной вязкостью при 0,1 рад/с при 30°С, составляющей 1,0е7 П. Силикон-акриловый гибридный PSA серии 7-6302, характеризующийся отношением силикона к акрилату, составляющим 50/50, характеризуется вязкостью раствора при 25°С и приблизительно 50% содержании твердых веществ в этилацетате, составляющей 1500 сП, и комплексной вязкостью при 0,1 рад/с при 30°С, составляющей 4,0е6 П.
[0158] В зависимости от растворителя, в котором поставляют силикон-акриловый гибридный приклеивающийся при надавливании адгезив, расположение силиконовой фазы и акриловой фазы, обеспечивающих силиконовую или акриловую непрерывную внешнюю фазу и соответствующую дискретную внутреннюю фазу, является различным. Если силикон-акриловый гибридный приклеивающийся при надавливании адгезив предусмотрен в н-гептане, композиция содержит непрерывную, силиконовую внешнюю фазу и дискретную, акриловую внутреннюю фазу. Если силикон-акриловый гибридный приклеивающийся при надавливании адгезив поставляется в этилацетате, композиция содержит непрерывную, акриловую внешнюю фазу и дискретную, силиконовую внутреннюю фазу. После испарения растворителя, в котором поставляется силикон-акриловый гибридный приклеивающийся при надавливании адгезив, расположение фаз полученной приклеивающейся при надавливании адгезивной пленки или слоя соответствует расположению фаз содержащей растворитель адгезивной композиции для покрытия. Например, при отсутствии какого-либо вещества, которое может индуцировать инверсию расположения фаз в силикон-акриловой гибридной приклеивающейся при надавливании адгезивной композиции, приклеивающийся при надавливании адгезивный слой, полученный из силикон-акрилового гибридного приклеивающегося при надавливании адгезива в н-гептане, обеспечивает непрерывную силиконовую внешнюю фазу и дискретную акриловую внутреннюю фазу, приклеивающийся при надавливании адгезивный слой, полученный из силикон-акрилового гибридного приклеивающегося при надавливании адгезива в этилацетате, обеспечивает непрерывную акриловую внешнюю фазу и дискретную силиконовую внутреннюю фазу. Расположение фаз композиций, например, можно определить в испытаниях на отрывное усилие с приклеивающимися при надавливании адгезивными пленками или слоями, полученными из силикон-акриловых гибридных PSA композиций, которые прикреплены к силиконизированному защитному покрытию. Приклеивающаяся при надавливании адгезивная пленка содержит непрерывную, силиконовую внешнюю фазу, если силиконизированное защитное покрытие нельзя удалить или лишь с трудом можно удалить с приклеивающейся при надавливании адгезивной пленки (ламинированной на наружную пленку) из-за блокирования двух силиконовых поверхностей. Блокирование является результатом сцепления двух силиконовых слоев, которые содержат сходную поверхностную энергию. Силиконовый адгезив демонстрирует хорошее растекание на силиконизированном покрытии и, следовательно, может создавать хорошую адгезию с покрытием. Если силиконизированное защитное покрытие можно легко удалить, приклеивающаяся при надавливании адгезивная пленка содержит непрерывную акриловую внешнюю фазу. Акриловый адгезив не обладает хорошим растеканием вследствие различных поверхностных энергий и, таким образом, характеризуется низкой адгезией или практически отсутствием адгезии к силиконизированному покрытию.
[0159] Согласно предпочтительному варианту осуществления настоящего изобретения силикон-акриловый гибридный полимер представляет собой силикон-акриловый гибридный приклеивающийся при надавливании адгезив, получаемый из кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу. Следует понимать, что кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, может включать в себя только акрилатную функциональную группу, только метакрилатную функциональную группу или как акрилатную функциональную группу, так и метакрилатную функциональную группу.
[0160] Согласно определенным вариантам осуществления настоящего изобретения силикон-акриловый гибридный приклеивающийся при надавливании адгезив содержит продукт реакции: (а) кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, (b) этиленненасыщенный мономер и (с) инициатор. Иными словами, силикон-акриловый гибридный приклеивающийся при надавливании адгезив представляет собой продукт химической реакции между этими реагентами ((а), (b) и (с)). В частности, силикон-акриловый гибридный приклеивающийся при надавливании адгезив включает в себя продукт реакции: (а) кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, (b) (мет)акрилатный мономер и (с) инициатор (т.е. в присутствии инициатора). Иными словами, силикон-акриловый гибридный приклеивающийся при надавливании адгезив включает в себя продукт химической реакции между этими реагентами ((а), (b) и (с)).
[0161] Продукт реакции (а) кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, (b) этиленненасыщенный мономер и (с) инициатор, может содержать непрерывную силиконовую внешнюю фазу и дискретную акриловую внутреннюю фазу или продукт реакции (а), (b) и (с) может содержать непрерывную акриловую внешнюю фазу и дискретную силиконовую внутреннюю фазу.
[0162] Кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу (а), как правило, присутствует в силикон-акриловом гибридном приклеивающемся при надавливании адгезиве в количестве 5-95, более типично, 25-75 частей по массе из расчета на 100 частей по массе гибридного приклеивающегося при надавливании адгезива.
[0163] Этиленненасыщенный мономер (b), как правило, присутствует в силикон-акриловом гибридном приклеивающемся при надавливании адгезиве в количестве 5-95, более типично, 25-75 частей по массе из расчета на 100 частей по массе гибридного приклеивающегося при надавливании адгезива.
[0164] Инициатор (с), как правило, присутствует в силикон-акриловом гибридном приклеивающемся при надавливании адгезиве в количестве 0,005-3, более типично 0,01-2 частей по массе из расчета на 100 частей по массе гибридного приклеивающегося при надавливании адгезива.
[0165] Согласно определенным вариантам осуществления настоящего изобретения кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу (а), содержит продукт реакции конденсации: (a1) силиконовая смола, (а2) силиконовый полимер и (а3) кремний-содержащий блокирующий агент, который обеспечивает указанную акрилатную или метакрилатную функциональную группу. Силиконовая смола (a1) может также называться силикатной смолой или силикагелевой смолой. Предпочтительно силиконовый полимер (а2) представляет собой полисилоксан, предпочтительно полидиметилсилоксан. Следует понимать, что (a1) и (а2) образуют приклеивающийся при надавливании адгезив на основе силикона путем поликонденсации, и что акрилатную или метакрилатную функциональную группу вводят путем реакции с (а3).
[0166] Согласно определенным вариантам осуществления настоящего изобретения кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу (а), содержит продукт реакции конденсации:
(a1) силиконовая смола,
(а2) силиконовый полимер, и
(а3) кремний-содержащий блокирующий агент, который обеспечивает указанную акрилатную или метакрилатную функциональную группу, причем указанный кремний-содержащий блокирующий агент характеризуется общей формулой XYR'bSiZ3-b, где
X представляет собой одновалентный радикал согласно общей формуле АЕ-
где Е представляет собой -О- или -NH-, и А представляет собой акриловую группу или метакриловую группу,
Y представляет собой двухвалентный алкиленовый радикал с 1-6 атомами углерода,
R' представляет собой метальный или фенильный радикал,
Z представляет собой одновалентный гидролизуемый органический радикал или галоген, и
b составляет 0 или 1;
причем силиконовая смола и силиконовый полимер реагируют с образованием приклеивающегося при надавливании адгезива, причем кремний-содержащий блокирующий агент вводят перед, во время или после реакции силиконовой смолы и силиконового полимера, и где:
кремний-содержащий блокирующий агент реагирует с приклеивающимся при надавливании адгезивом после того, как силиконовая смола и силиконовый полимер подверглись реакции конденсации с образованием приклеивающегося при надавливании адгезива; или
кремний-содержащий блокирующий агент реагирует in situ с силиконовой смолой и силиконовым полимером.
[0167] Согласно определенным вариантам осуществления настоящего изобретения кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, содержит продукт реакции конденсации приклеивающегося при надавливании адгезива и кремний-содержащего блокирующего агента, который обеспечивает указанную акрилатную или метакрилатную функциональную группу. Иными словами, кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, представляет собой по существу приклеивающийся при надавливании адгезив, который был блокирован на концах с помощью кремний-содержащего блокирующего агента, который обеспечивает указанную акрилатную или метакрилатную функциональную группу, где приклеивающийся при надавливании адгезив содержит продукт реакции конденсации силиконовой смолы и силиконового полимера. Предпочтительно силиконовая смола реагирует в количестве 30-80 частей по массе, с образованием приклеивающегося при надавливании адгезива, и силиконовый полимер реагирует в количестве 20-70 частей по массе, с образованием приклеивающегося при надавливании адгезива. В этих обоих случаях части по массе представлены из расчета на 100 частей по массе приклеивающегося при надавливании адгезива. Хотя это не обязательно, приклеивающийся при надавливании адгезив может содержать каталитическое количество катализатора конденсации. Широкий спектр силиконовых смол и силиконовых полимеров является походящим для получения приклеивающегося при надавливании адгезива.
[0168] Согласно определенным вариантам осуществления настоящего изобретения силикон-акриловый гибридный приклеивающийся при надавливании адгезив представляет собой продукт реакции:
(а) кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, которая содержит продукт реакции конденсации:
(a1) силиконовая смола,
(а2) силиконовый полимер, и
(а3) кремний-содержащий блокирующий агент, который обеспечивает указанную акрилатную или метакрилатную функциональную группу, причем указанный кремний-содержащий блокирующий агент характеризуется общей формулой XYR'bSiZ3-b, где
X представляет собой одновалентный радикал согласно общей формуле АЕ-
где Е представляет собой -О- или -NH-, и А представляет собой акриловую группу или метакриловую группу,
Y представляет собой двухвалентный алкиленовый радикал, характеризующийся 1-6 атомами углерода,
R' представляет собой метальный или фенильный радикал,
Z представляет собой одновалентный гидролизуемый органический радикал или галоген, и
b составляет 0 или 1;
причем силиконовая смола и силиконовый полимер реагируют с образованием приклеивающегося при надавливании адгезива, причем кремний-содержащий блокирующий агент вводят перед, во время или после реакции силиконовой смолы и силиконового полимера, и где:
кремний-содержащий блокирующий агент реагирует с приклеивающимся при надавливании адгезивом после того, как силиконовая смола и силиконовый полимер подверглись реакции конденсации с образованием приклеивающегося при надавливании адгезива; или
кремний-содержащий блокирующий агент реагирует in situ с силиконовой смолой и силиконовым полимером;
(b) этиленненасыщенный мономер; и
(c) инициатор.
[0169] Силикон-акриловую гибридную композицию, используемую в настоящем изобретении, можно описать путем ее получения с помощью способа, предусматривающего следующие стадии:
(i) получение кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу, которая содержит продукт реакции конденсации:
силиконовая смола,
силиконовый полимер, и
кремний-содержащий блокирующий агент, который обеспечивает указанную акрилатную или метакрилатную функциональную группу, причем указанный кремний-содержащий блокирующий агент характеризуется общей формулой XYR'bSiZ3-b, где
X представляет собой одновалентный радикал согласно общей формуле АЕ-
где Е представляет собой -О- или -NH-, и А представляет собой акриловую группу или метакриловую группу,
Y представляет собой двухвалентный алкиленовый радикал, характеризующийся 1 -6 атомами углерода,
R' представляет собой метальный или фенильный радикал,
Z представляет собой одновалентный гидролизуемый органический радикал или галоген, и
b составляет 0 или 1;
причем силиконовая смола и силиконовый полимер реагируют с образованием приклеивающегося при надавливании адгезива, причем кремний-содержащий блокирующий агент вводят перед, во время или после реакции силиконовой смолы и силиконового полимера, и где:
кремний-содержащий блокирующий агент реагирует с приклеивающимся при надавливании адгезивом после того, как силиконовая смола и силиконовый полимер подверглись реакции конденсации с образованием приклеивающегося при надавливании адгезива; или
кремний-содержащий блокирующий агент реагирует in situ с силиконовой смолой и силиконовым полимером;
(ii) полимеризация этиленненасыщенного мономера и кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу, стадии (i) в присутствии инициатора с образованием силикон-акриловой гибридной композиции, необязательно при температуре от 50°С до 100°С или от 65°С до 90°С.
[0170] Во время полимеризации этиленненасыщенного мономера и кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу, отношение силикона к акрилу можно контролировать и оптимизировать при необходимости. Отношение силикона к акрилу можно контролировать с помощью широкого разнообразия механизмов при осуществлении и во время способа. Иллюстративный пример одного такого механизма представляет собой контролируемое по скорости добавление этиленненасыщенного мономера или мономеров к кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу. В определенных применениях может быть желательно, чтобы подвид на основе силикона, или общее содержания силикона, превышал подвид на основе акрилата, или общее содержание акрила. В других применениях может быть желательно, чтобы имело место противоположное. Независимо от конечного применения, в общем предпочтительным, как уже описано выше, является то, что кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, предпочтительно присутствует в силикон-акриловой гибридной композиции в количестве от приблизительно 5 до приблизительно 95 частей по массе, более предпочтительно от приблизительно 25 до приблизительно 75 частей по массе и еще более предпочтительно от приблизительно 40 до приблизительно 60 частей по массе из расчета на 100 частей по массе силикон-акриловой гибридной композиции.
[0171] Согласно определенным вариантам осуществления настоящего изобретения силикон-акриловую гибридную композицию, используемую в настоящем изобретении, можно описать путем ее получения с помощью способа, предусматривающего следующие стадии:
(i) получение кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу, которая содержит продукт реакции конденсации:
силиконовая смола,
силиконовый полимер, и
кремний-содержащий блокирующий агент, который обеспечивает указанную акрилатную или метакрилатную функциональную группу, причем указанный кремний-содержащий блокирующий агент характеризуется общей формулой XYR'bSiZ3-b, где
X представляет собой одновалентный радикал согласно общей формуле АЕ-
где Е представляет собой -О- или -NH-, и А представляет собой акриловую группу или метакриловую группу,
Y представляет собой двухвалентный алкиленовый радикал, характеризующийся 1-6 атомами углерода,
R' представляет собой метальный или фенильный радикал,
Z представляет собой одновалентный гидролизуемый органический радикал или галоген, и
b составляет 0 или 1;
причем силиконовая смола и силиконовый полимер реагируют с образованием приклеивающегося при надавливании адгезива, причем кремний-содержащий блокирующий агент вводят перед, во время или после реакции силиконовой смолы и силиконового полимера, и где:
кремний-содержащий блокирующий агент реагирует с приклеивающимся при надавливании адгезивом после того, как силиконовая смола и силиконовый полимер подверглись реакции конденсации с образованием приклеивающегося при надавливании адгезива; или
кремний-содержащий блокирующий агент реагирует in situ с силиконовой смолой и силиконовым полимером;
(ii) полимеризация этиленненасыщенного мономера и кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу, стадии (i) в первом растворителе в присутствии инициатора при температуре от 50°С до 100°С с образованием силикон-акриловой гибридной композиции;
(iii) удаление первого растворителя; и
(iv) добавление второго растворителя с образованием силикон-акриловой гибридной композиции, причем расположение фаз силикон-акриловой гибридной композиции селективно контролируют с помощью выбора второго растворителя.
[0172] Силикон-акриловую гибридную PSA композицию, используемую в настоящем изобретении, можно описать путем ее получения с помощью способа, предусматривающего следующие стадии:
(i) получение кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу, которая содержит продукт реакции конденсации:
силиконовая смола,
силиконовый полимер, и
кремний-содержащий блокирующий агент, который обеспечивает указанную акрилатную или метакрилатную функциональную группу, причем указанный кремний-содержащий блокирующий агент характеризуется общей формулой XYR'bSiZ3-b, где
X представляет собой одновалентный радикал согласно общей формуле АЕ-
где Е представляет собой -О- или -NH-, и А представляет собой акриловую группу или метакриловую группу,
Y представляет собой двухвалентный алкиленовый радикал, характеризующийся 1-6 атомами углерода,
R' представляет собой метальный или фенильный радикал,
Z представляет собой одновалентный гидролизуемый органический радикал или галоген, и
b составляет 0 или 1;
причем силиконовая смола и силиконовый полимер реагируют с образованием приклеивающегося при надавливании адгезива, причем кремний-содержащий блокирующий агент вводят перед, во время или после реакции силиконовой смолы и силиконового полимера, и где:
кремний-содержащий блокирующий агент реагирует с приклеивающимся при надавливании адгезивом после того, как силиконовая смола и силиконовый полимер подверглись реакции конденсации с образованием приклеивающегося при надавливании адгезива; или
кремний-содержащий блокирующий агент реагирует in situ с силиконовой смолой и силиконовым полимером;
(ii) полимеризация этиленненасыщенного мономера и кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу, стадии (i) в первом растворителе в присутствии инициатора при температуре от 50°С до 100°С с образованием силикон-акриловой гибридной композиции;
(iii) добавление обрабатывающего растворителя, причем обрабатывающий растворитель характеризуется более высокой точкой кипения, чем первый растворитель, и
(iv) применение нагревания при температуре от 70°С до 150°С, так что основная часть первого растворителя селективно удаляется;
(v) удаление обрабатывающего растворителя; и
(vi) добавление второго растворителя с образованием силикон-акриловой гибридной композиции, причем расположение фаз силикон-акриловой гибридной композиции селективно контролируют с помощью выбора второго растворителя.
[0173] Силиконовая смола согласно предыдущим абзацам может содержать сополимер, содержащий триорганосилокси-звенья согласно формуле RX3SiO1/2 и тетрафункциональные силокси-звенья согласно формуле SiO4/2 в отношении, составляющем 0,1-0,9, предпочтительно приблизительно 0,6-0,9 триорганосилокси-звеньев на каждое тетрафункциональное силокси-звено. Предпочтительно каждый RX независимо обозначает одновалентный углеводородный радикал, содержащий 1-6 атомов углерода, винильную, гидроксильную или фенильную группы.
[0174] Силиконовый полимер согласно предыдущим абзацам может содержать по меньшей мере один полидиорганосилоксан и является предпочтительно блокированным на концах с помощью функциональной группы, выбранной из группы, состоящей из: гидроксильные группы, алкоксигруппы, гидридные группы, винильные группы или их смеси. Диорганозаместитель можно выбрать из группы, состоящей из: диметил, метилвинил, метилфенил, дифенил, метилэтил, (3,3,3-трифторпропил)метил и их смеси. Предпочтительно диорганозаместители содержат только метальные группы. Молекулярная масса полидиорганосилоксана, как правило, будет находиться в диапазоне от приблизительно 50000 до приблизительно 1000000, предпочтительно от приблизительно 80000 до приблизительно 300000. Предпочтительно полидиорганосилоксан содержит звенья ARXSiO, оканчивающиеся концевыми блокирующими звеньями TRXASiO1/2, причем полидиорганосилоксан характеризуется вязкостью, составляющей приблизительно 100 сП - приблизительно 30000000 сП при 25°С, каждый радикал А независимо выбран из RX или галогенуглеводородных радикалов, характеризующихся 1-6 атомами углерода, каждый радикал Т независимо выбран из группы, состоящей из RX, ОН, Н или ORY, и каждый RY представляет собой независимо алкильный радикал, характеризующийся 1-4 атомами углерода.
[0175] В качестве примера с использованием форм предпочтительной силиконовой смолы и предпочтительного силиконового полимера, один тип приклеивающегося при надавливании адгезива получают путем: смешивания: (i) 30-80 включительно частей по массе по меньшей мере одного сополимера смолы, содержащего связанные с силиконом гидроксильные радикалы и состоящего по существу из звеньев RX3SiO1/2 и звеньев SiO4/2 в мольном отношении, составляющем 0,6-0,9 звеньев RX3SiO1/2 на каждое присутствующее звено SiO4/2, (ii) от приблизительно 20 до приблизительно 70 частей по массе по меньшей мере одного полидиорганосилоксана, содержащего звенья ARXSiO, оканчивающиеся концевыми блокирующими звеньями TRXASiO1/2, причем полидиорганосилоксан характеризуется вязкостью, составляющей от приблизительно 100 сП до приблизительно 30000000 сП при 25°С, и каждый RX представляет собой одновалентный органический радикал, выбранный из группы, состоящей из углеводородных радикалов с 1-6 включительно атомами углерода, каждый радикал А независимо выбран из RX или галогенуглеводородных радикалов, характеризующихся 1-6 включительно атомами углерода, каждый радикал Т независимо выбран из группы, состоящей из RX, ОН, Н или ORY, и каждый RY независимо представляет собой алкильный радикал с 1-4 включительно атомами углерода; достаточное количество: (iii) по меньшей мере один из кремний-содержащих блокирующих агентов, также называемых в настоящем документе как концевыми блокирующими агентами, которые описаны ниже и способны обеспечивать содержание или концентрацию силанола в диапазоне, составляющем 5000-15000, более типично 8000-13000 м.д., при необходимости дополнительное каталитическое количество (iv) мягкого катализатора конденсации силанола в том случае, если ни один из них не предусмотрен в (ii), и при необходимости эффективное количество (у) органического растворителя, который является инертным в отношении (i), (ii), (iii) и (iv), для снижения вязкости смеси (i), (ii), (iii) и (iv), и конденсация смеси (i), (ii), (iii) и (iv) по меньшей мере до тех пор, пока значительное количество кремний-содержащего блокирующего агента или агентов не вступит в реакцию с гидроксильными радикалами, связанными с силиконом, и радикалами Т в (i) и (ii). Дополнительные органосиликоновые концевые блокирующие агенты можно использовать в сочетании с кремний-содержащим блокирующим агентом или агентами (iii) согласно настоящему изобретению.
[0176] Кремний-содержащий блокирующий агент согласно предыдущим абзацам можно выбрать из следующей группы: силаны с акрилатной функциональной группой, силазаны с акрилатной функциональной группой, дисилазаны с акрилатной функциональной группой, дисилоксаны с акрилатной функциональной группой, силаны с метакрилатной функциональной группой, силазаны с метакрилатной функциональной группой, дисилазаны с метакрилатной функциональной группой, дисилоксаны с метакрилатной функциональной группой и их комбинации, и их можно описать как характеризующиеся общей формулой XYR'bSiZ3-b, где X представляет собой одновалентный радикал согласно общей формуле АЕ-, где Е представляет собой -О- или -NH-, и А представляет собой акриловую группу или метакриловую группу, Y представляет собой двухвалентный алкиленовый радикал, характеризующийся 1-6 атомами углерода, R' представляет собой метальный или фенильный радикал, Z представляет собой одновалентный гидролизуемый органический радикал или галоген, и b составляет 0, 1 или 2. Предпочтительно одновалентный гидролизуемый органический радикал характеризуется общей формулой R''0-, где R'' представляет собой алкиленовый радикал. Наиболее предпочтительно этот конкретный концевой блокирующий агент выбран из следующей группы: 3-метакрилоксипропилдиметилхлорсилан, 3-метакрилоксипропилдихлорсилан, 3-метакрилоксипропилтрихлорсилан, 3-метакрилоксипропилд иметилметоксисилан, 3-метакрилоксипропилметилд иметоксисилан, 3-метакрилоксипропилтриметоксисилан, 3-метакрилоксипропилдиметилэтоксисилан, 3-метакрилоксипропилметилдиэтоксисилан, 3-метакрилоксипропилтриэтоксисилан, (метакрилоксиметил)диметилметоксисилан, (метакрилоксиметил)метилдиметоксисилан, (метакрилоксиметил)триметоксисилан, (метакрилоксиметил)диметилэтоксисилан, (метакрилоксиметил)метилдиэтоксисилан, метакрилоксиметилтриэтоксисилан, метакрилоксипропилтриизопропоксисилан, 3-метакрилоксипропилдиметилсилазан, 3-акрилокси-пропилдиметилхлорсилан, 3-акрилоксипропилдихлорсилан, 3-акрилоксипропил-трихлорсилан, 3-акрилоксипропилд иметилметоксисилан, 3-акрилокси-пропилметилдиметоксисилан, 3-акрилоксипропилтриметоксисилан, 3-акрилоксипропил-диметилсилазан и их комбинации.
[0177] Этиленненасыщенный мономер согласно предыдущим абзацам может представлять собой любой мономер, характеризующийся по меньшей мере одной углерод-углеродной двойной связью. Предпочтительно этиленненасыщенный мономер согласно предыдущим абзацам может представлять собой соединение, выбранное из группы, состоящей из следующего: алифатические акрилаты, алифатические метакрилаты, циклоалифатические акрилаты, циклоалифатические метакрилаты и их комбинации. Следует понимать, что каждое из следующих соединений: алифатические акрилаты, алифатические метакрилаты, циклоалифатические акрилаты и циклоалифатические метакрилаты, включают в себя алкильный радикал. Алкильные радикалы указанных соединений могут включать в себя вплоть до 20 атомов углерода. Алифатические акрилаты, которые можно выбрать в качестве одного из этиленненасыщенных мономеров, выбирают из группы, состоящей из следующего: метилакрилат, этилакрилат, пропилакрилат, н-бутилакрилат, изобутилакрилат, трет-бутилакрилат, гексилакрилат, 2-этилгексилакрилат, изооктилакрилат, изононилакрилат, изопентилакрилат, тридецилакрилат, стеарилакрилат, лаурилакрилат и их смеси. Алифатические метакрилаты, которые можно выбрать в качестве одного из этиленненасыщенных мономеров, выбирают из группы, состоящей из следующего: метилметакрилат, этилметакрилат, пропилметакрилат, н-бутилметакрилат, изобутилметакрилат, трет-бутилметакрилат, гексилметакрилат, 2-этилгексилметакрилат, изооктилметакрилат, изононилметакрилат, изопентилметакрилат, тридецилметакрилат, стеарилметакрилат, лаурилметакрилат и их смеси. Циклоалифатический акрилат, который можно выбрать в качестве одного из этиленненасыщенных мономеров, представляет собой циклогексилакрилат, и циклоалифатический метакрилат, который можно выбрать в качестве одного из этиленненасыщенных мономеров, представляет собой циклогексилметакрилат.
[0178] Следует понимать, что этиленненасыщенный мономер, используемый для получения силикон-акрилового гибридного приклеивающегося при надавливании адгезива, может представляет собой больше одного этиленненасыщенного мономера. Иными словами, комбинацию этиленненасыщенных мономеров можно подвергнуть полимеризации, более конкретно подвергнуть сополимеризации вместе с кремний-содержащей приклеивающейся при надавливании адгезивной композицией, содержащей акрилатную или метакрилатную функциональную группу и инициатор. Согласно определенному варианту осуществления настоящего изобретения силикон-акриловый гибридный приклеивающийся при надавливании адгезив получают путем использования по меньшей мере двух различных этиленненасыщенных мономеров, предпочтительно выбранных из группы 2-этилгексилакрилата и метилакрилата, более предпочтительно в отношении, составляющем 50% 2-этилгексилакрилата и 50% метилакрилата, или в отношении, составляющем 60% 2-этилгексилакрилата и 40% метилакрилата в качестве акрилового мономера.
[0179] Инициатор согласно предыдущим абзацам может представлять собой любое вещество, которое является походящим для инициации полимеризации кремний-содержащей приклеивающейся при надавливании адгезивной композиции, содержащей акрилатную или метакрилатную функциональную группу, и этиленненасыщенного мономера с образованием силикон-акрилового гибрида. Например, можно использовать свободнорадикалные инициаторы, выбранные из группы пероксидов, азосоединений, окислительно-восстановительных инициаторов и фотоинициаторов.
[0180] Дополнительные походящие силиконовые смолы, силиконовые полимеры, кремний-содержащие блокирующие агенты, этиленненасыщенные мономеры и инициаторы, которые можно использовать в соответствии с предыдущими абзацами, подробно описаны в WO 2007/145996, ЕР 2599847 А1 и WO 2016/130408.
[0181] Согласно определенному варианту осуществления настоящего изобретения силикон-акриловый гибридный полимер содержит продукт реакции силиконового полимера, силиконовой смолы и акрилового полимера, где акриловый полимер ковалентно поперечно сшит сам с собой и ковалентно соединен с силиконовым полимером и/или силиконовой смолой.
[0182] Согласно определенному другому варианту осуществления настоящего изобретения силикон-акриловый гибридный полимер содержит продукт реакции силиконового полимера, силиконовой смолы и акрилового полимера, где силиконовая смола содержит триорганосилокси-звенья R3SiO1/2, где R представляет собой органическую группу, и тетрафункциональные силокси-звенья SiO4/2 в мольном отношении, составляющем от 0,1 до 0,9 звеньев R3SiO1/2 на каждое звено SiO4/2.
[0183] Акриловый полимер может содержать по меньшей мере мономер с алкоксисилильной функциональной группой, полисилоксан-содержащий мономер, мономер с галогенсилильной функциональной группой или мономер с алкоксигалогенсилильной функциональной группой. Предпочтительно акриловый полимер получают из мономеров с алкоксисилильной функциональной группой, выбранных из группы, состоящей из следующего: триалкоксилсилильные (мет)акрилаты, диалкоксиалкилсилильные (мет)акрилаты и их смеси, или он содержит блокированные концевые алкоксисилильные функциональные группы. Алкоксисилильные функциональные группы можно предпочтительно выбрать из группы, состоящей из триметоксилсилильных групп, диметоксиметилсилильных групп, триэтоксилсилильных, диэтоксиметилсилильных групп и их смесей.
[0184] Акриловый полимер также можно получить из смеси, содержащей полисилоксан-содержащие мономеры, предпочтительно из смеси, содержащей полидиметилсилоксанмоно(мет)акрилат.
[0185] Мономеры с силильной функциональной группой, как правило, будут использовать в количествах, составляющих от 0,2 до 20% по массе акрилового полимера, более предпочтительно количество мономеров с силильной функциональной группой будет находиться в диапазоне от приблизительно 1,5 до приблизительно 5% по массе акрилового полимера.
[0186] Количество полисилоксан-содержащего мономера, как правило, будут использовать в количествах, составляющих от 1,5 до 50% по массе акрилового полимера, более предпочтительно количество полисилоксан-содержащих мономеров будет находиться в диапазоне 5-15% по массе акрилового полимера.
[0187] Альтернативно, акриловый полимер содержит блок-сополимер или привитой сополимер акрила и полисилоксана. Пример полисилоксанового блок-сополимера представляет собой полидиметилсилокеан-акриловый блок-сополимер. Предпочтительное количество силоксанового блока составляет 10-50% по массе всего блок-полимера.
[0188] Акриловый полимер содержит мономеры алкил(мет)акрштата. Предпочтительные алкил(мет)акрилаты, которые можно использовать, содержать вплоть до приблизительно 18 атомов углерода в алкильной группе, предпочтительно 1 - приблизительно 12 атомов углерода в алкильной группе. Предпочтительные алкилакрилаты с низкой температурой стеклования (Tg) с Tg гомополимера, составляющей меньше чем приблизительно 0°С, содержат приблизительно 4 - приблизительно 10 атомов углерода в алкильной группе и включают в себя бутилакрилат, амилакрилат, гексилакрилат, 2-этилгексилакрилат, октилакрилат, изооктилакрилат, децилакрилат, их изомеры и их комбинации. Особенно предпочтительными являются бутилакрилат, 2-этилгексилакрилат и изооктилакрилат. Компоненты акрилового полимера могут дополнительно содержать (мет)акрилатные мономеры, характеризующиеся высокой Tg, такие как метилакрилат, этилакрилат, метилметакрилат и изобутилметакрилат.
[0189] Компонент акрилового полимера может дополнительно содержать полиизобутиленовую группу для улучшения вытекание адгезивного вещества из-под пластыря свойства полученного адгезива.
[0190] Компоненты акрилового полимера могут содержать азот-содержащие полярные мономеры. Примеры включают в себя N-винилпирролидон, N-винилкапролактам, N-третичный октилакриламид, диметилакриламид, диацетонакриламид, N-третичный бутилакриламид, N-изопропилакриламид, цианоэтилакрилат, N-винилацетамид и N-винилформамид.
[0191] Компонент акрилового полимера может содержать один или несколько гидроксил-содержащих мономеров, таких как 2-гидроксиэтилакрилат, 2-гидроксиэтилметакрилат, гидроксипропилакрилат и/или гидроксипропилметакрилат.
[0192] Компоненты акрилового полимера при необходимости могут содержать содержащие карбоновые кислоты мономеры. Применимые карбоновые кислоты предпочтительно содержат от приблизительно 3 до приблизительно 6 атомов углерода и включают в себя, среди прочего, акриловую кислоту, метакриловую кислоту, итаконовую кислоту, β-карбоксиэтилакрилат и тому подобное. Акриловая кислота является особенно предпочтительной.
[0193] Другие применимые, хорошо известные сомономеры включают в себя винилацетат, стирол, циклогексилакрилат, алкилди(мет)акрилаты, глицидилметакрилат и аллилглицидиловый эфир, а также макромеры, такие как, например, поли(стирил)метакрилат.
[0194] Один компонент акрилового полимера, который можно использовать при осуществлении на практике настоящего изобретения, представляет собой акриловый полимер, который содержит от приблизительно 90 до приблизительно 99,5% по массе бутилакрилата и от приблизительно 0,5 до приблизительно 10% по массе диметоксиметилсилилметакрилата.
[0195] Согласно определенному варианту осуществления настоящего изобретения силикон-акриловый гибридный полимер можно получить следующим образом: а) реакция силиконового полимера с силиконовой смолой с образованием полученного продукта, b) реакция полученного продукта из а) с акриловым полимером, содержащим реакционноспособную функциональную группу, причем компоненты реагируют в органическом растворителе.
[0196] Согласно определенному варианту осуществления настоящего изобретения силикон-акриловый гибридный полимер можно получить следующим образом: а) реакция силиконовой смолы с акриловым полимером, содержащим реакционноспособную функциональную группу, с образованием полученного продукта, b) реакция полученного продукта из а) с силиконовым полимером, причем компоненты реагируют в органическом растворителе.
[0197] Согласно определенному варианту осуществления настоящего изобретения силикон-акриловый гибридный полимер можно получить следующим образом: а) реакция силиконового полимера с акриловым полимером, содержащим реакционноспособную функциональную группу с образованием полученного продукта, b) реакция полученного продукта из а) с силиконовой смолой, причем компоненты реагируют в органическом растворителе.
[0198] Дополнительные походящие акриловые полимеры, силиконовые смолы и силиконовые полимеры, которые можно использовать для химической реакции вместе с силиконовым полимером, силиконовой смолой и акриловым полимером для получения силикон-акрилового гибридного полимера согласно предыдущим абзацам подробно описаны в международной патентной публикации WO 2010/124187.
[0199] Согласно определенным вариантам осуществления настоящего изобретения силикон-акриловый гибридный полимер, используемый в TTS, смешивают с одним или несколькими негибридными полимерами, предпочтительно силикон-акриловый гибридный полимер смешивают с одним или несколькими негибридными приклеивающимися при надавливании адгезивами (например, приклеивающимися при надавливании адгезивами на основе полисилоксана или акрилатов).
Негибридные полимеры
[0200] TTS согласно настоящему изобретению содержит по меньшей мере один силиконовый полимер и необязательно по меньшей мере один дополнительный полимер, который может представлять собой негибридный полимер, такой как акрилатный полимер.
[0201] Негибридные полимеры (например, негибридные приклеивающиеся при надавливании адгезивы) представляют собой полимеры (например, приклеивающиеся при надавливании адгезивы на основе полимера), которые не включают в себя гибридный вид. Предпочтительными являются негибридные полимеры (например, негибридные приклеивающиеся при надавливании адгезивы) на основе полисилоксанов, акрилатов, полиизобутиленов или блок-сополимеров стирола-изопрена-стирола.
[0202] Негибридные полимеры (например, негибридные приклеивающиеся при надавливании адгезивы) могут содержаться в содержащей активное средство слоистой структуре и/или в адгезивном верхнем слое.
[0203] Негибридные приклеивающиеся при надавливании адгезивы, как правило, поставляются и используются в растворителях, таких как н-гептан и этилацетат. Содержание твердых веществ приклеивающихся при надавливании адгезивов составляет, как правило, от 30% до 80%.
[0204] Походящие негибридные полимеры согласно настоящему изобретению являются коммерчески доступными, например, под торговыми марками BIO-PSA (приклеивающиеся при надавливании адгезивы на основе полисилоксанов), Oppanol™ (полиизобутилены), JSR-SIS (сополимер стирола-изопрена-стирола) или Duro-Tak™ (акриловые полимеры).
[0205] Полимеры на основе полисилоксанов могут также называться полимерами на основе силикона или силиконовыми полимерами, или силиконами. Приклеивающиеся при надавливании адгезивы на основе полисилоксанов могут также называться приклеивающимися при надавливании адгезивами на основе силикона, или силиконовыми приклеивающимися при надавливании адгезивами. Указанные приклеивающиеся при надавливании адгезивы на основе полисилоксанов обеспечивают подходящую липкость и быстрое приклеивание к различным типам кожи, включая в себя влажную кожу, подходящие адгезионные и когезионные свойства, длительную адгезию к коже, высокую степень гибкости, проницаемость для влаги и совместимость со многими активными средствами и пленками-подложками. Можно обеспечить им достаточную аминостойкость и, следовательно, повышенную стабильность в присутствии аминов. Такие приклеивающиеся при надавливании адгезивы основаны на концепции смола-в-полимере, где, путем реакции конденсации полидиметилсилоксана с блокированной концевой силанольной группой и силикатной смолы (также носящей название силикагелевая смола), получают приклеивающийся при надавливании адгезив на основе полисилоксана, причем для аминостойкости остаточную силанольную функциональную группу дополнительно блокируют с помощью триметилсилоксигрупп. Содержание полидиметилсилоксана с блокированной концевой силанольной группой придает вязкому компоненту вязкоупругие свойства, и влияет на свойства смачиваемости и растекаемости адгезива. Смола действует в качестве обеспечивающего липкость агента и армирующего агента и участвует в эластичном компоненте. Правильный баланс между полидиметилсилоксаном с блокированной концевой силанольной группой и смолой обеспечивает правильные адгезионные свойства.
[0206] С учетом вышеизложенного, полимеры на основе силикона, и в частности приклеивающиеся при надавливании адгезивы на основе силикона, как правило, можно получить с помощью поликонденсации полидиметилсилоксана с блокированной концевой силанольной группой и силикатной смолы. Аминосовместимые полимеры на основе силикона, и в частности аминосовместимые приклеивающиеся при надавливании адгезивы на основе силикона, можно получить путем реакции полимера на основе силикона, в частности приклеивающегося при надавливании адгезива на основе силикона с триметилсилилом (например, гексаметилдисилазаном) для снижения содержания силанола в полимере. В результате остаточную силанольную функциональную группу по меньшей мере частично, предпочтительно в основном или полностью блокируют с помощью триметилсилоксигрупп.
[0207] Как указано выше, липкость по меньшей мере одного полимера на основе силикона можно модифицировать с помощью отношения смолы к полимеру, т.е. отношения полидиметилсилоксана с блокированной концевой силанольной группой к силикатной смоле, которое находится предпочтительно в диапазоне, составляющем 70:30-50:50, предпочтительно 65:35-55:45. Липкость будет увеличиваться с увеличением количеств полидиметилсилоксана относительно смолы. Полимеры на основе силикона с высокой липкостью предпочтительно характеризуются отношением смолы к полимеру, составляющим 55:45, полимеры на основе силикона со средней липкостью предпочтительно характеризуются отношением смолы к полимеру, составляющим 60:40, и полимеры на основе силикона с низкой липкостью предпочтительно характеризуются отношением смолы к полимеру, составляющим 65:35. Полимеры на основе силикона с высокой липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×106 П, полимеры на основе силикона со средней липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×107 П, и полимеры на основе силикона с низкой липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×108 П. Аминосовместимые полимеры на основе силикона с высокой липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×106 П, аминосовместимые полимеры на основе силикона со средней липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×108 П, и аминосовместимые полимеры на основе силикона с низкой липкостью предпочтительно характеризуются комплексной вязкостью при 0,01 рад/с и 30°С, составляющей 5×109 П.
[0208] Примеры композиций PSA на основе силикона, которые являются коммерчески доступными, включают в себя серии стандартного BIO-PSA (серии 7-4400, 7-4500 и 7-4600), серии аминосовместимого (блокированного на концах) BIO-PSA (серии 7-4100, 7-4200 и 7-4300), изготавливаемые и, как правило, поставляемые в н-гептане или этилацетате компанией Dow Corning, и серии адгезивов для нежной кожи (7-9800), изготавливаемые и, как правило, поставляемые без растворителя компанией Dow Corning. Например, BIO-PSA 7-4201 характеризуется вязкостью раствора при 25°С и приблизительно 73% содержании твердых веществ в гептане, составляющей 450 мПа⋅с, и комплексной вязкостью при 0,01 рад/с при 30°С, составляющей 1×108 П. BIO-PSA 7-4301 характеризуется вязкостью раствора при 25°С и приблизительно 73% содержании твердых веществ в гептане, составляющей 500 мПа⋅с, и комплексной вязкостью при 0,01 рад/с при 30°С, составляющей 5×106 П.
[0209] Силиконовые полимеры поставляют и используют в растворителях, таких как н-гептан, этилацетат или другие летучие силиконовые жидкости. Для настоящего изобретения н-гептан является предпочтительным. Содержание твердых веществ силиконовых полимеров в растворителях составляет, как правило, от 60 до 80%, предпочтительно от 70 до 80% или от 60 до 70%. Специалисту в настоящей области техники понятно, что содержание твердых веществ можно модифицировать путем добавления походящего количества растворителя.
[0210] Предпочтительные приклеивающиеся при надавливании адгезивы на основе полисилоксанов согласно настоящему изобретению характеризуются вязкостью раствора при 25°С и 60% содержании твердых веществ в н-гептане, составляющей больше чем приблизительно 150 мПа⋅с, или приблизительно 200 мПа⋅с - приблизительно 700 мПа⋅с, предпочтительно как измерено с использованием вискозиметра Brookfield RVT, оборудованного измерительным наконечником №5 при 50 об/мин. Они могут также характеризоваться комплексной вязкостью при 0,01 рад/с при 30°С, составляющей меньше чем приблизительно 1×109 П или приблизительно 1×105 - приблизительно 9×108 П.
[0211] Походящие полиизобутилены согласно настоящему изобретению доступны под торговой маркой Oppanol®. Можно использовать комбинации высокомолекулярных полиизобутиленов (В100/В80) и низкомолекулярных полиизобутиленов (B10, В11, В12, В13). Походящие отношения низкомолекулярного полиизобутилена к высокомолекулярному полиизобутилену находятся в диапазоне, составляющем от 100:1 до 1:100, предпочтительно от 95:5 до 40:60, более предпочтительно от 90:10 до 80:20. Предпочтительный пример комбинации полиизобутиленов представляет собой В10/В100 в отношении, составляющем 85/15. Oppanol® В100 характеризуется средневязкостной молекулярной массой Mv, составляющей 1110000, и среднемассовой молекулярной массой Mw, составляющей 1550000, и средним молекулярно-массовым распределением Mw/Mn, составляющим 2,9. Oppanol® В10 характеризуется средневязкостной молекулярной массой Mv, составляющей 40000, и среднемассовой молекулярной массой Mw, составляющей 53000, и средним молекулярно-массовым распределением Mw/Mn, составляющим 3,2. Согласно определенным вариантам осуществления полибутен можно добавить к полиизобутиленам. Содержание твердых веществ полиизобутиленов в растворителях, как правило, составляет 30-50%, предпочтительно 35-40%. Специалисту в настоящей области техники понятно, что содержание твердых веществ можно модифицировать путем добавления походящего количества растворителя.
[0212] Приклеивающиеся при надавливании адгезивы на основе акрилатов могут также называться приклеивающимися при надавливании адгезивами на основе акрилата, или акрилатными приклеивающимися при надавливании адгезивами. Приклеивающиеся при надавливании адгезивы на основе акрилатов могут характеризоваться содержанием твердых веществ, составляющим предпочтительно 30%-60%. Такие приклеивающиеся при надавливании адгезивы на основе акрилата могут содержать или могут не содержать функциональные группы, такие как гидроксигруппы, группы карбоновых кислот, нейтрализованные группы карбоновых кислот и их смеси. Таким образом, термин "функциональные группы", в частности, относится к гидроксигруппам и группам карбоновых кислот, и депротонированным группам карбоновых кислот.
[0213] Соответствующее коммерческие продукты являются доступными, например, от Henkel под торговой маркой Duro Так®. Такие приклеивающиеся при надавливании адгезивы на основе акрилата основаны на мономерах, выбранных из одного или нескольких из следующего: акриловая кислота, бутилакрилат, 2-этилгексилакрилат, глицидилметакрилат, 2-гидроксиэтилакрилат, метилакрилат, метилметакрилат, т-октилакриламид и винилацетат, и поставляются в этилацетате, гептанах, н-гептане, гексане, метаноле, этаноле, изопропаноле, 2,4-пентандионе, толуоле или ксилене или их смесях.
[0214] Конкретные приклеивающиеся при надавливании адгезивы на основе акрилата являются доступными как:
- Duro-Tak™ 387-2287 или Duro-Tak™ 87-2287 (сополимер на основе винилацетата, 2-этилгексил-акрилата, 2-гидроксиэтил-акрилата и глицидил-метакрилата, предоставленный в виде раствора в этилацетате без поперечно-сшивающего агента),
- Duro-Tak™ 387-2516 или Duro-Tak™ 87-2516 (сополимер на основе винилацетата, 2-этилгексил-акрилата, 2-гидроксиэтил-акрилата и глицидил-метакрилата, предоставленный в виде раствора в этилацетате, этаноле, н-гептане и метаноле с титановым поперечно-сшивающим агентом),
- Duro-Tak™ 387-2051 или Duro-Tak™ 87-2051 (сополимер на основе акриловой кислоты, бутилакрилата, 2-этилгексилакрилата и винилацетата, предоставленный в виде раствора в этилацетате и гептане),
- Duro-Tak™ 387-2353 или Duro-Tak™ 87-2353 (сополимер на основе акриловой кислоты, 2-этилгексилакрилата, глицидилметакрилата и метилакрилата, предоставленный в виде раствора в этилацетате и гексане),
- Duro-Tak™ 87-4098 (сополимер на основе 2-этилгексил-акрилата и винилацетата, предоставленный в виде раствора в этилацетате).
[0215] Дополнительные полимеры также можно добавить для усиления когезии и/или адгезии.
[0216] Определенные полимеры, в частности, снижают вытекание адгезивного вещества из-под пластыря и, таким образом, в частности, являются походящими в качестве дополнительного полимера. Полимерная матрица может демонстрировать вытекание адгезивного вещества из-под пластыря, поскольку такие полимерные композиции часто проявляются, несмотря на очень высокую вязкость, способность очень медленно течь. Таким образом, во время хранения матрица может вытекать до определенной степени за пределы подложки. Это является проблемой стабильности при хранении, и ее можно предотвратить путем добавления определенных полимеров. Основный акрилатный полимер (например, Eudragit® E100), например, можно использовать для снижения вытекания адгезивного вещества из-под пластыря. Таким образом, согласно определенным вариантам осуществления композиция матричного слоя содержит дополнительно основный полимер, в частности, акрилат с функциональной аминогруппой, как, например, Eudragit® E100. Eudragit® E100 представляет собой катионный сополимер на основе диметиламиноэтилметакрилата, бутилметакрилата и метилметакрилата с отношением, составляющим 2:1:1. Мономеры случайным образом распределены вдоль цепи сополимера. На основании способа SEC (гель-фильтрация) среднемассовая молярная масса (Mw) Eudragit® E100 составляет приблизительно 47000 г/моль. Кроме того, такие полимеры, как Plastoid В, акриловые полимеры, такие как Eudragit, хитозан, целлюлозы и их производные, и полистирол можно применять для увеличения степени сухости адгезива (например, матричного слоя).
Дополнительные вспомогательные вещества
[0217] TTS согласно настоящему изобретению, и в частности гуанфацин-содержащий слой, может дополнительно содержать по меньшей мере одно вспомогательное вещество или вспомогательное средство. Особенно предпочтительные вспомогательные вещества согласно настоящему изобретению включают в себя диспергирующие агенты, усилители проницаемости и солюбилизаторы. Подробности в этом отношении представлены выше. Тем не менее, TTS согласно настоящему изобретению, и в частности гуанфацин-содержащий слой, может также включать в себя дополнительные вспомогательные вещества или вспомогательные средства.
[0218] Как правило, вспомогательные вещества или вспомогательные средства предпочтительно выбирают из группы, состоящей из следующего: диспергирующие агенты, солюбилизаторы, усилители проницаемости, пленкообразующие агенты, мягчители/пластификаторы, придающие липкость агенты, вещества для ухода за кожей, регуляторы рН, консерванты, стабилизирующие агенты и наполнители. Такие вспомогательные вещества могут присутствовать в гуанфацин-содержащем слое в количестве 0,001%-15% по массе, например, 0,5-10% по массе или 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя, и где мас.% количества относятся к одному вспомогательному веществу.
[0219] Следует отметить, что в фармацевтических составах компоненты состава можно классифицировать согласно их физико-химическим и физиологическим свойствам, и согласно их функции. Это означает, в частности, что вещество или соединение, попадающее в одну категорию, не исключено из другой категории компонента состава. Например, определенный полимер может представлять собой пленкообразующий агент, но также и придающий липкость агент. Некоторые вещества могут, например, представлять собой типичный мягчитель, но в то же время действуют как усилитель проницаемости. Специалист в настоящей области техники способен определить на основании своих общих знаний, какой категории или категориям компонентов состава принадлежит определенное вещество или соединение. Далее приведены подробности в отношении вспомогательных средств и вспомогательных веществ, которые, тем не менее, не следует понимать как исключающие. Другие вещества, явно не перечисленные в настоящем описании, также можно использовать согласно настоящему изобретению, и не исключено, что вещества и/или соединения, явно перечисленные для одной категории компонента состава, можно использовать для другого компонента состава в смысле настоящего изобретения.
[0220] Согласно одному варианту осуществления гуанфацин-содержащий слой содержит диспергирующий агент, как определено выше, предпочтительно диспергирующий агент выбран из группы, состоящей из следующего: сложные эфиры жирных кислот с многоатомными спиртами, жирные спирты, полиэтиленгликоли, характеризующиеся среднечисловой молекулярной массой, составляющей 300-400, алкилэфиры полиэтиленгликоля. Как объяснено выше, диспергирующий агент представляет собой предпочтительно С8-С20-алкилэфир полиэтиленгликоля, характеризующийся 2-10 звеньями ЕО, в частности лауриловый эфир полиоксиэтилена (4). Альтернативно или дополнительно, полиэфирсиликоны можно использовать в качестве диспергирующих агентов. Диспергирующий агент является полезным для того, чтобы гомогенно диспергировать гуанфацин в пределах гуанфацин-содержащего слоя, в частности гуанфацин-содержащего матричного слоя, тем самым улучшая свойства высвобождения TTS.
[0221] Согласно одному варианту осуществления гуанфацин-содержащий слой содержит солюбилизатор. Солюбилизатор предпочтительно улучшает диспергируемость гуанфацина в гуанфацин-содержащем слое и стабилизирует гуанфацин-содержащий слой. Более того, солюбилизатор может положительно влиять на когезию. Предпочтительные солюбилизаторы включают в себя, например, следующее: сложные эфиры глицерина, полиглицерина, пропиленгликоля и полиоксиэтилена и жирные кислоты со средней и/или длинной цепью, такие как глицерилмонолинолеат, глицериды со средней длиной цепи и триглицериды со средней длиной цепи, неионные солюбилизаторы, полученные реакцией касторового масла с этиленоксидом, и любые их смеси, которые могут дополнительно содержать жирные кислоты или жирные спирты; целлюлоза и метилцеллюлоза и их производные, такие как гидроксипропилцеллюлоза и сукцинат ацетата гипромеллозы; различные циклодекстрины и их производные; неионные триблок-сополимеры, характеризующиеся центральной гидрофобной цепью полиоксипропилена, фланкированной двумя гидрофильными цепями полиоксиэтилена, известные как полоксамеры; водорастворимые производные витамина Е; фармацевтической степени чистоты или агломерированный сферический изомальт; привитой сополимер на основе полиэтиленгликоля, поливинилацетата и поливинилкапролактама, также сокращенно обозначаемый как PVAc-PVCap-PEG и известный как Soluplus®; сополимеры винилпирролидона-винилацетата, такие как Kollidon® VA64; очищенные сорта натурального касторового масла, полиэтиленгликоля 400, полиоксиэтиленсорбитанмоноолеата (такого как полисорбат 80) или пропиленгликолей; моноэтиловый эфир диэтиленгликоля; глюконо-дельта-лактон; кукурузный и картофельный крахмал; а также любой из упомянутых ниже растворимых поливинилпирролидонов, но также нерастворимые/поперечно сшитые поливинилпирролидоны, такие как кросповидоны.
[0222] Тем не менее, также усилители проницаемости, упомянутые ниже, могут действовать как солюбилизаторы. Более того, описанные ниже пленкообразующие агенты также могут действовать одновременно как солюбилизаторы и наоборот.
[0223] Согласно одному варианту осуществления гуанфацин-содержащий слой содержит усилитель проницаемости. Предпочтительные варианты в этом отношении приведены выше. Усилители проницаемости представляют собой вещества, которые влияют на барьерные свойства рогового слоя в смысле увеличения проницаемости активного средства. Некоторыми примерами усилителей проницаемости являются многоатомные спирты, такие как дипропиленгликоль, пропиленгликоль и полиэтиленгликоль; масла, такие как оливковое масло, сквален и ланолин; жирные эфиры, такие как цетиловый эфир и олеиловый эфир; сложные эфиры жирных кислот, такие как изопропилмиристат; мочевина и производные мочевины, такие как аллантоин; полярные растворители, такие как диметилдецилфосфоксид, метилцетилсульфоксид, диметилауриламин, додецилпирролидон, изосорбит, диметилацетонид, диметилсульфоксид, децилметилсульфоксид и диметилформамид; салициловая кислота; аминокислоты; бензилникотинат; и алифатические поверхностно-активные вещества с более высокой молекулярной массой, такие как лаурилсульфатные соли. Другие агенты включают в себя олеиновую и линолевую кислоты, аскорбиновую кислоту, пантенол, бутилированный гидрокситолуол, токоферол, токоферилацетат, токофериллинолеат, пропилолеат и изопропилпальмитат. Если гуанфацин-содержащий слой содержит усилитель проницаемости, усилитель проницаемости предпочтительно выбирают из группы, состоящей из моноэтилового эфира диэтиленгликоля (транскутол), олеиновой кислоты, левулиновой кислоты, триглицеридов каприловой/каприновой кислоты, диизопропиладипата, изопропилмиристата, изопропилпальмитата, лауриллактата, триацетина, диметилпропиленмочевины и олеилового спирта, и предпочтительно он представляет собой олеиловый спирт.
[0224] Согласно одному варианту осуществления гуанфацин-содержащий слой дополнительно содержит пленкообразующий агент. Следует понимать, что представленные выше упомянутые солюбилизаторы, такие как Soluplus®, также могут действовать в качестве пленкообразующих агентов и контролировать когезию. Походящие примеры дополнительных пленкообразующих агентов включают в себя поливинилпирролидон, сополимеры винилацетата-винилпирролидона и производные целлюлозы, предпочтительно поливинилпирролидон, более предпочтительно растворимый поливинилпирролидон.
[0225] Если требуется, чтобы гуанфацин-содержащий слой обладал самоклеящимися свойствами и выбран один или несколько полимеров, которые не обеспечивают достаточных самоклеящихся свойств, добавляют придающий липкость агент. Предпочтительные придающие липкость агенты включают в себя миглиол, который представляет собой жидкий сложный эфир воска на основе длинноцепочечных ненасыщенных жирных кислот с четным числом атомов и длинноцепочечных ненасыщенных жирных спиртов с четным числом атомов растительного происхождения и полиэтиленгликоли. В частности, придающий липкость агент можно выбрать из поливинилпирролидона (который, благодаря своей способности поглощать воду, способен сохранять адгезионные свойства матричного слоя и, таким образом, может рассматриваться как придающий липкость агент в широком смысле), триглицеридов, полиэтиленгликолей, дипропиленгликоля, смол, сложных эфиров смол, терпенов и их производных, этиленвинилацетатных адгезивов, диметилполисилоксанов и полибутенов, предпочтительно поливинилпирролидона и более предпочтительно растворимого поливинилпирролидона. Предпочтительно придающий липкость агент можно выбрать из поливинилпирролидона, триглицеридов, дипропиленгликоля, смол, сложных эфиров смолы, терпенов и их производных, этиленвинилацетатных адгезивов, диметилполисилоксанов и полибутенов, предпочтительно поливинилпирролидона и более предпочтительно растворимого поливинилпирролидона.
[0226] Термин "растворимый поливинилпирролидон" относится к поливинилпирролидону, также известному как повидон, который является растворимым с более чем 10% по меньшей мере в этаноле, предпочтительно также в воде, диэтиленгликоле, метаноле, н-пропаноле, 2-пропаноле, н-бутаноле, хлороформе, метиленхлориде, 2-пирролидоне, макроголе 400, 1,2-пропиленгликоле, 1,4-бутандиоле, глицерине, триэтаноламине, пропионовой кислоте и уксусной кислоте. Примеры поливинилпирролидонов, которые являются коммерчески доступными, включают в себя Kollidon® 12 PF, Kollidon® 17 PF, Kollidon® 25, Kollidon® 30 и Kollidon® 90 F, поставляемые BASF, или повидон K90F. Различные марки Kollidon® определяют с точки зрения значения K, отражающего среднюю молекулярную массу марок поливинилпирролидона. Kollidon® 12 PF характеризуется диапазоном значений K от 10,2 до 13,8, что соответствует номинальному значению K, составляющему 12. Kollidon® 17 PF характеризуется диапазоном значений K от 15,3 до 18,4, что соответствует номинальному значению, составляющему K 17. Kollidon® 25 характеризуется диапазоном значений K от 22,5 до 27,0, что соответствует номинальному значению K, составляющему 25, Kollidon® 30 характеризуется диапазоном значений K от 27,0 до 32,4, что соответствует номинальному значению K, составляющему 30. Kollidon® 90 F характеризуется диапазоном значений K от 81,0 до 97,2, что соответствует номинальному значению K, составляющему 90. Предпочтительными марками Kollidon® являются Kollidon® 12 PF, Kollidon® 30 и Kollidon® 90 F. Используемый в настоящем изобретении термин "значение K" относится к значению, рассчитанному из относительной вязкости поливинилпирролидона в воде в соответствии с монографиями "Повидон" Европейской Фармакопеи (Ph.Eur.) и Фармакопеи США (USP).
[0227] Согласно одному варианту осуществления гуанфацин-содержащий слой дополнительно содержит мягчитель/пластификатор. Иллюстративные мягчители/пластификаторы включают в себя линейные или разветвленные, насыщенные или ненасыщенные спирты, характеризующиеся от 6 до 20 атомами углерода, триглицериды и полиэтиленгликоли.
[0228] Согласно одному варианту осуществления гуанфацин-содержащий слой дополнительно содержит стабилизирующий агент. Стабилизирующие агенты включают в себя токоферол и его сложноэфирные производные и аскорбиновую кислоту и ее сложноэфирные производные. Дополнительные стабилизирующие агенты включают в себя метабисульфит натрия, аскорбиловые эфиры жирных кислот, такие как аскорбилпальмитат, аскорбиновую кислоту, бутилированный гидрокситолуол, токоферол, токоферилацетат и токофериллинолеат.
[0229] Согласно одному варианту осуществления гуанфацин-содержащий слой дополнительно содержит регулятор рН. Подходящие регуляторы рН включают в себя слабые кислоты и основания, включая в себя производные амина, производные неорганических щелочей и полимеры с основной или кислотной функциональной группой.
[0230] Согласно одному варианту осуществления гуанфацин-содержащий слой дополнительно содержит консервант. Походящие консерванты включают в себя парабены, формальдегидные высвобождающие вещества, изотиазолиноны, феноксиэтанол и органические кислоты, такие как бензойная кислота, сорбиновая кислота, левулиновая кислота и анисовая кислота.
[0231] Согласно одному варианту осуществления гуанфацин-содержащий слой дополнительно содержит дополнительно содержит вещество для ухода за кожей. Такие вещества можно использовать для предотвращения или уменьшения раздражения кожи, которое можно определить по шкале ответа кожи. Подходящие вещества для ухода за кожей включают в себя соединения стерина, такие как холестерин, декспантенол, альфа-бисаболол и антигистаминные препараты.
[0232] Согласно одному варианту осуществления гуанфацин-содержащий слой дополнительно содержит наполнитель. Наполнители, такие как силикагели, диоксид титана и оксид цинка, можно использовать в сочетании с полимером, чтобы влиять на определенные физические параметры, такие как когезия и прочность связи, желаемым образом.
Характеристики высвобождения
[0233] TTS согласно настоящему изобретению предназначены для трансдермального введения гуанфацина в системный кровоток в течение заданного продолжительного периода времени, предпочтительно в течение по меньшей мере 24 часов, более предпочтительно по меньшей мере 72 часов, в частности в течение приблизительно 84 часов.
[0234] Согласно одному варианту осуществления TTS согласно настоящему изобретению обеспечивает с помощью трансдермальной доставки в равновесном состоянии среднюю концентрацию гуанфацина в плазме, составляющую 1-20 нг/мл, предпочтительно 1-15 нг/мл, более предпочтительно 1-10 нг/мл.
[0235] Предпочтительно TTS обеспечивает терапевтически эффективные концентрации гуанфацина в плазме в пределах меньше чем 8 часов, предпочтительно меньше чем 6 часов, более предпочтительно меньше чем 4 часов после нанесения TTS на кожу. Более того, терапевтически эффективные концентрации в плазме предпочтительно поддерживаются в течение всего периода введения, составляющего по меньшей мере 24 часа, предпочтительно по меньшей мере 72 часа, более предпочтительно приблизительно 84 часа.
[0236] Согласно одному варианту осуществления TTS согласно настоящему изобретению обеспечивает AUC0-244, составляющую 10-600 нг*ч/мл, предпочтительно 20
- 400 нг*ч/мл. Согласно другому варианту осуществления TTS согласно настоящему изобретению обеспечивает AUC0-724, составляющую 30-1800 нг*ч/мл, предпочтительно 60
- 1200 нг*ч/мл. Согласно другому варианту осуществления TTS согласно настоящему изобретению обеспечивает AUC0-844, составляющую 35-2100 нг*ч/мл, предпочтительно 70
- 1400 нг*ч/мл. Следует понимать, что значения AUC предпочтительно относятся к значениям AUC, полученным в равновесном состоянии.
[0237] Согласно одному варианту осуществления TTS согласно настоящему изобретению обеспечивает отношение Cmax к С84, составляющее меньше чем 3,5. Согласно другому варианту осуществления TTS согласно настоящему изобретению обеспечивает отношение Cmax к С72, составляющее меньше чем 3,0. Согласно другому варианту осуществления TTS согласно настоящему изобретению обеспечивает отношение Cmax к С24, составляющее меньше чем 2,0. Указанные отношения указывают на плоскую кривую концентрации в плазме крови, что является благоприятным с точки зрения непрерывного лечения пациента.
[0238] Согласно одному варианту осуществления TTS согласно настоящему изобретению обеспечивает скорость чрескожного проникновения гуанфацина, как измерено в диффузионной ячейке Франца с помощью дерматомированной кожи человека, составляющую:
0,01 мкг/(см2*ч) - 8 мкг/(см2*ч) в первые 24 часа,
0,05 мкг/(см2*ч) - 10 мкг/(см2*ч) от 24 до 72 часов.
[0239] Согласно одному варианту осуществления TTS согласно настоящему изобретению обеспечивает скорость чрескожного проникновения гуанфацина, как измерено в диффузионной ячейке Франца с помощью дерматомированной кожи человека, составляющую 0,05 мг/см2 - 0,7 мг/см2, предпочтительно 0,1 мг/см2 - 0,6 мг/см2, в течение периода времени, составляющего 72 часа.
[0240] С учетом вышеизложенного, настоящее изобретение согласно одному аспекту также относится к трансдермальной терапевтической системе для трансдермального введения гуанфацина, содержащей гуанфацин-содержащую слоистую структуру,
причем трансдермальная терапевтическая система обеспечивает с помощью трансдермальной доставки один или несколько фармакокинетических параметров, выбранных из группы, состоящей из следующего:
AUC0-24 10-600 (нг/мл)⋅ч,
AUC0-72 30-1800 (нг/мл)⋅ч,
AUC0-84 35-2100 (нг/мл)⋅ч,
отношение Cmax к C24, составляющее меньше чем 2,0,
отношение Cmax к C72, составляющее меньше чем 3,0, и
отношение Cmax к C84, составляющее меньше чем 3,5.
[0241] Согласно предпочтительному варианту осуществления настоящего изобретения относится к трансдермальной терапевтической системе для трансдермального введения гуанфацина, содержащей гуанфацин-содержащую слоистую структуру,
причем трансдермальная терапевтическая система обеспечивает с помощью трансдермальной доставки один или несколько фармакокинетических параметров, выбранных из группы, состоящей из следующего:
AUC0-24 20-400 (нг/мл)⋅ч,
AUC0-72 60-1200 (нг/мл)⋅ч,
AUC0-84 70-1400 (нг/мл)⋅ч,
отношение Cmax к C24, составляющее меньше чем 1,5,
отношение Cmax к C72, составляющее меньше чем 2,5, и
отношение Cmax к C84, составляющее меньше чем 3,0.
Способ лечения/медицинское применение
[0242] Согласно одному варианту осуществления настоящего изобретения TTS согласно настоящему изобретению являются походящими для применения в способе лечения пациента-человека, предпочтительно пациента в возрасте, составляющем 6-17 лет. В частности, TTS согласно настоящему изобретению являются походящими для применения в способе лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) и/или в качестве дополнительной терапии к лекарственным средствам-стимуляторам у пациента-человека, предпочтительно у пациента-человека в возрасте, составляющем 6-17 лет.
[0243] Согласно предпочтительному варианту осуществления в связи с представленным выше медицинским применением TTS наносят на кожу пациента в течение по меньшей мере 24 часов, предпочтительно по меньшей мере 72 часов, более предпочтительно приблизительно 84 часов.
[0244] Согласно одному варианту осуществления настоящее изобретение относится к способу лечения пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем нанесения трансдермальной терапевтической системы, как определено в одном из пунктов 1-37, на кожу пациента. В частности, настоящее изобретение относится к способу лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) у пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем нанесения трансдермальной терапевтической системы согласно настоящему изобретению на кожу пациента.
[0245] Согласно предпочтительному варианту осуществления представленных выше способов лечения трансдермальную терапевтическую систему наносят на кожу пациента в течение по меньшей мере 24 часов, предпочтительно по меньшей мере 72 часов, более предпочтительно приблизительно 84 часов.
[0246] С учетом вышеизложенного, настоящее изобретение согласно одному аспекту относится к трансдермальной терапевтической системе, содержащей гуанфацин, для применения в способе лечения пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем трансдермального введения гуанфацина, причем трансдермальную терапевтическую систему наносят на кожу пациента в течение по меньшей мере 24 часов, предпочтительно по меньшей мере 72 часов, более предпочтительно приблизительно 84 часов. Согласно предпочтительному варианту осуществления трансдермальная терапевтическая система предусмотрена для применения в способе лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) и/или в качестве дополнительной терапии к лекарственным средствам-стимуляторам у пациента-человека. Согласно более предпочтительному варианту осуществления трансдермальная терапевтическая система представляет собой трансдермальную терапевтическую систему согласно настоящему изобретению, в частности трансдермальную терапевтическую систему, обеспечивающую один или несколько фармакокинетических параметров, выбранных из группы, состоящей из следующего:
AUC0-24 10-600 (нг/мл)⋅ч,
AUC0-72 30-1800 (нг/мл)⋅ч,
AUC0-84 35-2100 (нг/мл)⋅ч,
отношение Cmax к C24, составляющее меньше чем 2,0,
отношение Cmax к C72, составляющее меньше чем 3,0, и
отношение Cmax к C84, составляющее меньше чем 3,5;
и предпочтительно выбранных из группы, состоящей из следующего:
AUC0-24 20-400 (нг/мл)⋅ч,
AUC0-72 60-1200 (нг/мл)⋅ч,
AUC0-84 70-1400 (нг/мл)⋅ч,
отношение Cmax к C24, составляющее меньше чем 1,5,
отношение Cmax к C72, составляющее меньше чем 2,5, и
отношение Cmax к C84, составляющее меньше чем 3,0.
[0247] Согласно другому аспекту настоящее изобретение относится к гуанфацину для применения в способе лечения пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем трансдермального введения гуанфацина с помощью трансдермальной терапевтической системы, причем трансдермальную терапевтическую систему наносят на кожу пациента в течение по меньшей мере 24 часов, предпочтительно по меньшей мере 72 часов, более предпочтительно приблизительно 84 часов. Согласно предпочтительному варианту осуществления гуанфацин предусмотрен для применения в способе лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) и/или в качестве дополнительной терапии к лекарственным средствам-стимуляторам у пациента-человека. Согласно более предпочтительному варианту осуществления трансдермальная терапевтическая система представляет собой трансдермальную терапевтическую систему согласно настоящему изобретению, в частности трансдермальную терапевтическую систему, обеспечивающую один или несколько фармакокинетических параметров, выбранных из группы, состоящей из следующего:
AUC0-24 10-600 (нг/мл)⋅ч,
AUC0-72 30-1800 (нг/мл)⋅ч,
AUC0-84 35-2100 (нг/мл)⋅ч,
отношение Cmax к C24, составляющее меньше чем 2,0,
отношение Cmax к C72, составляющее меньше чем 3,0, и
отношение Cmax к C84, составляющее меньше чем 3,5;
и предпочтительно выбранных из группы, состоящей из следующего:
AUC0-24 20-400 (нг/мл)⋅ч,
AUC0-72 60-1200 (нг/мл)⋅ч,
AUC0-84 70-1400 (нг/мл)⋅ч,
отношение Cmax к C24, составляющее меньше чем 1,5,
отношение Cmax к C72, составляющее меньше чем 2,5, и
отношение Cmax к C84, составляющее меньше чем 3,0.
[0248] Согласно другому аспекту настоящее изобретение относится к способу лечения пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем трансдермального введения гуанфацина, причем трансдермальную терапевтическую систему наносят на кожу пациента в течение по меньшей мере 24 часов, предпочтительно по меньшей мере 72 часов, более предпочтительно приблизительно 84 часов. Согласно предпочтительному варианту осуществления способ предусмотрен для лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) и/или в качестве дополнительной терапии к лекарственным средствам-стимуляторам у пациента-человека. Согласно более предпочтительному варианту осуществления трансдермальная терапевтическая система представляет собой трансдермальную терапевтическую систему согласно настоящему изобретению, в частности трансдермальную терапевтическую систему, обеспечивающую один или несколько фармакокинетических параметров, выбранных из группы, состоящей из следующего:
AUC0-24 10-600 (нг/мл)⋅ч,
AUC0-72 30-1800 (нг/мл)⋅ч,
AUC0-84 35-2100 (нг/мл)⋅ч,
отношение Cmax к C24, составляющее меньше чем 2,0,
отношение Cmax к C72, составляющее меньше чем 3,0, и
отношение Cmax к C84, составляющее меньше чем 3,5;
и предпочтительно выбранных из группы, состоящей из следующего:
AUC0-24 20-400 (нг/мл)⋅ч,
AUC0-72 60-1200 (нг/мл)⋅ч,
AUC0-84 70-1400 (нг/мл)⋅ч,
отношение Cmax к С24, составляющее меньше чем 1,5,
отношение Cmax к С72, составляющее меньше чем 2,5, и
отношение Cmax к С84, составляющее меньше чем 3,0.
[0249] В связи с вышеупомянутыми применениями и способами лечения TTS согласно настоящему изобретению предпочтительно наносят по меньшей мере на одну поверхность тела субъекта, выбранную из верхней наружной области, верхней части груди, верхней части спины или боковой части груди, в течение определенных интервалов между введениями доз.
[0250] Предпочтительное время нанесения TTS согласно настоящему изобретению составляет по меньшей мере 24 часа (1 день), предпочтительно по меньшей мере 72 часа (3 дня), более предпочтительно приблизительно 84 часа (3,5 дней). По истечении этого времени TTS можно удалять и необязательно можно наносить новую TTS, чтобы обеспечить круглосуточное лечение.
Способ получения
[0251] Настоящее изобретение дополнительно относится к способу получения гуанфацин-содержащего слоя, предпочтительно гуанфацин-содержащего матричного слоя, для применения в трансдермальной терапевтической системе.
[0252] Согласно настоящему изобретению способ получения гуанфацин-содержащего слоя для применения в трансдермальной терапевтической системе согласно настоящему изобретению предусматривает следующие стадии:
1) объединение по меньшей мере следующих компонентов:
i) гуанфацин; и
ii) по меньшей мере один силиконовый полимер; и для получения композиции для покрытия;
2) нанесение композиции для покрытия на подложку или защитное покрытие для получения нанесенной композиции для покрытия; и
3) сушка нанесенной композиции для покрытия с образованием гуанфацин-содержащего слоя.
[0253] На стадии 1) представленного выше способа получения гуанфацин предпочтительно диспергируют в полимере для получения гомогенной композиции для покрытия.
[0254] Следует понимать, что на стадии 1) можно добавлять также дополнительные ингредиенты, предпочтительно по меньшей мере один дополнительный полимер и/или по меньшей мере одно вспомогательное вещество, как определено выше.
[0255] Предпочтительно растворитель добавляют на стадии 1) способа и/или растворитель присутствует, поскольку один или несколько полимеров предусмотрены в форме раствора. Растворитель предпочтительно выбран из спиртовых растворителей, в частности метанола, этанола, изопропанола и их смесей, и из неспиртовых растворителей, в частности этилацетата, гексана, гептана, петролейного эфира, толуола и их смесей, и более предпочтительно выбран из неспиртовых растворителей, и наиболее предпочтительно представляет собой этилацетат или н-гептан.
[0256] Согласно предпочтительному варианту осуществления по меньшей мере один силиконовый полимер предусмотрен в виде раствора с содержанием твердых веществ, составляющим 40-60% по массе.
[0257] На стадии 2) способа композицию для покрытия наносят на подложку или защитное покрытие. В результате получают нанесенную композицию для покрытия, т.е. композицию для покрытия, нанесенную на подложку или защитное покрытие.
[0258] После этого гуанфацин-содержащий слой образуется на стадии 3), способ, таким образом, может дополнительно предусматривать стадию, на которой защитное покрытие или подложку наносят на другую сторону гуанфацин-содержащего слоя.
[0259] На стадии 3) представленного выше способа получения сушку проводят предпочтительно при температуре, составляющей 20-90°С, более предпочтительно 40-70°С. Сушка может предпочтительно занимать по меньшей мере 1 час, предпочтительно по меньшей мере 8 часов, например, один день.
ПРИМЕРЫ
[0260] Настоящее изобретение теперь будет более полно описано со ссылкой на прилагаемые примеры. Тем не менее, следует понимать, что нижеследующее описание является только иллюстративным и никоим образом не должно рассматриваться как ограничение настоящего изобретения. Числовые значения, приведенные в примерах в отношении количества ингредиентов в композиции или массы площади, могут незначительно отличаться из-за изменчивости производственного процесса.
ПРИМЕР 1A-D
Композиция для покрытия
[0261] Составы гуанфацин-содержащих композиций для покрытия согласно примерам 1a-d обобщенно представлены в таблице 1.1а и 1.1b ниже. Значения в % относятся к количествам (кол-во) в % по массе.
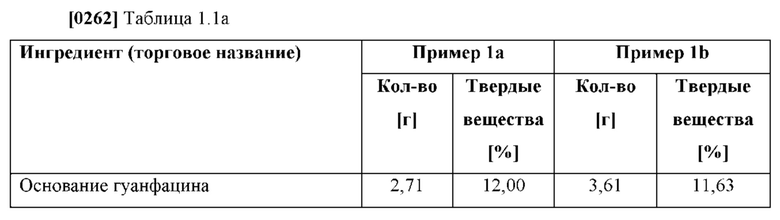
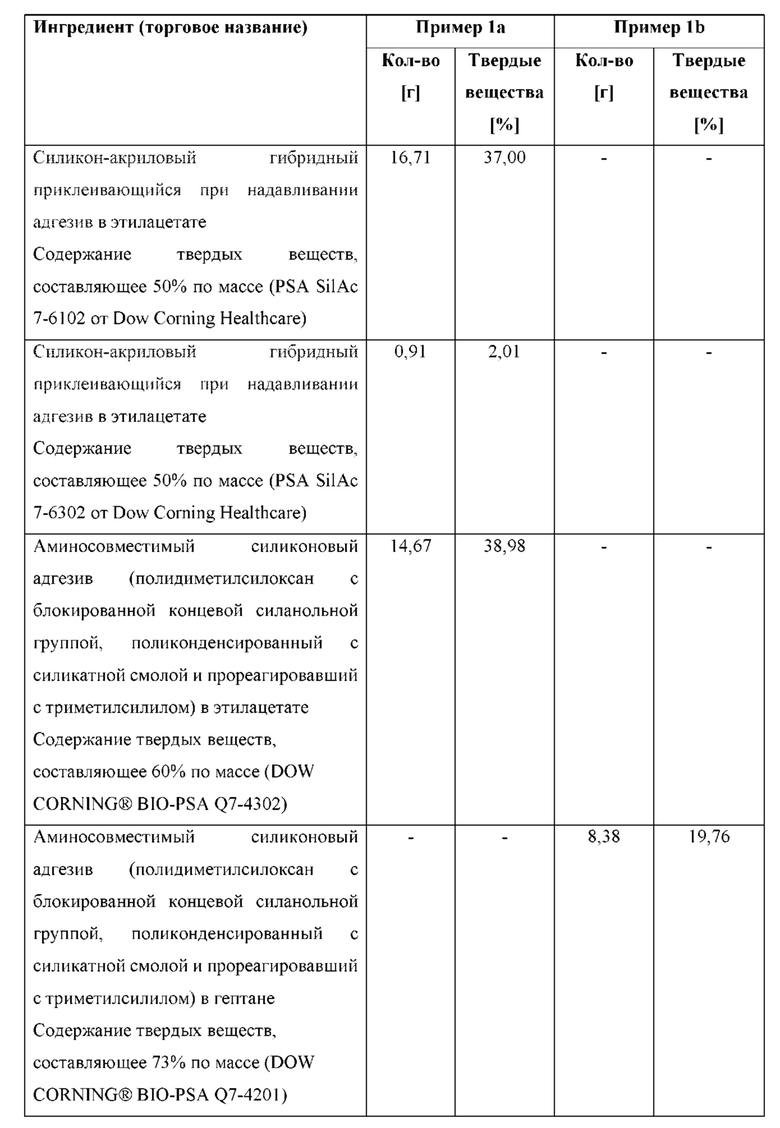
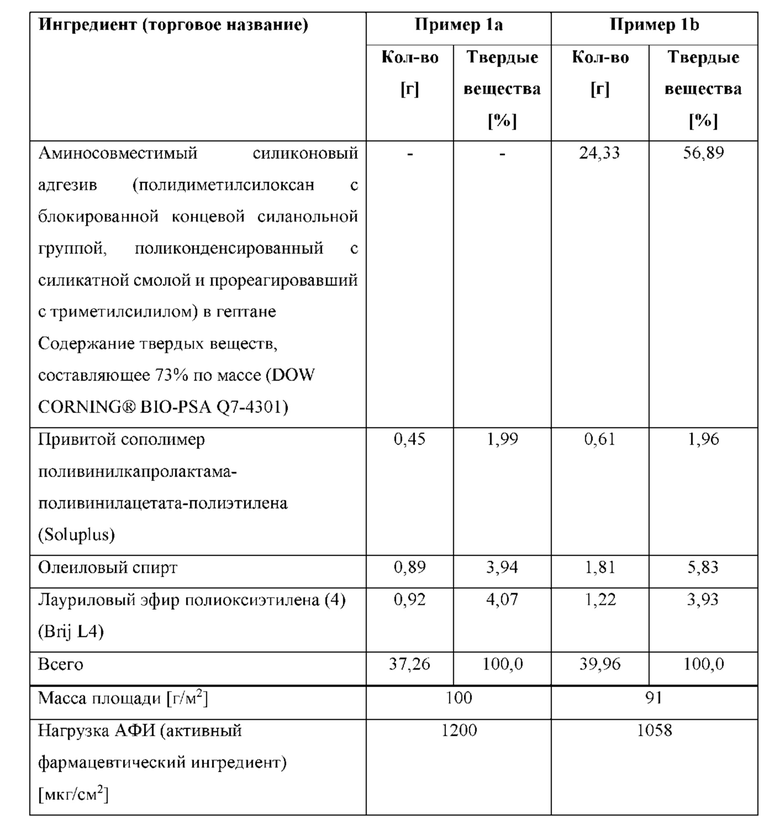
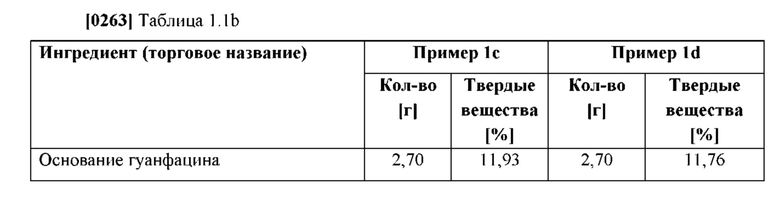
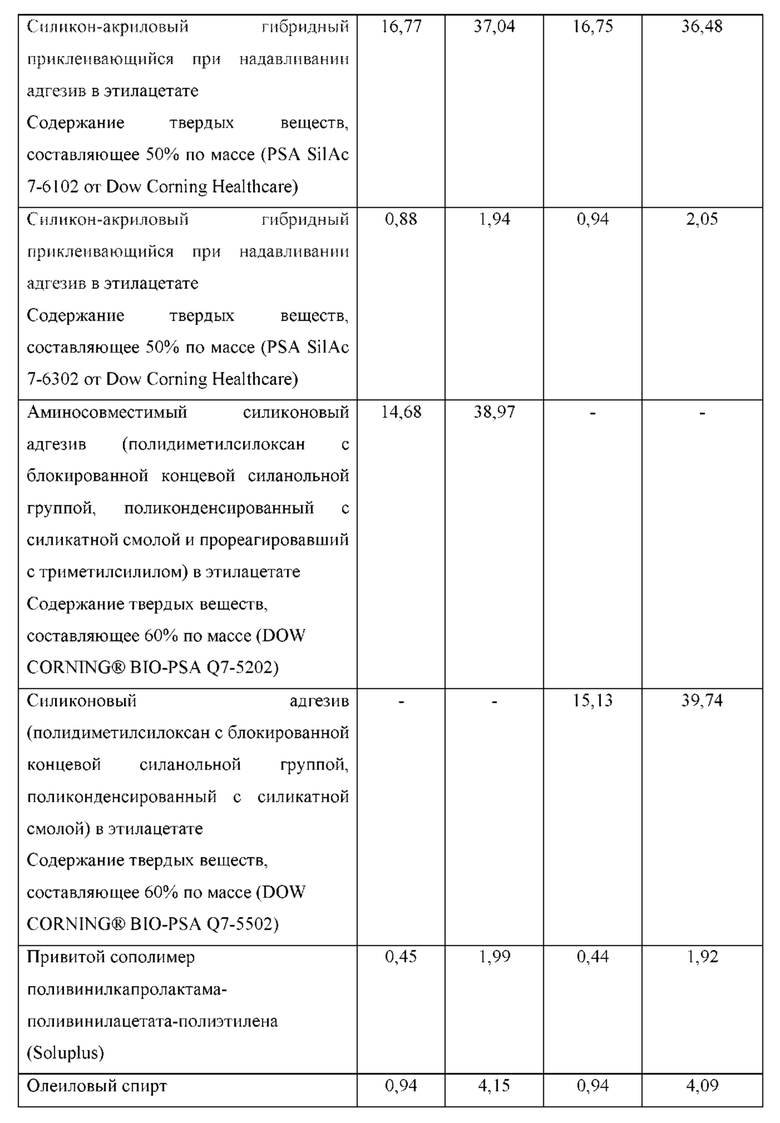
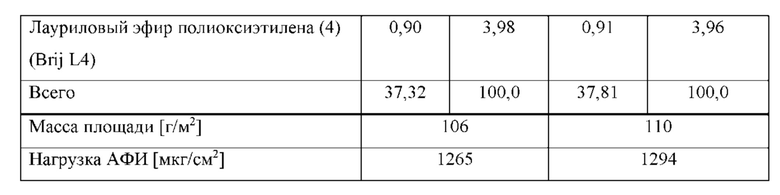
Получение композиции для покрытия
Активный фармацевтический ингредиент и используемые усилители диспергировали в растворителе этилацетате и обрабатывали ультразвуком в течение приблизительно 10 мин. Добавляли адгезивы. Указанные две стадии также можно проводить в обратном порядке. С помощью мешалки для растворения смесь гомогенизировали при 2000 об/мин в течение 2 минут. Soluplus добавляли и массу перемешивали в течение дополнительных 2 минут при 2000 об/мин и дополнительно гомогенизировали при 1500 об/мин в течение по меньшей мере 30 минут.
В случае композиции 1b усилитель лауриловый эфир полиоксиэтилена (4) и Soluplus диспергировали в растворителе этаноле и обрабатывали ультразвуком в течение 10 минут. Добавляли активный фармацевтический ингредиент и усилитель олеиловый спирт и смесь обрабатывали ультразвуком в течение дополнительных 10 минут. Добавляли адгезивы.
В случае композиции 1d активный фармацевтический ингредиент и используемые усилители диспергировали в растворителе этилацетате и обрабатывали ультразвуком в течение 10 минут. Добавляли адгезивы и Soluplus. С помощью мешалки для растворения смесь гомогенизировали при 2000 об/мин в течение 2 минут. Массу дополнительно перемешивали при 1500 об/мин в течение по меньшей мере 30 минут.
Нанесение композиции для покрытия
[0264] Полученную гуанфацин-содержащую композицию для покрытия наносили на полиэтилентерефталатную пленку (Scotchpak 9755, которая может функционировать в качестве защитного покрытия) с использованием, например, аппликатора пленки от компании Erichsen в соответствии с содержанием твердых веществ рассматриваемой смеси с требуемой сухой массой покрытия и высушивали при приблизительно 50°С в течение приблизительно 10 мин. В зависимости от целевой массы площади соответствующий зазор аппликатора пленки составляет 150-350 мкм.
[0265] Толщину покрытия выбирали так, что удаление раствора дает в результате массу площади гуанфацин-содержащего слоя, составляющую приблизительно 100 (пример 1а), 91 (пример 1b), 106 (пример 1с), 110 (пример 1d) г/м2. Высушенную пленку затем ламинировали с помощью подложки (PET, 15 мкм, прозрачный, MN 19) с получением гуанфацин-содержащей самоклеящейся слоистой структуры.
Получение TTS (применительно ко всем примерам)
[0266] Отдельные системы (TTS) затем получали штампованием из гуанфацин-содержащей самоклеящейся слоистой структуры, полученной, как описано выше. Затем, TTS запечатывали в пакеты из первичного упаковочного материала.
Измерение проницаемости кожи
[0267] Проникшее количество TTS, полученной согласно примерам 1a-d, определяли с помощью экспериментов в соответствии с руководством OECD (принятым 13 апреля 2004 г.) проводили с помощью 10,0 мл диффузионной ячейки Франца. Использовали разделенную по толщине кожу человека, полученную от косметических операций (например, живот женщины, дата рождения - 1966 г.). Использовали дерматом для получения кожи толщиной, составляющей 500 мкм, с неповрежденным эпидермисом для всех TTS. Отрезки с площадью высвобождения, составляющей 1,188 см2, получали штампованием из TTS. Измеряли проникшее количество гуанфацина в рецепторной среде диффузионной ячейки Франца (фосфатный буферный раствор рН 5,5 с 0,1% азидом натрия в качестве антибактериологического агента) при температуре, составляющей 32±1°С и рассчитывали соответствующее кумулятивное проникшее количество.
[0268] Результаты показаны в таблице 1.2 и на фиг. 1.
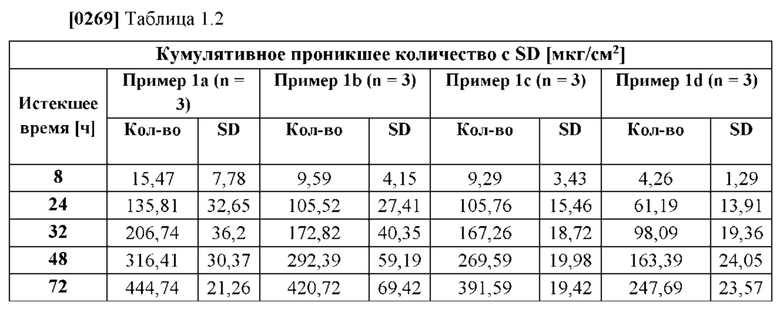
ПРИМЕР 2А-В
Композиция для покрытия
[0270] Составы гуанфацин-содержащих композиций для покрытия согласно примерам 2а-b обобщенно представлены в таблице 2.1. Значения в % относятся к количествам в % по массе.
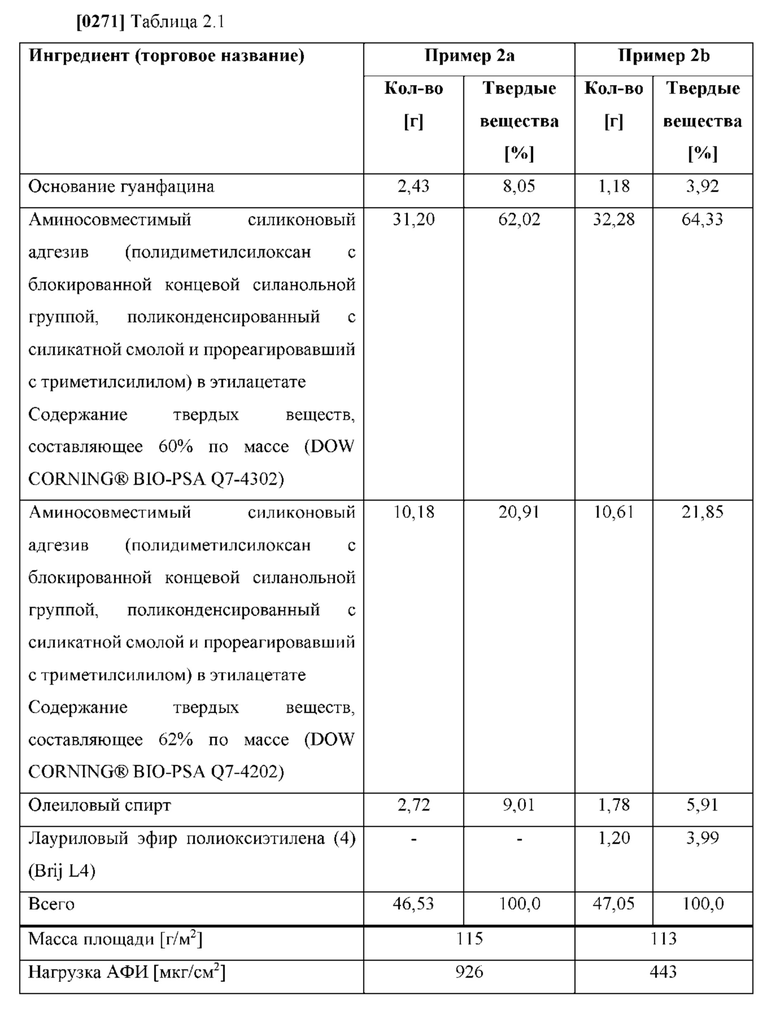
Получение композиции для покрытия
[0272] Активный фармацевтический ингредиент и используемые усилители диспергировали в растворителе этилацетате и обрабатывали ультразвуком в течение приблизительно 10 минут. Добавляли адгезивы. Указанные две стадии также можно проводить в обратном порядке. С помощью мешалки для растворения смесь гомогенизировали при 2000 об/мин в течение 2 минут. Массу перемешивали снова в течение 10 минут при 1000 об/мин.
Нанесение композиции для покрытия
[0273] См. пример 1a-d в отношении процесса нанесения покрытия. Толщина покрытия давала массу площади гуанфацин-содержащего слоя, составляющую 115 (пример 2а) и 113 (пример 2b) г/м2. Высушенную пленку ламинировали с помощью подложки (например, силиконизированный MN 19) для получения гуанфацин-содержащей самоклеящейся слоистой структуры.
Получение TTS
[0274] См. пример 1.
Измерение проницаемости кожи
[0275] Проникшее количество TTS, полученной согласно примерам 2а-b, определяли, как описано для примеров 1a-d выше. Отрезки с площадью высвобождения, составляющей 1,188 см2, получали штампованием из TTS.
[0276] Результаты показаны в таблице 2.2 и на фиг. 2.
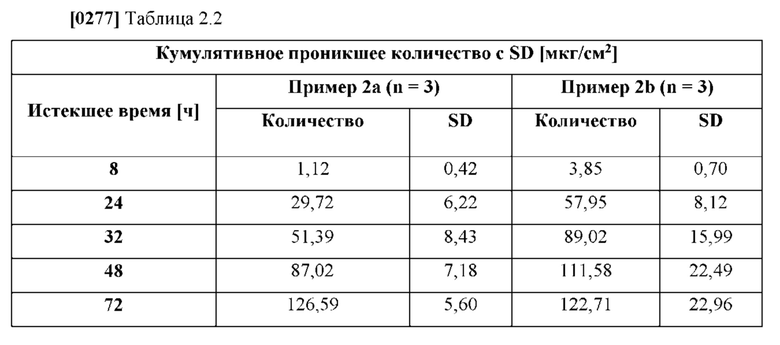
ПРИМЕР 3А-В
[0278] Составы гуанфацин-содержащих композиций для покрытия согласно примерам 3а-b обобщенно представлены в таблице 3.1 ниже. Значения в % относятся к количествам в % по массе.

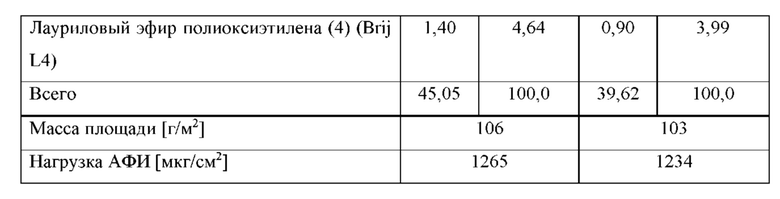
Получение композиции для покрытия
[0280] Активный фармацевтический ингредиент и используемые усилители диспергировали в растворителе этилацетате и обрабатывали ультразвуком в течение приблизительно 10 минут. Добавляли адгезивы. Указанные две стадии также можно проводить в обратном порядке. С помощью мешалки для растворения смесь гомогенизировали при 2000 об/мин в течение 2 минут. Добавляли Soluplus и массу перемешивали в течение дополнительных 2 мин при 2000 об/мин и дополнительно гомогенизировали при 1500 об/мин в течение 30 мин.
Нанесение композиции для покрытия
[0281] См. пример 1a-d в отношении процесса нанесения покрытия. Толщина покрытия давала массу площади гуанфацин-содержащего слоя, составляющую 106 (пример 3а) и 103 (пример 3b) г/м2. Высушенную пленку ламинировали с помощью подложки (например, силиконизированный MN 19) для получения гуанфацин-содержащей самоклеящейся слоистой структуры.
Получение TTS
[0282] См. пример 1.
Измерение проницаемости кожи
[0283] Проникшее количество TTS, полученной согласно примерам 3а-b определяли, как описано для примеров 1a-d выше. Отрезки с площадью высвобождения, составляющей 1,188 см2, получали штампованием из TTS.
[0284] Результаты показаны в таблице 3.2 и на фиг. 3.
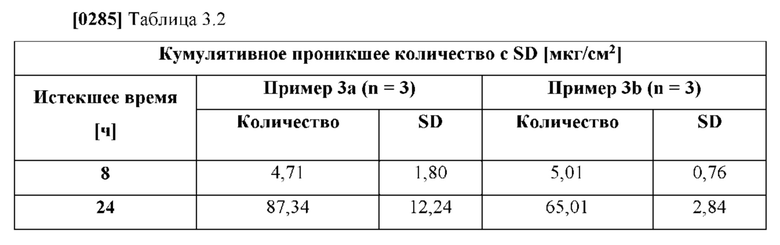
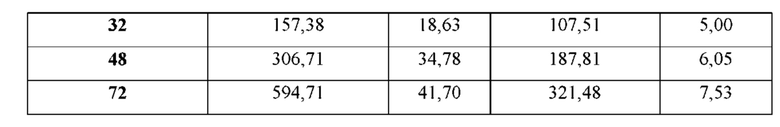
ПРИМЕР 4А
[0286] Составы гуанфацин-содержащих композиций для покрытия согласно примерам 4а обобщенно представлены в таблице 4.1 ниже. Значения в % относятся к количествам в % по массе.
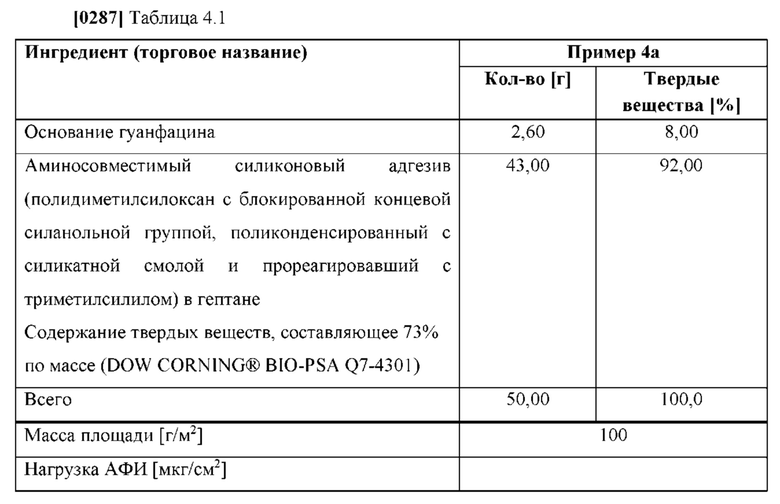
Получение композиции для покрытия
[0288] Активный фармацевтический ингредиент диспергировали в растворителе н-гептане и обрабатывали ультразвуком в течение приблизительно 45 минут. Добавляли адгезив. Указанные две стадии также можно проводить в обратном порядке. С помощью мешалки для растворения смесь гомогенизировали при 1000 об/мин в течение 15 минут.
Нанесение композиции для покрытия
[0289] См. пример 1a-d в отношении процесса нанесения покрытия. Толщина покрытия давала массу площади гуанфацин-содержащего слоя, составляющую 100 (пример 4а) г/м2. Высушенную пленку ламинировали с помощью подложка (хостафан, 15 мкм) для получения гуанфацин-содержащей самоклеящейся слоистой структуры.
Получение TTS
[0290] См. пример 1.
Измерение проницаемости кожи
[0291] Проникшее количество TTS, полученной согласно примерам 4а, определяли, как описано для примеров 1a-d выше. Отрезки с площадью высвобождения, составляющей 1,188 см2, получали штампованием из TTS.
[0292] Результаты показаны в таблице 4.2 и на фиг. 10.
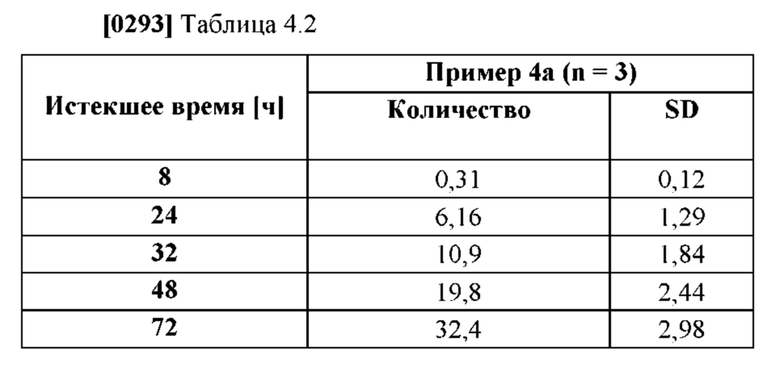
СРАВНИТЕЛЬНЫЙ ПРИМЕР 1
[0294] Сравнительный пример 1 представляет собой смесь Oppanol В10 и Oppanol В100 с отношением, составляющим 15/85 и основание гуанфацина. Состав гуанфацин-содержащей композиции для покрытия согласно сравнительному примеру 1 обобщенно представлен в таблице 4.1 ниже. Значения в % относятся к количествам в % по массе
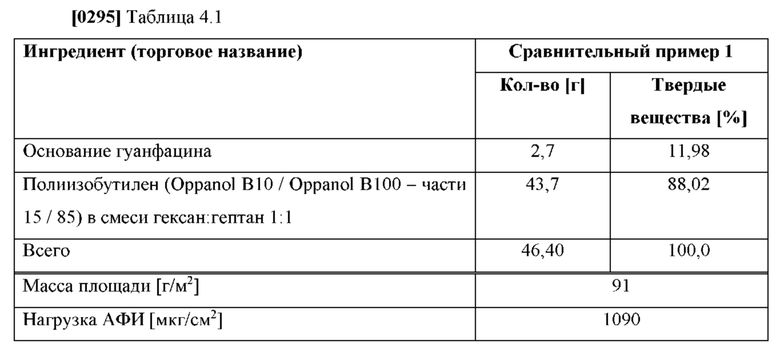
Получение композиции для покрытия
[0296] Активный фармацевтический ингредиент диспергировали в растворителе н-гептане и обрабатывали ультразвуком в течение 10 мин. Затем добавляли адгезивную смесь. Указанные две стадии также можно проводить в обратном порядке. С помощью мешалки для растворения смесь гомогенизировали при 100-500 об/мин в течение 30 минут.
Нанесение композиции для покрытия
[0297] См. пример 1a-d в отношении процесса нанесения покрытия. Толщина покрытия давала массу площади гуанфацин-содержащего слоя, составляющую 91 г/м2. Высушенную пленку ламинировали с помощью подложки (силиконизированный MN 19) для получения гуанфацин-содержащей самоклеящейся слоистой структуры.
Получение TTS
[0298] См. пример 1.
Измерение проницаемости кожи
[0299] Проникшее количество TTS, полученной согласно сравнительному примеру 1, определяли, как описано для примеров 1a-d выше. Отрезки с площадью высвобождения, составляющей 1,188 см2, получали штампованием из TTS.
[0300] Результаты показаны в таблице 4.2 и на фиг. 1.
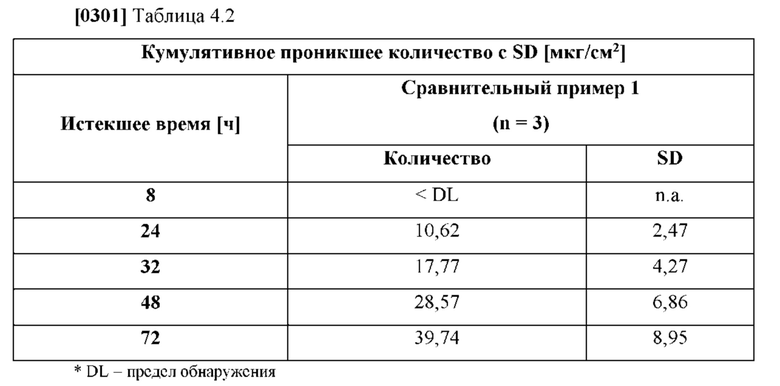
СРАВНИТЕЛЬНЫЙ ПРИМЕР 2А-В
Композиция для покрытия
[0302] Составы гуанфацин-содержащих композиций для покрытия согласно сравнительным примерам 2а-b обобщенно представлены в таблице 5.1 ниже. Значения в % относятся к количествам в % по массе.

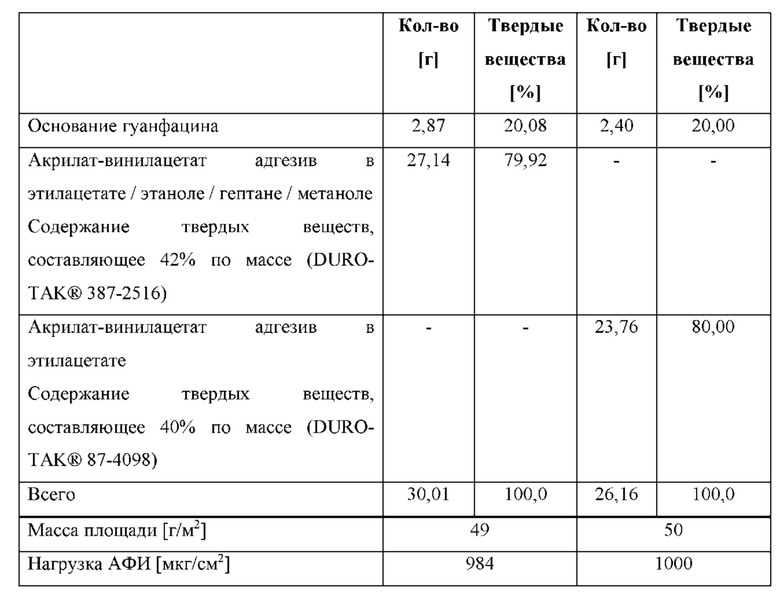
Получение композиции для покрытия
[0304] Активный фармацевтический ингредиент диспергировали в растворителе этилацетате и обрабатывали ультразвуком в течение приблизительно 5 мин. Затем добавляли адгезивы. Указанные две стадии также можно проводить в обратном порядке. С помощью мешалки для растворения смесь гомогенизировали при 500-800 об/мин в течение приблизительно 10 минут.
В случае сравнительного примера 2а активный фармацевтический ингредиент диспергировали непосредственно в адгезиве. Смесь перемешивали при 500 об/мин в течение приблизительно 10 минут.
Нанесение композиции для покрытия
[0305] См. пример 1a-d в отношении процесса нанесения покрытия. Для сравнительного примера 2b композицию для покрытия наносили на 100 мкм PET пленку. Толщина покрытия давала массу площади гуанфацин-содержащего слоя, составляющую 49 (сравнительный пример 2а) и 50 (сравнительный пример 2b) г/м2. Высушенную пленку ламинировали с помощью подложки (PET, 15 мкм, прозрачный) для получения гуанфацин-содержащей самоклеящейся слоистой структуры.
Получение TTS
[0306] См. пример 1.
Измерение проницаемости кожи
[0307] Проникшее количество TTS, полученной согласно сравнительному примеру 2а-b, определяли с помощью экспериментов в соответствии с руководством OECD (принятым 13 апреля 2004 г.) проводили с помощью 10,0 мл диффузионной ячейки Франца. Использовали разделенную по толщине кожу геттингенской карликовой свиньи (самка). Дерматом использовали для получения кожи толщиной, составляющей 800 мкм, с неповрежденным эпидермисом для всех TTS. Отрезки с площадью высвобождения, составляющей 1,165 см2, получали штампованием из TTS. Измеряли проникшее количество гуанфацина в рецепторной среде диффузионной ячейки Франца (фосфатный буферный раствор рН 5,5 с 0,1% азидом натрия в качестве антибактериологического агента) при температуре, составляющей 32±1°С и рассчитывали соответствующее кумулятивное проникшее количество.
[0308] Результаты показаны в таблице 5.2 и на фиг. 4.
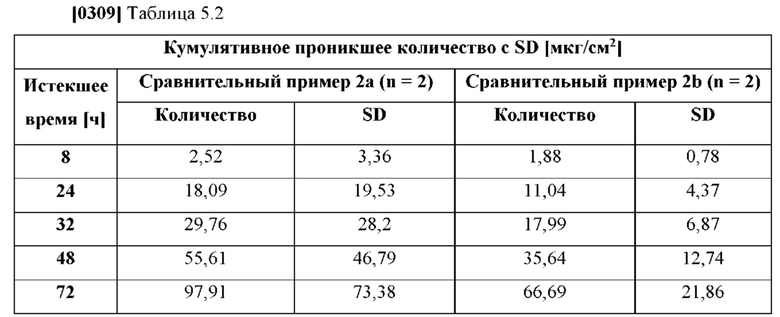
Настоящее изобретение относится, в частности, к следующим дополнительным пунктам:
1. Трансдермальная терапевтическая система для трансдермального введения гуанфацина, содержащая гуанфацин-содержащую слоистую структуру, причем указанная гуанфацин-содержащая слоистая структура содержит следующее:
A) подложка; и
B) гуанфацин-содержащий слой;
где трансдермальная терапевтическая система содержит по меньшей мере один силиконовый полимер.
2. Трансдермальная терапевтическая система по п. 1,
где гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, содержащий следующее:
i) гуанфацин; и
ii) по меньшей мере один силиконовый полимер.
3. Трансдермальная терапевтическая система по любому из пп. 1 или 2, где гуанфацин-содержащая слоистая структура является самоклеящейся и предпочтительно не содержит дополнительный контактирующий с кожей слой.
4. Трансдермальная терапевтическая система по любому из пп. 1-3, где по меньшей мере один силиконовый полимер представляет собой силиконовый приклеивающийся при надавливании адгезив.
5. Трансдермальная терапевтическая система по любому из пп. 1-4, где гуанфацин-содержащая слоистая структура содержит терапевтически эффективное количество гуанфацина.
6. Трансдермальная терапевтическая система по любому из пп. 1-5, где гуанфацин в гуанфацин-содержащей слоистой структуре присутствует в форме свободного основания, которое предпочтительно диспергировано в гуанфацин-содержащем слое.
7. Трансдермальная терапевтическая система по любому из пп. 1-6, где гуанфацин-содержащая слоистая структура содержит гуанфацин в количестве 1-100 мг/TTS, предпочтительно 8-72 мг/TTS.
8. Трансдермальная терапевтическая система по любому из пп. 1-7, где гуанфацин-содержащий слой содержит гуанфацин в количестве 1-20%, более предпочтительно 3-16% по массе в расчете на общую массу гуанфацин-содержащего слоя.
9. Трансдермальная терапевтическая система по любому из пп. 1-8, где гуанфацин-содержащий слой содержит по меньшей мере один силиконовый полимер в количестве 20-99%, предпочтительно 30-97%, наиболее предпочтительно 35-90% по массе в расчете на общую массу гуанфацин-содержащего слоя.
10. Трансдермальная терапевтическая система по любому из пп. 1-9, где по меньшей мере один силиконовый полимер можно получить с помощью поликонденсации полидиметилсилоксана с блокированной концевой силанольной группой и силикатной смолы.
11. Трансдермальная терапевтическая система по пункту 10, где остаточную силанольную функциональную группу по меньшей мере одного силиконового полимера блокируют с помощью триметилсилоксигрупп.
12. Трансдермальная терапевтическая система по любому из пп. 1-11, где гуанфацин-содержащий слой содержит по меньшей мере один дополнительный полимер, выбранный из группы, состоящей из следующего: акрилатные полимеры, силикон-акриловые гибридные полимеры, полиизобутилены и блок-сополимеры стирола-изопрена-стирола, предпочтительно выбранный из группы, состоящей из акрилатных полимеров и силикон-акриловых гибридных полимеров.
13. Трансдермальная терапевтическая система по любому из пп. 1-12, где гуанфацин-содержащий слой содержит первый полимер, который представляет собой силиконовый полимер, в количестве 35-70% по массе, и второй полимер, который выбран из группы, состоящей из следующего: силиконовые полимеры, акрилатные полимеры и силикон-акриловые гибридные полимеры, в количестве 15-45% по массе, в каждом случае в расчете на общую массу гуанфацин-содержащего слоя.
14. Трансдермальная терапевтическая система по любому из пп. 12 или 13, где акрилатный полимер можно получить из одного или нескольких мономеров, выбранных из следующего: акриловая кислота, бутилакрилат, 2-этилгексилакрилат, глицидилметакрилат, 2-гидроксиэтилакрилат, метилакрилат, метилметакрилат, т-октилакриламид и винилацетат, предпочтительно из одного или нескольких мономеров, выбранных из этилгексилакрилата, глицидилметакрилата, 2-гидроксиэтилакрилата и винилацетата.
15. Трансдермальная терапевтическая система по любому из пп. 12-14, где силикон-акриловый гибридный полимер содержит силиконовую фазу и акрилатную фазу в массовом отношении, составляющем от 60:40 до 40:60
16. Трансдермальная терапевтическая система по любому из пп. 12-15, где силикон-акриловый гибридный полимер содержит продукт реакции силиконового полимера, силиконовой смолы и акрилового полимера, где акриловый полимер ковалентно поперечно сшит сам с собой и ковалентно соединен с силиконовым полимером и/или силиконовой смолой.
17. Трансдермальная терапевтическая система по любому из пп. 12-15, где силикон-акриловый гибридный полимер представляет собой силикон-акриловый гибридный приклеивающийся при надавливании адгезив, получаемый из следующего:
(а) кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу.
18. Трансдермальная терапевтическая система по любому из пп. 12-15 или 17, где силикон-акриловый гибридный полимер представляет собой силикон-акриловый гибридный приклеивающийся при надавливании адгезив, содержащий продукт реакции следующего:
(a) кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу;
(b) этиленненасыщенный мономер; и
(c) инициатор.
19. Трансдермальная терапевтическая система по любому из пп. 17 или 18, где кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, содержит продукт реакции конденсации следующего:
(a1) силиконовая смола, и
(а2) силиконовый полимер, и
(а3) кремний-содержащий блокирующий агент, содержащий акрилатную или метакрилатную функциональную группу.
20. Трансдермальная терапевтическая система по любому из пп. 17-19, где кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу, содержит продукт реакции конденсации следующего:
(a1) силиконовая смола, и
(а2) силиконовый полимер, и
(а3) кремний-содержащий блокирующий агент, содержащий акрилатную или метакрилатную функциональную группу, где указанный кремний-содержащий блокирующий агент характеризуется общей формулой XYR'bSiZ3-b, где X представляет собой одновалентный радикал согласно общей формуле АЕ, где Е представляет собой -О- или -NH-, и А представляет собой акриловую группу или метакриловую группу, Y представляет собой двухвалентный алкиленовый радикал, характеризующийся 1-6 атомами углерода, R' представляет собой метильный или фенильный радикал, Z представляет собой одновалентный гидролизуемый органический радикал или галоген, и b составляет 0 или 1;
причем силиконовая смола и силиконовый полимер реагируют с образованием приклеивающегося при надавливании адгезива, причем кремний-содержащий блокирующий агент вводят перед, во время или после реакции силиконовой смолы и силиконового полимера,
и где кремний-содержащий блокирующий агент реагирует с приклеивающимся при надавливании адгезивом после того, как силиконовая смола и силиконовый полимер подверглись реакции конденсации с образованием приклеивающегося при надавливании адгезива, или кремний-содержащий блокирующий агент реагирует in situ с силиконовой смолой и силиконовым полимером.
21. Трансдермальная терапевтическая система по любому из пп. 18-20, где этиленненасыщенный мономер выбран из группы, состоящей из следующего: алифатические акрилаты, алифатические метакрилаты, циклоалифатические акрилаты, циклоалифатические метакрилаты и их комбинации, причем каждое из указанных соединений содержит вплоть до 20 атомов углерода в алкильном радикале, и где этиленненасыщенный мономер представляет собой предпочтительно комбинацию 2-этилгексилакрилата и метилакрилата, особенно предпочтительно в отношении, составляющем от 40:60 до 70:30.
22. Трансдермальная терапевтическая система по любому из пп. 18-21, где продукт реакции следующего:
(a) кремний-содержащая приклеивающаяся при надавливании адгезивная композиция, содержащая акрилатную или метакрилатную функциональную группу;
(b) этиленненасыщенный мономер; и
(c) инициатор,
содержит непрерывную акриловую внешнюю фазу и дискретную силиконовую внутреннюю фазу.
23. Трансдермальная терапевтическая система по любому из пп. 1-22, где гуанфацин-содержащий слой дополнительно содержит по меньшей мере одно вспомогательное вещество, выбранное из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов, или по меньшей мере два вспомогательных вещества, выбранных из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов, предпочтительно так, что присутствует комбинация диспергирующего агента и усилителя проницаемости, или комбинация диспергирующего агента и солюбилизатора, или комбинация усилителя проницаемости и солюбилизатора, или по меньшей мере три вспомогательных вещества, выбранных из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов, предпочтительно так, что присутствует комбинация диспергирующего агента, усилителя проницаемости и солюбилизатора.
24. Трансдермальная терапевтическая система по п. 23, где диспергирующий агент выбран из группы, состоящей из следующего: сложные эфиры жирных кислот с многоатомными спиртами, жирные спирты, полиэтиленгликоли, характеризующиеся среднечисловой молекулярной массой, составляющей 300-400, алкилэфиры полиэтиленгликоля, и где диспергирующий агент представляет собой предпочтительно C8-С20-алкилэфир полиэтиленгликоля, характеризующийся 2-10 звеньями ЕО.
25. Трансдермальная терапевтическая система по п. 23 или 24, где усилитель проницаемости выбран из группы, состоящей из следующего: моноэтиловый эфир диэтиленгликоля (транскутол), олеиновая кислота, левулиновая кислота, триглицериды каприловой/каприновой кислоты, диизопропиладипат, изопропилмиристат, изопропилпальмитат, лауриллактат, триацетин, диметилпропиленмочевина и олеиловый спирт, и предпочтительно представляет собой олеиловый спирт.
26. Трансдермальная терапевтическая система по любому из пп. 23-25, где солюбилизатор выбран из группы, состоящей из следующего: сополимеры, полученные из сложных эфиров акриловой и метакриловой кислоты, поливинилпирролидон, сополимеры винилпирролидона-винилацетата и привитые сополимеры поливинилкапролактама-поливинилацетата-полиэтиленгликоля, и предпочтительно представляет собой привитой сополимер поливинилкапролактама-поливинилацетата-полиэтиленгликоля.
27. Трансдермальная терапевтическая система по любому из пп. 23-26, где по меньшей мере одно вспомогательное вещество присутствует в количестве 0,5-10% по массе или 1-10% по массе в расчете на общую массу гуанфацин-содержащего слоя.
28. Трансдермальная терапевтическая система по любому из пп. 1-27, где площадь высвобождения находится в диапазоне от 1 до 100 см2, предпочтительно от 2,5 до 50 см2; и/или где масса площади гуанфацин-содержащего слоя находится в диапазоне от 40 до 250 г/м2, предпочтительно от 50 до 150 г/м2.
29. Трансдермальная терапевтическая система по любому из пп. 1-28, где нагрузка гуанфацином трансдермальной терапевтической системы находится в диапазоне от 0,2 до 2,4 мг/см2, предпочтительно от 0,2 до 1,5 мг/см2.
30. Трансдермальная терапевтическая система по любому из пп. 1-29, где трансдермальная терапевтическая система обеспечивает с помощью трансдермальной доставки в равновесном состоянии среднюю концентрацию гуанфацина в плазме, составляющую 1-20 нг/мл, предпочтительно 1-15 нг/мл.
31. Трансдермальная терапевтическая система по любому из пп. 1-30, обеспечивающая скорость чрескожного проникновения гуанфацина, как измерено в диффузионной ячейке Франца с помощью дерматомированной кожи человека, составляющую:
0,01 мкг/(см2*ч) - 8 мкг/(см2*ч) в первые 24 часа,
0,05 мкг/(см2*ч) - 10 мкг/(см2*ч) от 24 до 72 часов.
32. Трансдермальная терапевтическая система по любому из пп. 1-31, обеспечивающая кумулятивное проникшее количество гуанфацина, как измерено в диффузионной ячейке Франца с помощью дерматомированной кожи человека, составляющее 0,05 мг/см2 - 0,7 мг/см2, предпочтительно 0,1-0,6 мг/см2 в течение периода времени, составляющего 72 часа.
33. Трансдермальная терапевтическая система по любому из пп. 1-32 для применения в способе лечения пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет.
34. Трансдермальная терапевтическая система по любому из пп. 1-32 для применения в способе лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) и/или в качестве дополнительной терапии к лекарственным средствам-стимуляторам у пациента-человека, предпочтительно у пациента-человека в возрасте, составляющем 6-17 лет.
35. Трансдермальная терапевтическая система для применения по любому из пп. 33 или 34, причем трансдермальную терапевтическую систему наносят на кожу пациента в течение по меньшей мере 24 часов, предпочтительно по меньшей мере 72 часов, более предпочтительно приблизительно 84 часов.
36. Способ лечения пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем нанесения трансдермальной терапевтической системы, как определено в одном из пп. 1-32, на кожу пациента.
37. Способ лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) у пациента-человека, предпочтительно пациента-человека в возрасте, составляющем 6-17 лет, путем нанесения трансдермальной терапевтической системы, как определено в одном из пп. 1-32, на кожу пациента.
38. Способ лечения пациента-человека по любому из пп. 36 или 37, при котором трансдермальную терапевтическую систему наносят на кожу пациента в течение по меньшей мере 24 часов, предпочтительно по меньшей мере 72 часов, более предпочтительно приблизительно 84 часов.
39. Способ получения гуанфацин-содержащего слоя для применения в трансдермальной терапевтической системе по любому из пп. 1-32, предусматривающий следующие стадии:
1) объединение по меньшей мере следующих компонентов:
i) гуанфацин;
ii) по меньшей мере один силиконовый полимер; и для получения композиции для покрытия;
2) нанесение композиции для покрытия на подложку или защитное покрытие для получения нанесенной композиции для покрытия; и
3) сушка нанесенной композиции для покрытия с образованием гуанфацин-содержащего слоя.
40. Способ получения гуанфацин-содержащего слоя по п. 39, при котором силиконовый полимер предусмотрен в виде раствора, причем растворитель представляет собой этилацетат или н-гептан.
41. Трансдермальная терапевтическая система, получаемая с помощью способа согласно одному из пп. 40 или 41.
42. Трансдермальная терапевтическая система для трансдермального введения гуанфацина, содержащая гуанфацин-содержащую слоистую структуру, причем указанная гуанфацин-содержащая слоистая структура содержит следующее:
A) подложка; и
B) гуанфацин-содержащий слой, предпочтительно гуанфацин-содержащий матричный слой, содержащий следующее:
i) гуанфацин в количестве 3-13% по массе в расчете на общую массу гуанфацин-содержащего слоя;
ii) по меньшей мере один силиконовый полимер в количестве 35-90% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iii) по меньшей мере один диспергирующий агент в количестве 2-6% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iv) по меньшей мере один усилитель проницаемости в количестве 2-10% по массе в расчете на общую массу гуанфацин-содержащего слоя; и
v) необязательно по меньшей мере один солюбилизатор в количестве 0,5-4% по массе в расчете на общую массу гуанфацин-содержащего слоя.
43. Трансдермальная терапевтическая система по п. 42, где гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, который содержит следующее:
i) гуанфацин в количестве 3-13% по массе в расчете на общую массу гуанфацин-содержащего слоя;
ii) по меньшей мере один силиконовый полимер в количестве 35-90% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iii) C8-С20-алкилэфир полиэтиленгликоля, характеризующийся 2-10 звеньями ЕО, в количестве 2-6% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iv) олеиловый спирт в количестве 2-10% по массе в расчете на общую массу гуанфацин-содержащего слоя; и
v) необязательно привитой сополимер поливинилкапролактама-поливинилацетата-полиэтиленгликоля в количестве 0,5-4% по массе в расчете на общую массу гуанфацин-содержащего слоя.
44. Трансдермальная терапевтическая система по п. 42 или 43, где гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, который содержит следующее:
i) гуанфацин в количестве 3-13% по массе в расчете на общую массу гуанфацин-содержащего слоя;
ii) первый силиконовый полимер в количестве 50-70% по массе в расчете на общую массу гуанфацин-содержащего слоя, и второй силиконовый полимер в количестве 15-25% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iii) С8-C20-алкилэфир полиэтиленгликоля, характеризующийся 2-10 звеньями ЕО, предпочтительно лауриловый эфир полиоксиэтилена (4), в количестве 3-5% по массе в расчете на общую массу гуанфацин-содержащего слоя;
iv) олеиловый спирт в количестве 5-9% по массе в расчете на общую массу гуанфацин-содержащего слоя; и
v) необязательно привитой сополимер поливинилкапролактама-поливинилацетата-полиэтиленгликоля в количестве 0,5-3% по массе в расчете на общую массу гуанфацин-содержащего слоя.
45. Трансдермальная терапевтическая система по любому из пп. 42-44, где масса площади гуанфацин-содержащего слоя находится в диапазоне от 80 до 120 г/м2, предпочтительно от 90 до 120 г/м2.
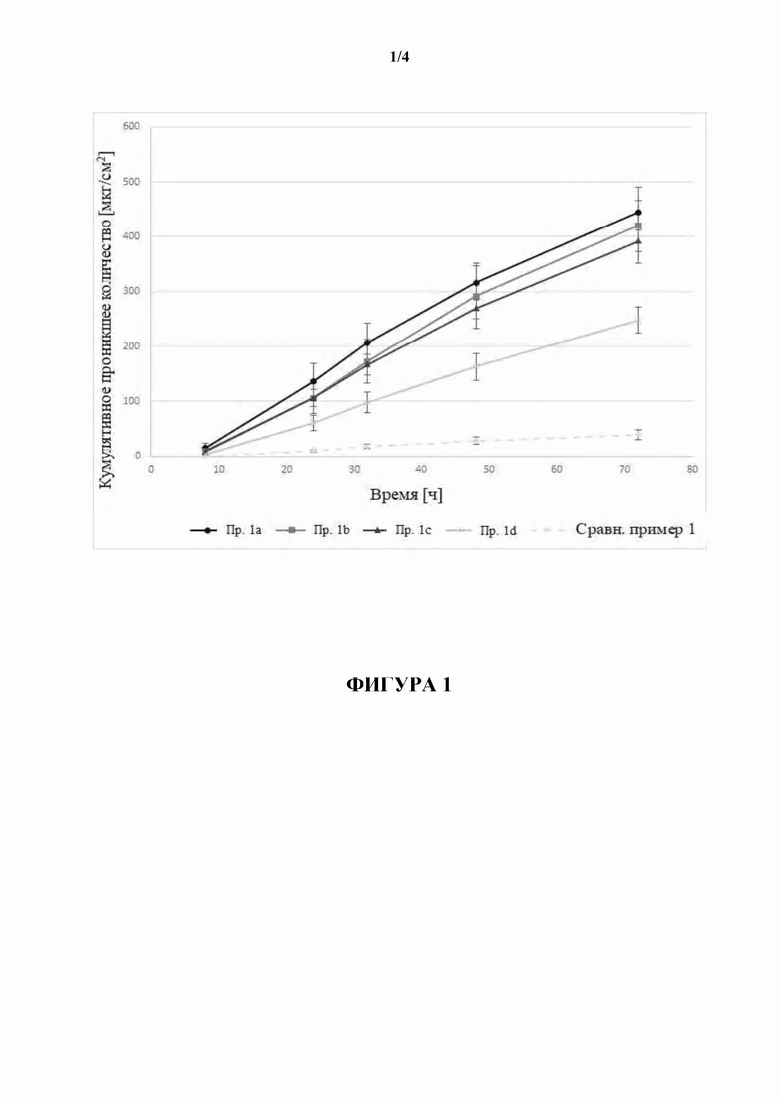
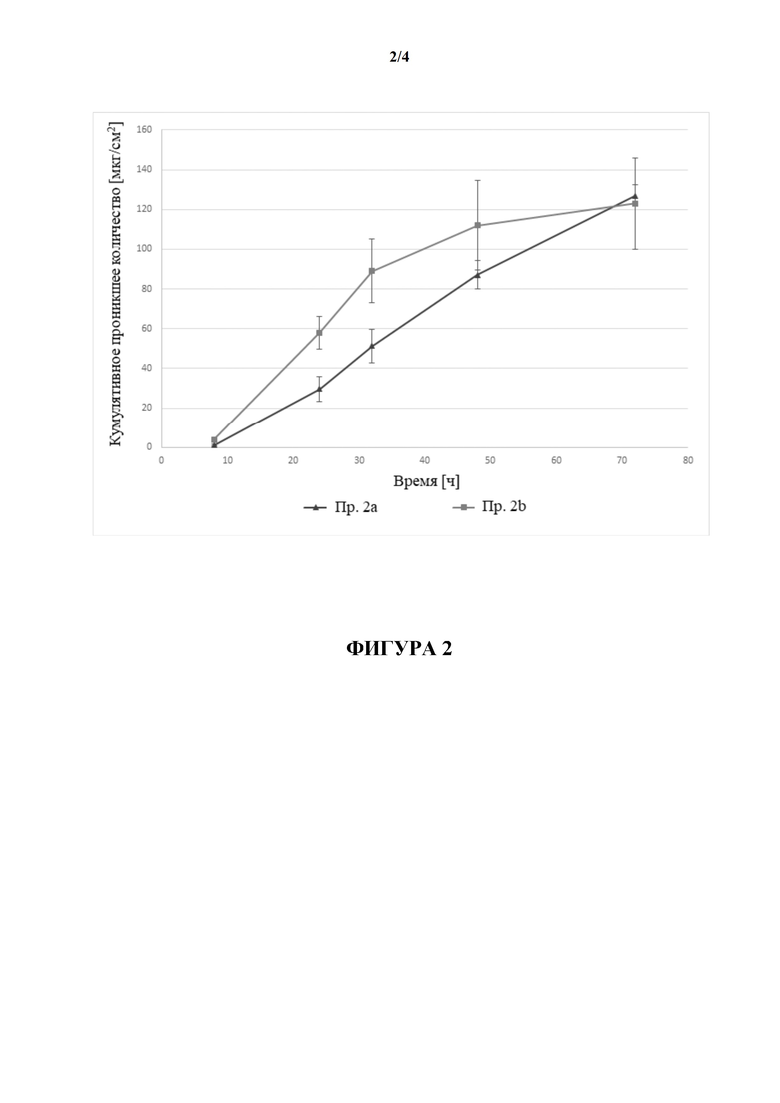
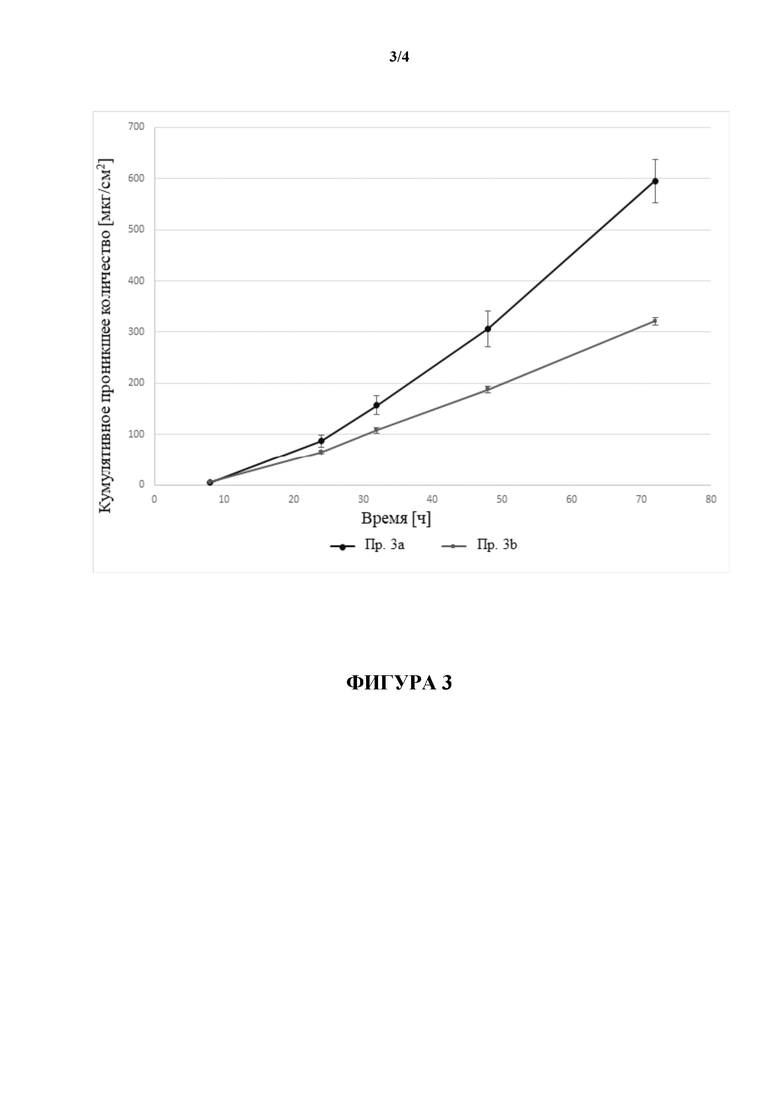
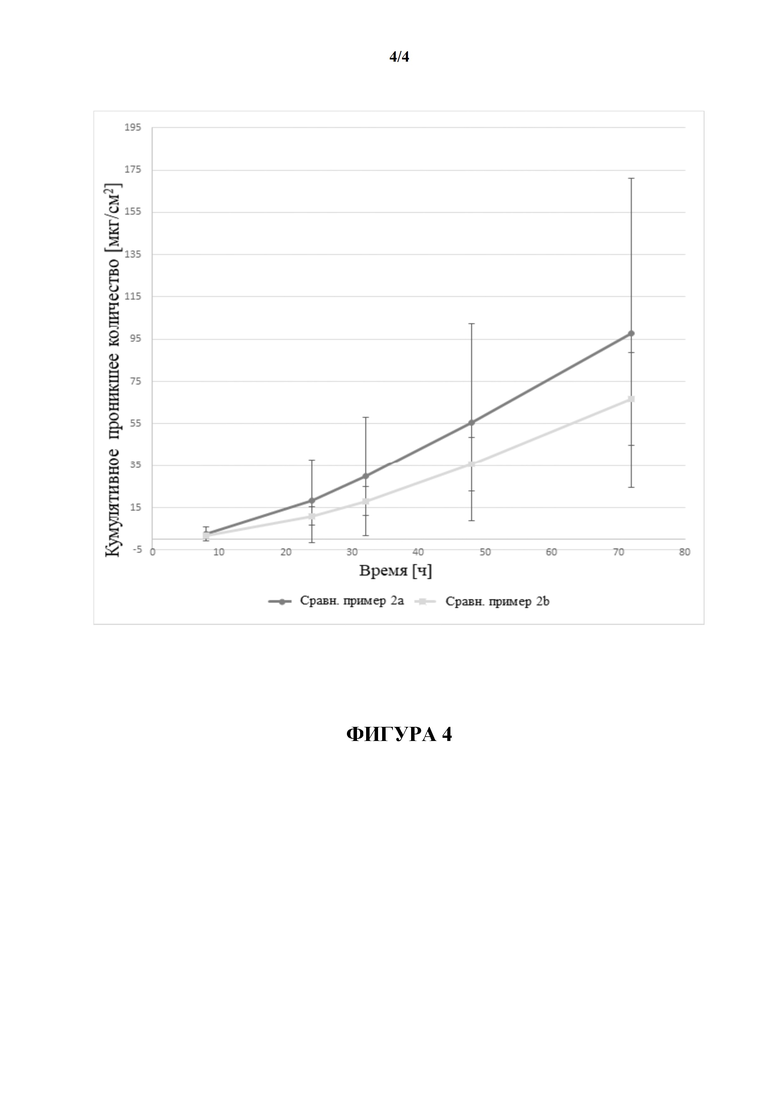
Группа изобретений относится к области медицины и описывает трансдермальную терапевтическую систему (TTS) для трансдермального введения гуанфацина, содержащую гуанфацин-содержащую слоистую структуру, причем указанная гуанфацин-содержащая слоистая структура содержит: A) подложку; и B) гуанфацин-содержащий слой; причем тpансдермальная терапевтическая система содержит по меньшей мере один силиконовый полимер; где гуанфацин-содержащий слой содержит по меньшей мере один силиконовый полимер в количестве 30 - 97%; и где гуанфацин-содержащий слой дополнительно содержит по меньшей мере два вспомогательных вещества, выбранных из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов, где каждое из по меньшей мере двух вспомогательных веществ присутствует в количестве 0,5 - 10% по массе в расчете на общую массу гуанфацин-содержащего слоя. Также группа изобретений раскрывает применение трансдермальной терапевтической системы в способе лечения пациента-человека в возрасте, составляющем 6 - 17 лет и применение трансдермальной терапевтической системы по любому в способе лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) и/или в качестве дополнительной терапии к лекарственным средствам-стимуляторам y пациента-человека в возрасте, составляющем 6 - 17 лет. Технический результат заключается в повышении эффективности трансдермальной терапевтической системы (TTS) для трансдермального введения гуанфацина. 3 н. и 13 з.п. ф-лы, 13 табл., 4 ил., 6 пр.
1. Трансдермальная терапевтическая система (TTS) для трансдермального введения гуанфацина, содержащая гуанфацин-содержащую слоистую структуру, причем указанная гуанфацин-содержащая слоистая структура содержит:
A) подложку; и
B) гуанфацин-содержащий слой;
причем трансдермальная терапевтическая система содержит по меньшей мере один силиконовый полимер;
где гуанфацин-содержащий слой содержит по меньшей мере один силиконовый полимер в количестве 30 - 97%;
и где гуанфацин-содержащий слой дополнительно содержит по меньшей мере два вспомогательных вещества, выбранных из группы, состоящей из диспергирующих агентов, усилителей проницаемости и солюбилизаторов, где каждое из по меньшей мере двух вспомогательных веществ присутствует в количестве 0,5 - 10% по массе в расчете на общую массу гуанфацин-содержащего слоя.
2. Трансдермальная терапевтическая система по п. 1,
где гуанфацин-содержащий слой представляет собой гуанфацин-содержащий матричный слой, содержащий:
i) гуанфацин; и
ii) по меньшей мере один силиконовый полимер.
3. Трансдермальная терапевтическая система по любому из пп. 1 или 2,
где гуанфацин-содержащая слоистая структура является самоклеящейся и предпочтительно не содержит дополнительный контактирующий c кожей слой.
4. Трансдермальная терапевтическая система по любому из пп. 1 - 3,
где гуанфацин в гуанфацин-содержащей слоистой структуре находится в форме свободного основания, которое предпочтительно диспергировано в гуанфацин-содержащем слое, и/или
где гуанфацин-содержащая слоистая структура содержит гуанфацин в количестве 1 - 75 мг/TTS, предпочтительно 3 - 30 мг/TTS.
5. Трансдермальная терапевтическая система по любому из пп. 1 - 4,
где гуанфацин-содержащий слой содержит гуанфацин в количестве 1 - 20%, более предпочтительно 3 - 16% по массе в расчете на общую массу гуанфацин-содержащего слоя.
6. Трансдермальная терапевтическая система по любому из пп. 1 - 5,
где гуанфацин-содержащий слой содержит по меньшей мере один силиконовый полимер в количестве 35 - 90% по массе в расчете на общую массу гуанфацин-содержащего слоя.
7. Трансдермальная терапевтическая система по любому из пп. 1 - 6,
где по меньшей мере один силиконовый полимер можно получить c помощью поликонденсации полидиметилсилоксана c блокированной концевой силанольной группой и силикатной смолы.
8. Трансдермальная терапевтическая система по любому из пп. 1 - 7,
где гуанфацин-содержащий слой содержит первый полимер, который представляет собой силиконовый полимер в количестве 35 - 70% по массе, и второй полимер, который выбран из группы, состоящей из: силиконовых полимеров, акрилатных полимеров и силикон-акриловых гибридных полимеров в количестве 15 - 45% по массе, в каждом случае в расчете на общую массу гуанфацин-содержащего слоя.
9. Трансдермальная терапевтическая система по любому из пп. 1-8, где диспергирующий агент выбран из группы, состоящей из: сложные эфиры жирны кислот c многоатомными спиртами, жирные спирты, полиэтиленгликоли, характеризующиеся среднечисловой молекулярной массой 300 - 400, алкилэфиры полиэтиленгликоля, и где диспергирующий агент представляет собой предпочтительно С8-С20-алкилэфир полиэтиленгликоля, характеризующийся 2 - 10 звеньями ЕО.
10. Трансдермальная терапевтическая система по любому из пп. 1-9, где усилитель проницаемости выбран из группы, состоящей из: моноэтиловый эфир диэтиленгликоля (транскутол), олеиновая кислота, левулиновая кислота, триглицериды каприловой/каприновой кислоты, диизопропиладипат, изопропилмиристат, изопропилпальмитат, лауриллактат, триацетин, диметилпропиленмочевина и олеиловый спирт, и предпочтительно представляет собой олеиловый спирт.
11. Трансдермальная терапевтическая система по любому из пп. 1 - 10, где солюбилизатор выбран из группы, состоящей из: сополимеры, полученные из сложны эфиров акриловой и метакриловой кислоты, поливинилпирролидон, сополимеры винилпирролидона-винилацетата и привитые сополимеры поливинилкапролактама-поливинилацетата-полиэтиленгликоля, и предпочтительно представляет собой привитой сополимер поливинилкапролактама-поливинилацетата-полиэтиленгликоля.
12. Трансдермальная терапевтическая система по любому из пп. 1 - 11, где каждое из по меньшей мере двух вспомогательных веществ присутствует в количестве 1 - 10% по массе в расчете на общую массу гуанфацин-содержащего слоя.
13. Трансдермальная терапевтическая система по любому из пп. 1 - 12,
где масса площади гуанфацин-содержащего слоя находится в диапазоне от 40 до 250 г/м2, предпочтительно от 50 до 150 г/м2; и/или
где площадь высвобождения находится в диапазоне от 1 до 100 см2, предпочтительно от 2,5 до 50 см2.
14. Применение трансдермальной терапевтической системы по любому из пп. 1 - 13 в способе лечения пациента-человека в возрасте, составляющем 6 - 17 лет.
15. Применение трансдермальной терапевтической системы по любому из пп. 1 - 13 в способе лечения гипертензии или синдрома дефицита внимания с гиперактивностью (ADHD) и/или в качестве дополнительной терапии к лекарственным средствам-стимуляторам y пациента-человека в возрасте, составляющем 6 - 17 лет.
16. Применение по любому из пп. 14 или 15, причем трансдермальная терапевтическая система наносится на кожу пациента на по меньшей мере 24 часа или по меньшей мере 72 часа или приблизительно 84 часа.
| US 2015342899 A1, 03.12.2015 | |||
| JOSEPHINE ELIA et al., "Methylphenidate transdermal system: clinical applications for attention-deficit/ hyperactivity disorder" | |||
| Expert Rev | |||
| Clin | |||
| Pharmacol | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ приготовления массы для карандашей | 1921 |
|
SU311A1 |
| GABRIEL KAPLANMD, et al., "Pharmacotherapy for Child and Adolescent Attention-deficit Hyperactivity Disorder" | |||
| Pediatric Clinics of | |||
Авторы
Даты
2023-03-24—Публикация
2018-10-11—Подача