Настоящее изобретение относится к полипептидам, содержащим фрагмент инвариантной цепи из костистой рыбы, необязательно, слитый с одним или несколькими антигенами, или инвариантную цепь из костистой рыбы, слитую с одним или несколькими антигенами или их антигенными фрагментами, к полинуклеотиду, кодирующему такие полипептиды, векторам, содержащим такие полинуклеотиды, группе векторов, содержащих такие полинуклеотиды, и к применению таких полипептидов, полинуклеотидов, векторов для лечения или предупреждения заболеваний, в частности, опухолевых заболеваний. Полипептиды инвариантной цепи костистой рыбы или их фрагменты действуют как «энхансер Т-клеточного ответа», превращающий неиммуногенные антигенные последовательности в иммуногенные Т-клеточные антигены.
Предшествующий уровень техники настоящего изобретения
Иногда вакцины вызывают субоптимальный Т-клеточный иммунный ответ или не вызывают его. Это явление слабой индукции Т-клеточного иммунного ответа чаще наблюдают в случае вакцинаций, нацеленных на антигены, которые представляют собой либо полностью аутологичные молекулы, например, специфические для злокачественных опухолей антигены, либо частично аутологичные, например, специфические для злокачественных опухолей неоантигены. Специфические для злокачественных опухолей неоантигены преимущественно являются результатом точковых мутаций в кодирующих участках генов, которые дают в результате несинонимичные однонуклеотидные варианты, приводящие в результате к изменению одной аминокислоты. Изменение одной аминокислоты в последовательности белка очень редко создает новый эпитоп, способный индуцировать сильный иммунный ответ. В большинстве случаев это небольшое изменение либо совсем не создает новый эпитоп, либо оно может создавать очень слабый эпитоп. Вследствие существующей центральной толерантности к аутоантигенам индукция сильных иммунных ответов в отношении специфических для злокачественных опухолей антигенов при вакцинации остается сложной задачей. Чтобы преодолеть отсутствие иммуногенности или слабую иммуногенность специфических для злокачественных опухолей антигенов и неоантигенов, использовали несколько стратегий для устранения отсутствия иммуногенности/слабой иммуногенности некоторых генетических вакцин. Было показано, что инвариантная цепь (INV) усиливает индукцию CD8+ Т-клеток в условиях генетической вакцинации. Инвариантная цепь представляет собой белок-шаперон молекул главного комплекса гистосовместимости (МНС) II класса, требующийся для их созревания и сборки.
INV также играет роль в презентировании антигенных пептидов и, как было продемонстрировано, повышает индукцию Т-клеток в случае, когда она слита с антигеном, в условиях генетической вакцинации. Была описана улучшенная способность к иммунизации при использовании лентивирусного вектора, экспрессирующего овальбумин, слитый с INV (Rowe et al 2006 Mol Ther 13(2) 310-9). В дальнейшем различные сообщения документально подтвердили усиленную индукцию CD8+ Т-клеточных ответов векторами на основе аденовируса 5 человека и плазмидной ДНК, экспрессирующими слитые с INV антигены.
При противораковой вакцинации важно избежать ускользания опухоли от воздействия иммунной системы вследствие появления новых специфических для злокачественных опухолей антигенов, не распознаваемых индуцированными вакциной Т-клетками. Трудность в излечении рака в случае противораковой вакцины заключается в индукции разнообразной популяции иммунных Т-клеток, способных к распознаванию и уничтожению максимально возможного числа раковых клеток сразу, чтобы уменьшить вероятность того, что раковые клетки могут «ускользнуть» от Т-клеточного ответа. Таким образом, желательно, чтобы вакцина кодировала достаточно большое количество специфических для злокачественных опухолей антигенов. Это особенно уместно в случае недавно описанного персонализированного подхода к созданию вакцин на основе специфических для злокачественных опухолей неоантигенов. Для того чтобы оптимизировать вероятность успешного исхода, вакцина должна быть нацелена на как можно большее число неоантигенов, тем не менее, максимальный размер вставки в векторы ограничен. Последовательности полноразмерных INV или их крупные фрагменты занимают относительно большую часть вставки с вакцинным антигеном. Следовательно, применение короткого полипептида в качестве энхансера Т-клеточного ответа является предпочтительным в условиях противораковой вакцинации, в особенности, при применении нескольких специфических для злокачественных опухолей антигенов в вакцине.
Было показано, что платформы для генетической вакцинации на основе аденовируса, в частности, вирусный вектор на основе аденовируса высших приматов (GAd), являются очень эффективными в отношении индукции Т-клеточных ответов, и аденовирусы высших приматов являются подходящими для кодирования крупных антигенов в формате искусственных генов, состоящих из полинуклеотидов, которые кодируют фрагменты из различных белков, соединенных один за другим (Borthwick, N., et al., Mol Ther, 2014. 22(2): p. 464-75). Неожиданно, при применении в отношении специфических для злокачественных опухолей неоантигенов опосредуемый Т-клетками иммунный ответ не индуцировался.
Авторы настоящего изобретения идентифицировали специфические последовательности INV, способные восстанавливать иммуногенность, которые в данной заявке также называются «аминокислотной последовательностью энхансера Т-клеточных ответов». Такие аминокислотные последовательности энхансера Т-клеточных ответов являлись подходящими в преодолении отсутствия иммуногенности или слабой иммуногенности специфических для злокачественных опухолей неоантигенов. В частности, идентифицировали два коротких фрагмента отличных от человеческих INV из представителей Teleostei, причем оба из них не включали в себя трансмембранный домен, и при этом они действовали как эффективные энхансеры Т-клеточных ответов.
Применение человеческих INV или INV филогенетически близкородственных видов может приводить в результате к нежелательной индукции иммунного ответа против этой аутологичной последовательности в условиях вакцинации. В этом случае аутоиммунная реакция будет направлена на нормальные ткани, в которых экспрессируется INV. Авторы настоящего изобретения неожиданно обнаружили, что INV костистых рыб, несмотря на то что они достаточно отличаются от INV млекопитающих, повышают Т-клеточный ответ на антигены у млекопитающих, то есть эффект усиления Т-клеточного ответа проявляется в отношении нескольких антигенов, слитых с инвариантной цепью костистой рыбы, и что даже короткого фрагмента INV костистых рыб достаточно для того, чтобы вызвать этот ответ. Таким образом, настоящее изобретение обеспечивает среди прочего: (i) улучшенный энхансер Т-клеточного ответа на антигены у млекопитающих с уменьшенной вероятностью того, что он вызывает нежелательные Т-клеточные ответы в отношении здоровой ткани, (ii) энхансер Т-клеточного ответа на несколько антигенов, и (iii) короткий фрагмент, способный вызывать образование Т-клеток, что максимально повышает способность к слиянию с большим количеством антигенов или их антигенных фрагментов.
Краткое раскрытие настоящего изобретения
В соответствии с первым аспектом настоящее изобретение относится к полипептиду, содержащему:
(а) фрагмент инвариантной цепи (INV) из представителя Teleostei, который имеет активность энхансера Т-клеточного ответа, содержащий или состоящий из 16-27 аминокислот проксимального по отношению к мембране домена (MPD) INV из представителя Teleostei, причем MPD предпочтительно характеризуется следующей аминокислотной последовательностью:
X1 QKX2 QIHTLQKX3 SX4 RX5 X6 X7 QX8 TRX9 SX10 AV,
в которой
X1 представляет собой G, D, S или N;
X2 представляет собой E или Q;
Х3 представляет собой N или S;
Х4 представляет собой D или Е;
Х5 представляет собой М или L;
Х6 представляет собой G, N, S или Т;
Х7 представляет собой K или R;
Х8 представляет собой L или М;
Х9 представляет собой S, Т или А; и
Х10 представляет собой Q или Н;
и при этом 16-27 аминокислот MPD предпочтительно являются по меньшей мере на 70% идентичными SEQ ID NO: 7;
и, необязательно, один или несколько антигенов или их антигенных фрагментов; или
(b) полноразмерную INV из представителя Teleostei с SEQ ID NO: 1 или ее вариант, которые характеризуются активностью энхансера Т-клеточного ответа, причем аминокислотная последовательность MPD у варианта является по меньшей мере на 80% идентичной SEQ ID NO: 7, и один или несколько антигенов или их антигенных фрагментов.
В соответствии со вторым аспектом настоящее изобретение относится к полинуклеотиду, кодирующему полипептид согласно первому аспекту настоящего изобретения.
В соответствии с третьим аспектом настоящее изобретение относится к вектору, содержащему полинуклеотид согласно второму аспекту настоящего изобретения.
В соответствии с четвертым аспектом настоящее изобретение относится к группе из двух или более отличающихся векторов, причем каждый из отличающихся векторов содержит полинуклеотид согласно второму аспекту настоящего изобретения, кодирующий отличающийся полипептид согласно первому аспекту настоящего изобретения.
В соответствии с пятым аспектом настоящее изобретение относится к фармацевтической композиции, содержащей полипептид согласно первому аспекту настоящего изобретения, полинуклеотид согласно второму аспекту настоящего изобретения, или вектор согласно третьему аспекту настоящего изобретения, или группу векторов согласно четвертому аспекту настоящего изобретения и фармацевтически приемлемое вспомогательное вещество и, необязательно, один или несколько адъювантов.
В соответствии с шестым аспектом настоящее изобретение относится к набору, содержащему фармацевтическую композицию согласно пятому аспекту настоящего изобретения и отдельно упакованный по меньшей мере один иммуномодулятор, например, модулятор молекулы-контрольной точки (МСМ), или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, например, МСМ, или вектор, содержащий полинуклеотид, который кодирует иммуномодулятор, например, МСМ.
В соответствии с седьмым аспектом настоящее изобретение относится к полипептиду согласно первому аспекту настоящего изобретения, полинуклеотиду согласно второму аспекту настоящего изобретения или к вектору или группе векторов согласно третьему или четвертому аспекту настоящего изобретения для применения в качестве лекарственного препарата.
В соответствии с восьмым аспектом настоящее изобретение относится к полипептиду согласно первому аспекту настоящего изобретения, полинуклеотиду согласно второму аспекту настоящего изобретения, или к вектору или группе векторов согласно третьему или четвертому аспекту настоящего изобретения, или к фармацевтической композиции согласно пятому аспекту настоящего изобретения, или к наборам, содержащим такие фармацевтические композиции, согласно шестому аспекту настоящего изобретения для применения в предупреждении или лечении пролиферативного заболевания, предпочтительно, рака, вирусного заболевания или бактериального заболевания.
Краткое описание чертежей
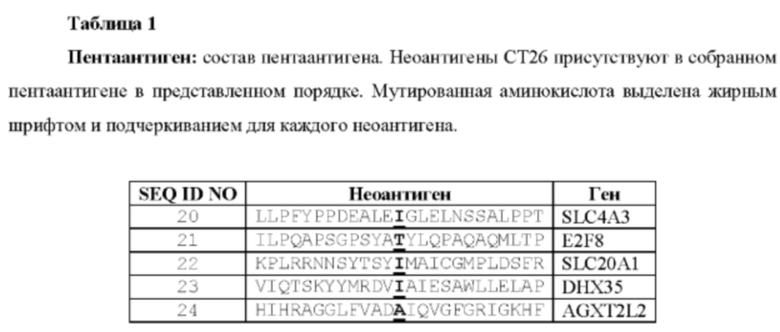
Фиг. 1. Иммуногенность векторов на основе GAd в дозах 5×107 vp (вирусных частиц) или 5×108vp. Векторы кодируют полноразмерную INV китайского окуня (MF_INV_FL), короткий вариант INV китайского окуня (остатки 1-81, MF_INV_SH), варианты А (остатки 62-88, MF_INV_А) и В (остатки 66-81, MF_INV_В) INV китайского окуня, связанные с пентатопным антигеном СТ26. Penta представляет пентатопный антиген СТ26 без последовательности INV китайского окуня или ее фрагмента, а только с начальным метионином. Представленные значения были получены с помощью анализа методом ELISpot на клетках селезенки из иммунизированных животных. Спленоциты стимулировали ex vivo через две недели после вакцинации пулом из пяти синтетических пептидов, соответствующих последовательностям пяти специфических для злокачественных опухолей неоантигенов, которые содержат мутацию. Ответы выражены в виде количества Т-клеток, продуцирующих IFNγ, на миллион спленоцитов. Снизу представлено количество мышей, демонстрирующих положительный ответ, из общего числа 6 иммунизированных мышей для каждой исследуемой векторной конструкции. Пунктирной линией показано пороговое значение для положительного ответа.
Фиг. 2. Выравнивание инвариантных цепей из различных видов Teleostei. Первая рамка характеризует 26-аминокислотный трансмембранный домен (TMD). Проксимальный по отношению к мембране домен (MPD) находится непосредственно возле TMD со стороны С-конца и выделен второй рамкой. Расположение и протяженность короткого 16-аминокислотного фрагмента MF_INV_В длинной инвариантной цепи, содержащегося в MPD, выделено рядом звездочек (*) под второй рамкой. Последовательности INV представлены сверху вниз в виде аминокислотных последовательностей, соответствующих SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: SEQ ID NO: 1 и SEQ ID NO: 2.
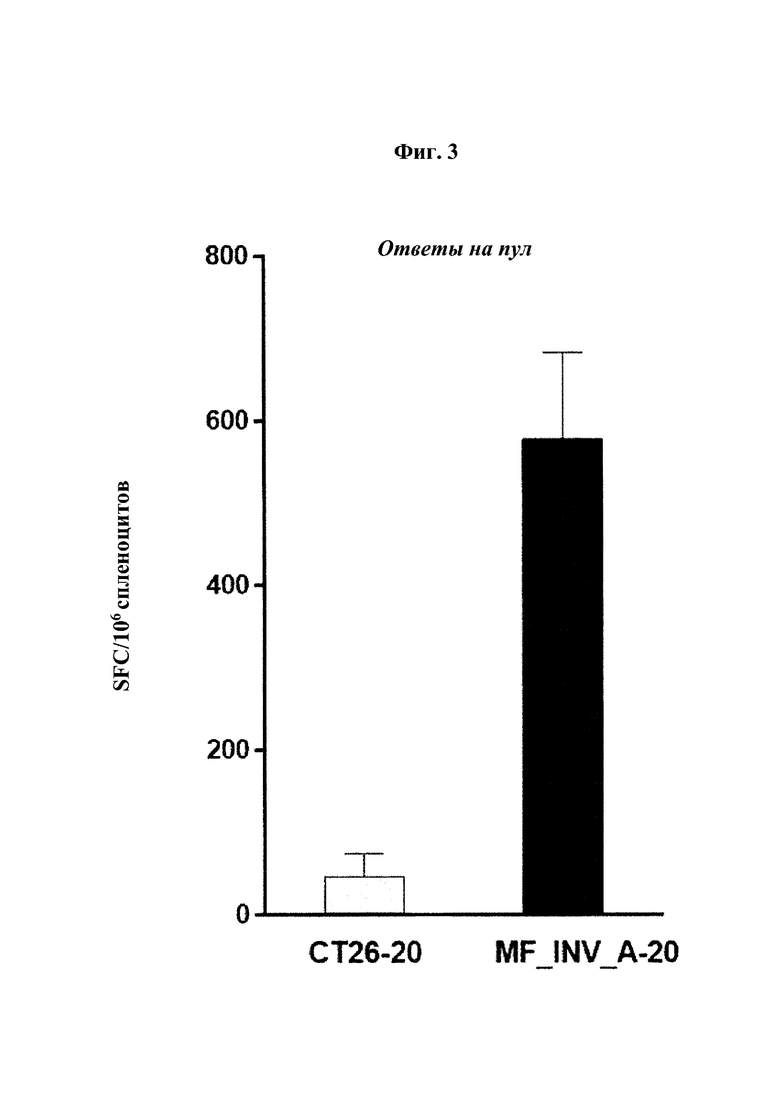
Фиг. 3. Иммуногенность векторов на основе GAd, кодирующих двадцать неоантигенов СТ26. Мышей иммунизировали 5×107 каждого вектора на основе GAd (MF_INV_A-20, включающий в себя FRAG_A инвариантной цепи MF, без СТ26-20) и спустя 2 недели иммунные ответы измеряли с помощью анализа методом ELISpot на клетках селезенки. Показаны ответы (количество Т-клеток, продуцирующих IFNγ, на миллионы спленоцитов) на пул из 20 синтетических пептидов, соответствующих последовательностям 20 кодируемых неоантигенов. Значения представлены в виде среднего значения +/-SEM от измерений, выполненных на 6 мышах/группа.
Подробное раскрытие настоящего изобретения
Перед тем как настоящее изобретение будет описано ниже более подробно, следует понимать, что настоящее изобретение не ограничено конкретной методикой, протоколами и реактивами, описанными в данном документе, поскольку они могут изменяться. Также следует понимать, что терминология, используемая в данном документе, предназначена только для описания конкретных вариантов осуществления, и не предполагается, что она ограничивает объем настоящего изобретения, который будет ограничиваться только пунктами прилагаемой формулы изобретения. Если не указано иное, все технические и научные термины, используемые в данном документе, имеют те же значения, которые обычно понятны квалифицированному специалисту в данной области техники.
Предпочтительно, термины, используемые в данном документе, определены, как описано в многоязычном толковом словаре биотехнологических терминов "A multilingual glossary of biotechnological terms: (IUPAC Recommendations)", Leuenberger, H.G.W, Nagel, B. and Klbl, H. eds. (1995), Helvetica Chimica Acta, CH-4010 Basel, Switzerland), и как описано в "Pharmaceutical Substances: Syntheses, Patents, Applications" за авторством Axel Kleemann and Jurgen Engel, Thieme Medical Publishing, 1999; "Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals", под редакцией Susan Budavari et al., CRC Press, 1996, и в статье 25 Фармакопеи США/Национальном формуляре 20, опубликованных Фармакопейной конвенцией Соединенных Штатов Америки United States Pharmcopeial Convention, Inc., Rockville Md., 2001.
Будет понятно, что во всем данном описании и пунктах следующей формулы изобретения, если контекст не требует иного, слово «содержать» и его варианты, такие как «содержит» и «содержащий», предполагают включение изложенного признака, целого числа или стадии или группы признаков, целых чисел или стадий, а не исключение любого другого признака, целого числа или стадии или группы целых чисел или стадий. В следующих абзацах различные аспекты настоящего изобретения определены более подробно. Каждый определенный аспект может быть объединен с любым другим аспектом или аспектами, если явно не указано противоположное. В частности, любой признак, указанный как предпочтительный или преимущественный, можно объединить с любым другим признаком или признаками, указанными как предпочтительные или преимущественные.
Несколько документов цитируются в тексте данного описания. Каждый из документов, цитируемых в данном документе (в том числе все патенты, патентные заявки, научные публикации, технические данные, инструкции производителя и т.д.) или выше, или ниже, таким образом включен в данный документ посредством ссылки во всей своей полноте. Ничто в данном документе не следует толковать как допущение, что настоящему изобретению может быть противопоставлено такое раскрытие в силу более ранней даты изобретения.
Определения
Ниже представлены некоторые определения терминов, часто используемых в данном описании. В каждом случае их использования в остальной части описания эти термины будут иметь соответственно определенное значение и предпочтительные значения.
Термин «трансмембранный домен» (TMD), используемый в контексте настоящего изобретения, относится к TMD последовательностей инвариантной цепи (INV) и определен как аминокислотный сегмент, начинающийся в 17 остатках со стороны N-конца от остатка Gln (Q), консервативного во всех INV, и заканчивающийся в 8 остатках со стороны С-конца от консервативного Q, таким образом включая в себя в общей сложности 26 остатков.
Термин «проксимальный по отношению к мембране домен» (MPD), используемый в контексте настоящего изобретения, относится к сегменту из 27 остатков, расположенному непосредственно вблизи TMD со стороны С-конца INV.
Термин «адъювант» используется в контексте настоящего изобретения применительно к веществам, которые усиливают иммунный ответ на антиген. Кроме того, адъюванты также эволюционировали как вещества, которые могут помочь в стабилизации составов с антигенами. Адъюванты добавляют к вакцинам для стимуляции ответа иммунной системы на целевой антиген, но сами по себе не обеспечивают иммунитет. Адъюванты необходимы для улучшения направления и адаптивных иммунных ответов на антигены. Адъюванты проявляют свои эффекты посредством разных механизмов. Например, посредством продления присутствия антигена в крови, или/и помощи в поглощении антигена антиген-презентирующими клетками, и/или активации макрофагов и лимфоцитов, и/или поддержки продуцирования цитокинов. Некоторые адъюванты, такие как квасцы, функционируют как системы доставки посредством создания депо, которые удерживают антигены в месте инъекции, обеспечивая медленное высвобождение, которое продолжает стимулировать иммунную систему. В числе описанных типов адъювантов присутствуют i) неорганические соединения: квасцы, гидроксид алюминия, фосфат алюминия, гидроксифосфат кальция; ii) минеральное масло: вазелиновое масло; iii) бактериальные продукты: убитые бактерии Bordetella pertussis, Mycobacterium bovis, анатоксины; iv) небактериальные органические соединения: сквален; v) системы доставки: детергенты (Quil A), vi) растительные сапонины из квилайи (см. Quillaia), сои, Polygala senega; vii) цитокины: IL-1, IL-2, IL-12; viii) комбинация: полный адъювант Фрейнда, неполный адъювант Фрейнда.
Термин «иммуномодулятор», используемый в контексте настоящего изобретения, относится к любому лекарственному средству или веществу, которое оказывает воздействие на иммунную систему. Иммуномодулятор может корректировать иммунный ответ до надлежащего уровня посредством: i) укрепления слабых иммунных систем; ii) контроля гиперактивных иммунных систем. Конкретный класс иммуномодуляторов, способных к укреплению слабых иммунных систем, представляют собой модуляторы молекул-иммунологических контрольных точек (МСМ), состоящих из
i) агонистических активирующих МСМ, подобных члену суперсемейства фактора некроза опухолей (TNF), предпочтительно, CD27, CD40, ОХ40, GITR или CD137;
ii) антагонистических ингибирующих МСМ, подобных PD-1, CD274, A2AR, В7-Н3, В7-Н4, BTLA, CTLA-4, IDO, KIR, LAG3, TIM-3, VISTA или члену супер семейства B7-CD28, CD28 или ICOS или антагониста их лиганда.
Еще одним классом иммуномодуляторов, которые могут укреплять слабую иммунную систему, являются цитокины, которые действуют как факторы роста Т-клеток. Предпочтительными примерами таких цитокинов являются IL-2, IL-12, IL-15 или IL-17.
Термин «антиген», используемый в контексте настоящего изобретения, относится к любой структуре, распознаваемой молекулами, обеспечивающими иммунный ответ, например, антителами, Т-клеточными рецепторами (TCR) и т.п.Предпочтительные антигены являются клеточными или чужеродными, например, вирусные, бактериальные или грибные белки, которые являются ассоциированными с конкретным заболеванием. Антигены распознаются высоковариабельными антигенными рецепторами (В-клеточным рецептором или Т-клеточным рецептором) адаптивной иммунной системы и могут вызывать гуморальный или клеточный иммунный ответ. Антигены, которые вызывают такой ответ, также называются иммуногеном. Часть белков внутри клеток, вне зависимости от того, являются ли они чужеродными или клеточными, подвергаются процессингу в меньшие пептиды и презентируются главным комплексом гистосовместимости (МНС).
Термин «его антигенный фрагмент» относится к части заданного антигена, которая все еще будет распознаваться молекулой иммунной системы. Антигенный фрагмент будет содержать по меньшей мере один эпитоп или антигенную детерминанту. Предпочтительно, антигенные фрагменты согласно настоящему изобретению содержат по меньшей мере один Т-клеточный эпитоп.
Термин «эпитоп», также известный как антигенная детерминанта, используемый в контексте настоящего изобретения, относится к сегменту антигена, предпочтительно, пептиду, который связывается молекулами иммунной системы, например, В-клеточные рецепторы, Т-клеточные рецепторы или антитела. Эпитопы, связываемые антителами или В-клетками, называются «В-клеточными эпитопами», и эпитопы, связываемые Т-клетками, называются «Т-клеточными эпитопами». В этом контексте термин «связывание» предпочтительно относится к специфическому связыванию, которое определено как связывание с константой ассоциации между антителом или Т-клеточным рецептором (TCR) и соответствующим эпитопом, составляющей 1×105 М-1 или выше, предпочтительно, 1×106 М-1, или выше. Квалифицированному специалисту хорошо известно, как определить константу ассоциации (см., например, Caoili, S.E. (2012) Advances in Bioinformatics Vol. 2012). Предпочтительно, специфическое связывание антител с эпитопом опосредуется Fab (антигенсвязывающий фрагмент) участком антитела, специфическое связывание В-клетки опосредуется Fab участком антитела, содержащегося в В-клеточном рецепторе, и специфическое связывание Т-клетки опосредуется вариабельным (V) участком Т-клеточного рецептора. Т-клеточные эпитопы презентируются на поверхности антиген-презентирующей клетки, где они связаны с молекулами главного комплекса гистосовместимости (МНС). Существует по меньшей мере два разных класса молекул МНС, называемых МНС I и II класса, соответственно. Эпитопы, презентируемые посредством пути с участием MHC-I, вызывают ответ с помощью цитотоксических Т-лимфоцитов (CD8+ клеток), в то время как эпитопы, презентируемые посредством пути с участием МНС-II, вызывают ответ с помощью Т-хелперных клеток (CD4+ клеток). Т-клеточные эпитопы, презентируемые молекулами МНС I класса, как правило, представляют собой пептиды длиной от 8 до 11 аминокислот, и Т-клеточные эпитопы, презентируемые молекулами МНС II класса, как правило, представляют собой пептиды длиной от 13 до 17 аминокислот. Молекулы МНС III класса также презентируют непептидные эпитопы в виде гликолипидов. Соответственно, термин «Т-клеточный эпитоп», предпочтительно, относится к пептиду длиной 8-11 или 13-17 аминокислот, который может презентироваться либо молекулой МНС I класса, либо молекулой МНС II класса. Эпитопы обычно состоят из химически активных поверхностных группировок аминокислот, которые могут нести или не нести боковые цепи в виде Сахаров, и обычно имеют специфические характеристики трехмерной структуры, а также специфические характеристики заряда. Конформационные и неконформационные эпитопы отличаются тем, что связывание с первым, а не с последним теряется в присутствии денатурирующих растворителей.
Термин «специфический для злокачественных опухолей антиген», используемый в контексте настоящего изобретения, относится к белку, который специфически экспрессируется в раковых клетках или является более распространенным в раковых клетках, чем в здоровых клетках. Специфические для злокачественных опухолей антигены включают в себя следующие типы антигенов:
(i) онкофетальные (как правило, экспрессирующиеся только в фетальных тканях и в злокачественных соматических клетках); или
(ii) онковирусные (кодируемые онкогенными трансформирующими вирусами); или
(iii) сверхэкспрессирующиеся/аккумулирующиеся (экспрессирующиеся как нормальной тканью, так и тканью новообразований, причем уровень экспрессии сильно повышен в новообразовании), например, тирозиназа при меланомах или рецептор Her-2 при раке молочной железы; или
(iv) антигены рака/яичка (экспрессирующиеся только раковыми клетками и взрослыми репродуктивными тканями, такими как яичко и плацента); или
(v) линиеспецифические (экспрессирующиеся преимущественно одним раковым гистотипом); или
(vi) специфические для злокачественных опухолей изоформы (изменение экзонного состава транскрипта).
Термин «специфический для злокачественных опухолей неоантиген», используемый в контексте настоящего изобретения, относится к антигену, не присутствующему в нормальных/зародышевых клетках, но который встречается в трансформированных, в частности, в злокачественных клетках. Специфический для злокачественных опухолей неоантиген может содержать один или несколько, например, 2, 3, 4, 5 или больше неоэпитопов. Предпочтительно, чтобы длина каждого специфического для злокачественных опухолей неоантигена, включенного в полипептид согласно настоящему изобретению, была выбрана таким образом, чтобы удостовериться, что существует низкая вероятность содержания в нем эпитопов, которые встречаются в нормальных/зародышевых клетках. Как правило, можно удостовериться в том, что специфический для злокачественных опухолей неоантиген содержит 12 или меньше аминокислот со стороны С-конца и/или N-конца от измененной(измененных) аминокислоты(аминокислот), которые создают неоэпитоп.
Специфический для злокачественных опухолей неоантиген предпочтительно образуется при мутации, происходящей на уровне ДНК, и при этом мутированный белок может содержать
a) одно или несколько изменений отдельных аминокислот, вызванных точковой мутацией с несинонимичной SNV; и/или
b) аминокислотную последовательность, отличную от дикого типа, образование которой вызвано вставками/делециями, приводящими в результате к пептиду со сдвигом рамки считывания; и/или
c) аминокислотную последовательность, отличную от дикого типа, образование которой вызвано изменением границ экзонов или мутациями, вызывающими сохранение интрона; и/или
d) мутированный белок злокачественной опухоли, образующийся вследствие явления слияния генов.
Неоантиген, который является результатом одного или нескольких изменений отдельных аминокислот, вызванных точковой мутацией в несинонимичный SNV в геноме, называется в контексте настоящего изобретения пептидом, мутантным по одной аминокислоте.
Термин «пептид со сдвигом рамки считывания», используемый в контексте настоящего изобретения, относится к полному продукту трансляции, не относящемуся к дикому типу, белок-кодирующего сегмента полинуклеотида, содержащего мутации-вставки или делеции, вызывающие сдвиг открытой рамки считывания (ORF).
Термин «открытая рамка считывания», сокращенно «ORF», используемый в контексте настоящего изобретения, относится к последовательности нуклеотидов, которая может транслироваться в последовательную цепь аминокислот. Как правило, ORF содержит старт-кодон, следующий за ним участок, имеющий длину, которая кратна 3 нуклеотидам, но не содержит стоп-кодон (TAG, ТАА, TGA, UAG, UAA или UGA) в данной рамке считывания.
ORF кодирует белок, в котором аминокислоты, в которые она может транслироваться, образуют цепь, связанную пептидными связями.
Термин «полинуклеотид» или «нуклеиновая кислота» включает в себя как одно цепочечные, так и двухцепочечные нуклеотидные полимеры. Нуклеотиды, содержащие полинуклеотид, могут представлять собой рибонуклеотиды или дезоксирибонуклеотиды или модифицированную форму любого типа нуклеотида. Указанные модификации включают в себя модификации оснований, такие как бромуридин и производные инозина, модификации рибозы, такие как 2',3'-дидезоксирибоза, и модификации межнуклеотидных связей, такие как фосфоротиоат, фосфородитиоат, фосфороселеноат, фосфородиселеноат, фосфороанилотиоат, фосфораниладат и фосфороамидат. Примерами полинуклеотидов являются ДНК и РНК.
«Выделенный полинуклеотид» представляет собой ДНК или РНК геномного происхождения, мРНК, кДНК синтетического происхождения или некую их комбинацию, которая не ассоциирована со всем полинуклеотидом или частью полинуклеотида, в котором выделенный полинуклеотид обнаруживается в природе, или является связанным с полинуклеотидом, с которым он не связан в природе.
Термин «экспрессионная кассета», используемый в контексте настоящего изобретения, относится к полинуклеотиду, содержащему по меньшей мере одну последовательность нуклеиновой кислоты, которую нужно экспрессировать, например, нуклеиновую кислоту, кодирующую отрезок из специфических для злокачественных опухолей неоантигенов, слитых с инвариантной цепью согласно настоящему изобретению или ее фрагментами, функционально связанную с последовательностями контроля транскрипции и/или трансляции. Предпочтительно, экспрессионная кассета включает в себя цис-регуляторные элементы для эффективной экспрессии заданного гена, такие как промотор, сайт инициации и/или сайт полиаденилирования. Предпочтительно, экспрессионная кассета содержит все дополнительные элементы, требующиеся для экспрессии полинуклеотида в клетке пациента. Таким образом, типичная экспрессионная кассета содержит промотор, функционально связанный с последовательностью полинуклеотида, которую нужно экспрессировать, и сигналы, требующиеся для эффективного полиаденилирования транскрипта, сайты связывания рибосом и сигналы терминации трансляции. Дополнительные элементы кассеты могут включать в себя, например, энхансеры. Предпочтительно, экспрессионная кассета также содержит участок терминации транскрипции ниже по ходу транскрипции относительно структурного гена для обеспечения эффективной терминации. Участок терминации можно получить из того же гена, что и промоторную последовательность, или его можно получить из отличающегося гена.
Термин «функционально связанный», используемый в контексте настоящего изобретения, относится к расположению элементов в определенном порядке, причем описанные таким образом компоненты сконфигурированы так, чтобы они выполняли свою обычную функцию. Полинуклеотид является «функционально связанным», когда он помещен в функциональную связь с другой последовательностью нуклеиновой кислоты. Например, промотор является функционально связанным с одним или несколькими трансгенами, если он оказывает воздействие на транскрипцию одного или нескольких трансгенов. Кроме того, управляющие элементы, функционально связанные с кодирующей последовательностью, способные к осуществлению экспрессии кодирующей последовательности. Управляющие элементы не обязательно должны быть смежными с кодирующей последовательностью при условии, что они функционируют, управляя ее экспрессией. Таким образом, например, промежуточные нетранслируемые, но при этом транскрибируемые последовательности могут присутствовать между промоторной последовательностью и кодирующей последовательностью, и промоторная последовательность все еще считается «функционально связанной» с кодирующей последовательностью.
Термины «вектор» или «экспрессионный вектор» используются взаимозаменяемо и относятся к полинуклеотиду, полинуклеотиду внутри оболочки некоего типа, например, вирусной оболочки или липосомы, или полинуклеотиду в составе комплекса с белками, способному вводиться или вводить полинуклеотид согласно настоящему изобретению в клетку, предпочтительно, клетку млекопитающего. Примеры векторов включают в себя, без ограничения, плазмиды, космиды, фаги, липосомы, вирусы или искусственные хромосомы. В частности, вектор применяют для переноса промотора и полинуклеотида согласно настоящему изобретению в подходящую клетку-хозяин. Экспрессионные векторы могут содержать последовательности «репликона» полинуклеотида, которые облегчают автономную репликацию экспрессионного вектора в клетке-хозяине. После того как он оказывается в клетке-хозяине, экспрессионный вектор может реплицироваться независимо или совместно с хромосомной ДНК хозяина, и могут образовываться несколько копий вектора и вставленной в него ДНК. В случае, когда применяют репликационно-некомпетентные экспрессионные векторы, часто из соображений безопасности, вектор может не реплицироваться, а только управлять экспрессией полинуклеотида. В зависимости от типа экспрессионного вектора экспрессионный вектор может исчезать из клетки, т.е. только временно экспрессирует неоантигены, кодируемые полинуклеотидом, или может быть стабильным в клетке. Экспрессионные векторы, как правило, содержат экспрессионные кассеты, т.е. необходимые элементы, которые обеспечивают возможность транскрипции полинуклеотида в молекулу мРНК. Если полинуклеотид представляет собой РНК, транскрипция не нужна, и, следовательно, для молекул РНК требуется только элементы для управления трансляцией.
Термин «аминокислотная последовательность усилителя Т-клеточного ответа» относится к полипептидным последовательностям, которые при слиянии с антигенной последовательностью повышают индукцию Т-клеток в условиях генетической вакцинации.
Термин «активность усилителя Т-клеточного ответа» относится к соединениям, в частности, полипептидам, которые повышают ответ Т-клеток, провоцируемых антигеном. Примером такого соединения будет полипептид согласно настоящему изобретению, в частности, если он связан с антигенной последовательностью. Полипептид будет повышать Т-клеточный ответ на указанные антигены по сравнению с Т-клеточным ответом на антиген отдельно в условиях вакцинации. Подходящие анализы для измерения Т-клеточного ответа являются известными в уровне техники и включают в себя измерение цитокинов, высвобождаемых активированными Т-клетками, как например, интерферона гамма (IFN-γ) с помощью метода ELISpot, или внутриклеточное окрашивание цитокинов (ICS), которое выявляет продуцирование и накопление цитокинов внутри эндоплазматического ретикулума после стимуляции клеток. Соединение с активностью усилителя Т-клеточного ответа повышает ответ Т-клеток, что иллюстрируется, например, увеличением высвобождения цитокинов.
Предполагается, что термины «препарат» и «композиция», используемые в контексте настоящего изобретения, включают в себя состав с активным соединением, например, аденовирус высших приматов согласно настоящему изобретению с носителем и/или вспомогательным веществом.
«Фармацевтически приемлемый» в контексте настоящего изобретения означает одобренный регулирующим органом федерального правительства США или правительством штата или приведенный в Фармакопее США или другой общепризнанной фармакопее для применения у животных и, более конкретно, у людей.
Термин «носитель», используемый в контексте данного документа, относится к фармакологически неактивному веществу, такому как, без ограничения, разбавитель, вспомогательное вещество, поверхностно-активные вещества, стабилизаторы, физиологические буферные растворы или среды, с которыми вводят терапевтически активный ингредиент. Такие фармацевтические носители могут быть жидкими или твердыми. Жидкий носитель включает в себя, без ограничения, стерильные жидкости, такие как солевые растворы в воде и маслах, в том числе, без ограничения, в маслах, происходящих из нефти, маслах животного, растительного или синтетического происхождения, таких как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п. Солевые растворы и водные растворы декстрозы и глицерина также можно использовать в качестве жидких носителей, в особенности, для инъекционных растворов. Солевой раствор является предпочтительным носителем в случае, когда фармацевтическую композицию вводят внутривенно. Примеры подходящих фармацевтических носителей описаны в "Remington's Pharmaceutical Sciences" за авторством Е. W. Martin.
Подходящие фармацевтические вспомогательные вещества включают в себя крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, глицеринмоностеарат, тальк, хлорид натрия, высушенное обезжиренное молоко, глицерин, пропилен, гликоль, воду, этанол и т.п.
«Поверхностно-активные вещества» включают в себя анионные, катионные и неионные поверхностно-активные вещества, такие как, без ограничения, дезоксихолат натрия, додецилсульфат натрия, Triton Х-100 и полисорбаты, такие как полисорбат 20, полисорбат 40, полисорбат 60, полисорбат 65 и полисорбат 80.
«Стабилизаторы» включают в себя, без ограничения, маннит, сахарозу, трегалозу, альбумин, а также антагонисты протеазы и/или нуклеазы.
«Физиологический буферный раствор», который можно применять в контексте настоящего изобретения, включает в себя, без ограничения, раствор хлорида натрия, деминерализованную воду, а также подходящие органические или неорганические буферные растворы, такие как, без ограничения, фосфатный буфер, цитратный буфер, Трис-буфер (три(гидроксиметил)амино метан), буфер HEPES ([4(2-гидроксиэтил)пиперазино]этансульфоновая кислота) или буфер MOPS (3-морфолино-1-пропансульфоновая кислота кислота). Выбор соответствующего буфера обычно зависит от желаемой молярности буфера. Фосфатный буфер является подходящим, например, для инъекционных и инфузионных растворов.
«Эффективное количество» или «терапевтически эффективное количество» представляет собой количество терапевтического средства, достаточное для достижения намеченной цели. Эффективное количество заданного терапевтического средства будет варьировать в зависимости от таких факторов, как природа средства, путь введения, размер и видовая принадлежность животного, получающего терапевтическое средство, и цель введения. Эффективное количество в каждом отдельном случае может быть определено эмпирически квалифицированным специалистом в соответствии с общепринятыми способами из уровня техники.
В контексте данного документа термины «лечить», «осуществление лечения», «лечение» или «терапия» заболевания или нарушения означают осуществление одного или нескольких из следующего: (а) снижение тяжести нарушения; (b) ограничение или предупреждение развития симптомов, характерных для нарушения(нарушений), лечение которого (которых) осуществляют; (с) задержка ухудшения симптомов, характерных для нарушения(нарушений), лечение которого(которых) осуществляют; (d) ограничение или предупреждение рецидива нарушения(нарушений) у индивида, который ранее имел нарушение(нарушения); и (е) ограничение или предупреждение повторного появления симптомов у индивидов, у которых ранее присутствовали симптомы нарушения(нарушений).
Варианты осуществления настоящего изобретения
В соответствии с первым аспектом настоящее изобретение относится к полипептиду, содержащему:
(a) фрагмент INV из представителя Teleostei, который предпочтительно характеризуется активностью усилителя Т-клеточного ответа, содержащий или состоящий из 16-27 смежных аминокислот проксимального по отношению к мембране домена (MPD) INV из представителя Teleostei, причем MPD предпочтительно характеризуется следующей аминокислотной последовательностью (SEQ ID NO: 31):
X1 QKX2 QIHTLQKX3 SX4 RX5 X6 X7 QX8 TRX9 SX10 AV, в которой
X1 представляет собой G, D, S или N, предпочтительно, G или S; и более предпочтительно, G;
X2 представляет собой Е или Q; предпочтительно, Е;
Х3 представляет собой N или S; предпочтительно, N;
Х4 представляет собой D или Е; предпочтительно, Е;
Х5 представляет собой М или L; предпочтительно, М;
Х6 представляет собой G, N, S или Т; предпочтительно, S, G или Т и, более предпочтительно, S;
Х7 представляет собой K или R; предпочтительно, K;
Х8 представляет собой L или М; предпочтительно, L;
Х9 представляет собой S, Т или А; предпочтительно, S; и
Х10 представляет собой Q или Н; предпочтительно, Q;
и при этом 16-27 аминокислот в MPD предпочтительно являются по меньшей мере на 70% идентичными SEQ ID NO: 7;
и, необязательно, один или несколько антигенов или их антигенных фрагментов;
или
(b) полноразмерную INV из представителя Teleostei с SEQ ID NO: 1 или ее вариант, которые характеризуются активностью усилителя Т-клеточного ответа, причем аминокислотная последовательность MPD у варианта является по меньшей мере на 80% идентичной SEQ ID NO: 7;
и один или несколько антигенов или их антигенных фрагментов.
В целом, желательно, чтобы фрагмент INV был максимально коротким, насколько это возможно, при этом сохраняя свой эффект стимулирования Т-клеток антигеном. Предпочтительно, фрагмент содержит, более предпочтительно, состоит из 16-27, 17-26,18-25, 19-24, 20-23, 21-22 смежных аминокислот MPD INV.
Несмотря на то, что фрагмент INV может содержать дополнительные последовательности со стороны N- и/или С-конца относительно MPD, предпочтительно, чтобы такие последовательности не содержались в фрагменте, и, следовательно, предпочтительно, чтобы фрагмент состоял из соответствующей непрерывной отрезок аминокислот MPD.
Если фрагмент INV содержит дополнительные последовательности, расположенные со стороны N- и/или С-конца относительно MPD, предпочтительно, чтобы фрагмент содержал полный MPD, т.е. 27 аминокислот. Предпочтительно, чтобы фрагмент не содержал TMD, а содержал дополнительные С-концевые аминокислоты INV. Предпочтительно, эти С-концевые аминокислоты располагаются непосредственно следом за MPD.
Последовательность MPD, предпочтительно, имеет в основе последовательность MPD из китайского окуня, соответствующую SEQ ID NO: 7. Предпочтительно, фрагмент содержит или состоит из 16-27 аминокислот MPD, причем MPD является по меньшей мере на 75%, более предпочтительно, по меньшей мере на 80%, более предпочтительно, по меньшей мере на 85%, более предпочтительно, по меньшей мере на 90%, более предпочтительно, по меньшей мере на 95% идентичным SEQ ID NO: 7.
Фрагмент может содержать дополнительные N- и/или С-концевые аминокислотные последовательности INV. Таким образом, предпочтительно, чтобы общая длина фрагмента INV составляла 16-80, 17-72, 18-55, 19-50, 20-45, 21-40, 22-35, 23-30 смежных аминокислот.
В соответствии с предпочтительным вариантом осуществления фрагмент содержит или состоит из MPD, характеризующегося аминокислотной последовательностью SEQ ID NO: 31. Предпочтительно, этот MPD содержит по меньшей мере аминокислотную последовательность QIHTLQKX3 SX4 RX5 X6 Х7 QX8 (SEQ ID NO: 51), в которой
Х3 представляет собой N или S; предпочтительно, N;
Х4 представляет собой D или Е; предпочтительно, Е;
Х5 представляет собой М или L; предпочтительно, М;
Х6 представляет собой G, N, S или Т; предпочтительно, S, G или Т и, более предпочтительно, S;
X7 представляет собой K или R; предпочтительно, K;
Х8 представляет собой L или М; предпочтительно, L.
В контексте этого предпочтительного варианта осуществления особенно предпочтительно, чтобы этот фрагмент содержал SEQ ID NO: 51 и от 0 до 11, т.е. 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11 дополнительных аминокислот в MPD, который может присутствовать со стороны N- и/или С-конца относительно SEQ ID NO: 51. Предпочтительно, эти 1-11 дополнительных аминокислот являются по меньшей мере на 70% идентичными SEQ ID NO: 7. Предпочтительно, полный фрагмент, включающий в себя коровую последовательность, соответствующую SEQ ID NO: 51, является по меньшей мере на 70% идентичным SEQ ID NO: 7, более предпочтительно, по меньшей мере на 75%, более предпочтительно, по меньшей мере на 80%, еще более предпочтительно, по меньшей мере на 85% или по меньшей мере на 90% идентичным SEQ ID NO: 7. В каждом случае предпочтительно, чтобы фрагмент характеризовался активностью усилителя Т-клеточного ответа. Кроме того, предпочтительно, чтобы не присутствовали дополнительные последовательности цепи INV, продолжающиеся со стороны N- и С-конца относительно фрагмента, и более предпочтительно, чтобы фрагмент являлся единственной последовательностью INV в полипептиде.
В соответствии с предпочтительным вариантом осуществления полипептида согласно первому аспекту настоящего изобретения аминокислотная последовательность:
(a) MPD согласно альтернативе (а) первого аспекта представляет собой любую из SEQ ID NO: 7-12, т.е. 7, 8, 9, 10, 11 или 12; или
(b) фрагмента INV согласно альтернативе (а) первого аспекта настоящего изобретения содержит любую из SEQ ID NO: 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 или 18, предпочтительно, 7 или 13; или состоит из любой из SEQ ID NO: 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 или 18, предпочтительно, из 7 или 13; или
(c) инвариантной цепи из представителя Teleostei согласно альтернативе (b) первого аспекта настоящего изобретения представляет собой любую из SEQ ID NO: 1-6.
Если фрагмент состоит из 16-27 аминокислот MPD INV, предпочтительные фрагменты имеют длину, составляющую 16-27, 17-26, 18-25, 19-24, 20-23, 21-22 непрерывных аминокислот MPD INV, что соответствует SEQ ID NO: 7-12.
В каждом изложенном выше случае фрагмент или вариант характеризуется активностью усилителя Т-клеточного ответа. Активность усилителя Т-клеточного ответа можно измерить, как известно в уровне техники, или как изложено в приложенной экспериментальной части. Предпочтительно, чтобы активность усилителя Т-клеточного ответа составляла по меньшей мере 50%, предпочтительно, по меньшей мере 80% от активности усилителя Т-клеточного ответа у фрагмента INV, соответствующего SEQ ID NO: 13, когда он связан с тем же антигеном или цепью из антигенов.
В соответствии с конкретным вариантом осуществления полипептида согласно альтернативе (а) первого аспекта настоящего изобретения фрагмент состоит по меньшей мере из 16-27 N-концевых аминокислот в MPD и:
(i) 1-26 последовательных аминокислот трансмембранного домена (TMD) INV из представителя Teleostei, расположенных непосредственно возле MPD со стороны N-конца, причем TMD INV из представителя Teleostei предпочтительно характеризуется следующей аминокислотной последовательностью (SEQ ID NO: 32):
AY1KY2AY3LTTLY4CLLY5Y6SQVFTAYY7VF, в которой
Y1 представляет собой L или F, предпочтительно, L;
Y2 представляет собой I или V, предпочтительно, V;
Y3 представляет собой G или А, предпочтительно, G;
Y4 представляет собой Т или А, предпочтительно, Т;
Y5 представляет собой L или V, предпочтительно, L;
Y6 представляет собой А или S, предпочтительно, А; и
Y7 представляет собой М или Т, предпочтительно, М; и/или
(ii) 1-19 последовательных аминокислот в INV из представителя Teleostei, расположенных непосредственно возле MPD со стороны С-конца, предпочтительно, характеризующихся следующей аминокислотной последовательностью (SEQ ID NO: 33):
APZ1Z2MZ3Z4PMZ5SLPZ6Z7Z8DZ9Z10, в которой
Z1 представляет собой М, V или А, предпочтительно, М или V, более предпочтительно, М;
Z2 представляет собой R или K, предпочтительно, K;
Z3 представляет собой Н, А или Q, предпочтительно, М или Н, более предпочтительно, Н;
Z4 представляет собой М или L, предпочтительно, М;
Z5 представляет собой N или S, предпочтительно, N;
Z6 представляет собой М или L, предпочтительно, L;
Z7 представляет собой М, L или V, предпочтительно, L;
Z8 представляет собой М или S, предпочтительно, М;
Z9 представляет собой F или Y, предпочтительно, F; и
Z10 представляет собой Т или S, предпочтительно, Т.
Если фрагмент содержит дополнительные N- и/или С-концевые аминокислотные последовательности INV, предпочтительно, чтобы общая длина фрагмента INV составляла 28-72, 30-65 или 35-46 смежных аминокислот.
Авторами настоящего изобретения было неожиданно обнаружено, что сильный Т-клеточный ответ на два или больше антигенов, предпочтительно, неоантигенов, может индуцироваться при слиянии фрагмента INV согласно альтернативе (а) первого аспекта настоящего изобретения или INV согласно альтернативе (b) первого аспекта настоящего изобретения с двумя или более антигенами и/или их антигенными фрагментами. Это обеспечивает возможность одновременной индукции Т-клеточного ответа в отношении нескольких антигенов. Таким образом, применительно как к альтернативе (а) первого аспекта настоящего изобретения, так и к альтернативе (b) первого аспекта настоящего изобретения предпочтительно, чтобы полипептид содержал несколько антигенов и/или их антигенных фрагментов. Например, предпочтительно, чтобы полипептид содержал по меньшей мере 5 отличающихся антигенов и/или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 отличающихся антигенов и/или их антигенные фрагменты, еще более предпочтительно, по меньшей мере 50 отличающихся антигенов и/или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 100 отличающихся антигенов и/или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 200 отличающихся антигенов и/или их антигенных фрагментов и, еще более предпочтительно, по меньшей мере 300 отличающихся антигенов и/или их антигенных фрагментов.
Для того чтобы вместить максимальное количество отличающихся антигенов в пределах одного полипептида, особенно предпочтительно, чтобы полипептид содержал антигенные фрагменты антигенов.
Антигены выбирают в зависимости от соответствующего терапевтического применения. Если желательна терапевтическая или профилактическая вакцинация против пролиферативного заболевания, антиген выбран из специфического для злокачественных опухолей антигена или специфического для злокачественных опухолей неоантигена. Как изложено выше, в частности, в контексте противораковой вакцинации, предпочтительно, чтобы полипептид согласно первому аспекту содержал два или более отличающихся антигенов. Предпочтительно, чтобы полипептид содержал по меньшей мере 5 отличающихся специфических для злокачественных опухолей антигенов или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 отличающихся специфических для злокачественных опухолей антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 50 отличающихся специфических для злокачественных опухолей антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 100 отличающихся специфических для злокачественных опухолей антигены или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 200 отличающихся специфических для злокачественных опухолей антигенов или их антигенных фрагментов и, еще более предпочтительно, по меньшей мере 300 отличающихся специфических для злокачественных опухолей антигенов или их антигенных фрагментов. В качестве альтернативы, предпочтительно, чтобы полипептид содержал по меньшей мере 5 отличающихся специфических для злокачественных опухолей неоантигенов или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 отличающихся специфических для злокачественных опухолей неоантигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 50 отличающихся специфических для злокачественных опухолей неоантигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 100 отличающихся специфических для злокачественных опухолей неоантигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 200 отличающихся специфических для злокачественных опухолей неоантигенов или их антигенных фрагментов и, еще более предпочтительно, по меньшей мере 300 отличающихся специфических для злокачественных опухолей неоантигенов или их антигенных фрагментов. В качестве альтернативы, предпочтительно, чтобы полипептид содержал по меньшей мере 5 отличающихся специфических для злокачественных опухолей антигенов или неоантигенов или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 отличающихся специфических для злокачественных опухолей антигенов или неоантигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 50 отличающихся специфических для злокачественных опухолей антигенов или неоантигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 100 отличающихся специфических для злокачественных опухолей антигенов или неоантигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 200 отличающихся специфических для злокачественных опухолей антигенов или неоантигенов или их антигенных фрагментов и, еще более предпочтительно, по меньшей мере 300 отличающихся специфических для злокачественных опухолей антигенов или неоантигенов или их антигенных фрагментов.
В качестве альтернативы, антиген представляет собой вирусный белок или его антигенный фрагмент, бактериальный белок или его антигенный фрагмент или грибной белок или его антигенный фрагмент.
Обычно профилактическая или терапевтическая вакцинация против вирусной, бактериальной или грибковой инфекции не требует столь большого количества отличающихся антигенов, чтобы она являлась эффективной, как вакцинация при терапии пролиферативных заболеваний. Тем не менее, существуют некоторые вирусы, подобные, например, ВИЧ, которые имеют большое разнообразие эпитопов, в частности, белков оболочки. Чтобы вызвать полиспецифический иммунный ответ могут быть включены несколько антигенов. Таким образом, предпочтительно, чтобы полипептид содержал по меньшей мере 5 отличающихся вирусных антигенов или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 отличающихся вирусных антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 50 отличающихся вирусных антигенов или антигенного фрагмента, еще более предпочтительно, по меньшей мере 100 отличающихся вирусных антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 200 отличающихся вирусных антигенов или их антигенных фрагментов и, еще более предпочтительно, по меньшей мере 300 отличающихся вирусных антигенов или их антигенных фрагментов. Антигены могут быть выбраны из отличающихся штаммов одного и того же вируса и/или разных видов вирусов. В последнем случае вакцина позволяет иммунизацию против ряда отличающихся видов вирусов.
В качестве альтернативы, предпочтительно, чтобы полипептид содержал по меньшей мере 5 отличающихся бактериальных антигенов или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 отличающихся бактериальных антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 50 отличающихся бактериальных антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 100 отличающихся бактериальных антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 200 отличающихся бактериальных антигенов или их антигенных фрагментов и, еще более предпочтительно, по меньшей мере 300 отличающихся бактериальных антигенов или их антигенных фрагментов.
В качестве альтернативы, предпочтительно, чтобы полипептид содержал по меньшей мере 5 отличающихся грибных антигенов или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 отличающихся грибных антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 50 отличающихся грибных антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 100 отличающихся грибных антигенов или их антигенных фрагментов, еще более предпочтительно, по меньшей мере 200 отличающихся грибных антигенов или их антигенных фрагментов и, еще более предпочтительно, по меньшей мере 300 отличающихся грибных антигенов или их антигенных фрагментов.
В соответствии со всеми вышеуказанными вариантами осуществления предпочтительно, чтобы антигены представляли собой Т-клеточные антигены. Т-клеточные антигены представляют собой антигены, которые презентируются МНС и вызывают Т-клеточный ответ.
Предпочтительно, антиген или каждый из антигенов или их антигенных фрагментов имеет(имеют) длину от 6 до 100 аминокислот, более предпочтительно, 7-50 и, более предпочтительно, 8-30 аминокислот.
В соответствии с предпочтительным вариантом осуществления полипептида согласно первому аспекту настоящего изобретения один или несколько антигенов и/или один или несколько их антигенных фрагментов расположены со стороны С-конца относительно фрагмента INV согласно альтернативе (а) первого аспекта настоящего изобретения или полноразмерного INV согласно альтернативе (b) первого аспекта настоящего изобретения. Особенно предпочтительно, чтобы антигены и/или их антигенные фрагменты располагались непосредственно со стороны С-конца относительно INV согласно альтернативе (а) или (b) первого аспекта настоящего изобретения.
Предпочтительно, чтобы полипептиды согласно настоящему изобретению продуцировались внутри клеток пациента, подлежащего вакцинации. Внутриклеточная экспрессия является предварительным условием для презентирования МНС и, следовательно, стимуляции Т-клеточного ответа. Соответственно, согласно второму аспекту настоящее изобретение относится к полинуклеотиду, кодирующему полипептид согласно первому аспекту настоящего изобретения. Предпочтительно, полинуклеотид представляет собой ДНК или РНК. Более предпочтительно, полинуклеотид представляет собой ДНК. РНК предпочтительно применяют для того, чтобы непосредственно вызвать трансляцию кодируемого полипептида. ДНК, кодирующая полипептид согласно первому аспекту, как правило, вставлена в экспрессионные кассеты, которые управляют транскрипцией мРНК, кодирующей полипептиды согласно настоящему изобретению. Тем не менее, полинуклеотид также может представлять собой РНК, если полинуклеотид содержится в векторе, и вектор представляет собой РНК-вирус. Предпочтительной РНК для непосредственного применения является самоамплифицирующаяся РНК (SAM).
В соответствии с третьим аспектом настоящее изобретение относится к вектору, содержащему полинуклеотид согласно второму аспекту настоящего изобретения. Предпочтительно, полинуклеотид согласно настоящему изобретению является функционально связанным с последовательностью для контроля экспрессии.
Два или больше векторов используют, если количество отличающихся антигенов или их антигенных фрагментов, которые нужно доставить пациенту, является столь большим, что полинуклеотид, кодирующий гибридный полипептид INV и всех антигенов или их антигенных фрагментов, не может уместиться в выбранном векторе. Соответственно, согласно четвертому аспекту настоящее изобретение относится к группе из двух или более отличающихся векторов, причем каждый из отличающихся векторов содержит полинуклеотид согласно второму аспекту настоящего изобретения, кодирующий отличающийся полипептид согласно первому аспекту настоящего изобретения.
Вектор согласно третьему аспекту или группа векторов согласно четвертому аспекту, причем вектор в каждом случае является независимо выбранным из группы, состоящей из плазмиды; космиды; липосомной частицы, вирусного вектора или вирусоподобной частицы; предпочтительно, из альфавирусного вектора, вектора на основе вируса венесуэльского энцефалита лошадей (VEE), вектор на основе вируса Синдбис (SIN), вектора на основе вируса леса Семлики (SFV), вектора на основе цитомегаловируса (CMV) обезьян или человека, вектора на основе вируса лимфоцитарного хориоменингита (LCMV), ретровирусного вектора, лентивирусного вектора, аденовирусного вектора, вектора на основе аденоассоциированного вируса, вектора на основе поксвируса, вектора на основе вируса коровьей оспы или вектора на основе модифицированного вируса осповакцины Ankara (MVA). Предпочтительно, чтобы группу векторов, в которой каждый член группы содержит полинуклеотид, кодирующий отличающийся антиген или его фрагменты, и которую, следовательно, как правило, вводят одновременно, применяли такой же тип вектора, например, вектор, полученный из аденовируса.
Наиболее предпочтительными векторами являются аденовирусные векторы, в частности, аденовирусные векторы, полученные от человека или высших приматов, отличных от человека. Предпочтительные высшие приматы, из которых получены аденовирусы, представляют собой шимпанзе (Pan), гориллу (Gorilla) и орангутанов (Pongo), предпочтительно, бонобо (Pan paniscus) и обыкновенного шимпанзе (Pan troglodytes). Как правило, встречающиеся в естественных условиях аденовирусы высших приматов, отличных от человека, выделяют из образцов кала соответствующего высшего примата. Наиболее предпочтительные векторы представляют собой нереплицирующиеся аденовирусные векторы на основе hAd5, hAd11, hAd26, hAd35, hAd49, ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd55, ChAd63, ChAd73, ChAd82, ChAd83, ChAd146, ChAd147, векторы на основе PanAd1, PanAd2 и PanAd3 или репликационно-компетентные векторы Ad4 и Ad7. Аденовирусы человека hAd4, hAd5, hAd7, hAd11, hAd26, hAd35 и hAd49 являются хорошо известными в уровне техники. Векторы на основе встречающихся в естественных условий ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd63 и ChAd82 подробно описаны в международной заявке WO 2005/071093. Векторы на основе встречающихся в естественных условиях PanAd1, PanAd2, PanAd3, ChAd55, ChAd73, ChAd83, ChAd146 и ChAd147 подробно описаны в международной заявке WO 2010/086189.
В соответствии с пятым аспектом настоящее изобретение относится к фармацевтической композиции, содержащей полипептид согласно первому аспекту настоящего изобретения, полинуклеотид согласно второму аспекту настоящего изобретения, или вектор согласно третьему аспекту настоящего изобретения, или группу векторов согласно четвертому аспекту настоящего изобретения и фармацевтически приемлемое вспомогательное вещество и, необязательно, один или несколько адъювантов.
Авторы настоящего изобретения обнаружили, что введение по меньшей мере одного иммуномодулятора, например, модулятора молекулы-контрольной точки (МСМ), дополнительно улучшает силу Т-клеточного ответа на антиген или его фрагмент. Таким образом, в соответствии с предпочтительным вариантом осуществления шестого аспекта фармацевтическая композиция содержит по меньшей мере один иммуномодулятор, например, МСМ, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, например, МСМ, или вектор или липосомную частицу, содержащую полинуклеотид, который кодирует иммуномодулятор, например, МСМ.
В соответствии с шестым аспектом настоящее изобретение относится к набору, содержащему фармацевтическую композицию согласно пятому аспекту настоящего изобретения и отдельно упакованный по меньшей мере один иммуномодулятор, например, МСМ, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, например, МСМ, или вектор, содержащий полинуклеотид, кодирующий иммуномодулятор, например, МСМ.
В соответствии с предпочтительным вариантом осуществления пятого аспекта или шестого аспекта иммуномодулятор представляет собой МСМ и является выбранным из группы, состоящей из:
(a) агониста члена суперсемейства факторов некроза опухолей (TNF), предпочтительно, CD27 (например, варлилумаб), CD40 (например, СР-870,893), ОХ40 (например, INCAGN01949 или MEDI0562), GITR (например, MEDI1873) или CD137 (например, утомилумаб);
(b) антагониста PD-1 (например, пембролизумаб или ниволумаб), CD274 (атезолизумаб или дурвалумаб), A2AR (например, преладенант), В7-НЗ (например, MGA271), В7-Н4, BTLA, CTLA-4 (например, тремелимумаб или AGEN1884), IDO, KIR, LAG3, TIM-3 (например, СА-327 или RMT3-23) или VISTA (например, СА-170), или антагониста члена суперсемейства B7-CD28, предпочтительно, CD28 или ICOS, или антагониста их лиганда.
Другие предпочтительные иммуномодуляторы представляют собой цитокины, которые действуют как факторы роста Т-клеток, в частности, IL-2, IL-12 или IL-15.
В соответствии с седьмым аспектом настоящее изобретение относится к полипептиду согласно первому аспекту настоящего изобретения, полинуклеотиду согласно второму аспекту настоящего изобретения или к вектору или группе векторов согласно третьему или четвертому аспекту настоящего изобретения для применения в качестве лекарственного препарата.
В соответствии с восьмым аспектом настоящее изобретение относится к полипептиду согласно первому аспекту настоящего изобретения, полинуклеотиду согласно второму аспекту настоящего изобретения, или к вектору или группе векторов согласно третьему или четвертому аспекту настоящего изобретения, или к фармацевтической композиции согласно пятому аспекту настоящего изобретения, или к наборам, содержащим такие фармацевтические композиции, согласно шестому аспекту настоящего изобретения для применения в предупреждении или лечении пролиферативного заболевания, предпочтительно, рака, вирусного заболевания, грибкового заболевания или бактериального заболевания.
В соответствии с предпочтительным вариантом осуществления полипептид согласно первому аспекту настоящего изобретения, полинуклеотид согласно второму аспекту настоящего изобретения, или вектор или группа векторов согласно третьему или четвертому аспекту настоящего изобретения, или фармацевтическая композиция или наборы, содержащие такие фармацевтические композиции, согласно пятому аспекту настоящего изобретения, причем рак является выбранным из группы, состоящей из злокачественных новообразований губ, ротовой полости, глотки, пищеварительного органа, органа дыхания, органа грудной полости, кости, суставного хряща, кожи, мезотелиальной ткани, мягкой ткани, молочной железы, женских половых органов, мужских половых органов, мочевых путей, головного мозга и других частей центральной нервной системы, щитовидной железы, желез внутренней секреции, лимфоидной ткани и гемопоэтической ткани.
В соответствии с предпочтительным вариантом осуществления полипептид согласно первому аспекту настоящего изобретения, полинуклеотид согласно второму аспекту настоящего изобретения, или вектор или группа векторов согласно третьему или четвертому аспекту настоящего изобретения, или фармацевтическая композиция или наборы, содержащие такие фармацевтические композиции, согласно пятому аспекту настоящего изобретения, причем по меньшей мере один иммуномодулятор, например, МСМ, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, например, МСМ, или вектор или липосомная частица, содержащая полинуклеотид, кодирующий иммуномодулятор, например, МСМ, вводят до, одновременно или после введения полипептида согласно первому аспекту настоящего изобретения, полинуклеотида согласно второму аспекту настоящего изобретения, или вектора или группы векторов согласно третьему или четвертому аспекту настоящего изобретения, или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции, согласно пятому аспекту настоящего изобретения.
В соответствии с предпочтительным вариантом осуществления восьмого аспекта настоящего изобретения введение модулятора молекулы-контрольной точки начинают до начала введения вакцины, или при этом введение ингибитора контрольной точки начинают после начала введения вакцины, или при этом введение ингибитора контрольной точки начинают одновременно с началом введения вакцины.
В соответствии с предпочтительным вариантом осуществления восьмого аспекта настоящего изобретения схема вакцинации представляет собой гетерологичную прайм-буст вакцинацию (heterologous prime boost) двумя отличающимися вирусными векторами. Предпочтительными комбинациями являются вектор на основе аденовируса высших приматов для примирования и вектор на основе поксвируса, вектор на основе вируса коровьей оспы или вектор на основе модифицированного вируса осповакцины Ankara (MVA) для бустер-иммунизации организма. Предпочтительно, их вводят последовательно с интервалом по меньшей мере в 1 неделю, предпочтительно, 6 недель.
ПРИМЕРЫ
Пример 1. Слияние неоантигенов с инвариантной цепью китайского окуня или ее фрагментами создает иммуногенность в условиях вакцинации аденовирусом высших приматов
Выбранные специфические для злокачественных опухолей неоантигены получают с помощью 5 несинонимичных однонуклеотидных вариантов (SNV), наиболее частого типа мутаций, обнаруживаемых в опухолях. Аминокислотная последовательность каждого специфического для злокачественных опухолей неоантигена имеет мутированную аминокислоту, помещенную в ее центр и фланкированную и спереди, и сзади 12 аминокислотами дикого типа (wt), при этом общая длина составляет 25 аминокислот (таблица 1). Последовательности неоантигенов соединены по типу «голова к хвосту» с образованием искусственного антигена.
Вектор на основе аденовируса высших приматов (GAd), кодирующий пентатоп, содержащий 5 специфических для злокачественных опухолей неоантигенов (таблица 1), перед которыми находится инициирующий метионин (Penta: SEQ ID NO: 25), и полученный из мышиной опухоли СТ26, не способен индуцировать иммунный ответ в отношении специфических для злокачественных опухолей неоантигенов (фиг. 1), если последовательность инвариантной цепи китайского окуня (INV) (MF_INV_FL: SEQ ID NO: 26), или усеченный вариант INV китайского окуня, содержащий остатки 1-81, который включает в себя трансмембранный домен (MF_INV_SH, SEQ ID NO:27), или фрагмент последовательности INV китайского окуня, которому предшествует инициирующий метионин (MF_INV-A: SEQ ID NO: 28; MF_INV_В: SEQ ID NO: 29), не помещены на N-конец пентатопа. Во всех конструкциях последовательность пептида НА (SEQ ID NO: 30) встраивают посредством слияния ниже пентатопа с целью мониторинга экспрессии.
Иммуногенность оценивали на инбредных мышах Ba1BC после одной внутримышечной иммунизации в дозе 5×108 или 5×107 вирусных частиц (vp) GAd для каждой из вакцинных конструкций. Спленоциты собирали через три недели после иммунизации и анализировали в отношении IFN-γ методом ELISpot, стимулируя клетки в присутствии пула синтетических пептидов из 25 мономерных звеньев, соответствующих каждому из 5 специфических для злокачественных опухолей неоантигенов. Анализы IFN-γ методом ELISpot осуществляли на суспензиях отдельных клеток из селезенок. Планшеты MSIP S4510 (Millipore, Биллерика, Массачусетс, США) покрывали 10 мкг/мл антитела к мышиному IFN-γ (U-CyTech, Утрехт, Нидерланды) и инкубировали в течение ночи при 4°С. После отмывки и блокирования мышиные спленоциты высевали в двух параллелях с двумя разными плотностями (1×106 и 5×105 клеток на лунку) и стимулировали в течение ночи пулом пептидов, содержащим пять пептидов из 25 мономерных звеньев в конечной концентрации, составляющей 1 мкг/мл. Разбавитель для пептида в виде диметилсульфоксида (Sigma-Aldrich, Милан, Италия) использовали в качестве отрицательного контроля. Планшеты проявляли посредством последующего инкубирования с биотинилированным антителом к мышиному IFN-γ (U-CyTech, Утрехт, Нидерланды), конъюгатом стрептавидин-щелочная фосфатаза (BD Biosciences, Сан-Хосе, Калифорния, США) и, наконец, с растворами 5-бром-4-хлор-3-индоил-фосфата/нитросинего тетразолия для анализа по технологии 1-Step (Thermo Fisher Scientific, Рокфорд, Иллинойс, США). Автоматический планшет-ридер с автоматизированной видеосистемой для анализа ELISA-spot применяли для анализа планшетов. Данные анализа ELISpot были выражены в SFC IFN-γ на миллион спленоцитов.
Иммунные ответы (количество Т-клеток, продуцирующих IFN-γ, на миллион спленоцитов) представлены на фиг. 1. Ответы считали положительными, если (i) среднее значение для лунок с антигенами составляло больше чем 20 образующих пятно колоний SFC/106 РВМС и (ii) 3-кратно превышало фоновое значение для лунок, инкубируемых с разбавителем для пептидов в виде DMSO. Как показано на фиг. 1, добавление либо INV китайского окуня, либо его фрагмента превращало неиммуногенный пентаантиген в иммуногенный антиген со 100% показателем ответа у животных, вакцинируемых MF_INV_FL, или у животных, вакцинируемых MF_INV_А в дозе, составляющей 5×108 vp.В частности, вакцинация в дозе 5×108vp конструкциями, содержащими короткие фрагменты MF_INV_A или MF_INV_B, индуцировала иммуногенность на уровнях, сравнимых с наблюдаемыми в случае конструкций, содержащих полноразмерную INV китайского окуня (MF_INV_FL) или усеченный вариант INV китайского окуня, содержащий остатки 1-81, который включает в себя трансмембранный домен (MF_INV_SH). Вакцинация в дозе 5×107 vp (фиг. 1) может дифференцировать активность отличающегося усилителя Т-клеточных ответов, при этом только конструкции, содержащие короткие фрагменты MF_INV_А, были способны сохранять иммуногенность у 100% мышей на уровнях, сравнимых с наблюдаемыми для конструкций, содержащих полноразмерную INV китайского окуня (MF_INV_FL).
Усеченный вариант INV китайского окуня, содержащий остатки 1-81, который включает в себя трансмембранный домен (MF_INV_SH), наоборот, проявляет себя хуже, чем MF_INV_A, и способен индуцировать иммунный ответ в более низкой дозе только у 1 из 6 мышей.
Пример 2
Способность фрагмента MF INV А инвариантной цепи китайского окуня (SEQ ID NO: 7) усиливать индуцируемый вакциной иммунный ответ затем дополнительно исследовали с применением нового искусственного антигена, содержащего большее количество (20) неоантигенов из мышиной модели СТ26. Все пять неоантигенов, присутствующих в конструкции MF_INV_А из примера 1 (таблица 1), включали в новый антиген, но в отличающемся порядке по сравнению с MF_INV_А (таблица 2). Получали два вектора на основе GAd, каждый из которых кодирует те же 20 неоантигенов, соединенные по типу «голова к хвосту» в порядке, представленном в таблице 2: конструкция СТ26-20, в которой перед антигеном находится только инициирующий метионин (SEQ ID NO: 49), и конструкция MF_INV_А-20, в которой FRAG_А инвариантной цепи китайского окуня (SEQ ID NO: 7), перед которым находится инициирующий метионин, помещен на N-конце антигена (SEQ ID NO: 50). В обеих конструкциях последовательность пептида НА (SEQ ID NO: 30) встроены посредством слияния ниже антигена с целью мониторинга экспрессии.
Иммунные ответы оценивали in vivo на инбредных мышах BalBC (n=6 на группу) после одной внутримышечной иммунизации в дозе, составляющей 5×107 вирусных частиц (vp). Спленоциты собирали через две недели после иммунизации и анализировали в отношении IFNγ методом ELISpot, стимулируя клетки в присутствии пула из 20 синтетических пептидов, соответствующих последовательностям кодируемых неоантигенов. Как наблюдали выше для небольшого пентатопного антигена, присутствие FRAG_А инвариантной цепи MF (SEQ ID NO: 7) значительно усиливало Т-клеточные ответы после вакцинации (фиг. 3) независимо от порядка и общего количества кодируемых неоантигенов.

| название | год | авторы | номер документа |
|---|---|---|---|
| Противораковая вакцина с инвариантной цепью из костистых рыб | 2019 |
|
RU2808567C2 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2782261C2 |
| ПЕПТИДЫ MPHOSPH1 И ВАКЦИНЫ, ВКЛЮЧАЮЩИЕ ИХ | 2012 |
|
RU2612905C2 |
| ПЕПТИДЫ NEIL3 И ВКЛЮЧАЮЩИЕ ИХ ВАКЦИНЫ | 2010 |
|
RU2600888C2 |
| ПЕПТИДЫ KNTC2 И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2014 |
|
RU2671395C2 |
| ПЕПТИДЫ UBE2T И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2013 |
|
RU2663350C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ИММУНОТЕРАПИИ | 2014 |
|
RU2680010C2 |
| ПЕПТИДЫ ТОРК И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2012 |
|
RU2633503C2 |
| ПЕПТИДЫ NEIL3 И ВКЛЮЧАЮЩИЕ ИХ ВАКЦИНЫ | 2010 |
|
RU2733985C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ И ДИАГНОСТИКИ РАКА ЛЕГКИХ | 2001 |
|
RU2311920C2 |



























Настоящее изобретение относится к области биотехнологии, в частности к усилителю иммунного ответа на вакцину, и может быть использовано в медицине. Предложенный укороченный вариант фрагмента инвариантной цепи китайского окуня Teleostei сохраняет иммуногенность полной инвариантной цепи и может быть применим для стимулирования иммунного ответа на более крупные антигенные последовательности для их доставки в векторах ограниченного размера. 10 н. и 9 з.п. ф-лы, 2 пр., 2 табл., 3 ил.
1. Полипептид, обладающий активностью энхансера Т-клеточного ответа, содержащий:
фрагмент инвариантной цепи (INV) Teleostei, содержащий или состоящий из 16-27 аминокислот проксимального по отношению к мембране домена (MPD) INV Teleostei, причем MPD характеризуется следующей аминокислотной последовательностью (SEQ ID NO: 31):
X1QKX2QIHTLQKX3SX4 RX5X6X7QX8TRX9SX10AV,
в которой
X1 представляет собой G, D, S или N;
X2 представляет собой E или Q;
X3 представляет собой N или S;
X4 представляет собой D или E;
X5 представляет собой M или L;
X6 представляет собой G, N, S или T;
X7 представляет собой K или R;
X8 представляет собой L или M;
X9 представляет собой S, T или A и
X10 представляет собой Q или H;
и при этом указанные 16-27 аминокислот MPD являются по меньшей мере на 70% идентичными последовательности SEQ ID NO: 7.
2. Полипептид, обладающий активностью энхансера Т-клеточного ответа, содержащий:
фрагмент инвариантной цепи (INV) Teleostei, содержащий или состоящий из 16-27 аминокислот проксимального по отношению к мембране домена (MPD) INV Teleostei, причем MPD характеризуется следующей аминокислотной последовательностью (SEQ ID NO: 31):
X1QKX2QIHTLQKX3SX4RX5X6X7QX8TRX9SX10AV,
в которой
X1 представляет собой G, D, S или N;
X2 представляет собой E или Q;
X3 представляет собой N или S;
X4 представляет собой D или E;
X5 представляет собой M или L;
X6 представляет собой G, N, S или T;
X7 представляет собой K или R;
X8 представляет собой L или M;
X9 представляет собой S, T или A и
X10 представляет собой Q или H;
и при этом указанные 16-27 аминокислот MPD являются по меньшей мере на 70% идентичными последовательности SEQ ID NO: 7;
и один или несколько антигенов и/или один или несколько их антигенных фрагментов.
3. Полипептид по п. 1 или 2, в котором аминокислотная последовательность:
(a) MPD согласно п. 1 или 2 представляет собой любую из SEQ ID NO: 7–12; или
(b) фрагмент согласно п. 1 или 2 содержит или состоит из любой из SEQ ID NO: 7–18.
4. Полипептид по пп. 1, 2 или согласно альтернативе (a) или (b) п. 3, в котором фрагмент состоит из по меньшей мере 16-27 N-концевых аминокислот MPD и:
(i) 1-26 последовательных аминокислот трансмембранного домена (TMD) INV Teleostei, расположенных непосредственно на N-конце MPD, причем TMD INV Teleostei предпочтительно характеризуется следующей аминокислотной последовательностью (SEQ ID NO: 32):
AY1KY2AY3LTTLY4CLLY5Y6SQVFTAYY7VF,
в которой
Y1 представляет собой L или F;
Y2 представляет собой I или V;
Y3 представляет собой G или A;
Y4 представляет собой T или A;
Y5 представляет собой L или V;
Y6 представляет собой A или S и
Y7 представляет собой M или T; и/или
(ii) 1-19 последовательных аминокислот INV Teleostei, расположенных непосредственно на C-конце MPD, предпочтительно характеризующихся следующей аминокислотной последовательностью (SEQ ID NO: 33):
APZ1Z2MZ3Z4PMZ5SLPZ6Z7Z8DZ9Z10,
в которой
Z1 представляет собой M, V или A;
Z2 представляет собой R или K;
Z3 представляет собой H, A или Q;
Z4 представляет собой M или L;
Z5 представляет собой N или S;
Z6 представляет собой M или L;
Z7 представляет собой M, L или V;
Z8 представляет собой M или S;
Z9 представляет собой F или Y и
Z10 представляет собой T или S.
5. Полипептид по любому из пп. 2-4, в котором антиген в каждом случае независимо выбран из группы, состоящей из специфического для злокачественных опухолей антигена, специфического для злокачественных опухолей неоантигена или вирусного белка, бактериального белка, при этом предпочтительно:
(i) полипептид содержит по меньшей мере пять отличающихся антигенов и/или их антигенных фрагментов
и/или
(ii) один или несколько антигенов и/или один или несколько их антигенных фрагментов находятся со стороны C-конца фрагмента INV согласно п. 2.
6. Полинуклеотид, кодирующий полипептид по любому из пп. 1-5, где полинуклеотид предпочтительно представляет собой ДНК или РНК, более предпочтительно ДНК.
7. Экспрессионный вектор, содержащий полинуклеотид по п. 6.
8. Коллекция из двух или более разных экспрессионных векторов для одновременного введения экспрессионных векторов, где каждый из разных векторов содержит полинуклеотид по п. 6, кодирующий разный полипептид по любому из пп. 1-5.
9. Вектор по п. 7 или коллекция векторов по п. 8, где вектор в каждом случае независимо выбран из группы, состоящей из плазмиды; космиды; липосомной частицы, вирусного вектора или вирусоподобной частицы; предпочтительно из альфавирусного вектора, вектора на основе вируса венесуэльского энцефалита лошадей (VEE), вектора на основе вируса Синдбис (SIN), вектора на основе вируса леса Семлики (SFV), вектора на основе цитомегаловируса (CMV) обезьян или человека, вектора на основе вируса лимфоцитарного хориоменингита (LCMV), ретровирусного вектора, лентивирусного вектора, аденовирусного вектора, вектора на основе аденоассоциированного вируса, вектора на основе поксвируса, вектора на основе вируса коровьей оспы или вектора на основе модифицированного вируса осповакцины Ankara (MVA), при этом аденовирусный вектор предпочтительно представляет собой вектор на основе аденовируса высших приматов, более предпочтительно вектор на основе аденовируса шимпанзе, или бонобо, или гориллы.
10. Фармацевтическая композиция, обладающая активностью энхансера Т-клеточного ответа, содержащая эффективное количество полипептида по любому из пп. 1-5, эффективное количество полинуклеотида по п. 6 или эффективное количество вектора(ов) по любому из пп. 7-9, фармацевтически приемлемое вспомогательное вещество и, необязательно, один или несколько адъювантов.
11. Фармацевтическая композиция по п. 10, содержащая по меньшей мере один иммуномодулятор, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, или вектор или липосомную частицу, содержащую полинуклеотид, кодирующий иммуномодулятор.
12. Набор для усиления активности Т-клеточного ответа, содержащий фармацевтическую композицию по п. 10 и отдельно упакованный по меньшей мере один иммуномодулятор, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, или вектор, содержащий полинуклеотид, кодирующий иммуномодулятор.
13. Фармацевтическая композиция по п. 10 или набор по п. 12, где:
(i) иммуномодулятор представляет собой MCM и выбран из группы, состоящей из:
(a) агониста члена суперсемейства рецепторов фактора некроза опухолей (TNF), предпочтительно CD27, CD40 (например, CP-870,893), OX40, GITR или CD137; и/или
(b) антагониста PD-1, CD274, A2AR, B7-H3 (например, MGA271), B7-H4, BTLA, CTLA-4, IDO, KIR, LAG3, TIM-3 или VISTA, или антагониста члена суперсемейства B7-CD28, предпочтительно CD28 или ICOS, или антагониста их лиганда;
и/или
(ii) иммуномодулятор представляет собой фактор роста T-клеток, предпочтительно IL-2, IL-12 или IL-15.
14. Способ профилактики или лечения заболевания, которое будет получать благоприятный эффект в результате усиления Т-клеточного ответа, включающий введение субъекту, нуждающемуся в этом, полипептида по любому из пп. 1-5, полинуклеотида по п. 6, вектора или коллекции векторов по любому из пп. 7-9 или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции по любому из пп. 10-13, для предупреждения или лечения пролиферативного заболевания, вирусного заболевания, грибкового заболевания или бактериального заболевания.
15. Способ усиления Т-клеточного ответа против антигена, включающий введение субъекту, нуждающемуся в этом, полипептида по любому из пп. 1-5, полинуклеотида по п. 6, вектора или коллекции векторов по любому из пп. 7-9 или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции по любому из пп. 10-13, для предупреждения или лечения пролиферативного заболевания, вирусного заболевания, грибкового заболевания или бактериального заболевания.
16. Применение полипептида по любому из пп. 1-5, полинуклеотида по п. 6,
вектора или коллекции векторов по любому из пп. 7-9 или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции по любому из пп. 10-13, для усиления Т-клеточного ответа против антигена для предупреждения или лечения пролиферативного заболевания, вирусного заболевания, грибкового заболевания или бактериального заболевания.
17. Способ по п. 14 или 15 или применение по п. 16, где пролиферативное заболевание представляет собой рак.
18. Способ или применение по п. 17, где рак выбран из группы, состоящей из злокачественных новообразований губ, ротовой полости, глотки, пищеварительного органа, органа дыхания, органа грудной полости, кости, суставного хряща, кожи, мезотелиальной ткани, мягкой ткани, молочной железы, женских половых органов, мужских половых органов, мочевых путей, головного мозга и других частей центральной нервной системы, щитовидной железы, желез внутренней секреции, лимфоидной ткани и гемопоэтической ткани.
19. Способ или применение по п. 17 или 18, причем по меньшей мере один иммуномодулятор, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, или вектор или липосомная частица, содержащие полинуклеотид, который кодирует иммуномодулятор, вводятся до, одновременно или после введения полипептида по любому из пп. 1-5, полинуклеотида по п. 6, вектора или коллекции векторов по любому из пп. 7-9 или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции, по любому из пп. 10-13.
| WO 2015082922 A1, 11.06.2015 | |||
| CAPONE S | |||
| et al.: "Fusion of HCV nonstructural antigen to MHC class II-associated invariant chain enhances T-cell responses induced by vectored vaccines in nonhuman primates", Mol Ther., 2014, v | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| SPENCER A.J | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
Авторы
Даты
2023-04-12—Публикация
2018-11-02—Подача