Настоящее изобретение относится к полипептидам, содержащим фрагмент инвариантной цепи из костистых рыб, необязательно слитый с одним или несколькими антигенами, или инвариантную цепь из костистых рыб, слитую с одним или несколькими антигенами или их антигенными фрагментами, полинуклеотид, кодирующий такие полипептиды, векторы, содержащие такие полинуклеотиды, набор векторов, содержащих такие полинуклеотиды, и применение таких полипептидов, полинуклеотидов, векторов для лечения или предотвращения пролиферативного заболевания, предпочтительно рака, вирусного заболевания, грибкового заболевания или бактериального заболевания. Полипептиды инвариантных цепей из костистых рыб или их фрагменты действуют как «усилитель Т-клеток», преобразуя неиммуногенные антигенные последовательности в иммуногенные Т-клеточные антигены.
Уровень техники изобретения
Иногда вакцины вызывают субоптимальный или не являющийся Т-клеточным иммунный ответ. Данный феномен слабой индукции Т-клеточного иммунного ответа чаще наблюдается в случае вакцинации, нацеленной на антигены, которые являются либо полностью собственными молекулами, например, специфичными для рака антигенами, либо частично собственными, например, раковыми неоантигенами. Специфичные для рака неоантигены, в основном, происходят из точечных мутаций в кодирующих областях генов, которые приводят к несинонимичным однонуклеотидным вариантам, приводящим к изменению одной аминокислоты. Изменение одной аминокислоты в последовательности белка очень редко приводит к появлению нового эпитопа, способного вызвать мощный иммунный ответ. В большинстве случаев такое небольшое изменение либо вообще не приводит к созданию нового эпитопа, либо может генерировать очень слабый. Из-за ранее существовавшей центральной толерантности к аутоантигенам индукция мощных иммунных ответов против онкоспецифических антигенов посредством вакцинации остается сложной задачей. Чтобы преодолеть недостаток или низкую иммуногенность онкоспецифических антигенов и неоантигенов, было использовано несколько стратегий для восстановления недостаточной/низкой иммуногенности некоторых генетических вакцин. Было показано, что инвариантная цепь (Invariant chain (INV)) усиливает индукцию CD8+ Т-клеток в контексте генетической вакцинации. Инвариантная цепь представляет собой белок-шаперон, относящийся к молекулам класса II главного комплекса гистосовместимости (МНС), необходимый для их созревания и сборки. INV также играет роль в представлении антигенных пептидов, и было продемонстрировано, что она увеличивает индукцию Т-клеток при слиянии с антигеном в контексте генетической вакцинации. Описана улучшенная способность к иммунизации лентивирусным вектором, экспрессирующим овальбумин, слитый с INV (Rowe et al, 2006 Mol Ther 13(2) 310-9). Впоследствии в различных сообщениях была документально подтверждена повышенная индукция CD8+ Т-клеточных ответов аденовирусом 5 человека и векторами плазмидной ДНК, экспрессирующими слитые с INV антигены.
При противораковой вакцинации важно предотвращать избегания опухолью иммунологического ответа благодаря появлению новых онкоспецифических антигенов, не распознаваемых индуцированными вакциной Т-клетками. Задача противораковой вакцины в лечении рака состоит в том, чтобы индуцировать разнообразную популяцию иммунных Т-клеток, способных распознавать и устранять как можно большее количество раковых клеток одновременно, чтобы снизить вероятность того, что раковые клетки смогут «ускользнуть» от ответа Т-лимфоцитов. Следовательно, желательно, чтобы вакцина кодировала довольно большое количество онкоспецифических антигенов. Это особенно актуально для недавно описанного подхода персонализированной вакцинации на основе онкоспецифических неоантигенов. Чтобы оптимизировать вероятность успеха, вакцина должна быть направлена на как можно большее количество неоантигенов, однако, максимальный размер вставки в вектор ограничен. Полноразмерные последовательности INV или их большие фрагменты занимают относительно большую часть вставки вакцинного антигена. Следовательно, применение короткого полипептида в качестве усилителя Т-клеток предпочтительно в контексте противораковой вакцинации, особенно при использовании в вакцине нескольких онкоспецифических антигенов.
Платформы для генетической вакцинации на основе аденовируса, в частности, вирусный вектор аденовируса, происходящего от человекообразных обезьян (Great Apes derived Adenovirus (GAd)), оказались очень эффективными для индукции Т-клеточных ответов, и аденовирусы, полученные от человекообразных обезьян, подходят для кодирования больших антигенов в формате искусственных генов, состоящих из полинуклеотидов, кодирующих фрагменты из разных белков, связанных друг за другом (Borthwick, N., et al., Mol Ther, 2014. 22(2): p.464-75). Неожиданно, при использовании в контексте онкоспецифических неоантигенов опосредованный Т-клетками иммунный ответ не индуцировался.
Авторы настоящего изобретения идентифицировали специфические последовательности INV, способные восстанавливать иммуногенность. Такие последовательности INV были подходящими для преодолевания отсутствия или слабой иммуногенности онкоспецифических неоантигенов. В частности, были идентифицированы два коротких фрагмента не относящейся к человеку INV костистых рыб (Teleostei), оба не включающие трансмембранный домен, которые действовали как мощные усилители Т-клеток.
Использование человеческих INV или INV филогенетически близких видов может привести к нежелательной индукции иммунного ответа против данной собственной последовательности в контексте вакцинации. В данном случае, аутоиммунный ответ будет направлен на нормальные ткани, в которых экспрессируется INV. Авторы настоящего изобретения неожиданно обнаружили, что INV костистых рыб, хотя и сильно отличаясь от INV у млекопитающих, усиливают Т-клеточный ответ на антигены у млекопитающих, что данный эффект усиления Т-клеточного ответа проявляется для множества антигенов, слитых с инвариантной цепью костистых рыб, и что уже короткого фрагмента INV костистых рыб достаточно, чтобы вызвать такой ответ. Таким образом, настоящее изобретение обеспечивает, помимо прочего: (i) улучшенный усилитель Т-клеточного ответа на антигены у млекопитающих, отличающийся пониженной вероятностью индукции нежелательного Т-клеточного ответа против здоровой ткани, (ii) усилитель Т-клеточного ответа против множества антигенов и (iii) короткий фрагмент, способный вызывать иммунный ответ Т-клетки, что максимально увеличивает способность к слиянию большого количества антигенов или их антигенных фрагментов.
Краткое содержание изобретения
В первом аспекте изобретения изобретение относится к полипептиду, содержащему: (а) фрагмент инвариантной цепи (INV) Teleostei (группы костистых рыб), включающий или состоящий из от 16 до 27 смежных аминокислот мембранного проксимального домена (membrane proximal domain (MPD)) в INV Teleostei, где фрагмент обладает активностью, усиливающей Т-клеточный ответ, и MPD характеризуется аминокислотной последовательностью, выбранной из:
(i) NQRX1DIKSLEEQX2SX3LX4X5X6X7TX8GRSX9X10 (SEQ ID NO: 001) в которой
X1 представляет собой G или N, Х2 представляет собой Н или N, Х3 представляет собой G или N, Х4 представляет собой N или Q, Х5 представляет собой Е или А, Х6 представляет собой Q или Е, Х7 представляет собой L или М, X8 представляет собой K или R, Х9 представляет собой А или V и Х10 представляет собой S или А; и где фрагмент предпочтительно по меньшей мере на 60% идентичен SEQ ID NO: 3; или
(ii) DQKQQIQZ1LQZ2Z3NQRZ4EKQZ5Z6Z7RZ8RZ9S (SEQ ID NO: 8) в которой
Z1 представляет собой G или D, Z2 представляет собой Т или A, Z3 представляет собой Т или S, Z4 представляет собой L или М, Z5 представляет собой М или V, Z6 представляет собой G или S, Z7 представляет собой Q или L, Z8 представляет собой Р или S, и Z9 представляет собой Е или V;
и где фрагмент предпочтительно по меньшей мере на 60% идентичен SEQ ID NO: 10;
и необязательно один или несколько антигенов и/или один или несколько их антигенных фрагментов;
или
(b) полноразмерную INV Teleostei, выбранную из SEQ ID NO: 2, 5, 9 или 12, или их вариантов, которая обладает активностью, усиливающей Т-клеточный ответ, где аминокислотная последовательность MPD варианта по меньшей мере на 60% идентична SEQ ID NO: 3 или 10, и один или несколько антигенов и/или один или несколько их антигенных фрагментов.
Во втором аспекте изобретение дополнительно относится к полинуклеотиду, кодирующему полипептид согласно первому аспекту изобретения, где полинуклеотид представляет собой ДНК или РНК, предпочтительно ДНК.
В третьем аспекте изобретение относится к вектору, содержащему полинуклеотид согласно второму аспекту изобретения.
В четвертом аспекте изобретение относится к набору из двух или более различных векторов, где каждый из различных векторов содержит полинуклеотид согласно второму аспекту изобретения, кодирующий отличный от других полипептид согласно первому аспекту изобретения.
В пятом аспекте изобретение относится к фармацевтической композиции, содержащей полипептид по первому аспекту изобретения, полинуклеотид по второму аспекту изобретения или вектор/набор векторов по третьему или четвертому аспекту изобретения, фармацевтически приемлемый наполнитель и необязательно один или несколько адъювантов.
В шестом аспекте изобретение относится к набору из частей, содержащему фармацевтическую композицию по пятому аспекту изобретения и отдельно упакованный по меньшей мере один иммуномодулирующий полинуклеотид или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, или вектор, содержащий полинуклеотид, кодирующий иммуномодулятор.
В седьмом аспекте изобретение относится к полипептиду согласно первому аспекту, полинуклеотиду согласно второму аспекту, вектору или набору векторов согласно третьему или четвертому аспекту, или фармацевтической композиции или наборам, включающим такие фармацевтические композиции согласно пятому или шестому аспекту для применения в предотвращении или лечении пролиферативного заболевания, предпочтительно рака, вирусного заболевания, грибкового заболевания или бактериального заболевания.
Список фигур
Далее описывается содержание фигур, содержащихся в данном описании. В данном контексте также обратитесь к подробному описанию изобретения выше и/или ниже.
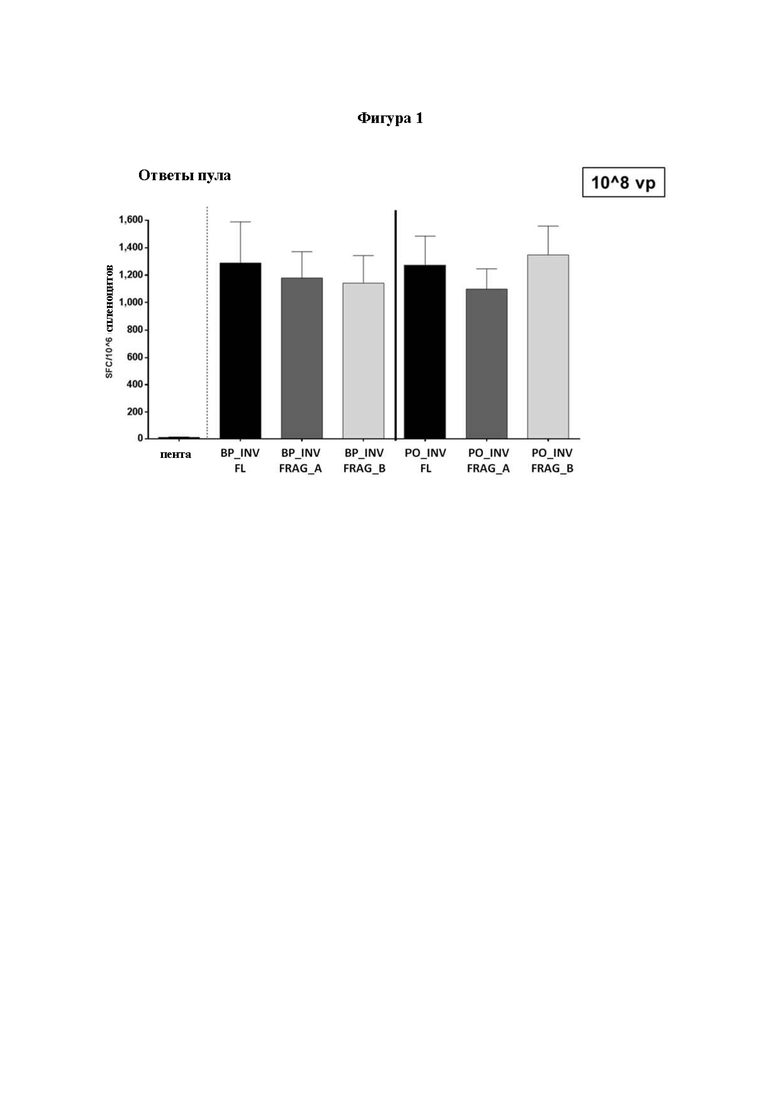
Фигура 1; Иммуногенность векторов GAd-пента (пента) и GAd, кодирующих полноразмерные инвариантные цепи BP и РО (BP_INV FL [SEQ ID NO: 9] и PO_INV_FL [SEQ ID NO: 2]) или их фрагменты FRAG_A (BP_INV FRAG_A [SEQ ID NO: 10] и PO_INV FRAG_A [SEQ ID NO: 3]) и FRAG_В (BP_INV FRAG_В [SEQ ID NO: 11] и PO_INV FRAG_В [SEQ ID NO: 4]), связанные с N-концом пента-антигена. Мышей (n=5-6/группу) иммунизировали с 108 vp каждого вектора и через 2 недели измеряли иммунные ответы с помощью анализа ELISpot на селезенке. Показаны средние ответы (количество Т-клеток, продуцирующих IFNγ на миллионы спленоцитов) на пул из 5 синтетических пептидов, соответствующих последовательностям неоантигенов, кодируемых пентатопом. Показанные значения являются средними +/- SEM из измерений, проведенных на 5-6 мышах/группа.
Подробное описание изобретения
Прежде чем настоящее изобретение будет подробно описано ниже, следует понимать, что данное изобретение не ограничивается конкретной методологией, протоколами и реагентами, описанными в данном документе, поскольку они могут варьироваться. Также следует понимать, что используемая в данном документе терминология предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения, которое будет ограничено только прилагаемой формулой изобретения. Если не указано иное, все технические и научные термины, используемые в данном документе, имеют те же значения, которые обычно понимаются специалистом в данной области техники.
Предпочтительно, чтобы используемые в данном документе термины были определены, как описано в «А multilingual glossary of biotechnological terms: (IUPAC Recommendations)», Leuenberger, HGW, Nagel, B. and Klbl, H. eds. (1995), Helvetica Chimica Acta, CH-4010 Basel, Switzerland) и как описано в Pharmaceutical Substances: Syntheses, Patents, Applications)) Axel Kleemann and Jurgen Engel, Thieme Medical Publishing, 1999; the "Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals", edited by Susan Budavari et al., CRC Press, 1996, и the United States Pharmacopeia-25/National Formulary-20, published by United States Pharmcopeial Convention, Inc., Rockville Md., 2001.
Во всем данном описании и формуле изобретения, которая следует за ним, если контекст не требует иного, слово «содержать» и варианты, такие как «включает» и «содержащий», будут пониматься как подразумевающие включение указанного признака, целого числа, стадии или группы признаков, целых чисел или стадий, но не исключение любого другого признака, целого числа, стадии или группы целых чисел или стадий. В следующих отрывках более подробно описаны различные аспекты изобретения. Каждый аспект, определенный таким образом, может быть объединен с любым другим аспектом или аспектами, если явно не указано иное. В частности, любой признак, указанный как предпочтительный или преимущественный, может быть объединен с любым другим признаком или признаками, указанными как предпочтительные или преимущественные.
В тексте данной спецификации цитируется несколько документов. Каждый из документов, процитированных в данном документе (включая все патенты, заявки на патенты, научные публикации, спецификации производителя, инструкции и т.д.), как выше, так и ниже, полностью включен сюда посредством ссылки. Ничто в данном документе не должно толковаться как признание того, что изобретение не имеет права датировать такое раскрытие задним числом на основании предшествующего изобретения. Некоторые из процитированных в данном документе документов охарактеризованы как «включены посредством ссылки». В случае противоречия между определениями или идеями таких включенных ссылок и определениями или идеями, изложенными в настоящем описании, текст настоящего описания имеет преимущественную силу.
Далее будут описаны элементы настоящего изобретения. Данные элементы перечислены с конкретными вариантами осуществления, однако, следует понимать, что они могут быть объединены любым способом и в любом количестве для создания дополнительных вариантов осуществления. Различные описанные примеры и предпочтительные варианты осуществления не должны толковаться как ограничивающие настоящее изобретение только явно описанными вариантами осуществления. Следует понимать, что данное описание поддерживает и охватывает варианты осуществления, которые объединяют явно описанные варианты осуществления с любым количеством раскрытых и/или предпочтительных элементов. Кроме того, любые перестановки и комбинации всех описанных элементов в данной заявке должны считаться раскрытыми в описании настоящей заявки, если контекст не указывает иное.
Определения
Для практического применения настоящего изобретения, если не указано иное, используются обычные способы химии, биохимии и технологии рекомбинантной ДНК, которые описаны в соответствующей литературе (см., например, Molecular Cloning: А Laboratory Manual, 2nd Edition, J. Sambrook et al. eds., Cold Spring Harbor Laboratory Press, Cold Spring Harbor 1989).
Далее приведены некоторые определения терминов, часто используемых в данной спецификации. Данные термины в каждом случае их использования в оставшейся части описания будут иметь соответственно определенное значение и предпочтительные значения.
Как используется в данном описании и прилагаемой формуле изобретения, формы единственного числа включают в себя ссылки во множественном числе, если содержание явно не указывает иное.
Термин трансмембранный домен (TMD), используемый в настоящем изобретении для обозначения TMD последовательностей инвариантной цепи (INV), определяется как аминокислотный сегмент, начинающийся с 17 остатков, расположенных в направлении N-конца от остатка Gln (Q), консервативного во всех INV, и заканчивающийся 8 остатками, расположенными в направлении С-конца от консервативного Q, таким образом, включая в общей сложности 26 остатков.
Термин «мембранный проксимальный домен» (MPD) используется в настоящем изобретении для обозначения сегмента из 27 остатков непосредственно с С-конца TMD INV-последовательностей.
Термин «адъювант» используется в настоящем изобретении как вещества, которые усиливают иммунный ответ на антиген. Кроме того, адъювантами также служат вещества, которые могут помочь в стабилизации составов антигенов. Адъюванты добавляются к вакцинам для стимуляции ответа иммунной системы на целевой антиген, но сами по себе не обеспечивают иммунитета. Адъюванты необходимы для улучшения маршрутизации и адаптивного иммунного ответа на антигены. Эффекты адъювантов обусловлены различными механизмами. Например, увеличивая присутствие антигена в крови и/или помогая антигенпрезентирующим клеткам поглощать антиген, и/или активируя макрофаги и лимфоциты, и/или поддерживая продукцию цитокинов. Некоторые адъюванты, такие как квасцы, действуют как системы доставки, генерируя депо, которые улавливают антигены в месте инъекции, обеспечивая медленное высвобождение, которое продолжает стимулировать иммунную систему. Среди описанных типов адъювантов: i) Неорганические соединения: квасцы, гидроксид алюминия, фосфат алюминия, гидроксид фосфата кальция ii) Минеральное масло: парафиновое масло iii) Бактериальные продукты: убитые бактерии Bordetella pertussis, Mycobacterium bovis, токсоиды iv) Небактериальные органические вещества: сквален, v) Системы доставки: детергенты (Quil A), vi) растительные сапонины из Quillaja (см. Quillaia), сои, Polygala senega, vii) Цитокины: IL-1, IL-2, IL-12, viii) Комбинация: полный адъювант Фрейнда, неполный адъювант Фрейнда.
Термин «иммуномодулятор» используется в настоящем изобретении для обозначения любого лекарственного препарата или вещества, которое оказывает влияние на иммунную систему. Иммуномодулятор может регулировать иммунный ответ до нужного уровня посредством: i) усиления слабой иммунной системы; ii) контроля сверхактивной иммунной системы. Особым классом иммуномодуляторов, способных усиливать слабую иммунную систему, являются модуляторы молекул иммунологических контрольных точек (МСМ), состоящие из
i) агонистических активаторных МСМ, таких как член суперсемейства рецепторов фактора некроза опухоли (TNF), предпочтительно CD27, CD40, ОХ40, GITR или CD137
ii) антагонистических ингибирующих МСМ, таких как PD-1, CD274, A2AR, В7-Н3, В7-Н4, BTLA, CTLA-4, IDO, KTR, LAG3, TIM-3, VISTA или член суперсемейства B7-CD28, CD28 или ICOS, или антагонист его лиганда.
Другой класс иммуномодуляторов, которые могут усилить слабую иммунную систему, представляет собой цитокины, которые действуют как факторы роста Т-клеток. Предпочтительными примерами таких цитокинов являются IL-2, IL-12, IL-15 или TL-17.
Термин «антиген» используется в контексте настоящего изобретения для обозначения любой структуры, распознаваемой молекулами иммунного ответа, например, антител, рецепторов Т-клеток (TCR) и тому подобного. Предпочтительные антигены представляют собой клеточные или чужеродные (например, вирусные, бактериальные или грибковые) белки, которые связаны с конкретным заболеванием. Антигены распознаются высоковариабельными антигенными рецепторами (В-клеточным рецептором или Т-клеточным рецептором) адаптивной иммунной системы и могут вызывать гуморальный или клеточный иммунный ответ. Антигены, которые вызывают такой ответ, также называют иммуногенами. Часть белков внутри клеток, независимо от того, являются ли они чужеродными или клеточными, перерабатываются в более мелкие пептиды и представляются главным комплексом гистосовместимости (МНС).
Термин «его антигенный фрагмент» относится к части данного антигена, которая все еще распознается молекулой иммунной системы. Антигенный фрагмент будет содержать по меньшей мере один эпитоп или антигенную детерминанту. Предпочтительно антигенные фрагменты по изобретению содержат по меньшей мере один Т-клеточный эпитоп.
Термин «эпитоп», также известный как антигенная детерминанта, используется в контексте настоящего изобретения для обозначения сегмента антигена, предпочтительно пептида, который связывается молекулами иммунной системы, например, рецепторами В-клеток, Т-клеточными рецепторами или антителами. Эпитопы, связанные с антителами или В-клетками, называются «эпитопами В-клеток», и эпитопы, связанные с Т-клетками, называются «эпитопами Т-клеток». В данном контексте термин «связывание» предпочтительно относится к специфическому связыванию, которое определяется как связывание с константой ассоциации между антителом или Т-клеточным рецептором (TCR) и соответствующим эпитопом, составляющей 1 х 105 М-1 или выше, предпочтительно 1 х 106 М-1, 107 М-1, 1 х 108 М-1 или выше. Квалифицированный специалист хорошо знает, как определить константу ассоциации (см., например, Caoili, SE (2012) Advances in Bioinformatics Vol.2012). Предпочтительно, специфическое связывание антителе эпитопом опосредуется участком Fab ((fragment, antigen binding) фрагмент, связывание антигена) антитела, специфическое связывание В-клетки опосредуется Fab-участком антитела, содержащимся в В-клеточном рецепторе, и специфическое связывание Т-клетки опосредуется вариабельной (V) областью Т-клеточного рецептора. Т-клеточные эпитопы представлены на поверхности антигенпрезентирующей клетки, где они связаны с молекулами главной гистосовместимости (МНС). Существует по меньшей мере два разных класса молекул МНС, называемых МНС классом I и II, соответственно. Эпитопы, представленные через путь MHC-I, вызывают ответ цитотоксических Т-лимфоцитов (CD8+ клетки), тогда как эпитопы, представленные через путь МНС-II, вызывают ответ Т-хелперных клеток (CD4+ клетки). Т-клеточные эпитопы, представленные молекулами МНС класса I, обычно представляют собой пептиды длиной от 8 до 11 аминокислот, и Т-клеточные эпитопы, представленные молекулами МНС класса II, обычно представляют собой пептиды длиной от 13 до 17 аминокислот. Молекулы МНС класса III также представляют непептидные эпитопы в виде гликолипидов. Соответственно, термин «Т-клеточный эпитоп» предпочтительно относится к пептиду длиной от 8 до 11 или от 13 до 17 аминокислот, который может быть представлен молекулой МНС класса I или МНС класса II. Эпитопы обычно состоят из химически активных поверхностных группировок аминокислот, которые могут нести или не содержать боковые цепи сахара и обычно имеют специфические трехмерные структурные характеристики, а также специфические характеристики заряда. Конформационные и неконформационные эпитопы различаются тем, что связывание с первыми, но не со вторыми, теряется в присутствии денатурирующих растворителей.
Понятие «специфичный для рака антиген» используется в контексте настоящего изобретения для обозначения белка, который специфически экспрессируется в раковых клетках или более распространен в раковых клетках, чем в здоровых клетках. Специфичные для рака антигены включают следующие типы антигенов:
(i) онкофетальный (обычно экспрессируется только в тканях плода и в раковых соматических клетках); или
(ii) онковиральный (кодируется онкогенными трансформирующими клетки вирусами); или
(iii) сверхэкспрессии/накопления (экспрессируется как нормальной, так и неопластической тканью, с высоким уровнем экспрессии при неоплазии), например, тирозиназа в меланомах или рецептор Her-2 при раке груди; или
(iv) рак-яичко (экспрессируется только раковыми клетками и репродуктивными тканями взрослых, такими как семенники и плацента); или
(v) ограниченный по происхождению (экспрессируемый, в основном, одним гистотипом рака); или
(vi) специфическая для рака изоформа (изменение экзонного состава транскрипта).
Понятие «онкоспецифический неоантиген» используется в контексте настоящего изобретения для обозначения антигена, не присутствующего в нормальных клетках/к летках зародышевой линии, но встречающегося в трансформированных, в частности, раковых клетках. Онкоспецифический неоантиген может содержать один или несколько, например, 2, 3, 4, 5 или более неоэпитопов. Предпочтительно, чтобы длина каждого онкоспецифического неоантигена, включенного в полипептид по настоящему изобретению, была выбрана таким образом, чтобы убедиться, что они имеют низкую вероятность включения эпитопов, которые встречаются в нормальных клетках/клетках зародышевой линии. Обычно это подтверждается тем, что онкоспецифический неоантиген содержит 12 или менее аминокислот на С-конце и/или на N-конце аминокислотного изменения (изменений), которое привело к образованию неоэпитопа.
Онкоспецифический неоантиген предпочтительно генерируется мутацией, происходящей на уровне ДНК, и где мутированный белок может включать а) одно или несколько одиночных аминокислотных (аа) изменений, вызванных несинонимичной точечной мутацией SNV; и/или
b) аминокислотную последовательность не дикого типа в результате вставок/делеций, приводящих к пептиду со сдвигом рамки считывания; и/или
c) аминокислотную последовательность не дикого типа в результате изменения границ экзонов или мутаций, вызывающих удержание интрона; и/или
d) мутированный онкобелок, образованный в результате слияния генов.
Неоантиген, который является результатом одного или нескольких изменений одной аминокислоты, вызванного геномной точечной мутацией несинонимичного SNV, в контексте настоящего изобретения упоминается как мутантный пептид по одной аминокислоте.
Термин «полинуклеотид» или «нуклеиновая кислота» включает полимеры как одноцепочечных, так и двухцепочечных нуклеотидов. Нуклеотиды, составляющие полинуклеотид, могут быть рибонуклеотидами или дезоксирибонуклеотидами или модифицированной формой любого типа нуклеотида. Указанные модификации включают модификации оснований, такие как производные бромуридина и инозина, модификации рибозы, такие как 2',3'-дидезоксирибоза, и модификации межнуклеотидных связей, такие как фосфоротиоат, фосфородитиоат, фосфороселеноат, фосфородиселеноат, фосфоранилотиоат, фосфорораниладат и фосфориладат. Примерами полинуклеотидов являются ДНК и РНК.
«Выделенный полинуклеотид» представляет собой ДНК или РНК геномного, мРНК, кДНК или синтетического происхождения или их комбинацию, которая не связана со всем или с частью полинуклеотида, в котором выделенный полинуклеотид встречается в природе, или связан с полинуклеотидом, с которым он не связан в природе.
Термин «экспрессионная кассета» используется в контексте настоящего изобретения для обозначения полинуклеотида, который содержит по меньшей мере одну последовательность нуклеиновой кислоты, которая должна быть экспрессирована, например, нуклеиновую кислоту, кодирующую цепочку онкоспецифических неоантигенов, слитых с инвариантной цепью по настоящему изобретению или ее фрагментами, функционально связанную с последовательностями контроля транскрипции и/или трансляции. Предпочтительно экспрессионная кассета включает цис-регулирующие элементы для эффективной экспрессии данного гена, такие как промотор, сайт инициации и/или сайт полиаденилирования. Предпочтительно экспрессионная кассета содержит все дополнительные элементы, необходимые для экспрессии полинуклеотида в клетке пациента. Таким образом, типичная экспрессионная кассета содержит промотор, оперативно связанный с экспрессируемой полинуклеотидной последовательностью, и сигналы, необходимые для эффективного полиаденилирования транскрипта, сайтов связывания рибосом и терминации трансляции. Дополнительные элементы кассеты могут включать, например, усилители. Кассета экспрессии предпочтительно также содержит область терминации транскрипции ниже структурного гена по направлению транскрипции для обеспечения эффективной терминации. Терминаторная область может быть получена из того же гена, что и промоторная последовательность, или может быть получена из другого гена.
Термин «оперативно связанный», используемый в контексте настоящего изобретения, относится к расположению элементов, при котором компоненты так описаны и составлены, чтобы выполнять свои обычные функции. Полинуклеотид является «оперативно связанным», если он находится в функциональной связи с последовательностью другой нуклеиновой кислоты. Например, промотор оперативно связан с одним или несколькими трансгенами, если он воздействует на транскрипцию одного или нескольких трансгенов. Кроме того, элементы управления, оперативно связанные с кодирующей последовательностью, способны воздействать на экспрессию кодирующей последовательности. Элементы управления не обязательно должны прилегать к кодирующей последовательности, до тех пор, пока они функционируют как направляющие ее экспрессию. Таким образом, например, между промоторной последовательностью и кодирующей последовательностью могут присутствовать промежуточные нетранслируемые, но транскрибируемые последовательности, и промоторная последовательность все еще может рассматриваться как «оперативно связанная» с кодирующей последовательностью.
Термины «вектор» или «экспрессионный вектор» используются взаимозаменяемо и относятся к полинуклеотиду, полинуклеотиду в оболочке некоторого типа, например, вирусной оболочке или липосоме, или полинуклеотиду в комплексе с белками, которые могут вводиться или вводить полинуклеотид по настоящему изобретению в клетку, предпочтительно клетку млекопитающего. Примеры векторов включают, но не ограничиваются ими, плазмиды, космиды, фаги, липосомы, вирусы или искусственные хромосомы. В частности, вектор используется для транспортировки промотора и полинуклеотида по изобретению в подходящую клетку-хозяин. Экспрессионные векторы могут содержать полинуклеотидные последовательности «репликон», которые способствуют автономной репликации экспрессионного вектора в клетке-хозяине. Попав в клетку-хозяин, экспрессионный вектор может реплицироваться независимо от хромосомной ДНК хозяина или одновременно с ней, и могут быть созданы несколько копий вектора и вставленной в него ДНК. В случае использования экспрессионных векторов, не способных к репликации, что часто имеет место по соображениям безопасности, вектор может не реплицироваться, а просто направлять экспрессию полинуклеотида. В зависимости от типа экспрессионного вектора, экспрессионный вектор может быть утерян из клетки, то есть он только временно экспрессирует неоантигены, кодируемые полинуклеотидом, или он может быть стабильным в клетке. Экспрессионные векторы обычно содержат экспрессионные кассеты, т.е. необходимые элементы, которые позволяют транскрипцию полинуклеотида в молекулу мРНК. Если полинуклеотид представляет собой РНК, транскрипция не требуется и, следовательно, молекулам РНК требуются только элементы контроля трансляции.
Понятие «аминокислотная последовательность усилителя Т-клеток» относится к полипептидной последовательности, которая, при слиянии с антигенной последовательностью, увеличивает индукцию Т-клеток в контексте генетической вакцинации.
Термины «препарат» и «композиция», используемые в контексте настоящего изобретения, предназначены для включения состава активного соединения, например, вектора аденовируса человекообразных обезьян по настоящему изобретению, с носителем и/или наполнителем.
«Фармацевтически приемлемый», используемый в контексте настоящего изобретения, означает одобренный регулирующим органом федерального правительства или правительства штата или перечисленный в Фармакопее США или другой общепризнанной фармакопее для применения у животных и, более конкретно, у людей.
Термин «носитель», используемый в данном документе, относится к фармакологически неактивному веществу, такому как, но не ограничиваясь ими, разбавитель, наполнитель, поверхностно-активные вещества, стабилизаторы, физиологические буферные растворы или носители, с которыми вводят терапевтически активный ингредиент. Такие фармацевтические носители могут быть жидкими или твердыми. Жидкий носитель включает, но не ограничивается ими, стерильные жидкости, такие как солевые растворы в воде и маслах, включая, но не ограничиваясь ими, жидкости нефтяного, животного, растительного или синтетического происхождения, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и тому подобные. Солевые растворы и водные растворы декстрозы и глицерина также можно использовать в качестве жидких носителей, особенно для растворов для инъекций. Солевой раствор является предпочтительным носителем при внутривенном введении фармацевтической композиции. Примеры подходящих фармацевтических носителей описаны в "Remington's Pharmaceutical Sciences" E.W. Martin.
Подходящие фармацевтические «вспомогательные вещества» включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропилен, гликоль, воду, этанол и тому подобное.
«Поверхностно-активные вещества» включают анионные, катионные и неионные поверхностно-активные вещества, такие как, но не ограничиваются ими, дезоксихолат натрия, додецилсульфат натрия, Тритон Х-100, и полисорбаты, такие как полисорбат 20, полисорбат 40, полисорбат 60, полисорбат 65 и полисорбат 80.
«Стабилизаторы» включают, но не ограничиваются ими, маннит, сахарозу, трегалозу, альбумин, а также антагонисты протеаз и/или нуклеаз.
«Физиологический буферный раствор», который можно использовать в контексте настоящего изобретения, включает, но не ограничивается ими, раствор хлорида натрия, деминерализованную воду, а также подходящие органические или неорганические буферные растворы, такие как, но не ограничиваясь ими, фосфатный буфер, цитратный буфер, трис-буфер (трис(гидроксиметил)аминометан), буфер HEPES ([4(2-гидроксиэтил)пиперазино]этансульфоновая кислота) или буфер MOPS (3-морфолино-1-пропансульфоновая кислота). Выбор соответствующего буфера обычно зависит от желаемой молярности буфера. Фосфатный буфер подходит, например, для растворов для инъекций и инфузий.
«Эффективное количество» или «терапевтически эффективное количество» представляет собой количество терапевтического средства, достаточное для достижения намеченной цели. Эффективное количество данного терапевтического средства будет варьироваться в зависимости от таких факторов, как природа средства, способ введения, размер и вид животного, получающего терапевтическое средство, и цель введения.
Эффективное количество в каждом индивидуальном случае может быть определено эмпирически специалистом в соответствии со способами, установленными в данной области техники.
Используемые в данном документе термины «лечить», «пролечить», «лечение» или «терапия» заболевания или расстройства означают выполнение одного или нескольких из следующих действий: (а) снижение тяжести расстройства; (b) ограничение или предотвращение развития симптомов, характерных для расстройств, подлежащих лечению; (c) подавление обострения симптомов, характерных для расстройств, подлежащих лечению; (d) ограничение или предотвращение рецидива расстройства (расстройств) у человека, который ранее страдал данным расстройством (расстройствами); и (е) ограничение или предотвращение повторения симптомов у людей, у которых ранее проявлялись симптомы расстройства (расстройств).
Варианты осуществления
Ниже более подробно описаны различные аспекты изобретения. Каждый аспект, определенный таким образом, может быть объединен с любым другим аспектом или аспектами, если явно не указано иное. В частности, любой признак, указанный как предпочтительный или преимущественный, может быть объединен с любым другим признаком или признаками, указанными как предпочтительные или преимущественные.
В первом аспекте изобретения изобретение относится к полипептиду, содержащему: (а) фрагмент инвариантной цепи (INV) Teleostei (группы костистых рыб), включающий или состоящий из от 16 до 27 смежных аминокислот мембранного проксимального домена (membrane proximal domain (MPD)) в INV из Teleostei, где фрагмент обладает активностью, усиливающей Т-клеточный ответ, и MPD характеризуется аминокислотной последовательностью, выбранной из:
(i) NQRX1DIKSLEEQX2SX3LX4X5X6X7TX8GRSX9X10 (SEQ ID NO: 001)
в которой
X1 представляет собой G или N, Х2 представляет собой Н или N, Х3 представляет собой G или N, Х4 представляет собой N или Q, Х5 представляет собой Е или А, Х6 представляет собой Q или Е, Х7 представляет собой L или М, X8 представляет собой K или R, Х9 представляет собой А или V и Х10 представляет собой S или А;
и где фрагмент предпочтительно по меньшей мере на 60% идентичен SEQ ID NO: 3; или
(ii) DQKQQIQZ1LQZ2Z3NQRZ4EKQZ5Z6Z7RZ8RZ9S (SEQ ID NO: 8)
в которой
Z1 представляет собой G или D, Z2 представляет собой Т или A, Z3 представляет собой Т или S, Z4 представляет собой L или М, Z5 представляет собой М или V, Z6 представляет собой G или S, Z7 представляет собой Q или L, Z8 представляет собой Р или S, и Z9 представляет собой Е или V;
и где фрагмент предпочтительно по меньшей мере на 60% идентичен SEQ ID NO: 10;
и необязательно один или несколько антигенов и/или один или несколько их антигенных фрагментов;
или
(b) полноразмерную INV Teleostei, выбранную из SEQ ID NO: 2, 5, 9 или 12, или их вариантов, которая обладает активностью, усиливающей Т-клеточный ответ, где аминокислотная последовательность MPD варианта по меньшей мере на 60% идентична SEQ ID NO: 3 или 10, и один или несколько антигенов и/или один или несколько их антигенных фрагментов. Обычно желательно, чтобы фрагмент INV был как можно короче, сохраняя при этом свое стимулирующее действие на Т-клеточный антиген. Предпочтительно фрагмент содержит, более предпочтительно состоит из от 16 до 27, от 17 до 26, от 18 до 25, от 19 до 24, от 20 до 23, от 21 до 22 непрерывно расположенных аминокислот MPD INV, предпочтительно MPD согласно SEQ ID NO: 3 [MPD в PO] или 10 [MPD в ВР].
Предпочтительный минимальный фрагмент согласно альтернативе (i) первого аспекта изобретения имеет аминокислотную последовательность:
DTKSLEEQX2SX3LX4X5X6X7 (SEQ ID NO: 28) с указанным выше значением для от Х2 до Х7.
Более предпочтительный минимальный фрагмент согласно альтернативе (i) первого аспекта изобретения имеет аминокислотную последовательность DIKSLEEQHSGLNEQL (SEQ ID NO: 4) или DIKSLEEQNSNLQAEM (SEQ ID NO: 7), причем наиболее предпочтительный минимальный фрагмент представляет собой аминокислотную последовательность DIKSLEEQHSGLNEQL (SEQ ID NO: 4).
Предпочтительный минимальный фрагмент согласно альтернативе (ii) первого аспекта изобретения имеет аминокислотную последовательность:
QIQZ1LQZ2Z3NQRZ4EKQZ5 (SEQ ID NO: 29) с указанным выше значением для от Z1 до Z5.
Более предпочтительный минимальный фрагмент согласно альтернативе (ii) первого аспекта изобретения представляет собой аминокислотную последовательность QIQGLQTSNQRLEKQM (SEQ ID NO: 11) или QIQDLQATNQRMEKQV (SEQ ID NO: 14), причем наиболее предпочтительный минимальный фрагмент имеет аминокислотную последовательность QIQGLQTSNQRLEKQM (SEQ ID NO: 11).
Хотя фрагмент INV может содержать дополнительные последовательности на N-и/или С-конце MPD, предпочтительно, чтобы такие последовательности не содержались во фрагменте, и, таким образом, предпочтительно, чтобы фрагмент состоял из соответствующего непрерывного участка аминокислот MPD.
Если фрагмент INV содержит дополнительные последовательности на N- и/или С-конце MPD, предпочтительно, чтобы данный фрагмент содержал весь MPD, т.е. 27 аминокислот. Предпочтительно, чтобы фрагмент не содержал TMD, но содержал дополнительные С-концевые аминокислоты INV. Предпочтительно, чтобы данные С-концевые аминокислоты располагались непосредственно после MPD.
Последовательность MPD предпочтительно основана на последовательности MPD из Paralichthys olivaceus (PO) согласно SEQ ID NO: 003 или Boleophthalmus pectinirostris (BP) согласно SEQ ID NO: 010. Предпочтительно фрагмент содержит или состоит из 16 до 27 аминокислот MPD, причем MPD по меньшей мере на 60%, более предпочтительно по меньшей мере на 70%, более предпочтительно, по меньшей мере на 75%, более предпочтительно по меньшей мере на 80%, более предпочтительно по меньшей мере на 90% идентичен SEQ ID NO: 3 или SEQ ID NO: 010.
Фрагмент может содержать дополнительные N- и/или С-концевые аминокислотные последовательности INV. Таким образом, предпочтительно, чтобы общая длина фрагмента INV составляла от 16 до 80, от 17 до 72, от 18 до 55, от 19 до 50, от 20 до 45, от 21 до 40, от 22 до 35, от 23 до 30 смежных аминокислот.
В предпочтительном варианте осуществления полипептида по первому аспекту изобретения полипептид включает фрагмент инвариантной цепи (INV) Teleostei, содержащий или состоящий из от 16 до 27 смежных аминокислот проксимального домена мембраны (MPD) INV из Teleostei, где фрагмент обладает активностью, усиливающей Т-клеточный ответ, и MPD характеризуется аминокислотной последовательностью DIKSLEEQX2SX3LX4X5X6X7 (SEQ ID NO: 28), где Х2 представляет собой Н или N, Х3 представляет собой G или N, Х4 представляет собой N или Q, Х5 представляет собой Е или А, Х6 представляет собой Q или Е, Х7 представляет собой L или М, и при этом фрагмент предпочтительно не менее чем на 60% идентичен SEQ ID NO: 003 и, необязательно, где полипептид содержит один или несколько антигенов и/или один или несколько их антигенных фрагментов. В предпочтительном варианте осуществления полипептида по первому аспекту изобретения полипептид включает фрагмент инвариантной цепи (INV) Teleostei, содержащий или состоящий из от 16 до 27 смежных аминокислот проксимального домена мембраны (MPD) INV Teleostei, где фрагмент обладает активностью, усиливающей Т-клеточный ответ, hMPD характеризуется аминокислотной последовательностью QIQZ1LQZ2Z3NQRZ4EKQZ5 (SEQ ID NO: 29), где Z1 представляет собой G или D, Z2 представляет собой Т или A, Z3 представляет собой Т или S, Z4 представляет собой L или М, Z5 представляет собой М или V, и при этом фрагмент предпочтительно не менее чем на 60% идентичен SEQ ID NO: 10 и, необязательно, где полипептид содержит один или несколько антигенов и/или один или несколько их антигенных фрагментов.
В предпочтительном варианте осуществления полипептида по первому аспекту изобретения аминокислотная последовательность:
(a) MPD, согласно альтернативе (a) (i) по п. 1, представляет собой любую из SEQ ID NO: 3 [MPD PO] и 6 [MPDZ1];
(b) MPD, согласно альтернативе (a) (ii) по п. 1, представляет собой любую из SEQ ID NO: 10 [MPD BP] и 13 [MPD Z2]; и/или
(c) инвариантной цепи Teleostei, согласно альтернативе (b) по п. 1, представляет собой любую из SEQ ID NO: 2 и 9.
Если фрагмент состоит из от 16 до 27 аминокислот MPD из INV, предпочтительные фрагменты имеют длину от 16 до 27, от 17 до 26, от 18 до 25, от 19 до 24, от 20 до 23, от 21 до 22 непрерывных аминокислот MPD из INV согласно SEQ ID NO: 3, 6, 10 и 13.
В каждом случае, описанном выше, фрагмент или вариант обладает активностью усилителя Т-клеточного ответа. Активность усилителя Т-клеточного ответа можно измерить, как известно в данной области техники, или как изложено в прилагаемых экспериментах. Предпочтительно, чтобы активность усилителя Т-клеточного ответа составляла по меньшей мере 50%, предпочтительно по меньшей мере 80% активности усилителя Т-клеточного ответа фрагмента INV в соответствии с SEQ ID NO: 004, когда он связан с тем же антигеном или цепочкой антигенов.
В предпочтительном варианте осуществления полипептида по первому аспекту изобретения фрагмент состоит по меньшей мере из от 16 до 27 N-концевых аминокислот MPD и от 1 до 26 последовательных аминокислот трансмембранного домена (TMD) INV Teleostei непосредственно на N-конце MPD, причем TMD из INV Teleostei предпочтительно характеризуется следующей аминокислотной последовательностью (SEQ ID NO: 15)
AB1KB2B3GB4TB5LB6CB7LB8B9B10QB11B12B13B14YB15B16B17
в которой
B1 представляет собой V, L или Y, В2 представляет собой V или I, В3 представляет собой V или А, В4 представляет собой L, I или F, В5 представляет собой V, Т или L, B6 представляет собой А или V, В7 представляет собой V или L, B8 представляет собой V или I, В9 представляет собой М, S или А, В10 представляет собой S, А или G, В11 представляет собой А или V, В12 представляет собой М или F, В13 представляет собой I или Т, В14 представляет собой I или А, В15 представляет собой F или М, B16 представляет собой L, М или V, В17 представляет собой V, F или L. Если фрагмент содержит дополнительные N- и/или С-концевые аминокислотные последовательности из INV, предпочтительно, чтобы общая длина фрагмента INV составляла от 28 до 72, от 30 до 65 или от 35 до 46 смежных аминокислот.
Авторы настоящего изобретения неожиданно обнаружили, что сильный Т-клеточный ответ на два или более антигенов, предпочтительно неоантигенов, может быть индуцирован путем слияния фрагмента INV альтернативы (а) первого аспекта изобретения или INV альтернативы (b) первого аспекта изобретения с двумя или более антигенами и/или их антигенными фрагментами. Это позволяет одновременно вызывать Т-клеточный ответ против нескольких антигенов. Таким образом, что касается как альтернативы (а) первого аспекта изобретения, так и альтернативы (b) первого аспекта изобретения, предпочтительно, чтобы полипептид содержал несколько антигенов и/или их антигенных фрагментов. Например, предпочтительно, чтобы полипептид содержал по меньшей мере 5 различных антигенов и/или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 различных антигенов и/или их антигенных фрагментов, еще более предпочтительно по меньшей мере 50 различных антигенов и/или или их антигенных фрагментов, даже более предпочтительно, по меньшей мере 100 различных антигенов и/или их антигенных фрагментов, еще более предпочтительно по меньшей мере 200 различных антигенов и/или их антигенных фрагментов и даже более предпочтительно, по меньшей мере 300 различных антигенов и/или их антигенных фрагментов.
Для размещения максимального количества различных антигенов в одном полипептиде особенно предпочтительно, чтобы полипептид содержал антигенные фрагменты антигенов.
Антигены выбирают в зависимости от соответствующего терапевтического применения. Если желательна терапевтическая или профилактическая вакцинация против пролиферативного заболевания, антиген выбирают из онкоспецифического антигена или онкоспецифического неоантигена. Как указано выше, в частности, в контексте вакцинации против рака, предпочтительно, чтобы полипептид согласно первому аспекту содержал два или более разных антигена. Предпочтительно, чтобы полипептид содержал по меньшей мере 5 различных онкоспецифических антигенов или их антигенных фрагментов, более предпочтительно по меньшей мере 20 различных онкоспецифических антигенов или их антигенных фрагментов, еще более предпочтительно по меньшей мере 50 различных онкоспецифических антигенов или их антигенных фрагментов, даже больше предпочтительно, по меньшей мере 100 различных онкоспецифических антигенов или их антигенных фрагментов, еще более предпочтительно по меньшей мере 200 различных онкоспецифических антигенов или их антигенных фрагментов и даже более предпочтительно, по меньшей мере 300 различных онкоспецифических антигенов или их антигенных фрагментов. В качестве альтернативы, предпочтительно, чтобы полипептид содержал по меньшей мере 5 различных онкоспецифических неоантигенов или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 различных онкоспецифических неоантигенов или их антигенных фрагментов, даже более предпочтительно, по меньшей мере 50 различных онкоспецифических неоантигенов или их антигенных фрагментов, еще более предпочтительно по меньшей мере 100 различных онкоспецифических неоантигенов или их антигенных фрагментов, еще более предпочтительно по меньшей мере 200 различных онкоспецифических неоантигенов или их антигенных фрагментов и еще более предпочтительно по меньшей мере 300 различных онкоспецифических неоантигенов или их антигенных фрагментов. В качестве альтернативы, предпочтительно, чтобы полипептид содержал по меньшей мере 5 различных онкоспецифических антигенов или неоантигенов или их антигенных фрагментов, более предпочтительно, по меньшей мере 20 различных онкоспецифических антигенов или неоантигенов или их антигенных фрагментов, еще более предпочтительно по меньшей мере 50 различных онкоспецифических антигенов или неоантигены, или их антигенных фрагментов, даже более предпочтительно, по меньшей мере 100 различных онкоспецифических антигенов, или неоантигенов, или их антигенных фрагментов, еще более предпочтительно по меньшей мере 200 различных онкоспецифических антигенов, или неоантигенов, или их антигенных фрагментов, и даже более предпочтительно, по меньшей мере 300 различных онкоспецифических антигенов, или неоантигенов, или их антигенных фрагментов.
В качестве альтернативы, антиген представляет собой вирусный белок или его антигенный фрагмент, бактериальный белок или его антигенный фрагмент, или грибковый белок или его антигенный фрагмент.
Как правило, чтобы быть эффективной, профилактическая или терапевтическая вакцинация против вирусной, бактериальной или грибковой инфекции не требует такого количества различных антигенов, как вакцинация при терапии пролиферативных заболеваний. Тем не менее, есть некоторые вирусы, такие как, например, ВИЧ, которые характеризуются большим разнообразием эпитопов, в частности, в белках оболочки. Чтобы вызвать широкий иммунный ответ, можно включить несколько антигенов. Таким образом, предпочтительно, чтобы полипептид содержал по меньшей мере 5 различных вирусных антигенов или их антигенный фрагмент, более предпочтительно по меньшей мере 20 различных вирусных антигенов или их антигенный фрагмент, даже более предпочтительно по меньшей мере 50 различных вирусных антигенов или их антигенный фрагмент, еще более предпочтительно по меньшей мере 100 различных вирусных антигенов или их антигенный фрагмент, еще более предпочтительно по меньшей мере 200 различных вирусных антигенов или их антигенный фрагмент и еще более предпочтительно по меньшей мере 300 различных вирусных антигенов или их антигенный фрагмент. Антигены могут быть выбраны из разных штаммов одного и того же вируса и/или из разных вирусных видов. В последнем случае, вакцина позволяет иммунизовать против множества различных видов вирусов.
В качестве альтернативы, предпочтительно, чтобы указанный полипептид содержал по меньшей мере 5 различных бактериальных антигенов или антигенный фрагмент, более предпочтительно, по меньшей мере 20 различных бактериальных антигенов или антигенный фрагмент, еще более предпочтительно по меньшей мере 50 различных бактериальных антигенов или антигенный фрагмент, еще более предпочтительно по меньшей мере 100 различных бактериальных антигенов или их антигенный фрагмент, еще более предпочтительно по меньшей мере 200 различных бактериальных антигенов или их антигенный фрагмент и еще более предпочтительно по меньшей мере 300 различных бактериальных антигенов или их антигенный фрагмент.
В качестве альтернативы, предпочтительно, чтобы указанный полипептид содержал по меньшей мере 5 различных грибковых антигенов или антигенный фрагмент, более предпочтительно по меньшей мере 20 различных грибковых антигенов или антигенный фрагмент, даже более предпочтительно по меньшей мере 50 различных грибковых антигенов или антигенный фрагмент, еще более предпочтительно по меньшей мере 100 различных грибковых антигенов или их антигенный фрагмент, еще более предпочтительно по меньшей мере 200 различных грибковых антигенов или их антигенный фрагмент и еще более предпочтительно по меньшей мере 300 различных грибковых антигенов или их антигенный фрагмент.
Во всех вышеперечисленных вариантах осуществления предпочтительно, чтобы антигены были Т-клеточными антигенами. Т-клеточные антигены представляет собой антигены, которые презентируются МНС и вызывают Т-клеточный ответ.
Предпочтительно, антиген или каждый из антигенов или их антигенных фрагментов имеет (имеют) длину от 8 до 100 аминокислот, более предпочтительно от 8 до 50 и более предпочтительно от 8 до 30 аминокислот.
В предпочтительном варианте осуществления полипептида по первому аспекту изобретения один или несколько антигенов и/или один или несколько его антигенных фрагментов расположены на С-конце фрагмента INV согласно альтернативе (а) первого аспекта изобретения или полноразмерной INV согласно альтернативе (b) первого аспекта изобретения. Особенно предпочтительно, чтобы антигены и/или их антигенные фрагменты находились непосредственно на С-конце INV согласно альтернативе (а) или (b) первого аспекта изобретения.
Предпочтительно, чтобы полипептиды по изобретению продуцировались внутри клеток вакцинируемого пациента. Внутриклеточная экспрессия является предпосылкой для презентации МНС и, таким образом, стимуляции Т-клеточного ответа. Соответственно, во втором аспекте настоящее изобретение относится к полинуклеотиду, кодирующему полипептид согласно первому аспекту настоящего изобретения. Предпочтительно полинуклеотид представляет собой ДНК или РНК. РНК предпочтительно используется для прямого вызова трансляции кодируемого полипептида. ДНК, кодирующую полипептид согласно первому аспекту, обычно вставляют в экспрессионные кассеты, которые направляют транскрипцию мРНК, кодирующей полипептиды по изобретению. Однако полинуклеотид также может быть РНК, если полинуклеотид содержится в векторе и вектор представляет собой РНК-вирус. Предпочтительной РНК для прямого применения является самоамплифицирующаяся РНК (SAM). Наиболее предпочтительно полинуклеотид представляет собой ДНК.
В третьем аспекте настоящее изобретение относится к вектору, содержащему полинуклеотид согласно второму аспекту изобретения. Предпочтительно полинуклеотид по настоящему изобретению функционально связан с последовательностью контроля экспрессии.
Используют два или более векторов, если количество различных антигенов или их антигенных фрагментов, которые должны быть доставлены пациенту, настолько велико, что полинуклеотид, кодирующий полипептид слияния INV и всех антигенов или их антигенных фрагментов, не может быть размещен в выбранном векторе. Соответственно, в четвертом аспекте настоящее изобретение относится к набору двух или более различных векторов, где каждый из различных векторов содержит полинуклеотид согласно второму аспекту настоящего изобретения, кодирующий отличный от других полипептид согласно первому аспекту настоящего изобретения.
Вектор по третьему аспекту или набор векторов по четвертому аспекту, где вектор в каждом случае независимо выбран из группы, состоящей из плазмиды; космиды; липосомной частицы, вирусного вектора или вирусоподобной частицы; предпочтительно альфавирусного вектора, вектора вируса венесуэльского конского энцефалита (VEE), вирусного вектора sindbis (SIN), вирусного вектора вируса леса Семлики (SFV), вектора обезьяньего или человеческого цитомегаловируса (CMV), вектора вируса лимфоцитарного хориоменингита (LCMV), ретровирусного вектора, лентивирусного вектора, аденовирусного вектора, аденоассоциированного вирусного вектора, поксвирусного вектора, вектора вируса осповакцины или модифицированнрого вектора коровьей оспы (MVA). Предпочтительно, чтобы в наборе векторов, в котором каждый член набора содержит полинуклеотид, кодирующий отличный от других антиген или его фрагменты, и который, таким образом, обычно вводят одновременно, использовался вектор того же типа, например, вектор, полученный из аденовируса.
Наиболее предпочтительными векторами являются аденовирусные векторы, в частности, аденовирусные векторы, полученные от человекообразных или не относящихся к человеку человекообразных обезьян. Предпочтительными человекообразными обезьянами, от которых происходят аденовирусы, являются шимпанзе (Pan), гориллы (Gorilla) и орангутаны (Pongo), предпочтительно бонобо (Pan paniscus) и обыкновенные шимпанзе (Pan troglodytes). Обычно встречающиеся в природе аденовирусы человекообразных обезьян, не относящихся к человеку, выделяют из образцов стула соответствующей обезьяны. Наиболее предпочтительными векторами являются нереплицирующиеся аденовирусные векторы на основе векторов hAd5, hAd11, hAd26, hAd35, hAd49, ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd55, ChAd63, ChAd73, ChAd82, ChAd83, ChAd146, ChAd147, PanAd1, PanAd2 и PanAd3 или векторов Ad4 и Ad7, способных к репликации. Аденовирусы человека hAd4, hAd5, hAd7, hAd11, hAd26, hAd35 и hAd49 хорошо известны в данной области техники. Векторы на основе встречающихся в природе ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd63 и ChAd63 и ChAd63 подробно описаны в WO 2005/071093. Векторы на основе встречающихся в природе PanAd1, PanAd2, PanAd3, ChAd55, ChAd73, ChAd83, ChAd146 и ChAd147 подробно описаны в WO 2010/086189.
В пятом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей полипептид согласно первому аспекту настоящего изобретения, полинуклеотид согласно второму аспекту настоящего изобретения или вектор согласно третьему аспекту настоящего изобретения или набор векторов согласно четвертому аспекту изобретения и фармацевтически приемлемый эксципиент и необязательно один или несколько адъювантов.
Авторы настоящего изобретения обнаружили, что введение по меньшей мере одного иммуномодулятора, например, модулятора молекулы контрольной точки (МСМ), дополнительно увеличивает силу Т-клеточного ответа на антиген или его фрагмент. Таким образом, в предпочтительном варианте осуществления пятого аспекта фармацевтическая композиция содержит по меньшей мере один иммуномодулятор, например, МСМ, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, например, МСМ, или вектор или липосомную частицу, содержащую полинуклеотид, кодирующий иммуномодулятор, например, МСМ.
В шестом аспекте настоящее изобретение относится к набору из частей, содержащему фармацевтическую композицию по пятому аспекту настоящего изобретения и отдельно упакованный по меньшей мере один иммуномодулятор, например, МСМ, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, например, МСМ или вектор, содержащий полинуклеотид, кодирующий иммуномодулятор, например, МСМ.
В предпочтительном варианте осуществления пятого или шестого аспекта иммуномодулятор представляет собой МСМ и выбран из группы, состоящей из:
(a) агониста члена суперсемейства рецепторов фактора некроза опухоли (TNF), предпочтительно CD27 (например, Варлилумаб), CD40 (например, СР-870,893), ОХ40 (например, INCAGN01949 или MEDI0562), GITR (например, MEDI1873) или CD137 (например, Утомилумаб);
(b) антагониста PD-1 (например, пембролизумаб или ниволумаб), CD274 (атезолизумаб или дурвалумаб), A2AR (например, преладенант), В7-Н3 (например, MGA271), В7-Н4, BTLA, CTLA-4 (например, Тремелимумаб или AGEN1884), IDO, KIR, LAG3, ТГМ-3 (например, СА-327 или RMT3-23) или VISTA (например, СА-170) или антагониста члена суперсемейства B7-CD28, предпочтительно CD28 или ICOS, или антагониста его лиганда.
Другими предпочтительными иммуномодуляторами являются цитокины, которые действуют как факторы роста Т-клеток, в частности, IL-2, IL-12 или IL-15.
В седьмом аспекте настоящее изобретение относится к полипептиду согласно первому аспекту изобретения, полинуклеотиду согласно второму аспекту изобретения или вектору или набору векторов согласно третьему или четвертому аспекту изобретения, или к фармацевтической композиции согласно пятому аспекту изобретения или наборам, содержащим такие фармацевтические композиции согласно шестому аспекту изобретения, или их применению в предотвращении или лечении пролиферативного заболевания, предпочтительно рака, вирусного заболевания, грибкового заболевания или бактериального заболевания.
В предпочтительном варианте осуществления полипептид согласно первому аспекту изобретения, полинуклеотид согласно второму аспекту изобретения, или вектор или набор векторов согласно третьему или четвертому аспекту изобретения, или фармацевтическая композиция или наборы, содержащие такие фармацевтические композиции согласно пятому аспекту изобретения, где рак выбран из группы, состоящей из злокачественных новообразований губы, полости рта, глотки, органа пищеварения, органа дыхания, внутригрудного органа, кости, суставного хряща, кожи, мезотелиальной ткани, мягкой ткани, груди, женских половых органов, мужских половых органов, мочевыводящих путей, головного мозга и других частей центральной нервной системы, щитовидной железы, эндокринных желез, лимфоидной ткани и кроветворной ткани.
В предпочтительном варианте осуществления полипептид согласно первому аспекту изобретения, полинуклеотид согласно второму аспекту изобретения, или вектор или набор векторов согласно третьему или четвертому аспекту изобретения, или фармацевтическая композиция или наборы, содержащие такие фармацевтические композиции согласно пятому аспекту изобретения, где по меньшей мере один иммуномодулятор, например, МСМ, или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, например, МСМ, или вектор или липосомную частицу, содержащую полинуклеотид, кодирующий иммуномодулятор, например, МСМ вводят до, одновременно с или после введения полипептида согласно первому аспекту изобретения, полинуклеотида согласно второму аспекту изобретения, или вектора или набора векторов согласно третьему или четвертому аспекту изобретения, или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции согласно пятому аспекту изобретения.
В предпочтительном варианте осуществления седьмого аспекта изобретения введение модулятора молекулы контрольной точки начинается до начала введения вакцины, или введение ингибитора контрольной точки начинается после начала введения вакцины, или введение ингибитора контрольной точки начинается одновременно с началом введения вакцины.
В предпочтительном варианте осуществления седьмого аспекта изобретения схема вакцинации представляет собой гетерологичную первичную иммунизацию двумя разными вирусными векторами. Предпочтительными комбинациями являются аденовирусный вектор, происходящий от человекообразных обезьян, для праймирования, и поксвирусный вектор, вектор вируса осповакцины или модифицированный вектор коровьей оспы (MVA) для бустинга. Предпочтительно их вводят последовательно, с интервалом по меньшей мере в 1 неделю, предпочтительно 6 недель.
В восьмом аспекте настоящее изобретение относится к полипептиду согласно первому аспекту изобретения, полинуклеотиду согласно второму аспекту изобретения или вектору или набору векторов согласно третьему или четвертому аспекту изобретения для применения в качестве лекарства.
Примеры
Инвариантные цепи из костистых рыб и их фрагменты превращают неиммуногенные раковые антигены в iiviviyiioi снныс антигены.
Иммуногенность аденовекторов человекообразных обезьян, кодирующих пять раковых неоантигенов (таблица 1, SEQ ID NO: 16-20), полученных из линии опухолевых клеток мыши СТ26, оценивали на инбредных мышах BalBC. Вектор GAd-penta, кодирующий только пять раковых неоантигенов, соединенных в направлении «голова к хвосту» (пента), плюс исходный Met и С-концевой тег НА (SEQ ID NO: 21), как было обнаружено, не являлся иммуногенным до тех пор, пока к N-концу пентаантигена (SEQ ID NO: 22-27) не были добавлены полноразмерные последовательности инвариантных цепей Teleostei (BP_INV FL [SEQ ID NO: 9] или PO_INV FL [SEQ ID NO: 2]) или их фрагменты (фрагмент BP_FRAG_A [SEQ ID NO: 10] или BP_FRAG_B [SEQ ID NO: 11] или PO_FRAG_A [SEQ ID NO: 3] или PO_FRAG_B [SEQ ID NO: 4]). Мышей иммунизировали однократной внутримышечной иммунизацией GAd в дозах 108 вирусных частиц (viral particles (vp)). Спленоциты собирали через две недели после иммунизации и тестировали с помощью TFN-γ ELISpot путем стимуляции Т-клеток в присутствии синтетических пептидов, соответствующих аминокислотной последовательности пяти неоантигенов. Культуры отрицательного контроля включали клетки, стимулированные одной культуральной средой, но содержащей растворитель диметилсульфоксид (ДМСО), используемый для получения пептидов. Иммунные ответы (количество Т-клеток, продуцирующих IFN-γ на миллион спленоцитов) показаны на фигуре 1. Ответы считались положительными, если (i) было обнаружено не менее 20 специфических пятен на миллион спленоцитов; (ii) количество пятен, обнаруженных в положительных лунках, в три раза превышало количество пятен, обнаруженных в имитационных контрольных лунках (ДМСО). Как показано на фигуре 1, связывание BP_INV FL или PO_INV FL или их фрагментов FRAG_A или FRAG_B с N-концом пентаантигена преобразовало неиммуногенную вакцинную конструкцию Gad-Penta в высокоиммуногенные конструкции, причем 100% вакцинированных животных показали положительные иммунологические ответы.

Материалы и способы
Иммунизация мышей
Шестинедельные самки мышей BalBC были приобретены в лабораториях Envigo. Всех мышей вакцинировали внутримышечно (в четырехглавую мышцу) путем инъекции 50 мкл вирусных векторов в каждую сторону (общий объем 100 мкл) в дозах 108 vp.
IFNγ ELISpot
Т-клетки, продуцирующие IFNγ, оценивали с помощью анализа ELISPOT через 2 недели после вакцинации. Планшеты MSIP S4510 (Millipore) покрывали 10 мкг/мл антимышиного IFN-γ (U-CyTech Utrecht, Нидерланды) в течение ночи при 4°С. После промывки и блокирования мышиные спленоциты высевали в двух экземплярах с двумя разными плотностями (2,5 × 105 и 5 × 105 клеток/лунка) и стимулировали в течение ночи пулом 25-мерных синтетических пептидов, соответствующих последовательности антигенной вакцины (фигура 1), при конечной концентрации 2 мкг/мл каждого пептида. Пептидный разбавитель ДМСО (Sigma-Aldrich, Milan, Italy) и ConA (Sigma-Aldrich, Milan, Italy) использовали соответственно в качестве отрицательного и положительного контролен. Планшеты обрабатывали путем последующей инкубации с биотинилированным антителом против IFN-γ мыши (U-CyTech Utrecht, The Netherlands), конъюгатом стрептавидин-щелочная фосфатаза (BD Biosciences, NJ) и, наконец, с 1-стадийным раствором BCIP/NBT (Thermo Fisher Scientific, Rockford, IL). Планшеты были считаны и проанализированы автоматическим считывателем планшетов CTL. Ответ ELISpot считали положительным, когда были выполнены все из следующих условий: присутствие IFN-y продукции в Con-А стимулированных лунках; не менее 20 специфических пятен на миллион спленоцитов; количество пятен, обнаруженных в положительных лунках, в три раза больше, чем количество, обнаруженное в ложных контрольных лунках (ДМСО); и снижение ответов при разведении клеток. Данные ELISpot выражали как IFN-γ пятнообразующие клетки (SFC) на миллион спленоцитов.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСИЛИТЕЛЬ T-КЛЕТОЧНОГО ОТВЕТА НА ВАКЦИНУ | 2018 |
|
RU2794196C2 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2782261C2 |
| КОМПОЗИЦИЯ МИКОБАКТЕРИАЛЬНЫХ АНТИГЕНОВ | 2011 |
|
RU2576007C2 |
| КОМПОЗИЦИЯ ВИРУСОПОДОБНЫХ ЧАСТИЦ | 2013 |
|
RU2705301C2 |
| КОМПОЗИЦИИ РЕКОМБИНАНТНОГО CDV И ЕЕ ПРИМЕНЕНИЕ | 2011 |
|
RU2567337C2 |
| ВАКЦИНЫ ПРОТИВ FMDV НА ОСНОВЕ РЕКОМБИНАНТНОГО АДЕНОВИРУСНОГО ВЕКТОРА И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725495C2 |
| ВАКЦИНЫ ПРОТИВ МАЛЯРИИ | 2014 |
|
RU2702163C2 |
| ТЕРАПЕВТИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2002 |
|
RU2328506C2 |
| СЛИТЫЕ БЕЛКИ FMDV-E2 И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2714428C2 |
| РЕКОМБИНАНТНАЯ ВАКЦИНА ОТ ПТИЧЬЕГО ГРИППА И ЕЁ ПРИМЕНЕНИЕ | 2009 |
|
RU2559527C2 |
Настоящее изобретение относится к биотехнологии. Предложен полипептид, обладающий активностью, усиливающей Т-клеточный ответ, содержащий: (a) фрагмент инвариантной цепи (INV) Teleostei, включающий или состоящий из от 16 до 27 смежных аминокислот мембранного проксимального домена (MPD) из INV Teleostei, где фрагмент обладает активностью, усиливающей Т-клеточный ответ, и фрагмент содержит аминокислотную последовательность, выбранную из SEQ ID NO: 11 и 4; и один или несколько онкоспецифических антигенов или онкоспецифических неоантигенов и/или один или несколько их антигенных фрагментов; или (b) полноразмерную INV Teleostei, выбранную из SEQ ID NO: 2 или 9, и один или несколько онкоспецифических антигенов или онкоспецифических неоантигенов и/или один или несколько их антигенных фрагментов. Предложен полинуклеотид, кодирующий заявленный полипептид; экспрессионный вектор, содержащий указанный полинуклеотид; коллекция из двух или более различных векторов для предотвращении или лечения пролиферативного заболевания; фармацевтическая композиция для предотвращения или лечения пролиферативного заболевания; набор для предотвращения или лечения пролиферативного заболевания; применение полипептида, полинуклеотида, вектора или коллекции векторов, или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции, для предотвращения или лечения пролиферативного заболевания. Полипептиды инвариантных цепей костистых рыб или их фрагменты действуют как «усилитель Т-клеток», преобразуя неиммуногенные антигенные последовательности в иммуногенные Т-клеточные антигены. 7 н. и 10 з.п. ф-лы, 1 ил., 1 табл., 1 пр.
1. Полипептид, обладающий активностью, усиливающей Т-клеточный ответ, содержащий:
(a) фрагмент инвариантной цепи (INV) Teleostei, включающий или состоящий из от 16 до 27 смежных аминокислот мембранного проксимального домена (MPD) из INV Teleostei, где фрагмент обладает активностью, усиливающей Т-клеточный ответ, и фрагмент содержит аминокислотную последовательность, выбранную из SEQ ID NO: 11 и 4; и один или несколько онкоспецифических антигенов или онкоспецифических неоантигенов и/или один или несколько их антигенных фрагментов;
или
(b) полноразмерную INV Teleostei, выбранную из SEQ ID NO: 2 или 9, и один или несколько онкоспецифических антигенов или онкоспецифических неоантигенов и/или один или несколько их антигенных фрагментов.
2. Полипептид по п. 1, где аминокислотная последовательность:
(a) MPD, согласно альтернативе (а) по п. 1, представляет собой SEQ ID NO: 3; или
(b) MPD, согласно альтернативе (а) по п. 1, представляет собой SEQ ID NO: 10.
3. Полипептид по п. 1 (а) или 2 (а) или (b), где фрагмент состоит по меньшей мере из от 16 до 27 N-концевых аминокислот MPD и от 1 до 26 последовательных аминокислот трансмембранного домена (TMD) из INV Teleostei непосредственно на N-конце MPD, причем TMD из INV Teleostei предпочтительно характеризуется следующей аминокислотной последовательностью (SEQ ID NO: 15)
AB1KB2B3GB4TB5LB6CB7LB8B9B10QB11B12B13B14YB15B16B17,
в которой
B1 представляет собой V, L или Y, В2 представляет собой V или I, В3 представляет собой V или А, В4 представляет собой L, I или F, В5 представляет собой V, Т или L, B6 представляет собой А или V, В7 представляет собой V или L, В8 представляет собой V или I, В9 представляет собой М, S или А, В10 представляет собой S, А или G, В11 представляет собой А или V, В12 представляет собой М или F, В13 представляет собой I или Т, В14 представляет собой I или А, В15 представляет собой F или М, B16 представляет собой L, М или V, В17 представляет собой V, F или L.
4. Полипептид по любому из пп. 1-3, где
(i) полипептид включает по меньшей мере пять различных онкоспецифичных антигенов или онкоспецифических неоантигенов и/или их антигенных фрагментов;
и/или
(ii) один или несколько онкоспецифичных антигенов или онкоспецифических неоантигенов и/или один или несколько их антигенных фрагментов находятся на С-конце фрагмента INV согласно альтернативе (а) по п. 1.
5. Полинуклеотид, кодирующий полипептид по любому из пп. 1-4, где полинуклеотид представляет собой ДНК или РНК, предпочтительно ДНК.
6. Экспрессионный вектор, содержащий полинуклеотид по п. 5.
7. Коллекция из двух или более различных векторов для предотвращении или лечения пролиферативного заболевания, причем каждый из различных векторов содержит полинуклеотид по п. 5, кодирующий отличный от других полипептид по пп. 1-4.
8. Вектор по п. 6 или коллекция векторов по п. 7, где вектор в каждом случае независимо выбран из группы, состоящей из плазмиды; космиды; липосомной частицы, вирусного вектора или вирусоподобной частицы; предпочтительно альфавирусного вектора, вектора вируса венесуэльского конского энцефалита (VEE), вирусного вектора sindbis (SIN), вирусного вектора вируса леса Семлики (SFV), вектора обезьяньего или человеческого цитомегаловируса (CMV), вектора вируса лимфоцитарного хориоменингита (LCMV), ретровирусного вектора, лентивирусного вектора, аденовирусного вектора, аденоассоциированного вирусного вектора, поксвирусного вектора, вектора вируса осповакцины или модифицированнрого вектора коровьей оспы (MVA), причем аденовирусный вектор предпочтительно представляет собой аденовирусный вектор человекообразных обезьян, более предпочтительно аденовирусный вектор шимпанзе, бонобо или гориллы.
9. Фармацевтическая композиция для предотвращения или лечения пролиферативного заболевания, содержащая полипептид по любому из пп. 1-4, полинуклеотид по п. 5 или вектор/коллекцию векторов по пп. 6-8, фармацевтически приемлемый эксципиент.
10. Фармацевтическая композиция по п. 9, дополнительно содержащая один или несколько адъювантов.
11. Фармацевтическая композиция по п. 9 или 10, содержащая по меньшей мере один иммуномодулятор или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, или вектор или липосомную частицу, содержащую полинуклеотид, кодирующий иммуномодулятор.
12. Набор для предотвращения или лечения пролиферативного заболевания, содержащий фармацевтическую композицию по любому из пп. 9, 10 или 11 и отдельно упакованный по меньшей мере один иммуномодулятор или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, или вектор, содержащий полинуклеотид, кодирующий иммуномодулятор.
13. Фармацевтическая композиция по пп. 9-11 или набор по п. 12, где:
(i) иммуномодулятор представляет собой МСМ и выбран из группы, состоящей из:
(a) агониста члена суперсемейства рецепторов фактора некроза опухоли (TNF), предпочтительно CD27, CD40, ОХ40, GITR или CD137; и/или
(b) антагониста PD-1, CD274, A2AR, В7-Н3, В7-Н4, BTLA, CTLA-4, IDO, KIR, LAG3, TIM-3 или VISTA или антагониста члена суперсемейства В7-CD28, предпочтительно CD28 или ICOS, или антагониста его лиганда;
и/или
(ii) иммуномодулятор представляет собой фактор роста Т-клеток, предпочтительно IL-2, IL-12 или IL-15.
14. Применение полипептида по пп. 1-4, полинуклеотида по п. 5, вектора или коллекции векторов по пп. 6-8, или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции по пп. 9-13, для предотвращения или лечения пролиферативного заболевания.
15. Применение по п. 14, где пролиферативное заболевание представляет собой рак.
16. Применение по п. 15, где рак выбран из группы, состоящей из злокачественных новообразований губы, полости рта, глотки, органа пищеварения, органа дыхания, внутригрудного органа, кости, суставного хряща, кожи, мезотелиальной ткани, мягкой ткани, груди, женских половых органов, мужских половых органов, мочевыводящих путей, головного мозга и других частей центральной нервной системы, щитовидной железы, эндокринных желез, лимфоидной ткани и кроветворной ткани.
17. Применение по любому из пп. 14-16, где по меньшей мере один иммуномодулятор или по меньшей мере один полинуклеотид, кодирующий иммуномодулятор, или вектор или липосомную частицу, содержащую полинуклеотид, кодирующий иммуномодулятор, вводят до, одновременно или после введения полипептида по пп. 1-4, полинуклеотида по п. 5, вектора или коллекции векторов по пп. 6-8, или фармацевтической композиции или наборов, содержащих такие фармацевтические композиции, по пп. 9-13.
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| UPI000A1C2E91, весь документ пп | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| CAPONE STEFANIA ET | |||
Авторы
Даты
2023-11-29—Публикация
2019-10-18—Подача