Изобретение относится к области медицины, а именно к медицинской генетике, педиатрии, детской эндокринологии, и связано с разработкой способа диагностики заболевания щитовидной железы у детей, проживающих в условиях Крайнего Севера.
Изобретение может быть использовано для постановки диагноза как в специализированных клиниках при обследовании детей, так и в обычных учреждениях здравоохранения.
В наше время заболевания щитовидной железы являются актуальной проблемой. Так, по данным ВОЗ (всемирная организация здравоохранения), около 31% населения планеты страдает от тиреоидных заболеваний, причем в России заболевания такого характера встречаются довольно часто и составляют около 40% населения, а в некоторых районах доходит и до 95%. Повышенный уровень заболеваемости по классу патологий щитовидной железы является актуальной проблемой для России, так как значительная часть территории страны, включая регионы Крайнего Севера, находится в зоне дефицита йода. Заболевания щитовидной железы широко распространены среди детского населения данного региона. Различные индивидуумы в зависимости от конкретных особенностей их генома и соответствующей функциональной активности продуктов экспрессии характеризуются модифицированной восприимчивостью к действию повреждающих факторов окружающей среды.
В настоящее время существуют различные клинико-лабораторные способы оценки предрасположенности и диагностирования заболеваний щитовидной железы (далее - ЩЖ). Причем эти способы условно можно разделить на четыре группы: способы с использованием клинических
показателей; способы с использованием методов ультразвукового исследования; методы установления онкологических заболеваний ЩЖ с использованием генетических прогностических критериев; способы прогнозирования риска возникновения заболеваний ЩЖ.
Из патента РФ №2305846 известен способ прогнозирования заболевания щитовидной железы у людей, занятых на вредном производстве. Для этого определяют содержание кадмия и ртути в волосах. При уровне кадмия выше 0,25 мкг/г и уровне ртути выше 1,0 мкг/г человека относят к группе риска по развитию гиперплазии щитовидной железы. Использование способа позволяет осуществить своевременное прогнозирование развития гиперплазии щитовидной железы на донозологическом этапе.
А из патента РФ №2421127 известен способ прогнозирования риска заболеваний щитовидной железы у женщин перименопаузального возраста. Определяют данные о причине менопаузы, применении препаратов эстрогенов, величине индекса массы тела и объема щитовидной железы, концентрации антител к тиреоидной пероксидазе и тиреотропного гормона. На основании полученных данных вычисляют прогностический индекс, позволяющий спрогнозировать наличие или отсутствие риска развития заболеваний щитовидной железы в ближайшие пять лет.
Недостатками известных способов является то, что данные способы не учитывают генетическую предрасположенность к развитию заболевания ЩЖ, полиморфизм которых может лежать в основе заболевания.
Из способов с использованием методов ультразвукового исследования известны следующие:
- известен способ диагностики аутоиммунных заболеваний ЩЖ (Патент РФ №2104531). При его реализации при ультразвуковом исследовании щитовидной железы проводят сравнительную оценку эхогенности тиреоидной ткани с эхогенностью ткани околоушной слюнной железы как индивидуальной нормы. И по снижению эхогенности относительно околоушной слюнной железы диагностируют аутоиммунное заболевание. Сравнительную оценку проводят по интенсивности окраски полученных изображений.
- известен способ диагностики аутоиммунных заболеваний щитовидной железы, включающий ультразвуковое исследование щитовидной железы с количественным определением ее эхогенности (Нарр J., Cordes U., Jost-Kostering S., Puhahn М. Quantitative determination of echogenicity of diffuse inflammatory thyroid gland diseases. / Bildgebung. 1993, Bd 60, N 3, p. 131-134). Способ заключается в том, что у пациента при ультразвуковом исследовании щитовидной железы гистографическим методом на денситометрической аппаратуре измеряют показатель эхоплотности тиреоидной ткани, и при его величине, менее нижней границы стандартной эхогенности щитовидной железы здорового человека, устанавливают наличие аутоиммунной патологии. Однако указанный способ имеет ряд недостатков. Они связаны как с техническими проблемами, а именно - с отсутствием в традиционно эксплуатируемой ультразвуковой аппаратуре общего назначения специальной денситометрической функции, которая значительно удорожает приборы, так и с отсутствием надежных стандартов нормы, особенно для детей.
- известен также способ диагностики аутоиммунных заболеваний щитовидной железы, в котором выявляют снижение эхогенности тиреоидной ткани, сравнивая ее с эхогенностью мышечной ткани. В качестве эталона нормальной эхогенности используют ультразвуковой параметр плотности двуглавой мышцы плеча (Васильев С.А., Анчуков В.Б. Ультразвуковая диагностика заболеваний щитовидной железы. / В кн.: "Актуальные вопросы злокачественных новообразований и аутоиммунных процессов щитовидной железы". Под ред. В.А. Привалова. Челябинск. 1990, с. 27-30). Однако к недостаткам этого способа относится невысокая точность, низкая специфичность и воспроизводимость результатов.
Кроме того, указанные способы предназначены для диагностирования уже состоявшегося заболевания и не предназначены для выявления предрасположенности.
Из методов по установления онкологических заболеваний ЩЖ с использованием генетических прогностических критериев известны следующие:
- Известен способ дифференциальной диагностики новообразований щитовидной железы (Патент РФ №2705110). При его реализации выполняют УЗИ щитовидной железы, выявляют узловые образования щитовидной железы. Проводят пункционную биопсию, последующее цитологическое исследование пунктата. При неопределенных цитологических заключениях выполняют молекулярно-генетическое исследование, при котором предварительно высушенный цитологический препарат с цитологических стекол смывают 200 мкл лизирующего буфера. Далее производят выделение ДНК и микроРНК из цитологических препаратов тонкоигольной аспирационной пункционной биопсии (ТАПБ) новообразований ЩЖ с помощью наборов для выделения. Производят детекцию и количественную оценку диагностически значимых микроРНК, основанную на методе полимеразной цепной реакции (ПЦР) с флуоресцентной регистрацией результата анализов в реальном времени с помощью термоциклера CFX96(Bio-Rad Laboratories, США). При условии показателей HMGA2 более 0,09, микроРНК 221 более 0,0105 и микроРНК 375 более -12,1213, определяют фолликулярную опухоль с признаками злокачественности. При условии показателей микроРНК-146b более 0,1721, определяют папиллярный рак. При показателях миРНК-375 более 5,2514, определяют медуллярный рак. Показатель соотношения митохондриальной ДНК/ядерной ДНК более 5716,3013 определяет В-клеточный рак.
- из патента РФ №2757347 известен способ дифференциальной диагностики узловых образований щитовидной железы человека. Осуществляют взятие образца ткани узлового образования щитовидной железы, выделение суммарного пула РНК из образца, анализ уровня экспрессии гена HMGA2, митохондриальной ДНК, а также определение мутации V600E в гене BRAF. Измеряют уровень экспрессии микроРНК-146b, -221, -375. Дополнительно измеряют уровень экспрессии гена GCM2. Заключение о наличии и характере узлового образования составляют на основании дерева принятия решений, согласно которому анализируемый образец относят к одному, выбранному из следующей группы: узловое образование паращитовидной железы, доброкачественное узловое образование щитовидной железы, злокачественное узловое образование щитовидной железы, включающее папиллярный рак, медуллярный рак, гюртлеклеточный рак, фолликулярные опухоли с маркерами злокачественности.
- из патента РФ №2300106 известен способ дифференциальной диагностики злокачественных опухолей щитовидной железы у детей и подростков. Сущность изобретения состоит в том, что у детей и подростков с узловыми образованиями щитовидной железы до начала лечения определяют антигены главного комплекса гистосовместимости (HLA-фенотип), и при наличии антигенов: А10, В7, В35, а также неполном фенотипе по локусам HLA-A и HLA-B диагностируют папиллярный рак щитовидной железы, а при отсутствии вышеперечисленных признаков HLA-фенотипа диагностируют фолликулярный вариант опухоли.
Однако указанные известные способы предназначены для диагностирования уже состоявшегося заболевания и не предназначены для выявления предрасположенности к нарушению функции ЩЖ, т.е. на ранних стадиях.
Из уровня техники известны следующие способы прогнозирования риска нарушения функционального состояния щитовидной железы:
- из патента РФ №2688207 известен способ выявления риска нарушения функционального состояния щитовидной железы у коренного и местного населения Арктической зоны Российской Федерации. При этом в период увеличения продолжительности светового дня, а именно с февраля по апрель, включающий определение в крови обследуемых людей зрелого возраста, а именно мужчин в возрасте от 22 до 60 лет и женщин в возрасте от 21 до 55 лет содержания тиреотропного гормона (ТТГ), свободного тироксина (сТ4) и свободного трийодтиронина (сТ3) и расчет, на основании полученных данных, интегрального тиреоидного индекса (ИТИ) по формуле ИТИ=(сТ3+сТ4)/ТТГ и, при выявлении отклонения, у коренных малочисленных народов - коми и ненцев ИТИ от значений 6,3-13,0, а у местного европеоидного населения - русских, проживающих в данной зоне, не менее чем в 3 поколениях, ИТИ от значений 8,9-19,6 свидетельствует о риске возникновения нарушений функционального состояния щитовидной железы. Изобретение обеспечивает своевременное выявление и правильную интерпретацию полученных данных в зависимости от возрастной и этнической принадлежности обследуемых лиц, что способствует сохранению здоровья трудоспособного населения Арктической зоны Российской Федерации.
- известен способ оценки функционального состояния щитовидной железы, включающий расчет интегрального тиреоидного индекса (ИТИ) как отношение суммы концентраций свободного трийодтиронина и свободного тироксина к содержанию тиреотропного гормона: ИТИ=(сТ3+сТ4)/ТТГ. За нормативные пределы принимается диапазон значений ИТИ от 7,04 до 27,2. Повышение данного индекса - наиболее ранний признак гипертиреоза, тогда как снижение ИТИ отражает даже начальные стадии гипотиреоза. (Информационное письмо для врачей ЛПУ Ханты-Мансийского автономного округа, бюджетного учреждения ХМАО-Югры "ОКД "ЦД и ССХ" https://www.okd.ru/doctor/informational_letter/doc/letter_l.pdf).
Недостатком указанных способов является то, что используемые критерии позволяют констатировать уже имеющиеся изменения функции щитовидной железы по уровню гормонов щитовидной железы и ТТГ и не отражают опасность возникновения нарушений в перспективе, то есть не характеризуют предрасположенность к функциональным нарушениям щитовидной железы.
При этом из уровня техники не были выявлены известные способы диагностики нарушения функционального состояния щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера, поэтому сделать выбор ближайшего аналога к заявляемому объекту не представляется возможным.
Технический результат, достигаемый предлагаемым изобретением, заключается в обеспечении достоверности выявления предрасположенности к развитию заболевания щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера, с обеспечением возможности в последующем судить о развитии таких состояний у детей уже на ранних стадиях их формирования.
Указанный технический результат достигается предлагаемым способом диагностики нарушения функционального состояния щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера, согласно которому отбирают у ребенка пробу мочи и пробу буккального эпителия, в пробе мочи ребенка определяют содержание йода, а из пробы буккального эпителия осуществляют выделение дезоксирибонуклеиновой кислоты ДНК, затем на детектирующем амплификаторе с использованием полимеразной цепной реакции проводят генотипирование полиморфизма гена белка-переносчика органических анионов 1 В1 ОАТР1 В1 (rs2306283) с использованием праймеров; и при одновременном выполнении следующих условий: наличия вариантного гомозиготного генотипа полиморфизма rs2306283, а также понижения уровня йода в моче более чем в 1,5 раза по сравнению с нижней границей физиологической нормы, равной 10,0 мкг/100 см3, диагностируют нарушение функционального состояния щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера.
Предлагаемый технический результат достигается благодаря следующему.
В качестве диагностических критериев реализации прогнозирования риска нарушения функционального состояния щитовидной железы у детей 4-10 лет рекомендуется использовать генотип гена-кандидата: генотип СС (вариантная гомозигота) гена ОАТР1 В1 (rs2306283), а также пониженный уровень йода в моче более чем в 1,5 раза по сравнению с нижней границей физиологической нормы (норма равна 10,0 - 50,0 мкг/100 см3). Аллельное состояние гена ОАТР1 В1 предусматривает следующие его состояния: гетерозиготное - ТС, или дикое гомозиготное - ТТ, или вариантное гомозиготное - СС.
Повышенный уровень распространенности йододефицитных заболеваний, включая патологию щитовидной железы, является чрезвычайно актуальной и социально значимой проблемой для России, так как значительная часть территории страны находится в зоне дефицита йода. Территория Крайнего Севера России также является йододефицитным регионом вследствие вечной мерзлоты, особенностей водосбора в период таяния снегов, недостаточного проникновения на эти территории воздушных масс с океана, что в сумме приводит к абсолютному дефициту йода в биосфере Артики. Йод является жизненно важным микроэлементом, необходимым для нормального роста и развития человека и является составной частью гормонов щитовидной железы - тироксина (Т4) и трийодтиронина (ТЗ).
На территориях в зоне дефицита йода наблюдается повышенный уровень заболеваемости по классу патологий щитовидной железы, включая эндемический зоб, гипотиреоз и другие болезни щитовидной железы, связанные с йодной недостаточностью. Так, на территории Крайнего Севера частота патологии щитовидной железы среди детей составляет до 70%.
Полиморфные варианты генов, в частности, гена ОАТР1В1, ассоциируются с функциональными изменениями продуктов экспрессии и, как следствие, определяют уровень ферментативной активности соответствующих белков. Поэтому различные индивидуумы могут обладать повышенной устойчивостью либо избыточной чувствительностью к действию повреждающих факторов окружающей среды в зависимости от конкретных особенностей их генома и функциональной активности конкретных ферментов.
Поддержание гомеостаза у детского населения в условиях йодного дефицита, оптимизация соотношения и гиперактивация тиреоидных гормонов обеспечиваются и контролируются гипофиз-тиреоидной системой. Следовательно, полиморфизм генов-транспортеров тиреоидных гормонов, включая ген белка-переносчика органических анионов 1В1 (ОАТР1В1), приводит к изменению их функциональной активности, что создает повышенный риск развития патологии щитовидной железы у детей, проживающих в условиях дефицита йода на территории Крайнего Севера.
Результаты клинико-лабораторного анализа биологических сред свидетельствуют о снижении содержания йода в моче детей с патологией щитовидной железы относительно группы сравнения и референтного уровня (р<0,05). Данные приведены в таблице 1.

При этом уровень ТТГ превышает аналогичные значения в группе сравнения (р<0,05). Данные приведены в таблице 2.

Полиморфизм гена белка переносчика органических анионов 1В1 ОАТР1В1 (rs2306283) у детей с заболеваниями щитовидной железы характеризуется повышенной частотой С-аллеля по отношению к группе сравнения (OR=1,79: CI: 1,03-3,09; р<0,05), что может быть связано с ингибированием транспорта гормонов щитовидной железы. Данные приведены в таблице 3.
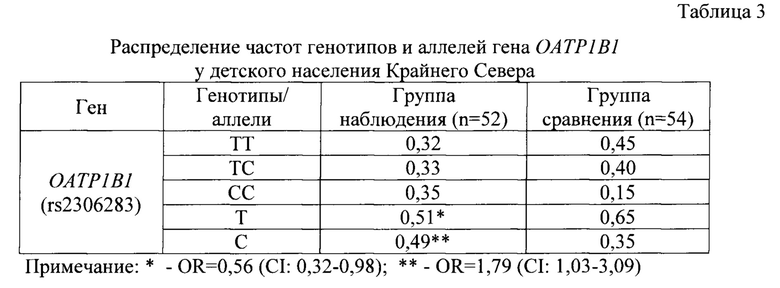
Таким образом, эндокринный профиль детей с патологией щитовидной железы, проживающих в условиях йододефицита на Крайнем Севере, характеризуется дисбалансом гипофиз-тиреоидной системы по критерию повышения содержания ТТГ на фоне снижения содержания йода в моче (р<0,05), что свидетельствует о снижении функциональной активности щитовидной железы. Установленная повышенная частота С-аллеля гена ОАТР1В1 (rs2306283) указывает на формирование патогенетических тенденций в транспорте йодсодержащих гормонов щитовидной железы при наличии заболеваний щитовидной железы в условиях естественного дефицита йода, так и может указывать на формирование компенсаторных механизмов, как вариант адаптации в условиях естественного дефицита поступления йода.
Определение полиморфного маркера генотипа гена ОАТР1В1 (rs2306283), ассоциированного с избыточным уровнем ТТГ на фоне дефицита йода в биосредах может быть использовано для профилактики, ранней диагностики и индивидуальной терапии заболеваний щитовидной железы у населения йододефицитных территорий.
Благодаря использованию в качестве исследуемого материала проб мочи, а также стандартных методик изучения генетических параметров, обеспечивается простота, надежность и доступность исследований, а также получение результатов нужной информативности.
Благодаря использованию в качестве исследуемого материала буккального эпителия (пробы биологического материала со слизистой щеки), обеспечивается простота и надежность исследований, а также получение нужной информативности в плане выделения из указанной пробы ДНК и посредством полимеразной цепной реакции (ПНР) проведения генотипирования полиморфизма указанного гена ОАТР1В1. При этом предлагается использовать в качестве праймера участок ДНК гена ОАТР1В1 (rs2306283), устанавливая при этом для каждого гена одно из следующих его состояний: гетерозиготное, или дикое гомозиготное, или вариантное гомозиготное.
Именно благодаря расширению информационных показателей, связанных с полиморфными вариантами указанного гена, и будет обеспечена точность прогнозирования риска потенциального нарушения функционального состояния ЩЖ у ребенка.
Исходя из вышеизложенного, можно сделать вывод, что поставленный технический результат обеспечивается за счет совокупности операций предлагаемого способа, их последовательности и режимов его реализации.
Предлагаемый способ реализуется следующим образом.
1. Проводят отбор группы детей 4-10 лет одной этнической популяции, родившихся и проживающих в условиях Крайнего Севера (выше 66,5° северной широты).
Затем проводят отбор пробы мочи у обследуемого ребенка - для определения содержания йода. Содержание указанного показателя определяют церий-арсенитовым методом (Wawschinek О., 1985 г.), в модификации лаборатории клинической биохимии ЭНЦ РАМН «Определение уровня экскреции йода с мочой в разовой порции мочи».
Устанавливают, имеется ли понижение его концентрации в пробе мочи над нижним пределом физиологической нормы (физиологическая норма содержания йода в моче составляет 10-50 мкг/100 см3).
2. Также у указанного ребенка отбирают пробу буккального эпителия (в виде мазка со слизистой оболочки щеки). После забора материала тампон (рабочую часть зонда с ватным тампоном) помещают в стерильную пробирку типа «Эппендорф» с 500 мкл транспортной среды (стерильный 0,9%-ный раствор NaCl). Пробирку с раствором и рабочей частью зонда закрывают.
Далее производят выделение ДНК из пробы. Для этого пробы в количестве 100 мкл лизируют 300 мкл лизирующего раствора, представляющего собой 0,5%-ный раствор саркозила и протеиназы К (20 мг/мл) в ацетатном буфере (рН 7,5). Затем добавляют сорбент (каолин) и последовательными процедурами промывки отмывают фосфатно-солевым буфером (рН 7,2) пробы от белков и смесью изопропиловый спирт: ацетон от липидов. Нуклеиновые кислоты остаются при этом на сорбенте. Далее адсорбированные на сорбенте ДНК из пробы экстрагируют ТЕ-буфером, представляющим собой смесь 10 мМ трис-HCl и 1 мМ ЭДТА (рН 8,0). Экстракт подвергают центрифугированию. После центрифугирования пробирки надосадочная жидкость содержит очищенную ДНК.
Полученный материал готов к постановке полимеразной цепной реакции (ПЦР). ПЦР проводят на детектирующем амплификаторе с гибридизационно-флуоресцентной детекцией в режиме «реального времени» с использованием готового набора праймеров и зондов производства ЗАО «Синтол», Россия, в котором в качестве праймеров использовались участки ДНК гена ОАТР1В1 (rs2306283).
Проводят реакцию амплификации, это достигается тем, что для исследования аллельного состояния гена у отдельного ребенка готовят свою реакционную смесь. В каждую пробирку вносят 0,1 мкл готовой смеси праймеров (принятый в генетике термин, обозначающий конечные нуклеотиды с меткой, ограничивающие (отрезающие) амплифицируемую цепочку нуклеотидов гена) и зондов для выбранного гена ОАТР1В1 (rs2306283) (использован набор реагентов для определения полиморфизма ОАТР1В1 (rs2306283) ЗАО «Синтол», Россия). В каждую пробирку добавляют остальные компоненты необходимые для осуществления ПЦР: нуклеотиды (дезоксинуклеозидтрифосфаты: по 10 мМ дАТФ, дТТФ, дГТФ, дЦТФ), буфера (100 мМ трис-HCl-буфера, 500 мМ KCl, 40 мМ MgCl2) и Tag F-полимеразы. Вносят пробу в количестве 10 мкл. Таким образом, общий объем реакционной смеси составляет 25 мкл. Каждая пробирка плотно закрывается пробкой и устанавливается в амплификатор.
При проведении ПЦР амплификацию и детекцию проводят на детектирующем амплификаторе CFX96 фирмы Bio-Rad.
Используется универсальная программа амплификации, подобранная производителем реактивов. Она включает в себя несколько этапов: 1 этап - активация TaqF-полимеразы (режим «горячего старта») продолжается 15 мин при 95°С; 2 этап - установочные циклы амплификации без измерения флуоресценции (5 циклов); 3 этап - рабочие циклы амплификации с измерением флюоресценции (40 циклов).
Каждый цикл амплификации включает в себя денатурацию ДНК (5 с при 95°С), отжиг праймеров (20 с при 60°С) и саму реакцию полимеризации ДНК (15 с при 72°С).
Регистрация сигнала флюоресценции, возникающего при накоплении продуктов амплификации участков ДНК проводится в режиме «реального времени» после стадии отжига праймеров для выбранных генов по каналу VIC - для детекции одного из аллельных вариантов генов, и по каналу FAM - для альтернативного варианта.
Результаты интерпретируются на основании наличия (или отсутствия) пересечения кривой флюоресценции с установленной на заданном уровне пороговой линией, что соответствует наличию (или отсутствию) значения порогового цикла (N) в соответствующей графе в таблице результатов, отображаемой в программном обеспечении для амплификатора CFX96.
По соотношению пороговых циклов, полученных по двум каналам детекции, определяют состояние гена ОАТР1В1 в исследуемом участке ДНК rs2306283 (метод аллельной дискриминации). Возможных вариантов состояния гена было два: гомозиготное - в случае, когда одно из значений порогового цикла не определяется (ниже пороговой линии) и гетерозиготное - в случае, когда получено два значения пороговых циклов и по этим каналам получены параболические кривые флюоресценции. В зависимости от того, накопление какого продукта амплификации происходит в реакции, устанавливается гетерозиготное, или дикое гомозиготное, или вариантное гомозиготное состояние гена ОАТР1В1 (rs2306283).
3. И при выполнении следующих условий: при одновременном наличии комбинации СС генотипа гена ОАТР1В1 (rs2306283), понижении содержания йода в моче более, чем в 1,5 раза по сравнению с нижней границей физиологической нормы (норма 10-50 мкг/100 см3), делают вывод о высокой предрасположенность к развитию заболеваний щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера.
При проведении испытаний по реализации предлагаемого способа были сформированы две группы: группа наблюдения и группа сравнения.
Группу наблюдения составили 52 ребенка в возрасте 4-10 лет с диагностированными заболеваниями щитовидной железы по МКБ-10: Е00 Синдром врожденной йодной недостаточности; Е01 Болезни щитовидной железы, связанные с йодной недостаточностью, и сходные состояния; Е01.2 Зоб (эндемический), связанный с йодной недостаточностью, неуточненный; Е03.9 Гипотиреоз неуточненный.
Группа сравнения - 54 ребенка в возрасте 4-10 лет без патологий эндокринной системы.
Группы исследования были сопоставимы по возрасту, полу, этническому составу, сопутствующей патологии, социально-экономическому уровню семьи, качеству и составу питания.
У всех обследуемых детей была взята проба мочи, исследование которой проводилось по вышеуказанной схеме. Также была взята проба буккального эпителия для установления по реакции ПЦР полиморфизма исследуемых генов.
Определение йода в моче проводилось с использованием унифицированной методики на спектрофотометре ПЭ-5400УФ («Экросхим», Россия). Определение уровня ТТГ в крови проводилось методом ИФА («Хема-медика», Россия) на анализаторе Е1х808 (BioTek, США).
Генотипирование по полиморфизму гена белка-транспортера анионов ОАТР1В1 (rs2306283) проведено методом ПЦР в режиме реального времени на приборе CFX96 (Bio-Rad, США). Генетический материал выделен из буккального эпителия с применением набора реагентов для экстракции ДНК из клинического материала («Синтол», Россия). Генотип человека определяли методом аллельной дискриминации в программе TaqMan.
Для статистической обработки результатов применялись методы параметрической (t-критерий Стьюдента) и непараметрической (U-критерий Манна-Уитни) математической статистики с использованием пакета программ Statistica 6.0 (StatSoft, USA). Результаты представлены в виде среднего арифметического (М) и его стандартной ошибки (ш) изученных показателей. Анализ ассоциаций вариантных генотипов с развитием патологии щитовидной железы проводили с использованием показателя отношения шансов (OR) и его доверительного интервала (CI). Различия между группами считали статистически значимыми при р<0,05.
Данные, полученные в результате исследований для детей из группы наблюдения и группы сравнения, приведены в таблице 4.
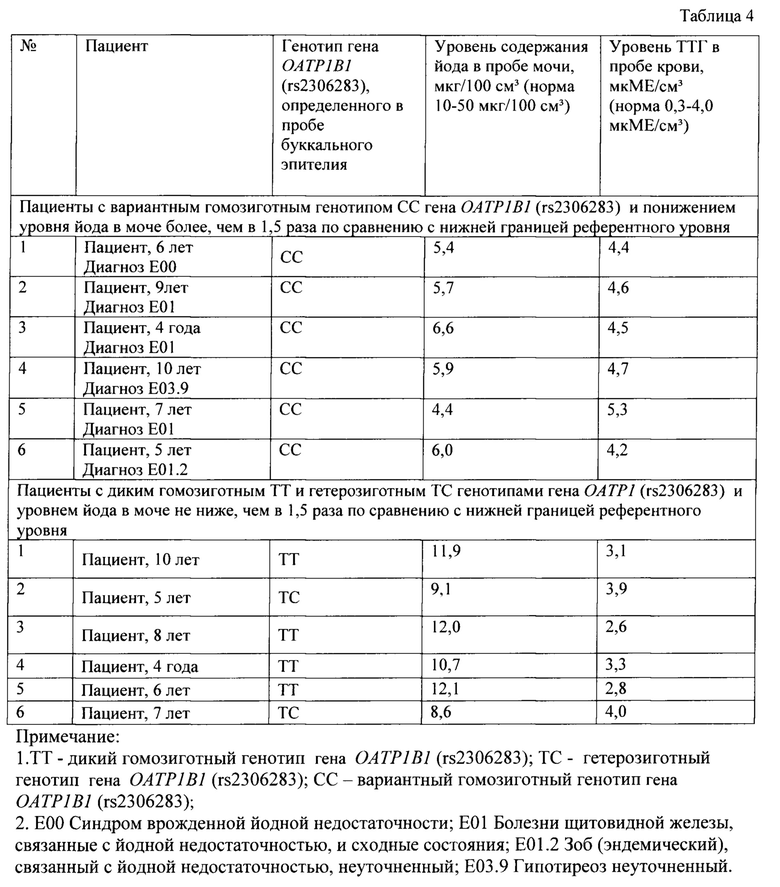
В результате биохимического анализа биологических сред детского населения Крайнего Севера показано, что у детей с заболеваниями щитовидной железы достоверно снижено содержание йода в моче по отношению к аналогичным значениям группы сравнения и к референтному уровню (р<0,05). При этом содержание йода в моче у детей группы сравнения сопоставимо с нижней границей референтного уровня (таблица 4).
При изучении показателей эндокринной регуляции обследованных детей по критерию уровня гормонов щитовидной железы было обнаружено, что содержание тиреотропного гормона у детей группы наблюдения в 1,2 раза и более выше, чем в группе сравнения (р<0,05).
Уровень тиреотропного гормона в крови точно отражает функциональное состояние щитовидной железы. Повышение уровня ТТГ свидетельствует о снижении функциональной активности щитовидной железы, что негативно сказывается на росте и развитии детского организма. По установленным нормам уровень ТТГ более 4 мЕд/л свидетельствует о патологии щитовидной железы.
Полиморфизм гена белка переносчика органических анионов 1В1 ОАТР1В1 (rs2306283) у детей с заболеваниями щитовидной железы характеризуется повышенной частотой С-аллеля по отношению к группе сравнения (OR=1,79: CI: 1,03-3,09; р<0,05): 35% детей группы наблюдения имели гомозиготный минорный генотип СС (15% в группе сравнения).
Таким образом, эндокринный профиль детей с установленной патологией щитовидной железы, проживающих в условиях йододефицита на Крайнем Севере, характеризуется дисбалансом системы щитовидной железы. Пониженное содержание йода в моче обследованных детей сочетается с избыточным содержанием ТТГ, что свидетельствует о снижении функциональной активности щитовидной железы. Установленная повышенная частота С-аллеля гена ОАТР1В1 (rs2306283) указывает на формирование патогенетических тенденций в транспорте гормонов щитовидной железы при наличии заболеваний щитовидной железы в условиях естественного дефицита йода. Определение полиморфного маркера генотипа гена ОАТР1В1 (rs2306283), ассоциированного с избыточным уровнем ТТГ на фоне дефицита йода в биосредах, может быть использовано для ранней диагностики, индивидуальной терапии и профилактики заболеваний щитовидной железы у детей Крайнего Севера, отнесенного к йододефицитной территории.
Для иллюстрации реализации предлагаемого способа приведены два примера по конкретным пациентам одного возраста и этнической принадлежности.
Пример 1. Пациент, 6 лет, русский, родился от родителей, проживающих в Заполярье на уровне 69 градусов северной широты. Ds: Е01 Болезнь щитовидной железы, связанная с йодной недостаточностью. Установлено наличие вариантного гомозиготного генотипа гена ОАТР1В1 (rs2306283) - СС. Значение содержания йода в пробе мочи: 6,4 мкг/100 см3 т.е. в 1,56 раза ниже нижней границы нормы (норма 10-50 мкг/100 см3). Содержание ТТГ в сыворотке крови - маркера регуляции экспрессии гормонов щитовидной железы 4,4 мкМЕ/см3, т.е. выше верхней границы диапазона нормы (0,3-4,0 мкМЕ/см3). Таким образом, установлены низкие значения содержания йода в организме (по уровню его экскреции с мочой) и гиперпродукция тропного к ткани щитовидной железы гормона (ТТГ) на фоне полиморфизма кандидатного гена транспортера органических анионов - наличие вариантного гомозиготного генотипа гена ОАТР1В1 (rs2306283) - СС, кодирующего протеин, ответственный за транспортировку гормонов щитовидной железы, что в совокупности указывает на наличие генетической предрасположенности к нарушению процессов доставки к тканям необходимых для метаболизма гормонов щитовидной железы, что на фоне природогенного дефицита йода приводит к ускорению формирования и утяжелению патологии щитовидной железы.
Это говорит о том, что, согласно предлагаемому способу, у данного ребенка состояние в условиях полиморфизма кандидатного гена ОАТР1В1 (rs2306283) оценивается, как формирование ранних нарушений и вероятность развития болезней ассоциированных с щитовидной железой, имеющих генетическую предрасположенность.
Анализируя представленные данные, можно сделать вывод, что у пациента имеются изменения связанные с дефицитом йода, в частности, наличие избыточного содержания тиреотропного гормона (ТТГ), которое характеризует наличие функциональных нарушений эндокринной регуляции обмена веществ, связанных с дефицитом гормонов щитовидной железы и их транспортом (доставкой) к тканям, что запускает процессы ведущие к формированию патологических процессов в щитовидной железе.
Пример 2. Пациент, 8 лет, русский, родился и проживает в Заполярье на уровне 69 градусов северной широты. Заболеваний щитовидной железы не выявлено. Установлено наличие дикого гомозиготного генотипа гена ОАТР1В1 (rs2306283) - ТТ. Значение содержания йода в пробе мочи: 12,0 мкг/100 см3 т.е. выше нижней границы нормы (норма 10-50 мкг/100 см3). Содержание ТТГ в сыворотке крови - маркера регуляции экспрессии гормонов щитовидной железы 2,6 мкМЕ/см3, т.е. в границах диапазона нормы (0,3-4,0 мкМЕ/см3). Таким образом, отсутствие полиморфизма гена ОАТР1В1 (rs2306283) на фоне соответствия границам нормы уровня содержания йода в организме (по уровню его экскреции с мочой) и отсутствия гиперпродукции тропного гормона ТТГ не приводит к развитию негативных эффектов в виде патологии щитовидной железы, связанной с йодным дефицитом, то есть в отсутствии негативной генетической программы не происходит формирования болезней и функциональных отклонений от нормы в щитовидной железе у данного пациента. Наблюдение за ребенком в течение года не выявили у него в последующем отклонений в функциональном состоянии ЩЖ.
Анализируя представленные данные, можно сделать вывод, что у обследуемого пациента отсутствуют нарушения функции щитовидной железы.
Таким образом, приведенные данные показывают, что при реализации предлагаемого способа с использованием предлагаемых критериев обеспечивается его назначение.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ установления предрасположенности к формированию "синдрома полярного напряжения" у школьников 7-13 лет, проживающих в условиях Заполярья | 2022 |
|
RU2793062C1 |
| Способ диагностики расстройства вегетативной нервной системы у девочек дошкольного возраста, ассоциированного с избыточной контаминацией биосред детей марганцем | 2021 |
|
RU2773830C1 |
| Способ определения предрасположенности к развитию ожирения у детей в условиях избыточной контаминации алюминием | 2019 |
|
RU2700565C1 |
| Способ оценки индивидуального риска формирования избыточной массы тела и ожирения у детей, потребляющих питьевую воду с повышенным содержанием хлороформа и тетрахлорметана | 2016 |
|
RU2619872C1 |
| Способ диагностики у детей астено-вегетативного синдрома в условиях экспозиции алюминием | 2018 |
|
RU2687731C1 |
| Способ оценки влияния нитрозаминов на апоптоз у детей, проживающих в неблагоприятных условиях среды обитания | 2016 |
|
RU2626516C1 |
| Способ выявления предрасположенности к развитию метаболического синдрома в виде ожирения у школьников 7-10 лет | 2022 |
|
RU2779085C1 |
| Способ оценки у детей влияния стронция на апоптоз, ассоциированный с аллельными вариантами гена FAS | 2016 |
|
RU2621155C1 |
| Способ диагностики синдрома утомляемости после перенесенной вирусной болезни у детей 4-7 лет в условиях контаминации алюминием | 2023 |
|
RU2811523C1 |
| Способ выявления нарушений физиологической иммуносупрессии у детей в первом поколении по мужской линии с отягощенной наследственностью в условиях избыточной экспозиции алюминием | 2017 |
|
RU2655658C1 |
Изобретение относится к медицине, а именно к медицинской генетике, педиатрии, детской эндокринологии, и может быть использовано для диагностики нарушения функционального состояния щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера. Отбирают у ребенка пробу мочи и пробу буккального эпителия. В пробе мочи определяют содержание йода. Из пробы буккального эпителия выделяют ДНК. На детектирующем амплификаторе с использованием полимеразной цепной реакции проводят генотипирование полиморфизма гена белка-переносчика органических анионов 1В1 ОАТР1В1 (rs2306283) с использованием праймеров. При наличии вариантного гомозиготного генотипа полиморфизма rs2306283 и понижения уровня йода в моче более чем в 1,5 раза по сравнению с нижней границей физиологической нормы, равной 10,0 мкг/100 см3, диагностируют нарушение функционального состояния щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера. Способ обеспечивает возможность достоверного выявления заболевания щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера за счет определения наличия вариантного гомозиготного генотипа полиморфизма rs2306283 и снижения содержания йода в моче. 4 табл., 2 пр.
Способ диагностики нарушения функционального состояния щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера, характеризующийся тем, что отбирают у ребенка пробу мочи и пробу буккального эпителия, в пробе мочи ребенка определяют содержание йода, а из пробы буккального эпителия осуществляют выделение дезоксирибонуклеиновой кислоты ДНК, затем на детектирующем амплификаторе с использованием полимеразной цепной реакции проводят генотипирование полиморфизма гена белка-переносчика органических анионов 1В1 ОАТР1В1 (rs2306283) с использованием праймеров; и при одновременном выполнении следующих условий: наличия вариантного гомозиготного генотипа полиморфизма rs2306283, а также понижения уровня йода в моче более чем в 1,5 раза по сравнению с нижней границей физиологической нормы, равной 10,0 мкг/100 см3, диагностируют нарушение функционального состояния щитовидной железы у детей 4-10 лет, проживающих в условиях Крайнего Севера.
| СПОСОБ ВЫЯВЛЕНИЯ РИСКА НАРУШЕНИЯ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ЩИТОВИДНОЙ ЖЕЛЕЗЫ У КОРЕННОГО И МЕСТНОГО НАСЕЛЕНИЯ АРКТИЧЕСКОЙ ЗОНЫ РОССИЙСКОЙ ФЕДЕРАЦИИ | 2018 |
|
RU2688207C1 |
| Способ дифференциальной диагностики йоддефицитного и йодиндуцированного нарушения функции щитовидной железы у лиц, проживающих в регионах с йодным дефицитом | 2019 |
|
RU2728261C2 |
| КОТЛОВСКИЙ М.Ю | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Сибирское медицинское обозрение | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| AKLILLU E | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Eur J Clin Pharmacol | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
Авторы
Даты
2023-04-12—Публикация
2022-06-22—Подача