Изобретение относится к области тонкого органического синтеза, медицине и вирусологии, а именно к использованию органических биологически активных соединений общей формулы Ia-d (фиг.1) в качестве ингибиторов ортопоксвирусов и перспективных химических соединений при создании препаратов для лечения и экстренной профилактики ортопоксвирусных заболеваний у человека и животных.
С 1980 года была прекращена всеобщая вакцинация населения против оспы, возбудителем которой является вирус натуральной оспы (ВНО), в связи с объявлением Всемирной организацией здравоохранения (ВОЗ) о полной ликвидации этого заболевания на планете. Поэтому в настоящее время более половины населения Земли лишено противооспенного иммунитета. Традиционная вакцинация с использованием живого вируса осповакцины опасна для людей с иммунодефицитом, число которых ежегодно увеличивается [UNAIDS date 2017; Pelkonen P.M, Tarvainen K., Hynninen A., Kallio E.R., Henttonen K., Palva A., Vaheri A., Vapalahti O. Cowpox with severe generalized eruption, Finland. Emerg. Infect. Dis. 2003. 9:1458-1461]. Следует отметить, что в РФ нет официально зарегистрированных химиопрепаратов для лечения поствакцинальных осложнений и профилактики оспенных заболеваний.
Нуклеозидный внутривенный препарат Цидофовир (Cidofovir, Vistide®, CDV) избирательно ингибирует вирусную ДНК-полимеразу и проявляет антиортопоксвирусную активность в экспериментах in vitro и in vivo [J. Gen. Virol. 2016. 97(5):1229-1239]. Проявляет активность в летальных моделях ортопоксвирусной инфекции у мышей и обезьян. Однако существенными недостатками Цидофовира являются низкая пероральная биодоступность и потенциальная нефротоксичность. Кроме того, этот препарат оказался неэффективным при его применении после проявления оспенных поражений у зараженных BHO обезьян [Идентификационный номер ВОЗ: WHO/HSE/GAR/BDP/2010.3/RUS. Всемирная организация здравоохраниения. Научный обзор исследований вируса натуральной оспы, 1999-2010 гг. 2011. 132 с.].
Модификацией химиопрепарата Цидофовир (Cidofovir) является современный, эффективный и биодоступный при пероральном введении противовирусный химический препарат Бринцидофовир (Brincidofovir, CMX001 [Chimerix Receives U.S. Food and Drug Administration Approval for TEMBEXA® (brincidofovir) for the Treatment of Smallpox (URL: https://www.globenewswire.com/news-release/2021/06/04/2242292/25619/en/Chimerix-Receives-U-S-Food-and-Drug-Administration-Approval-for-TEMBEXA-brincidofovir-for-the-Treatment-of-Smallpox.html; 04.06.2021]. Недостатком его применения является развитие резистентности при пассивировании ортопоксвирусов in vitro в присутствии CMX00l [Идентификационный номер ВОЗ: WHO/HSE/GAR/BDP/2010.4. Всемирная организация здравоохранения. Консультативная группа независимых экспертов ВОЗ по обзору программы исследования натуральной оспы (AGIES). Замечания к «Научному обзору исследований вируса натуральной оспы 1999-2010 гг.» 2010. 43 с.].
Также препаратом, разрешенным для лечения натуральной оспы и оспы обезьян, является Тековиримат (Tecovirimat, содержащий в качестве активной фармацевтической субтанции (АФС) N-{3,5-Диоксо-4-азатетрацикло[5.3.2.0{2,6}.0{8,10}]додец-11-ен-4-ил}-4-(трифторметил)бензамид (ST-246) [FDA approves the first drug with an indication for treatment of smallpox. FDA News Release. https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm613496.htm; 13.07.2018]. ST-246 был разработан SIGA Technologies Inc. (США). Его механизм действия отличается от механизма действия CDV, мишенью ST-246 является высококонсервативный вирусный кодируемый белок р37, присутствующий во всех ортопоксвирусах. Недостатком данного препарата является развитие резистентности ортопоксвирусов при его длительном использовании [Идентификационный номер ВОЗ: WHO/HSE/GAR/BDP/2010.4. Всемирная организация здравоохранения. Консультативная группа независимых экспертов ВОЗ по обзору программы исследования натуральной оспы (AGIES). Замечания к «Научному обзору исследований вируса натуральной оспы 1999-2010 гг.» 2010. 43 с.].
Недавно была завершена 1 фаза клинических испытаний нового отечественного препарата НИОХ-14, который является пролекарством ST-246, а по механизму действия также как ST-246 является ингибитором вирусного белка р37. НИОХ-14 проявляет высокую противовирусную активность против ортопоксвирусов, в том числе ВНО [Мазурков О.Ю., Шишкина Л.Н., Бормотов Н.И., Скарнович М.О., Мазуркова Н.А., Черноносов А.А., Тихонов А.Я., Селиванов Б.А. Оценка абсолютной биодоступности химической субстанции противооспенного препарата НИОХ-14 в экспериментах на мышах. Бюллетень экспериментальной биологии и медицины. 2020. Т. 170, № 8. - С. 173-177. Doi: http://iramn.ru/journals/bbm/2020/8/5903/].
Эксперты ВОЗ рекомендуют продолжать исследования по созданию новых препаратов, обладающих активностью в отношении ортопоксвирусов. Направленность действия новых противовирусных препаратов может касаться разных стадий вирусного цикла [Идентификационный номер ВОЗ: WHO/HSE/GAR/BDP/2010.4. Всемирная организация здравоохранения. Консультативная группа независимых экспертов ВОЗ по обзору программы исследования натуральной оспы (AGIES). Замечания к «Научному обзору исследований вируса натуральной оспы 1999-2010 гг.» 2010. 43 с.].
В связи с этим разработка новых противооспенных препаратов, обладающих высокой противовирусной активностью и низкой цитотоксичностью, является важной задачей для обеспечения безопасности здоровья и жизни людей.
Технической задачей предлагаемого изобретения является синтез нового класса ингибиторов с высоким индексом селективности в отношении ортопоксвирусов.
Техническим результатом является расширение ряда соединений, обладающих высокой антивирулентной активностью в отношении ортопоксвирусов.
Поставленная задача решается путем синтеза новых соединений общей формулы Ia-d (фиг.1), обладающих высоким индексом селективности в отношении ортопоксвирусов.
Синтез производных 1-гидрокси- и 1-метокси-2-(4-нитрофенил)имидазола Ia-d осуществляют путём взаимодействия соответствующих оксимов с нитробензальдегидом и ацетатом аммония в ледяной уксусной кислоте при комнатной температуре с получением 1-гидрокси-2-(4-нитрофенил)имидазолов Ia-Ib и последующим метилированием при комнатной температуре в присутствии гидроксида калия в ДМФА с получением 1-метокси-2-(4-нитрофенил)имидазолов Iс-d (фиг.2).
Цитотоксичность и противовирусную активность синтезированных производных в отношении вирусов оспавакцины, оспы коров и оспы мышей оценивают с использованием адаптированного колориметрического метода в культуре клеток Vero [Селиванов Б.А., Тихонов А.Я., Беланов Е.Ф., Бормотов Н.И., и др. Химико-фармацевтический журнал. (2017) 51(6), 13-17]. В качестве положительного контроля используют коммерчески доступный препарат Cidofovir (HeritageConsumerProducts, LLC, США).
В известном уровне техники отсутствуют сведения о заявляемых соединениях, обладающих высокой противовирусной активностью и низкой цитотоксичностью.
Изобретение подтверждается следующими примерами:
Пример 1. 1-(1-гидрокси-4-метил-2-(4-нитрофенил)-1Н-имидазол-5-ил)этанон Ia.
Смесь 4,53 г (30,0 ммоль) 4-нитробензальдегида, 3,87 г (30,0 ммоль) 3-гидроксиамино-2,4-пентандиона и 2,53 г (32,5 ммоль) ацетата аммония в 25 мл ледяной уксусной кислоты перемешивают при комнатной температуре в течение 12 часов и оставляют на двое суток. Выпавший осадок отфильтровывают и промывают 15 мл диэтилового эфира и кипятят в 200 мл н-гексана. Получают 5,06 г (65 %) 1-(1-гидрокси-4-метил-2-(4-нитрофенил)-1Н-имидазол-5-ил)этанона (Ia) в виде желтого порошка с т.пл. 182-184°С.
1Н ЯМР (300 МГц, CDCl3, 298 К), δ (м.д.): 14,14 (с, 1H, OH); 8,44 (д, J=9,2 Гц, 2H, H-Ar); 8,32 (д, J=9,1 Гц, 2H, H-Ar); 2,63 (с, 6H, 2CH3)
1Н ЯМР (400 МГц, DMSO-d6, 295 К), δ (м.д.): 12,63 (уш. с, 1H, OH); 8,40-8,34 (м, 4H, H-Ar); 2,55 (с, 3H, CH3); 2,42 (с, 3H, CH3) м.д.
13С ЯМР (100,62 МГц, DMSO-d6), δ (м.д.): 188,5, 147,6, 134,0, 128,5, 127,9, 124,4, 124,3, 30,3, 16,3.
ИК (KBr, ν, см-1): 2300-2800 (N-H…O=C); 1648 (C=O); 1513, 1339 (NO2).
Пример 2. 3-гидрокси-6,6-диметил-2-(4-нитрофенил)-3,5,6,7-тетрогидро-4Н-бензимидазол-4-он Ib.
Смесь 4,53 г (30 ммоль) 4-нитробензальдегида, 5,07 г (30 ммоль) 2-(гидроксиимино)-5,5-диметилциклогексан-1,3-диона и 2,69 г (35 ммоль) ацетата аммония в 30 мл ледяной уксусной кислоты перемешивают при комнатной температуре в течение 6 часов. Выпавший осадок отфильтровывают и промывают 20 мл воды. Получают 6,26 г (69%) 3-гидрокси-6,6-диметил-2-(4-нитрофенил)-3,5,6,7-тетрогидро-4Н-бензимидазол-4-она (Ib) в виде порошка желтого цвета. Т.пл. 130-132°С.
1Н ЯМР (400 МГц, DMSO-d6, 295 К), δ (м.д.): 2,81 (уш. с, 1H, OH); 8,34 (с, 4H, H-Ar); 2,68 (с, 2H, CH2); 2,39 (с, 2H, CH2); 1,06 (с, 6H, 2CH3).
13С ЯМР (100,62 МГц, DMSO-d6), δ (м.д.): 186,8, 172,5, 150,4, 147,9, 142,6, 134,3, 129,0, 124,4, 124,3, 53,0, 38,8, 35,8, 28,4, 21,5.
ИК (KBr, ν, см-1): 2300-2800 (N-ОH…O=C); 1666 (C=O); 1520, 1342 (NO2).
Пример 3. 1-(1-метокси-4-метил-2-(4-нитрофенил)-1Н-имидазол-5-ил)этанон Ic.
Смесь 2,00 г (8 ммоль) 1-(1-гидрокси-4-метил-2-(4-нитрофенил)-1Н-имидазол-5-ил)этанона Iа, 0,50 г (9 ммоль) гидроксида калия в 20 мл ДМФА охлаждают при перемешивании до 4°С и добавляют 0,5 мл (1,14 г, 8 моль) йодистого метила. Реакционную массу выдерживают в течение 4 часов при комнатной температуре, затем выливают в 60 мл воды, перемешивают в течение 20 минут. Выпавший осадок отфильтровывают и промывают водой на фильтре. Затем кипятят в 22 мл н-гексана. Получают 1,56 г (71 %) 1-(1-метокси-4-метил-2-(4-нитрофенил)-1Н-имидазол-5-ил)этанона (Ic) в виде порошка ярко-желтого цвета. Т.пл. 122-124°С.
1Н ЯМР (300 МГц, CDCl3, 303 К), δ (м.д.): 8,36 (д, J=9,3 Гц, 2H, H-Ar); 8.32 (д, J=9,1 Гц, 2H, H-Ar); 3,97 (с, 3H, ОCH3); 2,60 (с, 3H, CH3); 2,59 (с, 3H, CH3).
1Н ЯМР (400 МГц, DMSO-d6, 294 К), δ (м.д.): 8,37 (д, J= 9,1 Гц, 1H, Н-Ar); 8,30 (д, J=9,0 Гц, 1H, Н-Ar); 3,96 (с, 3H, ОСН3); 3,55 (с, 3H, CH3); 2,47 (с, 3H, CH3).
13С ЯМР (150,94 МГц, DMSO-d6), δ (м.д.): 187,3, 148,1, 143,8, 139,5, 133,5, 128,9, 125,8, 124,7, 67,9, 30,2, 17,1.
ИК (KBr, ν, см-1): 3116, 3010, 2925 (2CH3; OCH3); 1657 (C=O); 1511, 1338 (NO2).
Пример 4. 3-метокси-6,6-диметил-2-(4-нитрофенил)-3,5,6,7-тетрагидро-4Н-бензимидазол-4-она Id.
Смесь 2,1 г (7 ммоль) 3-гидрокси-6,6-диметил-2-(4-нитрофенил)-3,5,6,7-тетрогидро-4Н-бензимидазол-4-она Ib, 0,56 г (10 ммоль) гидроксида калия в 20 мл ДМФА охлаждают при перемешивании до 4°С и добавляют 0,4 мл (0,99 г, 7 ммоль) йодистого метила. Реакционную массу выдерживают в течение 4 часов при комнатной температуре и оставляют на двое суток. Затем выливают в 100 мл воды, перемешивают в течение 20 мин. Выпавший осадок отфильтровывают и промывают водой на фильтре. Затем кипятят в 20 мл воды, отфильтровывают в горячем виде. Получают 1,60 г (73%) 3-метокси-6,6-диметил-2-(4-нитрофенил)-3,5,6,7-тетрагидро-4Н-бензимидазол-4-она (Id) в виде порошка ярко-желтого цвета. Т.пл. 148-150°С.
1Н ЯМР (400 МГц, DMSO-d6, 291 К), δ (м.д.): 8,39-8,32 (м, 4H, H-Ar); 4,08 (с, 3H, ОCH3); 2,72 (с, 2H, CH2); 2,45 (с, 2H, CH2); 1,08 (с, 6H, 2CH3).
13С ЯМР (100,62 МГц, DMSO-d6), δ (м.д.): 186,5, 151,2, 148,3, 141,9, 133,5, 129,0, 124,6, 122,7, 67,7, 52,7, 38,8, 35,8, 28,4.
ИК (KBr, ν, см-1): 3086, 2963, 2893 (2CH3; OCH3); 1666 (C=O); 1520, 1342 (NO2).
Спектральный анализ полученных соединений проведён на спектрометре Bruker Avance TM 400 (рабочая частота 1Н: 400 МГц, 13С: 100.62 МГц) с использованием дейтерированных растворителей (CDCl3, DMSO-d6). В качестве внутренних стандартов использованы остаточные сигналы растворителей. ИК-спектр зарегистрирован на фурье-спектрофотометре Shimadzu IRAffinity-1 FTIR в таблетках KBr.
Температуры плавления измерены на приборе для измерения температуры плавления ПТП(М) и не корректированы.
Пример 5. Определение цитотоксичности и противовирусного действия соединений Ia-d в отношении вирусов осповакцины (штамм Копенгаген), оспы коров (штамм Гришак) и оспы мышей (штамм К-1) в культуре клеток Vero
Цитотоксичность и противовирусную активность синтезированных производных в отношении вирусов оспавакцины, оспы коров и оспы мышей оценивают с использованием адаптированного колориметрического метода в культуре клеток Vero [Селиванов Б.А., Тихонов А.Я., Беланов Е.Ф., Бормотов Н.И., и др. Химико-фармацевтический журнал. (2017) 51(6), 13-17]. В качестве положительного контроля используют коммерчески доступный препарат Cidofovir (HeritageConsumerProducts, LLC, США).
Противовирусную активность и цитотоксичность заявляемых соединений Ia-d проверяют в культуре клеток Vero. В качестве модели используют вирусы осповакцины (штамм Копенгаген), оспы коров (штамм Гришак) и оспы мышей - эктромелии (штамм К-1) как типичных представителей семейства ортопоксвирусов из Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ БВ «Вектор» Роспотребнадзора.
Монослой клеток Vero выращивают в 96-луночных планшетах. Из исследуемых соединений Ia-d готовят растворы в диметилсульфоксиде с концентрацией 20 мг/мл. Из приготовленных растворов готовят серии разведений в питательной среде с 5-кратным или 3-кратным шагом, начальная концентрация препарата в лунке планшета составляет 100 или 400 мкг/мл.
Разведения препаратов вносят в лунки планшетов с монослоем клеток, затем в половину лунок планшета вносят вирус, а вторую половину лунок планшета используют для оценки цитотоксичности соединений.
В качестве препарата сравнения (или прототипа) используют препарат Цидофовир (Cidofovir производства Gilead Sciences Inc., США).
После инкубации в течение 4 суток в лунки добавляют витальный краситель нейтральный красный, который поглощают только живые клетки. Клетки, которые разрушает вирус или повреждает токсическое воздействие соединения, не поглощают витальный краситель. Монослой клеток отмывают от непоглощённого красителя физиологическим раствором, и вносят в лунки лизирующий буфер, разрушающий клетки с поглощенным красителем и растворяющий этот краситель.
Светопоглощение (оптическую плотность - ОП) растворов в лунках планшетов измеряют при длине волны 490 нм на планшетном спектрофотометре E-Max (Molecular Devises США). ОП пропорциональна количеству жизнеспособных клеток, она отражает противовирусную активность соединения в сравнении с ОП в контроле вируса или характеризует цитотоксичность этого соединения в сравнении с ОП в контроле клеток.
Результаты обрабатывают с помощью программы Soft Max Pro 4.0, которая вычисляет 50 %-ю цитотоксическую концентрацию (СС50 мкг/мл) и 50 %-ю концентрацию, ингибирующую вирус (IC50 мкг/мл). На основании показателей СС50 и IC50 определяют индекс селективности (SI)
SI = СC50 / IC50.
Величина SI менее 8 считается неприемлемой для соединений, которые могут быть перспективными в качестве противовирусных препаратов [J. Gen. Virol. 2016. 97(5):1229-1239].
Расчет и сравнение средних величин CС50 и IC50 проводят стандартными методами описательной статистики с помощью пакета анализа данных Microsoft Excel.
Результаты изучения цитотоксического и противовирусного действия соединений приведены в таблице 1.
(M.m.)
мкг/мл (мкмоль)
(SI=CC50/IC50)
оспы коров
(261,24)
(28,48±7,01)
(0,65±0,19)
(43,5)
(2,45±0,80)
(11,6)
(1,30±0,38)
(21,8)
(301,30)
(142,42±48,32)
(0,13±0,03)
(1072,8)
(1,16±0,36)
(122,6)
(0,40±0,13)
(357,6)
(275,26)
(443,6±150,2)
(4,76±0,11)
(93,2)
(15,91±5,70)
(27,9)
(13,88±1,13)
(32,0)
(315,33)
(1154,3±272,2)
(3,96±0,22)
(291,2)
(17,92±4,88)
(64,4)
(12,53±0,57)
(92,2)
(279,19)
(прототип)
(1111,5±215,2)
(47,14±15,01)
(23,8)
(91,55±15,94)
(12,1)
(22,14±9,38)
(50,22)
Примечание:
СC50 - 50 %-я цитотоксическая концентрация препаратов, при которой разрушаются 50 % клеток в неинфицированном монослое.
IC50 - 50 %-я вирус ингибирующая концентрация препаратов, при которой сохраняется 50 % клеток в инфицированном монослое.
Значения СC50 и IC50 представлены в виде М±Sm, где М - среднее значение, Sm - стандартное отклонение при числе измерений n=3.
SI - индекс селективности препаратов (СC50/IC50).
M.m. - молекулярная масса.
* - отличие от показателей СC50 всех других препаратов при р≤0,05.
** - отличие от соответствующих показателей IC50 Цидофовира при р≤0,05.
& - тенденция к отличию от показателей IC50 Цидофовира при р≤0,9.
Как видно из таблицы 1, производные 1-гидрокси- и 1-метокси-2-(4-нитрофенил)имидазола - соединения Ia-d более активные в отношении вирусов осповакцины, оспы коров и оспы мышей (эктромелии), чем препарат сравнения (прототип) Цидофовир.
Таким образом, заявляемый ряд соединений Ia-d является новым типом эффективных ингибиторов ортопоксвирусов, патогенных для человека и животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ БОРНИЛАМИНА В КАЧЕСТВЕ ИНГИБИТОРОВ ОРТОПОКСВИРУСОВ | 2018 |
|
RU2687254C1 |
| МЕТИЛ, ХЛОР И НИТРОПРОИЗВОДНЫЕ N-{3, 5-ДИОКСО-4-АЗАТЕТРАЦИКЛО[5.3.2.0.0]ДОДЕЦ-11-ЕН-4-ИЛ}-2-ГИДРОКСИБЕНЗАМИДА-ПРОТИВОВИРУСНЫЕ ПРЕПАРАТЫ, ИНГИБИРУЮЩИЕ РЕПЛИКАЦИЮ РАЗЛИЧНЫХ ВИДОВ ОРТОПОКСВИРУСОВ | 2010 |
|
RU2440983C1 |
| Амиды, сочетающие адамантановый и монотерпеновый фрагменты, используемые в качестве ингибиторов ортопоксвирусов | 2019 |
|
RU2712135C1 |
| 7-[N'-(4-ТРИФТОРМЕТИЛБЕНЗОИЛ)-ГИДРАЗИНОКАРБОНИЛ]-ТРИЦИКЛО[3.2.2.0]НОН-8-ЕН-6-КАРБОНОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2412160C1 |
| Амиды, содержащие адамантановые и ароматические фрагменты, используемые в качестве ингибиторов репродукции ортопоксвирусов | 2021 |
|
RU2798665C2 |
| {3,5-ДИОКСО-4-АЗАТЕТРАЦИКЛО[5.3.2.0.0]ДОДЕЦ-11-ЕН-4-ИЛ}ТИОМОЧЕВИНА, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ОРТОПОКСВИРУСОВ | 2009 |
|
RU2412167C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО ПРОТИВ ВИРУСА НАТУРАЛЬНОЙ ОСПЫ И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2013 |
|
RU2543338C1 |
| N-{3,5-ДИОКСО-4-АЗАТЕТРАЦИКЛО[5.3.2.0.0]ДОДЕЦ-11-ЕН-4-ИЛ}-4-ГИДРОКСИБЕНЗАМИД, ПРОТИВОВИРУСНЫЙ ПРЕПАРАТ, ИНГИБИРУЮЩИЙ РЕПЛИКАЦИЮ РАЗЛИЧНЫХ ВИДОВ ОРТОПОКСВИРУСОВ | 2010 |
|
RU2424800C1 |
| 2-ЦИКЛОАЛКИЛИМИНО-5-(4-НИТРОФЕНИЛ)-1,3,4-ТИАДИАЗИНЫ, ОБЛАДАЮЩИЕ БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ ПРОТИВ ВИРУСОВ ОСПЫ | 2005 |
|
RU2281946C1 |
| N-БОРНИЛ- И N-ФЕНХИЛКАРБОКСАМИДЫ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ ОРТОПОКСВИРУСОВ | 2022 |
|
RU2800448C1 |
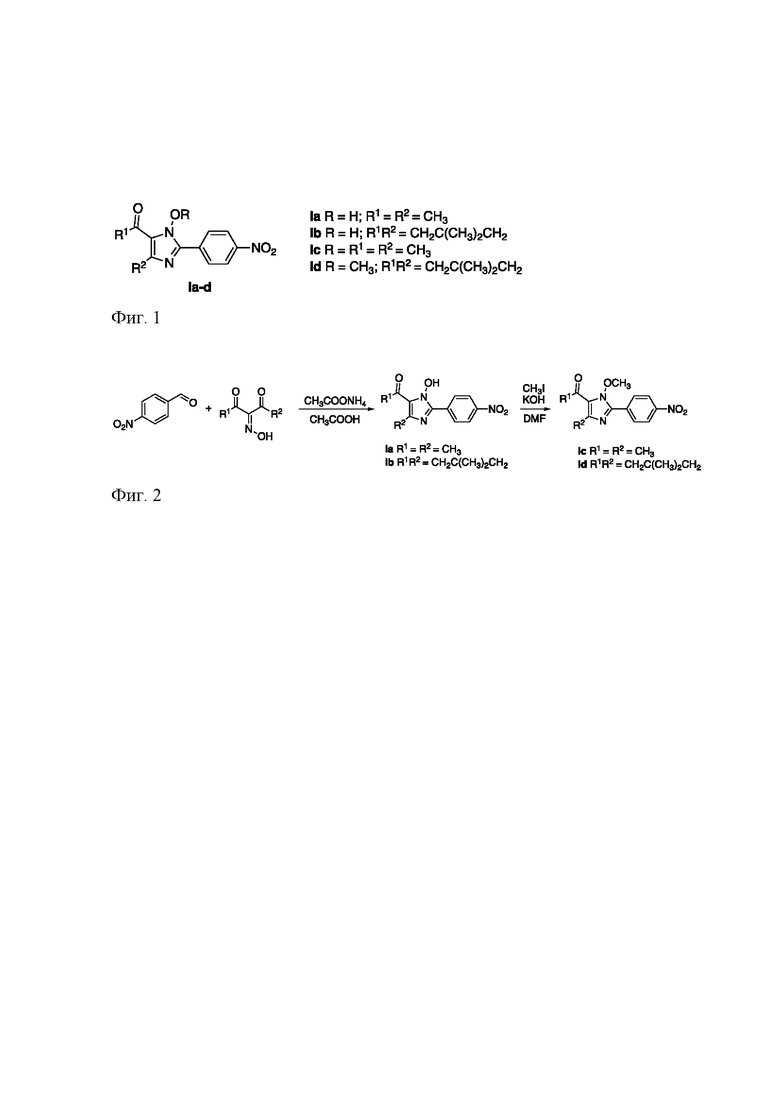
Изобретение относится к области органической химии, а именно к новым производным 1-гидрокси- и 1-метокси-2-(4-нитрофенил)имидазола общей формулы Ia-d, обладающим противовирусной активностью в отношении ортопоксвирусов. В соединениях формулы Ia-d R = H; R1 = R2 = CH3 (Ia); R = H; R1R2 = CH2C(CH3)2CH2 (Ib); R = R1 = R2 = CH3 (Ic); R = CH3; R1R2 = CH2C(CH3)2CH2 (Id). 2 ил., 1 табл., 5 пр.
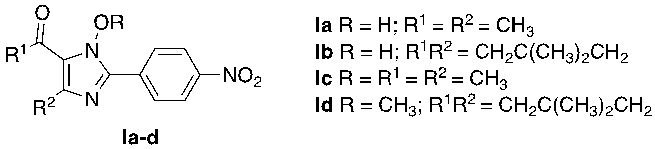
Производные 1-гидрокси- и 1-метокси-2-(4-нитрофенил)имидазола общей формулы Ia-d
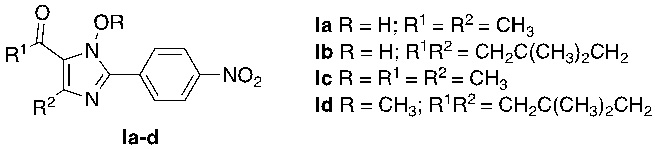 ,
,
обладающие противовирусной активностью в отношении ортопоксвирусов.
| ERTEL H | |||
| ET AL., Synthese von 1-Hydroxyimidazolen und 1-Hydroxyimidazol-3-oxiden, JUSTUS LIEBIGS ANNALEN DER CHEMIE, 1974 (9), pp | |||
| Устройство лопаток осевых паровых турбин | 1924 |
|
SU1399A1 |
| RU 2014109441 A, 20.09.2015 | |||
| KR 101194995 B1, 29.10.2012 | |||
| US 2012058080 A1, 08.03.2012 | |||
| ПРОИЗВОДНЫЕ ИНДОЛА, ОБЛАДАЮЩИЕ АНТИВИРУСНОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2217421C2 |
Авторы
Даты
2023-04-24—Публикация
2022-08-15—Подача