Изобретение относится к медицине, а именно к пульмонологии и предназначено для прогнозирования отдаленного исхода хронической обструктивной болезни легких (ХОБЛ).
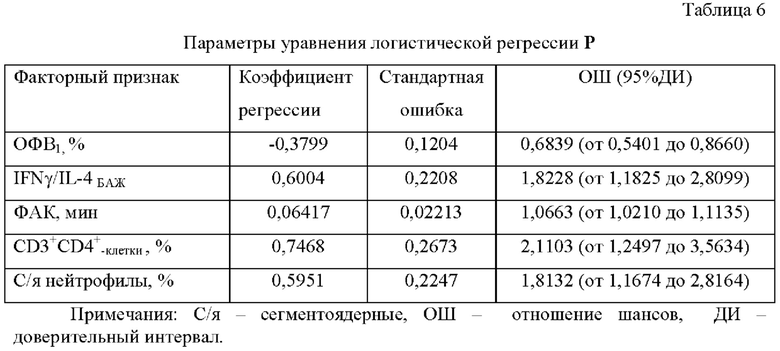
ХОБЛ - тяжелое, широко распространенное во всем мире заболевание, с высоким уровнем инвалидизации и смертности больных. В настоящее время ХОБЛ является третьей по величине причиной смертности во всем мире [18, 21]. По современным представлениям, ХОБЛ - это предотвратимое, поддающееся лечению заболевание, «характеризующееся ограничением скорости воздушного потока, которое не полностью обратимо, обычно прогрессирует и связано с патологическими воспалительным ответом легких на действие ингалируемых патогенных частиц или газов», и также сопровождающееся «существенными внелегочными проявлениями, способными дополнительно отягощать течение болезни у отдельных пациентов». Обострение ХОБЛ, определяемое как «острое ухудшение респираторных симптомов, которые приводят к дополнительной терапии», является основной причиной высокого уровня госпитализации и смертности у пациентов с ХОБЛ [12, 21]. Основными факторами риска ХОБЛ являются сигаретный дым, загрязнение воздуха и генетические факторы, вызывающие или усугубляющие ХОБЛ [11]. Сигаретный дым и другие агрессивные аэрозоли вызывают гиперпродукцию провоспалительных цитокинов (TNF-α, IL-1β, IL-6, IL-8 и IL-17A) в легочной ткани, усиление воспалительной реакции и усугубление повреждения легких [20, 23]. Вирусные или бактериальные респираторные инфекции приводят к обострениям ХОБЛ, проявляющимся усилением воспалительного процесса в дыхательных путях и секреции слизи [13, 21]. Избыточное образование провоспалительных цитокинов обусловливает системное воспаление при ХОБЛ [14, 15, 16], что приводит к преобладанию катаболических процессов в организме больных, снижению массы тела, миопении, остеопорозу. Гиперпродукция провоспалительных цитокинов вызывает изменения в системе гемостаза - повышение уровней прокоагулятных факторов и вторичную активацию фибринолиза [7]. Инвалидизация больных ХОБЛ наступает в среднем через 10 лет после установки диагноза [3].
Обострение, связанное с усилением воспаления дыхательных путей и избыточной продукцией слизи, является основной причиной неблагоприятных исходов и смертности при ХОБЛ [21]. Смертельный исход преимущественно наблюдается у больных с тяжелым и крайне тяжелым течением ХОБЛ. При этом даже при своевременном установлении риска неблагоприятного исхода возможность предотвращения смертельного исхода очень мала; в то время как легкое и среднетяжелое течение ХОБЛ характеризуется меньшей летальностью.
Диагностика ХОБЛ затруднена на ранних стадиях, когда еще отсутствуют явные респираторные симптомы. ХОБЛ выявляется на основании снижения спирометрического показателя - индекса Тиффно - отношения постбронхолитического объема форсированного выдоха за 1-ю секунду (ОФВ1) к форсированной жизненной емкости легких (ФЖЕЛ) менее 70% от должных значений. В клинической практике в настоящее время рекомендуют использовать для прогнозирования исхода ХОБЛ индекс BODE [9, 17], включающий 4 показателя в баллах: индекс массы тела - ИМТ (Body mass index) (значения менее 21 кг/м2 соответствует 1 баллу, более 21 кг/м2 - 0), спирометрический показатель ОФВ1 в % от должного, снижение которого отражает выраженность бронхиальной обструкции (Obstruction), значение шкалы MRC (Medical Research Council Dyspnea Scale), характеризующее выраженность одышки (Dyspnea) и расстояние, пройденное при выполнении 6-минутной шаговой пробы (табл. 1). Суммарное количество баллов может колебаться в пределах от 0 до 10. Максимальное число баллов соответствует высокому риску наступления смертельного исхода.
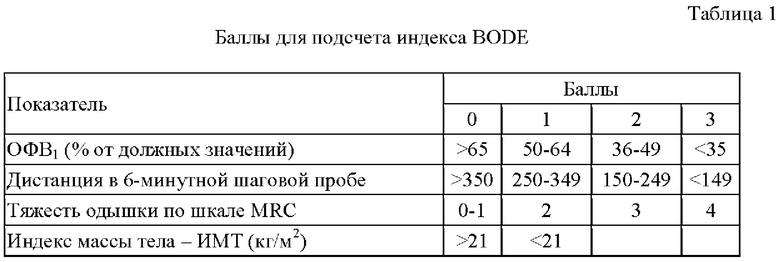
Ключевым недостатком данного метода является то, что подсчет индекса BODE включает проведение 6-минутной шаговой пробы, условием проведения которой является стабилизация ХОБЛ, и, следовательно, данный прогностический метод невозможно использовать во время обострения заболевания на госпитальном этапе лечения. Другим недостатком является то, что данный способ предполагает анализ лишь клинико-функциональных признаков ХОБЛ и не учитывает патогенетически значимые показатели заболевания, что снижает точность прогностической эффективности способа. Кроме того, данный метод прогнозирования исхода ХОБЛ в большей степени подходит для прогноза тяжелого течения заболевания, так как в качестве одного из предикторов неблагоприятного исхода предлагается снижение ИМТ - внелегочного признака, характерного для больных с тяжелым и крайне тяжелым течением ХОБЛ (GOLD3, GOLD4).
Описан способ прогнозирования неблагоприятного исхода ХОБЛ в сочетании с артериальной гипертензией в течение 2 лет [2], в соответствии с которым используют формулу (модель) логистического регрессионного анализа:
y=6,2-0,32×a-1,7×б-2,1×в-1,0×г-0,8×д-1,2×е,
где а, б, в, г, д, е - значения показателей модели:
а - спирометрический показатель ОФВ1 <70% (0 - нет, 1 - да),
б - наличие спонтанной агрегации лейкоцитарно-тромбоцитарной суспензии (число лейкоцитов 6-8×109/л, тромбоцитов - 220-240×1012/л) по методу Born [8] (0 - нет, 1 - да),
в - длительность артериальной гипертензии более 10 лет (0 - нет, 1 - да),
г - длительность ХОБЛ более 10 лет (0 - нет, 1 - да),
д - обострения ХОБЛ более 2 в год (0 - нет, 1 - да),
д - гнойная мокрота при обострении (0 - нет, 1 - да).
Затем полученное значение у вставляют в формулу определения индивидуального риска неблагоприятных исходов ХОБЛ с АГ (в течение 2 лет):
Р=еу/(1+еу), где е - основание натурального логарифма = 2,718,
Р вероятность развития неблагоприятного события ХОБЛ с АГ (развитие инсультов, инфарктов миокарда и летальный исход). Значения Р ниже 0,25 свидетельствуют о низком риске неблагоприятного исхода ХОБЛ, значения от 0,26 до 0,75 - о среднем и значения более 0,76 - о высоком риске.
Недостатком описанного способа можно считать то, что он позволяет прогнозировать риск неблагоприятных событий в отношении инсультов, инфарктов миокарда, летальных исходов лишь в целом и не предназначен для оценки вероятности развития конкретного неблагоприятного события летального исхода. Данный способ может быть использован преимущественно для прогноза неблагоприятного исхода тяжелых случаев ХОБЛ в сочетании с сердечно-сосудистой патологией. К тому же прогностическая модель не содержит патогенетически значимые показатели заболевания.
Известен способ «Прогнозирование исходов у пациентов с хронической обструктивной болезнью легких» [1], который позволяет оценить риск смертности пациентов с ХОБЛ в течение 2 лет и заключается в том, что используют 3 показателя из 4-х показателей индекса BODE в сочетании с одним из следующих биомаркеров: 1) прокальцитонина (РСТ), 2) среднерегионального проадреномедуллина (MR-proADM), 3) среднерегионального предсердного натрийуретического пептида (MR-pro-ANP) или 4) копептина. Значения биомаркеров, как и значений индекса BODE, выражают в баллах в зависимости от их абсолютных значений:
- РСТ: <0,07 нг/мл - 0;
>0,07 нг/мл и ≤0,1 нг/мл - 2 балла;
>0,1 нг/мл - 4 балла;
- копептин: <2 пмоль/л - 0;
>2 пмоль/л и ≤14 пмоль/л - 2 балла;
>14 пмоль/л - 4 балла;
- MR-proANP: <50 пмоль/л - 0;
>50 пмоль/л и ≤140 пмоль/л - 2 балла;
>140 пмоль/л - 4 балла;
- MR-proADM: <0,5 нмоль/л 0;
>0,5 нмоль/л и ≤0,8 нмоль/л - 2 балла;
>0,8 нмоль/л - 4 балла.
В последующем баллы, соответствующие уровням биомаркеров, суммируют с баллами показателей индекса BODE. При этом значения баллов от 0 до 3 соответствует низкому уровню смертности пациентов с ХОБЛ в течение 2 лет, значения баллов от 4 до 6 - среднему уровню, а значения баллов от 7 до 13 - высокому риску. Авторы показали, что модель, включающая биомаркер (в виде непрерывной или категориальной переменной), являлась в прогностическом плане значительно лучше, чем модель с использованием только параметров индекса BODE. Прогностическая значимость была выше, когда биомаркер комбинировали с легко оцениваемыми параметрами - ИМТ и выраженностью одышки и не учитывали результат теста с 6-минутной ходьбой и ОФВ1, которые являются относительно сложными для определения. Недостатком метода является необходимость использования высокозатратных коммерческих тест-систем для определения биомаркеров. Предлагаемая модель включает внелегочный предиктор - снижение ИМТ, следовательно, предназначена преимущественно для прогнозирования исхода заболевания у пациентов с тяжелым и крайне тяжелым течением ХОБЛ. К тому же прогностическая модель не содержит важные патогенетически значимые иммунологические показатели.
Наиболее близким аналогом к заявленному изобретению является решение по патенту №2711453 «Способ оценки развития неблагоприятного течения хронической обструктивной болезни легких и артериальной гипертензии при их сочетании» [5], которое может быть использовано для оценки развития неблагоприятного течения хронической обструктивной болезни легких (ХОБЛ) и артериальной гипертензии (АГ) при их сочетании.
У больного ХОБЛ с АГ определяют показатели клеточного иммунитета: содержание Т-лимфоцитов (CD3+- и CD4+-клетки) в крови и показатели вариабельности сердечного ритма (ВСР): SDNN - среднее квадратичное отклонение величин интервалов R-R, RMSSD - среднеквадратичное значение между длительностью соседних R-R интервалов по электрокардиограмме. Оценивают риск развития неблагоприятного течения ХОБЛ с АГ, используя математическую формулу: p=1/(1+ez), где р - вероятность развития неблагоприятного течения ХОБЛ с АГ;
z=3,4*×Н1+0,8*×Н2-2,3*×Н3-1,7*×Н4+(-7,74),
H1 - Т-лимфоциты CD3+ (×109 клеток /л), Н2 - Т-лимфоциты CD4+ (×109 клеток /л), Н3 - SDNN (сек), Н4 - RMSSD (сек). При значении р от 0,1 до 0,5 риск развития неблагоприятного течения ХОБЛ с АГ оценивают как низкий риск. При р от 0,5 до 0,8 как высокий. При р от 0,9 до 1,1 как очень высокий. Чувствительность модели - 76%, специфичность 91%. Преимуществом данного способа является то, что модель включает патогенетически значимые иммунологические показатели число Т-лимфоцитов (CD3+-клетки) и число Т-клеточной субпопуляции - Т-хелперы (CD4+-клетки), а также показатели вегетативных реакций организма - показатели вариабельности сердечного ритма.
Недостатком способа является то, что не учитывается такой важный функциональный показатель при ХОБЛ, как ОФВ1. Входящие в математическую модель показатели вариабельности сердечного ритма могут зависеть от назначаемой при ХОБЛ фармакотерапии М-холинолитиками и β2-агонистами, способной влиять как на частоту сердечных сокращений, так и на значения артериального давления. К тому же, при выборе независимых переменных логистического регрессионного анализа, на основе которого составлена прогностическая модель, не учтены важные условия анализа не использовать взаимозависимые показатели. В модель входят: 1) два зависимых друг от друга иммунологических показателя - абсолютное число CD3+-клеток и абсолютное число CD4+-клеток: в состав популяции CD3+-клеток входят клетки CD4+-популяции; 2) абсолютные числа данных клеток высчитываются относительно общего числа лимфоцитов, что также увеличивает взаимозависимость абсолютных значений CD3+- и CD4+-клеток. При этом и другая пара показателей - SDNN и RMSSD, отражающих вариабельность пульса, также зависимы друг от друга.
Задачей заявляемого изобретения является разработка высокочувствительного и высокоспецифичного способа прогнозирования отдаленного исхода (в течение 15 лет) у больных с нетяжелым проявлением ХОБЛ, с сохранением показателей ФВ1 более 50% от должных величин, то есть у пациентов с легкой и среднетяжелой ХОБЛ (GOLD1, GOLD2). При раннем прогнозировании высокого риска смертельного исхода сохраняется шанс на отдаление сроков наступления смерти за счет коррекции схемы лечения, направленной на уменьшение частоты обострений путем усиления антимикробной и патогенетической терапии.
Техническим результатом настоящего предложения является повышение чувствительности и специфичности прогноза выживаемости на ранних стадиях ХОБЛ, преимущественно у больных со среднетяжелой степенью бронхообструкции (GOLD2) без сопутствующих заболеваний сердечно-сосудистой системы, неврологических расстройств, за счет анализа патогенетически значимых данных лабораторных исследований в комбинации с показателем степени бронхиальной обструкции ОФВ1.
Этот технический результат достигается тем, что при прогнозировании исхода хронической обструктивной болезни легких (ХОБЛ) у больного со среднетяжелым течением болезни, включающим анализ патогенетически значимых при ХОБЛ лабораторных показателей., в анализ включают определение степени бронхиальной обструкции по величине ОФВ1, причем, в первые сутки после госпитализации в стационар по поводу обострения ХОБЛ среднетяжелого течения проводят определение постбронходилатационного объема форсированного выдоха за первую секунду (ОФВ1), фибринолитической активности крови эуглобулиновым методом, иммунологические исследования определение в бронхоальвеолярной жидкости цитокинов интерферона-гамма (IFNγ), интерлейкина-4 (IL-4) методом иммуноферментного анализа, относительного содержания CD3+CD4+-клеток методом прямой иммунофлюоресценции и сегментоядерных нейтрофилов в периферической крови, при этом значения данных показателей вносят в уравнение:
Z=-53,0571-0,3799×ХОФВ1+0,6004×XIFNg/IL-4 БАЖ+0,06417×ХФАК+0,7468×XCD3CD4%+0,5951×Хс/я нейтр. %, где
(-53,0571) - константа, соответствующая теоретическому значению Z при нулевых значениях всех предикторов смертельного исхода ХОБЛ;
(-0,3799; 0,6004; 0,06417; 0,7468; 0,5951) - коэффициенты предикторов;
ХОФВ1 - значение постбронхолитического ОФВ1 в % от должного значения,
XIFNg/IL-4 БАЖ. - значение соотношения IFNγ/IL-4 в бронхоальвеолярной жидкости,
ХФАК - значение фибринолитической активности крови в минутах,
XCD3CD4 - число CD3+CD4+-клеток в %,
Хс/я нейтр. % - число сегментоядерных нейтрофилов в периферической крови в %,
затем полученное значение Z вносят в формулу для вычисления показателя вероятности смертельного исхода Р:
Р=1/(1+e-Z)×100% (е - основание натурального логарифма, равно 2,718), при получении значения Р больше 44,8% прогнозируют летальный исход ХОБЛ в течение 15 лет, при значении показателя, равном или меньше 44,8%, прогнозируют благоприятный исход.
Первым этапом решения поставленной задачи явилось исследование по изучению отдаленной выживаемости больных ХОБЛ. В исследовании учитывались показатели анализов больных, госпитализированных по поводу обострения впервые диагностированной в 2005 году ХОБЛ среднетяжелого течения. Основным критерием включения пациента в исследование являлось сохранение значения показателя ОФВ1 более 50% от должной величины, рассчитанной по коэффициентам, которые соответствовали росту и возрасту пациента. Критериями исключения служили: сопутствующие заболевания сердечно-сосудистой системы, неврологические расстройства. В составе исследуемой группы преобладали больные со среднетяжелой ХОБЛ (GOLD2) в связи с тем, что на стадии легкого течения (GOLD1), когда еще нет заметных симптомов ХОБЛ, заболевание диагностируется очень редко. Результаты исследования показали, что к 2020 году, через 15 лет от начала наблюдения, из 116 пациентов с ХОБЛ среднетяжелого течения в живых остались 44 пациента 37,9% от общего числа больных. Средняя продолжительность жизни пациентов с момента установления диагноза ХОБЛ у умерших больных составила 12,5 года. Обзор доступной литературы и патентный поиск показали, что к настоящему времени не известны способы прогнозирования отдаленного исхода ХОБЛ. В то время как это весьма актуально в настоящее время в связи с тем, что экспертами GOLD было установлено, что ХОБЛ заболевание, прогрессирование которого можно остановить [19]. Установление факторов неблагоприятного исхода ХОБЛ может помочь уточнить патогенетические механизмы прогрессирования ХОБЛ и лечь в основу разработки программ предотвращения неблагоприятного исхода ХОБЛ на ранних стадиях заболевания.
Известно, что ХОБЛ развивается у курильщиков с большим стажем (индекс курения более 10 пачко-лет) или у лиц, вынужденных вдыхать другие воздушные химически агрессивные поллютанты (дым жилищ при их печном отоплении, выхлопные газы, производственные химические вещества). Изучение патогенетических механизмов ХОБЛ показало, что ремоделирование воздухоносных путей при ХОБЛ связано с аутоиммунным процессом, происходящим в респираторном дереве и обусловленным активностью Т-лимфоцитов. Иммунная агрессия не ограничивается иммунными реакциями на местном уровне. При обострении ХОБЛ наблюдают повышение уровней цитокинов в сыворотке крови и связанные с этим признаки системного воспаления [21, 22]. С целью установления преобладающего типа иммунного ответа, развивающегося у больных ХОБЛ, проводили исследование уровней цитокинов интерлейкина-4 (IL-4) и интерферона-гамма (IFNγ) в бронхоальвеолярной жидкости, в последующем рассчитывали соотношение IFNγ/IL-4. Продукция IL-4 связана с гуморальным типом адаптивного иммунитета, в то время как образование IFNγ происходит преимущественно при усилении активности клеточного иммунитета. Кроме того, проводили иммунофенотипирование лимфоцитов методом прямой иммунофлюоресценции с использованием моноклональных антител CD3, CD4, CD8, CD20. Определяли показатели гемостазиограммы.
Полученные данные анализировали непараметрическими методами статистического анализа с использованием программ «Statistica 10.0» (США) и «MedCalc Software» (Бельгия). Для интегральной оценки диагностических качеств изучаемых показателей применяли логистический бинарный регрессионный анализ и ROC-анализ (построение характеристических кривых). Диагностическую эффективность показателей оценивали с помощью определения их чувствительности и специфичности. Чувствительность определяли как долю пациентов, у которых данный тест правильно спрогнозировал летальный исход в ближайшие 15 лет жизни. Специфичность определяли по доле больных, которым не был прогнозирован смертельный исход в группе выживших больных.
Результаты исследования выявили существенные различия по изучаемым показателям в исследуемых группах больных (табл. 2). Так, для группы умерших в течение 15 лет больных были характерны более выраженные изменения в спирограмме, свидетельствующие о нарушении бронхиальной проходимости. Отклонения в лабораторных показателях демонстрировали в этой же группе более глубокие изменения в содержании цитокинов в бронхоальвеолярной жидкости (БАЖ) и крови, популяционном и субпопуляционном составе клеток периферической крови, в гемостазиограмме, свидетельствующие в целом об активации воспалительного процесса на системном уровне, о преобладании активации клеточного механизма адаптивного иммунитета на местном уровне, сдвиге в системе гемостаза в сторону преобладания гиперкоагуляции со вторичным усилением фибринолитической активности.


Корреляционный анализ выявил связь основного патофизиологического проявления ХОБЛ снижения бронхиальной проходимости с повышением цитокинового индекса IFNγ/IL-4 в бронхоальвеолярной жидкости (в БАЖ) и содержания Т-хелперных клеток в крови, а также с изменениями в системе гемостаза (табл. 3). Эти данные свидетельствуют о том, что увеличение в периферической крови клеток воспаления - нейтрофилов, преобладание уровня IFNγ в БАЖ, увеличение клеток с хелперным фенотипом (CD3+CD4+-клетки) в периферической крови, изменения в системе гемостаза ассоциированы с основными патогенетическими механизмами ХОБЛ.
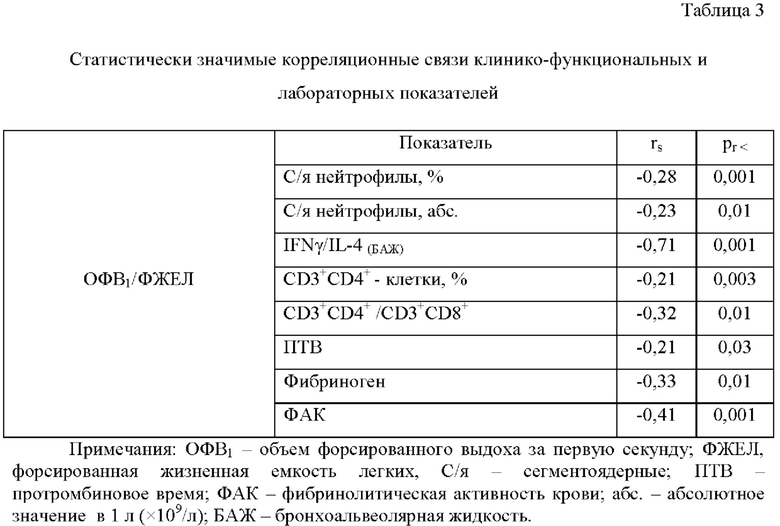
Летальный исход ХОБЛ в течение 15 лет коррелировал с рядом лабораторных показателей - значением соотношения IFNγ/IL-4(БАЖ), числом Т-хелперных клеток, спирометрическими и клиническими показателями, параметрами гемостазиограммы (табл. 4), что побудило к поиску нового способа прогнозирования долгосрочного исхода ХОБЛ.
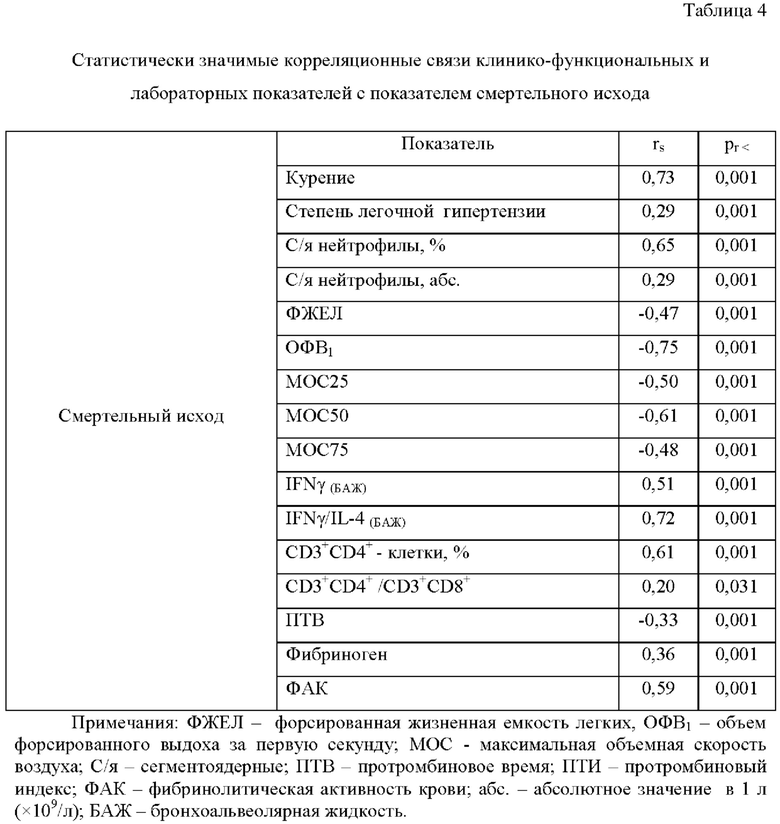
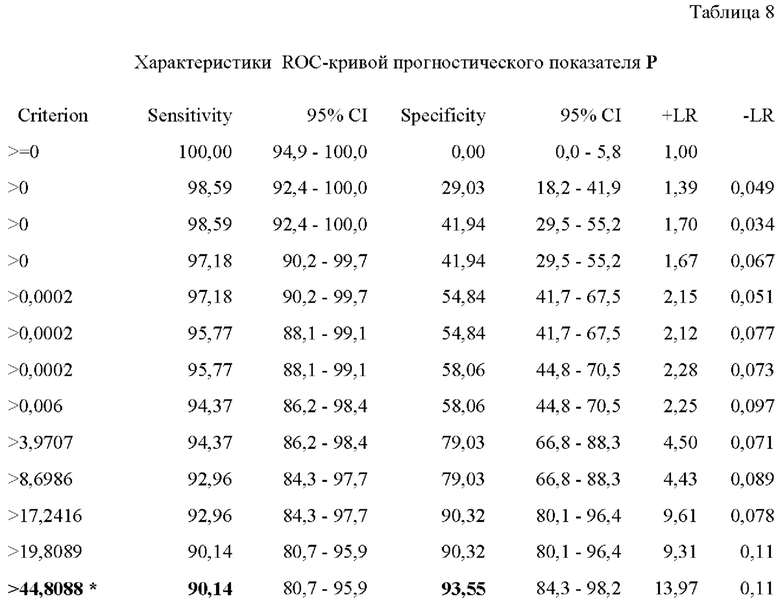
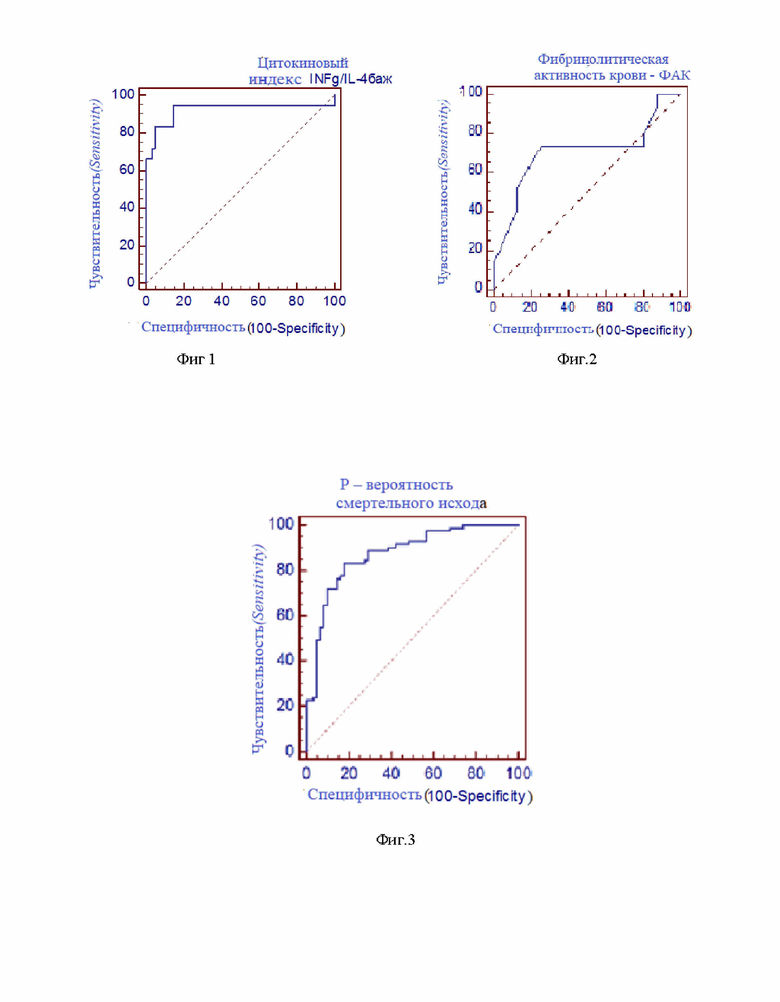
Для составления модели, позволяющей прогнозировать смертельный исход, был применен ROC (Receiver Operator Characteristic) - анализ в составе компьютерной программы «MedCalc Software» (Бельгия). Для каждого из 7 показателей (курение, С/я нейтрофилы, ОФВ1, МОС50, IFNγ/IL-4(БАЖ), CD3+CD4+-клетки, ФАК), проявивших среднюю или высокую степень корреляционной связи с показателем «смертельный исход», была построена ROC-кривая, или кривая ошибок, показывающая зависимость количества верно классифицированных положительных (истинно положительных) случаев от количества неверно классифицированных отрицательных (ложно отрицательных) случаев [6]. Доля истинно положительных случаев определяет чувствительность (Sensitivity) показателя, доля истинно отрицательных случаев - специфичность (Specificity). Чем ближе кривая к верхнему левому углу, где доля истинно положительных случаев составляет 100%, тем более качественен прогностический показатель, и чем ниже изгиб кривой, тем менее качественен. В качестве примера представлены ROC-кривые двух предикторов - 1) отношения IFNγ/IL-4(БАЖ) (фиг. 1) и 2) ФАК (фиг. 2), визуальное сравнение которых позволяет считать прогностические качества отношения IFNγ/IL-4(БАЖ) превосходящими. Такие же качества у показателя ФАК, так как кривая у первого показателя ближе к левому верхнему углу. Программа по проведению ROC-анализа позволяет рассчитать численный показатель площади под ROC-кривой, обозначаемой как AUC (Area Under Curve). Значения AUC в пределах 0,9-1,0 характеризуют отличное прогностическое качество показателя; 0,8-0,9 - очень хорошее; 0,7-0,8 - хорошее; 0,6-0,7 - среднее. Показатель, претендующий на роль предиктора, должен иметь AUC больше 0,5 [4]. AUC у отношения IFNγ/IL-4(БАЖ) оказалась равной 0,820, у показателя ФАК - 0,702, что также подтверждает превосходство прогностической ценности отношения IFNγ/IL-4(БАЖ)..
Программа по проведению ROC-анализа предоставляет также возможность определять ряд показателей AUC ROC-кривой: 95% ДИ - 95% доверительный интервал, стандартную ошибку, р - статистическую достоверность различия относительно AUC, равной 0,5. Кроме того, определяется так называемая область отсечения (cut-off), соответствующая численному значению показателя-предиктора, обеспечивающему оптимальное соотношение чувствительности и специфичности теста. Пять показателей из семи имели AUC ROC-кривых больше 0,5, что позволило рассматривать их как прогностические показатели (табл. 4).
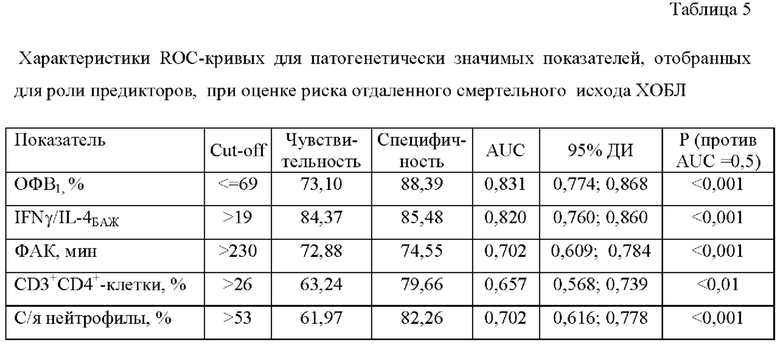

Для повышения прогностической эффективности пять отобранных показателей двух групп больных ХОБЛ выживших и умерших (в течение 15 лет после первого обострения заболевания) анализировали методом бинарного логистического регрессионного анализа (табл. 5) для формирования регрессионной модели (формулы):
Z=-53,0571-0,3799×Х ОФВ1+0,6004×X IFNγ/IL-4(БАЖ)+0,06417×Х ФАК+0,7468×X CD3CD4%+0,5951×Хс/я нейтр. %,
Р=1/(1+e-Z)×100%,
где Р вероятность смертельного исхода, е основание натурального логарифма, равно 2,718.
Для изучения прогностических характеристик показателя вероятности смертельного исхода Р проводили ROC-анализ данного показателя. На рис. 2 представлена ROC-кривая данного показателя. Приближение кривой к верхнему левому углу, соответствующему 100% чувствительности (доле истинно положительных случаев), свидетельствует о высоком прогностическом качестве показателя Р.
Численное значение AUC, равное 0,958, и высокая степень достоверности его отличия от площади под кривой, равной 0,5 (табл. 6), подтверждает высокую прогностическую ценность показателя вероятности смертельного исхода Р.

Был определен порог (cut-off) значений Р, обеспечивающий сочетание максимальных значений чувствительности и специфичности предложенной прогностической модели, который составил 44,8% (табл. 7). Значения Р больше 44,8% свидетельствуют о высокой вероятности смертельного исхода ХОБЛ в течение ближайших 15 лет.
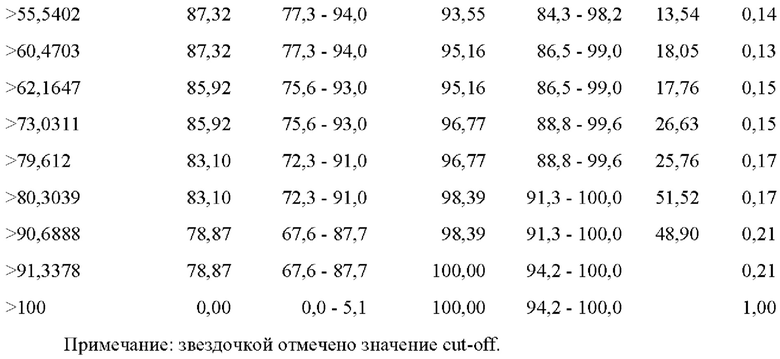
Прогностическая эффективность модели, соответствующая доле правильно предсказанных исходов, равна 91% (105 случаев из 116). Чувствительность предложенной модели составила 90,14%, специфичность - 93,55%. Высокая чувствительность и специфичность прогностической модели достигнуты благодаря включению патогенетически значимых показателей иммунного статуса, содержания цитокинов на местном уровне - в БАЖ.
Способ прогнозирования используется в период обострения ХОБЛ среднетяжелого течения. При этом до назначения лечения в стационаре пациенту проводят:
- спирометрию, определяют постбронхолитическую величину ОФВ1 в процентах от должностного значения,
- общий анализ крови: фиксируют относительное содержание сегментоядерных нейтрофилов,
- определение показателя фибринолитической активности крови традиционным эуглобулиновым методом в минутах,
- диагностическую бронхоскопию, после проведения которой производят забор бронхоальвеолярной жидкости (БАЖ) из участка легкого с помощью вакуумного контура путем продвижения бронхоскопа до «заклинивания» в сегментарный или субсегментарный бронх [10];
- иммунологические исследования:
1) иммунофенотипирование лимфоцитов с использованием моноклональных антител (МКАТ) CD3 и CD4 в % в реакции прямой иммунофлюоресценции,
2) определение уровней цитокинов IFNγ и IL-4 в пг/мл в бронхоальвеолярной жидкости методом иммуноферментного анализа с последующим расчетом соотношения IFNγ/IL-4;
- полученные данные вносят в формулу (модель):
Z=-53,0571-0,3799×ХОФВ1+0,6004×X IFNγ/IL-4(БАЖ)+0,06417×ХФАК+0,7468×XCD3CD4%+0,5951×Хс/я нейтр. %,
где -53,0571 константа, соответствующая теоретическому значению Z при нулевых значениях всех предикторов смертельного исхода ХОБЛ; -0,3799; 0,6004; 0,06417; 0,7468; 0,5951 - коэффициенты предикторов; ХОФВ1 - значение ОФВ1 в % от должного значения, XIFNg/IL-4 (БАЖ). - значение соотношения IFNγ/IL-4 в бронхоальвеолярной жидкости, ХФАК - значение фибринолитической активности крови в минутах, XCD3CD4_ - число CD3+CD4+-клеток в % в периферической крови, Хс/я нейтр. % - число сегментоядерных нейтрофилов в периферической крови в %,
затем полученное значение Z вносят в формулу для вычисления показателя Р:
Р=1/(1+e-Z)×100%, где Р - вероятность смертельного исхода, е - основание натурального логарифма, равно 2,718.
Значение Р больше 44,8%, дает основание прогнозировать неблагоприятный (смертельный) исход ХОБЛ у пациента в течение ближайших 15 лет жизни.
Для иллюстрации возможности использования предложенной модели приводим примеры:
Пример 1. Больной А., история болезни №476/171, дата рождения 25.06.1948 г. Госпитализирован с жалобами на кашель с отделением слизисто-гнойной мокроты, одышку при физической нагрузке, повышение температуры тела до 37,7°С, связанными с обострением ХОБЛ, в пульмонологическое отделение Республиканской клинической больницы Минздрава Чувашии 16.02.2005. Не курит. Клинический диагноз: ХОБЛ, бронхитический тип, клиническая группа В, среднетяжелое течение (GOLD 2), обострение. Постбронходилатационное значение ОФВ1 - 77%, Содержание цитокинов в БАЖ: IFNγ - 290 пг/мл, IL-4 - 17 пг/мл, IFNγ/IL-4 - 17. В крови: ФАК - 240 мин, CD3+CD4+-клетки - 25%, сегментоядерные нейтрофилы - 33%. Значения подставляем в предложенную модель:
Z=-53,0571-0,3799×77-0,6004×17=0,06417×240+0,7468×25+0,5951×33=-18,3935 и
Р=1/(1+2,718-(-18,3935))×100%=0,00000102755%.
Значение Р, равное 0,00000102755%, исключает вероятность отсроченного смертельного исхода в течение 15 лет. Действительно, при обследовании в 2020 году больной оказался жив.
Пример 2. Больной С., история болезни №2407/258, дата рождения 18.02.1937 г. Госпитализирован с обострением ХОБЛ в пульмонологическое отделение Республиканской клинической больницы Минздрава Чувашии 09.03.2005. Продолжительность периода табакокурения - 16 лет, индекс курения - 12. Клинический диагноз: ХОБЛ, смешанный тип, клиническая группа В, среднетяжелое течение (GOLD 2), обострение. Постбронходилатационное значение ОФВ1 - 72%. Содержание цитокинов в БАЖ: IFNγ - 305,6 пг/мл, IL-4 - 21,83 пг/мл, IFNγ - 14. В крови: ФАК - 80 мин, CD3+CD4+-клетки - 43%, сегментоядерные нейтрофилы - 51%.
Z=-53,0571-0,3799×72-0,6004×14+0,06417×80+0,7468×43+0,5951×51=-4,4082
Р=1-(1-2,718-(-4,4082))×100%=1,2033%.
Значение Р намного ниже порогового значения, равного 44,8%, что с большой вероятностью исключает возможность развития неблагоприятного исхода в течение 15 лет, что и подтвердилось в 2020 г., когда пациент был обнаружен в группе выживших.
Пример 3. Больной Э., история болезни №826/288, дата рождения 13.01.1939 г. Госпитализирован по поводу обострения ХОБЛ в пульмонологическое отделение Республиканской клинической больницы Минздрава Чувашии 23.03.2005. При поступлении в стационар жаловался на усиление выделения слизисто-гнойной мокроты, одышку при ходьбе, повышение температуры тела 38,1°С. Табакокурение - в течение 16 лет, индекс курения - 13,6. Клинический диагноз: ХОБЛ, бронхитический тип, клиническая группа В, среднетяжелое течение (GOLD 2), обострение. Постбронходилатационное значение ОФВ1 - 49%. Содержание цитокинов в БАЖ: IFNγ - 583 пг/мл, IL-4 - 10 пг/мл, IFNγ/IL-4 - 58,3. В крови: ФАК - 300 мин, CD3+CD4-клетки - 10%, сегментоядерные нейтрофилы - 55%.
Z=-53,0571-0,3799×49-0,6004×58,3-0,06417×300+0,7468×10+0,5951×55=22,78062
Р=1/(1+2,718-22,78062)×100%=99,99%.
Рассчитанное значение Р превышает порог 44,8%, что свидетельствует о высоком риске неблагоприятного исхода в течение 15 лет. Действительно, пациент значился в 2020 г. в группе умерших пациентов. В данном случае у больного выявлен дефицит массы массы, высокий уровень продукции провоспалительного цитокина IFNγ в БАЖ, что свидетельствует об активации иммунного ответа по преобладанию клеточного типа адаптивного иммунитета, подавление которой могло бы замедлить прогрессирование ХОБЛ и продлить жизнь пациента. В роли препаратов, подавляющих активность иммунного ответа, правомочно использование системных глюкокортикостероидов в период обострения на стационарном этапе. Больному следует рекомендовать на амбулаторный этап для снижения риска обострения ХОБЛ вакцинацию против пневмококковой инфекции и гриппа.
Включение в прогностическую модель иммунологических показателей позволило добиться высокой чувствительности и специфичности прогностического показателя. Установление связи неблагоприятного исхода ХОБЛ с иммунопатогенетическими показателями является основой для рекомендации добавления в стандартную схему бронхолитической, противомикробной и противовоспалительной терапии, а также средств иммунотерапии и иммунопрофилактики (системные глюкокортикостероиды в период обострения ХОБЛ и вакцины, бактериолизаты в период ремиссии).
Источники информации, принятые во внимание при составлении описания и формулы изобретения:
1. Гирсдорф Свен (De), Тамм Михаэль (Ch), Штольц Дайана (Ch) Прогнозирование исходов у пациентов с хронической обструктивной болезнью легких: Патент на изобретение RU 2688168. Опубл. 27.04.2016. Бюл. №12.
2. Козловский В.И., Ковтун О.М., Дусова Т.Н. и др. Возможности прогнозирования неблагоприятных исходов у пациентов с артериальной гипертензией в сочетании с хронической обструктивной болезнью легких. Журнал Гродненского государственного медицинского университета. 2015; №4: 80-84.
3. Кокосов А.Н. Хронический бронхит и обструктивная болезнь легких: аналитический очерк. Тер. арх. 2000; №3: 75-77.
4. Петри А., Сэбин К. Наглядная медицинская статистика: учеб. пособие / пер. с анг. под ред. В.П. Леонова. 3-е изд., перераб. и доп. М.: ГЭОТАР-Медиа. 2015. 216 с.
5. Смирнова Л.Е., Смирнова Е.Н., Яковлева М.В., Алексеев Д.В. Способ оценки развития неблагоприятного течения хронической обструктивной болезни легких и артериальной гипертензии при их сочетании: Патент на изобретение RU 2711453. Опубл. 17.01.2020. Бюл. №2.
6. Файнзильберг Л.С. Гарантированная оценка эффективности диагностических тестов на основе усиленного ROC-анализа // Управляющие системы и машины. 2009. №5. С. 3-13.
7. Ashitani J., Mukae Н., Arimura Y., Matsukura S.. Elevated plasma procoagulant and fibrinolytic markers in patients with chronic obstructive pulmonary disease. Intern Med. 2002; 41(3): 181-5. doi: 10.2169/internalmedicine.41.181
8. Born G.V.R. Aggregation of blood platelet by adenosine diphosphate and its reversal. Nature. 1962; 194: 927-929.
9. Celli B.R., Cote C.G., Marin J.M. et al. The body-mass index, airflow obstruction, dyspnea, and exercise capacity index in chronic obstructive pulmonary disease. N Engl J Med. 2004; 350: 1005-12. doi: 10.1056/NEJMoa021322.
10. Clinical guidelines and indications for bronchoalveolar lavage (BAL): Report of the European Society of Pneumology Task Group on BAL. Eur Respir J. 1990; 3(8): 937-76.
11. Hattab Y., Alhassan S., Balaan M. et al. Chronic Obstructive Pulmonary Disease. Crit. CareNurs. Q. 2016; 39: 124-130. doi: 10.1097/CNQ. 0000000000000105.
12. Li M., Han G., Chen Y. et al. Efficacy of Oseltamivir Compared with Zanamivir in COPD Patients with Seasonal Influenza Virus Infection: a Randomized Controlled Trial. Braz. J. Med. Biol. Res. 2020; 54 (2), e9542. doi: 10.1590/1414-431X20209542.
13. MacLeod M., Papi A., Contoli M. et al. Chronic Obstructive Pulmonary Disease Exacerbation Fundamentals: Diagnosis, Treatment, Prevention and Disease Impact. Respirology. 2021; 26: 532-551. doi: 10.1111/resp.14041.
14. Miossec P., Kolls J.K. Targeting IL-17 and TH17 Cells in Chronic Inflammation. Nat. Rev. DrugDiscov. 2012; 11 (10): 763-776. doi: 10.1038/nrd3794.
15. Ni L., Dong C. Roles of Myeloid and Lymphoid Cells in the Pathogenesis of Chronic Obstructive Pulmonary Disease. Front. Immunol. 2018; 9: 1431. doi: 10.3389/fimmu.2018.01431.
16. Ponce-Gallegos M., Ramirez-Venegas A., Falfan-Valencia R. Th17 Profile in COPD Exacerbations. Int. J. Chron. Obstruct. Pulmon. Dis. 2017; 12: 1857-1865. doi: 10.2147/COPD.S 136592.
17. Puhan M.A., Garcia-Aymerich J., Frey M. et al. Expansion of the prognostic assessment of patients with chronic obstructive pulmonary disease: the updated BODE index and the ADO index. Lancet. 2009; 374: 704-11. doi: 10.1016/S0140-6736(09)61301-5.
18. Rabe K.F., Watz H. Chronic Obstructive Pulmonary Disease. The Lancet. 2017; 389(10082): 1931-1940. doi: 10.1016/S0140-6736(17)31222-9.
19. Vogelmeier C.F., Criner G.J., Martinez F.J. et al. Global Strategy for the Diagnosis, Management and Prevention of Chronic Obstructive Lung Disease 2017 Report: GOLD Executive Summary. Respirology. 2017; 22(3): 575-601. doi: 10.1111/resp.13012.].
20. Wang C., Zhou J., Wang J. et al. Progress in the Mechanism and Targeted Drug Therapy for COPD. Sig. Transduct. Target Ther. 2020; 5 (1): 248. doi: 10.1038/s41392-020-00345-x.
21. Whittaker Brown S.-A., Braman S. Recent Advances in the Management of Acute Exacerbations of Chronic Obstructive Pulmonary Disease. Med. Clin. North America. 2020; 104(4): 615-630. doi: 10.1016/j.mcna.2020.02.003.
22. Xiao C., Cheng S., Li R. et al. Isoforskolin Alleviates AECOPD by Improving Pulmonary Function and Attenuating Inflammation Which Involves Downregulation of Th17/IL-17A and NF-κB/NLRP3. Front Pharmacol. 2021; 12: 721273. doi: 10.3389/fphar.2021.721273.
23. Zhang Z., Cheng X., Yue L. et al. Molecular Pathogenesis in Chronic Obstructive Pulmonary Disease and Therapeutic Potential by Targeting AMP-Activated Protein Kinase. J. Cell. Physiol. 2018; 233 (3): 1999-2006. doi: 10.1002/jcp.25844.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИНФЕКЦИОННОГО ОСЛОЖНЕНИЯ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ | 2015 |
|
RU2595853C1 |
| Способ оценки развития неблагоприятного течения хронической обструктивной болезни легких и артериальной гипертензии при их сочетании | 2018 |
|
RU2711453C1 |
| Способ прогнозирования обострений хронической обструктивной болезни легких у лиц, работающих в условиях воздействия промышленных аэрозолей | 2021 |
|
RU2774206C1 |
| СПОСОБ ОЦЕНКИ РИСКА ПРОГРЕССИРОВАНИЯ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЁГКИХ | 2022 |
|
RU2805829C1 |
| Способ прогнозирования на ранних стадиях хронической обструктивной болезни легких риска прогрессирования заболевания | 2020 |
|
RU2740071C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ГЛЮКОКОРТИКОИДНОЙ ТЕРАПИИ У БОЛЬНЫХ С ОБОСТРЕНИЕМ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ | 2011 |
|
RU2490645C2 |
| CПОСОБ ПРОГНОЗА ПРОГРЕССИРОВАНИЯ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ | 2008 |
|
RU2370773C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОБОСТРЕНИЙ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ У ПАЦИЕНТОВ С НАРУШЕНИЕМ СНА | 2018 |
|
RU2681272C1 |
| Способ отбора больных хронической обструктивной болезнью легких фенотипа "с редкими обострениями" для лечения рофлумиластом | 2019 |
|
RU2726228C1 |
| СПОСОБ ПРОГНОЗА ПРОГРЕССИРОВАНИЯ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ (ХОБЛ) | 2015 |
|
RU2599349C1 |
Изобретение относится к медицине, а именно к пульмонологии, и может быть использовано для оценки развития неблагоприятного течения хронической обструктивной болезни легких (ХОБЛ). У больного со среднетяжелым течением болезни проводят анализ патогенетически значимых при ХОБЛ лабораторных показателей, при котором в первые сутки после госпитализации в стационар по поводу обострения ХОБЛ среднетяжелого течения проводят определение постбронхолитического объема форсированного выдоха за первую секунду (ОФВ1), фибринолитической активности крови эуглобулиновым методом, иммунологические исследования путем определения в бронхоальвеолярной жидкости цитокинов - интерферона-гамма (IFNγ), интерлейкина-4 (IL-4) методом иммуноферментного анализа, относительного содержания CD3+CD4+-клеток методом прямой иммунофлюоресценции и сегментоядерных нейтрофилов в периферической крови, при этом значения данных показателей вносят в уравнение для определения показателя Z. Затем полученное значение Z вносят в формулу для вычисления показателя вероятности смертельного исхода P=1/(1+e-Z)×100%, где e - основание натурального логарифма, равное 2,718. При получении значения Р больше 44,8 % прогнозируют летальный исход ХОБЛ в течение 15 лет, а при значении показателя, равном или меньше 44,8%, прогнозируют благоприятный исход. Изобретение обеспечивает повышение чувствительности и специфичности прогноза выживаемости на ранних стадиях ХОБЛ, преимущественно у больных со среднетяжелой степенью бронхообструкции (GOLD2) без сопутствующих заболеваний сердечно-сосудистой системы и неврологических расстройств. 3 ил., 8 табл., 3 пр.
Способ прогнозирования исхода хронической обструктивной болезни легких (ХОБЛ) у больного со среднетяжелым течением болезни, включающий анализ патогенетически значимых при ХОБЛ лабораторных показателей, при котором в анализ включают определение степени бронхиальной обструкции по величине ОФВ1, причем в первые сутки после госпитализации в стационар по поводу обострения ХОБЛ среднетяжелого течения проводят определение постбронхолитического объема форсированного выдоха за первую секунду (ОФВ1), фибринолитической активности крови эуглобулиновым методом, иммунологические исследования путем определения в бронхоальвеолярной жидкости цитокинов - интерферона-гамма (IFNγ), интерлейкина-4 (IL-4) методом иммуноферментного анализа, относительного содержания CD3+CD4+-клеток методом прямой иммунофлюоресценции и сегментоядерных нейтрофилов в периферической крови, при этом значения данных показателей вносят в уравнение:
Z=-53,0571-0,3799×ХОФВ1+0,6004×XIFNg/IL-4 БАЖ +0,06417×ХФАК+0,7468×XCD3CD4%+0,5951×Хс/я нейтр. %,
где
(-53,0571) - константа, соответствующая теоретическому значению Z при нулевых значениях всех предикторов смертельного исхода ХОБЛ;
(-0,3799; 0,6004; 0,06417; 0,7468; 0,5951) - коэффициенты предикторов;
ХОФВ1 _ значение постбронхолитического ОФВ1 от должного значения, %;
XIFNg/IL-4 БАЖ - значение соотношения IFNγ/IL-4 в бронхоальвеолярной жидкости;
ХФАК - значение фибринолитической активности крови, мин;
XCD3CD4 - число CD3+CD4+ - клеток в крови, %
Хс/я нейтр. % - число сегментоядерных нейтрофилов в периферической крови, %,
затем полученное значение Z вносят в формулу для вычисления показателя вероятности смертельного исхода Р:
Р=1/(1+e-Z)×100% (е - основание натурального логарифма, равное 2,718),
причем при получении значения Р больше 44,8% прогнозируют летальный исход ХОБЛ в течение 15 лет, при значении показателя, равном или меньше 44,8%, прогнозируют благоприятный исход.
| Способ прогнозирования выживаемости при хронической обструктивной болезни легких | 2021 |
|
RU2756025C1 |
| ПРОГНОЗИРОВАНИЕ ИСХОДОВ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНЬЮ ЛЕГКИХ | 2013 |
|
RU2688168C2 |
| СПОСОБ ОЦЕНКИ ДВУХЛЕТНЕЙ ВЫЖИВАЕМОСТИ БОЛЬНЫХ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНЬЮ ЛЕГКИХ, ОСЛОЖНЕННОЙ ДЕКОМПЕНСИРОВАННЫМ ХРОНИЧЕСКИМ ЛЕГОЧНЫМ СЕРДЦЕМ | 2006 |
|
RU2315552C1 |
| CПОСОБ ПРОГНОЗА ПРОГРЕССИРОВАНИЯ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ | 2008 |
|
RU2370773C1 |
| WO 2000073803 A1, 07.12.2000 | |||
| А.К | |||
| СО и др | |||
| Предикторы неблагоприятного исхода при обострении хронической обструктивной болезни легких | |||
| Пульмонология, 2018, 28(4): 446-452 | |||
| АЛЕКСЕЕВА Е.П | |||
| и др | |||
| ХОБЛ: предикторы неблагоприятного течения | |||
Авторы
Даты
2023-05-02—Публикация
2021-11-26—Подача