ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[010] Настоящее изобретение в целом относится к низкомолекулярным ингибиторам мембранного белка микобактерий Large 3 (MmpL3) и к их применению в качестве терапевтических средств, например, при лечении заболеваний, таких как инфекции.
[020] УРОВЕНЬ ТЕХНИКИ
[030] микобактерии принадлежат к актиномицетам, содержащим миколовые кислоты, и основным признаком является то, что клеточная стенка содержит большое количество липидов, в основном миколовую кислоту. Это тесно связано с их способностью к окрашиванию, характеристиками роста, патогенностью и резистентностью. Как правило, они окрашиваются с трудом. Их также называют кислотоустойчивыми бациллами, если они остаются окрашенными или разрушаются при обесцвечивании с помощью мощного обесцвечивающего средства, представляющего собой хлористоводородную кислоту. Указанный род микроорганизмов лишен жгутиков, не имеет спор, не производит эндотоксин и экзотоксин, и его патогенность связана с бактериальными компонентами. Существует множество типов, которые можно поделить на комплекс Mycobacterium tuberculosis, нетуберкулезные микобактерии и Mycobacterium leprae.
[040] Mycobacterium tuberculosis (Mtb) представляет собой патогенную бактерию, которая вызывает туберкулез (TB) и относится к типу микобактерий. Она передается в основном через дыхательные пути и может обуславливать такие симптомы как кашель, боль в груди, кровохарканье и затрудненное дыхание. Здоровые люди, инфицированные туберкулезом, не заболевают обязательно, за исключением случаев, когда ухудшается иммунитет организма. Туберкулез занимает девятое место среди главных причин смертности в мире и является главной причиной смертности от инфекции, вызванной отдельным патогеном, выше, чем ВИЧ/СПИД. Согласно оценкам, в 2016 году 1,3 миллиона человек умерли от туберкулеза среди ВИЧ-отрицательных людей (меньше по сравнению с 1,7 миллиона в 2000 году). Что касается ВИЧ-положительных людей, от туберкулеза умерли 374000 человек. Согласно оценкам, в 2016 году в мире зарегистрировано 10,4 миллиона новых случаев туберкулеза, в том числе 90% взрослых, 65% мужчин, 10% людей, живущих с ВИЧ (74% в Африке), и на Индию, Индонезию, Китай, Филиппины и Пакистан приходится 56% новых случаев туберкулеза.
[050] Mycobacterium tuberculosis (Mtb) была открыта в 1882 году немецким микробиологом Робертом Кохом. Под микроскопом Mtb выглядит как тонкая или прямая бацилла. Mycobacterium tuberculosis представляет собой облигатную аэробную бактерию, которая растет очень медленно. На твердой среде период роста Mtb составляет 18-20 часов, и период культивирования занимает от 8 дней до 8 недель. Колония является шероховатой на большинстве типов среды. Mtb имеет воскообразную клеточную стенку, чрезвычайно устойчивую к сухим условиям и действию сильных кислот и оснований, и через нее не проникает множество химических дезинфицирующих веществ. Комплекс Mycobacterium tuberculosis включает человеческий тип, бычий тип, мышиный тип и африканский тип, из которых человеческий, бычий и африканский типы являются патогенными.
[060] Mycobacterium bovis является короткой и утолщенной, и Mycobacterium avium является плеоморфной. Ветвление наблюдается у клеток на застаревшей среде. В отличие от большинства грамположительных бактерий, клеточная стенка данной бактерии представляет собой не только пептидогликан, но также и особый гликолипид. Вследствие эффекта гликолипидов окраска по Граму является затрудненной, в то время как окраска для кислотоустойчивых бактерий приводит к окрашиванию в красный цвет. Бацилла Кальметта-Герена (BCG) выделена из аттенуированной Mycobacterium bovis, обладает теми же характеристиками, что и Mycobacterium bovis, является менее патогенной и легко растет на глицеринсодержащей среде.
[070] Mycobacterium smegmatis представляет собой кислотоустойчивый штамм микобактерий, длина которых составляет от 3 до 5 мкм, и которые имеют форму палочки и могут быть окрашены флуоресцентным способом с применением аурамина-O-родамина. Поскольку он является «быстро растущим» и непатогенным, он применялся исследователями в качестве простой модели для исследования других типов микобактерий. Данная бактерия имеет более 2000 генов, гомологичных по отношению к Mtb, и имеет такую же уникальную структуру клеточной стенки, как у Mtb и других видов микобактерий. Следовательно, исследователи часто применяют ее при фенотипическом скрининге лекарственных средств для лечения туберкулеза.
[080] Mycobacterium marinum представляет собой разновидность бактерий, существующих в морской и пресной воде, которые относятся к микобактериям и относятся к тому же роду, что и Mycobacterium tuberculosis. Она представляет собой несимбиотическую бактерию, которая может обуславливать развитие оппортунистических инфекций после проникновения в человеческий организм. Бациллы средней длины или длинные, часто рассеянные, обычно инокулируют на плотной яичной среде с разбавлением при 30°C в течение 7 дней или более, и колонии имеют вид от гладких до шероховатых. Колонии, выращиваемые в темноте, не имеют пигмента; являются светлыми при воздействии света или при краткосрочном воздействии света, и молодые колонии имеют ярко-желтый цвет. Mycobacterium marinum является наиболее активной при 28-32°C, и ей более сложно выжить при температуре выше 37°C. Следовательно, при проникновении в организм человека она распространяется только в фасции тела человека и не проникает во внутренние органы, имеющие более высокую температуру.
[090] Mycobacterium leprae, общеизвестная как возбудитель лепры, может вызывать лепру, которая представляет собой хроническое инфекционное заболевание. морфологическое строение и способ окраски Mycobacterium leprae были схожими с таковыми для Mycobacterium tuberculosis: тонкие, слегка изогнутые, часто в виде пучков. И окраска по Граму, и окраска с применением способа для кислотоустойчивых бактерий имели положительный результат.после лечения они могут иметь короткую палочковидную форму, обладать полиморфизмом в виде гранул или розеток, что может быть характерно для вариантов L-типа. Неполное излечение может приводить к рецидиву. Окраска Mycobacterium leprae с применением способа для кислотоустойчивых бактерий приводила к окрашиванию в красный цвет, и окраска по Граму имела положительный результат. Репродуктивная способность сохраняется в течение 7 дней в сухих условиях. При длительном существовании в условиях низкой температуры они могут выживать в течение нескольких месяцев при температуре от -60°C до -13°C и выживают в течение 3 недель при 0°C.
[100] Закодированный в геноме Mycobacterium MmpL3 представляет собой интегральный мембранный белок, имеющий 12 трансмембранных спиралей, функция которого состоит в экспортировании миколовой кислоты в форме мономиколята трегалозы (TMM), необходимого для интерстициальной или внешней мембраны. мембранный белок микобактерий Large 3 (MmpL3) является необходимым для обеспечения выживания и патогенности микобактерий in vivo, таким образом, мембранный белок MmpL3 представляет собой ключевую мишень для лекарственного средства, направленного на Mycobacterium tuberculosis и другие микобактерии. Сообщалось, что SQ109 нацеливается на мембранный белок MmpL3 из Mycobacterium tuberculosis, и лекарственное средство вступило в фазу II клинических испытаний. Кроме того, соединение римонабант, известное как ингибитор каннабиноидного рецептора (CB1), представляет собой новый тип таблеток для похудения. Имеются сообщения о том, что римонабант обладает значительным эффектом в отношении Mycobacterium tuberculosis (H37Rv), и биологические исследования демонстрировали нацеливание римонабанта на MmpL3.
[110] ОПИСАНИЕ
[120] В данном документе предусмотрены соединения или их фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, которые являются пригодными при лечении и/или предупреждении бактериальной инфекции, такой как микобактериальная инфекция.
[130] В определенных вариантах осуществления предусмотрены соединения, которые подавляют активность MmpL3.
[140] В определенных вариантах осуществления предусмотрены соединения формулы I:
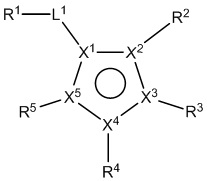 I,
I,
или их фармацевтически приемлемая соль, сольват, таутомер, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров,
где
кольцо A представляет собой 5-членный гетероарил, где X1 представляет собой C или N, X2, X3, X4 и X5 независимо выбраны из C, N, O и S, при условии, что не более чем один из X2, X3, X4 и X5 представляет собой O или S, и по меньшей мере один из X1, X2, X3, X4 и X5 представляет собой C;
L1 представляет собой *-N(R1b)CO-, *-CON(R1b)-, *-OCO-, *-COO-, *-N(R1b)SO2-, *-SO2N(R1b)-, *-N(R1c)CON(R1b)-, *-CO-L1a-CO-, *-L1a-CO- или алкилен, где необязательно одна или более из групп CH2 алкилена замещены группой, независимо выбранной из группы, состоящей из CO, NR1b, NR1c, O, S, SO, SO2 и 5- или 7-членного гетероциклилена;
* обозначает точку соединения с R1;
L1a представляет собой 5-, 6- или 7-членный гетероциклилен;
каждый R1b независимо представляет собой H или C1-3алкил;
каждый R1c независимо представляет собой H или C1-3алкил;
каждый из m и n независимо равняется 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10;
R1 представляет собой C7-15циклоалкил, необязательно замещенный R1a в количестве от одного до десяти;
каждый R1a независимо выбран из галогена, -CN, -NO2, C1-3алкила, C1-3галогеналкила, -OR6, -SR6, -N(R6)2, -C(O)R6, -C(O)OR6, -S(O)R6, -S(O)2R6, -C(O)N(R6)2, -NR6C(O)R6, -NR6C(O)OR6, -NR6C(O)N(R6)2, -NHS(O)R6, -S(O)(NH)R6, циклоалкила, арила, гетероциклила, гетероарила или их комбинации;
если X2 представляет собой C, то R2 представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R2a в количестве от одного до пяти, алкенил, необязательно замещенный R2a в количестве от одного до пяти, алкинил, необязательно замещенный R2a в количестве от одного до пяти, циклоалкил, необязательно замещенный R2a в количестве от одного до пяти, арил, необязательно замещенный R2a в количестве от одного до пяти, гетероциклил, необязательно замещенный R2a в количестве от одного до пяти, или гетероарил, необязательно замещенный R2a в количестве от одного до пяти,
если X2 представляет собой N, то R2 отсутствует или представляет собой H, прямой или разветвленный алкил, необязательно замещенный R2a в количестве от одного до пяти, алкенил, необязательно замещенный R2a в количестве от одного до пяти, алкинил, необязательно замещенный R2a в количестве от одного до пяти, циклоалкил, необязательно замещенный R2a в количестве от одного до пяти, арил, необязательно замещенный R2a в количестве от одного до пяти, гетероциклил, необязательно замещенный R2a в количестве от одного до пяти, или гетероарил, необязательно замещенный R2a в количестве от одного до пяти,
если X2 представляет собой O или S, то R2 отсутствует;
если X3 представляет собой C, то R3 представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R3a в количестве от одного до пяти, алкенил, необязательно замещенный R3a в количестве от одного до пяти, алкинил, необязательно замещенный R3a в количестве от одного до пяти, циклоалкил, необязательно замещенный R3a в количестве от одного до пяти, арил, необязательно замещенный R3a в количестве от одного до пяти, гетероциклил, необязательно замещенный R3a в количестве от одного до пяти, или гетероарил, необязательно замещенный R3a в количестве от одного до пяти,
если X3 представляет собой N, то R3 отсутствует или представляет собой H, прямой или разветвленный алкил, необязательно замещенный R3a в количестве от одного до пяти, алкенил, необязательно замещенный R3a в количестве от одного до пяти, алкинил, необязательно замещенный R3a в количестве от одного до пяти, циклоалкил, необязательно замещенный R3a в количестве от одного до пяти, арил, необязательно замещенный R3a в количестве от одного до пяти, гетероциклил, необязательно замещенный R3a в количестве от одного до пяти, или гетероарил, необязательно замещенный R3a в количестве от одного до пяти,
если X3 представляет собой O или S, то R3 отсутствует;
если X4 представляет собой C, то R4 представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R4a в количестве от одного до пяти, алкенил, необязательно замещенный R4a в количестве от одного до пяти, алкинил, необязательно замещенный R4a в количестве от одного до пяти, циклоалкил, необязательно замещенный R4a в количестве от одного до пяти, арил, необязательно замещенный R4a в количестве от одного до пяти, гетероциклил, необязательно замещенный R4a в количестве от одного до пяти, или гетероарил, необязательно замещенный R4a в количестве от одного до пяти,
если X4 представляет собой N, то R4 отсутствует или представляет собой H, прямой или разветвленный алкил, необязательно замещенный R4a в количестве от одного до пяти, алкенил, необязательно замещенный R4a в количестве от одного до пяти, алкинил, необязательно замещенный R4a в количестве от одного до пяти, циклоалкил, необязательно замещенный R4a в количестве от одного до пяти, арил, необязательно замещенный R4a в количестве от одного до пяти, гетероциклил, необязательно замещенный R4a в количестве от одного до пяти, или гетероарил, необязательно замещенный R4a в количестве от одного до пяти,
если X4 представляет собой O или S, то R4 отсутствует;
если X5 представляет собой C, то R5 представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R5a в количестве от одного до пяти, алкенил, необязательно замещенный R4a в количестве от одного до пяти, алкинил, необязательно замещенный R4a в количестве от одного до пяти, циклоалкил, необязательно замещенный R5a в количестве от одного до пяти, арил, необязательно замещенный R5a в количестве от одного до пяти, гетероциклил, необязательно замещенный R5a в количестве от одного до пяти, или гетероарил, необязательно замещенный R5a в количестве от одного до пяти,
если X5 представляет собой N, то R5 отсутствует или представляет собой H, прямой или разветвленный алкил, необязательно замещенный R5a в количестве от одного до пяти, алкенил, необязательно замещенный R5a в количестве от одного до пяти, алкинил, необязательно замещенный R5a в количестве от одного до пяти, циклоалкил, необязательно замещенный R5a в количестве от одного до пяти, арил, необязательно замещенный R5a в количестве от одного до пяти, гетероциклил, необязательно замещенный R5a в количестве от одного до пяти, или гетероарил, необязательно замещенный R5a в количестве от одного до пяти,
если X5 представляет собой O или S, то R5 отсутствует;
каждый из R2a, R3a, R4a или R5a независимо выбран из галогена, C1-3алкила, C1-3галогеналкила, -CN, -NO2, -OR6, -SR6, -N(R6)2, -C(O)R6, -C(O)OR6, -S(O)R6, -S(O)2R6, -C(O)N(R6)2, -NR6C(O)R6, -NR6C(O)OR6, -NR6C(O)N(R6)2, -NHS(O)R6, -S(O)(NH)R6, циклоалкила, арила, гетероциклила, гетероарила или их комбинации; и
каждый R6 независимо представляет собой водород, C1-3алкил, C1-3галогеналкил, C3-6циклоалкил, арил, гетероарил или гетероциклил.
[150] В определенных вариантах осуществления предусмотрена фармацевтическая композиция, содержащая соединение, описанное в данном документе, или его фармацевтически приемлемую соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, и фармацевтически приемлемый носитель.
[160] В определенных вариантах осуществления предусмотрен способ лечения или предупреждения микобактериальной инфекции у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту эффективного количества фармацевтической композиции, содержащей соединение, описанное в данном документе, или его фармацевтически приемлемую соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров.
[170] В настоящем изобретении также предусмотрены соединения и композиции, в том числе фармацевтические композиции, наборы, которые содержат соединения, и способы применения (или введения) и получения соединений. В настоящем изобретении дополнительно предусмотрены соединения и композиции на их основе для применения в способе лечения заболевания, нарушения или состояния, опосредованного, по меньшей мере частично, активностью MmpL3. Более того, в настоящем изобретении предусмотрены пути применения соединений или композиций на их основе при изготовлении лекарственного препарата для лечения бактериальной инфекции.
[180] ПОДРОБНОЕ ОПИСАНИЕ
[190] В следующем описании изложены иллюстративные варианты осуществления настоящего изобретения. Следует понимать, однако, что такое описание не предназначено в качестве ограничения объема настоящего изобретения, а, напротив, представлено в качестве описания иллюстративных вариантов осуществления.
[200] 1. Определения
[210] Предполагается, что используемые в данном описании следующие слова, выражения и символы, как правило, имеют значения, изложенные ниже, за исключением случаев, где в контексте, в котором они используются, указано иное.
[220] Тире («-»), которое находится не между двумя буквами или символами, используется для обозначения точки присоединения заместителя. Например, -C(O)NH2 присоединен посредством атома углерода. Тире в начале или в конце химической группы используется для удобства; химические группы могут быть изображены с использованием одного или более тире или без них без потери их обычного значения. Волнистая линия или пунктирная линия, проведенная через линию в структуре, обозначает указанную точку присоединения группы. За исключением случаев, где это требуется с химической или структурной точки зрения, направленность или стереохимия не указывается или подразумевается в соответствии с порядком, в котором химическая группа написана или названа.
[230] Приставка «Cu-v» указывает на то, что следующая группа содержит от u до v атомов углерода. Например, «C1-6алкил» указывает на то, что алкильная группа содержит от 1 до 6 атомов углерода.
[240] Упоминание термина «приблизительно» в отношении значения или параметра в данном документе включает (и описывает) варианты осуществления, которые направлены на данное значение или параметр как таковые. В определенных вариантах осуществления термин «приблизительно» включает указанное количество ±10%. В других вариантах осуществления термин «приблизительно» включает указанное количество ±5%. В определенных других вариантах осуществления термин «приблизительно» включает указанное количество ±1%. Кроме того, термин «приблизительно X» включает описание «X». Кроме того, формы единственного числа включают соответствующие формы множественного числа, если в контексте явно не указано иное. Таким образом, например, упоминание «соединения» в единственном числе включает множество таких соединений, и упоминание «способа» в единственном числе включает упоминание одного или более способов.
[250] Термин «кольцо A» означает кольцо, содержащее X1, X2, X3, X4 и X5, определенные в данном документе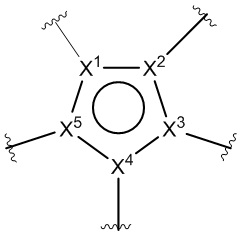 .
.
[260] Термин «алкил» означает неразветвленную или разветвленную насыщенную углеводородную цепь. В некоторых вариантах осуществления алкил содержит указанное число атомов углерода. В некоторых вариантах осуществления алкил содержит от 1 до 20 атомов углерода (т.е. C1-20алкил), от 1 до 12 атомов углерода (т.е. C1-12алкил), от 1 до 8 атомов углерода (т.е. C1-8алкил), от 1 до 6 атомов углерода (т.е. C1-6алкил) или от 1 до 4 атомов углерода (т.е. C1-4алкил). Примеры алкильных групп включают, например, метил, этил, пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, пентил, 2-пентил, изопентил, неопентил, гексил, 2-гексил, 3-гексил и 3-метилпентил. Если алкильный остаток, содержащий определенное число атомов углерода, указывается с помощью химического названия или определяется молекулярной формулой, то могут охватываться все позиционные изомеры, содержащие данное число атомов углерода; таким образом, например, термин «бутил» включает н-бутил (т.е. -(CH2)3CH3), втор-бутил (т.е. -CH(CH3)CH2CH3), изобутил (т.е. -CH2CH(CH3)2) и трет-бутил (т.е. -C(CH3)3); и термин «пропил» включает н-пропил (т.е. -(CH2)2CH3) и изопропил (т.е. -CH(CH3)2).
[270] могут использоваться определенные часто используемые альтернативные химические названия. Например, двухвалентная группа, такая как двухвалентная «алкильная» группа, двухвалентная «арильная группа» и т.д., может также называться «алкиленовой» группой, «ариленовой» группой соответственно. Кроме того, если явно не указано иное, в случаях, где комбинации групп упоминаются в данном документе как один фрагмент, например, арилалкил или аралкил, указанная в последнюю очередь группа содержит атом, посредством которого фрагмент присоединен к остальной части молекулы.
[280] Термин «алкенил» означает алкильную группу, содержащую по меньшей мере одну двойную связь углерод-углерод. В некоторых вариантах осуществления алкенил содержит указанное число атомов углерода. В некоторых вариантах осуществления алкенил содержит от 2 до 20 атомов углерода (т.е. C2-20алкенил), от 2 до 8 атомов углерода (т.е. C2-8алкенил), от 2 до 6 атомов углерода (т.е. C2-6алкенил) или от 2 до 4 атомов углерода (т.е. C2-4алкенил). Примеры алкенильных групп включают, например, этенил, пропенил, бутадиенил (в том числе 1,2-бутадиенил и 1,3-бутадиенил).
[290] Термин «алкинил» означает алкильную группу, содержащую по меньшей мере одну тройную связь углерод-углерод. В некоторых вариантах осуществления алкинил содержит указанное число атомов углерода. В некоторых вариантах осуществления алкинил содержит от 2 до 20 атомов углерода (т.е. C2-20алкинил), от 2 до 8 атомов углерода (т.е. C2-8алкинил), от 2 до 6 атомов углерода (т.е. C2-6алкинил) или от 2 до 4 атомов углерода (т.е. C2-4алкинил). Термин «алкинил» также включает указанные группы, содержащие одну тройную связь и одну двойную связь.
[300] Термин «алкокси» означает группу «алкил-O-». Примеры алкоксигрупп включают, например, метокси, этокси, н-пропокси, изопропокси, н-бутокси, трет-бутокси, втор-бутокси, н-пентокси, н-гексокси и 1,2-диметилбутокси.
[310] Термин «алкоксиалкил» означает группу «алкил-O-алкил».
[320] Термин «амино» означает группу -NRyRz, где Ry и Rz независимо представляют собой водород, алкил, алкенил, алкинил, циклоалкил, гетероциклил, арил, гетероалкил или гетероарил; каждый из которых может быть необязательно замещен, как определено в данном документе.
[330] Термин «арил» означает ароматическую карбоциклическую группу, содержащую одно кольцо (например, моноциклическую) или несколько колец (например, бициклическую или трициклическую), в том числе конденсированные системы. В некоторых вариантах осуществления арил содержит от 6 до 20 атомов углерода в кольце (т.е. C6-20арил), от 6 до 12 атомов углерода в кольце (т.е. C6-12арил) или от 6 до 10 атомов углерода в кольце (т.е. C6-10арил). Примеры арильных групп включают, например, фенил, нафтил, флуоренил и антрил. Арил, однако, не охватывает и не совпадает каким-либо образом с гетероарилом, определение которого представлено ниже. Если одна или более арильных групп конденсированы с гетероарилом, то полученная кольцевая система представляет собой гетероарил. Если одна или более арильных групп конденсированы с гетероциклилом, то полученная кольцевая система представляет собой гетероциклил.
[340] Термин «арилалкил» или «аралкил» означает группу «арил-алкил-».
[350] Термин «циклоалкил» означает насыщенную или частично ненасыщенную циклическую алкильную группу, содержащую одно кольцо или несколько колец, в том числе конденсированные, мостиковые и спирокольцевые системы. Термин «циклоалкил» включает циклоалкенильные группы (т.е. циклическую группу, содержащую по меньшей мере одну двойную связь) и карбоциклические конденсированные кольцевые системы, содержащие по меньшей мере один sp3-атом углерода (т.е. по меньшей мере одно неароматическое кольцо). В некоторых вариантах осуществления циклоалкил содержит от 3 до 20 атомов углерода в кольце (т.е. C3-20циклоалкил), от 3 до 12 атомов углерода в кольце (т.е. C3-12циклоалкил), от 3 до 10 атомов углерода в кольце (т.е. C3-10циклоалкил), от 3 до 8 атомов углерода в кольце (т.е. C3-8циклоалкил) или от 3 до 6 атомов углерода в кольце (т.е. C3-6циклоалкил). моноциклические группы включают, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Полициклический циклоалкил означает циклоалкил, содержащий по меньшей мере два кольца, который может представлять собой конденсированную, мостиковую или спирокольцевую систему. Полициклические группы включают, например, бицикло[2.2.1]гептанил, бицикло[2.2.2]октанил, адамантил, норборнил, декалинил, 7,7-диметил-бицикло[2.2.1]гептанил и т.п. Термин «спироциклоалкил» означает полициклическую циклоалкильную групу, где по меньшей мере два кольца связаны вместе посредством одного общего атома, например, спиро[2.5]октанил, спиро[4.5]деканил или спиро[5.5]ундеканил. Спироциклоалкил может содержать конденсированные кольца в кольцевой системе, но не мостиковые кольца. Термин «конденсированный циклоалкил» означает полициклическую циклоалкильную группу, где по меньшей мере два кольца связаны вместе посредством двух общих атомов, где два общих атома соединены посредством ковалентной связи. Конденсированный циклоалкил не содержит каких-либо спиро- или мостиковых колец в кольцевой системе. Термин «мостиковый циклоалкил» означает полициклический циклоалкил, который содержит мостик - алкиленовую (такую как C1-4алкиленовая) группу, которая соединяет два атома «в голове мостика». Неограничивающие примеры мостикового циклоалкила включают бицикло[2.2.1]гептанил, бицикло[2.2.2]октанил, адамантил, норборнил и 7,7-диметил-бицикло[2.2.1]гептанил. мостиковый циклоалкил может содержать конденсированные и/или спиро-кольца в кольцевой системе. Кроме того, предполагается, что термин «циклоалкил» охватывает любое неароматическое кольцо, которое может быть конденсировано с арильным кольцом вне зависимости от места присоединения к остальной части молекулы.
[360] Термин «циклоалкилалкил» означает группу «циклоалкил-алкил-».
[370] Термин «имино» означает группу -C(NRy)Rz, где каждый из Ry и Rz независимо представляет собой водород, алкил, алкенил, алкинил, циклоалкил, гетероциклил, арил, гетероалкил или гетероарил; каждый из которых может быть необязательно замещен, как определено в данном документе.
[380] Термин «галоген» или «галогено» означает атомы, занимающие группу VIIA периодической таблицы элементов, такие как фтор, хлор, бром или йод.
[390] Термин «галогеналкил» означает неразветвленную или разветвленную алкильную группу, определенную выше, где один или более (например, от 1 до 6, от 1 до 5 или от 1 до 3) атомов водорода замещены атомом галогена. Например, в случае, если остаток замещен более чем одним атомом галогена, это может обозначаться с помощью приставки, соответствующей числу присоединенных галогеновых фрагментов. Дигалогеналкил и тригалогеналкил означают алкил, замещенный двумя («ди») или тремя («три») галогеновыми группами, которые могут, но необязательно, представлять собой один и тот же галоген. Примеры галогеналкила включают, например, трифторметил, дифторметил, фторметил, трихлорметил, 2,2,2-трифторэтил, 1,2-дифторэтил, 3-бром-2-фторпропил, 1,2-дибромэтил и т.п.
[400] Термин «галогеналкокси» означает алкоксигруппу, определенную выше, где один или более (например, от 1 до 6, от 1 до 5 или от 1 до 3) атомов водорода замещены атомом галогена.
[410] Термин «гидроксиалкил» означает алкильную группу, определенную выше, где один или более (например, от 1 до 6, от 1 до 5 или от 1 до 3) атомов водорода замещены гидроксигруппой.
[420] Термин «гетероалкил» означает алкильную группу, в которой каждый из одного или более, но не всех атомов углерода (и любых связанных атомов водорода) независимо замещен одинаковой или отличающейся группой, содержащей гетероатом, при условии, что точка присоединения к остальной части молекулы обеспечивается посредством атома углерода. Термин «гетероалкил» включает неразветвленную или разветвленную насыщенную цепь, содержащую углерод и гетероатомы. В качестве примера, 1, 2 или 3 атома углерода могут быть независимо замещены одинаковыми или отличающимися группами, содержащими гетероатом. Группы, содержащие гетероатом, включают без ограничения -NRy-, -O-, -S-, -S(O)-, -S(O)2- и т.п., где Ry представляет собой водород, алкил, алкенил, алкинил, циклоалкил, гетероциклил, арил, гетероалкил или гетероарил; каждый из которых может быть необязательно замещен, как определено в данном документе. Примеры гетероалкильных групп включают, например, простые эфиры (например, -CH2OCH3, -CH(CH3)OCH3, -CH2CH2OCH3, -CH2CH2OCH2CH2OCH3 и т. д.), простые тиоэфиры (например, -CH2SCH3, -CH(CH3)SCH3, -CH2CH2SCH3, -CH2CH2SCH2CH2SCH3 и т. д.), сульфоны (например, -CH2S(O)2CH3, -CH(CH3)S(O)2CH3, -CH2CH2S(O)2CH3, -CH2CH2S(O)2CH2CH2OCH3 и т. д.) и амины (например, -CH2NRyCH3, -CH(CH3)NRyCH3, -CH2CH2NRyCH3, -CH2CH2NRyCH2CH2NRyCH3 и т. д., где Ry представляет собой водород, алкил, алкенил, алкинил, циклоалкил, гетероциклил, арил, гетероалкил или гетероарил; каждый из которых может быть необязательно замещен, как определено в данном документе). В некоторых вариантах осуществления гетероалкил содержит от 1 до 10 атомов углерода (C1-10гетероалкил), от 1 до 8 атомов углерода (C1-8гетероалкил) или от 1 до 4 атомов углерода (C1-4гетероалкил); а также от 1 до 3 гетероатомов, от 1 до 2 гетероатомов или 1 гетероатом.
[430] Термин «гетероалкилен» означает двухвалентную алкильную группу (т.е. алкилен), в которой каждый из одного или более (например, от одного до пяти или от одного до трех) атомов углерода (и любых связанных атомов водорода) независимо замещен одинаковой или отличающейся группой, содержащей гетероатом. «Гетероалкиленовые» группы должны содержать по меньшей мере один атом углерода и по меньшей мере одну группу, содержащую гетероатом, в составе цепи. Точка присоединения гетероалкилена к остальной части молекулы может обеспечиваться посредством атома углерода или гетероатома. Термин «гетероалкилен» включает неразветвленную или разветвленную насыщенную цепь, содержащую углерод и гетероатомы. В качестве примера, 1, 2 или 3 атома углерода могут быть независимо замещены одинаковыми или отличающимися группами, содержащими гетероатом. Группы, содержащие гетероатом, включают без ограничения -NRy-, -O-, -S-, -S(O)-, -S(O)2- и т.п., где Ry представляет собой водород, алкил, алкенил, алкинил, циклоалкил, гетероциклил, арил, гетероалкил или гетероарил; каждый из которых может быть необязательно замещен, как определено в данном документе. Примеры гетероалкиленовых групп включают, например, -CH2OCH2-, -CH(CH3)OCH2-, -CH2CH2OCH2-, -CH2CH2OCH2CH2OCH2-, -CH2SCH2-, -CH(CH3)SCH2-, -CH2CH2SCH2-, -CH2CH2SCH2CH2SCH2-, -CH2S(O)2CH2-, -CH(CH3)S(O)2CH2-, -CH2CH2S(O)2CH2-, -CH2CH2S(O)2CH2CH2OCH2-, -CH2NRyCH2-, -CH(CH3)NRyCH2-, -CH2CH2NRyCH2-, -CH2CH2NRyCH2CH2NRyCH2- и т.д., где Ry представляет собой водород, алкил, алкенил, алкинил, циклоалкил, гетероциклил, арил, гетероалкил или гетероарил; каждый из которых может быть необязательно замещен, как определено в данном документе). В некоторых вариантах осуществления гетероалкилен содержит от 1 до 10 атомов углерода (C1-10гетероалкилен), от 1 до 8 атомов углерода (C1-8гетероалкилен) или от 1 до 4 атомов углерода (C1-4гетероалкилен); а также от 1 до 3 гетероатомов, от 1 до 2 гетероатомов или 1 гетероатом.
[440] Термин «гетероарил» означает ароматическую группу, содержащую одно кольцо, несколько колец или несколько конденсированных колец, при этом один или более гетероатомов в кольце независимо выбраны из азота, кислорода и серы. При использовании в данном документе, гетероарил содержит от 1 до 20 атомов углерода в кольце (т.е. C1-20гетероарил), от 3 до 12 атомов углерода в кольце (т.е. C3-12гетероарил) или от 3 до 8 атомов углерода в кольце (т.е. C3-8гетероарил), а также от 1 до 5 гетероатомов в кольце, от 1 до 4 гетероатомов в кольце, от 1 до 3 гетероатомов в кольце, от 1 до 2 гетероатомов в кольце или 1 гетероатом в кольце, независимо выбранных из азота, кислорода и серы. В определенных случаях гетероарил содержит 5-10-членные кольцевые системы, 5-7-членные кольцевые системы или 5-6-членные кольцевые системы, каждая из которых независимо содержит от 1 до 4 гетероатомов в кольце, от 1 до 3 гетероатомов в кольце, от 1 до 2 гетероатомов в кольце или 1 гетероатом в кольце, независимо выбранных из азота, кислорода и серы. Примеры гетероарильных групп включают, например, акридинил, бензимидазолил, бензотиазолил, бензиндолил, бензофуранил, бензотиазолил, бензотиадиазолил, бензонафтофуранил, бензоксазолил, бензотиенил (бензотиофенил), бензотриазолил, бензо[4,6]имидазо[1,2-a]пиридил, карбазолил, циннолинил, дибензофуранил, дибензотиофенил, фуранил, изотиазолил, имидазолил, индазолил, индолил, индазолил, изоиндолил, изохинолил, изоксазолил, нафтиридинил, оксадиазолил, оксазолил, 1-оксидопиридинил, 1-оксидопиримидинил, 1-оксидопиразинил, 1-оксидопиридазинил, феназинил, фталазинил, птеридинил, пуринил, пирролил, пиразолил, пиридинил, пиразинил, пиримидинил, пиридазинил, хиназолинил, хиноксалинил, хинолинил, хинуклидинил, изохинолинил, тиазолил, тиадиазолил, триазолил, тетразолил и триазинил. Примеры конденсированных гетероарильных колец включают без ограничения бензо[d]тиазолил, хинолинил, изохинолинил, бензо[b]тиофенил, индазолил, бензо[d]имидазолил, пиразоло[1,5-a]пиридинил и имидазо[1,5-a]пиридинил, где гетероарил может быть связан посредством любого из колец конденсированной системы. Любое ароматическое кольцо, характеризующееся наличием одного или нескольких конденсированных колец, содержащее по меньшей мере один гетероатом, считается гетероарилом вне зависимости от места присоединения к остальной части молекулы (т.е. посредством любого из конденсированных колец). Гетероарил не охватывает арил, определенный выше, и не совпадает с ним.
[450] Термин «гетероарилалкил» означает группу «гетероарил-алкил-».
[460] Термин «гетероциклил» означает насыщенную или частично ненасыщенную циклическую алкильную группу, содержащую один или более гетероатомов в кольце, независимо выбранных из азота, кислорода и серы. Термин «гетероциклил» включает гетероциклоалкенильные группы (т.е. гетероциклильную группу, содержащую по меньшей мере одну двойную связь), мостиковые гетероциклильные группы, конденсированные гетероциклильные группы и спирогетероциклильные группы. Гетероциклил может представлять собой одно кольцо или несколько колец, где несколько колец могут представлять собой конденсированные, мостиковые или спиро-кольца, а также могут содержать один или более (например, от 1 до 3) оксо- (=O) или N-оксидных (-O-) фрагментов. Любое неароматическое кольцо, содержащее по меньшей мере один гетероатом, считается гетероциклилом вне зависимости от места присоединения (т.е. может быть присоединено посредством атома углерода или гетероатома). Кроме того, предполагается, что термин «гетероциклил» охватывает любое неароматическое кольцо, содержащее по меньшей мере один гетероатом, где кольцо может быть конденсировано с арильным или гетероарильным кольцом вне зависимости от места присоединения к остальной части молекулы. При использовании в данном документе, гетероциклил содержит от 2 до 20 атомов углерода в кольце (т.е. C2-20гетероциклил), от 2 до 12 атомов углерода в кольце (т.е. C2-12гетероциклил), от 2 до 10 атомов углерода в кольце (т.е. C2-10гетероциклил), от 2 до 8 атомов углерода в кольце (т.е. C2-8гетероциклил), от 3 до 12 атомов углерода в кольце (т.е. C3-12гетероциклил), от 3 до 8 атомов углерода в кольце (т.е. C3-8гетероциклил) или от 3 до 6 атомов углерода в кольце (т.е. C3-6гетероциклил); при этом содержит от 1 до 5 гетероатомов в кольце, от 1 до 4 гетероатомов в кольце, от 1 до 3 гетероатомов в кольце, от 1 до 2 гетероатомов в кольце или 1 гетероатом в кольце, независимо выбранные из азота, серы или кислорода. В определенных случаях гетероциклил включает 3-10-членный гетероциклил, содержащий в общем 3-10 атомов в кольце, 5-7-членный гетероциклил, содержащий в общем 5-7 атомов в кольце, или 5- или 6-членный гетероциклил, содержащий в общем 5 или 6 атомов в кольце. Примеры гетероциклильных групп включают, например, азетидинил, азепинил, бензодиоксолил, бензо[b][1,4]диоксепинил, 1,4-бензодиоксанил, бензопиранил, бензодиоксинил, бензопиранонил, бензофуранонил, диоксоланил, дигидропиранил, гидропиранил, тиенил[1,3]дитианил, декагидроизохинолил, фуранонил, имидазолинил, имидазолидинил, индолинил, индолизинил, изоиндолинил, изотиазолидинил, изоксазолидинил, морфолинил, октагидроиндолил, октагидроизоиндолил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, оксазолидинил, оксиранил, оксетанил, фенотиазинил, феноксазинил, пиперидинил, пиперазинил, 4-пиперидонил, пирролидинил, пиразолидинил, хинуклидинил, тиазолидинил, тетрагидрофурил, тетрагидропиранил, тритианил, тетрагидрохинолинил, тиофенил (т.е. тиенил), тетрагидропиранил, тиоморфолинил, тиаморфолинил, 1-оксо-тиоморфолинил и 1,1-диоксо-тиоморфолинил. Термин «гетероциклил» также включает «спирогетероциклил», где по меньшей мере два кольца связаны вместе посредством одного общего атома. Примеры спирогетероциклильных колец включают, например, бициклические и трициклические кольцевые системы, такие как 2-окса-7-азаспиро[3.5]нонанил, 2-окса-6-азаспиро[3.4]октанил и 6-окса-1-азаспиро[3.3]гептанил. Примеры конденсированных гетероциклильных колец включают без ограничения 1,2,3,4-тетрагидроизохинолинил, 4,5,6,7-тетрагидротиено[2,3-c]пиридинил, индолинил и изоиндолинил, где гетероциклил может быть связан посредством любого из колец конденсированной системы. Гетероциклилен означает двухвалентную гетероциклильную группу.
[470] Термин «гетероциклилалкил» означает группу «гетероциклил-алкил-».
[480] Термин «оксим» означает группу -CRy(=NOH), где Ry представляет собой водород, алкил, алкенил, алкинил, циклоалкил, гетероциклил, арил, гетероалкил или гетероарил; каждый из которых может быть необязательно замещен, как определено в данном документе.
[490] Термины «необязательный» или «необязательно» означают, что описанное после них событие или обстоятельство может реализоваться или не реализоваться, и что описание включает случаи, где указанное событие или обстоятельство реализуется, и случаи, где оно не реализуется. Кроме того, термин «необязательно замещенный» означает обозначенный атом или группу, где любой один или более (например, от 1 до 5 или от 1 до 3) атомов водорода при обозначенном атоме или группе могут быть замещены или могут быть не замещены фрагментом, отличным от водорода.
[500] В определенных вариантах осуществления термин «замещенный» включает любую из вышеуказанных алкильных, гетероалкильных, алкенильных, алкинильных, циклоалкильных, гетероциклильных, арильных или гетероарильных групп, где один или более (например, от 1 до 5 или от 1 до 3) атомов водорода независимо замещены атомом галогена, циано, нитро, азидо, оксо, алкилом, алкенилом, алкинилом, галогеналкилом, циклоалкилом, гетероциклилом, арилом, гетероарилом, -NRgRh, -NRgC(=O)Rh, -NRgC(=O)NRgRh, -NRgC(=O)ORh, -NRgS(=O)1-2Rh, -C(=O)Rg, -C(=O)ORg, -OC(=O)ORg, -OC(=O)Rg, -C(=O)NRgRh, -OC(=O)NRgRh, -ORg, -SRg, -S(=O)Rg, -S(=O)2Rg, -OS(=O)1-2Rg, -S(=O)1-2ORg, -NRgS(=O)1-2NRgRh, =NSO2Rg, =NORg, -S(=O)1-2NRgRh, -SF5, -SCF3 или -OCF3. В определенных вариантах осуществления термин «замещенный» также означает любую из вышеперечисленных групп, где один или более (например, от 1 до 5 или от 1 до 3) атомов водорода замещены -C(=O)Rg, -C(=O)ORg, -C(=O)NRgRh, -CH2SO2Rg или -CH2SO2NRgRh. Как изложено выше, Rg и Rh являются одинаковыми или отличающимися и независимо представляют собой водород, алкил, алкенил, алкинил, алкокси, тиоалкил, арил, аралкил, циклоалкил, циклоалкилалкил, галогеналкил, гетероциклил, гетероциклилалкил, гетероарил и/или гетероарилалкил. В определенных вариантах осуществления «замещенный» означает любую из вышеперечисленных групп, где один или более (например, от 1 до 5 или от 1 до 3) атомов водорода замещены связью с амино, циано, гидроксилом, имино, нитро, оксо, тиоксо, атомом галогена, алкилом, алкокси, алкиламино, тиоалкилом, арилом, аралкилом, циклоалкилом, циклоалкилалкилом, галогеналкилом, гетероциклилом, N-гетероциклилом, гетероциклилалкилом, гетероарилом и/или гетероарилалкилом, или два из Rg, и Rh, и Ri взяты вместе с атомами, к которым они присоединены, с образованием гетероциклильного кольца, необязательно замещенного оксо, атомом галогена или алкилом, необязательно замещенными оксо, атомом галогена, амино, гидроксилом или алкокси.
[510] Предполагается, что полимеры или подобные им структуры неопределенной длины, полученные путем описания заместителей с дополнительными заместителями, присоединяемыми до бесконечности (например, замещенный арил, содержащий замещенный алкил, который сам является замещенным замещенной арильной группой, которая дополнительно замещена замещенной гетероалкильной группой, и т.д.), не включены в данный документ.если не указано иное, максимальное число серийных замещений в соединениях, описанных в данном документе, равно трем. Например, серийные замещения замещенных арильных групп двумя другими замещенными арильными группами ограничены структурой ((замещенный арил)замещенный арил)замещенный арил. Подобным образом, предполагается, что вышеупомянутые определения не включают недопустимые схемы замещения (например, метил, замещенный 5 атомами фтора, или гетероарильные группы, содержащие два смежных атома кислорода в кольце). Такие недопустимые схемы замещения являются общеизвестными специалисту в данной области техники. В случае использования для модификации химической группы, термин «замещенный» может описывать другие химические группы, определенные в данном документе.
[520] В определенных вариантах осуществления используемое в данном документе выражение «один или более» означает число от одного до пяти. В определенных вариантах осуществления используемое в данном документе выражение «один или более» означает число от одного до трех.
[530] Также предполагается, что любое соединение или структура, приведенные в данном документе, представляют собой немеченые формы, а также меченные изотопом формы соединений. Такие формы соединений также могут называться «обогащенными изотопом аналогами». меченные изотопом соединения обладают структурами, изображенными в данном документе, за исключением того, что один или более атомов замещены атомом, имеющим выбранную атомную массу или массовое число. Примеры изотопов, которые могут быть включены в раскрытые соединения, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора, хлора и йода, такие как 2H, 3H, 11C, 13C, 14C, 13N, 15N, 15O, 17O, 18O, 31P, 32P, 35S, 18F, 36Cl, 123I и 125I соответственно. Представлены разнообразные меченные изотопом соединения по настоящему изобретению, например, соединения, в которые включены радиоактивные изотопы, такие как 3H, 13C и 14C. Такие меченные изотопом соединения могут быть пригодными в исследованиях метаболизма, исследованиях кинетики реакций, методиках обнаружения или визуализации, таких как позитронно-эмиссионная томография (PET) или однофотонная эмиссионная компьютерная томография (SPECT), в том числе анализы тканевого распределения лекарственного средства или субстрата, или при лечении субъектов с применением радиоактивных средств.
[540] Термин «обогащенные изотопом аналоги» включает «дейтерированные аналоги» соединений, описанных в данном документе, где один или более атомов водорода замещены атомом дейтерия, например, атом водорода при атоме углерода. Такие соединения могут проявлять повышенную устойчивость в отношении метаболизма и, таким образом, являются пригодными для увеличения периода полувыведения любого соединения при введении млекопитающему, в частности, человеку. См., например, Foster, «Deuterium Isotope Effects in Studies of Drug Metabolism», Trends Pharmacol. Sci. 5(12):524-527 (1984). Такие соединения синтезируют посредством способов, общеизвестных из уровня техники, например, путем применения исходных материалов, в которых один или более атомов водорода замещены атомом дейтерия.
[550] меченные или замещенные дейтерием терапевтические соединения по настоящему изобретению обладают улучшенными свойствами DMPK (метаболизм и фармакокинетика лекарственного средства), связанными с распределением, метаболизмом и выведением (ADME). Замещение более тяжелыми изотопами, такими как дейтерий, может обеспечивать определенные терапевтические преимущества вследствие более высокой метаболической стабильности, например, увеличение периода полувыведения in vivo, снижение требуемой дозы и/или улучшение в отношении терапевтического индекса. Меченное 18F, 3H, 11C соединение может быть пригодным для PET, или SPECT, или других исследований, основанных на визуализации. меченные изотопом соединения по настоящему изобретению, как правило, можно получать путем осуществления процедур, раскрытых на схемах или в примерах и способах получения, описанных ниже, путем замены общедоступным меченным изотопом реагентом не меченного изотопом реагента.
[560] Концентрация такого более тяжелого изотопа, в частности дейтерия, может выражаться коэффициентом изотопного обогащения. Подразумевается, что в соединениях по настоящему изобретению любой атом, явно не обозначенный как определенный изотоп, представляет собой любой стабильный изотоп данного атома. Если не указано иное, в случае если атом представлен в виде своего названия или буквенного обозначения, такого как H, C, O или N, следует понимать, что атом характеризуется своим природным изотопным составом. Например, если положение конкретно обозначено как «H» или «водород», то подразумевается, что положение содержит водород в его природном изотопном составе. Соответственно, подразумевается, что в соединениях по настоящему изобретению любой атом, конкретно обозначенный как дейтерий (D), представляет собой дейтерий.
[570] Во многих случаях соединения по настоящему изобретению обладают способностью к образованию солей кислот и/или оснований в результате наличия аминогрупп, и/или карбоксильных групп, или им подобных групп.
[580] Предусмотрены также фармацевтически приемлемая соль, обогащенный изотопом аналог, дейтерированный аналог, стереоизомер и смесь стереоизомеров соединений, описанных в данном документе. Термин «фармацевтически приемлемый» или «физиологически приемлемый» означает соединения, соли, композиции, дозированные лекарственные формы и другие материалы, которые являются применимыми в получении фармацевтической композиции, которая является подходящей для фармацевтического применения в ветеринарии или медицине.
[590] Термин «фармацевтически приемлемая соль» заданного соединения означает соли, которые сохраняют биологическую эффективность и свойства заданного соединения и которые не являются нежелательными с биологической или иной точки зрения. Термин «фармацевтически приемлемые соли» или «физиологически приемлемые соли» включает, например, соли неорганических кислот и соли органических кислот. Кроме того, если соединения, описанные в данном документе, получают в виде соли присоединения кислоты, то свободное основание можно получать путем повышения основности раствора соли кислоты. И наоборот, если продукт представляет собой свободное основание, то соль присоединения, в частности, фармацевтически приемлемую соль присоединения, можно получать путем растворения свободного основания в подходящем органическом растворителе и обработки раствора кислотой в соответствии с традиционными процедурами получения солей присоединения кислоты из основных соединений. Специалист в данной области определит разнообразные методологии синтеза, которые могут применяться для получения нетоксичных фармацевтически приемлемых солей присоединения. Фармацевтически приемлемые соли присоединения кислоты можно получать из неорганических и органических кислот. Соли, полученные из неорганических кислот, включают, например, хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, азотную кислоту, фосфорную кислоту и т.п. Соли, полученные из органических кислот, включают, например, уксусную кислоту, пропионовую кислоту, глюконовую кислоту, гликолевую кислоту, пировиноградную кислоту, щавелевую кислоту, яблочную кислоту, малоновую кислоту, янтарную кислоту, малеиновую кислоту, фумаровую кислоту, винную кислоту, лимонную кислоту, бензойную кислоту, коричную кислоту, миндальную кислоту, метансульфоновую кислоту, этансульфоновую кислоту, п-толуолсульфоновую кислоту, салициловую кислоту и т.п. Аналогичным образом, фармацевтически приемлемые соли присоединения основания можно получать из неорганических и органических оснований. Соли, полученные из неорганических оснований, включают, только в качестве примера, соли натрия, калия, лития, алюминия, аммония, кальция и магния. Соли, полученные из органических оснований, включают без ограничения соли первичных, вторичных и третичных аминов, таких как алкиламины (т.е. NH2(алкил)), диалкиламины (т.е. HN(алкил)2), триалкиламины (т.е. N(алкил)3), замещенные алкиламины (т.е. NH2(замещенный алкил)), ди(замещенный алкил)амины (т.е. HN(замещенный алкил)2), три(замещенный алкил)амины (т.е. N(замещенный алкил)3), алкениламины (т.е. NH2(алкенил)), диалкениламины (т.е. HN(алкенил)2), триалкениламины (т.е. N(алкенил)3), замещенные алкениламины (т.е. NH2(замещенный алкенил)), ди(замещенный алкенил)амины (т.е. HN(замещенный алкенил)2), три(замещенный алкенил)амины (т.е. N(замещенный алкенил)3, моно-, ди- или трициклоалкиламины (т.е. NH2(циклоалкил), HN(циклоалкил)2, N(циклоалкил)3), моно-, ди- или триариламины (т.е. NH2(арил), HN(арил)2, N(арил)3) или смешанные амины и т.д. Конкретные примеры подходящих аминов включают, только в качестве примера, изопропиламин, триметиламин, диэтиламин, три(изопропил)амин, три(н-пропил)амин, этаноламин, 2-диметиламиноэтанол, пиперазин, пиперидин, морфолин, N-этилпиперидин и т.п.
[600] Некоторые из соединений существуют в виде таутомеров. Таутомеры находятся в равновесии друг с другом. Например, содержащие амид соединения могут существовать в равновесии с таутомерами имидокислоты. Вне зависимости от того, какой таутомер показан, и вне зависимости от природы равновесия среди таутомеров, специалисту средней квалификации в данной области техники понятно, что соединения включают таутомеры. Таким образом, подразумевается, что содержащие амид соединения включают их таутомеры имидокислоты. Аналогичным образом, подразумевается, что содержащие имидокислоту соединения включают их амидные таутомеры.
[610] Термин «стереоизомер» означает соединение, образованное из одних и тех же атомов, связанных с помощью таких же связей, но имеющее другие пространственные структуры, которые не являются взаимозаменяемыми. В настоящем изобретении рассматриваются разнообразные стереоизомеры и их смеси, и они включают следующее.
[620] Стереоизомеры включают энантиомеры, диастереомеры и другие формы стереоизомеров, которые можно определить с точки зрения абсолютной стереохимии как (R)- или (S)-, или как (D)- или (L)- в случае аминокислот. Подразумевается, что настоящее изобретение включает все возможные такие изомеры, а также их рацемические и оптически чистые формы. Оптически активные (+)- и (-)-, (R)- и (S)-, или (D)- и (L)-изомеры можно получать с применением хиральных синтонов или хиральных реагентов, или выделять с применением традиционных методик, например, хроматографии и фракционной кристаллизации. Традиционные методики получения/выделения отдельных энантиомеров включают хиральный синтез из подходящего оптически чистого предшественника или разделение рацемата (или рацемата соли или производного) с применением, например, хиральной жидкостной хроматографии при высоком давлении (HPLC). Стереоизомеры также включают геометрические изомеры, если соединения, описанные в данном документе, содержат олефиновые двойные связи или другие центры геометрической асимметрии. Если не указано иное, предполагается, что такие соединения включают геометрические изомеры, как E-, так и Z-.
[630] «Энантиомеры» представляют собой два стереоизомера, молекулы которых представляют собой не совпадающие при наложении зеркальные отображения друг друга. «Диастереомеры» представляют собой стереоизомеры, которые содержат по меньшей мере два асимметричных атома, однако которые не являются зеркальными отображениями друг друга.
[640] Относительные центры соединений, изображенных в данном документе, обозначены графически с использованием стиля «утолщенных связей» (жирных или параллельных линий), и абсолютная стереохимия изображена с использованием клиновидных связей (жирных или параллельных линий).
[650] Термин «сольват» означает комплекс, образованный путем объединения соединения, описанного в данном документе, или его соли или кристаллической формы и растворителя. При использовании в данном документе термин «сольват» включает гидрат (т.е. сольват, если растворитель представляет собой воду).
[660] 2. Соединения
[670] В данном документе предусмотрены соединения, которые подавляют активность MmpL3, которые могут также называться низкомолекулярными ингибиторами MmpL3, ингибиторами мембранного белка микобактерий MmpL3 или низкомолекулярными ингибиторами мембранного белка микобактерий MmpL3, при этом указанные названия используют взаимозаменяемо.
[680] В определенных вариантах осуществления предусмотрено соединение формулы I:
 I,
I,
или его фармацевтически приемлемая соль, сольват, таутомер, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров,
где
кольцо A представляет собой 5-членный гетероарил, где X1 представляет собой C или N, X2, X3, X4 и X5 независимо выбраны из C, N, O и S, при условии, что не более чем один из X2, X3, X4 и X5 представляет собой O или S, и по меньшей мере один из X1, X2, X3, X4 и X5 представляет собой C;
L1 представляет собой *-N(R1b)CO-, *-CON(R1b)-, *-OCO-, *-COO-, *-N(R1b)SO2-, *-SO2N(R1b)-, *-N(R1c)CON(R1b)-, *-CO-L1a-CO-, *-L1a-CO- или алкилен, где необязательно одна или более из групп CH2 алкилена замещены группой, независимо выбранной из группы, состоящей из CO, NR1b, NR1c, O, S, SO, SO2 и 5-, 6- или 7-членного гетероциклилена;
* обозначает точку соединения с R1;
L1a представляет собой 5-, 6- или 7-членный гетероциклилен;
каждый R1b независимо представляет собой H или C1-3алкил;
каждый R1c независимо представляет собой H или C1-3алкил;
каждый из m и n независимо равняется 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10;
R1 представляет собой C7-15циклоалкил, необязательно замещенный R1a в количестве от одного до десяти;
каждый R1a независимо выбран из галогена, -CN, -NO2, C1-3алкила, C1-3галогеналкила, -OR6, -SR6, -N(R6)2, -C(O)R6, -C(O)OR6, -S(O)R6, -S(O)2R6, -C(O)N(R6)2, -NR6C(O)R6, -NR6C(O)OR6, -NR6C(O)N(R6)2, -NHS(O)R6, -S(O)(NH)R6, циклоалкила, арила, гетероциклила, гетероарила или их комбинации;
если X2 представляет собой C, то R2 представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R2a в количестве от одного до пяти, алкенил, необязательно замещенный R2a в количестве от одного до пяти, алкинил, необязательно замещенный R2a в количестве от одного до пяти, циклоалкил, необязательно замещенный R2a в количестве от одного до пяти, арил, необязательно замещенный R2a в количестве от одного до пяти, гетероциклил, необязательно замещенный R2a в количестве от одного до пяти, или гетероарил, необязательно замещенный R2a в количестве от одного до пяти,
если X2 представляет собой N, то R2 отсутствует или представляет собой H, прямой или разветвленный алкил, необязательно замещенный R2a в количестве от одного до пяти, алкенил, необязательно замещенный R2a в количестве от одного до пяти, алкинил, необязательно замещенный R2a в количестве от одного до пяти, циклоалкил, необязательно замещенный R2a в количестве от одного до пяти, арил, необязательно замещенный R2a в количестве от одного до пяти, гетероциклил, необязательно замещенный R2a в количестве от одного до пяти, или гетероарил, необязательно замещенный R2a в количестве от одного до пяти,
если X2 представляет собой O или S, то R2 отсутствует;
если X3 представляет собой C, то R3 представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R3a в количестве от одного до пяти, алкенил, необязательно замещенный R3a в количестве от одного до пяти, алкинил, необязательно замещенный R3a в количестве от одного до пяти, циклоалкил, необязательно замещенный R3a в количестве от одного до пяти, арил, необязательно замещенный R3a в количестве от одного до пяти, гетероциклил, необязательно замещенный R3a в количестве от одного до пяти, или гетероарил, необязательно замещенный R3a в количестве от одного до пяти,
если X3 представляет собой N, то R3 отсутствует или представляет собой H, прямой или разветвленный алкил, необязательно замещенный R3a в количестве от одного до пяти, алкенил, необязательно замещенный R3a в количестве от одного до пяти, алкинил, необязательно замещенный R3a в количестве от одного до пяти, циклоалкил, необязательно замещенный R3a в количестве от одного до пяти, арил, необязательно замещенный R3a в количестве от одного до пяти, гетероциклил, необязательно замещенный R3a в количестве от одного до пяти, или гетероарил, необязательно замещенный R3a в количестве от одного до пяти,
если X3 представляет собой O или S, то R3 отсутствует;
если X4 представляет собой C, то R4 представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R4a в количестве от одного до пяти, алкенил, необязательно замещенный R4a в количестве от одного до пяти, алкинил, необязательно замещенный R4a в количестве от одного до пяти, циклоалкил, необязательно замещенный R4a в количестве от одного до пяти, арил, необязательно замещенный R4a в количестве от одного до пяти, гетероциклил, необязательно замещенный R4a в количестве от одного до пяти, или гетероарил, необязательно замещенный R4a в количестве от одного до пяти,
если X4 представляет собой N, то R4 отсутствует или представляет собой H, прямой или разветвленный алкил, необязательно замещенный R4a в количестве от одного до пяти, алкенил, необязательно замещенный R4a в количестве от одного до пяти, алкинил, необязательно замещенный R4a в количестве от одного до пяти, циклоалкил, необязательно замещенный R4a в количестве от одного до пяти, арил, необязательно замещенный R4a в количестве от одного до пяти, гетероциклил, необязательно замещенный R4a в количестве от одного до пяти, или гетероарил, необязательно замещенный R4a в количестве от одного до пяти,
если X4 представляет собой O или S, то R4 отсутствует;
если X5 представляет собой C, то R5 представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R5a в количестве от одного до пяти, алкенил, необязательно замещенный R5a в количестве от одного до пяти, алкинил, необязательно замещенный R5a в количестве от одного до пяти, циклоалкил, необязательно замещенный R5a в количестве от одного до пяти, арил, необязательно замещенный R5a в количестве от одного до пяти, гетероциклил, необязательно замещенный R5a в количестве от одного до пяти, или гетероарил, необязательно замещенный R5a в количестве от одного до пяти,
если X5 представляет собой N, то R5 отсутствует или представляет собой H, прямой или разветвленный алкил, необязательно замещенный R5a в количестве от одного до пяти, алкенил, необязательно замещенный R5a в количестве от одного до пяти, алкинил, необязательно замещенный R5a в количестве от одного до пяти, циклоалкил, необязательно замещенный R5a в количестве от одного до пяти, арил, необязательно замещенный R5a в количестве от одного до пяти, гетероциклил, необязательно замещенный R5a в количестве от одного до пяти, или гетероарил, необязательно замещенный R5a в количестве от одного до пяти,
если X5 представляет собой O или S, то R5 отсутствует;
каждый из R2a, R3a, R4a или R5a независимо выбран из галогена, C1-3алкила, C1-3галогеналкила, -CN, -NO2, -OR6, -SR6, -N(R6)2, -C(O)R6, -C(O)OR6, -S(O)R6, -S(O)2R6, -C(O)N(R6)2, -NR6C(O)R6, -NR6C(O)OR6, -NR6C(O)N(R6)2, -NHS(O)R6, -S(O)(NH)R6, циклоалкила, арила, гетероциклила, гетероарила или их комбинации; и
каждый R6 независимо представляет собой водород, C1-3алкил, C1-3галогеналкил, C3-6циклоалкил, арил, гетероарил или гетероциклил.
[690] В определенных вариантах осуществления кольцо A представляет собой пиррол, имидазол, триазол, фуран, тиофен, оксазол, изоксазол, тиазол, изотиазол, оксадиазол или тиадиазол.
[700] В определенных вариантах осуществления предусмотрено соединение формулы
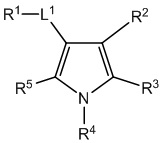 ,
, 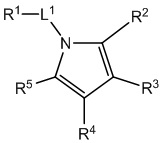 ,
, 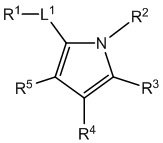 ,
, 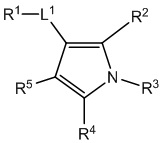 ,
, 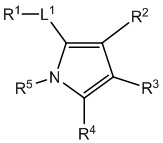 ,
, 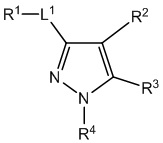 ,
, 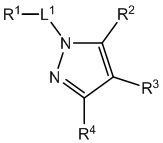 ,
, 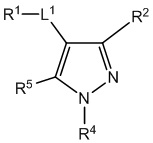 ,
, 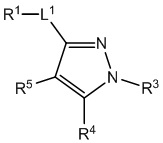 ,
, 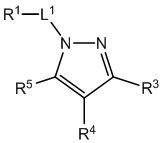 ,
, 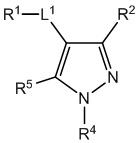 ,
, 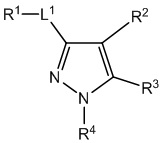 ,
, 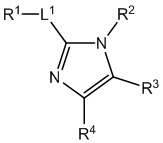 ,
, 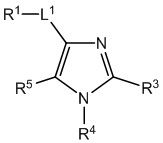 ,
, 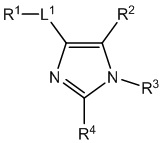 ,
, 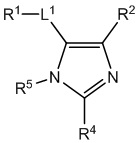 ,
, 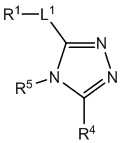 ,
, 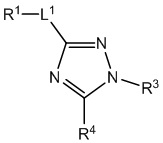 ,
, 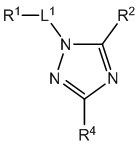 ,
, 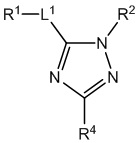 ,
, 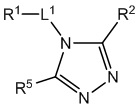 ,
, 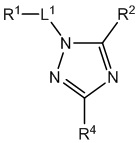 ,
, 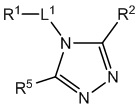 ,
, 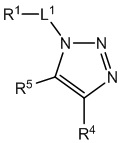 ,
, 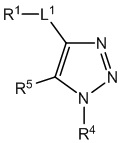 ,
, 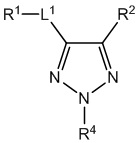 ,
, 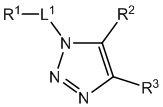 ,
, 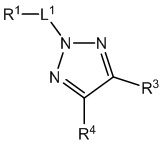 ,
, 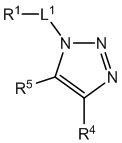 ,
, 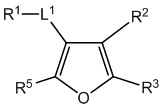 ,
, 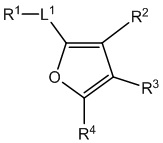 ,
, 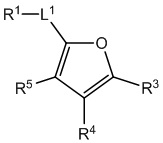 ,
, 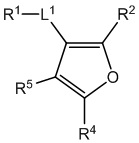 ,
, 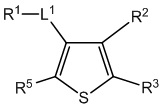 ,
, 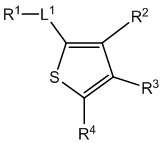 ,
, 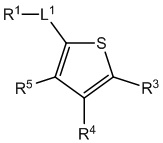 ,
, 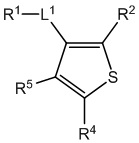 ,
, 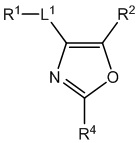 ,
, 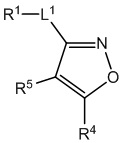 ,
, 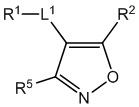 ,
, 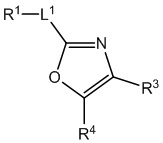 ,
, 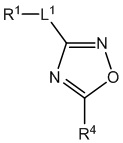 ,
, 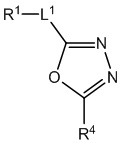 ,
, 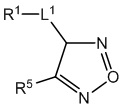 ,
, 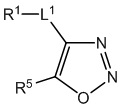 ,
, 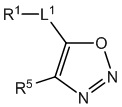 ,
, 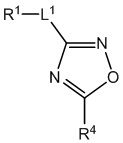 ,
, 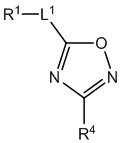 ,
, 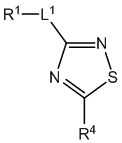 ,
, 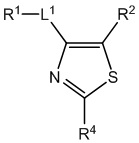 ,
, 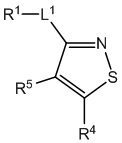 ,
, 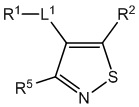 ,
, 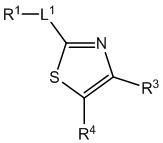 ,
, 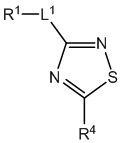 ,
, 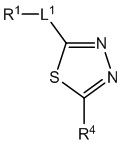 ,
, 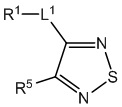 ,
, 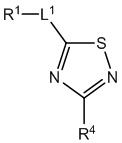 ,
, 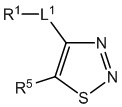 или
или 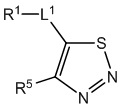 ,
,
или его фармацевтически приемлемая соль, сольват, таутомер, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров.
[710] В определенных вариантах осуществления по меньшей мере один из R2, R3, R4 или R5 представляет собой циклоалкил, необязательно замещенный R5a в количестве от одного до пяти, арил, необязательно замещенный R5a в количестве от одного до пяти, гетероциклил, необязательно замещенный R5a в количестве от одного до пяти, или гетероарил, необязательно замещенный R5a в количестве от одного до пяти. В определенных вариантах осуществления по меньшей мере один из R2, R3, R4 или R5 представляет собой арил, необязательно замещенный R5a в количестве от одного до пяти. В определенных вариантах осуществления по меньшей мере один из R2, R3, R4 или R5 представляет собой фенил, необязательно замещенный R5a в количестве от одного до пяти. В определенных вариантах осуществления по меньшей мере один из R2, R3, R4 или R5 представляет собой гетероарил, необязательно замещенный R5a в количестве от одного до пяти. В определенных вариантах осуществления по меньшей мере один из R2, R3, R4 или R5 представляет собой 5-членный гетероарил, необязательно замещенный R5a в количестве от одного до пяти. В определенных вариантах осуществления по меньшей мере один из R2, R3, R4 или R5 представляет собой 6-членный гетероарил, необязательно замещенный R5a в количестве от одного до пяти. В определенных вариантах осуществления по меньшей мере один из R2, R3, R4 или R5 представляет собой пиридил, необязательно замещенный R5a в количестве от одного до пяти. В определенных вариантах осуществления по меньшей мере один из R2, R3, R4 или R5 представляет собой замещенный арил или замещенный гетероарил.
[720] В определенных вариантах осуществления по меньшей мере один из R3 или R4 представляет собой необязательно замещенный арил или необязательно замещенный гетероарил. В определенных вариантах осуществления по меньшей мере один из R2 и R5 независимо отсутствует, представляет собой H, галоген, прямой или разветвленный C1-3алкил, необязательно замещенный R2a в количестве от одного до пяти, или C3-6циклоалкил, необязательно замещенный R2a в количестве от одного до пяти.
[730] В определенных вариантах осуществления R3 представляет собой фенил, необязательно замещенный R3a в количестве от одного до двух. В определенных вариантах осуществления R3 представляет собой пиридил, необязательно замещенный R4a в количестве от одного до двух. В определенных вариантах осуществления R3a независимо представляет собой галоген, CN, метил, метокси или трифторметил. В определенных вариантах осуществления R3a представляет собой хлор. В определенных вариантах осуществления R3 представляет собой 4-хлорфенил или 2,4-дихлорфенил.
[740] В определенных вариантах осуществления R4 представляет собой фенил, необязательно замещенный R4a в количестве от одного до двух. В определенных вариантах осуществления R4 представляет собой пиридил, необязательно замещенный R4a в количестве от одного до двух. В определенных вариантах осуществления R4a независимо представляет собой галоген, CN, метил, метокси или трифторметил. В определенных вариантах осуществления R4a представляет собой хлор. В определенных вариантах осуществления R4 представляет собой 4-хлорфенил или 2,4-дихлорфенил.
[750] В определенных вариантах осуществления L1 представляет собой *-(CH2)m-N(R1b)CO-, *-(CH2)m-CON(R1b)-, *-(CH2)n-OCO-, *-(CH2)n-COO-, *-(CH2)m-N(R1b)SO2-, *-(CH2)m-SO2N(R1b)- или *-(CH2)n-N(R1c)CON(R1b)-.
[760] В определенных вариантах осуществления L1 представляет собой алкилен, где необязательно одна или более из групп CH2 алкилена замещены группой, независимо выбранной из CO, NR1b, NR1c, O, S, SO, SO2 и 5-, 6- или 7-членного гетероциклилена. В некоторых вариантах осуществления две смежные группы CH2 алкилена вместе замещены -N(R1b)CO-, -CON(R1b)-, -N(R1b)SO2- или SO2N(R1b)-. В некоторых вариантах осуществления три смежные группы CH2 алкилена вместе замещены -N(R1c)CON(R1b)-. В некоторых вариантах осуществления три смежные группы CH2 алкилена вместе замещены -N(R1b)-N(R1b)-(CO)-. В дополнительных вариантах осуществления первая группа CH2 алкилена замещена группой, независимо выбранной из CO, NR1b, NR1c, O, S, SO, SO2 и 5-, 6- или 7-членного гетероциклилена, и две или три следующие смежные группы CH2 алкилена замещены группой, независимо выбранной из -N(R1b)CO-, -CON(R1b)-, -N(R1b)SO2-, SO2N(R1b)- или -N(R1b)-N(R1b)-(CO)-.
[770] В некоторых вариантах осуществления одна группа CH2 алкилена замещена пиперазинильным кольцом. В некоторых вариантах осуществления две смежные группы CH2 алкилена вместе замещены 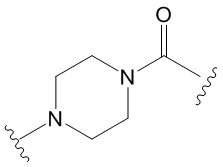 или
или 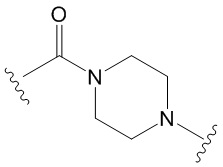 .
.
[780] В некоторых вариантах осуществления три смежные группы CH2 алкилена вместе замещены 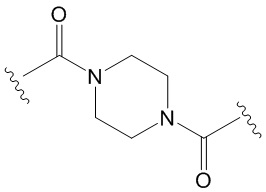 .
.
[790] В определенных вариантах осуществления L1 представляет собой *-N(R1b)CO-, *-(CH2)k-N(R1b)CO-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)CO-, *-(CH2)n-(O(CH2)m)p-O(CH2)k-N(R1b)CO-, *-(CH2)m-CO-L1a-CO-, *-(CH2)m-L1a-CO-, *-(CH2)n-NHCONH-(CH2)m-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)-(CH2)m-, *-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-SO2N(R1b)-(CH2)m-, *-(CH2)n-SO2N(R1b)-(CH2)m- или *-(CH2)n-OCO-; где
* обозначает точку соединения с R1;
L1a представляет собой 5-, 6- или 7-членный гетероциклилен;
R1b представляет собой H или C1-3алкил;
R1c представляет собой H или C1-3алкил;
k равняется 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10; и
каждый из m, n и p независимо равняется 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
[800] В определенных вариантах осуществления L1 представляет собой *-N(R1b)CO-, *-(CH2)k-N(R1b)CO-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)CO-, *-(CH2)n-(O(CH2)m)p-O(CH2)k-N(R1b)CO-, *-(CH2)m-CO-L1a-CO-, *-(CH2)m-L1a-CO-, *-(CH2)n-NHCONH-(CH2)m-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)-(CH2)m-, *-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-SO2N(R1b)-(CH2)m-, *-(CH2)n-SO2N(R1b)-(CH2)m-, *-(CH2)n-OCO-, *-(CH2)n-L1a-(CH2)m-, *-N(R1c)-(CH2)n-N(R1b)-(CH2)m- или *-N(R1c)-(CO)-(CH2)n-N(R1b)-N(R1b)-(CO)-; где
* обозначает точку соединения с R1;
L1a представляет собой 5-, 6- или 7-членный гетероциклилен;
R1b представляет собой H или C1-3алкил;
R1c представляет собой H или C1-3алкил;
k равняется 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10; и
каждый из m, n и p независимо равняется 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
[810] В определенных вариантах осуществления L1 представляет собой алкилен, где необязательно одна или более из групп CH2 алкилена замещены группой, независимо выбранной из CO, NR1b, NR1c, O, S, SO, SO2 и 5- или 6-членного гетероциклилена, такой как *-(CH2)k-N(R1b)CO-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)CO-, *-(CH2)n-(O(CH2)m)p-O(CH2)k-N(R1b)CO-, *-(CH2)m-CO-L1a-CO-, *-(CH2)m-L1a-CO-, *-(CH2)n-NHCONH-(CH2)m-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)-(CH2)m-, *-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-SO2N(R1b)-(CH2)m- или *-(CH2)n-SO2N(R1b)-(CH2)m-. В определенных вариантах осуществления L1 представляет собой C1-20алкилен, где необязательно от одной до десяти групп CH2 C1-20алкилена замещены группой, независимо выбранной из CO, NR1b, NR1c, O, S, SO, SO2 и 5- или 6-членного гетероциклилена.
[820] В определенных вариантах осуществления L1 представляет собой *-N(R1b)CO-.
[830] В определенных вариантах осуществления L1 представляет собой *-(CH2)k-N(R1b)CO-.
[840] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-N(R1c)-(CH2)k-N(R1b)CO-.
[850] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-(O(CH2)m)p-O(CH2)k-N(R1b)CO-.
[860] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-CO-L1a-CO-. В определенных вариантах осуществления L1a представляет собой пиперазин.
[870] В определенных вариантах осуществления L1 представляет собой *-(CH2)m-L1a-CO-. В определенных вариантах осуществления L1a представляет собой пиперазин.
[880] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-NHCONH-(CH2)m-.
[890] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-N(R1c)-(CH2)k-N(R1b)-(CH2)m-.
[900] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-CON(R1b)-(CH2)m-.
[910] В определенных вариантах осуществления L1 представляет собой *-N(R1c)-(CH2)n-CON(R1b)-(CH2)m-.
[920] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-N(R1c)-(CH2)n-SO2N(R1b)-(CH2)m-.
[930] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-SO2N(R1b)-(CH2)m-.
[940] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-N(R1c)-(CH2)n-N(R1b)SO2-(CH2)m-.
[950] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-N(R1b)SO2-(CH2)m-.
[960] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-OCO-.
[970] В определенных вариантах осуществления L1 представляет собой *-(CH2)n-L1a-(CH2)m-.
[980] В определенных вариантах осуществления L1 представляет собой *-N(R1c)-(CH2)n-N(R1b)-(CH2)m-.
[990] В определенных вариантах осуществления L1 представляет собой *-N(R1c)-(CO)-(CH2)n-N(R1b)-N(R1b)-(CO)-.
[1000] В определенных вариантах осуществления L1 выбран из *-NHCONH-, *-NHCONHCH2-, *-CH2NHCONHCH2-, *-(CH2)2NHCONHCH2-, *-(CH2)3NHCONHCH2-, *-(CH2)4NHCONHCH2-, *-(CH2)5NHCONHCH2-, *-(CH2)6NHCONHCH2-, *-NHCH2NHCO-, *-NH(CH2)2NHCO-, *-NH(CH2)3NHCO-, *-NH(CH2)4NHCO-, *-NH(CH2)5NHCO-, *-NH(CH2)6NHCO-, *-NH(CH2)7NHCO-, *-CH2NHCH2NHCO-, *-CH2NH(CH2)2NHCO-, *-CH2NH(CH2)3NHCO-, *-CH2NH(CH2)4NHCO-, *-CH2NH(CH2)5NHCO-, *-CH2NH(CH2)6NHCO-, *-CH2NH(CH2)7NHCO-, *-CH2NHCO-, *-(CH2)2NHCO-, *-(CH2)3NHCO-, *-(CH2)4NHCO-, *-(CH2)5NHCO-, *-(CH2)6NHCO-, *-(CH2)7NHCO-, *-(CH2)8NHCO-, *-NHCO-, *-O(CH2)2NHCO-, *-CH2NHCO-, *-CH2O(CH2)2NHCO-, *-(CH2)2O(CH2)2NHCO-, *-(CH2)3O(CH2)2NHCO-, *-O(CH2)2O(CH2)2NHCO-, *-CH2O(CH2)2O(CH2)2NHCO-, *-(CH2)2O(CH2)2O(CH2)2NHCO-, *-(CH2)3O(CH2)2O(CH2)2NHCO-, *-O(CH2)3NHCO-, *-NH(CH2)2NHCH2-, *-NH(CH2)4NHCH2-, *-NH(CH2)2SO2NHCH2-, *-OC(O)-, *-CH2O(CH2)3NHCO-, *-CH2NH(CH2)2NHCH2-, *-CH2NH(CH2)4NHCH2-, *-CH2NH(CH2)2SO2NHCH2-, *-CH2OC(O)-,
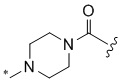 ,
, 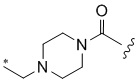 ,
, 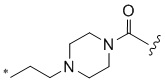 ,
, 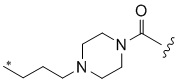 ,
, 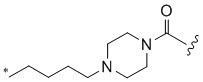 ,
, 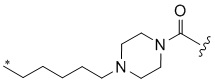 ,
, 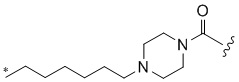 ,
, 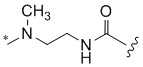 ,
, 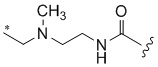 ,
, 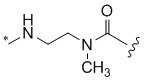 ,
, 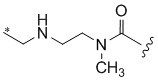 ,
, 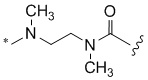 ,
, 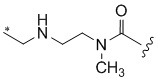 ,
, 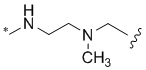 ,
, 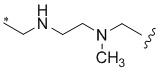 ,
, 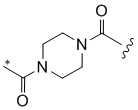 ,
, 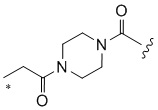 ,
, 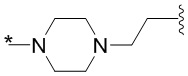 ,
, 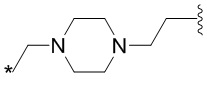 ,
, 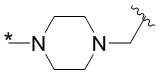 ,
, 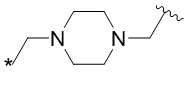 ,
, 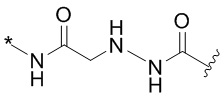 и
и 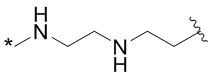 .
.
[1010] В определенных вариантах осуществления R1 представляет собой полициклический C7-15циклоалкил, необязательно замещенный R1a в количестве от одного до десяти. В определенных вариантах осуществления R1 представляет собой мостиковый C7-15циклоалкил, необязательно замещенный R1a в количестве от одного до десяти. В определенных вариантах осуществления R1 представляет собой незамещенный мостиковый C7-15циклоалкил.
[1020] В определенных вариантах осуществления R1 необязательно замещен R1a в количестве от одного до десяти, R1a в количестве от 1 до 9, R1a в количестве от 1 до 8, R1a в количестве от 1 до 7, R1a в количестве от 1 до 6, R1a в количестве от 1 до 5, R1a в количестве от 1 до 4, R1a в количестве от 1 до 3 или R1a в количестве от 1 до 2, или 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 R1a.
[1030] В определенных вариантах осуществления R1 представляет собой адамантил, необязательно замещенный R1a в количестве от одного до десяти, R1a в количестве от 1 до 9, R1a в количестве от 1 до 8, R1a в количестве от 1 до 7, R1a в количестве от 1 до 6, R1a в количестве от 1 до 5, R1a в количестве от 1 до 4, R1a в количестве от 1 до 3 или R1a в количестве от 1 до 2, или 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 R1a.
[1040] В определенных вариантах осуществления R1 представляет собой 1-адамантил, 2-адамантил, 3-адамантил, 4-адамантил, 5-адамантил, 6-адамантил, 7-адамантил, 8-адамантил, 9-адамантил или 10-адамантил, каждый из которых необязательно замещен R1a в количестве от 1 до 10, R1a в количестве от 1 до 9, R1a в количестве от 1 до 8, R1a в количестве от 1 до 7, R1a в количестве от 1 до 6, R1a в количестве от 1 до 5, R1a в количестве от 1 до 4, R1a в количестве от 1 до 3 или R1a в количестве от 1 до 2, или 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 R1a.
[1050] В определенных вариантах осуществления R1 представляет собой бицикло[2.2.1]гептил, необязательно замещенный R1a в количестве от одного до десяти, R1a в количестве от 1 до 9, R1a в количестве от 1 до 8, R1a в количестве от 1 до 7, R1a в количестве от 1 до 6, R1a в количестве от 1 до 5, R1a в количестве от 1 до 4, R1a в количестве от 1 до 3 или R1a в количестве от 1 до 2, или 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 R1a. В определенных вариантах осуществления R1 представляет собой 1-бицикло[2.2.1]гептил, 2-бицикло[2.2.1]гептил, 3-бицикло[2.2.1]гептил, 4-бицикло[2.2.1]гептил, 5-бицикло[2.2.1]гептил, 6-бицикло[2.2.1]гептил или 7-бицикло[2.2.1]гептил, каждый из которых необязательно замещен R1a в количестве от одного до десяти, R1a в количестве от 1 до 9, R1a в количестве от 1 до 8, R1a в количестве от 1 до 7, R1a в количестве от 1 до 6, R1a в количестве от 1 до 5, R1a в количестве от 1 до 4, R1a в количестве от 1 до 3 или R1a в количестве от 1 до 2, или 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 R1a. В определенных вариантах осуществления R1 представляет собой 1,7,7-триметилбицикло[2.2.1]гептан. В определенных вариантах осуществления R1 представляет собой метил.
[1060] В определенных случаях R1 представляет собой мостиковый C7-15циклоалкил, где мостиковый C7-15циклоалкил представляет собой замещенный адамантил или замещенный бицикло[2.2.1]гептил. В определенных случаях R1 представляет собой мостиковый C7-15циклоалкил, где мостиковый C7-15циклоалкил представляет собой незамещенный адамантил или незамещенный бицикло[2.2.1]гептил.
[1070] В определенных вариантах осуществления R1 выбран из
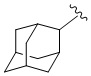 ,
, 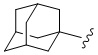 ,
, 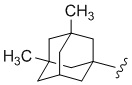 ,
, 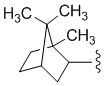 ,
, 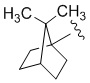 или
или 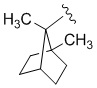 .
.
[1080] В определенных вариантах осуществления R1 выбран из
 ,
,  ,
,  ,
,
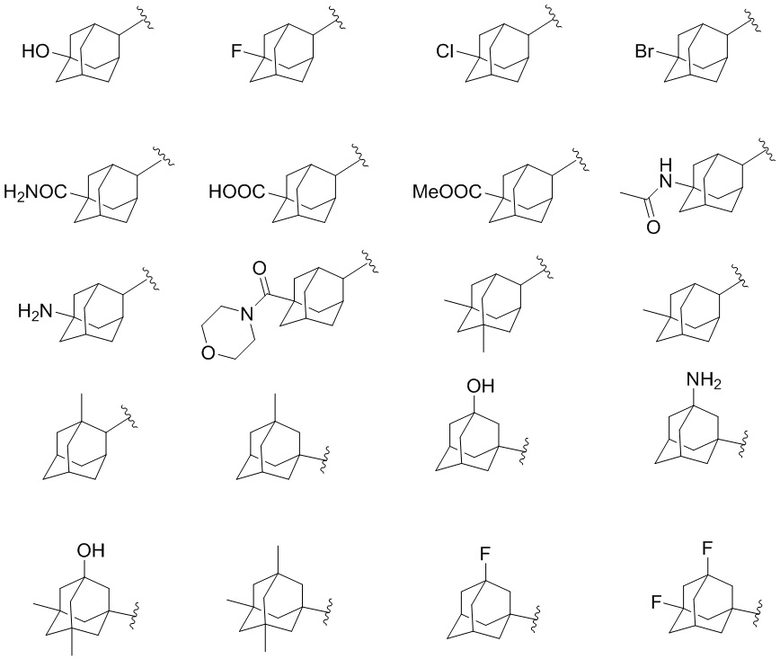
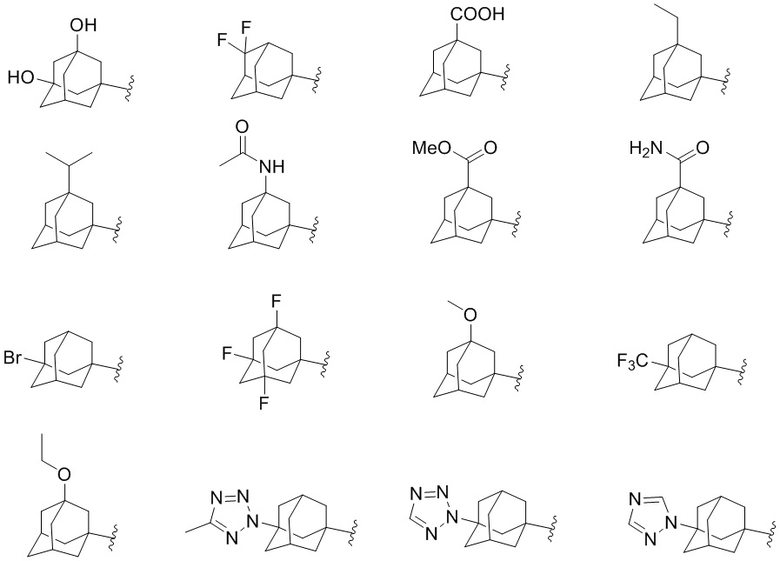
 ,
,  ,
,  ,
,
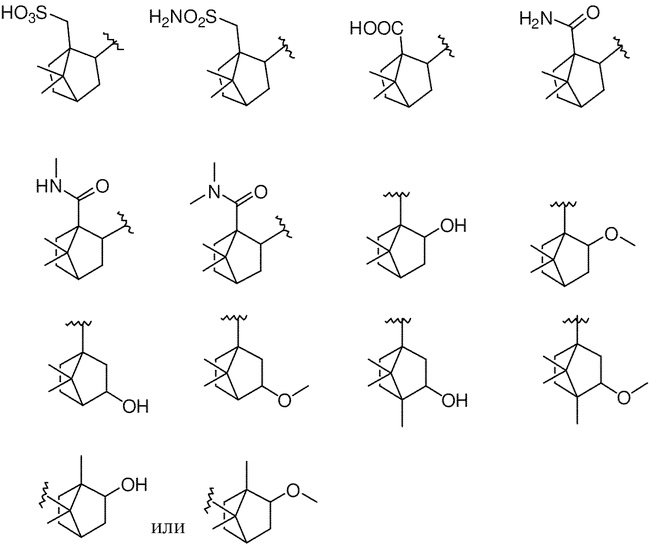 .
.
[1090] В определенных вариантах осуществления предусмотрено соединение формулы, выбранной из:
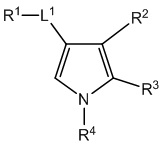 ,
, 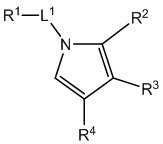 ,
, 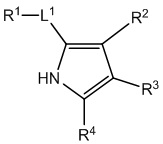 ,
, 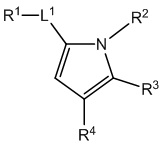 ,
, 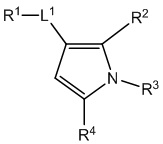 ,
,  ,
, 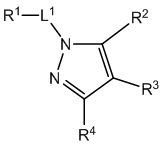 ,
, 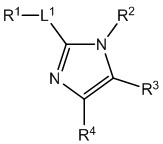 ,
, 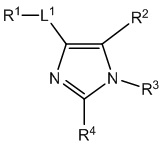 ,
, 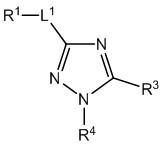 ,
, 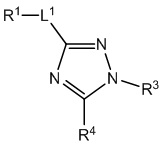 ,
, 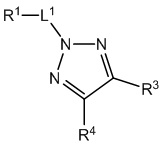 ,
, 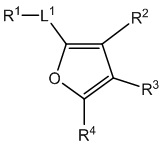 или
или 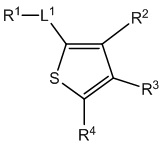 ,
,
или его фармацевтически приемлемая соль, таутомер, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров,
где
R1 представляет собой мостиковый C7-15циклоалкил, необязательно замещенный R1a в количестве от одного до десяти;
каждый R1a независимо выбран из галогена, C1-3алкила, C1-3алкокси и C1-3галогеналкила;
L1 представляет собой *-N(R1b)CO-, *-(CH2)k-N(R1b)CO-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)CO-, *-(CH2)n-(O(CH2)m)p-O(CH2)k-N(R1b)CO-, *-(CH2)m-CO-L1a-CO-, *-(CH2)m-L1a-CO-, *-(CH2)n-NHCONH-(CH2)m-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)-(CH2)m-, *-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-SO2N(R1b)-(CH2)m-, *-(CH2)n-SO2N(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-N(R1b)SO2-(CH2)m-, *-(CH2)n-N(R1b)SO2-(CH2)m-, или *-(CH2)n-OCO-, *-(CH2)n-L1a-(CH2)m-, *-N(R1c)-(CH2)n-N(R1b)-(CH2)m- или *-N(R1c)-(CO)-(CH2)n-N(R1b)-N(R1b)-(CO)-;
* обозначает точку соединения с R1;
L1a представляет собой 5- или 6-членный гетероциклилен;
R1b представляет собой H или C1-3алкил;
R1c представляет собой H или C1-3алкил;
k равняется 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10;
каждый из m, n и p независимо равняется 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10;
R2 отсутствует или представляет собой H, галоген, прямой или разветвленный алкил, необязательно замещенный R2a в количестве от одного до пяти, или циклоалкил, необязательно замещенный R2a в количестве от одного до пяти;
R3 представляет собой прямой или разветвленный алкил, необязательно замещенный R3a в количестве от одного до пяти, циклоалкил, необязательно замещенный R3a в количестве от одного до пяти, арил, необязательно замещенный R3a в количестве от одного до пяти, гетероциклил, необязательно замещенный R3a в количестве от одного до пяти, или гетероарил, необязательно замещенный R3a в количестве от одного до пяти;
R4 представляет собой прямой или разветвленный алкил, необязательно замещенный R4a в количестве от одного до пяти, циклоалкил, необязательно замещенный R4a в количестве от одного до пяти, арил, необязательно замещенный R4a в количестве от одного до пяти, гетероциклил, необязательно замещенный R4a в количестве от одного до пяти, или гетероарил, необязательно замещенный R4a в количестве от одного до пяти;
при условии, что по меньшей мере один из R3 или R4 представляет собой необязательно замещенный арил или необязательно замещенный гетероарил; и
каждый из R2a, R3a или R4a независимо выбран из галогена, -CN, C1-3алкила, C1-3алкокси, C1-3галогеналкила, C3-6циклоалкила, фенила, 3-6-членного гетероциклила и 5-6-членного гетероарила.
[1100] В определенных вариантах осуществления, если R2 присутствует, то он представляет собой H, C1-3алкил или C3-6циклоалкил.
[1110] В определенных вариантах осуществления, если R5 присутствует, то он представляет собой H, C1-3алкил или C3-6циклоалкил.
[1120] В определенных вариантах осуществления R3 представляет собой фенил, необязательно замещенный R3a в количестве от одного до двух. В определенных вариантах осуществления R3 представляет собой пиридил, необязательно замещенный R4a в количестве от одного до двух. В определенных вариантах осуществления R3a независимо представляет собой галоген, CN, метил, метокси или трифторметил. В определенных вариантах осуществления R3a представляет собой хлор. В определенных вариантах осуществления R3 представляет собой 4-хлорфенил или 2,4-дихлорфенил.
[1130] В определенных вариантах осуществления R4 представляет собой фенил, необязательно замещенный R4a в количестве от одного до двух. В определенных вариантах осуществления R4 представляет собой пиридил, необязательно замещенный R4a в количестве от одного до двух. В определенных вариантах осуществления R4a независимо представляет собой галоген, CN, метил, метокси или трифторметил. В определенных вариантах осуществления R4a представляет собой хлор. В определенных вариантах осуществления R4 представляет собой 4-хлорфенил или 2,4-дихлорфенил.
[1140] В определенных вариантах осуществления каждый R2a, R3a или R4a независимо выбран из галогена, -CN, C1-3алкила, C1-3алкокси и C1-3галогеналкила.
[1150] В определенных вариантах осуществления предусмотрено соединение формулы II:
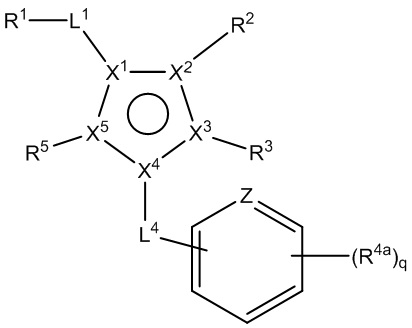 II,
II,
или его фармацевтически приемлемая соль, таутомер, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров,
где
X1, X2, X3, X4, X5, R1, R2, R3, R5, R4a и L1 определены в данном документе,
Z представляет собой CR4a или N;
q равняется 0, 1, 2 или 3; и
L4 представляет собой связь или CH2.
[1160] В определенных вариантах осуществления предусмотрено соединение формулы III:
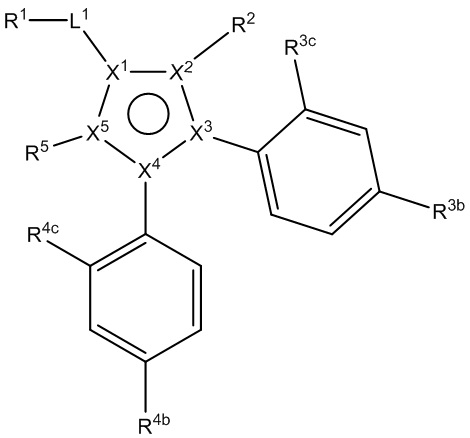 III,
III,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров,
где
X1, X2, X3, X4, X5, R1, R2, R3, R4, R5, R4a и L1 определены в данном документе,
каждый R3b и R3c независимо представляет собой H или R3a; и
каждый R4b и R4c независимо представляет собой H или R4a.
[1170] В определенных вариантах осуществления по меньшей мере один из R3b, R3c, R4b и R4c выбран из F, Cl, CN, метила, метокси или трифторметила. В определенных вариантах осуществления по меньшей мере два из R3b, R3c, R4b и R4c выбраны из F, Cl, CN, метила, метокси или трифторметила. В определенных вариантах осуществления по меньшей мере три из R3b, R3c, R4b и R4c выбраны из F, Cl, CN, метила, метокси или трифторметила. В определенных вариантах осуществления R3c представляет собой H, и R3b, R4b и R4c выбраны из F, Cl, CN, метила, метокси или трифторметила. В определенных вариантах осуществления R3c представляет собой H, и R3b, R4b и R4c представляют собой Cl.
[1180] В определенных вариантах осуществления предусмотрено соединение, представленное формулой I-C:
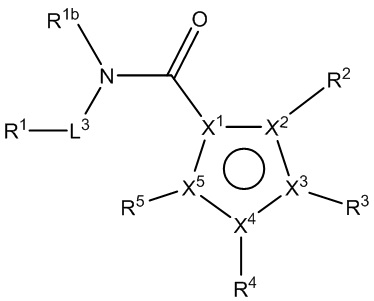 I-C,
I-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где L3 представляет собой *-(CH2)n-, *-(CH2)n-N(R1c)-(CH2)k- или *-(CH2)n-(O(CH2)m)p-O(CH2)k-, и каждый из m, n, k, p, X1, X2, X3, X4, X5, R1, R1b, R1c, R2, R3, R4 и R5 определен в данном документе.
[1190] В определенных вариантах осуществления предусмотрено соединение, представленное формулой II-C:
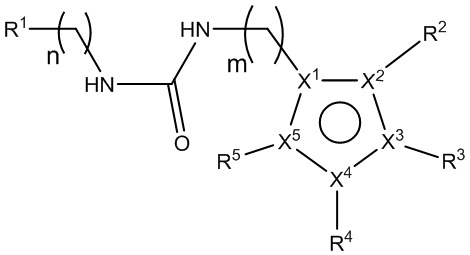 II-C,
II-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где каждый из m, n, X1, X2, X3, X4, X5, R1, R2, R3, R4 и R5 определен в данном документе.
[1200] В определенных вариантах осуществления предусмотрено соединение, представленное формулой III-C:
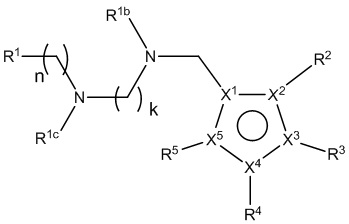 III-C,
III-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где каждый из k, n, X1, X2, X3, X4, X5, R1b, R1c, R1, R2, R3, R4 и R5 определен в данном документе.
[1210] В определенных вариантах осуществления предусмотрено соединение, представленное формулой IV-C:
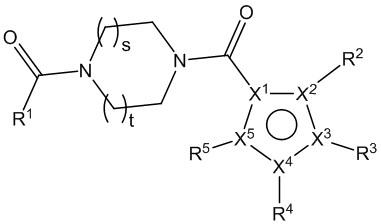 IV-C,
IV-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где s и t независимо равняются 0, 1 или 2, и каждый из X1, X2, X3, X4, X5, R1, R2, R3, R4 и R5 определен в данном документе. В определенных вариантах осуществления каждый из s и t равняется 1.
[1220] В определенных вариантах осуществления предусмотрено соединение, представленное формулой V-C:
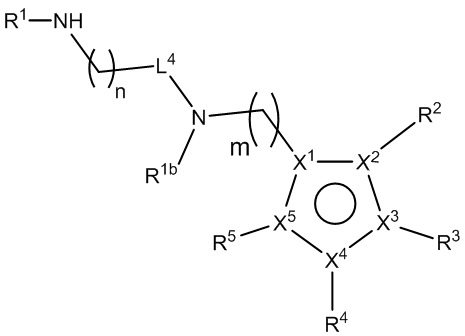 V-C,
V-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где L4 представляет собой CO или SO2, и каждый из m, n, X1, X2, X3, X4, X5, R1b, R1, R2, R3, R4 и R5 определен в данном документе.
[1230] В определенных вариантах осуществления предусмотрено соединение, представленное формулой VI-C:
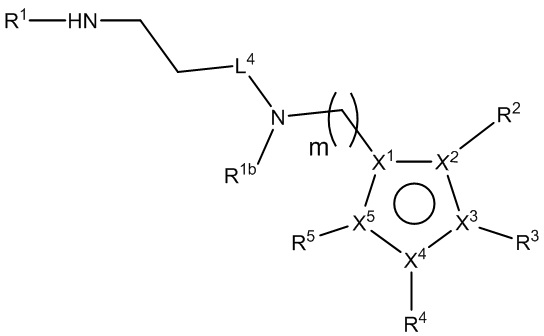 VI-C,
VI-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где L4 представляет собой CO или SO2, и каждый из m, X1, X2, X3, X4, X5, R1b, R1, R2, R3, R4 и R5 определен в данном документе.
[1240] В определенных вариантах осуществления предусмотрено соединение, представленное формулой VII-C:
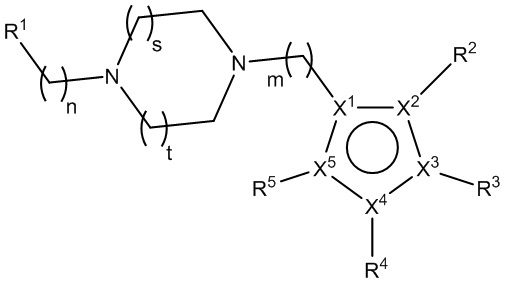 VII-C,
VII-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где каждый из m, n, s, t, X1, X2, X3, X4, X5, R1, R2, R3, R4 и R5 определен в данном документе.
[1250] В определенных вариантах осуществления предусмотрено соединение, представленное формулой VIII-C:
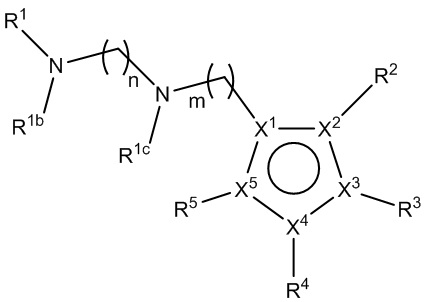 VIII-C,
VIII-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где каждый из m, n, X1, X2, X3, X4, X5, R1b, R1c, R1, R2, R3, R4 и R5 определен в данном документе.
[1260] В определенных вариантах осуществления предусмотрено соединение, представленное формулой IX-C:
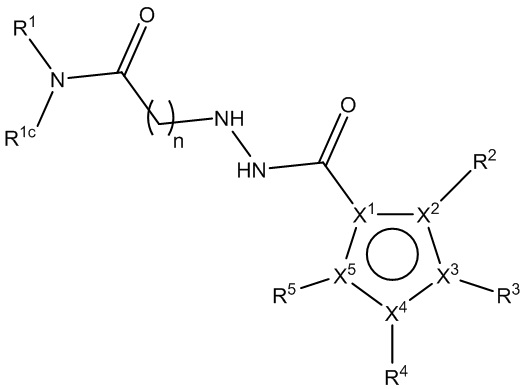 IX-C,
IX-C,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где каждый из n, X1, X2, X3, X4, X5, R1c, R1, R2, R3, R4 и R5 определен в данном документе.
[1270] В определенных вариантах осуществления в данном документе предусмотрено соединение, представленное любой одной или более из формул I-C-IX-C, в том числе любыми двумя, любыми тремя, любыми четырьмя, любыми пятью, любыми шестью, любыми семью, любыми восемью или всеми из формул I-C-IX-C, описанных в данном документе.
[1280] В определенных вариантах осуществления предусмотрено соединение формулы:
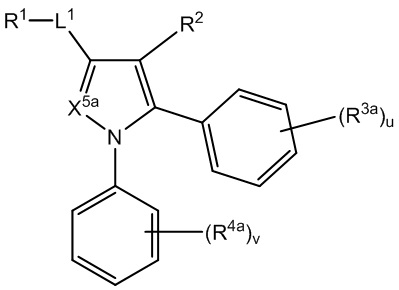 ,
,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где X5a представляет собой N или CH, каждый из u и v независимо равняется 0, 1, 2, 3, 4 или 5, R2 представляет собой H, C1-3алкил или C3-6циклоалкил, каждый из L1, R1, R2, R3a и R4a определен в данном документе.
[1290] Предусмотрено соединение, выбранное из
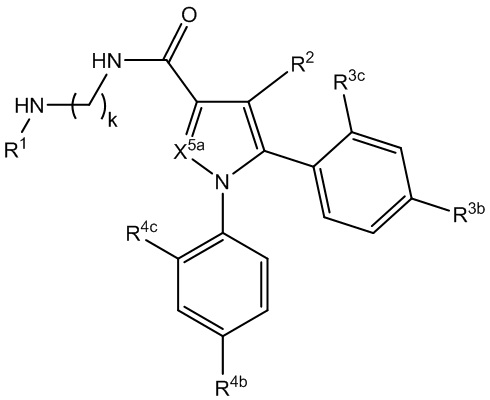 ,
, 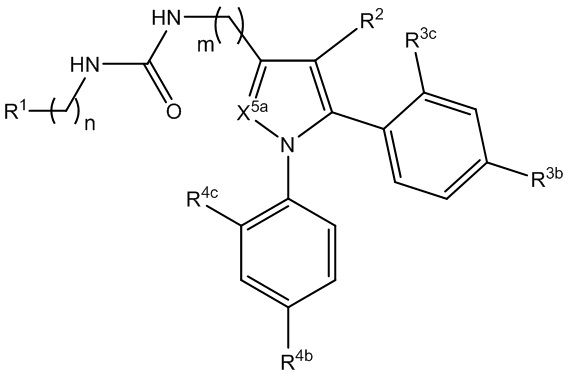 ,
,
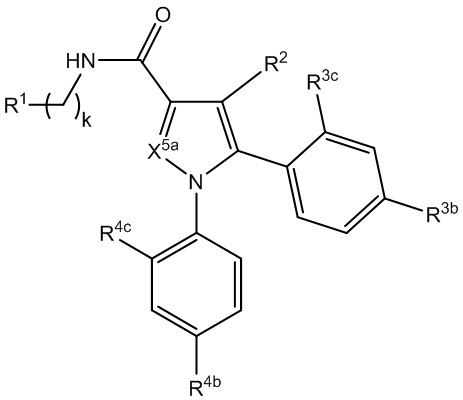 ,
, 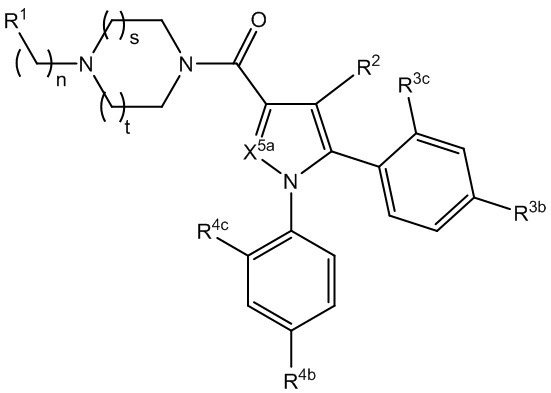 ,
, 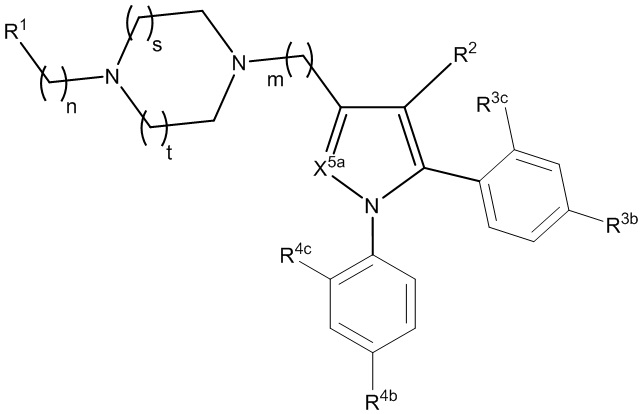 ,
, 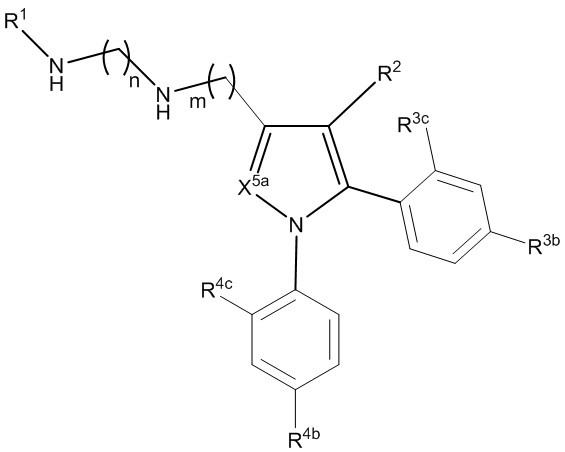
или 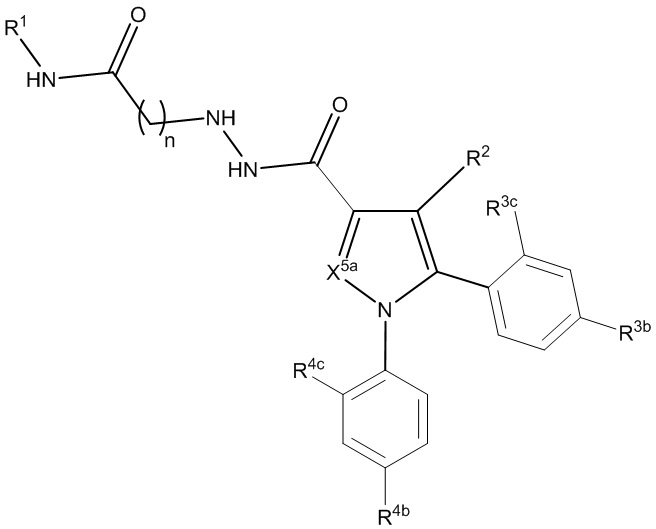 ,
,
или его фармацевтически приемлемая соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров, где X5a представляет собой N или CH, R2 представляет собой H, C1-3алкил или C3-6циклоалкил, каждый из k, m, n, s, t, R1, R3b, R3c, R4b и R4c определен в данном документе.
[1300] В определенных вариантах осуществления в данном документе предусмотрено соединение, выбранное из таблицы 1 ниже, или его фармацевтически приемлемая соль, сольват, таутомер, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров. В определенных вариантах осуществления в данном документе предусмотрено соединение, выбранное из раздела «Примеры» в данном документе, или его фармацевтически приемлемая соль, сольват, таутомер, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров.
Таблица 1
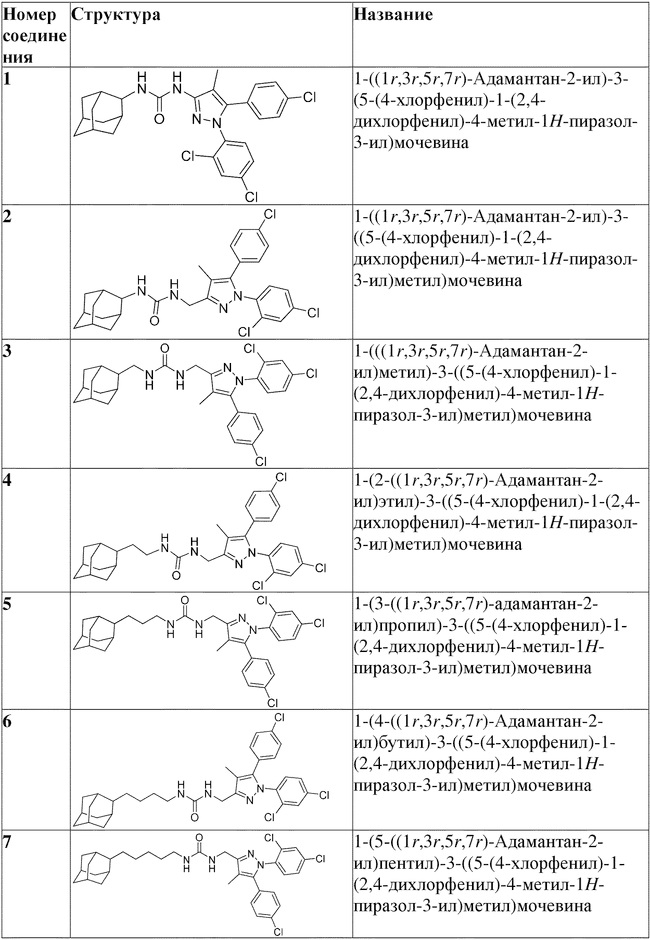
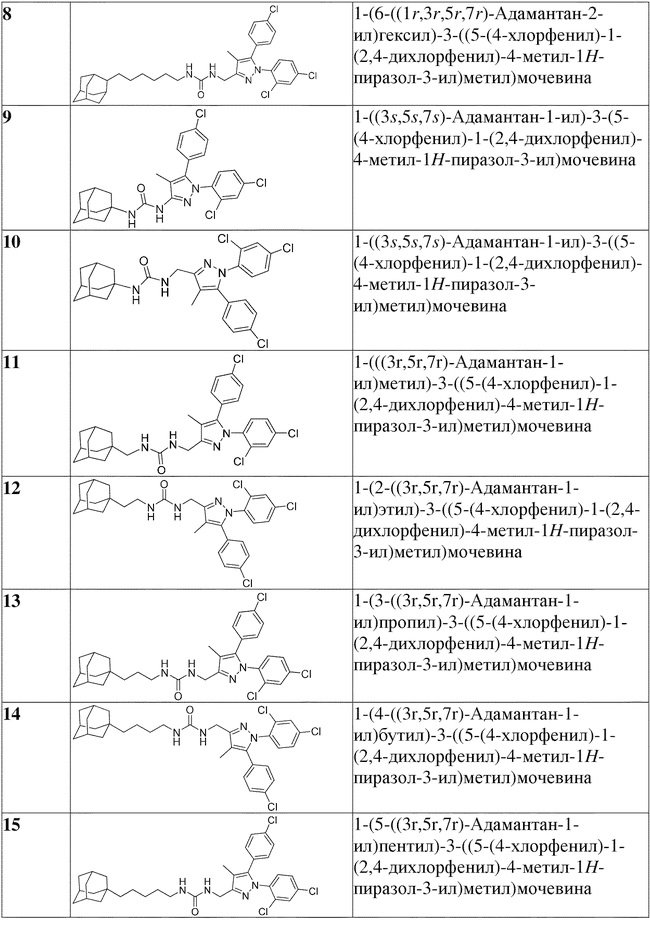
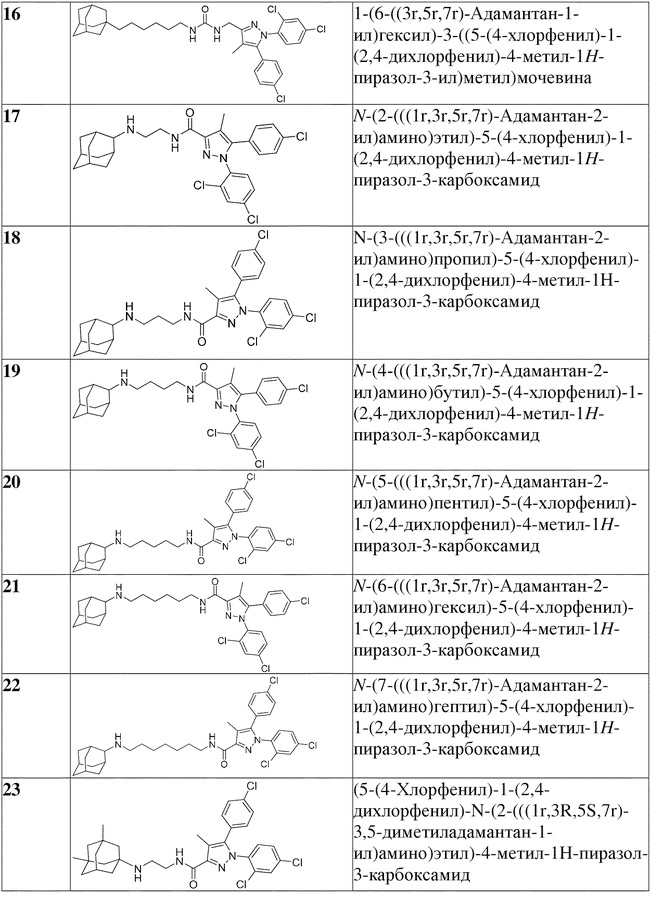
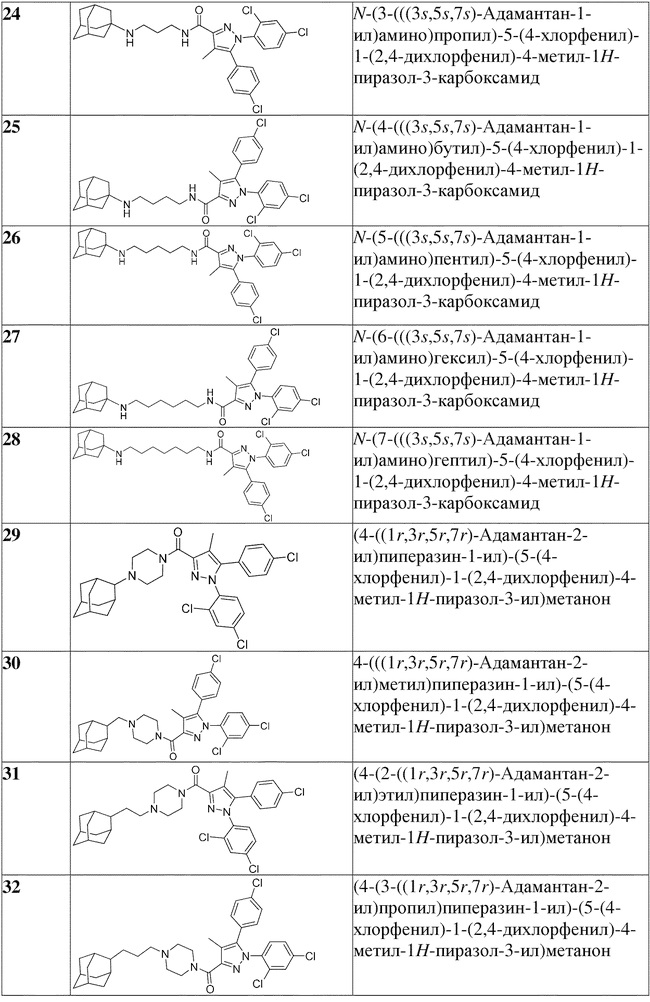
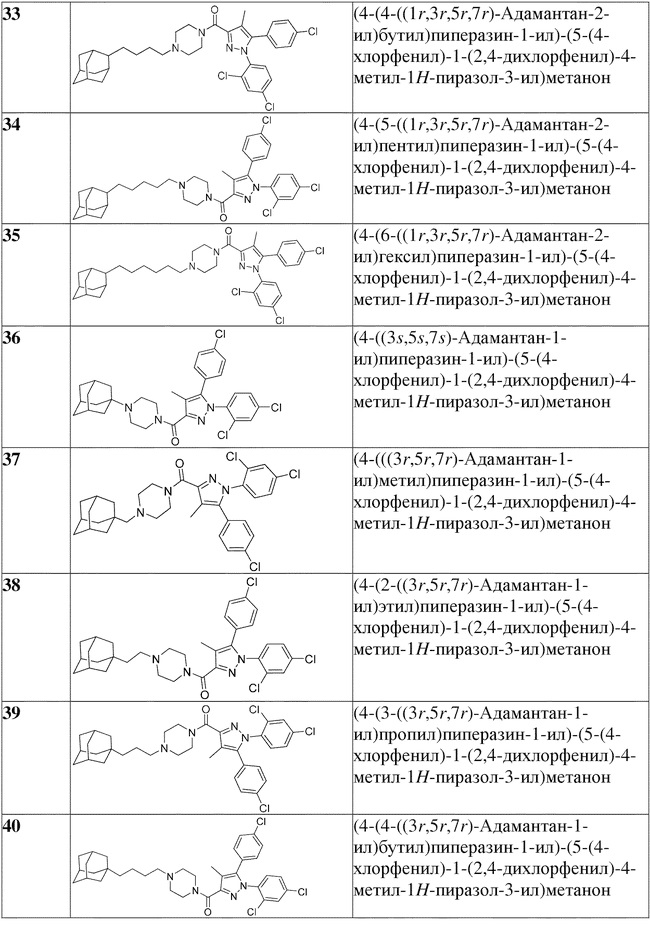
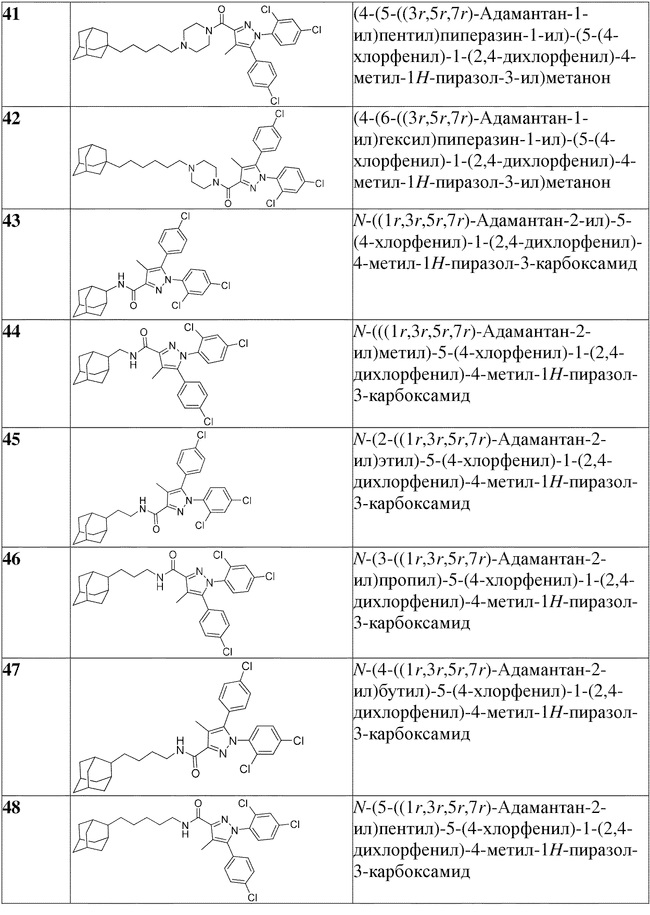
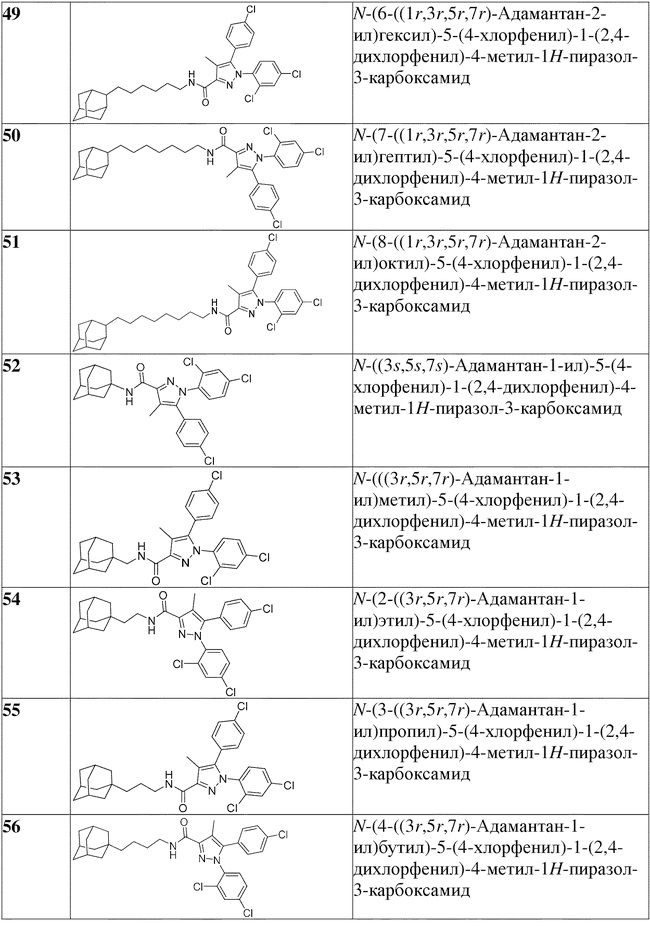
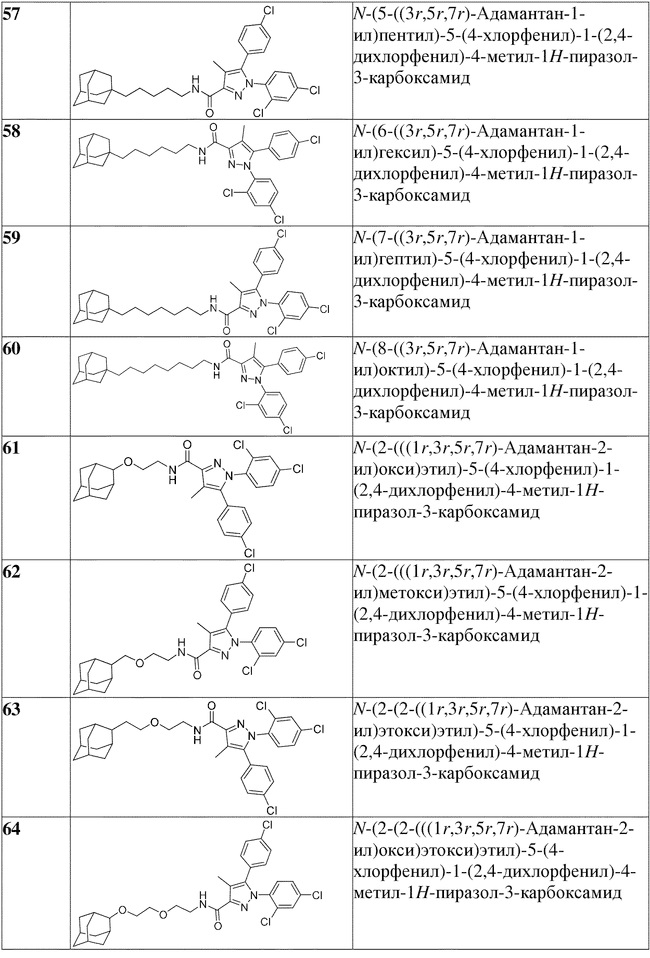
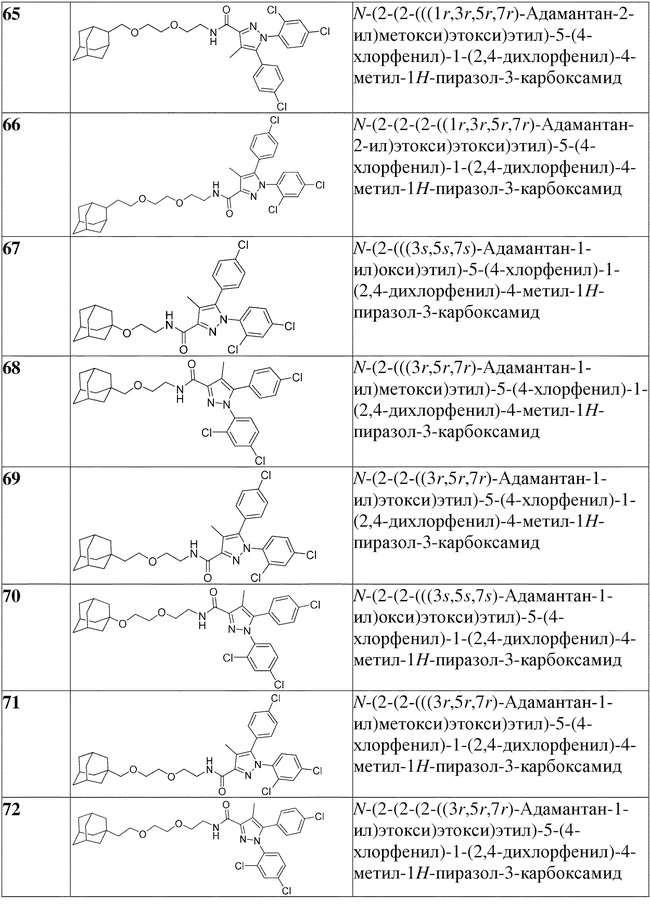
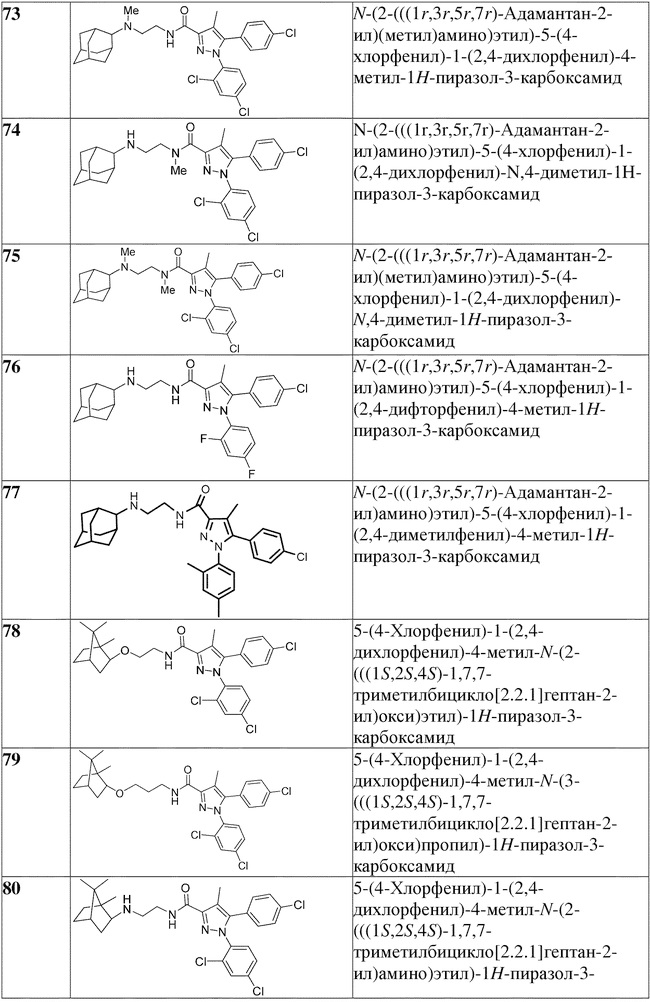
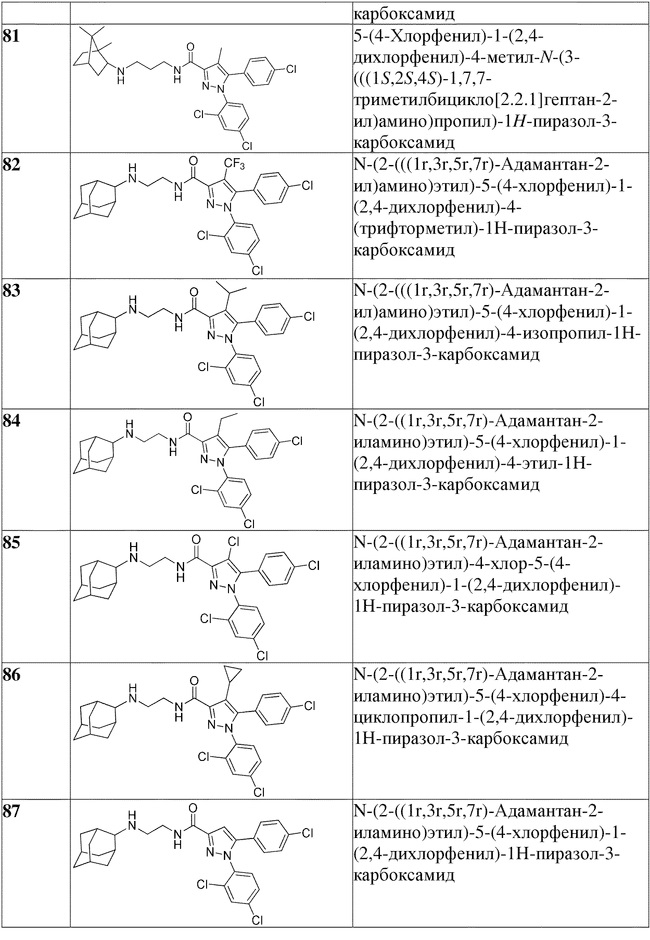
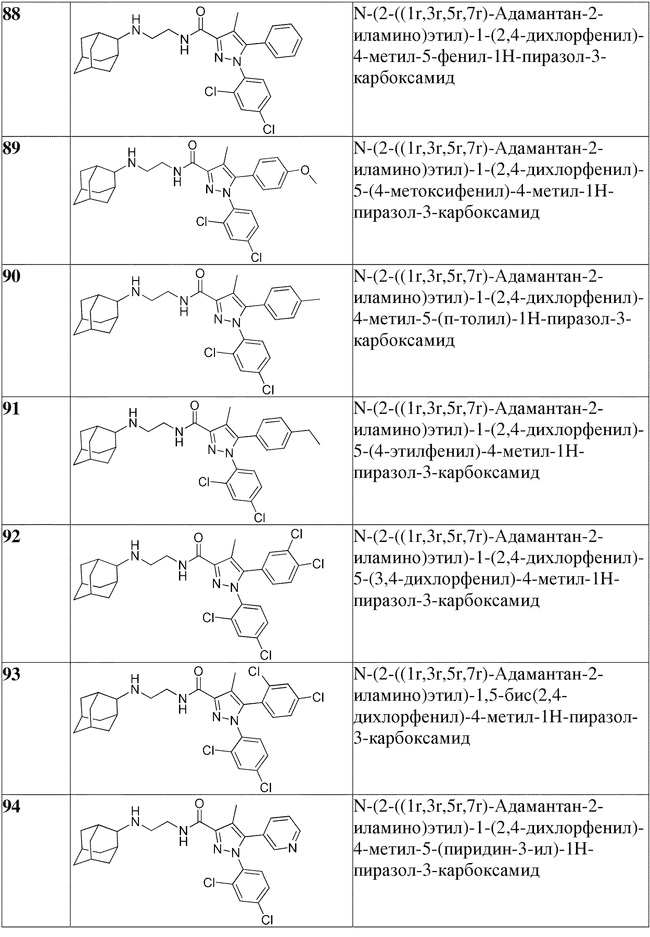
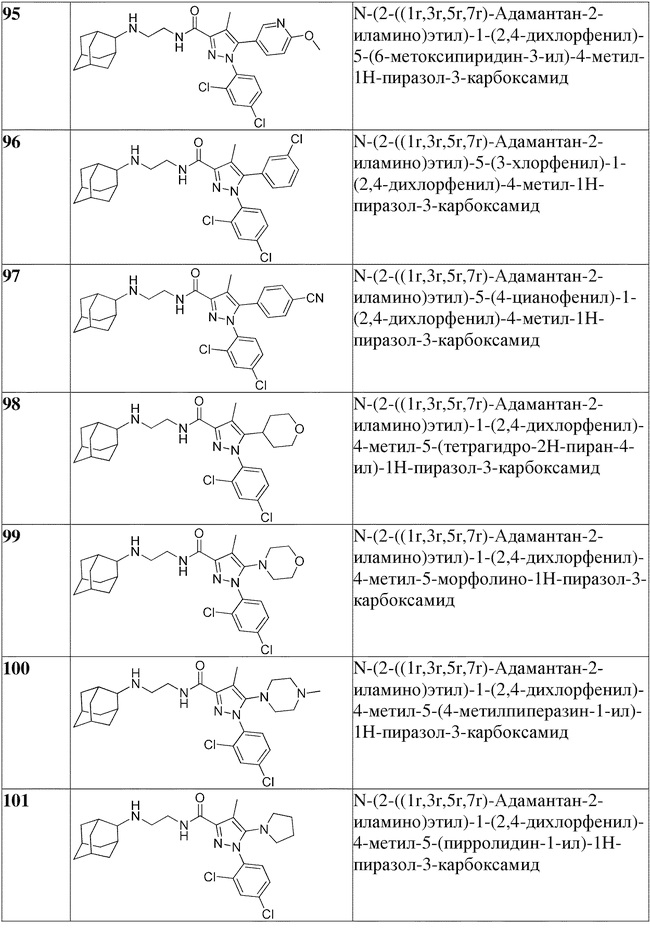
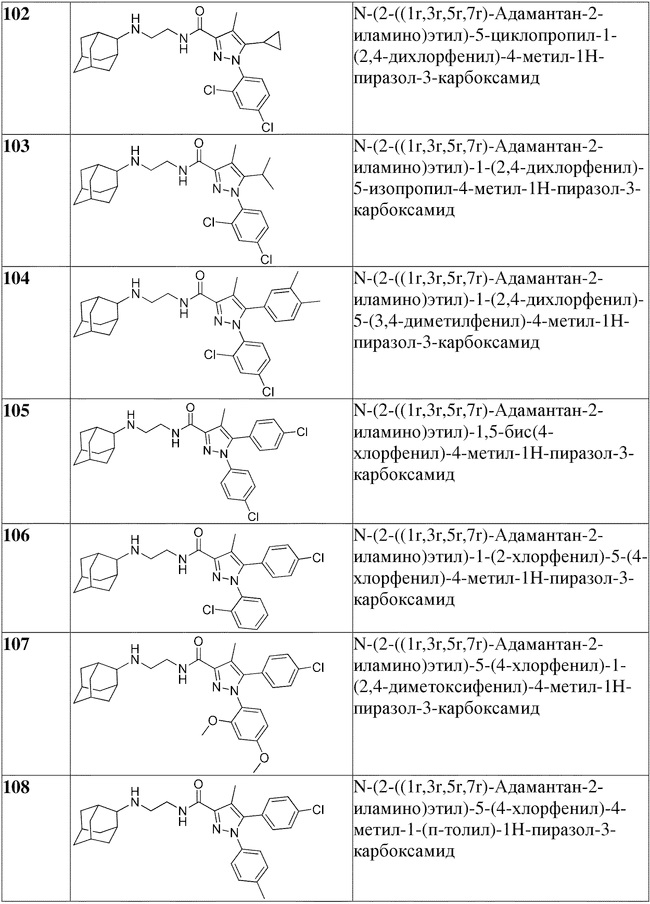
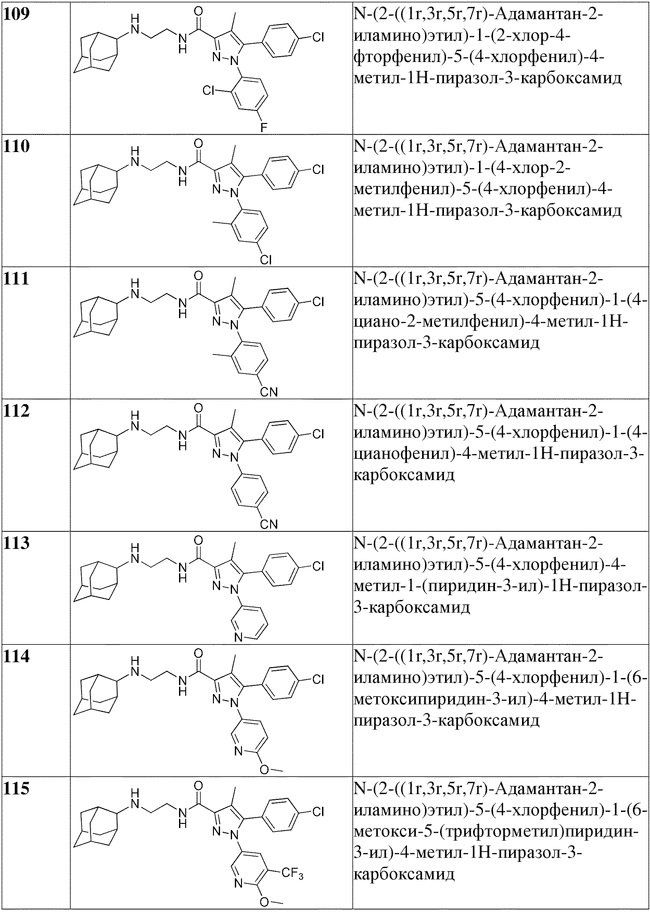
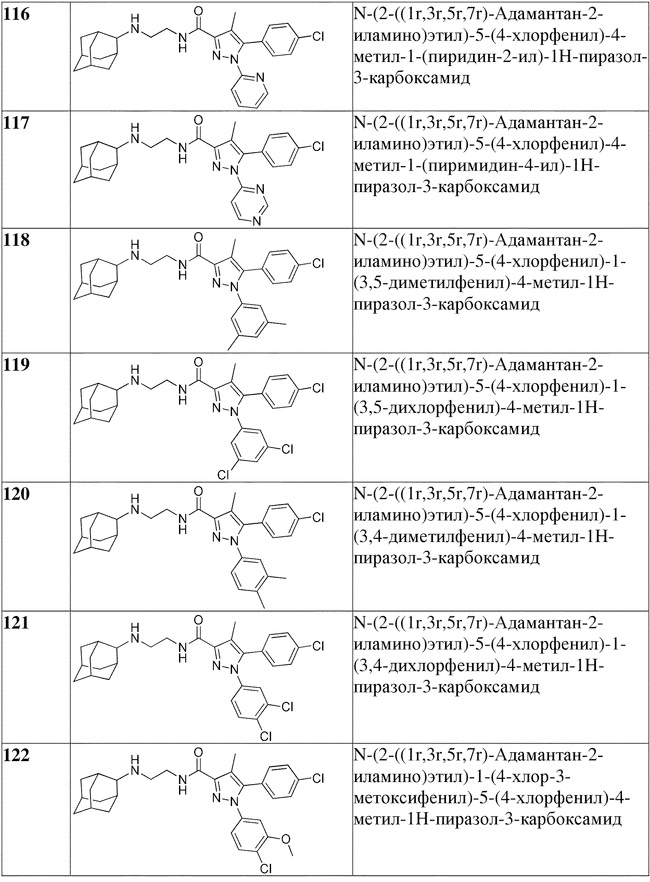
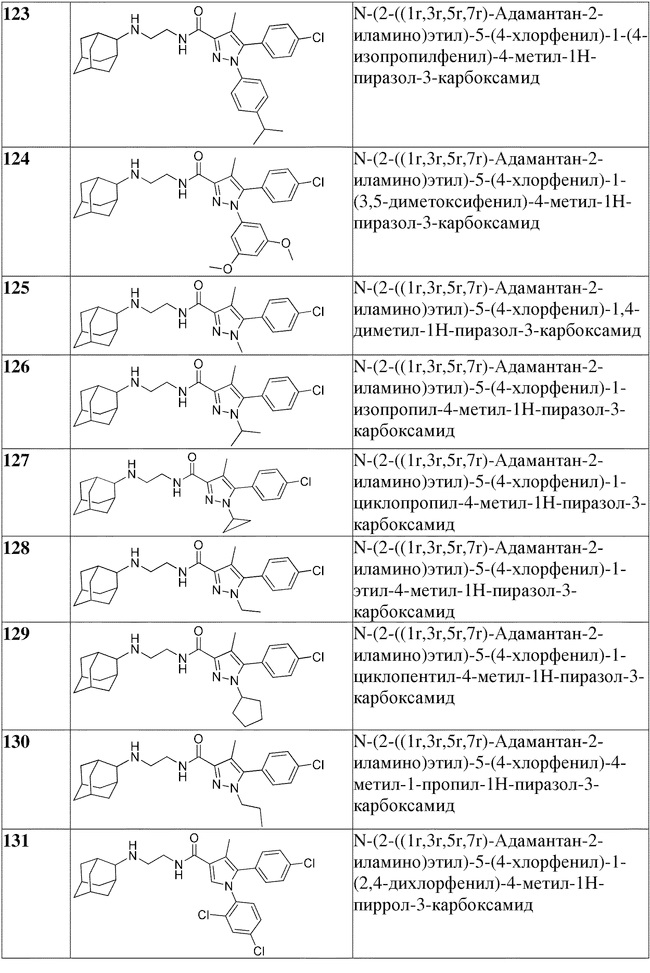
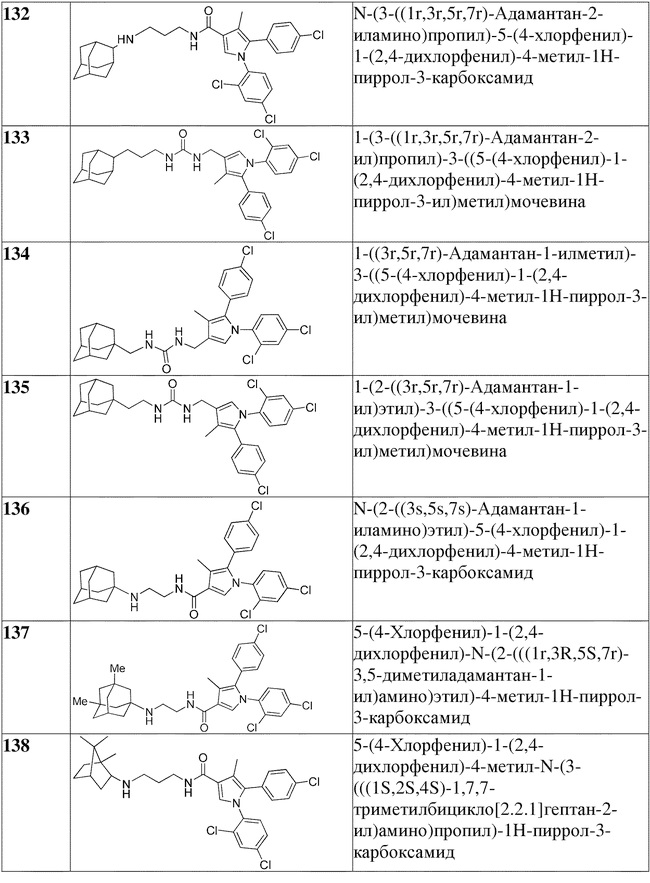
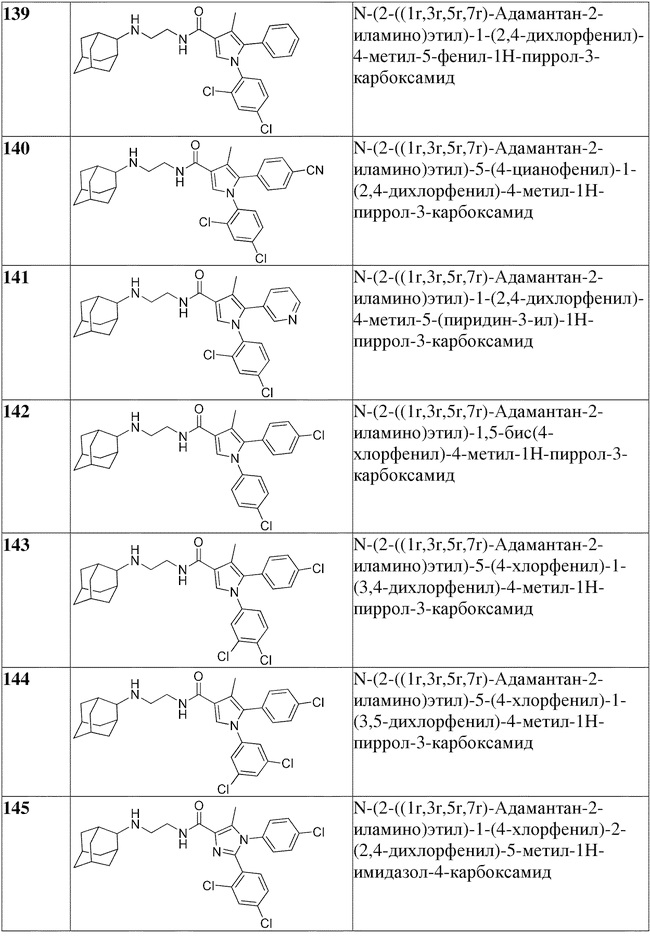
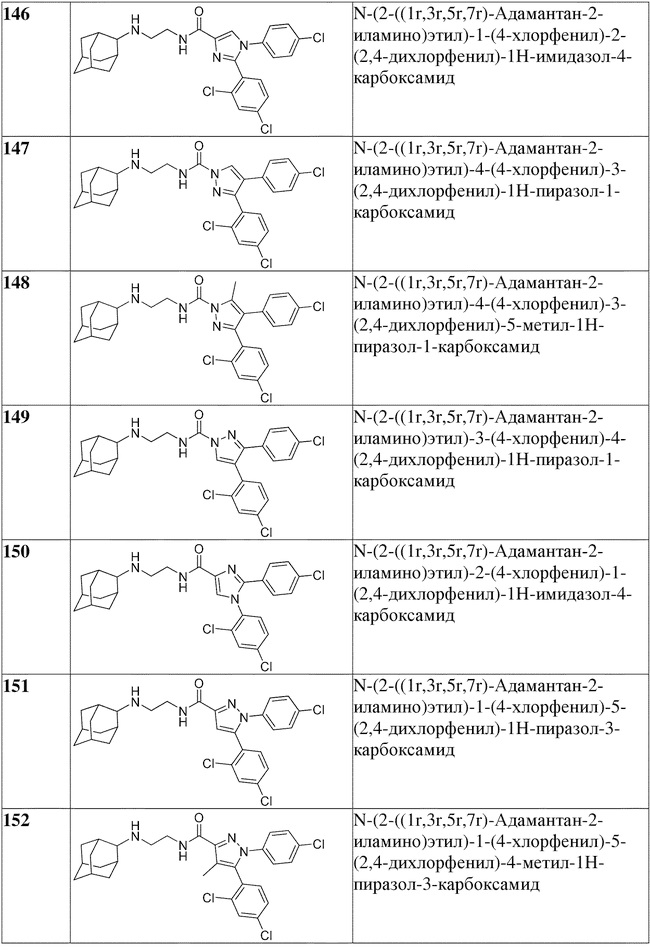
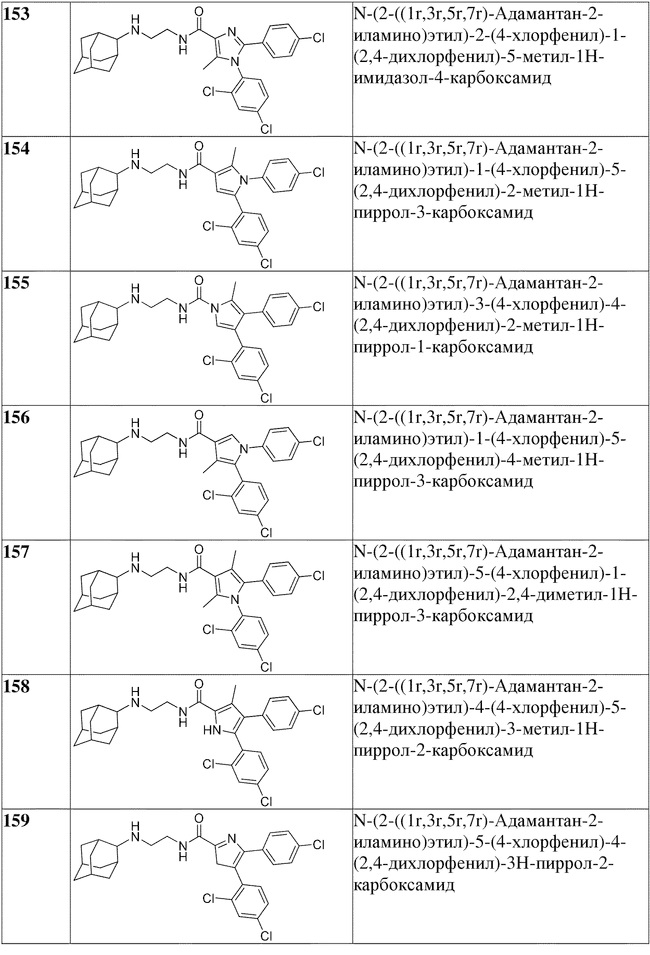
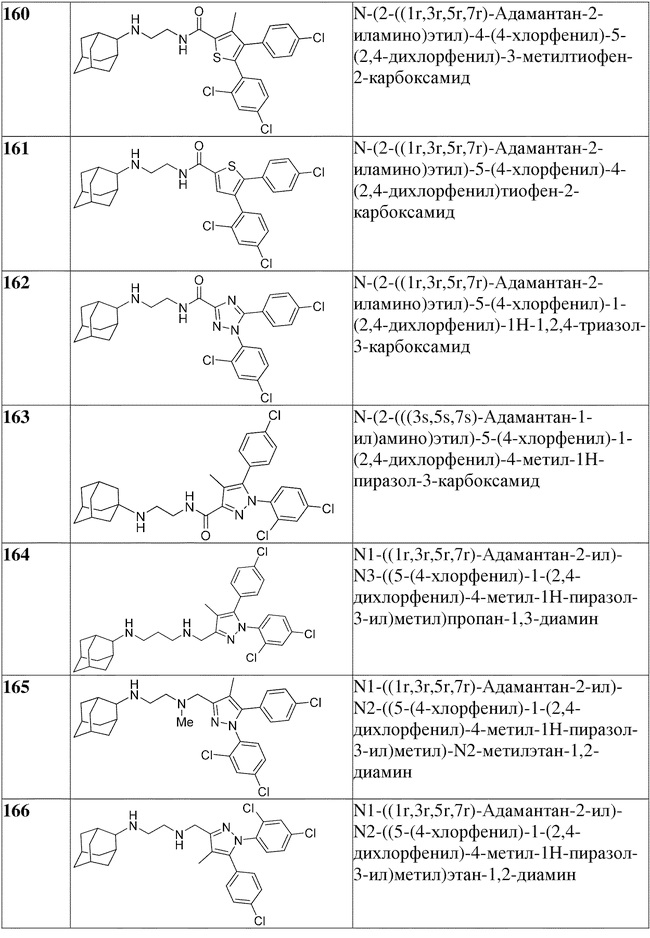
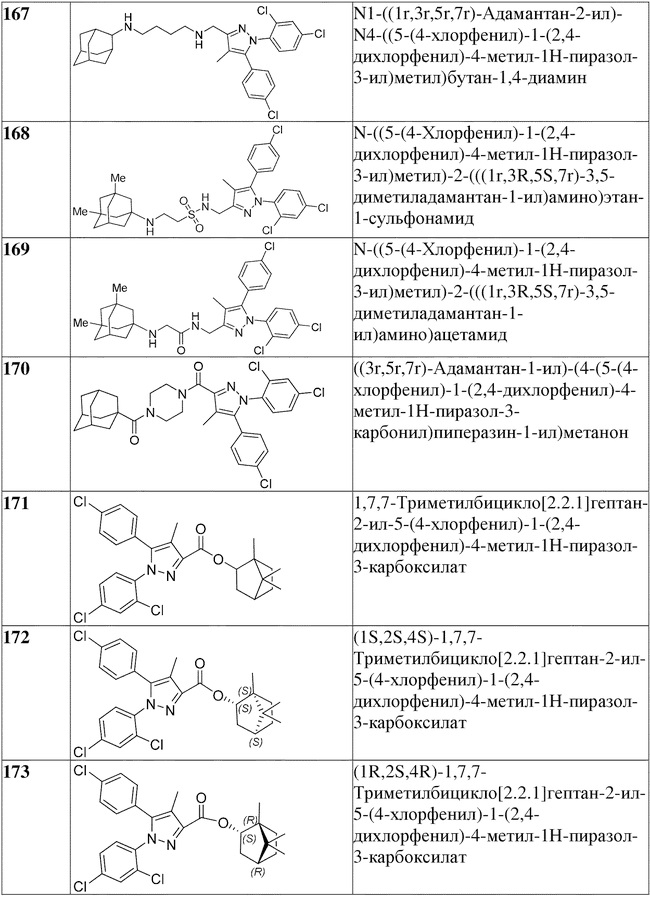
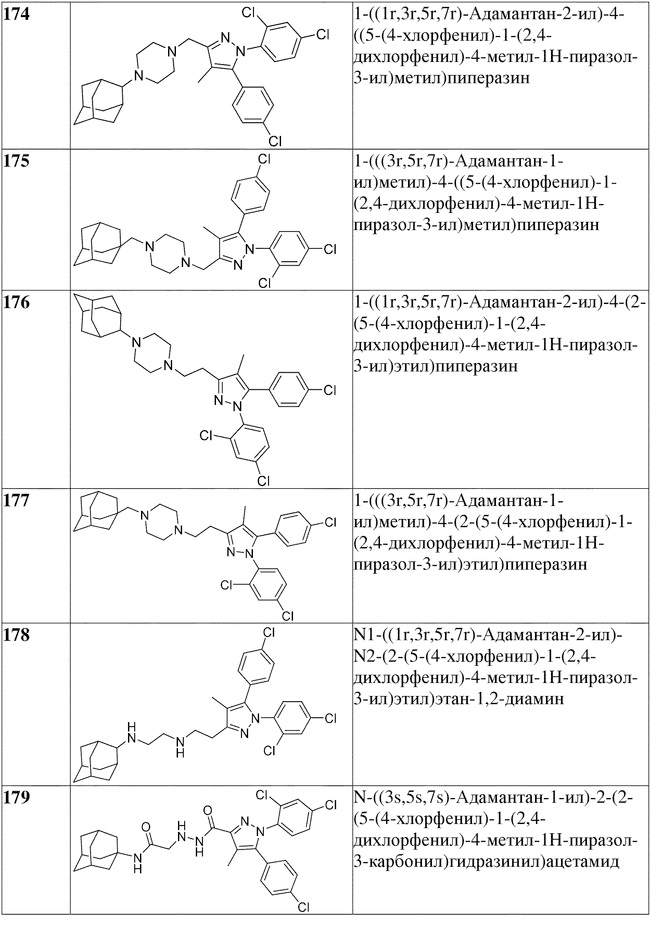
3. Способы и пути применения
[1310] В определенных вариантах осуществления соединения, описанные в данном документе, применяют при лечении заболевания или состояния, такого как инфекция.
[1320] «Лечение» или «осуществление лечения» представляет собой подход к получению благоприятных или желательных результатов, включающих клинические результаты. Благоприятные или желательные клинические результаты могут включать один или более из следующего: a) подавление заболевания или состояния (например, уменьшение выраженности одного или более симптомов, обусловленных заболеванием или состоянием, и/или уменьшение степени заболевания или состояния); b) замедление или остановка развития одного или более клинических симптомов, связанных с заболеванием или состоянием (например, стабилизация заболевания или состояния, предупреждение или замедление ухудшения или прогрессирования заболевания или состояния и/или предупреждение или замедление распространения (например, метастазов) заболевания или состояния); и/или c) облегчение заболевания, а именно, вызывание регрессии клинических симптомов (например, облегчение статуса заболевания, обеспечение частичной или полной ремиссии заболевания или состояния, усиление эффекта другого лекарственного средства, замедление прогрессирования заболевания, повышение качества жизни и/или продление жизни.
[1330] Термин «предупреждение» или «осуществление предупреждения» обозначает любое лечение заболевания или состояния, которое предотвращает развитие клинических симптомов заболевания или состояния. В некоторых вариантах осуществления соединения могут вводиться субъекту (в том числе человеку), имеющему риск развития или семейный анамнез заболевания или состояния.
[1340] Термин «субъект» означает животное, такое как млекопитающее (в том числе человек), которое являлось или будет являться объектом лечения, наблюдения или эксперимента. Способы, описанные в данном документе, могут быть пригодными в путях практического применения в терапии человека и/или в ветеринарии. В некоторых вариантах осуществления субъектом является млекопитающее. В определенных вариантах осуществления субъектом является человек.
[1350] Термин «терапевтически эффективное количество» или «эффективное количество» соединения, описанного в данном документе (которое может быть представлено в форме его фармацевтически приемлемой соли, обогащенного изотопом аналога, стереоизомера или смеси стереоизомеров), означает количество, достаточное для осуществления лечения при введении субъекту, для обеспечения терапевтического эффекта, такого как уменьшение интенсивности симптомов или замедление прогрессирования заболевания. Например, терапевтически эффективное количество может представлять собой количество, достаточное для уменьшения выраженности симптома заболевания или состояния, описанного в данном документе. Терапевтически эффективное количество может варьировать в зависимости от субъекта и заболевания или состояния, подлежащих лечению, веса и возраста субъекта, степени тяжести заболевания или состояния, а также способа введения, что может быть легко определено специалистом средней квалификации в данной области техники.
[1360] В некоторых вариантах осуществления предусмотрено соединение, описанное в данном документе, для предупреждения и/или лечения инфекции, вызванной микроорганизмом, экспрессирующим мембранные белки микобактерий large 3 (MmpL3), или заболевания, обусловленного такой инфекцией. В некоторых вариантах осуществления предусмотрено соединение, описанное в данном документе, для предупреждения и/или лечения микобактериальной инфекции или заболевания, обусловленного инфекцией. В некоторых вариантах осуществления микобактериальная инфекция включает без ограничения инфекцию, вызванную Mycobacterium tuberculosis, инфекцию, вызванную Mycobacterium leprae, инфекцию, вызванную Mycobacterium ulcerans, инфекцию, вызванную Mycobacterium abscessus, инфекцию, вызванную Mycobacterium bovis, и инфекцию, вызванную Mycobacterium marine.
[1370] В некоторых вариантах осуществления заболевание включает без ограничения туберкулез, обусловленный инфекцией, вызванной Mycobacterium tuberculosis, лепру, обусловленную Mycobacterium leprae, язву Бурули, обусловленную Mycobacterium ulcerans, инфекционное заболевание, обусловленное инфекцией, вызванной Mycobacterium abscessus, инфекционное заболевание, обусловленное инфекцией, вызванной Mycobacterium bovis, или инфекционное заболевание, обусловленное инфекцией, вызванной Mycobacterium marine.
[1380] В некоторых вариантах осуществления в данном документе предусмотрены способы лечения или предупреждения инфекции, вызванной микроорганизмом, экспрессирующим мембранные белки микобактерий large 3 (MmpL3), у субъекта, нуждающегося в этом, предусматривающие введение субъекту терапевтически эффективного количества соединения, описанного в данном документе. В дополнительном аспекте настоящего изобретения также предусмотрен способ лечения или предупреждения микобактериальной инфекции или заболевания, обусловленного инфекцией, у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения, описанного в данном документе.
[1390] В некоторых вариантах осуществления микобактериальные инфекции включают без ограничения инфекцию, вызванную Mycobacterium tuberculosis, инфекцию, вызванную Mycobacterium leprae, инфекцию, вызванную Mycobacterium ulcerans, инфекцию, вызванную Mycobacterium abscessus, инфекцию, вызванную Mycobacterium bovis, или инфекцию, вызванную Mycobacterium marine. В некоторых вариантах осуществления заболевание представляет собой лепру, обусловленную Mycobacterium leprae, язву Бурули, обусловленную Mycobacterium ulcerans, инфекционные заболевания, обусловленные инфекцией, вызванной Mycobacterium abscessus, инфекцией, вызванной Mycobacterium bovis, и инфекционные заболевания, обусловленные инфекцией, вызванной Mycobacterium marine.
[1400] В некоторых вариантах осуществления в данном документе предусмотрено применение соединения, описанного в данном документе, в способе лечения инфекции, вызванной микроорганизмом, экспрессирующим мембранные белки микобактерий large 3 (MmpL3), у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения, описанного в данном документе.
[1410] В некоторых вариантах осуществления в данном документе предусмотрено применение соединения, описанного в данном документе, для изготовления лекарственного препарата для лечения инфекции, вызванной микроорганизмом, экспрессирующим мембранные белки микобактерий large 3 (MmpL3), у субъекта.
[1420] В некоторых вариантах осуществления микроорганизм представляет собой микобактерии. В некоторых вариантах осуществления микобактериальные инфекции включают без ограничения инфекцию, вызванную Mycobacterium tuberculosis, инфекцию, вызванную Mycobacterium leprae, инфекцию, вызванную Mycobacterium ulcerans, инфекцию, вызванную Mycobacterium abscessus, инфекцию, вызванную Mycobacterium bovis, или инфекцию, вызванную Mycobacterium marine. В некоторых вариантах осуществления заболевание представляет собой лепру, обусловленную Mycobacterium leprae, язву Бурули, обусловленную Mycobacterium ulcerans, инфекционные заболевания, обусловленные инфекцией, вызванной Mycobacterium abscessus, Mycobacterium bovis, и инфекционные заболевания, обусловленные инфекцией, вызванной Mycobacterium marine.
[1430] В некоторых вариантах осуществления микроорганизм представляет собой Mycobacterium tuberculosis.
[1440] В некоторых вариантах осуществления субъект страдает туберкулезом или лепрой.
[1450] В некоторых вариантах осуществления субъект представляет собой человека.
[1460] Способы или пути применения, описанные в данном документе, могут применяться в отношении популяций клеток in vivo или ex vivo. Термин «in vivo» означает в пределах организма живого индивидуума, как, например, в пределах организма животного или человека. В данном контексте способы, описанные в данном документе, могут применяться в качестве терапии у индивидуума. Термин «ex vivo» означает за пределами организма живого индивидуума. Примеры популяций клеток ex vivo включают культуры клеток и биологические образцы in vitro, включающие образцы биологической жидкости или ткани, полученные от индивидуумов. Такие образцы можно получать с помощью способов, общеизвестных из уровня техники. Иллюстративные образцы биологической жидкости включают кровь, спинномозговую жидкость, мочу и слюну. В данном контексте соединения и композиции, описанные в данном документе, можно применять для разнообразных целей, в том числе для терапевтических и экспериментальных целей. Например, соединения и композиции, описанные в данном документе, можно применять ex vivo для определения активности соединения по настоящему изобретению в отношении заданного показания, типа клеток, индивидуума и других параметров. Информация, полученная в ходе такого применения, может применяться для экспериментальных целей или в клинической практике для установления протоколов лечения in vivo. Другие пути применения ex vivo, для которых соединения и композиции, описанные в данном документе, могут являться подходящими, описаны ниже или будут очевидны специалистам в данной области техники.
[1470] Введение одного или более соединений, описанных в данном документе, может привести к по меньшей мере 10% уменьшению (например, по меньшей мере 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или даже 100% уменьшению в отношении инфекции, описанной в данном документе, заболевания, обусловленного инфекцией, или симптома заболевания, как, например, величины бактериальной нагрузки у субъекта.
4. Наборы
[1480] В данном документе также предусмотрены наборы, которые содержат соединение по настоящему изобретению (в том числе фармацевтически приемлемую соль, обогащенный изотопом аналог, стереоизомер или смесь стереоизомеров соединения) и подходящую упаковку. В некоторых вариантах осуществления набор дополнительно содержит инструкции по применению. В одном аспекте набор содержит соединение по настоящему изобретению, а также этикетку и/или инструкции по применению соединений при лечении показаний, в том числе заболеваний или состояний, описанных в данном документе.
[1490] В данном документе также предусмотрены готовые изделия, которые включают соединение, описанное в данном документе, в подходящем контейнере. Контейнер может представлять собой флакон, сосуд, ампулу, предварительно заполненный шприц и пакет для раствора для внутривенного введения.
5. Фармацевтические композиции и способы введения
[1500] Соединения, предусмотренные в данном документе, обычно вводят в форме фармацевтических композиций. Таким образом, в данном документе также предусмотрены фармацевтические композиции, которые содержат одно или более из соединений, описанных в данном документе (которые могут быть представлены в форме их фармацевтически приемлемой соли, стереоизомера, смеси стереоизомеров), и одна или более фармацевтически приемлемых сред-носителей, выбранных из носителей, вспомогательных средств и вспомогательных веществ. Подходящие фармацевтически приемлемые носители могут включать, например, инертные твердые разбавители и наполнители, разбавители, в том числе стерильный водный раствор и разнообразные органические растворители, усилители проницаемости, солюбилизаторы и вспомогательные средства. Такие композиции получают с помощью способа, общеизвестного в области фармации. См., например, Remington’s Pharmaceutical Sciences, Mace Publishing Co., Филадельфия, Пенсильвания. 17th Ed. (1985); и Modern Pharmaceutics, Marcel Dekker, Inc. 3rd Ed. (G.S. Banker and C.T. Rhodes, Eds.). Композиции могут содержать от приблизительно 0,1% до приблизительно 90% соединения, раскрытого в данном документе, в пересчете на общий вес композиции.
[1510] Фармацевтические композиции могут вводиться либо в виде однократной дозы, либо в виде многократных доз. Фармацевтическая композиция, содержащая соединения, описанные в данном документе, может быть получена для подходящего пути введения (в том числе без ограничения интраназального введения, ингаляционного введения, местного введения, перорального введения, введения через слизистую оболочку полости рта, ректального введения, внутриплеврального введения, внутрибрюшинного введения, вагинального введения, внутримышечного введения, подкожного введения, трансдермального введения, эпидурального введения, интратекального введения и внутривенного введения). Подходящие формы препаратов включают составы в виде спрея, пластыри, таблетки, капсулы, драже, пастилки для рассасывания, порошки, гранулы, порошки или жидкие препараты (например, суспензии, растворы, эмульсии или сиропы).
[1520] Один способ введения представляет собой парентеральное введение, например, посредством инъекции. Формы, в которых фармацевтические композиции, описанные в данном документе, могут быть включены для введения посредством инъекции, включают, например, водные или масляные суспензии, или эмульсии, с кунжутным маслом, кукурузным маслом, хлопковым маслом или арахисовым маслом, а также настойки, маннит, декстрозу или стерильный водный раствор, а также сходные фармацевтические носители.
[1530] Пероральное введение может представлять собой другой путь введения соединений, описанных в данном документе. Введение может осуществляться посредством, например, капсулы или таблеток, покрытых энтеросолюбильной оболочкой. При изготовлении фармацевтических композиций, которые включают по меньшей мере одно соединение, описанное в данном документе, активный ингредиент обычно разбавляют вспомогательным веществом и/или заключают в такой носитель, который может быть представлен в форме капсулы, саше, бумажного или другого контейнера. Если вспомогательное вещество выполняет функцию разбавителя, то оно может быть представлено в форме твердого, полутвердого или жидкого материала, который выполняет функцию вспомогательного среды-носителя, носителя или среды для активного ингредиента. Таким образом, композиции могут быть представлены в форме таблеток, пилюль, порошков, пастилок для рассасывания, саше, крахмальных капсул, настоек, суспензий, эмульсий, растворов, сиропов, аэрозолей (в виде твердого вещества или в жидкой среде), мазей, содержащих, например, не более 10% по весу активного соединения, мягких и твердых желатиновых капсул, стерильных растворов для инъекции и упакованных стерильных порошков.
[1540] Некоторые примеры подходящих вспомогательных веществ включают, например, лактозу, декстрозу, сахарозу, сорбит, маннит, виды крахмала, аравийскую камедь, фосфат кальция, альгинаты, трагакант, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, стерильную воду, сироп и метилцеллюлозу. Составы могут дополнительно включать смазывающие средства, такие как тальк, стеарат магния и минеральное масло; смачивающие средства; эмульгирующие и суспендирующие средства; консерванты, такие как метил и пропилгидроксибензоаты; подсластители и ароматизаторы.
[1550] Композиции, которые содержат по меньшей мере одно соединение, описанное в данном документе, могут быть составлены таким образом, чтобы обеспечивать быстрое, замедленное или отсроченное высвобождение активного ингредиента после введения субъекту, посредством применения процедур, известных из уровня техники. Системы доставки для контролируемого высвобождения лекарственного средства для перорального введения включают системы на основе осмотической помпы и системы для растворения, содержащие резервуары, покрытые полимером, или составы на основе матрицы лекарственное средство-полимер. В другом составе для применения в способах, раскрытых в данном документе, применяются устройства для трансдермальной доставки («пластыри»). Такие трансдермальные пластыри могут применяться для обеспечения непрерывной или прерывистой инфузии соединений, описанных в данном документе, в контролируемых количествах. Конструирование и применение трансдермальных пластырей для доставки фармацевтических средств являются общеизвестными из уровня техники. Такие пластыри могут быть сконструированы для непрерывной, пульсирующей доставки фармацевтических средств или доставки фармацевтических средств «по требованию».
[1560] Для получения твердых композиций, таких как таблетки, основной активный ингредиент можно смешивать с фармацевтическим вспомогательным веществом с образованием твердой предварительно составленной композиции, содержащей однородную смесь соединения, описанного в данном документе. При упоминании этих предварительно составленных композиций как гомогенных, активный ингредиент может быть равномерно диспергирован по композиции таким образом, чтобы композиция могла быть легко разделена на одинаково эффективные стандартные дозированные лекарственные формы, такие как таблетки, пилюли и капсулы.
[1570] На таблетки или пилюли на основе соединений, описанных в данном документе, можно наносить покрытие или их можно иным образом составлять с получением лекарственной формы, обеспечивающей преимущество пролонгированного действия, или с целью защиты от кислотных условий в желудке. Например, таблетка или пилюля может содержать внутренний и внешний компонент дозы, при этом второй представлен в форме оболочки вокруг первого. Два компонента могут быть отделены энтеросолюбильным слоем, обеспечивает препятствование распаду в желудке и обеспечивает возможность внутреннему компоненту проходить в интактном виде в двенадцатиперстную кишку или задерживать его высвобождение. Для таких энтеросолюбильных слоев или покрытий можно применять разнообразные материалы, в том числе ряд полимерных кислот и смеси полимерных кислот с такими материалами как шеллак, цетиловый спирт и ацетат целлюлозы.
[1580] Композиции для ингаляции или инсуффляции могут содержать растворы и суспензии в фармацевтически приемлемых водных или органических растворителях или их смесях, а также порошки. Жидкие или твердые композиции могут содержать подходящие фармацевтически приемлемые вспомогательные вещества, описанные в данном документе. В некоторых вариантах осуществления композиции вводят путем вдыхания через рот или нос для обеспечения местного или системного эффекта. В других вариантах осуществления композиции в фармацевтически приемлемых растворителях можно распылять путем применения инертных газов. Распыленные растворы могут вдыхаться непосредственно из распыляющего устройства, или распыляющее устройство может быть присоединено к маске для ингаляции или аппарату искусственной вентиляции легких в режиме перемежающейся вентиляции с положительным давлением. Композиции в виде раствора, суспензии или порошка можно вводить, предпочтительно перорально или интраназально, из устройств, которые доставляют состав подходящим способом.
[1590] В некоторых вариантах осуществления фармацевтическая композиция дополнительно содержит одно или более дополнительных лекарственных средств для лечения или предупреждения инфекции, вызванной микроорганизмом.
6. Дозирование
[1600] Конкретный уровень дозы соединения по настоящему описанию может зависеть от разнообразных факторов, включающих активность конкретного используемого соединения, возраста, веса тела, общего состояния здоровья, пола, рациона питания, времени введения, пути введения, а также скорости выведения, комбинации лекарственных препаратов и тяжести конкретного заболевания, подвергаемого терапии. Например, доза может выражаться в количестве миллиграммов соединения, описанного в данном документе, на килограмм веса тела субъекта (мг/кг). Дозы, составляющие от приблизительно 0,1 мг/кг до 150 мг/кг, могут являться подходящими. В некоторых вариантах осуществления доза, составляющая от приблизительно 0,1 мг/кг до 100 мг/кг, может являться подходящей. В других вариантах осуществления доза, составляющая от приблизительно 0,5 мг/кг до 60 мг/кг, может являться подходящей. В некоторых вариантах осуществления доза, составляющая от приблизительно 0,0001 мг до приблизительно 100 мг на кг веса тела в сутки, от приблизительно 0,001 мг до приблизительно 50 мг соединения на кг веса тела или от приблизительно 0,01 мг до приблизительно 10 мг соединения на кг веса тела, может являться подходящей. Общую суточную дозу можно вводить один раз в день или вводить два раза, три раза, четыре раза или большее число раз в течение дня в виде разделенных доз.
7. Синтез соединений
[1610] Соединения можно получать с применением способов, раскрытых в данном документе, и их стандартных модификаций, которые будут очевидны с учетом приведенного в данном документе описания и способов, широко известных из уровня техники. можно применять традиционные и общеизвестные способы синтеза в дополнение к идеям, представленным в данном документе. Синтез типичных соединений, описанных в данном документе, может осуществляться в соответствии с описанием в следующих примерах. При их доступности реагенты и исходные материалы можно приобретать из коммерческих источников, например, у Sigma Aldrich или у других поставщиков химических реагентов.
[1620] Следует понимать, что в то время как приводятся типичные или предпочтительные условия способа (например, значения температуры осуществления реакции, времени, молярных соотношений веществ, вступающих в реакцию, растворители, значения давления и т.д.), также можно применять другие условия способа, если не указано иное. Оптимальные условия осуществления реакции могут варьировать в зависимости от конкретных применяемых веществ, вступающих в реакцию, или растворителя, однако такие условия могут быть определены специалистом в данной области техники посредством обычных процедур оптимизации.
[1630] Кроме того, могут требоваться традиционные защитные группы с целью предотвращения вступления определенных функциональных групп в нежелательные реакции. Подходящие защитные группы для разнообразных функциональных групп, а также подходящие условия для введения и удаления защитной группы для конкретных функциональных групп являются общеизвестными из уровня техники. Например, ряд защитных групп описан в Wuts, P. G. M., Greene, T. W. and Greene, T. W. (2006). Greene’s protective groups in organic synthesis. Hoboken, N.J., Wiley-Interscience, а также в литературных источниках, цитируемых в данном источнике.
[1640] Кроме того, соединения по настоящему изобретению могут содержать один или более хиральных центров. Соответственно, при необходимости такие соединения могут быть получены или выделены в виде чистых стереоизомеров, например, в виде отдельных энантиомеров, или диастереомеров, или в виде обогащенных стереоизомерами смесей. Все такие стереоизомеры (и обогащенные смеси) включены в пределах объема настоящего изобретения, если не указано иное. Чистые стереоизомеры (или обогащенные смеси) можно получать с применением, например, оптически активных исходных материалов или стереоселективных реагентов, общеизвестных из уровня техники. В качестве альтернативы, рацемические смеси таких соединений можно выделять с применением, например, хиральной колоночной хроматографии, средств для хирального разделения и т.п.
[1650] Пригодные исходные материалы представляют собой общеизвестные соединения или могут быть получены с помощью известных процедур или их модификаций. Например, многие из исходных материалов являются доступными у коммерческих поставщиков, таких как Aldrich Chemical Co. (Милуоки, Висконсин, США), Bachem (Торранс, Калифорния, США), Emka-Chemce или Sigma (Сент-Луис, миссури, США). Другие можно получать путем осуществления процедур или их модификаций, описанных в стандартных справочниках, таких как Fieser and Fieser’s Reagents for Organic Synthesis, Volumes 1-15 (John Wiley, and Sons, 1991), Rodd’s Chemistry of Carbon Compounds, Volumes 1-5, and Supplementals (Elsevier Science Publishers, 1989) organic Reactions, Volumes 1-40 (John Wiley, and Sons, 1991), March’s Advanced Organic Chemistry, (John Wiley, and Sons, 5th Edition, 2001) и Larock’s Comprehensive Organic Transformations (VCH Publishers Inc., 1989).
[1660] Промежуточные соединения и продукты можно выделять из реакционных смесей и очищать с помощью общепринятых способов, таких как экстрагирование, выпаривание, осаждение, фильтрация, кристаллизация и хроматография. Промежуточные соединения можно также непосредственно применять в следующей реакции без очистки или без отделения.
Общий синтез
[1670] В определенных вариантах осуществления предусмотрен способ получения соединения по настоящему изобретению. В определенных вариантах осуществления соединения можно получать в соответствии с общими схемами I-VI с применением исходных материалов и реагентов, которые могут быть приобретены или получены с помощью способов, известных специалисту в данной области техники. На схемах I-VI m, n, X1, X2, X3, X4, X5, R1, R1b, R2, R3, R4 и R5 определены в данном документе.
Схема I
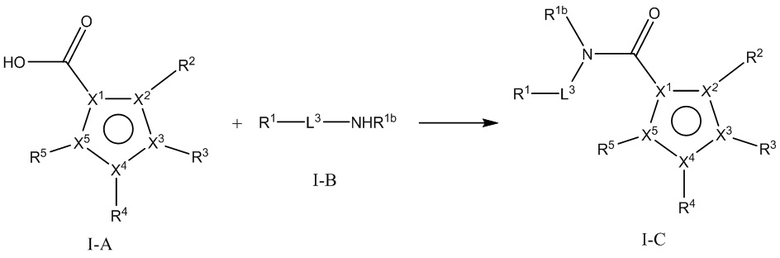
На схеме I L3 представляет собой *-(CH2)n-, *-(CH2)n-N(R1c)-(CH2)k- или *-(CH2)n-(O(CH2)m)p-O(CH2)k-, и *, n, k, p и R1c определены в данном документе. Соединение I-A вступает в реакцию с соединением I-B при условиях реакции сочетания амида с получением соединения I-C. Условия реакции сочетания амида в целом являются известными из уровня техники и, как правило, включают реагент для реакции сочетания, например, карбодиимиды, такие как N,N'-дициклогексилкарбодиимид (DCC), N,N'-диизопропилкарбодиимид (DIC) и 1-этил-3-(3'-диметиламинопропил)карбодиимид (EDCI). Карбодиимиды могут применяться в сочетании с добавками, такими как DMAP или HOBt. Часто встречающиеся реагенты для реакции сочетания амида также включают без ограничения оксихлорид фосфора (POCl3), ангидрид 2-пропанфосфоновой кислоты (T3P), карбонилдиимидазол (CDI), 2-хлор-4,6-диметокси-1,2,5-триазин (CDMT). Реагенты для реакции сочетания амида также включают реагенты на основе аминия и фосфония, такие как N-оксид гексафторфосфата N-[(диметиламино)-1H-1,2,3-триазоло[4,5-b]пиридин-1-илметилен]-N-метилметанаминия (HATU), N-оксид гексафторфосфата N-[(1H-бензотриазол-1-ил)(диметиламино)метилен]-N-метилметанаминия (HBTU) и гексафторфосфат бензотриазол-1-ил-N-окси-трис(пирролидино)фосфония (PyBOP). Условия реакции сочетания амида могут включать растворитель, такой как DMF, THF, DCM, ацетон, DMA, EtOAc, ацетонитрил или их смесь, а также могут включать органическое основание, такое как пиридин, TEA, DIPEA, DMAP, NMM или их смесь. Условия реакции сочетания могут включать температуру в диапазоне от -10°C до комнатной температуры.
Схема II
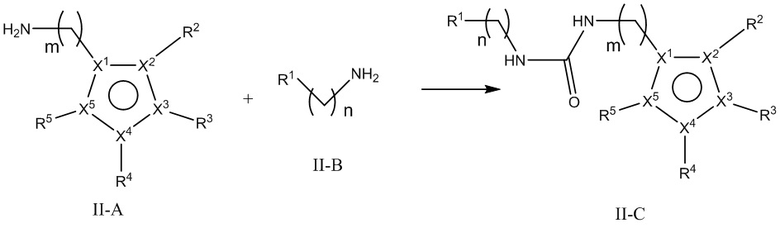
[1690] На схеме II соединение II-A вступает в реакцию с соединением II-B в присутствии трифосгена с получением соединения II-C. Реакцию, как правило, осуществляют в растворителе, таком как THF или DCM, в присутствии органического основания, такого как TEA или DIPEA, и в условиях охлаждения, например, на ледяной бане.
Схема III
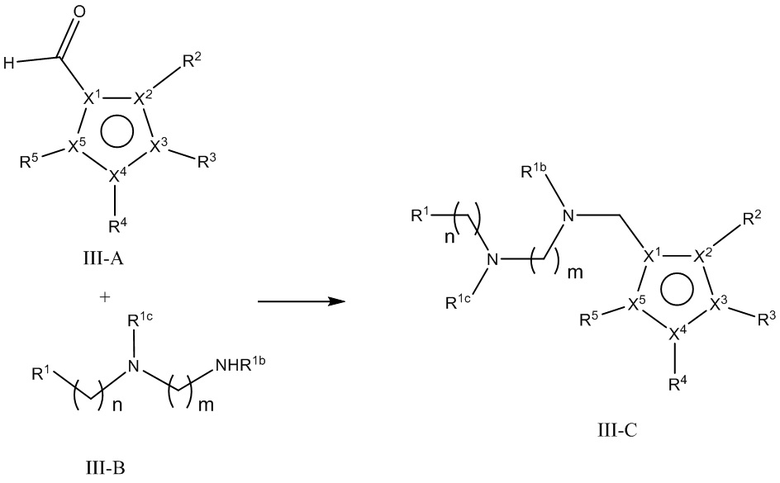
[1700] На схеме III соединение III-A вступает в реакцию с соединением III-B в условиях восстановительного аминирования с получением соединения III-C. Условия восстановительного аминирования в целом являются известными в уровне техники и, как правило, включают растворитель, такой как MeOH, EtOH, DCM, THF или диоксан, восстановитель, такой как NaBH4, NaBH3CN или NaBH(OCOCH3)3, и необязательно кислоты Льюиса, такие как Ti(iPrO)4 или ZnCl2, и молекулярное сито.
Схема IV
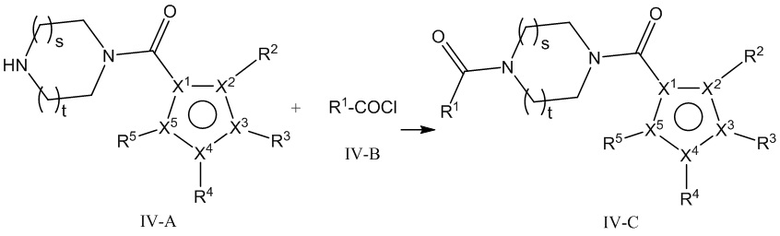
[1710] На схеме IV s и t независимо равняются 0, 1 или 2. Соединение IV-A вступает в реакцию с соединением IV-B в присутствии трифосгена с получением соединения IV-C. Реакцию, как правило, осуществляют в растворителе, таком как DCM, в присутствии органического основания, такого как TEA или DIPEA, и при температуре в диапазоне от приблизительно -10°C до приблизительно 40°C или от приблизительно 0°C до приблизительно 25°C.
Схема V
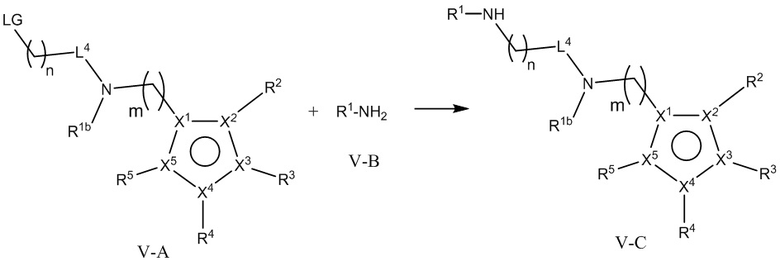
[1720] На схеме V L4 представляет собой CO или SO2, и LG представляет собой уходящую группу, такую как галоген. Соединение V-A вступает в реакцию с соединением V-B с получением соединения V-C. Реакцию, как правило, осуществляют в растворителе, таком как безводный CH3CN, в присутствии основания, такого как K2CO3, в условиях нагревания, например, с обратным холодильником.
Схема VI
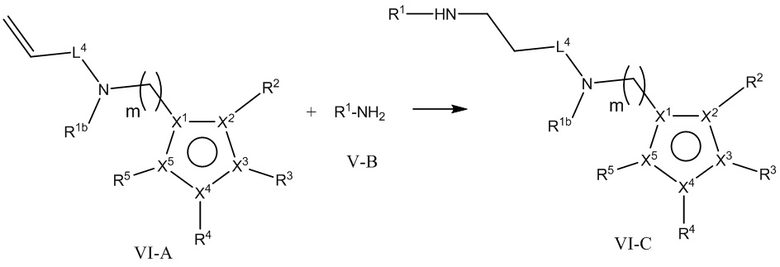
[1730] На схеме VI L4 представляет собой CO или SO2. Соединение VI-A вступает в реакцию с соединением VI-B с получением соединения VI-C. Реакцию, как правило, осуществляют в растворителе, таком как MeOH, в условиях нагревания, например, с обратным холодильником.
Схема VII
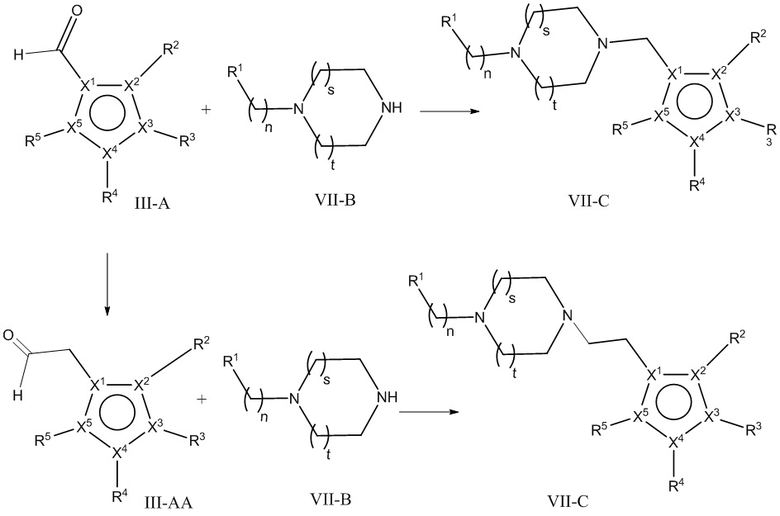
[170] На схеме VII соединение III-A вступает в реакцию с соединением VII-B с получением соединения VII-C, где m равняется 1. В дополнительных вариантах осуществления соединение III-A можно превращать в соединение III-AA, и соединение III-AA вступает в реакцию с соединением VII-B с получением соединения VII-C, где m равняется 2. Реакцию, как правило, осуществляют в условиях восстановительного аминирования с получением соединения VII-C. Условия восстановительного аминирования в целом являются известными в уровне техники и, как правило, включают растворитель, такой как MeOH, EtOH, DCM, THF или диоксан, восстановитель, такой как NaBH4, NaBH3CN или NaBH(OCOCH3)3, и необязательно кислоты Льюиса, такие как Ti(iPrO)4 или ZnCl2, и молекулярное сито.
Схема VIII
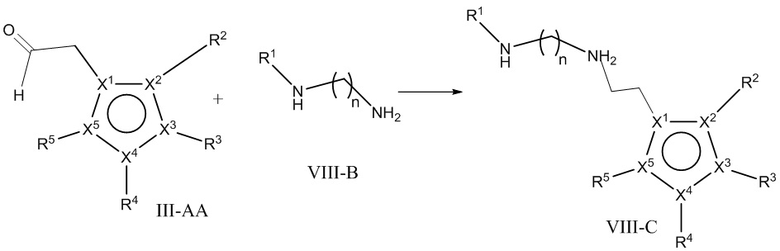
[1750] На схеме VIII соединение III-AA вступает в реакцию с соединением VIII-B с получением соединения VIII-C. Реакцию, как правило, осуществляют в условиях восстановительного аминирования с получением соединения VIII-C. Условия восстановительного аминирования в целом являются известными в уровне техники и, как правило, включают растворитель, такой как MeOH, EtOH, DCM, THF или диоксан, восстановитель, такой как NaBH4, NaBH3CN, или NaBH(OCOCH3)3, и необязательно кислоты Льюиса, такие как Ti(iPrO)4 или ZnCl2, и молекулярное сито.
Схема IX
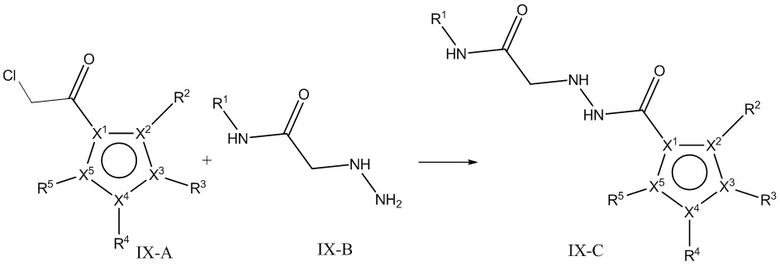
[1760] На схеме IX соединение IX-A вступает в реакцию с соединением IX-B с получением соединения IX-C. Реакцию, как правило, осуществляют в растворителе, таком как EtOH, с нагреванием или без нагревания, например, при комнатной температуре или с обратным холодильником.
ПРИМЕРЫ
[1770] Следующие примеры включены с целью демонстрации конкретных вариантов осуществления настоящего изобретения. Специалистам в данной области техники будет понятно, что методики, раскрытые в примерах, которые следуют ниже, представляют собой методики, работающие надлежащим образом при практической реализации настоящего изобретения, и которые, таким образом, можно считать основанием для конкретных способов его практической реализации. Однако в свете настоящего изобретения специалистам в данной области техники будет понятно, что в отношении конкретных вариантов осуществления, которые раскрыты, можно осуществлять множество изменений и по-прежнему получать сходные или подобные результаты без отступления от сущности и объема настоящего изобретения.
[1780] Общие экспериментальные способы
[1790] Все применяемые растворители являлись коммерчески доступными и применялись без дополнительной очистки. Реакции, как правило, осуществляли с применением безводных растворителей в инертной атмосфере азота.
ЯМР-спектроскопия
[1800] В соответствии с настоящим изобретением, 1H ЯМР-спектр измеряли с помощью спектрометра ядерного магнитного резонанса типа Bruker-500 MHz с применением 0,1% TMS в CD3OD в качестве растворителя, где CD3OD (δ = 3,31 ppm) применяют в качестве внутреннего стандарта; 0,1% TMS в CDCl3 в качестве растворителя, где CDCl3 (δ = 7,26 ppm) применяют в качестве внутреннего стандарта; или 0,03% TMS в DMSO-d6 в качестве растворителя, где DMSO-d6 (δ = 2,50 ppm) применяют в качестве внутреннего стандарта. LRMS-спектры определяли с помощью масс-спектрометра AB Triple 4600, препараты HPLC определяли с помощью прибора типа SHIMADZU LC-20AP и чистоту в соответствии с HPLC определяли с помощью прибора SHIMADZU LC-30AP или Waters 1525. Если не указано иное, все реакции осуществляли в атмосфере воздуха; и после осуществления реакций выполняли TLC или LC-MS. Характерные химические сдвиги (δ) приводятся в частях на миллион с использованием традиционных сокращений для обозначения главных пиков: например, s: синглет; d: дублет; t: триплет; q: квартет; dd: дублет дублетов; dt: дублет триплетов; br: широкий сигнал.
[1810] Растворители и реагенты
[1820] Если не указано иное, растворитель, применяемый для осуществления реакций, такой как DCM, DMF, безводный EtOH, безводный MeOH, приобретали у Sinopharm Group; вещества степени очистки для HPLC получали с применением CH3CN и деионизированной воды; и другие реагенты применяли непосредственно в том виде, в котором их приобретали у изготовителей.
Пример 1. Получение соединения 43
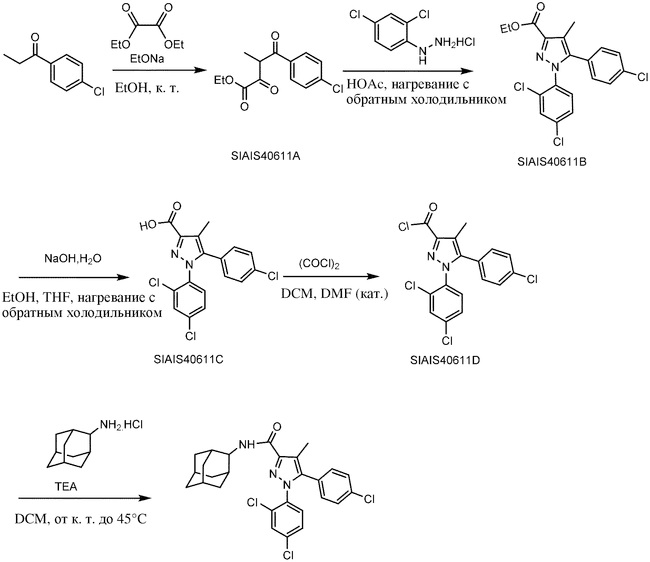
Стадия 1
[1830] В раствор диэтилоксалата (11,7 г, 80,1 ммоль) в EtOH (100 мл) добавляли по каплям раствор этоксида натрия (36,3 г, 20% вес/вес, 106,8 ммоль) в атмосфере азота. После перемешивания при комнатной температуре в течение 10 мин. добавляли 4'-хлорпропиофенон (9 г, 53,4 ммоль, растворенный в 100 мл EtOH). Реакционную смесь перемешивали в течение 24 часов при комнатной температуре. После израсходования исходного материала реакционную смесь гасили ледяной водой и pH раствора регулировали до 3-4 с помощью 1 м HCl (водн.). Смесь экстрагировали дихлорметаном, промывали солевым раствором, высушивали над безводным Na2SO4. Растворитель выпаривали при пониженном давлении и остаток очищали с помощью колоночной хроматографии на силикагеле с получением SIAIS40611A с выходом 76,9% в виде желтого твердого вещества (11,0 г). 1H ЯМР (400 мГц, CDCl3) δ 1,28 (t, J = 7,2 Гц, 3H), 1,43 (d, J = 7,1 Гц, 3H), 4,25 (q, J = 7,2 Гц, 2H), 4,98 (q, J = 7,1 Гц, 1H), 7,47 (d, J = 8,3 Гц, 2H), 7,91 (d, J = 8,6 Гц, 2H).
[1840] Стадия 2
[1850] В раствор SIAIS40611A (1,4 г, 5,21 ммоль) в уксусной кислоте (14 мл) добавляли гидрохлорид 2,4-дихлорфенилгидразина (1,13 г, 5,31 ммоль) при комнатной температуре в атмосфере азота. Затем смесь нагревали с обратным холодильником при 130°C в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры и концентрировали в вакууме. Остаток растворяли с помощью 50 мл этилацетата и последовательно промывали водным раствором фосфорной кислоты (0,5 м, 30 мл × 3), насыщенным водным раствором NaHCO3 и солевым раствором. Полученное высушивали над безводным Na2SO4, фильтровали и концентрировали в вакууме с получением соединения SIAIS40611B (в виде желтого твердого вещества, 2,0 г, выход = 93,9%) без дополнительной очистки.
Стадия 3
В раствор SIAIS40611B (1,3 г, 3,17 ммоль) в EtOH/THF (7 мл/13 мл) добавляли водный раствор NaOH (1,2 г, 31,7 ммоль, 6 мл). Смесь нагревали с обратным холодильником при 75°C в течение 2,5 часа, затем охлаждали до комнатной температуры и концентрировали в вакууме. Остаток растворяли с помощью 50 мл H2O и pH раствора регулировали до 2-3 с помощью 1М HCl (водн.). Полученное экстрагировали с помощью EA (50 мл × 2) и органическую фазу промывали с помощью 50 мл солевого раствора. Полученное высушивали над Na2SO4, фильтровали и концентрировали в вакууме с получением SIAIS40611C (в виде желтого твердого вещества, 1,1 г, выход = 91,6%), которое применяли без дополнительной очистки.
Стадия 4
[1870] В раствор SIAIS40611C (0,5 г, 1,31 ммоль) в 8 мл DCM добавляли оксалилхлорид (0,33 г, 2,62 ммоль). Добавляли одну каплю DMF для катализа реакции и смесь перемешивали при комнатной температуре в течение 18 часов. Концентрировали в вакууме с получением SIAIS40611D в виде бледно-желтого твердого вещества (0,52 г, выход = 99,2%), которое применяли без дополнительной очистки.
Стадия 5
[1890] Охлаждали раствор гидрохлорида 2-адамантанамина (0,32 г, 1,69 ммоль) и TEA (0,46 г, 4,55 ммоль) в 10 мл DCM на водяной бане со льдом в атмосфере азота и затем добавляли по каплям раствор SIAIS40611D (0,52 г, 1,30 ммоль) в 10 мл DCM. После перемешивания при комнатной температуре в течение 21 часа смесь нагревали с обратным холодильником при 45°C еще в течение 8 часов. Смесь охлаждали до комнатной температуры и гасили с помощью 20 мл воды. Органический слой отделяли и водный слой экстрагировали с помощью DCM (30 мл × 2). Затем органическую фазу объединяли, промывали солевым раствором, высушивали над безводным Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле и получали соединение 43 в виде белого твердого вещества (0,33 г, выход = 50,0%). 1H ЯМР (400 мГц, DMSO-d6) δ 1,54 (d, J = 12,5 Гц, 2H), 1,67 (br. s., 2H), 1,79 (br. s., 8H), 1,91 (br. s., 2H), 2,21 (s, 3H), 4,02 (d, J = 6,36 Гц, 1H), 7,19 (d, J = 8,1 Гц, 2H), 7,37-7,49 (m, 3H), 7,51-7,59 (m, 1H), 7,72 (d, J = 11,5 Гц, 2H); рассч. посредством HRMS (ESI) значение для C27H27Cl3N3O+ [M+H]+, 514,1214; обнаруженное значение 514,1209.
Пример 2. Получение SIAIS40612A
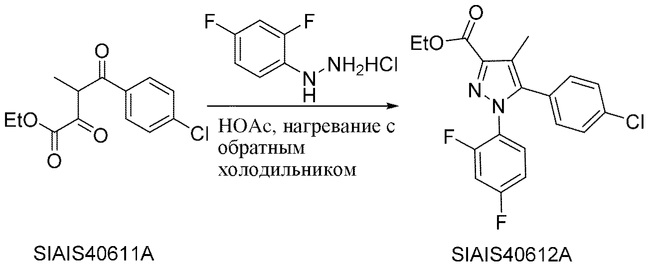
[1900] Нагревали раствор SIAIS40611A (2,5 г, 9,3 ммоль) и гидрохлорида 2,4-дифторфенилгидразина (1,68 г, 9,3 ммоль) в 8 мл уксусной кислоты до 130°C и нагревали с обратным холодильником в течение 3 часов в атмосфере азота. Смесь охлаждали до комнатной температуры и концентрировали в вакууме. Полученный остаток растворяли в 50 мл EA, последовательно промывали насыщенным водным раствором NaHCO3 (30 мл × 2) и солевым раствором. Высушивали над безводным Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле и получали соединение SIAIS40612A в виде белого твердого вещества (2,0 г, выход = 57,1%). 1H ЯМР (400 мГц, CDCl3) δ 1,41 (t, J = 7,1 Гц, 3H) 2,30 (s, 3H), 4,44 (q, J = 7,1 Гц, 2H), 6,71-6,81 (m, 1H), 6,91 (t, J = 7,8 Гц, 1H), 7,06 (d, J = 8,3 Гц, 2H), 7,30 (d, J = 8,6 Гц, 2H), 7,41-7,45 (m, 1H).
Пример 3. Получение SIAIS40614A
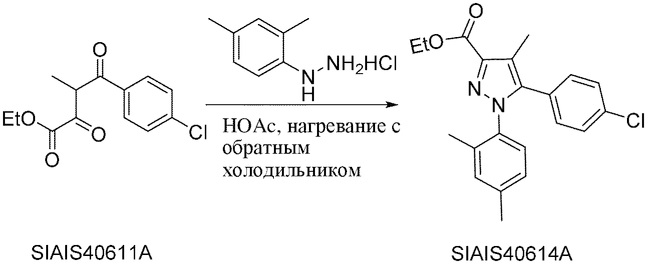
[1910] Нагревали раствор SIAIS40611A (2,0 г, 7,4 ммоль) и гидрохлорида 2,4-диметилфенилгидразина (1,28 г, 7,4 ммоль) в 15 мл уксусной кислоты до 130℃ и нагревали с обратным холодильником в течение 5 часов в атмосфере азота. Смесь охлаждали до комнатной температуры и концентрировали в вакууме. Полученный остаток растворяли в 50 мл EA, последовательно промывали насыщенным водным раствором NaHCO3 (30 мл × 2) и солевым раствором. Высушивали над безводным Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле и получали соединение SIAIS40614A в виде белого твердого вещества (2,0 г, выход = 72,8%). 1H ЯМР (400 мГц, CDCl3) δ 1,40 (t, J = 7,1 Гц, 3H), 1,84 (s, 3H), 2,28 (s, 3H), 2,33 (s, 3H), 4,42 (q, J = 7,1 Гц, 2H), 6,89-6,97 (m, 2H), 7,02 (d, J = 8,6 Гц, 2H), 7,07 (d, J = 7,8 Гц, 1H), 7,22-7,26 (m, 2H).
Пример 4. Получение соединения 17
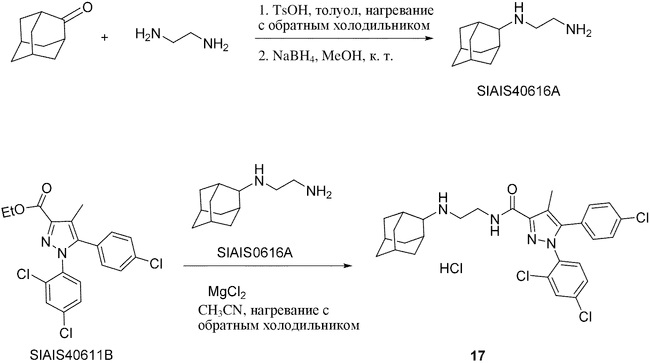
Стадия 1
[1920] Нагревали с обратным холодильником раствор 2-адамантанона (10,0 г, 66,57 ммоль), этилендиамина (25 мл) и TsOH (1,3 г, 6,66 ммоль) в 100 мл толуола при 130°C в течение 8 часов, в то же время отделяли воду. Затем смесь охлаждали до комнатной температуры и концентрировали в вакууме. Полученный остаток растворяли в 50 мл метанола и охлаждали на водяной бане со льдом, к нему добавляли NaBH4 (5,0 г, 130 ммоль) за 3 порции и осуществляли реакцию в течение 4 часов. Реакционную смесь гасили водой (100 мл) и удаляли метанол. Водную фазу экстрагировали с помощью EA (200 мл × 3) и органическую фазу объединяли, промывали с помощью 50 мл солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле и получали SIAIS40616A в виде светло-желтого масла (10,5 г, выход = 81,4%). 1H ЯМР (400 мГц, CDCl3) δ 1,45 (s, 3H), 1,48 (s, 2H), 1,72-1,63 (m, 4H), 1,78-1,72 (m, 1H), 1,86-1,78 (m, 5H), 1,93 (d, J = 12,2 Гц, 2H), 2,67-2,60 (m, 2H), 2,68 (s, 1H), 2,78 (dd, J = 6,5, 5,2 Гц, 2H).
Стадия 2
[1930] В атмосфере азота нагревали раствор SIAIS40611B (0,50 г, 1,22 ммоль), SIAIS40616A (0,95 г, 4,88 ммоль), MgCl2 (0,58 г, 6,10 ммоль) в 25 мл CH3CN нагревали до 90°C и выдерживали в течение 8 часов. После того как исходный материал израсходовался, смесь охлаждали до комнатной температуры и гасили с помощью 30 мл воды. Водную фазу экстрагировали с помощью EA (50 мл × 3). Объединенную органическую фазу промывали с помощью 50 мл солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле и получали соединение 17 в виде желтого твердого вещества (0,52 г, выход = 76,5%). 1H ЯМР (400 мГц, DMSO-d6) δ 1,50 (d, J = 12,9 Гц, 2H), 1,79-1,71 (m, 8H), 2,15-2,01 (m, 4H), 2,22 (s, 3H), 2,88-2,91 (m, 1H), 3,06 (t, J = 6,5 Гц, 2H), 3,30-3,31 (m, 1H), 3,62 (t, J = 6,3 Гц, 2H), 7,24-7,15 (m, 2H), 7,46-7,39 (m, 2H), 7,56 (dd, J = 8,5, 2,3 Гц, 1H), 7,70 (d, J = 8,5 Гц, 1H), 7,75 (d, J = 2,3 Гц, 1H), 8,54 (t, J = 5,9 Гц, 1H), 8,87 (s, 2H). Рассч. с помощью HRMS (ESI) значение для C29H32Cl3N4O+ [M + H]+ 557,1636; обнаруженное значение 557,1649.
Пример 5. Получение соединения 76
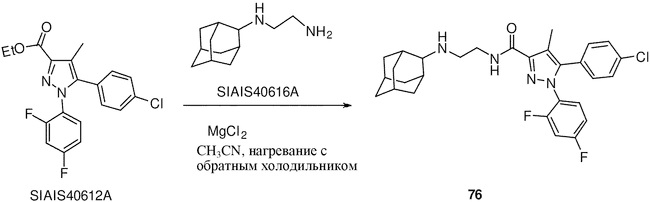
[1940] Нагревали раствор SIAIS40612A (0,30 г, 0,80 ммоль), SIAIS40616A (0,78 г, 4,0 ммоль), MgCl2 (0,30 г, 3,2 ммоль) в 16 мл CH3CN до 90°C и выдерживали в течение 4 часов в атмосфере азота. После того как исходный материал израсходовался, смесь охлаждали до комнатной температуры и гасили с помощью 30 мл воды. Водную фазу экстрагировали с помощью EA (50 мл × 3). Объединенную органическую фазу промывали с помощью 50 мл солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле и получали соединение 76 в виде белого твердого вещества (0,30 г, выход = 71,4%). 1H ЯМР (400 мГц, DMSO-d6) δ 1,34 (d, J=11,7 Гц, 2H), 1,60-1,64 (m, 5H), 1,71-1,82 (m, 5H), 1,93-2,04 (m, 2H), 2,21 (s, 3H), 2,71-2,82 (m, 3H), 3,31-3,34 (m, 2H), 7,13-7,28 (m, 3H), 7,33-7,52 (m, 3H), 7,60-7,74 (m, 1H), 8,23 (br. s., 1H). Рассч. с помощью HRMS (ESI) значение для C29H32ClF2N4O+ [M + H]+: 525,2227; обнаруженное значение: 525,2236.
Пример 6. Получение соединения 77
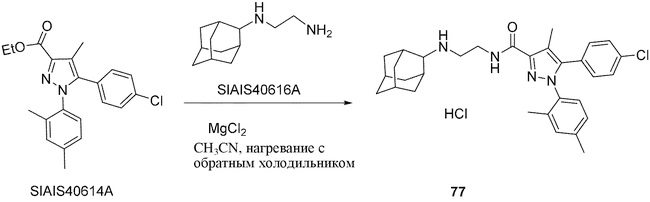
[1950] Нагревали раствор SIAIS40614A (0,60 г, 1,63 ммоль), SIAIS40616A (1,26 г, 6,52 ммоль), MgCl2 (0,77 г, 8,15 ммоль) в 25 мл CH3CN до 90°C и выдерживали в течение 10 часов в атмосфере азота. После того как исходный материал израсходовался, смесь охлаждали до комнатной температуры и гасили с помощью 30 мл воды. Водную фазу экстрагировали с помощью EA (50 мл × 3). Объединенную органическую фазу промывали с помощью 50 мл солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле, 2 раза промывали разбавленным водным раствором HCl и получали соединение 77 в виде белого твердого вещества (0,78 г, выход = 92,8%). 1H ЯМР (400 мГц, DMSO-d6) δ 1,50 (d, J = 12,8 Гц, 2H), 1,68 (d, J = 17,9 Гц, 4H), 1,79 (d, J = 11,2 Гц, 4H), 1,85 (s, 3H), 2,10 (d, J = 17,6 Гц, 4H), 2,23 (d, J = 7,6 Гц, 6H), 3,07 (t, J = 6,3 Гц, 2H), 3,31-3,33 (m, 1H), 3,63 (t, J = 6,2 Гц, 2H), 7,22-6,96 (m, 5H), 7,42-7,34 (m, 2H), 8,52 (t, J = 5,9 Гц, 1H), 9,02 (s, 2H). Рассч. с помощью HRMS (ESI) значение для C31H38ClN4O+ [M + H]+ 517,2729; обнаруженное значение: 517,2730.
Пример 7. Получение соединения 74
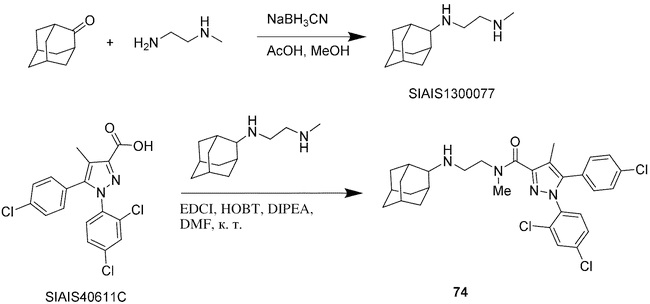
Стадия 1
[1960] В раствор 2-адамантанона (0,20 г, 1,33 ммоль) в 8 мл метанола добавляли N-метилэтандиамин (0,15 г, 2,0 ммоль). После перемешивания в течение 15 мин. при комнатной температуре добавляли уксусную кислоту (0,34 мл) и NaBH3CN (0,25 г, 4,0 ммоль) и осуществляли реакцию в течение ночи. Смесь гасили с помощью 10 мл воды и экстрагировали с помощью EA (25 мл × 2). Органическую фазу объединяли, промывали с помощью 50 мл солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали с получением SIAIS1300077 в виде неочищенного продукта (0,24 г, выход = 86%). 1H ЯМР (500 мГц, CD3OD) δ 3,11-3,04 (m, 2H), 2,95 (dd, J = 6,8, 5,2 Гц, 2H), 2,89 (d, J = 2,4 Гц, 1H), 2,68 (s, 3H), 2,10-2,02 (m, 2H), 2,02-1,92 (m, 4H), 1,93-1,78 (m, 6H), 1,70-1,58 (m, 2H). 13C ЯМР (126 мГц, CD3OD) δ 61,97, 48,49, 42,49, 37,38, 37,05, 32,68, 31,37, 30,54, 27,63, 27,46. Рассч. с помощью HRMS (ESI) значение для C13H25N2+ [M + H]+: 209,2012; обнаруженное значение: 209,2015.
Стадия 2
[1970] В раствор SIAIS1300077 (23 мг, 0,11 ммоль) и SIAIS40611C (41 мг, 0,11 ммоль) в 2 мл DMF последовательно добавляли EDCI (32 мг, 0,17 ммоль), HOBT (15 мг, 0,11 ммоль) и DIPEA (18 мкл, 0,11 ммоль) и осуществляли реакцию в течение ночи. Смесь гасили с помощью 0,2 мл воды, очищали с помощью препаративной HPLC и получали соединение 74 в виде белого порошка (32 мг, выход = 49%). 1H ЯМР (500 мГц, CD3OD) δ 7,71-7,43 (m, 3H), 7,39 (d, J = 8,5 Гц, 2H), 7,22 (d, J = 8,0 Гц, 2H), 3,99 (d, J = 57,1 Гц, 2H), 3,60-3,39 (m, 3H), 3,35 (s, 1,5H, NCH3), 3,17 (s, 1,5H, NCH3), 2,23 (s, 1H), 2,19 (s, 3H), 2,07-1,78 (m, 8H), 1,72 (s, 2H), 1,54 (s, 3H). Рассч. с помощью HRMS (ESI) значение для C30H34Cl3N4O [M + H]+: 571,1793; обнаруженное значение: 571,1799.
Пример 8. Получение соединения 18
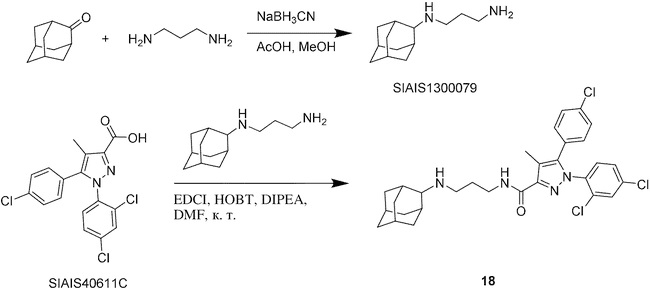
Стадия 1
[1980] В раствор 2-адамантанона (0,20 г, 1,33 ммоль) в 8 мл метанола добавляли 1,3-диаминопропан (0,30 г, 4,0 ммоль) и перемешивали в течение 15 мин. при комнатной температуре. Добавляли уксусную кислоту (0,34 мл) и NaBH3CN (0,25 г, 4,0 ммоль) и осуществляли реакцию в течение ночи. Смесь гасили с помощью 10 мл воды и экстрагировали с помощью EA (25 мл × 2), затем органическую фазу объединяли и промывали с помощью 50 мл солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали. В результате образования соли с помощью раствора HCl и промывания с помощью EA получали SIAIS1300079 в виде неочищенного продукта (0,22 г, выход = 67%).
Стадия 2
В раствор SIAIS1300079 (27 мг, 0,11 ммоль) и SIAIS40611C (41 мг, 0,11 ммоль) в 2 мл DMF последовательно добавляли EDCI (32 мг, 0,17 ммоль), HOBT (15 мг, 0,11 ммоль) и DIPEA (18 мкл, 0,11 ммоль) и осуществляли реакцию в течение ночи. Смесь гасили с помощью 0,2 мл воды, очищали с помощью препаративной HPLC и получали соединение 18 в виде белого порошка (16 мг, выход = 25%). 1H ЯМР (500 мГц, CD3OD) δ 7,61 (d, J = 2,2 Гц, 1H), 7,54 (d, J = 8,5 Гц, 1H), 7,48 (dd, J = 8,5, 2,2 Гц, 1H), 7,42-7,38 (m, 2H), 7,24-7,20 (m, 2H), 3,74-3,67 (m, 1H), 3,60-3,57 (m, 1H), 3,54 (t, J = 6,2 Гц, 2H), 3,44 (s, 1H), 3,14 (t, J = 7,1 Гц, 2H), 2,34 (s, 3H), 2,22 (d, J = 8,3 Гц, 2H), 2,14-2,00 (m, 6H), 1,96 (d, J = 6,4 Гц, 2H), 1,88 (d, J = 13,1 Гц, 4H), 1,79 (d, J = 13,7 Гц, 2H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C30H34Cl3N4O [M + H]+: 571,1793; обнаруженное значение: 571,1785.
Пример 9. Получение соединения 19
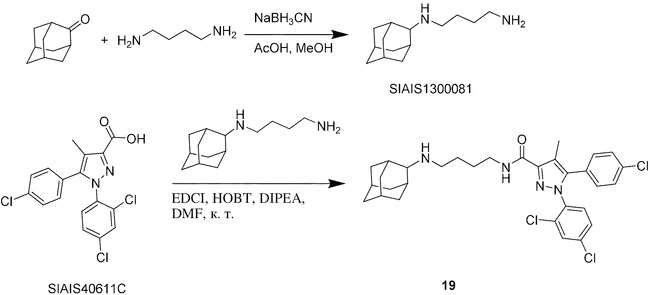
Стадия 1
[2000] В раствор 2-адамантанона (0,20 г, 1,33 ммоль) в 8 мл метанола добавляли 1,4-диаминобутан (0,35 г, 4,0 ммоль) и перемешивали в течение 15 мин. при комнатной температуре. Добавляли уксусную кислоту (0,34 мл) и NaBH3CN (0,25 г, 4,0 ммоль) и осуществляли реакцию в течение ночи. Смесь гасили с помощью 10 мл воды и экстрагировали с помощью EA (25 мл × 2), затем органическую фазу объединяли и промывали с помощью 50 мл солевого раствора, высушивали над безводным Na2SO4, фильтровали и концентрировали. В результате образования соли с помощью раствора HCl и промывания с помощью EA получали SIAIS1300081 в виде неочищенного продукта (0,32 г, выход = 93%).
Стадия 2
[2010] В раствор SIAIS1300081 (27 мг, 0,11 ммоль) и SIAIS40611C (41 мг, 0,11 ммоль) в 2 мл DMF последовательно добавляли EDCI (32 мг, 0,17 ммоль), HOBT (15 мг, 0,11 ммоль) и DIPEA (18 мкл, 0,11 ммоль) и осуществляли реакцию в течение ночи. Смесь гасили с помощью 0,2 мл воды, очищали с помощью препаративной HPLC и получали соединение 19 в виде белого порошка (16 мг, выход = 24%). 1H ЯМР (500 мГц, CD3OD) δ 7,62 (d, J = 2,4 Гц, 1H), 7,56 (d, J = 8,5 Гц, 1H), 7,50 (dd, J = 8,5, 2,3 Гц, 1H), 7,46-7,37 (m, 2H), 7,30-7,16 (m, 2H), 3,47 (t, J = 6,2 Гц, 2H), 3,42 (s, 1H), 3,20-3,09 (m, 2H), 2,35 (s, 3H), 2,06-1,92 (m, 7H), 1,91-1,71 (m, 11H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C31H36Cl3N4O [M + H]+: 585,1949; обнаруженное значение: 585,1953.
Пример 10. Получение соединения 52
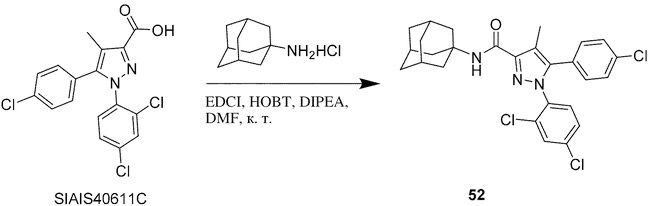
[2020] В раствор гидрохлорида 1-адамантанамина (20 мг, 0,11 ммоль) и SIAIS40611C (41 мг, 0,11 ммоль) в 2 мл DMF последовательно добавляли EDCI (32 мг, 0,17 ммоль), HOBT (15 мг, 0,11 ммоль) и DIPEA (18 мкл, 0,11 ммоль) и осуществляли реакцию в течение ночи. Смесь гасили с помощью 0,2 мл воды, очищали с помощью препаративной HPLC и получали соединение 52 в виде белого порошка (40 мг, выход = 72%). 1H ЯМР (500 мГц, CD3OD) δ 7,60 (d, J = 2,2 Гц, 1H), 7,55 (d, J = 8,5 Гц, 1H), 7,48 (dd, J = 8,4, 2,2 Гц, 1H), 7,42-7,36 (m, 2H), 7,26-7,15 (m, 2H), 2,30 (s, 3H), 2,17 (d, J = 2,9 Гц, 6H), 2,16-2,08 (m, 3H), 1,78 (d, J = 2,9 Гц, 6H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C27H27Cl3N3O+ [M + H]+: 514,1214; обнаруженное значение: 514,1220.
Пример 11. Получение соединения 163
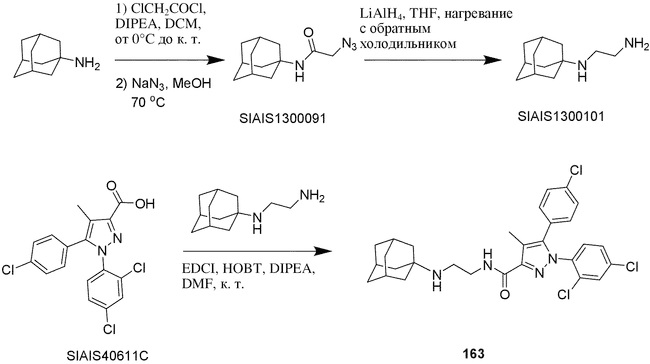
Стадия 1
[2030] Охлаждали раствор гидрохлорида 1-адамантанамина (1,0 г, 5,3 ммоль) в 8 мл DCM до 0°C, в него последовательно добавляли хлорацетилхлорид (0,90 г, 8,0 ммоль) и DIPEA (1,36 г, 1,76 мл). Реакцию осуществляли при комнатной температуре в течение ночи и смесь гасили с помощью 20 мл воды. Водную фазу экстрагировали с помощью DCM (25 мл × 2) и объединенную органическую фазу промывали солевым раствором, высушивали над безводным Na2SO4, фильтровали и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением белого твердого вещества (0,91 г, выход = 75%).
Стадия 2
[2040] Продукт стадии 1 растворяли в 8 мл метанола, к нему добавляли NaN3 (0,50 г, 7,7 ммоль) и смесь нагревали с обратным холодильником в течение 24 часов. Смесь концентрировали в вакууме и полученный остаток очищали с помощью колоночной хроматографии на силикагеле, SIAIS1300091 получали в виде белого твердого вещества (0,77 г, выход = 82%). 1H ЯМР (500 мГц, CDCl3) δ 5,93 (s, 1H), 3,88 (s, 2H), 2,11 (s, 3H), 2,03 (s, 6H), 1,72 (s, 6H). 13C ЯМР (126 мГц, CDCl3) δ 165,28, 53,17, 52,25, 41,47, 36,24, 29,40. Рассч. с помощью HRMS (ESI) значение масса/заряд для C12H19N4O+ [M + H]+: 235,1553; обнаруженное значение: 235,1549.
Стадия 3
[2050] В раствор SIAIS1300091 (0,50 г, 2,1 ммоль) в 20 мл THF добавляли LiAlH4 (0,41 г, 10,7 ммоль) и смесь нагревали с обратным холодильником в течение 24 часов. Реакционную смесь последовательно гасили с помощью 0,41 мл H2O, 0,41 мл 15% NaOH (водн.) и 1,2 мл H2O. Смесь фильтровали и раствор концентрировали в вакууме с получением SIAIS1300101 (0,47 г, выход = 95%), которое применяли без дополнительной очистки.
Стадия 4
[2060] В раствор SIAIS1300101 (27 мг, 0,11 ммоль) и SIAIS40611C (41 мг, 0,11 ммоль) в 2 мл DMF последовательно добавляли EDCI (32 мг, 0,17 ммоль), HOBT (15 мг, 0,11 ммоль) и DIPEA (18 мкл, 0,11 ммоль). Реакцию осуществляли в течение ночи и смесь гасили с помощью 0,2 мл воды, затем непосредственно очищали с помощью препаративной HPLC. Соединение 163 получали в виде белого порошка (23 мг, выход = 36%). 1H ЯМР (500 мГц, CD3OD) δ 7,62 (d, J = 2,2 Гц, 1H), 7,55 (d, J = 8,4 Гц, 1H), 7,49 (dd, J = 8,5, 2,3 Гц, 1H), 7,43-7,34 (m, 2H), 7,28-7,17 (m, 2H), 3,72-3,68 (m, 2H), 3,58 (dd, J = 5,5, 4,0 Гц, 2H), 2,35 (s, 3H), 2,24 (s, 3H), 1,96 (d, J = 2,9 Гц, 6H), 1,83 (d, J = 12,7 Гц, 3H), 1,75 (d, J = 12,8 Гц, 3H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C29H32Cl3N4O+[M + H]+: 557,1636; обнаруженное значение: 557,1631.
Пример 12. Получение соединения 23
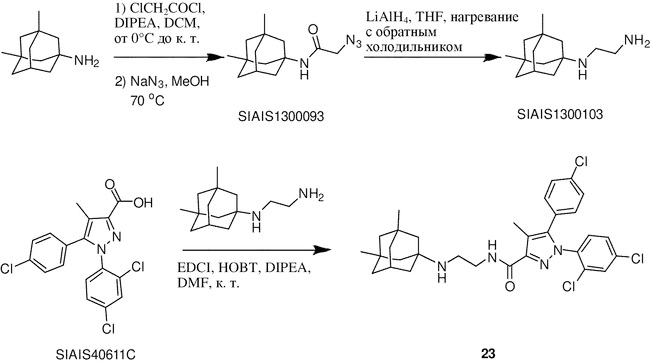
Стадия 1
[2070] Охлаждали раствор мемантина-HCl (1,0 г, 4,6 ммоль) в 8 мл DCM до 0°C, в него последовательно добавляли хлорацетилхлорид (0,78 г, 7,0 ммоль) и DIPEA (1,18 г, 1,52 мл). Реакцию осуществляли при комнатной температуре в течение ночи и смесь гасили с помощью 20 мл воды. Водную фазу экстрагировали с помощью DCM (25 мл × 2) и органическую фазу объединяли, промывали солевым раствором, высушивали над безводным Na2SO4, фильтровали и концентрировали. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением белого твердого вещества (0,98 г, выход = 83%).
Стадия 2
[2080] Продукт стадии 1 растворяли в 8 мл метанола, к нему добавляли NaN3 (0,50 г, 7,7 ммоль) и нагревали с обратным холодильником в течение 24 часов. Смесь концентрировали в вакууме и остаток очищали с помощью колоночной хроматографии на силикагеле, получали SIAIS1300093 в виде белого твердого вещества (0,81 г, выход = 80%). 1H ЯМР (500 мГц, CDCl3) δ 5,95 (s, 1H), 3,88 (s, 2H), 2,18 (p, J = 3,2 Гц, 1H), 1,92-1,81 (m, 2H), 1,75-1,63 (m, 4H), 1,45-1,40 (m, 2H), 1,39-1,29 (m, 2H), 1,24-1,13 (m, 2H), 0,88 (s, 6H). 13C ЯМР (126 мГц, CDCl3) δ 165,37, 53,83, 53,17, 50,49, 47,43, 42,55, 39,99, 32,44, 30,09, 30,00. Рассч. с помощью HRMS (ESI) значение масса/заряд для C14H23N4O+ [M + H]+: 263,1866; обнаруженное значение: 263,1863.
Стадия 3
В раствор SIAIS1300091 (0,50 г, 1,9 ммоль) в 20 мл THF добавляли LiAlH4 (0,41 г, 10,7 ммоль) и смесь нагревали с обратным холодильником в течение 24 часов. Реакционную смесь последовательно гасили с помощью 0,41 мл H2O, 0,41 мл 15% NaOH (водн.), 1,2 мл H2O. Затем смесь фильтровали и раствор концентрировали в вакууме с получением SIAIS1300103 (0,44 г, выход = 89%), которое применяли без дополнительной очистки.
Стадия 4
[2100] В раствор SIAIS1300103 (28 мг, 0,11 ммоль) и SIAIS40611C (41 мг, 0,11 ммоль) в 2 мл DMF последовательно добавляли EDCI (32 мг, 0,17 ммоль), HOBT (15 мг, 0,11 ммоль) и DIPEA (18 мкл, 0,11 ммоль). Реакцию осуществляли в течение ночи и смесь гасили с помощью 0,2 мл воды, затем непосредственно очищали с помощью препаративной HPLC. Соединение 23 получали в виде белого порошка (20 мг, выход = 30%). 1H ЯМР (500 мГц, CD3OD) δ 7,60 (d, J = 2,2 Гц, 1H), 7,52 (d, J = 8,5 Гц, 1H), 7,46 (dd, J = 8,5, 2,3 Гц, 1H), 7,42-7,35 (m, 2H), 7,27-7,12 (m, 2H), 3,66 (dd, J = 5,5, 3,8 Гц, 2H), 3,23 (t, J = 6,1 Гц, 2H), 2,33 (s, 3H), 1,78 (d, J = 3,2 Гц, 2H), 1,66-1,49 (m, 4H), 1,43 (d, J = 3,0 Гц, 4H), 1,35-1,16 (m, 3H), 0,94 (s, 6H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C31H36Cl3N4O+ [M + H]+: 585,1949; обнаруженное значение: 585,1941.
Пример 13. Получение соединения 54
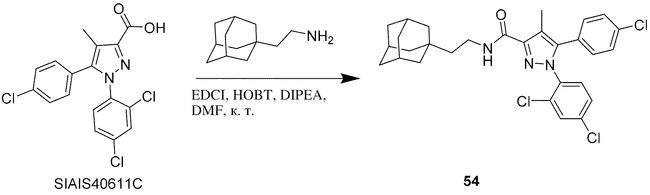
[2110] В раствор 2-(1-адамантил)этанамина (20 мг, 0,11 ммоль) и SIAIS40611C (41 мг, 0,11 ммоль) в 2 мл DMF последовательно добавляли EDCI (32 мг, 0,17 ммоль), HOBT (15 мг, 0,11 ммоль) и DIPEA (18 мкл, 0,11 ммоль). Реакцию осуществляли в течение ночи и смесь гасили водой (0,2 мл) и непосредственно очищали с помощью препаративной HPLC. Соединение 54 получали в виде белого порошка (24 мг, выход = 40%). 1H ЯМР (500 мГц, CD3OD) δ 7,57 (d, J = 2,3 Гц, 1H), 7,52 (d, J = 8,5 Гц, 1H), 7,44 (dd, J = 8,5, 2,3 Гц, 1H), 7,42-7,33 (m, 2H), 7,24-7,14 (m, 2H), 3,63-3,58 (m, 1H), 3,42-3,36 (m, 2H), 2,30 (s, 3H), 2,00-1,48 (m, 17H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C29H31Cl3N3O+ [M + H]+: 542,1527; обнаруженное значение: 542,1531.
Пример 14. Получение SIAIS1300172
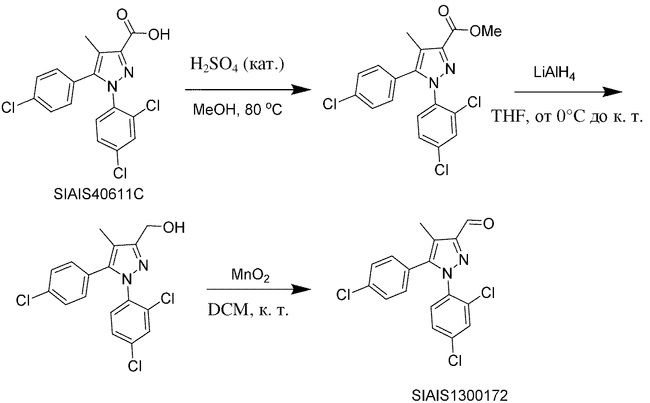
Стадия 1
[2120] В раствор SIAIS40611C (2,0 г, 5,2 ммоль) в 25 мл метанола добавляли 10 капель H2SO4 (конц.) и смесь нагревали с обратным холодильником при 70°C в течение 12 часов, пока раствор не становился прозрачным. Реакционную смесь гасили с помощью 50 мл воды и водную фазу экстрагировали с помощью DCM (50 мл × 2). Органическую фазу объединяли, последовательно промывали насыщенным раствором NaHCO3 и солевым раствором, выпаривали в вакууме с получением неочищенного продукта, который применяли на следующей стадии без дополнительной очистки.
Стадия 2
[2130] Вышеуказанный продукт растворяли в 25 мл THF и охлаждали до 0°C, к нему порциями добавляли LiAlH4 (0,20 г, 5,2 ммоль). Раствор нагревали естественным путем до комнатной температуры и выдерживали в течение 1 часа, после чего гасили с помощью 0,20 мл H2O, 0,20 мл 15% NaOH (водн.), 0,6 мл H2O. Смесь фильтровали и выпаривали в вакууме с получением неочищенного продукта, который применяли на следующей стадии без дополнительной очистки.
Стадия 3
[2140] Продукт стадии 2 растворяли в 50 мл DCM, к нему добавляли активированный MnO2 (4,5 г, 52 ммоль) и перемешивали в течение 12 часов при комнатной температуре. После израсходования исходного материала смесь фильтровали, концентрировали в вакууме и очищали с помощью колоночной хроматографии на силикагеле с получением SIAIS1300172 в виде белого твердого вещества (1,26 г, выход = 66%). 1H ЯМР (500 мГц, CDCl3) δ 10,06 (s, 1H), 7,38 (dd, J = 1,9, 0,6 Гц, 1H), 7,35-7,21 (m, 4H), 7,08-6,94 (m, 2H), 2,28 (s, 3H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C17H12Cl3N2O+ [M + H]+: 365,0010; обнаруженное значение: 365,0015.
Пример 15. Получение соединения 164
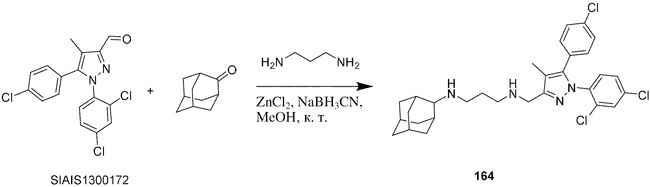
[2150] В раствор 2-адамантанона (25 мг, 0,16 ммоль) и 1,3-диаминопропана (12 мг, 0,16 ммоль) в 1 мл метанола добавляли молекулярные сита с размером пор 3Å (25 мг). После перемешивания в течение 1 часа в раствор добавляли SIAIS1300172 (20 мг, 0,055 ммоль) и его перемешивали еще в течение 15 мин., затем охлаждали до 0°C. Добавляли последовательно NaBH3CN (30 мг, 0,49 ммоль) и ZnCl2 (33 мг, 0,24 ммоль). Раствор выдерживали при 0°C в течение 2 часов и нагревали до комнатной температуры в течение ночи. Реакционную смесь гасили с помощью 10 мл воды и водную фазу экстрагировали с помощью EA (10 мл × 2). Органическую фазу объединяли, промывали солевым раствором и выпаривали в вакууме. Полученный остаток очищали с помощью препаративной HPLC с получением соединения 164 в виде белого твердого вещества (7,3 мг, выход = 21%). 1H ЯМР (500 мГц, CD3OD) δ 7,47 (d, J = 2,1 Гц, 1H), 7,41 (d, J = 8,4 Гц, 1H), 7,34 (dd, J = 8,5, 2,2 Гц, 1H), 7,26 (d, J = 8,0 Гц, 2H), 7,09 (d, J = 8,1 Гц, 2H), 4,30 (s, 2H), 3,33 (s, 1H), 3,22 (d, J = 6,9 Гц, 2H), 3,10 (t, J = 8,0 Гц, 2H), 2,22 (q, J = 8,4, 7,8 Гц, 2H), 2,11 (s, 2H), 2,07 (s, 3H), 1,99-1,92 (m, 2H), 1,88 (d, J = 12,4 Гц, 2H), 1,86-1,79 (m, 2H), 1,79-1,69 (m, 4H), 1,64 (d, J = 13,6 Гц, 2H). 13C ЯМР (126 мГц, CD3OD) δ 144,87, 144,09, 137,45, 137,18, 136,16, 134,07, 132,62, 132,17, 131,07, 129,93, 129,30, 128,81, 116,07, 64,72, 45,73, 43,95, 43,81, 38,04, 37,75, 31,16, 30,50, 28,35, 28,06, 23,87, 8,32. Рассч. с помощью HRMS (ESI) значение масса/заряд для C30H36Cl3N4+ [M + H]+: 557,2000; обнаруженное значение: 557,1995.
Пример 16. Получение соединения 165
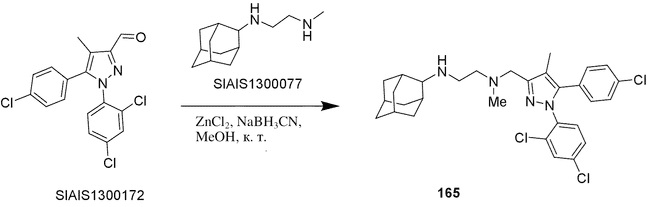
[2160] В раствор SIAIS1300172 (20 мг, 0,055 ммоль) в 1 мл метанола добавляли SIAIS1300077 (17 мг, 0,082 ммоль), смесь перемешивали в течение 15 мин. и затем охлаждали до 0°C. Последовательно добавляли NaBH3CN (30 мг, 0,49 ммоль) и ZnCl2 (33 мг, 0,24 ммоль) и реакционную среду выдерживали при 0°C в течение 2 часов, после чего нагревали до комнатной температуры. Реакцию осуществляли в течение ночи и затем реакционную смесь гасили с помощью 10 мл воды. Водную фазу экстрагировали с помощью EA (10 мл × 2) и органическую фазу объединяли, промывали солевым раствором и выпаривали в вакууме. Полученный остаток очищали с помощью препаративной HPLC с получением соединения 165 в виде белого твердого вещества (23 мг, выход = 67%). 1H ЯМР (500 мГц, CD3OD) δ 7,61 (dd, J = 5,3, 2,3 Гц, 2H), 7,46 (dt, J = 8,5, 2,1 Гц, 1H), 7,38 (dd, J = 8,6, 2,3 Гц, 2H), 7,25-7,16 (m, 2H), 4,60 (s, 2H), 3,65 (s, 2H), 3,50 (s, 1H), 3,32-3,29 (m, 2H), 3,11-3,00 (m, 3H), 2,22 (s, 5H), 2,08 (d, J = 14,2 Гц, 2H), 1,98 (d, J = 12,8 Гц, 2H), 1,91 (s, 2H), 1,82 (s, 4H), 1,73 (d, J = 13,8 Гц, 2H). 13C ЯМР (126 мГц, CD3OD) δ 144,40, 142,78, 137,33, 137,24, 136,23, 134,11, 132,80, 132,32, 131,01, 129,90, 129,29, 128,61, 117,97, 65,72, 52,46, 52,22, 41,56, 37,99, 37,67, 31,25, 30,48, 28,29, 28,02, 8,80. Рассч. с помощью HRMS (ESI) значение масса/заряд для C30H36Cl3N4+ [M + H]+: 557,2000; обнаруженное значение: 557,2000.
Пример 17. Получение соединения 166
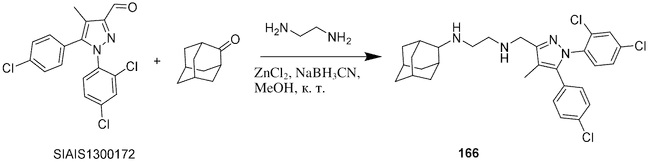
[2170] В раствор 2-адамантанона (42 мг, 0,28 ммоль) и этилендиамина (16 мг, 0,28 ммоль) в 1 мл метанола добавляли молекулярные сита с размером пор 3Å (25 мг) и перемешивали в течение 1 часа. Добавляли SIAIS1300172 (20 мг, 0,055 ммоль) и смесь перемешивали еще в течение 15 мин. После охлаждения до 0°C последовательно добавляли NaBH3CN (30 мг, 0,49 ммоль) и ZnCl2 (33 мг, 0,24 ммоль). Раствор выдерживали при 0°C в течение 2 часов и нагревали до комнатной температуры. Перемешивали в течение ночи, реакционную смесь гасили с помощью 10 мл воды и водную фазу экстрагировали с помощью EA (10 мл × 2). Органическую фазу объединяли, промывали солевым раствором и выпаривали в вакууме. Полученный остаток очищали с помощью препаративной HPLC с получением соединения 166 в виде белого твердого вещества (8,5 мг, выход = 25%). 1H ЯМР (500 мГц, CD3OD) δ 7,59 (d, J = 2,3 Гц, 1H), 7,51 (d, J = 8,5 Гц, 1H), 7,45 (dd, J = 8,4, 2,2 Гц, 1H), 7,41-7,33 (m, 2H), 7,23-7,14 (m, 2H), 4,47 (s, 2H), 3,68 (t, J = 6,9 Гц, 2H), 3,54-3,50 (m, 2H), 3,49 (s, 1H), 2,22 (s, 2H), 2,19 (s, 3H), 2,12-1,71 (m, 12H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C29H34Cl3N4+ [M + H]+, 543,1844; обнаруженное значение: 543,1838.
Пример 18. Получение соединения 167
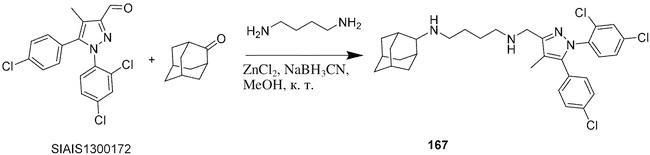
[2180] В раствор 2-адамантанона (25 мг, 0,16 ммоль) и 1,4-диаминобутана (9,7 мг, 0,11 ммоль) в 1 мл метанола добавляли молекулярные сита с размером пор 3Å (25 мг). После перемешивания в течение 1 часа добавляли SIAIS1300172 (20 мг, 0,055 ммоль), перемешивали еще в течение 15 мин. и затем охлаждали до 0°C. В раствор последовательно добавляли NaBH3CN (30 мг, 0,49 ммоль) и ZnCl2 (33 мг, 0,24 ммоль) при 0°C и выдерживали в течение 2 часов. Раствор нагревали до комнатной температуры и перемешивали в течение ночи. Реакционную смесь гасили с помощью 10 мл воды и экстрагировали с помощью EA (10 мл × 2). Органическую фазу объединяли, промывали солевым раствором и выпаривали в вакууме. Полученный остаток очищали с помощью препаративной HPLC с получением соединения 167 в виде белого твердого вещества (6,1 мг, выход = 17%). 1H ЯМР (500 мГц, CD3OD) δ 7,59 (d, J = 2,0 Гц, 1H), 7,50-7,43 (m, 2H), 7,42-7,34 (m, 2H), 7,26-7,12 (m, 2H), 4,37 (s, 2H), 3,41 (s, 1H), 3,25 (s, 2H), 3,10 (s, 2H), 2,19 (s, 2H), 2,16 (s, 3H), 2,05-1,71 (m, 16H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C31H38Cl3N4+ [M + H]+: 571,2157; обнаруженное значение: 571,2154.
Пример 19. Получение SIAIS230018
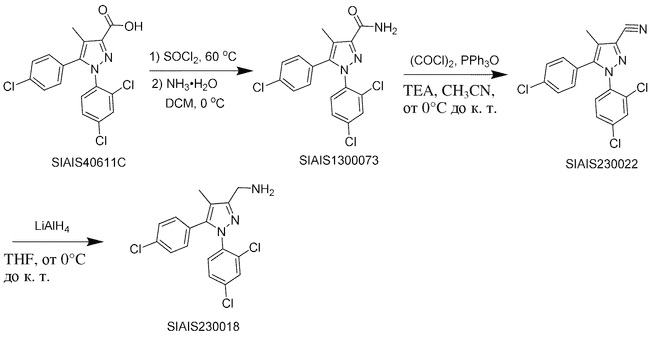
Стадия 1
[2190] Смешивали SIAIS40611C (0,50 г, 1,31 ммоль) с 2 мл SOCl2 и осуществляли реакцию при 60°C в течение 2 часов. После завершения реакции избыток SOCl2 удаляли в вакууме. Полученное твердое вещество растворяли в 5 мл DCM и охлаждали до 0°C, затем добавляли по каплям 5 мл NH3·H2O (водн.). Смесь нагревали до комнатной температуры и осуществляли реакцию в течение еще 1 часа. Смесь отделяли и водную фазу экстрагировали с помощью DCM (20 мл × 2). Органическую фазу объединяли, промывали солевым раствором и высушивали над безводным Na2SO4. Раствор фильтровали и концентрировали в вакууме с получением SIAIS1300073 в виде белого твердого вещества (0,45 г, выход = 90%).
Стадия 2
[2200] В раствор SIAIS1300073 (0,20 г, 0,52 ммоль) в 5 мл CH3CN добавляли Ph3PO (1,5 мг, 0,005 ммоль) и TEA (0,16 г, 1,56 ммоль). Смесь охлаждали до 0°C и добавляли по каплям оксалилхлорид (0,13 г, 1,04 ммоль). Раствор нагревали до комнатной температуры и перемешивали еще в течение 20 мин., затем концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле с получением SIAIS230022 в виде бесцветного масла (0,16 г, выход = 84%). 1H ЯМР (500 мГц, CDCl3) δ 7,36 (d, J = 2,1 Гц, 1H), 7,27-7,18 (m, 4H), 7,04-6,92 (m, 2H), 2,18 (s, 3H). 13C ЯМР (126 мГц, CDCl3) δ 142,22, 136,65, 135,66, 135,27, 132,74, 130,51, 130,45, 130,32, 129,20, 128,07, 127,76, 126,05, 121,01, 113,17, 8,81.
Стадия 3
Охлаждали раствор SIAIS230022 (0,28 г, 0,76 ммоль) в 10 мл THF до 0°C, в него добавляли порциями LiAlH4 (58 мг, 1,52 ммоль). Реакцию осуществляли в течение ночи. Реакционную смесь гасили с помощью 58 мкл H2O, 58 мкл 15% NaOH (водн.), 0,17 мл H2O. Смесь фильтровали и раствор концентрировали в вакууме. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле с получением SIAIS230018 в виде белого твердого вещества (0,22 г, выход = 80%). 1H ЯМР (500 мГц, DMSO-d6) δ 8,48 (s, 3H), 7,77 (dd, J = 1,8, 0,8 Гц, 1H), 7,58 (d, J = 1,8 Гц, 2H), 7,52-7,40 (m, 2H), 7,26-7,12 (m, 2H), 4,12 (d, J = 5,4 Гц, 2H), 2,09 (s, 3H). 13C ЯМР (126 мГц, DMSO-d6) δ 145,88, 141,56, 135,93, 134,71, 133,58, 131,82, 131,67, 130,86, 129,73, 128,85, 128,45, 127,55, 113,80, 34,58, 7,92. Рассч. с помощью HRMS (ESI) значение масса/заряд для C17H15Cl3N3+ [M + H]+: 366,0326; обнаруженное значение: 366,0321.
Пример 20. Получение соединения 10
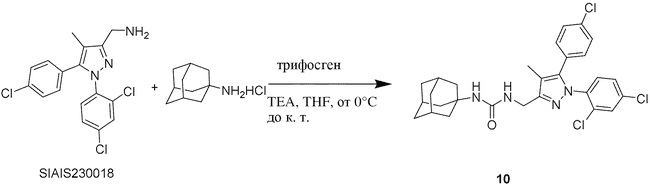
[2220] В раствор SIAIS230018 (25 мг, 0,068 ммоль) и гидрохлорида 1-адамантанамина (26 мг, 0,136 ммоль) в 2 мл THF добавляли TEA (69 мг, 0,68 ммоль). Смесь охлаждали до 0°C и в раствор добавляли трифосген (20 мг, 0,068 ммоль). Реакцию осуществляли в течение ночи и смесь очищали с помощью колоночной хроматографии на силикагеле с получением соединения 10 в виде белого твердого вещества (9,2 мг, выход = 25%). 1H ЯМР (500 мГц, CDCl3) δ 7,40 (d, J = 2,2 Гц, 1H), 7,29-7,21 (m, 4H), 7,04 (d, J = 8,5 Гц, 2H), 4,81 (t, J = 5,2 Гц, 1H), 4,40 (d, J = 5,2 Гц, 2H), 4,35 (s, 1H), 2,08 (s, 3H), 2,07-1,59 (m, 15H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C28H30Cl3N4O+ [M + H]+: 543,1480; обнаруженное значение: 543,1478.
Пример 21. Получение соединения 11
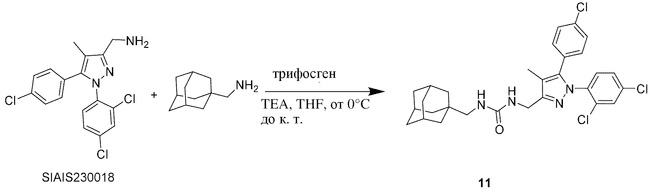
В раствор SIAIS230018 (25 мг, 0,068 ммоль) и 1-адамантанметиламина (23 мг, 0,136 ммоль) в 2 мл THF добавляли TEA (69 мг, 0,68 ммоль). Смесь охлаждали до 0°C и в раствор добавляли трифосген (20 мг, 0,068 ммоль). Полученное перемешивали в течение ночи и смесь очищали с помощью колоночной хроматографии на силикагеле с получением соединения 11 в виде белого твердого вещества (11,7 мг, выход = 31%). 1H ЯМР (500 мГц, CDCl3) δ 7,41 (d, J = 2,2 Гц, 1H), 7,34-7,19 (m, 4H), 7,12-7,01 (m, 2H), 4,98 (t, J = 5,3 Гц, 1H), 4,76 (s, 1H), 4,44 (d, J = 5,1 Гц, 2H), 2,88 (d, J = 6,0 Гц, 2H), 2,09 (d, J = 1,5 Гц, 3H), 1,99-1,52 (m, 15H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C29H32Cl3N4O+ [M + H]+: 557,1636; обнаруженное значение: 557,1628.
Пример 22. Получение соединения 12
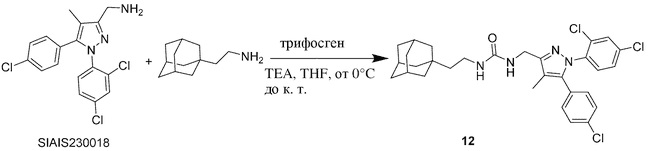
[2240] В раствор SIAIS230018 (25 мг, 0,068 ммоль) и 2-(1-адамантил)этанамина (24 мг, 0,136 ммоль) в 2 мл THF добавляли TEA (69 мг, 0,68 ммоль). Смесь охлаждали до 0°C и в раствор добавляли трифосген (20 мг, 0,068 ммоль). Полученное перемешивали в течение ночи и смесь очищали с помощью колоночной хроматографии на силикагеле с получением соединения 12 в виде белого твердого вещества (9,7 мг, выход = 25%). 1H ЯМР (500 мГц, CDCl3) δ 7,41 (d, J = 2,2 Гц, 1H), 7,34-7,19 (m, 4H), 7,10-7,00 (m, 2H), 4,93 (t, J = 5,3 Гц, 1H), 4,48 (s, 1H), 4,44 (d, J = 5,2 Гц, 2H), 3,25-3,14 (m, 2H), 2,09 (s, 3H), 2,01-1,40 (m, 17H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C30H34Cl3N4O+ [M + H]+: 571,1793; обнаруженное значение: 571,1792.
Пример 23. Получение SIAIS230032
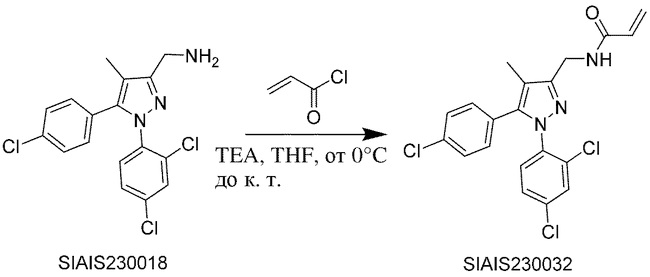
[2250] Охлаждали раствор SIAIS230018 (50 мг, 0,14 ммоль) в 2 мл THF до 0°C, в него последовательно добавляли TEA (44 мг, 0,34 ммоль), акрилилхлорид (19 мг, 0,20 ммоль). Реакцию осуществляли в течение ночи и раствор концентрировали в вакууме. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле с получением SIAIS230032 в виде белого твердого вещества (50 мг, выход = 87%). 1H ЯМР (500 мГц, CDCl3) δ 7,34 (d, J = 2,1 Гц, 1H), 7,25-7,15 (m, 4H), 7,03-6,95 (m, 2H), 6,27 (dd, J = 17,0, 1,5 Гц, 1H), 6,25 (s, 1H), 6,09 (dd, J = 17,0, 10,3 Гц, 1H), 5,60 (dd, J = 10,3, 1,4 Гц, 1H), 4,55 (d, J = 5,1 Гц, 2H), 2,02 (s, 3H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C20H17Cl3N3O+ [M + H]+: 420,0432; обнаруженное значение: 420,0429.
Пример 24. Получение соединения 168
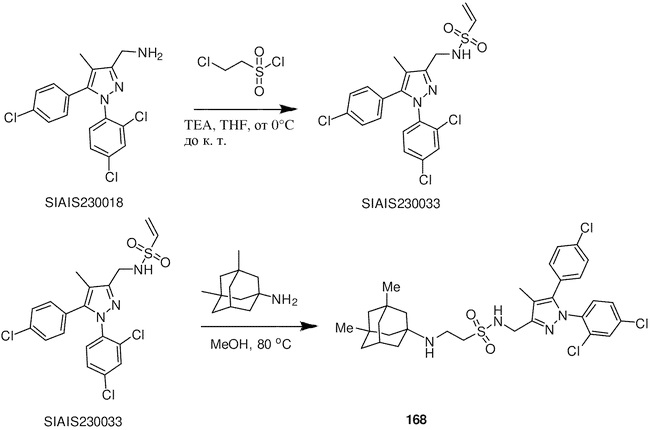
Стадия 1
[2260] Охлаждали раствор SIAIS230018 (50 мг, 0,14 ммоль) в 2 мл THF до 0°C и последовательно добавляли TEA (44 мг, 0,34 ммоль) и 2-хлорэтансульфонилхлорид (24 мг, 0,15 ммоль). Реакцию осуществляли в течение ночи и раствор концентрировали в вакууме. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле с получением SIAIS230033 в виде белого твердого вещества (37 мг, выход = 59%). 1H ЯМР (500 мГц, CDCl3) δ 7,34 (d, J = 2,2 Гц, 1H), 7,23-7,19 (m, 4H), 7,15 (d, J = 8,5 Гц, 1H), 7,00-6,95 (m, 2H), 6,48 (dd, J = 16,5, 10,0 Гц, 1H), 6,22 (d, J = 16,6 Гц, 1H), 5,87 (d, J = 9,9 Гц, 1H), 4,22 (d, J = 5,5 Гц, 2H), 2,02 (s, 3H). 13C ЯМР (126 мГц, CDCl3) δ 147,79, 142,23, 136,12, 135,70, 135,62, 134,75, 132,91, 130,58, 130,51, 130,27, 128,91, 127,90, 127,61, 126,86, 113,66, 39,54, 8,23. Рассч. с помощью HRMS (ESI) значение масса/заряд для C19H17Cl3N3O2S+ [M + H]+: 456,0102; обнаруженное значение: 456,0095.
Стадия 2
В раствор SIAIS230033 (10 мг, 0,022 ммоль) в 1 мл метанола добавляли мемантин (8,1 мг, 0,045 ммоль). Смесь нагревали с обратным холодильником в течение 24 часов и затем очищали с помощью препаративной HPLC. Соединение 168 получали в виде белого твердого вещества (8,6 мг, выход = 58%). 1H ЯМР (500 мГц, CD3OD) δ 7,65-7,57 (m, 1H), 7,46 (dd, J = 3,5, 2,1 Гц, 2H), 7,36 (d, J = 8,5 Гц, 2H), 7,17 (d, J = 8,5 Гц, 2H), 4,42 (s, 2H), 3,44 (d, J = 1,2 Гц, 4H), 2,29-2,21 (m, 1H), 2,14 (s, 3H), 1,70 (s, 2H), 1,58-1,44 (m, 4H), 1,46-1,33 (m, 4H), 1,33-1,13 (m, 2H), 0,92 (s, 6H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C31H38Cl3N4O2S+ [M + H]+: 635,1776; обнаруженное значение: 635,1770.
Пример 25. Получение соединения 169
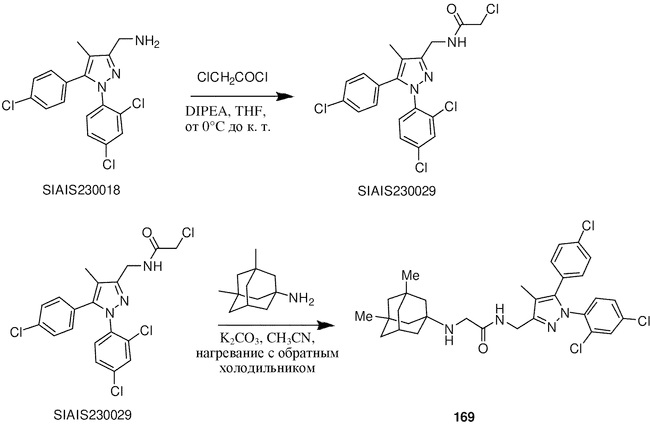
Стадия 1
[2280] Охлаждали раствор SIAIS230018 (100 мг, 0,27 ммоль) в 5 мл THF до 0°C. В раствор последовательно добавляли DIPEA (87 мг, 0,68 ммоль) и хлорацетилхлорид (46 мг, 0,41 ммоль). Реакцию осуществляли в течение ночи и раствор концентрировали в вакууме. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле с получением SIAIS230029 в виде белого твердого вещества (0,11 г, выход = 91%). 1H ЯМР (500 мГц, CDCl3) δ 7,35 (d, J = 2,1 Гц, 1H), 7,26-7,15 (m, 4H), 7,10 (s, 1H), 7,03-6,93 (m, 2H), 4,52 (d, J = 5,1 Гц, 2H), 4,04 (s, 2H), 2,02 (s, 3H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C19H16Cl4N3O+ [M + H]+: 442,0042; обнаруженное значение: 442,0032.
Стадия 2
[2290] В раствор SIAIS230029 (10 мг, 0,023 ммоль) в 1 мл CH3CN добавляли мемантин (8,1 мг, 0,045 ммоль) и K2CO3 (4,7 мг, 0,035 ммоль). Смесь нагревали с обратным холодильником в течение 24 часов и очищали с помощью препаративной HPLC. Соединение 169 получали в виде белого твердого вещества (12 мг, выход = 85%). 1H ЯМР (500 мГц, CD3OD) δ 7,57 (d, J = 2,0 Гц, 1H), 7,49-7,40 (m, 2H), 7,40-7,32 (m, 2H), 7,21-7,03 (m, 2H), 4,56 (s, 2H), 3,79 (s, 2H), 2,32-2,21 (m, 1H), 2,11 (s, 3H), 1,76 (d, J = 3,2 Гц, 2H), 1,64-1,45 (m, 4H), 1,42 (d, J = 3,0 Гц, 4H), 1,35-1,13 (m, 2H), 0,93 (s, 6H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C31H36Cl3N4O+ [M + H]+: 585,1949; обнаруженное значение: 585,1950.
Пример 26. Получение соединения 170
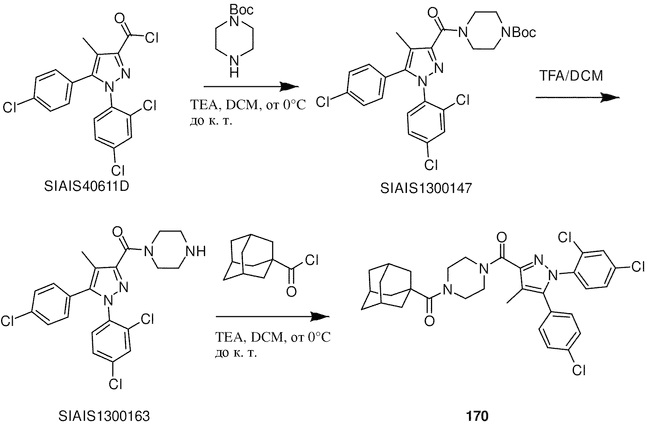
Стадия 1
[2300] Охлаждали раствор SIAIS40611D (0,52 г, 1,31 ммоль) в 15 мл DCM до 0°C. В него добавляли 1-Boc-пиперазин (0,24 г, 1,3 ммоль) и TEA (0,14 г, 1,4 ммоль). Обеспечивали осуществление реакции в смеси в течение ночи и затем ее очищали с помощью колоночной хроматографии на силикагеле с получением SIAIS1300147 в виде белого твердого вещества (0,67 г, выход = 94%). 1H ЯМР (500 мГц, CDCl3) δ 7,38 (d, J = 2,2 Гц, 1H), 7,25-7,21 (m, 2H), 7,19-7,17 (m, 1H), 7,09 (d, J = 8,5 Гц, 1H), 7,05-6,95 (m, 2H), 3,73 (dt, J = 20,5, 5,1 Гц, 4H), 3,44 (dt, J = 24,1, 5,1 Гц, 4H), 2,14 (s, 3H), 1,41 (s, 9H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C26H28Cl3N4O3+ [M + H]+: 549,1222; обнаруженное значение: 549,1222.
Стадия 2
[2310] Растворяли SIAIS1300147 (0,20 г, 0,36 ммоль) в растворе DCM/TFA (1 мл/1 мл) и осуществляли реакцию в течение ночи. Раствор концентрировали в вакууме и очищали с помощью колонки с обращенной фазой с получением SIAIS1300163 в виде белого твердого вещества (0,13 г, выход = 79%). 1H ЯМР (500 мГц, CD3OD) δ 7,63 (d, J = 2,0 Гц, 1H), 7,47-7,42 (m, 2H), 7,41-7,37 (m, 2H), 7,22-7,18 (m, 2H), 4,09 (d, J = 63,8 Гц, 4H), 3,36-3,32 (m, 4H), 2,19 (s, 3H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C21H20Cl3N4O+ [M + H]+: 449,0697; обнаруженное значение: 449,0703.
Стадия 3
[2320] Охлаждали раствор 1-адамантанкарбонилхлорида (12 мг, 0,067 ммоль) в 2 мл DCM до 0°C. В него добавляли SIAIS1300163 (20 мг, 0,044 ммоль) и TEA (14 мг, 0,134 ммоль) и естественным путем нагревали раствор до комнатной температуры. Обеспечивали осуществление реакции в смеси в течение 12 часов и растворитель удаляли в вакууме. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле с получением соединения 170 в виде белого твердого вещества (8,6 мг, выход = 32%). 1H ЯМР (500 мГц, CDCl3) δ 7,39 (d, J = 2,3 Гц, 1H), 7,28-7,21 (m, 3H), 7,11 (d, J = 8,5 Гц, 1H), 7,06-6,95 (m, 2H), 3,79 (d, J = 5,6 Гц, 2H), 3,74 (s, 4H), 3,66 (t, J = 5,2 Гц, 2H), 2,14 (s, 3H), 1,99 (s, 3H), 1,94 (d, J = 2,8 Гц, 6H), 1,73-1,63 (m, 6H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C32H34Cl3N4O2+ [M + H]+: 611,1742; обнаруженное значение: 611,1734.
Пример 27. Получение соединения 171
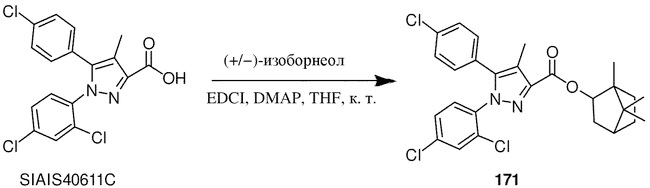
[2330] Последовательно добавляли SIAIS40611C (0,13 г, 0,34 ммоль), (±)-изоборнеол (0,05 г, 0,32 ммоль), DMAP (10 мг) и EDCI (0,068 г, 0,35 ммоль) к 3 мл THF и смесь перемешивали при комнатной температуре в течение 12 часов. После израсходования исходного материала реакционную смесь гасили с помощью 5 мл воды и водную фазу экстрагировали с помощью EA (10 мл × 3). Органическую фазу объединяли, промывали солевым раствором и высушивали над безводным Na2SO4. Раствор фильтровали и концентрировали в вакууме. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле с получением соединения 171 в виде белого твердого вещества (0,10 г, выход = 60%). 1H ЯМР (500 мГц, CDCl3) δ 7,38 (d, J = 2,2 Гц, 1H), 7,32 (t, J = 5,8 Гц, 1H), 7,31-7,28 (m, 3H), 7,07-7,05 (m, 2H), 5,00 (dd, J = 7,5, 4,3 Гц, 1H), 2,30 (s, 3H), 1,97 (dd, J = 10,1, 5,9 Гц, 1H), 1,79 (q, J = 4,2 Гц, 1H), 1,76-1,70 (m, 1H), 1,69 (s, 1H), 1,65-1,58 (m, 1H), 1,28-1,23 (m, 1H), 1,18-1,12 (m, 1H), 1,10 (s, 3H), 0,99 (s, 3H), 0,88 (s, 4H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C27H28Cl3N2O2 [M+H]+: 517,1216; обнаруженное значение: 517,1209.
Пример 28. Получение соединения 172
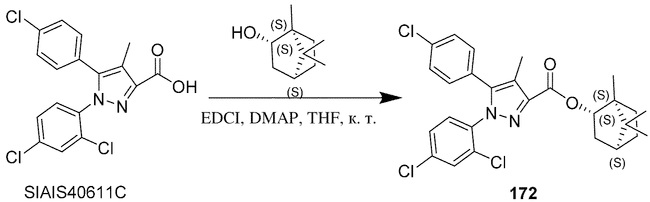
[2340] Соединение 172 получали в соответствии с процедурой, подобной описанной в примере 27, с применением (-)-борнеола в качестве исходного материала (белое твердое вещество, выход = 50%). 1H ЯМР (500 мГц, CDCl3) δ 7,38 (d, J = 2,2 Гц, 1H), 7,36-7,34 (m, 1H), 7,32-7,28 (m, 3H), 7,09-7,05 (m, 2H), 5,22 (ddd, J = 9,9, 3,4, 2,2 Гц, 1H), 2,54-2,47 (m, 1H), 2,33 (s, 3H), 2,17-2,11 (m, 1H), 1,83-1,76 (m, 1H), 1,74 (t, J = 4,5 Гц, 1H), 1,43-1,38 (m, 1H), 1,35-1,29 (m, 1H), 1,20 (dd, J = 13,9, 3,5 Гц, 1H), 0,98 (s, 3H), 0,95 (s, 3H), 0,92 (s, 3H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C27H28Cl3N2O2+ [M+H]+: 517,1216; обнаруженное значение: 517,1212.
Пример 29. Получение соединения 173
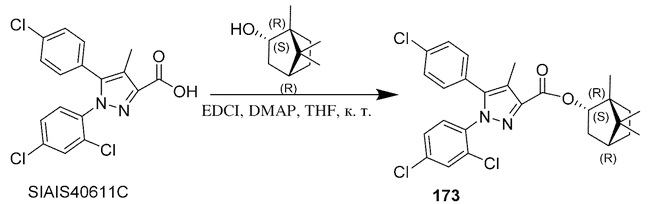
[2350] Соединение 173 получали в соответствии с процедурой, подобной описанной в примере 27, с применением (+)-борнеола в качестве исходного материала. (белое твердое вещество, выход = 65%). 1H ЯМР (500 мГц, CDCl3) δ 7,38 (d, J = 2,2 Гц, 1H), 7,37-7,34 (m, 1H), 7,29 (td, J = 6,9, 3,4 Гц, 3H), 7,07 (d, J = 8,4 Гц, 2H), 5,31-5,09 (m, 1H), 2,54-2,47 (m, 1H), 2,33 (s, 3H), 2,17-2,11 (m, 1H), 1,83-1,76 (m, 1H), 1,74 (t, J = 4,4 Гц, 1H), 1,43-1,38 (m, 1H), 1,35-1,30 (m, 1H), 1,20 (dd, J = 13,8, 3,5 Гц, 1H), 0,98 (s, 3H), 0,95 (s, 3H), 0,92 (s, 3H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C27H28Cl3N2O2+ [M+H]+: 517,1216; обнаруженное значение: 517,1207.
Пример 30. Получение соединения 174
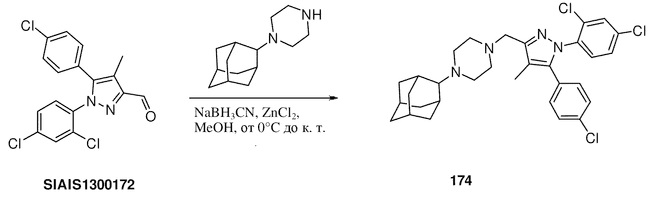
[2360] Соединение 174 получали в соответствии с процедурой, подобной описанной в примере 16. (белое твердое вещество, выход = 70%), 1H ЯМР (500 мГц, CD3OD) δ 7,58 (d, J = 8,6 Гц, 2H), 7,44 (dd, J = 8,7, 2,2 Гц, 1H), 7,38 (d, J = 8,2 Гц, 2H), 7,21 (d, J = 8,2 Гц, 2H), 4,52 (s, 2H), 4,04 (s, 2H), 3,85 (s, 4H), 3,55-3,30 (m, 3H), 2,43 (s, 2H), 2,20 (s, 3H), 2,25-2,15 (m, 2H), 2,06 (d, J = 12,9 Гц, 2H), 1,94 (d, J = 11,4 Гц, 2H), 1,86 (d, J = 15,1 Гц, 4H), 1,74 (d, J = 13,6 Гц, 2H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C31H36Cl3N4+ [M+H]+: 569,2000; обнаруженное значение: 569,2078.
Пример 31. Получение соединения 175
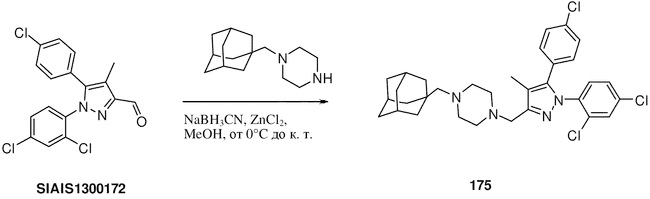
[2370] Соединение 175 получали в соответствии с процедурой, подобной описанной в примере 16, с применением 1-(((3r,5r,7r)-адамантан-1-ил)метил)пиперазина в качестве исходного материала вместо указанного. 1H ЯМР (500 мГц, CD3OD) δ 7,60 (s, 1H), 7,55 (dd, J = 14,4, 8,5 Гц, 1H), 7,44 (d, J = 8,5 Гц, 1H), 7,38 (d, J = 8,0 Гц, 2H), 7,21 (d, J = 8,3 Гц, 2H), 4,42 (d, J = 30,7 Гц, 2H), 3,90-3,70 (br, s, 4H), 3,70-3,30 (br, s, 4H), 2,96 (s, 2H), 2,20 (s, 3H), 2,04 (s, 3H), 1,85-1,70 (m, 12H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C32H38Cl3N4+ [M+H]+: 583,2157; обнаруженное значение: 583,2215.
Пример 32. Получение соединения 178
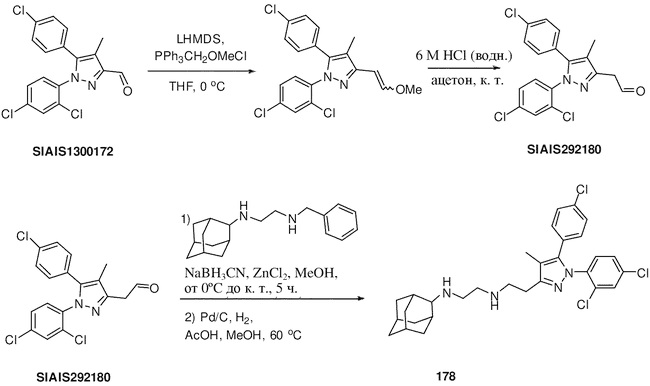
[2380] Стадия 1. Растворяли хлорид (метоксиметил)трифенилфосфония (200 мг, 0,58 ммоль) в 8 мл безводного THF и охлаждали до -78°C. К нему добавляли по каплям раствор 1 м LHMDS в THF (0,84 мл, 0,84 ммоль). Естественным путем нагревали до 0°C, затем добавляли SIAS292180 (212 мг, 0,58 ммоль) и осуществляли реакцию в течение ночи. Реакционную смесь гасили водой и органическую фазу экстрагировали с помощью DCM (20 мл × 3). Органический раствор выпаривали и остаток очищали с помощью колоночной хроматографии на силикагеле.
Вышеуказанный продукт растворяли в ацетоне и подвергали гидролизу с помощью 6 м HCl (водн.) в течение 4 ч. с получением соединения SIAIS292180 в виде белого твердого вещества (0,13 г, выход = 58%). Рассч. с помощью MS (ESI) значение масса/заряд для C18H14Cl3N2O+ [M+H]+: 379,02; обнаруженное значение: 379,14.
[2390] Стадия 2. Соединение 178 получали в соответствии с процедурой, подобной описанной в примере 16, с применением N1-((1r,3r,5r,7r)-адамантан-2-ил)-N2-бензилэтан-1,2-диамина в качестве исходного материала вместо указанного и с последующим гидрированием в растворе MeOH при 60°C в течение 24 ч. 1H ЯМР (500 мГц, CD3OD) δ 7,62 (s, 1H), 7,57 (d, J = 8,5 Гц, 1H), 7,47 (d, J = 8,5 Гц, 1H), 7,38 (d, J = 7,8 Гц, 2H), 7,22 (d, J = 7,9 Гц, 2H), 4,56 (s, 2H), 3,82 (s, 2H), 3,41 (s, 1H), 3,04 (s, 2H), 2,97 (s, 2H), 2,41 (s, 2H), 2,20 (s, 3H), 2,00 (d, J = 13,3 Гц, 3H), 1,88 (d, J = 17,5 Гц, 3H), 1,78 (s, 4H), 1,67 (s, 2H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C30H36Cl3N4+ [M+H]+: 557,2000; обнаруженное значение: 557,1998.
Пример 33. Получение соединения 179
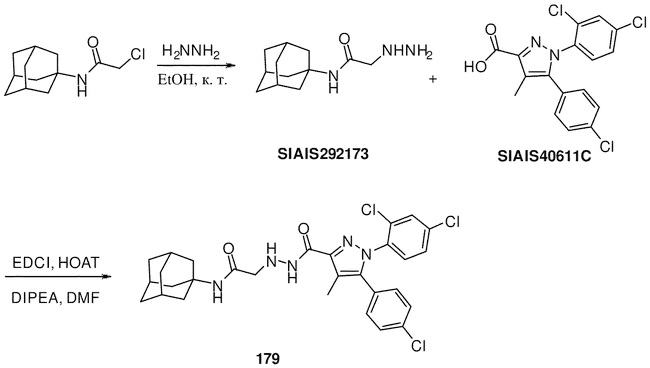
[2400] Стадия 1. SIAIS292173 получали в соответствии с процедурой, подобной процедуре для SIAIS1300093, с применением гидрата гидразина вместо NaN3, с применением EtOH в качестве растворителя, и реакцию осуществляли при комнатной температуре.
Стадия 2. Соединение 179 получали с применением процедуры, подобной процедуре, описанной в примере 13. 1H ЯМР (500 мГц, CD3OD) δ 7,56 (s, 1H), 7,52 (d, J = 8,5 Гц, 1H), 7,44 (d, J = 8,3 Гц, 1H), 7,37 (d, J = 8,2 Гц, 2H), 7,20 (d, J = 8,2 Гц, 2H), 3,44 (s, 2H), 2,32 (s, 3H), 2,13-1,97 (m, 9H), 1,72 (d, J = 2,9 Гц, 6H). Рассч. с помощью HRMS (ESI) значение масса/заряд для C29H31Cl3N5O2+ [M+H]+: 586,1538; обнаруженное значение: 586,1540.
Пример испытания биологической активности 1
[2420] Микропланшетный способ с использованием резазурина применяли для измерения MIC (минимальной ингибирующей концентрации) низкомолекулярных ингибиторов MmpL3 в отношении Mycobacterium smegmatis.
[2430] Эксперимент осуществляли в соответствии со способами, описанными в литературных источниках (SQ109 targets MmpL3, a membrane transporter of trehalose monomycolate involved in mycolic acid donation to the cell wall core of Mycobacterium tuberculosis. [J] Antimicrobial Agents and Chemotherapy, 2012, 4 (56) 1797-1809).
[2440] (1) Получение жидкого материала для посева: Штамм Mycobacterium smegmatis (mc2155) выращивали в жидкой среде 7H9 (агар 7H9, 50% глицерина, 0,05% Tween 80 и 10,05% ADS) в соотношении 1:100 на стерильном рабочем столе, подвергали колебаниям при 37°C, 220 об/мин. После достижения OD600 значения 1,0 клетки центрифугировали при 8000 об/мин в течение 10 мин и собирали путем добавления 1 мл 50% глицерина (стерилизованного) и 1 мл жидкой среды 7H9 на стерильном рабочем столе. Штаммы замораживали при -80°C после упаковки по частям. Жидкий материал для посева представлял собой штамм Mycobacterium smegmatis (mc2155), подвергавшийся выращиванию до OD600=1,0, свежесть которого поддерживали путем обновления каждые три недели.
[2450] (2) Активация жидкого материала для посева: жидкий материал для посева инокулировали в 5 мл жидкой среды 7H9 в соотношении 1:100 на стерильном рабочем столе и подвергали колебаниям при 37°C, 220 об/мин до достижения значения OD600, составлявшего 0,5 (фаза логарифмического роста). OD600 культивируемых бактерий доводили до 0,15 с помощью жидкой среды 7H9 и затем разбавляли 100-кратно для применения.
[2460] (3) Разбавление соединения из положительного контроля, представляющего собой римонабант: римонабант применяли в качестве положительного контроля в ходе эксперимента. Римонабант представляет собой ингибитор каннабиноидного рецептора типа I (CB1), новый тип лекарственного препарата для похудения, вышедший на рынок. Исследования показали, что римонабант также является ингибитором MmpL3 и обладает значительным ингибирующим эффектом в отношении Mycobacterium tuberculosis (H37Rv). Римонабант получали в следующих градиентных разбавлениях: 543,9024392 мкг/мл, 271,9512196 мкг/мл, 135,9756098 мкг/мл, 67,98780492 мкг/мл, 33,99390246 мкг/мл, 16,99695123 мкг/мл, 8,498475615 мкг/мл, 4,249237808 мкг/мл, 2,124618904 мкг/мл, 1,062309452 мкг/мл, 0,531154726 мкг/мл, 0,265577363 мкг/мл. Как правило, шестой градиент разбавления гарантированно представлял собой минимальную ингибирующую концентрацию соединения в отношении штаммов дикого типа. MIC римонабанта в отношении штамма M. smegmatis составляет 16,99695123 мкг/мл.
[2470] (4) Разбавление низкомолекулярных ингибиторов мембранного белка Mycobacterium MmpL3: соединения разбавляли в соответствии с 2-кратным градиентным разбавлением. Градиентные разбавления для каждого низкомолекулярного соединения приведены в виде следующего перечня. Градиентные разбавления соединения 17 представляли собой 380,48 мкг/мл, 190,24 мкг/мл, 95,12 мкг/мл, 47,56 мкг/мл, 23,78 мкг/мл, 11,89 мкг/мл, 5,945 мкг/мл, 2,9725 мкг/мл, 1,48625 мкг/мл, 0,743125 мкг/мл, 0,3715625 мкг/мл, 0,18578125 мкг/мл; градиентные разбавления соединения 76 представляли собой 468,288 мкг/мл, 234,144 мкг/мл, 117,072 мкг/мл, 58,536 мкг/мл, 29,268 мкг/мл, 14,634 мкг/мл, 7,317 мкг/мл, 3,6585 мкг/мл, 1,82925 мкг/мл, 0,914625 мкг/мл, 0,4573125 мкг/мл, 0,22865625 мкг/мл; градиентные разбавления соединения 77 представляли собой 331,52 мкг/мл, 165,76 мкг/мл, 82,88 мкг/мл, 41,44 мкг/мл, 20,72 мкг/мл, 10,36 мкг/мл, 5,18 мкг/мл, 2,59 мкг/мл, 1,295 мкг/мл, 0,6475 мкг/мл, 0,32375 мкг/мл, 0,161875 мкг/мл; градиентные разбавления соединения 74 представляли собой 107,32 мкг/мл, 53,66 мкг/мл, 26,83 мкг/мл, 13,415 мкг/мл, 6,7075 мкг/мл, 3,35375 мкг/мл, 1,676875 мкг/мл, 0,8384375 мкг/мл, 0,41921875 мкг/мл, 0,209609375 мкг/мл; градиентные разбавления соединения 18 представляли собой 97,56 мкг/мл, 48,78 мкг/мл, 24,39 мкг/мл, 12,195 мкг/мл, 6,0975 мкг/мл, 3,04875 мкг/мл, 1,524375 мкг/мл, 0,7621875 мкг/мл, 0,38109375 мкг/мл, 0,190546875 мкг/мл; градиентные разбавления соединения 19 представляли собой 107,32 мкг/мл, 53,66 мкг/мл, 26,83 мкг/мл, 13,415 мкг/мл, 6,7075 мкг/мл, 3,35375 мкг/мл, 1,676875 мкг/мл, 0,8384375 мкг/мл, 0,41921875 мкг/мл, 0,209609375 мкг/мл; градиентные разбавления соединения 163 представляли собой 117,0732 мкг/мл, 58,5366 мкг/мл, 29,2683 мкг/мл, 14,6341 мкг/мл, 7,3171 мкг/мл, 3,6585 мкг/мл, 1,8293 мкг/мл, 0,9146 мкг/мл, 0,4573 мкг/мл, 0,2287 мкг/мл, 0,1143 мкг/мл, 0,0572 мкг/мл; градиентные разбавления соединения 23 представляли собой 117,0732 мкг/мл, 58,5366 мкг/мл, 29,2683 мкг/мл, 14,6341 мкг/мл, 7,3171 мкг/мл, 3,6585 мкг/мл, 1,8293 мкг/мл, 0,9146 мкг/мл, 0,4573 мкг/мл, 0,2287 мкг/мл, 0,1143 мкг/мл, 0,0572 мкг/мл; градиентные разбавления соединения 164 представляли собой 207,3171 мкг/мл, 103,6585 мкг/мл, 51,8293 мкг/мл, 25,9146 мкг/мл, 12,9573 мкг/мл, 6,4787 мкг/мл, 3,2393 мкг/мл, 1,6197 мкг/мл, 0,8098 мкг/мл, 0,4049 мкг/мл, 0,2025 мкг/мл, 0,1012 мкг/мл; градиентные разбавления соединения 165 представляли собой 231,7073 мкг/мл, 115,8537 мкг/мл, 57,9268 мкг/мл, 28,9634 мкг/мл, 14,4817 мкг/мл, 7,2409 мкг/мл, 3,6204 мкг/мл, 1,8102 мкг/мл, 0,9051 мкг/мл, 0,4526 мкг/мл, 0,2263 мкг/мл, 0,1131 мкг/мл; градиентные разбавления соединения 10 представляли собой 170,7317 мкг/мл, 85,3659 мкг/мл, 42,6829 мкг/мл, 21,3415 мкг/мл, 10,6707 мкг/мл, 5,3354 мкг/мл, 2,6677 мкг/мл, 1,3338 мкг/мл, 0,6669 мкг/мл, 0,3335 мкг/мл, 0,1667 мкг/мл, 0,0834 мкг/мл; градиентные разбавления соединения 11 представляли собой 134,1463 мкг/мл, 67,0732 мкг/мл, 33,5366 мкг/мл, 16,7683 мкг/мл, 8,3841 мкг/мл, 4,1921 мкг/мл, 2,0960 мкг/мл, 1,0480 мкг/мл, 0,5240 мкг/мл, 0,2620 мкг/мл, 0,1310 мкг/мл, 0,0655 мкг/мл; градиентные разбавления соединения 12 представляли собой 121,9512 мкг/мл, 60,9756 мкг/мл, 30,4878 мкг/мл, 15,2439 мкг/мл, 7,6220 мкг/мл, 3,8110 мкг/мл, 1,9055 мкг/мл, 0,9527 мкг/мл, 0,4764 мкг/мл, 0,2382 мкг/мл, 0,1191 мкг/мл, 0,0595 мкг/мл; градиентные разбавления соединения 171 представляли собой 200,0000 мкг/мл, 100,0000 мкг/мл, 50,0000 мкг/мл, 25,0000 мкг/мл, 12,5000 мкг/мл, 6,2500 мкг/мл, 3,1250 мкг/мл, 1,5625 мкг/мл, 0,7813 мкг/мл, 0,3906 мкг/мл, 0,1953 мкг/мл, 0,0977 мкг/мл; градиентные разбавления соединения 172 представляли собой 337,8049 мкг/мл, 168,9024 мкг/мл, 84,4512 мкг/мл, 42,2256 мкг/мл, 21,1128 мкг/мл, 10,5564 мкг/мл, 5,2782 мкг/мл, 2,6391 мкг/мл, 1,3196 мкг/мл, 0,6598 мкг/мл, 0,3299 мкг/мл, 0,1649 мкг/мл; градиентные разбавления соединения 173 представляли собой 231,7073 мкг/мл, 115,8537 мкг/мл, 57,9268 мкг/мл, 28,9634 мкг/мл, 14,4817 мкг/мл, 7,2409 мкг/мл, 3,6204 мкг/мл, 1,8102 мкг/мл, 0,9051 мкг/мл, 0,4526 мкг/мл, 0,2263 мкг/мл, 0,1131 мкг/мл; градиентные разбавления соединения 166 представляли собой 243,9024 мкг/мл, 121,9512 мкг/мл, 60,9756 мкг/мл, 30,4878 мкг/мл, 15,2439 мкг/мл, 7,6220 мкг/мл, 3,8110 мкг/мл, 1,9055 мкг/мл, 0,9527 мкг/мл, 0,4764 мкг/мл, 0,2382 мкг/мл, 0,1191 мкг/мл; градиентные разбавления соединения 167 представляли собой 268,2927 мкг/мл, 134,1463 мкг/мл, 67,0732 мкг/мл, 33,5366 мкг/мл, 16,7683 мкг/мл, 8,3841 мкг/мл, 4,1921 мкг/мл, 2,0960 мкг/мл, 1,0480 мкг/мл, 0,5240 мкг/мл, 0,2620 мкг/мл, 0,1310 мкг/мл; градиентные разбавления соединения 169 представляли собой 243,9024 мкг/мл, 121,9512 мкг/мл, 60,9756 мкг/мл, 30,4878 мкг/мл, 15,2439 мкг/мл, 7,6220 мкг/мл, 3,8110 мкг/мл, 1,9055 мкг/мл, 0,9527 мкг/мл, 0,4764 мкг/мл, 0,2382 мкг/мл, 0,1191 мкг/мл; градиентные разбавления соединения 168 представляли собой 341,4634 мкг/мл, 170,7317 мкг/мл, 85,3659 мкг/мл, 42,6829 мкг/мл, 21,3415 мкг/мл, 10,6707 мкг/мл, 5,3354 мкг/мл, 2,6677 мкг/мл, 1,3338 мкг/мл, 0,6669 мкг/мл, 0,3335 мкг/мл, 0,1667 мкг/мл; градиентные разбавления соединения 170 представляли собой 292,6829 мкг/мл, 146,3415 мкг/мл, 73,1707 мкг/мл, 36,5854 мкг/мл, 18,2927 мкг/мл, 9,1463 мкг/мл, 4,5732 мкг/мл, 2,2866 мкг/мл, 1,1433 мкг/мл, 0,5716 мкг/мл, 0,2858 мкг/мл, 0,1429 мкг/мл.
[2480] (5) Добавляли 40 мкл жидкой среды 7H9 (содержащей Tween-80 и ADS) в 96-луночные планшеты. Для каждого градиента устанавливали три повторности. Добавляли 2 мкл соединений с различными градиентами и 40 мкл разбавленных культивированных бактерий (mc2155) и перемешивали путем острожного встряхивания. Планшеты инкубировали в инкубаторе при 37°C в течение 48 часов.
[2490] (6) Добавляли 0,02% (вес/об.) раствор резазурина в лунки на стерильном рабочем столе и продолжали инкубировать планшеты в инкубаторе в течение 4 часов. Рост бактерий наблюдали под инвертированным микроскопом. MIC определяли как минимальную концентрацию соединения, при которой останавливался рост бактерий. Резазурин имел розовую окраску при остановке роста бактерий и голубую окраску при продолжении роста.
Пример испытания биологической активности 2
[2500] Микропланшетный способ с использованием резазурина применяли для измерения MIC низкомолекулярных ингибиторов MmpL3 в отношении штамма Mycobacterium bovis BCG и штамма Mycobacterium tuberculosis H37Ra.
[250] (1) Получение жидкого материала для посева: штамм BCG и штамм H37Ra выращивали в жидкой среде 7H9 (агар 7H9, 50% глицерина, 0,05% Tween 80 и 10,05% ADS) в соотношении 1:100 на стерильном рабочем столе, подвергали колебаниям при 37°C, 110 об./мин. После достижения OD600 значения 1,0 клетки центрифугировали при 8000 об./мин. в течение 10 мин. и собирали путем добавления 1 мл 50% глицерина (стерилизованного) и 1 мл жидкой среды 7H9 на стерильном рабочем столе. Штаммы замораживали при -80°C после упаковки по частям. Жидкий материал для посева представлял собой штамм, подвергавшийся выращиванию до OD600=1,0, свежесть которого поддерживали путем обновления каждые три недели.
[2520] (2) Активация жидкого материала для посева: жидкий материал для посева инокулировали в 5 мл жидкой среды 7H9 в соотношении 1:100 на стерильном рабочем столе и подвергали колебаниям при 37°C, 110 об/мин до достижения значения OD600, составлявшего 0,5 (фаза логарифмического роста). OD600 культивируемых бактерий доводили до 0,15 с помощью жидкой среды 7H9 и затем разбавляли 100-кратно для применения.
[2530] (3) Разбавление соединения из положительного контроля, представляющего собой римонабант: римонабант применяли в качестве положительного контроля в ходе эксперимента. Римонабант представляет собой ингибитор каннабиноидного рецептора типа I (CB1), новый тип лекарственного препарата для похудения, вышедший на рынок. Исследования показали, что римонабант также является ингибитором MmpL3 и обладает значительным ингибирующим эффектом в отношении Mycobacterium tuberculosis (H37Rv). Римонабант получали в следующих градиентных разбавлениях: 543,9024392 мкг/мл, 271,9512196 мкг/мл, 135,9756098 мкг/мл, 67,98780492 мкг/мл, 33,99390246 мкг/мл, 16,99695123 мкг/мл, 8,498475615 мкг/мл, 4,249237808 мкг/мл, 2,124618904 мкг/мл, 1,062309452 мкг/мл, 0,531154726 мкг/мл, 0,265577363 мкг/мл. Как правило, шестой градиент разбавления гарантированно представлял собой минимальную ингибирующую концентрацию соединения в отношении штаммов дикого типа. MIC римонабанта в отношении штамма BCG и штамма H37Ra составляла 33,99390246 мкг/мл и 16,99695123 мкг/мл соответственно.
[2540] (4) Разбавление низкомолекулярных ингибиторов мембранного белка Mycobacterium MmpL3: соединения разбавляли в соответствии с 2-кратным градиентным разбавлением. Градиентные разбавления для каждого низкомолекулярного соединения приведены в виде следующего перечня. Градиентные разбавления соединения 17 представляли собой 380,48 мкг/мл, 190,24 мкг/мл, 95,12 мкг/мл, 47,56 мкг/мл, 23,78 мкг/мл, 11,89 мкг/мл, 5,945 мкг/мл, 2,9725 мкг/мл, 1,48625 мкг/мл, 0,743125 мкг/мл, 0,3715625 мкг/мл, 0,18578125 мкг/мл; градиентные разбавления соединения 76 представляли собой 468,288 мкг/мл, 234,144 мкг/мл, 117,072 мкг/мл, 58,536 мкг/мл, 29,268 мкг/мл, 14,634 мкг/мл, 7,317 мкг/мл, 3,6585 мкг/мл, 1,82925 мкг/мл, 0,914625 мкг/мл, 0,4573125 мкг/мл, 0,22865625 мкг/мл; градиентные разбавления соединения 77 представляли собой 331,52 мкг/мл, 165,76 мкг/мл, 82,88 мкг/мл, 41,44 мкг/мл, 20,72 мкг/мл, 10,36 мкг/мл, 5,18 мкг/мл, 2,59 мкг/мл, 1,295 мкг/мл, 0,6475 мкг/мл, 0,32375 мкг/мл, 0,161875 мкг/мл; градиентные разбавления соединения 74 представляли собой 107,32 мкг/мл, 53,66 мкг/мл, 26,83 мкг/мл, 13,415 мкг/мл, 6,7075 мкг/мл, 3,35375 мкг/мл, 1,676875 мкг/мл, 0,8384375 мкг/мл, 0,41921875 мкг/мл, 0,209609375 мкг/мл; градиентные разбавления соединения 18 представляли собой 97,56 мкг/мл, 48,78 мкг/мл, 24,39 мкг/мл, 12,195 мкг/мл, 6,0975 мкг/мл, 3,04875 мкг/мл, 1,524375 мкг/мл, 0,7621875 мкг/мл, 0,38109375 мкг/мл, 0,190546875 мкг/мл; градиентные разбавления соединения 19 представляли собой 107,32 мкг/мл, 53,66 мкг/мл, 26,83 мкг/мл, 13,415 мкг/мл, 6,7075 мкг/мл, 3,35375 мкг/мл, 1,676875 мкг/мл, 0,8384375 мкг/мл, 0,41921875 мкг/мл, 0,209609375 мкг/мл; градиентные разбавления соединения 163 представляли собой 117,0732 мкг/мл, 58,5366 мкг/мл, 29,2683 мкг/мл, 14,6341 мкг/мл, 7,3171 мкг/мл, 3,6585 мкг/мл, 1,8293 мкг/мл, 0,9146 мкг/мл, 0,4573 мкг/мл, 0,2287 мкг/мл, 0,1143 мкг/мл, 0,0572 мкг/мл; градиентные разбавления соединения 23 представляли собой 117,0732 мкг/мл, 58,5366 мкг/мл, 29,2683 мкг/мл, 14,6341 мкг/мл, 7,3171 мкг/мл, 3,6585 мкг/мл, 1,8293 мкг/мл, 0,9146 мкг/мл, 0,4573 мкг/мл, 0,2287 мкг/мл, 0,1143 мкг/мл, 0,0572 мкг/мл; градиентные разбавления соединения 164 представляли собой 207,3171 мкг/мл, 103,6585 мкг/мл, 51,8293 мкг/мл, 25,9146 мкг/мл, 12,9573 мкг/мл, 6,4787 мкг/мл, 3,2393 мкг/мл, 1,6197 мкг/мл, 0,8098 мкг/мл, 0,4049 мкг/мл, 0,2025 мкг/мл, 0,1012 мкг/мл; градиентные разбавления соединения 165 представляли собой 231,7073 мкг/мл, 115,8537 мкг/мл, 57,9268 мкг/мл, 28,9634 мкг/мл, 14,4817 мкг/мл, 7,2409 мкг/мл, 3,6204 мкг/мл, 1,8102 мкг/мл, 0,9051 мкг/мл, 0,4526 мкг/мл, 0,2263 мкг/мл, 0,1131 мкг/мл; градиентные разбавления соединения 10 представляли собой 170,7317 мкг/мл, 85,3659 мкг/мл, 42,6829 мкг/мл, 21,3415 мкг/мл, 10,6707 мкг/мл, 5,3354 мкг/мл, 2,6677 мкг/мл, 1,3338 мкг/мл, 0,6669 мкг/мл, 0,3335 мкг/мл, 0,1667 мкг/мл, 0,0834 мкг/мл; градиентные разбавления соединения 11 представляли собой 134,1463 мкг/мл, 67,0732 мкг/мл, 33,5366 мкг/мл, 16,7683 мкг/мл, 8,3841 мкг/мл, 4,1921 мкг/мл, 2,0960 мкг/мл, 1,0480 мкг/мл, 0,5240 мкг/мл, 0,2620 мкг/мл, 0,1310 мкг/мл, 0,0655 мкг/мл; градиентные разбавления соединения 12 представляли собой 121,9512 мкг/мл, 60,9756 мкг/мл, 30,4878 мкг/мл, 15,2439 мкг/мл, 7,6220 мкг/мл, 3,8110 мкг/мл, 1,9055 мкг/мл, 0,9527 мкг/мл, 0,4764 мкг/мл, 0,2382 мкг/мл, 0,1191 мкг/мл, 0,0595 мкг/мл; градиентные разбавления соединения 171 представляли собой 200,0000 мкг/мл, 100,0000 мкг/мл, 50,0000 мкг/мл, 25,0000 мкг/мл, 12,5000 мкг/мл, 6,2500 мкг/мл, 3,1250 мкг/мл, 1,5625 мкг/мл, 0,7813 мкг/мл, 0,3906 мкг/мл, 0,1953 мкг/мл, 0,0977 мкг/мл; градиентные разбавления соединения 172 представляли собой 337,8049 мкг/мл, 168,9024 мкг/мл, 84,4512 мкг/мл, 42,2256 мкг/мл, 21,1128 мкг/мл, 10,5564 мкг/мл, 5,2782 мкг/мл, 2,6391 мкг/мл, 1,3196 мкг/мл, 0,6598 мкг/мл, 0,3299 мкг/мл, 0,1649 мкг/мл; градиентные разбавления соединения 173 представляли собой 231,7073 мкг/мл, 115,8537 мкг/мл, 57,9268 мкг/мл, 28,9634 мкг/мл, 14,4817 мкг/мл, 7,2409 мкг/мл, 3,6204 мкг/мл, 1,8102 мкг/мл, 0,9051 мкг/мл, 0,4526 мкг/мл, 0,2263 мкг/мл, 0,1131 мкг/мл; градиентные разбавления соединения 166 представляли собой 243,9024 мкг/мл, 121,9512 мкг/мл, 60,9756 мкг/мл, 30,4878 мкг/мл, 15,2439 мкг/мл, 7,6220 мкг/мл, 3,8110 мкг/мл, 1,9055 мкг/мл, 0,9527 мкг/мл, 0,4764 мкг/мл, 0,2382 мкг/мл, 0,1191 мкг/мл; градиентные разбавления соединения 167 представляли собой 268,2927 мкг/мл, 134,1463 мкг/мл, 67,0732 мкг/мл, 33,5366 мкг/мл, 16,7683 мкг/мл, 8,3841 мкг/мл, 4,1921 мкг/мл, 2,0960 мкг/мл, 1,0480 мкг/мл, 0,5240 мкг/мл, 0,2620 мкг/мл, 0,1310 мкг/мл; градиентные разбавления соединения 169 представляли собой 243,9024 мкг/мл, 121,9512 мкг/мл, 60,9756 мкг/мл, 30,4878 мкг/мл, 15,2439 мкг/мл, 7,6220 мкг/мл, 3,8110 мкг/мл, 1,9055 мкг/мл, 0,9527 мкг/мл, 0,4764 мкг/мл, 0,2382 мкг/мл, 0,1191 мкг/мл; градиентные разбавления соединения 168 представляли собой 341,4634 мкг/мл, 170,7317 мкг/мл, 85,3659 мкг/мл, 42,6829 мкг/мл, 21,3415 мкг/мл, 10,6707 мкг/мл, 5,3354 мкг/мл, 2,6677 мкг/мл, 1,3338 мкг/мл, 0,6669 мкг/мл, 0,3335 мкг/мл, 0,1667 мкг/мл; градиентные разбавления соединения 170 представляли собой 292,6829 мкг/мл, 146,3415 мкг/мл, 73,1707 мкг/мл, 36,5854 мкг/мл, 18,2927 мкг/мл, 9,1463 мкг/мл, 4,5732 мкг/мл, 2,2866 мкг/мл, 1,1433 мкг/мл, 0,5716 мкг/мл, 0,2858 мкг/мл, 0,1429 мкг/мл.
[2550] (5) Добавляли 40 мкл жидкой среды 7H9 (содержащей Tween-80 и ADS) в 96-луночные планшеты. Для каждого градиента устанавливали три повторности. Добавляли 2 мкл соединений с различными градиентами и 40 мкл разбавленных культивированных бактерий (штамм BCG или штамм H37Ra) и перемешивали путем острожного встряхивания. Планшеты инкубировали в инкубаторе при 37°C в течение 168 часов.
[2560] (6) Добавляли 0,02% (вес/об.) раствор резазурина в лунки на стерильном рабочем столе и продолжали инкубировать планшеты в инкубаторе в течение 4 часов. Рост бактерий наблюдали под инвертированным микроскопом. MIC определяли как минимальную концентрацию соединения, при которой останавливался рост бактерий. Резазурин имел розовую окраску при остановке роста бактерий и голубую окраску при продолжении роста.
[2570] Результаты определения MIC для низкомолекулярных ингибиторов MmpL3 в отношении Mycobacterium smegmatis, Mycobacterium bovis BCG и Mycobacterium tuberculosis H37Ra показаны в таблице 2.
Таблица 2
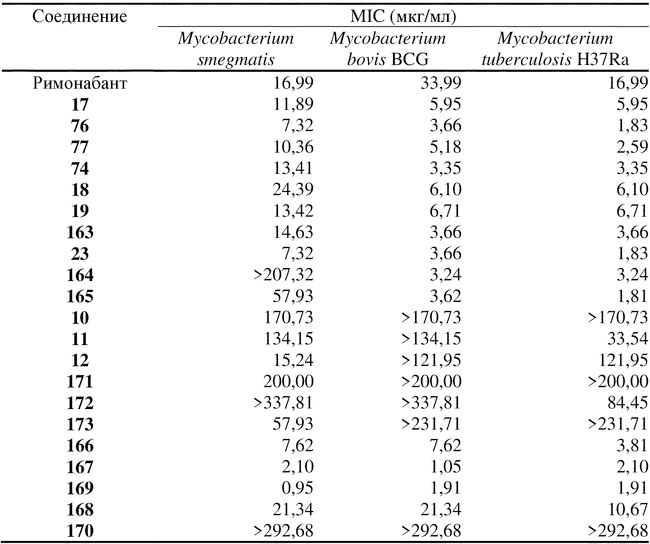
[2580] Данные в таблице 2 показывали, что в отношении штаммов м. smegmatis, BCG и H37Ra все из соединений 17, 76, 77, 74, 18, 19, 163 и 23 обладали надлежащим ингибирующим эффектом. Среди них соединение 76 и соединение 23 превосходят другие соединения в отношении широкого спектра противомикробной активности и могут применяться в качестве потенциальных лекарственных средств, направленных в отношении инфекции, вызванной Mycobacterium.
[2590] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют те же значения, которые обычно являются понятными специалисту средней квалификации в области техники, к которой относится настоящее изобретение.
[2600] Настоящее изобретение, иллюстративно описанное в данном документе, может быть реализовано на практике соответствующим образом при отсутствии какого-либо элемента или элементов, ограничения или ограничений, конкретно не раскрытых в данном документе. Таким образом, например, термины «предусматривающий», «включающий», «содержащий» и т.д. следует толковать расширительно и без ограничения. Кроме того, термины и выражения, используемые в данном документе, используются в качестве описательных, а не ограничивающих терминов, и такие термины и выражения не предназначаются для исключения каких-либо эквивалентов показанных и описанных элементов или их частей, а подразумевается, что различные модификации являются возможными в пределах объема заявляемого изобретения.
[2610] Все публикации, заявки на патент, патенты и другие литературные источники, упомянутые в данном документе, явным образом включены в данный документ посредством ссылки во всей своей полноте в той же степени, как если бы каждый из них был включен посредством ссылки по отдельности. В случае конфликта настоящее описание, в том числе определения, будет иметь преимущество.
[2620] Следует понимать, что хотя настоящее изобретение описано в сочетании с вышеописанными вариантами осуществления, вышеуказанное описание и примеры предназначены для иллюстрации и не предназначены для ограничения объема настоящего изобретения. Настоящее изобретение не ограничено вариантами осуществления, показанными и описанными выше, однако может быть изменено в пределах объема формулы изобретения. Другие аспекты, преимущества и модификации в пределах объема настоящего изобретения будут очевидны специалистам в области техники, к которой относится настоящее изобретение.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2,5-ДИЗАМЕЩЕННЫЕ АРИЛСУЛЬФОНАМИДНЫЕ АНТАГОНИСТЫ CCR3 | 2010 |
|
RU2532515C2 |
| (АЛЬФА-ЗАМЕЩЕННЫЕ АРАЛКИЛАМИНО- И ГЕТЕРОАРИЛАЛКИЛАМИНО)ПИРИМИДИНИЛ- И 1, 3, 5-ТРИАЗИНИЛБЕНЗИМИДАЗОЛЫ, ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2608742C2 |
| ИНГИБИТОРЫ ГЛИКОЛАТОКСИДАЗЫ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2805308C2 |
| АНТАГОНИСТЫ АРИЛСУЛЬФОНАМИДА CCR3 | 2010 |
|
RU2539591C2 |
| ПРОИЗВОДНЫЕ ДИАЗАГОМОАДАМАНТАНА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2549551C2 |
| СТЕРОИДЫ, ВЫСВОБОЖДАЮЩИЕ ОКСИД АЗОТА | 2008 |
|
RU2442790C2 |
| АНТИГИПЕРТЕНЗИВНЫЕ СОЕДИНЕНИЯ ДВОЙНОГО ДЕЙСТВИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2008 |
|
RU2476427C2 |
| ИНГИБИТОРЫ ИОННОГО КАНАЛА, ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ И ПРИМЕНЕНИЕ | 2016 |
|
RU2746188C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ, КОТОРЫЕ МОЖНО ИСПОЛЬЗОВАТЬ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ ATR | 2012 |
|
RU2677292C2 |
| КЛАСС КОНДЕНСИРОВАННЫХ КОЛЬЦЕВЫХ СОЕДИНЕНИЙ И ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2021 |
|
RU2831125C1 |
Изобретение относится к новым ингибиторам мембранного белка микобактерий MmpL3 формулы I. Технический результат: получены новые соединения, которые являются ингибиторами мембранного белка микобактерий MmpL3 и могут быть использованы в способе лечения микобактериальной инфекции. 8 н. и 4 з.п. ф-лы, 2 табл., 35 пр.
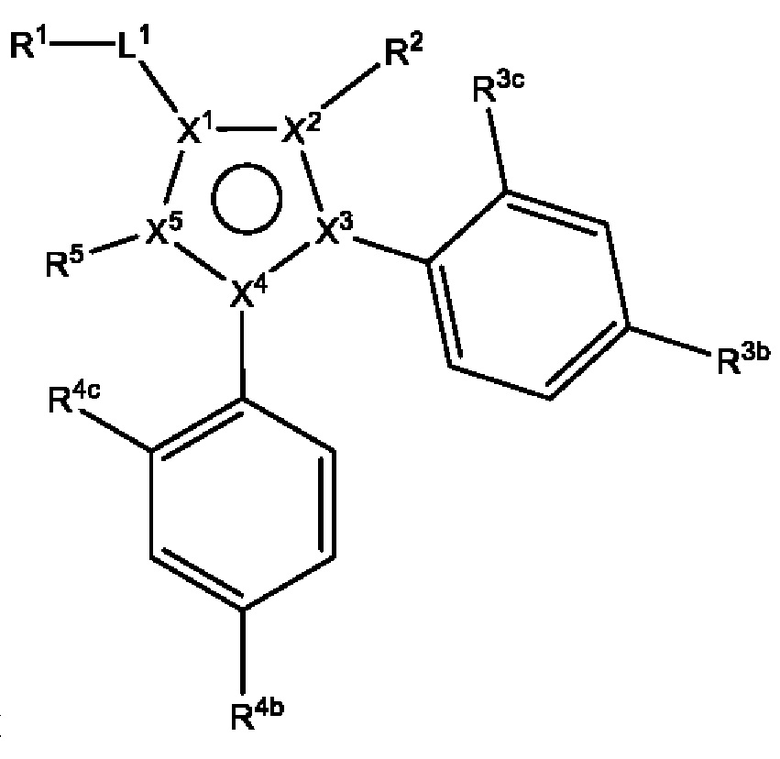
1. Соединение формулы I:
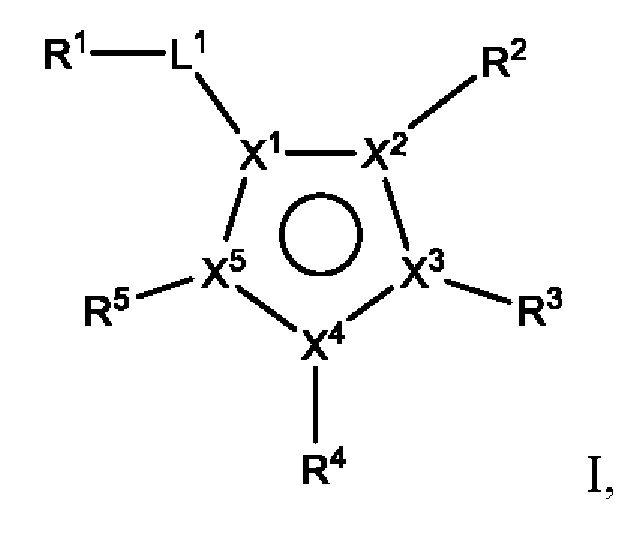
или его фармацевтически приемлемая соль, стереоизомер или смесь стереоизомеров,
где
формула I представляет собой 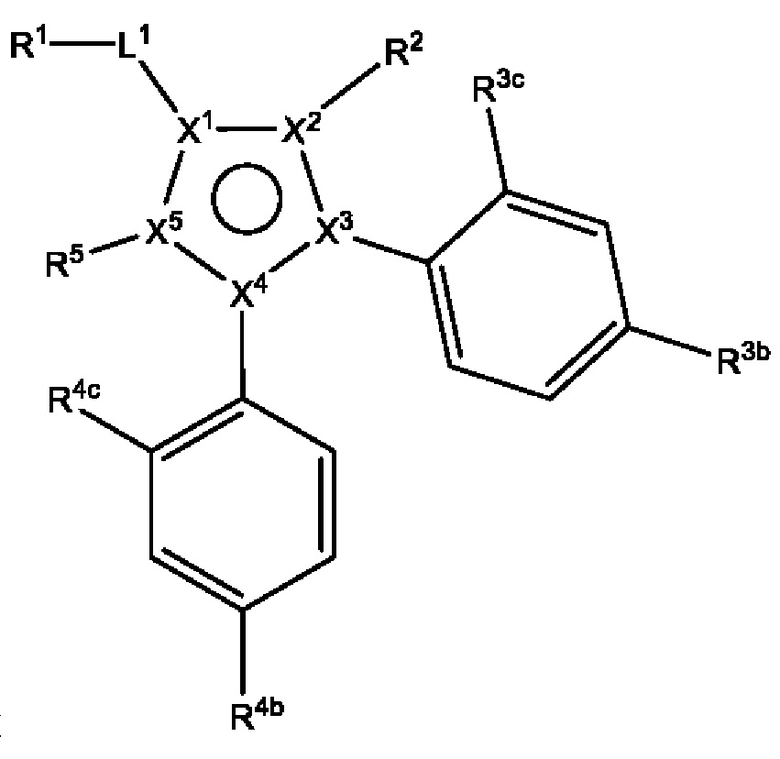 ;
;
X1, X2 и X3 представляют собой С; X4 и X5 представляют собой N;
L1 представляет собой *-(CH2)n-N(R1c)-(CH2)k-N(R1b)CO-, *-(CH2)m-CO-L1a-CO-, *-(CH2)n-NHCONH-(CH2)m-, *-(CH2)n-N(R1c)-(CH2)k-N(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-CON(R1b)-(CH2)m-, *-(CH2)p-N(R1c)-(CH2)n-SO2N(R1b)-(CH2)m- или *-(CH2)n-OCO-;
* обозначает точку соединения с R1;
L1a представляет собой 5- или 6-членный гетероциклилен; где гетероатомы представляют собой азот, а количество гетероатомов равно двум;
каждый R1b независимо представляет собой Н или С1-3алкил;
каждый R1c независимо представляет собой Н или С1-3алкил;
k равняется 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10; и
каждый из m, n и р независимо равняется 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10;
R1 представляет собой адамантил, замещенный R1a в количестве от одного до пяти, бицикло[2.2.1]гептил, замещенный R1a в количестве от одного до пяти или незамещенный адамантил;
каждый R1a независимо представляет собой С1-3алкил;
R2 представляет собой С1-3алкил;
каждый R3b и R3c независимо представляет собой Н или R3a; и
каждый R4b и R4c независимо представляет собой Н или R4a;
R3a и R4a независимо выбраны из галогена и С1-3алкила;
R5 отсутствует.
2. Соединение формулы I-C, II-С, III-С, IV-C, V-C и VIII-C, или его фармацевтически приемлемая соль, стереоизомер, или смесь стереоизомеров:
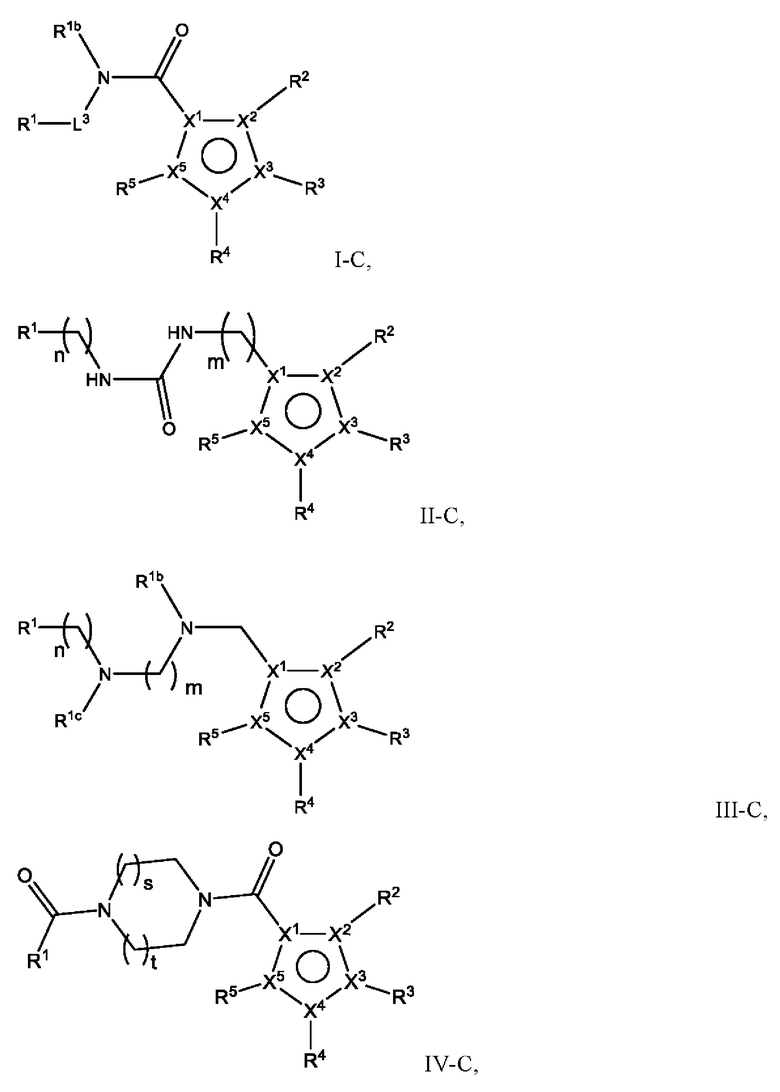
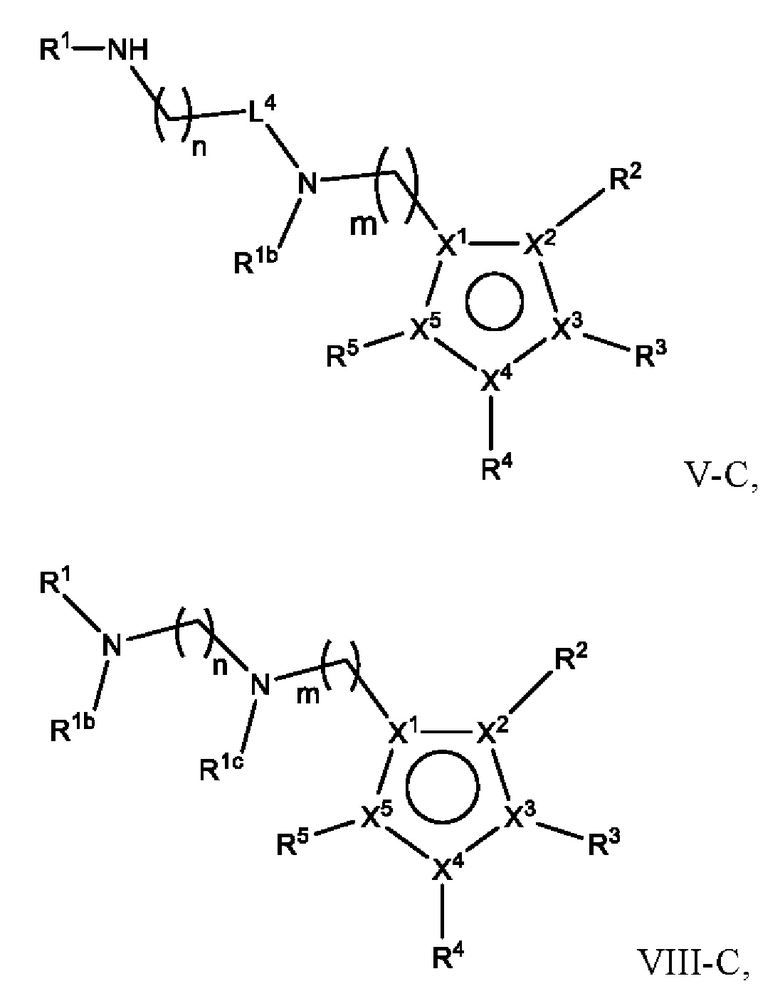
или его фармацевтически приемлемая соль, стереоизомер или смесь стереоизомеров, где
L3 представляет собой *-(CH2)n-N(R1c)-(CH2)k-,
L4 представляет собой SO2,
s и t независимо равняются 0, 1 или 2, и
каждый из m, n, k, р, X1, X2, X3, X4, X5, R1b, R1c, R1, R2, R3, R4 и R5 определены в п. 1.
3. Соединение формулы VI-С, или его фармацевтически приемлемая соль, стереоизомер, или смесь стереоизомеров,
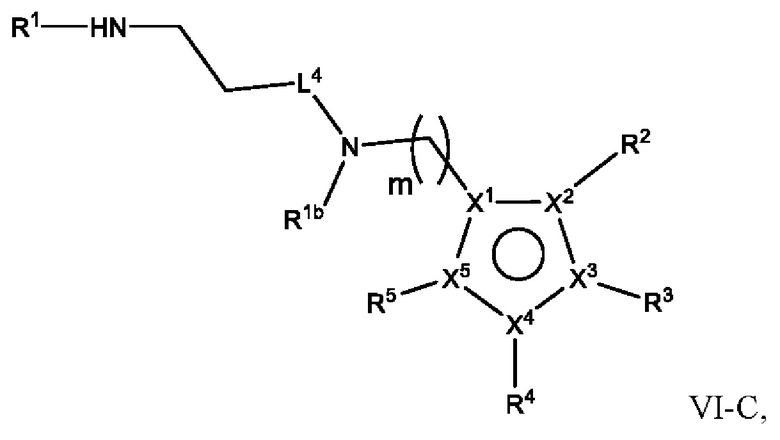
где L4 представляет собой SO2,
каждый из m, X1, X2, X3, X4, X5, R1b, R1c, R1, R2, R3, R4 и R5 определены в п. 1.
4. Соединение по п. 1, где L1 выбран из *-NHCONH-, *-NHCONHCH2-, *-CH2NHCONHCH2-, *-(CH2)2NHCONHCH2-, *-(CH2)3NHCONHCH2-, *-(CH2)4NHCONHCH2-, *-(CH2)5NHCONHCH2-, *-(CH2)6NHCONHCH2-, *-NHCH2NHCO-, *-NH(CH2)2NHCO-, *-NH(CH2)3NHCO-, *-NH(CH2)4NHCO-, *-NH(CH2)5NHCO-, *-NH(CH2)6NHCO-, *-NH(CH2)7NHCO-, *-CH2NHCH2NHCO-, *-CH2NH(CH2)2NHCO-, *-CH2NH(CH2)3NHCO-, *-CH2NH(CH2)4NHCO-, *-CH2NH(CH2)5NHCO-, *-CH2NH(CH2)6NHCO-, *-CH2NH(CH2)7NHCO-, *-NH(CH2)2NHCH2-, *-NH(CH2)4NHCH2-, *-NH(CH2)2SO2NHCH2-, *-OC(O)-, *-CH2NH(CH2)2NHCH2-, *-CH2NH(CH2)4NHCH2-, *-CH2NH(CH2)2SO2NHCH2-, *-CH2OC(O)-,
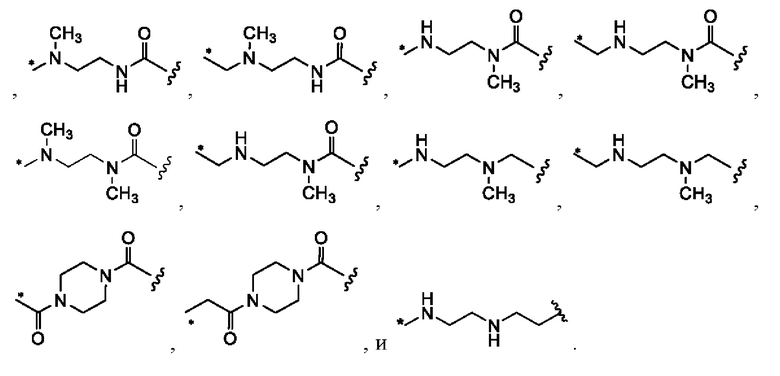
5. Соединение по любому из пп. 1-4, где R1 выбран из:
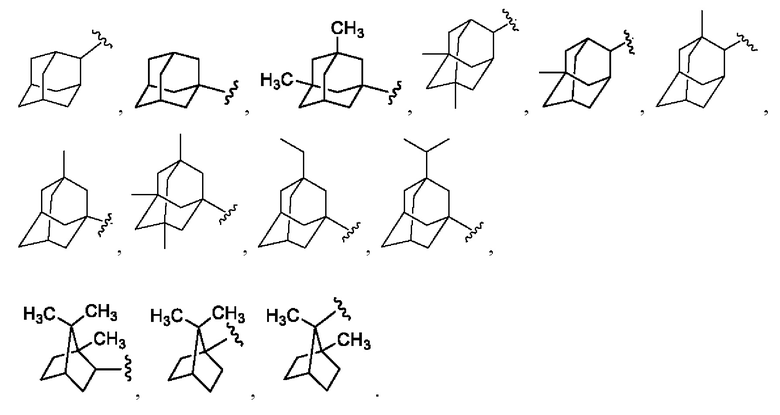
6. Соединение, или его фармацевтически приемлемая соль, стереоизомер или смесь стереоизомеров, где соединение выбрано из любого из следующих соединений:

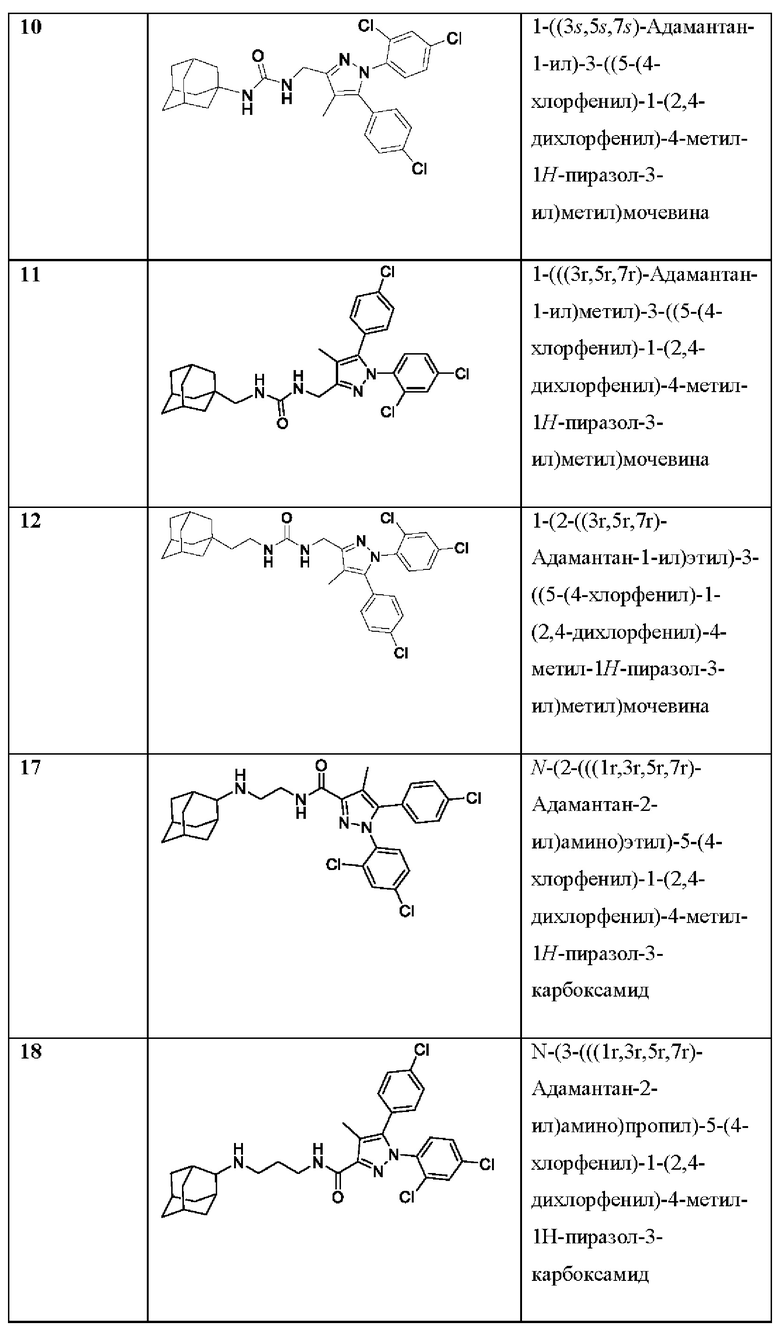
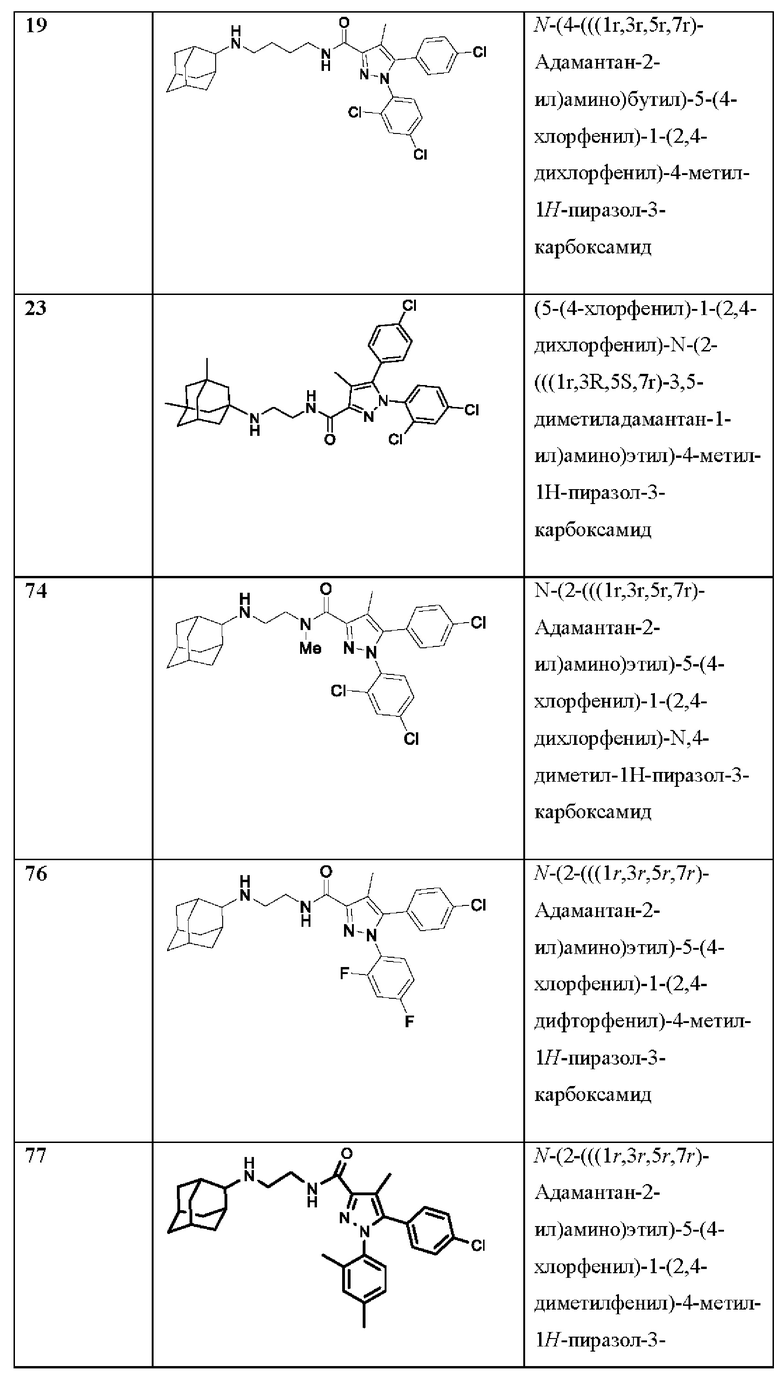
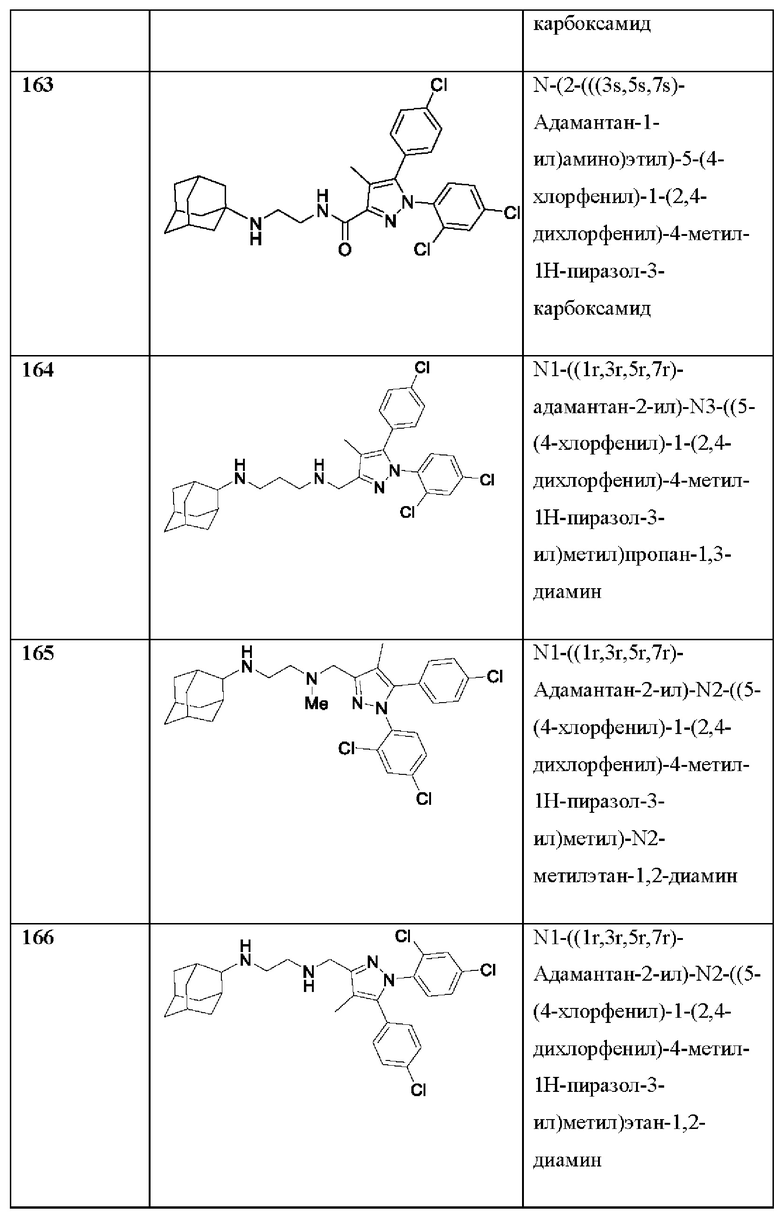
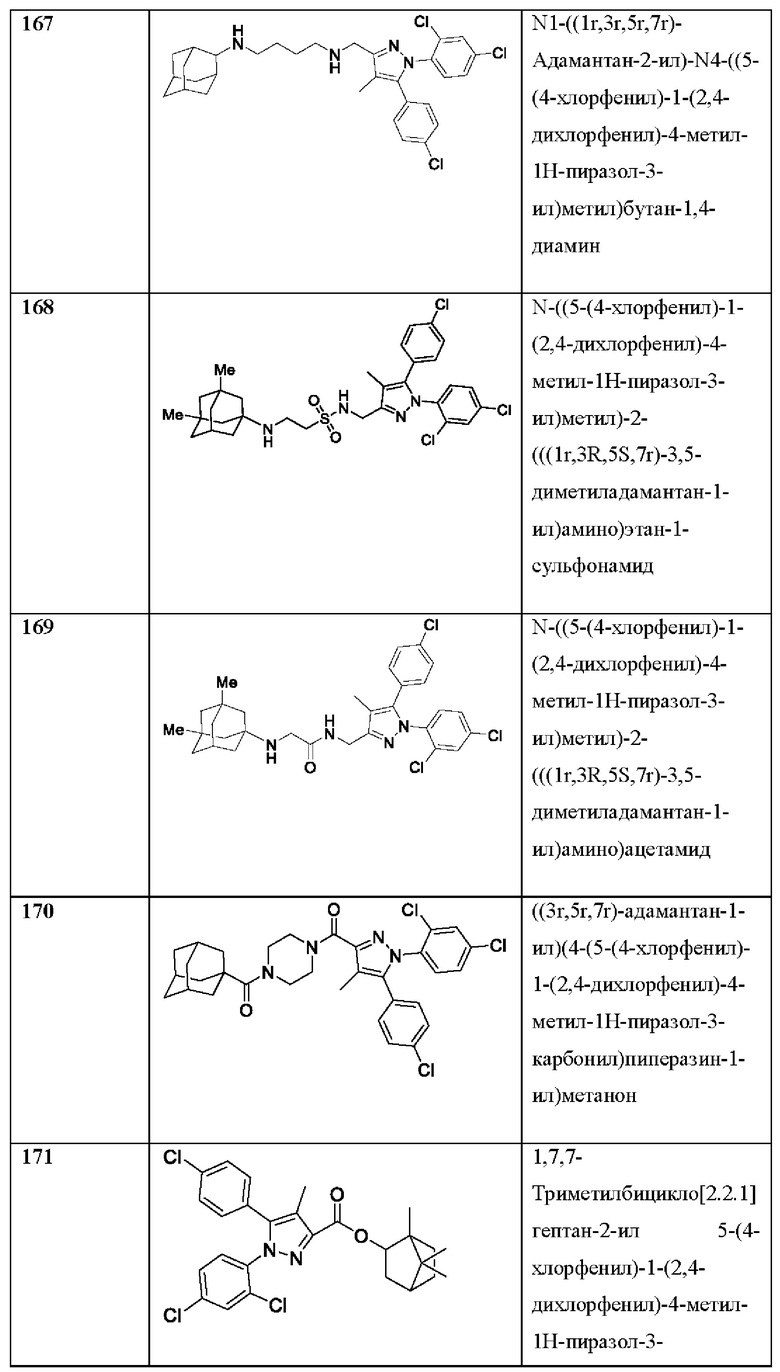
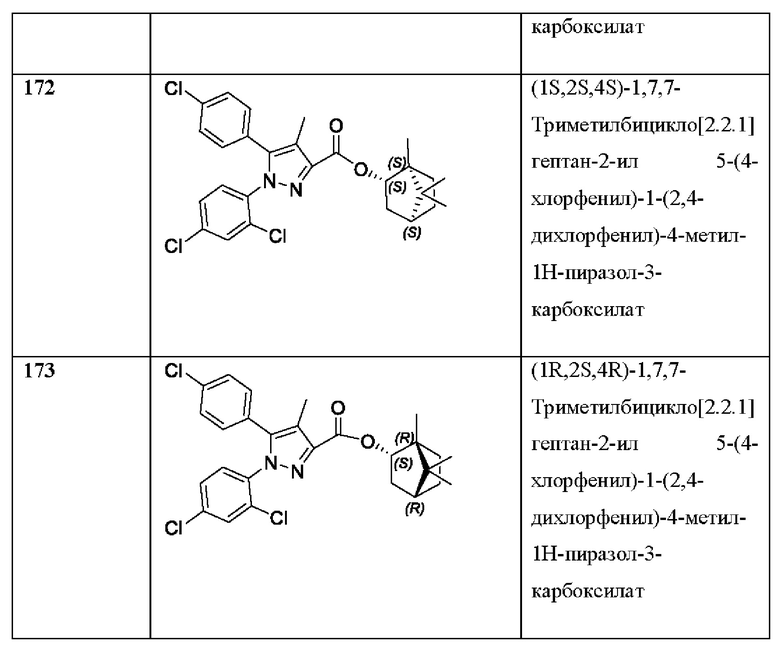
7. Способ ингибирования мембранного белка микобактерий Large 3 у субъекта, нуждающегося в этом, предусматривающий введение субъекту эффективного количества соединения по любому из пп. 1-6.
8. Способ лечения микобактериальной инфекции у субъекта, нуждающегося в этом, предусматривающий введение субъекту эффективного количества соединения по любому из пп. 1-6, при этом микобактериальная инфекция представляет собой инфекцию, вызванную Mycobacterium tuberculosis, инфекцию, вызванную Mycobacterium leprae, инфекцию, вызванную Mycobacterium ulcerans, инфекцию, вызванную Mycobacterium abscessus, инфекцию, вызванную Mycobacterium bovis, или инфекцию, вызванную Mycobacterium marinum.
9. Способ лечения заболевания, обусловленного микобактериальной инфекцией, у субъекта, нуждающегося в этом, предусматривающий введение субъекту эффективного количества соединения по любому из пп. 1-6, при этом заболевание, обусловленное микобактериальной инфекцией, представляет собой туберкулез, обусловленный инфекцией, вызванной Mycobacterium tuberculosis, лепру, обусловленную Mycobacterium leprae, язву Бурули, обусловленную Mycobacterium ulcerans, инфекционное заболевание, обусловленное Mycobacterium abscessus, инфекционное заболевание, обусловленное инфекцией, вызванной Mycobacterium bovis, или инфекционное заболевание, обусловленное инфекцией, вызванной Mycobacterium marinum.
10. Применение соединения по любому из пп. 1-6 в изготовлении лекарственного препарата для предупреждения или лечения микобактериальной инфекции или заболевания, обусловленного микобактериальной инфекцией.
11. Применение по п. 10, где микобактериальная инфекция представляет собой инфекцию, вызванную Mycobacterium tuberculosis, инфекцию, вызванную Mycobacterium leprae, инфекцию, вызванную Mycobacterium ulcerans, инфекцию, вызванную Mycobacterium abscessus, инфекцию, вызванную Mycobacterium bovis, или инфекцию, вызванную Mycobacterium marinum.
12. Применение по п. 10, где заболевание, обусловленное микобактериальной инфекцией, представляет собой туберкулез, обусловленный инфекцией, вызванной Mycobacterium tuberculosis, лепру, обусловленную Mycobacterium leprae, язву Бурули, обусловленную Mycobacterium ulcerans, инфекционное заболевание, обусловленное Mycobacterium abscessus, инфекционное заболевание, обусловленное инфекцией, вызванной Mycobacterium bovis, или инфекционное заболевание, обусловленное инфекцией, вызванной Mycobacterium marinum.
| ПРОИЗВОДНЫЕ 1Н-ИМИДАЗОЛА, ОБЛАДАЮЩИЕ CB-АГОНИСТИЧЕСКОЙ, ЧАСТИЧНОЙ CB-АГОНИСТИЧЕСКОЙ ИЛИ CB-АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2299200C2 |
| CN 1921849 A, 28.02.2007 | |||
| US 2005124660 A1, 09.06.2005 | |||
| ПРОИЗВОДНЫЕ 1H-1,2,4-ТРИАЗОЛ-3-КАРБОКСАМИДА В КАЧЕСТВЕ ЛИГАНДОВ РЕЦЕПТОРА КАННАБИНОИДОВ | 2003 |
|
RU2325382C2 |
| WO 2014174457 A1, 30.10.20140. | |||
Авторы
Даты
2023-05-02—Публикация
2019-11-20—Подача