Изобретение относится к медицине, в частности к иммунологии, и может быть использовано в клинической практике для оценивания и интерпретации показателей клеточного иммунитета, в том числе с целью оценки рисков возникновения и развития хронических заболеваний, а также принятия оперативного и обоснованного решения о вакцинации [МПК G01N 33/48, G01N 33/53, A61P 37/02, A61K 35/74].
Из уровня техники известен СПОСОБ ОЦЕНКИ ТЕЧЕНИЯ РАНЕВОГО ПРОЦЕССА [RU 2184972, опубл. 10.07.2002], включающий исследование клеточного звена иммунитета больного, отличающийся тем, что осуществляют забор раневого содержимого после операции и определяют в нем содержание иммуноглобулинов А, М, G и фенотипические показатели лимфоцитов: Т лимфоцитов (CD-3+), Т- хелперов (CD-4+), Т-супрессоров (CD-8+), CD22, CD56, CD+HLA-DR+ и иммунорегуляторный индекс (хелперы/супрессоры) и при показателях содержания иммуноглобулинов: А - 2,3 + -0,06 г/л; М - 4 + -0,08 г/л; G - 18 + -0,2 г/л и фенотипических параметров лимфоцитов: CD3 - 72 + -6,5%, CD4 - 48 + -5,4%; CD8 - 24 + -5,7%; CD22 - 2 + -0,6%; CD56 - 4 + -0,4%; CD + HLA - DR + - 14 + -1/2%; иммунорегуляторный индекс - 2,5% + -0,3 оценивают течение раневого процесса как неосложненное, а при отличии от данных величин оценивают как осложненное течение.
Из уровня техники известен СПОСОБ ОЦЕНКИ ТЯЖЕСТИ БОЛЬНЫХ С ПОСТНЕКРОТИЧЕСКИМИ СВИЩАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ [RU2442162, опубл. 10.02.2012], осуществляемый путем исследования крови больного, при котором методом проточной цитометрии определяют субпопуляционный состав лимфоцитов, рассчитывают соотношение CD3+4+ Т-хелперов к CD3+8+ Т-цитотоксическим лимфоцитам, определяя таким образом иммунорегуляторный индекс (ИРИ) и при его уровне 0,5-0,3 оценивают состояние больного как тяжелое.
Общими недостатками приведенных аналогов является ограниченность применения результатов интерпретации полученных показателей крови (только для оценки течения раневого процесса либо оценки тяжести больных с постнекротическими свищами поджелудочной железы), что не позволяет интерпретировать ИРИ для оценивания рисков возникновения и течения других воспалительных процессов в организме, а также ограниченный диапазон значений ИРИ, рассматриваемый при оценке состояния пациентов.
Из уровня техники известен способ, который реализован в ЛЕКАРСТВЕННОМ СРЕДСТВЕ ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ [RU 2595807, опубл. 27.08.2016], которое содержит активированную - потенцированную форму антител к гамма-интерферону человека в сочетании с активированной - потенцированной формой антител к CD4 рецептору Т-лимфоцитов и активированной - потенцированной формой антител к гистамину в виде гомеопатически активированного - потенцированного водного или водно-спиртового раствора, либо в твердой лекарственной форме, и получено путем многократного последовательного разведения и промежуточного внешнего воздействия из соответствующих матричных аффинно-очищенных антител с концентрацией 0,5÷5,0 мг/мл, при этом предложенное лекарственное средство применяют для лечения вирусных инфекционных заболеваний, вызываемых ВИЧ или ассоциированных с ВИЧ, в том числе СПИДа, различных вирусных гепатитов, герпесвирусной инфекции, заболеваний, вызванных вирусом гриппа, острых респираторных вирусных инфекций, бактериальных инфекционных заболеваний, вызванных различными возбудителями, в том числе для лечения псевдотуберкулеза, коклюша, иерсиниоза, пневмонии различной этиологии.
Недостатком аналога является ограниченность возможности оценивания качества лечения предложенным лекарственным средством, поскольку связь положительного эффекта от приема предложенного лекарственного средства с повышением значения ИРИ исследуется только в отношении ВИЧ-инфицированных пациентов, при этом оценивание изменений значения ИРИ после приема предложенного лекарственного средства при других заболеваниях не производится.
Наиболее близким по технической сущности является СПОСОБ ПРОГНОЗИРОВАНИЯ ВЕРОЯТНОСТИ УХУДШЕНИЯ КЛИНИЧЕСКОГО ТЕЧЕНИЯ ПСОРИАЗА, ПЕРЕХОДА ЕГО В ЭРИТРОДЕРМИЮ С УЧЕТОМ ИММУНОЛОГИЧЕСКИХ ПОКАЗАТЕЛЕЙ, ДЕТОКСИКАЦИОННОЙ И МЕТАБОЛИЧЕСКОЙ ФУНКЦИИ ПЕЧЕНИ [RU 2508903, опубл. 10.03.2014], при котором проводят интегрированную оценку патогенетической значимости выявленных факторов риска, способствующих ухудшению заболевания. Определяют прогностический коэффициент (ПК) для таких признаков, как: пол; возраст; рабочие нефтехимического производства; сельхозрабочие; строители; водители; служащие; гиперинсоляция; неблагоприятные условия сельхозтруда (контакт с пестицидами, удобрениями); контакт с нефтепродуктами; контакт со стройматериалами; нерациональное применение лекарств; наличие очагов хронической бактериальной и/или грибковой инфекции; часто рецидивирующие ОРВИ; хронические заболевания желудочно-кишечного тракта и/или печени; хронические заболевания легких; хронические заболевания ЛОР-органов; нарушения детоксикационной функции печени; нарушения метаболической функции печени; увеличение уровня циркулирующих иммунных комплексов; увеличение уровня иммуноглобулинов; увеличение иммунорегуляторного индекса; уменьшение индекса стимуляции; уменьшение цитотоксического индекса; увеличение уровня противотканевых аутоантител; наличие кожного антигена в крови; увеличение индекса торможения миграции лейкоцитов. При отсутствии фактора его ПК принимают за ноль. Суммируют полученные ПК. При значении суммы ПК 5,64-16,24 прогнозируют низкую вероятность ухудшения клинического течения псориаза и благоприятный прогноз заболевания, 16,25-26,85 - среднюю вероятность и относительно благоприятный прогноз, 26,86-37,86 и выше - высокую вероятность и неблагоприятный прогноз, возможность перехода псориаза в эритродермию.
Основными техническими проблемами прототипа являются ограниченность применения способа (лечение псориаза и эритродермии), а также отсутствие четкого разделения значений ИРИ на поддиапазоны при оценивании связи течения болезни и эффективности лечения с изменением значений ИРИ, что не позволяет однозначно интерпретировать конкретные значения ИРИ и учитывать их при назначении лечения.
Задачей изобретения является устранение недостатков прототипа.
Техническим результатом изобретения является повышение точности диагностики организма человека и повышение уровня ИРИ.
Указанный технический результат достигается за счет того, что:
Способ диагностики состояния организма человека путем исследования крови, характеризующийся тем, что посредством блока определения субпопуляционного состава лимфоцитов 1 получают значения антигенов CD4+ и CD8+ и передают эти значения в блок вычисления значения иммунорегуляторного индекса 2, посредством которого вычисляют значение иммунорегуляторного индекса R как соотношение R = CD4+ / CD8+, отличающийся тем, что передают значение R в блок сравнения значения иммунорегуляторного индекса с эталонными значениями из первого столбца матрицы интерпретации значений иммунорегуляторного индекса 3 M[n × k+1], где n=5 – количество поддиапазонов интерпретации значений иммунорегуляторного индекса, k=5 – количество критериев интерпретации значений иммунорегуляторного индекса, причем под значением критерия M[n, 2] понимают риск возникновения хронического воспалительного заболевания, под значением критерия M[n, 3] понимают риск течения хронического воспалительного заболевания в средней и тяжелой формах, под значением критерия M[n, 4] понимают риск развития лекарственной устойчивости к антибактериальным препаратам, под значением критерия M[n, 5] понимают риск развития вирусного заболевания в период эпидемии в средней и тяжелой форме вне зависимости от факта вакцинации, под значением критерия M[n, 6] понимают рекомендации по вакцинации от гриппа/Covid19, при этом из блока хранения матрицы интерпретации значений иммунорегуляторного индекса 4 передают для проведения процедуры сравнения в блок сравнения значения иммунорегуляторного индекса с эталонными значениями 3 значения элементов первого столбца матрицы M, путем последовательного сравнения ранее вычисленного в блоке вычисления значения иммунорегуляторного индекса 2 значения иммунорегуляторного индекса R и эталонных значений элементов M[1:n, 1] определяют поддиапазон n интерпретации иммунорегуляторного индекса, в который попадает ранее вычисленное в блоке вычисления значения иммунорегуляторного индекса 2 значение иммунорегуляторного индекса R, при этом если R<1,2, то n=1, M[n, 2] = 95…98%, M[n, 3] = 100%, M[n, 4] = 100%, M[n, 5] = 90%, M[n, 6] = {"вакцинация от гриппа/Covid19 противопоказана всем по причине недостаточного уровня клеточного иммунитета для формирования устойчивого вторичного специфического иммунитета, существует высокий риск первичных и вторичных осложнений, риск заболевания после вакцинации в средне-тяжелой форме не уменьшается"};
если 1,2≤R≤1,5, то n=2, M[n, 2] = M[n, 3] = 90% при R=1,2, M[n, 2] = M[n, 3] = 80% при R=1,3, M[n, 2] = M[n, 3] = 70% при R=1,4, M[n, 2] = M[n, 3] = 60% при R=1,5, M[n, 4] = 60%, M[n, 5] = 60%, M[n, 6] = {"вакцинация от гриппа/Covid19 рекомендована, кроме случаев наличия любого хронического воспалительного заболевания и возрасте старше 50 лет, риск заболевания после вакцинации в средне-тяжелой форме уменьшается до 60%"};
если 1,6≤R≤1,8, то n=3, M[n, 2] = M[n, 3] = 45% при R=1,6, M[n, 2] = M[n, 3] = 30% при R=1,7, M[n, 2] = M[n, 3] = 15% при R=1,8, M[n, 4] = 30%, M[n, 5] = 30%, M[n, 6] = {"вакцинация от гриппа/Covid19 рекомендована всем, риск заболевания после вакцинации в средне-тяжелой форме уменьшается до 30%"};
если 1,9≤R≤2,6, то n=4, M[n, 2] = M[n, 3] = 0%, M[n, 4] = 0%, M[n, 5] = 0…3%, M[n, 6] = {"риск заболевания в средне-тяжелой форме после вакцинации от гриппа/Covid19 достоверно не изменяется ввиду того, что изначальный риск минимален"};
если R>2,6, то n=5, M[n, 2] = 10%, M[n, 3] = 0%, M[n, 4] = 0%, M[n, 5] = 0…3%, M[n, 6] = {"вакцинация от гриппа/Covid19 противопоказана при наличии аллергических и аутоиммунных заболеваний, риск заболевания в средне-тяжелой форме после вакцинации от гриппа/Covid19 достоверно не изменяется ввиду того, что изначальный риск минимален"}, после чего сохраняют текущий вектор состояния M[n, 1:k], соответствующий текущему значению R, в блоке хранения результатов интерпретации значения иммунорегуляторного индекса 5.
Способ повышения иммунорегуляторного индекса, включающий диагностику по п. 1 и введение в организм человека препарата, содержащего в качестве действующего вещества липополисахарид Salmonella typhi, отличающийся тем, что препарат вводят в форме стерильного раствора путем внутримышечного введения через день курсом протяженностью 17 дней по схеме 3 инъекции из расчета 0,5 мкг/кг массы пациента, после чего 3 инъекции из расчета 1,0 мкг/кг массы пациента, после чего 3 инъекции из расчета 1,5 мкг/кг массы пациента.
Способ повышения иммунорегуляторного индекса, включающий диагностику по п. 1 и введение в организм человека препарата, содержащего в качестве действующего вещества липополисахарид Salmonella typhi, отличающийся тем, что, препарат вводят в форме суппозиториев ректальных ежедневно курсом протяженностью 12 дней по схеме 3 дня по 50 мкг, после чего 3 дня по 100 мкг, после чего 3 дня по 150 мкг, после чего 3 дня по 200 мкг.
Применение вещества липополисахарид Salmonella typhi в качестве средства для повышения иммунорегуляторного индекса.
Краткое описание чертежей
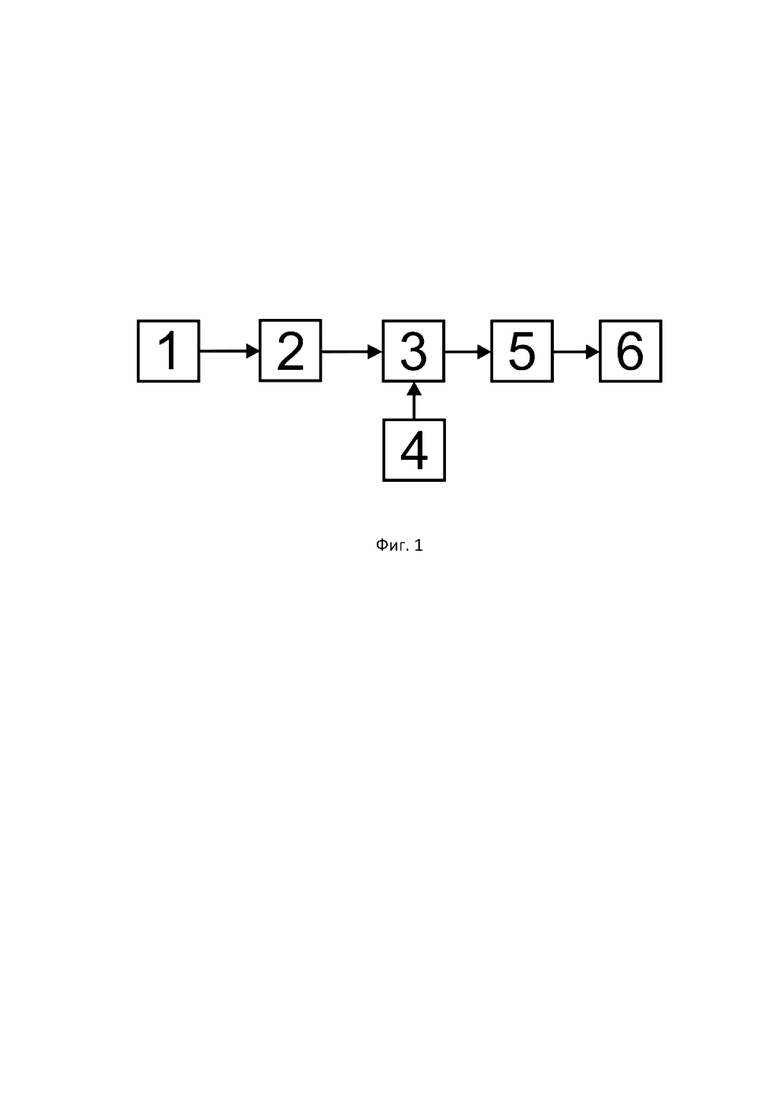
На фиг.1 показана блок-схема способа диагностики состояния организма человека и повышения иммунорегуляторного индекса.
На фиг.1 обозначено: 1 – блок определения субпопуляционного состава лимфоцитов, 2 – блок вычисления значения иммунорегуляторного индекса, 3 – блок сравнения значения иммунорегуляторного индекса с эталонными значениями из матрицы интерпретации значений иммунорегуляторного индекса, 4 – блок хранения матрицы интерпретации значений иммунорегуляторного индекса, 5 – блок хранения результатов интерпретации значения иммунорегуляторного индекса, 6 – блок назначения терапии.
Осуществление изобретения
Иммунитет - это система организма, защищающая человека от инфекций и различных заболеваний (онкологические, аутоиммунные и др.). Главными клетками иммунной защиты являются лимфоциты, которые обеспечивают как гуморальный, так и клеточный иммунитет.
Лимфоциты делятся на 3 вида (популяции) в зависимости от выполняемых функций: В-клетки, Т-клетки и NK-клетки. Основной популяцией являются Т-клетки, представляющие собой до 80% от общего числа лимфоцитов. В свою очередь, Т-лимфоциты делятся на 2 основные субпопуляции: Т-киллеры (цитотоксические клетки) и Т-хелперы (клетки-помощники).
Каждая из субпопуляций в норме имеет на своей поверхности различные молекулы-антигены. Помимо общих антигенов, каждая субпопуляция имеет на поверхности, то есть экспрессирует, специфический только для нее антиген. Для Т-киллеров это CD8+, а для Т-хелперов CD4+. Эти молекулы делают эти клетки узнаваемыми среди других, что позволяет использовать это при комплексном анализе иммунного статуса.
Одним из основных лабораторных показателей удовлетворительного состояния иммунной системы является ИРИ. ИРИ представляет собой соотношение CD4+ и CD8+ Т-лимфоцитов. Определение ИРИ проводится с целью количественной оценки клеток в крови, является одним из показателей адаптивности клеточного иммунитета и позволяет дать объективную оценку иммунному ответу.
Изобретение касается качественного улучшения интерпретации ИРИ по нескольким направлениям.
Для реализации предложенного способа посредством блока определения субпопуляционного состава лимфоцитов 1 у пациента производят забор венозной крови в количестве 5-7 мл в вакумную пробирку с ЭДТА, которую помещают в контейнер для проб проточного цитометра типа Navios, определяют субпопуляционный состав лимфоцитов, в том числе CD4+ и CD8+, и посредством блока вычисления значения иммунорегуляторного индекса 2 определяют их соотношение и таким образом вычисляют значение ИРИ, после чего запрашивают значения элементов матрицы М из блока хранения матрицы интерпретации значений иммунорегуляторного индекса 4 и посредством блока сравнения значения иммунорегуляторного индекса с эталонными значениями из матрицы интерпретации значений иммунорегуляторного индекса 3 осуществляют сравнение вычисленного значения ИРИ и эталонных значений ИРИ из первого столбца матрицы М, путем сравнения определяют поддиапазон значений ИРИ, в который попадает вычисленное значение ИРИ, ставят ему в соответствие текущую строку n, значения элементов которой являются интерпретацией вычисленного значения ИРИ, записывают в текущий вектор состояния значения элементов строки n матрицы М, соответствующей определенному ранее поддиапазону значений ИРИ, и сохраняют текущий вектор состояния M[n, 1:k], соответствующий текущему значению ИРИ, в блоке хранения результатов интерпретации значения иммунорегуляторного индекса 5.
Матрица М представлена ниже в виде таблицы 1:
Таблица 1
1,3 -80%
1,4 – 70%
1,5 – 60%
1,3 -80%
1,4 – 70%
1,5 – 60%
1,7 -30%
1,8 – 15%
1,7 -30%
1,8 – 15%
Далее выводят из широкого диапазона значений ИРИ целевой диапазон (1,9…2,7), при попадании в который с вероятностью 99% делается вывод о том, что пациент:
1) защищен от хронического воспалительного заболевания, в том числе хронического простатита, хронического цистита, хронического синусита, хронического тонзиллита, хронического эндометрита и сальпингоофорита, хронического бронхита, ларингита, трахеита; если у человека уже есть одно из указанных заболеваний, то делают вывод о том, что значение ИРИ с вероятностью 99% ниже 1,9, при этом если у человека, имеющего хроническое заболевание, значение ИРИ составляет менее 1,9, то его поднятие до целевого диапазона позволяет добиться ремиссии заболевания сроком от одного года;
2) защищен от протекания сезонных ОРВИ, в том числе гриппа и Covid19, в средней и тяжелой форме (по шкале NEWS); если у человека уже есть одно из вышеперечисленных заболеваний в средней и тяжелой форме, то делают вывод о том, что значение ИРИ с вероятностью 99% ниже 1,9, при этом в аспекте вакцинации от гриппа и Covid19:
- пациентам из целевого диапазона вакцинация от гриппа и Covid19 напрямую не показана и решение принимается на усмотрение гражданина, если у врачей нет других противопоказаний;
- пациентам со значением ИРИ ниже 1,9 вакцинация обязательна;
- пациентам со значением ИРИ ниже 1,2 вакцинация противопоказана без консультации иммунолога ввиду высокого риска осложнений;
3) защищен от возникновения злокачественных новообразований (уменьшает вероятность «феномена ускользания» от мутировавшей раковой клетки до 1%); исключения составляют профессиональные интоксикации, облучающая радиация, аутоиммунные заболевания; у пациентов с впервые выявленным злокачественным образованием ИРИ с вероятностью 99% ниже 1,9, при этом достижение целевого диапазона увеличивает у таких пациентов эффективность химио- и иммунотерапии (в том числе дендритными клетками);
4) устойчив к антибактериальной терапии; при значениях ИРИ в целевом диапазоне препараты максимально эффективны; при снижении значения ИРИ до 1,5 возникает избирательная устойчивость, преимущественно к грамотрицательным бактериям, уреаплазме, микоплазме; при снижении значения ИРИ ниже 1,5 возникает множественная устойчивость к широкому диапазону возбудителей: это обусловлено тем, что адаптация возбудителя (в основном через мутации с новыми свойствами) происходит быстрее, чем новые штаммы успевает обнаружить и уничтожить Т-клеточная регуляция.
После этого посредством блока назначения терапии 6 вводят в организм человека препарат для повышения иммунорегуляторного индекса.
Для подтверждения достижения заявленного технического результата была проведена наблюдательная программа по мониторингу ИРИ у различных категорий пациентов в общем количестве более 6000 измерений.
Для изучения значимости величины ИРИ были выбраны две группы пациентов: в первую группу вошли пациенты с хроническими воспалительными заболеваниями (заболевания, вызванные бактериальной флорой, стажем более года и имеющие хотя бы одно обострение в год): хронический простатит, хронический цистит, хронический синусит, хронический тонзиллит, хронический эндометрит и сальпингоофорит, хронический бронхит, ларингит, трахеит; во вторую группу вошли пациенты без хронического воспалительного заболевания.
В первой группе (144 человека) средний уровень ИРИ составил 1,45±0,15 г/л, а во второй (89 человек) - 1,95±0,05 г/л (данные представлены в формате M±m), сравниваемые совокупности имеют нормальное распределение.
Чтобы сделать вывод о статистической значимости полученных различий и эффективности нового алгоритма интерпретации, был использован t-критерий Стьюдента, рассчитываемый как разность средних значений, поделенная на сумму квадратов ошибок:
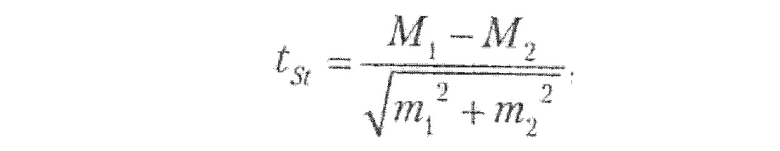

Таким образом, при M1=1,95 и M2=1,45, m1=0,05 и m2=0,15 получили значение t-критерия равным 3,16.
Число степеней свободы: 144+89-2=231.
Таблица 2
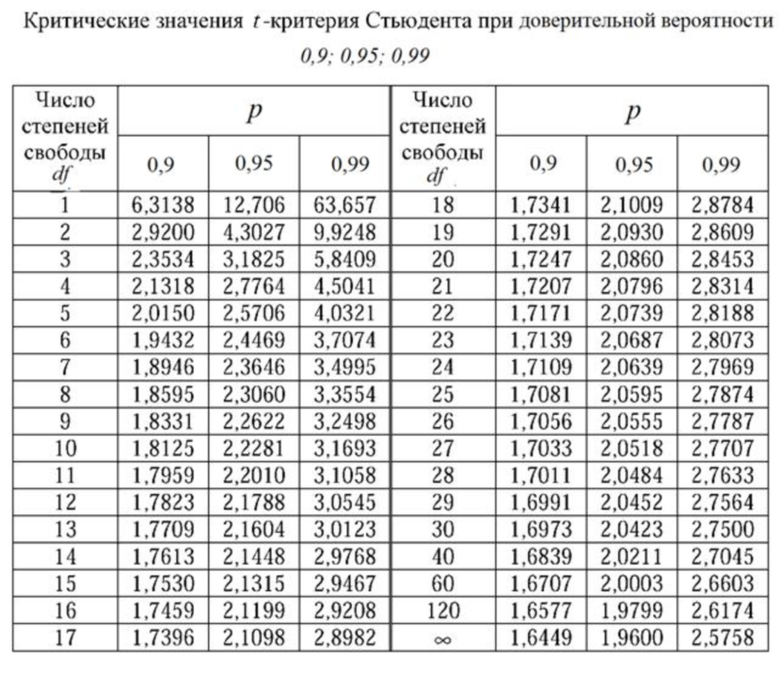
Сравнение полученного значения t-критерия Стьюдента с критическими значениями из таблицы 2 показало, что доверительная вероятность гипотезы составляет более 99%, а вероятность ошибки р≤0,01, из чего был сделан вывод о том, что при значениях ИРИ не ниже 1,9 клеточный иммунитет защищает от хронизации вышеперечисленных заболеваний с вероятностью более 99%.
Реализация предложенных способов интерпретации и повышения ИРИ позволила:
- осуществлять страхование от хронических воспалительных заболеваний и риска заболевания гриппом и Covid19 вне зависимости от возраста, профессии, статуса вакцинации и т.д. в системе добровольного медицинского страхования: чем выше значение ИРИ у застрахованного, тем ниже цена страховки – это единственный необходимый маркер;
- экономить время и средства медицинских учреждений на лабораторных анализах, диагностических процедурах, медикаментах при лечении хронического воспалительного заболевания, гриппа, Covid19;
- осуществлять принятие врачом и пациентом оперативного и обоснованного решения о вакцинации, основываясь на точных показателях иммунитета.
К дополнительному техническому результату можно отнести увеличение количества диапазонов значений ИРИ, подлежащих интерпретации, расширение перечня заболеваний, диагностируемых с помощью интерпретации упомянутых значений ИРИ, экономию времени и средств медицинских учреждений на лабораторных анализах, диагностических процедурах, медикаментах при лечении хронических воспалительных заболеваний, гриппа, Covid19, а также увеличение достоверности способов повышения ИРИ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ИНФЕКЦИОННО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2023 |
|
RU2813422C1 |
| Способ прогнозирования исходов COVID-19 | 2023 |
|
RU2830374C1 |
| Способ лечения неосложненного некротизирующего энтероколита у новорожденных с бактериальной инфекцией и при подозрении на наличие внутриутробной инфекции | 2021 |
|
RU2771856C1 |
| СПОСОБ ДИАГНОСТИКИ РАННЕГО ВРОЖДЕННОГО СИФИЛИСА МАНИФЕСТНОГО | 2009 |
|
RU2402775C1 |
| Способ прогнозирования неблагоприятного течения хронического посттравматического увеита после однократного проникающего хирургического вмешательства на глазном яблоке | 2020 |
|
RU2733745C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ОСЛОЖНЕНИЯ ПОСЛЕ COVID-19 У ЛИЦ С КОМОРБИДНЫМ ФОНОМ В АРКТИЧЕСКОМ РЕГИОНЕ | 2023 |
|
RU2812780C1 |
| СПОСОБ ЛЕЧЕНИЯ УГРЕВОЙ БОЛЕЗНИ | 2011 |
|
RU2455009C1 |
| СПОСОБ ПРОГНОЗА ОСЛОЖНЕНИЙ ИММУНОТЕРАПИИ АЛЛЕРГЕНАМИ ПРИ СЕЗОННОМ АЛЛЕРГИЧЕСКОМ РИНИТЕ | 2003 |
|
RU2262951C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ГЛЮКОКОРТИКОИДНОЙ ТЕРАПИИ У БОЛЬНЫХ С ОБОСТРЕНИЕМ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ | 2011 |
|
RU2490645C2 |
| СПОСОБ ЛЕЧЕНИЯ СИАЛОАДЕНИТА | 2007 |
|
RU2413507C2 |
Изобретение относится к медицине, а именно к иммунологии, и может быть использовано для определения показания к вакцинации против гриппа/COVID-19. Определяют иммунорегуляторный индекс R = CD4+ / CD8+. Если 1,2≤R≤1,5, то вакцинация против гриппа/COVID-19 рекомендована, кроме случаев наличия любого хронического воспалительного заболевания и возраста старше 50 лет. Если 1,6≤R≤1,8, то вакцинация против гриппа/COVID-19 рекомендована без ограничений. Если 1,9≤R≤2,6, то риск заболевания в среднетяжелой форме после вакцинации против гриппа/СOVID-19 достоверно не изменяется. Если R>2,6, то вакцинация против гриппа/COVID-19 противопоказана при наличии аллергических и аутоиммунных заболеваний, риск заболевания в среднетяжелой форме после вакцинации против гриппа/COVID-19 достоверно не изменяется. Способ обеспечивает возможность принятия решения о вакцинации за счет показателей иммунитета. 1 ил., 2 табл.
Способ определения показания к вакцинации против гриппа/COVID-19, включающий определение иммунорегуляторного индекса по соотношению R = CD4+ / CD8+ и,
если 1,2≤R≤1,5, то вакцинация против гриппа/COVID-19 рекомендована, кроме случаев наличия любого хронического воспалительного заболевания и возраста старше 50 лет,
если 1,6≤R≤1,8, то вакцинация против гриппа/COVID-19 рекомендована без ограничений,
если 1,9≤R≤2,6, то риск заболевания в среднетяжелой форме после вакцинации против гриппа/СOVID-19 достоверно не изменяется,
если R>2,6, то вакцинация против гриппа/COVID-19 противопоказана при наличии аллергических и аутоиммунных заболеваний, риск заболевания в среднетяжелой форме после вакцинации против гриппа/COVID-19 достоверно не изменяется.
| RU 2184972 C2, 10.07.2002 | |||
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ БОЛЬНЫХ С ПОСТНЕКРОТИЧЕСКИМИ СВИЩАМИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2010 |
|
RU2442162C1 |
| СПОСОБ ИММУНОКОРРИГИРУЮЩЕЙ ТЕРАПИИ ЗАБОЛЕВАНИЙ | 2000 |
|
RU2163488C1 |
| НОВИКОВ Д | |||
| К | |||
| и др | |||
| Иммунокоррекция, иммунопрофилактика, иммунореабилитация | |||
| Витебск, ВГМУ, 2006, 198 с | |||
| OBERHARDT V | |||
| et al | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Nature | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| LU W | |||
| et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2023-05-05—Публикация
2022-01-13—Подача