Область техники
Изобретение относится к области извлечения и восстановления редкоземельных элементов.
Более конкретно, изобретение относится к применению смеси экстрагентов, обладающей синергетическим эффектом, для извлечения по меньшей мере одного редкоземельного элемента, присутствующего в водной среде, содержащей фосфорную кислоту, такой как водный раствор фосфорной кислоты, полученный в результате воздействия серной кислотой на фосфатную руду.
Изобретение может найти применение, в частности, при обработке фосфатных руд с целью переработки редкоземельных элементов, присутствующих в этих рудах.
Уровень техники
К редкоземельным элементам (далее "РЗЭ") относятся металлы, характеризующиеся аналогичными свойствами, а именно, скандий (Sc), иттрий (Y) и все лантаноиды, включающие в себя 15 химических элементов, перечисленных в Периодической таблице Менделеева, в интервале от лантана (La) с атомным номером 57 до лютеция (Lu) с атомным номером 71.
В эту группу входят "легкие" РЗЭ, т.е. имеющие атомный номер не выше 61 (скандий, иттрий, лантан, церий, празеодим и неодим), и "тяжелые" РЗЭ, т.е. имеющие атомный номер не ниже 62 (самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий и иттербий).
Особая электронная конфигурация РЗЭ и, в частности, их ненасыщенная электронная 4f-подоболочка придает им уникальные химические, структурные и физические свойства. Эти свойства используются в промышленных применениях, которые столь же разнообразны, как и сложны: стекольная и керамическая промышленность, полировка, катализ (в частности, нефтяной и автомобильный), производство высокотехнологичных сплавов, постоянных магнитов, оптических устройств (в частности, фотоаппаратов и камер), люминофоров, аккумуляторов для электрических или гибридных транспортных средств, генераторов для ветряных турбин и т. д.
Следовательно, РЗЭ составляют часть так называемых "технологических" металлов, получение которых является стратегическим, но при этом находится под угрозой из-за мирового роста и спроса на эти конкретные металлы.
В настоящее время РЗЭ производятся из традиционных ресурсов, таких как месторождения твердых пород бастнезита, а также аллювиальные месторождения монацита и ксенотима. Однако существуют и другие нетрадиционные ресурсы, такие как фосфатные руды (также называемые природными фосфатами), которые используются для производства фосфорной кислоты и фосфорных удобрений и в которых концентрация РЗЭ, безусловно, меньше, но, тем не менее, может привести к прибыльному производству РЗЭ.
Обработка фосфатных руд с целью получения фосфорной кислоты и фосфорных удобрений начинается с разрушающего воздействия (или выщелачивания), на эти руды, предварительно раздробленные и измельченные, концентрированной кислотой, обычно 98% серной кислотой, которая превращает трехкальциевый фосфат в фосфорную кислоту H3PO4 и нерастворимый сульфат кальция (или фосфогипс). В результате этого воздействия образуются водные растворы фосфорной кислоты с концентрацией более 4 моль/л, которые содержат различные концентрации РЗЭ в зависимости от их содержания в исходных рудах и в соответствии с методом обработки, применяемым к таким рудам.
Один из методов извлечения РЗЭ из водного раствора фосфорной кислоты, образующегося в результате выщелачивания фосфатной руды серной кислотой, заключается в том, что после фильтрации и концентрирования этот водный раствор подвергают жидкостно-жидкостной экстракции или экстракции растворителем, при которой водный раствор приводят в контакт с органическим раствором, содержащим один или несколько экстрагентов в органическом разбавителе, имеющем сродство к РЗЭ, чтобы обеспечить перенос РЗЭ в органический раствор.
Такая экстракция должна быть одновременно эффективной и селективной по отношению ко многим другим металлам (далее "металлические примеси"), которые также присутствуют в водных растворах фосфорной кислоты, образующихся в результате выщелачивания фосфатных руд серной кислотой и, в частности, по отношению к железу, присутствующему в форме ионов Fe3+, концентрация которого в растворах этого типа обычно превышает 1 г/л.
Анализ научной литературы показал, что небольшое количество экстрагентов было протестировано для извлечения РЗЭ из среды фосфорной кислоты (см. S. Wu et al., Chemical Engineering Journal 2018, 335, 774-800, далее ссылка [1])).
Были изучены два больших класса экстрагентов, а именно:
- катионообменные экстрагенты, также называемые кислотными экстрагентами, которые в основном представляют собой фосфорорганические соединения, такие как фосфорорганические кислоты, органофосфоновые кислоты или органофосфиновые кислоты; это, например, ди-2-этилгексилфосфорная кислота (или D2EHPA, или HDEHP), ди(н-октилфенил) фосфорная кислота (или DOPPA), 2-этилгексил-2-этилгексилфосфоновая кислота (или HEH [EHP] или PC88A) и бис(триметил-2,4,4-пентил) фосфиновая кислота (продается под наименованием Cyanex™ 272); и
- сольватирующие экстрагенты, также называемые нейтральными экстрагентами, такие как фосфаты, оксиды фосфина или дигликольамиды; это, например, три-н-бутилфосфат (или TBP), оксид триоктилфосфина (или TOPO) и N, N, N’, N’-тетраоктил-дигликольамид (или TODGA).
Что касается фосфорорганических кислот, оказывается, что экстракция РЗЭ этими кислотами сильно зависит от кислотности среды, в которой присутствуют РЗЭ. Поэтому D2EHPA и его аналоги (например, DOPPA) позволяют эффективно извлекать тяжелые РЗЭ при кислотности выше 4 моль/л фосфорной кислоты, но не позволяют извлекать легкие РЗЭ при такой кислотности. Это связано с тем, что количественное извлечение легких РЗЭ можно обеспечить только при кислотности ниже 0,5 моль/л фосфорной кислоты и, следовательно, по меньшей мере в восемь раз ниже, чем водные растворы фосфорной кислоты, получаемые в результате выщелачивания фосфатных руд серной кислотой.
Фосфорорганические кислоты также имеют недостатки, заключающиеся в медленной кинетике экстракции и сродстве к переходным металлам и, в частности, к железу. Поэтому конкурентная экстракция ионов Fe3+ с помощью D2EHPA значительно снижает экстракцию РЗЭ этим экстрагентом, тогда как присутствие других металлических примесей, таких как Al3+, Ca2+ или Mg2+, по-видимому, мало влияет на эту экстракцию (см. L. Wang et al., Hydrometallurgy 2010, 101 (1-2), 41-47, далее ссылка [2]).
Первой возможностью преодоления этой недостаточной селективности было бы восстановлении ионов Fe3+ до ионов Fe2+ (которые очень мало экстрагируются фосфорорганическими кислотами) с помощью восстанавливающего агента перед тем, как приступить к экстракции РЗЭ; тем не менее, затраты на такую операцию могут оказаться очень высокими по сравнению с экономической выгодой, обеспечиваемой прямым селективным извлечением РЗЭ. Второй возможностью могло бы быть добавление операций, направленных на удаление железа из водных растворов фосфорной кислоты перед извлечением из них РЗЭ, например, путем селективного осаждения железа с последующим удалением осадка фильтрацией, но это бы сначала привело к трудно реализуемому и поэтому малоинтересному для промышленности методу, а во-вторых, к риску изменения конечного качества производимой фосфорной кислоты.
Известно, что применение смесей экстрагентов, содержащих, например, катионообменник и сольватирующий обменник, в некоторых случаях может позволить значительно повысить производительность жидкостно-жидкостной экстракции по сравнению с производительностью, достигаемой при использовании только экстрагентов.
Однако исследования показывают, что в присутствии среды, содержащей фосфорную кислоту, смеси, содержащие фосфорорганическую кислоту, такую как D2EHPA, и сольватирующий экстрагент, такой как TBP или оксид фосфина (CyanexTM 923), оказывают антагонистическое действие на экстракцию РЗЭ в том, что эффективность экстракции (определяемая коэффициентами распределения РЗЭ) ниже, чем достигаемая только фосфорорганической кислотой (см. вышеупомянутую ссылку [2]; DK Singh et al., Desalination and Water Treatment 2012, 38 (1) -3), 292-300, далее ссылка [3]).
Что касается DGA, они представляют собой семейство экстрагентов, которые были разработаны японской группой в контексте исследований по переработке отработанного ядерного топлива с целью совместного извлечения трехвалентных актинидов и лантанидов из рафината процесса PUREX, но которые также изучались в отношении возможности восстановления РЗЭ из лома производства постоянных магнитов NdFeB.
Так, в международной заявке PCT WO2016/046179, далее ссылка [4], показано, что липофильные симметричные DGA с 24 атомами углерода или более, такие как TODGA, позволяют извлекать диспрозий, празеодим и неодим из водного раствора азотной кислоты, полученного в результате обработки постоянных магнитов NdFeB, не только количественно, но и селективно по отношению к другим металлическим элементам, присутствующим в этой фазе, в частности, по отношению к железу и бору.
В ссылке [4] указано, что хотя водный раствор, из которого экстрагируются РЗЭ, предпочтительно является раствором азотной кислоты, он также может быть раствором серной или фосфорной кислоты. Однако в этой ссылке не сообщается ни об одном экспериментальном результате, относящемся к экстракции РЗЭ с помощью TODGA из раствора фосфорной кислоты, когда известно, что ионы фосфата, присутствующие в этом типе раствора, являются гораздо более сильно комплексообразующими, чем ионы нитрата, присутствующие в растворе азотной кислоты.
С другой стороны, в международной заявке PCT WO2016/177695, далее ссылка [5], показано, что извлечение лантана, неодима, гадолиния, диспрозия и иттербия из водного раствора, содержащего от 0,5 до 5 моль/л фосфорной кислоты, с помощью органической фазы, содержащей TODGA, приводит ко всем процентным показателям экстракции ниже 2%, и это касается всех протестированных концентраций фосфорной кислоты.
Следовательно, ссылка [5] подтверждает, что эффективность экстракции, достигаемую при использовании TODGA для извлечения РЗЭ из водного раствора азотной кислоты, невозможно перенести на извлечение РЗЭ из водного раствора фосфорной кислоты.
И наконец, хотя это относится скорее к переработке отработавшего ядерного топлива, чем к извлечению РЗЭ из водных растворов фосфорной кислоты, образующихся в результате выщелачивания фосфатных руд серной кислотой, необходимо процитировать работу P.K. Nayak et al., впервые опубликованную в J. Environ. Chem. Англ. 2013, 1 (3), 559-565, далее ссылка [6], и, во-вторых, в Sep. Sci. Technol. 2014, 49 (8), 1186-1191, далее ссылка [7].
В этой работе показано, что смесь экстрагентов, содержащая фосфорорганическую кислоту, в данном случае D2EHPA, и липофильный симметричный DGA, в данном случае N, N, N', N'-тетра(2-этилгексил) дигликольамид (или TEHDGA), в n-додекане приводит к очень значительной экстракции ионов Fe3+, присутствующих в водном растворе азотной кислоты с высокой активностью. Например, для смеси, содержащей 0,25 моль/л D2EHPA и 0,1 моль/л TEHDGA в n-додекане, коэффициент распределения железа составляет около 1,2 в тесте партии, и более 80% присутствующего железа экстрагируется в органической фазе в тесте смесителя-отстойника (см. ссылку [5]).
Также показано, что если концентрация азотной кислоты в водном растворе, содержащем америций и европий, превышает 1 моль/л, способность смеси экстрагентов, содержащих D2EHPA и TODGA, извлекать европий из этого раствора такая же, как полученная только с TODGA (см. ссылку [6]).
Следовательно, эта работа позволяет сделать вывод, что применение смеси экстрагентов, содержащих фосфорорганическую кислоту и DGA, не имеет никаких преимуществ по сравнению с использованием только DGA, когда речь идет об извлечении РЗЭ из водного раствора азотной кислоты, содержащего железо, и/или имеющего концентрацию азотной кислоты более 1 моль/л.
Принимая во внимание вышеизложенное, существует реальная потребность в экстрагенте или смеси экстрагентов, которые позволили бы экстрагировать все РЗЭ, легкие и тяжелые, из водного раствора фосфорной кислоты, имеющего кислотность того же типа, что и водные растворы, полученные в результате выщелачивания фосфатных руд серной кислотой, и делать это эффективно и селективно по отношению к другим металлам, которые могут присутствовать в данном растворе, в частности, по отношению к железу.
Однако в контексте своей работы авторы изобретения неожиданно обнаружили, что смесь экстрагентов, включающая в себя фосфорорганическую кислоту, такую как H2EHPA, и липофильный симметричный дигликольамид, такой как TODGA, позволяет эффективно и селективно по отношению к железу экстрагировать все РЗЭ, которые присутствуют в водном растворе, содержащем фосфорную кислоту, даже при концентрации кислоты более 4 моль/л.
Они также обнаружили, что эта смесь экстрагентов оказывает синергетический эффект на экстракцию РЗЭ из такого водного раствора фосфорной кислоты, поскольку:
- во-первых, как известно из уровня техники и подтверждено авторами (см. пример 2 ниже), фосфорорганические кислоты, такие как D2EHPA, не подходят для извлечения легких РЗЭ из водной среды, содержащей более 4 моль/л фосфорной кислоты, и
- во-вторых, как известно из ссылки [5] и подтверждено авторами изобретения (см. пример 1 ниже), липофильные симметричные DGA, такие как TODGA, при их использовании по отдельности не позволяют извлекать редкоземельные элементы из водной среды, содержащей более 0,5 моль/л фосфорной кислоты.
Эти экспериментальные результаты положены в основу настоящего изобретения.
Сущность изобретения
Таким образом, объектом изобретения является применение смеси, содержащей
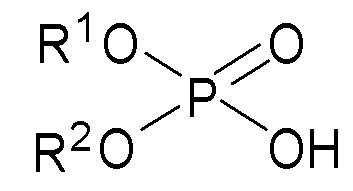
- первый экстрагент, представляющий собой фосфорорганическую кислоту и соответствующий следующей формуле (I):
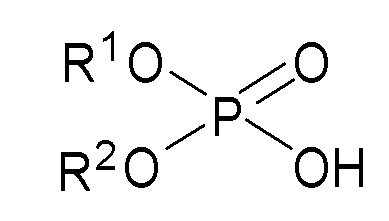 (I)
(I)
где R1 and R2, одинаковые или разные, представляют собой насыщенную или ненасыщенную, линейную или разветвленную углеводородную группу, содержащую от 6 до 12 атомов углерода, или фенильную группу, необязательно замещенную насыщенной или ненасыщенной, линейной или разветвленной углеводородной группой, содержащую от 1 до 10 атомов углерода; и
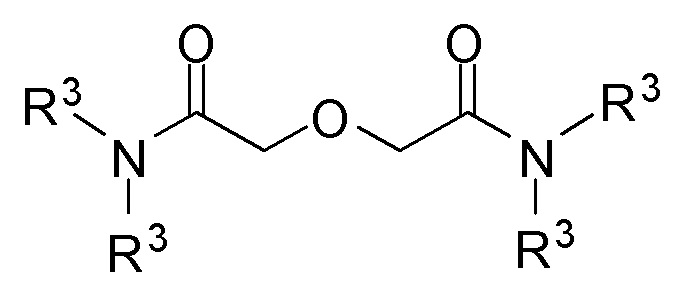
- второй экстрагент, представляющий собой липофильный симметричный DGA и соответствующий следующей формуле (II):
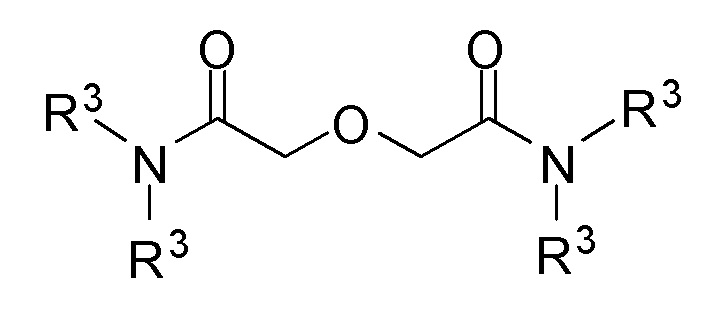 (II)
(II)
где R3 представляет собой линейную или разветвленную алкильную группу, содержащую от 6 до 12 атомов углерода;
для извлечения по меньшей мере одного РЗЭ из водной среды, содержащей фосфорную кислоту.
Использованный выше и в дальнейшем признак "насыщенная или ненасыщенная, линейная или разветвленная углеводородная группа, содержащая от 6 до 12 атомов углерода", означает любую алкильную, алкенильную или алкинильную группу с линейной цепью или с одним или несколькими разветвлениями, и содержащую в совокупности 6, 7, 8, 9, 10, 11 или 12 атомов углерода.
Аналогичным образом, признак "насыщенная или ненасыщенная, линейная или разветвленная углеводородная группа, содержащая от 1 до 10 атомов углерода" означает любую алкильную, алкенильную или алкинильную группу, с линейной цепью или с одной или несколькими разветвлениями и содержащую в совокупности 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов углерода.
Кроме того, признак "линейная или разветвленная алкильная группа, содержащая от 6 до 12 атомов углерода" означает любую алкильную группу с линейной цепью или с одной или несколькими разветвлениями и содержащую в совокупности 6, 7, 8, 9, 10, 11 или 12 атомов углерода.
Выше и далее термины "водная среда", "водный раствор" и "водная фаза" эквивалентны и взаимозаменяемы, так же как и эквивалентны и взаимозаменяемы термины "органический раствор" и "органическая фаза".
Выражение "от… до…" применительно к диапазону концентраций подразумевает, что включены границы этого диапазона.
В соответствии с изобретением в приведенной выше формуле (I) R1 и R2, одинаковые или разные, предпочтительно представляют собой линейную или разветвленную алкильную группу, содержащую от 6 до 12 атомов углерода, или фенильную группу, замещенную линейной или разветвленной алкильной группой, содержащей от 1 до 10 атомов углерода.
Кроме того, предпочтительно, чтобы R1 и R2, одинаковые или разные, представляли собой:
- линейную или разветвленную алкильную группу, содержащую от 8 до 10 атомов углерода, такую как группа, включающая в себя n-октил, изооктил, n-нонил, изононил, n-децил, изодецил, 2-этилгексил, 2-бутилгексил, 2-метилгептил, 2-метилоктил, 1,5-диметилгексил, 2,4,4-триметилпентил, 1,2-диметилгептил, 2,6-диметилгептил, 3,5,5-триметилгексил, 3,7-диметилоктил, 2,4,6-триметилгептил и т.д.; или
- фенильную группу, замещенную линейной или разветвленной алкильной группой, содержащей от 6 до 10 атомов углерода, такой как группа, включающая в себя n-гексил, изогексил, n-гептил, изогептил, n-октил, изооктил, n-нонил, изононил, n-децил, изодецил, 1-этилпентил, 2-этилгексил, 2-бутилгексил, 2-метилгептил, 2-этилгептил, 2-метилоктил, 2-метилнонил, 1,5-диметилгексил, 2,4,4-триметилпентил, 1,2-диметилгептил, 2,6-диметилгептил, 3,5,5-триметилгексил, 3,7-диметилпентил, 2,4,6-триметилгептил и т.д.
Кроме того, R1 и R2 предпочтительно идентичны друг другу.
Среди экстрагентов указанной выше формулы (I) особое предпочтение отдается тем, в которых R1 и R2, идентичные друг другу, представляют собой разветвленную алкильную группу, содержащую от 8 до 10 атомов углерода.
Таким экстрагентом является, например, D2EHPA, которая соответствует приведенной выше формуле (I), где R1 и R2 представляют собой 2-этилгексильную группу.
В соответствии с изобретением в приведенной выше формуле (II) R3 предпочтительно представляет собой линейную или разветвленную алкильную группу, содержащую от 8 до 10 атомов углерода, такую как группа, включающая в себя n-октил, изооктил, n-нонил, изононил, n-децил, изодецил, 2-этилгексил, 2-бутилгексил, 2-метилгептил, 2-метилоктил, 1,5-диметилгексил, 2,4,4-триметилпентил, 1,2-диметилгептил, 2,6-диметилгептил, 3,5,5-триметилгексил, 3,7-диметилоктил, 2,4,6-триметилгептил и т.д.
Среди экстрагентов указанной выше формулы (II) особое предпочтение отдается тем, в которых R3 представляет собой линейную алкильную группу, содержащую от 8 до 10 атомов углерода.
Таким экстрагентом является, например, TODGA, соответствующий приведенной выше формуле (II), в которой R3 представляет собой n-октильную группу.
В соответствии с изобретением смесь экстрагентов предпочтительно представляет собой смесь D2EHPA и TODGA.
Более того, смесь экстрагентов предпочтительно используется в растворе в органическом разбавителе, которым может быть любой неполярный органический разбавитель, использование которого было предложено для солюбилизации липофильных экстрагентов, таких как углеводород или смесь алифатических и/или ароматических углеводородов. В качестве примеров такого разбавителя можно упомянуть n-додекан, гидрированный тетрапропилен (TPH), керосин и разбавители, которые продаются под наименованиями IsaneTM IP-185 (Total), IsaneTM IP-175 (Total), ShellsolTM D90 (Shell Chemicals) и EscaidTM 110 Fluid (Exxon Mobil), предпочтение отдается IsaneTM IP-185.
Кроме того, смесь экстрагентов предпочтительно используется для извлечения одного или нескольких РЗЭ из водной среды, в которой он (они) присутствуют, путем жидкостно-жидкостной экстракции, и в этом случае использование данной смеси включает в себя, по меньшей мере, контакт водной среды с не смешиваемым в водой органическим раствором, содержащим смесь экстрагентов в органическом разбавителе, и затем отделение водной среды от органического раствора, в результате чего получается органический раствор, содержащий один или несколько РЗЭ.
Органический раствор, который контактирует с водной средой, обычно содержит от 0,2 моль/л до 2 моль/л первого экстрагента и от 0,05 моль/л до 2 моль/л второго экстрагента.
Само собой разумеется, что выбор концентрации для каждого из первого и второго экстрагентов в этих диапазонах будет зависеть от используемых экстрагентов, а также, возможно, одного или нескольких РЗЭ, которые желательно извлечь.
Таким образом, например, для смеси, содержащей D2EHPA в качестве первого экстрагента и TODGA в качестве второго экстрагента, органический раствор предпочтительно будет содержать от 0,2 моль/л до 1,5 моль/л D2EHPA и от 0,1 моль/л до 0,5 моль/л. ТОДГА.
В соответствии с изобретением после извлечения одного или нескольких РЗЭ из водной среды путем жидкостно-жидкостной экстракции предпочтительно следует отгонка этого РЗЭ или этих РЗЭ из органического раствора, из которого они (они) извлекались (экстрагировались); в этом случае отгонка включает в себя, по меньшей мере, контакт органического раствора с кислотным или основным водным раствором, а затем отделение органического раствора от водного раствора, в результате чего получается водный раствор, содержащий один или несколько РЗЭ.
Водная среда, из которой извлекаются один или несколько РЗЭ, предпочтительно содержит от 0,5 моль/л до 10 моль/л, предпочтительно от 2 моль/л до 6 моль/л и еще лучше от 4 моль/л до 5 моль/л фосфорной кислоты.
Такая водная среда может, в частности, представлять собой водный раствор фосфорной кислоты, полученный в результате выщелачивания фосфатной руды серной кислотой.
Водный раствор может содержать РЗЭ в общей концентрации от 30 мг/л до 1200 мг/л, точнее от 100 мг/л до 1000 мг/л, а также определенное количество металлических примесей, включая железо, а также магний, алюминий, кальций, цинк, хром, ванадий и др.
В любом случае один или несколько РЗЭ предпочтительно выбираются из иттрия, лантана, неодима, диспрозия, иттербия и их смесей.
Другие существенные признаки и преимущества изобретения станут очевидными из следующего дополнительного описания со ссылками на прилагаемые чертежи.
Само собой разумеется, что это дополнительное описание приводится только для иллюстрации объекта изобретения и ни в коем случае не должно интерпретироваться как его ограничение.
Краткое описание чертежей
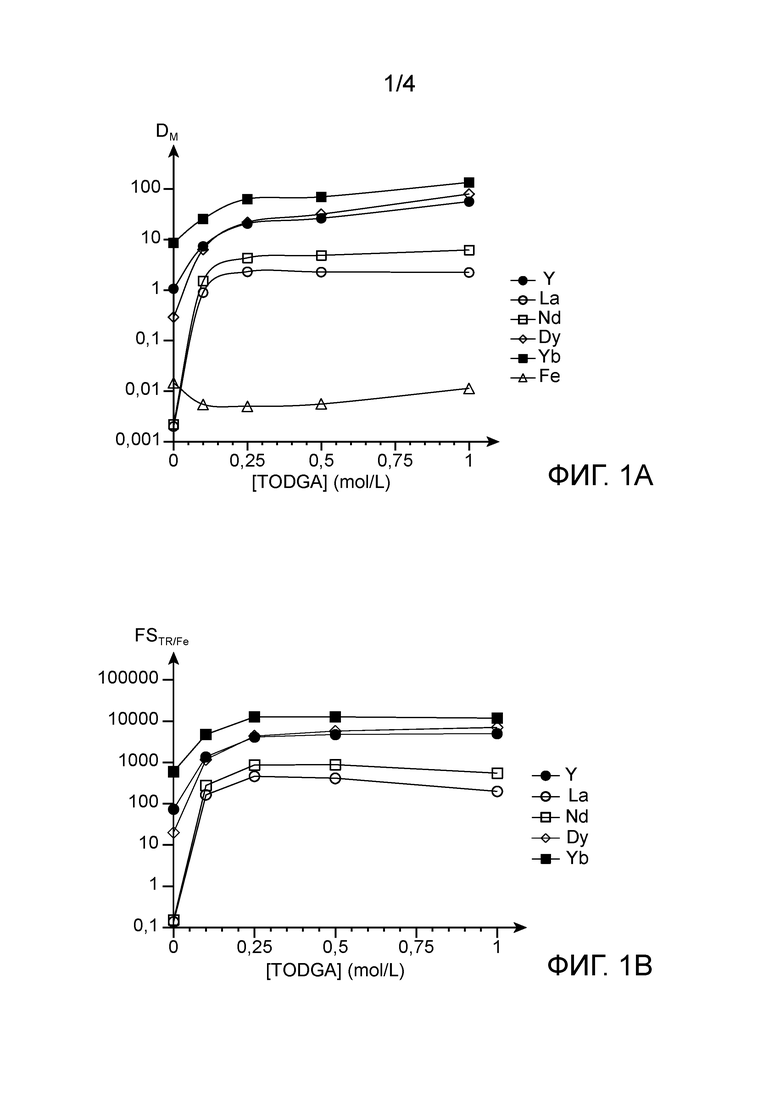
Фиг.1A и 1B иллюстрируют результаты тестов экстракции, выполненных на водных фазах фосфорной кислоты, содержащих пять РЗЭ, а именно иттрий, лантан, неодим, диспрозий и иттербий, а также железо, с использованием органических фаз, содержащих 0,5 моль/л D2EHPA и переменную молярную концентрацию TODGA; на фиг.1A показано изменение коэффициентов распределения РЗЭ и железа, обозначенных DM и представленных на логарифмической шкале, в зависимости от молярной концентрации TODGA, обозначенного [TODGA], в органических фазах, а на фиг.1B показано изменение коэффициентов разделения между РЗЭ и железом, обозначенное FSTR/Fe и также представленное на логарифмической шкале, в зависимости от концентрации TODGA; для сравнения на этих фигурах также показаны значения DM и FSTR/Fe, полученные при одинаковых рабочих условиях с органической фазой, содержащей только D2EHPA в качестве экстрагента.
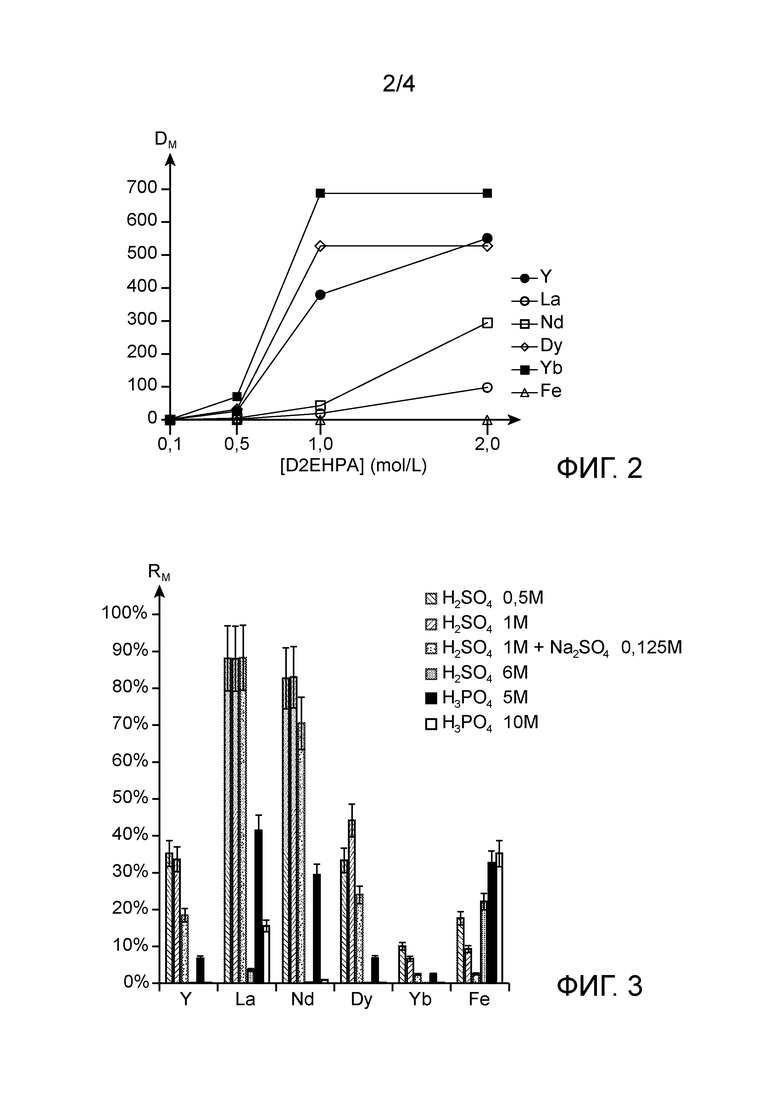
На фиг.2 показаны результаты тестов экстракции, выполнявшихся на водных фазах фосфорной кислоты, которые содержали упомянутые выше пять РЗЭ и железо, с использованием органических фаз, содержащих переменную молярную концентрацию D2EHPA и 0,5 моль/л TODGA; более конкретно, на этой фигуре показано изменение коэффициентов распределения РЗЭ и железа, обозначенное как DM и представленное на арифметической шкале, в зависимости от молярной концентрации D2EHPA, обозначенной как [D2EHPA], в органических фазах.
На фиг.3 показан выход отгонки, обозначенный как RM и выраженный в %, полученный во время тестов отгонки, которые выполнялись на органической фазе, содержащей упомянутые пять РЗЭ, железо, 0,5 моль/л D2EHPA и 0,25 моль/л TODGA, с использованием различных кислых водных фаз.
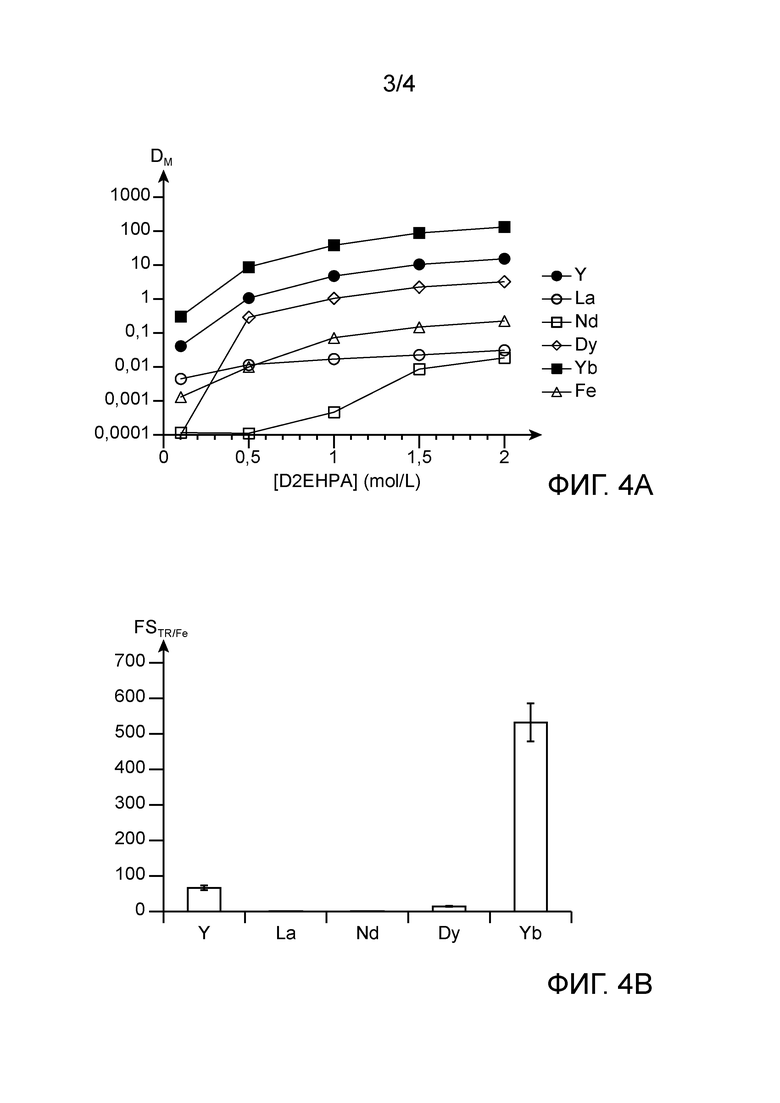
Фигуры 4A и 4B иллюстрируют для сравнения результаты тестов экстракции, которые выполнялись на водных фазах фосфорной кислоты, содержащей упомянутые пять РЗЭ и железо, с использованием органических фаз, содержащих только D2EHPA в качестве экстрагента, при различных молярных концентрациях; на фиг.4A показано изменение коэффициентов распределения РЗЭ и железа, обозначенных DM и представленных на логарифмической шкале, в зависимости от молярной концентрации D2EHPA, обозначенной как [D2EHPA], в органических фазах, а на фиг.4B показаны коэффициенты разделения РЗЭ и железа, обозначенные как FSTR/Fe, полученные с органической фазой, содержащей 1 моль/л D2EHPA.
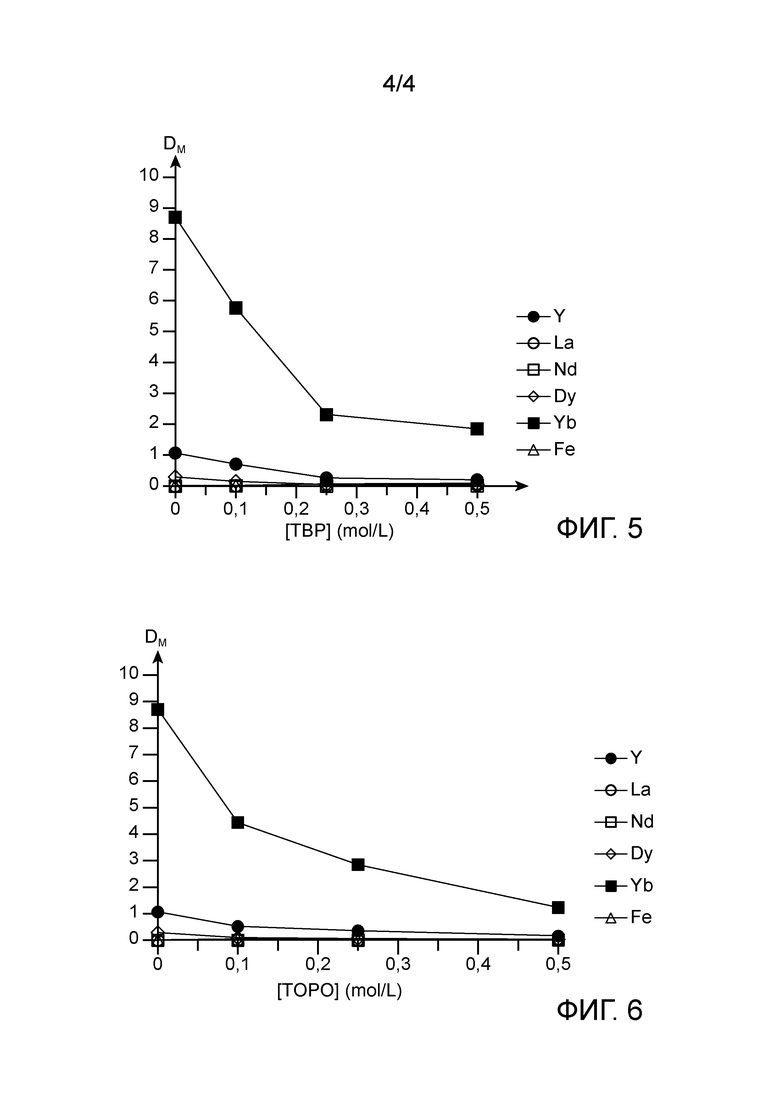
Фиг.5 иллюстрирует для сравнения результаты тестов экстракции, которые выполнялись на водных фазах фосфорной кислоты, содержащих упомянутые выше пять РЗЭ и железо, с использованием органических фаз, содержащих 0,5 моль/л D2EHPA и переменную молярную концентрацию TBP; более конкретно, на этой фигуре показано изменение коэффициентов распределения РЗЭ и железа, обозначенных как DM и представленных на арифметической шкале, в зависимости от молярной концентрации TBP, обозначенного как [TBP], в органических фазах; на этой фигуре также указаны значения DM, полученные при тех же рабочих условиях с органической фазой, содержащей только D2EHPA в качестве экстрагента.
Фиг.6 иллюстрирует для сравнения результаты тестов экстракции, которые выполнялись на водных фазах фосфорной кислоты, содержащих упомянутые пять РЗЭ и железо, с использованием органических фаз, содержащих 0,5 моль/л D2EHPA и переменную молярную концентрацию TOPO; более конкретно, на этой фигуре показано изменение коэффициентов распределения РЗЭ и железа, обозначенных DM и представленных на арифметической шкале, в зависимости от молярной концентрации TOPO, обозначенного как [TOPO], в органических фазах; на этой фигуре также указаны DM, полученные в тех же рабочих условиях с органической фазой, содержащей только D2EHPA в качестве экстрагента.
На фигурах 3 и 4B планки погрешностей соответствуют относительной неопределенности 10%, которая включает в себя различные аналитические и экспериментальные погрешности.
Описание вариантов осуществления
Все тесты экстракции, представленные в следующих примерах, выполнялись с использованием в качестве водных фаз аликвот синтетического водного раствора, представляющего водные растворы фосфорной кислоты, реально полученные во время производства H3PO4 выщелачиванием природных фосфатов с помощью H2SO4.
Этот синтетический водный раствор содержит, кроме фосфорной кислоты, три легких РЗЭ, а именно иттрий, лантан и неодим, два тяжелых РЗЭ, а именно диспрозий и иттербий, и главную и вредную примесь, а именно железо. Раствор был приготовлен путем растворения оксидов соответствующих металлов со степенью окисления +3 в растворе концентрированной H3PO4 с последующим доведением концентрации H3PO4 в этом растворе до 4,6 моль/л.
В таблице I ниже представлен массовый состав металлических элементов в растворе.
Таблица I
Органические фазы получали с использованием IsaneTM IP185 в качестве органического разбавителя и предварительно уравновешивали их путем контакта с водным раствором, содержащим 4,6 моль/л H3PO4.
Кроме того, все тесты экстракции и отгонки, которые описаны в следующих примерах, выполнялись в микропробирках объемом менее 1,5 мл при температуре 45°C с объемным отношением органических фаз к водным фазам (O/A) равным 1, при однократном контакте этих фаз течение 20 минут с перемешиванием мешалкой VibraxTM. После центрифугирования органическую и водную фазы разделяли путем отстаивания.
Коэффициенты распределения, коэффициенты разделения и выход отгонки определяли в соответствии с общепринятыми условиями в области жидко-жидкостной экстракции, а именно:
- коэффициент распределения металлического элемента M, обозначаемый DM, между двумя фазами, соответственно, органической и водной, равен:
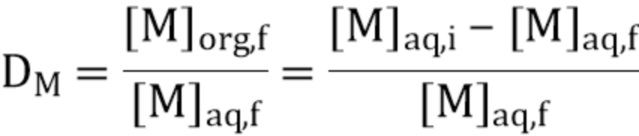
где:
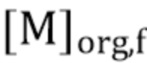 = концентрация M в органической фазе после экстракции (или отгонки),
= концентрация M в органической фазе после экстракции (или отгонки),
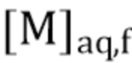 = концентрация M в водной фазе после экстракции (или отгонки), и
= концентрация M в водной фазе после экстракции (или отгонки), и
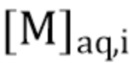 = концентрация M в водной фазе перед экстракцией (или отгонкой);
= концентрация M в водной фазе перед экстракцией (или отгонкой);
- коэффициент разделения между двумя металлическими элементами M1 и M2, обозначенный как FSM1/M2, равен:
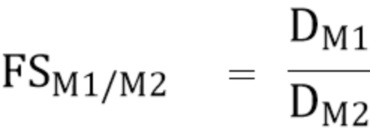
где:
DM1=коэффициент распределения металлического элемента M1, и
DM2=коэффициент распределения металлического элемента M2;
- выход отгонки металлического элемента M, обозначенный как RM, органической фазы равен:
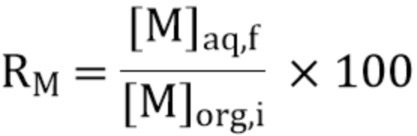
где:
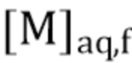 = концентрация M в водной фазе после отгонки, и
= концентрация M в водной фазе после отгонки, и
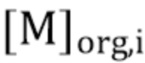 = концентрация M в органической фазе перед отгонкой.
= концентрация M в органической фазе перед отгонкой.
Многоэлементные анализы водных или органических фаз, содержащих РЗЭ (исходный синтетический раствор, водная и органическая фазы после экстракции, водные фазы после отгонки и т.д.), выполнялись методом атомно-эмиссионной спектрометрии, источником которой является плазма аргона, генерируемая посредством индуктивной связи, после разбавления для доведения металлических элементов до измеримых концентраций.
ПРИМЕР 1: Экстракция РЗЭ смесями экстрагентов D2EHPA/TODGA в соответствии с изобретением.
1.1 - Тесты экстракции:
* Первая серия тестов:
Тесты экстракции проводились с использованием в качестве органических фаз растворов, содержащих 0,5 моль/л D2EHPA и TODGA, при концентрации 0,1 моль/л, 0,25 моль/л, 0,5 моль/л или 1 моль/л и, для сравнения, раствора, содержащего 0,5 моль/л D2EHPA, но не содержащего TODGA.
На фиг.1А показано изменение коэффициентов распределения РЗЭ и железа, DM, полученных в конце этих тестов, в зависимости от концентрации TODGA в органических фазах.
Как видно на этой фигуре, добавление TODGA к D2EHPA приводит к значительному увеличению коэффициентов распределения РЗЭ и, следовательно, к их экстракции водной фазы фосфорной кислоты.
Смеси D2EHPA/TODGA обладают особенно высоким сродством к диспрозию, иттербию и иттрию.
Это сродство существенно ниже к лантану и неодиму, однако все же остается высоким (DLamax=2,3) по сравнению с тем, которое имеет только D2EHPA (DLa <0,01).
Более того, добавление TODGA к D2EHPA приводит к снижению коэффициента распределения железа в 3 раза по сравнению с коэффициентом, полученным с использованием только D2EHPA. Этот коэффициент распределения очень мал (DFe=0,005) для концентраций TODGA в диапазоне до 0,25 моль/л, что ясно показывает отличную селективность для РЗЭ по отношению к железу, которую имеют смеси D2EHPA/TODGA.
На фиг.1B показано изменение коэффициентов разделения РЗЭ и железа, FSTR/Fe, в зависимости от концентрации TODGA в органических фазах.
Эта фигура демонстрирует, что максимальные значения FSTR/Fe очень важны для тяжелых РЗЭ, таких как иттербий (FSYb/Fe>12500), и остаются вполне удовлетворительными для легких РЗЭ, таких как лантан (FSLa/Fe=460).
Для сравнения: лучший коэффициент разделения между РЗЭ и железом, который достигается при использовании только D2EHPA, при концентрации 0,5 моль/л в органической фазе, - это коэффициент разделения между иттербием и железом, который как минимум в 20 раз меньше (FSYb/Fe≈600), чем полученный со смесями D2EHPA/TODGA.
* Вторая серия тестов:
Тесты проводились с использованием в качестве органических фаз растворов, содержащих 0,5 моль/л TODGA и D2EHPA при концентрации 0,1 моль/л, 0,5 моль/л, 1 моль/л или 2 моль/л.
На фиг.2 показано изменение коэффициентов распределения РЗЭ и железа, DM, полученных в конце этих тестов, в зависимости от концентрации D2EHPA в органических фазах.
Как видно на этой фигуре, добавление D2EHPA к TODGA приводит к значительному увеличению коэффициентов распределения РЗЭ и, следовательно, к их экстракции в водной фазе фосфорной кислоты.
Для получения хороших характеристик экстракции для всех РЗЭ необходима концентрация D2EHPA в смеси выше 0,1 моль/л. Например, коэффициент распределения лантана очень низкий, когда концентрация D2EHPA в смеси составляет 0,1 моль/л (DLa=0,06), но значительно возрастает, когда концентрация D2EHPA в смеси составляет 0,5 моль/л (DLa=2,2). Для сравнения, сродство к лантану одного D2EHPA при концентрации 0,5 моль/л очень мало (DLa=0,01).
Эти результаты подтверждают данные из ссылки [5], а именно, что использование только TODGA не позволяет извлекать РЗЭ из водной фазы фосфорной кислоты.
С другой стороны, они демонстрируют, что использование концентрации D2EHPA, по крайней мере, равной концентрации TODGA и предпочтительно вдвое большей, чем концентрация TODGA, позволяет получить хорошую экстракцию всех РЗЭ.
1.2 - Тесты отгонки:
Тесты отгонки проводились с использованием:
- в качестве органических фаз: аликвот органической фазы, полученных в результате теста экстракции, который проводился по пункте 1.1 выше, со смесью, содержащей 0,5 моль/л D2EHPA и 0,25 моль/л TODGA; и
- в качестве водных фаз: водных растворов, содержащих:
* 0,5 моль/л, 1 моль/л или 6 моль/л H2SO4,
* или 1 моль/л H2SO4 и 0,125 моль/л Na2SO4,
* или 5 моль/л или 10 моль/л H3PO4.
На фиг.3 показан выход отгонки, RM, полученный в конце этих испытаний.
Как видно на этой фигуре, водные растворы высококонцентрированной H3PO4 (5 моль/л или 10 моль/л) также позволяют отделять лантан и неодим, и еще железо, но не позволяют отделять иттрий, диспрозий и иттербий, которые остаются в органической фазе.
Водные растворы разбавленной H2SO4 (0,5 моль/л и 1 моль/л) фактически позволяют количественно отделить лантан и неодим, частично иттрий, диспрозий и иттербий. Раствор H2SO4 с концентрацией 1 моль/л обеспечивает лучшую селективность отделения РЗЭ по отношению к железу, чем раствор H2SO4 с концентрацией 0,5 моль/л. Добавление Na2SO4 в количестве 0,125 моль/л дополнительно повышает эту селективность, однако приводит к падению выхода иттрия, неодима и диспрозия при отгонке.
На фиг.3 также показано, что железо частично, но селективно отделяется водным раствором, содержащим 6 моль/л H2SO4.
Следовательно, можно предусмотреть реализацию схемы, в которой органическая фаза, полученная в результате экстракции РЗЭ, будет подвергнута стадии промывки водным раствором, содержащим, например, 6 моль/л H2SO4, чтобы селективно удалить железо, присутствующее в этой органической фазе перед тем, как подвергнуть стадии удаления РЗЭ, например, с помощью раствора разбавленной H2SO4, необязательно с добавлением Na2SO4.
Результаты, полученные с водным раствором, содержащим как серную кислоту, так и сульфат натрия, также могут позволить создать схему, при которой РЗЭ, присутствующие в водном растворе после отгонки, извлекались бы осаждением, например, в форме двойных сульфатов РЗЭ и натрия, карбонатов, оксалатов и т.д.; этот тип осаждения описан в литературе.
ПРИМЕР 2: Экстракция РЗЭ с использованием только D2EHPA (сравнительный пример)
Для сравнения, тесты экстракции выполнялись с использованием в качестве органических фаз растворов, содержащих 0,1 моль/л, 0,5 моль/л, 1 моль/л, 1,5 моль/л или 2 моль/л D2EHPA.
На фиг.4А показано изменение коэффициентов распределения РЗЭ и железа, DM, полученных в конце этих испытаний, в зависимости от концентрации D2EHPA в органических фазах.
Эта фигура ясно показывает, что экстракция РЗЭ с помощью D2EHPA уменьшается с увеличением ионного радиуса РЗЭ. Таким образом, D2EHPA имеет хорошее сродство к РЗЭ с небольшим ионным радиусом, таким как иттрий, диспрозий и иттербий, но делает невозможным или почти невозможным извлечение РЗЭ с более высоким ионным радиусом, таких как лантан и неодим (DM<0,1 независимо от концентрации D2EHPA в органической фазе).
Кроме того, на фиг.4B показаны коэффициенты разделения между РЗЭ и железом, FSTR/Fe, полученные при концентрации D2EHPA в органической фазе 1 моль/л. Эти коэффициенты разделения являются удовлетворительными для иттербия (FSYb/Fe=500). Но с другой стороны, они совершенно не подходят для других РЗЭ.
Следует отметить, что не наблюдается значительного изменения этих коэффициентов разделения в зависимости от концентрации D2EHPA в органической фазе.
ПРИМЕР 3: Экстракция РЗЭ с использованием смесей D2EHPA/TBP и D2EHPA/TOPO (сравнительный пример)
Поскольку TODGA является сольватирующим экстрагентом, были проведены тесты экстракции, чтобы проверить, будут ли смеси, содержащие D2EHPA и сольватирующий экстрагент, отличный от TODGA, проявлять такой же синергетический эффект, который наблюдается при использовании D2EHPA в смеси с TODGA.
Эти тесты экстракции проводились с использованием в качестве органических фаз растворов, содержащих 0,5 моль/л D2EHPA и:
- три-n-бутилфосфат (или TBP) в концентрации 0,1 моль/л, 0,25 моль/л или 0,5 моль/л;
или оксид триоктилфосфина (или ТОРО) в концентрации 0,1 моль/л, 0,25 моль/л или 0,5 моль/л.
Результаты, полученные в конце этих тестов, проиллюстрированы коэффициентами распределения DM на фиг.5 для смесей D2EHPA/TBP и на фиг.6 для смесей D2EHPA/TOPO.
Как показано на фиг.5, добавление TBP к D2EHPA приводит к заметному снижению коэффициентов распределения РЗЭ и, следовательно, к их экстракции водной фазой фосфорной кислоты, за исключением случая лантана и неодима, поскольку они еще не экстрагированы только D2EHPA.
Таким образом, это снижение DM, которое тем больше, чем больше концентрация TBP в органической фазе, показывает наличие антагонистического эффекта смесей D2EHPA/ТВФ на экстракцию РЗЭ из водного раствора фосфорной кислоты.
Аналогичным образом на фиг.6 показано постоянное снижение коэффициентов распределения РЗЭ в зависимости от концентрации TOPO в органической фазе, а также показано наличие антагонистического эффекта смесей D2EHPA/TOPO на экстракцию РЗЭ из водного раствора фосфорной кислоты.
Эти результаты согласуются с данными, приведенными в вышеупомянутых ссылках [2] и [3] для смесей D2EHPA/TBP и D2EHPA/TOPO, и подтверждают, что применение смеси, содержащей фосфорорганическую кислоту, такую как D2EHPA, и сольватирующий экстрагент, в принципе не представляет интереса, если требуется извлечь РЗЭ из водного раствора, содержащего фосфорную кислоту.
Список литературы:
[1] S. Wu et al., Chemical Engineering Journal 2018, 335, 774-800
[2] L. Wang et al., Hydrometallurgy 2010, 101(1-2), 41-47
[3] D.K. Singh et al., Desalination and Water Treatment 2012, 38(1-3), 292-300
[4] Международная заявка PCT WO2016/046179
[5] Международная заявка PCT WO2016/177695
[6] P.K. Nayak et al., J. Environ. Chem. Eng. 2013, 1(3), 559-565
[7] P.K. Nayak et al., Sep. Sci. Technol. 2014, 49(8), 1186-1191.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ ЭКСТРАГЕНТ, ИСПОЛЬЗУЕМЫЙ ДЛЯ ЭКСТРАКЦИИ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ ИЗ ВОДНОГО РАСТВОРА ФОСФОРНОЙ КИСЛОТЫ, И ЕГО ПРИМЕНЕНИЕ | 2017 |
|
RU2762074C2 |
| СУММАРНОЕ ИЗВЛЕЧЕНИЕ АКТИНОИДОВ ИЗ СИЛЬНОКИСЛОЙ ВОДНОЙ ФАЗЫ С ПОМОЩЬЮ СОЛЬВАТИРУЮЩИХ ЭКСТРАГЕНТОВ В ВЫСАЛИВАЮЩЕЙ СРЕДЕ | 2007 |
|
RU2456689C2 |
| ПРИМЕНЕНИЕ НОВЫХ СОЕДИНЕНИЙ ДЛЯ СЕЛЕКТИВНОГО ЭКСТРАГИРОВАНИЯ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ ИЗ ВОДНЫХ РАСТВОРОВ, СОДЕРЖАЩИХ ФОСФОРНУЮ КИСЛОТУ, И СООТВЕТСТВУЮЩИЙ СПОСОБ ЭКСТРАКЦИИ | 2016 |
|
RU2718439C2 |
| ЭКСТРАКЦИОННАЯ СМЕСЬ ДЛЯ ИЗВЛЕЧЕНИЯ ТПЭ И РЗЭ ИЗ ВЫСОКОАКТИВНОГО РАФИНАТА ПЕРЕРАБОТКИ ОЯТ АЭС И СПОСОБ ЕЁ ПРИМЕНЕНИЯ (ВАРИАНТЫ) | 2016 |
|
RU2623943C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ГАДОЛИНИЯ ЭКСТРАКЦИЕЙ ФОСФОРОРГАНИЧЕСКИМИ СОЕДИНЕНИЯМИ | 2012 |
|
RU2518619C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ МЕТАЛЛА ИЗ ЕГО ОРГАНИЧЕСКОГО КОМПЛЕКСА | 1994 |
|
RU2125477C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ (РЗМ) ПРИ ПЕРЕРАБОТКЕ АПАТИТОВОГО КОНЦЕНТРАТА | 2021 |
|
RU2752770C1 |
| СПОСОБ ОТДЕЛЕНИЯ АМЕРИЦИЯ ОТ ДРУГИХ МЕТАЛЛИЧЕСКИХ ЭЛЕМЕНТОВ, ПРИСУТСТВУЮЩИХ В КИСЛОТНОЙ ВОДНОЙ ИЛИ ОРГАНИЧЕСКОЙ ФАЗЕ, И ВАРИАНТЫ ЕГО ПРИМЕНЕНИЯ | 2011 |
|
RU2577640C2 |
| СПОСОБ РАЗДЕЛЕНИЯ ТЕРБИЯ И ДИСПРОЗИЯ | 2023 |
|
RU2830550C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ГОЛЬМИЯ (III) ИЗ РАСТВОРОВ СОЛЕЙ | 2014 |
|
RU2584626C1 |
Изобретение относится к применению синергетической смеси экстрагентов для извлечения по меньшей мере одного редкоземельного элемента из водной среды, содержащей фосфорную кислоту. Изобретение может быть использовано при обработке фосфатных минералов для извлечения содержащихся в них редкоземельных элементов (РЗЭ). Упомянутая смесь содержит: первый экстрагент с формулой (I)
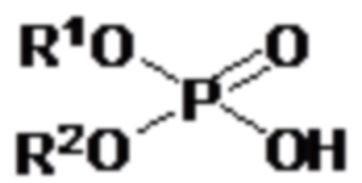 (I),
(I),
где R1 и R2, одинаковые или разные, представляют собой насыщенную или ненасыщенную, линейную или разветвленную углеводородную группу, содержащую от 6 до 12 атомов углерода, или фенильную группу, необязательно замещенную насыщенной или ненасыщенной, линейной или разветвленной углеводородной группой, содержащую от 1 до 10 атомов углерода; и второй экстрагент с формулой (II)
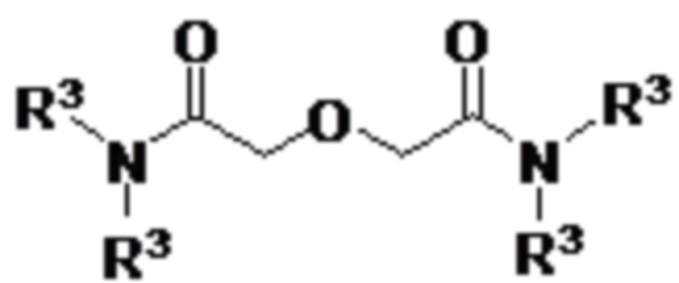 (II),
(II),
где R3 представляет собой линейную или разветвленную алкильную группу, содержащую от 6 до 12 атомов углерода. Смесь позволяет эффективно и селективно по отношению к железу экстрагировать все РЗЭ, которые присутствуют в водном растворе фосфорной кислоты, даже при концентрации кислоты более 4 моль/л. 14 з.п. ф-лы, 6 ил., 1 табл., 3 пр.
1. Применение смеси, содержащей
первый экстрагент с формулой (I)
 (I),
(I),
где R1 и R2, одинаковые или разные, представляют собой насыщенную или ненасыщенную, линейную или разветвленную углеводородную группу, содержащую от 6 до 12 атомов углерода, или фенильную группу, необязательно замещенную насыщенной или ненасыщенной, линейной или разветвленной углеводородной группой, содержащую от 1 до 10 атомов углерода, и
второй экстрагент с формулой (II)
 (II),
(II),
где R3 представляет собой линейную или разветвленную алкильную группу, содержащую от 6 до 12 атомов углерода,
для извлечения по меньшей мере одного редкоземельного элемента из водной среды, содержащей фосфорную кислоту.
2. Применение по п. 1, в котором R1 и R2 представляют собой линейную или разветвленную алкильную группу, содержащую от 6 до 12 атомов углерода, или фенильную группу, замещенную линейной или разветвленной алкильной группой, содержащей от 1 до 10 атомов углерода.
3. Применение по п. 1 или 2, в котором R1 и R2 представляют собой линейную или разветвленную алкильную группу, содержащую от 8 до 10 атомов углерода, или фенильную группу, замещенную линейной или разветвленной алкильной группой, содержащей от 6 до 10 атомов углерода.
4. Применение по любому из пп. 1-3, в котором R1 и R2 идентичны друг другу.
5. Применение по любому из пп. 1-4, в котором первый экстрагент представляет собой ди(2-этилгексил) фосфорную кислоту.
6. Применение по любому из пп. 1-5, в котором R3 представляет собой линейную или разветвленную алкильную группу, содержащую от 8 до 10 атомов углерода.
7. Применение по п. 6, в котором второй экстрагент представляет собой N, N, N’, N’-тетраоктил-дигликольамид.
8. Применение по любому из пп. 1-7, в котором смесь экстрагентов содержит ди(2-этилгексил) фосфорную кислоту и N, N, N’, N’-тетраоктил-дигликольамид.
9. Применение по любому из пп. 1-8, в котором смесь экстрагентов используют в растворе в органическом разбавителе.
10. Применение по любому из пп. 1-9, которое включает в себя по меньшей мере один контакт водной среды с органическим раствором, не смешиваемым с водой, содержащим смесь экстрагентов в органическом разбавителе, и затем отделение водной среды от органического раствора, в результате чего получают органический раствор, содержащий, по меньшей мере, редкоземельный элемент.
11. Применение по п. 10, в котором органический раствор содержит от 0,2 до 2 моль/л первого экстрагента и от 0,05 до 2 моль/л второго экстрагента.
12. Применение по п. 10 или 11, которое дополнительно включает в себя по меньшей мере один контакт органического раствора, содержащего по меньшей мере редкоземельный элемент, с кислотным или основным водным раствором и затем отделение органического раствора от водного раствора, в результате чего получают водный раствор, содержащий по меньшей мере редкоземельный элемент.
13. Применение по любому из пп. 1-12, в котором водная среда содержит от 0,5 до 10 моль/л фосфорной кислоты.
14. Применение по любому из пп. 1-13, в котором водная среда представляет собой водный раствор фосфорной кислоты, полученный в результате выщелачивания фосфатной руды серной кислотой.
15. Применение по любому из пп. 1-14, в котором редкоземельный элемент выбран из иттрия, лантана, неодима, диспрозия, иттербия и их смесей.
| WANG L et al | |||
| Recovery of rare earths from wet-process phosphoric acid., Hydrometallurgy, v.101, no | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Механический грохот | 1922 |
|
SU41A1 |
| FENG XIE et al | |||
| A critical review on solvent extraction of rare earth from aqueous solutions., Mineral Engineering, 2014-02-01, vol | |||
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| WO 2016046179 A1, 31.03.2016 | |||
| WO 2018085234 A1, 11.05.2018 | |||
| СПОСОБ ИЗВЛЕЧЕНИЯ И РАЗДЕЛЕНИЯ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ ПРИ ПЕРЕРАБОТКЕ АПАТИТОВОГО КОНЦЕНТРАТА | 2016 |
|
RU2640479C2 |
Авторы
Даты
2023-05-22—Публикация
2019-09-24—Подача