Изобретение относится к области фармацевтики, в частности к липосомальным лекарственным формам препаратов. Предложенный препарат липосом обладает способностью специфически связываться с поверхностью опухолевой клетки и осуществлять доставку цитотоксического агента гранзима Б человека для инициации в ней апоптоза, что позволяет эффективно лечить онкологические заболевания, для которых характерна экспрессия таргетных антигенов.
Изобретение относится также к области пассивной иммунотерапии онкологических заболеваний, в частности к применению иммунопрепарата, которым может быть антитело, специфически распознающее антиген, присутствующий на опухолевой клетке, и связанное с липосомой, содержащей гранзим Б человека.
Некоторые сигнальные каскады и белки связаны с инициированием апоптоза клеток. Инициация этих сигнальных каскадов возможна при доставке в цитоплазму клеток специальных активаторов. Соответственно, можно осуществлять доставку специальных молекул для активации клеточной гибели с целью устранения нежелательных клеток, которыми могут быть опухолевые клетки. Доставку можно осуществлять при помощи наноконтейнеров, в частности с помощью липосом. В липосомы могут быть включены вещества, активирующие сигнальные каскады клеточной гибели.
В настоящее время создано множество препаратов на основе липосом, содержащих различные цитостатические агенты, например доксорубицин [Green А.Е., Rose P.G., 2006]. Подобные носители могут быть использованы для терапии онкологических заболеваний, таких как рак яичника. Для более специфического взаимодействия с опухолью и достижения большей безопасности препарата на поверхности липосомы могут быть размещены либо целые антитела, либо антиген-распознающие фрагменты антител, в результате чего получают иммунолипосомы [Application of МСС-465 or doxorubicin (DXR) encapsulated in PEG immunolyposome, in patients with metastatic stomach cancer]. Другой подход для терапии онкологических заболеваний представляет собой создание CART-клеток - лимфоцитов, в которые введены конструкции, предназначенные для экспрессии химерных рецепторов, связывающихся с опухолевой клеткой [Pehlivan К.С., 2018]. Подобная разработка позволяет повысить вероятность сближения Т-клетки и опухолевой клетки в пространстве и увеличивает цитотоксическую активность Т-лимфоцита, результатом чего становится лизис опухолевой клетки. Несмотря на большое разнообразие препаратов на основе липосом и CART-клеток, случаи полного излечения больных наблюдаются редко, что во многом обусловлено недостатками перечисленных подходов.
К недостаткам липосомальных препаратов относится ограниченная возможность загрузки цитостатических препаратов, мало или практически нерастворимых в воде.
В результате в каждой отдельно взятой липосоме оказывается относительно немного молекул действующего вещества. Так как основная цель применения цитостатических препаратов заключается в остановке пролиферации и индукции гибели опухолевых клеток, попадание небольшого количества препарата становится неэффективным ввиду связывания большого количества молекул лекарства со структурными компонентами опухолевой клетки, что приводит к незначительным последствиям для ее жизнедеятельности. С другой стороны, увеличение концентрации химиопрепарата может сделать лекарственную форму более токсичной для здоровых тканей. Вместе с этим возрастает риск внесения мутаций в нормальные клетки с последующим развитием новых онкологических заболеваний. Наконец, применение липосомального химиопрепарата увеличивает стоимость терапии по сравнению с использованием того же химиопрепарата в его обычной форме.
Изготовление CART-клеток, несмотря на высокую эффективность в отдельных случаях, является очень сложной технологией, которую приходится воспроизводить заново при каждом новом запросе на терапию. Основой CART-клеток обычно служат лимфоциты самого больного. В тех случаях, когда больной получил химиотерапию, способность к пролиферации и цитотоксичность его Т-клеток заметно снижается, что отражается на качестве получаемых CART-клеток. Применение клеток донора может приводить к таким последствиям, как реакция «трансплантат против хозяина», вызванной частичной несовместимостью по репертуару молекул HLA. CART-клеточная вакцина не хранится долго, так как представляет собой живую вакцину. CART-клетки могут быть инактивированы опухолью при воздействии молекул PDL1 и PDL2 опухоли с PD1 модифицированного лимфоцита. Кроме этого, возможно развитие нежелательного явления «цитокинового шторма», вызванного гиперактивностью CART-клеток. Хотя каждая из этих проблем имеет решение, выведение CART-клеток из организма в случае нежелательных эффектов может быть затруднительной, а общая стоимость CART-клеточной терапии при сопоставлении с традиционной химиотерапией остается высокой. Практически непреодолимой проблемой является наработка большого количества CART-клеток для введения больному, так как для этого требуется время, которого в период прогрессии заболевания зачастую может не хватить. Наконец, использование векторов для доставки генетического материала в CART-клетки может с одной стороны привести к иммортализации этих клеток, с другой стороны - стать источником генетического материала для рекомбинации с вирусами, находящимися в латентном состоянии в геноме больного. В результате может возникнуть лейкозо-подобное заболевание либо появление вирусной инфекции нового типа.
Главную роль в развитии цитотоксических реакций CART-клеток играет белок гранзим Б (Granzyme В, сокращенно GrB, представляющий собой сериновую протеазу). Этот небольшой и хорошо растворимый белок представляет собой протеазу, активирующую прокаспазы 8, 10, 7 и 3, что эффективно активирует апоптоз [Afonina I.S., 2010]. Появление активной каспазы-3 в клетке приводит к ее быстрой гибели путем апоптоза. Апоптозу могут подвергаться также те опухолевые клетки, которые резистентны к химиопрепаратам. Гранзим Б достаточно стабилен, и может храниться длительное время. Таким образом, свойства гранзима Б позволяют использовать его как цитотоксический агент для терапии онкологических заболеваний.
Для активации апоптоза гранзим Б должен попадать внутрь клетки. Во время проведения лизиса клетки Т-лимфоцит выделяет белки перфорины, которые формируют поры в мембране клетки-мишени. Через эту пору гранзим Б проникает в цитоплазму. В отсутствие перфорина гранзим Б остается в межклеточном пространстве. Белок не может перфорировать клеточную мембрану, оставаясь безопасным для нормальных клеток и неэффективным для устранения опухолевых. Для активации гранзима Б также необходим белок катепсин. Катепсин в основном экспрессируется в клетках, пораженных вирусами, либо в опухолевых клетках, но не активен в нормальных. По этой причине гранзим Б, попавший в цитоплазму неопухолевых или не зараженных клеток, не будет активирован и не запустит апоптоз. В отличие от химиопрепаратов, гранзим Б не является мутагеном, так как не взаимодействует с ДНК клеток. Гранзим Б также не способен проводить трансформацию клеток по механизму, наблюдаемому при гормональном канцерогенезе. Примечательно, что в некоторых случаях для запуска апоптоза достаточно всего одной молекулы гранзима Б на клетку. В случае химиопрепаратов количество молекул исчисляется сотнями и более. Большинство химиопрепаратов воздействует на небольшой спектр онкологических заболеваний. Гранзим Б не избирателен в своем действии, и может активировать апоптоз в опухолевых клетках любого происхождения. Таким образом, гранзим Б человека может быть одновременно более эффективным и безопасным, чем химиопрепараты. Так как гранзим Б хорошо растворим в растворах с нейтральным рН, можно использовать любые безвредные для человека растворы со значением рН, близким к 7,0. Гранзим не обладает способностью проходить через липидные мембраны, и освобождение белка из липосомальной формы возможно только в случае прямого разрушения липосом, либо слияния липосом с мембраной опухолевых клеток. В организме живого человека условия относительно стабильны, и липосомальная форма гранзима Б будет практически не подвержена спонтанному разрушению.
Одним из решений для транспортировки гранзима Б в клетку является создание дуплекса из гранзима Б и транспортного пептида. В патенте US9724378B2 предлагается связывание молекулы гранзима Б с одним из множества пептидов, способных связываться с мембраной клетки и проходить сквозь нее. Таким образом находящийся во внеклеточном пространстве гранзим Б сможет проходить через мембрану клеток вместе с пептидом. Достоинства такого подхода позволяют создать большое количество доставляемых внутрь клетки молекул гранзима Б. Недостатком является неизбирательность действия, вследствие чего дуплекс гранзима Б и пептида будет проникать во все клетки, в том числе и в здоровые, и стимулировать их гибель.
Цитотоксичность гранзима Б, доставленного в опухолевую клетку тем или иным способом, можно увеличить посредством внесения изменений в молекулу белка. Опухолевые клетки могут экспрессировать ингибитор протеаз 9 (IP-9), который блокирует функции гранзима Б. Гранзим Б, используемый в лекарственной форме, может быть синтезирован с заменой лизина, находящегося в положении 27 белка, на аланин [Sun J., 2011] и аргинина в положении 201 белка на лизин или аланин [Losasso V., 2012].
В случаях, если опухолевые клетки экспрессируют катепсин на низком уровне, или не экспрессируют его вообще, попавший в их цитоплазму гранзим Б может оставаться в неактивной форме, и не сможет запустить апоптоз. Чтобы увеличить эффективность препарата, можно использовать мутантный гранзим Б, который с самого начала не требует активации катепсином. Для этого в структуре гранзима Б должны быть удалены глицин и глутаминовая кислота, находящиеся в положении 19 и 20 в незрелом белке. С другой стороны, перед гранзим Б может быть активирован белком катепсином еще перед загрузкой в липосомы.
В настоящее время гранзим Б коммерчески доступен, но может быть произведен в лабораторных условиях, в бактериальном штамме.
Новизна настоящего изобретения заключается в создании препарата, аналогичного Т-клеткам с химерным рецептором, но при этом лишенного недостатка модифицированных Т-клеток. Липосомы с заключенным внутрь гранзимом Б и оснащенные антителами для таргетной доставки гранзима потенциально легче произвести и хранить, они не имеют проблем с гистосовместимостью с реципиентом, а побочные эффекты в виде «цитокинового шторма» легче купировать. Так как подобная конструкция не имеет собственного генома, нет проблемы «оставшихся» модифицированных Т-клеток, которые сами могут стать причиной аутоиммунных заболеваний.
Проблемой, на решение которой направлено данное изобретение, является разработка способа получения липосомальной формы биологически активного гранзима Б, при котором возможно осуществить доставку препарата в цитоплазму опухолевой клетки без необходимости привлечения перфорина, без риска поражения нормальных клеток и стимулирования развития опухолевых заболеваний, при этом удобного в производстве, легко сохраняемого и вводимого в организм. Гранзим Б человека можно как выделять из лимфоцитов, так и производить в форме рекомбинантного белка в генетически модифицированных организмах бактерий либо растений.
Техническим результатом является доставка в клетку млекопитающего биологически активной формы гранзима Б, в количестве, достаточном для инициации цитотоксичности и активирования апоптоза в опухолевых клетках.
Полученные липосомальные формы препарата могут быть использованы для введения в кровоток больных онкологическими заболеваниями. Для опухолевой ткани характерно явление повышенной проницаемости сосудов, что делает опухолевую ткань предпочтительным местом накопления липосом, содержащих гранзим Б. Попав в опухолевую ткань, липосомы сливаются с клеточной мембраной, освобождая свое содержимое в цитоплазму. Попав в цитоплазму, гранзим Б взаимодействует с прокаспазами 8, 10, 7 и 3, что активирует апоптоз [Afonina I.S., 2010].
Липосомальные формы человеческого гранзима Б к настоящему моменту не разрабатывались как лекарственное средство и никогда не производились. В одной из работ созданы везикулы с упакованным в них гранзимом Б в качестве модели, демонстрирующей неспособность гранзима каким-либо способом спонтанно проходить через мембрану [Besenicar М.Р., 2008]. В работе, где гранзим Б представлен как перспективное лекарственное средство для терапии опухолей, предлагается создавать химерный гранзим, объединенный с другими белками [Hlongwane Р., 2018].
Ранее проводились эксперименты по созданию липосом с загруженными в них протеолитическими ферментами. Так, в 1988 году Alkhalaf с коллегами сделали липосомальную протеиназу, которую использовали для ускорения созревания сыра [el Soda М., 1988]. Методика предусматривала приготовление раствора 400 мг протеиназы в 20 мл трисового буфера с рН 7.0. Этот раствор использовался для захвата фермента в липосомы. Получали тонкую липидную пленку, которую растворяли в 40 мл диэтилового эфира, смешивали с раствором протеиназы, встряхивали и выпаривали эфир при +30°С при периодическом встряхивании вручную. Для отделения липосом от несвязавшегося белка использовали центрифугирование при 100000 g по способу, предложенному Piard и соавт. [Piard J.-С., 1986]. Способ Alkhalaf может рассматриваться в качестве прототипа заявленного изобретения.
Заявленный метод основан на получении тонкой липидной пленки, которая формируется при удалении растворителя из ранее полученного органического раствора липидов путем отгона под вакуумом на роторном испарителе. Растворение всех точно отмеренных компонентов липидного бислоя проводят в неполярных органических растворителях, в которых они хорошо растворяются. Если массу всех компонентов тщательно взвешивают, то объем растворителя не так важен для конечного результата, поскольку в процессе работы растворитель полностью выпаривается. Полученные таким способом липосомы можно легко отсортировать по размеру и очистить от невключившегося в них гранзима Б.
В предлагаемом нами методе получения липосомального гранзима Б смесь липидов (яичный либо соевый фосфатидилхолин, холестерин, mPEG2000-DSPE и PNP-PEG3000-DOPE в диапазоне молярных соотношений (6-7):(2-4):(0,005-0,014):(0,0001-0,01) смешивали с органическим растворителем (хлороформ). Полученный раствор помещали в круглодонную колбу и упаривали на роторном испарителе. Посредством выпаривания растворителя при температуре 37±1°С при использовании яичного фосфатидилхолина (Lipoid, Германия) или 40±1°С при получении липосом из соевого фосфатидилхолина (Lipoid, Германия) в условиях пониженного давления формировалась полупрозрачная липидная пленка. Полученную пленку досушивали под вакуумом (120 мбар) до постоянной массы. Затем пленку диспергировали с гранзимом Б, растворенным в буфере PBS, либо в деионизованной воде. Скорость вращения ротора составляла 25-30 об/мин. Для улучшения формирования липосомальной дисперсии и полного инкапсулирования гранзима Б в липосомы собирали всю липидную пленку. При этом раз в 5 минут меняли угол вращения колбы на роторном испарителе.
Полученные в результате дисперсии последовательно пропускали через нейлоновые мембранные фильтры (Pall Corporation, США или ООО Палл Евразия, Россия) с диаметром пор 1,2 мкм (1 раз), 0,45 мкм (1 раз) и 0,22 мкм (1-5 раз). Анализ среднего диаметра полученных липосом и оценку их распределения по размерам проводили с использованием метода корреляционной спектроскопии светорассеяния (динамического лазерного светорассеяния) на устройстве дзетасайзер Nanoseries Nano-ZS 3600 (Malvern, Великобритания). Для этого к 10 мкл липосомальной дисперсии добавляли воду, очищенную до 1 мл и полученный раствор переносили в полистирольную кювету, после чего кювету помещали в прибор и проводили измерение. Все расчетные операции проводили на компьютере в автоматическом режиме.
Для очистки липосом предлагается хроматографический метод. Для этого на хроматографическую колонку (NAP-5 (Amersham Biosciences, Швеция)), заполненную сефадексом (G-25 Medium (Amersham Biosciences, Швеция)), наносили 1 мл воды для инъекций. После прохождения воды на сухую поверхность колонки медленно наносили 1 мл дисперсии. На выходе из колонки получали 2 фракции: I фракция - липосомальный гранзим Б (мутная окрашенная жидкость), II фракция - невключившийся в липосомы гранзим Б (прозрачный бесцветный раствор). Фиксация смены фракций производилась визуально.
Для определения содержания гранзима Б в липосомах предлагается метод спектрофотометрии на приборе Cary 100 (Varian, Inc., Австралия) с использованием рабочего стандартного образца (СО) гранзима Б при длине волны 279±2 нм.
Измерение оптической плотности спиртовых растворов липосом с гранзимом Б и СО гранзима Б предлагается проводить относительно 95% этилового спирта в кюветах с толщиной оптического слоя 10 мм. Содержание гранзима Б (X, мг) рассчитывали по формуле (1).
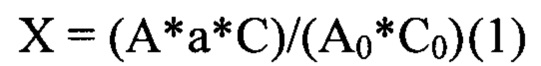
где А - оптическая плотность раствора образца; А0 - оптическая плотность СО гранзима Б; С - величина разбавления образца; С0 - величина разбавления СО гранзима Б; а - навеска СО гранзима Б, мг.
Эффективность включения гранзима Б в липосомы (В, %) рассчитывали по формуле (2).
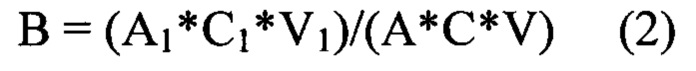
где A1 - оптическая плотность раствора фракции с очищенным липосомальным гранзимом Б; А - оптическая плотность раствора исходной липосомальной дисперсии; C1 - величина разбавления фракции с очищенным липосомальным гранзимом Б; С - величина разбавления исходной липосомальной дисперсии; V1 - объем фракции с очищенным липосомальным гранзимом Б, мл; V - объем исходной липосомальной дисперсии, нанесенной на колонку, мл.
Доставку гранзима Б в опухолевую клетку можно сделать более эффективной при помощи модификации липосом. Модификации позволяют придать им способность к избирательному связыванию с поверхностью опухолевых клеток и проникновению в них. Это может быть достигнуто путем присоединения к поверхности липосом структур, связывающихся с антигенами, расположенными на поверхности преимущественно опухолевых клеток. Среди таких антигенов могут быть белки CD1, CD2, CD3, CD4, CD5, CD7, CD8, CD10, CD11a, CD11c, CD13, CD14, CD15, CD16, CD18, CD19, CD20, CD21, CD22, CD23, CD25, CD28, CD30, CD33, CD34, CD36, CD38, CD40, CD41, CD44, CD45, CD51, CD52, CD56, CD62L, CD70, CD79b, CD80, CD95, CD117, CD125, CD137, CD138, CD147, CD242, CD319, гликофорин А, антигены легкой и/или тяжелой цепи иммуноглобулина, Т-клеточный рецептор, ACVR2B, VEGF, VEGFR, VEGFR2, PCSK9, HLA-DR, ВСМА, BAFF, EGFR, FGFR2, ЕрСАМ, RANKL, GD2, SLAMF7, CCR4, СБА, DPP4, RTN4, PDGFRa, Notch 1, HER2, В7-Н3, Nectin-4, ICAM-1, CTLA4, PD-L1, PD-L2, SOST, CSF1R, MUC1, VWF, DLL4, MUC5AC, RANKL, DR5, AXL, HER3, NKG2A, MCP-1, PDCP1, PD-1, MCAM, PTK7, IGHE, TFPI, GCGR, CCR2, PCSK9, PRAME и других. Структурами, которые могут связывать данные антигены, могут быть антитела, в том числе человеческие, мышиные, химерные, гуманизированные, крысиные, верблюжьи и иные антитела или их фрагменты, содержащие антиген-распознающие участки, либо белки человека, способные связываться с перечисленными антигенами по принципам лиганд-рецептор. Подобная лекарственная форма, так называемая иммунолипосомальная форма, обладает значительно большим сродством к опухолевой клетке, и вероятность успешного проникновения гранзима Б в цитоплазму увеличивается.
Иммунолипосомальную форму гранзима Б можно использовать для лечения таких заболеваний как гемангиома печени, рак прямой кишки, меланома кожи, увеальная меланома, опухоли матки, опухоли простаты, рак гортани, желудка, кожи, кости, легких, мозга, опухоли гипофиза, мочевого пузыря, печени, пищевода, почки, киста яичника, рак простаты, саркома молочной железы, хондросаркома, рак слюнной железы, шейки матки, щитовидной железы, яичка, яичника, острый миелоидный лейкоз, острый лимфоидный лейкоз, хронический В-клеточный лимфоидный лейкоз, хронический Т-клеточный лимфоидный лейкоз, волосатоклеточный лейкоз, множественная миелома, хронический миелоидный лейкоз, лимфома Беркитта, фолликулярная лимфома, диффузная В-крупноклеточная лимфома, лимфома из клеток маргинальной зоны селезенки, лимфома из клеток зоны мантии, Т-клеточные лимфомы кожи, миелодиспластический синдром и другие.
Мы предлагаем создавать иммунолипосомальную форму гранзима Б по методу, аналогичному способу получения липосомальной формы гранзима Б на этапах от формирования липидной пленки до ее гидратирования раствором PBS или воды. На этапе загрузки к полученным пустым липосомам добавляется раствор гранзима Б в 10 mM буфера HEPES с рН 8,2-8,4. После этого рН дисперсии доводится до значений 8,5-8,6 с помощью 3М раствора NaOH. Затем проводится инкубирование на водяной бане при температуре +45°С в течение 1,5 ч. После этого к дисперсии добавляется раствор необходимых моноклональных антител в молярном соотношении антитело/pNp-PEG3000-lipid 1:40. После этого проводится инкубирование в течение 12 ч при +4°С при постоянном перемешивании. Очистка липосомальной дисперсии от невключившегося в гранзима Б проводится методом колоночной хроматографии по протоколу, предложенному для создания липосомального гранзима Б. Количественное определение содержания гранзима Б внутри иммунолипосом и оценки эффективности его инкапсулирования проводится согласно рекомендациям, аналогичным предложенным для создания липосомального гранзима Б.
Липосомы и иммунолипосомы способны доставить гранзим Б к целевой клетке, слиться с ее мембраной и освободить содержимое внутрь. Таким образом гранзим Б попадает в цитоплазму, где может активировать апоптоз. Действие иммунолипосом потенциально более избирательное.
Доставляемые в цитоплазму клеток липосомы зачастую сливаются с лизосомой и содержимое липосом деградирует под действием низкого рН и комплекса ферментов, содержащихся в липосомах. Гранзим Б может быстро потерять стабильность в лизосоме, в связи с чем необходимо защитить его. Это возможно путем создания рН-чувствительных липосом, стенка которых реагирует на снижение рН. Липосома, в составе стенки которой находится, например, N-ацилфосфатидилэтаноламин, при попадании в лизосому сливается с мембраной лизосомы, и содержимое липосомы освобождается в цитоплазму клетки. Подобные свойства липосоме придает также полиэтиленгликоль. Если в стенку липосомы встроить вещества из группы ненасыщенных фосфатидилэтаноламинов, таких как диацетилен-фосфатидил-этаноламин, пальмитоил-олеоил-фосфатидил-этаноламин и диолеоил-фосфатидил-этаноламин, подобная липосома, в случае ее попадания в лизосому, способна разрушить как свою собственную мембрану, так и мембрану лизосомы. В этом случае в цитоплазму клетки будут освобождены как гранзим Б, так и ферменты, содержащиеся в лизосоме. Выброс лизосомальных ферментов не будет препятствовать выполнению гранзимом Б его основной задачи.
Полученный препарат потенциально обладает значительной цитотоксической активностью, а возможность использования антитела для таргетной доставки позволяет использовать его практически при любых онкологических и онкогематологических заболеваниях. Каждый отдельный компонент, используемый в настоящее время при создании липосом и иммунолипосом, нетоксичен. Сочетания этих компонентов друг с другом также не токсичны. В отличие от химиопрепаратов, полученный препарат не будет обладать мутагенным действием. Липосомы и иммунолипосомы с гранзимом Б легко дозировать при введении больным. Препарат легко хранить в лиофилизированной форме, так как гранзим Б - стабильный белок. Благодаря этому липосомальный гранзим Б можно накапливать в больших количествах и сохранять, используя при необходимости, что не достижимо в случае CART-клеток.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение липосомального гранзима Б
Получение липосомального гранзима Б осуществлялось по предложенному нами методу. Для формирования пленки использовались реагенты яичный фосфатидилхолин, холестерин и mPEG2000-DSPE в молярных соотношениях 7:2:0,005, растворенных в хлороформе. Пленку гидратировали гранзимом Б, растворенным в 2 мл воды для инъекций. Средний диаметр полученных липосом составил 320 нм. Эффективность включения составила 96% от исходной массы использованного белка гранзима Б.
Пример 2. Получение липосомального гранзима Б с использованием PNP-PEG3000-DOPE
Получение липосомального гранзима Б осуществлялось по предложенному нами способу. Для формирования пленки использовались реагенты яичный фосфатидилхолин, холестерин, mPEG2000-DSPE и PNP-PEG3000-DOPE в молярных соотношениях 7:3:0,014:0,01, растворенных в хлороформе. Пленку гидратировали гранзимом Б, растворенным в 2 мл воды для инъекций. Средний диаметр полученных липосом составил 320 нм. Эффективность включения составила 95% от исходной массы использованного белка гранзима Б.
Пример 3. Получение иммунолипосомального гранзима Б с антителом 5D3
Получение иммунолипосомального гранзима Б осуществлялось по предложенному нами способу для липосомального гранзима с дополнением для создания иммунолипосом. Для формирования пленки использовались реагенты соевый фосфатидилхолин, холестерин, mPEG2000-DSPE, pNp-PEG3000-lipid и в молярных соотношениях 6:4:0,014:0,01, растворенных в хлороформе. Пленку гидратировали гранзимом Б, растворенным в 10 mM буфера HEPES с рН 8,2. К дисперсии липосом были добавлены моноклональные гуманизированные антитела 5D3, распознающие антиген PRAME. Средний диаметр полученных липосом составил 320 нм. Эффективность включения составила 93% от исходной массы использованного белка гранзима Б.
Пример 4. Сборка иммунолипосомального гранзима Б с антителом против CD117
Сборка иммунолипосомального гранзима Б осуществлялась по предложенному нами протоколу для липосомального гранзима с дополнением для создания иммунолипосом. Для формирования пленки использовались реагенты соевый фосфатидилхолин, холестерин, mPEG2000-DSPE и pNp-PEG3000-lipid в молярных соотношениях 7:3:0,01:0,014, растворенных в хлороформе. Пленку гидратировали гранзимом Б, растворенным в 10 mM буфера HEPES с рН 8,4. К дисперсии липосом были добавлены моноклональные мышиные антитела ICO-406, распознающие антиген CD117. Средний диаметр полученных липосом составил 320 нм. Чистота - около 98%. Эффективность включения составила 96% от исходной массы использованного белка гранзима Б.
Пример 5. Цитотоксичность иммунолипосомального гранзима Б против клеток меланомы mel Kor
CD117-экспрессирующие опухолевые клетки линии mel Kor (метастатическая меланома) в количестве 50*103 в 180 мкл среды RPMI, содержащей 10% эмбриональной телячьей сыворотки, были посажены в ячейки 96-луночного планшета. Клетки были инкубированы в течение 24 ч при +37°С в атмосфере, содержащей 5% СО2. После этого в лунки были добавлены серии разведений иммунолипосомального гранзима Б, конъюгированного с антителом против антигена CD117, в объеме 20 мкл на лунку. Разведения были двухкратными начиная с концентрации 5 мг/мл гранзима, заключенного в липосомы. В качестве контроля использовались пустые иммунолипосомы, которые были собраны без добавления гранзима Б. Всего было 10 разведений по три повтора каждого. Клетки с иммунолипосомальным гранзимом Б были инкубированы в течение 24 ч при +37°С в атмосфере, содержащей 5% СО2. Для оценки цитотоксичности проводился МТТ-тест по стандартной методике. Было установлено, что клетки линии mel Kor погибали после инкубирования с иммунолипосомальным гранзимом Б. Чем больше была концентрация иммунолипосомального гранзима Б, тем большая доля клеток погибла. При инкубировании с пустыми липосомами клетки mel Kor не погибали.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОЛИПОСОМАЛЬНАЯ ФОРМА ФОТОСЕНСИБИЛИЗАТОРА | 2009 |
|
RU2410090C1 |
| БИНАРНАЯ ИММУНОЛИПОСОМАЛЬНАЯ НАНОСИСТЕМА АДРЕСНОЙ ДОСТАВКИ К КОННЕКСИН-43 ПОЛОЖИТЕЛЬНЫМ ОПУХОЛЕВЫМ КЛЕТКАМ | 2009 |
|
RU2422154C2 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО НА ОСНОВЕ ИММУНОЛИПОСОМАЛЬНОЙ БИОЛОГИЧЕСКОЙ КОНСТРУКЦИИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ВЕКТОРНОЙ ДОСТАВКИ В ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ ПРИ ОПУХОЛЕВОМ ПРОЦЕССЕ | 2007 |
|
RU2336901C1 |
| ТЕРАПЕВТИЧЕСКИЕ АГЕНТЫ, СОДЕРЖАЩИЕ ПРОАПОПТОЗНЫЕ БЕЛКИ | 2002 |
|
RU2319709C2 |
| СРЕДСТВО, УЛУЧШАЮЩЕЕ ПРОТИВООПУХОЛЕВЫЙ ЭФФЕКТ, СОДЕРЖАЩЕЕ ЛИПОСОМАЛЬНОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ОКСАЛИПЛАТИН, И ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ЛИПОСОМАЛЬНОЕ СРЕДСТВО | 2009 |
|
RU2492863C2 |
| ЛИПОСОМНЫЕ КОМПОЗИЦИИ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2015 |
|
RU2757110C2 |
| ЛИПОСОМНЫЕ КОМПОЗИЦИИ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2005 |
|
RU2574926C2 |
| СРЕДСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2016 |
|
RU2646834C1 |
| Композиция для ингибирования роста и стимуляции апоптоза клеток колоректального рака | 2016 |
|
RU2644675C1 |
| Фармацевтическая композиция, включающая доксорубицин в составе фосфолипидных наночастиц, с использованием селективных молекул ДНК-аптамера для направленного транспорта в опухолевые клетки | 2021 |
|
RU2794798C1 |
Группа изобретений относится к липосомальной лекарственной форме, предназначенной для транспортировки гранзима Б в клетки млекопитающих. Способ получения липосом с загруженным в них белком гранзим Б включает получение липидного бислоя, растворенного в хлороформе, диспергирование его с раствором протеиназы, встряхивание и выпаривание, диспергирование полученной пленки с гранзимом Б, при этом для получения липидного бислоя растворенные в неполярном растворителе компоненты берут в следующих диапазонах молярных соотношений: фосфатидилхолин (от 6 до 7): холестерин (от 2 до 4): mPEG2000-DSPE (от 0,005 до 0,014). Также раскрыты липосомы, содержащие гранзим Б, и применение липосом для доставки гранзима Б в клетку млекопитающего и инициации в ней цитотоксической активности. Группа изобретений обеспечивает доставку в клетку млекопитающего биологически активной формы гранзима Б. 3 н. и 10 з.п. ф-лы, 5 пр.
1. Способ получения липосом с загруженным в них белком гранзим Б, включающий получение липидного бислоя, растворенного в хлороформе, диспергирование его с раствором протеиназы, встряхивание и выпаривание, диспергирование полученной пленки с гранзимом Б, при этом для получения липидного бислоя растворенные в неполярном растворителе компоненты берут в следующих диапазонах молярных соотношений: фосфатидилхолин (от 6 до 7) : холестерин (от 2 до 4) : mPEG2000-DSPE (от 0,005 до 0,014).
2. Способ по п. 1, где среди компонентов липосомы дополнительно используется pNP-PEG3000-DOPE в молярном соотношении от 0,0001 до 0,01.
3. Способ по п. 1, где фосфатидилходин представляет собой яичный.
4. Способ по п. 3, где растворитель выпаривают при температуре 37±1°С
5. Способ по п. 1, где фосфатидилходин представляет собой соевый.
6. Способ по п. 5, где растворитель выпаривают при температуре 40±1°С.
7. Способ по п. 1, где полученную пленку липидного бислоя досушивают под вакуумом до постоянной массы и диспергируют с протеолитическим ферментом, растворённым в буфере PBS или в деионизированной воде.
8. Способ по п. 7, где скорость вращения ротора при диспергировании составляет приблизительно 25−30 об/мин.
9. Способ по п. 1, где полученные в результате дисперсии липосомы последовательно пропускают через нейлоновые мембранные фильтры с диаметром пор 1,2 мкм, 0,45 мкм и 0,22 мкм.
10. Способ по п. 1, где на поверхности липосомы размещены молекулы для таргетной доставки везикулы к определенному типу клеток.
11. Способ по п. 10, где прикрепленные молекулы представляют собой антитела или пептиды.
12. Липосомы, содержащие гранзим Б, полученные способом по п. 1.
13. Применение липосом по п. 12 для доставки гранзима Б в клетку млекопитающего и инициации в ней цитотоксической активности.
| ALKHALAF W | |||
| et al | |||
| Liposomes as Proteinase Carriers for the Accelerated Ripening of Saint-Paulin Type Cheese // Journal of Food Science, 1998, 53(6), р | |||
| Прибор для проверки исправности запальных свечей | 1924 |
|
SU1674A1 |
| DE 60331228 D1, 25.03.2010 | |||
| US 9724378 B2, 08.08.2017 | |||
| ТЕРАПЕВТИЧЕСКИЕ АГЕНТЫ, СОДЕРЖАЩИЕ ПРОАПОПТОЗНЫЕ БЕЛКИ | 2002 |
|
RU2319709C2 |
Авторы
Даты
2023-05-29—Публикация
2021-04-19—Подача