Изобретение относится к медицине, в частности к акушерству-гинекологии и клинической лабораторной диагностике, и может быть использовано для прогнозирования рецидива тяжелой ранней преэклампсии по данным уровня плацентарных микровезикул в плазме периферической крови женщины.
Преэклампсия (ПЭ) остается ведущей причиной материнской и перинатальной заболеваемости/смертности из-за неэффективной стратегии прогнозирования на этапе возможного проведения профилактики. Несмотря на достаточное количество предложенных биомаркеров для прогнозирования ПЭ, они показали свою недостаточную эффективность. Известно, что ПЭ с клиническими проявлениями до 34 недель относится к ранней преэклампсии, связана с задержкой роста плода, имеет тяжелое клиническое течение и неблагоприятный прогноз как для матери, так и для новорожденного (Magee L.A., Pels A., Helewa М., Rey Е., von Dadelszen P. Diagnosis, evaluation and management of the hypertensive disorders of pregnancy: execultive summary // J. Obstet. Gynaecol. Can. 2014. Vol. 36. N5. P. 416-441). Кроме того, доказано, что ранняя ПЭ в личном анамнезе связана с 35,4% неблагоприятных комбинированных исходов и 20,8% рецидивов ПЭ во время последующей беременности (Gottardi Е, Lecarpentier Е, Villette С, Berman A, Redel D, Tsatsaris V, Goffmet F, Haddad В. Preeclampsia before 26 weeks of gestation: Obstetrical prognosis for the subsequent pregnancy. J Gynecol Obstet Hum Reprod. 2021 Mar; 50(3): 102000. doi: 10.1016/j.jogoh.2020.102000. Epub 2020 Nov 19. PMID: 33221560.).
Биологическая основа реализации ПЭ, основывается на аномальной плацентации и неадекватном ремоделировании спиральных артерий. При физиологической беременности повышенный оксидативный стресс в зоне инвазии синцитиотрофобласта предрасполагает к освобождению плацентарных микровезикул (EVs), которые могут связываться с моноцитами и стимулировать выработку провоспалительных цитокинов, что обеспечивает состояние иммунотолерантности к аллоиммунному плоду. Однако при нарушении процесса становления плаценты продукция плацентарных EVs может быть нарушена, вызывая патологический ответ организма матери (Pillay Р, Maharaj N, Moodley J, Mackraj I. Placental exosomes and pre-eclampsia: Maternal circulating levels in normal pregnancies and, early and late onset preeclamptic pregnancies. Placenta. 2016 Oct; 46: 18-25. doi: 10.1016/j.placenta.2016.08.078. Epub 2016 Aug 21. PMID: 27697217.). Впервые многоядерные клетки плацентарного происхождения в легочной ткани женщин, умерших от эклампсии обнаружил и описал в 1893 году немецкий врач и патолог Кристиан Георг Шморль (Schmorl G. Pathologisch-anatomischeuntersuchungenuber puerperal-eklampsie (pathological and anatomical examinations of puerperal-eclampsia). Leipzig: FCW Vogel. 1893: 106.).
Плацентарные EVs имеют принципиальное отличие от фрагментов депортированного сцинтиотрофобласта (ДС). Это частицы примитивного строения - продукт вакуольной трансформации щеточной каймы, размером от 30 до 1000 нм, которые в противоположность ДС легко проходят легочные капилляры и попадают в системный кровоток (Tannetta D.S., Hunt K., Jones C.I. et al. Syncytiotrophoblast extracellular vesicles from preeclampsia placentas differentially affect platelet function. PLoS One. 2015; 10(11): e0142538. https://doi.org/10.1371/journal.pone.0142538). В процессе биогенеза плацентарных EVs внутри концентрируются молекулы, содержащие генетическую и протеомную информацию, которая может служить прямыми маркерами осложнений, связанных с дисфункцией плаценты.
Известно, что плацента высвобождает EVs в материнский кровоток с ранних сроков беременности (Morgan Т.K. Cell- and size-specific analysis of placental extracellular vesicles in maternal plasma and pre-eclampsia. Transl. Res. 2018; 201: 40-48. doi: 10.1016/j.trsl.2018.08.004.), а с увеличением срока гестации количество EVs плацентарного происхождения в плазме крови нарастает (Motta-Mejia С., Kandzija N., Zhang W. et al. Placental Vesicles Carry Active Endothelial Nitric Oxide Synthase and Their Activity is Reduced in Preeclampsia. Hypertension. 2017; 70: 372-381. doi: 10.1161/HYPERTENSIONAHA.l 17.09321.). Имеется гипотеза, что при избыточном образовании плацентарных EVs изменяет иммунный ответ матери, что обусловливает развитие гестационных осложнений, включая ПЭ. Причем посредством математических моделей предложена теория, что срок реализации ПЭ зависит от уровня плацентарных EVs в плазме крови матери (McElrath TF, Cantonwine DE, Gray KJ, Mirzakhani H, Doss RC, Khaja N, Khalid M, Page G, Brohman B, Zhang Z, Sarracino D, Rosenblatt KP. Late first trimester circulating microparticle proteins predict the risk of preeclampsia <35 weeks and suggest phenotypic differences among affected cases. Sci Rep. 2020 Oct 21; 10(1): 17353. doi: 10.1038/s41598-020-74078-w. PMID: 33087742; PMCID: PMC7578826.). Необходимо отметить, что имеющиеся предпосылки требуют клинических доказательств, которые позволят рассматривать плацентарные EVs в качестве биологических маркеров, прогнозирующих риск развития ПЭ.
Существует достаточное количество способов прогнозирования тяжелой ПЭ, основанных на изучение биомаркеров в плазме крови матери.
Так, например, предложен способ прогнозирования развития тяжелой ПЭ с полиорганной недостаточностью (ПОН) (Патент РФ, 2013 год: RU 2204833) путем комплексного исследования нескольких систем организма. Цель достигается тем, что исследуют системы организма: эндотелиальную, гемостаза, гематологическую, иммунную и гемодинамики, анализируют полученные данные с учетом теории функциональных систем на основании системного подхода, выявляют меж- и внутризвеньевые интеграционные межклеточные взаимодействия, ответственные за формирование полиорганной недостаточности. С помощью метода распознавания образов выявляют информативные показатели гомеостаза: число свободных эндотелиоцитов, уровень D-димеров, фибриногена, число тромбоцитов, количество лимфоцитов III типа, уровень интерлейкина 6, индекс активности лейкоцитов, общее периферическое сосудистое сопротивление и выводят решающее правило (F). При F>0 делают заключение о вероятной принадлежности беременной женщины к группе риска на развитие ПОН. При F<0 делают заключение о вероятной принадлежности беременной женщины к группе, где ПОН не будет развиваться в течение беременности.
Недостатком заявленного способа является трудоемкость постановки лабораторных тестов по заданным параметрам, необходимость выполнять сложные математические расчеты и высокая стоимость реактивов.
Имеется способ прогнозирования преэклампсии в поздние сроки беременности (патент РФ, 2019 год: RU 2691114), основанный на определении концентрации ADAM 12 и RBP 4 в сроке гестации 12 недель у женщин группы риска развития ПЭ. При увеличении концентрации данных маркеров: ADAM12 более 2,33 нг/мл и RBP 4 более 87,90 мкг/мл прогнозируют развитие преэклампсии, которая развивается после 34 недель беременности. Недостатком заявленного способа является возможность прогнозировать развитие заболевания только поздней ПЭ, реализующейся после 34 недель беременности.
Заявлен способ прогнозирования тяжести течения ранней преэклампсии (патент РФ, 2021 год: RU 2753463), в котором авторы путем количественного определения в плазме крови матриксной металлопротеиназы 2 типа (ММП-2) у беременных с установленным диагнозом «умеренная преэклампсия» в сроке гестации 24-34 недели прогнозируют риск тяжелого течения ПЭ. При значении ММП-2 равном или превышающем 379 нг/мл прогнозируется высокий риск тяжелого течения преэклампсии, при чувствительности и специфичности метода 70% и 85%, соответственно.
Основным недостатком метода является его информативность только у пациенток с установленным диагнозом «умеренная преэклампсия» в сроке гестации 24-34 недели. Однако необходимо отметить, что ранняя ПЭ манифестирует сразу тяжелой степенью состояния пациентки, требующей неотложного принятия решения о досрочном родоразрешении. В связи с чем целевая когорта для использования заявленного метода малочисленна.
Прототипом заявляемого способа выбрана работа исследователей из США, в которой авторы по уровню циркулирующих белков EVs, включая EVs плацентарного происхождения предсказывают риск развития ранней тяжелой ПЭ в конце первого триместра (McElrath TF, Cantonwine DE, Gray KJ, Mirzakhani H, Doss RC, Khaja N, Khalid M, Page G, Brohman B, Zhang Z, Sarracino D, Rosenblatt KP. Late first trimester circulating microparticle proteins predict the risk of preeclampsia <35 weeks and suggest phenotypic differences among affected cases. Sci Rep. 2020 Oct 21; 10(1): 17353. doi: 10.103 8/s41598-020-74078-w. PMID: 33087742; PMCID: PMC7578826.). Авторы, с помощью хроматографии, с использованием глобального профилирования протеома на основе масс-спектрометрии проанализировали 226 белков у пациенток двух групп: с физиологическим течением беременности и при развитии ПЭ. Далее, посредством логистического анализа определены наиболее эффективные модели прогнозирования ПЭ, включающие не более 4 предикторов. Также, авторы изучили случаи кластеризации K-средних для фенотипических подтипов ПЭ и обогащения биологических путей. Результаты исследования показали, что белки, отличающие случаи заболевания от контрольных, обогащены биологическими путями, участвующими в свертывании крови, гемостазе и восстановлении тканей. Панель, состоящая из 4 биомаркеров и включающая компонент дополнения C1r (C1RL), тромбоцитарный гликопротеин Ib, альфа цепь (GP1BA), витронектин (VTNC) и цинк-альфа-2-гликопротеин (ZA2G), продемонстрировала наилучшие прогностические характеристики (AUC 0,79), при этом наиболее значимые изменения определены для ранней тяжелой ПЭ.
Основным недостатком заявленного метода является возможность проведения представленного диагностического алгоритма только для научных исследований, что обусловлено технической сложностью преаналитической подготовки биоматериала, дорогостоящими расходными материалами и наличием высокотехнологично оснащенной лабораторией.
Авторы предлагают простой, доступный способ прогнозирования рецидива тяжелой ранней ПЭ у пациенток с тяжелой ПЭ в анамнезе, позволяющий своевременно стратифицировать беременных в группу для проведения дополнительных методов обследования и профилактических мероприятий. В основе метода лежит оценка количества внеклеточных везикул, произошедших от синцитиотрофобласта (плацентарные микровезикулы) в различные сроки гестации.
Технический результат заявленного метода достигается путем измерения количества плацентарных мировезикул (PLAP + события) в объеме безтромбоцитарной плазмы крови в сроки гестации 11-13 и 27-28 недель.
Способ осуществляют следующим образом.
Забор крови и пробоподготовка
Кровь для исследования забирают утром, натощак, из локтевой вены в пробирки "VACUETTE" 4,5 мл, содержащие забуференный раствор цитрата натрия 3,2%, соотношение объемов крови и цитрата натрия - 9:1. Кровь должна быть обработана в течение 1 часа после сбора. Кровь последовательно центрифугируют до получения свободной от тромбоцитов плазмы (PFP или СТП), которая подвергается дальнейшему анализу. Сначала центрифугирование проводят при 2500×g в течение 15 минут при комнатной температуре для получения бедной тромбоцитами плазмы (БТП). Верхний слой (3/4) БТП еще дважды центрифугируют при 2500×g в течение 15 минут при комнатной температуре, отбирая на каждом этапе 3/4 верхнего слоя супернатанта для получения свободной от тромбоцитов плазмы (PFP или СТП).
При необходимости образцы безтромбоцитарной плазмы переносят в криопробирки и проводят заморозку в жидком азоте (-196°С) с последующим хранением при -70°С до проведения анализа (но не более чем 6 месяцев). В день проведения анализа образцы плазмы размораживают (если они были заморожены) при +37°С на водяной бане. Далее образцы из криопробирок переносят в микроцентрифужные пробирки и проводят дополнительное центрифугирование 3000×g 10 минут для удаления возможных ассоциатов. После центрифугирования супернатант (3/4) используют для анализа. Подготовка конъюгированных антител и настройка прибора Для окрашивания внеклеточных везикул синцитиотрофобласта используются антитела против щелочной фосфатазы плацентраного типа (PLAP) коньюгированные с любым коммерчески доступным флуорофором. Перед работой с антителами необходима их подготовка для устранения шума: антитела разводят в 20 раз фосфатно-солевым буфером и подвергают центрифугированию 18000×g - 15 минут для удаления возможных конъюгатов.
Окрашивание проводят смешиванием 10 мкл коньюгированных антител с 50 мкл образца, перемешиванием и последующей экспозицией в темном месте в течение 20-30 минут. В качестве отрицательного контроля допустимо использование как неокрашенных образцы в тех же разведениях, что и окрашенный образец, так и соответствующего изотипического контроля.
Непосредственное измерение событий может проводится на любом проточном цитофлюориметре с пределом обнаружения событий не менее 200 нм. Например, CytoFlex (Beckman Coulter, США), который использует боковое светорассеяние на более короткой длине волны 405 нм (фиолетовый лазер) в качестве триггерного сигнала, что повышает чувствительность и разрешения исследуемых объектов, позволяя обнаруживать частицы с диаметром менее 500 нм (предел обнаружения на уровне 150-200 нм). Для отнесения PLAP + событий к внеклеточным везикулам используется параметр размера (0,1-1 мкм), гейт для которого формируются в ходе использования микрогранул фиксированного размера с пришитой флуоресцентной меткой (0,1-1,0 мкм). Например, Flow Cytometry Sub-micron Particle Size Reference Kit, Thermofisher, США, с набором калибровочных шариков 0.1, 0.2, 0.5, и 1.0 мкм, по которым выставляется ориентировочный гейт в диапазоне от 0,1 до 1 мкм.
Обязательным в описываемом методе проведение проверки на возможный вклад в «шум» для фосфатно-солевого буфера, для антител, разведенных в фосфатно-солевом буфере в тех же пропорциях, что и окрашенные образцы. Только после этого можно переходить к измерению для неокрашенных проб, по которым выставляется граница для «PLAP-» гейта. Соответственно все события, превышающие по величине сигнала отрицательный гейт относят к положительным событиям.
Окрашенные пробы по истечении 20-30 минут инкубации повторно встряхивают и проводят измерение после разбавления пробы фосфатно-солевым буфером достаточным, чтобы избежать эффекта роя (или совпадения). В каждом анализе проводится запись 1 млн всех событий на скорости 10 мкл/мин, предварительно убеждаясь, что в анализируемой области нет объектов более 1000 нм.
После измерения окрашенной пробы выборочно может проводится тест с тритоном XI00 (детергент, разрушающий мембраны эукариотических клеток).
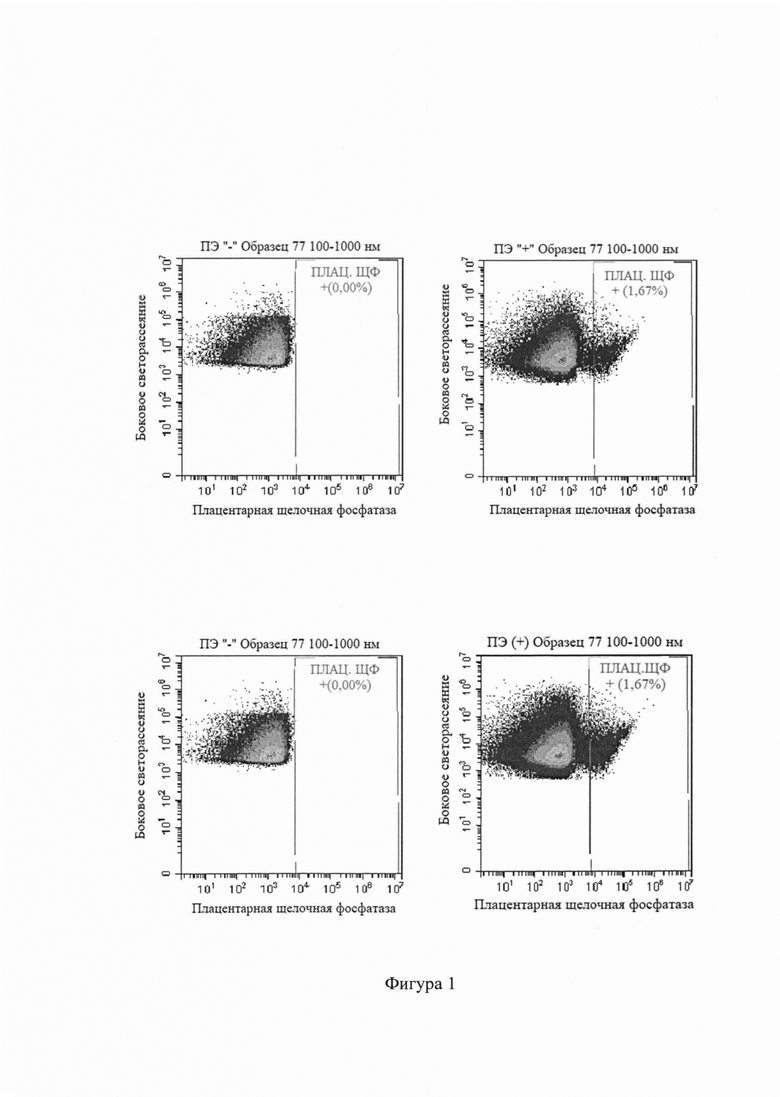
Графически технический результат представлен на фигуре 1. Для статистической обработки использовали параметр количества событий (внеклеточных везикул) в 1 мкл.
Для подтверждения эффективности заявляемого способа проведено проспективное наблюдательное когортное исследование, с включением 137 пациенток. Первично сформированы 2 группы. Контрольная группа представлена 40 беременными с физиологическим течением беременности, родами в сроке гестации больше 37 недель и не имеющими отягощенного анамнеза по ПЭ. Основную группу составили 97 беременных, имеющих в личном анамнезе эпизод ранней тяжелой преэклампсии, то есть относящихся к высокому риску развития преэклампсии в настоящую беременность.
Критерии включения в контрольную группу: возраст матери до 35 лет, отсутствие соматических заболеваний, таких как: артериальная гипертензия, сахарный диабет, повышение массы тела (индекс массы тела не более 25 до момента вступления в беременность), отсутствие семейной истории ПЭ, наличие срочных родов в анамнезе, подтвержденная маточная беременность, в сроке 7-8 недель по данными ультразвукового исследования.
Критерии включения в основную группу сравнения: возраст матери до 35 лет; подтвержденная маточная беременность, в сроке 7-8 недель по данными ультразвукового исследования; наличие в анамнезе беременности с реализованной тяжелой ранней преэклампсией.
Критерии исключения из исследования: беременность, наступившая в программах вспомогательных репродуктивных технологий, первая беременность, аномалии развития половых органов, возраст пациентки старше 35 лет, отказ пациентки от участия в исследовании.
По окончанию гестационного процесса основная группа рандомизирована в зависимости от исходов настоящей беременности в две подгруппы: основная ПЭ (-) и основная ПЭ (+). В группу основная ПЭ (-) вошли 59 пациенток, беременность которых протекала благоприятно и закончилась родами в сроке гестации более 37 недель живыми новорожденными. Группу основная ПЭ (+) составили 38 женщин, у которых произошел рецидив ранней тяжелой ПЭ в сроке гестации менее 34 недель.
У всех пациенток, включенных в исследование, с целью изучения уровня плацентарных микровезикул в сроки гестации 11-13, 27-28 и за 6-8 часов до родоразрешения забиралось 4,5 мл периферической венозной крови.
Медиана возраста пациенток групп исследования была сопоставима, и составила в контрольной группе 28,0 [95%CI 24,0-33,1] лет, в группе основная ПЭ (-) - 28,1 [95%CI 24,5-34,1] лет, в основная ПЭ (+) - 27,1 [95%CI 22,8-34,3] лет. Группы были сопоставимы по социальному статусу.
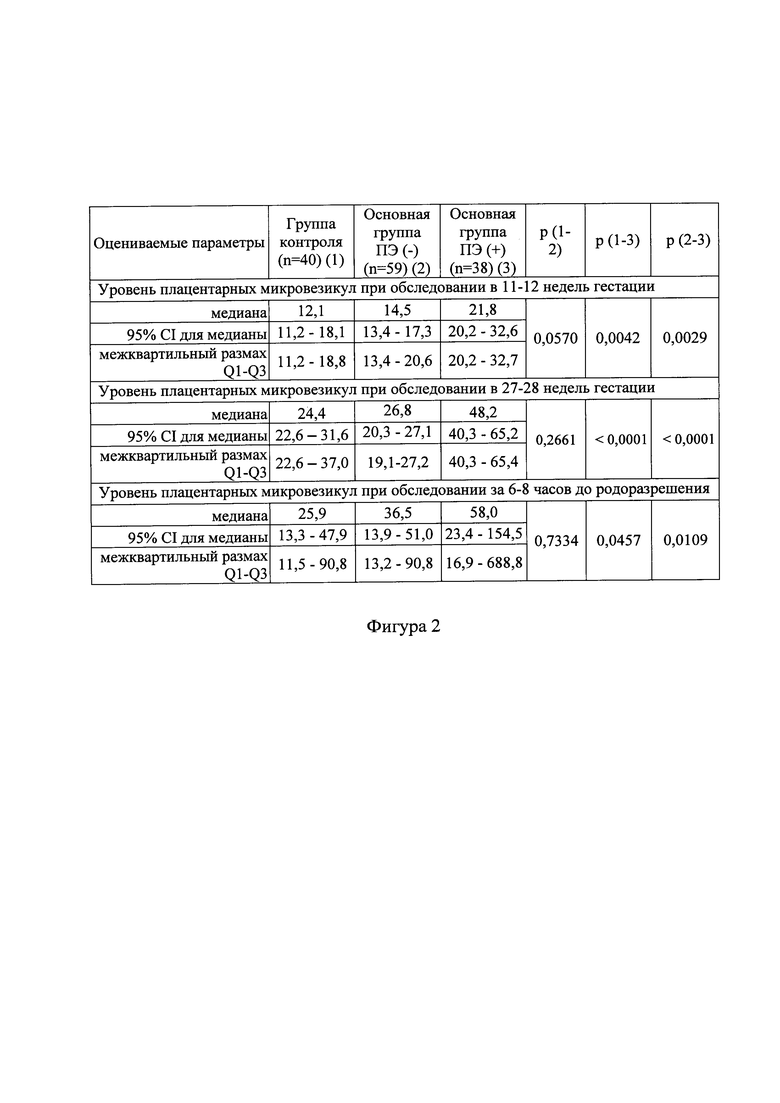
Медиана (Me) уровня плацентарных микровезикул при обследовании в контрольных точках гестации в основной группе была значимо больше, чем в группе контроля и в группе сравнения (Фиг. 2).
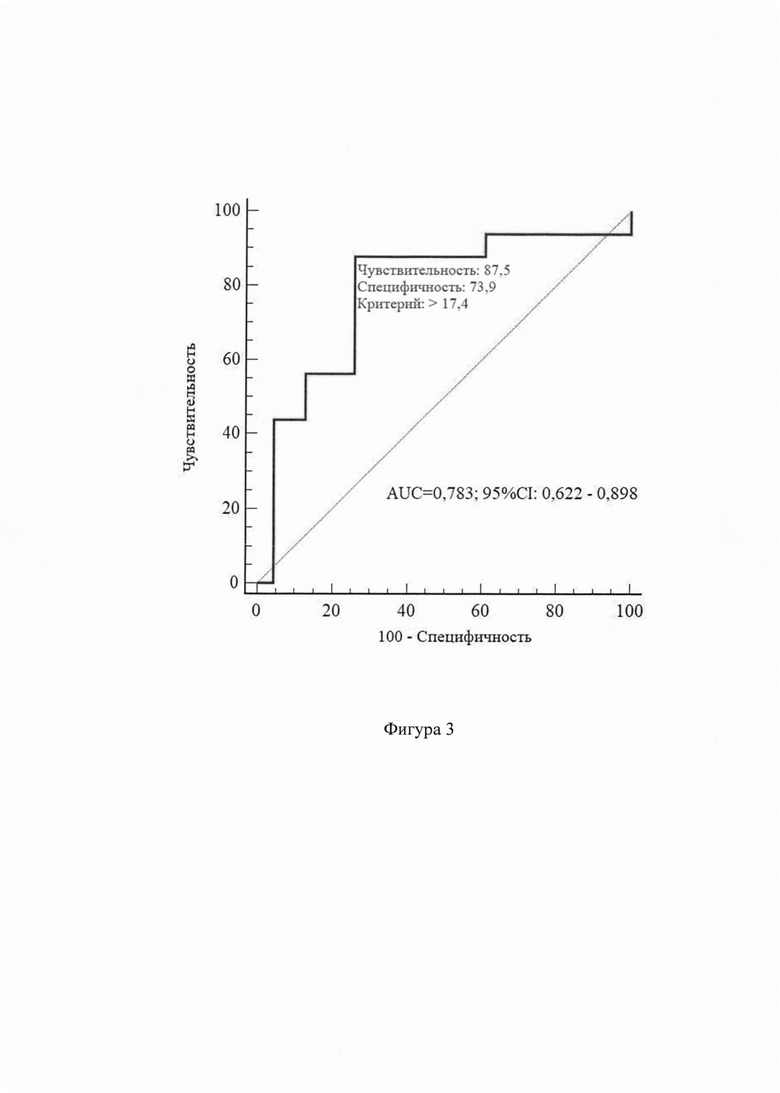
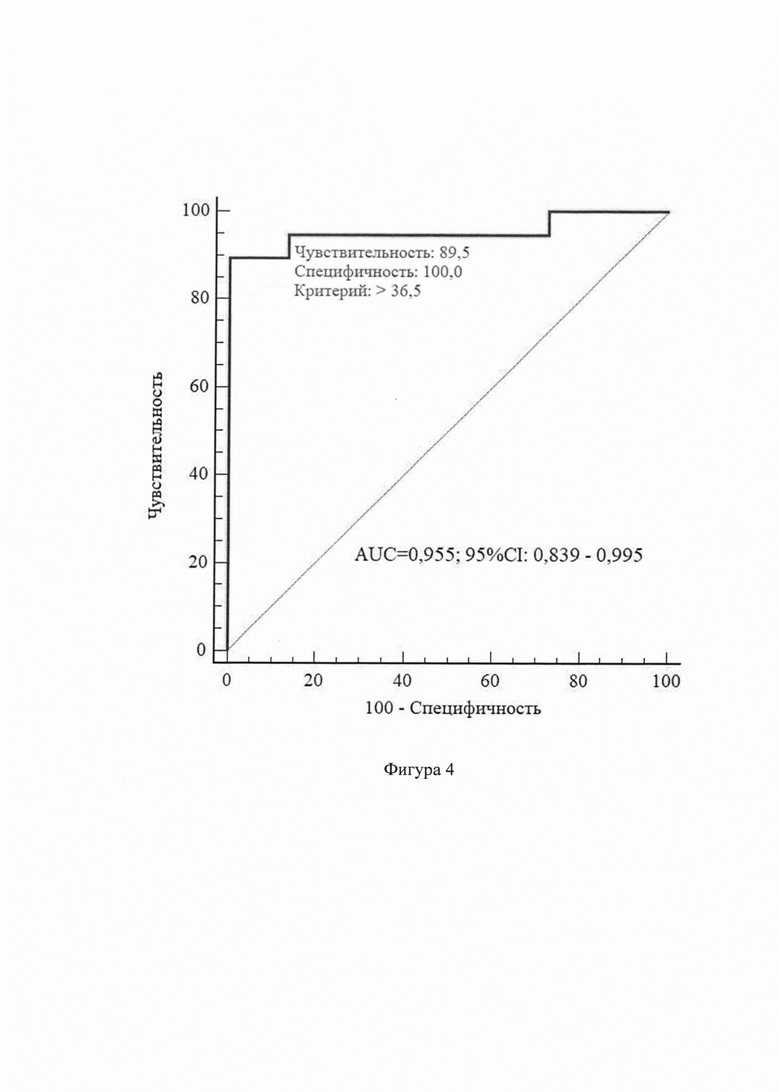
Для определения критической величины показателя (порог отсечки) «уровень плацентарных микровезикул» и степени прогностической информативности теста проведен ROC-анализ для точек гестации 11-13 и 27-28 недель. Определено, что при значении уровня плацентарных микровезикул в плазме крови в сроки гестации 11-13 недель >17,4 событий/мкл риск развития ранней тяжелой преэклампсии прогнозируется в 78,3% случаев (Фиг. 3), а при значении уровня плацентарных микровезикул в плазме крови в сроки гестации 27-28 недель >36,5 событий/мкл риск развития ранней тяжелой преэклампсии прогнозируется в 95,5% случаев (Фиг. 4).
Статистически значимое повышение уровня плацентарных микровезикул в плазме крови беременных женщин с тяжелой преэклампсией в личном анамнезе в различные сроки гестации, позволяет рассматривать плацентарные микровезикулы в качестве биомаркера тяжелой ранней преэклампсии с раннего срока беременности.
Клиническое наблюдение 1
С.К.Н. - повторнородящая 26 лет. Менструальная функция не нарушена, гинекологический анамнез не отягощен. В анамнезе, 3 года назад, индуцированные преждевременные роды абдоминальным путем (кесарево сечение) в сроке гестации 32 недели в связи с реализацией тяжелой ранней преэклампсии (систолическое артериальное давление до 200 мм рт.ст, протеинурия до 6 г/литр). Родилась девочка 1850 г, 42 см, живая до настоящего времени. Дополнительно после родов обследовалась, соматические заболевания отрицает. Беременность желанная, но не запланированная, прегравидарную подготовку не получала. При взятии на диспансерный учет рост пациентки 167, вес 60 кг, ИМТ=21,51. Консультацию посещала регулярно, мониторируемая группа высокого риска по развитию ПЭ. При обследовании в первом триместре отклонений в лабораторных показателях не зарегистрировано. Первый ультразвуковой скрининг в сроке гестации 11,5 недели. Ультразвуковых маркеров хромосомной патологии не обнаружено. Ультразвуковая анатомия плода без патологии. Рассчитан риск развития акушерских осложнений в программе Astraia как высокий (риск ПЭ до 37 недель беременности - 1 на 79, риск по задержке роста плода до 37 недель беременности - 1 на 173). По данным цитометрии определен уровень плацентарных микровезикул 20,4 событий/мкл
При проведении второго ультразвукового скрининга в сроке гестации 19,5 недель: ультразвуковых маркеров хромосомной патологии не обнаружено. Ультразвуковая анатомия плода без патологии. Показатели фетометрии в пределах референсных значений. По данным доплерометрии патологические кровотоки в маточных артериях, сосудах пуповины не зарегистрированы. По данным цитометрии, проведенной в сроке гестации 27,4 недели определен уровень плацентарных микровезикул 75,69 событий/мкл
В 30 недель на фоне полного благополучия появилась сильная головная боль, не купируемая приемом анальгетиков (принимала по совету родственников). При обращении в стационар АД 210/120; протеинурия в разовой порции мочи 6 граммов/литр, уровень плацентарных микровезикул определен как 1716 событий/мкл. Переведена в отделение реанимации и интенсивной терапии (диагноз: беременность 30,2 недели; тяжелая преэклампсия), при стабилизации состояния (через 4 часа) экстренно родоразрешена абдоминальным путем. Родилась недоношенная девочка, весом 1650. Кровопотеря в родах составила 650 мл. Стабилизация пациентки на 3 сутки после родоразрешения. Переведена с ребенком на второй этап выхаживания новорожденных.
Клиническое наблюдение 2.
М.О.К - повторнородящая, 32 лет. Менструальная функция не нарушена, гинекологические заболевания отрицает. В анамнезе один артифициальный аборт 5 лет назад в сроке гестации 6-7 недель и одни индуцированные преждевременные роды (7 лет назад) абдоминальным путем (кесарево сечение) в сроке гестации 33 недели в связи с реализацией тяжелой ранней преэклампсии (систолическое артериальное давление до 210 мм рт.ст, протеинурия до 7 г/литр). Родилась девочка 1790 г, 42 см, живая до настоящего времени. Соматические заболевания отрицает. Беременность желанная, запланированная. При взятии на диспансерный учет рост пациентки 161, вес 64 кг, ИМТ=24,69. Консультацию посещала регулярно. При обследовании в первом триместре отклонений в лабораторных показателях не зарегистрировано.
Первый ультразвуковой скрининг в сроке гестации 11,4 недели: КТР 50,2 мм, соответствует сроку 11,6 недели. Ультразвуковых маркеров хромосомной патологии не обнаружено. Ультразвуковая анатомия плода без патологии. Допплерометрические характеристики маточно-плацентарного кровотока в норме. Рассчитан риск развития акушерских осложнений в программе Astraia как высокий (риск ПЭ до 37 недель беременности - 1 на 82, риск по задержке роста плода до 37 недель беременности - 1 на 279).
При проведении второго ультразвукового скрининга в сроке гестации 20,1 недель: фетометрически плод соответствует сроку 20,1 недель. Ультразвуковых маркеров хромосомной патологии не обнаружено. Ультразвуковая анатомия плода без патологии. Течение беременности благоприятное.
В 27,1 уровень плацентарных микровезикул определен как 1724,69 событий/мкл. В 29 недель после ночного сна появилась сильная головная боль и пациентка направлена в краевой перинатальный центр. При обращении в стационар АД 180/110; протеинурия в разовой порции мочи 7 граммов/литр, уровень плацентарных микровезикул определен как 13496 событий/мкл. Переведена в отделение реанимации и интенсивной терапии (диагноз: беременность 29,3 недели; тяжелая преэклампсия). При стабилизации состояния (через 3 часа) экстренно родоразрешена абдоминальным путем. Родился недоношенный мальчик, весом 1450. Кровопотеря в родах составила 900 мл. Пациентка сутки находилась на продленном ИВЛ, стабилизация пациентки на 5 сутки после родоразрешения. На 10 сутки переведена с ребенком на второй этап выхаживания новорожденных.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования рецидива ранней преэклампсии по маркерам эндотелиальной дисфункции | 2022 |
|
RU2795090C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЯЖЕСТИ ТЕЧЕНИЯ РАННЕЙ ПРЕЭКЛАМПСИИ | 2021 |
|
RU2753463C1 |
| Способ прогнозирования ранней преэклампсии по данным уровня прокоагулянтной активности тканевого фактора в плазме крови в сроки гестации 19-21 неделя у пациенток группы низкого риска | 2022 |
|
RU2795083C1 |
| Прогнозирование плацентарной преэклампсии по данным плацентометрии в сроки гестации 19-21 неделя у пациентов группы низкого риска | 2021 |
|
RU2771762C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЯЖЁЛОЙ ПРЕЭКЛАМПСИИ | 2024 |
|
RU2831487C1 |
| Способ прогнозирования эффективности лечения преэклампсии средней тяжести | 2020 |
|
RU2752715C1 |
| Способ прогнозирования риска развития преэклампсии | 2023 |
|
RU2817206C1 |
| Способ прогнозирования тяжелой преэклампсии у беременных при носительстве мутации гена протромбина, генотип F2G20210A | 2019 |
|
RU2723627C1 |
| Способ прогнозирования риска развития преэклампсии у женщин с учетом генетических маркеров | 2022 |
|
RU2795660C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ У БЕРЕМЕННЫХ С САХАРНЫМ ДИАБЕТОМ 1 И 2 ТИПОВ | 2020 |
|
RU2751139C1 |
Изобретение относится к медицине, а именно к клинической лабораторной диагностике, акушерству и гинекологии, и может быть использовано для прогнозирования рецидива ранней тяжелой преэклампсии (ПЭ) у пациенток с тяжелой ПЭ в личном анамнезе. Исследуют уровень плацентарных микровезикул в плазме крови. При уровне плацентарных микровезикул более 17,4 событий/мкл на сроке гестации 11-13 недель риск развития рецидива тяжелой ранней ПЭ прогнозируют в 78,3% случаев. При уровне плацентарных микровезикул более 36,5 событий/мкл на сроке гестации 27-28 недель риск развития рецидива тяжелой ранней ПЭ прогнозируют в 95,5% случаев. Способ обеспечивает эффективное прогнозирование рецидива ранней тяжелой ПЭ у пациенток с тяжелой ПЭ в анамнезе за счет измерения количества плацентарных микровезикул в сроки гестации 11-13 и 27-28 недель. 4 ил., 2 пр.
Способ прогнозирования рецидива ранней тяжелой преэклампсии по результатам исследования уровня плацентарных микровезикул в плазме крови у пациенток с тяжелой преэклампсией в личном анамнезе, отличающийся тем, что при уровне плацентарных микровезикул более 17,4 событий/мкл в сроке гестации 11-13 недель риск развития рецидива тяжелой ранней преэклампсии прогнозируют в 78,3% случаев, а при уровне плацентарных микровезикул более 36,5 событий/мкл в сроке гестации 27-28 недель риск развития рецидива тяжелой ранней преэклампсии прогнозируют в 95,5% случаев.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЯЖЕСТИ ТЕЧЕНИЯ РАННЕЙ ПРЕЭКЛАМПСИИ | 2021 |
|
RU2753463C1 |
| WO 2017217844 A1, 21.12.2017 | |||
| КЕРКЕШКО Г.О | |||
| и др | |||
| Роль взаимодействия экстраклеточных микровезикул трофобласта с клетками иммунной системы и эндотелия в патогенезе преэклампсии | |||
| Медицинская иммунология | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| MCELRATH T.F | |||
| et al | |||
| Late first trimester circulating microparticle proteins predict the risk of | |||
Авторы
Даты
2023-06-23—Публикация
2022-08-29—Подача