Настоящее изобретение относится к синбиотическому препарату, содержащему по меньшей мере один пробиотический штамм и по меньшей мере одну аминокислоту или ее производное, выбранные из глутамина, глутаминовой кислоты или ее солей, конъюгированного глутамина или олигопептидов длиной 2-10 аминокислотных структурных единиц, при этом указанные аминокислотные структурные единицы представляют собой природные аминокислоты, и по меньшей мере одна аминокислотная структурная единица является структурной единицей, представляющей собой глутамин или глутаминовую кислоту.
Микробиота желудочно-кишечного тракта влияет на состояние здоровья, а следовательно стала объектом вмешательств для улучшения состояния здоровья людей и животных. Стратегии, направленные на микробиоту, включают применение пребиотиков, пробиотиков и иногда даже фекальные трансплантации для изменения состава и активности микробиоты. Пробиотики представляют собой живые микроорганизмы, которые при введении в адекватных количествах приносят пользу здоровью хозяина [1]. Наиболее часто исследуемые и коммерчески доступные пробиотики представляют собой в основном микроорганизмы из видов родов Lactobacillus и Bifidobacterium. Кроме того, также используются некоторые другие, такие как Propionibacterium, Streptococcus, Bacillus, Enterococcus, Escherichia coli и дрожжи. Различные бактериальные штаммы одного и того же рода и вида могут оказывать различные эффекты в отношении хозяина.
По определению, пробиотики приносят пользу хозяину за счет своей активности в организме человека, при этом представленный способ действия включает нормализацию микробиоты хозяина, ингибирование патогенов, взаимодействие с иммунной системой и их собственную метаболическую активность. Более конкретно, благоприятные эффекты в отношении состава микробиоты могут включать увеличение таксонов, принадлежащих к группе Clostridium IV (также известной как группа Clostridium leptum) и группе Clostridium XIVa (также известной как группа Clostridium Coccoides), при этом обе группы принадлежат к группе облигатных экстремофильных анаэробов, и уменьшение таксонов Clostridium группы XI. Например, группа Clostridium soredelli принадлежит к кластеру XI и вызывает пневмонию, эндокардит, артрит, перитонит и мионекроз.
Кластер Clostridium XIVa включает виды, принадлежащие к родам Clostridium, Eubacterium, Ruminococus, Coporococcus, Dorea, Lachnospira, Roseburia и Butyrivibrio. Кластер Clostridium IV состоит из родов Clostridium, Eubacterium, Ruminococcus и Anaerofilum [2]. Кластер Clostridium XI содержит патогенные виды, такие как Clostridium difficile. Кластеры Clostridium XIVa и IV составляют значительную часть (10-40%) от общего числа бактерий в микробиоте кишечника [3], которая играет важную роль в защитных механизмах и устойчивости к инфекциям.
Функциональность микробиоты описывается продуцированием таких веществ, как органические кислоты, диацетил, короткоцепочечные жирные кислоты, биосурфактанты, газы, модифицированные желчные кислоты, фитохимические вещества и антибактериальные вещества, такие как бактериоцины и перекись водорода. Среди благоприятных короткоцепочечных жирных кислот (SCFA) находятся, в частности, ацетат и н-бутират. Например, ацетат улучшает состояние здоровья за счет подавления энтеропатогенов.
Добавление в рацион некоторых пищевых ингредиентов может способствовать развитию полезных бактерий. Так называемые пребиотики определяются как селективно ферментированные ингредиенты, которые приводят к определенным изменениям в составе и/или активности микробиоты желудочно-кишечного тракта, что приносит пользу для состояния здоровья хозяина. Пребиотики часто действуют как улавливающие матрицы во время транзита пищи по желудочно-кишечному тракту, дополнительно высвобождая микроорганизмы в кишечнике, а затем выступая в качестве ферментируемых субстратов [4]. Большинство пребиотиков представляют собой сложные углеводы растительного происхождения. Пребиотики и пробиотики можно комбинировать с поддержкой выживания и метаболической активности последних, а полученные в результате продукты принадлежат к классу синбиотиков. Синбиотики относятся к пищевым ингредиентам или диетическим добавкам, сочетающим пробиотики и пребиотики в форме синергизма, следовательно синбиотичным [5]. Обновленным определением термина пребиотики является: «субстрат, который избирательно используется микроорганизмами хозяев, принося пользу для состояния здоровья» [6], относится таким образом не только к определенным углеводам, но также, например, к аминокислотам и пептидам.
Пищевые добавки представляют собой концентрированные источники питательных веществ или других веществ с питательным или физиологическим эффектом, целью которых является дополнить обычный рацион (www.efsa.europa.eu/en/topics/topic/food-supplements). Например, для L-глутамина описано, что пероральная добавка изменяет состав микробиоты кишечника у людей с избыточным весом, снижая соотношение Firmicutes и Bacteriodetes, что также наблюдалось в программах похудения [7]. Благоприятными эффектами в отношении активности микробиоты могут быть повышенное продуцирование ацетата и н-бутирата и снижение выработки короткоцепочечных жирных кислот с разветвленной цепью, таких как изобутират и изовалерат. Н-бутират можно использовать в качестве так называемого топлива толстой кишки для биосинтеза липидов и выработки гормонов кишечника. Кроме того, масляная кислота является физиологическим компонентом среды толстой кишки, который обладает противовоспалительными и противоопухолевыми свойствами [8], а также поддерживает многие дополнительные функции человеческого организма, предупреждающие возникновение неинфекционных заболеваний [9, 10]. Уменьшение изоформ бутирата и валерата указывает на снижение ферментации белка в кишечнике и уменьшение количества вредных продуктов ферментации.
Хотя некоторые пробиотики продемонстрировали многообещающие результаты в научных исследованиях, убедительных научных доказательств в поддержку конкретных путей применения пробиотиков для большинства случаев состояний здоровья не хватает. Управление США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) и Европейское управление по безопасности пищевых продуктов (EFSA) до сих пор не одобрило никаких пробиотиков для предупреждения или лечения проблем с состоянием здоровья. Некоторые пробиотические стратегии не увенчались успехом, поскольку микроорганизмы часто плохо выживают и не колонизируются в желудочно-кишечном тракте. Ограничивающие факторы включают низкий pH в желудке, а также присутствие желчных и пищеварительных ферментов, низкое содержание кислорода и присутствие других микроорганизмов в кишечнике. Кроме того, не только жизнеспособность, но и поддержание метаболической активности штаммов важны для функциональности пробиотиков [11].
В некоторых случаях лечение пробиотиками может иметь недостаточное влияние на дисбактериоз, что связано со многими расстройствами и отсутствием модуляции местных полезных и патогенных микроорганизмов. Кроме того, отсутствуют некоторые полезные микроорганизмы для применения в качестве добавок (например, Faecalibacterium prausnitzii и другие). Такие методы как трансплантация фекальной микробиоты (FMT), также известная как бактериотерапия, сложны и включают риск непреднамеренных неблагоприятных последствий.
Хотя снижение кишечных патогенов часто рассматривалось как принадлежащее к благоприятным эффектам пребиотиков, это не было достоверно продемонстрировано. Как и другие неперевариваемые углеводы, пребиотики ферментируются кишечными бактериями, в результате чего SCFA известны своими полезными для состояния здоровья свойствами. Фактически, на продуцирование SCFA влияет потребление пищи и состав микробиоты кишечника. Эти молекулы участвуют в формировании кишечной среды и физиологии толстой кишки, поскольку они являются источниками энергии для клеток-хозяев и кишечной микробиоты, а также участвуют в различных механизмах передачи сигналов хозяина [12]. Ацетат, пропионат и бутират являются SCFA, которые имеются в изобилии в кишечнике. Пропионат может быть включен в глюконеогенез путем синтеза жирных кислот с нечетным числом атомов. Предшественником для образования SCFA является лактат.
Таким образом, пребиотические стратегии в основном включают ферментируемые олигосахариды, дисахариды, моносахариды и полиолы (FODMAP) и нацелены на увеличение продуцирования этих метаболитов, а также на увеличение содержания полезных микроорганизмов. Однако эти углеводы часто вызывают нежелательные побочные эффекты, например, диарею, запор и метеоризм. Диета с низким содержанием FODMAP эффективно уменьшает эти симптомы у пациентов с синдромом раздраженного кишечника [13].
Безусловно, существует потребность в стратегиях, нацеленных на микробиоту желудочно-кишечного тракта, чтобы вызвать благоприятные изменения в их составе и активности с достижением благоприятных эффектов в отношении состояния здоровья хозяина. Такая концепция должна быть сосредоточена конкретно на эффектах в отношении клостридий, поскольку они принадлежат к ведущим игрокам в поддержании гомеостаза кишечника [14]. Эти палочковидные бактерии типа Firmicutes являются грамположительными и составляют значительную часть от общего числа бактерий в микробиоте кишечника. Они начинают заселять кишечник младенцев, вскармливаемых грудью, в течение первого месяца жизни и создавать популяции на определенном участке слизистой оболочки кишечника в тесной взаимосвязи с клетками кишечника. Эта месторасположение дает им возможность участвовать в качестве решающих факторов в модулировании физиологических, метаболических и иммунных процессов в кишечнике на протяжении всей жизни посредством взаимодействия с другими резидентными популяциями микроорганизмов, но также и обеспечивая специфические и неотъемлемые функции.
Различные пробиотические штаммы и их применение в качестве корма и пищевой добавки были описаны ранее (только в качестве примера ссылка дана на WO 2017/207371 A1 и WO 2017/207372 A1). Однако для известных пробиотических штаммов ранее не был описан так подробно эффект в отношении состава микробиоты кишечника в отношении конкретных бактериальных штаммов и их распределения.
Таким образом, целью настоящего изобретения было обеспечить новые комбинации пробиотических штаммов, которые проявляют положительные эффекты в отношении микробиоты желудочно-кишечного тракта, вызывая благоприятные изменения в их составе, в частности в отношении клостридий, и способствуя продуцированию благоприятных SCFA, таких как ацетат и н-бутират, в желудочно-кишечном тракте.
Таким образом, субъектом настоящего изобретения является синбиотический препарат, содержащий по меньшей мере один пробиотический штамм, выбранный из Bacillus subtilis, Bacillus licheniformis, Bacillus amyloliquefaciens и Bacillus pumilus, и по меньшей мере одну аминокислоту, выбранную из глутамина, глутаминовой кислоты или ее солей, конъюгированного глутамина или олигопептидов длиной 2-10 аминокислотных структурных единиц, при этом указанные аминокислотные структурные единицы представляют собой природные аминокислоты, и по меньшей мере одна аминокислотная структурная единица является структурной единицей, представляющей собой глутамин или глутаминовую кислоту.
Этот новый синбиотический препарат, содержащий бактериальный штамм и глутамин или производные глютамина, способствует выработке таксонов, продуцирующих н-бутират, и повышению уровня н-бутирата в кишечнике.
Бактерии рода Bacillus оказались особенно подходящими для данного эффекта. Следовательно, в предпочтительной конфигурации настоящего изобретения пробиотический штамм содержит бактериальный штамм из рода Bacillus. В частности, бактериальные штаммы из видов Bacillus subtilis, Bacillus licheniformis и Bacillus amyloliquefaciens эффективно увеличивают долю членов группы Clostridium XIVa и в то же время сокращают таксоны группы Clostridium XI в кишечнике. Данный эффект сопровождается повышением уровней лактата, ацетата и н-бутирата, но одновременно снижением уровней изобутирата и изовалерата. Неожиданно было обнаружено, что L-глутамин и глутаминовая кислота и их производные сильно индуцируют таксоны группы Clostridium XIVa и ингибируют таксоны группы Clostridium XI. Как и эффект Bacillus subtilis, данный эффект микробиоты был связан с увеличением уровней ацетата и н-бутирата и уменьшением уровней изобутирата и изовалерата. Повышение уровней ацетата и н-бутирата можно объяснить наличием пути ферментации глутаминовой кислоты, который используется определенными Clostridia [15]. Более того, комбинации штаммов Bacillus subtilis с глутамином или его производными действуют синергетически и оказывают более сильные эффекты в отношении клостридиальных кластеров и продуцирования короткоцепочечных жирных кислот, чем отдельные компоненты. Использование штамма Bacillus в качестве пробиотической и/или синбиотической пищевой добавки имеет дополнительное преимущество в виде возможного применения устойчивых к нагреванию и кислотам спор, что невозможно, например, для неспорообразующих лактобацил.
Большим преимуществом пробиотиков по сравнению с антибиотиками является то, что они не уничтожают бактерии без разбора и не приводят к появлению устойчивых к антибиотикам штаммов патогенных бактерий. Обычно они способны избирательно конкурировать с патогенными бактериями путем продуцирования антимикробных веществ с определенной эффективностью, а в идеале они способны одновременно усиливать рост и жизнеспособность полезной микрофлоры кишечника. Кроме того, они предпочтительно способны стимулировать системный иммунный ответ у подвергнутых лечению животных или людей.
В предпочтительном варианте осуществления пробиотический штамм выбран из одного из следующих: Bacillus subtilis DSM 32315 (который подробно описан в WO 2017/207372 A1), Bacillus subtilis DSM 32540 и Bacillus amyloliquefaciens CECT 5940, Bacillus subtilis DSM 32592, Bacillus pumilus DSM 32539, Bacillus licheniformis DSM 32314 (который подробно описан в WO 2017/207371 A1).
В соответствии с настоящим изобретением аминокислота или ее производное выбраны из глутамина, глутаминовой кислоты или ее солей, конъюгированного глутамина или олигопептидов длиной 2-10 аминокислотных структурных единиц, при этом указанные аминокислотные структурные единицы представляют собой природные аминокислоты, и по меньшей мере одна аминокислотная структурная единица является структурной единицей, представляющей собой глутамин или глутаминовую кислоту.
Положительные эффекты глутамина известны из литературы, например, было показано, что пероральная добавка с глутамином снижает смертность у морских свинок, обработанных дозами метотрексата, вызывающими некротический энтероколит [16]. Более того, в исследованиях баланса задних конечностей на послеоперационных анестезированных собаках было показано, что аминокислоты аланилглутамина, введенного посредством инфузии, извлекаются скелетными мышцами почти так же, как и из смесей аланина и глутамина [17].
Под «аминокислотой» в контексте настоящего изобретения следует понимать молекулу, содержащую функциональную аминогруппу (-NH2) и функциональную группу карбоновой кислоты (-COOH) вместе с боковой цепью, специфичной для соответствующей аминокислоты. В контексте настоящего изобретения включены как альфа-, так и бета-аминокислоты. Предпочтительные аминокислоты по настоящему изобретению представляют собой альфа-аминокислоты, в частности 20 «природных аминокислот», приведенных ниже.
В контексте настоящего изобретения следует понимать, что выражение «природные аминокислоты» включает как L-форму, так и D-форму перечисленных выше 20 аминокислот. Однако предпочтительной является L-форма. В одном варианте осуществления термин «аминокислота» также включает аналоги или производные этих аминокислот.
Под «свободной аминокислотой» в соответствии с настоящим изобретением подразумевается аминокислота, содержащая ее амино- и ее (альфа-) карбоксильную функциональную группу в свободной форме, т.е. не связанной ковалентно с другими молекулами, например аминокислотой, не образуя пептидную связь. Свободные аминокислоты также могут присутствовать в виде солей или в форме гидрата. При упоминании аминокислоты как части олигопептида или в олигопептиде следует понимать как относящееся к той части соответствующей структуры олигопептида, которая происходит из соответствующей аминокислоты, в соответствии с известными механизмами биохимии и биосинтеза пептидов.
Под «олигопептидом» в соответствии с настоящим изобретением следует понимать пептидное соединение, состоящее из 2-20 аминокислот. Более предпочтительными олигопептидами по настоящему изобретению являются олигопептиды, состоящие из 2-10 аминокислот, 2-6 аминокислот, 2-5 аминокислот, 2-4 аминокислот или 2-3 аминокислот. Наиболее предпочтительными олигопептидами в соответствии с настоящим изобретением являются дипептиды.
Предпочтение меньших пептидов согласуется с ранней литературой, которая показывает, что исследования на молодых животных предполагают, что транспорт дипептидов имеет большее количественное значение, чем транспорт свободных аминокислот во время раннего роста [18, 19]. Более того, в исследованиях перфузии кишечника человека поглощение ди- и трипептидов ингибировалось меньше, чем поглощение свободных аминокислот после 2 недель голодания [20].
Под «пептидом» следует понимать молекулу, содержащую по меньшей мере две аминокислоты, ковалентно связанные друг с другом пептидной связью (R1-CO-NH-R2).
В альтернативном варианте осуществления настоящего изобретения олигопептид дополнительно содержит аланин или глицин.
В дополнительном альтернативном варианте осуществления олигопептид представляет собой дипептид, выбранный из глицин-глутамина, глицин-глутаминовой кислоты, аланин-глутамина, аланин-глутаминовой кислоты и их ацетилированных форм.
Дипептид аланин-глутамин (Ala-Gln) является особенно предпочтительным в соответствии с предпочтительным вариантом осуществления настоящего изобретения.
В соответствии с настоящим изобретением общее количество пробиотического штамма и аминокислоты или олигопептида составляет по меньшей мере 40 вес. %, предпочтительно по меньшей мере 50 вес. %, более предпочтительно по меньшей мере 60 вес. %, наиболее предпочтительно по меньшей мере 70 вес. % от общего веса препарата.
Особенно предпочтительно, когда препарат дополнительно содержит энтеросолюбильное покрытие в соответствии с настоящим изобретением, для прямой доставки симбиотической композиции в толстую кишку индивидуума. Композиция энтеросолюбильного покрытия может включать одно или более из следующего: сополимеры метилакрилата и метакриловой кислоты, фталат ацетата целлюлозы (CAP), сукцинат ацетата целлюлозы, фталат гидроксипропилметилцеллюлозы, сукцинат ацетата гидроксипропилметилцеллюлозы (сукцинат ацетата гипромеллозы), поливинилацетатфталат (PVAP), сополимеры метилметакрилата и метакриловой кислоты, шеллак, тримеллитат ацетата целлюлозы, альгинат натрия, зеин.
В качестве энтеросолюбильного покрытия предпочтительно использовать полимер, полимеризованный от 10 до 30% по весу метилметакрилата, от 50 до 70% по весу метилакрилата и от 5 до 15% по весу метакриловой кислоты.
Как раскрыто, полимерная дисперсия может предпочтительно содержать от 15 до 50% по весу полимера, полимеризованного от 20 до 30% по весу метилметакрилата, от 60 до 70% по весу метилакрилата и от 8 до 12% по весу метакриловой кислоты. Наиболее предпочтительный полимер является полимеризованным из 25% по весу метилметакрилата, 65% по весу метилакрилата и 10% по весу метакриловой кислоты.
30% по весу водной дисперсии полимера, полимеризованного из 25% по весу метилметакрилата, 65% по весу метилакрилата и 10% по весу метакриловой кислоты, соответствует коммерческому продукту EUDRAGUARD® biotic.
Процентное содержание мономеров составляет в сумме 100%. Функциональный полимер используют в количестве 2-30 мг/см2, предпочтительно 5-20 мг/см2.
Одним из субъектов настоящего изобретения является применение препарата в соответствии с настоящим изобретением в качестве кормовой или пищевой добавки.
Дополнительным субъектом настоящего изобретения является также применение препарата по настоящему изобретению в качестве синбиотического ингредиента в кормовых или пищевых продуктах. В соответствии с настоящим изобретением термин «синбиотичный» должен относиться к композиции, содержащей пребиотический и пробиотический компоненты. Более того, настоящее изобретение относится к обновленному определению термина «пребиотик», означающему субстрат, который селективно используется микроорганизмами и приносит пользу для состояния здоровья, и также должен включать аминокислоты и пептиды. Таким образом, симбиотическая композиция в соответствии с настоящим изобретением представляет собой композицию, содержащую пробиотический штамм и аминокислоту или олигопептид в качестве пребиотика.
Предпочтительными пищевыми продуктами в соответствии с настоящим изобретением являются молочные продукты, в частности йогурт, сыр, молоко, масло и творог.
Клетки штаммов по настоящему изобретению могут присутствовать, в частности в композициях по настоящему изобретению, в виде спор (которые находятся в состоянии покоя), в виде вегетативных клеток (которые растут), в виде клеток переходного состояния (которые переходят из фазы роста к фазе образования спор) или в виде комбинации из по меньшей мере двух, в частности всех этих типов клеток. В предпочтительном варианте осуществления композиция по настоящему изобретению содержит в основном или только споры.
Дополнительным субъектом настоящего изобретения является кормовая или пищевая композиция, содержащая препарат в соответствии с настоящим изобретением и по меньшей мере один дополнительный кормовой или пищевой ингредиент, предпочтительно выбранный из белков, углеводов, жиров, дополнительных пробиотиков, пребиотиков, ферментов, витаминов, иммуномодуляторов, заменителей молока, микроэлементов, аминокислот, кокцидиостатиков, продуктов на основе кислот, лекарственных средств и их комбинаций.
Композиция корма или пищевого продукта в соответствии с настоящим изобретением также включает диетические добавки в форме пилюли, капсулы, таблетки или жидкости.
Композиции по настоящему изобретению, в частности кормовые, пищевые и фармацевтические композиции, предпочтительно содержат штаммы по настоящему изобретению и вводятся животным или людям в количестве от приблизительно 1×103 до приблизительно 2×1012 КОЕ/г корма/продукта питания или мл воды, в частности в количестве от приблизительно 1×103, или приблизительно 1×104, или приблизительно 1×105, или приблизительно 1×106, или приблизительно 1×107, или приблизительно 1×108, или приблизительно 1×109, или приблизительно 1×1010, или приблизительно 1×1011, или приблизительно 1×1012 КОЕ/г корма/продукта питания или мл воды, предпочтительно в количестве от приблизительно 1×104 до приблизительно 1×1010 КОЕ/г корма/продукта питания или мл воды, более предпочтительно в количестве от 1×104 до 1×107 КОЕ/г корма/продукта питания или мл воды.
Соответственно, предпочтительные количества препаратов по настоящему изобретению в кормовых или пищевых композициях по настоящему изобретению предпочтительно находятся в диапазоне от 0,1 вес. % до 10 вес. %, более предпочтительно от 0,2 вес. % до 5 вес. %, в частности от 0,3 вес. % до 3 вес. %.
Дополнительным субъектом настоящего изобретения является фармацевтическая композиция, содержащая препарат в соответствии с настоящим изобретением и фармацевтически приемлемый носитель.
Препараты в соответствии с настоящим изобретением при введении животным или людям предпочтительно улучшают состояние здоровья, в частности, состояние здоровья кишечника, состояние здоровья сердечно-сосудистой системы, контроль здорового веса или здоровый иммунитет животного или человека.
Таким образом, дополнительным субъектом настоящего изобретения является композиция по настоящему изобретению для применения в предупреждении или лечении диареи, запора, синдрома раздраженного кишечника, болезни Крона, язвенного колита, колоректального рака, рака кишечника, сердечно-сосудистого заболевания, артериосклероза, жировой болезни печени, гиперлипидемии, гиперхолестеринемии, ожирения, адипоза, диабета 2 типа, метаболического синдрома, хронических воспалительных заболеваний и аллергических заболеваний.
Преимущественная конфигурация в соответствии с настоящим изобретением представляет собой композицию для улучшения состояния здоровья кишечника животного или человека с помощью одно или более из следующего:
- увеличения общего количества бактерий группы Clostridium XIVa в микробиоме кишечника,
- уменьшения общего количества бактерий группы Clostridium XI в микробиоме кишечника,
- увеличения продуцирования короткоцепочечных жирных кислот, предпочтительно н-бутирата, пропионата, ацетата и лактата, и
- ингибирования образования короткоцепочечных жирных кислот с разветвленной цепью, предпочтительно изобутирата и изовалерата.
Дополнительным субъектом настоящего изобретения является капсула, содержащая по меньшей мере один пробиотический штамм, выбранный из Bacillus subtilis, Bacillus licheniformis, Bacillus amyloliquefaciens, Bacillus pumilus, и по меньшей мере один дипептид, выбранный из глицин-глутамина, глицин-глутаминовой кислоты, аланин-глутамина, аланин-глутаминовой кислоты и их ацетилированных форм.
В предпочтительном варианте осуществления пробиотический штамм представляет собой Bacillus subtilis, предпочтительно Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus subtilis DSM 32592.
Капсула предпочтительно содержит от 1×108 до 2×1010 КОЕ пробиотического штамма и от 50 мг до 800 мг дипептида.
Также предпочтительно, когда количество пробиотического штамма и дипептида составляет по меньшей мере 40 вес. %, предпочтительно по меньшей мере 50 вес. %, более предпочтительно по меньшей мере 60 вес. %, наиболее предпочтительно по меньшей мере 70 вес. % от общего веса содержимого капсулы.
Капсула может дополнительно содержать дополнительные витамины или микроэлементы. Витамины предпочтительно выбраны из витамина А (в виде полностью транс-ретинола, полностью транс-ретиноловых сложных эфиров, а также полностью транс-бета-каротина и других каротиноидов провитамина А), витамина B1 (тиамина), витамина B2 (рибофлавина), витамина B3 (ниацина), витамина B5 (пантотеновой кислоты), витамина B6 (пиридоксина), витамина B7 (биотина), витамина B9 (фолиевой кислоты или фолата), витамина B12 (кобаламинов), витамина C (аскорбиновой кислоты), витамина D (кальциферолов), витамина E (токоферолов и токотриенолов) и витамина K (хинонов).
Микроэлементы предпочтительно выбраны из серы, железа, хлора, кальция, хрома, кобальта, меди, цинка, магния, марганца, молибдена, йода и селена.
Капсула может дополнительно содержать один или более пребиотических ингредиентов, предпочтительно выбранных из инулинов, фруктоолигосахаридов (FOS), галактоолигосахаридов (GOS), крахмала, пектина, бета-глюканов и ксилоолигосахаридов.
Капсула может дополнительно содержать один или более растительных экстрактов, где растения предпочтительно выбраны из брокколи, маслины, граната, черной смородины, черники, голубики, облепихи, каму-каму, бойзеновой ягоды, куркумы, имбиря, чеснока, виноградных косточек, ягоды асаи, черноплодной рябины, ягоды годжи, хрена, босвеллии пильчатой, спирулины, женьшеня обыкновенного, каннабидиола, шиповника, пуэра, сенча, эхинацеи и листьев зеленого чая.
В предпочтительной конфигурации капсула содержит энтеросолюбильное покрытие, где энтеросолюбильное покрытие содержит одно или более из следующего: сополимеров метилакрилата и метакриловой кислоты, фталата ацетата целлюлозы (CAP), сукцината ацетата целлюлозы, фталата гидроксипропилметилцеллюлозы, сукцината ацетата гидроксипропилметилцеллюлозы (сукцината ацетата гипромеллозы), поливинилацетатфталата (PVAP), сополимеров метилметакрилата и метакриловой кислоты, шеллака, тримеллитата ацетата целлюлозы, альгината натрия, зеина.
Демонстрационные примеры
Пример 1. Штаммы Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940 способны сохраняться в микробиоте толстой кишки человека
Скрининговая модель кишечника
Для определения эффекта пробиотических штаммов Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940 в отношении микробиоты толстой кишки взрослых использовали скрининговую модель кишечника (i-screen, TNO, Нидерланды). Таким образом, модель i-screen инокулировали с помощью стандартного материала фекальной микробиоты взрослого человека, который состоял из объединенных фекалий от 6 здоровых взрослых добровольцев (европеоид, европейский образ жизни и питание). Фекальный материал смешивали и выращивали в ферментере периодического действия с подпиткой в течение 40 часов для создания стандартизированной микробиоты, как описано ранее [21]. Эти стандартные наборы кишечной микробиоты взрослых хранили при -80°C в 12% глицерине.
Кишечную микробиоту культивировали in vitro в модифицированной стандартной среде оттока из подвздошной кишки (SIEM), состав которой был описан [22] и модифицирован следующим образом: 0,047 г/л пектина, 0,047 г/л ксилана, 0,047 г/л арабиногалактана, 0,047 г/л амилопектина, 0,392 г/л крахмала, 24,0 г/л казеина, 24,0 бактопептона, 0,4 бычьей желчи и 0,2 г/л цистеина. Все компоненты были поставлены от Trititium Microbiology (Велдховен, Нидерланды). Доводили pH среды до 5,8.
Для ферментаций i-screen предварительно культивированный стандартизованный фекальный инокулят разбавляли в 50 раз в 1350 мкл модифицированной SIEM. Все эксперименты осуществляли в трех повторностях. Штаммы Bacillus subtilis (DSM 32315), Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940 предварительно культивировали отдельно в 50 мл среды LBKelly [23] в течение приблизительно 16 ч. Инкубацию осуществляли во встряхиваемых колбах при 37°C в аэробных условиях. После инкубации плотность бактерий определяли путем измерения оптической плотности при 600 нм. Конечный исходный раствор 1×1010 клеток/мл получали в 1 мл буферного раствора (0,1 мМ MES, pH 6). Суспензию каждого штамма вводили в i-screen до конечного уровня приблизительно 109 клеток/мл, соответственно.
Инкубацию i-screen осуществляли при следующих газовых условиях: 0,2% O2, 0,2% CO2, 10% H2, 89,6% N2.
Выделение ДНК
Выделение ДНК для секвенирования генов, кодирующих 16S rRNA, осуществляли, как описано Ladirat et al. (2013), с небольшими изменениями. Приблизительно 100 мкл культурального материала добавляли в лунки 96-луночного планшета, содержащего на лунку по 300 мкл лизирующего буфера (Mag Mini DNA Isolation Kit, LGC ltd, Великобритания), 500 мкл циркониевых гранул (0,1 мм; BioSpec products, Бартлсвилл, Оклахома, США) и 500 мкл фенола, насыщенного трис-HCl (pH 8,0; Carl Roth GMBH, Германия). Помещали 96-луночный планшет в Mini-BeadBeater-96 (BioSpec products, Бартлсвилл, Оклахома, США) на 2 мин. при 2100 колебаний/мин. Затем ДНК очищали с использованием набора для выделения ДНК Agowa Mag Mini в соответствии с рекомендациями производителя. Выделенную ДНК элюировали в конечном объеме буфера 60 мкл.
Секвенирование гена 16S rRNA V4
Состав микробиоты анализировали с помощью секвенирования ампликона гена 16S rRNA гипервариабельной области V4. Это было достигнуто путем ряда стадий.
Количество бактериальной ДНК в образцах ДНК i-screen определяли с помощью количественной полимеразной цепной реакции (qPCR) с использованием праймеров, специфичных для бактериального гена 16S rRNA: Прямой праймер - CGAAAGCGTGGGGAGCAAA; обратный праймер - GTTCGTACTCCCCAGGCGG; зонд - 6FAM-ATTAGATACCCTGGTAGTCCA-MGB.
Затем создавали ПЦР-ампликоны гипервариабельной области V4 гена 16S rRNA для отдельных образцов путем амплификации 500 пг ДНК, как описано [24] (2013), с использованием праймеров F515/R806 [25]. Праймеры включали адаптеры Illumina и уникальный ключ индексной последовательности из 8 нуклеотидов [24]. Был включен имитационный контроль для технического контроля качества. Количество амплифицированной ДНК в образце определяли количественно с использованием набора реагентов dsDNA 910 на анализаторе фрагментов (Advanced Analytical). Библиотеки ампликонов объединяли в эквимолярных количествах и очищали из 1,2% агарозного геля с использованием набора Gel Extraction Kit (Qiagen). Библиотеку количественно оценивали с помощью набора для анализа dsDNA Quant-iT™ PicoGreen® (Thermo Fisher Scientific). Парное секвенирование ампликонов осуществляли на платформе Illumina MiSeq (Illumina, Эйндховен, Нидерланды).
Эти последовательности обрабатывали с помощью Mothur v.1.36.1 [26] в соответствии с mothur MiSeq SOP [24]. Перед объединением пар чтения области низкого качества обрезали с помощью Btrim [27] с размером скользящего окна 5 нуклеотидов и средним показателем качества 25. После слияния последовательности фильтровали по длине, в то время как неоднозначные основания не допускались. Уникальные последовательности выравнивали с эталонным выравниванием бактериальных SILVA SEED, выпуск 102 (доступно по адресу: http://www.mothur.org/wiki/Silva_reference_files); слишком короткие последовательности удаляли с помощью screen.seqs с параметрами «optimize=start-end, criteria=90». Химерные последовательности идентифицировали для каждого образца с помощью UCHIME [28] в режиме de novo и удаляли. Затем удаляли последовательности, встречающиеся менее чем 10 раз во всем наборе данных. Таксономические названия присваивали всем последовательностям с использованием не подвергавшегося воздействию байесовского классификатора Ribosomal Database Project (RDP) с доверительным порогом 60% и 1000 итераций [29] и версии обучающего набора RDP v.9 в формате mothur (trainset9_032012).
Последовательности группировали с помощью алгоритма Minimum Entropy Decomposition (MED), который чувствительным образом группирует ампликоны гена 16S rRNA [30]. Для фильтрации шума фильтр «минимального существенного содержания» устанавливали на 200.
Микробиота толстой кишки человека в i-screen также была дополнена жизнеспособными вегетативными клетками Bacillus spp. каждого пробиотического штамма.
На основе секвенирования MiSeq гипервариабельной области V4 кодирующего гена 16S rRNA можно было визуализировать специфические эффекты в отношении состава микробиоты, связанные с отдельными штаммами.
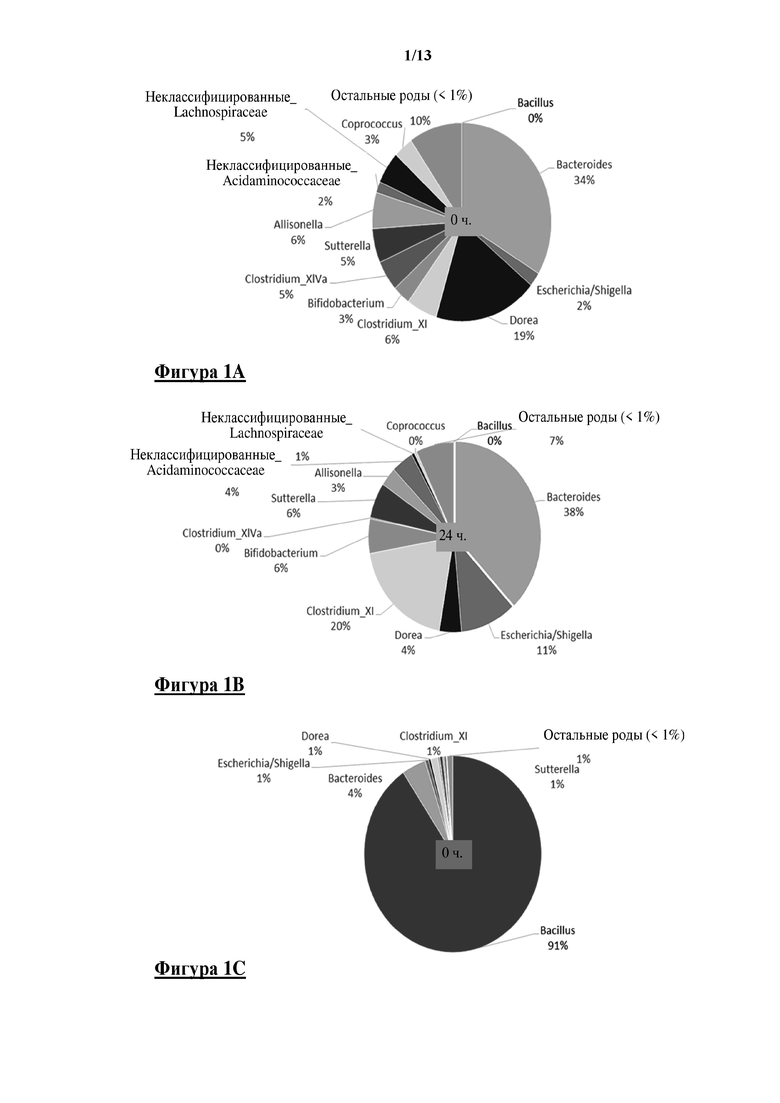
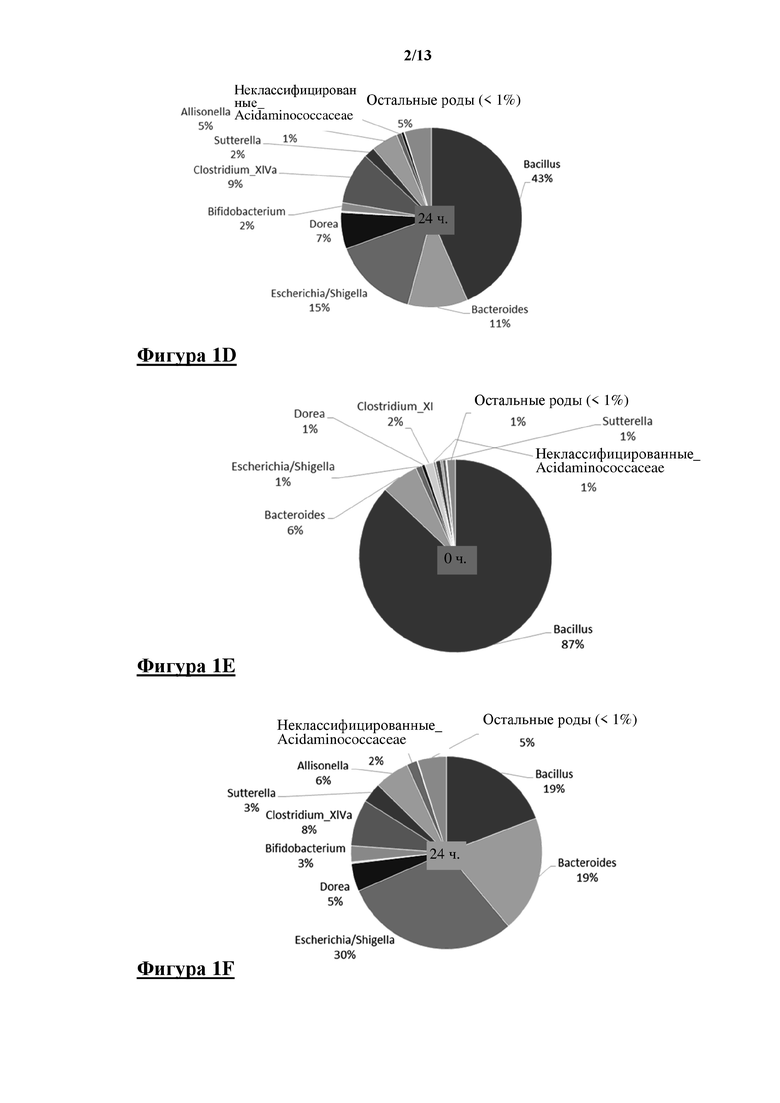
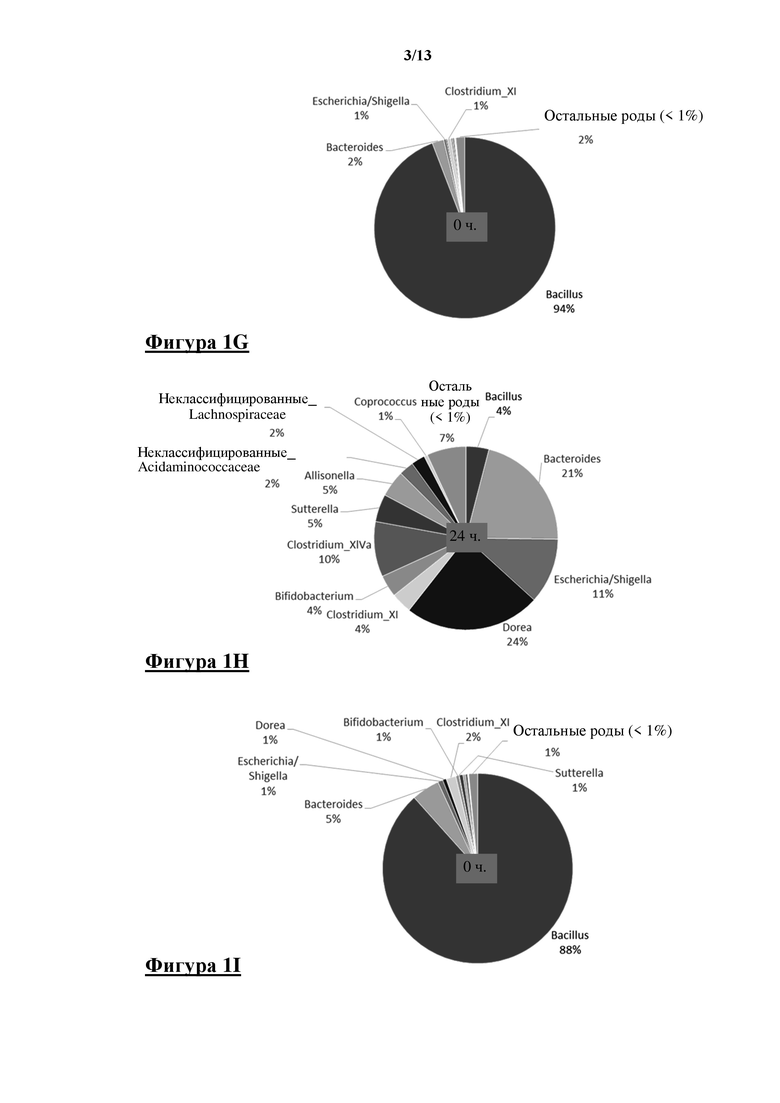
Исходя из числа прочтений последовательности, содержание бацилл было высоким в начале эксперимента i-screen (приблизительно 109 КОЕ/мл), и таким образом Bacillus subtilis DSM 32315 составляла примерно 91% от общей бактериальной популяции при t=0 ч. (фигура 1 C), Bacillus subtilis DSM 32540 составляла примерно 87% от общей бактериальной популяции в при t=0 ч. (фигура 1 E), Bacillus licheniformis DSM 32314 составляла примерно 94% от общей бактериальной популяции при t=0 ч. (фигура 1 G) и Bacillus amyloliquefaciens CECT 5940 составляла примерно 88% от общей бактериальной популяции в момент времени t=0 ч. (фигура 1 I).
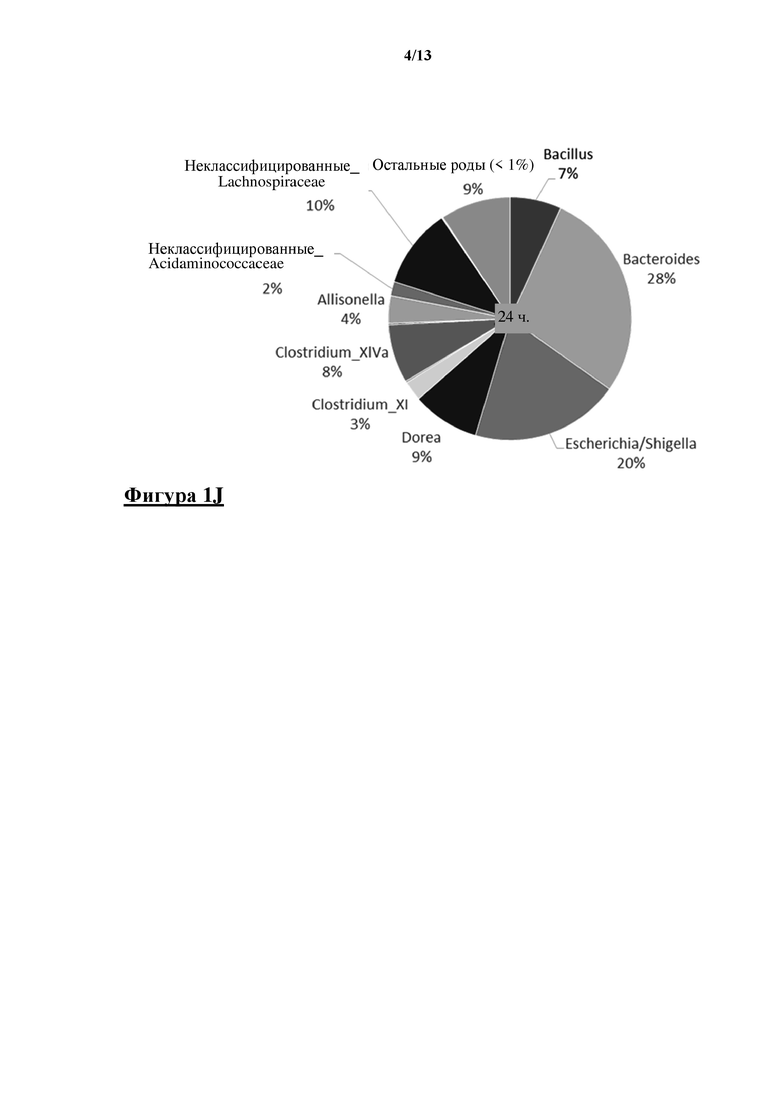
Контроль без добавления штамма Bacillus spp. показан в момент времени 0 ч (фигура 1 A) и через 24 ч. инкубации (фигура 1 B). После 24 ч. инкубации фекальная микробиота смогла восстановиться за счет относительного присутствия бацилл. Оказалось, что клетки DSM 32315 сохраняли присутствие на уровне 41% в i-screen после 24 ч. инкубации (фигура 1 D), клетки DSM 32540 сохраняли присутствие на уровне 19% в i-screen после 24 ч. инкубации (фигура 1 F), клетки DSM 32314 сохраняли присутствие на уровне 4% в i-screen после 24 ч. инкубации (фигура 1 H) и клетки CECT 5940 сохраняли присутствие на уровне 7% в i-screen после 24 ч. инкубации (фигура 1 J).
На фигуре 1 показаны круговые диаграммы, показывающие образцы ферментации i-screen на уровне родов на основе секвенирования MiSeq гипервариабельной области V4 гена области, кодирующей 16S rRNA. Обнаруженные роды и их относительное содержание представлены заштрихованными участками. A) 0 ч. инкубации без добавления, B) после 24 ч. инкубации без добавления, C) 0 ч. после добавления вегетативных клеток Bacillus subtilis DSM 32315, D) 24 ч. после добавления вегетативных клеток Bacillus subtilis DSM 32315, E) 0 ч. после добавления вегетативных клеток Bacillus subtilis DSM 32540, F) через 24 ч. после добавления вегетативных клеток Bacillus subtilis DSM 32540, G) 0 ч. после добавления вегетативных клеток Bacillus licheniformis DSM 32314, H) 24 ч. после добавления вегетативных клеток Bacillus licheniformis DSM 32314, I) 0 ч. после добавления вегетативных клеток Bacillus amyloliquefaciens CECT 5940, J) 24 ч. после добавления вегетативных клеток Bacillus amyloliquefaciens CECT 5940.
Пример 2. Пробиотические штаммы Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940 продуцируют значительные уровни лактата.
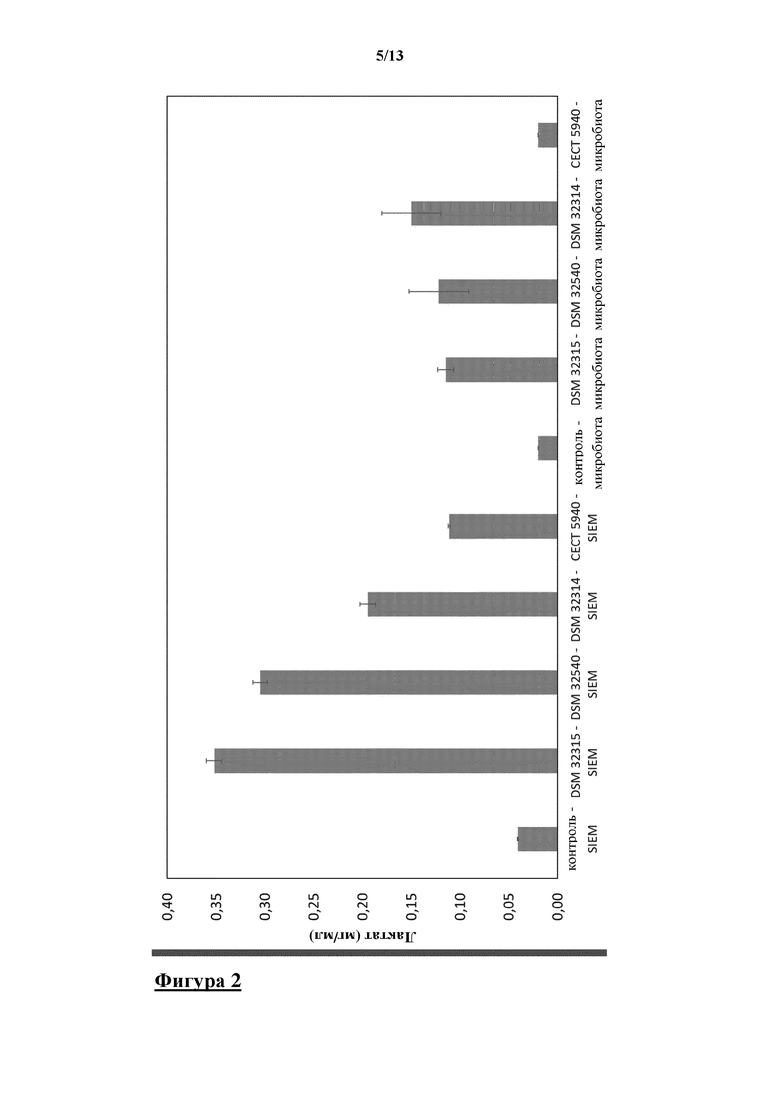
В SIEM вначале выявляли низкий уровень лактата, составляющий приблизительно 0,04 мг/мл, который полностью исчезал в присутствии микробиоты с содержанием лактата <0,02 мг/мл через 24 ч. (фигура 2). Штаммы Bacillus продуцировали значительные уровни лактата в SIEM без сообщества бактерий толстой кишки через 24 ч. Клетки DSM 32315 продуцировали 0,35 мг/мл, клетки DSM 32540 продуцировали 0,31 мг/мл, клетки DSM 32314 продуцировали 0,19 мг/мл и клетки CECT 5940 продуцировали 0,11 мг/мл.
После 24 ч. инкубации с микробиотой кишечника человека количество лактата все еще значительно увеличивалось до 0,12 мг/мл в присутствии клеток DSM 32315 или DSM 32540 и до 0,15 мкг/мл в присутствии DSM 32314, соответственно.
Таким образом, эти пробиотические штаммы вызывали значительное образование лактата микробиотой кишечника человека. Это можно интерпретировать как положительный эффект, поскольку лактат может превращаться в полезные для здоровья SCFA.
На фигуре 2 показаны измеренные концентрации лактата в мг/мл в SIEM после 24 ч. инкубации в SIEM и в присутствии микробиоты толстой кишки, содержащей Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940, соответственно. Предел обнаружения лактата составлял 0,02 мг/мл.
Пример 3. Пробиотические штаммы Bacillus subtilis DSM 32315, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940, соответственно, поддерживали продуцирование ацетата сообществом микробиоты человека
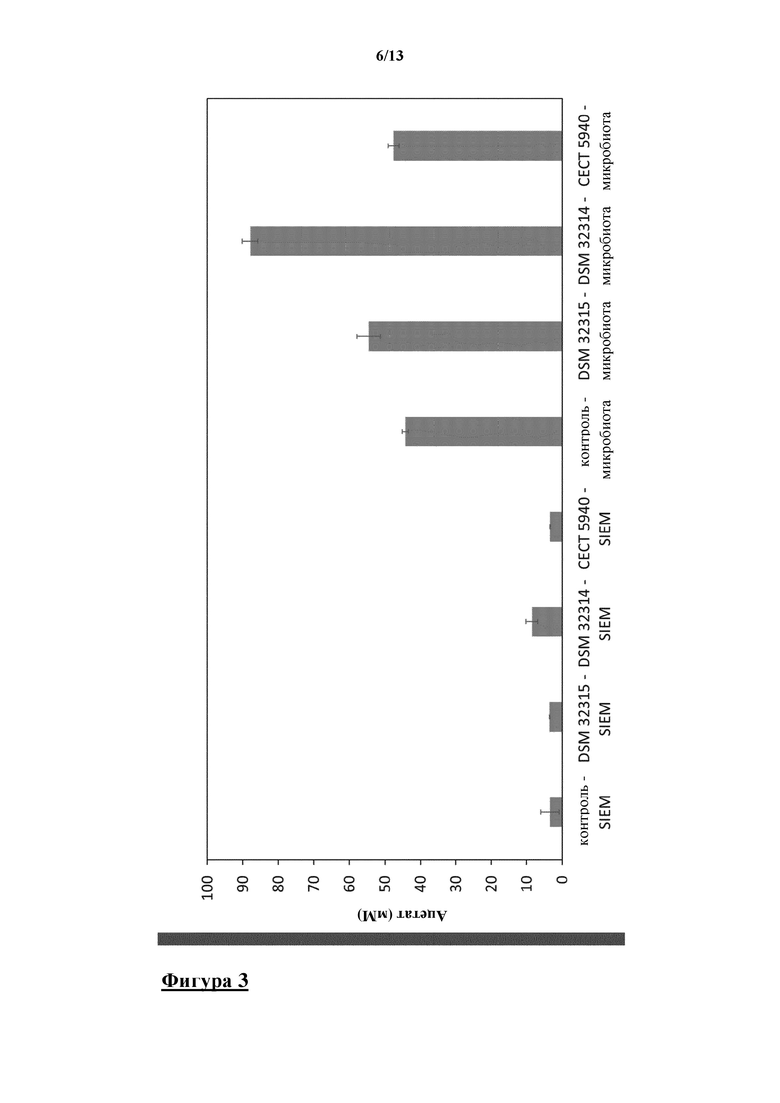
Штаммы Bacillus DSM 32315, DSM 32314 и CECT 5940 вызывали значительное увеличение продуцирования ацетата кишечной микробиотой. На фигуре 3 показан средний уровень ацетата, составляющий приблизительно 44 мМ, в i-screen после 24 ч. воздействия без добавления пробиотических штаммов, в то время как ацетат с 3,4 мМ был с трудом выявляемым в SIEM.
После 24 ч. инкубации увеличение концентрации ацетата на 10,4 мМ, 43,7 мМ и 3,3 мМ наблюдали в присутствии штаммов DSM 32315, DSM 32314 и CECT 5940, соответственно (фигура 3).
Значение p для всех данных составляло ниже 0,05, что означает то, что они статистически значимы. Таким образом, пробиотические штаммы DSM 32315, DSM 32314 и CECT 5940 поддерживали продуцирование ацетата, который оказывал благотворное влияние на кишечник человека.
На фигуре 3 показаны измеренные концентрации ацетата в мМ в SIEM после 24 ч. инкубации в SIEM и в присутствии микробиоты толстой кишки, содержащей Bacillus subtilis DSM 32315, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940, соответственно.
Пример 4. Пробиотические штаммы Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940, соответственно, поддерживали продуцирование пропионата микробиотой человека
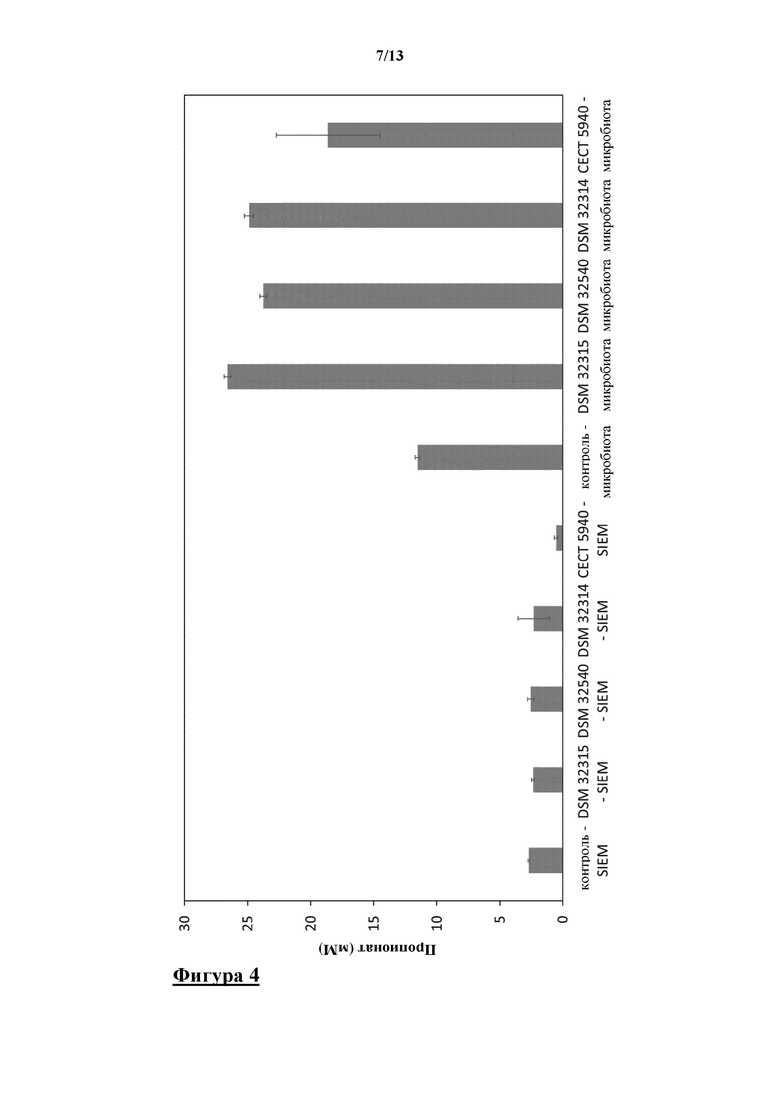
Штаммы Bacillus DSM 32315, DSM 32540, DSM 32314 и CECT 5940 не продуцировали пропионата в SIEM, однако они значительно (значение p<0,05) ускоряли продуцирование пропионата микробиотой человека (фигура 4). Штаммы значительно поддерживали продуцирование пропионата микробиотой кишечника по сравнению с контролем. На фигуре 4 показан средний уровень пропионата, составляющий приблизительно 11,5 мМ, в i-screen после 24 ч. воздействия без добавления пробиотических штаммов, в то время как пропионат с 2,7 мМ был с трудом выявляемым в SIEM. В присутствии вегетативных клеток Bacillus subtilis DSM 32315 количество пропионата было на 15,1 мМ выше через 24 ч., чем в контроле. В присутствии вегетативного Bacillus subtilis DSM 32540 количество пропионата было на 12,2 мМ выше. В присутствии DSM 32314 количество было на 13,4 мМ выше, а в присутствии CECT 5940 количество пропионата было на 7,1 мМ выше.
Пропионат полезен для состояния здоровья кишечника человека, потому что он может быть включен в глюконеогенез.
На фигуре 4 показаны измеренные концентрации пропионата в мМ в SIEM после 24 ч. инкубации в SIEM и в присутствии микробиоты толстой кишки, содержащей Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940, соответственно.
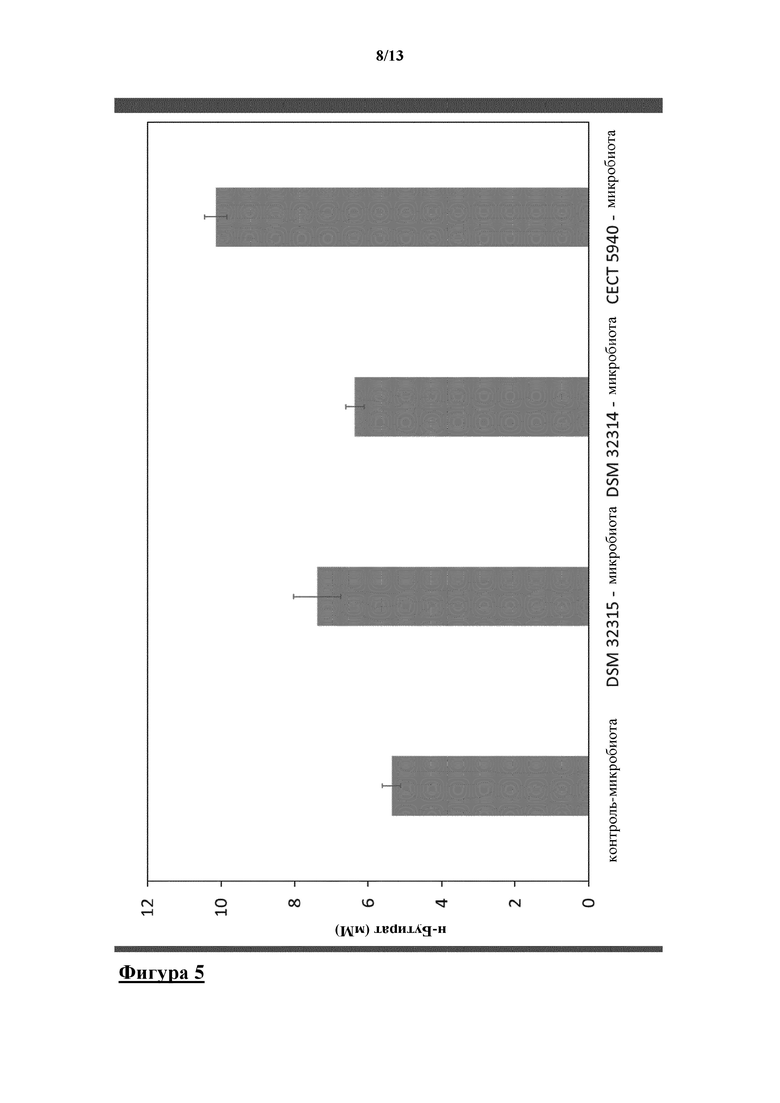
Пример 5. Пробиотические штаммы Bacillus subtilis DSM 32315, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940,соответственно, поддерживали продуцирование н-бутирата в составе микробиоты человека
Пробиотические штаммы Bacillus subtilis DSM 32315, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940 не продуцировали выявляемых уровней н-бутирата после воздействия в SIEM в течение 24 ч., однако они оказывали значительные положительные влияния (p-значения <0,05) на уровень продуцирования н-бутирата микробиотой человека (фигура 5). На фигуре 5 показан средний уровень н-бутирата, составляющий приблизительно 5,4 мМ, в i-screen после 24 ч. воздействия без добавления пробиотических штаммов, в то время как пропионат был с трудом выявляемым в SIEM с 0,3 мМ. В присутствии вегетативных клеток Bacillus subtilis DSM 32315 количество н-бутирата было на 2,0 мМ выше через 24 ч., чем в контроле. В присутствии вегетативных клеток DSM 32314 количество н-бутирата было на 1,0 мМ выше, а в присутствии вегетативных клеток CECT 5940 количество н-бутирата было на 4,8 мМ выше. Получение более высоких количеств н-бутирата может быть полезным для биосинтеза липидов, например производства гормонов кишечника.
На фигуре 5 показаны измеренные концентрации н-бутирата в мМ в SIEM после 24 ч. инкубации в присутствии микробиоты толстой кишки, содержащей Bacillus subtilis DSM 32315, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940, соответственно.
Пример 6. Штаммы Bacillus subtilis DSM 32315 и DSM 32540, соответственно, уменьшали образование изобутирата и изовалерата в составе микробиоты человека
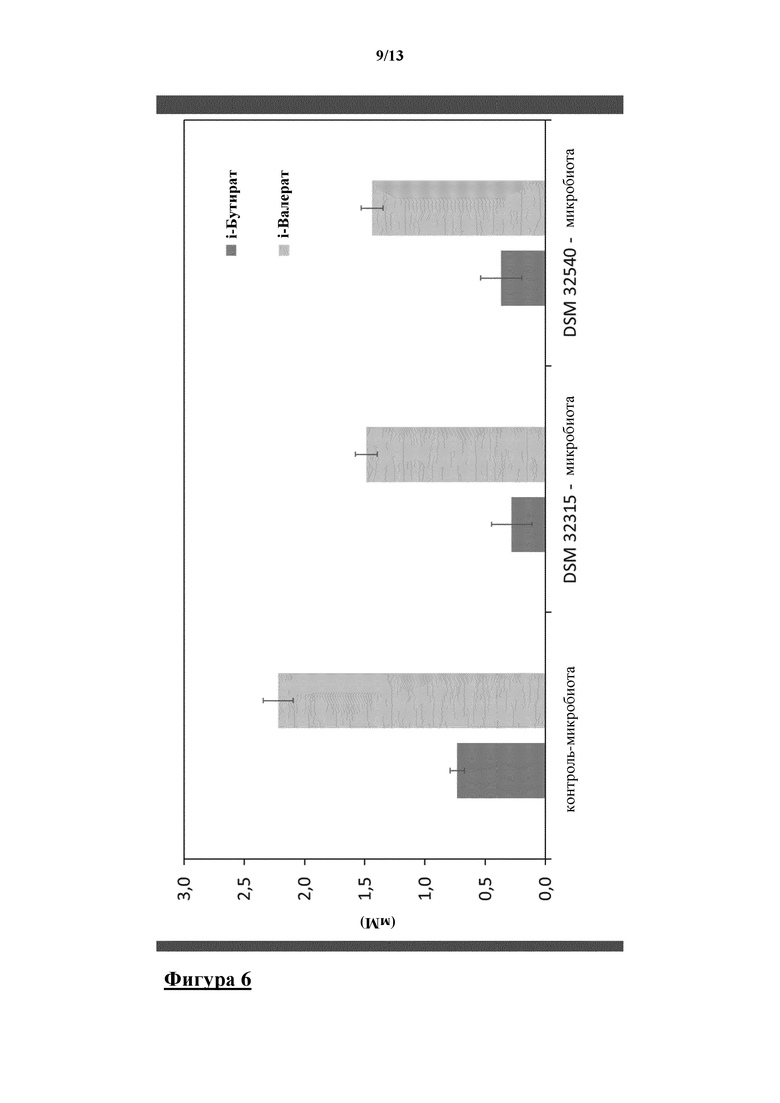
На рисунке 6 показан средний уровень изобутирата, составляющий приблизительно 0,73 мМ, и средний уровень изовалерата, составляющий приблизительно 2,2 мМ, в i-screen после 24 ч. воздействия без добавления пробиотических штаммов, в то время как изобутират не был выявляемым, а содержание изовалерата составляло 0,24 мМ в SIEM.
В частности, штаммы DSM 32315 и DSM 32540 значительно снижали (значение p<0,05) продуцирование изобутирата и изовалерата микробиотой кишечника человека. После 24 ч. инкубации содержание изобутирата было соответственно на 0,5 мМ ниже в присутствии клеток DSM 32315 и на 0,4 мМ ниже в присутствии клеток DSM 32540 по сравнению с контролем.
Штаммы Bacillus DSM 32315 и DSM 32540 также оказывали отрицательное влияние на уровень продуцирования изовалерата при добавлении к микробиоте человека. Концентрация значительно (значение p<0,05) уменьшилась на i-screen соответственно на 0,7 мМ и 0,8 мМ по сравнению с контролем.
При введении штаммов Bacillus DSM 32315 в микробиоту кишечника в i-screen клетки поддерживали продуцирование н-бутирата и подавляли образование изобутирата и изовалерата. Это может быть признаком замедленного процесса ферментации белка в кишечнике, что также указывает на снижение продуцирования вредных побочных продуктов.
На фигуре 6 показаны измеренные через 24 ч. инкубации в SIEM концентрации изобутирата и изовалерата в мМ в присутствии микробиоты толстой кишки, содержащей соответственно Bacillus subtilis DSM 32315 и Bacillus subtilis DSM 32540.
Пример 7. Присутствие Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314 и Bacillus amyloliquefaciens CECT 5940, соответственно, снижали содержание кластера Clostridium XI. Штаммы DSM 32315, DSM 32314 и CECT 5940, соответственно, увеличивали содержание кластера Clostridium XIVa
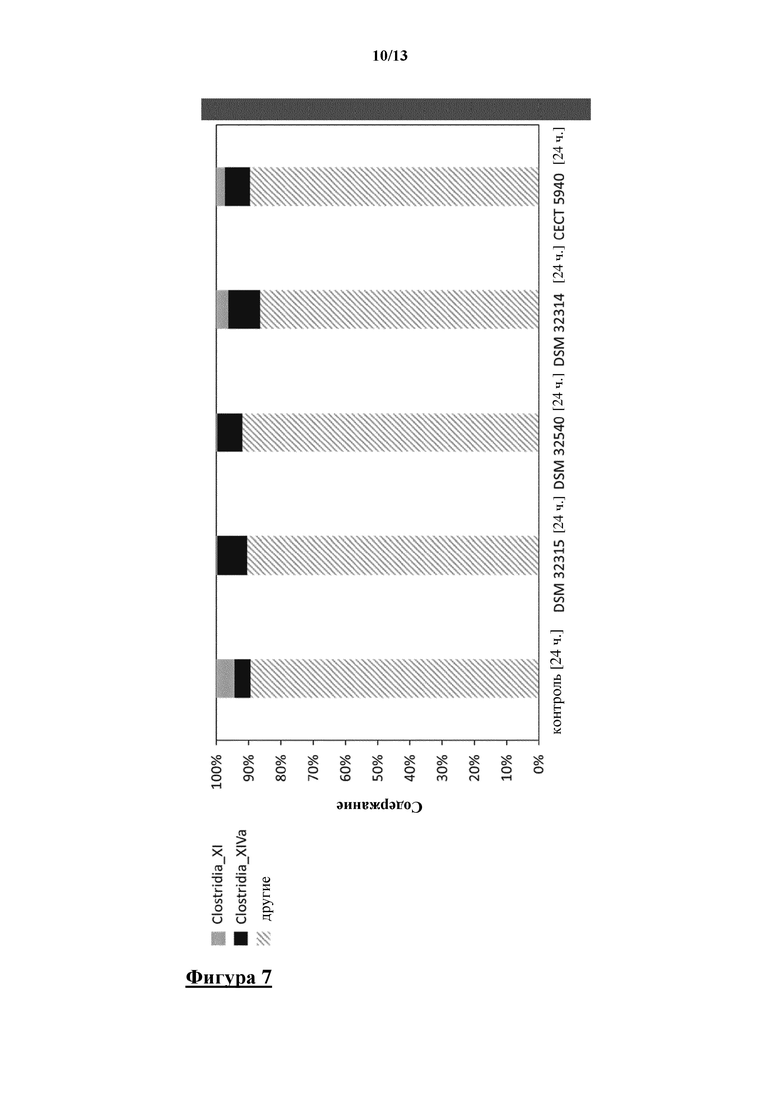
По сравнению с контролем в начальный момент времени 0 ч. (фигура 1) и развитием микробиоты через 24 ч. присутствие штаммов DSM 32315, DSM 32540, DSM 32314 и CECT 5940 снижало содержание кластера Clostridium XI с 6% до значений ниже 3% от всего микробного сообщества (фигура 7). Кластер Clostridium XIVa увеличивался через 24 ч. с 5% в контроле до значения, составляющего не более чем по меньшей мере 8% от всего сообщества в присутствии пробиотических клеток, соответственно. Инкубацию i-screen осуществляли при следующих газовых условиях: 0,2% O2, 0,2% CO2, 10% H2, 89,6% N2.
Таким образом, в присутствии этих пробиотических штаммов состав микробиоты человека смещается в сторону более здорового сообщества.
На фигуре 7 показана круговая гистограмма, показывающая образцы ферментации i-screen на уровне родов на основе секвенирования MiSeq гипервариабельной области V4 гена области, кодирующей 16S rRNA. Заштрихованные столбцы представляют выявленные роды Clostridium XI и Clostridium XIVa и их относительное содержание.
Пример 8. Добавление глутамина или его производных значительно изменяло микробное сообщество человека
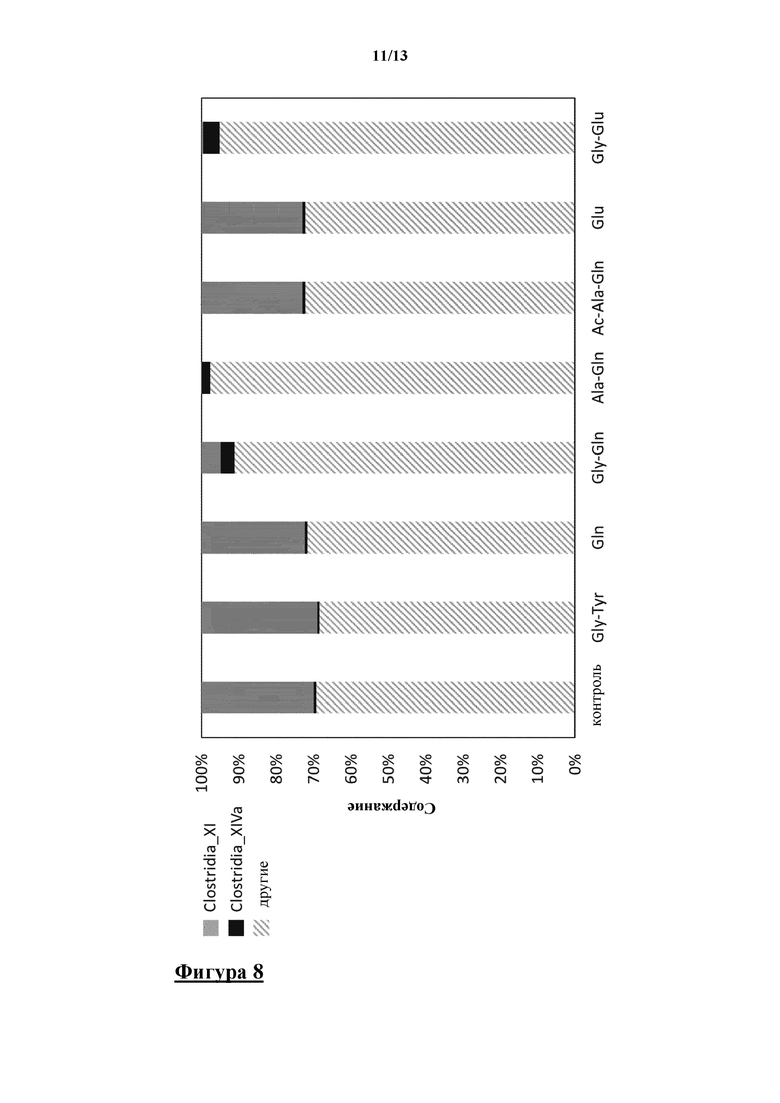
Присутствие дипептидов, содержащих глутамин или глутаминовую кислоту, влияло на микробное сообщество за счет перехода к устраненной группе Clostridium XI и увеличенной группе Clostridium XIVa (фигура 8). Отдельные аминокислоты добавляли до концентрации 3,5 мМ, а дипептиды до концентрации 7 мМ. Воздействие i-screen выполняли, как описано в примере 1, при следующих газовых условиях: 0% O2, 0.2% CO2, 10% H2, 90% N2. Более того, Ala-Gln и Gly-Glu почти полностью уменьшали группу Clostridia XI, что связано с сильными благоприятными эффектами в отношении состояния здоровья кишечника. В качестве контролей были протестированы дипептид Gly-Tyr, не содержащий глутамина или глутаминовой кислоты, а также отдельные аминокислоты глутамин (Gln) и глутамат (Glu), которые не оказывали положительного эффекта на микробное сообщество.
На фигуре 8 показана круговая гистограмма, показывающая образцы ферментации i-screen на уровне родов на основе секвенирования MiSeq гипервариабельной области V4 гена области, кодирующей 16S rRNA. Заштрихованные столбцы представляют выявленные роды Clostridium XI и Clostridium XIVa и их относительнуое содержание.
Пример 9. Комбинированное добавление Bacillus subtilis (DSM 32315), Bacillus licheniformis (DSM 32314) или Bacillus amyloliquefaciens (CECT 5940) с глутамином или его производными продемонстрировало синергетические эффекты в отношении изменения микробного сообщества и продуцирование ним короткоцепочечной кислоты по сравнению с отдельными компонентами
Эффект комбинации различных пробиотических штаммов, вместе с несколькими пептидами, содержащими глутамин и глутаминовую кислоту, был подробно проанализирован способом, описанным в примере 7. В качестве контроля проанализировали эффекты глутамина (Gln), глутаминовой кислоты (Glu) и дипептида, не содержащего Glu/не содержащего Gln, глицина-тирозина (Gly-Tyr) отдельно и в комбинации с пробиотическими штаммами. Отдельные аминокислоты добавляли до концентрации 3,5 мМ, а дипептиды до концентрации 7 мМ.
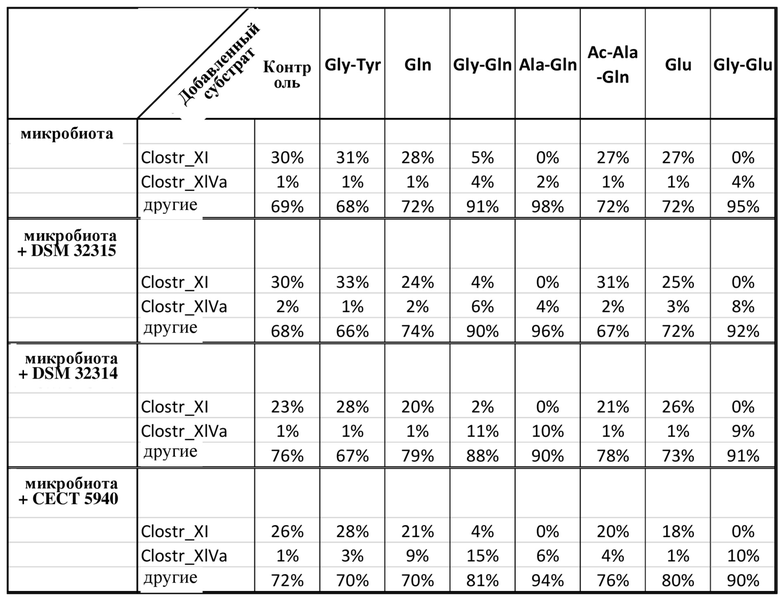
Состав микробиоты анализировали после 24 ч. инкубации. Наблюдались синергетические положительные эффекты нескольких комбинаций в отношении состава микробного сообщества, о чем свидетельствовало более сильное увеличение процента группы Clostridium XIVa и более сильное уменьшение группы Clostridium XI по сравнению с однократным добавлением аминокислоты или дипептида и пробиотических клеток. Этот синергетический эффект наблюдался в отношении комбинации B. subtilis (DSM 32315) с Ala-Gln, Gly-Glu и Gly-Gln, для B. licheniformis (DSM 32314) с Ala-Gln, Gly-Glu и Gly-Gln, а для B. amyloliquefaciens (CECT 5940) с Ala-Gln, Gln, Gly-Glu и Gly-Gln (таблица 1).
Таким образом, в присутствии этих пробиотических штаммов в сочетании с дипептидами, содержащими глутамин или глутаминовую кислоту, состав микробиоты человека смещался в сторону более здорового сообщества.
Таблица 1. Через 24 ч. инкубации микробиоты человека в SIEM с добавленными аминокислотами, дипептидами и/или пробиотическими клетками (B. subtilis DSM 32315, B. licheniformis DSM 32314 или B. amyloliquefaciens CECT 5940) были выявлены роды Clostridium XI (Clostr_XI), Clostridium XIVa (Clostr_XIVa) и другие, а также их относительное обилие.
Пример 10. Комбинированное добавление B. subtilis (DSM 32315), B. licheniformis (DSM 32314) или B. amyloliquefaciens (CECT 5940) с глутамином или дипептидами, содержащими глутамин или глутаминовую кислоту, продемонстрировало синергетические эффекты в отношении продуцирования н-бутирата микробным сообществом
Эффект комбинации различных пробиотических штаммов вместе с глутамином или дипептидами, содержащими глутамин или глутаминовую кислоту, в отношении продуцирования н-бутирата микробным сообществом анализировали для штамма B. subtilis (DSM 32315), как описано в примерах 1 и 5. Отдельные аминокислоты добавляли до концентрации 3,5 мМ, а дипептиды до концентрации 7 мМ.
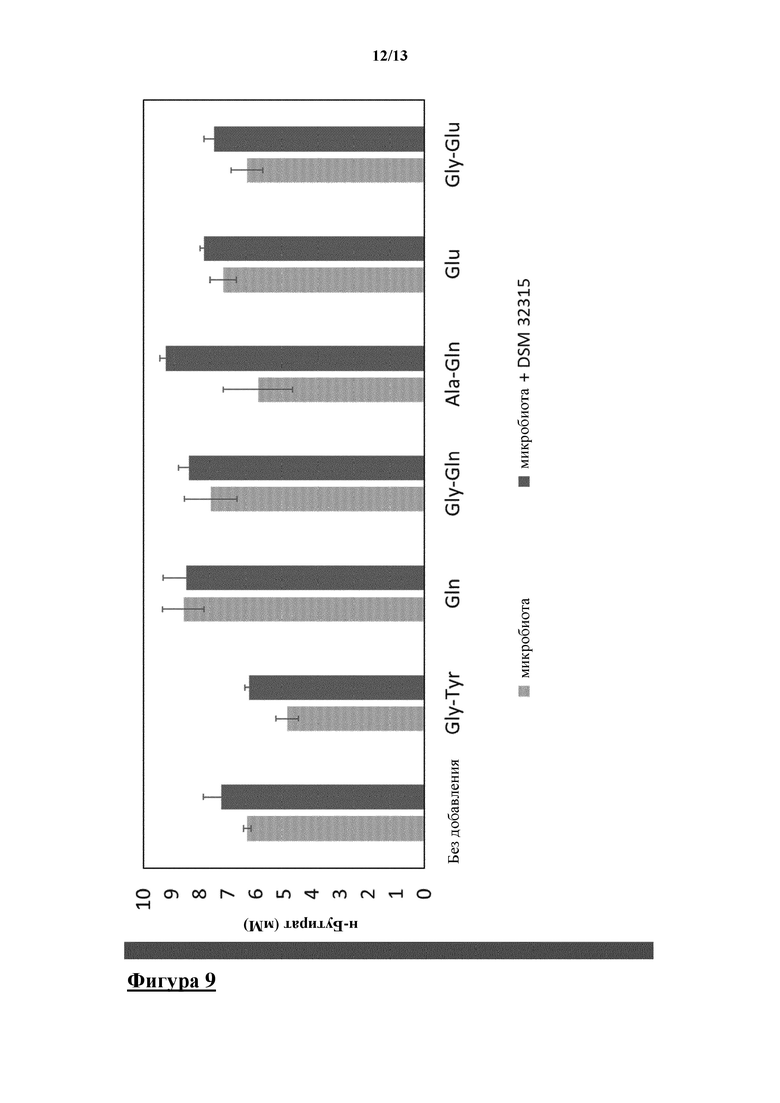
Содержание н-бутирата анализировали после 24 ч. инкубации. Синергетические положительные эффекты в отношении концентрации н-бутирата наблюдались для комбинаций B. subtilis (DSM 32315) с Gln, Gly-Gln, Ala-Gln, Glu или Gly-Glu (фигура 9). Это показывает, что этот пробиотический штамм в сочетании с глутамином, или глутаминовой кислотой, или глутаминсодержащими пептидами, оказывал ускоряющий эффект в отношении полезного продуцирования н-бутирата микробным сообществом. В качестве отрицательного контроля тестировали дипептид Gly-Tyr, не содержащий глутамина или глутаминовой кислоты, который не оказывал положительного эффекта в отношении продуцирования н-бутирата.
На фигуре 9 показаны измеренные концентрации н-бутирата в мМ после 24 ч. инкубации в SIEM с микробиотой человека в присутствии микробиоты толстой кишки, содержащей различные аминокислоты или дипептиды с комбинацией клеток B. subtilis DSM 32315 и без нее, соответственно.
Пример 11. Комбинированное добавление клеток B. licheniformis (DSM 32314) или B. amyloliquefaciens (CECT 5940) с глутамином, дипептидами, содержащими глутамин или глутаминовую кислоту, оказывало синергетические эффекты в отношении продуцирования н-бутирата микробным сообществом
Эффекты комбинации различных пробиотических штаммов вместе с глутамином или дипептидами, содержащими глутамин или глутаминовую кислоту, в отношении продуцирования н-бутирата микробным сообществом анализировали для штаммов B. licheniformis (DSM 32314) и B. amyloliquefaciens (CECT 5940), как описано в примерах 1, 5 и 10. Отдельные аминокислоты добавляли до концентрации 3,5 мМ, а дипептиды до концентрации 7 мМ.
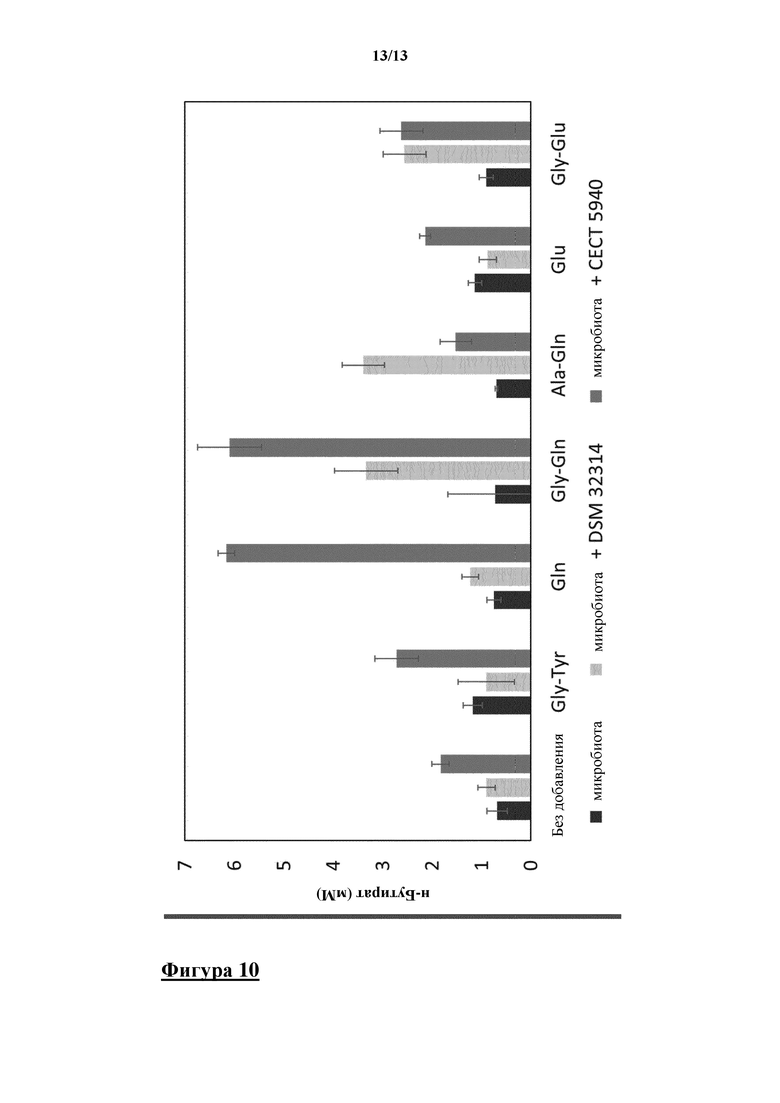
Содержание н-бутирата анализировали после 24 ч. инкубации. Синергетические положительные эффекты в отношении концентрации н-бутирата наблюдались для комбинаций B. licheniformis (DSM 32314) с Gly-Gln, Ala-Gln или Gly-Glu (фигура 10). А также для комбинаций B. amyloliquefaciens (CECT 5940) с Gln и Gly-Gln.
Это показывает, что этот пробиотический штамм в сочетании с глутамином, или глутаминовой кислотой, или глутаминсодержащими пептидами, оказывал ускоряющий эффект в отношении полезного продуцирования н-бутирата микробным сообществом. В качестве отрицательного контроля тестировали дипептид Gly-Tyr, не содержащий глутамина или глутаминовой кислоты, который не оказывал положительного эффекта в отношении продуцирования н-бутирата.
На фигуре 10 показаны измеренные концентрации н-бутирата в мМ после 24 ч. инкубации в SIEM с микробиотой человека в присутствии микробиоты толстой кишки, содержащей различные аминокислоты или дипептиды с комбинацией клеток соответственно B. licheniformis (DSM 32314) или B. amyloliquefaciens (CECT 5940) и без них.
Пример 12. Капсулы, содержащие Bacillus subtilis и дипептиды в качестве пребиотика
Следующие компоненты заполняли капсулы из HPMC (размер 3).
Таблица 2. Препараты для заполнения капсул HPMC
Капсулы могут дополнительно содержать дополнительные пребиотические ингредиенты, выбранные из инулинов, фруктоолигосахаридов (FOS), галактоолигосахаридов (GOS), крахмала, пектина, бета-глюканов и ксилоолигосахаридов.
Капсулы могут дополнительно содержать один или более растительных экстрактов, выбранных из брокколи, маслины, граната, черной смородины, черники, голубики, облепихи, каму-каму, бойзеновой ягоды, куркумы, имбиря, чеснока, виноградных косточек, ягоды асаи, черноплодной рябины, ягоды годжи, хрена, босвеллии пильчатой, спирулины, женьшеня обыкновенного, каннабидиола, шиповника, пуэра, сенча, эхинацеи и листьев зеленого чая.
Капсулы могут содержать дополнительные витамины, выбранные из витамина A, витамина B1 (тиамина), витамина B2 (рибофлавина), витамина B3 (ниацина), витамина B5 (пантотеновой кислоты), витамина B9 (фолиевой кислоты или фолата), витамина C (аскорбиновой кислоты), витамина D (кальциферолов), витамина E (токоферолов и токотриенолов) и витамина K (хинононов), или микроэлементы, выбранные из серы, железа, хлора, кальция, хрома, кобальта, меди, магния, марганца, молибдена, йода и селена.
Пример 13. Капсулы, содержащие Bacillus subtilis и дипептиды в качестве пребиотика и энтеросолюбильного покрытия
Капсулы, полученные в примере 12, были покрыты композицией энтеросолюбильного покрытия.
Таблица 3. Композиция для нанесения покрытия
[%]
[%]
[%]
Литературные источники
1. Hill C, Guarner F, Reid G, Gibson GR, Merenstein DJ, Pot B, Morelli L, Canani RB, Flint HJ, Salminen S et al: Expert consensus document. The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nat Rev Gastroenterol Hepatol 2014, 11(8): 506-514.
2. Collins MD, Lawson PA, Willems A, Cordoba JJ, Fernandez-Garayzabal J, Garcia P, Cai J, Hippe H, Farrow JA: The phylogeny of the genus Clostridium: proposal of five new genera and eleven new species combinations. Int J Syst Bacteriol 1994, 44(4): 812-826.
3. Hold GL, Pryde SE, Russell VJ, Furrie E, Flint HJ: Assessment of microbial diversity in human colonic samples by 16S rDNA sequence analysis. FEMS Microbiol Ecol 2002, 39(1): 33-39.
4. Koh JH, Choi SH, Park SW, Choi NJ, Kim Y, Kim SH: Synbiotic impact of tagatose on viability of Lactobacillus rhamnosus strain GG mediated by the phosphotransferase system (PTS). Food Microbiol 2013, 36(1): 7-13.
5. Pandey KR, Naik SR, Vakil BV: Probiotics, prebiotics and synbiotics- a review. J Food Sci Technol 2015, 52(12): 7577-7587.
6. Gibson GR, Hutkins R, Sanders ME, Prescott SL, Reimer RA, Salminen SJ, Scott K, Stanton C, Swanson KS, Cani PD et al: Expert consensus document: The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of prebiotics. Nat Rev Gastroenterol Hepatol 2017, 14(8): 491-502.
7. de Souza AZ, Zambom AZ, Abboud KY, Reis SK, Tannihao F, Guadagnini D, Saad MJ, Prada PO: Oral supplementation with L-glutamine alters gut microbiota of obese and overweight adults: A pilot study. Nutrition 2015, 31(6): 884-889.
8. Celasco G, Moro L, Aiello C, Mangano K, Milasi A, Quattrocchi C, R DIM: Calcium butyrate: Anti-inflammatory effect on experimental colitis in rats and antitumor properties. Biomed Rep 2014, 2(4): 559-563.
9. Riviere A, Selak M, Lantin D, Leroy F, De Vuyst L: Bifidobacteria and Butyrate-Producing Colon Bacteria: Importance and Strategies for Their Stimulation in the Human Gut. Front Microbiol 2016, 7: 979.
10. Vital M, Karch A, Pieper DH: Colonic Butyrate-Producing Communities in Humans: an Overview Using Omics Data. mSystems 2017, 2(6).
11. Gueimonde M, Sanchez B: Enhancing probiotic stability in industrial processes. Microb Ecol Health Dis 2012, 23.
12. Rios-Covian D, Ruas-Madiedo P, Margolles A, Gueimonde M, de Los Reyes-Gavilan CG, Salazar N: Intestinal Short Chain Fatty Acids and their Link with Diet and Human Health. Front Microbiol 2016, 7: 185.
13. Halmos T, Suba I: [Physiological patterns of intestinal microbiota. The role of dysbacteriosis in obesity, insulin resistance, diabetes and metabolic syndrome]. Orv Hetil 2016, 157(1): 13-22.
14. Lopetuso LR, Chowdhry S, Pizarro TT: Opposing Functions of Classic and Novel IL-1 Family Members in Gut Health and Disease. Front Immunol 2013, 4: 181.
15. Schlegel H: Allgemeine Mikrobiologie. Georg Thieme Verlag 1992.
16. Fox AD, Kripke SA, De Paula J, Berman JM, Settle RG, Rombeau JL: Effect of a glutamine-supplemented enteral diet on methotrexate-induced enterocolitis. JPEN J Parenter Enteral Nutr 1988, 12(4): 325-331.
17. Roth E, Karner J, Ollenschlager G, Karner J, Simmel A, Furst P, Funovics J: Alanylglutamine reduces muscle loss of alanine and glutamine in post-operative anaesthetized dogs. Clin Sci (Lond) 1988, 75(6): 641-648.
18. Guandalini S, Rubino A: Development of dipeptide transport in the intestinal mucosa of rabbits. Pediatr Res 1982, 16(2): 99-103.
19. Miller PM, Burston D, Brueton MJ, Matthews DM: Kinetics of uptake of L-leucine and glycylsarcosine into normal and protein malnourished young rat jejunum. Pediatr Res 1984, 18(6): 504-508.
20. Vazquez JA, Morse EL, Adibi SA: Effect of starvation on amino acid and peptide transport and peptide hydrolysis in humans. Am J Physiol 1985, 249(5 Pt 1): G563-566.
21. Ladirat SE, Schols HA, Nauta A, Schoterman MH, Keijser BJ, Montijn RC, Gruppen H, Schuren FH: High-throughput analysis of the impact of antibiotics on the human intestinal microbiota composition. J Microbiol Methods 2013, 92(3): 387-397.
22. Minekus M, Smeets-Peeters M, Bernalier A, Marol-Bonnin S, Havenaar R, Marteau P, Alric M, Fonty G, Huis in't Veld JH: A computer-controlled system to simulate conditions of the large intestine with peristaltic mixing, water absorption and absorption of fermentation products. Appl Microbiol Biotechnol 1999, 53(1): 108-114.
23. Scholz R, Molohon KJ, Nachtigall J, Vater J, Markley AL, Sussmuth RD, Mitchell DA, Borriss R: Plantazolicin, a novel microcin B17/streptolysin S-like natural product from Bacillus amyloliquefaciens FZB42. J Bacteriol 2011, 193(1): 215-224.
24. Kozich JJ, Westcott SL, Baxter NT, Highlander SK, Schloss PD: Development of a dual-index sequencing strategy and curation pipeline for analyzing amplicon sequence data on the MiSeq Illumina sequencing platform. Appl Environ Microbiol 2013, 79(17): 5112-5120.
25. Caporaso JG, Lauber CL, Costello EK, Berg-Lyons D, Gonzalez A, Stombaugh J, Knights D, Gajer P, Ravel J, Fierer N et al: Moving pictures of the human microbiome. Genome Biol 2011, 12(5): R50.
26. Schloss PD, Westcott SL, Ryabin T, Hall JR, Hartmann M, Hollister EB, Lesniewski RA, Oakley BB, Parks DH, Robinson CJ et al: Introducing mothur: open-source, platform-independent, community-supported software for describing and comparing microbial communities. Appl Environ Microbiol 2009, 75(23): 7537-7541.
27. Kong Y: Btrim: a fast, lightweight adapter and quality trimming program for next-generation sequencing technologies. Genomics 2011, 98(2): 152-153.
28. Edgar RC, Haas BJ, Clemente JC, Quince C, Knight R: UCHIME improves sensitivity and speed of chimera detection. Bioinformatics 2011, 27(16): 2194-2200.
29. Wang Q, Garrity GM, Tiedje JM, Cole JR: Naive Bayesian classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy. Appl Environ Microbiol 2007, 73(16): 5261-5267.
30. Eren AM, Maignien L, Sul WJ, Murphy LG, Grim SL, Morrison HG, Sogin ML: Oligotyping: Differentiating between closely related microbial taxa using 16S rRNA gene data. Methods Ecol Evol 2013, 4(12).
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Эвоник Текнокеми ГмбХ
<120> СИНБИОТИЧЕСКИЕ КОМПОЗИЦИИ
<130> Файл: 201800108
<210> 1
<211> 19
<212> ДНК, прямой праймер
<213> бактериальный ген 16S rRNA
<400> 1
cgaaagcgtg gggagcaaa
<210> 2
<211> 19
<212> ДНК, обратный праймер
<213> бактериальный ген 16S rRNA
<400> 2
gttcgtactc cccaggcgg
<210> 3
<211> 21
<212> ДНК, зонд ПЦР
<213> бактериальный ген 16S rRNA
<400> 3
attagatacc ctggtagtcc a
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ФЕРМЕНТАЦИОННЫЕ БУЛЬОНЫ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2810249C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ БАКТЕРИИ, ПРОДУЦИРУЮЩИЕ БАЦИЛЛЕН, ИЛИ ЕГО ПРЕПАРАТЫ | 2020 |
|
RU2804144C2 |
| Функциональная вода с пробиотиками | 2019 |
|
RU2775077C1 |
| КОМПОНЕНТЫ НА ОСНОВЕ МИКРООРГАНИЗМА РОДА BACILLUS ДЛЯ ИНГИБИРОВАНИЯ ИЛИ ЗАМЕДЛЕНИЯ РОСТА ENTEROCOCCUS SPP. У ЖИВОТНЫХ | 2017 |
|
RU2789148C2 |
| КОМПОЗИЦИЯ ПАЛОЧКОВИДНЫХ БАКТЕРИЙ, УСТОЙЧИВЫХ К ЖЕЛЧИ И СЕКРЕТИРУЮЩИХ ВЫСОКИЕ УРОВНИ НЕЗАМЕНИМЫХ АМИНОКИСЛОТ | 2009 |
|
RU2564127C2 |
| КОМПОЗИЦИЯ КОРМОВОЙ ДОБАВКИ | 2016 |
|
RU2754276C2 |
| МЕТАБИОТИЧЕСКАЯ КОМПОЗИЦИЯ С СОРБИРУЮЩИМИ СВОЙСТВАМИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2023 |
|
RU2833932C2 |
| Композиция с использованием метаболитов Bacillus subtilis для лечения заболеваний мочевыводящих путей | 2022 |
|
RU2840322C2 |
| МЕТАБИОТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ LACTOBACILLUS REUTERI И BACILLUS SUBTILIS | 2023 |
|
RU2835358C2 |
| Кормовая добавка с пробиотической активностью для рыб | 2022 |
|
RU2802073C1 |
Группа изобретений относится к области фармацевтики и пищевой промышленности. Предложен синбиотический препарат, содержащий по меньшей мере один пробиотический штамм, выбранный из Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314, Bacillus amyloliquefaciens CECT 5940, и по меньшей мере одну аминокислоту, выбранную из глутамина, глутаминовой кислоты или ее солей, конъюгированного глутамина или олигопептидов длиной 2-10 аминокислотных структурных единиц, при этом указанные аминокислотные структурные единицы представляют собой природные аминокислоты, и по меньшей мере одна аминокислотная структурная единица является единицей, представляющей собой глутамин или глутаминовую кислоту, причем общее количество пробиотического штамма и аминокислоты или олигопептида составляет по меньшей мере 40 вес.%. Также предложены применение синбиотического препарата в качестве кормовой или пищевой добавки, в качестве синбиотического ингредиента в кормовых или пищевых продуктах, кормовая или пищевая композиция, содержащая указанный препарат, фармацевтическая композиция, содержащая указанный препарат, применение этой фармацевтической композиции в предупреждении или лечении различных заболеваний, капсула с синбиотическим препаратом. Предложенный синбиотический препарат способствует выработке таксонов, продуцирующих н-бутират, и повышению уровня н-бутирата в кишечнике. 7 н. и 11 з.п. ф-лы, 10 ил., 3 табл., 13 пр.
1. Синбиотический препарат, содержащий
- по меньшей мере один пробиотический штамм, выбранный из Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314, Bacillus amyloliquefaciens CECT 5940, и
- по меньшей мере одну аминокислоту, выбранную из глутамина, глутаминовой кислоты или ее солей, конъюгированного глутамина или олигопептидов длиной 2-10 аминокислотных структурных единиц, при этом указанные аминокислотные структурные единицы представляют собой природные аминокислоты, и по меньшей мере одна аминокислотная структурная единица является единицей, представляющей собой глутамин или глутаминовую кислоту;
при этом общее количество пробиотического штамма и аминокислоты или олигопептида составляет по меньшей мере 40 вес.%.
2. Препарат по п. 1, где олигопептид дополнительно содержит аланин или глицин.
3. Препарат по любому из предыдущих пунктов, где олигопептид представляет собой дипептид, выбранный из глицин-глутамина, глицин-глутаминовой кислоты, аланин-глутамина, аланин-глутаминовой кислоты и их ацетилированных форм.
4. Препарат по любому из предыдущих пунктов, где общее количество пробиотического штамма и аминокислоты или олигопептида составляет по меньшей мере 50 вес.%, более предпочтительно по меньшей мере 60 вес.%, наиболее предпочтительно по меньшей мере 70 вес.% от общего веса препарата.
5. Препарат по любому из предыдущих пунктов, где препарат содержит энтеросолюбильное покрытие, где энтеросолюбильное покрытие содержит одно или более из следующего: сополимеров метилакрилата и метакриловой кислоты, фталата ацетата целлюлозы (САР), сукцината ацетата целлюлозы, фталата гидроксипропилметилцеллюлозы, сукцината ацетата гидроксипропилметилцеллюлозы (сукцината ацетата гипромеллозы), поливинилацетатфталата (PVAP), сополимеров метилметакрилата и метакриловой кислоты, шеллака, тримеллитата ацетата целлюлозы, альгината натрия, зеина.
6. Применение препарата по любому из предыдущих пунктов в качестве кормовой или пищевой добавки.
7. Применение препарата по любому из пп. 1-5 в качестве синбиотического ингредиента в кормовых или пищевых продуктах.
8. Кормовая или пищевая композиция, содержащая препарат по любому из пп. 1-5 и по меньшей мере один дополнительный кормовой или пищевой ингредиент, предпочтительно выбранный из белков, углеводов, жиров, дополнительных пробиотиков, пребиотиков, ферментов, витаминов, иммуномодуляторов, заменителей молока, микроэлементов, аминокислот, кокцидиостатиков, продуктов на основе кислот, лекарственных средств и их комбинаций.
9. Фармацевтическая композиция, содержащая препарат по любому из пп. 1-5 и фармацевтически приемлемый носитель.
10. Применение композиции по п. 8 или 9 в предупреждении или лечении диареи, запора, синдрома раздраженного кишечника, болезни Крона, язвенного колита, колоректального рака, рака кишечника, сердечно-сосудистого заболевания, артериосклероза, жировой болезни печени, гиперлипидемии, гиперхолестеринемии, ожирения, адипоза, диабета 2 типа, метаболического синдрома, хронических воспалительных заболеваний и аллергических заболеваний.
11. Капсула с синбиотическим препаратом, содержащая по меньшей мере один пробиотический штамм, выбранный из Bacillus subtilis DSM 32315, Bacillus subtilis DSM 32540, Bacillus licheniformis DSM 32314, Bacillus amyloliquefaciens CECT 5940, и по меньшей мере один дипептид, выбранный из глицин-глутамина, глицин-глутаминовой кислоты, аланин-глутамина, аланин-глутаминовой кислоты и их ацетилированных форм.
12. Капсула по п. 11, где капсула содержит от 1×108 до 2×1010 КОЕ пробиотического штамма и от 50 до 800 мг дипептида.
13. Капсула по п. 11 или 12, где количество пробиотического штамма и дипептида составляет по меньшей мере 40 вес.%, предпочтительно по меньшей мере 50 вес.%, более предпочтительно по меньшей мере 60 вес.%, наиболее предпочтительно по меньшей мере 70 вес.% от общего веса содержимого капсулы.
14. Капсула по п. 11 или 13, дополнительно содержащая один или более витаминов, выбранных из витамина А (в виде полностью транс-ретинола, полностью транс-ретиноловых сложных эфиров, а также полностью транс-бета-каротина и других каротиноидов провитамина А), витамина В1 (тиамина), витамина В2 (рибофлавина), витамина В3 (ниацина), витамина В5 (пантотеновой кислоты), витамина В6 (пиридоксина), витамина В7 (биотина), витамина В9 (фолиевой кислоты или фолата), витамина В12 (кобаламинов), витамина С (аскорбиновой кислоты), витамина D (кальциферолов), витамина Е (токоферолов и токотриенолов) и витамина K (хинонов).
15. Капсула по любому из пп. 11-14, дополнительно содержащая один или более микроэлементов, выбранных из серы, железа, хлора, кальция, хрома, кобальта, меди, цинка, магния, марганца, молибдена, йода и селена.
16. Капсула по любому из пп. 11-15, дополнительно содержащая один или более пребиотиков, выбранных из инулинов, фруктоолигосахаридов (FOS), галактоолигосахаридов (GOS), крахмала, пектина, бета-глюканов и ксилоолигосахаридов.
17. Капсула по любому из пп. 11-16, дополнительно содержащая один или более растительных экстрактов, где растения предпочтительно выбраны из брокколи, маслин, граната, черной смородины, черники, голубики, облепихи, каму-каму, бойзеновой ягоды, куркумы, имбиря, чеснока, виноградных косточек, ягоды асаи, черноплодной рябины, ягоды годжи, хрена, босвеллии пильчатой, спирулины, женьшеня обыкновенного, каннабидиола, шиповника, пуэра, сенча, эхинацеи и листьев зеленого чая.
18. Капсула по любому из пп. 11-17, где капсула содержит энтеросолюбильное покрытие, где энтеросолюбильное покрытие содержит одно или более из следующего: сополимеров метилакрилата и метакриловой кислоты, фталата ацетата целлюлозы (САР), сукцината ацетата целлюлозы, фталата гидроксипропилметилцеллюлозы, сукцината ацетата гидроксипропилметилцеллюлозы (сукцината ацетата гипромеллозы), поливинилацетатфталата (PVAP), сополимеров метилметакрилата и метакриловой кислоты, шеллака, тримеллитата ацетата целлюлозы, альгината натрия, зеина.
| US 20180042972 A1, 15.02.2018 | |||
| WO 2017207371 A1, 07.12.2017 | |||
| WO 2017207372 A1, 07.12.2017 | |||
| US 20140220662 A1, 07.08.2014 | |||
| WO 2014020226 A1, 06.02.2014 | |||
| US 20150017144 A1, 15.01.2015 | |||
| Y.XIE ET AL | |||
| Optimization of Glutamine Peptide Production from Soybean Meal and Analysis of Molecular Weight Distribution of Hydrolysates | |||
| Int | |||
| J | |||
| Mol | |||
| Sci | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
Авторы
Даты
2023-07-05—Публикация
2019-04-18—Подача