ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТИ, ПРЕДСТАВЛЕННЫЙ В ЭЛЕКТРОННОМ ВИДЕ
[0001] Содержимое представленного в электронном виде перечня последовательностей в текстовом файле ASCII (имя: 4268.014PC01_SequenceListing_ST25.txt; размер: 8737 байт; и дата создания: 29 марта 2019 г. ), поданном вместе с заявкой, полностью включено в данный документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к бактериальным композициям, которые могут модулировать уровень желчных кислот при введении субъекту. Такие бактериальные композиции применимы для лечения и/или предотвращение осложнений и побочных эффектов, ассоциированных с воспалительными заболеваниями кишечника.
УРОВЕНЬ ТЕХНИКИ
[0003] Воспалительное заболевание кишечника (ВЗК) - это хроническое заболевание желудочно-кишечного тракта, характеризующееся воспалением кишечника или толстой кишки. Симптомы ВЗК могут быть разными, но обычно включают спазмы в животе, персистирующую диарею и колоректальное кровотечение. ВЗК может быть изнурительным и иметь опасные для жизни осложнения в случае отсутствия лечения.
[0004] Язвенный колит и болезнь Крона представляют собой две основные формы ВЗК. Хотя оба являются расстройствами, вызывающими воспаление пищеварительного тракта, они отличаются по своей природе и локализации воспалительных реакций в желудочно-кишечном тракте (ЖКТ). Язвенный колит поражает только толстую кишку и анус, а вызванное им воспаление поражает только слизистую оболочку. Напротив, болезнь Крона может поражать весь желудочно-кишечный тракт, то есть от рта до ануса, хотя обычно поражает нижнюю часть тонкой кишки (подвздошную кишку).
[0005] Известных способов лечения ВЗК нет. Текущие варианты лечения включают лекарственные препараты (например, противовоспалительные средства, иммунодепрессанты и антибиотики), пищевые добавки и хирургическое вмешательство. Хотя такие методы лечения могут уменьшить признаки и симптомы заболевания, они, как правило, имеют ограниченную эффективность и/или нежелательные побочные эффекты. См., например, Martinez-Montiel М.Р., et al., Clin Exp Gastroenterol 8:257-269 (2015); Cunliffe R.N., et al., Aliment Pharmacol Ther 16(4):647-662 (2002). Более того, несмотря на доступные варианты лечения, ВЗК остается серьезной медицинской проблемой, поскольку как частота, так и распространенность ВЗК возрастают во всем мире. M'Koma, А.Е., Clin Med Insights Gastroenterol 6: 33-47 (2013). Соответственно, существует острая потребность в новых вариантах лечения ВЗК, которые были бы более безопасными и эффективными.
[0006] Желчные кислоты вместе с холестерином, фосфолипидами и билирубином составляют основные компоненты желчи. Они синтезируются из холестерина в печени и секретируются гепатоцитами в желчные каналы, а затем сохраняются в желчном пузыре. После приема пищи желчь попадает в двенадцатиперстную кишку, где она способствует солюбилизации и перевариванию жирорастворимых питательных веществ. Thomas et al., Nat Rev Drug Discov 7(8): 678-693 (2008). Соответственно, желчные кислоты традиционно считаются важными для солюбилизации холестерина в ЖКТ и для стимуляции абсорбции холестерина, жирорастворимых витаминов и липидов в кишечнике. Hylemon Р.В., et al., J Lipid Res 50(8): 1509-1520 (2009).
[0007] Совсем недавно было описано, что желчные кислоты играют важную роль во многих других биологических процессах. Например, теперь известно, что желчные кислоты действуют, по меньшей мере частично, через сопряженные с G-белком рецепторы (GPCR) (например, TGR5), и рецепторы ядерных гормонов (например, фарнезоидный Х-рецептор, прегнан Х-рецептор и рецептор витамина D) и опосредуют не только свой собственный биосинтез, но также опосредуют метаболизм других молекул липидов (например, холестерина и триглицерида) и глюкозы. Thomas et al., Nat Rev Drug Discov 7(8): 678-693 (2008). Также было описано, что желчные кислоты играют роль в модуляции как врожденного, так и адаптивного иммунитета. Zhu С., et al., Clin Exp Rheumatol 34: 25-31 (2016). Следовательно, биологические агенты, которые могут модулировать уровни желчных кислот, могут быть применимыми вариантами лечения ВЗК.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008] Данное описание относится к композиции, содержащей очищенную популяцию бактерий, при этом очищенная популяция бактерий содержит Flavonifractor_SC49, Clostridium leptum или их комбинации, и при этом композиция может модулировать уровень вторичной желчной кислоты при введении субъекту. В некоторых вариантах осуществления очищенная популяция бактерий содержит Flavonifractor_SC49. В других вариантах осуществления очищенная популяция бактерий содержит Clostridium leptum. В дополнительных вариантах осуществления очищенная популяция бактерий содержит как Flavonifractor_SC49, так и Clostridium leptum.
[0009] В некоторых вариантах осуществления Flavonifractor_SC49 содержит последовательность 16S рДНК, которая по меньшей мере на 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере на 98%, по меньшей мере 99% или на 100% идентична последовательности 16S рДНК эталонной ОТЕ Flavonifractor_SC49 (SEQ ID NO: 1, 3 или 4).
[0010] В некоторых вариантах осуществления Clostridium leptum содержит последовательность 16S рДНК, которая по меньшей мере на 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере на 98%, по меньшей мере 99% или на 100% идентична последовательности 16S рДНК эталонной ОТЕ Clostridium leptum (SEQ ID NO: 2).
[0011] В некоторых вариантах осуществления вторичная желчная кислота включает дезоксихолевую кислоту (ДХК), 3α-12-оксодезоксихолевую кислоту, 3β-12α-дезоксихолевую кислоту (3-изодезоксихолевую кислоту), 7α-3-оксохенодезоксихолевую кислоту, литохолевую кислоту (ЛХК), 3-оксо-ЛХК или их комбинации.
[0012] В некоторых вариантах осуществления вторичная желчная кислота включает урсодезоксихолевую кислоту (УДХК).
[0013] В данном документе также предложен способ модуляции уровня вторичной желчной кислоты у нуждающегося в этом субъекта, включающий введение субъекту эффективного количества композиции, описанной в настоящем документе. В данном документе также предложен способ облегчения одного или более признаков или симптомов воспалительного заболевания кишечника (ВЗК) или поддержания ремиссии ВЗК у нуждающегося в этом субъекта, включающий введение субъекту эффективного количества композиции, описанной в данном документе.
[0014] В некоторых вариантах осуществления вторичная желчная кислота включает дезоксихолевую кислоту (ДХК), 3α-12-оксодезоксихолевую кислоту, 3β-12α-дезоксихолевую кислоту (3-изодезоксихолевую кислоту), 7α-3-оксохенодезоксихолевую кислоту, литохолевую кислоту (ЛХК), 3-оксо-ЛХК или их комбинации. В некоторых вариантах осуществления введение композиции, описанной в данном документе, повышает уровень вторичной желчной кислоты у субъекта. В некоторых вариантах осуществления уровень вторичной желчной кислоты повышается по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере 90% у субъекта по сравнению с эталоном (например, соответствующим уровнем у субъекта, который не получал композицию). В некоторых вариантах осуществления повышение уровня вторичной желчной кислоты ассоциируется с ремиссией ВЗК. В некоторых вариантах осуществления вторичная желчная кислота может снижать выработку ФНО-α и/или повышать выработку ИЛ-10 в моноцитах, стимулированных липополисахаридами (ЛИС) in vitro. В дополнительных вариантах осуществления вторичная желчная кислота может снижать выработку ФНО-α и/или повышать выработку ИЛ-10 в ЛПС-стимулированных мононуклеарных клетках периферической крови (МКПК) in vitro. В некоторых вариантах осуществления вторичная желчная кислота может снижать выработку ИЛ-8 в ФНОα-стимулированных эпителиальных клетках кишечника in vitro.
[0015] В некоторых вариантах осуществления вторичная желчная кислота включает урсодезоксихолевую кислоту (УДХК). В некоторых вариантах осуществления введение снижает уровень УДХК у субъекта. В некоторых вариантах осуществления уровень УДХК снижен по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90% у субъекта по сравнению с эталоном (например, соответствующим уровнем у субъекта, который не получал композицию). В некоторых вариантах осуществления снижение уровня УДХК ассоциировано с ремиссией ВЗК.
[0016] В некоторых вариантах осуществления ВЗК представляет собой язвенный колит или болезнь Крона.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0017] На ФИГ. 1 показано сравнение относительных концентраций (измеренных в мкг/г образца кала, сухой вес) вторичных желчных кислот, ассоциированных с путем 7α-дегидроксилазы (т.е., ДХК, ЛХК, 3-оксо-ЛХК, 3α 12-оксодезоксихолевой кислоты и 3β 12α-дезоксихолевой кислоты), измеренных в образцах кала, полученных от разных групп пациентов с язвенным колитом. Пациенты с язвенным колитом получали одну из следующих схем: (А) только плацебо; (В) плацебо с последующим еженедельным дозированием популяции спор, полученных из фекалий здорового человека («ПСЗЧ»); (С) ванкомицин с последующим еженедельным введением ПСЗЧ; и (D) ванкомицин с последующим ежедневным дозированием ПСЗЧ. Концентрации желчных кислот измеряли в четырех различных временных точках: (1) исходный уровень (т.е. до введения ванкомицина или ПСЗЧ) («Визит 1»); (2) сразу после лечения ванкомицином (при необходимости) («Визит 4»); (3) через 2 недели после начала введения ПСЗЧ (при необходимости) («Визит 6»); и (4) через 8 недель после начала введения спорообразующей фракции (при необходимости) («Визит 12»). Концентрации, показанные на Визитах 4, 6 и 12, относятся к концентрациям общих желчных кислот, измеренным на исходном уровне.
[0018] На ФИГ. 2A-2G показано сравнение концентрации (измеренной в мкг/г образца кала, сухой вес) различных желчных кислот, измеренных в образцах кала пациентов с язвенным колитом, которые находятся в стадии ремиссии (т.е. пациенты с ремиссией, светло-серый) или пациентов, у которых не наблюдается ремиссии (т.е. пациенты без ремиссии, темно-серый). Показанные пациенты получали одну из схем, описанных на ФИГ. 1. Концентрации желчных кислот измеряли в четырех разных временных точках, как описано на ФИГ. 1. На ФИГ. 2А показана концентрация дезоксихолевой кислоты (ДХК). На ФИГ. 2 В показана концентрация литохолевой кислоты (ЛХК). На ФИГ. 2С показана концентрация 3α-12-оксо-ДХК (12-оксо-3α). ФИГ. 2D показана концентрация 7α-3-оксо-СДХК (3-оксо-7α). ФИГ. 2Е показана концентрация 3-оксо-ЛХК. ФИГ. 2F показана концентрация 3β-12α-ДХК (3β-12α). На ФИГ. 2G показана концентрация урсодезоксихолевой кислоты (УДХК).
[0019] На ФИГ. 3A-3G показано сравнение концентрации (измеренной в мкг/г образца кала, сухой вес) различных желчных кислот, измеренных в образцах кала пациентов с язвенным колитом, получавших ванкомицин, с последующим ежедневным дозированием популяции спор, полученных из фекалий здорового человека (ПСЗЧ). Концентрации желчных кислот измеряли в четырех разных временных точках, как описано на ФИГ. 1. Для каждой временной точки пациенты с язвенным колитом были разделены на две группы: (i) в стадии ремиссии (т.е. пациенты с ремиссией, светло-серый) или (ii) пациентов, у которых не наблюдается ремиссии (т.е. пациенты без ремиссии, темно-серый). На ФИГ. 3А показана концентрация дезоксихолевой кислоты (ДХК). На ФИГ. 3 В показана концентрация литохолевой кислоты (ЛХК). На ФИГ. 3С показана концентрация 3α-12-оксо-ДХК (12-оксо 3α). ФИГ. 3D показана концентрация 7α-3-оксо-СДХК (3-оксо-7α). ФИГ. 3Е показана концентрация 3-оксо-ЛХК. ФИГ. 3F показана концентрация 3β-12α-ДХК (3β-12α). На ФИГ. 3G показана концентрация урсодезоксихолевой кислоты (УДХК).
[0020] На Фиг. 4А и 4В показано влияние различных желчных кислот на выработку ФНО-α (ФИГ. 4А) и ИЛ-10 (ФИГ. 4В) в ЛПС-стимулированных мононуклеарных клетках периферической крови (МКПК) in vitro. Показанные желчные кислоты включают: (i) конъюгированные первичные желчные кислоты (конъюг. 1°) - таурохолевую кислоту (тХК), гликохолевую кислоту (гХК), таурохенодезоксихолевую кислоту (тХДХК) и гликоль-хенодезоксихолевую кислоту (гХДХК); (ii) первичные желчные кислоты (1°) - холевую кислоту (ХК) и хенодезоксихолевую кислоту (ХДХК); (iii) вторичные желчные кислоты (2°) - дезоксихолевую кислоту (ДХК) и литохолевую кислоту (ЛХК); (iv) изо-желчные кислоты (изо-ЖК) - урсодезоксихолевую кислоту (УДХК); и (v) конъюгированные вторичные желчные кислоты (конъюг. 2°) - тауродезоксихолевую кислоту (тДХК), гликодезоксихолевую кислоту (гДХК) и тауросульфолитохолевую кислоту (тЛХК). Для каждой желчной кислоты показанные столбцы соответствуют концентрации использованной желчной кислоты (т.е. 0, 12,5, 25 и 50 мкМ) с повышением концентрации слева направо. Звездочка указывает на возможную токсичность при данной концентрации желчной кислоты.
[0021] На ФИГ. 5А и 5В показано влияние различных желчных кислот на выработку ФНО-α (ФИГ. 5А) и ИЛ-10 (ФИГ. 5 В) в ЛПС-стимулированных моноцитах in vitro. Показанные желчные кислоты включают: (i) конъюгированные первичные желчные кислоты (конъюг. 1°) - таурохолевую кислоту (тХК), гликохолевую кислоту (гХК), таурохенодезоксихолевую кислоту (тХДХК) и гликоль-хенодезоксихолевую кислоту (гХДХК); (ii) первичные желчные кислоты (1°) - холевую кислоту (ХК) и хенодезоксихолевую кислоту (ХДХК); (iii) вторичные желчные кислоты (2°) - дезоксихолевую кислоту (ДХК) и литохолевую кислоту (ЛХК); (iv) конъюгированные вторичные желчные кислоты (конъюг. 2°) - тауродезоксихолевую кислоту (тДХК), гликодезоксихолевую кислоту (гДХК) и тауросульфолитохолевую кислоту (тЛХК). Для каждой желчной кислоты показанные столбцы соответствуют концентрации использованной желчной кислоты (т.е. 0, 12,5, 25 и 50 мкМ) с повышением концентрации слева направо.
[0022] На ФИГ. 6 показано влияние различных желчных кислот на выработку ИЛ-8 в ФНО-α-стимулированных эпителиальных клетках кишечника («ЭКК»). Показанные желчные кислоты включают: (i) конъюгированные первичные желчные кислоты (конъюг. 1°) - таурохолевую кислоту (тХК), гликохолевую кислоту (гХК), таурохенодезоксихолевую кислоту (тХДХК) и гликоль-хенодезоксихолевую кислоту (гХДХК); (ii) первичные желчные кислоты (1°) - холевую кислоту (ХК) и хенодезоксихолевую кислоту (ХДХК); (iii) вторичные желчные кислоты (2°) - дезоксихолевую кислоту (ДХК) и литохолевую кислоту (ЛХК); (iv) изо-желчные кислоты (изо-ЖК) - урсодезоксихолевую кислоту (УДХК); и (v) конъюгированные вторичные желчные кислоты (конъюг. 2°) - тауродезоксихолевую кислоту (тДХК), гликодезоксихолевую кислоту (гДХК) и тауросульфолитохолевую кислоту (тЛХК). Для каждой желчной кислоты показанные столбцы соответствуют концентрации использованной желчной кислоты (т.е. 62,5, 125 и 250 мкМ) с повышением концентрации слева направо. Количество ИЛ-8, вырабатываемого в присутствии различных желчных кислот, показано относительно контроля без желчных кислот. Звездочка указывает на возможную токсичность при данной концентрации желчной кислоты.
[0023] На ФИГ. 7 представлено сравнение общего содержания некоторых вторичных желчных кислот (т.е. тех, которые ассоциированы с путем 7α-дегидроксилазы - ДХК, ЛХК, 3-оксо-ЛХК, 3α, 12-оксо-дезоксихолевой кислоты и 3β-12-α-дезоксихолевой кислоты), измеренное в образцах кала от разных пациентов с язвенным колитом, на наличие или отсутствие видов, включающих Flavonifractor_SC49 и/или Clostridium leptum. Перед измерением вторичных желчных кислот пациенты с язвенным колитом получали одну из схем, описанных на ФИГ. 1. Образцы пациентов были разделены в зависимости от наличия Flavonifractor_SC49 и Clostridium leptum: (i) ни одного («1»); (ii) только Flavonifractor_SC49 («2»); (iii) только Clostridium leptum («3»); или (iv) оба («4»).
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0024] Для того, чтобы настоящее описание было более понятным, сначала определены некоторые термины. Дополнительные определения приведены в подробном описании.
[0025] Следует отметить, что термины в форме единственного числа включают ссылки на одно или более; например, «нуклеотидная последовательность» означает одну или более нуклеотидных последовательностей. Следовательно, термины в форме единственного числа, а также выражения «один или более» и «по меньшей мере один» могут использоваться в данном документе взаимозаменяемо.
[0026] Кроме того, в данном контексте «и/или» следует рассматривать как конкретное описание каждого из двух указанных признаков или компонентов с другим или без него. Таким образом, термин «и/или», используемый в такой фразе, как «А и/или В», предназначен для включения «А и В», «А или В»; «А» (отдельно) и «В» (отдельно). Аналогично, термин «и/или», используемый в такой фразе, как «А, В и/или С», предназначен для охвата каждого из следующих аспектов: А, В и С; А, В или С; А или С; А или В; В или С; А и С; А и В; В и С; А (отдельно); В (отдельно); и С (отдельно).
[0027] Следует понимать, что в тех случаях, когда аспекты описаны в данном документе с формулировкой «содержащий», в противном случае также предложены аналогичные аспекты, описанные в терминах «состоящий из» и/или «состоящий в основном из».
[0028] Если не указано иное, все используемые в данном документе технические и научные термины имеют общепринятые значения, понятные специалисту в области техники, к которой относится данное изобретение. Например, Concise Dictionary of Biomedicine and Molecular Biology, Juo, Pei-Show, 2nd ed., 2002, CRC Press; Dictionary of Cell and Molecular Biology, 3rd ed., 1999, Academic Press; и Oxford Dictionary of Biochemistry and Molecular Biology, Revised, 2000, Oxford University Press, обеспечивают специалиста общим словарем многих терминов, используемых в данном описании.
[0029] Единицы, префиксы и символы обозначаются в их общепринятой форме Международной системы единиц измерения (СИ). Числовые диапазоны включают числа, определяющие диапазон. Если не указано иное, нуклеиновые кислоты записываются слева направо в ориентации от 5'- до 3'-конца. Аминокислотные последовательности записываются слева направо в ориентации от амино до карбокси. Заголовки, представленные в данном документе, не являются ограничениями различных аспектов изобретения, которые могут быть осуществлены со ссылкой на спецификацию в целом. Соответственно, термины, определенные ниже, определены в более полном объеме со ссылкой на спецификацию в целом.
[0030] В контексте данного документа термин «около» применяется для обозначения приблизительно, примерно, около или в области. Если около термин «около» используется в сочетании с числовым диапазоном, то он изменяет этот диапазон, расширяя границы выше и ниже указанных числовых значений. В целом, термин «около» может изменить числовое значение выше и ниже указанного значение с отклонением, например, 10 процентов, 5 процентов, 3 процента, 2 процента или 1 процент; вверх или вниз (выше или ниже).
[0031] Термин «желчные кислоты» относится к семейству молекул, состоящему из стероидной структуры с четырьмя кольцами, пяти- или восьмиуглеродной боковой цепью, оканчивающейся карбоновой кислотой, присоединенной в 17-м положении стероидного каркаса, а также с наличием и ориентацией разного количества гидроксигрупп. Структура желчных кислот может варьироваться в зависимости от ткани. Например, при синтезе в печени желчные кислоты конъюгируются с остатками таурина или глицина («конъюгированные первичные желчные кислоты»), а затем выводятся из организма и хранятся в желчном пузыре. Во время пищеварения конъюгированные первичные желчные кислоты секретируются в просвет кишечника. В некоторых вариантах осуществления первичными конъюгированными желчными кислотами являются гликохолевая кислота (гХК), таурохолевая кислота (тХК), гликохенодезоксихолевая кислота (гХДХК) или таурохенодезоксихолевая кислота (тХДХК).
[0032] Внутри просвета кишечника резидентные кишечные бактерии экспрессируют ферменты (например, гидролазу желчной соли (BSH)), которые деконъюгируют конъюгированные первичные желчные кислоты с образованием «первичных желчных кислот». В некоторых вариантах осуществления первичные желчные кислоты включают холевую кислоту (ХК) или хенодезоксихолевую кислоту (ХДХК). Затем первичные желчные кислоты обрабатываются (с помощью ферментов, таких как гидроксистероиддегидрогеназа (ГСДГ) или 7α-дегидрогеназа) с превращением во «вторичные желчные кислоты». В некоторых вариантах осуществления вторичные желчные кислоты включают дезоксихолевую кислоту (ДХК), оксодезоксихолевую кислоту (3 или 12), изо-дезоксихолевую кислоту (3 или 12), оксохолевую кислоту (3, 7 или 12), изо-холевую кислоту (3, 7 или 12), литохолевую кислоту (ЛХК), оксо-ЛХК, изо-ЛХК, оксо-хенодезоксихолевую кислотуа (3 или 7) или изо-хенодезоксихолевую кислоту (3 или 7).
[0033] Вторичные желчные кислоты, вырабатываемые в просвете кишечника, могут циркулировать обратно в печень, где они повторно конъюгируются с превращением в «конъюгированные вторичные желчные кислоты». В некоторых вариантах осуществления вторичные конъюгированные желчные кислоты по настоящему описанию включают глико-изо-дезоксихолевую кислоту (3 или 12), тауро-изо-дезоксихолевую кислоту (3 или 12), глико-дезоксихолевую кислоту, тауро-дезоксихолевую кислоту, глико-изо-холевую кислоту (3, 7 или 12), тауро-изо-холевую кислоту (3, 7 или 12), сульфо-литохолевую кислоту, глико-сульфо-литохолевую кислоту, тауро-сульфо-литохолевую кислоту, глико-изо-хенодезоксихолевую кислоту (3 или 7), тауро-изо-хенодезоксихолевую кислоту (3 или 7), глико-оксо-хенодезоксихолевую кислоту (3 или 7) или тауро-оксо-хенодезоксихолевую кислоту (3 или 7).
[0034] Термин «клада» относится к ОТЕ или представителям филогенетического дерева, которые находятся ниже от статистически достоверного узла в филогенетическом дереве. Клада включает набор терминальных листьев на филогенетическом дереве, которые представляют собой отдельную монофилетическую эволюционную единицу и которые имеют некоторую степень сходства последовательностей.
[0035] Термин «микробиота» относится к экологическому сообществу микроорганизмов, которые встречаются (устойчиво или временно) в организме животного и на нем, обычно млекопитающего, такого как человек, включая эукариоты, археи, бактерии и вирусы (включая бактериальные вирусы, т.е. фаг).
[0036] Термин «микробном» относится к микроорганизмам, которые живут в человеческом теле и на нем, как устойчиво, так и временно, включая эукариоты, археи, бактерии и вирусы (включая бактериальные вирусы (т.е. фаг)). В контексте данного документа термин «генетическое содержание» включает геномную ДНК, РНК, такую как рибосомную РНК, эпигеном, плазмиды и все другие типы генетической информации.
[0037] В контексте данного документа термин «увеличение числа микроорганизмов» или просто «увеличение» относится к созданию или значительному увеличению популяции микроорганизмов, которые (i) отсутствуют или не поддаются обнаружению (как определено с использованием стандартных геномных и микробиологических методов) из вводимой терапевтической композиции микроорганизмов, (ii) отсутствуют, не поддаются обнаружению или редко встречаются в нише хозяина (например, в желудочно-кишечном тракте, на коже, в ноздрях или во влагалище) до доставки композиции микроорганизмов, и (iii) обнаруживаются после введения композиции микроорганизмов или значительно увеличиваются в количестве после введения композиции микроорганизмов, например, в 2 раза, 5 раз, 1×102 раз, 1×103 раз, 1×104 раз, 1×105 раз, 1×106 раз, 1×107 или больше, чем 1×108 раз, в случаях, когда микроорганизмы редко встречаются. Микроорганизмы, обладающие расширенной экологией, могут быть получены из экзогенных источников, таких как пища и окружающая среда, или могут расти из микрониш внутри хозяина, где они редко встречаются.
[0038] Не придерживаясь какой-либо теории, введение терапевтической композиции микроорганизмов может вызвать изменение среды в целевой нише, что способствует благоприятным условиям для роста определенных комменсальных микроорганизмов. При отсутствии лечения терапевтической композицией микроорганизмов, хотя хозяин может подвергаться воздействию этих микроорганизмов, устойчивый рост и положительные эффекты для состояния здоровья, связанные со стабильной популяцией повышенных уровней микроорганизмов, составляющих улучшенную экологию, не наблюдаются или наблюдаются реже в целевой популяции.
[0039] Термин «приживление микроорганизмов» или «приживление» относится к созданию ОТЕ, содержащих терапевтическую композицию микроорганизмов, например, бактериальную композицию, в целевой нише, которые отсутствуют или не поддаются обнаружению у получавшего лечения хозяина до лечения. Микроорганизмы входящие в состав приживленной экологии, присутствуют в терапевтической композиции микроорганизмов и являются компонентами экологии микроорганизмов у хозяина на фоне лечения. Приживление ОТЕ может происходить в течение переходного периода времени или они могут демонстрировать долговременную стабильность в экологии микроорганизмов, которые заселяют хозяина после лечения терапевтической композицией микроорганизмов. Не придерживаясь какой-либо теории, приживленная экология может вызвать изменение среды в целевой нише, что способствует благоприятным условиям для роста комменсальных микроорганизмов, способных катализировать переход от дисбиотической экологии к еще одному типичному состоянию здоровья.
[0040] Термин «экологическая ниша» или «ниша» относится к экологическому пространству, в котором находится организм или группа организмов. Ниша описывает, как организм, популяция или организмы реагируют на распределение ресурсов, физических параметров (например, пространство тканей хозяина) и конкурентов (например, путем роста, когда ресурсов много, а хищников, паразитов и патогенов мало), и как это в свою очередь изменяет те же факторы (например, ограничение доступа к ресурсам для других организмов, выступающих в качестве источника пищи для хищников и потребителей добычи).
[0041] Термин «дисбиоз» относится к состоянию микробиоты ЖКТ или другой области тела субъекта, включая поверхности слизистой оболочки или кожи, при котором нарушается нормальное разнообразие и/или функция экологической сети. Это нездоровое состояние может быть связано с уменьшением разнообразия, чрезмерным ростом одного или более патогенов или патобионтов, симбиотических организмов, способных вызывать заболевание только при наличии определенных генетических и/или окружающих условий у субъекта, или переходом к экологической микробной сети, которая больше не обеспечивает важную функцию для субъекта-хозяина и, следовательно, более не поддерживает здоровье.
[0042] В контексте данного документа термин «операционная таксономическая единица», «ОТЕ» (или в множественном числе «ОТЕ») относится к терминальному листу в филогенетическом дереве и определяется последовательностью нуклеиновой кислоты, например, полным геномом или конкретной генетической последовательностью, и всеми последовательностями, которые имеют идентичность последовательности с этой последовательностью нуклеиновой кислоты на уровне видов. В некоторых вариантах осуществления конкретная генетическая последовательность может представлять собой последовательность 16S рДНК или часть последовательности 16S рДНК. В других вариантах осуществления полные геномы двух объектов секвенируют и сравнивают. В другом варианте осуществления можно генетически сравнивать отдельные области, такие как маркеры мультилокусных последовательностей (MLST), конкретные гены или наборы генов. В вариантах осуществления 16S ОТЕ, которые имеют 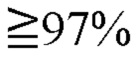 средней идентичности нуклеотидов по всей 16S или вариабельной области последовательности 16S рДНК, например, в области V4, считаются одной и той же ОТЕ (см., например, Claesson М J, Wang Q, O'Sullivan О, Greene-Diniz R, Cole J R, Ros R P, and O'Toole P W. 2010. Сравнение двух технологий секвенирования следующего поколения для разрешения очень сложного микробиома с использованием тандемных вариабельных областей гена 16S рРНК. Nucleic Acids Res 38: е200. Konstantinidis K Т, Ramette A, and Tiedje J M. 2006. The bacterial species definition in the genomic era. Philos Trans R Soc Lond В Biol Sci 361: 1929-1940). В вариантах осуществления, включающих полный геном, MLST, специфические гены или наборы генов, ОТЕ, которые имеют
средней идентичности нуклеотидов по всей 16S или вариабельной области последовательности 16S рДНК, например, в области V4, считаются одной и той же ОТЕ (см., например, Claesson М J, Wang Q, O'Sullivan О, Greene-Diniz R, Cole J R, Ros R P, and O'Toole P W. 2010. Сравнение двух технологий секвенирования следующего поколения для разрешения очень сложного микробиома с использованием тандемных вариабельных областей гена 16S рРНК. Nucleic Acids Res 38: е200. Konstantinidis K Т, Ramette A, and Tiedje J M. 2006. The bacterial species definition in the genomic era. Philos Trans R Soc Lond В Biol Sci 361: 1929-1940). В вариантах осуществления, включающих полный геном, MLST, специфические гены или наборы генов, ОТЕ, которые имеют 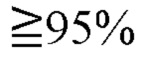 средней идентичности нуклеотидов, считаются одной и той же ОТЕ (см., например, Achtman М, and Wagner М. 2008. Microbial diversity and the genetic nature of microbial species. Nat. Rev. Microbiol. 6: 431-440. Konstantinidis K T, Ramette A, and Tiedje J M. 2006. The bacterial species definition in the genomic era. Philos Trans R Soc bond В Biol Sci 361: 1929-1940.). ОТЕ часто определяются путем сравнения последовательностей организмов. Как правило, последовательности с идентичностью последовательностей менее 95% не считаются частью одной и той же ОТЕ. ОТЕ также могут быть характеризованы по любой комбинации нуклеотидных маркеров или генов, в частности высококонсервативных генов (например, генов «домашнего хозяйства»), или их комбинацией. В таком определении характеристик используются, например, данные WGS или полногеномная последовательность.
средней идентичности нуклеотидов, считаются одной и той же ОТЕ (см., например, Achtman М, and Wagner М. 2008. Microbial diversity and the genetic nature of microbial species. Nat. Rev. Microbiol. 6: 431-440. Konstantinidis K T, Ramette A, and Tiedje J M. 2006. The bacterial species definition in the genomic era. Philos Trans R Soc bond В Biol Sci 361: 1929-1940.). ОТЕ часто определяются путем сравнения последовательностей организмов. Как правило, последовательности с идентичностью последовательностей менее 95% не считаются частью одной и той же ОТЕ. ОТЕ также могут быть характеризованы по любой комбинации нуклеотидных маркеров или генов, в частности высококонсервативных генов (например, генов «домашнего хозяйства»), или их комбинацией. В таком определении характеристик используются, например, данные WGS или полногеномная последовательность.
[0043] В контексте данного документа термин «филогенетическое дерево»относится к графическому представлению эволюционных взаимоотношений одной генетической последовательности с другой, которое создается с использованием определенного набора алгоритмов филогенетической реконструкции (например, экономичность, максимальная вероятность или байесовский метод). Узлы на дереве представляют различные предковые последовательности, и надежность любого узла обеспечивается бутстрепом или байесовской апостериорной вероятностью, которая измеряет неопределенность ветвления.
[0044] «Остаточные продукты среды обитания» относятся к материалу, полученному из среды обитания микробиоты внутри тела или на теле человека или животного, за исключением микробиоты. Микробиота человека находится, например, в кале в желудочно-кишечном тракте, на самой коже, в слюне, слизи дыхательных путей или выделениях мочеполовых путей, все из которых содержат биологические и другие вещества, ассоциированные с микробным сообществом. «По существу не содержит остаточных продуктов среды обитания» означает, что бактериальная композиция содержит пониженное количество биологического вещества, ассоциированного с микробной средой на или в теле человека или животного, и на 100%, 99%, 98%, 97%, 96% или 95% не содержит каких-либо загрязняющих биологических веществ, ассоциированных с микробным сообществом или загрязняющих веществ, ниже уровня обнаружения. Остаточные продукты среды обитания могут включать абиотические материалы (включая непереваренную пищу) или могут включать нежелательные микроорганизмы. По существу не содержит остаточных продуктов среды обитания может также означать, что бактериальная композиция микроорганизмов не содержит поддающихся обнаружению клеток человека или животного и, что обнаруживаются только клетки микроорганизмов. В некоторых вариантах осуществления по существу не содержит остаточных продуктов среды обитания может означать, что бактериальная композиция не содержит поддающихся обнаружению вирусных (включая бактериальные вирусы (т.е. фаг)), грибковых, микоплазменных примесей. В других вариантах осуществления это означает, что менее 1×10-2%, 1×10-3%, 1×10-4%, 1×10-5%, 1×10-6%, 1×10-7%, 1×10-8% жизнеспособных клеток в бактериальной композиции представляют собой клетки человека или животного по сравнению с клетками микроорганизмов. Есть несколько способов уменьшить присутствие остаточных продуктов среды обитания, ни один из которых не является ограничивающим. Таким образом, загрязнение может быть уменьшено путем выделения желаемых составляющих с помощью нескольких этапов штриховой разводки до отдельных колоний на твердой среде до тех пор, пока повторяющиеся (например, но не ограничиваясь двумя) штриховые разводки из серийных отдельных колоний не покажут морфологию только одной колонии. В качестве альтернативы, снижение загрязнения может быть достигнуто с помощью нескольких циклов серийных разведений отдельных желаемых клеток (например, разведения 10-8 или 10-9), например, с помощью нескольких 10-кратных серийных разведений. Это можно дополнительно подтвердить, продемонстрировав, что несколько выделенных колоний имеют сходные формы клеток и характер окрашивания по Граму. Другие способы подтверждения адекватного сокращения остаточных продуктов среды обитания включают генетический анализ (например, ПЦР, секвенирование ДНК), серологический и антигенный анализ, ферментативный и метаболический анализ, а также способы с использованием таких инструментов, как проточная цитометрия с реагентами, которые позволяют отличать желаемые компоненты от загрязняющих веществ.
[0045] Термин «секвенирование 16S», или «16S рДНК», или «16S» относится к последовательности, полученной путем характеристики нуклеотидов, составляющих ген(ы) 16S рибосомной РНК. Бактериальная 16S рДНК имеет длину приблизительно 1500 нуклеотидов и используется для реконструкции эволюционных взаимоотношений и сходства последовательностей одного бактериального изолята с другим с использованием филогенетических подходов. Последовательности 16S используются для филогенетической реконструкции, поскольку они в целом высококонсервативны, но содержат специфические гипервариабельные области, которые обладают достаточным нуклеотидным разнообразием для дифференциации родов и видов большинства бактерий.
[0046] Термин «области V1-V9» 16S рРНК относится к гипервариабельным областям с первой по девятую гена 16S рРНК, которые используются для генетического типирования бактериальных образцов. Эти области в бактериях определяются нуклеотидами 69-99, 137-242, 433-497, 576-682, 822-879, 986-1043, 1117-1173, 1243-1294 и 1435-1465, соответственно, с использованием нумерации на основе номенклатурной системы Е.coli. Brosius et al., Complete nucleotide sequence of a 16S ribosomal RNA gene from Escherichia coli, PNAS 75(10):4801-4805 (1978). В некоторых вариантах осуществления по меньшей мере одна из областей V1, V2, V3, V4, V5, V6, V7, V8 и V9 используется для характеристики ОТЕ. В некоторых вариантах осуществления области V1, V2 и V3 используются для характеристики ОТЕ. В другом варианте осуществления области V3, V4 и V5 используются для характеристики ОТЕ. В другом варианте осуществления область V4 используется для характеристики ОТЕ. Специалист в данной области техники может идентифицировать конкретные гипервариабельные области кандидатной 16S рРНК, сравнивая рассматриваемую кандидатную последовательность с эталонной последовательностью и идентифицируя гипервариабельные области на основании сходства с эталонными гипервариабельными областями или, в качестве альтернативы, можно использовать характеристику микроорганизмов или микробного сообщества при помощи полного геномного секвенирования методом дробовика.
[0047] В контексте данного документа термин «субъект» относится к любому животному-субъекту, включая людей, лабораторных животных (например, приматов, крыс, мышей), сельскохозяйственных животных (например, коров, овец, коз, свиней, индеек и кур) и домашних питомцев (например, собак, кошек и грызунов). Субъект может страдать дисбиозом, включая, но не ограничиваясь этим, инфекцию, вызванную желудочно-кишечным патогеном, или может иметь риск развития или передачи другим инфекции из-за желудочно-кишечного патогена. В некоторых вариантах осуществления субъект страдает воспалительным заболеванием кишечника (например, язвенным колитом или болезнью Крона).
[0048] В контексте данного документа термин «субъект, страдающий воспалительным заболеванием кишечника» является синонимом термина «субъект, у которого диагностировано воспалительное заболевание кишечника», и означает пациента, имеющего болезнь Крона или язвенный колит. Болезнь Крона (регионарный энтерит) представляет собой заболевание с хроническим воспалением, которое может поражать любую часть желудочно-кишечного тракта. Обычно поражаются дистальная часть тонкой кишки (подвздошная кишка) и слепая кишка. В других случаях заболевание ограничивается тонкой кишкой, толстой кишкой или аноректальной областью. Болезнь Крона иногда поражает двенадцатиперстную кишку и желудок, реже пищевод и полость рта. Применимые композиции, описанные в данном документе, могут облегчить или предотвратить один или более признаков или симптомов ВЗК, неограничивающие примеры которых описаны в данном документе.
[0049] Различные клинические проявления болезни Крона частично являются результатом различной анатомической локализации заболевания. Наиболее частыми симптомами БК являются боль в животе, диарея и рецидивирующая лихорадка. БК обычно ассоциируется с кишечной непроходимостью или свищом, который, например, является аномальным проходом между пораженными петлями кишечника. Болезнь Крона также включает такие осложнения, как воспаление глаз, суставов и кожи; заболевание печени; камни в почках или амилоидоз. Кроме того, БК ассоциируется с повышенным риском рака кишечника.
[0050] Для патологии болезни Крона характерно несколько особенностей. Воспаление, связанное с БК, известное как трансмуральное воспаление, поражает все слои стенки кишечника. Утолщение и отек, например, обычно также появляются по всей стенке кишечника, при этом фиброз также присутствует при длительном заболевании. Воспаление, характерное для БК, также является прерывистым в том плане, что сегменты воспаленной ткани, известные как «сегментарные поражения», разделены явно нормальным кишечником. Кроме того, линейные изъязвления, отек и воспаление переходной ткани приводят к появлению симптома «булыжной мостовой» слизистой оболочки кишечника, что характерно для БК.
[0051] Отличительным признаком болезни Крона является присутствие дискретных скоплений воспалительных клеток, известных как гранулемы, которые обычно обнаруживаются в подслизистой оболочке. В некоторых случаях болезни Крона наблюдаются типичные дискретные гранулемы, в других -неспецифическое трансмуральное воспаление. В результате наличие дискретных гранулем указывает на БК, хотя отсутствие гранулем также согласуется с заболеванием. Таким образом, трансмуральное или прерывистое воспаление, а не наличие гранулем, является предпочтительным диагностическим признаком болезни Крона (Rubin and Farber, Pathology (Second Edition) Philadelphia: J. B. Lippincott Company (1994)).
[0052] Язвенный колит (ЯК) представляет собой заболевание толстой кишки, характеризующееся хронической диареей со спазматической болью в животе, ректальным кровотечением и жидкими выделениями крови, гноя и слизи. Проявления язвенного колита широко варьируются. Характер обострений и ремиссий типичен для клинического течения заболевания большинства пациентов с ЯК (70%), хотя у некоторых пациентов с ЯК наблюдаются продолжительные симптомы без ремиссии. К местным и системным осложнениям ЯК относятся артрит, воспаление глаз, такое как увеит, язвы кожи и заболевание печени. Кроме того, язвенный колит и, в частности длительное обширное заболевание, связано с повышенным риском рака толстой кишки.
[0053] ЯК отличается от других воспалительных заболеваний кишечника несколькими патологическими особенностями. Язвенный колит - это диффузное заболевание, которое обычно простирается от самой дистальной части прямой кишки на различное расстояние в проксимальном направлении. Термин левосторонний колит описывает воспаление, которое поражает дистальную часть толстой кишки, доходя до изгиба селезенки. Сохранение прямой кишки или поражение только правой части (проксимальной части) толстой кишки является нетипичным при язвенном колите. Воспалительный процесс при язвенном колите ограничивается толстой кишкой и не поражает, например, тонкую кишку, желудок или пищевод. Кроме того, язвенный колит отличается поверхностным воспалением слизистой оболочки, которое обычно не затрагивает более глубокие слои стенки кишечника. Абсцессы крипт, при которых дегенерированные кишечные крипты заполнены нейтрофилами, также типичны для язвенного колита (Rubin and Farber, supra, 1994).
[0054] По сравнению с болезнью Крона, которая представляет собой очаговое заболевание с частым отсутствием поражения прямой кишки, язвенный колит характеризуется непрерывным воспалением толстой кишки, которое обычно характеризуется более тяжелым поражением в дистальной, чем в проксимальной части. Воспаление при язвенном колите носит поверхностный характер, поскольку обычно ограничивается слоем слизистой оболочки и характеризуется острым воспалительным инфильтратом с нейтрофилами и абсцессами крипт. Напротив, болезнь Крона поражает всю толщину стенки кишечника, при этом часто, хотя и не всегда, присутствуют гранулемы. Заболевание, которое заканчивается у илеоцекального клапана или в толстой кишке дистальнее него, свидетельствует о язвенном колите, тогда как поражение терминального отдела подвздошной кишки, в виде «булыжной мостовой», отдельные язвы или свищи предполагают наличие болезни Крона.
[0055] Помимо ВЗК, описанные в данном документе бактериальные композиции также могут быть применимы для лечения других иммуноопосредованных желудочно-кишечных расстройств, включая, но не ограничиваясь ими, лимфоцитарный колит; микроскопический колит; коллагенозный колит; аутоиммунная энтеропатия, включая аутоиммунный энтерит и аутоиммунный энтероколит; аллергические заболевания желудочно-кишечного тракта; и эозинофильное желудочно-кишечное заболевание, включая эозинофильный гастроэнтерит и эозинофильную энтеропатию.
[0056] В контексте данного документа термин «спора» или «эндоспора» относится к объекту, в частности, к бактериальному объекту, который находится в стадии покоя, невегетативной и нерепродуктивной стадии. Споры обычно устойчивы к стрессам окружающей среды, таким как радиация, высушивание, ферментативная обработка, изменение температуры, лишение питательных веществ и химические дезинфицирующие средства. В некоторых вариантах осуществления спора или популяция спор устойчива к 50% этанолу.
[0057] «Популяция спор» относится к множеству спор, присутствующих в композиции. В контексте данного документа синонимичные термины включают состав спор, препарат спор, фракцию спор, обработанную этанолом, и экологию спор. Популяция спор может быть очищена из образца кала, например, с помощью этанола или тепловой обработки, или разделения в градиенте плотности, или любой комбинации описанных здесь способов для повышения чистоты, активности и/или концентрация спор в образце. Альтернативно, популяция спор может быть получена с помощью способов культивирования, начиная с выделенных спорообразующих видов или спорообразующих ОТЕ, или из смеси таких видов, либо в вегетативной форме, либо в форме спор.
[0058] В некоторых вариантах осуществления препарат спор содержит спорообразующие виды, в которых остаточные неспорообразующие виды были инактивированы химической или физической обработкой, включая этанол, детергент, нагревание, обработку ультразвуком и тому подобное; или в которых виды, не образующие споры, были удалены из препарата спор с помощью различных стадий разделения, включая градиенты плотности, центрифугирование, фильтрацию и/или хроматографию; или при этом способы инактивации и разделения объединены для получения препарата спор. В еще одном варианте осуществления препарат спор включает спорообразующие виды, которые обогащены жизнеспособными не образующими споры микроорганизмами или вегетативными формами спорообразующих микроорганизмов. В данном варианте осуществления споры обогащены в 2, 5, 10, 50, 100, 1000, 10000 или более чем в 10000 раз по сравнению со всеми вегетативными формами бактерий. В еще одном варианте осуществления споры в препарате спор подвергаются частичному прорастанию во время обработки и составления, так что конечная композиция включает споры и вегетативные бактерии, происходящие от спорообразующих видов.
[0059] Термин «средство, способствующее прорастанию» относится к материалу, композиции или физико-химическому процессу, способному вызывать вегетативный рост бактерии, которая находится в спящей форме спор, или группы бактерий в форме спор, напрямую или опосредованно в организме хозяина и/или in vitro.
[0060] Термин «индуцирующий спорообразование агент» относится к материалу или физико-химическому процессу, который способен вызывать образование спор у бактерии, напрямую или опосредованно в организме хозяина и/или in vitro.
[0061] Термин «увеличение выработки бактериальных спор» включает агент, индуцирующий активность или образование спор. «Выработка» в контексте данного документа включает преобразование вегетативных бактериальных клеток в споры и увеличение скорости такого преобразования, а также снижение прорастания бактерий в форме спор, уменьшение скорости разложения спор in vivo или ex vivo, или увеличение общего выхода спор (например, за счет увеличения объемного выхода фекального материала).
[0062] «Колонизация» организма-хозяина включает постоянное наличие бактерии или другого микроскопического организма. В контексте данного документа термин «уменьшение колонизации» желудочно-кишечного тракта субъекта-хозяина (или любой другой микробиотической ниши) патогенными бактериями включает сокращение времени пребывания патогена в желудочно-кишечном тракте, а также снижение количества (или концентрации) патогена в желудочно-кишечном тракте или прилипшего к поверхности просвета желудочно-кишечного тракта. Измерение уменьшения количества прикрепившихся патогенов может быть продемонстрировано, например, с помощью биопсийного образца, или уменьшение может быть измерено опосредованно, например, путем измерения патогенной нагрузки в стуле млекопитающего-хозяина.
[0063] «Комбинация» двух или более бактерий включает физическое сосуществование двух бактерий либо в одном материале или продукте, либо в физически связанных продуктах, а также временное совместное введение или совместную локализацию двух бактерий.
[0064] «Цитотоксическая» активность бактерии включает способность уничтожать бактериальную клетку, такую как патогенная бактериальная клетка. «Цитостатическая» активность бактерии включает способность подавлять, частично или полностью, рост, метаболизм, и/или пролиферация бактериальной клетки, такой как патогенная бактериальная клетка.
[0065] Отсутствие «несъедобных продуктов» означает, что бактериальная композиция или другой материал, представленный в данном документе, не содержит значительного количества несъедобного продукта, например продукта или материала, который является несъедобным, вредным или иным образом нежелательным в продукте, который подходит для введения, например, перорального введения человеку. Несъедобные продукты часто встречаются в препаратах бактерий из предшествующего уровня техники.
[0066] В случае нуклеиновых кислот термин «существенная гомология» указывает, что две нуклеиновые кислоты или их указанные последовательности при оптимальном выравнивании и сравнении являются идентичными, с учетом соответствующих нуклеотидных вставок и делеций, в по меньшей мере около 80% нуклеотидов, по меньшей мере от около 90% до 95%, или по меньшей мере от около 98% до 99,5% нуклеотидов. В альтернативном варианте существенная гомология существует, когда сегменты гибридизируются в селективных условиях гибридизации, с комплементарной последовательностью цепи.
[0067] В случае полипептидов термин «существенная гомология» указывает, что два полипептида или их указанные последовательности при оптимальном выравнивании и сравнении являются идентичными, с учетом соответствующих аминокислотных вставок и делеций, в по меньшей мере около 80% аминокислот, по меньшей мере от около 90% до 95%, или по меньшей мере от около 98% до 99,5% аминокислот.
[0068] Процент идентичности между двумя последовательностями является функцией от числа совпадающих позиций в последовательностях (т.е. % гомологии = число идентичных позиций/общее число позиций × 100) с учетом числа гэпов и длины каждого гэпа, которые необходимо вносить для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями можно осуществлять с помощью математического алгоритма, как описано в неограничивающих примерах ниже.
[0069] Процент идентичности между двумя нуклеотидными последовательностями может быть определен с помощью программы GAP в пакете программного обеспечения GCG (доступно на веб-сайте worldweb.gcg.com), используя матрицу NWSgapdna.CMP и штраф за открытие гэпа 40, 50, 60, 70 или 80 и штраф за продолжение гэпа 1, 2, 3, 4, 5 или 6. Процент идентичности между двумя нуклеотидными или аминокислотными последовательностями также можно определять, используя алгоритм Е. Meyers и W. Miller (CABIOS, 4: 11-17 (1989)), который был включен в программу ALIGN (версия 2.0), используя таблицу весов замен остатков РАМ120, штраф за продолжение гэпа 12 и штраф за открытие гэпа 4. Процент идентичности между двумя аминокислотными последовательностями можно определять, используя алгоритм Needleman и Wunsch (J. Mol Biol. (48):444-453 (1970)), который был включен в программу GAP из пакета программного обеспечения GCG (доступно на веб-сайте www.gcg.com), используя матрицу Blossum 62 или матрицу РАМ250 и штраф за открытие гэпа 16, 14, 12, 10, 8, 6 или 4, и штраф за продолжение гэпа 1, 2, 3, 4, 5 или 6.
[0070] Последовательности нуклеиновых кислот и белков, описанные в данном документе, дополнительно можно использовать в качестве «запрашиваемой последовательности» для проведения поиска по общедоступным базам данных, например, для определения родственных последовательностей. Такой поиск можно проводить, используя программы NBLAST и XBLAST (версия 2.0) по Altschul, et al. (1990) J. Mol. Biol. 215:403-10. Нуклеотидный поиск BLAST можно осуществлять с помощью программы NBLAST, показатель = 100, длина слова = 12, для получения нуклеотидных последовательностей, гомологичных с молекулами нуклеиновых кислот, описанных в данном документе. Белковый поиск BLAST можно осуществлять с помощью программы XBLAST, показатель = 50, длина слова = 3, для получения аминокислотных последовательностей, гомологичных с белковыми молекулами, описанными в данном документе. Для получения выравнивания с внесенными в целях сравнения гэпами можно использовать BLAST с гэпами, как описано в Altschul et al., (1997) Nucleic Acids Res. 25(17):3389-3402. При использовании программ BLAST и BLAST с гэпами можно использовать параметры по умолчанию соответствующих программ (например, XBLAST и NBLAST). См. worldwideweb.ncbi.nlm.nih.gov. Могут использоваться другие методы определения идентичности, известные в данной области.
[0071] Термины «лечить», «процесс лечения» и «лечение» в контексте данного документа относятся к любому типу вмешательства или процессу, выполняемому у субъекта, или введению активного агента субъекту с целью обращения, улучшения, облегчения, ингибирования или замедления или предотвращения прогрессирования, развития, тяжести или рецидива симптома, осложнения, состояния или биохимических показателей, ассоциированных с заболеванием, или повышения общей выживаемости. Лечение может относиться к субъекту, страдающему заболеванием, или субъекту, у которого нет заболевания (например, в целях профилактики).
[0072] Термин «эффективная доза» или «эффективная дозировка» определяется как количество, достаточное для достижения или по меньшей мере частичного достижения желаемого эффекта. «Терапевтически эффективное количество» или «терапевтически эффективная дозировка» лекарственного препарата или терапевтического агента представляет собой любое количество лекарственного препарата, которое при использовании отдельно или в комбинации с другим терапевтическим агентом способствует регрессии заболевания, о чем свидетельствует уменьшение тяжести симптомов заболевания, увеличение частоты и продолжительности периодов без симптомов заболевания или предотвращению нарушений или инвалидности из-за болезни. Терапевтически эффективное количество или дозировка лекарственного препарата включает «профилактически эффективное количество» или «профилактически эффективную дозировку», которая представляет собой любое количество лекарственного препарата, которое при введении отдельно или в комбинации с другим терапевтическим агентом субъекту с риском развития заболевание или рецидива заболевания ингибирует развитие или рецидив заболевания. Способность терапевтического агента способствовать регрессии заболевания или ингибировать развитие или рецидив заболевания может быть оценена с использованием множества способов, известных квалифицированному практикующему врачу, например, у людей во время клинических испытаний, в системах животных моделей, предсказывающих эффективность применения у людей или путем анализа активности агента в анализах in vitro.
[0073] Термин «пациент», включает людей и других субъектов-млекопитающих, которые получают либо профилактическое, либо терапевтическое лечение.
[0074] В контексте данного документа термин «субъект» включает любого человека или животного, не являющегося человеком. Например, способы и композиции, описанные в данном документе, можно использовать для лечения субъекта, имеющего рак. Термин «отличное от человека животное» включает всех позвоночных, например, млекопитающих и не млекопитающих, таких как отличные от человека приматы, овцы, собаки, коровы, куры, амфибии, рептилии и т.д.
[0075] В контексте данного документа термины «μg» и «μМ» используются взаимозаменяемо с «мкг» и «мкМ», соответственно.
[0076] Различные аспекты, описанные в данном документе, более подробно описаны в следующих подразделах.
I. Бактериальные композиции
[0077] В данном документе описаны бактерии и комбинации бактерий микробиоты желудочно-кишечного тракта человека, способные изменять уровень одной или более желчных кислот у субъекта. В некоторых вариантах осуществления модуляция уровня желчной кислоты может лечить, предотвращать, задерживать или улучшать один или более признаков или симптомов, связанных с желудочно-кишечным расстройством, например воспалительным заболеванием кишечника (например, язвенным колитом или болезнью Крона). Не ограничиваясь конкретным механизмом, считается, что повышение и/или понижение содержания некоторых желчных кислот может снизить содержание провоспалительных медиаторов (например, ФНО-α или ИЛ-8), вырабатываемых активированными клетками (например, моноцитами, МКПК или эпителиальными клетками кишечника). В некоторых вариантах осуществления повышение и/или снижение содержания некоторых желчных кислот может повысить содержание противовоспалительных медиаторов (например, ИЛ-10), вырабатываемых активированными клетками.
[0078] В некоторых вариантах осуществления бактериальная композиция, описанная в данном документе, содержит два типа бактерий (называемых «бинарными комбинациями» или «бинарными парами»). В некоторых вариантах осуществления бактериальная композиция содержит более двух типов бактерий. Соответственно, в некоторых вариантах осуществления бактериальная композиция по настоящему изобретению содержит по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14, по меньшей мере 15, по меньшей мере 16, по меньшей мере 17, по меньшей мере 18, по меньшей мере 19, по меньшей мере 20 или по меньшей мере 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39 или по меньшей мере 40, по меньшей мере 50 или по более 50 типов бактерий, как определено видом или операционной таксономической единицей (ОТЕ), или иным образом, как указано в данном документе.
[0079] В некоторых вариантах осуществления типы бактерий, обнаруженные в бактериальной композиции, описанной в данном документе, представляют собой те типы, которые, как обнаружено, истощены у пациентов с ВЗК и/или обычно присутствуют только на низких уровнях или отсутствуют у пациентов с диагностированным ВЗК (например, у пациентов с активным заболеванием). В некоторых вариантах осуществления бактериальная композиция включает одну или более дополнительных бактерий, которые часто присутствуют в популяции здоровых людей.
[0080] В некоторых вариантах осуществления первый и/или второй тип бактерий включает последовательность 16S рДНК, которая по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% идентична последовательности 16S рДНК эталонной ОТЕ Flavonifractor_SC49 (SEQ ID NO: 1, 3 или 4). Flavonifractor_SC49, описанный в данном документе представляет собой новый вид, который принадлежит к роду семейства Ruminococcaceae. В некоторых вариантах осуществления первый и/или второй тип бактерий включает последовательность 16S рДНК, которая по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% идентична последовательности 16S рДНК эталонной ОТЕ Clostridium leptum (SEQ ID NO: 2). В некоторых вариантах осуществления первый тип бактерий включает последовательность 16S рДНК, которая по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% идентична SEQ ID NO: 1, 3 или 4, а второй тип бактерий включает последовательность 16S рДНК, которая по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% идентична SEQ ID NO: 2. В некоторых вариантах осуществления бактерии Flavonifractor_SC49 и/или Clostridium leptum более распространены у пациентов с ВЗК, находящихся в стадии ремиссии (т.е. без активной фазы обострения заболевания), по сравнению с пациентами с ВЗК с активным заболеванием.
[0081] В некоторых вариантах осуществления штамм ОТЕ, применимый для настоящего изобретения (например, ОТЕ, описанная в данном документе), может быть получен из общедоступного центра биологических ресурсов, такого как АТСС (atcc.org), DSMZ (dsmz.de) или Riken (en.brc.riken.jp). Способы определения идентичности последовательностей известны в данной области техники.
[0082] В некоторых вариантах осуществления бактериальная композиция может модулировать уровень желчной кислоты у субъекта. В некоторых вариантах осуществления бактериальная композиция повышает уровень вторичной желчной кислоты, при этом вторичная желчная кислота выбрана из группы, состоящей из дезоксихолевой кислоты (ДХК), 3α-12-оксо-дезоксихолевой кислоты, 3β-12α-дезоксихолевой кислоты (3-изо-дезоксихолевой кислоты), 7α-3-оксо-хенодезоксихолевой кислоты, литохолевой кислоты (ЛХК), 3-оксо-ЛХК, оксо-ЛХК, изо-ЛХК и их комбинаций. В некоторых вариантах осуществления уровень вторичной желчной кислоты повышается по меньшей мере на 1%, по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 100% по сравнению с соответствующим уровнем в эталонном образце. В некоторых вариантах осуществления эталонный образец представляет собой биологический образец (например, образец кала), полученный от субъекта до введения бактериальной композиции, описанной в данном документе. В других вариантах осуществления эталонный образец представляет собой биологический образец (например, образец кала), полученный от субъекта в активной фазе обострения воспалительного заболевания кишечника (например, язвенного колита или болезни Крона).
[0083] В некоторых вариантах осуществления повышение уровня вторичной желчной кислоты снижает содержание провоспалительных медиаторов (например, ФНО-α или ИЛ-8), вырабатываемых активированными клетками (например, ЛПС-стимулированными моноцитами, ЛПС-стимулированными МКПК или ФНО-α-стимулированными эпителиальными клетками кишечника). В некоторых вариантах осуществления повышение уровня вторичной желчной кислоты повышает содержание противовоспалительных медиаторов (например, ИЛ-10), вырабатываемых активированными клетками. В определенных вариантах осуществления количество вырабатываемых противовоспалительных медиаторов снижается по меньшей мере на 1%, по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 100% по сравнению с эталонным образцом (например, активированными клетками, необработанными повышенной концентрацией вторичной желчной кислоты). В некоторых вариантах осуществления количество вырабатываемых противовоспалительных медиаторов повышается по меньшей мере на 1%, по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 100% по сравнению с эталонным образцом (например, активированными клетками, необработанными повышенной концентрацией вторичной желчной кислоты). Соответственно, в некоторых вариантах осуществления бактериальная композиция по данному изобретению оказывает противовоспалительное действие при введении субъекту.
[0084] В некоторых вариантах осуществления бактериальная композиция также может снижать уровень урсодезоксихолевой кислоты (УДХК). В некоторых вариантах осуществления уровень УДХК снижается по меньшей мере на 1%, по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 100% по сравнению с соответствующим уровнем в эталонном образце. В определенных вариантах осуществления эталонный образец представляет собой биологический образец (например, образец кала), полученный от субъекта до введения бактериальной композиции, описанной в данном документе. В других вариантах осуществления эталонный образец представляет собой биологический образец (например, образец кала), полученный от субъекта в активной фазе обострения воспалительного заболевания кишечника (например, язвенного колита или болезни Крона). В некоторых вариантах осуществления УДХК может повышать содержание провоспалительного медиатора (например, ИЛ-8), вырабатываемого, например, эпителиальными клетками кишечника. Соответственно, в некоторых вариантах осуществления снижение уровня УДХК может снизить количество одного или более провоспалительных медиаторов (например, ИЛ-8), вырабатываемых, например, эпителиальными клетками кишечника.
[0085] В некоторых вариантах осуществления бактериальная композиция может модулировать уровень желчной кислоты у субъекта путем изменения активности одного или более ферментов, задействованных в синтезе желчной кислоты. В некоторых вариантах осуществления бактериальная композиция может модулировать активность гидролазы солей желчных кислот (BSH), 7α-дегидроксилазы и/или гидроксистероиддегидрогеназы (ГСДГ).
[0086] В некоторых вариантах осуществления бактериальная композиция по данному изобретению содержит бактерии, способные образовывать споры (т.е. спорообразующие бактерии). Соответственно, в некоторых вариантах осуществления бактериальная композиция содержит очищенную популяцию бактерий, в которой бактерии находятся в форме спор. В некоторых вариантах осуществления бактерии в композиции находятся в форме спор. В других вариантах осуществления некоторые бактерии находятся в форме спор, тогда как другие бактерии не находятся в форме спор (т.е. находятся в вегетативном состоянии). В некоторых вариантах осуществления бактериальная композиция содержит очищенную популяцию спорообразующих бактерий, при этом все бактерии находятся в вегетативном состоянии.
[0087] В контексте данного документа термины «очищать», «очищенный» и «процесс очищения» относятся к состоянию популяции (например, множеству известных или неизвестных количеств и/или концентраций) желаемых бактерий или бактериальных спор, которые прошли один или более процессов очистки, например, отбор или обогащение желаемой бактерии и/или бактериальной споры или, альтернативно, удаление или уменьшение остаточных продуктов среды обитания, как описано в данном документе. В некоторых вариантах осуществления очищенная популяция не имеет обнаруживаемой нежелательной активности или, альтернативно, уровень или количество нежелательной активности находится на приемлемом уровне или в приемлемом количестве или ниже приемлемого уровня или количества. В других вариантах осуществления очищенная популяция имеет количество и/или концентрацию желаемых бактерий или бактериальных спор, например, в целом или отдельных видов, в приемлемом количестве или выше и/или концентрации. В других вариантах осуществления соотношение желаемой и нежелательной активности (например, спор по сравнению с вегетативными бактериями) изменилось в 2-, 5-, 10-, 30-, 100-, 300-, 1×104, 1×105, 1×106, 1×107, 1×108 или более, чем 1×108 раз. В других вариантах осуществления очищенная популяция бактериальных спор обогащена по сравнению с исходным материалом (например, фекальным материалом), из которого получена популяция. Это обогащение может составлять 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99%, 99,9%, 99,99%, 99,999%, 99,9999%, 99,9999% или более 99,999999% по сравнению с исходным материалом.
[0088] В некоторых вариантах осуществления очищенная популяция бактерий имеет пониженные или неподдающиеся определению уровни одной или более патогенных активностей, таких как токсичность, способность вызывать инфекцию у млекопитающего-реципиента, нежелательную иммуномодулирующую активность, аутоиммунный ответ, метаболический ответ или воспалительный ответ или неврологический ответ. В некоторых вариантах осуществления патогенная активность бактерий снижается по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% по сравнению с эталонными бактериями. В некоторых вариантах осуществления очищенная популяция бактерий имеет пониженное содержание сенсорных компонентов по сравнению с каловыми массами, таких как ослабленный запах, вкус, внешний вид и вкус белковых веществ.
[0089] В некоторых вариантах осуществления бактериальная композиция, описанная в данном документе, по существу не содержит остаточных продуктов среды обитания и/или по существу не содержит поддающегося обнаружению уровня патогенного материала (например, не содержит поддающегося обнаружению вирусных (включая бактериальные вирусы (т.е. фаг)), грибковых, микоплазменных или токсоплазменных загрязняющих веществ или эукариотических паразитов, таких как гельминты. В некоторых вариантах осуществления бактериальная композиция по существу не содержит бесклеточного материала (например, ДНК, материала вирусной оболочки или нежизнеспособного бактериального материала).
[0090] В некоторых вариантах осуществления бактериальная композиция включает популяцию бактерий, чувствительных к одному или более антибиотикам, которые можно использовать у человека. В некоторых вариантах осуществления бактерии композиции устойчивы к одному или более антибиотикам, которые используются для профилактического лечения пациентов с активным ВЗК (например, в острой фазе обострения). Такие антибиотики включают, но не ограничиваются ими, β-лактамы, ванкомицин, аминогликозиды, фторхинолоны и даптомицин.
[0091] В некоторых вариантах осуществления бактериальная композиция содержит популяцию бактерий, очищенных от биологического материала (например, фекальных материалов, таких как кал или материалы, выделенные из различных сегментов тонкого и толстого кишечника), полученных от субъекта-донора, являющегося млекопитающим. В некоторых вариантах осуществления биологический материал (например, фекальный материал) может быть получен от нескольких доноров (например, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 200, 300, 400, 500, 750, 1000 или от более чем 1000 доноров), где такие материалы затем объединяют перед очисткой от желаемых бактерий. В других вариантах осуществления биологический материал может быть получен от одного донора несколько раз и объединен из нескольких образцов, например, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 32, 35, 40, 45, 48, 50, 100 образцов от одного донора.
[0092] Субъекты-доноры, являющиеся млекопитающими, применимые для настоящего описания, обычно имеют хорошее состояние здоровья и микробиоту, соответствующую такому хорошему состоянию здоровья. Как правило, субъекту-донору не вводили антибиотические соединения в течение определенного периода до сбора фекального материала. В некоторых вариантах осуществления субъект-донор не страдает ожирением или избыточной массой тела и может иметь показатель индекса массы тела (ИМТ) ниже 25, например от 18,5 до 24,9. В других вариантах осуществления субъект-донор не является психически больным или не имеет в анамнезе или семейном анамнезе психических заболеваний, таких как тревожное расстройство, депрессия, биполярное расстройство, расстройства аутистического спектра, шизофрения, панические расстройства, расстройство дефицита внимания (гиперактивности), расстройства пищевого поведения или расстройства настроения. В других вариантах осуществления у субъекта-донора нет заболевания раздраженного кишечника (например, болезни Крона или язвенного колита), синдрома раздраженного кишечника, целиакии, колоректального рака или этих заболеваний в семейном анамнезе. В других вариантах осуществления субъект-донор прошел скрининг на переносимые с кровьюпатогены, и патогены, передаваемые через фекалии, с использованием стандартных методов, известных специалисту в данной области техники (например, тестирование нуклеиновых кислот, серологическое тестирование, тестирование на антигены, методы культивирования, ферментативные анализы, анализы бесклеточных фекальных фильтратов, предназначенные для выявления токсинов на чувствительных субстратах клеточных культур).
[0093] В некоторых вариантах осуществления донор также выбран по наличию определенных родов и/или виды, которые обеспечивают повышенную эффективность терапевтических композиций, содержащих эти роды или виды. В некоторых вариантах осуществления донор выбран по наличию Flavornifactor_SC49 и/или Clostridium leptum. В некоторых вариантах осуществления донор выбран по наличию бактерий, содержащих последовательность 16S рДНК, которая по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% идентична последовательности 16S рДНК эталонной ОТЕ Flavonifractor_SC49 (SEQ ID NO: 1, 3 или 4) или эталонной ОТЕ Clostridium leptum (SEQ ID NO: 2). В других вариантах осуществления выбран донор, который вырабатывает относительно более высокие концентрации спор в фекальном материале, чем другие доноры. В дополнительных вариантах осуществления выбран донор, который предоставляет фекальный материал, из которого очищаются споры, обладающие повышенной эффективностью; эта повышенная эффективность измеряется с помощью исследований in vitro или на исследований животных, как описано ниже. В некоторых вариантах осуществления донор может быть подвергнут одной или более процедурам лечения перед сдачей образца, чтобы снизить содержание нежелательного материала в фекальном материале и/или увеличить желаемую популяцию спор.
[0094] Предпочтительно проводить скрининг состояния здоровья субъекта-донора до и, необязательно, один или более раз после сбора фекального материала. Такой скрининг выявляет доноров, несущих патогенные материалы, такие как вирусы (ВИЧ, гепатит, полиомиелит) и патогенные бактерии. После сбора доноры проходят скрининг в течение одной недели, двух недель, трех недель, одного месяца, двух месяцев, трех месяцев, шести месяцев, одного года или более одного года, и частота такого скрининга может быть ежедневной, еженедельной, каждые две недели, ежемесячной, каждые два месяца, раз в полгода или ежегодной. Доноры, прошедшие скрининг и не имеющие положительного результата ни до, ни после сдачи образцов, или и того, и другого, считаются «утвержденными» донорами.
[0095] Способы очистки бактерий из биологического образца (например, образца кала) от субъектов-доноров известны в данной области техники, как описано, например, в патенте США №9 011 834, который полностью включен в настоящий документ посредством ссылки.
II. Составы
[0096] Кроме того, в данном документе представлены составы для введения людям и другим нуждающимся в этом субъектам (например, пациентам с ВЗК, например, пациентам с язвенным колитом). Как правило, описанная в данном документе бактериальная композиция комбинируется с дополнительными активными и/или неактивными материалами для получения конечного продукта, который может быть в единичной лекарственной форме или в многодозовой лекарственной форме.
[0097] В некоторых вариантах осуществления бактериальная композиция содержит по меньшей мере один углевод. «Углевод» относится к сахару или полимеру сахаров. Термины «сахарид», «полисахарид», «углевод» и «олигосахарид» могут использоваться взаимозаменяемо. Большинство углеводов представляют собой альдегиды или кетоны с множеством гидроксильных групп, обычно по одной на каждый углеродный атом молекулы. Углеводы обычно имеют молекулярную формулу CnH2nOn. Углевод может представлять собой моносахарид, дисахарид, трисахарид, олигосахарид или полисахарид. Самый основной углевод - это моносахарид, такой как глюкоза, сахароза, галактоза, манноза, рибоза, арабиноза, ксилоза и фруктоза. Дисахариды представляют собой два соединенных моносахарида. Примеры дисахаридов включают сахарозу, мальтозу, целлобиозу и лактозу. Обычно олигосахарид включает от трех до шести моносахаридных звеньев (например, рафинозу, стахиозу), а полисахариды включают шесть или более моносахаридных звеньев. Примеры полисахаридов включают крахмал, гликоген и целлюлозу. Углеводы могут содержать модифицированные сахаридные звенья, такие как 2'-дезоксирибоза, в которой удалена гидроксильная группа, 2'-фторорибоза, в которой гидроксильная группа заменена фтором или N-ацетилглюкозамин, азотсодержащая форма глюкозы (например, 2'-фторорибоза, дезоксирибоза и гексоза). Углеводы могут существовать во многих различных формах, например, конформерах, циклических формах, ациклических формах, стереоизомерах, таутомерах, аномерах и изомерах.
[0098] В некоторых вариантах осуществления бактериальная композиция содержит по меньшей мере один липид. В контексте данного документа термин «липид» включает жиры, масла, триглицериды, холестерин, фосфолипиды, жирные кислоты в любой форме, включая свободные жирные кислоты. Жиры, масла и жирные кислоты могут быть насыщенными, ненасыщенными (цис или транс) или частично ненасыщенными (цис или транс). В некоторых вариантах осуществления липид содержит по меньшей мере одну жирную кислоту, выбранную из лауриновой кислоты (12:0), миристиновой кислоты (14:0), пальмитиновой кислоты (16:0), пальмитолеиновой кислоты (16:1), маргариновой кислоты (17:0), гептадеценовой кислоты (17:1), стеариновой кислоты (18:0), олеиновой кислоты (18:1), линолевой кислоты (18:2), линоленовой кислоты (18:3), октадекатетраеновой кислоты (18:4), арахиновой кислоты (20:0), эйкозеновой кислоты (20:1), эйкозадиеновой кислоты (20:2), эйкозатетраеновой кислоты (20:4), эйкозапентаеновой кислоты (20:5) (ЭПК), докозановой кислоты (22:0), докозеновой кислоты (22:1), докозапентаеновой кислоты (22:5), докозагексаеновой кислоты (22:6) (ДГК) и тетракозановой кислоты (24:0). В некоторых вариантах осуществления композиция содержит по меньшей мере один модифицированный липид, например липид, модифицированный путем варки.
[0099] В некоторых вариантах осуществления бактериальная композиция содержит по меньшей мере один дополнительный минерал или минеральный источник. Примеры минералов включают, без ограничения: хлорид, натрий, кальций, железо, хром, медь, иод, цинк, магний, марганец, молибден, фосфор, калий и селен. Подходящие формы любого из вышеупомянутых минералов включают растворимые минеральные соли, малорастворимые минеральные соли, нерастворимые минеральные соли, хелатные минералы, минеральные комплексы, нереактивные минералы, такие как карбонильные минералы, и восстановленные минералы, а также их комбинации.
[0100] В некоторых вариантах осуществления бактериальная композиция содержит по меньшей мере один дополнительный витамин. По меньшей мере, один витамин может быть жиро- или водорастворимым витамином. Подходящие витамины включают, но не ограничиваются ими, витамин С, витамин А, витамин Е, витамин В12, витамин K, рибофлавин, ниацин, витамин D, витамин В6, фолиевую кислоту, пиридоксин, тиамин, пантотеновую кислоту и биотин. Подходящими формами любого из вышеперечисленного являются соли витамина, производные витамина, соединения, обладающие такой же или подобной активностью витамина, а также метаболиты витамина.
[0101] В некоторых вариантах осуществления бактериальная композиция содержит наполнитель. Неограничивающие примеры подходящих наполнителей включают буферный агент, консервант, стабилизатор, связующий агент, уплотняющий агент, смазывающий агент, усилитель дисперсии, дезинтегрирующий агент, ароматизатор, подсластитель и красящее вещество.
[0102] В некоторых вариантах осуществления наполнитель может представлять собой буферный агент. Неограничивающие примеры подходящих буферных агентов включают цитрат натрия, карбонат магния, бикарбонат магния, карбонат кальция и бикарбонат кальция.
[0103] В некоторых вариантах осуществления наполнитель включает консервант. Неограничивающие примеры подходящих консервантов включают антиоксиданты, такие как альфа-токоферол и аскорбат, и противомикробные средства, такие как парабены, хлорбутанол и фенол.
[0104] В некоторых вариантах осуществления бактериальная композиция содержит связующий агент в качестве наполнителя. Неограничивающие примеры подходящих связующих агентов включают крахмалы, прежелатинизированные крахмалы, желатин, поливинилпиролидон, целлюлозу, метилцеллюлозу, карбоксиметилцеллюлозу натрия, этилцеллюлозу, полиакриламиды, поливинилоксоазолидон, поливиниловые спирты, спирт жирных кислот С12-С18, полиэтиленгликоль, полиолы, сахариды, олигосахариды и их комбинации.
[0105] В некоторых вариантах осуществления бактериальная композиция содержит смазывающий агент в качестве наполнителя. Неограничивающие примеры подходящихсмазывающих агентов включают стеарат магния, стеарат кальция, стеарат цинка, гидрогенизированные растительные масла, стеротекс, моностеарат полиоксиэтилена, тальк, полиэтиленгликоль, бензоат натрия, лаурилсульфат натрия, лаурилсульфат магния и легкое минеральное масло.
[0106] В некоторых вариантах осуществления бактериальная композиция содержит усилитель дисперсии в качестве наполнителя. Неограничивающие примеры подходящих диспергирующих агентов включают крахмал, альгиновую кислоту, поливинилпирролидоны, гуаровую камедь, каолин, бентонит, очищенную древесную целлюлозу, крахмалгликолят натрия, изоаморфный силикат и микрокристаллическую целлюлозу в качестве поверхностно-активных эмульгаторов с высоким значением HLB.
[0107] В некоторых вариантах осуществления бактериальная композиция содержит разрыхлитель в качестве наполнителя. В некоторых вариантах осуществления разрыхлитель представляет собой нешипучий разрыхлитель. Неограничивающие примеры подходящих разрыхлителей включаюткрахмалы, такие как кукурузный крахмал, картофельный крахмал, их прежелатенизированные и модифицированные формы, подсластители, глины, такие как бентонит, микрокристаллическую целлюлозу, альгинаты, натрия крахмал гликолят, камеди, такие как агар, гуар, плоды рожкового дерева, карайя, пектин и трагакант. В некоторых вариантах осуществления разрыхлитель представляет собой шипучий разрыхлитель. Неограничивающие примеры подходящих шипучих разрыхлителей включают бикарбонат натрия в комбинации с лимонной кислотой и бикарбонат натрия в комбинации с винной кислотой.
[0108] В некоторых вариантах осуществления наполнитель включает ароматизатор. Ароматизаторы могут быть выбраны из синтетических ароматизирующих масел и ароматизирующих отдушек; натуральных масел; экстрактов из растений, листьев, цветов, и плодов; и их комбинации. В некоторых вариантах осуществления ароматизатор выбран из масел корицы; гаультериевого масла; масла мяты перечной; масла клевера; масла сенны; анисового масла; эвкалипта; ванили; масла цитрусовых, такого как масло лимона, масло апельсина, масло винограда и грейпфрута; и фруктовых эссенций, включая яблоко, персик, грушу, клубнику, малину, вишню, сливу, ананас и абрикос.
[0109] В некоторых вариантах осуществления наполнитель включает подсластитель. Неограничивающие примеры подходящих подсластителей включают глюкозу (кукурузный сироп), декстрозу, инвертный сахар, фруктозу и их смеси (когда не используется в качестве носителя); сахарин и его различные соли, такие как натриевая соль; дипептидные подсластители, такие как аспартам; дигидрохальконовые соединения, глицирризин; стевию медовую (стевиозид); хлорпроизводные сахарозы, такие как сукралоза; и сахарные спирты, такие как сорбит, маннит, силит и тому подобное. Также рассматриваются гидрогенизированные гидролизаты крахмала и синтетический подсластитель 3,6-дигидро-6-метил-1,2,3-оксатиазин-4-он-2,2-диоксид, в частности соль калия (ацесульфам-К) и их соли натрия и кальция.
[0110] В некоторых вариантах осуществления бактериальная композиция содержит красящее вещество. Неограничивающие примеры подходящих красителей включают пищевые, лекарственные и косметические красители (FD&C), лекарственные и косметические красители (D&C), наружные лекарственные и косметические красители (Ext. D&C). Красящие вещества можно использовать в качестве красителей или их соответствующих пигментов.
[0111] Массовая доля наполнителя или комбинации наполнителей в составе обычно составляет около 99% или менее, например, около 95% или менее, около 90% или менее, около 85% или менее, около 80% или менее, около 75% или менее, около 70% или менее, около 65% или менее, около 60% или менее, около 55% или менее, 50% или менее, около 45% или менее, около 40% или менее, около 35% или менее, около 30% или менее, около 25% или менее, около 20% или менее, около 15% или менее, около 10% или менее, около 5% или менее, около 2% или менее, около 1% или менее от общей массы композиции.
[0112] Описанные в данном документе бактериальные композиции могут быть составлены в различных формах и введены рядом различных способов. Бактериальную композицию можно принимать перорально, вводить ректально или парентерально в составах, содержащих традиционно приемлемые носители, адъюванты и несущие среды, если желательно. Термин «парентеральный» в контексте данного документа включает подкожные инъекции, внутривенную, внутримышечную, интрастернальную инъекцию или методы инфузии. В иллюстративном варианте осуществления бактериальную композицию принимают перорально.
[0113] Твердые лекарственные формы для перорального применения включают капсулы, таблетки, каплеты, пилюли, троше, пастилки, порошки и гранулы. Капсула как правило содержит материал сердцевины, содержащий бактериальную композицию, и стенку оболочки, которая инкапсулирует материал сердцевины. В некоторых вариантах осуществления материал сердцевины включает по меньшей мере одно из твердого вещества, жидкости и эмульсии. В некоторых вариантах осуществления материал стенки оболочки содержит по меньшей мере одно из мягкого желатина, твердого желатина и полимера. Подходящие полимеры включают, но не ограничиваются ими: целлюлозные полимеры, такие как гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза (НРМС), метилцеллюлоза, этилцеллюлоза, ацетат целлюлозы, фталат ацетата целлюлозы, тримеллитат ацетата целлюлозы, гидроксипропилметалтилцеллюлозы, сукцинат гидроксипропилметилцеллюлозы и натрийкарбоксиметилцеллюлоза; полимеры и сополимеры акриловой кислоты, такие как те, которые образованы из акриловой кислоты, метакриловой кислоты, метилакрилата, аммонийметилакрилата, этилакрилата, метилметакрилата и/или этилметакрилата (например, те сополимеры, которые продаются под торговым наименованием «Eudragit»); виниловые полимеры и сополимеры, такие как поливинилпирролидон, поливинилацетат, поливинилацетатфталат, сополимер винилацетата и кротоновой кислоты, и сополимеры этилена и винилацетата; и шеллак (очищенный лак). В некоторых вариантах осуществления по меньшей мере один полимер действует в качестве вещества, корригирующего вкус.
[0114] Таблетки, пилюли и тому подобное могут быть запрессованы, многократно запрессованы, многослойными и/или с покрытыми оболочкой. Покрытие может быть однослойным или многослойным. В некоторых вариантах осуществления материал покрытия содержит по меньшей мере один из сахарида, полисахарида и гликопротеинов, экстрагированных по меньшей мере из одного растения, гриба и микроорганизма. Неограничивающие примеры включают кукурузный крахмал, пшеничный крахмал, картофельный крахмал, крахмал тапиоки, целлюлозу, гемицеллюлозу, декстраны, мальтодекстрин, циклодекстрины, инулины, пектин, маннаны, гуммиарабик, камедь рожкового дерева, мескитовую камедь, гуаровую камедь, камедь карайи, гаттиевую камедь, трагакантовую камедь, фунори, каррагинаны, агар, альгинаты, хитозаны или геллановую камедь. В некоторых вариантах осуществления материал покрытия содержит белок. В некоторых вариантах осуществления материал покрытия содержит по меньшей мере одно из жира и масла. В некоторых вариантах осуществления по меньшей мере одно из жира и масла плавится при высокой температуре. В некоторых вариантах осуществления по меньшей мере одно из жира и масла гидрогенизировано или частично гидрогенизировано. В некоторых вариантах осуществления по меньшей мере одно из жира и масла получено из растения. В некоторых вариантах осуществления по меньшей мере одно из жира и масла содержит по меньшей мере одно из глицеридов, свободных жирных кислот и сложных эфиров жирных кислот. В некоторых вариантах осуществления материал покрытия содержит по меньшей мере один пищевой воск. Пищевой воск может быть получен из животных, насекомых или растений. Неограничивающие примеры включают пчелиный воск, ланолин, воск восковицы, карнаубский воск и воск из рисовых отрубей. Таблетки и пилюли могут быть дополнительно приготовлены с энтеросолюбильным покрытием.
[0115] В качестве альтернативы порошки или гранулы, содержащие бактериальную композицию, описанную в данном документе, могут быть включены в пищевой продукт. В некоторых вариантах осуществления пищевой продукт представляет собой напиток для перорального применения. Неограничивающие примеры подходящего напитка включают фруктовый сок, фруктовый напиток, напиток с искусственным вкусом, напиток с искусственным подслащением, газированный напиток, спортивный напиток, жидкий молочный продукт, коктейль, алкогольный напиток, напиток с кофеином, детские смеси и так далее. Другие подходящие средства для перорального применения включают водные и неводные растворы, эмульсии, суспензии и растворы и/или суспензии, восстановленные из нешипучих гранул, содержащие по меньшей мере один из подходящих растворителей, консервантов, эмульгаторов, суспендирующих агентов, разбавителей, подсластителей, красящих веществ и ароматизаторов.
[0116] В некоторых вариантах осуществления пищевой продукт представляет собой твердый пищевой продукт. Подходящие примеры твердых пищевых продуктов включают без ограничения пищевой батончик, энергетический батончик, печенье, пирожное, маффин, крекер, брикет мороженого, брикет замороженного йогурта и т.п.
[0117] В некоторых вариантах осуществления бактериальная композиция, описанная в данном документе, включается в лечебный продукт питания. В некоторых вариантах осуществления лечебный продукт питания представляет собой готовый к употреблению продукт, который необязательно содержит некоторые или все основные макроэлементы и микроэлементы. В некоторых вариантах осуществления бактериальная композиция, описанная в данном документе, включена в дополнительный продукт питания, который предназначен для смешивания с пищей. В некоторых вариантах осуществления дополнительный продукт питания содержит некоторые или все основные макроэлементы и микроэлементы. В некоторых вариантах осуществления бактериальная композиция, описанная в данном документе, смешивается с существующим пищевым продуктом или добавляется к нему для усиления белкового содержания пищевого продукта. Примеры включают основные продукты питания (зерновые культуры, соль, сахар, растительное масло, маргарин), напитки (кофе, чай, газированные напитки, пиво, спиртные напитки, спортивные напитки), закуски, сладости и другие продукты.
[0118] В некоторых вариантах осуществления составами заполняют желатиновые капсулы для перорального применения. Примером подходящей капсулы является желатиновая капсула 250 мг, содержащая от 10 (до 100 мг) лиофилизированного порошка (от 108 до 1011 бактерий), 160 мг микрокристаллической целлюлозы, 77,5 мг желатина и 2,5 мг стеарата магния. В других вариантах осуществления можно использовать от 105 до 1012 бактерий, от 105 до 107, от 106 до 107 или от 108 до 1010, с соответствующими корректировками наполнителей, при необходимости. В дополнительных вариантах осуществления можно использовать капсулу или таблетку с энтеросолюбильным покрытием или с буферной или защитной композицией.
[0119] В некоторых вариантах осуществления количество бактерий каждого типа может присутствовать в одном и том же количестве или в разных количествах. Например, в бактериальной композиции с двумя типами бактерий бактерии могут присутствовать в соотношении от 1:10000 до соотношения 1:1, в соотношении от 1:10000 до соотношения 1:1000, в соотношении от 1:1000 до соотношения 1:100 соотношение, в соотношении от 1:100 до соотношения 1:50, в соотношении от 1:50 до соотношения 1:20, в соотношении от 1:20 до соотношения 1:10, в соотношении от 1:10 до соотношения 1:1. В случае бактериальных композиций, содержащих по меньшей мере три типа бактерий, соотношение типов бактерий может быть выбрано попарно из соотношений для бактериальных композиций с двумя типами бактерий. Например, в бактериальной композиции, содержащей бактерии А, В и С, по меньшей мере одно из соотношения между бактериями А и В, соотношения между бактериями В и С и соотношения между бактериями А и С может быть выбрано независимо, из парных комбинаций, представленных выше.
III. Способы лечения субъекта
[0120] Композиции, описанные в данном документе, могут быть использованы для лечения воспалительного заболевания кишечника (ВЗК) (например, язвенного колита или болезни Крона), например, путем облегчения одного или более признаков или симптомов заболевания (например, индукции ремиссии), и/или для уменьшения рецидивов активного заболевания (например, для поддержания ремиссии).
[0121] В некоторых вариантах осуществления лечение составом, описанным в данном документе, повышает уровень вторичной желчной кислоты, при этом вторичная желчная кислота выбрана из группы, состоящей из дезоксихолевой кислоты (ДХК), 3α-12-оксо-дезоксихолевой кислоты, 3β-12α-дезоксихолевой кислоты (3-изо-дезоксихолевой кислоты), 7α-3-оксо-хенодезоксихолевой кислоты, литохолевой кислоты (ЛХК), 3-оксо-ЛХК, оксо-ЛХК, изо-ЛХК и их комбинаций. В некоторых вариантах осуществления лечение составом по данному изобретению снижает уровень вторичной желчной кислоты, при этом вторичной желчной кислотой является УДХК. В некоторых вариантах осуществления УДХК может повышать содержание провоспалительных медиаторов (например, ИЛ-8), вырабатываемых, например, эпителиальными клетками кишечника.
[0122] В некоторых вариантах повышение и/или снижение содержания некоторых вторичных желчных кислот ассоциируется по меньшей мере с одним из следующих факторов: (i) повышением разнообразия микробиома желудочно-кишечного тракта (ЖКТ) у пациента с диагнозом ВЗК (например, язвенный колит или болезнь Крона), (ii) уменьшением воспаления желудочно-кишечного тракта у пациента (например, с диагнозом ВЗК), (iii) улучшением целостности слизистых оболочек и эпителиального барьера в популяции пациентов с ВЗК по сравнению с пациентами с ВЗК, не получавшими лечения, (iv) улучшением целостности слизистых оболочек и эпителиального барьера у пациента с ВЗК по сравнению с состоянием до лечения, (v) содействием заживлению слизистой оболочки (которое можно оценить, например, по снижению количества баллов по шкале Майо при эндоскопическом исследовании), и (vi) другими улучшениями по крайней мере одного признака или симптома ВЗК (например, ремиссия заболевания). Такие улучшения могут также включать, например, улучшения, обнаруживаемые с помощью биомаркеров, такие как снижение уровня фекального кальпротектина после лечения. Оценки по шкале Майо известны в данной области техники, например, см. globalrph.com/mayo_clinic_score.htm. Снижение общего балла по шкале Майо по сравнению с баллом до лечения и/или улучшение при ректальном кровотечении и/или оценки по эндоскопической подшкале указывают на терапевтический эффект.
[0123] В некоторых вариантах осуществления частота клинической ремиссии после лечения описанным в данном документе составом составляет не менее 20%, 25%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 90%, 95% или 100%. В некоторых вариантах осуществления показатель клинической ремиссии улучшается по сравнению с плацебо, например, по меньшей мере на 60% по сравнению с 30%, соответственно. В некоторых вариантах осуществления клиническая ремиссия представляет собой оценку по шкале Майо ≤2 балла, без индивидуальной оценки по подшкале >1. В некоторых вариантах осуществления клинический ответ на лечение составом улучшается по сравнению с плацебо, например, по меньшей мере на 60% по сравнению с 30%, соответственно. Заживление слизистой оболочки определяется как 0 или 1 по эндоскопической подшкале шкалы Майо. В некоторых вариантах осуществления клинический ответ представляет собой снижение по сравнению с исходным уровнем оценки по шкале Майо на ≥30% и ≥3 балла, сопровождающееся уменьшением балла по подшкале ректального кровотечения на ≥1 или балл по подшкале ректального кровотечения от 0 до 1. В некоторых вариантах осуществления клинический ответ определяется как снижение общей модифицированной оценки по шкале Майо (TMMS - англ.: Total Modified Mayo Score) на ≥3 балла по сравнению с исходным уровнем, наряду с по меньшей мере одним из снижением на >1 балл по подшкале ректального кровотечения или подшкале абсолютного ректального кровотечения 0 или 1. Полная ремиссия определяется как TMMS < 2 и балл по эндоскопической подшкале 0 без эритемы, крови и признаков воспаления. Эндоскопическое улучшение определяется как снижение общей модифицированной оценки по эндоскопической подшкале Майо > 1.
[0124] Описанные в данном документе составы могут быть применимы в различных клинических ситуациях. Например, состав можно вводить в качестве дополнительного лечения антибиотиками, когда пациент страдает острой инфекцией, чтобы снизить риск рецидива после утихания острой инфекции или, если пациент будет находиться в непосредственной близости от других с серьезными желудочно-кишечными инфекциями или риском их развития (врачи, медсестры, работники больницы, члены семей заболевших или госпитализированных).
[0125] Составы по данному описанию можно вводить животным, включая людей, лабораторных животных (например, приматов, крыс и мышей), сельскохозяйственных животных (например, коров, овец, коз, свиней, индеек и кур) и домашних питомцев (например, собак, кошек и грызунов). В некоторых вариантах осуществления состав вводят человеку. В некоторых вариантах осуществления у субъекта-человека имеется один или более признаков или симптомов ВЗК (например, язвенного колита или болезни Крона), например, диареи (например,, содержащей кровь или гной); боли в животе и спазмы; ректальная боль; ректальное кровотечение; императивные позывы к дефекации; невозможность дефекации, несмотря на императивные позывы; потеря массы тела; усталость; повышенная температура тела; задержка роста (у детей); сильное кровотечение; перфорированная толстая кишка; сильное обезвоживание; заболевание печени; остеопороз; воспаление кожи, суставов или глаз; язвы во рту; повышенный риск рака толстой кишки; токсичный мегаколон; или повышенный риск образования тромбов в венах и артериях. Терапевтически эффективное лечение с использованием состава, предложенного в данном документе, может улучшить один или более из таких признаков и симптомов.
[0126] В некоторых вариантах осуществления субъект (например, пациент-человек) получает протокол предварительного лечения перед введением состава, при этом протокол предварительного лечения подготавливает желудочно-кишечный тракт для приема бактериальной композиции. В некоторых вариантах осуществления протокол предварительного лечения включает лечение антибиотиками, при этом лечение антибиотиками изменяет состав бактерий у пациента. В других вариантах осуществления протокол предварительного лечения включает очистку толстой кишки (например, клизму), при которой очистка толстой кишки по существу опустошает содержимое толстой кишки пациента. В контексте данного документа термин «существенное опорожнение содержимого толстой кишки» относится к удалению по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95%, или около 100% содержимого обычного объема содержимого толстой кишки. Протоколу очищения толстой кишки может предшествовать лечение антибиотиками.
[0127] В некоторых вариантах осуществления протокол предварительного лечения вводят пациенту по меньшей мере за 1 день, 2 дня, 3 дня, 5 дней, 6 дней, 7 дней, 10 дней или 15 дней до введения описанного в данном документе состава. В некоторых вариантах осуществления субъект получает несколько доз состава. В некоторых вариантах осуществления у субъекта имеется по меньшей мере один признак или симптом ВЗК (например, язвенного колита или болезни Крона) до введения состава. В других вариантах осуществления у субъекта не проявляется признак или симптом ВЗК (например, язвенного колита или болезни Крона) до введения состава, например, состав вводят в профилактических целях, чтобы снизить риск признака или симптома активного ВЗК.
[0128] В некоторых вариантах осуществления описанный в данном документе состав вводится энтерально, другими словами, путем доступа в желудочно-кишечный тракт. Это включает пероральное применение, ректальное введение (включая клизму, суппозиторий или колоноскопию), через оральный или назальный зонд (назогастральный, назоеюнальный, оральный желудочный или оральноеюнальный) или любой другой способ, известный в данной области.
[0129] В некоторых вариантах осуществления состав вводят по меньшей мере в одну область желудочно-кишечного тракта, включая рот, пищевод, желудок, тонкую кишку, толстую кишку и прямую кишку. В других вариантах осуществления состав вводят во все области желудочно-кишечного тракта. В некоторых вариантах осуществления состав вводят перорально в форме лекарственных средств, таких как порошки, капсулы, таблетки, гели или жидкости. Состав также можно вводить в форме геля или жидкости пероральным путем или через назогастральный зонд или ректальным путем в форме геля или жидкости, при помощи клизмы, или инсталляции через колоноскоп, или суппозиторий.
[0130] В некоторых вариантах осуществления бактерии и бактериальные композиции представлены в лекарственной форме. В некоторых вариантах осуществления лекарственная форма предназначена для введения по меньшей мере одной ОТЕ или их комбинации, описанных в данном документе, при этом общее количество вводимой бактериальной композиции выбрано из от 0,1 нг до 10 г, от 10 нг до 1 г, от 100 нг до 0,1 г, от 0,1 мг до 500 мг, от 1 мг до 100 мг или от 10 до 15 мг. В некоторых вариантах осуществления бактериальная композиция потребляется в количестве от 0,1 нг до 10 г в день, от 10 нг до 1 г в день, от 100 нг до 0,1 г в день, от 0,1 до 500 мг в день, от 1 до 100 мг в день или от 10-15 мг в день и более.
[0131] В некоторых вариантах осуществления период лечения составляет по меньшей мере 1 день, по меньшей мере 2 дня, по меньшей мере 3 дня, по меньшей мере 4 дня, по меньшей мере 5 дней, по меньшей мере 6 дней, по меньшей мере 1 неделю, по меньшей мере 2 недели, по меньшей мере 3 недели, по меньшей мере 4 недели, по меньшей мере 1 месяц, по меньшей мере 2 месяца, по меньшей мере 3 месяца, по меньшей мере 4 месяца, по меньшей мере 5 месяцев, по меньшей мере 6 месяцев или по меньшей мере 1 год. В некоторых вариантах осуществления период лечения составляет от 1 дня до 1 недели, от 1 недели до 4 недель, от 1 месяца до 3 месяцев, от 3 месяцев до 6 месяцев, от 6 месяцев до 1 года или более года.
[0132] В некоторых вариантах осуществления от 105 до 1012 микроорганизмов вводят пациенту в данной лекарственной форме. В некоторых вариантах осуществления эффективное количество может быть предоставлено в количестве от 1 до 500 мл или от 1 до 500 граммов бактериальной композиции, содержащей от 107 до 1011 бактерий на мл или на грамм, или в капсуле, таблетке или суппозитории, содержащих от 1 мг до 1000 мг лиофилизированного порошка, содержащего от 107 до 1011 бактерий. В некоторых вариантах осуществления пациенты, получающие острое лечение, получают более высокие дозы, чем те, кто получает постоянное лечение (например, работники больницы или пациенты, госпитализированные в учреждения длительного ухода).
[0133] В некоторых вариантах осуществления описанный в данном документе состав вводят один раз, один раз или несколько раз, например, один раз в день в течение нескольких дней или более одного раза в день в день введения (включая два раза в день, три раза в день или до пяти раз в день). В некоторых вариантах осуществления состав вводят с перерывами в соответствии с установленным графиком, например, один раз в неделю, один раз в месяц или в случае рецидива основного заболевания у пациента. В других вариантах осуществления состав вводят на длительной основе людям, которые подвержены риску заражения этими патогенами или, которые могут быть носителями этих патогенов, включая людей, которым предстоит проведение инвазивной медицинской процедуры (например, хирургической операции), которые будут госпитализированы, проживающих в учреждении долговременного ухода или реабилитации, подверженных воздействию патогенов в силу своей профессии (работники отрасли животноводства) или, которые могут быть переносчиками патогенов (включая работников больниц, таких как врачи, медсестры и другие специалисты в области здравоохранения).
[0134] В некоторых вариантах осуществления бактериальную композицию по настоящему описанию вводят с другими агентами (например, антимикробными агентами или пребиотиками) в качестве режима комбинированной терапии. В некоторых вариантах осуществления введение является последовательным в течение часов или дней. В других вариантах осуществления введение является одновременным.
[0135] В некоторых вариантах осуществления бактериальная композиция включена в комбинированную терапию одним или более антимикробными средствами, которые включают антибактериальные средства, противогрибковые средства, противовирусные средства и антипаразитарные средства.
[0136] Антибактериальные средства включают цефалоспориновые антибиотики (цефалексин, цефуроксим, цефадроксил, цефазолин, цефалотин, цефаклор, цефамандол, цефокситин, цефпрозил и цефтобипрол); фторхинолоновые антибиотики (ципро, леваквин, флоксин, текин, авелокс и норфлокс); тетрациклиновые антибиотики (тетрациклин, миноциклин, окситетрациклин и доксициклин); пенициллиновые антибиотики (амоксициллин, ампициллин, пенициллин V поколения, диклоксациллин, карбенициллин, ванкомицин и метициллин); и карбапенемные антибиотики (эртапенем, дорипенем, имипенем/циластатин и меропенем).
[0137] Противовирусные средства включают абакавир, ацикловир, адефовир, ампренавир, атазанавир, цидофовир, дарунавир, делавирдин, диданозин, докозанол, эфавиренц, элвитегравир, эмтрицитабин, энфувиртид, этравирин, фамцикловир, фоскарнет, фомивирсен, ганцикловир, индинавир, идоксуридин, ламивудин, лопинавир, маравирок, МК-2048, нельфинавир, невирапин, пенцикловир, ралтегравир, рилпивирин, ритонавир, саквинавир, ставудин, тенофовир, трифлуридин, валацикловир, валганцикловир, видарабин, ибацитабин, амантадин, осельтамивир, римантидин, типранавир, зальцитабин, занамивир и зидовудин.
[0138] Примеры противогрибковых соединений включают, но не ограничиваются ими, полиеновые противогрибковые средства, такие как натамицин, римоцидин, филипин, нистатин, амфотерицин В, кандицин и хамицин; имидазольные противогрибковые средства, такие как миконазол, кетоконазол, клотримазол, эконазол, омоконазол, бифоназол, бутоконазол, фентиконазол, изоконазол, оксиконазол, сертаконазол, сульконазол и тиоконазол; триазольные противогрибковые средства, такие как флуконазол, итраконазол, изавуконазол, равуконазол, позаконазол, вориконазол, терконазол и альбаконазол; тиазольные противогрибковые средства, такие как абафунгин; аллиламиновые противогрибковые средства, такие как тербинафин, нафтифин и бутенафин; и противогрибковые средства на основе эхинокандина, такие как анидулафунгин, каспофунгин и микафунгин. Другие соединения, которые обладают противогрибковыми свойствами, включают, но не ограничиваются ими, полигодиал, бензойную кислоту, циклопирокс, толнафтат, ундециленовую кислоту, флуцитозин или 5-фторцитозин, гризеофульвин и галопрогин.
[0139] В некоторых вариантах осуществления бактериальная композиция включена в комбинированную терапию одним или более кортикостероидами, месалазином, месаламином, сульфасалазином, производными сульфасалазина, иммунодепрессантами, циклоспорином А, меркаптопурином, азатиопурином, преднизоном, метотрексатом, антигистаминными препаратами, глюкокортикоидами, адреналином, теофиллином, кромолином натрия, антилейкотриенами, антихолинергическими препаратами для лечения ринита, антихолинергическими противоотечными средствами, стабилизаторами тучных клеток, моноклональными антителами против IgE, вакцинами и их комбинацией.
[0140] Пребиотик представляет собой селективно ферментированный ингредиент, который допускает определенные изменения как в составе так и/или в активности микробиоты желудочно-кишечного тракта, которая способствует благополучию и здоровью хозяина. Пребиотики могут включать сложные углеводы, аминокислоты, пептиды или другие важные пищевые компоненты для выживания бактериальной композиции. Пребиотики включают, но не ограничиваются ими, аминокислоты, биотин, фруктоолигосахарид, галактоолигосахариды, инулин, лактулозу, маннановые олигосахариды, обогащенный олигофруктозой инулин, олигофруктозу, олигодекстрозу, тагатозу, трансгалактоолигосахарид и ксхаолигосахарид.
[0141] Данное описание наиболее полно понимается в свете основополагающих ссылок, цитируемых в описании. Варианты осуществления в рамках описания обеспечивают иллюстрацию вариантов осуществления и не должны толковаться как ограничение объема. Специалисту в данной области техники будет понятно, что охватываются многие другие варианты осуществления. Все публикации, патенты и патентные заявки, цитируемые в данном описании, включены в данный документ посредством ссылки во всей своей полноте. В тех случаях, когда включенный посредством ссылки материал противоречит или не согласуется с данным описанием, данное описание имеет приоритет относительно любого такого материала. Цитирование любых ссылок в данном документе не является признанием того, что такие ссылки являются предшествующим уровнем техники.
[0142] Если не указано иное, все числа, выражающие количества ингредиентов, условия реакции и т.д., используемые в описании, включая формулу изобретения, следует понимать как измененные во всех случаях термином «примерно». Соответственно, если не указано иное, числовые параметры являются приблизительными и могут варьироваться в зависимости от желаемых свойств, которые должны быть получены. По меньшей мере, и не как попытка ограничить применение доктрины эквивалентов к объему формулы изобретения, каждый числовой параметр должен истолковываться с учетом числа сообщаемых значимых цифр и обычных методов округления.
[0143] Следующие примеры приведены с целью иллюстрации, а не с целью ограничения. Содержание всех ссылок, процитированных в данной заявке, специально включено в данный документ посредством ссылки.
ПРИМЕРЫ
Пример 1: Анализ уровня желчных кислот у пациентов с язвенным колитом после введения популяции спор, полученных из фекалий здорового человека (ПСЗЧ)
[0144] Для понимания роли желчных кислот в воспалительных заболеваниях кишечника (ВЗК) уровни вторичных желчных кислот, ассоциированных с путем 7α-дегидроксилазы (т.е. ДХК, ЛХК, 3-оксо-ЛХК, 3α-12-оксо-дезоксихолевой кислоты и 3β-12α-дезоксихолевой кислоты), были количественно определены в образцах кала, полученных от пациентов с язвенным колитом, которые получали различные схемы лечения. Схемы лечения включали одно из следующих: (А) только плацебо; (В) плацебо с последующим еженедельным дозированием популяции спор, полученных из фекалий здорового человека («ПСЗЧ»); (С) ванкомицин с последующим еженедельным введением ПСЗЧ; и (D) ванкомицин с последующим ежедневным дозированием ПСЗЧ. Концентрации желчных кислот измеряли в четырех различных временных точках: (1) исходный уровень (т.е. до введения ванкомицина или ПСЗЧ) («Визит 1»); (2) сразу после лечения ванкомицином (при необходимости) («Визит 4»); (3) через 2 недели после начала введения ПСЗЧ (при необходимости) («Визит 6»); и (4) через 8 недель после начала введения спорообразующей фракции (при необходимости) («Визит 12»).
Экстракция желчных кислот из образцов кала человека
[0145] Образцы кала человека были разделены на аликвоты, взвешены и гомогенизированы в 10-кратном мас./об. буфере для экстракции (50% метанол в воде). Образцы экстрагировали на льду в течение 1 часа, а затем дополнительно экстрагировали равным объемом холодного ацетонитрила. Затем экстракты центрифугировали и супернатант фильтровали через фильтр с размером пор 0,22 мкм перед анализом методом жидкостной хроматографии с тандемной масс-спектрометрией (ЖХ-МС). В стандарты меченых желчных кислот добавляли добавки до и после экстракции, чтобы обеспечить контроль качества экстракции и анализа метаболитов. Аликвоту каждого образца также взвешивали, а затем сушили для определения содержания воды в образце и сухого веса.
Анализ ЖХ-МС желчных кислот
[0146] Желчные кислоты разделяли с использованием Agilent 1260 HPLC, снабженной колонкой Microsolv bidentate С18, которой предшествовал 0,2-мкм предколоночный фильтр. Разделение осуществляли с использованием воды и градиента ацетонитрила с 0,1% муравьиной кислотой при скорости потока 0,4 мл/мин. Образцы вводили в объеме 5 мкл. Система ВЭЖХ была присоединена к времяпролетному квадрупольному микромасс-спектрометру Bruker Compass™ qTOF, откалиброванному до диапазона масс от 50 до 1700 м/з с использованием смеси для настройки Agilent Low-mass tuning mix. Каждый прогон был дополнительно откалиброван по эталонному раствору массы, введенному в начале каждого прогона. Желчные кислоты были обнаружены в режиме определения отрицательных ионов и идентифицированы по уникальным м/з и времени удерживания по сравнению с известными чистыми стандартами. Площадь под пиком была определена с использованием программного обеспечения для анализа данных Bruker. Желчные кислоты определяли количественно с использованием калибровочных кривых, полученных из чистых стандартов, в концентрации от 0,001 мкМ до 100 мкМ. Желчные кислоты, обнаруженные методом ЖХ-МС, приведены в таблице 1 ниже
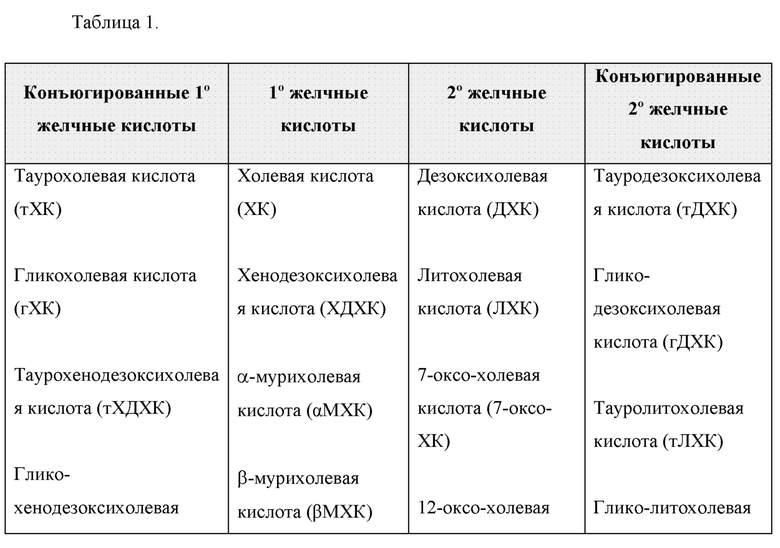
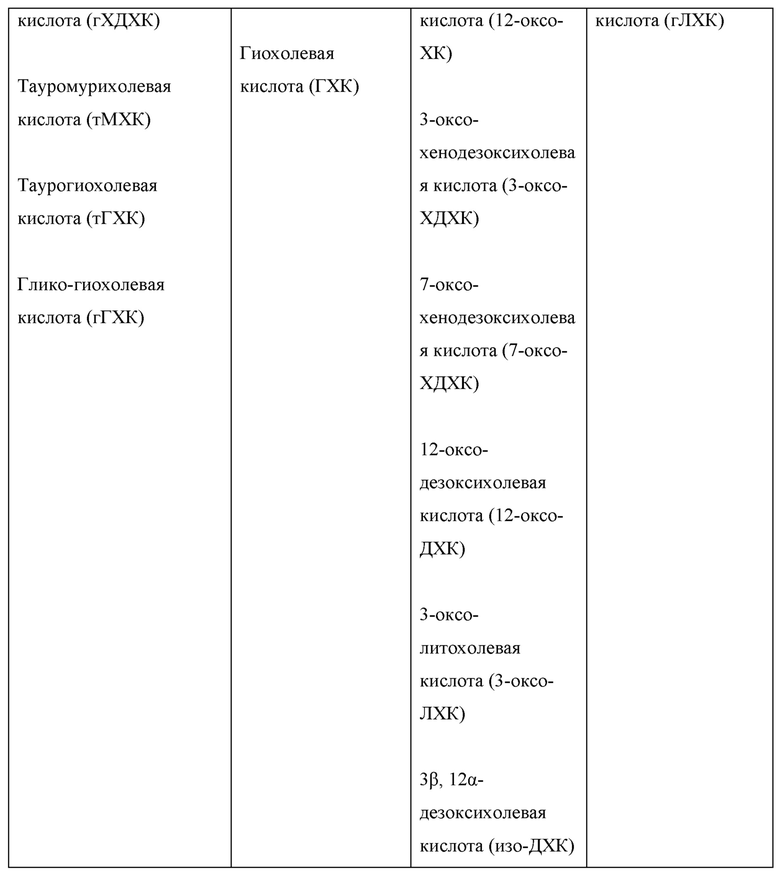
[0147] Как показано на ФИГ. 1, пациенты с язвенным колитом, получавшие ванкомицин с последующим введением ПСЗЧ (С и D), имели повышенные уровни вторичных желчных кислот, ассоциированных с путем 7α-дегидроксилазы в их образцах кала по сравнению с соответствующими уровнями у пациентов до введения. Наибольшее повышение наблюдалось у пациентов, получавших ванкомицин с последующим ежедневным дозированием ПСЗЧ (D). Напротив, у пациентов, получавших только плацебо, не было заметного повышения концентрации измеренных вторичных желчных кислот (А). Этот результат предполагает, что одна или более спорообразующих бактерий, присутствующих в ПСЗЧ, могут отвечать за повышение концентраций желчных кислот, наблюдаемое у пациентов с язвенным колитом.
Пример 2: Анализ уровня желчных кислот у пациентов с язвенным колитом в стадии ремиссии
[0148] Для оценки потенциальной взаимосвязи между уровнями желчных кислот и ремиссией заболевания, уровни различных желчных кислот сравнивали между пациентами с язвенным колитом, находящимися в стадии ремиссии («пациенты с ремиссией»), и теми, у кого было активное заболевание («пациенты без ремиссии»). Пациенты с язвенным колитом получали одну из схем лечения, описанных в Примере 1. Желчные кислоты экстрагировали из образцов фекалий и количественно определяли, как описано в Примере 1 выше.
[0149] Как показано на ФИГ. 2A-2F и ФИГ. 3A-3F, пациенты с ремиссией экспрессировали более высокие уровни следующих вторичных желчных кислот по сравнению с пациентами без ремиссии: дезоксихолевая кислота (ДХК) (ФИГ. 2А и 3А), ЛХК (ФИГ. 2В и 3В), 3α-12-оксо-дезоксихолевая кислота (ФИГ. 2С и 3С), 7α-3-оксохенодезоксихолевая кислота (ФИГ. 2D и 3D), 3-оксо-ЛХК (ФИГ. 2Е и 3Е) и 3β-12α-оксо-дезоксихолевая кислота (3-изодезоксихолевая кислота) (ФИГ. 2F и 3F). Напротив, уровень УДХК (ФИГ. 2G и 3G) был значительно выше у пациентов без ремиссии по сравнению с пациентами с ремиссией, что позволяет предположить, что не все вторичные желчные кислоты имеют сходные профили при воспалительном заболевании кишечника (например, язвенном колите). Приведенные выше данные также показывают, что ремиссия ВЗК напрямую связана с повышением содержания некоторых желчных кислот (например, тех, которые ассоциированы с путем 7α-дегидроксилазы) и снижением уровней УДХК.
[0150] Эти данные указывают на то, что изменение уровня вторичных желчных кислот может быть применимо для лечения воспалительного заболевания кишечника.
Пример 3: Оценка противовоспалительного действия вторичных желчных кислот на активированные моноциты и МКПК
[0151] Для лучшего понимания возможной свяи между повышенным уровнем некоторых вторичных желчных кислот и ремиссией язвенного колита, моноциты и МКПК активировали ЛПС в присутствии различных концентраций разных первичных и вторичных желчных кислот в их конъюгированных и неконъюгированных формах. Количество ФНО-α и ИЛ-10, вырабатываемое активированными клетками, измеряли, как описано ниже.
Анализ секреции ФНО-α и ИЛ-10
[0152] Лейкоцитарная пленка человека была получена от компании Bioreclamation и транспортирована в течение ночи на льду. Лейкоцитарную пленку разбавляли в соотношении 1:1 с применением ФСБ и накладывали слоями поверх Фиколл-Пак (GE Healthcare, номер по каталогу 17-1440-03) в пробирках типа Falcon объемом 50 мл. Образцы центрифугировали при 500 × g в течение 20 мин при комнатной температуре без торможения. МКПК аспирировали в градиентном слое Percoll и промывали 3 раза ФСБ. Число клеток подсчитывали с помощью гемоцитометра для определения жизнеспособности и концентрации клеток. Клетки высевали на 96-луночный планшет и инкубировали при 37°С, 5% CO2 в течение 1 часа. После этого добавляли желчные кислоты в конечной концентрации 12,5 мкМ, 25 мкМ и 50 мкМ в течение одного часа перед добавлением ЛПС (1 нг/мл). После инкубации в течение 16-20 часов среды для культивирования клеток собирали для анализа цитокинов. Цитокины анализировали с использованием набора Milliplex Human Cytokine (Luminex; Millipore), анализируя ИЛ-10 и ФНО-α. Моноциты выделяли из МКПК с использованием набора для выделения моноцитов Miltenyi Biotec Pan (№по каталогу: 130-096-537) в соответствии с инструкциями производителя и анализировали, как описано выше.
[0153] Как показано на ФИГ. 4А и 4В при увеличении концентрации большинства показанных желчных кислот ЛПС-активированные МКПК выратабывали более высокие уровни ИЛ-10 и более низкие уровни ФНО-α, что подчеркивает противовоспалительное действие этих желчных кислот. Наибольшие противовоспалительные эффекты наблюдались у вторичных желчных кислот (ДХК и ЛХК) и их конъюгированных производных (тДХК, гДХК и тЛХК). Аналогичные результаты наблюдались с ЛПС-стимулированными моноцитами. См. Фиг. 5А и 5В. В соответствии с Примером 2 повышение концентрации УДХК не оказывало противовоспалительного действия на ЛРС-стимулированные моноциты или МКПК.
Пример 4: Оценка противовоспалительного действия вторичных желчных кислот на активированные эпителиальные клетки кишечника
[0154] Поскольку ВЗК в первую очередь поражает ткани кишечника, оценивали, были ли отмечены противовоспалительные эффекты, наблюдаемые в моноцитах и МКПК, также и в эпителиальных клетках кишечника (НТ29), как описано ниже.
Анализ секреции IL-8
[0155] Клетки НТ29, культивируемые в среде McCoys с добавлением 10% ФБС, GlutaMAX и Pen/Strep высевали на планшет с плотностью 50 тыс. клеток/лунку в 96-луночном формате и оставляли расти в течение 5 дней до полного слияния. Питательную среду меняли каждые два дня. На 5-й день клетки предварительно обрабатывали в течение 1 часа 250 мкМ, 125 мкМ или 62,5 мкМ соединениями желчной кислоты перед воздействием 1,25 нг/мл ФНО-α. Клетки инкубировали в течение ночи (16 ч) и культуральные супернатанты собирали для количественного определения белка ИЛ-8 методом ИФА. Уровни ИЛ-8 в исследуемых образцах были нормализованы к воспалительным контрольным образцам, предварительно обработанным ДМСО образцам (т.е. без желчных кислот), которые подвергали воздействию 1,25 нг/мл ФНО-α.
[0156] В соответствии с ранее полученными данными, эпителиальные клетки кишечника активировались в присутствии нескольких различных желчных кислот, включая конъюгированные вторичные желчные кислоты (например, т-ЛХК, т-ДХК и г-ДХК), и снижалась выработка ИЛ-8 в организме человека дозозависимым образом. См. ФИГ. 6. В соответствии с данными, представленными выше, в отличие от других исследуемых вторичных желчных кислот, УДХК не оказывала противовоспалительного действия на активированные эпителиальные клетки кишечника. Вместо этого УДХК, по-видимому, повышала выработку ИЛ-8 активированными эпителиальными клетками кишечника дозозависимым образом.
[0157] В совокупности приведенные выше данные указывают на то, что повышение уровня некоторых вторичных желчных кислот (например, дезоксихолевой кислоты (ДХК), литохолевой кислоты (ЛХК) или 3-оксо-ЛХК) и/или снижение уровня УДХК может усиливать противовоспалительное действие, что приводит к ремиссии заболевания у пациентов с язвенным колитом.
[0158] Эти данные предоставляют дополнительные доказательства того, что бактериальные композиции, которые могут влиять на изменения содержания желчных кислот, например, вторичных желчных кислот, могут быть применимы для лечения воспалительного заболевания кишечника.
Пример 5: Выявление бактерий, ответственных за повышение уровня некоторых вторичных желчных кислот при язвенном колите в стадии ремиссии
[0159] Для идентификации бактерий, которые могут быть ответственны за повышение уровня количества желчных кислот, ассоциированных с противовоспалительным действием, описанным в приведенных выше примерах, образцы кала от различных пациентов с язвенным колитом (т.е. как пациентов с ремиссией, так и пациентов без ремиссии, которые получали одну из схем лечения, описанных в примере 1), были разделены в зависимости от наличия Flavonifractor_SC49 и Clostridium leptum. Затем было измерено количество вторичных желчных кислот, ассоциированных с путем 7α-дегидроксилазы (т.е. ДХК, 3α-12-оксодезоксихолевой кислотой, 3β-12α-дезоксихолевой кислотой (3-изо-дезоксихолевой кислотой), ЛХК и 3-оксо-ЛХК), как описано ранее в Примере 1.
[0160] Как показано на ФИГ. 7, образцы кала, содержащие либо Flavonifractor_SC49, либо Clostridium leptum имели значительно более высокие уровни исследуемых вторичных желчных кислот по сравнению с образцами кала, в которых отсутствовали обе бактерии. Самые высокие уровни исследуемых вторичных желчных кислот были измерены в образцах кала, содержащих как Flavonifractor_SC49, так и Clostridium leptum. Эти данные показывают, что эти виды бактерий, например, в бактериальной композиции, могут быть применимы для стимуляции ремиссии заболевания у пациента с ВЗК путем модуляции уровней определенных желчных кислот у пациентов с язвенным колитом.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> СЕРЕС ТЕРАПЕУТИКС, ИНК.
< 120> КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ
КИШЕЧНИКА
<130> 4268.014PC01/ELE/JBF/DKC
<150> US 62/650 002
<151> 29.03.2018
<160> 4
<170> PatentIn версия 3.5
<210> 1
<211> 1529
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Flavonifractor_SC49
<400> 1
tattgagagt ttgatcctgg ctcaggatga acgctggcgg cgtgcttaac acatgcaagt
60
cgaacggagt gctcatgaca gaggattcgt ccaatggagt gagttactta gtggcggacg
120
ggtgagtaac gcgtgagtaa cctgccttgg agtggggaat aacaggtgga aacatctgct
180
aataccgcat gatgcagttg ggtcgcatgg ctctgactgc caaagattta tcgctctgag
240
atggactcgc gtctgattag ctggttggcg gggtaacggc ccaccaaggc gacgatcagt
300
agccggactg agaggttggc cggccacatt gggactgaga cacggcccag actcctacgg
360
gaggcagcag tggggaatat tgggcaatgg gcgcaagcct gacccagcaa cgccgcgtga
420
aggaagaagg ctttcgggtt gtaaacttct tttctcaggg acgaagcaag tgacggtacc
480
tgaggaataa gccacggcta actacgtgcc agcagccgcg gtaatacgta ggtggcgagc
540
gttatccgga tttactgggt gtaaagggcg tgtaggcggg actgcaagtc agatgtgaaa
600
accatgggct caacctgtgg cctgcatttg aaactgtagt tcttgagtac tggagaggca
660
gacggaattc ctagtgtagc ggtgaaatgc gtagatatta ggaggaacac cagtggcgaa
720
ggcggtctgc tggacagcaa ctgacgctga ggcgcgaaag cgtggggagc aaacaggatt
780
agataccctg gtagtccacg ctgtaaacga tggatactag gtgtgggggg tctgaccccc
840
tccgtgccgc agttaacaca ataagtatcc cacctgggga gtacgatcgc aaggttgaaa
900
ctcaaaggaa ttgacggggg cccgcacaag cggtggagta tgtggtttaa ttcgaagcaa
960
cgcgaagaac cttaccaggg cttgacatcc cggtgaccgg tgtagagata caccttcttc
1020
ttcggaagcg ccggtgacag gtggtgcatg gttgtcgtca gctcgtgtcg tgagatgttg
1080
ggttaagtcc cgcaacgagc gcaaccctta ttgttagttg ctacgcaaga gcactctagc
1140
gagactgccg ttgacaaaac ggaggaaggt ggggacgacg tcaaatcatc atgcccctta
1200
tgtcctgggc cacacacgta ctacaatggt ggtcaacaga gggaagcaag accgcgaggt
1260
ggagcaaacc cctaaaagcc atcccagttc ggattgcagg ctgcaactcg cctgtatgaa
1320
gttggaatcg ctagtaatcg cggatcagca tgccgcggtg aatacgttcc cgggccttgt
1380
acacaccgcc cgtcacacca tgagagtcgg gaacacccga agtccgtagc ctaaccgcaa
1440
ggggggcgcg gccgaaggtg ggttcgataa ttggggtgaa gtcgtaacaa ggtagccgta
1500
tcggaaggtg cggctggatc acctccttt
1529
<210> 2
<211> 1548
<212> ДНК
<213> Clostridium leptum
<400> 2
tttagagagt ttgatcctgg ctcaggacga acgctggcgg cgtgcctaac acatgcaagt
60
cgaacggagt taaattcgac acccgagtat ccggccggga ggcggggtgc tgggggttgg
120
atttaactta gtggcggacg ggtgagtaac gcgtgagtaa cctgcctttc agagggggat
180
aacgttctga aaagaacgct aataccgcat aacatcaatt tatcgcatga taggttgatc
240
aaaggagcaa tccgctggaa gatggactcg cgtccgatta gccagttggc ggggtaacgg
300
cccaccaaag cgacgatcgg tagccggact gagaggttga acggccacat tgggactgag
360
acacggccca gactcctacg ggaggcagca gtgggggata ttgcacaatg ggggaaaccc
420
tgatgcagca acgccgcgtg agggaagaag gttttcggat tgtaaacctc tgttcttagt
480
gacgataatg acggtagcta aggagaaagc tccggctaac tacgtgccag cagccgcggt
540
aatacgtagg gagcgagcgt tgtccggatt tactgggtgt aaagggtgcg taggcggcga
600
ggcaagtcag gcgtgaaatc tatgggctta acccataaac tgcgcttgaa actgtcttgc
660
ttgagtgaag tagaggtagg cggaattccc ggtgtagcgg tgaaatgcgt agagatcggg
720
aggaacacca gtggcgaagg cggcctactg ggctttaact gacgctgaag cacgaaagca
780
tgggtagcaa acaggattag ataccctggt agtccatgcc gtaaacgatg attactaggt
840
gtggggggtc tgaccccctc cgtgccgcag ttaacacaat aagtaatcca cctggggagt
900
acggccgcaa ggttgaaact caaaggaatt gacgggggcc cgcacaagca gtggagtatg
960
tggtttaatt cgaagcaacg cgaagaacct taccaggtct tgacatccgt ctaacgaagc
1020
agagatgcat taggtgccct tcggggaaag gcgagacagg tggtgcatgg ttgtcgtcag
1080
ctcgtgtcgt gagatgttgg gttaagtccc gcaacgagcg caacccttgt ttctagttgc
1140
tacgcaagag cactctagag agactgccgt tgacaaaacg gaggaaggtg gggacgacgt
1200
caaatcatca tgccccttat gacctgggcc acacacgtac tacaatggct gtaaacagag
1260
ggaagcaaag ccgcgaggtg gagcaaaacc ctaaaagcag tcccagttcg gatcgcaggc
1320
tgcaacccgc ctgcgtgaag tcggaattgc tagtaatcgc ggatcagcat gccgcggtga
1380
atacgttccc gggccttgta cacaccgccc gtcacaccat gggagccggt aatacccgaa
1440
gccagtagtt caaccgcaag gagagcgctg tcgaaggtag gattggcgac tggggtgaag
1500
tcgtaacaag gtagccgtat cggaaggtgc ggctggatca cctccttt
1548
<210> 3
<211> 1529
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Flavonifractor_SC49
<400> 3
tattgagagt ttgatcctgg ctcaggatga acgctggcgg cgtgcttaac acatgcaagt
60
cgaacggagt gctcatgaca gaggattcgt ccaatggagt gagttactta gtggcggacg
120
ggtgagtaac gcgtgagtaa cctgccttgg agtggggaat aacaggtgga aacatctgct
180
aataccgcat gatgcagttg ggtcgcatgg ctctgactgc caaagattta tcgctctgag
240
atggactcgc gtctgattag ctagttggcg gggtaacggc ccaccaaggc gacgatcagt
300
agccggactg agaggttggc cggccacatt gggactgaga cacggcccag actcctacgg
360
gaggcagcag tggggaatat tgggcaatgg gcgcaagcct gacccagcaa cgccgcgtga
420
aggaagaagg ctttcgggtt gtaaacttct tttctcaggg acgaagcaag tgacggtacc
480
tgaggaataa gccacggcta actacgtgcc agcagccgcg gtaatacgta ggtggcgagc
540
gttatccgga tttactgggt gtaaagggcg tgtaggcggg actgcaagtc agatgtgaaa
600
accatgggct caacctgtgg cctgcatttg aaactgtagt tcttgagtac tggagaggca
660
gacggaattc ctagtgtagc ggtgaaatgc gtagatatta ggaggaacac cagtggcgaa
720
ggcggtctgc tggacagcaa ctgacgctga ggcgcgaaag cgtggggagc aaacaggatt
780
agataccctg gtagtccacg ctgtaaacga tggatactag gtgtgggagg tctgaccccc
840
tccgtgccgc agttaacaca ataagtatcc cacctgggga gtacgatcgc aaggttgaaa
900
ctcaaaggaa ttgacggggg cccgcacaag cggtggagta tgtggtttaa ttcgaagcaa
960
cgcgaagaac cttaccaggg cttgacatcc cggtgaccgg tgtagagata caccttcttc
1020
ttcggaagcg ccggtgacag gtggtgcatg gttgtcgtca gctcgtgtcg tgagatgttg
1080
ggttaagtcc cgcaacgagc gcaaccctta ttgttagttg ctacgcaaga gcactctagc
1140
gagactgccg ttgacaaaac ggaggaaggt ggggacgacg tcaaatcatc atgcccctta
1200
tgtcctgggc cacacacgta ctacaatggt ggtcaacaga gggaagcaag accgcgaggt
1260
ggagcaaacc cctaaaagcc atcccagttc ggattgcagg ctgcaactcg cctgtatgaa
1320
gttggaatcg ctagtaatcg cggatcagca tgccgcggtg aatacgttcc cgggccttgt
1380
acacaccgcc cgtcacacca tgagagtcgg gaacacccga agtccgtagc ctaaccgcaa
1440
ggggggcgcg gccgaaggtg ggttcgataa ttggggtgaa gtcgtaacaa ggtagccgta
1500
tcggaaggtg cggctggatc acctccttt
1529
<210> 4
<211> 1376
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Flavonifractor_SC49
<220>
<221> прочий_признак
<222> (543)..(543)
<223> n представляет собой a, c, g или t
<220>
<221> прочий_признак
<222> (955)..(956)
<223> n представляет собой a, c, g или t
<400> 4
aacggagtgc tcatgacaga ggattcgtcc aatggagtga gttacttagt ggcggacggg
60
tgagtaacgc gtgagtaacc tgccttggag tggggaataa caggtggaaa catctgctaa
120
taccgcatga tgcagttgag tcgcatggct ctgactgcca aagatttatc gctctgagat
180
ggactcgcgt ctgattagct ggttggcggg gtaacggccc accaaggcga cgatcagtag
240
ccggactgag aggttggccg gccacattgg gactgagaca cggcccagac tcctacggga
300
ggcagcagtg gggaatattg ggcaatgggc gcaagcctga cccagcaacg ccgcgtgaag
360
gaagaaggct ttcgggttgt aaacttcttt tctcagggac gaagcaagtg acggtacctg
420
aggaataagc cacggctaac tacgtgccag cagccgcggt aatacgtagg tggcgagcgt
480
tatccggatt tactgggtgt aaagggcgtg taggcgggac tgcaagtcag atgtgaaaac
540
cangggctca acctgtggcc tgcatttgaa actgtagttc ttgagtactg gagaggcaga
600
cggaattcct agtgtagcgg tgaaatgcgt agatattagg aggaacacca gtggcgaagg
660
cggtctgctg gacagcaact gacgctgagg cgcgaaagcg tggggagcaa acaggattag
720
ataccctggt agtccacgct gtaaacgatg gatactaggt gtggggggtc tgaccccctc
780
cgtgccgcag ttaacacaat aagtatccca cctggggagt acgatcgcaa ggttgaaact
840
caaaggaatt gacgggggcc cgcacaagcg gtggagtatg tggtttaatt cgaagcaacg
900
cgaagaacct taccagggct tgacatcccg gtgaccggtg tagagataca ccttnntctt
960
cggaagcacc ggtgacaggt ggtgcatggt tgtcgtcagc tcgtgtcgtg agatgttggg
1020
ttaagtcccg caacgagcgc aacccttatt gttagttgct acgcaagagc actctagcga
1080
gactgccgtt gacaaaacgg aggaaggtgg ggacgacgtc aaatcatcat gccccttatg
1140
tcctgggcca cacacgtact acaatggtgg tcaacagagg gaagcaagcc cgcgaggagg
1200
agcaaacccc taaaagccat cccagttcgg attgcaggct gcaactcgcc tgtatgaagt
1260
tggaatcgct agtaatcgcg gatcagcatg ccgcggtgaa tacgttcccg ggccttgtac
1320
acaccgcccg tcacaccatg agagtcggga acacccgaag tccgtagcct aaccgc
1376
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ГЕПАТОПРОТЕКТОРА И ПРЕБИОТИКА, ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2006 |
|
RU2318538C1 |
| КОМПОЗИЦИИ И СПОСОБЫ | 2014 |
|
RU2664479C2 |
| МАНИПУЛЯЦИЯ МЕТАБОЛИЗМОМ ТРИПТАМИНОВ | 2018 |
|
RU2794244C2 |
| РАЗРАБОТАННЫЕ БАКТЕРИАЛЬНЫЕ КОМПОЗИЦИИ | 2016 |
|
RU2773327C2 |
| СПОСОБ ДИАГНОСТИКИ КОЛОРЕКТАЛЬНОГО РАКА ИЗ ОБРАЗЦА КАЛА ЧЕЛОВЕКА С ПОМОЩЬЮ КОЛИЧЕСТВЕННОЙ ПЦР, ПРАЙМЕРОВ И НАБОРА | 2015 |
|
RU2692555C2 |
| ПРИМЕНЕНИЕ КАРОТИНОИДА МИКРОБНОГО ПРОИСХОЖДЕНИЯ, ВЛИЯЮЩЕГО НА СОСТАВ МИКРООРГАНИЗМОВ КИШЕЧНИКА | 2017 |
|
RU2759600C2 |
| ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ Lactobacillus plantarum | 2018 |
|
RU2772025C2 |
| КОМПЛЕКТ ДЛЯ ПРОГНОЗИРОВАНИЯ ИЛИ ДИАГНОСТИКИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ И СПОСОБ ДИАГНОСТИКИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ | 2020 |
|
RU2800086C1 |
| ШТАММ Bacillus subtilis, ВЫРАБАТЫВАЮЩИЙ ПЕПТИД С ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИНГИБИРОВАНИЯ НЕЖЕЛАТЕЛЬНЫХ МИКРООРГАНИЗМОВ В МАТЕРИАЛЕ С ИСПОЛЬЗОВАНИЕМ ШТАММА | 2011 |
|
RU2553547C2 |
| ИСПОЛЬЗОВАНИЕ МИКРОБНЫХ СООБЩЕСТВ ДЛЯ ЛЕЧЕНИЯ ЧЕЛОВЕКА И ЖИВОТНЫХ | 2017 |
|
RU2758387C2 |
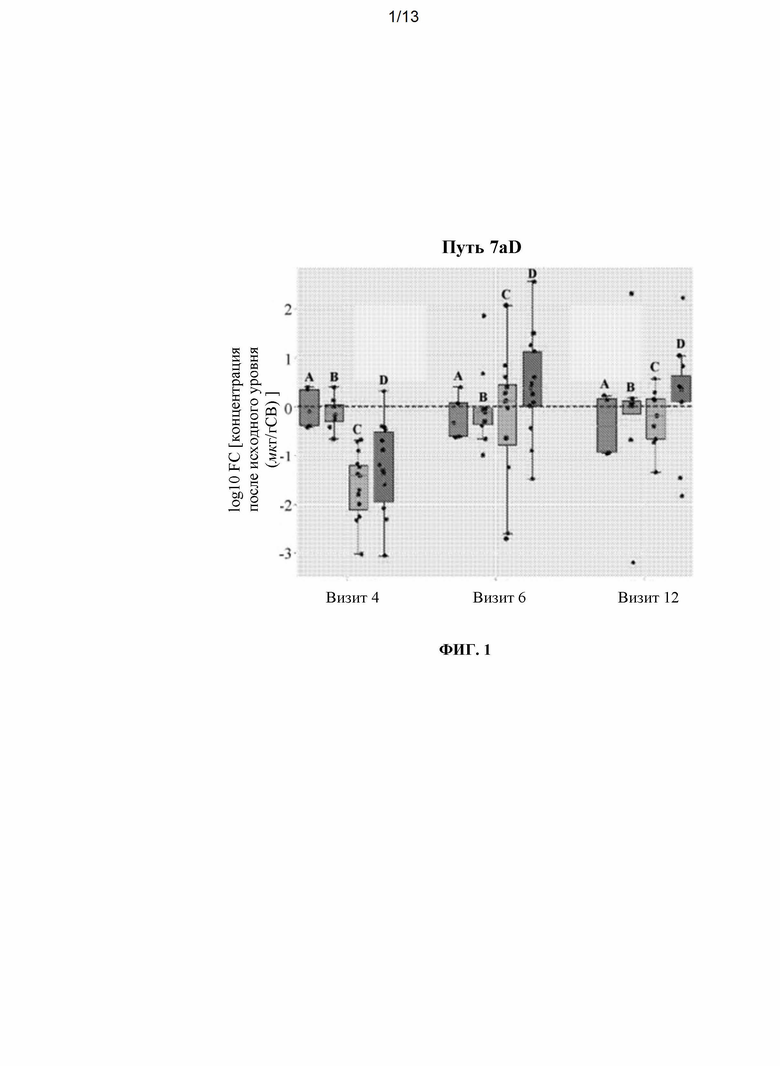
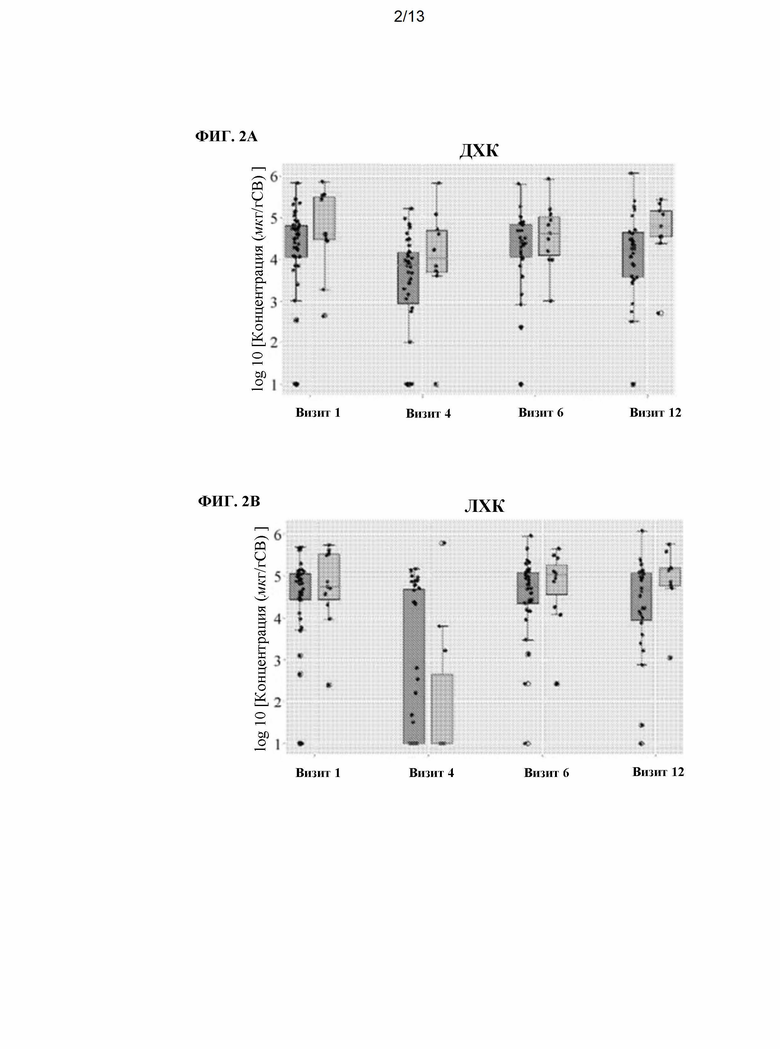
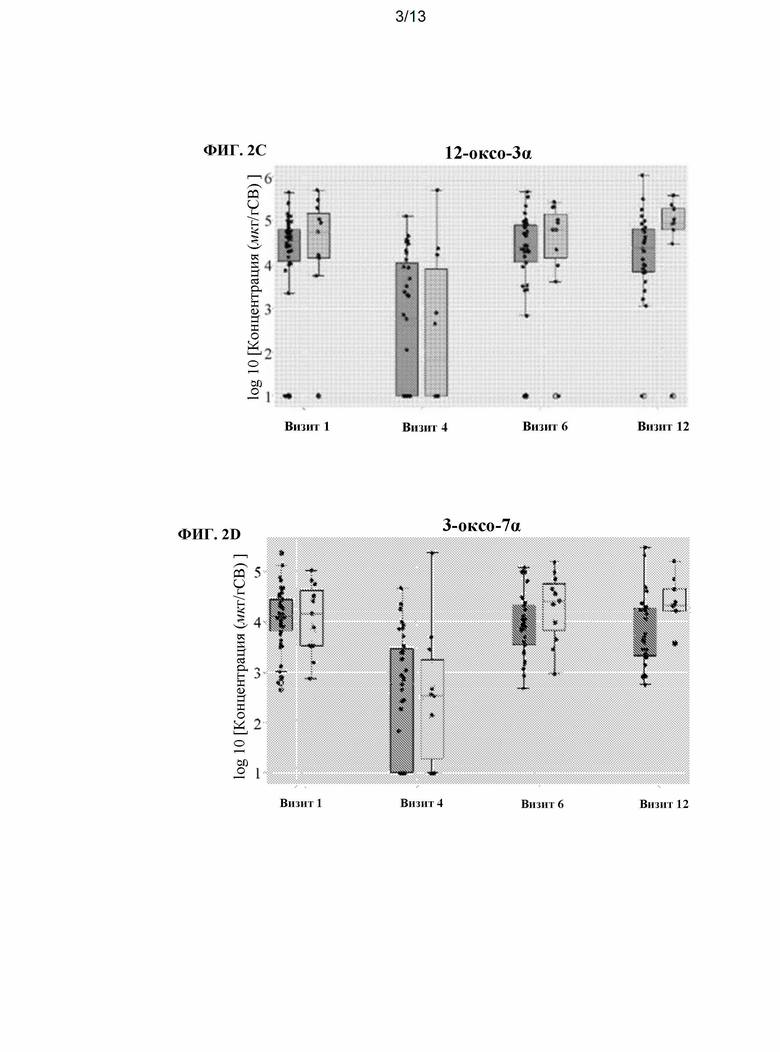
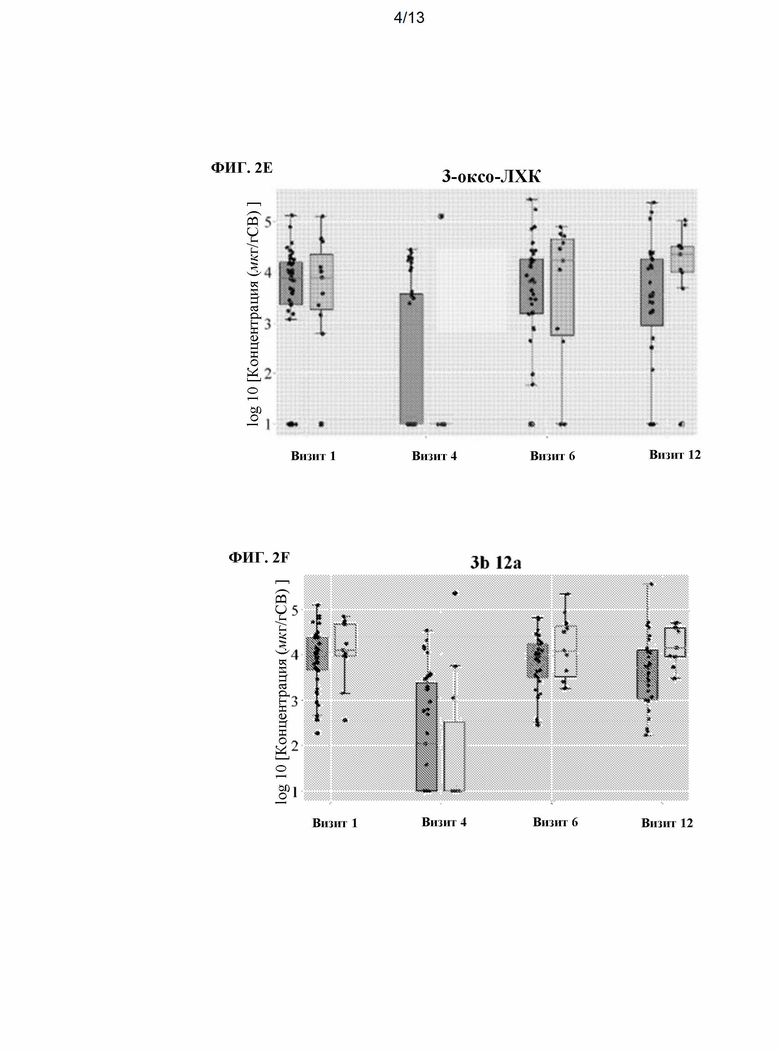

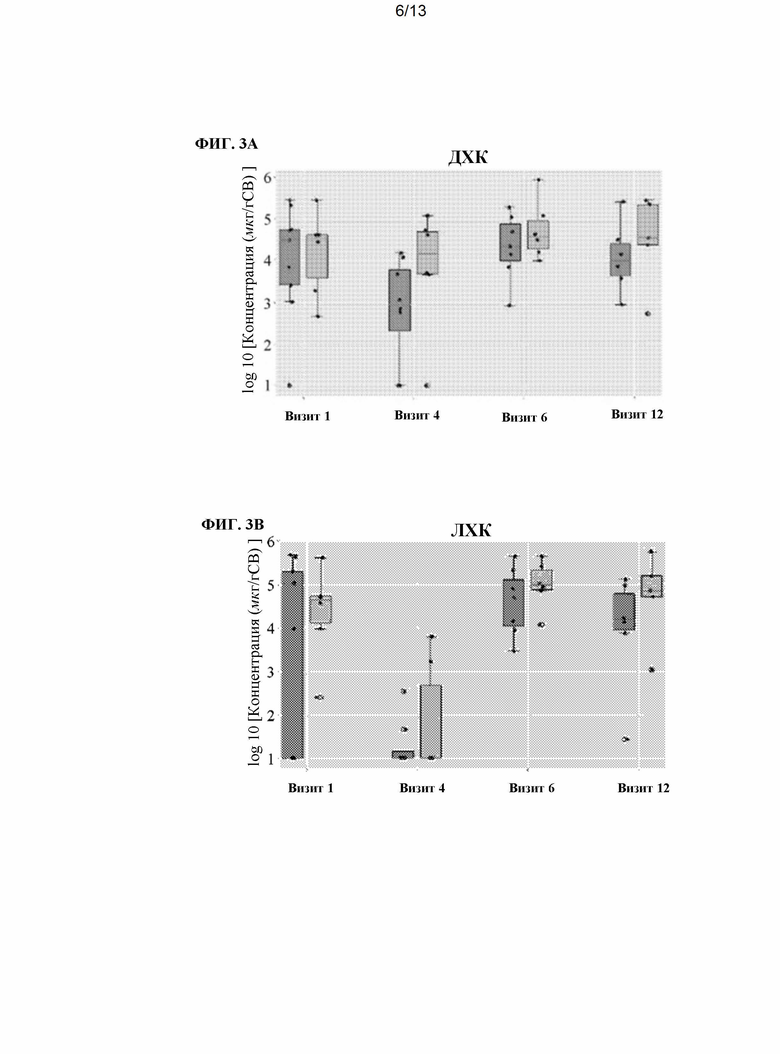
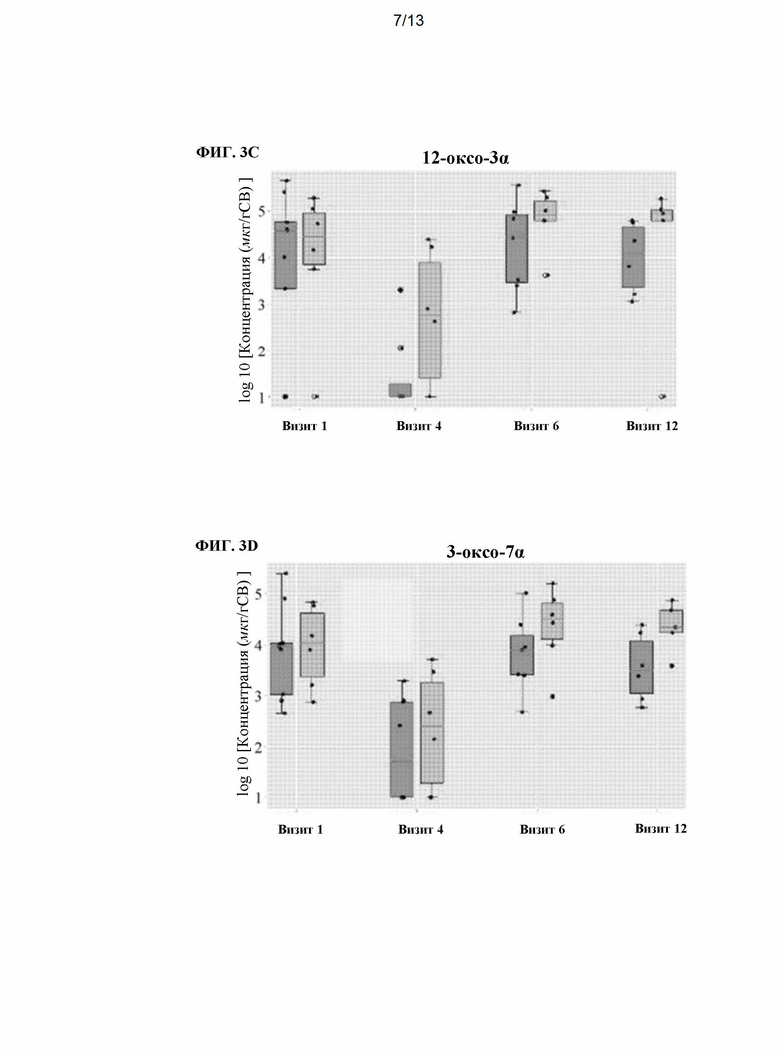
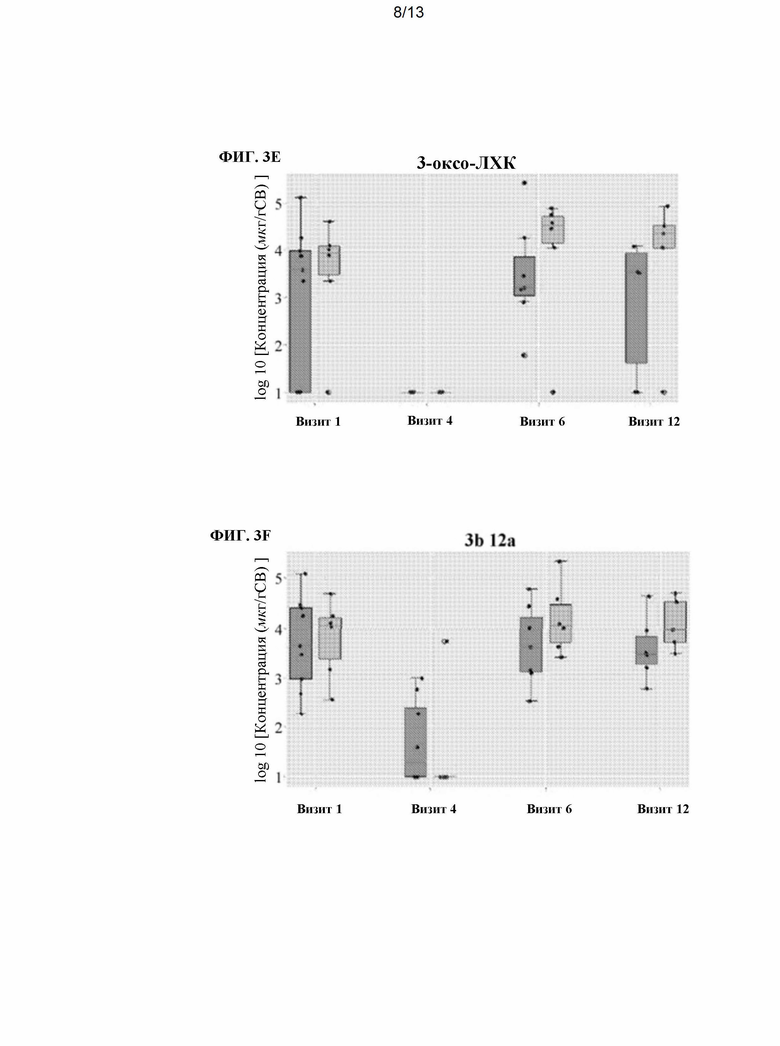
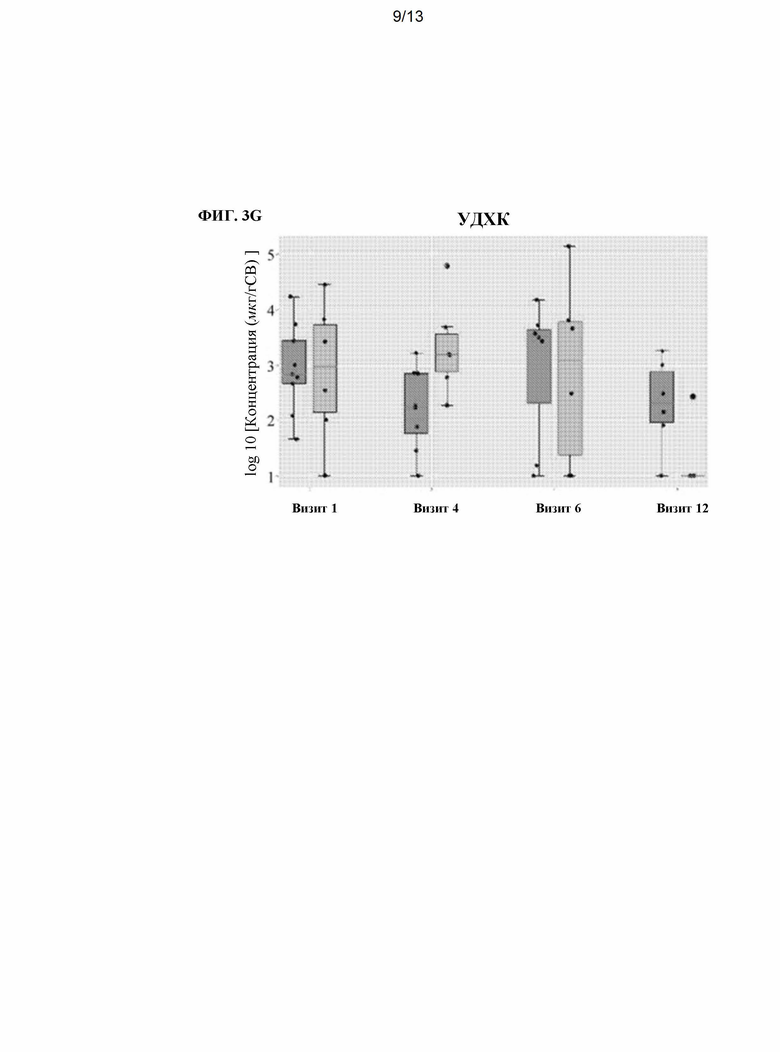
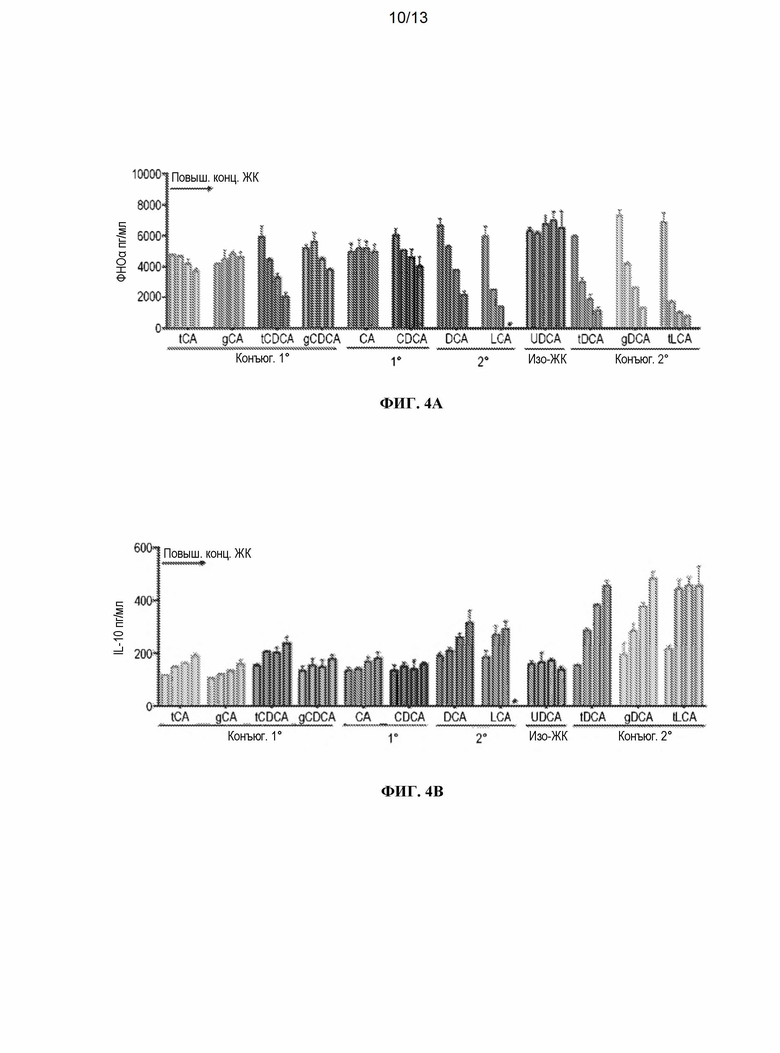
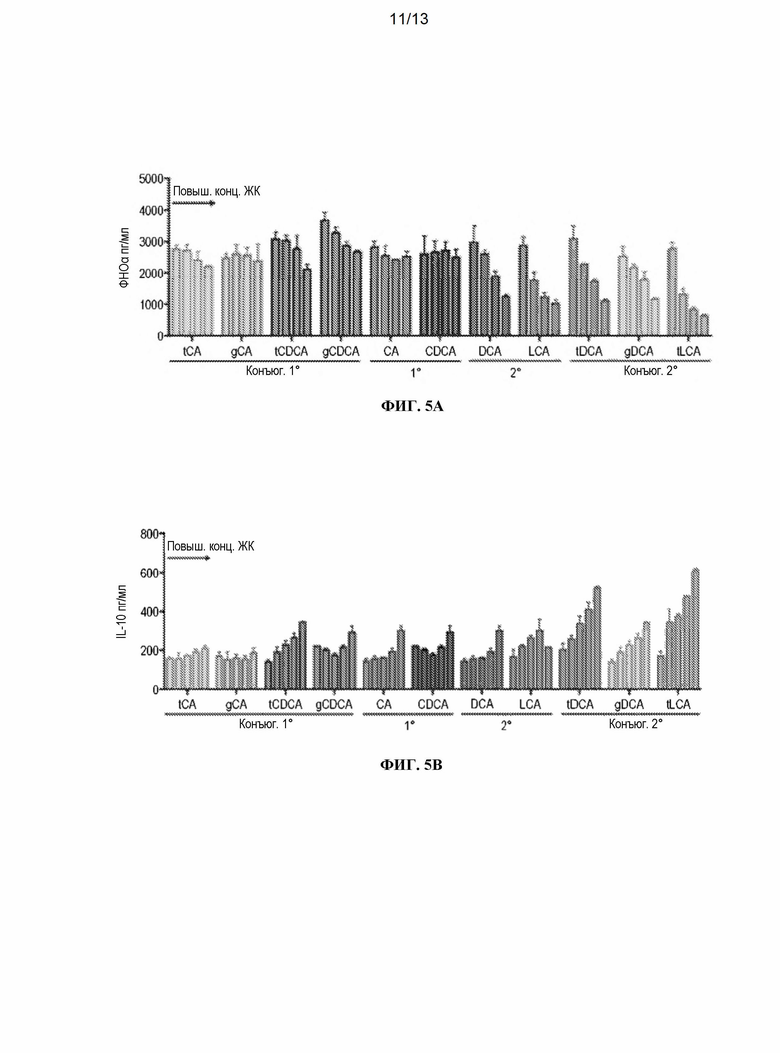

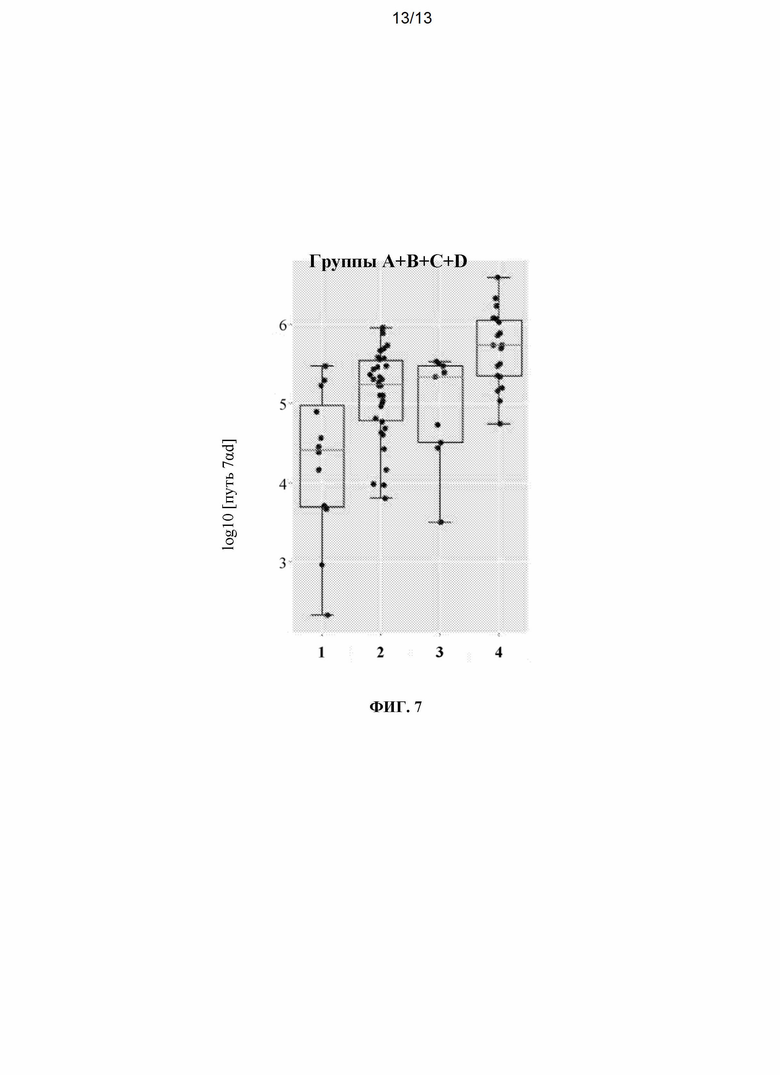
Группа изобретений относится к области медицины, а именно к терапии и гастроэнтерологии, и предназначена для модулирования уровня вторичной желчной кислоты при введении субъекту. Композиция содержит очищенную популяцию бактерий, при этом очищенная популяция бактерий содержит вид бактерий, который содержит последовательность 16S рДНК, которая по меньшей мере на 97% идентична последовательности 16S рДНК, представленной в любой из SEQ ID NOs: 1, 3, и 4. Также представлен фармацевтический состав, включающий указанную композицию и один или более дополнительный агент. В других воплощениях обеспечиваются способ модуляции уровня вторичной желчной кислоты и способ лечения воспалительного заболевания кишечника (ВЗК) у нуждающегося в этом субъекта, включающие введение субъекту указанной композиции или указанного фармацевтического состава. Использование группы изобретений позволяет модулировать уровень вторичных желчных кислот. 4 н. и 18 з.п. ф-лы, 7 ил., 1 табл., 5 пр.
1. Композиция, содержащая очищенную популяцию бактерий, при этом очищенная популяция бактерий содержит вид бактерий, который содержит последовательность 16S рДНК, которая по меньшей мере на 97% идентична последовательности 16S рДНК, представленной в любой из SEQ ID NOs: 1, 3, и 4.
2. Композиция по п. 1, в которой указанный вид бактерий содержит последовательность 16S рДНК, которая по меньшей мере на 98% идентична последовательности 16S рДНК, представленной в любой из SEQ ID NOs: 1, 3, и 4.
3. Композиция по п. 1, в которой указанный вид бактерий содержит последовательность 16S рДНК, которая по меньшей мере на 99% идентична последовательности 16S рДНК, представленной в любой из SEQ ID NOs: 1, 3, и 4.
4. Композиция по п. 1, в которой указанный вид бактерий содержит последовательность 16S рДНК, представленную в любой из SEQ ID NOs: 1, 3, и 4.
5. Композиция по любому из пп. 1-4, в которой указанный вид бактерий находится в вегетативной форме.
6. Композиция по любому из пп. 1-5, в которой очищенная популяция бактерий дополнительно содержит Clostridium leptum.
7. Композиция по п. 6, в которой Clostridium leptum содержит последовательность 16S рДНК, которая по меньшей мере на 97% идентична последовательности 16S рДНК, представленной в SEQ ID NO: 2.
8. Композиция по любому из пп. 1–7, которая способна повышать уровень вторичной желчной кислоты при введении субъекту, причем вторичная желчная кислота включает дезоксихолевую кислоту (ДХК), 3α-12-оксодезоксихолевую кислоту, 3β-12α-дезоксихолевую кислоту (3-изодезоксихолевую кислоту), 7α-3-оксо-хенодезоксихолевую кислоту, литохолевую кислоту (ЛХК), 3-оксо-ЛХК или их комбинации.
9. Композиция по любому из пп. 1–7, которая способна понижать уровень вторичной желчной кислоты при введении субъекту, причем вторичная желчная кислота включает урсодезоксихолевую кислоту (УДХК).
10. Композиция по любому из пп. 1–9, которая дополнительно содержит энтеросолюбильное покрытие.
11. Фармацевтический состав, включающий композицию по любому из пп. 1–10 и один или более дополнительный агент.
12. Способ модуляции уровня вторичной желчной кислоты у нуждающегося в этом субъекта, включающий введение субъекту композиции по любому из пп. 1–10 или фармацевтического состава по п. 11.
13. Способ по п. 12, в котором вторичная желчная кислота включает дезоксихолевую кислоту (ДХК), 3α-12-оксодезоксихолевую кислоту, 3β-12α-дезоксихолевую кислоту (3-изодезоксихолевую кислоту), 7α-3-оксо-хенодезоксихолевую кислоту, литохолевую кислоту (ЛХК), 3-оксо-ЛХК или их комбинации.
14. Способ по п. 12 или 13, в котором введение повышает уровень вторичной желчной кислоты у субъекта.
15. Способ по п. 14, в котором субъект страдает воспалительным заболеванием кишечника (ВЗК), и в котором повышение уровня вторичной желчной кислоты ассоциируется с ремиссией ВЗК.
16. Способ по любому из пп. 12-15, в котором вторичная желчная кислота может: (i) снижать выработку ФНО-α и/или повышать выработку ИЛ-10 в моноцитах, стимулированных липополисахаридами (ЛПС), in vitro, (ii) снижать выработку ФНО-α и/или повышать выработку ИЛ-10 в ЛПС-стимулированных мононуклеарных клетках периферической крови (МКПК) in vitro, (iii) может снижать выработку ИЛ-8 в ФНОα-стимулированных эпителиальных клетках кишечника in vitro, или (iv) любая комбинация (i)-(iii).
17. Способ по п. 12, в котором вторичная желчная кислота включает урсодезоксихолевую кислоту (УДХК).
18. Способ по п. 17, в котором введение снижает у субъекта уровень УДХК.
19. Способ по п. 18, в котором субъект страдает воспалительным заболеванием кишечника (ВЗК), и в котором снижение уровня УДХК ассоциируется с ремиссией ВЗК.
20. Способ лечения воспалительного заболевания кишечника (ВЗК) у нуждающегося в этом субъекта, включающий введение субъекту композиции по любому из пп. 1–10 или фармацевтического состава по п. 11.
21. Способ по п. 20, в котором указанное лечение включает: (i) поддержание ремиссии ВЗК у указанного субъекта, (ii) улучшение целостности слизистых оболочек и/или эпителиального барьера у указанного субъекта, (iii) уменьшение воспаления желудочно-кишечного тракта у указанного субъекта, или (iv) любую комбинацию (i)-(iii).
22. Способ по любому из пп. 15, 16 и 19-21, в котором ВЗК включает язвенный колит, болезнь Крона, или и то, и другое.
| US 2016184370 A1, 30.06.2016 | |||
| US 2016271188 A1, 22.09.2016 | |||
| WO 2017091783 A2, 01.06.2017 | |||
| WO 2016122889 A1, 04.08.2016 | |||
| KABEERDOSS J et al | |||
| Clostridium leptum group bacteria abundance and diversity in the fecal microbiota of patients with inflammatory bowel disease: a case-control study in India | |||
| BMC Gastroenterol., 2013, 13:20. |
Авторы
Даты
2023-07-06—Публикация
2019-03-29—Подача