Настоящее изобретение относится к реминерализационному стоматологическому материалу, содержащему по меньшей мере один катион и по меньшей мере один анион, которые выступают в качестве взаимодействующих ионов для образования реминерализационного вещества. Следующие объекты настоящего изобретения представляют собой применение этого стоматологического материала, способ его применения и набор для его изготовления.
Существуют известные стоматологические материалы для всех типов консервативного лечения дефектов твердого вещества зубов. Поскольку такие материалы проявляют минерализационный эффект, задача заключается в том, чтобы стабилизировать природное твердое вещество зубов, которое остается после инвазивного лечения, например, чтобы предотвратить последующее разрушение, которое могут вызывать, например, бактерии. В этом случае минерализация может быть индуцирована посредством высвобождения из материала определенных ионов, таких как Са2+ или F-, с введением подходящих противоположно заряженных ионов из слюны на поверхности или в объеме твердой ткани зубов. После этого образуется новый неорганический твердый материал, имеющий низкую растворимость, который восполняет потери минерального материала (осуществляет минерализацию) в твердом веществе зубов. Другие подходы сосредоточены на образовании твердых минеральных веществ, представляющих собой, главным образом, гидроксилапатит или другие апатиты, без необходимости введения ионов Са2+ или фосфатных ионов из слюны. При этом, согласно предшествующему уровню техники, основное применение находят так называемые биоактивные стекла.
Минерализационный потенциал материалов на основе предшествующего уровня техники, как правило, оказывается ограниченным. Причины этого представляют собой, с одной стороны, ограниченное количество доступных, т.е. частично растворимых подходящих ионов, которые содержат рассматриваемые материалы (например, иономерные стеклоцементы), и, с другой стороны, тот факт, что в материалах рассматриваемых классов, вследствие природы этих материалов, оказывается возможным применение лишь ограниченных количеств источников ионов (например, композиционных материалов с биоактивными стеклами) с учетом приемлемых физических свойств. Для таких материалов является ограниченным количество высвобождаемых ионов и/или образующегося минерального заместителя, и, следовательно оно может оказаться недостаточным для надежной стабилизации твердого вещества зубов.
В документе WO2017/161179A1 раскрыта реминерализационная композиция, которая содержит смесь биостекла 45S5 и полиаспарагиновой кислоты в соотношении 60:40. Эта смесь обеспечивает лишь низкую концентрацию высвобождаемых ионов. Кроме того, существуют ограничения в отношении возможностей выбора и сочетания высвобождаемых ионов, и, следовательно, в отношении природы реминерализации.
В документе US2010/0272764A1 раскрыт полимеризуемый стоматологический смоляной композиционный материал, обладающий способностями реминерализации. Этот композиционный материал содержит микрокапсулы, каждая из которых содержит раствор нитрата кальция, раствор гидрофосфата калия и раствор фторида натрия. Ионы высвобождаются через полупроницаемую мембрану капсул под действием концентрационного градиента. Указано, что эти микрокапсулы могут быть получены в результате комплексной коацервации противоположно заряженных полиэлектролитов. Здесь недостаток представляет собой низкую концентрацию высвобождаемых ионов.
Основная задача, которую должно решить настоящее изобретение, заключается в том, чтобы создать стоматологический материал указанного типа, который обеспечивает эффективную реминерализацию.
Для решения этой задачи согласно настоящему изобретению предложено, что по меньшей мере один из взаимодействующих ионов является многозарядным и присутствует в качестве противоположно заряженного иона в коацервате.
Прежде всего, будет представлено разъяснение некоторых терминов, используемых в контексте настоящего изобретения.
Настоящее изобретение относится к реминерализационному стоматологическому материалу.
Реминерализация и деминерализация представляют собой биологические процессы, которые происходят поочередно на границе раздела между зубом и полостью рта, и в которых неорганические ионы растворяются или повторно внедряются посредством слюны. Деминерализация означает, как правило, индуцированную кислотой (источником которой является, например, вызывающий кариес зубной налет) потерю минерального вещества зуба в процессе растворения неорганических, главным образом, содержащих гидроксилапатит составляющих компоненты зуба, что представляет собой первичный процесс образования кариеса (статья P. Shellis в книге «Кариес» под ред. H. Meyer-Lückel, S. Paris, K.R. Ekstrand, издательство G. Thieme, 2012, с. 23).
Реминерализация в более узком смысле представляет собой восполнение истощенного минерального материала, основу которого составляет апатит, в области поверхности зубов (статья P. Shellis в процитированной выше книге, с.23, 26; статья S. Twetmann, K.R. Ekstrand в процитированной выше книге, с. 210). В случае предшествующего повреждения зубного вещества в результате деминерализации процесс реминерализации этого типа приводит к определенному устранению дефектов. Восстановительный материал может накапливаться на существующих кристаллах апатита в составе зуба, что приводит к росту кристаллов, хотя также могут образовываться и новые кристаллы апатита. Принимая во внимание современное состояние исследований, авторы предполагают, что природный процесс реминерализации ускоряется в присутствии фторида даже низких концентрациях.
Реминерализация в смысле настоящего изобретения означает любой процесс, в котором неорганический материал накапливается в ходе осаждения на существующем твердом веществе зубов, потенциально поврежденных в результате деминерализации. Это осаждение может обеспечивать рост существующих кристаллов апатита в зубном веществе или, в качестве альтернативы, может приводить к образованию нового неорганического материала в области реминерализации. Подходящие неорганические материалы могут представлять собой материалы, произведенные из апатита, или, в качестве альтернативы, они могут представлять собой другие биосовместимые соединения, имеющие низкую растворимость. В рамках настоящего изобретения они называются термином «реминерализационное вещество».
Зубное вещество означает любое минерализованное зубное вещество, в частности, зубную эмаль, дентин и зубной цемент.
Взаимодействующие ионы представляют собой катионы и анионы, которые способны совместно образовывать реминерализационное вещество.
Термин «коацервация» означает разделение двух жидких фаз. Ионный полимер или макроион (например, ионный полифосфат) вместе с многозарядным противоположно заряженным ионом (например, ионом кальция) образует коацерват, который представляет собой относительно обогащенную полимером фазу в составе полимерного раствора.
Коацерваты представляют собой полиэлектролиты, сшитые посредством многозарядных противоположно заряженных ионов. В водной среде, коацерваты присутствуют в форме фазы, имеющей более высокую вязкость. В зависимости от величины молекулярных масс исходных полиэлектролитов, коацерваты присутствуют в форме жидких вязких или вязкопластичных веществ, которые образуют отдельную фазу в водной среде. Коацерваты существуют только в пределах определенного диапазона соотношения количества вещества полиэлектролитов и многозарядных противоположно заряженных ионов, а также только выше определенной минимальной концентрации полиэлектролита. Если содержание противоположных заряженных ионов является чрезмерно низким, или если концентрация образующих коацерваты веществ (многозарядных противоположно заряженных ионов и полиэлектролитов) является чрезмерно низкой, то в водной среде не происходит разделение фаз.
Подходящие коацерваты образуют анионные или катионные полиэлектролиты и многозарядные катионы или многозарядные анионы. Подходящие коацерваты содержат ионный полиэлектролит и многозарядные противоположно заряженные ионы, которые сшивают этот полиэлектролит.
Коацерваты предпочтительно получают посредством смешивания водных растворов, содержащих анионные или катионные полиэлектролиты и многозарядные катионы или анионы. В этом контексте анионные полиэлектролиты и многозарядные катионы являются смешанными, и катионные полиэлектролиты и многозарядные анионы также являются смешанными.
Коацерваты образуют отдельную жидкую фазу повышенной вязкости в смеси. Коацерваты предпочтительно выделяют. Это осуществляют в каждом случае, используя подходящие известные способы, такие как декантирование или центрифугирование. Выделенные коацерваты предпочтительно очищают. Это осуществляют предпочтительно посредством простого промывания растворителем, предпочтительно водой.
Настоящее изобретение продемонстрировало, что взаимодействующие ионы реминерализационного материала, имеющие высокий потенциал минерализации в отношении твердого вещества зубов, могут быть сделаны доступными в стоматологическом материале, если по меньшей мере один из указанных взаимодействующих ионов присутствует в качестве противоположно заряженного иона в коацервате. Поскольку такие материалы проявляют минерализационный эффект, задача заключается в том, чтобы стабилизировать природное твердое вещество зубов, которое остается после инвазивного лечения, например, чтобы предотвратить последующее разрушение, которое могут вызывать, например, бактерии. В этом случае минерализация может быть индуцирована посредством высвобождения из материала определенных ионов, таких как Са2+ или F-, с введением подходящих противоположно заряженных ионов из слюны на поверхности или в объеме твердой ткани зубов. После этого образуется новый неорганический твердый материал, имеющий низкую растворимость, который восполняет потери минерального материала (осуществляет минерализацию) в твердом веществе зубов.
С другой стороны, минерализационный потенциал известных стоматологических материалов является ограниченным. Одна из причин этого заключается в том, что известные компоненты, производящие минерализационный эффект, могут быть введены в стоматологический материал лишь в ограниченных количествах, чтобы не ухудшались другие физический свойства указанного материала. Следующая причина представляет собой ограничение скорости и количества возможного введения ионов в соответствующий стоматологический материал и/или их высвобождения из стоматологического материала, например, в случае известных иономерных стеклоцементов.
Для применения согласно настоящему изобретению стоматологические материалы, производящие минерализационный эффект, присутствуют преимущественно в жидкой или пастообразной форме, но по меньшей мере в приемлемой форме, и их наносят в этой форме на твердое вещество зубов, подлежащих лечению. При этом их вручную наносят на поверхность и, возможно, придают им соответствующую форму. Поскольку процессы реминерализации, как правило, происходят очень медленно, материал должен оставаться в области применения по меньшей мере в течение определенного времени после затвердевания. В применении, которое является особенно подходящим для успешного долгосрочного результата лечения, материал затвердевает после истечения определенного времени, и продолжительность затвердевания должна быть достаточной для осуществления ручных операций с этим материалом. В этом случае материал в затвердевшей форме также служит для защиты области реминерализации от механического и/или химического разрушения. До и, если это предусмотрено, после затвердевания материалы должны сохранять способность высвобождения ионов для минерализации твердого вещества зубов посредством восполнения минерального вещества.
Согласно одному предпочтительному применению стоматологические материалы, обладающие потенциалом минерализации, предназначены для применения соответствующим образом в целях стабилизации зубной эмали. Она может представлять собой зубную эмаль, частично разрушенную кариозными процессами, зубную эмаль в области, открытой для инвазивного лечения зубов, или в областях, имеющих недостаточную минерализацию в результате неправильного образования зубной эмали, например, при моляро-резцовой гипоминерализации (MIH). Желательный стоматологический материал обеспечивает минерализацию находящегося с ним в контакте недостаточно минерализованного твердого вещества зубов и покрывает такие области по меньшей мере в течение периода, который требуется для минерализации областей зубной эмали. Кроме того, может быть предусмотрено постоянное воздействие в случае применения пломбировочного материала. Его применение приводит к стабилизации вещества зуба, которая обеспечивает реминерализацию и физическую защиту в течение периода, который требуется для реминерализации. В случае такого применения рассматриваемый материал также обеспечивает идеальное сцепление в области, подлежащей лечению.
Следующее желательное специфическое применение минерализационных стоматологических материалов осуществляется с целью стабилизации существующего или оставшегося дентина. Такие применения направлены, например, на открытый дентин в области открытой шейки зуба. Как известно, это клиническое состояние оказывается наиболее сложным для лечения, потому что долгосрочная и непроницаемая герметизация в этой области является весьма затруднительной. Это оказывается особенно актуальным в лечении кариеса шейки зуба, клиническое лечение которого является затруднительным. В случае такого применения материал также производит одновременно эффект физической защиты и минерализационный эффект и, таким образом, своим действием обеспечивает стабилизацию. В этом случае также, по клиническим соображениям, материал должен быть способным к адгезионному самоотверждению на стадии его применения на поверхности дентина.
Следующее предпочтительное применение таких материалов связано с их пригодностью в качестве корректирующего материала, в частности, когда присутствуют глубокие полости, и в некоторых обстоятельствах деминерализованный дентин остается в полости. В этом случае также цель представляет собой эффекты стабилизации и продолжительной защиты. В случае материалов предшествующего уровня техники проблема заключается в том, что корректирующие материалы на основе неорганических соединений не всегда обладают достаточной химической устойчивостью и/или не обеспечивают или обеспечивают лишь недостаточное сцепление с подложкой.
Предпочтительное требование к образованию восполняющего минерального материала заключается в том, что в химическом отношении он должен быть по меньшей мере таким же устойчивым в кислой водной среде, как твердое вещество зубов (гидроксилапатит), и предпочтительнее является более устойчивым. Устойчивость в кислой водной среде означает устойчивость к растворению в такой среде. Образование такого химически устойчивого минерального заместителя предотвращает растворение материала на поверхности, например, в условиях микробиологического воздействия и образования кислоты.
Согласно настоящему изобретению оказывается предпочтительным, что один из взаимодействующих ионов является многозарядным и присутствует в качестве противоположно заряженного иона в коацервате, и второй взаимодействующий ион присутствует в водном растворе.
Согласно этому варианту осуществления может оказаться предпочтительным дополнительное присутствие второго полиэлектролита, имеющего иной заряд, чем полиэлектролит коацервата. Если при этом полиэлектролит коацервата представляет собой катионный пол и электролит, этот второй полиэлектролит представляет собой анионный полиэлектролит, и наоборот. Было обнаружено, что введение такого второго полиэлектролита означает обеспечение дополнительной глубины минерализации в зубном веществе (более конкретно, в дентине). Это представляет собой преимущество, в частности, в случае деминерализованного дентина, которое заключается в том, что потенциал минерализации может быть улучшен посредством глубины проникновения взаимодействующего иона, который содержится в коацервате, что обеспечивает улучшенную реминерализацию в глубину дентина.
Согласно настоящему изобретению оба взаимодействующих иона могут быть многозарядными и присутствуют в качестве противоположно заряженных ионов соответствующего коацервата. Предпочтительнее один из взаимодействующих ионов является двухзарядным, т.е. заряд составляет 2. Предпочтительные величины заряда составляют +3, +2, -2 и -3.
Помимо многозарядных катионов/анионов, коацерваты также могут содержать однозарядные катионы/анионы. Может оказаться предпочтительным, что некоторые из многозарядных или однозарядных катионов обладают противомикробными свойствами. Подходящие катионы, имеющие указанные свойства, представляют собой, например, ионы серебра или ионы меди. Может оказаться предпочтительным, что некоторые из многозарядных или однозарядных анионов производят биологические эффекты или, в качестве альтернативы, способствующие реминерализации эффекты. Оказывается особенно предпочтительным, когда фторид присутствует в качестве однозарядного аниона.
Анионные полиэлектролиты для образования коацерватов с многозарядными катионами могут быть предпочтительно выбраны из группы органических полиэлектролитов, которую предпочтительно составляют:
полимеры и сополимеры, которые содержат группы карбоновых кислот, группы фосфорных кислот, группы фосфоновых кислот и/или группы сульфоновых кислот, а также соответствующие соли и соответствующие неполные сложные эфиры; предпочтительно поликарбоновые кислоты, полиалкиленфосфорные кислоты, полиалкиленфосфоновые кислоты, например, поливинилфосфоновая кислота, и полисульфоновые кислоты, а также соответствующие соли и соответствующие неполные сложные эфиры; предпочтительнее поли(мет)акриловая кислота, полиаспарагиновая кислота, полиитаконовая кислота, и полиглутаминовая кислота, а также соответствующие соли;
кислые белки, производные кислых белков и соответствующие соли, которые предпочтительно образуют лизоцим или желатин (тип В);
кислые полисахариды и соответствующие соли, которые предпочтительно образуют каррагенан, пектин, альгиновая кислота и гиалуроновая кислота.
Анионные полиэлектролиты для образования коацерватов с многозарядными катионами предпочтительно имеют средние молекулярные массы (среднемассовые значения Mw), составляющие от 3 кДа до 1500 кДа, предпочтительнее от 5 до 500 кДа, предпочтительнее от 8 кДа до 200 кДа, еще предпочтительнее от 8 до 50 кДа.
Многозарядные катионы предпочтительно выбраны из группы, которую составляют минералообразующие катионы; предпочтительно катионы металлов; предпочтительнее металлы групп 2А, 3В, и 3А Периодической системы элементов, а также лантаниды; предпочтительнее Ва2+, Са2+, Sr2+, Tb3+ и Yb3+; предпочтительнее Са2+ и/или смеси катионов металлов, содержащие Са2+.
Оказываются возможными коацерваты, содержащие смеси катионов, например, посредством частичного замещения ионов Са2+, в частности, ионами Sr2+ в содержащих кальций коацерватах.
Согласно одному предпочтительному варианту осуществления в случае коацервата на основе полиакриловой кислоты и ионов Са2+ для образования желательного выделяемого коацервата используют значение рН, составляющее по меньшей мере 5, и концентрацию полиакриловой кислоты, составляющую по меньшей мере 1 мг/мл, предпочтительнее по меньшей мере 10 мг/мл.
Катионные полиэлектролиты для образования коацерватов с многозарядными анионами предпочтительно выбраны из органических полиэлектролитов, предпочтительно из группы, которую составляют полимеры и сополимеры, которые содержат первичные, вторичные и/или третичные аминогруппы, а также соответствующие соли; предпочтительно полиамины; предпочтительнее полиаллиламин, линейный или разветвленный полиэтиленимин, хитозан, полибетаин и полиаргинин, а также соответствующие соли; предпочтительнее гидрохлорид полиаллиламина (РАН).
Согласно одному варианту осуществления коацерваты на основе катионных полиэлектролитов могут представлять собой сочетание гидрохлорида полиаллиламина (РАН) с фосфатом или гидрофосфатом, представляющим собой противоположно заряженный ион. Согласно этому варианту осуществления должно быть обеспечено, чтобы в целях изготовления коацервата полиаллиламин присутствовал в максимально возможной протонированной форме, и фосфатный ион присутствовал в максимально возможной депротонированной форме.
Катионные полиэлектролиты для образования коацерватов с многозарядными анионами предпочтительно имеют средние молекулярные массы (среднемассовые значения Mw), составляющие от 3 кДа до 1500 кДа, предпочтительно от 5 до 500 кДа, предпочтительнее от 8 кДа до 200 кДа, еще предпочтительнее от 8 до 50 кДа.
Многозарядные анионы предпочтительно выбраны из группы, которую составляют минералообразующие анионы, предпочтительно ортофосфатные ионы, дифосфатные ионы, метафосфатные ионы, силикатные ионы, более конкретно, неорганические силикатные ионы, предпочтительно ортосиликатные, иносиликатные и имеющие запрещенную зону силикатные ионы, и частично модифицированные органическими группами силикатные ионы, более конкретно, алкилоксисиликатные ионы, сульфатные ионы, вольфраматные ионы, ванадатные ионы, молибдатные ионы, и карбонатные ионы, предпочтительнее ортофосфатные ионы, дифосфатные ионы, метафосфатные ионы, сульфатные ионы, вольфраматные ионы, ванадатные ионы, молибдатные ионы, предпочтительнее ортофосфатные ионы и/или смеси ортофосфатных ионов с минералообразующими анионами.
Согласно одному варианту осуществления настоящего изобретения стоматологический материал предпочтительно представляет собой жидкость и/или эмульсию и/или суспензию, предпочтительно имеющую динамическую вязкость, составляющую более чем 50 мПа⋅с, предпочтительно более чем 100 мПа⋅с.
Согласно следующему варианту осуществления настоящего изобретения стоматологический материал предпочтительно представляет собой твердое вещество, предпочтительнее порошок.
Согласно следующему варианту осуществления настоящего изобретения стоматологический материал предпочтительно представляет собой гель или пасту.
Стоматологический материал может содержать от 1 до 100 мас. % взаимодействующих ионов и коацерват; при этом предпочтительные нижние пределы и верхние пределы составляют 5, 10, 15, 25 и так далее вплоть до 95 мас. %. Указанные интервалы, составляющие 5 мас. %, в каждом случае могут быть объединены произвольным образом согласно настоящему изобретению с образованием диапазонов нижних пределов и верхних пределов.
Стоматологический материал согласно настоящему изобретению предпочтительно содержит воду, составляющую предпочтительно от 5 до 95 мас. %; при этом предпочтительные нижние пределы и верхние пределы составляют 5, 10, 15, 25 и так далее вплоть до 95 мас. %. Указанные интервалы, составляющие 5 мас. %, в каждом случае могут быть объединены произвольным образом согласно настоящему изобретению с образованием диапазонов нижних пределов и верхних пределов.
Согласно одному варианту осуществления настоящему изобретению коацерват согласно может иметь содержание воды, составляющее от 0,1 до 90 мас. %, предпочтительно от 1 до 75 мас. %, предпочтительнее от 5 до 60 мас. %.
Согласно предпочтительному варианту осуществления после высушивания, например, коацерват может иметь содержание воды, составляющее от 0,1 до 50 мас. %, предпочтительно от 1 до 25 мас. %, предпочтительнее от 5 до 25 мас. %.
Согласно настоящему изобретению оказывается предпочтительным, что концентрация полиэлектролита, который образует коацерваты, и соответствующих противоположно заряженных ионов в коацервате составляет от 10 до 100 мас. %; при этом нижние пределы составляют предпочтительно 25 или 40, предпочтительнее 45 мас. %; верхние пределы составляют предпочтительно 55 или 75, предпочтительнее 85, 90 и 95 мас. %.
Согласно настоящему изобретению оказывается предпочтительным, что фторидные ионы присутствуют в качестве взаимодействующих ионов.
Согласно настоящему изобретению оказывается предпочтительным, что взаимодействующие ионы в стоматологическом материале присутствуют, в основном, в растворимой форме (в частности, перед образованием реминерализационного вещества).
Стоматологический материал согласно настоящему изобретению может присутствовать в самоотверждающейся конфигурации.
Согласно настоящему изобретению оказывается предпочтительным, что стоматологический материал имеет продолжительность действия и/или продолжительность затвердевания, составляющую от 1 до 5 минут согласно стандарту ISO 9917:2007.
Согласно настоящему изобретению оказывается предпочтительным, что отвержденный стоматологический материал является самосклеивающимся и предпочтительно имеет на зубной эмали и/или дентине прочность сцепления при сдвиге, составляющую по меньшей мере 3,5 МПа.
Отвержденный стоматологический материал предпочтительно имеет прочность при сжатии, составляющую более чем 50, предпочтительно более чем 100, предпочтительнее более чем 200 МПа, и прочность при изгибе, составляющую более чем 20, предпочтительно более чем 25 МПа согласно стандарту ISO 9917:2007.
Стоматологический материал согласно настоящему изобретению имеет высокий потенциал минерализации в отношении твердого вещества зубов и, в частности, в своей предпочтительной форме образует минеральный замещающий материал, который имеет растворимость кислой среде при рН 4,2, которая является ниже, чем растворимость гидроксилапатита.
Согласно настоящему изобретению стоматологический материал может содержать добавки, такие как пигменты, красители, антиоксиданты, консерванты, наполнители или другие восстановители консистенции, которые могут быть добавлены, например, для регулирования реологических свойств. Для улучшения механических свойств оказывается возможным введение в стоматологический материал инертных неорганических или органических наполнителей, таких как силикаты, стекла, ZrO2, BaSO4, SiO2, а также форполимеры. Кроме того, могут быть использованы наполнители, способные активно воздействовать на процесс минерализации. В качестве иллюстративных примеров здесь можно привести высвобождающие ионы стекла, такие как иономерные стекла и биоактивные стекла, частицы гидроксилапатита, аморфный фосфат кальция (АСР) или тетракальцийфосфат (TCP). Особенно предпочтительным является гидроксилапатит, более конкретно, в форме наночастиц, у которых средний диаметр частицы составляет от 5 до 100 нм. Кроме того, посредством добавления растворимых в воде частиц, высвобождающих взаимодействующие ионов согласно настоящему изобретению, в частности, солей, содержащих ионы кальция, фосфатные и фторидные ионы, более конкретно, частиц CaCl2 и частиц (NH4)2HPO4, оказывается возможным достижение дополнительного увеличения содержания минеральных веществ и источников ионов в указанных частицах. Растворимые в воде цитраты представляют собой еще одну предпочтительную добавку. В целях окрашивания оказывается возможным добавление неорганических или органических цветных пигментов. Указанные пигменты могут служить для совмещения цвета материала с цветом твердого вещества зубов или, в качестве альтернативы, обеспечивать контраст между материалом и зубом.
В качестве следующих возможных добавок оказывается возможным введение в систему мономеров, представляющих собой, например, (мет)акрилаты или содержащие двойные связи полиэлектролиты. Посредством дополнительной возможности отверждения полиэлектролитной системы по второму механизму отверждения можно дополнительно воздействовать на свойства описанного стоматологического материала. В зависимости от архитектуры, полимеризуемые мономерные звенья могут быть сшиты с полиэлектролитами. Кроме того, оказывается возможной частичная функционализация используемых коацерватов.
Согласно настоящему изобретению термин «водный раствор» также распространяется на такие растворы, которые содержат воду в гомогенной системе, например, вместе с органическими растворителями. Такие растворы содержат предпочтительно более чем 10 мас. % воды, предпочтительнее более чем 50 мас. % воды, и особенно предпочтительно вода представляет собой единственный растворитель.
Полиэлектролиты можно рассматривать, в частности, как полимеры, которые содержат заряженные группы, прикрепленные непосредственно или через промежуточные группы к полимерной цепи. Указанные заряженные группы могут представлять собой отрицательно заряженные группы или положительно заряженные группы. Оказывается предпочтительным, что в каждой полимерной цепи присутствуют заряды только одного знака. При этом число заряженных групп в полимерной цепи может варьироваться в пределах широкого диапазона. Например, полимерная цепь подходящего полиэлектролита может содержать не только мономерные звенья, в которых присутствуют носители заряда, но также мономерные звенья, в которых отсутствуют носители заряда. Подходящий полиэлектролит предпочтительно обладает растворимостью, составляющей более чем 1 мг/мл.
Коацерваты получают, как правило, посредством обмена противоположно заряженных ионов растворенных полиионов, которые образуют коацерваты с полиионами. Стадию получения этого типа осуществляют посредством простого смешивания полиионов в водном растворе с соответствующими образующими коацерваты противоположно заряженными ионами в водном растворе. Получаемые в результате коацерваты после этого освобождают от избыточных остаточных ионов, осуществляя простые операции промывания, а затем они могут быть выделены в качестве материалов, состояние которых варьируется от сиропоподобного до высоковязкого или вязкоупругого. В качестве простого примера, натриевую соль полиакриловой кислоты смешивают с CaCl2. Выше определенной концентрации ионов Са2+ в растворе и соответствующего соотношения ионов Са2+ и карбоксилатных ионов происходит разделение фаз, и может быть выделен жидкий водный коацерват. Коацерваты могут быть использованы в жидкой форме в непрерывной/макроскопической фазе. Характеристика коацерватов согласно настоящему изобретению представляет собой переменное содержание воды. Из коацерватной фазы, выделенной из раствора, воду можно удалять, например, до тех пор, пока не будет получено твердое вещество. Это удаление воды является обратимым. После этого коацерваты могут быть использованы предпочтительно в измельченной форме, представляющей собой порошок. Порошки получают предпочтительно посредством высушивания и последующего измельчения высушенных коацерватов. Высушивание происходит при температурах ниже 250°C, предпочтительно ниже 100°C, например, при 60°C и стандартном давлении, при 40°C и стандартном давлении, или предпочтительно посредством лиофилизация. Измельчение может быть осуществлено с применением множества технологий, описанных в документах предшествующего уровня техники, в сухом или влажном состоянии, в подходящей жидкой среде. Следующая возможность представляет собой применение в форме суспензий или эмульсий. Далее порошки, суспензии или эмульсии в совокупности могут быть упомянуты с применением термина «тонкоизмельченные формы».
Далее для целей простоты коацерват на основе анионных полиэлектролитов называется термином «коацерват (а)», и коацерват на основе анионных полиэлектролитов называется термином «коацерват (b)».
Когда коацерват вступает в контакт с водным раствором, содержащим ион (взаимодействующий ион), который способен образовывать соединение, имеющее низкую растворимость в воде, со сшивающим противоположно заряженным ионом коацервата, происходит медленное осаждение соединения, имеющего низкую растворимость, на границе раздела с коацерватом.
Согласно одному варианту осуществления водный коацерват содержит в качестве основы полиакриловую кислоту и ионы Са2+. Согласно этому варианту осуществления, фосфат может быть использован в качестве взаимодействующего иона. Для целей минерализации в такой форме было показано, что преимущество имеет раствор, содержащий (NH4)2HPO4 в концентрации, составляющей от 10 мМ до 250 мМ, предпочтительно 130 мМ. Аналогичным образом, согласно этому варианту осуществления значение рН производит решающее воздействие на образование минерального заместителя. В течение минерализации значение рН снижается без применения дополнительных буферных растворов. Применение буферного раствора, например, такого как TRIS, может оказываться благоприятным для свойств стоматологического материала.
Согласно следующему варианту осуществления водный коацерват содержит в качестве основы полиаллиламинфосфатные ионы. В этом случае ионы Са2+ могут быть использованы в качестве взаимодействующих ионов. В целях минерализации имеют доказанное преимущество растворы, содержащие CaCl2 в концентрации, составляющей от 10 мМ до 250 мМ, предпочтительнее 130 мМ. Кроме того, согласно этому варианту осуществления значение рН также производит решающее воздействие на образование минерального заместителя.
Согласно одному варианту осуществления в течение определенного периода времени поверхность зуба находится в контакте с раствором, содержащим взаимодействующий ион. Затем на эту поверхность наносят коацерват, который распространяется по ее площади (например, в форме пленки) и остается на ней до тех пор, пока не будет осуществлена достаточная минерализация вещества зуба. Необязательная возможность представляет собой нанесение коацервата другого типа на эту обработанную поверхность.
В случае применения таким образом коацерват может быть нанесен, с одной стороны, в форме вязкой жидкости. На стороне, обращенной от зуба, поверхность затем может быть защищена в течение желательного периода, таким образом, чтобы не происходила преждевременная потеря коацерватного слоя. В случае применения другим образом коацерват может быть нанесен в тонкоизмельченной форме на поверхность зуба, обработанного с применением взаимодействующего иона. В этом случае применение коацервата в форме порошка также оказывается возможным, поскольку в среде полости рта всегда присутствует достаточное количество воды, которая является необходимой дл процессов минерализации.
Согласно следующему варианту осуществления коацерват смешивают в тонкоизмельченной форме с раствором взаимодействующего иона наносят в этой форме на поверхность зуба, подлежащего лечению. В этом случае минеральный заместитель также образуется, начиная с границ раздела коацерватных частиц, которые также способны воздействовать на вещество зуба.
Сочетание коацерватов на основе противоположно заряженных полиэлектролитов приводит, во-первых, к образованию сшитых высокой степени и твердых интеролимерных комплексов указанных полиэлектролитов, причем указанные комплексы являются нерастворимыми в воде. Во-вторых, в случае подходящего выбора противоположно заряженных ионов, образуется минеральный заместитель. То есть материал претерпевает затвердевание с образованием неорганических твердых веществ, предшественники которых составляют часть исходных компонентов в форме коацерватов.
В принципе, компоненты, содержащие коацерваты (а) и (b), можно смешивать друг с другом в форме жидких компонентов и выделять в составе вещества, которое затем очень быстро превращается в твердое вещество. Может оказаться более предпочтительным применение тонкоизмельченных коацерватов, которые смешивают в присутствии воды в процессе применения. Продолжительность действия и продолжительность затвердевания таких сочетаний коацерватов можно в каждом случае регулировать посредством выбора частиц или распределения частиц по размеру. Другая возможность представляет собой нанесение послойное коацерватов друг за другом.
Согласно одному предпочтительному варианту осуществления тонкоизмельченные компоненты, содержащие коацерваты (а) и (b), смешивают в присутствии водных растворов и наносят на вещество зуба, подлежащего лечению. Они претерпевают затвердевание, главным образом, в результате образования нерастворимых интерполимерных комплексов. По мере протекания реакции образующие минеральный заместитель ионы высвобождаются из коацерватов, и минеральный заместитель образуется в области, открытой для коацерватных смесей, а также в области твердого вещества зубов.
Согласно одному способу применения, в котором высушенные измельченные компоненты, содержащие коацерваты (а) и (b), смешивают друг с другом, оказывается необходимым добавление в смесь воды или водных растворов перед нанесением на вещество зуба, чтобы обеспечить протекание реакции. Это добавление в смесь воды или водных растворов происходит предпочтительно перед нанесением на вещество зуба, например, посредством перемешивания вручную или с применением автоматических способов, таких как перемешивание с применением капсулы.
Порошок и воду или водный раствор смешивают предпочтительно в массовом соотношении, составляющем от 5:1 до 1:50, предпочтительно от 2:1 до 1:10 и предпочтительнее от 2:1 до 1:2. Согласно одному предпочтительному варианту осуществления коацерваты (а) и (b) смешивают в форме порошков в массовом соотношении (суммы количеств (а) и (b) и количества воды или водного раствора), составляющем от 2:1 до 1:10, предпочтительно от 2:1 до 1:1 и предпочтительнее 3:2.
Кроме того, оказывается возможным нанесение индивидуальных порошков или смеси порошков на влажную поверхность зуба, где происходят реакции, которые указаны выше.
Согласно одному предпочтительному аспекту указанные смешанные измельченные коацерваты представляют собой смесь коацервата, содержащего полиакрилат кальция, и коацервата, содержащего полиаллиламинфосфата. В случае этого смешанного коацервата является преимущественным массовое соотношение, составляющее 1:1. Кроме того, оказываются возможными массовые соотношения, составляющие от 5:3 вплоть до 3:5. Количество воды, необязательно добавляемой в смесь, определяется целевой консистенцией смеси, которая требуется для конкретного применения.
Согласно следующему варианту осуществления неводную дисперсию смеси высушенных порошков компонентов с коацерватами (а) и (b), которая содержит полностью смешиваемый с водой растворитель (например, глицерин), перед применением перемешивают с дополнительным водным компонентом. Эту смесь затем наносят на вещество зуба, подлежащего лечению, где происходят процессы затвердевания и минерализации.
Может оказаться предпочтительным смешивание друг с другом перед применением водных эмульсий компонентов, содержащих коацерваты (а) и (b) в каждом случае и необязательно содержат дополнительно растворимые образующие минеральный заместитель соли в водной фазе. Эту смесь наносят на вещество зуба, подлежащего лечению, где и в этом случае происходят процессы затвердевания и минерализации.
Водная эмульсия коацервата или множества коацерватов в качестве стоматологического материала содержит по меньшей мере 1 процент по массе, предпочтительно по меньшей мере 2 процента по массе, предпочтительнее по меньшей мере 5 процентов по массе коацервата.
Смешивание может быть осуществлено в каждом случае вручную или с применением способов автоматического смешивания, таких как, например, перенос двухкомпонентного материала из двойных картриджей и смешивание посредством статического или динамического смесителя.
Согласно одному предпочтительному применению, в целях получения ускоренного сцепления между поверхностью зуба и стоматологическим материалом, перед нанесением компонентов коацерватов (а) и (b), смешанных друг с другом, твердое вещество зубов, подлежащих лечению, обрабатывают водным раствором, содержащим поликислоту или полиоснование, или соответствующие соли. Оказывается особенно предпочтительным нанесение поликислоты, а затем смеси (а) и (b) на поверхность вещество зуба, подлежащего лечению. Согласно следующему применению водный раствор поликислоты сначала наносят на вещество зуба, а затем наносят водный раствор полиоснования, прежде чем, наконец, наносят смесь (а) и (b). Согласно настоящему изобретению применение поликислоты или полиоснования, которые описаны в настоящем документе, перед применением стоматологического материала следует отличать от аналогичного предусмотренного настоящим изобретением добавления такой поликислоты или такого полиоснования в указанный стоматологический материал согласно настоящему изобретению.
Благодаря своим свойствам образования минерального заместителя и минерализации с течением времени, стоматологический материал согласно настоящему изобретению проявляет более интенсивное взаимодействие с твердым веществом зубов и, таким образом, противодействует эффекту дестабилизации сцеплению в результате воздействия окружающей среды. Такое взаимодействие может включать, например, построение мостиков из минерального заместителя между стоматологическим материалом и твердым веществом зубов.
Поскольку количества подвижных ионов в коацерватах является сравнительно большими, потенциал минерализации коацерватов для твердого вещества зубов является соответственно высоким. Посредством выбора сочетания противоположно заряженных ионов в коацервате оказывается также возможным воздействие на природу минерального заместителя и, таким образом, на его химическую устойчивость.
Следующий объект настоящего изобретения представляет собой набор для изготовления реминерализационного стоматологического материала согласно настоящему изобретению, который содержит следующие составляющие компоненты:
первый компонент, который содержит по меньшей мере один коацерват с одним из взаимодействующих ионов в качестве противоположно заряженного иона коацервата;
второй компонент, который содержит воду;
при этом второй из взаимодействующих ионов присутствует в качестве свободного иона в водном растворе во втором компоненте и/или в качестве противоположно заряженного иона второго коацервата в одном из двух компонентов.
Предпочтительно по меньшей мере один из компонентов представляет собой твердое вещество, предпочтительнее порошок.
Согласно следующему предпочтительному варианту осуществления по меньшей мере один из компонентов представляет собой жидкость, предпочтительно имеющую динамическую вязкость при 23°C, составляющую более чем 10 мПа⋅с, предпочтительнее более чем 50 мПа⋅с, еще предпочтительнее более чем 100 мПа⋅с.
Согласно следующему предпочтительному варианту осуществления по меньшей мере два из компонентов представляют собой пасты.
Согласно следующему предпочтительному варианту осуществления по меньшей мере два из компонентов представляют собой гели.
Согласно настоящему изобретению оказывается предпочтительным, что по меньшей мере один из компонентов, предпочтительно по меньшей мере два из компонентов, имеют значение рН, составляющее от 7 до 9 при 23°C.
Набор предпочтительно содержит дополнительный компонент с, который предпочтительно имеет значение рН, составляющее менее чем 7, и содержит усилитель адгезии. Усилитель адгезии предпочтительно представляет собой поликислоту или полиамин, который является протонированным, предпочтительно в степени, составляющей по меньшей мере 10%. Описанное здесь применение поликислоты или полиамина перед нанесением стоматологического материала согласно настоящему изобретению следует отличать от аналогичного предусмотренного настоящим изобретением добавления указанных материалов в указанный стоматологический материал согласно настоящему изобретению. Аналогичным образом, согласно настоящему изобретению оказывается возможным, что такой компонент выполняет двойную функцию в качестве усилителя адгезии, с одной стороны, и в качестве составляющего компонента указанного стоматологического материала с другой стороны.
Предпочтительно компоненты а и b содержатся в устройстве, подходящем для смешивания, предпочтительно в смесительной капсуле, содержащей предпочтительно порошок и/или жидкость, и/или в многокамерном картридже в качестве части системы картриджей для экструзии компонентов через смесительную иглу, содержащую предпочтительно две пасты или два геля.
Согласно одному предпочтительному варианту осуществления один из взаимодействующих ионов является многозарядным и присутствует в качестве противоположно заряженного иона в коацервате; второй взаимодействующий ион присутствует в водном растворе. По меньшей мере, один из компонентов дополнительно содержит второй полиэлектролит, который имеет иной заряд, чем полиэлектролит коацервата.
Согласно настоящему изобретению оказывается предпочтительным, что компонент а содержит по меньшей мере один коацерват (а) или (b) и содержит по меньшей мере один пол и электролит, который имеет иной заряд, чем полиэлектролит коацервата, и не присутствует в форме коацервата.
Согласно настоящему изобретению оказывается предпочтительным, что компонент а содержит по меньшей мере один коацерватный порошок, содержащий многозарядные анионы в качестве противоположно заряженных ионов, и по меньшей мере один порошок анионного полиэлектролита.
Согласно настоящему изобретению оказывается предпочтительным, что компонент а содержит по меньшей мере один коацерватный порошок, содержащий многозарядные катионы в качестве противоположно заряженных ионов и по меньшей мере один порошок катионного полиэлектролита.
Согласно настоящему изобретению оказывается предпочтительным, что компонент а содержит по меньшей мере один первый коацерватный порошок, содержащий ионы щелочноземельных металлов, предпочтительно ионы кальция, в качестве противоположно заряженных ионов, и по меньшей мере один второй коацерватный порошок, содержащий многозарядные анионы в качестве взаимодействующих ионов.
Следующий объект настоящего изобретения представляет собой способ применения набора согласно настоящему изобретению, включающий следующие стадии:
i. нанесение составляющего компонента b на дентин и/или зубную эмаль, предпочтительно в форме жидкости
ii. нанесение составляющего компонента а на дентин с составляющим компонентом b и/или на зубную эмаль с составляющим компонентом b, предпочтительно в форме порошка, пасты, геля или вязкой жидкости.
Аналогичным образом, объект настоящего изобретения представляет собой способ применения набора согласно настоящему изобретению, включающий следующие стадии:
i. смешивание составляющего компонента а и составляющего компонента b,
ii. нанесение смеси на дентин и/или на зубную эмаль, предпочтительно в форме пасты или геля.
Следующий объект настоящего изобретения представляет собой применение стоматологического материала согласно настоящему изобретению в качестве герметизирующего материала, покровного материала, корректирующего материала и/или пломбировочного материала, в качестве временного пломбировочного цемента, для покрытия пульпы, в качестве костного цемента, в качестве стоматологического лака, в качестве герметизирующего трещины материала, в качестве десенсибилизирующего вещества, в качестве реминерализационного вещества в профилактике или лечении кариозных поражений; или в целях изготовления указанных материалов.
Рабочие примеры настоящего изобретения продемонстрированы ниже.
Методы
Потеря массы при высушивании
В каждом случае немедленно после синтеза коацерваты взвешивали, а затем выдерживали в вакуумном сушильном шкафу Heraeus VT6025 от компании Thermo Scientific при температуре 40°C и давлении 50 мбар в течение по меньшей мере 24 часов. Потерю массы при высушивании вычисляли как разность начальной массы и конечной массы.
Термогравиметрический анализ (ТГА)
Термогравиметрический анализ (ТГА) осуществляли на воздухе при температуре от 25°C до 1000°C и скорости нагревания 10 К/мин с применением прибора STA 449FS Jupiter от компании Netzsch.
Оцениваемый параметр представлял собой потерю массы до 250°C, которая соответствовала остаточному содержанию воды, при получении лиофилизированных порошков.
Энергодисперсионная рентгеновская спектроскопия (ЭДРС)
Содержание элементов было определено с применением следующих приборов: настольный сканирующий электронный микроскоп (СЭМ)/ЭДРС ТМ 3000 М от компании Hitachi и детектор ЭДРС Quantax от компании Bruker. Были использованы лиофилизированные порошки.
Прочность при сжатии
Исследуемые образцы были изготовлены с применением двухкомпонентной формы, которая была изготовлена из нержавеющей стали и содержала шесть цилиндрических отверстий, имеющих высоту 4±0,02 мм и диаметр 2±0,01 мм. Форму помещали на стеклянную пластинку, и стоматологический материал вводили в отверстия. Когда отверстия были наполнены материалом, края отверстий были выровнены. Образцы выдерживали в форме в условиях температуры 37°C и почти 100% относительной влажности в течение одного часа. После этого образцы вместе с формой были извлечены из влажной камеры. Форму открывали, образцы, у которых высота составляла приблизительно 4 мм, и диаметр составлял приблизительно 2 мм, извлекали, и прочность при сжатии измеряли с применением универсальной испытательной машины модели Z 010/TN2A от компании Zwick, определяя прочность при сжатии через 1 час. Для определения прочность при сжатии через 4 суток, извлеченные из формы исследуемые образцы снова выдерживали во влажной камере в условиях температуры 37°C и 100% относительной влажности в течение 4 суток. После этого образцы извлекали из камеры, и прочность при сжатии с применением указанной универсальной испытательной машины от компании Zwick в следующих условиях:
постоянная скорость движения: 1,0 мм/мин;
вычисление прочности при сжатии (CS) согласно следующей формуле: CS [МПа]=F/(п⋅r2), в которой:
F представляет собой максимальное усилие (в ньютонах), приложенное к образцу;
r представляет собой радиус (в миллиметрах) образца.
Измерение осуществляли в каждом случае для шести образцов, и среднее значение определяли по шести измеренным значениям.
Прочность сцепления при сдвиге
Чтобы определить прочность сцепления при сдвиге (SBS), бычьи резцы без пульпы погружали в полимеризующуюся на холоде смолу Viscovoss GTS с отвердителем на основе метилэтилкетонпероксида (МЕКР) МЕН от компании Voss Chemie. Непосредственно перед испытанием используемые зубы подвергали абразивной обработке во влажном состоянии на зубной эмали или дентин с применением наждачной бумаги Р120, а затем повторно обрабатывали во влажном состоянии с применением тонкой наждачной бумаги Р500. Перед испытанием зубы выдерживали в деминерализованной воде. Для измерения зубы извлекали из деминерализованной воды. Затем двухкомпонентную тефлоновую форму с отверстием диаметром 3,0 мм согласно стандарту ISO/TS 11405:2003 устанавливали и фиксировали с помощью металлической скобки, и полость наполняли стоматологическим материалом. После наполнения полости помещали пленку Hostaphan, и стеклянную пластинку устанавливали и фиксировали с помощью другой металлической скобки. Наполненные формы выдерживали во влажной камере при температуре 37°C в течение 4 суток, и после этого извлекали содержимое форм. Исследуемые образцы затем подвергали измерению с применением устройства для сдвига согласно стандарту ISO10477:2004 и устройства для определения диаграммы сила-расстояние модели Z010/TN2A от компании Zwick GmbH & Со. (Ульм, Германия) при скорости движения 0,5 мм/мин. В каждом случае исследование осуществляли для трех образцов.
Динамическая вязкость
Вязкость измеряли при температуре 23°C, используя динамический вискозиметр с двумя пластинами (динамический реометр для измерения напряжения сдвига от компании Rheometric Scientific Inc.). Измерение осуществляли в режиме развертки стационарного напряжения с размерами зазора от 0,1 до 0,5 мм при напряжении сдвига в диапазоне от 0 до 50 Па.
Минерализация/рентгеновская дифрактометрия (РД)
Стоматологический материал, полученный в примере 6, отверждали в форме тонкого слоя. Материал затем выдерживали во влажной камере при температуре 37°C в течение 5 суток. Высушенный материал измельчали в ступке и анализировали в таком состоянии с применением рентгеновского дифрактометра D8 Discover от компании Bruker.
Были использованы коацерваты (а) и взаимодействующие ионы в водном растворе (примеры 9 и 10).
После окончания времени минерализации смесь центрифугировали, декантировали и промывали три раза ультрачистой водой 1,75. Промытые центрифугированные остатки затем высушивали при температуре 37°C.
В каждом случае высушенные продукты в форме порошков исследовали методом рентгеновской дифрактометрии (РД) для определения соответствующих минеральных фаз.
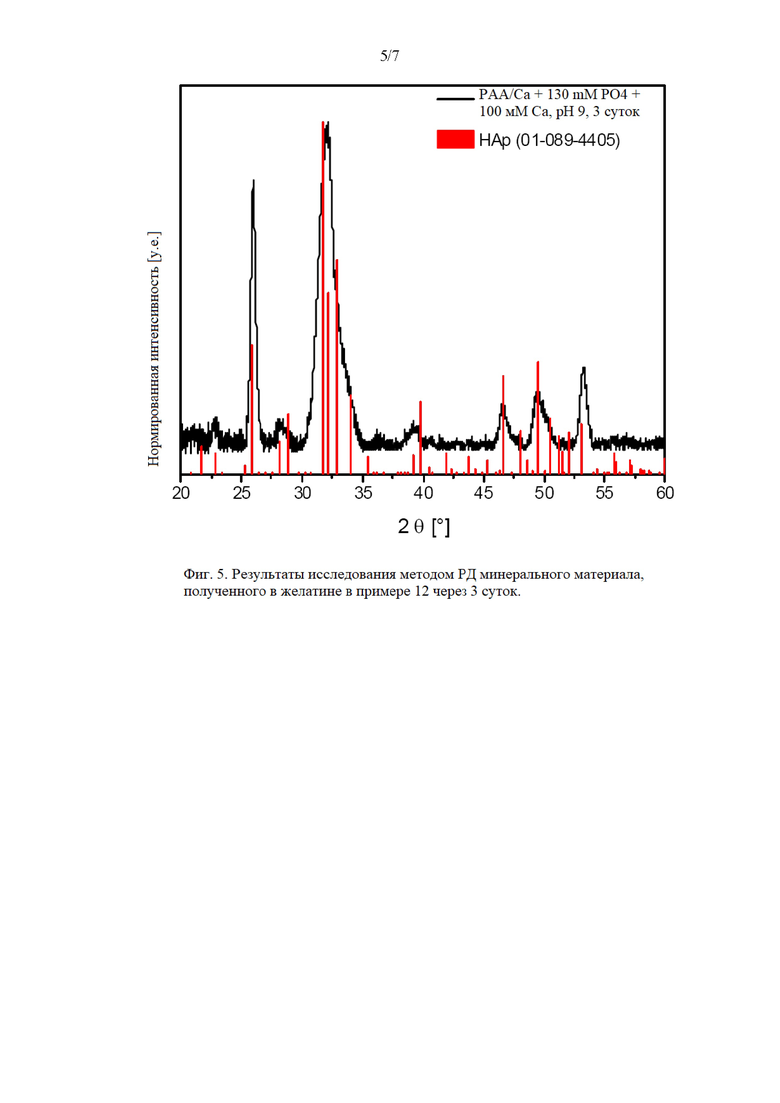
В примерах 11 и 12 минерализованный материал извлекали из внутренней части гелевого продукта и анализировали в таком состоянии с применением рентгеновского дифрактометра D8 Discover от компании Bruker.
Определение размеров частиц
Для определения распределения частиц по размерам 250 мг лиофилизированных и измельченных коацерватов диспергировали в 20 мл этанола в течение 5 минут в ультразвуковой ванне. После этого размер частиц измеряли с применением анализатора размеров частиц методом дифракции Фраунгофера (лазерный дифракционный анализатор размеров частиц LS 13 320 с универсальным жидкостным модулем от компании Beckmann Coulter) в денатурированном этаноле.
Используемые химические вещества
- Раствор натриевой соли полиакриловой кислоты (NaPAA15, Mw=15 кДа, раствор 35 мас. % от компании Sigma Aldrich)
- Полиакриловая кислота (РАА100, Mw=100 кДа, раствор 35 мас. % от компании Sigma Aldrich)
- Гидрохлорид полиаллиламина (РАН15, Mw=15 кДа, раствор 15 мас. % от компании Polyscience
- Порошок гидрохлорида полиаллиламина (Mw=17,5 кДа от компании Sigma)
- Тетрагидрат трехзамещенного цитрата натрия (Sigma Aldrich)
- Дигидрат хлорида кальция (Roth)
- Гидрофосфат диаммония (Sigma Aldrich)
- Хлорид стронция (Roth)
- Гидроксид натрия (Merck)
- Хлористоводородная кислота (Merck)
- Ультрачистая вода (MilliQ, Merck Millipore)
- Желатин (300 блюм, тип А)
Синтез коацерватов на основе солей полиакриловой кислоты (примеры 1-4)
В водный раствор натриевой соли полиакриловой кислоты при интенсивном перемешивании медленно добавляли водный раствор хлорида кальция или водный раствор хлорида стронция. В процессе добавления наблюдали разделение фаз. После завершения добавления перемешивание продолжали в течение пяти минут, а затем смесь выдерживали в состоянии покоя в течение 10 минут для дальнейшего разделения. Образовавшийся верхний раствор сливали, и оставшуюся фазу промывали три раза, используя каждый раз по 400 мл ультрачистой воды. Была получена вязкая жидкость.
Значения рН в каждом случае регулировали с применением растворов хлористоводородной кислоты и/или гидроксида натрия. Количества, концентрации и значения рН используемых растворов представлены в таблице 1.

Синтез коацервата на основе гидрохлорида полиаллиламина (пример 5)
В водный раствор гидрохлорида полиаллиламина при интенсивном перемешивании медленно добавляли водный раствор (NH4)2HPO4. В процессе добавления наблюдали разделение фаз. После завершения добавления перемешивание продолжали в течение пяти минут, а затем осуществляли центрифугирование при ускорении 7700 g в течение 3 минут для дальнейшего разделения. Образовавшийся верхний раствор сливали, и оставшуюся фазу промывали три раза, используя каждый раз по 10 мл ультрачистой воды. Была получена вязкая жидкость.
Значения рН в каждом случае регулировали с применением растворов хлористоводородной кислоты и/или гидроксида натрия. Количества, концентрации и значения рН используемых растворов представлены в таблице 2.

Содержание воды/потеря массы при высушивании вязких жидкостей, полученных в примерах 1, 4 и 5
Содержание воды в вязких жидкостях определяли по потере массы при высушивании. Потеря массы при высушивании представлена как содержание воды в таблице 3а.
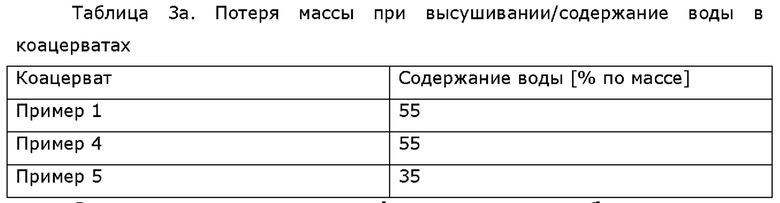
Содержание ионов в лиофилизированных образцах вязких жидкостей, полученных в примерах 1, 4 и 5
Содержание ионов определяли как содержание элементов методом энергодисперсионной рентгеновской спектроскопии (ЭДРС). Остаточное содержание воды в лиофилизированных вязких гелях определяли методом термогравиметрии (ТГА). Остаточное содержание воды и содержание элементов представлено в таблице 3b.
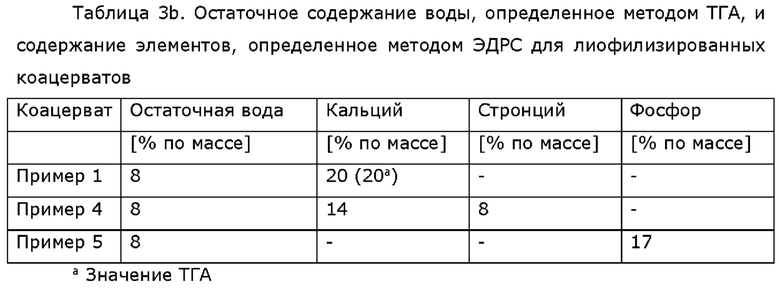
Получение коацерватных порошков
Коацерватный порошок (Р1)
Воду удаляли из вязкой жидкости, полученной в примере 1, посредством лиофилизации. Полученный в результате материал измельчали в вибрационной мельнице (Pulverisette 0 от компании Fritsch) в течение 7 часов, затем в дробильной мельнице (Pulverisette 2 от компании Fritsch) в течение 6 часов и, наконец, в шаровой мельнице (распределение шаров: 55×16 мм, 14×25 мм, 4×40 мм) в течение 18 часов.
Остаточное содержание воды в полученном белом порошке определяли методом ТГА. Остаточное содержание воды составляло 8% по массе. Распределение частиц по размерам: D10=1,0 мкм и D50=4,4 мкм.
Коацерватный порошок (Р2)
Воду удаляли из вязкой жидкости, полученной в примере 5, посредством лиофилизации. Полученный в результате материал измельчали в вибрационной мельнице (Pulverisette 0 от компании Fritsch) в течение 7 часов, затем в капсульном смесителе (1 мл; диаметр шаров: 3,15 мм; Silamat от компании Ivoclar Vivadent) в течение 60 секунд, и, наконец, в капсульном смесителе (1 мл; диаметр шаров: 0,1 мм; Silamat от компании Ivoclar-Vivadent) в течение 60 секунд.
Остаточное содержание воды в полученном белом порошке определяли методом ТГА. Остаточное содержание воды составляло 8% по массе. Распределение частиц по размерам: D10=2,4 мкм и D50=24,6 мкм
Порошок гидрохлорида полиаллиламина (Р3)
Этот порошок представляет собой второй катионный полиэлектролит, который, в соответствии с настоящим изобретением, может быть использован вместе с коацерватом, содержащим анионный полиэлектролит, и который обеспечивает глубину минерализация таким образом, как уже было описано выше и проиллюстрировано в примерах.
Пример 6. Получение самоклеящегося самоотверждающегося стоматологического материала из коацерватных порошков Р1 и Р2
Для получения стоматологического материала 150 мг порошка Р1 смешивали с 150 мг порошка Р2. Эту смесь порошков, а также 0,2 мл воды раздельно вводили из одной смесительной капсулы в другую смесительную капсулу Applicap от компании DMG (Гамбург).
Порошок и жидкость перемешивали с применением вибрационного смесителя (Silamat от компании Ivoclar Vivadent AG) в течение 20 секунд и получали готовый к применению стоматологический материал.
Немедленно после перемешивания полученный в результате стоматологический материал извлекали из смесительной капсулы с применением иглы смесительной капсулы и подвергали обработке.
Пример 7. Получение самоклеящегося самоотверждающегося стоматологического материала из коацерватного порошка Р1
Вручную перемешивали с помощью шпателя на лотке 300 мг порошка Р1 и 0,2 мл раствора (NH^HPCm (130 мМ, рН 9) в течение приблизительно 30 секунд и получали готовый к применению стоматологический материал.
Пример 8. Получение самоклеящегося самоотверждающегося стоматологического материала из коацерватного порошка Р1
Вручную перемешивали 300 мг измельченного порошка Р1 и 0,2 мл раствора, содержащего 130 мМ (NH4)2HPO4 и 100 мМ цитрата натрия и доведенного до рН 9, в течение приблизительно 30 секунд и получали готовый к применению стоматологический материал. По сравнению с примером 7, этот материал затвердевает значительно быстрее.
Пример 9
Вручную перемешивали с помощью шпателя 40 мг измельченного порошка Р1 и 1,75 мл раствора 130 мМ (NH4)2HPO4, доведенного до рН 9, в течение приблизительно 30 секунд в реакционном резервуаре (пробирке Эппендорфа) объемом 2 мл, встряхивали в течение непродолжительного времени, а затем выдерживали в горизонтальном положении при комнатной температуре в течение 5 минут и 24 часов, соответственно.
Пример 10
Перемешивали 40 мг коацерватного порошка Р1 смешивали с 1,75 мл водного раствора, содержащего 130 мМ (NH4)2HPO4 и 100 мМ цитрата натрия (по аналогии с примером 8) в реакционном резервуаре (пробирке Эппендорфа) объемом 2 мл, встряхивали в течение непродолжительного времени, а затем выдерживали в горизонтальном положении при комнатной температуре в течение 5 минут и 24 часов, соответственно.
Исследование
Прочность при сжатии определяли для стоматологических материалов, полученных в примерах 6-8. Значения прочности при сжатии представлены в таблице 4.
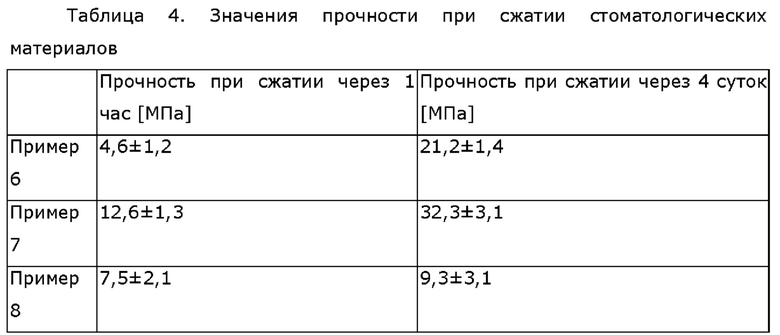
Прочность при сжатии оказалась наиболее высокой для материала, полученного в примере 7. Для всех стоматологических материалов значения прочности при сжатии были выше через 4 суток, чем через 1 час после обработки.
Прочность сцепления при сдвиге (SBS)
Прочность сцепления при сдвиге измеряли в примерах 6-8. Стоматологический материал является самоклеящимся. В образцах наблюдались трещины или деформации, которые возникали перед разрушением при сдвиге.
Минерализация
Минерализацию смесей, полученных в примерах 6, 9 и 10, исследовали методом РД. Обнаруженные минеральные фазы представлены в таблице 5.
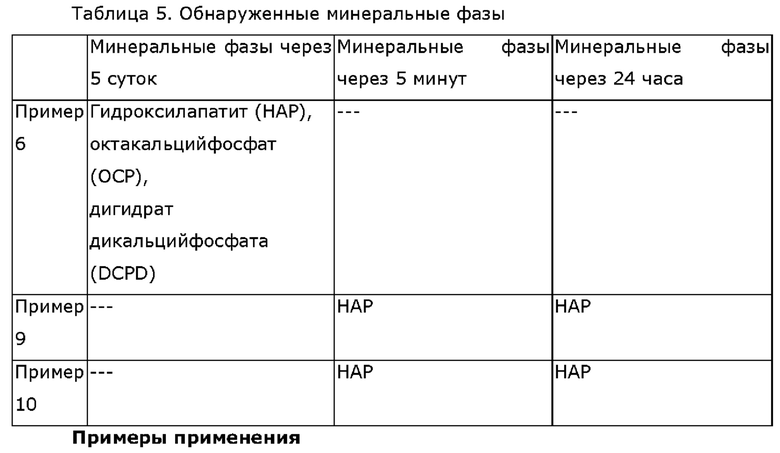
Получение модельного вещества
Для представленных ниже примеров применения были сначала получены модельные вещества для деминерализованного дентина. Каждое модельное вещество состоит из геля, который является твердым при комнатной температуре.
При температуре 40°C растворяли 10 г желатина (тип А, 300 блюм) в 90 мл водного раствора, имеющего рН 9 и содержащего 130 мМ гидрофосфата диаммония и 100 мМ тетрагидрата трехзамещенного цитрата натрия. Полученный в результате желатиновый раствор помещали в стандартные 24-луночные титровальные планшеты и выдерживали для охлаждения до комнатной температуры. Немедленно после достижения комнатной температуры образцы твердого геля извлекали из титровального планшета с помощью шпателя и помещали в водный раствор.
Нанесение стоматологических материалов на модельные вещества
Стоматологические материалы в каждом случае наносили на поверхность модельного вещества, т.е. на верхние поверхности дискообразных образцов геля, а затем выдерживали при комнатной температуре в 10 мл водного раствора, имеющего рН 9 и содержащего 130 мМ гидрофосфата диаммония и 100 мМ тетрагидрата трехзамещенного цитрата натрия, таким образом, что стоматологический материал и модельное вещество были покрыты раствором, или их выдерживали в шкафу для кондиционирования в условиях 100% относительной влажности воздуха и комнатной температуры. Через 2 суток, 3 суток, 4 суток, 8 суток или 12 суток образцы геля извлекали и промывали ультрачистой водой. Затем с помощью бритвенного лезвия были получены поперечные сечения дискообразных образцов геля. Эти поперечные сечения были исследованы оптическими методами, чтобы определить, присутствует ли минерализованный материал под поверхностью модельного вещества, и насколько глубоко проникает этот материал в модельное вещество.
Примеры 11-13
Самоклеящиеся самоотверждающиеся стоматологические материалы были получены таким же способом, как в примере 6. Порошки/смеси порошков и жидкости, используемые в этом случае, представлены ниже в таблице 6 ниже.
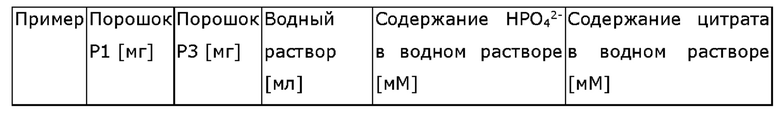
Используемый жидкий составляющий компонент представляет собой водный раствор, содержащий (NH4)2HPO4 и цитрат натрия, который также был уже использован в примере 8.
В примерах 12 и 13 смесь порошков содержит порошок Р3 в качестве второго катионного пол и электролит, который используется вместе с коацерватом, содержащим анионный полиэлектролит (порошок Р1), и который обеспечивает глубину минерализация таким способом, как уже было указано выше.
Для получения стоматологического материала 150 мг соответствующего порошка/смеси порошков, а также жидкого составляющего компонента вводили раздельно из одной смесительной капсулы в другую смесительную капсулу Applicap от компании DMG (Гамбург). Порошок и жидкость перемешивали с применением вибрационного смесителя (Silamat от компании Ivoclar Vivadent AG) в течение 20 секунд и получали готовый к применению стоматологический материал.
Немедленно после перемешивания полученный в результате стоматологический материал извлекали из смесительной капсулы с применением иглы смесительной капсулы и подвергали обработке.
Полученные таким способом стоматологические материалы наносили на модельное вещество, и минерализацию исследовали в соответствии с приведенными ниже примерами применения.
Пример 11
Стоматологический материал, полученный в примере 11 и указанный выше в таблице 6, наносили на модельное вещество и выдерживали в водном растворе, как описано выше
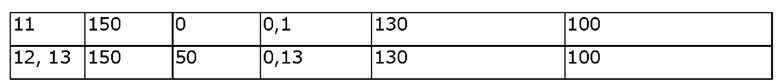
Через 4 суток наблюдалась небольшая глубина минерализации. Через 12 суток наблюдаемая глубина минерализации оставалась небольшой (фиг. 1). Для минерального материала, полученного в желатине, кальций, углерод, фосфор и кислород были обнаружено по всей глубине (фиг. 2). Минеральный материал был идентифицирован как гидроксилапатит методом РД (фиг. 3).
Пример 12
Стоматологический материал, полученный в примере 12 и указанный выше в таблице 6, наносили на модельное вещество и выдерживали в водном растворе, как описано выше
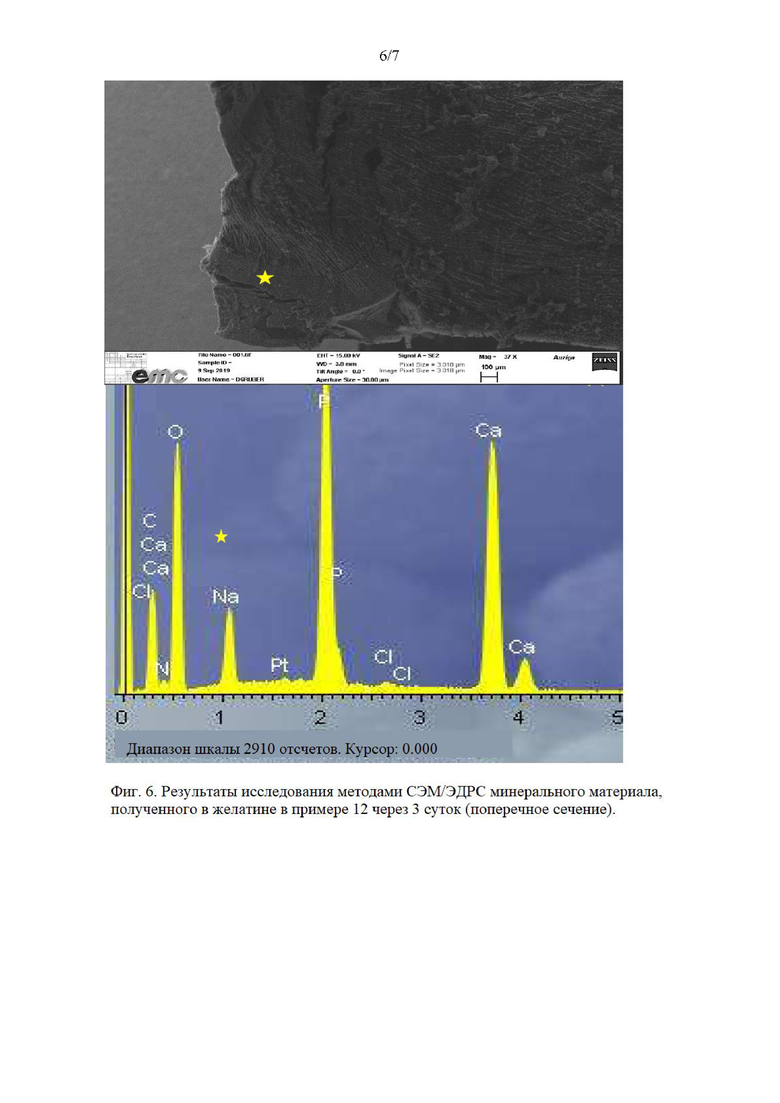
Уже через 3 суток наблюдалась значительная глубина минерализации (фиг. 4). Стоматологический материал, нанесенный на желатиновую поверхность, обеспечивает сцепление с поверхностью, проявляет устойчивость и не разрушается. Полученный минеральный материал может быть идентифицирован как гидроксилапатит при измерении методом РД (фиг. 5). Для минерального материала, полученного в желатине, кальций, углерод, фосфор и кислород могут быть обнаружены в результате анализа методом ЭДРС (фиг. 6).
Пример 13
Стоматологический материал, полученный в примере 13 и указанный выше в таблице 6, наносили на модельное вещество и выдерживали в камере для кондиционирования, как описано выше
Уже через 2 суток наблюдалась значительная глубина минерализации (фиг. 7). Стоматологический материал, нанесенный на желатиновую поверхность, обеспечивает сцепление с поверхностью, проявляет устойчивость и не разрушается. Полученный минеральный материал был идентифицирован как гидроксилапатит методом РД.



Группа изобретений относится к области материалов для реминерализации зубов и их применению. Предлагается реминерализационный стоматологический материал, содержащий по меньшей мере один катион и по меньшей мере один анион, которые выступают в качестве взаимодействующих ионов для образования реминерализационного вещества, причем по меньшей мере один из взаимодействующих ионов является многозарядным и присутствует в качестве противоположно заряженного иона с полиэлектролитом в коацервате; а также применение указанного выше стоматологического материала в качестве герметизирующего материала, покровного материала, корректирующего материала и/или пломбировочного материала. Предлагается набор для изготовления указанного выше реминерализационного материала, который содержит: a. первый компонент, который содержит по меньшей мере один коацерват с одним из взаимодействующих ионов, представляющим собой противоположно заряженный ион коацервата; b. второй компонент, содержащий воду; причем второй из взаимодействующих ионов присутствует в качестве свободного иона в водном растворе в компоненте b и/или в качестве противоположно заряженного иона второго коацервата в одном из двух компонентов. Варианты способа применения указанного выше набора включают следующие стадии: i. нанесение составляющего компонента b на дентин и/или зубную эмаль, ii. нанесение составляющего компонента a на дентин с составляющим компонентом b и/или на зубную эмаль с составляющим компонентом b, или: i. смешивание составляющего компонента a и составляющего компонента b, ii. нанесение смеси на дентин и/или на зубную эмаль. Использование группы изобретений обеспечивает эффективную реминерализацию. 5 н. и 29 з.п. ф-лы, 7 ил., 7 табл., 13 пр.
1. Реминерализационный стоматологический материал, содержащий по меньшей мере один катион и по меньшей мере один анион, которые выступают в качестве взаимодействующих ионов для образования реминерализационного вещества, причем по меньшей мере один из взаимодействующих ионов является многозарядным и присутствует в качестве противоположно заряженного иона с полиэлектролитом в коацервате.
2. Стоматологический материал по п. 1, в котором один из взаимодействующих ионов является многозарядным и присутствует в качестве противоположно заряженного иона в коацервате, и второй взаимодействующий ион присутствует в водном растворе.
3. Стоматологический материал по п. 1 или 2, в котором дополнительно присутствует второй полиэлектролит, который имеет иной заряд, чем полиэлектролит коацервата.
4. Стоматологический материал по п. 1, в котором оба взаимодействующих иона являются многозарядными и присутствуют в качестве противоположно заряженных ионов соответствующего коацервата.
5. Стоматологический материал по любому из пп. 1-4, в котором анионные полиэлектролиты для образования коацерватов с многозарядными катионами выбраны из группы органических полиэлектролитов, которую предпочтительно составляют:
a. полимеры и сополимеры, которые содержат группы карбоновых кислот, группы фосфорных кислот, группы фосфоновых кислот и/или группы сульфоновых кислот, а также соответствующие соли и соответствующие неполные сложные эфиры; предпочтительно поликарбоновые кислоты, полиалкиленфосфорные кислоты, полиалкиленфосфоновые кислоты и полисульфоновые кислоты, а также соответствующие соли и соответствующие неполные сложные эфиры; предпочтительнее поли(мет)акриловая кислота, полиаспарагиновая кислота, полиитаконовая кислота и полиглутаминовая кислота, а также соответствующие соли;
b. кислые белки, производные кислых белков и соответствующие соли, которые предпочтительно образует лизоцим или желатин (тип B); c. кислые полисахариды и соответствующие соли, которые предпочтительно образуют каррагенан, пектин, альгиновая кислота и гиалуроновая кислота.
6. Стоматологический материал по любому из пп. 1-5, в котором анионные полиэлектролиты для образования коацерватов с многозарядными катионами имеют средние молекулярные массы (среднемассовые значения Mw), составляющие от 3 до 1500 кДа, предпочтительно от 5 до 500 кДа, предпочтительнее от 8 до 200 кДа, еще предпочтительнее от 8 до 50 кДа.
7. Стоматологический материал по любому из пп. 1-6, в котором многозарядные катионы выбраны из группы, которую составляют минералообразующие катионы; предпочтительно катионы металлов; предпочтительнее металлов групп 2A, 3B, и 3A Периодической системы элементов, а также лантанидов; предпочтительнее Ba2+, Ca2+, Sr2+, Tb3+и Yb3+; предпочтительнее Ca2+ и/или смеси катионов металлов, содержащие Ca2+.
8. Стоматологический материал по любому из пп. 1-7, в котором катионные полиэлектролиты для образования коацерватов с многозарядными анионами выбраны из органических полиэлектролитов, предпочтительно из группы, которую составляют полимеры и сополимеры, которые содержат первичные, вторичные и/или третичные аминогруппы, а также соответствующие соли; предпочтительно полиамины; предпочтительнее полиаллиламин, линейный или разветвленный полиэтиленимин, хитозан, полибетаин и полиаргинин, а также соответствующие соли; предпочтительнее гидрохлорид полиаллиламина (PAH).
9. Стоматологический материал по любому из пп. 1-8, в котором катионные полиэлектролиты для образования коацерватов с многозарядными анионами имеют средние молекулярные массы (среднемассовые значения Mw), составляющие от 3 до 1500 кДа, предпочтительно от 5 до 500 кДа, предпочтительнее от 8 до 200 кДа, еще предпочтительнее от 8 до 50 кДа.
10. Стоматологический материал по любому из пп. 1-9, в котором многозарядные анионы выбраны из группы, которую составляют минералообразующие анионы, предпочтительно ортофосфатные ионы, дифосфатные ионы, метафосфатные ионы, силикатные ионы, более конкретно, неорганические силикатные ионы, предпочтительно ортосиликатные, иносиликатные и имеющие запрещенную зону силикатные ионы, и частично модифицированные органическими группами силикатные ионы, более конкретно, алкилоксисиликатные ионы, сульфатные ионы, вольфраматные ионы, ванадатные ионы, молибдатные ионы, и карбонатные ионы, предпочтительнее ортофосфатные ионы, дифосфатные ионы, метафосфатные ионы, сульфатные ионы, вольфраматные ионы, ванадатные ионы, молибдатныеионы, предпочтительнее ортофосфатные ионы и/или смеси ортофосфатных ионов с минералообразующими анионами.
11. Стоматологический материал по любому из пп. 1-10, в котором доля коацерватного компонента составляет более чем 1 процент по массе, предпочтительно более чем 2 процента по массе, предпочтительнее более чем 5 процентов по массе.
12. Стоматологический материал по любому из пп. 1-11, который представляет собой жидкость, и/или эмульсию, и/или суспензию.
13. Стоматологический материал по любому из пп. 1-11, который представляет собой гель.
14. Стоматологический материал по любому из пп. 1-11, который представляет собой пасту.
15. Стоматологический материал по любому из пп. 1-14, который содержит от 1 до 95 мас.% взаимодействующих ионов и коацерват; при этом предпочтительные нижние пределы и/или верхние пределы составляют 5, 10, 15, 25 и так далее вплоть до 95 мас.%.
16. Стоматологический материал по любому из пп. 1-15, который содержит воду, составляющую предпочтительно от 5 до 95 мас.%, при этом предпочтительные нижние пределы и/или верхние пределы составляют 5, 10, 15, 25 и так далее вплоть до 95 мас.%.
17. Стоматологический материал по любому из пп. 1-16, в котором коацерват имеет содержание воды, составляющее от 0,1 до 90 мас.%, предпочтительно от 1 до 75 мас.%, предпочтительнее от 5 до 60 мас.%.
18. Стоматологический материал по любому из пп. 1-17, в котором концентрация полиэлектролита, образующего коацерваты, и соответствующих противоположно заряженных ионов в коацервате составляет от 10 до 95 мас.%; при этом предпочтительные нижние пределы составляют 25 или 40, предпочтительнее 45 мас.%, предпочтительные верхние пределы составляют 55 или 75, предпочтительнее 85 и 90 мас.%.
19. Стоматологический материал по любому из пп. 1-18, в котором фторидные ионы присутствуют в качестве взаимодействующих ионов.
20. Стоматологический материал по любому из пп. 1-19, причем взаимодействующие ионы присутствуют в стоматологическом материале, в основном, в растворимой форме.
21. Стоматологический материал по любому из пп. 1-20, который является самоотверждающимся.
22. Набор для изготовления реминерализационного стоматологического материала по любому из пп. 1-21, который содержит следующие составляющие компоненты:
a. первый компонент, который содержит по меньшей мере один коацерват с одним из взаимодействующих ионов, представляющим собой противоположно заряженный ион коацервата;
b. второй компонент, содержащий воду;
причем второй из взаимодействующих ионов присутствует в качестве свободного иона в водном растворе в компоненте b и/или в качестве противоположно заряженного иона второго коацервата в одном из двух компонентов.
23. Набор по п. 22, в котором по меньшей мере один из компонентов представляет собой твердое вещество, предпочтительно порошок.
24. Набор по п. 22, в котором по меньшей мере один из компонентов представляет собой жидкость, предпочтительно имеющую динамическую вязкость, составляющую более чем 10 мПа⋅с, предпочтительно более чем 50 мПа⋅с, предпочтительнее более чем 100 мПа⋅с.
25. Набор по п. 22, в котором оба компонента представляют собой пасты.
26. Набор по п. 22, в котором оба компонента представляют собой гели.
27. Набор по любому из пп. 22-26, в котором по меньшей мере у одного из компонентов, предпочтительно по меньшей мере у двух из компонентов значение pH, составляющее от 7 до 10 при 23°C.
28. Набор по любому из пп. 22-27, который содержит дополнительный компонент c, который предпочтительно содержит усилитель адгезии.
29. Набор по любому из пп. 22-28, в котором компоненты a и b содержатся в устройстве, подходящем для смешивания, предпочтительно в смесительной капсуле, содержащей предпочтительно порошок или жидкость, и/или в многокамерном картридже, представляющем собой часть системы картриджей для экструзии компонентов через смесительную иглу, содержащую предпочтительно две пасты или два геля.
30. Набор по любому из пп. 22-29, в котором один из взаимодействующих ионов является многозарядным и присутствует в качестве противоположно заряженного иона с полиэлектролитом в коацервате, и второй взаимодействующий ион присутствует в водном растворе, причем по меньшей мере один из компонентов дополнительно содержит второй полиэлектролит, который имеет иной заряд, чем полиэлектролит коацервата.
31. Набор по любому из пп. 22-24, 27-29, в котором компонент a содержит по меньшей мере один первый коацерватный порошок, содержащий ионы щелочноземельных металлов, предпочтительно ионы кальция в качестве противоположно заряженных ионов, и по меньшей мере один второй коацерватный порошок, содержащий многозарядные анионы в качестве взаимодействующих ионов.
32. Способ применения набора по любому из пп. 22-31, включающий следующие стадии:
i. нанесение составляющего компонента b на дентин и/или зубную эмаль, предпочтительно в форме жидкости,
ii. нанесение составляющего компонента a на дентин с составляющим компонентом b и/или на зубную эмаль с составляющим компонентом b, предпочтительно в форме порошка, пасты, геля или вязкой жидкости.
33. Способ применения набора по любому из пп. 22-31, включающий следующие стадии:
i. смешивание составляющего компонента a и составляющего компонента b,
ii. нанесение смеси на дентин и/или на зубную эмаль, предпочтительно в форме пасты или геля.
34. Применение стоматологического материала по любому из пп. 1-21 в качестве герметизирующего материала, покровного материала, корректирующего материала и/или пломбировочного материала.
| SHU-CHEN HUANG et al | |||
| A carbonate controlled-addition method for amorphous calcium carbonate spheres stabilized by poly(acrylic acid)s | |||
| Langmuir, 2007, V | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| УСТРОЙСТВО ДЛЯ ТЕЛЕФОНИРОВАНИЯ | 1924 |
|
SU12086A1 |
| Найдено в PubMed, PMID: 17963412, DOI: 10.1021/la701972n | |||
| CANTAERT B | |||
| et al.Think Positive: Phase Separation Enables a Positively | |||
Авторы
Даты
2023-07-18—Публикация
2020-04-08—Подача