ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к соединениям, пригодным для лечения заболеваний, вызванных вирусом гепатита В, у животных, в частности для лечения заболеваний, вызванных вирусом гепатита В, у людей.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
[0001] Гепатит В представляет собой вирусное заболевание, передающееся парентерально через зараженный материал, такой как кровь и продукты крови, зараженные иглы, половым путем и вертикально от инфицированной матери или матери-носителя к ее детям. В тех регионах мира, где это заболевание является обычным явлением, вертикальная передача в раннем возрасте приводит к тому, что высокая доля инфицированных людей становятся хроническими носителями гепатита В. По оценкам Всемирной организации здравоохранения, во всем мире инфицировано более 2 миллиардов человек, происходит около 4 миллионов острых случаев в год, 1 миллион смертей в год и имеется 350-400 миллионов хронических носителей. Примерно 25% носителей умирают от хронического гепатита, цирроза или рака печени, и почти 75% хронических носителей являются людьми азиатской расы. Вирус гепатит В (ВГВ) - второй по значимости канцероген после табака, вызывающий от 60% до 80% всех случаев первичного рака печени. ВГВ в 100 раз более заразен, чем ВИЧ.
[0002] ВГВ передается через кожный или парентеральный контакт с инфицированной кровью, биологическими жидкостями и при половом акте. ВГВ может оставаться на любой поверхности, с которой соприкасается, около недели, например, столешницы, бритвенные лезвия, пятна крови, не теряя заразности. Однако ВГВ не может проникать через кожу или барьер слизистой оболочки. Для передачи требуется некоторый прорыв этого барьера, который может быть минимальным и незначительным.
[0003] ВГВ представляет собой небольшой ДНК-вирус с оболочкой, принадлежащий к семейству гепаднавирусов. Вирус реплицируется через промежуточную форму РНК путем обратной транскрипции, что на практике связывает их с ретровирусами, такими как ВИЧ. Хотя репликация происходит в печени, вирус распространяется через кровь, где вирусные белки и антитела против них обнаруживаются у инфицированных людей. ВГВ во много раз более заразен, чем ВИЧ, из-за более высоких концентраций вируса ВГВ, обнаруживаемых в кровотоке в любой момент времени.
[0004] Инфекция ВГВ приводит к образованию двух разных частиц: 1) самого вируса ВГВ (или частицы Дейна), который включает вирусный капсид, собранный из белка корового антигена ВГВ (HBcAg) и покрытый поверхностным антигеном гепатита В (HBsAg), способный повторно инфицировать клетки; и 2) субвирусные частицы (или СВЧ), которые представляют собой липопротеиноподобные частицы высокой плотности, состоящие из липидов, холестерина, сложных эфиров холестерина, а также малых и средних форм поверхностного антигена гепатита В (HBsAg), которые являются неинфекционными. На каждую произведенную вирусную частицу в кровь попадает от 1000 до 10000 СВЧ. Таким образом, СВЧ (и белок HBsAg, который они несут) представляют собой подавляющее большинство вирусного белка в крови. Инфицированные ВГВ клетки также секретер уют растворимый протеолитический продукт пре-корового белка, называемый е-антигеном ВГВ (HBeAg).
[0005] Вирус гепатита D (ВГД) использует HBsAg для формирования своей вирусной структуры (Taylor, 2006, Virology, 344: 71-76), и поэтому инфекция ВГД может возникать только у субъектов с сопутствующей инфекцией ВГВ. В то время как частота сочетанной инфекции ВГД у бессимптомных носителей ВГВ и хронических заболеваний печени, связанных с ВГВ, низкая в странах с низкой заболеваемостью ВГВ-инфекцией, это является серьезным осложнением у ВГВ - инфицированных субъектов в странах с высокой заболеваемостью ВГВ-инфекцией и может увеличивать скорость прогрессирования болезни печени до скоротечного гепатита. Таким образом, очевидная неудовлетворенная медицинская потребность в лечении инфекции ВГВ становится еще более актуальной для субъектов с совместной инфекцией ВГВ / ВГД.
[0006] Современные общепринятые методы лечения ВГВ включают иммунотерапию на основе интерферона или тимозина α1 и подавление вирусной продукции посредством ингибирования полимеразы ВГВ (например, "ядер"). Ингибиторы полимеразы ВГВ эффективны в снижении вирусной продукции, но практически не влияют на быстрое снижение уровня HBsAg в крови или могут медленно снижать HBsAg при длительном лечении у ограниченного числа пациентов (как в случае с тенофовир дизопроксил фумаратом). Иммунотерапия на основе интерферона может привести к снижению производства вируса и раннему удалению HBsAg из крови, но только у небольшого процента пациентов, прошедших лечение. Общепризнанная роль HBsAg в крови состоит в том, чтобы изолировать анти-HBsAg антитела и позволить инфекционным вирусным частицам ускользнуть от иммунного обнаружения, что, вероятно, является одной из причин того, что инфекция ВГВ остается хроническим заболеванием. Кроме того, HBsAg, HBeAg и HBcAg обладают иммуноингибирующими свойствами, как это обсуждается ниже, и стойкость этих вирусных белков в крови пациентов после введения любого из доступных в настоящее время методов лечения ВГВ, как описано выше, вероятно, оказывает значительное влияние на трудность достижения пациентами иммунологического контроля над их инфекцией ВГВ.
[0007] Хотя все три основных белка ВГВ (HBsAg, HBeAg и HBcAg) обладают иммуноингибирующими свойствами (см. ниже), HBsAg составляет подавляющее большинство белка ВГВ, циркулирующего в крови у субъектов, инфицированных ВГВ. Кроме того, хотя удаление (посредством сероконверсии) HBeAg или снижение виремии в сыворотке крови не коррелируют с развитием устойчивого контроля инфекции ВГВ после лечения, удаление HBsAg в сыворотке крови (и сероконверсия) при инфекции ВГВ - это всеобще признанный превосходный прогностический индикатор противовирусного ответа на лечение, который позволит контролировать инфекцию ВГВ после лечения (хотя это происходит только у небольшой части пациентов, получающих иммунотерапию). Таким образом, хотя уменьшение всех трех основных белков ВГВ (HBsAg, HBeAg и HBcAg) может привести к оптимальному устранению ингибирующего эффекта, удаление одного HBsAg может быть достаточным само по себе для устранения основной части подавления вирусами иммунной функции у субъектов с ВГВ-инфекцией.
[0008] Следовательно, в отсутствие какой-либо текущей схемы лечения, которая может восстановить иммунологический контроль ВГВ у значительной части пациентов, необходимо обеспечить эффективное лечение инфекции ВГВ и совместной инфекции ВГВ/ВГД, которые могут восстановить иммунологический контроль у большинства пациентов.
[0009] Вирусные инфекции гепатита В в сочетании с вирусными инфекциями гепатита D представляют собой постоянную медицинскую проблему, потому что, как и любой быстро реплицирующийся инфекционный агент, они вызывают возникновение мутаций, которые помогают некоторым субпопуляциям ВГВ стать устойчивыми к текущим схемам лечения. В настоящее время не существует эффективных терапевтических средств для лечения людей, инфицированных вирусом гепатита В и/или гепатита D (HDV), которые приводят к сероконверсии вируса в организме, или которые приводят к снижению уровня антигена на 90% по сравнению с исходным уровнем у лиц, страдающих вирусной инфекцией гепатита В. В настоящее время методы лечения хронической ВГВ и/или ВГД-инфекции, рекомендованные Американской ассоциацией по изучению заболеваний печени (AASLD) и Европейской ассоциацией изучения печени (EASL), включают интерферон альфа (IFNα), пегилированный интерферон альфа-2а (Peg-IFN2a), энтекавир и тенофовир. Однако типичная терапия интерфероном длится 48 недель и приводит к серьезным и неприятным побочным эффектам, а сероконверсия HBeAg через 24 недели после прекращения терапии колеблется только в диапазоне 27-36%. Сероконверсия HBsAg еще ниже - сразу после прекращения лечения наблюдается лишь 3%, а через 5 лет она увеличивается до 12%.
[0010] Нуклеозидная и нуклеотидная терапии энтекавиром и тенофовиром успешны в снижении вирусной нагрузки, но уровни сероконверсии HBeAg и потери HBsAg даже ниже, чем при использовании терапии IFNα. Также используются другие аналогичные методы лечения, включая ламивудин (3ТС), телбивудин (LdT) и адефовир, но для нуклеозидной / нуклеотидной терапии в целом появление резистентности ограничивает терапевтическую эффективность.
[0011] Недавние клинические исследования обнаружили корреляцию между сероконверсией и снижением HBeAg (Fried и др. (2008) Hepatology 47: 428) и снижением HBsAg (Moucari и др. (2009) Hepatology 49: 1151). Снижение уровней антигенов могло позволить иммунологический контроль инфекции ВГВ, поскольку считается, что высокие уровни антигенов вызывают иммунологическую толерантность. Современные методы нуклеозидной терапии ВГВ способны резко снизить уровни ВГВ в сыворотке, но мало влияют на уровни HBeAg и HBsAg. Антисмысловая терапия отличается от нуклеозидной терапии тем, что она может напрямую воздействовать на транскрипты антигенов и тем самым снижать уровни HBeAg и HBsAg в сыворотке. Но антисмысловая терапия стоит дорого и требует внутривенного введения.
[0012] Таким образом, в данной области техники существует потребность в открытии и разработке новых противовирусных методов лечения. В частности, существует потребность в новых методах лечения против ВГВ, способных повысить частоту сероконверсии HBeAg и HBsAg. Эти сывороточные маркеры указывают на иммунологический контроль инфекции ВГВ и приводят к улучшению прогноза, то есть предотвращению заболевания печени и прогрессированию цирроза, профилактике печеночной недостаточности, профилактике гепатоцеллюлярного рака (ГЦК), профилактике трансплантации, связанной с заболеванием печени, и предотвращение смерти.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0013] Вариантами осуществления настоящего изобретения являются соединения Формулы I:
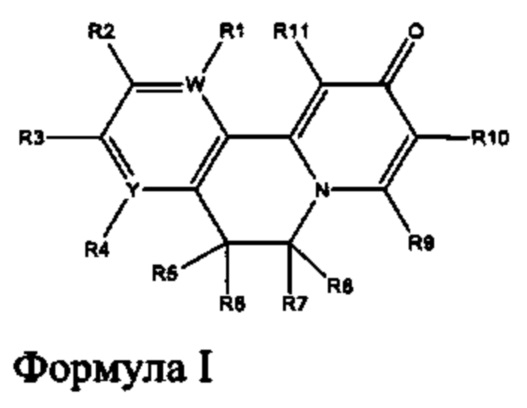
где
[0014] W и Y независимо являются С или N, при условии, что W и Y оба не являются С;
при этом
[0015] если W является С, то R1 является водородом, гидрокси, галогеном, циано, амино или замещенным амино, тио или замещенным тио, алкилом или замещенным алкилом, алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; алкенилом или замещенным алкенилом; от 3- до 8-членным гетероциклоалкилом или замещенным от 3- до 8-членным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, пирролидинилом, -СхН2х-фенилом, -О-CxH2x-фенилом или -(C1-6 алкил)N-CxH2x-фенилом, при этом х представляет собой 0, 1, 2, 3, 4, 5, 6; или -OR12; и
[0016] если Y представляет собой С, то R4 представляет собой водород, гидрокси, галоген, циано, амино или замещенный амино, тио или замещенный тио, алкил или замещенным алкил, алкокси или замещенным алкокси; циклоалкил или замещенный циклоалкил; алкенил или замещенный алкенил; от 3- до 8-членный гетероциклоалкил или замещенный от 3- до 8-членный гетероциклоалкил, арил или замещенный арил, гетероарил или замещенный гетероарил, пирролидинил, -CxH2x-фенил, -О-CxH2x-фенил, или -(C1-6 алкил)N- СхН2х-фенил, при этом х равно 0, 1, 2, 3,4, 5, 6; или -OR12;
при этом
[0017] если W представляет собой N, то R1 отсутствует; и
[0018] если Y представляет собой N, то R4 отсутствует;
[0019] R2 и R3 независимо являются группой, выбранной из водорода, гидрокси, галогена, циано, амино или замещенного амино, тио или замещенного тио, алкила или замещенного алкила, алкокси или замещенного алкокси; циклоалкила или замещенного циклоалкила; алкенила или замещенного алкенила; от 3- до 8-членного гетероциклоалкила или замещенного от 3- до 8-членного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила, пирролидинила, -СхН2х-фенила, О-CxH2x-фенила, или -(C1-6 алкил)N-СхН2х-фенила, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12; R5 и R6 независимо являются водородом, гидрокси, галогеном, циано, амино алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным арилом, -СхН2х-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[0020] R7 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[0021] или R5 и R6 вместе являются от 3- до 8-членным циклоалкиловым кольцом или от 3- до 8-членным гетероциклоалкильным кольцом, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', при этом указанное от 3- до 8-членный гетероциклоалкильное кольцо является необязательно замещенным R13, R13', R14 и/или R14';
[0022] или R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или гетероциклоалкильное кольцо, включающее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляет собой NR20 и указанные два или более гетероатомов являются группой, выбранной из N, NR22, О, S, SR22 и SR22R22';
[0023] или R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R17', R18 и/или R18', при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[0024] R9 представляет собой связь, водород, гидрокси, галоген, циано, амино, алкил или замещенный алкил, алкокси или замещенный алкокси, циклоалкил или замещенный циклоалкил, алкенил или замещенный алкенил, гетероциклоалкил или замещенный гетероциклоалкил, арил или замещенный арил, гетероарил или замещенный гетероарил, -CxH2x-фенил или -О-CxH2x-фенил, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[0025] R10 представляет собой заместитель, показанный в Таблице 2 или его таутомер;
[0026] или R9 представляет собой связь, и R9 и R10 вместе образуют оксабороловое кольцо;
[0027] R11 представляет собой водород, гидрокси, галоген, пиано, амино, алкил или замещенный алкил; алкенил или замещенный алкенил; алкокси или замещенный алкокси; циклоалкил или замещенный циклоалкил; гетероциклоалкил или замещенный гетероциклоалкил, арил, гетероарил, -CxH2x-фенил или -О-CxH2x-фенил, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[0028] R12 представляет собой водород; алкил или замещенный алкил, алкокси или замещенный алкокси, циклоалкил или замещенный циклоалкил, гетероциклоалкил или замещенный гетероциклоалкил, арил или замещенный арил, гетероарил или замещенный гетероарил;
[0029] R13, R13', R14 и R14' независимо являются водородом, гидрокси, галогеном, амино, аминоалкилом, циано, C1-6 алкилом, C1-6 алкокси, карбонилом, карбоксамидом, амидом; или R13 и R13' или R14 и R14' вместе образуют от 3- до 8-членный циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, С1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[0030] R15, R15', R16 и R16' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6 алкилом, или C1-6 алкокси; или R15 и R15' или R16 и R16' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[0031] R17, R17', R18 и R18' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6 алкилом, или C1-6 алкокси; или R17 и R18 или R17' и R18' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце является О, N, NR22, S, SR22 или SR22R22';
[0032] R19, R19' и R19" независимо являются водородом, C1-6алкилом, С3-8 циклоалкилом, С2-6 алкенилом, C1-6алкокси, фенилом, С1-6 алкилимидазолом, C1-6 алкилтриазолом, C1-6 алкилтетразолом, С1-6алкилтиазолом, C1-6алкилоксазолом, C1-6 алкилдиоксазолом; C1-6 алкилоксазолидоном; и
[0033] R20 и R21 независимо представляют собой водород, C1-6 алкил, С3-8 циклоалкил, С2-6алкенил, C1-6 алкокси, фенил, С1-6 алкилимидазол, C1-6алкилтриазол, C1-6 алкилтетразол, С1-6алкилтиазол, C1-6 алкилоксазол, С1-6алкилдиоксазол; C1-6 алкилоксазолидон, или R20 и R21 вместе с азотом, к которому они присоединены, образуют незамещенный пирролидинил, незамещенный пиперидинил, или незамещенный морфолинил; или образуют карбоксил-замещенный пирролидинил, карбоксил-замещенный пиперидинил или карбоксил-замещенный морфолинил; и
[0034] R22 и R22' независимо являются группой, выбранной из водорода, кислорода, C1-6 алкила или замещенного C1-6 алкила, C1-6 алкокси или замещенного C1-6 алкокси, С3-8 циклоалкила или замещенного С3-8 циклоалкила, С2-6 алкенила или замещенного С2-6 алкенила, арила или замещенного арила, включая замещенный или незамещенный C1-6 алкилимидазол, замещенный или незамещенный C1-6 алкилтриазол, C1-6 алкилтетразол, С1-6 алкилтиазол, замещенный или незамещенный C1-6 алкилоксазол, C1-6алкилдиоксазол; C1-6 алкилоксазолидон; -COR19, -COOR19', -CSOR19", -CONR20R21,
или его фармацевтически приемлемую соль.
[0035] Еще один вариант осуществления обеспечивает соединение Формулы IA или Формулы IB:
[0036] 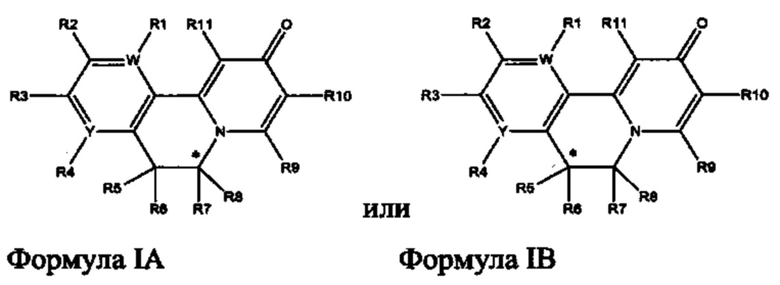
при этом
[0037] С* представляет собой стереоцентр при атоме углерода, который имеет конфигурацию, являющуюся (R) или (S);
[0038] W и Y независимо являются С или N, при условии, что W и Y оба не являются С;
[0039] при этом если W представляет собой С, то R1 является водородом, гидрокси, галогеном, циано, амино или замещенным амино, тио или замещенным тио, алкилом или замещенным алкилом, алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; алкенилом или замещенным алкенилом; от 3- до 8-членным гетероциклоалкилом или замещенным от 3- до 8-членным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, пирролидинилом, -CxH2x-фенилом, -О-CxH2x-фенилом, или -(C1-6 алкил)N-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12; и
[0040] если Y представляет собой С, то R4 является водородом, гидрокси, галогеном, циано, амино или замещенным амино, тио или замещенным тио, алкилом или замещенным алкилом, алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; алкенилом или замещенным алкенилом; от 3- до 8-членным гетероциклоалкилом или замещенным от 3- до 8-членным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, пирролидинилом, -CxH2x-фенилом, -О-CxH2x-фенилом, или -(C1-6 алкил)N-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12;
при этом
[0041] если W представляет собой N, то R1 отсутствует; и
[0042] если Y представляет собой N, то R4 отсутствует;
[0043] R2 и R3 независимо являются группой, выбранной из водорода, гидрокси, галогена, циано, амино или замещенного амино, тио или замещенного тио, алкила или замещенного алкила, алкокси или замещенного алкокси; циклоалкила или замещенного циклоалкила; алкенила или замещенного алкенила; от 3- до 8-членного гетероциклоалкила или замещенного от 3- до 8-членного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила, пирролидинила, -CxH2x-фенила, -О-CxH2x-фенила, или -(C1-6 алкил)N-СхН2х-фенила, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12;
[0044] R5 и R6 независимо являются водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным арилом, -CxH2x-фенилом или -О-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[0045] R7 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом, -СхН2х-фенилом или -О-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[0046] или R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, при этом указанным гетероатомом в указанном гетероциклоалкильном кольце являются О, N, NR22, S, SR22 или SR22R22', при этом указанное от 3- до 8-членное гетероциклоалкильное кольцо является необязательно замещенным R13, R13', R14 и/или R14';
[0047] или R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанным одним гетероатомом в указанном гетероалкильном кольце является NR20, а указанные два или более гетероатомов являются группой, выбранной из N, NR22, О, S, SR22 и SR22R22';
[0048] или R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R17', R18 и/или R18', при этом указанным гетероатомом в указанном гетероциклоалкильном кольце является О, N, NR22, S, SR22 или SR22R22';
[0049] R9 представляет собой связь, водород, гидрокси, галоген, циано, амино, алкил или замещенный алкил, алкокси или замещенный алкокси, циклоалкил или замещенный циклоалкил, алкенил или замещенный алкенил, гетероциклоалкил или замещенный гетероциклоалкил, арил или замещенный арил, гетероарил или замещенный гетероарил, -CxH2x-фенил или -О-CxH2x-фенил, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[0050] R10 представляет собой заместитель, показанный в Таблице 2, или его таутомер;
[0051] или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо;
[0052] R11 является водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом; алкенилом или замещенным алкенилом; алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; гетероциклоалкилом или замещенным гетероциклоалкилом, арилом, гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[0053] R12 является водородом; алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, гетероциклоалкилом или замещенным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом;
[0054] R13, R13', R14 и R14' независимо являются водородом, гидрокси, галогеном, амино, аминоалкилом, циано, С1-6алкилом, C1-6алкокси, карбонилом, карбоксамидом, амидом; или R13 и R13' или R14 и R14' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6алкокси, при этом указанным гетероатомом в указанном гетероциклоалкильном кольце является О, N, NR22, S, SR22 или SR22R22';
[0055] R15, R15', R16 и R16' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6 алкилом, или C1-6 алкокси; или R15 и R15' или R16 и R16' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[0056] R17, R17', R18 и R18' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6 алкилом, или C1-6 алкокси; или R17 и R18 или R17' и R18' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[0057] R19, R19' и R19" независимо являются водородом, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом, C1-6 алкокси, фенилом, C1-6 алкилимидазолом, C1-6 алкилтриазолом, C1-6 алкилтетразолом, C1-6 алкилтиазолом, C1-6 алкилоксазолом, C1-6 алкилдиоксазолом; C1-6алкилоксазолидоном; и
[0058] R20 и R21 независимо представляют собой водород, C1-6 алкил, С3-8 циклоалкил, С2-6 алкенил, C1-6 алкокси, фенил, C1-6 алкилимидазол, C1-6 алкилтриазол, C1-6 алкилтетразол, C1-6 алкилтиазол, C1-6 алкилоксазол, C1-6 алкилдиоксазол; C1-6 алкилоксазолидон, или R20 и R21 вместе с азотом к которому они присоединены, образуют незамещенный пирролидинил, незамещенный пиперидинил, или незамещенный морфолинил; или образуют карбоксил-замещенный пирролидинил, карбоксил-замещенный пиперидинил или карбоксил-замещенный морфолинил; и
[0059] R22 и R22' независимо являются группой, выбранной из водорода, кислорода, C1-6 алкила или замещенного C1-6 алкила, C1-6 алкокси или замещенного C1-6 алкокси, С3-8 циклоалкила или замещенного С3-8 циклоалкила, С2-6 алкенила или замещенного С2-6 алкенила, арила или замещенного арила, включая замещенный или незамещенный C1-6 алкилимидазол, замещенный или незамещенный C1-6 алкилтриазол, C1-6 алкилтетразол, С1-6 алкилтиазол, замещенный или незамещенный C1-6 алкилоксазол, C1-6 алкилдиоксазол; C1-6 алкилоксазолидон; -COR19, -COOR19', CSOR19", -CONR20R21,
или его фармацевтически приемлемую соль.
[0060] В другом конкретном варианте осуществления настоящего изобретения обеспечиваются соединения Формулы I, Формулы IA или Формулы IB, приведенных в настоящем описании, включая их соли и пролекарства,
[0061] при этом
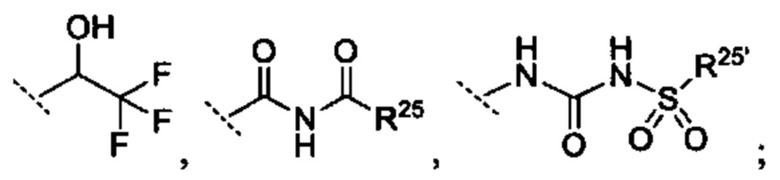
R10 выбрано из группы -CO2H, -В(ОН)2, -NHSO2R25', -NCO2R25, 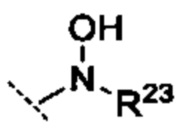
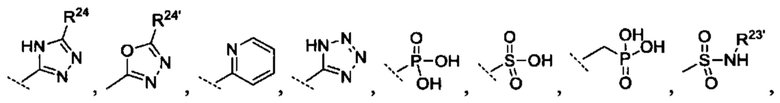
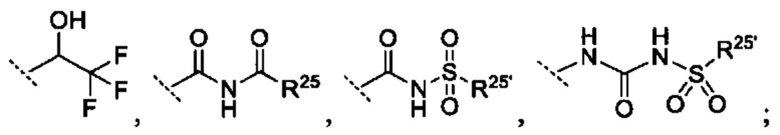
при этом
[0062] R23 и R23' независимо являются группой, выбранной из Н, алкила или замещенного алкила, циклоалкила или замещенного циклоалкила, алкенила или замещенного алкенила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила
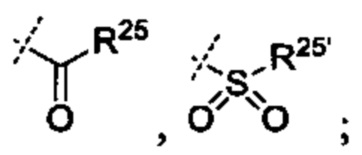
[0063] R24 и R24' независимо являются группой, выбранной из Н, гидроксила, амино или замещенного амино, алкила или замещенного алкила, циклоалкила или замещенного циклоалкила, алкенила или замещенного алкенила, тиола или тиоалкила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила; и
[0064] R25 и R25' независимо являются группой, выбранной из Н, ОН, алкила или замещенного алкила, циклоалкила или замещенного циклоалкила, алкенила или замещенного алкенила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила и гетероарила или замещенного гетероарила; или их фармацевтически приемлемой соли.
[0065] В другом конкретном варианте осуществления настоящего изобретения обеспечиваются соединения Формулы I, Формулы IA или Формулы IB, включая их соли и пролекарства, при этом
[0066] R1, R2, R3, R4, R5, R6, R7, R9 и R11 представляют собой группы, как они определены в настоящем описании;
[0067] R8 представляет собой изопропил; и
R10 выбрано из группы -CO2H, -В(ОН)2, -NHSO2R25', -NCO2R25, 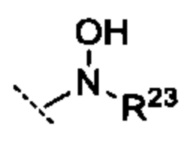
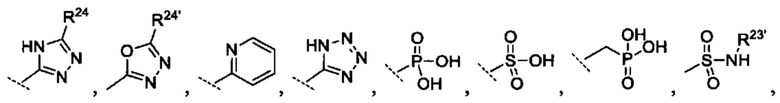
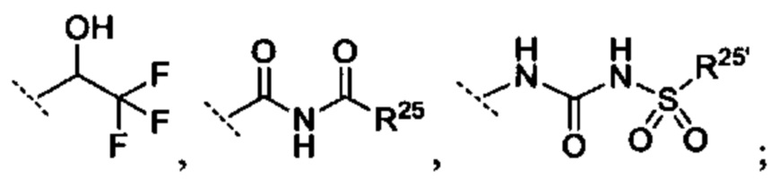
при этом
[0068] R23 и R23' независимо являются группой, выбранной из Н, алкила или замещенного алкила, циклоалкила или замещенного циклоалкила, алкенила или замещенного алкенила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила,
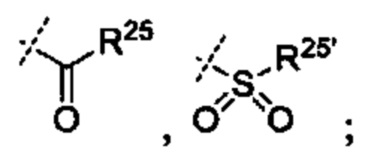
[0069] R24 и R24' независимо являются группой, выбранной из Н, гидроксила, амино или замещенного амино, алкила или замещенного алкила, циклоалкила или замещенного циклоалкила, алкенила или замещенного алкенила, тиола или тиоалкила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила; и
[0070] R25 и R25' независимо являются группой, выбранной из Н, ОН, алкила или замещенного алкила, циклоалкила или замещенного циклоалкила, алкенила или замещенного алкенила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила и гетероарила или замещенного гетероарила; или их фармацевтически приемлемой соли.
[0071] В другом варианте осуществления обеспечивают соединение Формулы I, Формулы IA или Формулы IB, включая их соли и пролекарства, при этом
[0072] R1, R2, R3, R4, R9 и R11, как определены в настоящем описании;
[0073] R5, R6 и R7 представляют собой H;
[0074] R8 представляет собой изопропил;
R10 выбрано из группы -CO2H, -В(ОН)2, -NHSO2R25', -NCO2R25, 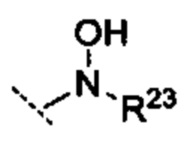
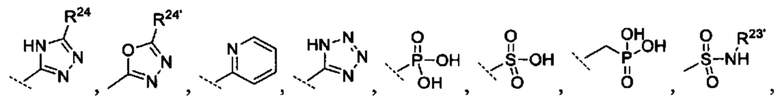
при этом
[0075] R23 и R23' независимо являются группой, выбранной из Н, алкила или замещенного алкила, цикло алкила или замещенного циклоалкила, алкенила или замещенного алкенила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила,
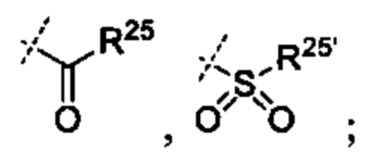
[0076] R24 и R24' независимо являются группой, выбранной из Н, гидроксила, амино или замещенного амино, алкила или замещенного алкила, циклоалкила или замещенного циклоалкила, алкенила или замещенного алкенила, тиола или тиоалкила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила; и
[0077] R25 и R25' независимо являются группой, выбранной из Н, ОН, алкила или замещенного алкила, циклоалкила или замещенного циклоалкила, алкенила или замещенного алкенила, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила и гетероарила или замещенного гетероарила; или их фармацевтически приемлемой соли.
[0078] В конкретных вариантах осуществления обеспечивают способ лечения инфекции гепатита В или совместной инфекции гепатита В и гепатита D, в частности способ лечения инфекции гепатита В или совместной инфекции гепатита В и гепатита D у человека, включающий введение субъекту, нуждающемуся в таком лечении, соединения Формулы I, IA или IB, приведенной в настоящем описании.
[0079] В еще одном варианте осуществления настоящее изобретение обеспечивает способ лечения инфекции гепатита В или совместной инфекции гепатита В и гепатита D, в частности способ лечения инфекции гепатита В или совместной инфекции гепатита В и гепатита D у человека, включающий введение субъекту, нуждающемуся в таком лечении, первого фармацевтически приемлемого агента, содержащего соединение Формулы I, Формулы IA или Формулы IB, приведенной в настоящем описании, в комбинации со вторым фармацевтически приемлемым агентом, который стимулирует иммунную функцию и третьим фармацевтически приемлемым агентом, содержащим антивирусное соединение.
[0080] В еще одном варианте осуществления введение соединения Формулы I, IA или IB, приведенной в настоящем описании, ингибирует высвобождение поверхностного антигена гепатита В (HBsAg), белка корового антигена НВ (HBcAg), и/или пре-корового белка гепатита В, известного как е-антигена антигена ВГВ (HBeAg), из инфицированных гепатоцитов.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
[0081] Варианты осуществления настоящего изобретения включают соединения, которые ингибируют уровни антигенов НВе и/или HBs у субъекта, инфицированного вирусом гепатита В, и поэтому пригодного для лечения инфекций вируса гепатита В у человека, и заболеваний и симптомов, ассоциированных с таким вирусными инфекциями. Признаки настоящего изобретения будут более подробно разъяснены со ссылкой на следующее подробное описание со ссылкой на приложенные Таблицы, в которых:
[0082] в Таблице 1 приведен список соединений Формулы I, приведенной в настоящем описании,
[0083] в Таблице 2 приведен список заместителей R10 для соединений Формулы I, приведенной в настоящем описании.
[0084] в Таблице 3 приведены результаты исследования ELISA клеток HepAD38 HBsAg и исследования цитотоксичности, показывающие значения ЕС50, измеренные для исследованных соединений в отношении антигенов HBs (HBsAg).
ПОДРОБНОЕ ОПИСАНИЕ КОНКРЕТНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0085] В этой заявке делаются ссылки на различные варианты осуществления, относящиеся к соединениям, композициям и способам. Различные описанные варианты осуществления предназначены для раскрытия множества иллюстративных примеров и не должны рассматриваться как описания альтернативных видов. Скорее следует отметить, что описания различных вариантов осуществления, представленные в данном документе, могут иметь перекрывающийся объем. Обсуждаемые здесь варианты осуществления являются исключительно иллюстративными и не предназначены для ограничения объема настоящего изобретения.
[0086] Следует понимать, что терминология, используемая в данном документе, предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения. В этом описании и в последующей формуле изобретения будут сделаны ссылки на ряд терминов, которые должны иметь следующие значения.
[0087] В данном контексте, если не указано иное, "алкил" относится к одновалентной насыщенной алифатической углеводородной группе, имеющей от 1 до 14 атомов углерода и, в некоторых вариантах реализации, от 1 до 6 атомов углерода. Термин "алкил" включает в себя в качестве примера линейные и разветвленные углеводородные группы, такие как метил (CH3-), этил-(СН3СН2-), n-пропил (СН3СН2СН2-), изопропил ((СН3)2СН-), n-бутил (СН3СН2СН2СН2-), изобутил ((СН3)2СНСН2-), sec-бутил ((СН3)(СН3СН2)СН-), t-бутил ((СН3)3С-), n-пентил (СН3СН2СН2СН2СН2-), и неопентил ((СН3)3ССН2-). Алкильные группы также могут быть замещены, например, одним или более алкилом, циклоалкилом, гетероциклоалкилом, алкокси, амино, аминоалкилом, тиолом, тиоалкилом, арилом, гетероарилом, галогенными или галогеналкильными заместителями.
[0088] "Алкокси" или "алкоксил" относится к -О-алкильной группе, при этом алкил представляет собой группу, определенную в настоящем описании. Алкокси включает в качестве примера метокси, этокси, n-пропокси, изопропокси, n-бутокси, t-бутокси, sec-бутокси, n-пентокси, морфолинилпропокси, пиперидинилэтокси. Алкоксильные группы также могут быть замещены, например, одним или более алкилом, циклоалкилом, гетероциклоалкилом, алкокси, амино, аминоалкилом, тиолом, тиоалкилом, арилом, гетероарилом, галогенными или галогеналкильными заместителями.
[0089] "Амино" относится к группе -NRaRb, где Ra и Rb независимо являются группой, выбранной из водорода, гидрокси, алкила или замещенного алкила, алкенила или замещенного алкенила, арила или замещенного арила, циклоалкила или замещенного циклоалкила, гетероциклоалкила или замещенного гетероциклоалкила, гетероарила или замещенного гетероарила, и при этом необязательно Ra и Rb, соединенные с азотом, образуют гетероциклическую группу. Когда Ra представляет собой водород, a Rb представляет собой алкил, указанная аминогруппа иногда относится к алкиламино или аминоалкилу. Когда Ra и Rb являются алкилами, указанная аминогруппа иногда относится к даалкиламино. Когда идет отсылка к монозамещенному амино, это означает, что либо Ra, либо Rb является водородом, но не оба одновременно. Когда идет отсылка к дизамещенному амино, это означает, что ни Ra, ни R6 не являются водородом.
[0090] "Арил" относится к ароматической группе, образованной из от 5 до 14 атомов углерода без гетероатомов в кольце и имеющей одно кольцо (например, фенил) или несколько конденсированных колец (например, нафтил или антрил). Для систем с несколькими кольцами, включая конденсированные, мостиковые и спирокольца, содержащих ароматические и неароматические кольца, которые не содержат гетероатомы в кольце, термин "арил" или "Ar" применяется, когда местом присоединения является ароматический атом углерода (например, 5,6,7,8 тетрагидронафтален-2-ил представляет собой арильную группу, в которой местом ее присоединения является положение 2 в ароматическом фенильном кольце). Арильные группы также могут быть замещены, например, одним или более алкилом, циклоалкилом, гетероциклоалкилом, алкокси, амино, аминоалкилом, тиолом, тиоалкилом, арилом, гетероарилом, галогенными или галогеналкильными заместителями.
[0091] "Циклоалкил" относится к насыщенной или частично насыщенной циклической группе, образованной из от 3 до 14 атомов углерода, не содержащей кольцевые гетероатомы и имеющей одно кольцо или несколько колец, включая конденсированные, мостиковые и спиро кольцевые системы. Для систем с множеством колец, имеющих ароматические и неароматические кольца, которые не содержат гетероатомы в кольце, термин "циклоалкил" применяют когда местом присоединения является неароматический атом углерода (например 5,6,7,8-тетрагидронафтален-5-ил). Термин "циклоалкил" включает циклоалкенильные группы, такие как циклогексенил. Примеры циклоалкильных групп включают, например, адамантил, циклопропил, циклобутил, циклогексил, циклопентил, циклооктил, циклопентенил и циклогексенил. Примерами циклоалкильных групп, которые включают множественные бициклоалкильные кольцевые системы, являются бициклогексил, бициклопентил, бициклоостил и подобные им. Циклоалкильные группы также могут быть замещены, например, одним или более алкилом, циклоалкилом, гетероциклоалкилом, алкокси, амино, аминоалкилом, тиолом, тиоалкилом, арилом, гетероарилом, галогенными или галогеналкильными заместителями.
[0092] "Гало" или "галоген" относится к фтору, хлору, брому и йоду.
[0093] "Галоалкил" относится к замещенным алкильным группам с от 1 до 9 (например, когда указанная алкильная группа имеет 4 атома углерода, такая как t-бутильная группа, полностью замещенная галогеном) или в некоторых вариантах осуществления от 1 до 3 галогенных групп (например, трифторметил).
[0094] "Гидрокси" или "гидроксил" относится к группе -ОН.
[0095] "Гетероарил" относится к ароматической группе, образованной из от 1 до 14 атомов углерода и от 1 до 6 гетероатомов, выбранных из кислорода, азота, серы, фосфора, кремния и бора, и включает системы с одним кольцом (например, имидазолил) и несколькими кольцами (например, бензимидазол-2-ил и бензимидазол-6-ил). Для систем с множеством колец, включающих конденсированные, мостиковые, и спиро кольцевые системы, содержащих ароматические и неароматические кольца, термин "гетероарил" применяется, если присутствует по меньшей мере один кольцевой гетероатом и местом присоединения является атом ароматического кольца (например, 1,2,3,4-тетрагидрохинолин-6-ил и 5,6,7,8-тетрагидрохинолин-3-ил). В некоторых вариантах осуществления, указанные кольцевые атомы азота и/или серы указанной гетероарильной группы необязательно окислены с образованием N-оксида (N→O), сульфинила или сульфонила. Более конкретно термин гетероарилом включает, но не ограничиваются ими, пиридин, фуранил, тиенил, тиазолил, изотиазолил, триазолил, имидазолил, имидазолинил, изоксазолил, пирролил, пиразолил, пиридазинил, пиримидинил, пуринил, фталазил, нафтил, нафтилпиридил, оксазолил, хинолил, бензофуранил, тетрагидробензофуранил, изобензофуранил, бензотиазолил, бензоизотиазолил, бензотриазолил, индолил, изоиндолил, индолизинил, дигидроиндолил, индазолил, индолинил, бензоксазолил, хинолил, изохинолил, хинолизил, хианазолил, хиноксалил, тетрагидрохинолинил, изохинолил, хиназолинонил, бензимидазолил, бензизоксазолил, бензотиенил, бензопиридазинил, птеридинил, карбазолил, карболинил, фенантридинил, акридинил, фенантролинил, феназинил, феноксазинил, фенотиазинил и фталимидил, но не ограничиваются ими. Гетероарильные группы также могут быть замещены, например, одним или более алкилом, циклоалкилом, гетероциклоалкилом, алкокси, амино, аминоалкилом, тиолом, тиоалкилом, арилом, гетероарилом, галогенными или галогеналкильными заместителями.
[0096] "Гетероциклический" или "гетероцикл" или "гетероциклоалкил" или "гетероциклил" относится к насыщенной или частично насыщенной циклической группе, содержащей от 1 до 14 атомов углерода и от 1 до 6 гетероатомов, выбранных из азота, серы, фосфора или кислорода, и имеющей одно кольцо и систему с множеством колец, включая конденсированные, мостиковые, и спиро-кольцевые системы. Для систем с множеством колец, имеющих ароматические и/или неароматические кольца, термины "гетероциклический, "гетероцикл", "гетероциклоалкил" или "гетероциклил" применяют, когда имеется по меньшей один гетероатом в кольце, а местом присоединения является атом неароматического кольца (например, 1,2,3,4-тетрагидрохинолин-3-ил, 5,6,7,8-тетрагидрохинолин-6-ил, и декагидрохинолин-6-ил). В одном варианте осуществления атомы азота, фосфора и/или серы указанной гетероциклической группы необязательно окислены с получением N-оксида, фосфинан оксида, сульфинильного, сульфонильного остатков. Более конкретно указанный гетероциклил включает тетрагидропиранил, пиперидинил, пиперазинил, 3-пирролидинил, 2-пирролидон-1-ил, морфолинил, и пирролидинил, но не ограничиваются ими. Префикс, указывающий количество атомов углерода (например, С3-С10) относится к общему количеству атомов углерода в части указанной гетероциклильной группы, не включающему количество гетероатомов. Гетероциклил или алкильные группы гетероцикла также могут быть замещены, например, одним или более алкилом, циклоалкилом, гетероциклоалкилом, алкокси, амино, аминоалкилом, тиолом, тиоалкилом, арилом, гетероарилом, галогенными или галогеналкильными заместителями.
[0097] Примеры гетероциклических и гетероарильных групп включают азетидин, пиррол, имидазол, пиразол, пиридин, пиразин, пиримидин, пиридазин, пиридон, индолизин, изоиндол, индол, дигидроиндол, индазол, пурин, хинолизинол, хинолин, фталазин, нафтилпиридин, хиноксалин, хиназолин, циннолин, птеридин, карбазол, карболин, фенантридин, акридин, фенантролин, изотиазол, феназин, изоксазол, феноксазин, фенотиазин, имидазолиперолин, имидазолидин, имидазолидин, нафразолин, фталимид, хинолин, 1,2,3,4 тетрагидроизохинолин, 4,5,6,7-тетрагидробензо[b]тиофен, тиазол, циклопентатиазол, тиазолидин, тиофен, бензо[b]тиофен, морфолин, тиоморфолин (также называемый тиаморфолином), пиперидин, пирролидин, и тетрагидрофуранил, но не ограничиваются ими.
[0098] "Конденсированные гетероциклические" или "конденсированный гетероциклил" относится к от 3 до 10-членному циклическому заместителю, образованному замещением двух атомов водорода при различных атомах углерода в циклоалкильной кольцевой структуре, как в следующей циклопентатиазольной структуре:

Конденсированные гетероциклильные группы также могут быть замещены, например, одним или более алкилом, циклоалкилом, гетероциклоалкилом, алкокси, амино, аминоалкилом, тиолом, тиоалкилом, арилом, гетероарилом, галогенными или галогеналкильными заместителями.
[0099] "Конденсированный арил" и "конденсированный гетероарил" относится к от 5 до 6-членной арильной структуре или гетероарильной структуре, конденсированной с от 5- до 6-членным арилом, гетероарилом или циклоалкильным кольцом с различными атомами углерода в указанной арильной структуре или указанной гетероарильной структуре, которая может быть замещена при одном из атомов углерода в указанном конденсированном ариле или конденсированном гетероариле и соединена с кором молекулы при различных атомах углерода, как в следующих структурах циклопентилтиазола, хинолина или нафталина, приведенных в качестве примера:
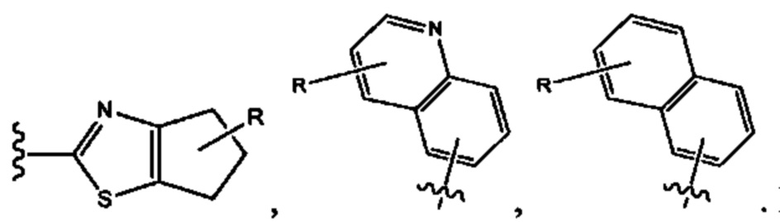
Конденсированные арильные и конденсированные гетероарильные группы также могут быть замещены, например, одним или более алкилом, циклоалкилом, гетероциклоалкилом, алкокси, амино, аминоалкилом, тиолом, тиоалкилом, арилом, гетероарилом, галогенными или галогеналкильными заместителями.
[00100] Термины "соединение", "соединения", "химическое соединение" и "химические соединения", используемые в настоящем описании относятся к соединению, охарактеризованному общей Формулой, приведенной в настоящем описании, любым подвидам указанной общей Формулы, и любым формам соединений, включенных в указанную Формулу и подвиды указанной Формулы, включая рацематы, стереоизомеры и таутомеры указанного соединения или соединений.
[00101] Термин "гетероатом" означает азот, кислород или серу и включает любую окисленную форму азота, такую как N(O) {N+-О-}, и серы, такую как S(O) и S(O)2, и четвертичную форму любого основного азота.
[00102] "Оксазол" и "оксазолил" относится к 5-членному гетероциклическому кольцу, содержащему один азот и один кислород в качестве гетероатомов, и также содержит три атома углерода и может замещать один из трех атомов углерода и может быть связан с другой молекулой при другом из трех атомов углерода, как проиллюстрировано любой из следующих структур, где оксазолидиноновые группы, показанные в настоящем описании, связаны с родительской молекулой, что обозначено волнистой линией в связи с родительской молекулой:
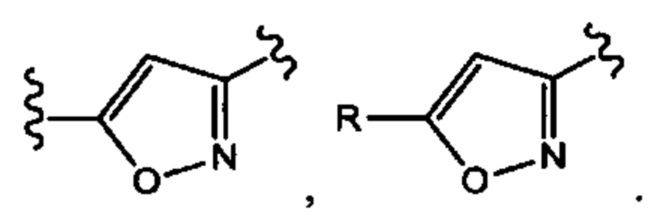
[00103] "Оксопирролидин" и "оксопирролидинил" относится к 5-членному гетероциклическому кольцу, содержащему азот и 4 атома углерода, которое замещает один из атомов углерода в гетероциклическом кольце через карбонил и может быть связан с другим заместителем у другого атома углерода в гетероциклическом кольце, как в структуре, приведенной ниже в качестве примера:
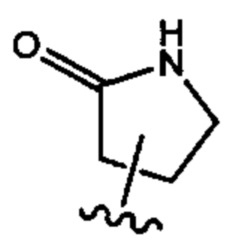
[00104] "Пиридин" и "пиридинил" относятся к 6-членным гетероарильным кольцам, содержащим один азот и 5 атомов углерода, которые также могут быть замещены у одного или нескольких атомов углерода в гетероарильном кольце, и могут быть связаны с другим заместителем у другого углерода в гетероарильном кольце, как в структуре, приведенной ниже в качестве примера:
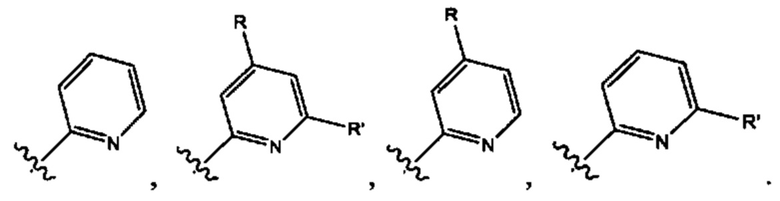
[00105] "Тиазол" и "тиазолил" относятся к 5-членным гетероарилам, содержащим один атом серы и один атом азота в гетероарильном кольце и 3 атома углерода в гетероарильном кольце, которые также могут замещать один или несколько атомов углерода в гетероарильном кольце, и может быть связан с другим заместителем у другого атома углерода в гетероарильном кольце, как в структуре, приведенной ниже в качестве примера:
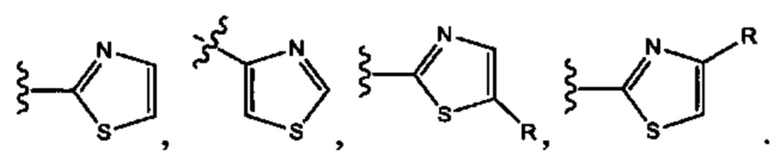
[00106] "Пиримидин" и "пиримидинил" относится к 6-членному гетероарильному кольцу, содержащему два азота в гетероарильном кольце и 4 атома углерода в гетероарильном кольце, которое может быть замещено по одному или нескольким атомам углерода в гетероарильном кольце, и может быть соединено с другим заместителем при другом атоме углерода в гетероарильном кольце, как в структуре, приведенной ниже в качестве примера:
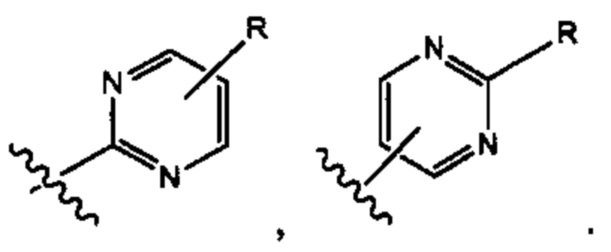
[00107] "Рацематы" относятся к смеси энантиомеров. В одном из вариантов осуществления настоящего изобретения соединения Формулы I или его фармацевтически приемлемую соль энантиомерно обогащены одним энантиомером, где все указанные хиральные атомы углерода находятся в одной конфигурации. В общем, ссылка на энантиомерно обогащенное соединение или соль означает, что указанный энантиомер будет составлять более 50% по массе от общей массы всех энантиомеров соединения или соли.
[00108] "Сольват" или "сольваты" соединения относятся к тем соединениям, как определено выше, которые связаны со стехиометрическим или нестехиометрическим количеством растворителя. Сольваты соединения включают сольваты всех форм соединения. В некоторых вариантах осуществления растворители являются летучими, нетоксичными и/или пригодными для введения человеку в следовых количествах. Подходящие сольваты включают воду.
[00109] "Стереоизомер" или "стереоизомеры" относятся к соединениям, которые различаются хиральностью одного или нескольких стереоцентров. Стереоизомеры включают энантиомеры и диастереомеры.
[00110] "Таутомер" относится к альтернативным формам соединения, которые различаются положением протона, таким как енол-кето и имин-енамин таутомеры, или таутомерные формы гетероарильных групп, содержащие кольцевой атом, присоединенный как к кольцевому фрагменту -NH-, так и кольцевому фрагменту =N-, например пиразолы, имидазолы, бензимидазолы, триазолы и тетразолы.
[00111] "Тио" или "тиол" относится к группе -SR, где R выбрано из группы водорода, алкила, алкенила, арила, циклоалкила, гетероциклоалкила, гетероарила, гетероцикла. Когда R представляет собой Н, указанная тиогруппа иногда относится к тиольной группе, а когда R представляет собой алкил, указанная тиогруппа иногда относится в настоящем описании к тиоалкильной группе или алкилтиогруппе. Указанный атом серы также может быть связан с другим атомом углерода или атомом в той же молекуле с образованием гетероциклической группы.
[00112] "Фармацевтически приемлемая соль" относится к фармацевтически приемлемым солям, полученным из множества органических и неорганических противоионов, хорошо известных в данной области, и включает, только в качестве примера, натрий, калий, кальций, магний, аммоний и тетраалкиламмоний, и когда молекула содержит основную функциональную группу, соли органических или неорганических кислот, такие как гидрохлорид, гидробромид, тартрат, мезилат, ацетат, малеат и оксалат. Подходящие соли включают соли, описанные в P. Heinrich Stahl, Camille G. Wermuth (Eds.), Handbook of Pharmaceutical Salts Properties, Selection, and Use; 2002.
[00113] "Пациент" или "субъект" относится к млекопитающим и включает людей и млекопитающих, не являющихся людьми.
[00114] "Лечение" заболевания у пациента относится к 1) предотвращению возникновения заболевания у пациента, который предрасположен или еще не проявляет симптомов заболевания; 2) подавлению заболевания или остановке его развития; или 3) облегчению или регрессу заболевания.
[00115] Если пунктирные линии встречаются рядом с одинарными связями, обозначенными сплошными линиями, то пунктирная линия представляет необязательную двойную связь в этом положении. Аналогичным образом, везде, где в кольцевых структурах появляются пунктирные кружки, обозначенные сплошными линиями или сплошными кружками, пунктирные кружки представляют от одной до трех необязательных двойных связей, расположенных в соответствии с их надлежащей валентностью, с учетом того, есть ли в кольце какие-либо необязательные замещения вокруг кольца, известные специалисту в данной области. Например, пунктирная линия в приведенной ниже структуре может указывать либо на двойную связь в этом положении, либо на одинарную связь в этом положении:
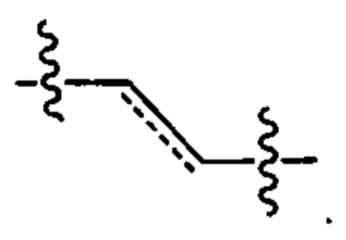
[00116] Точно так же кольцо А, приведенном ниже, может быть циклогексильным кольцом без каких-либо двойных связей или это также может быть фенильным кольцом, имеющим три двойные связи, расположенные в любом положении, которое все еще отражает правильную валентность фенилового кольца. Аналогично, в кольце В, приведенном ниже, любой из X1-Х5 может быть группой, выбранной из: С, СН, или СН2, N, или NH, и пунктирный кружок означает, что кольцо В может быть циклогексильным или фениловым кольцом или N-содержащим гетероциклом без двойных связей или N-содержащим гетероарильным кольцом с одной-тремя двойными связями, расположенными в любом положении, которое все еще отражает правильную валентность:
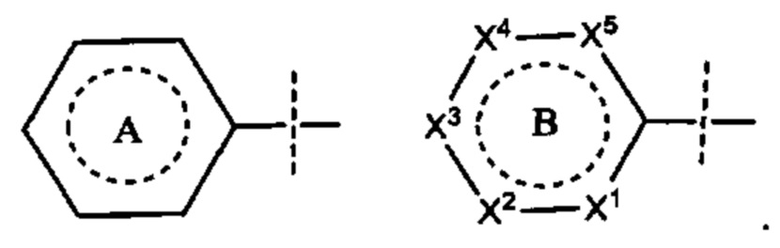
[00117] Если показаны конкретные соединения или общие Формулы, которые имеют ароматические кольца, такие как кольца с арилом или гетероарилом, тогда специалисту в данной области будет понятно, что конкретное ароматическое расположение любых двойных связей представляет собой смесь эквивалентных положений даже если они нарисованы в разных местах от соединения к соединению или от Формулы к Формуле. Например, в двух пиридиновых кольцах (А и В), приведенных ниже, двойные связи нарисованы в разных местах, однако, как известно, они имеют одинаковую структуру и представляют собой одно и то же соединение:
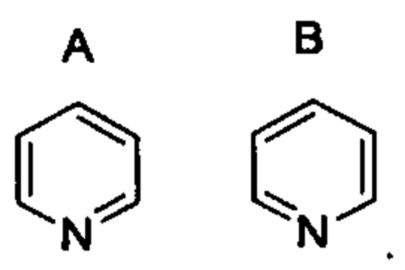
[00118] Если не указано иное, номенклатура заместителей, которые явно не определены в данном документе, достигаются путем обозначения концевой части функциональности, за которой следуют смежные функциональные группы в направлении точки присоединения. Например, заместитель "арилалкилоксикарбонил" относится к группе (арил)(алкил)ОС(O). В терминах, таких как "-C(Rx)2", следует понимать, что две группы Rx могут быть одинаковыми или они могут быть разными, если Rx определяется как имеющий более одной возможной идентичности. Кроме того, некоторые заместители обозначены как -RxRy, где "-" указывает на связь, примыкающую к исходной молекуле, а Ry представляет собой терминальную часть функциональности. Точно так же понятно, что приведенные выше определения не предназначены для включения недопустимых схем замещения (например, замещения 5 фторгруппами). Такие недопустимые схемы замещения хорошо известны специалисту в данной области.
[00119] В соответствии с одним вариантом осуществления настоящего изобретения, обеспечиваются соединения Формулы I или их соли или пролекарства,
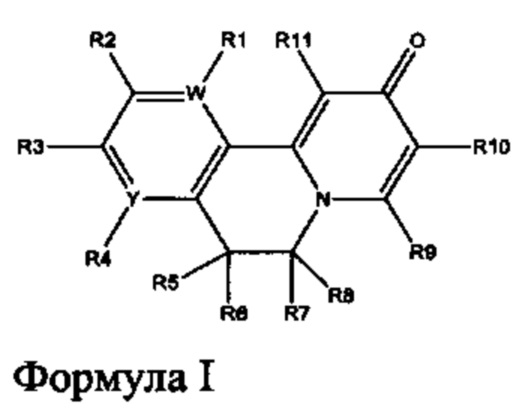
при этом
[00120] W и Y независимо являются С или N, при условии, что W и Y оба не являются С;
при этом
[00121] если W представляет собой С, то R1 представляет собой водород, гидрокси, галоген, циано, амино или замещенный амино, тио или замещенный тио, алкил или замещенный алкил, алкокси или замещенный алкокси; циклоалкил или замещенный циклоалкил; алкенил или замещенный алкенил; от 3- до 8-членный гетероциклоалкил или замещенный от 3- до 8-членный гетероциклоалкил, арил или замещенный арил, гетероарил или замещенный гетероарил, пирролидинил, -CxH2x-фенил, -О-CxH2x-фенил, или -(C1-6 алкил)N-СхН2х-фенил, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12; и
[00122] если Y представляет собой С, то R4 является водородом, гидрокси, галогеном, циано, амино или замещенным амино, тио или замещенным тио, алкилом или замещенным алкилом, алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; алкенилом или замещенным алкенилом; от 3- до 8-членным гетероциклоалкилом или замещенным от 3- до 8-членным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, пирролидинилом, -CxH2x-фенилом, -О-CxH2x-фенилом, или -(C1-6 алкил)N-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12;
при этом
[00123] если W представляет собой N, то R1 отсутствует; и
[00124] если Y представляет собой N, то R4 отсутствует;
[00125] R2 и R3 независимо являются группой, выбранной из водорода, гидрокси, галогена, циано, амино или замещенного амино, тио или замещенного тио, алкила или замещенного алкилом, алкокси или замещенного алкокси; циклоалкилом или замещенного циклоалкилом; алкенилом или замещенным алкенилом; от 3- до 8-членным гетероциклоалкилом или замещенным от 3- до 8-членным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, пирролидинилом, -CxH2x-фенилом, -О-CxH2x-фенилом, или -(C1-6алкилом)N-CxH2x-фенилом, при этом х равно 0,1, 2, 3,4, 5, 6; или -OR12;
[00126] R5 и R6 независимо являются водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00127] R7 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x- фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00128] или R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', при этом указанное от 3- до 8-членное гетероциклоалкильное кольцо необязательно замещено R13, R13', R14 и/или R14';
[00129] или R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляет собой NR20, а указанные два или более гетероатомов являются группой, выбранной из N, NR22,O, S, SR22 и SR22R22';
[00130] или R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R17', R18 и/или R18', при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00131] R9 представляет собой связь, водород, гидрокси, галоген, циано, амино, алкил или замещенный алкил, алкокси или замещенный алкокси, циклоалкил или замещенный циклоалкил, алкенил или замещенный алкенил, гетероциклоалкил или замещенный гетероциклоалкил, арил или замещенный арил, гетероарил или замещенный гетероарил, -CxH2x-фенил или -О-CxH2x-фенил, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00132] R10 представляет собой заместитель, показанный в Таблице 2, или его таутомер;
[00133] или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо;
[00134] R11 является водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом; алкенилом или замещенным алкенилом; алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; гетероциклоалкилом или замещенным гетероциклоалкилом, арилом, гетероарилом, -СхН2х-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00135] R12 является водородом; алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, гетероциклоалкилом или замещенным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом;
[00136] R13, R13', R14 и R14' независимо являются водородом, гидрокси, галогеном, амино, аминоалкилом, циано, C1-6 алкилом, C1-6 алкокси, карбонилом, карбоксамидом, амидом; или R13 и R13' или R14 и R14' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00137] R15, R15', R16 и R16' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6 алкилом или C1-6 алкокси; или R15 и R15' или R16 и R16' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00138] R17, R17', R18 и R18' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6 алкилом, или C1-6 алкокси; или R17 и R18 или R17' и R18' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00139] R19, R19' и R19" независимо являются водородом, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом, C1-6 алкокси, фенил, С1-6 алкилимидазолом, C1-6 алкилтриазолом, C1-6 алкилтетразолом, C1-6 алкилтиазолом, C1-6алкилоксазолом, C1-6 алкилдиоксазолом; C1-6 алкилоксазолидоном; и
[00140] R20 и R21 независимо являются водородом, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом, С1-6 алкокси, фенилом, C1-6 алкилимидазолом, C1-6 алкилтриазолом, C1-6 алкилтетразолом, С1-6 алкилтиазолом, C1-6алкилоксазолом, C1-6 алкилдиоксазолом; C1-6 алкилоксазолидоном, или R20 и R21 вместе с азотом, к которому они присоединены, образуют незамещенный пирролидинил, незамещенный пиперидинил, или незамещенный морфолинил; или образуют карбоксил-замещенный пирролидинил, карбоксил-замещенный пиперидинил или карбоксил-замещенный морфолинил; и
[00141] R22 и R22' независимо являются группой, выбранной из водорода, кислорода, C1-6 алкила или замещенного C1-6 алкила, C1-6 алкокси или замещенного C1-6 алкокси, С3-8 циклоалкила или замещенного С3-8 циклоалкила, С2-6 алкенила или замещенного С2-6 алкенила, арила или замещенного арила, включая замещенный или незамещенный C1-6 алкилимидазол, замещенный или незамещенный C1-6 алкилтриазол, C1-6 алкилтетразол, C1-6 алкилтиазол, замещенный или незамещенный C1-6 алкилоксазол, C1-6 алкилдиоксазол; C1-6 алкилоксазолидон; -COR19, -COOR19', -CSOR19", -CONR20R21,
или их фармацевтически приемлемую соль.
[00142] Один конкретный вариант осуществления обеспечивает соединение в соответствии с Формулой I, Формулой IA или Формулой IB, приведенной в настоящем описании, при этом:
[00143] R1 выбрано из группы водорода, гидрокси, галогена, циано, амино, пирролидинила, незамещенного C1-6 алкила или галогензамещенного C1-6 алкила, незамещенного C1-6 алкокси или галогензамещенного C1-6 алкилокси; С3-7 циклоалкила или галогензамещенного С3-7 циклоалкила; N-содержащего моноциклического гетероциклоалкила, пирролидинила, -CxH2x-фенила, -О-СхН2х-фенила, или -(C1-6 алкил)N- СхН2х-фенила, при этом х равно 0, 1, 2, 3, 4, 5 или 6; или -OR12;
[00144] R2 и R3 независимо являются OR12;
[00145] R4 выбрано из группы водорода, гидрокси, галогена, пиано, амино, пирролидинила, незамещенного C1-6 алкила или галогензамещенного C1-6 алкила, незамещенного C1-6 алкокси или галогензамещенного C1-6 алкилокси; С3-7 циклоалкила или галогензамещенного С3-7 циклоалкила; N-содержащего моноциклического гетероциклоалкила, пирролидинила, -CxH2x-фенила, -О-CxH2x-фенила, или -(C1-6 алкил)N-СхН2х-фенила, при этом х равно 0, 1, 2, 3, 4, 5 или 6; или -OR12;
[00146] R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляет собой NR20 и указанные два или более гетероатомов являются группой, выбранной из N, NR22, О, S, SR22"SR22R22'; R11 представляет собой водород; R12 - как приведено в настоящем описании; и R15 и R16 или R15' и R16' вместе образуют от 3- до 8-членное циклоалкильное кольцо или гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', или его фармацевтически приемлемую соль.
[00147] Еще один вариант осуществления обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенной в настоящем описании, R9 - как приведено в настоящем описании и R10 представляет собой заместитель, показанный в Таблице 2, или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо; или его фармацевтически приемлемую соль.
[00148] Еще один конкретный вариант осуществления обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, R9 - как приведено в настоящем описании и R10 представляет собой заместитель, показанный в Таблице 2, или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо; и R12 является незамещенным C1-6 алкилом; или его фармацевтически приемлемую соль.
[00149] Еще один конкретный вариант осуществления обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, при этом W и Y - как приведено в настоящем описании, R1, R2, R3 и R4 независимо являются OR12; R9 - как приведено в настоящем описании и R10 представляет собой заместитель, показанный в Таблице 2, или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо; и R12 - как приведено в настоящем описании; или его фармацевтически приемлемую соль.
[00150] Другой вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемую соль, приведенное в настоящем описании, при этом R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо.
[00151] Другой вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемую соль, приведенное в настоящем описании, при этом
[00152] W и Y - как приведено в настоящем описании;
[00153] R1 и R4, - как описано;
[00154] R2 и R3 независимо являются группой, выбранной из водорода, гидрокси, галогена, циано, амино, тио, C1-6 алкила или замещенного C1-6 алкила, C1-6 алкокси или замещенного C1-6 алкокси; С3-8 циклоалкила или замещенного С3-8 циклоалкила; С2-8 алкенила или замещенного С2-8 алкенила; от 3- до 8-членного гетероциклоалкила или замещенного от 3- до 8-членного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила, или -OR12;
[00155] R5 и R6 независимо являются водородом, гидрокси, галогеном, циано, амино, C1-6 алкилом или замещенным C1-6 алкилом, C1-6 алкокси или замещенным C1-6 алкокси, С3-8 циклоалкилом или замещенным С3-8 циклоалкилом, С2-8 алкенилом или замещенным С2-8 алкенилом; арилом или замещенным арилом, гетероарилом или замещенным арилом, -CxH2x-фенилом или -О-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00156] R7 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино, C1-6 алкилом или замещенным С1-6 алкилом, С1-6 алкокси или замещенным С1-6 алкокси, С3-8 циклоалкилом или замещенным С3-8 циклоалкилом, С2-8 алкенилом или замещенным С2-8 алкенилом; арилом или замещенным арилом, гетероарилом или замещенным арилом, -СхН2х-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00157] или R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', при этом указанное от 3- до 8-членное гетероциклоалкильное кольцо необязательно замещено R13, R13', R14 и/или R14';
[00158] R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляет собой NR20 и указанные два или более гетероатомов являются группой, выбранной из N, NR22, О, S, SR22 и SR22R22';
[00159] или R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R17', R18 и/или R18', при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00160] R9 представляет собой связь, водород, гидрокси, галоген, циано, амино, алкил или замещенный алкил, алкокси или замещенный алкокси, циклоалкил или замещенный циклоалкил, алкенил или замещенный алкенил, гетероциклоалкил или замещенный гетероциклоалкил, арил или замещенный арил, гетероарил или замещенный гетероарил, -CxH2x-фенил или -О-CxH2x-фенил, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00161] R10 представляет собой заместитель, показанный в Таблице 2, или его таутомер;
[00162] или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо;
[00163] R11 является водородом, гидрокси, галогеном, циано, амино, C1-6 алкилом или замещенным C1-6 алкилом, C1-6 алкокси или замещенным C1-6 алкокси, С3-8 циклоалкилом или замещенным С3-8 циклоалкилом, С2-8 алкенилом или замещенным С2-8 алкенилом; арилом или замещенным арилом, гетероарилом или замещенным арилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00164] R12 является водородом; C1-6 алкилом или замещенным C1-6 алкилом, C1-6 алкокси или замещенным C1-6 алкокси, С3-8 циклоалкилом или замещенным С3-8 циклоалкилом, С3-8 гетероциклоалкилом или замещенным С3-8 гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом; и
[00165] R22 и R22' независимо являются группой, выбранной из водорода, кислорода, C1-6 алкила или замещенного C1-6 алкила, C1-6 алкокси или замещенного С1-6 алкокси, С3-8 циклоалкила или замещенного С3-8 циклоалкила, С2-6 алкенила или замещенного С2-6 алкенила, арила или замещенного арила, -COR19, -COOR19', -CSOR19", -CONR20R21.
[00166] Другой вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемую соль, приведенное в настоящем описании, при этом каждый из W и Y представляет собой N.
[00167] Конкретный вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемую соль, приведенное в настоящем описании, при этом
[00168] W и Y - как приведено в настоящем описании;
[00169] R1, R2, R3 и R4 независимо являются Н или OR12; и
[00170] R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', при этом указанное от 3- до 8-членное гетероциклоалкильное кольцо необязательно замещено R13, R13', R14 и/или R14'.
[00171] Еще один вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемую соль, приведенное в настоящем описании, при этом
[00172] W и Y - как приведено в настоящем описании;
[00173] R2 и R3 независимо являются Н или OR12; и
[00174] R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляет собой NR20 и указанные два или более гетероатомов являются группой, выбранной из N, NR22, O, S, SR22 и SR22R22'.
[00175] Еще один вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемую соль, приведенные в настоящем описании, при этом
[00176] R1, R2, R3 и R4 независимо являются Н или OR12; и
[00177] R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17 и R18, при этом указанный гетероатом в указанном гетероциклоалкильном кольце выбрано из группы О, N, NR22, S, SR22 или SR22R22'.
[00178] Еще один конкретный вариант осуществления обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, при этом R2 и R3 независимо являются OR12; R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R13 и R14, при этом указанный гетероатом в указанном гетероалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22'; R10 представляет собой заместитель, показанный в Таблице 2, или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо; R11 представляет собой Н; R12 является незамещенным C1-6 алкилом; и R13 и R14 или R13' и R14' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22'; или его фармацевтически приемлемую соль.
[00179] Еще один конкретный вариант осуществления обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, при этом R2 и R3 независимо являются OR12; R7 и R8 вместе образуют от 3- до 8-членное кольцо, необязательно замещенное R17 и R18; R10 представляет собой заместитель, показанный в Таблице 2, или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо; R11 представляет собой Н; R12 является незамещенным C1-6 алкилом; и R17 и R18 или R17' и R18' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22'; или его фармацевтически приемлемую соль.
[00180] Еще один конкретный вариант осуществления обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, при этом R2 и R3 независимо являются OR12; и R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членным гетероциклоалкильное кольцо, необязательно замещенное R13, R14, R13' и/или R14', при этом указанный гетероатом в указанном гетероалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', или его фармацевтически приемлемую соль.
[00181] Еще один конкретный вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, при этом R2 и R3 независимо являются OR12; и R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R18, R17' и/или R18', при этом указанный гетероатом в указанном гетероалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', или его фармацевтически приемлемую соль.
[00182] Еще один конкретный вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемую соль, приведенное в настоящем описании, при этом
[00183] R1, R2, R3 и R4 - как описано в настоящем документе; и
[00184] (A) R5 и R6 независимо являются гидрокси, галогеном, циано, амино алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6; или R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R13, R13', R14 и/или R14', при этом указанный гетероатом в указанном гетероциклоалкильном кольце выбрано из группы О, N, NR22, S, SR22 или SR22R22'; и
[00185] R7 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6; или
[00186] (В) R5 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6; и
[00187] R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляет собой NR20, а указанные два или более гетероатомов являются группой, выбранной из N, NR22, О, S, SR22 и SR22R22'; или
[00188] (С) R5 и R6 независимо являются водородом, гидрокси, галогеном,
циано, амино алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6; и
[00189] R7 и R8 независимо являются гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом, -CxH2x-фенилом или -O-СхН2х-фенилом, при этом x равно 0, 1, 2, 3, 4, 5 или 6; или R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R18', R17 и/или R18', при этом указанный гетероатом в указанном гетероциклоалкильном кольце выбрано из группы О, N, NR22, S, SR22 или SR22R22'.
[00190] В другом конкретном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формула IA, или Формула IB, как описано выше, при этом указанное соединение выбрано из группы соединений, приведенных в Таблице 1, при этом R10 - как приведено в настоящем описании или заместитель, показанный в Таблице 2, или его таутомер.
[00191] В конкретных вариантах осуществления настоящее изобретение обеспечивает соединение Формулы I, приведенной в настоящем описании, или его фармацевтически приемлемую соль, при этом W представляет собой N; Y представляет собой С; R1 отсутствует; R2 и R3 независимо являются группой, выбранной из группы, представленной водородом, гидрокси, галогеном, C1-6 алкилом или замещенным C1-6 алкилом, C1-6 алкокси или замещенным C1-6 алкокси, С3-8 циклоалкилом или замещенным С3-8 циклоалкилом, С2-8 алкенилом или замещенным С2-8 алкенилом, или -OR12, R4 представляет собой Н; R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо, необязательно замещенное R15, R15', R16 и/или R16'; R11 представляет собой Н; и R15, R15', R16 и/или R16' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6алкилом, или C1-6алкокси.
[00192] В конкретном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, приведенной в настоящем описании, или его фармацевтически приемлемую соль, при этом W представляет собой N; Y представляет собой С; R1 отсутствует; R2 является галогеном; R3 представляет собой OR12; и R4 представляет собой Н.
[00193] В другом конкретном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, приведенной в настоящем описании, или его фармацевтически приемлемую соль, при этом W представляет собой N; Y представляет собой С; R1 отсутствует; R2 является галогеном и R3 представляет собой -OR12; R4 представляет собой Н; R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо, необязательно замещенное R15, R15', R16 и/или R16'; R11 представляет собой Н; и R15, R15', R16 и/или R16' независимо являются C1-6 алкилом.
[00194] В другом конкретном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, приведенной в настоящем описании, или его фармацевтически приемлемую соль, при этом: R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо, необязательно замещенное R15, R15', R16 и/или R16'.
[00195] В другом конкретном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, приведенной в настоящем описании, или его фармацевтически приемлемую соль, при этом: R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17 и R18, при этом указанный гетероатом в указанном гетероциклоалкильном кольце выбрано из группы О, N, NR22, S, SR22 или SR22R22'.
[00196] В одном конкретном варианте осуществления настоящее изобретение обеспечивает соединение, выбранное из группы, состоящей из следующих соединений:
[00197] (4bR,7aS)-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00198] (4bS,7aR)-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00199] (4bR,7aS)-2-циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00200] 2-циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00201] (7aR)-2-циклопропил-4b-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00202] (7aR)-2-хлор-4b-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00203] (7aR)-2-хлор-4b-метокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00204] (4bR,7aS)-2-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00205] (4bR,7aS)-2-хлор-3-гидрокси-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00206] 2-хлор-6-(1-гидрокси-2-метилпропан-2-ил)-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00207] (S)-6-(трет-бугил)-2-хлор-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00208] (S)-6-(трет-бутил)-3-(циклопропилметокси)-2-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00209] (S)-6-(трет-бутил)-3-(3-метоксипропокси)-2-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00210] (S)-6-(трет-бутил)-2-циклопропил-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00211] (S)-6-(трет-бутил)-2-циклопропил-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00212] (R)-6-(трет-бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00213] (S)-6-(трет-бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-6,10-дигадро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00214] (S)-6-(трет-бутил)-3-(циклопропилметокси)-2-гидрокси-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00215] (S)-6-(трет-бутил)-2-метокси-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00216] (S)-6-(трет-бутил)-2-гидрокси-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00217] (S)-6-(трет-бутил)-3-(3-метоксипропокси)-10-оксо-2-(проп-1-ен-2-ил)-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00218] (S)-6-(трет-бутил)-2-изопропил-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00219] (S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-8-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00220] (S)-6-(трет-бутил)-2-(гидроксиметил)-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00221] (s)-6-(трет-бутил)-2-циклопропил-11-гидрокси-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00222] (2-хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00223] (2-хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00224] 2-циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00225] 2-циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00226] 6-(трет-бугил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота;
[00227] 2'-хлор-3'-(циклопропилметокси)-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловая кислота;
[00228] 2',3'-диметокси-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловая кислота;
[00229] 6-изопропил-2,3-диметил-10-оксо-5,10-дигидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксиловая кислота;
[00230] 2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
[00231] 3'-(циклопропилметокси)-2,-(дифторметил)-11'-фтор-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловая кислота;
[00232] 2'-(дифторметил)-11'-фтор-10'-оксо-3'-((тетрагидрофуран-3-ил)метокси)-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловая кислота;
[00233] (S)-3-(циклопропилметокси)-2-(дифторметил)-11-фтор-6-изопропил-6-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота; и
[00234] (6S)-2-(дифторметил)-11-фтор-6-изопропил-6-метил-10-оксо-3-((тетрагидрофуран-3-ил)метокси)-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота; или их фармацевтически приемлемая соль или таутомер.
[00235] В одном конкретном варианте осуществления настоящее изобретение обеспечивает соединение, выбранное из группы соединений:
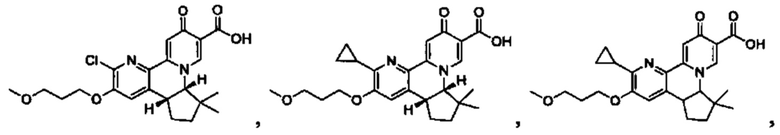
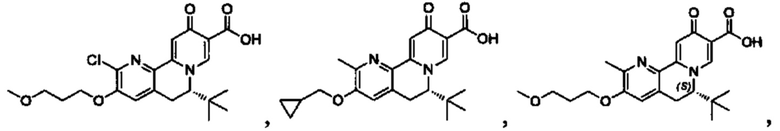
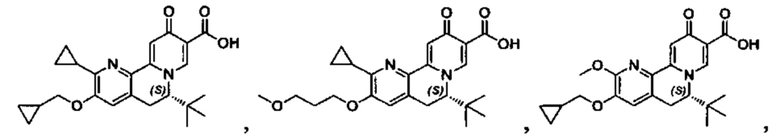
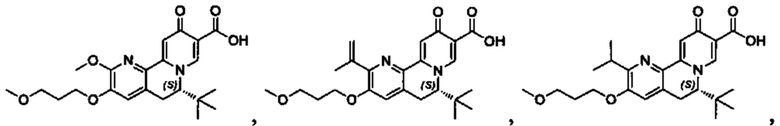
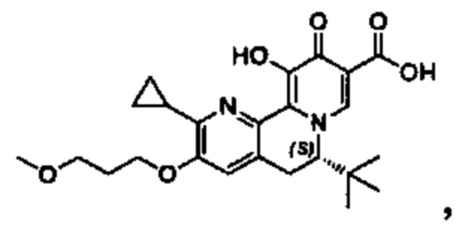 или
или 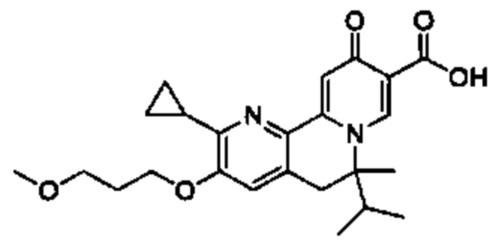
или его фармацевтически приемлемая соль.
[00236] В конкретном варианте осуществления настоящее изобретение обеспечивает соединение, имеющее следующую структуру:
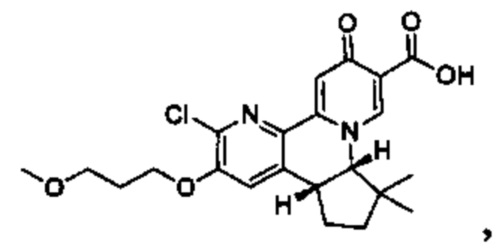 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00237] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
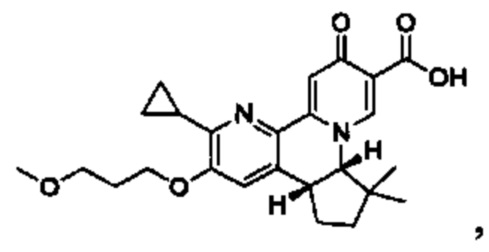 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00238] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
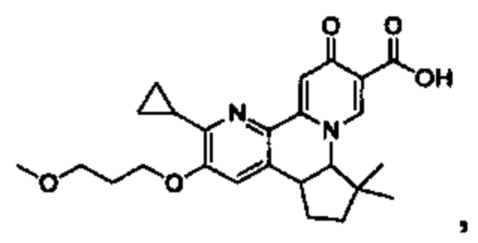 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00239] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
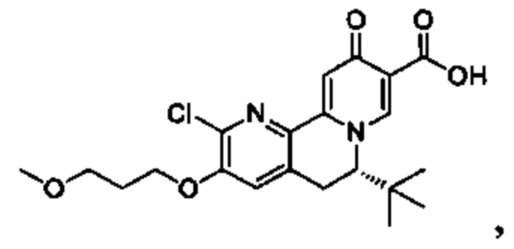 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00240] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
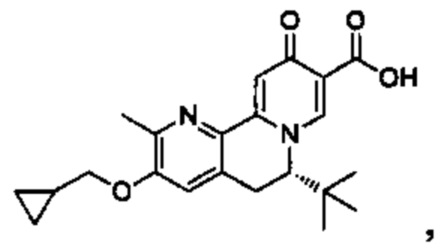 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00241] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
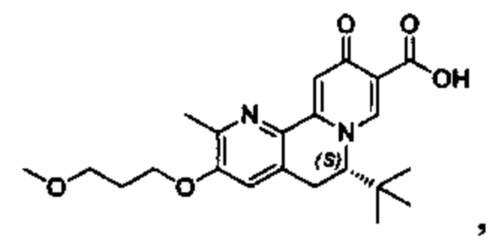 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00242] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
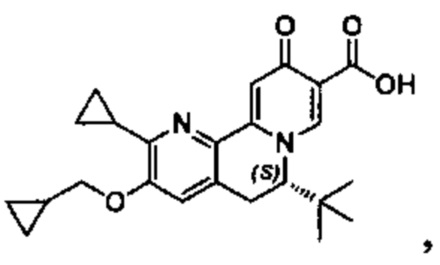 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00243] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
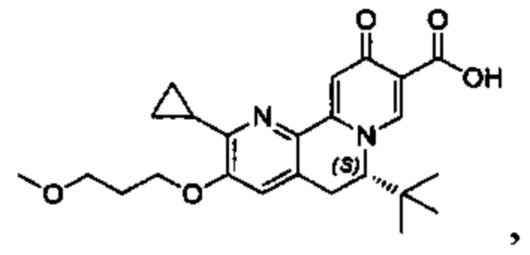 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00244] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
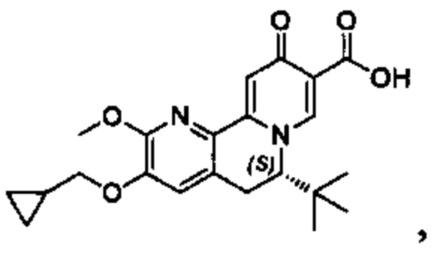 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00245] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
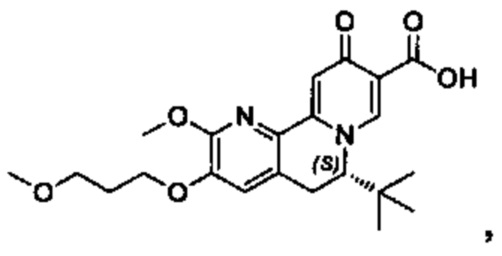 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00246] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
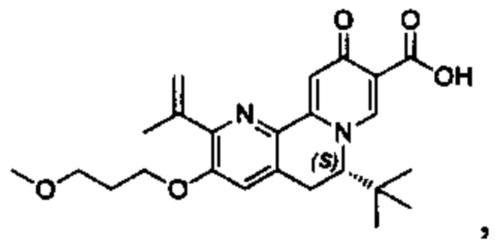 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00247] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
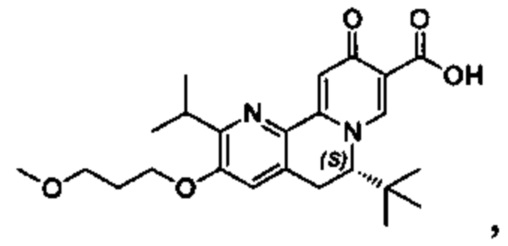 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00248] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
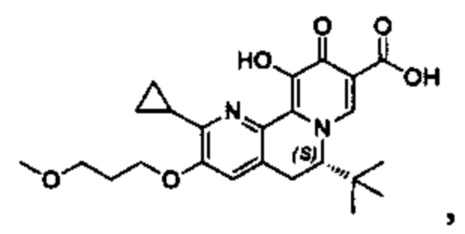 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00249] В конкретном варианте осуществления настоящее изобретение обеспечивают соединение, имеющее следующую структуру:
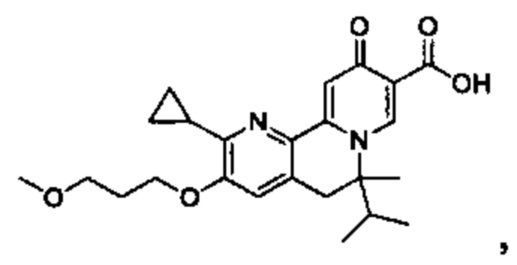 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[00250] В соответствии с одним вариантом осуществления настоящее изобретение обеспечивает соединение, имеющее структуру Формулы I, IA или IB, при этом указанное соединение выбрано из группы соединений:
[00251]
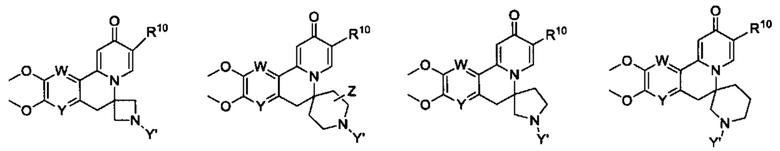
при этом W и Y независимо являются N или С, при условии, что W и Y оба не являются С, и при этом R10 - как приведено в настоящем описании или заместитель, показанный в Таблице 2 и
Y' представляет собой 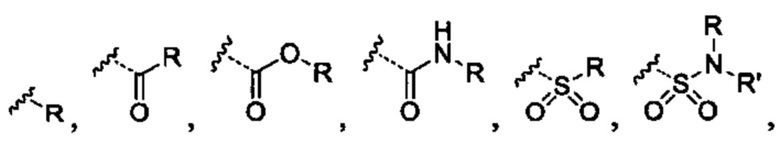 гетероцикл или замещенный гетероцикл, гетероарил или замещенный гетероарил, при этом R и R' независимо являются алкилом или замещенным алкилом.
гетероцикл или замещенный гетероцикл, гетероарил или замещенный гетероарил, при этом R и R' независимо являются алкилом или замещенным алкилом.
[00252] В конкретных вариантах осуществления настоящее изобретение обеспечивает соединения Формулы I, IA или IB, при этом указанное соединение выбрано из группы:
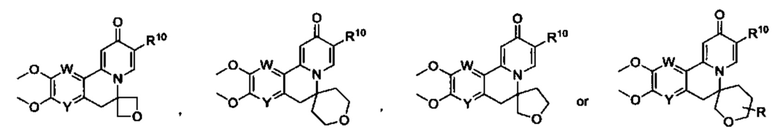
при этом W и Y независимо являются N или С, при условии, что W и Y оба не являются С, и при этом R10 - как приведено в настоящем описании или заместитель, показанный в Таблице 2.
[00253] В других конкретных вариантах осуществления настоящее изобретение обеспечивает соединение Формулы I, IA или IB, при этом указанное соединение выбрано из группы:
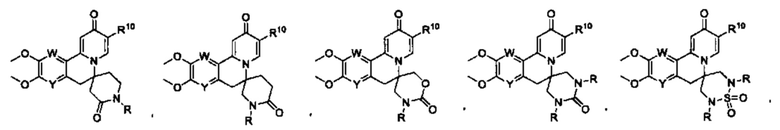
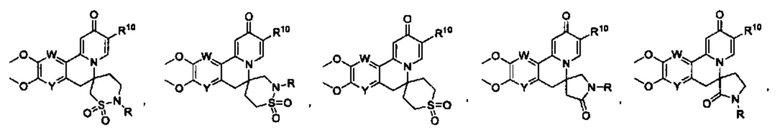
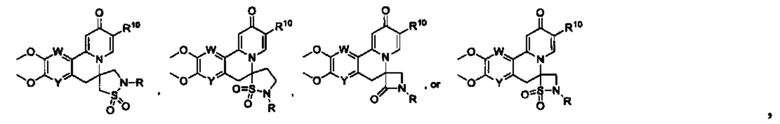
при этом W и Y независимо являются N или С, при условии, что W и Y оба не являются С, и при этом R10 представляет собой заместитель, приведенный в настоящем описании, или заместитель, показанный в Таблице 2, и R представляет собой Н, алкил или замещенный алкил.
[00254] В другом варианте осуществления настоящего изобретения соединение Формулы I, Формулы IA или Формулы IB выбрано из группы:
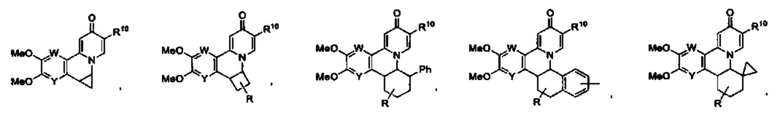
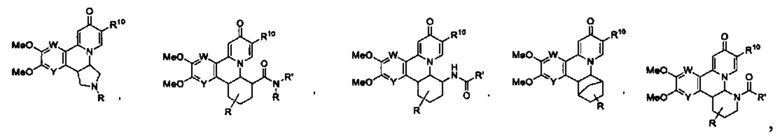
при этом W и Y независимо являются N или С, при условии, что W и Y оба не являются С, и при этом R10 представляет собой заместитель, приведенный в настоящем описании, или заместитель, показанный в Таблице 2, и R является водородом, гидрокси,  гетероциклоалкилом или замещенным гетероциклоалкилом, гетероарилом или замещенным гетероарилом, при этом R' и R'' независимо являются алкилом или замещенным алкилом.
гетероциклоалкилом или замещенным гетероциклоалкилом, гетероарилом или замещенным гетероарилом, при этом R' и R'' независимо являются алкилом или замещенным алкилом.
[00255] В другом варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, как показано ниже:
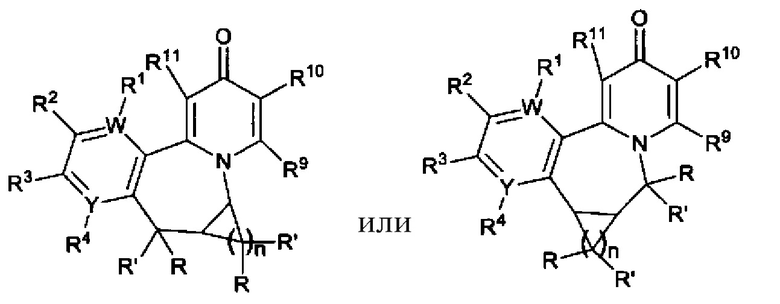
[00256] при этом R1, R2, R3, R4, R9 и R11 - как описано в настоящем документе, W и Y независимо являются N или С, при условии, что W и Y оба не являются С, и при этом R10 - как приведено в настоящем описании или группа, выбранная из заместителей, показанных в Таблице 2, и R' и R независимо являются группой, выбранной из водорода, гидроксила, галогена, алкила или замещенного алкила, алкиломена или замещенного алкиломена, карбоцикла или замещенного карбоцикла, гетероциклоалкила или замещенного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила, при этом указанные замещенные группы R и R' могут быть замещены гидроксилом, галогеном, алкилом, алкиломеном, циклоалкилом, гетероциклом, арилом, гетероарилом, 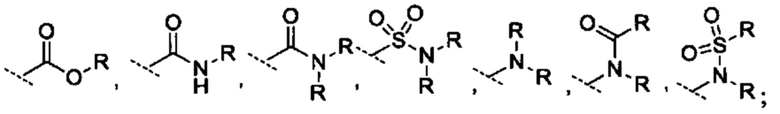 или R и R' вместе образуют спиро, конденсированное или мостиковое карбоциклическое или гетероциклическое кольцо.
или R и R' вместе образуют спиро, конденсированное или мостиковое карбоциклическое или гетероциклическое кольцо.
[00257] В другом варианте осуществления настоящее изобретение обеспечивает соединение, имеющее структуру Формулы I, IA или IB, при этом указанное соединение выбрано из группы:
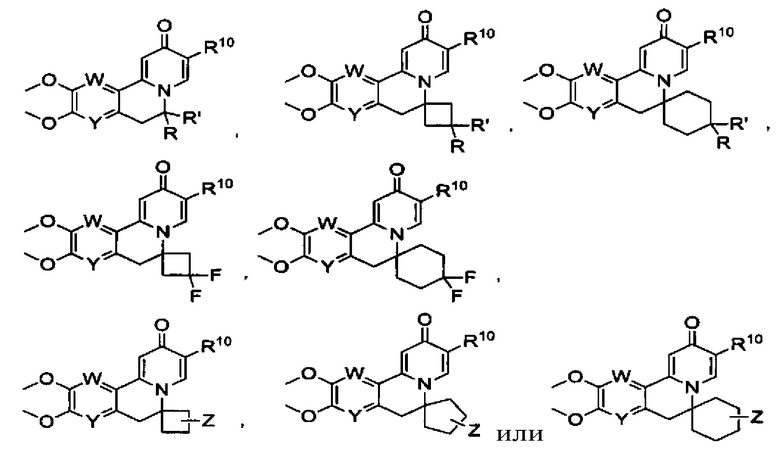
при этом W и Y независимо являются N или С, при условии, что W и Y оба не являются С, и при этом R10 - как приведено в настоящем описании или выбрано из группы заместителей, показанных в Таблице 2, R и R' независимо являются Н, гидроксилом, алкилом или замещенным алкилом, ацилом, сложным эфиром, карбамоилом, сульфонилмочевиной или мочевиной, и при этом Z представляет собой Н, ОН, NH2, SH, или замещенным С, О, N или S.
[00258] В другом конкретном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, IA или IB, как указано ниже:
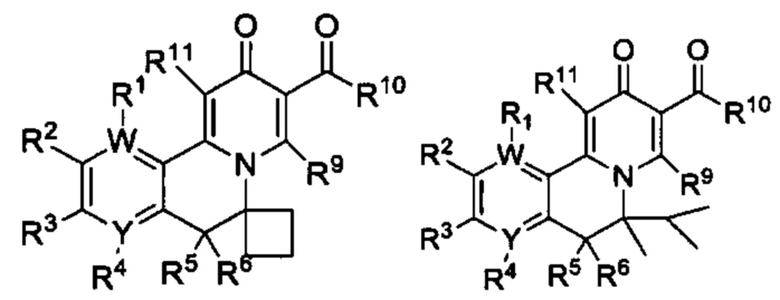
при этом R4, R5, R6, R9, и R11 - как описано в настоящем документе, W и Y независимо являются N или С, при условии, что W и Y оба не являются С, и при этом R10 - как приведено в настоящем описании или выбрано из группы заместителей, показанных в Таблице 2, R1 - как определено в настоящем документе, R2 и R3 независимо являются группой, выбранной из: 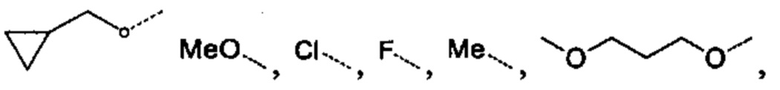
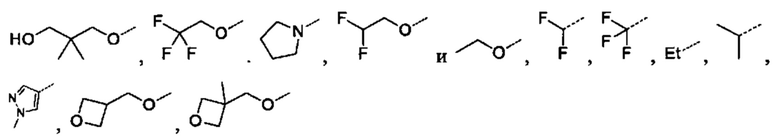
[00259] Некий вариант осуществления настоящего изобретения обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенной в настоящем описании, или его фармацевтически приемлемую соль, при этом:
[00260] (A) R5 и R6 независимо являются гидрокси, галогеном, циано, амино алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0,1,2, 3,4, 5 или 6; или R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R13, R13', R14 и/или R14', при этом указанный гетероатом в указанном гетероциклоалкильном кольце выбран из группы О, N, NR22, S, SR22 или SR22R22'; и
[00261] R7 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -O-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6; или
[00262] (В) R5 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6; и
[00263] R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляет собой NR20, а указанные два или более гетероатомов выбраны из группы N, NR22, О, S, SR22 и SR22R22'; или
[00264] (С) R5 и R6 независимо являются водородом, гидрокси, галогеном, циано, амино алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6; и
[00265] R7 и R8 независимо являются гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6; или R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R18', R17 и/или R18', при этом указанный гетероатом в указанном гетероциклоалкильном кольце выбран из группы О, N, NR22, S, SR22 или SR22R22'.
[00266] В одном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, или его фармацевтически приемлемую соль, при этом указанное соединение выбрано из группы соединений в Таблице 1, и при этом R10 - как приведено в настоящем описании или представляет собой заместитель, показанный в Таблице 2, или его таутомер.
[00267] В одном варианте осуществления настоящее изобретение обеспечивает способ лечения или предотвращения вирусной инфекции у субъекта, подверженного или страдающего указанной вирусной инфекцией, включающий введение указанному субъекту ингибитора антигена НВе или HBs, при этом указанный ингибитор представляет собой соединение Формулы I, Формулы IA или Формулы IB, приведенной в настоящем описании.
[00268] В одном варианте осуществления настоящее изобретение обеспечивает способ лечения или предотвращения вирусной инфекции гепатита В у субъекта, подверженного или страдающего от указанной вирусной инфекции гепатита В, включающий введение указанному субъекту ингибитора антигенов НВе или HBs, при этом указанный ингибитор представляет собой соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании.
[00269] В одном варианте осуществления настоящее изобретение обеспечивает способ лечения или предотвращения вирусной инфекции гепатита В у субъекта, подверженного или страдающего от указанной вирусной инфекции гепатита В, включающий введение указанному субъекту ингибитора антигенов НВе или HBs, при этом указанный ингибитор содержит соединение из Таблицы 1, при этом R10 представляет собой заместитель, показанный в Таблице 2, или его таутомер, или при этом указанный ингибитор представляет собой соединение из Таблицы IB.
[00270] В одном варианте осуществления настоящее изобретение обеспечивает способ ингибирования уровня антигенов НВе или HBs у млекопитающего, включающий введение указанному млекопитающему терапевтически эффективного количества соединения Формулы I, Формулы IA или Формулы IB, приведенного в настоящем описании, или его фармацевтически приемлемой соли, сольвата или гидрата.
[00271] В конкретном варианте осуществления настоящее изобретение обеспечивает способ ингибирования уровня антигенов НВе или HBs у млекопитающего, включающий введение указанному млекопитающему терапевтически эффективного количества соединения Формулы I, Формулы IA или Формулы IB, приведенного в настоящем описании, или его фармацевтически приемлемой соли, сольвата или гидрата, при этом указанное млекопитающее является человеком.
[00272] В одном варианте осуществления настоящее изобретение обеспечивает фармацевтическую композицию, содержащую фармацевтически приемлемый разбавитель и терапевтически эффективное количество соединения Формулы I, Формулы IA или Формулы IB, приведенного в настоящем описании.
[00273] В одном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, или его фармацевтическую композицию для применения в указанной терапии.
[00274] В одном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, или его фармацевтическую композицию для применения в лечении вирусной инфекции.
[00275] В одном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, или его фармацевтическую композицию для применения в лечении вирусной инфекции, при этом указанной вирусной инфекцией является вирусная инфекция гепатита В.
[00276] В одном варианте осуществления настоящее изобретение обеспечивает применение соединения Формулы I, Формулы IA или Формулы IB, приведенного в настоящем описании, или его фармацевтической композиции для производства лекарственного средства для применения в лечении вирусной инфекции гепатита В у человека.
[00277] В одном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, или его фармацевтическую композицию для применения в медицинской терапии.
[00278] В одном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, или его фармацевтическую композицию для применения в лечении для предотвращения вирусной инфекции гепатита В у человека.
[00279] В одном варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, приведенное в настоящем описании, или его фармацевтическую композицию для применения в ингибировании уровня антигенов НВе или HBs у млекопитающего HBsAg in vitro.
[00281] Соединения, описанные в настоящем документе, могут существовать в конкретных геометрических или стереоизомерных формах. Настоящее изобретение включает в себя все такие соединения, включая цис- и транс-изомеры, (-)- и (+)-энантиомеры, (R)- и (S)-энантиомеры, диастереомеры, (D)-изомеры, (L)-изомеры, их рацемические смеси и другие смеси, такие как энантиомерно или диастереомерно обогащенные смеси, как попадающие в рамки настоящего изобретения. Дополнительные асимметричные атомы углерода могут присутствовать в заместителях, таких как алкильная группа. Все такие изомеры, а также их смеси, включены в рамки настоящего изобретения.
[00282] Оптически активные (R) - и (S)-изомеры и D и L-изомеры могут быть получены с использованием хиральных синтонов или хиральных реагентов или могут быть разделены с использованием обычных методик. Если, например, желательно получение конкретного энантиомера соединения согласно настоящему изобретению, он может быть получен асимметричным синтезом или дериватизацией с хиральным вспомогательным веществом, где полученная диастереомерная смесь разделяется, а вспомогательная группа отщепляется с получением чистых желаемых энантиомеров. Альтернативно, если молекула содержит основную функциональную группу, такую как аминогруппа, или кислотную функциональную группу, такую как карбоксильная группа, диастереомерные соли могут быть образованы с подходящей оптически активной кислотой или основанием с последующим разделением диастереомеров, полученных таким образом, фракционной кристаллизацией или хроматографическими методами, известными в данной области, и последующим выделением чистых энантиомеров. Кроме того, разделение энантиомеров и диастереомеров часто проводят с использованием хроматографии с использованием хиральных неподвижных фаз, необязательно в сочетании с химической дериватизацией (например, образованием карбаматов из аминов).
[00283] В другом варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB для применения в указанной терапии.
[00284] В другом варианте осуществления настоящее изобретение обеспечивает соединение Формулы I, Формулы IA или Формулы IB, для применения в лечении вирусной инфекции.
[00285] В другом варианте осуществления настоящее изобретение обеспечивает применение соединения Формулы I, Формулы IA или Формулы IB для производства лекарственного средства для применения в лечении вирусной инфекции у человека.
[00286] В другом варианте осуществления настоящее изобретение обеспечивает фармацевтическую лекарственную форму, содержащую фармацевтически приемлемый разбавитель и терапевтически эффективное количество соединения, описанного Формулой I, Формулой IA или Формулой IB.
[00287] В одном варианте осуществления указанная фармацевтическая лекарственная форма, содержащая соединение Формулы I, Формулы IA или Формулы IB или его соль, представляет собой лекарственную форму, адаптированную для парентерального введения. В другом варианте осуществления, указанной лекарственной формой является лекарственная форма продолжительного действия. В еще одном варианте осуществления указанной лекарственной формой является лекарственная форма с наночастицами.
[00288] В одном варианте осуществления, указанная фармацевтическая лекарственная форма, содержащая соединение Формулы I, Формулы IA или Формулы IB или его соль, представляет собой лекарственную форму, адаптированную для орального, ректального, местного или внутривенного введения, при этом указанная фармацевтическая лекарственная форма необязательно содержит любой один или более фармацевтически приемлемый носитель, адъювант или наполнитель.
[00289] В одном варианте осуществления настоящего изобретения, указанное соединение Формулы I, Формулы IA или Формулы IB выполнено в виде лекарственной формы для орального введения, и может вводиться в виде обычного препарата, например, в виде любой дозированной формы твердого агента, такой как таблетки, порошки, гранулы, капсулы и подобные им; водного агента; масляной суспензии; или жидкого средства, такого как сироп и эликсир. В одном варианте осуществления, указанное соединение Формулы I, Формулы IA или Формулы IB выполнено в виде лекарственной формы для парентерального введения, и может вводиться в виде водной или масляной суспензии для инъекций или капель в нос. При приготовлении парентеральной лекарственной формы с соединением Формулы I, Формулы IA или Формулы IB, обычные вспомогательные вещества, связующие вещества, смазывающие вещества, водные растворители, масляные растворители, эмульгаторы, суспендирующие агенты, консерванты, стабилизаторы и подобные им вещества могут быть использованы произвольно. В качестве противовирусного лекарственного средства предпочтительнее, в частности, пероральное средство. Препарат соединения Формулы I, Формулы IA или Формулы IB может быть получен путем объединения (например, смешивания) терапевтического количества соединения Формулы I, Формулы IA или Формулы IB с фармацевтически приемлемым носителем или разбавителем.
[00290] Фармацевтическая лекарственная форма, адаптированная для орального введения, может быть представлена в виде дискретных единиц, таких как капсулы или таблетки; порошки или гранулы; растворы или суспензии в водных или неводных жидкостях; пены съедобные или взбитые; или жидкие эмульсии «масло в воде» или жидкие эмульсии «вода в масле».
[00291] Например, для орального введения в форме таблетки или капсулы, указанное соединение Формулы I, Формулы IA или Формулы IB можно комбинировать с пероральным нетоксичным фармацевтически приемлемым инертным носителем, таким как этанол, глицерин, вода и другие, подобные им. Порошки получают путем измельчения указанного соединения Формулы I, Формулы IA или Формулы IB до подходящего мелкого размера и смешивания с аналогичным измельченным фармацевтическим носителем, таким как съедобные углеводы, например крахмал или маннит. Также могут присутствовать ароматизатор, консервант, диспергирующий агент и краситель.
[00292] Капсулы изготавливают путем приготовления порошковой смеси, как описано выше, и заполнения сформированных желатиновых оболочек. Глиданты и смазывающие вещества, такие как коллоидный диоксид кремния, тальк, стеарат магния, стеарат кальция или твердый полиэтиленгликоль, могут быть добавлены к порошковой смеси перед операцией заполнения. Разрыхлитель или солюбилизирующий агент, такой как агар-агар, карбонат кальция или карбонат натрия, также может быть добавлен для улучшения доступности лекарственного средства при проглатывании капсулы.
[00293] Кроме того, при желании или необходимости в смесь также могут быть включены подходящие связующие вещества, смазывающие вещества, дезинтегрирующие агенты и красители. Подходящие связующие вещества включают крахмал, желатин, натуральные сахара, такие как глюкоза или бета-лактоза, кукурузные подсластители, натуральные и синтетические камеди, такие как акация, трагакант или альгинат натрия, карбоксиметилцеллюлоза, полиэтиленгликоль, воски и подобные им вещества. Смазочные материалы, используемые в этих лекарственных формах, включают олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и подобные им вещества. Дезинтеграторы включают крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и подобные им вещества, но не ограничиваются ими. Таблетки выполнены в виде лекарственной формы, например, путем приготовления порошковой смеси, гранулирования или ударного уплотнения, добавления лубриканта и дезинтегранта и прессования в таблетки. Порошковую смесь готовят путем смешивания указанного соединения, измельченного подходящим образом, с разбавителем или основой, как описано выше, и, необязательно, со связующим, таким как карбоксиметилцеллюлоза, алигинат, желатин или поливинилпирролидон, замедлитель растворения, такой как парафин, ускоритель резорбции, такой как четвертичная соль и/или абсорбент, такой как бентонит, каолин или дикальцийфосфат. Порошковая смесь может быть гранулирована путем смачивания связующим веществом, таким как сироп, крахмальная паста, смола из акадии или растворов целлюлозных или полимерных материалов, и продавливанием через сито. В качестве альтернативы гранулированию порошковую смесь можно пропустить через таблетировочную машину, в результате чего плохо сформированные слитки разбиваются на гранулы. Гранулы можно смазывать для предотвращения прилипания к формующим формам для таблеток путем добавления стеариновой кислоты, стеаратной соли, талька или минерального масла. Смесь со смазкой затем прессуют в таблетки. Указанное соединение согласно настоящему изобретению также можно комбинировать со свободно текущим инертным носителем и напрямую прессовать в таблетки, минуя стадии гранулирования или ударного уплотнения. Может быть предусмотрено прозрачное или непрозрачное защитное покрытие, состоящее из герметизирующего слоя шеллака, покрытия из сахара или полимерного материала и полирующего покрытия из воска. К этим покрытиям можно добавлять красители, чтобы различать различные стандартные дозировки.
[00294] Жидкости для перорального применения, такие как растворы, сиропы и эликсиры, могут быть приготовлены в форме единичной дозировки, так что заданное количество жидкости содержит заданное количество указанного соединения. Сиропы можно приготовить путем растворения указанного соединения в водном растворе с подходящим вкусом, а эликсиры - с использованием нетоксичного спиртового носителя. Суспензии могут быть приготовлены диспергированием указанного соединения в нетоксичном транспортном средстве. Также могут быть добавлены солюбилизаторы и эмульгаторы, такие как этоксилированные изостеариловые спирты и полиоксиэтиленовые эфиры сорбита, консерванты, вкусовые добавки, такие как масло перечной мяты или натуральные подсластители, сахарин или другие искусственные подсластители и т.п.
[00295] При необходимости, стандартная дозировка лекарственной формы для орального введения может быть микрокапсулирована. Указанная лекарственная форма соединений Формулы I, Формулы IA или Формулы IB также может быть приготовлена в виде формы для продленного или длительного высвобождения указанного соединения, например, путем нанесения покрытия или заключения материала в виде частиц в полимеры, воск или подобные им вещества.
[00296] Указанное соединение Формулы I, Формулы IA или Формулы IB или его соли, сольват или его гидраты также можно вводить в форме липосомных систем доставки, таких как маленькие однослойные везикулы, большие однослойные везикулы и многослойные везикулы. Липосомы могут быть сформированы из множества фосфолипидов, таких как холестерин, стеариломамин или фосфатидилхолины.
[00297] Указанное соединение Формулы I, Формулы IA или Формулы IB или его соли, сольваты или его гидраты также могут быть доставлены с использованием моноклональных антител в качестве индивидуальных носителей, с которыми связаны молекулы указанного соединения. Указанное соединение также может быть связано с растворимыми полимерами в качестве целевых носителей лекарственного средства. Такие полимеры могут включать поливинилпирролидон, пирансополимер, полигидроксипропилметакриламид-фенол, полигидроксиэтиласпартамид-фенол или пальмитоил, замещенный полизтиленоксидполилизиновыми остатками. Кроме того, указанное соединение может быть связано с классом биоразлагаемых полимеров, полезных для достижения контролируемого высвобождения лекарственного средства, например, полимолочной кислоты, полепсилон-капролактон, полигидрокси масляной кислоты, сложных полиортоэфиров, полиацеталей, полидигидропиранов, полицианоакрилатов и сшитых или амфипатических блок-сополимеров, гидрогелей.
[00298] Фармацевтическая лекарственная форма, адаптированная для трансдермального введения, может быть представлена в виде отдельных пластырей, предназначенных для сохранения тесного контакта с эпидермисом реципиента в течение продолжительного периода времени. Например, указанное соединение Формулы I, Формулы IA или Формулы IB может быть доставлено из пластыря с помощью ионтофореза, как в целом описано в Pharmaceutical Research, 3 (6), 318 (1986).
[00299] Фармацевтическая лекарственная форма, адаптированная для местного применения, может быть изготовлена в виде мазей, кремов, суспензий, лосьонов, порошков, растворов, паст, гелей, спреев, аэрозолей или масел. При изготовлении лекарственной формы в виде мази активный ингредиент может использоваться либо с парафиновой, либо с водорастворимой мазевой основой. В качестве альтернативы, активный ингредиент может быть добавлен в крем на основе типа "масло в воде" или основе "воды в масле".
[00300] Фармацевтическая лекарственная форма, адаптированная для ректального введения, может быть представлена в виде суппозиториев или клизм.
[00301] Фармацевтическая лекарственная форма, адаптированная для назального введения, когда носитель представляет собой твердое вещество, включая крупнозернистый порошок, имеющий размер частиц, например, в диапазоне от 20 до 500 микрон, может вводиться таким же способом, как нюхательный табак, то есть путем быстрого вдыхания через носовой проход из контейнера с порошком, поднесенного близко к носу. Подходящая лекарственная форма, когда носитель представляет собой жидкость, которая может вводиться в виде назального спрея или в виде назальных капель, включает водные или масляные растворы активного ингредиента.
[00302] Фармацевтические лекарственные формы, адаптированные для введения путем ингаляции, включают мелкодисперсные частицы пыли или спрея, которые могут образовываться с помощью различных типов дозированных аэрозолей под давлением, распылителей или инсуффляторов.
[00303] Фармацевтическая лекарственная форма, адаптированная для парентерального введения, включает водные и неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостатики и растворенные вещества, которые делают лекарственную форму изотонической с кровью предполагаемого реципиента; и водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты и загустители. Указанная лекарственная форма может быть представлена в одноразовых или многодозовых контейнерах, например, запечатанных ампулах и флаконах, и может храниться в лиофилизированном состоянии, требующем только добавления стерильного жидкого носителя, например, воды для инъекций, непосредственно перед использованием. Инъекционные растворы и суспензии для немедленного приема могут быть приготовлены из стерильных порошков, гранул и таблеток.
[00304] Следует понимать, что в дополнение к ингредиентам, в частности, упомянутым выше, лекарственная форма, описанная в настоящем описании, может включать другие агенты, обычные в данной области техники, с учетом рассматриваемого типа лекарственной формы, например, лекарственные формы, подходящие для орального введения могут включать ароматизаторы.
[00305] Терапевтические эффективные количества соединения Формулы I, Формулы IA или Формулы IB будут зависеть от ряда факторов, включая возраст и вес человека или другого животного, точное состояние, требующее лечения, и его тяжесть, характер заболевания, лекарственную форму и способ введения, и в конечном итоге будет определяться на усмотрение лечащего врача или ветеринара. Эффективное количество соли или гидрата может быть определено как пропорция эффективного количества указанного соединения Формулы I, Формулы IA или Формулы IB или их солей, сольвата или гидратов как таковых.
[00306] Варианты осуществления настоящего изобретения предусматривают введение соединений Формулы I, Формулы IA или Формулы IB здоровому или инфицированному вирусом пациенту либо в виде одного агента, либо в комбинации с (а) другим агентом, который эффективен для лечения или предотвращения вируса гепатита В или вируса гепатита D, (b) другим агентом, который улучшает иммунный ответ и устойчивость, или (с) другим агентом, который уменьшает воспаление и/или боль.
[00307] Указанное соединение Формулы I, Формулы IA или Формулы IB или их соли, сольвата или их гидраты, как полагают, обладают активностью в предотвращении, прекращении или снижении эффектов вируса Гепатит В путем ингибирования антигенов НВе и/или HBs, тем самым препятствуя или предотвращая присутствие вируса в клетке-хозяине и делая вирус неспособным к репликации.
[00308] Соответственно осуществляют способ лечения вируса гепатита В и/или вируса гепатита D путем введения млекопитающему терапевтически эффективного количества соединения Формулы I, Формулы IA или Формулы IB, или его фармацевтически приемлемой соли, сольвата или гидрата. В одном варианте осуществления, указанное млекопитающее является человеком.
[00309] В другом аспекте настоящее изобретение обеспечивает способ снижения уровня антигенов НВе и/или HBs у млекопитающих путем введения указанному млекопитающему терапевтически эффективного количества соединения Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемой соли, сольвата или гидрата. В одном варианте осуществления, указанное млекопитающее является человеком.
[00310] В других вариантах осуществления указанное соединение согласно настоящему изобретению может использоваться в комбинации с одним или более противовирусными терапевтическими агентами или противовоспалительными агентами, полезными для профилактики или лечения вирусных заболеваний или связанной с ними патофизиологии. Таким образом, указанное соединение согласно настоящему изобретению и его соль, сольват или их другие приемлемые производные можно использовать отдельно или в комбинации с другими противовирусными или противовоспалительными терапевтическими агентами.
[00311] Указанное соединение согласно настоящему изобретению и любой другой фармацевтически активный агент(ы) можно вводить вместе или отдельно, и при раздельном введении указанное введение может происходить одновременно или последовательно, в любом порядке. Количества указанного соединения согласно настоящему изобретению и другого фармацевтически активного(ых) агента(ов) и относительное время введения выбирают для достижения желаемого комбинированного терапевтического эффекта. Введение в комбинации соединения согласно настоящему изобретению и его соли, сольвата или других фармацевтически приемлемых производных с другими лечебными агентами может осуществляться в комбинации путем одновременного введения в виде: (1) единой фармацевтической композиции, включающей оба соединения; или (2) отдельных фармацевтических композиций, каждая из которых включает одно указанное соединение.
[00312] В качестве альтернативы, указанную комбинацию можно вводить отдельно последовательным образом, при этом один лечебный агент вводится первым, а другой - вторым, или наоборот. Такое последовательное введение может быть близким по времени или удаленным по времени. Количества указанного соединения(й) Формулы I, Формулы IA или Формулы IB или его соли и другого фармацевтически активного агента(ов) и относительные сроки введения выбирают для достижения желаемого комбинированного терапевтического эффекта.
[00313] Более конкретно, варианты осуществления настоящего изобретения обеспечивают способ, как описано в настоящем документе, включающий введение дополнительного агента, выбранного из группы, включающей противовирусный агент, антибиотик, анальгетик, нестероидный противовоспалительный (NSAED) агент, противогрибковый агент, противопаразитарное средство, агент против тошноты, антидиарейный агент или иммунодепрессант. В некоторых вариантах осуществления настоящего изобретения указанный противовирусный агент представляет собой агент против гепатита В или агент против гепатита С. Еще более конкретно, дополнительный агент вводят как часть одной дозировки указанной фармацевтической лекарственной формы или как отдельную дозированную форму.
[00314] Настоящее изобретение направлено на создание соединения, композиции и фармацевтической композиции, которые могут использоваться в качестве новых методов лечения и/или профилактических терапий вирусных инфекций. Не ограничиваясь какой-либо конкретной теорией, считается, что соединения согласно настоящему изобретению способны ингибировать уровни антигенов НВе и HBs у человека, инфицированного вирусом гепатита В или страдающего от хронической вирусной инфекции гепатита В. Снижая уровни НВе и HBs антигенов у инфицированного вирусом гепатита В пациента, соединения, описанные в настоящем документе, эффективны при лечении инфекций, вызванных вирусом гепатита В, и вторичных заболеваний, таких как цирроз печени, печеночная недостаточность и рак печени, которые часто связаны с инфекциями вируса гепатита В.
[00315] Таким образом, в другом варианте осуществления настоящего изобретения обеспечивают способ лечения или предотвращения вирусной инфекции гепатита у субъекта страдающего от инфекции ВГВ, включающий введение указанному субъекту ингибитора антигенов НВе и/или HBs, при этом указанный ингибитор представляет собой соединение Формулы I, Формулы IA или Формулы IB.
[00316] Другим вариантом осуществления настоящего изобретения является способ лечения вирусной инфекции гепатита В и/или заражения вирусом гепатита D у субъекта, страдающего от указанной вирусной инфекции, включающий введение указанному субъекту соединения из Таблицы 1.
[00317] В некоторых вариантах осуществления предоставляется способ лечения вирусной инфекции у субъекта, опосредованной, по меньшей мере частично, вирусом семейства гепатита В и или семейства гепатита D, включающий введение указанному субъекту композиции, содержащей соединение любой Формулы I, Формулы IA или Формулы IB или его фармацевтически приемлемую соль.
[00318] В еще одном аспекте другой вариант осуществления настоящего изобретения предусматривает способ ингибирования прогрессировал™ вирусной инфекции у субъекта с риском инфицирования вирусом гепатита В и/или вирусом гепатита D, включающий введение указанного субъекту терапевтически эффективного количества указанного соединения Формулы I, Формулы IA или Формулы IB, или его фармацевтически приемлемой соли.
[00319] В еще одном аспекте другой вариант осуществления настоящего изобретения обеспечивает способ предотвращения вирусной инфекции у субъекта, подверженного риску заражения вирусом гепатита В и/или вирусом гепатита D, включающий введение указанному субъекту терапевтически эффективного количества указанного соединения Формулы I или Формула IA, или его фармацевтически приемлемой соли.
[00320] В еще одном аспекте другой вариант осуществления настоящего изобретения обеспечивает способ лечения вирусной инфекции у субъекта, страдающего от указанной вирусной инфекции, включающий введение указанному субъекту терапевтически эффективного количества указанного соединения Формулы I, Формулы IA или Формулы IB, или его фармацевтически приемлемой соли.
[00321] В настоящем документе раскрыты соединения, способы и фармацевтические композиции для лечения вирусных инфекций путем введения соединений Формулы I, Формулы IA или Формулы IB в терапевтически эффективных количествах. Также раскрыты способы получения соединений Формулы I, Формулы IA или Формулы IB и способы использования указанного соединения и их фармацевтических композиций. В частности, описаны лечение и профилактика вирусных инфекций, таких как инфекции, вызываемые гепатитом В и/или гепатитом D.
[00322] В других вариантах осуществления настоящего изобретения указанное соединение, описанное в настоящем документе, пригодно для лечения инфекций у субъекта, при этом указанная инфекция вызвана штаммом вируса гепатита В и/или вируса гепатит D с множественной лекарственной устойчивостью.
[00323] В дополнительных вариантах осуществления настоящего изобретения указанное соединение согласно настоящему изобретению или его практически приемлемую соль выбирают из указанного соединения, представленного в Таблице 1.
ПРИМЕРЫ
[00324] Схемы синтеза
[00325] Указанное соединение согласно настоящему изобретению, имеющее Формулу I, Формулу IA или Формулу IB
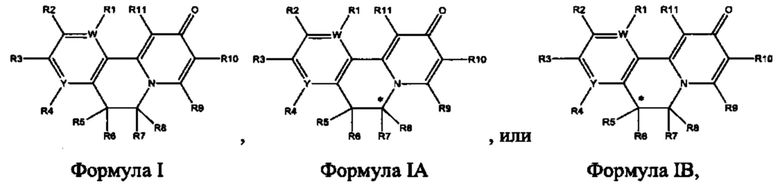
[00326] или его соответствующие фармацевтически приемлемые соли получают с использованием традиционных методов органического синтеза, при этом:
[00327] С* представляет собой стереоцентр при атоме углерода, который имеет конфигурацию (R) или (S);
[00328] W и Y независимо являются С или N, при условии, что W и Y оба не являются С;
при этом
[00329] если W является С, то R1 является водородом, гидрокси, галогеном, циано, амино или замещенным амино, тио или замещенным тио, алкилом или замещенным алкилом, алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; алкенилом или замещенным алкенилом; от 3- до 8-членным гетероциклоалкилом или замещенным от 3- до 8-членным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, пирролидинилом, -CxH2x-фенилом, -О-CxH2x-фенилом, или -(C1-6 алкил)N-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12; и
[00330] если Y является С, то R4 является водородом, гидрокси, галогеном, циано, амино или замещенным амино, тио или замещенным тио, алкилом или замещенным алкилом, алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; алкенилом или замещенным алкенилом; от 3- до 8-членным гетероциклоалкилом или замещенным от 3- до 8-членным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, пирролидинилом, -CxH2x-фенилом, -О-CxH2x-фенилом, или -(C1-6 алкилом)N-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12;
при этом
[00331] если W является N, то R1 отсутствует; и
[00332] если Y является N, то R4 отсутствует;
[00333] R2 и R3 независимо являются группой, выбранной из водорода, гидрокси, галогена, циано, амино или замещенного амино, тио или замещенного тио, алкила или замещенного алкила, алкокси или замещенного алкокси; циклоалкила или замещенного циклоалкила; алкенила или замещенного алкенила; от 3- до 8-членного гетероциклоалкила или замещенного от 3- до 8-членного гетероциклоалкила, арила или замещенного арила, гетероарила или замещенного гетероарила, пирролидинила, -CxH2x-фенила, -О-СхН2х-фенила, или -(C1-6 алкилом)N-СхН2х-фенила, при этом х равно 0, 1, 2, 3, 4, 5, 6; или -OR12;
[00334] R5 и R6 независимо являются водородом, гидрокси, галогеном, циано, амино алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом или замещенным арилом, -СхН2х-фенилом или -О-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00335] R7 и R8 независимо являются водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом; арилом или замещенным арилом, гетероарилом, -СхН2х-фенилом или -О-СхН2х-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00336] или R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', при этом указанное от 3- до 8-членное гетероциклоалкильное кольцо необязательно замещено R13, R13', R14 и/или R14';
[00337] или R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляет собой NR20 и указанные два или более гетероатомов выбраны из группы N, NR22, О, S, SR22 и SR22R22';
[00338] или R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R17', R18 и/или R18', при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00339] R9 является связью, водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, алкенилом или замещенным алкенилом, гетероциклоалкилом или замещенным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00340] R10 представляет собой заместитель, показанный в Таблице 2 или его таутомер;
[00341] или R9 представляет собой связь и R9 и R10 вместе образуют оксабороловое кольцо;
[00342] R11 является водородом, гидрокси, галогеном, циано, амино, алкилом или замещенным алкилом; алкенилом или замещенным алкенилом; алкокси или замещенным алкокси; циклоалкилом или замещенным циклоалкилом; гетероциклоалкилом или замещенным гетероциклоалкилом, арилом, гетероарилом, -CxH2x-фенилом или -О-CxH2x-фенилом, при этом х равно 0, 1, 2, 3, 4, 5 или 6;
[00343] R12 является водородом; алкилом или замещенным алкилом, алкокси или замещенным алкокси, циклоалкилом или замещенным циклоалкилом, гетероциклоалкилом или замещенным гетероциклоалкилом, арилом или замещенным арилом, гетероарилом или замещенным гетероарилом;
[00344] R13, R13', R14 и R14' независимо являются водородом, гидрокси, галогеном, амино, аминоалкилом, циано, С1-6 алкилом, C1-6 алкокси, карбонилом, карбоксамидом, амидом; или R13 и R13' или R14 и R14' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00345] R15, R15', R16 и R16' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6 алкилом, или C1-6 алкокси; или R15 и R15' или R16 и R16' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6 алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00346] R17, R17', R18 и R18' независимо являются водородом, гидрокси, галогеном, амино, циано, C1-6 алкилом, или C1-6 алкокси; или R17 и R18 или R17' и R18' вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное кислородом, галогеном, гидрокси, амино, циано, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом или C1-6алкокси, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22';
[00347] R19, R19' и R19'' независимо являются водородом, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом, C1-6 алкокси, фенилом, C1-6 алкилимидазолом, C1-6 алкилтриазолом, C1-6 алкилтетразолом, C1-6 алкилтиазолом, C1-6 алкилоксазолом, C1-6 алкилдиоксазолом; C1-6 алкилоксазолидоном; и
[00348] R20 и R21 независимо являются водородом, C1-6 алкилом, С3-8 циклоалкилом, С2-6 алкенилом, C1-6 алкокси, фенилом, C1-6 алкилимидазолом, C1-6 алкилтриазолом, C1-6 алкилтетразолом, C1-6 алкилтиазолом, C1-6 алкилоксазолом, C1-6 алкилдиоксазолом; C1-6 алкилоксазолидоном, или R20 и R21 вместе с азотом, к которому они присоединены, образуют незамещенный пирролидинил, незамещенный пиперидинил, или незамещенный морфолинил; или образуют карбоксил-замещенный пирролидинил, карбоксил-замещенный пиперидинил или карбоксил-замещенный морфолинил; и
[00349] R22 и R22' независимо являются группой, представленной водородом, кислородом, C1-6 алкилом или замещенным C1-6 алкилом, C1-6 алкокси или замещенным C1-6 алкокси, С3-8 циклоалкилом или замещенным С3-8 циклоалкилом, С2-6 алкенилом или замещенным С2-6 алкенилом, арилом или замещенным арилом, включая замещенный или незамещенный C1-6 алкилимидазол, замещенный или незамещенный C1-6 алкилтриазол, C1-6 алкилтетразол, C1-6 алкилтиазол, замещенный или незамещенный С1-6 алкилоксазол, C1-6 алкилдиоксазол; C1-6алкилоксазолидон; -COR19, -COOR19', -CSOR19'', -CONR20R21,
или его фармацевтически приемлемую соль.
[00350] В других вариантах осуществления представлены соединения Формулы I, Формулы IA или Формулы IB или их фармацевтически приемлемые соли, приведенные в настоящем описании, при этом:
[00351] R5 и R6 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22', при этом указанное от 3- до 8-членное гетероциклоалкильное кольцо необязательно замещено R13, R13', R14 и/или R14'.
[00352] Другие конкретные варианты осуществления настоящего изобретения обеспечивают соединения Формулы I, Формулы IA или Формулы IB или их фармацевтически приемлемые соли, приведенные в настоящем описании, при этом:
[00353] R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо или гетероциклоалкильное кольцо, содержащее один гетероатом или два или более гетероатомов, необязательно замещенное R15, R15', R16 и/или R16', при этом указанный один гетероатом в указанном гетероалкильном кольце представляется собой NR20 и указанные два или более гетероатомов выбраны из группы N, NR22, О, S, SR22 и SR22R22'.
[00354] Другие конкретные варианты осуществления настоящего изобретения обеспечивают соединения Формулы I, Формулы IA или Формулы IB или их фармацевтически приемлемые соли, приведенные в настоящем описании, при этом:
[00355] R7 и R8 вместе образуют от 3- до 8-членное циклоалкильное кольцо или от 3- до 8-членное гетероциклоалкильное кольцо, необязательно замещенное R17, R17', R18 и/или R18', при этом указанный гетероатом в указанном гетероциклоалкильном кольце представляет собой О, N, NR22, S, SR22 или SR22R22'.
[00356] Подходящие пути синтеза изображены ниже на следующих общих схемах реакций. Квалифицированный специалист поймет, что если описанный в настоящем документе заместитель несовместим с описанными методами синтеза, заместитель может быть защищен подходящей защитной группой, которая стабильна в условиях реакции. Защитная группа может быть удалена в подходящий момент в последовательности реакции с получением желаемого промежуточного соединения или целевого соединения. Подходящие защитные группы и способы защиты и снятия защиты различных заместителей с использованием таких подходящих защитных групп хорошо известны специалистам в данной области; их примеры можно найти в Т. Greene и P. Wuts, Protecting Groups in Chemical Synthesis (3-е изд.), John Wiley & Sons, NY (1999). В некоторых случаях заместитель может быть специально выбран так, чтобы он был реактивным в используемых условиях реакции. В этих условиях условия реакции превращают выбранный заместитель в другой заместитель, который либо полезен в качестве промежуточного соединения, либо является желаемым заместителем в целевом соединении.
[00357] Сокращения
[00358] При описании примеров химические элементы идентифицируются в соответствии с Периодической таблицей элементов. Аббревиатуры и символы, используемые в настоящем документе, соответствуют обычному использованию таких сокращений и символов специалистами в области химии. В данном документе используются следующие сокращения:
АсОН - уксусная кислота
AC2O - уксусный ангидрид
aq - водный
B4 - (S)-2-(((бензилокси)карбонилом)амино)-3-(4-(трифторметил)пиперидин-1-ил)пропановая кислота
ВОС (Boc) - N-трет-бутоксикарбонил или трет-бутилоксикарбонил
CBz - карбоксибензил
dba - дибензилиденацетон или дибензалацетон
DCE - дихлорэтан
DCM - дихлорметан
DCM/EA - дихлорметан/этанол
DDQ - 2,3-дихлор-5,6-дицианобензохинон
DIPEA (or DIEA) - N,N-диизопропилэтиламин, или Основание Хунига
DME - диметоксиэтан
DMEM - среда Игла в модификации Дульбекко
ДМФА - диметилформамид
DMP - периодинан Десса-Мартина
DMSO-d6 - дейтерированный диметилсульфоксид
DMSO - диметилсульфоксид
DPPA - дифенилфосфорилазид
ЕС50 - 50% эффективная концентрация
EDTA - этилендиаминтетрауксусная кислота
Et - этил
Et2O - диэтиловый эфир
EtOH - этанол
EtOAc, ЕА, AcOEt - этилацетат
GlutaMAX™ - дополнение к культуре клеток от Life Technologies
h - час(ы)
HEPES - 4-(2-гидроксиэтил)-1-пиперазинэтансульфоновая кислота
ВЭЖХ - высокоэффективная жидкостная хроматография
IC50 - 50% ингибирующая концентрация
iPrOH - изопропиловый спирт или изопропанол
LCMS - жидкостная хроматография - масс-спектроскопия
LDA - диизопропиламид лития
Me - метил
МеОН - метанол
NBS - N-бромсукцинимид
NCS - N-хлорсукцинимид
NIS - N-йодсукцинимид
NXS - N-галосукцинимид
NaBH(OAc)3 - триацетоксиборгидрид натрия
ЯМР - спектроскопия ядерного магнитного резонанса
Pd2(dba)3 - трис(дибензилиденацетон)дипалладий(0)
РЕ - петролейный эфир
PPh3 - трифенилфосфин
Pr - пропил
RB - круглодонная
rt или r.t. - комнатная температура
RT - время удерживания
SFC - жидкостная хроматография со сверхкритической фазой
SO3pyr - комплекс триоксида серы и пиридина формулы C5H5NSO3
SPhos - 2-дициклогексилфосфин-2',6'-диметоксибифенил или дициклогексил(2',6'-диметокси-[1,1'-бифенил]-2-ил)
t-BuOMe - метил-t-бутиловый эфир
Т3Р - раствор 1-пропанфосфонового ангидрида, 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфоринан-2,4,6-триоксид
TFA, ТФУ - трифторуксусная кислота
THF, ТГФ - тетрагидрофуран
УФ – ультрафиолет.
[00359] Если не указано иное, все исходные материалы были получены от коммерческих поставщиков и использовались без дополнительной очистки. Если не указано иное, все температуры выражены в °С (градусах Цельсия). Если не указано иное, все реакции проводили в инертной атмосфере при температуре окружающей среды.
[00360] Все температуры даны в градусах Цельсия, все растворители имеют наивысшую доступную чистоту и все реакции протекают в безводных условиях в атмосфере аргона (Ar) или азота (N2), если это необходимо.
[00361] Следующие ниже примеры иллюстрируют настоящее изобретение. Эти примеры не предназначены для ограничения объема настоящего изобретения, а скорее служат руководством для квалифицированного специалиста по приготовлению и использованию указанного соединения, композиций и способов согласно настоящему изобретению.
[00362] Хотя описаны конкретные варианты осуществления настоящего изобретения, квалифицированный специалист поймет, что различные изменения и модификации могут быть сделаны без отклонения от сущности и объема настоящего изобретения.
[00363] [00363] Используемые в настоящем документе символы и условные обозначения, используемые в процессах, схемах и примерах, соответствуют тем, которые используются в современной научной литературе, например, в Журнале американского химического общества (Journal of the American Chemical Society) или Журнале биологической химии (Journal of Biological Chemistry). Если не указано иное, все исходные материалы были получены от коммерческих поставщиков и использовались без дополнительной очистки.
[00364] Все ссылки на простой эфир относятся к диэтиловому эфиру; солевой раствор относится к насыщенному водному раствору NaCl. Если не указано иное, все температуры выражены в °С (градусах Цельсия). Все реакции проводят в инертной атмосфере при комнатной температуре, если не указано иное, и все растворители имеют самую высокую доступную чистоту, если не указано иное.
[00365] Спектры 1Н ЯМР (далее также "ЯМР") регистрировали на спектрометре Varian Unity-400. Химические сдвиги выражаются в частях на миллион (ppm, единицах δ). Константы взаимодействия выражены в герцах (Гц). Паттерны расщепления описывают кажущиеся множественности и обозначаются как s (синглет), d (дублет), t (триплет), q (квартет), quint (квинтет), m (мультиплет), br (широкий).
[00366] Жидкостную хроматографию проводили на Merck Силикагель 60 (230-400 меш) или на Teledyne Isco Combiflash® Companion с одноразовыми флэш-колонками Redi-Sep® с нормальной фазой. Масс-спектры снимали в системе LC-MS открытого доступа с ионизацией электрораспылением. Аналитические масс-спектры низкого разрешения (МС) записывали на приборе Waters SQD. Анализ UPLC проводили на колонке Phenomenex® Kinetex® 1,7 мкм, 2,1×50 мм ХВ-С18 при 40CSQ с использованием метода градиентного элюирования. Растворитель А: 0,2% муравьиной кислоты (МК) в воде; растворитель В: 0,15% МК в ацетонитриле; градиент 1% - 99% растворителя В за 1,1 минуты и постоянное удержание при 99% растворителя В еще 0,4 минуты при скорости потока 1 мл/мин.
[00367] Получение соединений посредством синтеза
[00368] Общие протоколы получения соединений, приведенных в настоящем описании, показаны ниже на Схемах 1-15.
[00369] Схема 1
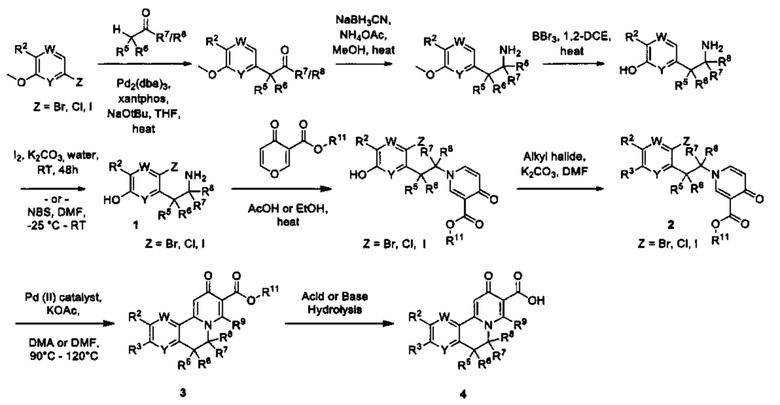
Обозначения: heat - нагревание, water - вода, catalyst - катализатор, acid or base hydrolysis - кислотный или щелочной гидролиз.
[00370] Конкретные соединения, описанные в настоящем документе, могут быть получены в соответствии со Схемой 1. Например, соединение 4 может быть получено посредством введения в реакцию соединения 1 с соответствующим образом замещенным 4-пираноном, как показано, в уксусной кислоте или этаноле, при нагревании. Восстановительная циклизация соединения 2 посредством обработки соединения 2 с катализатором Pd(II) с подходящим основанием, таким как ацетат калия, в подходящем растворителе, таком как N,N-диметилацетамид (DMA) или N,N-диметилформамид (ДМФА) при 90-120°С, приводит к образованию конденсированного трициклического карбоксилатного соединения 3. Соединение 3 затем подвергают гидролизу эфирной связи в кислых или основных условиях с образованием карбоксиловой кислоты 4. Дальнейшие химические манипуляции с указанной карбоксиловой кислотой могут привести к введению дополнительных групп R10.
[00371] В качестве альтернативы, соединения, описанные в настоящем документе, могут быть получены в соответствии со Схемой 2.
[00372] Схема 2
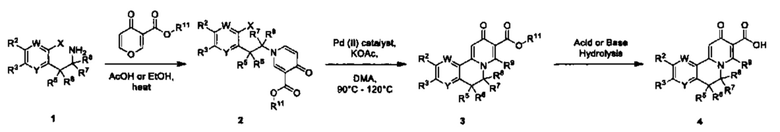
где X представляет собой Br или I, а W, Y, R5, R6, R7 и R8 - как указано в настоящем документе.
Обозначения: heat - нагревание, catalyst - катализатор, acid or base hydrolysis - кислотный или щелочной гидролиз.
[00373] Как показано на Схеме 2, соединение 2 может быть получено посредством введения в реакцию соединения 1 с соответствующим образом замещенным 4-пираноном, как показано, в уксусной кислоте или этанола, при нагревании. Восстановительная циклизация соединения 2 посредством обработки соединения 2 с катализатором Pd(II) с подходящим основанием, таким как ацетат калия в подходящем растворителе, таком как N,N-диметилацетамид (DMA) или N,N-диметилформамид (ДМФА) при 90-120°С, приводит к образованию конденсированного трициклического карбоксилатного соединения 3. Соединение 3 затем подвергают гидролизу эфирной связи в кислых или основных условиях с образованием указанной карбоксиловой кислоты 4. Также как в Схеме 1, дальнейшие химические манипуляции с указанной карбоксиловой кислотой могут привести к введению дополнительных групп R10.
[00374] Схема 3 С получением соединения Примера 1 (Соединение 220)
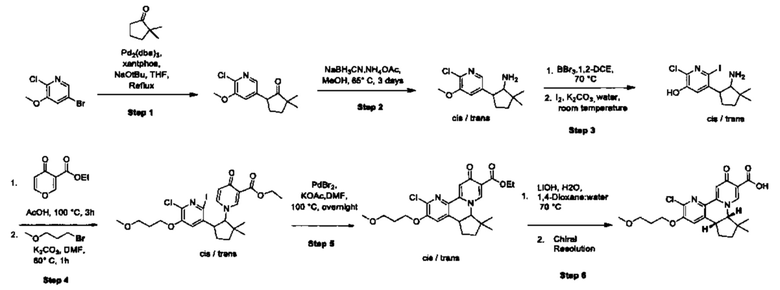
Обозначения: reflux - нагревание с обратным холодильником, water - вода, room temperature - комнатная температура, cis/trans - цис/транс, overnight - в течение ночи, dioxane - диоксан, chiral resolution - хиральное разделение.
[00375] Пример 1. Получение А (Соединение 220)
[00376] (4bR,7aS)-2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,71нафтиридин-10-карбоксиловая кислота
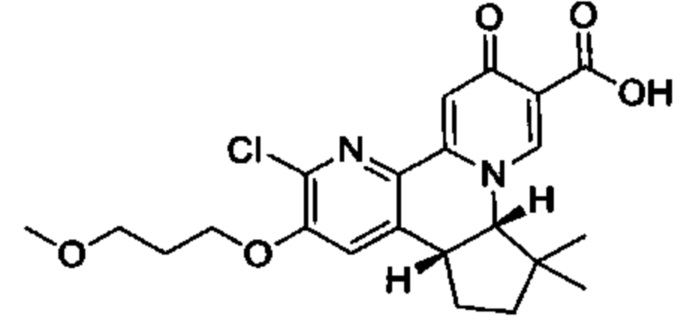
[00377] Стадия 1: 5-(6-Хлор-5-метоксипиридин-3-ил)-2,2-диметилцикло-пентанон
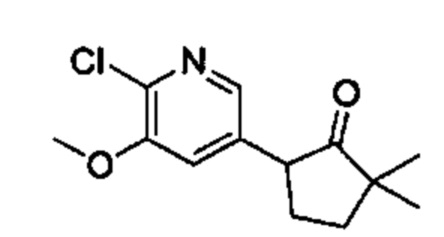
[00378] В колбу помещали мешалку, 5-бром-2-хлор-3-метоксипиридин (16,5 г, 74,2 ммоль), трис(дибензилиденацетон)дипалладий(0) (1,02 г, 1,11 ммоль), ксантфос (1,16 г, 2,00 ммоль), и трет-бутоксид натрия (12,6 г, 131 ммоль). Указанную колбу продували потоком азота в течение 30 минут. Тетрагидрофуран (ТГФ) (300 мл) дегазировали азотом в течение 30 минут. 2,2-диметилциклопентан-1-он (11,2 мл, 89 ммоль) добавляли к указанному дегазированному тетрагидрофурану (ТГФ) (300 мл) и этот раствор добавляли в указанную колбу, продутую азотом, содержащую исходное соединение. Указанную смесь нагревали с обратным холодильником в атмосфере азота в течение 3 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и отфильтровывали через кремниевую пробку в атмосфере азота. Указанную пробку промывали тетрагидрофураном и полученный фильтрат концентрировали. Полученный осадок растворяли в минимальном количестве дихлорметана и вводили в колонку с диоксидом кремния. Указанную колонку элюировали 1 минуту гексанами, а затем быстрым градиентом (3 минуты) до 20% этилацетат/гексаны, а затем изократически 20% этилацетат/гексаны до элюции продукта. Фракции концентрировали и получали 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-он (10,7 г, 42,1 ммоль, 56,8% выход) в виде масла. LCMS (ESI) m/z 254,2 (М+1).
[00379] Стадия 2: 5-(6-Хлор-5-метоксипиридин-3 -ил)-2,2-диметилциклопентанамин (смесь цис/транс)
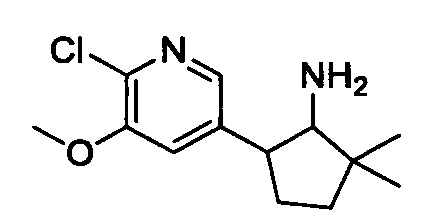
[00380] Перемешиваемую смесь 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-она (смесь цис/транс) (10,7 г, 42,2 ммоль) и ацетата аммония (32,5 г, 422 ммоль) в метаноле (200 мл) дегазировали потоком азота в течение 25 минут. Цианоборгидрид натрия (5,30 г, 84 ммоль) добавляли и указанную смесь нагревали при 65°С в течение выходных. Обратный холодильник удаляли и масляную баню грели при 80°С, до концентрации указанной реакционной смеси до ~70% от начального объема в течение 4 часов. Обратный холодильник присоединяли обратно и указанную смесь сильно нагревали с обратным холодильником в течение ночи (масляная баня при 80°С). Указанную смесь концентрировали и полученный осадок суспендировали в ~300 мл дихлорметана. Указанную смесь энергично взбалтывали в течение ~30 минут. Твердую фракцию отфильтровывали и осадок на фильтре промывали дихлорметаном. Полученный фильтрат концентрировали и получали 22 г неочищенного 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-амина (смесь цис/транс). Указанный неочищенный материал очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 10% 2М аммиак/метанол в дихлорметане. Фракции концентрировали и получали 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-амин (смесь цис/транс) (9,04 г, 35,5 ммоль, 84% выход). LCMS (ESI) m/z 255,2 (М+1).
[00381] Стадия 3: 5-(2-Амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ол (смесь цис/транс)
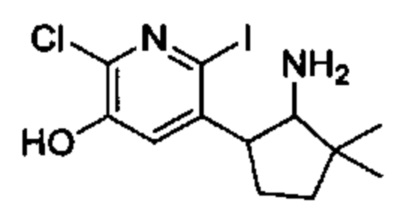
[00382] Трибромид бора (6,71 мл, 71,0 ммоль) медленно добавляли по каплям к энергично перемешиваемому раствору 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-амина (смесь цис/транс) (9,04 г, 35,5 ммоль) в 1,2-дихлорэтане (DCE) (175 мл). Указанную смесь взбалтывали при комнатной температуре в течение 30 минут, а затем нагревали при 70°С в течение ночи. Указанную смесь охлаждали в ледяной бане, а затем осторожно гасили медленным добавлением метанола. Добавляли дополнительный метанол (100 мл). Указанную смесь нагревали до комнатной температуры, перемешивали в течение 30 минут, и концентрировали с получением ~17 г неочищенного 5-(2-амино-3,3-диметилциклопентил)-2-хлорпиридин-3-ола (смесь цис/транс). К указанному неочищенному материалу добавляли воду (200 мл) и перемешивали с мешалкой. Карбонат калия (24,5 г, 177 ммоль) добавляли порциями медленно и осторожно для того, чтобы контролировать вспенивание. Указанную смесь взбалтывали в течение 10 минут после полного добавления карбоната калия. Указанную водную смесь проверяли рН-бумажкой, чтобы убедиться, что указанная смесь была щелочной. Указанную водную смесь экстрагировали 1 раз 100 мл дихлорметана. LC-MS выявила примеси только в органической фазе и только 5-(2-амино-3,3-диметилциклопентил)-2-хлоргшридин-3-ол (смесь цис/транс) в водной фазе. Указанную органическую фазу выбрасывали и указанную водную фазу переносили из делительной воронки в круглодонную колбу перед добавлением йода (18,0 г, 71,0 ммоль). Указанную смесь взбалтывали в течение ночи при комнатной температуре. Избыток сульфата натрия (~4 экв.) добавляли порциями. 2-Метилтетрагидрофуран (100 мл) добавляли и указанную смесь перемешивали. Избыток уксусной кислоты осторожно добавляли, чтобы нейтрализовать указанную водную фазу, контролируя вспенивание. К указанной водной фазе добавляли твердый хлорид натрия. Указанную смесь экстрагировали 3 раза 2-метилтетрагидрофураном. Объединенные органические фазы промывали 2 раза солевым раствором. Указанную органическую фазу осушали над сульфатом натрия, концентрировали и получали 12,6 г неочищенного материала. Указанный материал очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 20% 2М аммиак/метанол в дихлорметане. Фракции концентрировали и получали 5-(2-амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ол (смесь цис/транс) (6,6 г, 18 ммоль, 50,7% выход). LCMS (ESI) m/z 367,1 (М+1).
[00383] Стадия 4: Этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (смесь цис/транс)
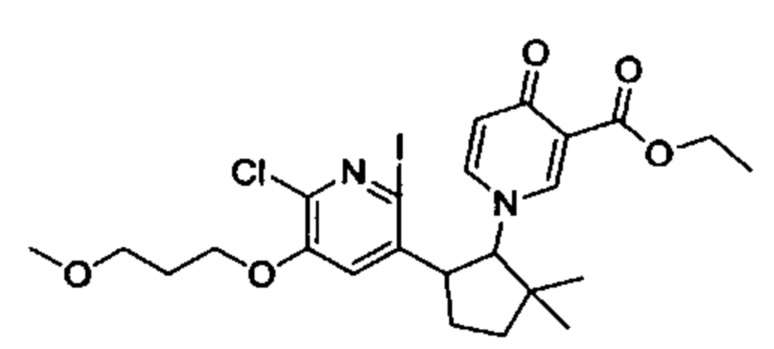
[00384] 5-(2-Амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ол (смесь цис/транс) (6,6 г, 18 ммоль) и этил-4-оксо-4Н-пиран-3-карбоксилат (3,94 г, 23,4 ммоль) в уксусной кислоте (150 мл) перемешивали при 100°С в течение 3 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и концентрировали досуха под вакуумом. Толуол добавляли и упаривали на роторе несколько раз, чтобы избавиться от остатков уксусной кислоты. Финальное упаривание дало неочищенный этил-1-(5-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат. LCMS (ESI) m/z 517,1 (М+1). Неочищенный этил-1-(5-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат растворяли в N,N-диметилформамиде (ДМФА) (75 мл) перед добавлением карбоната калия (12,4 г, 90 ммоль) и 1-бром-3-метоксипропана (4,05 мл, 36,0 ммоль). Указанную смесь оставляли перемешиваться при комнатной температуре в течение 15 минут, а затем нагревали при 60°С в течение 1 часа. Полученную реакционную смесь охлаждали в ледяной бане и гасили водой. Твердую фазу осаждали. Указанную смесь экстрагировали 3 раза этил ацетатом. Твердые компоненты плавали на границе раздела фаз и указанную смесь экстрагировали 1 раз дихлорметаном. Твердую фракцию растворяли и продукт обнаруживали в указанной органической фазе. Объединенные органические фазы промывали 2 раза 5% хлоридом лития, промывали 1 раз солевым раствором, осушали над сульфатом натрия, и концентрировали. Полученный осадок суспендировали в этиловом эфире и указанный осадок собирали фильтрацией. Указанный осадок сушили на воздухе и получали этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (рацемат транс) (5,21 г, 8,85 ммоль, 49,1% выход) в виде бледно-коричневого твердого вещества. LCMS (ESI) m/z 589,2 (М+1). Полученный фильтрат концентрировали и полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 10% метанола в дихлорметане. Фракции концентрировали и получали этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (смесь цис/транс) (2,59 г, 3,08 ммоль, 17,1% выход, 70% чистота). LCMS (ESI) m/z 589,2 (М+1).
[00385] Стадия 5: Этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксилат (смесь цис/транс)
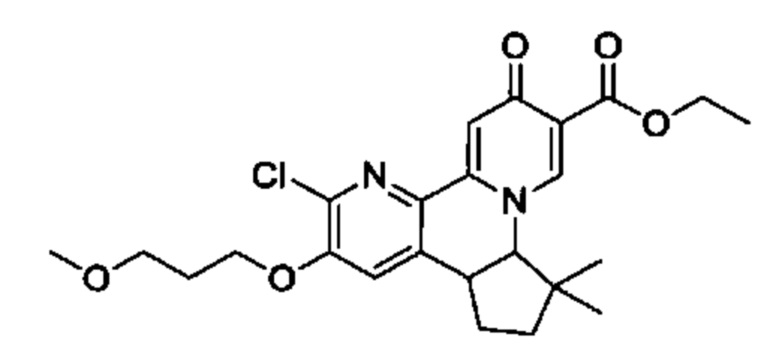
[00386] Круглодонную колбу, содержащую мешалку, этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (смесь цис/транс) (5,57 г, 9,46 ммоль), ацетат калия (4,64 г, 47,3 ммоль), и бромид палладия (II) (0,504 г, 1,89 ммоль) продували азотом в течение 20 минут с использованием мембраны с вдвигаемой и выдвигаемой иглой. N,N-Диметилформамид (ДМФА) (75 мл) продували азотом в течение 20 минут перед добавлением в колбу с реакционной смесью. Указанную колбу с реакционной смесью помещали в масляную баню, предварительно нагретую до 100°С, и указанную смесь перемешивали в течение ночи. Указанную смесь оставляли охлаждаться до комнатной температуры и отфильтровывали через целитовую прокладку. Указанную целитовую прокладку промывали дихлорметаном и полученный фильтрат концентрировали. Полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 10% метанола в дихлорметане. Фракции концентрировали и получали этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксилат (смесь цис/транс) (3,15 г, 6,83 ммоль, 72,2% выход) в виде бледно-коричневого твердого вещества. LCMS (ESI) m/z 461,3 (М+1).
[00387] Стадия 6: (4bR,7aS)-2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
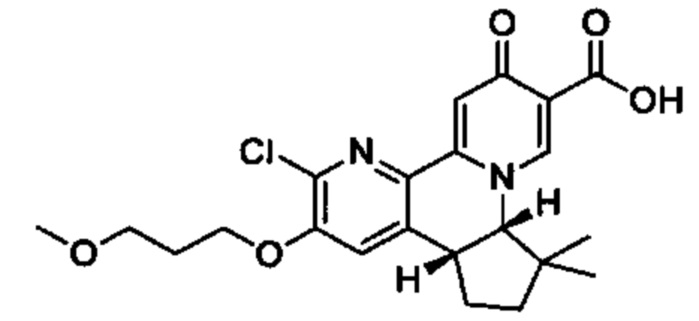
[00388] К раствору этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксилата (смесь цис/транс) (3,15 г, 6,83 ммоль) в 1,4-диоксане (40 мл) добавляли раствор моногидрата гидроксида лития (1,434 г, 34,2 ммоль) в воде (30 мл). Указанную смесь нагревали при 70°С в течение 3 часов. LC-MS показала полное превращение в желаемый рацемический цис продукт. Указанную смесь оставляли охлаждаться до комнатной температуры и разбавляли 0,5М соляной кислотой (100 мл). Указанный осадок собирали фильтрацией и осадок на фильтре тщательно промывали водой. Осадок на фильтре сушили на воздухе в течение нескольких часов с использованием вакуума на воронке Бюхнера до тех пор, пока твердая фракция не содержала влагу при визуальном осмотре. Осадок на фильтре растворяли в 150 мл дихлорметана. Для полного растворения требовалось перемешивание в течение нескольких минут. Указанный раствор осушали над сульфатом натрия, концентрировали и получали 2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (рацемат цис) (2,6 г, 6,01 ммоль, 88% выход).
[00389] Указанный рацемат очищали в несколько приемов с использованием следующих условий: Колонка = Chiralpak IC, 10 мм × 250 мм (5u); Подвижная фаза = 3:1 МеОН/EtOH+0,1% ТФУ; Скорость потока = 10 мл/мин; Объем инъекции = 500 мкл (концентрация 30 мг/мл, DCM использовали в качестве растворителя для инъекции); Длина волны детекции = 254 нм. Фракции, соответствующие пику 1, концентрировали. Полученные осадки суспендировали в этиловом эфире, обрабатывали ультразвуком, перемешивали в течение 10 минут, а затем указанную перемешиваемую смесь охлаждали в ледяной бане. Твердую фракцию собирали с помощью вакуумной фильтрации, сушили на воздухе, и осушали под глубоким вакуумом и получали (4bR,7aS)-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (1,24 г, 2,87 ммоль, 42% выход) в виде белой твердой фракции. LCMS (ESI) m/z 433,2 (М+1). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,62 (s, 1 H), 7,63 (s, 1 H), 7,43 (s, 1 H), 4,72 (d, J=8,98 Hz, 1 H), 4,19-4,39 (m, 2 H), 3,94 (td, J=8,68, 3,32 Hz, 1 H), 3,51 (t, J=6,05 Hz, 2 H), 3,26 (s, 3 H), 2,35-2,46 (m, 1 H), 2,19-2,31 (m, 1 H), 2,03 (quin, J=6,25 Hz, 2 H), 1,55-1,67 (m, 1 H), 1,40-1,50 (m, 1 H), 1,15 (s, 3 H), 0,40 (s, 3 H).
Схема 4 - Альтернативный синтез Соединения 220. Пример 1
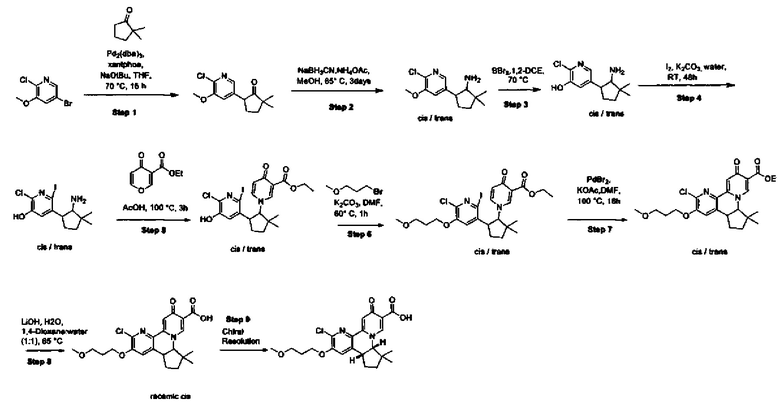
Обозначения: step - стадия, water - вода, cis/trans - цис/транс, chiral resolution - хиральное разделение.
[00390] Пример 1 Получение В (Соединение 220)
[00391] (4bR,7aS)-2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
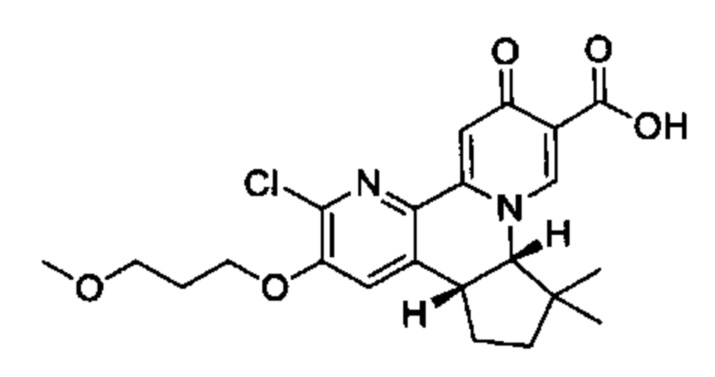
[00392] Стадия 1: 5-(6-Хлор-5-метоксипиридин-3-ил)-2,2-диметилдиклопентан-1-он
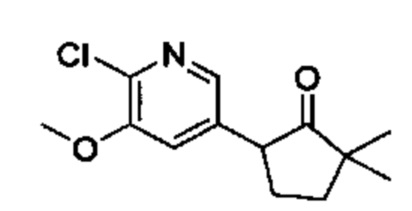
[00393] К раствору 5-бром-2-хлор-3-метоксипиридина (100 г, 449 ммоль) в ТГФ (2 L) добавляли NaOtBu (76,02 г, 791 ммоль), ксантфос (7,01 г, 12,1 ммоль) и 2,2-диметилциклопентан-1-он (65,56 г, 584,6 ммоль). Полученную реакционную смесь дегазировали азотом в течение 30 минут. Pd2(aba)3 добавляли к указанной реакционной смеси и полученную реакционную смесь взбалтывали при 70°С в течение 3 ч. После завершения реакции, полученную реакционную смесь отфильтровывали через подушку силикагеля (60-120) и промывали ТГФ. Указанный растворитель удаляли при пониженном давлении и указанный неочищенный продукт очищали с использованием хроматографической колонки (230-400 силикагель) с использованием 0-30% этилацетата в петролейном эфире в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии, (61 г, 54% выход), LCMS (ESI) m/z 253,9 (М+1).
[00394] Стадия 2: 5-(6-Хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-амин (смесь цис/транс)
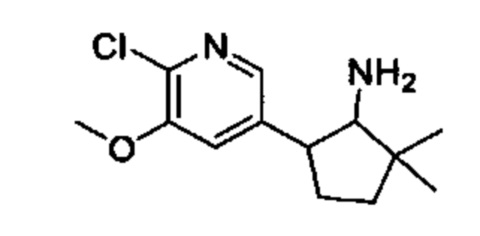
[00395] К раствору 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-она (60 г, 236,5 ммоль) в метаноле (1,2 L) добавляли NH4OAc (182 г, 2365 ммоль). Полученную реакционную смесь дегазировали азотом в течение 30 минут. К полученной реакционной смеси добавляли NaBH3CN (29,7 г, 473 ммоль) и полученную реакционную смесь взбалтывали при 65°С в течение 3 суток. После завершения реакции, указанный растворитель удаляли при пониженном давлении с получением неочищенного соединения, указанного в названии, (55 г). LCMS (ESI) m/z: 255,7(М+1). Указанное соединение использовали на следующей стадии без дальнейшей очистки.
[00396] Стадия 3: Получение 5-(2-амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ола (смесь цис/транс)
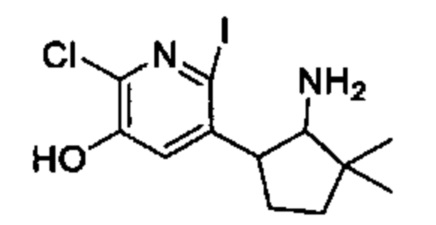
[00397] К раствору 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-амина (60 г, 236 ммоль) в 1,2-дихлорэтане (DCE) (1300 мл) добавляли BBr3 (22,27 мл, 236 ммоль) и полученную реакционную смесь взбалтывали при 70°С в течение 16 ч. После завершения реакции, метанол (1,5 л) добавляли к реакционной смеси медленно по каплям при 0°С и перемешивали при комнатной температуре в течение 30 минут. Полученную реакционную смесь концентрировали и полученный осадок помещали в воду (1 л) и доводили рН до щелочного значения с использованием карбоната калия (325 г, 2355 ммоль). Указанную водную фазу промывали DCM (200 мл). К указанной водной фазе добавляли йод (120 г, 471 ммоль) и перемешивали при комнатной температуре в течение 16 ч. После завершения реакции, добавляли сульфат натрия (200 г) чтобы нейтрализовать избыток йода. Добавляли уксусную кислоту (250 мл) и экстрагировали 2-метил-ТГФ (2×1 л). Указанную органическую фазу отделяли и осушали над сульфатом натрия. Указанный растворитель удаляли при пониженном давлении и указанный неочищенный продукт перетирали с 20% дихлорметаном в гексане (2 × 600 мл). Полученную твердую фазу отфильтровывали и осушали с получением соединения, указанного в названии (35 г, выход 21,89%). LCMS (54%) (ESI) m/z: 367 (М+1).
[00398] Стадия 4: Этил-1-(5-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-2,2-диметилвдклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (смесь цис/транс)
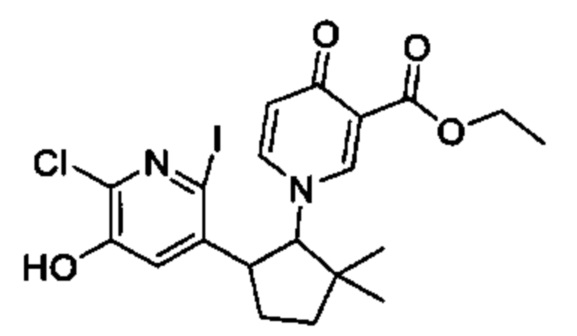
[00399] Суспензию 5-(2-амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ола (87 г, 237 ммоль), этил-4-оксо-4Н-пиран-3-карбоксилата (45,9 г, 273 ммоль) и уксусной кислоты (1,8 L) взбалтывали при 100°С в течение 3 ч. После завершения реакции полученную реакционную смесь концентрировали и совместно упаривали с толуолом (4 × 200 мл). Полученный осадок очищали с использованием хроматографической колонки (230-400 силикагель) с использованием 10~15% МеОН в DCM в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии, (51 г, 22% выход) в виде темно-коричневого твердого вещества. LCMS (53%) (ESI) m/z: 517 (М+1).
[00400] Стадия 5: Этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-оксо-1,4-дигидропиридин-3-карбоксилат (смесь цис/транс)
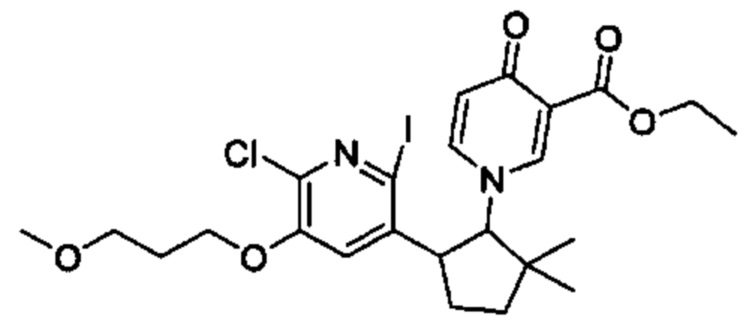
[00401] К раствору этил-1-(5-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилата (51 г, 99 ммоль) в N,N-диметилформамиде (580 мл) добавляли К2СО3 (68,2 г, 493 ммоль) и 1-бром-3-метоксипропан (30,2 г, 197 ммоль). Полученную реакционную смесь взбалтывали при 60°С в течение 1 ч. После завершения реакции полученную реакционную смесь гасили ледяной водой (1500 мл) и экстрагировали DCM (2 L). Объединенные органические фазы промывали солевым раствором (500 мл), осушали над Na2SO4 и концентрировали. Неочищенное вещество очищали с использованием хроматографической колонки (230-400 силикагель) с использованием 0~10% метанола в DCM в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии (52 г, 84% выход). LCMS (ESI) m/z: 588,8 (М+1).
Стадия 6: Этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-][1,7]нафтиридин-10-карбоксилат (смесь цис/транс)
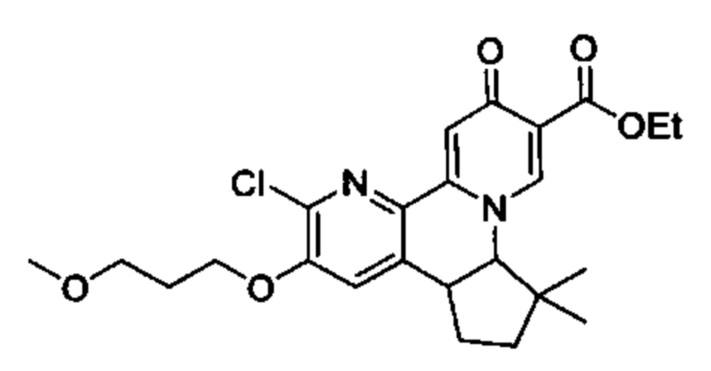
[00402] К раствору этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилата (52 г, 88 ммоль) в N,N-диметилформамиде (550 мл) добавляли ацетат калия (43,3 г, 442 ммоль). Полученную реакционную смесь дегазировали азотом в течение 20 минут. Бромид палладия (II) (4,70 г, 17,66 ммоль) добавляли к полученной реакционной смеси и полученную реакционную смесь взбалтывали при 100°С в течение 16 ч. После завершения реакции полученную реакционную смесь отфильтровывали через целит и промывали DCM. Указанную органическую фазу промывали водой (250 мл), осушали над Na2SO4 и концентрировали. Неочищенное вещество очищали с использованием хроматографической колонки (230-400 силикагель) с использованием 2~5% МеОН в DCM в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии (20 г, 42% выход). LCMS (ESI) m/z: 461,1 (М+1).
[00403] Стадия 7: (4bR,7aS)-2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
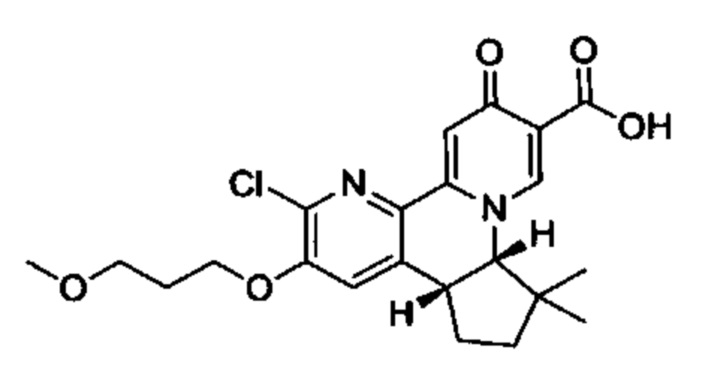
[00404] К раствору этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7] нафтиридин-10-карбоксилата (17,5 г, 38 ммоль) в 1,4-диоксане (150 мл) и воде (150 мл) добавляли гидроксид лития (7,9 г, 190,14 ммоль). Полученную реакционную смесь нагревали до 70°С в течение 2 ч. После завершения реакции полученную реакционную смесь концентрировали и полученный осадок переносили в DCM (250 мл). К этой смеси добавляли 1,5 N HCl до тех пор, пока не установился рН=6. Указанную органическую фазу отделяли и осушали над Na2SO4 и концентрировали с получением 15 г (выход: 91%) рацемической смеси. Эту рацемическую смесь очищали с помощью препаративной ВЭЖХ с получением соединения, указанного в названии, (5,5 г, 73% выход) в виде бледно-желтого твердого вещества. Метод хиральной ВЭЖХ: Chiralpak IC (21*250), 5 mics, Подвижная фаза А: 0,1% ТФУ в метаноле, В: 0,1% ТФУ в этаноле; А: В:75:25, Скорость потока: 2 5 мл/мин. Время удерживания первого пика: 5,4. 1Н ЯМР 400 MHz, DMSO-d6: δ 8,62 (s, 1Н), 7,63 (s, 1H), 7,43 (s, 1H), 4,73 (d, J=8,96 Hz, 1H), 4,33-4,28 (m, 2H), 3,95-3,94 (m, 1H), 3,53-3,50 (m, 2H), 3,27 (s, 3H), 2,39-2,38 (m, 1H), 2,28-2,27 (m, 1H), 2,04-2,01 (m, 2H), 1,61-1,60 (m, 1H), 1,47-1,44 (m, 1H), 1,15 (s, 3H), 0,40 (s, 3H). LCMS (ESI) m/z: 432,9 (M+1).
[00405] Пример 2 (Соединение 221)
[00406] (4bS,7aR)-2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
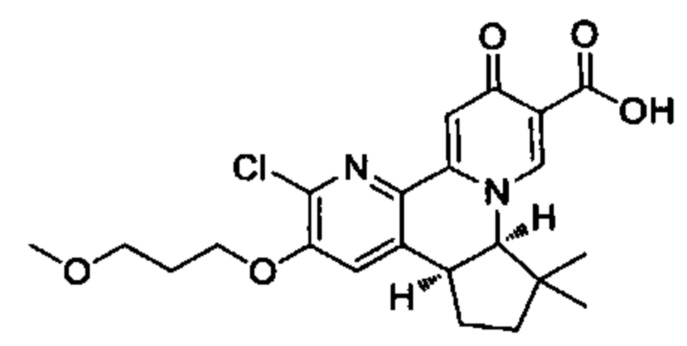
[00407] Стадия 1: (4bS,7aR)-2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
[00408] 2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагадроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (рацемат цис) (500 мг) очищали с помощью хиральной хроматографии. Колонка = Chiralpak IC, 10 мм × 250 мм (5и), Подвижная фаза = 3:1 МеОН/EtOH + 0,1% ТФУ, Скорость потока=10 мл/мин, Объем инъекции = 500 мкл (30 мг/мл концентрация); DCM использовали в качестве растворителя для инъекции, длина волны детекции = 254 нм. Пик 2 концентрировали и получали (4bS,7aR)-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (190 мг, 0,438 ммоль, 38% выход) в виде белого твердого вещества. LCMS (EST) m/z 433,3 (М+1). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,59 (s, 1 H), 7,60 (s, 1 H), 7,40 (s, 1 H), 4,69 (d, J=8,98 Hz, 1 H), 4,18-4,36 (m, 2 H), 3,84-3,96 (m, 1 H), 3,48 (t, J=6,25 Hz, 2 H), 3,23 (s, 3 H), 2,30-2,43 (m, 1 H), 2,18-2,28 (m, 1 H), 2,00 (quin, J=6,15 Hz, 2 H), 1,53-1,64 (m, 1 H), 1,37-1,48 (m, 1 H), 1,12 (s, 3 H), 0,37 (s, 3 H).
[00409] Пример 3: (Соединение 222)
[00410] (4bR,7aS)-2-Циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1.2-h][1,7]нафтиридин-10-карбоксиловая кислота
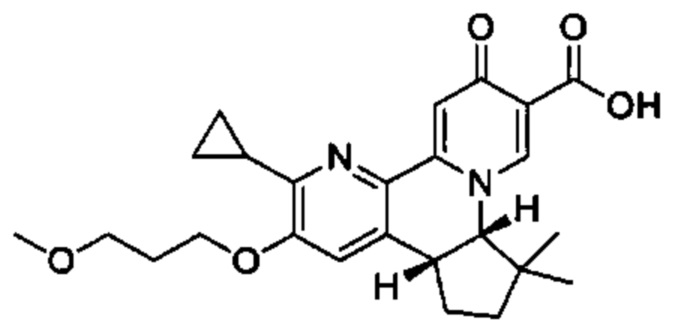
[00411] Стадия 1: (4bR,7aS)-2-Циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагадроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
[00412] Реакционную виалу, содержащую мешалку, (4bR,7aS)-2-xnop-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (81 мг, 0,19 ммоль), карбонат калия (103 мг, 0,748 ммоль), циклопропилборную кислоту (32,1 мг, 0,374 ммоль) и тетракис(трифенилфосфин)палладий(0) (43,2 мг, 0,037 ммоль) тщательно продували потоком азота (вдвигаемая/выдвигаемая игла). Добавляли 1,4-диоксан (2 мл) и указанную реакционную виалу помещали в нагревательный блок, предварительно нагретый до 100°С. Указанную смесь нагревали при 100°С в течение ночи. Полученную реакционную смесь оставляли охлаждаться до комнатной температуры, а затем разбавляли 2-метилтетрагидрофураном и водой. Уксусную кислоту добавляли медленно и осторожно (из-за вспенивания) до тех пор, пока Указанную водную фазу не была нейтрализована. Указанную смесь экстрагировали 2 раза 2-метилтетрагидрофураном. Объединенные органические фазы промывали солевым раствором и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции комбинировали и концентрировали до тех пор, пока не образовался белый осадок. Добавляли небольшое количество ацетонитрила и указанный раствор становился прозрачным. Указанный раствор лиофилизировали и получали (4bR,7aS)-2-циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (67 мг, 0,151 ммоль, 81% выход) в виде белого порошка. LCMS (ESI) m/z 439,1 (М+1). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,54 (s, 1 Н), 7,46 (s, 1 Н), 7,31 (s, 1 Н), 4,64 (d, J=8,98 Hz, 1 H), 4,08-4,33 (m, 2 H), 3,79-3,91 (m, 1 H), 3,50 (t, J=6,25 Hz, 2 H), 3,24 (s, 3 H), 2,39-2,45 (m, 1 Н), 2,16-2,38 (m, 2 Н), 2,01 (quin, J=6,15 Hz, 2 H), 1,51-1,63 (m, 1 H), 1,32-1,45 (m, 1 H), 1,12 (s, 3 H), 0,92-1,05 (m, 4 H), 0,34 (s, 3 H).
[00413] Пример 4: (Соединение 223)
[00414] 2-Циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота (рацемат цис)
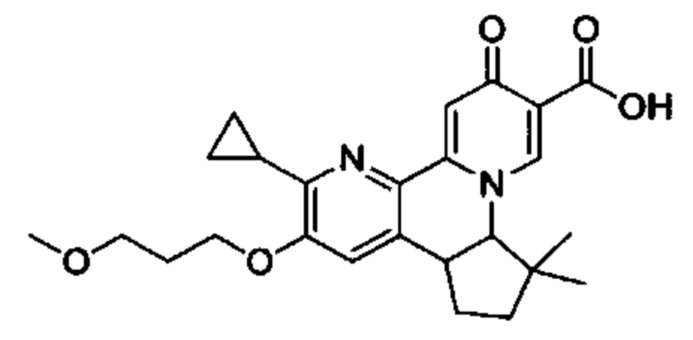
[00415] Стадия 1: 2-Циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексатдроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота (рацемат цис)
[00416] Реакционную виалу, содержащую мешалку, этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-b][1,7]нафтиридин-10-карбоксилат (рацемат цис) (200 мг, 0,434 ммоль), карбонат калия (240 мг, 1,74 ммоль), циклопропилборную кислоту (74,5 мг, 0,868 ммоль), и тетракис(трифенилфосфин)палладий(0) (100 мг, 0,087 ммоль) тщательно продували потоком азота (вдвигаемая/выдвигаемая игла). Добавляли 1,4-диоксан (4 мл) и указанную реакционную виалу помещали нагревательный блок, предварительно нагретый до 100°С. Указанную смесь нагревали при 100°С в течение 3 часов. Дополнительно добавляли циклопропилборную кислоту (74,5 мг, 0,868 ммоль) и тетракис(трифенилфосфин)палладий(0) (100 мг, 0,087 ммоль) и указанную смесь продолжали нагревать при 100°С в течение 2 часов. Указанную смесь оставляли охлаждаться и отфильтровывали через целитную заглушку. Указанную целитную заглушку промывали этилацетатом. Полученный фильтрат концентрировали и получали неочищенный этил-2-циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксилат. Неочищенное промежуточное вещество растворяли в метаноле (2 мл) перед тем, как добавляли раствор моногидрата гидроксида лития (182 мг, 4,34 ммоль) в воде (2 мл). Указанную смесь нагревали при 60°С в течение 3 часов и охлаждали до комнатной температуры. Указанную смесь очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали 2-циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]-пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (рацемат цис) (50 мг, 0,114 ммоль, 26,3% выход) в виде бледно-коричневого порошка. LCMS (ESI) m/z 439,3 (М+1). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,54 (s, 1 H), 7,46 (s, 1 H), 7,31 (s, 1 H), 4,64 (d, J=8,98 Hz, 1 H), 4,11-4,28 (m, 2 H), 3,79-3,91 (m, 1 H), 3,50 (t, J=6,25 Hz, 2 H), 3,24 (s, 3 H), 2,39-2,45 (m, 1 H), 2,16-2,38 (m, 2 H), 1,96-2,04 (m, 2 H), 1,51-1,64 (m, 1 H), 1,34-1,44 (m, 1 H), 1,12 (s, 3 H), 0,93-1,06 (m, 4 H), 0,34 (s, 3 H).
[00417] Схема 5 - Получение соединений, таких как Пример 5
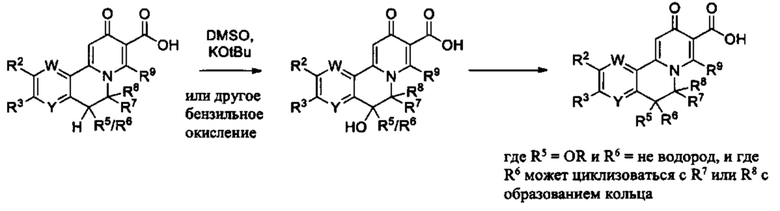
[00418] Пример 5: (Соединение 224)
[00419] (7aR)-2-Циклопропил-4b-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
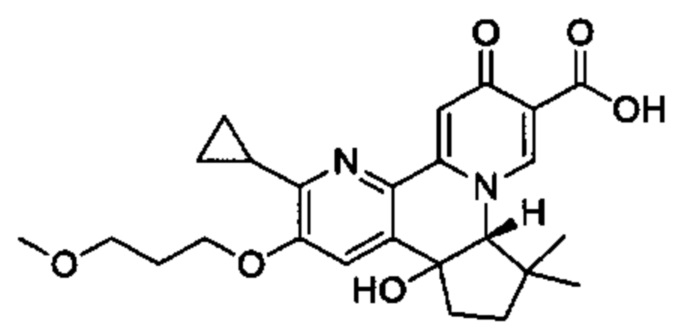
[00420] Стадия 1: (7aR)-2-Циклопропил-4b-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
[00421] Трет-бутоксид калия (13,3 мг, 0,119 ммоль) добавляли к раствору (4bR,7aS)-2-циклопропил-3-(3-метокситэопокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловой кислоты (13 мг, 0,030 ммоль) в диметилсульфоксиде (DMSO) (0,5 мл) при комнатной температуре и перемешивали в течение ночи. Указанную смесь вводили в хроматографическую колонку среднего давления с обращенной фазой и элюировали (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали (7aR)-2-циклопропил-4b-гадрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (единичный изомер) (6 мг, 0,013 ммоль, 43,6% выход) в виде серовато-белого порошка. LC-MS и ЯМР подтвердили получение желаемого продукта. LCMS (ESI) m/z 455,3 (М+1). 1H ЯМР (400 MHz, DMSO-d6) δ ppm 8,68 (s, 1 H), 7,50 (s, 2 H), 6,11 (s, 1 H), 4,62 (s, 1 H), 4,12-4,35 (m, 2 H), 3,51 (t, J=6,05 Hz, 2 H), 3,24 (s, 3 H), 2,57-2,68 (m, 1 H), 2,11-2,24 (m, 1 H), 2,02 (quin, J=6,15 Hz, 2 H), 1,56-1,70 (m, 1 H), 1,13-1,26 (m, 4 H), 0,97-1,10 (m, 4 H), 0,24 (s, 3 H).
[00422] Пример 6: (Соединение 225)
[00423] (7aR)-2-Хлор-4b-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
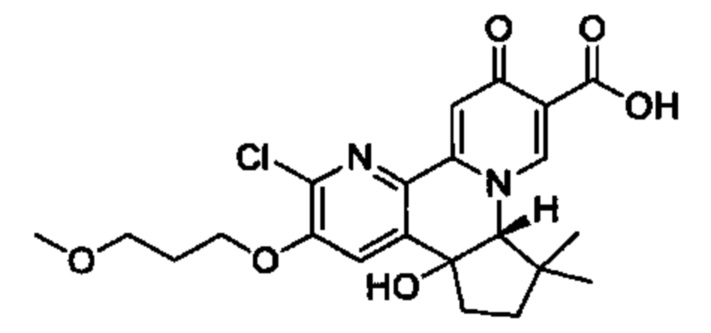
[00424] Стадия 1: (7aR)-2-Хлор-4b-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
[00425] Трет-бутоксид калия (15,5 мг, 0,139 ммоль) добавляли к раствору (4bR,7aS)-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловой кислоты (15 мг, 0,035 ммоль) в диметилсульфоксиде (DMSO) (1 мл) при комнатной температуре и перемешивали в течение 2 часов. Указанную смесь вводили в хроматографическую колонку среднего давления с обращенной фазой и элюировали (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали (7aR)-2-хлор-4b-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагадроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (7 мг, 0,015 ммоль, 44,6% выход) в виде белого порошка. LCMS (ESI) m/z 449,1 (М+1). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,74 (s, 1 H), 7,78 (s, 1 H), 7,44 (s, 1 H), 6,28 (s, 1 H), 4,70 (s, 1 H), 4,18-4,43 (m, 2 H), 3,49 (t, J=6,25 Hz, 2 H), 3,24 (s, 3 H), 2,59-2,73 (m, 1 H), 2,21 (dt, J=13,47, 8,88 Hz, 1 H), 2,01 (quin, J=6,15 Hz, 2 H), 1,58-1,71 (m, 1 H), 1,21-1,29 (m, 1 H), 1,18 (s, 3 H), 0,27 (s, 3 H).
[00426] Пример 7: (Соединение 226)
[00427] (7aR)-2-Хлор-4b-метокси-3-(3-метоксипропрокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
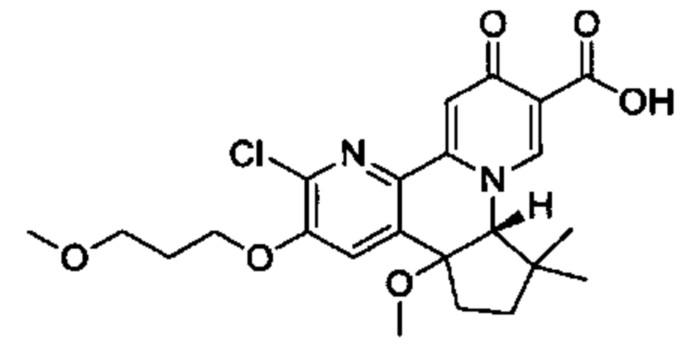
[00428] Стадия 1: (7aR)-2-Хлор-4b-метокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагадроциклопента[f]пиридо[1,2-b][1,71нафтиридин-10-карбоксиловая кислота
[00429] Гидрид натрия (60% в минеральном масле) (1,87 мг, 0,047 ммоль) добавляли к перемешиваемому раствору (7aR)-2-хлор-4b-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]-пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловой кислоты (7 мг, 0,016 ммоль) и метилйодида (2,9 мкл, 0,047 ммоль) в N,N-диметилформамиде (ДМФА) (0,5 мл). Указанную смесь взбалтывали в течение 2 часов. Указанную смесь нагревали до 80°С в течение 2 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и гасили водой. Указанную смесь перемешивали в течение 20 минут. Указанную смесь вводили в колонку обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали (4bS,7aR)-2-хлор-4b-метокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагадроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту в виде серовато-белого порошка. LCMS (ESI) m/z 463,2 (М+1). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,79 (s, 1 H), 7,78 (s, 1 H), 7,46 (s, 1 H), 4,92 (s, 1 H), 4,26-4,42 (m, 2 H), 3,49 (t, J=6,25 Hz, 2 H), 3,24 (s, 3 H), 2,94 (s, 3 H), 2,66 (dt, J=13,56, 6,68 Hz, 1 H), 2,19-2,33 (m, 1 H), 2,01 (quin, J=6,15 Hz, 2 H), 1,63-1,74 (m, 1 H), 1,28-1,40 (m, 1 H), 1,19 (s, 3 H), 0,29 (s, 3 H).
[00430] Пример 8 (Соединение 227) и Пример 9 (Соединение 228)
[00431] (4bR,7aS)-2-Гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
[00432] (4bR,7aS)-2-Хлор-3-гидрокси-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота
[00433] 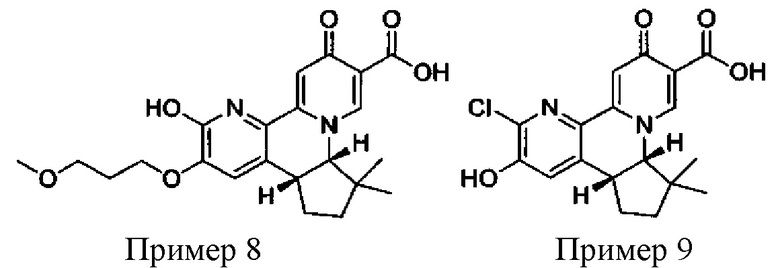
[00434] Смесь (4bR,7aS)-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловой кислоты (61 мг, 0,141 ммоль) в гидроксиде натрия (2М) (4 мл, 8 ммоль) нагревали при 150°С в микроволновом реакторе в течение 1 часа. Указанную смесь вводили в хроматографическую колонку среднего давления с обращенной фазой и элюировали (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 0% до 100%). 2 набора фракций лиофилизировали раздельно и получали:
[00435] Пример 8: (4bR,7aS)-2-Гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (20 мг, 0,048 ммоль, 34% выход). LCMS (ESI) m/z 415,2 (M+1). 1H ЯМР (400 MHz, DMSO-d6) δ ppm 11,15-11,71 (m, 1 H), 8,53 (s, 1 H), 7,44 (s, 1 H), 6,97-7,27 (m, 1 H), 4,61 (d, J=8,98 Hz, 1 H), 4,00-4,19 (m, 2 H), 3,73 (br. s., 1 H), 3,45 (t, J=6,05 Hz, 2 H), 3,23 (s, 3 H), 2,11-2,33 (m, 2 H), 1,96 (quin, J=6,25 Hz, 2 H), 1,50-1,61 (m, 1 H), 1,31-1,45 (m, 1 H), 1,11 (s, 3 H), 0,42 (s, 3 H).
[00436] Пример 9: (4bR,7aS)-2-Хлор-3-гидрокси-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (8 мг, 0,022 ммоль, 15,6% выход). LCMS (ESI) m/z 361,1 (M+1). 1H ЯМР (400 MHz, DMSO-d6) δ ppm 11,85 (br. s, 1 H), 8,57 (s, 1 H), 7,37 (s, 1 H), 7,24 (s, 1 H), 4,66 (d, J=8,98 Hz, 1 H), 3,80-3,94 (m, 1 H), 2,25-2,43 (m, 2 H), 1,94-2,08 (m, 1 H), 1,52-1,64 (m, 1 H), 1,38-1,49 (m, 1 H), 1,11 (s, 3 H), 0,37 (s, 3 H).
[00437] Пример 10: (Соединение 229)
[00438] 2-Хлор-6-(1-гидрокси-2-метилпропан-2-ил)-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
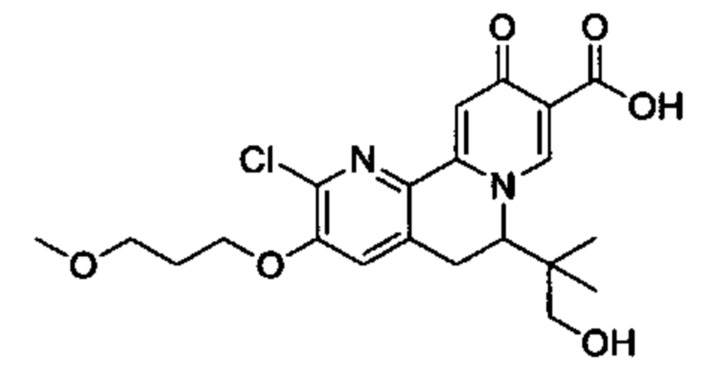
[00439] Стадия 1: 4-(Бензилокси)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-он
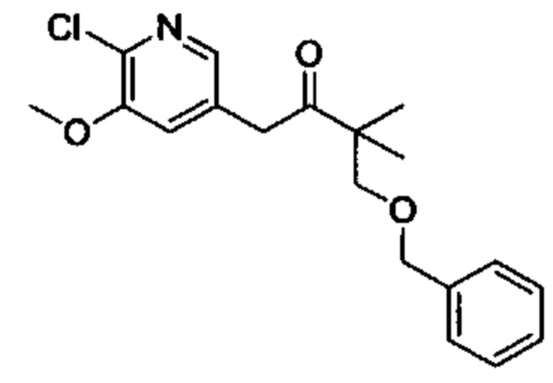
[00440] В колбу помещали мешалку, 5-бром-2-хлор-3-метоксипиридин (5,8 г, 26 ммоль), трис(дибензилиденацетон)дипалладий(0) (0,358 г, 0,391 ммоль), и трет-бутоксид натрия (4,41 г, 45,9 ммоль). Указанную колбу продували потоком азота перед добавлением 4-(бензилокси)-3,3-диметилбутан-2-она (5,45 г, 26,4 ммоль) в тетрагидрофуране (ТГФ) (100 мл). Указанную смесь нагревали с обратным холодильником в течение 3 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и разбавляли водой. Указанную смесь экстрагировали 3 раза этил ацетатом. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия, и концентрировали. Полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 50% этилацетата в гексанах. Полученные Фракции концентрировали и получали 4-(бензилокси)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-он (5,62 г, 16,2 ммоль, 62% выход) в виде бледно-желтого масла. LCMS (ESI) m/z 348,2 (М+1). 1Н ЯМР (400 MHz, хлороформ-d) δ ppm 7,70 (d, J=1,95 Hz, 1 Н), 7,21-7,39 (m, 5 Н), 7,01 (d, J=1,56 Hz, 1 Н), 4,49 (s, 2 Н), 3,79 (s, 5 Н), 3,52 (s, 2 Н), 1,22 (s, 6 Н).
[00441] Стадия 2: 4-(Бензилокси)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-амин
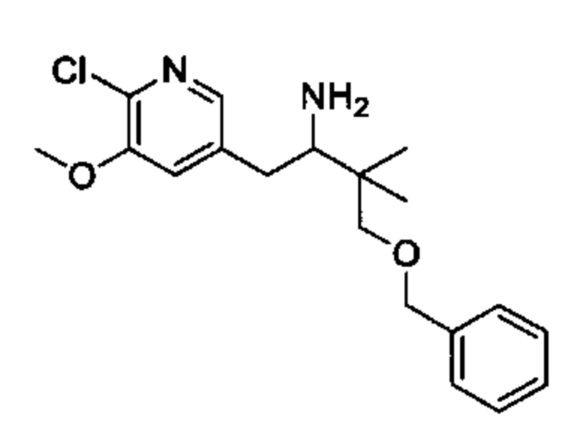
[00442] Смесь 4-(бензилокси)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-она (3 г, 8,6 ммоль) и ацетата аммония (9,97 г, 129 ммоль) в метаноле (50 мл) перемешивали при комнатной температуре в течение ночи. Добавляли цианоборгидрид натрия (1,08 г, 17,3 ммоль) и указанную смесь нагревали при 60°С в течение ночи. Указанную смесь оставляли охлаждаться до комнатной температуры, концентрировали до -15 мл, гасили 1М гидроксидом натрия, и экстрагировали 3 раза этил ацетатом. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия, концентрировали и получали неочищенный 4-(бензилокси)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-амин (2,84 г, 5,62 ммоль, 65% выход). LCMS (ESI) m/z 349,3 (М+1).
[00443] Стадия 3: 5-(2-Амино-4-гидрокси-3,3-диметилбутил)-2-хлорпиридин-3-ол
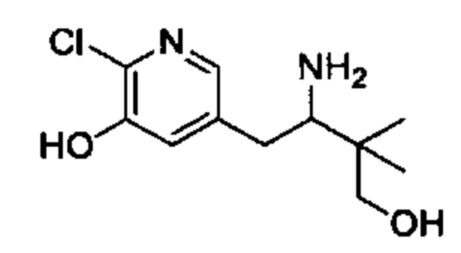
[00444] Трибромид бора (2,66 мл, 28,1 ммоль) добавляли по каплям к раствору 4-(бензилокси)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-амина (2,84 г, 5,62 ммоль) в 1,2-дихлорзтане (DCE) (100 мл) при 0°С. Указанную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 4 часов. Маслянистое твердое вещество осаждалось на дне колбы. Указанную твердую фракцию соскребали со стенок колбы и указанную смесь энергично перемешивали при комнатной температуре в течение ночи. Маслянистое твердое вещество осаждалось на дне колбы. Указанную жидкую фазу декантировали и выливали в лед. Указанный осадок в исходной реакционной колбе суспендировали в свежем 1,2-дихлорэтане (DCE) (100 мл) и перемешивали, пока по каплям добавляли 1 мл (~2 экв.) свежего трибромида бора при комнатной температуре. Указанную смесь нагревали при 70°С в течение 4 часов, а затем оставляли охлаждаться до комнатной температуры. Указанную смесь охлаждали в ледяной бане, гасили медленным осторожным добавлением 100 мл метанола, нагретого до комнатной температуры, и перемешивали в течение 1 часа. Указанную смесь концентрировали и полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 /ацетонитрил / вода / 0,1% муравьиная кислота / градиент от 0% до 20%). Фракции лиофилизировали и получали 5-(2-амино-4-гадрокси-3,3-диметилбутил)-2-хлорпиридин-3-ол (910 мг, 3,72 ммоль, 66,2% выход) в виде белого порошка. LCMS (ESI) m/z 245,2 (М+1). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 7,80 (d, J=1,95 Hz, 1 H), 7,59 (br. s., 3 H), 7,25 (d, J=1,95 Hz, 1 H), 3,31-3,38 (m, 2 H), 3,19-3,29 (m, 1 H), 2,92-3,02 (m, 1 H), 2,53-2,63 (m, 1 H), 0,95 (s, 3 H), 0,90 (s, 3 H).
[00445] Стадия 4: 5-(2-Амино-4-гидрокси-33-диметилбутил)-2-хлор-6-йодпиридин-3-ол
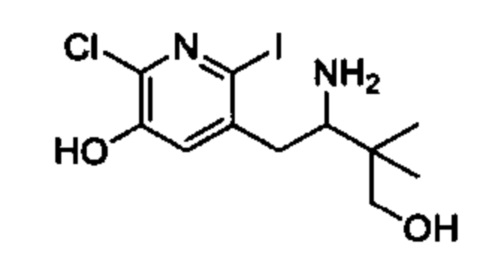
[00446] Йод (233 мг, 0,919 ммоль) добавляли к перемешиваемой смеси 5-(2-амино-4-гидрокси-3,3-диметилбутил)-2-хлорпиридин-3-ола (225 мг, 0,919 ммоль) и карбоната калия (381 мг, 2,76 ммоль) в воде (10 мл). Указанную смесь взбалтывали при комнатной температуре в течение 2 часов. Твердый сульфат натрия добавляли порциями к указанной смеси до тех пор, пока не исчез цвет. Указанную водную смесь вводили в колонку С18 среднего давления с обращенной фазой, а затем элюировали градиентом от 0% до 50% смеси ацетонитрил / вода / 0,1% муравьиная кислота. Объединенные фракции лиофилизировали и получали 5-(2-амино-4-гидрокси-3,3-диметилбутил)-2-хлор-6-йодпиридин-3-ол (164 мг, 0,443 ммоль, 48,1% выход) в виде белого твердого вещества. LCMS (ESI) m/z 371,0 (М+1). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,23 (s, 1 H), 7,20 (s, 1 H), 3,13-3,41 (m, 2 H), 2,70-2,88 (m, 2 H), 2,29-2,39 (m, 1 H), 0,92 (s, 3 H), 0,84 (s, 3 H).
[00447] Стадия 5: Этил-1-(4-ацетокси-1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
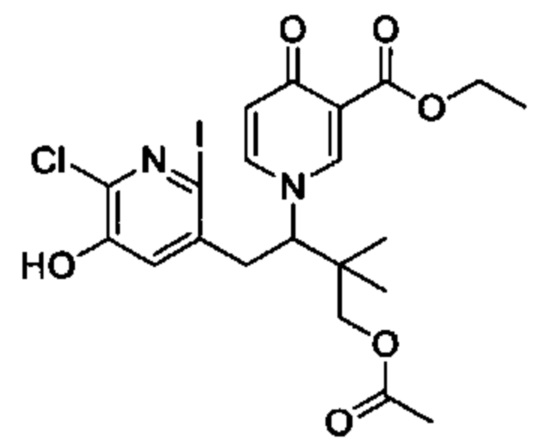
[00448] 5-(2-Амино-4-гадрокси-3,3-диметилбутил)-2-хлор-6-йодпиридин-3-ол (164 мг, 0,443 ммоль) и этил-4-оксо-4Н-пиран-3-карбоксилат (83 мг, 0,494 ммоль) в уксусной кислоте (4 мл) перемешивали при 100°С в течение 4 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент от 0% до 100%). 2 набора фракций концентрировали раздельно и получали этил-1-(1-(6-хлор-5-ил)окси-2-йодпиридин-3-ил)-4-гидрокси-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигадропиридин-3-карбоксилат (83 мг, 0,16 ммоль, 36% выход) и этил-1-(4-ацетокси-1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (27 мг, 0,048 ммоль, 11% выход). LCMS (EST) m/z 563,2 (М+1).
[00449] Стадия 6: Этил-1-(4-ацетокси-1-(6-хлор-2-йод-5-(3-метоксипропокси)-пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
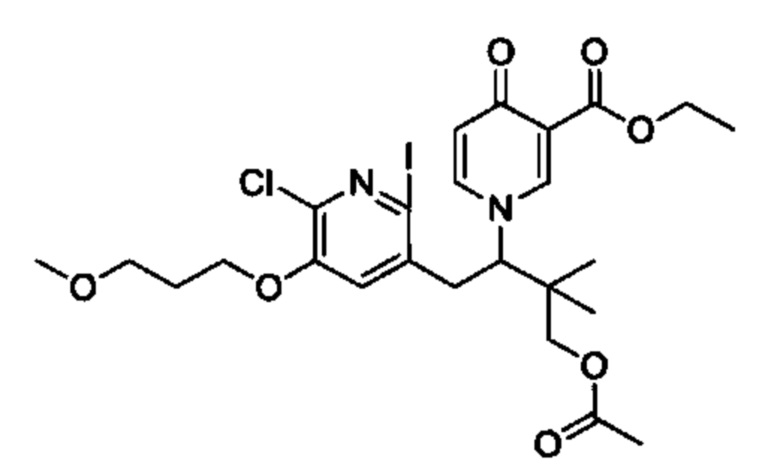
[00450] Этил-1-(4-ацетокси-1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (27 мг, 0,048 ммоль), карбонат калия (26,5 мг, 0,192 ммоль), и 1-бром-3-метоксипропан (19 мг, 0,124 ммоль) перемешивали при комнатной температуре в течение ночи. Указанную смесь гасили водой и 2 раза экстрагировали этил ацетатом. Объединенные органические фазы промывали солевым раствором, промывали 5% хлоридом лития (волн.), и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали этил-1-(4-ацетокси-1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигропиридин-3-карбоксилат (15 мг, 0,024 ммоль, 49,2% выход) в виде белого порошка. LCMS (ESI) m/z 635,9 (М+1).
[00451] Стадия 7: 2-Хлор-6-(1-гидрокси-2-метилпропан-2-ил)-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
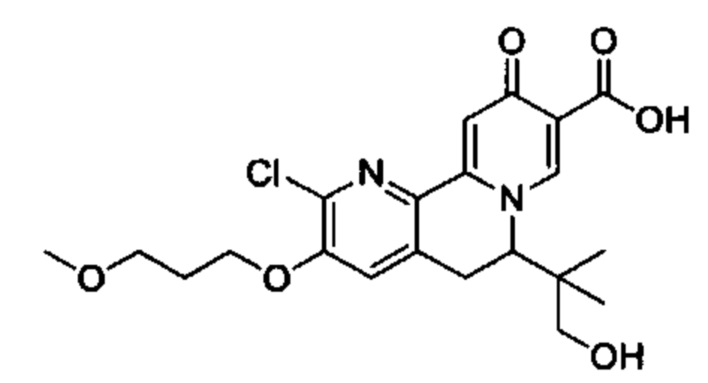
[004S2] Круглодонную колбу, содержащую мешалку, этил-1-(4-ацетокси-1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (14 мг, 0,022 ммоль), ацетат калия (4,33 мг, 0,044 ммоль), и бромид палладия (II) (1,2 мг, 4,4 мкмоль) продували азотом в течение 15 минут. N,N-Диметилацетамид (DMA) (1 мл) продували азотом в течение 5 минут перед добавлением в колбу с реакционной смесью. Указанную колбу с реакционной смесью помещали в масляную баню, предварительно нагретую до 90°С и указанную смесь перемешивали в течение 3 часов. Указанную смесь оставляли охлаждаться до комнатной температуры, отфильтровывали через целит и полученный фильтрат очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции комбинировали и защелачивали 1М гидроксидом натрия. Указанную смесь нагревали при 60°С в течение ночи, охлаждали до комнатной температуры, и концентрировали. Полученный осадок растворяли в воде и закисляли до рН=3-4 1М соляной кислотой. Указанную смесь очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 0% до 100%). Фракции лиофилизировали и получали 2-хлор-6-(1-гидрокси-2-метилпропан-2-ил)-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловую кислоту (3 мг, 6,9 мкмоль, 31% выход). LCMS (ESI) m/z 437,2 (М+1).
[00453]
[00454] Общая схема 6 с получением соединений Примеров 11-25
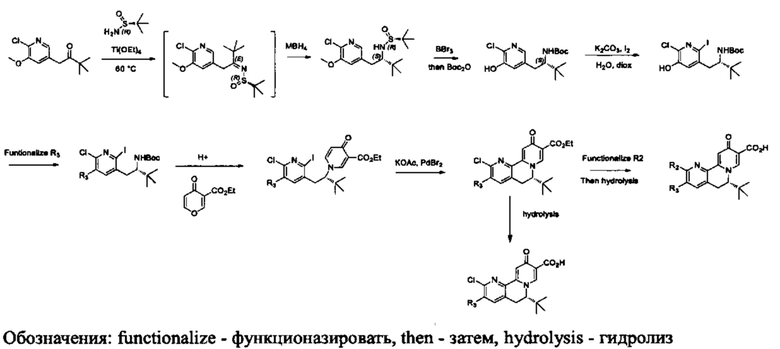
[00455] Пример 11 (Соединение 230)
[00456] (S)-6-(трет-Бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
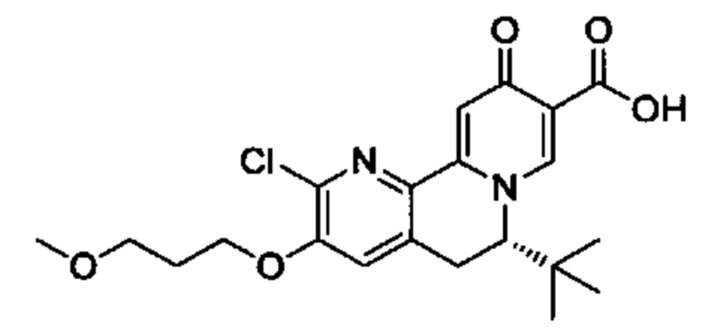
[00457] Стадия 1: (R)-N-((S)-1-(6-Хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-ил)-2-метилпропан-2-сульфинамид
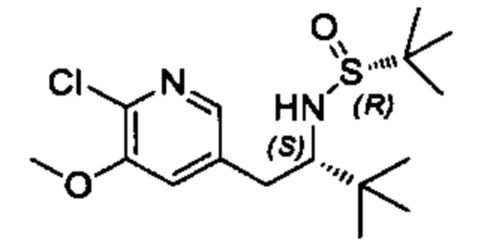
[00458] Раствор 1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-она (2,54 г, 10,50 ммоль), (R)-2-метилпропан-2-сульфинамида (2,55 г, 21,00 ммоль) и Ti(OEt)4 (5,99 г, 26,3 ммоль) в толуоле (8,5 мл) взбалтывали в течение 10 минут при 60°С, а затем указанный сосуд упаривали. Полученную реакционную смесь взбалтывали при 60°С под вакуумом в течение 24 ч. Указанный сосуд наполняли азотом и добавляли толуол (5 мл) и ТГФ (35 мл). Медленно добавляли раствор LiBH4 (15,8 мл, 2М в ТГФ, 31,5 ммоль). Полученную реакционную смесь взбалтывали при комнатной температуре в течение ночи. Полученную реакционную смесь разбавляли ТГФ (130 мл) и насыщенным солевым раствором (3 мл), перемешивали в течение 30 мин, а затем отфильтровывали через целит. Полученный фильтрат упаривали и очищали с помощью хроматографии на силикагеле (0-100% EtOAc/гексаны) с получением (R)-N-((S)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-ил)-2-метилпропан-2-сульфинамида (2,58 г, 71%) в виде основного диастереомера. LCMS (m/z, ES+)=346,9, 348,1 (М+1).
[00459] Стадия 2: (S)-5-(2-Амино-3,3-диметилбутил)-2-хлорпиридин-3-ол
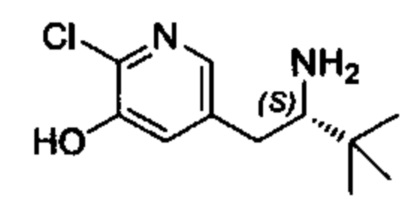
[00460] Раствор (R)-N-((S)-1-(6-хлор-5-метоксш1иридин-3-ил)-3,3-диметилбутан-2-ил)-2-метилпропан-2-сульфинамида (2,56 г, 7,38 ммоль) в 1,2-дихлорзтане (36,9 мл) взбалтывали при 0°С. Медленно добавляли трибромид бора (4,88 мл, 51,7 ммоль). Полученную реакционную смесь удаляли из охлаждающей бани и перемешивали в течение ночи при комнатной температуре. Указанный раствор охлаждали до 0°С и гасили посредством медленного добавления МеОН. Полученную суспензию упаривали. Добавляли EtOAc и полученный твердый остаток собирали фильтрацией, промывали EtOAc и осушали с получением (S)-5-(2-амино-3,3-диметилбутил)-2-хлорпиридин-3-ола в виде бис-соли HBr. (2,89 г, рассчетн.) LCMS (m/z, ES+)=229,1,231,1 (М+1).
[00461] Стадия 3: (S)-трет-Бутил (1-(6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамат
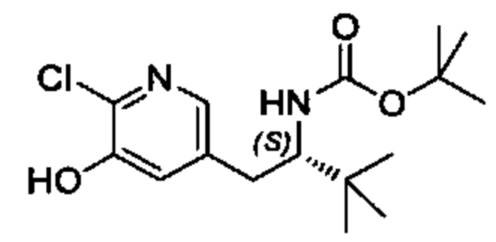
[00462] Триэтиламин (0,95 мл, 6,85 ммоль) добавляли к перемешиваемой суспензии (S)-5-(2-амино-3,3-диметилбутил)-2-хлорпиридин-3-ола 2HBr (1,36 г, 3,42 ммоль) и Вос-ангидрида (0,87 мл, 3,73 ммоль) в ТГФ (34,2 мл) и полученную реакционную смесь взбалтывали при 60°С в течение 1 ч, а затем упаривали досуха. Полученный твердый остаток суспендировали в диэтиловом эфире, отделяли с помощью фильтрации, а затем разделяли между EtOAc и водой. Указанную водную фазу экстрагировали CH2Cl2 (4х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением (S)-трет-бутил (1-(6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (предполагаемый рассчетн.). LCMS (m/z, ES+)=329,6, 331,2 (М+1).
[00463] Стадия 4: (S)-трет-Бутил (1-(6-хлор-5-гадрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамат
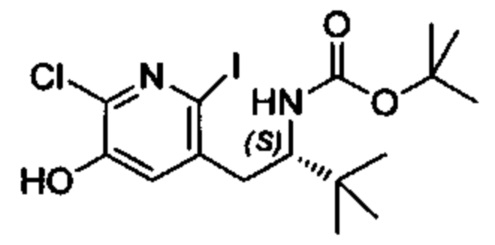
[00464] Йод (0,87 г, 3,42 ммоль) добавляли к перемешиваемому раствору трет-бутил-(S)-(1-(6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамату (1,13 г, 3,42 ммоль) и К2СО3 (1,42 г, 10,26 ммоль) в воде (8,6 мл) и 1,4-диоксане (8,6 мл). Полученную реакционную смесь взбалтывали в течение ночи при комнатной температуре. Добавляли дополнительный йод (0,20 г, 0,79 ммоль) и К2СО3 (0,40 г, 7,23 ммоль) и полученную реакционную смесь нагревали при 40°С в течение 5 ч. Твердый Na2SO3 добавляли при перемешивании до тех пор, пока указанный раствор переставал быть темно-коричневым. Указанный раствор разбавляли солевым раствором и EtOAc. Указанную водную фазу экстрагировали EtOAc. Объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением (S)-трет-бутил-(1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата в виде желтой пены (1,56 г, рассчетн.). LCMS (m/z, ES+)=455,1,457,1 (M+1).
[00465] Стадия 5: (S)-трет-Бутил (1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)карбамат
[00466] 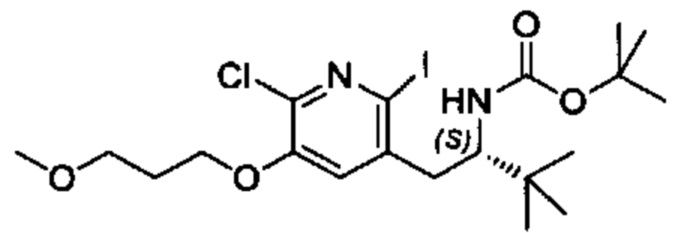
[00467] Раствор трет-бутил-(S)-(1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (0,83 г, 1,84 ммоль), К2СО3 (0,76 г, 5,51 ммоль) и 1-бром-3-метоксипропана (0,56 г, 3,67 ммоль) в ДМФА (12,2 мл) нагревали при 80°С в течение 3 ч. Полученную реакционную смесь упаривали досуха и полученный осадок переносили в CH2Cl2 и Н2О. Указанную водную фазу экстрагировали CH2Cl2 (2х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали, и упаривали с получением трет-бутил-(S)-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (0,97 г, рассчетн.) в виде серовато-белого твердого вещества. LCMS (m/z, ES+)=527,2, 529,2 (M+1).
[00468] Стадия 6: (S)-Этил-1-(1-(6-хлор-2-йод-5-(3-метокситэопокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
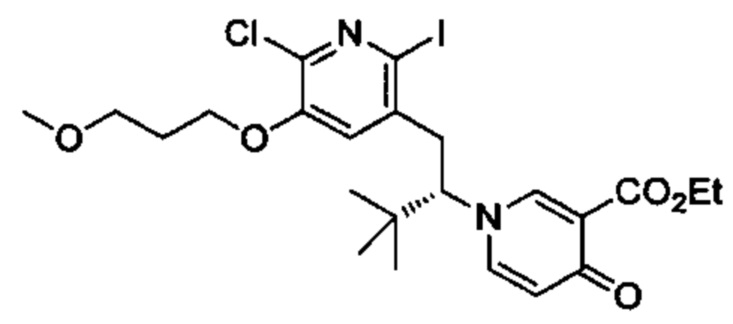
[00469] 4 М Соляную кислоту в диоксане (6,89 мл, 27,5 ммоль) добавляли к раствору трет-бутил-(S)-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (967 мг, 1,84 ммоль) в CH2Cl2 (7 мл). Полученную реакционную смесь взбалтывали при комнатной температуре в течение 3 ч и упаривали досуха. Полученный твердый остаток растворяли в CH2Cl2 (1 мл) и Et3N (1 мл), а затем упаривали досуха. Полученный осадок переносили в насыщенный NaHCO3 и CH2Cl2. Указанную водную фазу экстрагировали CH2Cl2 (2х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением (S)-1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-амина. Раствор вышеуказанного амина и этил-4-оксо-4Н-пиран-3-карбоксилата (340 мг, 2,02 ммоль) в уксусной кислоте (18,4 мл) взбалтывали при 100°С в течение 7 ч. Полученную реакционную смесь упаривали досуха и полученный осадок очищали с помощью обращенно-фазовой хроматографии (10-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением этил-(S)-1-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дитидропиридин-3-карбоксилата (593 мг, 56%) в виде светло-коричневого твердого вещества. LCMS (m/z, ES+)=577,7, 579,2 (М+1).
[00470] Стадия 7: (S)-Этил-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
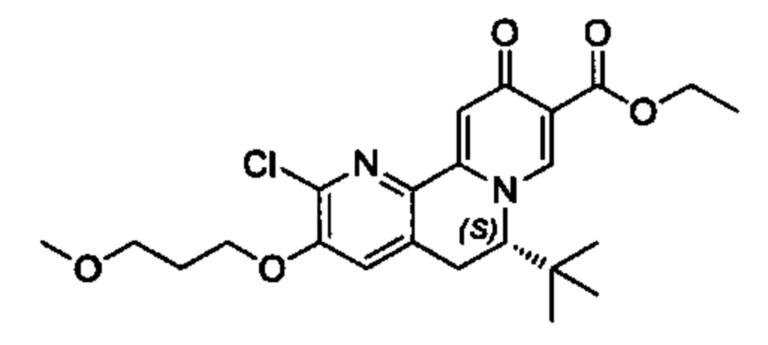
[00471] Колбу, содержащую этил-(S)-1-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (0,59 г, 1,03 ммоль), ацетат калия (0,20 г, 2,06 ммоль) и бромид палладия (II) (0,055 г, 0,21 ммоль) продували азотом. Добавляли дегазированный N,N-диметилацетамид (DMA) (10,3 мл) и полученную реакционную смесь нагревали при 90°С в течение 24 ч. Указанный растворитель удаляли упариванием и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением этил-(S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (326 мг, 71%) в виде серовато-белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,18 (s, 1 Н), 7,49 (s, 1 Н), 7,02 (s, 1 Н), 4,40 (q, J=7,0 Hz, 2 H), 4,13-4,26 (m, 2 H), 3,93 (d, J=6,6 Hz, 1 H), 3,62 (m, 2 H), 3,42-3,51 (m, 1 H), 3,38 (s, 3 H), 3,17-3,25 (m, 1 H), 2,15 (quin, J=6,0 Hz, 2 H), 1,41 (t, J=7,2 Hz, 3 H), 0,86 (s, 9 H); LCMS (m/z, ES+)=449,3,451,3 (M+1).
[00472] Стадия 8: (S)-6-(трет-Бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
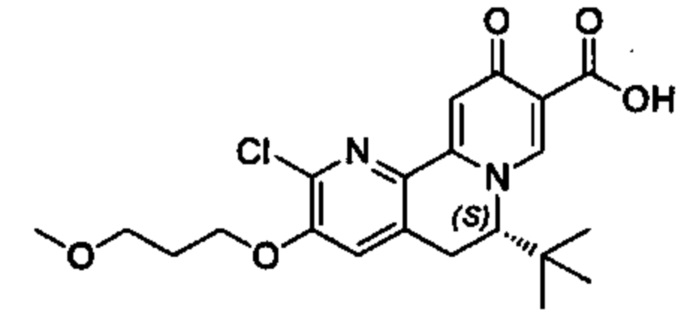
[00473] Раствор этил-(S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (42 мг, 0,094 ммоль) в 1М LiOH (1,7 мл) и МеОН (1,7 мл) взбалтывали при 50°С в течение 1,5 ч. Добавляли 1М лимонную кислоту (2 мл) и полученную реакционную смесь взбалтывали в течение нескольких минут. Указанное белое вещество собирали фильтрацией, промывали водой и осушали с получением (S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (35,5 мг, 90%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 16,31 (s, 1 H), 8,81 (s, 1 H), 7,75 (s, 1 H), 7,30 (s, 1 H), 4,68 (d, J=6,3 Hz, 1 H), 4,19-4,32 (m, 2 H), 3,40-3,60 (m, 4 H), 3,26 (s, 3 H), 2,04 (quin, J=6,2 Hz, 2 H), 0,75 (s, 9 H); LCMS (m/z, ES+)=421,3, 423,2 (M+1).
[00474] Пример 12 (Соединение 231)
[00475] (S)-6-(трет-Бутил)-3-(циклопропилметокси)-2-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
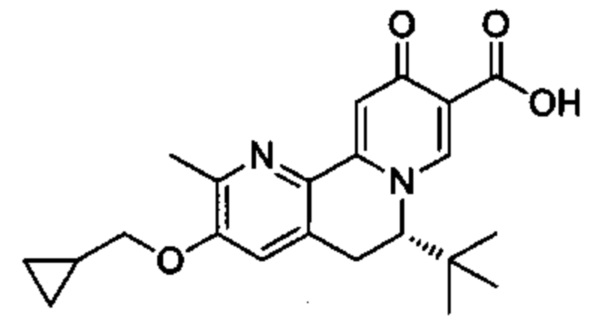
[00476] Стадия 1: (S)-трет-Бутил-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметидбутан-2-ил)карбамат
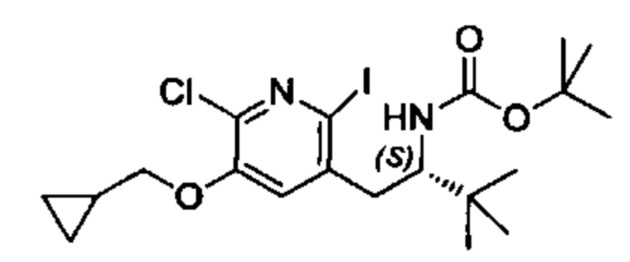
[00477] Раствор трет-бутил-(S)-(1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (0,73 г, 1,60 ммоль), K2СО3 (0,66 г, 4,78 ммоль) и (бромметил)циклопропана (0,43 г, 3,19 ммоль) в ДМФА (10,6 мл) нагревали при 80°С в течение 3 ч. Полученную реакционную смесь упаривали досуха и полученный осадок переносили в CH2Cl2 и Н2О. Указанную водную фазу экстрагировали CH2Cl2 (2х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением трет-бутил-(S)-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (0,81 г, рассчетн.) в виде серовато-белого твердого вещества. LCMS (m/z, ES+)=508,8, 511,1 (М+1).
[00478] Стадия 2: (S)-Этил-1-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
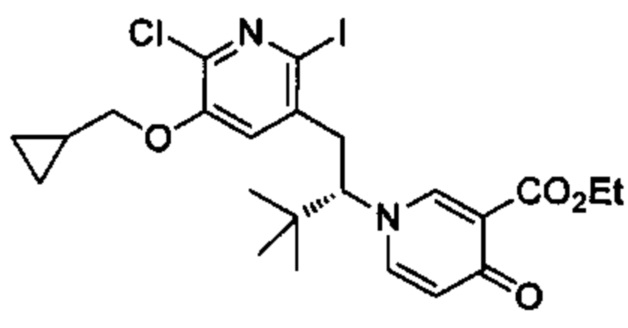
[00479] 4 М Соляную кислоту в диоксане (5,98 мл, 23,9 ммоль) добавляли к раствору трет-бутил (S)-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (812 мг, 1,60 ммоль) в CH2Cl2 (6 мл). Полученную реакционную смесь взбалтывали при комнатной температуре в течение 3 ч и упаривали досуха. Полученный твердый остаток растворяли в CH2Cl2 (1 мл) и Et3N (1 мл), а затем упаривали досуха. Полученный осадок переносили в насыщенный NaHCO3 и CH2Cl2. Указанную водную фазу экстрагировали CH2Cl2 (2х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением (S)-1-(6-хлор-2-йод-5-(циклопропилметокси)пиридин-3-ил)-3,3-диметилбутан-2-амина. LCMS (m/z, ES+)=409,1,411,1 (М+1).
[00480] Раствор вышеуказанного амина и этил-4-оксо-4Н-пиран-3-карбоксилата (295 мг, 1,76 ммоль) в уксусной кислоте (16,0 мл) взбалтывали при 100°С в течение 7 ч. Полученную реакционную смесь упаривали досуха и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением этил-(S)-1-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилата(453 мг, 51%) в виде светло-коричневого твердого вещества. LCMS (m/z, ES+)=559,4, 561,1 (M+1).
[00481] Стадия 3: (S)-Этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
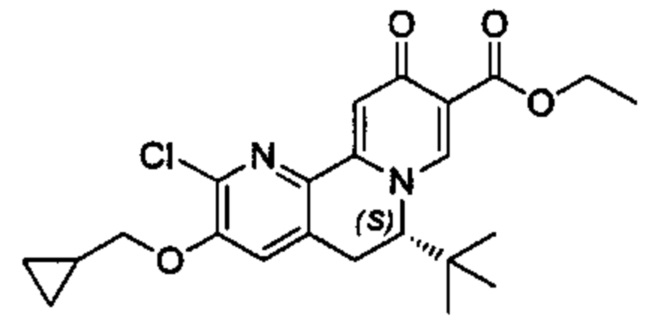
[00482] Колбу, содержащую этил-(S)-1-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (0,45 г, 0,81 ммоль), ацетат калия (0,16 г, 1,62 ммоль), и бромид палладия (II) (0,043 г, 0,16 ммоль), продували азотом. Добавляли дегазированный N,N-диметилацетамид (DMA) (8,1 мл) и полученную реакционную смесь нагревали при 90°С в течение 24 ч. Указанный растворитель удаляли упариванием и полученный осадок переносили в CH2Cl2 и воду и отфильтровывали через целит. Указанную органическую фазу упаривали досуха и полученный осадок очищали с помощью обращенно-фазовой хроматографии (10-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением этил-(S)-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (216 мг, 62%) в виде серовато-белого твердого вещества. LCMS (m/z, ES+)=431,2,433,2 (M+1); >97% энантиомерный избыток по данным хиральной ВЭЖХ.
[00483] Стадия 4: (S)-6-(трет-Бутил)-3-(циклопропилметокси)-2-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00484] 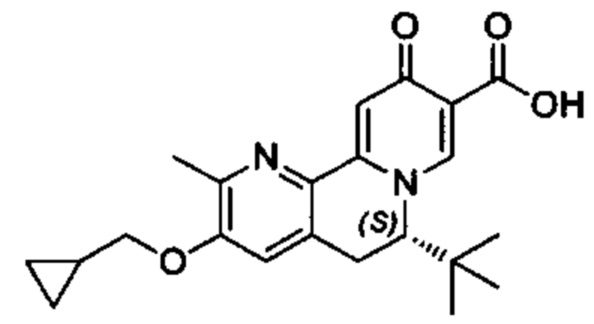
[00485] Раствор этил-(S)-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (52,7 мг, 0,12 ммоль), Pd(PPh3)4 (28 мг, 0,024 ммоль), карбоната калия (34 мг, 0,25 ммоль), и триметилбороксина (46 мг, 0,37 ммоль) в 1,4-диоксане (0,61 мл) нагревали при 100°С в течение ночи. Полученную реакционную смесь разбавляли CH2Cl2 и отфильтровывали через целит. Полученный фильтрат упаривали и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением (S)-этил-6-(трет-бутил)-3-(циклопропилметокси)-2-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (36,5 мг, 73%). 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,18 (s, 1 Н), 7,56 (s, 1 Н), 6,80 (s, 1 Н), 4,40 (q, J=7,0 Hz, 2 H), 3,87 (s, 3 H), 3,39-3,48 (m, 1 H), 3,10-3,18 (m, 1 H), 2,50 (s, 3 H), 1,41 (t, J=7,0 Hz, 3 H), 0,69 (m, 2 H), 0,40 (m, 2 H); LCMS (m/z, ES+)=411,4 (M+1).
[00486] Раствор вышеуказанного эфира в 1M LiOH (0,9 мл) и МеОН (0,9 мл) нагревали при 50°С в течение 1,5 ч. 1М лимонную кислоту (1,2 мл) добавляли и полученную реакционную смесь взбалтывали в течение 15 мин. Полученный твердый остаток собирали фильтрацией, промывали водой и осушали с получением (S)-6-(трет-бутил)-3-(циклопропилметокси)-2-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-р][1,7]нафтиридин-9-карбоксиловой кислоты (27,7 мг, 59% для 2-х стадий) в виде белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 16,53 (br. s., 1 H), 8,77 (s, 1 H), 7,44 (s, 1 H), 7,42 (s, 1 H), 4,58-4,69 (m, 1 H), 3,98 (m, 2 H), 3,46-3,55 (m, 2 H), 2,43 (s, 3H), 1,22-1,36 (m, 1 H), 0,73 (s, 9 H), 0,65-0,55 (m, 2 H), 0,33-0,44 (m, 2 H); LCMS (m/z, ES+)=383,2 (M+1).
[00487] Пример 13 (Соединение 232)
[00488] (S)-6-(трет-Бутил)-3-(3-метоксипропокси)-2-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00489] 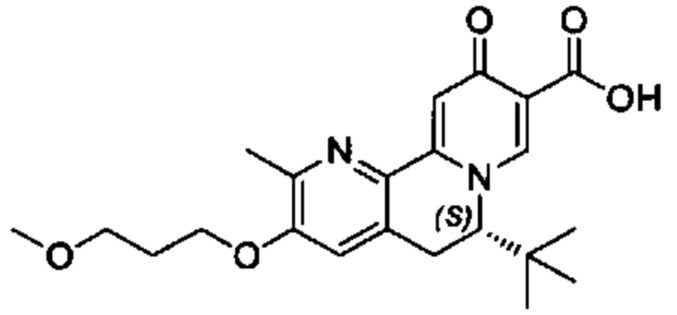
[00490] Раствор этил-(S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (47,7 мг, 0,11 ммоль), Pd(PPh3)4 (25 мг, 0,021 ммоль), карбоната калия (29 мг, 0,21 ммоль) и триметилбороксина (40 мг, 0,32 ммоль) в 1,4-диоксане (0,53 мл) нагревали при 100°С в течение ночи. Полученную реакционную смесь разбавляли CH2Cl2 и отфильтровывали через целит. Полученный фильтрат упаривали и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% (3:1 EtOAc:EtOH) в гексанах) с получением (S)-этил-6-(трет-бутил)-3-(3-метоксипропокси)-2-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (41,3 мг, 91%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,17 (s, 1 H), 7,27 (s, 1 H), 6,86 (s, 1 H), 4,39 (q, J=7,0 Hz, 2 H), 4,05-4,17 (m, 2 H), 3,91 (d, J=6,6 Hz, 1 H), 3,63-3,55 (m, 2 H), 3,49-3,41 (m, 1 H), 3,38 (s, 3 H), 3,15 (d, J=16,8 Hz, 1 H), 2,46 (s, 3 H), 2,12 (quin, J=6,1 Hz, 2 H), 1,40 (t, J=7,0 Hz, 3 H), 0,84 (s, 9 H); LCMS (m/z, ES+)=429,4 (M+1).
[00491] Раствор вышеуказанного эфира в 1M LiOH (1 мл) и МеОН (1 мл) нагревали при 50°С в течение 1,5 ч. Добавляли 1М лимонную кислоту (1,2 мл) и полученную реакционную смесь взбалтывали в течение 15 мин. Полученный твердый остаток собирали фильтрацией, промывали водой и осушали с получением (S)-6-(трет-бутил)-3-(3-метоксипропокси)-2-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h] [1,7]нафтиридин-9-карбоксиловой кислоты (27,6 мг, 65% для 2-х стадий) в виде белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 16,53 (s, 1 Н), 8,77 (s, 1 Н), 7,46 (s, 1 Н), 7,44 (s, 1 Н), 4,64 (d, J=6,3 Hz, 1 H), 4,09-4,23 (m, 2 H), 3,47-3,56 (m, 3 H), 3,38-3,32 (m, 1H), 3,26 (s, 3 H), 2,42 (s, 3 H), 2,02 (quin, J=6,2 Hz, 2 H), 0,74 (s, 9 H); LCMS (m/z, ES+)=401,2 (M+1).
[00492] Пример 14 (Соединение 233)
[00493] (S)-6-(трет-Бутил)-2-циклопропил-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00494] 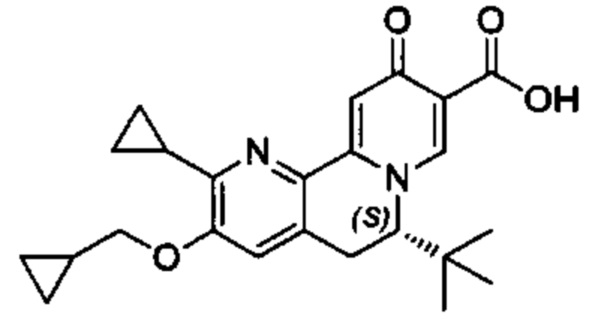
[00495] Раствор этил-(S)-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (53 мг, 0,12 ммоль), Pd(PPh3)4 (28 мг, 0,025 ммоль), карбоната калия (51 мг, 0,37 ммоль) и циклопропилборной кислоты (21 мг, 0,25 ммоль) в 1,4-диоксане (1,2 мл) нагревали при 100°С в течение ночи. Полученную реакционную смесь разбавляли CH2Cl2 и отфильтровывали через целит. Полученный фильтрат упаривали и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% (3:1 EtOAc:EtOH) в гексанах) с получением (S)-этил-6-(трет-бутил)-2-циклопропил-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пирвдо[1,2-h][1,7]нафтиридин-9-карбоксилата (53,3 мг, 99%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,14 (s, 1 Н), 7,42 (s, 1 Н), 6,77 (s, 1 Н), 4,38 (q, J=7,3 Hz, 2 H), 3,88 (m, J=6,8,2,1 Hz, 2 H), 3,43 (dd, J=16,8, 7,0 Hz, 1 H), 3,11 (d, J=16,8 Hz, 1 H), 2,56-2,47 (m, 1 H), 1,39 (t, J=7,0 Hz, 3 H), 1,35-1,29 (m, 1 H), 1,22-1,29 (m, 1 H), 1,04-1,19 (m, 2 H), 0,93-1,01 (m, 2 H), 0,82 (s, 9 H), 0,63-0,73 (m, 2 H), 0,44-0,38 (m, 2 H); LCMS (m/z, ES+)=437,4 (M+1).
[00496] Раствор вышеуказанного эфира в 1M LiOH (1,2 мл) и МеОН (1,2 мл) нагревали при 50°С в течение 2 ч. Добавляли 1М лимонную кислоту (1,5 мл) и полученную реакционную смесь взбалтывали в течение 15 мин. Полученный твердый остаток собирали фильтрацией, промывали водой и осушали с получением (S)-6-(трет-бутил)-2-циклопропил-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (38,8 мг, 77% для 2-х стадий) в виде белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 16,53 (s, 1 Н), 8,76 (s, 1 Н), 7,38 (s, 1 Н), 7,35 (s, 1 Н), 4,62 (d, J=6,3 Hz, 1 H), 4,05-3,94 (m, 2 H), 3,42-3,55 (m, 1 H), 3,30-3,28 (m, 1H), 1,26-1,44 (m, 1 H), 0,93-1,06 (m, 4 H), 0,72 (s, 9 H), 0,65-0,59 (m, 2 H), 0,43-0,5 (m, 2 H); LCMS (m/z, ES+)=409,2 (M+1).
[00497] Пример 15 (Соединение 234)
[00498] (S)-6-(трет-Бутил)-2-циклопропил-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00499] 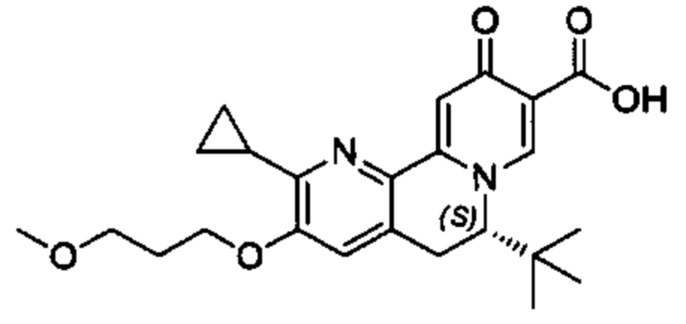
[00500] Раствор этил-(S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (46 мг, 0,10 ммоль), Pd(PPh3)4, (24 мг, 0,020 ммоль), карбоната калия (42 мг, 0,31 ммоль) и циклопропилборной кислоты (18 мг, 0,21 ммоль) в 1,4-диоксане (1,0 мл) нагревали при 100°С в течение ночи. Полученную реакционную смесь разбавляли CH2Cl2 и отфильтровывали через целит. Полученный фильтрат упаривали и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% (3:1 EtOAc:EtOH) в гексанах) с получением (S)-этил-6-(трет-бутил)-2-циклопропил-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (43,6 мг, 94%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,16 (s, 1 Н), 7,45 (s, 1 Н), 6,83 (s, 1 Н), 4,39 (q, J=7,0 Hz, 2 H), 4,13 (m, 2 H), 3,89 (d, J=6,6 Hz, 1 H), 3,62 (m, 2 H), 3,39-3,46 (m, 1 H), 3,38 (s, 3 H), 3,13 (d, J=16,8 Hz, 1 H), 2,40-2,50 (m, 1 H), 2,15 (quin, J=6,1 Hz, 2 H), 1,40 (t, J=7,0 Hz, 3 H), 1,14-1,22 (m, 1 H), 1,04-1,12 (m, 1 H), 0,93-1,02 (m, 2 H), 0,83 (s, 9 H); LCMS (m/z, ES+)=455,5 (M+1).
[00501] Раствор вышеуказанного эфира в 1М LiOH (1,2 мл) и МеОН (1,2 мл) нагревали при 50°С в течение 2 ч. Добавляли 1М лимонную кислоту (1,5 мл) и полученную реакционную смесь взбалтывали в течение 15 мин. Полученный твердый остаток собирали фильтрацией, промывали водой, и осушали с получением (S)-6-(трет-бутил)-2-циклопропил-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (27,2 мг, 62%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 16,53 (s, 1 H), 8,76 (s, 1 H), 7,43 (s, 1 H), 7,35 (s, 1 H), 4,62 (d, J=6,3 Hz, 1 H), 4,11-4,24 (m, 2 H), 3,42-3,57 (m, 4 H), 3,26 (s, 3 H), 2,41-2,46 (m, 1 H), 2,05 (quin, J=6,2 Hz, 2 H), 0,94-1,06 (m, 4 H), 0,73 (s, 9 H); LCMS (m/z, ES+)=427,2 (M+1).
[00502] Пример 16 (Соединение 235)
[00503] (R)-6-(трет-Бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00504] 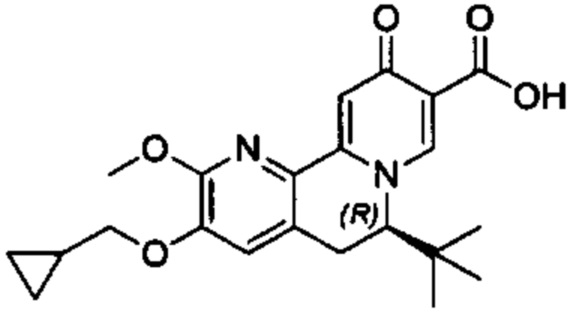
[00505] Стадия 1: (S)-N-((R)-1-(6-Хлор-5-метокситфидин-3-ил)-3,3-диметилбутан-2-ил)-2-метилпропан-2-сульфинамидом и (S)-N-((S)-1-(6-Хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-ил)-2-метилпропан-2-сульфинамид
[00506] 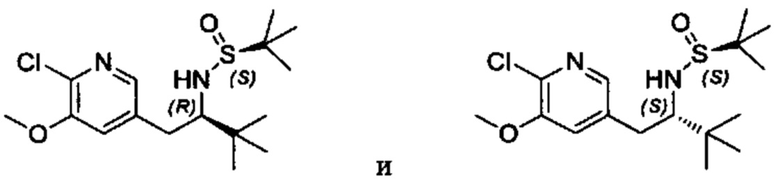
[00507] Раствор 1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-она (2,56 г, 10,57 ммоль), (S)-2-метилпропан-2-сульфинамида (2,56 г, 21,14 ммоль), Ti(OEt)4 (6,03 г, 26,4 ммоль) в толуоле (8,5 мл) взбалтывали в течение 10 минут при 60°С и указанный сосуд упаривали. Полученную реакционную смесь взбалтывали при 60°С под вакуумом в течение 24 ч. Указанный сосуд наполняли азотом, добавляли толуол (5 мл) и Ti(OEt)4 (2,4 г, 10,5 ммоль) и полученную реакционную смесь взбалтывали под вакуумом в течение 4 ч.
Указанный сосуд наполняли азотом, добавляли толуол (5 мл) и полученную реакционную смесь взбалтывали под вакуумом в течение дополнительных 3 ч. Указанную вязкую реакционную смесь затем переносили в ТГФ (70,5 мл), добавляли дополнительный Ti(OEt)4 (2,4 г, 10,5 ммоль) и указанный раствор NaBH4 (1,20 г, 31,7 ммоль), охлажденный до -30°С, добавляли порциями. Затем полученную реакционную смесь оставляли медленно нагреваться до комнатной температуры в течение ночи. Полученную реакционную смесь разбавляли ТГФ (130 мл) и насыщенным солевым раствором (3 мл), перемешивали в течение 30 мин, а затем отфильтровывали через целит. Полученный фильтрат упаривали и очищали с помощью хроматографии на силикагеле с получением двух указанных диастереомеров.
[00508] Основной диастереомер представляет собой белое твердое вещество: (S)-N-((R)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-ил)-2-метилпропан-2-сульфинамид (1,8 г, 50%). 1Н ЯМР (400 MHz, CDCl3) δ ppm 7,81 (d, J=2,0 Hz, 1 H), 7,40 (d, J=2,0 Hz, 1 H), 3,97 (s, 3 H), 3,26 (m, 1 H), 3,06-3,15 (m, 2 H), 2,72 (dd, J=14,8, 8,2 Hz, 1 H), 1,17 (s, 9 H), 0,99 (s, 9 H); LCMS (m/z, ES+)=346,8, 348,5 (M+1).
[00509] Другой диастереомер представляет собой прозрачное масло: (S)-N-((S)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-ил)-2-метилпропан-2-сульфинамид (1,2 г, 33%). 1Н ЯМР (400 MHz, CDCl3) δ ppm 7,77 (d, J=1,6 Hz, 1 H), 7,07 (d, J=1,6 Hz, 1 H), 3,93 (s, 3 H), 3,19-3,33 (m, 2 H), 3,02 (dd, J=14,1, 2,7 Hz, 1 H), 2,55 (dd, J=14,1, 10,5 Hz, 1 H), 1,08 (s, 9 H), 0,98 (s, 9 H); LCMS (m/z, ES+)=346,8, 348,0 (M+1).
[00510] Стадия 2: (R)-5-(2-Амино-3,3-диметилбутил)-2-хлорпиридин-3-ол
[00511] 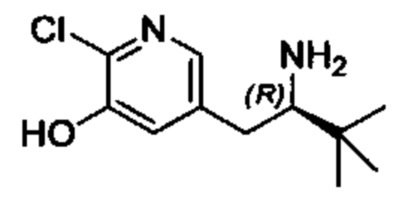
[00512] Раствор (S)-N-((R)-1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-ил)-2-метилпропан-2-сульфинамида (1,82 г, 5,26 ммоль) в 1,2-дихлорэтане (26,3 мл) взбалтывали при 0°С. Медленно добавляли трибромид бора (3,48 мл, 36,8 ммоль). Полученную реакционную смесь удаляли из охлаждающей бани и перемешивали в течение ночи при комнатной температуре. Указанный раствор охлаждали до 0°С и гасили посредством медленного добавления МеОН. Полученную суспензию упаривали. Добавляли EtOAc и полученный твердый остаток собирали фильтрацией, промывали EtOAc и осушали с получением (S)-5-(2-амино-3,3-диметилбутил)-2-хлорпиридин-3-ола, в виде бис-соли HBr. (2,1 г, рассчетн.) LCMS (m/z, ES+)=229,2, 231,2 (M+1).
[00513] Стадия 3: (R)-трет-Бутил (1-(6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамат
[00514] 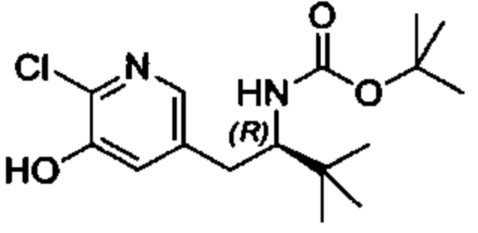
г, 2,51 ммоль) и Вос-ангидрида (0,80 г, 3,67 ммоль) в ТГФ (25,1 мл) взбалтывали при 60°С в течение 1,5 ч. Добавляли ТГФ (10 мл) и триэтиламин (0,35 мл, 2,51 ммоль) и полученную реакционную смесь взбалтывали в течение дополнительных 30 минут. Добавляли дополнительный триэтиламин (0,35 мл, 2,51 ммоль) и полученную реакционную смесь взбалтывали при 60°С в течение 1 ч. Указанный раствор затем упаривали досуха. Полученный твердый остаток суспендировали в диэтиловом эфире, отделяли с помощью фильтрации и промывали дополнительной порцией диэтилового эфира. Полученный твердый остаток переносили в EtOAc и промывали разбавленным водным NaHCCO3, и насыщенным солевым раствором. Указанную органическую фазу осушали (Na2SO4), отфильтровывали и упаривали с получением (R)-трет-бутил (1-(6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (1,01 г, 99%) в виде светло-желтого твердого вещества. LCMS (m/z, ES+) = 329,2, 331,2 (М+1).
[00516] Стадия 4: (R)-трет-Бутил-(1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамат
[00517] 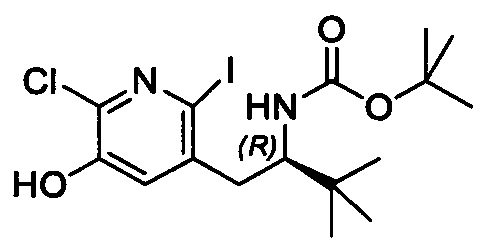
[00518] Йод (0,64 г, 2,51 ммоль) добавляли к перемешиваемому раствору трет-бутил-(R)-(1-(6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (0,83 г, 2,51 ммоль) и К2СО3 (1,04 г, 7,53 ммоль) в воде (6,3 мл) и 1,4-диоксане (6,3 мл). Полученную реакционную смесь взбалтывали при комнатной температуре в течение 1,5 ч.
[00519] Твердый Na2SO3 добавляли при перемешивании до тех пор, пока указанный раствор переставал быть темно-коричневым. Указанный раствор разбавляли солевым раствором и EtOAc. Указанную водную фазу экстрагировали EtOAc. Объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением (R)-трет-бутил-(1-(6-хлор-5-гадрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата в виде желтой пены (0,38 г, 34%). LCMS (m/z, ES+) = 455,4,457,1 (М+1).
[00520] Стадия 5: (R)-трет-Бутил-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамат
[00521] 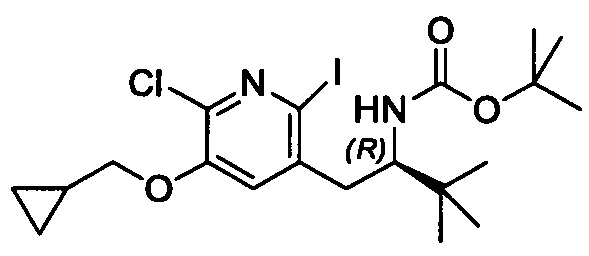
[00522] Раствор трет-бутил-(R)-(1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (0,3819 г, 0,840 ммоль), K2СО3 (0,35 г, 2,52 ммоль) и (бромметил)циклопропана (0,23 г, 1,68 ммоль) в ДМФА (5,6 мл) нагревали при 80°С в течение 3 ч. Полученную реакционную смесь упаривали досуха и полученный осадок переносили в CH2Cl2 и Н2О. Указанную водную фазу экстрагировали CH2Cl2 (2х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением трет-бутил-(E)-(1-(6-хлор-5-(1щклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (415,4 мг, 97%) в виде серовато-белого твердого вещества. LCMS (m/z, ES+) = 509,2, 511,2 (М+1).
[00523] Стадия 6: Этил-(R)-1-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
[00524] 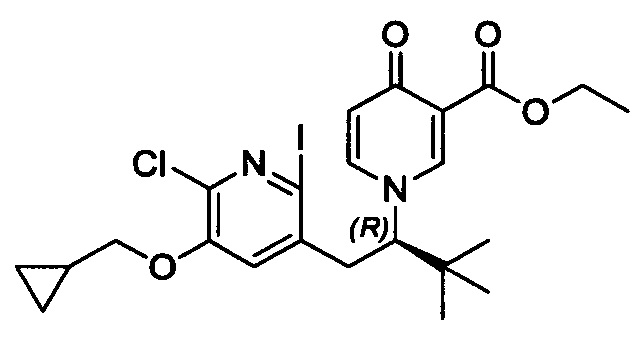
[00525] 4 М Соляную кислоту в диоксане (3,06 мл, 12,25 ммоль) добавляли к раствору трет-бутил (R)-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (0,42 г, 0,82 ммоль) в CH2Cl2 (3 мл). Полученную реакционную смесь взбалтывали при комнатной температуре в течение 3 ч и упаривали досуха. Полученный твердый остаток растворяли в CH2Cl2 (1 мл) и Et3N (1 мл), перемешивали, а затем упаривали досуха. Полученный осадок переносили в насыщенный NaHCO3 и CH2Cl2.Указанную водную фазу экстрагировали CH2Cl2 (2х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением (R)-1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-амина. Раствор вышеуказанного амина и этил-4-оксо-4Н-пиран-3-карбоксилата (151 мг, 0,90 ммоль) в уксусной кислоте (8,2 мл) взбалтывали при 100°С в течение 7 ч. Полученную реакционную смесь упаривали досуха и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением этил-(R)-1-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (389 мг, 85%) в виде светло-коричневого твердого вещества. LCMS (m/z, ES-) = 575,2, 577,2 (М-1).
[00526] Стадия 7: (R)-Этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
[00527] 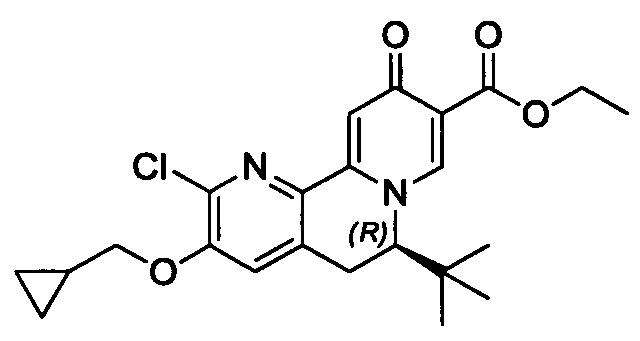
[00528] Колбу, содержащую этил-(R)-1-(1-(6-хлор-5-(циклопропилметокси)-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (0,39 г, 0,70 ммоль), ацетат калия (0,14 г, 1,39 ммоль), и бромид палладия (П) (0,037 г, 0,14 ммоль), продували азотом. Добавляли дегазированный N,N-диметилацетамид (DMA) (7,0 мл) и полученную реакционную смесь нагревали при 90°С в течение 24 ч. Указанный раствор очищали с помощью обращенно-фазовой хроматографии (10-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением этил-(R)-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (167 мг, 56%). 1H ЯМР (400 MHz, CDCl3) δ ppm 8,18 (s, 1Н), 7,49 (s, 1Н), 6,96 (s, 1Н), 4,40 (q, J=7,3 Hz, 2Н), 3,96 (d, J=7,0 Hz, 2H), 3,93 (d, J=6,6 Hz, 1H), 3,46 (dd, J=17,0, 6,8 Hz, 1H), 3,19 (d, J=16,8 Hz, 1H), 1,41 (t, 7=7,0 Hz, 3H), 1,30-1,37 (m, 1H), 0,85 (s, 9H), 0,76-0,70 (m, 2H), 0,41-0,48 (m, 2 H); LCMS (m/z, ES-) = 429,4,431,4 (M-1).
[00529] Стадия 8: (R)-6-(трет-Бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00530] 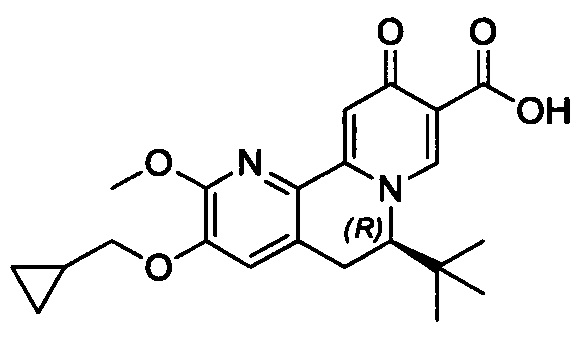
[00531] Раствор этил-(R)-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (33 мг, 0,077 ммоль), NaB(OMe)4 (36 мг, 0,23 ммоль), tBuXPhos (6,5 мг, 0,015 ммоль) и Pd2(dba)3 (7,0 мг, 7,66 мкмоль) в ДМФА (0,77 мл) нагревали при 80°С в течение 2 ч. Полученную реакционную смесь отфильтровывали через целит и указанный целит промывали EtOAc и CH2Cl2. Полученный фильтрат упаривали и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% (3:1 EtOAc:EtOH) в гексанах) с получением этил-(R)-6-(трет-бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (27 мг, 83%). 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,17 (s, 1Н), 7,42 (s, 1Н), 6,80 (s, 1Н), 4,39 (q, 7=7,0 Hz, 2H), 4,05 (s, 3H), 3,94-3,85 (m, 3H), 3,42 (dd, 7=16,6,6,8 Hz, 1H), 3,09 (d, J=16,8 Hz, 1H), 1,37-1,40 (t, 7=7,2 Hz, 4H), 1,27-1,37 (m, 1H), 0,85 (s, 9H), 0,66-0,75 (m, 2H), 0,42-0,37 (m, 2H); LCMS (m/z, ES+) = 427,4 (M+1).
[00532] Раствор вышеуказанного эфира в 1M LiOH (1 мл) и МеОН (1 мл) нагревали при 50°С в течение 2 ч. Полученную реакционную смесь отфильтровывали через фильтр Acrodisc для удаления оставшихся мелких частиц и к указанному чистому фильтрату добавляли 1М лимонную кислоту (1 мл). Указанный осадок собирали фильтрацией, промывали водой и осушали с получением (R)-6-(трет-бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (19 мг, 62% для 2-х стадий) в виде серовато-белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 16,53 (s, 1H), 8,77 (s, 2H), 7,40 (s, 2H), 7,36 (s, 2H), 4,62 (d, J=6,8 Hz, 1H), 3,97 (s, 3H), 3,96-3,89 (m, 2H), 3,49-3,40 (m, 1H), 1,22-1,32 (m, 1H), 0,75 (s, 9H), 0,57-0,65 (m, 2H), 0,31-0,40 (m, 2H); LCMS (m/z, ES+) = 399,2 (M+1).
[00533] Пример 17 (Соединение 236)
[00534] (S)-6-(трет-Бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00535] 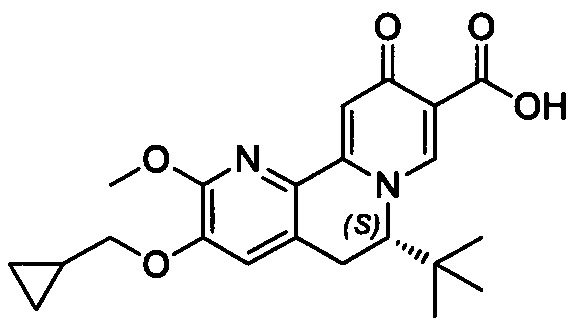
[00536] Раствор этил-(S)-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-b][1,7]нафтиридин-9-карбоксилата (52 мг, 0,12 ммоль), NaB(OMe)4 (57 мг, 0,36 ммоль), tBuXPhos (10,3 мг, 0,024 ммоль) и Pd2(dba)3 (11,0 мг, 0,012 ммоль) в ДМФА (1,2 мл) нагревали при 80°С в течение 2 ч. Полученную реакционную смесь отфильтровывали через целит и указанный целит промывали EtOAc и CH2Cl2. Полученный фильтрат упаривали и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% (3:1 EtOAc:EtOH) в гексанах) с получением этил-(S)-6-(трет-бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафгиридин-9-карбоксилата (32 мг, 62%). 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,17 (s, 1Н), 7,44 (s, 1Н), 6,80 (s, 1Н), 4,40 (q, 7=7,2 Hz, 2H), 4,06 (s, 3H), 3,89 (m, 3H), 3,42 (dd, 7=16,8, 7,0 Hz, 1H), 3,09 (d, J=16,4 Hz, 1H), 1,40 (t, 7=7,0 Hz, 3H), 1,31-1,37 (m, 1H), 0,84 (s, 9H), 0,68-0,75 (m, 2H), 0,36-0,43 (m, 2 H); LCMS (m/z, ES+) = 427,4 (M+1).
[00537] Раствор вышеуказанного эфира в 1М LiOH (0,75 мл) и МеОН (0,75 мл) нагревали при 50°С в течение 2 ч, к полученной реакционной смеси добавляли 1М лимонную кислоту (0,75 мл) и указанный осадок собирали фильтрацией, промывали водой и осушали с получением (S)-6-(трет-бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (26,5 мг, 55% для 2-х стадий) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 16,11 (s, 1H), 8,45 (s, 1H), 7,65 (s, 1H), 6,83 (s, 1H), 4,08 (s, 3H), 4,04 (d,.7=6,8 Hz, 1H), 3,92 (m, 2H), 3,48 (dd, J=17,1, 7,3 Hz, 1H), 3,16 (d, J=17,1 Hz, 1H), 1,31-1,43 (m, 1H), 0,86 (s, 9H), 0,69-0,78 (m, 2H), 0,41 (m, 2 H); LCMS (m/z, ES+) = 399,3 (M+1).
[00538] Пример 18 (Соединение 237)
[00539] (S)-6-(трет-Бутил)-3-(циклопропилметокси)-2-гидрокси-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1.7]нафтиридин-9-карбоксиловая кислота
[00540] 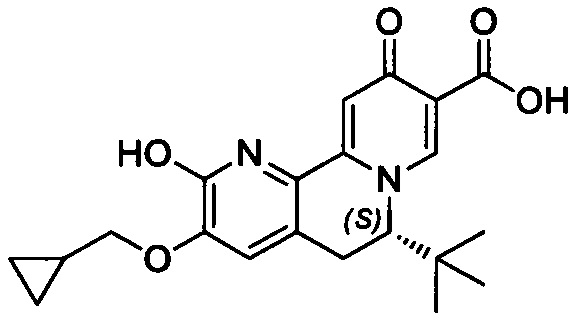
[00541] Деметилированный продукт образовывался в качестве побочного продукта реакции, в которой получали этил-(S)-6-(трет-бутил)-3-(циклопропилметокси)-2-метокси-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат, и его собирали в виде смешанных фракций, которые затем комбинировали. Повторная очистка с помощью обращенно-фазовой хроматографии (10-100% CH3CN/H2O (0,1% муравьиная кислота)) позволила получить (S)-этил-6-(трет-бутил)-3-(циклопропилметокси)-2-гидрокси-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат(8,3 мг, 17%). 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,18 (s, 1Н), 6,85 (s, 1Н), 6,55 (s, 1Н), 4,37 (q, J=7,0 Hz, 2H), 3,83-3,97 (m, 3H), 3,33 (dd, J=16,8, 6,6 Hz, 1H), 2,95 (d, J=17,2 Hz, 1H), 1,33-1,42 (m, 4H), 0,65-0,74 (m, 2H), 0,40 (m, 2 H); LCMS (m/z, ES+) = 413,3 (M+1).
[00542] Раствор вышеуказанного эфира в 1М LiOH (0,5 мл) и МеОН (0,5 мл) нагревали при 50°С в течение 2 ч. 1М лимонную кислоту (0,5 мл) добавляли к полученной реакционной смеси и указанный раствор очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением (S)-6-(трет-бутил)-3-(циклопропилметокси)-2-гидрокси-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (6,4 мг, 14% для 2-х стадий) в виде желтого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 15,72 (br. s., 1H), 8,44 (s, 1H), 7,38 (s, 1H), 6,66 (s, 1H), 4,04 (d, J=4,9 Hz, 1H), 3,96 (d, J=6,8 Hz, 2H), 3,40-3,53 (m, 1H), 3,04 (d, J=17,1 Hz, 1H), 1,34-1,45 (m, 1H), 0,89 (s, 9H), 0,77-0,72 (m, 2H), 0,47-0,42 (m, 2 H); LCMS (m/z, ES+) = 385,2 (M+1).
[00543] Пример 19 (Соединение 238)
[00544] (S)-6-(трет-Бутил)-2-метокси-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1.2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00545] 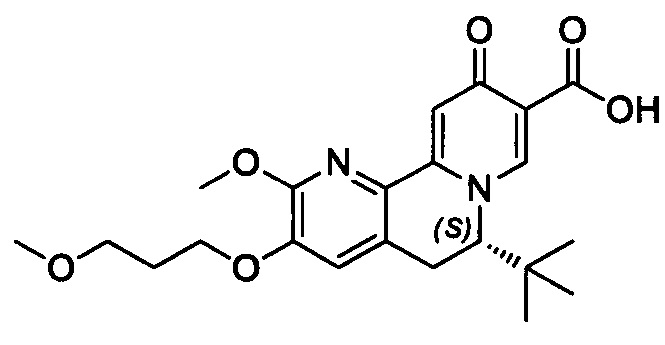
[00546] Раствор этил-(8)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-b][1,7]нафтиридин-9-карбоксилата (46,8 мг, 0,10 ммоль), NaB(OMe)4 (49 мг, 0,31 ммоль), tBuXPhos (8,9 мг, 0,021 ммоль) и Pd2(dba)3 (9,6 мг, 0,010 ммоль) в ДМФА (1,0 мл) нагревали при 80°С в течение 2 ч. Полученную реакционную смесь отфильтровывали через целит и указанный целит промывали CH2Cl2. Полученный фильтрат упаривали и полученный осадок использовали в тех же условиях указанной реакционной смеси с дополнительными реагентами: NaB(OMe)4 (49 мг, 0,31 ммоль), tBuXPhos (8,9 мг, 0,021 ммоль) и Pd2(dba)3 (9,6 мг, 0,010 ммоль) в ДМФА (1,0 мл) при 80°С в течение дополнительных 3 ч. Полученную реакционную смесь отфильтровывали через целит и указанный целит промывали CH2Cl2. Полученный фильтрат упаривали и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% (3:1 EtOAc:EtOH) в гексанах) с получением этил-(S)-6-(трет-бутил)-2-метокси-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата в виде светло-коричневого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,18 (s, 1Н), 7,44 (s, 1Н), 6,86 (s, 1Н), 4,40 (q, 7=7,3 Hz, 2H), 4,19 - 4,12 (m, 2H), 4,05 (s, 3H), 3,90 (d, J=6,6 Hz, 1H), 3,61-3,55 (m, 2H), 3,42 (dd, J=16,8, 7,0 Hz, 1H), 3,37 (s, 3H), 3,11 (d, J=16,8 Hz, 1H), 2,15 (quin, J=6,2 Hz, 2H), 1,40 (t, J=7,0 Hz, 3H), 0,86 (s, 9H); LCMS (m/z, ES+) = 445,0 (M+1).
[00547] Раствор вышеуказанного эфира в 1М LiOH (0,75 мл) и МеОН (0,75 мл) нагревали при 50°С в течение 2 ч. К полученной реакционной смеси добавляли 1М лимонную кислоту (0,75 мл) и указанный раствор очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением (S)-6-(трет-бутил)-2-метокси-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (19,6 мг, 45% для 2-х стадий) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 16,12 (s, 1H), 8,46 (s, 1H), 7,65 (s, 1H), 6,90 (s, 1H), 4,24-4,13 (m, 2H), 4,06 (s, 1H), 3,63-3,55 (m, 2H), 3,49 (dd, J=16,6, 6,3 Hz, 1H), 3,38 (s, 3H), 3,18 (d, J=17,1 Hz, 1H), 2,16 (quin, J=6,1 Hz, 2H), 0,87 (s, 9H); LCMS (m/z, ES+) = 417,2 (M+1).
[00548] Пример 20 (Соединение 239)
[00549] (S)-6-(трет-Бутил)-2-гидрокси-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1.2-h][1.7]нафтиридин-9-карбоксиловая кислота
[00550] 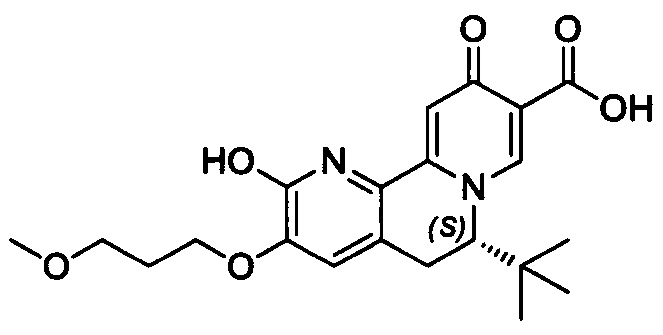
[00551] Деметилированный продукт образовывался в качестве побочного продукта реакции, в которой получали этил-(S)-6-(трет-бутил)-2-метокси-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат, и его собирали в виде смешанных фракций, которые затем комбинировали и подвергали гидролизу без дальнейшей очистки. Раствор указанного эфира в 1М LiOH (0,5 мл) и МеОН (0,5 мл) нагревали при 50°С в течение 2 ч. К полученной реакционной смеси добавляли 1М лимонную кислоту (0,5 мл) и указанный раствор очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением (S)-6-(трет-бутил)-2-гидрокси-3-(3-метоксигфопокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (3,4 мг, 8% для 2-х стадий) в виде желтого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 15,76 (br. s., 1H), 8,42 (s, 1H), 7,47 (s, 1H), 6,70 (s, 1H), 4,20 (t, 7=6,1 Hz, 2H), 4,04 (d, J=6,3 Hz, 1H), 3,61-3,76 (m, 2H), 3,48 (dd, J=17,1, 6,8 Hz, 1H), 3,41 (s, 3H), 3,04 (d, J=17,1 Hz, 1H), 2,21 (quin, J=6,0 Hz, 2H), 0,89 (s, 9H); LCMS (m/z, ES+) = 403,2 (M+1).
[00552] Пример 21 (Соединение 240)
[00553] (S)-6-(трет-Бутил)-3-(3-метоксипропокси)-10-оксо-2-(проп-1-ен-2-ил)-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00554] 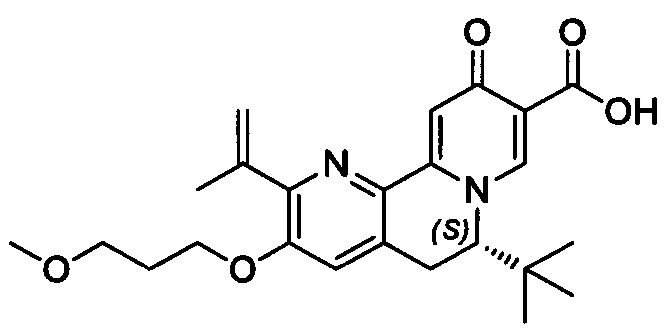
[00555] Стадия 1: (S)-Этил-6-(трет-бутил)-3-(3-метоксипропокси)-10-оксо-2-(проп-1-ен-2-ил)-6,10-дигидро-5Н-пиридо[1.2-h][1.7]нафтиридин-9-карбоксилат
[00556] 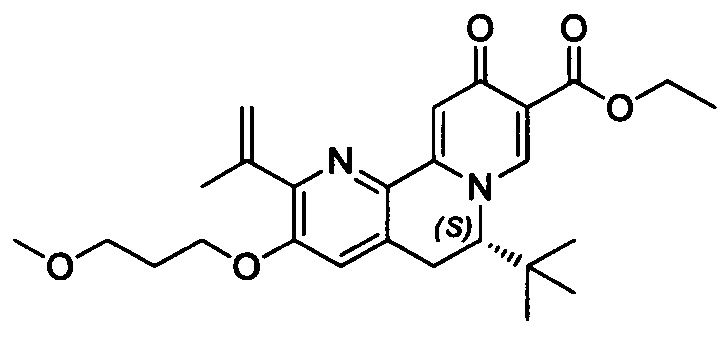
[00557] Раствор этил-(S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (88,4 мг, 0,20 ммоль), изопропенилтрифторбората калия (58 мг, 0,39 ммоль),карбоната натрия (63 мг, 0,59 ммоль) и Pd(PPh3)4 (23 мг, 0,020 ммоль) в этаноле (2,0 мл) взбалтывали при 80°С в течение ночи. Полученную реакционную смесь разбавляли CH2Cl2 и отфильтровывали через целит. Полученный фильтрат упаривали и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% (3:1 EtOAc:EtOH) в гексанах) с получением этил-(S)-6-(трет-бутил)-3-(3-метоксипропокси)-10-оксо-2-(проп-1-ен-2-ил)-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (87,5 мг, 98%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,18 (s, 1Н), 7,54 (s, 1Н), 7,00 (s, 1Н), 5,91 (s, 1Н), 5,54 (s, 1Н), 4,39 (q, J=7,0 Hz, 2H), 4,07-4,22 (m, 2H), 3,93 (d, J=6,6 Hz, 1H), 3,61-3,56 (m, 2H), 3,48 (dd, J=17,0, 6,8 Hz, 1H), 3,37 (s, 3H), 3,19 (d, J=16,8 Hz, 1H), 2,25 (s, 3H), 2,13 (quin, J=6,1 Hz, 2H), 1,40 (t, 7=7,2 Hz, 3H), 0,85 (s, 9H); LCMS (m/z, ES+) = 455,9 (M+1).
[00558] Стадия 2: (S)-6-(трет-Бутил)-3-(3-метоксипропокси)-10-оксо-2-(проп-1-ен-2-ил)-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00559] 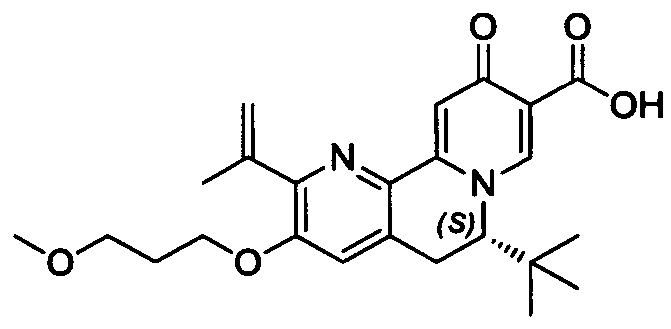
[00560] Соединение, указанное в названии выделяли в качестве побочного продукта с помощью гидролиза в щелочных условиях в процессе реакции окисления этил-(S)-6-(трет-бутил)-3-(3-метоксипропокси)-10-оксо-2-(проп-1-ен-2-ил)-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (30,3 мг, 0,067 ммоль) с помощью йодида триметилсульфоксония (31 мг, 0,14 ммоль) и KOtBu (15 мг, 0,13 ммоль) в DMSO (0,64 мл) и ТГФ (0,27 мл). Очистка полученной реакционной смеси с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) приводила к получению (S)-6-(трет-бутил)-3-(3-метоксипропокси)-10-оксо-2-(проп-1-ен-2-ил)-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (4,8 мг, 17%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 16,16 (s, 1H), 8,47 (s, 1H), 7,78 (s, 1H), 7,04 (s, 1H), 5,95 (s, 1H), 5,59 (s, 1H), 4,26-4,12 (m, 2H), 4,07 (d, J=6,8 Hz, 1H), 3,62-3,57 (m, 2H), 3,53 (dd, J=17,3, 7,1 Hz, 1H), 3,38 (s, 3H), 3,26 (d, J=17,1 Hz, 1H), 2,26 (s, 3H), 2,15 (quin, J=6,0 Hz, 2H), 0,87 (s, 9H); LCMS (m/z, ES+) = 427,3 (M+1).
[00561] Пример 22: (Соединение 241)
[00562] (S)-6-(трет-Бутил)-2-изопропил-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00563] 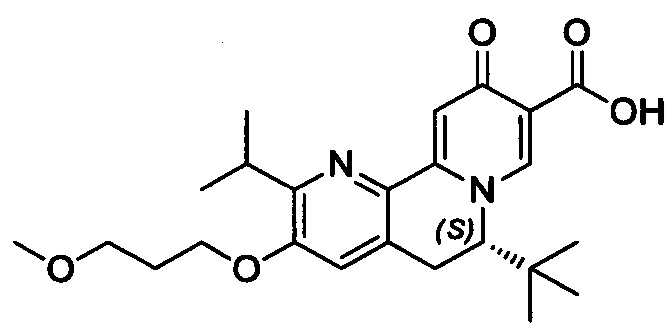
[00564] Раствор этил-(S)-6-(трет-бутил)-3-(3-метоксипропокси)-10-оксо-2-(проп-1-ен-2-ил)-5,10-дигадро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (11,9 мг, 0,026 ммоль) и 10% Pd/C (каталитический) в МеОН (1 мл) взбалтывали в условиях 60 фунт/кв. дюйм H2 в течение 1,5 ч. Полученную реакционную смесь отфильтровывали через целит и упаривали досуха с получением неочищенного вещества (S)-этил-6-(трет-бутил)-2-изопропил-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата, который использовали без дальнейшей очистки.
[00565] Раствор вышеуказанного эфира в 1М LiOH (0,7 мл) и МеОН (0,7 мл) нагревали при 50°С в течение 2 ч. 1М лимонную кислоту (0,8 мл) добавляли и полученную реакционную смесь взбалтывали в течение 15 мин. Указанный осадок собирали фильтрацией, промывали водой и осушали с получением (S)-6-(трет-бутил)-2-изопропил-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (9,3 мг, 83% для двух стадий) в виде серовато-белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 16,26 (s, 1H), 8,46 (s, 1H), 7,83 (s, 1H), 6,91 (s, 1H), 4,08-4,21 (m, 2H), 4,05 (d, J=6,8 Hz, 1H), 3,66-3,58 (m, 2H), 3,41-3,55 (m, 2H), 3,38 (s, 3H), 3,22 (d, J=17,1 Hz, 1H), 2,14 (quin, J=6,0 Hz, 2H), 1,27 (d, J=6,8 Hz, 6 H), 0,85 (s, 9H); LCMS (m/z, ES+) = 429,3 (M+1).
[00566] Пример 23: (Соединение 243)
[00567] (S)-6-(трет-Бутил)-2-хлор-3-(3-метоксипропокси)-8-метил-10-оксо-6,10-дигидро-5Н-пиридо[1.2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00568] 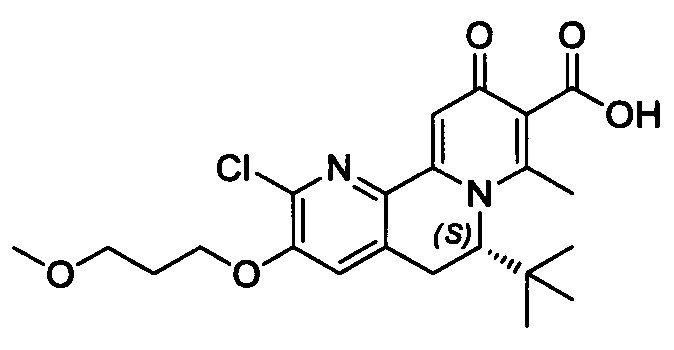
[00569] Стадия 1: Этил-2-метил-4-оксо-4Н-пиран-3-карбоксилат
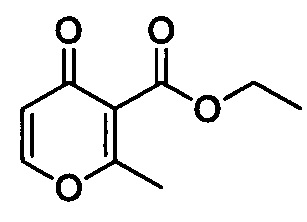
[00570] Раствор этил-3-оксобутаноата (3,64 г, 28 ммоль) в 20 мл ТГФ добавляли с помощью шприцевого насоса (по каплям) в сосуд, содержащий NaH (60% дисперсия в минеральном масле) (1,176 г, 29,4 ммоль), который охлаждали при 0°С в процессе добавления. Полученную реакционную смесь взбалтывали при комнатной температуре в течение 1 ч после того, как добавление было завершено, а затем охлаждали обратно до 0°С.Раствор 3-хлоракрилоилхлорида (3,50 г, 28 ммоль) в 20 мл ТГФ медленно добавляли к указанной охлаждаемой реакционной смеси с помощью шприцевого насоса в течение более 1 ч. После того, как добавление было завершено, полученную реакционную смесь взбалтывали при комнатной температуре в течение ночи, а затем грели с обратным холодильником в течение 2,5 ч. Полученную реакционную смесь разбавляли водой и экстрагировали Et2O (4х) и CH2Cl2 (2х). Объединенные органические экстракты осушали (Na2SO4), отфильтровывали, упаривали и очищали с помощью хроматографии на силикагеле (0-100% EtOAc/гексаны) с получением этил-2-метил-4-оксо-4Н-пиран-3-карбоксилата (2,65 г, 52%) в виде коричневой жидкости. 1Н ЯМР (400 MHz, CDCl3) δ ppm 7,66 (d, J=5,9 Hz, 1H), 6,36 (d, J=5,9 Hz, 1H), 4,39 (q, J=7,3 Hz, 2H), 2,38 (s, 3H), 1,38 (t, J=7,2 Hz, 3H); LCMS (m/z, ES+) = 183,1 (M+1).
[00571] Стадия 2: (S)-Этил-1-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбуган-2-ил)-2-метил-4-оксо-1,4-дигидропиридин-3-карбоксилат
[00572] 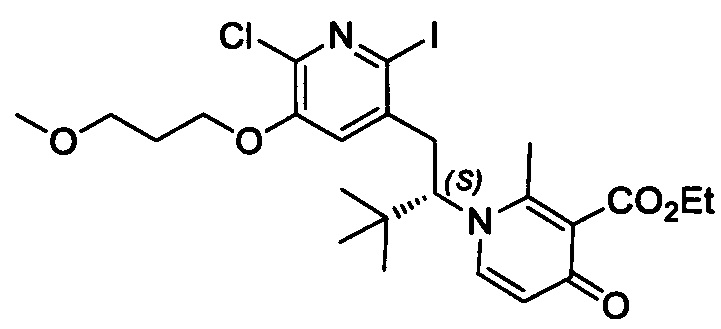
[00573] Раствор (S)-1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-амина, соляной кислоты (196 мг, 0,42 ммоль) и этил-2-метил-4-оксо-4Н-пиран-3-карбоксилата (0,23 г, 1,27 ммоль) в НОАс (4,2 мл) взбалтывали при 100°С в течение 10 ч. Полученную реакционную смесь упаривали досуха, растворяли в CH2Cl2 и насыщенном NaHCO3 и перемешивали в течение 1 ч. Указанную органическую фазу выделяли, осушали (Na2SO4), отфильтровывали и упаривали. Полученный осадок взбалтывали с дополнительным этил-2-метил-4-оксо-4Н-пиран-3-карбоксилатом (200 мг, 1,10 ммоль) в НОАс (4,2 мл) при 100°С в течение ночи. Полученную реакционную смесь упаривали досуха и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением этил-(S)-1-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-2-метил-4-оксо-1,4-дигидропиридин-3-карбоксилата (67,4 мг, 27%) в виде коричневого твердого вещества. LCMS (m/z, ES+) = 591,2, 593,2 (M+1).
[00574] Стадия 3: (S)-Этил-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-8-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
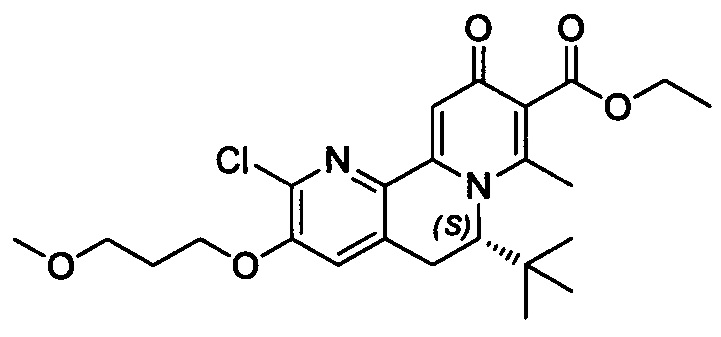
[00575] Колбу, содержащую этил-(S)-1-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-2-метил-4-оксо-1,4-дигидропиридин-3-карбоксилат (67,4 мг, 0,11 ммоль), ацетат калия (22 мг, 0,23 ммоль) и бромид палладия (II) (6,1 мг, 0,023 ммоль), продували азотом. Добавляли дегазированный ДМФА (1,1 мл) и полученную реакционную смесь нагревали при 90°С в течение 24 ч. Указанный раствор охлаждали до комнатной температуры, добавляли дополнительный бромид палладия (II) (6,1 мг, 0,023 ммоль) и полученную реакционную смесь нагревали при 90°С еще в течение 6 ч. Указанный растворитель удаляли упариванием и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% 3:1 (EtOAc/EtOH) в гексанах) с получением этил-(S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-8-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата(12,1 мг, 23%) в виде коричневого масла. 1Н ЯМР (400 MHz, CDCl3) δ ppm 7,48 (s, 1Н), 7,00 (s, 1Н), 4,34-4,45 (m, 3 Н), 4,13-4,24 (m, 2Н), 3,65-3,58 (m, 2Н), 3,31-3,41 (m, 4Н), 3,15 (d, J=16,8 Hz, 1H), 2,45 (s, 3H), 2,12-2,19 (m, 2H), 1,38 (t, J=7,2 Hz, 3H), 0,80 (s, 9H); LCMS (m/z, ES+) = 463,3,465,3 (M+1).
[00576] Стадия 4: (S)-6-(трет-Бутил)-2-хлор-3-(3-метоксипропокси)-8-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00577] 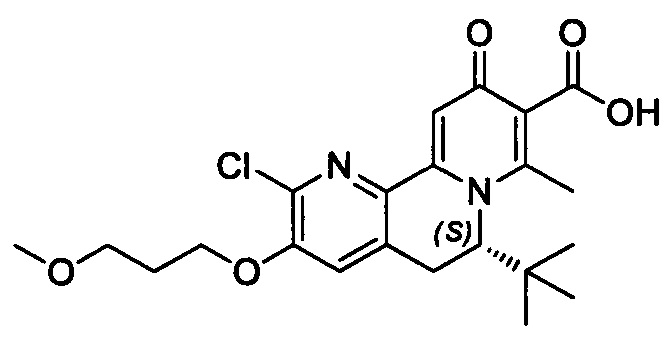
[00578] Раствор (S)-этил-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-8-метил-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (12,1 мг, 0,026 ммоль) в 1М LiOH (0,5 мл) и МеОН (0,5 мл) нагревали при 50°С в течение 2 ч, а затем при 60°С в течение 2 ч. К полученной реакционной смеси добавляли 1М лимонную кислоту (0,7 мл). Указанный раствор упаривали досуха и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-90% CH3CN/H2O (0,1% муравьиная кислота)) с получением (S)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-8-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (7,0 мг, 62%) в виде белого твердого вещества. 1H ЯМР (400 MHz, CDCl3) δ ppm 17,61 (br. s., 1H), 7,82 (s, 1H), 7,05 (s, 1H), 4,81 (d, J=5,4 Hz, 1H), 4,15-4,28 (m, 2H), 3,67-3,57 (m, 2H), 3,49-3,41 (m, 1H), 3,38 (s, 3H), 3,25 (d, J=17,6 Hz, 1H), 3,18 (s, 3H), 2,17 (quin, 7=6,0 Hz, 2H), 0,81 (s, 9H); LCMS (m/z, ES+) = 435,2, 437,2 (M+1).
[00579] Пример 24: (Соединение 243)
[00580] (S)-6-(трет-Бутил)-2-(гидроксиметил)-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00581] 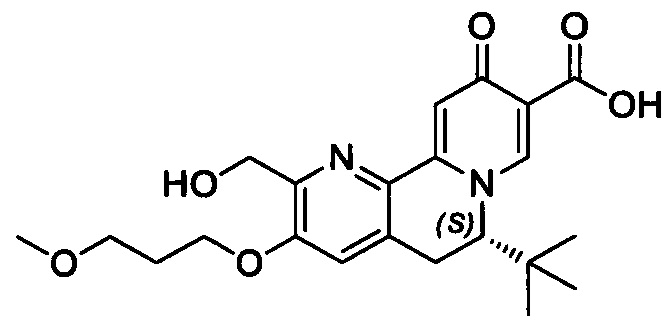
[00582] Стадия 1: (S)-трет-Бутил-(1-(5-(бензилокси)-6-хлор-2-йодпиридин-3-ил)-3,3-диметилбуган-2-ил)карбамат
[00583] 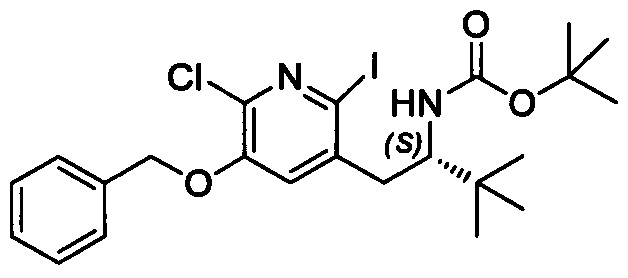
[00584] Раствор трет-бутил-(S)-(1-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (2,18 г, 4,79 ммоль), K2СО3 (1,99 г, 14,38 ммоль), (бромметил)бензола (0,86 мл, 7,19 ммоль) в ДМФА (32,0 мл) нагревали при 80°С в течение 3 ч. Полученную реакционную смесь упаривали досуха и полученный осадок переносили в CH2Cl2 и водой. Указанную водную фазу экстрагировали CH2Cl2 (2х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали с получением трет-бутил-(S)-(1-(5-(бензилокси)-6-хлор-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (расчетное количество), который переносили на следующую стадию без дальнейшей очистки. LCMS (m/z, ES+) = 545,4, 547,0 (M+1).
[00585] Стадия 2: Этил-(S)-1-(1-(5-(бензилокси)-6-хлор-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
[00586] 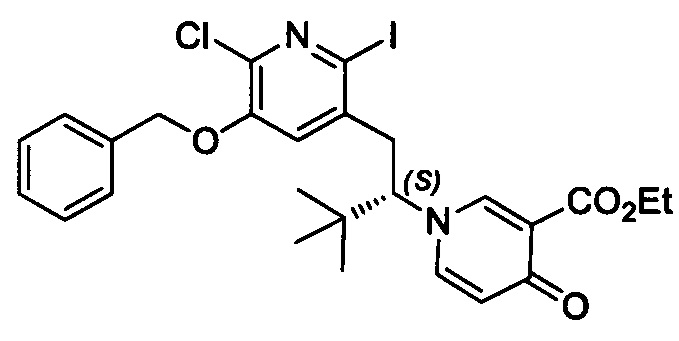
[00587] HCl (4М в диоксане) (11,98 мл, 47,9 ммоль) добавляли к раствору трет-бутил-(S)-(1-(5-(бензилокси)-6-хлор-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (2,61 г, 4,79 ммоль) в CH2Cl2 (6 мл) и полученную реакционную смесь взбалтывали при комнатной температуре в течение 3 ч. Указанную смесь упаривали досуха и полученный осадок переносили в насыщенный NaHCO3 и CH2Cl2. Указанную водную фазу экстрагировали CH2Cl2 (2х) и объединенные органические фазы осушали (Na2SO4), отфильтровывали, упаривали и получали коричневое масло.
[00588] Раствор вышеуказанного амина и этил-4-оксо-4Н-пиран-3-карбоксилата (0,89 г, 5,27 ммоль) в НОАс (24 мл) взбалтывали при 100°С в течение 7 ч. Полученную реакционную смесь упаривали, полученный осадок переносили в CH2Cl2 и насыщенный NaHCO3, и указанный раствор энергично взбалтывали в течение 30 мин. Указанную водную фазу экстрагировали CH2Cl2 (5×10 мл), и объединенные органические фазы осушали (Na2SO4), отфильтровывали, упаривали и очищали с помощью хроматографии на силикагеле (0-100% (3:1 EtOAc:EtOH) в гексанах) с получением этил-(S)-1-(1-(5-(бензилокси)-6-хлор-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилата (1,39 г, 49%) в виде коричневого твердого вещества. LCMS (m/z, ES+) = 596,1, 597,2 (M+1).
[00589] Стадия 3: Этил-(S)-3-(бензилокси)-6-(трет-бутил)-2-хлор-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
[00590] 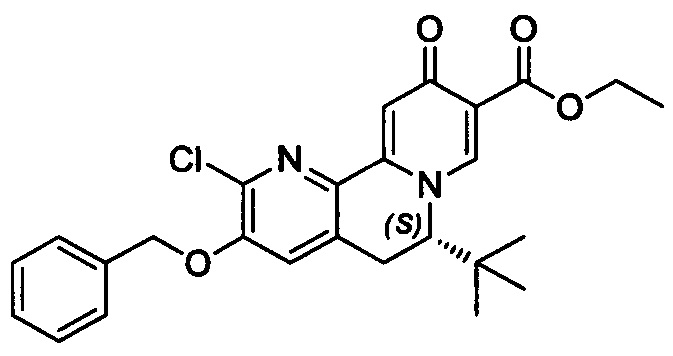
[00591] Колбу, содержащую этил-(S)-1-(1-(5-(бензилокси)-6-хлор-2-йодпиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (1,39 г, 2,34 ммоль), ацетат калия (460 мг, 4,68 ммоль), и бромид палладия (II) (125 мг, 0,47 ммоль) продували азотом. Добавляли дегазированный ДМФА (23,4 мл) и полученную реакционную смесь нагревали при 90°С в течение 24 ч. Указанный растворитель удаляли упариванием и полученный осадок растворяли в CH2Cl2, отфильтровывали через целит и очищали с помощью хроматографии на силикагеле (0-100% 3:1 (EtOAc/EtOH) в гексанах) с получением этил-(S)-3-(бензилокси)-6-(трет-бутил)-2-хлор-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (706 мг, 65%) в виде коричневого твердого вещества. LCMS (m/z, ES+) = 467,3,469,3 (M+1).
[00592] Стадия 4: Этил-(S)-3-(бензилокси)-6-(трет-бутил)-10-оксо-2-винил-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
[00593] 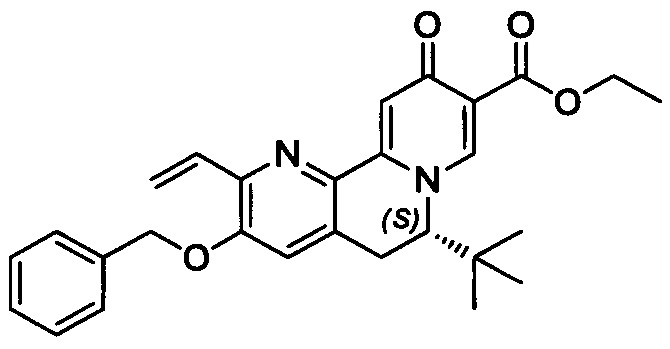
[00594] Раствор этил-(S)-3-(бензилокси)-6-(трет-бутил)-2-хлор-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (0,34 г, 0,74 ммоль), калиевой соли трифтор(винил)-14-борана (0,20 г, 1,48 ммоль), карбоната натрия (0,24 г, 2,22 ммоль) и Pd(PPh3)4 (85 мг, 0,074 ммоль) в EtOH (7,4 мл) взбалтывали при 80°С в течение ночи. Полученную реакционную смесь разбавляли CH2Cl2, отфильтровывали через целит, и упаривали. Полученный осадок очищали с помощью хроматографии на силикагеле (0-100% 3:1 (EtOAc/EtOH) в гексанах) с получением этил-(S)-3-(бензилокси)-6-(трет-бутил)-10-оксо-2-винил-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (251 мг, 74%) в виде сероватой пены. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,21 (s, 1H), 7,39-7,73 (m, 7H), 7,00 (s, 1H), 6,59 (d, J=6,6 Hz, 1H), 5,54 (d, J=10,5 Hz, 1H), 5,09-5,24 (m, 2H), 4,40 (q, J=7,0 Hz, 2H), 3,90-4,01 (m, 1H), 3,39-3,55 (m, 1H), 3,13-3,24 (m, 1H), 1,41 (t, J=7,0 Hz, 3H), 0,84 (s., 9H); LCMS (m/z, ES+) = 459,1,460,4 (M+1).
[00595] Стадия 5: (S)-Этил-6-(трет-бутил)-3-гидрокси-2-(гидроксиметил)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
[00596] 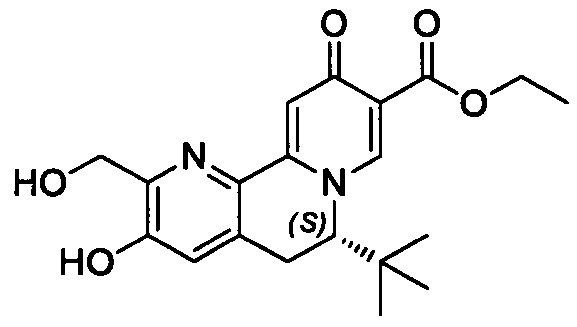
[00597] К раствору этил-(S)-3-(бензилокси)-6-(трет-бутил)-10-оксо-2-винил-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (251 мг, 0,55 ммоль) в ТГФ (5,5 мл) и воде (1,4 мл) при 0°С добавляли дигидрат осмата калия (20,2 мг, 0,055 ммоль), а затем перйодат натрия (468 мг, 2,19 ммоль). После того, как добавление было завершено, полученную реакционную смесь взбалтывали при комнатной температуре в течение 2 ч. Полученную реакционную смесь разбавляли CH2Cl2 и водой, перемешивали и отфильтровывали через целит. Объединенные органические фазы осушали (Na2SO4), отфильтровывали, упаривали и очищали с помощью хроматографии на силикагеле (0-100% 3:1 (EtOAc/EtOH) в CH2Cl2) с получением этил-(S)-3-(бензилокси)-6-(трет-бутил)-2-формил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (предполагаемый расчет). LCMS (m/z, ES+) = 461,3 (M+1).
[00598] Раствор вышеуказанного альдегида и 10% Pd/C (каталитический) в EtOH (20 мл) взбалтывали при 60 фунт/кв. дюйм H2 в течение ночи. Полученную реакционную смесь отфильтровывали через целит и упаривали с получением этил-(S)-6-(трет-бутил)-3-гидрокси-2-(гидроксиметил)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (122,1 мг, 60%), который переносили на следующую стадию без очистки. LCMS (m/z, ES+) = 373,3 (M+1).
[00599] Стадия 6: Этил-(S)-6-(трет-бутил)-2-(гидроксиметил)-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1.7]нафтиридин-9-карбоксилат
[00600] 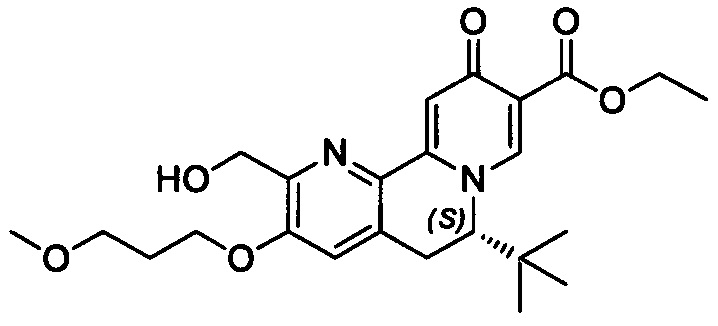
[00601] 1-Бром-3-метоксипропан (44,3 мкл, 0,39 ммоль) добавляли к раствору этил-(S)-6-(трет-бутил)-3-гидрокси-2-(гидроксиметил)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (122,1 мг, 0,33 ммоль) и карбоната калия (136 мг, 0,98 ммоль) в ДМФА (3,3 мл) и полученную реакционную смесь взбалтывали при комнатной температуре в течение ночи. Добавляли дополнительный карбонат калия (100 мг, 0,72 ммоль) и 1-бром-3-метоксипропан (44,3 мкл, 0,39 ммоль) и полученную реакционную смесь нагревали при 40°С в течение 2,5 ч, а затем перемешивали при комнатной температуре в течение ночи. Указанный растворитель упаривали и полученный осадок разбавляли CH2Cl2 и насыщенным солевым раствором. Указанную органическую фазу осушали (Na2SO4), отфильтровывали, упаривали и очищали с помощью хроматографии на силикагеле (0-100% 3:1 (EtOAc/EtOH) в CH2Cl2) с получением этил-(S)-6-(трет-бутил)-2-(гидроксиметил)-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (62,8 мг, 43%) в виде желтого масла. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,18 (s, 1Н), 7,44 (s, 1Н), 6,98 (s, 1Н), 4,72 (s, 2Н), 4,39 (q, J=7,2 Hz, 2H), 4,22-4,12 (m, 2H), 3,90-4,06 (m, 2H), 3,61-3,53 (m, 3H), 3,37 (s, 3H), 3,21 (d, J=16,8 Hz, 1H), 2,11 (quin, J=6,0 Hz, 2H), 1,40 (t, J=7,2 Hz, 3H), 0,83 (s, 9H); LCMS (m/z, ES+) = 445,3 (M+1).
[00602] Стадия 7: (S)-6-(трет-Бутил)-2-(гидроксиметил)-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
[00603] 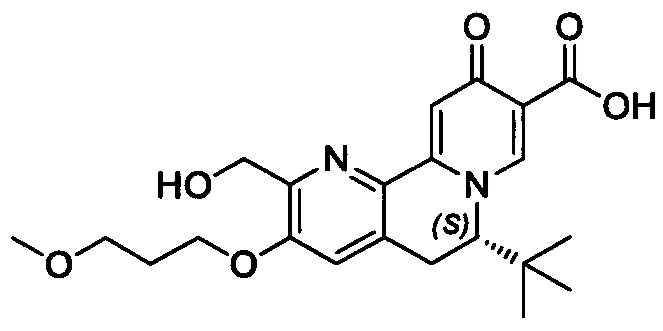
[00604] Раствор этил-(S)-6-(трет-бутил)-2-(гидроксиметил)-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (29 мг, 0,065 ммоль) в 1М LiOH (0,65 мл) и МеОН (0,65 мл) нагревали при 50°С в течение 2 ч. Добавляли 1М лимонную кислоту (1 мл) и полученную реакционную смесь упаривали досуха. Полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-90% CH3CN/H2O (0,1% муравьиная кислота)) с получением (S)-6-(трет-бутил)-2-(гидроксиметил)-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (18,5 мг, 68%) в виде белого твердого вещества. 1H ЯМР (400 MHz, CDCl3) δ ppm 15,96 (s, 1Н), 8,49 (s, 1Н), 7,74 (s, 1Н), 7,02 (s, 1Н), 4,79 (d, J=4,4 Hz, 2H), 4,14-4,27 (m, 2H), 4,10 (d, J=6,3 Hz, 1H), 3,90 (t, J=4,9 Hz, 1H), 3,62-3,53 (m, 3H), 3,37 (s, 3H), 3,29 (d, J=17,1 Hz, 1H), 2,13 (quin, J=5,9 Hz, 2H), 0,86 (s, 9H); LCMS (m/z, ES-) = 415,3 (M-1).
[00605] Пример 25: (Соединение 244)
[00606] (S)-6-(трет-Бутил)-2-циклопропил-11-гидрокси-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
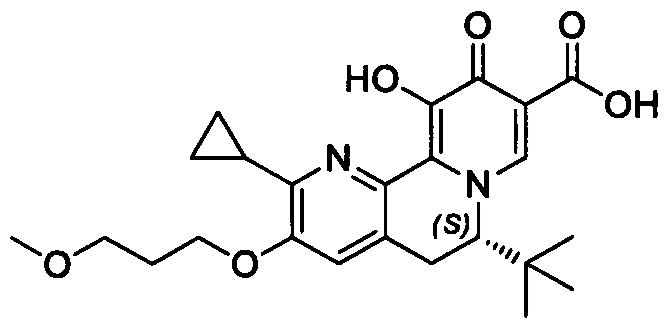
[00607] Стадия 1: Этил-4-(бензилокси)-2-((диметиламино)метилен)-3-оксобутаноат
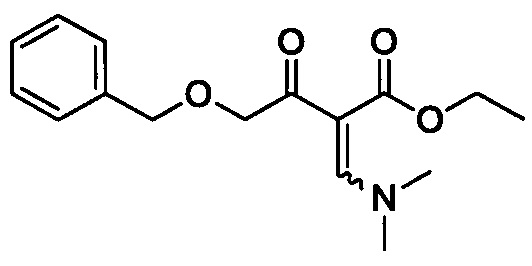
[00608] ДМФ-ДМА (5,70 мл, 42,5 ммоль) добавляли к раствору этил-4-(бензилокси)-3-оксобутаноата (6,70 г, 28,4 ммоль) в толуоле (30 мл) и полученную реакционную смесь взбалтывали в течение ночи и упаривали досуха. Полученный осадок очищали с помощью хроматографии на силикагеле (0-100% EtOAc в гексанах) с получением этил-4-(бензилокси)-2-((диметиламино)метилен)-3-оксобутаноата (6,78 г, 82%) в виде желтого масла. LCMS (m/z, ES+) = 292,6 (M+1).
[00609] Стадия 2: Этил-5-(бензилокси)-4-оксо-4Н-пиран-3-карбоксилат
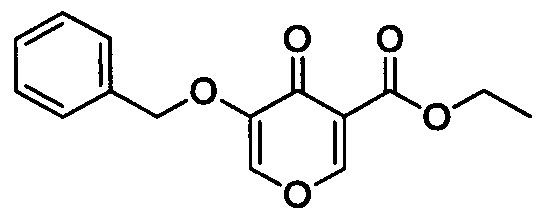
[00610] Этилформат (10,2 мл, 126 ммоль) медленно добавляли к суспензии трет-бутоксида калия (3,54 г, 31,6 ммоль) в 24 мл ТГФ при 0°С. После того как добавление было завершено, полученную реакционную смесь взбалтывали еще в течение 15 мин при 0°С и раствор этил-4-(бензилокси)-2-((диметиламино)метилен)-3-оксобутаноата (4,6 г, 15,8 ммоль) в 24 мл ТГФ добавляли по каплям с использованием дополнительной воронки. После того как добавление было завершено, полученную реакционную смесь удаляли из ледяной бани и перемешивали при комнатной температуре в течение ночи. Добавляли 1 М HCl (50 мл) и указанный раствор экстрагировали EtOAc (2х). Объединенные органические фазы осушали (Na2SO4), отфильтровывали, упаривали и очищали с помощью хроматографии на силикагеле (0-100% EtOAc в гексанах) с получением этил-5-(бензилокси)-4-оксо-4Н-пиран-3-карбоксилата (1,48 г, 34%) в виде светло-желтого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,41 (s, 1H), 7,55 (s, 1H), 7,32-7,43 (m, 5 H), 5,12 (s, 2H), 4,37 (q, J=7,0 Hz, 2H), 1,38 (t, J=7,2 Hz, 3H); LCMS (m/z, ES+) = 275,5 (M+1).
[00611] Стадия 3: (S)-Этил-5-(бензилокси)-1-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбуган-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
[00612] 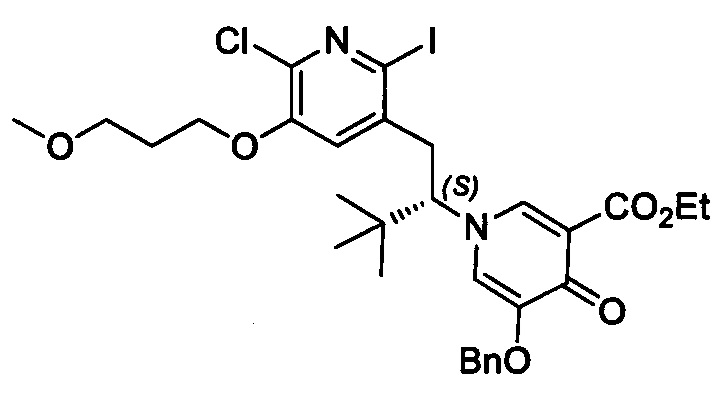
[00613] Раствор указанного (S)-1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-амина, соляной кислоты (0,402 г, 0,87 ммоль) и этил-5-(бензилокси)-4-оксо-4Н-пиран-3-карбоксилата (0,38 г, 1,37 ммоль) в НОАс (8,7 мл) взбалтывали при 100°С в течение 10 ч. Полученную реакционную смесь упаривали досуха, переносили в CH2Cl2 и насыщенный NaHCO3 и перемешивали в течение 1 ч. Указанную водную фазу экстрагировали CH2Cl2 и EtOAc (2х). Объединенные органические фазы осушали (Na2SO4), отфильтровывали и упаривали. Полученный осадок растворяли в EtOH (8 мл) и нагревали при 80°С в течение ночи. Полученную реакционную смесь упаривали досуха и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением этил-(S)-5-(бензилокси)-1-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилата(89,8 мг, 15%) в виде коричневого твердого вещества. LCMS (m/z, ES+) = 683,7, 685,7 (M+1).
[00614] Стадия 4: (S)-Этил-11-(бензилокси)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
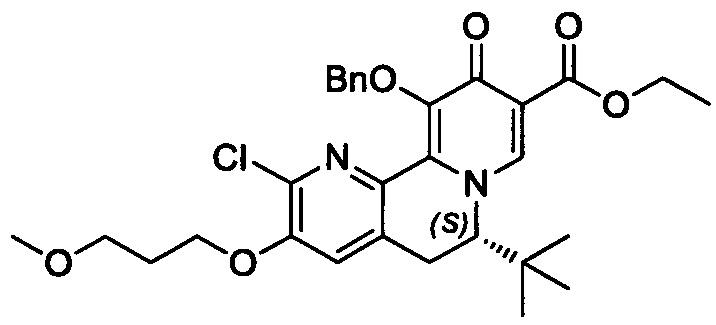
[00615] Колбу, содержащую этил-(S)-5-(бензилокси)-1-(1-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигадропиридин-3-карбоксилат (89,8 мг, 0,13 ммоль), ацетат калия (26 мг, 0,26 ммоль) и бромид палладия (II) (7,0 мг, 0,03 ммоль) продували азотом. Добавляли дегазированный ДМФА (1,3 мл) и полученную реакционную смесь нагревали при 90°С в течение 24 ч. Полученную реакционную смесь отфильтровывали через целит, указанный растворитель удаляли упариванием и полученный осадок очищали с помощью хроматографии на силикагеле (0-100% 3:1 (EtOAc/EtOH) в гексанах) с получением этил-(S)-11-(бензилокси)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (47,9 мг, 66%) в виде коричневого масла. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,15 (s, 1H), 7,73 (d, J=6,2 Hz, 2H), 7,28-7,36 (m, 3H), 6,94 (s, 1H), 5,26 (br. s., 2H), 4,35 (q, J=6,4 Hz, 2H), 4,21-4,10 (m, 2H), 3,82-3,92 (m, 1H), 3,56-3,67 (m, 2H), 3,46-3,37 (m, 1H), 3,39 (s, 3H), 2,98 (d, J=16,0 Hz, 1H), 2,13 (quin, J=5,9 Hz, 2H), 1,40-1,31 (m, 3H), 0,71 (s, 9H); LCMS (m/z, ES+) = 555,4, 557,3 (M+1).
[00616] Стадия 5: (S)-Этил-11-(бензилокси)-6-(трет-бутил)-2-циклопропил-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
[00617] 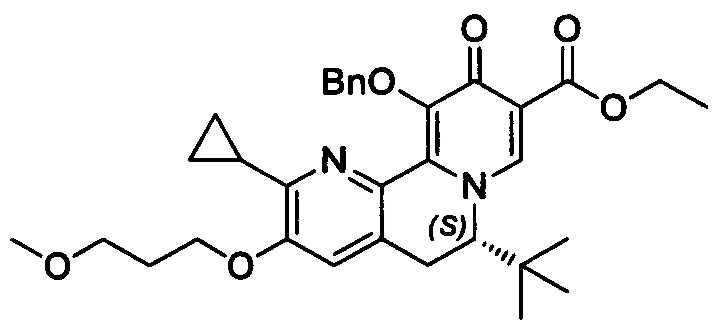
[00618] Раствор этил-(S)-11-(бензилокси)-6-(трет-бутил)-2-хлор-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (47,9 мг, 0,086 ммоль), Pd(PPh3)4 (20 мг, 0,017 ммоль), карбоната калия (36 мг, 0,26 ммоль) и циклопропилборной кислоты (15 мг, 0,17 ммоль) в 1,4-диоксане (0,9 мл) нагревали при 100°С в течение 2 суток. Полученную реакционную смесь разбавляли CH2Cl2 и отфильтровывали через целит. Полученный фильтрат упаривали и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-100% CH3CN/H2O (0,1% муравьиная кислота)) с получением (S)-этил-11-(бензилокси)-6-(трет-бутил)-2-циклопропил-3-(3-метоксипропокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (14,7 мг, 30%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,18 (s, 1Н), 7,66 (d, J=7,0 Hz, 2H), 7,27-7,20 (m, 3H), 6,82 (s, 1H), 5,45 (d, J=10,9 Hz, 1H), 5,21 (d, J=10,9 Hz, 1H), 4,46-4,38 (m, 2H), 4,04-4,20 (m, 2H), 3,89 (d, J=5,5 Hz, 1H), 3,65-3,56 (m, 2H), 3,38 (s, 3H), 3,30 (dd, J=16,0, 6,2 Hz, 1H), 3,03 (d, J=16,0 Hz, 1H), 2,39-2,49 (m, 1H), 2,13 (quin, J=6,1 Hz, 2H), 1,42 (t, J=7,2 Hz, 3H), 1,07-1,15 (m, 1H), 0,96-1,04 (m, 1H), 0,88-0,96 (m, 1H), 0,80-0,86 (m, 1H), 0,77 (s, 9H); LCMS (m/z, ES+) = 561,8 (M+1).
[00619] Стадия 6: (S)-6-(трет-Бутил)-2-циклопропил-11-гидрокси-3-(3-метоксипропокси)-10-оксо-5,10-дигадро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
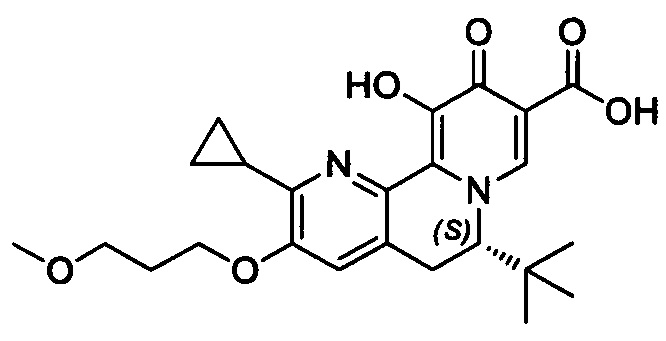
[00620] Раствор этил-(S)-11-(бензилокси)-6-(трет-бутил)-2-вдпшопропил-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (14,7 мг, 0,026 ммоль) и 10% Pd/C (каталитический) в МеОН (5 мл) взбалтывали в 1 атм Н2 в течение 1,5 ч. Полученную реакционную смесь отфильтровывали через целит и упаривали досуха. Полученный осадок переносили в МеОН (0,5 мл) и 1М LiOH (0,5 мл) и указанный раствор нагревали при 50°С в течение 2 ч. Добавляли 1М лимонную кислоту (1,5 мл), указанную смесь упаривали досуха и полученный осадок очищали с помощью обращенно-фазовой хроматографии (5-90% CH3CN/H2O (0,1% муравьиная кислота)) с получением (S)-6-(трет-бутил)-2-циклопропил-11-гидрокси-3-(3-метоксипропокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловойкислоты (6,3 мг, 54%) в виде белого твердого вещества. 1Н ЯМР (400 MHz, CDCl3) δ ppm 15,79 (s, 1Н), 13,96 (s, 1Н), 8,28 (s, 1Н), 7,08 (s, 1Н), 4,25-4,16 (m, 2Н), 4,06 (d, J=6,3 Hz, 1H), 3,58-3,69 (m, 2H), 3,51 (dd, J=17,1, 6,8 Hz, 1H), 3,39 (s, 3H), 3,25 (d, J=17,1 Hz, 1H), 2,49-2,59 (m, 1H), 2,18 (quin, J=6,1 Hz, 2H), 1,06-1,19 (m, 4H), 0,84 (s, 9H); LCMS (m/z, ES+) = 443,7 (M+1).
[00621] Общая схема 7 с получением соединений, таких как Примеры 26, 27
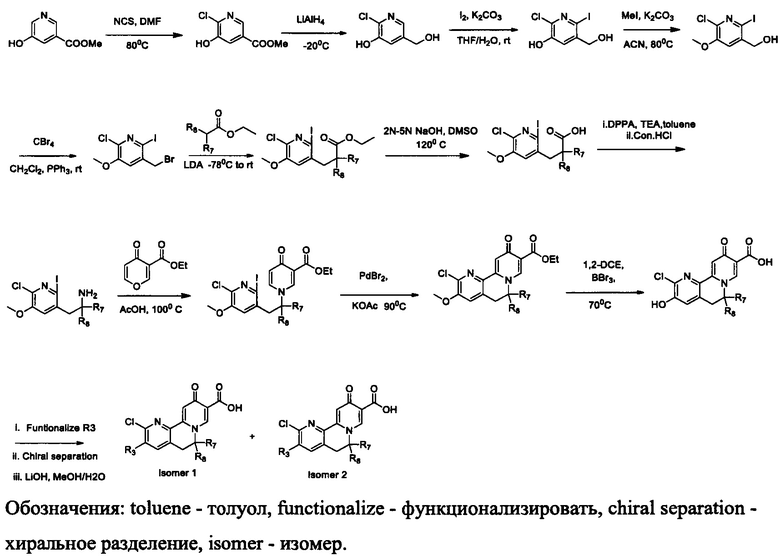
[00622] Конкретная Схема синтеза 8 для Соединений Примера 26,2
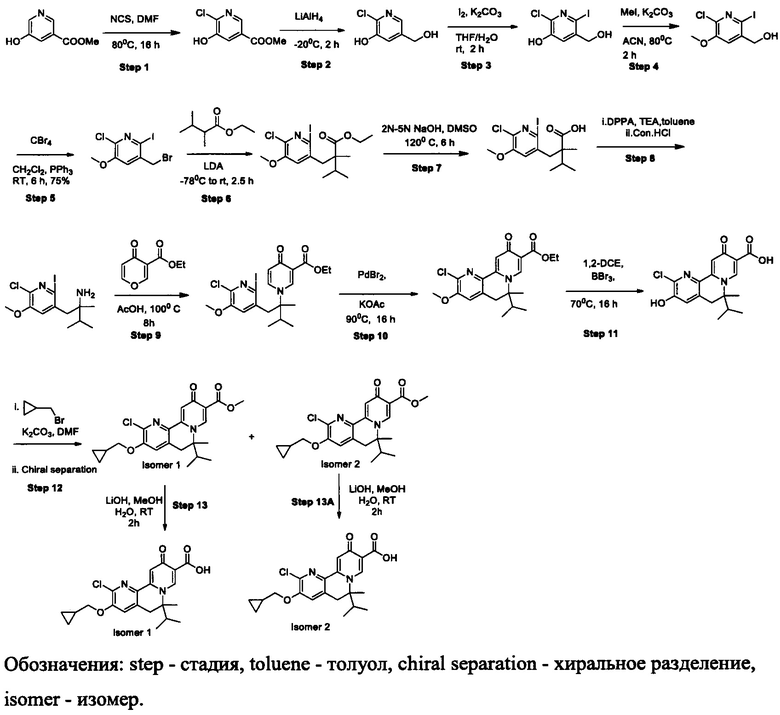
[00623] Пример 26: (Соединение 245)
[00624] (2-Хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота - Изомер-1
[00625] Пример 27: (Соединение 246)
[00626] (2-Хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота - Изомер-2
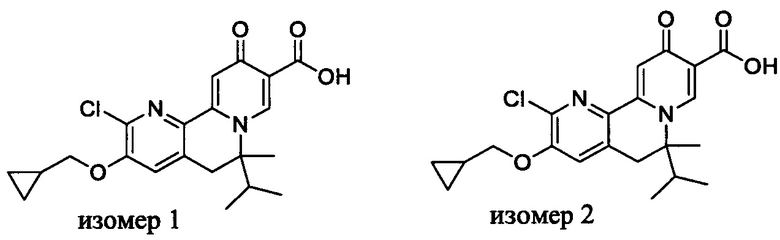
[00627] Стадия 1: Метил 6-хлор-5-гидроксиникотинат
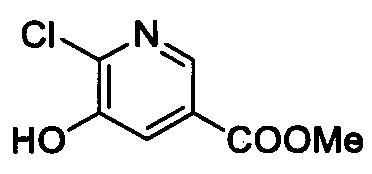
[00628] К раствору метил 5-гидроксиникотината (100 г, 0,65 моль) в ДМФА (1000 мл), NCS (130,5 г, 0,97 моль) добавляли и полученную реакционную смесь нагревали до 80°С в течение 16 ч. Полученную реакционную смесь охлаждали до комнатной температуры и указанный растворитель удаляли при пониженном давлении. Полученный осадок переносили в EtOAc (2L) и промывали насыщенным раствором хлорида натрия (500 мл). Указанную органическую фазу осушали над Na2SO4 и концентрировали. Указанный неочищенный продукт очищали с использованием хроматографической колонки на силикагеле 230-400 с использованием 0-30% этил ацетата в петролейном эфире в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии, в виде желтого масла (60 г, 49% выход), LCMS (ESI) m/z 187,9 (M+1).
[00629] Стадия 2: 2-Хлор-5-(гидроксиметил)пиридин-3-ол
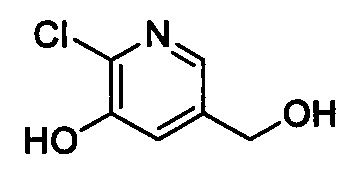
[00630] Раствор метил-6-хлор-5-гидроксиникотината (60 г, 0,32 моль) в ТГФ (600 мл) добавляли по каплям к алюмогидриду лития (160 мл, 0,32 моль, 2,0 М в ТГФ) при -50°С в атмосфере азота. Полученную реакционную смесь взбалтывали при -25°С в течение 2 ч. EtOAc (1000 мл), воду (50 мл) и насыщенный водный раствор тартрата натрия и калия (500 мл) добавляли к полученной реакционной смеси по каплям при -25°С. Указанную смесь отфильтровывали через целитовую подушку, промывали 20% МеОН в DCM (500 мл). Полученный фильтрат концентрировали при пониженном давлении с получением соединения, указанного в названии, (40 г, 80% выход) в виде серовато-белого твердого вещества. LCMS (ESI) m/z 157,9 (М-Н).
[00631] Стадия 3: 2-Хлор-5-(гидроксиметил)-6-йодпиридин-3-ол
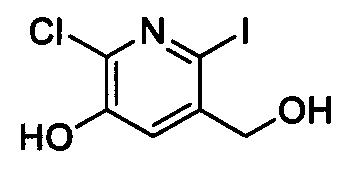
[00632] К раствору 2-хлор-5-(гидроксиметил)пиридин-3-ола (3,5 г, 22,01 ммоль) в ТГФ (35 мл) добавляли воду (35 мл), K2СО3 (6,1 г, 44,24 ммоль) и йод (5,84 г, 23,11 ммоль) и полученную реакционную смесь взбалтывали при комнатной температуре в течение 2 ч. Полученную реакционную смесь охлаждали до 0°С и гасили водным раствором сульфата натрия (50 мл). К ней добавляли этил ацетат (150 мл), органический слой отделяли и выбрасывали. Указанную водную фазу закисляли 1,5 N водным раствором HCl до рН=6 и экстрагировали этил ацетатом (150 мл). Указанную органическую фазу отделяли, промывали водой (25 мл) и сушили над сульфатом натрия. Растворитель удаляли при пониженном давлении с получением соединения, указанного в названии, в виде сероватого твердого вещества (4 г, 64,5% выход). LCMS (ESI) m/z: 283,7 (М-Н).
[00633] Стадия 4: (6-Хлор-2-йод-5-метоксипиридин-3-ил)метанол

[00634] К раствору 2-хлор-5-(гидроксиметил)-6-йодпиридин-3-ола (4 г, 14,03 ммоль) в ацетонитриле (50 мл), добавляли K2СО3 (3,87 г, 28,06 ммоль) и метилйодид (Mel) (5,97 г, 42,10 ммоль) и полученную реакционную смесь нагревали до 80°С в течение 2 ч в запаянной трубке. Полученную реакционную смесь гасили водой (100 мл), закисляли 1,5N HCl (рН=6) и экстрагировали этил ацетатом (150 мл). Указанную органическую фазу промывали солевым раствором, осушали над Na2SO4 и концентрировали. Неочищенное вещество очищали с использованием хроматографической колонки на 230-400 силикагеле с использованием 0-30% этил ацетата в петролейном эфире в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии в виде сероватого твердого вещества (3,3 г, 80% выход). LCMS (ESI) m/z: 299,8 (М+1).
[00635] Стадия 5: 3-(Броммегил)-6-хлор-2-йод-5-метоксипиридин

[00636] К раствору (6-хлор-2-йод-5-метоксипиридин-3-ил)метанола (2,2 г, 7,35 ммоль) в DCM (20 мл) добавляли CBr4 (3,6 г, 11,35 ммоль) и PPh3 (2,3 г, 8,82 ммоль) в ТГФ (20 мл). Полученную реакционную смесь взбалтывали при комнатной температуре в течение 6 ч. Растворитель удаляли при пониженном давлении с получением неочищенного продукта. Его очищали с использованием хроматографической колонки на силикагеле 60-120 меш с использованием 0-20% EtOAc в петролейном эфире в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии, в виде сероватого твердого вещества (2,4 г, 92% выход). LCMS (ESI) m/z: 363,6 (М+Н).
[00637] Стадия 6: Этил-2-((6-хлор-2-йод-5-метоксипиридин-3-ил)метил)-2,3-диметилбутаноат
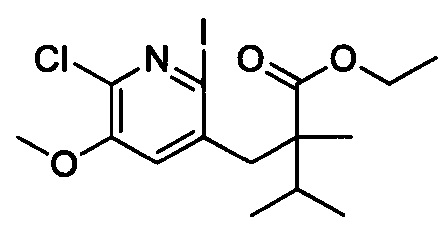
[00638] К раствору диизопропиламина (2,43 мл, 17,38 ммоль) в сухом ТГФ (20 мл) добавляли n-BuLi (10,86 мл, 17,38 ммоль, 1,6М в гексане) по каплям при -78°С. Полученную реакционную смесь взбалтывали при той же температуре в течение 30 мин. К полученной реакционной смеси добавляли этил-2,3-диметилбутаноат (2,3 г, 16,57 ммоль) в ТГФ (20 мл) и полученную реакционную смесь взбалтывали при -78°С в течение 1 ч. При той же температуре по каплям добавляли 3-(бромметил)-6-хлор-2-йод-5-метоксипиридин (3 г, 8,28 ммоль) в ТГФ (20 мл) и полученную реакционную смесь нагревали до комнатной температуры и перемешивали при комнатной температуре в течение 1 ч. Полученную реакционную смесь охлаждали до 0°С, гасили насыщенным раствором NH4Cl (50 мл), разбавляли водой (20 мл) и экстрагировали EtOAc (3×50 мл). Объединенные органические фазы промывали солевым раствором (20 мл), осушали над безводным Na2SO4 и отфильтровывали. Растворители удаляли при пониженном давлении с получением неочищенного продукта. Указанный неочищенный продукт очищали с использованием хроматографической колонки на силикагеле 230-400 меш с использованием 0-10% EtOAc в петролейном эфире в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии, в виде желтого масла (3 г, 85% выход). LCMS (ESI) m/z: 426 (М+Н).
[00639] Стадия 7: 2-((6-Хлор-2-йод-5-метоксипиридин-3-ил)метил)-2,3-диметилмасляная кислота
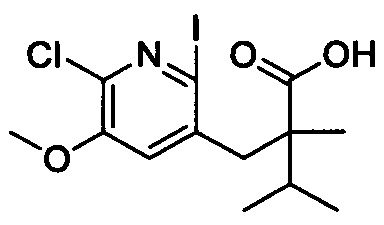
[00640] К раствору этил-2-((6-хлор-2-йод-5-метоксипиридин-3-ил)метил)-2,3-диметилбутаноата (3 г, 7,05 ммоль) в DMSO (9 мл) добавляли раствор 5М NaOH (21,6 мл, 98,11 ммоль) и полученную реакционную смесь взбалтывали при 120°С в течение 6 ч. Полученную реакционную смесь охлаждали до 0°С, закисляли концентрированной HCl до рН=1. После разбавления водой (50 мл) ее экстрагировали EtOAc (2×100 мл). Объединенные органические фазы промывали солевым раствором (50 мл), осушали над безводным Na2SO4 и отфильтровывали. Указанный растворитель удаляли при пониженном давлении с получением указанного неочищенного продукта. Указанный неочищенный продукт очищали с использованием хроматографической колонки на силикагеле 230-400 с использованием 0-10% МеОН в DCM с получением 2-((6-хлор-2-йод-5-метоксипиридин-3-ил)метил)-2,3-диметилмасляной кислоты (500 мг, 18% выход) (LCMS (ESI) m/z: 397,8 (M+1)).
[00641] Стадия 8: 1-(6-Хлор-2-йод-5-метоксипиридин-3-ил)-2,3-диметилбутан-2-амин
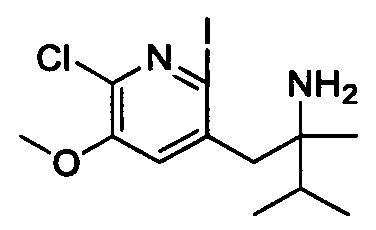
[00642] К раствору 2-((6-хлор-2-йод-5-метоксипиридин-3-ил)метил)-2,3-диметилмасляной кислоты (1 г, 2,5 ммоль) в толуоле (30 мл) добавляли тризтиламин (0,57 г, 5,5 ммоль) и дифенил фосфорил азид (1,52 г, 5,5 ммоль) и полученную реакционную смесь взбалтывали при 80°С в течение 2 ч. Полученную реакционную смесь охлаждали до комнатной температуры и концентрировали HCl (8,4 мл) добавляли к полученной реакционной смеси по каплям более 30 мин при 0°С. Полученную реакционную смесь взбалтывали при 60°С в течение 2 ч. Полученную реакционную смесь охлаждали до 0°С и защелачивали 1N водным раствором NaOH до рН=10. Полученную реакционную смесь разбавляли водой (20 мл) и экстрагировали EtOAc (2×50 мл). Объединенные органические фазы промывали солевым раствором (20 мл), осушали над безводным Na2SO4, отфильтровывали и концентрировали с получением коричневого резиноподобного твердого вещества. Его очищали с использованием хроматографической колонки на силикагеле 230-400 с использованием 0-3% МеОН в DCM с получением соединения, указанного в названии, в виде желтого масла (800 мг, 87% выход). LCMS (ESI) m/z: 368,8 (M+1).
[00643] Стадия 9: Этил-1-(1-(6-хлор-2-йод-5-метоксипиридин-3-ил)-2,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
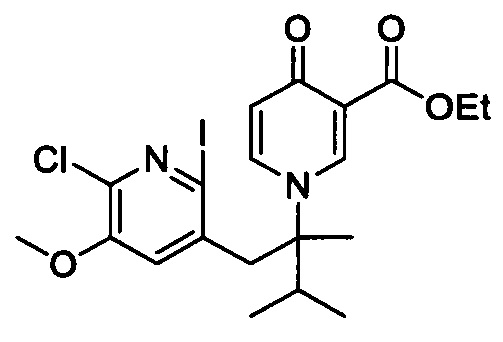
[00644] К раствору 1-(6-хлор-2-йод-5-метоксипиридин-3-ил)-2,3-диметилбутан-2-амина (800 мг, 2,17 ммоль) в уксусной кислоте (25 мл) добавляли этил-4-оксо-4Н-пиран-3-карбоксилат (0,547 г, 3,2 ммоль) и полученную реакционную смесь взбалтывали при 100°С в течение 8 ч. Полученную реакционную смесь охлаждали до комнатной температуры. Указанный растворитель удаляли при пониженном давлении и полученный осадок очищали с использованием хроматографической колонки на силикагеле 230-400 с использованием 0-10% МеОН в DCM в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии, (400 мг, 35% выход) в виде коричневого твердого вещества. LCMS (ESI) m/z: 518,7 (М+1).
[00645] Стадия 10: Этил-2-хлор-6-изопропил-3-метокси-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
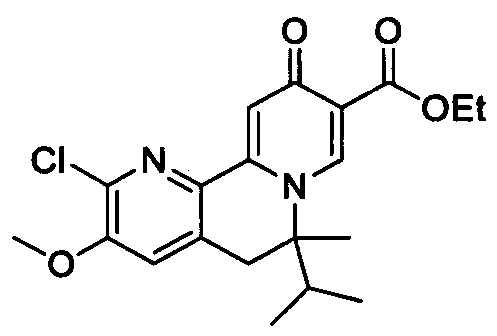
[00646] К раствору этил-1-(1-(6-хлор-2-йод-5-метоксипиридин-3-ил)-2,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилата (300 мг, 0,57 ммоль) в N,N-диметилформамиде (7,5 мл) добавляли ацетат калия (283 мг, 2,89 ммоль). Полученную реакционную смесь дегазировали азотом в течение 20 минут. Бромид палладия (II) (30 мг, 0,11 ммоль) добавляли к полученной реакционной смеси взбалтывали при 90°С в течение 16 ч. Полученную реакционную смесь охлаждали до комнатной температуры, отфильтровывали через целит и промывали DCM. Указанный растворитель удаляли при пониженном давлении и неочищенное вещество очищали с использованием хроматографической колонки на силикагеле 230-400 с использованием 0-10% МеОН в DCM в качестве элюента. Фракции собирали и концентрировали с получением соединения, указанного в названии, (150 мг, 68% выход) в виде коричневого твердого вещества. LCMS (ESI) m/z: 390,9 (М+1).
[00647] Стадия 11: 2-Хлор-3-гидрокси-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
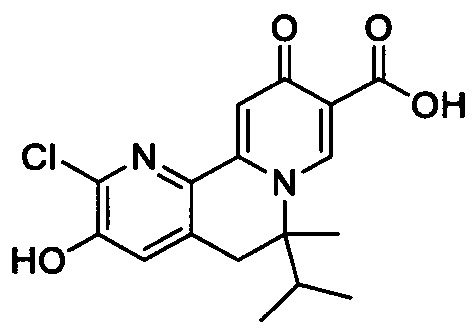
[00648] К раствору этил-2-хлор-6-изопропил-3-метокси-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (150 мг, 0,38 ммоль) в 1,2-дихлорэтане (DCE) (6,45 мл) добавляли BBr3 (288 мг, 1,15 ммоль) и полученную реакционную смесь взбалтывали при 70°С в течение 16 ч. Полученную реакционную смесь охлаждали до -10°С, метанол (15 мл) добавляли к реакционной смеси по каплям, а затем перемешивали при комнатной температуре в течение 30 минут. Полученную реакционную смесь концентрировали с получением неочищенного соединения (150 мг) в виде коричневого твердого вещества. LCMS (ESI) m/z: 348,9 (М+1). Этот неочищенный продукт использовали на следующей Стадии.
[00649] Стадия 12: Метил-2-хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат-Изомер-1 и метил-2-хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат - Изомер-2
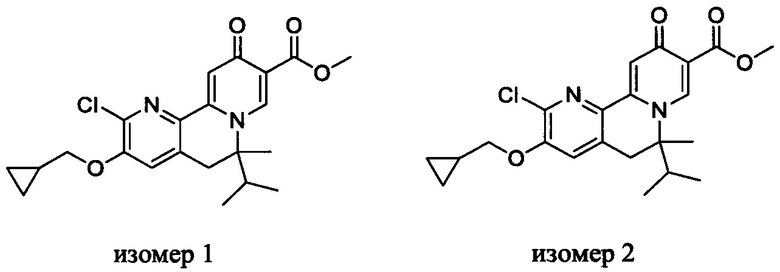
[00650] К раствору 2-хлор-3-гидрокси-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловой кислоты (150 мг, 0,43 ммоль) в ДМФА (2 мл) добавляли К2СО3 (594 мг, 4,3 ммоль) и (бромметил)циклопропан (464 мг, 3,44 ммоль) и полученную реакционную смесь взбалтывали при 80°С в течение 5 ч. Полученную реакционную смесь охлаждали до комнатной температуры, Указанный растворитель удаляли при пониженном давлении и полученный осадок взбалтывали с МеОН (10 мл) при комнатной температуре в течение 30 мин. Растворитель удаляли при пониженном давлении и разбавляли DCM (20 мл). Органический слой промывали водой (15 мл) и осушали над безводным сульфатом натрия, отфильтровывали и концентрировали при пониженном давлении с получением указанного соединения в виде смеси изомеров, которые разделяли с помощью хиральной хроматографии со сверхкритической подвижной фазой (SFC). Полученные фракции Изомера-1 (первый пик элюции) и Изомера-2 (второй пик элюции) концентрировали при пониженном давлении с получением метил-2-хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-1 (50 мг, 28% выход) в виде сероватого твердого вещества LCMS (ESI) m/z: 417,9 (М+1) и метил-2-хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-2 (50 мг, 28% выход) в виде сероватого твердого вещества. LCMS (ESI) m/z: 417,9 (M+1).
[00651] Стадия 13: (2-Хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота - Изомер-1
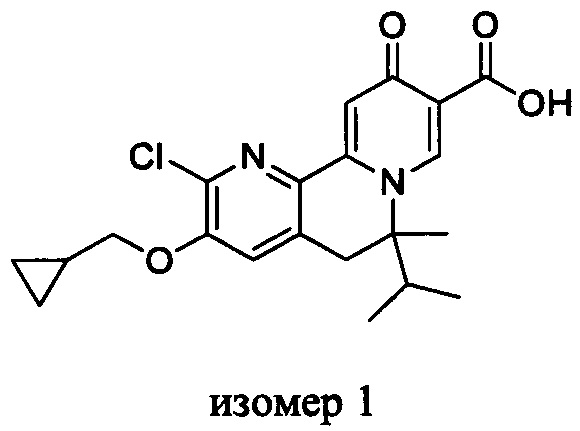
[00652] К раствору метил-2-хлор-3-(циклопропилметокси)-6-изогфопил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-1 (50 мг, 0,11 ммоль) в метаноле (2 мл) и Н2О (0,5 мл) добавляли гидроксид лития (25 мг, 0,59 ммоль) и полученную реакционную смесь взбалтывали при комнатной температуре в течение 2 ч. Указанный растворитель удаляли при пониженном давлении и полученный осадок растворяли в воде (3 мл) и закисляли 1,5 N HCl до рН~3. Полученное твердое вещество отфильтровывали, промывали водой (5 мл), осушали под вакуумом и очищали с помощью преп-ВЭЖХ с получением соединения, указанного в названии, (15 мг, выход 31,2%) в виде сероватого твердого вещества. LCMS (ESI) m/z: 403,1 (M+1). 1H ЯМР; 400 MHz, DMSO-d6: δ ppm 8,57 (s, 1H), 7,72 (s, 1H), 7,39 (s, 1H), 4,10-4,07 (m, 2H), 3,36-3,35 (m, 2H), 1,91-1,84 (m, 1H), 1,70 (s, 3H), 1,35-1,25 (m, 1H), 0,85-0,82 (m, 3H), 0,65-0,63 (m, 5H), 0,42-0,39 (m, 2H).
[00653] Стадия 13 А: 2-хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота - Изомер-2
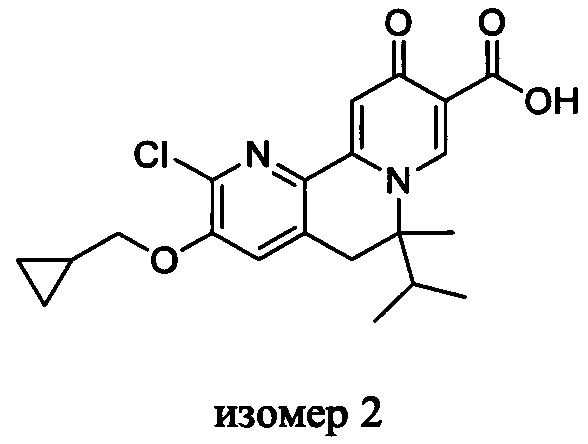
[00654] К раствору метил-2-хлор-3-(циклопропилметокси)-6-изопропил-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-2 (50 мг, 0,11 ммоль) в метаноле (2 мл) и H2O (0,5 мл) добавляли гидроксид лития (25 мг, 0,59 моль) и полученную реакционную смесь взбалтывали при комнатной температуре в течение 2 ч. Указанный растворитель удаляли при пониженном давлении и полученный осадок растворяли в воде (3 мл) и закисляли 1,5 N HCl до рН~3. Полученное твердое вещество отфильтровывали, промывали водой (5 мл), осушали под вакуумом в течение 16 ч с получением соединения, указанного в названии, в виде сероватого твердого вещества (30 г, выход 62%). LCMS (ESI) m/z: 402,9 (M+1). 1H ЯМР; 400 MHz, DMSO-d6: δ ppm 8,57 (s, 1H), 7,71 (s, 1H), 7,39 (s, 1H), 4,09-4,08 (m, 2H), 3,39-3,38 (m, 2H), 1,90-1,87 (m, 1H), 1,70 (s, 3H), 1,32-1,28 (m, 1H), 1,11-1,07 (m, 3H), 0,83-0,81 (m, 5H), 0,63-0,62 (m, 2H).
[00655] Пример 28: (Соединение 247)
[00656] 2-Циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота - Изомер-1
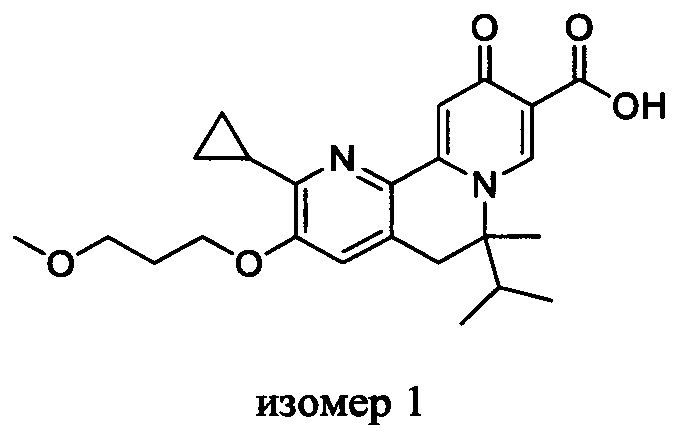
[00657] Пример 29: (Соединение 248)
[00658] 2-Циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота - Изомер-2
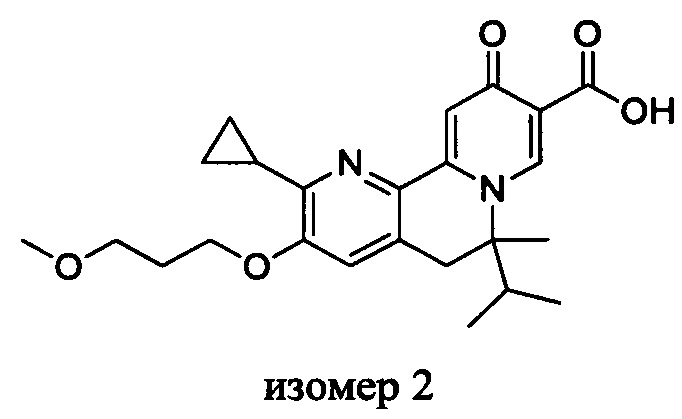
[00659] Общая схема синтеза 9 для Соединений, таких как Пример 28, 29:
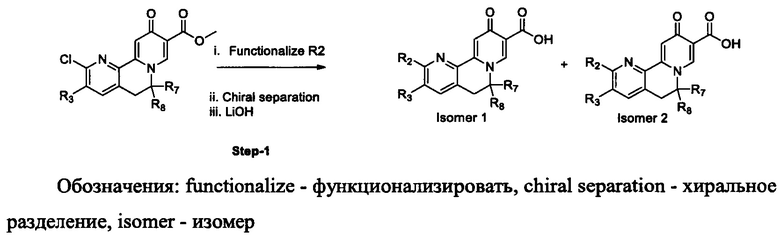
[00660] Конкретная схема синтеза 10 для Соединений Примера 28, 29:
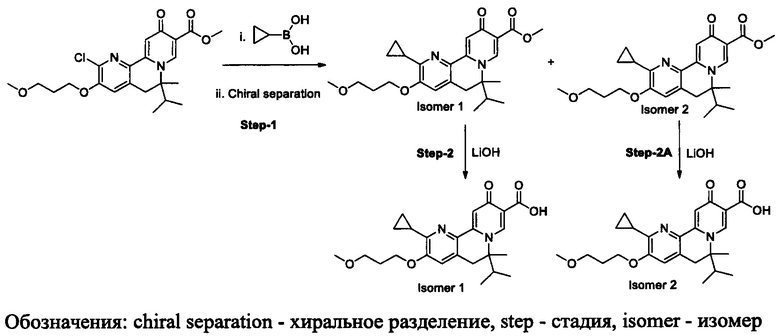
[00661] Стадия 1: Метил-2-циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат - Изомер-1 и метил-2-циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-2
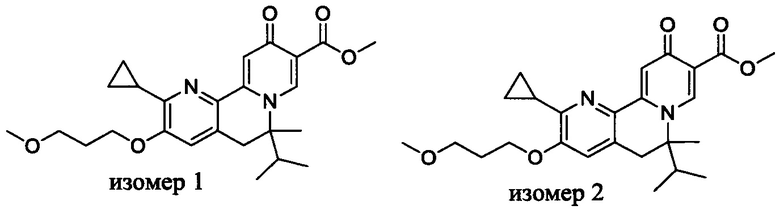
[00662] К перемешиваемому раствору метил-2-хлор-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (570 мг, 1,311 ммоль) в 1,4-диоксане (11,4 мл) добавляли карбонат калия (362 мг, 2,62 ммоль) и продували азотом в течение 5 мин. Добавляли циклопропилборную кислоту (225 мг, 2,62 ммоль), а затем Pd(PPh3)4 (303 мг, 0,262 ммоль) и продували азотом в течение 5 мин. Полученную реакционную смесь нагревали до 100°С в запаянной трубке в течение 16 ч. Полученную реакционную смесь концентрировали полностью при пониженном давлении и полученный осадок разбавляли DCM (100 мл), промывали водой (40 мл), насыщенным солевым раствором (40 мл). Указанную органическую фазу отделяли, осушали над сульфатом натрия, концентрировали и неочищенное вещество очищали с помощью хроматографии Isolera™ на силикагеле и элюировали 3% МеОН в DCM. Собранные фракции концентрировали полностью с получением указанного соединения в виде смеси изомеров. Затем указанное соединение очищали с помощью препаративной ВЭЖХ, а затем хиральной SFC. Собранные фракции Изомера-1 (первый пик элюции) и Изомер-2 (второй пик элюции) концентрировали раздельно при пониженном давлении с получением метил-2-циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-1 (60 мг, выход 10,3%) в виде бесцветного масла и метил-2-циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-2(90 мг, 13,97% выход) в виде бесцветного масла. LCMS (ESI) m/z: 441,0 (M+1).
[00663] Стадия 2: 2-Циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота - Изомер-1
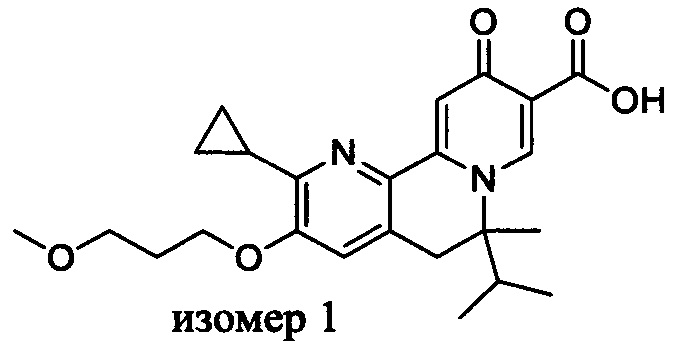
[00664] К раствору метил-2-циклопрогшл-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-1 (60 мг, 0,136 ммоль) в метаноле (2,4 мл) при комнатной температуре добавляли LiOH (16,31 мг, 0,681 ммоль) и воду (0,60 мл) и полученную реакционную смесь взбалтывали при комнатной температуре в течение 2 ч. Растворители из полученной реакционной смеси удаляли при пониженном давлении и полученный осадок растворяли в воде (2 мл). Этот раствор закисляли 1,5N HCl до рН 6 при 0°С. Полученный твердый остаток отфильтровывали, промывали водой, н-пентаном и осушали с получением соединения, указанного в названии в виде бледно-коричневого твердого вещества (15 мг, 25,3%). LCMS (ESI) m/z: 427,2 (M+1). 1H ЯМР (400 MHz, DMSO-d6): δ ppm 8,54 (s, 1H), 7,44 (s, 2H), 4,19-4,18 (m, 2H), 3,53 (t, J=6 Hz, 2H), 3,29-3,27 (m, 5H), 2,05 (t, J=6 Hz, 2H), 1,84-1,82 (m, 1H), 1,68 (s, 3H), 1,03-1,01 (m, 4H), 0,82 (d, J=6,5 Hz 3H), 0,61 (d, J=6,6 Hz, 3H)
[00665] Стадия 2A: 2-Циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота - Изомер-2
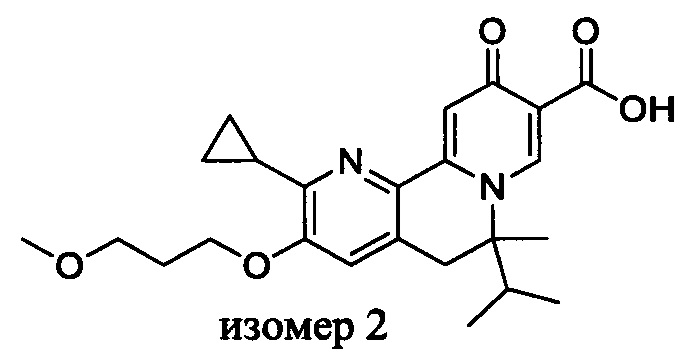
[00666] К раствору метил-2-циклопропил-6-изопропил-3-(3-метоксипропокси)-6-метил-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата - Изомер-2 (90 мг, 0,204 ммоль) в метаноле (3,6 мл) при комнатной температуре добавляли LiOH (24,46 мг, 1,021 ммоль) и воду (0,90 мл), и полученную реакционную смесь взбалтывали при комнатной температуре в течение 2 ч. Растворители из полученной реакционной смеси удаляли при пониженном давлении и полученный осадок растворяли в воде (2 мл). Этот раствор закисляли 1,5N HCl до рН 6 при 0°С. Полученный твердый остаток отфильтровывали, промывали водой, н-пентаном и осушали с получением соединения, указанного в названии в виде бледно-коричневого твердого вещества (26 мг, 29,3%). LCMS (ESI) m/z: 427,2 (M+1). 1H ЯМР (400 MHz, DMSO-d6): δ ppm 8,53 (s, 1H), 7,44 (s, 2H), 4,25-4,12 (m, 2H), 3,56-3,52 (m, 2H), 3,23-3,18 (m, 5H), 2,10-2,01 (m, 3H), 1,81-1,62 (m, 4H), 1,05-0,99 (m, 4H), 0,85-0,81 (m, 3H), 0,65-0,61 (m, 3H).
[00667] Общая схема 11 - Получение типа соединений, таких как Соединение 249
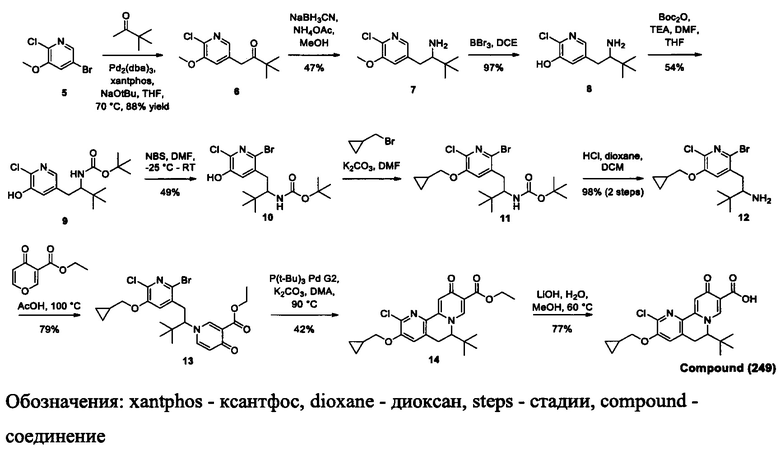
[00668] Соединение 249 может быть получено в соответствии с общей процедурой синтеза, описанной в Схеме 11, приведенной выше, и как описано более подробно ниже.
[00669] Пример 30 (Соединение 249 (рацемат))
[00670] 6-(трет-Бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
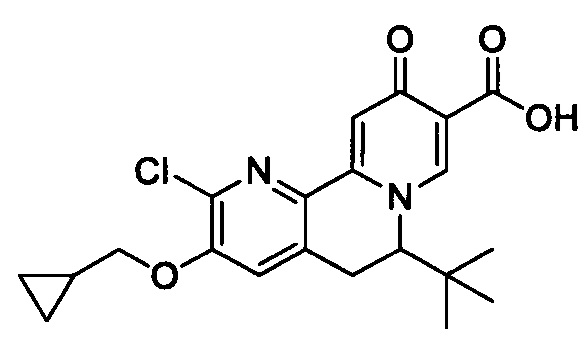
[00671] Стадия 1: 1-(6-Хлор-5-метокситфидин-3-ил)-3,3-диметилбутан-2-он
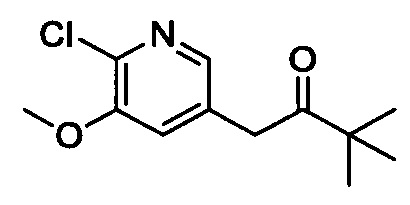
[00672] В колбу помещали мешалку, ксантфос (0,225 г, 0,388 ммоль), трис(дибензилиденацетон)дипалладий(0) (0,198 г, 0,216 ммоль), и трет-бутоксид натрия (2,43 г, 25,3 ммоль). Указанную колбу продували потоком азота перед добавлением раствора 5-бром-2-хлор-3-метоксипиридина (3,2 г, 14,4 ммоль) и 3,3-диметилбутан-2-она (2,16 мл, 17,3 ммоль) в тетрагидрофуране (ТГФ) (50 мл). Указанную смесь нагревали с обратным холодильником в течение ночи. Указанную смесь оставляли охлаждаться до комнатной температуры и разбавляли водой. Указанную смесь экстрагировали 3 раза этил ацетатом. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия, концентрировали и получали 1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-он (3,07 г, 12,7 ммоль, 88% выход). 1Н ЯМР (400 MHz, хлороформ-d) δ ppm 7,74 (d, J=1,56 Hz, 1Н), 7,10 (d, J=1,56 Hz, 1H), 3,89 (s, 3H), 3,77 (s, 2H), 1,20 (s, 9H).
[00673] Стадия 2: 1-(6-Хлор-5-метоксипиридин-3-ил)-3,3-диметилбуган-2-амин
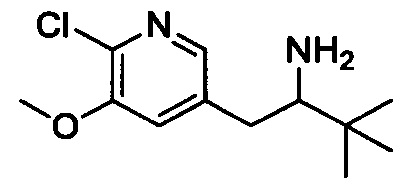
[00674] Смесь 1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-она(3,07 г, 12,7 ммоль) и ацетата аммония (14,7 г, 191 ммоль) в метаноле (50 мл) перемешивали в течение 1 часа при комнатной температуре перед порционным добавлением цианоборгидрида натрия (2,00 г, 31,8 ммоль). Указанную смесь взбалтывали в течение выходных при комнатной температуре, а потом защелачивали 1М гидроксидом натрия. Указанную смесь экстрагировали 3 раза дихлорметаном. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия, концентрировали и получали 1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-амин (2,82 g) в виде прозрачного масла. Полученное вещество очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 0% до 100%). Фракции комбинировали, защелачивали 1М гидроксидом натрия и экстрагировали 3 раза этил ацетатом. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия, концентрировали и получали 1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-амин (1,45 г, 5,97 ммоль, 47,0% выход) в виде прозрачного масла. 1Н ЯМР (400 MHz, хлороформ-d) δ ppm 7,83 (d, J=1,56 Hz, 1Н), 7,08 (d, J=1,56 Hz, 1Н), 3,90 (s, 3Н), 2,91 (dd, J=13,48,2,15 Hz, 1H), 2,62 (dd, J=10,94, 1,95 Hz, 1H), 2,22 (dd, J=13,48, 11,13 Hz, 1H), 1,12-1,36 (m, 2H), 0,98 (s, 9H).
LCMS(ES+)(w/z): 243, 245 (M+1).
[00675] Стадия 3: 5-(2-Амино-3,3-диметилбугил)-2-хлорпиридин-3-ол
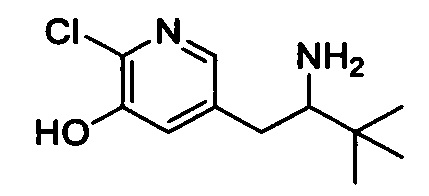
[00676] Трибромид бора (2,82 мл, 29,9 ммоль) добавляли по каплям к раствору 1-(6-хлор-5-метоксипиридин-3-ил)-3,3-диметилбутан-2-амина (1,45 г, 5,97 ммоль) в 1,2-дихлорэтане (DCE) (30 мл) при 0°С. Указанную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. Данные LC-MS продемонстрировали существенную конверсию в желаемый продукт, однако исходный материал все еще присутствовал. Твердую фракцию, которая образовалась в течение ночи, измельчали и указанную смесь перемешивали в течение дополнительных 24 часов при комнатной температуре. Указанную смесь охлаждали до 0°С и осторожно гасили добавлением метанола по каплям. После того, как избыток BBr3 был полностью погашен, добавляли дополнительный метанол (100 мл). Указанную смесь взбалтывали в течение 1 часа и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 0% до 100%). Фракции лиофилизировали и получали 5-(2-амино-3,3-диметилбутил)-2-хлорпиридин-3-ол (1,33 г, 5,81 ммоль, 97% выход) в виде белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,21 (s, 1Н), 7,83-8,16 (m, 2Н), 7,74 (d, J=1,95 Hz, 1H), 7,21 (d, J=1,56 Hz, 1H), 2,82-3,02 (m, 2H), 2,35-2,43 (m, 1H), 0,94 (s, 9H). LCMS(ES+)(m/z): 229,231 (M+1).
[00677] Стадия 4: трет-Бутил (1-(6-хлор-5-гидроксигофидин-3-ил)-3,3-диметилбутан-2-ил)карбамат
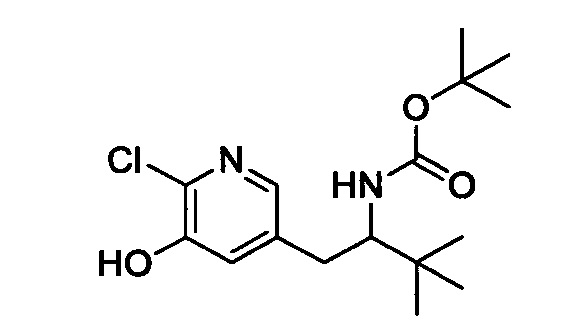
[00678] ди-трет-Бутилдикарбонат (1,52 г, 6,98 ммоль) добавляли к перемешиваемой смеси 5-(2-амино-3,3-диметилбутил)-2-хлоргофидин-3-ола (1,33 г, 5,81 ммоль) и триэтиламина (2,43 мл, 17,4 ммоль) в N,N-диметилформамиде (ДМФ) (30 мл). Указанную смесь взбалтывали при комнатной температуре в течение 1 часа. Данные LC-MS продемонстрировали минимальную конверсию. Указанная твердая фракция полностью не растворялась. Добавляли тетрагидрофуран (ТГФ) (50 мл) и указанная твердая фракция переходила в раствор. Указанную смесь взбалтывали в течение 2 часов, концентрировали, и полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции концентрировали, а затем полученный осадок лиофилизировали (ацетонитрил / водой) и получали трет-бутил-(1-(6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамат (1,04 г, 3,16 ммоль, 54,4% выход). 1Н ЯМР (400 MHz, Темп. = 80°С, DMSO-d6) δ ppm 9,81-10,14 (m, 1Н), 7,68 (d, J=1,56 Hz, 1H), 7,15 (d, J=1,56 Hz, 1H), 6,13-6,46 (m, 1H), 3,24-3,46 (m, 1H), 2,76 (dd, J=14,05,2,34 Hz, 1H), 2,31-2,42 (m, 1H), 1,21 (br. s., 9H), 0,91 (s, 9H). LCMS(ES+)(/n/z): 329, 331 (M+1).
[00679] Стадия 5: трет-Бутил-(1-(2-бром-6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбуган-2-ил)карбамат

[00680] В атмосфере азота раствор N-бромсукцинимида (471 мг, 2,65 ммоль) в 2 мл ДМФА медленно добавляли по каплям к охлажденному до 0°С раствору трет-бутил-(1-(6-хлор-5-гадроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (791 мг, 2,405 ммоль) в N,N-диметилформамиде (ДМФА) (25 мл) и указанную смесь перемешивали в реакционной виале, которая была защищена от света с помощью алюминиевой фольги. Температуру охлаждающей бани поддерживали между -25°С и -20°С в течение 30 минут. Указанную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение ночи. Указанную смесь гасили водой и экстрагировали 3 раза этилацетатом. Объединенные органические фазы промывали солевым раствором и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент от 10% до 60%, затем изократически 60%, затем градиент с 60% до 100%). Фракции концентрировали и получали трет-бутил (1-(2-бром-6-хлор-5-гидроксшшридин-3-ил)-3,3-диметилбутан-2-ил)карбамат (485 мг, 1,19 ммоль, 49,5% выход). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 10,81 (br. s., 1H), 7,23 (s, 1H), 6,60 (d, J=10,15 Hz, 1H), 3,35-3,50 (m, 1H), 2,73-2,89 (m, 1H), 2,18-2,37 (m, 1H), 1,15 (s, 9H), 0,83-0,91 (m, 9H). LCMS(ES+)(m/z): 407, 409, 411 (M+1).
[00681] Стадия 6: 1-(2-Бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)-3,3-диметилбутан-2-амин
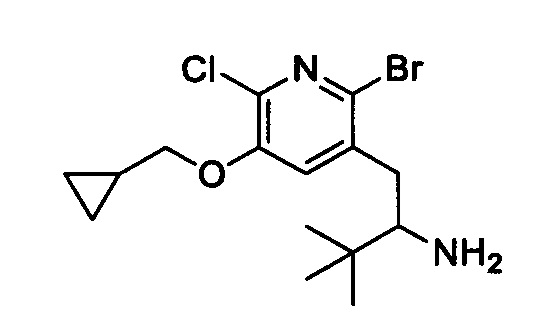
[00682] (Бромметил)циклопропан (0,231 мл, 2,38 ммоль) добавляли к перемешиваемой смеси трет-бутил-(1-(2-бром-6-хлор-5-гидроксипиридин-3-ил)-3,3-диметилбутан-2-ил)карбамата (485 мг, 1,19 ммоль) и карбоната калия (658 мг, 4,76 ммоль) в N,N-диметилформамиде (ДМФА) (5 мл). Указанную смесь взбалтывали при комнатной температуре в течение ночи. Указанную смесь гасили водой и 2 раза экстрагировали этил ацетатом. Объединенные органические фазы промывали 5% хлоридом лития, промывали солевым раствором, осушали над сульфатом натрия, концентрировали и получали неочищенный трет-бутил (1-(2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)карбамат. Указанное промежуточное соединение растворяли в дихлорметане (DCM) (5,00 мл) перед добавлением соляной кислоты (4М в диоксане) (5 мл, 20 ммоль). Указанную смесь взбалтывали в течение 4 часов, концентрировали и получали белое твердое вещество. Добавляли насыщенный раствор бикарбонат натрия и указанную смесь 2 раза экстрагировали этил ацетатом. Объединенные органические фазы осушали над сульфатом натрия, концентрировали и получали 1-(2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)-3,3-диметилбутан-2-амин (423 мг, 1,17 ммоль, 98% выход) в виде прозрачного масла. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 7,62 (s, 1H), 3,96 (d, J=7,03 Hz, 2H), 2,89 (dd, J=12,88, 1,95 Hz, 1H), 2,43-2,46 (m, 1H), 2,20-2,33 (m, 1H), 1,19-1,36 (m, 3H), 0,92 (s, 9H), 0,52-0,66 (m, 2H), 0,26-0,42 (m, 2H). LCMS(ES+)(m/z): 361, 363, 365 (M+1).
[00683] Стадия 7: Этил-1-(1-(2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)-33-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
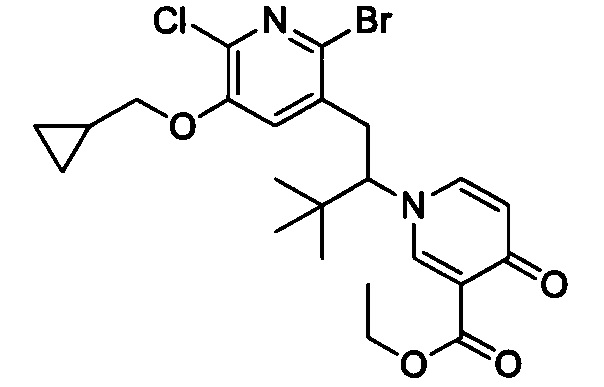
[00684] 1-(2-Бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)-3,3-диметилбутан-2-амин (375 мг, 1,04 ммоль) и этил-4-оксо-4Н-пиран-3-карбоксилат (174 мг, 1,04 ммоль) в уксусной кислоте (10 мл) перемешивали при 100°С в течение 4 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода / 0,1% муравьиная кислота / градиент с 0% до 100%). Фракции концентрировали и полученный осадок лиофилизировали (вода / ацетонитрил) и получали этил-1-(1-(2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (420 мг, 0,821 ммоль, 79% выход) в виде белого порошка. LCMS(ES+)(w/z): 511, 513, 515 (М+1).
[00685] Стадия 8: Этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат
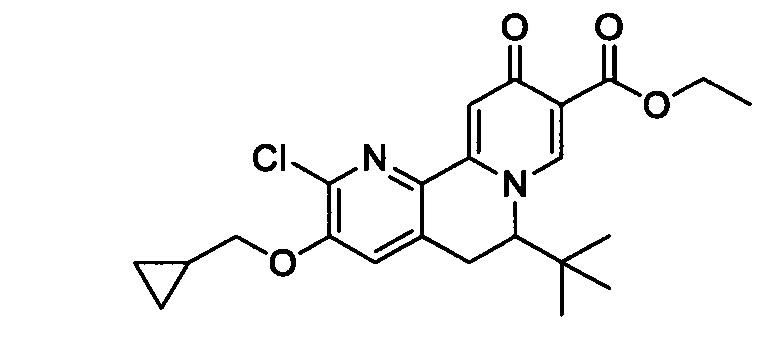
[00686] Реакционную виалу, содержащую мешалку, этил-1-(1-(2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)-3,3-диметилбутан-2-ил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (395 мг, 0,772 ммоль), ацетат калия (151 мг, 1,543 ммоль) и хлор[(три-трет-бутилфосфин)-2-(2-аминобифенил)]палладий(II) (79 мг, 0,15 ммоль), продували азотом в течение 15 минут. N,N-Диметилацетамид (DMA) (8 мл) продували азотом в течение 5 минут перед добавлением к указанной реакционной смеси. Указанную реакционную виалу помещали в нагревательный блок, предварительно нагретый до 90°С и указанную смесь перемешивали в течение ночи. Полученную реакционную смесь оставляли охлаждаться до комнатной температуры, отфильтровывали через хлопковую пробку и очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции концентрировали и полученный осадок подвергали азеотропной перегонке с ацетонитрилом для удаления всей оставшейся воды. Полученный осадок растворяли в дихлорметане и гексанах, затем концентрировали и получали этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат (140 мг, 0,325 ммоль, 42,1% выход) в виде бледно-желтого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,38 (s, 1Н), 7,66 (s, 1Н), 6,90 (s, 1Н), 4,40 (d, J=6,25 Hz, 1H), 4,21 (q, J=7,03 Hz, 2H), 3,99-4,10 (m, 2H), 3,37-3,50 (m, 1H), 3,31-3,37 (m, 1H), 1,22-1,37 (m, 4H), 0,74 (s, 9H), 0,59-0,67 (m, 2H), 0,34-0,45 (m, 2H). LCMS(ES+)(m/z): 431, 433 (M+1).
[00687] Стадия 9: 6-(трет-Бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота
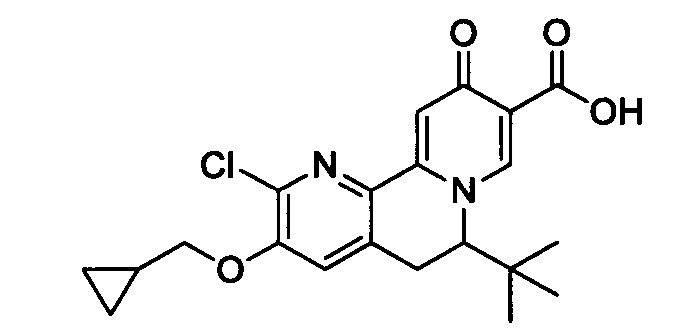
[00688] Раствор моногидрата гидроксида лития (1,6 мг, 0,039 ммоль) в воде (1 мл) добавляли к раствору этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дипшро-5Н-пиридо[1,2-11][1,7]нафтиридин-9-карбоксилата (2,0 мг, 3,9 мкмоль) в метаноле (1 мл) и указанную смесь нагревали при 60°С в течение 3 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции концентрировали и полученный осадок осушали и получали 6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловую кислоту (1,2 мг, 2,9 мкмоль, 77% выход) в виде белого твердого вещества. 1Н ЯМР (400 MHz, метанол-d4) δ ppm 8,70 (br. s., 1Н), 7,54 (br. s., 1H), 7,47 (br. s., 1H), 4,44-4,55 (m, 1H), 3,97-4,14 (m, 2H), 3,39-3,61 (m, 2H), 1,33 (br. s., 1H), 1,12 (br. s., 1H), 0,83 (s, 9H), 0,63-0,71 (m, 2H), 0,34-0,50 (m, 2H). LCMS(ES+)(m/z): 403,405 (M+1).
[00689] Пример 30-а (Соединение 249 Изомер 1)
[00690] 6-(трет-Бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота (изомер 1)
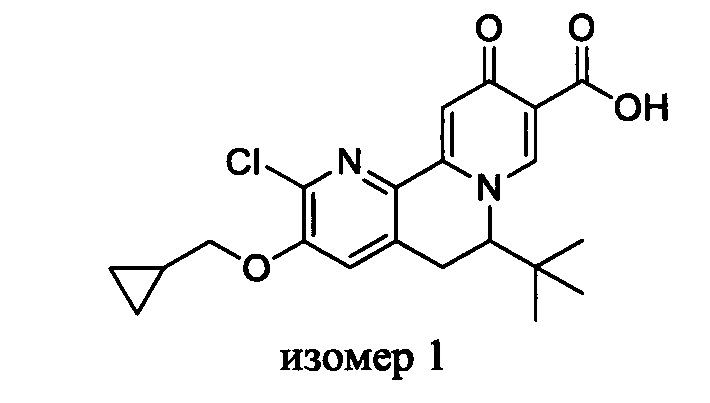
[00691] Стадия 1: Этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат (изомер 1)
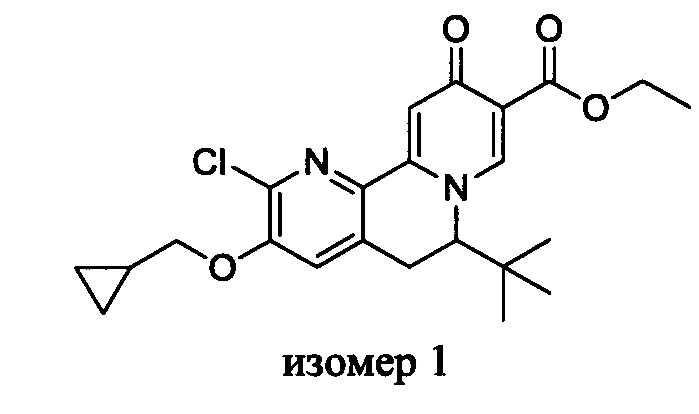
[00692] Рацемат этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигадро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (153 мг) очищали с помощью хиральной хроматографии с использованием следующих условий: Колонка = Chiralpak IC, 10 мм × 250 мм (5u); Подвижная фаза = 95:5 MeCN/H2O + 0,1% муравьиная кислота; Скорость потока = 10 мл/мин: Объем инъекции = 300 мкл (18 мг/мл концентрация); Длина волны детекции: 254 нм. Фракции концентрировали и получали этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат (изомер 1) (48 мг). LCMS(ES+)(m/z): 431,433 (М+1).
[00693] Стадия 2: 6-(трет-Бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота (изомер 1)
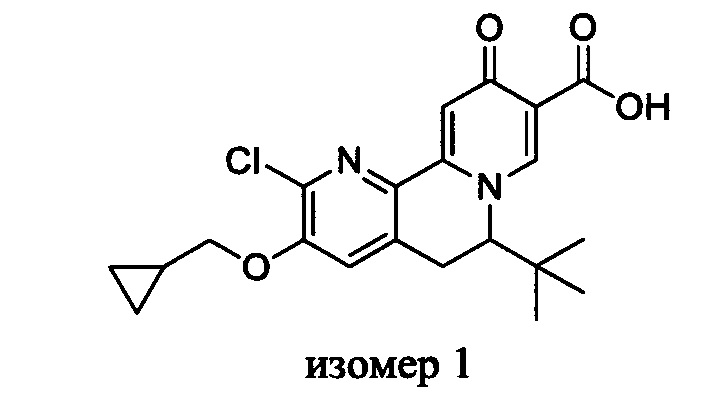
[00694] Раствор моногидрата гидроксида лития (38,8 мг, 0,925 ммоль) в воде (2 мл) добавляли к раствору этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (изомер 1) (48 мг, 0,092 ммоль) в метаноле (2 мл) и указанную смесь нагревали при 60°С в течение 3 часов. Указанную смесь охлаждали до комнатной температуры и закисляли 3 мл 1М соляной кислоты. Твердую фракцию собирали фильтрацией. Полученный фильтрат вводили в хроматографическую колонку среднего давления с обращенной фазой. Собранное твердое вещество растворяли в ДМФА и вводили в колонку с обращенной фазой. Указанную колонку элюировали (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали 6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловую кислоту (изомер 1) (33 мг, 0,082 ммоль, 89% выход) в виде белого порошка. 1H ЯМР (400 MHz, DMSO-d6) δ ppm 8,75 (br. s., 1H), 7,66 (s, 1H), 7,24 (br. s., 1H), 4,55-4,68 (m, 1H), 3,93-4,10 (m, 2H), 3,39-3,54 (m, 2H), 1,27 (d, J=5,08 Hz, 1H), 0,70 (s, 9H), 0,55-0,62 (m, 2H), 0,30-0,39 (m, 2H). LCMS(ES+)(/w/z): 403,405 (M+1).
[00695] Пример 30-b (Соединение 249 Изомер 2)
[00696] 6-(трет-Бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6,10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота (изомер 2)
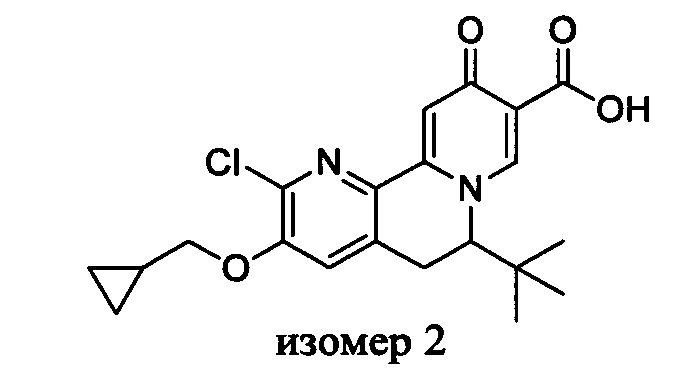
[00697] Стадия 1: Этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат (изомер 2)
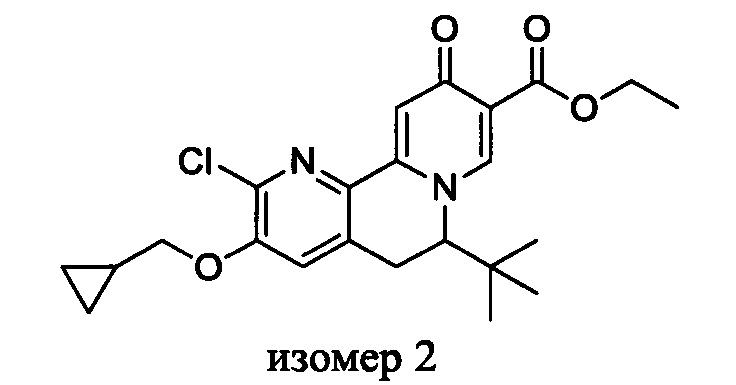
[00698] Рацемат этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (153 мг) очищали с помощью хиральной хроматографии с использованием следующих условий: Колонка = Chiralpak IC, 10 мм × 250 мм (5u); Подвижная фаза = 95:5 MeCN/H2O + 0,1% муравьиная кислота; Скорость потока = 10 мл/мин: Объем инъекции = 300 мкл (18 мг/мл концентрация); Длина волны детекции: 254 нм. Фракции концентрировали и получали этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилат (изомер 2) (46 мг). LCMS(ES+)(m/z): 431,433 (М+1).
[00699] Стадия 2: 6-(трет-Бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-6.10-дигидро-5Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловая кислота (изомер 2)
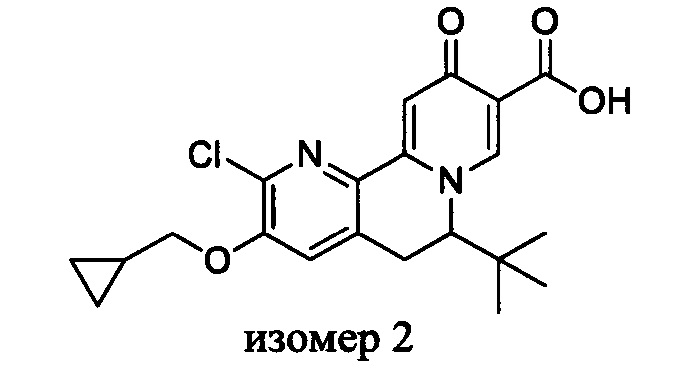
[00700] Раствор моногидрата гидроксида лития (37,2 мг, 0,886 ммоль) в воде (2 мл) добавляли к раствору этил-6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксилата (изомер 2) (46 мг, 0,089 ммоль) в метаноле (2 мл) и указанную смесь нагревали при 60°С в течение 3 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и закисляли 3 мл 1М соляной кислоты. Твердую фракцию собирали фильтрацией. Полученный фильтрат вводили в хроматографическую колонку среднего давления с обращенной фазой. Собранное твердое вещество растворяли в ДМФА и также вводили в колонку с обращенной фазой. Указанную колонку элюировали (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали 6-(трет-бутил)-2-хлор-3-(циклопропилметокси)-10-оксо-5,10-дигидро-6Н-пиридо[1,2-h][1,7]нафтиридин-9-карбоксиловую кислоту (изомер 2) (34 мг, 0,084 ммоль, 95% выход) в виде белого порошка. 1H ЯМР (400 MHz, DMSO-d6) δ ppm 8,76 (s, 1Н), 7,67 (s, 1Н), 7,25 (s, 1Н), 4,63 (d, J=6,64 Hz, 1H), 3,96-4,11 (m, 2H), 3,33-3,54 (m, 2H), 1,19-1,33 (m, 1H), 0,70 (s, 9H), 0,56-0,62 (m, 2H), 0,30-0,42 (m, 2H). LCMS(ES+)(m/z): 403, 405 (M+1).
[00701] Схема 12 - Получение соединений Типа YYYY (например. Соединения 250.251.255 и 256)
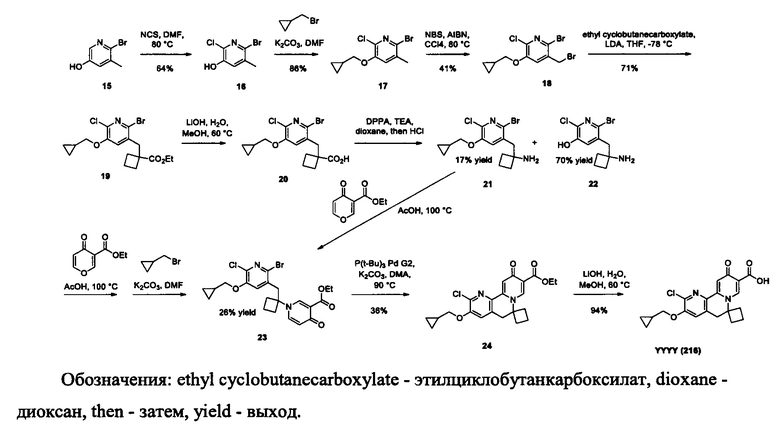
[00702] Пример 31 (Соединение 250)
2'-Хлор-3'-(циклопропилметокси)-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловая кислота
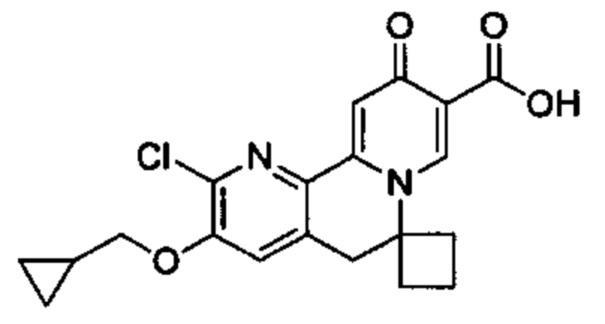
[00703] Стадия 1: 6-Бром-2-хлор-5-метилпиридин-3-ол
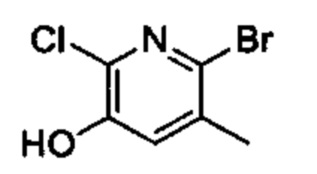
[00704] 6-Бром-5-метилпиридин-3-ол (10,4 г, 55,3 ммоль) и NCS (8,12 г, 60,8 ммоль) в N,N-диметилформамиде (ДМФА) (150 мл) нагревали при 80°С в течение 2 часов. Указанную смесь оставляли охлаждаться до комнатной температуры, гасили солевым раствором и экстрагировали 3 раза этилацетатом. Объединенные органические фазы промывали 5% хлоридом лития, промывали солевым раствором, осушали над сульфатом натрия и концентрировали. Полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 50% этилацетата в гексанах. Фракции концентрировали и получали 6-бром-2-хлор-5-метилпиридин-3-ол (7,85 г, 35,3 ммоль, 63,8% выход) в виде белого порошка. LCMS(ES+)(m/z): 222, 224, 226 (М+1).
[00705] Стадия 2: 2-Бром-6-хлор-5-(циклопропилметокси)-3-метилпиридин
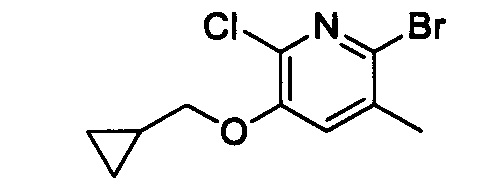
[00706] 6-Бром-2-хлор-5-метилпиридин-3-ол (1,1 г, 4,9 ммоль), карбонат калия (2,73 г, 19,8 ммоль) и (бромметил)циклопропан (1,01 мл, 10,4 ммоль) в N,N-диметилформамиде (ДМФА) (10 мл) перемешивали при комнатной температуре в течение ночи. Указанную смесь разбавляли водой и экстрагировали 2 раза этил ацетатом. Объединенные органические фазы промывали 5% хлоридом лития, промывали солевым раствором, осушали над сульфатом натрия, концентрировали и получали 2-бром-6-хлор-5-(циклопропилметокси)-3-металлиридин (1,18 г, 4,27 ммоль, 86% выход) в виде белого твердого вещества. LCMS(ES+)(m/z): 276, 278, 280 (М+1).
[00707] Стадия 3: 2-Бром-3-(бромметил)-6-хлор-5-(циклопропилметокси)пиридин
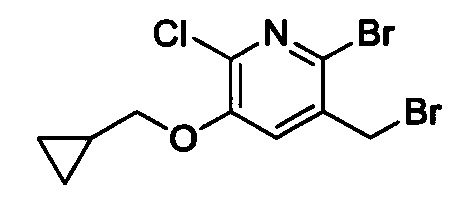
[00708] N-Бромсукцинимид (0,801 г, 4,50 ммоль) и AIBN (0,049 г, 0,30 ммоль) добавляли к перемешиваемому раствору 2-бром-6-хлор-5-(циклопропилметокси)-3-метилпиридина (1,0 г, 3,0 ммоль) в тетрахлорметане (15 мл). Указанную смесь нагревали при 85°С в течение 5 часов. Добавляли дополнительный AIBN (0,049 г, 0,300 ммоль) и указанную смесь оставляли нагреваться в течение ночи. Указанную смесь оставляли охлаждаться до комнатной температуры и твердую фракцию собирали фильтрацией. Полученный фильтрат гасили водой и 2 раза экстрагировали дихлорметаном. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия, и концентрировали. Полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией 10% этил ацетатом в гексанах. Фракции концентрировали и получали 2-бром-3-(бромметил)-6-хлор-5-(циклопропилметокси)пиридин (730 мг, 1,23 ммоль, 60% чистота, 41% выход). Указанный материал представлял собой смесь ~60:40 желаемого продукта / исходного материала. LCMS(ES+)(/w/z): 354, 356, 358 (М+1).
[00709] Стадия 4: Этил-1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобуганкарбоксилат
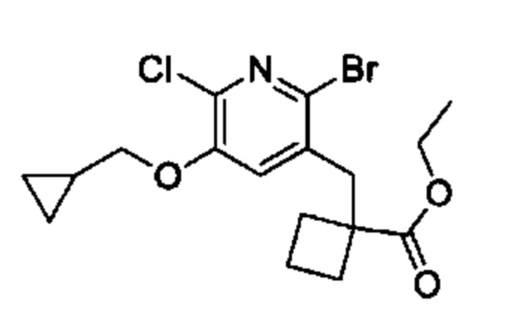
[00710] n-Бутиллитий (2,5 М в гексанах) (1,04 мл, 2,59 ммоль) добавляли по каплям к охлажденному до -78°С раствору диизопропиламина (0,369 мл, 2,59 ммоль) в тетрагидрофуране (ТГФ) (10 мл). Указанную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 15 минут. Указанную смесь охлаждали до -78°С перед добавлением этилциклобутанкарбоксилата (0,317 мл, 2,46 ммоль), который добавляли по каплям. Указанную смесь нагревали до 0°С и перемешивали в течение 15 минут. Раствор 2-бром-3-(бромметил)-6-хлор-5-(циклопропилметокси)пиридина (730 мг, 1,23 ммоль) в тетрагидрофуране (ТГФ) (3,33 мл) добавляли по каплям. Указанную смесь взбалтывали дополнительно 10 минут при 0°С, а затем гасили насыщенным хлоридом аммония. Указанную смесь экстрагировали 2 раза этил ацетатом. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия, и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции концентрировали и получали этил-1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутан-1-карбоксилата (350 мг, 0,869 ммоль, 70,5% выход) в виде масла. LCMS(ES+)(m/r): 402, 404, 406 (М+1).
[00711] Стадия 5: 1-((2-Бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутанкарбоксиловая кислота
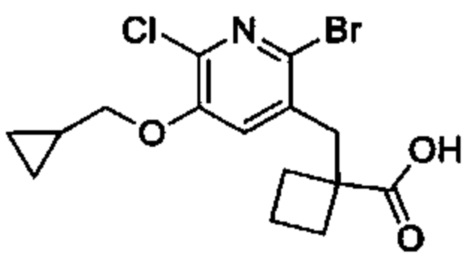
[00712] Раствор моногидрата гидроксида лития (365 мг, 8,69 ммоль) в воде (3 мл) добавляли К раствору этил-1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутан-1-карбоксилата (350 мг, 0,869 ммоль) в 1,4-диоксане (5 мл) и Указанную смесь нагревали при 60°С в течение 4 часов. Указанную смесь оставляли охлаждаться до комнатной температуры, гасили насыщенным раствором хлорида аммония и экстрагировали 3 раза этил ацетатом. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия, концентрировали и получали 1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутан-1-карбоксиловую кислоту (325 мг, 0,867 ммоль, количественно) в виде белого твердого вещества. LCMS(ES+)(m/z): 374, 376, 378 (М+1).
[00713] Стадия 6: 1-((2-Бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутанамин и 5-((1-аминоциклобутил)метил)-6-бром-2-хлорпиридин-3-ол
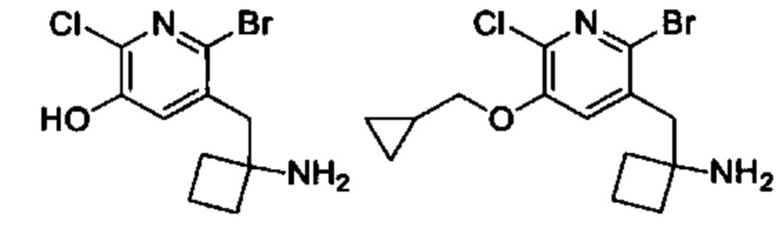
[00714] Дифенилфосфоразидат (0,394 мл, 1,83 ммоль) добавляли по каплям к охлажденной до 0°С перемешиваемой смеси 1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутан-1-карбоксиловой кислоты (311 мг, 0,830 ммоль) и триэтиламина (0,255 мл, 1,83 ммоль) в толуоле (10 мл). Указанную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 15 минут, затем нагревали при 80°С в течение 1 часа. Данные LC-MS продемонстрировали чистую конверсию в 2-бром-6-хлор-5-(циклопропилметокси)-3-((1-изоцианатциклобутил)метил)пиридин. Указанную смесь оставляли охлаждаться до комнатной температуры перед добавлением 5N соляной кислоты (5 мл, 25 ммоль) и 1,4-диоксана (10 мл). Указанную смесь нагревали при 80°С с энергичным взбалтыванием в течение 3 часов. Указанную смесь концентрировали и полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Два набора фракций концентрировали раздельно и получали следующие продукты:
[00715] 5-((1-аминоциклобутил)метил)-6-бром-2-хлорпиридин-3-ол (170 мг, 0,583 ммоль, 70,2% выход). LCMS(ES+)(m/z): 291, 293, 295 (М+1)
[00716] 1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутан-1-амин (50 мг, 0,145 ммоль, 17,43% выход). LCMS(ES+)(/n/z): 345, 347, 349 (М+1).
[00717] Стадия 7: Этил-4-оксо-4Н-пиран-3-карбоксилат
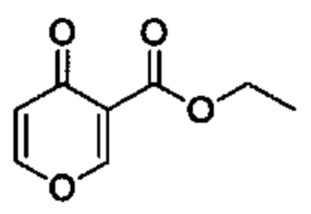
[00718] Этилформат (23,6 мл, 292 ммоль) медленно добавляли к суспензии KOtBu (6,06 г, 54,0 ммоль) в 50 мл ТГФ при 0°С. Полученную реакционную смесь перемешивали в течение 15 мин при 0°С и предварительно охлажденный (0°С) раствор этил-2-((диметиламино)метилен)-3-оксобутаноата (5 г, 27,0 ммоль) в 45 мл ТГФ добавляли с помощью канюли. После того, как добавление было завершено, указанный раствор удаляли из охлаждающей бани, перемешивали при комнатной температуре в течение ночи, и гасили добавлением 1М водной HCl (80 мл). Указанную смесь экстрагировали EtOAc (3×25 мл) и CH2Cl2 (5×25 мл). Указанные органические фазы объединяли, осушали (Na2SO4), отфильтровывали, упаривали и очищали с помощью хроматографии на силикагеле (0-100% EtOAc/гексаны) с получением этил-4-оксо-4Н-пиран-3-карбоксилата (1,8994 г, 41,8% выход) в виде коричневого масла. 1Н ЯМР (400 MHz, CDCl3) δ ppm 8,47 (d, J=0,78 Hz, 1H), 7,72 (dd, J=5,86, 0,78 Hz, 1H), 6,47 (d, J=5,86 Hz, 1H), 4,37 (q, J=7,29 Hz, 2H), 1,38 (t, J=7,03 Hz, 3H). LCMS (ESI) m/z: 169,05 (M+1)+.
[00719] Стадия 8: Этил-1-(1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутил)-4-оксо-1,4-дигидропиридин-3-карбоксилат
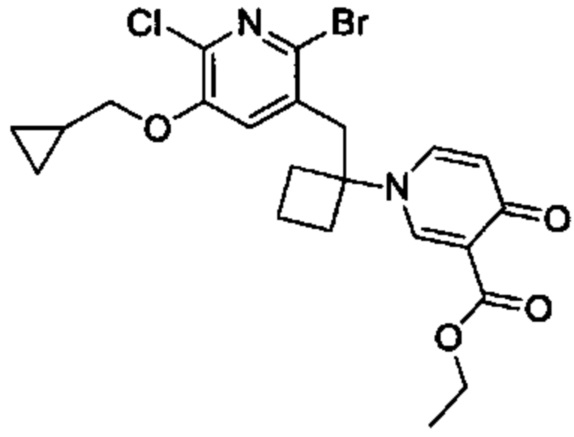
[00720] 5-((1-Аминоциклобутил)метил)-6-бром-2-хлорпиридин-3-ол (170 мг, 0,583 ммоль) и этил-4-оксо-4Н-пиран-3-карбоксилат (98 мг, 0,58 ммоль) в уксусной кислоте (5 мл) перемешивали при 100°С в течение 4 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и концентрировали. Полученный осадок разбавляли в толуоле и указанную смесь концентрировали для удаления оставшейся уксусной кислоты. Полученный осадок растворяли в N,N-диметилформамиде (ДМФА) (2 мл) перед добавлением карбоната калия (322 мг, 2,33 ммоль) и (бромметил)циклопропана (0,113 мл, 1,17 ммоль). Указанную смесь взбалтывали при комнатной температуре в течение 6 часов и получали неочищенную смесь этил-1-(1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутил)-4-оксо-1,4-дигидропиридин-3-карбоксилата в ДМФ. В отдельной реакционной колбе перемешивали 1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутан-1-амин (50 мг, 0,145 ммоль) и этил-4-оксо-4Н-пиран-3-карбоксилат (24,3 мг, 0,145 ммоль) в уксусной кислоте (1 мл) при 100°С в течение ночи. Указанную смесь оставляли охлаждаться до комнатной температуры, а затем объединяли с указанной предыдущей неочищенной смесью этил-1-(1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутил)-4-оксо-1,4-дигидропиридин-3-карбоксилата в ДМФА, описанной выше. Указанную смесь разбавляли водой и экстрагировали 2 раза этилацетатом. Объединенные органические фазы промывали 5% хлоридом лития, промывали солевым раствором, осушали над сульфатом натрия и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции концентрировали до тех пор, пока они не замутнели. Добавляли ацетонитрил до полного растворения и указанный раствор лиофилизировали и получали этил-1-(1-((2-бром-6-хлор-5-(циклопропилметокси)пиридин-3-ил)метил)циклобутил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (100 мг, 0,202 ммоль, 26% выход) в виде бледно-желтого твердого вещества. LCMS(ES+)(/n/z): 495, 497,499 (М+1).
[00721] Стадия 9: Этил-2'-хлор-3'-(циклопропилметокси)-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксилат
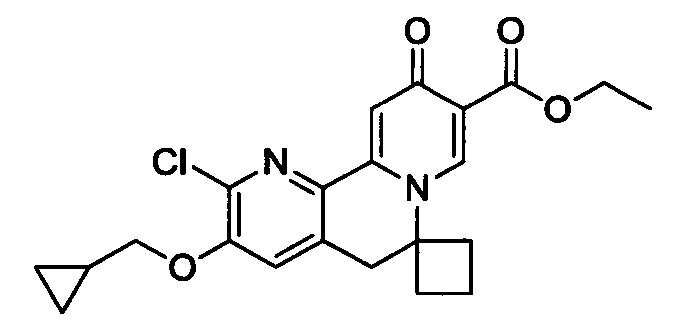
[00722] Реакционную виалу, содержащую мешалку, этил-1-(1-((2-бром-6-хлор-5-(циклопропилметокси)гшридин-3-ил)метил)циклобутил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (100 мг, 0,202 ммоль), ацетат калия (39,6 мг, 0,403 ммоль) и хлор[(три-трет-бутилфосфин)-2-(2-аминобифенил)]палладий(II) (20,7 мг, 0,040 ммоль) продували азотом в течение 15 минут. N,N-Диметилацетамид (DMA) (2 мл) продували азотом в течение 5 минут перед добавлением к указанной реакционной смеси в виале. Указанную реакционную виалу помещали в нагревательный блок, предварительно нагретый до 90°С и указанную смесь перемешивали в течение ночи. Полученную реакционную смесь оставляли охлаждаться до комнатной температуры, отфильтровывали через хлопковую пробку и очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода / 0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали этил-2'-хлор-3'-(циклопропилметокси)-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксилат (30 мг, 0,072 ммоль, 35,9% выход) в виде серовато-белого твердого вещества. LCMS(ES+)(m/z): 415, 417 (М+1).
[00723] Стадия 10: 2'-Хлор-3'-(циклопропилметокси)-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,71нафтиридин]-9'-карбоксиловая кислота
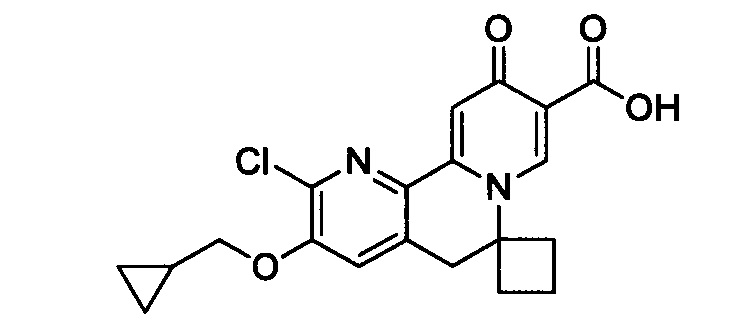
[00724] Раствор моногидрата гидроксида лития (25,2 мг, 0,600 ммоль) в воде (1 мл) добавляли к раствору этил-2'-хлор-3'-(циклопропилметокси)-10'-оксо-5',10'-дигидроспиро [циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксилата (30 мг, 0,060 ммоль) в метаноле (1 мл) и указанную смесь нагревали при 60°С в течение 3 часов. Указанную смесь оставляли охлаждаться до комнатной температуры и закисляли 1М соляной кислотой. Указанную смесь разбавляли ДМФА для растворения образца, а затем очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода / 0,1% муравьиная кислота / градиент с 10% до 100%). Объединенные фракции лиофилизировали и получали 2,-хлор-3'-(1циклопропилметокси)-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловую кислоту (22 мг, 0,056 ммоль, 94% выход) в виде серовато-белого порошка. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,79 (s, 1H), 7,68 (s, 1H), 7,27 (s, 1H), 4,07 (d, J=7,03 Hz, 2H), 3,44 (s, 2H), 2,61-2,75 (m, 2H), 2,00-2,12 (m, 2H), 1,78-1,95 (m, 2H), 1,25-1,37 (m, 1H), 0,57 -0,68 (m, 2H), 0,33-0,40 (m, 2H). LCMS(ES+)(m/z): 387, 389 (M+1).
[00725] Пример 32 (Соединение 251)
[00726] 2',3',-Диметокси-10'-оксо-5',10,-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловая кислота
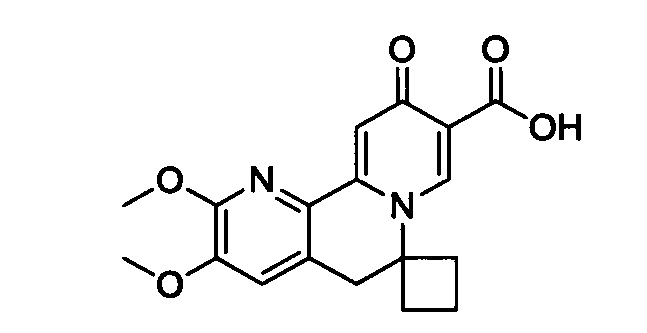
[00727] Стадия 1: 2',3'-Диметокси-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловая кислота
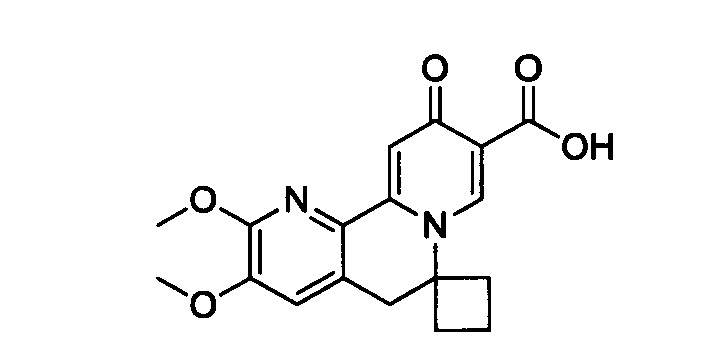
[00728] 2'-Хлор-3'-(циклопропилметоксти)-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловую кислоту (10 мг, 0,026 ммоль) и метилат натрия (0,5 М в метаноле) (0,517 мл, 0,259 ммоль) нагревали при 65°С в течение 2 часов. Добавляли диоксан (0,5 мл) и указанную смесь грели при 100°С. Указанную виалу оставляли изначально незакрытой, так что большая часть метанола испарилась. Указанную реакционную виалу закрывали крышкой и перемешивали при 100°С в течение 1,5 часов. Указанную смесь оставляли охлаждаться до комнатной температуры, закисляли 1N HCl, очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 10% до 100%). Фракции лиофилизировали и получали 2',3'-диметокси-10'-оксо-5',10'-дигидроспиро[циклобутан-1,6'-пиридо[1,2-h][1,7]нафтиридин]-9'-карбоксиловую кислоту (1,5 мг, 4,03 мкмоль, 15,6% выход) в виде белого твердого вещества. 1Н ЯМР (400 MHz, хлороформ-d) δ ppm 8,90 (s, 1Н), 7,65 (s, 1Н), 6,93 (s, 1Н), 4,08 (s, 3Н), 3,97 (s, 3Н), 3,26 (s, 2Н), 2,57-2,75 (m, 2Н), 2,15-2,29 (m, 2Н), 2,00-2,12 (m, 2Н). LCMS(ES-)(w/z): 341 (M-1)-.
[00729] Схема 13-Получение соединений, таких как Пример 33 (Соединение 252)
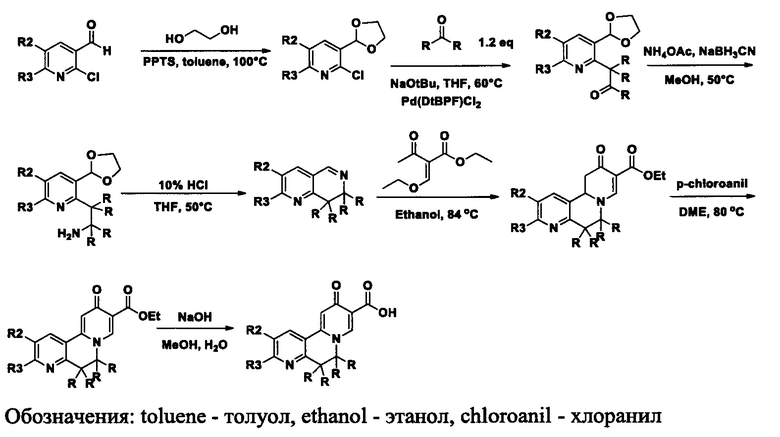
[00730] Схема 14-Получение Примера 33 (Соединение 252)

[00731] Пример 33 (Соединение 252)
6-Изопропил-2,3-диметил-10-оксо-5,10-дигидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксиловая кислота
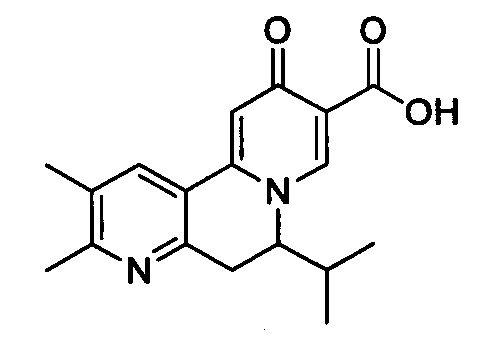
[00732] Стадия 1: 2-Хлор-5.6-диметилникотиннитрил
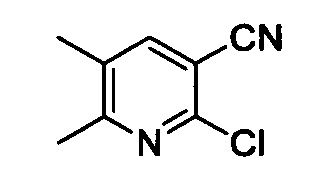
[00733] Смесь 2-гадрокси-5,6-диметилникогиннитрила (10 г, 67,5 ммоль) в POCl3 (100 мл) нагревали с обратным холодильником в течение 10 ч и концентрировали. Полученный осадок защелачивали 10% водным раствором NaOH и отфильтровывали. Осадок на фильтре промывали Н2О. Полученный фильтрат экстрагировали DCM (200 мл × 2). Указанные органические фазы комбинировали, промывали солевым раствором (200 мл), осушали над безводным Na2SO4, концентрировали и получали 9,8 г неочищенного 2-хлор-5,6-диметилникотиннитрила в виде желтого твердого вещества. LCMS (ESI) m/z: 167,1, 169,1 (М/М+2)+.
[00734] Стадия 2: 2-Хлор-5,6-диметилникотинальдегид
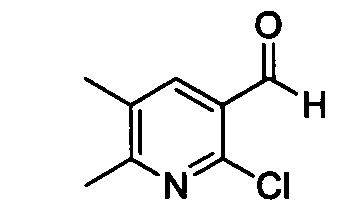
[00735] К охлажденному до -78°С раствору 2-хлор-5,6-диметилникотиннитрила (1,6 г, 9,6 ммоль) в DCM (20 мл) добавляли DIBAL-H (5,76 мл, 2 моль/л в гексане). Полученную смесь взбалтывали при той же температуре в течение 2 ч. Указанную реакционную смесь гасили добавлением ледяной воды. Затем указанную смесь закисляли 1N HCl до рН= ~6 и экстрагировали DCM (100 мл × 2). Указанные органические фазы комбинировали, промывали солевым раствором (50 мл), осушали над безводным Na2SO4, концентрировали и получали 1,5 г неочищенный 2-хлор-5,6-диметилникотинальдегид в виде белого твердого вещества. LCMS (ESI) m/z: 170,1, 172,1 (М/М+2)+.
[00736] Стадия 3: 2-Хлор-3-(1,3-диоксолан-2-ил)-5,6-диметилпиридин
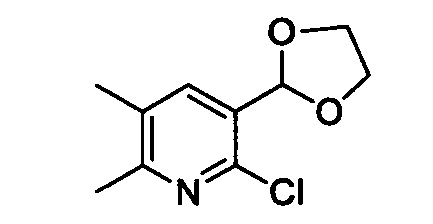
[00737] Смесь 2-хлор-5,6-диметилникотинальдегида (1,5 г, 8,84 ммоль), этан-1,2-диола (1,1 г, 17,68 ммоль), PPTS (444,3 мг, 1,768 ммоль) в толуоле (20 мл) нагревали с обратным холодильником в течение 12 ч. Полученную реакционную смесь охлаждали до комнатной температуры и экстрагировали EtOAc (100 мл × 2). Указанные органические фазы комбинировали, промывали водным раствором NaHCO3 (50 мл), осушали над безводным Na2SO4 и концентрировали. Полученный осадок очищали с помощью колоночной флеш-хроматографии (силикагель, 0-50% EtOAc в РЕ) с получением 2-хлор-3-(1,3-диоксолан-2-ил)-5,6-диметилпиридина(1,35 г, 71,5% выход) в виде бесцветного масла. LCMS (ESI) m/z: 214,1, 216,1(М/М+2)+.
[00738] Стадия 4: 1-(3-(1,3-Диоксолан-2-ил)-5,6-диметилпиридин-2-ил)-3-метилбутан-2-он

[00739] Смесь 2-хлор-3-(1,3-диоксолан-2-ил)-5,6-диметилпиридина (1,35 г, 6,32 ммоль), 3-метилбутан-2-она (653 мг, 7,58 ммоль), Pd(dtbpf)Cl2(411,9 мг, 0,632 ммоль) и t-BuONa (1,52 г, 15,8 ммоль) в ТГФ (20 мл) нагревали при 60°С в течение 3 ч. Полученную реакционную смесь охлаждали до комнатной температуры и отфильтровывали. Полученный фильтрат концентрировали и полученный осадок очищали с помощью колоночной флеш-хроматографии (силикагель, 0-70% EtOAc в РЕ) с получением 1-(3-(1,3-даоксолан-2-ил)-5,6-диметилпиридин-2-ил)-3-метилбутан-2-она(231 мг, 14% выход) в виде желтого твердого вещества. LCMS (ESI) m/z: 264,3 (М+1)+.
[00740] Стадия 5: 1-(3-(1,3-Диоксолан-2-ил)-5,6-диметилпиридин-2-ил)-3-метилбуган-2-амин

[00741] К раствору 1-(3-(1,3-даоксолан-2-ил)-5,6-диметилпиридин-2-ил)-3-метилбутан-2-она (231 мг, 0,878 ммоль) в МеОН (10 мл) добавляли NH4OAc (683,1 мг, 8,78 ммоль) при комнатной температуре. После перемешивания указанной смеси в течение 30 мин к указанной смеси при 0°С добавляли NaBH3CN (82,8 мг, 1,317 ммоль). Затем полученную смесь взбалтывали при 50°С в течение 10 ч. Полученную реакционную смесь охлаждали до комнатной температуры и концентрировали. Полученный осадок разбавляли Н2О (20 мл), защелачивали до рН~10 10% раствором NaOH. Указанную водную смесь экстрагировали DCM (2х). Указанные органические фазы комбинировали, промывали солевым раствором (30 мл), осушали над безводным Na2SO4 и концентрировали при пониженном давлении с получением 236 мг неочищенного 1-(3-(1,3-диоксолан-2-ил)-5,6-диметилпиридин-2-ил)-3-метилбутан-2-амина. LCMS (ESI) m/z: 265,3 (М+1)+.
[00742] Стадия 6: 7-Изопропил-2,3-диметил-7,8-дигидро-1,6-нафтиридин
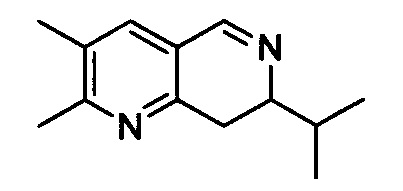
[00743] К раствору 1-(3-(1,3-диоксолан-2-ил)-5,6-диметилпиридин-2-ил)-3-метилбутан-2-амина (70 мг, 0,264 ммоль) в ТГФ (10 мл) добавляли 10% водный раствор HCl (2 мл). Полученную смесь нагревали при 50°С в течение 10 ч. После охлаждения до комнатной температуры указанную смесь концентрировали. Полученный осадок очищали с использованием хроматографической колонки (силикагель, 0-10% МеОН в DCM) и получали 7-изопропил-2,3-диметил-7,8-дигадро-1,6-нафтиридин (20 мг, 37,3% выход). LCMS (ESI) m/z: 203,27 (М+1)+.
[00744] Стадия 7: Этил-6-изопропил-2,3-диметил-10-оксо-5,10,11,11а-тетрагидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксилат
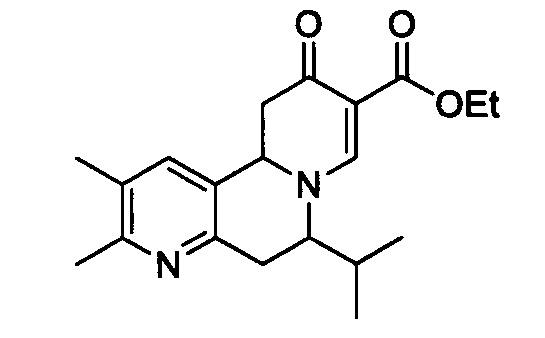
[00745] Раствор 7-изопропил-2,3-диметил-7,8-дигидро-1,6-нафтиридина (20 мг, 0,099 ммоль) и этил-2-(этоксиметилен)-3-оксо-бутаноата (55,86 мг, 0,3 ммоль) в EtOH (5 мл) нагревали при 85°С в течение 10 ч. После охлаждения до комнатной температуры указанную смесь концентрировали. Полученный осадок очищали с использованием хроматографической колонки (силикагель, 0-10% МеОН в DCM) и получали этил-6-изопропил-2,3-диметил-10-оксо-5,10,11,11а-тетрагидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксилат (20 мг, 58,9% выход). LCMS (ESI) m/z: 343,2 (М+1)+.
[00746] Стадия 8: Этил-6-изопропил-2,3-диметил-10-оксо-5,10-дигидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксилат
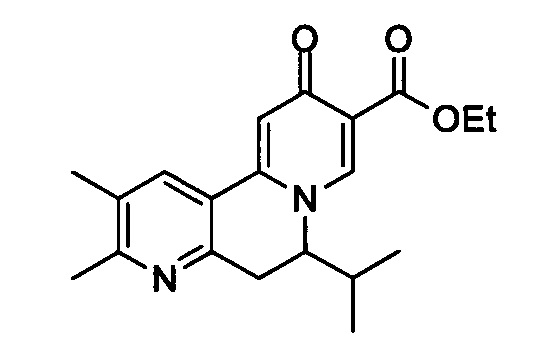
[00747] К раствору этил-6-изопропил-2,3-диметил-10-оксо-5,10,11,11а-тетрагидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксилата (20 мг, 0,058 ммоль) в DME (5 мл) добавляли р-хлоранил (12,3 мг, 0,05 ммоль). Указанную смесь нагревали при 80°С в течение 3 ч. После охлаждения до комнатной температуры указанную смесь концентрировали. Полученный осадок очищали с использованием хроматографической колонки (силикагель, 0-10% МеОН в DCM) с получением этил-6-изопропил-2,3-диметил-10-оксо-5,10-дигидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксилата (15 мг, 76% выход). LCMS (ESI) m/z: 341,2 (M+1)+.
[00748] Стадия 9: 6-Изопропил-2,3-диметил-10-оксо-5Л0-дигидро-6Н-пиридо[2,1-][1,6]нафтиридин-9-карбоксиловая кислота
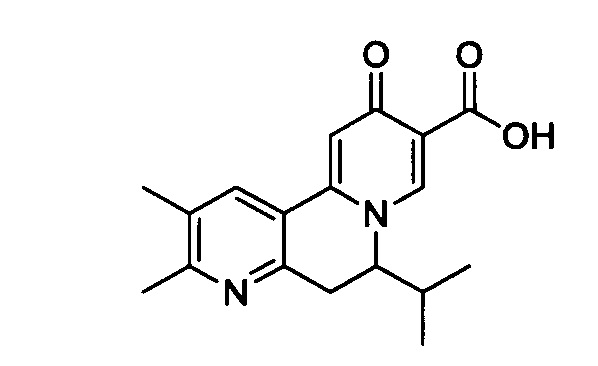
[00749] К раствору этил-6-изопропил-2,3-диметил-10-оксо-5,10-дигидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксилата (15 мг, 0,044 ммоль) в МеОН (5 мл) добавляли NaOH (7 мг, 0,176 ммоль), растворенного в H2O (1 мл). Полученную смесь взбалтывали при комнатной температуре в течение 2 ч. Полученную реакционную смесь закисляли до рН~5 с помощью 1N HCl. Затем указанную смесь разбавляли EtOAc (20 мл) и H2O (20 мл), а затем экстрагировали EtOAc (20 мл × 2). Объединенные органические фазы осушали над безводным Na2SO4 и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой ВЭЖХ (колонка С18, 5% - 100% MeCN в H2O с 0,1% муравьиная кислота в Н2О) и получали 6-изопропил-2,3-диметил-10-оксо-5,10-дигидро-6Н-пиридо[2,1-f][1,6]нафтиридин-9-карбоксиловую кислоту (5 мг, 36,3% выход) в виде белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ 8,87 (s, 1Н), 8,25 (s, 1H), 7,43 (s, 1H), 4,63-4,58 (m, 1H), 3,56-3,50 (m, J=16,8, 5,3 Hz, 1H), 3,18 (d, J=16,6 Hz, 1H), 2,48 (s, 3H), 2,31 (s, 3H), 1,64-1,57 (m, 1H), 0,84 (d, J=6,6 Hz, 3H), 0,69 (d, J=6,7 Hz, 3H). LCMS (ESI) m/z: 313,2 (M+1)+.
[00750] Пример 34 (Соединение 253)
[00751] 2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота (рацемат цис)
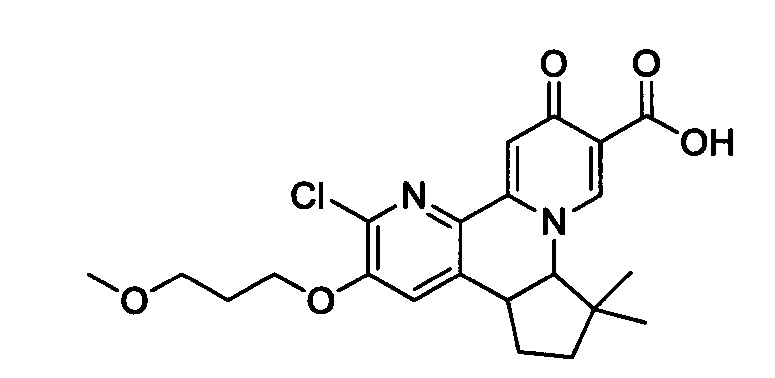
[00752] Стадия 1: 5-(6-Хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентанон
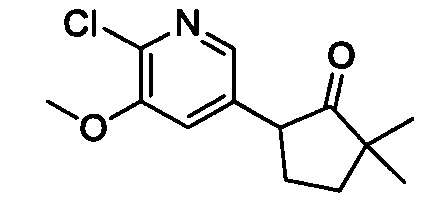
[00753] В колбу помещали мешалку, 5-бром-2-хлор-3-метоксипиридин (9,9 г, 44 ммоль), трис(дибензилиденацетон)дипалладий(0) (0,611 г, 0,668 ммоль), ксантфос (0,695 г, 1,202 ммоль) и трет-бутоксид натрия (7,5 г, 78 ммоль). Указанную колбу продували потоком азота перед добавлением 2,2-диметилциклопентан-1-она (8,38 мл, 66,8 ммоль) в тетрагидрофуране (ТГФ) (200 мл). Указанную смесь нагревали с обратным холодильником в течение 3 часов. Указанную смесь оставляли охлаждаться до комнатной температуры, отфильтровывали и осадок на фильтре промывали этил ацетатом. Полученный фильтрат разбавляли дополнительным этилацетатом, промывали солевым раствором, концентрировали и полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 30% этилацетатом в гексанах. Фракции концентрировали и получали 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметщщиклопентан-1-он (4,6 г, 18 ммоль, 41% выход) в виде масла. 1Н ЯМР (400 MHz, хлороформ-d) δ ppm 7,82 (d, J=1,56 Hz, 1Н), 7,13 (d, J=1,95 Hz, 1H), 3,91 (s, 3H), 3,36-3,47 (m, 1H), 2,45 (m, 1H), 1,96-2,17 (m, 2H), 1,79-1,92 (m, 1H), 1,18 (s, 3H), 1,07 (s, 3H). LCMS(ES+)(m/z): 254,2 (M+1).
[00754] Стадия 2: 5-(6-Хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентанамин (цис/транс изомеры)
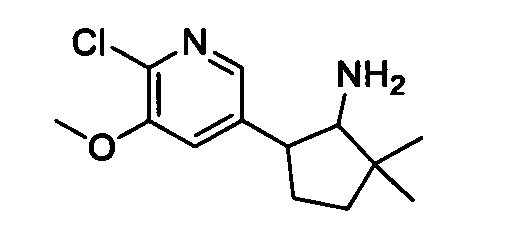
[00755] Смесь 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-она (4,6 г, 18 ммоль) и ацетата аммония (21 г, 270 ммоль) в метаноле (75 мл) перемешивали при комнатной температуре в течение 1 часа. Добавляли цианоборгидрид натрия (2,28 г, 36,3 ммоль) и указанную смесь нагревали при 60°С в течение ночи, а затем при 65°С в течение дополнительных 24 часов. Указанную смесь оставляли охлаждаться до комнатной температуры, концентрировали до ~20 мл, гасили 1М гидроксидом натрия и экстрагировали 3 раза 2-метилтетрагидрофураном. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия и концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 0% до 100%). Фракции концентрировали и получали 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-амин (2,63 г, 10,3 ммоль, 57% выход) в виде смеси цис/транс изомеров. LCMS(ES+)(m/z): 255,2 (М+1).
[00756] Стадия 3: 5-(2-Амино-3,3-диметилциклопентил)-2-хлорпиридин-3-ол(цис/транс изомеры)
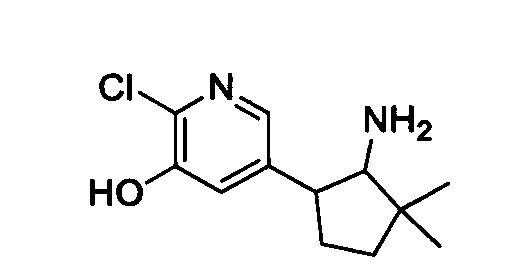
[00757] Трибромид бора (4,82 мл, 51,0 ммоль) медленно добавляли по каплям к энергично перемешиваемому раствору 5-(6-хлор-5-метоксипиридин-3-ил)-2,2-диметилциклопентан-1-амина (2,6 г, 10,2 ммоль) (цис/транс изомеры). Указанную смесь нагревали при 70°С в течение ночи. Указанную смесь оставляли охлаждаться до комнатной температуры, а затем охлаждали до 0°С. Указанную смесь осторожно гасили медленным добавлением метанола. Добавляли дополнительные 50 мл метанола и указанную смесь перемешивали в течение 30 минут, затем концентрировали. Полученный осадок очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода /0,1% муравьиная кислота / градиент с 0% до 100%). Фракции лиофилизировали и получали 5-(2-амино-3,3-диметилциклопентил)-2-хлорпиридин-3-ол (цис/транс изомеры) (2,17 г, 9,01 ммоль, 88% выход) в виде белого твердого вещества. LCMS(ES+)(m/z): 241,2 (М+1).
[00758] Стадия 4: 5-(2-Амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ол (рацемат цис) и 5-(2-амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ол (рацемат транс)
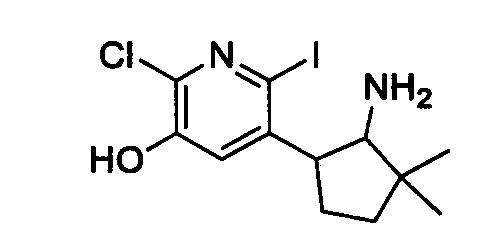
[00759] Йод (2,29 г, 9,01 ммоль) добавляли к перемешиваемой смеси 5-(2-амино-3,3-диметилциклопентил)-2-хлорпиридин-3-ола (2,17 г, 9,01 ммоль) и карбоната калия (3,74 г, 27,0 ммоль) в воде (40 мл). Указанную смесь взбалтывали при комнатной температуре в течение 2 часов. Порциями добавляли твердый сульфат натрия (2,39 г, 18,9 ммоль) и указанную смесь перемешивали в течение 30 минут. Указанную водную смесь доводили рН=~3 3N соляной кислотой. Указанную смесь отфильтровывали. Данные LC-MS продемонстрировали, что полученный твердый остаток содержал небольшое количество продукта и его отбрасывали. Промывку концентрировали до ~50 мл и вводили в обращенно-фазовую колонку среднего давления С18 ISCO, которую элюировали системой ацетонитрил / вода /0,1% муравьиная кислота / градиент с 0% до 100%. 2Набора фракций лиофилизировали раздельно.
[00760] Пик 1 = 5-(2-амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ол (рацемат транс) (1,17 г, 3,19 ммоль, 35% выход). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,23 (s, 1H), 7,26 (s, 1H), 2,99-3,15 (m, 2H), 2,05-2,19 (m, 1H), 1,51-1,64 (m, 2H), 1,22-1,35 (m, 1H), 1,09 (s, 3H), 0,95 (s, 3H). LCMS(ES+)(m/z): 367,1 (M+1).
[00761] Пик 2 = 5-(2-амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ол (рацемат цис, загрязненный ~20% рацематом транс) (924 мг, 2,01 ммоль, 22% выход). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,27 (s, 1Н), 7,20 (s, 1Н), 3,41-3,53 (m, 1Н), 3,28 (d, J=5,86 Hz, 1H), 2,07-2,19 (m, 1H), 1,81-1,95 (m, 1H), 1,68-1,77 (m, 1H), 1,47-1,57 (m, 1H), 1,14 (s, 3H), 1,08 (s, 3H). LCMS(ES+)(m/z): 367,1 (M+1).
[00762] Стадия 5: Этил-1-(5-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (рацемат цис)
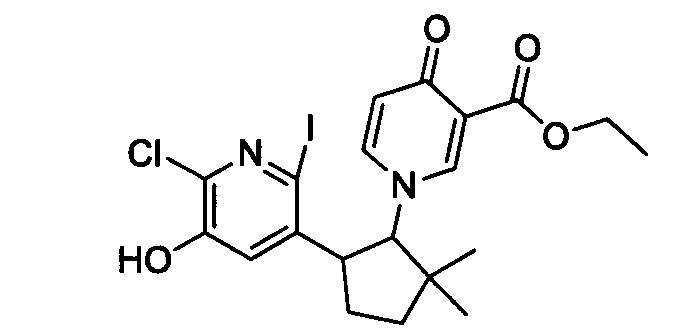
[00763] 5-(2-Амино-3,3-диметилциклопентил)-2-хлор-6-йодпиридин-3-ол (рацемат цис) (924 мг, 2,02 ммоль) (загрязненный ~20% рацематом транс) и этил-4-оксо-4Н-пиран-3-карбоксилат (466 мг, 2,77 ммоль) в уксусной кислоте (13 мл) перемешивали при 100°С в течение 4 часов. Указанную смесь оставляли охлаждаться до комнатной температуры, разбавляли водой и экстрагировали 2 раза дихлорметаном. Насыщенный солевой раствор добавляли к указанной водной фазе и указанную смесь еще 2 раза экстрагировали дихлорметаном. Объединенные органические фазы промывали солевым раствором, осушали над сульфатом натрия и концентрировали. Полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 10% метанола в дихлорметане. Фракции концентрировали и получали этил-1-(5-(6-хлор-5-гадрокси-2-йодпиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (рацемат цис) (346 мг, 0,670 ммоль, 33% выход). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 10,92 (br. s., 1H), 7,78 (d, J=1,95 Hz, 1H), 7,43 (dd, J=7,81, 2,34 Hz, 1H), 7,07 (s, 1H), 6,04 (d, J=7,42 Hz, 1H), 4,54 (d, J=7,42 Hz, 1H), 4,03-4,17 (m, 2H), 3,82-3,95 (m, 1H), 2,15-2,27 (m, 2H), 1,99 (dt, J=13,66, 7,22 Hz, 1H), 1,74-1,87 (m, 1H), 1,24-1,31 (m, 3H), 1,14-1,23 (m, 3H), 0,92 (s, 3H). LCMS(ES+)(m/z): 517,1 (M+1).
[00764] Стадия 6: Этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (рацемат цис)
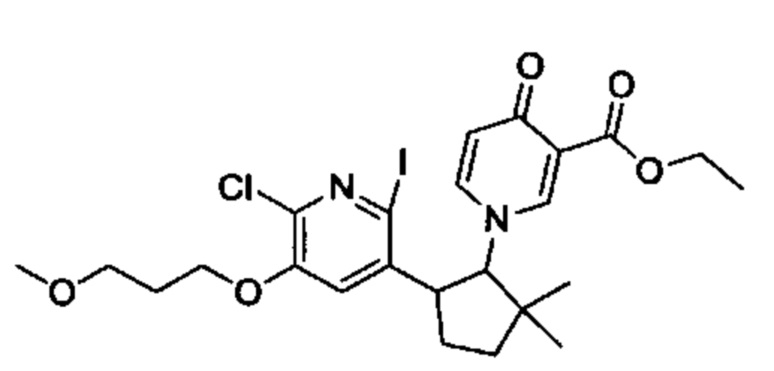
[00765] Этил-1-(5-(6-хлор-5-гидрокси-2-йодпиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-кар (рацемат цис) (346 мг, 0,670 ммоль), карбонат калия (463 мг, 3,35 ммоль) и 1-бром-3-метоксипропан (205 мг, 1,34 ммоль) в N,N-диметилформамиде (ДМФА) (5 мл) перемешивали при комнатной температуре в течение ночи. Указанную смесь гасили водой и экстрагировали 3 раза этил ацетатом. Объединенные органические фазы промывали солевым раствором и концентрировали. Полученный осадок очищали с помощью хроматографии и получали этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (341 мг, 0,579 ммоль, 86% выход). LCMS(ES+)(w/z): 589,2 (М+1).
[00766] Стадия 7: Этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксилата (рацемат цис)
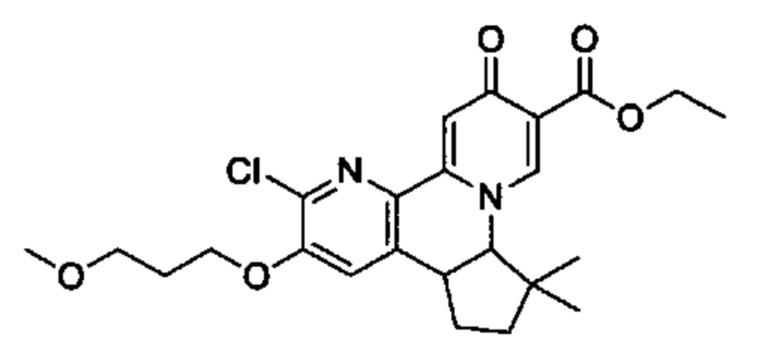
[00767] Круглодонную колбу, закрытую диафрагмой и содержащую мешалку, этил-1-(5-(6-хлор-2-йод-5-(3-метоксипропокси)пиридин-3-ил)-2,2-диметилциклопентил)-4-оксо-1,4-дигидропиридин-3-карбоксилат (341 мг, 0,579 ммоль), ацетат калия (114 мг, 1,16 ммоль) и бромид палладия (II) (30,8 мг, 0,116 ммоль) продували азотом в течение 15 минут. N,N-Диметилацетамид (DMA) (5 мл) продували азотом в течение 5 минут перед добавлением в колбу с реакционной смесью. Указанную колбу с реакционной смесью помещали в масляную баню, предварительно нагретую до 90°С, и указанную смесь перемешивали в течение 4 часов. Полученную реакционную смесь оставляли охлаждаться до комнатной температуры, разбавляли этилацетатом и отфильтровывали через хлопковую пробку. Указанную смесь промывали солевым раствором, осушали над сульфатом натрия и концентрировали. Полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 10% метанола в дихлорметане. Фракции концентрировали. Желаемый продукт выделяли, но оставляли значительное количество DMA. Затем указанный продукт очищали с помощью обращенно-фазовой хроматографии среднего давления (С18 / ацетонитрил / вода / 0,1% муравьиная кислота / градиент с 10% до 100%). Фракции концентрировали и получали этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексатадроциклопента[1]пиридо[1,2-h][1,7]нафтиридин-10-карбоксилат (рацемат цис) (150 мг, 0,325 ммоль, 56% выход). 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,21 (s, 1H), 7,55 (s, 1H), 7,00 (s, 1H), 4,43 (d, J=8,98 Hz, 1H), 4,15-4,31 (m, 4H), 3,79-3,88 (m, 1H), 3,47 (t, J=6,05 Hz, 2H), 3,23 (s, 3H), 2,27-2,38 (m, 1H), 2,12-2,25 (m, 1H), 1,99 (quin, J=6,15 Hz, 2H), 1,50-1,60 (m, 1H), 1,35-1,45 (m, 1H), 1,24 (t, J=7,22 Hz, 3H), 1,11 (s, 3H), 0,39 (s, 3H). LCMS(ES+)(m/z): 461,3 (M+1).
[00768] Стадия 8: 2-Хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота (рацемат цис)
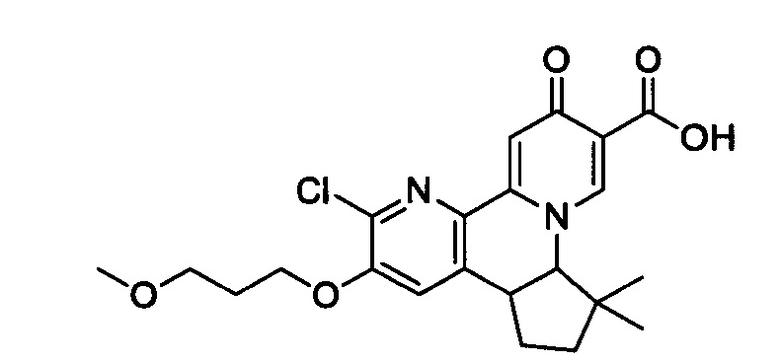
[00769] Раствор моногидрата гидроксида лития (113 мг, 2,70 ммоль) в воде (2 мл) добавляли к раствору этил-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[1]пиридо[1,2-h][1,7]нафтиридин-10-карбоксилата (рацемат цис) (150 мг, 0,270 ммоль) в метаноле (3 мл) и указанную смесь нагревали при 65°С в течение 1 часа. Указанную смесь оставляли охлаждаться, разбавляли водой, закисляли 1М HCl и экстрагировали 3 раза 2-метилтетрагидрофураном. Объединенные органические фазы промывали солевым раствором и концентрировали. Полученный осадок очищали с помощью хроматографии на диоксиде кремния элюцией градиентом от 0% до 10% метанол в дихлорметане. Фракции концентрировали и получали 2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[1]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловую кислоту (рацемат цис) (95 мг, 0,219 ммоль, 81% выход) в виде белого твердого вещества. 1Н ЯМР (400 MHz, DMSO-d6) δ ppm 8,62 (s, 1H), 7,63 (s, 1H), 7,43 (s, 1H), 4,72 (d, J=9,37 Hz, 1H), 4,21-4,39 (m, 2H), 3,89-3,99 (m, 1H), 3,51 (t, J=6,05 Hz, 2H), 3,26 (s, 3H), 2,33-2,44 (m, 1H), 2,19-2,31 (m, 1H), 1,96-2,08 (m, 2Н), 1,55-1,66 (m, 1Н), 1,40-1,51 (m, 1Н), 1,15 (s, 3Н), 0,40 (s, 3Н). LCMS(ES+)(m/z): 433,3 (M+1).
[00770] Дополнительные общие протоколы синтеза для получения соединений, приведенных в настоящем описании, приведены ниже на Схеме 15.
[00771] Схема 15-Соединения типа Соединений, у которых R10 выбран из Таблицы 2)

Биологические Примеры
[00772] Пример 35-Обработка соединениями первичных гепатоцитов человека, инфицированных ВГВ
[00773] Ингибиторы ВГВ-Ag
[00774] Виалы с криосохраненными первичными гепатоцитами человека помещали в водяную баню температуры 37°С до тех пор, пока они не оттаивали. Указанные объединяли, аккуратно ресуспендировали в среде для дифференциации (среда Вильямса, содержащая добавку для дифференциации GlutaMax-1™ и пенициллин/стрептомицин) и число клеток подсчитывали с использованием гемацитометра. Указанные клетки осаждали с помощью центрифугирования при 1000 g в течение 10 минут и ресуспендировали до плотности 5,5×105 клеток/мл в среде для дифференциации. 100 мкл суспензии клеток помещали в каждую лунку 96-луночного планшета, покрытого коллагеном. Указанные планшеты инкубировали при 37°С и 5% СО2 в течение 2 суток перед инфицированием.
[00775] Исходные растворы с ВГВ получали с помощью ультрафильтрации среды от культуры клеток HepG2,2,15. Для получения рабочего исходного раствора с множественностью инфицирования (MOI), равной 100, исходные растворы ВГВ добавляли к среде для дифференцирования, содержащей 4% полиэтиленгликоля, до достижения концентрации ДНК ВГВ 5,5×107 копий/мл. Указанную среду клеток перемещали с 100 мкл рабочего исходного раствора вируса в колонки 1-11 и со средой для дифференцировки-в колонку 12. Указанные планшеты инкубировали при 37°С и 5% СО2 в течение приблизительно 24 часов.
[00776] Соединения ресуспендировали в DMSO и серийно разбавляли в 3 раза в DMSO для получения серии разведений из 10 точек при 200х конечных желаемых концентрациях. Колонки 11 и 12 содержали DMSO. С использованием a Biomek FX в 96-луночные планшеты с U-образным дном помещали 2,5 мкл каждого разведения соединения в 3-х повторах. Указанные планшеты с соединениями герметично закрывали и хранили при -20°С. После нагревания до комнатной температуры указанные планшеты с соединениями разбавляли 200-кратной средой для исследования (среда для дифференцировки плюс 1 мм АВТ). Среду в клеточных планшетах замещали 150 мкл разбавленных растворов соединений. Набольшая конечная концентрация соединения составляла 20 мкМ. Указанные планшеты инкубировали при 37°С и 5% СО2. Указанную обработку соединениями повторяли на 4-е и 9-е сутки после первоначальной обработки. Снятие показаний производили методом ELISA с использованием HBsAg и HBeAg на 9-е и 14-е сутки.
[00777] На 9-е сутки после первоначальной обработки указанную среду переносили из каждой лунки планшета в планшет с U-образным дном и хранили при -80°С. На 14-е сутки после первоначальной обработки планшеты с клетками один раз промывали PBS и хранили при -80°С.
[00778] ELISA с использованием HBs Ag
[00779] Замороженные планшеты, содержащие собранные среды, оставляли нагреваться до комнатной температуры в боксе микробиологической безопасности в течение приблизительно 30 мин. Набор ELISA с HBsAg использовали в соответствии с рекомендациями производителя. Вкратце, планшеты ELISA и растворы оставляли нагреваться до комнатной температуры в течение приблизительно 1 часа и указанные планшеты промывали один раз 300 мкл 1х буфера для промывки. 100 мкл 1х раствора конъюгированного фермента, 120 мкл PBS, содержащего 10% FBS, и 30 мкл полученной среды помещали в каждую лунку. Планшеты для исследования герметично закрывали и инкубировали при 37°С в течение приблизительно 2 часов. Указанные планшеты 4 раза промывали 195 мл 1х буфера для промывки и тщательно осушали, перевернув на бумажные полотенца. 195 мкл раствора хромаген/субстрат добавляли в каждую лунку и инкубировали при комнатной температуре в течение приблизительно 5 мин. 100 мкл стоп-раствора добавляли в каждую лунку и указанные планшеты считывали на считывателе планшетов Molecular Devices SpectraMax® 384 Plus при 450 нм. Значения IC50 определяли с использованием GraphPad Prism: четырех-параметрическая логистическая кривая с уравнением Y=Bottom+(Top-Bottom)/(1+10∧((LogIC50-X)*HillSlope)).
[00780] ELISA с использованием НВе Ag
[00781] Замороженные планшеты, содержащие собранные среды оставляли нагреваться до комнатной температуры в боксе биологической безопасности в течение приблизительно 30 мин. Набор ELISA с HBeAg использовали в соответствии с рекомендациями производителя. Вкратце, указанные планшеты ELISA и растворы оставляли нагреваться до комнатной температуры в течение приблизительно 1 часа и указанные планшеты промывали один раз 300 мкл 1х буфера для промывки. 80 мкл PBS, содержащего 10% FBS, и 20 мкл собранной среды помещали в каждую лунку. Планшеты для исследования герметично закрывали и инкубировали при 37°С в течение приблизительно 1 ч. Указанные планшеты промывали два раза 300 мл 1х буфера для промывки и тщательно осушали, перевернув на бумажные полотенца. 100 мкл 1х раствора конъюгированного фермента помещали в каждую лунку. Планшеты для исследования герметично закрывали и инкубировали при 37°С в течение по меньшей мере 1 ч. Указанные планшеты промывали 3 раза 300 мл 1х буфера для промывки и тщательно осушали, перевернув на бумажные полотенца. 100 мкл раствора хромаген/субстрат добавляли в каждую лунку и инкубировали при комнатной температуре в течение приблизительно 5 мин. 100 мкл стоп-раствора добавляли в каждую лунку и указанные планшеты считывали на считывателе планшетов Molecular Devices SpectraMax 384 Plus при 450 нм.
[00782] Анализ данных
[00783] Значения IC50 определяли с использованием GraphPad Prism: четырех-параметрическая логистическая кривая с уравнением Y=Bottom+(Тор-Bottom)/(1+10∧((LogIC50-X)*HillSlope)). Значения IC50 по 50% снижению антигенов HBs и НВе для исследованных соединений показаны в Таблице 1 для 9-х и 14-х суток. Как видно из указанных значений IC50, исследованные соединения демонстрировали 50% ингибирование антигенов НВе и HBs при значениях концентраций между менее ~0,22 мкМ и 0,0069 мкМ.
[00784] Указанные варианты осуществления настоящего изобретения, описанные выше, приведены исключительно в иллюстративных целях; множество вариантов и модификаций очевидны специалисту в данной области техники. Такие варианты и модификации как таковые входят в рамки настоящего изобретения, определенные в приложенной формуле изобретения.
[00785] Пример 36. Клетки HepAD38-HBsAg ELISA и исследование цитотоксичности
[00786] Клетки HepAD38 поддерживали в колбах, покрытых коллагеном, в среде для выращивания клеток (DMEM/F12, содержащая 10% фетальной бычьей сыворотки (FBS), GlutaMax-1, пенициллин/стрептомицин, не незаменимые аминокислоты, пируват натрия, 250 мкг/мл генецитин и 1 мкг/мл доксициклин). Растворы соединений получали в DMSO и соединения серийно разбавляли до конечных концентраций 4000, 1000,250, 62,5, 15,6, 3,91, 0,977, 0,244, 0,061, и 0,015 нМ. Затем указанные клетки обрабатывали трипсином и высевали при концентрации 10,000 клеток на лунку. Планшеты инкубировали при 37°С, 5% СО2 в течение 4 суток. Среду замещали новой средой с соединениями для обработки. Затем указанные планшеты инкубировали при 37°С, 5% СО2 в течение 3-х дополнительных суток до достижения полного времени обработки в размере 7 суток. Для оценки антивирусного ответа измеряли уровень HBsAg с использованием набора ELISA с HBsAg (International Immuno-diagnostics) в соответствии с предоставленной инструкцией. Для ELISA использовали 100 мкл образцов клеточной среды. Оптическое поглощение измеряли на считывателе планшетов Spectramax® 384 (Molecular Devices) при 450 нм. Для оценки клеточной цитотоксичности использовали реагент теста на выживаемость клеток CellTiter-Glo® Luminescent (Promega). Люминесценцию измеряли на считывателе Envision Multilabel Reader (Perkin Elmer). Полученные данные анализировал и в сравнении с контролем DMSO.
[00787] % ингибирования = (1-(неизвестное/наибольшее значение контроля))*100
[00788] Значения среднего % ингибирования по данным двух повторов исследования на планшетах использовали для построения графика с использованием GraphPad Prism для определения одного значения IC: четырехпараметрическая логистическая кривая с уравнением Y=Bottom+(Top-Bottom)/(1+10∧((LogIC50-X)*HillSlope))
[00789] pIC50=log(-IC50 в M)
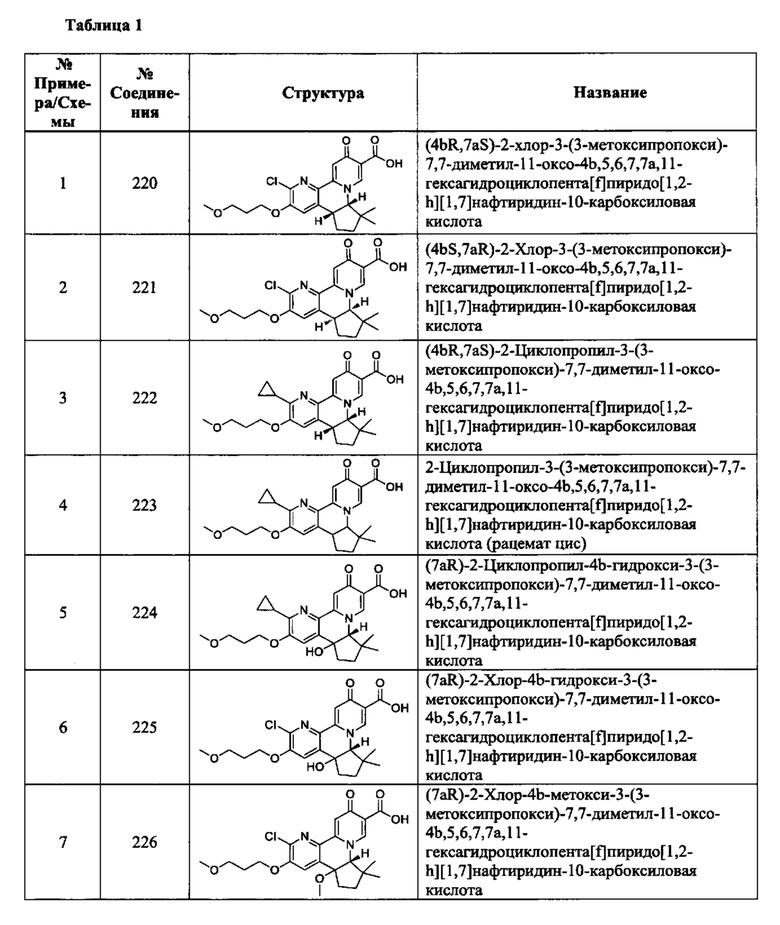
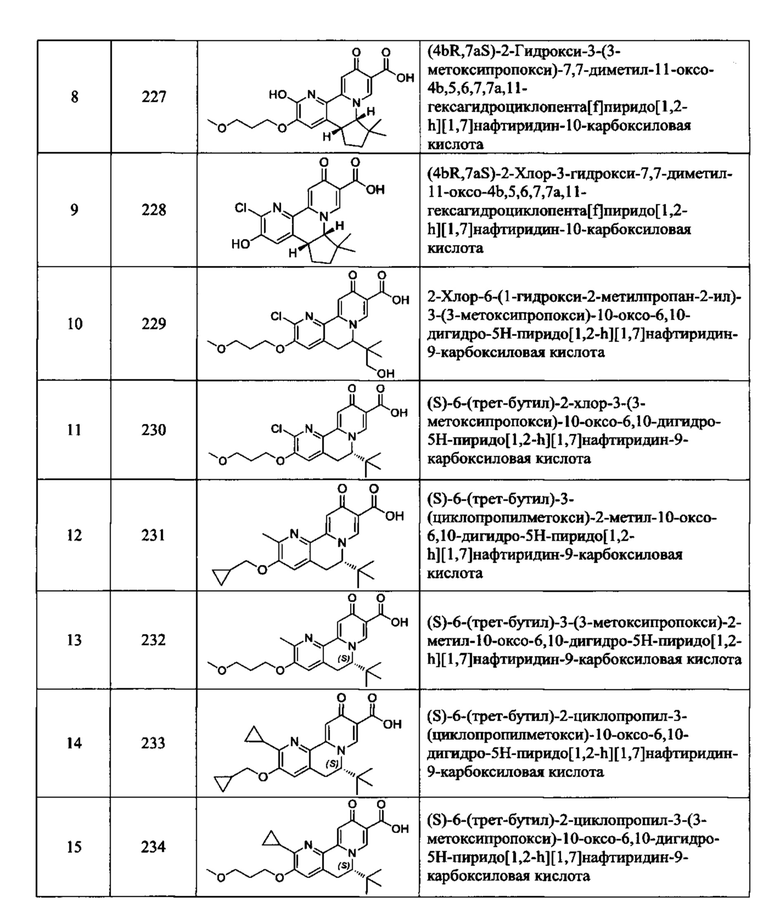
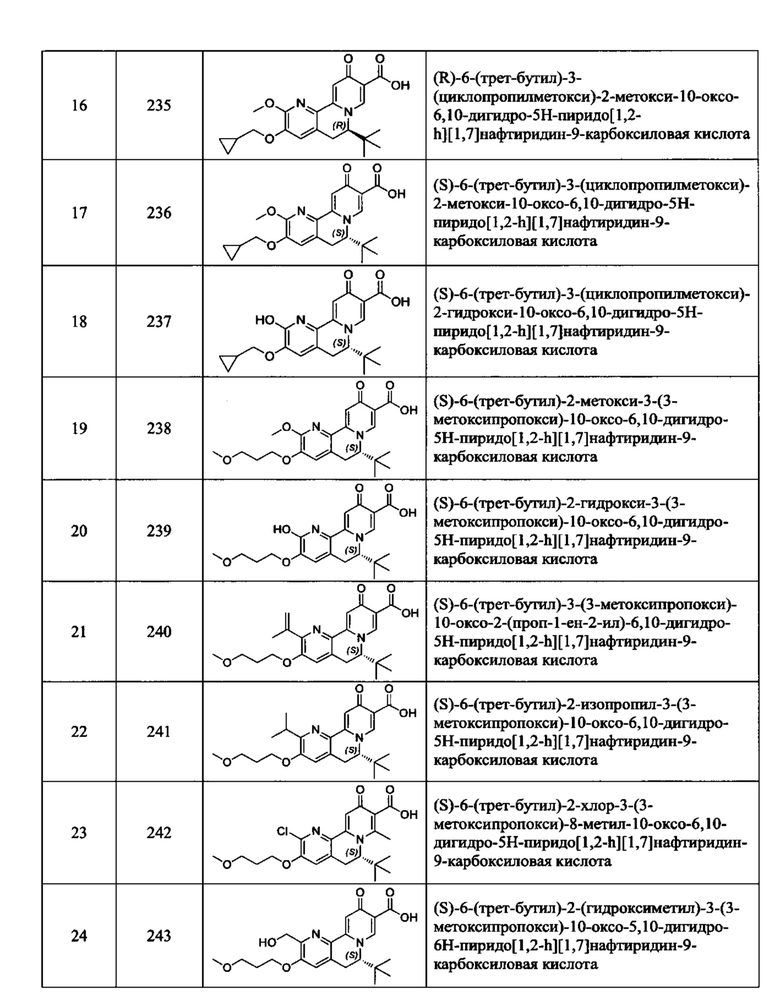
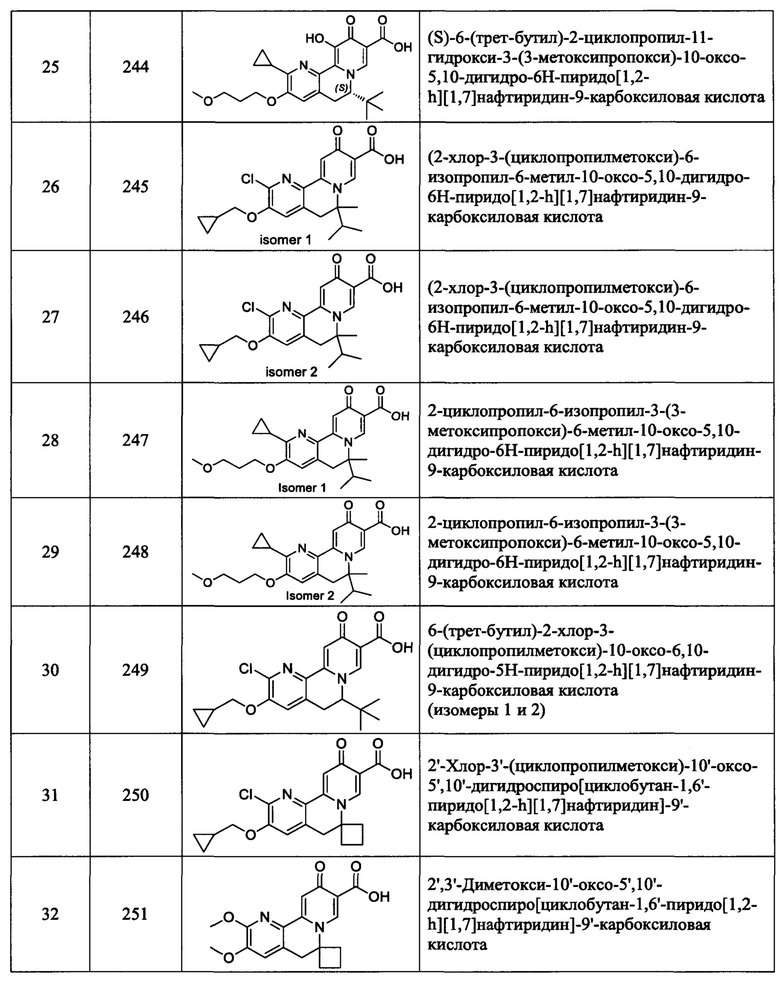
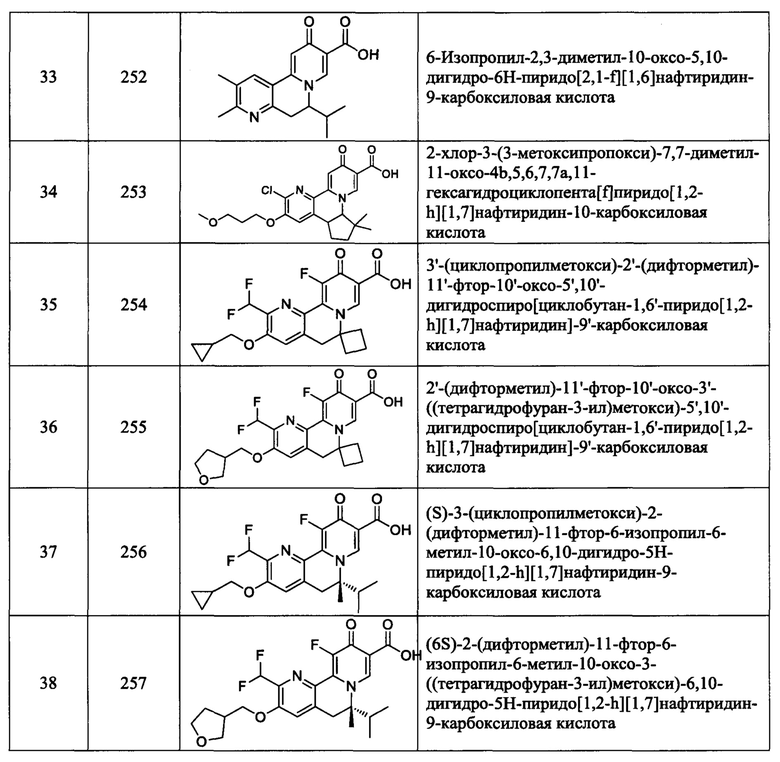
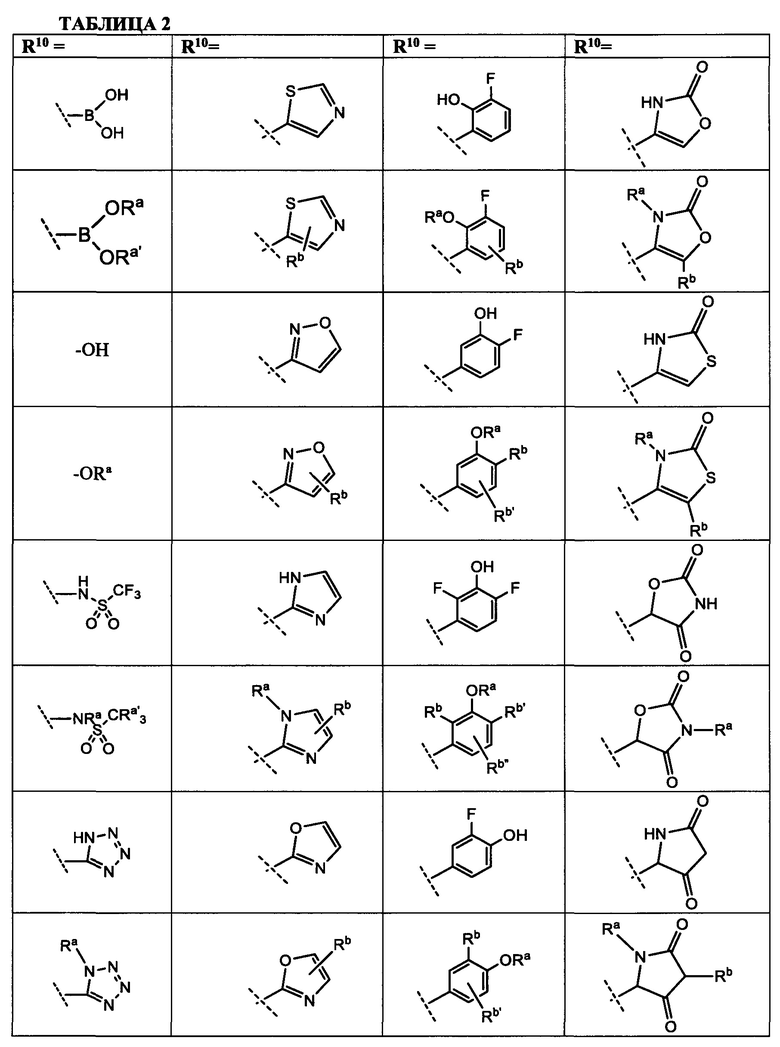
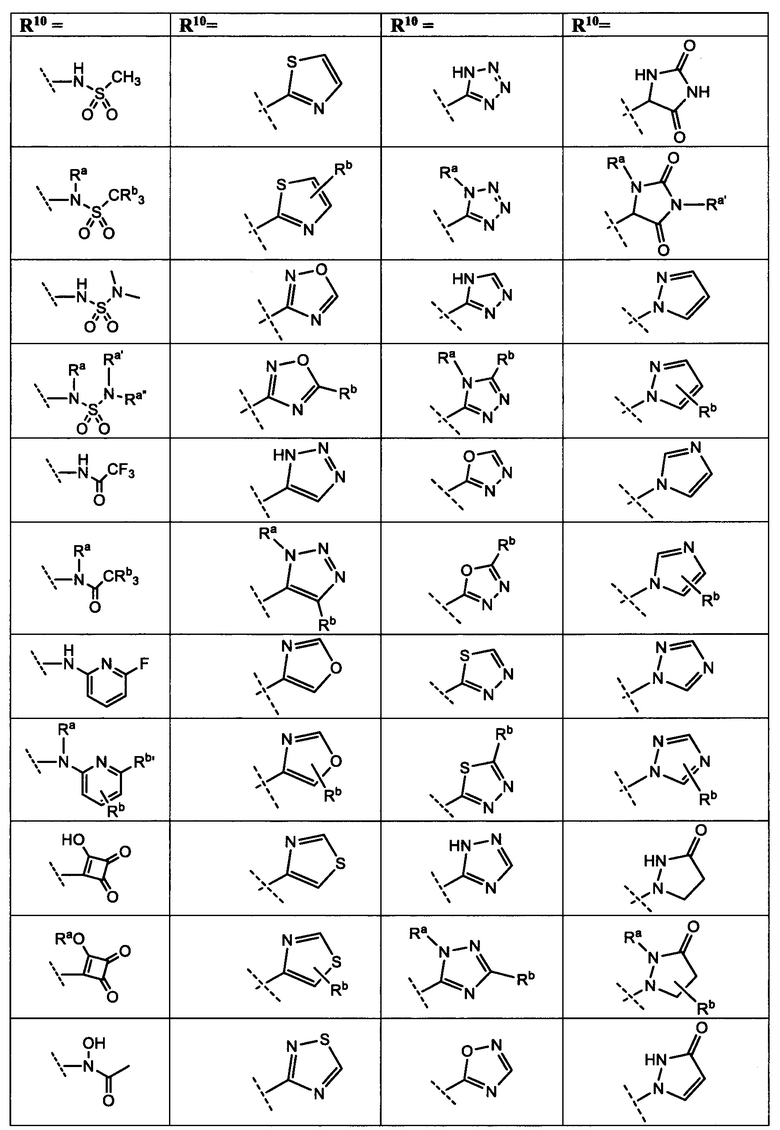
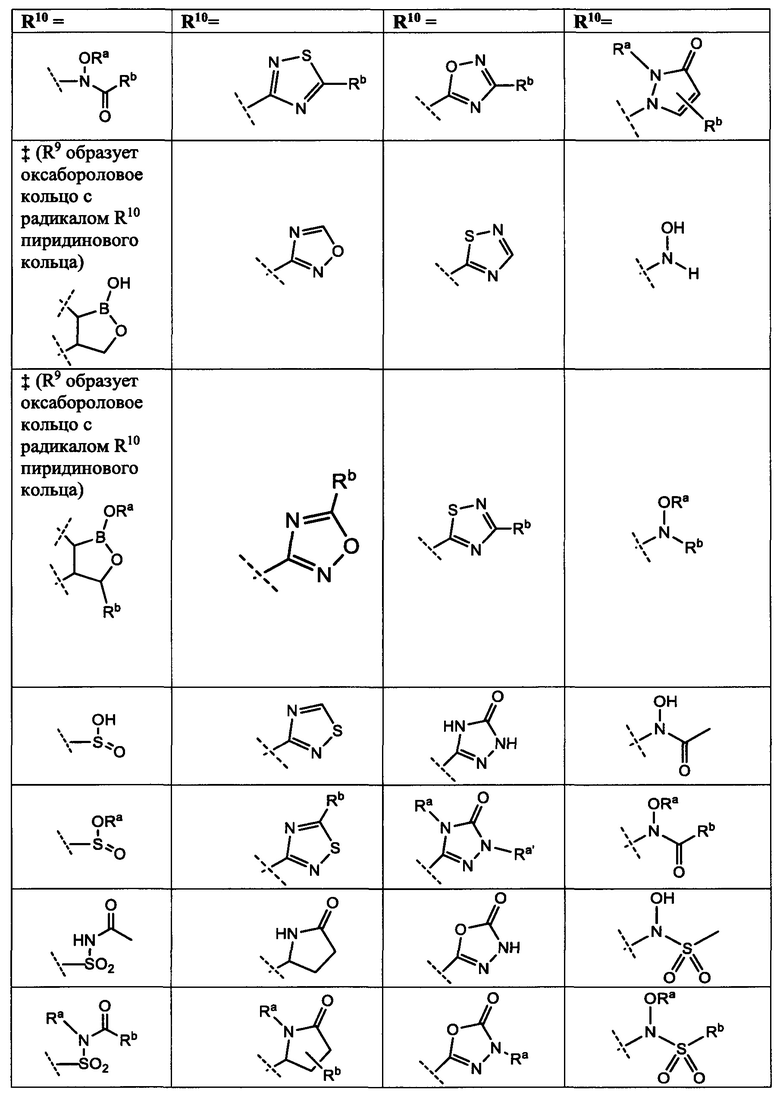
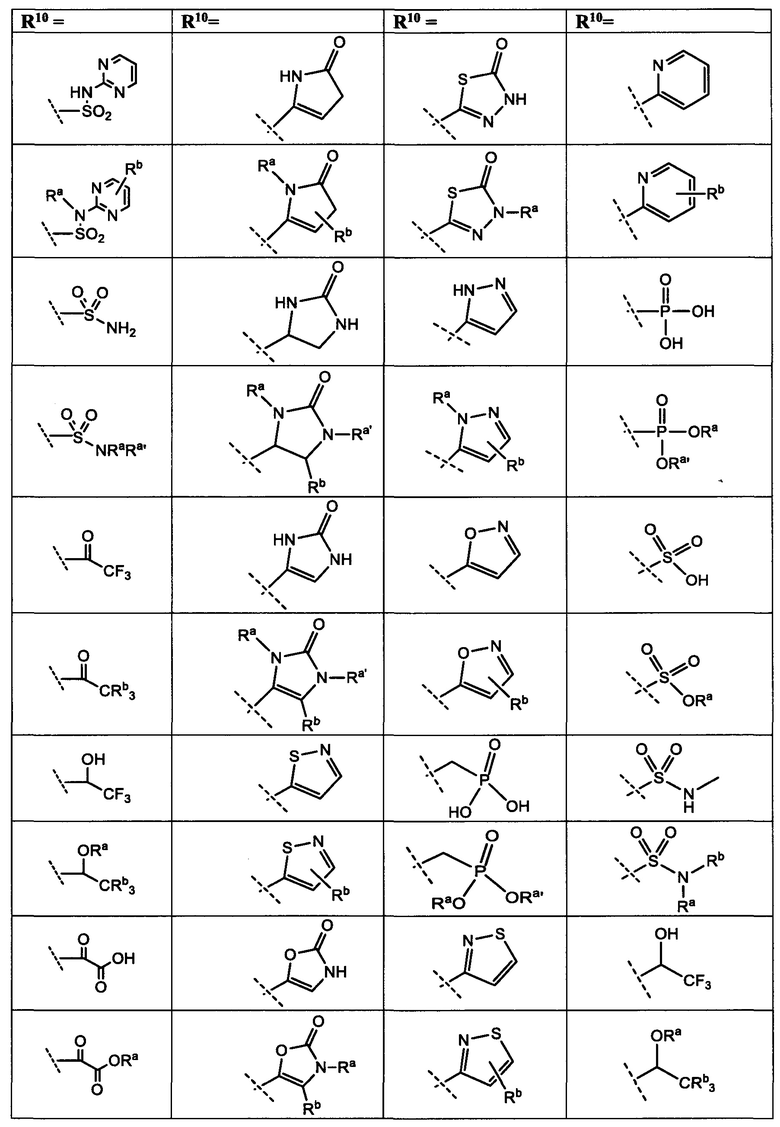
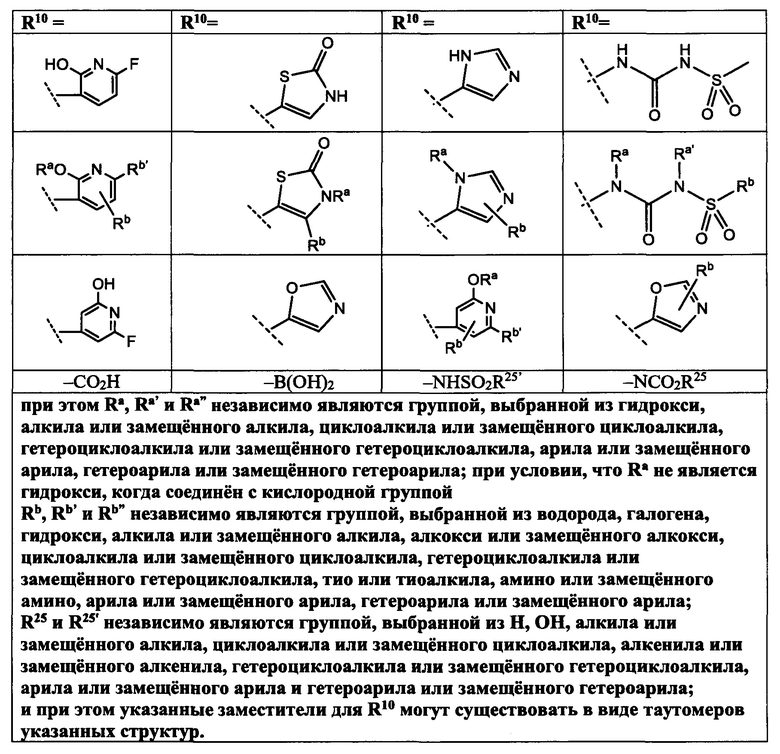
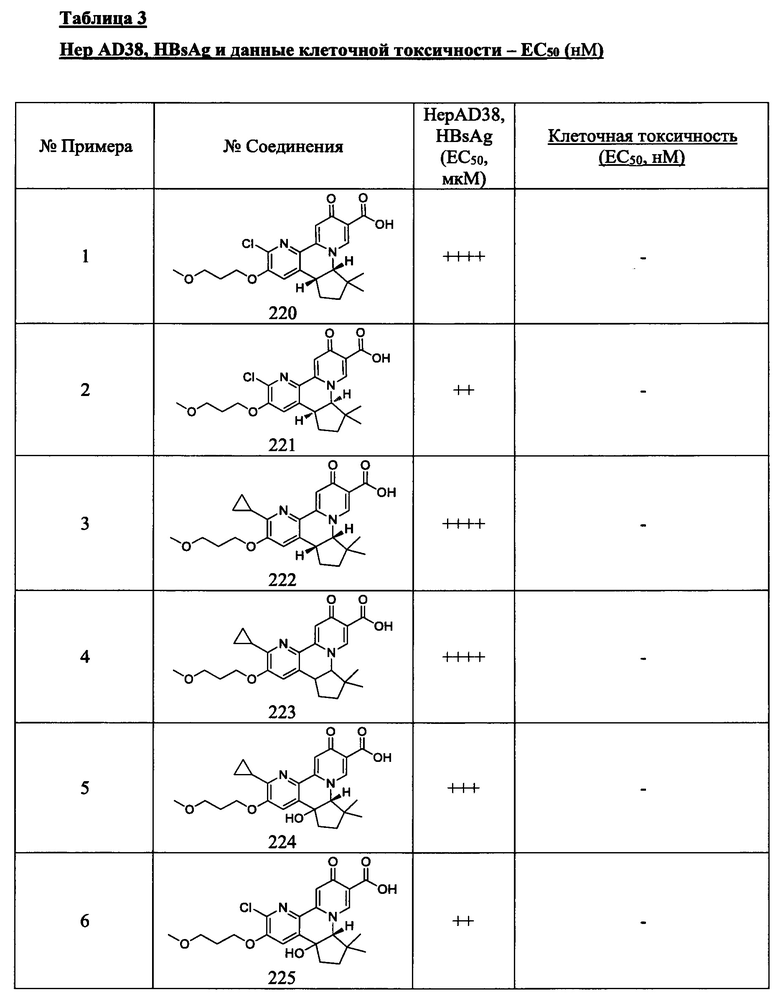
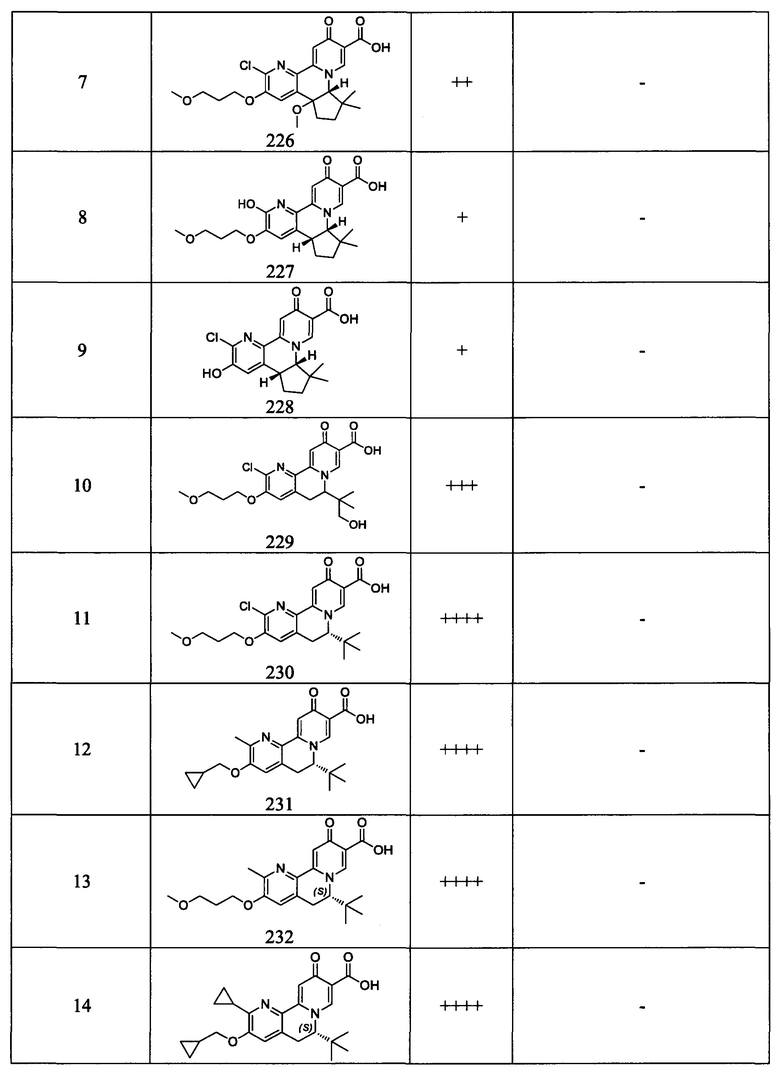
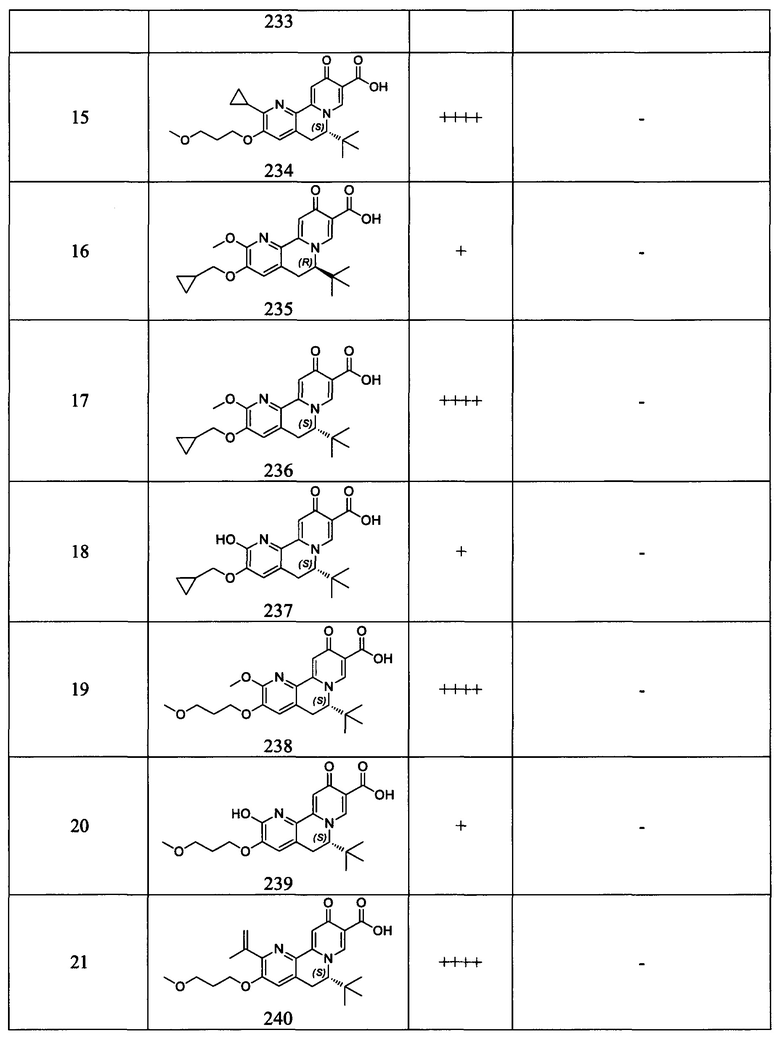
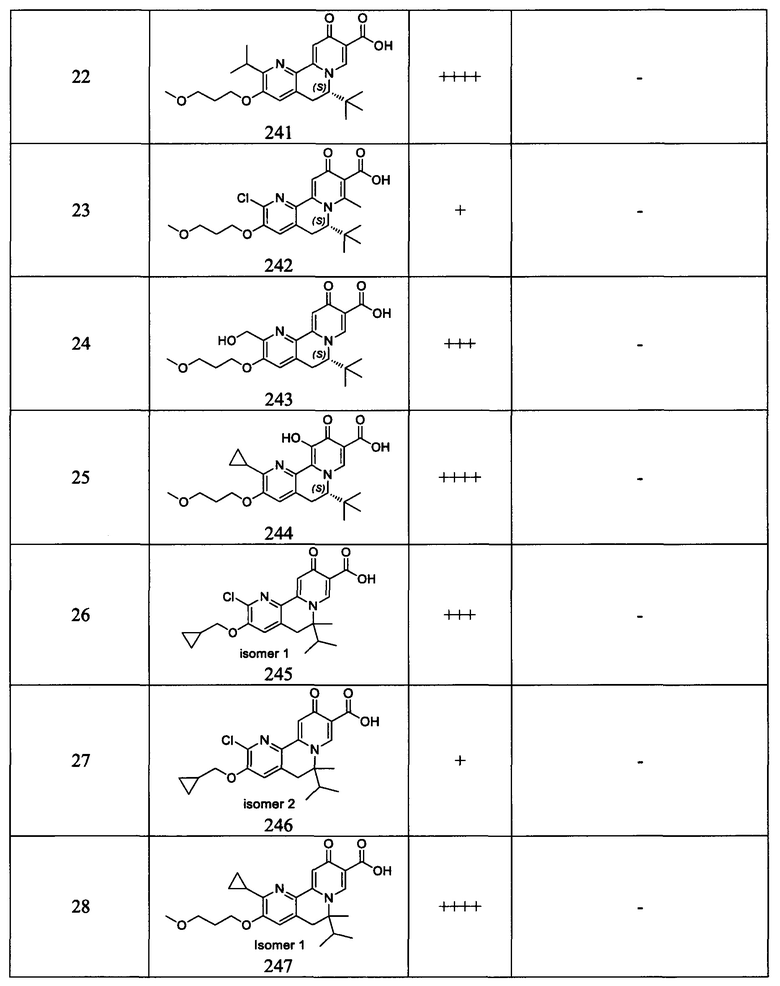
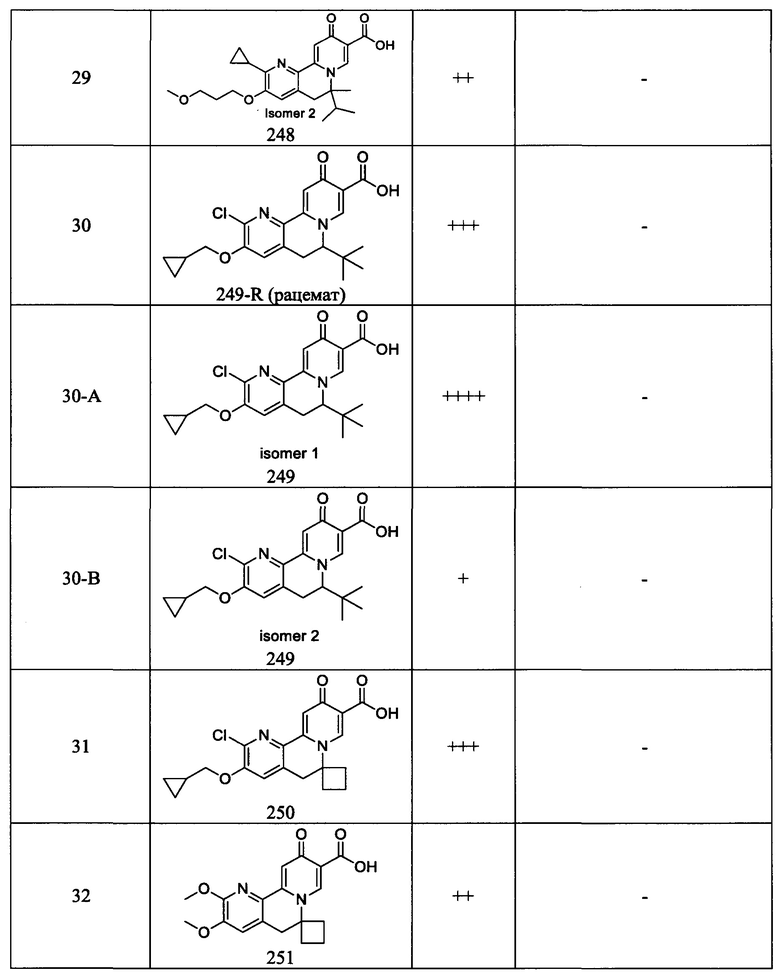
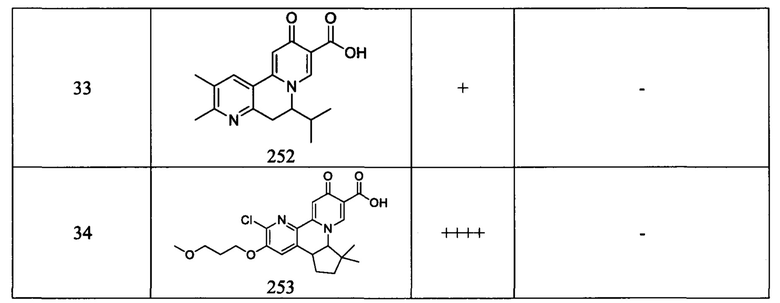
ппи этом:

| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ НА ОСНОВЕ ДИГИДРОНАФТИРИДИНОНА, И СПОСОБ ЕГО ПОЛУЧЕНИЯ, И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2021 |
|
RU2809869C1 |
| Спироконденсированные пирролидиновые производные в качестве ингибиторов деубиквитилирующих ферментов (DUB) | 2017 |
|
RU2730552C2 |
| БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ | 2019 |
|
RU2794894C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ | 2020 |
|
RU2830113C2 |
| БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ | 2019 |
|
RU2794895C2 |
| ПРОИЗВОДНОЕ НИТРОИМИДАЗОЛА ПРОТИВ ТУБЕРКУЛЕЗА ЛЕГКИХ | 2016 |
|
RU2675622C1 |
| ИНГИБИТОР PDE9 И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2793732C2 |
| СПОСОБ ЛЕЧЕНИЯ | 2012 |
|
RU2621148C2 |
| ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ | 2015 |
|
RU2702732C1 |
| ЗАМЕЩЕННЫЕ 1,2-ДИГИДРО[2,7]-НАФТИРИДИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2003 |
|
RU2243218C1 |
Изобретение относится к соединению Формулы I или к его фармацевтически приемлемой соли, в котором W представляет собой N; Y представляет собой С; R1 отсутствует; R2 представляет собой галоген, гидрокси или циклоалкил; R3 представляет собой -OR12; R4 представляет собой Н; R5 представляет собой Н; R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо, необязательно замещенное R15, R15', R16 и/или R16'; R8 представляет собой Н; R9 представляет собой Н; R10 представляет собой -СООН; R11 представляет собой Н; R12 представляет собой C1-6 алкил, замещенный метокси или циклопропилом; и R15, R15, R16 и/или R16' независимо являются C1-6 алкилом. Изобретение также относится к фармацевтической композиции, содержащей терапевтически эффективное количество соединения Формулы I. Технический результат – получены новые соединения и фармацевтическая композиция на их основе, которые могут найти применение в медицине в качестве эффективных средств для лечения гепатита В. 2 н. и 6 з.п. ф-лы, 3 табл., 36 пр.
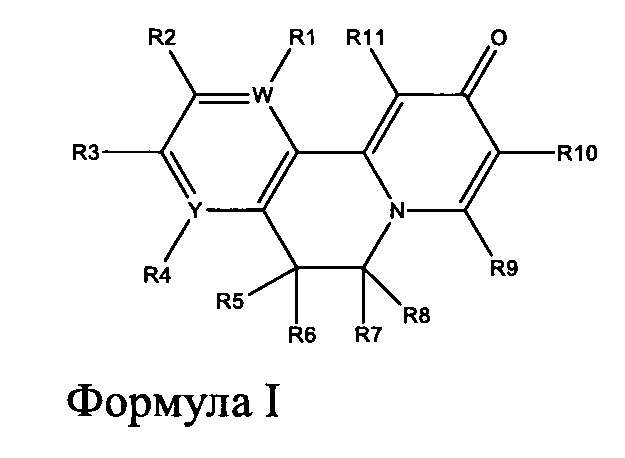
1. Соединение Формулы I или его фармацевтически приемлемая соль 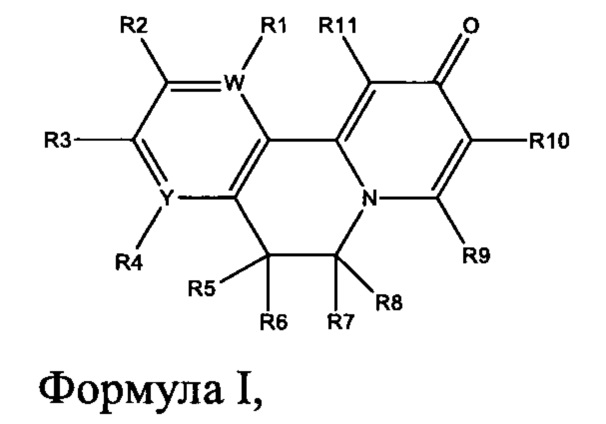
в котором
W представляет собой N;
Y представляет собой С;
R1 отсутствует;
R2 представляет собой галоген, гидрокси или циклоалкил;
R3 представляет собой -OR12;
R4 представляет собой Н;
R5 представляет собой Н;
R6 и R7 вместе образуют от 3- до 8-членное циклоалкильное кольцо, необязательно замещенное R15, R15', R16 и/или R16';
R8 представляет собой Н;
R9 представляет собой Н;
R10 представляет собой -СООН;
R11 представляет собой Н;
R12 представляет собой C1-6 алкил, замещенный метокси или циклопропилом; и
R15, R15, R16 и/или R16' независимо являются C1-6 алкилом.
2. Соединение по п. 1 или его фармацевтически приемлемая соль, отличающееся тем, что
R2 представляет собой галоген;
R8 представляет собой водород; и
R12 представляет собой C1-6 алкил, замещенный метокси или циклопропилом.
3. Соединение по п. 1, выбранное из указанной группы:
(4bR,7aS)-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7a,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
(4bS,7aR)-2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
(4bR,7aS)-2-циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
2-циклопропил-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
(4bR,7aS)-2-гидрокси-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
2-хлор-3-(3-метоксипропокси)-7,7-диметил-11-оксо-4b,5,6,7,7а,11-гексагидроциклопента[f]пиридо[1,2-h][1,7]нафтиридин-10-карбоксиловая кислота;
или его фармацевтически приемлемая соль.
4. Соединение по п. 1, выбранное из группы:
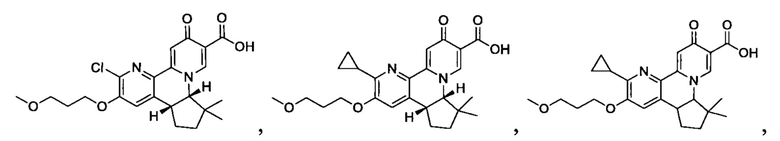
или его фармацевтически приемлемая соль.
5. Соединение по п. 1, имеющее структуру
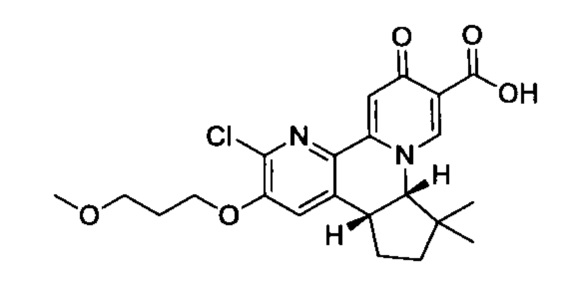
или его фармацевтически приемлемая соль.
6. Соединение по п. 1, имеющее структуру
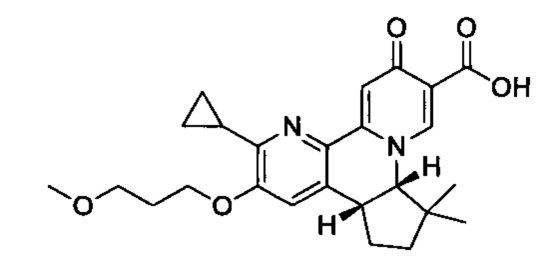
или его фармацевтически приемлемая соль.
7. Соединение по п. 1, имеющее структуру
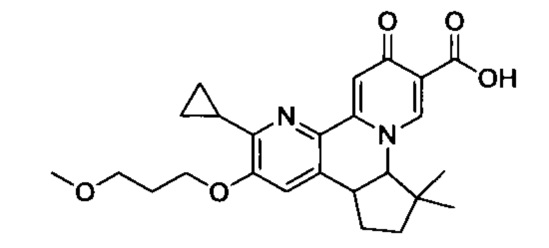
или его фармацевтически приемлемая соль
8. Фармацевтическая композиция для лечения гепатита В, содержащая фармацевтически приемлемый разбавитель и терапевтически эффективное количество соединения по любому из пп. 1-7 или его фармацевтически приемлемой соли.
| WO 2016071215 A1, 12.05.2016 | |||
| WO 2015173164 A1, 19.11.2015 | |||
| ДИАФРАГМЕННЫЙ НАСОС | 1926 |
|
SU5011A1 |
| ЗАМЕЩЕННЫЕ 1,2-ДИГИДРО[2,7]-НАФТИРИДИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2003 |
|
RU2243218C1 |
Авторы
Даты
2023-07-19—Публикация
2018-10-05—Подача