Изобретение относится к медицине, а именно к кардиологии и медицинской генетике, и может быть использовано для прогнозирования риска развития у пациента инфаркта миокарда (ИМ) с подъемом сегмента ST (HMпST).
Сердечно-сосудистые заболевания (ССЗ) стабильно занимают лидирующие позиции в структуре причин инвалидизации и смертности населения во всем мире. Главная роль в группе заболеваний сердечнососудистой системы отводится ишемической болезни сердца (ИБС), которая является причиной смерти более половины умерших от болезней системы кровообращения.
Согласно современной классификации ВОЗ ишемическая болезнь сердца включает следующие восемь видов ишемии (https://serdce.biz/zabolevaniya/ibs/klassifikatsiya-ibs-po-voz.html;
https://serdce5.ru/zabolevaniya/ishemiya/klassifikatsiya-ibs-po-voz-pos1ednyaya.html):
1 - стенокардия (обычно появляется при сильных нагрузках, после приема большого количества пищи, вследствие стресса и т.д.);
2 - внезапная коронарная смерть. Причиной является резкое нарушение электрической активности сердца;
3 - безболевая ишемия. Недостаточное кровоснабжение миокарда вызывает кратковременное изменение уровня метаболизма и электрической активности в сердце, однако не сопровождается грудной болью. Основные причины возникновения - физические нагрузки, курение, стресс и т.д.;
4 - постинфарктный кардиосклероз. Сердечные волокна миокарда замещаются соединительной тканью, что приводит к различным нарушениям;
5 - кардиомиопатия - болезнь миокарда, при которой происходит увеличение сердечной полости. Наиболее частая причина - атеросклероз коронарных артерий;
6 - сердечная недостаточность - синдром, при котором нарушение работы сердца приводит к недостаточному кровоснабжению органов и тканей. При острой сердечной недостаточности нарушается сократительная функция сердечной мышцы, что вызывает как легкие, так и тяжелые нарушения (сердечная астма, отек легких, кардиогенный шок, остановка сердца и т.д.);
7 - аритмические нарушения. Из-за сужения коронарной артерии нарушается приток крови к сердцу, однако это приводит лишь к нарушению ритма;
8 - инфаркт миокарда (ИМ) - необратимое повреждение миокарда, которое чаще всего наступает при сужении артерии на 70 и более процентов площади ее сечения, что приводит к частичному некрозу его тканей.
В настоящее время ИМ рассматривается в соответствии с рекомендациями «Четвертого универсального определения инфаркта миокарда (2018)» (chetvertoe-universalnoe-opredelenie-infarkta-miokarda-2018.pdf).
ИМ можно классифицировать на основании морфологических, клинических, прогностических критериев, а также в зависимости от терапевтических стратегий.
С точки зрения быстрого определения стратегии лечения выделяют ИМ с подъемом (с элевацией) сегмента ST (ИМпST) и ИМ без элевации сегмента ST (ИМбпST). ИМпST, ИМбпST и нестабильную стенокардию объединяют в понятие «острый коронарный синдром» (ОКС).
ИМпST определяют при наличии подъема сегмента ST в двух последовательных отведениях, пороговый уровень ≥1 мм для всех отведений, кроме отведений V2-V3, для которых пороговое значение составляет ≥2 мм для мужчин в возрасте 40 лет и более, ≥2,5 мм для мужчин моложе 40 лет или ≥1,5 мм для женщин независимо от возраста (https://scardio.ru/content/Guidelines/05_rkj_ 18_recomendation.pdf).
ИМ занимает одну из ведущих позиций среди ИБС. Несмотря на активное развитие рентген-эндоваскулярной хирургии, смертность от ИМ остается высокой. К тому же ИМ приводит к осложнениям, как в ближайшем, так и отдаленном периоде, в том числе к развитию повторных сосудистых катастроф, которые в последующем становятся причиной смерти пациентов.
Известно много способов прогнозирования в отношении ИМ, например, способов, защищенных патентами РФ №№2436501, 2682488, 2611891, 2485884, 2565103, 2373542, 2649517 и т.д. Эти способы относятся к прогнозированию неблагоприятного исхода ИМ, развития осложнений, развития повторного ИМ, внезапной смерти больного и т.д., но не к прогнозированию риска развития ИМ.
Известен «Способ прогнозирования острого инфаркта миокарда» по патенту РФ №2105981, но он также относится к прогнозированию течения острого ИМ.
Известен способ прогнозирования инфаркта миокарда по патенту РФ №2168937, но он относится к прогнозированию развития ИМ у больных гипертонической болезнью.
Известен способ генетической диагностики неблагоприятных исходов (нефатальный ИМ и смерть) у больных в течение одного года после ОКС с подъемом сегмента ST (ОКСпST) (патент РФ 2502474).
В данной работе исследовались следующие полиморфизмы, которые генотипировали у больных ОКСпST: rs4291 и rs4343 гена АСЕ; rs1801252 гена ADRB1; rs1042713 и rs1042714 гена ADRB2; rs699 гена AGT; rs5186 гена AGTR1; rs1800775 и rs5882 гена СЕТР; rs1799963 гена F2; rs6027, rs6025 и rs 1800595 гена F5; rs5918 гена ITGB3; rs 1800588 гена LIPC; rs328 гена LPL; rs 1801131 и rs 1l801133 гена MTHFR; rs 2069542 гена MYH7; rs 2070744 и rs 1799983 гена NOS3; rs662 и rs854560 гена PON1; rs 1801282 гена PPARG; rs7903146 гена TCF7L2; rs5370 гена EDN1; rs5443 гена GNB3; rs1052373 гена MYBPC3; rs28357372 гена MTND2; rs1800629 гена TNF; rs10811661 гена CDKN2A/B.
Из представленного набора полиморфизмов генов-кандидатов были выделены варианты, при носительстве которых можно с высокой точностью прогнозировать развитие неблагоприятного исхода OKCnST (смерти или нефатального инфаркта миокарда) в течение 12 месяцев - полиморфизм rs4291 гена АСЕ, rs6025 гена F5, rs5918 гена IGTB3.
В данной работе не был исследован ген LMOD1, кодирующий актин-связывающий протеин леймодин 1, который играет важную роль в сокращении гладкомышечных волокон и проведении импульса по проводящей системе сердца.
В работе «Генетические предикторы развития острого коронарного синдрома» авторов Ложкиной Н.Г., Козик В.А., Найдены Е.А., Хасановой М.Х, Стафеевой Е.А., Толмачевой А.А., Барбарич В.Б., Куимова А.Д., Максимова В.Н., Воеводы М.И. (Современные проблемы науки и образования. - 2018. - №5) содержится следующая информация:
 низкая экспрессия гена CPNE3 служит потенциальным независимым фактором риска ОИМ;
низкая экспрессия гена CPNE3 служит потенциальным независимым фактором риска ОИМ;
 марокканские ученые в своем исследовании доказали, что I/D полиморфизм гена АСЕ (ангиотензинпревращающего фермента, локализуется на хромосоме 17q23.3) может быть связан с возникновением инфаркта миокарда среди пациентов младше 45 лет;
марокканские ученые в своем исследовании доказали, что I/D полиморфизм гена АСЕ (ангиотензинпревращающего фермента, локализуется на хромосоме 17q23.3) может быть связан с возникновением инфаркта миокарда среди пациентов младше 45 лет;
 новосибирские ученые рассмотрели связь семи однонуклеотидных полиморфизмов (rs17465637, rs4804611, rs2549513, rs499818, rs619203, rs1333049, rs1376251) с ОКС и ИМ, в частности, в группах пациентов до 55 лет и старше. В исследование были включены 160 пациентов с ИМ (113 мужчин и 47 женщин). Была доказана связь однонуклеотидного полиморфизма (ОНП, SNP) rs 1333049 с развитием ИМ независимо от пола и возраста;
новосибирские ученые рассмотрели связь семи однонуклеотидных полиморфизмов (rs17465637, rs4804611, rs2549513, rs499818, rs619203, rs1333049, rs1376251) с ОКС и ИМ, в частности, в группах пациентов до 55 лет и старше. В исследование были включены 160 пациентов с ИМ (113 мужчин и 47 женщин). Была доказана связь однонуклеотидного полиморфизма (ОНП, SNP) rs 1333049 с развитием ИМ независимо от пола и возраста;
 изучалась связь генотипа СТ полиморфизма rs2820315 гена LMOD1 с риском возникновения повторного ОКС, но на данный момент его связь с неблагоприятным прогнозом ИМ не доказана.
изучалась связь генотипа СТ полиморфизма rs2820315 гена LMOD1 с риском возникновения повторного ОКС, но на данный момент его связь с неблагоприятным прогнозом ИМ не доказана.
В статье «Проверка взаимосвязи между девятью однонуклеотидными полиморфизмами и инфарктом миокарда на сибирской популяции» авторов В.Н. Максимова, И.В. Куликова, П.С. Орлова, В.В. Гафарова, С.К. Малютиной, А.Г. Ромащенко, М.И. Воеводы (Вестник РАМН, 2012, №5) описано исследование, в которое были включены жители Новосибирска: 200 больных ИМ (129 мужчин, 71 женщина) и контрольная группа - лица без ИМ (420 человек), сопоставимые по полу и возрасту. Изучали следующие ОНП: rs28711149, rs499818, rs619203, rs10757278 и rs1333049 (хр. 9), rs1376251, rs2549513, rs4804611, rs17465637.
Для 4 из 9 исследованных ОНП была подтверждена их ассоциация с ИМ: rs1333049 (хр. 9), rs10757278 (хр. 9), rs499818 (хр. 6), rs619203 гена ROS1.
Известны следующие работы в отношении гена LMOD1 и ССЗ.
«Fifteen new risk loci for coronary artery disease highlight arterial-wall-specific mechanisms» / Joanna M M Howson, Wei Zhao, Daniel R Barnes, Weang-Kee Ho, Robin Young, Dirk S Paul and others (Nature Genetics, 2017, http://dx.doi.org/10.1038/ng.3874).
В исследование были включены пациенты европейской, азиатской, африканской популяций. В работе упоминается полиморфизм rs2820315 гена LMOD1, но речь идет о сборной группе больных ИБС. Пациенты с ИМ не были выделены и не были проанализированы. В качестве аллеля риска ИБС в данной статье указан аллель Т (т.е генотипы ТТ и СТ) rs2820315 гена LMOD1. Он связан с повышенной экспрессией LMOD1 в сальниковой и подкожной жировой ткани (MuTHER, β=0,11, Р=1,43×10-11).
В статье «Functional regulatory mechanism of smooth muscle cell-restricted LMOD1 coronary artery disease (CAD) locus / Nanda V, Wang T, Pjanic M, Liu B, Nguyen T, Matic LP, Hedin U, Koplev S and others (PLoS Genet. 2018 Nov 16; 14(11):e1007755. doi: 10.1371/journal.pgen.1007755. eCollection 2018 Nov.) речь также идет об ИБС без конкретизации вида ишемии. В статье не упоминается ИМ (т.е. больных с ИМ отдельно не исследовали). В качестве аллеля риска ИБС также указан аллель Т (т.е. генотипы ТТ и СТ) rs2820315 гена LMOD1. Кроме rs2820315 исследовали полиморфизм rs34091558 гена LMOD1 в этой же когорте пациентов (с ИБС). Как предрасполагающий к ИБС указан генотип ТТ данного полиморфизма.
Раскрытие изобретения
Сущность заявляемого способа определения (прогнозирования) риска развития инфаркта миокарда с подъемом сегмента ST (ИМпST) у пациентов - жителей г. Новосибирска характеризуется тем, что у пациента определяют генотип по полиморфизму rs2820315 гена LMOD1. При этом наличие генотипа СС свидетельствует о повышенном риске развития ИМпST у пациента, наличие генотипа СТ по данному ОНП свидетельствует о пониженном риске развития ИМпST у пациента, т.е. о протективной роли данного генотипа в отношении ИМпST.
Техническими результатами предлагаемого способа являются следующие:
1) заявляемый способ позволяет определить риск развития наиболее тяжелой формы ИБС - ИМпST (если не считать внезапную сердечную смерть);
2) способ позволяет определить как повышенный, так и пониженный риск развития ИМпST у пациента;
3) способ разработан на сибирской популяции, конкретно, в результате обследования пациентов г. Новосибирска;
4) предлагаемый способ достаточно осуществить один раз в жизни пациента. Он не требует повторения, поскольку генетический набор пациента не меняется в течение жизни;
5) предлагаемый способ позволяет выявить повышенный или пониженный риск развития ИМпST у пациента в результате исследования только одного полиморфизма одного гена.
Обоснование способа
С целью выявления генетических предикторов, определяющих риск развития ИМпST у пациента - жителя г. Новосибирска, были изучены 4 ОНП: rs9349379 гена PHACTR1, rs2820315 гена LMOD1, rs1799883 гена FABP2, rs867186 гена PROCR. В таблице 1 представлен перечень 12 генотипов исследованных полиморфизмов.

Ген PHACTR1 картирован на хромосоме 6р24.1, является ответственным за синтез регулятора актина 1 и фосфатазы. Данный регулятор играет важную роль в развитии сосудистой стенки и в гемостазе. Наиболее изучаемым ОНП гена PHACTR1 является rs9349379. Китайские ученые подтвердили ассоциацию генотипа GG полиморфизма rs9349379 гена PHACTR1 с риском развития ИБС среди женщин. При этом генотип AG исследуемого полиморфизма показал протективные свойства в отношении риска развития ССЗ среди мужчин, проживающих в Китае [PHACTR1 regulates oxidative stress and inflammation to coronary artery endothelial cells via interaction with NF-κB/p65. Zhang Z, Jiang F, Zeng L, Wang X, Tu S. Atherosclerosis. 2018 Nov; 278:180-189. doi: 10.1016/j.atherosclerosis. 2018.08.041; PHACTR1 gene polymorphism with the risk of coronary artery disease in Chinese Han population. Chen L, Qian H, Luo Z. Postgrad Med J. 2019 Feb 18. pii: postgradmedj-2018-136298. doi: 10.1136/postgradmedj -2018-136298].
Ассоциация полиморфизма rs9349379 гена PHACTR1 с риском развития ИМ, ИБС и с повышенным риском кальцификации коронарных артерий, что тесно связано патогенезом атеросклероза, была подтверждена в ряде других зарубежных исследований, проводимых в Европе и Соединенных Штатах Америки [PHACTR1 Functional Clues Linking a Genome-Wide Association Study Locus to Coronary Artery Disease. Adam W. Turner, Ruth McPherson. Arterioscler Thromb Vase Biol. 2015;35:1293-1295. DOI: 10.1161/ATVBAHA.l 15.305680; Myocardial Infarction-Associated SNP at 6p24 Interferes With MEF2 Binding and Associates With PHACTR1 Expression Levels in Human Coronary Arteries. Melissa Beaudoin, Rajat M. Gupta, Hong-Hee Won. Arterioscler Thromb Vase Biol is available at http://atvb.ahajournals.org. DOI: 10.1161/ATVBAHA.l 15.305534].
В публикациях, указанных в предыдущем абзаце, авторы проанализировали связь между ИМ (без выделения ИМпST и ИМбпST) и 45 ОНП в популяции французских канадцев (отбирались образцы анализов пациентов из биобанка Монреальского института сердца (МHI)). Группу пациентов, перенесших ИМ, составили 1176 человек. Самая сильная связь с ИМ была у ОНП rs9349379 (G-аллель, OR=1,37, Р=8,4×10-6). Поскольку ОНП PHACTR1 не связаны с традиционными факторами риска для ИМ, такими как липидный профиль пациента, артериальное давление или сахарный диабет, авторы предполагают, что PHACTR1 может влиять на риск развития ИМ через неизвестные пока механизмы, связанные с эндотелием сосудов.
Ген FABP2 (Fatty acid-binding protein 2) находится в хромосоме 4q26, кодирует белок, связывающий жирные кислоты в кишечнике. Данный белок принимает участие во внутриклеточном транспорте и метаболизме жирных кислот. Во многих странах мира проведены исследования, целью которых было выявление ассоциации гена FABP2 с развитием ССЗ. В одном из таких проектов ученые подтвердили взаимосвязь генотипа GT rs1799883 гена FABP2 с риском развития ССЗ путем влияния на липидный профиль пациентов. Авторы проанализировали данные 523 пациентов-мексиканцев и доказали ассоциацию генотипа GT rs 1799883 гена FABP2 с повышенным уровнем общего холестерина (ОХ), холестерина липопротеинов низкой плотности (ЛПНП) и распространенностью гиперхолестеринемии, что играет важную роль в патогенезе ССЗ [Associations of the lipid genetic variants Thr54 (FABP2) and -493T (MTTP) with total cholesterol and low-density lipoprotein cholesterol levels in Mexican subjects. Gonzalez-Becerra K, Ramos-Lopez O, Garcia-Cazarin ML, Barron-Cabrera E, Panduro A, Martinez-Lopez E.J Int Med Res. 2018 Apr;46(4):1467-1476. doi: 10.1177/0300060517748518].
Ген PROCR (protein С receptor) картирован на хромосоме 20q11.22, кодирует рецептор протеина С.Активированный протеин С, взаимодействующий через соответствующий рецептор, синтез которого кодируется геном PROCR, выполняет антикоагуляционную функцию за счет инактивации коагуляционных факторов гемостаза - V и VIII. Кроме этого активированный протеин С стимулирует фибринолиз. Соответственно, при патологии, связанной с взаимодействием протеина С с одноименным рецептором, повышается риск тромбообразования и развития сосудистых катастроф. Это объясняет повышенный интерес исследователей к изучению гена PROCR в отношении риска развития ССЗ и ИМ. Так, например, авторы крупного мета-анализа (см. ниже) провели оценку данных 64374 пациентов с ИБС и 130681 пациентов без ИБС.Пациенты принадлежали к европейско-азиатской популяции. Исследователи пришли к выводу, что полиморфизм rs867186 гена PROCR ассоциирован с риском развития ИБС. Отдельно группу пациентов с ИМ авторы не анализировали [Plasma levels of the anti-coagulation protein С and the risk of ischaemic heart disease. A Mendelian randomisation study. Schooling CM, Zhong Y. Thromb Haemost. 2017 Jan 26; 117(2):262-268. doi: 10.1160/TH16-07-0518. Epub 2016 Nov 24].
Ген LMOD1 (Leiomodin 1) находится в хромосоме 1. Он кодирует актин-связывающий протеин леймодин 1, который играет важную роль в сокращении гладкомышечных волокон и проведении импульса по проводящей системе сердца.
В Регионарном сосудистом центре №1 г. Новосибирска было проведено генотипирование двух групп пациентов. В основную группу вошли 210 пациентов с ИМпST (119 мужчин и 91 женщин в возрасте 18-75 лет), в контрольную - 246 пациентов без ИМпST (141 мужчин, 105 женщин 18-75 лет). Группы были сопоставимы по полу и возрасту.
Все обследованные пациенты были жителями города Новосибирска.
Критерии включения пациентов в основную группу были следующими: мужчины и женщины, перенесшие ИМпST, подтвержденный типичной клиникой, ЭКГ, реакцией кардиоспецефических ферментов (КК, МВКК, тропонин I), ЭХОКГ. Диагноз ИМпST устанавливался по совокупности критериев, разработанных Европейским обществом кардиологов, Американской коллегией кардиологов и Российским кардиологическим обществом (2015, 2017 г.г).
Критерии включения в контрольную группу: мужчины и женщины без перенесенного ИМпST на момент исследования и в анамнезе.
Критерии исключения, общие для основной и контрольной группы пациентов, были следующими: обструктивная, дилатационная и рестриктивная кардиомиопатия; злокачественные новообразования; острые воспалительные процессы печени, почек, эндокринных желез и других органов и систем и хронические заболевания в фазе обострения и неполной ремиссии; сахарный диабет 1 и 2 типа с инсулиновой недостаточностью; тяжелая печеночная и почечная недостаточность; хронический алкоголизм и психические расстройства.
У всех обследованных пациентов были проведены следующие виды обследований:
- общеклиническое обследование с оценкой жалоб и клинического статуса;
- лабораторное обследование с проведением общего и биохимического анализа крови, общего анализа мочи;
- инструментальные обследования: электрокардиография (ЭКГ), R-графия органов грудной клетки, эхокардиография (Эхо-КГ), селективная коронарография (КАГ), холтеровское (суточное) мониторирование ЭКГ (ХМ ЭКГ) при наличии специальных показаний - нарушения ритма или проводимости;
- определение толерантности к физической нагрузке (оценивали по тесту 6-минутной ходьбы);
- оценка риска неблагоприятных госпитальных исходов по шкалам TIMI и GRACE;
- генетическое обследование пациентов, которое включало 3 этапа:
1) забор 10 мл венозной крови пациента в пробирки с этилендиаминтетрауксусной кислотой (ЭДТА);
2) выделение геномной ДНК из 10 мл венозной крови методом фенол-хлороформной экстракции;
3) генотипирование методом ПЦР в режиме реального времени (Realtime PCR) на приборе ABI 7900НТ в соответствии с протоколом фирмы-производителя (зонды TaqMan, AppliedBiosystems, USA). Исследовали четыре ОНП: rs1799883 гена FABP2, rs867186 гена PROCR, rs9349379 гена PHACTR1, rs2820315 гена LMOD1.
В таблице 2 показано распределение генотипов изучавшихся полиморфизмов в группе больных ИМпST и в контрольной группе.
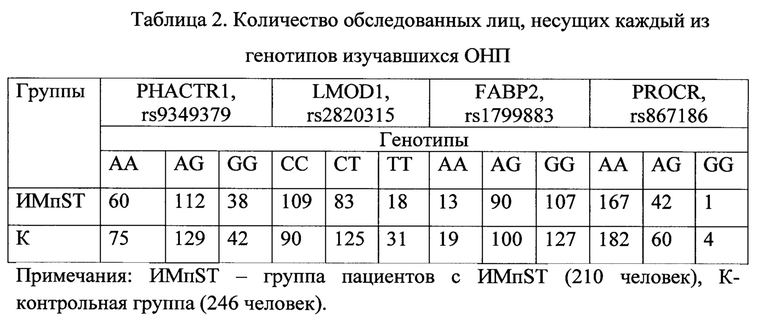
Для оценки статистической значимости влияния конкретного генотипа каждого ОНП на риск развития у пациента ИМпST использовали показатель отношение шансов (ОШ) - показатель, который позволяет описать в численном выражении, насколько наличие или отсутствие конкретного генотипа каждого ОНП связано с присутствием или отсутствием ИМпST в конкретной статистической группе.
ОШ определяли по формуле: ОШ=ШИМпST/Шк, где
ШИМпST - шанс наличия конкретного исследуемого генотипа ОНП в группе пациентов с ИМпST;
Шк - шанс наличия того же генотипа в контрольной группе пациентов.
ШИМпST и Шк определяли по формулам:
ШИМпST=pИМпST/(1-pИМпST), где pИМпST - вероятность наличия данного генотипа в группе пациентов с ИМпST;
Шк=рк/(1-рк), где рк - вероятность наличия данного генотипа в контрольной группе пациентов.
В таблице 3 приведены полученные значения ОШ, верхних и нижних границ доверительных интервалов (ДИ) и p-значений (р-значения - вероятность ошибки первого рода при отклонении нулевой гипотезы. Принятие нулевой гипотезы говорит об отсутствии значимого отличия между вероятностями pИМпST и рк, т.е. исследуемый генотип не ассоциирован с риском развития ИМпST. Принятие альтернативной гипотезы говорит о достоверной значимости отличия в вероятностях pИМпST и pк т.е. об ассоциации исследуемого генотипа с риском развития ИМпST). 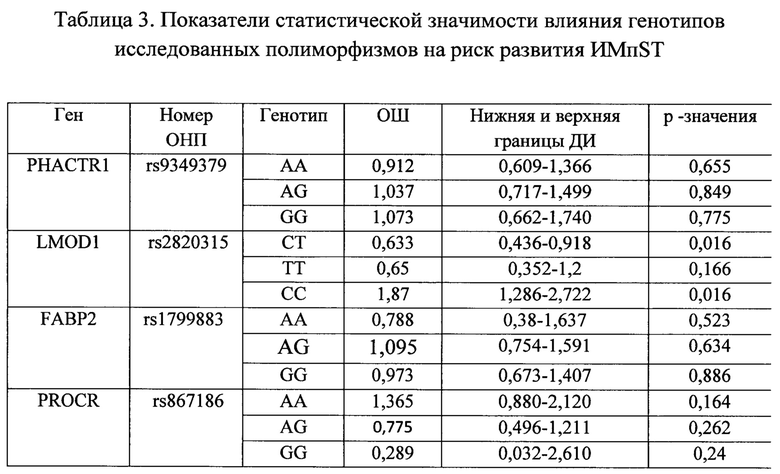
Примечания: ОШ - отношение шансов, номер ОНП - номер ОНП в международной классификации.
Как показывают приведенные выше данные, статистически значимой является связь между генотипом СС полиморфизма rs2820315 гена LMOD1 и развитием ИМпST (ОШ 1,87; 95% ДИ 1,286-2,722).
Генотип СТ полиморфизма rs2820315 гена LMOD1 играет протективную роль в отношении ИМпST (ОШ 0,633; 95% ДИ 0,436-0,918).
При анализе генотипов полиморфизма rs2820315 гена LMOD1 в контрольной и основной группах, разделенных по полу, были выявлены статистические значимые различия.
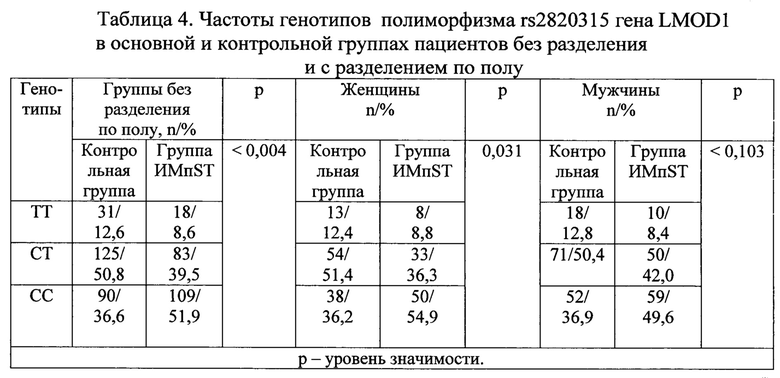
Как без разделения, так и при тендерном делении основной (ИМпST) и контрольной групп, частота генотипа СС в основной группе была достоверно выше, чем в контрольной (54,9% против 36,2% у женщин; 49,6% против 36,9% у мужчин).
Анализ генов PHACTR1, FABP2 и PROCR не выявил достоверных различий в основной и контрольной группе.
Заявляемый способ позволяет выделить приоритетную группу пациентов для проведения персонализированной первичной (отказ от вредных привычек, правильное питание, динамические физические нагрузки) и вторичной профилактики риска развития ИМ (правильная схема и длительность медикаментозной терапии, длительное диспансерное наблюдение).
Способ подтверждается следующими клиническими примерами.
Пример №1. Больной А., 58 лет, мужчина, работающий, поступил в приемное отделение с диагнозом ИМпST. Время от начала болевого синдрома до поступления в стационар составило 1 час 30 мин. Рост пациента -176 см, вес - 82 кг. Частота пульса при поступлении - 100 уд/мин, артериальное давление - 150/90 мм рт.ст. Жалобы при поступлении: жгучая боль за грудиной в течение 1 часа 30 минут без эффекта от нитроглицерина, купированная наркотическими анальгетиками на этапе скорой помощи.
В анамнезе: артериальная гипертензия в течение 10 лет, курение 20 лет (индекс пачка/лет равен 10), установлена гиперхолестеринемия. Наследственность отягощена по материнской линии (артериальная гипертензия). Инсульт, сахарный диабет отрицает.
На ЭКГ у пациента: синусовый ритм с ЧСС 80 уд/мин., элевация сегмента ST по задней стенке левого желудочка, нарушений проводимости нет. Тяжесть сердечной недостаточности расценена как Killip I (аускультативно хрипы в легких не обнаруживаются; рентгенологически отсутствуют признаки гипертензии малого круга кровообращения). По данным ЭхоКГ, выполненной на 7-е сутки от поступления в стационар, фракция выброса левого желудочка составляет 44%. Концентрация креатинина в сыворотке крови при поступлении - 84 мкмоль/л, при выписке - 82 мкмоль/л, концентрация общей креатинкиназы - 428 Е/л, изоформы MB креатинкиназы - 62 Е/л. Результаты коронароангиографии были следующими: окклюзия правой коронарной артерии в проксимальном сегменте; стеноз передней нисходящей артерии в проксимальном отделе более 50%.
Проведена ангиопластика со стентированием правой коронарной артерии.
Проведено генотипирование по четырем молекулярно-генетическим маркерам: rs9349379 гена PHACTR1, rs2820315 гена LMOD1, rs1799883 гена FABP2, rs867186 гена PROCR.
У пациента выявлен генотип СС по полиморфизму rs2820315 гена LMOD1.
В течение госпитального периода рецидивов ангинозных болей не было, толерантность к физическим нагрузкам - средняя. Пациент выписан со стандартной двойной антитромбоцитарной терапией в сочетании с бета-блокаторами, ингибиторами ангиотензинпревращающего фермента (иАПФ) и статинами.
Пример №2. Пациент Д., 49 лет, мужчина, работающий. На момент осмотра жалоб на ангинозные боли не предъявляет, обратился с целью ежегодного планового обследования и коррекции гипотензивной терапии в связи с повышением артериального давления выше 140/90 мм. рт.ст.1-2 раза в месяц.
В анамнезе: артериальная гипертензия в течение 5 лет, максимальное АД 165/90 мм.рт.ст., адаптирован к 120-130/80-90 мм.рт.ст., гипотензивную терапию принимает регулярно (лозартан 50 мг 1/д), курит 20 лет (индекс пачка лет равен 15), дислипидемия была диагностирована 1 год назад, гиполипидемическую терапию не принимает. Наследственность по ССЗ не отягощена. Инсульт, ИМ, сахарный диабет ранее не диагностировались. Операций, травм не было.
Объективный осмотр: состояние удовлетворительное. Рост - 178 см, вес - 86 кг. Индекс массы тела равен 27,1 кг/м2. Кожные покровы и видимые слизистые обычной окраски и влажности. Грудная клетка правильной формы, перкуторно выявляется легочный звук. Дыхание везикулярное, хрипов нет. ЧДД 16 в минуту. Тоны сердца ясные, ритмичные, шумов нет. ЧСС 68 уд/мин. Пульс удовлетворительного наполнения, ритмичный, 68 уд/мин. АД 130/80 мм.рт.ст. Живот обычной формы, участвует в акте дыхания, безболезненный при пальпации во всех отделах. Печень пальпируется по краю реберной дуги. Периферических отеков нет.Физиологические отправления в норме.
На ЭКГ у пациента: синусовый ритм с ЧСС 68 уд/мин., признаков гипертрофии миокарда левого желудочка нет. По данным ЭхоКГ: акинезии и гипокинезии стенок левого желудочка (ЛЖ) нет, фракция выброса ЛЖ составляет 58%. В биохимическом анализе крови: ОХ - 5,9 ммоль/л, ЛГЛНП 3,1 ммоль/л, ЛПВП - 1,4 ммоль/л, TP- 1,4 ммоль/л.
Пациенту проведено генотипирование по следующим ОНП: rs9349379 гена PHACTR1, rs2820315 гена LMOD1, rs1799883 гена FABP2, rs867186 гена PROCR. У пациента выявлен генотип СТ по полиморфному варианту rs2820315 гена LMOD1. Даны рекомендации по образу жизни, рациону питания, отказу от вредных привычек, проведена коррекция гипотензивной терапии согласно клиническим рекомендациям и стандартам лечения артериальной гипертензии (иАПФ, антагонисты кальция, статины).
Как видно из примеров, достаточно похожие пациенты изначально имели разную генетическую предрасположенность к развитию ИМпST. Соответственно, при своевременном определении генетического риска, пациентам была бы подобрана правильная персонализированная программа профилактики, направленная на снижение ССР и определена необходимая тактика ведения пациента (частота амбулаторных приемов и участия пациента в школах здоровья, периодичность обследования и т.д.).
Это позволило бы предотвратить или отсрочить время наступления ИМпST у пациента №1.
Изобретение относится к области медицины, в частности к кардиологии и медицинской генетике. Предложен способ определения риска развития инфаркта миокарда с подъемом сегмента ST (ИМпST). У пациента определяют генотип по полиморфизму rs2820315 гена LMOD1. Наличие генотипа СС свидетельствует о повышенном риске развития ИМпST. Наличие генотипа СТ свидетельствует о пониженном риске развития ИМпST. Изобретение позволяет определить риск развития ИМпST посредством выявления полиморфизма rs2820315 гена LMOD1. 4 табл., 2 пр.
Способ определения риска развития инфаркта миокарда с подъемом сегмента ST (ИМпST) у пациентов - жителей г. Новосибирска, характеризующийся тем, что у пациента определяют генотип по полиморфизму rs2820315 гена LMOD1: наличие генотипа СС свидетельствует о повышенном риске развития ИМпST у данного пациента, наличие генотипа СТ свидетельствует о пониженном риске развития ИМпST у данного пациента.
| СПОСОБ ГЕНЕТИЧЕСКОЙ ДИАГНОСТИКИ НЕБЛАГОПРИЯТНЫХ ИСХОДОВ У БОЛЬНЫХ В ТЕЧЕНИЕ ОДНОГО ГОДА ПОСЛЕ ОСТРОГО КОРОНАРНОГО СИНДРОМА С ПОДЪЕМОМ СЕГМЕНТА ST | 2012 |
|
RU2502474C1 |
| KR 20120016897 A, 27.02.2012 | |||
| NANDA V | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| PLoS Genet | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
Авторы
Даты
2020-01-17—Публикация
2019-09-23—Подача