Изобретение относится к медицине, а именно к хирургии и комбустиологии, и может быть использовано для закрытия раневых дефектов кожи и доставки лекарственных веществ в область раневого дефекта кожи.
Из литературы известно покрытие на основе коллаген-хитозанового комплекса для восстановления дефектов кожи в виде губки, геля, коллоидного раствора, пленки [1]. Описано биодеградируемое раневое покрытие и способ получения биодеградируемого раневого покрытия на основе хитозана [2].
Наиболее близким по технической сущности является покрытие для лечения ран на гидрофильной тканевой основе, гидрогелевого слоя, содержащего акриловую кислоту и акриламид, водорастворимого биодеградирующего полимера на основе желатина с поли-N-винилпирролидоном и биологически активными компонентами [3]. Ее недостаток - наличие в составе акриловой кислоты, которую требуется нейтрализовать и акриламида с N,N'-метилен-бис-акриламидом в качестве сшивающего агента, который также требует активирования окислительно-восстановительной системой на основе персульфата аммония и тетраметилэтилендиамина, необходимость контроля реакции полимеризации.
Для получения покрытия в данном изобретении предлагается структурирование и упрочнение покрытия на основе гидрофильного биополимера ПЭГ-1500 и пищевого желатина за счет введения в состав углеродных наноматериалов - нанотрубок и нановолокон. Наноуглеродные материалы играют роль армирующего каркаса, способствующего получению более прочных пленочных покрытий. Использовали одностенные углеродные нанотрубки (с диспергентом поли-N-винилпирролидоном или Na-карбоксиметилцеллюлозой) или углеродные нановолокна [4].
Известно, что углеродные наноматериалы используют для повышения прочности и твердости композитных материалов [5]. Углеродные наноматериалы могут быть использованы для получения бионанопленок, визуализации опухолей, таргетной доставки лекарственных и диагностических веществ [6, 7].
Методика получения. Биополимерные пленки получали растворением желатина и ПЭГ-1500 в пропорции 1:1 по 10 г в 100 мл дистиллированной воды, перемешивали и помещали в термостат (ТС-80, Россия) при температуре 37С на 24 часа. Затем в смесь добавляли по 40 мг (0,04%) одностенных углеродных нанотрубок высокой чистоты Tuball-99™ (группа компаний OCSiAl, Россия) в виде водной дисперсии Tuball Batt H2O, содержавшей 0,4% масс. Tuball и 0,8% масс. поли-N-винилпирролидона (C6H9NO)n молекулярной массой 12600±2700 в качестве дисперсанта (ОУНТ-ПВП) или водной дисперсии Tuball Batt H2O, содержавшей 0,4% масс. Tuball и 0,6% масс.Na-карбоксиметилцеллюлозы в качестве дисперсанта (ОУНТ-СМС) или углеродных нановолокон НП-44, перемешивали до получения однообразной массы. Помещали полученную биомассу в емкости с обеспечением образования равномерного слоя покрытия с высотой 5 мм и формирования пленки путем высушивания биомассы в течение 72 час. в термостате при температуре 37°С.
Микрофотографии образцов после сушки (ув. х10) представлены на Рисунке 1:
Контрольный образец (желатин + полиэтиленгликоль) полупрозрачный сероватого оттенка, в котором прослеживается наличие паутинообразных нитей, которые могут быть следствием неполного гидролизирования волокон коллагена (Рис. 1а).
Образцы, армированные углеродными нанотрубками ОУНТ-СМС (Рис. 1б) и ОУНТ-ПВН (Рис. 1 в) сероватого цвета со сниженной прозрачностью, в которой отчетливо видны участки скопления ОУНТ, но при этом менее заметны остатки волокон коллагена.
Образец, армированный углеродным нановолокном НП-44, черного цвета, в котором отчетливо видны участки скопления ОУНТ, но при этом менее заметны остатки волокон коллагена (Рис. 1 г).
Для оценки способности образцов к удержанию воды, образцы пленок с размерами (1×1 см) взвешивали, помещали в дистиллированную воду на 24 часа при комнатной температуре, далее образцы извлекали, промокали фильтровальной бумагой для удаления излишка влаги и взвешивали. Рассчитывал % удержания воды (набухания) = [(конечная масса-исходная масса)/исходная масса] × 100%. Биодеградацию образцов оценивали в растворе хлорида натрия при 37°С в течение 14 дней.
Токсичность полученных образцов в отношение первичной культуры дермальных фибробластов человека (чДФб) оценивали в МТТ тесте [7]. Для этого, исследуемые образцы размеров 1,5×1,5 см помещели в лунку 6-луночного культурального планшета, на поверхность образца наносили в 200 мкл 1 млн. чДФб в питательной среде (RPMI-1640, 10% эмбриональной телячьей сыворотки, 2 мM L-глутамина, 5 MMHEPPES-буфера, 1% антибиотик/антимикотик), в лунку вносили 1 мл питательной среды, инкубировали в СО2-инкубаторе при 37°С и воздушной смеси 5% CO2/95% атмосферный воздух в течение 72 часов. Жизнеспособность клеток определяли по внутриклеточной активности НАДФ-Н-зависимых оксидоредуктаз, делали микрофотографии. Результаты приведены в примерах. Оценка жизнеспособности первичной культуры фибробластов кожи человека на поверхности образцов представлена на Рисунке 2.
Пример 1. Образец на основе желатина и ПЭГ-1500 (контроль) способен к удержанию влаги (383±29,4%), биодеградация/распад образца в водной фазе начинается на 7 сутки и практически завершается к 14 суткам (происходит расслоение биомассы с формированием комков в водной среде), утрачивается гомогенность биомассы. На поверхности образца чДФб формируют очаги скопления клеток, в которых сохранена активность НАДФ-Н-зависимых оксидоредуктаз, но не формируется монослоя клеток, что указывает на сохранность метаболической активности клеток, т.е. жизнеспособность тестируемых клеток до 95% (Рис. 2а).
Пример 2. Образец на основе желатина, ПЭГ-1500 и ОУНТ-ПВП способен к удержанию влаги на значениях близких к контролю (300±20%), искомый образец сохраняет целостность в течение 7 суток в водной фазе и далее биодеградирует к 14 суткам. На поверхности образца чДФб располагаются отдельными клетками, имеют округлую форму, восстанавливают тетразолевый краситель, что указывает на сохранность метаболической активности клеток, т.е. жизнеспособность тестируемых клеток клеток до 95% (Рис. 26).
Пример 3. Образец на основе желатина, ПЭГ-1500 и ОУНТ-СМС способен к удержанию влаги на значениях ниже контроля (166,67±16,5%), целостность структуры образца сохранна до 7 суток с последующим биодеградированием образца в водной фазе к 14 суткам наблюдения. На поверхности образца чДФб располагаются мелкими скоплениями клеток, имеют округлую форму, что указывает на сохранность метаболической активности клеток, т.е. жизнеспособность тестируемых клеток клеток до 95% (Рис. 2в).
Пример 4. Образец на основе основе желатина, ПЭГ-1500 и НП-44 способен к удержанию влаги на значениях ниже контроля (161,33±9,81%), анализ биодеградации образца во влажной среде выявил ее сохранность до 10 суток с последующим распадом образца по периферии и сохранности в центре к 14 суткам. На поверхности образца чДФб располагаются мелкими скоплениями клеток, имеют округлую форму, восстанавливают тетразолевый краситель, что указывает на сохранность метаболической активности клеток, т.е. жизнеспособность тестируемых клеток клеток до 95% (Рис. 2 г).
Данные приведенные в примерах представлены в таблице.
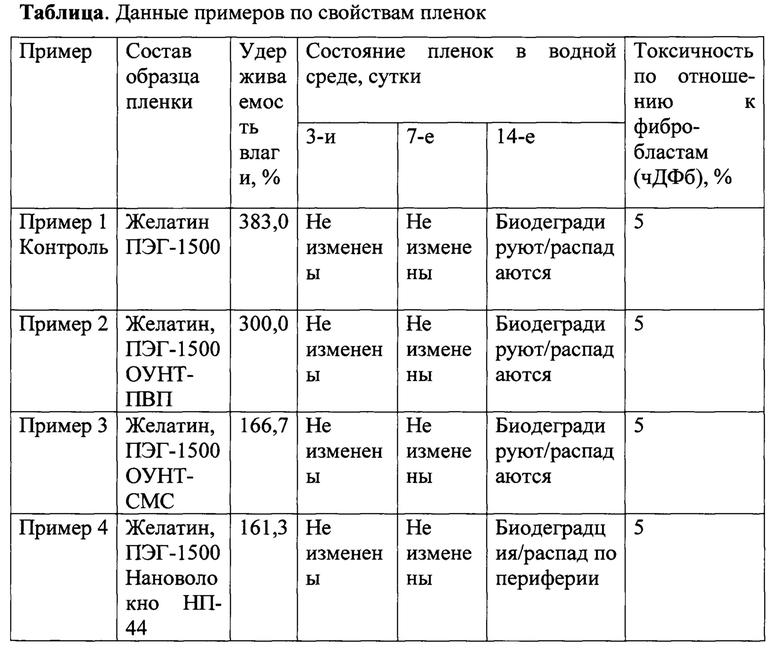
Из приведенных примеров видно, что как желатин-ПЭГ-1500, так и желатин-ПЭГ-углеродные наноматериалы пленки обладают способностью к удержанию влаги, биодеградируют, не подавляют метаболические процессы в клетках и удерживают воду в сравнении с контролем на 50-80%. К достоинтсву пленок из желатина-ПЭГ-углеродных наноматериалов следует отнести их простоту приготовления, возможность наносить композиции на марлевую или иную трикотажную основу, что позволит, при их наложении на раневые дефекты кожи, легко удалять их без трамвирования раны. Кроме этого, в состав пленок можно вводить антибактериальные средства, ионы металлов с антимикробной активностью, вещества способствующие ускорению процесса эпителизации раневых дефектов кожи и другие терапевтические средства.
Цитируемые источники
1. Патент РФ №2254145, 2005.
2. Патент РФ №2519168, 2014
3. Патент РФ №2372944, 2009.
4. Lykov A., Rachkovskaya L., Poveshchenko О., Rachkovsky Е., Surovtseva М., Kim I., Bondarenko N., Volodin A., Bauman Y., Mishakov I, Vedyagin A. Biocompatability of the complex of aluminium oxide and polydimethylsiloxane modified with carbon nanofiber. 2021 IEE Ural-Siberian conference of computation technologies in cognitive science, genomics and biomedicine, CSGB 2021. 2021. P. 180-183.
5. Вигдорович В.И., Цыганкова Л.Е., Шель H.B., Осетров А.Ю., Зверева А.А. Углеродные наноматериалы и композиты на их основе. Вестник ТГУ. 2013. Т. 18. Т. 4. С.1220-1229.
6. Митрофанова И.В., Мильто И.В., Суходоло И.В., Васюков Г.Ю. Возможности биомедицинского применения углеродных нанотрубок. Бюллетень сибирской медицины. 2014. Т. 13. №1. С.145-154.
7. Alexander Lykov, Lubov Rachkovskaya, Olga Poveshchenko, Maria Surovtseva, Irina Kim, Evgenia Yankaite, Edmond Rachkovsky, Alexander Volodin, Vladimir Konenkov. Single wall carbon Nanotubes functionalized with composition of y-aluminum oxide and polydimethylsiloxane properties. 2019 International multi-conference of engineering, computer and information sciences (SIBIRCON). https://doi.org: 10/1109/SIBIRCON48585.2019:0297-03000.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФИЛЬТРУЮЩИЙ ЭЛЕМЕНТ, МЕДИЦИНСКАЯ МАСКА И РЕСПИРАТОР | 2021 |
|
RU2750600C1 |
| Биосовместимая матрица на основе бактериальной целлюлозы и пептидов природного происхождения для активизации репаративных процессов поврежденных тканей | 2023 |
|
RU2824664C1 |
| БИОПОЛИМЕРНОЕ ВОЛОКНО, СОСТАВ ФОРМОВОЧНОГО РАСТВОРА ДЛЯ ЕГО ПОЛУЧЕНИЯ, СПОСОБ ПРИГОТОВЛЕНИЯ ФОРМОВОЧНОГО РАСТВОРА, ПОЛОТНО БИОМЕДИЦИНСКОГО НАЗНАЧЕНИЯ, СПОСОБ ЕГО МОДИФИКАЦИИ, БИОЛОГИЧЕСКАЯ ПОВЯЗКА И СПОСОБ ЛЕЧЕНИЯ РАН | 2010 |
|
RU2468129C2 |
| ПОКРЫТИЕ ДЛЯ ФОТОВОЛЬТАИЧЕСКОЙ ЯЧЕЙКИ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2577174C1 |
| Углеродминеральный пористый сорбент на основе оксида алюминия, полидиметилсилоксана и одностенных углеродных нанотрубок | 2019 |
|
RU2727378C1 |
| МОДИФИЦИРУЮЩАЯ ДОБАВКА В АСФАЛЬТОБЕТОН | 2023 |
|
RU2801276C1 |
| Биологически активный материал для покрытия раневой поверхности | 2022 |
|
RU2804197C1 |
| ПЕРЕВЯЗОЧНОЕ СРЕДСТВО НА БИОПОЛИМЕРНОЙ ОСНОВЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИНФЕКЦИЙ ПРИ ОЖОГАХ, ТРОФИЧЕСКИХ ЯЗВАХ И НЕКРОЗЕ МЯГКИХ ТКАНЕЙ | 2016 |
|
RU2666012C1 |
| МНОГОСЛОЙНЫЙ МАТЕРИАЛ С ХИТОЗАНОВЫМ СЛОЕМ ИЗ НАНО- И УЛЬТРАТОНКИХ ВОЛОКОН | 2013 |
|
RU2522216C1 |
| Наномодификатор строительных материалов | 2016 |
|
RU2637246C1 |


Настоящее изобретение относится к области медицины, а именно к биополимерной пленке для использования в хирургии и комбустиологии, получаемой на основе желатина и гидрофильного биополимера ПЭГ-1500 в пропорции 1:1, структурированной углеродными наноматериалами: ОУНТ-ПВП, или ОУНТ-СМС, или НП-44 в количестве 0,04% масс. Настоящее изобретение обеспечивает углеродные наноматериалы пленки, которые обладают способностью к удержанию влаги, биодеградируют, не подавляют метаболические процессы в клетках и удерживают воду в сравнении с контролем на 50-80%. 4 пр., 1 табл., 2 ил.
Биополимерная пленка для использования в хирургии и комбустиологии, получаемая на основе желатина и гидрофильного биополимера ПЭГ-1500 в пропорции 1:1, структурированная углеродными наноматериалами: ОУНТ-ПВП, или ОУНТ-СМС, или НП-44 в количестве 0,04% масс.
| US 4243656 A, 06.01.1981 | |||
| УСТРОЙСТВО для УПРАВЛЕНИЯ ОБЖИГОМ КЕРАМИЧседйХ- ПЛИТОК В ЩЕЛЕВОЙ ПЕЧИ | 0 |
|
SU380930A1 |
| WO 2005082775 A1, 09.09.2005 | |||
| Gholamreza Kavoosi et al., Investigation of gelatin/multi-walled carbon nanotube nanocomposite films as packaging materials / Food Science & Nutrition, 2014, Vol.2, N.1, pp.65-73 | |||
| Monica Puri Sikka et al., The role of biopolymers and biodegradable polymeric | |||
Авторы
Даты
2023-08-01—Публикация
2022-06-06—Подача