Изобретение относится к медицине, а именно к радионуклидной диагностике в кардиологии, и предназначено для выявления пациентов c повышенным риском осложненного течения раннего послеоперационного периода после хирургического лечения ишемической кардиомиопатии (ИКМП) в целях улучшения отбора пациентов на данный вид лечения и выбора тактики ведения их в послеоперационном периоде. Способ может быть использован в кардиологических отделениях лечебно-диагностических учреждений, оснащенных радиоизотопными лабораториями.
Известно, что ишемическая болезнь сердца (ИБС) остается одной из главных причин смертности и инвалидизации населения в мире, а также одним из основных факторов развития хронической сердечной недостаточности [1]. Прогрессирование ИБС, сопровождающееся расширением полостей сердца и выраженной контрактильной дисфункцией носит название ИКМП [2]. Данное состояние ассоциировано с наихудшим прогнозом по сравнению с остальными вариантами ИБС [3]. В ходе большого количества исследований было продемонстрировано, что хирургическое лечение данной патологии имеет значительно лучший результат по сравнению с применением консервативной терапии [4]. Однако, поскольку данный вид лечения всегда подразумевает открытое и продолжительное оперативное вмешательство, у части пациентов в раннем послеоперационном периоде наблюдается ряд тяжелых осложнений, связанных с нарушением инотропной функции сердца [5-7].
Таким образом, имеется потребность в оценке вероятности развития осложнений в раннем послеоперационном периоде на дооперационном этапе, чтобы при высокой вероятности была возможность рассмотреть альтернативную тактику лечения или оптимизировать риски.
Радионуклидные методы исследования отличаются высокими показателями воспроизводимости и низкой операторзависимостью [8]. В последние перспективным объектом исследования становится стресс-индуцированная механическая диссинхрония сердца (МД), которую можно оценить посредством таких радионуклидных модальностей, как перфузионная сцинтиграфия миокарда [9] и радионуклидная томовентрикулография (РТВГ) [8]. Первый из указанных методов может давать некорректные результаты у пациентов с обширными дефектами перфузии, что наблюдается у пациентов с ИКМП [10]. В отличие от перфузионной сцинтиграфии миокарда, РТВГ визуализирует пул крови и не подвержен влиянию дефектов перфузии на вычисление показателей МД [8]. Из исследуемых показателей наиболее малоизученным, однако весьма перспективным, является Entropy, который отражает степень разнородности фазовой гистограммы [11]. Данный метод слабее подвержен влиянию помех измерения [11] и продемонстрировал прогностическую роль [8,11,12]. Однако, его роль в аспекте прогнозирования осложненного течения раннего послеоперационного периода ранее не изучалась.
Известны способы прогнозирования осложнений послеоперационного периода, основанные на оценке различных показателей, полученных в ходе операции и на послеоперационном этапе [13-17]. Данные способы не позволяют предсказывать осложненное течение раннего послеоперационного периода до проведения операции, таким образом исключаются возможность корректировки тактики ведения пациента и, в случае высокого риска послеоперационных осложнений - выбора альтернативного метода лечения.
Известен способ прогнозирования осложнений у пациентов с хронической сердечной недостаточностью после кардиохирургических операций в условиях искусственного кровообращения [18], основанный на определении концентрации мелатонина сульфата в ночной фракции мочи на дооперационном этапе методом иммуноферментного анализа. Недостатком данного метода является то, что пик концентрации мелатонина может смещаться в зависимости от многих факторов (хронотип, режим питания и т.д.) [19]. Кроме того, указанный метод продемонстрировал показатели специфичности по данным ROC-анализа, равные 86,7% (для концентрации мелатонина сульфата 17,4 нг/мл), что значительно уступает предложенному методу.
Известен способ прогнозирования риска развития осложнений в раннем госпитальном периоде у пациентов после коронарного шунтирования в условиях искусственного кровообращения [20], заключающийся в определении ряда маркеров почечного повреждения (цистатин С (Х,мг/л), липокалин, ассоциированный с желатиназой нейтрофилов - NGAL (X, нг/мл), микроальбумин (Х, мг/сут), интерлейкин-18 - ИЛ-18 (Х, пг/мл) и молекул повреждения почек 1 типа - КИМ-1 (Х, нг/мл)), после чего вычисляют интегральный показатель повреждения почек по соответствующей формуле. Недостатками данного метода является сложная логистическая модель, включающая 5 показателей, что значительно увеличивает вероятность ошибки.
Известен способ прогнозирования неблагоприятного исхода у пациентов с ишемической болезнью сердца, перенесших аортокоронарное шунтирование [21], заключающийся в определении роста сгустка методом тромбодинамики и расчете прогностического коэффициента по оригинальной формуле. Недостатком данного метода является выявление осложнений, связанных исключительно с нарушением свертывания крови, и игнорирование осложнений, связанных с нарушением инотропной функции сердца вследствие нарушения обменных процессов и роста внутрижелудочковой диссинхронии.
Известен способ прогнозирования риска развития повторного ремоделирования миокарда левого желудочка сердца в течение 12 месяцев после хирургического лечения ишемической кардиомиопатии [22], основанный на способе определения сократительного резерва левого желудочка сердца у пациентов с ИКМП проведении радионуклидной томовентрикулографии (РТВГ) сердца с 99mTc-пирофосфатом в состоянии покоя и на фоне инфузии добутамина в дозах 5, 10, 15 мкг/кг/мин [23]. Данный способ характеризуется наиболее высокими показателями воспроизводимости и низкой операторзависимостью по сравнению с другими визуализирующими методиками в отношение определения функции левого желудочка сердца [24,25]. Проведение данного исследования на гамма-камере с ультрабыстрыми CZT-детекторами позволяет значительно снизить дозу вводимого радиофармпрепарата, таким образом снизить лучевую нагрузку и значительно сократить время исследования. Благодаря этим факторам стало возможным проведение данного исследования у пациентов с высокими классами сердечной недостаточности на фоне нагрузочных стресс-тестов. Недостатком способа является отсутствие данных о его возможностях в отношении прогнозирования повышенного риска осложненного течения раннего послеоперационного периода у больных ишемической кардиомиопатией на дооперационном этапе.
Данный способ является наиболее близким к заявляемому по технической сущности и достигаемому результату и выбран в качестве прототипа.
Целью изобретения является улучшение качества отбора пациентов для хирургического лечения ИКМП посредством выделения тех из них, кто имеет повышенный риск развития сердечно-сосудистых осложнений в раннем послеоперационном периоде, и, в случае выявления высокого риска - выбора альтернативного метода лечения.
Поставленная цель достигается проведением радионуклидной томовентрикулографии (РТВГ) сердца с 99mTc-пирофосфатом в состоянии покоя и на фоне инфузии добутамина в дозах 5,10,15 мкг/кг/мин в течении 5 минут каждая, по результатам которой определяют показатели стресс-индуцированного изменения Entropy фазовой гистограммы (∆Entropy, %), а также рутинного эхокардиографического исследования (ЭхоКГ) с вычислением конечно-систолического объема левого желудочка сердца (КСО) и состояния митрального клапана для определения показаний к оперативному вмешательству на нем. Прогностическую вероятность развития осложнений в раннем послеоперационном периоде после хирургического лечения ИКМП высчитывается по формуле:
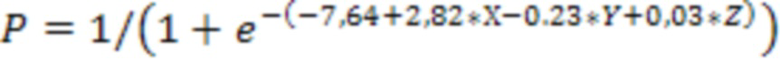
где P - прогностическая вероятность;
e - основание натурального логарифма (математическая константа; e=2,718);
-7,64 - константа логистической регрессии;
2,82; 0,23; 0,03 - весовые коэффициенты соответствующих показателей;
Х - наличие операции на митральном клапане;
Y - ΔEntropy ЛЖ, определяются по формуле: Entropy ЛЖ на пике стресс-теста - Entropy ЛЖ в состоянии покоя;
Z - конечно-систолический объем левого желудочка сердца по данным ЭхоКГ;
и при значении P больше 0,5 прогнозируют высокую вероятность развития осложнений в раннем послеоперационном периоде после хирургического лечения ИКМП.
Существенные признаки изобретения проявляют в заявленной совокупности новые свойства, что приводит к достижению нового положительного эффекта, явным образом не вытекающего из уровня техники в данной области и не являющегося очевидными для специалиста.
Идентичной совокупности признаков в известных решениях по данным патентной и научно-методической литературы не обнаружено.
Предлагаемый способ может быть использован в практическом здравоохранении как дополнительный критерий отбора пациентов для повышения качества кардиохирургического лечения ИКМП.
Исходя из выше сказанного, следует считать предлагаемое изобретение соответствующим условия патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применяемость».
Изобретение будет понятно из следующего описания и предложенных к нему фигур.
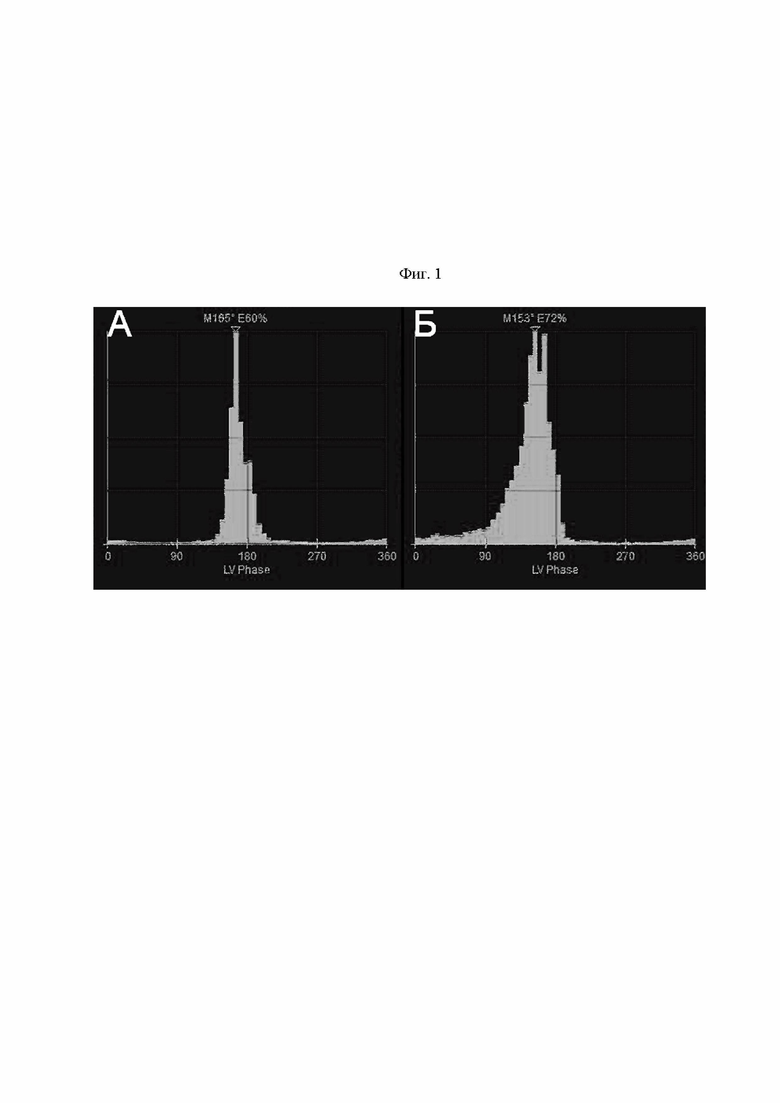
На Фиг. 1 представлена фазовая гистограмма с показателем Entropy, полученные при исследовании в состоянии функционального покоя пациента (А) и на фоне стресс-теста (Б).
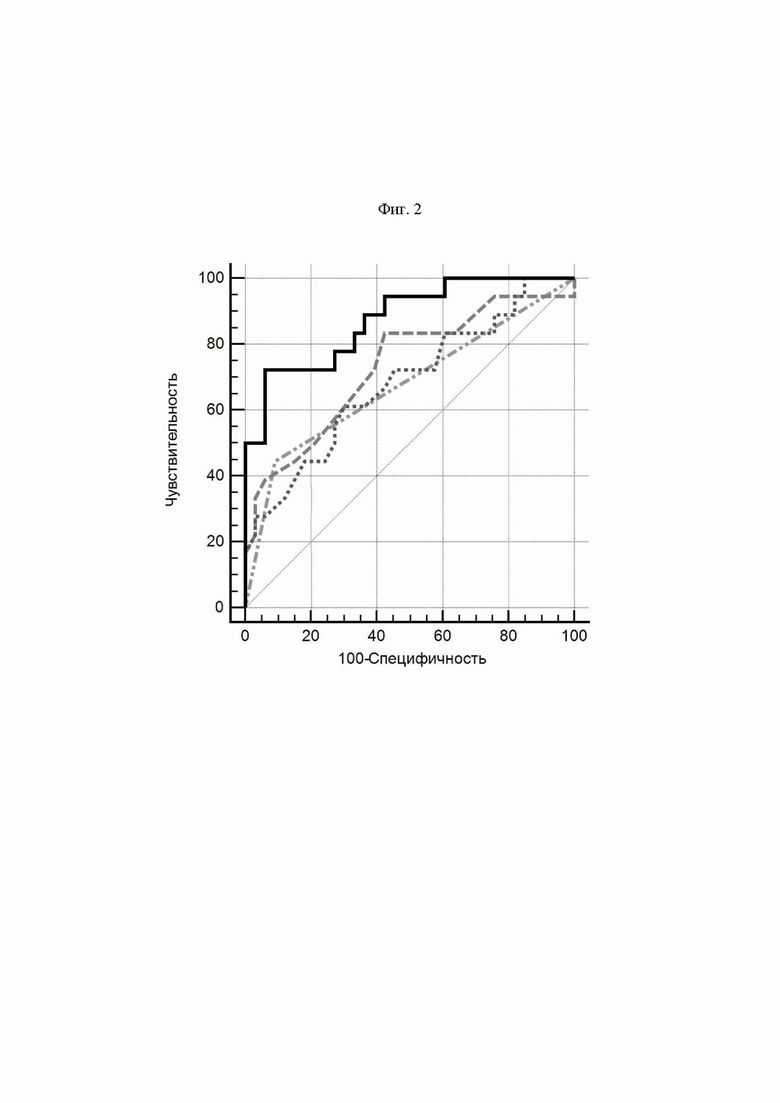
На Фиг. 2 изображены ROC-кривые, полученные при анализе КСО ЛЖ по данным эхокардиографического исследования  ΔEntropy ЛЖ
ΔEntropy ЛЖ  наличия вмешательства на митральном клапане
наличия вмешательства на митральном клапане  и выявленной прогностической модели
и выявленной прогностической модели  в определении прогноза осложненного течения раннего послеоперационного периода.
в определении прогноза осложненного течения раннего послеоперационного периода.
Способ осуществляют следующим образом. Пациенту проводят рутинное эхокардиографическое исследование, в ходе которого высчитывается КСО и степень регургитации митрального клапана [25]. Затем пациенту проводится нагрузочная РТВГ: за 24 часа до исследования пациентам рекомендуется исключить употребление кофеин-содержащих напитков, блокаторов кальциевых каналов и бетта-блокаторов. За 30 минут до исследования в локтевую вену обследуемого устанавливается внутривенный катетер. Метка эритроцитов in vivo производится согласно стандартному протоколу с введенением 555-740 мБк Tc99m- пирофосфата (препарат «Пирфотех» фирмы «Диамед», Россия). Пациент располагается на диагностическом столе однофотонного эмиссионного компьютерного томографа лежа на спине с отведенными за голову руками. Детекторы центрированы на области сердца. Центр энергетического окна устанавливается на фотопик 99mTc - 140 кЭв; ширина энергетического окна симметрична (20%). Производится регистрация ЭКГ и АД в состоянии покоя. Затем производится запись РТВГ в состоянии покоя. После этого через установленный катетер посредством инфузомата производится серия последовательных инфузий добутамина в дозах 5,10,15 мкг/кг/мин продолжительностью 5 мин каждая с параллельной записью РТВГ. Все записи проводятся в ЭКГ-синхронизированном режиме. В ходе введения каждой дозы добутамина производится контроль ЭКГ и АД. Обработка полученных данных проводится в автоматическом и полуавтоматическом режиме. Вычисляются показатель ΔEntropy ЛЖ на пике нагрузки и их разница по сравнению с показателями покоя по формуле: [значение показателя на пике стресс-теста - значение показателя в покое].
Для получения формулы, позволяющей прогнозировать вероятность развития повторного ремоделирования сердца, в исследование было включено 74 пациента с установленным диагнозом ИКМП, направленных на оперативное лечение. Перед интервенционным лечением все пациенты прошли полное клиническое, лабораторное и инструментальное обследование, а также всем пациентам выполняли РТВГ на фоне введения добутамина для оценки сократимости обоих желудочков сердца.
Сцинтиграфические исследования проводили с использованием однофотонного эмиссионного компьютерного томографа Discovery NM/CT 570c (GE Healthcare, США), оснащенного гамма-камерой с CZT детекторами.
В раннем послеоперационном периоде пациенты были разделены на 2 подгруппы в зависимости от наличия осложнений в раннем послеоперационном периоде (смерть от сердечных причин, необходимость использования внутриаортальной баллонной контрпульсации, необходимость инотропной поддержи в отделении реанимации более 5 дней): группа 1 (n=23: смерть - 3, ВАБГ - 9, необходимость инотропной поддержки в ОАР >5 дней - 11) - с наличием осложнений; группа 2 (n=51) - без осложнений в раннем послеоперационном периоде.
Статистическую обработку результатов проводили в программном пакете STATISTICA v10 и MedCalc 12.1.14.0. Для оценки распределения количественных признаков был использован критерий Шапиро-Уилка Для определения диагностической эффективности исследуемых методик использовали ROC-анализ (Receiver Operating Characteristic Analysis). Информативность диагностического теста определяли путем оценки площади под кривой — Area Under Curve (AUC), а также сравнения показателей чувствительности и специфичности. Для сравнения ROC-кривых использовался непараметрический тест Делонга. Для построения модели прогнозирования развития повторного ремоделирования использовали регрессионный анализ в виде бинарной логистической регрессии: рассчитаны отношения шансов (ОШ) и доверительный интервал (ДИ). Статистически значимыми считались различия при p<0,05.
По данным многофакторного логистического регрессионного анализа независимыми предикторами осложненного течения раннего послеоперационного периода у больных ИКМП явились вмешательство на митральном клапане (ОШ = 9,8; ДИ 1,92; 7,9; р = 0,005), ΔEntropy ЛЖ (ОШ=1,35; ДИ 1,07; 1,7; р=0,009), КСО ЛЖ (ОШ = 1,04; ДИ 1,0; 1,08; р = 0,008).
Используя коэффициенты регрессии выявленных сцинтиграфических показателей, было выведено уравнение для расчета прогностической вероятности осложненного течения раннего послеоперационного периода после оперативного лечения пациентов с ИКМП:
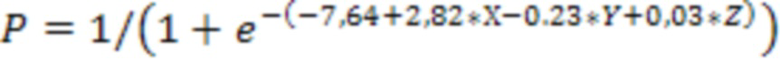
где P - прогностическая вероятность;
e - основание натурального логарифма (математическая константа; e=2,718);
-7,64 - константа логистической регрессии;
2,82; 0,23; 0,03 - весовые коэффициенты соответствующих показателей;
Х - наличие операции на митральном клапане;
Y - ΔEntropy ЛЖ, определяются по формуле: Entropy ЛЖ на пике стресс-теста - Entropy ЛЖ в состоянии покоя;
Z - конечно-систолический объем левого желудочка сердца по данным ЭхоКГ,
и при значении P больше 0,5 прогнозируют высокую вероятность развития осложнений в раннем послеоперационном периоде после хирургического лечения ИКМП.
По результатам ROC-анализа наличие вмешательства на митральном клапане имело значение чувствительности 40% и специфичности 86% (AUC=0,633), КСО ЛЖ имело значение чувствительности 60% и специфичности 70% для порогового значения >148мл (AUC=0,690), ΔEntropy ЛЖ показало значение чувствительности 86% и специфичности 54% для значения >0 (AUC=0,740). Логистическая модель, учитывающая все указанные показатели, имела чувствительность 74%, специфичность 95% и AUC=894, что оказалось достоверно больше показателей AUC, полученных при анализе каждого указанного выше (р<0,05) показателя по отдельности.
Клинический пример 1 (осложненное течение раннего послеоперационного периода).
Пациентка 57 год. Диагноз - ишемическая кардиомиопатия, хроническая сердечная недостаточность III функционального класса (NYHA). По данным эхокардиографии ФВ ЛЖ = 33%, КСО ЛЖ = 167мл. По данным ангиографии - стеноз ПНА 75%, ПКА - 75%, ОА - 60%. По результатам РТВГ с добутамином ΔEntropy ЛЖ составила +10%. Используя полученные данные было рассчитано значение вероятности:
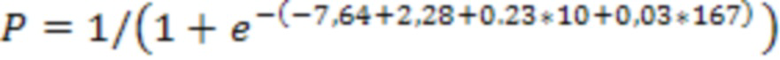
P=0,87
Полученное значение P=0,87 позволяет на предоперационном этапе предположить, что у данной пациентки следует ожидать тяжелое течение раннего послеоперационного периода.
Пациентке была выполнена операция аорто-коронарного шунтирования, пластика левого желудочка и пластика МК. В раннем послеоперационном периоде ввиду отсутствия адекватного восстановления сократительной функции и необходимости использования внутриаортальной баллонной контрпульсации, пациентка 12 дней провела в отделении реанимации на фоне инотропной поддержки.
Клинический пример 2 (отсутствие осложнений в раннем послеоперационном периоде).
Пациентка 59 лет. Диагноз - ишемическая кардиомиопатия, хроническая сердечная недостаточность III функционального класса (NYHA). По данным эхокардиографии ФВ ЛЖ = 29%, КСО ЛЖ = 145мл. По данным ангиографии - стеноз ПНА 75%, ПКА, 70%, ЗНА - 90%. По результатам РТВГ с добутамином ΔEntropy ЛЖ составила -5%. Используя полученные данные было рассчитано значение вероятности:

P=0,01
Полученное значение P=0,01 позволяет на предоперационном этапе предположить, что у данного пациента низкие шансы развития осложнений в раннем послеоперационном периоде.
Пациенту была выполнена операция аорто-коронарного шунтирования и пластика ЛЖ. После операции через 24 часа пациент был переведен из отделения реанимации в палату, течения послеоперационного периода нормальное.
Предлагаемый в качестве изобретения способ апробирован на 74 больных и позволяет повысить точность выявления пациентов c высоким риском осложненного течения раннего послеоперационного периода на дооперационном этапе и скорректировать тактику ведения пациентов с ИКМП.
Список использованной литературы
1. World Health Statistics 2012 // http://www.who.int URL: http://www.who.int/gho/publications/world_health_statistics/WHS2012_IndicatorCompendium.pdf?ua=1 (дата обращения: 02.11.2018)]
2. Burch G.E. lschemic cardiomyopathy / Burch G.E., Tsui C.Y., Harb J.M. // Am Heart J. - 1972. - №3. - 340-350.
3. Шипулин В.М., Пряхин А.С., Андреев С.Л., Шипулин В.В., Чумакова С.П., Рябова Т.Р., Стельмашенко А.И., Беляева С.А., Лелик Е.В. Современные клинико-фундаментальные аспекты в диагностике и лечении пациентов с ишемической кардиомиопатией (обзор). Сибирский журнал клинической и экспериментальной медицины. 2021;36(1):20-29. https://doi.org/10.29001/2073-8552-2021-36-1-20-29
4. Orlandini A., Castellana N., Pascual A. et al. Myocardial viability for decision-making concerning revascularization in patients with left ventricular dysfunction and coronary artery disease: a meta-analysis of non-randomized and randomized studies // Int J Cardiol. - 2015 Mar 1. - Vol. 182. - P. 494-499. doi: 10.1016/j.ijcard.2015.01.025. Epub 2015 Jan 7. PMID: 25617608
5. Шипулин В.М., Андреев С.Л., Пряхин А.С. и др. Значение стресс-методов в оценке риска ранних послеоперационных осложнений у пациентов с ишемической кардиомиопатией // Кардиология и сердечно-сосудистая хирургия. - 2020. - № 13 (6). - С. 502-509. https://doi.org/10.17116/kardio202013061502
6. Nadeem R., Agarwal S., Jawed S., Yasser A., Altahmody K. Impact of cardiopulmonary bypass time on postoperative duration of mechanical ventilation in patients undergoing cardiovascular surgeries: a systemic review and regression of metadata // Cureus. - 2019. - Nov 6. - Vol. 11 (11). - P. e6088. doi: 10.7759/cureus.6088. PMID: 31857920; PMCID: PMC6897343
7. Ruggieri V.G., Bounader K., Verhoye J.P. et al. Prognostic impact of prolonged cross-clamp time in coronary artery bypass grafting // Heart Lung Circ. - 2018. - Dec. - Vol. 27 (12). - P. 1476-1482. doi: 10.1016/j.hlc.2017.09.006. Epub 2017 Oct 6. PMID: 29276146.
8. Shipulin VV, Andreev SL, Pryakhin AS, et al. Low-dose dobutamine stress gated blood pool SPECT assessment of left ventricular contractile reserve in ischemic cardiomyopathy: a feasibility study. Eur J Nucl Med Mol Imaging. 2022;10.1007/s00259-022-05714-y. doi:10.1007/s00259-022-05714-y
9. Chen J., Bax J.J., Henneman M.M., Boogers M.J., Garcia E.V. Is nuclear imaging a viable alternative technique to assess dyssynchrony? // Europace. - 2008. - Vol. 10 (3). - P. 101-105. DOI: 10.1093/europace/eun221
10. AlJaroudi W, Jaber WA, Cerqueira MD. Effect of tracer dose on left ventricular mechanical dyssynchrony indices by phase analysis of gated single photon emission computed tomography myocardial perfusion imaging. J Nucl Cardiol. 2012;19(1):63-72. doi:10.1007/s12350-011-9463-z
11. Nakajima K, Okuda K, Matsuo S, Slomka P. Making the invisiblevisible: Phase dyssynchrony has potential as a new prognostic marker. J Nucl Cardiol. 2019;26:298-302
12. Shimizu M, Iiya M, Fujii H, Kimura S, Suzuki M, Nishizaki M. Left ventricular end-systolic contractile entropy can predict cardiac prognosis in patients with complete left bundle branch block. J Nucl Cardiol 2019.
13. Заболотских И.Б., Власов Г.С., Малышев Ю.П., Филиппова Е.Г. Способ прогнозирования послеоперационных осложнений. Патент № 2149580 РФ, МПК А61 В 5/04. № 97101026/14; Заявл.23.01.1997; Опубл. 27.05.2000, Бюл.№ 15.
14. Загатин М.М., Зорин А.Б. Государственное образовательное учреждение Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова. Способ прогнозирования результатов кардиохирургических операций в раннем послеоперационном периоде у больных с изолированными, сочетанными и комбинированными поражениями клапанного аппарата сердца. Патент № 2251964 РФ, МПК А61В 5/02 № 2003129625/14, Заявл. 30.09.2003, Опубл. 20.05.2005, Бюл. № 14.
15. Базарный В.В., Тихонина Е.А., Кондрашов К.В. Государственное бюджетное образовательное учреждение высшего профессионального образования "Уральская государственная медицинская академия Министерства здравоохранения и социального развития Российской Федерации" (ГБОУ ВПО УГМА Минздравсоцразвития России). Способ прогнозирования послеоперационных осложнений при аортокоронарном шунтировании. Патент № 2480757 РФ, МПК G01N 33/50 № 2012108264/15, Заявл. 05.03.2012, Опубл. 27.04.2013, Бюл. № 12.
16. Семенова А.С., Шигаев М.Ю., Агапов В.В. Способ прогнозирования осложнений после операций шунтирования коронарных артерий в условиях искусственного кровообращения. Патент № 2536279 РФ, МПК A61B 5/00, № 2013152204/14, Заявл. 25.11.2013, Опубл. 20.12.2014, Бюл. № 35 /
17. Дорофейков В.В., Шешурина Т.А., Вавилова Т.В., Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр имени В.А. Алмазова" Министерства здравоохранения Российской Федерации, Федеральное государственное бюджетное образовательное учреждение высшего образования "Национальный государственный университет физической культуры, спорта и здоровья имени П.Ф. Лесгафта, Санкт-Петербург". Способ оценки повреждения миокарда и риска развития осложнений после операций на сердце в условиях искусственного кровообращения. Патент № 2760242 РФ, МПК G01N 33/48, A61B 5/021, № 2021105348, Заявл. 01.03.2021, Опубл. 23.11.2021, Бюл. № 33.
18. Лискова Ю.В., Чернышева Т.В., Стадников А.А., Саликова С.П., Рожков В.О., Твердохлиб Н.В. Федеральное государственное бюджетноеобразовательное учреждение высшего образования "Оренбургский государственный медицинский университет" Министерства здравоохранения Российской Федерации. Способ прогнозирования осложнений у пациентов с хронической сердечной недостаточностью после кардиохирургических операций в условиях искусственного кровообращения. Патент № 2680602 РФ, МПК G01N 33/74, № 2017142520, Заявл. 05.12.2017, Опубл. 25.02.2019, Бюл. №6.
19. Mirza-Aghazadeh-Attari M, Reiter RJ, Rikhtegar R, et al. Melatonin: An atypical hormone with major functions in the regulation of angiogenesis. IUBMB Life. 2020;72(8):1560-1584. doi:10.1002/iub.2287
20. Плотников Г.П., Шафранская К.С., Каган Е.С., Шукевич Д.Л., Рубцов М.С., Барбараш О.Л. Федеральное государственноебюджетное научное учреждение"Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний" (НИИКПССЗ). Способ прогнозирования риска развития осложнений в раннем госпитальном периоде у пациентов после коронарного шунтирования в условиях искусственного кровообращения. Патент № 2642238 РФ, МПК G01N 33/48, № 2017109321, Заявл. 20.03.2017, Опубл. 24.01.2018, Бюл. №3.
21. Шлык И.Ф., Сидоров Р.В., Демидова А.А., Дроботя Н.В., Шлык С.В., Шлык Ирина Федоровна, Способ прогнозирования неблагоприятного исхода у пациентов с ишемической болезнью сердца, перенесших аортокоронарное шунтирование. Патент № 2688241 РФ, МПК A61B 5/145, № 2018146340, Заявл. 24.12.2018, Опубл. 21.05.2019, Бюл. № 15.
22. Шипулин В.В., Андреев С.Л., Пряхин А.С., Завадовский К.В. Федеральное государственное научное учреждение "Томский национальный исследовательский медицинский центр Российской академии наук" (Томский НИМЦ). Способ прогнозирования риска развития повторного ремоделирования миокарда левого желудочка сердца в течение 12 месяцев после хирургического лечения ишемической кардиомиопатии. Патент № 2745473 РФ, МПК А61В 5/00, № 2020117057, Заявл. 12.05.2020, Опубл. 25.03.2021, Бюл. № 9.
23. Завадовский К.В., Андреев С.Л., Шипулин В.В., "Томский национальный исследовательский медицинский центр Российской академии наук" (Томский НИМЦ), Cпособ неинвазивной оценки сократительного резерва левого желудочка сердца у пациентов с ишемической кардиомиопатией. Патент № 2695902 РФ, МПК А61В 6/03, А61К 51/00, А61Р 43/00, № 2018115379, Заявл. 24.04.2018, Опубл. 29.07.2019, Бюл. № 22 /
24. Шипулин В.В., Мишкина А.И., Гуля М.О., Варламова Ю.В., Андреев С. Л., Пряхин А. С., Шипулин В.М., Завадовский К.В. Отдаленный прогноз повторного ремоделирования левого желудочка после хирургического лечения ишемической кардиомиопатии: возможности нагрузочной радионуклидной томовентрикулографии. Российский кардиологический журнал. 2020;25(11):3831. doi:10.15829/1560-4071-2020-3831
25. McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure [published correction appears in Eur Heart J. 2021 Oct 14;:]. Eur Heart J. 2021;42(36):3599-3726. doi:10.1093/eurheartj/ehab368
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития повторного ремоделирования миокарда левого желудочка сердца в течение 12 месяцев после хирургического лечения ишемической кардиомиопатии | 2020 |
|
RU2745473C1 |
| Способ неинвазивной оценки сократительного резерва левого желудочка сердца у пациентов с ишемической кардиомиопатией | 2018 |
|
RU2695902C1 |
| Способ прогнозирования ранних послеоперационных сердечно-сосудистых осложнений у пациентов с ишемической кардиомиопатией | 2022 |
|
RU2793654C1 |
| Способ прогнозирования эффективности процедуры прямой реваскуляризации у пациентов с ишемической болезнью сердца, осложненной выраженным снижением сократительной способности левого желудочка | 2023 |
|
RU2814402C1 |
| Способ диагностики развития ишемической кардиомиопатии у больных ишемической болезнью сердца | 2021 |
|
RU2765598C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННОГО РЕМОДЕЛИРОВАНИЯ СЕРДЦА У БОЛЬНЫХ ИШЕМИЧЕСКОЙ КАРДИОМИОПАТИЕЙ | 2006 |
|
RU2310372C1 |
| Способ прогнозирования положительного ответа на кардиоресинхронизирующую терапию у пациентов с хронической сердечной недостаточностью II и III функционального класса | 2022 |
|
RU2786467C1 |
| Способ прогнозирования ответа на сердечную ресинхронизирующую терапию у пациентов с хронической сердечной недостаточностью | 2019 |
|
RU2721821C1 |
| Способ предоперационной подготовки пациентов с терминальной сердечной недостаточностью перед имплантацией механического устройства гемодинамической поддержки левого желудочка | 2023 |
|
RU2833849C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МИТОХОНДРИАЛЬНОЙ ДИСФУНКЦИИ МИОКАРДА ПОСЛЕ ТРАНСПЛАНТАЦИИ СЕРДЦА С ИСПОЛЬЗОВАНИЕМ РАДИОНУКЛИДНОГО МЕТОДА | 2018 |
|
RU2687584C1 |
Изобретение относится к медицине, а именно к радионуклидной диагностике в кардиологии, и может быть использовано для прогнозирования развития осложненного течения раннего послеоперационного периода у больных ишемической кардиомиопатией на дооперационном этапе. Проводят эхокардиографию (ЭхоКГ) и определяют конечный систолический объём левого желудочка (КСО ЛЖ). Проводят радионуклидную равновесную вентрикулографию с 99mTc-пирофосфатом в состоянии покоя и на фоне последовательных внутривенных инфузий добутамина в дозах 5, 10, 15 мкг/кг/мин в течение 5 минут на каждую дозу. Определяют Entropy ЛЖ в состоянии покоя и Entropy ЛЖ на пике стресс-теста. Вычисляют прогностическую вероятность развития осложненного течения раннего послеоперационного периода у больных ишемической кардиомиопатией (P) по формуле: Р=1/(1+e(-(-7,64+2,82*Х-0.23×Y+0,03*Z))), где Х равно 1 в случае наличия у больной операции на митральном клапане, равно 0 в случае отсутствия у больной операции на митральном клапане; Y - ΔEntropy ЛЖ, вычисляемая по формуле ΔEntropy ЛЖ = (Entropy ЛЖ на пике стресс-теста – Entropy ЛЖ в состоянии покоя); Z - КСО ЛЖ. При значении P больше 0,5 прогнозируют развитие осложнений в раннем послеоперационном периоде после хирургического лечения ишемической кардиомиопатии. Способ обеспечивает возможность отбора пациентов с повышенным риском развития сердечно-сосудистых осложнений в раннем послеоперационном периоде за счет эхокардиографических и радионуклидных признаков. 2 ил., 2 пр.
Способ прогнозирования развития осложненного течения раннего послеоперационного периода у больных ишемической кардиомиопатией на дооперационном этапе, заключающийся в том, что проводят эхокардиографию (ЭхоКГ) и определяют конечный систолический объём левого желудочка (КСО ЛЖ), проводят радионуклидную равновесную вентрикулографию с 99mTc-пирофосфатом в состоянии покоя и на фоне последовательных внутривенных инфузий добутамина в дозах 5, 10, 15 мкг/кг/мин в течение 5 минут на каждую дозу и определяют Entropy ЛЖ в состоянии покоя и Entropy ЛЖ на пике стресс-теста, после чего вычисляют прогностическую вероятность развития осложненного течения раннего послеоперационного периода у больных ишемической кардиомиопатией (P) по формуле:
Р=1/(1+e(-(-7,64+2,82*Х-0.23×Y+0,03*Z))), где
Х равно 1 в случае наличия у больной операции на митральном клапане, равно 0 в случае отсутствия у больной операции на митральном клапане;
Y - ΔEntropy ЛЖ, вычисляемая по формуле ΔEntropy ЛЖ = (Entropy ЛЖ на пике стресс-теста – Entropy ЛЖ в состоянии покоя);
Z - КСО ЛЖ;
и при значении P больше 0,5 прогнозируют развитие осложнений в раннем послеоперационном периоде после хирургического лечения ишемической кардиомиопатии.
| Способ диагностики развития ишемической кардиомиопатии у больных ишемической болезнью сердца | 2021 |
|
RU2765598C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННОГО РЕМОДЕЛИРОВАНИЯ СЕРДЦА У БОЛЬНЫХ ИШЕМИЧЕСКОЙ КАРДИОМИОПАТИЕЙ | 2006 |
|
RU2310372C1 |
| Способ прогнозирования риска развития повторного ремоделирования миокарда левого желудочка сердца в течение 12 месяцев после хирургического лечения ишемической кардиомиопатии | 2020 |
|
RU2745473C1 |
| АНДРЕЕВ С.Л | |||
| и др | |||
| Критерий прогнозирования течения послеоперационного периода у больных ишемической кардиомиопатией по данным магнитно-резонансной томографии | |||
| Сибирский медицинский журнал (г | |||
| Томск), 2015, том 30, номер 2, стр | |||
| Способ приготовления пищевого продукта сливкообразной консистенции | 1917 |
|
SU69A1 |
| ЛЕЖНЕВ А.А | |||
| и др | |||
| Метод оценки | |||
Авторы
Даты
2023-08-02—Публикация
2022-07-04—Подача