ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к производным пептидных нуклеиновых кислот, дополнительно целенаправленно воздействующим на пре-мРНК матриксной металлопротеиназы-1 человека, для изменения к лучшему старения кожи при посредничестве матриксной металлопротеиназы-1.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Старению кожи уделяется значительное внимание, так как признаки старения наиболее заметны на коже. Поскольку предупреждение и лечение старения кожи очень важно для качества жизни, не только уже немолодые люди, но и молодежь заинтересованы в соответствующей здоровой пище, косметике, медикаментах, медицинских принадлежностях и так далее. Существуют два основных процесса старения кожи. Одним из них является старение, вызванное воздействием внутренних факторов или естественное старение, которое сопровождает старение, и другим является старение, вызванное воздействием внешних факторов, которое вызвано экзогенным происхождением, таким как солнечное облучение, курение и недостаточное питание.
Воздействие ультрафиолетового облучения на кожу ускоряет экспрессию матриксной металлопротеиназы-1 (ММП-1), приводя к ускорению разрушения коллагена, основного структурного компонента дермы. Кроме того, курение индуцирует мРНК матриксной металлопротеиназы-1 в коже, что приводит к тем же результатам, что и воздействие ультрафиолетового облучения на кожу [J. Cosmetic Dermatology vol 6, 40-50 (2007)].
Коллаген является основным структурным белком во внеклеточном пространстве в различных соединительных тканях, таких как кожа, кровеносный сосуд, кость, зуб и мышца. Так как коллаген отвечает за поддержку большинства тканей и структуры клеток, его разрушение и деформация могут сильно повлиять на старение кожи [J. Pathol, vol 211, 241-251 (2007)].
Матриксные металлопротеиназы представляют собой ферменты, которые секретируются из фибробласта, кератиноцита и т.д., которые способны к разрушению всех видов внеклеточных матриц (extracellular matrix, ЕСМ) и базальных мембран (basement membrane, BM). Выявлено более 26 видов матриксных металлопротеиназ, таких как ММП-1 (интерстициальная коллагеназа), ММП-2 (желатиназа), ММП-3 (стромелизин), ММП-7 (Матрилизин), ММП-8 (нейтрофильная коллагеназа) и ММП-12 (металлоэластаза) [J. Biol. Chem. vol 277, 451-454 (2002); J. Matrix. Biol, vol 15, 519-526 (1997)].
Активные формы кислорода, вызванные воздействием ультрафиолетового облучения и курения, были известны по причине сверхэкспрессии матриксной металлопротеиназы-1. Для лечения старения кожи в некотором смысле были разработаны антиоксиданты и функциональное питание для противоокислительного действия, такие как витамин А (ретинол), витамин С (аскорбиновая кислота), витамин Е (токоферол), каротиноид, флавоноид, зеленый чай и селен, и в настоящее время ведется исследование механизма их действия [Int. J. Food Sci. Technol. vol 73, 989-996 (2005); Kor. J. Aesthet. Cosmetol. vol 11, 649-654 (2013); Int. J. Mol. Med. vol 38, 357-363 (2016)].
Принимая во внимание значимость металлопротеиназы-1 при старении кожи, было бы очень интересно и необходимо разработать фармацевтические препараты или косметику на основе механизма экспрессии металлопротеиназы-1, которая может улучшить и предотвратить состояние старения кожи.
Пре-мРНК: Генетическая информация осуществляется на ДНК (2-дезоксирибонуклеиновая кислота). ДНК транскрибируется для продуцирования пре-мРНК (пре-информационная (матричная) рибонуклеиновая кислота) в ядре. Пре-мРНК млекопитающих обычно состоит из экзонов и интронов, а экзон и интрон взаимосвязаны друг с другом, как схематично приведено ниже. Экзоны и интроны пронумерованы, как проиллюстрировано на рисунке ниже:
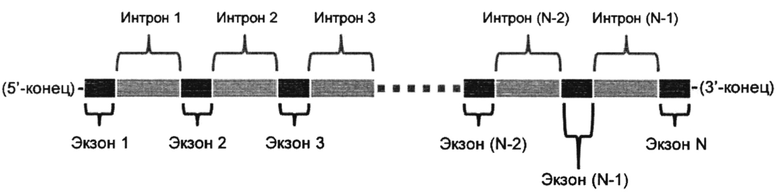
Сплайсинг пре-мРНК: Пре-мРНК подвергается процессингу в мРНК после удаления интронов серией сложных реакций в совокупности называемых "сплайсингом", который схематически обобщен ниже на диаграмме. [Ann. Rev. Biochem. 72(1), 291-336 (2003); Nature Rev. Mol. Cell Biol. 6(5), 386-398 (2005); Nature Rev. Mol. Cell Biol. 15(2), 108-121 (2014)].
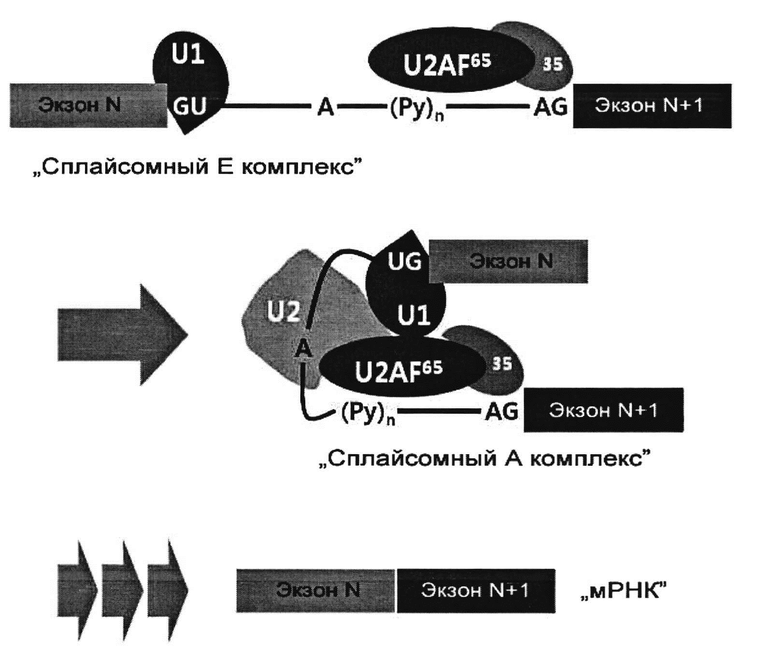
Сплайсинг инициируется образованием "сплайсомного Е комплекса" (т.е. ранний сплайсомный комплекс) между пре-мРНК и адапторными факторами сплайсинга. В "сплайсомном Е комплексе", U1 связывается с областью соединения экзона N и интрона N, и U2AF35 связывает область соединения интрона N и экзона (N+1). Таким образом, области соединения экзон/интрон или интрон/экзон являются критическими для образования раннего сплайсомного комплекса. "Сплайсомный Е комплекс" превращается в "сплайсомный А комплекс " при дополнительном комплексообразовании с U2. "Сплайсомный А комплекс" претерпевает серию сложных реакций для удаления или сплайсирования интрона, чтобы присоединить соседние экзоны.
Синтез рибосомного белка: Белки кодируются ДНК (2-дезоксирибонуклеиновая кислота). В ответ на клеточную стимуляцию или спонтанно ДНК транскрибируется для продуцирования пре-мРНК (прематричная рибонуклеиновая кислота) в ядре. Интроны пре-мРНК ферментативным путем сплайсируются для получения мРНК (матричная рибонуклеиновая кислота), которая затем транслоцируется в цитоплазму. В цитоплазме комплекс трансляционной структуры, вызванной рибосомой, связывается с мРНК и осуществляется синтез белка, поскольку он сканирует генетическую информацию, кодируемую по мРНК. [Biochemistry vol 41, 4503-4510 (2002); Cancer Res. vol 48, 2659-2668 (1988)].
Антисмысловой олигонуклеотид (ACQ) (Antisense Oligonucleotide, ASO): Связывание олигонуклеотида с нуклеиновой кислотой, включая ДНК, мРНК и пре-мРНК, в сиквенс-специфичном методе (т.е. комплементарно) называется антисмысловым олигонуклеотидом (АСО).
Если АСО прочно связывается с мРНК в цитоплазме, например, АСО может ингибировать синтез рибосомного белка по мРНК. Необходимо, чтобы АСО присутствовал внутри цитоплазмы для того, чтобы ингибировать синтез рибосомного белка его белка-мишени.
Антисмысловое ингибирование сплайсинга: Если АСО прочно связывается с пре-мРНК в ядре, АСО сможет ингибировать или модулировать сплайсинг пре-мРНК в мРНК. Необходимо, чтобы АСО присутствовал внутри ядра для того, чтобы ингибировать или модулировать сплайсинг пре-мРНК в мРНК. Такое антисмысловое ингибирование сплайсинга продуцирует мРНК или мРНКы, не содержащие экзона, таргетированного с помощью АСО. Такая(ие) мРНК(ы) называется(ются) "сплайс-вариантом(ами)", и кодирует(ют) белок(и) меныний(ие), чем белок, кодируемый полноразмерной мРНК.
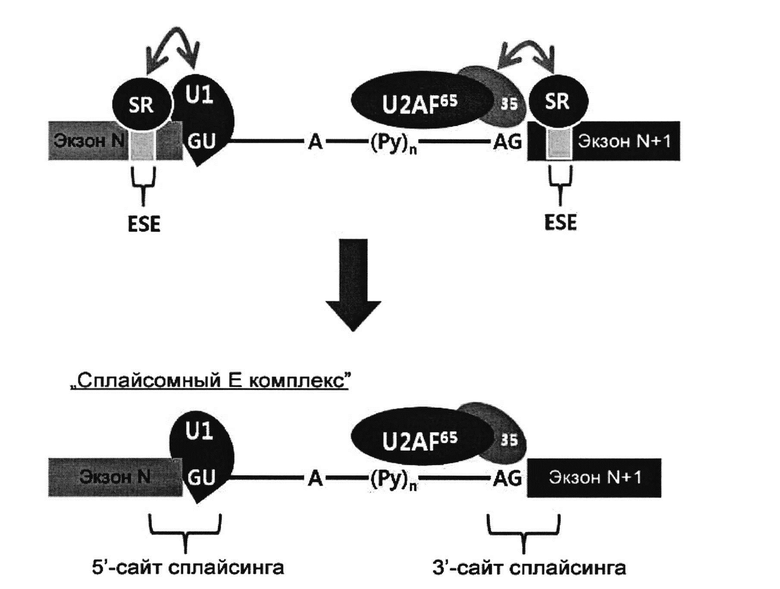
В принципе, сплайсинг может быть нарушен при ингибировании образования «сплайсомного Е комплекса». Если АСО прочно связывается с областью соединения (5'→3') экзон-интрон, т.е. "5' сайт сплайсинга», то АСО блокирует образование комплекса между пре-мРНК и фактором U1, и, следовательно, образование «сплайсомного Е комплекса». Аналогичным образом, «сплайсомный Е комплекс» не может образоваться, если АСО прочно связывается с областью соединения (5'→3') интрон-экзон, т.е. «3' сайт сплайсинга».
3' сайт сплайсинга и 5' сайт сплайсинга схематически проиллюстрированы на рисунке, приведенном ниже.
Олигонуклеотиды не природного происхождения: ДНК- или РНК-олигонуклеотиды подвержены деградации эндогенными нуклеазами, ограничивая их терапевтическую ценность. В настоящее время были разработаны и интенсивно исследованы многие виды олигонуклеотидов не природного происхождения (не встречающиеся в природе). [Clin. Exp.Pharmacol. Physiol, vol 33, 533-540 (2006)]. Некоторые из них показывают длительную метаболическую стабильность по сравнению с ДИК и РНК. Ниже приведены химические структуры для нескольких типичных олигонуклеотидов не природного происхождения. Такие олигонуклеотиды предсказуемо связываются с комплементарной нуклеиновой кислотой, как это делает ДНК или РНК.
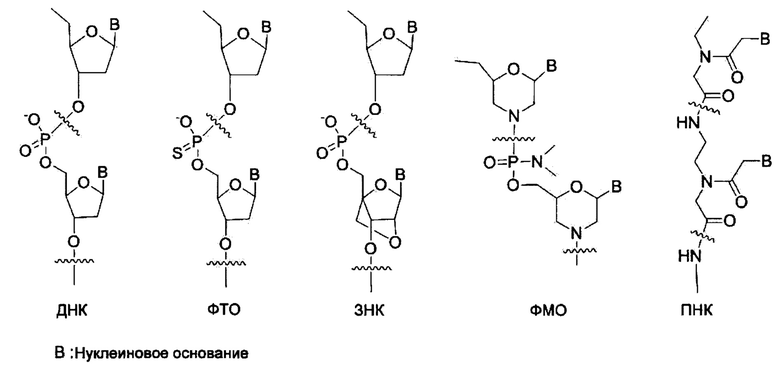
Фосфоротиоатный олигонуклеотид: Фосфоротиоатный олигонуклеотид (ФТО) (Phosphorothioate oligonucleotide, РТО) является аналогом ДНК с одним остовом атомов фосфатного кислорода, замещенных атомом серы в мономере. Такое небольшое структурное изменение сделало ФТО сравнительно устойчивым к деградации нуклеазами. [Ann. Rev. Biochem. vol 54, 367-402 (1985)].
Отражая структурное сходство в остове ФТО и ДНК, они оба плохо проникают в клеточную мембрану в большинстве типов клеток млекопитающих. При этом, для некоторых типов клеток, чрезмерно экспрессирующих транспортер(ы) ДНК, ДНК и ФТО показывают хорошее проникновение в клетки. Известно, что системно вводимые ФТО(ы) легко распределяются в печени и почках. [Nucleic Acids Res. vol 25, 3290-3296 (1997)].
Для того, чтобы облегчить проникновение в клетки ФТО in vitro, обычно на практике применяют липофекцию. Однако, липофекция физически изменяет клеточную мембрану, вызывает цитотоксичность, и поэтому не будет идеальным для долгосрочного терапевтического применения in vivo.
За прошедшие 30 лет антисмысловые ФТО(ы) и варианты ФТО(ов) были клинически оценены для лечения рака, иммунологических расстройств, метаболических заболеваний и так далее. [Biochemistry vol 41, 4503-4510 (2002); Clin. Exp.Pharmacol. Physiol, vol 33, 533-540 (2006)]. Многие из таких кандидатов антисенс-препаратов не были успешно разработаны отчасти из-за плохого проникновения в клетки ФТО. Для того, чтобы преодолеть плохое проникновение в клетки, ФТО необходимо вводить в высокой дозе для терапевтической активности.
Однако, известно, что ФТО(ы) связаны с дозолимитирующей токсичностью, включающей увеличенное время свертывания, активацию комплемента, тубулярную нефропатию, активацию купферовых клеток и иммунную стимуляцию, включая спленомегалию, лимфоидную гиперплазию, мононуклеарную клеточную инфильтрацию. [Clin. Exp. Pharmacol. Physiol, vol 33, 533-540 (2006)].
Было найдено, что многие антисмысловые ФТО(ы) показывают надлежащую клиническую активность при заболеваниях со значительной ролью печени или почек. Мипомерсен является аналогом ФТО, который ингибирует синтез ароВ-100, белка, вовлеченного в транспорт холестерина липопротеинов низкой плотности (LDL). Мипомерсен проявлял надлежащую клиническую активность у больных атеросклерозом, скорее всего, из-за его избирательного распределения в печени. [Circulation vol 118(7), 743-753 (2008)]. ISIS-113715 является антисмысловым аналогом ФТО, ингибирующего синтез протеинтирозинфосфатазы 1B (РТР1 В), и было установлено, что показывает терапевтическую активность у больных сахарным диабетом II типа. [Curr. Opin. Mol. Ther. vol 6, 331-336 (2004)].
Запертая нуклеиновая кислота: В запертой нуклеиновой кислоте (ЗНК) (locked nucleic acid, LNA) рибозное кольцо остова РНК структурно затрудняет увеличить связывающую способность для РНК или ДНК. Таким образом, ЗНК можно рассматривать как аналог ДНК или РНК высокой аффинности. [Biochemistry vol 45, 7347-7355 (2006)].
Фосфородиамидат морфолиновый олигонуклеотид: В фосфородиамидат морфолиновом олигонуклеотиде (ФМО) (phosphorodiamidate morpholino oligonucleotide, РМО) фосфатный остов и 2-дезоксирибоза ДНК заменяются фосфорамидатом и морфолином, соответственно. [Appl. Microbiol. Biotechnol. vol 71, 575-586 (2006)]. При этом остов ДНК отрицательно заряжен, ФМО остов не заряжен. Таким образом, связывание между ФМО И мРНК не имеет электростатического отталкивания между остовами и оказывается, как правило, сильнее, чем таковое между ДНК и мРНК. Так как ФМО структурно очень сильно отличается от ДНК, ФМО не будет распознаваться печеночным(и) транспортером(ами), распознающим(ими) ДНК или РНК. При этом ФМО не легко проникает в клеточную мембрану.
Пептидная нуклеиновая кислота: Пептидная нуклеиновая кислота (ПНК) (peptide nucleic acid, PNA) является полипептидом с N-(2-аминоэтил)глицином в качестве остовного звена и была открыта Dr. Nielsen и коллегами. [Science vol 254, 1497-1500 (1991)]. Химическая структура и сокращенная номенклатура ПНК иллюстрируются на представленном ниже рисунке. Подобно ДНК и РНК, ПНК также селективно связывается с комплементарной нуклеиновой кислотой. [Nature (London) vol 365, 566-568 (1992)]. При связывании с комплементарной нуклеиновой кислотой N-конец ПНК рассматривается как эквивалент «5'-конца» ДНК или РНК и С-конец ПНК как эквивалент «3'-конца» ДНК или РНК.
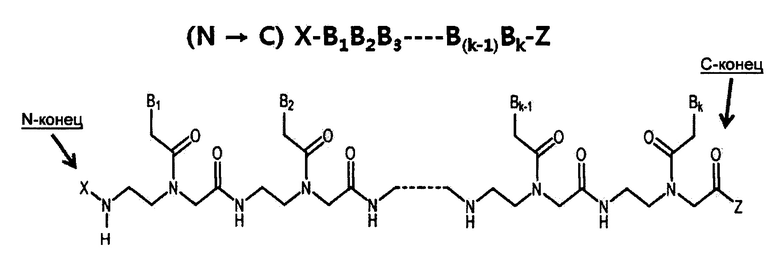
Подобно ФМО, остов ПНК не заряжен. Таким образом, связывание между ПНК и РНК оказывается, как правило, сильнее, чем связывание между ДНК и РНК. Так как ПНК заметно отличается от ДНК по химической структуре, ПНК не будет распознаваться печеночным(ми) транспортером(ами), распознающим(ими) ДНК, и будет показывать профиль распределения в тканях, отличный от такого для ДНК или ФТО. Однако, ПНК также плохо проникает в мембрану клеток млекопитающих. (Adv. Drug Delivery Rev. vol 55, 267-280, 2003).
Модифицированные нуклеиновые основания для улучшения мембранной проницаемости ПНК; ПНК была получена высоко проницаемой для мембраны клеток млекопитающих путем введения модифицированных нуклеиновых оснований с катионным липидом или его эквивалентном ковалентно к нему присоединенным. Химические структуры таких модифицированных нуклеиновых оснований приведены ниже. Было найдено, что такие модифицированные нуклеиновые основания цитозина, аденина и гуанина предсказуемо и комплементарно гибридизируются с гуанином, тимином и цитозином, соответственно. [РСТ Appl. No. PCT/KR2009/001256; ЕР2268607; US8680253].
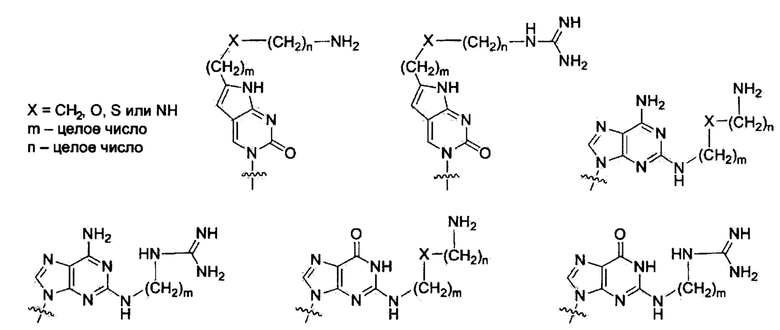
Включение таких модифицированных нуклеиновых оснований в ПНК имеет сходство с ситуациями липофекции. При липофекции молекулы олигонуклеотида с фосфатным остовом скрыты катионными липидными молекулами, такими как липофектамин, и такие липофектамин/олигонуклеотидные комплексы склонны проникать в мембрану довольно легко по сравнению с оголенными молекулами олигонуклеотидов.
Было найдено, что в дополнение к хорошей мембранной проницаемости, эти производные ПНК обладают ультра-сильным сродством к комплементарной нуклеиновой кислоте. Например, введение от 4 до 5 модифицированных нуклеиновых оснований в 11-13-мерные производные ПНК легко дало прирост Tm в 20°С или выше при дуплексном образовании с комплементарной ДНК. Такие производные ПНК очень чувствительны к ошибочному спариванию пары оснований. Ошибочное спаривание пары оснований привело к потере Tm от 11 до 22°С в зависимости от типа модифицированного основания, а также последовательности ПНК.
Малая интерферирующая РНК (siPHK) (small Interfering RNA, siRNA): Малая интерферирующая РНК (siPHK) относится к двухцепочечной РНК из 20-25 пар оснований. [Microbiol. Mol. Biol. Rev. vol 67(4), 657-685 (2003)]. Антисмысловая цепь siPHK каким-то образом взаимодействует с белками, образуя «индуцированный РНК комплекс сайленсинга» (RNA-induced Silencing Complex, RISC). Затем RISC связывается с определенной частью мРНК, комплементарной к антисмысловой цепи siPHK. мРНК, образовавшая комплекс с RISC, подвергается расщеплению. Таким образом, siPHK каталитически индуцирует расщепление своей и целевой мРНК, и, следовательно, подавляет экспрессию белка с помощью мРНК. RISC не всегда связывается с полной комплементарной последовательностью в пределах целевой мРНК, что вызывает опасения, связанные с ненаправленными действиями лекарственного действия siPHK. Как и другие классы олигонуклеотида с остовом ДНК или РНК, siPHK обладает плохой клеточной проницаемостью и, следовательно, имеет тенденцию показывать плохую терапевтическую активность in vitro или in vivo, если должным образом не подготовлена или химически не модифицирована для получения хорошей мембранной проницаемости.
siPHK матриксной металлопротеиназы-1: Сообщалось, что siPHK ММП-1, целенаправленно воздействующая на 19-мерную последовательность РНК в мРНК ММП-1 человека, ингибирует экспрессию мРНК и белка ММП-1 в хондросаркоме человека после липофекции при 100 нМ [J. Orthop.Res. vol 23, 1467-1474 (2005)]. Этот результат может быть полезен при изучении метастаза при раке, связанного с ММП-1, и разработке медицинских препаратов от рака.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Проблема, подлежащая решению
Были разработаны антиоксиданты и функциональный пищевой продукт антиокислительного действия для лечения старения кожи с контролируемой эффективностью и в настоящее время проводится изучение механизма действия. Сообщалось, что хотя siPHK, связанная с ММП-1, ингибирует экспрессию мРНК и белка ММП-1 in vitro, siPHK-ы являются слишком дорогими для производства, и они должны быть доставлены в кожу с помощью транс-дермального введения для надлежащего соответствия указаниям по применению. Поэтому, учитывая значимость металлопротеиназы-1 при старении кожи, очень интересно и необходимо развивать фармацевтику и косметику на основе механизма экспрессии металлопротеиназы-1, что может улучшить состояние кожи и предотвратить ее старение.
Решение проблемы
Данное изобретение предлагает производное пептидной нуклеиновой кислоты, представленное формулой I, или его фармацевтически приемлемую соль:
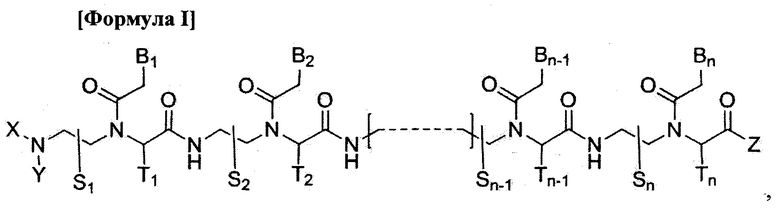
где
n - целое число от 10 до 21;
соединение формулы I обладает по меньшей мере 10-мерным комплементарным перекрыванием с 16-мерной последовательностью пре-мРНК [(5'→3') CAUAUAUGGUGAGUAU] в пре-мРНК ММП-1 человека;
соединение формулы I полностью комплементарно пре-мРНК ММП-1 человека или частично комплементарно пре-мРНК ММП-1 человека с одним или двумя ошибочными спариваниями;
S1, S2, …, Sn-1, Sn, T1, Т2, …, Tn-1 и Tn независимо обозначают атом водорода, атом дейтерия, замещенную или незамещенную алкилгруппу или замещенную или незамещенную арилгруппу;
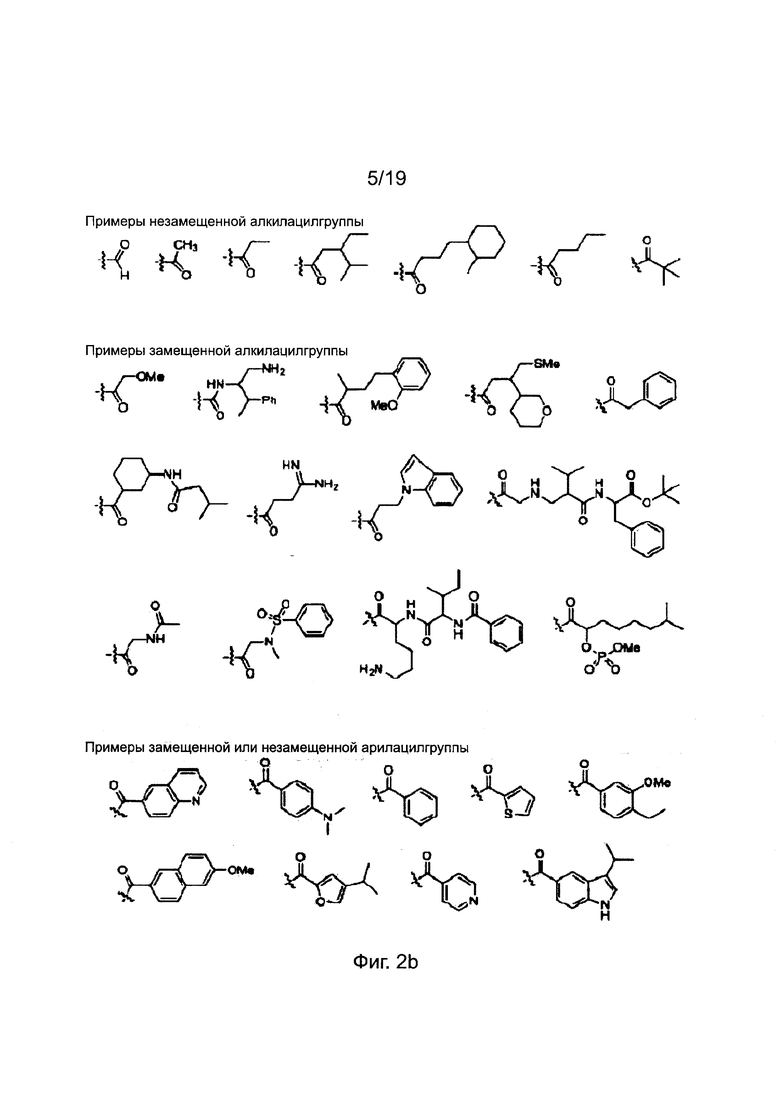
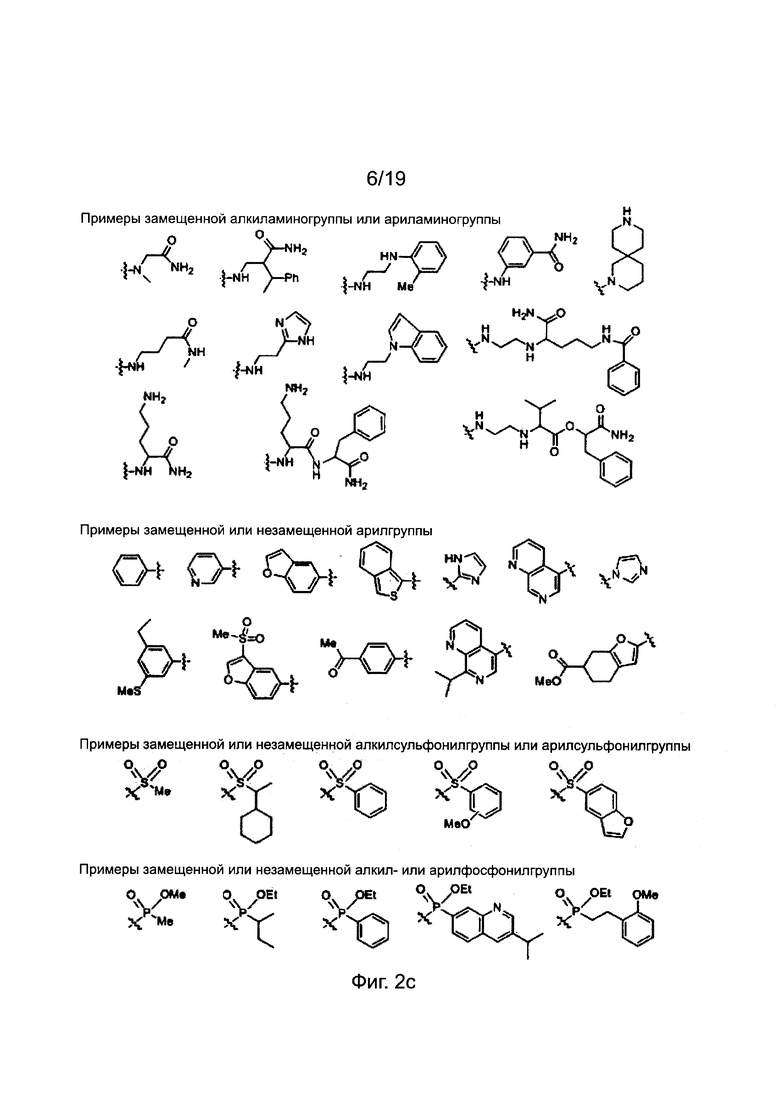
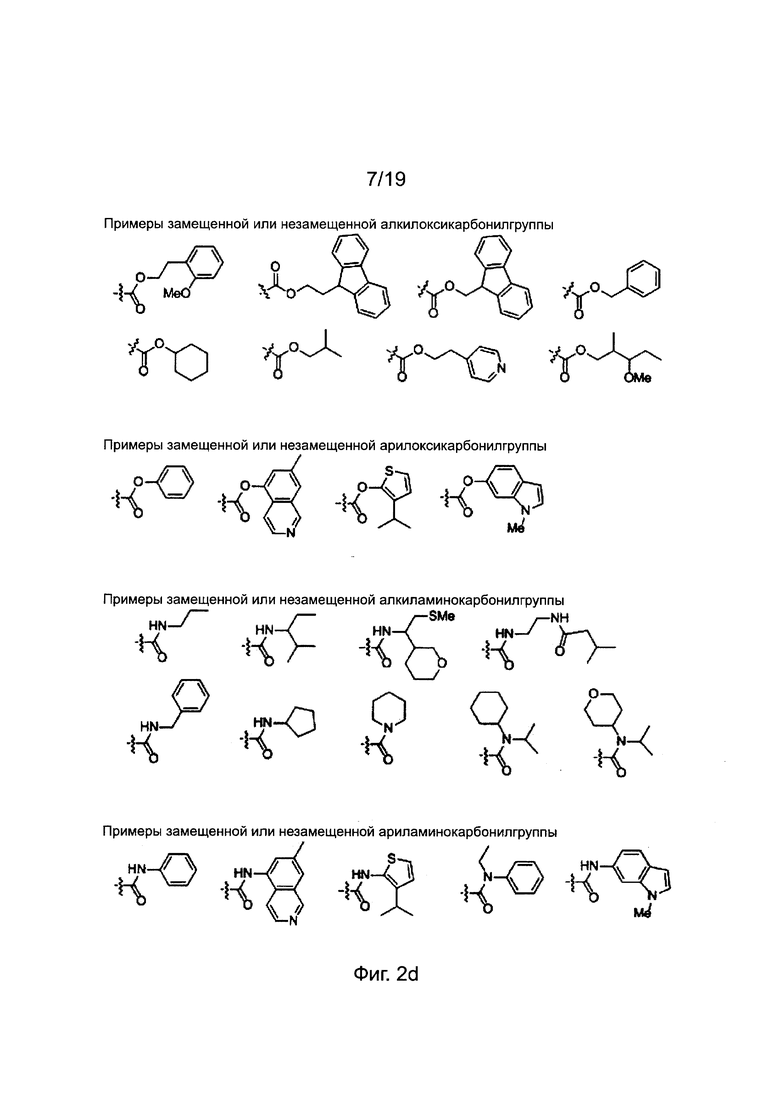
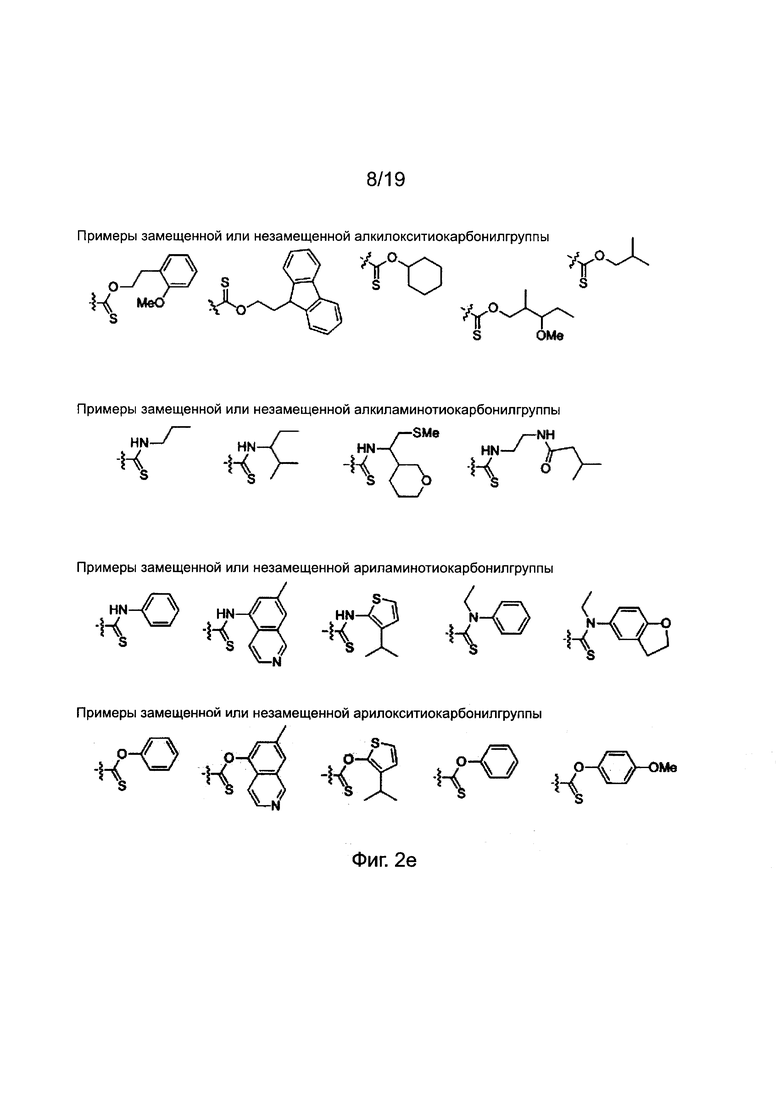
X и Y независимо обозначают атом водорода, атом дейтерия, формилгруппу [Н-С(=O)-], аминокарбонилгруппу [NH2-C(=O)-], аминотиокарбонилгруппу [NH2-C(=S)-], замещенную или незамещенную алкилгруппу, замещенную или незамещенную арилгруппу, замещенную или незамещенную алкилоксисигруппу, замещенную или незамещенную арилоксигруппу, замещенную или незамещенную алкилацилгруппу, замещенную или незамещенную арилацилгруппу, замещенную или незамещенную алкилоксикарбонилгруппу, замещенную или незамещенную арилоксикарбонилгруппу, замещенную или незамещенную алкиламинокарбонилгруппу, замещенную или незамещенную ариламинокарбонилгруппу, замещенную или незамещенную алкиламинотиокарбонилгруппу, замещенную или незамещенную ариламинотиокарбонилгруппу, замещенную или незамещенную алкилокситиокарбонилгруппу, замещенную или незамещенную арилокситиокарбонилгруппу, замещенную или незамещенную алкилсульфонилгруппу, замещенную или незамещенную арилсульфонилгруппу, замещенную или незамещенную алкилфосфонилгруппу или замещенную или незамещенную арилфосфонилгруппу.
Z обозначает атом водорода, атом дейтерия, гидроксигруппу, замещенную или незамещенную алкилоксигруппу, замещенную или незамещенную арилоксигруппу, замещенную или незамещенную аминогруппу, замещенную или незамещенную алкилгруппу или замещенную или незамещенную арилгруппу;
B1, В2, …, Bn-1 и Bn независимо выбраны из природных нуклеиновых оснований, включая аденин, тимин, гуанин, цитозин и урацил, и нуклеиновых оснований не природного происхождения; и
по меньшей мере четыре из B1, В2, …, Bn-1 и Bn независимо выбраны из нуклеиновых оснований не природного происхождения с замещенной или незамещенной аминогруппой, ковалентно связанной с остатком нуклеинового основания.
Соединение формулы I индуцирует пропуск «экзона 5» в пре-мРНК ММП-1 человека, дает сплайс-вариант(ы) мРНК ММП-1 человека, не содержащий(ие) «экзона 5», и, следовательно, пригодно для ингибирования функциональной активности гена, считывающего пре-мРНК ММП-1 человека.
Условие, что «n представляет собой целое число от 10 до 21» буквально означает, что п является целым числом, выбираемым из группы целых чисел 11, 12, 13, 14, 15, 16, 17, 18, 19 и 20.
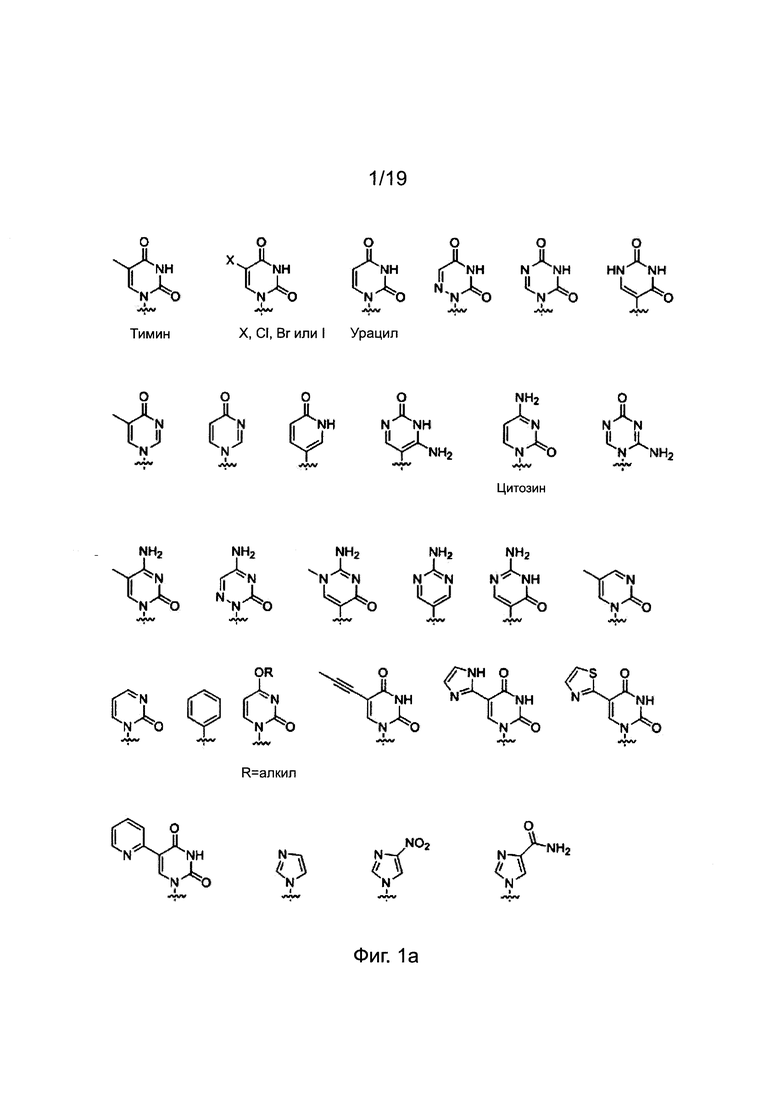
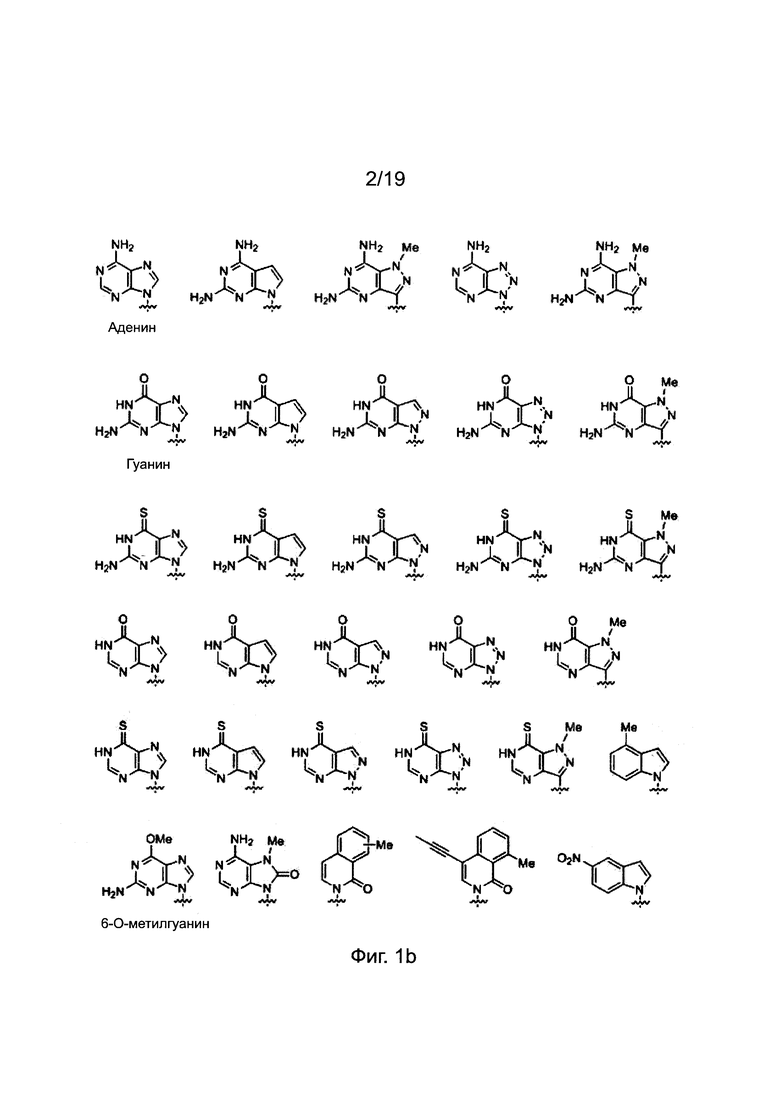
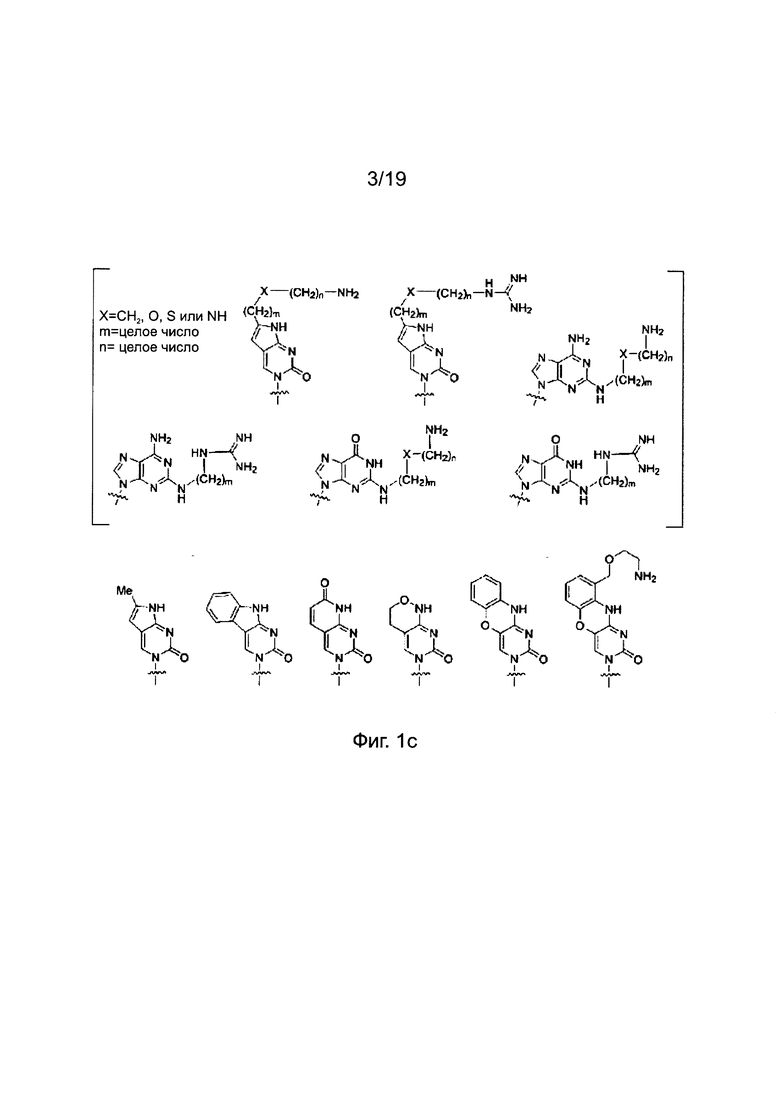
Химические структуры природных нуклеиновых оснований или нуклеиновых оснований не природного происхождения в производном ПНК формулы I подтверждаются примерами на Фиг. 1а-1с. Природные (т.е. встречающиеся в природе) нуклеиновые основания или нуклеиновые основания не природного происхождения (т.е. не встречающиеся в природе), описанные в настоящем изобретении, включают, но не ограничиваются нуклеиновыми основаниями, представленными на Фиг. 1а-1с. Обеспечение таких нуклеиновых оснований не природного происхождения является иллюстрацией разнообразия приемлемых нуклеиновых оснований, и поэтому не должно быть истолковано для ограничения объема настоящего изобретения.
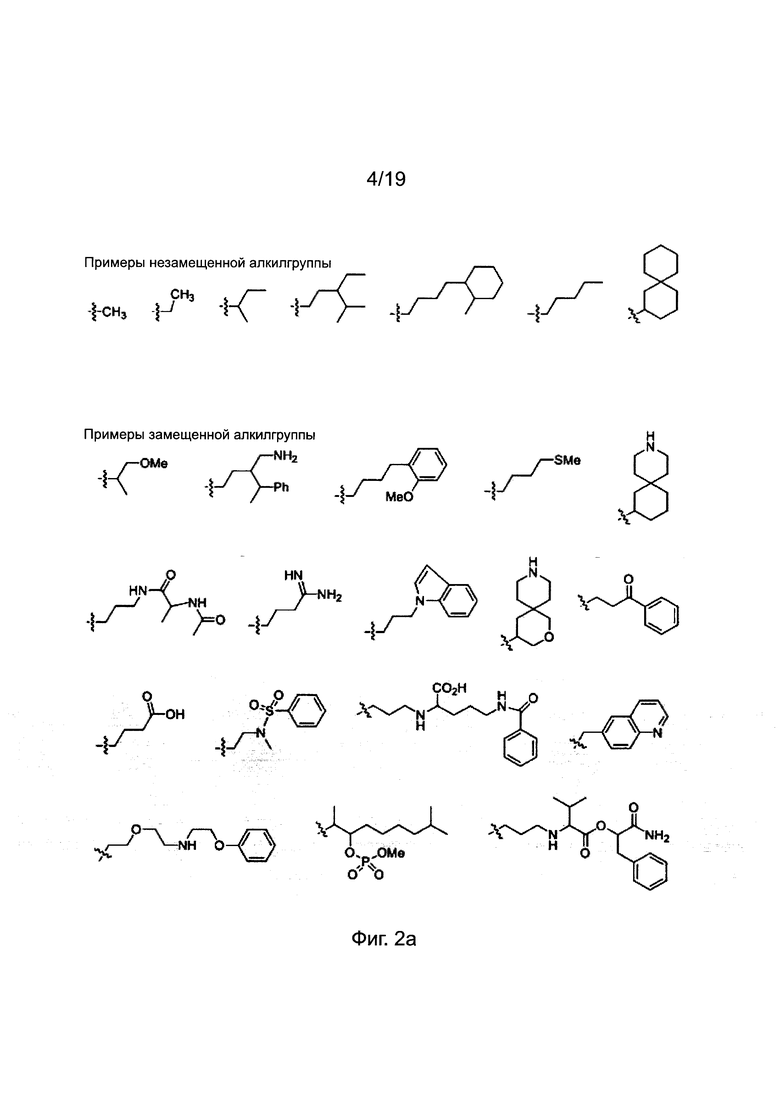
Заместители, выбранные для описания производного ПНК формулы I, приведены на фиг. 2а-2е. Фиг. 2а приводит примеры для замещенных или незамещенных алкилгрупп. Замещенные или незамещенные алкилацилгруппы и замещенные или незамещенные арилацилгруппы приведены на фиг. 2b. Фиг. 2с иллюстрирует примеры для замещенной или незамещенной алкиламиногруппы, замещенной или незамещенной ариламиногруппы, замещенной или незамещенной арилгруппы, замещенной или незамещенной алкилсульфонилгруппы или арилсульфонилгруппы и замещенной или незамещенной алкилфосфонилгруппы или арилфосфонилгруппы. Фиг. 2d приводит примеры для замещенной или незамещенной алкилоксикарбонилгруппы или арилоксикарбонилгруппы, замещенной или незамещенной алкиламинокарбонилгруппы или ариламинокарбонилгруппы. На фиг. 2е приведены примеры для замещенной или незамещенной алкиламинотиокарбонилгруппы, замещенной или незамещенной ариламинотиокарбонилгруппы, замещенной или незамещенной алкилокситиокарбонилгруппы и замещенной или незамещенной арилокситиокарбонилгруппы. Обеспечение таких типичных заместителей является иллюстрацией разнообразия приемлемых заместителей, и поэтому не должно быть истолковано для ограничения объема настоящего изобретения. Специалист в данной области может легко додумать, что олигонуклеотидная последовательность является ключевым фактором для сиквенс-специфичного связывания олигонуклеотида с целевой последовательностью пре-мРНК по сравнению с заместителями в N-конце или С-конце.
Соединение формулы 1 прочно связывается с комплементарной ДНК, пример которой приведен в предшествующем уровне техники [PCT/KR2009/001256]. Дуплекс между производным ПНК формулы I и его полноразмерной комплементарной ДНК или РНК обладает значением Tm слишком высоким для достоверного определения в водном буфере. Соединение ПНК формулы I дает высокие значения Tm с комплементарными ДНКами более короткой длины.
Соединение формулы I комплементарно связывается с 5' сайтом сплайсинга "экзона 5" пре-мРНК ММП-1 человека. [NCBI Reference Sequence: NG_011740]. 16-мерная последовательность [(5'→3') CAUAUAUGGUGAGUAU] охватывает область соединения «экзона 5» и "интрона 5" в пре-мРНК ММП-1 человека, и состоит из 8-мерной от "экзона 5" и 8-мерной от "интрона 5". Таким образом, 16-мерная последовательность пре-мРНК может обычно обозначаться как [(5'→3') CAUAUAUG |gugaguau], где последовательность экзона и интрона определяется соответственно "заглавными" и "строчными" буквами и область соединения экзона-интрона выражается "|". Традиционное обозначение для пре-мРНК дополнительно иллюстрируется 30-мерной последовательностью [(5'→3') UCCAAGCCAUAUAUG |gugaguauggggaaa], охватывающей область соединения "экзона 5" и "интрона 5" в пре-мРНК ММП-1 человека.
Соединение формулы I прочно связывается с целевым 5' сайтом сплайсинга пре-мРНК ММП-1 человека, считанного с гена ММП-1 человека, и препятствует образованию «раннего сплайсомного комплекса» для получения сплайс-варианта(ов) мРНК ММП-1, не содержащего(их) "экзона 5" (пропуск экзона 5).
Сильное сродство РНК позволяет соединению формулы I вызвать пропуск "экзона 5" ММП-1, даже если производное ПНК имеет одно или два ошибочных спаривания с целевым 5' сайтом сплайсинга в пре-мРНК ММП-1. Подобным образом производное ПНК формулы I все еще может индуцировать пропуск "экзона 5" ММП-1 в мутантной пре-мРНК ММП-1, обладающей одним или двумя однонуклеотидными полиморфизмами (single nucleotide polymorphism, SNPs) в целевом сайте сплайсинга.
Соединение формулы I обладает хорошей клеточной проницаемостью и может быть легко доставлено в клетку как «оголенный» олигонуклеотид, примером чего является предшествующий уровень техники [PCT/KR2009/001256], Таким образом, соединение, описанное в настоящем изобретении, индуцирует пропуск "экзона 5" в пре-мРНК ММП-1 и дает сплайс-вариант(ы) мРНК ММП-1, не содержащий(ие) "экзона 5" ММП-1 в клетках, обработанных соединением формулы I как «оголенным» олигонуклеотидом. Соединение формулы I не требует каких-либо средств или составов для доставки в клетку, чтобы мощно индуцировать пропуск целевого экзона в клетках. Соединение формулы I легко индуцирует пропуск "экзона 5" ММП-1 в клетках, обработанных соединением, описанным в настоящем изобретении, как «оголенным» олигонуклеотидом при субфемтомолярной концентрации.
Вследствие хорошей клеточной или мембранной проницаемости, производное ПНК формулы I может местно вводиться как «оголенный» олигонуклеотид для индуцирования пропуска "экзона 5" ММП-1 в коже. Соединению формулы I не требуется лекарственная форма для увеличения трансдермальной доставки в ткань-мишень с точки зрения надлежащей терапевтической или биологической активности. Обычно соединение формулы I растворяют в воде и сорастворителе и наружно или трансдермально вводят при субпикомолярной концентрации, чтобы вызвать желаемую терапевтическую или биологическую активность в коже-мишени. Соединение, описанное в настоящем изобретении, не обязательно должно быть интенсивно или агрессивно вводиться, чтобы вызвать топическую терапевтическую активность. Тем не менее, производное ПНК формулы I может входить в состав с косметическими ингредиентами или адъювантами в качестве наружного крема или лосьона. Такой наружный косметический крем или лосьон может быть пригоден для лечения старения кожи.
Соединение, описанное в настоящем изобретении, может вводиться местно пациенту при терапевтически или биологически эффективной концентрации в диапазоне от 1 аМ до более чем 1 нМ, которая будет варьироваться в зависимости от схемы приема препарата, состояний или ситуаций пациента и так далее.
Производное ПНК формулы I может различным образом входить в состав, включая, но не ограничиваясь инъекциями, назальным спреем, трансдермальным пластырем и так далее. Кроме того, производное ПНК формулы I может вводиться пациенту в терапевтически эффективной дозе и доза введения может варьироваться в зависимости от показания, способа введения, схемы введения доз, состояний или ситуаций пациента и так далее.
Соединение формулы I может использоваться в сочетании с фармацевтически приемлемой кислотой или основанием, включая, но не ограничиваясь, гидроксид натрия, гидроксид калия, соляную кислоту, метансульфоновую кислоту, лимонную кислоту, трифторуксусную кислоту и другие.
Производное ПНК формулы I или его фармацевтически приемлемая соль может вводиться пациенту вместе с фармацевтически приемлемым адъювантом, включая, но не ограничиваясь, лимонную кислоту, соляную кислоту, винную кислоту, стеариновую кислоту, полиэтиленгликоль, полипропиленгликоль, этанол, изопропанол, бикарбонат натрия, дистиллированную воду, консервант(ы) и другие.
Предпочтительным является производное ПНК формулы I или его фармацевтически приемлемая соль:
где
n - целое число от 10 до 21;
соединение формулы I обладает по меньшей мере 10-мерным комплементарным перекрыванием с 16-мерной последовательностью пре-мРНК [(5'→3') CAUAUAUGGUGAGUAU] в пре-мРНК ММП-1 человека;
соединение формулы I полностью комплементарно пре-мРНК ММП-1 человека или частично комплементарно пре-мРНК ММП-1 человека с одним или двумя ошибочными спариваниями;
S1, S2, …, Sn-1, Sn, T1, Т2, …, Tn-1 и Tn независимо обозначают атом водорода, атом дейтерия;
X и Y независимо обозначают атом водорода, атом дейтерия, формилгруппу [Н-С(=O)-], аминокарбонилгруппу [NH2-C(=O)-], аминотиокарбонилгруппу [NH2-C(=S)-], замещенную или незамещенную алкилгруппу, замещенную или незамещенную арилгруппу, замещенную или незамещенную алкилоксигруппу, замещенную или незамещенную арилоксигруппу, замещенную или незамещенную алкилацилгруппу, замещенную или незамещенную арилацилгруппу, замещенную или незамещенную алкилоксикарбонилгруппу, замещенную или незамещенную арилоксикарбонилгруппу, замещенную или незамещенную алкиламинокарбонилгруппу, замещенную или незамещенную ариламинокарбонилгруппу, замещенную или незамещенную алкиламинотиокарбонилгруппу, замещенную или незамещенную ариламинотиокарбонилгруппу, замещенную или незамещенную алкилокситиокарбонилгруппу, замещенную или незамещенную арилокситиокарбонилгруппу, замещенную или незамещенную алкилсульфонилгруппу, замещенную или незамещенную арилсульфонилгруппу, замещенную или незамещенную алкилфосфонилгруппу или замещенную или незамещенную арилфосфонилгруппу;
Z обозначает атом водорода, гидроксигруппу, замещенную или незамещенную алкилоксигруппу, замещенную или незамещенную арилоксигруппу или замещенную или незамещенную аминогруппу;
B1, В2, …, Bn-1 и Bn независимо выбраны из природных нуклеиновых оснований, включая аденин, тимин, гуанин, цитозин и урацил, и нуклеиновых оснований не природного происхождения;
по меньшей мере четыре из B1, В2, …, Bn-1 и Bn независимо выбраны из нуклеиновых оснований не природного происхождения, представленных формулой II, формулой III или формулой IV:
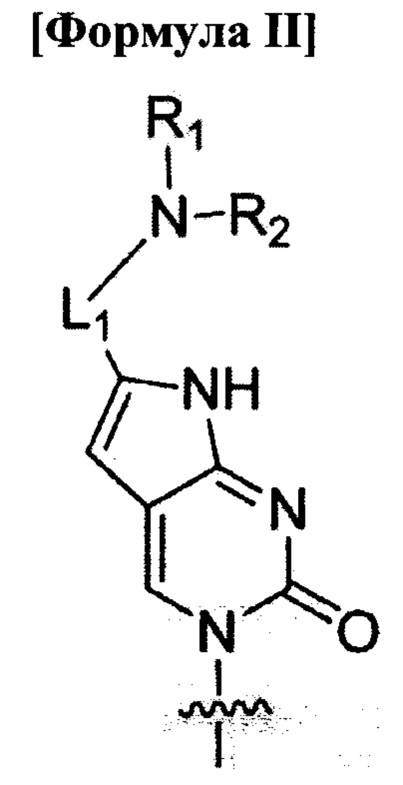
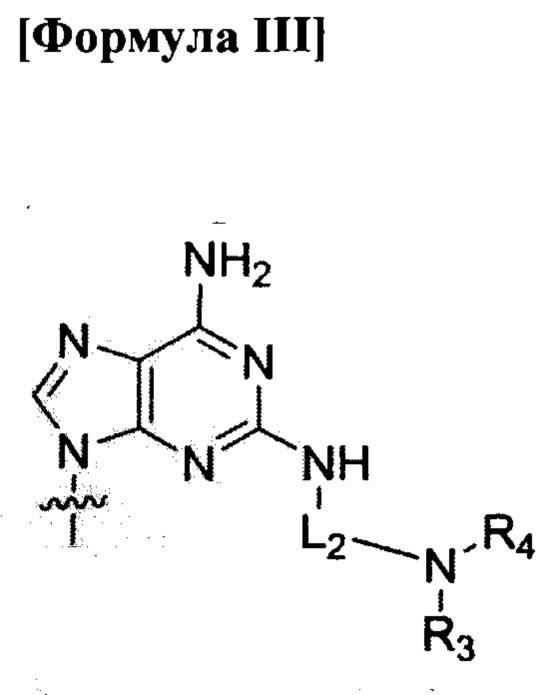
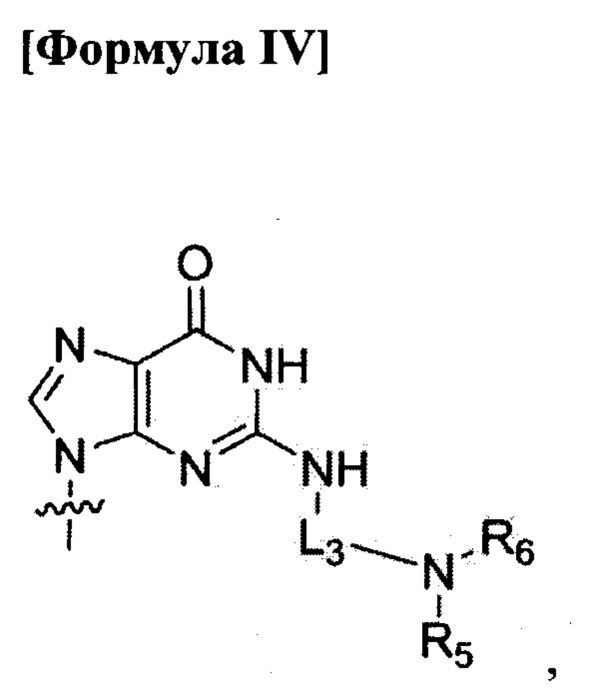
где
R1, R2, R3, R4, R5 и R6 независимо выбраны из атома водорода и замещенной или незамещенной алкилгруппы;
L1, L2 и L3 являются ковалентным линкером, представленным формулой V, ковалентно соединяющий основную аминогруппу с остатком нуклеинового основания:
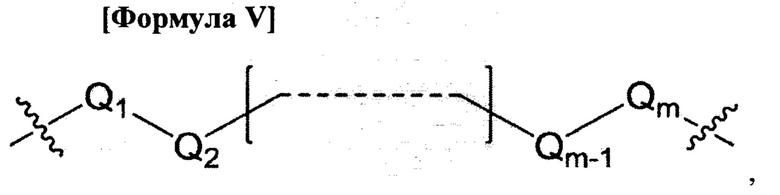
Где
Q1 и Qm представляют собой замещенную или незамещенную метиленгруппу (-СН2-) и Qm непосредственно связывается с основной аминогруппой;
Q2, Q3, …, и Qm-1 независимо выбраны из замещенной или незамещенной метиленгруппы, атома кислорода (-O-), атома серы (-S-) и замещенной или незамещенной аминогруппы [-N(H)- или -N(заместитель)-]; и
m - целое число от 1 до 15.
Представляет интерес олигомер ПНК формулы I или его фармацевтически приемлемая соль: где
n - целое число от 11 до 16;
соединение формулы I обладает по меньшей мере 10-мерным комплементарным перекрыванием с 16-мерной последовательностью пре-мРНК [(5'→3') CAUAUAUGGUGAGUAU] в пре-мРНК ММП-1 человека;
соединение формулы I полностью комплементарно пре-мРНК ММП-1 человека;
S1, S2, …, Sn-1, Sn, T1, Т2, …, Tn-1 и Tn представляют собой атом водорода;
X и Y независимо обозначают атом водорода, замещенную или незамещенную алкилацилгруппу или замещенную или незамещенную алкилоксикарбонилгруппу;
Z обозначает замещенную или незамещенную аминогруппу;
B1, В2, …, Bn-1 и Bn независимо выбраны из природных нуклеиновых оснований, включая аденин, тимин, гуанин, цитозин и урацил, и нуклеиновых оснований не природного происхождения;
по меньшей мере пять из В1, В2, …, Bn-1 и Bn независимо выбраны из нуклеиновых оснований не природного происхождения, представленных формулой II, формулой III или формулой IV;
R1, R2, R3, R4, R5 и R6 являются атомом водорода;
Q1 и Qm представляют собой метиленгруппу и Qm непосредственно связывается с основной аминогруппой;
Q2, Q3, … и Qm-1 независимо выбраны из метиленгруппы и атома кислорода; и
m - целое число от 1 до 9.
Представляет интерес производное ПНК формулы I или его фармацевтически приемлемая соль:
где
n - целое число от 11 до 16;
соединение формулы I обладает по меньшей мере 10-мерным комплементарным перекрыванием с 16-мерной последовательностью пре-мРНК [(5'→3') CAUAUAUGGUGAGUAU] в пре-мРНК ММП-1 человека;
соединение формулы I полностью комплементарно пре-мРНК ММП-1 человека;
S1, S2, …, Sn-1, Sn, T1, T2, …, Tn-1 и Tn представляют собой атом водорода; X представляет собой атом водорода;
Y обозначает замещенную или незамещенную алкилоксикарбонилгруппу;
Z обозначает замещенную или незамещенную аминогруппу;
B1, В2, …, Bn-1 и Bn независимо выбраны из природных нуклеиновых оснований, включая аденин, тимин, гуанин, цитозин и урацил, и нуклеиновых оснований не природного происхождения;
по меньшей мере пять из B1, В2, …, Bn-1 и Bn независимо выбраны из нуклеиновых оснований не природного происхождения, представленных формулой II, формулой III или формулой IV;
R1, R2, R3, R4, R5 и R6 являются атомами водорода;
L1 обозначает-(СН2)2-O-(СН2)2-группу,-CH2-O-(CH2)2-группу,
-СН2-O-(СН2)3-группу, -СН2-O-(СН2)4-группу или -СН2-O-(СН2)5-группу с правым концом, непосредственно связанным с основной аминогруппой; и
L2 и L3 независимо выбраны из -(СН2)2-O-(СН2)2-группы, -(СН2)3-O-(СН2)2-группы, -(СН2)2-O-(СН2)3-группы, -(СН2)2-группы, -(СН2)3-группы, -(СН2)4-группы, -(CH2)5-группы, -(СН2)6-группы, -(СН2)7-группы и -(СН2)8-группы с правым концом, непосредственно связанным с основной аминогруппой.
Представляет интерес производное ПНК формулы I, которое является-соединением, приведенным ниже (АСО 1, антисмысловой олигонуклеотид 1), или его фармацевтически приемлемая соль:
(N→C) Fethoc-TA(6)C-TCA(6)-CC(1O2)A(6)-TA(6)T-A(6) T-NH2,
где
А, Т и С представляют собой мономеры ПНК с природным нуклеиновым основанием аденином, тимином и цитозином, соответственно;
C(pOq) и А(р) представляют собой мономеры ПНК с нуклеиновым основанием не природного происхождения, представленным формулой VI и формулой VII, соответственно;


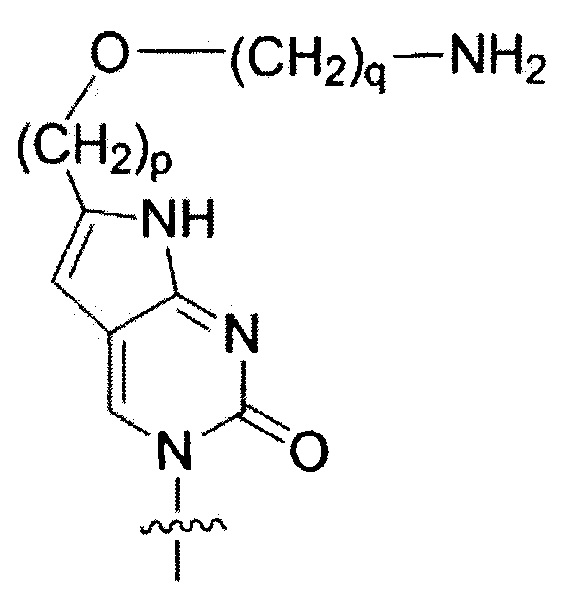
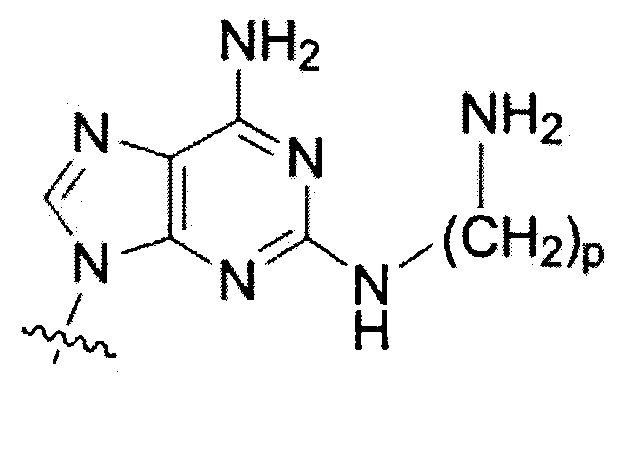
где
p и q - целые числа; и р равно 1 или 6 и q равно 2 в АСО 1; и,
" Fethoc-" представляет собой сокращение для "[2-(9-фторенил)этил-1-окси]карбонилгруппы" и "-NH2" - для незамещенной "аминогруппы".
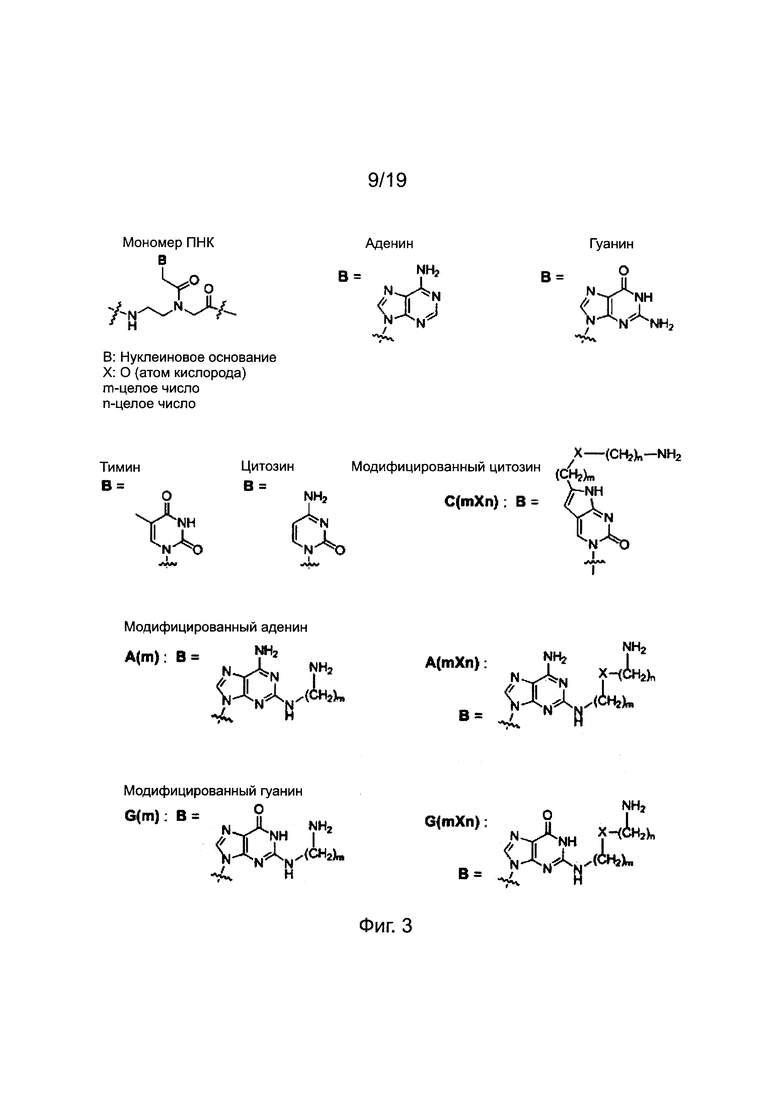
Фиг. 3 в совокупности и недвусмысленно представляет химические структуры для мономеров ПНК, сокращенных как A, G, Т, С, C(pOq), А(р), A(pOq), G(p) и G(pOq). Как обсуждалось в предшествующем уровне техники [PCT/KR2009/001256], C(pOq) рассматривается как мономер ПНК с "модифицированным цитозином" вследствие его гибридизации в "гуанин". А(р) и A(pOq) принимаются за мономеры ПНК с "модифицированным аденином" вследствие их гибридизации в "тимин".
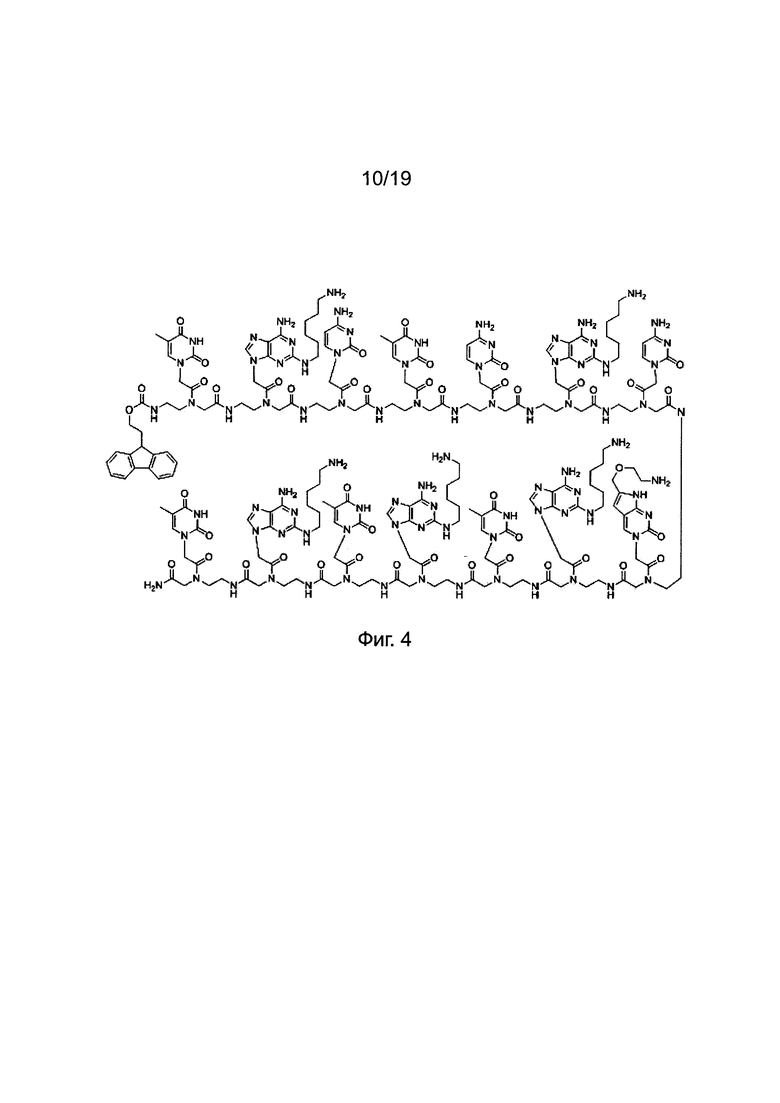
Для того, чтобы проиллюстрировать сокращения, применяемые для таких производных ПНК, химическая структура АСО 1 приведена на Фиг. 4.
АСО 1 эквивалентен последовательности ДНК "(5'→3') ТАС-ТСА-ССА-ТАТ-АТ" для комплементарного связывания с пре-мРНК. 14-мерная ПНК имеет 14-мерное комплементарное перекрывание с 14-мерной последовательностью, обозначенной "жирным шрифтом" и "подчеркнутой" в 30-мерной последовательности РНК [(5'→3')
UCCAAGCCAUAUAUG |gugaguauggggaaa], охватывающей область соединения "экзона 5" и "интрона 5" в пре-мРНК ММП-1 человека.
Одним из аспектов настоящего изобретения является способ лечения заболеваний или состояний, связанных с транскрипцией гена ММП-1 человека, включающий введение пациенту производного пептидной нуклеиновой кислоты в соответствии с настоящим изобретением или его фармацевтически приемлемой соли.
Одним из аспектов настоящего изобретения является способ лечения старения кожи, включающий введение пациенту производного пептидной нуклеиновой кислоты в соответствии с настоящим изобретением или его фармацевтически приемлемой соли.
Одним из аспектов настоящего изобретения является фармацевтическая композиция для лечения заболеваний или состояний, связанных с транскрипцией гена ММП-1 человека, включающая производное пептидной нуклеиновой кислоты в соответствии с настоящим изобретением или его фармацевтически приемлемую соль.
Одним из аспектов настоящего изобретения является косметическая композиция для лечения заболеваний или состояний, связанных с транскрипцией гена ММП-1 человека, включающая производное пептидной нуклеиновой кислоты в соответствии с настоящим изобретением или его фармацевтически приемлемую соль.
Одним из аспектов настоящего изобретения является фармацевтическая композиция для лечения старения кожи, включающая производное пептидной нуклеиновой кислоты в соответствии с настоящим изобретением или его фармацевтически приемлемую соль.
Одним из аспектов настоящего изобретения является косметическая композиция для лечения старения кожи, включающая производное пептидной нуклеиновой кислоты в соответствии с настоящим изобретением или его фармацевтически приемлемую соль.
Заболевания или состояния, связанные с транскрипцией гена ММП-1 человека, можно лечить введением производного ПНК формулы I или его фармацевтически приемлемой соли.
Заболевания или состояния, связанные со старением кожи, можно лечить введением производного ПНК формулы I или его фармацевтически приемлемой соли.
Краткое пояснение фигур
Фиг: 1а-1с. Примеры природных нуклеиновых оснований или нуклеиновых оснований не природного происхождения (модифицированных), выбираемых для производного пептидной нуклеиновой кислоты формулы I.
Фиг, 2а-2е. Примеры заместителей, выбираемых для производного пептидной нуклеиновой кислоты формулы I.
Фиг. 3. Химические структуры мономеров ПНК с природным или модифицированным нуклеиновым основанием.
Фиг. 4. Химическая структура "АСО 1".
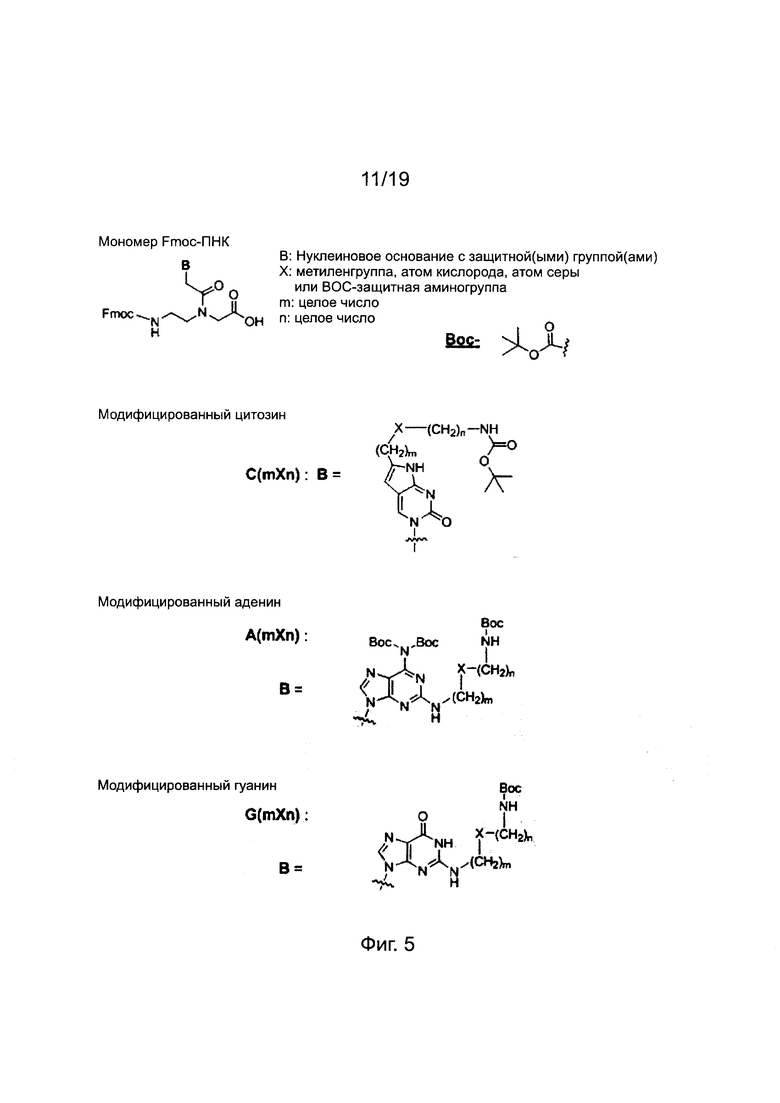
Фиг. 5. Химические структуры мономеров Fmoc-ПНК, используемых для синтеза производных ПНК данного изобретения.
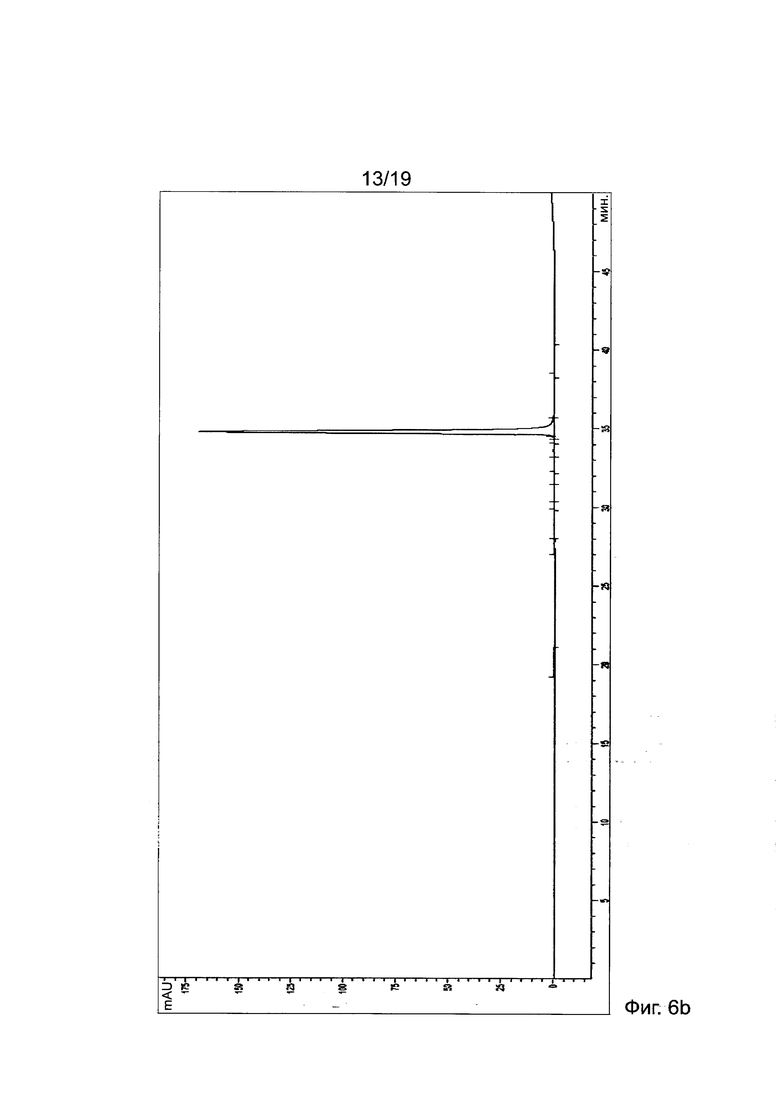
Фиг. 6а-6b. С18-обращенно-фазовые ВЭЖХ хроматограммы"АСО 1" до и после ВЭЖХ очистки, соответственно.
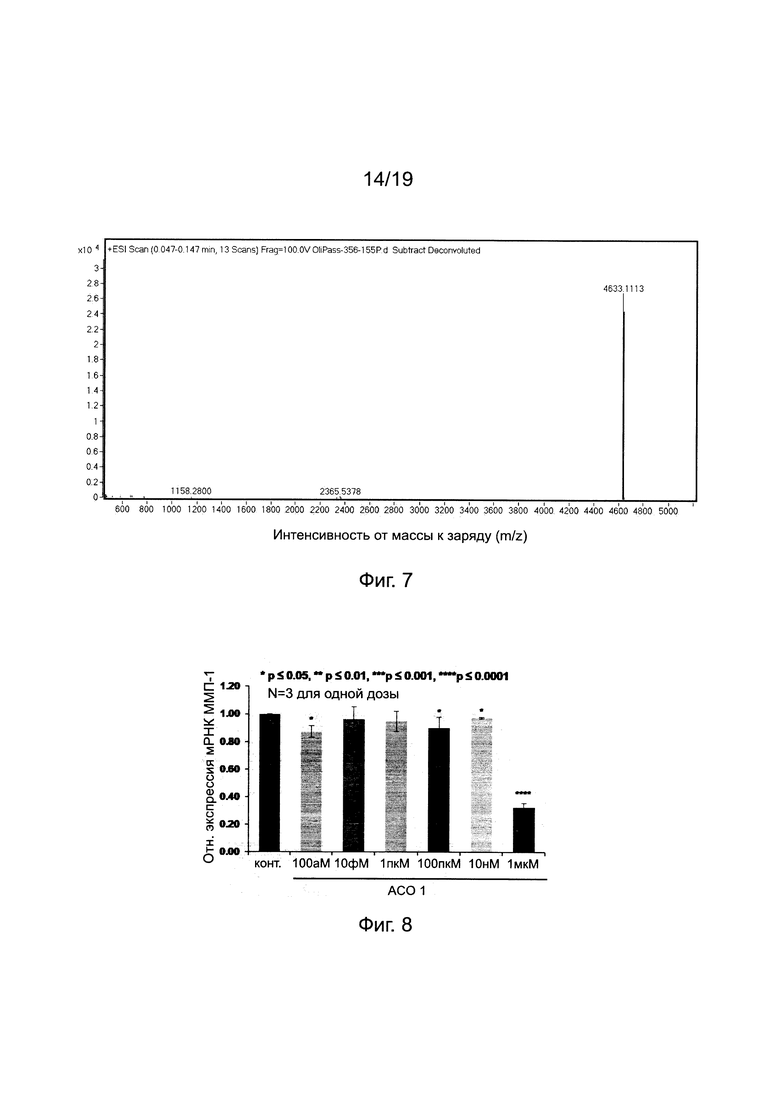
Фиг. 7. ESI-TOF масс-спектр "АСО 1", очищенного C18-RP препаративной ВЭЖХ.
Фиг. 8. Ингибирование образования мРНК ММП-1 с помощью "АСО 1" в HDF (HDF - human dermal fibroblasts, дермальные фибробласты человека) (количественная ПЦР с детекцией в реальном времени).
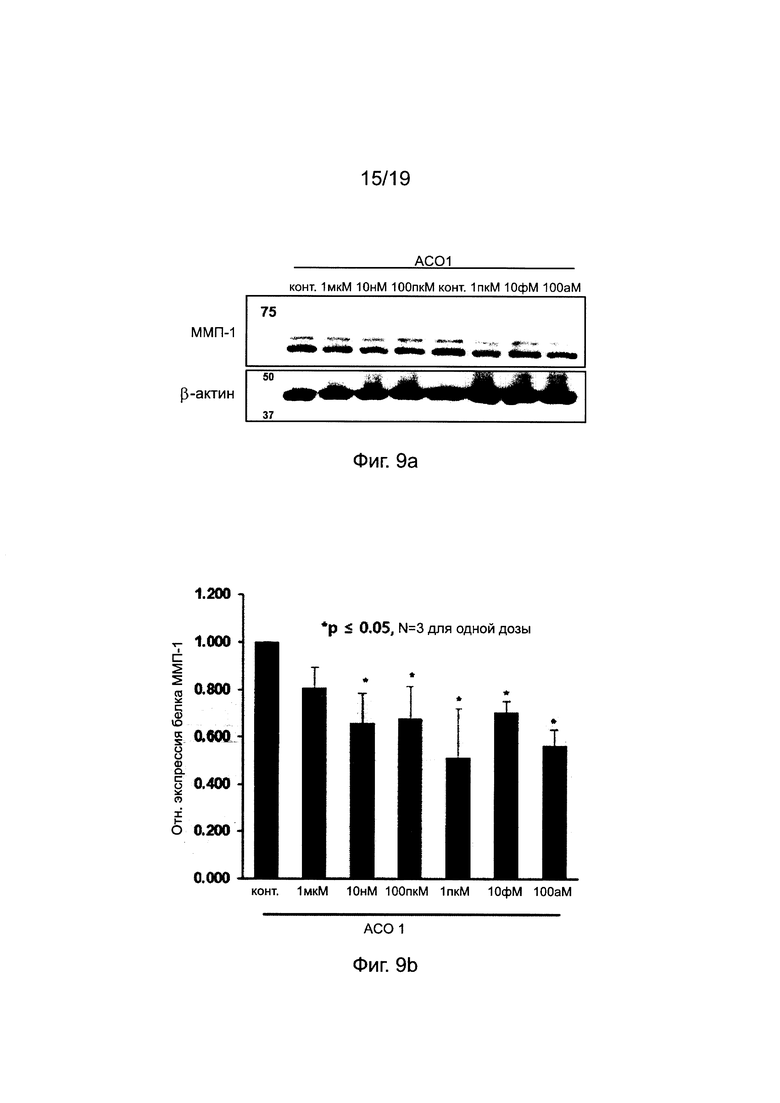
Фиг. 9а-9b. Ингибирование экспрессии белка ММП-1 с помощью "АСО 1" в HDF (вестерн-блоттинг и график изменений уровней экспрессии белка).
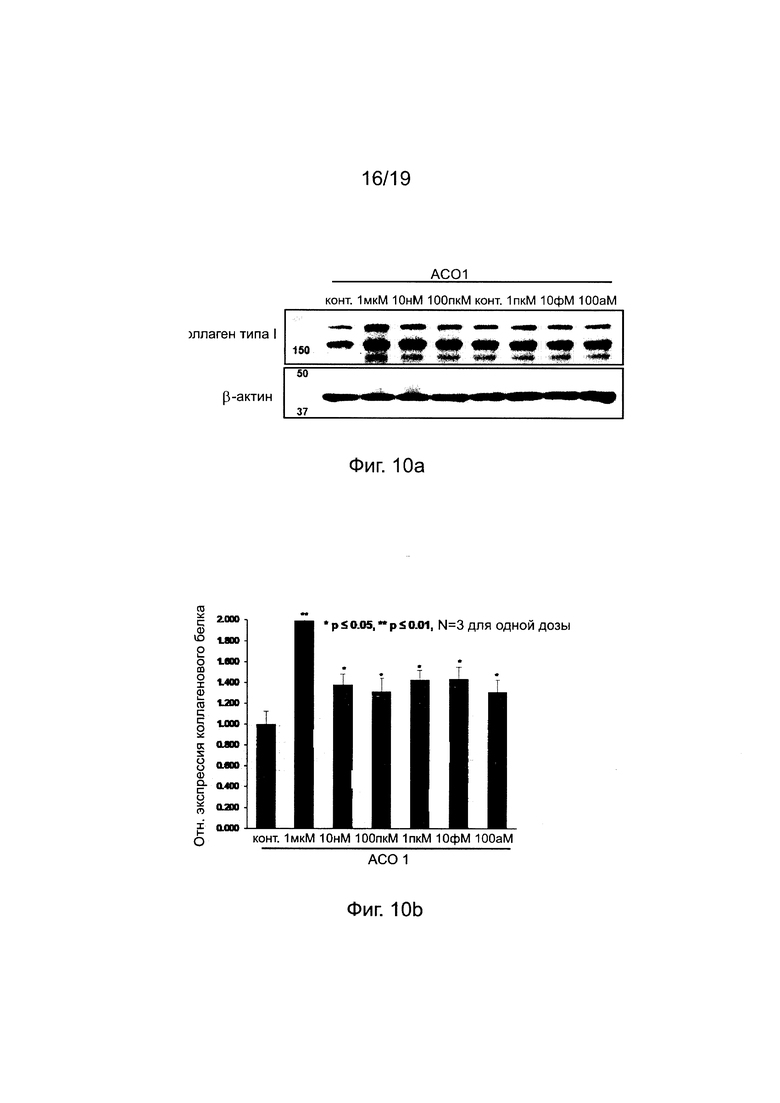
Фиг. 10а-10b. Увеличение экспрессии коллагенового белка с помощью "АСО 1" в HDF (вестерн-блоттинг и график изменений уровней экспрессии белка).
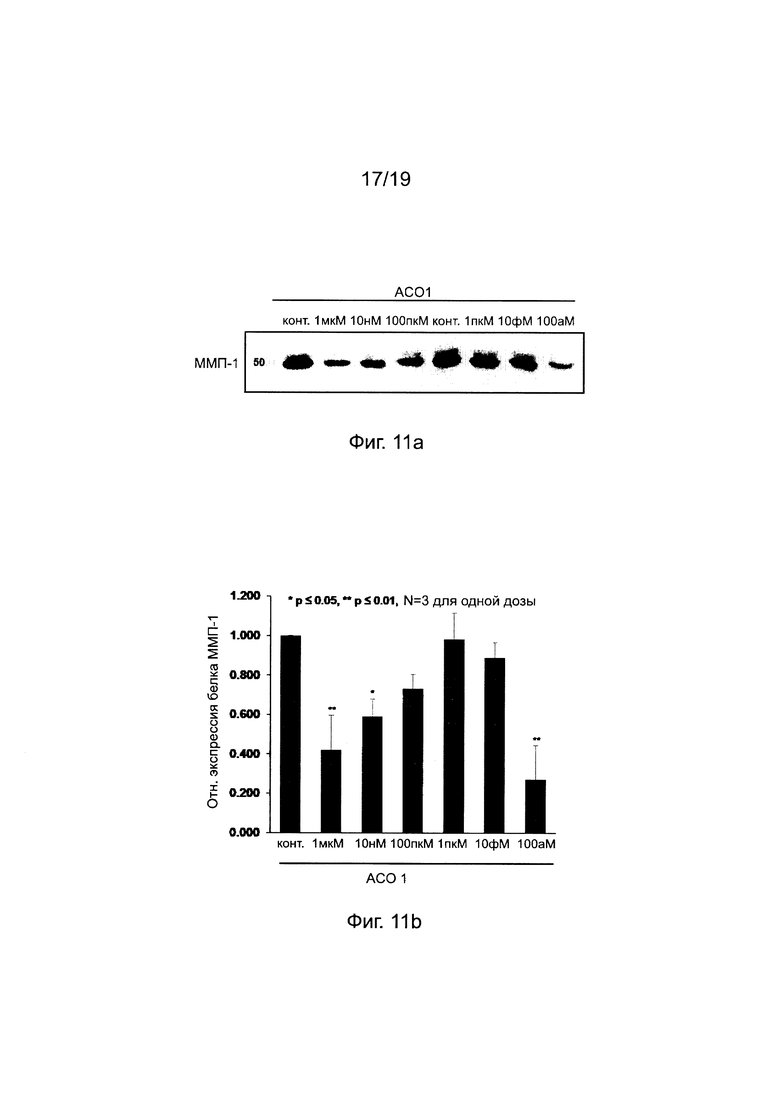
Фиг. 11a-11b. Ингибирование экспрессии белка ММП-1 с помощью "АСО 1" во внеклеточной жидкости (вестерн-блоттинг и график изменений уровней экспрессии белка).
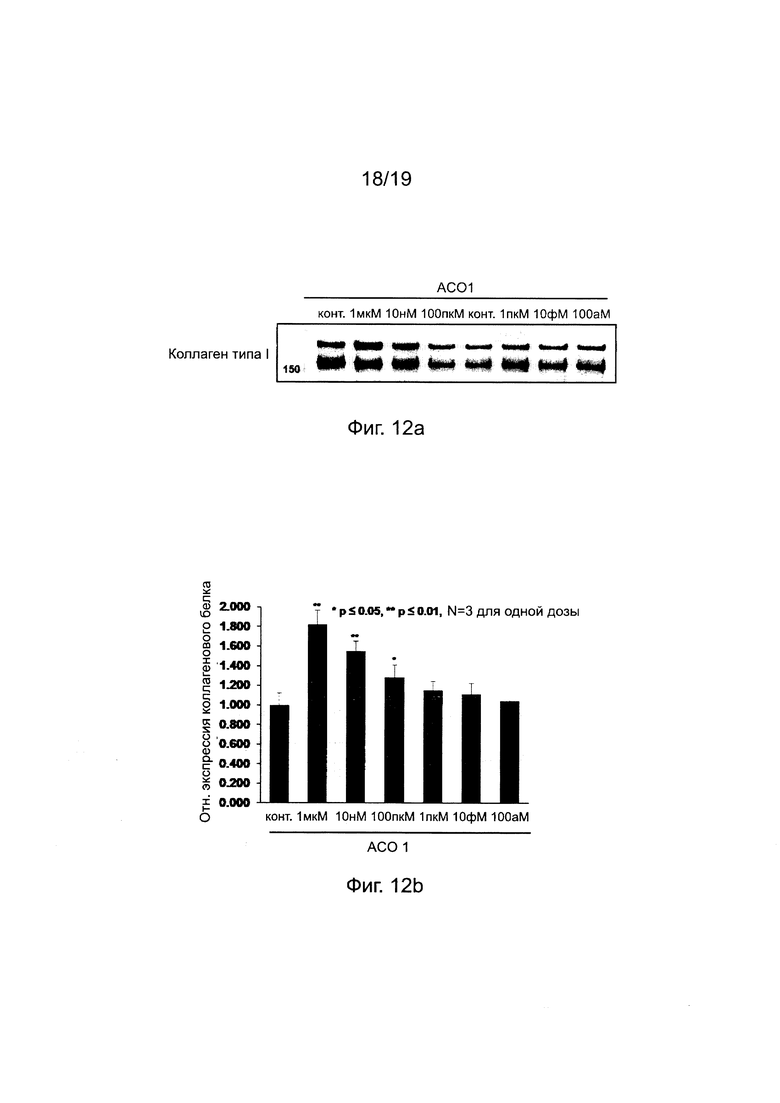
Фиг. 12а-12b. Увеличение экспрессии коллагенового белка с помощью "АСО 1" во внеклеточной жидкости (вестерн-блоттинг и график изменений уровней экспрессии белка).
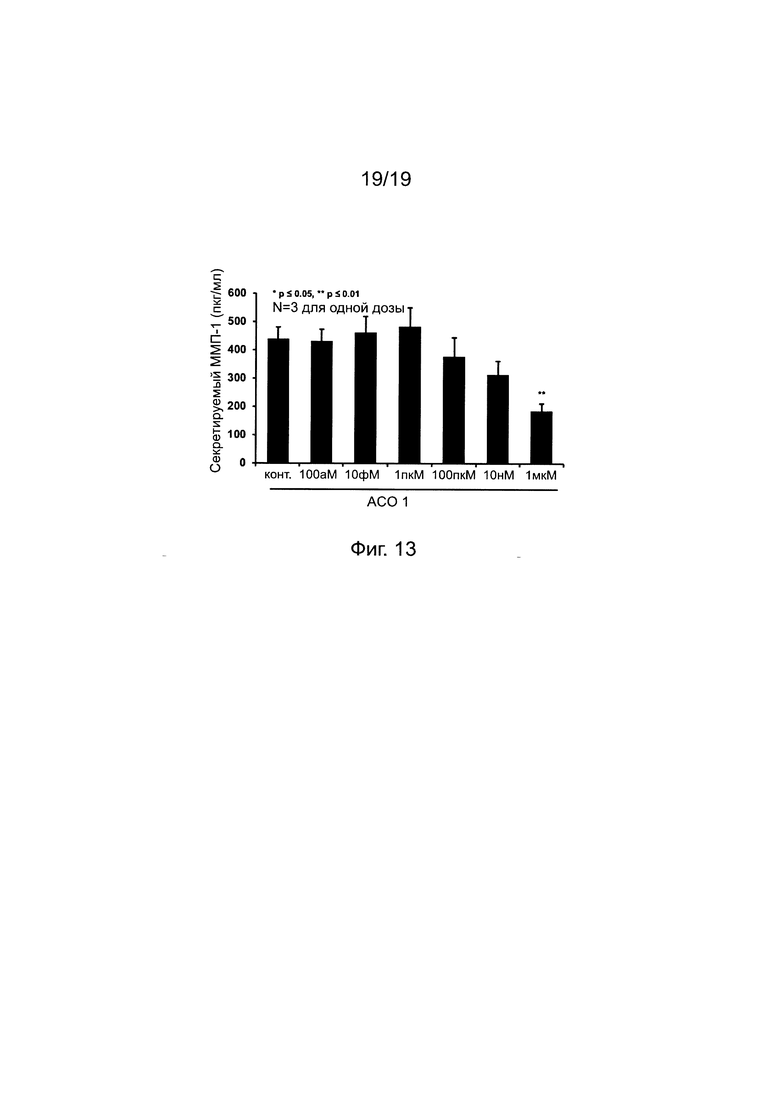
Фиг. 13. Ингибирование экспрессии белка ММП-1 с помощью "АСО 1" во внеклеточной жидкости (ELISA).
Лучший вариант осуществления изобретения
Общие методики приготовления олигомеров ПНК
Олигомеры ПНК синтезировали с помощью твердофазного пептидного синтеза (solid phase peptide synthesis, SPPS), основанного на Fmoc-химии в соответствии со способом, раскрытым в предшествующем уровне техники [US6,133,444; WO96/40685] с незначительными, но требуемыми изменениями. Твердая подложка, применяемая в данном исследовании, представляла собой амидную смолу H-Rink Amide-ChemMatrix, закупленную в PCAS BioMatrix Inc. (Квебек, Канада). Мономеры Fmoc-ПНК с модифицированным нуклеиновым основанием синтезировали, как описано в предшествующем уровне техники [PCT/KR 2009/001256] или с незначительными изменениями. Для синтеза производных ПНК настоящего изобретения использовались конкретные мономеры Fmoc-ПНК с модифицированным нуклеиновым основанием и мономеры Fmoc-ПНК с нуклеиновым основанием природного происхождения. Олигомеры ПНК очищали с помощью С18-обращено-фазовой ВЭЖХ (вода/ацетонитрил или вода/метанол с 0,1% TFA) и характеризовали масс-спектрометрией, включая ESI/TOF/MS.
Схема 1 иллюстрирует типичный цикл удлинения мономеров, принятый в SPPS данного исследования, и синтетические детали (тонкости) приведены ниже. Однако, для специалиста в данной области имеется много незначительных изменений, очевидно, возможных при эффективном проведении таких реакций SPPS на автоматическом пептидном синтезаторе или неавтоматическом пептидном синтезаторе. Каждая стадия реакции в схеме 1 кратко представлена, как изложено ниже.
[Схема 1]
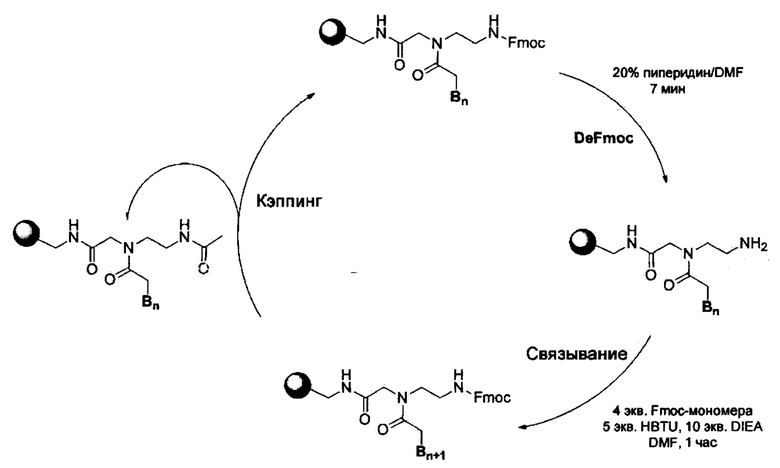
[DeFmoc] Смолу встряхивали в 1,5 мл 20% пиперидина/DMF в течение 7 мин, и DeFmoc раствор отфильтровывали. Смолу промывали в течение 30 сек последовательно каждый раз 1,5 мл МС, 1,5 мл DMF, 1,5 мл МС, 1,5 мл DMF и 1,5 мл МС. Полученные свободные амины на твердой подложке тотчас подвергали связыванию с мономером Fmoc-ПНК.
[Связывание с мономером Fmoc-ПНК] Свободные амины на твердой подложке связывались с мономером Fmoc-ПНК следующим образом. 0,04 ммолей мономера ПНК, 0,05 ммолей HBTU и 10 ммолей DIEA инкубировали в течение 2 мин в 1 мл безводного DMF и прибавляли к смоле со свободными аминами. Раствор смолы встряхивали в течение 1 часа и реакционную смесь фильтровали. Затем смолу промывали 30 сек последовательно каждый раз 1,5 мл МС, 1,5 мл DMF и 1,5 мл МС. Химические структуры мономеров Fmoc-ПНК с модифицированным нуклеиновым основанием, используемом в данном изобретении, представлены на фиг. 6. Мономеры Fmoc-ПНК с модифицированным нуклеиновым основанием, представленные на фиг. 6, должны быть приняты в качестве примеров и, следовательно, не должны рассматриваться для ограничения объема данного изобретения. Специалист в данной области может легко догадаться о целом ряде изменений в мономерах Fmoc-ПНК для синтеза производного ПНК формулы I.
[Кэпирование] После реакции связывания непрореагированные свободные амины копировали при встряхивании в течение 5 минут в 1,5 мл раствора кэпирования (5% уксусный ангидрид и 6% 2,6-лейтидин в DMF). Затем раствор кэпирования отфильтровывали и промывали в течение 30 сек последовательно каждый раз 1,5 мл МС, 1,5 мл DMF и 1,5 мл МС.
[Введение группы "Fethoc-" в N-конец] Группу "Fethoc-" вводили в N-конец при взаимодействии свободного амина на смоле с "Fethoc-OSu" при основных условиях связывания. Химическая структура "Fethoc-OSu" [CAS No. 179337-69-0, C20H17NO5, М.В.351,36] приведена, как указано ниже.
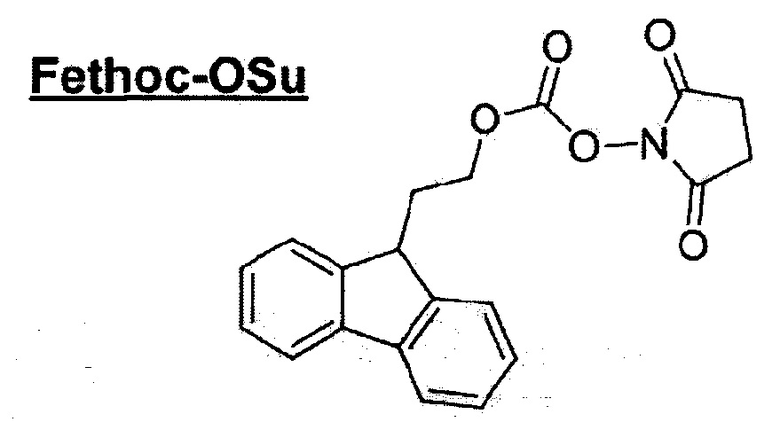
[Отщепление смолы] Олигомеры ПНК, связанные со смолой, отщепляли от смолы встряхиванием в течение 3 часов в 1,5 мл отщепляющего раствора (2,5% триизопропилсилана и 2,5% воды в трифторуксусной кислоте). Смолу отфильтровывали и фильтрат концентрировали при пониженном давлении. Полученный остаток растирали в порошок с помощью диэтилового эфира и полученный осадок собирали с помощью фильтрации для очистки обращено-фазовой ВЭЖХ.
[Анализ ВЭЖХ и очистка] После отщепления смолы технический продукт производного ПНК очищали с помощью С18-обращено-фазовой ВЭЖХ, элюируя водой/ацетонитрилом или водой/метанолом (градиентный метод), содержащих 0,1% TFA. Фиг. 6a и 6b представляют типичные хроматограммы ВЭЖХ для "АСО 1" до и после очистки ВЭЖХ, соответственно.
Синтетические примеры для производного ПНК формулы I
Для того, чтобы комплементарно целенаправленно воздействовать на 5' сайт сплайсинга "экзона 5" в пре-мРНК ММП-1 человека, производное ПНК данного изобретения получали согласно методикам синтеза, приведенным выше, или с незначительными изменениями. Предоставление таких производных ПНК, целенаправленно воздействующих на пре-мРНК ММП-1 человека, является примером производных ПНК формулы I, и не должно быть истолковано для ограничения объема данного изобретения.

Таблица 1 приводит производное ПНК, комплементарно целенаправленно воздействующее на 5' сайт сплайсинга "экзона 5" в пре-мРНК ММП-1 человека, считанной с гена ММП-1 человека [Стандартная/эталонная последовательность NCBI (Национального центра биотехнологической информации): NG 011740], а также данные по структурному исследованию с помощью масс-спектрометрии. Предоставление производного пептидной нуклеиновой кислоты в таблице 1 является примером производного ПНК формулы I, и не должно быть истолковано для ограничения объема данного изобретения.
"АСО 1" имеет 14-мерное комплементарное перекрывание с 14-мерной последовательностью, обозначенной "жирным шрифтом" и "подчеркнутой" в пределах 30-мерной последовательности РНК [(5'→3')
UCCAAGCCAUAUAUG |gugaguauggggaaa], охватывающей область соединения "экзона 5" и "интрона 5" в пре-мРНК ММП-1 человека. Таким образом, "АСО 1" имеет 7-мерное перекрывание с "экзоном 5" и 7-мерное перекрывание с "интроном 5" в пределах пре-мРНК ММП-1 человека.
Связывающая аффинность "ACQ 1" для комплементарной ДНК
Величины Tm определяли на спектрометре с УФ и видимой областями спектра следующим образом. Смешанный раствор 4 мкМ олигомера ПНК и 4 мкМ комплементарной 14-мерной ДНК в 4 мл водного буфера (рН 7,16, 10 мМ фосфата натрия, 100 мМ NaCl) в 15 мл полипропиленовой пробирке фирмы Falcon инкубировали при 90°С в течение минуты и медленно охлаждали до обычной температуры. Затем раствор переносили в 3 мл кварцевую УФ кювету, снабженную герметичной крышкой, и подвергали измерению Tm при 260 нм на спектрофотометре (Agilent 8453) с УФ и видимой областями спектра. Изменения поглощения при 260 нм регистрировали с повышением температуры кюветы либо на 0,5, либо 1,0°С в минуту. Из кривой абсорбции от температуры, температуру, показывающую самую высокую интенсивность абсорбции, считывали как температуру плавления Tm от ПНК до ДНК. 14-мерные комплементарные ДНК(ы) для измерения Tm приобретали от Bioneer (www.bioneer.com, Dajeon, Республика Корея) и использовали без дополнительной очистки.
"АСО 1" показал значение Tm в 72,67°С для дуплекса с 14-мерной комплементарной ДНК.
Примеры биологических активностей производных ПНК формулы I
Производные ПНК в данном изобретении оценивали in vitro на антисмысловые активности ММП-1 в дермальных фибробластах человека (human dermal fibroblasts, HDF) с помощью количественной полимеразной цепной реакции с детекцией в реальном времени (real-time quantitative polymerase chain reaction, RT qPCR) и т.д.. Биологические примеры предусмотрены в качестве примеров для иллюстрации биологических профилей производных ПНК формулы I, и поэтому не должны быть истолкованы для ограничения объема нынешнего изобретения.
Пример 1. Ингибирование образования мРНК ММП-1 с помощью "АСО 1" bHDF.
"АСО 1" оценивали с помощью вестерн-блоттинга по его способности подавлять образование мРНК ММП-1 в HDF, как описано ниже.
[Культура клеток и обработка АСО] Клетки HDF поддерживали в базальной среде для фибробластов (АТСС PCS-201-030), подкрепленной набором роста фибробластов с низким содержанием сыворотки (АТСС PCS-201-041) и 1% стрептомицина/пенициллина, которую выращивали при 37°С и при условии 5% СО2. HDF клетки (3×105), стабилизированные в течение 24 часов в 60 мм чашке для культивирования, инкубировали в течение 24 часов с "АСО 1" при 0 (негативный контроль) и 100 аМ до 1 мкМ.
[Экстракция РНК и синтез кДНК] Суммарную РНК экстрагировали с помощью RNeasy Mini kit (Qiagen, Cat. No. 714106) согласно инструкциям производителя из АСО 1 обработанных клеток и кДНК получали из 400 нг РНК с помощью набора для синтеза 1-ой цепи кДНК PrimeScript™ (Takara, Cat. No. 6110A). К смеси 400 нг РНК, 1 мкл случайного гексамера и 1 мкл dNTP (дезоксинуклеозидтрифосфат) (10 мМ) в ПЦР пробирке прибавляли воду, обработанную DEPC, до общего объема 10 мкл, которая реагировала при 65°С в течение 5 минут. кДНК синтезировали прибавлением 10 мкл PrimeScript RTase к реакционной смеси и проведением реакции при 30°С в течение 10 минут и при 42°С в течение 60 минут, последовательно.
[Количественная ПЦР в реальном времени] Для того, чтобы оценить уровень экспрессии мРНК ММП-1 человека, количественную ПЦР в реальном времени проводили с синтезированной кДНК, используя линейный разрушаемый зонд. Смесь кДНК, линейного разрушаемого зонда, IQ супермикса (BioRad, Cat. No. 170-8862) и воды без нуклеазной активности в ПЦР пробирке реагировала с помощью CFX96 слепого метода в реальном времени (BioRad) согласно условиям циклов, указанным, как описано далее: 95°С в течение 3 мин (первичная денатурация) с последующими 50 циклами по 10 сек при 95°С (денатурация), 30 сек при 60°С (отжиг) и 30 сек при 72°С (полимеризация). Интенсивность флуоресценции измеряли в конце каждого цикла и результат ПЦР оценивали с помощью кривой плавления. После пороговый цикл (Ct) каждого гена стандартизировали благодаря GAPDH, изменение Ct сравнивали и анализировали.
[Уменьшение мРНК ММП-1 с помощью АСО] Как можно видеть из фиг. 8, по сравнению с контрольным экспериментом количество уменьшенной мРНК ММП-1 составляло 65% при 1 мкМ обработке "АСО 1" и от 10 до 15% при 100 аМ до 10 нМ мкМ обработке "АСО 1", соответственно.
Пример 2. Ингибирование экспрессии белка ММП-1 с помощью "АСО 1" в HDF.
"АСО 1" оценивали с помощью вестерн-блоттинга по его способности подавлять экспрессию белка ММП-1 в HDF, как описано ниже.
[Вестерн-блоттинг] HDF клетки выращивали так, как в примере 1, и 48 часами позже промывали 2 раза холодным PBS (phosphate buffered saline, забуференный фосфатом физиологический раствор) и растворяли в 50 мМ Tris-Cl (рН 7,5), 150 мМ NaCl, 1% NP-40, 0,5% дезоксихолата натрия и 0,1% SDS, ингибитор протеазы. Белок количественно определяли раствором ВСА (Thermo, Cat. No. 23225) и очищали электрофорезом в полиакриламидном геле в присутствии 8% додецилсульфата натрия (SDS-PAGE Gel). Белок переносили на мембрану PVDF (polyvinylidene fluoride membrane, поливинилиденфторидная мембрана) (Millipore, Cat. Нет.IPVH00010), которую блокировали в буфере обезжиренного молока в течение 1 часа. Мембрану опробовали с анти-ММП-1 (SantaCruz, Cat. No 58377) и анти-Р-актином (Sigma, Cat. No. A3854) в качестве первичного антитела и в качестве вторичного антитела использовали козьи антимышиные антитела (CST, Cat. No 7076V). SuperSignal™ West Pico (PierAce, USA) использовали для обнаружения хемилюминесцентного сигнала и интенсивность сигнала измеряли с помощью системы Gel Doc (АТТО). На основе результатов вестерн-блоттинга каждой из полос количественно определяли относительные уровни экспрессии ММП-1 с помощью Image-J программы.
[Ингибирование экспрессии белка ММП-1 с помощью АСО] Как показано на фиг. 9а и 9b, по сравнению с контрольным экспериментом сниженная величина уровня экспрессии белка ММП-1 составляла от 20 до 50% при 100 аМ до 1 мкМ обработки "АСО 1". Таким образом, было доказано, что "АСО 1" показал свою способность подавлять экспрессию белка ММП-1 в HDF.
Пример 3. Увеличение экспрессии коллагенового белка с помощью "АСО 1" b HDF.
"АСО 1" оценивали с помощью вестерн-блоттинга по его способности активировать экспрессию коллагенового белка типа I в HDF, связанного (ассоциированного) с уменьшением экспрессии белка ММП-1, как описано ниже.
[Вестерн-блоттинг] HDF клетки выращивали, как в примере 1, и 48 часами позже промывали 2 раза холодным PBS (phosphate buffered saline, забуференный фосфатом физиологический раствор) и растворяли в 50 мМ Tris-Cl (рН 7,5), 150 мМ NaCl, 1% NP-40, 0,5% дезоксихолата натрия и 0,1% SDS, ингибитор протеазы. Белок количественно определяли раствором ВСА (Thermo, Cat. No. 23225) и очищали электрофорезом в полиакриламидном геле в присутствии 8% додецилсульфата натрия (SDS-PAGE Gel). Белок переносили на мембрану PVDF (polyvinylidene fluoride membrane, поливинилиденфторидная мембрана) (Millipore, Cat. Нет.IPVH00010), которую блокировали в буфере обезжиренного молока в течение 1 часа. Мембрану опробовали с анти-ММП-1 (SantaCruz, Cat. No 58377) и анти-Р-актином (Sigma, Cat. No. A3854) в качестве первичного антитела и в качестве вторичного антитела использовали кроличьи анти-козьи антитела (Santacruz, Cat. No. 2768). SuperSignal™ West Pico (PierAce, USA) использовали для обнаружения хемилюминесцентного сигнала и интенсивность сигнала измеряли с помощью системы Gel Doc (АТТО). На основе результатов вестерн-блоттинга каждой из полос количественно определяли относительные уровни экспрессии ММП-1 с помощью Image-J программы.
[Увеличение экспрессии коллагенового белка типа I с помощью АСО] Как показано на фиг. 10а и 10b, по сравнению с контрольным экспериментом повышенная величина уровня экспрессии коллагенового белка тира I составляла более 30% при 100 аМ до 1 мкМ обработки "АСО 1". Таким образом, было доказано, что индуцированное "АСО 1" снижение экспрессии белка ММП-1 показало свою способность повышать экспрессию коллагенового белка типа I в HDF.
Пример 4. Ингибирование экспрессии белка ММП-1 с помощью "АСО 1" во внеклеточной жидкости (вестерн-блоттинг)
Снижение экспрессии белка ММП-1, вызванное "АСО 1" в клетке, в результате, может повлиять на уровень экспрессии белка ММП-1, секретируемого вне клетки. В этом смысле, "АСО 1" оценивали с помощью вестерн-блоттинга по его способности подавлять экспрессию белка ММП-1 в культуральной жидкости клеток через 48 часов после обработки "АСО 1", как описано ниже.
[Вестерн-блоттинг] HDF клетки выращивали, как в примере 1, и 48 часами позже собранную культуральную жидкость клеток очищали электрофорезом в полиакриламидном геле в присутствии 8% додецилсульфата натрия (SDS-PAGE Gel). Выделенный белок переносили на мембрану PVDF (polyvinylidene fluoride membrane, поливинилиденфторидная мембрана) (Millipore, Cat. No. IPVH00010), которую блокировали в буфере обезжиренного молока в течение 1 часа. Мембрану опробовали с анти-ММП-1 (SantaCruz, Cat. No. 58377) в качестве первичного антитела и в качестве вторичного антитела использовали козьи антимышиные антитела (CST, Cat. No. 7076V). SuperSignal™ West Pico (PierAce, USA) использовали для обнаружения хемилюминесцентного сигнала и интенсивность сигнала измеряли с помощью системы Gel Doc (АТТО). На основе результатов вестерн-блоттинга каждой из полос количественно определяли относительные уровни экспрессии ММП-1 с помощью Image-J программы.
[Ингибирование экспрессии белка ММП-1 с помощью АСО] Как показано на фиг.11а и 11b, по сравнению с контрольным экспериментом пониженная величина уровня экспрессии белка ММП-1 составляла от 10% до 60% при 100 пкМ до 1 мкМ обработки "АСО 1" во внеклеточной жидкости. Таким образом, было доказано, что "АСО 1" показал свою способность подавлять экспрессию белка ММП-1 во внеклеточной жидкости.
Пример 5. Увеличение экспрессии коллагенового белка с помощью "АСО 1" в во внеклеточной жидкости
"АСО 1" оценивали с помощью вестерн-блоттинга по его способности активировать экспрессию коллагенового белка типа I во внеклеточной жидкости, как описано ниже.
[Вестерн-блоттинг] HDF клетки выращивали, как в примере 1, и 48 часами позже собранную культуральную жидкость клеток очищали электрофорезом в полиакриламидном геле в присутствии 8% додецилсульфата натрия (SDS-PAGE Gel). Выделенный белок переносили на мембрану PVDF (polyvinylidene fluoride membrane, поливинилиденфторидная мембрана) (Millipore, Cat. No. IPVH00010), которую блокировали в буфере обезжиренного молока в течение 1 часа. Мембрану опробовали с анти-ММП-1 (SantaCruz, Cat. No. 58377) в качестве первичного антитела и в качестве вторичного антитела использовали кроличьи анти-козьи антитела (Santacruz, Cat. No. 2768). SuperSignal™ West Pico (PierAce, USA) использовали для обнаружения хемилюминесцентного сигнала и интенсивность сигнала измеряли с помощью системы Gel Doc (АТТО). На основе результатов вестерн-блоттинга каждой из полос количественно определяли относительные уровни экспрессии ММП-1 с помощью Image-J программы.
[Увеличение экспрессии коллагенового белка типа I с помощью АСО] Как показано на фиг. 12а и 12b, по сравнению с контрольным экспериментом повышенная величина уровня экспрессии коллагенового белка составляла 20% при 1 пкМ и 80% при 1 мкМ обработке "АСО 1", соответственно. Таким образом, было доказано, что снижение экспрессии белка ММП-1, индуцированное "АСО 1" в HDF, показало его способность активировать экспрессию коллагенового белка типа I во внеклеточной жидкости.
Пример 6. Ингибирование экспрессии белка ММП-1 с помощью "АСО 1" во внеклеточной жидкости (ELISA).
Снижение экспрессии белка ММП-1, вызванное "ASO 1" в клетке, в результате, может повлиять на уровень экспрессии белка ММП-1, секретируемого вне клетки. В этом смысле, "АСО 1" оценивали с помощью ферментного иммуносорбентного теста (ELISA, enzyme linked immunosorbent assay) по его способности подавлять экспрессию белка ММП-1 в культуральной жидкости клеток через 48 часов после обработки "АСО 1", как описано ниже.
[ELISA] HDF клетки выращивали, как в примере 1, и 48 часами позже в собранной культуральной жидкости клеток оценивали уровень экспрессии ММП-1 с помощью абсорбции (Sunrise, TEC AN) комплектом ELISA ММП-1 человека (abeam, Cat. No. ab 100603) согласно инструкции производителя.
[Ингибирование экспрессии белка ММП-1 с помощью АСО] Как показано на фиг. 13, по сравнению с контрольным экспериментом величина пониженного уровеня экспрессии белка ММП-1 составляла от 15% до 30% при 100 пкМ до 10 нМ и 50% при 1 мкМ обработке "АСО 1", соответственно. Таким образом, было доказано, что "АСО 1" показал свою способность подавлять экспрессию белка ММП-1 во внеклеточной жидкости.
Пример 7. Получение соединения формулы I, содержащего сыворотку для местного применения (вес/вес.%)
Соединение формулы I, например "АСО 1", входило в состав в виде сыворотки для местного применения для пациентов. Сыворотку для местного применения получали, как описано ниже. Учитывая, что существует множество вариантов возможной Сыворотки для местного применения, данный препарат следует рассматривать в качестве примера и не следует интерпретировать для ограничения объема нынешнего изобретения.


В отдельном стакане растворяли смешанные вещества части А и части В при 25°С, соответственно. Часть А и часть В смешивали и превращали в эмульсию с помощью гомогенизатора с 3600 об/мин при 25°С в течение 5 минут. Эмульгированную часть С фильтровали через фильтр с отверстиями в 50 меш и фильтрат прибавляли к смеси частей А и В. Полученную смесь превращали в эмульсию с помощью гомогенизатора с 3600 об/мин при 80°С в течение 5 минут. После добавления части D в смесь частей А, В и С полученную смесь превращали в эмульсию с помощью гомогенизатора с 2500 об/мин при 25°С в течение 3 минут. Наконец, обеспечить однородную дисперсию и полное уничтожение пены.
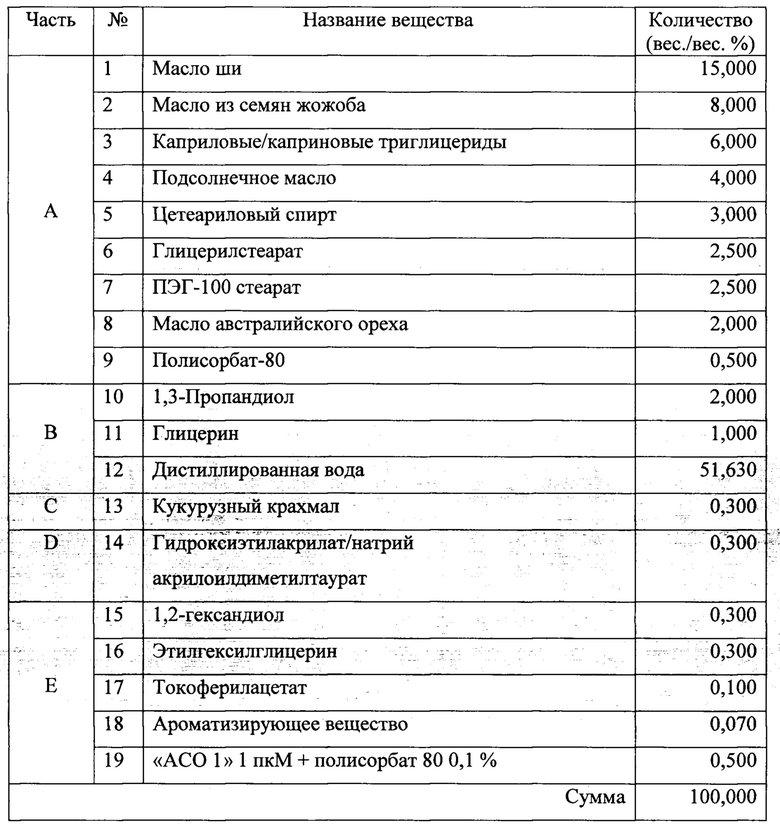
Пример 8. Получение крема для местного применения, содержащего соединение формулы I (вес/вес.%)
Соединение формулы I, например "АСО 1", входило в состав в виде крема для местного применения для пациентов. Крем для местного применения получали, как описано ниже. Учитывая, что существует множество вариантов возможного крема для местного применения, данный препарат следует рассматривать в качестве примера и не следует интерпретировать для ограничения объема нынешнего изобретения.
В отдельном стакане растворяли вещества части А при 80°С и части В при 85°С, соответственно. Часть А и часть В смешивали и превращали в эмульсию с помощью гомогенизатора с 3600 об/мин при 80°С в течение 5 минут. После прибавления частей С и D к смеси частей А и В, полученную смесь превращали в эмульсию с помощью гомогенизатора с 3600 об/мин при 80°С в течение 5 минут. После прибавления части Е к смеси частей А, В, С и D при 35°С, полученную смесь превращали в эмульсию с помощью гомогенизатора с 3600 об/мин при 35°С в течение 3 минут. Наконец, обеспечить однородную дисперсию и полное уничтожение пены при 25°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИСМЫСЛОВЫЕ ОЛИГОНУКЛЕОТИДЫ АЦЕТИЛ-СОА-КАРБОКСИЛАЗЫ-2 | 2019 |
|
RU2807629C2 |
| АНТИСМЫСЛОВЫЕ ОЛИГОНУКЛЕОТИДЫ ТИРОЗИНАЗЫ | 2018 |
|
RU2778786C2 |
| АНТИСМЫСЛОВЫЕ ОЛИГОНУКЛЕОТИДЫ К HIF-1-АЛЬФА | 2017 |
|
RU2753517C2 |
| ПРОПУСК ЭКЗОНОВ С ПОМОЩЬЮ ПРОИЗВОДНЫХ ПЕПТИДО-НУКЛЕИНОВЫХ КИСЛОТ | 2017 |
|
RU2786637C2 |
| АНТИСМЫСЛОВЫЕ ОЛИГОНУКЛЕОТИДЫ АНДРОГЕНОВОГО РЕЦЕПТОРА | 2017 |
|
RU2753966C2 |
| АНТИСМЫСЛОВЫЕ ОЛИГОНУКЛЕОТИДЫ ДЛЯ SNAP25 | 2017 |
|
RU2766701C2 |
| АНТИСМЫСЛОВОЕ ДЛЯ SCN9A ОБЕЗБОЛИВАЮЩЕЕ СРЕДСТВО | 2018 |
|
RU2762293C2 |
| АНТИСМЫСЛОВЫЕ ОЛИГОНУКЛЕОТИДЫ ПРОТИВ SCN9A | 2017 |
|
RU2748834C2 |
| ПРОИЗВОДНЫЕ ПЕПТИДО-НУКЛЕИНОВЫХ КИСЛОТ С ХОРОШЕЙ КЛЕТОЧНОЙ ПЕНЕТРАЦИЕЙ И СИЛЬНОЙ АФФИННОСТЬЮ К НУКЛЕИНОВОЙ КИСЛОТЕ | 2009 |
|
RU2564032C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛЯЦИИ SMN2 СПЛАЙСИНГА У СУБЪЕКТА | 2010 |
|
RU2566724C9 |

Группа изобретений относится к производным пептидных нуклеиновых кислот (ПНК), целенаправленно воздействующим на пре-мРНК матриксной металлопротеиназы-1 человека (ММП-1), и их применению для лечения состояний старения кожи, связанных с белком ММП-1 человека. Предложено производное ПНК формулы I или его фармацевтически приемлемая соль для индуцирования пропуска экзона в пре-мРНК ММП-1 человека. Производное ПНК обладает по меньшей мере 14-мерным комплементарным перекрыванием с 16-мерной последовательностью пре-мРНК [(5'→3') CAUAUAUGGUGAGUAU] в пре-мРНК ММП-1 человека. Также предложены фармацевтическая композиция и косметическая композиция для снижения старения кожи, связанного с ММП-1 человека, способ снижения старения кожи. Производное ПНК обладает хорошей клеточной или мембранной проницаемостью, может местно вводиться как «оголенный» олигонуклеотид для индуцирования пропуска "экзона 5" ММП-1 в коже, улучшить состояние кожи и предотвратить ее старение. 4 н. и 2 з.п. ф-лы, 13 ил., 8 пр.
1. Производное пептидной нуклеиновой кислоты, представленное формулой I, или его фармацевтически приемлемая соль для индуцирования пропуска экзона в пре-мРНК матриксной металлопротеиназы-1 (ММП-1) человека:
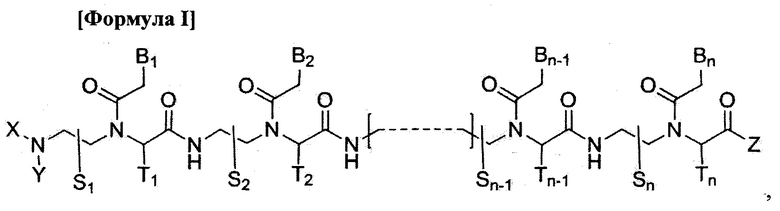
где
n - целое число от 14 до 21;
соединение формулы I обладает по меньшей мере 14-мерным комплементарным перекрыванием с 16-мерной последовательностью пре-мРНК 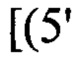
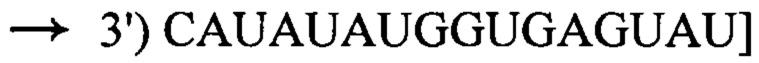 в пре-мРНК ММП-1 человека;
в пре-мРНК ММП-1 человека;
соединение формулы I полностью комплементарно пре-мРНК ММП-1 человека или частично комплементарно пре-мРНК ММП-1 человека с одним ошибочным спариванием;
S1, S2, …, Sn-1, Sn, T1, T2, …, Tn-1 и Tn обозначают атом водорода;
X обозначает атом водорода;
Y обозначает замещенную или незамещенную алкилоксикарбонилгруппу, в которой замещенную или незамещенную алкилоксикарбонилгруппу выбирают из:
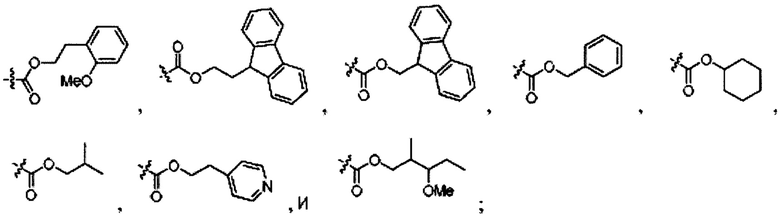
Z обозначает аминогруппу;
B1, В2, …, Bn-1 и Bn независимо выбраны из природных нуклеиновых оснований, включая аденин, тимин, гуанин, цитозин и урацил, и нуклеиновых оснований неприродного происхождения; в которых количество нуклеиновых оснований неприродного происхождения равно 6 и нуклеиновые основания неприродного происхождения независимо выбраны из формулы II, формулы III или формулы IV:
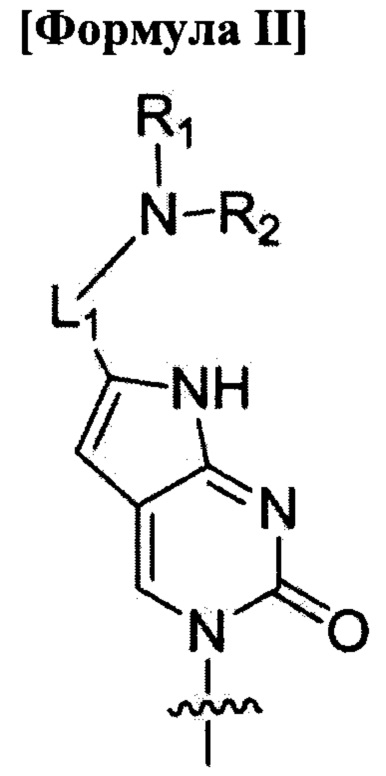
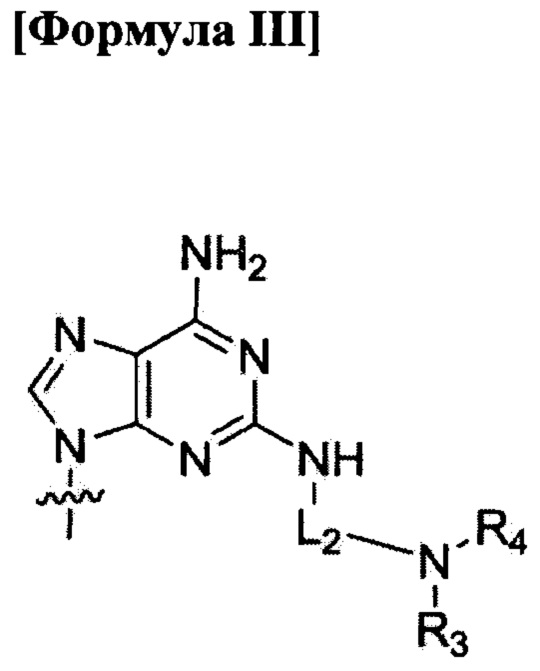
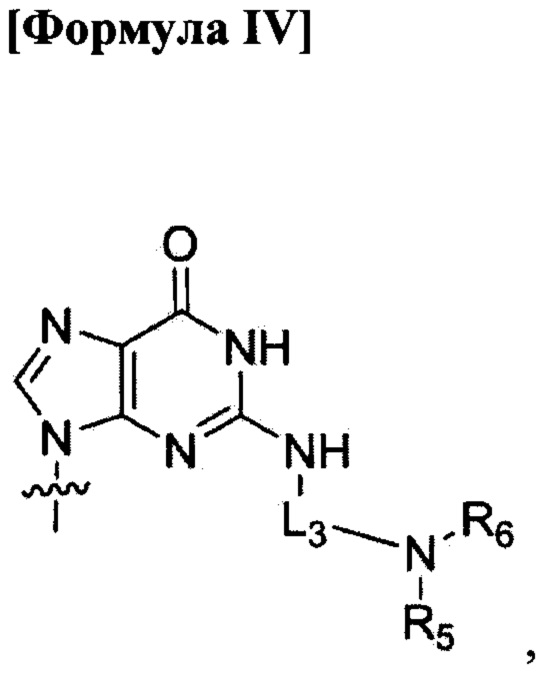
где
R1, R2, R3, R4, R5 и R6 обозначают атом водорода;
L1, L2 и L3 являются ковалентным линкером, представленным формулой V, ковалентно соединяющим основную аминогруппу с остатком нуклеинового основания:
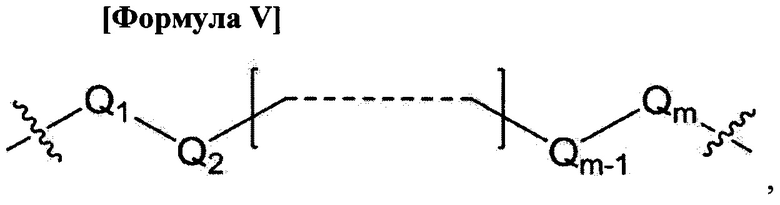
где
Q1 и Qm представляют собой метиленгруппу (-СН2-) и Qm непосредственно связывает основную аминогруппу;
Q2, Q3, … и Qm-1 независимо выбраны из метиленгруппы и атома кислорода; и m - целое число от 1 до 15.
2. Производное пептидной нуклеиновой кислоты по п. 1 или его фармацевтическая соль, где
n - целое число от 14 до 18;
соединение формулы I обладает по меньшей мере 14-мерным комплементарным перекрыванием с 16-мерной последовательностью пре-мРНК 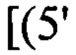
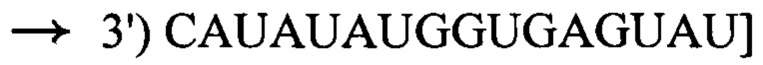 в пре-мРНК ММП-1 человека;
в пре-мРНК ММП-1 человека;
соединение формулы I полностью комплементарно пре-мРНК ММП-1 человека;
S1, S2, …, Sn-1, Sn, T1, T2, …, Tn-1 и Tn представляют собой атом водорода;
X является атомом водорода;
Y обозначает замещенную или незамещенную алкилоксикарбонилгруппу;
Z обозначает аминогруппу;
B1, В2, …, Bn-1 и Bn независимо выбраны из природных нуклеиновых оснований, включая аденин, тимин, гуанин, цитозин и урацил, и нуклеиновых оснований неприродного происхождения, в которых количество нуклеиновых оснований неприродного происхождения равно 6 и нуклеиновые основания неприродного происхождения независимо выбраны из формулы II, формулы III или формулы IV;
R1, R2, R3, R4, R5 и R6 являются атомами водорода;
L1 обозначает -(СН2)2-O-(СН2)2-, -СН2-O-(СН2)2-, -СН2-O-(СН2)3-, -СН2-O-(СН2)4- или -СН2-O-(СН2)5- с правым концом непосредственно связывается с основной аминогруппой; и
L2 и L3 независимо выбраны из -(СН2)2-O-(СН2)2-, -(СН2)3-O-(СН2)2-, -(СН2)2-O-(СН2)3-, -(СН2)2-, -(СН2)3-, -(СН2)4-, -(СН2)5-, -(СН2)б-, -(СН2)7- и -(СН2)8- с правым концом непосредственно связывается с основной аминогруппой.
3. Производное пептидной нуклеиновой кислоты по п. 2, которое является производным пептидной нуклеиновой кислоты, приведенным ниже, или его фармацевтически приемлемой солью:
(N→C) Fethoc-TA(6)C-TCA(6)-CC(1O2)A(6)-TA(6)T-A(6)T-NH2,
где
А, Т и С представляют собой мономеры пептидной нуклеиновой кислоты с природным нуклеиновым основанием аденином, тимином и цитозином, соответственно;
C(pOq) и А(р) представляют собой мономеры пептидной нуклеиновой кислоты с нуклеиновым основанием неприродного происхождения, представленным формулой VI и формулой VII, соответственно;
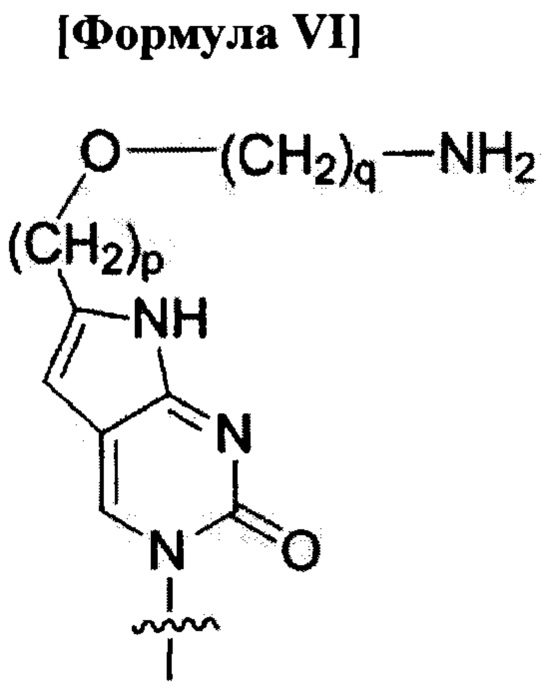
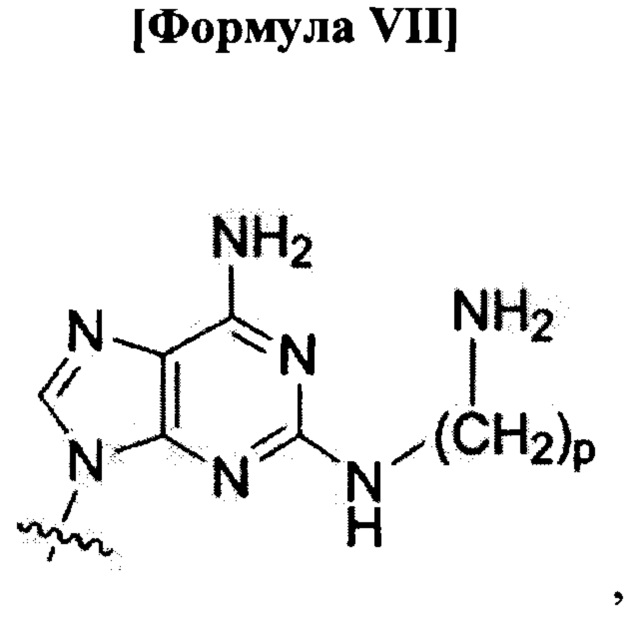
где
р и q - целые числа и р равен 1 или 6, и q равен 2; и
"Fethoc-" представляет собой сокращение для "[2-(9-фторенил)этил-1-окси]карбонилгруппы".
4. Способ снижения старения кожи, связанного с повышенной экспрессией ММП-1, включающий введение пациенту производного пептидной нуклеиновой кислоты по п. 1 или его фармацевтически приемлемой соли.
5. Фармацевтическая композиция для снижения старения кожи, связанного с повышенной экспрессией ММП-1, включающая производное пептидной нуклеиновой кислоты по п. 1 или его фармацевтически приемлемую соль и фармацевтически приемлемый адъювант.
6. Косметическая композиция для снижения старения кожи, связанного с повышенной экспрессией ММП-1, включающая производное пептидной нуклеиновой кислоты по п. 1 или его фармацевтически приемлемую соль и косметические ингредиенты.
| WO 2018029517 A1, 15.02.2018 | |||
| WO 2018069764 A1, 19.04.2018 | |||
| US 6617422 B1, 09.09.2003 | |||
| ПРОИЗВОДНЫЕ ПЕПТИДО-НУКЛЕИНОВЫХ КИСЛОТ С ХОРОШЕЙ КЛЕТОЧНОЙ ПЕНЕТРАЦИЕЙ И СИЛЬНОЙ АФФИННОСТЬЮ К НУКЛЕИНОВОЙ КИСЛОТЕ | 2009 |
|
RU2564032C2 |
| KR 20120073536 A, 05.07.2012 | |||
| US 2015240239 A1, 27.08.2015 | |||
| WO 2016037071 A2, 10.03.2016 | |||
| УКЛАДЧИК БУРИЛЬНЫХ СВЕЧЕЙ | 0 |
|
SU177384A1 |
| WO 03033659 A2, 24.04.2003. | |||
Авторы
Даты
2023-08-28—Публикация
2019-05-03—Подача