Изобретение относится к медицине, а именно к анестезиологии-реаниматологии, интенсивной терапии, акушерству и гинекологии и может быть использовано при лечении преэклампсии.
Преэклампсия (ПЭ) - синдром полиорганной дисфункции, индуцированный беременностью, основными клиническими характеристиками которого являются впервые возникшая гипертензия - артериальное давление (АД) более 140/90 мм рт.ст. после 20-й недели беременности и протеинурия, купирующиеся в послеродовом периоде. ПЭ развивается в течение 2-8% беременностей и является основной причиной материнской заболеваемости и смертности плода. Частота развития полиорганной недостаточности при ПЭ достигает более 52%, частота индуцированного досрочного родоразрешения - 20-30%, показатель материнской смертности превышает популяционный в 5-6 раз (25-30%о); перинатальная смертность почти в 8-10 раз выше популяционной (75%о от числа живорожденных) [Радзинский, В.Е. Преэклампсия как угрожающее жизни состояние / B. Е. Радзинский, А.С. Оленев, В.А. Новикова // Акушерство и гинекология. - 2020. -№3. - C. 48-57]. Наиболее тяжелым, быстро прогрессирующим течением, высокими цифрами материнской и перинатальной заболеваемости и смертности характеризуется ранняя преэклампсия, в 46,2% случаев сопровождающаяся развитием синдрома задержки развития плода (СЗРП) [Стрижаков А.Н. Новые возможности дифференциального прогнозирования ранней и поздней преэклампсии / Тимохина Е.В., Ибрагимова СМ., Белоусова B.C., Мартиросян Я.О. // Акушерство, гинекология и репродукция. - 2018. -Т. 12. -№2.-С.55-61].
Формирование патогенетической основы ранней ПЭ происходит с момента вскрытия трофобластом просвета спиральных артерий в области зоны преимущественной инвазии хориона и начала становления маточно-хориального кровотока. Патофизиология ПЭ остается неясной, предполагается участие многих факторов в развитии этого состояния: провоспалительных медиаторов, антиангиогенных факторов с их преобладанием над ангиогенными, определямыми как соотношение sFlt-1 и PLGF, нарушений липидного обмена. Исследования показывают, что во время нормально протекающей беременности липидный профиль меняется на атерогенный фенотип с еще более резкими изменениями при ПЭ. Метаанализ 24 исследований случай-контроль (2720 женщин) покачал, что высокие уровни триглицеридов связаны с 4-кратным увеличением распространенности ПЭ [Сидорова, И.С. Преэклампсия как гестационный иммунокомплексный комплементопосредованный эндотелиоз / И.С. Сидорова, Н.А. Никитина // Российский вестник акушера-гинеколога. - 2019. - Т. 19. - №1. - С.5-11].
В настоящее время методом контроля раннего развития клинических симптомов ПЭ, имеющим очень ограниченные возможности, является назначение антигипертензивных препаратов и сульфата магния для предотвращения судорог [Рокотянская, Е.А. Патогенетическое обоснование персонифицированной программы ведения беременных женщин при гипертензивных расстройствах: дис. докт. мед. наук: 14.01.01 / Рокотянская Елена Аркадьевна. Иваново, 2019. - 484 с]. При прогрессировании симптомов ПЭ единственным методом лечения является преждевременное родоразрешение путем кесарева сечения, что значительно ухудшает неонатальные исходы.
Описан способ лечения беременных с ПЭ средней тяжести (RU 2657768 С1, Волкова, 15.06.2018). Этот способ предполагает инъекционное введение экулизумаба под контролем за гемодинамическими, лабораторными показателями беременной и функциональным состоянием плода. Изобретение обеспечивает пролонгирование беременности у пациенток с ПЭ средней тяжести за счет снижения патологической активности системы компонентов комплемента. Необходимо отметить, что в настоящее время не выделяют преэклампсию средней степени тяжести, как это указано в описанном способе. В соответствии с современными классификациями выделяют умеренную и тяжелую преэклампсию, преэклампсию раннюю с началом развития до 34 недель беременности и позднюю с манифестацией после 34 недель беременности, а также осложнения тяжелой преэклампсии: эклампсию и HELLP-синдром [Клинические рекомендации «Преэклампсия. Эклампсия. Отеки, протеинурия и гипертензивные расстройства во время беременности, в родах и послеродовом периоде», 2021] [1]. Препарат экулизумаб подавляет терминальную активность комплемента человека, обладая высокой аффинностью к его С5-компоненту. Как следствие, полностью блокируется расщепление компонента С5 на С5а и C5b и образование терминального комплекса комплемента C5b-9, который принимает участие в развитии таких заболеваний как пароксизмальная ночная гемоглобинурия (ПНГ) и атипичный гемолитико-уремический синдром (аГУС). Активация альтернативного пути комплемента с прогрессированием микротромбозов является крайне редким состоянием, развивающимся у пациенток с генетическими нарушениями или, реже, аутоиммунными реакциями, приводящими к патологии системы комплемента [Кирсанова, Т.В. Имитаторы тяжелой преэклампсии и HELLP-синдрома: различные виды тромботической микроангиопатии, ассоциированной с беременностью / Т.В. Кирсанова, М.А. Виноградова, Т.А. Федорова // Акушерство и гинекология. - 2016. - №12. - С. 5-14.]. Необходимо отметить, что, несмотря на то, что в настоящее время тяжелую преэклампсию и HELLP-синдром, так же как и ПНГ и аГУС относят к группе тромботических микроангиопатии (ТМА), ни ПН Г. ни аГУС не являются осложнениями ПЭ. Патогенетическое обоснование для применения препарата экулизумаб при лечении ПЭ на сегодняшний день отсутствует.Кроме того, в инструкции к препарату экулизумаб отмечено, что применение при беременности возможно только в том случае, когда предполагаемая польза для матери превосходит потенциальный риск для плода. Это положение противоречит основной идее пролонгирования беременности при ПЭ, поскольку продолжение беременности при развитии этого осложнения всегда обусловлено интересами плода в первую очередь: рождение ближе к доношенному сроку, снижение рисков неонатальных осложнений, связанных с недоношенностью.
В соответствии с современными представлениями о патогенезе ранней ПЭ описано применение методов терапевтического афереза патогенетически значимых факторов развития ПЭ. Возможности терапевтического афереза для пролонгирования беременности и улучшения исходов для новорожденных были показаны в работе R.Thadhani с соавт.[Thadhani, R. et al. Removal of soluble Fms-like tyrosine kinase-1 by dextran sulfate apheresis in preeclampsia /J. Am. Soc. Nephrol.//2016 Mar;27(3):903-13.] при использовании отрицательно заряженных колонок на основе декстрансульфатцеллюлозы (DSC-аферез) для удаления растворимой FMS-подобной L-тирозинкиназы-1 (sFlt-1), являющейся антиангиогенным фактором, и улучшения соотношения проангиогенных и антиангиогенных факторов. В работах K.Winkler et al. [Winkler K. et al. Treatment of very preterm preeclampsia via heparin-mediated extracorporeal LDL-precipitation (H.E.L.P.) apheresis: The Freiburg preeclampsia H.E.L.P.-Apheresis study / Pregnancy Hypertens.// 2018 Apr;12:136-143.] была показана эффективность гепарин-опосредованной преципитации ЛПНП (H.E.L.P.- афереза). Ограничением указанных выше методик является селективность удаления тех или иных компонентов, в то время как в патогенетический механизм развития ПЭ включает каскад взаимосвязанных между собой реакций с участием большого количества медиаторов.
Описан способ профилактики тяжелых форм гестозов, который относится к эфферентным методам лечения, и может быть использован для профилактики тяжелых форм гестозов (RU 2295981 С2, Уральский НИИ охраны материнства и младенчества, 27.03.2007). Женщинам с выявленным эндотоксикозом на сроке беременности 20-24 недели проводят курс карбогемосорбции, состоящий из 2-х процедур. Продолжительность процедуры составляет 60-90 минут. Способ обеспечивает предупреждение развития тяжелых осложнений беременности (гестозов) на ранних сроках, после завершения процессов органо- и гистеогенеза плода и, соответственно, пролонгирование беременности до сроков жизнеспособности плода за счет выбора оптимального срока проведения курса карбогемосорбции, что также существенно снижает медикаментозную нагрузку в группе пациенток высокого риска. К недостаткам данного метода можно отнести характеристики используемых угольных сорбентов. Подобные материалы проявляют неселективную сорбционную активность по отношению к веществам с молекулярной массой от 0,5 до 50 кДа. В результате, при использовании угольных сорбентов, в спектр удаляемых веществ попадают не только патогенные молекулы средней и низкой массы, к которым относятся медиаторы воспаления и, отчасти поврежденные структуры ДНК (НВЛ), но и молекулы с защитным действием с молекулярной массой до 50 кДа, такие как проангиогенный фактор PLGF (фактор роста плаценты) и альбумин. Это может не только нивелировать положительный эффект процедуры, но и ухудшить состояние пациентки, поскольку естественное снижение PLGF является фактором, утяжеляющим течение ПЭ, а уменьшение концентрации альбумина плазмы крови способствует снижению онкотического давления крови, прогрессированию отечного синдрома, гемодинамических нарушений и нарушений перфузии органов и тканей. С другой стороны, при использовании угольных сорбентов не происходит элиминации sFlt-1 и липопротеидов низкой плотности, играющих ведущую роль в развитии и прогрессировании преэклампсии.
Наиболее близким к патентуемому является способ профилактики развития эклампсий, описанный в патенте RU 2161990 С2, ООО "НОРД КОМПЬЮТЕР", 20.01.2001 - прототип. В период до 32-й недели беременности проводят диагностический тест Ганта и при положительном тесте выполняют с интервалом в 2-3 дня 2-3 сеанса плазмафереза с эксфузией не более 900 мл плазмы за сеанс при скорости качания 60-100 мл/мин.
К недостаткам данного метода следует отнести неселективность методики, в результате которой происходит удаление из кровяного русла не только молекул, ответственных за развитие ПЭ, но и полезных веществ. В настоящее время определены основные молекулярные структуры, ответственные за прогрессирование ПЭ, к ним относятся антиангиогенные факторы, прежде всего, растворимая FMS-подобной L-тирозинкиназы-1 (sFlt-1) и ее преобладание над фактором роста плаценты (PLGF), а также липопротеиды низкой плотности (атерогенные липопротеиды). При проведении плазмаферезов по указанной методике вместе с удалением молекул, способствующих развитию преэклампсии, удаляются и вещества, препятствующие ее развитию. К полезным веществам относятся белки плазмы крови, в первую очередь, альбумин, фактор роста плаценты, факторы свертывания крови, иммуноглобулины. Это может приводить к снижению онкотического давления крови, усилению отечного синдрома, гиповолемии с компенсаторной гипертензией, снижению иммунитета и дальнейшему прогрессированию преэклампсии. Кроме того, удаление за один сеанс до 900 мл плазмы крови превышает рекомендуемый объем при однократной эксфузии плазмы у беременных, который должен быть не более 350-500 мл [Кровесберегающие технологии в акушерской практике. Клинические рекомендации, 2014], что также может быть причиной осложнений. Предлагаемый способ не способствует предотвращению прогрессирования ПЭ и пролонгированию беременности в интересах плода, а лишь, как указано, профилактирует развитие эклампсии, одного из редких осложнений беременности, за счет улучшения точности диагностики этого осложнения.
Настоящее изобретение направлено на решение проблемы пролонгирования сроков беременности и улучшение неонатальных исходов при ранней преэклампсии.
Патентуемый способ ведения беременности при ранней преэклампсии включает проведение процедуры мембранного плазмафереза.
Отличие состоит в том. что на следующие сутки после проведения мембранного плазмафереза проводят с интервалом три дня два сеанса каскадной плазмофильтрации, состоящей в последовательной перфузии крови через два фильтра, при этом на первом фильтре кровь разделяют на форменные элементы, которые возвращают в кровяное русло, а полученную плазму направляют на второй фильтр с точкой отсечения веществ с молекулярной массой более 70 кДа, при этом за один сеанс фильтруют весь объем циркулирующей плазмы, после чего ее возвращают пациентке.
Способ может характеризоваться тем, что в процессе мембранного плазмафереза отбирают не более 500 мл плазмы.
Способ может характеризоваться и тем, что в качестве первого фильтра используют фильтр ПФМ-500 производства ЗАО «Плазмофильтр», а также тем, что в качестве второго фильтра используют последовательно установленные фильтр ПФМ-500 производства ЗАО «Плазмофильтр» и фракционатор плазмы Evaflux 2А20 производства фирмы Kawasumi Laboratories, Япония.
Технический результат изобретения - пролонгирование сроков беременности и улучшение неонатальных исходов за счет удаления антиангиогенного фактора растворимой fms-подобной тирозинкиназы-1 и атерогенных липопротеидов при сохранении содержания альбумина и плацентарного фактора роста. Обеспечивается более высокий вес при рождении, более высокая оценка по шкале Апгар при рождении, меньшая потребность в сурфактанте, меньшая потребность в респираторной поддержке и ее длительности, снижение продолжительности пребывания в отделении реанимации по сравнению с группой контроля.
Способ осуществляют следующим образом.
У пациенток с развитием ПЭ в сроки до 34 недель беременности проводится процедура плазмафереза с удалением 500 мл плазмы. После процедуры плазмафереза с интервалом 3 дня проводятся два сеанса каскадной плазмофильтрации. Процедура каскадной плазмофильтрации заключается в последовательной перфузии крови через два фильтра. Первый фильтр разделяет кровь пациентки на клеточные элементы и плазму. Клеточные элементы возвращают в кровяное русло пацинтки, а плазма поступает на второй фильтр, в который содержит фракционатор с точкой отсечения веществ с молекулярной массой более 70 кДа. Соответственно, в спектр удаляемых патологических элементов попадают антиангиогенный фактор - растворимая fms-подобная тирозинкиназа-1 (sFlt-1) с молекулярной массой 90кДа и атерогенные липопротеиды. но при этом сохраняются молекулы, играющие протективную роль - альбумин и PLGF. Проведение предварительного сеанса плазмафереза позволяет оценить состояние венозного русла пациентки, улучшить реологические свойства крови, что способствует улучшению пропускной способности фильтров и эффективности проведения последующих сеансов каскадной плазмофильтрации.
Результатом применения патентуемого способа является снижение отношения sFlt-1/ PLGF и уровня триглицеридов, что является подтверждением эффективности удаления молекул, играющих ведущую роль в развитии преэклампсии. Это обуславливает значительное пролонгирование сроков беременности и улучшение неонатальных исходов: более высокий вес при рождении, более высокая оценка по шкале Апгар при рождении, меньшая потребность в сурфактанте, меньшая потребность в респираторной поддержке и ее длительности, снижение продолжительности пребывания в отделении реанимации по сравнению с группой контроля.
Для подтверждения эффективности проведено сравнительное исследование исходов беременности у пациенток с ранним развитием преэклампсии при использовании патентуемого способа (группа исследования, n=15) и при применении стандартной терапии (группа контроля, n=15). При включении в исследование группы не отличались по возрасту и сроку беременности (Таблица №1).
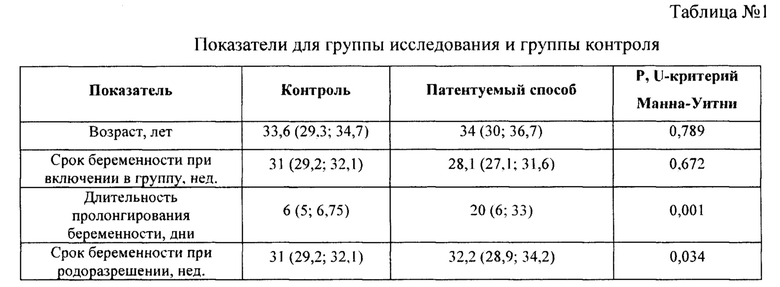
Выявлены значительные статистически и клинически значимые различия по сроку беременности при родоразрешении, а также длительности пролонгирования беременности. Основной лабораторный показатель тяжести ПЭ - отношение sFlt-1 и PLGF был значительно выше в группе исследования перед началом терапии (Таблица №2).
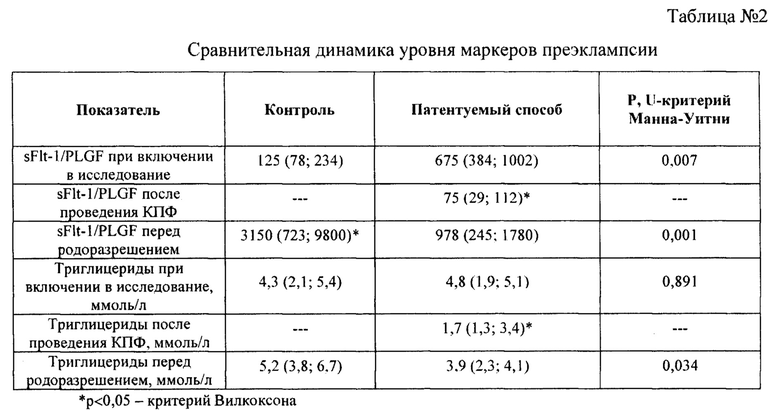
После проведения лечения предлагаемым способом этот показатель статистически и клинически значимо снижался и перед родоразрешением оставался значительно ниже, чем в контрольной группе. Атерогенные липопротеиды (триглицериды) также статистически и клинически значимо снижались после применения предлагаемого способа и перед родоразрешением также оставались значительно ниже, чем в этой группе перед началом исследования и ниже, чем в контрольной группе.
При применении предлагаемого способа пролонгирования беременности при ранней ПЭ значительно улучшились исходы для новорожденных (Таблица №3).

Статистически значимо вес при рождении в группе исследования превышал вес новорожденных в группе контроля. Длительность лечения в палате реанимации в группе контроля также была статистически значимо выше в группе контроля. Респираторная поддержка в виде инвазивной искусственной вентиляции легких статистически значимо реже требовалась при лечении с использованием патентуемого способа: Отношение шансов 2,5 95%ДИ (0,37; 16,88). В группе исследования значительно реже применялся антиателектатический препарат сурфактант: Отношение шансов 4,33 95% ДИ (1,02; 18,6).
Таким образом, способ пролонгирования беременности при раннем развитии ПЭ путем применения сочетания одной процедуры плазмафереза с удалением 500 мл плазмы с последующим проведением 2-х процедур каскадной плазмофильтрации с интервалом 3 дня между ними позволяет значительно снизить соотношение sFlt-1/PLGF, уровень атерогенный липопротеидов, которые являются основным показателями тяжести преэклампсии, и соответственно пролонгировать беременность и улучшить исходы для новорожденных.
Клинический пример №1. Пациентка Н., 40 лет, была доставлена бригадой скорой помощи в приемное отделение Видновского перинатального центра переводом из роддома города Ступино с жалобами на повышение артериального давления до 160/100 мм рт.ст., нарастание отеков нижних конечностей, кистей рук, лица, которые появились за несколько дней до поступления. Из анамнеза известно, что пациентка перенесла субтотальную резекцию щитовидной железы в 2009 году (постоянно принимает заместительную гормональную терапию), в 2010 году - кесарево сечение в связи с развитием тяжелой преэклампсии. Из сопутствующей патологии отмечается хроническая артериальная гипертензия, вне беременности отмечает повышение АД до 140/90, периодически принимала гипотензивные препараты. Множественные кисты почек. На учете в женской консультации состояла с 10 недель беременности. Беременность протекала без осложнений. В течение беременности АД в пределах 120/80 - 130/80 мм рт.стб., гипотензивные препараты не принимала.
При поступлении АД - 150/100 мм рт.ст., суточная протеинурия - 1 г/л. Клинический, биохимический анализы крови, коагулограмма - в пределах нормы. Но при исследовании отношения sFlt-1/PLGF выявлено его увеличение до 180, что значительно превышает норму для данного срока беременности (норма - 38-85), увеличение уровня триглицеридов - 6,1 ммол/л. Подсчет уровня НВЛ также показал увеличение этого показателя до 18 (при норме до 10). На основании жалоб пациентки, клинических признаков и лабораторных показателей выставлен диагноз: Беременность 32 недели. Тяжелая преэклампсия. Хроническая артериальная гипертензия. Поликистоз почек. Медикаментозно компенсированный гипотиреоз.
В соответствии с клиническими рекомендациями [1], начата терапия с применением гипотензивной, магнезиальной и симптоматической терапии. Учитывая срок беременности 32 недели (ранняя недоношенность) и высокий риск преждевременных родов, проведена профилактика респираторного дистресс-синдрома (РДС) новорожденных. В связи с отсутствием клинически значимых изменений в стандартных лабораторных показателях (Таблица №4) и стабилизацию АД на фоне назначенной комбинированной гипотензивной терапии, а также отсутствием нарушений со стороны плода по данным допплерографии и кардиотокографии (КТГ), с целью пролонгирования беременности проведен сеанс мембранного плазмафереза. Использовался фильтр ПФМ-500 производства ЗАО «Плазмофильтр» с удалением 500 мл плазмы.
На следующий день после плазмафереза проведен первый сеанс селективной каскадной плазмофильтрации, а затем через 3 дня - второй сеанс. Селективная каскадная плазмофильтрация осуществлялась через два последовательно соединенных фильтра. На первом фильтре ПФМ-500 кровь разделяли на форменные элементы, которые возвращались в кровяное русло, а полученную плазму направляли на второй фильтр, образованный последовательно соединенными фильтром ПФМ-500 и фракционатором «Evaflux 2А20» с точкой отсечения веществ с молекулярной массой более 70 кДа. При этом за один сеанс фильтровали весь объем циркулирующей плазмы (2000-2500 мл), после чего ее возвращали пациентке.
Отмечено снижение отношения sFlt-1/PLGF, снижение уровня триглицеридов до 2,1 ммоль/л, снижение суточной протеинурии до 0,5 г/л, стабилизация АД на уровне 130/80-140/80 мм рт.ст. без увеличения суточной дозировки гипотензивных препаратов, уменьшение выраженности периферических отеков. Уровень НВЛ ловушек снизился незначительно, концентрация общего белка и альбумина плазмы не изменилась (Таблица №4). Состояние плода по данным допплерографии, КТГ после проведенного лечения не ухудшилось. Учитывая улучшение состояния пациентки и отсутствие ухудшения со стороны плода, пациентка выписана из стационара для амбулаторного наблюдения в удовлетворительном состоянии с диагнозом: Беременность 33,6 недель. Умеренная преэклампсия. Отягощенный акушерско-гинекологический анамнез. Вторичное бесплодие 7 лет, смешанный фактор. Поликистоз почек. Хроническая артериальная гипертензия. Постоперационный гипотиреоз, медикаментозная компенсация. Состояние после тиреоидэктомии от 2009 г, осложнения: Экстракорпоральное оплодотворение и перенос эмбриона. Рубец на матке после операции кесарева сечения. Хроническая фетоплацентарная недостаточность, компенсация. Нарушение плацентарного кровотока 1А степени.
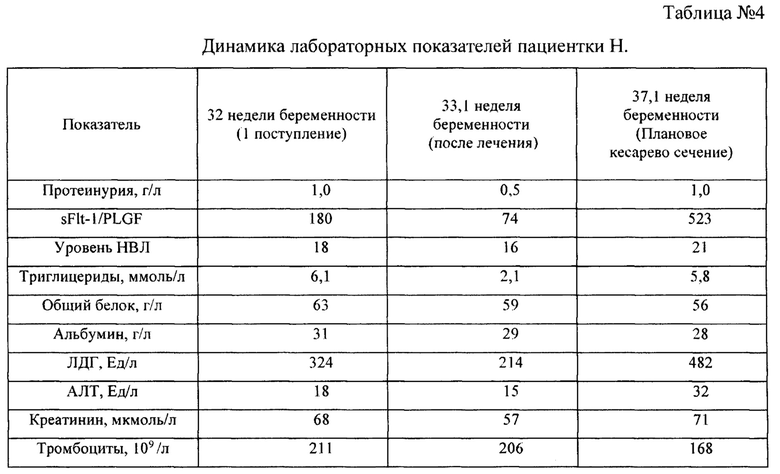
Проведена повторная плановая госпитализация при сроке беременности 37,1 недель для оперативного родоразрешения. При поступлении состояние пациентки удовлетворительное. Активных жалоб нет. Умеренные отеки нижних конечностей, рук, лица. АД 140/90 мм рт.ст. Суточная протеинурия 1 г/л. По лабораторным данным отмечено увеличение отношения sFlt-1/PLGF, увеличение уровня НВЛ, увеличение уровня триглицеридов, что подтверждает выставленный при первом обращении диагноз ПЭ. Остальные исследованные лабораторные показатели находились в пределах нормальных значений для данного срока беременности. После стандартной предоперационной подготовки пациентке проведено плановое кесарево сечение. Родилась живая доношенная девочка с весом 2420 г, ростом 47 см с оценкой по шкале Апгар - 8-9 баллов. Течение послеоперационного периода у матери и раннего неонатального периода у новорожденной протекало без осложнений. На 4-е сутки пациентка с ребенком выписаны из стационара.
Таким образом, применение патентуемого способа позволило улучшить состояние пациентки Н., предотвратить быстрое прогрессирование ранней преэклампсии и продлить беременность на 36 дней до доношенного срока.
Клинический пример №2. Пациентка Б., 37 лет, поступила в Видновский перинатальный центр по каналу скорой помощи с жалобами на бессимптомное повышение АД до 150/100 мм рт.ст. в последние несколько дней. Срок беременности при поступлении 33,1 неделя. Данная беременность первая у пациентки с сопутствующей патологией: ревматоидный артрит, серонегативный, суставная форма, стадия 2, активность 1. ФН 2. Гестационный сахарный диабет, диетотерапия. Протеинурия при поступлении 1 г/л. На учете в женской консультации состоит с 7 недель беременности, беременность протекала без осложнений, повышений АД, изменений в лабораторных данных до поступления в стационар не отмечалось. В анамнезе бесплодие в течение 23 лет, не обследовалась.
Учитывая впервые выявленное повышение АД и протеинурию, пациентка для дообследования и стабилизации состояния госпитализирована в палату интенсивной терапии с диагнозом умеренная преэклампсия с высоким риском прогрессирования до тяжелой. В палате интенсивной терапии начата комбинированная гипотензивная терапия в сочетании с магнезиальной терапией, проведена профилактика РДС плода, выполнена расширенная лабораторная диагностика (Таблица №5). Проведен суточный мониторинг артериального давления (СМАД): Суточный профиль АД изменен по гипертоническому типу, диастолическая артериальная гипертензия с эпизодом смешанной в первой половине ночного сна.
Полученные лабораторные данные и результаты СМАД подтвердили диагноз преэклампсии. Учитывая стабильное состояние пациентки и удовлетворительное состояние плода по данным допплерографии и КТГ, принято решение о проведении сеанса плазмафереза с последующим проведением двух сеансов селективной каскадной плазмофильтрации.
На фоне продолжения комбинированной гипотензивной терапии, согласно действующим клиническим рекомендациям [1], проведен один сеанс плазмафереза с применением фильтра ПФМ-500 с удалением 500 мл плазмы. На следующий день проведен первый сеанс селективной каскадной плазмофильтрации, с последовательной перфузией крови через фильтр ПФМ-500, где кровь разделяют на форменные элементы, которые возвращают в кровяное русло, а полученную плазму направляют на второй фильтр - фракционатор «Evaflux 2А20» с точкой отсечения веществ с молекулярной массой более 70кДа, который размещен последовательно после фильтра ПФМ-500. Второй сеанс селективной каскадной плазмофильтрации проводился через 3 дня.
Объем фильтрованной плазмы за два сеанса составил 2100 и 1800 мл соответственно. После проведенного курса отмечено значительное улучшение лабораторных показателей (Таблица №5), стабилизация показателей АД и общего самочувствия. Выписана домой в удовлетворительном состоянии.
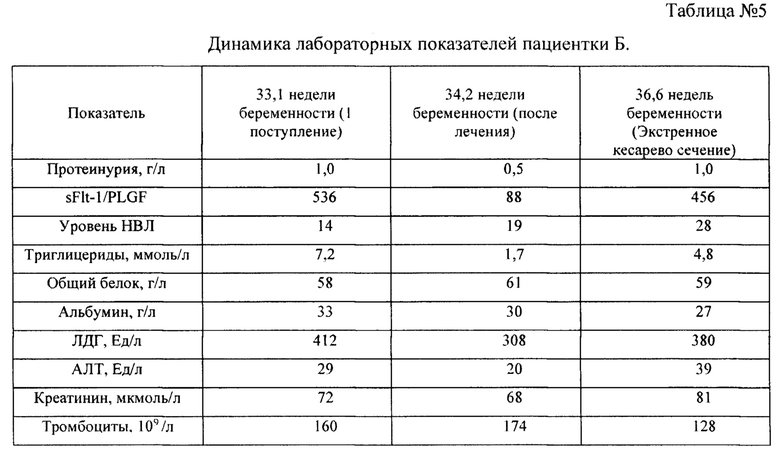
Повторная госпитализация через 28 дней в сроке 36,6 недель. Отмечает повышение АД до 170/100 мм рт.ст. на фоне проводимой терапии, эпизоды тяжести в затылочной области, головокружение. По лабораторным данным отмечено повторное повышение уровня sFlt-1/PLGF, НВЛ, триглицеридов, снижение содержания тромбоцитов, протеинурию 1 г/л. Пациентка госпитализирована в палату интенсивной терапии с диагнозом: Первая беременность в 37 лет, 36,6 недель. Первичное бесплодие 23 года. Ревматоидный артрит, серонегативный, суставная форма, стадия 2, активность 1. ФН 2.
Нарушение жирового обмена 2 ст.Осложнения: Тяжелая преэклампсия. Гестационный сахарный диабет, диетотерапия. После стабилизации состояния выполнено экстренное кесарево сечение. Родилась живая доношенная девочка весом 2600 г, ростом 47 см, с оценкой по шкале Апгар 8-9 баллов, переведена в отделение новорожденных. Пациентка с новорожденной выписаны из стационара на 6-е сутки после родов без осложнений. В представленном клиническом случае, несмотря на прогрессирование тяжести преэклампсии при повторном поступлении пациентки, благодаря патентуемому способу удалось пролонгировать беременность на 30 дней. В результате родился доношенный ребенок, не потребовавший респираторной поддержки и госпитализации в отделение реанимации. Состояние матери также быстро стабилизировалось сразу после родоразрешения.
Клинический пример №3. Пациентка Л., 38 лет, доставлена бригадой скорой помощи в приемное отделение ГБУЗ МО «Видновский перинатальный центр» по направлению из женской консультации, где во время приема был впервые отмечен подъем АД до 160/100 мм рт.ст. При поступлении состояние расценено как средней тяжести. Предъявляет жалобы на общую слабость, головокружение. При осмотре АД 160/100 мм рт.ст. на правой руке, 150/90 мм рт.ст. - на левой. Нарушений зрения нет. Выявлена отечность верхних и нижних конечностей, лица, протеинурия 1 г/л. Из сопутствующей патологии отмечает хронический пиелонефрит в стадии ремиссии, киста левой почки, аллергический ринит в стадии ремиссии. НЖО 1 степени. С диагнозом 3 беременность в головном предлежании 30,3 недель в 38 лет, умеренная преэклампсия переведена в палату интенсивной терапии для стабилизации состояния и динамического наблюдения.
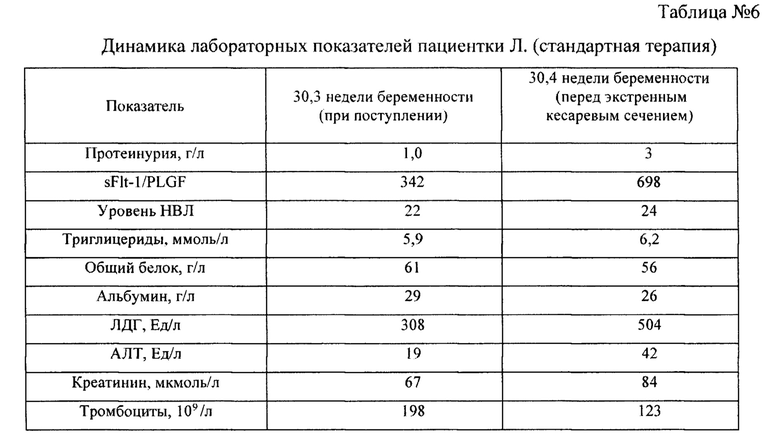
При поступлении в палату интенсивной терапии отмечается повышение уровня триглицеридов до 5.9 ммоль/л, sFlt-1/PLGF до 342, уровень НВЛ - 22. Остальные лабораторные показатели в пределах нормы для данного срока беременности (Таблица №6).
В отделении интенсивной терапии начата терапия в соответствии с клиническими рекомендациями [1] и профилактика РДС плода. Через 24 часа на фоне проводимой терапии и снижения АД до 130/80 мм рт.ст. пациентка пожаловалась на головную боль, появление мелькания «мушек» перед глазами. По лабораторным данным отмечена отрицательная динамика (Таблица №6). В связи с прогрессированием симптомов тяжелой преэклампсии, угрозой жизни матери и плода в экстренном порядке переведена в операционную для оперативного родоразрешения. Родился живой недоношенный мальчик весом - 1440, рост - 29 см с оценкой по Апгар - 7-8 баллов. Сразу после рождения проведен комплекс реанимационных мероприятий, для улучшения функции дыхания введено 2 дозы препарата сурфактанта. Тяжелое состояние новорожденного, обусловленное дыхательной недостаточностью, потребовало проведения инвазивной респираторной поддержки в течение 72 часов и последующей неинвазивной респираторной терапии в режиме CP АР в течение 52 часов. Продолжительность лечения в отделении реанимации новорожденных составила 12 суток с последующим переводом на второй этап выхаживания в отделение патологии новорожденных, где ребенок находился на лечении еще 22 дня.
Пациентка выписана на 6-е сутки с рекомендациями наблюдения в динамике в амбулаторных условиях с заключительным диагнозом: 2 преждевременные оперативные роды в 31,2 недель. Проведение срочного кесарева сечения. Сопутствующие: Отягощенный акушерско-гинекологический анамнез. Хронический пиелонефрит, ремиссия. Киста почки слева. Аллергический ринит, ремиссия. Ожирение 1 степени. Осложнения: Тяжелая преэклампсия. Повышение резистентности в маточных артериях. Повышение резистентности в артерии пуповины. Внутрипеченочный холестаз беременных. Тазовое предлежание плода. Задержка роста плода. Рубец на матке после операции кесарева сечения.
Актуальные на настоящее время клинические рекомендации [1] четко определяют критерии постановки диагноза тяжелой преэклампсии, схему медикаментозной поддержки, которая предназначена для стабилизации состояния пациентки и подготовки к экстренному родоразрешению. Единственным методом лечения тяжелой преэклампсии на настоящий момент остается экстренное родоразрешение в интересах матери. При раннем развитии преэклампсии и преждевременных родах рекомендуется предварительная подготовка легких плода проведением курса стероидной терапии, который, как правило, занимает 12-24 часа. Наиболее благоприятные условия для родоразрешения с точки зрения подготовленности легких плода создаются при наличии интервала от 24 часов и более между завершением профилактики РДС плода и родоразрешением.
В приведенных клинических примерах №1 и №2 пациенткам была применена методика по патентуемому способу, что позволило не только подготовить легкие плода к рождению, но и стабилизировать состояние женщин с уменьшением лабораторных и клинических проявлений этого осложнения и продлить беременность до доношенного срока (пример №1) или почти доношенного (пример №2). В результате применения предлагаемого способа новорожденным не требовались реанимационные мероприятия в период новорожденности, после рождения они были переведены в палату совместного пребывания матери и ребенка и выписаны домой в обычные сроки. В отличие от приведенных первых двух клинических примеров, в клиническом примере №3 пациентке проведено стандартное лечение в соответствии с рекомендациями [1], проведена профилактика РДС плода. Тем не менее, состояние пациентки прогрессивно ухудшалось и потребовало экстренного родоразрешения. В этих условиях ребенок родился глубоко недоношенным с недостаточной подготовкой респираторной системы, что потребовало длительной терапии в условиях реанимации.
Результаты исследований подтверждают достижение технического результата в части пролонгирования сроков беременности и улучшения неонатальных исходов за счет удаления антиангиогенного фактора растворимой fms-подобной тирозинкиназы-1 и атерогенных липопротеидов при сохранении содержания альбумина и плацентарного фактора роста. Это обеспечивает более высокий вес при рождении, более высокую оценку по шкале Апгар при рождении, меньшую потребность в сурфактанте, меньшую потребность в респираторной поддержке и ее длительности, снижение продолжительности пребывания в отделении реанимации по сравнению с группой контроля.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ дифференциальной диагностики изолированной преэклампсии и преэклампсии, развившейся на фоне недиагностированной хронической артериальной гипертензии | 2019 |
|
RU2713436C1 |
| Способ диагностики преэклампсии у беременных с хронической болезнью почек | 2016 |
|
RU2623057C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ВЕДЕНИЯ БЕРЕМЕННЫХ С ПРЕЭКЛАМПСИЕЙ СРЕДНЕЙ СТЕПЕНИ ТЯЖЕСТИ | 2011 |
|
RU2477481C1 |
| Способ прогнозирования эффективности лечения преэклампсии средней тяжести | 2020 |
|
RU2752715C1 |
| СПОСОБ ЛЕЧЕНИЯ ПРЕЭКЛАМПСИИ СРЕДНЕЙ СТЕПЕНИ ТЯЖЕСТИ У ЖЕНЩИН С АЛИМЕНТАРНЫМ ОЖИРЕНИЕМ | 2014 |
|
RU2549668C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПРЕЭКЛАМПСИИ У БЕРЕМЕННЫХ С ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТЬЮ | 2013 |
|
RU2545760C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ У БЕРЕМЕННЫХ С САХАРНЫМ ДИАБЕТОМ 2 ТИПА | 2022 |
|
RU2800716C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЯЖЕСТИ ТЕЧЕНИЯ РАННЕЙ ПРЕЭКЛАМПСИИ | 2021 |
|
RU2753463C1 |
| Способ формирования группы риска развития преэклампсии | 2021 |
|
RU2762204C1 |
| Способ прогнозирования эффективности лечения преэклампсии средней тяжести | 2019 |
|
RU2705374C1 |
Изобретение относится к медицине, а именно к анестезиологии-реаниматологии, интенсивной терапии, акушерству и гинекологии, и может быть использовано при пролонгировании беременности при ранней преэклампсии. Выполняют процедуру мембранного плазмафереза. Затем на следующие сутки с интервалом три дня проводят два сеанса каскадной плазмофильтрации, состоящей в последовательной перфузии крови через два фильтра, при этом на первом фильтре кровь разделяют на форменные элементы, которые возвращают в кровяное русло, а полученную плазму направляют на второй фильтр с точкой отсечения веществ с молекулярной массой более 70 кДа. При этом за один сеанс фильтруют весь объем циркулирующей плазмы, после чего ее возвращают пациентке. Способ позволяет осуществить пролонгирование сроков беременности, улучшить неонатальные исходы, а именно: более высокий вес при рождении, более высокая оценка по шкале Апгар при рождении, меньшая потребность в сурфактанте, меньшая потребность в респираторной поддержке и снижение ее длительности, путем удаления антиангиогенного фактора растворимой fms-подобной тирозинкиназы-1 и атерогенных липопротеидов при сохранении содержания альбумина и плацентарного фактора роста за счет совокупности приемов заявленного изобретения. 3 з.п. ф-лы, 6 табл., 3 пр.
1. Способ ведения беременности при ранней преэклампсии, включающий проведение процедуры мембранного плазмафереза,
отличающийся тем, что
на следующие сутки после проведения мембранного плазмафереза с интервалом три дня проводят два сеанса каскадной плазмофильтрации, состоящей в последовательной перфузии крови через два фильтра, при этом на первом фильтре кровь разделяют на форменные элементы, которые возвращают в кровяное русло, а полученную плазму направляют на второй фильтр с точкой отсечения веществ с молекулярной массой более 70 кДа, при этом за один сеанс фильтруют весь объем циркулирующей плазмы, после чего ее возвращают пациентке.
2. Способ по п. 1, отличающийся тем, что в процессе мембранного плазмафереза отбирают не более 500 мл плазмы.
3. Способ по п. 1, отличающийся тем, что в качестве первого фильтра используют фильтр ПФМ-500 производства ЗАО «Плазмофильтр».
4. Способ по п. 1, отличающийся тем, что в качестве второго фильтра используют последовательно установленные фильтр ПФМ-500 производства ЗАО «Плазмофильтр» и фракционатор плазмы Evaflux 2А20 производства фирмы Kawasumi Laboratories, Япония.
| БЕЛОЦЕРКОВЦЕВА Л.Д | |||
| и др | |||
| Опыт применения каскадной плазмофильтрации при ранней преэклампсии | |||
| Вопросы гинекологии, акушерства и перинатологии | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Способ закалки пил | 1915 |
|
SU140A1 |
| Прибор для сложения и вычитания | 1929 |
|
SU22970A1 |
| БЕЛОЦЕРКОВЦЕВА Л.Д | |||
| и др | |||
| Ранняя преэклампсия и возможность пролонгирования беременности с точки зрения патогенетического подхода | |||
| Общая реаниматология | |||
Авторы
Даты
2023-09-15—Публикация
2023-02-16—Подача