Область техники
Настоящее изобретение относится к фармацевтической промышленности и касается новых производных полиенового антибиотика натамицина, полученных амидированием карбоксильной группы, а также их медицинского применения для лечения грибковых инфекций, вызванных дрожжеподобными грибками рода Candida.
Уровень техники
Внутрибольничные системные микозы являются одной из основных причин смертности пациентов с угнетенной иммунной системой, вызванной онкологическими заболеваниями или активной формой ВИЧ (СПИД), а также иммуносупресссией при трансплантациях органов и тканей. В период пандемии COVID-19 под угрозой заражения системными микозами оказались также и пациенты с тяжелой формой протекания коронавирусной инфекции [Segrelles-Calvo G., de S 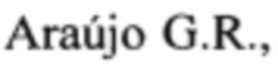 Frases S. Future Microbiol. 2020, 15, 1405-1413]. Для терапии микозов препаратами выбора являются азолы и эхинокандины; однако их широкое применение привело к снижению их эффективности - ряд исследований подтверждает распространение штаммов патогенных грибов, устойчивых и к азолам, и к эхинокандинам [Shields R.K., Nguyen Μ.Η., Clancy C.J. Curr. Opin. Infect. Dis. 2015, 28 (6), 514-522; Whaley S.G., Berkow E.L., Rybak J.M. et al. Front. Microbiol. 2017, 7, 2173]. Препаратом резерва для лечения резистентных грибковых инфекций является амфотерицин В (1). Этот полиеновый макролидный антибиотик используется в клинической практике с 1958 года, и несмотря на длительную историю применения в качестве противогрибкового средства, случаи резистентности к нему регистрируются крайне редко. Его близкий аналог нистатин (2) широко применяют для профилактики и лечения кандидозов. Еще один противогрибковый полиеновый антибиотик - натамицин (3), используется в качестве консерванта в пищевой промышленности, а также применяется для местного лечения микозов кожи и слизистых оболочек. Несмотря на это, случаи возникновения резистентности к натамицину или перекрестной резистентности к другим полиенам практически не встречаются [Streekstra Η., Verkermis А.Е.Е., Jacobs R. et al. Int. J. Food Microbiol. 2016, 238, 15-22]. Однако крайне низкая растворимость в воде, высокая нефротоксичность и гемолитическое действие природных полиенов серьезно ограничивают их использование для терапии микозов.
Frases S. Future Microbiol. 2020, 15, 1405-1413]. Для терапии микозов препаратами выбора являются азолы и эхинокандины; однако их широкое применение привело к снижению их эффективности - ряд исследований подтверждает распространение штаммов патогенных грибов, устойчивых и к азолам, и к эхинокандинам [Shields R.K., Nguyen Μ.Η., Clancy C.J. Curr. Opin. Infect. Dis. 2015, 28 (6), 514-522; Whaley S.G., Berkow E.L., Rybak J.M. et al. Front. Microbiol. 2017, 7, 2173]. Препаратом резерва для лечения резистентных грибковых инфекций является амфотерицин В (1). Этот полиеновый макролидный антибиотик используется в клинической практике с 1958 года, и несмотря на длительную историю применения в качестве противогрибкового средства, случаи резистентности к нему регистрируются крайне редко. Его близкий аналог нистатин (2) широко применяют для профилактики и лечения кандидозов. Еще один противогрибковый полиеновый антибиотик - натамицин (3), используется в качестве консерванта в пищевой промышленности, а также применяется для местного лечения микозов кожи и слизистых оболочек. Несмотря на это, случаи возникновения резистентности к натамицину или перекрестной резистентности к другим полиенам практически не встречаются [Streekstra Η., Verkermis А.Е.Е., Jacobs R. et al. Int. J. Food Microbiol. 2016, 238, 15-22]. Однако крайне низкая растворимость в воде, высокая нефротоксичность и гемолитическое действие природных полиенов серьезно ограничивают их использование для терапии микозов.
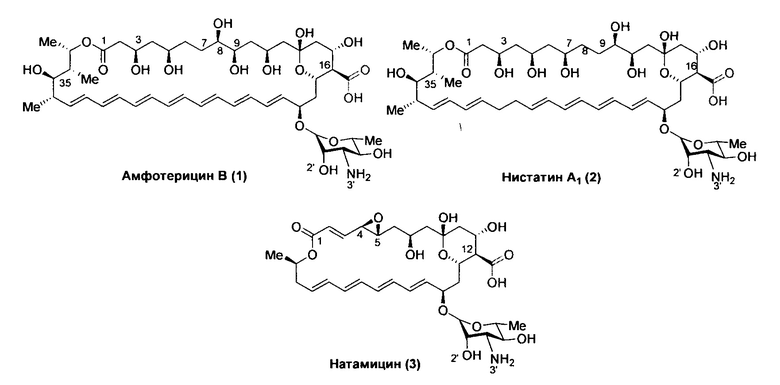
Общей структурной особенностью полиеновых макролидов является наличие 20-44-членного макролактонового кольца, содержащего от 3 до 7 сопряженные двойные связи. Физико-химические и биологические свойства этих антибиотиков во многом обусловлены амфотерным характером и цвиттерионным строением (карбоксильная группа несет отрицательный заряд, а аминогруппа микозамина - положительный), а также амфифильным характером их молекул (одна половина макроцикла (полиольная цепь) - гидрофильная, вторая (полиеновая) - гидрофобная).
Несмотря на длительную историю успешного применения в медицине, механизм противогрибкового действия полиенов до сих пор окончательно не установлен. Считается, что основной механизм действия полиеновых антибиотиков связан с нарушением нормальной функции клеточной мембраны за счет взаимодействия с эргостерином (в клетках грибов) или холестерином (в клетках млекопитающих) и порообразующей активностью в случае амфотерицина В (1) и нистатина (2). В отличие от них, натамицин (3) с макролактонным кольцом меньшего размера (26 атомов в кольце в сравнении с 38 атомами в случае амфотерицина В и нистатина) не образует пор в мембранах грибковых клеток, а его противогрибковый эффект основан только на специфическом связывании с эргостерином [Welscher Y.M., Napel Н.Н. ten, Balague М.М. et al. J. Biol. Chem., 2008, 283(10), 6393-6401].
Ранее был описан ряд примеров химической модификации полиеновых антибиотиков амфотерицина В (1) и нистатина (2) по карбоксильной группе и показано, что введение аминогрупп с дополнительным основным фрагментом значительно повышает растворимость, а также в ряде случаев усиливает противогрибковую активность антибиотиков [Seco Ε.Μ., Cuesta Т., Fotso S., Laatsch H., Malpartida F. Chem. Biol. 2005, 12(5), 535-543;  de Vries A.H., Espinosa-Caballero M. et al. PLOS ONE 2016, 11 (9), e0162171; Tevyashova A.N., Bychkova E.N., Solovieva S.E. et al. ACS Infect. Dis. 2020, 6 (8), 2029-2044; Amir Α., Levin-Khalifa M., Dvash T. ACS Med. Chem. Lett. 2022, 13 (2), 182-187]. Введение аминогрупп с дополнительным основным фрагментом в структуру полиенового антибиотика натамицина (2) для улучшения его свойств ранее не предпринималось, и является новым перспективным направлением создания эффективных противогрибковых препаратов.
de Vries A.H., Espinosa-Caballero M. et al. PLOS ONE 2016, 11 (9), e0162171; Tevyashova A.N., Bychkova E.N., Solovieva S.E. et al. ACS Infect. Dis. 2020, 6 (8), 2029-2044; Amir Α., Levin-Khalifa M., Dvash T. ACS Med. Chem. Lett. 2022, 13 (2), 182-187]. Введение аминогрупп с дополнительным основным фрагментом в структуру полиенового антибиотика натамицина (2) для улучшения его свойств ранее не предпринималось, и является новым перспективным направлением создания эффективных противогрибковых препаратов.
Раскрытие изобретения
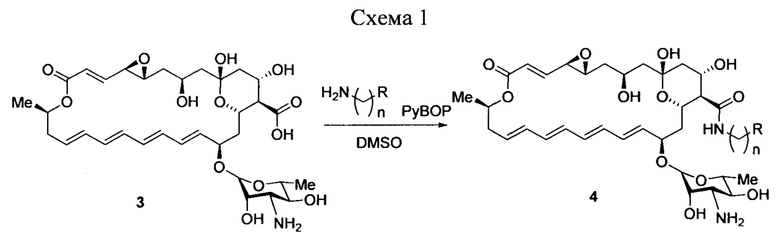
Целью настоящего изобретения ставится создание более эффективных противогрибковых средств на основе новых полусинтетических амидов натамицина (3), в частности, производных, содержащих амидную группу в С12 положении макроцикла, в структуре которых содержится дополнительная группа основного характера. Производные этого хемотипа обладают значительно более высокой растворимостью в водных фармацевтически приемлемых средах, а также в некоторых случаях обладают большей активностью в отношении дрожжеподобных грибков Candida spp., по сравнению с природным антибиотиком. Настоящее изобретение включает соединения, соответствующие структурной формуле 4, их метод одностадийного синтеза, а также применение соединений формулы 4, а также их фармакологически приемлемых солей и их сольватов для лечения микозов, прежде всего, вызванных штаммами Candida spp.
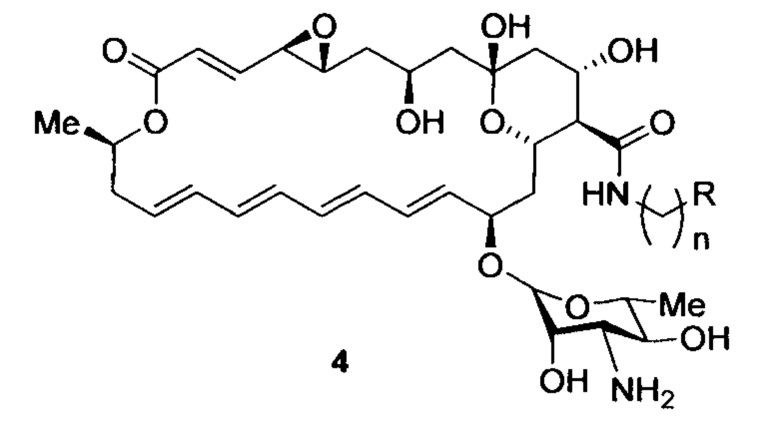
где R - независимо означает аминогруппу; алкиламиногруппу, необязательно замещенную арилом, галогенарилом или гидроксигруппой; пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, необязательно кватернизованные алкильной группой; n=1-4.
Амиды натамицина, соответствующие формуле 4, могут быть получены конденсацией натамицина (3) и аминопроизводного, с использованием методов, хорошо известных из текущего уровня техники [Bailey P.D., Collier I.D., Morgan K.М. 5.06 -Amides /Eds.: A.R. Katritzky, O. Meth-Cohn, C.W. Rees. Elsevier Science. 1995, 257-307]. Так, для синтеза могут быть использованы конденсирующие агенты (РуВОР, ВОР, TBTU, HBTU, HCTU, TCTU, HATU, COMU) [Han S.-Y., Kim Y.-A. Tetrahedron, 2004, 60(11), 2447-2467], а также в качестве оснований амины или их соли, необходимые для поддержания оптимального рН (7.5-9) в подходящем инертном апротонном растворителе (Схема 1). На предварительном этапе аминогруппа натамицина и/или одна из аминогрупп диамина может быть защищена получением соответствующего карбамата (9-флуоренилметилкарбамата, трет-бутоксикарбамата), с использованием методов, хорошо известных из текущего уровня техники [Wuts P. G. М., Greene Т. W. Greene's protective groups in organic synthesis. - John Wiley & Sons, 2006]. Так, для ацилирования аминогрупп могут быть использованы ди-трет-бутилдикарбонат, 9-флуоренилметилхлорформиат, N-(9-флуоренилметоксикарбонилокси)сукцинимид, а также подходящие основания и инертные растворители. После проведения конденсации защитные группы могут быть сняты в подходящих условиях, хорошо известных из текущего уровня техники (Вос-защита - действием HCl в метаноле, трифторуксусной кислоты, метансульфокислоты и других подходящих кислот; Fmoc-защита - действием аминов - пиперидина, морфолина, диизопропилэтиламина и других подходящих оснований) [Wuts P. G. М., Greene Т. W. Greene's protective groups in organic synthesis. - John Wiley & Sons, 2006]. Предпочтительным является одностадийный метод конденсации без использования защитных групп.
Сравнительное исследование противогрибковых свойств новых производных натамицина, соответствующих формуле 4, и природного антибиотика натамицина (3) на контрольных штаммах С parapsilosis АТСС 22019, С.albicans АТСС 10231, A. fumigatus АТСС 46645, а также в отношении Т. rubrum 2002 и A. niger 37а и широкой панели клинических изолятов штаммов Candida spp.показало, что новая модификация карбоксильной группы натамицина позволяет повысить анти-кандидозную активность производных, в т.ч. в отношении резистентных к флуконазолу штаммов. На модели кандидозного сепсиса in vivo показана возможность применения водорастворимых производных натамицина для лечения системных микозов.
Таким образом, изобретение также включает способ лечения грибковых инфекций, вызванных штаммами Candida spp., в том числе, нечувствительными или малочувствительными к другим классам противогрибковых препаратов (азолам и эхинокандинам), предусматривающий введение нуждающемуся субъекту терапевтически эффективного количества производного натамицина, соответствующего формуле 4.
Если не указано иное, термины, используемые в описании заявки и пунктах формулы изобретения, имеют значения, указанные ниже. Следует отметить, что, если не указано иное, используемые в описании и пунктах формулы формы единственного числа включают также формы множественного числа.
«Алкил» означает одновалентный насыщенный углеводородный радикал с прямой или разветвленной цепью, включающий только атомы углерода и водорода и содержащий от 1 до включительно 14 атомов углерода.
«Алкиламино» означает радикалы -NHR и -NR2, где R означает указанный выше алкильный радикал.
«Арил» означает моноциклическое кольцо или конденсированную бициклическую систему, состоящую из атомов углерода и водорода, отвечающую критериям ароматичности, включает без ограничения перечисленным такие радикалы, как фенил и нафтил.
«Галоген» означает радикал фтора, брома, хлора, йода.
«Галогенарил» означает указанный выше арильный радикал, независимо замещенный 1, 2 или 3 атомами галогенов.
«Конденсирующий агент» означает органические соединения, используемые для активации (повышения реакционной способности) карбоксильной группы в реакциях амидирования [Han S.-Y., Kim Y.-A. Tetrahedron, 2004, 60(11), 2447-2467] и независимо относящиеся по химической природе к фосфониевым солям, включающим без ограничения перечисленным такие реактивы, как ВОР, РуВОР, PyBrOP, урониевыем/аминиевым солям, включающим без ограничения перечисленным такие вещества, как HBTU, HATU, TBTU, COMU и карбодиимиды, включающим без ограничения перечисленным такие вещества, как DCC, EDC, DIC.
«Инертный органический растворитель» означает растворитель, инертный в условиях описываемой в тексте реакции, включающий, например, Ν,Ν-диметилформамид, Ν,Ν-диметилацетамид, N-метилпирролидон, диметилсульфоксид, сульфолан, бензол, толуол, ацетонитрил, тетрагидрофуран, хлороформ, дихлорметан, дихлорэтан, этилацетат, ацетон, метилэтилкетон, метанол, этанол, пропанол, изопропанол, трет-бутаноп, диоксан, пиридин и т.п. Если не указано иное, растворители, использованные в реакциях по настоящему изобретению, являются инертными растворителями.
«Сольваты» означает сольватированные формы, содержащие стехиометрическое или нестехиометрическое количество растворителя. Некоторые соединения способны удерживать в кристаллической решетке фиксированное количество молекул растворителя, образуя сольват. Гидраты образуются в том случае, если в качестве растворителя используется вода, а алкоголяты образуются в том случае, если растворителем является спирт.
«Субъект» означает млекопитающих, т.е. любого члена класса млекопитающих, включая, без ограничения перечисленным, человека, сельскохозяйственных животных, лабораторных животных и т.п., предпочтительно, человека. Термин субъект не означает конкретный возраст или пол пациента.
«Терапевтически эффективное количество» означает количество соединения, которое при введении субъекту (пациенту) для лечения патологического состояния является достаточным для оказания фармакологического действия при лечении патологического состояния субъекта. Терапевтически эффективное количество варьируется в зависимости от типа соединения, патологического состояния подлежащего лечению, тяжести болезни, возраста и относительного состояния здоровья субъекта, от способа и формы введения, от мнения лечащего врача или практикующего ветеринара и других факторов.
«Фармакологическое действие» означает термин, используемый в описании заявки, включает результаты воздействия на субъект, при которых достигается предполагаемая цель терапии. Например, фармакологическое действие означает такие результаты воздействия, которые приводят к излечению или замедлению развития заболевания, предупреждению его рецидива.
«Фармацевтически приемлемый» означает материал, который используют при получении фармацевтической композиции, и который обычно является безопасным, не токсичным, безопасным в биологическом или ином отношении и включает материал, приемлемый как в ветеринарии, так и в фармацевтике.
«Фармацевтически приемлемые соли» соединений означают соли, которые являются фармацевтически приемлемыми и обладают необходимой фармакологической активностью исходного соединения. Такие соли включают кислотно-аддитивные соли неорганических кислот, таких, как хлористоводородная кислота, бромистоводородная кислота, серная кислота, фосфорная кислота и т.п., или органических кислот, таких, как уксусная кислота, бензойная кислота, лимонная кислота, фумаровая кислота, глутаминовая кислота, гликолевая кислота, молочная кислота, малеиновая кислота, яблочная кислота, метансульфоновая кислота, пропионовая кислота, салициловая кислота, янтарная кислота, винная кислота, толуолсульфоновая кислота и т.п. Подразумевается, что фармацевтически приемлемые соли включают сольваты или кристаллические формы (полиморфные образования) указанной кислотно-аддитивной соли. Предпочтительными фармацевтически приемлемыми солями являются соли соляной кислоты, серной кислоты, метансульфоновой кислоты, уксусной кислоты, адипиновой кислоты, янтарной кислоты, фумаровой кислоты, щавелевой кислоты, фосфорной кислоты.
Исходный натамицин (3), РуВОР, диизопропилэтиламин, триэтиламин гидрохлорид, диметилсульфоксид, растворители и прочие реагенты являются коммерческими химическими соединениями, поставляемыми фирмами, такими, как Aldrich, Merck или Acros. Исходные амины также могут быть коммерчески доступными химическими соединениями или могут быть получены методами, известными специалисту в данной области или описанными в литературе [Wang et al., Tetrahedron, 2009, 65, 50, 10377; Moiseenko E.I. et al., Macroheterocycles, 2019, 12 (1), 98].
Примеры, показывающие возможность получения новых производных натамицина, соответствующих формуле 4, являющихся предметом настоящего изобретения, а также их физико-химические свойства, антибактериальная активность и терапевтическая эффективность in vivo, описанные ниже, приводятся лишь для иллюстрации настоящего изобретения, а не для ограничения объема притязаний.
Пример 1. Диацетат N-(2-аминоэтил)амида натамицина (4-1)
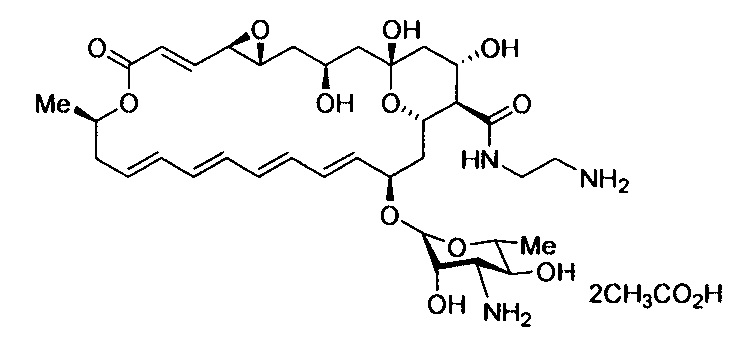
Метод А. К раствору натамицина (3, 0.70 г, 1.05 ммоль) в ДМСО (7 мл) при перемешивании прибавляют этилендиамин (0.32 г, 5.26 ммоль), затем в течение 1.5 ч равными частями прибавляют РуВОР (0.82 г, 1.58 ммоль). Реакционную смесь перемешивают при комнатной температуре 3 ч, затем прибавляют диэтиловый эфир (20 мл). Смесь интенсивно встряхивают 3 мин, слой диэтилового эфира удаляют и повторяют процедуру несколько раз до тех пор, пока не сформируется вязкое масло. К маслу прибавляют метанол (5 мл) и диэтиловый эфир (50 мл); образующийся осадок отфильтровывают, промывают эфиром и сушат в эксикаторе. Полученный продукт очищают методом обращено-фазовой хроматографии (элюент А - вода, водн. NH4OH и водн. АсОН, элюент В - ацетонитрил (MeCN)): 0,5% водн. NH4OH/MeCN (В: 0→20%), затем H2O/MeCN (В: 20%), 0,5% водн. АсОН /MeCN (20→60%). Фракции, содержащие целевое вещество, объединяют, прибавляют изопропиловый спирт и упаривают до минимального объема. К раствору прибавляют Et2O, выпавший осадок отфильтровывают и сушат. Контроль прохождения реакции и хроматографической очистки производится с помощью тонкослойной хроматографии в системе н-PrOH-EtOAc-NH4OH, 3:3:2. Чистота конечного соединения определяется методом ВЭЖХ (элюент А - 0.2% HCOONH4 при рН 4.5, элюент В - ацетонитрил). Выход 274 мг (33%), порошок желто-бежевого цвета, т.пл. 174-176°С (разл.); Rf 0.44; Rt (В, %: 30→60% в течение 15 мин) 5.70 мин; чистота 97.4%; HRMS (ESI) m/z: [М+Н]+ вычислено для C35H54N3O12+ 708.3702; найдено 708.3705. Найдено, %: С 56.34, Η 7.34, N 5.07; вычислено для C35H54N3O12*2СН3СООН*4H2O, %: С 56.58, Η 7.43, N 5.08. ЯМР 1H (δ, м.д.): 8,15 (1Н, NH); 6,50 (1Н, СН); 6,27 (1Н, СН); 6,22 (1Н, СН); 6,17 (1Н, СН); 6,16 (1Н, СН); 6,11 (1Н, СН); 6,10 (1Н, СН); 6,06 (1Н, СН); 5,87 (1Н, СН); 5,60 (1Н, СН); 4,68 (1Н, СН); 4,34 (1Н, НС-О); 4,26 (1Н, СН); 4,24 (1Н, НС-О); 4,14 (1Н, СН); 4,05 (1Н, СН); 3,64 (1Н, СН); 3,23 (1Н, НС-О); 3,15 (2Н, СН2); 3,03 (1Н, СН); 2,93(1Н, СН); 2,75 (1Н, НС-О); 2,65 (2Н, СН2); 2,47 (1Н, СН); 2,38 (1Н, СН2); 2,20 (1Н, СН2); 1,98 (1Н, СН2); 1,96 (1Н, СН2); 1,88 (1Н, СН); 1,84 (1Н, СН2); 1,58 (1Н, СН2); 1,50 (1Н, СН2); 1,47 (1Н, СН2); 1,25 (3Н, СН3); 1,14 (3Н, СН3); 1,15 (1Н, СН2); 1,10 (1Н, СН2). ЯМР 13С (δ, м.д.): 172,1; 164,4; 144,6; 136,5; 135,4; 133,4; 131,9; 131,4; 131,2; 128,6; 128,5; 124,5; 97,0; 96,8; 74,3; 73,1; 72,6; 69,6; 69,3; 66,1; 65,1; 64,6; 58,0; 57,4; 56,4; 53,6; 46,3; 44,4; 40,8; 40,6; 40,6; 39,1, 36,6; 20,2; 17,9.
Метод Б. К раствору натамицина (3, 0.70 г, 1.05 ммоль) в ДМСО (7 мл) при перемешивании прибавляют этилендиамин (0.32 г, 5.26 ммоль) и гидрохлорид триэтиламина (0.72 г, 5.26 ммоль), затем в течение 1.5 ч равными частями прибавляют РуВОР (0.82 г, 1.58 ммоль). Реакционную смесь перемешивают при комнатной температуре 3 ч, затем прибавляют диэтиловый эфир (20 мл). Смесь интенсивно встряхивают 3 мин, слой диэтилового эфира удаляют и повторяют процедуру несколько раз до тех пор, пока не сформируется вязкое масло. К маслу прибавляют метанол (5 мл) и диэтиловый эфир (50 мл); образующийся осадок отфильтровывают, промывают эфиром и сушат в эксикаторе. Полученный продукт очищают методом обращено-фазовой хроматографии (элюент А - вода, водн. ΝΗ4ΟΗ и водн. АсОН, элюент В - ацетонитрил (MeCN)): 0,5% водн. NH4OH/MeCN (В: 0→20%), затем H2O/MeCN (В: 20%), 0,5% водн. АсОН /MeCN (20→60%). Фракции, содержащие целевое вещество, объединяют, прибавляют изопропиловый спирт и упаривают до минимального объема. К раствору прибавляют Et20, выпавший осадок отфильтровывают и сушат. Контроль прохождения реакции и хроматографической очистки производится с помощью тонкослойной хроматографии в системе н-PrOH-EtOAc-NH4OH, 3:3:2. Чистота конечного соединения определяется методом ВЭЖХ (элюент А - 0.2% HCOONH4 при рН 4.5, элюент В - ацетонитрил). Выход 430 мг (52%), порошок желто-бежевого цвета, т.пл. 174-176°С (разл.); Rf 0.44; Rt (В, %: 30→60% в течение 15 мин) 5.70 мин; чистота 95.2%; HRMS (ESI) m/z: [М+Н]+ вычислено для C35H54N3O12+ 708.3702; найдено 708.3705.
Пример 2. Гидрохлорид N-((1-тетрадецилпиридин-1-иум-3-ил)метил)амида натамицина (4-2)
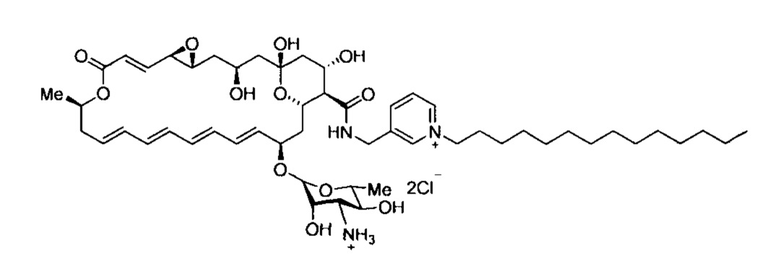
К раствору натамицина (3, 0.70 г, 1.05 ммоль) в ДМСО (7 мл) при перемешивании прибавляют гидрохлорид 3-(аминометил)-1-тетрадецилпиридиния (1.98 г, 5.26 ммоль) и триэтиламин (0.53 г, 5.26 ммоль), затем в течение 1.5 ч равными частями прибавляют РуВОР (0.82 г, 1.58 ммоль). Реакционную смесь перемешивают при комнатной температуре 3 ч, прибавляют диэтиловый эфир (20 мл). Смесь интенсивно встряхивают в 3 мин, затем слой диэтилового эфира удаляют и повторяют процедуру несколько раз до тех пор, пока не сформируется вязкое масло. К маслу прибавляют метанол (5 мл) и диэтиловый эфир (50 мл); образующийся осадок отфильтровывают, промывают эфиром и сушат в эксикаторе. Полученный продукт очищают методом обращено-фазовой хроматографии (элюент А - вода, водн. NH4OH и водн. АсОН, элюент В - MeCN): 0,5% водн. NH4OH/MeCN (В: 0→20%), затем H2O/MeCN (В: 20%), 0,5% водн. АсОН /MeCN (20→60%). Фракции, содержащие целевое вещество, объединяют, прибавляют 0.2 мл 5 Μ HCl в метаноле, перемешивают 10 мин, затем прибавляют изопропиловый спирт и упаривают до небольшого объема. К раствору прибавляют Et20, выпавший осадок отфильтровывают и сушат. Контроль прохождения реакции и хроматографической очистки производится с помощью тонкослойной хроматографии в системе н-PrOH-EtOAc-NH4OH, 3:3:2. Чистота конечного соединения определяется методом ВЭЖХ (элюент А - 0.2%) HCOONH4 при рН 4.5, элюент В - ацетонитрил). Выход 530 мг (53%), порошок бежевого цвета, т.пл. 167-169°С (разл.); Rf 0.48; Rt (В, %: 40-»90% в течение 30 мин) 15.20 мин; чистота 95.5%; HRMS (ESI) m/z: [М]+ вычислено для C53H82N3O12+ 952.5893; найдено 952.5892. ЯМР 1H (δ, м.д.): 8,97 (1Н, СН); 8,94 (1Н, СН); 8,84 (1Н, NH); 8,48 (1Н, СН); 8,12 (1Н, СН); 6,51 (1Н, СН); 6,27 (1Н, СН); 6,23 (1Н, СН); 6,19 (1Н, СН); 6,16 (1Н, СН); 6,12 (1Н, СН); 6,12 (1Н, СН); 6,07 (1Н, СН); 5,88 (1Н, СН); 5,61 (1Н, СН); 4,69 (1Н, СН); 4,69 (2Н, СН2); 4,53 (2Н, СН2); 4,39 (1Н, НС-О); 4,30 (1Н, СН); 4,30 (1Н, НС-О); 4,15 (1Н, СН); 4,10 (1Н, СН); 3,68 (1Н, СН); 3,24 (1Н, НС-О); 3,13 (1Н, СН); 3,03 (1Н, СН); 2,75 (1Н, НС-О); 2,65 (1Н, СН); 2,38 (1Н, СН2); 2,19 (1Н, СН2); 2,05 (1Н, СН); 1,96 (1Н, СН2); 1,93 (1Н, СН2); 1,89 (2Н, СН2); 1,61 (1Н, СН2); 1,53 (1Н, СН2); 1,27-1,20 (22Н, 11СН2); 1,26 (3Н, СН3); 1,19 (1Н, СН2); 1,19 (1Н, СН2); 1,16 (3Н, СН3); 0,85 (3Н, с, СН3). ЯМР 13С (δ, м.д.): 172,8; 164,4; 144,5; 143,4; 143,0; 142,5; 140,6; 135,8; 135,4; 133,3; 131,8; 131,6; 131,5; 128,8; 128,8; 127,6; 124,6; 97,1; 96,2; 74,3; 73,0; 70,8; 69,6; 68,3; 66,2; 65,3; 64,9; 61,0; 57,9; 57,1; 56,0; 53,7; 46,1; 44,0; 40,8; 39,2; 39,0; 36,7; 31,2; 30,7; 28,9; 28,4; 28,3; 25,5; 22,0; 20,2; 17,8; 13,9.
Пример 3. Диацетат N-((2-(2-фторфенил-1 -метил)амино)этил)амида натамицина (4-3)
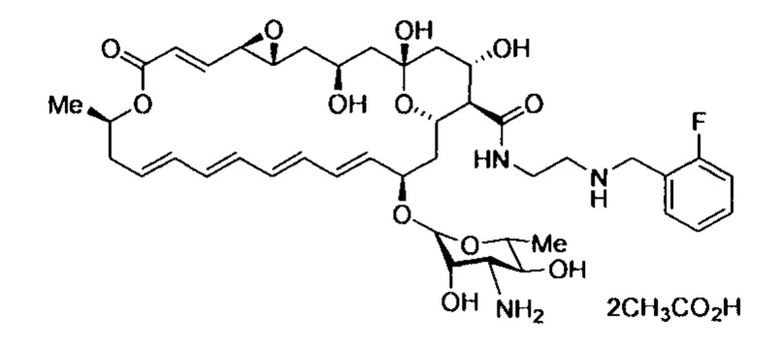
Получают по методике, аналогичной приведенной в примере 1 из натамицина (3) и N-(2-фторбензил)этан-1,2-диамина. Выход 273 мг (32%), порошок бежевого цвета, т.пл. 177-179°С (разл.); Rf 0.55; Rt (В, %: 20→60% в течение 30 мин) 14.39 мин; чистота 95.0%; HRMS (ESI) m/z: [М+Н]+ вычислено для C42H59FN3O12+ 816.4077; найдено 816.4081. ЯМР 1H (δ, м.д.): 8,21 (1Н, NH); 7,56 (1H, CH); 7,50 (1H, CH); 7,31 (1H, CH); 7,30 (1H, CH); 6,50 (1H, CH); 6,26 (1H, CH); 6,22 (1H, CH); 6,19 (1H, CH); 6,16 (1H, CH); 6,13 (1H, CH); 6,12 (1H, CH); 6,07 (1H, CH); 5,87 (1H, CH); 5,62 (1H, CH); 4,67 (1H, CH); 4,36 (1H, HC-O); 4,34 (1H, CH); 4,25 (1H, HC-O); 4,19 (2H, CH2); 4,14 (1H, CH); 4,03 (1H, CH); 3,84 (1H, CH); 3,45 (1H, CH2); 3,29 (1H, CH2); 3,24 (1H, CH); 3,24 (1H, HC-O); 3,12 (1H, CH); 3,00 (2H, CH2); 2,87 (1H, HC-O); 2,87 (1H, CH); 2,38 (1H, CH2); 2,19 (1H, CH2); 1,87 (1H, CH2); 1,86 (1H, CH); 1,96 (1H, CH2); 1,93 (1H, CH2); 1,59 (1H, CH2); 1,52 (1H, CH2); 1,51 (1H, CH2); 1,25 (3H, CH3); 1,15 (1H, CH2); 1,12 (1H, CH2); 1,18 (3Н, CH3). ЯМР 13C (δ, м.д.): 172,7; 164,4; 160,6 (д, JCF=247 Гц); 144,5; 135,8; 135,4; 133,3; 132,1; 131,8; 131,6; 131,5; 131,5; 128,8; 128,8; 124,8; 124,8; 115,6 (д, JCF=21 Гц); 97,0; 95,6; 74,5; 72,9; 69,6; 68,5; 67,0; 66,2; 64,9; 64,9; 57,3; 55,4; 55,4; 53,7; 46,6; 46,2; 44,4; 43,9; 40,8; 39,1; 36,6; 35,4; 20,2; 17,6.
Пример 4. N-(2-((2-Гидроксиэтил)амино)этил)амид натамицина (4-4)
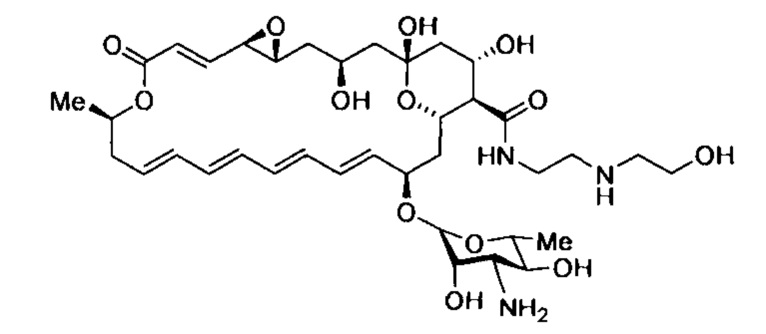
К раствору натамицина (3, 0.70 г, 1.05 ммоль) в ДМСО (7 мл) при перемешивании прибавляют N-(2-гидроксиэтил)этилендиамин (0.55 г, 5.26 ммоль) и триэтиламина гидрохлорид (0.72 г, 5.26 ммоль), затем в течение 1.5 ч равными частями прибавляют РуВОР (0.82 г, 1.58 ммоль). Реакционную смесь перемешивают при комнатной температуре 3 ч, затем прибавляют диэтиловый эфир (20 мл). Смесь интенсивно встряхивают 3 мин, затем слой диэтилового эфира удаляют и повторяют процедуру несколько раз до тех пор, пока не сформируется вязкое масло. К маслу прибавляют метанол (5 мл) и диэтиловый эфир (50 мл); образующийся осадок отфильтровывают, промывают эфиром и сушат в эксикаторе. Полученный продукт очищают методом обращено-фазовой хроматографии (элюент А - вода и водн. NH4OH, элюент В - MeCN): 0,5% водн. NH4OH/MeCN (В: 0→20%), затем H2O/MeCN (В: 20→80%). Фракции, содержащие целевое вещество, объединяют, прибавляют изопропиловый спирт и упаривают до небольшого объема. К раствору прибавляют Et20, выпавший осадок фильтруют и сушат. Выход 220 мг (28%), порошок светло-бежевого цвета, т.пл. 171-173°С (разл.); Rf 0.46; Rt (В, %: 30→60% в течение 15 мин) 5.78 мин, чистота 95.7%; HRMS (ESI) m/z: [М+Н]+ вычислено для C37H58N3O13+ 752.3964; найдено 752.3959. Найдено, %: С 59.14, Η 7.56, N 5.65; вычислено для C37H57N3O13*6H2O, %: С 59.11; Η 7.64; N 5.59. ЯМР 1H (δ, м.д.): 7,94 (1Н, NH); 6,50 (1H, CH); 6,26 (1H, CH); 6,21 (1H, CH); 6,19 (1H, CH); 6,15 (1H, CH); 6,11 (1H, CH); 6,10 (1H, CH); 6,06 (1H, CH); 5,87 (1H, CH); 5,60 (1H, CH); 4,66 (1H, CH); 4,35 (1H, HC-O); 4,27 (1H, CH); 4,24 (1H, HC-O); 4,13 (1H, CH); 4,04 (1H, CH); 3,64 (1H, CH); 3,22 (1H, HC-O); 3,18 (2H, CH2); 3,02 (1H, CH); 2,95 (1H, CH); 2,75 (1H, HC-O); 2,61 (2H, CH2); 2,60 (2H, CH2); 2,44 (2H, CH2); 2,44 (H, CH); 2,38 (1H, CH2); 2,19 (1H, CH2); 1,97 (1H, CH2); 1,96 (1H, CH2); 1,87 (1H, CH); 1,84 (1H, CH2); 1,58 (1H, CH2); 1,49 (1H, CH2); 1,44 (1H, CH2); 1,25 (3H, CH3); 1,15 (1H, CH2); 1,14 (3H, CH3); 1,10 (1H, CH2). ЯМР 13C (δ, м.д.): 171,9; 164,4; 144,6; 136,3; 135,4; 133,5; 131,9; 131,4; 131,2; 128,6; 128,4; 124,6; 96,9; 96,7; 74,2; 73,1; 72,4; 69,6; 69,3; 66,2; 65,0; 64,6; 57,9; 57,3; 56,5; 56,4; 53,6; 51,1; 48,4; 46,2; 44,4; 40,8; 39,1; 38,4; 36,4; 20,2; 17,9.
Пример 5. N-(2-(Диметиламино)этил)амид натамицина (4-5)
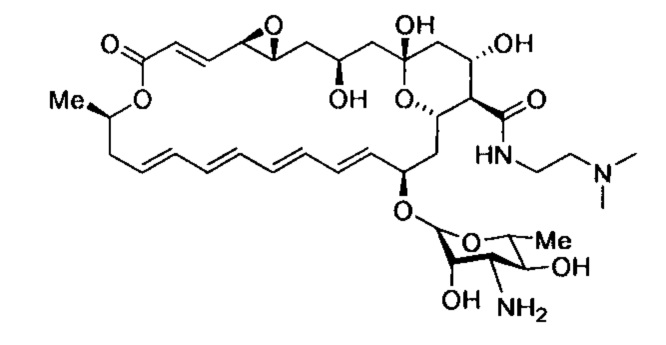
Получают по методике, аналогичной приведенной в примере 4 из натамицина (3) и Ν,Ν-диметилэтилендиамина. Выход 294 мг (38%), порошок белого цвета, т.пл. 194-196°С (разл.); Rf 0.53; Rt (В, %: 20→60% в течение 30 мин) 14.03 мин, чистота 98.3%; HRMS (ESI) m/z: [М+Н]+ вычислено для C37H58N3O12+ 736.4015; найдено 736.4012. ЯМР 1H (δ, м.д.): 7,84 (1Н, NH); 6,49 (1Н, СН); 6,26 (1H, СН); 6,19 (1Н, СН); 6,17 (1Н, СН); 6,15 (1Н, СН); 6,11 (1Н, СН); 6,09 (1Н, СН); 6,06 (1Н, СН); 5,87 (1Н, СН); 5,60 (1Н, СН); 4,66 (1Н, СН); 4,35 (1Н, НС-О); 4,26 (1Н, СН); 4,23 (1Н, НС-О); 4,13 (1Н, СН); 4,02 (1Н, СН); 3,58 (1Н, СН); 3,22 (1Н, НС-О); 3,18 (1Н, СН2); 3,13 (1Н, СН2); 3,00 (1Н, СН); 2,87 (1Н, СН); 2,75 (1Н, НС-О); 2,38 (1Н, СН2); 2,31 (1Н, СН); 2,28 (2Н, СН2); 2,19 (1Н, СН2); 2,15 (6Н, с, 2СН3); 1,96 (1Н, СН2); 1,96 (1Н, СН2); 1,86 (1Н, СН); 1,83 (1Н, СН2); 1,57 (1Н, СН2); 1,49 (1Н, СН2); 1,44 (1Н, СН2); 1,25 (3Н, СН3); 1,16 (1Н, СН2); 1,14 (3Н, СН3); 1,09 (1Н, СН2). ЯМР 13С (δ, м.д.): 171,7; 164,4; 144,5; 136,5; 135,4; 133,5; 131,9; 131,3; 131,1; 128,5; 128,2; 124,5; 96,9; 96,9; 74,0; 73,3; 73,1; 69,9; 69,6; 66,1; 65,1; 64,6; 58,2; 57,9; 57,2; 56,7; 53,6; 46,3; 45,1; 44,4; 40,8; 39,0; 36,8; 36,4; 20,1; 17,9.
Пример 6. N-(3-(Метиламино)пропил)амид натамицина (4-6)
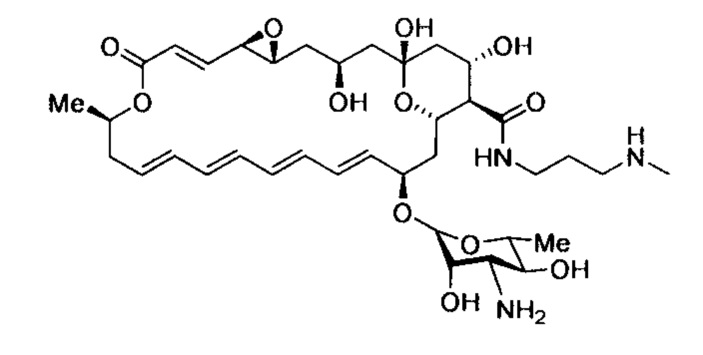
Получают по методике, аналогичной приведенной в примере 4 из натамицина (3) и N-метил-1,3-пропандиамина. Выход 472 мг (61%), порошок оранжевого цвета, т.пл. 182-184°С (разл.); Rf 0.35; Rt (В, %: 20→60% в течение 30 мин) 14.00 мин, чистота 95.3%; HRMS (ESI) m/z: [М+Н]+ вычислено для C37H58N3O12+ 736.4015; найдено 736.4016. ЯМР 1H (δ, м.д.): 8,11 (1Н, NH); 6,50 (1H, CH); 6,26 (1H, CH); 6,21 (1H, CH); 6,19 (1H, CH); 6,16 (1H, CH); 6,11 (1H, CH); 6,09 (1H, CH); 6,06 (1H, CH); 5,86 (1H, CH); 5,60 (1H, CH); 4,67 (1H, CH); 4,34 (1H, HC-O); 4,25 (1H, CH); 4,23 (1H, HC-O); 4,13 (1H, CH); 4,05 (1H, CH); 3,61 (1H, CH); 3,22 (1H, HC-O); 3,13 (1H, CH2); 3,08 (1H, CH2); 3,01 (1H, CH); 2,91 (1H, CH); 2,75 (1H, HC-O); 2,58 (2H, CH2); 2,39 (1H, CH); 2,38 (1H, CH2); 2,30 (3H, CH3); 2,19 (1H, CH2); 1,97 (1H, CH2); 1,95 (1H, CH2); 1,85 (1H, CH); 1,63 (1H, CH2); 1,60 (2H, CH2); 1,57 (1H, CH2); 1,49 (1H, CH2); 1,45 (1H, CH2); 1,25 (3H, CH3); 1,15 (1H, CH2); 1,14 (3H, CH3); 1,09 (1H, CH2). ЯМР 13C (δ, м.д.): 171,9; 164,4; 144,6; 136,3; 135,4; 133,5; 131,9; 131,4; 131,2; 128,6; 128,4; 124,5; 97,0; 97,0; 74,4; 73,1; 72,8; 69,6; 69,5; 66,1; 65,3; 64,5; 57,9; 57,2; 56,5; 53,6; 47,9; 46,3; 44,5; 40,8; 39,1; 36,6; 36,4; 34,7; 28,0; 20,2; 17,9.
Пример 7. Диацетат N-(4-аминобутил)амида натамицина (4-7). 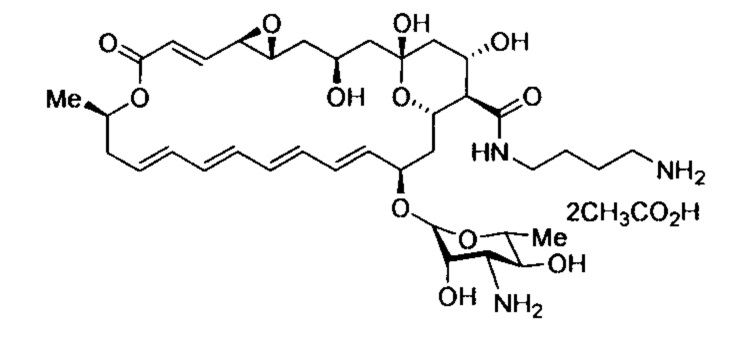
Получают по методике, аналогичной приведенной в примере 1 из натамицина (3) и 1,4-бутандиамина. Выход 437 мг (55%), порошок белого цвета, т.пл. 175-177°С (разл.); Rf 0.36; Rt (В, %: 20→60% в течение 30 мин) 14.03 мин, чистота 95.4%; HRMS (ESI) m/z: [М+Н]+ вычислено для C37H58N2O12+ 736.4015; найдено 736.4014. ЯМР 1H (δ, м.д.): 7,93 (1Н, NH); 6,50 (1Н, СН); 6,26 (1Н, СН); 6,20 (1Н, СН); 6,17 (1Н, СН); 6,15 (1Н, СН); 6,12 (1Н, СН); 6,09 (1Н, СН); 6,06 (1Н, СН); 5,87 (1Н, СН); 5,60 (1Н, СН); 4,67 (1Н, СН); 4,35 (1Н, НС-О); 4,25 (1Н, СН); 4,23 (1Н, НС-О); 4,13 (1Н, СН); 4,05 (1Н, СН); 3,56 (1Н, СН); 3,22 (1Н, НС-О); 3,13 (1Н, СН2); 2,99 (1Н, СН); 2,96 (1Н, СН2); 2,85 (1Н, СН); 2,75 (1Н, НС-О); 2,54 (2Н, СН2); 2,38 (1Н, СН2); 2,27 (1Н, СН); 2,19 (1Н, СН2); 1,97 (1Н, СН2); 1,95 (1Н, СН2); 1,85 (1Н, СН); 1,83 (1Н, СН2); 1,57 (1Н, СН2); 1,49 (2Н, СН2); 1,44 (1Н, СН2); 1,42 (2Н, СН2); 1,37 (2Н, СН2); 1,25 (3Н, СН3); 1,15 (1Н, СН2); 1,13 (3Н, СН3); 1,09 (1Н, СН2). ЯМР 13С (δ, м.д.): 171,5; 164,4; 144,6; 136,5; 135,5; 133,6; 132,0; 131,4; 131,2; 128,7; 128,4; 124,6; 97,1; 97,1; 74,2; 73,6; 73,2; 70,0; 69,6; 66,2; 65,3; 64,5; 58,0; 57,2; 56,8; 53,7; 46,3; 44,6; 41,1; 40,9; 39,1; 38,5; 36,4; 30,4; 26,7; 20,2; 18,0.
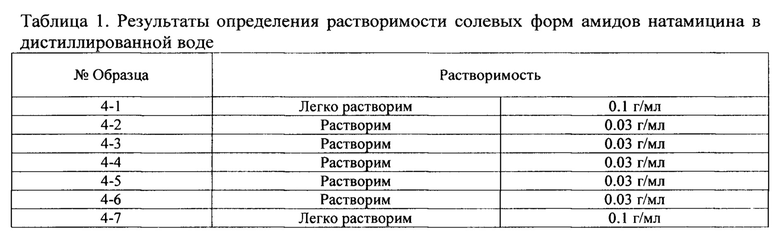
Пример 8. Растворимость солевых форм амидов натамицина 4-1 - 4-7.
В качестве растворителя использовалась дистиллированная вода.
Методика определения растворимости: к навеске исследуемого вещества прибавляют отмеренное количество растворителя и непрерывно встряхивают в течение 10 мин при комнатной температуре. Наблюдение и визуальную оценку растворимости проводят в проходящем свете. Вещество считают растворившимся, если при наблюдении в растворе не обнаруживаются частицы веществ. Для медленно растворимых веществ допускается нагревание на водяной бане. В данном случае наблюдение и оценку растворимости проводят после охлаждения раствора до комнатной температуры и встряхивания в течение 1-2 мин. Растворимость веществ классифицировали согласно ОФС.1.2.1.0005.15 «Растворимость» Государственной Фармакопеи Российской Федерации (XIV издание).
К навескам по 100 мг производных натамицина 4-1 (пример 1), 4-2 (пример 2), 4-3 (пример 3), 4-7 (пример 7) прибавляли 1 мл дистиллированной воды и перемешивали 10 мин. при 20°С. Приготовленные растворы оценивали визуально, и в случае обнаружения нерастворенных частиц добавляли 2 мл дистиллированной воды. К навескам по 100 мг производных натамицина 4-4 (пример 4), 4-5 (пример 5), 4-6 (пример 6) прибавляли 1 мл дистиллированной воды, содержащей 2 экв. АсОН, и перемешивали 10 мин. при 20°С. Приготовленные растворы оценивали визуально, и в случае обнаружения нерастворенных частиц добавляли 2 мл дистиллированной воды. Результаты определения растворимости амидов натамицина представлены в Таблице 1.
Пример 9. Противогрибковая активность новых производных натамицина в отношении штаммов Candida spp. и филаментозных грибов
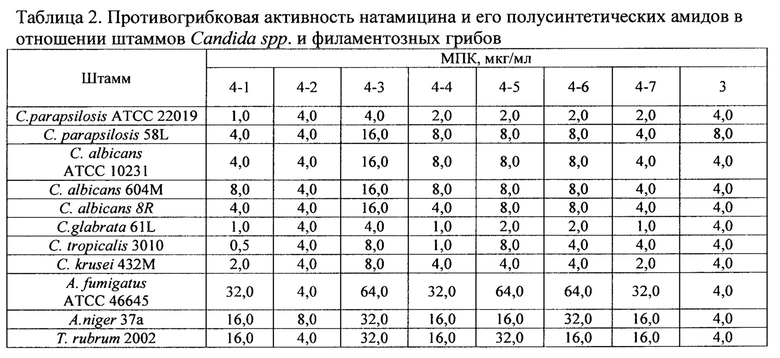
Противогрибковая активность полусинтетических амидов натамицина, являющихся предметом настоящего изобретения, изучена в сравнении с натамицином (3) на широкой панели штаммов грибов рода Candida: референсных штаммов С.parapsilosis АТСС 22019, С albicans АТСС 10231, клинических изолятов, чувствительных к флуконазолу С.parapsilosis 58L, С.albicans 604М, Cglabrata 61L, С.tropicalis 3010, и флуконазол-устойчивых штаммов изолятов С krusei 432М, С.albicans 8R, а также в отношении штаммов филаментозных грибов A. fumigatus АТСС 46645, A. niger 37а, Т. rubrum 2002. Штаммы были получены из медицинской микробиологической лаборатории Государственного научного центра по антибиотикам (ГНЦА, Москва, Россия). Минимальную подавляющую рост микроорганизмов концентрацию (МПК) для тестируемых соединений определяли микрометодом серийных разведений в бульоне, в соответствии с рекомендациями CLSI.
Полученные результаты, представленные в таблице 2, свидетельствуют, что в большинстве случаев новые амиды натамицина, являющиеся предметом настоящего изобретения, в отношении штаммов Candida spp.по активности in vitro сравнимы с природным натамицином (3) и менее активны в отношении филаментозных грибов. Так, диацетат N-(2-аминоэтил)амида натамицина (4-1, пример 1), превосходит по антикандидозной активности препарат сравнения - натамицин (3), обладая в 2-8 раз большей активностью в отношении большинства протестированных штаммов Candida spp.
Пример 10. Антикандидозная эффективность N-(2-аминоэтил)амида натамицина (4-1) in vivo
Сравнительное исследование эффективности диацетата N-(2-аминоэтил)амида натамицина (4-1, пример 1) и амфотерицина В (1) проведено на модели кандидозного сепсиса мышей. В качестве препарата сравнения был использован полиеновый антибиотик амфотерицин В, применяемый в клинике для лечения системных микозов.
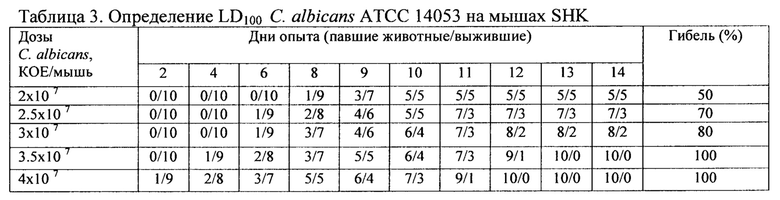
Исследования проведены на мышах SHK, массой 18-22 г, полученных из Питомника ФГБУН «НЦБМТ» ФМБА России «Андреевка». Первоначально определялась 100% летальная доза (LDioo) для С.albicans АТСС 14053 на мышах SHK. С этой целью звесь суточной культуры С.albicans разводили до 2x107, 2,5x107, 3,0x107, 3,5x107, 4,0x107 КОЕ/мышь. Внутривенно заражали этими дозами по 10 мышей в группе. Срок наблюдения - 14 дней. За LD100 принимали минимальную заражающую дозу С.albicans, сопровождающуюся 100% гибелью мышей. Она составила 3.5x107 КОЕ/мышь (табл. 3).
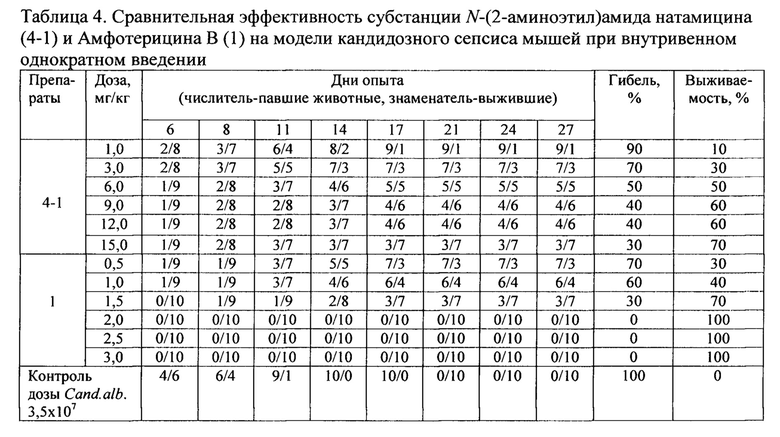
Сравнение противогрибковой эффективности производного 4-1 (N-(2-аминоэтил)амид натамицин) и амфотерицина В (1) проведено на модели кандидозного сепсиса при внутривенном введении препаратов при однократном введении. Диапазон доз для 4-1 составлял от 1 до 15 мг/кг, для амфотерицина В (1) - от 0,5 до 3 мг/кг (табл. 4).
Для количественной оценки эффективности испытуемых препаратов использовался показатель 50% эффективной дозы - ЕД50, которая определялась по методу Беренса (метод накопления частот). На основании экспериментальных данных о выживаемости мышей (таблица 4) были рассчитаны значения показателей эффективности испытуемых препаратов (ED50):
• ED50 N-(2-аминоэтил)амида натамицина (4-1)=6,64 мг/кг
• ED50 амфотерицина В (1)=1,16 мг/кг
Пример 11. Острая токсичность N-(2-аминоэтил)амида натамицина (4-1)
Исследования острой токсичности диацетата N-(2-аминоэтил)амида натамицина (4-1, пример 1) проведены на мышах SHK самках, массой 18-22 г, полученных из Питомника ФГБУН «НЦБМТ» ФМБА России «Андреевка». После двухнедельного карантина из клинически здоровых животных формировали группы по 6 животных в каждой.
Производное 4-1 (пример 1) растворяли в 5% растворе глюкозы до 0,05% концентрации и вводили мышам однократно в хвостовую вену в диапазоне доз от 30 до 70 мг/кг. Наблюдение за состоянием и поведением животных производили в течение 5-х часов после введения препарата и далее ежедневно. Отмечали количество павших животных и сроки их гибели. Через 30 дней после введения препарата выживших животных подвергали эвтаназии при помощи эфира и вскрывали. Расчет доз, характеризующих токсичность, проводили при помощи программы «StatPlus-2006».
В результате исследования показано, что амид 4-1, введенный в смертельных дозах, вызывал гибель животных от 15-20 мин до 1-3 суток после введения (таблица 5).
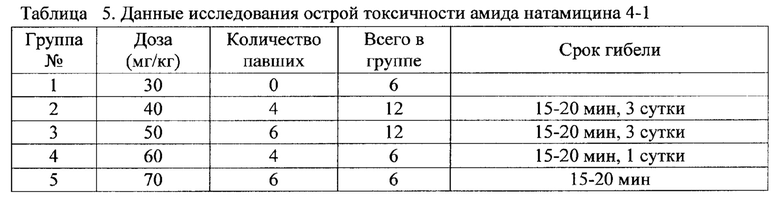
На основании экспериментальных данных о выживаемости мышей (таблица 5) были рассчитаны значения показателей острой токсичности испытуемых препаратов (LDn - доза, при которой гибнут n% испытуемых, MTD - максимальная переносимая доза):
LD50=49,1 (40,2÷60,0) мг/кг
MTD=27,6 (22,6÷33,7) мг/кг
Уровень значимости р≤0,05.
Наличие in vivo активности у диацетата N-(2-аминоэтил)амида натамицина (4-1, пример 1) на модели кандидозного сепсиса и наличие значительного интервала между величинами эффективной (ED50) и максимальной переносимой дозами указывают на возможность использования полусинтетических амидов натамицина для терапии системных микозов, в отличие от природного антибиотика натамицина (3), область медицинского применения которого ограничена только локальной терапией микозов кожных покровов и слизистых оболочек.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения противогрибкового полусинтетического полиенового антибиотика | 2020 |
|
RU2751333C1 |
| Противогрибковый полусинтетический полиеновый антибиотик, его водорастворимые соли и фармацевтические композиции на их основе | 2018 |
|
RU2688658C1 |
| СОЕДИНЕНИЕ ПЕПТИДНОЙ ПРИРОДЫ, ОБЛАДАЮЩЕЕ СПОСОБНОСТЬЮ СВЯЗЫВАТЬСЯ С ПСМА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2823164C2 |
| ЦИТОТОКСИЧЕСКИЕ ЛИНЕЙНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ АНТРАЦЕНДИОНА, СОДЕРЖАЩИЕ В БОКОВОЙ ЦЕПИ ЦИКЛИЧЕСКИЕ ДИАМИНЫ, АКТИВНЫЕ В ОТНОШЕНИИ ОПУХОЛЕВЫХ КЛЕТОК С МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ | 2009 |
|
RU2412166C1 |
| СПИРО[2.3]ГЕКСАНОВЫЕ АМИНОКИСЛОТЫ - КОНФОРМАЦИОННО-ЖЕСТКИЕ АНАЛОГИ γ-АМИНОМАСЛЯНОЙ КИСЛОТЫ - И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2016 |
|
RU2629357C1 |
| Оксазолидиноны на основе производных пиридоксина, обладающие антибактериальной активностью | 2024 |
|
RU2836570C1 |
| 2-ЗАМЕЩЕННЫЕ-1,2,4,5-ТЕТРАГИДРО-3H-ПИРРОЛО[1,2-a][1,4]ДИАЗЕПИН-3-ОНЫ | 2011 |
|
RU2472795C1 |
| Производные 1,4-диоксида хиноксалин-2-карбонитрила, ингибирующие рост опухолевых клеток | 2016 |
|
RU2640304C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗО[7,8]АЗОНИНО[5,4-b]ИНДОЛОВ, 7,9-ЭТЕНОАЗЕЦИНО[5,4-b]ИНДОЛОВ И 7,9-ЭТАНОАЗЕЦИНО[5,4-b]ИНДОЛОВ | 2009 |
|
RU2397984C1 |
| ЛИГАНДЫ, ТРОПНЫЕ К ПРОСТАТИЧЕСКОМУ СПЕЦИФИЧЕСКОМУ МЕМБРАННОМУ АНТИГЕНУ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ДВОЙНЫХ КОНЪЮГАТОВ С ТЕРАПЕВТИЧЕСКИМИ АГЕНТАМИ НА ИХ ОСНОВЕ ДЛЯ КОМБИНИРОВАННОЙ ТЕРАПИИ ПСМА ЭКСПРЕССИРУЮЩИХ ОПУХОЛЕЙ | 2023 |
|
RU2841078C1 |
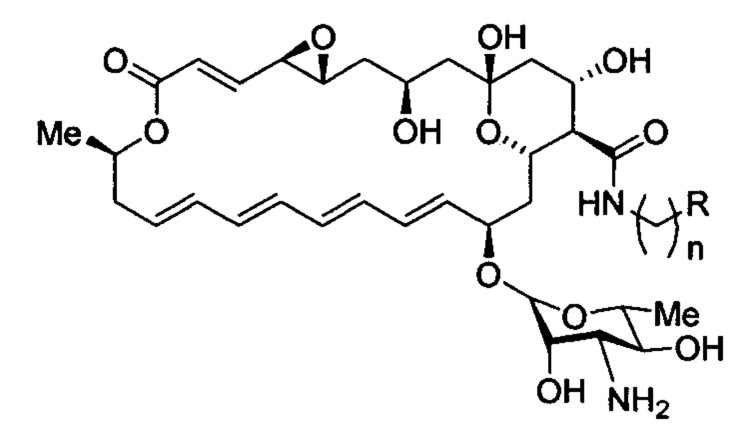
Изобретение относится к фармацевтической промышленности и касается производного натамицина, модифицированного по карбоксильной группе остатком амина, в структуре которого содержится дополнительная основная группа, соответствующего следующей формуле:
 ,
,
а также его фармацевтически приемлемых солей и сольватов. В указанной формуле: R независимо означает аминогруппу; алкиламиногруппу, содержащую от 1 до включительно 6 атомов углерода, необязательно замещенную фенилом, галогенфенилом или гидроксигруппой; пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, необязательно кватернизованные алкильной группой, содержащей от 1 до включительно 14 атомов углерода; n = 1-4. Также предложены способ получения производного натамицина и способ лечения системных грибковых инфекционных заболеваний, вызванных штаммами Candida spp. Изобретение позволяет создать более эффективные противогрибковые средства на основе новых полусинтетических амидов натамицина. 3 н. и 2 з.п. ф-лы, 5 табл., 11 пр.
1. Производное натамицина, модифицированное по карбоксильной группе остатком амина, в структуре которого содержится дополнительная основная группа, а также его фармацевтически приемлемые соли и сольваты, соответствующее формуле:
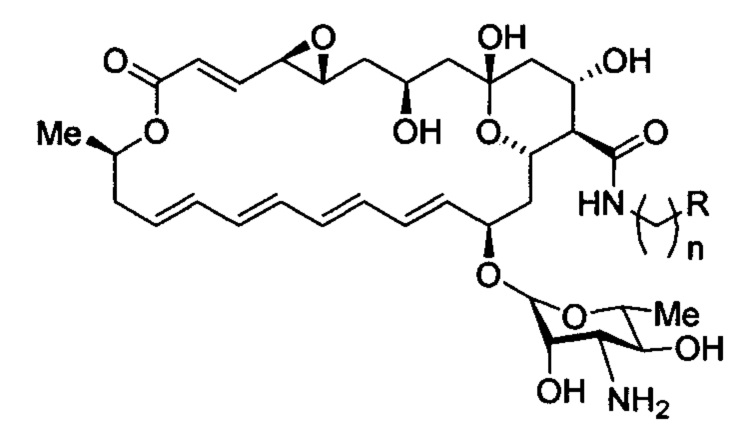
где R - независимо означает аминогруппу; алкиламиногруппу, содержащую от 1 до включительно 6 атомов углерода, необязательно замещенную фенилом, галогенфенилом или гидроксигруппой; пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, необязательно кватернизованные алкильной группой, содержащей от 1 до включительно 14 атомов углерода; n = 1-4.
2. Способ получения соединений по п. 1, который заключается в одностадийной конденсации природного антибиотика натамицина с аминами или их солями в присутствии конденсирующего агента, выбранного из РуВОР, ВОР, TBTU, HBTU, HCTU, TCTU, HATU, COMU в подходящем инертном апротонном растворителе в присутствии основания.
3. Способ получения соединений по п. 2, отличающийся тем, что в реакции в качестве оснований используются амины или их соли для поддержания оптимального рН 7,5-9.
4. Способ лечения системных грибковых инфекционных заболеваний, вызванных штаммами Candida spp., предусматривающий введение нуждающемуся субъекту терапевтически эффективного количества вещества по п. 1.
5. Способ лечения грибковых инфекций по п. 4, в котором возбудитель имеет резистентность в отношении других противогрибковых средств.
| WELSCHER Y.M | |||
| et al., Natamycin Blocks Fungal Growth by Binding Specifically to Ergosterol without Permeabilizing the Membrane, J | |||
| Biol | |||
| Chem., 2008, v | |||
| ПРИБОР ДЛЯ ОПРЕДЕЛЕНИЯ ОСАДКИ ВАЛОВ ПАРОВЫХ ТУРБИН | 1917 |
|
SU283A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Ветряный двигатель барабанного типа | 1926 |
|
SU6393A1 |
| TEVYASHOVA A.N | |||
| et al., Discovery of Amphamide, a Drug Candidate for the Second Generation of Polyene Antibiotics, ACS Publications, 2020, v | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Устройство разъемной опоры для подшипников велосипедных осей | 1924 |
|
SU2029A1 |
| AMIR A | |||
Авторы
Даты
2023-09-19—Публикация
2022-08-16—Подача