ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее раскрытие относится к варианту гидролизующей глутамин GMP-синтазы (гуанозинмонофосфат-синтаза) и способу получения пуринового нуклеотида с его использованием.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Пуриновые нуклеотиды, которые представляют собой тип веществ на основе нуклеиновой кислоты, широко используются для приправ или пищи и привлекают внимание в качестве усиливающих вкус приправ на основе нуклеиновой кислоты.
Для получения пуриновых нуклеотидов проводили разные исследования для разработки микроорганизмов с высокоэффективной продукцией и технологии процесса ферментации. Например, главным образом используют подходы, специфичные в отношении целевого вещества, такие как увеличение экспрессии генов, кодирующих ферменты, участвующие в биосинтезе пуриновых нуклеотидов, или удаление генов, не являющихся необходимыми в биосинтезе (ЕР 3722430 А1 и US 2020-0347346 А1).
По мере того, как возрастает потребность в пуриновых нуклеотидах, все еще необходимы исследования эффективной продукции пуриновых нуклеотидов.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКАЯ ПРОБЛЕМА
Согласно настоящему изобретению предложен вариант гидролизующей глутамин GMP-синтазы.
ТЕХНИЧЕСКОЕ РЕШЕНИЕ
Одним аспектом настоящего изобретения является предложение варианта гидролизующей глутамин GMP-синтазы.
Другим аспектом настоящего изобретения является предложение полинуклеотида, кодирующего данный вариант.
Еще одним другим аспектом настоящего изобретения является предложение микроорганизма, содержащего вариант полинуклеотида, кодирующего данный вариант.
Еще одним другим аспектом данного изобретения является предложение способа получения пуринового нуклеотида, включающего культивирование данного микроорганизма.
Полезные эффекты
Варианты по настоящему изобретению можно использовать для получения пуриновых нуклеотидов с высокой эффективностью.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение будет конкретно описано следующим образом. Каждое описание и воплощение, раскрытое в данном изобретении, также может применяться к другим описаниям и воплощениям. То есть, все комбинации разных элементов, раскрытых в данномизобретении, попадают в пределы объема настоящего изобретения. Кроме того, объем настоящего изобретения не ограничивается приведенным ниже конкретным описанием. Кроме того, во всем данном описании изобретения дается ссылка на многие статьи и патентные документы, и приводятся их цитирования. Изобретения процитированных статей и патентных документов включаются в настоящее описание изобретения во всей их полноте посредством ссылки, и уровень технической области, в пределы которого попадает настоящее раскрытие, и подробности настоящего изобретения объясняются более ясно.
Согласно одному аспекту настоящего изобретения предложен вариант гидролизующей глутамин GMP-синтазы, в котором аминокислота, соответствующая положению 29 в SEQ ID NO: 3, заменена другой аминокислотой.
Термин «вариант гидролизующей глутамин GMP-синтазы» относится к варианту, включающему замену аминокислоты, соответствующей положению 29 от N-конца SEQ ID NO: 3, другой аминокислотой в полипептиде, имеющем активность гидролизующей глутамин GMP-синтазы, или в гидролизующей глутамин GMP-синтазе.
В настоящем изобретении «гидролизующая глутамин GMP-синтаза» представляет собой фермент, участвующий в превращении 5'-ксантозинмонофосфата (ХМР) в 5'-гуанозинмонофосфат (далее GMP).
Гидролизующая глутамин GMP-синтаза по настоящему изобретению может представлять собой гидролизующую глутамин GMP-синтазу или полипептид, имеющий активность гидролизующей глутамин GMP-синтазы, которые подлежат модификации для получения варианта гидролизующей глутамин GMP-синтазы, предложенного в настоящем изобретении.
В частности, данный полипептид может представлять собой встречающийся в природе полипептид или полипептид дикого типа, или его зрелый полипептид и может включать его вариант или функциональный фрагмент, но включается любой полипептид без ограничения, при условии, что он может быть родительским в отношении варианта гидролизующей глутамин GMP-синтазы по настоящему изобретению.
В одном воплощении гидролизующая глутамин GMP-синтаза по настоящему изобретению может происходить из рода Corynebacterium и, более конкретно, Corynebacterium stationis, но не ограничиваясь этим.
В одном воплощении гидролизующая глутамин GMP-синтаза по настоящему изобретению может представлять собой полипептид SEQ ID NO: 3. В одном воплощении гидролизующая глутамин GMP-синтаза по настоящему изобретению может представлять собой полипептид, имеющий по меньшей мере примерно 60%-ную, 70%-ную, 75%-ную, 80%-ную, 85%-ную, 90%-ную, 93%-ную, 95%-ную, 96%-ную, 97%-ную, 98%-ную или 99%-ную идентичность последовательности с полипептидом SEQ ID NO: 3, и включает любой полипептид, который имеет активность, идентичную или соответствующую активности полипептида, состоящего из аминокислотной последовательности SEQ ID NO: 3, без ограничения, в пределах ряда гидролизующих глутамин GMP-синтаз. В частности, гидролизующая глутамин GMP-синтаза может иметь, содержать или по существу состоять из аминокислотной последовательности, изложенной в SEQ ID NO: 3, но не ограничивается ей.
Гидролизующая глутамин GMP-синтаза, подлежащая мутированию в настоящем изобретении, может представлять собой гидролизующую глутамин GMP-синтазу, происходящую из вида Corynebacterium, и, в частности, полипептид/белок, содержащий аминокислотную последовательность, изложенную в SEQ ID NO: 3, или любой полипептид/белок, имеющий такую же активность, что и эта синтеза, может быть включен без ограничения. Например, данный полипептид/белок может содержать аминокислотную последовательность SEQ ID NO: 3 или аминокислотную последовательность, имеющую по меньшей мере 80%-ную гомологию или идентичность с ней, но не ограничиваясь ими. В частности, данный полипептид/белок может содержать аминокислотную последовательность, имеющую по меньшей мере 80%-ную, 85%-ную, 90%-ную, 95%-ную, 96%-ную, 97%-ную, 98%-ную или 99%-ную гомологию или идентичность с SEQ ID NO: 3. Полипептид/белок, имеющий делецию, модификацию, замену или вставку в части его последовательности очевидно включается в настоящем изобретении в пределы ряда полипептидов/белков, подлежащих мутации, при условии, что он представляет собой полипептид/белок, имеющий такую гомологию или идентичность, и демонстрирующий активность гидролизующей глутамин GMP-синтазы.
Последовательность гидролизующей глутамин GMP-синтазы по настоящему изобретению может быть доступна в GenBank NCBI (Национальный центр биотехнологической информации), известной базе данных. Например, гидролизующая глутамин GMP-синтаза по настоящему изобретению может представлять собой полипептид, кодируемый геном guaA. Например, гидролизующая глутамин GMP-синтаза по настоящему изобретению может происходить из Corynebacterium stationis, Corynebacterium casei или Corynebacterium ammoniagenes, и ее примеры могут представлять собой фермент, экспрессируемый эталонной последовательностью NCBI WP_194285183.1, WP_006823296.1 или WP_040355890.1, но не ограничиваясь ими.
Термин «гомология» или «идентичность» в том виде, как он здесь используется, относится к степени сходства между двумя данными аминокислотными последовательностями или нуклеотидными последовательностями, и она может быть выражена в виде процентной доли. Термины «гомология» и «идентичность» часто могут использоваться взаимозаменяемо.
Гомология или идентичность последовательности консервативных полинуклеотидов или полипептидов может определяться стандартным алгоритмом выравнивания, и можно совместно использовать штрафы за пробел по умолчанию, установленные программой. По существу, гомологичные или идентичные последовательности обычно могут гибридизоваться друг с другом целиком или частично при умеренных или сильно жестких условиях. Очевидно, что гибридизация также включает гибридизацию с полинуклеотидом, содержащим обычные кодоны или кодоны с учетом вырожденности кодонов в данном полинуклеотиде.
Гомологию, сходство или идентичность между любыми двумя последовательностями полинуклеотидов или полипептидов можно определять с использованием известных компьютерных алгоритмов, таких как программа «FASTA», с использованием параметров по умолчанию как в Pearson et al., (1988) Proc. Natl. Acad. Sci. USA 85: 2444. В качестве альтернативы, гомология, сходство или идентичность могут быть определены с использованием алгоритма Needleman-Wunsch (Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443-4153), который осуществляется в программе Needleman пакета European Molecular Biology Open Software Suite (EMBOSS) (включая Rice et al., 2000, Trends Genet. 16: 276-277) (версия 5.0.0 или более поздняя) (программный пакет GCG (Devereux, J., et at, Nucleic Acids Research 12: 387 (1984)), BLASTP, BLASTN, FASTA (Atschul, S.F., et at, JMOLEC BIOL 215:403 (1990); Guide to Huge Computers, Martin J. Bishop, ed., Academic Press, San Diego, 1994; и CARILLO et at (1988) SIAM J Applied Math 48: 1073). Например, гомология, сходство или идентичность могут определяться с использованием BLAST или ClustalW из базы данных Национального центра биотехнологической информации.
Гомологию, сходство или идентичность между полинуклеотидами или полипептидами можно определять посредством сравнения информации по последовательности с использованием компьютерной программы GAP, как, например, вводится Needleman et at (1970), J Mol Biol. 48: 443, как раскрыто Smith and Waterman, Adv. Appl. Math (1981) 2: 482. Вкратце, программа GAP определяет гомологию, сходство или идентичность как значение, полученное делением числа аналогичных выровненных символов (т.е. нуклеотидов или аминокислот) на общее число символов в более короткой из двух последовательностей. Параметры по умолчанию для программы GAP могут включать: (1) матрицу двоичных сравнений (содержащую значение 1 для идентичности и 0 для неидентичности) и матрицу взвешенных сравнений Gribskov et al., (1986) Nucl. Acids Res. 14: 6745, как раскрыто в Schwartz and Dayhofr", eds., Atlas Of Protein Sequence And Structure, National Biomedical Research Foundation, pp. 353-358 (1979) (или матрицу замен EDNAFULL (EMBOSS версии NCBI NUC4.4)); (2) штраф 3,0 для каждого пропуска и дополнительный штраф 0,10 для каждого символа в каждом пропуске (или штраф 10 за открытие пропуска и штраф 0,5 за удлинение пропуска); и (3) отсутствие штрафа за концевые пропуски.
Термин «вариант» в том виде, как он здесь используется, относится к полипептиду, который имеет другую последовательность, но сохраняет функции или свойства, сравнимые с аминокислотной последовательностью перед мутацией посредством консервативной замены и/или модификации по меньшей мере одной аминокислоты. Такой вариант обычно может быть идентифицирован посредством модифицирования одной или более чем одной аминокислоты в аминокислотной последовательности данного полипептида и осуществления оценки свойств модифицированного полипептида. То есть, способность данного варианта может быть увеличена, оставаться неизменной или снижаться по сравнению со способностью полипептида перед мутацией. Некоторые варианты могут включать вариант, в котором по меньшей мере одна часть, такая как N-концевая лидерная последовательность или транс мембранный домен, удалена. Другие варианты могут включать вариант, в котором удаляется часть N-конца и/или С-конца зрелого белка. Термин «вариант» также может использоваться взаимозаменяемо с «модификацией», «модифицированным белком», «модифицированным полипептидом», «мутантом», «мутеином», «дивергентом» или тому подобными, и любой термин, который используется в смысле мутирования, можно использовать без его ограничения.
Кроме того, данный вариант может включать делеции или вставки аминокислот, которые имеют минимальное влияние на свойства и вторичные структуры полипептида. Например, с N-концом данного варианта может быть конъюгирована сигнальная (или лидерная) последовательность N-конца белка, которая котрансляционно или посттрансляционно направляет перенос данного белка. Кроме того, данный вариант также может быть конъюгирован с другой последовательностью или линкером таким образом, что данный вариант идентифицирован, очищен или синтезирован.
Вариант гидролизующей глутамин GMP-синтазы, предложенный в настоящем изобретении, может представлять собой полипептид, содержащий аминокислотную последовательность, в которой аминокислота, соответствующая положению 29 в SEQ ID NO: 3, заменена другой аминокислотой. В частности, данная другая аминокислота может быть выбрана из глицина, аланина, валина, лейцина, изолейцина, метионина, фенилаланина, триптофана, пролина, серина, треонина, цистеина, тирозина, аспарагина, глутамина, аспарагиновой кислоты, глутаминовой кислоты, лизина и гистидина.
Данная «другая аминокислота» не ограничен, при условии, что данная аминокислота отличается от аминокислоты перед заменой. Выражение «заменена конкретной аминокислотой» в настоящем изобретении является очевидным в качестве замены отличной аминокислотой от аминокислоты перед заменой, даже если конкретно не утверждается «замена другой аминокислотой».
В одном воплощении вариант по настоящему изобретению может представлять собой вариант, в котором аминокислота, соответствующая положению 29 в аминокислотной последовательности SEQ ID NO: 3 в качестве эталонного белка, представляет собой одну аминокислоту за исключением аргинина. В частности, аминокислота, соответствующая положению 29 в SEQ ID NO: 3 данного варианта может быть выбрана из глицина, аланина, валина, лейцина, изолейцина, метионина, фенилаланина, триптофана, пролина, серина, треонина, цистеина, тирозина, аспарагина, глутамина, аспарагиновой кислоты, глутаминовой кислоты, лизина и гистидина.
В одном воплощении вариант гидролизующей глутамин GMP-синтазы по настоящему изобретению может содержать аминокислотную последовательность, в которой аминокислота, соответствующая положению 29 в аминокислотной последовательности, изложенной в SEQ ID NO: 3, представляет собой аминокислоту за исключением аргинина, и которая имеет по меньшей мере 70%-ную, 75%-ную, 80%-ную, 85%-ную, 90%-ную, 95%-ную, 96%-ную, 97%-ную, 98%-ную, 99%-ную, 99,5%-ную, 99,7%-ную или 99,8%-ную гомологию или идентичность с аминокислотной последовательностью, изложенной в SEQ ID NO: 3.
Например, вариант гидролизующей глутамин GMP-синтазы по настоящему изобретению может состоять из аминокислотной последовательности SEQ ID NO: 1 или может содержать аминокислотную последовательность, имеющую по меньшей мере 70%-ную, 75%-ную, 80%-ную, 85%-ную, 90%-ную, 95%-ную, 96%-ную, 97%-ную, 98%-ную, 99%-ную, 99,5%-ную, 99,7%-ную или 99,8%-ную идентичность с ней, но не ограничиваясь ей.
Очевидно то, что даже вариант, имеющий аминокислотную последовательность с делецией, модификацией, заменой, консервативной заменой или вставкой в его части, также может быть включен в пределы объема настоящего изобретения, при условии, что данная аминокислотная последовательность имеет такую гомологию или идентичность и демонстрирует активность, соответствующую варианту по настоящему изобретению.
Например, может быть вставка или делеция последовательности, встречающаяся в природе мутация, молчащая мутация или консервативная замена, которая не изменяет функции варианта по настоящему изобретению, в N-конце, С-конце и/или внутри данной аминокислотной последовательности.
Термин «консервативная замена» относится к замене одной аминокислоты другой аминокислотой, имеющей аналогичные с ней структурные и/или химические свойства. Такая аминокислотная замена обычно может происходить на основе сходств в полярности, заряде, растворимости, гидрофобности, гидрофильности и/или амфипатической природе остатков. Обычно консервативная замена может иметь малый эффект или не иметь эффекта на активность белка или полипептида.
Термин «соответствующий» в том виде, как он здесь используется, относится к аминокислотному остатку в положении, перечисленном в полипептиде, или к аминокислотному остатку, аналогичному, идентичному или гомологичному остатку, перечисленному в полипептиде. Идентификация аминокислоты в соответствующем положении может представлять собой определение конкретной аминокислоты последовательности, относящейся к конкретной последовательности. Термин «соответствующая область» в том виде, как он здесь используется, обычно относится к аналогичному или соответствующему сайту в родственном белке или эталонном белке.
Например, любая аминокислотная последовательность выравнивается с SEQ ID NO: 3, и на основе этого каждый аминокислотный остаток данной аминокислотной последовательности может быть пронумерован относительно числовому положению аминокислотного остатка, соответствующего аминокислотному остатку SEQ ID NO: 3. Например, алгоритм выравнивания последовательности, как описано в настоящем изобретении, может идентифицировать положение аминокислоты или положение появления модификаций, таких как замена, вставка или делеция, по сравнению с запрашиваемой последовательностью (также именуемой «эталонная последовательность»).
Для такого выравнивания, например, можно использовать алгоритм Needleman Wunsch (Needleman and Wunsch, 1970, J. Mot Biol. 48: 443-453) или программу Needle пакета EMBOSS (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, Trends Genet. 16: 276-277), но не ограничиваясь ими, можно использовать программу выравнивания последовательностей, алгоритм попарного сравнения последовательностей или тому подобное, которые известны в данной области, в зависимости от обстоятельств.
Согласно другому аспекту настоящего изобретения предложен полинуклеотид, кодирующий вариант по настоящему изобретению.
Термин «полинуклеотид» в том виде, как он здесь используется, относится к нити ДНК или РНК, имеющей более чем определенную длину, в виде нуклеотидного полимера, который представляет собой длинную цепь нуклеотидных мономеров, связанных ковалентными связями.
Например, полинуклеотид, кодирующий гидролизующую глутамин GMP-синтазу по настоящему изобретению, может иметь или содержать последовательность, кодирующую нуклеотидную последовательность SEQ ID NO: 4. Например, полинуклеотид, кодирующий гидролизующую глутамин GMP-синтазу, может состоять или по существу состоит из последовательности SEQ ID NO: 4.
Полинуклеотид по настоящему изобретению может быть по-разному модифицирован в его кодирующей области в пределах интервала, в котором аминокислотная последовательность варианта по настоящему изобретению не изменяется, учитывая вырожденность кодонов или кодоны, предпочитаемые организмом, в котором подлежит экспрессии вариант по настоящему изобретению.
В частности, полинуклеотид, кодирующий вариант гидролизующей глутамин GMP-синтазы по настоящему изобретению, может иметь или содержать нуклеотидную последовательность, имеющую по меньшей мере 70%-ную, по меньшей мере 75%-ную, по меньшей мере 80%-ную, по меньшей мере 85%-ную, по меньшей мере 90%-ную, по меньшей мере 95%-ную, по меньшей мере 96%-ную, по меньшей мере 97%-ную, по меньшей мере 98%-ную, по меньшей мере 99%-ную и меньше, чем 100%-ную гомологию или идентичность с последовательностью SEQ ID NO: 4, или может состоять или по существу состоит из нуклеотидной последовательности, имеющей по меньшей мере 70%-ную, по меньшей мере 75%-ную, по меньшей мере 80%-ную, по меньшей мере 85%-ную, по меньшей мере 90%-ную, по меньшей мере 95%-ную, по меньшей мере 96%-ную, по меньшей мере 97%-ную, по меньшей мере 98%-ную и меньше, чем 100%-ную гомологию или идентичность с последовательностью SEQ ID NO: 4, но не ограничивается ими. В последовательностях, имеющих такую гомологию или идентичность, кодон, кодирующий аминокислоту, соответствующую положению 29 в SEQ ID NO: 3, может представлять собой один из кодонов, кодирующих любые аминокислоты, кроме аргинина.
Кроме того, полинуклеотид по настоящему изобретению может включать, без ограничения, последовательность, которая может гибридизоваться при жестких условиях с зондом, который можно получать из последовательности известного гена, например, последовательности, комплементарной части или всей последовательности полинуклеотида по настоящему изобретению. Термин «жесткие условия» относится к условиям, которые обеспечивают специфичную гибридизацию между полинуклеотидами. Данные условия подробно описываются в литературе (см. J. Sambrook et al., Molecular Cloning, A Laboratory Manual, 2nd Edition, Cold Spring Harbor Laboratory press, Cold Spring Harbor, New York, 1989 и F. M. Ausubel et at, Current Protocols in Molecular Biology, John Wiley & Sons, Inc., New York, 9.50-9.51, 11.7-11.8). Например, такие условия могут включать условия, при которых полинуклеотиды, имеющие высокую гомологию или идентичность, такие как полинуклеотиды, имеющие по меньшей мере 70%-ную, по меньшей мере 75%-ную, по меньшей мере 80%-ную, по меньшей мере 85%-ную, по меньшей мере 90%-ную, по меньшей мере 95%-ную, по меньшей мере 96%-ную, по меньшей мере 97%-ную, по меньшей мере 98%-ную или по меньшей мере 99%-ную гомологию или идентичность между ними, гибридизуются друг с другом, но полинуклеотиды, имеющие меньшую гомологию или идентичность, не гибридизуются друг с другом; или условия промывки для типичной саузерн-гибридизации, при которых промывка проводится при концентрации соли и температуре, соответствующих 60°С, 1×SSC (цитратно-солевой раствор), 0,1% SDS (додецилсульфат натрия); конкретно 60×С, 0,1×SSC, 0,1% SDS; и более конкретно 68°С, 0,1×SSC, 0,1% SDS, один раз, конкретно дважды или три раза.
Для гибридизации требуется, чтобы две нуклеиновые кислоты имели комплементарные последовательности, хотя и могут быть возможны несоответствия между основаниями, в зависимости от жесткости гибридизации. Термин «комплементарность» используется для описания связи между нуклеотидными основаниями, которые могут гибридизоваться друг с другом. Например, для ДНК аденин является комплементарным тимину, а цитозин является комплементарным гуанину. Следовательно, полинуклеотид по настоящему изобретению также может включать выделенные фрагменты нуклеиновой кислоты, комплементарные всей последовательности, а также по существу аналогичные нуклеиново-кислотные последовательности.
В частности, полинуклеотид, имеющий гомологию с полинуклеотидом по настоящему изобретению или идентичный ему, может быть выявлен с использованием условий гибридизации, включающих стадию гибридизации при Тm (температура плавления) 55°С и с использованием вышеописанных условий. Кроме того, значение Тm может составлять 60°С, 63°С или 65°С, но не ограничиваясь ими, и может подходящим образом контролироваться специалистом в данной области согласно цели.
Подходящая жесткость для гибридизации полинуклеотидов зависит от длины полинуклеотидов и степени комплементарности, и ее переменные хорошо известны в данной области (например, Sambrook et al., выше).
Согласно еще одному другому аспекту настоящего изобретения предложен вектор, включающий полинуклеотид, кодирующий вариант по настоящему изобретению. Данный вектор может представлять собой экспрессионный вектор для осуществления экспрессии полинуклеотида в клетке-хозяине, но не ограничивается этим.
«Вектор» по настоящему изобретению может включать ДНК-конструкцию, содержащую нуклеотидную последовательность полинуклеотида, кодирующего целевой полипептид, связанного функциональным образом с подходящей областью контроля экспрессии (или последовательностью контроля экспрессии) таким образом, чтобы экспрессировать целевой полипептид в подходящем хозяине. Данная область контроля экспрессии может включать промотор, способный инициировать транскрипцию, последовательность любого оператора для осуществления контроля такой транскрипции, последовательность для кодирования подходящего сайта связывания рибосомы с мРНК и последовательность для осуществления контроля терминации транскрипции и трансляции. Данный вектор после трансформации в подходящую клетку-хозяина может реплицироваться или функционировать независимо от генома хозяина или сам может интегрировать в данный геном.
Вектор, используемый в настоящем изобретении, конкретно не ограничен, и можно использовать любой вектор, известный в данной области. Примеры вектора, который обычно используется, могут включать природные или рекомбинантные плазмиды, космиды, вирусы и бактериофаги. Например, в качестве фаговых векторов или космидных векторов можно использовать pWE15, М13, MBL3, MBL4, IXII, ASHII, АРII, t10, t11, Charon4A и Charon21A, и в качестве плазмидных векторов можно использовать векторы на основе pBR, на основе pUC, на основе pBluescript II, на основе pGEM, на основе pTZ, на основе pCL и на основе рЕТ. В частности, можно использовать векторы pDZ, pDC, pDCM2, pACYC177, pACYC184, pCL, pECCG117, pUC19, pBR322, pMW118 и рСС1BAC.
Например, полинуклеотид, кодирующий целевой полипептид, можно вставлять в хромосому посредством вектора для хромосомной вставки в клетке. Вставку данного полинуклеотида в хромосому можно осуществлять с использованием любого способа, известного в данной области, например, гомологичной рекомбинации, но не ограничиваясь ей. Данный вектор может дополнительно включать селективный маркер для исследования встраивания или невстраивания в хромосому. Данный селективный маркер служит для отбора клеток, трансформированных вектором, то есть, осуществления идентификации вставки целевой молекулы нуклеиновой кислоты, и можно использовать маркеры, придающие селектируемый фенотип, такой как устойчивость к лекарственным средствам, ауксотрофия, устойчивость к цитотоксическим агентам или экспрессия поверхностного белка. При обстоятельствах обработки селективным агентом могут выживать или демонстрировать другие фенотипические признаки только клетки, экспрессирующие селективные маркеры, таким образом, могут быть отобраны трансформированные клетки.
Термин «трансформация» в том виде, как он здесь используется, означает, что вектор, содержащий полинуклеотид, кодирующий целевой полипептид, вводится в клетку-хозяина или микроорганизм для обеспечения экспрессии в клетке-хозяине полипептида, кодируемого данным полинуклеотидом. Примеры трансформированного полинуклеотида могут включать любой полипептид, при условии, что он может экспрессироваться в клетке-хозяине, независимо от того, встроен ли он и локализован в хромосоме клетки-хозяина или локализован вне хромосомы. Кроме того, примеры данного полинуклеотида включают ДНК и/или РНК, кодирующую целевой белок. Данный полинуклеотид может быть введен в любой форме, при условии, что данный полинуклеотид может быть введен в клетку-хозяина и может экспрессироваться. Например, данный полинуклеотид может быть введен в виде экспрессионной кассеты, которая представляет собой генетическую конструкцию, содержащую все факторы, требующиеся для автономной экспрессии. Данная экспрессионная кассета обычно может включать промотор, связанный функциональным образом с полинуклеотидом, сигнал терминации транскрипции, сайт связывания рибосомы и сигнал терминации трансляции. Данная экспрессионная кассета может представлять собой экспрессионный вектор, способный к автономной репликации. Кроме того, данный полинуклеотид может быть введен в клетку-хозяина в том виде, в котором он находится, для связывания функциональным образом с последовательностью, требующейся для экспрессии в клетке-хозяине, но не ограничиваясь им.
В приведенном выше термин «связанный функциональным образом» относится к функциональной связи между последовательностью промотора для инициирования и опосредования транскрипции полинуклеотида, кодирующего вариант по настоящему изобретению, и последовательностью данного полинуклеотида.
Согласно еще одному другому аспекту настоящего изобретения предложен микроорганизм, содержащий вариант по настоящему изобретению или полинуклеотид, кодирующий указанный вариант.
Микроорганизм по настоящему изобретению может содержать вариант по настоящему изобретению, полинуклеотид, кодирующий указанный вариант, или вектор, включающий указанный полинуклеотид.
Термин «микроорганизм (или штамм)» в том виде, как он здесь используется, охватывает все микроорганизмы дикого типа или естественно или искусственно генетически модифицированные микроорганизмы, относится к микроорганизму, в котором ослаблен или усилен конкретный механизм из-за вставки экзогенного гена или усиления активности, или инактивации эндогенного гена, и он может представлять собой микроорганизм, включающий генетическую модификацию для продуцирования целевого полипептида, белка или продукта.
Микроорганизм по настоящему изобретению может представлять собой микроорганизм, включающий по меньшей мере один вариант по настоящему изобретению, полинуклеотид, кодирующий вариант по настоящему изобретению, и вектор, включающий полинуклеотид, кодирующий вариант по настоящему изобретению; микроорганизм, модифицированный для экспрессии варианта по настоящему изобретению или полинуклеотида, кодирующего вариант по настоящему изобретению; микроорганизм (например, рекомбинантный штамм), экспрессирующий вариант по настоящему изобретению или полинуклеотид, кодирующий вариант по настоящему изобретению; или микроорганизм (например, рекомбинантный штамм), имеющий активность варианта по настоящему изобретению, но не ограничивается ими.
Микроорганизмы по настоящему изобретению могут иметь способность к продукции пуриновых нуклеотидов.
Микроорганизм по настоящему изобретению может представлять собой микроорганизм, имеющий природную способность к продуцированию гидролизующей глутамин GMP-синтазы или пуриновых нуклеотидов, или микроорганизм, получаемый введением варианта по настоящему изобретению или кодирующего его полинуклеотида (или вектора, включающего данный полинуклеотид) в родительский штамм без способности к продуцированию гидролизующей глутамин GMP-синтазы или пуринового нуклеотида, и/или придание родительскому штамму способности к продуцированию пуринового нуклеотида, но не ограничиваясь этим. Например, микроорганизм по настоящему изобретению может представлять собой микроорганизм, имеющий способность к продуцированию пуринового нуклеотида, придаваемую введением варианта гидролизующей глутамин GMP-синтазы по настоящему изобретению. Например, микроорганизм по настоящему изобретению может представлять собой микроорганизм, имеющий способность к продуцированию пуринового нуклеотида, усиленную введением варианта гидролизующей глутамин GMP-синтазы по настоящему изобретению. Однако микроорганизм по настоящему изобретению не ограничивается этим.
Например, штамм по настоящему изобретению представляет собой клетку или микроорганизм, трансформированный вектором, включающим полинуклеотид по настоящему изобретению или полинуклеотид, кодирующий вариант по настоящему изобретению, и, таким образом, экспрессирует вариант по настоящему изобретению, и, в целях настоящего изобретения, штамм по настоящему изобретению охватывает все микроорганизмы, которые могут продуцировать пуриновый нуклеотид, посредством включения варианта по настоящему изобретению. Например, штамм по настоящему изобретению может представлять собой рекомбинантный штамм, имеющий повышенную способность к продукции пуринового нуклеотида посредством экспрессии варианта гидролизующей глутамин GMP-синтазы посредством введения полинуклеотида, кодирующего вариант по настоящему изобретению, в природный микроорганизм дикого типа или в микроорганизм, продуцирующий пуриновый нуклеотид. Данный рекомбинантный штамм имеет повышенную способность к продуцированию пуринового нуклеотида по сравнению с природным микроорганизмом дикого типа или микроорганизмом, не модифицированным гидролизующей глутамин GMP-синтазой (т.е. микроорганизмом, экспрессирующим гидролизующую глутамин GMP-синтазу дикого типа (SEQ ID NO: 3), или микроорганизмом, не экспрессирующим модифицированный белок), но не ограничивается этим.
Термин «немодифицированный микроорганизм» в том виде, как он здесь используется, может относиться к штамму дикого типа или природному штамму в том виде, в котором он встречается в природе, или к штамму перед трансформацией из-за генетической мутации, вызванной природными или искусственными факторами, не исключая штаммы, включающие мутации, которые могут встречаться у микроорганизмов в природе. Например, немодифицированный микроорганизм может относиться к штамму, в который не введен описанный здесь вариант гидролизующей глутамин GMP-синтазы, или перед его введением. Термин «немодифицированный микроорганизм» может использоваться взаимозаменяемо с терминами «штамм до модификации», «микроорганизм до модификации», «неизмененный штамм», «немодифицированный штамм», «неизмененный микроорганизм» или «эталонный микроорганизм».
В одном воплощении микроорганизм по настоящему изобретению может представлять собой микроорганизм рода Corynebacterium. Например, микроорганизм по настоящему изобретению может представлять собой Corynebacterium stationis, Corynebacterium crudilactis, Corynebacterium deserti, Corynebacterium efficiens, Corynebacterium callunae, Corynebacterium glutamicum, Corynebacterium singulare, Corynebacterium halotolerans, Corynebacterium striatum, Corynebacterium ammoniagenes, Corynebacterium pollutisoli, Corynebacterium imitans, Corynebacterium testudinoris или Corynebacterium flavescens. В частности, микроорганизм по настоящему изобретению может представлять собой Corynebacterium stationis, но не ограничивается им.
Термин «пуриновый нуклеотид» здесь относится к нуклеотиду, содержащему структуру на основе пурина. Данный пуриновый нуклеотид может представлять собой ХМР (ксантозинмонофосфат), IMP (инозинмонофосфат), GMP (гуанозинмонофосфат) или AMP (аденозинмонофосфат) и, в частности, IMP, ХМР или GMP. Более конкретно, данный пуриновый нуклеотид может представлять собой ХМР или GMP, но не ограничивается ими.
«Инозин-5'-монофосфат или 5'-инозиновая кислота (IМР)» и «гуанозин-5'-монофосфат или 5'-гуаниловая кислота (GMP)» по настоящему изобретению, которые являются промежуточными соединениями в метаболических системах биосинтеза нуклеиновых кислот, имеют физиологически важную роль в организме и широко используются в пищевых продуктах, фармацевтических средствах и тому подобном. В частности, известно, что сам IMP придает вкус говядины, a GMP, происходящий из ХМР, известен как придающий грибной вкус. Известно, что оба вещества усиливают вкус мононатрия глутамата (MSG) и, таким образом, привлекали значительное внимание в качестве усиливающей вкус приправы на основе нуклеиновой кислоты.
В одном воплощении GMP может быть получен посредством превращения из ХМР, но не ограничиваясь этим. Например, уровень продукции GMP может быть увеличен посредством превращения усиленно продуцируемого ХМР в GMP, и, таким образом, GMP также включается в пределы объема настоящего изобретения.
«ХМР» по настоящему изобретению также называется ксантозин-5'-монофосфат или 5'-ксантиловая кислота и может образоваться из IMP посредством действия IMP-дегидрогеназы, или превращаться в GMP посредством действия GMP-синтазы.
Термин «микроорганизм, продуцирующий пуриновый нуклеотид» в том виде, как он здесь используется, охватывает все микроорганизмы дикого типа или природно или искусственно генетически модифицированные микроорганизмы и относится к микроорганизму, у которого ослаблен или усилен конкретный механизм из-за вставки экзогенного гена или усиления или инактивации активности эндогенного гена, где данный микроорганизм может иметь генетическую мутацию или увеличенную активность в отношении продукции целевого пуринового нуклеотида.
Микроорганизм по настоящему изобретению, продуцирующий пуриновый нуклеотид, может сохранять повышенную способность к продуцированию целевого пуринового нуклеотида посредством содержания варианта гидролизующей глутамин GMP-синтазы по настоящему изобретению.
В одном воплощении микроорганизм, продуцирующий пуриновый нуклеотид, или микроорганизм, имеющий способность к продуцированию пуринового нуклеотида, в настоящем изобретении может представлять собой микроорганизм, у которого некоторые из генов, участвующих в биосинтезе пуриновых нуклеотидов, усилены или ослаблены, или некоторые из генов, участвующих в пути деградации пуриновых нуклеотидов, усилены или ослаблены.
Термин «уменьшение» активности полипептида в том виде, как он здесь используется, имеет идею всего из снижения активности или отсутствия активности по сравнению с эндогенной активностью. Термин «уменьшение» можно использовать взаимозаменяемо с терминами «инактивация», «недостаточность», «понижающая регуляция», «снижение», «падение», «ослабление» или тому подобными.
Уменьшение также может включать: случай, где активность самого полипептида уменьшена или устранена по сравнению с активностью полипептида, которой обладал исходный микроорганизм, из-за мутации полинуклеотида, кодирующего данный полипептид, или тому подобного; случай, где активность и/или концентрация (уровень экспрессии) всех полипептидов в клетке ниже по сравнению с природным штаммом из-за ингибирования экспрессии гена полинуклеотида, кодирующего полипептид, или ингибирования трансляции в полипептид, кодирующий полинуклеотид, или ингибирования трансляции в данный полипептид; случай, где экспрессия данного полинуклеотида не осуществляется; и/или случай, где данный полипептид не имеет активности, несмотря на экспрессию данного полинуклеотида. Термин «собственная активность» относится к активности конкретного полипептида, которой исходно обладал родительский штамм перед модификацией или микроорганизм дикого типа или немодифицированный микроорганизм, когда данный штамм или микроорганизм трансформирован посредством генетической мутации, вызванной природными или искусственными факторами. Данный термин может использоваться взаимозаменяемо с фразой «активность перед модификацией». Термины «инактивация, недостаточность, снижение, понижающая регуляция, уменьшение или ослабление» активности полипептида по сравнению с его собственной активностью означают, что активность данного полипептида снижена по сравнению с активностью конкретного полипептида, которой исходно обладал родительский штамм перед трансформацией или немодифицированный микроорганизм.
Уменьшение активности полипептида может осуществляться любым способом, известным в данной области, но не ограничивается ими, и может достигаться применением разных способов, хорошо известных в данной области (например, Nakashima N. et al., Bacterial cellular engineering by genome editing and gene silencing. Int J Mol Sci. 2014; 15 (2): 2773-2793 и Sambrook et al. Molecular Cloning 2012 и т.д.).
В частности, уменьшение активности полипептида по настоящему изобретению может достигаться посредством:
1) делеции части или всего гена, кодирующего данный полипептид;
2) модификации области контроля экспрессии (или последовательности контроля экспрессии) для уменьшения экспрессии гена, кодирующего данный полипептид;
3) модификации аминокислотной последовательности, составляющей данный полипептид, для устранения или уменьшения активности данного полипептида (например делеция/замена/вставка по меньшей мере одной аминокислоты в аминокислотной последовательности);
4) модификации последовательности гена, кодирующего данный полинуклеотид, для устранения или уменьшения активности данного полипептида (например делеция/замена/вставка по меньшей мере одного нуклеотида в нуклеотидной последовательности гена данного полипептида для кодирования полипептида, модифицированного для устранения или уменьшения активности данного полипептида);
5) модификации нуклеотидной последовательности, кодирующей инициирующий кодон 5'-UTR (нетранслируемой) области транскрипта гена, кодирующего данный полипептид;
6) введения антисмыслового олигонуклеотида (например антисмысловой РНК), комплементарно связывающегося с транскриптом гена, кодирующего данный полипептид;
7) добавления последовательности, комплементарной последовательности Шайна-Далгарно (Shine Dalgarno) гена, кодирующего данный полипептид, выше последовательности Шайна-Далгарно с образованием вторичной структуры, которая делает невозможным присоединение рибосом;
8) добавления промотора, который подлежит обратной транскрипции, к 3'-концу открытой рамки считывания (ORF) последовательности гена, кодирующего данный полипептид (инженерия обратной транскрипции (RTE); или
9) комбинации двух или более чем двух, выбранных из пунктов (1)-(8), но конкретно не ограничиваясь ими.
Например, они описываются следующим образом.
Делецией части или всего гена, кодирующего полипептид в п. (1), может быть устранение всего полинуклеотида, кодирующего эндогенный целевой белок в хромосоме, замена полинуклеотидом с делецией некоторых нуклеотидов или замена маркерным геном.
Модификацией области контроля экспрессии (или последовательности контроля экспрессии) в п. (2) может быть мутация области контроля экспрессии (или последовательности контроля экспрессии) посредством делеции, вставки, неконсервативной или консервативной замены или их комбинации, или замена последовательностью, имеющей более пониженную активность. Область контроля экспрессии включает промотор, последовательность оператора, последовательность для кодирования сайта связывания рибосомы и последовательность для осуществления контроля терминации транскрипции и трансляции, но не ограничивается ими.
Модификацией аминокислотной последовательности или полинуклеотидной последовательности по пп. (3) и (4) может быть модификация последовательности посредством делеции, вставки, неконсервативной или консервативной замены, или их комбинации в аминокислотной последовательности полипептида или полинуклеотидной последовательности, кодирующей данный полипептид, или замена аминокислотной последовательностью или полинуклеотидной последовательностью, модифицированной таким образом, чтобы иметь более пониженную активность, или аминокислотной последовательностью, или полинуклеотидной последовательностью, улучшенной для того, чтобы не иметь активности, так, чтобы уменьшить активность данного полипептида. Например, экспрессия данного гена может ингибироваться или ослабляться посредством введения мутации в данную последовательность полинуклеотида с образованием кодона терминации.
Модификация нуклеотидной последовательности, кодирующей инициирующий кодон или 5'-UTR область транскрипта гена, кодирующего полипептид по п. (5), может представлять собой, например, замену кодирующей нуклеотидной последовательностью, а не эндогенным инициирующим кодоном, другим инициирующим кодоном, имеющим меньшую скорость экспрессии полипептида, но не ограничиваясь ими.
На введение антисмыслового олигонуклеотида (например, антисмысловой РНК), комплементарно связывающегося с транскриптом гена, кодирующим полипептид по п. (6), например, может приводиться ссылка в литературе (Weintraub, Н. et al., Antisense-RNA as a molecular tool for genetic analysis, Reviews - Trends in Genetics, Vol. 1(1) 1986].
Добавление последовательности, комплементарной последовательности Шайна-Далгарно гена, кодирующего данный полипептид, к расположенной выше последовательности Шайна-Далгарно таким образом, чтобы образовать вторичную структуру, которая делает невозможным присоединение рибосом в п. (7), может делать невозможной трансляцию мРНК или уменьшать ее скорость.
Добавление промотора, который подлежит обратной транскрипции, к 3'-концу открытой рамки считывания (ORF) последовательности гена, кодирующей данный полипептид (инженерия обратной транскрипции (RTE)) в п. (8), может делать антисмысловой нуклеотид комплементарным транскрипту гена, кодирующего данный полипептид, с уменьшением, посредством этого, активности данного полипептида.
Термин «усиление» активности полипептида в том виде, как он здесь используется, относится к увеличению активности данного полипептида по сравнению с его собственной активностью. Термин «усиление» может использоваться взаимозаменяемо с «активацией», «повышающей регуляцией», «сверхэкспрессией», «увеличением» или тому подобным. Здесь «активация», «усиление», «повышающая регуляция», «сверхэкспрессия» и «увеличение» могут включать все из демонстрирования активности, которой исходно не обладали, или демонстрирования повышенной активности по сравнению с собственной активностью или активностью перед модификацией. Термин «собственная активность» относится к активности конкретного полипептида, которой исходно обладал родительский штамм перед его трансформацией, или немодифицированный микроорганизм, когда данный штамм или микроорганизм трансформируют генетической мутацией, вызванной природными или искусственными факторами. Данный термин можно использовать взаимозаменяемо с «активностью перед модификацией». «Усиление», «повышающая регуляция», «сверхэкспрессия» или «увеличение» активности полипептида по сравнению с его собственной активностью означает улучшение активности и/или концентрации (уровня экспрессии) конкретного полипептида, которым исходно обладал родительский штамм перед трансформацией или немодифицированный микроорганизм.
Данное усиление может достигаться посредством введения экзогенного полипептида или увеличения активности и/или концентрации (уровня экспрессии) эндогенного полипептида. Усиление активности данного полипептида может быть идентифицировано по увеличению уровня активности или уровня экспрессии соответствующего полипептида или количества продукта, продуцируемого из соответствующего полипептида.
Усиление активности данного полипептида может достигаться применением разных способов, хорошо известных в данной области, и не ограничивается при условии, что данный способ может увеличивать активность целевого полипептида по сравнению с микроорганизмом перед трансформацией. В частности, можно использовать генную инженерию и/или белковую инженерию, хорошо известные специалисту в данной области, которая является традиционным способом молекулярной биологии, но не ограничиваясь ей (например, Sitnicka et al. Functional Analysis of Genes. Advances in Cell Biology. 2010, Vol. 2. 1-16, Sambrook et al. Molecular Cloning 2012 или тому подобные).
В частности, усиление активности полипептида по настоящему изобретению может достигаться посредством:
1) увеличения числа внутриклеточных копий полинуклеотида, кодирующего данный полипептид;
2) замены области контроля экспрессии гена на хромосоме, кодирующей данный полипептид, последовательностью, имеющей более высокую активность;
3) модификации нуклеотидной последовательности, кодирующей инициирующий кодон или 5'-UTR область транскрипта гена, кодирующего данный полипептид;
4) модификации аминокислотной последовательности полипептида для усиления активности данного полипептида;
5) модификации полинуклеотидной последовательности, кодирующей полипептид, для усиления активности данного полипептида (например, модификации полинуклеотида последовательности гена полипептида для кодирования модифицированного полипептида с усилением активности данного полипептида);
6) введения экзогенного полипептида, демонстрирующего активность данного полипептида, или кодирующего его экзогенного полинуклеотида;
7) оптимизации кодонов полинуклеотида, кодирующего данный полипептид;
8) модификации или химической модификации экспонированного сайта, выбранного анализом третичной структуры полипептида; или
9) комбинации двух или более чем двух, выбранных из пп. (1) - (8), но конкретно не ограничиваясь ими.
Более конкретно, усиление полипептида описывается следующим образом.
Увеличение числа внутриклеточных копий полинуклеотида, кодирующего полипептид по п. (1), может достигаться введением в клетку-хозяина вектора, в котором полинуклеотид, кодирующий соответствующий полипептид, связан функциональным образом, и который может реплицироваться и функционировать независимо от хозяина. В качестве альтернативы, увеличение по п. (1) может достигаться введением одной или более чем одной копии полинуклеотида, кодирующего соответствующий полипептид, в хромосому в клетке-хозяине. Введение в хромосому может осуществляться введением в клетку-хозяина вектора, способного вставлять данный полинуклеотид в хромосому в клетке-хозяине. Данный полинуклеотид является таким, как описано выше.
Замена области контроля экспрессии гена на хромосоме, кодирующей полипептид, последовательностью с сильной активностью по п. (2), например, может представлять собой модификацию в последовательности посредством делеции, вставки, неконсервативной или консервативной замены или их комбинации, или замену последовательностью, имеющей более сильную активность, для дальнейшего усиления активности области контроля экспрессии. Данная область контроля экспрессии может включать промотор, последовательность оператора, последовательность, кодирующую сайт связывания рибосомы, последовательность, контролирующую терминацию транскрипции и трансляции и тому подобное, но конкретно не ограничивается ими.
Например, она может представлять собой замену исходного промотора более сильным промотором, но не ограничиваясь ей.
Примеры известного более сильного промотора могут представлять собой промоторы CJ1-CJ7 (US 7662943 В2), промотор lac, промотор trp, промотор trc, промотор tac, промотор PR фага лямбда, промотор PL, промотор tet, промотор gapA, промотор SPL7, промотор SPL13 (sm3) (US 10584338 В2), промотор O2 (US 10273491 В2), промотор tkt, промотор усе А и тому подобные, но не ограничиваясь ими.
Модификация нуклеотидной последовательности, кодирующей инициирующий кодон или 5'-UTR область транскрипта гена, кодирующего полипептид по п. 3), может представлять собой, например, замену кодирующей нуклеотидной последовательностью, а не эндогенным инициирующим кодоном, другим инициирующим кодоном, имеющим более высокую скорость экспрессии полипептида, но не ограничивается ими.
Модификация аминокислотной последовательности или полинуклеотидной последовательности в пп. (4) и (5) может представлять собой модификацию последовательности посредством делеции, вставки, неконсервативной или консервативной замены, или их комбинацию в аминокислотной последовательности полипептида или полинуклеотидной последовательности, кодирующей данный полипептид, или замену аминокислотной последовательностью или полинуклеотидной последовательностью, модифицированной так, чтобы иметь более сильную активность, или аминокислотной последовательностью или полинуклеотидной последовательностью, модифицированной так, чтобы иметь повышенную активность, для усиления активности данного полипептида. В частности, данная замена может осуществляться вставкой полинуклеотида в хромосому посредством гомологичной рекомбинации, но не ограничиваясь ей. Использованный здесь вектор может дополнительно включать селективный маркер для проверки вставки в хромосому. Данный селективный маркер является таким, как описывается выше.
Введение экзогенного полипептида, демонстрирующего активность данного полипептида, в п. (6) может представлять собой введение в клетку-хозяина экзогенного полинуклеотида, кодирующего полипептид, демонстрирующий такую же/аналогичную активность относительно данного полипептида. Экзогенный полинуклеотид не ограничивается по его происхождению или последовательности, при условии, что экзогенный полинуклеотид демонстрирует такую же/аналогичную активность относительно данного полинуклеотида. Введение может осуществляться любым известным способом трансформации, подходящим образом выбранным специалистом в данной области, и посредством экспрессии введенного полинуклеотида в клетке-хозяине продуцируется полипептид, и его активность может быть увеличена.
Оптимизация кодонов полинуклеотида, кодирующего данный полипептид, в п. (7) может представлять собой оптимизацию кодонов эндогенного полинуклеотида с увеличением его транскрипции или трансляции в клетке-хозяине или оптимизацию кодонов экзогенного полинуклеотида для обеспечения его оптимизированной транскрипции или трансляции в клетке-хозяине.
Модификация или химическая модификация экспонированного сайта, выбранного анализом третичной структуры полипептида в п. (8), может представлять собой, например, модификацию или химическую модификацию экспонированного сайта, подлежащего модификации или химической модификации, посредством сравнения информации по последовательности полинуклеотида, подлежащего анализу, с базой данных, которая хранит информацию по последовательностям существующих белков, определяя шаблонный белок-кандидат согласно сходству последовательностей и идентифицируя структуру на его основе.
Такое усиление активности полипептида может означать, что активность, концентрация или уровень экспрессии соответствующего полипептида увеличены относительно активности или концентрации полипептида, экспрессируемого у дикого типа или микробного штамма перед модификацией, или что количество продукта, продуцируемого из соответствующего полипептида, увеличеноя, но не ограничивается этим.
Модификация части или всего полинуклеотида в микроорганизме по настоящему изобретению может индуцироваться следующим: (а) редактирование генома с применением гомологичной рекомбинации или генетически модифицированной нуклеазы (например, CRISPR-Cas9) с использованием вектора для хромосомной вставки в микроорганизм и/или (б) обработка светом, таким как ультрафиолетовый свет и излучение, и/или химическими реактивами, но не ограничиваясь ими. Способ модифицирования части или всего гена может включать способ генной инженерии. Например, нуклеотидная последовательность или вектор, содержащий нуклеотидную последовательность, гомологичную гену-мишени, может быть введен в микроорганизм для осуществления гомологичной рекомбинации, приводя к делеции части или всего гена. Нуклеотидная последовательность или вектор, подлежащий введению, могут включать маркер доминантного отбора, но не ограничиваясь им.
Согласно еще одному другому аспекту настоящего изобретения предложен способ получения пуринового нуклеотида, включающий культивирование микроорганизма, включающего вариант по настоящему изобретению или полинуклеотид, кодирующий данный вариант.
Способ получения пуринового нуклеотида по настоящему изобретению может включать культивирование в среде микроорганизма, содержащего вариант по настоящему изобретению, кодирующий его полинуклеотид или вектор, включающий указанный полинуклеотид.
Термин «культивирование» в том виде, как он здесь используется, относится к выращиванию микроорганизма по настоящему изобретению в подходящим образом скорректированных условиях среды. Методику культивирования по настоящему изобретению можно проводить согласно подходящим средам или условиям культивирования, известным в данной области. Такое культивирование может легко корректироваться согласно выбранному штамму специалистом в данной области. В частности, данное культивирование может быть периодического типа, непрерывного типа и/или типа с подпиткой, но не ограничивается ими.
Термин «среда» в том виде, как он здесь используется, относится к смеси, содержащей, в качестве главных ингредиентов, питательные вещества, требующиеся для культивирования микроорганизма, где данная среда поставляет питательные вещества, факторы роста и тому подобное, включая воду, которые являются важными для выживания и роста. В частности, в том, что касается среды и других условий культивирования, используемых для культивирования микроорганизма по настоящему изобретению, можно использовать любую среду, которая используется для обычного культивирования микроорганизмов, без конкретного ограничения. Однако микроорганизмы по настоящему изобретению могут культивироваться в аэробных условиях в традиционной среде, содержащей подходящие источники углерода, источники азота, источники фосфора, неорганические соединения, аминокислоты и/или витамины, тогда как температура, рН и тому подобное корректируются.
В частности, культуральная среда для штамма рода Corynebacterium может быть найдена в литературе ("Manual of Methods for General Bacteriology" by the American Society for Bacteriology (Washington D.C., USA, 1981)).
В настоящем изобретении источник углерода может включать углеводы, такие как глюкоза, сахароза, лактоза, фруктоза, сахар и мальтоза; сахароспирты, такие как маннит и сорбит; органические кислоты, такие как пировиноградная кислота, молочная кислота и лимонная кислота; и аминокислоты, такие как глутаминовая кислота, метионин и лизин. Кроме того, можно использовать природные источники органических питательных веществ, такие как гидролизаты крахмала, мелассы, сырые мелассы, рисовые отруби, маниок, жом сахарного тростника и жидкий кукурузный экстракт, и, в частности, можно использовать углеводы, такие как глюкоза и стерильные предобработанные мелассы (т.е. мелассы, превращенные в восстанавливающие сахара), и можно использовать подходящие количества других источников углерода без ограничения. Данные источники углерода могут использоваться одни или в комбинации двух или более чем двух, но не ограничиваясь ими.
В том, что касается источников азота, можно использовать неорганические источники азота, такие как аммиак, сульфат аммония, хлорид аммония, ацетат аммония, фосфат аммония, карбонат аммония и нитрат аммония; аминокислоты, такие как глутаминовая кислота, метионин и глутамин; и органические источники азота, такие как пептон, NZ-амин, мясные экстракты, дрожжевые экстракты, солодовые экстракты, жидкий кукурузный экстракт, гидролизаты казеина, рыбу или продукты ее разложения, обезжиренный соевый жмых или его продукты деградации и тому подобное. Данные источники азота можно использовать одни или в комбинации двух или более чем двух из них, но они не ограничиваются ими.
Примеры источников фосфата могут включать одноосновный фосфат калия, двухосновный фосфат калия и соответствующие им натрийсодержащие соли. В том, что касается неорганических соединений, можно использовать хлорид натрия, хлорид кальция, хлорид железа, сульфат магния, сульфат железа, сульфат марганца, карбонат кальция и тому подобное, и, кроме того, можно включать аминокислоты, витамины и/или подходящие предшественники. Данные составляющие ингредиенты или предшественники можно добавлять в среду партиями или непрерывным способом. Однако настоящее раскрытие не ограничивается ими.
рН среды может корректироваться добавлением в среду подходящим способом таких соединений, как гидроксид аммония, гидроксид калия, аммиак, фосфорная кислота и серная кислота, во время культивирования микроорганизма по настоящему изобретению. Кроме того, можно добавлять пеногаситель, такой как сложный полигликолевый эфир жирной кислоты, для подавления образования пены во время культивирования. Кроме того, в среду можно инъецировать кислород или кислородсодержащий газ для поддержания аэробного состояния среды, или можно инъецировать газообразный азот, водород или диоксид углерода, или можно не инъецировать газ для поддержания анаэробного или неаэробного состояния среды, но не ограничиваясь ими.
При культивировании по настоящему изобретению может поддерживаться температура культивирования от 20°С до 45°С, в частности, от 25°С до 40°С, и данное культивирование может проводиться в течение примерно от 10 часов до 160 часов, но не ограничиваясь ими.
Пуриновый нуклеотид, продуцируемый культивированием по настоящему изобретению, может высвобождаться в среду или может сохраняться в клетках без высвобождения.
Способ получения пуринового нуклеотида по настоящему изобретению может дополнительно включать получение микроорганизма по настоящему изобретению, приготовление среды для культивирования данного микроорганизма или комбинацию данных стадий (независимо от порядка, в любом порядке), например, до или после стадии культивирования.
Способ получения пуринового нуклеотида по настоящему изобретению может дополнительно включать выделение пуринового нуклеотида из среды, образующейся в результате культивирования (среда, в которой осуществлялось культивирование), или из микроорганизма. Стадия выделения может быть дополнительно включена после стадии культивирования.
Выделение может представлять собой отбор желательного пуринового нуклеотида с использованием подходящего способа, известного в данной области, согласно способу культивирования микроорганизма по настоящему изобретению, например, культивированию периодического, непрерывного типа или с подпиткой. Например, можно использовать центрифугирование, фильтрование, обработку агентом, осаждающим кристаллизованный белок (высаливание), экстракцию, ультразвуковое разрушение, ультрафильтрацию, диализ, разные типы хроматографии, такую как хроматографию на молекулярных ситах (гель-фильтрация), адсорбционную хроматографию, ионообменную хроматографию и аффинную хроматографию, ВЭЖХ (высокоэффективная жидкостная хроматография) и комбинацию данных способов, и желательный пуриновый нуклеотид может быть выделен из среды или микроорганизма с использованием подходящего способа, известного в данной области.
Способ получения пуринового нуклеотида по настоящему изобретению может дополнительно включать стадию очистки. Очистка может проводиться с использованием подходящего способа, известного в данной области. В типичном воплощении, когда способ получения пуринового нуклеотида по настоящему изобретению включает и стадию выделения, и стадию очистки, стадия выделения и стадия очистки могут осуществляться непрерывно или прерывисто, независимо от порядка, или могут осуществляться одновременно или интегрироваться в одну стадию, но не ограничиваясь ими.
В типичном воплощении способ получения GMP по настоящему изобретению может дополнительно включать превращение ХМР в GMP. В способе получения GMP по настоящему изобретению стадия превращения может быть дополнительно включена после стадии культивирования или стадии превращения. Данная стадия превращения может проводиться с использованием подходящего способа, известного в данной области. Например, превращение может проводиться с использованием коринебактерии, Е. coli или аминазы 5'-ксантиловой кислоты (KR 10-0655902 В1, US 2013-0095529 A1 или тому подобные), но не ограничиваясь ими.
В способе по настоящему изобретению вариант, полинуклеотид, вектор, штамм, пуриновый нуклеотид и тому подобные являются такими, как описано в других аспектах, приведенных выше.
Еще одним другим аспектом настоящего изобретения является предложение композиции для получения пуринового нуклеотида, содержащей вариант по настоящему изобретению, полинуклеотид, кодирующий указанный вариант, микроорганизм, включающий вектор, включающий полинуклеотид, или полинуклеотид по настоящему изобретению; среды, полученной культивированием данного микроорганизма; или ее композиции.
Композиция по настоящему изобретению может дополнительно содержать любой подходящий эксципиент, который обычно используют в композиции для получения пуринового нуклеотида, и примеры данного эксципиента могут включать консервант, увлажнитель, диспергент, суспендирующий агент, буфер, стабилизатор или изотоничный агент, но не ограничиваются ими.
В композиции по настоящему изобретению вариант, полинуклеотид, вектор, микроорганизм, среда, пуриновый нуклеотид и тому подобные являются такими, как описано в других аспектах выше.
Еще одним другим аспектом настоящего изобретения является предложение способа увеличения способности микроорганизма к продуцированию пуринового нуклеотида, включающий модифицирование указанного микроорганизма для экспрессии варианта по настоящему изобретению.
В способе по настоящему изобретению вариант, полинуклеотид, вектор, микроорганизм, среда, пуриновый нуклеотид и тому подобное являются такими, как описано в других аспектах выше.
Согласно еще одному другому аспекту настоящего изобретения предложено применение варианта по настоящему изобретению для получения пуринового нуклеотида.
Согласно еще одному другому аспекту настоящего изобретения предложено применение варианта по настоящему изобретению, полинуклеотида, кодирующего указанный вариант, или микроорганизма, включающего вектор, содержащий указанный полинуклеотид.
Данный вариант, полинуклеотид, вектор, микроорганизм и тому подобные являются такими, как описано в других аспектах выше.
Способ осуществления изобретения
Ниже настоящее раскрытие будет подробно описано со ссылкой на примеры и опытные примеры. Однако данные примеры и опытные примеры приводятся для конкретного иллюстрирования настоящего изобретения, и объем настоящего изобретения не ограничивается ими.
Пример 1: получение варианта с ослабленной синтазой guaA
Для обнаружения варианта guaA для получения ХМР конструировали библиотеку мутантного guaA - гена, кодирующего данный вариант.
Пример 1-1: Получение вектора, содержащего guaA
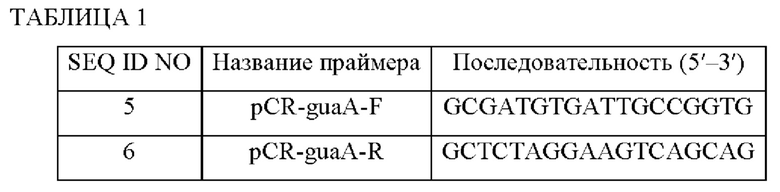
Для получения библиотеки мутантного guaA сначала конструировали рекомбинантный вектор, содержащий guaA. Проводили ПЦР (полимеразная цепная реакция) с использованием хромосомы Corynebacterium stationis АТСС6872 в качестве матрицы, наряду с праймерами SEQ ID NO: 5 и SEQ ID NO: 6, и продукт амплификации клонировали в вектор pCR2.1 с использованием набора для клонирования ТОРО (Invitrogen), и образующийся вектор называли pCR-guaA.
Пример 1-2: Конструирование библиотеки мутантного guaA
Библиотеку мутантного guaA конструировали с использованием в качестве матрицы вектора pCR-guaA, сконструированного в Примере 1-1. Данную библиотеку получали с использованием набора для ПЦР ПЦР пониженной точности, допускающей ошибки (набор для случайного ПЦР-мутагенеза Clontech Diversify®), и получали ПЦР-продукты в виде мутантных guaA с разными последовательностями посредством случайного мутагенеза с использованием праймеров SEQ ID NO: 7 и 8 согласно руководству изготовителя. Продукты амплификации клонировали с использованием набора для клонирования ТОРО (Invitrogen), затем трансформировали в Е. coli DH5α и распределяли на твердой среде LB (лизогенная среда), содержащей канамицин (25 мг/л). Трансформированные колонии Е. coli собирали для выделения плазмид, которые называли pCR-guaA-библиотекой.

Пример 1-3: Оценка сконструированной библиотеки и выбор штамма
pCR-guaA-библиотеку, полученную в Примере 1-2, трансформировали в штамм Corynebacterium stationis АТСС6872 дикого типа электропорацией, и затем данный штамм распределяли на питательной среде, содержащей 25 мг/л канамицина, с получением 5000 колоний штамма, в которые был вставлен мутантный ген. Соответствующие колонии были названы от C.st ATCC6872_pCR_guaA(mt)1 до C.st ATCC6872_pCR_guaA(mt)5000.
- Питательная среда: 1% пептона, 1% говяжьего экстракта, 0,25% хлорида натрия, 1% дрожжевого экстракта, 150 мг/л аденина, 150 мг/л гуанина, 2% агара, рН 7,2 (но основе 1 л дистиллированной воды).
Каждую из 5000 полученных колоний автоклавировали под давлением, инокулировали в 100 мкл посевной среды, содержащей канамицин (25 мг/л), культивировали в 96-глубоколуночном планшете со встряхиванием при 30°С, 1200 об./мин в течение 24 часов с использованием шейкера для микропланшетов (TAITAC) и затем использовали в качестве посевной культуры. 320 мкл автоклавированной ферментационной среды (240 мкл основной среды плюс 80 мкл отдельной стерилизованной среды) распределяли в 96-глубоколуночном планшете, и затем в него инокулировали каждые 15 мкл посевной культуры с последующим культивированием со встряхиванием при тех же самых условиях, что и выше, в течение 72 часов.
Для анализа количества ХМР, продуцированного в культуре, 640 мкл стерильной воды дозировали в культуру после завершения культивирования с последующим центрифугированием при 4000 об./мин в течение 15 минут, и затем 3 мкл супернатанта переносили в 96-луночный УФ (ультрафиолет) планшет, в который дозировали 297 мкл дистиллированной воды. Затем использовали микропланшет-ридер для осуществления встряхивания в течение 30 секунд, и использовали спектрофотометр для измерения поглощения при 25°С и длине волны 260 нм. Затем отбирали десять колоний мутантных штаммов, демонстрирующих увеличение поглощения по сравнению со штаммом дикого типа. Другие колонии демонстрировали аналогичные или сниженные уровни поглощения по сравнению с контролем.
Десять отобранных штаммов многократно измеряли на поглощение посредством приведенного выше способа и исследовали на уровень продукции ХМР, и отбирали один вид штамма (C.st ATCC6872_pCR_guaA(mt)726), имеющий значительно повышенную способность к продукции ХМР по сравнению со штаммом дикого типа.
Для подтверждения правильности отобранного в конечном итоге штамма, осуществляли анализ титра ферментации.
Штамм Corynebacterium stationis АТСС6872 дикого типа и отобранный штамм C.st ATCC6872_pCR_guaA(mt)726 инокулировали в пробирки на14 мл, содержащие 2,5 мл приведенной ниже посевной среды, и культивировали со встряхиванием при 170 об./мин в течение 24 часов при 30°С. В колбу на 250 мл с угловыми перегородками, содержащую 32 мл следующей продукционной среды (24 мл основной среды плюс 8 мл отдельной стерильной среды), инокулировали 0,7 мл посевной культуры и культивировали со встряхиванием при 170 об./мин в течение 75 часов при 30°С.
Составы посевной среды, основной среды и отдельной стерильной среды являются следующими.
ХМР посевная среда для колбы
30 г/л глюкозы, 15 г/л пептона, 15 г/л дрожжевого экстракта, 2,5 г/л хлорида натрия, 3 г/л мочевины, 150 мг/л аденина, 150 мг/л гуанина, рН 7,0 (на основе 1 л дистиллированной воды).
ХМР продукционная среда для колбы (основная среда)
50 г/л глюкозы, 10 г/л сульфата магния, 3 г/л дрожжевого экстракта, 100 мг/л хлорида кальция, 20 мг/л сульфата железа, 10 мг/л сульфата магранца, 10 мг/л сульфата цинка, 0,8 мг/л сульфата меди, 20 мг/л гистидина, 15 мг/л цистина, 15 мг/л бета-аланина, 100 мкг/л биотина, 5 мг/л тиамина, 50 мг/л аденина, 25 мг/л гуанина, 15 мг/л ниацина, рН 7,0 (на основе 1 л дистиллированной воды).
ХМР продукционная среда для колбы (отдельная стерильная среда)
18 г/л одноосновного фосфата калия, 42 г/л двухосновного фосфата калия, 7 г/л мочевины, 5 г/л сульфата аммония (на основе 1 л дистиллированной воды).
Результаты измерения уровня продукции ХМР способом с использованием ВЭЖХ после завершения культивирования показаны в Таблице 3.
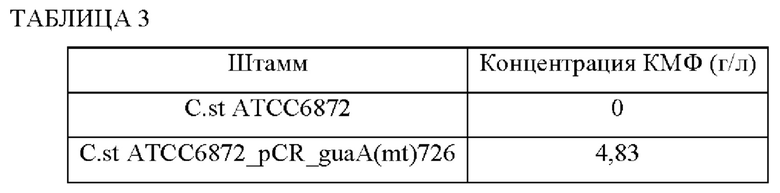
Как показано в Таблице 3, концентрация продуцированного ХМР составляла 4,83 г/л в C.st ATCC6872_pCR guaA(mt)726 по сравнению со штаммом дикого типа.
Пример 1-4: Идентификация мутации посредством секвенирования гена
Для идентификации последовательности варианта guaA штамма C.st ATCC6872_pCR_guaA(mt)726, данный штамм C.st ATCC6872_pCR_guaA(mt)726 подвергали ПЦР с использованием праймеров SEQ ID NO: 8 и 9, и секвенированию. В результате сравнения с последовательностью гена guaA штамма дикого типа идентифицировали, что штамм C.st ATCC6872_pCR_guaA(mt)726 включает мутацию, в которой аминокислота в положении 29 в гене guaA заменяется с аргинина на цистеин (нуклеотид в положении 85 заменяется от с до t: SEQ ID NO: 2).
Данный идентифицированный вариант последовательности показан в Таблице 4.

В следующих примерах исследовали, имела ли мутация guaA влияние на продукцию ХМР.
Пример 2: Идентификация влияния варианта guaA
Пример 2-1: конструирование вектора для экспрессии варианта guaA
Для исследования влияния на продукцию КМФ варианта (R29C; SEQ ID NO: 1), в котором аргинин в положении 29 аминокислотной последовательности фермента guaA был заменен цистеином, конструировали вектор для получения его экспрессионного штамма следующим образом с использованием плазмиды pDCM2 (корейская публикация №10-2020-0136813) для вставки и замены гена в хромосоме Corynebacterium.
ПЦР проводили с использованием хромосомы Corynebacterium stationis АТСС6872 в качестве матрицы, наряду с парами праймеров SEQ ID NO: 10 и 11, и SEQ ID NO: 12 и 13. ДНК-полимеразу Solg™ Pfu-X использовали в качестве полимеразы, и ПЦР проводили при следующих условиях ПЦР-амплификации: денатурация при 95°С в течение 5 минут, 30 циклов денатурации при 95°С в течение 30 секунд, отжиг при 58°С в течение 30 секунд, полимеризация при 72°С в течение 60 секунд и затем реакция полимеризации при 72°С в течение 5 минут для получения, посредством этого, каждого ПЦР-продукта. Продукт амплификации смешивали с вектором pDCM2, полученным ранее расщеплением рестрикционным ферментом SmaI, и клонировали способом сборки по Gibson (DG Gibson et al., NATURE METHODS, Vol. 6 No. 5, MAY 2009, NEBuilder HiFi DNA Assembly Master Mix) с получением рекомбинантной плазмиды, которую назвали pDCM2-guaA(R29C). Клонирование осуществляли смешиванием реактива сборки Gibson и каждого из генных фрагментов при расчетном числе молей, с последующим консервированием при 50°С в течение 1 часа.
Пример 2-2: Получение штамма, экспрессирующего вариант guaA
Вектор pDCM2-guaA(R29C), сконструированный в приведенном выше примере, трансформировали в штамм Corynebacterium stationis АТСС6872 посредством электропорации, и штаммы, имеющие данный вектор, вставленный в хромосому посредством рекомбинации гомологичных последовательностей, отбирали на среде, содержащей 25 мг/л канамицина. Отобранные первичные штаммы подвергали вторичному кроссинговеру для отбора штамма, имеющего мутацию, введенную в целевой ген. Введение генной мутации в заключительный трансформированный штамм исследовали посредством ПЦР с использованием пары праймеров SEQ ID NO: 14 и SEQ ID NO: 15 и секвенирования, и подтвержденный штамм назвали C.st ATCC6872::guaA(R29C).
Пример 2-3: Сравнение способности к продуцированию ХМР штамма, экспрессирующего вариант guaA
Способности к продуцированию ХМР штамма C.st ATCC6872::guaA(R29C), полученного в Примере 2-2, и штамма дикого типа исследовали посредством способа оценки титра ферментации в Примере 1-3. После завершения культивирования уровень продукции ХМР измеряли посредством ВЭЖХ, и результаты культивирования демонстрируются в Таблице 5.
Данный анализ повторяли три раза, и средние значения результатов анализа показаны в Таблице 5.

Как показано в Таблице 5, концентрация продуцированного ХМР в штамме C.st ATCC6872::guaA(R29C) составляла 5,21 г/л.
Данный штамм C.st ATCC6872::guaA(R29C) был обозначен как CN02-2299, его депонировали в Корейский центр сохранения микроорганизмов, депозитарный институт, работающий согласно Будапештскому соглашению, 9 августа 2021 г., и ему был присвоен номер доступа KССМ13029Р.
Пример 3: Замена аминокислоты другими аминокислотами в мутации guaA
Пример 3-1: конструирование вектора для замены и вставки аминокислоты для мутации guaA
Посредством приведенного выше примера идентифицировали, что ХМР мог быть получен посредством введения мутации в guaA(R29C). Для исследования позиционной важности мутации guaA конструировали векторы для замены аминокислоты в положении 29 другими аминокислотами, и исследовали влияние на способность к продуцированию ХМР. Проводили сайт-направленный мутагенез с использованием вектора pDCM2-guaA(R29C), сконструированного в Примере 2-1, в качестве матрицы.
В частности, ПЦР проводили с использованием пар праймеров SEQ ID NO: 10 и 16, и SEQ ID NO: 17 и 13, пар праймеров SEQ ID NO: 10 и 18, и SEQ ID NO: 19 и 13, пар праймеров SEQ ID NO: 10 и 20, и SEQ ID NO: 21 и 13, пар праймеров SEQ ID NO: 10 и 22, и SEQ ID NO: 23 и 13, пар праймеров SEQ ID NO: 10 и 24, и SEQ ID NO: 25 и 13, пар праймеров SEQ ID NO: 10 и 26, и SEQ ID NO: 27 и 13, пар праймеров SEQ ID NO: 10 и 28, и SEQ ID NO: 29 и 13, пар праймеров SEQ ID NO: 10 и 30, и SEQ ID NO: 31 и 13, пар праймеров SEQ ID NO: 10 и 32, и SEQ ID NO: 33 и 13, пар праймеров SEQ ID NO: 10 и 34, и SEQ ID NO: 35 и 13, пар праймеров SEQ ID NO: 10 и 36, и SEQ ID NO: 37 и 13, пар праймеров SEQ ID NO: 10 и 38, и SEQ ID NO: 39 и 13, пар праймеров SEQ ID NO: 10 и 40, и SEQ ID NO: 41 и 13, пар праймеров SEQ ID NO: 10 и 42, и SEQ ID NO: 43 и 13, пар праймеров SEQ ID NO: 10 и 44, и SEQ ID NO: 45 и 13, пар праймеров SEQ ID NO: 10 и 46, и SEQ ID NO: 47 и 13, пар праймеров SEQ ID NO: 10 и 48, и SEQ ID NO: 49 и 13, и пар праймеров SEQ ID NO: 10 и 50, и SEQ ID NO: 51 и 13. В качестве полимеразы использовали ДНК-полимеразу Solg™ Pfu-X, и ПЦР проводили при следующих условиях ПЦР-амплификации: с денатурацией при 95°С в течение 5 минут, 30 циклами денатурации при 95°С в течение 30 секунд, отжигом при 58°С в течение 30 секунд, полимеризацией при 72°С в течение 60 секунд и затем реакцией полимеризации при 72°С в течение 5 минут для получения, посредством этого, каждого ПЦР-продукта. Соответствующие продукты амплификации смешивали с вектором pDCM2, полученным ранее расщеплением рестрикционным ферментом SmaI, и клонировали способом сборки по Gibson с получением рекомбинантных плазмид, и информация по плазмидам, полученным таким образом, показана в Таблице 6. Клонирование осуществляли смешиванием реактива сборки Gibson и соответствующих фрагментов при расчетном числе молей, с последующим консервированием при 50°С в течение 1 часа.

Пример 3-2: Получение штаммов, имеющих мутации в виде замены в варианте guaA другими аминокислотами и сравнение способности к продуцированию ХМР
18 векторов для введения мутации, полученных в Примере 3-1, трансформировали в штамм Corynebacterium stationis АТСС6872 дикого типа, и штаммы, имеющие векторы, вставленные в хромосому посредством рекомбинации гомологичных последовательностей, отбирали на среде, содержащей 25 мг/л канамицина. Отобранные первичные штаммы подвергали вторичному кроссинговеру для отбора штаммов, имеющих мутацию, введенную в целевой ген. Введение мутации гена в наконец трансформированные штаммы исследовали посредством ПЦР с использованием пары праймеров SEQ ID NO: 14 и SEQ ID NO: 15 и секвенирования, и названия штаммов согласно вставленным мутациям показаны в Таблице 7 ниже.

Полученные штаммы, штамм C.st ATCC6872::guaA(R29C) и штамм дикого типа, культивировали и анализировали на концентрацию ХМР посредством способа оценки титра ферментации в Примере 1-3. Данный анализ повторяли три раза, и средние значения результатов анализа показаны в Таблице 8.
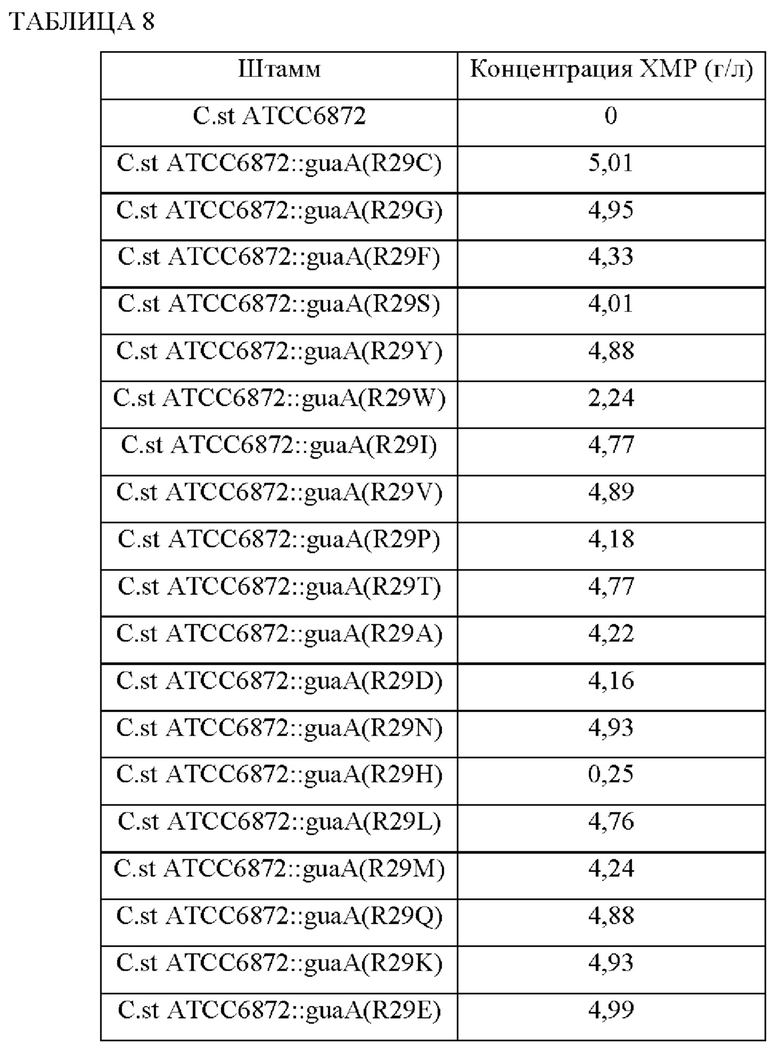
Ссылаясь на Таблицу 8, идентифицировали, что штаммы, включающие guaA, в котором аминокислота в положении 29 в аминокислотной последовательности, кодируемой геном guaA, заменена другими аминокислотами, за исключением аргинина, продуцируют ХМР по сравнению со штаммом дикого типа. То есть, аминокислота в положении 29 в аминокислотной последовательности, кодируемой геном guaA, соответствовала положению главной мутации при продукции ХМР и, более конкретно, при замене аминокислоты в положении 29 в аминокислотной последовательности, кодируемой геном guaA, другими аминокислотами, за исключением аргинина (цистеином, глицином, фенилаланином, серином, тирозином, триптофаном, изолейцином, валином, пролином, треонином, аланином, аспарагиновой кислотой, аспарагином, гистидином, лейцином, метионином, глутамином, лизином и глутаминовой кислотой), количества ХМР, продуцированные микроорганизмами, содержащими такую мутацию, могут быть значительно увеличены.
Следовательно, можно видеть, что варианты, имеющие замены аминокислоты в положении 29 в guaA другими аминокислотами, могут эффективно использоваться в продукции пуринового нуклеотида.
Пример 4: Идентификация способности к продуцированию GMP штамма, экспрессирующего вариант quaА
Продукцию GMP исследовали с использованием ХМР культуры C.st ATCC6872::guaA(R29C) в качестве штамма, продуцирующего ХМР, посредством следующего способа (см. корейский патент № KR 10-0655902 В1 и патентную публикацию США № US 2013-0095529 A1).
Штамм C.st ATCC6872::guaA(R29C) культивировали посредством способа оценки титра ферментации в Примере 1-3. После завершения культивирования уровень продукции ХМР измеряли способом с использованием ВЭЖХ. Для реакции превращения продуцированного ХМР в GMP добавляли следующие добавки реакции превращения и ХМР-аминазу Е. coli в ферментационную жидкость в колбе с угловыми перегородками для осуществления реакции превращения при 40°С в течение 2,5 часов.
Добавки реакции превращения
1,8 г/л фитиновой кислоты, 4,8 г/л сульфата магния, 3 мл/л nymeen, 2% ксилола, 100 мг/л аденина, 7,7 г/л двухосновного фосфата натрия (Na2HPO4), 2 г/л глутамина, 46 г/л глюкозы.
В результате данного анализа показатель превращения, указывающий уровень продукции GMP по сравнению с уровнем потребления ХМР, показан в Таблице 9.

Как показано в Таблице 9, 3,54 г/л GMP продуцировалось посредством реакции превращения из ХМР, продуцированного штаммом C.st ATCC6872::guaA(R29C).
Следовательно, идентифицировали, что вариант, имеющий замену аминокислоты в положении 29 в guaA другой аминокислотой, увеличивал продукцию GMP, и, таким образом, можно видеть, что вариант, предложенный в настоящеми зобретении, может эффективно использоваться в продукции пуринового нуклеотида.
Как изложено выше, специалист в области, к которой относится настоящее раскрытие, сможет понять то, что настоящее раскрытие может быть воплощено в других конкретных формах без отступления от его технической сущности или существенных характеристик. Следовательно, описанные выше воплощения следует истолковывать как иллюстрирующие примерами и не ограничивающие настоящее раскрытие. Следует понимать то, что согласно объему настоящего изобретения все изменения или модификации, полученные из определений и объемов формулы изобретения и ее эквивалентов, будут попадать в пределы объема данного изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> CJ CheilJedang Corporation
<120> НОВЫЙ ВАРИАНТ ГИДРОЛИЗУЮЩЕЙ ГЛУТАМИН GMP-СИНТАЗЫ И СПОСОБ
ПОЛУЧЕНИЯ ПУРИНОВОГО НУКЛЕОТИДА С ЕГО ИСПОЛЬЗОВАНИЕМ
<130> OPA21333
<150> KR 10-2021-0125841
<151> 2021-09-23
<160> 51
<170> KoPatentIn 3.0
<210> 1
<211> 524
<212> PRT
<213> Artificial Sequence
<220>
<223> guaA_R29C
<400> 1
Met Thr Gln Pro Ala Thr Thr Pro Arg Pro Val Leu Val Val Asp Phe
1 5 10 15
Gly Ala Gln Tyr Ala Gln Leu Ile Ala Arg Arg Val Cys Glu Ala Ser
20 25 30
Ile Tyr Ser Glu Val Val Pro His Ser Ala Thr Val Lys Glu Ile Lys
35 40 45
Ala Lys Asn Pro Ala Ala Leu Ile Leu Ser Gly Gly Pro Ser Ser Val
50 55 60
Tyr Ala Asp Gly Ala Pro Gln Leu Lys Pro Glu Leu Leu Glu Leu Gly
65 70 75 80
Val Pro Val Phe Gly Ile Cys Tyr Gly Phe Gln Ala Met Asn His Ala
85 90 95
Leu Gly Gly Asn Val Ala Gln Thr Gly Asp Arg Glu Tyr Gly Arg Thr
100 105 110
Glu Ile Thr His Thr Gly Gly Val Leu His Asp Gly Leu Glu Glu Asn
115 120 125
His Lys Val Trp Met Ser His Gly Asp Ala Val Asp Lys Ala Pro Glu
130 135 140
Gly Phe Thr Val Thr Ala Ser Ser Ala Gly Ala Pro Val Ala Ala Met
145 150 155 160
Glu Cys Val Ala Lys Gln Met Ala Gly Val Gln Tyr His Pro Glu Val
165 170 175
Met His Ser Pro His Gly Gln Glu Val Leu Val Arg Phe Leu Thr Glu
180 185 190
Val Ala Gly Leu Glu Gln Thr Trp Thr Ser Ala Asn Ile Ala Gln Gln
195 200 205
Leu Ile Asp Asp Val Arg Ala Gln Ile Gly Pro Glu Gly Arg Ala Ile
210 215 220
Cys Gly Leu Ser Gly Gly Val Asp Ser Ala Val Ala Ala Ala Leu Val
225 230 235 240
Gln Arg Ala Ile Gly Asp Arg Leu Thr Cys Val Phe Val Asp His Gly
245 250 255
Leu Leu Arg Ala Gly Glu Arg Glu Gln Val Glu Lys Asp Phe Val Ala
260 265 270
Ser Thr Gly Ala Lys Leu Ile Thr Ala His Glu Ala Asp Ala Phe Leu
275 280 285
Ser Lys Leu Ala Gly Val Thr Asp Pro Glu Ala Lys Arg Lys Ala Ile
290 295 300
Gly Ala Glu Phe Ile Arg Ser Phe Glu Arg Ala Val Ala Gln Ala Leu
305 310 315 320
Glu Glu Ser Pro Glu Asp Ser Thr Val Asp Phe Leu Val Gln Gly Thr
325 330 335
Leu Tyr Pro Asp Val Val Glu Ser Gly Gly Gly Asp Gly Thr Ala Asn
340 345 350
Ile Lys Ser His His Asn Val Gly Gly Leu Pro Asp Asp Val Glu Phe
355 360 365
Glu Leu Val Glu Pro Leu Arg Leu Leu Phe Lys Asp Glu Val Arg Ala
370 375 380
Val Gly Arg Glu Leu Gly Leu Pro Glu Glu Ile Val Ala Arg Gln Pro
385 390 395 400
Phe Pro Gly Pro Gly Leu Gly Ile Arg Ile Ile Gly Glu Val Thr Glu
405 410 415
Glu Arg Leu Glu Ile Leu Arg Gln Ala Asp Leu Ile Ala Arg Thr Glu
420 425 430
Leu Thr Asn Ala Gly Leu Asp Gly Asp Ile Trp Gln Cys Pro Val Val
435 440 445
Leu Leu Ala Asp Val Arg Ser Val Gly Val Gln Gly Asp Gly Arg Thr
450 455 460
Tyr Gly His Pro Ile Val Leu Arg Pro Val Ser Ser Glu Asp Ala Met
465 470 475 480
Thr Ala Asp Trp Thr Arg Val Pro Tyr Asp Val Leu Glu Lys Ile Ser
485 490 495
Thr Arg Ile Thr Asn Glu Val Asn Asp Val Asn Arg Val Val Val Asp
500 505 510
Ile Thr Ser Lys Pro Pro Gly Thr Ile Glu Trp Glu
515 520
<210> 2
<211> 1575
<212> DNA
<213> Artificial Sequence
<220>
<223> guaA_c85t
<400> 2
gtgactcaac ctgcaacaac tccgcgccca gtcctcgtgg tggatttcgg tgcccaatac 60
gcacagctga ttgctcgtcg cgtatgtgag gcatcgattt actccgaggt agtcccacat 120
tccgccaccg ttaaagagat taaagctaaa aaccctgcag ctttgatttt gtccggtggc 180
ccgtcctctg tttatgccga tggcgccccg caattaaagc ctgaactgct cgagcttggt 240
gtgccagtct ttggcatctg ctacggcttc caagccatga accatgcttt gggtggcaac 300
gttgcgcaaa ccggtgaccg tgaatacggc cgcaccgaaa tcacccatac cggtggtgtg 360
ctgcacgacg gcttagaaga aaaccacaag gtctggatgt cccacggtga tgctgtggat 420
aaggcacctg agggctttac cgtgaccgca tcgtcggctg gtgcgccggt tgcagcgatg 480
gaatgcgtgg ccaagcaaat ggctggtgtg caataccacc ccgaggttat gcattcccca 540
cacggacagg aagtactcgt tcgcttcctc accgaggtag cagggctaga gcagacctgg 600
acctcggcaa atattgcgca gcagcttatc gatgatgtcc gcgcgcaaat cggccctgaa 660
ggccgcgcta tttgtggcct gtcgggcggc gtggactccg cagtcgctgc agcgctcgtg 720
cagcgcgcca ttggcgaccg tttgacctgt gtgttcgtgg accacggtct gctgcgcgcc 780
ggtgagcgtg agcaggtaga aaaggacttc gtggcttcga ctggtgcgaa gctgattacc 840
gcgcatgaag ctgatgcttt cttgtctaag ctcgccggtg ttaccgatcc tgaggctaag 900
cgcaaggcta tcggcgcgga attcatccgt tcctttgagc gtgctgtggc acaggctttg 960
gaagaatctc ctgaagactc cacagtggac ttcctggtcc agggcacctt gtatccggat 1020
gtggttgaat ccggcggcgg tgacggcacc gcaaatatca agtcccacca caatgttggc 1080
ggcctgccag acgatgtcga attcgaactc gtcgagccac tacgcctgct gtttaaggac 1140
gaagtccgtg ccgtcggccg cgagctcggc ctgcctgagg aaatcgttgc ccgccagcca 1200
ttccctggcc ctggcctagg catccgcatc atcggtgaag tcaccgagga gcgtctagaa 1260
atcctgcgtc aagcagacct gattgcgcgt accgagctga ccaacgctgg cctcgacggt 1320
gatatctggc agtgcccagt cgtactgctt gccgatgtcc gctccgtcgg agtccaaggc 1380
gacggccgca cctacggcca cccaatcgtg ctgcgcccag tgtcatccga ggatgccatg 1440
accgccgact ggacccgcgt tccttacgac gtcctagaga aaatctccac ccgcattacc 1500
aacgaagtca acgacgtcaa ccgcgtggtc gtcgacatca cctccaagcc accgggaacc 1560
atcgagtggg agtaa 1575
<210> 3
<211> 524
<212> PRT
<213> Unknown
<220>
<223> Corynebacterium stationis
<400> 3
Met Thr Gln Pro Ala Thr Thr Pro Arg Pro Val Leu Val Val Asp Phe
1 5 10 15
Gly Ala Gln Tyr Ala Gln Leu Ile Ala Arg Arg Val Arg Glu Ala Ser
20 25 30
Ile Tyr Ser Glu Val Val Pro His Ser Ala Thr Val Lys Glu Ile Lys
35 40 45
Ala Lys Asn Pro Ala Ala Leu Ile Leu Ser Gly Gly Pro Ser Ser Val
50 55 60
Tyr Ala Asp Gly Ala Pro Gln Leu Lys Pro Glu Leu Leu Glu Leu Gly
65 70 75 80
Val Pro Val Phe Gly Ile Cys Tyr Gly Phe Gln Ala Met Asn His Ala
85 90 95
Leu Gly Gly Asn Val Ala Gln Thr Gly Asp Arg Glu Tyr Gly Arg Thr
100 105 110
Glu Ile Thr His Thr Gly Gly Val Leu His Asp Gly Leu Glu Glu Asn
115 120 125
His Lys Val Trp Met Ser His Gly Asp Ala Val Asp Lys Ala Pro Glu
130 135 140
Gly Phe Thr Val Thr Ala Ser Ser Ala Gly Ala Pro Val Ala Ala Met
145 150 155 160
Glu Cys Val Ala Lys Gln Met Ala Gly Val Gln Tyr His Pro Glu Val
165 170 175
Met His Ser Pro His Gly Gln Glu Val Leu Val Arg Phe Leu Thr Glu
180 185 190
Val Ala Gly Leu Glu Gln Thr Trp Thr Ser Ala Asn Ile Ala Gln Gln
195 200 205
Leu Ile Asp Asp Val Arg Ala Gln Ile Gly Pro Glu Gly Arg Ala Ile
210 215 220
Cys Gly Leu Ser Gly Gly Val Asp Ser Ala Val Ala Ala Ala Leu Val
225 230 235 240
Gln Arg Ala Ile Gly Asp Arg Leu Thr Cys Val Phe Val Asp His Gly
245 250 255
Leu Leu Arg Ala Gly Glu Arg Glu Gln Val Glu Lys Asp Phe Val Ala
260 265 270
Ser Thr Gly Ala Lys Leu Ile Thr Ala His Glu Ala Asp Ala Phe Leu
275 280 285
Ser Lys Leu Ala Gly Val Thr Asp Pro Glu Ala Lys Arg Lys Ala Ile
290 295 300
Gly Ala Glu Phe Ile Arg Ser Phe Glu Arg Ala Val Ala Gln Ala Leu
305 310 315 320
Glu Glu Ser Pro Glu Asp Ser Thr Val Asp Phe Leu Val Gln Gly Thr
325 330 335
Leu Tyr Pro Asp Val Val Glu Ser Gly Gly Gly Asp Gly Thr Ala Asn
340 345 350
Ile Lys Ser His His Asn Val Gly Gly Leu Pro Asp Asp Val Glu Phe
355 360 365
Glu Leu Val Glu Pro Leu Arg Leu Leu Phe Lys Asp Glu Val Arg Ala
370 375 380
Val Gly Arg Glu Leu Gly Leu Pro Glu Glu Ile Val Ala Arg Gln Pro
385 390 395 400
Phe Pro Gly Pro Gly Leu Gly Ile Arg Ile Ile Gly Glu Val Thr Glu
405 410 415
Glu Arg Leu Glu Ile Leu Arg Gln Ala Asp Leu Ile Ala Arg Thr Glu
420 425 430
Leu Thr Asn Ala Gly Leu Asp Gly Asp Ile Trp Gln Cys Pro Val Val
435 440 445
Leu Leu Ala Asp Val Arg Ser Val Gly Val Gln Gly Asp Gly Arg Thr
450 455 460
Tyr Gly His Pro Ile Val Leu Arg Pro Val Ser Ser Glu Asp Ala Met
465 470 475 480
Thr Ala Asp Trp Thr Arg Val Pro Tyr Asp Val Leu Glu Lys Ile Ser
485 490 495
Thr Arg Ile Thr Asn Glu Val Asn Asp Val Asn Arg Val Val Val Asp
500 505 510
Ile Thr Ser Lys Pro Pro Gly Thr Ile Glu Trp Glu
515 520
<210> 4
<211> 1575
<212> DNA
<213> Unknown
<220>
<223> Corynebacterium stationis
<400> 4
gtgactcaac ctgcaacaac tccgcgccca gtcctcgtgg tggatttcgg tgcccaatac 60
gcacagctga ttgctcgtcg cgtacgtgag gcatcgattt actccgaggt agtcccacat 120
tccgccaccg ttaaagagat taaagctaaa aaccctgcag ctttgatttt gtccggtggc 180
ccgtcctctg tttatgccga tggcgccccg caattaaagc ctgaactgct cgagcttggt 240
gtgccagtct ttggcatctg ctacggcttc caagccatga accatgcttt gggtggcaac 300
gttgcgcaaa ccggtgaccg tgaatacggc cgcaccgaaa tcacccatac cggtggtgtg 360
ctgcacgacg gcttagaaga aaaccacaag gtctggatgt cccacggtga tgctgtggat 420
aaggcacctg agggctttac cgtgaccgca tcgtcggctg gtgcgccggt tgcagcgatg 480
gaatgcgtgg ccaagcaaat ggctggtgtg caataccacc ccgaggttat gcattcccca 540
cacggacagg aagtactcgt tcgcttcctc accgaggtag cagggctaga gcagacctgg 600
acctcggcaa atattgcgca gcagcttatc gatgatgtcc gcgcgcaaat cggccctgaa 660
ggccgcgcta tttgtggcct gtcgggcggc gtggactccg cagtcgctgc agcgctcgtg 720
cagcgcgcca ttggcgaccg tttgacctgt gtgttcgtgg accacggtct gctgcgcgcc 780
ggtgagcgtg agcaggtaga aaaggacttc gtggcttcga ctggtgcgaa gctgattacc 840
gcgcatgaag ctgatgcttt cttgtctaag ctcgccggtg ttaccgatcc tgaggctaag 900
cgcaaggcta tcggcgcgga attcatccgt tcctttgagc gtgctgtggc acaggctttg 960
gaagaatctc ctgaagactc cacagtggac ttcctggtcc agggcacctt gtatccggat 1020
gtggttgaat ccggcggcgg tgacggcacc gcaaatatca agtcccacca caatgttggc 1080
ggcctgccag acgatgtcga attcgaactc gtcgagccac tacgcctgct gtttaaggac 1140
gaagtccgtg ccgtcggccg cgagctcggc ctgcctgagg aaatcgttgc ccgccagcca 1200
ttccctggcc ctggcctagg catccgcatc atcggtgaag tcaccgagga gcgtctagaa 1260
atcctgcgtc aagcagacct gattgcgcgt accgagctga ccaacgctgg cctcgacggt 1320
gatatctggc agtgcccagt cgtactgctt gccgatgtcc gctccgtcgg agtccaaggc 1380
gacggccgca cctacggcca cccaatcgtg ctgcgcccag tgtcatccga ggatgccatg 1440
accgccgact ggacccgcgt tccttacgac gtcctagaga aaatctccac ccgcattacc 1500
aacgaagtca acgacgtcaa ccgcgtggtc gtcgacatca cctccaagcc accgggaacc 1560
atcgagtggg agtaa 1575
<210> 5
<211> 18
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 5
gcgatgtgat tgccggtg 18
<210> 6
<211> 18
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 6
gctctaggaa gtcagcag 18
<210> 7
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 7
tgcccaatac gcacagctg 19
<210> 8
<211> 16
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 8
ggctggggct ttgtcc 16
<210> 9
<211> 18
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 9
ggcttagcaa gacctggc 18
<210> 10
<211> 37
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 10
gtgaattcga gctcggtacc cgcaccgcag ttagccc 37
<210> 11
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 11
taaatcgatg cctcacatac gcgacgagca atc 33
<210> 12
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 12
gattgctcgt cgcgtatgtg aggcatcgat tta 33
<210> 13
<211> 39
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 13
ggtcgactct agaggatccc ccgaggtcca ggtctgctc 39
<210> 14
<211> 17
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 14
ggaatccgaa gcggagc 17
<210> 15
<211> 18
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 15
caggccacaa atagcgcg 18
<210> 16
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 16
taaatcgatg cctcgcctac gcgacgagca atc 33
<210> 17
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 17
gattgctcgt cgcgtaggcg aggcatcgat tta 33
<210> 18
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 18
taaatcgatg cctcgaatac gcgacgagca atc 33
<210> 19
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 19
gattgctcgt cgcgtattcg aggcatcgat tta 33
<210> 20
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 20
taaatcgatg cctcggatac gcgacgagca atc 33
<210> 21
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 21
gattgctcgt cgcgtatccg aggcatcgat tta 33
<210> 22
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 22
taaatcgatg cctcgtatac gcgacgagca atc 33
<210> 23
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 23
gattgctcgt cgcgtatacg aggcatcgat tta 33
<210> 24
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 24
taaatcgatg cctcccatac gcgacgagca atc 33
<210> 25
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 25
gattgctcgt cgcgtatggg aggcatcgat tta 33
<210> 26
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 26
taaatcgatg cctcgattac gcgacgagca atc 33
<210> 27
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 27
gattgctcgt cgcgtaatcg aggcatcgat tta 33
<210> 28
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 28
taaatcgatg cctccactac gcgacgagca atc 33
<210> 29
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 29
gattgctcgt cgcgtagtgg aggcatcgat tta 33
<210> 30
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 30
taaatcgatg cctctggtac gcgacgagca atc 33
<210> 31
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 31
gattgctcgt cgcgtaccag aggcatcgat tta 33
<210> 32
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 32
taaatcgatg cctcggttac gcgacgagca atc 33
<210> 33
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 33
gattgctcgt cgcgtaaccg aggcatcgat tta 33
<210> 34
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 34
taaatcgatg cctctgctac gcgacgagca atc 33
<210> 35
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 35
gattgctcgt cgcgtagcag aggcatcgat tta 33
<210> 36
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 36
taaatcgatg cctcatctac gcgacgagca atc 33
<210> 37
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 37
gattgctcgt cgcgtagatg aggcatcgat tta 33
<210> 38
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 38
taaatcgatg cctcgtttac gcgacgagca atc 33
<210> 39
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 39
gattgctcgt cgcgtaaacg aggcatcgat tta 33
<210> 40
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 40
taaatcgatg cctcgtgtac gcgacgagca atc 33
<210> 41
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 41
gattgctcgt cgcgtacacg aggcatcgat tta 33
<210> 42
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 42
taaatcgatg cctccagtac gcgacgagca atc 33
<210> 43
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 43
gattgctcgt cgcgtactgg aggcatcgat tta 33
<210> 44
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 44
taaatcgatg cctccattac gcgacgagca atc 33
<210> 45
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 45
gattgctcgt cgcgtaatgg aggcatcgat tta 33
<210> 46
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 46
taaatcgatg cctcctgtac gcgacgagca atc 33
<210> 47
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 47
gattgctcgt cgcgtacagg aggcatcgat tta 33
<210> 48
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 48
taaatcgatg cctcctttac gcgacgagca atc 33
<210> 49
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 49
gattgctcgt cgcgtaaagg aggcatcgat tta 33
<210> 50
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 50
taaatcgatg cctcttctac gcgacgagca atc 33
<210> 51
<211> 33
<212> DNA
<213> Artificial Sequence
<220>
<223> праймер
<400> 51
gattgctcgt cgcgtagaag aggcatcgat tta 33
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Новая аденилосукцинат-синтетаза и способ получения нуклеотидов пурина с ее использованием | 2018 |
|
RU2770464C1 |
| Новый вариант аспартокиназы и способ получения L-аминокислоты с использованием этого варианта | 2018 |
|
RU2730025C1 |
| Новый вариант цитратсинтазы и способ получения L-аминокислот c его применением | 2022 |
|
RU2836733C1 |
| Новый вариант О-сукцинилгомосеринтрансферазы и способ получения О-сукцинилгомосерина с использованием этого варианта | 2018 |
|
RU2747493C1 |
| МУТИРОВАННЫЙ БЕЛОК SPOT И СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ С ЕГО ПРИМЕНЕНИЕМ | 2022 |
|
RU2837657C2 |
| НОВЫЙ ВАРИАНТ DAHP СИНТАЗЫ И СПОСОБ ПОЛУЧЕНИЯ L-ЛИЗИНА С ЕГО ПРИМЕНЕНИЕМ | 2021 |
|
RU2794484C1 |
| НОВЫЙ ВАРИАНТ МИКОТИОНРЕДУКТАЗЫ И СПОСОБ ПОЛУЧЕНИЯ L-ЛИЗИНА С ЕГО ПРИМЕНЕНИЕМ | 2021 |
|
RU2793438C1 |
| Новый вариант экспортирующей медь АТФазы А Р-типа и способ получения L-триптофана с его применением | 2021 |
|
RU2790565C1 |
| НОВЫЙ ВАРИАНТ ЦИТРАТСИНТАЗЫ II ТИПА И СПОСОБ ПОЛУЧЕНИЯ L-ЛИЗИНА С ЕГО ИСПОЛЬЗОВАНИЕМ | 2021 |
|
RU2793434C1 |
| Новый вариант гидролазы и способ получения L-триптофана | 2021 |
|
RU2793185C1 |
Изобретение относится к биотехнологии. Предложен полипептид, участвующий в получении пуринового нуклеотида, выбранного из группы XMP (ксантозинмонофосфат) или GMP (гуанозинмонофосфат), в котором аминокислота, соответствующая положению 29 в SEQ ID NO: 3, заменена другой аминокислотой, выбранной из глицина, аланина, валина, лейцина, изолейцина, метионина, фенилаланина, триптофана, пролина, серина, треонина, цистеина, тирозина, аспарагина, глутамина, аспарагиновой кислоты, глутаминовой кислоты, лизина и гистидина. Также предложены полинуклеотид, кодирующий указанный полипептид, микроорганизм для получения пуринового нуклеотида, выбранного из группы XMP или GMP, содержащий указанный полипептид или полинуклеотид, кодирующий указанный полипептид, способ получения пуринового нуклеотида, выбранного из группы XMP или GMP. Также предложены композиция для получения пуринового нуклеотида, выбранного из группы XMP или GMP, и способ увеличения способности микроорганизма к продуцированию XMP или GMP. Изобретение позволяет получить пуриновые нуклеотиды с высокой эффективностью. 6 н. и 2 з.п. ф-лы, 9 табл., 4 пр.
1. Полипептид, участвующий в получении пуринового нуклеотида, выбранного из группы XMP (ксантозинмонофосфат) или GMP (гуанозинмонофосфат), в котором аминокислота, соответствующая положению 29 в SEQ ID NO: 3, заменена другой аминокислотой, выбранной из глицина, аланина, валина, лейцина, изолейцина, метионина, фенилаланина, триптофана, пролина, серина, треонина, цистеина, тирозина, аспарагина, глутамина, аспарагиновой кислоты, глутаминовой кислоты, лизина и гистидина.
2. Полинуклеотид, кодирующий полипептид по п. 1.
3. Микроорганизм для получения пуринового нуклеотида, выбранного из группы XMP или GMP, содержащий полипептид, в котором аминокислота, соответствующая положению 29 в SEQ ID NO: 3, заменена другой аминокислотой, выбранной из глицина, аланина, валина, лейцина, изолейцина, метионина, фенилаланина, триптофана, пролина, серина, треонина, цистеина, тирозина, аспарагина, глутамина, аспарагиновой кислоты, глутаминовой кислоты, лизина и гистидина, или полинуклеотид, кодирующий указанный полипептид.
4. Микроорганизм по п. 3, где указанный микроорганизм представляет собой Corynebacterium stationis.
5. Способ получения пуринового нуклеотида, выбранного из группы XMP или GMP, включающий культивирование микроорганизма по п. 3 или 4.
6. Способ по п. 5, дополнительно включающий выделение XMP или GMP из культуральной среды или указанного микроорганизма.
7. Композиция для получения пуринового нуклеотида, выбранного из группы XMP или GMP, содержащая эксципиент, обычно используемый в композиции для получения пуринового нуклеотида, и по меньшей мере одно из следующего: полипептид, в котором аминокислота, соответствующая положению 29 в SEQ ID NO: 3, заменена другой аминокислотой, выбранной из глицина, аланина, валина, лейцина, изолейцина, метионина, фенилаланина, триптофана, пролина, серина, треонина, цистеина, тирозина, аспарагина, глутамина, аспарагиновой кислоты, глутаминовой кислоты, лизина и гистидина; и микроорганизм, содержащий указанный полипептид.
8. Способ увеличения способности микроорганизма к продуцированию XMP или GMP, включающий введение полипептида по п. 1 или полинуклеотида, кодирующего его, в указанный микроорганизм.
| NCBI Reference Sequence: WP_194285183.1, 16.11.2020 | |||
| Glutamine-hydrolyzing GMP synthase [Corynebacterium stationis] Найдено онлайн: https://www.ncbi.nlm.nih.gov/protein/WP_194285183.1/ Дата обращения 17.03.2023 | |||
| Микроорганизм рода Corynebacterium, продуцирующий ксантозин-5'-монофосфат, и способ получения ксантозин-5'-монофосфата c использованием этого микроорганизма | 2018 |
|
RU2720520C1 |
| US 20110033898 A1, 10.02.2011 | |||
| WO 2019147078 A1, 01.08.2019 | |||
| PEIFER S | |||
| ET AL | |||
| Metabolic engineering of the | |||
Авторы
Даты
2023-09-26—Публикация
2021-12-17—Подача