Технология синтеза новых производных нафтиридина, которые могут найти применение в медицине.
Изобретение относится к области получения новых замещенных бензонафтиридинов.
Предлагается способ получения производных нафтиридина общей формулы (1)
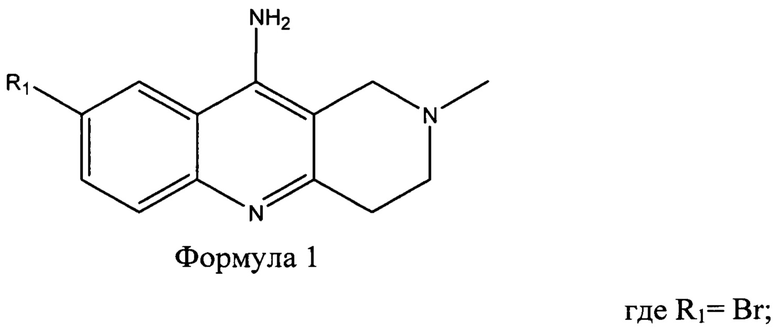
УРОВЕНЬ ТЕХНИКИ
Обнаружено, что соединение общей формулы 1, с заместителями в положении 8, где R1=галоген, а заместитель в положении 2 простой алкил, могут являться полезными модификатором антихолинэстеразного действия. Однако производство фармацевтических продуктов может столкнуться с непредвиденными затруднениями и необходимыми методиками получения. Нафтиридины общей формулы 1, согласно настоящему изобретению, подходят для применения в лекарственных средствах, в частности, в качестве агентов для лечения расстройств, вызванных процессами неверно направленной передачи клеточных сигналов у человека, млекопитающих и домашней птицы.
Сведениями об аналогах изобретения. Известны способы получения соединения 3b и 4b, где R1=Н. Из «GATTA F. et al., Synthesis of 10-Amino-1,2,3,4-tetrahydrobenzo[b][1,6]-naphthyridines and Related Derivatives, J. Heterocyclic Chem., 1996, v. 33» из простых компонентов, таких как изатин и 4-пиперидон с барботажем аммиака при температуре 150-160°С в течение часа. В издании говорится о способе получения 98 соединения 4b по средством реакции Гофмана, при этом автор отмечает о неприменимости данного способа. Также в издании раскрывается возможность получения соединений типа 3а и 4а, где R1=Cl; F; Из уровня техники известны методики по усовершенствованию молекулы такрина, а именно изменение заместителей и структуры в положении 10 и 2 «KALAI Т. et al., Synthesis and functional survey of new Tacrine analogs modified with nitroxides or their precursors, European Journal of Medicinal Chemistry, 2014, v. 77». «KHADEEVA V.A. et al., INVESTIGATION OF NAPHTHYRIDINES. VII. SYNTHESIS OF 10-ALKYLAMINO-1,2,3,4-TETRAHYDROBENZO[B]-1,6-NAPHTHYRIDINES, Chemistry of Heterocyclic Compounds, 1976, v. 12». В издании «GB 1186061 A (American Home Products Corparation), 16.02.1968» описывается получения соединения с замещенным атомом в положении 8, где R1=галоген. Известные способы получения соединений общей формулы 1 разработаны для структур с различными функциональными группами в разных положениях, что может не удовлетворять условиям получения структуры, где в качестве заместителей используется: Br, NH2, СН3.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Целью изобретения является разработка способа, на основе известных методов, получения новых производных 2,8-бензонафтиридинов, по реакции Пфитцингера и реакции Гофмана, с ценными фармакологическими свойствами на основе известных в литературе способов.
Важность и индивидуальность данного вещества в том, что ранее не удавалось получить аминогруппу в положении 10. Целевое вещество, полученное по схеме 1, близкое по структуре к Такрину и Ипидакрину, с высокой долей вероятности, может ингибировать ацетилхолинэстеразу. Изобретение иллюстрируется следующими данными.
Схема 1

Способ получения 8-бромо-2-метил-1,2,3,4-тетрагидробензо[b][1,6]-нафтиридин-10-иламин (соединение 4а, где [R1=Br]) включает способ получения амид 8-бромо-2-метил-1,2,3,4-тетрагидро-бензо[b]-1,6-нафтиридин-10-карбоновой кислоты (соединение 3а, где [R1=Br]), а также 5-бромизатина, для получения замещенных атомов.
ПОЛУЧЕНИЕ АМИД 8-БРОМО-2МЕТИЛ-1,2,3,4-ТЕТРАГИДРОБЕНЗО[В] [1,6] НАФТИРИДИНОВ-10-КАРБОНОВОЙ КИСЛОТЫ. (3а [R1=Br]);
18,5 г 5-бромизатина растворяли при нагреве в 200 мл этиленгликоля. После растворения барботировании реакционную массу аммиаком, при достижении температуры реакционной массы 70°С, добавляли 10,63 мл N-метилпиперидона, перемешивали 3 часа при температуре 115-120°С.
Далее в 925 мл дистиллированной воды, предварительно охлажденной, с высоким перемешивание, тонкой струйкой добавляли горячую реакционную массу. Оставляли перемешиваться около часа. Затем массу фильтровали под вакуумом.
Правели анализ субстанции методом ТСХ в сорбент DC Kieselgel 60 F254. Температура плавления полученного соединения составляет 192-193°С. Субстанция - кристаллический порошок, цвет от белого до серых оттенков.
ПОЛУЧЕНИЕ 8-БРОМО-2-МЕТИЛ-1,2,3,4-ТЕТРАГИДРОБЕНЗО [В] [1,6]-НАФТИРИДИН-10-ИЛАМИН. (4а [R1=Br]);
Пример 1
К метанолу 175 мл добавляли 8-бромо-1,2,3,4-тетрагидробензо[b][1,6]нафтиридин-10-карбоксиламида 9 г. (0,025 моль), доводили реакционную смесь до кипения. К раствору добавляли KF/Al2O3 (22 г. KF, 32,6 г Al2O3. 50% массы от 3а) и NaOCl (75 мл 10%-го водного раствора), смесь кипятили с обратным холодильником в течение 2 часов. После охлаждения реакционной смеси, до комнатной температуры, твердый осадок отфильтровали. Отфильтрованное вещество анализируем при помощи ТСХ, сорбент DC Kieselgel 60 F254.
Целевой продукт был выделен колоночной хроматографией. Получен 1 г, выход реакции 13%. Температура плавления полученного соединения составляет 236-238°С. Субстанция - кристаллический порошок, цвет от светло желтого до оранжевых оттенков.
Пример 2
К метанолу 350 мл добавляли 8-бромо-1,2,3,4-тетрагидробензо[b][1,6]нафтиридин-10-карбоксиламида 18 г. (0,05 моль), доводили реакционную смесь до кипения. К раствору добавляли KF/Al2O3 (44 г. KF, 65 г Al2O3. 40% массы от 3а) и NaOCl (150 мл 10%-го водного раствора), смесь кипятили с обратным холодильником в течение 2 суток. После охлаждения реакционной смеси, до комнатной температуры, твердый осадок отфильтровали. Отфильтрованное вещество анализируем при помощи ТСХ, сорбент DC Kieselgel 60 F254. Получено 7 г. вещества с чистотой 65% по ВЭЖХ, выход реакции 57%. Температура плавления полученного соединения составляет 236-238°С. Субстанция - кристаллический порошок, цвет от светло желтого до оранжевых оттенков.
ОЧИСТКА
В изопропиловом спирте 100 мл растворяли 23,27 грамма продукта, кипятили раствор 20 минут, охлаждали в холодильнике при 5°С, в течение 1 часа. Фильтровали и промывали осадок 30 мл ИПС. Получено 15 г.. продукта с чистотой 90% по ВЭЖХ, выход реакции 64%. Субстанция - кристаллический порошок, цвет от светло желтого до оранжевых оттенков.
ПОЛУЧЕНИЕ АМИД-2-МЕТИЛ-1,2,3,4-ТЕТРАГИДРО-БЕНЗО[В]-1,6-НАФТИРИДИНОВ-10 КАРБОНОВОЙ КИСЛОТЫ. (3b [R1=H]);
Этиленгликоль 1 л, барботировании NH3 в течение 15 мин. Вносили 100 г. изатина (0,68 моль), нагревали реакционную массу до 70°С. После добавления 87 мл (0,745 моль) 1-метил-4пиперидона, реакционную смесь перемешивали 3 часа при Т=115-120°С. Весь процесс происходил при непрерывной подаче NH3. Контроль прохождения реакции осуществлялся при помощи тонкослойной хроматографии. В мерный стакан объемом 4 л, помещали 3 л дистиллированной воды, предварительно охлажденной. Тонкой струйкой добавляли горячую реакционную массу в воду. Массу оставили перемешиваться около 3 часов, после поместили в холодильник на сутки при 3-5°С. Массу фильтруем под вакуумом. Провели анализ ТСХ, сорбент DCKieselgel 60 F254. Температура плавления полученного соединения составляет 218-219°С. Масса высушенного при 45°С под вакуумом, 54 г.. с чистотой 85% по ВЭЖХ, выход реакции 33%. Субстанция - кристаллический порошок, цвет от бежевого до белого.
ПОЛУЧЕНИЕ 2-МЕТИЛ-1,2,3,4-ТЕТРАГИДРОБЕНЗО [В] [1,6]-НАФТИРИДИН-10-ИЛАМИН. (4b [R1=Н]);
Пример 1
Метанол 500 мл и амид-2-метил-1,2,3,4-тетрагидро-бензо[b]-1,6-нафтиридинов-10 карбоновой кислоты (0,083 моль). Включали подогрев и доводим реакционную смесь до кипения. К раствору добавляем KF/Al2O3 (65,6 г. KF, 98 г Al2O3. 40% массы от 4b) и NaOCl (240 мл 4%-го водного раствора), смесь кипятили с обратным холодильником в течение 3 часов. После охлаждения реакционной смеси до комнатной температуры, твердый осадок отфильтровали. Правели анализ субстанции методом ТСХ, сорбент DCKieselgel 60 F254. Контроль прохождения реакции осуществлялся при помощи тонкослойной хроматографии. Масса полученного вещества 12 г. с чистотой 65%) по ВЭЖХ, выход реакции 72%). Т Температура плавления полученного соединения составляет 170-175°С; Субстанция - кристаллический порошок, цвет от белого до бежевого.
Пример 2
Метанол 200 мл и амид-2-метил-1,2,3,4-тетрагидро-бензо[b]-1,6-нафтиридинов-10 карбоновой кислоты (0,04 моль). Включали подогрев и доводим реакционную смесь до кипения. К раствору добавляем KF/Al2O3 (30,6 г. KF, 50 г Al2O3. 40% массы от 4b) и NaOCl (200 мл 10%-го водного раствора), смесь кипятили с обратным холодильником в течение суток. После охлаждения реакционной смеси до комнатной температуры, твердый осадок отфильтровали. Правели анализ субстанции методом ТСХ в качестве элюента хлороформ: метанол (20:1), сорбент DCKieselgel 60 F254. Контроль прохождения реакции осуществлялся при помощи тонкослойной хроматографии. Масса полученного вещества 5 г. с чистотой 70% по ВЭЖХ, выход реакции 62%. Температура плавления 170-175°С. Субстанция - кристаллический порошок, цвет от белого до бежевого.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВОЕ ТРИЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2009 |
|
RU2470934C1 |
| ТРИЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ СОЕДИНЕНИЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТАКОЕ СОЕДИНЕНИЕ | 2016 |
|
RU2715413C2 |
| ПРОИЗВОДНЫЕ ФТОРХИНОЛИН-3-КАРБОНОВОЙ КИСЛОТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2109014C1 |
| НИЗКОМОЛЕКУЛЯРНЫЕ ЛИГАНДЫ АСИАЛОГЛИКОПРОТЕИНОВОГО РЕЦЕПТОРА НА ОСНОВЕ ХИНОЛИН-4-КАРБОНОВОЙ КИСЛОТЫ | 2020 |
|
RU2769859C1 |
| ПРОИЗВОДНЫЕ ХИНОЛИНА ДЛЯ КОРРЕКЦИИ СИСТЕМЫ ГЕМОСТАЗА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СРЕДСТВО ДЛЯ КОРРЕКЦИИ ГЕМОСТАЗА | 2000 |
|
RU2177317C1 |
| НОВЫЕ КРИСТАЛЛИЧЕСКИЕ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ ТРИЦИКЛИЧЕСКОГО ПРОИЗВОДНОГО ИЛИ ИХ ГИДРАТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2572820C1 |
| ДИСПИРОИНДОЛИНОНЫ НА ОСНОВЕ РОДАНИНОВ КАК ИНГИБИТОРЫ Р53-MDM2 БЕЛОК-БЕЛКОВОГО ВЗАИМОДЕЙСТВИЯ | 2019 |
|
RU2730286C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗО(B)НАФТИРИДИНОВ И ПРОИЗВОДНЫЕ БЕНЗО(B)НАФТИРИДИНОВ | 1992 |
|
RU2105007C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ ГИДАНТОИНА В КАЧЕСТВЕ ИНГИБИТОРОВ МЕТАЛЛОПРОТЕИНАЗ | 2005 |
|
RU2378269C2 |
| ЗАМЕЩЕННЫЕ 1,2-ДИГИДРО[2,7]-НАФТИРИДИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2003 |
|
RU2243218C1 |
Изобретение относится к способу получения замещенных бензонафтиридинов общей формулы 1:

где R1=Br или Н. Способ включает взаимодействие 5-бромизатина или изатина с N-метилпиперидоном по реакции Пфитцингера в этиленгликоле при непрерывной подаче NH3 с получением амида формулы:
 ,
,
и проведение деструкции полученного амида по реакции Гофмана в присутствии катализатора KF/Al2O3, где содержание KF составляет 40 мас.% от массы катализатора, и 10%-ного водного раствора NaOCl в течение не менее суток. Техническим результатом изобретения является разработка способа получения производных 2,8-бензонафтиридинов, которые могут использоваться в лекарственных средствах, в частности, в качестве модификатора антихолинэстеразного действия. 4 пр.
Способ получения замещенных бензонафтиридинов общей формулы 1:

где R1=Br или Н, включающий взаимодействие 5-бромизатина или изатина с N-метилпиперидоном по реакции Пфитцингера в этиленгликоле при непрерывной подаче NH3 с получением амида формулы:
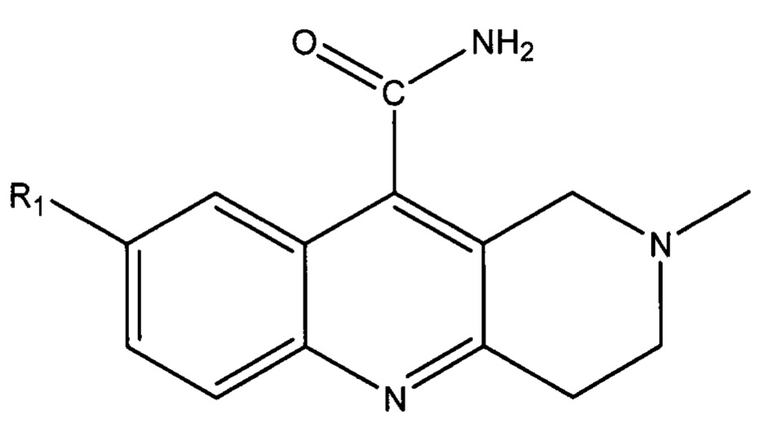 ,
,
и проведение деструкции полученного амида по реакции Гофмана в присутствии катализатора KF/Al2O3, где содержание KF составляет 40 мас.% от массы катализатора, и 10%-ного водного раствора NaOCl в течение не менее суток.
| GATTA F | |||
| et al., Synthesis of 10-Amino-1,2,3,4-tetrahydrobenzo[b][1,6]-naphthyridines and Related Derivatives, J | |||
| Heterocyclic Chem., 1996, v | |||
| Способ сопряжения брусьев в срубах | 1921 |
|
SU33A1 |
| KALAI T | |||
| et al., Synthesis and functional survey of new Tacrine analogs modified with nitroxides or their precursors, European Journal of Medicinal Chemistry, 2014, v | |||
| Спускная труба при плотине | 0 |
|
SU77A1 |
| GB | |||
Авторы
Даты
2023-10-09—Публикация
2022-02-19—Подача