Изобретение относится к медицине, а именно к хирургии и онкологии. Способ предназначен для использования в качестве вспомогательного инструмента в работе врача при планировании лечения в послеоперационном периоде для пациентов, перенесших гастрэктомию по поводу рака желудка со спленэктомией или с сохранением селезенки.
Рак желудка остается одним из самых распространенных злокачественных новообразований, наибольшее число пациентов с этой нозологией приходится трудоспособный возраст, что является значимой клинической и социальной проблемой.
Основным методом лечения резектабельных форм рака желудка является хирургический, объем операции зависит от стадии, морфологической структуры и распространенности опухолевого процесса.
Оценка вероятности послеоперационной летальности и развития осложнений наиболее важные задачи, способы решения которых должен оценить хирург-онколог при планировании лечения пациента с раком желудка.
Известен способ прогнозирования развития послеоперационных осложнений при панкреатодуоденальной резекции у больных раком органов биллиопанкреато дуоденальной зоны [пат.RU №2650984]. Авторы предлагают через сутки после операции на основании данных общего анализа крови с помощью компьютерной программы «Антистресс» оценивать в баллах характер и напряженности адапатационной реакций больного и при значениях этого показателя 18 баллов и ниже прогнозируют развитие послеоперационных осложнений.
Способ требует дополнительного обеспечения в виде специального программного обеспечения, что сводит возможность широкого использования способа в клинике к минимуму.
Известен способ прогнозирования развития острого послеоперационного панкреатита у онкологических больных [RU 2466399]. Способ позволяет выявить пациентов, предрасположенных к развитию острого послеоперационного панкреатита после гастрэктомии с показаниями к спленэктомии. Авторы предлагают за сутки до операции определять в плазме крови активность протеиназы узкой субстратной специфичности калликреина и содержание его предшественника прекалликреина. Рассчитывают коэффициент прекалликреин/калликреин. При величине от 1,02 до 1,2 прогнозируют развитие острого послеоперационного панкреатита в 1-8 сутки после операции; при величине более 1,2 прогнозируют течение послеоперационного периода без панкреатита.
Недостатки способа: требует выполнения иммуноферментного анализа, что не всегда возможно в условиях реальной клинической ситуации.
Известен способ прогнозирования послеоперационных осложнений после радикальных операций у больных раком желудка [пат. RU №2706696]. В крови больных раком желудка на первые сутки после операции определяют иммунологические показатели CD3, CD4, CD8 и HLA-DRpr, описывают показатели люминол-зависимой и люцигенин-зависимой хемилюминесценции, индуцированной зимозаном и St. epidermidis: I max (sp) с люм + зим, I max (sp) с люц + зим, Т max (in) с люм + st, I max (in) с люм + st, ИА с люм + st, определяют иммунорегуляторный индекс (ИРИ), проводят статистический анализ и выводят линейные дискриминантные функции, для отсутствия (D1) и для развития (D2) послеоперационных осложнений. При D1>D2 делают вывод о низком, а при D1<D2 - о высоком риске развития послеоперационных осложнений.
Способ трудоемок, требует участия специалистов лаборатории иммунологического анализа, дорогостоящих реактивов и сложных вычислений.
Известен способ прогнозирования развития острого послеоперационного панкреатита (ОПП) [пат. RU №2722672].
Авторы выявляют у пациента факторы риска на дооперационном и раннем послеоперационном этапе, а именно оценивают в баллах вид оперативного вмешательства, объем выполненной лимфодиссекции, наличие фонового хронического панкреатита, пенетрация язвы и врастание опухоли в поджелудочную железу, язвенный анамнез, дуоденостаз и показатели D-димера в 1-е сутки после операции. Баллы суммируют, сумма до трех баллов прогнозирует низкий риск развития ОПП, при сумме балов 4-6 - средний риск развития ОПП, свыше 6 баллов - высокий риск развития ОПП. Способ позволяет добиться выраженного профилактического эффекта, что позволяет проводить раннюю профилактику и улучшение показателей выживаемости оперированных больных, а также значительно улучшает качество жизни данной категории пациентов за счет оценки комплекса наиболее значимых факторов риска.
Авторы используют результаты стандартных обследований, что является положительным моментом, однако для более точного прогнозирования вероятности развития осложнений, а так же для оценки возможности развития иных, кроме панкреатита, осложнений, необходим арсенал разнообразных методик.
Технический результат - возможность оценки развития послеоперационных осложнений в кратчайшие сроки после завершения операции; индивидуальное, для каждого пациента в зависимости от анамнестических данных и особенностей выполнения оперативного вмешательства, планирование послеоперационного ведения; предупреждение развития тяжелых форм течения послеоперационных осложнений. Грамотно выстроенное послеоперационное лечение способствует сокращению летальности пациентов, перенесших гастрэктомию по поводу рака желудка.
Способ основан на результатах наблюдения ста тридцати пациентов, перенесших гастрэктомию по поводу рака желудка, со спленэктомией или с сохранением селезенки.
Всем пациентам проводили дооперационное обследование в соответствии с рекомендациями «Клинические рекомендации. Рак желудка» [разработаны общероссийским национальным союзом «Ассоциация онкологов России» и общероссийской общественной организацией «Российское общество клинической онкологии», 2020, найдено в интернет https://oncology-association.ru/wp-content/uploads/2020/09rak_zheludka.pdf]
В течение месяца наблюдали за течением послеоперационного периода. У четырех пациентов отмечено развитие кровотечения (один человек), реактивного панкреатита (два человека), перитонита (один человек).
Используя представленные выше данные пациентов строили регрессионное уравнение, где в качестве зависимой, то есть прогнозируемой переменной выступало наличие ранних послеоперационных осложнений (табл. 1).
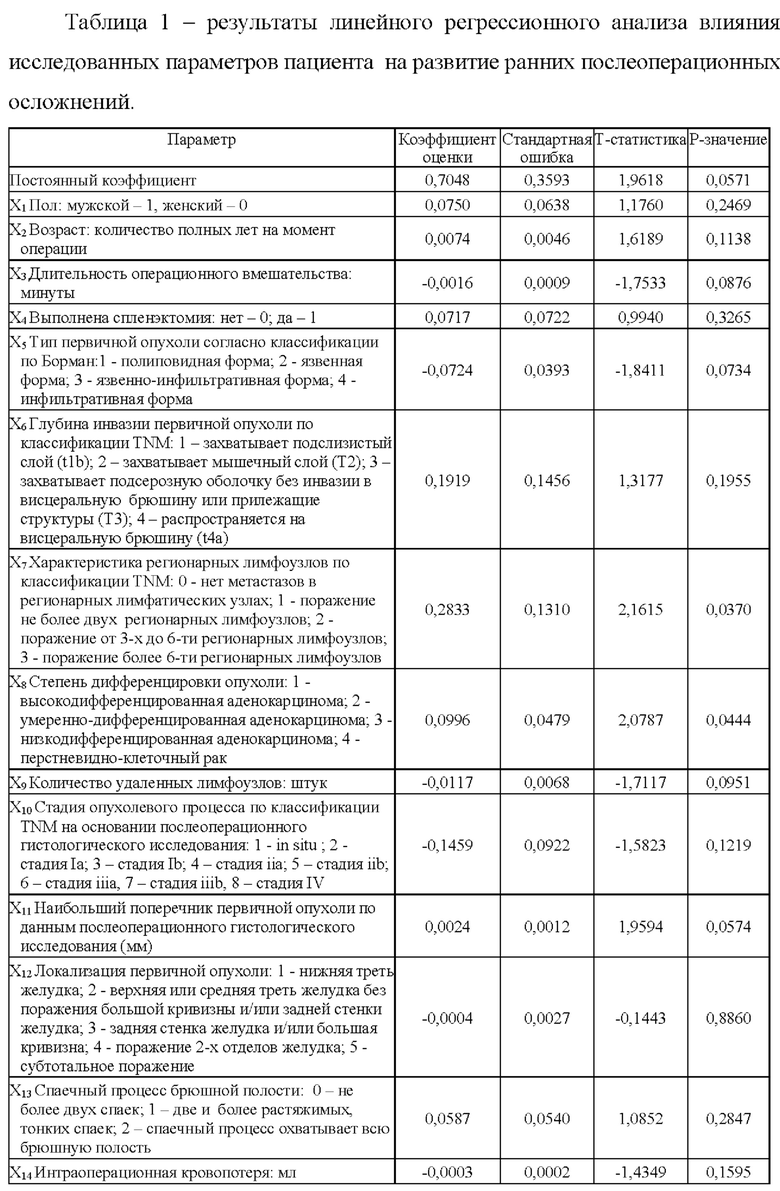
Уравнение, позволяющее прогнозировать развитие ранних послеоперационных осложнений следующее:
Кпрогноз = 0,7048 + x1*0,075 + х2*0,0074 - х3*0,0016 + х4*0,0717 - х5*0,0724 + х6*0,1919 + х7*0,2833 + х8*0,0996 - х9*0,0117 - х10*0,1459 + х11*0,0024 - x12*0,0004 + x13*0,0587 - х14*0,0003
Далее по обучающей выборке рассчитывали средние значения коэффициентов прогнозирования в группе пациентов, не имевших ранних послеоперационных осложнений и в группе пациентов, у которых такие осложнения развивались в течение месяца после операции (табл. 2).
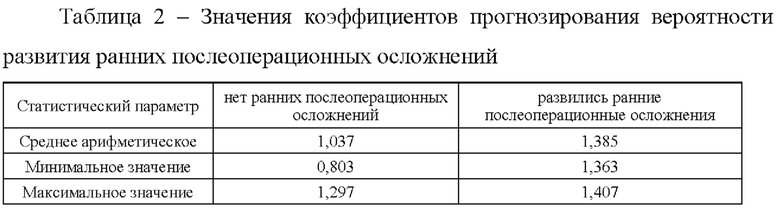
Из данных таблицы следует, что пересекающихся диапазонов значений коэффициентов прогнозирования в группе пациентов не имевших послеоперационных осложнений и в группе с резвившимися осложнениями нет.
Таким образом, можно сформулировать общее правило: если коэффициент прогнозирования вероятности развития ранних послеоперационных осложнений, рассчитанный по предлагаемой формуле не превышает 1,297, то осложнения не разовьются. Если величина коэффициента составляет 1,297 и более, то вероятно развитие ранних послеоперационных осложнений.
Правило, полученное на обучающей выборке, было проверено на клинических примерах. Прогнозируемый и реально наблюдаемый результаты совпали.
Клинический пример. Пациентка П., (x1=0), 64 лет (х2=64). Диагноз по МКБ-10: С16 Злокачественное новообразование желудка. Высоко дифференцированная аденокарцинома с прорастанием в подслизистый слой. Реактивная гиперплазия регионарных лимфоузлов. Хронический холецистит.
Выполнена расширенно-комбинированная дистальная субтотальная резекция желудка, селезенка сохранена (х4=0).
По результатам оперативного лечения установлено: длительность операции 90 минут (х3=90). Тип первичной опухоли согласно классификации по Борман: полиповидная форма (x5=1); первичная опухоль захватывает подслизистый слой (х6=1). Метастазов в регионарных лимфатических узлах нет (х7=0), высоко дифференцированная аденокарцинома (х8=1). Удалено шесть лимфоузлов (х9=6). Стадия опухолевого процесса по классификации TNM на основании послеоперационного гистологического исследования Ia (х10=2). Наибольший поперечник первичной опухоли по данным послеоперационного гистологического исследования 16 мм (х11=16).
Локализация первичной опухоли в верхней трети желудка, большая кривизна и задняя стенки желудка не поражены (x12=2). Спаечный процесс брюшной полости не распространенный, две растяжимые, тонкие спайки (x13=0). Объем интраоперационной кровопотери 150 мл (x14=150).
Коэффициент прогнозирования вероятности развития ранних послеоперационных осложнений, рассчитанный по предложенной формуле:
Кпрогноз=0,7048 +х1*0,075 + х2*0,0074 - х3*0,0016 + х4*0,0717 - х5*0,0724 + х6*0,1919 + х7*0,2833 + х8*0,0996 - х9*0,0117 - х10*0,1459 + х11*0,0024 - x12*0,0004 + x13*0,0587 - x14*0,0003
Кпрогноз=0,7048+0*0,075+64*0,0074-90*0,0016+0*0,0717 - 1*0,0724 + 1*0,1919 + 0*0,2833 + 1*0,0996 - 6*0,0117 - 2*0,1459 + 16*0,0024 - 2*0,0004 + 0*0,0587 - 150*0,0003 = 0,8841
Согласно величине коэффициента прогнозирования ранние послеоперационные осложнения не разовьются.
По результатам динамического наблюдения послеоперационный период протекал спокойно, жалоб на ухудшение самочувствия пациентка не предъявляла.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования послеоперационных осложнений у больной, перенесшей хирургическое лечение рака молочной железы | 2017 |
|
RU2683692C1 |
| Способ прогнозирования риска развития лимфогенных осложнений после радикальной простатэктомии с тазовой лимфаденэктомией | 2021 |
|
RU2752949C1 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ РИСКА НЕБЛАГОПРИЯТНОГО ИСХОДА ЗАБОЛЕВАНИЯ У БОЛЬНЫХ РАКОМ ЖЕЛУДКА | 2016 |
|
RU2662085C1 |
| СПОСОБ ДИАГНОСТИКИ РАКА У БОЛЬНЫХ С ДООПЕРАЦИОННЫМ ЦИТОЛОГИЧЕСКИМ ДИАГНОЗОМ "ФОЛЛИКУЛЯРНАЯ ОПУХОЛЬ" ЩИТОВИДНОЙ ЖЕЛЕЗЫ С ПОМОЩЬЮ МАТЕМАТИЧЕСКОГО МОДЕЛИРОВАНИЯ | 2011 |
|
RU2493770C2 |
| Способ оценки риска неблагоприятного исхода острого инфаркта миокарда у больных сахарным диабетом 2 типа | 2021 |
|
RU2790520C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПОСЛЕОПЕРАЦИОННЫХ КАРДИАЛЬНЫХ ИШЕМИЧЕСКИХ ОСЛОЖНЕНИЙ У БОЛЬНОГО РАКОМ ЛЕГКОГО | 2022 |
|
RU2798781C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ОСЛОЖНЕНИЙ МОНОПОЛЯРНОЙ ТРАНСУРЕТРАЛЬНОЙ ЭНУКЛЕАЦИИ ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2018 |
|
RU2698623C1 |
| Способ прогнозирования ранней несостоятельности колоректального анастомоза. | 2022 |
|
RU2807932C1 |
| Способ прогнозирования риска развития отдаленных метастазов у больных операбельными формами рака молочной железы с метастазами в регионарные лимфоузлы | 2020 |
|
RU2733697C1 |
| Способ прогнозирования послеоперационных осложнений после радикальных операций у больных раком желудка | 2019 |
|
RU2706696C1 |
Изобретение относится к медицине, а именно к хирургии и онкологии, и может быть использовано для прогнозирования развития ранних послеоперационных осложнений у пациентов, перенесших гастрэктомию по поводу рака желудка. Проводят оценку анамнестических и интраоперационных параметров. Коэффициент прогнозирования рассчитывают по формуле: Кпрогноз=0,7048+Х1*0,075+Х2*0,0074–Х3*0,0016+Х4*0,0717–Х5*0,0724+Х6*0,1919+Х7* 0,2833+Х8*0,0996–Х9*0,0117-Х10*0,1459+Х11*0,0024-Х12*0,0004+Х13*0,0587-Х14*0,0003, где Х1 пол, обозначенный мужской – 1, женский – 0; Х2 - возраст в количестве полных лет на момент операции; Х3 - длительность операционного вмешательства в минутах; Х4 - спленэктомия, не выполнялась – 0, выполнена – 1; Х5 - тип первичной опухоли согласно классификации по Борман, 1 - полиповидная форма, 2 - язвенная форма, 3 - язвенно-инфильтративная форма, 4 - инфильтративная форма; Х6 - глубина инвазии первичной опухоли по классификации TNM: 1 – захватывает подслизистый слой; 2 – захватывает мышечный слой; 3 – захватывает подсерозную оболочку без инвазии в висцеральную брюшину или прилежащие структуры; 4 – распространяется на висцеральную брюшину; Х7- характеристика регионарных лимфоузлов по классификации TNM: 0 - нет метастазов в регионарных лимфатических узлах, 1 - поражение не более двух регионарных лимфоузлов, 2 - поражение от 3-х до 6-ти регионарных лимфоузлов, 3 - поражение более 6-ти регионарных лимфоузлов; Х8 - степень дифференцировки опухоли: 1 - высокодифференцированная аденокарцинома, 2 - умереннодифференцированная аденокарцинома, 3 – низкодифференцированная аденокарцинома, 4 - перстневидно-клеточный рак; Х9 - количество удаленных лимфоузлов; Х10- стадия опухолевого процесса по классификации TNM: 1 - in situ, 2 - стадия Ia, 3 – стадия Ib, 4 – стадия IIa, 5 – стадия IIb, 6 – стадия IIIa, 7 – стадия IIIb, 8 – стадия IV; Х11 - наибольший поперечник первичной опухоли по данным послеоперационного гистологического исследования (мм); Х12 - локализация первичной опухоли: 1 - нижняя треть желудка, 2 - верхняя или средняя треть желудка без поражения большой кривизны и/или задней стенки желудка, 3 - задняя стенка желудка и/или большая кривизна, 4 - поражение 2-х отделов желудка, 5 - субтотальное поражение; Х13 - спаечный процесс брюшной полости: 0 – не более двух спаек, 1 – две и более растяжимых тонких спаек, 2 – спаечный процесс охватывает всю брюшную полость; Х14 - интраоперационная кровопотеря в мл. Если коэффициент прогнозирования развития ранних послеоперационных осложнений не превышает 1,297, прогнозируют отсутствие послеоперационных осложнений; если величина коэффициента составляет более 1,297, то прогнозируют развитие ранних послеоперационных осложнений. Способ обеспечивает возможность оценить вероятность развития послеоперационных осложнений в кратчайшие сроки после завершения операции, индивидуально, для каждого пациента за счет анализа анамнестических данных и особенностей выполнения оперативного вмешательства. 2 табл., 1 пр.
Способ прогнозирования развития ранних послеоперационных осложнений у пациентов, перенесших гастрэктомию по поводу рака желудка, включающий оценку анамнестические и интраоперационных параметров, отличающийся тем, что коэффициент прогнозирования рассчитывают по формуле: Кпрогноз=0,7048+Х1*0,075+Х2*0,0074–Х3*0,0016+Х4*0,0717–Х5*0,0724+Х6*0,1919+Х7*0,2833+Х8*0,0996–Х9*0,0117-Х10*0,1459+Х11*0,0024–Х12*0,0004+Х13*0,0587–Х14*0,0003, где Х1 пол, обозначенный мужской – 1, женский – 0; Х2 возраст в количестве полных лет на момент операции; Х3 длительность операционного вмешательства в минутах; Х4 спленэктомия не выполнялась – 0, выполнена – 1; Х5 тип первичной опухоли согласно классификации по Борман 1 - полиповидная форма, 2 - язвенная форма, 3 - язвенно-инфильтративная форма, 4 - инфильтративная форма; Х6 глубина инвазии первичной опухоли по классификации TNM: 1 – захватывает подслизистый слой; 2 – захватывает мышечный слой; 3 – захватывает подсерозную оболочку без инвазии в висцеральную брюшину или прилежащие структуры; 4 – распространяется на висцеральную брюшину; Х7 характеристика регионарных лимфоузлов по классификации TNM: 0 - нет метастазов в регионарных лимфатических узлах, 1 - поражение не более двух регионарных лимфоузлов, 2 - поражение от 3-х до 6-ти регионарных лимфоузлов, 3 - поражение более 6-ти регионарных лимфоузлов; Х8 степень дифференцировки опухоли: 1 - высокодифференцированная аденокарцинома, 2 - умереннодифференцированная аденокарцинома, 3 - низкодифференцированная аденокарцинома, 4 - перстневидно-клеточный рак; Х9 количество удаленных лимфоузлов; Х10 стадия опухолевого процесса по классификации TNM: 1 - in situ, 2 - стадия Ia, 3 – стадия Ib, 4 – стадия IIa, 5 – стадия IIb, 6 – стадия IIIa, 7 – стадия IIIb, 8 – стадия IV; Х11 наибольший поперечник первичной опухоли по данным послеоперационного гистологического исследования (мм); Х12 локализация первичной опухоли: 1 - нижняя треть желудка, 2 - верхняя или средняя треть желудка без поражения большой кривизны и/или задней стенки желудка, 3 - задняя стенка желудка и/или большая кривизна, 4 - поражение 2-х отделов желудка, 5 - субтотальное поражение; Х13 спаечный процесс брюшной полости: 0 – не более двух спаек, 1 – две и более растяжимых, тонких спаек, 2 – спаечный процесс охватывает всю брюшную полость; Х14 интраоперационная кровопотеря в мл; если коэффициент прогнозирования развития ранних послеоперационных осложнений не превышает 1,297, прогнозируют отсутствие послеоперационных осложнений; если величина коэффициента составляет более 1,297, то прогнозируют развитие ранних послеоперационных осложнений.
| Способ прогнозирования развития острого послеоперационного панкреатита | 2019 |
|
RU2722672C1 |
| Способ прогнозирования послеоперационных осложнений после радикальных операций у больных раком желудка | 2019 |
|
RU2706696C1 |
| Звуковая коробка для граммофона | 1929 |
|
SU22948A1 |
| Рогозянская М.И | |||
| и др | |||
| Сравнительный анализ и пути улучшения ближайших и отдаленных результатов хирургического лечения рака желудка | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| Ke L, Tong ZH, Li WQ, Wu C, Li N, Windsor JA, Li JS, Petrov MS | |||
Авторы
Даты
2023-10-09—Публикация
2023-02-13—Подача