Изобретение относится к медицине и может быть использовано для эндоскопической биопсии периферических образований легких.
Диагностика периферических образования легких является крайне важной клинической проблемой. Так, еще в 2015 году общее число ежегодного выявляемых периферических образований по данным компьютерной томографии органов грудной клетки в США превышало 1,6 млн человек [1]. По данным ряда исследований, частота выявления периферических образований колеблется от 8 до 51% популяции, в зависимости от критериев скрининга и оценки [2].
Подавляющее большинство пациентов с выявленными периферическими образованиями не нуждаются в дальнейшем обследовании и верификации, однако, от 5 до 10% выявленных образований нуждаются в выполнении различных модальностей биопсий.
Долгое время «золотым стандартном» верификации периферических образований легких считалась трансторакальная биопсия легкого под контролем КТ (TTNA), обеспечивающая верификацию диагноза у более, чем 90% пациентов [3]. Вместе с тем, существенная частота осложнений в виде пневмотораксов и кровотечений, достигающая зачастую 20-25% [4], а также невозможность адекватно верифицировать образования, расположенные в средней и внутренней трети легкого, не позволяют применить этот метод во всех случаях диагностики.
Альтернативой TTNA в настоящее время является диагностическая навигационная бронхоскопия, когда биопсия «цели» в легочной ткани осуществляется под контролем средств навигации - рентгеноскопии [5], компьютерной томографии [6], радиального эндобронхиального ультразвука [7], виртуальной бронхоскопии [8].
Эффективность навигационной бронхоскопии при периферических образованиях легких колеблется в пределах 55-78% [9].
В последнее десятилетие получают все большее распространение роботические бронхоскопические системы, которые позволяют обеспечить доступ эндоскопа в наиболее мелкие ветвления бронхиального дерева (7-9 генерации), тем самым, приближаясь к зоне патологических изменений в паренхиме легкого [10].
Эффективность верификации периферических образований легких превышает 85-90%, однако распространение методики ограничено высокой стоимостью как самой системы, так и расходного инструментария.
Известен способ диагностической биопсии [RU 2324431, C1, А61В 17/00, 20.05.2008], характеризующийся тем, что по данным предварительно проведенных исследований на коже пациента отмечают точку в проекции выявленных наиболее выраженных изменений париетальной плевры, под местной анестезией через намеченную точку по ходу межреберья выполняют разрез кожи и подкожной жировой клетчатки длиной 2,5-3,0 см, подлежащие мышцы расслаивают по ходу волокон до межреберья и разводят в стороны, межреберные мышцы рассекают на протяжении 2,5-3,0 см до подплевральной фасции по верхнему краю нижележащего ребра, расширяют межреберный промежуток путем введения в углы раны двух крючков Фарабефа, которые разворачивают на 90° в виде распорок, после чего через образованную апертуру раны вдоль верхнего и нижнего ребер рассекают плевральную шварту до висцеральной плевры, соединяя горизонтальные разрезы вертикальными, зажимом берут иссеченный фрагмент за угол и, оттягивая его от легкого, проводят препаровку плевральной шварты от висцеральной плевры на протяжении 4-5 мм, после чего в проекции намеченной точки под визуальным контролем выполняют биопсию, иссекая одним блоком участок ткани, включающий париетальную и висцеральную плевру, затем рану послойно ушивают.
Недостатком этого технического решения является относительно узкая область применения, которая относится к диагностической биопсии плевры.
Наиболее близким по технической сущности к предложенному является способ [RU 2744532, C1, А61В 6/12, 10.03.2021], характеризующийся тем, что проводят компьютерную томографию легких (КТ) и ультразвуковое исследование легких (УЗИ) с последующим совмещением в режиме реального времени полученных изображений КТ и поперечного среза легких, полученного при проведении УЗИ, при этом, в качестве костных «ориентиров» при совмещении используют при локализации опухолевого узла в передних отделах легкого - грудинно-реберное или грудинно-ключичное сочленение, при локализации опухолевого узла в задних отделах легкого - гребень и/или углы лопатки, после достижения совмещения КТ и УЗ изображений при помощи игл для трепан-биопсии выполняют прицельную пункционную Fusion-биопсию выявленного новообразования с забором ткани для исследований.
Недостатком наиболее близкого технического решения является относительно низкая эффективность диагностической биопсии периферических образований легких, в частности, в области периферического образования мелких ветвлений бронхиального дерева.
Задачей изобретения является разработка способа диагностической эндоскопической биопсии периферических образований легких, обладающего более высокой эффективностью диагностической биопсии периферических образований легких, в частности, в области периферического образования мелких ветвлений бронхиального дерева.
Требуемый технический результат заключается в повышении эффективности диагностической биопсии периферических образований легких, в частности, в области периферического образования мелких ветвлений бронхиального дерева.
Поставленная задача решается, а требуемый технический результат достигается тем, что в способе, характеризующемся тем, что пациенту на предварительном этапе проводится компьютерная томография органов грудной клетки (КТ) и на основании полученных изображений КТ и их постпроцессинговой обработки выполняют прицельную биопсию периферических образования с забором ткани для исследований, согласно изобретению, на основании данных КТ используют холангиоскоп с дополнительным каналом для подачи физиологического раствора, подогретого до температуры 37°С, и биопсийным инструментарием, который проводится через трахею, один из главных бронхов до уровня мелких ветвлений бронхиального дерева в области наличия периферического образования, далее под визуальным контролем выполняют биопсию.
Кроме того, требуемый технический результат достигается, что, в качестве биопсийного инструментария используют гибкие щипцы.
Кроме того, требуемый технический результат достигается, что используют гибкие щипцы с диаметром 1.2 мм.
Кроме того, требуемый технический результат достигается, что в качестве биопсийного инструментария используют одноразовый криозонд.
Кроме того, требуемый технический результат достигается, что используют одноразовый криозонд с диаметром 1,1 мм.
На чертеже представлены:
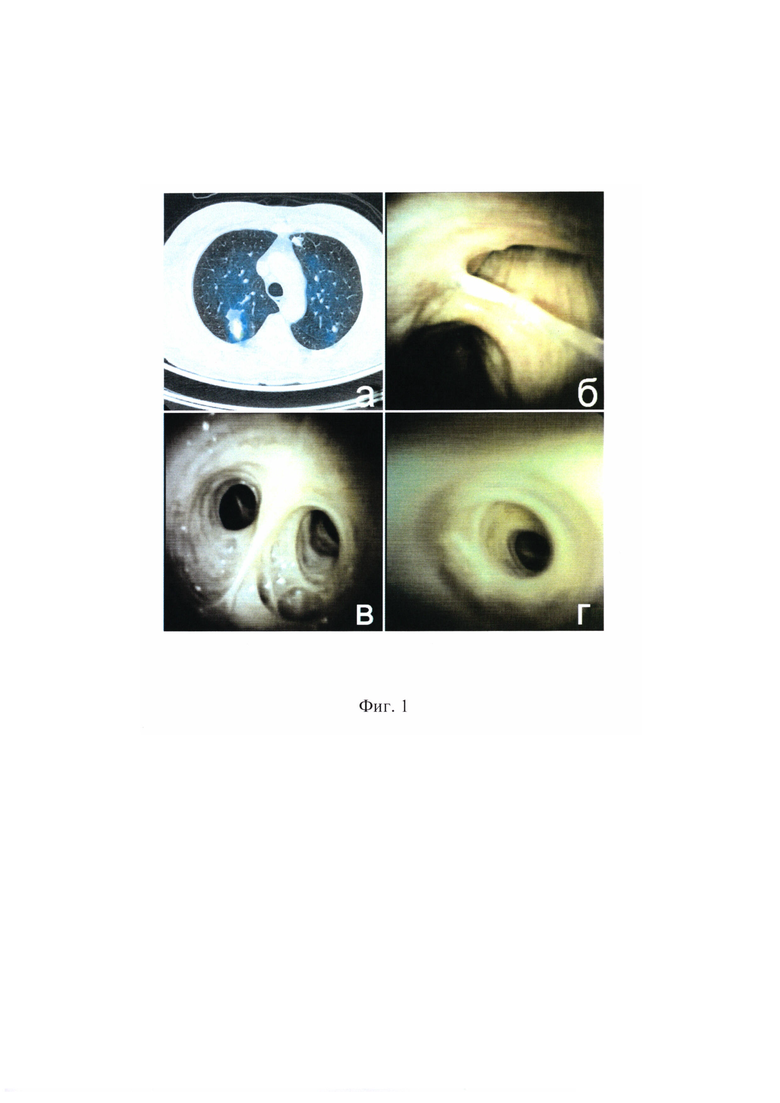
на фиг. 1 - образование в верхней доле правого легкого легкого;
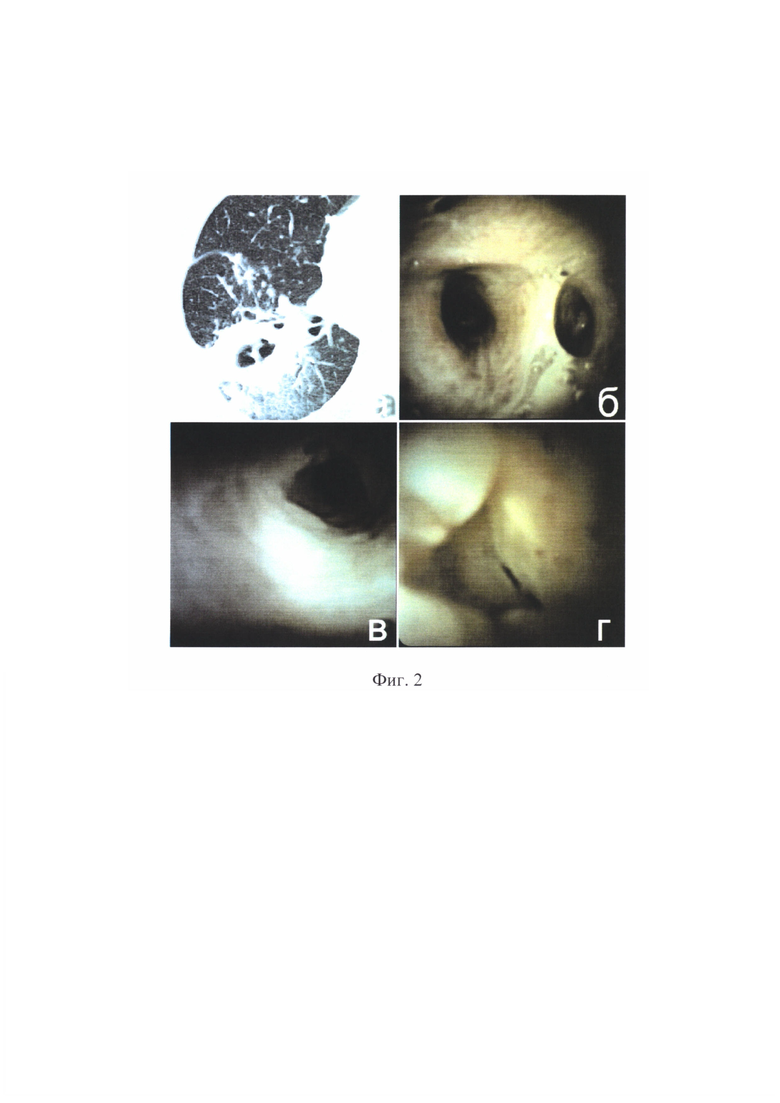
на фиг. 2 - полостное образование в нижней доле правого легкого на фоне тракционных бронхоэктазов и выраженных ретикулярных изменений;
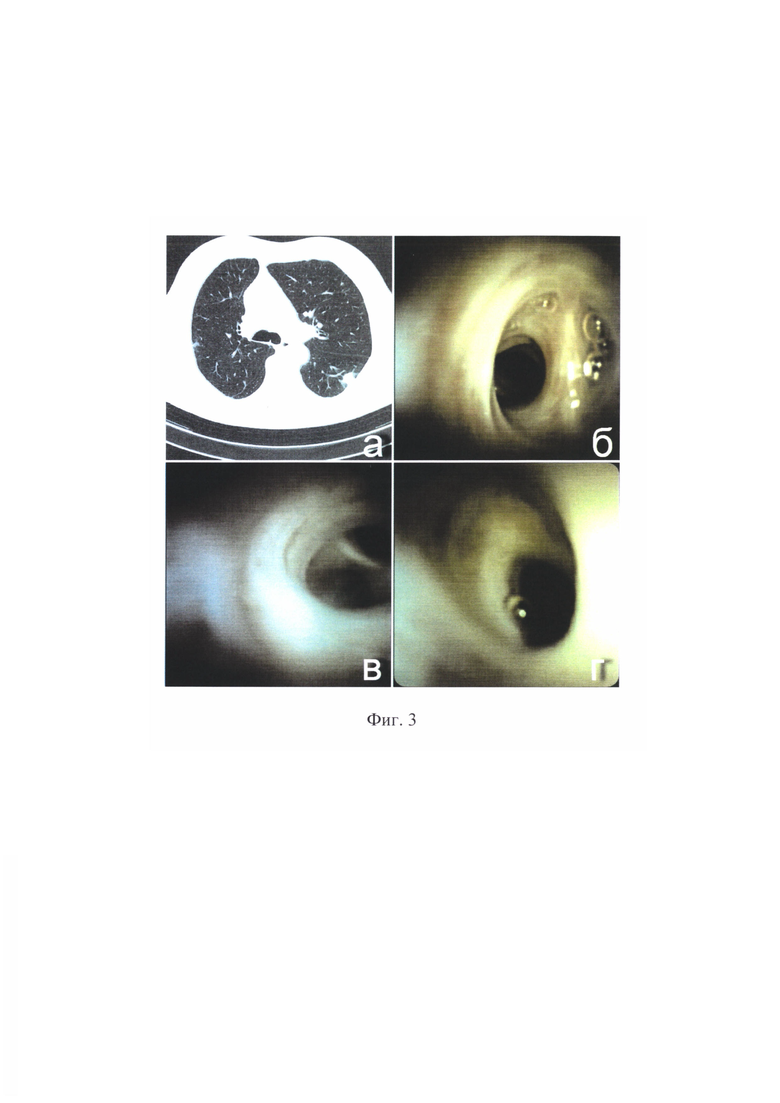
на фиг. 3 - образования в нижней доле левого легкого.
Предложенное изобретение используется следующим образом.
Задачей изобретения является создание способа навигационной бронхоскопии с возможностью выполнения прецизионной биопсии периферических образований легких.
Для этого в рамках поднаркозной ригидной бронхоскопии жесткими бронхоскопами выполняется навигационная бронхоскопия с помощью, например, гибкого цифрового тонкого холангиоскопа для визуализации печеночных/панкреатических протоков, выполнения биопсии, а также реканализации просвета желчных путей от конкрементов.
Навигация гибкого цифрового холангиоскопа проводится по данным КТ органов грудной клетки, управление гибким холангиоскопом осуществляется с помощью двух винтов управления, с возможностью фиксации последних в определенном положении, что является преимуществом перед любыми иными эндоскопическими методиками навигационной бронхоскопии. За счет возможности управления дистальным концом холангиоскопа в двух плоскостях вместо одной при использовании гибкого бронхоскопа, достигается четкое позиционирование как эндоскопа, так и биопсийного инструментария, становятся доступными самые мелкие ветвления периферических бронхов. В момент выполнения биопсии гибкий холангиоскоп позволяет постоянно контролировать чистоту эндоскопического изображения за счет возможности подачи теплого физиологического раствора даже в момент биопсии, тем самым обеспечивая «смывание» примеси крови, сгустков и отделяемого бронхиального дерева, обеспечивая тем самым возможность выполнения прецизионной биопсии в режиме реального времени. Такая возможность при выполнении как роботической бронхоскопии, так и навигационной бронхоскопии с помощью тонкого бронхоскопа отсутствует, в связи с отсутствием в иных эндоскопах отдельного канала для подачи жидкости.
Подача подогретого до 37°С физиологического раствора через специальный канал омывания гибкого цифрового холедохоскопа преследует три цели:
а) раскрытие просвета спавшихся дистальных мелких бронхов, что позволяет осуществлять их визуализацию и поэтапное продвижение холедохоскопа на периферию бронхиального дерева;
б) за счет температуры в 37°С осуществляется профилактика бронхоспазма, который может развиться при введении жидкости более низкой температуры, тем самым также поддерживается постоянный просвет бронхиального ветвления;
в) при выполнении биопсий за счет вводимой жидкости происходит постоянное омывание линзы гибкого холедохоскопа, сохраняя визуальный контроль за областью биопсии, причем, для этого нет необходимости задействовать рабочий канал холедохоскопа и тем самым устраняется нужда в извлечении инструментария и сокращается время, потребное на выполнение биопсии, равно как и снижается техническая сложность выполнения последней.
На основании данных компьютерной томографии и рентгеноскопического контроля холангиоскоп проводится через трахею, один из главных бронхов до уровня мелких ветвлений бронхиального дерева (6-9 генерация) в области наличия периферического образования. Далее под визуальным/рентгеноскопическим контролем выполняется биопсия с помощью гибких щипцов диаметром 1.2 мм, либо тонкого одноразового криозонда диаметром 1,1 мм.
Заявленный способ позволяет повысить эффективность диагностики периферических образований легких в сравнении с классической бронхобиопсией с помощью стандартных гибких фибро- и видеобронхоскопов.
Такие параметры цифрового холангиоскопа позволяют проводить его в самые тонкие, отдаленные ветвления бронхиального дерева. По своим характеристикам цифровой холангиоскоп при применении его в бронхиальном дереве близок к дорогостоящим системам роботической бронхоскопии, но имеет ряд преимуществ - так, доступен постоянный эндоскопический контроль, имеется дополнительный канал для подачи жидкостей без необходимости удаления инструмента из рабочего канала, доступен разнообразный биопсийный инструментарий.
На основании данных компьютерной томографии, виртуальной бронхоскопии, а, при необходимости, и рентгеноскопического контроля холангиоскоп проводится через трахею, один из главных бронхов до уровня мелких ветвлений бронхиального дерева (6-9 генерация) в области наличия периферического образования. Далее под визуальным/рентгеноскопическим контролем выполняется биопсия с помощью гибких щипцов с диаметром 1.2 мм, либо тонкого одноразового криозонда диаметром 1,1 мм.
Заявленный способ позволяет повысить эффективность диагностики периферических образований легких в сравнении с классической бронхобиопсией с помощью стандартных гибких фибро- и видеобронхоскопов.
Заявляемое изобретение далее поясняется примерами, но не ограничено ими.
Пример 1.
Пациент У., 65 лет. Госпитализирован в стационар в связи с выявлением по данным компьютерной томографии при плановом обследовании образования в верхней доле правого легкого, позитивного по данным позитронно-эмиссионной томографии (фиг. 1, а). Пациенту выполнена навигационная бронхоскопия в условиях тотальной внутривенной анестезии с проведением ряда этапов:
Интубация трахеи тубусом ригидного бронхоскопа Karl Storz 11 размера;
Навигационная бронхоскопия цифровым холангиоскопом (система SpyGlass DS II, Boston Scientific Corp, USA) - проведена поэтапная визуализация долевого, сегментарного, субсегментарного бронхов и более глубоких их ветвлений до 8 порядка (фиг. 1, б, 1, в, 1, г).
В зоне интереса, наиболее близко расположенной к области поражения, выполнен ряд биопсий, на основании которых цитоморфологически подтверждена аденокарцинома легкого. В ходе продвижения гибкого холангиоскопа по мелким ветвлениям бронхиального дерева для раскрытия устьев мелких бронхов использована возможность подачи подогретого до 37°С физиологического раствора, также во время биопсий проводилась подача подогретого до 37°С физиологического раствора с целью визуального контроля зоны биопсии.
Пример 2.
Пациентка П., 36 лет. У пациентки с длительным течением саркоидоза легких, на фоне системной кортикостероидной терапии по данным компьютерной томографии выявлено полостное образование в нижней доле правого легкого на фоне тракционных бронхоэктазов и выраженных ретикулярных изменений (фиг. 2, а). Пациентке выполнена навигационная бронхоскопия в условиях тотальной внутривенной анестезии с проведением ряда этапов:
Интубация трахеи тубусом ригидного бронхоскопа.
Навигационная бронхоскопия цифровым холангиоскопом, проведена поэтапная визуализация долевого, сегментарного, субсегментарного бронхов и более глубоких их ветвлений до 9 порядка (фиг. 2, б, 2, в, 2, г).
По данным навигацинной бронхоскопии с помощью цифрового холангиоскопа эндоскопически подтверждено наличие полости, выполнен ряд биопсий, на основании которых цитоморфологически и микробиологически подтверждена аспергиллома легкого. В ходе продвижения гибкого холангиоскопа по мелким ветвлениям бронхиального дерева для раскрытия устьев мелких бронхов использована возможность подачи подогретого до 37°С физиологического раствора, также во время биопсий проводилась подача подогретого до 37°С физиологического раствора с целью визуального контроля зоны биопсии.
Пример 3.
Пациент Б., 77 лет. Госпитализирован в стационар в связи с выявлением по данным компьютерной томографии при плановом обследовании образования в нижней доле левого легкого (фиг. 3, а). Ранее пациенту выполнена навигационная бронхоскопия под контролем рентгеноскопии - материал неинформативен. По данным иммунологических тестов (Диаскин-тест, проба Манту, T-SPOT) заподозрен туберкулез легких. Пациенту выполнена навигационная бронхоскопия в условиях тотальной внутривенной анестезии с проведением ряда этапов:
Интубация трахеи тубусом ригидного бронхоскопа.
Навигационная бронхоскопия цифровым холангиоскопом проведена поэтапная визуализация долевого, сегментарного, субсегментарного бронхов и более глубоких их ветвлений до 8 порядка (фиг. 3, б, 3, в, 3, г).
В ходе продвижения гибкого холангиоскопа по мелким ветвлениям бронхиального дерева для раскрытия устьев мелких бронхов использована возможность подачи подогретого до 37°С физиологического раствора.
В зоне интереса, наиболее близко расположенной к области поражения, выполнен диагностический бронхоальвеолярный лаваж, на основании ПЦР-исследования, которого установлен диагноз туберкулеза легких.
Таким образом, в предложении заявителя реализуется требуемый технический результат, который заключается в повышении эффективности диагностической биопсии периферических образований легких, в частности, в области периферического образования мелких ветвлений бронхиального дерева.
Литература
1. Gould MK, Tang Т, Liu IL, Lee J, Zheng C, Danforth KN, et al. Recent trends in the identification of incidental pulmonary nodules. Am J Respir Crit Care Med. 2015; 192(10):1208-14
2. Wahidi MM, Govert JA, Goudar RK, Gould MK, DC MC, American College of Chest Physicians. Evidence for the treatment of patients with pulmonary nodules: when is it lung cancer?: ACCP evidencebased clinical practice guidelines (2nd edition). Chest. 2007; 132 (3 Suppl):94s-107s.
3. Yang W, Jiang H, Khan AN, Allen C, Bertolaccini L, Lv T, Song Y; written on behalf of the AME Lung Cancer Collaborative Group.Transthoracic needle aspiration in solitary pulmonary nodule. Transl Lung Cancer Res. 2017 Feb; 6(1):76-85. doi: 10.21037/tlcr.2017.02.03. PMID: 28331827; PMCID: PMC5344843.
4. Chockalingam A, Hong K. Transthoracic needle aspiration: the past, present and future. J Thorac Dis. 2015 Dec; 7(Suppl 4):S292-9. doi: 10.3978/j.issn.2072-1439.2015.12.01. PMID: 26807277; PMCID: PMC4700378.
5. Uchida J, Imamura F, Takenaka A, Yoshimura M, Ueno K, Oda K, Nakayama T, Tsukamoto Y, Higashiyama M, Kusunoki Y. Improved diagnostic efficacy by rapid cytology test in fluoroscopy-guided bronchoscopy. J Thorac Oncol. 2006 May; 1(4):314-8. PMID: 17409876.
6. Matsuno Y, Asano F, Shindoh J, Abe T, Shiraki A, Ando M, Suzuki T, Seko A, Moriwaki H. CT-guided ultrathin bronchoscopy: bioptic approach and factors in predicting diagnosis. Intern Med. 2011; 50(19):2143-8. doi: 10.2169/internalmedicine.50.5666. Epub 2011 Oct 1. PMID: 21963732.
7. ЭФФЕКТИВНОСТЬ ЭНДОБРОНХИАЛЬНОЙ УЛЬТРАСОНОГРАФИИ В ДИАГНОСТИКЕ ПЕРИФЕРИЧЕСКИХ ОБРАЗОВАНИЙ ЛЕГКИХ // Сивокозов И.В., Зайцев А.А., Фокин А.В., Артемкин Э.Н. Вестник рентгенологии и радиологии. 2013. №2. С. 16-20.
8. СРАВНИТЕЛЬНАЯ ЭФФЕКТИВНОСТЬ ВИРТУАЛЬНОЙ БРОНХОСКОПИИ И ЭНДОБРОНХИАЛЬНОЙ УЛЬТРАСОНОГРАФИИ В МАЛОИНВАЗИВНОЙ ДИАГНОСТИКЕ ПЕРИФЕРИЧЕСКИХ ОБРАЗОВАНИЙ ЛЕГКИХ: ПЕРВЫЙ ОПЫТ // Чесалина Я.О., Карпина Н.Л., Березовский Ю.С., Шишова С. В., Сивокозов И.В Пульмонология. 2021. Т. 31. №6. С.718-728.
9. Kemp SV. Navigation Bronchoscopy. Respiration. 2020; 99(4):277-286. doi: 10.1159/000503329. Epub 2019 Oct 10. PMID: 31600761.
10. Kurimoto N. Robotic-assisted bronchoscopy approaches for peripheral pulmonary lesions. Respirology. 2023 Jan; 28(1):15-16. doi: 10.1111/resp.14385. Epub 2022 Sep 27. PMID: 36168720.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭНДОСКОПИЧЕСКОЙ ДИАГНОСТИКИ САРКОИДОЗА ОРГАНОВ ДЫХАНИЯ ПУТЕМ СЕРИЙНОЙ ЭНДОБРОНХИАЛЬНОЙ КРИОБИОПСИИ | 2024 |
|
RU2836009C1 |
| СПОСОБ ВЕРИФИКАЦИИ ЭТИОЛОГИИ ДЕФОРМАЦИЙ ТРАХЕОБРОНХИАЛЬНОГО ДЕРЕВА | 2021 |
|
RU2766671C1 |
| СПОСОБ КОМБИНИРОВАННОЙ ЭНДОСКОПИЧЕСКОЙ ДИАГНОСТИКИ РЕНТГЕНОНЕГАТИВНЫХ СИНХРОННЫХ ЦЕНТРАЛЬНЫХ РАКОВ ЛЕГКИХ | 2016 |
|
RU2628649C1 |
| СПОСОБ ДИАГНОСТИКИ ПЕРИФЕРИЧЕСКИХ НОВООБРАЗОВАНИЙ ЛЕГКИХ С ЭНДОСОНОГРАФИЧЕСКИМ КОНТРОЛЕМ ПОЛОЖЕНИЯ ЭНДОСКОПИЧЕСКОГО ИНСТРУМЕНТА В ПАТОЛОГИЧЕСКОМ ОЧАГЕ | 2019 |
|
RU2719666C1 |
| СПОСОБ ЭНДОСКОПИЧЕСКОГО ЛЕЧЕНИЯ АБСЦЕССА ЛЕГКОГО | 2019 |
|
RU2719662C1 |
| Транспортная коаксиальная система для трансторакальной доставки игл к новообразованиям легкого и средостения с функцией перманентной анестезии | 2022 |
|
RU2797628C1 |
| СПОСОБ ПРОВЕДЕНИЯ БРОНХОАЛЬВЕОЛЯРНОГО ЛАВАЖА ПАЦИЕНТАМ С МАССИВНОЙ ОБСТРУКЦИЕЙ БРОНХИАЛЬНЫМ СЕКРЕТОМ | 2011 |
|
RU2443393C1 |
| СИСТЕМЫ ПОДАЧИ ЭНЕРГИИ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2721647C2 |
| СПОСОБ ВЫБОРА ТАКТИКИ ЭНДОСКОПИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С ОПУХОЛЕВЫМИ СТЕНОЗАМИ БИФУРКАЦИИ ТРАХЕИ И БРОНХОВ 1-3 ПОРЯДКА | 2024 |
|
RU2835734C1 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ ОТСЛЕЖИВАНИЯ ПРИ МЕДИЦИНСКОЙ ПРОЦЕДУРЕ | 2010 |
|
RU2544807C2 |
Изобретение относится к медицине и может быть использовано при диагностической биопсии периферических образований легких. Пациенту на предварительном этапе проводят компьютерную томографию органов грудной клетки (КТ) и на основании полученных изображений КТ и их постпроцессинговой обработки выполняют прицельную биопсию периферического образования с забором ткани для исследований, для чего на основании данных КТ используют холангиоскоп с дополнительным каналом для подачи физиологического раствора, подогретого до температуры 37°С, и биопсийным инструментарием, который проводится через трахею, один из главных бронхов до уровня мелких ветвлений бронхиального дерева в области наличия периферического образования, далее под визуальным контролем выполняют биопсию. Способ, за счет использования холангиоскопа с дополнительным каналом для подачи физиологического раствора, позволяет повысить эффективность диагностической биопсии периферических образований легких, в частности, в области периферического образования мелких ветвлений бронхиального дерева. 4 з.п. ф-лы, 3 ил., 3 пр.
1. Способ диагностической биопсии периферических образований легких, характеризующийся тем, что пациенту предварительно проводят компьютерную томографию органов грудной клетки (КТ) и на основании полученных изображений КТ выполняют прицельную биопсию периферического образования легкого с забором ткани для исследований, отличающийся тем, что на основании данных КТ используют холангиоскоп с дополнительным каналом для подачи жидкости физиологического раствора, подогретого до температуры 37°С, и биопсийным инструментарием, который проводится через трахею, один из главных бронхов до уровня мелких ветвлений бронхиального дерева в области наличия периферического образования, далее под визуальным контролем выполняют биопсию.
2. Способ по п. 1, отличающийся тем, что в качестве биопсийного инструментария используют гибкие щипцы.
3. Способ по пп. 1, 2, отличающийся тем, что используют гибкие щипцы с диаметром 1,2 мм.
4. Способ по п. 1, отличающийся тем, что в качестве биопсийного инструментария используют одноразовый криозонд.
5. Способ по пп. 1, 4, отличающийся тем, что используют одноразовый криозонд с диаметром 1,1 мм.
| СПОСОБ ДИАГНОСТИКИ ПЕРИФЕРИЧЕСКИХ НОВООБРАЗОВАНИЙ ЛЕГКИХ С ЭНДОСОНОГРАФИЧЕСКИМ КОНТРОЛЕМ ПОЛОЖЕНИЯ ЭНДОСКОПИЧЕСКОГО ИНСТРУМЕНТА В ПАТОЛОГИЧЕСКОМ ОЧАГЕ | 2019 |
|
RU2719666C1 |
| Способ выполнения прицельной пункционной FUSION-биопсии легких | 2020 |
|
RU2744532C1 |
| RU 2011125192 A, 27.12.2012 | |||
| WO 2015137870 A1, 17.09.2015 | |||
| US 2016242737 A1, 25.08.2016 | |||
| ЧЕСАЛИНА Я.О | |||
| и др | |||
| Сравнительная эффективность виртуальной бронхоскопии и эндобронхиальной ультрасонографии в малоинвазивной диагностике периферических образований легких: первый опыт, Пульмонология, | |||
Авторы
Даты
2023-10-16—Публикация
2023-02-17—Подача